JP4801445B2 - 生体分子の検出方法及びそれに用いる標識色素並びに標識キット - Google Patents
生体分子の検出方法及びそれに用いる標識色素並びに標識キット Download PDFInfo
- Publication number
- JP4801445B2 JP4801445B2 JP2005516510A JP2005516510A JP4801445B2 JP 4801445 B2 JP4801445 B2 JP 4801445B2 JP 2005516510 A JP2005516510 A JP 2005516510A JP 2005516510 A JP2005516510 A JP 2005516510A JP 4801445 B2 JP4801445 B2 JP 4801445B2
- Authority
- JP
- Japan
- Prior art keywords
- group
- dye
- biomolecule
- organic
- substituent
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- 0 CC1(C2)C(*)=C(*)N=C(*)C2(C)c2c1c(*)c(C1(C)NN=IC3(C)C1)c3c2* Chemical compound CC1(C2)C(*)=C(*)N=C(*)C2(C)c2c1c(*)c(C1(C)NN=IC3(C)C1)c3c2* 0.000 description 2
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/58—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving labelled substances
- G01N33/582—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving labelled substances with fluorescent label
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/531—Production of immunochemical test materials
- G01N33/532—Production of labelled immunochemicals
- G01N33/533—Production of labelled immunochemicals with fluorescent label
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6813—Hybridisation assays
- C12Q1/6816—Hybridisation assays characterised by the detection means
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/62—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light
- G01N21/63—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light optically excited
- G01N21/64—Fluorescence; Phosphorescence
- G01N21/6428—Measuring fluorescence of fluorescent products of reactions or of fluorochrome labelled reactive substances, e.g. measuring quenching effects, using measuring "optrodes"
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/62—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light
- G01N21/63—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light optically excited
- G01N21/64—Fluorescence; Phosphorescence
- G01N21/645—Specially adapted constructive features of fluorimeters
- G01N21/6452—Individual samples arranged in a regular 2D-array, e.g. multiwell plates
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/52—Use of compounds or compositions for colorimetric, spectrophotometric or fluorometric investigation, e.g. use of reagent paper and including single- and multilayer analytical elements
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/58—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving labelled substances
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/62—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light
- G01N21/63—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light optically excited
- G01N21/64—Fluorescence; Phosphorescence
- G01N21/6428—Measuring fluorescence of fluorescent products of reactions or of fluorochrome labelled reactive substances, e.g. measuring quenching effects, using measuring "optrodes"
- G01N2021/6439—Measuring fluorescence of fluorescent products of reactions or of fluorochrome labelled reactive substances, e.g. measuring quenching effects, using measuring "optrodes" with indicators, stains, dyes, tags, labels, marks
Description
Science 283,1,January,1999,83-87
すなわち、有機EL色素は固体状態(固体及び半固体を含む)で高い量子収率を有しており高い蛍光強度を有している。さらに、有機EL色素はCy3やCy5に比べ安価であるので、より低コストで生体分子の検出を行うことができる。また、有機EL色素は生体分子とほぼ定量的に反応し、高い取り込み率を有しているので、高い検出感度を得ることができる。また、蛍光波長の選択の自由度が増加し、オレンジ、イエロー、グリーン、ブルーなど多くの蛍光波長を用いることができる。これにより、ストークスシフトの大きい(励起波長と蛍光波長の差が大きい)2種以上の蛍光色素を用いることが可能となるので、一つの試料中に含まれる複数の標的核酸を同時に検出することも可能となる。また、Cy3やCy5は冷凍保存する必要があるのに対し、有機EL色素は化学的に安定であり、常温での長期保存に耐えることができるので、取り扱いが容易である。
2 電極
3 電極
4 プローブ核酸
4a 有機EL色素
5 標的核酸
本発明に用いる有機EL色素は、一対の陽極と陰極との間に固体状態で挟持され、陽極から注入された正孔と陰極から注入された電子とが再結合する際のエネルギーにより発光可能な色素であれば特に限定されない。例えば、テトラフェニルブタジエンやペリレン等の多環芳香族化合物、シクロペンタジエン誘導体、ジスチリルピラジン誘導体、アクリドン誘導体、キナクドリン誘導体、スチルベン誘導体、フェノチアジン誘導体、ピラジノピリジン誘導体、アゾール誘導体、イミダゾール誘導体、カルバゾール誘導体そしてテトラフェニルチオフェン誘導体等を用いることができる。さらに、分子内にカルボン酸基を有し、又はカルボン酸基を導入可能な色素であることが好ましい。以下に述べるように、生体分子と結合するための反応性基の導入を容易に行うことができるからである。
以下に、縮合多環化合物の具体例について説明する。
R'は芳香環を含んでも良いアルキル基又はアルケニル基等の脂肪族炭化水素基あるいは芳香族炭化水素基、An-は、Cl-、Br-、I-等のハロゲン化物イオン、CF3SO3 -、BF4 -、PF6 -を示す。なお、以下の一般式においても、特に断らない限り同様である。
また、チオフェン誘導体の場合、非縮合系の化合物であり、以下の一般式で示される2,3,4,5-テトラフェニルチオフェン誘導体を用いることもできる。
また、以下の一般式で示される2,3,4,5-テトラフェニルチオフェン誘導体を用いることもできる。
また、以下の一般式で示されるカルバゾール誘導体を用いることもできる。
(DNAマイクロアレイ法)
本検出方法は、検出すべき標的核酸に有機EL色素を反応させて有機EL色素で標識する一方、標的核酸に対して相補的な塩基配列を有する一本鎖のプローブ核酸を用意し、一本鎖に変成させた標的核酸とプローブ核酸とを基板上でハイブリダイズさせ、標的核酸の蛍光を測定する。本検出方法では、基板に固定するプローブ核酸には、遺伝子の発現を調べる場合、cDNA等をcDNAのライブラリー、ゲノムのライブラリー又は全ゲノムをテンプレートとしてPCR法により増幅して調製したものを用いることができる。また、遺伝子の変異等を調べる場合、標準となる既知の配列をもとにして、変異等に対応する種々のオリゴヌクレオチドを合成したものを用いることができる。
(PCR法)
(PCR法)
本検出方法は、検出すべき標的核酸の塩基配列に相補的なプローブを有機EL色素で標識し、標的核酸の増幅に先立って、あるいは増幅させた後、標的核酸とプローブとを反応させ、標的核酸の蛍光を測定する。具体的には、標的核酸の伸長反応は酵素(DNAポリメラーゼ、RNAポリメラーゼ)によって行われ、このとき標的核酸とオリゴヌクレオチドからなるプライマーとが形成した2本鎖核酸配列を酵素が認識し、その認識した位置から伸長反応が行われ、目的とする遺伝子領域だけを増幅させる。酵素が合成を行う際ヌクレオチド(dNTP、NTP)を原料として合成反応が行われる。このとき通常のヌクレオチド(dNTP、NTP)に、例えば、図27に示すような、色素を有するヌクレオチドを任意の割合で混合すると、その割合の色素が導入された核酸を合成することができる。または、PCRにより、任意の割合でアミノ基を有するヌクレオチドを導入した後に有機EL色素を結合させ、有機EL色素が導入された核酸を合成することも可能である。
これらを生細胞において動的に観察することで細胞のシグナル伝達の観察を行うことができる。
合成例1.
有機EL色素として1, 2, 5,-オキサジアゾロ-[3, 4-c]ピリジン誘導体を用いた。
以下に、1, 2, 5,-オキサジアゾロ-[3, 4-c]ピリジンの活性エステル体(以下、EL-OSuと略す。)の合成スキームを示す。
500mL三口フラスコに4-メトキシアセトフェノン(1)37.5 g (0.25 mol)、亜硝酸ナトリウム0.15 gを酢酸100 mLに溶解した。水浴中、HNO3 100 mLを酢酸100 mLに溶解したものを2時間かけて滴下した。その後、室温で2日間撹拌した。反応混合物を500mLの水にゆっくりと入れ、沈殿を生成させた。沈殿物は濾過し、クロロホルムに溶解した。クロロホルム相を飽和重曹水で洗浄し、10% NaCl 水溶液で2回洗浄した。MgSO4で脱水した後、減圧下、クロロホルムを留去し、オキサジアゾール-N-オキサイド(2)を34.5 g (収率78%)で得た。
500mL三口フラスコにオキサジアゾール-N-オキサイド(2)17.7 g (0.05 mol)をアセトニトリル400 mLに溶解した。それにZn 12.0 g、AcOH 7 mL、Ac2O 20mLを添加した。水浴中で反応温度が30℃を超えないように冷却した。12時間撹拌して反応終点とした。反応混合物を濾過し、不溶分を除去した。アセトニトリルを減圧下留去して残渣を得た。残渣をクロロホルムで再結晶し、オキサジアゾール-N-オキサイド(3)を10.2 g (収率60%)で得た。
500mL三口フラスコでオキサジアゾール-N-オキサイド(3)15.6 g (0.046 mol)をブタノール300 mLに溶解した。そこへグリシンエチルエステル塩酸塩 32.0 g (0.23 mol)を添加した。24時間加熱還流を行った。ブタノールを減圧下留去し、残渣を得た。残渣を200mLのクロロホルムに溶解し、10% HCl、飽和NaHCO3、10%NaClで洗浄した。MgSO4で乾燥し、溶媒を留去した。得られた残渣をクロロホルムで再結晶し、オキサジアゾロピリジンエチルエステル(4)を13.0 g (収率 70%)で得た。
500mL三口フラスコでオキサジアゾロピリジンエチルエステル(4)3.0 g (0.007 mol)を200 mLのエタノールに溶解した。そこへKOH 0.62 g (0.01 mol)を添加した。5時間加熱環流を行った後、反応混合物を200 mLの水へ添加した。この水溶液に濃塩酸を滴下してpH 1に調整したところ沈殿が生じた。沈殿物を濾過し、クロロホルムに溶解した。クロロホルム相を10% NaHCO3水溶液、水で洗浄した。クロロホルムを留去して残渣を得た。残渣を水-エタノール (1:1)で再結晶し、2.1 g (収率 81%)のオキサジアゾロピリジンカルボン酸(5)を得た。
50 mL 三口フラスコでオキサジアゾロピリジンカルボン酸(5)1.0 g (0.0026 mol)とN-ヒドロキシスクシンイミド0.30 g (0.0026 mol)をDMF 20mLに溶解した。これにN, N'-ジシクロヘキシルカルボジイミド 0.54 g (0.0026 mol)を30分かけて滴下した。滴下後、室温で30時間撹拌した。減圧下、DMFを留去した。残渣をシリカゲルカラムクロマトグラフィー(クロロホルム)で単離精製し、オキサジアゾロピリジン活性エステル体(6)を0.76 g (収率62%)得た。
有機EL色素としてイミダゾロピリジンエチルエステル誘導体を用いた。以下に、イミダゾロピリジンエチルエステルの活性エステル体(以下、im-EL-OSuと略す。)の合成スキームを示す。
500mL三口フラスコでエステル体1 0.5 g (1.5 mmol)を50 mLのエタノールに溶解した。そこへKOH 0.12 g (2.1 mol)を添加した。5時間加熱環流を行った後、反応混合物を50 mLの水へ添加した。この水溶液に濃塩酸を滴下してpH 1に調整したところ沈殿が生じた。沈殿物を濾過し、クロロホルムに溶解した。クロロホルム相を10% NaHCO3水溶液、水で洗浄した。クロロホルムを留去して残渣を得た。残渣を水で再結晶し、0.3 g (収率 63%)のカルボン酸 2 を得た。
50 mL 三口フラスコでカルボン酸誘導体2 0.2 g (0.6 mmol)とN-ヒドロキシスクシンイミド0.07 g (0.6 mmol)をDMF 10mLに溶解した。これにN, N'-ジシクロヘキシルカルボジイミド 0.12 g (0.6 mmol)を30分かけて滴下した。滴下後、室温で30時間撹拌した。減圧下、DMFを留去した。残渣をシリカゲルカラムクロマトグラフィー(クロロホルム)で単離精製し、活性エステル体3を0.14 g (収率55%)得た。
〈オリゴヌクレオチドの色素標識及び検出(1)〉
1.オリゴヌクレオチドの色素標識
オリゴヌクレオチドの色素標識は、以下のスキーム5で行った。
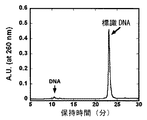
H2N-dT20(40 mmol)を含むNa2CO3/NaHCO3buffer(pH 9.0)40 μlに、有機EL色素の活性エステル5.0 μmol(2.4 mg)を含む無水 DMSO溶液12 μlを加えて室温で6時間振とうした。振とう後、全量が1mlになるように0.1M TEAA(triethylamine-acetic acid)buffer(pH7.0)を加え、NAP-10カラム(Parmacia SephadexG-25)を用いてオリゴヌクレオチドに由来する成分を分取した。その際、NAP-10カラムはあらかじめ0.1M TEAA buffer 15mlで平衡化させた後使用した。全量が1mlになるようにメスアップした試料をカラムに充填し、1mlの溶液が溶出した後、0.1M TEAA bufferを1.5mlチャージした。この直後からの溶出液1.5mlを分取した。この得られた溶液を一晩凍結乾燥し、滅菌蒸留水20μlを加えて逆相HPLCにより分析した。HPLCにインジェクトした溶液は、40分の1に希釈して分析した。
カラム:Lichrospher RP-18(Cica-MERCK) 流速:1ml/min
検出波長:260nm 試料注入溶媒:超純水
溶離液A:0.1M TEAA buffer(pH7.0), 10% CH3CN溶液
溶離液B:0.1M TEAA buffer(pH7.0), 40% CH3CN溶液
次に、以下の表2に示すように、標識されたオリゴヌクレオチドの濃度の異なる溶液を調製した。次いで、その溶液1nLをガラス基板上にスポット(5×5)した。スポット後、ガラス基板を乾燥した。
ここで、検出機器には、BIO-RAD モレキュラーイメージャー FX Proを用いた。レーザの波長は488 nm、スキャン間隔は50nmである。
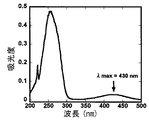
今回、検出に用いた励起光は488 nmのレーザ光であり、蛍光色素の励起波長は438 nmである。それにも拘わらず、標識されたオリゴヌクレオチドの相対濃度の検出限界は0.5 fmol (500 amol)であり高感度な検出が可能であった。また、DNAとの反応はほぼ定量的であり、反応時間も従来の24時間程度から6時間程度に短縮することが可能であった。さらに、このEL色素は安定であり、15日間、室温下で保存したEL色素を用いて再測定しても、同等の結果が得られた。
〈オリゴヌクレオチドの色素標識及び検出(2)〉
1.オリゴヌクレオチドの色素標識
オリゴヌクレオチドの色素標識は、以下のスキーム6で行った。標識の条件は実施例1の場合と同様である。イミダゾール誘導体の付加反応は速やかに且つほぼ定量的に進行した。
カラム:Lichrospher RP-18(Cica-MERCK) 流速:1ml/min
検出波長:260nm 試料注入溶媒:超純水
溶離液A:0.1M TEAA buffer(pH7.0), 10% CH3CN溶液
溶離液B:0.1M TEAA buffer(pH7.0), 40% CH3CN溶液
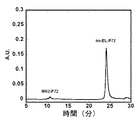
なお、HPLC測定のグラジエント条件は実施例1の場合と同様である。標識されたオリゴヌクレオチドのHPLCスペクトルと目的物のUVスペクトルをそれぞれ図4Aと図4Bに示す。HPLCの結果、RT=25 min付近に目的物由来のピークが得られたと判断し、HPLC分取を行った。
標識されたオリゴヌクレオチドの相対濃度の検出限界は10fmolであり高感度な検出が可能であった。また、オリゴヌクレオチドとEL色素との反応はほぼ定量的であった。
〈ペプチド類の標識及び検出〉
1.Ac-Lys(EL)-Lys-Lys-Lys(Acr)-Lys-Lys-Lys(Acr)-Lys-Lys-NH2の合成
(1)Ac-Lys(Mtt)-(Lys(Boc))2-Lys(Acr)-(Lys(Boc))2-Lys(Acr)-(Lys(Boc))2-Resinの合成
(実験操作)
リアクションベッセルにFmoc-NH-SAL Resin 0.15g(0.61mmol/g)を入れ、カートリッジ3, 6にFmoc-Lys(Acr)-OHを0.26gずつ、カートリッジ1,2,4,5,7,8にFmoc-Lys(Boc)-OHを0.18gずつ、カートリッジ9にFmoc-Lys(Mtt)-OHを0.23g入れた。後は、Applied Biosystems社の431A peptide synthesizerを用いて合成を行った。Methodは、standard Fmoc法で行い、N末端はアセチル化した。黄色固体のペプチドレジンが得られ、収量は0.30gであった。
(実験操作)
i)Mtt基の脱保護
スクリュー管に1で合成したペプチドレジン0.30g入れ、これに過剰のジクロロメタン(DCM)を加えて30分かけて膨潤させた後、過剰のDCMを窒素ガスで除いた。その後、DCM:TFA:TIPS(トリイソプロピルシラン)=94:1:5の混合溶液4mlを加えて2分攪拌し、窒素ガスで溶媒を除いた。この操作を5回繰り返した後、吸引濾過しDCM、トリエチルアミン、DCMで洗浄後、減圧乾燥させた。
ii)メトキシ型有機EL色素の修飾
減圧乾燥させたペプチドレジンにNMP 6mlを加えて30分間攪拌して膨潤させ、トリエチルアミン 0.15mlを加えて攪拌した。さらに、活性エステル(6)0.2gを加えて室温で24時間攪拌した。その後吸引濾過し、NMP、DCMで洗浄して減圧乾燥させた。
iii)レジンからの切り出し及び側鎖の脱保護
減圧乾燥させたペプチドレジンにm-クレゾール 0.08ml、チオアニソール 0.48ml、TFA 3.44mlを加えて室温で1時間半撹拌した。その後、吸引濾過しTFAで洗浄した。TFAを減圧留去した後、氷浴中でエーテル15ml加えた。超音波処理後、しばらく放置し、上澄み液を取り除いた。次に、氷浴中で酢酸エチル15mlを加えて、超音波処理後、しばらく放置した。その後、吸引濾過しエーテルで洗浄後、減圧乾燥させた。
実施例1と同様の方法により、ガラス基板上にスポットした標識ペプチドの検出を行った。検出機器には、BIO-RAD モレキュラーイメージャー FX Proを用いた。レーザの波長は488 nm、スキャン間隔は50nmである。
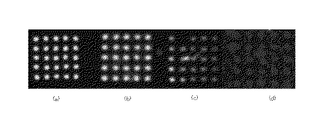
図8は標識されたペプチドの発光パターンであり、(a)、(b)、(c)、(d)、(e)は、それぞれ10fmol、5fmol、1fmol、0.5fmol、0.1fmolの結果を示す。標識されたペプチドの相対濃度の検出限界は0.1 fmol (100 amol)であり高感度な検出が可能であった。また、ペプチドとEL色素との反応はほぼ定量的であった。
〈タンパク質の色素標識及び検出〉
1.タンパク質の色素標識
BSAのリジン残基のアミノ基と有機EL色素の活性エステルを反応させてアミド結合を形成させて、BSAの標識化を行った。具体的には、BSA(Bovine Serium Albumin) 4.0 mg(58 nmol)を含む炭酸buffer(pH9.0) 58 μlに、有機EL色素の活性エステル(EL-OSu)3.6 mg(8.6 μmol)を含むDMSO溶液40μl加えて37℃で24時間振盪した。その後全量が1 mlになるように0.1 M TEAA buffer(pH7.0)を加え、NAP-10カラム(Parmacia SephadexG-25)を用いてBSAに由来する成分を分取し、分取した溶液を一晩凍結乾燥した。
(結果)
調製したBSAは、図10に示すように固体状態で蛍光を発した。このように有機EL色素活性エステルにより、タンパク質を標識化できることが明らかとなった。
Claims (11)
- 生体分子試料と、有機EL色素で標識されたプローブとを反応させ、該生体分子試料の蛍光を測定する生体分子の検出方法であって、
上記有機EL色素が以下の一般式(1)で示されるアゾール誘導体あるいは以下の一般式(4)で表されるイミダゾール誘導体である生体分子の検出方法。
(式中、R2、R 3 は、それぞれ独立に、炭素数1から4のアルキル基またはアルコキシ基を有してもよい芳香族炭化水素基を示し、R1は水素原子、ハロゲン原子、エステル基、置換基としてヒドロキシル基、シアノ基あるいはスルホニル基を有してもよい芳香族炭化水素基又は炭化水素基又は複素環基又はヘテロ原子を環内に含む芳香族基を示し、Xは置換基を有していてもよい酸素原子を示す。)
(式中、R2、R3、R 4 は、それぞれ、置換基としてヒドロキシル基、シアノ基あるいはスルホニル基を有しても良い芳香族炭化水素基を示し、R2、R3、R 4 は同じでも異なっていても良く、R1は水素原子、ハロゲン原子、エステル基、置換基としてヒドロキシル基、シアノ基あるいはスルホニル基を有してもよい芳香族炭化水素基又は炭化水素基又は複素環基又はヘテロ原子を環内に含む芳香族基を示す。) - 上記生体分子試料が核酸であり、上記プローブには該核酸の塩基配列に相補的なオリゴヌクレオチド又はPNAを用いる請求項1記載の検出方法。
- 上記オリゴヌクレオチドがプライマー又はターミネータであり、上記核酸を増幅させて蛍光を測定する請求項2記載の検出方法。
- 上記核酸の増幅に先立ってプライマーを有機EL色素で標識する請求項3記載の検出方法。
- 上記オリゴヌクレオチド又はPNAがモレキュラービーコンである請求項2記載の検出方法。
- 生体分子試料を電気泳動によりサイズ分離する工程を含み、該電気泳動に先立ってあるいは該電気泳動後に生体分子試料を有機EL色素で標識する生体分子の検出方法であって、
上記有機EL色素が以下の一般式(1)で示されるアゾール誘導体あるいは以下の一般式(4)で表されるイミダゾール誘導体である生体分子の検出方法。
(式中、R2、R 3 は、それぞれ独立に、炭素数1から4のアルキル基またはアルコキシ基を有してもよい芳香族炭化水素基を示し、R1は水素原子、ハロゲン原子、エステル基、置換基としてヒドロキシル基、シアノ基あるいはスルホニル基を有してもよい芳香族炭化水素基又は炭化水素基又は複素環基又はヘテロ原子を環内に含む芳香族基を示し、Xは置換基を有していてもよい酸素原子を示す。)
(式中、R2、R3、R 4 は、それぞれ、置換基としてヒドロキシル基、シアノ基あるいはスルホニル基を有しても良い芳香族炭化水素基を示し、R2、R3、R 4 は同じでも異なっていても良く、R1は水素原子、ハロゲン原子、エステル基、置換基としてヒドロキシル基、シアノ基あるいはスルホニル基を有してもよい芳香族炭化水素基又は炭化水素基又は複素環基又はヘテロ原子を環内に含む芳香族基を示す。) - 上記生体分子試料が核酸であり、電気泳動画像に基づいて該核酸の塩基配列を決定する請求項6記載の検出方法。
- 上記生体分子試料がタンパク質であり、電気泳動画像に基づいて取り出したタンパク質を質量分析する請求項6記載の検出方法。
- 組織又は細胞試料中の生体分子を有機EL色素で標識する組織又は細胞の染色方法であって、
上記有機EL色素が以下の一般式(1)で示されるアゾール誘導体あるいは以下の一般式(4)で表されるイミダゾール誘導体である組織又は細胞の染色方法。
(式中、R2、R 3 は、それぞれ独立に、炭素数1から4のアルキル基またはアルコキシ基を有してもよい芳香族炭化水素基を示し、R1は水素原子、ハロゲン原子、エステル基、置換基としてヒドロキシル基、シアノ基あるいはスルホニル基を有してもよい芳香族炭化水素基又は炭化水素基又は複素環基又はヘテロ原子を環内に含む芳香族基を示し、Xは置換基を有していてもよい酸素原子を示す。)
(式中、R2、R3、R 4 は、それぞれ、置換基としてヒドロキシル基、シアノ基あるいはスルホニル基を有しても良い芳香族炭化水素基を示し、R2、R3、R 4 は同じでも異なっていても良く、R1は水素原子、ハロゲン原子、エステル基、置換基としてヒドロキシル基、シアノ基あるいはスルホニル基を有してもよい芳香族炭化水素基又は炭化水素基又は複素環基又はヘテロ原子を環内に含む芳香族基を示す。) - 上記生体分子が核酸又はタンパク質である請求項9記載の染色方法。
- 組織又は細胞試料の染色に用いる染色色素であって、組織又は細胞中の生体分子と結合する反応性基を有する有機EL色素から成る染色色素であって、
であって、
上記有機EL色素が以下の一般式(1)で示されるアゾール誘導体あるいは以下の一般式(4)で表されるイミダゾール誘導体である染色色素。
(式中、R2、R 3 は、それぞれ独立に、炭素数1から4のアルキル基またはアルコキシ基を有してもよい芳香族炭化水素基を示し、R1は水素原子、ハロゲン原子、エステル基、置換基としてヒドロキシル基、シアノ基あるいはスルホニル基を有してもよい芳香族炭化水素基又は炭化水素基又は複素環基又はヘテロ原子を環内に含む芳香族基を示し、Xは置換基を有していてもよい酸素原子を示す。)
(式中、R2、R3、R 4 は、それぞれ、置換基としてヒドロキシル基、シアノ基あるいはスルホニル基を有しても良い芳香族炭化水素基を示し、R2、R3、R 4 は同じでも異なっていても良く、R1は水素原子、ハロゲン原子、エステル基、置換基としてヒドロキシル基、シアノ基あるいはスルホニル基を有してもよい芳香族炭化水素基又は炭化水素基又は複素環基又はヘテロ原子を環内に含む芳香族基を示す。)
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2005516510A JP4801445B2 (ja) | 2003-12-24 | 2004-12-22 | 生体分子の検出方法及びそれに用いる標識色素並びに標識キット |
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2003427268 | 2003-12-24 | ||
| JP2003427268 | 2003-12-24 | ||
| JP2005516510A JP4801445B2 (ja) | 2003-12-24 | 2004-12-22 | 生体分子の検出方法及びそれに用いる標識色素並びに標識キット |
| PCT/JP2004/019215 WO2005062046A1 (ja) | 2003-12-24 | 2004-12-22 | 生体分子の検出方法及びそれに用いる標識色素並びに標識キット |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JPWO2005062046A1 JPWO2005062046A1 (ja) | 2007-12-13 |
| JP4801445B2 true JP4801445B2 (ja) | 2011-10-26 |
Family
ID=34708888
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2005516510A Expired - Fee Related JP4801445B2 (ja) | 2003-12-24 | 2004-12-22 | 生体分子の検出方法及びそれに用いる標識色素並びに標識キット |
Country Status (8)
| Country | Link |
|---|---|
| US (1) | US7662555B2 (ja) |
| EP (1) | EP1712911B1 (ja) |
| JP (1) | JP4801445B2 (ja) |
| KR (1) | KR101171253B1 (ja) |
| CN (1) | CN1902490B (ja) |
| AT (1) | ATE520983T1 (ja) |
| HK (1) | HK1097046A1 (ja) |
| WO (1) | WO2005062046A1 (ja) |
Families Citing this family (17)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20040137368A1 (en) * | 2003-01-13 | 2004-07-15 | 3D Systems, Inc. | Stereolithographic resins containing selected oxetane compounds |
| US8304259B2 (en) * | 2005-07-28 | 2012-11-06 | Shinichiro Isobe | Labeling dye for detecting biomolecule, labeling kit, and method for detecting biomolecule |
| JP4860352B2 (ja) * | 2006-05-23 | 2012-01-25 | 信一郎 礒部 | 診断薬及びそれを用いた測定方法 |
| WO2008018129A1 (fr) * | 2006-08-09 | 2008-02-14 | Shinichiro Isobe | Procédé de détection de protéine et colorant fluorescent utilisé à cet effet |
| FR2910278A1 (fr) * | 2006-12-26 | 2008-06-27 | Oreal | Compositions comprenant un colorant direct et un tensioactif, procede et utilisation pour la coloration notamment eclaircissante des matieres keratiniques |
| FR2910277A1 (fr) * | 2006-12-26 | 2008-06-27 | Oreal | Compositions comprenant un colorant direct et un epaississant, procede et utilisation pour la coloration notamment eclaircissante des matieres keratiniques |
| KR101360014B1 (ko) | 2010-11-12 | 2014-02-11 | 신에쓰 가가꾸 고교 가부시끼가이샤 | 근적외광 흡수 색소 화합물, 근적외광 흡수막 형성 재료, 및 이것에 의해 형성되는 근적외광 흡수막 |
| JP5539920B2 (ja) * | 2011-03-18 | 2014-07-02 | 信一郎 礒部 | 診断薬及びそれを用いた測定方法 |
| US20130277384A1 (en) * | 2012-04-24 | 2013-10-24 | Ivan TYUSHKEVICH | Dispenser for flat flexible items |
| EP2906720A4 (en) | 2012-10-10 | 2016-06-01 | Univ Arizona | SYSTEMS AND DEVICES FOR DETECTING MOLECULES AND METHOD FOR THE PRODUCTION THEREOF |
| EP3462167A1 (en) * | 2013-03-05 | 2019-04-03 | Arizona Board of Regents on behalf of Arizona State University | Translocation of a polymer through a nanopore |
| US10336713B2 (en) | 2014-02-27 | 2019-07-02 | Arizona Board Of Regents, Acting For And On Behalf Of, Arizona State University | Triazole-based reader molecules and methods for synthesizing and use thereof |
| JP6808818B2 (ja) | 2017-03-30 | 2021-01-06 | 富士フイルム株式会社 | 生体試料中の測定対象物質を測定するためのキット及び方法 |
| CN110520731B (zh) | 2017-03-30 | 2023-04-28 | 富士胶片株式会社 | 用于对测定对象物质进行测定的试剂盒、方法及试剂 |
| KR20190120329A (ko) * | 2017-03-30 | 2019-10-23 | 후지필름 가부시키가이샤 | 생체 시료 중의 측정 대상 물질을 측정하기 위한 키트 및 방법 |
| CN107488657A (zh) * | 2017-08-15 | 2017-12-19 | 苏州泽科生物科技有限公司 | 核酸的活性染料偶联标记、检测及提纯方法 |
| CN107354155A (zh) * | 2017-08-25 | 2017-11-17 | 苏州泽科生物科技有限公司 | 三基色核酸分子量标准试剂盒及其使用方法 |
Citations (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH04308689A (ja) * | 1991-04-08 | 1992-10-30 | Mitsubishi Kasei Corp | 有機電界発光素子 |
| JPH09505464A (ja) * | 1993-09-22 | 1997-06-03 | イゲン,インコーポレーテッド | 自立性配列複製電気化学発光核酸測定法 |
| JP2000095766A (ja) * | 1998-09-24 | 2000-04-04 | Minolta Co Ltd | 新規ベンゾイミダゾール化合物、その製造法および用途 |
| JP2001153870A (ja) * | 1999-11-25 | 2001-06-08 | Hitachi Software Eng Co Ltd | ハイブリダイゼーション装置、ケース、支持体、及び、標識試薬 |
| JP2001288197A (ja) * | 2000-04-10 | 2001-10-16 | Fuji Photo Film Co Ltd | 蛍光ヌクレオチド |
| JP2002161135A (ja) * | 2000-09-14 | 2002-06-04 | Fuji Photo Film Co Ltd | アミン系高分子複合体及びその製造方法、有機el素子及びその製造方法、並びに、光電変換有機デバイス |
| JP2002173673A (ja) * | 2000-12-05 | 2002-06-21 | Keio Gijuku | 発光材料及び有機el素子 |
| JP2003027049A (ja) * | 2001-07-23 | 2003-01-29 | Toyo Ink Mfg Co Ltd | 有機エレクトロルミネッセンス素子材料及びそれを使用した有機エレクトロルミネッセンス素子 |
| JP2003532790A (ja) * | 2000-05-05 | 2003-11-05 | コールター インターナショナル コーポレイション | 未成熟赤血球細胞における核酸の検出用色素及び方法 |
Family Cites Families (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5132206A (en) * | 1984-06-11 | 1992-07-21 | Dreyer William J | Fluorescent pigments for tagging biological molecules |
| US5075215A (en) * | 1984-06-11 | 1991-12-24 | Dreyer William J | Use of daylight fluorescent pigments for tagging biological molecules |
| DE19504198A1 (de) * | 1995-02-09 | 1996-08-14 | Behringwerke Ag | Kompetitiver Immuntest unter Verwendung komplexierter Analytderivate |
| US5753439A (en) * | 1995-05-19 | 1998-05-19 | Trustees Of Boston University | Nucleic acid detection methods |
| EP2295988A2 (en) * | 1996-12-31 | 2011-03-16 | High Throughput Genomics, Inc. | Multiplexed molecular analysis apparatus and its fabrication method |
| JP2002060744A (ja) | 2000-08-21 | 2002-02-26 | Showa Denko Kk | 有機エレクトロルミネッセンス素子材料、それを用いた有機エレクトロルミネッセンス素子及びその製造方法 |
| US7138506B2 (en) * | 2001-05-09 | 2006-11-21 | Genetic Id, Na, Inc. | Universal microarray system |
| US20030114399A1 (en) * | 2001-07-23 | 2003-06-19 | Blakely Randy D. | Human and mouse choline transporter cDNA |
| JP4274403B2 (ja) * | 2002-03-25 | 2009-06-10 | 大日本印刷株式会社 | 蛍光発光色素材料 |
| JP2004187563A (ja) | 2002-12-10 | 2004-07-08 | Peptide Door Co Ltd | IgGに結合性を有するペプチド又は該ペプチドを表面に呈示したファージを用いたIgGの検出方法 |
| JP3881667B2 (ja) * | 2003-12-24 | 2007-02-14 | 信一郎 礒部 | 生体分子の検出方法及びそれに用いる標識色素並びに標識キット |
-
2004
- 2004-12-22 KR KR1020067014817A patent/KR101171253B1/ko not_active IP Right Cessation
- 2004-12-22 CN CN2004800387729A patent/CN1902490B/zh not_active Expired - Fee Related
- 2004-12-22 US US10/584,089 patent/US7662555B2/en not_active Expired - Fee Related
- 2004-12-22 EP EP04807572A patent/EP1712911B1/en not_active Expired - Fee Related
- 2004-12-22 JP JP2005516510A patent/JP4801445B2/ja not_active Expired - Fee Related
- 2004-12-22 AT AT04807572T patent/ATE520983T1/de active
- 2004-12-22 WO PCT/JP2004/019215 patent/WO2005062046A1/ja active Application Filing
-
2007
- 2007-04-27 HK HK07104496.4A patent/HK1097046A1/xx not_active IP Right Cessation
Patent Citations (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH04308689A (ja) * | 1991-04-08 | 1992-10-30 | Mitsubishi Kasei Corp | 有機電界発光素子 |
| JPH09505464A (ja) * | 1993-09-22 | 1997-06-03 | イゲン,インコーポレーテッド | 自立性配列複製電気化学発光核酸測定法 |
| JP2000095766A (ja) * | 1998-09-24 | 2000-04-04 | Minolta Co Ltd | 新規ベンゾイミダゾール化合物、その製造法および用途 |
| JP2001153870A (ja) * | 1999-11-25 | 2001-06-08 | Hitachi Software Eng Co Ltd | ハイブリダイゼーション装置、ケース、支持体、及び、標識試薬 |
| JP2001288197A (ja) * | 2000-04-10 | 2001-10-16 | Fuji Photo Film Co Ltd | 蛍光ヌクレオチド |
| JP2003532790A (ja) * | 2000-05-05 | 2003-11-05 | コールター インターナショナル コーポレイション | 未成熟赤血球細胞における核酸の検出用色素及び方法 |
| JP2002161135A (ja) * | 2000-09-14 | 2002-06-04 | Fuji Photo Film Co Ltd | アミン系高分子複合体及びその製造方法、有機el素子及びその製造方法、並びに、光電変換有機デバイス |
| JP2002173673A (ja) * | 2000-12-05 | 2002-06-21 | Keio Gijuku | 発光材料及び有機el素子 |
| JP2003027049A (ja) * | 2001-07-23 | 2003-01-29 | Toyo Ink Mfg Co Ltd | 有機エレクトロルミネッセンス素子材料及びそれを使用した有機エレクトロルミネッセンス素子 |
Also Published As
| Publication number | Publication date |
|---|---|
| ATE520983T1 (de) | 2011-09-15 |
| US7662555B2 (en) | 2010-02-16 |
| HK1097046A1 (en) | 2007-06-15 |
| CN1902490B (zh) | 2012-06-27 |
| EP1712911A1 (en) | 2006-10-18 |
| WO2005062046A1 (ja) | 2005-07-07 |
| KR101171253B1 (ko) | 2012-08-06 |
| JPWO2005062046A1 (ja) | 2007-12-13 |
| EP1712911B1 (en) | 2011-08-17 |
| KR20070003827A (ko) | 2007-01-05 |
| EP1712911A4 (en) | 2008-04-09 |
| CN1902490A (zh) | 2007-01-24 |
| US20070154890A1 (en) | 2007-07-05 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5638734B2 (ja) | 生体分子用標識色素及び標識キット並びに生体分子の検出方法 | |
| JP4801445B2 (ja) | 生体分子の検出方法及びそれに用いる標識色素並びに標識キット | |
| US20200124613A1 (en) | Single molecule peptide sequencing | |
| JP3881667B2 (ja) | 生体分子の検出方法及びそれに用いる標識色素並びに標識キット | |
| JP5539635B2 (ja) | 蛍光色素 | |
| US11435358B2 (en) | Single molecule peptide sequencing | |
| JP5881624B2 (ja) | 蛍光色素 | |
| JP4860352B2 (ja) | 診断薬及びそれを用いた測定方法 | |
| JP2008156556A (ja) | 蛍光色素及びその製造方法 | |
| EP3137898B1 (en) | Fluorescent molecular sensor for targeting changes in protein surfaces, and methods of use thereof | |
| JP2016196608A (ja) | 蛍光色素 | |
| JP5539920B2 (ja) | 診断薬及びそれを用いた測定方法 | |
| JP2019031604A (ja) | 蛍光色素 | |
| JP2019048908A (ja) | 蛍光色素 | |
| JP2002107364A (ja) | ノンラベル検出用生物試薬アレイ及びその作製方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20071221 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20071221 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20101109 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20101224 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20110125 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20110425 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20110623 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20110712 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20110805 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20140812 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 4801445 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |