JP4339906B2 - 試料ろ過フィルターを用いる簡易メンブレンアッセイ方法及びキット - Google Patents
試料ろ過フィルターを用いる簡易メンブレンアッセイ方法及びキット Download PDFInfo
- Publication number
- JP4339906B2 JP4339906B2 JP2007269365A JP2007269365A JP4339906B2 JP 4339906 B2 JP4339906 B2 JP 4339906B2 JP 2007269365 A JP2007269365 A JP 2007269365A JP 2007269365 A JP2007269365 A JP 2007269365A JP 4339906 B2 JP4339906 B2 JP 4339906B2
- Authority
- JP
- Japan
- Prior art keywords
- sample
- filter
- membrane
- specimen
- substance
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Landscapes
- Sampling And Sample Adjustment (AREA)
- Investigating Or Analysing Biological Materials (AREA)
Description
(1)強剛性フィルターを含むフィルターにより構成されたろ過フィルターを備えた検体試料用ろ過チューブ、及び
(2)検体試料中の被検出物を捕捉するための捕捉物質が結合したメンブレンを備えたアッセイ装置、
により解決される。
(簡易メンブレンアッセイ方法及びアッセイ装置)
本発明の方法は、被検出物を捕捉するための捕捉物質が結合したメンブレンを備えたアッセイ装置を用いる、検体試料中の被検出物の簡易メンブレンアッセイ法であって、強剛性フィルターを含むフィルターにより構成されたろ過フィルターを用いて被検出物を含む検体から調製した検体試料をろ過した後に前記メンブレン上に滴下し、前記検体試料中の被検出物の存在を検出あるいは定量することを特徴とする方法である。
(1)ウイルスや細菌等に感染した疑いがある患者の咽頭、鼻腔あるいは直腸等から綿棒等の検体採取器具を用いて直接採取した検体試料を、後述するような検体浮遊液に浮遊させる。あるいは患者から採取した鼻腔吸引液、尿、便等の被分析対象物から綿棒等の検体採取器具を用いて採取した検体試料を、後述するような検体浮遊液に浮遊させる。
(2)この浮遊液を、ろ過フィルターを備えた検体試料用ろ過チューブ中に入れてろ過する。
(3)このろ過液を、メンブレンを備えたアッセイ装置中の被検出物に特異的に結合して被検出物を捕捉する捕捉試薬が結合したメンブレンに滴下等により添加して、被検出物をメンブレン上に捕捉させる。この際、ろ過液をサンプル滴下パッドに滴下することにより、毛細管現象により被検出物がメンブレンに流れていく。
(4)前記メンブレン上に、被検出物に特異的に結合する検出試薬である標識物質を滴下等により添加し、捕捉試薬/被検出物/標識物質の複合体を形成させる。この際、標識物質はあらかじめアッセイ装置に組み込んでおいてもよい。この場合、検体試料を含む浮遊液をアッセイ装置に添加することにより、該浮遊液がアッセイ装置上を流れ、検出試薬を含むパッド部分に到達すると、検出試薬が前記浮遊液に溶解し、被検体とともにメンブレンに到達し、メンブレンの捕捉試薬との間で複合体を形成する。
(5)前記複合体中の標識物質により、複合体の存在を検出することにより、検体試料中の被検出物の有無を測定する。複合体の存在の検出の前に、必要に応じて反応停止液を用いて反応を停止させてもよい。
検体採取するための器具としては、綿棒、白金耳、スポイト又はさじ形状の用具等を用いることができる。特に人体を被験体とし、鼻腔ぬぐい液、鼻腔吸引液、咽頭ぬぐい液、肺胞洗浄液、便懸濁液又は直腸拭い液を検体とする場合は、検体採取器具として主として綿棒を用いることが多い。
本発明の方法において、患者から採取した検体は検体浮遊液に浮遊させて検体試料とした後、アッセイ装置中のメンブレンの目詰まりや偽陽性を防止するために、ろ過フィルターを用いてろ過される。特に検体採取器具としてブラシ状綿棒を用いた場合、通常の綿棒を用いた場合よりも多くの被検出物を採取することが可能であるが、同時に検体採取部位から剥落した細胞や分泌物、排泄物の成分等もより多く採取するため、メンブレンの目詰まりや偽陽性もより発生しやすい。したがってろ過工程の重要性もより高くなる。ろ過フィルターはメンブレンの目詰まりや偽陽性及びろ過フィルター自身の目詰まりを防ぐため、1種類だけではなく、材質の異なるもの、孔径又は保留粒子径の異なるものをいくつか組み合わせても良いが、本発明においては、少なくとも1種の強剛性フィルターを含むことが必要である。
ろ過チューブ中に検体浮遊液に浮遊させた検体試料を入れて、先端に取り付けた強剛性フィルターを含むろ過フィルターを通してろ過し、ろ液をメンブレンアッセイ装置中のメンブレンに滴下する際に、フィルターはろ過チューブ内の検体試料等の液体や空気の圧力を受ける。このとき、フィルターの厚さ方向の潰れや湾曲等の変形が発生する可能性があるが、これらの現象はフィルター内部のろ液の流路を塞ぎ、フィルター自身が目詰まりする原因となる。本発明に用いる強剛性フィルターは、ろ過チューブ中に検体浮遊液に浮遊させた検体試料を入れて、先端に取り付けた強剛性フィルターを含むろ過フィルターを通してろ過し、ろ液をメンブレンアッセイ装置中のメンブレンに滴下する際に、フィルターの厚さ方向に潰れにくく、または、湾曲等の変形をしにくい剛性を備えているフィルターをいう。別の表現をすれば、ろ液の圧力によってもフィルター内部のろ液の流路を塞ぎ難い剛性を備えたフィルターのことをいう。
上記ろ過フィルターは、本発明の簡易メンブレンアッセイ法又はキットにおいて、検体試料用ろ過チューブの先端に取り付けて使用されることが好ましい。すなわち、ろ過チューブ中に検体浮遊液に浮遊させた検体試料を入れて、先端に取り付けたろ過フィルターを通してろ過し、ろ液をメンブレンアッセイ装置中のメンブレンに滴下する方法が簡便であり、好ましい。このろ過チューブの一実施態様の模式図を図5及び図6に示す。ろ過チューブは例えば図5及び図6に記載されるように先端部(ろ過ノズル)nと本体部pからなる形状であり、先端部の内部に図5に示されるようにろ過フィルターo1〜o3が備えつけられている。図5のろ過ノズルにおいて、図下部がノズル底面であり、ろ過フィルターo1、o2及びo3は、それぞれ3段目フィルター、2段目フィルター及び1段目フィルターである。図6に示すような本体部に検体を浮遊液に浮遊させた調製した検体試料を入れ、ろ過フィルターを備えた先端部を取り付ける。ろ過フィルターを通して検体試料をろ過し、ろ液をメンブレンアッセイ装置に滴下する。本体部がポリエチレン、ポリエチレンテレフタレート(PET)等のフレキシブルな材質からなる場合、ろ過フィルターを取り付け、内部に検体試料を入れた状態で、手などにより内部に圧力を加えることで、容易に検体試料をろ過することができるため、好ましい。
本発明でいう被検出物にはインフルエンザウイルス、RSウイルス、アデノウイルス、A群溶連菌、肺炎マイコプラズマ、下痢症の原因微生物、例えばノロウイルス、ロタウイルス、サポウイルス、下痢症アデノウイルス等の病原微生物若しくは該病原微生物由来のタンパク質等の物質又はそれらに対する抗体、ペプチドホルモン、ステロイド、生理活性アミン類、ビタミン類、プロスタングランジン類、テトラサイクリン等の抗生物質、細菌等が産生する毒素、各種腫瘍マーカー、農薬、及び病原微生物に由来する核酸成分に相補的なヌクレオチド等を挙げることができる。上記の病原微生物若しくは該病原微生物由来のタンパク質等の物質又はそれらに対する抗体等を非検出物として用いる場合、特にインフルエンザウイルス、RS(Respiratory Syncytial)ウイルス、アデノウイルス、A群溶連菌、肺炎マイコプラズマ、ロタウイルス及びノロウイルス等のように、大流行し、ごく短時間に特定する必要がある病原体の診断に、極めて有用である。
被検出物を捕捉するための捕捉物質は、被検出物と、抗原抗体反応のような特異的反応により結合して、複合体を形成する物質である。従って、被検出物により使用する捕捉物質が異なることは当然であるが、一般には被検出物が細菌、ウイルス、ホルモン、その他臨床マーカー等の場合には、これらに対し特異的に反応して結合するポリクローナル抗体、モノクローナル抗体等が挙げられる。そのほか、ウイルス抗原、ウイルス中空粒子、遺伝子組換え大腸菌発現タンパク質、遺伝子組換え酵母発現タンパク質等が挙げられる。このような捕捉物質を上述したメンブレン表面に結合させる方法としては、物理的吸着であってもよく、又は化学的な結合によるものであってもよい。固相化は、タンパク質をニトロセルロースメンブレン等の固相に固相化するための公知の方法で行うことができる。捕捉物質が結合したメンブレンの調製は、例えば、捕捉物質を緩衝液等に希釈した溶液をメンブレンに吸着してその後乾燥することにより行われる。補足物質は、例えばライン状に固相化すればよい。
本発明において、検体浮遊液とは、患者や環境等から採取した被検出物を含む可能性がある検体を浮遊又は懸濁するための溶液であり、該検体を浮遊又は懸濁した浮遊液は検体試料としてアッセイ装置に滴下等により添加されて、アッセイに供される。
採取検体には被検出物以外にも様々な物質が含まれている。例えば、病原体感染測定のため、人から検体を採取する際には鼻腔、咽頭又は直腸より綿棒等で採取することが多いが、この検体中には患者由来の組織片や分泌物の他、被検出物である病原体の組織が含まれている場合がある。これらの一部は検体浮遊液中に凝集物として存在し、一部は検体試料中に溶解した状態で存在する。これらを含んだ状態で検体試料をアッセイ装置に添加すると、非特異反応により偽陽性が発生する場合がある。凝集物を除去するためにはアッセイ装置に添加する前にろ過用のメンブレンを通過させてろ過する方法が有効であるが、溶解物の場合、ろ過により除去することはできないので、検体浮遊液の組成を工夫する必要がある。
上記のような工夫によっても偽陽性の発生を減じることができるが、完全に防ぐことはできない。
本明細書において、検出試薬とは、被検出物に特異的に結合し、被検出物と複合体を形成しうるものである。また、標識物質とは、被検出物と複合体を形成した後に何らかの手段で検出可能なように標識された検出試薬を意味する。例えば、被検出物がウイルス等の抗原物質である場合には、そのウイルスに対する抗体であって、酵素等で標識化された抗体が挙げられる。このように酵素で標識された場合には、該酵素により触媒される反応により、比色法、蛍光法により検出可能な物質を生成する該酵素の基質を添加することにより、複合体の検出を行うことができる。標識化される前の検出試薬としては、捕捉試薬について述べたものと同じものが挙げられる。また、標識は、酵素、蛍光発光性標識、磁性体標識、放射性同位元素、金コロイド、着色ラテックス等が挙げられる。検出試薬は、検体試料をアッセイ装置に添加した後に、アッセイ装置に添加してもよく、またあらかじめアッセイ装置に組み込んでおいてもよい。検出試薬をアッセイ装置に組み込む場合、例えば、検出試薬を含浸させて乾燥させたパッドをサンプル滴下パッドと捕捉物質を含むメンブレンの間に組み込んでおけばよい。この場合、検体試料を含む浮遊液をアッセイ装置に添加することにより、該浮遊液がアッセイ装置上を流れ、検出試薬を含むパッド部分に到達すると、検出試薬が前記浮遊液に溶解し、被検体とともにメンブレンに到達し、メンブレンの捕捉試薬との間で複合体を形成する。検出試薬を含むパッド部は、例えば、セルロース、ガラス繊維などでできた不織布等が用いられる。
標識物質の標識として酵素標識を用いた場合には、通常その酵素に対する基質であって、該酵素により触媒される反応により、比色法、蛍光法により検出可能な物質を生成するものを添加する。具体例としては、5−ブロモ−4−クロロ−3−インドリルリン酸(BCIP)/ニトロテトラゾリウムブルー(NBT)、テトラメチルベンチジン(TMB)、グルコース‐6‐リン酸NAD+が挙げられる。
本発明のキットにはさらに必要により、例えば酵素と基質との反応を停止させるための反応停止液が含まれていてもよい。このような反応停止液としては、例えば、クエン酸、硫酸等が挙げられる。
本発明の装置は、吸収パッド部を備えていてもよい。吸収パッド部は、本発明のエンザイムイムノアッセイデバイスの一端に設けられデバイスを展開する液体を吸収することによりメンブレン上の液体の流れを促進する。吸収パッド部は、多量の液を吸収できるよう、吸水性の材質でできており、例えば、セルロース、ガラス繊維などでできた不織布等が用いられる。また、その大きさは、特に限定されないが、通常、3mm〜15mm×10mm〜40mm、厚さ0.5mm〜3mm程度である。
本発明の簡易メンブレンアッセイキットは、上述した本発明の簡易メンブレンアッセイ法に用いるキットである。本発明の簡易メンブレンアッセイキットは少なくとも以下の(i)及び(ii)を含む。
(i) 強剛性フィルターを含むフィルターにより構成されるろ過フィルター、及び
(ii) 被検出物を捕捉するための捕捉物質が結合したメンブレンを備えたアッセイ装置。
1.モノクローナル抗体の作製
(1)抗A型インフルエンザウイルスNP(Nucleoprotein;核蛋白)モノクローナル抗体(マウス)の作製
精製A型インフルエンザウイルス抗原を免疫し、一定期間維持したBALB/cマウスから脾臓を摘出し、ケラーらの方法(Kohler et al., Nature, vol, 256, p495-497(1975))によりマウスミエローマ細胞(P3×63)と融合した。
精製B型インフルエンザウイルス抗原を免疫し、一定期間維持したBALB/cマウスから脾臓を摘出し、ケラーらの方法(Kohler et al., Nature, vol.256, p495-497(1975))によりマウスミエローマ細胞(P3×63)と融合した。得られた融合細胞(ハイブリドーマ)は、37℃下にてインキュベーター中で維持し、B型インフルエンザウイルスNP抗原固相プレートを用いたELISAにより上清の抗体活性を確認しながら細胞の純化(単クローン化)を行った。取得した該細胞2株をそれぞれプリスタン処理したBALB/cマウスに腹腔投与し、約2週間後、抗体含有腹水を採取した。得られた腹水からProteinAカラムクロマトグラフィー(アマシャム社製)によってIgGを精製し、2種類の精製抗B型インフルエンザウイルスNPモノクローナル抗体を得た。
ヒトRSウイルスのFP(Fusion Protein)のアミノ酸配列の一部を合成したポリペプチドを免役し、一定期間維持したBALB/cマウスから脾臓を摘出し、ケラーらの方法(Kohler et al., Nature, vol, 256, p495-497(1975))によりマウスミエローマ細胞(P3×63)と融合した。
(1)ラテックス粒子標識抗A型インフルエンザウイルス抗体の調製
抗A型インフルエンザウイルスNPモノクローナル抗体のうち1種類を50mM MES(2-Morpholinoethanesulfonic acid, monohydrate;同仁化学社)緩衝液(pH6.0)溶液で透析後、O.D.280nm=0.5になるように同じ緩衝液で希釈した溶液を10mL調製した。次に10(W/V)%赤色ポリスチレンラテックス粒子(粒径0.45μm、表面官能基はカルボキシル基、官能基密度65Å2/COOH基;Magsphere社)と液量比40:1になるように混合し、反応させた。次に、1(W/V)%のEDAC(N-(3-Dimethlaminopropyl)-N'-ethylcarbodiimide hydrochloride;Sigma社)を最終濃度0.1%になるように添加した後、2時間反応させた。洗浄後、最終浮遊液(5mMTris, 0.04(W/V)% BSA(ウシ血清アルブミン), 0.4Mトレハロース, 0.2(V/V)% TritonX-100)20mL中に浮遊し、超音波分散装置(オリンパス社)にかけ、ラテックス粒子を分散させた。
抗B型インフルエンザウイルスNPモノクローナル抗体のうち1種類を50mM MES(2-Morpholinoethanesulfonic acid,monohydrate;同仁化学社)緩衝液(pH6.0)溶液で透析後、O.D.280nm=0.5になるように同じ緩衝液で希釈した溶液を10mL調製した。次に10(W/V)%青色ポリスチレンラテックス粒子(粒径0.45μm, 表面官能基はカルボキシル基, 官能基密度65Å2/COOH基;Magsphere社)と液量比40:1になるように混合し、反応させた。次に、1(W/V)%のEDAC(N-(3-Dimethlaminopropyl)-N'-ethylcarbodiimide hydrochloride;Sigma社)を最終濃度0.1%になるように添加した後、2時間反応させた。洗浄後、最終浮遊液(5mMTris, 0.04(W/V)% BSA(ウシ血清アルブミン), 0.4Mトレハロース,0.2(V/V)% TritonX-100)20mL中に浮遊し、超音波分散装置(オリンパス社)にかけ、ラテックス粒子を分散させた。
抗RSウイルスFPモノクローナル抗体のうち1種類を50mM MES緩衝液(pH6.0)溶液で透析後、O.D.280nm=0.5になるように同じ緩衝液で希釈した溶液を10mL調製した。次に10(W/V)%緑色ポリスチレンラテックス粒子(粒径0.49μm, 表面官能基はカルボキシル基, 官能基密度69Å2/COOH基;メルク社)と液量比40:1になるように混合し、反応させた。次に、1(W/V)%のEDAC(N-(3-Dimethlaminopropyl)-N'-ethylcarbodiimide hydrochloride;Sigma社)を最終濃度0.1%になるように添加した後、2時間反応させた。洗浄後、最終浮遊液(5mMTris, 0.04(W/V)% BSA(ウシ血清アルブミン), 0.4Mトレハロース,0.2(V/V)% TritonX-100)20mL中に浮遊し、超音波分散装置(オリンパス社)にかけ、ラテックス粒子を分散させた。
(1)ラテックス粒子標識抗体の混合
上記2.(1)、(2)及び(3)で作製したラテックス粒子標識抗A型インフルエンザウイルス抗体、ラテックス粒子標識抗B型インフルエンザウイルス抗体及びラテックス粒子標識抗RSウイルス抗体をラテックス濃度がそれぞれ0.3(W/V)%になるように、上記2.(1)記載の最終浮遊液で希釈後、室温下にて150rpmで5分間撹拌して等量混合した。
3.(1)で作製したラテックス粒子標識抗体を陽圧噴霧装置(BioJet;BioDot社)を用いて8μL/cmの塗布量でリール状に巻いた幅15mmのセルロース不織布全面に噴霧した。噴霧後、50℃の温風を1分間吹きつけて乾燥させ、ラテックス粒子標識抗体乾燥パッドを作製した。
(1)固相用抗A型インフルエンザウイルス抗体の調製
上記1.(1)で作製した精製抗A型インフルエンザウイルスNPモノクローナル抗体のうち標識に用いなかった方を、固相液(10mM Tris-HCl(pH7.5))に透析し、透析後に0.22μmろ過を行い、O.D.280nm=4.0になるように固相液で希釈して固相用抗A型インフルエンザウイルス抗体を調製した。
上記1.(2)で作製した精製抗B型インフルエンザウイルスNPモノクローナル抗体のうち標識に用いなかった方を、固相液(10mM Tris-HCl(pH7.5))に透析し、透析後に0.22μmろ過を行い、O.D.280nm=3.0になるように固相液で希釈して固相用抗B型インフルエンザウイルス抗体を調製した。
上記1.(3)で作製した精製抗RSウイルスFPモノクローナル抗体のうち標識に用いなかった方を、固相液(10mM Tris-HCl(pH7.5),1(W/V)%トレハロース)に透析し、透析後に0.22μmろ過を行い、O.D.280nm=3.0になるように固相液で希釈して固相用抗RSウイルス抗体を調製した。
インフルエンザ及びRSウイルス検出用ラテラルフロー式メンブレンアッセイ装置は、図1及び図2に示すものと同様の構成のものを用いた。
メンブレンは、幅3cm×長さ10cmのニトロセルロースメンブレン(孔径12μm;ワットマン社製)シート(白色)を用いた(図1及び図2のd)。その長軸側の一端(この端を上流端、反対側を下流端とする)から6mm離れたeの位置に固相用抗A型インフルエンザウイルス抗体を1μL/cmの塗布量で陽圧噴霧装置(BioJet;BioDot社)を用いて線状に塗布し、10mm離れたfの位置に固相用抗B型インフルエンザウイルス抗体を1μL/cmの塗布量で陽圧噴霧装置(BioJet;BioDot社)を用いて線状に塗布し、14mm離れたgの位置に固相用抗RSウイルス抗体を1μL/cmの塗布量で陽圧噴霧装置(BioJet;BioDot社)を用いて線状に塗布した。22mm離れたhの位置に抗マウスIgG抗体をO.D.280nm=1.0に希釈し、1μL/cmの塗布量で陽圧噴霧装置(BioJet;BioDot社)を用いて線状に塗布した。塗布後、45℃の温風を10分間吹き付けて乾燥した。
図5のnに示した様なろ過用ノズルを用意し、表1に示す部材を円形(直径0.7cm)に打ち抜き、ノズルの底面に装填し、表2に示すような構成の試料ろ過フィルターを作製した。ろ過フィルターとして2枚以上の部材を重ねた場合には底面の側から1段目、2段目、3段目と数えた。
(1)検体の採取と検体試料の調製
臨床的にインフルエンザウイルスあるいはRSウイルス感染が疑われる患者から鼻腔吸引液を採取した。まず、そのうち一部を2mLのウイルス分離用培地に浮遊し、この浮遊液を用いてRT-PCR法により検体中にインフルエンザウイルス遺伝子又はRSウイルス遺伝子が存在するかを確認した。インフルエンザウイルス遺伝子検出のためのRT-PCR法は、清水の方法(感染症学雑誌、第71巻、第6号、p522-526)で実施した。またRSウイルス遺伝子検出のためのRT-PCR方はStockton等の方法(Journal of Clinical Microbiology 、第36巻、p2990-2995、1998年)で実施した。その結果より、A型インフルエンザウイルス遺伝子が検出された鼻腔吸引液を10検体、B型インフルエンザウイルス遺伝子が検出された鼻腔吸引液を10検体、RSウイルス遺伝子が検出された鼻腔吸引液を10検体及びいずれの遺伝子も検出されなかった鼻腔吸引液を10検体それぞれ選び出し、以後の試験に用いた。
鼻腔吸引液1検体より調製した検体試料の入った6本のチューブの先端に6.で作製した各種の試料ろ過フィルターをそれぞれ2個ずつ装着した。検体採取に用いた綿棒の種類と試料ろ過フィルターの種類の組み合わせを表3に示した。
試験の結果を表3に示す。
A型インフルエンザ陽性:RT-PCRにてA型インフルエンザウイルス遺伝子が検出された検体から調製された検体試料を用いてメンブレンアッセイ法にて試験した際にA型インフルエンザウイルスのみ陽性と判定された場合
B型インフルエンザ陽性:RT-PCRにてB型インフルエンザウイルス遺伝子が検出された検体から調製された検体試料を用いてメンブレンアッセイ法にて試験した際にB型インフルエンザウイルスのみ陽性と判定された場合
RS陽性:RT-PCRにてRSウイルス遺伝子が検出された検体から調製された検体試料を用いてメンブレンアッセイ法にて試験した際にRSウイルスのみ陽性と判定された場合
陰性:RT-PCRにていずれの遺伝子も検出されなかった検体から調製された検体試料を用いてメンブレンアッセイ法にて試験した際に陰性と判定された場合
非特異:試験した際にRT-PCRにて検体から遺伝子が検出されなかったウイルスがメンブレンアッセイ法にて陽性であると判定された場合(RT-PCRにて遺伝子が検出されたウイルスに加えて、遺伝子が検出されなかったウイルスもメンブレンアッセイ法にて陽性と判定された場合を含む)
無効:メンブレンアッセイ法にてhの位置に発色が認められなかった場合
1.インフルエンザ及びRSウイルス検出用ラテラルフロー式メンブレンアッセイ装置の作製
実施例1で用いたものを使用した。
2.試料ろ過フィルターの作製
図5のnに示した様なろ過用ノズルを用意し、表4に示す部材を円形(直径0.7cm)に打ち抜き、ノズルの底面に装填し、表5に示すような構成の試料ろ過フィルターを作製した。ろ過フィルターとして2枚以上の部材を重ねた場合には底面の側から1段目、2段目、3段目と数えた。また、試料ろ過フィルターに含まれる2種類のフィルターのうち、孔径の小さいフィルターを精密ろ過用フィルターと、孔径の大きいフィルターを粗ろ過用フィルターと呼ぶ。
(1)検体の採取と検体試料の調製
実施例1で用いた鼻腔吸引液の中から、実施例1に記載の方法によりA型インフルエンザウイルス遺伝子が検出された鼻腔吸引液を10検体、B型インフルエンザウイルス遺伝子が検出された鼻腔吸引液を7検体、RSウイルス遺伝子が検出された鼻腔吸引液を10検体及びいずれの遺伝子も検出されなかった鼻腔吸引液を10検体それぞれ選び出し、以後の試験に用いた。
鼻腔吸引液に頭部がナイロン繊維からなるブラシ状綿棒を10秒間浸した後に引き上げ、図6に示した様なチューブ内に分注した検体浮遊液(20mM MES緩衝液(pH6.0)、1(W/V)% TritonX-100、5(W/V)% アルギニン塩酸塩、1.0(W/V)%ウシ血清アルブミン)0.3mL中に浮遊し、検体試料を調製した。鼻腔吸引液1検体につき6本の検体試料を調製した。
鼻腔吸引液1検体より調製した検体試料の入った6本のチューブの先端に上記2.で作製したA、D、E、F、G及びHの各種試料ろ過フィルターをそれぞれ1個ずつ装着し、実施例1と同じ方法で試験を実施した。
試験の結果を表6に示す。尚、結果の説明は実施例1の表3に記載したものと同じである。
1.インフルエンザ及びRSウイルス検出用ラテラルフロー式メンブレンアッセイ装置の作製
実施例1で用いたものを使用した。
実施例1及び2で作製した試料ろ過フィルターのうちA、C及びDを用いた。
(1)検体の採取と検体試料の調製
臨床的にインフルエンザウイルスあるいはRSウイルス感染が疑われる患者から頭部がナイロン繊維からなるブラシ状綿棒(検体採取部分の水分吸収量90μL;microRheologics社)を用いて鼻腔拭い液を3本、咽頭拭い液を1本採取した。まず、そのうち咽頭拭い液を2mLのウイルス分離用培地に浮遊し、この浮遊液を用いて実施例1の7.(1)記載のRT-PCR法により検体中にインフルエンザウイルス遺伝子又はRSウイルス遺伝子が存在するかを確認した。その結果より、採取した咽頭拭い液中からA型インフルエンザウイルス遺伝子が検出された患者を5人、B型インフルエンザウイルス遺伝子が検出された患者を5人、RSウイルス遺伝子が検出された患者を5人及びいずれの遺伝子も検出されなかった患者を5人選び出し、その患者から採取した鼻腔拭い液を図6に示した様なチューブ内に分注した検体浮遊液(20mM MES緩衝液(pH6.0)、1(W/V)% TritonX-100、5(W/V)% アルギニン塩酸塩、1.0(W/V)%ウシ血清アルブミン)0.3mL中にそれぞれ浮遊し、検体試料を調製した。
1人の患者より採取した鼻腔拭い液から調製した検体試料の入った3本のチューブの先端に2.で作製したA、C及びDの各種試料ろ過フィルターをそれぞれ1個ずつ装着し、実施例1と同じ方法で試験を実施した。
試験の結果を表7に示す。尚、結果の説明は実施例1の表3に記載したものと同じである。
1.インフルエンザ及びRSウイルス検出用ラテラルフロー式メンブレンアッセイ装置の作製
実施例1で用いたものを使用した。
実施例1及び2で作製した試料ろ過フィルターのうちA、C及びDを用いた。
(1)検体の採取と検体試料の調製
臨床的にインフルエンザウイルスあるいはRSウイルス感染が疑われる患者から頭部がナイロン繊維からなるブラシ状綿棒(検体採取部分の水分吸収量90μL;microRheologics社)を用いて咽頭拭い液を3本、鼻腔拭い液を1本採取した。まず、そのうち鼻腔拭い液を2mLのウイルス分離用培地に浮遊し、この浮遊液を用いて実施例1の7.(1)記載のRT-PCR法により検体中にインフルエンザウイルス遺伝子又はRSウイルス遺伝子が存在するかを確認した。その結果より、採取した咽頭拭い液中からA型インフルエンザウイルス遺伝子が検出された患者を5人、B型インフルエンザウイルス遺伝子が検出された患者を5人、RSウイルス遺伝子が検出された患者を5人及びいずれの遺伝子も検出されなかった患者を5人を5人選び出し、その患者から採取した鼻腔拭い液を図6に示した様なチューブ内に分注した検体浮遊液(20mM MES緩衝液(pH6.0)、1(W/V)% TritonX-100、5(W/V)% アルギニン塩酸塩、1.0(W/V)%ウシ血清アルブミン)0.3mL中にそれぞれ浮遊し、検体試料を調製した。
1人の患者より採取した咽頭拭い液より調製した検体試料の入った3本のチューブの先端に2.で作製したA、C及びDの各種試料ろ過フィルターをそれぞれ1個ずつ装着し、実施例1と同じ方法で試験を実施した。
試験の結果を表8に示す。尚、結果の説明は実施例1の表3に記載したものと同じである。
1.モノクローナル抗体の作製
(1)アデノウイルスヘキソン蛋白モノクローナル抗体(マウス)
ヒトアデノウイルスのヘキソン蛋白のアミノ酸配列の一部を合成したポリペプチドを免疫し、一定期間維持したBALB/cマウスから脾臓を摘出し、ケラーらの方法(Kohler et al., Nature, vol, 256, p495-497(1975))によりマウスミエローマ細胞(P3×63)と融合した。
(1)ラテックス粒子標識抗アデノウイルスヘキソン蛋白抗体の調製
抗アデノウイルスヘキソン蛋白抗体のうち1種類を50mM MES(2-Morpholinoethanesulfonic acid,monohydrate;同仁化学社)緩衝液(pH6.0)溶液で透析後、O.D.280nm=0.5になるように同じ緩衝液で希釈した溶液を10mL調製した。次に10(W/V)%青色ポリスチレンラテックス粒子(粒径0.45μm、表面官能基はカルボキシル基、官能基密度65Å2/COOH基;Magsphere社)と液量比40:1になるように混合し、反応させた。次に、1(W/V)%のEDAC(N-(3-Dimethlaminopropyl)-N'-ethylcarbodiimide hydrochloride;Sigma社)を最終濃度0.1%になるように添加した後、2時間反応させた。洗浄後、最終浮遊液(5mM Tris, 0.04(W/V)% BSA(ウシ血清アルブミン), 0.4Mトレハロース,0.2(V/V)% TritonX-100)20mL中に浮遊し、超音波分散装置(オリンパス社)にかけ、ラテックス粒子を分散させた。
(1)ラテックス粒子標識抗体乾燥パッドの作製
2.で作製したラテックス粒子標識抗体を陽圧噴霧装置(BioJet;BioDot社)を用いて8μL/cmの塗布量でリール状に巻いた幅15mmのセルロース不織布全面に噴霧した。噴霧後、50℃の温風を1分間吹きつけて乾燥させ、ラテックス粒子標識抗体乾燥パッドを作製した。
(1)固相用抗アデノウイルスヘキソン蛋白抗体の調製
上記1.(1)で作製した精製抗アデノウイルスヘキソン蛋白抗体のうち標識に用いなかった方を、固相液(10mM Tris-HCl(pH7.5))に透析し、透析後に0.22μmろ過を行い、O.D.280nm=4.0になるように固相液で希釈して固相用抗アデノウイルスヘキソン蛋白抗体を調製した。
アデノウイルス検出用ラテラルフロー式メンブレンアッセイ装置は、図1及び図2に示すものと同様の構成のものを用いた。
メンブレンは、幅3cm×長さ10cmのニトロセルロースメンブレン(孔径12μm;ワットマン社製)シート(白色)を用いた(図1及び図2のd)。その長軸側の一端(この端を上流端、反対側を下流端とする)から6mm離れたeの位置に固相用抗アデノウイルスヘキソン蛋白抗体を1μL/cmの塗布量で陽圧噴霧装置(BioJet;BioDot社)を用いて線状に塗布し、22mm離れたhの位置に抗マウスIgG抗体をO.D.280nm=1.0に希釈し、1μL/cmの塗布量で陽圧噴霧装置(BioJet;BioDot社)を用いて線状に塗布した。fとgの位置には何も塗布しなかった。塗布後、45℃の温風を10分間吹き付けて乾燥した。
実施例1及び2で作製した試料ろ過フィルターのうちA、C及びDを用いた。
(1)検体の採取と検体試料の調製
臨床的にアデノウイルス感染が疑われる患者から頭部がナイロン繊維からなるブラシ状綿棒(検体採取部分の水分吸収量90μL;microRheologics社)を用いて咽頭拭い液を4本採取した。まず、そのうち1本を2mLのウイルス分離用培地に浮遊し、この浮遊液を用いてFujimoto等の方法(Single-tube multiplex PCR for rapid and sensitive diagnosis of subgenus B and other subgenera adenovirus in clinical samples. Microbiology and Immunology. 44. 821-826, 2000)を用いたPCR法により検体中にアデノウイルス遺伝子が存在するかを確認した。その結果より、採取した咽頭拭い液中からアデノウイルス遺伝子が検出された患者を5人及びアデノウイルス遺伝子が検出されなかった患者を5人選び出し、その患者から採取した咽頭拭い液を図6に示した様なチューブ内に分注した検体浮遊液(20mM MES緩衝液(pH6.0)、1(W/V)% TritonX-100、5(W/V)% アルギニン塩酸塩、1.0(W/V)%ウシ血清アルブミン)0.3mL中にそれぞれ浮遊し、検体試料を調製した。
1人の患者より採取した咽頭拭い液より調製した検体試料の入った3本のチューブの先端に2.で作製したA、C及びDの各種試料ろ過フィルターをそれぞれ1個ずつ装着し、実施例1と同じ方法で試験を実施した。
試験の結果を表9に示す。10分後、アッセイ装置を観察し、図1あるいは図2のhの位置(コントロールライン)に青色の発色が認められた場合を有効とし、eの位置に青色の発色が認められた場合にアデノウイルス陽性と判定した。またhの位置に発色が認められない場合を無効とした。
アデノウイルス陽性:PCRにてアデノウイルス遺伝子が検出された検体から調製された検体試料を用いてメンブレンアッセイ法にて試験した際にアデノウイルス陽性と判定された場合
陰性:PCRにてアデノウイルス遺伝子が検出されなかった検体から調製された検体試料を用いてメンブレンアッセイ法にて試験した際に陰性と判定された場合
非特異:試験した際にPCRにて検体からアデノウイルス遺伝子が検出されなかった検体から調製された検体試料を用いてメンブレンアッセイ法にて試験した際にアデノウイルス陽性であると判定された場合
無効:メンブレンアッセイ法にてhの位置に発色が認められなかった場合
1.モノクローナル抗体の作製
(1)抗ノロウイルスキャプシド蛋白モノクローナル抗体(マウス)
ノロウイルスのキャプシド蛋白をコードする遺伝子を導入した組換えバキュロウイルスによるタンパク質発現によりウイルス中空粒子(VLPs)を作製した。これを免疫し、一定期間維持したBALB/cマウスから脾臓を摘出し、ケラーらの方法(Kohler et al., Nature, vol, 256, p495-497(1975))によりマウスミエローマ細胞(P3×63)と融合した。
(1)ラテックス粒子標識抗ノロウイルスキャプシド蛋白抗体の調製
抗ノロウイルスキャプシド蛋白抗体のうち1種類を50mM MES(2-Morpholinoethanesulfonic acid,monohydrate;同仁化学社)緩衝液(pH6.0)溶液で透析後、O.D.280nm=0.5になるように同じ緩衝液で希釈した溶液を10mL調製した。次に10(W/V)%青色ポリスチレンラテックス粒子(粒径0.45μm、表面官能基はカルボキシル基、官能基密度65Å2/COOH基;Magsphere社)と液量比40:1になるように混合し、反応させた。次に、1(W/V)%のEDAC(N-(3-Dimethlaminopropyl)-N'-ethylcarbodiimide hydrochloride;Sigma社)を最終濃度0.1%になるように添加した後、2時間反応させた。洗浄後、最終浮遊液(5mM Tris, 0.04(W/V)% BSA(ウシ血清アルブミン), 0.4Mトレハロース,0.2(V/V)% TritonX-100)20mL中に浮遊し、超音波分散装置(オリンパス社)にかけ、ラテックス粒子を分散させた。
(1)ラテックス粒子標識抗体乾燥パッドの作製
2.で作製したラテックス粒子標識抗体を陽圧噴霧装置(BioJet;BioDot社)を用いて8μL/cmの塗布量でリール状に巻いた幅15mmのセルロース不織布全面に噴霧した。噴霧後、50℃の温風を1分間吹きつけて乾燥させ、ラテックス粒子標識抗体乾燥パッドを作製した。
(1)固相用抗ノロウイルスキャプシド蛋白抗体の調製
上記1.(1)で作製した精製抗ノロウイルスキャプシド蛋白抗体のうち標識に用いなかった方を、固相液(10mM Tris-HCl(pH8.0))に透析し、透析後に0.22μmろ過を行い、O.D.280nm=3.0になるように固相液で希釈して固相用抗ノロウイルスキャプシド蛋白抗体を調製した。
ノロウイルス検出用ラテラルフロー式メンブレンアッセイ装置は、図1及び図2に示すものと同様の構成のものを用いた。
メンブレンは、幅3cm×長さ10cmのニトロセルロースメンブレン(孔径12μm;ワットマン社製)シート(白色)を用いた(図1及び図2のd)。その長軸側の一端(この端を上流端、反対側を下流端とする)から6mm離れたeの位置に固相用抗ノロウイルスキャプシド蛋白抗体を1μL/cmの塗布量で陽圧噴霧装置(BioJet;BioDot社)を用いて線状に塗布し、22mm離れたhの位置に抗マウスIgG抗体をO.D.280nm=1.0に希釈し、1μL/cmの塗布量で陽圧噴霧装置(BioJet;BioDot社)を用いて線状に塗布した。fとgの位置には何も塗布しなかった。塗布後、45℃の温風を10分間吹き付けて乾燥した。
実施例1及び2で作製した試料ろ過フィルターのうちA、C及びDを用いた。
(1)検体の採取と検体試料の調製
臨床的にノロウイルス感染が疑われる患者から頭部がナイロン繊維からなるブラシ状綿棒(検体採取部分の水分吸収量90μL;microRheologics社)を用いて直腸拭い液を4本採取した。まず、そのうち1本を2mLのウイルス分離用培地に浮遊し、この浮遊液を用いてRT-PCR法(平成15年11月5日付食安監発第1105001号厚生労働省医薬食品局食品安全部監視安全課長通知に準拠)により検体中にノロウイルス遺伝子が存在するかを確認した。その結果より、採取した直腸拭い液中からノロウイルス遺伝子が検出された患者を5人及びノロウイルス遺伝子が検出されなかった患者を5人選び出し、その患者から採取した直腸拭い液を図6に示した様なチューブ内に分注した検体浮遊液(20mM MES緩衝液(pH6.0)、1(W/V)% TritonX-100、5(W/V)% アルギニン塩酸塩、1.0(W/V)%ウシ血清アルブミン)0.3mL中にそれぞれ浮遊し、検体試料を調製した。
1人の患者より採取した直腸拭い液より調製した検体試料の入った3本のチューブの先端に2.で作製したA、C及びDの各種試料ろ過フィルターをそれぞれ1個ずつ装着し、実施例1と同じ方法で試験を実施した。
試験の結果を表10に示す。10分後、アッセイ装置を観察し、図1あるいは図2のhの位置(コントロールライン)に青色の発色が認められた場合を有効とし、eの位置に青色の発色が認められた場合にノロウイルス陽性と判定した。またhの位置に発色が認められない場合を無効とした。
ノロウイルス陽性:RT-PCRにてノロウイルス遺伝子が検出された検体から調製された検体試料を用いてメンブレンアッセイ法にて試験した際にノロウイルス陽性と判定された場合
陰性:RT-PCRにてノロウイルス遺伝子が検出されなかった検体から調製された検体試料を用いてメンブレンアッセイ法にて試験した際に陰性と判定された場合
非特異:試験した際にRT-PCRにて検体からノロウイルス遺伝子が検出されなかった検体から調製された検体試料を用いてメンブレンアッセイ法にて試験した際にノロウイルス陽性であると判定された場合
無効:メンブレンアッセイ法にてhの位置に発色が認められなかった場合
1.ノロウイルス検出用ラテラルフロー式メンブレンアッセイ装置の作製
実施例6で用いたものを使用した。
実施例1及び2で作製した試料ろ過フィルターのうちA、C及びDを用いた。
(1)検体の採取と検体試料の調製
臨床的にノロウイルス感染が疑われる患者の糞便より頭部がナイロン繊維からなるブラシ状綿棒(検体採取部分の水分吸収量90μL;microRheologics社)を用いて検体を4本採取した。まず、そのうち1本を2mLのウイルス分離用培地に浮遊し、この浮遊液を用いてRT-PCR法(平成15年11月5日付食安監発第1105001号厚生労働省医薬食品局食品安全部監視安全課長通知に準拠)により検体中にノロウイルス遺伝子が存在するかを確認した。その結果より、採取した糞便中からノロウイルス遺伝子が検出された患者を5人及びノロウイルス遺伝子が検出されなかった患者を5人選び出し、その患者から採取した糞便を図6に示した様なチューブ内に分注した検体浮遊液(20mM MES緩衝液(pH6.0)、1(W/V)% TritonX-100、5(W/V)% アルギニン塩酸塩、1.0(W/V)%ウシ血清アルブミン)0.3mL中にそれぞれ浮遊し、検体試料を調製した。
1人の患者より採取した糞便より調製した検体試料の入った3本のチューブの先端に2.で作製したA、C及びDの各種試料ろ過フィルターをそれぞれ1個ずつ装着し、実施例1と同じ方法で試験を実施した。
試験の結果を表11に示す。10分後、アッセイ装置を観察し、図1あるいは図2のhの位置(コントロールライン)に青色の発色が認められた場合を有効とし、eの位置に青色の発色が認められた場合にノロウイルス陽性と判定した。またhの位置に発色が認められない場合を無効とした。
実施例6と同じ。
b:ラテックス粒子標識抗体乾燥パッド(標識物質乾燥パッド)
c:サンプル吸収パッド
d:ニトロセルロースメンブレン
e〜g:被検出物に特異的に結合する捕捉物質がd上でライン状に結合している位置
h:標識物質を結合することができる物質がd上でライン状に結合している位置
i:バッキングシート
j:透明プラスチックラミネート
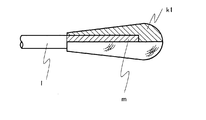
k1:綿を巻き付けた綿球からなる検体採取部分
k2:繊維をブラシ状に配置した検体採取部分
l:軸部
m:頭部
n:ろ過用ノズル
o1〜o3:ろ過フィルター
p:検体浮遊液チューブ
Claims (14)
- 検体中の被検出物を捕捉するための捕捉試薬が結合したメンブレンを備えたアッセイ装置上で検体中の被検出物の存在を検出又は定量することを含む簡易メンブレンアッセイ法において、繊維がブラシ状に配置されたブラシ状綿棒を検体採取器具として用いて、ヒト又は他の動物の咽頭拭い液、鼻腔拭い液、鼻腔吸引液、鼻腔洗浄液、肺胞洗浄液、便懸濁液及び直腸拭い液からなる群から選択される検体を採取し、ブラシ状綿棒により採取した検体を検体浮遊液に浮遊させ試料を調製し、調製した試料を強剛性フィルターが含まれるろ過フィルターを用いて加圧ろ過することを含む、簡易メンブレンアッセイ方法。
- フレキシブルな材質からなり検体から調製した試料をろ過することができるろ過チューブの内部に前記試料を入れた状態で、内部に圧力を加えることで、検体から調製した試料を加圧ろ過することを特徴とする請求項1に記載の簡易メンブレンアッセイ方法
- 強剛性フィルターが焼結フィルターである請求項1または2に記載の簡易メンブレンアッセイ方法。
- 焼結フィルターの素材がポリプロピレン、ポリエチレン、ポリスチレン及びポリメチルメタクリレートからなる群から選択される請求項3に記載の簡易メンブレンアッセイ方法。
- 検体中の被検出物が呼吸器感染症の原因微生物若しくは該微生物由来の物質又はそれらに対する抗体である請求項1〜4のいずれか1項に記載の簡易メンブレンアッセイ方法。
- 検体中の被検出物がインフルエンザウイルス、RSウイルス、アデノウイルス、A群溶連菌及び肺炎マイコプラズマからなる群から選択される病原微生物若しくは該微生物由来の物質又はそれらに対する抗体である請求項5に記載の簡易メンブレンアッセイ方法。
- 検体中の被検出物が下痢症の原因微生物若しくは該微生物由来の物質又はそれらに対する抗体である請求項1〜4のいずれか1項に記載の簡易メンブレンアッセイ方法。
- 検体中の被検出物がノロウイルス、ロタウイルス、サポウイルス及び下痢症アデノウイルスからなる群から選択される病原微生物若しくは該微生物由来の物質又はそれらに対する抗体である請求項7に記載の簡易メンブレンアッセイ方法。
- フロースルー式又はラテラルフロー式メンブレンアッセイ方法である、請求項1〜8のいずれか1項に記載の簡易メンブレンアッセイ方法。
- ろ過フィルターが孔径の異なる複数のフィルターを重ねて構成されており、最小孔径を有するフィルターの孔径が、メンブレンを備えたアッセイ装置のメンブレンの孔径以下であり、最大孔径を有するフィルターの孔径が前記メンブレンの孔径以上でありかつ200μm以下である、請求項1〜9のいずれか1項に記載の簡易メンブレンアッセイ方法。
- 試料を最初に最大孔径を有するフィルターを通過させ、次いでより小さい孔径を有するフィルターを通過させる請求項10記載の簡易メンブレンアッセイ方法。
- 以下を含む、検体中の被検出物の存在を検査するための簡易メンブレンアッセイキット;
(1)強剛性フィルターを含むフィルターにより構成されたろ過フィルターを備えた検体試料用加圧ろ過チューブ、
(2)検体中の被検出物を捕捉するための捕捉物質が結合したメンブレンを備えたアッセイ装置、及び
(3)繊維がブラシ状に配置されたブラシ状綿棒。 - さらに、以下の(4)から(7)の少なくとも1つを含む請求項12記載の簡易メンブレンアッセイキット;
(4)検体浮遊液、
(5)洗浄液組成物、
(6)標識物質、及び
(7)コントロール液。 - ろ過フィルターが孔径の異なる複数のフィルターを重ねて構成されており、最小孔径を有するフィルターの孔径が、メンブレンを備えたアッセイ装置のメンブレンの孔径以下であり、最大孔径を有するフィルターの孔径が前記メンブレンの孔径以上でありかつ200μm以下である、請求項12又は13に記載の簡易メンブレンアッセイキット。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2007269365A JP4339906B2 (ja) | 2006-10-19 | 2007-10-16 | 試料ろ過フィルターを用いる簡易メンブレンアッセイ方法及びキット |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2006285113 | 2006-10-19 | ||
| JP2007269365A JP4339906B2 (ja) | 2006-10-19 | 2007-10-16 | 試料ろ過フィルターを用いる簡易メンブレンアッセイ方法及びキット |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2008286739A Division JP5586842B2 (ja) | 2006-10-19 | 2008-11-07 | 試料ろ過フィルターを用いる簡易メンブレンアッセイ方法及びキット |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2008122372A JP2008122372A (ja) | 2008-05-29 |
| JP2008122372A5 JP2008122372A5 (ja) | 2008-12-25 |
| JP4339906B2 true JP4339906B2 (ja) | 2009-10-07 |
Family
ID=39507256
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2007269365A Active JP4339906B2 (ja) | 2006-10-19 | 2007-10-16 | 試料ろ過フィルターを用いる簡易メンブレンアッセイ方法及びキット |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP4339906B2 (ja) |
Families Citing this family (18)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP5290131B2 (ja) * | 2009-11-16 | 2013-09-18 | デンカ生研株式会社 | 生物学的検体の採取用スワブ、該スワブの製造方法及び該スワブを用いたキット |
| ES2436358T3 (es) * | 2010-04-21 | 2013-12-30 | Puritan Medical Products Company, Llc | Material y dispositivo de recogida |
| JP5567932B2 (ja) | 2010-08-03 | 2014-08-06 | 田中貴金属工業株式会社 | イムノクロマトグラフィー用試薬組成物およびそれを用いた測定方法 |
| JP6004744B2 (ja) * | 2012-05-28 | 2016-10-12 | 栄研化学株式会社 | 検体希釈浮遊液およびそれを含む容器 |
| JP5686853B2 (ja) * | 2013-06-13 | 2015-03-18 | デンカ生研株式会社 | 生物学的検体の採取用スワブ、該スワブの製造方法及び該スワブを用いたキット |
| JP6454274B2 (ja) | 2013-06-21 | 2019-01-16 | アルフレッサファーマ株式会社 | Rsvを検出するためのイムノクロマトグラフィー装置 |
| FR3025315B1 (fr) * | 2014-08-29 | 2018-08-24 | Biomerieux | Dispositif d'obtention de matiere biologique et/ou d'information biologique a partir d'un echantillon a matrice heterogene |
| WO2017038711A1 (ja) * | 2015-08-28 | 2017-03-09 | 栄研化学株式会社 | 免疫学的測定用試薬組成物およびその用途 |
| CN108884488A (zh) * | 2017-03-15 | 2018-11-23 | 东洋纺株式会社 | 基因检测方法及基因检测试剂盒 |
| CN107727851A (zh) * | 2017-11-15 | 2018-02-23 | 北京舜雷科技有限公司 | 一种免疫凝集和胶体金层析试纸条相结合的用于检测hit抗体的系统 |
| WO2019208487A1 (ja) * | 2018-04-27 | 2019-10-31 | 公益財団法人筑波メディカルセンター | 病原性微生物の核酸検出方法 |
| JP7187175B2 (ja) * | 2018-04-27 | 2022-12-12 | 公益財団法人筑波メディカルセンター | 病原性微生物の核酸検出方法 |
| CN108479233B (zh) * | 2018-06-05 | 2023-05-09 | 山西省生态环境监测和应急保障中心(山西省生态环境科学研究院) | 一种烟尘采样滤膜的自动分离、拾取装置及方法 |
| JP7291659B2 (ja) * | 2020-04-16 | 2023-06-15 | デンカ株式会社 | アデノウイルスの免疫測定方法及び免疫測定器具 |
| JP7436274B2 (ja) * | 2020-04-16 | 2024-02-21 | デンカ株式会社 | アデノウイルスの免疫測定方法及び免疫測定器具 |
| CN113720831A (zh) * | 2020-05-26 | 2021-11-30 | 德路通(石家庄)生物科技有限公司 | 可即时识别目标物的装置及即时目标物识别方法 |
| JPWO2023112859A1 (ja) * | 2021-12-13 | 2023-06-22 | ||
| CN116448494A (zh) * | 2022-01-10 | 2023-07-18 | 浙江东方基因生物制品股份有限公司 | 一种生产制造收集样本的收集器的设备 |
Family Cites Families (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP3613876B2 (ja) * | 1995-02-15 | 2005-01-26 | 和光純薬工業株式会社 | 糞便採取用具 |
| JP2740489B2 (ja) * | 1995-10-31 | 1998-04-15 | 本多プラス株式会社 | 糞便採取容器 |
| AUPP323798A0 (en) * | 1998-04-28 | 1998-05-21 | Chandler, Howard Milne | Sample collection method |
| US7879293B2 (en) * | 2001-09-28 | 2011-02-01 | Orasure Technologies, Inc. | Sample collector and test device |
| ITMI20030643A1 (it) * | 2003-04-01 | 2004-10-02 | Copan Innovation Ltd | Tampone per il prelievo di campioni biologici |
| JP4199607B2 (ja) * | 2003-06-30 | 2008-12-17 | シスメックス株式会社 | 免疫クロマトグラフィー検査キットおよび免疫クロマトグラフィー検査方法 |
| JP4262616B2 (ja) * | 2004-03-01 | 2009-05-13 | 積水メディカル株式会社 | 検体の免疫学的検査方法及びその方法に用いる検査器具 |
| TW200643396A (en) * | 2005-03-14 | 2006-12-16 | Nipro Corp | Specimen material collection liquid container |
-
2007
- 2007-10-16 JP JP2007269365A patent/JP4339906B2/ja active Active
Also Published As
| Publication number | Publication date |
|---|---|
| JP2008122372A (ja) | 2008-05-29 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5639730B2 (ja) | 試料ろ過フィルターを用いる簡易メンブレンアッセイ方法及びキット | |
| JP4339906B2 (ja) | 試料ろ過フィルターを用いる簡易メンブレンアッセイ方法及びキット | |
| US8404479B2 (en) | Simple membrane assay method and kit | |
| JP5845033B2 (ja) | マイコプラズマ・ニューモニエ検出用イムノクロマトグラフィー試験デバイスおよびキット | |
| JP4286157B2 (ja) | メンブレンアッセイ法 | |
| JP2014098715A (ja) | 着色ラテックス粒子を用いるメンブレンアッセイ法およびキット | |
| JP2008014751A (ja) | 着色ラテックス粒子を用いるメンブレンアッセイ法およびキット | |
| JP3848599B2 (ja) | 簡易メンブレンアッセイ法及びキット | |
| JP4976068B2 (ja) | 簡易イムノアッセイ用検体浮遊液およびアッセイ方法 | |
| JP4365329B2 (ja) | 複数の被検出物を検出する簡易アッセイ装置及び方法 | |
| JP2006084351A (ja) | 検体浮遊液組成物、キット及び検査方法 | |
| JP5911404B2 (ja) | 簡易メンブレンアッセイ法及びキット | |
| JP2006118936A (ja) | メンブランエンザイムイムノアッセイ法 | |
| JP2012083370A (ja) | 着色ラテックス粒子を用いるメンブレンアッセイ法およびキット | |
| JP6405339B2 (ja) | 簡易メンブレンアッセイ法及びキット | |
| JP2009002961A (ja) | 簡易メンブレンアッセイ法及びキット | |
| EP4703727A1 (en) | Strip for lateral flow-type measurement method using wet nonwoven fabric for marker part | |
| WO2015093439A1 (ja) | ヘリコバクター・ピロリの検出方法 | |
| JP4276898B2 (ja) | メンブレンアッセイ法 | |
| JP6405269B2 (ja) | 簡易メンブレンアッセイ法及びキット | |
| JP2010044094A (ja) | 簡易メンブレンアッセイ法及びキット | |
| JP2006215044A (ja) | 簡易メンブレンアッセイ法及びキット | |
| JP2017078723A (ja) | 簡易メンブレンアッセイ法及びキット | |
| JP2020046436A (ja) | 簡易メンブレンアッセイ法及びキット |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20081107 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20081107 |
|
| A871 | Explanation of circumstances concerning accelerated examination |
Free format text: JAPANESE INTERMEDIATE CODE: A871 Effective date: 20081107 |
|
| A975 | Report on accelerated examination |
Free format text: JAPANESE INTERMEDIATE CODE: A971005 Effective date: 20081211 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20090120 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20090323 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20090616 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20090702 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 4339906 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20120710 Year of fee payment: 3 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20120710 Year of fee payment: 3 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20130710 Year of fee payment: 4 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| S111 | Request for change of ownership or part of ownership |
Free format text: JAPANESE INTERMEDIATE CODE: R313111 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |