JP2022075813A - ジクアホソル含有点眼液 - Google Patents
ジクアホソル含有点眼液 Download PDFInfo
- Publication number
- JP2022075813A JP2022075813A JP2022039183A JP2022039183A JP2022075813A JP 2022075813 A JP2022075813 A JP 2022075813A JP 2022039183 A JP2022039183 A JP 2022039183A JP 2022039183 A JP2022039183 A JP 2022039183A JP 2022075813 A JP2022075813 A JP 2022075813A
- Authority
- JP
- Japan
- Prior art keywords
- diquafosol
- sodium
- ophthalmic solution
- chelating agent
- acid
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/08—Solutions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7084—Compounds having two nucleosides or nucleotides, e.g. nicotinamide-adenine dinucleotide, flavine-adenine dinucleotide
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/08—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite containing oxygen, e.g. ethers, acetals, ketones, quinones, aldehydes, peroxides
- A61K47/12—Carboxylic acids; Salts or anhydrides thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/16—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite containing nitrogen, e.g. nitro-, nitroso-, azo-compounds, nitriles, cyanates
- A61K47/18—Amines; Amides; Ureas; Quaternary ammonium compounds; Amino acids; Oligopeptides having up to five amino acids
- A61K47/183—Amino acids, e.g. glycine, EDTA or aspartame
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/24—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite containing atoms other than carbon, hydrogen, oxygen, halogen, nitrogen or sulfur, e.g. cyclomethicone or phospholipids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0048—Eye, e.g. artificial tears
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
- A61P27/04—Artificial tears; Irrigation solutions
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Veterinary Medicine (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Public Health (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Epidemiology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Oil, Petroleum & Natural Gas (AREA)
- Molecular Biology (AREA)
- Ophthalmology & Optometry (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Biophysics (AREA)
- Organic Chemistry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Medicinal Preparation (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
【解決手段】0.0001~1%(w/v)の濃度のキレート剤を含有するジクアホソル点眼液では、ジクアホソル点眼液で認められる保存中の不溶性析出物の発生、および製造過程(ろ過滅菌過程)におけるろ過性の低下が抑制された。また、キレート剤を含有するジクアホソル点眼液では、キレート剤を含有しないジクアホソル点眼液に比して、眼刺激性の軽減および保存効力の増強も確認された。したがって、本発明は、製造および流通過程ならびに患者による保存過程においても安定した物理化学的性質を有する上、眼刺激性の軽減および保存効力の増強も確認された。特に、キレート剤を含有するジクアホソル点眼液は、製造過程(ろ過滅菌過程)におけるろ過性の低下が抑制されているため、製造過程では効率的なろ過滅菌が可能であり、製造コストの抑制に寄与する。
【選択図】図1
Description
また、本発明は、0.1~10%(w/v)の濃度のジクアホソルまたはその塩を含有する水性点眼液の製造方法であって、ジクアホソルまたはその塩および該水性点眼液中のキレート剤の最終濃度が0.0001~1%(w/v)となる量のキレート剤を混合して不溶性析出物の発生が抑制された水溶液を得るステップを含む製造方法(以下、単に「本製造方法」ともいう)についても提供する。
本発明において、「キレート剤」とは、金属イオンをキレート化する化合物であれば特に制限はされないが、例えば、エデト酸(エチレンジアミン四酢酸)、エデト酸一ナトリウム、エデト酸二ナトリウム、エデト酸三ナトリウム、エデト酸四ナトリウム、エデト酸二カリウム、エデト酸三カリウム、エデト酸四カリウムなどのエデト酸またはその塩;クエン酸、クエン酸一ナトリウム、クエン酸二ナトリウム、クエン酸三ナトリウム、クエン酸一カリウム、クエン酸二カリウム、クエン酸三カリウムなどのクエン酸またはその塩;メタリン酸、メタリン酸ナトリウム、メタリン酸カリウムなどのメタリン酸またはその塩;ピロリン酸、ピロリン酸四ナトリウム、ピロリン酸四カリウムなどのピロリン酸またはその塩;ポリリン酸、ポリリン酸ナトリウム、ポリリン酸カリウムなどのポリリン酸またはその塩;リンゴ酸一ナトリウム、リンゴ酸二ナトリウム、リンゴ酸一カリウム、リンゴ酸二カリウムなどのリンゴ酸またはその塩;酒石酸ナトリウム、酒石酸カリウム、酒石酸カリウムナトリウムなどの酒石酸またはその塩;フィチン酸ナトリウム、フィチン酸カリウムなどのフィチン酸またはその塩、などを挙げることができる。なお、本発明において、「エデト酸、クエン酸、メタリン酸、ピロリン酸、ポリリン酸、リンゴ酸、酒石酸、フィチン酸、およびそれらの塩」には、それぞれのフリー体またはそれらの塩の水和物および有機溶媒和物も含まれるものとする。
ジクアホソル点眼液の保存中の性状変化の有無を目視で確認するとともに、キレート剤であるエデト酸塩が該性状変化に及ぼす影響を検討した。
・キレート剤非含有処方
ジクアホソルナトリウム3g、リン酸水素ナトリウム水和物0.2g、塩化ナトリウム0.41g、塩化カリウム0.15gおよびベンザルコニウム塩化物0.0075gを水に溶解して100mLとし、pH調節剤を添加して、pH7.5、浸透圧比1.0とした。
ジクアホソルナトリウム3g、リン酸水素ナトリウム水和物0.2g、塩化ナトリウム0.41g、塩化カリウム0.15g、エデト酸ナトリウム水和物0.001gまたは0.1gおよびベンザルコニウム塩化物0.002gを水に溶解して100mLとし、pH調節剤を添加して、pH7.5、浸透圧比1.0とした。
上記キレート剤非含有処方および0.001または0.1%(w/v)エデト酸塩含有処方をガラス容器中で、25℃で3ヶ月間保存した後、目視によりその性状の変化の有無を確認した。
試験結果を表1に示す。
キレート剤を含有するジクアホソル点眼液については、流通過程および患者による保存過程においても、不溶性析出物が発生しないか、または該析出物の発生頻度および量が低減されることが示唆された。
ジクアホソル点眼液のろ過滅菌時のろ過性能の経時的変化を確認するとともに、キレート剤であるエデト酸塩が該変化に及ぼす影響を検討した。
・キレート剤非含有処方
ジクアホソルナトリウム30g、リン酸水素ナトリウム水和物2g、塩化ナトリウム4.1g、塩化カリウム1.5gおよびベンザルコニウム塩化物0.075gを水に溶解して1000mLとし、pH調節剤を添加して、pH7.5、浸透圧比1.0とした。
ジクアホソルナトリウム30g、リン酸水素ナトリウム水和物2g、塩化ナトリウム4.1g、塩化カリウム1.5g、エデト酸ナトリウム水和物0.01gおよびベンザルコニウム塩化物0.075gを水に溶解して1000mLとし、pH調節剤を添加して、pH7.5、浸透圧比1.0とした。
各調製物を、ろ過フィルターとして親水性PVDFメンブレンフィルター(日本ポール社製、フロロダインIIディスクフィルターφ47mm、ポアサイズ0.2μm(型式FTKDFL)を2段使用し、ろ過圧力200kPa、室温でろ過を行なった。そのときのろ過時間とろ過量を測定し、その関係をプロットした。
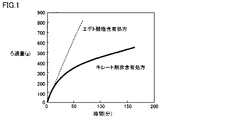
図1は、エデト酸塩含有処方、キレート剤非含有処方それぞれのジクアホソル点眼液でのろ過性能試験の結果を示すグラフであり、縦軸はろ過量(g)、横軸はろ過時間(分)である。図1から明らかなように、キレート剤非含有処方については、ろ過滅菌中にろ過量の低下(ろ過率の低下)が認められる一方、エデト酸塩含有処方では、ろ過率の低下が完全に抑制されることが示された。
キレート剤を含有するジクアホソル点眼液については、製造過程(ろ過滅菌過程)におけるろ過率の低下が完全に抑制されることから、キレート剤を含有しないジクアホソル点眼液と比較して、効率的にろ過滅菌できることが示唆された。なお、キレート剤を含有しないジクアホソル点眼液において認められたろ過率の低下は、不溶性析出物(目視できないものも含まれる)の目詰まりが原因であるものと考えられる。
エデト酸塩およびエデト酸塩以外のキレート剤が、ジクアホソル点眼液のろ過滅菌時のろ過性能の経時的変化に及ぼす影響を比較検討した。
・キレート剤非含有処方
ジクアホソルナトリウム30g、リン酸水素ナトリウム水和物2g、塩化ナトリウム4.1g、塩化カリウム1.5gおよびベンザルコニウム塩化物0.075gを水に溶解して1000mLとし、pH調節剤を添加して、pH7.5、浸透圧比1.0とした。
ジクアホソルナトリウム30g、リン酸水素ナトリウム水和物2g、塩化ナトリウム4.1g、塩化カリウム1.5g、エデト酸ナトリウム水和物0.1gおよびベンザルコニウム塩化物0.075gを水に溶解して1000mLとし、pH調節剤を添加して、pH7.5、浸透圧比1.0とした。
ジクアホソルナトリウム30g、リン酸水素ナトリウム水和物2g、塩化ナトリウム4.1g、塩化カリウム1.5g、クエン酸一水和物0.1gおよびベンザルコニウム塩化物0.075gを水に溶解して1000mLとし、pH調節剤を添加して、pH7.5、浸透圧比1.0とした。
ジクアホソルナトリウム30g、リン酸水素ナトリウム水和物2g、塩化ナトリウム4.1g、塩化カリウム1.5g、メタリン酸ナトリウム0.1gおよびベンザルコニウム塩化物0.075gを水に溶解して1000mLとし、pH調節剤を添加して、pH7.5、浸透圧比1.0とした。
ジクアホソルナトリウム30g、リン酸水素ナトリウム水和物2g、塩化ナトリウム4.1g、塩化カリウム1.5g、ポリリン酸ナトリウム0.1gおよびベンザルコニウム塩化物0.075gを水に溶解して1000mLとし、pH調節剤を添加して、pH7.5、浸透圧比1.0とした。
各調製物を、ろ過フィルターとして親水性PVDFメンブレンフィルター(日本ポール社製、フロロダインIIディスクフィルターφ25mm、ポアサイズ0.2μm(型式FTKDFL)を2段使用し、ろ過圧力200kPa、室温でろ過を行なった。そのときのろ過時間と有効ろ過面積あたりのろ過量を測定し、その関係をプロットした。
図2は、キレート剤非含有処方、またはエデト酸塩、クエン酸、メタリン酸塩もしくはポリリン酸塩含有処方のそれぞれのジクアホソル点眼液でのろ過性能試験の結果を示すグラフであり、縦軸は有効ろ過面積あたりのろ過量(g/cm2)、横軸はろ過時間(分)を示す。図2から明らかなように、キレート剤非含有処方については、ろ過滅菌中にろ過量の低下(ろ過率の低下)が認められる一方、クエン酸、メタリン酸塩またはポリリン酸塩含有処方では、エデト酸塩含有処方同様に、ろ過率の低下が完全に抑制されることが示された。
キレート剤を含有するジクアホソル点眼液については、製造過程(ろ過滅菌過程)におけるろ過率の低下が完全に抑制されることから、キレート剤を含有しないジクアホソル点眼液と比較して、効率的にろ過滅菌できることが示唆された。
キレート剤を含有しないジクアホソル点眼液である「ジクアス(登録商標)点眼液3%」の添付文書には、同点眼液を使用したドライアイ患者の6.7%で副作用として眼刺激感が認められたことが記載されている。そこで、ドライアイ患者同様に角膜上皮が障害されたn-ヘプタノール角膜上皮剥離モデルを用いて、キレート剤の添加がジクアホソル点眼液の眼刺激性にどのような影響を及ぼすか否かを検討した。
・3%(w/v)ジクアホソルナトリウム含有/キレート剤非含有処方
ジクアホソルナトリウム3g、リン酸水素ナトリウム水和物0.2g、塩化ナトリウム0.41g、塩化カリウム0.15gおよびベンザルコニウム塩化物0.0075gを水に溶解して100mLとし、pH調節剤を添加して、pH7.2~7.8、浸透圧比1.0~1.1とした。
ジクアホソルナトリウム3g、リン酸水素ナトリウム水和物0.2g、塩化ナトリウム0.41g、塩化カリウム0.15g、エデト酸ナトリウム水和物0.01gおよびベンザルコニウム塩化物0.002gを水に溶解して100mLとし、pH調節剤を添加して、pH7.2~7.8、浸透圧比1.0~1.1とした。
ジクアホソルナトリウム8g、リン酸水素ナトリウム水和物0.2gおよびベンザルコニウム塩化物0.0075gを水に溶解して100mLとし、pH調節剤を添加して、pH7.2~7.8、浸透圧比1.0~1.1とした。
ジクアホソルナトリウム8g、リン酸水素ナトリウム水和物0.2g、エデト酸ナトリウム水和物0.01gおよびベンザルコニウム塩化物0.002gを水に溶解して100mLとし、pH調節剤を添加して、pH7.2~7.8、浸透圧比1.0~1.1とした。
リン酸水素ナトリウム水和物0.2g、塩化ナトリウム0.75g、塩化カリウム0.15gおよびベンザルコニウム塩化物0.0075gを水に溶解して100mLとし、pH調節剤を添加して、pH7.2~7.8、浸透圧比1.0~1.1とした。
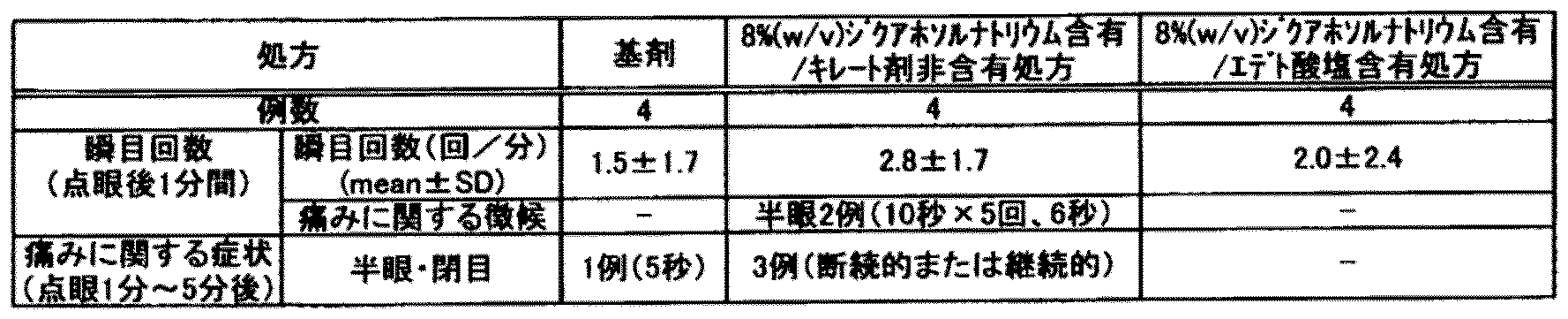
ウサギの左眼の角膜にn-ヘプタノール処置(1分間)を行なった後、角膜上皮を剥離し、その16~18時間後に、基剤、3%(w/v)ジクアホソルナトリウム含有/キレート剤非含有処方、または3%(w/v)ジクアホソルナトリウム含有/エデト酸塩含有処方を1回点眼し(50μL/眼)、点眼後1分間の瞬目回数の測定および点眼時の痛みに関連する症状の観察を行なった。その後続けて、点眼5分後までの閉目および半眼などの痛みに関する徴候を観察した(1群4例)。
試験結果を表2および表3に示す。
以上のように、ジクアホソル点眼液は、ドライアイ患者同様に角膜上皮が障害されたn-ヘプタノール角膜上皮剥離モデルにおいて、痛みに関する徴候である半眼・閉目を高頻度で引き起こす一方、該点眼液にキレート剤を添加することで、これらの事象の発現頻度は基剤レベルまで軽減されることが示唆された。すなわち、キレート剤を含有しないジクアホソル点眼液をドライアイ患者に点眼した場合に一定頻度で認められる副作用としての眼刺激は、キレート剤の添加により軽減されるものと思われる。
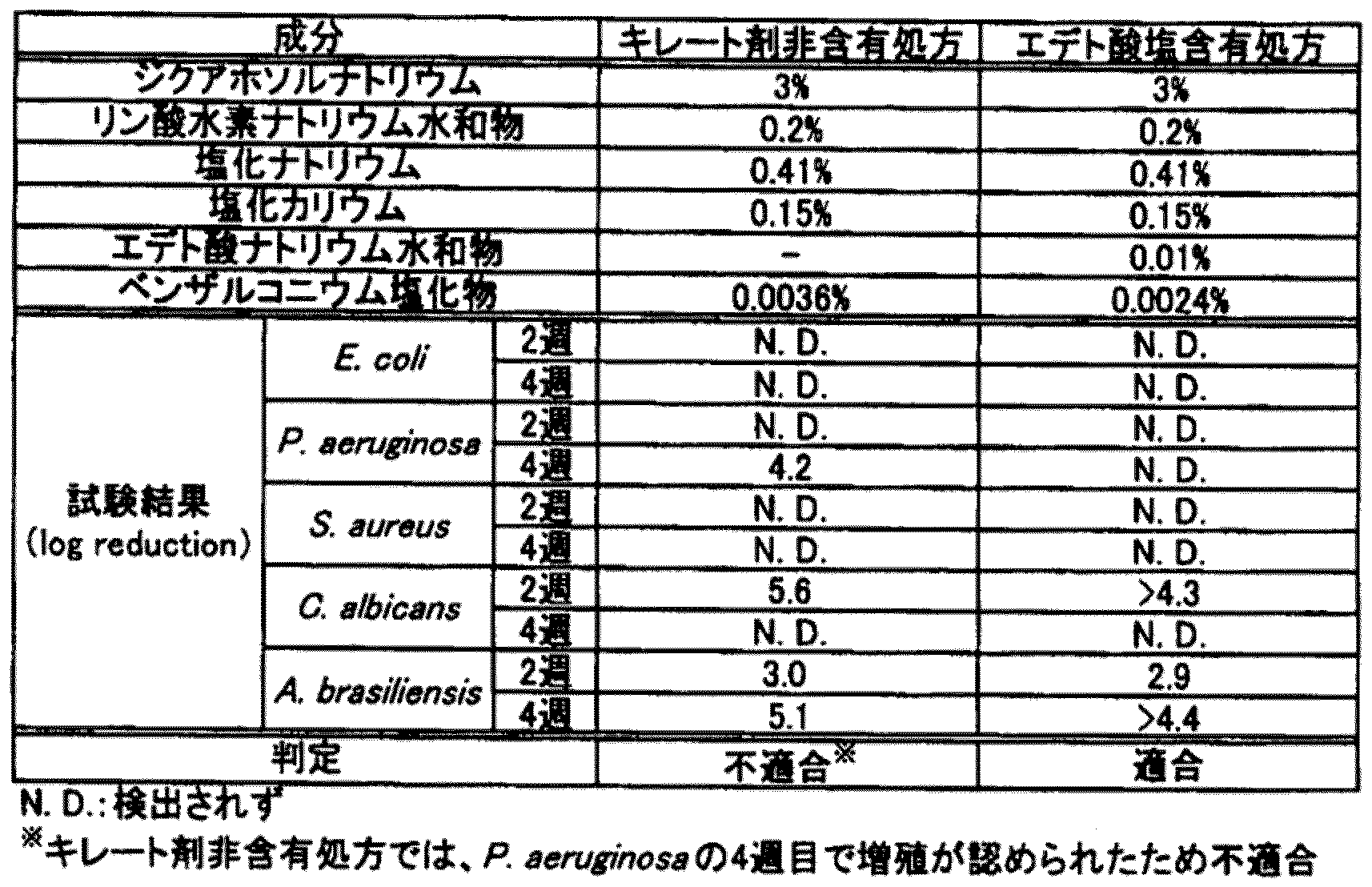
キレート剤がジクアホソル点眼液の保存効力に与える影響を確認するため、保存効力試験を行った。
・キレート剤非含有処方
ジクアホソルナトリウム3g、リン酸水素ナトリウム水和物0.2g、塩化ナトリウム0.41g、塩化カリウム0.15gおよびベンザルコニウム塩化物0.0036gを水に溶解して100mLとし、pH調節剤を添加して、pH7.2~7.8、浸透圧比1.0~1.1とした。
ジクアホソルナトリウム3g、リン酸水素ナトリウム水和物0.2g、塩化ナトリウム0.41g、塩化カリウム0.15g、エデト酸ナトリウム水和物0.01gおよびベンザルコニウム塩化物0.0024gを水に溶解して100mLとし、pH調節剤を添加して、pH7.2~7.8、浸透圧比1.0~1.1とした。
保存効力試験は、第十五改正日本薬局方の保存効力試験法に準拠して行なった。本試験では、試験菌として、Esherichia Coli(E.coli)、Pseudomonas aeruginosa(P.aeruginosa)、Staphylococcus aureus(S.aureus)、Candida albicans(C.albicans)およびAspergillus braziliensis(A.braziliensis)を用いた。
試験結果を表4に示す。
上記の結果から、ジクアホソル点眼液にキレート剤を添加することで、その保存効力が顕著に向上することが示唆された。すなわち、本点眼液については、キレート剤を含有しないジクアホソル点眼液と比して、点眼液中の防腐剤濃度を低下させ得るものと考えられる。
製剤例を挙げて本発明の薬剤をさらに具体的に説明するが、本発明はこれらの製剤例にのみ限定されるものではない。
100ml中
ジクアホソルナトリウム 3g
リン酸水素ナトリウム水和物 0.1~0.5g
塩化ナトリウム 0.01~1g
塩化カリウム 0.01~1g
エデト酸ナトリウム水和物 0.0001~0.1g
滅菌精製水 適量
滅菌精製水にジクアホソルナトリウムおよびそれ以外の上記成分を加え、これらを十分に混合することで上記点眼剤を調製できる。
100ml中
ジクアホソルナトリウム 3g
リン酸水素ナトリウム水和物 0.1~0.5g
塩化ナトリウム 0.01~1g
塩化カリウム 0.01~1g
BAK-C12 0.1~10g
エデト酸ナトリウム水和物 0.0001~0.1g
滅菌精製水 適量
滅菌精製水にジクアホソルナトリウムおよびそれ以外の上記成分を加え、これらを十分に混合することで上記点眼剤を調製できる。
100ml中
ジクアホソルナトリウム 3g
リン酸水素ナトリウム水和物 0.1~0.5g
塩化ナトリウム 0.01~1g
塩化カリウム 0.01~1g
BAK-C12 0.1~10g
クエン酸一水和物 0.0001~0.1g
滅菌精製水 適量
滅菌精製水にジクアホソルナトリウムおよびそれ以外の上記成分を加え、これらを十分に混合することで上記点眼剤を調製できる。
100ml中
ジクアホソルナトリウム 3g
リン酸水素ナトリウム水和物 0.1~0.5g
塩化ナトリウム 0.01~1g
塩化カリウム 0.01~1g
BAK-C12 0.1~10g
メタリン酸ナトリウム 0.0001~0.1g
滅菌精製水 適量
滅菌精製水にジクアホソルナトリウムおよびそれ以外の上記成分を加え、これらを十分に混合することで上記点眼剤を調製できる。
100ml中
ジクアホソルナトリウム 3g
リン酸水素ナトリウム水和物 0.1~0.5g
塩化ナトリウム 0.01~1g
塩化カリウム 0.01~1g
BAK-C12 0.1~10g
ポリリン酸ナトリウム 0.0001~0.1g
滅菌精製水 適量
滅菌精製水にジクアホソルナトリウムおよびそれ以外の上記成分を加え、これらを十分に混合することで上記点眼剤を調製できる。
Claims (1)
- 明細書に記載の発明。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2012069157 | 2012-03-26 | ||
| JP2012069157 | 2012-03-26 | ||
| JP2019022692A JP7042762B2 (ja) | 2012-03-26 | 2019-02-12 | ジクアホソル含有点眼液 |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2019022692A Division JP7042762B2 (ja) | 2012-03-26 | 2019-02-12 | ジクアホソル含有点眼液 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2022075813A true JP2022075813A (ja) | 2022-05-18 |
| JP7447176B2 JP7447176B2 (ja) | 2024-03-11 |
Family
ID=49259901
Family Applications (6)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2013062270A Active JP5625081B2 (ja) | 2012-03-26 | 2013-03-25 | ジクアホソル含有点眼液 |
| JP2014082821A Active JP6126041B2 (ja) | 2012-03-26 | 2014-04-14 | ジクアホソル含有点眼液 |
| JP2017075167A Active JP6389544B2 (ja) | 2012-03-26 | 2017-04-05 | ジクアホソル含有点眼液 |
| JP2018020154A Active JP6483299B2 (ja) | 2012-03-26 | 2018-02-07 | ジクアホソル含有点眼液 |
| JP2019022692A Active JP7042762B2 (ja) | 2012-03-26 | 2019-02-12 | ジクアホソル含有点眼液 |
| JP2022039183A Active JP7447176B2 (ja) | 2012-03-26 | 2022-03-14 | ジクアホソル含有点眼液 |
Family Applications Before (5)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2013062270A Active JP5625081B2 (ja) | 2012-03-26 | 2013-03-25 | ジクアホソル含有点眼液 |
| JP2014082821A Active JP6126041B2 (ja) | 2012-03-26 | 2014-04-14 | ジクアホソル含有点眼液 |
| JP2017075167A Active JP6389544B2 (ja) | 2012-03-26 | 2017-04-05 | ジクアホソル含有点眼液 |
| JP2018020154A Active JP6483299B2 (ja) | 2012-03-26 | 2018-02-07 | ジクアホソル含有点眼液 |
| JP2019022692A Active JP7042762B2 (ja) | 2012-03-26 | 2019-02-12 | ジクアホソル含有点眼液 |
Country Status (26)
| Country | Link |
|---|---|
| US (4) | US9486529B2 (ja) |
| EP (2) | EP3431092A1 (ja) |
| JP (6) | JP5625081B2 (ja) |
| KR (5) | KR101536885B1 (ja) |
| CN (2) | CN113018259A (ja) |
| AU (3) | AU2013241507A1 (ja) |
| BR (1) | BR112014023402B1 (ja) |
| CA (1) | CA2868390C (ja) |
| DK (1) | DK2832359T3 (ja) |
| EA (1) | EA028848B1 (ja) |
| ES (1) | ES2702575T3 (ja) |
| GE (1) | GEP20166470B (ja) |
| HK (1) | HK1204922A1 (ja) |
| HU (1) | HUE041671T2 (ja) |
| IN (1) | IN2014DN08632A (ja) |
| MX (1) | MX353874B (ja) |
| MY (1) | MY169816A (ja) |
| NZ (1) | NZ631041A (ja) |
| PH (1) | PH12014501955B1 (ja) |
| PL (1) | PL2832359T3 (ja) |
| PT (1) | PT2832359T (ja) |
| SG (2) | SG10201607872PA (ja) |
| TR (1) | TR201820073T4 (ja) |
| TW (4) | TWI625135B (ja) |
| UA (1) | UA113981C2 (ja) |
| WO (1) | WO2013146649A1 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2023165142A (ja) * | 2022-05-02 | 2023-11-15 | 株式会社三洋物産 | 遊技機 |
Families Citing this family (22)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2750229B2 (ja) | 1991-05-30 | 1998-05-13 | 信越石英株式会社 | 大型軽量化反射鏡 |
| JP2750234B2 (ja) | 1991-12-25 | 1998-05-13 | 信越石英株式会社 | シリカ質軽量反射鏡の製造方法 |
| EA028848B1 (ru) | 2012-03-26 | 2018-01-31 | Сантен Фармасьютикал Ко., Лтд. | Офтальмологический раствор, содержащий диквафасол |
| SG11201605366QA (en) * | 2014-01-10 | 2016-08-30 | Santen Pharmaceutical Co Ltd | Pharmaceutical composition containing pyridylaminoacetic acidcompound |
| MX384935B (es) * | 2014-12-25 | 2025-03-14 | Santen Pharmaceutical Co Ltd | Solucion oftalmica acuosa. |
| TWI711453B (zh) * | 2015-06-05 | 2020-12-01 | 日商參天製藥股份有限公司 | 抑制水性點眼液中之洛赫西定類的殘存率降低之方法 |
| ES2999137T3 (en) * | 2015-06-05 | 2025-02-24 | Santen Pharmaceutical Co Ltd | Therapeutic agent for dry eye characterized by being to be dropped into eye of dry eye patient wearing soft contact lens |
| CN107709345A (zh) * | 2015-06-29 | 2018-02-16 | 雅玛山酱油株式会社 | P1,p4‑二(尿苷5′)‑四磷酸晶体的保存方法 |
| JP6688057B2 (ja) * | 2015-12-01 | 2020-04-28 | 日水製薬株式会社 | グラム染色用後染色試液及びグラム染色方法 |
| SG11202007977RA (en) * | 2018-02-28 | 2020-09-29 | Santen Pharmaceutical Co Ltd | Ophthalmic composition comprising diquafosol and cationic polymer |
| CN108403625A (zh) * | 2018-04-11 | 2018-08-17 | 东莞解石医药科技有限公司 | 一种含有螯合剂的地夸磷索四钠滴眼液 |
| US11918603B2 (en) * | 2018-08-30 | 2024-03-05 | Harrow Ip, Llc | Ocular lubricant formulations |
| TWI848171B (zh) * | 2019-08-27 | 2024-07-11 | 日商參天製藥股份有限公司 | 含有迪夸弗索(diquafosol)或其鹽、及聚乙烯吡咯烷酮之水性眼科用組合物 |
| CN113720924B (zh) * | 2020-05-25 | 2025-01-10 | 南京帝昌医药科技有限公司 | 一种地夸磷索四钠的含量及有关物质检测方法 |
| JPWO2022107790A1 (ja) * | 2020-11-18 | 2022-05-27 | ||
| WO2022107791A1 (ja) * | 2020-11-18 | 2022-05-27 | 参天製薬株式会社 | ポリヘキサメチレンビグアナイドまたはその塩を含有する水性点眼液 |
| KR102548710B1 (ko) | 2020-12-24 | 2023-06-28 | 주식회사 종근당 | 디쿠아포솔 또는 이의 약제학적으로 허용가능한 염과 토코페롤을 함유하는 건성안 예방 또는 치료용 약제학적 조성물 |
| CN112933040A (zh) * | 2021-02-04 | 2021-06-11 | 合肥博思科创医药科技有限公司 | 一种舒更葡糖钠注射液的制备方法 |
| WO2023195718A1 (ko) * | 2022-04-04 | 2023-10-12 | 서울대학교산학협력단 | 감미 억제용 조성물 및 식품의 감미 억제 방법 |
| KR102794468B1 (ko) * | 2022-04-04 | 2025-04-14 | 서울대학교산학협력단 | 감미 억제용 조성물 및 식품의 감미 억제 방법 |
| CN116019767A (zh) * | 2023-01-12 | 2023-04-28 | 上海阿尔福斯医药科技有限公司 | 眼用制剂及其制备方法 |
| CN117838628B (zh) * | 2024-03-01 | 2024-05-28 | 广州市桐晖药业有限公司 | 一种地夸磷索钠滴眼液及其制备方法 |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP6389544B2 (ja) * | 2012-03-26 | 2018-09-12 | 参天製薬株式会社 | ジクアホソル含有点眼液 |
Family Cites Families (36)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH075456B2 (ja) * | 1988-10-01 | 1995-01-25 | 参天製薬株式会社 | 点眼液 |
| JP2530491B2 (ja) | 1988-12-20 | 1996-09-04 | 参天製薬株式会社 | ヒアルロン酸点眼液 |
| TW200402B (ja) | 1990-08-13 | 1993-02-21 | Senju Pharma Co | |
| US5504113A (en) | 1994-03-02 | 1996-04-02 | Allergan, Inc. | Enhancement of benzalkonium chloride preservative activity in formulations containing an incompatible drug |
| US5900407A (en) * | 1997-02-06 | 1999-05-04 | Inspire Pharmaceuticals, Inc. | Method of treating dry eye disease with uridine triphosphates and related compounds |
| EP0981534B1 (en) | 1997-02-06 | 2006-05-03 | Inspire Pharmaceuticals, Inc. | Dinucleotides and their uses |
| ATE261982T1 (de) | 1997-07-25 | 2004-04-15 | Inspire Pharmaceuticals Inc | Salze von di(uridine 5'-tetraphosphate), verfahren zur herstellung und verwendungen davon |
| KR19990074047A (ko) | 1998-03-03 | 1999-10-05 | 김수복 | 콘택트렌즈용 세척, 소독 및 보존제 조성물 |
| JP5138128B2 (ja) | 1998-08-21 | 2013-02-06 | 千寿製薬株式会社 | 水性液剤 |
| JP4880808B2 (ja) * | 1999-11-15 | 2012-02-22 | 久光製薬株式会社 | 人工涙液型点眼剤組成物 |
| CA2413928C (en) | 2000-05-30 | 2011-01-25 | Santen Pharmaceutical Co., Ltd. | Corneal epithelial migration promoter |
| JP4003008B2 (ja) * | 2000-05-30 | 2007-11-07 | 参天製薬株式会社 | 角膜上皮伸展促進剤 |
| US6555675B2 (en) * | 2000-08-21 | 2003-04-29 | Inspire Pharmaceuticals, Inc. | Dinucleoside polyphosphate compositions and their therapuetic use as purinergic receptor agonists |
| US6583181B1 (en) | 2000-11-22 | 2003-06-24 | Lonza Inc. | Antimicrobial quaternary ammonium compositions with reduced ocular irritation |
| JP2003160491A (ja) * | 2001-09-11 | 2003-06-03 | Santen Pharmaceut Co Ltd | ジウリジンリン酸含有点眼液 |
| CN1228053C (zh) * | 2001-09-11 | 2005-11-23 | 参天制药株式会社 | 含有二尿苷磷酸的滴眼液 |
| US20030109488A1 (en) | 2001-10-11 | 2003-06-12 | Alcon, Inc. | Methods for treating dry eye |
| ES2298672T3 (es) | 2003-04-14 | 2008-05-16 | Wyeth Holdings Corporation | Composiciones que contienen piperacilina y tazobactam utiles para inyeccion. |
| JP4806956B2 (ja) | 2004-04-20 | 2011-11-02 | 大正製薬株式会社 | 点眼用液剤 |
| US20060073172A1 (en) | 2004-10-01 | 2006-04-06 | Schneider L W | Stabilized ophthalmic solution for the treatment of glaucoma and lowering intraocular pressure |
| KR20070067189A (ko) | 2004-12-02 | 2007-06-27 | 비너스 레머디스 리미티드 | 주사제에 유용한 베타-락타마제 억제제를 이용한베타-락타마제-매개 항생제 내성에 대처하기 위한 조성물 |
| KR100870104B1 (ko) * | 2005-11-28 | 2008-11-26 | 주식회사 머젠스 | 안구건조증 치료 및 예방용 조성물 |
| JP4168071B2 (ja) | 2005-12-08 | 2008-10-22 | 興和株式会社 | 点眼用組成物 |
| JP2008247828A (ja) | 2007-03-30 | 2008-10-16 | Wakamoto Pharmaceut Co Ltd | ラタノプロストを含有する水性医薬組成物。 |
| JP2009040727A (ja) * | 2007-08-09 | 2009-02-26 | Towa Yakuhin Kk | ラタノプロストを有効成分とする安定な点眼液剤 |
| CN100534423C (zh) * | 2007-11-30 | 2009-09-02 | 张咏梅 | 一种保质期长的氯霉素滴眼液及其制备方法 |
| US8119112B2 (en) | 2008-01-31 | 2012-02-21 | Bausch & Lomb Incorporated | Ophthalmic compositions with an amphoteric surfactant and hyaluronic acid |
| CN101461778A (zh) * | 2009-01-06 | 2009-06-24 | 河北科技大学 | 不含抑菌剂的盐酸环丙沙星滴眼液及其制备方法 |
| WO2010085572A1 (en) * | 2009-01-23 | 2010-07-29 | Inspire Pharmaceuticals, Inc. | Method of treating dry eye disease with azithromycin |
| CN102100693A (zh) * | 2009-12-16 | 2011-06-22 | 沈阳兴齐制药有限公司 | 一种含有肌肽的人工泪液及其制备方法 |
| KR20110104367A (ko) | 2010-03-16 | 2011-09-22 | 삼천당제약주식회사 | 무보존제 안과용 조성물 |
| AU2011281035B2 (en) | 2010-07-21 | 2014-10-02 | Cumberland Pharmaceuticals, Inc. | Acetycysteine compositions and methods of use thereof |
| EA026680B1 (ru) | 2010-09-10 | 2017-05-31 | Сантен Фармасьютикал Ко., Лтд. | Средство для лечения синдрома сухого глаза, характеризующееся комбинированием агониста рецептора p2yи гиалуроновой кислоты или ее соли, способ лечения синдрома сухого глаза и применение агониста рецептора p2yи гиалуроновой кислоты или ее соли |
| US20140221306A1 (en) | 2010-12-28 | 2014-08-07 | Santen Pharmaceutical Co. Ltd | Ophthalmic solution comprising diquafosol, method for producing the same, and method for inhibiting formation of insoluble precipitate |
| WO2012141334A1 (en) * | 2011-04-12 | 2012-10-18 | R-Tech Ueno, Ltd. | Aqueous ophthalmic composition |
| JP2015514705A (ja) | 2012-03-26 | 2015-05-21 | ディラフォール・アクチボラゲットDilafor Ab | 分娩停止の処置のための方法 |
-
2013
- 2013-03-25 EA EA201491771A patent/EA028848B1/ru unknown
- 2013-03-25 EP EP18193430.8A patent/EP3431092A1/en not_active Withdrawn
- 2013-03-25 JP JP2013062270A patent/JP5625081B2/ja active Active
- 2013-03-25 SG SG10201607872PA patent/SG10201607872PA/en unknown
- 2013-03-25 TW TW102110422A patent/TWI625135B/zh active
- 2013-03-25 NZ NZ631041A patent/NZ631041A/en not_active IP Right Cessation
- 2013-03-25 TR TR2018/20073T patent/TR201820073T4/tr unknown
- 2013-03-25 EP EP13770386.4A patent/EP2832359B1/en active Active
- 2013-03-25 MX MX2014011468A patent/MX353874B/es active IP Right Grant
- 2013-03-25 AU AU2013241507A patent/AU2013241507A1/en not_active Abandoned
- 2013-03-25 HK HK15105452.3A patent/HK1204922A1/xx unknown
- 2013-03-25 CN CN202110358504.0A patent/CN113018259A/zh active Pending
- 2013-03-25 MY MYPI2014002576A patent/MY169816A/en unknown
- 2013-03-25 SG SG11201405799TA patent/SG11201405799TA/en unknown
- 2013-03-25 PL PL13770386T patent/PL2832359T3/pl unknown
- 2013-03-25 KR KR1020147028142A patent/KR101536885B1/ko not_active Ceased
- 2013-03-25 UA UAA201411576A patent/UA113981C2/uk unknown
- 2013-03-25 TW TW109124203A patent/TWI757799B/zh active
- 2013-03-25 KR KR1020187018799A patent/KR101935484B1/ko not_active Ceased
- 2013-03-25 US US14/386,169 patent/US9486529B2/en not_active Expired - Fee Related
- 2013-03-25 IN IN8632DEN2014 patent/IN2014DN08632A/en unknown
- 2013-03-25 CA CA2868390A patent/CA2868390C/en active Active
- 2013-03-25 TW TW106124911A patent/TWI692364B/zh active
- 2013-03-25 KR KR1020207022714A patent/KR20200096708A/ko not_active Ceased
- 2013-03-25 TW TW109100132A patent/TWI723722B/zh active
- 2013-03-25 HU HUE13770386A patent/HUE041671T2/hu unknown
- 2013-03-25 ES ES13770386T patent/ES2702575T3/es active Active
- 2013-03-25 CN CN201380016616.1A patent/CN104203254A/zh active Pending
- 2013-03-25 KR KR1020157004372A patent/KR101875845B1/ko not_active Ceased
- 2013-03-25 PT PT13770386T patent/PT2832359T/pt unknown
- 2013-03-25 GE GEAP201313609A patent/GEP20166470B/en unknown
- 2013-03-25 WO PCT/JP2013/058519 patent/WO2013146649A1/ja not_active Ceased
- 2013-03-25 KR KR1020187037979A patent/KR20190002751A/ko not_active Ceased
- 2013-03-25 BR BR112014023402-7A patent/BR112014023402B1/pt not_active IP Right Cessation
- 2013-03-25 DK DK13770386.4T patent/DK2832359T3/en active
-
2014
- 2014-04-14 JP JP2014082821A patent/JP6126041B2/ja active Active
- 2014-09-01 PH PH12014501955A patent/PH12014501955B1/en unknown
-
2016
- 2016-02-23 AU AU2016201111A patent/AU2016201111A1/en not_active Withdrawn
- 2016-02-23 AU AU2016201110A patent/AU2016201110B2/en not_active Ceased
- 2016-10-10 US US15/289,273 patent/US10071113B2/en active Active
-
2017
- 2017-04-05 JP JP2017075167A patent/JP6389544B2/ja active Active
-
2018
- 2018-02-07 JP JP2018020154A patent/JP6483299B2/ja active Active
- 2018-08-14 US US16/103,328 patent/US10632139B2/en not_active Expired - Fee Related
-
2019
- 2019-02-12 JP JP2019022692A patent/JP7042762B2/ja active Active
-
2020
- 2020-03-16 US US16/819,974 patent/US11166974B2/en not_active Expired - Fee Related
-
2022
- 2022-03-14 JP JP2022039183A patent/JP7447176B2/ja active Active
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP6389544B2 (ja) * | 2012-03-26 | 2018-09-12 | 参天製薬株式会社 | ジクアホソル含有点眼液 |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2023165142A (ja) * | 2022-05-02 | 2023-11-15 | 株式会社三洋物産 | 遊技機 |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7042762B2 (ja) | ジクアホソル含有点眼液 | |
| US20140221306A1 (en) | Ophthalmic solution comprising diquafosol, method for producing the same, and method for inhibiting formation of insoluble precipitate |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20220411 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20230307 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20230414 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20230623 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20230905 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20231101 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20240130 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20240228 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7447176 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |