JP2013542053A - 浄水のための還元されたグラフェン酸化物ベースの複合体 - Google Patents
浄水のための還元されたグラフェン酸化物ベースの複合体 Download PDFInfo
- Publication number
- JP2013542053A JP2013542053A JP2013526567A JP2013526567A JP2013542053A JP 2013542053 A JP2013542053 A JP 2013542053A JP 2013526567 A JP2013526567 A JP 2013526567A JP 2013526567 A JP2013526567 A JP 2013526567A JP 2013542053 A JP2013542053 A JP 2013542053A
- Authority
- JP
- Japan
- Prior art keywords
- nanocomposite
- rgo
- adsorbent
- metal
- shape
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J20/00—Solid sorbent compositions or filter aid compositions; Sorbents for chromatography; Processes for preparing, regenerating or reactivating thereof
- B01J20/02—Solid sorbent compositions or filter aid compositions; Sorbents for chromatography; Processes for preparing, regenerating or reactivating thereof comprising inorganic material
- B01J20/10—Solid sorbent compositions or filter aid compositions; Sorbents for chromatography; Processes for preparing, regenerating or reactivating thereof comprising inorganic material comprising silica or silicate
- B01J20/103—Solid sorbent compositions or filter aid compositions; Sorbents for chromatography; Processes for preparing, regenerating or reactivating thereof comprising inorganic material comprising silica or silicate comprising silica
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J20/00—Solid sorbent compositions or filter aid compositions; Sorbents for chromatography; Processes for preparing, regenerating or reactivating thereof
- B01J20/02—Solid sorbent compositions or filter aid compositions; Sorbents for chromatography; Processes for preparing, regenerating or reactivating thereof comprising inorganic material
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J20/00—Solid sorbent compositions or filter aid compositions; Sorbents for chromatography; Processes for preparing, regenerating or reactivating thereof
- B01J20/02—Solid sorbent compositions or filter aid compositions; Sorbents for chromatography; Processes for preparing, regenerating or reactivating thereof comprising inorganic material
- B01J20/06—Solid sorbent compositions or filter aid compositions; Sorbents for chromatography; Processes for preparing, regenerating or reactivating thereof comprising inorganic material comprising oxides or hydroxides of metals not provided for in group B01J20/04
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J20/00—Solid sorbent compositions or filter aid compositions; Sorbents for chromatography; Processes for preparing, regenerating or reactivating thereof
- B01J20/02—Solid sorbent compositions or filter aid compositions; Sorbents for chromatography; Processes for preparing, regenerating or reactivating thereof comprising inorganic material
- B01J20/20—Solid sorbent compositions or filter aid compositions; Sorbents for chromatography; Processes for preparing, regenerating or reactivating thereof comprising inorganic material comprising free carbon; comprising carbon obtained by carbonising processes
- B01J20/205—Carbon nanostructures, e.g. nanotubes, nanohorns, nanocones, nanoballs
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J20/00—Solid sorbent compositions or filter aid compositions; Sorbents for chromatography; Processes for preparing, regenerating or reactivating thereof
- B01J20/28—Solid sorbent compositions or filter aid compositions; Sorbents for chromatography; Processes for preparing, regenerating or reactivating thereof characterised by their form or physical properties
- B01J20/28002—Solid sorbent compositions or filter aid compositions; Sorbents for chromatography; Processes for preparing, regenerating or reactivating thereof characterised by their form or physical properties characterised by their physical properties
- B01J20/28004—Sorbent size or size distribution, e.g. particle size
- B01J20/28007—Sorbent size or size distribution, e.g. particle size with size in the range 1-100 nanometers, e.g. nanosized particles, nanofibers, nanotubes, nanowires or the like
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J20/00—Solid sorbent compositions or filter aid compositions; Sorbents for chromatography; Processes for preparing, regenerating or reactivating thereof
- B01J20/28—Solid sorbent compositions or filter aid compositions; Sorbents for chromatography; Processes for preparing, regenerating or reactivating thereof characterised by their form or physical properties
- B01J20/28014—Solid sorbent compositions or filter aid compositions; Sorbents for chromatography; Processes for preparing, regenerating or reactivating thereof characterised by their form or physical properties characterised by their form
- B01J20/28016—Particle form
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J20/00—Solid sorbent compositions or filter aid compositions; Sorbents for chromatography; Processes for preparing, regenerating or reactivating thereof
- B01J20/30—Processes for preparing, regenerating, or reactivating
- B01J20/32—Impregnating or coating ; Solid sorbent compositions obtained from processes involving impregnating or coating
- B01J20/3202—Impregnating or coating ; Solid sorbent compositions obtained from processes involving impregnating or coating characterised by the carrier, support or substrate used for impregnation or coating
- B01J20/3204—Inorganic carriers, supports or substrates
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J20/00—Solid sorbent compositions or filter aid compositions; Sorbents for chromatography; Processes for preparing, regenerating or reactivating thereof
- B01J20/30—Processes for preparing, regenerating, or reactivating
- B01J20/32—Impregnating or coating ; Solid sorbent compositions obtained from processes involving impregnating or coating
- B01J20/3202—Impregnating or coating ; Solid sorbent compositions obtained from processes involving impregnating or coating characterised by the carrier, support or substrate used for impregnation or coating
- B01J20/3206—Organic carriers, supports or substrates
- B01J20/3208—Polymeric carriers, supports or substrates
- B01J20/3212—Polymeric carriers, supports or substrates consisting of a polymer obtained by reactions otherwise than involving only carbon to carbon unsaturated bonds
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J20/00—Solid sorbent compositions or filter aid compositions; Sorbents for chromatography; Processes for preparing, regenerating or reactivating thereof
- B01J20/30—Processes for preparing, regenerating, or reactivating
- B01J20/32—Impregnating or coating ; Solid sorbent compositions obtained from processes involving impregnating or coating
- B01J20/3231—Impregnating or coating ; Solid sorbent compositions obtained from processes involving impregnating or coating characterised by the coating or impregnating layer
- B01J20/3234—Inorganic material layers
- B01J20/3236—Inorganic material layers containing metal, other than zeolites, e.g. oxides, hydroxides, sulphides or salts
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B82—NANOTECHNOLOGY
- B82Y—SPECIFIC USES OR APPLICATIONS OF NANOSTRUCTURES; MEASUREMENT OR ANALYSIS OF NANOSTRUCTURES; MANUFACTURE OR TREATMENT OF NANOSTRUCTURES
- B82Y30/00—Nanotechnology for materials or surface science, e.g. nanocomposites
-
- C—CHEMISTRY; METALLURGY
- C02—TREATMENT OF WATER, WASTE WATER, SEWAGE, OR SLUDGE
- C02F—TREATMENT OF WATER, WASTE WATER, SEWAGE, OR SLUDGE
- C02F1/00—Treatment of water, waste water, or sewage
- C02F1/28—Treatment of water, waste water, or sewage by sorption
- C02F1/281—Treatment of water, waste water, or sewage by sorption using inorganic sorbents
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2220/00—Aspects relating to sorbent materials
- B01J2220/50—Aspects relating to the use of sorbent or filter aid materials
- B01J2220/56—Use in the form of a bed
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10T—TECHNICAL SUBJECTS COVERED BY FORMER US CLASSIFICATION
- Y10T428/00—Stock material or miscellaneous articles
- Y10T428/31504—Composite [nonstructural laminate]
- Y10T428/31678—Of metal
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10T—TECHNICAL SUBJECTS COVERED BY FORMER US CLASSIFICATION
- Y10T428/00—Stock material or miscellaneous articles
- Y10T428/31504—Composite [nonstructural laminate]
- Y10T428/31678—Of metal
- Y10T428/31681—Next to polyester, polyamide or polyimide [e.g., alkyd, glue, or nylon, etc.]
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10T—TECHNICAL SUBJECTS COVERED BY FORMER US CLASSIFICATION
- Y10T428/00—Stock material or miscellaneous articles
- Y10T428/31504—Composite [nonstructural laminate]
- Y10T428/31678—Of metal
- Y10T428/31703—Next to cellulosic
Abstract
【選択図】図1
Description
特に別段の定めがない限り、本明細書中で用いられる全ての技術用語および科学用語は、本発明が属する分野の通常の知識を有する者により通常理解されるのと同じ意味を有する。本明細書中で記載されるものと類似または同等の任意の方法および材料を本発明の実施または試験で用いることができるが、ここでは例示的方法および材料を記載する。
1つの態様において、本発明のナノ複合体は、GO/RGOと好適な金属/金属酸化物ナノ粒子との複合体を含んでもよい。ナノ複合体中に組み入れることができる金属としては、限定されないが、金、銀、白金、パラジウム、コバルト、マンガン、鉄、テルル、ロジウム、ルテニウム、銅、イリジウム、モリブデン、クロム、セリウム、またはそれらの組み合わせが挙げられる。ナノ複合体中に組み入れることができる金属酸化物としては、限定されないが、MnO2などが挙げられる。例示的ナノ複合体は、式RGO−Ag、RGO−Au、RGO−Pt、RGO−Pd、RGO−Fe、RGO−Rh、RGO−MnOx、RGO−CoO、RGO−TeO2、RGO−Ce2O3、RGO−Cr2O3およびそれらの組み合わせに対応する可能性がある。
1つの態様において、RGO−金属/金属酸化物ナノ複合体は、限定されないが、シリカなどの担持材料または基体上に固定されている。結果としての担持された複合体は、水から重金属廃棄物を除去するために用いられる。様々な態様において、担持材料は、アルミナ、ゼオライト、活性炭、セルロース繊維、ココナッツ繊維、クレー、バナナシルク、ナイロン、ヤシ殻およびそれらの組み合わせをさらに含んでもよい。1つの態様において、RGO−金属/金属酸化物ナノ複合体は、キトサンなどの好適な環境にやさしい結合剤を用いることによって、シリカに結合させることができる。結合剤は、ポリアニリン、ポリビニルアルコール、ポリビニルピロリドン(PVP)、およびそれらの組み合わせをさらに含んでもよい。
上述のように、RGO−金属/金属酸化物ナノ複合体は、水から重金属を除去するための吸着剤組成物として用いることができる。重金属の例としては、鉛(Pb(II))およびマンガン(Mn(II))、銅(Cu(II))、ニッケル(Ni(II))、カドミウム(Cd(II))および水銀(Hg(II))が挙げられるが、これらに限定されるものではない。例示的水源は、地下水源、工業原料、水道水、水源および/またはそれらの組み合わせのいずれかであり得る。
本開示のナノコーティングはさらに、スーパーコンデンサ、スズキカップリングなどの有機反応、水素化反応および脱水素化反応、ならびに石油のクラッキングにおいて、燃料電池、水素貯蔵などにおける酸素還元反応の触媒においても適用される可能性がある。
グラファイト粉末からの例示的GO合成は、Kovtyukhovaらによって報告されている修正されたHummers法(Hummers, W. S., Offeman, R. E., Preparation of graphitic oxide. J. Am. Chem. Soc. 1958, 80, 1339.; Kovtyukhova, N. I., Ollivier, P. J., Martin, B. R., Mallouk, T. E., Chizhik, S. A., Buzaneva, E. V., Gorchinskiy, A. D., Layer-by-Layer assembly of ultrathin composite films from micron-sized graphite oxide sheets and polycations. Chem. Mater. 1999, 11, 771)(その内容は、参照することによって本明細書中に組み込まれる)に基づいて実施した。容積をスケールアップして、実験要件に合わせた。完全な酸化は、予備酸化ステップを実際の酸化より先におこなうことによって確実にした。予備酸化されたグラファイトは酸化ステップ中に完全に酸化されてGOを形成し、その詳細は、Kovtyukhovaらによって報告されている。
RGO複合体をシリカ上に担持させるために、以下のプロトコルを採用した。最初に、調製したままのRGO−MnO2/RGO−Agおよびキトサン(Ch)溶液(1.5%酢酸中0.8%キトサン)を1:1比で混合した。混合物を十分に撹拌して、均質な分散液を得た。25mLの均質な分散液を10gのシリカに添加し、十分に混合した。混合物を約40℃にて一定して撹拌しながら乾燥して、均一なコーティングを確実にした。コーティングを安定化するために、乾燥試料をアンモニア溶液(35%)中に約1時間浸し、その後、洗浄水のpHがほぼ中性になるまで蒸留水で洗浄した。材料を40℃にて一晩乾燥し、さらなる使用のためにガラスビン中で保管した。
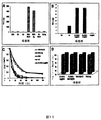
2つのRGO−金属/金属酸化物組成物(RGO−MnO2およびRGO−Ag)(担持および非担持形態の両方)を水性媒体からのHg(II)の除去におけるそれらの有用性について評価した。RGO、活性炭(AC)、Ag添着炭素(AC−Ag)、MnO2添着炭素(AC−MnO2)、シリカ、キトサン(Ch)をはじめとする様々な他の吸着剤のHg(II)取り込み能力をRGO−複合体と比較した。バッチ吸着実験を20mLのガラスビン中で実施し、作動容積を10mLに維持した。均質な吸着剤分散液をリアクター中にとり、標的汚染物質をこの溶液中に混合して、必要とされる濃度(1mg/L)のHg(II)を得た。シリカ上に固定された担持RGO複合体について、250mgの吸着剤を秤量し、1mg/LのHg(II)溶液10mLに添加した。全ての場合で、溶液を30(±2)℃にて撹拌し続けた。試料をあらかじめ決められた時間間隔で集め、残留水銀濃度について分析した。固液分離を、用いられる吸着剤に応じて膜ろ過によるかまたは単純な沈殿によって実施した。ろ過プロトコルは、200nm膜ろ紙(Sartorius Stedim(商標) biotech and biolab products)を通し、続いて100nm陽極酸化ろ紙(Whatman(商標)、Schleicher(商標)およびSchuell(商標))を通して吸着剤分散液をろ過することを含んでいた。真水中で吸着実験を実施するために、約1mg/LのHg(II)を地下水中にスパイクすることによって水を刺激した。地下水の水質特性を表1に記載する(図16中に示す)。他の重金属(Ni(II)、Cd(II)およびCu(II))の存在下での水性媒体からのHg(II)除去の特異性を試験するために、前述の手順によって示されるように、約1.0、2.0および5.0mg/Lの各4つの金属イオンの水溶液の混合物を用いることによって、選択的金属イオン吸着試験を実施した。溶液中に存在する残留金属イオン濃度は、PerkinElmer 5300 DVシリーズ誘導結合プラズマ(ICP−AES)分析器(商標)を用いることによって測定した。
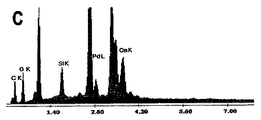
表面形態、元素分析および元素マッピング研究を、エネルギー分散型X線分析(EDX)(INCA, Oxford Instruments(商標)、英国)を備えた透過型電子顕微鏡(TEM)を用いて実施した。前述のようにした調製された試料を銅格子上に担持されたアモルファス炭素フィルム上にドロップキャストし、室温で乾燥した。走査型電子顕微鏡(SEM)(FEI quanta 200(商標))も同様に使用して、試料を特性化した。前述のようにして調製した試料をインジウムスズ酸化物(ITO)導電性ガラス上にスポットし、乾燥した。試料の高分解能透過型電子顕微鏡(HRTEM)画像をJEM 3010(JEOL JEM 3010(商標)、日本)で得た。Omicron NanotecnologyのESCA Probe TPD(商標)を用いてX線光電子分光(XPS)分析をおこなった。多色Mg KαをX線源(hν=1253.6eV)として使用した。必要な結合エネルギー範囲中のスペクトルを集め、平均をとった。試料の光線によって誘発された損傷は、X線フラックスを調節することによって低減した。284.5eVでのC1に関して結合エネルギーを較正した。Lambda 25分光計(Perkin-Elmer(商標)、米国)を用いてUV/Visスペクトルを測定した。ラマン分光器(WiTec GmbH CRM 200(商標)、独国)も使用して試料を特性化した。
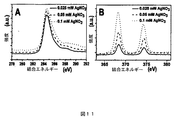
図1は、様々な金属イオンをRGO懸濁液に添加することに伴うUV/Visスペクトルの変化を示す。全てのスペクトルは金属イオン前駆体添加の12時間後に集めた。図1Aは、KMnO4をRGO溶液に添加した後に観察されるスペクトルの変化を示す。低濃度では、UV/VisスペクトルにおいてKMnO4に対応するピークはない。270nmでのRGOピークおよび金属酸化物(この場合はMnO2)に特徴的なブロードなピークだけが見られる。このピークと通常どおり作製されたMnO2ナノ粒子との比較によって、400nm付近のブロードな特性がMnO2ナノ粒子の形成によるものであることが裏付けられる。スペクトルの変化は、KMnO4のコロイド状MnO2ナノ粒子への還元を示す。565nmでのKMnO4特性は、添加されたKMnO4の濃度が0.1mMに達したら現れ始める。この濃度以降は、還元が不完全である。添加されたKMnO4の濃度が増大するにつれて、270でのグラフェンのピークについてブルーシフトがある。このブルーシフトは、RGOのGOへの酸化の徴候である。これらの結果は、GOおよびMnO2を作製するKMnO4によるグラフェンの酸化と解釈することができる。図1B〜Dは、RGOによるAu3+、Ag+およびPt2+の還元のUV/Visスペクトル特性を示す。全ての試験された元素は、添加された前駆体イオン濃度を増大させるとRGOピークでブルーシフトを示し、RGOの酸化を示す。
Claims (46)
- 還元されたグラフェン酸化物(RGO)ならびに少なくとも1つの金属および金属の酸化物のナノ粒子を含むナノ複合体であって、前記金属が、少なくとも1つの金、銀、白金、パラジウム、コバルト、マンガン、鉄、テルル、ロジウム、ルテニウム、銅、イリジウム、モリブデン、クロムおよびセリウムを含む、ナノ複合体。
- ナノ粒子が約1nm〜100nmの直径を有する、請求項1記載のナノ複合体。
- ナノ粒子が約3nm〜10nmの直径を有する、請求項1記載のナノ複合体。
- ナノ複合体が、RGO−Ag、RGO−Au、RGO−Pt、RGO−Pd、RGO−Fe、RGO−Rh、RGO−MnOx、RGO−CoO、RGO−TeO2、RGO−Ce2O3、RGO−Cr2O3の少なくとも1つを含む、請求項1記載のナノ複合体。
- ナノ粒子が非球状である、請求項1記載のナノ複合体。
- ナノ粒子が四面体形状、三角形状、角柱形状、ロッド形状、六角形状、立方体形状、リボン形状、管形状、らせん形状、樹枝形状、花形状、星形状、またはそれらの組み合わせのものである、請求項1記載のナノ複合体。
- ナノ複合体が、水から1以上の重金属を吸着することができる、請求項1記載のナノ複合体。
- 1以上の重金属が、少なくとも1つの鉛(Pb(II))およびマンガン(Mn(II))、銅(Cu(II))、ニッケル(Ni(II))、カドミウム(Cd(II))および水銀(Hg(II))金属を含む、請求項7記載のナノ複合体。
- ナノ複合体が、少なくとも1つのアルミナ、ゼオライト、活性炭、セルロース繊維、ココナッツ繊維、クレー、バナナシルク、ナイロン、またはヤシ殻を含む材料上に担持されている、請求項1記載のナノ複合体。
- ナノ複合体を含む吸着剤であって、前記ナノ複合体が、還元されたグラフェン酸化物(RGO)ならびに少なくとも1つの金属および金属の酸化物のナノ粒子を含み、前記金属が、金、銀、白金、パラジウム、コバルト、マンガン、鉄、テルル、ロジウム、ルテニウム、銅、イリジウム、モリブデン、クロムおよびセリウムの少なくとも1つを含む、吸着剤。
- 吸着剤が、水から1以上の重金属を吸着させるために用いられる、請求項10記載の吸着剤。
- 1以上の重金属が、少なくとも1つの銅鉛(Pb(II))およびマンガン(Mn(II))、(Cu(II))、ニッケル(Ni(II))、カドミウム(Cd(II))および水銀(Hg(II))金属を含む、請求項11記載の吸着剤。
- ナノ複合体が、少なくとも1つのアルミナ、ゼオライト、活性炭、セルロース繊維、ココナッツ繊維、クレー、バナナシルク、ナイロンおよびヤシ殻を含む材料上に担持されている、請求項12記載の吸着剤。
- 吸着剤を1以上の重金属で汚染された水と混合することによって吸着剤がバッチセットアップで使用される、請求項10記載の吸着剤。
- 吸着剤床に1以上の重金属で汚染された水を通過させることによって、吸着剤がカラムセットアップで使用される、請求項10記載の吸着剤。
- ナノ複合体を含む吸着剤であって、前記ナノ複合体が、還元されたグラフェン酸化物(RGO)ならびに少なくとも1つの金属および金属の酸化物のナノ粒子を含み、前記金属が、少なくとも1つの金、銀、白金、パラジウム、コバルト、マンガン、鉄、テルル、ロジウム、ルテニウム、銅、イリジウム、モリブデン、クロムおよびセリウムを含み、前記ナノ複合体が基体に結合している、吸着剤。
- 基体が、少なくとも1つのシリカ、アルミナ、ゼオライト、活性炭、セルロース繊維、ココナッツ繊維、クレー、バナナシルク、ナイロン、およびヤシ殻を含む、請求項16記載の吸着剤。
- ナノ複合体が、少なくとも1つのキトサン、ポリアニリン、ポリビニルアルコール、およびポリビニルピロリドン(PVP)を用いることによって基体に結合される、請求項16記載の吸着剤。
- 吸着剤が、1以上の重金属を水から吸着するために用いられる、請求項16記載の吸着剤。
- 1以上の重金属が、少なくとも1つの銅鉛(Pb(II))およびマンガン(Mn(II))、(Cu(II))、ニッケル(Ni(II))、カドミウム(Cd(II))および水銀(Hg(II))金属を含む、請求項16記載の吸着剤。
- ナノ複合体が、少なくとも1つのアルミナ、ゼオライト、活性炭、セルロース繊維、ココナッツ繊維、クレー、バナナシルク、ナイロン、およびヤシ殻を含む材料上に担持されている、請求項16記載の吸着剤。
- 吸着剤と1以上の重金属で汚染された水とを混合することによって、吸着剤がバッチセットアップで使用される、請求項16記載の吸着剤。
- 吸着剤床に1以上の重金属で汚染された水を通過させることによって、吸着剤がカラムセットアップで使用される、請求項16記載の吸着剤。
- ナノ複合体を含む吸着剤を含むろ過装置であって、前記ナノ複合体が、還元されたグラフェン酸化物(RGO)ならびに少なくとも1つの金属および金属の酸化物のナノ粒子を含み、前記金属が、金、銀、白金、パラジウム、コバルト、マンガン、鉄、テルル、ロジウム、ルテニウム、銅、イリジウム、モリブデン、クロムおよびセリウムの少なくとも1つを含み、前記ナノ複合体が基体に結合している、ろ過装置。
- 基体が、少なくとも1つのシリカ、アルミナ、ゼオライト、活性炭、セルロース繊維、ココナッツ繊維、クレー、バナナシルク、ナイロンおよびヤシ殻を含む、請求項24記載のろ過装置。
- 少なくとも1つのキトサン、ポリアニリン、ポリビニルアルコール、およびポリビニルピロリドン(PVP)を用いることによってナノ複合体を基体に結合させる、請求項25記載のろ過装置。
- ろ過装置が、キャンドル、放射状多孔性ブロック、垂直多孔性ブロック、濾床、パケットおよびバッグのうちの1つである、請求項24記載のろ過装置。
- ナノ複合体を作製する方法であって、金属前駆体を還元されたグラフェン酸化物(RGO)によって還元することを含む、方法。
- 金属前駆体がRGOによって約40℃までの温度で還元される、請求項28記載の方法。
- 金属前駆体がRGOによってその場で還元される、請求項28記載の方法。
- RGOが、グラフェン酸化物(GO)の化学的、生物学的、物理的、光化学的、または熱水還元によって得られる、請求項28記載の方法。
- 金属前駆体およびGOを同時に還元することをさらに含む、請求項31記載の方法。
- あらかじめ形成された金属またはあらかじめ形成された金属酸化物ナノ粒子およびRGOを混合することをさらに含む、請求項28記載の方法。
- 金属前駆体が、金、銀、白金、パラジウム、コバルト、マンガン、鉄、テルル、ロジウム、ルテニウム、銅、イリジウム、モリブデン、クロムおよびセリウムの1以上の化合物を含む、請求項28記載の方法。
- 金属前駆体中のカウンターイオンが、塩化物、硝酸塩、酢酸塩、硫酸塩、および重炭酸塩の1以上を含む、請求項34記載の方法。
- GOがグラファイト源を酸化することによって得られる、請求項31記載の方法。
- グラファイト源が少なくとも1つの化石燃料および糖を含む、請求項36記載の方法。
- 金属前駆体およびRGOの濃度を変えることによって、ナノ複合体のサイズを変えることをさらに含む、請求項28記載の方法。
- 吸着剤を作製する方法であって、請求項28記載のナノ複合体をシリカに結合させることを含む、方法。
- 請求項28記載の方法によって形成されるナノ複合体。
- 約50nm〜5μmの幅を有する、請求項1〜28記載のナノ複合体。
- ナノ複合体が、球状、四面体形状、三角形状、角柱形状、ロッド形状、六角形状、立方体形状、リボン形状、管形状、らせん形状、樹枝形状、花形状、星形状、シート形状またはそれらの組み合わせのものである、請求項1または28記載のナノ複合体。
- ナノ複合体がスーパーコンデンサで用いられる、請求項1または28記載のナノ複合体。
- ナノ複合体が、スズキカップリングを含む有機反応において用いられる、請求項1または28記載のナノ複合体。
- ナノ複合体が、スズキカップリング、水素化および脱水素化反応、ならびに石油のクラッキングの少なくとも1つを含む有機反応において使用される、請求項1または28記載のナノ複合体。
- ナノ複合体が、燃料電池および水素貯蔵における酸素還元反応の触媒として用いられる、請求項1または28記載のナノ複合体。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| IN2563CH2010 | 2010-09-03 | ||
| IN2563/CHE/2010 | 2010-09-03 | ||
| PCT/IB2011/002740 WO2012028964A2 (en) | 2010-09-03 | 2011-09-02 | Reduced graphene oxide-based-composites for the purification of water |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2016114309A Division JP2016193431A (ja) | 2010-09-03 | 2016-06-08 | 浄水のための還元されたグラフェン酸化物ベースの複合体 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2013542053A true JP2013542053A (ja) | 2013-11-21 |
| JP2013542053A5 JP2013542053A5 (ja) | 2014-10-16 |
Family
ID=45773317
Family Applications (3)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2013526567A Pending JP2013542053A (ja) | 2010-09-03 | 2011-09-02 | 浄水のための還元されたグラフェン酸化物ベースの複合体 |
| JP2016114309A Pending JP2016193431A (ja) | 2010-09-03 | 2016-06-08 | 浄水のための還元されたグラフェン酸化物ベースの複合体 |
| JP2018092904A Pending JP2018167262A (ja) | 2010-09-03 | 2018-05-14 | 浄水のための還元されたグラフェン酸化物ベースの複合体 |
Family Applications After (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2016114309A Pending JP2016193431A (ja) | 2010-09-03 | 2016-06-08 | 浄水のための還元されたグラフェン酸化物ベースの複合体 |
| JP2018092904A Pending JP2018167262A (ja) | 2010-09-03 | 2018-05-14 | 浄水のための還元されたグラフェン酸化物ベースの複合体 |
Country Status (5)
| Country | Link |
|---|---|
| US (2) | US20130240439A1 (ja) |
| JP (3) | JP2013542053A (ja) |
| CN (1) | CN103298550A (ja) |
| SG (2) | SG10201507003VA (ja) |
| WO (1) | WO2012028964A2 (ja) |
Cited By (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN103639421A (zh) * | 2013-12-04 | 2014-03-19 | 北京印刷学院 | 一种高电导率的石墨烯/银纳米复合材料的制备方法 |
| KR20160112632A (ko) * | 2015-03-20 | 2016-09-28 | 부산대학교 산학협력단 | 니켈 폼 및 그래핀 에어로겔을 이용한 직접탄소 연료전지용 바인더-프리 촉매전극의 제조방법 및 이를 이용하여 제조된 촉매전극 |
| CN107570212A (zh) * | 2017-10-10 | 2018-01-12 | 东南大学 | 一种以复合材料为载体的金属氧化物催化剂及其制备方法与应用 |
| KR101818481B1 (ko) | 2015-10-23 | 2018-02-21 | 이화여자대학교 산학협력단 | 녹조 제거용 부유성 필름, 및 폐수 정화용 부유성 필름 |
| WO2018066630A1 (ja) * | 2016-10-05 | 2018-04-12 | 学校法人関西学院 | イリジウム化合物-グラフェンオキサイド複合体 |
| US10035131B2 (en) | 2011-11-24 | 2018-07-31 | Indian Institute Of Technology | Multilayer organic-templated-boehmite-nanoarchitecture for water purification |
| JP2018534140A (ja) * | 2015-08-09 | 2018-11-22 | 済南聖泉集団股▲ふん▼有限公司Jinan Shengquan Group Share Holding Co., Ltd. | グラフェン吸着材、その製造方法とその適用、及びタバコフィルターとタバコ |
| WO2019054214A1 (ja) * | 2017-09-13 | 2019-03-21 | 株式会社大阪ソーダ | 重金属処理剤および重金属処理剤の製造方法 |
| CN112755962A (zh) * | 2021-01-25 | 2021-05-07 | 中国地质大学(北京) | 一种去除地下水中铅铜镉的吸附材料及其制备方法和应用 |
| WO2022195734A1 (ja) * | 2021-03-16 | 2022-09-22 | パナソニックホールディングス株式会社 | ガス捕捉材及び真空断熱部材製造用キット |
| JP7460128B2 (ja) | 2020-03-31 | 2024-04-02 | ナノサミット株式会社 | 酸化マンガン-ナノカーボン複合粒子及びその分散液並びにそれらの製造方法 |
Families Citing this family (73)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR101358883B1 (ko) | 2012-03-19 | 2014-02-07 | 인하대학교 산학협력단 | 금속이 담지된 그래핀 옥사이드와 금속-유기구조체의 복합화로 제조된 고효율 수소저장용 탄소나노복합체 제조방법 |
| WO2013156870A2 (en) * | 2012-04-17 | 2013-10-24 | Indian Institute Of Technology | Detection of quantity of water flow using quantum clusters |
| US9424505B2 (en) | 2012-05-25 | 2016-08-23 | Indian Institute Of Technology Madras | Luminescent graphene patterns |
| US9403112B2 (en) | 2012-06-12 | 2016-08-02 | The United States Of America As Represented By The Secretary Of The Air Force | Graphene oxide filters and methods of use |
| CN102718965B (zh) * | 2012-06-27 | 2014-04-09 | 沈阳理工大学 | 电化学合成氧化钴/聚苯胺复合材料的电解液 |
| CN102716722A (zh) * | 2012-07-11 | 2012-10-10 | 济南大学 | 基于石墨烯的纳米磁性生物吸附材料的制备方法 |
| JP6047742B2 (ja) * | 2012-10-31 | 2016-12-21 | 国立大学法人 熊本大学 | 鉄フタロシアニン/グラフェンナノ複合体、鉄フタロシアニン/グラフェンナノ複合体担持電極及びこれらの製造方法 |
| US9975776B2 (en) * | 2012-11-23 | 2018-05-22 | Nanyang Technological University | Composite film and method of forming the same |
| US20140183415A1 (en) * | 2012-12-31 | 2014-07-03 | Cheil Industries Inc. | Graphene-Based Composite and Method of Preparing the Same |
| CN103240063B (zh) * | 2013-05-22 | 2014-11-12 | 陕西科技大学 | 污水处理用氧化石墨烯/两性壳聚糖插层复合材料的制备方法 |
| CN103497476B (zh) * | 2013-10-16 | 2015-07-29 | 苏州大学 | 一种基于两性纤维素的复合材料及其应用 |
| JP6417183B2 (ja) * | 2013-10-16 | 2018-10-31 | 地方独立行政法人東京都立産業技術研究センター | 金属イオン捕集材 |
| IL230024A0 (en) * | 2013-12-19 | 2014-03-31 | Mekorot Israel Nat Water Company Ltd | Process, device and system for water treatment |
| CN104162410B (zh) * | 2014-05-15 | 2016-02-03 | 浙江海洋学院 | 一种天然材料吸附剂的制备方法及采用天然材料吸附剂的污水处理方法 |
| MX2016016145A (es) * | 2014-06-06 | 2017-10-12 | Univ Houston System | Polimeros de nanocompuestos porosos para tratamiento de agua. |
| CN104016438A (zh) * | 2014-06-20 | 2014-09-03 | 上海交通大学 | 一种用石墨烯吸附重金属离子的方法 |
| CN104162406A (zh) * | 2014-07-14 | 2014-11-26 | 宁夏宝塔石化科技实业发展有限公司 | 一种用于吸附天然气的微孔材料的组成与构型 |
| TWI531407B (zh) * | 2014-11-20 | 2016-05-01 | 中原大學 | 石墨烯過濾膜及其製作方法 |
| CN104607146A (zh) * | 2015-02-09 | 2015-05-13 | 中国人民解放军第三军医大学第二附属医院 | 氧化态石墨烯-纳米铂钯微型树枝状复合材料的制备方法及产品 |
| CN104772118B (zh) * | 2015-04-24 | 2018-09-18 | 河北工业大学 | 一种亲水性石墨烯基碳材料及其应用 |
| KR101702438B1 (ko) | 2015-07-13 | 2017-02-06 | 울산대학교 산학협력단 | 산화텅스텐 나노입자가 코팅된 탄소나노튜브 산화그래핀 하이브리드 기반 플렉시블 이산화질소 가스센서 및 그 제조방법 |
| CN105177379A (zh) * | 2015-08-19 | 2015-12-23 | 合肥市田源精铸有限公司 | 一种氧化石墨烯复合材料 |
| KR20170024409A (ko) | 2015-08-25 | 2017-03-07 | 울산대학교 산학협력단 | 자기조립 단분자막 백금/팔라듐 코아-셀 나노입자 기반 수소센서 및 그의 제조방법 |
| CN105597821B (zh) * | 2015-10-19 | 2018-05-15 | 华南理工大学 | 一种半纤维素-壳聚糖-钯催化剂及其制备方法与应用 |
| CN105289515B (zh) * | 2015-11-27 | 2018-04-13 | 安徽师范大学 | 一种磁性氧化石墨烯吸附剂材料的制备方法及应用 |
| CN105344329A (zh) * | 2015-11-30 | 2016-02-24 | 武汉科技大学 | 一种氧化石墨烯/壳聚糖微球及其制备方法 |
| CN105977041A (zh) * | 2016-04-07 | 2016-09-28 | 铜陵泰力电子有限公司 | 一种铈锰掺杂可延长循环寿命的超级电容器电极材料及其制备方法 |
| US20190120701A1 (en) * | 2016-04-09 | 2019-04-25 | Indian Institute Of Science | Reduced graphene oxide-silver nanocomposite films for temperature sensor application |
| WO2017175191A1 (en) * | 2016-04-09 | 2017-10-12 | Indian Institute Of Science | Reduced graphene oxide-silver nanocomposite films for temperature sensor application |
| US10052302B2 (en) | 2016-05-10 | 2018-08-21 | King Saud University | Green synthesis of reduced graphene oxide silica nanocomposite using nigella sativa seeds extract |
| US10150094B2 (en) | 2016-06-09 | 2018-12-11 | King Fahd University Of Petroleum And Minerals | Metal adsorbent and a method of making thereof |
| CN106105605A (zh) * | 2016-06-21 | 2016-11-16 | 天津师范大学 | 采用碳纳米材料提高草坪堆肥基质小型节肢动物数量的方法 |
| CN106258573A (zh) * | 2016-06-21 | 2017-01-04 | 天津师范大学 | 碳纳米材料提高草坪堆肥基质芽孢杆菌数量的方法 |
| CN106069245A (zh) * | 2016-06-21 | 2016-11-09 | 天津师范大学 | 采用碳纳米材料增进堆肥基质高羊茅根系生长的方法 |
| CN106105854A (zh) * | 2016-06-21 | 2016-11-16 | 天津师范大学 | 一种采用碳纳米管钝化草坪堆肥基质重金属的方法 |
| CN106111682A (zh) * | 2016-06-21 | 2016-11-16 | 天津师范大学 | 采用碳纳米材料对单一体系中Pb等温吸附的调控方法 |
| CN106105810A (zh) * | 2016-06-21 | 2016-11-16 | 天津师范大学 | 采用碳纳米材料调控草坪堆肥基质Pd形态与分布的方法 |
| CN106105853A (zh) * | 2016-06-21 | 2016-11-16 | 天津师范大学 | 采用碳纳米材料提高堆肥基质高羊茅初期地上生物量的方法 |
| CN106069036A (zh) * | 2016-06-21 | 2016-11-09 | 天津师范大学 | 采用羟基化多壁碳纳米管调控堆肥基质高羊茅绿度的方法 |
| EP3281695A1 (en) * | 2016-08-11 | 2018-02-14 | Freie Universität Berlin | Filtration device |
| US10682638B2 (en) * | 2016-10-21 | 2020-06-16 | Texas State University—San Marcos | Catalyst nanoarchitectures with high activity and stability |
| KR101913471B1 (ko) * | 2016-10-24 | 2018-10-30 | 영남대학교 산학협력단 | 공유결합으로 이루어진 환원된 산화그래핀/폴리아닐린 복합체 제조방법 |
| CN110114126A (zh) * | 2016-10-26 | 2019-08-09 | 标准石墨烯有限公司 | 包含还原氧化石墨烯层的水净化过滤器和包含其的水净化系统 |
| KR20180045793A (ko) * | 2016-10-26 | 2018-05-04 | 주식회사 스탠다드그래핀 | 환원된 산화 그래핀 층을 포함하는 수질 정화용 필터, 및 이를 포함하는 수질 정화용 시스템 |
| CN106735298B (zh) * | 2016-12-13 | 2018-09-18 | 浙江大学 | 一种方形钯纳米片及其制备方法 |
| CN106770772B (zh) * | 2016-12-28 | 2019-06-07 | 上海微谱化工技术服务有限公司 | 皮肤类用品中对羟基苯甲酸酯的分离及定性、定量方法 |
| CN107185489A (zh) * | 2016-12-30 | 2017-09-22 | 常州碳星科技有限公司 | 大气中有机污染物的吸附材料的制备方法 |
| CN106693920A (zh) * | 2017-02-14 | 2017-05-24 | 上海工程技术大学 | 一种磁性纳米复合材料及其制备方法和应用 |
| US10787374B2 (en) | 2017-05-04 | 2020-09-29 | Arizona Board Of Regents On Behalf Of Arizona State University | Silver-impregnated two-dimensional structures for bromide removal |
| CN107243326B (zh) * | 2017-05-16 | 2019-10-18 | 北京化工大学 | 一种氧化石墨烯/壳聚糖复合气凝胶微球的制备方法 |
| US10815580B2 (en) * | 2017-08-10 | 2020-10-27 | Board Of Trustees Of The University Of Arkansas | 3D reduced graphene oxide foams embedded with nanocatalysts, synthesizing methods and applications of same |
| US11577977B2 (en) * | 2017-09-26 | 2023-02-14 | The Board Of Trustees Of The University Of Arkansas | Composite zero valent iron nanoparticles and applications thereof |
| CN107785591B (zh) * | 2017-09-28 | 2021-03-19 | 东华大学 | 具有高电催化甲醇氧化活性的钯-铜合金/还原氧化石墨烯复合材料及其制备方法和应用 |
| CN108083377A (zh) * | 2017-12-25 | 2018-05-29 | 中国科学院合肥物质科学研究院 | 一种降低重金属砷毒性的方法 |
| US20210269311A1 (en) * | 2018-07-13 | 2021-09-02 | University Of Delaware | Methods for producing silver-amended carbon materials |
| CN109433193B (zh) * | 2018-10-15 | 2021-07-23 | 昆明理工大学 | 一种纳米Pd/M-rGO复合催化剂及其制备方法 |
| JP6950894B2 (ja) * | 2018-11-06 | 2021-10-13 | 潤 夏木 | 銀/酸化グラフェン複合体およびその製造方法 |
| CN111282594B (zh) * | 2018-12-06 | 2023-04-07 | 中国石油天然气股份有限公司 | 一种稠油水热裂解催化剂及其制备与应用 |
| CN109456758A (zh) * | 2018-12-24 | 2019-03-12 | 江苏经贸职业技术学院 | 一种RGO@Au复合纳米材料的合成方法 |
| US20220212958A1 (en) * | 2019-01-25 | 2022-07-07 | Graphene Leaders Canada (Glc) Inc. | Graphene oxide nanocomposites as granular active media |
| CN110092518B (zh) * | 2019-04-18 | 2020-08-04 | 清华大学 | 吸附法处理含有机物的废水并制备碳纳米材料的系统与方法 |
| CN110354816B (zh) * | 2019-05-31 | 2022-05-27 | 中国农业科学院茶叶研究所 | 一种壳聚糖/氧化石墨烯/硅藻土复合材料及其制备方法、应用 |
| CN110523375A (zh) * | 2019-08-15 | 2019-12-03 | 江苏大学 | 一种镧改性的还原氧化石墨烯/二氧化硅大介孔膜的制备方法及应用 |
| CN110514771B (zh) * | 2019-08-26 | 2021-07-27 | 首都师范大学 | 氧化石墨烯-二硫化钼毛细管电色谱柱及制备方法 |
| PL430984A1 (pl) * | 2019-08-29 | 2021-03-08 | Uniwersytet Warszawski | Sposób biologicznego wytwarzania materiału kompozytowego zredukowany tlenek grafenu / nanocząstki złota przy pomocy lizatu bakteryjnego oraz zastosowanie lizatu bakterii do biologicznego wytwarzania materiału kompozytowego zredukowany tlenek grafenu / nanocząstki złota |
| US11008425B1 (en) * | 2019-11-13 | 2021-05-18 | King Abdulaziz University | Method of producing metal nanoparticle-loaded biopolymer microgels |
| CN110813254B (zh) * | 2019-11-26 | 2022-05-10 | 合肥学院 | 一种用于从混合金属溶液中选择性分离铜的杂化膜的制备方法 |
| CN114976062B (zh) * | 2020-10-15 | 2024-01-26 | 昆明理工大学 | 氮掺杂rGO负载MnO纳米颗粒催化剂的制备方法 |
| CN112280073B (zh) * | 2020-10-30 | 2022-05-06 | 哈尔滨工业大学 | 一种多功能薄膜的制备方法 |
| CN112973633B (zh) * | 2021-03-01 | 2022-10-14 | 中国科学院城市环境研究所 | 一种活性炭基材料及其制备方法和用途 |
| US11332389B1 (en) | 2021-03-15 | 2022-05-17 | King Abdulaziz University | Recylable multifunctional composites for metal ion removal from water |
| KR102634276B1 (ko) | 2021-06-07 | 2024-02-06 | 한국생산기술연구원 | Co2 전환용 촉매 및 이의 제조방법 |
| CN114192109A (zh) * | 2021-12-06 | 2022-03-18 | 郑州师范学院 | 一种用于水中除砷的石墨烯铜铁氧化物复合吸附剂及其制备方法 |
Citations (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH10180093A (ja) * | 1996-10-21 | 1998-07-07 | Kuraray Chem Corp | 活性炭及びその複合吸着材の再生方法 |
| JPH11189481A (ja) * | 1997-12-26 | 1999-07-13 | Rengo Co Ltd | 多孔質機能材 |
| US20040050795A1 (en) * | 2002-09-18 | 2004-03-18 | Park Jae Kwang | Removal of arsenic and other anions using novel adsorbents |
| WO2009117628A1 (en) * | 2008-03-20 | 2009-09-24 | The Government Of The United States Of America, As Represented By The Secretary Of The Navy | Reduced graphene oxide film |
| JP2010275186A (ja) * | 2009-05-26 | 2010-12-09 | Belenos Clean Power Holding Ag | 溶液中の単層および多層グラフェンの安定な分散系 |
| JP2011168449A (ja) * | 2010-02-19 | 2011-09-01 | Fuji Electric Co Ltd | グラフェン膜の製造方法 |
| WO2011131722A1 (de) * | 2010-04-22 | 2011-10-27 | Basf Se | Verfahren zur herstellung von zweidimensionalen sandwich-nanomaterialien auf basis von graphen |
| WO2011141486A1 (de) * | 2010-05-14 | 2011-11-17 | Basf Se | Verahren zur einkapselung von metallen und metalloxiden mit graphen und die verwendung dieser materialien |
Family Cites Families (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20050025970A1 (en) * | 2002-12-06 | 2005-02-03 | Bozidar Stipanovic | Carbon beads |
| WO2007146352A2 (en) * | 2006-06-14 | 2007-12-21 | Inframat Corporation | Methods of making water treatment compositions |
| US8696938B2 (en) * | 2008-08-25 | 2014-04-15 | Nanotek Instruments, Inc. | Supercritical fluid process for producing nano graphene platelets |
| JP5470509B2 (ja) * | 2008-11-27 | 2014-04-16 | 独立行政法人産業技術総合研究所 | 電極用白金クラスター及びその製造方法 |
| CN101811696B (zh) * | 2010-04-28 | 2013-01-02 | 东南大学 | 一种石墨烯负载四氧化三钴纳米复合材料及其制备方法 |
-
2011
- 2011-09-02 US US13/820,403 patent/US20130240439A1/en not_active Abandoned
- 2011-09-02 CN CN2011800529433A patent/CN103298550A/zh active Pending
- 2011-09-02 SG SG10201507003VA patent/SG10201507003VA/en unknown
- 2011-09-02 JP JP2013526567A patent/JP2013542053A/ja active Pending
- 2011-09-02 SG SG2013015417A patent/SG188350A1/en unknown
- 2011-09-02 WO PCT/IB2011/002740 patent/WO2012028964A2/en active Application Filing
-
2016
- 2016-06-08 JP JP2016114309A patent/JP2016193431A/ja active Pending
-
2017
- 2017-08-25 US US15/686,294 patent/US20180221850A1/en not_active Abandoned
-
2018
- 2018-05-14 JP JP2018092904A patent/JP2018167262A/ja active Pending
Patent Citations (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH10180093A (ja) * | 1996-10-21 | 1998-07-07 | Kuraray Chem Corp | 活性炭及びその複合吸着材の再生方法 |
| JPH11189481A (ja) * | 1997-12-26 | 1999-07-13 | Rengo Co Ltd | 多孔質機能材 |
| US20040050795A1 (en) * | 2002-09-18 | 2004-03-18 | Park Jae Kwang | Removal of arsenic and other anions using novel adsorbents |
| WO2009117628A1 (en) * | 2008-03-20 | 2009-09-24 | The Government Of The United States Of America, As Represented By The Secretary Of The Navy | Reduced graphene oxide film |
| JP2010275186A (ja) * | 2009-05-26 | 2010-12-09 | Belenos Clean Power Holding Ag | 溶液中の単層および多層グラフェンの安定な分散系 |
| JP2011168449A (ja) * | 2010-02-19 | 2011-09-01 | Fuji Electric Co Ltd | グラフェン膜の製造方法 |
| WO2011131722A1 (de) * | 2010-04-22 | 2011-10-27 | Basf Se | Verfahren zur herstellung von zweidimensionalen sandwich-nanomaterialien auf basis von graphen |
| WO2011141486A1 (de) * | 2010-05-14 | 2011-11-17 | Basf Se | Verahren zur einkapselung von metallen und metalloxiden mit graphen und die verwendung dieser materialien |
Non-Patent Citations (1)
| Title |
|---|
| VIMLESH CHANDRA: "WATER-DISPERSIBLE MAGNETITE-REDUCED GRAPHENE OXIDE COMPOSITES FOR ARSENIC REMOVAL", ACS NANO, vol. V4 N7, JPN5013009952, June 2010 (2010-06-01), pages 3979 - 3986, ISSN: 0003055146 * |
Cited By (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US10035131B2 (en) | 2011-11-24 | 2018-07-31 | Indian Institute Of Technology | Multilayer organic-templated-boehmite-nanoarchitecture for water purification |
| CN103639421A (zh) * | 2013-12-04 | 2014-03-19 | 北京印刷学院 | 一种高电导率的石墨烯/银纳米复合材料的制备方法 |
| KR20160112632A (ko) * | 2015-03-20 | 2016-09-28 | 부산대학교 산학협력단 | 니켈 폼 및 그래핀 에어로겔을 이용한 직접탄소 연료전지용 바인더-프리 촉매전극의 제조방법 및 이를 이용하여 제조된 촉매전극 |
| KR101691198B1 (ko) * | 2015-03-20 | 2016-12-30 | 부산대학교 산학협력단 | 니켈 폼 및 그래핀 에어로겔을 이용한 직접탄소 연료전지용 바인더-프리 촉매전극의 제조방법 및 이를 이용하여 제조된 촉매전극 |
| JP2018534140A (ja) * | 2015-08-09 | 2018-11-22 | 済南聖泉集団股▲ふん▼有限公司Jinan Shengquan Group Share Holding Co., Ltd. | グラフェン吸着材、その製造方法とその適用、及びタバコフィルターとタバコ |
| KR101818481B1 (ko) | 2015-10-23 | 2018-02-21 | 이화여자대학교 산학협력단 | 녹조 제거용 부유성 필름, 및 폐수 정화용 부유성 필름 |
| WO2018066630A1 (ja) * | 2016-10-05 | 2018-04-12 | 学校法人関西学院 | イリジウム化合物-グラフェンオキサイド複合体 |
| JPWO2019054214A1 (ja) * | 2017-09-13 | 2020-10-29 | 株式会社大阪ソーダ | 重金属処理剤および重金属処理剤の製造方法 |
| WO2019054214A1 (ja) * | 2017-09-13 | 2019-03-21 | 株式会社大阪ソーダ | 重金属処理剤および重金属処理剤の製造方法 |
| CN107570212A (zh) * | 2017-10-10 | 2018-01-12 | 东南大学 | 一种以复合材料为载体的金属氧化物催化剂及其制备方法与应用 |
| CN107570212B (zh) * | 2017-10-10 | 2020-01-07 | 东南大学 | 一种以复合材料为载体的金属氧化物催化剂及其制备方法与应用 |
| JP7460128B2 (ja) | 2020-03-31 | 2024-04-02 | ナノサミット株式会社 | 酸化マンガン-ナノカーボン複合粒子及びその分散液並びにそれらの製造方法 |
| CN112755962A (zh) * | 2021-01-25 | 2021-05-07 | 中国地质大学(北京) | 一种去除地下水中铅铜镉的吸附材料及其制备方法和应用 |
| WO2022195734A1 (ja) * | 2021-03-16 | 2022-09-22 | パナソニックホールディングス株式会社 | ガス捕捉材及び真空断熱部材製造用キット |
Also Published As
| Publication number | Publication date |
|---|---|
| CN103298550A (zh) | 2013-09-11 |
| US20130240439A1 (en) | 2013-09-19 |
| WO2012028964A2 (en) | 2012-03-08 |
| JP2016193431A (ja) | 2016-11-17 |
| JP2018167262A (ja) | 2018-11-01 |
| WO2012028964A3 (en) | 2013-07-04 |
| SG10201507003VA (en) | 2015-10-29 |
| US20180221850A1 (en) | 2018-08-09 |
| SG188350A1 (en) | 2013-04-30 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2018167262A (ja) | 浄水のための還元されたグラフェン酸化物ベースの複合体 | |
| Ahmad et al. | Adsorption of methyl orange by synthesized and functionalized-CNTs with 3-aminopropyltriethoxysilane loaded TiO2 nanocomposites | |
| Farghali et al. | Functionalization of acidified multi-walled carbon nanotubes for removal of heavy metals in aqueous solutions | |
| Jayaramulu et al. | Graphene-based metal–organic framework hybrids for applications in catalysis, environmental, and energy technologies | |
| Fan et al. | Hybridization of graphene sheets and carbon-coated Fe 3 O 4 nanoparticles as a synergistic adsorbent of organic dyes | |
| Tang et al. | One-step synthesis of magnetic attapulgite/carbon supported NiFe-LDHs by hydrothermal process of spent bleaching earth for pollutants removal | |
| Liu et al. | Carbon spheres/activated carbon composite materials with high Cr (VI) adsorption capacity prepared by a hydrothermal method | |
| Li et al. | Adsorbent for chromium removal based on graphene oxide functionalized with magnetic cyclodextrin–chitosan | |
| Sreeprasad et al. | Reduced graphene oxide–metal/metal oxide composites: facile synthesis and application in water purification | |
| Koo et al. | Graphene‐Based Multifunctional Iron Oxide Nanosheets with Tunable Properties | |
| Gupta et al. | Chromium removal by combining the magnetic properties of iron oxide with adsorption properties of carbon nanotubes | |
| Siriwardane et al. | Synthesis and characterization of nano magnesium oxide impregnated granular activated carbon composite for H2S removal applications | |
| Li et al. | N-doped porous carbon with magnetic particles formed in situ for enhanced Cr (VI) removal | |
| Ai et al. | Removal of methylene blue from aqueous solution by a solvothermal-synthesized graphene/magnetite composite | |
| US9950311B2 (en) | Process for the synthesis of magnetically recoverable, high surface area carbon-Fe3O4 nano-composite using metal organic framework (MOF) | |
| Liang et al. | Adsorptive removal of gentian violet from aqueous solution using CoFe2O4/activated carbon magnetic composite | |
| Shehzad et al. | Synthesis of ultra-large ZrO2 nanosheets as novel adsorbents for fast and efficient removal of As (III) from aqueous solutions | |
| Li et al. | Adsorption mechanism of methylene blue on oxygen-containing functional groups modified graphitic carbon spheres: Experiment and DFT study | |
| Nayl et al. | Development of sponge/graphene oxide composite as eco-friendly filter to remove methylene blue from aqueous media | |
| Rathour et al. | Selective and multicycle removal of Cr (VI) by graphene oxide–EDTA composite: insight into the removal mechanism and ionic interference in binary and ternary associations | |
| Zhang et al. | Magnetic carbon-coated palygorskite loaded with cobalt nanoparticles for Congo Red removal from waters | |
| Liu et al. | Magnetic ZrO2/PEI/Fe3O4 functionalized MWCNTs composite with enhanced phosphate removal performance and easy separability | |
| Tao et al. | Ultrasound-assisted bottom-up synthesis of Ni-graphene hybrid composites and their excellent rhodamine B removal properties | |
| Li et al. | Facile and cost-effective synthesis of CNT@ MCo 2 O 4 (M= Ni, Mn, Cu, Zn) core–shell hybrid nanostructures for organic dye removal | |
| Wu et al. | Magnetically recoverable Ni@ C composites: The synthesis by carbonization and adsorption for Fe3+ |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20140901 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20140901 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20150420 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20150422 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20150717 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20150819 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20150918 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20151019 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20160208 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20160608 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20160802 |
|
| A912 | Re-examination (zenchi) completed and case transferred to appeal board |
Free format text: JAPANESE INTERMEDIATE CODE: A912 Effective date: 20160826 |