JP2007502124A - 改良ケトレダクターゼポリペプチドおよび関連ポリヌクレオチド - Google Patents
改良ケトレダクターゼポリペプチドおよび関連ポリヌクレオチド Download PDFInfo
- Publication number
- JP2007502124A JP2007502124A JP2006523448A JP2006523448A JP2007502124A JP 2007502124 A JP2007502124 A JP 2007502124A JP 2006523448 A JP2006523448 A JP 2006523448A JP 2006523448 A JP2006523448 A JP 2006523448A JP 2007502124 A JP2007502124 A JP 2007502124A
- Authority
- JP
- Japan
- Prior art keywords
- seq
- kred
- polypeptide
- sequence
- kred polypeptide
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N9/00—Enzymes; Proenzymes; Compositions thereof; Processes for preparing, activating, inhibiting, separating or purifying enzymes
- C12N9/0004—Oxidoreductases (1.)
- C12N9/0006—Oxidoreductases (1.) acting on CH-OH groups as donors (1.1)
Landscapes
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- Genetics & Genomics (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- Molecular Biology (AREA)
- Microbiology (AREA)
- Biotechnology (AREA)
- Biomedical Technology (AREA)
- Biochemistry (AREA)
- General Engineering & Computer Science (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Enzymes And Modification Thereof (AREA)
Abstract
Description
本発明は、酵素学の分野、特にケトレダクターゼの酵素学の分野に関する。より正確にはいえば、本発明は、増強された酵素活性を有するケトレダクターゼポリペプチド、および、改良ケトレダクターゼポリペプチドをコードするポリヌクレオチド配列に関する。
キラルγ−置換β−ヒドロキシ酪酸エステルは、薬の合成において商業的に重要な中間体である。これらの中間体は、HMG−CoAレダクターゼインヒビターの合成において光学活性中間体(例えば、アトルバスタチン、フルバスタチン、およびロスバスタチン)として利用され得る。いくつかのγ−置換β−ヒドロキシ酪酸エステルを生成する方法が記載されている。例えば、シアン化ナトリウムとの反応前に保護基によるヒドロキシ基の保護を必要とする4−ブロモ−3−ヒドロキシブチレートから、4−シアノ−3−ヒドロキシ酪酸を生成する方法が報告されている(非特許文献1)。Isbellら(非特許文献2)は、トレオニンの一水和物カルシウム塩と臭化水素とを反応させて、トレオニンのジブロモ形態を生成し、次いでブロモヒドリンに変換することによって、(R)−4−シアノ−3−ヒドロキシ酪酸エステルを合成する方法をさらに報告している(非特許文献2)。上記ブロモヒドリンのヒドロキシ基は、シアン化ナトリウムで反応させる前に保護される(非特許文献2)。あいにく、保護する工程および脱保護する工程を必要とする方法は、商業的に提供することが現実的ではない。
(KREDの特徴付け)
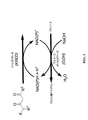
ケトレダクターゼ(KRED)またはカルボニルレダクターゼクラス(EC1.1.1.184)に属する酵素は、対応するプロキラルケトン基質から光学活性アルコールを合成するのに有用である。KREDは、代表的には、ケトン基質を対応するアルコール産物に変換するが、KREDはまた、逆反応(アルコール基質が対応するケトン/アルデヒド産物に酸化される反応)を触媒し得る。KREDのような酵素によるケトンの還元およびアルコールの酸化は、補因子(最も一般的には、還元型ニコチンアミドアニンジヌクレオチド(NADH)または還元型ニコチンアミドアデニンジヌクレオチドリン酸(NADPH)、およびニコチンアミドアデニンジヌクレオチド(NAD)またはニコチンアミドアデニンジヌクレオチドリン酸(NADP))を、酸化反応のために必要とする。NADHおよびNADPHは、電子ドナーとして働き、他方で、NADおよびNADPは、電子受容体として働く。ケトレダクターゼおよびアルコールデヒドレゲナーゼが(その酸化された状態および還元された状態にある)、リン酸化補因子または非リン酸化補因子のいずれかを受け取るが、両方を受け取らないことが、しばしば観察される。
生細胞における代謝は、デノボ合成および再生により還元反応のための補因子の十分な供給を保証する。したがって、生体触媒によるケトンの還元のために全細胞を使用することは、有利であり得るが、微生物は、代表的には、低い鏡像異性過剰率の少量の産物を導き得る多数のケトレダクターゼを有する。この理由から、Wongらは、半精製したケトレダクターゼ酵素を研究し、そして、より質の高い産物が得られ得ることを見出した(非特許文献6)。
本発明は、種々の局面を有する。一つの局面において、本発明は、配列番号2のKREDと比較して増強されたKRED活性を有するケトレダクターゼ(「KRED」)ポリペプチドに関し、この増強されたKRED活性は、この配列番号2のKRED活性の好ましくは少なくとも1.5倍、代表的には1.5〜50倍、より代表的には1.5〜約25倍の活性である。このような活性は、NADPHが酸化されて同時にケトンが対応するアルコールに還元されることに起因する、NADPHの吸光度の減少またはNADPHの蛍光の減少から測定される。別の局面において、本発明は、配列番号2のポリペプチドの少なくとも1.5倍、代表的には1.5〜50倍、より代表的には1.5〜約25倍のKRED活性を有するKREDポリペプチドに関し、このような活性は、NADPHの吸光度またはNADPHの蛍光の減少から測定されるか(例えば、実施例4)、あるいは、結合アッセイにおいて生成された産物から測定される(例えば、実施例5)。このKREDポリペプチドは、配列番号506、配列番号520、配列番号526、配列番号536、および配列番号538のアミノ酸配列と、少なくとも90%、好ましくは少なくとも95%、より好ましくは少なくとも97%、そして、最も好ましくは少なくとも99%相同である。別の局面において、本発明は、配列番号2のKREDと比較して増加したKRED残存活性を有するケトレダクターゼ(「KRED」)ポリペプチドに関し、50℃にて15〜24時間処理した後、この増加したKRED活性は、配列番号2のKRED活性の少なくとも1.5倍、代表的には1.5〜100倍、より代表的には1.5〜約60倍である。このような活性は、NADPHが酸化されて同時にケトンが対応するアルコールに還元されることに起因する、NADPHの吸光度の減少またはNADPHの蛍光の減少から測定される。なお別の局面において、本発明は、配列番号2のKREDと比較して増加したKRED残存活性を有するKREDポリペプチドに関し、50℃にて15〜24時間処理した後、この増加したKRED活性は、配列番号2のKRED活性の少なくとも1.5倍、代表的には1.5〜100倍、より代表的には1.5〜約60倍である。このような活性は、NADPHの吸光度の減少またはNADPHの蛍光の減少から測定されるか(例えば、実施例4)、あるいは、結合アッセイにおいて生成された産物から測定される(例えば、実施例5)。このKREDポリペプチドは、配列番号506、配列番号520、および配列番号526のアミノ酸配列と、少なくとも90%相同であり、好ましくは少なくとも95%、より好ましくは少なくとも97%、そして、最も好ましくは少なくとも99%相同である。一つの実施形態において、本発明はまた、本明細書中に記載される、単離されかつ精製された形態のKREDポリペプチド改変体に関する。別の実施形態において、上記単離されかつ精製されたKREDポリペプチド改変体は、凍結乾燥形態にある。なお別に実施形態において、本発明は、本明細書中に記載されるKREDポリペプチド改変体および適切なキャリア(代表的には緩衝溶液、より代表的には6.0と8.0との間のpHを有する緩衝溶液)を含む組成物に関する。この緩衝化KRED組成物が凍結乾燥形態であることもまた、本発明の範囲内である。
(a)配列番号224、配列番号244、配列番号246、配列番号250、配列番号252、配列番号254、配列番号256、配列番号260、配列番号304、配列番号344、配列番号354、配列番号358、配列番号360、配列番号364、配列番号368、配列番号374、配列番号382、配列番号386、配列番号388、配列番号400、配列番号408、配列番号438、配列番号440、配列番号448、配列番号470、配列番号484、配列番号486、配列番号488、配列番号490、配列番号502、配列番号506、配列番号508、配列番号512、配列番号514、配列番号516、配列番号518、配列番号520、配列番号522、配列番号524、配列番号526、配列番号528、配列番号530、配列番号532、配列番号534、配列番号536、配列番号538、配列番号540、または配列番号542のアミノ酸配列と、少なくとも90%の相同性、好ましくは少なくとも95%の相同性、より好ましくは少なくとも97%、そして、最も好ましくは少なくとも99%の相同性を有するアミノ酸配列(以下「相同ポリペプチド」)を有するか;
(b)(i)配列番号223、配列番号243、配列番号245、配列番号249、配列番号251、配列番号253、配列番号255、配列番号259、配列番号303、配列番号343、配列番号353、配列番号357、配列番号359、配列番号363、配列番号367、配列番号373、配列番号381、配列番号385、配列番号387、配列番号399、配列番号407、配列番号437、配列番号439、配列番号447、配列番号469、配列番号483、配列番号485、配列番号487、配列番号489、配列番号501、配列番号505、配列番号507、配列番号511、配列番号513、配列番号515、配列番号517、配列番号519、配列番号521、配列番号523、配列番号525、配列番号527、配列番号529、配列番号531、配列番号533、配列番号535、配列番号537、配列番号539、または配列番号541のヌクレオチド配列、(ii)少なくとも100ヌクレオチドの(i)の部分配列、または、(iii)(i)もしくは(ii)の相補鎖のうちのいずれかと、中程度のストリンジェンシー条件下においてハイブリダイズする核酸配列によってコードされるか(例えば、J.Sambrook,E.F.FritschおよびT.Maniatis,1989,Molecular Cloning,A Laboratory Manual,第二版、Cold Spring Harbor,N.Y.参照のこと);
(c)1〜6個のアミノ酸の置換、欠失、および/または挿入を含む、配列番号224、配列番号244、配列番号246、配列番号250、配列番号252、配列番号254、配列番号256、配列番号260、配列番号303、配列番号344、配列番号354、配列番号358、配列番号360、配列番号364、配列番号368、配列番号374、配列番号382、配列番号386、配列番号388、配列番号400、配列番号408、配列番号438、配列番号440、配列番号448、配列番号470、配列番号484、配列番号486、配列番号488、配列番号490、配列番号502、配列番号506、配列番号508、配列番号512、配列番号514、配列番号516、配列番号518、配列番号520、配列番号522、配列番号524、配列番号526、配列番号528、配列番号530、配列番号532、配列番号534、配列番号536、配列番号538、配列番号540、および配列番号542のポリペプチド改変体であるか;
(d)配列番号224、配列番号244、配列番号246、配列番号250、配列番号252、配列番号254、配列番号256、配列番号260、配列番号303、配列番号344、配列番号354、配列番号358、配列番号360、配列番号364、配列番号368、配列番号374、配列番号382、配列番号386、配列番号388、配列番号400、配列番号408、配列番号438、配列番号440、配列番号448、配列番号470、配列番号484、配列番号486、配列番号488、配列番号490、配列番号502、配列番号506、配列番号508、配列番号512、配列番号514、配列番号516、配列番号518、配列番号520、配列番号522、配列番号524、配列番号526、配列番号528、配列番号530、配列番号532、配列番号534、配列番号536、配列番号538、配列番号540、または配列番号542のポリペプチドからの少なくとも220アミノ酸残基のフラグメントであるか;あるいは、
(e)50℃にてpH7で60分間インキュベーションした後に、最初のKRED活性の60%より多くを保持する、(a)、(b)、(c)または(d)のポリペプチドであるか;
のいずれかである、KREDポリペプチドである。
(a)ポリペプチドの産生のために適切な条件下で、本発明のKREDポリペプチドをコードする核酸配列を含む核酸構築物を含む宿主細胞を培養する工程;および
(b)そのポリペプチドを回収する工程
を包含する、本発明のKREDポリペプチドを作製する方法に関する。
本明細書中に用いられる場合、用語「ケトレダクターゼ」および「KRED」は、ケトンの還元を触媒する能力を有するポリペプチドについて本明細書中で援用するために互換可能に用いられる。好ましくは、β−ケト酸中のケトンが、還元剤として還元型ニコチンアミドアデニンジヌクレオチド(NADH)または還元型ニコチンアミドアデニンジヌクレオチドリン酸(NADPH)を利用して、立体特異的様式で、対応するβ−ヒドロキシ酸になる。
(a)配列番号224、配列番号244、配列番号246、配列番号250、配列番号252、配列番号254、配列番号256、配列番号260、配列番号304、配列番号344、配列番号354、配列番号358、配列番号360、配列番号364、配列番号368、配列番号374、配列番号382、配列番号386、配列番号388、配列番号400、配列番号408、配列番号438、配列番号440、配列番号448、配列番号470、配列番号484、配列番号486、配列番号488、配列番号490、配列番号502、配列番号506、配列番号508、配列番号512、配列番号514、配列番号516、配列番号518、配列番号520、配列番号522、配列番号524、配列番号526、配列番号528、配列番号530、配列番号532、配列番号534、配列番号536、配列番号538、配列番号540、または配列番号542のアミノ酸配列と、少なくとも90%の相同性、好ましくは少なくとも95%の相同性、より好ましくは少なくとも97%、そして、最も好ましくは少なくとも99%の相同性を有するアミノ酸配列(以下「相同ポリペプチド」)を有するか;
(b)(i)配列番号223、配列番号243、配列番号245、配列番号249、配列番号251、配列番号253、配列番号255、配列番号259、配列番号303、配列番号343、配列番号353、配列番号357、配列番号359、配列番号363、配列番号367、配列番号373、配列番号381、配列番号385、配列番号387、配列番号399、配列番号407、配列番号437、配列番号439、配列番号447、配列番号469、配列番号483、配列番号485、配列番号487、配列番号489、配列番号501、配列番号505、配列番号507、配列番号511、配列番号513、配列番号515、配列番号517、配列番号519、配列番号521、配列番号523、配列番号525、配列番号527、配列番号529、配列番号531、配列番号533、配列番号535、配列番号537、配列番号539、または配列番号541のヌクレオチド配列、(ii)少なくとも100ヌクレオチドの(i)の部分配列、または(iii)(i)もしくは(ii)の相補鎖
のうちのいずれかと、中程度のストリンジェンシー条件下においてハイブリダイズする核酸配列によってコードされるか(例えば、J.Sambrook,E.F.FritschおよびT.Maniatis,1989,Molecular Cloning,A Laboratory Manual,第二版、Cold Spring Harbor,N.Y.参照のこと);
(c)1〜6個のアミノ酸の置換、欠失、および/または挿入を含む、配列番号224、配列番号244、配列番号246、配列番号250、配列番号252、配列番号254、配列番号256、配列番号260、配列番号303、配列番号344、配列番号354、配列番号358、配列番号360、配列番号364、配列番号368、配列番号374、配列番号382、配列番号386、配列番号388、配列番号400、配列番号408、配列番号438、配列番号440、配列番号448、配列番号470、配列番号484、配列番号486、配列番号488、配列番号490、配列番号502、配列番号506、配列番号508、配列番号512、配列番号514、配列番号516、配列番号518、配列番号520、配列番号522、配列番号524、配列番号526、配列番号528、配列番号530、配列番号532、配列番号534、配列番号536、配列番号538、配列番号540または配列番号542のポリペプチドの改変体であるか;
(d)配列番号224、配列番号244、配列番号246、配列番号250、配列番号252、配列番号254、配列番号256、配列番号260、配列番号303、配列番号344、配列番号354、配列番号358、配列番号360、配列番号364、配列番号368、配列番号374、配列番号382、配列番号386、配列番号388、配列番号400、配列番号408、配列番号438、配列番号440、配列番号448、配列番号470、配列番号484、配列番号486、配列番号488、配列番号490、配列番号502、配列番号506、配列番号508、配列番号512、配列番号514、配列番号516、配列番号518、配列番号520、配列番号522、配列番号524、配列番号526、配列番号528、配列番号530、配列番号532、配列番号534、配列番号536、配列番号538、配列番号540、または配列番号542のポリペプチドからの少なくとも220アミノ酸残基のフラグメントであるか;あるいは、
(e)50℃にてpH7で60分間インキュベーションした後に、最初のKRED活性の60%より多くを保持する、(a)、(b)、(c)または(d)のポリペプチドであるか;
のいずれかである。
のうちのいずれかと、中程度のストリンジェンシー条件下においてハイブリダイズする核酸配列によってコードされるKREDポリペプチドに関する(J.Sambrook,E.F.FritschおよびT.Maniatis,1989,Molecular Cloning,A Laboratory Manual,第二版、Cold Spring Harbor,N.Y.)。
その第2の局面において、本発明は、本発明のKREDポリペプチドをコードするポリヌクレオチド配列に関する。遺伝子コードの縮重を考慮すれば、本発明はまた、配列番号42、配列番号72、配列番号76、配列番号96、配列番号262、配列番号264、配列番号266、配列番号268、配列番号270、配列番号272、配列番号274、配列番号276、配列番号278、配列番号280、配列番号282、配列番号284、配列番号286、配列番号288、配列番号290、配列番号292、配列番号294、配列番号296、配列番号298、配列番号300、配列番号302、配列番号304、配列番号306、配列番号308、配列番号310、配列番号312、配列番号314、配列番号316、配列番号318、配列番号320、配列番号322、配列番号324、配列番号326、配列番号328、配列番号330、配列番号344、配列番号332、配列番号334、配列番号336、配列番号338、配列番号340、配列番号342、配列番号354、配列番号358、配列番号360、配列番号364、配列番号368、配列番号374、配列番号382、配列番号386、配列番号388、配列番号398、配列番号400、配列番号408、配列番号438、配列番号440、配列番号448、配列番号470、配列番号484、配列番号486、配列番号488、配列番号490、配列番号502、配列番号506、配列番号508、配列番号512、配列番号514、配列番号516、配列番号518、配列番号520、配列番号522、配列番号524、配列番号526、配列番号528、配列番号530、配列番号532、配列番号534、配列番号536、配列番号538、配列番号540または配列番号542のKREDポリペプチドをコードする任意のポリヌクレオチドに関する。
別の局面において、本発明は、核酸構築物に関し、この核酸構築物は、核酸構築物を生じるために遺伝子発現を制御する1つ以上の異種調節配列に作動可能に連結された、本発明のKREDポリペプチドをコードするポリヌクレオチド(例えば、発現ベクターまたは発現カセット)を含む。その後、得られた核酸構築物(例えば、発現ベクターまたは発現カセット)は、上記ポリヌクレオチド改変体によりコードされたKREDポリペプチドの究極的な発現のために、適切な宿主細胞に挿入された。
別の局面において、本発明は、本発明のKREDポリペプチドをコードするポリヌクレオチドを含む宿主細胞に関し、このポリヌクレオチドは、その宿主細胞におけるそのKREDポリペプチドの発現のために、1つ以上の制御配列に作動可能に連結される。本発明の発現ベクターによってコードされる上記KREDポリペプチドの発現における使用のための宿主細胞は、当該分野において周知であり、細菌細胞(例えば、E.coli細胞、Streptomyces細胞およびSalmonella typhimurium細胞);真菌細胞(例えば、酵母細胞(例えば、Saccharomyces cerevisiaeまたはPichia pastoris(ATCC登録番号 201178)));昆虫細胞(例えば、Drosophila S2細胞およびSpodoptera Sf9細胞);動物細胞(例えば、CHO細胞、CS細胞、293細胞およびBowes黒色腫細胞);および植物細胞が挙げられるが、これらに限定されない。上に記載される宿主細胞のための適切な培養培地および培養条件は、当該分野において周知である。
本発明のKREDポリペプチドが上記ポリヌクレオチド改変体によって発現されると、そのポリペプチドを、タンパク質精製のための任意の1つ以上の周知技術(リゾチーム処理、音波破砕、濾過、塩の適用、超遠心分離、アフィニティークロマトグラフィーなどを含む)を用いて、上記細胞および/または培養培地から精製した。細菌(例えば、E.coli)由来のタンパク質の溶解および高効率抽出のための適切な溶液は、St.Louis MOのSigma−Aldrichから、商標名CelLytic BTMで市販される。化学的プロセスにおける適用のために、細胞溶解産物から上記KREDポリペプチドを充分に精製するための適切なプロセスは、本明細書中の実施例3において開示される。
増強したKRED活性について、上記発現ライブラリーから上記KREDポリペプチドのクローンをスクリーニングすることは、代表的に、NADHまたはNADPHがNAD+またはNADP+に変換されるのに伴う(吸光度または蛍光の減少を介した)NADHまたはNADPHの減少速度をモニタリングする、標準的な生物化学的技術を用いて実施される。この反応において、上記ケトレダクターゼが、ケトン基質を対応するヒドロキシル基に立体特異的に還元するにつれて、上記NADHまたはNADPHは、そのケトレダクターゼによって使い果たされる(酸化される)。単位時間あたりのNADHまたはNADPHの減少速度は、吸光度または蛍光の減少により測定される場合、一定量の上記溶解産物(またはそれから作製された凍結乾燥粉末)における、上記KREDポリペプチドの相対(酵素)活性を示す。このような手順は、本明細書中の実施例4に記載されている。
Candida magnoliaeケトレダクターゼの遺伝子のアナログを、E.coliにおける発現のためにコドンを最適化し、そしてGenBank登録番号 JC7338として開示される公知の配列に基づいて合成した。上記アナログ遺伝子を、60マーのオリゴマーを用いて合成し、そしてlacプロモーター遺伝子およびlacIリプレッサー遺伝子の制御下にある発現ベクター(図3のpCK110900)中にクローン化して、プラスミドpKREDを作製した。上記発現ベクターはまた、P15a複製起点およびクロラムフェニコール耐性遺伝子を含んでいた。いくつかのクローンは、(実施例4の方法により)活性なケトレダクターゼを発現したことが見出され、そして上記合成遺伝子を配列決定した。CR2−5と呼ばれる配列(配列番号1)を、全てのさらなる変異およびシャッフリングのための出発物質として使用した。CR2−5は、野生型Candida magnoliaeケトレダクターゼ(GenBank登録番号 JC7338)と約60%の核酸同一性を有していた。
通気性振盪発酵槽において、0.528g/Lの硫酸アンモニウム、7.5g/Lのリン酸水素二カリウム三水和物、3.7g/Lのリン酸二水素カリウム、2g/LのTastone−154酵母抽出物、0.05g/Lの硫酸鉄および3ml/Lの微量元素溶液(2g/Lの塩化カルシウム二水和物、2.2g/Lの硫酸亜鉛七水和物、0.5g/Lの硫酸マンガン一水和物、1g/Lの硫酸銅四水和物、0.1g/Lのホウ酸ナトリウム十水和物および0.5g/LのEDTAを含有する)を含有する10.0Lの増殖培地を、30℃の温度まで上昇させた。
上記細胞ペーストを、細胞ペーストの湿重量の1容量に対して3倍容量の100mM トリス/硫酸塩(pH7.2)中に懸濁し、その後、Sorval 12BPにおいて40分間、5000gで遠心分離することによって洗浄した。上記洗浄した細胞ペーストを、2倍容量の100mM トリス/硫酸塩(pH7.2)に懸濁した。第1のパスについて14,000psigを用い、そして第2のパスについて8,000psigを用いた2パスのホモジナイザーに上記懸濁液を通すことによって、細胞内KREDを細胞から放出させた。上記溶解産物を室温まで温め、次いで、ポリエチレンイミン(PEI)(pH7.2)の10%w/v溶液をその溶解産物に添加して、0.75%w/vの最終PEI濃度とし、そして30分間攪拌した。上記処理したホモジネートを、Beckman実験用遠心分離機において、60分間、10,000rpmで遠心分離した。上記上清をデカントし、そして容器に再懸濁して、−20℃で凍らせ、凍結乾燥した。
細胞を、1%グルコースおよび30μg/mlのクロラムフェニコールを含有するterrific broth(TB)中で一晩増殖させた。その培養物を、30μg/mlのクロラムフェニコールを含有する新鮮なTB中に10倍希釈し、30℃で2時間増殖させた後、30μg/mlのクロラムフェニコールおよび8mMのIPTG(イソプロピルチオガラクトシド)を含有する1/8容量のTBを添加した。その培養物(0.5ml)を、30℃でさらに6時間増殖させた。
pH電極制御自動滴定器を備える100mLの容器に、100mLのトリエタノールアミン緩衝液(pH7、25mL)中のグルコース(7.5g)の溶液を注いだ。この溶液に、上記2つの酵素(100mg KRED;50mg GDH)およびNADP(6.25mg)を注いだ。次いで、酢酸ブチル(10mL)を注いだ。最後に、酢酸ブチル(10mL)中の4−クロロアセト酢酸エチル(6g)を、その容器に注いだ。4M NaOHを、(6.85のpHを、下限値として設定した)自動滴定器によって必要に応じて滴下して、そのpHを常に7.0に調整した。水酸化物(caustic)が必要とされなくなった時に、その反応は完了した。その反応速度を、単位時間あたりの添加された塩基の量を測定することによるか、またはその反応混合物のサンプルをとり、そのサンプルを等しい容量の酢酸エチルで3回抽出し、そしてその合わせた有機層をガスクロマトグラフィーで分析して、単位時間あたりの(S)−4−クロロ−3−ヒドロキシ酪酸エチルの量を決定することによって、決定した。
Claims (15)
- KREDポリペプチドであって、該KREDポリペプチドは、配列番号2のポリペプチドの少なくとも1.5倍のKRED活性を有し、かつ、該KREDポリペプチドは、配列番号2のアミノ酸配列に対して少なくとも90%相同性である、KREDポリペプチド。
- KREDポリペプチドであって、該KREDポリペプチドは、配列番号2のポリペプチドの少なくとも1.5倍〜約25倍のKRED活性を有するが、配列番号2の骨格と、A2V;K3E;F5LまたはF5C;N7K;E9GまたはE9K;A12V;P13L;P14A;A16GまたはA16V;T18A;K19I;N20DまたはN20S;E21K;S22NまたはS22T;Q24HまたはQ24R;V25A;N32SまたはN32D;A36T;S41G;S42N;I45L;A48T;V56A;V60I;Y64H;N65K、N65D、N65YまたはN65S;S66GまたはS66R;H67LまたはH67Q;D68GまたはD68N;G71D;E74KまたはE74G;K78R;K79R;K85R;A86V;N90D;S93NまたはS93C;D95N、D95G、D95V、D95YまたはD95E;K98R;Q99L、Q99R、またはQ99H;T100A;I101V;Q103R;I105VまたはI105T;K106RまたはK106Q;H110Y、H110CまたはH110R;V114A;A116G;I120V;K124R;D129GまたはD129N;D131GまたはD131V;D132N;K134M、K134V、K134EまたはK134R;D137NまたはD137G;Q138L;V140I;D143N;L144F;K145R;V147A;V150A;H153YまたはH153Q;H157Y;F158LまたはF158Y;R159K;E160GまたはE160V;F162YまたはF162S;E163GまたはE163K;E165D、E165GまたはE165K;K167IまたはK167R;A170S;V172I;F173C;M177VまたはM177T;H180Y;V184I;T190A;A193V;A194V;F201L;K203R;F209Y;V218I;N224S;E226K、E226GまたはE226D;S228T;D229A;V231IまたはV231A;Q223KまたはQ223R;E234GまたはE234D;T235KまたはT235A;N237Y;K238RまたはK238E;T251A;V255A;F260L;A262V;T272A;I274L;I275LまたはI275V;およびP283Rからなる群より選択される1〜20個の残基の変化とを有する、KREDポリペプチド。
- KREDポリペプチドであって、該KREDポリペプチドは、配列番号224、配列番号244、配列番号246、配列番号250、配列番号252、配列番号254、配列番号256、配列番号260、配列番号304、配列番号344、配列番号354、配列番号358、配列番号360、配列番号364、配列番号368、配列番号374、配列番号382、配列番号386、配列番号388、配列番号400、配列番号408、配列番号438、配列番号440、配列番号448、配列番号470、配列番号484、配列番号486、配列番号488、配列番号490、配列番号502、配列番号506、配列番号508、配列番号512、配列番号514、配列番号516、配列番号518、配列番号520、配列番号522、配列番号524、配列番号526、配列番号528、配列番号530、配列番号532、配列番号534、配列番号536、配列番号538、配列番号540、および配列番号542からなる群より選択されるアミノ酸を有する、KREDポリペプチド。
- KREDポリペプチドであって、該KREDポリペプチドは、配列番号2のポリペプチドの少なくとも1.5倍〜約25倍のケトレダクターゼ活性を有し、そして、該KREDポリペプチドは、
(a)配列番号224、配列番号244、配列番号246、配列番号250、配列番号252、配列番号254、配列番号256、配列番号260、配列番号304、配列番号344、配列番号354、配列番号358、配列番号360、配列番号364、配列番号368、配列番号374、配列番号382、配列番号386、配列番号388、配列番号400、配列番号408、配列番号438、配列番号440、配列番号448、配列番号470、配列番号484、配列番号486、配列番号488、配列番号490、配列番号502、配列番号506、配列番号508、配列番号512、配列番号514、配列番号516、配列番号518、配列番号520、配列番号522、配列番号524、配列番号526、配列番号528、配列番号530、配列番号532、配列番号534、配列番号536、配列番号538、配列番号540、および配列番号542と少なくとも90%の相同性を有するアミノ酸配列を有するか;
(b)(i)配列番号223、配列番号243、配列番号245、配列番号249、配列番号251、配列番号253、配列番号255、配列番号259、配列番号303、配列番号343、配列番号353、配列番号357、配列番号359、配列番号363、配列番号367、配列番号373、配列番号381、配列番号385、配列番号387、配列番号399、配列番号407、配列番号437、配列番号439、配列番号447、配列番号469、配列番号483、配列番号485、配列番号487、配列番号489、配列番号501、配列番号505、配列番号507、配列番号511、配列番号513、配列番号515、配列番号517、配列番号519、配列番号521、配列番号523、配列番号525、配列番号527、配列番号529、配列番号531、配列番号533、配列番号535、配列番号537、配列番号539、または配列番号541のヌクレオチド配列、(ii)少なくとも100ヌクレオチドの(i)の部分配列、または、(iii)(i)もしくは(ii)の相補鎖のうちのいずれかと、中程度のストリンジェンシー条件下においてハイブリダイズする核酸配列によってコードされるか;
(c)1〜6個のアミノ酸の置換、欠失、および/または挿入を含む、配列番号224、配列番号244、配列番号246、配列番号250、配列番号252、配列番号254、配列番号256、配列番号260、配列番号303、配列番号344、配列番号354、配列番号358、配列番号360、配列番号364、配列番号368、配列番号374、配列番号382、配列番号386、配列番号388、配列番号400、配列番号408、配列番号438、配列番号440、配列番号448、配列番号470、配列番号484、配列番号486、配列番号488、配列番号490、配列番号502、配列番号506、配列番号508、配列番号512、配列番号514、配列番号516、配列番号518、配列番号520、配列番号522、配列番号524、配列番号526、配列番号528、配列番号530、配列番号532、配列番号534、配列番号536、配列番号538、配列番号540、および配列番号542のポリペプチド改変体であるか;
(d)配列番号224、配列番号244、配列番号246、配列番号250、配列番号252、配列番号254、配列番号256、配列番号260、配列番号303、配列番号344、配列番号354、配列番号358、配列番号360、配列番号364、配列番号368、配列番号374、配列番号382、配列番号386、配列番号388、配列番号400、配列番号408、配列番号438、配列番号440、配列番号448、配列番号470、配列番号484、配列番号486、配列番号488、配列番号490、配列番号502、配列番号506、配列番号508、配列番号512、配列番号514、配列番号516、配列番号518、配列番号520、配列番号522、配列番号524、配列番号526、配列番号528、配列番号530、配列番号532、配列番号534、配列番号536、配列番号538、配列番号540、および配列番号542のポリペプチドからの少なくとも220アミノ酸残基フラグメントであるか;あるいは、
(e)50℃にてpH7で60分間インキュベーションした後に、最初のKRED活性の60%より多くを保持する、(a)、(b)、(c)または(d)のポリペプチドであるか;
のいずれかである、KREDポリペプチド。 - 請求項1、2、3または4のうちのいずれか1項に記載のKREDポリペプチドをコードする、ポリヌクレオチド。
- 請求5に記載のポリヌクレオチドを含むヌクレオチド構築物であって、遺伝子発現を制御する一つ以上の異種調節配列に対して作動可能に連結されている、ヌクレオチド構築物。
- 請求項5に記載のポリヌクレオチドを含むベクターであって、該ポリヌクレオチドは、該ポリヌクレオチドによってコードされる前記KREDポリペプチドの発現の制御配列に対して作動可能に結合されており、該ベクターは、宿主細胞内で該KREDポリペプチドを発現するように該宿主細胞を形質転換し得る、ベクター。
- 前記KREDポリペプチドをコードする請求項5に記載のポリヌクレオチドを含む宿主細胞であって、該ポリヌクレオチドは、該宿主細胞内で該KREDポリペプチドの発現のための一つ以上の制御配列に対して作動可能に連結されている、宿主細胞。
- 単離されかつ精製された、請求項1に記載のKREDポリペプチド。
- 凍結乾燥形態の請求項1に記載のKREDポリペプチド。
- 緩衝化媒体中に請求項1に記載のKREDポリペプチドを含む、組成物。
- 補因子としてNADHを用いることについて増加した特異性を有する請求項1に記載のKREDポリペプチドであって、配列番号2の骨格を有し、E226が変異している、KREDポリペプチド。
- 請求項12に記載のKREDポリペプチドであって、E226がG、D、またはKである、KREDポリペプチド。
- 増加した熱安定性を有する請求項1に記載のKREDポリペプチドであって、該KREDポリペプチドは、配列番号2の骨格を有し、P14、V140、V184またはA194が変異している、KREDポリペプチド。
- 請求項12に記載のKREDポリペプチドであって、P14がAであるか、またはV140がIであるか、またはV184がIであるか、またはA194がVである、KREDポリペプチド。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US49419503P | 2003-08-11 | 2003-08-11 | |
| US54568204P | 2004-02-18 | 2004-02-18 | |
| PCT/US2004/026655 WO2005017135A1 (en) | 2003-08-11 | 2004-08-11 | Improved ketoreductase polypeptides and related polynucleotides |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2007502124A true JP2007502124A (ja) | 2007-02-08 |
| JP2007502124A5 JP2007502124A5 (ja) | 2007-08-02 |
Family
ID=34197992
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2006523448A Pending JP2007502124A (ja) | 2003-08-11 | 2004-08-11 | 改良ケトレダクターゼポリペプチドおよび関連ポリヌクレオチド |
Country Status (6)
| Country | Link |
|---|---|
| US (2) | US7629157B2 (ja) |
| EP (1) | EP1654354A1 (ja) |
| JP (1) | JP2007502124A (ja) |
| CA (1) | CA2533838A1 (ja) |
| IL (1) | IL173191A (ja) |
| WO (1) | WO2005017135A1 (ja) |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2010539952A (ja) * | 2007-10-01 | 2010-12-24 | コデクシス, インコーポレイテッド | アゼチジノンの生産のためのケトレダクターゼポリペプチド |
| WO2011145211A1 (ja) * | 2010-05-21 | 2011-11-24 | 明治製菓株式会社 | ケトレダクターゼ変異体 |
| JP2022536500A (ja) * | 2019-06-13 | 2022-08-17 | アシムケム ラボラトリーズ (ティエンジン) カンパニー リミテッド | ケトレダクターゼ突然変異体及びキラルアルコールの生産方法 |
Families Citing this family (110)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE60336324D1 (de) | 2002-08-09 | 2011-04-21 | Codexis Inc | Enzymatische verfahren zur herstellung 4-substituierter 3-hydroxybuttersäure-derivate |
| MXPA06001718A (es) | 2003-08-11 | 2006-05-19 | Codexis Inc | Procedimiento enzimatico para la produccion de derivados de acido 3-hidroxibutirico 4-sustituido y esteres de acido carboxilico sustituido con ciano e hidroxi vecinales. |
| KR20080036098A (ko) * | 2005-07-20 | 2008-04-24 | 가부시키가이샤 가네카 | 광학 활성 2-(n-치환 아미노메틸)-3-히드록시부티르산에스테르류의 제조 방법 |
| AT502395B1 (de) | 2005-07-27 | 2007-03-15 | Iep Gmbh | Oxidoreduktasen zur stereoselektiven reduktion von ketoverbindungen |
| WO2008100251A1 (en) | 2007-02-13 | 2008-08-21 | Ls9, Inc. | Modified microorganism uses therefor |
| DE102006010994A1 (de) * | 2006-03-09 | 2007-09-13 | Wacker Chemie Ag | Verfahren zur enzymatischen Herstellung von chiralen Alkoholen |
| AT503486B1 (de) * | 2006-04-11 | 2008-05-15 | Iep Gmbh | Verfahren zur enantioselektiven reduktion von steroiden |
| US20100242345A1 (en) | 2006-05-19 | 2010-09-30 | LS9, Inc | Production of fatty acids & derivatives thereof |
| US8110670B2 (en) | 2006-05-19 | 2012-02-07 | Ls9, Inc. | Enhanced production of fatty acid derivatives |
| KR20090029708A (ko) | 2006-05-19 | 2009-03-23 | 엘에스9, 인코포레이티드 | 지방산 및 이의 유도체의 제조 |
| US7879585B2 (en) | 2006-10-02 | 2011-02-01 | Codexis, Inc. | Ketoreductase enzymes and uses thereof |
| JP2010517574A (ja) | 2007-02-08 | 2010-05-27 | コデクシス, インコーポレイテッド | ケトレダクターゼおよびその使用 |
| JP5863088B2 (ja) | 2007-03-28 | 2016-02-16 | アールイージー ライフ サイエンシズ リミテッド ライアビリティ カンパニー | 脂肪酸誘導体の増強された生産 |
| CN101784669B (zh) | 2007-08-24 | 2015-02-18 | 科德克希思公司 | 用于(r)-3-羟基四氢噻吩的立体选择性制备的改善的酮还原酶多肽 |
| EP2198018B1 (en) * | 2007-09-13 | 2013-11-20 | Codexis, Inc. | Ketoreductase polypeptides for the reduction of acetophenones |
| CN101889081B (zh) | 2007-09-28 | 2014-06-18 | 科德克希思公司 | 酮还原酶多肽及其用途 |
| TW200936764A (en) * | 2007-10-03 | 2009-09-01 | Teva Pharma | Processes for preparing an intermediate of sitagliptin via enzymatic reduction |
| CA2728285A1 (en) | 2008-03-03 | 2009-09-11 | Joule Unlimited, Inc. | Engineered co2 fixing microorganisms producing carbon-based products of interest |
| DK3023494T3 (en) | 2008-06-13 | 2019-02-25 | Codexis Inc | PROCEDURE FOR SYNTHESIS OF POLYNUCLEOTIDE VARIETIES |
| US20090312196A1 (en) | 2008-06-13 | 2009-12-17 | Codexis, Inc. | Method of synthesizing polynucleotide variants |
| EP2307419B1 (en) | 2008-06-24 | 2013-11-06 | Codexis, Inc. | Biocatalytic processes for the preparation of substantially stereomerically pure fused bicyclic proline compounds |
| WO2010027710A2 (en) | 2008-08-27 | 2010-03-11 | Codexis, Inc. | Ketoreductase polypeptides and uses thereof |
| SI2329013T1 (sl) | 2008-08-27 | 2016-03-31 | Codexis, Inc. | Polipeptidi ketoreduktaze za proizvodnjo 3-aril-3-hidroksipropanamina iz 3-aril-3-ketopropanamina |
| US8288141B2 (en) * | 2008-08-27 | 2012-10-16 | Codexis, Inc. | Ketoreductase polypeptides for the production of 3-aryl-3-hydroxypropanamine from a 3-aryl-3-ketopropanamine |
| EP2329014B1 (en) | 2008-08-29 | 2014-10-22 | Codexis, Inc. | Ketoreductase polypeptides for the stereoselective production of (4s)-3[(5s)-5(4-fluorophenyl)-5-hydroxypentanoyl]-4-phenyl-1,3-oxazolidin-2-one |
| CN103725717A (zh) | 2008-10-17 | 2014-04-16 | 焦耳无限科技公司 | 微生物的乙醇生产 |
| BRPI0923572B1 (pt) | 2008-12-23 | 2019-07-30 | REG Life Sciences, LLC | Enzima tioesterase modificada que converte um substrato acil-acp c10, c12 ou c14 em um derivado de ácido graxo, polinucleotídeo codificando a tioesterase modificada, vetor de expressão, célula hospedeira de microrganismo e método de fabricação de composição de derivado de ácido graxo c10, c12 ou c14 |
| DK2385983T3 (en) | 2009-01-08 | 2018-02-12 | Codexis Inc | Transaminase POLYPEPTIDES |
| EP2401369B1 (en) | 2009-02-26 | 2014-12-24 | Codexis, Inc. | Beta-glucosidase variant enzymes and related polynucleotides |
| CN102405281B (zh) | 2009-02-26 | 2015-05-13 | 科德克希思公司 | 转氨酶生物催化剂 |
| US8263601B2 (en) | 2009-02-27 | 2012-09-11 | Concert Pharmaceuticals, Inc. | Deuterium substituted xanthine derivatives |
| WO2010107644A2 (en) | 2009-03-17 | 2010-09-23 | Codexis, Inc. | Variant endoglucanases and related polynucleotides |
| WO2010126891A1 (en) | 2009-04-27 | 2010-11-04 | Ls9, Inc. | Production of fatty acid esters |
| BRPI1010920B1 (pt) | 2009-05-22 | 2020-04-28 | Codexis Inc | processo para a produção biológica de álcoois graxos |
| US8921079B2 (en) | 2009-06-22 | 2014-12-30 | Codexis, Inc. | Transaminase reactions |
| CN102482648B (zh) | 2009-06-22 | 2014-12-10 | 科德克希思公司 | 酮还原酶介导的产生α氯代醇的立体选择性途径 |
| CA2766585C (en) | 2009-06-30 | 2016-03-01 | Codexis, Inc. | Production of fatty alcohols with fatty alcohol forming acyl-coa reductases (far) |
| US9102959B2 (en) | 2009-08-19 | 2015-08-11 | Codexis, Inc. | Ketoreductase polypeptides for the preparation of phenylephrine |
| US20110082055A1 (en) * | 2009-09-18 | 2011-04-07 | Codexis, Inc. | Reduced codon mutagenesis |
| WO2011035105A1 (en) | 2009-09-18 | 2011-03-24 | Codexis, Inc. | Reduced codon mutagenesis |
| SG181535A1 (en) | 2009-12-08 | 2012-07-30 | Codexis Inc | Synthesis of prazole compounds |
| US8986965B2 (en) | 2010-03-31 | 2015-03-24 | Codexis, Inc. | Production of monoterpenes |
| HUE026367T2 (en) | 2010-05-04 | 2016-06-28 | Codexis Inc | Biocatalysts of ezetimibe synthesis |
| HUE038434T2 (hu) * | 2010-06-17 | 2018-10-29 | Codexis Inc | Biokatalizátorok és módszerek (S)-3(1-aminoetil)-fenol szintéziséhez |
| CA2804019A1 (en) | 2010-06-28 | 2012-01-12 | Codexis, Inc. | Fatty alcohol forming acyl reductases (fars) and methods of use thereof |
| EP2606139B1 (en) | 2010-08-16 | 2015-07-15 | Codexis, Inc. | Biocatalysts and methods for the synthesis of (1r,2r)-2-(3,4-dimethoxyphenethoxy)cyclohexanamine |
| US9006460B2 (en) | 2010-08-16 | 2015-04-14 | Cardiome International Ag | Process for preparing aminocyclohexyl ether compounds |
| WO2012024662A2 (en) | 2010-08-20 | 2012-02-23 | Codexis, Inc. | Expression constructs comprising fungal promoters |
| US9085788B2 (en) | 2010-09-01 | 2015-07-21 | Concert Pharmaceuticals, Inc. | Process for preparing an enantiomerically enriched, deuterated secondary alcohol from a corresponding ketone without reducing deuterium incorporation |
| US9074233B2 (en) | 2010-09-01 | 2015-07-07 | Concert Pharmaceuticals, Inc. | Process for preparing an enantiomerically enriched, deuterated secondary alcohol from a corresponding ketone without reducing deuterium incorporation |
| WO2012035402A1 (en) * | 2010-09-14 | 2012-03-22 | Council Of Scientific & Industrial Research | High flux hollow fiber ultrafiltration membranes and process for the preparation thereof |
| WO2012046254A2 (en) * | 2010-10-08 | 2012-04-12 | Cadila Healthcare Limited | Process for preparing an intermediate of sitagliptin via enzymatic conversion |
| EP2649187B1 (en) | 2010-12-08 | 2017-11-22 | Codexis, Inc. | Biocatalysts and methods for the synthesis of armodafinil |
| WO2012142302A2 (en) | 2011-04-13 | 2012-10-18 | Codexis, Inc. | Biocatalytic process for preparing eslicarbazepine and analogs thereof |
| EP2726651B1 (en) | 2011-06-28 | 2018-11-07 | Codexis, Inc. | Protein variant generation by region shuffling |
| US9109209B2 (en) | 2011-09-08 | 2015-08-18 | Codexis, Inc. | Biocatalysts and methods for the synthesis of substituted lactams |
| IN2014MN00850A (ja) | 2011-10-19 | 2015-04-17 | Cipla Ltd | |
| HUE046089T2 (hu) | 2011-11-18 | 2020-01-28 | Codexis Inc | Biokatalizátorok hidroxi-szubsztituált karbamátok elõállításához |
| US20140357727A1 (en) | 2011-12-20 | 2014-12-04 | Codexis, Inc. | Fatty alcohol forming acyl reductase (far) variants and methods of use |
| WO2013139987A1 (en) | 2012-03-23 | 2013-09-26 | Novartis Ag | Chemical process for preparing spiroindolones and intermediates thereof |
| SG11201405990PA (en) | 2012-03-23 | 2014-11-27 | Codexis Inc | Biocatalysts and methods for synthesizing derivatives of tryptamine and tryptamine analogs |
| WO2013159055A1 (en) | 2012-04-20 | 2013-10-24 | Codexis, Inc. | Production of fatty alcohols from engineered microorganisms |
| WO2013169725A2 (en) | 2012-05-08 | 2013-11-14 | Codexis, Inc. | Biocatalysts and methods for hydroxylation of chemical compounds |
| CN104428313B (zh) | 2012-05-11 | 2017-11-17 | 科德克希思公司 | 工程化亚胺还原酶以及用于酮和胺化合物的还原胺化的方法 |
| US9650655B2 (en) | 2012-07-20 | 2017-05-16 | Codexis, Inc. | Production of fatty alcohols from engineered microorganisms |
| WO2014093070A1 (en) | 2012-12-14 | 2014-06-19 | Codexis, Inc. | Modified native beta-ketoacyl-acp synthases and engineered microorganisms |
| SG11201504752YA (en) | 2012-12-21 | 2015-07-30 | Codexis Inc | Engineered biocatalysts and methods for synthesizing chiral amines |
| JP6486835B2 (ja) | 2013-01-18 | 2019-03-20 | コデクシス, インコーポレイテッド | カルバペネム合成に有用な人口生体触媒 |
| CA2902824C (en) | 2013-02-28 | 2021-06-22 | Codexis, Inc. | Engineered transaminase polypeptides for industrial biocatalysis |
| EP2970927A4 (en) | 2013-03-15 | 2016-10-12 | Merck Sharp & Dohme | IMMOBILIZED KETOREDUCTASES AND METHODS OF MAKING AND USING IMMOBILIZED KETOREDUCTASE |
| KR101876172B1 (ko) * | 2013-04-17 | 2018-07-10 | 카운슬 오브 사이언티픽 앤드 인더스트리얼 리서치 | 케톤의 거울상 이성질체 선택적 환원을 위한 디자이너 세포 및 거울상 이성질체 풍부한 알콜의 효율적인 생산에서의 이의 용도 |
| US9822346B2 (en) | 2013-11-13 | 2017-11-21 | Codexis, Inc. | Engineered imine reductases and methods for the reductive amination of ketone and amine compounds |
| US9133488B2 (en) | 2013-12-30 | 2015-09-15 | University Of Alaska Fairbanks | Synthetic methods and compounds related thereto |
| EP3134519B1 (en) | 2014-04-22 | 2018-06-06 | c-LEcta GmbH | Ketoreductases |
| US10696953B2 (en) | 2015-02-10 | 2020-06-30 | Codexis, Inc. | Ketoreductase polypeptides for the synthesis of chiral compounds |
| CN104659287B (zh) * | 2015-03-12 | 2017-05-31 | 京东方科技集团股份有限公司 | 像素界定层及制备方法、显示基板及制备方法、显示装置 |
| EP3292136B1 (en) | 2015-05-07 | 2021-02-17 | Codexis, Inc. | Penicillin-g acylases |
| EP3452587B1 (en) | 2016-05-05 | 2021-09-08 | Codexis, Inc. | Penicillin-g acylases |
| US10184117B2 (en) | 2016-06-09 | 2019-01-22 | Codexis, Inc. | Biocatalysts and methods for hydroxylation of chemical compounds |
| JP2019517801A (ja) | 2016-06-15 | 2019-06-27 | コデクシス, インコーポレイテッド | 操作されたβ−グルコシダーゼおよびグルコシル化方法 |
| IL264686B1 (en) | 2016-08-26 | 2024-03-01 | Codexis Inc | Engineered imine reductases and methods for reversible amination of ketone and amine compounds |
| KR20190102063A (ko) | 2017-01-05 | 2019-09-02 | 코덱시스, 인코포레이티드 | 페니실린 g 아실라아제 |
| IL268121B2 (en) | 2017-02-03 | 2024-01-01 | Codexis Inc | Transgenic glycosyltransferases and steviol glycoside glucosylation methods |
| EP3615058A4 (en) | 2017-04-27 | 2021-06-02 | Codexis, Inc. | KETOREDUCTASE-POLYPEPTIDES AND POLYNUCLEOTIDES |
| EP3635101B1 (en) | 2017-05-08 | 2021-08-18 | Codexis, Inc. | Engineered ligase variants |
| WO2018231462A1 (en) | 2017-06-14 | 2018-12-20 | Codexis, Inc. | Engineered transaminase polypeptides for industrial biocatalysis |
| US11643642B2 (en) | 2017-06-27 | 2023-05-09 | Codexis, Inc. | Penicillin-g acylases |
| US10738286B2 (en) | 2017-06-30 | 2020-08-11 | Codexis, Inc. | T7 RNA polymerase variants |
| AU2018292105A1 (en) | 2017-06-30 | 2019-12-19 | Codexis, Inc. | T7 RNA polymerase variants |
| WO2019012095A1 (en) | 2017-07-14 | 2019-01-17 | C-Lecta Gmbh | TCO-reductase |
| SG11202003094PA (en) | 2017-11-07 | 2020-05-28 | Codexis Inc | Transglutaminase variants |
| JP2021506252A (ja) | 2017-12-13 | 2021-02-22 | コデクシス, インコーポレイテッド | アミドカップリングのためのカルボキシエステラーゼポリペプチド |
| CA3085261A1 (en) | 2017-12-13 | 2019-06-20 | Glaxosmithkline Intellectual Property Development Limited | Carboxyesterase biocatalysts |
| GB201802383D0 (en) * | 2018-02-14 | 2018-03-28 | Givaudan Sa | Process |
| EP3587393B1 (en) | 2018-06-21 | 2024-01-17 | F.I.S.- Fabbrica Italiana Sintetici S.p.A. | Enzymatic process for the preparation of droxidopa |
| JP7462969B2 (ja) | 2018-07-09 | 2024-04-08 | コデクシス, インコーポレイテッド | 操作されたデオキシリボースリン酸アルドラーゼ |
| KR20210032950A (ko) | 2018-07-16 | 2021-03-25 | 노파르티스 아게 | 페닐피페리디닐 인돌 유도체를 제조하기 위한 화학적 방법 |
| WO2020028039A1 (en) | 2018-07-30 | 2020-02-06 | Codexis, Inc. | Engineered glycosyltransferases and steviol glycoside glucosylation methods |
| WO2020069100A1 (en) | 2018-09-26 | 2020-04-02 | Kalamazoo Holdings, Inc. | Enzymatic process for production of modified hop products |
| US20220047682A1 (en) * | 2018-10-26 | 2022-02-17 | Tami Bar | Compositions and methods for biodegrading alcohol |
| JP2022512847A (ja) | 2018-10-29 | 2022-02-07 | コデクシス, インコーポレイテッド | 操作されたdnaポリメラーゼバリアント |
| JP2022513199A (ja) | 2018-12-14 | 2022-02-07 | コデクシス, インコーポレイテッド | 操作されたチロシンアンモニアリアーゼ |
| JPWO2021100848A1 (ja) * | 2019-11-22 | 2021-05-27 | ||
| IL296841A (en) | 2020-04-10 | 2022-11-01 | Codexis Inc | Transaminase transaminase polypeptides |
| JP2023539634A (ja) | 2020-08-28 | 2023-09-15 | コデクシス, インコーポレイテッド | 操作されたアミラーゼバリアント |
| JP2023539632A (ja) | 2020-08-28 | 2023-09-15 | コデクシス, インコーポレイテッド | 操作されたプロテアーゼバリアント |
| WO2022066155A1 (en) | 2020-09-24 | 2022-03-31 | Kalamazoo Holdings, Inc. | Enzymatic process for production of modified hop products |
| CN112410276B (zh) * | 2020-11-27 | 2023-03-21 | 江苏阿尔法药业股份有限公司 | 一种2-氯-1-(3,4-二氟苯基)乙酮还原酶重组菌株及构建方法和应用 |
| CA3204825A1 (en) | 2020-12-18 | 2022-06-23 | Codexis, Inc. | Engineered uridine phosphorylase variant enzymes |
| WO2024044657A1 (en) | 2022-08-26 | 2024-02-29 | Tesaro, Inc. | Biocatalysts and methods thereof |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1998035025A1 (fr) * | 1997-02-07 | 1998-08-13 | Kaneka Corporation | Nouvelle carbonyle reductase, gene codant celle-ci et procede d'utilisation |
| WO1999023242A1 (en) * | 1997-11-04 | 1999-05-14 | Eli Lilly And Company | Ketoreductase gene and protein from yeast |
| WO2003004653A1 (fr) * | 2001-07-02 | 2003-01-16 | Kaneka Corporation | Methode permettant de modifier un enzyme et |
Family Cites Families (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB9512837D0 (en) | 1995-06-23 | 1995-08-23 | Zeneca Ltd | reduction of ketone groups |
| US6531308B2 (en) | 1997-11-04 | 2003-03-11 | Eli Lilly And Company | Ketoreductase gene and protein from yeast |
| HUP0100252A3 (en) | 1997-12-19 | 2002-12-28 | Warner Lambert Exp Ltd Dun Lao | Process for the synthesis of 1,3-diols |
| WO1999057109A1 (fr) | 1998-04-30 | 1999-11-11 | Kaneka Corporation | Procede de production de derives d'acide acetique 6-cyanomethyl-1,3-dioxane-4 |
| ATE486068T1 (de) | 1998-08-05 | 2010-11-15 | Kaneka Corp | Verfahren zur herstellung optisch aktiver 2-ä6- (hydroxymethyl)-1,3-dioxan-4-ylü-essigsäure- derivate |
| JP4707233B2 (ja) | 1998-11-12 | 2011-06-22 | ジェイエム エレクトロニクス リミテッド エルエルシー | 多重基準、高精度スイッチング増幅器 |
| WO2001004336A1 (de) | 1999-07-09 | 2001-01-18 | Forschungszentrum Jülich GmbH | Verfahren zur reduktion von keto-carbonsäuren und deren estern |
| AU1551701A (en) | 1999-12-03 | 2001-06-12 | Kaneka Corporation | Novel carbonyl reductase, gene thereof and method of using the same |
| US6492868B2 (en) | 2000-08-14 | 2002-12-10 | Larry Kirn | Dynamic range enhancement technique |
| AU2003214111A1 (en) | 2002-03-18 | 2003-09-29 | Ciba Specialty Chemicals Holding Inc. | Alcohol dehydrogenases with high solvent and temperature stability |
| DE60336324D1 (de) | 2002-08-09 | 2011-04-21 | Codexis Inc | Enzymatische verfahren zur herstellung 4-substituierter 3-hydroxybuttersäure-derivate |
| MXPA06001718A (es) * | 2003-08-11 | 2006-05-19 | Codexis Inc | Procedimiento enzimatico para la produccion de derivados de acido 3-hidroxibutirico 4-sustituido y esteres de acido carboxilico sustituido con ciano e hidroxi vecinales. |
| DE102004029112B4 (de) | 2004-06-11 | 2007-06-21 | Julich Chiral Solutions Gmbh | Alkoholdehydrogenase zur stereoselektiven Gewinnung von Hydroxyverbindungen |
-
2004
- 2004-08-11 WO PCT/US2004/026655 patent/WO2005017135A1/en active Application Filing
- 2004-08-11 EP EP04781365A patent/EP1654354A1/en not_active Withdrawn
- 2004-08-11 US US10/916,311 patent/US7629157B2/en active Active
- 2004-08-11 CA CA002533838A patent/CA2533838A1/en not_active Abandoned
- 2004-08-11 JP JP2006523448A patent/JP2007502124A/ja active Pending
-
2006
- 2006-01-17 IL IL173191A patent/IL173191A/en not_active IP Right Cessation
-
2009
- 2009-10-08 US US12/576,195 patent/US7833767B2/en active Active
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1998035025A1 (fr) * | 1997-02-07 | 1998-08-13 | Kaneka Corporation | Nouvelle carbonyle reductase, gene codant celle-ci et procede d'utilisation |
| WO1999023242A1 (en) * | 1997-11-04 | 1999-05-14 | Eli Lilly And Company | Ketoreductase gene and protein from yeast |
| WO2003004653A1 (fr) * | 2001-07-02 | 2003-01-16 | Kaneka Corporation | Methode permettant de modifier un enzyme et |
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2010539952A (ja) * | 2007-10-01 | 2010-12-24 | コデクシス, インコーポレイテッド | アゼチジノンの生産のためのケトレダクターゼポリペプチド |
| WO2011145211A1 (ja) * | 2010-05-21 | 2011-11-24 | 明治製菓株式会社 | ケトレダクターゼ変異体 |
| US8697409B2 (en) | 2010-05-21 | 2014-04-15 | Meiji Seika Pharma Co., Ltd. | Ketoreductase mutant |
| JP2022536500A (ja) * | 2019-06-13 | 2022-08-17 | アシムケム ラボラトリーズ (ティエンジン) カンパニー リミテッド | ケトレダクターゼ突然変異体及びキラルアルコールの生産方法 |
| JP7375052B2 (ja) | 2019-06-13 | 2023-11-07 | アシムケム ラボラトリーズ (ティエンジン) カンパニー リミテッド | ケトレダクターゼ突然変異体及びキラルアルコールの生産方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| US20100028972A1 (en) | 2010-02-04 |
| IL173191A (en) | 2010-12-30 |
| US7629157B2 (en) | 2009-12-08 |
| IL173191A0 (en) | 2006-06-11 |
| WO2005017135A1 (en) | 2005-02-24 |
| US20060195947A1 (en) | 2006-08-31 |
| EP1654354A1 (en) | 2006-05-10 |
| WO2005017135A8 (en) | 2012-06-14 |
| CA2533838A1 (en) | 2005-02-24 |
| US7833767B2 (en) | 2010-11-16 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US7629157B2 (en) | Ketoreductase polypeptides and related polynucleotides | |
| EP1660648B1 (en) | Improved glucose dehydrogenase polypeptides and related polynucleotides | |
| KR101502634B1 (ko) | 케토 환원 효소 및 이의 용도 | |
| US7790432B2 (en) | Alanine 2,3-aminomutases and related polynucleotides | |
| US20120040437A1 (en) | Alanine 2,3-aminomutases and related polynucleotides | |
| KR102093546B1 (ko) | 에탄올에서 아세토인의 생산방법 | |
| WO2007028729A1 (en) | Nocardia globerula alcohol dehydrogenase and use thereof | |
| ES2437615T3 (es) | Producción de compuestos de carbonilo alfa-oxifuncionalizados | |
| JP5230234B2 (ja) | 還元酵素及びその利用 | |
| AU2021102284A4 (en) | Peptide linker, fusion protein comprising the peptide linker and uses thereof | |
| WO2024010785A1 (en) | Ketoreductase enzymes for the synthesis of 1,3-diol substituted indanes | |
| JP2011205921A (ja) | ロドコッカス(Rhodococcus)属細菌組換体及びそれを用いた光学活性(R)−3−キヌクリジノールの製造方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20070601 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20070601 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20100421 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20100720 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20100727 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20100823 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20101210 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20110902 |