ES2945834T3 - Pirrolinas fusionadas que actúan como inhibidores de la proteasa 30 específica de ubiquitina (USP30) - Google Patents
Pirrolinas fusionadas que actúan como inhibidores de la proteasa 30 específica de ubiquitina (USP30) Download PDFInfo
- Publication number
- ES2945834T3 ES2945834T3 ES19791136T ES19791136T ES2945834T3 ES 2945834 T3 ES2945834 T3 ES 2945834T3 ES 19791136 T ES19791136 T ES 19791136T ES 19791136 T ES19791136 T ES 19791136T ES 2945834 T3 ES2945834 T3 ES 2945834T3
- Authority
- ES
- Spain
- Prior art keywords
- alkylene
- alkyl
- compound
- haloalkyl
- halogen
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D487/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00
- C07D487/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00 in which the condensed system contains two hetero rings
- C07D487/08—Bridged systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/12—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains three hetero rings
- C07D471/18—Bridged systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/415—1,2-Diazoles
- A61K31/4155—1,2-Diazoles non condensed and containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/4427—Non condensed pyridines; Hydrogenated derivatives thereof containing further heterocyclic ring systems
- A61K31/4439—Non condensed pyridines; Hydrogenated derivatives thereof containing further heterocyclic ring systems containing a five-membered ring with nitrogen as a ring hetero atom, e.g. omeprazole
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/14—Drugs for disorders of the nervous system for treating abnormal movements, e.g. chorea, dyskinesia
- A61P25/16—Anti-Parkinson drugs
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D209/00—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D209/02—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom condensed with one carbocyclic ring
- C07D209/52—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom condensed with one carbocyclic ring condensed with a ring other than six-membered
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/14—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings
- C07D417/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/08—Bridged systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D487/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00
- C07D487/12—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00 in which the condensed system contains three hetero rings
- C07D487/18—Bridged systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D491/00—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00
- C07D491/02—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00 in which the condensed system contains two hetero rings
- C07D491/10—Spiro-condensed systems
- C07D491/107—Spiro-condensed systems with only one oxygen atom as ring hetero atom in the oxygen-containing ring
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Neurosurgery (AREA)
- Neurology (AREA)
- Biomedical Technology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Life Sciences & Earth Sciences (AREA)
- Veterinary Medicine (AREA)
- General Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Pharmacology & Pharmacy (AREA)
- Medicinal Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Psychology (AREA)
- Epidemiology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Agricultural Chemicals And Associated Chemicals (AREA)
- Plural Heterocyclic Compounds (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
Abstract
La descripción se refiere a los compuestos inhibidores I de USP30, sus sales farmacéuticamente aceptables, composiciones farmacéuticas que los comprenden y usos médicos que implican los mismos. (I) (Traducción automática con Google Translate, sin valor legal)
Description
DESCRIPCIÓN
Pirrolinas fusionadas que actúan como inhibidores de la proteasa 30 específica de ubiquitina (USP30)
CAMPO TÉCNICO
Esta divulgación se refiere a la inhibición de la proteasa 30 específica de ubiquitina (USP30), incluyendo nuevos compuestos y métodos para inhibir la USP30. Los compuestos y los métodos relacionados son útiles en el campo de la medicina, incluyendo el desarrollo de nuevas terapias (por ejemplo, para el tratamiento de afecciones relacionadas con la inhibición terapéutica de USP30, como la enfermedad de Parkinson (PD)). Cualquier referencia a métodos de tratamiento en los párrafos posteriores de esta descripción debe interpretarse como referencia a los compuestos, composiciones farmacéuticas y medicamentos de la presente invención para su uso en un método para el tratamiento del cuerpo humano (o animal) mediante terapia (o para el diagnóstico).
ANTECEDENTES
El sistema de ubiquitinación es un proceso altamente regulado que afecta a una amplia variedad de actividades celulares y procesos fisiológicos. La ubiquitinación es un proceso reversible, facilitado por un grupo de proteínas conocidas como enzimas desubiquitinantes (DUB), que desconjugan la ubiquitina (Ub) del sustrato. Las DUB están codificadas por aproximadamente 100 genes humanos y se dividen en seis familias, la familia más grande siendo la de las proteasas específicas de ubiquitina (USP) con más de 50 miembros.
La ubiquitinación regula la dinámica y biogénesis mitocondrial, afectando la abundancia y función de estos orgánulos. Las mitocondrias cumplen muchas funciones para mantener la salud celular en los mamíferos, incluida la generación de ATP. A medida que las mitocondrias envejecen, se dañan, pierden su funcionalidad metabólica y comienzan a liberar proteínas proapoptóticas. Las mitocondrias autorregulan su calidad a través del mecanismo de la mitofagia, que es la eliminación selectiva de las mitocondrias dañadas de la célula. Se cree que la ubiquitinación de las proteínas mitocondriales contribuye a la dinámica mitocondrial en las células de los mamíferos, posiblemente "marcando" esas proteínas para su inactivación. La proteasa específica de ubiquitina 30 (USP30) está incrustada en la membrana externa de las mitocondrias, donde participa en el mantenimiento de la morfología mitocondrial.
La desactivación de mutaciones en PINK1 y Parkin puede deteriorar la mitofagia y dar como resultado la acumulación de mitocondrias dañadas y toxicidad neuronal, lo que se ha relacionado con la enfermedad de Parkinson. La USP30 se opone a la actividad ligasa de Parkin y es un regulador negativo de la mitofagia. Se espera que la inhibición de USP30 promueva la mitofagia y restablezca la salud mitocondrial.
La WO 2016/156816 describe compuestos y métodos para la fabricación de inhibidores de enzimas desubiquitilantes (DUB).
La WO 2018/060742 describe una clase de cianopirrolidinas sustituidas con actividad como inhibidores de enzimas desubiquitilantes.
La WO 2017/163078 describe compuestos y métodos para la fabricación de inhibidores de enzimas desubiquitilantes (DUB).
La WO 2017/103614 describe compuestos y métodos para la fabricación de inhibidores de enzimas desubiquitilantes (DUB).
La WO 2017/141036 describe compuestos y métodos para la fabricación de inhibidores de enzimas desubiquitilantes (DUB).
SUMARIO
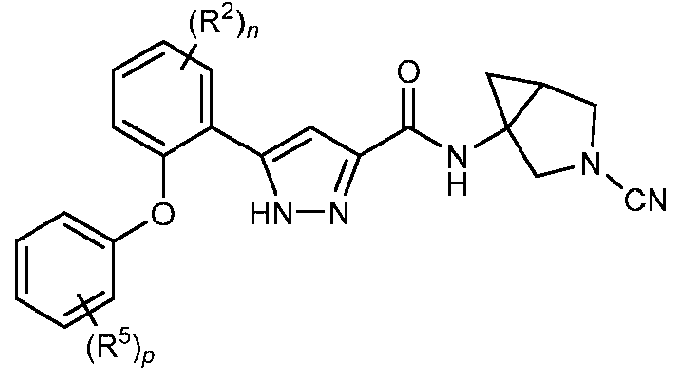
La divulgación proporciona compuestos útiles para inhibir USP30, incluyendo los compuestos inhibidores de USP30 como se definen en la presente. En algunas realizaciones, la divulgación proporciona un compuesto de fórmula (I):
o una sal farmacéuticamente aceptable del mismo, en donde
Ra, Rb, Rc, Rd, Re, Rf, Rg y Rh se definen de la siguiente manera:
(i) Ra y Rb forman un grupo alquileno C1-C4 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C4 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3; y Rc, Rd, Re, Rf, Rg y Rh son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3 ; o
(ii) Ra y Re forman un grupo alquileno C1-C2 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C2 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1 -C3 y haloalquilo C1-C3 ; y Rb, Rc, Rd, Re, Rf, Rg y Rh son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3 ; o
(iii) Ra y Rg forman un grupo alquileno C1-C3 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C3 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3 ; y Rb, Rc, Rd, Re, Rf y Rh son cada uno halógeno, alquilo C1-C3 o haloalquilo C1-C3 ; o
(iv) Rb y Rc forman un grupo alquileno C1-C4 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C4 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3; y Ra, Rd, Re, Rf, Rg y Rh son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3 ; o
(v) Rb y Re forman un grupo alquileno C1-C3 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C3 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3; y Ra, Rc, Rd, Rf, Rg y Rh son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3 ; o
(vi) Rb y Rg forman un grupo alquileno C1-C4 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C4 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3; y Ra, Rc, Rd, Re, Rf y Rh son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3 ; o
(vii) Rc y Rd junto con el átomo al que están unidos, forman un cicloalquilo o heterocicloalquilo de 3-6 miembros, en donde dicho cicloalquilo o heterocicloalquilo de 3-6 miembros está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3 ; y Ra, Rb,
Re, Rf, Rg y Rh sonn cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3; o
(viii) Rc y Rd juntos forman =O; y Ra, Rb, Re, Rf, Rg y Rh son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3 ; o
(ix) Rc y Re forman un grupo alquileno C1-C4 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C4 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3 ; y Ra, Rb, Rd, Rf, Rg y Rh son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3 ; o
(x) Rc y Rg forman un grupo alquileno C1-C3 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C3 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3; y Ra, Rb, Rd, Re, Rf y Rh son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3 ; o
(xi) Re y Rf junto con el átomo al que están unidos, forman un cicloalquilo o heterocicloalquilo de 3-6 miembros, en donde dicho cicloalquilo o heterocicloalquilo de 3-6 miembros está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3 ; y Ra, Rb,
Rc, Rd, Rg y Rh son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3 ; o
(xii) Re y Rf juntos forman =O; y Ra, Rb, Rc, Rd, Rg y Rh son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3; o
(xiii) Re y Rg forman un grupo alquileno C1-C3 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C3 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3 ; y Ra, Rb, Rc, Rd, Rf y Rh son cada uno halógeno, alquilo C1-C3 o haloalquilo C1-C3 ; o
(xiv) Rg y Rh junto con el átomo al que están unidos, forman un cicloalquilo o heterocicloalquilo de 3-6 miembros, en donde dicho cicloalquilo o heterocicloalquilo de 3-6 miembros está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3 ; y Ra, Rb,
Rc, Rd, Re y Rf son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3 ; o
(xv) Rg y Rh juntos forman =O; y Ra, Rb, Rc, Rd, Re y Rf son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3 ; y
Ar1 es fenileno o heteroarileno de 5-6 miembros, en donde dicho fenileno o heteroarileno está sustituido con m grupos R1; y
Ar2 es fenileno o heteroarileno de 5-10 miembros, en donde dicho fenileno o heteroarileno está sustituido con n grupos R2;
L es-O-, -S-, -NR3-, -C(R4)2-, -S(O)2-, o -S(O)-;
M es cicloalquilo de 3 a 6 miembros, fenilo o heteroarilo de 5 a 6 miembros, en donde dicho cicloalquilo, fenilo o
heteroarilo está sustituido con p grupos R5;
cada aparición de R1, R2 y R5 es independientemente halo, ciano, NO2, oxo, hidroxilo,-R6, -OR6, alquilo C1-C6, haloalquilo C1-C6 , hidroxialquilo C1-C6, -alquileno C1-C6-R6 , alcoxi C1-C6, haloalcoxi Ci-C6,-alquileno C0-C3-NR6R7,-alquileno C0-C3-NR7R8, -alquileno C0-C3-C(O)NR6R7, -alquileno C0-C3-C(O)NR7R8, -alquileno C0-C3-NR7C(O)R6, -alquileno C0-C3-NR7C(O)R8, -alquileno C0-C3-NR7S(O)2R6, -alquileno C0-C3-C(O)R6, -alquileno C0-C3-C(O)R7, -alquileno C0-C3 -SR6, -alquileno C0-C3-S(O)R6, -alquileno C0-C3-S(O)2R6, -alquileno C0-C3-S(O)2R7, -alquileno C0-C3S(O)2NR6R7, -alquileno C0-C3-S(O)2NR7R8, -alquileno C rC 3-NR7C(O)NR8R9, -alquileno C0-C3-n R7S(O)2NR8R9, -alquileno C0-C3-C(O)OR7, -alquileno C0-C3-C(O)OR6, -alquileno C0-C3-OC(O)R7, -alquileno C0-C3-OC(O)R6, -alquileno C0-C3 - NR7C(O)OR8, o -alquileno C0-C3-NR7S(O)2R8;
R3 es H, alquilo C1-C6 o haloalquilo C1-C6 ;
cada R4 es independientemente H, alquilo C1-C6 o haloalquilo C1-C6, o dos grupos R4 junto con el átomo de carbono al que están unidos forman un cicloalquilo o heterocicloalquilo de 3-6 miembros;
cada R6 es independientemente heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, arilo de 6-10 miembros o cicloalquilo de 3-8 miembros, en donde dicho heteroarilo, heterocicloalquilo, arilo o cicloalquilo está opcionalmente sustituido con de 1 a 5 sustituyentes seleccionados independientemente del grupo formado por halo, oxo, alquilo C1-C6, haloalquilo C1-C6 , hidroxialquilo C1-C6 , alcoxi C1-C6, haloalcoxi C1-C6, alquenilo C2-C6 6 , alquinilo C2-C6 6, heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, arilo de 6-10 miembros, cicloalquilo de 3-8 miembros, -NR10C(O)NR11R12, -NR10R11, -C(O)R10, -NR10C(O)R11, -NR10C(O)OR11, -S(O)2R10, -C(O)NR10R11, -C(O)OR10, - S(O)2NR10R11, -NR10S(O)2R11, -OR10, -OC(O)R10, -OS(O)2R10, -OC(O)NR10R11, -OC(O)OR10, - OS(O)2NR10R11, -C(O)NR10C(O)NR11R12, -C(O)C(O)R10, -C(O)NR10C(O)R11, - C(O)NR10C(O)OR11, -C(O)S(O)2R10, -C(O)C(O)NR10R11, -C(O)C(O)OR10, -C(O)S(O)2NR10R11, -C(O)NR10S(O)2R11, - alquileno C1-C6-R10, -alquileno C1-C6-NR10C(O)NR11R12, -alquileno C1-C6-NR10R11, -alquileno C1-C6-C(O)R10, -alquileno C1-C6-NR10C(O)R11, -alquileno C1-C6-NR10C(O)OR11, -alquileno C1-C6-S(O)2R10, -alquileno C1-C6-C(O)NR10R11, -alquileno C1-C6-C(O)OR10, -alquileno C ^ - S ^ N R ^ R 11, -alquileno C1-C6-NR10S(O)2R11, -alquenileno C1-C6-R10, -alquenileno C1-C6-NR10C(O)NR11R12, -alquenileno C1-C6-NR10R11, -alquenileno C1-C6-C(O)R10, -alquenileno C1-C6-NR10C(O)R11, -alquenileno C1-C6-NR10C(O)OR11, -alquenileno C1-C6-S(O)2R10, -alquenileno C1-C6-C(O)NR10R11, -alquenileno C1-C6-C(O)OR10, -alquenileno C1-C6-S(O)2NR10R11, y -alquenileno C1-C6-NR10S(O)2R11;
cada R7, R8 y R9 es independientemente hidrógeno o alquilo C1-C6 ;
cada R10, R11 y R12 es independientemente hidrógeno, alquilo C1-C6, heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, arilo de 6-10 miembros o cicloalquilo de 3-8 miembros;
m es 0-4;
n es 0-4; y
p es 0-4.
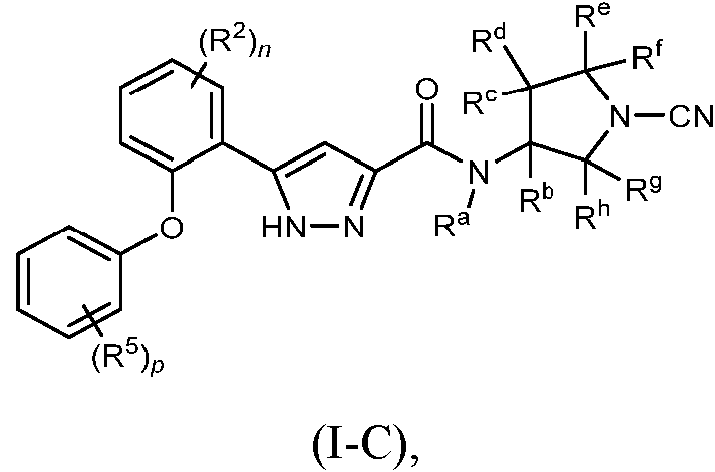
En algunas realizaciones, la divulgación proporciona un compuesto de fórmula (I-C):
o una sal farmacéuticamente aceptable del mismo, en donde R2, R5, n, p, Ra, Rb, Rc, Rd, Re, Rf, Rg y Rh son todos como se definen para la fórmula (I) anterior.
En algunas realizaciones, un compuesto inhibidor de USP30 es un compuesto seleccionado del grupo que consiste en:
y
en donde R2, R5, n y p son como se definen con respecto a la fórmula (I) en la presente, o una sal farmacéuticamente aceptable del mismo, que tiene un valor de IC50 de aproximadamente < 1 μM (y preferiblemente ≤ 0,5 μM o ≤ 0,1 μM) y > 0,001 μM como se mide en un ensayo de ubiquitina-rodamina 110 como se describe en el Ejemplo 1. En algunas realizaciones, se proporcionan compuestos de fórmula (I-C) donde R2 y R5 son ambos hidrógeno.
En algunas realizaciones, un compuesto inhibidor de USP30 es un compuesto de fórmula química:
en donde R2, R5, n y p son como se definen con respecto a la fórmula (I) en la presente, o una sal farmacéuticamente aceptable del mismo, que tiene un valor de IC50 de aproximadamente < 1 μM (y preferiblemente ≤ 0,5 μM o ≤ 0,1 μM) y > 0,001 μM como se mide en un ensayo de ubiquitina-rodamina 110 como se describe en el ejemplo 1.
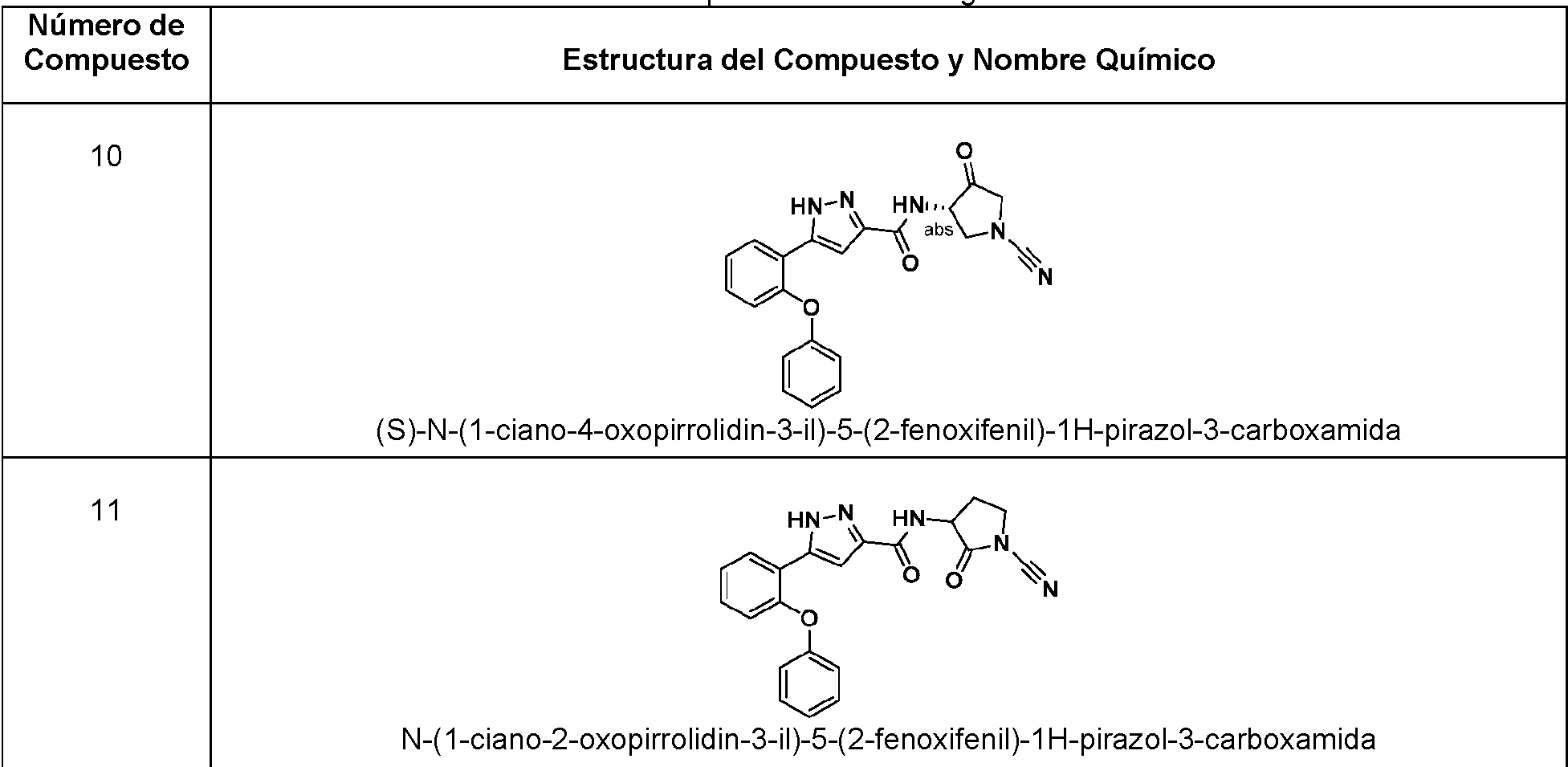
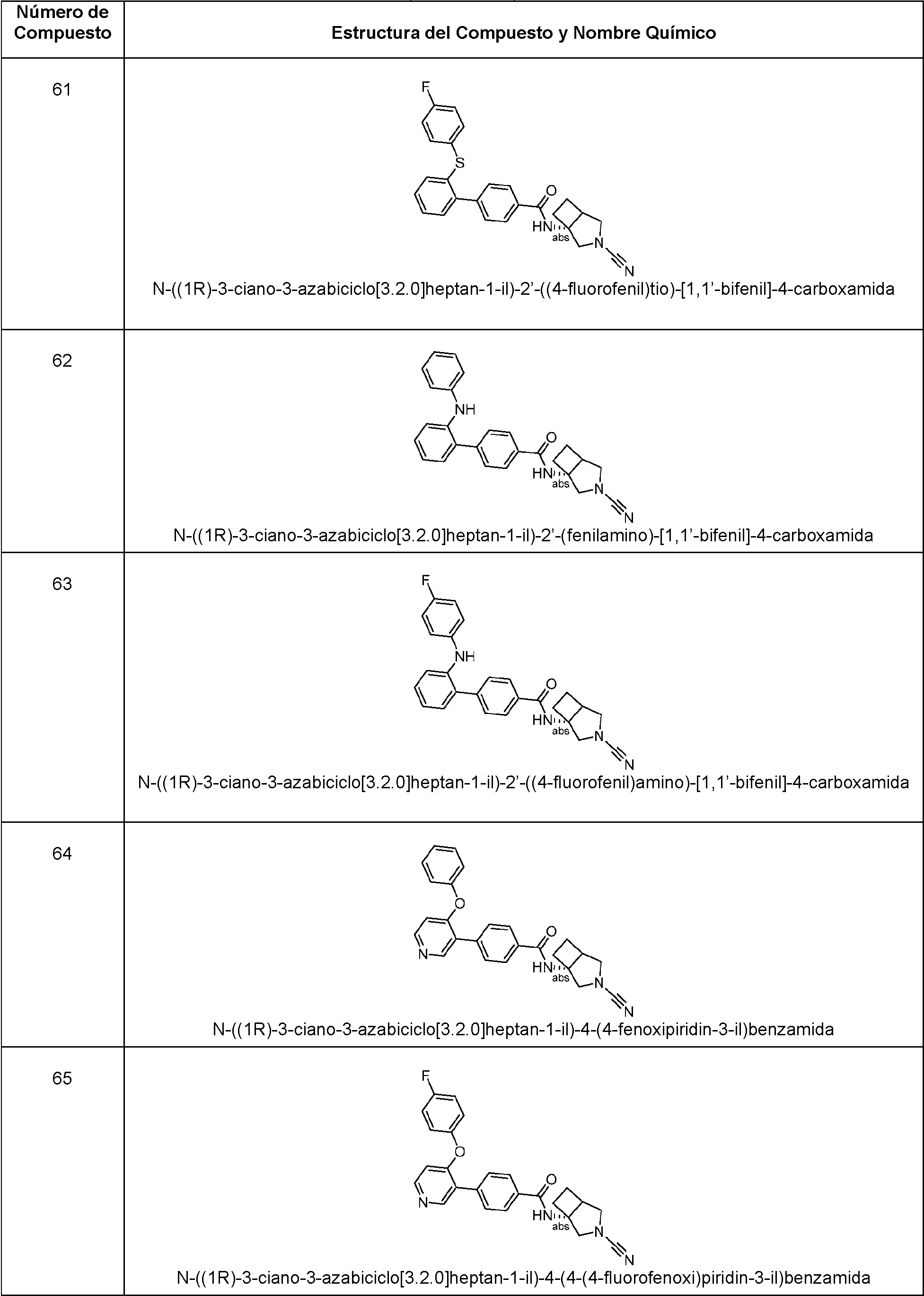
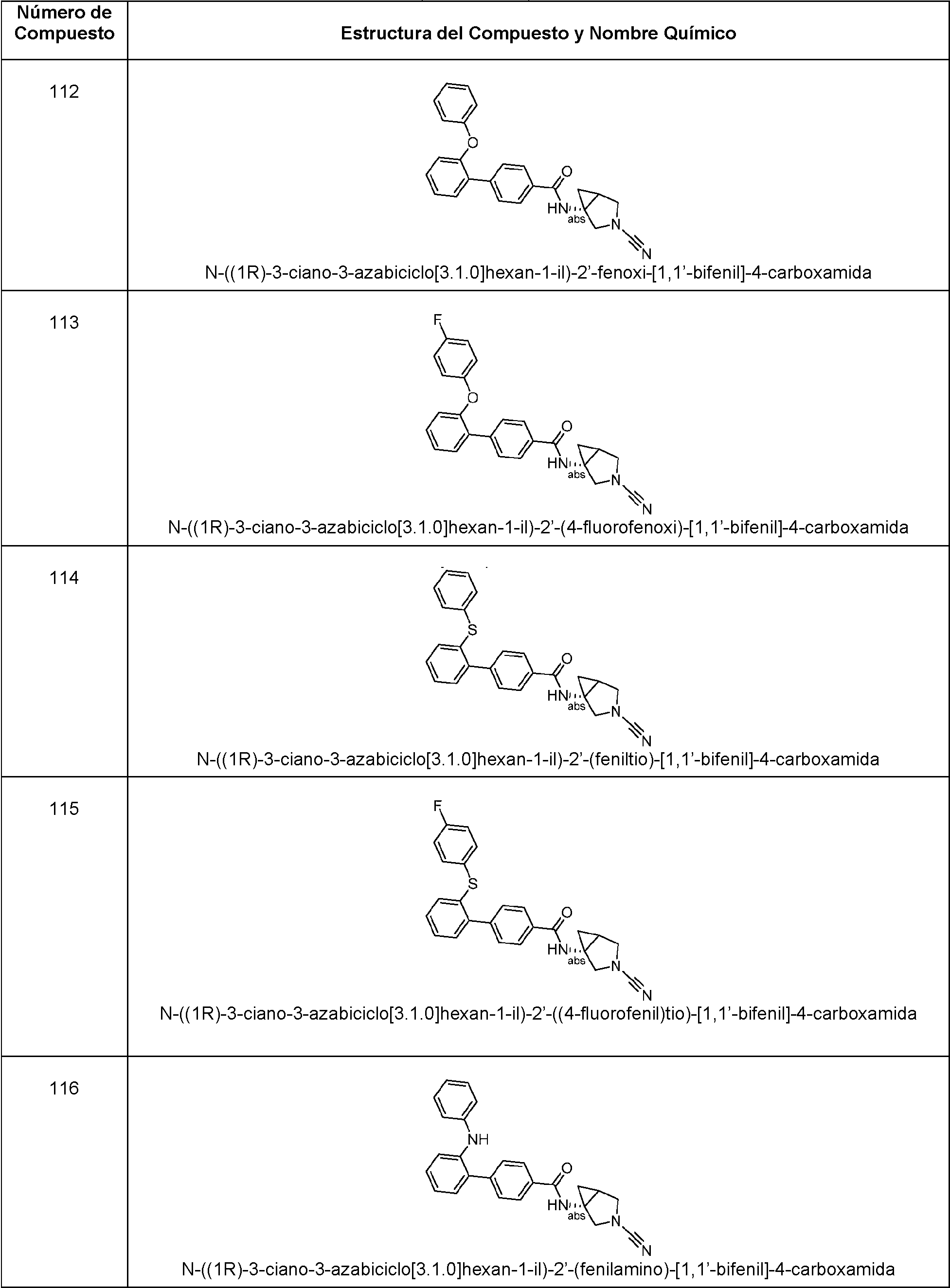
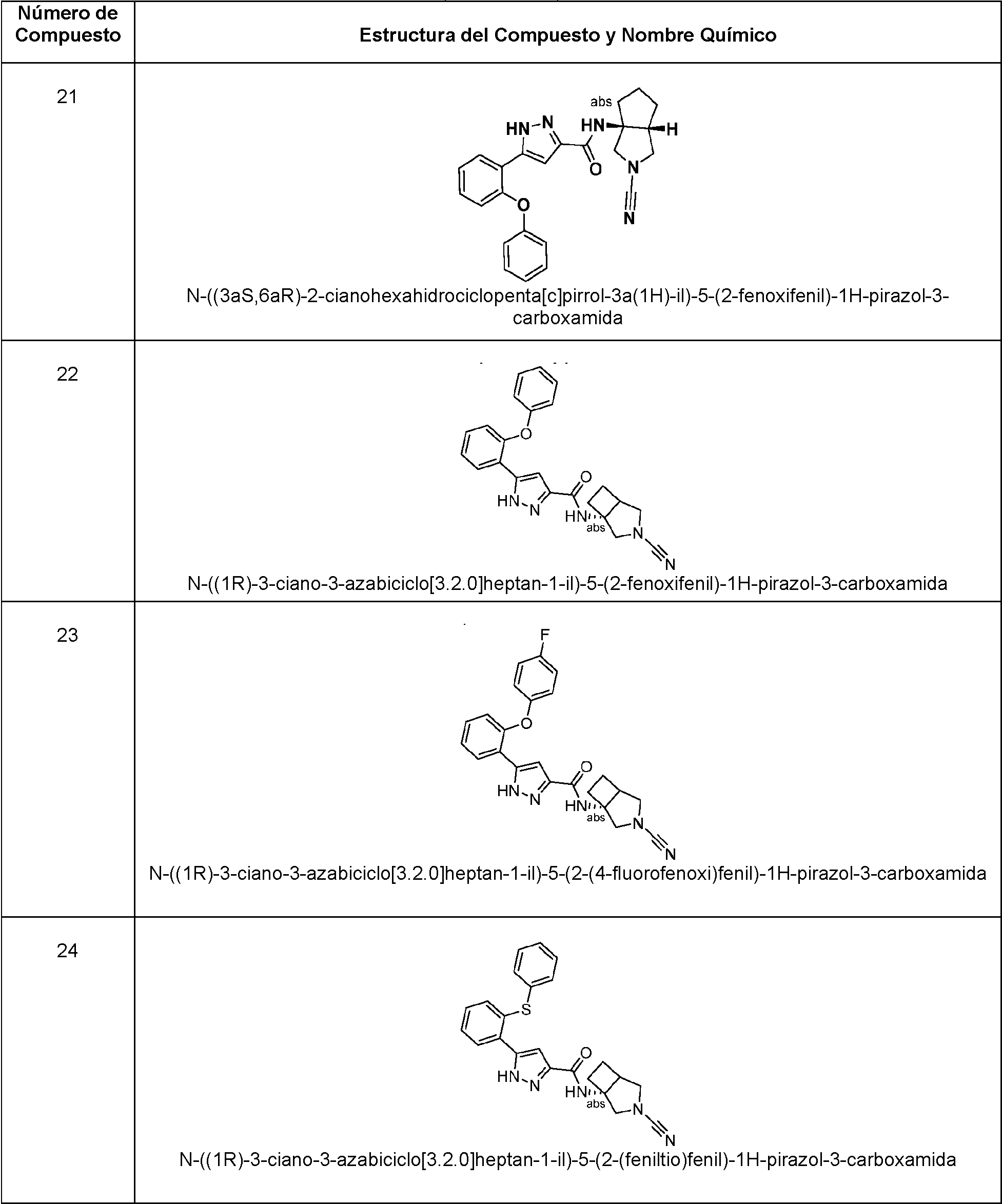
En algunas realizaciones, un compuesto es cualquier compuesto seleccionado de los compuestos enumerados en la Tabla 1 de la presente.
DESCRIPCIÓN DETALLADA
La presente divulgación se refiere a compuestos de fórmula (I), como se define en la presente, sales farmacéuticamente aceptables de los mismos, composiciones farmacéuticas que comprenden los mismos y usos médicos que implican los mismos. En algunas realizaciones, los compuestos de fórmula (I) son compuestos inhibidores de USP30. En otras realizaciones, los compuestos de fórmula (I) son útiles, por ejemplo, como herramientas analíticas y/o compuestos de control en ensayos biológicos (por ejemplo, compuestos de cualquiera de los siguientes aspectos y realizaciones que no son compuestos inhibidores de USP30).
Los Compuestos Inhibidores de USP30 son útiles en el desarrollo de nuevas terapias para la enfermedad de Parkinson (PD) y en métodos para tratar enfermedades o afecciones mediante la inhibición de USP30 (como la PD). Parkin (ubiquitina ligasa E3) y PINK1 (quinasa) son reguladores clave de la mitofagia. En las mitocondrias sanas, la localización de PINK1 en la membrana externa mitocondrial (MOM) y la exposición al citosol están limitadas por la rápida importación a la membrana interna mitocondrial (MIM). Una vez localizado en el MIM, PINK1 es procesado por varias proteasas, como la proteasa de tipo romboidal asociada a presenilina (PARL), para proporcionar una versión truncada de PINK1 que posteriormente es degradada por el proteasoma (Meissner et al., Autophagy. 2015, 11). (9), 1484-1498). Tras la despolarización o disfunción mitocondrial, PINK1 se acumula en la MOM, reclutando y activando Parkin a través de la fosforilación dependiente de PINK1 tanto de ubiquitina como de Parkin. Por consiguiente, Parkin activada ubiquitina las proteínas de MOM como TOMM20 para desencadenar mitofagia (Pickrell et al., Neuron. 2015, 85(2), 257-273). La USP30 está incrustada en la MOM con su dominio DUB catalítico orientado hacia el citosol y se ha demostrado que antagoniza la ubiquitinación mediada por Parkin de sustratos comunes, por lo que se opone a la mitofagia mediada por Parkin. El silenciamiento genético de USP30 da como resultado una ubiquitinación aumentada de varios sustratos de Parkin seguido de un aumento de la mitofagia. En organismos modelo, el agotamiento de USP30 es capaz de rescatar defectos de mitofagia provocados por mutaciones patógenas de Parkin, así como restaurar la morfología y función de las mitocondrias y los niveles de dopamina. (Nakamura, et al., Mol Biol Cell. 2008, 19(5), 1903-1911; Bingol, et al., Nature 2014, 510(7505):370-5). Por lo tanto, la inhibición de USP30 con un compuesto divulgado en la presente podría presentar un nuevo paradigma de tratamiento para la PD promoviendo el recambio mitocondrial.
Definiciones
Como se usa en la presente, el término "alquilo" significa una cadena hidrocarbonada sustituida o no sustituida que está completamente saturada, que incluye grupos alquilo de cadena lineal y grupos alquilo de cadena ramificada, y que tiene un único punto de unión al resto de la molécula. En algunas realizaciones, un alquilo de cadena lineal o cadena ramificada tiene aproximadamente 1-20 átomos de carbono en su estructura principal (por ejemplo, C1-C2 0 para cadena lineal, C2-C6 20 para cadena ramificada), y alternativamente, aproximadamente 1-10. En algunas realizaciones, un alquilo tiene aproximadamente 1-8 átomos de carbono. En algunas realizaciones, un alquilo tiene aproximadamente 1-6 átomos de carbono. En algunas realizaciones, un alquilo tiene aproximadamente 1-5 átomos de carbono. En algunas realizaciones, un alquilo tiene aproximadamente 1-4 átomos de carbono. En algunas realizaciones, un alquilo tiene aproximadamente 1-3 átomos de carbono. En algunas realizaciones, un alquilo tiene aproximadamente 1-2 átomos de carbono.
Como se usa en la presente, el término "alquileno" se refiere a un grupo alquilo bivalente. Los alquilenos ejemplares incluyen - -CH2-, -CH2CH2-, -CH(CH3)-, -CH2CH(CH3)-, -CH(CH3)c H3)-, etc. En algunas realizaciones, una "cadena de alquileno" es un grupo polimetileno, es decir, -(CH2)n-, en donde n es un número entero positivo, preferiblemente de 1 a 6, de 1 a 4, de 1 a 3, de 1 a 2, o de 2 a 3. Una cadena de alquileno sustituida es un grupo polimetileno en el que uno o más átomos de hidrógeno de metileno se reemplazan por un sustituyente.
Como se usa en la presente, el término "alquenilo" se refiere a un grupo alquilo, como se define en la presente, que tiene uno o más enlaces dobles.
Como se usa en la presente, el término "alquenileno" se refiere a un grupo alquenilo bivalente. Una cadena de alquenileno sustituida es un grupo polimetileno que contiene por lo menos un enlace doble en el que uno o más átomos de hidrógeno se reemplazan por un sustituyente.
Como se usa en la presente, el término "alquinilo" se refiere a un grupo alquilo, como se define en la presente, que tiene uno o más enlaces triples.
El término "arilo" se refiere a sistemas de anillos que tienen un total de cinco a catorce miembros del anillo, en donde por lo menos un anillo en el sistema es aromático y en donde cada anillo en el sistema contiene de 3 a 7 miembros del anillo. El término "arilo" puede usarse indistintamente con el término "anillo de arilo". En ciertas realizaciones de la presente divulgación, "arilo" se refiere a un sistema de anillos aromático y los grupos ejemplares
incluyen fenilo, bifenilo, naftilo, antracilo y similares, que pueden tener uno o más sustituyentes. También se incluye dentro del alcance del término "arilo", como se usa en la presente, un grupo en el que un anillo aromático se fusiona con uno o más anillos no aromáticos, como indanilo, ftalimidilo, naftimidilo, fenantridinilo o tetrahidronaftilo, y similares.
El término "arileno" se refiere a un grupo arilo bivalente (por ejemplo, fenileno).
Como se usa en la presente, el término "cicloalquilo" se refiere a un grupo alquilo cíclico (por ejemplo, un grupo alquilo monocíclico o un grupo alquilo bicíclico). En algunas realizaciones, "cicloalquilo" se refiere a un grupo cicloalquilo C3-C8 monocíclico. En algunas realizaciones, "cicloalquilo" se refiere a un grupo cicloalquilo C3-C6 monocíclico.
Los términos "halógeno" o "halo" significan F, Cl, Br o I.
El término "heteroarilo" se refiere a grupos que tienen de 5 a 10 átomos en el anillo, preferiblemente 5, 6 o 9 átomos en el anillo; que tienen 6, 10 o 14 electrones n compartidos en una matriz cíclica; y que tienen, además de los átomos de carbono, de uno a cinco heteroátomos en donde el término "heteroátomo" se refiere a nitrógeno, oxígeno o azufre, e incluye cualquier forma oxidada de nitrógeno o azufre, y cualquier forma cuaternizada de un nitrógeno básico. Los grupos heteroarilo ejemplares incluyen tienilo, furanilo, pirrolilo, imidazolilo, pirazolilo, triazolilo, tetrazolilo, oxazolilo, isoxazolilo, oxadiazolilo, tiazolilo, isotiazolilo, tiadiazolilo, piridilo, piridazinilo, pirimidinilo, pirazinilo, indolizinilo, purinilo, naftiridinilo y pteridinilo. El término "heteroarilo", como se usa en la presente, también incluye grupos en los que un anillo heteroaromático está fusionado con uno o más grupos arilo, cicloalifáticos, o anillos heterociclilo, donde el radical o punto de unión está en el anillo heteroaromático. Los grupos ejemplares incluyen indolilo, isoindolilo, benzotienilo, benzofuranilo, dibenzofuranilo, indazolilo, bencimidazolilo, benzotiazolilo, quinolilo, isoquinolilo, cinolinilo, ftalazinilo, quinazolinilo, quinoxalinilo, 4H-quinolizinilo, carbazolilo, acridinilo, fenacinilo, fenotiazinilo, fenoxazinilo, tetrahidroquinolinilo, tetrahidroisoquinolinilo y pirido[2,3-b]-1,4-oxazin-3(4H)-ona. Un grupo heteroarilo puede ser mono o bicíclico. El término "heteroarilo" puede usarse indistintamente con los términos "anillo de heteroarilo", "grupo heteroarilo" o "heteroaromático", cualquiera de estos términos incluye anillos que están opcionalmente sustituidos.
El término "heteroarileno" se refiere a un grupo heteroarilo bivalente.
Como se usa en la presente, el término "heterocicloalquilo" se refiere a una fracción cíclica monocíclica estable de 3 a 7 miembros o bicíclica de 7 a 10 miembros que está saturada y que tiene, además de átomos de carbono, uno o más, preferiblemente de uno a cuatro, heteroátomos seleccionados independientemente de nitrógeno, oxígeno y azufre, incluyendo cualquier forma oxidada de nitrógeno o azufre, y cualquier forma cuaternizada de nitrógeno básico. Como ejemplo, en un anillo saturado que tiene de 1 a 3 heteroátomos seleccionados de oxígeno, azufre o nitrógeno, el nitrógeno puede ser N (como en 3,4-dihidro-2H-pirrolilo), NH (como en pirrolidinilo) o NR (como en N-pirrolidinilo sustituido). Un anillo de heterocicloalquilo puede unirse a su grupo colgante en cualquier heteroátomo o átomo de carbono que dé como resultado una estructura estable y cualquiera de los átomos del anillo puede estar opcionalmente sustituido. Los ejemplos de tales radicales heterocicloalquilo incluyen tetrahidrofuranilo, tetrahidrotiofenilpirrolidinilo, piperidinilo, pirrolinilo, tetrahidroquinolinilo, tetrahidroisoquinolinilo, decahidroquinolinilo, oxazolidinilo, piperazinilo, dioxanilo, dioxolanilo, diazepinilo, oxazepinilo, tiazepinilo, morfolinilo y quinuclidinilo. El término "heterocicloalquilo" también incluye grupos en los que un anillo heterocicloalquilo está fusionado con uno o más anillos arilo, heteroarilo o cicloalifáticos, como indolinilo, 3H-indolilo, cromanilo, fenantridinilo o tetrahidroquinolinilo, donde el radical o punto de unión está en el anillo heterocicloalquilo.
Como se usa en la presente, un "compuesto inhibidor de USP30" se refiere a un compuesto que tiene una IC50 de aproximadamente 1 micromolar o menos (es decir, un valor de IC50 de < 1 j M y > 0,001 j M) en el ensayo de ubiquitina-rodamina 110 para USP30 como descrito en el Ejemplo 1 de la presente. Por ejemplo, un inhibidor de USP30 puede ser un compuesto de fórmula (I) que tiene un valor de IC50 de <0,5 j M y > 0,001 j M cuando se analiza en el ensayo bioquímico del Ejemplo 1. En algunas realizaciones, un inhibidor de USP30 es un compuesto de fórmula (I) que tiene un valor de IC50 de < 0,1 j M y > 0,001 j M cuando se prueba en el Ensayo Bioquímico del Ejemplo 1.
Como se usa en la presente, el término "sal farmacéuticamente aceptable" se refiere a las sales de tales compuestos que son apropiadas para su uso en contextos farmacéuticos, es decir, sales que son, dentro del alcance del buen criterio médico, adecuadas para su uso en contacto con los tejidos de humanos y animales inferiores sin toxicidad, irritación, respuesta alérgica y similares indebidos, y están en consonancia con una relación beneficio/riesgo razonable. Las sales farmacéuticamente aceptables son bien conocidas en la técnica. Por ejemplo, S.M. Berge, et al. describe sales farmacéuticamente aceptables en detalle en J. Pharmaceutical Sciences, 66: 1-19 (1977).
A menos que se indique lo contrario, se entenderá que todas las estructuras químicas y nombres químicos representados en la presente sin descriptores estereoquímicos incluyen todas las formas estereoisoméricas (por
ejemplo, enantioméricas o diastereoisómeras) del compuesto representado por la estructura o el nombre, así como todas las formas geométricas y conformacionales isoméricas del compuesto; por ejemplo, las configuraciones R y S para cada estereocentro. A menos que se indique lo contrario, se entenderá que tales estructuras y nombres incluyen una forma estereoquímicamente pura del compuesto y cualquier mezcla de enantiómeros, diastereómeros o isómeros geométricos (o conformacionales). A menos que se indique lo contrario, todas las formas tautoméricas de los compuestos de la divulgación están dentro del alcance de la divulgación.
A menos que se indique lo contrario, se entenderá que todas las estructuras químicas y nombres químicos representados en la presente con descriptores estereoquímicos (es decir, enlaces hash y cuña en las estructuras químicas; designadores (R)- y (S)- en los nombres químicos) se refieren a un compuesto que tiene la estereoquímica relativa (pero no necesariamente la estereoquímica absoluta) indicada por los descriptores estereoquímicos. A menos que se indique lo contrario, se entenderá que tales estructuras y nombres incluyen una forma enantioméricamente pura del compuesto que tiene la estereoquímica relativa indicada por los descriptores estereoquímicos o cualquier mezcla de enantiómeros. En algunas realizaciones, los enantiómeros están presentes en una mezcla racémica. En otras realizaciones, el enantiómero que tiene la estereoquímica absoluta sugerida por los descriptores estereoquímicos está presente en forma sustancialmente enantioméricamente pura. En otras realizaciones, el enantiómero que tiene la estereoquímica absoluta opuesta a la sugerida por los descriptores estereoquímicos está presente en forma sustancialmente enantioméricamente pura.
A menos que se indique lo contrario, se entenderá que todas las estructuras químicas y nombres químicos representados en la presente con descriptores estereoquímicos (es decir, enlaces hash y cuña en las estructuras químicas; designadores (R)- y (S)- en los nombres químicos) y un descriptor "absoluto" ("abs") se refieren a un compuesto que tiene la estereoquímica absoluta indicada por los descriptores estereoquímicos. A menos que se indique lo contrario, se entenderá que tales estructuras y nombres incluyen el compuesto en forma enantioméricamente pura o en una mezcla con su enantiómero. En algunas realizaciones, los enantiómeros están presentes en una mezcla racémica. En otras realizaciones, el enantiómero que tiene la estereoquímica absoluta indicada por los descriptores estereoquímicos está presente en forma sustancialmente enantioméricamente pura.
A menos que se indique lo contrario, también se pretende que las estructuras representadas en la presente incluyan compuestos que difieren solo en la presencia de uno o más átomos isotópicamente enriquecidos. Por ejemplo, los compuestos que tienen las presentes estructuras que incluyen la sustitución de hidrógeno por deuterio o tritio, o la sustitución de un carbono por un carbono enriquecido en 13C o 14C están dentro del alcance de esta divulgación.
Se apreciará que a lo largo de la presente divulgación, a menos que se indique lo contrario, se pretende que la referencia a un compuesto de fórmula (I) incluya también las fórmulas (I-1), (I-2), (I-3), (I-4), (I-A), (I-A-1), (I-A-2), (I-A-3), (I-A-4), (IB), (I-B-1), (I-B-2), (I-B-3), (I-B-4), (I-C), (I-C-1), (LC-2), (LC-3), (I-C-4), (I-C-a), (I-C-b), (I-C-c), (I-C-d), (I-C-e), (LC-f), (ID), (I-E), (I-E-1), (I-E-2), (I-E-3), (I-E-4), (I-F-1), (I-F-2), (I-G-1), (I-G-2), (I-H-1), (I-H-2), (I-J-1), (I-J-2), (I-K-1), (I-K-2), (IL-1), (I-L-2), (I-M), (I-M-1), (I-M-2), (I-M-3), y (I-M-4), y especies compuestas de tales fórmulas divulgadas en la presente.
Compuestos de la divulgación
En un aspecto, la divulgación se refiere a un compuesto de fórmula (I):
o una sal farmacéuticamente aceptable del mismo, en donde Ar1, Ar2, M, L, Ra, Rb, Rc, Rd, Re, Rf, Rg y Rh son todos como se definen para la fórmula (I) anterior.
En algunas realizaciones, la presente divulgación proporciona compuestos, o sales farmacéuticamente aceptables de los mismos, de fórmula (I-1):
en donde Ar1, Ar2, M, L, Ra, Rd, Re, Rf, Rg y Rh son todos como se definen para la fórmula (I Rk, Rm y Rn son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3.
En algunas realizaciones, la presente divulgación proporciona compuestos, o sales farmacéuticamente aceptables de los mismos, de fórmula (I-2):
en donde Ar1, Ar2, M, L, Ra, Rd, Re, Rf, Rg y Rh son todos como se define para la fórmul Rk son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3.
En algunas realizaciones, la presente divulgación proporciona compuestos, o sales farmacéuticamente aceptables de los mismos, de fórmula (I-3):
en donde Ar1, Ar2, M, L, Ra, Rd, Re, Rf, Rg y Rh son todos como se definen para la fórmula (I) anterior, y en donde RJ
Rk, Rm, Rn, Ro y Rp son cada uno independientemente hidrógeno, halógeno, alquilo C1 -C3 o haloalquilo C1 -C3.
En algunas realizaciones, la presente divulgación proporciona compuestos, o sales farmacéuticamente aceptables de los mismos, de fórmula (I-4):
en donde Ar1, Ar2, M, L, Ra, Rb, Rd, Rf, Rg y Rhson todos como se definen para la fórmula (I) anterior, y en donde Rq y Rr son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3.
En otro aspecto, la divulgación se refiere a un compuesto de fórmula (I-A):
(I-A);
o una sal farmacéuticamente aceptable del mismo, en donde:
X1 es C o N;
X2 es CH, CR1, O, S, N, NH o NR1, según lo permita la valencia;
X2 es CH, CR1, O, S, N, NH o NR1, según lo permita la valencia;
X4 es C o N;
X5 es un enlace, CH, CR1, O, S, N, NH o NR1, según lo permita la valencia;
X6 es CH, CR1, O, S, N, NH o NR1, según lo permita la valencia;
Y1 es C o N;
Y2 es C o N;
Y3 es CH, CR2, O, S, N, NH o NR2, según lo permita la valencia;
Y4 es un enlace, CH, CR2, O, S, N, NH o NR2, según lo permita la valencia;
Y5 es CH, CR2, O, S, N, NH o NR2, según lo permita la valencia;
Y6 es CH, CR2, O, S, N, NH o NR2, según lo permita la valencia,
siempre que el anillo que comprende X1, X2, X3, X4, X5 y X6 sea aromático, y
que el anillo que comprende Y1, Y2, Y3, Y4, Y5 e Y6 sea aromático;
y en donde L, M, R1, R2, R5, Ra, Rb, Rc, Rd, Re, Rf, Rg y Rh son todos anterior.
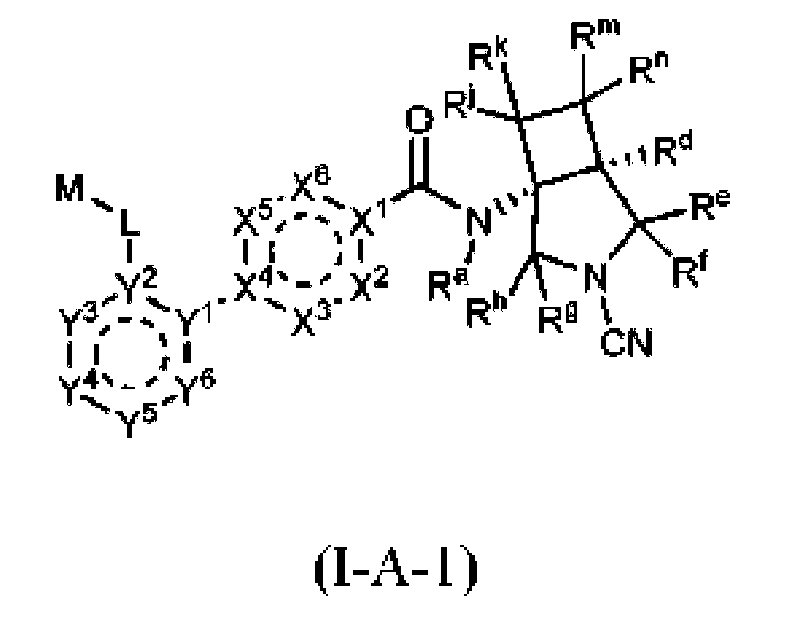
En algunas realizaciones, la presente divulgación proporciona compuestos, o sales farmacéuticamente aceptables de los mismos, de fórmula (I-A-1):
la fórmula (IA) anterior, y
en donde cada uno de Rj, Rk, Rm y Rn es independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo
C1-C3.
En algunas realizaciones, la presente divulgación proporciona compuestos, o sales farmacéuticamente aceptables de los mismos, de fórmula (I-A-2):
en donde M, L, X1, X2, X3, X4, X5, X6, Y1, Y2, Y3, Y4, Y5, Y6, Ra, Rd, Re, Rf la fórmula (I-A) anterior, y
en donde cada uno de Rj y Rk es independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3.
En algunas realizaciones, la presente divulgación proporciona compuestos, o sales farmacéuticamente aceptables de los mismos, de fórmula (I-A-3):
en donde M, L, X1, X2, X3, X4, X5, X6, Y1, Y2, Y3, Y4, Y5, Y6, Ra, Rd, Re, Rf, Rg y Rh son todos como se definen para la fórmula (I-A) anterior, y
en donde cada uno de Rj, Rk, Rm, Rn, Ro y Rp son independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1 -C3.
En algunas realizaciones, la presente divulgación proporciona compuestos, o sales farmacéuticamente aceptables de los mismos, de fórmula (I-A-4):
en donde Rq y Rr son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3.
En otro aspecto, la divulgación se refiere a un compuesto de fórmula (I-B):
o una sal farmacéuticamente aceptable del mismo, en donde:
Y3 es CH, CR2 o N;
Y4 es CH, CR2 o N;
Y5 es CH, CR2 o N;
Y6 es CH, CR2 o N; y
en donde X1, X2, X3, X4, X6, L, M, Ra, Rb, Rc, Rd, Re, Rf, Rg y Rh son todos como se definen para la fórmula (I) anterior.
En algunas realizaciones, la presente divulgación proporciona compuestos, o sales farmacéuticamente aceptables de los mismos, de fórmula (I-B-1):
en donde M, L, X1, X2, X3, X4, X6, Y3, Y4, Y5, Y6, Ra, Rd, Re, Rf, Rg y Rh son todos co (I-B) anterior, y
en donde cada uno de Rj, Rk, Rm y Rn es independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo
C1-C3.
En algunas realizaciones, la presente divulgación proporciona compuestos, o sales farmacéuticamente aceptables de los mismos, de fórmula (I-B-2):
en donde M, L, X1, X2, X3, X4, X6, Y3, Y4, Y5, Y6, Ra, Rd, Re, Rf, Rg y Rh son t (I-B) anterior, y
en donde cada uno de Rj y Rk es independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3.
En algunas realizaciones, la presente divulgación proporciona compuestos, o sales farmacéuticamente aceptables de los mismos, de fórmula (I-B-3):
en donde M, L, X1, X2, X3, X4, X6, Y3, Y4, Y5, Y6, Ra, Rd, Re, Rf, Rg y Rh son tod (I-B) anterior, y
en donde cada uno de Rj, Rk, Rm, Rn, Ro y Rp son independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3.
En algunas realizaciones, la presente divulgación proporciona compuestos, o sales farmacéuticamente aceptables de los mismos, de fórmula (I-B-4):
en donde M, L, X1, X2, X3, X4, X6, Y3, Y4, Y5, Y6, Ra, Rd, Re, Rf, Rg y Rh s (I-B) anterior, y
en donde Rq y Rr son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3.
En otro aspecto, la divulgación se refiere a un compuesto de fórmula (I-C):
o una sal farmacéuticamente aceptable del mismo, en donde R2, R5, n, p, Ra, Rb, Rc, Rd, Re, Rf, Rg y Rh son todos
como se define para la fórmula (I) anterior.
En algunas realizaciones, la presente divulgación proporciona compuestos, o sales farmacéuticamente aceptables de los mismos, de fórmula (I-C-1):
en donde R2, R5, n, p, Ra, Rd, Re, Rf, Rg y Rh son todos como se definen para la fórmula (I-C) anterior, y
en donde cada uno de Rj, Rk, Rm y Rn es independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo
C1-C3.
En algunas realizaciones, la presente divulgación proporciona compuestos, o sales farmacéuticamente aceptables de los mismos, de fórmula (I-C-2):
en donde R2, R5, n, p, Ra, Rd, Re, Rf, Rg y Rh son todos como se definen para la fórmula (I-C) anterior, y en donde cada uno de Rj y Rk es independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3.
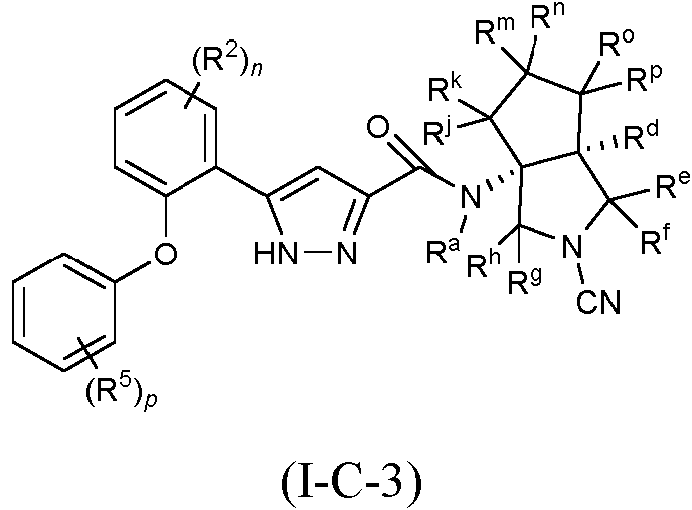
En algunas realizaciones, la presente divulgación proporciona compuestos, o sales farmacéuticamente aceptables de los mismos, de fórmula (I-C-3):
en donde R2, R5, n, p, Ra, Rd, Re, Rf, Rg y Rh son todos como se definen para la fórmula (I-C) anterior, y en donde cada uno de Rj, Rk, Rm, Rn, Ro y Rp son independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3.
En algunas realizaciones, la presente divulgación proporciona compuestos, o sales farmacéuticamente aceptables de los mismos, de fórmula (I-C-4):
en donde R2, R5, n, p, Ra, Rb, Rd, Rf, Rg y Rh son todos como se definen para la fórmula (I-C) anterior, y en donde Rq y Rr son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I-C), o una sal farmacéuticamente aceptable del mismo, en donde el compuesto es de fórmula (I-C-a):
en donde R2, R5, n y p son todos como se define para la fórmula (I-C) anterior.
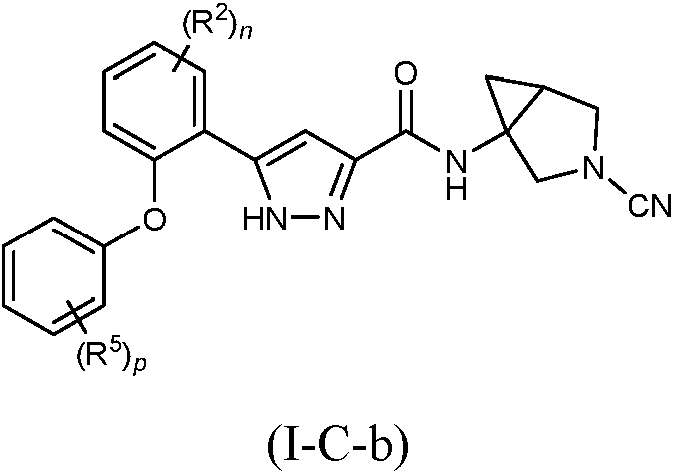
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I-C), o una sal farmacéuticamente aceptable del mismo, en donde el compuesto es de fórmula (I-C-b):
en donde R2, R5, n y p son todos como se define para la fórmula (I-C) anterior.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I-C), o una sal farmacéuticamente aceptable del mismo, en donde el compuesto es de fórmula (I-C-c):
en donde R2, R5, n y p son todos como se define para la fórmula (I-C) anterior.
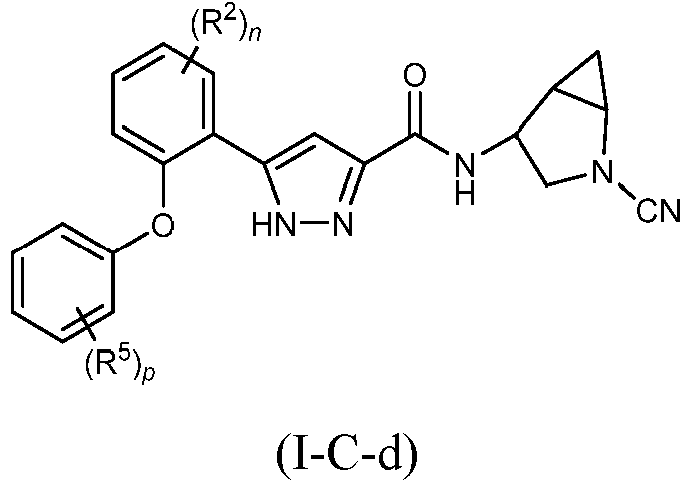
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I-C), o una sal farmacéuticamente aceptable del mismo, en donde el compuesto es de fórmula (I-C-d):
en donde R2, R5, n y p son todos como se define para la fórmula (I-C) anterior.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I-C), o una sal farmacéuticamente aceptable del mismo, en donde el compuesto es de fórmula (I-C-e):
en donde R2, R5, n y p son todos como se define para la fórmula (I-C) anterior.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I-C), o una sal farmacéuticamente aceptable del mismo, en donde el compuesto es de fórmula (I-C-f):
en donde R2, R5, n y p son todos como se define para la fórmula (I-C) anterior.
En otro aspecto, la divulgación se refiere a un compuesto de fórmula (I-D):
o una sal farmacéuticamente aceptable del mismo, en donde Ra, Rb, Rc, Rd, Re, Rf, Rg y Rh son todos como se definen para la fórmula (I) anterior.
En otro aspecto, la divulgación se refiere a un compuesto de fórmula (I-E):
o una sal farmacéuticamente aceptable del mismo, en donde Ra, Rb, Rc, Rd, Re, Rf y Rg son todos como se definen para la fórmula (I) anterior. En algunas realizaciones, la presente divulgación proporciona compuestos, o sales farmacéuticamente aceptables de los mismos, de fórmula (I-E-1):
En algunas realizaciones, el compuesto de fórmula (I-E-1) tiene la estereoquímica absoluta del primer isómero en eluir cuando se separa una mezcla racémica del compuesto de fórmula (I-E-1) mediante el procedimiento descrito en el Ejemplo 3, Paso 6. En algunas realizaciones, el compuesto de fórmula (I-E-1) tiene la estereoquímica absoluta del segundo isómero en eluir cuando se separa una mezcla racémica del compuesto de fórmula (I-E-1) mediante el procedimiento descrito en el Ejemplo 3, Paso 6.
En algunas realizaciones, el compuesto de fórmula (I-E-1) es:
En algunas realizaciones, el compuesto de fórmula (I-E-1) es:
En algunas realizaciones, la presente divulgación proporciona compuestos, o sales farmacéuticamente aceptables de los mismos, de fórmula (I-E-2):
En algunas realizaciones, el compuesto de fórmula (I-E-2) tiene la estereoquímica absoluta del primer isómero en eluir cuando se separa una mezcla racémica del compuesto de fórmula (I-E-2) mediante el procedimiento divulgado en el Ejemplo 4, Paso 6. En algunas realizaciones, el compuesto de fórmula (I-E-2) tiene la estereoquímica absoluta del segundo isómero en eluir cuando se separa una mezcla racémica del compuesto de fórmula (I-E-2) mediante el procedimiento descrito en el Ejemplo 4, Paso 6.
En algunas realizaciones, el compuesto de fórmula (I-E-2) es:
En algunas realizaciones; el compuesto de formula (I-E-2) es:
En algunas realizaciones, la presente divulgación proporciona compuestos, o sales farmacéuticamente aceptables de los mismos, de fórmula (I-E-3):
En algunas realizaciones, el compuesto de fórmula (I-E-3) tiene la estereoquímica absoluta del primer isómero en eluir cuando se separa una mezcla racémica del compuesto de fórmula (I-E-3) mediante el procedimiento descrito en el Ejemplo 2, Paso 7. En algunas realizaciones, el compuesto de fórmula (I-E-3) tiene la estereoquímica absoluta del segundo isómero en eluir cuando se separa una mezcla racémica del compuesto de fórmula (I-E-3) mediante el procedimiento descrito en el Ejemplo 2, Paso 7.
En algunas realizaciones, el compuesto de fórmula (I-E-3) es:
En algunas realizaciones, el compuesto de fórmula (I-E-3) es:
En algunas realizaciones, la presente divulgación proporciona compuestos, o sales farmacéuticamente aceptables de los mismos, de fórmula (I-E-4):
En algunas realizaciones, el compuesto de fórmula (I-E-4) tiene la estereoquímica absoluta del primer isómero en eluir cuando se separa una mezcla racémica del compuesto de fórmula (I-E-4) mediante el procedimiento descrito en el Ejemplo 2, Paso 7. En algunas realizaciones, el compuesto de fórmula (I-E-4) tiene la estereoquímica absoluta del segundo isómero en eluir cuando se separa una mezcla racémica del compuesto de fórmula (I-E-4) mediante el procedimiento descrito en el Ejemplo 2, Paso 7.
En algunas realizaciones, el compuesto de fórmula (I-E-4) es:
En algunas realizaciones, el compuesto de fórmula (I-E-4) es:
En otro aspecto, la divulgación se refiere a un compuesto de fórmula (I-F-1) o (I-F-2):
o una sal farmacéuticamente aceptable del mismo, en donde X1, X2, X3, X4, X5, X6, Y1, Y2, Y3, Y4, Y5, Y6, L y M son todos como se define para la fórmula (I-A) anterior.
En algunas realizaciones, los compuestos de fórmula (I-F-1) y (I-F-2) están presentes en una mezcla racémica. En otras realizaciones, el compuesto de fórmula (I-F-1) o (I-F-2) está presente en forma sustancialmente enantioméricamente pura. Los compuestos de fórmula (I-F-1) y (I-F-2) pueden separarse entre sí mediante HPLC quiral, como mediante el procedimiento descrito en el Ejemplo 2, Paso 7 o el Ejemplo 3, Paso 6.
En otro aspecto, la divulgación se refiere a un compuesto de fórmula (I-G-1) o (I-G-2):
o una sal farmacéuticamente aceptable del mismo, en donde X1, X2, X3, X4, X5, X6, Y1, Y2, Y3, Y4, Y5, Y6, L y M son todos como se define para la fórmula (I-A) anterior.
En algunas realizaciones, los compuestos de fórmula (I-G-1) e (I-G-2) están presentes en una mezcla racémica. En otras realizaciones, el compuesto de fórmula (I-G-1) o (I-G-2) está presente en forma sustancialmente enantioméricamente pura. Los compuestos de fórmula (I-G-1) y (I-G-2) pueden separarse entre sí mediante HPLC quiral, como mediante el procedimiento descrito en el Ejemplo 2, Paso 7, o el Ejemplo 4, Paso 6.
En otro aspecto, la divulgación se refiere a un compuesto de fórmula (I-H-1) o (I-H-2):
o una sal farmacéuticamente aceptable del mismo, en donde X1, X2, X3, X4, X5, X6, Y1, Y2, Y3, Y4, todos como se define para la fórmula (I-A) anterior.
En algunas realizaciones, los compuestos de fórmula (I-H-1) e (I-H-2) están presentes en una mezcla racémica. En otras realizaciones, el compuesto de fórmula (I-H-1) o (I-H-2) está presente en forma sustancialmente enantioméricamente pura. Los compuestos de fórmula (I-H-1) y (I-H-2) pueden separarse entre sí mediante HPLC quiral, como mediante el procedimiento descrito en el Ejemplo 2, Paso 7.
En otro aspecto, la divulgación se refiere a un compuesto de fórmula (I-J-1) o (I-J-2):
o una sal farmacéuticamente aceptable del mismo, en donde X1, X2, X3, X4, X5, X6, Y1, Y2, Y3, todos como se define para la fórmula (I-A) anterior.
En algunas realizaciones, los compuestos de fórmula (I-J-1) y (I-J-2) están presentes en una mezcla racémica. En otras realizaciones, el compuesto de fórmula (I-J-1) o (I-J-2) está presente en forma sustancialmente enantioméricamente pura. Los compuestos de fórmula (I-J-1) y (I-J-2) pueden separarse entre sí mediante HPLC quiral, como mediante el procedimiento descrito en el Ejemplo 2, Paso 7.
En algunas realizaciones, la presente divulgación proporciona compuestos, o sales farmacéuticamente aceptables de los mismos, de fórmula (I-K-1) o (I-K-2):
en donde M, L, X1, X2, X3, X4, X5, X6, Y1, Y2, Y3, Y4, Y5 e Y6 son todos como se definen para la fórmula (I-A) anterior.
En algunas realizaciones, la presente divulgación proporciona compuestos, o sales farmacéuticamente aceptables de los mismos, de fórmula (I-L-1) o (I-L-2):
en donde M, L, X1, X2, X3, X4, X5, X6, Y1, Y2, Y3, Y4, Y5 e Y6 son todos como se definen para la fórmu En algunas realizaciones, la presente divulgación proporciona compuestos, o sales farmacéuticamente aceptables de los mismos, de fórmula (I-M):
en donde M, L, X1, X2, X3, X4, X5, X6, Ra, Rb, Rc, Rd, Re, Rf, Rg y Rh son todos como se ha definido para las fórmulas
(I) y (I-A) anteriores.
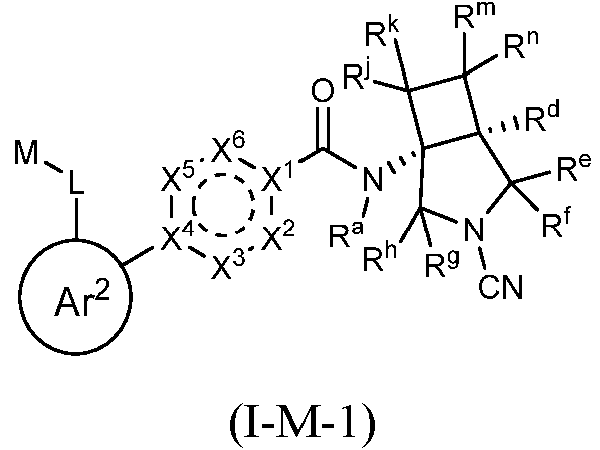
En algunas realizaciones, la presente divulgación proporciona compuestos, o sales farmacéuticamente aceptables de los mismos, de fórmula (I-M-1):
en donde M, L, X1, X2, X3, X4, X5, X6, Ra, Rd, Re, Rf, Rg y Rh son todos como se definen para la fórmula (I-M) anterior, y
en donde cada uno de Rj, Rk, Rm y Rn es independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo
C1-C3.
o En algunas realizaciones, la presente divulgación proporciona compuestos, o sales farmacéuticamente aceptables de los mismos, de fórmula (I-M-2):
en donde M, L, X1, X2, X3, X4, X5, X6, Ra, Rd, Re, Rf, Rg y Rh son todos como se definen para la fórmula (I-M) anterior, y
en donde cada uno de Rj y Rk es independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3.
En algunas realizaciones, la presente divulgación proporciona compuestos, o sales farmacéuticamente aceptables de los mismos, de fórmula (I-M-3):
en donde M, L, X1, X2, X3, X4, X5, X6, Ra, Rd, Re, Rf, Rg y Rh son todos como se definen para la fórmula (I-M)
arriba, y
en donde cada uno de Rj, Rk, Rm, Rn, Ro y Rp son independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1 -C3.
En algunas realizaciones, la presente divulgación proporciona compuestos, o sales farmacéuticamente aceptables de los mismos, de fórmula (I-M-4):
en donde M, L, X1, X2, X3, X4, X5, X6, Ra, Rb, Rd, Rf, Rg y Rh son t (I-M) anterior, y
en donde Rq y Rr son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I), (I-1), (I-2), (I-3) o (I-4), o
una sal farmacéuticamente aceptable del mismo, en donde Ar1 es independientemente fenileno o heteroarileno de 5
6 miembros, en donde dicho fenileno o heteroarileno está sustituido con m grupos R1. En algunas realizaciones, Ar1 es fenileno sustituido con m grupos R1 En algunas realizaciones, Ar1 es fenileno sustituido con 1-2 grupos R1 seleccionados del grupo que consiste en halo, ciano, hidroxilo, alquilo C1-C6, alcoxi C1-C6, haloalquilo C1-C6 e hidroxialquilo C1-C6. En algunas realizaciones, Ar1 es fenileno. En algunas realizaciones, Ar1 es heteroarileno de 5-6 miembros sustituido con m grupos R1. En algunas realizaciones, Ar1 es heteroarileno de 5-6 miembros sustituido con
1-2 grupos R1 seleccionados del grupo que consiste en halo, ciano, hidroxilo, alquilo C1-C6, alcoxi C1-C6, alcoxi C1-C6 haloalquilo e hidroxialquilo C1-C6. En algunas realizaciones, Ar1 es heteroarileno de 5 miembros sustituido con m grupos R1. En algunas realizaciones, Ar1 es pirazol. En algunas realizaciones, Ar1 es tiazol. En algunas realizaciones, Ar1 es heteroarileno de 6 miembros sustituido con m grupos R1.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I), (I-1), (I-2), (I-3), (I-4), (IM), (IM-1), (IM-2), (IM-3) o (IM-4), o una sal farmacéuticamente aceptable del mismo, en donde Ar2 es independientemente fenileno o heteroarileno de 5-10 miembros, en donde dicho fenileno o heteroarileno está sustituido con n grupos R2 En algunas realizaciones, Ar2 es fenileno o heteroarileno de 5-6 miembros, en donde dicho fenileno o heteroarileno está sustituido con n grupos R2 En algunas realizaciones, Ar2 es fenileno sustituido con n grupos R2 En algunas realizaciones, Ar2 es fenileno sustituido con 1-2 grupos R2 seleccionados del grupo que consiste en halo, ciano, hidroxilo, alquilo C1-C6 , alcoxi C1-C6 , haloalquilo C1-C6 e hidroxialquilo C1-C6. En algunas realizaciones, Ar2 es fenileno. En algunas realizaciones, Ar2 es heteroarileno de 5-10 miembros sustituido con n grupos R2. En algunas realizaciones, Ar2 es heteroarileno de 5-6 miembros sustituido con n grupos R2. En algunas realizaciones, Ar2 es heteroarileno de 5-6 miembros sustituido con 1-2 grupos R2 seleccionados del grupo que consiste en halo, ciano, hidroxilo, alquilo C1-C6, alcoxi C1-C6, haloalquilo C1-C6 y e hidroxialquilo C1-C6. En algunas realizaciones, Ar2 es heteroarileno de 5 miembros sustituido con n grupos R2. En algunas realizaciones, Ar2 es heteroarileno de 6 miembros sustituido con n grupos R2. En algunas realizaciones, Ar2 es piridina. En algunas realizaciones, Ar2 es heteroarileno de 7 miembros sustituido con n grupos R2. En algunas realizaciones, Ar2 es heteroarileno de 8 miembros sustituido con n grupos R2. En algunas realizaciones, Ar2 es heteroarileno de 9 miembros sustituido con n grupos R2. En algunas realizaciones, Ar2 es heteroarileno de 10 miembros sustituido con n grupos R2.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula(I), (I-1), (I-2), (I-3), (I-4), (I-A), (I-A-1), (I-A-2), (I-A-3), (I-A-4), (I-B), (I-B-1), (I-B-2), (I-B-3), (I-B-4), (IF-1), (I-F-2), (I-G-1), (I-G-2), (I-H-1), (I-H-2), (I-J-1), (I-J-2), (I-K-1), (I-K-2), (I-L-1), (I-L-2), (I-M), (I-M-1), (I-M-2), (I-M-3), o (I-M-4), o una sal farmacéuticamente aceptable del mismo, en donde L es -O-, -S-, -NR3-,-C(R4)2-, -S(O)2-, o -S(O)-. En algunas realizaciones, L es -O-, -S- o -NH-. En algunas realizaciones, L es -O-. En algunas realizaciones, L es -S-. En algunas realizaciones, L es -NR3-. En algunas realizaciones, L es -NH-. En algunas realizaciones, L es -C(R4)2-. En algunas realizaciones, L es -CH2-. En algunas realizaciones, L es -S(O)2-. En algunas realizaciones, L es -S(O)-.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I), (I-1), (I-2), (I-3), (I-4), (I-A), (I-A-1), (I-A-2), (I-A-3), (I-A-4), (I-B), (I-B-1), (I-B-2), (I-B-3), (I-B-4), (IF-1), (I-F-2), (I-G-1), (I-G-2), (I-H-1), (I-H-2), (I-J-1), (I-J-2), (I-K-1), (I-K-2), (I-L-1), (I-L-2), (I-M), (I-M-1), (I-M-2), (I-M-3), o (I-M-4), o una sal farmacéuticamente aceptable del mismo, en donde M es cicloalquilo de 3-6 miembros, fenilo o heteroarilo de 5-6 miembros, en donde dicho cicloalquilo, fenilo o heteroarilo está sustituido con p grupos R5. En algunas realizaciones, M es cicloalquilo de 3-6 miembros sustituido con p grupos R5. En algunas realizaciones, M es cicloalquilo de 3-6 miembros. En algunas realizaciones, M es cicloalquilo de 3-6 miembros sustituido con 1-2 grupos R5 seleccionados del grupo que consiste en halo, ciano, hidroxilo, alquilo C1-C6 , haloalquilo C1-C6 y hidroxialquilo C1-C6. En algunas realizaciones, M es fenilo sustituido con p grupos R5. En algunas realizaciones, M es fenilo. En algunas realizaciones, M es fenilo sustituido con 1-2 grupos R5 seleccionados del grupo que consiste en halo, ciano, hidroxilo, alquilo C1-C6 , haloalquilo C1-C6, alcoxi C1-C6 e hidroxialquilo C1-C6. En algunas realizaciones, M es fenilo sustituido con flúor. En algunas realizaciones, M es heteroarilo de 5-6 miembros sustituido con p grupos R5. En algunas realizaciones, M es heteroarilo de 5-6 miembros. En algunas realizaciones, M es heteroarilo de 5-6 miembros sustituido con 1-2 grupos R5 seleccionados del grupo que consiste en halo, ciano, hidroxilo, alquilo C1-C6 , alcoxi C1-C6, haloalquilo C1-C6 e hidroxialquilo C1-C6.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I), (I-1), (I-2), (I-3), (I-4), (I-A), (I-A-1), (I-A-2), (I-A-3), (I-A-4), (I-B), (I-B-1), (I-B-2), (I-B-3), (I-B-4), (I-C), (I-C-1), (LC-2), (LC-3), (I-C-4), (I-C-a), (I-C-b), (I-C-c), (I-C-d), (I-C-e), (LC-f), (LF-1), (IF-2), (I-G-1), (I-G-2), (LH-1), (LH-2), (I-J-1), (I-J-2), (I-K-1), (I-K-2), (I-L-1), (I-L-2), (I-M), (I-M-1), (I-M-2), (I-M-3), o (I-M-4), o una sal farmacéuticamente aceptable del mismo, en donde cada aparición de R1, R2 y R5 es independientemente halo, ciano, NO2 , oxo, hidroxilo, -R6, -OR6, alquilo C1-C6, haloalquilo C1-C6 , hidroxialquilo C1-C6 , -alquileno C1-C6-R6, alcoxi C1-C6 , haloalcoxi C1-C6 , -alquileno Cü-C3-NR6R7, -alquileno Cü-C3-NR7R8, -alquileno Cü-C3-C(O)NR6R7, -alquileno Cü-C3-C(O)NR7R8, -alquileno Cü-C3-NR7C(O)R6, -alquileno Co-C3-NR7C(O)R8, -alquileno C0-C3-NR7S(O)2R6, -alquileno C0-C3-C(O)R6, -alquileno C0-C3-C(O)R7, -alquileno C0-C3-SR6, -alquileno C0-C3-S(O)R6, -alquileno C0-C3-S(O)2R6, -alquileno C0-C3-S(O)2R7, -alquileno C0-C3 S(O)2NR6R7, -alquileno C0-C3-S(O)2NR7R8, -alquileno C0-C3-NR7C(O)NR8R9, -C0-C3 alquileno-NR7 S(O) 2 NR8 R9, -C0-C3 alquileno-C(O)OR7, -C0-C3 alquileno-C(O)OR6, -C0-C3 alquileno-OC(O)R7, -alquileno C0-C3-OC(O)R6, -alquileno C0-C3-NR7C(O)OR8, o -alquileno C0-C3-NR7S(O)2R8. En algunas realizaciones, cada aparición de R1 es independientemente halo, ciano, hidroxilo, alquilo C1-C6 , alcoxi C1-C6, haloalquilo C1-C6 e hidroxialquilo C1-C6. En algunas realizaciones, cada aparición de R1 es independientemente halo (por ejemplo, flúor, cloro, bromo o yodo). En algunas realizaciones, cada aparición de R1 es flúor. En algunas realizaciones, cada aparición de R1 es ciano. En algunas realizaciones, cada aparición de R1 es hidroxilo. En algunas realizaciones, cada aparición de R1 es alquilo C1-C6. En algunas realizaciones, cada aparición de R1 es alcoxi C1-C6. En algunas realizaciones, cada aparición de R1 es haloalquilo C1-C6. En algunas realizaciones, cada aparición de R1 es hidroxialquilo C1-C6. En algunas
realizaciones, cada aparición de R2 es independientemente halo, ciano, hidroxilo, alquilo C1-C6, alcoxi C1-C6 , haloalquilo C1-C6 e hidroxialquilo C1-C6. En algunas realizaciones, cada aparición de R2es independientemente halo
(por ejemplo, flúor, cloro, bromo o yodo). En algunas realizaciones, cada aparición de R2 es fluoro. En algunas realizaciones, cada aparición de R2 es ciano. En algunas realizaciones, cada aparición de R2 es hidroxilo. En algunas realizaciones, cada aparición de R2 es alquilo C1-C6. En algunas realizaciones, cada aparición de R2 es alcoxi C1-C6. En algunas realizaciones, cada aparición de R2 es haloalquilo C1-C6. En algunas realizaciones, cada aparición de R2 es hidroxialquilo C1-C6. En algunas realizaciones, cada aparición de R5 es independientemente halo, ciano, hidroxilo, alquilo C1-C6, alcoxi C1-C6, haloalquilo C1-C6 e hidroxialquilo C1-C6. En algunas realizaciones, cada aparición de R5 es independientemente halo (por ejemplo, flúor, cloro, bromo o yodo). En algunas realizaciones, cada aparición de R5 es fluoro. En algunas realizaciones, cada aparición de R5 es ciano. En algunas realizaciones, cada aparición de R5 es hidroxilo. En algunas realizaciones, cada aparición de R5 es alquilo C1-C6. En algunas realizaciones, cada aparición de R5 es alcoxi C1-C6. En algunas realizaciones, cada aparición de R5 es haloalquilo
C1-C6. En algunas realizaciones, cada aparición de R5 es hidroxialquilo C1-C6.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I), (I-1), (I-2), (I-3), (I-4), (I-A), (I-A-1), (I-A-2), (I-A-3), (I-A-4), (I-B), (I-B-1), (I-B-2), (I-B-3), (I-B-4), (IF-1), (I-F-2), (I-G-1), (I-G-2), (I-H-1), (I-H-2),
(I-J-1), (I-J-2), (I-K-1), (I-K-2), (I-L-1), (I-L-2), (I-M), (I-M-1), (I-M-2), (I-M-3), o (I-M-4), o una sal aceptable farmacéutico del mismo, en donde R3 es H, alquilo C1-C6 o haloalquilo C1-C6. En algunas realizaciones, R3 es H. En algunas realizaciones, R3 es alquilo C1-C6. En algunas realizaciones, R3 es haloalquilo C1-C6.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I), (I-1), (I-2), (I-3), (I-4), (I-A), (I-A-1), (I-A-2), (I-A-3), (I-A-4), (I-B), (I-B-1), (I-B-2), (I-B-3), (I-B-4), (IF-1), (I-F-2), (I-G-1), (I-G-2), (LH-1), (I-H-2),
(I-J-1), (I-J-2), (I-K-1), (I-K-2), (I-L-1), (I-L-2), (I-M), (I-M-1), (I-M-2), (I-M-3), o (I-M-4), o una sal aceptable farmacéutico del mismo, en donde cada R4 es independientemente H, alquilo C1-C6 o haloalquilo C1-C6, o dos grupos R4 junto con el átomo de carbono al que están unidos forman un cicloalquilo o heterocicloalquilo de 3-6 miembros. En algunas realizaciones, cada R4 es H. En algunas realizaciones, dos grupos R4 junto con el átomo de carbono al que están unidos forman un cicloalquilo de 3 a 6 miembros. En algunas realizaciones, dos grupos R4 junto con el átomo de carbono al que están unidos forman un heterocicloalquilo de 3 a 6 miembros.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I), (I-1), (I-2), (I-3), (I-4), (I-A), (I-A-1), (I-A-2), (I-A-3), (I-A-4), (I-B), (I-B-1), (I-B-2), (I-B-3), (I-B-4), (I-C), (I-C-1), (LC-2), (LC-3), (LC-4), (LC-a),
(LC-b), (I-C-c), (I-C-d), (I-C-e), (I-C-f), (LF-1), (IF-2), (I-G-1), (I-G-2), (I-H-1), (I-H-2), (I-J-1), (I-J-2), (I-K-1), (I-K-2),
(LL-1), (I-L-2), (I-M), (I-M-1), (I-M-2), (i-M-3), o (i-M-4), o una sal farmacéuticamente aceptable del mismo, en donde cada R6 es heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, arilo de 6-10 miembros o cicloalquilo de 3-8 miembros, en donde dicho heteroarilo, heterocicloalquilo, arilo o cicloalquilo está opcionalmente sustituido con
1-5 sustituyentes seleccionados independientemente del grupo que consiste en halo, oxo, alquilo C1-C6, haloalquilo
C1-C6 , hidroxialquilo C1-C6, alcoxi C1-C6, haloalcoxi C1-C6, alquenilo C2-C6 6, alquinilo C2-C6 6, heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, arilo de 6-10 miembros, cicloalquilo de 3-8 miembros, -NR10C(O)NR11R12, -NR10R11, -C(O)R10, - NR10C(O)R11, -NR10C(O)OR11, -S(O)2R10, -C(O)NR10R11, -C(O)OR10, -S(O)2NR10R11, - NR10S(O)2R11, -OR10, -OC(O)R10, -OS(O)2R10, -OC(O)NR10R11, -OC(O)OR10, -OS(O)2NR10R11, -C(O)NR10C(O)NR11R12, -C(O)C(O)R10, -C(O)NR10C(O)R11, -C(O)NR10C(O)OR11, - C(O)S(O)2R10, -C(O)C(O)NR10R11, -C(O)C(O)OR10, -C(O)S(O)2NR10R11, -C(O)NR10S(O)2R11, -alquileno C1-C6-R10, -alquileno C1-C6-NR10C(O)NR11R12, -alquileno C1-C6-NR10R11, -alquileno C1-C6-C(O)R10, -alquileno C1-C6-NR10C(O)R11, -alquileno C1-C6-NR10C(O)OR11, -alquileno C1-C6-S(O)2R10, -alquileno C1-C6-C(O)NR10R11, -alquileno C1-C6-C(O)OR10, -alquileno C1-C6 S(O)2NR10R11, -alquileno C1-C6-NR10S(O)2R11, -alquenileno C1-C6-R10, -alquenileno C1-C6-NR10C(O)NR11R12, -alquenileno C1-C6-NR10R11, -alquenileno C1-C6-C(O)R10, -alquenileno C1-C6-NR10C(O)R11, -alquenileno C1-C6-NR10C(O)OR11, -alquenileno C1-C6-S(O)2R10, -alquenileno C1-C6-C(O)NR10R11, -alquenileno C1-C6-C(O)OR10, -alquenileno C1-C6-S(O)2NR10R11, y -alquenileno C1-C6-NR10S(O)2R11. En algunas realizaciones, cada R6 es heteroarilo de 5-10 miembros opcionalmente independientemente sustituido. En algunas realizaciones, cada R6 es heterocicloalquilo de
4-10 miembros opcionalmente independientemente sustituido. En algunas realizaciones, cada R6 es arilo de 6-10 miembros opcionalmente independientemente sustituido. En algunas realizaciones, cada R6 es cicloalquilo de 3-8 miembros opcionalmente independientemente sustituido.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I), (I-1), (I-2), (I-3), (I-4), (I-A), (I-A-1), (I-A-2), (I-A-3), (I-A-4), (I-B), (I-B-1), (I-B-2), (I-B-3), (I-B-4), (I-C), (I-C-1), (I-C-2), (LC-3), (I-C-4), (I-C-a), (I-C-b), (I-C-c), (I-C-d), (I-C-e), (I-C-f), (LF-1), (IF-2), (I-G-1), (I-G-2), (I-H-1), (I-H-2), (I-J-1), (I-J-2), (I-K-1), (I-K-2), (I-L-1), (I-L-2), (I-M), (I-M-1), (I-M-2), (I-M-3), o (I-M-4), o una sal farmacéuticamente aceptable del mismo, en donde cada
R7, R8 y R9 es independientemente hidrógeno o alquilo C1-C6. En algunas realizaciones, cada R7, R8 independientemente hidrógeno.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I), (I-1), (I-2), (I-3), (I-4), (I-A), (I-A-1), (I-A-2), (I-A-3), (I-A-4), (I-B), (I-B-1), (I-B-2), (I-B-3), (I-B-4), (I-C), (I-C-1), (I-C-2), (LC-3), (LC-4), (I-C-a),
(LC-b), (I-C-c), (I-C-d), (I-C-e), (I-C-f), (LF-1), (IF-2), (I-G-1), (I-G-2), (I-H-1), (I-H-2), (I-J-1), (I-J-2), (I-K-1), (I-K-2),
(LL-1), (I-L-2), (I-M), (I-M-1), (I-M-2), (i-M-3), o (i-M-4), o una sal farmacéuticamente aceptable del mismo, en donde cada R10, R11 y R12 es independientemente hidrógeno, alquilo C1-C6, heteroarilo de 5-10 miembros,
heterocicloalquilo de 4-10 miembros, arilo de 6-10 miembros o cicloalquilo de 3-8 miembros. En algunas realizaciones, cada R10, R11 y R12 es independientemente hidrógeno.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I), (I-1), (I-2), (I-3) o (I-4), o una sal farmacéuticamente aceptable del mismo, en donde m es 0-4 (es decir, m es 0, 1, 2, 3 o 4). En algunas realizaciones, m es 0. En algunas realizaciones, m es 1. En algunas realizaciones, m es 2. En algunas realizaciones, m es 3. En algunas realizaciones, m es 4. En algunas realizaciones, m es 0, 1, o 2. En algunas realizaciones, m es 1 o 2.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I), (I-1), (I-2), (I-3), (I-4), (I-C), (I-C-1), (I-C-2), (I-C-3), (I-C-4), (I-C-a), (I-C-b), (I-C-c), (I-C-d), (I-C-e), (I-C-f), (I-M), (I-M-1), (I-M-2), (I-M-3), o (I-M-4), o una sal farmacéuticamente aceptable del mismo, en donde n es 0-4 (es decir, n es 0, 1, 2, 3 o 4). En algunas realizaciones, n es 0. En algunas realizaciones, n es 1. En algunas realizaciones, n es 2. En algunas realizaciones, n es 3. En algunas realizaciones, n es 4. En algunas realizaciones, n es 0, 1, o 2. En algunas realizaciones, n es 1 o 2.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I), (I-1), (I-2), (I-3), (I-4), (I-A), (I-A-1), (I-A-2), (I-A-3), (I-A-4), (I-B), (I-B-1), (I-B-2), (I-B-3), (I-B-4), (I-C), (I-C-1), (I-C-2), (I-C-3), (LC-4), (I-C-a), (I-C-b), (I-C-c), (I-C-d), (I-C-e), (I-C-f), (LF-1), (IF-2), (I-G-1), (I-G-2), (I-H-1), (I-H-2), (I-J-1), (I-J-2), (I-K-1), (I-K-2), (LL-1), (I-L-2), (I-M), (I-M-1), (I-M-2), (I-M-3), o (I-M-4), o una sal farmacéuticamente aceptable del mismo, en donde p es 0-4 (es decir, p es 0, 1, 2, 3 o 4). En algunas realizaciones, p es 0. En algunas realizaciones, p es 1. En algunas realizaciones, p es 2. En algunas realizaciones, p es 3. En algunas realizaciones, p es 4. En algunas realizaciones, p es 0, 1 o 2. En algunas realizaciones, p es 1 o 2. En algunas realizaciones, n y p son ambos 0. En algunas realizaciones, m y n son ambos 0. En algunas realizaciones, m y n son ambos 0. En algunas realizaciones, m, n y p son 0. En algunas realizaciones, m y n son 0 y p es 1.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I), (I-A), (I-B), (I-C), (I-D), (I-E) o (I-M), o una sal farmacéuticamente aceptable del mismo, en donde Ra y Rb forman un grupo alquileno C1-C4 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C4 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3. En algunas realizaciones, Ra y Rb forman un grupo alquileno C1-C4 entre los átomos a los que están unidos; y Rc, Rd, Re, Rf, Rg y Rh son cada uno hidrógeno. En algunas realizaciones, Ra y Rb forman un grupo alquileno C1 entre los átomos a los que están unidos; y Rc, Rd, Re, Rf, Rg y Rh son cada uno hidrógeno. En algunas realizaciones, Ra y Rb forman un grupo alquileno C2 entre los átomos a los que están unidos; y Rc, Rd, Re, Rf, Rg y Rh son cada uno hidrógeno. En algunas realizaciones, Ra y Rb forman un grupo alquileno C3 entre los átomos a los que están unidos; y Rc, Rd, Re, Rf, Rg y Rh son cada uno hidrógeno. En algunas realizaciones, Ra y Rb forman un grupo alquileno C4 entre los átomos a los que están unidos; y Rc, Rd, Re, Rf, Rg y Rh son cada uno hidrógeno.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I), (I-A), (I-B), (I-C), (I-D), (I-E) o (I-M), o una sal farmacéuticamente aceptable del mismo, en donde Ra y Re forman un grupo alquileno C1-C2 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C2 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3. En algunas realizaciones, Ra y Re forman un grupo alquileno C1-C2 entre los átomos a los que están unidos; y cada uno de Rb, Rc, Rd, Rf, Rg y Rh es hidrógeno. En algunas realizaciones, Ra y Re forman un grupo alquileno C1 entre los átomos a los que están unidos; y cada uno de Rb, Rc, Rd, Rf, Rg y Rh es hidrógeno. En algunas realizaciones, Ra y Re forman un grupo alquileno C2 entre los átomos a los que están unidos, y Rb, Rc, Rd, Rf, Rg y Rh son cada uno hidrógeno.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I), (I-A), (I-B), (I-C), (I-D), (I-E) o (I-M), o una sal farmacéuticamente aceptable del mismo, en donde Ra y Rg forman un grupo alquileno C1-C3 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C3 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3. En algunas realizaciones, Ra y R8 forman un grupo alquileno C1-C3 entre los átomos a los que están unidos; y Rb, Rc, Rd, Re, Rf y Rh son cada uno hidrógeno. En algunas realizaciones, Ra y Rg forman un grupo alquileno C1 entre los átomos a los que están unidos; y Rb, Rc, Rd, Re, Rf y Rh son cada uno hidrógeno. En algunas realizaciones, Ra y Rg forman un grupo alquileno C2 entre los átomos a los que están unidos; y Rb, Rc, Rd, Re, Rf y Rh son cada uno hidrógeno. En algunas realizaciones, Ra y Rg forman un grupo alquileno C3 entre los átomos a los que están unidos; y Rb, Rc, Rd, Re, Rf y Rh son cada uno hidrógeno.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I), (I-A), (I-B), (I-C), (I-D), (I-E) o (I-M), o una sal farmacéuticamente aceptable del mismo, en donde Rb y Rc forman un grupo alquileno C1-C4 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C4 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3. En algunas realizaciones, Rb y Rc forman un grupo alquileno C1-C4 entre los átomos a los que están unidos; y Ra, Rd, Re, Rf, Rg y Rh son cada uno hidrógeno. En algunas realizaciones, Rb y Rc forman un grupo alquileno C1-C3 entre los átomos a los que están unidos; y Ra, Rd, Re, Rf, Rg y Rh son cada uno hidrógeno. En algunas realizaciones, Rb y Rc forman un grupo alquileno C1 entre los átomos a los que están unidos; y Ra, Rd, Re, Rf, Rg y Rh son cada uno hidrógeno. En algunas
realizaciones, Rb y Rb forman un grupo alquileno C2 entre los átomos a los que están unidos; y Ra, Rd, Re, Rf, Rg y Rh son cada uno hidrógeno. En algunas realizaciones, Rb y Rc forman un grupo alquileno C3 entre los átomos a los que están unidos; y Ra, Rd, Re, Rf, Rg y Rh son cada uno hidrógeno. En algunas realizaciones, Rb y alquileno C4 entre los átomos a los que están unidos; y Ra, Rd, Re, Rf, Rg y Rh son cada uno hidrógeno.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I), (I-A), (I-B), (I-C), (I-D), (I-E) o (I-M), o una sal farmacéuticamente aceptable del mismo, en donde Rb y Re forman un grupo alquileno C1-C3 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C3 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3. En algunas realizaciones, Rb y
Re forman un grupo alquileno C1-C3 entre los átomos a los que están unidos; y Ra, Rc, Rd, Rf, Rg y Rh son cada uno hidrógeno. En algunas realizaciones, Rb y Re forman un grupo alquileno C1 entre los átomos a los que están unidos;
y Ra, Rc, Rd, Rf, Rg y Rh son cada uno hidrógeno. En algunas realizaciones, Rb y Re forman un grupo alquileno C2 entre los átomos a los que están unidos; y Ra, Rc, Rd, Rf, Rg y Rh son cada uno hidrógeno. En algunas realizaciones,
Rb y Re forman un grupo alquileno C3 entre los átomos a los que están unidos; y Ra, Rc, Rd, Rf, Rg y Rh son cada uno hidrógeno.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I), (I-A), (I-B), (I-C), (I-D), (I-E) o (I-M), o una sal farmacéuticamente aceptable del mismo, en donde Rb y Rg forman un grupo alquileno C1-C4 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C4 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3. En algunas realizaciones, Rb y
R8 forman un grupo alquileno C1-C4 entre los átomos a los que están unidos; y Ra, Rc, Rd, Re, Rf y Rh son cada uno hidrógeno. En algunas realizaciones, Rb y Rg forman un grupo alquileno C1 entre los átomos a los que están unidos;
y Ra, Rc, Rd, Re, Rf y Rh son cada uno hidrógeno. En algunas realizaciones, Rb y Rg forman un grupo alquileno C2 entre los átomos a los que están unidos; y Ra, Rc, Rd, Re, Rf y Rh son cada uno hidrógeno. En algunas realizaciones,
Rb y Rg forman un grupo alquileno C3 entre los átomos a los que están unidos; y Ra, Rc, Rd, Re, Rf y Rh son cada uno hidrógeno. En algunas realizaciones, Rb y Rg forman un grupo alquileno C4 entre los átomos a los que están unidos;
y Ra, Rc, Rd, Re, Rf y Rh son cada uno hidrógeno.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I), (I-A), (I-B), (I-C), (I-D), (I-E) o (I-M), o una sal farmacéuticamente aceptable del mismo, en donde Rc y Rd junto con el átomo al que están unidos, forman un cicloalquilo o heterocicloalquilo de 3-6 miembros, en donde dicho cicloalquilo o heterocicloalquilo de 3-6 miembros está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 , y haloalquilo C1-C3. En algunas realizaciones, Rc y Rd junto con el átomo al que están unidos, forman un cicloalquilo o heterocicloalquilo de 3-6 miembros; y Ra, Rb, Re, Rf, Rg y Rh son cada uno hidrógeno. En algunas realizaciones, Rc y Rd junto con el átomo al que están unidos, forman un cicloalquilo de 3 miembros o un heterocicloalquilo de 4 miembros; y Ra, Rb, Re, Rf, Rg y Rh son cada uno hidrógeno. En algunas realizaciones, Rc y
Rd junto con el átomo al que están unidos forman un cicloalquilo de 3 a 6 miembros; y Ra, Rb, Re, Rf, Rg y Rh son cada uno hidrógeno. En algunas realizaciones, Rc y Rd junto con el átomo al que están unidos, forman un cicloalquilo de 3 miembros; y Ra, Rb, Re, Rf, Rg y Rh son cada uno hidrógeno. En algunas realizaciones, Rc y Rd junto con el átomo al que están unidos, forman un cicloalquilo de 4 miembros; y Ra, Rb, Re, Rf, Rg y Rh son cada uno hidrógeno.
En algunas realizaciones, Rc y Rd junto con el átomo al que están unidos, forman un cicloalquilo de 5 miembros; y
Ra, Rb, Re, Rf, Rg y Rh son cada uno hidrógeno. En algunas realizaciones, Rc y Rd junto con el átomo al que están unidos, forman un cicloalquilo de 6 miembros; y Ra, Rb, Re, Rf, Rg y Rh son cada uno hidrógeno. En algunas realizaciones, Rc y Rd junto con el átomo al que están unidos, forman un anillo heterocicloalquilo de 3-6 miembros; y
Ra, Rb, Re, Rf, Rg y Rh son cada uno hidrógeno. En algunas realizaciones, Rc y Rd junto con el átomo al que están unidos, forman un anillo heterocicloalquilo de 3-6 miembros, en donde el anillo heterocicloalquilo de 3-6 miembros contiene O, S o NH; y Ra, Rb, Re, Rf, Rg y Rh son cada uno hidrógeno. En algunas realizaciones, Rc y Rd junto con el átomo al que están unidos, forman un anillo heterocicloalquilo de 3 miembros; y Ra, Rb, Re, Rf, Rg y Rh son cada uno hidrógeno. En algunas realizaciones, Rc y Rd junto con el átomo al que están unidos, forman un anillo heterocicloalquilo de 4 miembros; y Ra, Rb, Re, Rf, Rg y Rh son cada uno hidrógeno. En algunas realizaciones, Rc y
Rd junto con el átomo al que están unidos forman un anillo de oxetano; y Ra, Rb, Re, Rf, Rg y Rh son cada uno hidrógeno. En algunas realizaciones, Rc y Rd junto con el átomo al que están unidos, forman un anillo heterocicloalquilo de 5 miembros; y Ra, Rb, Re, Rf, Rg y Rh son cada uno hidrógeno. En algunas realizaciones, Rc y
Rd junto con el átomo al que están unidos, forman un anillo heterocicloalquilo de 6 miembros; y Ra, Rb, Re, Rf, Rg y
Rh son cada uno hidrógeno. En algunas realizaciones, Rc y Rd juntos forman =O. En algunas realizaciones, Rc y Rd juntos forman =O; y Ra, Rb, Re, Rf, Rg y Rh son cada uno hidrógeno.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I), (I-A), (I-B), (I-C), (I-D), (I-E) o (I-M), o una sal farmacéuticamente aceptable del mismo, en donde Rc y Re forman un grupo alquileno C1-C4 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C4 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3. En algunas realizaciones, Rc y
Re forman un grupo alquileno C1-C4 entre los átomos a los que están unidos; y Ra, Rb, Rd, Rf, Rg y Rh son cada uno hidrógeno. En algunas realizaciones, Rc y Re forman un grupo alquileno C1 entre los átomos a los que están unidos;
y Ra, Rb, Rd, Rf, Rg y Rh son cada uno hidrógeno. En algunas realizaciones, Rc y Re forman un grupo alquileno C2 entre los átomos a los que están unidos; y Ra, Rb, Rd, Rf, Rg y Rh son cada uno hidrógeno. En algunas realizaciones,
Rc y Re forman un grupo alquileno C3 entre los átomos a los que están unidos; y Ra, Rb, Rd, Rf, Rg y Rh son cada uno hidrógeno. En algunas realizaciones, Rc y Re forman un grupo alquileno C4 entre los átomos a los que están unidos; y Ra, Rb, Rd, Rf, Rg y Rh son cada uno hidrógeno.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I), (I-A), (I-B), (I-C), (I-D), (I-E) o (I-M), o una sal farmacéuticamente aceptable del mismo, en donde Rc y Rg forman un grupo alquileno C1-C3 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C3 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3. En algunas realizaciones, Rc y R8 forman un grupo alquileno C1-C3 entre los átomos a los que están unidos; y Ra, Rb, Rd, Re, Rf y Rh son cada uno hidrógeno. En algunas realizaciones, Rc y Rg forman un grupo alquileno C1-C2 entre los átomos a los que están unidos; y Ra, Rb, Rd, Re, Rf y Rh son cada uno hidrógeno. En algunas realizaciones, Rc y Rg forman un grupo alquileno C1 entre los átomos a los que están unidos; y Ra, Rb, Rd, Re, Rf y Rh son cada uno hidrógeno. En algunas realizaciones, Rc y Rg forman un grupo alquileno C2 entre los átomos a los que están unidos; y Ra, Rb, Rd, Re, Rf y Rh son cada uno hidrógeno. En algunas realizaciones, Rc y Rg forman un grupo alquileno C3 entre los átomos a los que están unidos; y Ra, Rb, Rd, Re, Rf y Rh son cada uno hidrógeno.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I), (I-A), (I-B), (I-C), (I-D), (I-E) o (I-M), o una sal farmacéuticamente aceptable del mismo, en donde Re y Rf junto con el átomo al que están unidos, forman un cicloalquilo o heterocicloalquilo de 3-6 miembros, en donde dicho cicloalquilo o heterocicloalquilo de 3-6 miembros está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 , y haloalquilo C1-C3. En algunas realizaciones, Re y Rf junto con el átomo al que están unidos, forman un cicloalquilo o heterocicloalquilo de 3-6 miembros; y Ra, Rb, Rc, Rd, Rg y Rh son cada uno hidrógeno. En algunas realizaciones, Re y Rf junto con el átomo al que están unidos, forman un cicloalquilo de 3 a 6 miembros; y Ra, Rb, Rc, Rd, Rg y Rh son cada uno hidrógeno. En algunas realizaciones, Re y Rf junto con el átomo al que están unidos, forman un cicloalquilo de 3 miembros; y Ra, Rb, Rc, Rd, Rg, y Rh son cada uno hidrógeno. En algunas realizaciones, Re y Rf junto con el átomo al que están unidos, forman un cicloalquilo de 4 miembros; y Ra, Rb, Rc, Rd, Rg y Rh son cada uno hidrógeno. En algunas realizaciones, Re y Rf junto con el átomo al que están unidos, forman un cicloalquilo de 5 miembros; y Ra, Rb, Rc, Rd, Rg y Rh son cada uno hidrógeno. En algunas realizaciones, Re y Rf junto con el átomo al que están unidos, forman un cicloalquilo de 6 miembros; y Ra, Rb, Rc, Rd, Rg y Rh son cada uno hidrógeno. En algunas realizaciones, Re y Rf junto con el átomo al que están unidos, forman un anillo heterocicloalquilo de 3-6 miembros; y Ra, Rb, Rc, Rd, Rg y Rh son cada uno hidrógeno. En algunas realizaciones, Re y Rf junto con el átomo al que están unidos, forman un anillo heterocicloalquilo de 3-6 miembros, en donde el anillo heterocicloalquilo de 3-6 miembros contiene O, S o NH; y Ra, Rb, Rc, Rd, Rg y Rh son cada uno hidrógeno. En algunas realizaciones, Re y Rf junto con el átomo al que están unidos, forman un anillo heterocicloalquilo de 3 miembros; y Ra, Rb, Rc, Rd, Rg y Rh son cada uno hidrógeno. En algunas realizaciones, Re y Rf junto con el átomo al que están unidos, forman un anillo heterocicloalquilo de 4 miembros; y Ra, Rb, Rc, Rd, Rg y Rh son cada uno hidrógeno. En algunas realizaciones, Re y Rf junto con el átomo al que están unidos, forman un anillo de oxetano; y Ra, Rb, Rc, Rd, Rg y Rh son cada uno hidrógeno. En algunas realizaciones, Re y Rf junto con el átomo al que están unidos, forman un anillo heterocicloalquilo de 5 miembros; y Ra, Rb, Rc, Rd, Rg y Rh son cada uno hidrógeno. En algunas realizaciones, Re y Rf junto con el átomo al que están unidos, forman un anillo heterocicloalquilo de 6 miembros; y Ra, Rb, Rc, Rd, Rg y Rh son cada uno hidrógeno. En algunas realizaciones, Re y Rf juntos forman =O. En algunas realizaciones, Re y Rf juntos forman =O; y Ra, Rb, Rc, Rd, Rg y Rh son cada uno hidrógeno.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I), (I-A), (I-B), (I-C), (I-D), (I-E) o (I-M), o una sal farmacéuticamente aceptable del mismo, en donde Re y Rg forman un grupo alquileno C1-C3 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C3 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3. En algunas realizaciones, Re y R8 forman un grupo alquileno C1-C3 entre los átomos a los que están unidos; y Ra, Rb, Rc, Rd, Rf y Rh son cada uno hidrógeno. En algunas realizaciones, Re y Rg forman un grupo alquileno C1 entre los átomos a los que están unidos; y Ra, Rb, Rc, Rd, Rf y Rh son cada uno hidrógeno. En algunas realizaciones, Re y Rg forman un grupo alquileno C2 entre los átomos a los que están unidos; y Ra, Rb, Rc, Rd, Rf y Rh son cada uno hidrógeno. En algunas realizaciones, Re y Rg forman un grupo alquileno C3 entre los átomos a los que están unidos; y Ra, Rb, Rc, Rd, Rf y Rh son cada uno hidrógeno.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I), (I-A), (I-B), (I-C), (I-D), (I-E) o (I-M), o una sal farmacéuticamente aceptable del mismo, en donde Rg y Rh junto con el átomo al que están unidos, forman un cicloalquilo o heterocicloalquilo de 3-6 miembros, en donde dicho cicloalquilo o heterocicloalquilo de 3-6 miembros está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 , y haloalquilo C1-C3. En algunas realizaciones, Rg y Rh junto con el átomo al que están unidos, forman un cicloalquilo o heterocicloalquilo de 3-6 miembros; y Ra, Rb, Rc, Rd, Re y Rf son cada uno hidrógeno. En algunas realizaciones, Rg y Rh junto con el átomo al que están unidos, forman un cicloalquilo de 3-6 miembros; y Ra, Rb, Rc, Rd, Re y Rf son cada uno hidrógeno. En algunas realizaciones, Rg y Rh junto con el átomo al que están unidos, forman un cicloalquilo de 3 miembros; y Ra, Rb, Rc, Rd, Re, y Rf son cada uno hidrógeno. En algunas realizaciones, R8 y Rh junto con el átomo al que están unidos, forman un cicloalquilo de 4 miembros; y Ra, Rb, Rc, Rd, Re y Rf son cada uno hidrógeno. En algunas realizaciones, Rg y Rh junto con el átomo al que están unidos, forman un cicloalquilo
de 5 miembros; y Ra, Rb, Rc, Rd, Re y Rf son cada uno hidrógeno. En algunas realizaciones, Rg y Rh junto con el átomo al que están unidos, forman un cicloalquilo de 6 miembros; y Ra, Rb, Rc, Rd, Re y Rf son cada uno hidrógeno.
En algunas realizaciones, Rg y Rh junto con el átomo al que están unidos, forman un anillo heterocicloalquilo de 3-6 miembros; y Ra, Rb, Rc, Rd, Re y Rf son cada uno hidrógeno. En algunas realizaciones, Rg y Rh junto con el átomo al que están unidos, forman un anillo heterocicloalquilo de 3-6 miembros, en donde el anillo heterocicloalquilo de 3-6 miembros contiene O, S o NH; y Ra, Rb, Rc, Rd, Re y Rf son cada uno hidrógeno. En algunas realizaciones, Rg y Rh junto con el átomo al que están unidos, forman un anillo heterocicloalquilo de 3 miembros; y Ra, Rb, Rc, Rd, Re y Rf son cada uno hidrógeno. En algunas realizaciones, Rg y Rh junto con el átomo al que están unidos, forman un anillo heterocicloalquilo de 4 miembros; y Ra, Rb, Rc, Rd, Re y Rf son cada uno hidrógeno. En algunas realizaciones, Rg y Rh junto con el átomo al que están unidos, forman un anillo de oxetano; y Ra, Rb, Rc, Rd, Re y Rf son cada uno hidrógeno. En algunas realizaciones, Rg y Rh junto con el átomo al que están unidos, forman un anillo heterocicloalquilo de 5 miembros; y Ra, Rb, Rc, Rd, Re y Rf son cada uno hidrógeno. En algunas realizaciones, Rg y
Rh junto con el átomo al que están unidos, forman un anillo heterocicloalquilo de 6 miembros; y Ra, Rb, Rc, Rd, Re y Rf son cada uno hidrógeno. En algunas realizaciones, Rg y Rh juntos forman =O. En algunas realizaciones, Rg y Rh juntos forman =O; y Ra, Rb, Rc, Rd, Re y Rf son cada uno hidrógeno.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I), (I-A), (I-B), (I-C), (I-D), (I-E) o (I-M), o una sal farmacéuticamente aceptable del mismo, en donde Ra, Rb, Rc, Rd, Re, Rf, Rg y Rh se definen de la siguiente manera:
(ii) Ra y Re forman un grupo alquileno C1-C2 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C2 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo
C1-C3 y haloalquilo C1-C3 ; y Rb, Rc, Rd, Rf, Rg y Rh son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3 ; o
(iv) Rb y Rc forman un grupo alquileno C1-C4 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C4 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo
C1-C3 y haloalquilo C1-C3; y Ra, Rd, Re, Rf, Rg y Rh son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3 ; o
(vii) Rc y Rd junto con el átomo al que están unidos, forman un cicloalquilo o heterocicloalquilo de 3-6 miembros, en donde dicho cicloalquilo o heterocicloalquilo de 3-6 miembros está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3; y Ra, Rb, Re, Rf, Rg y Rh son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3 ; o
(viii) Rc y Rd juntos forman =O; y Ra, Rb, Re, Rf, Rg y Rh son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3 ; o
(ix) Rc y Re forman un grupo alquileno C1-C4 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C4 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo
C1-C3 y haloalquilo C1-C3 ; y Ra, Rb, Rd, Rf, Rg y Rh son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3 ; o
(x) Rc y Rg forman un grupo alquileno C1-C3 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C3 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo
C1 -C3 y haloalquilo C1-C3 ; y Ra, Rb, Rd, Re, Rf y Rh son cada uno independientem alquilo C1-C3 o haloalquilo C1-C3 ; o
(xi) Re y Rf junto con el átomo al que están unidos, forman un cicloalquilo o heterocicloalquilo de 3-6 miembros, en donde dicho cicloalquilo o heterocicloalquilo de 3-6 miembros está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3; y Ra, Rb, Rc, Rd, Rg y Rh son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3 ; o
(xiii) Re y Rg forman un grupo alquileno C1-C3 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C3 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo
C1-C3 y haloalquilo C1-C3 ; y Ra, Rb, Rc, Rd, Rf y Rh son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3 ; o
(xv) Rg y Rh juntos forman =O; y Ra, Rb, Rc, Rd, Re y Rf son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I), (I-A), (I-B), (I-C), (I-D), (I-E) o (I-M), o una sal farmacéuticamente aceptable del mismo, en donde Ra, Rb, Rc, Rd, Re, Rf, Rg y Rh se definen de la siguiente manera:
(ii) Ra y Re forman un grupo alquileno C1-C2 entre los átomos a los que están unidos; y Rb, Rc, Rd, Rf, Rg y Rh son cada uno hidrógeno; o
(iv) Rb y Rc forman un grupo alquileno C1-C4 entre los átomos a los que están unidos; y Ra, Rd, Re, Rf, Rg y Rh son cada uno hidrógeno; o
(vii) Rc y Rd junto con el átomo al que están unidos, forman un cicloalquilo o heterocicloalquilo de 3-6 miembros; y
Ra, Rb, Re, Rf, Rg y Rh son cada uno hidrógeno; o
(viii) Rc y Rd juntos forman =O; y Ra, Rb, Re, Rf, Rg y Rh son cada uno hidrógeno; o
(ix) Rc y Re forman un grupo alquileno C1-C4 entre los átomos a los que están unidos; y Ra, Rb, Rd, Rf, Rg y Rh son
cada uno hidrógeno; o
(x) Rc y Rg forman un grupo alquileno C1-C3 entre los átomos a los que están unidos; y Ra, Rb, Rd, Re, Rf y Rh son cada uno hidrógeno; o
(xi) Re y Rf junto con el átomo al que están unidos, forman un cicloalquilo o heterocicloalquilo de 3-6 miembros; y Ra, Rb, Rc, Rd, Rg y Rh son cada uno hidrógeno; o
(xiii) Re y Rg forman un grupo alquileno C1-C3 entre los átomos a los que están unidos; y Ra, Rb, Rc, son cada uno independientemente hidrógeno; o
(xv) Rg y Rh juntos forman =O; y Ra, Rb, Rc, Rd, Re y Rf son cada uno hidrógeno.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I), (I-A), (I-B), (I-C), (I-D), (I-E) o (I-M), o una sal farmacéuticamente aceptable del mismo, en donde Ra, Rb, Rc, Rd, Re, Rf, Rg y Rh se definen de la siguiente manera:
(ii) Ra y Re forman un grupo alquileno C1-C2 entre los átomos a los que están unidos; y Rb, Rc, Rd, Rf, Rg y Rh son cada uno hidrógeno; o
(iv) Rb y Rc forman un grupo alquileno C1-C3 entre los átomos a los que están unidos; y Ra, Rd, Re, Rf, Rg y Rh son cada uno hidrógeno; o
(vii) Rc y Rd junto con el átomo al que están unidos, forman un cicloalquilo de 3 miembros o un heterocicloalquilo de 4 miembros; y Ra, Rb, Re, Rf, Rg y Rh son cada uno hidrógeno; o
(viii) Rc y Rd juntos forman =O; y Ra, Rb, Re, Rf, Rg y Rh son cada uno hidrógeno; o
(ix) Rc y Re forman un grupo alquileno C1 entre los átomos a los que están unidos; y Ra, Rb, Rd, cada uno hidrógeno; o
(x) Rc y Rg forman un grupo alquileno C1-C2 entre los átomos a los que están unidos; y Ra, Rb, Rd, Re, Rf y Rh son cada uno hidrógeno; o
(xi) Re y Rf junto con el átomo al que están unidos, forman un heterocicloalquilo de 4 miembros; y Ra, Rb, Rc, Rd, Rg y Rh son cada uno hidrógeno; o
(xiii) Re y Rg forman un grupo alquileno C2 entre los átomos a los que están unidos; y Ra, Rb, Rc, Rd, Rf y Rh son cada uno independientemente hidrógeno; o
(xv) Rg y Rh juntos forman =O; y Ra, Rb, Rc, Rd, Re y Rf son cada uno hidrógeno.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I), (I-A), (I-B), (I-C), (I-D), (I-E) o (I-M), o una sal farmacéuticamente aceptable del mismo, en donde Ra, Rb, Rc, Rd, Re, Rf, Rg y Rh se definen de la siguiente manera:
(ii) Ra y Re forman un grupo alquileno C1-C2 entre los átomos a los que están unidos; y cada uno de Rb, Rc, Rd, Rf y Rg es hidrógeno; o
(iv) Rb y Rc forman un grupo alquileno C1-C2 entre los átomos a los que están unidos; y Ra, Re, Rd, Rf y Rg son cada uno hidrógeno; o
(vii) Rc y Rd junto con el átomo al que están unidos, forman un cicloalquilo de 3 miembros; y Ra, Rb, Re, Rf y Rg son cada uno hidrógeno; o
(x) Rc y Rg forman un grupo alquileno C1-C2 entre los átomos a los que están unidos; y Ra, Rb, Rd, Re y Rf son cada uno hidrógeno; o
(xi) Re y Rf junto con el átomo al que están unidos, forman un heterocicloalquilo de 4 miembros; y Ra, Rb, Rc, Rd y Rg son cada uno hidrógeno; o
(xiii) Re y Rg forman un grupo alquileno C2 entre los átomos a los que están unidos; y Ra, Rb, Rc, Rd y Rf son cada uno independientemente hidrógeno.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I), (I-A), (I-B), (I-C), (I-D), (I-E) o (I-M), o una sal farmacéuticamente aceptable del mismo, en donde
se selecciona de:
En algunas realizaciones,
es
En algunas realizaciones,
En algunas realizaciones
En algunas realizaciones
es
En algunas realizadones;
es
En algunas realizadones;
En algunas realizaciones
En algunas realizaciones,
En algunas realizaciones
es
En algunas realizaciones
es
En algunas realizaciones,
es
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I-A), (IA-1), (I-A-2), (I-A-3), (I-A-4), (I-B), (I-B-1), (I-B-2), (I-B-3), (I-B-4), (I-F-1), (I-F-2), (I-G-1), (I-G-2), (LH-1), (I-H-2), (LJ-1), (I-J-2), (LK-1), (I-K-2), (I-L-1), (i-L-2), (I-M), (I-M-1), (I-M-2), (I-M-3) o (I-M-4), o una sal farmacéuticamente aceptable del mismo, en donde X1 es C o N. En algunas realizaciones, X1 es C. En algunas realizaciones, X1 es N.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I-A), (I-A-1), (I-A-2), (I-A-3), (I-A-4), (I-B), (I-B-1), (I-B-2), (I-B-3), (I-B-4), (I-F-1), (I-F-2), (I-G-1), (I-G-2), (I-H-1), (I-H-2), (I-J-1), (I-J-2), (I-K-1), (I-K-2), (I-L-1), (i-L-2), (I-M), (I-M-1), (I-M-2), (I-M-3) o (I-M-4), o una sal farmacéuticamente aceptable del mismo, en donde X2 es CH, CR1, O, S, N, NH o NR1, según lo permita la valencia. En algunas realizaciones, X2 es CH. En algunas realizaciones, X2 es CR1. En algunas realizaciones, X2 es O. En algunas realizaciones, X2 es S. En algunas realizaciones, X2 es N. En algunas realizaciones, X2es NH. En algunas realizaciones, X2 es NR1.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I-A), (I-A-1), (I-A-2), (I-A-3), (I-A-4), (I-B), (I-B-1), (I-B-2), (I-B-3), (I-B-4), (I-F-1), (I-F-2), (I-G-1), (I-G-2), (LH-1), (I-H -2), (LJ-1), (I-J-2), (LK-1), (I-K-2), (I-L-1), (I-L-2), (I-M), (I-M-1), (I-M-2), (I-M-3) o (I-M-4), o una sal farmacéuticamente aceptable del mismo, en donde X3 es CH, CR1, O, S, N, NH o NR1, según lo permita la valencia. En algunas realizaciones, X3 es CH. En algunas realizaciones, X3 es CR1. En algunas realizaciones, X3 es O. En algunas realizaciones, X3 es S. En algunas realizaciones, X3 es N. En algunas realizaciones, X3es NH. En algunas realizaciones, X3 es NR1.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I-A), (I-A-1), (I-A-2), (I-A-3), (I-A-4), (I-B), (I-B-1), (I-B-2), (I-B-3), (I-B-4), (IF-1), (IF-2), (IG-1), (IG-2), (LH-1), (I-H-2), (LJ-1), (I-J-2), (I-K-1), (I-K-2), (LL-1), (I-L-2), (I-m ), (I-M-1), (I-M-2), (I-M-3) o (I-M-4), o una sal farmacéuticamente aceptable del mismo, en donde X4 es C o N. En algunas realizaciones, X4 es C. En algunas realizaciones, X4 es N.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I-A), (I-A-1), (I-A-2), (I-A-3), (I-A-4), (I-F-1), (I-F-2), (I-G-1), (I-G-2), (I-H-1), (I-H-2), (I-J-1), (I-J-2), (I-K-1), (I-K-2), (I-L-1), (I-L-2), (I-M), (I-M-1), (I-M-2), (I-M-3) o (I-M-4), o una sal farmacéuticamente aceptable del mismo, en donde X5 es un enlace, CH, CR1, O, S, N, NH o NR1, según lo permita la valencia. En algunas realizaciones, X5 es un enlace. En algunas realizaciones, X5 es CH. En algunas realizaciones, X5 es CR1. En algunas realizaciones, X5 es O. En algunas realizaciones, X5 es S. En algunas realizaciones, X5es N. En algunas realizaciones, X5 es NH. En algunas realizaciones, X5 es NR1.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I-A), (I-A-1), (I-A-2), (I-A-3), (I-A-4), (I-B), (I-B-1), (I-B-2), (I-B-3), (I-B-4), (I-F-1), (I-F-2), (I-G-1), (I-G-2), (I-H-1), (IH -2), (I-J-1), (I-J-2), (I-K-1), (I-K-2), (I-L-1), (I-L-2), (I-M), (I-M-1), (I-M-2), (I-M-3) o (I-M-4), o una sal farmacéuticamente aceptable del mismo, en donde X6 es CH, CR1, O, S, N, NH o NR1, según lo permita la valencia. En algunas realizaciones, X6 es CH. En algunas realizaciones, X6 es CR1. En algunas realizaciones, X6 es O. En algunas realizaciones, X6 es S. En algunas realizaciones, X6 es N. En algunas realizaciones, X6es NH. En algunas realizaciones, X6 es NR1.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I-A), (I-A-1), (I-A-2), (I-A-3), (I-A-4), (I-F-1), (I-F-2), (I-G-1), (I-G-2), (I-H-1), (I-H-2), (I-J-1), (I-J-2), (I-K-1), (I-K-2), (I-L-1), (I-L-2), (I-M), (I-M-1), (I-M-2), (I-M-3) o (I-M-4), o una sal farmacéuticamente aceptable del mismo, en donde X1 es C; X2 es N; X3 es NH; X4 es C; X5 es un enlace; y X6 es CH.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I-A), (I-A-1), (I-A-2), (I-A-3), (I-A-4), (I-F-1), (I-F-2), (I-G-1), (I-G-2), (I-H-1), (I-H-2), (I-J-1), (I-J-2), (I-K-1), (I-K-2), (I-L-1), (I-L-2), (I-M), (I-M-1), (I-M-2), (I-M-3) o (I-M-4), o una sal farmacéuticamente aceptable del mismo, en donde X1 es C; X2 es N; X3 es CH; X4 es C; X5 es un enlace; y X6 es S.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I-A), (I-A-1), (I-A-2), (I-A-3), (I-A-4), (I-F-1), (I-F-2), (I-G-1), (I-G-2), (I-H-1), (I-H-2), (I-J-1), (I-J-2), (I-K-1), (I-K-2), (I-L-1), (I-L-2), (I-M), (I-M-1), (I-M-2), (I-M-3) o (I-M-4), o una sal farmacéuticamente aceptable del mismo, en donde X1 es C; X2 es CH; X3 es CH; X4 es C; X5 es CH; y X6 es C.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I-A), (I-A-1), (I-A-2), (I-A-3), (I-A-4), (I-F-1), (I-F-2), (I-G-1), (I-G-2), (I-H-1), (I-H-2), (I-J-1), (I-J-2), (I-K-1), (I-K-2), (I-L-1), o (I-L-2), o una sal farmacéuticamente aceptable del mismo, donde Y1 es C o N. En algunas realizaciones, Y1 es C. En algunas realizaciones, Y1 es N.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I-A), (I-A-1), (I-A-2), (I-A-3), (I-A-4), (I-F-1), (I-F-2), (I-G-1), (I-G-2), (I-H-1), (I-H-2), (I-J-1), (I-J-2), (I-K-1), (I-K-2), (I-L-1), o (I-L-2), o una sal farmacéuticamente aceptable del mismo, en donde Y2 es C o N. En algunas realizaciones, Y2 es C. En algunas realizaciones, Y2 es N.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I-A), (I-A-1), (I-A-2), (I-A-3), (I-A-4), (I-B), (I-B-1), (I-B-2), (I-B-3), (I-B-4), (I-F-1), (I-F-2), (I-G-1), (I-G-2), (I-H-1), (I-H-2), (I-J-1), (I-J-2), (I-K-1), (I-K-2), (I-L-1) o (I-L-2), o una sal farmacéuticamente aceptable del mismo, en donde Y3 es CH, CR2, O, S, N, NH o Nr 2, según lo permita la valencia. En algunas realizaciones, Y3 es CH. En algunas realizaciones, Y3 es CR2. En algunas realizaciones, Y3 es O. En algunas realizaciones, Y3 es S. En algunas realizaciones, Y3 es N. En algunas realizaciones, Y3 es NH. En algunas realizaciones, Y3 es NR2.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I-A), (I-A-1), (I-A-2), (I-A-3), (I-A-4), (I-B), (I-B-1), (I-B-2), (I-B-3), (I-B-4), (I-F-1), (I-F-2), (I-G-1), (I-G-2), (I-H-1), (I-H-2), (I-J-1), (I-J-2), (I-K-1), (I-K-2), (I-L-1) o (I-L-2), o una sal farmacéuticamente aceptable del mismo, en donde Y4 es un enlace, CH, CR2, O, S, N, NH o NR2, según lo permita la valencia. En algunas realizaciones, Y4 es un enlace. En algunas realizaciones, Y4 es CH. En algunas realizaciones, Y4 es CR2. En algunas realizaciones, Y4 es O. En algunas realizaciones, Y4 es S. En algunas realizaciones, Y4 es N. En algunas realizaciones, Y4 es NH. En algunas realizaciones, Y4 es NR2.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I-A), (I-A-1), (I-A-2), (I-A-3), (I-A-4), (I-B), (I-B-1), (I-B-2), (I-B-3), (I-B-4), (I-F-1), (I-F-2), (I-G-1), (I-G-2), (I-H-1), (I-H-2), (I-J-1), (I-J-2), (I-K-1), (I-K-2), (I-L-1) o (I-L-2), o una sal farmacéuticamente aceptable del mismo, en donde Y5 es CH, CR2, O, S, N, NH o Nr 2, según lo permita la valencia. En algunas realizaciones, Y5 es CH. En algunas realizaciones, Y5 es CR2. En algunas realizaciones, Y5 es O. En algunas realizaciones, Y5 es S. En algunas realizaciones, Y5 es N. En algunas realizaciones, Y5 es NH. En algunas realizaciones, Y5 es NR2.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I-A), (I-A-1), (I-A-2), (I-A-3), (I-A-4), (I-B), (I-B-1), (I-B-2), (I-B-3), (I-B-4), (I-F-1), (I-F-2), (I-G-1), (I-G-2), (I-H-1), (I-H-2), (I-J-1), (I-J-2), (I-K-1), (I-K-2), (I-L-1) o (I-L-2), o una sal farmacéuticamente aceptable del mismo, en donde Y6 es CH, CR2, O, S, N, NH o Nr 2, según lo permita la valencia. En algunas realizaciones, Y6 es CH. En algunas realizaciones, Y6 es CR2. En algunas realizaciones, Y6 es O. En algunas realizaciones, Y6 es S. En algunas realizaciones, Y6 es N. En algunas realizaciones, Y6 es NH. En algunas realizaciones, Y6 es NR2.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I-A), (I-A-1), (I-A-2), (I-A-3), (I-A-4), (I-F-1), (I-F-2), (I-G-1), (I-G-2), (I-H-1), (I-H-2), (I-J-1), (I-J-2), (I-K-1), (I-K-2), (I-L-1), o (I-L-2), o una sal farmacéuticamente aceptable del mismo, en donde Y1 es C; Y2 es C; Y3 es CH; Y4 es CH; Y5 es CH; e Y6 es CH.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I-A), (I-A-1), (I-A-2), (I-A-3),
(I-A-4), (I-F-1), (I-F-2), (I-G-1), (I-G-2), (I-H-1), (I-H-2), (I-J-1), (I-J-2), (I-K-1), (I-K-2), (I-L-1), o (I-L-2), o una sal farmacéuticamente aceptable del mismo, en donde Y1 es C; Y2 es C; Y3 es CR2; Y4 es CH; Y5 es CH; e Y6 es CH.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I-A), (I-A-1), (I-A-2), (I-A-3), (I-A-4), (I-F-1), (I-F-2), (I-G-1), (I-G-2), (I-H-1), (I-H-2), (I-J-1), (I-J-2), (I-K-1), (I-K-2), (I-L-1), o (I-L-2), o una sal farmacéuticamente aceptable del mismo, en donde Y1 es C; Y2 es C; Y3 es CH; Y4 es CR2; Y5 es CH; e Y6 es CH.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I-A), (I-A-1), (I-A-2), (I-A-3), (I-A-4), (I-F-1), (I-F-2), (I-G-1), (I-G-2), (I-H-1), (I-H-2), (I-J-1), (I-J-2), (I-K-1), (I-K-2), (I-L-1), o (I-L-2), o una sal farmacéuticamente aceptable del mismo, en donde Y1 es C; Y2 es C; Y3 es CH; Y4 es CH; Y5 es CR2; e Y6 es CH.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I-A), (I-A-1), (I-A-2), (I-A-3), (I-A-4), (I-F-1), (I-F-2), (I-G-1), (I-G-2), (I-H-1), (I-H-2), (I-J-1), (I-J-2), (I-K-1), (I-K-2), (I-L-1), o (I-L-2), o una sal farmacéuticamente aceptable del mismo, en donde Y1 es C; Y2 es C; Y3 es N; Y4 es CH; Y5 es CH; e Y6 es CR2. En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I-A), o una sal farmacéuticamente aceptable del mismo, en donde Y1 es C; Y2 es C; Y3 es N; Y4 es CH; Y5 es CH; y Y6 es CH.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I-A), (I-A-1), (I-A-2), (I-A-3), (I-A-4), (I-F-1), (I-F-2), (I-G-1), (I-G-2), (I-H-1), (I-H-2), (I-J-1), (I-J-2), (I-K-1), (I-K-2), (I-L-1), o (I-L-2), o una sal farmacéuticamente aceptable del mismo, en donde Y1 es C, Y2 es C; Y3 es CH; Y4 es N; Y5 es CH; e Y6 es CH.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I-A), (I-A-1), (I-A-2), (I-A-3), (I-A-4), (I-F-1), (I-F-2), (I-G-1), (I-G-2), (I-H-1), (I-H-2), (I-J-1), (I-J-2), (I-K-1), (I-K-2), (I-L-1), o (I-L-2), o una sal farmacéuticamente aceptable del mismo, en donde Y1 es C; Y2 es C; Y3 es CH; Y4 es CH; Y5 es N; e Y6 es CH.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I-A), (I-A-1), (I-A-2), (I-A-3), (I-A-4), (I-F-1), (I-F-2), (I-G-1), (I-G-2), (I-H-1), (I-H-2), (I-J-1), (I-J-2), (I-K-1), (I-K-2), (LL-1), o (I-L-2), o una sal farmacéuticamente aceptable del mismo, en donde Y1 es C; Y2 es C; Y3 es CH; Y4 es CH; Y5 es CH; e Y6 es N.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (LA-1), (I-A-2), (I-A-3), (I-A-4), (I-B-1), (I-B-2), (I-B -3), (I-B-4), (I-C-1), (I-C-2), (I-C-3), (I-C-4), (I-M-1), (I-M-2), (I-M-3), o (I-M-4), o una sal farmacéuticamente aceptable del mismo, en donde Rj, Rk, Rm, Rn, Ro, Rp, Rq y Rr, cuando están presentes, son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3. En algunas realizaciones, Rj, Rk, Rm, Rn, Ro, Rp, Rq y Rr, cuando están presentes, son cada uno hidrógeno.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I-B), (I-B-1), (I-B-2), (I-B-3) o (I-B-4), o una sal farmacéuticamente aceptable del mismo, en donde X1 es C; X2 es N; X3 es NH; X4 es C; y X6 es CH.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I-B), (I-B-1), (I-B-2), (I-B-3) o (I-B-4), o una sal farmacéuticamente aceptable del mismo, en donde X1 es C; X2 es N; X3 es CH; X4 es C; y X6 es S.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I-B), (I-B-1), (I-B-2), (I-B-3) o (I-B-4), o una sal farmacéuticamente aceptable del mismo, en donde Y3 es CH; Y4 es CH; Y5 es CH; e Y6 es CH.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I-B), (I-B-1), (I-B-2), (I-B-3) o (I-B-4), o una sal farmacéuticamente aceptable del mismo, en donde Y3 es CR2; Y4 es CH; Y5 es CH; e Y6 es CH.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I-B), (I-B-1), (I-B-2), (I-B-3) o (I-B-4), o una sal farmacéuticamente aceptable del mismo, en donde Y3 es CH; Y4 es CR2; Y5 es CH; e Y6 es CH.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I-B), (I-B-1), (I-B-2), (I-B-3) o (I-B-4), o una sal farmacéuticamente aceptable del mismo, en donde Y3 es CH; Y4 es CH; Y5 es CR2; e Y6 es CH.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I-B), (I-B-1), (I-B-2), (I-B-3) o (I-B-4), o una sal farmacéuticamente aceptable del mismo, en donde Y3 es CH; Y4 es CH; Y5 es CH; e Y6 es CR2.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I-B), (I-B-1), (I-B-2), (I-B-3) o (I-B-4), o una sal farmacéuticamente aceptable del mismo, en donde Y3 es N; Y4 es CH; Y5 es CH; e Y6 es CH.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I-B), (I-B-1), (I-B-2), (I-B-3) o (I-B-4), o una sal farmacéuticamente aceptable del mismo, en donde Y3 es CH; Y4 es N; Y5 es CH; e Y6 es CH.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I-B), (I-B-1), (I-B-2), (I-B-3) o (I-B-4), o una sal farmacéuticamente aceptable del mismo, en donde Y3 es CH; Y4 es CH; Y5 es N; e Y6 es CH.
En algunas realizaciones, la divulgación se refiere a un compuesto de fórmula (I-B), (I-B-1), (I-B-2), (I-B-3) o (I-B-4), o una sal farmacéuticamente aceptable del mismo, en donde Y3 es CH; Y4 es CH; Y5 es CH; e Y6 es N.
En algunas realizaciones, la divulgación se refiere a un compuesto proporcionado en la presente, o una sal farmacéuticamente aceptable del mismo, que es un compuesto inhibidor de USP30 que tiene un valor de IC50 de < 1 |jM y > 0,001 |jM como se mide en un ensayo de ubiquitina-rodamina 110 como se describe en Ejemplo 1.
En otro aspecto, la divulgación se refiere a un compuesto seleccionado de la Tabla 1, o una sal farmacéuticamente aceptable del mismo. Cada par de compuestos enumerados en la Tabla 1 (es decir, compuestos 1-a y 1-b, compuestos 2-a y 2-b, etc.) se obtuvo como una mezcla racémica y luego se separaron mediante HPLC quiral de acuerdo con el procedimiento descrito en el Ejemplo 2, Paso 7, o un método similar, para obtener los compuestos individuales en forma sustancialmente enantioméricamente pura. Para cada par de compuestos, el primer compuesto (es decir, los compuestos 1-a, 2-a, etc.) fue el primer isómero en eluiry el segundo compuesto (es decir, los compuestos 1-b, 2-b, etc.) el segundo isómero en eluir. Los descriptores estereoquímicos reflejan la estereoquímica relativa de cada compuesto. La estereoquímica absoluta de cada compuesto se asignó arbitrariamente. En algunas realizaciones, el compuesto seleccionado de la Tabla 1, o una sal farmacéuticamente aceptable del mismo, está presente en una mezcla racémica. En algunas realizaciones, el compuesto seleccionado de la Tabla 1, o una sal farmacéuticamente aceptable del mismo, está presente en forma sustancialmente enantioméricamente pura.
Tabla 1. Com uestos de la divul ación
continuación
continuación
continuación
continuación
En otro aspecto, la divulgación se refiere a un compuesto seleccionado de la Tabla 2, o una sal farmacéuticamente aceptable del mismo. En algunas realizaciones, el compuesto, o una sal farmacéuticamente aceptable del mismo, está presente en una mezcla racémica con su enantiómero. En algunas realizaciones, el compuesto, o una sal farmacéuticamente aceptable del mismo, está presente en forma sustancialmente enantioméricamente pura.
En otro aspecto, la divulgación se refiere a el enantiómero de un compuesto seleccionado de la Tabla 2, o una sal farmacéuticamente aceptable del mismo. En algunas realizaciones, el enantiómero, o una sal farmacéuticamente aceptable del mismo, está presente en una mezcla racémica. En algunas realizaciones, el enantiómero, o una sal farmacéuticamente aceptable del mismo, está presente en forma sustancialmente enantioméricamente pura.
continuación
continuación
continuación
continuación
continuación
continuación
continuación
continuación
continuación
continuación
continuación
continuación
continuación
continuación
continuación
continuación
continuación
continuación
continuación
continuación
continuación
continuación
continuación
continuación
continuación
continuación
continuación
continuación
continuación
continuación
continuación
continuación
continuación
continuación
continuación
continuación
continuación
continuación
continuación
continuación
continuación
continuación
En algunas realizaciones, un compuesto descrito en la presente se proporciona en forma no salina. En algunas realizaciones, un compuesto descrito en la presente se proporciona como una sal farmacéuticamente aceptable.
En otro aspecto, la divulgación se refiere a un compuesto, o una sal farmacéuticamente aceptable del mismo, preparado mediante un método que comprende: preparar un compuesto de la presente divulgación como una mezcla de estereoisómeros; separar los estereoisómeros por HPLC quiral de acuerdo con el procedimiento descrito en el Ejemplo 2, Paso 7; aislar uno o más estereoisómeros que son compuestos inhibidores de USP30 que tienen un valor de ICsode < 1 μM como se mide en un ensayo de ubiquitina-rodamina 110 como se describe en el Ejemplo 1; y opcionalmente tratar el estereoisómero aislado con un ácido o una base para proporcionar una sal farmacéuticamente aceptable del mismo.
En algunas realizaciones, el compuesto es el primer isómero en eluir. En algunas realizaciones, el compuesto es el segundo isómero en eluir. En algunas realizaciones, el compuesto es el tercer isómero en eluir. En algunas realizaciones, el compuesto es el cuarto isómero en eluir. En algunas realizaciones, el compuesto es el 5°, 6°, 7° u 8° isómero en eluir.
En algunas realizaciones, un compuesto de la presente divulgación, o una sal farmacéuticamente aceptable del mismo, es un compuesto inhibidor de USP30 que tiene un valor de IC50 de < 1 μM medido en un ensayo de ubiquitina-rodamina 110 como se describe en el Ejemplo 1. En algunas realizaciones, el valor de IC50 es < 0,1 μM.
Composiciones farmacéuticas y vías de administración
La divulgación también se refiere a una composición farmacéutica que comprende uno o más compuestos proporcionados en la presente, o una sal farmacéuticamente aceptable de los mismos, y un portador farmacéuticamente aceptable. En algunas realizaciones, la composición farmacéutica comprende una cantidad terapéuticamente eficaz de uno o más compuestos, o una sal farmacéuticamente aceptable de los mismos. En algunas realizaciones, la composición farmacéutica es para su uso en un método para tratar un trastorno neurodegenerativo, como la enfermedad de Parkinson.
Los compuestos y sales farmacéuticamente aceptables divulgados en la presente pueden administrarse a través de cualquier modo de administración de agentes terapéuticos, de acuerdo con las prácticas farmacéuticas convencionales. En algunas realizaciones, las composiciones farmacéuticas notificadas en la presente pueden proporcionarse en una forma de dosificación unitaria. En algunas realizaciones, las composiciones farmacéuticas notificadas en la presente pueden proporcionarse en una forma de dosificación oral. En algunas realizaciones, las composiciones farmacéuticas descritas en la presente se pueden proporcionar en una forma de dosificación oral sólida, como un comprimido, cápsula, polvo u oblea.
Las composiciones farmacéuticas descritas en la presente pueden prepararse de acuerdo con métodos convencionales de mezclado, granulado o recubrimiento. Por ejemplo, las formas de dosificación orales (por ejemplo, comprimidos) pueden prepararse mezclando en seco o granulando en seco. Las composiciones farmacéuticas descritas en la presente pueden contener de aproximadamente un 0,1% a aproximadamente un 99%, de aproximadamente un 5% a aproximadamente un 90%, o de aproximadamente un 1% a aproximadamente un 20% del compuesto o sal farmacéuticamente aceptable en peso o volumen. Los portadores farmacéuticamente
aceptables empleados en las composiciones farmacéuticas descritas en la presente pueden incluir uno o más excipientes farmacéuticos, como cargas, disgregantes, lubricantes, deslizantes, antiadherentes, antiestáticos, surfactantes o aditivos estabilizadores. En la técnica se conocen portadores sólidos adecuados, por ejemplo, carbonato de magnesio, estearato de magnesio, talco, azúcar o lactosa. Con algunos fármacos, la presencia de tales aditivos promueve la estabilidad y dispersabilidad del agente en solución. Los ejemplos adecuados, pero no limitativos, de aditivos estabilizadores incluyen goma acacia, gelatina, metilcelulosa, polietilenglicol, ácidos carboxílicos y sales de los mismos, y polilisina. En algunas realizaciones, los aditivos estabilizadores son goma acacia, gelatina y metilcelulosa. Ejemplos de portadores farmacéuticamente aceptables y métodos de fabricación para varias composiciones pueden encontrarse en A. Gennaro (ed.), Remington's Pharmaceutical Sciences, 18a Edición, (1990), Mack Publishing Co., Easton, Pa.
Las composiciones farmacéuticas descritas en la presente pueden contener el compuesto o la sal farmacéuticamente aceptable en forma sustancialmente pura, como por lo menos un 60% de pureza, más adecuadamente por lo menos un 75% de pureza, preferiblemente por lo menos un 85% de pureza y lo más preferible por lo menos un 98% de pureza (p/p).
Los compuestos y las sales farmacéuticamente aceptables descritos en la presente se administran preferentemente en una cantidad terapéuticamente eficaz (por ejemplo, una cantidad que tenga un índice terapéutico favorable adecuado). La cantidad y frecuencia de administración se regulará de acuerdo con el criterio del practicante clínico tratante considerando factores como la edad, género, condición y tamaño del paciente, así como la gravedad de la afección médica que se está tratando; la vía de administración; la función renal o hepática del paciente; y el compuesto particular o la sal farmacéuticamente aceptable empleada. Un médico o veterinario experto en la técnica puede determinar y prescribir fácilmente la cantidad eficaz del fármaco requerida para prevenir, contrarrestar o detener el progreso de la afección. Por conveniencia, la dosificación diaria total puede dividirse y administrarse en porciones a lo largo del día según se requiera.
Usos de los compuestos divulgados en la presente
La presente divulgación también proporciona usos de compuestos de fórmula (I). Los compuestos de fórmula (I) son útiles en medicina. Por ejemplo, los compuestos y composiciones descritos en la presente son inhibidores de USP30. Sin querer estar limitados por ninguna teoría en particular, tal inhibición de USP30 puede proporcionar el tratamiento de los síntomas y/o causas subyacentes de enfermedades o afecciones asociadas con la actividad de USP30. En algunas realizaciones, los inhibidores de USP30 pueden usarse para tratar enfermedades o afecciones neurológicas y neurodegenerativas, como la enfermedad de Parkinson.
En la presente se proporcionan compuestos y composiciones para su uso en métodos para tratar una enfermedad o trastorno asociado con una proteasa específica de ubiquitina (por ejemplo, USP30), que comprende administrar a un paciente con necesidad de ello una cantidad terapéuticamente eficaz de un compuesto o composición proporcionados en la presente. En algunas realizaciones, la enfermedad o trastorno asociado con una proteasa específica de ubiquitina (por ejemplo, USP30) es una enfermedad o trastorno neurodegenerativo (por ejemplo, enfermedad de Parkinson).
La presente divulgación también proporciona compuestos y composiciones para su uso en métodos de inhibición de una proteasa específica de ubiquitina (por ejemplo, USP30) en un paciente con necesidad de ello, que comprende administrar al paciente una cantidad terapéuticamente eficaz de un compuesto o composición proporcionada en la presente.
La presente divulgación también proporciona compuestos y composiciones para su uso en métodos de tratamiento de una enfermedad o trastorno neurodegenerativo (por ejemplo, la enfermedad de Parkinson) en un paciente con necesidad de ello, que comprende administrar al paciente una cantidad terapéuticamente eficaz de un compuesto o composición proporcionada en la presente.
La presente divulgación también proporciona compuestos para su uso en el método de inhibición de una proteasa específica de ubiquitina (por ejemplo, USP30) en un paciente con necesidad de ello. En algunas realizaciones, la presente divulgación proporciona compuestos para su uso en un método para tratar una enfermedad o trastorno neurodegenerativo (por ejemplo, la enfermedad de Parkinson) en un paciente con necesidad de ello.
Síntesis de compuestos divulgados en la presente
Los compuestos y las sales farmacéuticamente aceptables divulgados en la presente pueden prepararse mediante métodos conocidos en la técnica de la síntesis orgánica como se expone en parte mediante los siguientes esquemas sintéticos. En los esquemas que se describen a continuación, se entiende bien que se emplean grupos protectores para grupos sensibles o reactivos cuando sea necesario de acuerdo con los principios generales de la química. Los grupos protectores se manipulan de acuerdo con métodos estándar de síntesis orgánica (T.W. Greene
y P.G.M. Wuts, "Protective Groups in Organic Synthesis", Tercera edición, Wiley, Nueva York 1999). Estos grupos se eliminan en una etapa conveniente de la síntesis del compuesto usando métodos que son claramente evidentes para los expertos en la técnica.
En general, los compuestos de fórmula (I) pueden sintetizarse mediante los métodos descritos en el Esquema 1, mediante los procedimientos específicos analizados en los Ejemplos 2-4 y/o mediante métodos conocidos por los expertos en la técnica. Los materiales de partida para la síntesis descrita en el Esquema 1 están disponibles comercialmente o pueden prepararse mediante métodos conocidos por los expertos en la técnica.
Esquema 1. Síntesis de Compuestos de Fórmula I
(i) catalizador de acoplamiento cruzado (por ejemplo, XPhos-Pd), base (por ejemplo, K3PO4), solvente (por ejemplo, dioxano, H2O) (X es un grupo saliente, por ejemplo, Br; R es un grupo alquilo, por ejemplo, Me); (ii) Base (por ejemplo, LiOH), solvente (por ejemplo, THF, H2O); (iii) agente de acoplamiento de amida (por ejemplo, HATU), base (por ejemplo, DIEA), solvente (por ejemplo, DMF) (P es un grupo protector, por ejemplo, Boc); (iv) condiciones de desprotección (por ejemplo, ácido, por ejemplo, CF3COOH), solvente (por ejemplo, CH2Ch); (v) agente de cianación (por ejemplo, BrCN), base (por ejemplo, NaHCO3).
Realizaciones ejemplares
Las siguientes realizaciones numeradas, aunque no limitativas, son ejemplares de ciertos aspectos de la divulgación:
1. Un compuesto de fórmula (I):
o una sal farmacéuticamente aceptable del mismo, en donde:
Ar1 es fenileno o heteroarileno de 5-6 miembros, en donde dicho fenileno o heteroarileno está sustituido con m grupos R1;
Ar2 es fenileno o heteroarileno de 5-6 miembros, en donde dicho fenileno o heteroarileno está sustituido con n grupos R2;
L es -O-, -S-, -NR3-, -C(R4)2-, -S(O)2-, o -S(O)-;
M es cicloalquilo de 3-6 miembros, fenilo o heteroarilo de 5-6 miembros, en donde dicho cicloalquilo, fenilo o heteroarilo está sustituido con p grupos R5;
cada aparición de R1, R2 y R5 es independientemente halo, ciano, NO2, oxo, hidroxilo,-R6, -OR6, alquilo C1-C6 ,
haloalquilo C1-C6 , hidroxialquilo C1-C6 , -alquileno C1-C6-R6 , alcoxi C1-C6 , haloalcoxi Ci-C6,-alquileno C0-C3-NR6R7,-alquileno C0-C3-NR7R8, -alquileno C0-C3-C(O)NR6R7, -alquileno C0-C3-C(O)NR7R8, -alquileno C0-C3-NR7C(O)R6, -alquileno C0-C3-NR7C(O)R8, -alquileno C0-C3-NR7S(O)2R6, -alquileno C0-C3-C(O)R6, -alquileno
C0-C3-C(O)R7, -alquileno C0-C3-SR6, -alquileno C0-C3-S(O)R6, -alquileno C0-C3-S(O)2R6, -alquileno C0-C3-S(O)2R7, -alquileno C0-C3S(O)2NR6R7, -alquileno C0-C3-S(O)2NR7R8, -alquileno C0-C3-NR7C(O)NR8R9, -alquileno C0-C3-NR7S(O)2NR8R9, -alquileno C0-C3-C(O)OR7, -alquileno C0-C3-C(O)OR6, -alquileno C0-C3-OC(O)R7, -alquileno C0-C3-OC(O)R6, -alquileno C0-C3 - NR7C(O)OR8, o -alquileno C0-C3-NR7S(O)2R8;
R3 es H, alquilo C1-C6 o haloalquilo C1-C6 ;
cada R4 es independientemente H, alquilo C1-C6 o haloalquilo C1-C6 , o dos grupos R4 junto con el átomo de carbono al que están unidos forman un cicloalquilo o heterocicloalquilo de 3-6 miembros;
cada R6 es independientemente heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, arilo de
6-10 miembros o cicloalquilo de 3-8 miembros, en donde dicho heteroarilo, heterocicloalquilo, arilo o cicloalquilo está opcionalmente sustituido con de 1 a 5 sustituyentes seleccionados independientemente del grupo formado por halo, oxo, alquilo C1-C6, haloalquilo C1-C6, hidroxialquilo C1-C6 , alcoxi C1-C6, haloalcoxi C1-C6, alquenilo C2-C6, alquinilo C2-C6, heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, arilo de 6-10 miembros, cicloalquilo de 3-8 miembros, -NR10C(O)NR11R12, -NR10R11, -C(O)R10, -NR10C(O)R11, -NR10C(O)OR11, -S(O)2R10, -C(O)NR10R11, -C(O)OR10, - S(O)2NR10R11, -NR10S(O)2R11, -OR10, -OC(O)R10, -OS(O)2R10, -OC(O)NR10R11, -OC(O)OR10, - OS(O)2NR10R11, -C(O)NR10C(O)NR11R12, -C(O)C(O)R10, -C(O)NR10C(O)R11, - C(O)NR10C(O)OR11, -C(O)S(O)2R10, -C(O)C(O)NR10R11, -C(O)C(O)OR10, -C(O)S(O)2NR10R11, -C(O)NR10S(O)2R11, - alquileno C1-C6-R10, -alquileno C1-C6-NR10C(O)NR11R12, -alquileno
C1-C6-NR10R11, -alquileno C1-C6-C(O)R10, -alquileno C1-C6-NR10C(O)R11, -alquileno C1-C6-NR10C(O)OR11, -alquileno C1-C6-S(O)2R10, -alquileno C1-C6-C(O)NR10R11, -alquileno C1-C6-C(O)OR10, -alquileno C1-C6-S(O)2NR10R11, -alquileno C1-C6-NR10S(O)2R11, -alquenileno C1-C6-R10, -alquenileno C1-C6-NR10C(O)NR11R12, -alquenileno C1-C6-NR10R11, -alquenileno C1-C6-C(O)R10, -alquenileno C1-C6-NR10C(O)R11, -alquenileno C1-C6-NR10C(O)OR11, -alquenileno C1-C6-S(O)2R10, -alquenileno C1-C6-C(O)NR10R11, -alquenileno C1-C6-C(O)OR10, -alquenileno C1-C6-S(O)2NR10R11, y-alquenileno C1-C6-NR10S(O)2R11;
cada R7, R8 y R9 es independientemente hidrógeno o alquilo C1-C6 ;
cada R10, R11 y R12 es independientemente hidrógeno, alquilo C1-C6 , heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, arilo de 6-10 miembros o cicloalquilo de 3-8 miembros;
m es 0-4;
n es 0-4; y
p es 0-4;
Ra, Rb, Rc, Rd, Re, Rf, Rg y Rh se definen de la siguiente manera: (i)
(i) Ra y Rb forman un grupo alquileno C1-C4 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C4 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3; y Rc, Rd, Re, Rf, Rg y Rh son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3 ; o
(ii) Ra y Re forman un grupo alquileno C1-C2 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C2 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1 -C3 y haloalquilo C1-C3; y Rb, Rc, Rd, Re, Rf, Rg y Rh son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3 ; o
(iii) Ra y Rg forman un grupo alquileno C1-C3 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C3 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3 ; y Rb, Rc, Rd, Re, Rf y Rh so hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3; o
(iv) Rb y Rc forman un grupo alquileno C1-C4 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C4 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3; y Ra, Rd, Re, Rf, Rg y Rh son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3; o
(v) Rb y Re forman un grupo alquileno C1-C3 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C3 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3; y Ra, Rc, Rd, Rf, Rg y Rh son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3; o
(vi) Rb y Rg forman un grupo alquileno C1-C4 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C4 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3; y Ra, Rc, Rd, Re, Rf y Rh son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3; o
(vii) Rc y Rd junto con el átomo al que están unidos, forman un cicloalquilo o heterocicloalquilo de 3-6 miembros, en donde dicho cicloalquilo o heterocicloalquilo de 3-6 miembros está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3 ; y Ra,
Rb, Re, Rf, Rg y Rh sonn cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3; o
(viii) Rc y Rd juntos forman =O; y Ra, Rb, Re, Rf, Rg y Rh son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3 ; o
(ix) Rc y Re forman un grupo alquileno C1-C4 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C4 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3 ; y Ra, Rb, Rd, Rf, Rg y Rh so hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3; o
(x) Rc y Rg forman un grupo alquileno C1-C3 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C3 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3; y Ra, Rb, Rd, Re, Rf y Rh so hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3; o
(xi) Re y Rf junto con el átomo al que están unidos, forman un cicloalquilo o heterocicloalquilo de 3-6 miembros, en donde dicho cicloalquilo o heterocicloalquilo de 3-6 miembros está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3 ; y Ra,
Rb, Rc, Rd, Rg y Rh son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3; o
(xii) Re y Rf juntos forman =O; y Ra, Rb, Rc, Rd, Rg y Rh son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3; o
(xiii) Re y Rg forman un grupo alquileno C1-C3 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C3 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3 ; y Ra, Rb, Rc, Rd, Rf y Rh son cad hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3; o
(xiv) Rg y Rh junto con el átomo al que están unidos, forman un cicloalquilo o heterocicloalquilo de 3-6 miembros, en donde dicho cicloalquilo o heterocicloalquilo de 3-6 miembros está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3 ; y Ra,
Rb, Rc, Rd, Re y Rf son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3; o
(xv) Rg y Rh juntos forman =O; y Ra, Rb, Rc, Rd, Re y Rf son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3.
2. El compuesto de la realización 1, o una sal farmacéuticamente aceptable del mismo, en donde Rc y Rg forman un grupo alquileno C1-C3 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C3 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo
C1-C3 ; y Ra, Rb, Rd, Re, Rf y Rh son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3, o haloalquilo C1-C3.
3. El compuesto de la realización 1, o una sal farmacéuticamente aceptable del mismo, en donde Rb y Rc forman un grupo alquileno C1-C4 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C4 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo
C1-C3 ; y Ra, Rd, Re, Rf, Rg y Rh son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3, o haloalquilo C1-C3.
4. El compuesto de la realización 1, o una sal farmacéuticamente aceptable del mismo, en donde Rc y Rd junto con el átomo al que están unidos, forman un cicloalquilo o heterocicloalquilo de 3-6 miembros, en donde dicho cicloalquilo o heterocicloalquilo de 3-6 miembros está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3 ; y Ra, Rb, Re, Rf, Rg y Rh son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3.
5. El compuesto de la realización 1, en donde el compuesto tiene la fórmula (I-A):
(I-A);
o una sal farmacéuticamente aceptable del mismo, en donde:
X1 es C o N;
X2 es CH, CR1, O, S, N, NH o NR1;
X2 es CH, CR1, O, S, N, NH o NR1;
X4 es C o N;
X5 es un enlace, CH, CR1, O, S, N, NH o NR1;
X6 es CH, CR1, O, S, N, NH o NR1;
Y1 es C o N;
Y2 es C o N;
Y3 es CH, CR2, O, S, N, NH o NR2;
Y4 es un enlace, CH, CR2, O, S, N, NH o NR2;
Y5 es CH, CR2, O, S, N, NH o NR2;
Y6 es CH, CR2, O, S, N, NH o NR2;
Ra Rb, Rc, Rd, Re, Rf, Rg y Rh se definen de la siguiente manera
(ii) Ra y Re forman un grupo alquileno C1-C2 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C2 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3 ; y Rb, Rc, Rd, Rf, Rg y Rh son ca hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3; o
(iv) Rb y Rc forman un grupo alquileno C1-C4 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C4 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3; y Ra, Rd, Re, Rf, Rg y Rh son ca hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3; o
(vii) Rc y Rd junto con el átomo al que están unidos, forman un cicloalquilo o heterocicloalquilo de 3-6 miembros, en donde dicho cicloalquilo o heterocicloalquilo de 3-6 miembros está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3 ; y Ra,
Rd, Re, Rf, Rg y Rh son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3; o
(viii) Rc y Rd juntos forman =O; y Ra, Rb, Re, Rf, Rg y Rh son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3 ; o
(ix) Rc y Re forman un grupo alquileno C1-C4 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C4 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3 ; y Ra, Rb, Rd, Rf, Rg y Rh son ca hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3; o
(x) Rc y Rg forman un grupo alquileno C1-C3 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C3 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3; y Ra, Rb, Rd, Re, Rf y Rh son cad hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3; o
(xi) Re y Rf junto con el átomo al que están unidos, forman un cicloalquilo o heterocicloalquilo de 3-6 miembros, en donde dicho cicloalquilo o heterocicloalquilo de 3-6 miembros está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3 ; y Ra,
Rb, Rc, Rd, Rg y Rh son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3; o
(xiii) Re y Rg forman un grupo alquileno C1-C3 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C3 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3 ; y Ra, Rb, Rc, Rd, Rf y Rh son cad hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3; o
(xv) Rg y Rh juntos forman =O; y Ra, Rb, Rc, Rd, Re y Rf so halógeno, alquilo C1-C3 o haloalquilo C1-C3.
6. El compuesto de la realización 5, o una sal farmacéuticamente aceptable del mismo, en donde Rc y Rg forman un grupo alquileno C1-C3 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C3 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo
C1-C3 ; y Ra, Rb, Rd, Re, Rf y Rh son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3.
7. El compuesto de la realización 5, o una sal farmacéuticamente aceptable del mismo, en donde Rb y Rc forman un grupo alquileno C1-C4 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C4 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo
C1-C3 ; y Ra, Rd, Re, Rf, Rg y Rh son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3.
8. El compuesto de la realización 5, o una sal farmacéuticamente aceptable del mismo, en donde Rc y Rd junto con el átomo al que están unidos, forman un cicloalquilo o heterocicloalquilo de 3-6 miembros, en donde dicho cicloalquilo o heterocicloalquilo de 3-6 miembros está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3 ; y Ra, Rb, Re, Rf, Rg y Rh son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3.
9. El compuesto de cualquiera de las realizaciones 5-8, o una sal farmacéuticamente aceptable del mismo, en donde X1 es C; X2 es N; X3 es NH; X4 es C; X5 es un enlace; y X6 es CH.
10. El compuesto de cualquiera de las realizaciones 5-9, o una sal farmacéuticamente aceptable del mismo, en donde Y1 es C; Y2 es C; Y3 es CH; Y4 es CH; Y5 es CH; e Y6 es CH.
11. El compuesto de cualquiera de las realizaciones 5-10, o una sal farmacéuticamente aceptable del mismo, en donde L es O.
12. El compuesto de cualquiera de las realizaciones 5-11, o una sal farmacéuticamente aceptable del mismo, en donde M es fenilo sustituido con p grupos R5.
13. El compuesto de la realización 1, en donde el compuesto tiene la fórmula (I-B):
o una sal farmacéuticamente aceptable del mismo, en donde:
X1 es C o N;
X2 es CH, CR1, O, S, N, NH o NR1;
X3 es CH, CR1, O, S, N, NH o NR1;
X4 es Co N;
X6 es CH, CR1, O, S, N, NH o NR1;
Y3 es CH, CR2 o N;
Y4 es CH, CR2 o N;
Y5 es CH, CR2 o N;
Y6 es CH, CR2 o N;
Ra, Rb, Rc, Rd, Re, Rf, Rg y Rh se definen de la siguiente manera:
(ii) Ra y Re forman un grupo alquileno C1-C2 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C2 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3 ; y Rb, Rc, Rd, Rf, Rg y Rh son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3; o
(iv) Rb y Rc forman un grupo alquileno C1-C4 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C4 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3; y Ra, Rd, Re, Rf, Rg y Rh son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3; o
(vii) Rc y Rd junto con el átomo al que están unidos, forman un cicloalquilo o heterocicloalquilo de 3-6 miembros, en donde dicho cicloalquilo o heterocicloalquilo de 3-6 miembros está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3 ; y Ra, Rb, Re, Rf, Rg y Rh son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3; o
(viii) Rc y Rd juntos forman =O; y Ra, Rb, Re, Rf, Rg y Rh son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3 ; o
(ix) Rc y Re forman un grupo alquileno C1-C4 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C4 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3 ; y Ra, Rb, Rd, Rf, Rg y Rh son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3; o
(x) Rc y Rg forman un grupo alquileno C1-C3 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C3 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3; y Ra, Rb, Rd, Re, Rf y Rh son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3; o
(xi) Re y Rf junto con el átomo al que están unidos, forman un cicloalquilo o heterocicloalquilo de 3-6 miembros, en donde dicho cicloalquilo o heterocicloalquilo de 3-6 miembros está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3 ; y Ra, Rb, Re, Rf, Rg y Rh son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3; o
(xiii) Re y Rg forman un grupo alquileno C1-C3 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C3 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3 ; y Ra, Rb, Rc, Rd, Rf y Rh son cada uno independientemente
hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3; o
(xv) Rg y Rh juntos forman =O; y Ra, Rb, Rc, Rd, Re y Rf son cada uno indep halógeno, alquilo C1-C3 o haloalquilo C1-C3.
14. El compuesto de la realización 13, o una sal farmacéuticamente aceptable del mismo, en donde Rc y Rg forman un grupo alquileno C1-C3 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C3 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3 ; y Ra, Rb, Rd, Re, Rf y Rh son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3.
15. El compuesto de la realización 13, o una sal farmacéuticamente aceptable del mismo, en donde Rb y Rc forman un grupo alquileno C1-C4 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C4 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3 ; y Ra, Rd, Re, Rf, Rg y Rh son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3.
16. El compuesto de la realización 13, o una sal farmacéuticamente aceptable del mismo, en donde Rc y Rd junto con el átomo al que están unidos, forman un cicloalquilo o heterocicloalquilo de 3-6 miembros, en donde dicho cicloalquilo o heterocicloalquilo de 3-6 miembros está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3 ; y Ra, Rb, Re, Rf, Rg y Rh son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3.
17. El compuesto de cualquiera de las realizaciones 13-16, o una sal farmacéuticamente aceptable del mismo, en donde X1 es C; X2 es N; X3 es NH; X4 es C; y X6 es CH.
18. El compuesto de cualquiera de las realizaciones 13-17, o una sal farmacéuticamente aceptable del mismo, en donde Y1 es C; Y2 es C; Y3 es CH; Y4 es CH; Y5 es CH; e Y6 es CH.
19. El compuesto de cualquiera de las realizaciones 13-18, o una sal farmacéuticamente aceptable del mismo, en donde L es O.
20. El compuesto de cualquiera de las realizaciones 13-19, o una sal farmacéuticamente aceptable del mismo, en donde M es fenilo sustituido con p grupos R5.
21. El compuesto de la realización 1, en donde el compuesto tiene la fórmula (I-C):
o una sal farmacéuticamente aceptable del mismo, en donde:
Ra, Rb, Rc, Rd, Re, Rf, Rg y Rh se definen de la siguiente manera:
(ii) Ra y Re forman un grupo alquileno C1-C2 entre los átomos a los que están unidos; y Rb, Rc, Rd, Rf, Rg y Rh son cada uno hidrógeno; o
(iv) Rb y Rc forman un grupo alquileno C1-C4 entre los átomos a los que están unidos; y Ra, Rd, Re, Rf, Rg y Rh son cada uno hidrógeno; o
(vii) Rc y Rd junto con el átomo al que están unidos, forman un cicloalquilo o heterocicloalquilo de 3-6 miembros; y Ra, Rb, Re, Rf, Rg y Rh son cada uno hidrógeno; o
(viii) Rc y Rd juntos forman =O; y Ra, Rb, Re, Rf, Rg y Rh son cada uno hidrógeno; o
(ix) Rc y Re forman un grupo alquileno C1-C4 entre los átomos a los que están unidos; y Ra, Rb, Rd, Rf, Rg y Rh son cada uno hidrógeno; o
(x) Rc y Rg forman un grupo alquileno C1-C3 entre los átomos a los que están unidos; y Ra, Rb, Rd, Re, Rf y Rh son cada uno hidrógeno; o
(xi) Re y Rf junto con el átomo al que están unidos, forman un cicloalquilo o heterocicloalquilo de 3-6 miembros; y Ra, Rb, Rc, Rd, Rg y Rh son cada uno hidrógeno; o (xiii) Re y Rg forman un grupo alquileno C1-C3 entre los átomos a los que están unidos; y Ra, Rb, Rc, Rd, Rf y Rh son cada uno independientemente hidrógeno o
(xv) Rg y Rh juntos forman =O; y Ra, Rb, Rc, Rd, Re y Rf son cada uno hidrógeno.
22. El compuesto de la realización 21, o una sal farmacéuticamente aceptable del mismo, en donde Ra, Rb, Rc, Rd, Re, Rf, Rg y Rh se definen de la siguiente manera:
(ii) Ra y Re forman un grupo alquileno C1-C2 entre los átomos a los que están unidos; y Rb, Rc, Rd, Rf, Rg y Rh son cada uno hidrógeno; o
(iv) Rb y Rc forman un grupo alquileno C1-C3 entre los átomos a los que están unidos; y Ra, Rd, Re, Rf, Rg y Rh son cada uno hidrógeno; o
(vii) Rc y Rd junto con el átomo al que están unidos, forman un cicloalquilo de 3 miembros o un heterocicloalquilo de 4 miembros; y Ra, Rb, Re, Rf, Rg y Rh son cada uno hidrógeno; o
(viii) Rc y Rd juntos forman =O; y Ra, Rb, Re, Rf, Rg y Rh son cada uno hidrógeno; o
(ix) Rc y Re forman un grupo alquileno Ci entre los átomos a los que están unidos; y Ra, Rb, Rd, Rf, Rg y Rh son cada uno hidrógeno; o
(x) Rc y Rg forman un grupo alquileno C1-C2 entre los átomos a los que están unidos; y Ra, Rb, Rd, Re, Rf y Rh son cada uno hidrógeno; o
(xi) Re y Rf junto con el átomo al que están unidos, forman un heterocicloalquilo de 4 miembros; y Ra, Rb, Rc, Rd, Rg y Rh son cada uno hidrógeno; o
(xiii) Re y Rg forman un grupo alquileno C2 entre los átomos a los que están unidos; y Ra, Rb, Rc, son cada uno independientemente hidrógeno o
(xv) Rg y Rh juntos forman =O; y Ra, Rb, Rc, Rd, Re y Rf son cada uno hidrógeno.
23. El compuesto de la realización 22, o una sal farmacéuticamente aceptable del mismo, en donde Rc y Rg forman un grupo alquileno C1-C2 entre los átomos a los que están unidos; y Ra, Rb, Rd, Re, Rf y Rh son cada uno hidrógeno.
24. El compuesto de la realización 22, o una sal farmacéuticamente aceptable del mismo, en donde Rb y Rc forman un grupo alquileno C1-C3 entre los átomos a los que están unidos; y Ra, Rd, Re, Rf, Rg y Rh son cada uno hidrógeno.
25. El compuesto de la realización 22, o una sal farmacéuticamente aceptable del mismo, en donde Rc y Rd junto con el átomo al que están unidos, forman un cicloalquilo de 3 miembros o un heterocicloalquilo de 4 miembros; y Ra, Rb, Re, Rf, Rg y Rh son cada uno hidrógeno.
26. El compuesto de cualquiera de las realizaciones 21-25, o una sal farmacéuticamente aceptable del mismo, en donde n y p son 0.
27. El compuesto de la realización 1, o una sal farmacéuticamente aceptable del mismo, en donde el compuesto se selecciona de la Tabla 1.
28. El compuesto de la realización 1, o una sal farmacéuticamente aceptable del mismo, en donde el compuesto se selecciona de la Tabla 2.
29. El compuesto de cualquiera de las realizaciones 1-28, o una sal farmacéuticamente aceptable del mismo, que es un compuesto inhibidor de USP30 que tiene un valor IC50 de < 1 μM medido en un ensayo de ubiquitinarodamina 110 como se describe en el Ejemplo 1.
30. El compuesto de la realización 29, o una sal farmacéuticamente aceptable del mismo, en donde el valor de IC50 es < 0,1 μM.
31. Un compuesto de fórmula (I-C)
o una sal farmacéuticamente aceptable del mismo, que es un compuesto inhibidor de USP30 que tiene un valor de IC50 de < 1 μM y > 0,001 μM como se mide en un ensayo de Ubiquitina-Rodamina 110 como se describe en el
Ejemplo 1, en donde:
cada aparición de R2 y R5 es independientemente halo, ciano, hidroxilo, alquilo C1-C6, alcoxilo C1-C6, haloalquilo C1-C6 e hidroxialquilo C1-C6;
n es 0-4;
p es 0-4;
Rh es hidrógeno;
Ra, Rb, Rc, Rd, Re, Rf y Rg se definen de la siguiente manera:
(ii) Ra y Re forman un grupo alquileno C1-C2 entre los átomos a los que están unidos; y cada uno de Rb, Rc, Rd, Rf y Rg es hidrógeno; o
(iv) Rb y Rc forman un grupo alquileno C1-C2 entre los átomos a los que están unidos; y Ra, Re, Rd, Rf y Rg son cada uno hidrógeno; o
(vii) Rc y Rd junto con el átomo al que están unidos, forman un cicloalquilo de 3 miembros; y Ra, Rb, Re, Rf y Rg son cada uno hidrógeno; o
(x) Rc y Rg forman un grupo alquileno C1-C2 entre los átomos a los que están unidos; y Ra, Rb, Rd, Re y Rf son cada uno hidrógeno; o
(xi) Re y Rf junto con el átomo al que están unidos, forman un heterocicloalquilo de 4 miembros; y Ra, Rb, Rc, Rd y Rg son cada uno hidrógeno; o
(xiii) Re y Rg forman un grupo alquileno C2 entre los átomos a los que están unidos; y Ra, Rb, Rc, Rd y Rf son cada uno independientemente hidrógeno.
32. El compuesto de la realización 31, o una sal farmacéuticamente aceptable del mismo, en donde el compuesto tiene la siguiente fórmula
33. El compuesto de la realización 31, o una sal farmacéuticamente aceptable del mismo, en donde el compuesto tiene la siguiente fórmula
34. El compuesto de la realización 31, o una sal farmacéuticamente aceptable del mismo, en donde el compuesto tiene la siguiente fórmula
35. El compuesto de la realización 31, o una sal farmacéuticamente aceptable del mismo, en donde el compuesto tiene la siguiente fórmula
36. El compuesto de cualquiera de las realizaciones 31-35, o una sal farmacéuticamente aceptable del mismo, en donde n y p son 0.
37. Una composición farmacéutica que comprende el compuesto de cualquiera de las realizaciones 1-36, o una sal farmacéuticamente aceptable del mismo, y un portador farmacéuticamente aceptable.
38. Un método para inhibir una proteasa específica de ubiquitina en un paciente con necesidad de ello, que comprende administrar al paciente una cantidad terapéuticamente eficaz del compuesto de cualquiera de las realizaciones 1-36, o una sal farmacéuticamente aceptable del mismo, o la composición farmacéutica de la realización 37.
39. El método de la realización 38, en donde la proteasa específica de ubiquitina es USP30.
40. Un método para tratar un trastorno neurodegenerativo en un paciente con necesidad de ello, que comprende administrar al paciente una cantidad terapéuticamente eficaz del compuesto de cualquiera de las realizaciones 1 36, o una sal farmacéuticamente aceptable del mismo, o la composición farmacéutica de la realización 37.
41. El método de la realización 40, en donde el trastorno neurodegenerativo es la enfermedad de Parkinson. 42. Un compuesto de cualquiera de las realizaciones 1-36, o una sal farmacéuticamente aceptable del mismo, para su uso en un método para inhibir una proteasa específica de ubiquitina en un paciente con necesidad de ello.
43. El compuesto o sal farmacéuticamente aceptable para el uso de la realización 42, en donde la proteasa específica de ubiquitina es USP30.
44. Un compuesto de cualquiera de las realizaciones 1-36, o una sal farmacéuticamente aceptable del mismo, para su uso en un método para tratar un trastorno neurodegenerativo en un paciente con necesidad de ello. 45. El compuesto o sal farmacéuticamente aceptable para el uso de la realización 44, en donde el trastorno neurodegenerativo es la enfermedad de Parkinson.
46. Un compuesto inhibidor de USP30 de fórmula:
o una sal farmacéuticamente aceptable del mismo, en donde:
cada aparición de R2 y R5 es independientemente halo, ciano, hidroxilo, alquilo C1-C6, alcoxilo C1-C6, haloalquilo C1-C6 o hidroxialquilo C1-C6;
n es 0-4;
p es 0-4.
47. El compuesto de cualquiera de las realizaciones 1-36 o 44-46, que tiene un valor de IC50 de < 0,5 μM y > 0,001 μM como se mide en un ensayo de ubiquitina-rodamina 110 como se describe en el ejemplo 1
48. El compuesto de la realización 47, que tiene un valor de IC50 de < 0,1 μM y > 0,001 μM como se mide en un
ensayo de Ubiquitina-Rodamina 110 como se describe en el Ejemplo 1.
49. Un compuesto inhibidor de USP30 como se describe y proporciona en la presente.
50. El compuesto inhibidor de USP30 de la realización 49, que tiene un valor IC50 de < 1 μM y > 0,001 μM como se mide en un ensayo de ubiquitina-rodamina 110 como se describe en el ejemplo 1.
EJEMPLOS
Métodos generales
Todos los solventes usados estaban disponibles comercialmente y se usaron sin purificación adicional. Las reacciones se llevaron a cabo típicamente usando solventes anhidros en una atmósfera inerte de nitrógeno.
Los espectros de NMR de protones se registraron usando un espectrómetro de NMR Bruker Plus 400. El solvente deuterado (DMSO- de) contenía típicamente del 0,03% al 0,05% v/v de tetrametilsilano, que se usó como señal de referencia (establecida en 80,00 para 1H).
Los análisis de LCMS se realizaron en un SHIMADZU LCMS que consiste en un UFLC20-AD y detector LCMS 2020 MS. La columna usada fue una Shim-pack XR-ODS, 2,2 μm, 3,0 x 50 mm. El instrumento usa condiciones de fase inversa (acetonitrilo/agua, que contiene 0,05% de amoníaco).
Abreviaturas
A menos que se indique lo contrario, o cuando el contexto indique lo contrario, se entenderá que las siguientes abreviaturas tienen los siguientes significados:
8 cambio químico
ACN acetonitrilo
DIEA N,N-diisopropiletilamina
DMF N,N-dimetilformamida
DCM Diclorometano o cloruro de metileno
h hora
1H NMR resonancia magnética nuclear de protones
HATU hexafluorofosfato de 2-(3H-[1,2,3]triazolo[4,5-b]piridin-3-il)-1,1,3,3-tetrametilisouronio
HPLC cromatografía líquida de alto rendimiento
Hz Hercios
LCMS cromatografía líquida/espectrometría de masas
min minutos
MS espectrometría de masas
ppm partes por millón
RT tiempo de retención
SEMCl 2-clorometil 2-(trimetilsilil)etil éter
ATF Ácido trifluoroacético
THF tetrahidrofurano
XPos-Pd Cloro(2-diciclohexilfosfino-2',4',6'-triisopropil-1,1'-bifenil)[2-(2'-amino-1,1'-bifenil)]paladio(N) XPos-Pd-G3 (2-diciclohexilfosfino-2',4',6'-triisopropil-1,1'-bifenil)[2-(2'-amino-1,1'-bifenil)]paladio(N)
metanosulfonato
Ejemplo 1: Ensayo de ubiquitina-rodamina 110 para la actividad de USP30
El ensayo se realizó a un volumen final de 9 μl en tampón de ensayo que contenía Tris-HCl 20 mM (pH 8,0, (solución de Tris-HCl 1 M, pH 8,0; Corning 46-031-CM)), Gs H 1 mM (L-glutatión reducido, Sigma-Aldrich, G4251-100G), 0,03% de BGG (0,22 μM filtrado, Sigma, G7516-25G) y 0,01% de Triton X-100 (Sigma, T9284-10L). Se predispensaron cantidades de nanolitros de 10 puntos, dilución en serie de 3 veces en DMSO en 1536 placas de ensayo (Corning, N° 3724BC) para una concentración de prueba final de 25 μM a 1,3 nM, de la dosis más alta a la más baja, respectivamente. La concentración y los tiempos de incubación se optimizaron para obtener la máxima señal a fondo mientras se mantenían las condiciones de velocidad inicial a una concentración de sustrato fija. La concentración final de USP30 (USP30 recombinante humana, Boston Biochem, N° de cat. E-582) en el ensayo fue de 0,2 nM. Sustrato final (Ub-Rh110; Ubiquitina-Rodamina 110, UbiQ-126) la concentración fue de 25 nM con [Ub-Rh110]<<Km. Se añadieron 3 μl de USp30 2x a las placas de ensayo (preestampadas con el compuesto), se preincubaron durante 30 minutos y luego se trataron con 3 μl de Ub-Rh1102x. Las placas se incubaron durante 30 minutos a temperatura ambiente antes de añadir 3 μl de solución de parada (concentración final de ácido cítrico 10 mM (Sigma, 251275-500G)). La fluorescencia se leyó en el lector de fluorescencia Envision (excitación a 485 nm y emisión a 535 nm; Perkin Elmer) o en PheraSTAR (excitación a 485 nm y emisión a 535 nm; BMG Labtech).
Para todos los formatos de ensayo, los datos se informaron como el porcentaje de inhibición en comparación con los pocillos de control sobre la base de la siguiente ecuación: % inh = 1-((FLU - AveLow)/(AveHigh - AveLow)) donde f Lu = Fluorescencia medida, AveLow = Fluorescencia media de control sin enzima (n=16), y AveHigh= Fluorescencia media del contro de DMSO (n=16). Los valores de IC50 se determinaron mediante el ajuste de la curva del algoritmo de ajuste logístico estándar de 4 parámetros incluido en el paquete de software Activity Base: IDBS XE Designer Model205. Los datos se ajustan usando el algoritmo de Levenburg Marquardt.
En la Tabla 3 se indican los valores de IC50 calculados de los compuestos descritos en la presente, donde A representa una IC50 de < 0,1 j M, B representa una IC50 de 0,1 a 1,0 j M y C representa una 1C50 > 1,0 |jM. Los compuestos en el ensayo bioquímico USP30 se consideraron activos si la IC50 era < 1 j M.
Tabla 3. Valores IC50 de los com uestos en el ensa o de ubi uitina-rodamina 110
Ejemplo 2: Preparación de (1S,5R)-2-(5-(2-fenoxifenil)-1H-pirazol-3-carbonil)-2,6-diazabiciclor3.2.11octano-6-carbonitrilo (1-a) y (1R,5S)-2-(5-(2-fenoxifenil)-1H-pirazol-3-carbonil)-2,6-diazabiciclor3.2.11octano-6-carbonitrilo (1-b)
Los compuestos 1-a y 1-b se prepararon por la siguiente vía:
Paso 1. 5-bromo-1-[[2-(trimetilsilil)etoxi]metil]-1H-pirazol-3-carboxilato de metilo
Se añadió 2-clorometil 2-(trimetilsilil)etil éter (12,3 ml, 69,5 mmol) a una mezcla de 5-bromo-1H-pirazol-3-carboxilato de metilo (5,00 g, 23,2 mmol) y K2CO3 (18,0 g, 130 mmol) en DMF (50 ml) a 0° C en un baño de hielo/agua. La solución resultante se agitó durante 14 h a 25° C. La reacción se inactivó mediante la adición de agua (100 ml). La mezcla resultante se extrajo con acetato de etilo (3 x 100 ml). Las capas orgánicas combinadas se lavaron con salmuera (100 ml), se secaron sobre sulfato de sodio anhidro, se filtraron y se concentraron al vacío. El residuo se purificó por cromatografía en gel de sílice (eluyendo con éter de petróleo/acetato de etilo 15:1) para proporcionar 5-bromo-1-[[2-(trimetilsilil)etoxi]metil]-1H-pirazol-3-carboxilato de metilo como un aceite amarillo (6,20 g, 79%). LCMS (ES, m/z) 335, 337 [M+H]+.
Paso 2. 5-(2-fenoxifenil)-1-[[2-(trimetilsilil)etoxi]metil]-1H-pirazol-3-carboxilato de metilo
Se agitó una solución de 5-bromo-1-[[2-(trimetilsilil)etoxi]metil]-1H-pirazol-3-carboxilato de metilo (6,20 g, 18,4 mmol), ácido (2-fenoxifenil)borónico (4,96 g, 23,2 mmol), XPhos-Pd (2,90 g, 3,68 mmol) y K3PO4 (11,7 g, 55,2 mmol) en dioxano (120 ml) y H2O (24 ml) durante 15 ha 100° C en un baño de aceite. Después de enfriarla a 25° C, los sólidos se filtraron. El filtrado se concentró al vacío. El residuo se diluyó con agua (50 ml). La mezcla resultante se extrajo con acetato de etilo (3 x 50 ml). La capa orgánica combinada se secó sobre sulfato de sodio anhidro, se filtró y se concentró al vacío. El residuo se purificó por cromatografía de fase inversa (Columna: Columna XBridge Shield RP18 OBD, 5 |jm, 30 x 150 mm; Fase móvil, A: agua (que contenía 10 mmol/l NH4HCO3) y B: ACN (del 5% de B al 72% durante 20 min); detector: UV: 220 y 254 nm) para proporcionar 5-(2-fenoxifenil)-1-[[2-(trimetilsilil)etoxi]metil]-1H-pirazol-3-carboxilato de metilo como un sólido amarillo (3,20 g, 41%). LCMS (ES, m/z) 425 [M+H] .
Paso 3. Ácido 5-(2-fenoxifenil)-1-[[2-(trimetilsilil)etoxi]metil]-1H-pirazol-3-carboxílico
Se agitó una solución de 5-(2-fenoxifenil)-1-[[2-(trimetilsilil)etoxi]metil]-1H-pirazol-3-carboxilato de metilo (1,40 g, 3,30 mmol) y LiOH (0,810 g, 33,8 mmol) en t Hf (60 ml) y H2O (15 ml) durante 4 ha 50° C. La mezcla se dejó enfriar a 25° C y se concentró al vacío. El valor de pH del residuo se ajustó a 5-6 con ácido clorhídrico 3N. Los sólidos se recogieron por filtración y se secaron en un horno para proporcionar ácido 5-(2-fenoxifenil)-1-[[2-(trimetilsilil)etoxi]metil]-1H-pirazol-3-carboxílico como un sólido blanquecino (1,05 g, 78%). LCMS (ES, m/z) 411 [M+H]+.
Paso 4. 2-[5-(2-fenoxifenil)-1-[[2-(trimetilsilil)etoxi]metil]-1H-pirazol-3-carbonil]-2,6-diazabicido[3.2.1]octano-6-carboxilato de terc-butilo
Se agitó una solución de ácido 5-(2-fenoxifenil)-1-[[2-(trimetilsilil)etoxi]metil]-1H-pirazol-3-carboxílico (150 mg, 0,366 mmol), HATU (210 mg, 0,541 mmol), 2,6-diazabiciclo[3.2.1]octano-6-carboxilato de terc-butilo (75,0 mg, 0,346 mmol) y DIEA (0,2 ml, 1,40 mmol) en DMF (2 ml) durante 3 h a 25° C. La reacción se inactivó mediante la adición de agua (10 ml). La mezcla resultante se extrajo con acetato de etilo (3 x 20 ml). La capa orgánica combinada se lavó con salmuera (20 ml), se secó sobre sulfato de sodio anhidro, se filtró y se concentró a presión reducida. El residuo se purificó mediante cromatografía en columna de gel de sílice (eluyendo con éter de petróleo/acetato de etilo 1/1) para proporcionar 2-[5-(2-fenoxifenil)-1-[[2-(trimetilsilil)etoxi]metil]-1H-pirazol-3-carbonil]-2,6-diazabiciclo[3.2.1]octano-6-carboxilato de terc-butilo como un sólido blanco (100 mg, 45%). LCMS (ES, m/z): 605 [M+H]+.
Paso 5. 2,2,2-trifluoroacetato de 2-[5-(2-fenoxifenil)-1H-pirazol-3-carbonil]-2,6-diazabiciclo[3.2.1]octano
Se agitó una solución de 2-[5-(2-fenoxifenil)-1-[[2-(trimetilsilil)etoxi]metil]-1H-pirazol-3-carbonil]-2,6-diazabiciclo[3.2.1]octano-6-carboxilato de terc-butil (100 mg, 0,157 mmol) y TFA (1 ml) en DCM (2 ml) durante 2 h a 25° C. La mezcla resultante se concentró al vacío para proporcionar 2,2,2-trifluoroacetato de 2-[5-(2-fenoxifenil)-1H-pirazol-3-carbonil]-2,6-diazabiciclo[3.2.1]octano como un aceite incoloro (110 mg, bruto). LCMS (ES, m/z): 375 [M+H]+.
Paso 6. 2-[5-(2-fenoxifenil)-1H-pirazol-3-carbonil]-2,6-diazabiciclo[3.2.1]octano-6-carbonitrilo
Se añadió bromuro de cianógeno (17,8 mg, 0,170 mmol) a una mezcla a 0° C de 2,2,2-trifluoroacetato de 2-[5-(2-fenoxifenil)-1H-pirazol-3-carbonil]-2,6-diazabiciclo[3.2.1]octano (80,0 mg, 0,170 mmol) y NaHCO3 (82,0 mg, 0,957 mmol) en DMF (2 ml). La mezcla resultante se agitó durante 16 h a 25° C. La reacción se inactivó mediante la adición de agua (10 ml). La mezcla resultante se extrajo con acetato de etilo (3 x 20 ml). La capa orgánica combinada se secó sobre sulfato de sodio anhidro, se filtró y se concentró a presión reducida. El residuo se purificó por HPLC preparativa (Columna: Columna OBD XBridge Shield RP18, 5 μm, 19 x 150 mm; Fase móvil A: agua (que contenía 10 mmol/l de NH4HCO3) y B: CH3CN (30% a 55% en 8 min); Caudal: 25 ml/min; detector: 220 nm) para proporcionar 2-[5-(2-fenoxifenil)-1H-pirazol-3-carbonil]-2,6-diazabiciclo[3.2.1]octano-6-carbonitrilo como un sólido blanco (40,0 mg, 59%). LCMS (ES, m/z): 400 [M+H]+.
Paso 7. (1S,SR)-2-(5-(2-fenoxifenil)-1H-pirazol-3-carbonil)-2,6-diazabiciclo[3.2.1]octano-6-carbonitrilo y (1R,5S) -2-(5-(2-fenoxifenil)-1H-pirazol-3-carbonil)-2,6-diazabiciclo[3.2.1]octano-6-carbonitrilo
Se separó 2-[5-(2-fenoxifenil)-1H-pirazol-3-carbonil]-2,6-diazabiciclo[3.2.1]octano-6-carbonitrilo (40,0 mg, 0,100 mmol) mediante HPLC quiral (Columna: CHIRAL ART Celulosa-SB, 2 x 25 cm, 5um Fase móvil A: n-hexano y B: EtOH (mantener al 50% en 15 min) Caudal: 20 ml/min Detector: 254/220 nm RT1: 8,911 min y RT2 : 11,119 min). El primer isómero en eluir (RTi= 8,911 min) se recogió y se concentró al vacío, luego se liofilizó para obtener un compuesto cuya estereoquímica absoluta se asignó arbitrariamente como (1S,5R)-2-(5-(2-fenoxifenil)-1H -pirazol-3-carbonil)-2,6-diazabiciclo[3.2.1]octano-6-carbonitrilo (1-a) como un sólido blanco (13,8 mg, 35%). LCMS (ES, m/z): 400 [M+H]+; 1H-NMR (DMSO-de, 400 MHz) 6 (ppm): 13.63 (br s, 1H), 7.86-7.85 (m, 1H), 7.44-7.29 (m, 4H), 7.13-6.90 (m, 5H), 5.49-5.18 (m, 1H), 4.65-4.31 (m, 1H), 4.18-4.17 (m, 1H), 3.65-3.46 (m, 3H), 3.08-3.03 (m, 1H), 1.86-1.72 (m, 4H). El segundo isómero en eluir (RT2 = 11,119 min) se recogió y se concentró al vacío, luego se liofilizó para obtener un compuesto cuya estereoquímica absoluta se asignó arbitrariamente como (1R,SS)-2-(5-(2-fenoxifenil)-1H-pirazol-3-carbonil)-2,6-diazabiciclo[3.2.1]octano-6-carbonitrilo (1-b) como un sólido blanco (14,8 mg, 37%). LCMS (ES, m/z): 400 [M+H]+; 1H-NMR (DMSO-de, 400 MHz) 6 (ppm): 13.63 (br s, 1H), 7.88-7.85 (m, 1H), 7.44-7.29 (m, 4H), 7.14-6.90 (m, 5H), 5.48-5.17 (m, 1H), 4.65-4.31 (m, 1H), 4.18-4.17 (m, 1H), 3.65-3.48 (m, 3H), 3.08-3.03 (m, 1H), 1.86-1. 72 (m, 4H).
Los compuestos expuestos en la Tabla 4 se prepararon mediante métodos análogos a la preparación de los compuestos 1-a y 1-b. Cada par de compuestos enumerados en la Tabla 4 (es decir, compuestos 2-a y 2-b, compuestos 3-a y 3-b, etc.) se obtuvo como una mezcla racémica y luego se separó por HPLC quiral de acuerdo con el procedimiento descrito en el Ejemplo 2, Paso 7, para obtener los compuestos individuales en forma sustancialmente enantioméricamente pura. El primer y el segundo enantiómero en eluir de cada par de enantiómeros se identifican en la Tabla 4. La estereoquímica absoluta de cada enantiómero se asignó arbitrariamente.
T l 4. m i i n l r r m i n m n l
continuación
continuación
continuación
Ejemplo 3: Preparación de N-((1R.5S)-3-cvano-3-azabiciclo[3.2.01heptan-1-il)-5-(2-fenoxifenil)-1H-pirazol-3-carboxamida (6-a) y N-((1S.5R)-3-ciano-3-azabiciclo[3.2.01heptan-1-il)-5-(2-fenoxifenil)-1H-pirazol-3-carboxamida (6-b)
Los compuestos 6-a y 6-b se prepararon mediante la siguiente vía:
Paso 1. 5-bromo-1-[[2-(trimetilsilil)etoxi]metil]-1H-pirazol-3-carboxilato de metilo
Se añadió gota a gota cloruro de 2-(trimetilsMil)etoximetilo (12,2 ml, 68,8 mmol) a una solución a 0° C de 5-bromo-1H-pirazol-3-carboxilato de metilo (5,00 g, 24,5 mmol) y carbonato de potasio (18,0 g, 130 mmol) en DMF (10 ml). La mezcla resultante se agitó durante 14 h a 25° C. La reacción se inactivó con agua (20 ml) a 0° C. La mezcla resultante se extrajo con acetato de etilo (3 x 30 ml). Las capas orgánicas combinadas se lavaron con salmuera (2 x 100 ml), se secaron sobre sulfato de sodio anhidro y se filtraron. El filtrado se concentró al vacío. El residuo se purificó por cromatografía en gel de sílice (eluyendo con éter de petróleo/acetato de etilo 15:1) para proporcionar 5-bromo-1-[[2-(trimetilsilil)etoxi]metil]-1H-pirazol-3-carboxilato de metilo (6,20 g, 76%) como un aceite amarillo. LCMS (ES, m/z): 335, 337 [M+H]+.
Paso 2. 5-(2-fenoxifenil)-1-[[2-(trimetilsilil)etoxi]metil]-1H-pirazol-3-carboxilato de metilo
Se agitó una solución de 5-bromo-1-[[2-(trimetilsilil)etoxi]metil]-1H-pirazol-3-carboxilato de metilo (6,20 g, 18,5 mmol), ácido (2-fenoxifenil)borónico (4,96 g, 23,2 mmol)), XPhos-Pd-G3 (3,12 g, 36,9 mmol) y fosfato de potasio tribásico (25,4 mg, 37,1 mmol) en dioxano (120 ml) y agua (24 ml) durante 15 h a 100° C en un baño de aceite. La mezcla se enfrió a 25° C. La mezcla resultante se concentró al vacío. El residuo se diluyó con agua (30 ml). La mezcla resultante se extrajo con acetato de etilo (3 x 30 ml). Las capas orgánicas combinadas se secaron sobre sulfato de sodio anhidro, se filtraron y se concentraron. El residuo se purificó por cromatografía de fase inversa (Columna: Columna XBridge Shield RP18 OBD, 5 μm, 30 x 150 mm; Fase móvil, A: agua (que contenía 0,05% de hidrógeno amónico) y B: acetonitrilo (del 5% de B al 72% durante 20 minutos); detector: UV 220 y 254 nm) para proporcionar 5-(2-fenoxifenil)-1-[[2-(trimetilsilil)etoxi]metil]-1H-pirazol-3-carboxilato de metilo como un sólido amarillo (3,20 g, 41%). LCMS (ES, m/z): 425 [M+H]+.
Paso 3. Ácido 5-(2-fenoxifenil)-1-[[2-(trimetilsilil)etoxi]metil]-1H-pirazol-3-carboxílico
Se agitó una solución de 5-(2-fenoxifenil)-1-[[2-(trimetilsilil)etoxi]metil]-1H-pirazol-3-carboxilato de metilo (1,40 g, 3,30 mmol) e hidróxido de litio (810 mg, 34,0 mmol) en Th F (60,0 ml), agua (15,0 ml) y metanol (300 ml) durante 4 h a 50° C. La mezcla se enfrió a 25° C y se concentró al vacío. El valor de pH del residuo se ajustó a 3-4 con solución acuosa de ácido clorhídrico 3 N. La mezcla resultante se extrajo con acetato de etilo (3 x 30 ml). Las capas orgánicas combinadas se lavaron con salmuera (2 x 100 ml), se secaron sobre sulfato de sodio anhidro, se filtraron y se concentraron. El residuo se purificó por cromatografía en gel de sílice (eluyendo con éter de petróleo/acetato de etilo 2:1) para proporcionar ácido 5-(2-fenoxifenil)-1-[[2-(trimetilsilil)etoxi]metil]-1H-pirazol-3-carboxílico como un sólido blanquecino (1,00 g, 74%). LCMS (ES, m/z): 411 [M+H]+.
Paso 4. 1-(5-(2-fenoxifenil)-1-((2-(trimetilsilil)etoxi)metil)-1H-pirazol-3-carboxamido)-3-azabiciclo[3.2.0]heptano-3-carboxilato de terc-butilo
Se agitó una solución de ácido 5-(2-fenoxifenil)-1-[[2-(trimetilsilil)etoxi]metil]-1H-pirazol-3-carboxílico (300
mg, 0,723 mmol), 1-amino-3- azabiciclo[3.2.0]heptano-3-carboxilato de terc-butilo (154 mg, 0,723 mmol), HATU (275 mg, 0,723 mmol) y N,N-diisopropiletilamina (0,239 ml, 1,45 mmol) en DMF (2 ml) durante 40 min a 25° C. La reacción se inactivó con agua (5 ml). La mezcla resultante se extrajo con acetato de etilo ( 3 x 15 ml). Las capas orgánicas combinadas se lavaron con salmuera (2 x 30 ml), se secaron sobre sulfato de sodio anhidro, se filtraron y se concentraron. El residuo se purificó por cromatografía en gel de sílice (eluyendo con éter de petróleo/acetato de etilo 4:1) para proporcionar 1-(5-(2-fenoxifenil)-1-((2-(trimetilsilil)etoxi)metil)-1H-pirazol-3-carboxamido)-3-azabiciclo[3.2.0]heptano-3-carboxilato de terc-butilo como un sólido blanquecino (350 mg, 80%). LCMS (ES, m/z): 605 [M+H]+.
Paso 5. 2,2,2-trifluoroacetato de N-(3-azabiciclo[3.2.0]heptan-1-il)-5-(2-fenoxifenil)-1H-pirazol-3-carboxamida
Se agitó una solución de 1-(5-(2-fenoxifenil)-1-((2-(trimetilsilil)etoxi)metil)-1H-pirazol-3-carboxamido)-3-azabiciclo[3.2.0]heptano-3-carboxilato de terc-butilo (350 mg, 0,579 mmol) en ácido trifluoroacético (1 ml) y diclorometano (3 ml) durante 30 min a 25° C. La mezcla resultante se concentró al vacío para proporcionar 2,2,2-trifluoroacetato de N-(3-azabiciclo[3.2.0]heptan-1-il)-5-(2-fenoxifenil)-1H-pirazol-3-carboxamida como un aceite marrón (360 mg, bruto). LCMS (ES, m/z): 375 [M+H]+.
Paso 6. N-((1R,5S)-3-ciano-3-azabiciclo[3.2.0]heptan-1-il)-5-(2-fenoxifenil)-1H-pirazol-3-carboxamida (6-a) y N-((1S,5R)-3-ciano-3-azabiciclo[3.2.0]heptan-1-il)-5-(2-fenoxifenil)-1H-pirazol-3-carboxamida (6-b)
Se añadió gota a gota bromuro de cianógeno (72,8 mg, 0,687 mmol) a una solución a 0° C de 2,2,2-trifluoroacetato de N-(3-azabiciclo[3.2.0]heptan-1-il)-5-(2-fenoxifenil)-1H-pirazol-3-carboxamida (350 mg, 0,763 mmol) y bicarbonato de sodio (785 mg, 9,25 mmol) en DMF (2 ml). La mezcla se agitó durante 1 h a 25° C. Los sólidos se filtraron. El filtrado se purificó directamente mediante HPLC preparativa (Columna: Columna OBD XBridge Shield RP18, 5 |jm, 30 x 150 mm; Fase móvil, A: agua (que contenía 0,05% de hidrógeno amónico) y B: acetonitrilo (del 35% de B al 65% durante 7 min); Detector: UV 220 y 254 nm) para proporcionar N-(3-ciano-3-azabiciclo[3.2.0]heptan-1-il)-5-(2-fenoxifenil)-1H-pirazol-3-carboxamida como un sólido blanco (70,0 mg). Este material se separó por HPLC quiral (Columna: Chiralpak IG, 2 x 25 cm, 5 jm ; Fase móvil, A: MTBE y B: EtOH (mantenida al 15% en 24 min); Caudal: 20 ml/min; Detector: 220/254 nm). Se recogió el primer isómero en eluir y la estereoquímica absoluta se asignó arbitrariamente como (1R,5S): N-((1R,5S)-3-ciano-3-azabiciclo[32,01heptan-1-il)-5-(2-fenoxifenil)-1H-pirazol-3-carboxamida (RTi=10,9 min) como un sólido blanco (6-a, 28,5 mg, 10%). lCm S (e S, m/z): 400 [M+H]+. 1H-NMR (DMSO-de, 400 MHz) 6 (ppm): 13.68-13.62 (m, 1H), 8.92-8.61 (m, 1H), 8.03-7.86 (m, 1H), 7.42-7.23 (m, 4H), 7.21-7.12 (m, 1H), 7.03-6.89 (m, 4H) , 3.73-3.70 (m, 1H), 3.68-3.56 (m, 1H), 3.39-3.31 (m, 2H), 3.08-3.05 (m, 1H), 2.34-2.31 (m, 1H), 2.20-2.08 (m, 2H), 1.61-1.58 (m, 1H). Se recogió el segundo isómero en eluir y la estereoquímica absoluta se asignó arbitrariamente como (1S,5R): N-((1S,5R)-3-ciano-3-azabiciclo[3.2.0]heptan-1-il)-5 -(2-fenoxifenil)-1H-pirazol-3-carboxamida (RT2 = 12,7 min) como un sólido blanco (6-b, 20,6 mg, 8%). LCMS (ES, m/z): 400 [M+H]+. 1H-NMR (DMSO-de , 400 MHz) 6 (ppm): 13.68-13.62 (m, 1H), 8.92-8.61 (m, 1H), 8.03-7.86 (m, 1H), 7.42-7.29 (m, 4H), 7.21-7.12 (m, 1H), 7.04-6.89 (m, 4H), 3.73-3.70 (m, 1H), 3.68-3.54 (m, 1H), 3.39-3.31 (m, 2H), 3.08-3.05 (m, 1H), 2.34-2.31 (m, 1H), 2.20-2.08 (m, 2H), 1.61-1.58 (m, 1H). Alternativamente, la estereoquímica absoluta del primer y segundo isómero en eluir podría haberse asignado arbitrariamente como (1S,5R) y (1R,5S), respectivamente.
Ejemplo 4: Preparación de N-((1S,5R)-3-ciano-3-azabiciclo[3.1.01hexan-1-il)-5-(2-fenoxifenil)-1H-pirazol-3-carboxamida (3-a) y N-((1R.5S)-3-c¡ano-3-azab¡c¡clo[3.1.01hexan-1-il)-5-(2-fenox¡fen¡l)-1H-p¡razol-3-carboxam¡da (3-b)
Los compuestos 3-a y 3-b se prepararon por la siguiente vía:
Paso 1. 5-bromo-1-[[2-(trimetilsilil)etoxi]metil]-1H-pirazol-3-carboxilato de metilo
Se añadió gota a gota cloruro de 2-(trimetilsMil)etoximetilo (12,2 ml, 68,8 mmol) a una solución a 0° C de 5-bromo-1H-pirazol-3-carboxilato de metilo (5,00 g, 24,5 mmol) y carbonato de potasio (18,0 g, 130 mmol) en DMF (10 ml). La mezcla resultante se agitó durante 14 h a 25° C. La reacción se inactivó con agua (20 ml) a 0° C. La mezcla resultante se extrajo con acetato de etilo (3 x 30 ml). Las capas orgánicas combinadas se lavaron con salmuera (2 x 100 ml), se secaron sobre sulfato de sodio anhidro y se filtraron. El filtrado se concentró al vacío. El residuo se purificó por cromatografía en gel de sílice (eluyendo con éter de petróleo/acetato de etilo 15:1) para proporcionar 5-bromo-1-[[2-(trimetilsilil)etoxi]metil]-1H-pirazol-3-carboxilato de metilo (6,20 g, 76%) como un aceite amarillo. LCMS (ES, m/z): 335, 337 [M+H]+.
Paso 2. 5-(2-fenoxifenil)-1-[[2-(trimetilsilil)etoxi]metil]-1H-pirazol-3-carboxilato de metilo
Se agitó una solución de 5-bromo-1-[[2-(trimetilsilil)etoxi]metil]-1H-pirazol-3-carboxilato de metilo (6,20 g, 18,5 mmol), ácido (2-fenoxifenil)borónico (4,96 g, 23,2 mmol)), XPhos-Pd-G3 (3,12 g, 36,9 mmol) y fosfato de potasio tribásico (25,4 mg, 37,1 mmol) en dioxano (120 ml) y agua (24 ml) durante 15 h a 100° C en un baño de aceite. La mezcla se enfrió a 25° C. La mezcla resultante se concentró al vacío. El residuo se diluyó con agua (30 ml). La mezcla resultante se extrajo con acetato de etilo (3 x 30 ml). Las capas orgánicas combinadas se secaron sobre sulfato de sodio anhidro, se filtraron y se concentraron. El residuo se purificó por cromatografía de fase inversa (Columna: Columna XBridge Shield RP18 OBD, 5 μm, 30 x 150 mm; Fase móvil, A: agua (que contenía un 0,05% de hidrógeno amónico) y B: acetonitrilo (del 5% de B al 72% durante 20 minutos); detector: UV 220 y 254 nm) para proporcionar 5-(2-fenoxifenil)-1-[[2-(trimetilsilil)etoxi]metil]-1H-pirazol-3-carboxilato de metilo como un sólido amarillo (3,20 g, 41%). LCMS (ES, m/z): 425 [M+H]+.
Paso 3. Ácido 5-(2-fenoxifenil)-1-[[2-(trimetilsilil)etoxi]metil]-1H-pirazol-3-carboxílico
Se agitó una solución de 5-(2-fenoxifenil)-1-[[2-(trimetilsilil)etoxi]metil]-1H-pirazol-3-carboxilato de metilo (1,40 g, 3,30 mmol) e hidróxido de litio (810 mg, 34,0 mmol) en THF (60,0 ml), agua (15,0 ml) y metanol (30,0 ml) durante 4 h a 50° C. La mezcla se enfrió a 25° C y se concentró al vacío. El valor de pH del residuo se ajustó a 3-4 con solución acuosa de ácido clorhídrico 3 N. La mezcla resultante se extrajo con acetato de etilo (3 x 30 ml). Las capas orgánicas combinadas se lavaron con salmuera (2 x 100 ml), se secaron sobre sulfato de sodio anhidro, se filtraron y se concentraron. El residuo se purificó por cromatografía en gel de sílice (eluyendo con éter de petróleo/acetato de etilo 2:1) para proporcionar ácido 5-(2-fenoxifenil)-1-[[2-(trimetilsilil)etoxi]metil]-1H-pirazol-3-carboxílico como un sólido blanquecino (1,00 g, 74%). LCMS (ES, m/z): 411 [M+H]+.
Paso 4. terc-butil-(5-(2-fenoxifenil)-1-((2-(trimetilsilil)etoxi)metil)-1H-pirazol-3-carboxamido)-3-azabiciclo[3.1.0]hexano-3-carboxilato
Se agitó una solución de ácido 5-(2-fenoxifenil)-1-[[2-(trimetilsilil)etoxi]metil]-1H-pirazol-3-carboxílico (300 mg, 0,723 mmol), 1-amino-3- azabiciclo[3.1.0]hexano-3-carboxilato de terc-butilo (145 mg, 0,723 mmol), HATU (278 mg, 0,723 mmol) y N,N-diisopropiletilamina (0,242 ml, 1,47 mmol) en DMF (3 ml) durante 30 min a 25° C. La reacción se inactivó con agua (10 ml) a 25° C. La mezcla resultante se extrajo con acetato de etilo ( 3 x 10 ml). Las capas orgánicas combinadas se lavaron con salmuera (2 x 30 ml), se secaron sobre sulfato de sodio anhidro, se filtraron y se concentraron. El residuo se purificó por cromatografía en gel de sílice (eluyendo con éter de petróleo/acetato de etilo 4:1) para proporcionar 1-(5-(2-fenoxifenil)-1-((2-(trimetilsilil)etoxi)metil)-1H-pirazol-3-carboxamido)-3-azabiciclo[3.1.0]hexano-3-carboxilato de terc-butilo como un sólido blanquecino (280 mg, 67%).
LCMS (ES, m/z): 591 [M+H]+.
Paso 5. 2,2,2-trifluoroacetato de N-(3-azabiciclo[3.1.0]hexan-1-il)-5-(2-fenoxifenil)-1H-pirazol-3-carboxamida
Se agitó una solución de 1-(5-(2-fenoxifenil)-1-((2-(trimetilsilil)etoxi)metil)-1H-pirazol-3-carboxamido)-3-azabiciclo[3.1.0]hexano-3-carboxilato de terc-butilo (280 mg, 0,475 mmol) en ácido trifluoroacético (1 ml) y diclorometano (3 ml) durante 2 h a 25° C. La mezcla resultante se concentró al vacío para proporcionar 2,2,2-trifluoroacetato de N-(3-azabiciclo[3.1.0]hexan-1-il)-5-(2-fenoxifenil)-1H-pirazol-3-carboxamida como un aceite amarillo (285 mg, bruto). LCMS (ES, m/z): 361 [M+H]+.
Paso 6. N-((1S,SR)-3-ciano-3-azabiciclo[3.1.0]hexan-1-il)-S-(2-fenoxifenil)-1H-pirazol-3-carboxamida (3-a) y N-((1R,5S)-3-ciano-3-azabiciclo[3.1.0]hexan-1-il)-5-(2-fenoxifenil)-1H-pirazol-3-carboxamida (3-b)
Se añadió gota a gota bromuro de cianógeno (58,5 mg, 0,552 mmol) a una solución a 0° C de 2,2,2-trifluoroacetato de N-(3-azabiciclo[3.1.0]hexan-1-il)-5-(2-fenoxifenil)-1H-pirazol-3-carboxamida (280 mg, 0,613 mmol) y bicarbonato de sodio (653 mg, 7,69 mmol) en DMF (2 ml). La mezcla se agitó durante 1 h a 25° C. La reacción se enfrió a 0° C y se inactivó con agua (10 ml). La mezcla resultante se extrajo con acetato de etilo (3 x 10 ml). Las capas orgánicas combinadas se lavaron con salmuera (20 ml), se secaron sobre sulfato de sodio anhidro, se filtraron y se concentraron. El residuo se purificó por HPLC preparativa (Columna: Columna XBridge Shield RP18 OBD, 5 |jm, 30 x 150 mm; Fase móvil, A: agua (que contenía un 0,05% de hidrógeno amónico) y B: acetonitrilo (del 28% de
B al 48% durante 7 min); Detector: UV 220 y 254 nm) para proporcionar N-(3-ciano-3-azabiciclo[3.1.0]hexan-1-il)-5-(2-fenoxifenil)-1H-pirazol-3-carboxamida como un sólido blanco (60,0 mg). Este material se separó por HPLC quiral (Columna: Chiralpak IG, 2 x 25 cm, 5 jm ; Fase móvil, A: Mt Be y B: EtOH (manteniendo al 30% en 10,5 min);
Caudal: 13 ml/min; Detector: 220/254nm). Se recogió el primer isómero en eluir y la estereoquímica absoluta se asignó arbitrariamente como (1S,5R): N-((1S,SR)-3-ciano-3-azabiciclo[3.1.0]hexan-1-il)-5-(2-fenoxifenil)-1H-pirazol-3-carboxamida (RT1=6,45 min) como un sólido rosa (3-a, 30,3 mg, 14%). Lc MS (ES, m/z): 386 [M+H]+. 1H-NMR (DMSO-de, 400 MHz) 6 (ppm): 13.72-13.64 (m, 1H), 9.08-8.70 (m, 1H), 8.05-7.85 (m, 1H), 7.44-7.29 (m, 4H), 7.20 7.12 (m, 1H), 7.04-6.87 (m, 4H), 3.69-3.66 (m, 1H), 3.57-3.48 (m, 3H), 1.78-1.74 (m, 1H), 1.17-1.14 (m, 1H), 0.87 0.82 (m, 1H). Se recogió el segundo isómero en eluir y la estereoquímica absoluta se asignó arbitrariamente como (1R,5S); N-((1R,5S)-3-ciano-3-azabiciclo[3.1.0]hexan-1-il)-5-(2-fenoxifenil)-1H-pirazol-3-carboxamida (RT2=8,97 min) (3-b, 29,9 mg, 14%) como un sólido blanco. LCMS (ES, m/z): 386 [M+H]+. 1H-NMR (DMSO-de, 400 MHz) 6 (ppm):
13.72-13.64 (m, 1H), 9.08-8.70 (m, 1H), 8.05-7.85 (m, 1H), 7.44-7.29 (m, 4H), 7.22-7.12 (m, 1H), 7.04 -6.87 (m, 4H), 3.69-3.66 (m, 1H), 3.57-3.51 (m, 3H), 1.78-1.74 (m, 1H), 1.17-1.14 (m, 1H), 0.87-0.82 (m, 1H). Alternativamente, la estereoquímica absoluta del primer y segundo isómero en eluir podría haberse asignado arbitrariamente como (1R,5S) y (1S,5R), respectivamente.
Pueden realizarse muchas modificaciones y variaciones de las realizaciones descritas en la presente sin apartarse del alcance de las reivindicaciones, como es evidente para los expertos en la técnica. Las realizaciones específicas descritas en la presente se ofrecen únicamente a modo de ejemplo.
Claims (1)
- REIVINDICACIONES1. Un compuesto de fórmula (I):o una sal farmacéuticamente aceptable del mismo, en dondeRa, Rb, Rc, Rd, Re, Rf, Rg y Rh se definen de la siguiente manera:(i) Ra y Rb forman un grupo alquileno C1-C4 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C4 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno,alquilo C1-C3 y haloalquilo C1-C3; y Rc, Rd, Re, Rf, Rg y Rh son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3 ; o(ii) Ra y Re forman un grupo alquileno C1-C2 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C2 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno,alquilo C1 -C3 y haloalquilo C1-C3 ; y Rb, Rc, Rd, Re, Rf, Rg y Rh son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3 ; o(iii) Ra y Rg forman un grupo alquileno C1-C3 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C3 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno,alquilo C1-C3 y haloalquilo C1-C3 ; y Rb, Rc, Rd, Re, Rf y Rh son cada uno halógeno, alquilo C1-C3 o haloalquilo C1-C3 ; o(iv) Rb y Rc forman un grupo alquileno C1-C4 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C4 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno,alquilo C1-C3 y haloalquilo C1-C3; y Ra, Rd, Re, Rf, Rg y Rh son c halógeno, alquilo C1-C3 o haloalquilo C1-C3 ; o(v) Rb y Re forman un grupo alquileno C1-C3 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C3 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno,alquilo C1-C3 y haloalquilo C1-C3; y Ra, Rc, Rd, Rf, Rg y Rh son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3 ; o(vi) Rb y Rg forman un grupo alquileno C1-C4 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C4 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno,alquilo C1-C3 y haloalquilo C1-C3; y Ra, Rc, Rd, Re, Rf y Rh son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3 ; o(vii) Rc y Rd junto con el átomo al que están unidos, forman un cicloalquilo o heterocicloalquilo de 3-6 miembros, en donde dicho cicloalquilo o heterocicloalquilo de 3-6 miembros está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3 ; y Ra, Rb,Re, Rf, Rg y Rh sonn cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3; o(viii) Rc y Rd juntos forman =O; y Ra, Rb, Re, Rf, Rg y Rh son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3 ; o(ix) Rc y Re forman un grupo alquileno C1-C4 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C4 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno,alquilo C1-C3 y haloalquilo C1-C3 ; y Ra, Rb, Rd, Rf, Rg y Rh son cada uno i halógeno, alquilo C1-C3 o haloalquilo C1-C3 ; o(x) Rc y Rg forman un grupo alquileno C1-C3 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C3 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno,alquilo C1-C3 y haloalquilo C1-C3; y Ra, Rb, Rd, Re, Rf y Rh son cada uno i halógeno, alquilo C1-C3 o haloalquilo C1-C3 ; o(xi) Re y Rf junto con el átomo al que están unidos, forman un cicloalquilo o heterocicloalquilo de 3-6 miembros, en donde dicho cicloalquilo o heterocicloalquilo de 3-6 miembros está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3 ; y Ra, Rb,Rc, Rd, Rg y Rh son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3 ; o(xii) Re y Rf juntos forman =O; y Ra, Rb, Rc, Rd, Rg y Rh son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3; o(xiii) Re y Rg forman un grupo alquileno C1-C3 entre los átomos a los que están unidos, en donde dicho grupo alquileno C1-C3 está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno,alquilo C1-C3 y haloalquilo C1-C3 ; y Ra, Rb, Rc, Rd, Rf y Rh son cada uno halógeno, alquilo C1-C3 o haloalquilo C1-C3 ; o(xiv) Rg y Rh junto con el átomo al que están unidos, forman un cicloalquilo o heterocicloalquilo de 3-6 miembros, en donde dicho cicloalquilo o heterocicloalquilo de 3-6 miembros está sustituido con 0-4 sustituyentes seleccionados del grupo que consiste en halógeno, alquilo C1-C3 y haloalquilo C1-C3 ; y Ra, Rb, Rc, Rd, Re y Rf son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3 ; o (xv) Rg y Rh juntos forman =O; y Ra, Rb, Rc, Rd, Re y Rf son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3 ; yAr1 es fenileno o heteroarileno de 5-6 miembros, en donde dicho fenileno o heteroarileno está sustituido con m grupos R1; yAr2 es fenileno o heteroarileno de 5-10 miembros, en donde dicho fenileno o heteroarileno está sustituido con n grupos R2;L es-O-, -S-, -NR3-, -C(R4)2-, -S(O)2-, o -S(O)-;M es cicloalquilo de 3 a 6 miembros, fenilo o heteroarilo de 5 a 6 miembros, en donde dicho cicloalquilo, fenilo o heteroarilo está sustituido con p grupos R5;cada aparición de R1, R2 y R5 es independientemente halo, ciano, NO2, oxo, hidroxilo,-R6, -OR6, alquilo C1-C6, haloalquilo C1-C6 , hidroxialquilo C1-C6, -alquileno C1-C6-R6 , alcoxi C1-C6, haloalcoxi Ci-C6,-alquileno C0-C3-NR6R7,-alquileno C0-C3-NR7R8, -alquileno C rC 3-C(O)NR6R7, -alquileno C0-C3-C(O)NR7R8, -alquileno C0-C3-NR7C(O)R6, -alquileno C0-C3-NR7C(O)R8, -alquileno C0-C3-NR7S(O)2R6, -alquileno C0-C3-C(O)R6, -alquileno C0-C3-C(O)R7, -alquileno C0-C3 -SR6, -alquileno C0-C3-S(O)R6, -alquileno C0-C3-S(O)2R6, -alquileno C0-C3-S(O)2R7, -alquileno C rC 3S(O)2NR6R7, -alquileno C0-C3-S(O)2NR7R8, -alquileno C rC 3-NR7C(O)NR8R9, -alquileno C0-C3-n R7S(O)2NR8R9, -alquileno C0-C3-C(O)OR7, -alquileno C0-C3-C(O)OR6, -alquileno C0-C3-OC(O)R7, -alquileno C0-C3-OC(O)R6, -alquileno C0-C3 - NR7C(O)OR8, o -alquileno C0-C3-NR7S(O)2R8;R3 es H, alquilo C1-C6 o haloalquilo C1-C6 ;cada R4 es independientemente H, alquilo C1-C6 o haloalquilo C1-C6, o dos grupos R4 junto con el átomo de carbono al que están unidos forman un cicloalquilo o heterocicloalquilo de 3-6 miembros;cada R6 es independientemente heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, arilo de 6-10 miembros o cicloalquilo de 3-8 miembros, en donde dicho heteroarilo, heterocicloalquilo, arilo o cicloalquilo está opcionalmente sustituido con de 1 a 5 sustituyentes seleccionados independientemente del grupo formado por halo, oxo, alquilo C1-C6, haloalquilo C1-C6 , hidroxialquilo C1-C6 , alcoxi C1-C6, haloalcoxi C1-C6, alquenilo C2-C6 6 , alquinilo C2-C6 6, heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, arilo de 6-10 miembros, cicloalquilo de 3-8 miembros, -NR10C(O)NR11R12, -NR10R11, -C(O)R10, -NR10C(O)R11, -NR10C(O)OR11, -S(O)2R10, -C(O)NR10R11, -C(O)OR10, - S(O)2NR10R11, -NR10S(O)2R11, -OR10, -OC(O)R10, -OS(O)2R10, -OC(O)NR10R11, -OC(O)OR10, - OS(O)2NR10R11, -C(O)NR10C(O)NR11R12, -C(O)C(O)R10, -C(O)NR10C(O)R11, - C(O)NR10C(O)OR11, -C(O)S(O)2R10, -C(O)C(O)NR10R11, -C(O)C(O)OR10, -C(O)S(O)2NR10R11, -C(O)NR10S(O)2R11, - alquileno C1-C6-R10, -alquileno C1-C6-NR10C(O)NR11R12, -alquileno C1-C6-NR10R11, -alquileno C1-C6-C(O)R10, -alquileno C1-C6-NR10C(O)R11, -alquileno C1-C6-NR10C(O)OR11, -alquileno C1-C6-S(O)2R10, -alquileno C1-C6-C(O)NR10R11, -alquileno C1-C6-C(O)OR10, -alquileno C1-C6-S(O)2NR10R11, -alquileno C1-C6-NR10S(O)2R11, -alquenileno C1-C6-R10, -alquenileno C1-C6-NR10C(O)NR11R12, -alquenileno C1-C6-NR10R11, -alquenileno C1-C6-C(O)R10, -alquenileno C1-C6-NR10C(O)R11, -alquenileno C1-C6-NR10C(O)OR11, -alquenileno C1-C6-S(O)2R10, -alquenileno C1-C6-C(O)NR10R11, -alquenileno C1-C6-C(O)OR10, -alquenileno C1-C6-S(O)2NR10R11, y -alquenileno C1-C6-NR10S(O)2R11;cada R7, R8 y R9 es independientemente hidrógeno o alquilo C1-C6 ;cada R10, R11 y R12 es independientemente hidrógeno, alquilo C1-C6 , heteroarilo de 5-10 miembros, heterocicloalquilo de 4-10 miembros, arilo de 6-10 miembros o cicloalquilo de 3-8 miembros;m es 0-4;n es 0-4; yp es 0-4.2. El compuesto de la reivindicación 1, en donde el compuesto es:(a) de fórmula (I-B):o una sal farmacéuticamente aceptable del mismo, en donde:X1 es C o N;X2 es CH, CR1, O, S, N, NH o NR1, según lo permita la valencia;X3 es CH, CR1, O, S, N, NH o NR1, según lo permita la valencia;X4 es C o N;X6 es CH, CR, O, S, N, NH o NR1, según lo permita la valencia;Y3 esCH, CR2 oN;Y4 es CH, CR2 o N;Y5 esCH, CR2 o N;Y6 es CH, CR2 o N; y/o(b) de fórmula (I-C):o una sal farmacéuticamente aceptable del mismo; y/o(c) de fórmula (I-E):o una sal farmacéuticamente aceptable del mismo.3. El compuesto de la reivindicación 1 o la reivindicación 2, en donde Rb y Rc forman un grupo alquileno C1-C4 entre los átomos a los que están unidos, y Ra, Rd, Re, Rf, Rg y Rh son cada uno hidrógeno.4. El compuesto de cualquiera de las reivindicaciones 1-3, en donde el compuesto es:(a) de fórmula (I-1):o una sal farmacéuticamente aceptable del mismo, en donde Rj, Rk, Rm y Rn son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3,opcionalmente en donde:(i) el compuesto es de fórmula (I-B-1):o una sal farmacéuticamente aceptable del mismo; y/o(ii) el compuesto es de fórmula (I-C-1):o una sal farmacéuticamente aceptable del mismo; y/o(iii) Ra, Rd, Re, Rf, Rg, Rh, Rj, Rk, Rm y Rn son cada uno hidrógeno; o(b) de fórmula (I-2):o una sal farmacéuticamente aceptable del mismo, en donde Rj y Rk son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3, opcionalmente en donde:(i) el compuesto es de fórmula (I-B-2):o una sal farmacéuticamente aceptable del mismo; y/o(ii) el compuesto es de fórmula (I-C-2):o una sal farmacéuticamente aceptable del mismo; y/o(iii) Ra, Rd, Re, Rf, Rg, Rh, Rj y Rk son cada uno hidrógeno; o(c) de fórmula (I-3):o una sal farmacéuticamente aceptable del mismo, en donde Rj, Rk, Rm, Rn, Ro y Rp son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3 , opcionalmente en donde:(i) el compuesto es de fórmula (I-B-3):o una sal farmacéuticamente aceptable del mismo; y/o(ii) el compuesto es de fórmula (I-C-3):o una sal farmacéuticamente aceptable del mismo; y/o(iii) Ra, Rd, Re, Rf, Rg, Rh, Rj, Rk, Rm, Rn, Ro y Rp son cada uno hidrógeno.5. El compuesto de la reivindicación 1 o la reivindicación 2, en donde:(a) Rc y Re forman un grupo alquileno C1-C4 entre los átomos a los que están unidos; y Ra, Rb, Rd, cada uno hidrógeno; y/o(b) el compuesto es de fórmula (I-4):o una sal farmacéuticamente aceptable del mismo, donde Rq y Rr son cada uno independientemente hidrógeno, halógeno, alquilo C1-C3 o haloalquilo C1-C3 , opcionalmente en donde:(i) el compuesto es de fórmula (I-B-4):o una sal farmacéuticamente aceptable del mismo; y/o(ii) el compuesto es de fórmula (I-C-4):o una sal farmacéuticamente aceptable del mismo; y/o(iii) Ra, Rb, Rd, Rf, Rg, Rh, Rq y Rr son cada uno hidrógeno.6. El compuesto de la reivindicación 1 o la reivindicación 2, en donde:(a) Ra y Re forman un grupo alquileno C1-C2 entre los átomos a los que están unidos; y Rb, Rc, Rd, Rf, Rg y Rh son cada uno hidrógeno; o(b) R y Rd junto con el átomo al que están unidos, forman un cicloalquilo o heterocicloalquilo de 3-6 miembros; y Ra, Rb, Re, Rf, Rg y Rh son cada uno hidrógeno; o(c) Rc y Rg forman un grupo alquileno C1-C3 entre los átomos a los que están unidos; y Ra, Rb, Rd, Re, Rf y Rh son cada uno hidrógeno; o(d) Re y Rf junto con el átomo al que están unidos, forman un cicloalquilo o heterocicloalquilo de 3-6 miembros; y Ra, Rb, Rc, Rd, Rg y Rh son cada uno hidrógeno; o(e) Re y Rg forman un grupo alquileno C1-C3 entre los átomos a los que están unidos; y Ra, Rb, Rc, Rd, Rf y Rh son cada uno hidrógeno.7. El compuesto de cualquiera de las reivindicaciones anteriores, en donde Ar1 es:(a) heteroarileno de 5-6 miembros, opcionalmente en donde Ar1 es heteroarileno de 5 miembros; o (b) fenileno.8. El compuesto de cualquiera de las reivindicaciones anteriores, en donde Ar2 es:(a) heteroarileno de 5-10 miembros; o(b) fenileno; o(c) fenileno o heteroarileno de 5-6 miembros.9. El compuesto de cualquiera de las reivindicaciones anteriores, en donde L es:(a) -O-, -S- o -NH-; o(b) -O-.10. El compuesto de cualquiera de las reivindicaciones anteriores, en donde:(a) M es fenilo sustituido con p grupos R5,opcionalmente en donde M es opcionalmente fenilo; y/o(b) cada aparición de R1, R2 y R5 se selecciona independientemente de halo, ciano, hidroxilo, alquilo C1-C6, alcoxi C1-C6 , haloalquilo C1-C6 e hidroxialquilo C1-C6; y/o(c) m es 0; y/o(d) n es 0; y/o(e) p es 0 o 1,opcionalmente en donde p es 0.11. El compuesto de cualquiera de las reivindicaciones anteriores, en dondese selecciona de:12. Un compuesto de acuerdo con la reivindicación 1 o una sal farmacéuticamente aceptable del mismo, en donde el compuesto se selecciona de:continuacióncontinuacióncontinuacióncontinuaciónen donde el compuesto se selecciona decontinuacióncontinuacióncontinuacióncontinuacióncontinuacióncontinuacióncontinuacióncontinuacióncontinuacióncontinuacióncontinuacióncontinuacióncontinuacióncontinuacióncontinuacióncontinuacióncontinuacióncontinuacióncontinuacióncontinuacióncontinuacióncontinuacióncontinuacióncontinuacióncontinuacióncontinuacióncontinuacióncontinuacióncontinuacióncontinuacióncontinuacióncontinuacióncontinuacióncontinuacióncontinuacióncontinuacióncontinuacióncontinuacióncontinuacióncontinuacióncontinuacióncontinuación13. Una composición farmacéutica que comprende el compuesto de cualquiera de las reivindicaciones 1-12, o una sal farmacéuticamente aceptable del mismo, y un portador farmacéuticamente aceptable.14. Un compuesto de cualquiera de las reivindicaciones 1-12, o una sal farmacéuticamente aceptable del mismo, o una composición farmacéutica de la reivindicación 13 para su uso en un método para inhibir USP30 en un paciente con necesidad de ello, que comprende administrar al paciente una cantidad terapéuticamente eficaz del compuesto de cualquiera de las reivindicaciones 1-12, o una sal farmacéuticamente aceptable del mismo, o la composición farmacéutica de la reivindicación 13.15. Un compuesto de cualquiera de las reivindicaciones 1-12, o una sal farmacéuticamente aceptable del mismo, o una composición farmacéutica de la reivindicación 13 para su uso en un método para tratar un trastorno neurodegenerativo en un paciente con necesidad de ello, que comprende administrar al paciente una cantidad terapéuticamente eficaz del compuesto de cualquiera de las reivindicaciones 1-12, o una sal farmacéuticamente aceptable del mismo, o la composición farmacéutica de la reivindicación 13,opcionalmente en donde el trastorno neurodegenerativo es la enfermedad de Parkinson.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201862741945P | 2018-10-05 | 2018-10-05 | |
| PCT/US2019/054803 WO2020072964A1 (en) | 2018-10-05 | 2019-10-04 | Fused pyrrolines which act as ubiquitin-specific protease 30 (usp30) inhibitors |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2945834T3 true ES2945834T3 (es) | 2023-07-07 |
Family
ID=68296856
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES19791136T Active ES2945834T3 (es) | 2018-10-05 | 2019-10-04 | Pirrolinas fusionadas que actúan como inhibidores de la proteasa 30 específica de ubiquitina (USP30) |
Country Status (28)
| Country | Link |
|---|---|
| US (2) | US11535618B2 (es) |
| EP (2) | EP3860989B1 (es) |
| JP (1) | JP2022504211A (es) |
| KR (1) | KR20210072791A (es) |
| CN (1) | CN113166108A (es) |
| AU (1) | AU2019356011A1 (es) |
| BR (1) | BR112021003620A2 (es) |
| CA (1) | CA3110113A1 (es) |
| CL (1) | CL2021000793A1 (es) |
| CO (1) | CO2021005070A2 (es) |
| CY (1) | CY1126067T1 (es) |
| DK (1) | DK3860989T3 (es) |
| EA (1) | EA202190960A1 (es) |
| ES (1) | ES2945834T3 (es) |
| FI (1) | FI3860989T3 (es) |
| HR (1) | HRP20230409T1 (es) |
| HU (1) | HUE062240T2 (es) |
| IL (1) | IL281980A (es) |
| LT (1) | LT3860989T (es) |
| MA (1) | MA53816A (es) |
| MX (1) | MX2021002981A (es) |
| PE (1) | PE20211053A1 (es) |
| PL (1) | PL3860989T3 (es) |
| PT (1) | PT3860989T (es) |
| RS (1) | RS64321B1 (es) |
| SG (1) | SG11202102815SA (es) |
| SI (1) | SI3860989T1 (es) |
| WO (1) | WO2020072964A1 (es) |
Families Citing this family (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| AU2018346597B2 (en) | 2017-10-06 | 2023-07-13 | Forma Therapeutics, Inc. | Inhibiting Ubiquitin Specific Peptidase 30 |
| EP3860989B1 (en) | 2018-10-05 | 2023-04-05 | Forma Therapeutics, Inc. | Fused pyrrolines which act as ubiquitin-specific protease 30 (usp30) inhibitors |
| GB201912674D0 (en) | 2019-09-04 | 2019-10-16 | Mission Therapeutics Ltd | Novel compounds |
| JP2023520727A (ja) | 2020-04-08 | 2023-05-18 | ミッション セラピューティクス リミティド | Usp30阻害剤として活性を有するn-シアノピロリジン |
| EP4157834A1 (en) | 2020-05-28 | 2023-04-05 | Mission Therapeutics Limited | N-(1-cyano-pyrrolidin-3-yl)-5-(3-(trifluoromethyl)phenyl)oxazole-2-carboxamide derivatives and the corresponding oxadiazole derivatives as usp30 inhibitors for the treatment of mitochondrial dysfunction |
| CN115698001A (zh) | 2020-06-04 | 2023-02-03 | 特殊治疗有限公司 | 具有作为usp30抑制剂活性的n-氰基吡咯烷类化合物 |
| WO2021249909A1 (en) | 2020-06-08 | 2021-12-16 | Mission Therapeutics Limited | 1-(5-(2-cyanopyridin-4-yl)oxazole-2-carbonyl)-4-methylhexahydropyrrolo[3,4-b]pyr role-5(1h)-carbonitrile as usp30 inhibitor for use in the treatment of mitochondrial dysfunction, cancer and fibrosis |
| GB202016800D0 (en) | 2020-10-22 | 2020-12-09 | Mission Therapeutics Ltd | Novel compounds |
| WO2023099561A1 (en) | 2021-12-01 | 2023-06-08 | Mission Therapeutics Limited | Substituted n-cyanopyrrolidines with activity as usp30 inhibitors |
Family Cites Families (191)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20030191279A1 (en) | 1999-08-27 | 2003-10-09 | Goldstein Steven Wayne | Urea derivatives useful as anticancer agents |
| US6576632B1 (en) | 1999-08-27 | 2003-06-10 | Pfizer Inc | Biaryl compounds useful as anticancer agents |
| BR0014076A (pt) | 1999-09-17 | 2002-10-15 | Millennium Pharm Inc | Benzamidas e inibidores correlatos do fator xa |
| US6632815B2 (en) | 1999-09-17 | 2003-10-14 | Millennium Pharmaceuticals, Inc. | Inhibitors of factor Xa |
| CN1390206A (zh) | 1999-09-17 | 2003-01-08 | 千嬉药品公司 | 因子Xa的抑制剂 |
| CA2387892A1 (en) | 1999-10-18 | 2001-04-26 | University Of Connecticut | Pyrazole derivatives as cannabinoid receptor antagonists |
| EP1259485B1 (en) | 2000-02-29 | 2005-11-30 | Millennium Pharmaceuticals, Inc. | BENZAMIDES AND RELATED INHIBITORS OF FACTOR Xa |
| AU2001256981A1 (en) | 2000-04-06 | 2001-10-23 | Axys Pharmaceuticals, Inc. | Cathepsin cysteine protease inhibitors |
| CZ20031554A3 (cs) | 2000-12-06 | 2003-08-13 | Aventis Pharma Deutschland Gmbh | Guanidinové a amidinové deriváty jako inhibitory faktoru XA |
| EP1217000A1 (en) | 2000-12-23 | 2002-06-26 | Aventis Pharma Deutschland GmbH | Inhibitors of factor Xa and factor VIIa |
| WO2003007955A2 (en) | 2001-07-20 | 2003-01-30 | Cancer Research Technology Limited | Biphenyl apurinic/apyrimidinic site endonuclease inhibitors to treat cancer |
| JP2005507875A (ja) | 2001-08-31 | 2005-03-24 | ユニバーシティ オブ コネチカット | カンナビノイド受容体に作用する新規なピラゾール類似体 |
| JP4881559B2 (ja) | 2002-06-27 | 2012-02-22 | ノボ・ノルデイスク・エー/エス | 治療薬としてのアリールカルボニル誘導体 |
| WO2004014902A2 (en) | 2002-08-09 | 2004-02-19 | Astrazeneca Ab | Compounds having an activity at metabotropic glutamate receptors |
| EP1536790A2 (en) | 2002-08-09 | 2005-06-08 | AstraZeneca AB | Oxadiazoles as modulators of metabotropic glutamate receptor-5 |
| TW201018661A (en) | 2003-03-14 | 2010-05-16 | Ono Pharmaceutical Co | Heterocyclic rinf having nitrogen atom derivatives and medicament containing the derivatives as active ingredient |
| AR043633A1 (es) | 2003-03-20 | 2005-08-03 | Schering Corp | Ligandos de receptores de canabinoides |
| US7244739B2 (en) | 2003-05-14 | 2007-07-17 | Torreypines Therapeutics, Inc. | Compounds and uses thereof in modulating amyloid beta |
| GB0315111D0 (en) | 2003-06-27 | 2003-07-30 | Cancer Rec Tech Ltd | Substituted 5-membered ring compounds and their use |
| WO2005019200A2 (en) | 2003-08-14 | 2005-03-03 | Icos Corporation | Aryl piperidine derivatives as vla-1 integrin antagonists and uses thereof |
| GB0325956D0 (en) | 2003-11-06 | 2003-12-10 | Addex Pharmaceuticals Sa | Novel compounds |
| TWI316955B (en) | 2003-11-19 | 2009-11-11 | Chisso Corp | Photo-polymerization liquid composition,polymer or polymer co mposition and optical compensation device thereof |
| WO2005077373A2 (en) | 2004-02-03 | 2005-08-25 | Astrazeneca Ab | Treatment of gastro-esophageal reflux disease (gerd) |
| WO2005077368A2 (en) | 2004-02-03 | 2005-08-25 | Astrazeneca Ab | Treatment of gastro-esophageal reflux disease (gerd) |
| WO2005077345A1 (en) | 2004-02-03 | 2005-08-25 | Astrazeneca Ab | Compounds for the treatment of gastro-esophageal reflux disease |
| KR20070027503A (ko) | 2004-02-18 | 2007-03-09 | 아스트라제네카 아베 | 트리아졸 화합물 및 대사성 글루타메이트 수용체길항제로서 이들의 용도 |
| US7585881B2 (en) | 2004-02-18 | 2009-09-08 | Astrazeneca Ab | Additional heteropolycyclic compounds and their use as metabotropic glutamate receptor antagonists |
| CN1942186B (zh) | 2004-03-09 | 2010-10-06 | 国家卫生研究院 | 吡咯烷化合物 |
| WO2005112540A2 (en) | 2004-05-21 | 2005-12-01 | Merck Patent Gmbh | Liquid crystal compounds, liquid crystal medium and liquid crystal display |
| US8022063B2 (en) | 2004-05-29 | 2011-09-20 | 7Tm Pharma A/S | CRTH2 receptor ligands for medicinal uses |
| EP1758571A1 (en) | 2004-05-29 | 2007-03-07 | 7TM Pharma A/S | Crth2 receptor ligands for therapeutic use |
| WO2006015279A1 (en) | 2004-07-28 | 2006-02-09 | Neurogen Corporation | Heterocyclic diamine compounds as ligands of the melanin concentrating hormone receptor useful for the treatment of obesity, diabetes, eating and sexual disorders |
| MX2007002208A (es) | 2004-08-25 | 2007-05-08 | Targegen Inc | Compuestos hetrociclicos y metodos de uso. |
| ATE399832T1 (de) | 2004-09-06 | 2008-07-15 | Merck Patent Gmbh | Polymerisierbares flüssigkristallmaterial |
| DE102004051277A1 (de) | 2004-10-21 | 2006-04-27 | Merck Patent Gmbh | Heterocyclische Carbonylverbindungen |
| DE102004054666A1 (de) | 2004-11-12 | 2006-05-18 | Bayer Cropscience Gmbh | Substituierte Pyrazol-3-carboxamide, Verfahren zur Herstellung und Verwendung als Herbizide und Pflanzenwachstumsregulatoren |
| WO2006063113A2 (en) | 2004-12-07 | 2006-06-15 | Portola Pharmaceuticals, Inc. | Ureas as factor xa inhibitors |
| EP1845972A4 (en) | 2005-01-10 | 2010-12-22 | Univ Connecticut | CANNAPINOID RECEPTORS APPLYING NOVEL HETEROPYRROL ANALOGS |
| AU2006205220B2 (en) | 2005-01-10 | 2012-09-13 | Exelixis, Inc. | Heterocyclic carboxamide compounds as steroid nuclear receptors ligands |
| GB2424881B (en) | 2005-04-07 | 2010-11-24 | Merck Patent Gmbh | Halophenyl derivatives of bisalkylfluorene |
| US20060235028A1 (en) | 2005-04-14 | 2006-10-19 | Li James J | Inhibitors of 11-beta hydroxysteroid dehydrogenase type I |
| DE602006003432D1 (de) | 2005-05-13 | 2008-12-11 | Lilly Co Eli | Latoren des androgenrezeptors |
| GB0510139D0 (en) | 2005-05-18 | 2005-06-22 | Addex Pharmaceuticals Sa | Novel compounds B1 |
| WO2007024744A2 (en) | 2005-08-21 | 2007-03-01 | Exelixis, Inc. | Heterocyclic carboxamide compounds as steroid nuclear receptor ligands |
| WO2007061923A2 (en) | 2005-11-18 | 2007-05-31 | Takeda San Diego, Inc. | Glucokinase activators |
| US20080004273A1 (en) | 2006-05-30 | 2008-01-03 | Stephane Raeppel | Inhibitors of protein tyrosine kinase activity |
| EA200802417A1 (ru) | 2006-06-09 | 2009-06-30 | Икос Корпорейшн | Замещенные фенилуксусные кислоты как dp-2-антагонисты |
| TW200815437A (en) | 2006-06-13 | 2008-04-01 | Bayer Schering Pharma Ag | Substituted aminopyrazolopyridines and salts thereof, pharmaceutical compositions comprising same, methods of preparing same and uses of same |
| TW200815438A (en) | 2006-06-13 | 2008-04-01 | Bayer Schering Pharma Ag | Substituted pyrazolopyridines and salts thereof, pharmaceutical compositions comprising same, methods of preparing same and uses of same |
| WO2008028553A1 (en) | 2006-09-02 | 2008-03-13 | Merck Patent Gmbh | Particle beam process for the alignment of reactive mesogens |
| PT2101760E (pt) | 2006-12-08 | 2013-05-07 | Millennium Pharm Inc | Formulações de dose unitária e métodos de tratamento da trombose com um inibidor oral do fator xa |
| UY30796A1 (es) | 2006-12-15 | 2008-07-31 | Bayer Schering Pharma Ag | 3-h-pirazolopiridinas y sales de éstas, composiciones farmacéuticas que las comprenden, métodos para prepararlas, y sus usos |
| WO2008079291A2 (en) | 2006-12-20 | 2008-07-03 | Amgen Inc. | Substituted heterocycles and methods of use |
| AU2008253118B2 (en) | 2007-05-22 | 2013-11-21 | Madrigal Pharmaceuticals, Inc. | Diacylglycerol acyltransferase inhibitors |
| KR101077417B1 (ko) | 2007-06-12 | 2011-10-26 | 주식회사 엘지화학 | 위상차 필름, 이를 포함하는 편광판 및 액정 표시 장치 |
| WO2009011850A2 (en) | 2007-07-16 | 2009-01-22 | Abbott Laboratories | Novel therapeutic compounds |
| EP2017264A1 (de) | 2007-07-16 | 2009-01-21 | Bayer Cropscience Ag | Substituierte Phenylpropargylverbindungen, Verfahren zu deren Herstellung und deren Verwendung als Herbizide und Pflanzenwachstumsregulatoren |
| JP5057056B2 (ja) | 2007-08-03 | 2012-10-24 | Jsr株式会社 | 液晶配向剤、液晶配向膜の製造方法、ポリアミック酸およびポリイミドならびにジアミン化合物 |
| EP2197869B1 (en) | 2007-10-10 | 2013-04-24 | Basf Se | Sulphonium salt initiators |
| JP2009108152A (ja) | 2007-10-29 | 2009-05-21 | Sumitomo Chemical Co Ltd | 重合性化合物および光学フィルム |
| WO2009078992A1 (en) | 2007-12-17 | 2009-06-25 | Amgen Inc. | Linear tricyclic compounds as p38 kinase inhibitors |
| JP2009149754A (ja) | 2007-12-20 | 2009-07-09 | Sumitomo Chemical Co Ltd | 重合性化合物および該重合性化合物を重合してなる光学フィルム |
| US20090270418A1 (en) | 2008-01-09 | 2009-10-29 | Marianne Sloss | Pyrazole pyrazine amine compounds as kinase inhibitors, compositions thereof and methods of treatment therewith |
| JP5219583B2 (ja) | 2008-03-31 | 2013-06-26 | 住友化学株式会社 | 組成物、光学フィルムとその製造方法、光学部材及び表示装置 |
| TW201002317A (en) | 2008-04-18 | 2010-01-16 | Glaxo Group Ltd | Cathepsin C inhibitors |
| KR101892989B1 (ko) | 2008-06-27 | 2018-08-30 | 셀젠 카르 엘엘씨 | 헤테로아릴 화합물 및 이의 용도 |
| JP5443720B2 (ja) | 2008-09-05 | 2014-03-19 | 住友化学株式会社 | 組成物、光学フィルム及びその製造方法、光学部材ならびに表示装置 |
| JP2010066630A (ja) | 2008-09-12 | 2010-03-25 | Sumitomo Chemical Co Ltd | 光学フィルムの製造方法及び光学フィルム |
| WO2010048149A2 (en) | 2008-10-20 | 2010-04-29 | Kalypsys, Inc. | Heterocyclic modulators of gpr119 for treatment of disease |
| MX2011006332A (es) | 2008-12-23 | 2011-06-27 | Abbott Lab | Compuestos antivirales. |
| KR101641385B1 (ko) | 2009-03-16 | 2016-07-20 | 스미또모 가가꾸 가부시끼가이샤 | 화합물, 광학 필름 및 광학 필름의 제조 방법 |
| JP5899607B2 (ja) | 2009-03-16 | 2016-04-06 | 住友化学株式会社 | 化合物、光学フィルム及び光学フィルムの製造方法 |
| JP2011006360A (ja) | 2009-06-26 | 2011-01-13 | Sumitomo Chemical Co Ltd | 化合物、光学フィルム及び光学フィルムの製造方法 |
| KR101256018B1 (ko) | 2009-08-20 | 2013-04-18 | 한국과학기술연구원 | 단백질 키나아제 저해활성을 갖는 1,3,6-치환된 인돌 화합물 |
| JP2011042606A (ja) | 2009-08-20 | 2011-03-03 | Sumitomo Chemical Co Ltd | 化合物、光学フィルム及び光学フィルムの製造方法 |
| EP2470183B1 (en) | 2009-08-26 | 2015-09-16 | Merck Sharp & Dohme Corp. | Heterocyclic amide compounds as protein kinase inhibitors |
| EP2475254A4 (en) | 2009-09-11 | 2013-05-22 | Enanta Pharm Inc | HEPATITIS C-VIRUS HEMMER |
| WO2011053825A2 (en) | 2009-10-30 | 2011-05-05 | The United States Of America, As Represented By The Secretary, Department Of Health And Human Services | Compositions and methods for the treatment or prevention of mitochondrial diseases |
| TWI510241B (zh) | 2010-02-18 | 2015-12-01 | Vtv Therapeutice Llc | 苯基-雜芳基衍生物及其使用方法 |
| WO2011126903A2 (en) | 2010-03-30 | 2011-10-13 | Verseon, Inc. | Multisubstituted aromatic compounds as inhibitors of thrombin |
| CA2798325A1 (en) | 2010-05-13 | 2011-11-17 | Amgen Inc. | Heteroaryloxyheterocyclyl compounds as pde10 inhibitors |
| GB201010359D0 (en) | 2010-06-21 | 2010-08-04 | Univ Nottingham | Compounds for treating proliferative disorders |
| MY165584A (en) | 2010-07-29 | 2018-04-05 | Rigel Pharmaceuticals Inc | Ampk-activating heterocyclic compounds and methods for using the same |
| DK3366688T3 (da) | 2010-12-08 | 2022-05-02 | Us Health | Substituerede pyrazolpyrimidiner som glucocerebrosidaseaktivatorer |
| JP5728921B2 (ja) | 2010-12-10 | 2015-06-03 | コニカミノルタ株式会社 | 光学フィルム、及びそれを用いた偏光板、液晶表示装置 |
| EP2651927A4 (en) | 2010-12-15 | 2014-06-04 | Abbvie Inc | ANTIVIRAL CONNECTIONS |
| EP2651920A4 (en) | 2010-12-15 | 2014-12-17 | Abbvie Inc | ANTI-VIRAL COMPOUNDS |
| US9464065B2 (en) | 2011-03-24 | 2016-10-11 | The Scripps Research Institute | Compounds and methods for inducing chondrogenesis |
| RU2013150349A (ru) | 2011-04-13 | 2015-05-20 | Мерк Шарп И Доум Корп. | 5-замещенные иминотиазины и их моно- и диоксиды в качестве ингибиторов васе, содержащие их композиции и их применение |
| SG194625A1 (en) | 2011-05-23 | 2013-12-30 | Sanofi Sa | Process for the preparation of deuterated compounds containing n-alkyl groups |
| JP6007417B2 (ja) | 2011-05-31 | 2016-10-12 | レセプトス エルエルシー | 新規glp−1受容体安定剤および調節剤 |
| JP2014518223A (ja) | 2011-06-20 | 2014-07-28 | アルツハイマーズ・インスティテュート・オブ・アメリカ・インコーポレイテッド | 化合物とその治療用途 |
| JP6061922B2 (ja) | 2011-06-22 | 2017-01-18 | ザ ジェネラル ホスピタル コーポレイション | プロテイノパチーの処置方法 |
| EA025183B1 (ru) | 2011-09-27 | 2016-11-30 | Новартис Аг | 3-пиримидин-4-ил-оксазолидин-2-оны в качестве ингибиторов мутантной idh |
| EP2763532B1 (en) | 2011-10-05 | 2018-09-19 | The Board of Trustees of the Leland Stanford Junior University | Pi-kinase inhibitors with broad spectrum anti-infective activity |
| WO2013086229A1 (en) | 2011-12-07 | 2013-06-13 | Amgen Inc. | Bicyclic aryl and heteroaryl sodium channel inhibitors |
| WO2013106678A1 (en) | 2012-01-12 | 2013-07-18 | Envivo Pharmaceuticals, Inc. | Tetrasubstituted benzenes |
| TW201348231A (zh) | 2012-02-29 | 2013-12-01 | Amgen Inc | 雜雙環化合物 |
| JP5798066B2 (ja) | 2012-03-08 | 2015-10-21 | 富士フイルム株式会社 | 化合物、液晶組成物、高分子材料およびフィルム |
| US9013997B2 (en) | 2012-06-01 | 2015-04-21 | Broadcom Corporation | System for performing distributed data cut-through |
| EP2671885A1 (en) | 2012-06-05 | 2013-12-11 | Ares Trading S.A. | Imidazo-oxadiazole and Imidazo-thiadiazole derivatives |
| FR2992317B1 (fr) | 2012-06-22 | 2016-05-13 | Diverchim | Procede de preparation de peptides chiraux |
| KR102134572B1 (ko) | 2012-06-26 | 2020-07-16 | 메르크 파텐트 게엠베하 | 복굴절성 중합체 필름의 제조 방법 |
| CN110317811A (zh) | 2012-09-17 | 2019-10-11 | 霍夫曼-拉罗奇有限公司 | Usp30抑制剂及其使用方法 |
| WO2014068527A1 (en) | 2012-11-02 | 2014-05-08 | Pfizer Inc. | Bruton's tyrosine kinase inhibitors |
| ES2603931T3 (es) | 2012-11-07 | 2017-03-02 | F. Hoffmann-La Roche Ag | Compuestos de triazolo |
| CN103012428A (zh) | 2013-01-08 | 2013-04-03 | 中国药科大学 | 4-(五元杂环并嘧啶/吡啶取代)氨基-1H-3-吡唑甲酰胺类CDK/Aurora双重抑制剂及其用途 |
| JP2016518328A (ja) | 2013-03-12 | 2016-06-23 | キュアジェニックス インコーポレイテッド | 癌治療のための化合物 |
| CN104045552B (zh) | 2013-03-13 | 2019-06-11 | 江苏先声药业有限公司 | 作为神经保护剂的药用化合物 |
| US9744169B2 (en) | 2013-03-14 | 2017-08-29 | Curegenix, Inc. | Compounds for treatment of fibrosis diseases |
| US9393244B2 (en) | 2013-03-15 | 2016-07-19 | Georgetown University | Increasing parkin activity by administering a deubiquitinating enzyme inhibitor |
| KR20150128863A (ko) | 2013-03-15 | 2015-11-18 | 에프. 호프만-라 로슈 아게 | RORc 조절제로서 아릴 설파미드 및 설파메이트 유도체 |
| JP2014232188A (ja) | 2013-05-29 | 2014-12-11 | コニカミノルタ株式会社 | セルロースアシレートフィルム、円偏光板及び画像表示装置 |
| WO2015003816A2 (en) | 2013-07-12 | 2015-01-15 | Helmholtz-Zentrum für Infektionsforschung GmbH | Cystobactamides |
| WO2015011284A2 (en) | 2013-07-25 | 2015-01-29 | Fondazione Telethon | Inhibitors of fapp2 and uses thereof |
| WO2015010297A1 (en) | 2013-07-25 | 2015-01-29 | Agios Pharmaceuticals, Inc. | Therapeutically active compounds and their methods of use |
| KR101715090B1 (ko) | 2013-08-28 | 2017-03-13 | 한국화학연구원 | 신규한 화합물 또는 이의 약학적으로 허용가능한 염, 및 이를 유효성분으로 함유하는 인플루엔자 바이러스 감염으로 인한 질환의 예방 또는 치료용 약학적 조성물 |
| WO2015048547A2 (en) | 2013-09-26 | 2015-04-02 | Rigel Pharmaceuticals, Inc. | Methods for using and biomarkers for ampk-activating compounds |
| WO2015048662A2 (en) | 2013-09-30 | 2015-04-02 | X-Rx Discovery, Inc. | Substituted nicotinimide inhibitors of btk and their preparation and use in the treatment of cancer, inflammation and autoimmune disease |
| WO2015061247A2 (en) | 2013-10-21 | 2015-04-30 | Merck Patent Gmbh | Heteroaryl compounds as btk inhibitors and uses thereof |
| JP6505683B2 (ja) | 2013-10-21 | 2019-04-24 | メルク パテント ゲゼルシャフト ミット ベシュレンクテル ハフツングMerck Patent Gesellschaft mit beschraenkter Haftung | 複屈折ポリマーフィルムの調製方法 |
| WO2015085238A1 (en) | 2013-12-05 | 2015-06-11 | The Regents Of The University Of California, A California Corporation | Inhibitors of lpxc |
| WO2015095104A1 (en) | 2013-12-18 | 2015-06-25 | Merck Sharp & Dohme Corp. | Iminothiadiazepane dioxide compounds as bace inhibitors, compositions, and their use |
| WO2015106292A1 (en) | 2014-01-13 | 2015-07-16 | Coferon, Inc. | Bcr-abl tyrosine-kinase ligands capable of dimerizing in an aqueous solution, and methods of using same |
| EP3110420B8 (en) | 2014-02-25 | 2019-07-10 | Board of Regents, The University of Texas System | Salts of heterocyclic modulators of hif activity for treatment of disease |
| PT3143011T (pt) | 2014-05-13 | 2021-04-26 | Hoffmann La Roche | Compostos heterocíclicos deuterados e a sua utilização como agentes de imagiologia |
| KR102412045B1 (ko) | 2014-05-22 | 2022-06-22 | 놀스 차이나 파마수티칼 컴퍼니., 엘티디. | 혈액응고인자 Xa 억제제로서의 히드라지드 화합물 |
| US9511142B2 (en) | 2014-06-11 | 2016-12-06 | VenatoRx Pharmaceuticals, Inc. | Beta-lactamase inhibitors |
| GB201410653D0 (en) | 2014-06-14 | 2014-07-30 | Mission Therapeutics Ltd | Methodologies for measuring isopeptidase activity in biological samples in a high throughput manner |
| CN106065009B (zh) | 2014-06-28 | 2019-03-01 | 广东东阳光药业有限公司 | 作为丙型肝炎抑制剂的化合物及其在药物中的应用 |
| US10005724B2 (en) | 2014-07-07 | 2018-06-26 | Genentech, Inc. | Therapeutic compounds and methods of use thereof |
| EP3169683A4 (en) | 2014-07-16 | 2017-11-22 | Novogen Ltd. | Functionalised and substituted indoles as anti-cancer agents |
| WO2016019237A2 (en) | 2014-07-31 | 2016-02-04 | Pharmacyclics Llc | Inhibitors of bruton's tyrosine kinase |
| US9290457B2 (en) | 2014-07-31 | 2016-03-22 | Boehringer Ingelheim International Gmbh | Substituted dihydropyrimidinones and their use as inhibitors of neutrophil elastase activity |
| JP6695863B2 (ja) | 2014-09-05 | 2020-05-20 | メルク パテント ゲーエムベーハー | 調合物と電子素子 |
| WO2016040449A1 (en) | 2014-09-10 | 2016-03-17 | Raze Therapeutics, Inc. | 3-phosphoglycerate dehydrogenase inhibitors and uses thereof |
| GB201416754D0 (en) | 2014-09-23 | 2014-11-05 | Mission Therapeutics Ltd | Novel compounds |
| JP2016115940A (ja) | 2014-12-12 | 2016-06-23 | 出光興産株式会社 | 有機エレクトロルミネッセンス素子および電子機器 |
| CN104557862B (zh) | 2014-12-15 | 2017-05-17 | 苏州云轩医药科技有限公司 | 具有Wnt信号通路抑制活性的杂环化合物 |
| SI3240785T1 (sl) | 2014-12-29 | 2021-11-30 | THE UNITED STATES OF AMERICA, as represented by THE SECRETARY, DEPARTMENT OF HEALTH AND HUMAN SERVICES, OFFICE OF TECHNOLOGY TRANSFER, NATIONAL INSTITUTES OF HEALTH | Malomolekulski zaviralci laktat dehidrogenaze in postopki za uporabo le-teh |
| AU2016240033B2 (en) * | 2015-03-30 | 2020-04-16 | Mission Therapeutics Limited | 1-cyano-pyrrolidine compounds as USP30 inhibitors |
| US11040976B2 (en) | 2015-04-24 | 2021-06-22 | President And Fellows Of Harvard College | Substrate selective inhibitors of insulin-degrading enzyme (IDE) and uses thereof |
| WO2017002120A1 (en) | 2015-07-02 | 2017-01-05 | Yeda Research And Development Co. Ltd. | Selective inhibitors of senescent cells and uses thereof |
| WO2017010399A1 (ja) | 2015-07-10 | 2017-01-19 | 塩野義製薬株式会社 | RORγt阻害作用を有する化合物およびそれらを含有する医薬組成物 |
| EP3800186A1 (en) | 2015-07-14 | 2021-04-07 | Mission Therapeutics Limited | Cyanopyrrolidines as dub inhibitors for the treatment of cancer |
| WO2017019817A1 (en) | 2015-07-29 | 2017-02-02 | Medivation Technologies, Inc. | Methods and compositions for targeted therapeutics |
| WO2017019822A1 (en) | 2015-07-29 | 2017-02-02 | Medivation Technologies, Inc. | Pellet composition containing repair cells |
| WO2017019830A1 (en) | 2015-07-29 | 2017-02-02 | Medivation Technologies, Inc. | Methods and compositions for targeted therapeutics |
| US11124483B2 (en) | 2015-09-02 | 2021-09-21 | The Regents Of The University Of California | HER3 ligands and uses thereof |
| EP3344600B1 (en) | 2015-09-04 | 2021-02-24 | Dow Agrosciences LLC | Molecules having pesticidal utility, and intermediates, compositions, and processes, related thereto |
| WO2017066705A1 (en) | 2015-10-14 | 2017-04-20 | Aquinnah Pharmaceuticals, Inc. | Compounds, compositions and methods of use against stress granules |
| GB201521109D0 (en) | 2015-11-30 | 2016-01-13 | Mission Therapeutics Ltd | Novel compounds |
| CN108602806B (zh) | 2015-12-09 | 2022-07-12 | 研究三角协会 | 改进的爱帕琳肽受体(apj)激动剂及其用途 |
| GB201522267D0 (en) * | 2015-12-17 | 2016-02-03 | Mission Therapeutics Ltd | Novel compounds |
| GB201522768D0 (en) | 2015-12-23 | 2016-02-03 | Mission Therapeutics Ltd | Novel compounds |
| CN106986859B (zh) | 2016-01-20 | 2020-02-11 | 广东东阳光药业有限公司 | 吲哚衍生物及其用途 |
| GB201602854D0 (en) * | 2016-02-18 | 2016-04-06 | Mission Therapeutics Ltd | Novel compounds |
| GB201603779D0 (en) | 2016-03-04 | 2016-04-20 | Mission Therapeutics Ltd | Novel compounds |
| IL261606B (en) | 2016-03-16 | 2022-09-01 | Kura Oncology Inc | Inhibitors of converted menin-mll and methods of use |
| GB201604638D0 (en) | 2016-03-18 | 2016-05-04 | Mission Therapeutics Ltd | Novel compounds |
| GB201604647D0 (en) | 2016-03-18 | 2016-05-04 | Mission Therapeutics Ltd | Novel compounds |
| CN107226805A (zh) | 2016-03-24 | 2017-10-03 | 北京天诚医药科技有限公司 | 芳香族酰胺类衍生物、其制备方法及其在医药上的应用 |
| JP6959252B2 (ja) * | 2016-03-24 | 2021-11-02 | ミッション セラピューティクス リミティド | Dub阻害剤としての1−シアノピロリジン誘導体 |
| CN109715615A (zh) | 2016-06-29 | 2019-05-03 | 蒙特利尔大学 | 联芳甲基杂环 |
| CN107619388A (zh) | 2016-07-13 | 2018-01-23 | 南京天印健华医药科技有限公司 | 作为fgfr抑制剂的杂环化合物 |
| CN107619384B (zh) | 2016-07-13 | 2020-07-28 | 江苏恒瑞医药股份有限公司 | 苯并杂环衍生物、其制备方法及其在医药上的应用 |
| WO2018024188A1 (zh) | 2016-08-02 | 2018-02-08 | 上海迪诺医药科技有限公司 | 多环化合物、其制备方法、药物组合物及应用 |
| US11124628B2 (en) | 2016-08-30 | 2021-09-21 | Dow Global Technologies Llc | Method of attenuating concerntration of acrolein |
| EP3519385B1 (en) | 2016-09-27 | 2020-11-18 | Mission Therapeutics Limited | Cyanopyrrolidine derivatives with activity as inhibitors of usp30 |
| GB201616511D0 (en) | 2016-09-29 | 2016-11-16 | Mission Therapeutics Limited | Novel compounds |
| GB201616627D0 (en) * | 2016-09-30 | 2016-11-16 | Mission Therapeutics Limited | Novel compounds |
| TWI771327B (zh) | 2016-10-05 | 2022-07-21 | 英商使命醫療公司 | 新穎化合物 |
| WO2018106818A1 (en) | 2016-12-07 | 2018-06-14 | Kura Oncology, Inc. | Methods of promoting beta cell proliferation |
| WO2018106820A1 (en) | 2016-12-07 | 2018-06-14 | Kura Oncology, Inc. | Methods of promoting beta cell proliferation |
| RU2764980C2 (ru) | 2017-01-20 | 2022-01-24 | Лео Фарма А/С | Бициклические амины в качестве новых ингибиторов jak-киназы |
| ES2892330T3 (es) | 2017-02-08 | 2022-02-03 | Helmholtz Zentrum Dresden | Compuestos de Hg-197(m) estables in vivo, método para su producción y su uso en diagnóstico por medicina nuclear y terapia con endorradionúclidos (teranóstica) |
| US10744213B2 (en) | 2017-02-14 | 2020-08-18 | Colossus Biopharma Consultants Company, Limited | Fluorescent compounds for imaging of blood vessels and blood flow, and an in vivo screen for pro- and anti-angiogenic agents |
| WO2018160891A1 (en) | 2017-03-01 | 2018-09-07 | Achillion Pharmaceutical, Inc. | Pharmaceutical compounds for treatment of medical disorders |
| KR20190126322A (ko) | 2017-03-03 | 2019-11-11 | 장쑤 한서 파마슈티칼 그룹 캄파니 리미티드 | 아미드 유도체 억제제 및 그의 제조 방법 및 적용 |
| WO2018213150A1 (en) | 2017-05-15 | 2018-11-22 | Mitobridge, Inc. | Usp30 inhibitors |
| GB201708652D0 (en) | 2017-05-31 | 2017-07-12 | Mission Therapeutics Ltd | Novel compounds and uses |
| CN110831936B (zh) | 2017-06-20 | 2023-03-28 | 特殊治疗有限公司 | 具有dub抑制剂活性的取代氰基吡咯烷 |
| AU2018346597B2 (en) | 2017-10-06 | 2023-07-13 | Forma Therapeutics, Inc. | Inhibiting Ubiquitin Specific Peptidase 30 |
| GB2571731A (en) | 2018-03-06 | 2019-09-11 | Mission Therapeutics Ltd | Novel compounds and uses |
| MX2020012180A (es) | 2018-05-17 | 2021-01-29 | Forma Therapeutics Inc | Compuestos biciclicos fusionados utiles como inhibidores de la peptidasa 30 especifica de ubiquitina. |
| JP7434285B2 (ja) | 2018-08-14 | 2024-02-20 | アムジエン・インコーポレーテツド | N-シアノ-7-アザノルボルナン誘導体及びその使用 |
| EP3860989B1 (en) | 2018-10-05 | 2023-04-05 | Forma Therapeutics, Inc. | Fused pyrrolines which act as ubiquitin-specific protease 30 (usp30) inhibitors |
| GB201905371D0 (en) | 2019-04-16 | 2019-05-29 | Mission Therapeutics Ltd | Novel compounds |
| GB201905375D0 (en) | 2019-04-16 | 2019-05-29 | Mission Therapeutics Ltd | Novel compounds |
| GB201912674D0 (en) | 2019-09-04 | 2019-10-16 | Mission Therapeutics Ltd | Novel compounds |
| AU2020345962A1 (en) | 2019-09-11 | 2022-03-31 | Vincere Biosciences, Inc. | USP30 inhibitors and uses thereof |
-
2019
- 2019-10-04 EP EP19791136.5A patent/EP3860989B1/en active Active
- 2019-10-04 AU AU2019356011A patent/AU2019356011A1/en active Pending
- 2019-10-04 LT LTEPPCT/US2019/054803T patent/LT3860989T/lt unknown
- 2019-10-04 HU HUE19791136A patent/HUE062240T2/hu unknown
- 2019-10-04 JP JP2021518517A patent/JP2022504211A/ja active Pending
- 2019-10-04 SI SI201930533T patent/SI3860989T1/sl unknown
- 2019-10-04 US US17/282,521 patent/US11535618B2/en active Active
- 2019-10-04 DK DK19791136.5T patent/DK3860989T3/da active
- 2019-10-04 PT PT197911365T patent/PT3860989T/pt unknown
- 2019-10-04 EP EP23165482.3A patent/EP4218934A1/en active Pending
- 2019-10-04 KR KR1020217013165A patent/KR20210072791A/ko unknown
- 2019-10-04 FI FIEP19791136.5T patent/FI3860989T3/fi active
- 2019-10-04 PE PE2021000398A patent/PE20211053A1/es unknown
- 2019-10-04 CN CN201980080107.2A patent/CN113166108A/zh active Pending
- 2019-10-04 MA MA053816A patent/MA53816A/fr unknown
- 2019-10-04 CA CA3110113A patent/CA3110113A1/en active Pending
- 2019-10-04 MX MX2021002981A patent/MX2021002981A/es unknown
- 2019-10-04 WO PCT/US2019/054803 patent/WO2020072964A1/en active Application Filing
- 2019-10-04 BR BR112021003620-2A patent/BR112021003620A2/pt unknown
- 2019-10-04 EA EA202190960A patent/EA202190960A1/ru unknown
- 2019-10-04 PL PL19791136.5T patent/PL3860989T3/pl unknown
- 2019-10-04 ES ES19791136T patent/ES2945834T3/es active Active
- 2019-10-04 RS RS20230494A patent/RS64321B1/sr unknown
- 2019-10-04 HR HRP20230409TT patent/HRP20230409T1/hr unknown
- 2019-10-04 SG SG11202102815SA patent/SG11202102815SA/en unknown
-
2021
- 2021-03-29 CL CL2021000793A patent/CL2021000793A1/es unknown
- 2021-04-01 IL IL281980A patent/IL281980A/en unknown
- 2021-04-21 CO CONC2021/0005070A patent/CO2021005070A2/es unknown
-
2022
- 2022-10-20 US US18/048,079 patent/US11814386B2/en active Active
-
2023
- 2023-06-02 CY CY20231100267T patent/CY1126067T1/el unknown
Also Published As
| Publication number | Publication date |
|---|---|
| JP2022504211A (ja) | 2022-01-13 |
| MA53816A (fr) | 2022-04-06 |
| EP3860989A1 (en) | 2021-08-11 |
| HRP20230409T1 (hr) | 2023-07-07 |
| MX2021002981A (es) | 2021-05-14 |
| SG11202102815SA (en) | 2021-04-29 |
| RS64321B1 (sr) | 2023-08-31 |
| CO2021005070A2 (es) | 2021-04-30 |
| US20210355126A1 (en) | 2021-11-18 |
| CY1126067T1 (el) | 2023-11-15 |
| US11814386B2 (en) | 2023-11-14 |
| LT3860989T (lt) | 2023-06-12 |
| HUE062240T2 (hu) | 2023-10-28 |
| WO2020072964A1 (en) | 2020-04-09 |
| DK3860989T3 (da) | 2023-05-01 |
| FI3860989T3 (fi) | 2023-05-25 |
| EP3860989B1 (en) | 2023-04-05 |
| EA202190960A1 (ru) | 2021-06-28 |
| KR20210072791A (ko) | 2021-06-17 |
| AU2019356011A1 (en) | 2021-04-01 |
| CL2021000793A1 (es) | 2021-08-20 |
| SI3860989T1 (sl) | 2023-06-30 |
| US20230126252A1 (en) | 2023-04-27 |
| CN113166108A (zh) | 2021-07-23 |
| EP4218934A1 (en) | 2023-08-02 |
| US11535618B2 (en) | 2022-12-27 |
| PL3860989T3 (pl) | 2023-07-10 |
| PE20211053A1 (es) | 2021-06-07 |
| IL281980A (en) | 2021-05-31 |
| BR112021003620A2 (pt) | 2021-05-18 |
| CA3110113A1 (en) | 2020-04-09 |
| PT3860989T (pt) | 2023-06-30 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2945834T3 (es) | Pirrolinas fusionadas que actúan como inhibidores de la proteasa 30 específica de ubiquitina (USP30) | |
| KR100883003B1 (ko) | 알츠하이머병의 치료를 위한 글라이신 수송체1(glyt-1) 억제제로서 바이- 및 트라이사이클릭 치환된페닐 메탄온 | |
| ES2576182T3 (es) | Derivados de heterocíclicos novedosos y su uso en el tratamiento de trastornos neurológicos | |
| JP7449242B2 (ja) | ユビキチン特異的ペプチダーゼ30(usp30)阻害剤として有用な縮合二環化合物 | |
| EP3652168A1 (en) | 5-membered and bicyclic heterocyclic amides as inhibitors of rock | |
| ES2770047T3 (es) | Compuestos de azetidiniloxifenilpirrolidina | |
| KR20080087070A (ko) | 피리미딘 또는 트리아진 융합된 비시클릭 메탈로프로테아제억제제 | |
| US20140107109A1 (en) | Amino-dihydrothiazine and amino-dioxido dihydrothiazine compounds as beta-secretase antagonists and methods of use | |
| CN105732637A (zh) | 杂芳化合物及其在药物中的应用 | |
| ES2895904T3 (es) | Tetrahidroindazoles y usos médicos de los mismos | |
| CN105399756A (zh) | Btk抑制剂及其用途 | |
| CA3007653A1 (en) | Substituted benzazinones as antibacterial compounds | |
| ES2562903T3 (es) | Nuevo compuesto que tiene actividad inhibidora de PARP | |
| TW384285B (en) | Pharmaceutical composition containing quinoline or quinazoline derivatives and novel derivatives therefor | |
| CN105153154A (zh) | Btk抑制剂及其用途 | |
| JP6345651B2 (ja) | ヘテロアリール化合物及びその使用方法 | |
| CN101006055B (zh) | 作为酪蛋白激酶Iε抑制剂的3-取代的-5-和6-氨基烷基吲哚-2-羧酸酰胺以及相关类似物 | |
| ES2743183T3 (es) | Derivados de piridopirimidinodiona como supresores de mutaciones finalizadoras | |
| CA3225596A1 (en) | Inhibitors targeting ubiquitin specific protease 7 (usp7) | |
| KR20230104782A (ko) | Bcr-abl 티로신 키나제 억제용 7-아자인돌 화합물 | |
| ES2442293T3 (es) | Derivados de dihidro-oxazolobenzodiazepinona, procedimientos para su preparación y composiciones farmacéuticas que contienen estos compuestos | |
| EA045195B1 (ru) | Конденсированные пирролины, которые действуют как ингибиторы убиквитин-специфической протеазы 30 (usp30) | |
| US20240132499A1 (en) | Fused pyrrolines which act as ubiquitin-specific protease 30 (usp30) inhibitors | |
| RU2782469C2 (ru) | Апоптоз-индуцирующие агенты | |
| WO2023185073A1 (zh) | Parp7抑制剂及其用途 |