-
Diese
Anmeldung nimmt die Priorität
der U.S. Provisional Patentanmeldung Nr. 60/105,628, eingereicht
am 26. Oktober 1998, in Anspruch.
-
GEBIET DER
ERFINDUNG
-
Die
vorliegende Erfindung betrifft Therapeutika und Diagnostika für Krebs
und andere mit veränderten metabolischen
Enzymen assoziierte Krankheiten. Insbesondere betrifft die Erfindung
eine neue Klasse von therapeutischen Mitteln, welche Tumorzellen
und bestimmte andere Typen von Zellen, die in Krankheitsprozessen
involviert sind, selektiv angreifen und abtöten.
-
HINTERGRUND
DER ERFINDUNG
-
Alle
Säugerzellen
benötigen
zum Leben und Wachsen Energie. Zellen erhalten diese Energie durch den
Metabolismus von Nahrungsmolekülen.
Die große
Mehrheit normaler Zellen verwendet eine einzige Metabolismusroute,
um ihre Nahrungsmittel abzubauen. Der erste Schritt in dieser Metabolismusroute
ist der teilweise Abbau von Glucosemolekülen zu Pyruvat in einem Verfahren,
das als Glykolyse oder glykolytischer Zyklus bekannt ist. Das Pyruvat
wird weiter im Mitochondrium zu Wasser und Kohlendioxid abgebaut,
welches anschließend
eliminiert wird. Dies geschieht durch ein Verfahren, das als Tricarbonsäure (TCA)-Zyklus
bezeichnet wird. Die kritische Verbindung zwischen diesen beiden
Prozessen ist der große
Enzymkomplex mit mehreren Untereinheiten, der als Pyruvat-Dehydrogenase
("PDH")-Komplex bezeichnet
wird (nachfolgend "PDC"). PDC fungiert als
Katalysator, welcher das Pyruvat vom glykolytischen Zyklus zum TCA-Zyklus
leitet.
-
Die
meisten Krebsarten zeigen eine tiefgreifende Störung des Energiemetabolismus.
Diese Veränderung
im Energiemetabolismus stellt eine der robustesten und am besten
dokumentierten Korrelate bösartiger Transformationen
dar.
-
Da
Tumorzellen Glucose größtenteils
glykolytisch abbauen, d.h. ohne den TCA-Zyklus, müssen große Mengen an Pyruvat auf andere
alternative Arten abgebaut werden. Eine Hauptroute, die zum Abbau
des überschüssigen Pyruvats
verwendet wird, umfasst die Verbindung von zwei Pyruvatmolekülen, um
die neutrale Verbindung Acetoin zu bilden. Die Bildung von Acetoin
wird durch eine Tumor-spezifische Form von PDC katalysiert. Obgleich
der TCA-Zyklus in
Krebszellen immer noch funktioniert, ist der Tumorzellen-TCA-Zyklus
ein abweichender Zyklus, der auf Glutamin als primärer Energiequelle
beruht. Der Tumor-spezifische PDC spielt bei diesem abweichenden
TCA-Zyklus eine regulatorische Rolle. Somit kann die Inhibition
oder Inaktivierung eines einzigen Enzyms, nämlich des Tumor-spezifischen
PDC, die Bildung großer
Mengen an ATP sowie das Reduktionspotenzial in Tumorzellen blockieren.
-
Trotz
der intensiven Arbeit zur Charakterisierung des Tumorzellmetabolismus
hat man die systematische Veränderung
des Tumorzell-Energiemetabolismus noch nicht als Ziel für eine Krebs-Chemotherapie
genutzt. Viele bösartige
Krankheiten stellen immer noch große Herausforderungen an die
klinische Onkologie dar. Beispielsweise ist Prostatakrebs die zweihäufigste
Ursache für
Krebstod in Männern.
Derzeitige Behandlungsmethoden beruhen primär auf hormonellen Manipulationen.
Trotz der anfänglich
hohen Ansprechraten entwickeln die Patienten jedoch oft Hormon-unempfindliche
Tumore, was zu einem schnellen Krankheitsverlauf mit einer schlechten
Prognose führt.
Insgesamt waren die Ergebnisse einer cytotoxischen Chemotherapie enttäuschend,
was auf einen lang bestehenden Bedarf an neuen Ansätzen zur
Prävention
und Behandlung von fortgeschrittenen Krebsarten hindeutet. Weitere
Krankheiten, die von einer abnormen Zellreplikation herrühren, beispielsweise
metastatische Melanome, Hirntumore glialen Ursprungs (z.B. Astrozytome)
und Lungen-Adenokarzinome sind ebenfalls hochaggressive bösartige
Tumore mit einer schlechten Prognose. Die Häufigkeit von Melanomen und
Lungen-Adenokarzinomen ist in den vergangenen Jahren signifikant
angestiegen. Chirurgische Behandlungen von Hirntumoren erreichen
oft keine vollständige
Entfernung aller Tumorgewebe, was zu Rückfällen führt. Systemische Chemotherapie
wird durch Blutbarrieren behindert. Es besteht daher ein dringender
Bedarf an neuen Ansätzen
für die
Behandlung von humanen bösartigen
Tumoren, einschließlich
fortgeschrittenem Prostatakrebs, Melanom, Hirntumoren und anderen
bösartigen
Tumoren wie etwa Neuroblastomen, Lymphomen und Gliomen.
-
Die
Entwicklung von Verfahren und Zusammensetzungen der vorliegenden
Erfindung wurde durch die Theorie geleitet, dass Metabolismuseigenschaften,
welche Tumore von normalen Zellen unterscheiden, zu Zielen für eine therapeutische
Intervention führen
können.
Beispielsweise scheinen Tumorzellen metabolisch über einen tumorspezifischen
PDC zu funktionieren. Somit können
Inhibitoren dieses Enzymkomplexes verwendet werden, um den Tumorzellmetabolismus
zu blockieren, was zu einem selektiven Tumorzelltod führt.
-
Antikrebsaktivität wurde
für bestimmte
Palladium-enthaltende Lipoat-Verbindungen
vorgeschlagen, wobei das spezifische Mittel, welches den Antikrebseffekt
zeigt, als Palladium identifiziert wurde. U.S. Patent Nr. 5,463,093
und 5,679,697. Anders als im Stand der Technik betrifft die vorliegende
Erfindung eine neue Klasse von Lipoat-Verbindungen, welche kein
Palladium enthalten, die jedoch überraschenderweise
eine starke Antikrebsaktivität
besitzen. Diese Verbindungen funktionieren anscheinend durch PDC
und stellen daher eine wirksame Gegenmaßnahme gegen Krebs und andere
pathologische oder pathogene Zellen bereit, welche einen entsprechend
veränderten
Energiemetabolismus zeigen.
-
Es
ist somit eine allgemeine Aufgabe der Erfindung, eine neue Klasse
von therapeutischen Mitteln bereitzustellen, weiche Tumorzellen
wirksam angreifen und abtöten.
-
Es
ist eine weitere Aufgabe der Erfindung, pharmazeutische Zusammensetzungen
bereitzustellen, welche Liponsäurederivate
und einen pharmazeutisch annehmbaren Träger umfassen, die in der Lage
sind, Tumorzellen spezifisch anzugreifen und abzutöten.
-
Es
ist auch eine Aufgabe dieser Erfindung, ein Verfahren zur prophylaktischen
und therapeutischen Behandlung einer Vielzahl von Krebsarten bereitzustellen
unter Verwendung der hierin beschriebenen Liponsäurederivate.
-
Es
ist eine weitere Aufgabe der Erfindung, eine prophylaktische oder
therapeutische Behandlung von Pathologien, wie etwa bakteriellen,
Pilz-, Pflanzen- und Protozoen-Infektionen von Menschen und anderen
Tieren unter Verwendung der hierin beschriebenen Liponsäurederivate
bereitzustellen.
-
ZUSAMMENFASSUNG
DER ERFINDUNG
-
Die
vorliegende Erfindung stellt eine Klasse von Verbindungen zur Behandlung
verschiedener Pathologien in einem Patienten bereit. Die Klasse
von Verbindungen umfasst Liponsäurederivate
und pharmazeutisch annehmbare Salze davon. Die Erfindung stellt
eine Verbindung der Formel:
bereit, wobei:
x 0 bis
16 ist
R
1 und R
2 unabhängig Acyl
CH
3(CH
2)
n–1C(=O)-;
Alkyl C
nH
2+1; Alken
C
mH
2m; Alkin C
mH
2m–2; aromatisch; Aroyl; Alkylsulfid
CH
3(CH
2)
t-S-; Thiocarbaminsäureester CH
3(CH
2)
n–1C=NH-; und Semithioacetal
CH
3CH(OH)-S- sind; wobei n 1–10 ist; m 2–10 ist
und t 0–9
ist, zur Verwendung bei der Behandlung oder Prävention einer Krankheit.
-
Die
vorliegende Erfindung betrifft auch die Verwendung einer oben definierten
Verbindung zur Herstellung einer pharmazeutischen Zusammensetzung
zur Behandlung oder Prävention
einer Krankheit in einem Patienten, die durch eine Empfindlichkeit
auf Liponsäurederivate
gekennzeichnet ist. Derartige Verwendungen können ein Verfahren zur Behandlung
eines Säugetiers
umfassen, einschließlich
eines Menschen, das/der unter einer Krankheit leidet, wobei das
Verfahren die Verabreichung in einer therapeutisch wirksamen Menge mindestens
einer oben definierten Verbindung oder eines physiologisch annehmbaren
Salzes davon an das Säugetier
umfasst.
-
Die
Verbindungen sind für
ein Verfahren der Behandlung oder Prävention einer neoplastischen
Krankheit in einem Patienten geeignet, umfassend das Verabreichen
einer wirksamen Menge mindestens einer oben definierten Verbindung
oder eines physiologisch annehmbaren Salzes davon. Dieses Verfahren
umfasst ein Verfahren, bei dem die Verbindung allein oder in Kombination
mit einem weiteren Reagenz verabreicht wird. Die Kombinationsbehandlungsmethode
erlaubt die gleichzeitige, aufeinanderfolgende oder getrennte Verwendung
zur Behandlung solcher Krankheiten.
-
Die
hierin beschriebene Behandlung ermöglicht die Inhibition von Tumorzellen
in einem Patienten. Alternativ kann die Zusammensetzung verwendet
werden, um Zellen direkt zu kontaktieren und zu inhibieren oder
Tumorzellen in vitro abzutöten.
-
Es
können
jedoch auch andere Krankheitszustände eine Empfindlichkeit gegen
die Liponsäurederivate
zeigen. Demgemäß beinhaltet
die Erfindung die Verwendung von Liponsäurederivaten als wirksame Mittel gegen
Krankheiten eubakteriellen, archebakteriellen, Pilz-, Pflanzen-,
Algen- und Protozoen-Ursprungs,
da diese Krankheiten in Menschen und anderen Tieren auftreten.
-
Einige
der oben beschriebenen Verbindungen sind per se neu. Demgemäß betrifft
die vorliegende Erfindung solche Verbindungen wie in Anspruch 10
beansprucht und pharmazeutische Zusammensetzungen, welche eine oben definierte
Verbindung oder ein physiologisch annehmbares Salz davon umfassen,
zusammen mit einem oder mehreren physiologisch annehmbaren Trägern oder
Arzneistoffträgern.
-
BESCHREIBUNG
DER FIGUREN
-
1:
Gezeigt ist eine Krebszellen-spezifische Zellabtötung durch Bis-Benzoyl-Lipoat (120 μg/ml oder 120
mg/kg), ein Mitglied der neuen Klasse von Verbindungen, welche Gegenstand
dieser Erfindung sind. Siehe BEISPIEL 7. Die linke Spalte enthält das Gewebe
mit Krebsursprung und, in Klammern, die spezifische Bezeichnung
der Zelllinie. Die oberen drei Reihen zeigen drei unterschiedliche
Krebszelltypen – Lungenkrebs, Leberkrebs
und Embryonalkrebs. Im Gegensatz dazu zeigt die untere Reihe eine
normale (keine Krebszellen) Nieren-Epithelzelllinie. Die mittlere
Spalte zeigt die unbehandelten Proben (Kontrollen), während die
rechte Spalte die Wirkungen der Behandlung auf jeden Zelltyp zeigt
(experimentelle Proben). Jede der drei Krebszelltypen wird wirksam
abgetötet,
während
die normalen Zellen nicht nachweisbar beeinflusst werden. Diese
Bilder wurden etwa 48 Stunden nach der Verabreichung des Bis-Benzoyl-Lipoats
photographiert. Es wird darauf hingewiesen, dass fast alle der Krebszellen
zu diesem Zeitpunkt abgetötet
worden waren. Die wenigen verbleibenden Zellen oder Zellfragmente
haben eine charakteristische Morphologie von Zellen, die den Zelltod durchlaufen
(Apoptose; siehe BEISPIEL 9; siehe auch 2 und 3).
Diese wenigen verbleibenden Zellen in den behandelten Feldern werden
innerhalb der nächsten
wenigen Stunden absterben. Im Gegensatz dazu wird darauf hingewiesen,
dass die normalen, Nicht-Krebszellen (untere Reihe) nicht nachweisbar
durch die Behandlung beeinflusst werden.
-
2:
Gezeigt ist die selektive Abtötung
von ras-transformierten NIH3T3-Zellen
in Kultur durch das Bis-Benzoyl-Lipoat (120 μg/ml oder 120 mg/kg), ein Mitglied
der neuen Klasse von Verbindungen, die Gegenstand dieser Erfindung
sind. Siehe BEISPIELE 7 und 8. Die linke Spalte beschreibt die nicht-karzinöse (nicht-transformierte),
Ursprungs-NIH3T3-Zelllinie und eines ihrer Derivate (T24), das durch
Einführung
einer aktivierten Form des ras-Onkogens zu einem malignen (kanzerösen) Status
transformiert wurde. Die mittlere Spalte zeigt diese beiden Zelltypen
unbehandelt (Kontrollproben), und die rechte Spalte zeigt sie nach
etwa 24 Stunden Behandlung mit Bis-Benzoyl-Lipoat. Zunächst sind
die nicht-kanzerösen
Ursprungs-Zellen durch diese Behandlung nicht beeinträchtigt.
Zweitens sind im Gegensatz dazu nach 24 Stunden Behandlung ca. 50%
der kanzeröse
(transformierten) Zellen abgetötet
und die verbleibenden Zellen sind gerundet und durchlaufen den Zelltod.
Siehe 1 und 3 für Beispiele dieser charakteristischen
Zellrundung und Zelltod. Nach etwa 48 Stunden Behandlung werden
die Krebszellen fast vollständig
vernichtet (getötet)
sein, während die
entsprechenden nicht-kanzerösen Unsprungs-Zellen
unbeeinträchtigt
bleiben.
-
3:
Gezeigt ist das Ergebnis eines TUNEL-Assays, der zeigt, dass das
Bis-Benzoyl, ein Mitglied der neuen Klasse von Verbindungen, die
Gegenstand der vorliegenden Erfindung sind, Apoptose (programmierter
Zelltod) in Krebszellen induziert. In diesem Experiment werden HeLa-Zellen
(Gebärmutterhalskrebs) für ca. 24
Stunden so behandelt, dass der Zelltod begonnen hatte, aber so dass
eine signifikante Anzahl von lebenden Zellen verblieb. Alle Krebszellen
waren innerhalb von etwa 48 bis 60 Stunden unter diesen Bedingungen
abgetötet.
Siehe BEISPIEL 9. Die linken Photographien zeigen Phasenkontrast-Lichtmikrographe
der Zelle. Eine Zelle, welche die stark abgerundete, intern fragmentierte
Erscheinung einer Zelle zeigt, die Apoptose durchläuft, ist
durch den Pfeil angegeben. Die mittleren Photographien zeigen dieselben
Zellen, mit DAPI gefärbt
und durch indirekte Fluoreszenzmikroskopie untersucht. Dieses zeigt
die DNA, was zeigt, wo sich die Zellkerne befinden. Es wird auch
auf die charakteristische ungleichmäßige Färbung der DNA in den apoptotischen
Zellen hingewiesen (Pfeil). Die rechten Photographien zeigen das
Ergebnis des TUNEL-Assays derselben Zellen, untersucht durch indirekte
Fluoreszenzmikroskopie. Es wird auf den sehr geringen Grad der Färbung der
meisten Zellkerne hingewiesen, was eine kleine Anzahl von DNA-Brüchen widerspiegelt
(siehe BEISPIEL 9). Im Gegensatz dazu sieht man ein sehr starkes
Fluoreszenzsignal bei der apoptotischen Zelle (Pfeil). Dies ist
diagnostisch für
die große
Anzahl von DNA-Brüchen,
die für
Zellen charakteristisch sind, die den programmierten Zelltod durchlaufen
(Apoptose).
-
DETAILLIERTE
BESCHREIBUNG DER BEVORZUGTEN AUSFÜHRUNGSFORMEN
-
Strukturelle
Eigenschaften von Liponsäurederivaten
-
Die
Verbindungen unserer Erfindung umfassen Liponsäure, die an der Thiolgruppe
des Moleküls durch
organische Gruppen derivatisiert wurde. Lipon-/Dihydroliponsäure-Spezies mit längeren oder
kürzeren Kohlenstoffketten,
mit einer Länge
von bis zu 20 Kohlenstoffen, vorzugsweise zwischen 4 bis 10 Kohlenstoffen, können zur
Ausführung
dieser Erfindung verwendet werden. Die Varianten von Liponsäure der
vorliegenden Erfindung umfassen solche, in denen die Carbonsäuregruppe
unangetastet ist, und in denen ein oder beide Thiole und/oder Sulfhydryle
durch Derivatisierung blockiert sind, um Tumorzellen durch Eingriff
in Tumorzell-spezifische PDC-Funktionen gezielt abzutöten.
-
Die
vorliegende Erfindung betrifft eine Klasse von Liponsäurezusammensetzungen
der Formel:
wobei:
x von 0–16
ist und R
1 und R
2 unabhängig die
Folgenden sein können:
- (1) Eine durch eine Thioester-Bindung gebundene
Acylgruppe. Die Acylgruppe umfasst CH3(CH2)n–1(C=O)-, wobei n von
1–10 ist.
Beispiele von Acylgruppen umfassen, sind jedoch nicht beschränkt auf
Acetyl und Butyryl. Ein spezielles Beispiel einer mit Acyl derivatisierten
Liponsäure
ist Bis-Acetyl-Lipoat (Beispiel 1).
- (2) Eine durch eine Thioester-Bindung gebundene aromatische
Gruppe. Beispiele von aromatischen Gruppen umfassen, sind jedoch
nicht beschränkt
auf Benzoyl oder ein Benzoylderivat. Ein spezielles Beispiel einer
mit Benzoyl derivatisierten Liponsäure ist Bis-Benzoyl-Lipoat
(Beispiel 2).
- (3) Eine durch eine Thioether-Bindung gebundene Alkylgruppe.
Die Alkylgruppe umfasst CnH2n+1,
wobei n 1–10
ist. Solche Alkylgruppen können
mit weiteren Gruppen, wie etwa z.B. OH, Cl oder NH2,
substituiert sein. Beispiele von Alkylgruppen umfassen, sind jedoch
nicht beschränkt
auf Methyl, Ethyl, Butyl, Decanyl und 6,8-Bis-Carbamoyl-methyllipoat.
(BEISPIEL 3).
- (4) Eine durch eine Thioether-Bindung gebundene Alkengruppe.
Das Alken umfasst CnH2n,
wobei n von 2–10
ist. Beispiele von Alkengruppen umfassen, sind jedoch nicht beschränkt auf
Propylen, 2,3-Dimehtyl-2-buten
und Hepten.
- (5) Eine durch eine Thioether-Bindung gebundene Alkingruppe.
Das Alkin umfasst CnH2n–2, wobei n 2–10 ist.
Beispiele von Alkingruppen umfassen, sind jedoch nicht beschränkt auf
Acetylen, Propin und Octin.
- (6) Alkyl-, Alken- und Alkingruppen können entweder offene Ketten
oder alicyclisch sein. Alicyclische Gruppen können Additionen oder Substitutionen
an jedem der Kohlenstoffe aufweisen, um Heterocyclen zu bilden.
Beispiele von alicyclischen Gruppen umfassen, sind jedoch nicht
beschränkt
auf Cyclopropan, Cyclopenten und 6,8-Methylsuccinimidolipoat (BEISPIEL
4).
- (7) Alkyl-, Alken- und Alkingruppen können Additionen an jedem ihrer
Kohlenstoffe aufweisen. Beispiele von Additionen umfassen, sind
jedoch nicht beschränkt
auf Hydroxyle und Amine.
- (8) Eine durch eine Thioether-Bindung gebundene aromatische
Gruppe. Die aromatischen Gruppen können ein Benzol oder Benzolderivat
sein. Beispiele von Benzolderivaten umfassen, sind jedoch nicht
beschränkt
auf Toluol und Anilin.
- (9) Alkylsulfid (CH3(CH2)t-S-, wobei t 0–9 ist).
- (10) Thiocarbaminsäureestergruppe
[CH3(CH2)n–1C=NH-,
wobei n 1–10
ist], die durch eine Thioamid-Bindung gebunden ist; und
- (11) Semithioacetalgruppe [CH3CH(OH)-S-,
wobei R auf Verbindungen beschränkt
ist, die stark Elektronen-abziehende Substituenten haben. Beispiele
umfassen Trichloracetaldehyd und Brenztraubensäure.
-
R1 und R2 können auch
Thioester umfassen, die oxidiert sein können, um Sulfoxide oder Sulfone
zu ergeben, z.B. C-S(O)-R und C-S(O)2-R.
R1 und R2 können weiterhin
Disulfide umfassen, die oxidiert sein können, um Thiosulfin- oder Thiosulfonsäuren zu
ergeben, beispielsweise C-S(O)-S-R und C-S(O)2-S-R.
-
In
einer bevorzugten Ausführungsform
wird die Liponsäure
der vorliegenden Erfindung durch Addition einer Blockierungsgruppe(n)
an eine oder beide Sulfhydryle derivatisiert. Diese Blockierungsgruppen
können jede
Form haben, wie etwa aliphatische oder aromatische organische Substituenten,
die an ein oder beide Sulfhydryle gebunden werden. Die allgemeine
Struktur dieser Klasse von Lipoatderivaten ist unten dargestellt. Ein
spezielles Beispiel ist wie folgt:
Diethoxycarbonylierte
Liponsäure
-
Die
Verbindungen unserer Erfindung umfassen Liponsäure, die an der Thiolgruppe
des Moleküls durch
organische Gruppen derivatisiert wurde.
-
Es
sind Verbindungen erhältlich,
die spezifisch mit Thiolgruppen reagieren und die im Stand der Technik
wohlbekannt sind. Beispiele solcher Thiolspezifischen Reagenzien
umfassen N-Ethylmaleimid (NEM), 5,5-Dithiobis (2-nitrobenzoesäure) (DNTB), p-Chlor-Quecksilberbenzoesäure (PCMB)
und Ethylchloroformat (ECF). Im Allgemeinen bilden Thiol-reaktive
Reagenzien Thioether oder Thioester mit den reagierenden Thiol(en),
und alle derartigen Verbindungen sind von dieser Klasse umfasst.
-
Zusammensetzungen
von Liponsäurederivaten
für die
therapeutische Verwendung
-
Für therapeutische
Anwendungen wird eine pharmazeutische Zusammensetzung(en), umfassend eine
wirksame Menge der oben beschriebenen Liponsäurederivate zusammen mit einem
pharmazeutisch annehmbaren Träger
direkt an einen Patienten verabreicht. Die Zusammensetzungen können in
Form von Tabletten, Kapseln, Pulvern, Granulat, Pastillen, Zäpfchen,
rekonstituierbaren Pulvern oder flüssigen Zusammensetzungen, wie
etwa orale oder sterile parenterale Lösungen oder Suspensionen, vorliegen.
Für die
Konsistenz der Verabreichung ist es jedoch bevorzugt, dass die Liponsäurederivat-Zusammensetzung
in Form einer Einzelpackung vorliegt. Für die orale Verabreichung können Tabletten
und Kapseln herkömmliche
Arzneiträger enthalten,
wie etwa Bindemittel, Gleitmittel für die Tablettenherstellung,
oder pharmazeutisch annehmbare Benetzungsmittel, wie etwa Natriumlaurylsulfat.
-
Feste
orale Zusammensetzungen können
durch herkömmliche
Verfahren des Mischens, Füllens,
Tablettierens oder dgl. hergestellt werden. Wiederholte Mischvorgänge können eingesetzt
werden, um das Liponsäurederivat
in jeder Zusammensetzung, die Füllmittel
umfasst, zu verteilen. Solche Vorgänge sind natürlich im
Stand der Technik bekannt. Siehe z.B. Remington's Pharmaceutical Sciences, 17. Auflage
1985, Gennaro Herausgeber, Mack Pub. Co., PA, USA. Die Tabletten
können
gemäß allen
in der pharmazeutischen Praxis wohlbekannten Verfahren beschichtet
werden, insbesondere mit einer magensaftresistenten Beschichtung. Orale
flüssige
Zusammensetzungen können
in Form von beispielsweise Emulsionen, Sirupen oder Elixieren vorliegen,
oder sie können
als gefrorenes Produkt zur Rekonstituierung vor ihrer Verwendung
mit Wasser oder anderen geeigneten Vehikeln bereitgestellt werden.
Solche flüssigen
Zusammensetzungen können
herkömmliche
Zusätze,
wie etwa Suspensionsmittel, Emulgiermittel, nicht-wässrige Vehikel
(welche essbare Öle
umfassen können)
enthalten, und, falls gewünscht,
herkömmliche
Geschmacksmittel oder Farbstoffe.
-
Für die parenterale
Verabreichung werden Flüssig-Einzelpackungen
hergestellt, welche das Liponsäurederivat
in einem sterilen Vehikel verwenden, und, je nach der verwendeten
Konzentration, kann dieses entweder in dem Vehikel suspendiert oder
aufgelöst
sein. Bei der Herstellung von Lösungen
kann das Liponsäurederivat
zur Injektion in Wasser gelöst
und filtersterilisiert werden, bevor es in ein geeignetes Röhrchen oder
eine Ampulle eingefüllt
und verschlossen wird. Es können
auch Adjuvantien, wie etwa Lokalanästhetika, ein Konservierungsmittel
und Puffermittel im Vehikel gelöst
werden. Um die Stabilität
zu erhöhen,
kann die Zusammensetzung nach dem Abfüllen in das Röhrchen gefroren
werden und das Wasser unter Vakuum entfernt werden. Parenterale
Suspensionen werden im Wesentlichen auf die gleiche Weise hergestellt,
außer
dass das Liponsäurederivat
in dem sterilen Vehikel suspendiert wird. Ein oberflächenaktives
oder Benetzungsmittel kann in der Zusammensetzung umfasst sein,
um eine gleichmäßige Verteilung
des Liponsäurederivats
sicherzustellen.
-
In
den Verfahren zum Verhindern oder Inhibieren von Krebs können das
Liponsäurederivat
oder eine ein Liponsäurederivat
umfassende pharmazeutische Zusammensetzung über eine oder verschiedene
Routen verabreicht werden, einschließlich intravenös, intramuskulär, subkutan,
intradermal, intraperitoneal, intrathorazisch, intrapleural, intrauterin,
topisch oder intratumoral.
-
Der
Fachmann auf dem Gebiet wird erkennen, dass die Art der Verabreichung
des Liponsäurederivats vom
Krebstyp oder dem zu behandelnden Symptom abhängt. Beispielsweise wäre eine
bevorzugte Verabreichungsroute der Liponsäure zur Behandlung von Leukämie eine
intravenöse
Verabreichung, wohingegen bevorzugte Verfahren zur Behandlung von
Hautkrebs beispielsweise eine topische oder intradermale Verabreichung
umfassen würden.
-
Die
pharmazeutischen Zusammensetzungen der Erfindung können von
0,1 Gew.-% bis 99 Gew.-%, vorzugsweise von 10 Gew.-% bis 25 Gew.-%
des Liponsäurederivats
enthalten, je nach Verabreichungsverfahren.
-
Verfahren
zur Verwendung von Liponsäurederivaten
-
Die
Liponsäurederivate
der Erfindung können
in einem Verfahren zum Verhindern oder Inhibieren von Krankheiten,
welche eine veränderte
oder spezifische zelluläre
PDC-Aktivität
umfassen, verwendet werden. Solche Krankheiten sind charakterisiert
durch eine Empfindlichkeit gegen die Lipoatzusammensetzungen der vorliegenden
Erfindung. Einer der wichtigsten Vorteile unserer Liponsäurederivate
als chemotherapeutische Mittel ist ihre Spezifität. Zellen mit entsprechend
verändertem
oder gestörtem
Energiemetabolismus, d.h. veränderte
PDC-Aktivität,
werden gezielt angegriffen und abgetötet, während die umgebenden gesunden
Gewebe durch das Liponsäurereagenz
nicht beeinträchtigt
werden. Der Fachmann kann Krankheiten mit einer veränderten
PDC-Aktivität
leicht identifizieren. Alternativ hierzu kann der Fachmann die zu
behandelnde Krankheit auf ihre Empfindlichkeit auf die hier beschriebene
Klasse von Verbindungen screenen.
-
In
einem bevorzugten Behandlungsverfahren werden die hier beschriebenen
Liponsäurezusammensetzungen
für die
Prävention
und die Behandlung von Krebsarten, wie etwa primäres oder metastatisches Melanom,
Thymom, Lymphom, Sarcom, Lungenkrebs, Leberkrebs, Nicht-Hodgkin's Lymphom, Hodgin's Lymphom, Leukämien, Gebärmutterkrebs,
Gebärmutterhalskrebs,
Blasenkrebs, Nierenkrebs, Darmkrebs und Adenokarzinomen, wie etwa
Brustkrebs, Prostatakrebs, Eierstockkrebs, Bauchspeicheldrüsenkrebs,
verwendet. Eine große
Vielzahl an Tumorarten, einschließlich Gebärmutterhals-Karzinome und Brustkrebsarten reagieren
empfindlich auf diese neue Klasse von Verbindungen. Zelluläre Ergebnisse
zeigen, dass eine Krebs-spezifische Zellabtötung beobachtet werden kann,
beispielsweise in der hierin unten beschriebenen Tabelle 1.
-
Die
bevorzugte Dosis des Liponsäurederivats
oder einer pharmazeutischen Zusammensetzung daraus wird auf der
Basis von weiteren Kriterien ausgewählt, einschließlich der
besonderen verwendeten Zusammensetzung und dem Alter, Gewicht und
Zustand des Patienten. Es ist wichtig, dass die Menge an Liponsäurederivat
ausreichend ist, um Tumorzellen zu inhibieren oder abzutöten, während normale
Zellen im Wesentlichen unverletzt bleiben sollten. Im Allgemeinen
ist es wünschenswert,
dem Patienten eine Dosis von Liponsäurederivat von mindestens etwa
10 μM, vorzugsweise
mindestens 100 μM,
stärker
bevorzugt mindestens etwa 400 μM
zu verabreichen, während
ein Bereich von etwa 10 μM
bis etwa 1 mM verwendet werden kann. Es kann natürlich eine niedrigere oder
höhere
Dosis verabreicht werden, wobei die in den hierin beschriebenen Beispielen
offenbarten in vivo Daten als Richtschnur herangezogen werden können. Wie
oben beschrieben, beeinflussen eine Vielzahl von klinischen Faktoren
die bevorzugten Dosisbereiche.
-
Eine
weitere Ausführungsform
der Erfindung betrifft ein Verfahren zur Behandlung einer Krankheit,
die gegen Lipoatderivate empfindlich ist, umfassend die Verabreichung
einer wirksamen Menge einer Lipoatverbindung und eines zweiten Reagenzes,
um die Krankheit zu behandeln. Dieses zweite Reagenz ist vorzugsweise
ein Inhibitor des Energiemetabolismus in Mitochondrien und/oder
eines, welches Apoptose induziert. Solche Reagenzien umfassen Metabolismus-inhibitorische
Reagenzien. Viele solcher Reagenzien sind im Stand der Technik bekannt.
Ein besonders bevorzugtes Reagenz ist Dichloracetat. Dieses zweite
Reagenz kann nachfolgend, gleichzeitig oder separat verabreicht
werden, um das Ansprechen des Patienten auf das Behandlungsverfahren
zu verstärken.
-
Durch
Anpassung der hierin beschriebenen Behandlungen können die
Liponsäurederivate
auch in Verfahren zur Behandlung von anderen Krankheiten als Krebs
verwendet werden, bei denen die krankheitsverursachenden Zellen
ein verändertes
Metabolismusmuster zeigen. Beispielsweise sind eukaryontische Pathogene
von Menschen und anderen Tieren im Allgemeinen sehr schwieriger
zu behandeln als bakterielle Pathogene, da eukaryontische Zellen
den tierischen Zellen viel ähnlicher
sind als bakterielle Zellen. Solche eukaryontischen Pathogene umfassen
Protozoen, wie etwa jene, die Malaria verursachen, sowie Pilzpathogene und
Algenpathogene. Aufgrund des bemerkenswerten Mangels an Toxizität der Liponsäurederivate
der Erfindung gegenüber
normalen Menschen- und Tierzellen und weil viele eukaryontische
Pathogene Lebenszyklusstadien durchlaufen, in denen ihre PDCs gegenüber Mitgliedern
der neuen Klasse von hierin beschriebenen Lipoatderivaten empfindlich
sind, töten
einige dieser Mitglieder der neuen Klasse von Lipoatderivaten bakterielle
PDCs ab und stellen daher eine fundamental neue Klasse von antibakteriellen
Mitteln dar. Da gegen traditionelle Antibiotika resistente Bakterien
ein zunehmendes schwerwiegendes klinisches Problem darstellen, werden
diese Verbindungen sich in diesem Zusammenhang als von therapeutischer
Wichtigkeit erweisen.
-
In
noch weiteren Anwendungen werden die Liponsäurederivate der vorliegenden
Erfindung als diagnostische Mittel in vitro verwendet. Wie oben erwähnt, können die
verschiedenen Liponsäurederivate,
je nach der jeweiligen speziellen Tumorzelle oder Zelltyp mehr oder
weniger wirksam bei der Inhibierung unterschiedlicher Tumorklassen
sein. Somit stellt z.B. in Fällen,
bei denen die Diagnose oder Selektion einer geeigneten chemotherapeutischen
Strategie schwierig sein kann, das Testen einer Tumorzellkultur
in vitro mit Liponsäurederivaten,
von denen bekannt ist, dass sie spezifische Tumorzelltypen angreifen,
einen alternativen Ansatz zur Identifizierung von Tumortypen und
für wirksame
Behandlungen dar.
-
Beispiel 1
-
Um
die Existenz einer großen
neuen Klasse von Antikrebsmitteln, die aus blockierten und/oder
deaktivierten Liponsäurederivaten
bestehen, zu bestätigen,
wurde eine Anzahl neuer Liponsäurederivate
hergestellt und getestet. In diesem und den folgenden fünf BEISPIELEN
(1–5)
werden die Synthese, Struktur und Aufreinigung von sechs Verbindungen
beschrieben. Diese Verbindungen werden dann in späteren BEISPIELEN
(6–13)
getestet.
-
Herstellung von 6,8-Bisacetylmercaptooctansäure (Bis-Acetylliponsäure)
-
6,8-Bisacetylmercaptooctansäure (im
Folgenden als Bis-Acetylliponsäure
bezeichnet) wurde aus gewerblich erhältlicher Liponsäure unter
Verwendung eines dreischrittigen Verfahrens hergestellt. Diese Schritte waren
wie folgt: Liponsäure
wurde zunächst
zu 6,8-Bismercaptooctansäure
reduziert, welche anschließend acetyliert
wurde, um 6,8-Bisacetylmercaptooctansäure-Essigsäureanhydrid zu ergeben. Dieses
6,8-Bisacetylmercaptooctansäure-Essigsäureanhydrid
wurde dann selektiv hydrolysiert, um die 6,8-Bisacetylmercaptooctansäure zu ergeben.
-
Im
Detail wurden diese Schritte wie folgt durchgeführt.
-
SCHRITT
1: 6,8-Bismercapfooctansäure:
a-Liponsäure
(5,15 g, 25,0 mmol) wurde in 125 ml Wasser suspendiert und es wurde
Natriumbicarbonat (2,10 g, 25,0 mmol) hinzugefügt. Das Gemisch wurde mit Ultraschall
behandelt, um das Natriumsalz zu bilden. Die resultierende blassgelbe
Lösung
wurde in einem Eisbad gekühlt,
und es wurde festes Natriumborhydrid (1,90 g, 50,0 mmol) unter Rühren in
kleinen Portionen über
20 Minuten hinzugefügt.
Die Lösung
wurde bei Eisbadtemperatur weitere 30 Minuten gerührt und
anschließend bei
Raumtemperatur für
30 Minuten gerührt.
Die trübe
Lösung
wurde in einem Eisbad abgekühlt,
und der pH-Wert durch die langsame Zugabe von 2M Salzsäure auf
etwa 1 gebracht. Es erfolgte eine starke Freisetzung von Wasserstoff
bei der Zersetzung des überschüssigen Natriumborhydrids,
und es trennte sich eine ölige
Flüssigkeit
ab. Soweit als möglich
wurden die folgenden Schritte unter Stickstoff durchgeführt. Das
Gemisch wurde mit 3 × 50
ml Chloroform extrahiert. Die zusammengegebenen Chloroformextrakte
wurde über
Magnesiumsulfat getrocknet, filtriert und das Lösungsmittel unter verringertem
Druck bei Raumtemperatur verdampft. Das verbleibende Öl wurde
weiter unter Vakuum getrocknet, um die letzten Spuren an Lösungsmittel
zu entfernen. Die 6,8-Bismercaptooctansäure wurde als farbloses Öl isoliert,
welches 5,2 g wog (100% Ausbeute). Das Produkt wurde bei –20° unter Stickstoff
gelagert.
-
Die
Analyse ergab die folgenden Ergebnisse: 1H-NMR (CDCl3): 2,89 (Muliplett,
1H, S-C-H). 2,67 (Multiplett, 2H, S-CH2), 2,34 (t, J = 7,1 Hz, 2H,
CH2C(O)), 1,4 – 1,92
(Multipletts, 8H, (CH2)2), 1,33 (t, J = 8,0 Hz, 1H, S-H), 1,30 (t,
J = 7,6 Hz, 1H, S-H).
13C-NMR (CDCl3): 180,0, 42,7, 39,2, 38,6,
33,8, 26,4, 24,2, 22,2
-
SCHRITT
2: 6,8-Bisacetylmercaptooctansäure-Essigsäureanhydrid:
6,8-Bismercaptooctansäure (5,20
g, 25 mmol) wurde in 125 ml trockenem Methylenchlorid unter Stickstoff
gelöst,
und es wurde Triethylamin (8,10 g, 80,0 mmol, 11,25 ml) hinzugefügt. Die
Lösung
wurde in einem Eisbad gekühlt
und es wurde Acetylchlorid (6,30 g, 80,0 mmol) in 25 ml Methylenchlorid
gelöst
und tropfenweise unter Rühren über 15 Minuten hinzugegeben.
Während
dieser Zugabe fiel Triethylammoniumchlorid aus. Die Lösung selbst
blieb farblos. Das Rühren
wurde bei Raumtemperatur für
90 Minuten fortgeführt.
Das Volumen wurde auf 300 ml mit mehr Methylenchlorid (alle Feststoffe
gelöst)
gebracht und die Lösung
wurde in einen Separationstrichter überführt. Sie wurde schnell mit
300 ml 10 %iger Zitronensäure
(der pH-Wert der wässrigen
Phase wurde nach der Extraktion überprüft, um sicherzustellen,
dass er sauer war) extrahiert. Sie wurde ein zweites Mal mit 200
ml der Zitronensäurelösung extrahiert
und anschließend
mit 200 ml halbgesättigter
Salzlösung
gewaschen. Die organische Phase wurde über Magnesiumsulfat getrocknet,
filtriert und das Methylenchlorid verdampft. Es verblieb ein fast
farbloses Öl,
welches 8,0 g wog.
-
Die
Analyse ergab die folgenden Ergebnisse: 1H-NMR (CDCl3): 3,49 (Multiplett,
1H), 2,7 – 3,0
(Multiplett, 2H), 2,36 (t, 2H, CH2C(O), 2,27 (s, 3H, CH3), 2,26
(s, 3H, CH3), 2,15 (s, 3H, CH3), 1,3 – 1,9 (Multiplett, 8H).
13C-NMR (CDCl3):
195,4, 195,2, 168,9, 166,3, 43,2, 34,8, 34,5, 34,2, 30,6, 30,4,
26,3, 25,7, 23,7, 22,0. IR (KBr Pressling): 1821, 1749, 1691 cm-1.
-
SCHRITT
3: 6,8-Bisacetylmercapfooctansäure:
Das Anhydrid aus Schritt 2 (8,0 g) wurde mit 30 ml Wasser und 30
ml 2-Propanol gemischt und bei 40°C
für 4,25
Stunden gerührt.
Nach etwa 2 Stunden hatte sich eine klare Lösung gebildet. Das Lösungsmittel
wurde unter Vakuum (2 mm) bei 25° verdampft.
Das verbleibende Öl
wurde mit 10 ml Wasser verdampft, um alles verbleibende 2-Propanol
und Essigsäure
zu entfernen. Es wurde ein fast farbloses Öl isoliert, welches 6,8 g wog.
-
AUFREINIGUNG:
Ein Beispiel für
eine Aufreinigung ist wie folgt. Das Material aus Schritt 3 wurde
mit 5 ml Ethylacetat-Hexan-Essigsäure (100 : 100 : 1, v/v) gemischt,
hinzugefügt,
um es flüssiger
zu machen. Die Lösung
wurde auf eine 25 × 6,5
cm Silicagel 60-Säule
(etwa 300 g Flash-Silica) in Ethylacetat-Hexan-Essigsäure (100 : 100 : 1, v/v) gepackt.
Die Säule
wurde mit diesem Lösungsmittel
eluiert. 75 ml-Fraktionen wurden etwa bei 5 ml/min gesammelt. In
Fraktion 13 wurde ein etwa 1 : 1 Gemisch des Produkts und einer
etwas schneller eluierenden Verunreinigung gesammelt (Fraktion 13,
0,86 g). Fraktionen 14 (1,92 g) und 15 (1,61 g) enthielten das Produkt
mit viel weniger dieser Verunreinigung. Reines Material wurde in
den Fraktionen 16–20 (2,36
g) als farbloses Öl
gesammelt. Die Fraktionen 14 und 15 wurden re chromatographiert (separat),
auf einer 25 × 4,5
cm Säule
(150 g Silicagel). Daraus wurden jeweils 1,72 und 1,55 g reines
Produkt isoliert. Die Gesamtausbeute an reinem Produkt betrug 5,63
g (77% Ausbeute basierend auf 6,8-Bismercaptooctansäure).
-
Die
Analyse ergab die folgenden Ergebnisse: 1H-NMR
(CDCl3): 3,50 (Multiplett, 1H), 2,7 – 3,0 (Multiplet,
2H), 2,27 (t, 2H, CH2C(O)), 2,27 (s, 3H,
CH3), 2,26 (s, 3H, CH3), 1,1 – 1,8 (Multiplett,
8H).
13C-NMR (CDCl3):
195,76, 195,50, 179,59, 43,34, 34,60, 34,30, 33,71, 30,68, 30,48,
26,40, 26,01, 24,20.
IR (unverdünnte Flüssigkeit): 2935, 1736, 1691,
1423, 1355, 1134, 1118, 953, 744, 630.
TLC Rf =
0,40 (Ethylacetat-Hexan-Essigsäure,
100:100:1, v/v).
-
REINHEIT:
Die Analyse zeigt, dass das Endprodukt dieser Synthese (Bis-Acetyl-Liponsäure) mehr
als 98% Reinheit aufweist. Darüber
hinaus wurden fünf
unabhängige
Chargen im Rahmen dieser Studien erhalten, und die biologischen
Eigenschaften (in BEISPIEL 8 zusammengefasst) aller Chargen waren
in jedem getesteten Detail identisch. Die Struktur dieser Verbindung
ist unten dargestellt.
-
Beispiel 2
-
Herstellung von 6,8-Bisbenzoylmercaptooctansäure (Bisbenzoyl-Liponsäure)
-
Im Überblick
wurde 6,8-Bisbenzoylmercaptooctansäure in einem dreischrittigen
Verfahren aus gewerblicher α-Liponsäure hergestellt.
Die Liponsäure
wurde zunächst
mit Natriumborhydrid in Wasser unter leicht alkalischen Bedingungen
zu 6,8-Bismercaptooctansäure
reduziert. Dieses Produkt wurde mit drei Äquivalenten an Benzoylchlorid
in Gegenwart von Triethylamin benzoyliert, um das HCl-Nebenprodukt
abzufangen, um 6,8-Bisbenzoylmercaptooctansäure-Benzoesäureanhydrid zu ergeben. Das
Anhydrid wurde selektiv mit Dioxan/Wasser hydrolysiert, um 6,8-Bisbenzoylmercaptooctansäure zu ergeben,
ohne jedwede unerwünschte
Hydrolyse der Benzoylthioestergruppen. Das Produkt wurde durch Säulenchromatographie
auf Silicagel aufgereinigt. Die aufgereinigte Säure wurde in Methanol gelöst und durch
die langsame Zugabe einer wässrigen
Lösung,
die ein Mol Äquivalent
an Natriumbicarbonat enthielt, zu dem Natriumsalz konvertiert.
-
Im
Detail wurden diese Schritte wie erläutert durch das folgende Beispiel
durchgeführt:
-
SCHRITT
1: 6,8-Bismercaptooctansäure
wurde exakt wie in BEISPIEL 1 beschrieben hergestellt.
-
SCHRITT
2: 6,8-Bisbenzoylmercaptooctansäure-Benzoesäureanhydrid:
6,8-Bismercaptooctansäure (2,03
g, 10 mmol) wurde in 50 ml trockenem Methylenchlorid unter Stickstoff
gelöst,
und es wurde Triethylamin (3,24 g, 32 mmol, 4,50 ml) hinzugegeben.
Benzoylchlorid (4,50 g, 32 mmol) wurde in 20 ml Methylenchlorid gelöst und tropfenweise
unter Rühren über 20 Minuten
hinzugegeben. Triethylammoniumchlorid fiel aus, wenn etwa die Hälfte des
Benzoylchlorids hinzugefügt
worden war. Die Lösung
selbst blieb farblos. DA Rühren
wurde für
9 Stunden bei 25–27° fortgeführt. Das
Volumen wurde mit mehr Methylenchlorid (alle Feststoffe gelöst) auf
100 ml gebracht, und die Lösung
wurde in einen Separationstrichter überführt. Sie wurde schnell mit
2 × 50
ml 10%iger Zitronensäure
extrahiert (der pH-Wert der wässrigen
Phase wurde nach der Extraktion überprüft, um sicherzugehen,
dass er sauer war), und anschließend mit 50 ml gesättigter
Salzlösung
gewaschen. Die organische Phase wurde über Magnesiumsulfat getrocknet,
filtriert und das Methylenchlorid verdampft. Es verblieb ein fast
farbloses Öl,
welches 5,48 g wog.
-
SCHRITT
3: 6,8-Bisbenoylmercaptoocfansäure:
Das Roh-Anhydrid (5,48 g) wurde in 20 ml Dioxan gelöst, und
20 ml Wasser wurden hinzugefügt.
Dies führte
dazu, dass das Material ausölte.
Das Gemisch wurde bei 40–45° für 21 Stunden
gerührt.
Das Lösungsmittel
wurde unter Vakuum (2 mm) bei 30° verdampft.
Das verbleibende Öl
wurde in 80 ml Chloroform aufgenommen und mit 25 ml 5%iger wässriger
Zitronensäure
extrahiert. Die organische Phase wurde über Magnesiumsulfat getrocknet,
filtriert und das Lösungsmittel
verdampft. Ein blassgelbes Öl
wurde isoliert, welches 5,7 g wog. Die NMR-Spektren zeigten, dass nur etwa ein Drittel
des Anhydrids hydrolysiert worden war. Daher wurde das Rohmaterial
in 20 ml Dioxan wieder aufgelöst und
20 ml Wasser hinzugefügt.
Das Gemisch wurde bei 45° weitere
32 Stunden gerührt.
Das Lösungsmittel wurde
in vacuo verdampft. Nach dieser Behandlung war die Hydrolyse des
Anhydrids vollständig.
-
AUFREINGIUNG:
Das Produkt wurde mit 2 ml Ethylacetat gemischt und auf eine 25 × 4,5 cm
Silicagel 60-Säule
(150 g Flash-Silica), die in Hexan-Ethylacetat-Essigsäure (100 : 50 : 1, v/v) gepackt
war, gegeben. Die Säule
wurde mit diesem Lösungsmittel
eluiert. 40 ml-Fraktionen wurden bei etwa 5 ml/min gesammelt. Schneller
eluierendes Material wurde in den Fraktionen 10–12 (133 g eines weißen Feststoffs – wahrscheinlich Benzoesäure) gesammelt.
Eine kleine Menge dieses schneller eluierenden Materials wurde zusammen
mit dem Produkt in den Fraktionen 13–15 (0,66 g) gesammelt. Reines
Produkt wurde in den Fraktionen 16–21 (1,95 g farbloses Öl) gesammelt.
-
Die
Analyse ergab die folgenden Ergebnisse: 1H-NMR (CDCl3): 8,0 (Multiplett,
4H, ArH), 7,38 – 7,60 (Multiplett,
6H, ArH), 3,89 (Multiplett, 1H, CH-S), 3,0 – 3,3 (Multiplett, 2H, CH2S),
2,34 (t, J = 7,1 Hz, 2H, CH2C(O)), 1,1 – 2,2 (Multiplett, 8H, -CH2-).
13-C-NMR
(CDCl3): 191,71, 191,46, 179,72, 136,98, 136,92, 133,29, 128,51,
127,25, 127,14, 43,60, 34,98, 34,59, 33,76, 26,43, 26,19, 24,29.
TLC
Rf = 0,30 (Hexan-Ethylacetat-Essigsäure, 100 : 50 : 1, v/v).
IR
(unverdünnte
Flüssigkeit):
2937, 1710, 1704, 1662, 1667, 1655, 1448, 1207, 1175, 911, 773,
757, 733, 648, 688 cm-1.
-
NATRIUMSALZ:
Das Natriumsalz dieses Derivats ist besser löslich und leichter handhabbar.
Es ist daher im Allgemeinen bevorzugt, das Material in der Salzform,
wie im folgenden Beispiel erläutert,
herzustellen. Die Säure
(1,95 g, 4,7 mmol) wurde in 10 ml Methanol gelöst, und eine Lösung aus
Natriumbicarbonat (0,39 g, 4,7 mmol) in 10 ml Wasser wurde in kleinen
Portionen unter heftigem Schwenken über etwa 10 Minuten hinzugegeben.
Zunächst ölte Material
aus, aber, nachdem die Zugabe vollständig war, ergab sich eine farblose homogene
Lösung.
Die Lösung
wurde für
weitere 10 Minuten bei Raumtemperatur stehengelassen, anschließend wurde
das Lösungsmittel
unter Vakuum (2 mm) bei 20° entfernt,
was einen gummiartigen Feststoff ergab. Der Feststoff wurde in 10
ml Methanol gelöst
und das Lösungsmittel
in vacuo ausgeflasht. Dieses wurde ein zweites Mal wiederholt. Es
wurde ein schaumiger weißer
Feststoff erhalten. Dieser wurde in vacuo über P205 bei Raumtemperatur über Nacht
getrocknet. Es wurden 1,6 g des Salzes isoliert.
-
Die
Analyse ergab die folgenden Ergebnisse: 1H-NMR (D2O): 7,8 – 7,9 (Multiplett,
4H, ArH), 7,0 – 7,4 (Multiplett,
6H, ArH), 3,57 (Multiplett, 1H, -CH-S), 2,9 – 3,1 (Multiplett, 2H, CH2S),
2,06 (t, 2H, CH2C(O)), 1,0 – 2,1
(Multiplett, 8H, -CH2-).
13C-NMR (D2O): 193,49, 193,11, 183,39,
137,10, 137,00, 134,21, 129,21, 127,70, 127,58, 44,69, 38,15, 34,97,
27,23, 27,00, 26,46.
-
REINHEIT:
Die Analyse zeigte, dass die Präparationen
des Bis-Benzoyl-Lipoats zu mehr als 98% rein waren. Darüber hinaus
zeigte jede der drei unabhängigen
Präparationen
dieses Mittels identische biologische Eigenschaften (siehe BEISPIEL
6).
-
Die
Struktur dieser Verbindung ist unten erläutert.
-
Beispiel 3
-
Herstellung von 6,8-Biscarbamoylmethylmercaptooctansäure
-
6,8-Biscarbamoylmethylmercaptooctansäure: Jodacetamid
(1,11 g, 6,0 mmol) wurde zu einer Lösung aus 6,8-Bismercaptooctansäure (0,62
g, 3,0 mmol), gelöst
in 30 ml entgastem Methanolwasser (9:1, v/v) bei 0°C hinzugefügt. Die Lösung wurde
unter Stickstoff und unter gedämpftem
Licht gerührt,
und es wurde über
3 Minuten 1,0 M wässriges
Natriumhydroxid (9,0 ml, 9,0 mmol) hinzugefügt. Die klare Lösung wurde
bei 0°C
für 10
Minuten und anschließend
bei Raumtemperatur für
4 Stunden gerührt.
Der Großteil
an Methanol wurde unter verringertem Druck verdampft und das Volumen
mit entgastem Wasser auf 25 ml gebracht. Der pH-Wert wurde mit 2
M Salzsäure
auf 1 eingestellt. Das Wasser wurde in vacuo bei 25° verdampft
und das verbleibende blassgelbe Öl
mit 2 × 20
ml Ethylacetat geschüttelt.
Das Ethylacetat-unlösliche
Material wurde auf Silicagel unter Verwendung von Chloroform-Methanol-Essigsäure (120:60:1,
v/v) als Eluent chromatographiert, was 1,0 g (100%) der 6,8-Biscarbamoylmethyl-Mercaptooctansäure als
bräunlich-gelben
Feststoff ergab.
-
Die
Analyse ergab die folgenden Ergebnisse: 1H-NMR (D2O): 3,44 (s, 2H, – CH2C(O)NH2),
3,43 (s, 2H, -CH2C(O)NH2), 3,00 (m, 1H, -CHS), 2,88 (t, J = 7,44
Hz, 2H, CH2S), 2,51 (t, J = 7,1 Hz, 2H, -CH2COOH), 1,95 (m, 2H,
-CH2-), 1,5 – 1,8
(m, 6H, -CH2-).
13C-NMR (D2O): 180,07, 175,51, 175,24, 46,00,
35,65, 35,09, 34,11, 34,09, 34,03, 30,29, 26,29, 25,13.
TLC
Rf = 0,35; Silicagel G: Chloroform, Methanol, Essigsäure, 60
: 30 : 1, (v/v).
-
Beispiel 4
-
Herstellung von 6,8-Bis
[S-(N-methylsuccinimido)]mercaptooctansäure
-
6,8-Bis-[S-(N-methylsuccinimido)]mercaptooctansäure: 6,8-Bismercaptooctansäure (0,62
g, 3,0 mmol) wurde mit Natriumbicarbonat (0,25 g, 3,0 mmol), welches
in 25 ml entgastem Wasser gelöst
war, gemischt und unter Stickstoff bei Raumtemperatur gerührt, bis
sich eine klare Lösung
ergab. Es wurde N-Methylmaleimid (0,67 g, 6,0 mmol) hinzugefügt, und
das Gemisch wurde bei Raumtemperatur unter Stickstoff für 3 Stunden
gerührt.
Die Lösung
wurde filtriert, um Spuren von unlöslichem Material zu entfernen,
anschließend mit
20 ml Chloroform gewaschen. Der pH-Wert der wässrigen Phase wurde mit 2 M
Salzsäure
auf 1,5 eingestellt und das Gemisch mit 3 × 15 ml Chloroform extrahiert.
Die Chloroformextrakte wurden getrocknet (MgSO4), filtriert und
das Lösungsmittel
verdampft. Es verblieb ein farbloser Sirup, der 1,30 g wog. Die
TLC [Silicagel, (Chloroform-Methanol, 10:1, (v/v)] zeigte eine Anzahl überlappender
Spots mit Rf = 0,27, wie erwartet für das Gemisch von Diastereomeren,
was möglich
ist.
-
Die
Analyse ergab die folgenden Ergebnisse: 1H-NRM (CDCl3): 3,72 (m,
2H), 2,7 – 3,3
(m, 5H), 2,93 (s, 6H, CH3-), 2,25 – 2,55 (m, 4H), 2,0 – 1,35 (m,
8H).
13C-NMR (CDCl3): 178,73, 176,81, 176,77, 176,65, 176,62,
176,54, 176,50, 174,75, 175,69, 45,22, 44,78, 44,57, 39,11, 38,96,
38,90, 38,77, 38,59, 38,51, 38,00, 37,68, 36,35, 36,30, 36,24, 35,87,
35,85, 35,78, 34,49, 34,34, 33,96, 33,79, 33,67, 33,52, 29,08, 28,70,
28,66, 28,45, 25,92, 25,86, 25,58, 25,45, 25,02, 24,98, 24,21, 24,14.
-
Beispiel 5
-
Herstellung von Natrium
6,8-dihydroxyoctanoat
-
Natrium
6,8-dihydroxyoctanoat: Methyl 6,8-dihydroxyoctanoat (0,15 g, 0,80
mmol; enthaltend etwa 10% des 6,7-Isomers) wurde in 3 ml Methanol
gelöst,
und es wurde 1,00 M Natriumhydroxid in Methanol (0,80 ml, 0,80 mmol)
hinzugefügt.
Die Lösung
wurde unter Rückfluss
für 3 Stunden
gerührt.
Das Lösungsmittel
wurde in vacuo verdampft, was 0,15 g Natrium 6,8-dihydroxyoctanoat als weißes Pulver
ergab. Die Ausbeute war quantitativ.
-
Die
Analyse ergab die folgenden Ergebnisse: 1H-NMR (D2O): 3,74 (m, 1H, – CHOH-),
3,70 (t, J = 6,6 Hz, 2H, -CH2OH), 2,19 (t, J = 7,2 Hz, 2H, – CH2COOH),
1,2 – 1,9
(m, 8H, -CH2-).
13C-NMR (D2O): 184,47, 69,25, 59,42, 39,01,
38,21, 36,77, 26,47, 25,32.
-
Beispiel 6
-
Die
BEISPIELE 7–10
beschreiben Ergebnisse aus Kulturzellsystemen, was die Eigenschaften
und die Wirksamkeit der Liponsäurederivat-Verbindungen,
welche Gegenstand dieser Erfindung sind, zeigt. Tabelle 1 unten
fasst alle Ergebnisse, die in den BEISPIELEN 7–10 gefunden wurden, in verkürzter und
tabellenförmiger Form
zusammen.
-
Im Überblick
zeigten alle Beispiele, welche die Liponsäurederivate auf Gewebekulturzellen
anwendeten, dass die Liponsäurederivate
die Fähigkeit
besaßen,
Tumorzellen abzutöten,
während
sie in den geeigneten Dosisbereichen kontaktinhibierte, normale
Nicht-Krebszellen unverletzt ließen.
-
Zweitens
wurde jeder getestete Krebszelltyp durch eine oder mehrere Mitglieder
der Familie von blockierten Liponsäurederivaten abgetötet. Dies
deutete darauf hin, dass diese Mittel ein breites Spektrum an potenziellen
klinischen Anwendungen haben, einschließlich viele oder die meisten
der humanen Krebsarten.
-
Drittens
hatten unterschiedliche Liponsäurederivatverbindungen
etwas unterschiedliche chemische Eigenschaften, einschließlich beispielsweise
Löslichkeit
in polaren und nicht-polaren Umgebungen, mit entsprechenden Wirkungen
darauf, wie effizient verschiedene Derivate die Zellmembran durchqueren
und in die Zelle eindringen. Darüber
hinaus wiesen die Liponsäurederivate
unterschiedliche Verbrauchgeschwindigkeiten durch zelluläre Enzyme
auf, die normalerweise Liponsäure
selbst verarbeiten. Unter Berücksichtigung
dieser Eigenschaften wurde beobachtet, dass die verschiedenen Liponsäurederivate
etwas unterschiedliche Anti-Krebswirksamkeiten
aufwiesen. Einige Derivate hatten eine hohe Wirksamkeit, während andere
niedrigere, aber immer noch potenziell nützliche Wirksamkeiten aufwiesen.
-
Viertens
könnten,
da verschiedene Tumorzelltypen verschiedene physiologische Eigenschaften
aufwiesen, diese Eigenschaften indirekte Wirkungen sowohl auf die
Aufnahme und den Einbau von Liponsäurederivaten als auch auf die
toxischen Wirkungen dieses Einbaus ausüben. Somit wurde herausgefunden,
dass verschiedene Krebszelltypen signifikant unterschiedliche Grade
der Empfindlichkeit zeigten. Diese Empfindlichkeit der verschiedenen
Krebszellen variierte von relativ empfindlichen Krebszelltypen,
die durch alle getesteten Liponsäurederivate
abgetötet
wurden, bis hin zu relativ resistenten Krebszelltypen, die nur durch
die stärker
wirksamen Liponsäurederivatverbindungen
wirksam abgetötet
wurden.
-
Trotz
dieser Unterschiede in der Wirksamkeit ist es wichtig festzustellen,
dass die Liponsäurederivate in
den BEISPIELEN unten beschriebene gemeinsame Eigenschaften aufweisen.
-
-
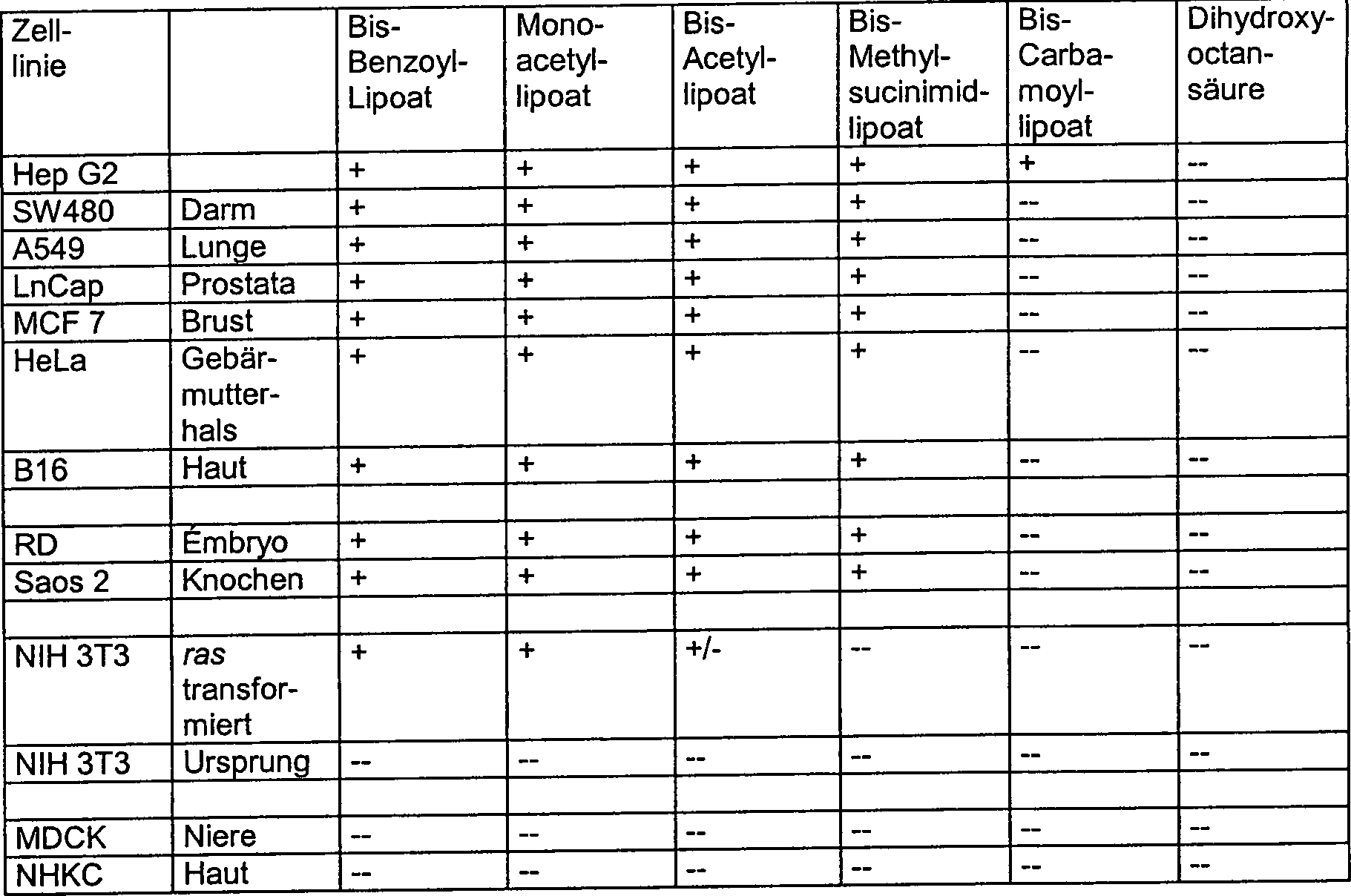
Tabelle
1: Es ist das Ansprechen von Zellen in Kultur auf das Abtöten durch
Beispielmitglieder der Familie von blockierten Lipoatderivaten zusammengefasst,
welche Gegenstand dieser Erfindung sind, sowie durch eine Kontrollverbindung
(Dihydroxyoctansäure).
Auf der rechten Seite ist die spezifische Zelllinie angegeben, gefolgt
vom Ursprungsgewebe der Zelllinie. Oben sind die spezifischen getesteten
Verbindungen aufgelistet. Jedes blockierte Lipoatderivat wurde zwei-
bis vierfach oberhalb seiner Schwellen- Abtötungskonzentration
verwendet. [Diese Konzentrationen waren im Bereich von 0,15 mM (60 μg/ml oder
60 mg/kg) bis 2,5 mM (800 μg/ml
oder 800 mg/kg) (siehe BEISPIEL 9).] Dihydroxyoctansäure wurde
bis zu Konzentrationen von 5 mM (3200 μg/ml oder 3200 mg/kg) ohne nachweisbare
Wirkung getestet. "+" zeigt, dass die
Zellen durch die Behandlung abgetötet wurden, während "–" zeigt, dass sie nicht abgetötet wurden. "+/–" zeigt ein langsames geringfügiges Ansprechen,
die nur in einigen speziellen Fällen
mit experimentell durch das Einführen
des ras-Oncogens transformierten Fibroblasten beobachtet wurde (BEISPIEL
10).
-
Beispiel 7
-
Dieses
Beispiel beweist, dass die Liponsäurederivate dieser Erfindung
Krebszellen mit hoher Spezifität
abtöten.
Genauer wird die Verwendung von Liponsäurederivaten in Kulturzellsystemen
beschrieben. Die Ergebnisse zeigen, dass die Lipoatderivate Krebszellen
(transformiert) unter Bedingungen, unter denen normale Nicht-Krebszellen
(nicht-transformiert) scheinbar unbeeinträchtigt waren, effizient abtöteten. Die
in TABELLE 1 in BEISPIEL 6 zusammengefassten Daten wurden unter
Verwendung der folgenden Vorgehensweise erzeugt:
Zunächst wurde
jeder zu testende Zelltyp bei geringen Dichten in die Vertiefungen
einer Standardgewebekulturplatte mit 6 × 24 Vertiefungen plattiert.
(Für jeden
Zelltyp wurden mehrfache Vertiefungen ausgesät.)
-
Zweitens
ließ man
die Zellen auf mittlere Dichte wachsen. Transformierte Zellen sind
in Kontakt, und nicht-transformierte Zellen sind kontaktinhibiert
unter diesen Bedingungen.
-
Drittens
wurden die zu testenden Lipoatderivate zu den einzelnen Vertiefungen
hinzugefügt.
In diesen Experimenten wurde jede Verbindung in einer zweifachen
bis vierfachen Konzentration oberhalb der Schwellen-Abtötungskonzentration
für Krebszellen
hinzugefügt
(BEISPIEL 9).
-
Viertens
wurden die Zellen über
die nächsten
Tage überwacht.
-
Für alle getesteten
blockierten Lipoatderivate wurde gefunden, dass jeder empfindliche
Krebszelltyp effizient abgetötet
wurde, während
jeder der vier verschiedenen normalen Nicht-Krebszelltypen, die
getestet wurden, nicht beeinträchtigt
wurde.
-
1 zeigt
die Ergebnisse von Experimenten unter Verwendung der Liponsäurederivate,
zum selektiven Abtöten
einer Reihe von Tumorzelltypen.
-
Beispiel 8
-
In
diesem Beispiel wurde das gut entwickelte Zellkultursystem NIH-3T3
zum Testen der Liponsäurederivate
dieser Erfindung verwendet. NIH-3T3-Zellen sind relative normale,
nicht-krebsartige Zellen. Wenn jedoch ein aktiviertes Allel des
ras-Oncogens in diese Zellen eingeführt wird, werden sie stark
bösartig
(krebsartig), wie durch verschiedene Tests nachgewiesen werden kann
(REFERENZ).
-
Unter
Verwendung des in BEISPIEL 7 beschriebenen Verfahrens wurde die
Empfindlichkeit auf Liponsäurederivate
von Ursprungs-NIH 3T3-Zellen und dem ras-transformierten T24-Derivat
dieser Zellen verglichen. Es wurde gefunden, dass die stärkeren blockierten
Lipoatderivate (siehe TABELLE 1, BEISPIEL 6) die transformierten
Zellen sehr effizient abtöteten,
während
die nicht-transformierten
Urpsrungs-Zellen unbeeinträchtigt
blieben. Die Ergebnisse sind in 2 gezeigt.
-
Somit
stellen diese Ergebnisse zusätzliche
Hinweise darauf dar, dass blockierte Lipoatderivate Krebszellen
mit hoher Spezifität
abtöten.
-
Beispiel 9
-
Dieses
Beispiel prüft
einige der Eigenschaften, welche die Liponsäurederivate der Erfindung gemeinsam
haben.
-
Zunächst tötete jede
Verbindung Krebszellen in Kultur bei oder oberhalb eines relativ
schmalen, spezifischen Konzentrationsbereiches ab, aber nicht darunter.
Die unten angegebenen Schwellenkonzentrationen stellen den ungefähren Mittelwert
dieses Bereichs dar, welcher sich grob über zweifach bis dreifach erstreckt. Dieses
Abtötungsprofil
zeigte, dass diese Verbindungen einen oder mehrere zelluläre Prozesse
oder Ziele absättigen,
um eine Abtötung
zu erreichen. Unterhalb dieser Absättigungsbereiche überlebten
empfindliche Zellen und wuchsen. Sie konnten entfernt und replattiert
werden, um, scheinbar unendlich, unter diesen Bedingungen weiterzuwachsen.
Im Gegensatz dazu hielt oberhalb dieser spezifischen Konzentrationsbereiche
des Liponsäuremittels
das Zellwachstum an, und es folgte der Zelltod. Dies war ein sehr
ungewöhnliches
Dosis/Ansprech-Profil. Die Schwellen-Abtötungskonzentrationen
(Bereiche) variierten zwischen einzelnen Verbindungen. Beispiele
dieser Schwellen-Abtötungskonzentrationen
waren wie folgt: Bis-Benzoyl-Lipoat (BEISPIEL 2) 60 mg/Liter (60
mg/kg); Bis-Acetyllipoat
(BEISPIEL 1) 600 mg/Liter (600 mg/kg).
-
Zweitens
erzeugte jedes getestete Liponsäurederivat
spezifische morphologische Veränderungen
in empfindlichen Zielzellen über
eine anfängliche
12–24-stündige Zeitdauer
der Behandlung. Diese Veränderungen
umfassten eine Abrundung sowie die häufige Bildung von Zellpaaren,
die durch brückenartige
Strukturen verbunden waren, die an zum Stillstand gebrachte Cytokinese
erinnerten. Auf diese Veränderungen
folgte letztendlich der Zelltod, wenn die Behandlung weitergeführt wurde.
Diese morphologischen Veränderungen wurden
jedoch rückgängig gemacht,
und die Zellen erholten sich, wenn das Lipoatderivat während dieses
anfänglichen
Ausgesetztseins entfernt wurde. Wie mit dem Dosis/Ansprech-Profil
des vorangegangenen Absatzes ist diese reversible Induzierung der
morphologischen Veränderung,
gefolgt von einer Zwangsläufigkeit
des Zelltods stark idiosynkratisch. Die Erkenntnis, dass dieses
Verhalten von allen getesteten Mitgliedern der Klasse von Verbindungen,
die Gegenstand dieser Erfindung sind, gezeigt wurde, war wiederum
ein sehr starker Hinweis darauf, dass diese Verbindungen tatsächlich eine
funktionell kohärente
Klasse sind.
-
Beispiel 10
-
Dieses
Beispiel stellt Hinweise bereit, dass die Liponsäurederivate, die Gegenstand
dieser Erfindung sind, Krebszellen durch die Induzierung von Apoptose
(programmierter Zelltod) abtöten.
Von Wichtigkeit ist, dass alle getesteten Mitglieder diese Eigenschaft
aufwiesen. Dies stellt einen starken zusätzlichen Beweis dar (ebenso,
siehe BEISPIELE 6, 7 und 9), dass diese Verbindungen auf die gleiche
Art und Weise fungieren. Tatsächlich
induzieren diese Verbindungen offensichtlich Krebszellen dahingehend, "Selbstmord zu begehen". Des Weiteren ist
die Induzierung von Apoptose im Gegensatz zur Nekrose eine vorteilhafte
Eigenschaft für
die klinische Verwendung dieser Verbindungen. Unter apoptotischen
Bedingungen ist der "Selbstmord" von Krebszellen
weniger störend
als Nekrose der umgebenden normalen Zellen.
-
Um
das in diesem Beispiel beschriebene Experiment zu verstehen, ist
es notwendig, die Einzelheiten betreffend den speziellen in den
Experimenten verwendeten Test zu betrachten. Zellkern-DNA von Zellen
ist normalerweise in sehr langen Molekülen vorhanden, die Chromosome
bilden. Diese sehr langen polymeren Moleküle haben nur sehr seltene freie
Enden. Im Gegensatz dazu führt
die Induzierung der Apoptose in der Zelle dazu, dass diese sich
selbst zerstört,
und in diesem Prozess wird eine extrem große Anzahl von Brüchen in
die DNA eingeführt,
und diese wird in ihre kleineren Monomer-Bestandteile zerkleinert.
Das geeignete Enzym – terminale
Transferase – addiert
Nukleotide an die freien Enden von DNA-Molekülen. Darüber hinaus verwendet dieses
Enzym Monomere (Nukleotide) für
diese Additionsreaktion, welche stark fluoreszierende Gruppen aufweisen.
Falls somit die Zellkerne von normalen Zellen – mit wenigen freien DNA-Enden – mit einer
terminalen Transferase und fluoreszierenden Monomeren behandelt
werden, wird sehr wenig Fluoreszenz zu diesen Zellkernen hinzugefügt. Im Gegensatz
dazu wird, wenn diese Komponenten zu den Zellkernen von Zellen hinzugefügt werden,
die einer Apoptose unterliegen, und eine große Anzahl von fluoreszierenden
Monomeren hinzugefügt
wird – zu
den sehr vielen DNA-Enden, die vorhanden sind, resultiert dies in
einer massiven Einführung
von Fluoreszenz. Der herkömmliche Assay,
der auf diesen Eigenschaften beruht, wird durch das Akronym TUNEL
bezeichnet.
-
Das
Folgende ist ein Beispiel der Experimente, welche zeigen, dass die
Lipoatderivate, die Gegenstand dieser Erfindung sind, Apoptose induzieren.
HeLa-Krebszellen wurden in mehrere Vertiefungen in einer Gewebekulturplatte
ausplattiert. Einige Vertiefungen (experimentell) wurden mit dem
Bis-Benzoyl-Lipoat-Derivat
(BEISPIEL 2) bei einer etwa zweifach höheren Konzentration als der
Schwellen-Abtötungskonzentration (BEISPIEL
9) behandelt, während
andere Vertiefungen (Kontrollen) unbehandelt belassen wurden. Nach
ca. 20 Stunden begannen die behandelten (experimentellen) Zellen,
abzusterben. Die experimentellen und Kontroll-Zellen wurden dann
fixiert, permeabilisiert und einer terminalen Transferase und fluoreszierende
Monomeren (Nukleotiden) ausgesetzt. Dieser Test zeigt, dass dieser
Untertyp von Krebszellen, welche in dem Moment des Tests aktiv absterben,
das TUNEL-Fluoreszenzsignal zeigen, das bei Zellen erwartet wird,
die eine Apoptose durchlaufen. Dies zeigt, dass alle getesteten
Mitglieder der Liponsäureverbindungen,
die Gegenstand dieser Erfindung sind, in Krebszellen Apoptose induzieren.
-
Die
Ergebnisse des obigen Experiments sind in 3 dargestellt.
-
Beispiel 11
-
Dieser
Abschnitt bespricht die Toxikologie in der Maus für die Liponsäurederivate
dieser Erfindung. Ein Schlüsselpunkt
bei der Untersuchung der praktischen klinischen Eignung von neuen
Anti-Krebsmitteln ist ihre Toxizität für Menschen und Tiere, in denen
sie verwendet werden sollen. Um sehr gut geeignet zu sein, müssen solche
Mittel unter Bedingungen, bei denen sie Krebszellen wirksam abtöten oder
inhibieren, im menschlichen oder tierischen Wirt relativ unschädlich sein.
Mitglieder der Familie von blockierten Lipoatderivaten zeigten diese
wünschenswerte,
essenzielle Eigenschaft, wie durch die folgenden Beobachtungen gezeigt
wird.
-
Es
ist seit vielen Jahren bekannt, dass selbst normal vorkommende,
biogene Moleküle
toxisch sind, wenn sie in ausreichend hohen Dosen verabreicht werden.
Liponsäure
ist offensichtlich keine Ausnahme. Bei ausreichenden Dosen kann
sie eine Maus töten.
Wir werden diese Tötung
im Folgenden als nicht spezifische Toxizität bezeichnen. Die getesteten
Mitglieder unserer neuen Klasse von Verbindungen haben nicht-spezifische
Toxizitäten,
die niedriger sind als bei normaler Liponsäure. Darüber hinaus haben die getesteten
Mitglieder dieser Klasse, welche die höchste Wirksamkeit gegen Tumore
in Zellkultur aufweisen, die niedrigsten nicht-spezifischen Toxizitäten.
-
Aus
diesem Grund können
stärker
wirksame Mitglieder dieser Klasse von Verbindungen in Dosen in Tiere
injiziert werden, die um ein Vielfaches höher sind als die Dosis, bei
der eine ausreichende Abtötung
von Tumorzellen in Zellkultursystemen erwartet wird, wobei keine
sichtbare Toxizität
in dem Tier auftritt.
-
Zusammengenommen
zeigen diese Ergebnisse, dass Mitglieder dieser Klasse von Mitteln
an Mäuse und
Menschen in Dosen verabreicht werden können, die höher sind als jene, die für die Behandlung
von Tumoren erforderlich sind, und zwar ohne signifikante Nebenwirkungen.
-
Die
relevanten Einzelheiten dieser Studie sind wie folgt:
Zunächst hat
Liponsäure
selbst (D, L razemisches Gemisch) eine LD-50 von ca. 500 mg/kg Körpergewicht
in Mäusen.
(Alle Studien, die in diesem Abschnitt beschrieben sind, wurden
durch intraperitoneale (IP) Injektion in C57/BL-Mäusen
durchgeführt.)
-
Zweitens
stellte sich heraus, dass die nicht-spezifische Toxizität des Bis-Acylliponsäurederivats
eine LD-50 von ca. 500 mg/kg ergab, mit einer maximalen gut tolerierten
Dosis von ca. 200 mg/kg. Es ist auch zu bemerken, dass dies eine
signifikant geringere nicht-spezifische Toxizität als für normales Lipoat darstellt.
[Es ist darauf hinzuweisen, dass die nicht-spezifische Toxizität dieser
und aller anderen getesteten Lipoatverbindungen akut war – Tod des
Tieres tritt innerhalb von Minuten der IP-Injektion auf. Sie schien
daher mit dem Zelltod, der über
eine Zeitdauer von Tagen in Krebszellen auftrat, die in Kultur mit
blockierten Lipoatderivaten behandelt wurden, nicht zusammenzuhängen (siehe
BEISPIELE 6–10).]
-
Drittens
hatte das Bis-Benzylliponsäurederivat
eine LD-50 von ca. 1000 mg/kg Körpergewicht
mit einer maximalen gut tolerierten Dosis von ca. 500 mg/kg. Dies
war eine signifikant geringere Toxizität als die von Bis-Acetyllipoat
(oben) und viel geringer als normales Lipoat.
-
Viertens
wurden auf der Grundlage dieser Ergebnisse die folgenden Berechnungen
durchgeführt:
Die Gesamtmasse des Tieres umfasste ca. 70 Wasser. Dies war wie
folgt verteilt. Ca. 50% der adulten Masse war intrazelluläres Wasser,
ca. 15% der Gesamtmasse war Nicht-Blutextrazelluläre Körperflüssigkeit
(im Allgemeinen als "interstitielle
Körperfüssigkeit" bezeichnet), und
ca. 5% der Gesamtmasse war Blut. Dies führte zu der folgenden hochgerechneten
Sequenz. Ca. 500 mg/kg des Bis-Benzylderivats
wurde in die Bauchhöhle
einer Maus injiziert. Dieses Material wurde schnell in das Blut
aufgenommen. Die wirksame Dosis des Bis-Benzylderivats in Zellkultur betrug
60 μg/ml
oder 60 mg/kg (siehe BEISPIELE 6 und 9). Es wurde erwartet, dass
diese IP-Injektion rasch mit Blut äquilibrieren würde, was
zu Konzentrationen führen
würde,
die übergangsweise
annähernd
10000 mg/kg oder ca. 167 mal die wirksame Konzentration dieses Mittels
im Blut erreichen würde.
Es wurde weiter erwartet, dass dies mit der interstitiellen Körperflüssigkeit äquilibrieren
würde,
was zu Konzentrationen von annähernd
2500 mg/kg oder ca. 42 mal der wirksamen Konzentration in dieser
Körperflüssigkeit ergeben
würde.
Dies äquilibrierte
anschließend
mit den Gesamtkörperflüssigkeiten,
um Konzentrationen von annähernd
715 mg/kg oder ca. 12 mal der wirksamen Dosis in den gesamten Körperflüssigkeiten
zu ergeben.
-
Zusammenfassend
führen
diese Ergebnisse zu zwei wichtigen Schlussfolgerungen. Erstens zeigen sie,
dass die wirksamen Konzentrationen leicht durch die stärker wirksamen
Mitglieder dieser Klasse von Mitteln erreicht werden konnten – einschließlich Bis-Benzoyl-Lipoat – von denen
erwartet wurde, dass sie ausreichend sein würden, um Krebszellen in dem
Tier abzutöten,
ohne das Tier in anderer Weise sichtbar zu beeinflussen. Diese Kombination
von niedriger, nicht-spezifischer Toxizität und hoher spezifischer Toxizität für Tumorzellen
war hervorstechend und zeigte, dass diese Klasse von Mitteln ein
hohes klinisches Potenzial haben. Zweitens zeigen die relativen
Eigenschaften der Bis-Acetyl- und Bis-Benzoyl-Mitglieder der Liponsäurederivatfamilie
diesen Punkt. Beide Derivate hatten eine spezifische Anti-Krebsaktivität, welche
normales Lipoat nicht aufwies, wobei sie gleichzeitig einen geringeren
Grad an nicht-spezifischer Toxizität haben. Des Weiteren wurde
ein ähnliches
Verhältnis
zwischen den blockierten Lipoatderivaten beobachtet, und zwar wie
folgt. Bis-Benzoyl-Lipoat hatte gleichzeitig eine niedrigere nicht-spezifische
Toxizität
und eine viel höhere
Anti-Krebswirksamkeit
als das Bis-Acetylderivat. Dieses und ähnliche Ergebnisse demonstrieren
eindeutig, dass die Anti-Krebsaktivität und nicht-spezifische Toxizität unabhängig voneinander
variieren.
-
Beispiel 12
-
Die
oben beschriebenen Entdeckungen zeigen, dass es möglich sein
sollte, Krebszellen abzutöten, ohne
dem behandelten Menschen oder Tier Schaden zuzufügen, wobei Mitglieder der neuen
Klasse von Verbindungen verwendet werden, die Gegenstand dieser
Erfindung sind (siehe insbesondere BEISPIELE 6 und 11). In diesem
Beispiel stützen
die Ergebnisse von Studien in Mäusen
diese Erwartung. Die relevanten Ergebnisse sind wie folgt.
-
Der
B-16-Melanomstamm wurde entweder subkutan oder intraperitoneal in
einzelne Mäuse
des C57/BL syngeneischen Mäusestamms
eingebracht (7). Wenn diese Mäuse
nicht behandelt wurden, entwickelten sie massive Tumore in der unmittelbaren
Umgebung der Injektion, sowie sekundäre Metastasen, die über das
ganze Tier verteilt waren – einschließlich der
Leber und der Lungen. Dieses bösartige
Zellwachstum resultiert in dem frühen Tod der Tiere. Darüber hinaus
bestand das resultierende bösartige
Zellwachstum aus dunkel pigmentierten bösartigen Melanozyten – was ihre
Untersuchung bequem und sehr verlässlich macht. Wir werden dieses
im Folgenden als das "B-16-System" bezeichnen.
-
Unter
Verwendung des B-16-Systems haben wir die Bis-Benzoyl- und Bis-Acetyllipoatmitglieder
verwendet, um zu demonstrieren, dass Mitglieder der neuen Klasse
von Verbindungen, die Gegenstand dieser Erfindung sind, eine Anti-Krebswirksamkeit
aufweisen, die auf der Grundlage der in den vorangegangenen Beispielen
beschriebenen Entdeckungen zu erwarten war. Die relevanten Ergebnisse
sind wie folgt.
-
Zuerst
wurden einer Gruppe von Mäusen
IP B16-Zellen injiziert. Die injizierte Gruppe wurde nach dem Zufallsprinzip
in zwei gleiche Untergruppen aufgeteilt. Einer Untergruppe (experimentell)
wurde IP zwei mal am Tag 100 mg/kg des Bis-Benzoyl-Lipoatmitglieds
der Verbindungsklasse in 200 μl
10 %igem Ethanol IP-injiziert. [Siehe BEISPIELE 2, 6 und 9 für Beschreibungen
des Bis-Benzoyl-Lipoats.]
Der zweiten Untergruppe (Kontrolle) wurden 200 μl 10 %iges Ethanol allein injiziert.
-
Nach
16 Tagen wurden die Tiere untersucht – einschließlich durch Sezieren, wo es
angemessen war. Die Kontrolltiere hatten viele massive IP-Tumormassen. Im Gegensatz
dazu hatten die entsprechenden experimentellen Tiere eine wesentlich
verringerte Tumoranzahl und -masse – weniger als 30–50% Masse
als die Kontrollprobe.
-
Zweitens
wurde einer Gruppe von Tieren an einer subkutanen Stelle B-16-Zellen injiziert.
Nach 6–8 Tagen
wurden große,
sphärische,
leicht fühlbare
Tumore (ca. 3–5
mm im Durchmesser) an der ursprünglichen Zell-Injektionsstelle
beobachtet. Zu diesem Zeitpunkt begann eine Gruppe der Tiere (experimentell)
mit einer zwei mal täglichen
Serie von Injektionen des Bis-Acetyllipoatderivats
(100 mg/kg in 100 μl
isotonischer Kochsalzlösung),
und eine zweite Gruppe (Kontrollen) mit entsprechenden Injektionen
des Kochsalzlösungsmittels allein.
[Siehe BEISPIELE 1, 6 und 9 für
die Einzelheiten des Bis-Acetyllipoatderivats.] In den experimentellen Tieren – aber nicht
in den Kontrollen – beobachteten
wir häufig
eine fühlbare
Aufweichung und scheinbar teilweise Verflüssigung der Tumormasse, gefolgt
von einer Stabilisierung oder einer Reduzierung der Größe. Dies zeigt,
dass das Bis-Acetylderivat in diesen Tumoren unter diesen Bedingungen
einen signifikanten Zelltod herbeiführt.
-
Drittens
wurden, wie im vorangegangenen Abschnitt, in mehreren Tieren subkutane
Tumore erzeugt. Nachdem die Tumore auf eine sichtbare, fühlbare Größe herangewachsen
waren, erhielten diese Tiere sowohl eine zwei mal tägliche IP
(systemische) Dosis von 50 mg/kg Bis-Benzoyl-Lipoat, sowie eine
zwei mal tägliche direkte
Injektion einer zweiten Dosis desselben Volumens direkt in die Tumormasse.
Diese Tiere zeigten sichtbar eine besonders massives Ansprechen,
einschließlich
eines Falls, in dem die Tumormasse drastisch sank und im Verlauf
der Behandlung im Wesentlichen oder vollständig verschwand.
-
Zusammenfassend
zeigen diese Resultate ganz klar, dass die Bis-Benzoyl- und Bis-Acetyllipoatderivate
eine zu erwartende Anti-Krebswirksamkeit und Spezifität im intakten
Tier aufweisen. Auf der Grundlage dieser Ergebnisse kann der Fachmann
auf dem Gebiet die Dosen und Dosisregimes so anpassen, um eine partielle
oder vollständige
Kontrolle und/oder Eliminierung dieser Tumore in diesen Tieren zu
erreichen.
-
Beispiel 13
-
Ein
möglicher
Mechanismus der Wirkung der blockierten Lipoatderivate, die Gegenstand
dieser Erfindung sind, ist, dass sie PDC spezifisch in Krebszellen
inhibieren, was zu einem Verlust der Polarisierung der Mitochondrienmembran
führt und
daher zu einer Induzierung der Apoptose in Krebszellen. Es ist zu
erwarten, dass blockierte Lipoatderivate synergistisch mit anderen
Mitteln wechselwirken könnten,
die entweder den Energiemetabolismus der Mitochondrien inhibieren
und/oder auf die eine oder andere Weise Apoptose induzieren.
-
Dies
wurde in diesem Beispiel mit Dichloracetat (im Folgenden als CDA
abgekürzt)
getestet (8). Diese Verbindung ist ein Pyruvatanalogon. Als solches ist
eine ihrer erwarteten Wirkungen die kompetitive Inhibierung von
PDC. Es wurde gefunden, dass diese Verbindung synergistisch mit
den blockierten Lipoatderivaten wechselwirkt, wie es zu erwarten
war. Eine relevante experimentelle Beobachtung ist wie folgt.
-
HeLa-Zellen
wurden in einer Serie von Vertiefungen in einer Gewebekulturplatte
mit mehreren Vertiefungen bei mittleren Dichten plattiert, und man
ließ sie
sich anheften und für
ca. 24 Stunden wachsen. Zu einzelnen Vertiefungen einer ersten Untergruppe
(Kontrolle) wurden jeweils Bis-Acetyllipoat
oder Bis-Benzoyl-Lipoat, jedes bei einer Dosis, die etwa zweifach
oberhalb der Schwellenbtötungsdosis
lag (BEISPIEL 9) – hinzugefügt.
-
Zu
einer gleichwertigen (experimentellen) Untergruppe von Vertiefungen
wurden dieselben Verbindungen bei der gleichen Dosis zusammen mit
einer gleichzeitigen Zugabe von DCA in einer 5 mM endgültigen Konzentration
hinzugegeben. Wir beobachten, dass die Zellen der experimentellen
Untergruppe etwa zwei mal so schnell wie in der Kontrolluntergruppe
abgetötet
werden.
-
Dies
war eine bemerkenswerte Wirkung. 24 Stunden nach der Behandlung
der experimentellen Gruppe war diese fast vollständig abgetötet, während ein ähnlicher Grad der fast vollständigen Abtötung in
der Kontrolluntergruppe nicht bis ca. 48 Stunden danach beobachtet
wurde.
-
Auf
der Grundlage dieser Art von experimentellen Beobachtungen ist es
wahrscheinlich, das diese Lipoatderivate dieser Erfindung mit anderen
Metabolismusinhibitoren und/oder anderen chemotherapeutischen Mitteln
synergistisch wechselwirken, um Krebszellen effizienter abzutöten. Es
ist in der Tat eine wirksame klinische Anwendung der neuen Verbindungen,
die Gegenstand dieser Erfindung sind, dass sie zusammen mit weiteren
Mitteln wirken können.
-
REFERENZEN
-
- (1) Baggetto, L G. 1992. Deviant energetic metabolism of
glycolytic cancer cells. Biochemie 74: 959–974.
- (2) Garrett, R H und Grisham, C M. 1995. Biochemistry. New York:
Saunders College Publishing.
- (3) Dvorak, H F. 1986. Tumors: wounds that do not heal. Similarities
between tumor stroma generation and wound healing. New England Journal
of Medicine 315: 1650–1659.
- (4) Whalen, G F. 1990. Solid tumors and wounds: transformed
cells misunderstood as injured tissue? Lancet 136: 1489–1492.
- (5) Patel, M S und Roche, T E. 1990. Molecular biology and biochemistry
of pyruvate dehydrogenase complexes. FASEB Journal 4: 3224–3233.
- (6) Johnson, L V, et al. 1980. Proceedings of the National Academy
of Sciences, USA 77: 990–994.
- (7) Fidler, I.J., Gersten, D.M. und Budman, M.B. 1976. Characterization
in vivo and in vitro of tumor cells selected for resistance to syngeneic
lymphocytemediated toxicity. Cancer Res. 36: 3160–3165.
- (8) Stacpoole, P.W., Henderson, G.N., Yan, Z., Cornett, R und
James, M.O. 1998. Pharmacokinetics, metabolism and toxicology of
dichloroacetate. Drug Metabolism Reviews. 30: 499–539.
- (9) Hill, S.A., Wilson, S., Chamber, A.F. 1988. Clonal heterogeneity,
experimental metastatic ability, and p21 expression in H-ras-transformed
NIH 3T3 cells. J. Natl. Cancer Inst. 80: 484–90.