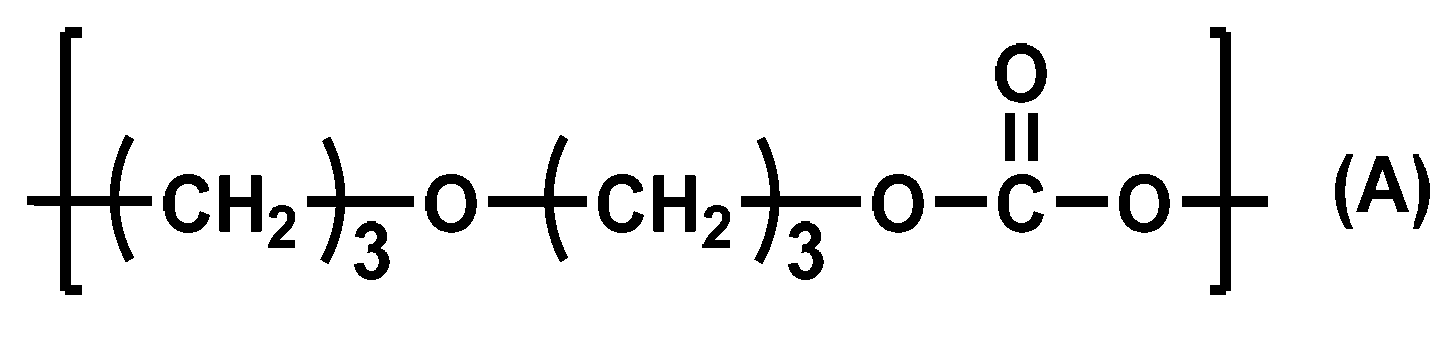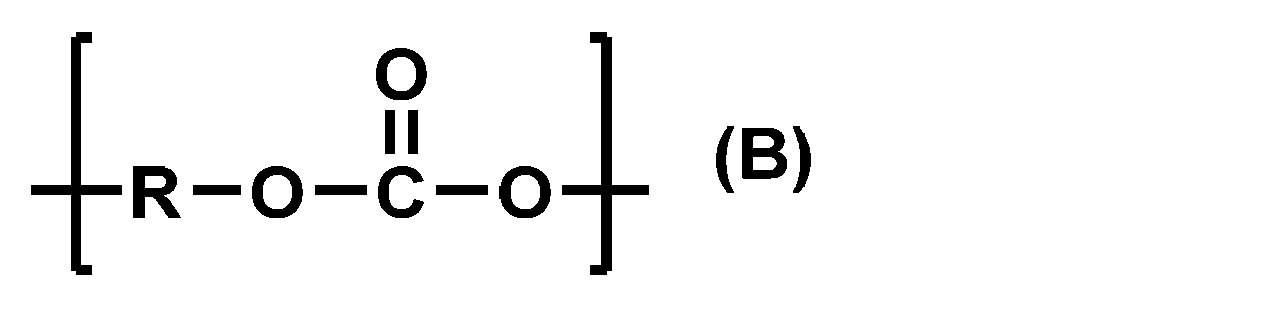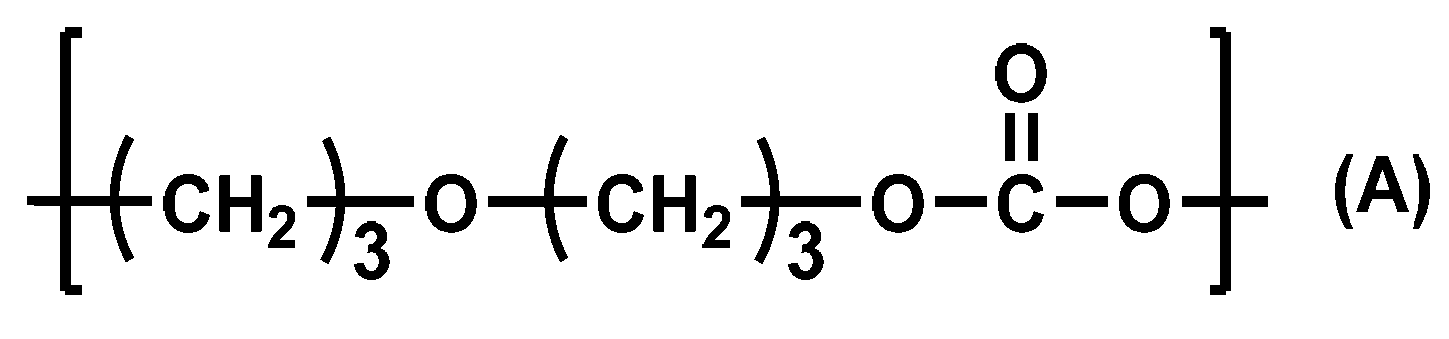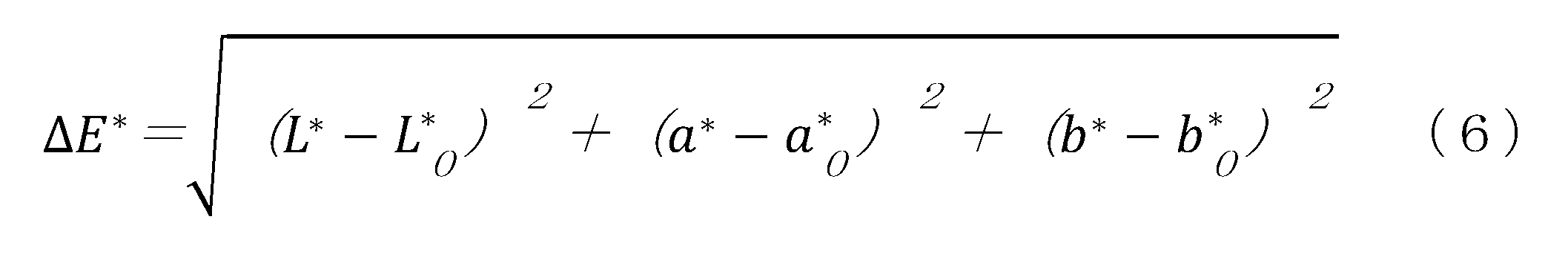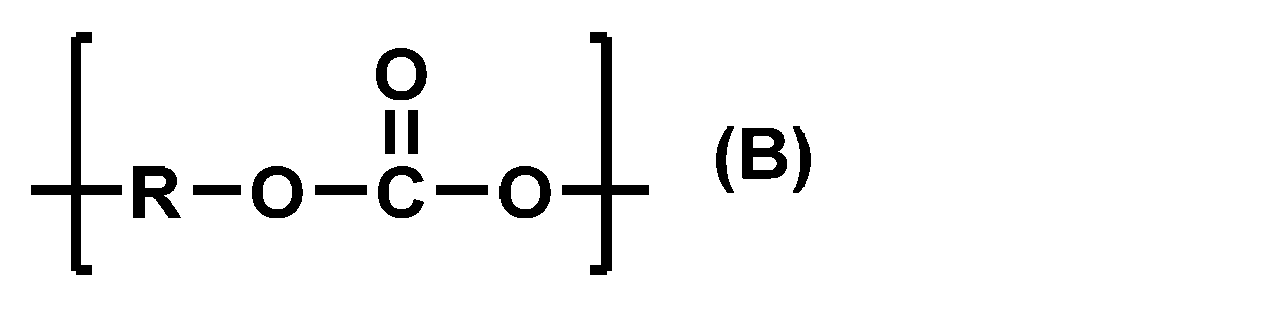WO2020179483A1 - ポリカーボネートジオール及びその用途 - Google Patents
ポリカーボネートジオール及びその用途 Download PDFInfo
- Publication number
- WO2020179483A1 WO2020179483A1 PCT/JP2020/006909 JP2020006909W WO2020179483A1 WO 2020179483 A1 WO2020179483 A1 WO 2020179483A1 JP 2020006909 W JP2020006909 W JP 2020006909W WO 2020179483 A1 WO2020179483 A1 WO 2020179483A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- polycarbonate diol
- mass
- formula
- polyurethane
- examples
- Prior art date
Links
- 0 C*(C)O[N+]([O-])OC(C)(C)C Chemical compound C*(C)O[N+]([O-])OC(C)(C)C 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G18/00—Polymeric products of isocyanates or isothiocyanates
- C08G18/06—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen
- C08G18/70—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen characterised by the isocyanates or isothiocyanates used
- C08G18/72—Polyisocyanates or polyisothiocyanates
- C08G18/73—Polyisocyanates or polyisothiocyanates acyclic
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G18/00—Polymeric products of isocyanates or isothiocyanates
- C08G18/06—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen
- C08G18/28—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen characterised by the compounds used containing active hydrogen
- C08G18/30—Low-molecular-weight compounds
- C08G18/32—Polyhydroxy compounds; Polyamines; Hydroxyamines
- C08G18/3203—Polyhydroxy compounds
- C08G18/3206—Polyhydroxy compounds aliphatic
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G18/00—Polymeric products of isocyanates or isothiocyanates
- C08G18/06—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen
- C08G18/08—Processes
- C08G18/0804—Manufacture of polymers containing ionic or ionogenic groups
- C08G18/0819—Manufacture of polymers containing ionic or ionogenic groups containing anionic or anionogenic groups
- C08G18/0823—Manufacture of polymers containing ionic or ionogenic groups containing anionic or anionogenic groups containing carboxylate salt groups or groups forming them
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G18/00—Polymeric products of isocyanates or isothiocyanates
- C08G18/06—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen
- C08G18/08—Processes
- C08G18/10—Prepolymer processes involving reaction of isocyanates or isothiocyanates with compounds having active hydrogen in a first reaction step
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G18/00—Polymeric products of isocyanates or isothiocyanates
- C08G18/06—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen
- C08G18/08—Processes
- C08G18/16—Catalysts
- C08G18/22—Catalysts containing metal compounds
- C08G18/24—Catalysts containing metal compounds of tin
- C08G18/244—Catalysts containing metal compounds of tin tin salts of carboxylic acids
- C08G18/246—Catalysts containing metal compounds of tin tin salts of carboxylic acids containing also tin-carbon bonds
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G18/00—Polymeric products of isocyanates or isothiocyanates
- C08G18/06—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen
- C08G18/28—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen characterised by the compounds used containing active hydrogen
- C08G18/30—Low-molecular-weight compounds
- C08G18/34—Carboxylic acids; Esters thereof with monohydroxyl compounds
- C08G18/348—Hydroxycarboxylic acids
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G18/00—Polymeric products of isocyanates or isothiocyanates
- C08G18/06—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen
- C08G18/28—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen characterised by the compounds used containing active hydrogen
- C08G18/40—High-molecular-weight compounds
- C08G18/42—Polycondensates having carboxylic or carbonic ester groups in the main chain
- C08G18/44—Polycarbonates
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G18/00—Polymeric products of isocyanates or isothiocyanates
- C08G18/06—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen
- C08G18/28—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen characterised by the compounds used containing active hydrogen
- C08G18/65—Low-molecular-weight compounds having active hydrogen with high-molecular-weight compounds having active hydrogen
- C08G18/66—Compounds of groups C08G18/42, C08G18/48, or C08G18/52
- C08G18/6633—Compounds of group C08G18/42
- C08G18/6659—Compounds of group C08G18/42 with compounds of group C08G18/34
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G18/00—Polymeric products of isocyanates or isothiocyanates
- C08G18/06—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen
- C08G18/70—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen characterised by the isocyanates or isothiocyanates used
- C08G18/72—Polyisocyanates or polyisothiocyanates
- C08G18/74—Polyisocyanates or polyisothiocyanates cyclic
- C08G18/75—Polyisocyanates or polyisothiocyanates cyclic cycloaliphatic
- C08G18/751—Polyisocyanates or polyisothiocyanates cyclic cycloaliphatic containing only one cycloaliphatic ring
- C08G18/752—Polyisocyanates or polyisothiocyanates cyclic cycloaliphatic containing only one cycloaliphatic ring containing at least one isocyanate or isothiocyanate group linked to the cycloaliphatic ring by means of an aliphatic group
- C08G18/753—Polyisocyanates or polyisothiocyanates cyclic cycloaliphatic containing only one cycloaliphatic ring containing at least one isocyanate or isothiocyanate group linked to the cycloaliphatic ring by means of an aliphatic group containing one isocyanate or isothiocyanate group linked to the cycloaliphatic ring by means of an aliphatic group having a primary carbon atom next to the isocyanate or isothiocyanate group
- C08G18/755—Polyisocyanates or polyisothiocyanates cyclic cycloaliphatic containing only one cycloaliphatic ring containing at least one isocyanate or isothiocyanate group linked to the cycloaliphatic ring by means of an aliphatic group containing one isocyanate or isothiocyanate group linked to the cycloaliphatic ring by means of an aliphatic group having a primary carbon atom next to the isocyanate or isothiocyanate group and at least one isocyanate or isothiocyanate group linked to a secondary carbon atom of the cycloaliphatic ring, e.g. isophorone diisocyanate
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G18/00—Polymeric products of isocyanates or isothiocyanates
- C08G18/06—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen
- C08G18/70—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen characterised by the isocyanates or isothiocyanates used
- C08G18/72—Polyisocyanates or polyisothiocyanates
- C08G18/74—Polyisocyanates or polyisothiocyanates cyclic
- C08G18/76—Polyisocyanates or polyisothiocyanates cyclic aromatic
- C08G18/7657—Polyisocyanates or polyisothiocyanates cyclic aromatic containing two or more aromatic rings
- C08G18/7664—Polyisocyanates or polyisothiocyanates cyclic aromatic containing two or more aromatic rings containing alkylene polyphenyl groups
- C08G18/7671—Polyisocyanates or polyisothiocyanates cyclic aromatic containing two or more aromatic rings containing alkylene polyphenyl groups containing only one alkylene bisphenyl group
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G18/00—Polymeric products of isocyanates or isothiocyanates
- C08G18/06—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen
- C08G18/70—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen characterised by the isocyanates or isothiocyanates used
- C08G18/72—Polyisocyanates or polyisothiocyanates
- C08G18/77—Polyisocyanates or polyisothiocyanates having heteroatoms in addition to the isocyanate or isothiocyanate nitrogen and oxygen or sulfur
- C08G18/78—Nitrogen
- C08G18/79—Nitrogen characterised by the polyisocyanates used, these having groups formed by oligomerisation of isocyanates or isothiocyanates
- C08G18/791—Nitrogen characterised by the polyisocyanates used, these having groups formed by oligomerisation of isocyanates or isothiocyanates containing isocyanurate groups
- C08G18/792—Nitrogen characterised by the polyisocyanates used, these having groups formed by oligomerisation of isocyanates or isothiocyanates containing isocyanurate groups formed by oligomerisation of aliphatic and/or cycloaliphatic isocyanates or isothiocyanates
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G64/00—Macromolecular compounds obtained by reactions forming a carbonic ester link in the main chain of the macromolecule
- C08G64/02—Aliphatic polycarbonates
- C08G64/0208—Aliphatic polycarbonates saturated
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G64/00—Macromolecular compounds obtained by reactions forming a carbonic ester link in the main chain of the macromolecule
- C08G64/20—General preparatory processes
- C08G64/30—General preparatory processes using carbonates
- C08G64/305—General preparatory processes using carbonates and alcohols
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09D—COATING COMPOSITIONS, e.g. PAINTS, VARNISHES OR LACQUERS; FILLING PASTES; CHEMICAL PAINT OR INK REMOVERS; INKS; CORRECTING FLUIDS; WOODSTAINS; PASTES OR SOLIDS FOR COLOURING OR PRINTING; USE OF MATERIALS THEREFOR
- C09D169/00—Coating compositions based on polycarbonates; Coating compositions based on derivatives of polycarbonates
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09D—COATING COMPOSITIONS, e.g. PAINTS, VARNISHES OR LACQUERS; FILLING PASTES; CHEMICAL PAINT OR INK REMOVERS; INKS; CORRECTING FLUIDS; WOODSTAINS; PASTES OR SOLIDS FOR COLOURING OR PRINTING; USE OF MATERIALS THEREFOR
- C09D175/00—Coating compositions based on polyureas or polyurethanes; Coating compositions based on derivatives of such polymers
- C09D175/04—Polyurethanes
- C09D175/06—Polyurethanes from polyesters
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09D—COATING COMPOSITIONS, e.g. PAINTS, VARNISHES OR LACQUERS; FILLING PASTES; CHEMICAL PAINT OR INK REMOVERS; INKS; CORRECTING FLUIDS; WOODSTAINS; PASTES OR SOLIDS FOR COLOURING OR PRINTING; USE OF MATERIALS THEREFOR
- C09D5/00—Coating compositions, e.g. paints, varnishes or lacquers, characterised by their physical nature or the effects produced; Filling pastes
- C09D5/02—Emulsion paints including aerosols
- C09D5/022—Emulsions, e.g. oil in water
Definitions
- the present invention relates to a polycarbonate diol and its use.
- a polycarbonate polyol As such a polycarbonate polyol, a polycarbonate polyol using 1,6-hexanediol alone as a diol component is generally used. However, since such a polycarbonate polyol is crystalline, it is solid at room temperature and has a problem that it is difficult to handle.
- Patent Document 1 discloses that a polycarbonate diol was synthesized using 1,5-pentanediol and 1,6-hexanediol.
- Patent Document 2 discloses that a polycarbonate diol was synthesized using dipropylene glycol having a branched chain and hexanediol. The resulting polycarbonate diol has a structure that is impaired, its crystallinity is lowered, and it becomes liquid at room temperature. Polyurethanes using these polycarbonate diols have been found to be highly flexible.
- polyurethane obtained by using a polycarbonate diol as a raw material compound as described in Patent Documents 1 and 2 has room for improvement in stain resistance. That is, a polycarbonate diol that can impart excellent stain resistance, low-temperature flexibility, and heat resistance when used as a raw material compound such as polyurethane has not been obtained so far.
- an object of the present invention is to provide, for example, a novel polycarbonate diol capable of imparting excellent stain resistance, low temperature flexibility and heat resistance when used as a raw material compound of polyurethane and its use.
- a polycarbonate diol having a specific repeating unit in a specific ratio is amorphous, and when used as a raw material compound for polyurethane or a thermoplastic elastomer, a general polycarbonate polyol is used.
- a general polycarbonate polyol is used.
- the present invention is as follows. (1) A polycarbonate diol in which the proportion of the repeating unit represented by the following formula (A) is 0.1% by mass or more and 99.9% by mass or less. (2) The polycarbonate diol according to (1), wherein the proportion of the repeating unit represented by the formula (A) is 0.1% by mass or more and 50.0% by mass or less. (3) The polycarbonate diol according to (1) or (2), further containing 0.1% by mass or more and 99.9% by mass or less of the repeating unit represented by the following formula (B).
- R represents a divalent hydrocarbon group having 3 to 20 carbon atoms, which may contain an oxygen atom in the carbon skeleton.
- R represents a divalent hydrocarbon group having 3 to 20 carbon atoms, which may contain an oxygen atom in the carbon skeleton.
- the present invention can provide a polycarbonate diol and its use that can impart excellent stain resistance, low-temperature flexibility and heat resistance when used as a raw material compound of polyurethane or thermoplastic elastomer, for example.
- this embodiment a mode for carrying out the present invention (hereinafter, abbreviated as “this embodiment”) will be described in detail.
- the present invention is not limited to the following embodiments, and can be variously modified and implemented within the scope of the gist.
- stain resistance means that the polycarbonate diol of the present embodiment is used as a raw material compound for polyurethane and thermoplastic elastomers. Properties that can impart properties, low-temperature flexibility, and heat resistance. Examples of the stain resistance include stains on daily life such as oil-based pens and blue jeans, and stains on food such as coffee, ketchup and olive oil.
- the proportion of the repeating unit represented by the following formula (A) is 0.1% by mass or more and 99.9% by mass or less. It is preferable that the polycarbonate diol of the present embodiment further contains a repeating unit represented by the following formula (B) in an amount of 0.1% by mass or more and 99.9% by mass or less.
- the carbon number R in the following formula (B) is more preferably 3 to 6.
- the polycarbonate diol of the present embodiment preferably has a number average molecular weight of 300 or more and 4,000 or less.
- the polycarbonate diol of this embodiment preferably has a primary hydroxyl group terminal ratio of 90% or more.
- R represents a divalent hydrocarbon group having 3 to 20 carbon atoms, which may contain an oxygen atom in the carbon skeleton.
- the polycarbonate diol of the present embodiment By providing the polycarbonate diol of the present embodiment with the above-mentioned constitution, for example, when it is used as a raw material compound of polyurethane or elastomer, excellent stain resistance and low temperature flexibility can be imparted.
- the mechanism by which the polycarbonate diol of the present embodiment exerts these effects is not clear, but it is presumed as follows.
- the present invention is not limited by this speculation. That is, the effect of disturbing the regularity of the structure of the polycarbonate diol is preferably obtained mainly because the polycarbonate diol contains the repeating unit represented by the above formula (A) in a specific ratio. From this, it is presumed that it has no crystallization orientation and, when used as a raw material compound for polyurethane, can impart excellent stain resistance and low-temperature flexibility.
- the ratio of the repeating unit represented by the above formula (A) is 0.1% by mass or more and 99.9% by mass or less, preferably 0.1% by mass or more and 50.0% by mass. % Or less, more preferably 1.0% by mass or more and 30.0% by mass or less.
- the polycarbonate diol of the present embodiment is excellent in stain resistance and low-temperature flexibility when the ratio is 0.1% by mass or more, and excellent in heat resistance when the ratio is 99.9% by mass or less. ..
- the ratio of the repeating unit represented by the above formula (A) is obtained by the following method. 1) Polycarbonate diol Mg (about 1 g), ethanol 30 g, and potassium hydroxide 4 g are added to a 100 mL eggplant flask and reacted at 100 ° C. for 1 hour to obtain a hydrolyzate. 2) After cooling the hydrolyzate to room temperature, add 2 to 3 drops of phenolphthalein as an indicator, neutralize with hydrochloric acid, and further cool in the refrigerator for 1 hour. 3) Diethylene glycol diethyl ether Cmol (about 0.5 g) is added as an internal standard, 30 g of acetone is further added, and the precipitated salt is removed by filtration.
- the peak area ratio D of 4-oxa-1,7-heptanediol to the peak area of the internal standard is determined by gas chromatography under the following conditions.
- Equipment Gas Chromatography GC-2014 (Shimadzu Corporation product) Column: DB-WAX (J & W company product) Detector: FID Temperature rising profile: Hold at 100° C. for 5 minutes, then heat up to 250° C. at 10° C./minute 5)
- the ratio of the repeating unit represented by the formula (A) is calculated by the following formula.
- the polycarbonate diol of the present embodiment preferably further contains a repeating unit represented by the above formula (B) in an amount of 0.1% by mass or more and 99.9% by mass or less.
- the proportion of the repeating unit represented by the above formula (B) is more preferably 50.0 mass% or more and 99.9 mass% or less, and further preferably 70.0 mass% or more and 99. It is 0% by mass or less.
- the polycarbonate diol of the present embodiment tends to be more excellent in stain resistance, low temperature flexibility and heat resistance by containing the repeating unit represented by the above formula (B) in the above range.
- the total proportion of the repeating unit represented by the above formula (A) and the repeating unit represented by the above formula (B) is preferably at least 50% by mass, and 60% by mass or more. Is more preferable, 70% by mass or more is further preferable, and 80% by mass or more is particularly preferable.
- the total ratio of the repeating unit represented by the formula (A) and the repeating unit represented by the formula (B) is at least the above lower limit value, the stain resistance and the heat resistance tend to be particularly excellent.
- the upper limit of the total ratio of the repeating unit represented by the above formula (A) and the repeating unit represented by the above formula (B) is not particularly limited, but is, for example, 100% by mass.
- the proportion of the repeating unit represented by the above formula (B) can be measured by the method described in Examples below.
- the divalent hydrocarbon group R having 3 to 20 carbon atoms and optionally containing an oxygen atom is not particularly limited, and examples thereof include linear diols, branched diols, cyclic diols and ethers. Hydrocarbon groups derived from group-containing diols can be mentioned.
- the linear diol is not particularly limited, but for example, 1,3-propanediol, 1,4-butanediol, 1,5-pentanediol, 1,6-hexanediol, 1,7-heptanediol, 1 , 8-octanediol, 1,9-nonanediol, 1,10-decanediol, 1,12-dodecanediol.
- the branched diol is not particularly limited, and examples thereof include 1,3-butanediol, 2-methyl-1,3-propanediol, 2-ethyl-1,3-propanediol, neopentyl glycol, 3-methyl- Examples thereof include 1,5-pentanediol and 2-methyl-1,8-octanediol.
- the cyclic diol is not particularly limited, and examples thereof include 1,2-cyclohexanediol, 1,3-cyclohexanediol, 1,4-cyclohexanediol, 1,4-cyclohexanedimethanol, and 2,2′-bis(4- Hydroxycyclohexyl) propane and the like.
- the ether group-containing diol is not particularly limited, and examples thereof include diethylene glycol, dipropylene glycol, 3-oxa-1,6-hexanediol, 3-oxa-1,7-heptanediol, 3-oxa-1,8- Octanediol, 3-oxa-1,9-nonanediol, 5-methyl-3-oxa-1,6-hexanediol, 6-methyl-3-oxa-1,8-octanediol and the like can be mentioned.
- the carbon number of R in the formula (B) is It is preferably 3 to 6.
- R in the formula (B) has 3 carbon atoms because it tends to further improve the low temperature flexibility of polyurethane.
- the number average molecular weight of the polycarbonate diol of the present embodiment is preferably 300 or more and 4,000 or less, more preferably 350 or more and 3,000 or less, and further preferably 400 or more and 2,400 or less.
- the polycarbonate diol of the present embodiment has a number average molecular weight of 300 or more, so that flexibility and low-temperature properties tend to be further excellent, and a number average molecular weight of 4,000 or less has low viscosity and molding. Workability tends to be further improved.
- the number average molecular weight of the polycarbonate diol can be measured by the method described in Examples described later.
- the primary hydroxyl group terminal ratio of the polycarbonate diol of the present embodiment is preferably 90% or more, more preferably 95% or more, still more preferably 97% or more.
- the upper limit of the primary hydroxyl group terminal ratio is not particularly limited, but the practical upper limit is 100%.
- the molecular weight of the polyurethane tends to be high when producing (synthesizing) polyurethane (particularly thermoplastic polyurethane) using the polycarbonate diol of the present embodiment as a raw material compound, and the heat resistance tends to be strong. It is in.
- the primary hydroxyl group terminal ratio is obtained by the following method.
- the proportion of primary hydroxyl groups is calculated by dissolving polycarbonate diol in CDCl 3 (deuterated chloroform), measuring 1 H-NMR (ECS400 manufactured by JEOL) at 400 MHz, and calculating the integrated value.
- the ratio of the primary hydroxyl group terminal is the sum of the integrated value of one proton of the primary hydroxyl group and the integrated value of all the hydroxyl groups of carbonate diol and carbonate ester terminal such as phenoxide terminal of each proton.
- the detection limit of the ratio of the primary hydroxyl terminal is 1.0 mol% with respect to the entire structure of the polycarbonate diol terminal.
- the method for producing the polycarbonate diol of the present embodiment is not particularly limited.
- the diol component may further contain other polyols.
- the 4-oxa-1,7-heptanediol may be a petroleum-derived compound or a plant-derived compound. It may also be purchased as a reagent or obtained by reduction of diethyl 3,3'-oxydipropionate. Regardless of which of these compounds is used, there is no difference in the physical properties of the polyurethane obtained by reacting the polycarbonate diol with the isocyanate.
- diol compound represented by the formula (C) examples include 1,3-propanediol, 1,4-butanediol, 1,5-pentanediol and 1,6-hexane.
- Linear diols such as diols, 1,7-heptanediol, 1,8-octanediol, 1,9-nonanediol, 1,10-decanediol and 1,12-dodecanediol, 1,3-butanediol, Branching of 2-methyl-1,3-propanediol, 2-ethyl-1,3-propanediol, neopentyl glycol, 3-methyl-1,5-pentanediol, 2-methyl-1,8-octanediol, etc.
- Cyclic diols such as diols, 1,2-cyclohexanediol, 1,3-cyclohexanediol, 1,4-cyclohexanediol, 1,4-cyclohexanedimethanol, 2,2′-bis(4-hydroxycyclohexyl)propane, diethylene glycol , Dipropylene glycol, 3-oxa-1,6-hexanediol, 3-oxa-1,7-heptanediol, 3-oxa-1,8-octanediol, 3-oxa-1,9-nonanediol, 5 Examples thereof include ether group-containing diols such as -methyl-3-oxa-1,6-hexanediol and 6-methyl-3-oxa-1,8-octanediol.
- diol compounds can be used alone or in combination of two or more.
- the diol compound preferably has 3 to 6 carbon atoms.
- the carbon number is within the above range, at least one of abrasion resistance, breaking strength and extensibility of the produced polyurethane tends to be further excellent.
- the trimethylene group has 3 carbon atoms. When the number of carbon atoms is in the above range, the low temperature flexibility of the produced polyurethane tends to be further excellent.
- the carbonic acid ester is not particularly limited, and examples thereof include alkylene carbonate, dialkyl carbonate, and diaryl carbonate.
- the alkylene carbonate is not particularly limited, and examples thereof include ethylene carbonate, trimethylene carbonate, 1,2-propylene carbonate, 1,2-butylene carbonate, 1,3-butylene carbonate, and 1,2-pentylene carbonate. Be done.
- the dialkyl carbonate is not particularly limited, and examples thereof include dimethyl carbonate, diethyl carbonate, linear dibutyl carbonate, branched dibutyl carbonate, and the like.
- the dialkylene carbonate is not particularly limited, and examples thereof include diphenyl carbonate. These carbonic acid esters can be used alone or in combination of two or more. Among these, ethylene carbonate, dimethyl carbonate, diethyl carbonate, linear butyl carbonate, and branched chain dibutyl carbonate are preferable.
- the reaction temperature for transesterification is not particularly limited, but is preferably 120 to 280°C, more preferably 140 to 230°C.
- a catalyst may be used from the viewpoint of improving the reaction rate during the transesterification reaction.
- the catalyst is not particularly limited, but for example, titanium compounds such as tetraisopropoxytitanium and tetra-n-butoxytitanium; tin compounds such as di-n-butyltin dilaurate, di-n-butyltin oxide and dibutyltin diacetate; acetic acid. Examples thereof include metal salts of acetic acid such as magnesium, calcium acetate, zinc acetate and lead acetate. These catalysts may be used alone or in combination of two or more. Among these, it is preferable to use a titanium compound.
- the content of these catalysts is preferably 1 mass ppm or more and 300 mass ppm or less, and more preferably 30 mass ppm or more and 200 mass ppm or less with respect to the total amount of the reaction raw materials.
- the method for producing the polycarbonate diol of the present embodiment is not particularly limited, and other methods include a method in which 4-oxa-1,7-heptanediol is added to the polycarbonate diol and the transesterification reaction is performed.
- the polycarbonate diol those obtained by the transesterification reaction between the diol compound represented by the above formula (C) and the above carbonic acid ester may be used, and those obtained by the ring opening of the cyclic carbonate may be used.
- the coating composition of this embodiment contains the above-mentioned polycarbonate diol.
- the coating composition of this embodiment may contain an isocyanate compound.
- the (NCO group / OH group) equivalent ratio is preferably 0.5 to 3.0, more preferably 0.6 to 2.0. , And more preferably 0.7 to 1.5.
- the isocyanate compound used in the present embodiment is preferably polyisocyanate derived from an aliphatic and / or alicyclic isocyanate compound, particularly from the viewpoint of weather resistance.
- polyisocyanates derived from aliphatic or alicyclic diisocyanates such as hexamethylene diisocyanate (HDI) and isophorone diisocyanate (IPDI).
- these polyisocyanates are blocked with a blocking agent such as lower alcohols such as butanol and 2-ethylhexanol, methylethylketone oxime, lactams, phenols, imidazoles, and active methylene compounds, so-called blocked isocyanate-based curing. Agents can also be used.
- the coating composition of the present embodiment may contain 1 to 95% by mass of an organic solvent, if necessary, in order to adjust the workability at the time of coating.
- the content of the organic solvent is more preferably 15 to 75% by mass, further preferably 30 to 60% by mass.
- the organic solvent used is not particularly limited, but is preferably an organic solvent that is substantially inactive with respect to the isocyanate compound and does not have active hydrogen.
- Examples thereof include, but are not particularly limited to, pentanes, hexane, heptane, octane, decane, petroleum ether, petroleum benzine, ligroin, petroleum spirit, cyclohexane, methylcyclohexane, and other hydrocarbons, trichlorofluoroethane, tetrachlorodifluoroethane.
- Perfluoroether and other fluorousylated oils perfluorocyclohexane, perfluorobutyl tetrahydrofuran, perfluorodecalin, perfluoro-n-butylamine, perfluoropolyether, dimethylpolysiloxane and the like alone or in admixture.
- a single solvent or a mixed solvent of methyl ethyl ketone, acetone, ethyl acetate, butyl acetate, toluene, xylene and the like can be mentioned.
- the coating composition of the present embodiment comprises 4-oxa-1,7-heptanediol, a diol compound (C) represented by the above formula (C), a polyether polyol, a polyester polyol, a polycarbonate polyol, and an acryl depending on the use. It may contain a polyol or a fluorine polyol.
- a polyether polyol or a polyester polyol is contained, chemical resistance can be imparted as compared with the case where they are used alone.
- an acrylic polyol or a fluorine polyol is contained, flexibility and scratch resistance can be imparted as compared with the case where they are used alone.
- Polyurethane particles may be used in the coating composition of the present embodiment in order to further enhance the softness of the obtained coating film.
- a matting agent for example, TS-100 manufactured by Evonik Industries, Inc.
- TS-100 manufactured by Evonik Industries, Inc.
- curing accelerators catalysts
- fillers flame retardants, dyes, organic or inorganic pigments, mold release agents, fluidity modifiers, plasticizers, antioxidants, UV absorbers, light stabilizers, quenchers
- a foaming agent, a leveling agent (for example, BYK-331 manufactured by Big Chemie), a coloring agent, an anticoloring agent (for example, Silkalean 3700 manufactured by Big Chemie), a solvent and the like can be added. These may be used alone or in combination of two or more.
- the aqueous polyurethane dispersion of the present embodiment contains water and a water-dispersible polyurethane obtained by using the above-mentioned polycarbonate diol.
- the water-dispersible polyurethane contained in the aqueous polyurethane dispersion of the present embodiment is obtained from the above-mentioned polycarbonate diol, an isocyanate compound, and a carboxyl group and / or a sulfone group-containing polyol or a salt thereof.
- the isocyanate compound is not particularly limited as long as it is an isocyanate compound containing two or more isocyanate groups in one molecule.
- the isocyanate compound include, for example, diphenylmethane diisocyanate (MDI), cyclohexane diisocyanate, tolylene diisocyanate (TDI), HDI, trimethylhexane diisocyanate, 1,5-naphthalene diisocyanate (NDI), xylylene diisocyanate (XDI), 2, Aromatic, aliphatic, alicyclic organic diisocyanates such as 6-diisocyanate methylcaproate, IPDI, methylcyclohexane-2,4- (or 2,6-) diisocyanate, dicyclohexylmethane diisocyanate (hydrogenated MDI), or Examples thereof include multimers containing polyfunctional isocyanate groups such as these bullets and isocyanurates,
- the carboxyl group- and/or sulfone group-containing polyol or salt thereof used in the present embodiment is a carboxylate for the purpose of self-emulsifying a water-dispersible polyurethane in water and imparting dispersion stability of an aqueous polyurethane dispersion.
- the carboxyl group-containing polyol is not particularly limited, and is, for example, 2,2-dimethylolpropionic acid (DMPA), 2,2-dimethylolbutanoic acid, 2,2-dimethylolheptanic acid, 2,2-dimethyloloctane. Examples include acid.
- Examples of the sulfonic group-containing polyol include sulfonic acid diol ⁇ 3-(2,3-dihydroxypropoxy)-1-propanesulfonic acid ⁇ and sulfamic acid diol ⁇ N,N-bis(2-hydroxyl)sulfamic acid ⁇ And its alkylene oxide adduct and the like.
- the salts of these carboxyl group and / or sulfone group-containing polyols are not particularly limited, but are, for example, ammonium salts and amine salts [primary amines having 1 to 12 carbon atoms (primary monoamines such as methylamine, ethylamine, propyl).
- Amine and octylamine) salts secondary monoamines (dimethylamine, diethylamine and dibutylamine) salts, tertiary monoamines (trimethylamine, triethylamine triethanolamine, N-methyldiethanolamine, N,N-methylethanolamine and other aliphatic tertiary compounds Monoamines; heterocyclic tertiary monoamines such as N-methylpiperidine and N-methylmorpholine; benzyldimethylamine, ⁇ -methylbenzyldimethylamine; and aromatic ring-containing tertiary monoamines such as N-dimethylaniline) salts], alkali metals (Sodium, potassium and lithium cation) salts, and combinations of two or more thereof.
- Preferred salts are amine salts, more preferred are aliphatic tertiary monoamine salts, and particularly preferred is triethylamine salt.
- a neutralizing agent may be used to neutralize the carboxyl group and/or sulfone group to a carboxylate group and/or sulfonate group. it can.
- the neutralizing agent is not particularly limited, and examples thereof include the alkaline compounds that form the cations mentioned as the counterions.
- examples thereof include the alkaline compounds that form the cations mentioned as the counterions.
- ammonia amine [a primary amine having 1 to 12 carbon atoms (a primary monoamine such as methylamine, ethylamine, propylamine and octylamine), a secondary monoamine (dimethylamine, Diethylamine and dibutylamine), tertiary monoamines (trimethylamine, triethylamine, triethanolamine, N-methyldiethanolamine and aliphatic tertiary monoamines such as N, N-dimethylethanolamine; heterocycles such as N-methylpiperidine and N-methylmorpholin.
- amine a primary amine having 1 to 12 carbon atoms (a primary monoamine such as methylamine, ethylamine, propylamine and octylamine), a secondary monoamine (
- tertiary monoamine benzyldimethylamine, ⁇ -methylbenzyldimethylamine; and aromatic ring-containing tertiary monoamine such as N-dimethylaniline)]
- alkali metal sodium, potassium and lithium cation
- alkali metal hydroxide alkali metal hydroxide
- amines preferred are amines, more preferred are aliphatic tertiary monoamines, and particularly preferred are triethylamine.
- the amount of the carboxyl group- and/or sulfone group-containing polyol or salt thereof used is preferably such that the carboxyl group and/or sulfone group becomes 0.01 to 10 mol% with respect to the water-dispersible polyurethane.
- the ratio of the carboxyl group and / or the sulfone group to the water-dispersible polyurethane is more preferably 0.1 to 7 mol%, still more preferably 0.5 to 5 mol%.
- the carboxyl group and/or the sulfone group is 0.01 mol% or more, the emulsion stability tends to be more excellent. Further, when the content is 10 mol% or less, the water resistance of the obtained coating film tends to be more excellent.
- the aqueous polyurethane dispersion of the present embodiment may contain a surfactant.
- the surfactant is not particularly limited, but is an anionic surfactant represented by, for example, higher fatty acid, resin acid, acidic fatty alcohol, sulfate ester, higher alkyl sulfonic acid, alkylaryl sulfonate, sulfonated castor oil, sulfosuccinic acid ester and the like. Examples thereof include activators or nonionic surfactants typified by known reaction products of ethylene oxide and long-chain fatty alcohols or phenols.
- the method for producing the aqueous polyurethane dispersion of the present embodiment is not particularly limited, but the following method may be mentioned.
- an organic solvent containing no active hydrogen-containing group in the molecule for example, acetone, methyl ethyl ketone, tetrahydrofuran, N, N-dimethylformamide, etc.
- one molecule contains two or more isocyanate groups.
- the (NCO group/OH group) equivalent ratio of the isocyanate compound, the polycarbonate diol, and the carboxyl group- and/or sulfone group-containing polyol or salt thereof is preferably in the range of 0.5 to 1.5, more preferably 0.
- Polyurethane is synthesized by urethanization reaction in the range of 8. to 1.2, more preferably 0.9 to 1.1 by the one-shot method or the multi-step method, and the polyurethane is neutralized if necessary. After neutralizing with the agent, water is added dropwise to the place where the obtained reaction solution is strongly stirred, and after the completion of the addition, the solvent is removed as necessary to obtain an aqueous polyurethane dispersion. It is also possible to obtain an aqueous polyurethane dispersion by adding and dispersing the obtained reaction solution in water with stirring, and then removing the solvent if necessary.
- the (NCO group/OH group) equivalent ratio When the (NCO group/OH group) equivalent ratio is 0.5 or more, the molecular weight of the obtained polyurethane can be increased, and a more stable aqueous polyurethane dispersion tends to be obtained. The strength and flexibility of the coating film formed by the water-based coating composition containing the above as a constituent tend to be more excellent. Further, when the (NCO group/OH group) equivalent ratio is 1.5 or less, similarly, the molecular weight of the obtained polyurethane can be increased, and a more stable aqueous polyurethane dispersion tends to be obtained. The strength and flexibility of the coating film formed by the water-based coating composition containing the water-based polyurethane dispersion as a constituent tend to be more excellent.
- an isocyanate compound, a polycarbonate diol, and a carboxyl group- and/or sulfone group-containing polyol or a salt thereof are preliminarily synthesized to prepare a prepolymer under an isocyanate excess condition. It is also possible to disperse this prepolymer in water and then add a chain extender to prepare an aqueous polyurethane dispersion.
- the chain extender is not particularly limited, but includes, for example, water, ethylene glycol, 1,3-propanediol, 1,4-butanediol and other short chain diols, hydrazine, ethylenediamine, diethyltriamine, triethylenetetramine, tetraethylene.
- Examples thereof include polyamines such as pentamine, pentaethylenehexamine, propylenediamine, hexamethylenediamine and cyclohexylenediamine.
- the amount of the chain extender added is usually 0 to 1.2 mol, preferably 0.1 to 0.6 mol, based on 1 mol of the isocyanate group of the urethane prepolymer.
- a known urethanization reaction catalyst can be used if necessary.
- the urethanization reaction catalyst is not particularly limited, but for example, an amine catalyst (for example, triethylamine, N-ethylmorpholin, triethylenediamine, etc.), a tin-based catalyst (for example, dibutyltin dilaurylate, dioctyltin dilaurylate, tin octylate, etc.), Examples thereof include titanium-based catalysts (for example, tetrabutyl titanate).
- the solid content of the aqueous polyurethane dispersion of the present embodiment is preferably 10 to 70% by mass, more preferably 20 to 60% by mass.
- the particle size of the polyurethane of the aqueous polyurethane dispersion of the present embodiment is preferably 500 nm or less, more preferably 200 nm or less, still more preferably 150 nm or less.
- the particle size of polyurethane is 500 nm or less, the appearance, strength and abrasion resistance of the coating film of the aqueous coating composition containing the aqueous polyurethane dispersion tend to be more excellent, which is preferable.
- the water-based coating composition of the present embodiment contains the above-mentioned water-based polyurethane dispersion.
- the content of the above-mentioned aqueous polyurethane dispersion is preferably 10 to 98% by mass, more preferably 20 to 95% by mass, and 30 to 90% by mass. It is more preferable to have.
- aqueous coating composition of the present embodiment depending on various uses, for example, fillers, flame retardants, dyes, organic or inorganic pigments, mold release agents, fluidity modifiers, plasticizers, antioxidants, UV absorption. Agents, light stabilizers, defoamers, leveling agents, colorants, solvents and the like can be added.
- the filler and pigment are not particularly limited, but include, for example, woven fabric, glass fiber, carbon fiber, polyamide fiber, mica, kaolin, bentonite, metal powder, azo pigment, carbon black, clay, silica, talc, gypsum, alumina.
- Commonly used materials such as white, barium carbonate, and resin fine particles can be used. Among them, resin fine particles are preferable, and polyurethane fine particles are more preferable, in order to obtain a soft feel.
- the release agent, fluidity adjuster, and leveling agent are not particularly limited, but for example, silicone, aerosil, wax, stearate, polysiloxane such as BYK-331 (manufactured by BYK Chemical Co., Ltd.) and the like are used.
- antioxidants are not particularly limited, examples thereof include phosphoric acid, aliphatic, aromatic or alkyl substituted aromatic esters of phosphorous acid, hypophosphorous acid derivatives, phenylsulfonic acid, phenylphosphinic acid, diphenylphosphonic acid, and poly(phosphoric acid).
- Phosphonates such as phosphonate, dialkylpentaerythritol diphosphite, dialkylbisphenol A diphosphite; phenolic derivatives, especially hindered phenol compounds, choethers, dithiolates; mercaptobenzimidazole, thiocarbanilides, thiodipropionic acid esters, etc.
- Compounds containing sulfur; tin-based compounds such as phosphorate and dibutyltin monooxide can be used. These may be used alone or in combination of two or more.
- the method for coating the water-based coating composition of the present embodiment is not particularly limited, but a method of applying each additive component to the water-based polyurethane dispersion and then applying it to the substrate by spraying, rolling, brushing or the like is illustrated. Will be done.
- the elastomer of this embodiment is obtained by reacting the above-mentioned polycarbonate diol with an isocyanate compound.
- the isocyanate compound used for producing the elastomer of the present embodiment is not particularly limited as long as it is an isocyanate compound containing two or more isocyanate groups in one molecule.
- isocyanate compounds include MDI, cyclohexane diisocyanate, TDI, HDI, trimethylhexane diisocyanate, NDI, XDI, 2,6-diisocyanate methylcaproate, IPDI, methylcyclohexane-2,4- (or 2,6-).
- Aromatic, aliphatic, alicyclic organic diisocyanates such as diisocyanates and hydrogenated MDIs, or multimers containing polyfunctional isocyanate groups such as bullets and isocyanurates thereof, or single or mixtures of these isocyanates. Can be mentioned.
- a chain extender may be used as a copolymerization component.
- the chain extender water, low molecular weight polyol, polyamine, high molecular weight polyol may be used in combination.
- the low molecular weight polyol a diol having a molecular weight of 300 or less is usually used.
- the low molecular weight polyol is not particularly limited, and examples thereof include ethylene glycol, 1,3-propanediol, 1,4-butanediol, 1,5-pentanediol, 1,6-hexanediol, neopentyl glycol, 1, Aliphatic diols such as 10-decanediol, alicyclic diols such as 1,1-cyclohexanedimethanol, 1,4-cyclohexanedimethanol and tricyclodecanedimethanol, xylylene glycol, bis(p-hydroxy)diphenyl, Bis(p-hydroxyphenyl)propane, 2,2-bis[4-(2-hydroxyethoxy)phenyl]propane, bis[4(2-hydroxy)phenyl]sulfone, 1,1-bis[4-(2- Aromatic
- the polyamine is not particularly limited, and examples thereof include hydrazine, ethylenediamine, diethyltriamine, triethylenetetramine, tetraethylenepentamine, pentaethylenehexamine, propylenediamine, hexamethylenediamine, cyclohexylenediamine, and isophoronediamine.
- the polymer polyol is not particularly limited, and examples thereof include polymer polyols such as polyether polyols, polyester polyols, and polycarbonate polyols.
- a known urethanization reaction catalyst can be used if necessary.
- the urethanization reaction catalyst is not particularly limited, and examples thereof include amine catalysts (eg, triethylamine, N-ethylmorpholine, triethylenediamine, etc.), tin-based catalysts (eg, dibutyltin dilaurylate, dioctyltin dilaurylate, tin octylate, etc.), A titanium-based catalyst (for example, tetrabutyl titanate or the like) can be used.
- amine catalysts eg, triethylamine, N-ethylmorpholine, triethylenediamine, etc.
- tin-based catalysts eg, dibutyltin dilaurylate, dioctyltin dilaurylate, tin octylate, etc.
- a titanium-based catalyst for example, tetrabutyl titanate or
- a solvent may be used in the process of producing the elastomer of the present embodiment.
- preferred solvents include, but are not particularly limited to, dimethylformamide, diethylformamide, dimethylacetamide, dimethyl sulfoxide, tetrahydrofuran, methyl isobutyl ketone, dioxane, cyclohexanone, methyl ethyl ketone, benzene, toluene, ethyl cellosolve, and the like.
- the elastomer of this embodiment may contain a stabilizer.
- the stabilizer include a heat stabilizer and a light stabilizer.
- the heat stabilizer is not particularly limited, and is, for example, an aliphatic, aromatic or alkyl group-substituted aromatic ester of phosphoric acid or phosphite, a hypophosphoric acid derivative, phenylphosphonic acid, phenylphosphinic acid, diphenylphosphonic acid, or polyphosphonate.
- the light stabilizer is not particularly limited, and examples thereof include an ultraviolet absorbing light stabilizer and a radical scavenging light stabilizer.
- examples of the ultraviolet absorbing light stabilizer are not particularly limited, and examples thereof include benzotriazole-based and benzophenone-based compounds.
- examples of the radical scavenging type light stabilizer are not particularly limited, and examples thereof include hindered amine compounds.
- These stabilizers may be used alone or in combination of two or more.
- the amount of these stabilizers added is 0.01 to 5 parts by mass, preferably 0.1 to 3 parts by mass, and more preferably 100 parts by mass of the elastomer obtained by reacting the above-mentioned polycarbonate diol with an isocyanate compound. It is 0.2 to 2 parts by mass.
- the elastomer of this embodiment may contain a plasticizer.
- the plasticizer is not particularly limited, and is, for example, phthalates such as dioctyl phthalate, dibutyl phthalate, diethyl phthalate, butyl benzyl phthalate, di-2-ethylhexyl phthalate, diisodecyl phthalate, diundecyl phthalate, and diisononyl phthalate, and trickre.
- Phosphoric acid esters such as dil phosphate, triethyl phosphate, tributyl phosphate, tri-2-ethylhexyl phosphate, trimethylhexyl phosphate, tris(chloroethyl)phosphate, tris(dichloropropyl)phosphate, trimellitic acid octyl ester, trimellitic acid isodecyl Esters, trimellitic acid esters, dipentaerythritol esters, dioctyl adipate, dimethyl adipate, di-2-ethylhexyl azelate, dioctyl azelate, dioctyl sebacate, di-2-ethylhexyl sebacate, methylacetyl ricinolate Phthalate acid esters such as fatty acid esters and phthalates octyl esters; epoxy-based plasticizers such as epoxidized soybean oil
- plasticizers can be used alone or in combination of two or more.
- the addition amount of the plasticizer is appropriately selected according to the required hardness and physical properties, but is preferably 0.1 to 50 parts by mass per 100 parts by mass of the elastomer obtained by reacting the above-mentioned polycarbonate diol with an isocyanate compound.
- the elastomer of this embodiment may contain additives.
- the additive is not particularly limited, and examples thereof include an inorganic filler, a lubricant, a colorant, a silicone oil, a foaming agent, and a flame retardant. Specific examples thereof include, but are not limited to, calcium carbonate, talc, magnesium hydroxide, mica, barium sulfate, silicic acid (white carbon), titanium oxide, carbon black and the like. These various additives can be used in amounts commonly used for conventional elastomers.
- the polystyrene reduced number average molecular weight (Mn) measured by gel permeation chromatography (GPC) analysis is preferably in the range of 5,000 to 200,000, respectively.
- the elastomer of the present embodiment obtained as described above is excellent in flexibility, heat resistance, low temperature characteristics, weather resistance, strength, molding processability, etc., and therefore various molded articles such as automobile parts, home electric appliance parts, toys, sundries, etc.
- Raw materials, especially molded products requiring strength such as hoses, sheets, industrial belts, automobile interior and exterior parts such as wind moldings, bumpers, instrument panel skins, grips, spandex, watch bands, shoes It is extremely useful as a raw material for molded products that require flexibility such as the bottom.
- the method for producing the elastomer of the present embodiment is not particularly limited, and examples thereof include the following methods.
- an organic solvent containing no active hydrogen-containing group in the molecule for example, acetone, methyl ethyl ketone, tetrahydrofuran, N, N-dimethylformamide, etc.
- one molecule contains two or more isocyanate groups.
- the (NCO group / active proton group) equivalent ratio of the isocyanate compound, the polycarbonate diol, and the chain extender is preferably in the range of 0.5 to 1.5, more preferably in the range of 0.8 to 1.2.
- the urethane reaction is carried out in the range of 0.9 to 1.1 by the one-shot method or the multi-step method.
- the obtained elastomer or elastomer solution may be processed into pellets, or may be applied to a base material and processed into a film.
- the stabilizer, the plasticizer and the additive may be added at any timing.
- acetylation reagent was prepared by measuring up 12.5 g of acetic anhydride with 50 mL of pyridine. 2.5-5.0 g of the sample was precisely weighed in a 100 mL eggplant flask. After adding 5 mL of the acetylation reagent and 10 mL of toluene with a whole pipette, a cooling tube was attached, and the mixture was stirred and heated at 100 ° C. for 1 hour. 2.5 mL of distilled water was added with a whole pipette, and the mixture was further heated and stirred for 10 minutes.
- the ratio of the repeating unit represented by the above formula (A) was determined by the following method. 1) Polycarbonate diol Mg (about 1 g), ethanol 30 g, and potassium hydroxide 4 g were added to a 100 mL eggplant flask and reacted at 100 ° C. for 1 hour to obtain a hydrolyzate. 2) After cooling the hydrolyzate to room temperature, 2-3 drops of phenolphthalein was added as an indicator, neutralized with hydrochloric acid, and further cooled in a refrigerator for 1 hour. 3) Cmol of diethylene glycol diethyl ether (about 0.5 g) was added as an internal standard, and the precipitated salt was removed by filtration.
- each ratio of the repeating unit represented by the formula (B) corresponding to each diol (C) was calculated by the following formula.
- Each ratio of the repeating unit represented by the formula (B) corresponding to each diol (C) (f' ⁇ C ⁇ D' ⁇ Mw / M) ⁇ 100 (Note: Mw is the molecular weight of the repeating unit represented by the above formula (B) corresponding to each diol (C))
- Mw is the molecular weight of the repeating unit represented by the above formula (B) corresponding to each diol (C)
- the ratio of the repeating units represented by the above formula (B) is the sum of the respective ratios of the repeating units represented by the above formula (B) corresponding to each diol (C) obtained in the above 6).
- the ratio of primary hydroxyl group ends in the polycarbonate diols obtained in each Example and Comparative Example was determined by the following method.
- the ratio of the primary hydroxyl group terminal was calculated by dissolving polycarbonate diol in CDCl 3 (deuterated chloroform) and measuring 1 H-NMR (ECS400 manufactured by JEOL) at 400 MHz, and calculating the integrated value.
- the ratio of the primary hydroxyl group terminal is the sum of the integrated value of one proton of the primary hydroxyl group and the integrated value of all the hydroxyl groups of carbonate diol and carbonate ester terminal such as phenoxide terminal of each proton. It was calculated from the ratio of.
- the detection limit of the ratio of the primary hydroxyl group terminal is 1.0 mol% with respect to the entire structure of the polycarbonate diol terminal.
- a polyurethane film or elastomer film having a thickness of 0.04 to 0.06 mm prepared in the shape of a white plate was colored with a red oil-based pen (Magic Ink, manufactured by Teranishi Chemical Industry Co., Ltd.). After 1 hour, the colored portion of each film was washed off with acetone and dried at 23° C. for 10 minutes. The stain resistance of each film was evaluated as follows based on the color difference ⁇ E * before coloring with an oil-based pen and after washing.
- ⁇ E * was calculated according to the following formula (6) by measuring the color of the coated plate before and after the test with a color meter (manufactured by Suga Test Instruments Co., Ltd., model number: SM-P45) according to the CIELab color system.
- a polyurethane film or elastomer film having a thickness of 0.04 to 0.06 mm was formed on the glass, and cut into strips having a width of 10 mm and a length of 50 mm.
- this film was subjected to a tensile test under conditions of a temperature of -20°C and a chuck distance of 20 mm, a tensile speed of 5 mm/min. From the obtained elongation at break, the low temperature flexibility of each film was evaluated as follows.
- Breaking elongation is 100% or more ⁇ : Breaking elongation is 30% or more and less than 100% X: Breaking elongation is less than 30%.
- a polyurethane film or elastomer film having a thickness of 0.04 to 0.06 mm was formed on the glass, and cut into strips having a width of 10 mm and a length of 50 mm.
- the film was heated at 120 degrees for 1 week.
- the film before and after the heating was subjected to a tensile test using a Universal Testing Machine (manufactured by Zwick Corp.) under room temperature conditions with a chuck distance of 20 mm and a tensile speed of 5 mm/min.
- the heat resistance of each film was evaluated as follows from the calculated breaking strength retention rate.
- Breaking strength retention rate 50% or more
- Breaking strength retention rate 30% or more and less than 50%
- Breaking strength retention rate Less than 30%
- Elastomer number average molecular weight The number average molecular weights of the elastomers obtained in Examples and Comparative Examples were measured by gel permeation chromatography (GPC).
- the GPC apparatus used was an HLC-8220 GPC apparatus manufactured by Tosoh, and was detected by an RI detector.
- DMF dimethylformamide
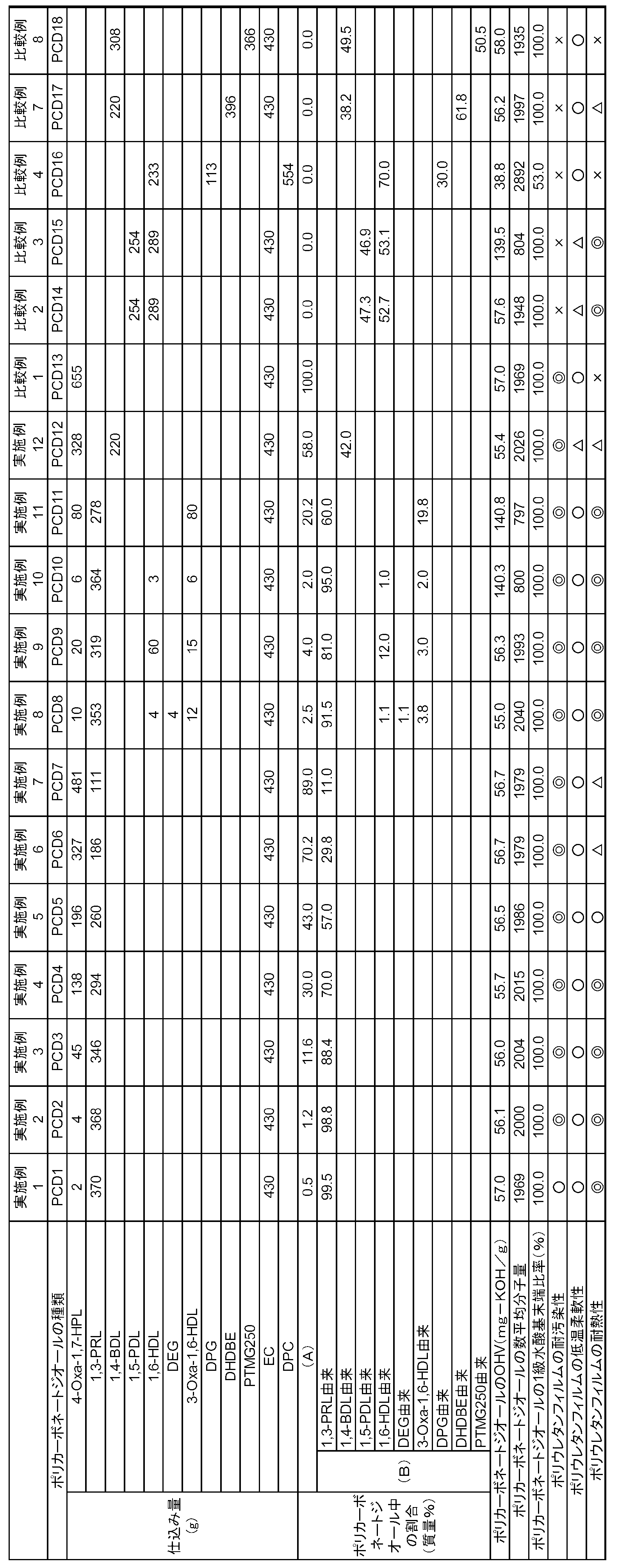
- Example 1 A 2-L separable flask equipped with a stirrer, a thermometer, and an Oldershaw with a vacuum jacket having a reflux head at the top was charged with 2 g of 4-oxa-1,7-heptanediol, 370 g of 1,3-propanediol, and 430 g of ethylene carbonate. Then, 0.08 g of tetrabudoxy titanium was added as a catalyst. The reaction was carried out for 18 hours while the internal temperature of the flask was 140 to 180° C. and the degree of vacuum was 15 to 3 kPa while removing a part of the fraction from the reflux head.
- PCD1 viscous liquid polycarbonate diol
- Example 2 to 12 Liquid polycarbonate diols (PCD2 to PCD12) viscous at room temperature were obtained in the same manner as in Example 1 except that the types of raw materials and the amount charged were changed as shown in Table 1.
- the viscosity of the obtained polyisocyanate at 25 ° C. was 1,600 mPa ⁇ s, the isocyanate group concentration was 23.0% by mass, the number average molecular weight was 660, and the residual HDI concentration was 0.2% by mass.
- the obtained coating composition was cast on a glass plate or an ABS plate, allowed to stand at room temperature for 5 minutes to remove the solvent, and then placed in a dryer at 80° C. for 1 hour to dry to obtain a polyurethane film. ..
- the obtained polyurethane film was cured in an environment of a temperature of 23 ° C. and a humidity of 50% for one week and used for each evaluation (stain resistance, low temperature flexibility and heat resistance).
- the OH value (OHV) and primary hydroxyl group end ratio of the polycarbonate diol of each Example and Comparative Example, and various characteristics when the polycarbonate diol of each Example and Comparative Example was used as a polyurethane film stain resistance, low temperature flexibility
- the evaluation results of (property and heat resistance) are shown in Table 1. It was confirmed that the polyurethane produced by using the polycarbonate diol of the present embodiment has excellent stain resistance, low temperature flexibility and heat resistance.
- 1,3-PRL represents 1,3-propanediol
- 1,4-BDL represents 1,4-butanediol
- 1,5-PDL represents 1,5-PDL.
- 1,6-HDL represents 1,6-hexanediol
- DEG represents diethylene glycol
- 3-Oxa-1,6-HDL represents. It represents 3-oxa-1,6-hexanediol
- 4-Oxa-1,7-HDL represents 4-oxa-1,7-heptanediol
- DPG represents dipropylene glycol.
- DHDBE represents 4,4'-dihydroxydibutyl ether
- PTMG250 represents polytetramethylene etherdiol having a molecular weight of 250
- EC represents ethylene carbonate
- DPC diphenyl carbonate.
- (A)” represents a repeating unit represented by the formula (A)
- (B) represents a repeating unit represented by the formula (B).
- Example 13 In a 2 L 4-necked flask equipped with a stirrer, a cooling tube, a nitrogen inflow tube, and a thermometer, under a nitrogen atmosphere, 33.3 g of isophorone diisocyanate (IPDI), 100 g of polycarbonate diol PCD4, and 6.7 g of dimethylolpropionic acid (DMPA). , 6.1 g of triethylamine (TEA) and 30 mL of methyl ethyl ketone (MEK) were added and reacted at 80 ° C. for 2.5 hours to obtain an NCO-terminated prepolymer solution.
- IPDI isophorone diisocyanate
- DMPA dimethylolpropionic acid
- the obtained aqueous polyurethane dispersion is cast on a glass plate or an ABS plate, left at room temperature for 5 minutes for curing, and then placed in a dryer at 80° C. for 1 hour to be dried to obtain a polyurethane film. It was.
- the obtained polyurethane film was aged for one week in an environment of a temperature of 23° C. and a humidity of 50% and used for each evaluation (stain resistance and heat resistance). Table 2 shows the stain resistance and heat resistance of the obtained polyurethane film.
- Example 14 to 15 Aqueous polyurethane dispersions (PUD17 to PUD18) and polyurethane films were obtained and evaluated in the same manner as in Example 13 except that PCD8 or PCD9 was used instead of the polycarbonate diol PCD4.
- Table 2 shows the polyurethane particle size of the obtained aqueous polyurethane dispersion and the stain resistance and heat resistance of the obtained polyurethane film.
- aqueous polyurethane dispersion (PUD19) and a polyurethane film were obtained and evaluated in the same manner as in Example 13 except that PCD14 was used instead of polycarbonate diol PCD4.
- Table 2 shows the polyurethane particle size of the obtained aqueous polyurethane dispersion and the stain resistance and heat resistance of the obtained polyurethane film.
- Example 16 To a 500 mL four-necked flask equipped with a stirrer, a cooling tube, a nitrogen inflow tube, and a thermometer, 30 g of polycarbonate diol PCD4 and 150 g of dimethylformamide were added under a nitrogen atmosphere, and the mixture was stirred at 40° C. until PCD4 was dissolved. 7.7 g of MDI (2.05 times mole of PCD4) was added and stirred for 4 hours to obtain a prepolymer.
- the obtained elastomer solution was spread on a glass plate or upstream of a white plate, left at room temperature for 5 minutes to cure, and then placed in a dryer at 80 ° C. for 1 hour to dry to obtain an elastomer film.
- the obtained elastomer film was cured in an environment of a temperature of 23 ° C. and a humidity of 50% for one week and used for evaluation (stain resistance and heat resistance).
- the properties of the obtained elastomer film (TPU21) are shown in Table 3.
- Example 17 to 18 Elastomer films were obtained and evaluated in the same manner as in Example 16 except that PCD8 or PCD9 was used instead of the polycarbonate diol PCD4.
- Table 3 shows the number average molecular weight of the obtained elastomer and the characteristics of the obtained elastomer films (TPU22 to TPU23).
- Example 6 Elastomer films were obtained and evaluated in the same manner as in Example 16 except that PCD14 was used instead of the polycarbonate diol PCD4. Table 3 shows the number average molecular weight of the obtained elastomer and the properties of the obtained elastomer film (TPU24).
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Medicinal Chemistry (AREA)
- Polymers & Plastics (AREA)
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Life Sciences & Earth Sciences (AREA)
- Wood Science & Technology (AREA)
- Manufacturing & Machinery (AREA)
- Oil, Petroleum & Natural Gas (AREA)
- Dispersion Chemistry (AREA)
- Polyurethanes Or Polyureas (AREA)
- Polyesters Or Polycarbonates (AREA)
- Paints Or Removers (AREA)
Abstract
Description
(1)
下記式(A)で表される繰り返し単位の割合が、0.1質量%以上99.9質量%以下である、ポリカーボネートジオール。
前記式(A)で表される繰り返し単位の割合が、0.1質量%以上50.0質量%以下である、(1)に記載のポリカーボネートジオール。
(3)
さらに、下記式(B)で表される繰り返し単位を0.1質量%以上99.9質量%以下含む、(1)又は(2)に記載のポリカーボネートジオール。
(4)
前記式(B)におけるRの炭素数が3~6である、(3)に記載のポリカーボネートジオール。
(5)
数平均分子量が300以上4,000以下である、(1)~(4)のいずれかに記載のポリカーボネートジオール。(6)
1級水酸基末端比率が90%以上である、(1)~(5)のいずれかに記載のポリカーボネートジオール。
(7)
(1)~(6)のいずれかに記載のポリカーボネートジオールを含有する塗料組成物。
(8)
(1)~(6)いずれかに記載のポリカーボネートジオールを用いて得られる水分散性ポリウレタンと、水とを含む、水性ポリウレタン分散体。
(9)
(8)に記載の水性ポリウレタン分散体を含む水性塗料組成物。
(10)
(1)~(6)いずれかに記載のポリカーボネートジオールとイソシアネート化合物とを反応させて得られるエラストマー。
本実施形態のポリカーボネートジオールは、下記式(A)で表される繰り返し単位の割合が、0.1質量%以上99.9質量%以下である。本実施形態のポリカーボネートジオールは、さらに、下記式(B)で表される繰り返し単位を0.1質量%以上99.9質量%以下含むことが好ましい。下記式(B)における炭素数Rは3~6であることがより好ましい。また、本実施形態のポリカーボネートジオールは、数平均分子量が300以上4,000以下であることが好ましい。さらにまた、本実施形態のポリカーボネートジオールは、1級水酸基末端比率が90%以上であることが好ましい。
1)100mLのナスフラスコにポリカーボネートジオールMg(約1g)、エタノール30g、水酸化カリウム4gを添加して、100℃で1時間反応し、加水分解物を得る。
2)加水分解物を室温まで冷却後、指示薬としてフェノールフタレインを2~3滴添加し、塩酸で中和し、さらに冷蔵庫で1時間冷却する。
3)内標としてジエチレングリコールジエチルエーテルCmol(約0.5g)を加え、更にアセトンを30g加え、沈殿した塩を濾過で除去する。
4)次の条件でガスクロマトグラフィーにより、内標のピーク面積に対する4-オキサ-1,7-ヘプタンジオールのピーク面積比Dを求める。
装置:ガスクロマトグラフィーGC-2014(島津製作所株式会社製品)
カラム:DB-WAX(J&W会社製品)
検出器:FID
昇温プロファイル:100℃で5分保持した後、250℃まで10℃/分で昇温
5)4-オキサ-1,7-ヘプタンジオール0.1g、内標(ジエチレングリコールジエチルエーテル)0.5g、エタノール30gを混合し、上記4)と同じ条件でガスクロマトグラフィー分析を行い、ファクターfを計算する。
6)ピーク面積値Dとファクターfとから、下記式により、式(A)で表される繰り返し単位の割合を計算する。
(注:160は上記式(A)で表される繰り返し単位の分子量)
本実施形態のポリカーボネートジオールにおいて、上記式(A)で表される繰り返し単位と、上記式(B)で表される繰り返し単位との合計割合は、少なくとも50質量%以上が好ましく、60質量%以上がより好ましく、70質量%以上がさらに好ましく、80質量%以上が特に好ましい。上記式(A)で表される繰り返し単位と上記式(B)で表される繰り返し単位との合計割合が上述した下限値以上であると、耐汚染性と耐熱性が特に優れる傾向にある。上記式(A)で表される繰り返し単位と上記式(B)で表される繰り返し単位との合計割合の上限値は特に限定されないが例えば100質量%である。
1級の水酸基末端の割合は、ポリカーボネートジオールをCDCl3(重クロロホルム)に溶解して400MHzにて1H-NMR(JEOL製ECS400)を測定、その積分値より算出する。1級の水酸基末端の割合は、1級の水酸基末端の1プロトン分の積分値と、ポリカーボネートジオールの全水酸基末端及びフェノキシド末端等の炭酸エステル由来末端、それぞれの1プロトン分の積分値の合計との比から求めており、1級の水酸基末端の割合の検出限界はポリカーボネートジオール末端の全構造に対して1.0モル%である。
次に本実施形態のポリカーボネートジオールの製造方法について説明する。
本実施形態のポリカーボネートジオールの製造方法は特に限定されないが、例えば、4-オキサ-1,7-ヘプタンジオールと式(C):HO-R-OH(式中、Rは、炭素骨格中に酸素原子を含んでもよい、炭素数3~20の二価の炭化水素基を表す。)で表されるジオール化合物を含むジオール成分と、炭酸エステルとのエステル交換反応により得る方法が挙げられる。ジオール成分は、さらに他のポリオールを含有してもよい。
本実施形態の塗料組成物は、上述したポリカーボネートジオールを含有する。
本実施形態の塗料組成物はイソシアネート化合物を含んでいてもよい。本実施形態の塗料組成物において、イソシアネート化合物を含む場合、(NCO基/OH基)当量比は0.5~3.0であることが好ましく、より好ましくは0.6~2.0であり、さらに好ましくは0.7~1.5である。(NCO基/OH基)当量比が前述の範囲にあることで塗膜の分子量が向上し耐熱性、耐薬品性等に優れる傾向にある。本実施形態で用いるイソシアネート化合物としては、特に耐候性の点から、脂肪族及び/又は脂環族イソシアネート化合物から誘導されたポリイソシアネート類であることが好ましい。具体的には、特に限定されないが、例えば、ヘキサメチレンジイソシアネート(HDI)、イソホロンジイソシアネート(IPDI)等の脂肪族又は脂環族ジイソシアネートから誘導されたポリイソシアネートが挙げられる。更には、これらのポリイソシアネートを、例えば、ブタノール、2-エチルヘキサノール等の低級アルコール、メチルエチルケトンオキシム、ラクタム類、フェノール類、イミダゾール類、活性メチレン化合物などブロック剤でブロックした、いわゆるブロックドイソシアネート系硬化剤を用いることもできる。
本実施形態の塗料組成物は、塗装時の作業性を調整するために、必要に応じて有機溶剤を1から95質量%含有することができる。有機溶剤の含有量は、15~75質量%であることがより好ましく、30~60質量%であることがさらに好ましい。用いる有機溶剤としては、特に限定されないが、実質的にイソシアネート化合物に対して不活性な有機溶媒であり且つ活性水素を有しないものであることが好ましい。その例としては、特に限定されないが、例えば、ペンタン、ヘキサン、ヘプタン、オクタン、デカン、石油エーテル、石油ベンジン、リグロイン、石油スピリット、シクロヘキサン、メチルシクロヘキサン等の炭化水素類、トリクロロフルオロエタン、テトラクロロジフルオロエタン、パーフルオロエーテル等の弗素化油等の弗素系不活性液体、パーフルオロシクロヘキサン、パーフルオロブチルテトラヒドロフラン、パーフルオロデカリン、パーフルオロ-n-ブチルアミン、パーフルオロポリエーテル、ジメチルポリシロキサン等の単独又は混合物が挙げられる。さらには、メチルエチルケトン、アセトン、酢酸エチル、酢酸ブチル、トルエン、キシレン等の単独又は混合溶媒が挙げられる。
本実施形態の塗料組成物は、用途に応じて4-オキサ-1,7-ヘプタンジオール、前記式(C)で表されるジオール化合物(C)、ポリエーテルポリオール、ポリエステルポリオール、ポリカーボネートポリオール、アクリルポリオール、フッ素ポリオールを含んでもよい。ポリエーテルポリオール、ポリエステルポリオールを含んだ場合、それらを単独で用いる場合と比較して耐薬品性を付与できる。アクリルポリオールやフッ素ポリオールを含んだ場合、それら単独で用いる場合と比較して柔軟性や耐擦り傷性を付与することができる。
本実施形態の塗料組成物は、得られる塗膜のソフト感をより高めるためにポリウレタン粒子を用いてもよい。またつや消し調塗膜を得るためにつや消し剤(例えばエボニック社製 TS-100)を用いてもよい。各種用途に応じて硬化促進剤(触媒)、充填剤、難燃剤、染料、有機又は無機顔料、離型剤、流動性調整剤、可塑剤、抗酸化剤、紫外線吸収剤、光安定剤、消泡剤、レベリング剤(例えばビックケミー製BYK-331)、着色剤、着色防止剤(例えばビックケミー製Silcalean3700等)、溶剤等を添加することができる。これらは単独で用いても2種以上組み合わせて用いてもよい。
本実施形態の水性ポリウレタン分散体は、上述したポリカーボネートジオールを用いて得られる水分散性ポリウレタンと、水とを含む。
本実施形態の水性ポリウレタン分散体に含まれる水分散性ポリウレタンは、上述したポリカーボネートジオールと、イソシアネート化合物と、カルボキシル基及び/又はスルホン基含有ポリオール若しくはその塩とから得られる。
前記イソシアネート化合物としては、1分子中にイソシアネート基を2つ以上含有するイソシアネート化合物であれば特に限定されない。イソシアネート化合物の例としては、例えば、ジフェニルメタンジイソシアネート(MDI)、シクロヘキサンジイソシアネート、トリレンジイソシアネート(TDI)、HDI、トリメチルヘキサンジイソシアネート、1,5-ナフタレンジイソシアネート(NDI)、キシリレンジイソシアネート(XDI)、2,6-ジイソシアネートメチルカプロエート、IPDI、メチルシクロヘキサン-2,4-(又は2,6-)ジイソシアネート、ジシクロヘキシルメタンジイソシアネート(水添MDI)などの芳香族、脂肪族、脂環族系有機ジイソシアネート、又はこれらのビュレット体、イソシアヌレート体等の多官能イソシアネート基を含有する多量体、又はこれらのイソシアネートの単独又は混合物が挙げられる。
本実施形態に用いるカルボキシル基及び/又はスルホン基含有ポリオール又はその塩は、水分散性ポリウレタンを水中に自己乳化させること、及び水性ポリウレタン分散体の分散安定性を付与することを目的として、カルボキシレート基又はスルホネート基導入のために使用される成分である。カルボキシル基含有ポリオールとしては、特に限定されないが、例えば2,2-ジメチロールプロピオン酸(DMPA)、2,2-ジメチロールブタン酸、2,2-ジメチロールヘプタン酸、2,2-ジメチロールオクタン酸などが挙げられる。また、スルホン基含有ポリオールとしては、例えば、スルホン酸ジオール{3-(2,3-ジヒドロキシプロポキシ)-1-プロパンスルホン酸}及びスルファミン酸ジオール{N,N-ビス(2-ヒドロキシルキル)スルファミン酸}及びそのアルキレンオキサイド付加物等が挙げられる。これらのカルボキシル基及び/又はスルホン基含有ポリオールの塩としては、特に限定されないが、例えば、アンモニウム塩、アミン塩[炭素数1~12の1級アミン(1級モノアミン、例えばメチルアミン、エチルアミン、プロピルアミン及びオクチルアミン)塩、2級モノアミン(ジメチルアミン、ジエチルアミン及びジブチルアミン)塩、3級モノアミン(トリメチルアミン、トリエチルアミントリエタノールアミン、N-メチルジエタノールアミン及びN,N-メチルエタノールアミン等の脂肪族3級モノアミン;N-メチルピペリジン及びN-メチルモルホリン等の複素環式3級モノアミン;ベンジルジメチルアミン、α―メチルベンジルジメチルアミン;及びN-ジメチルアニリン等の芳香環含有3級モノアミン)塩]、アルカリ金属(ナトリウム、カリウム及びリチウムカチオン)塩、並びにこれらの2種以上の併用が挙げられる。
また本実施形態の水性ポリウレタン分散体は、界面活性剤を含んでもよい。界面活性剤としては、特に限定されないが、例えば高級脂肪酸、樹脂酸、酸性脂肪アルコール、硫酸エステル、スルホン酸高級アルキル、スルホン酸アルキルアリール、スルホン化ひまし油、スルホコハク酸エステル等に代表されるアニオン性界面活性剤あるいはエチレンオキサイドと長鎖脂肪アルコール又はフェノール類との公知の反応生成物に代表されるノニオン性界面活性剤等が挙げられる。
本実施形態の水性ポリウレタン分散体の製造方法は、例えば、特に限定されないが、以下のような方法が挙げられる。分子内に活性水素含有基を含まない有機溶剤(例えば、アセトン、メチルエチルケトン、テトラヒドロフラン、N,N-ジメチルホルムアミド等)の存在下又は非存在下で、1分子中にイソシアネート基を2つ以上含有するイソシアネート化合物と、ポリカーボネートジオールと、カルボキシル基及び/又はスルホン基含有ポリオール又はその塩と、を(NCO基/OH基)当量比が、好ましくは0.5~1.5の範囲、より好ましくは0.8~1.2の範囲、さらに好ましくは0.9~1.1の範囲にてワンショット法、又は多段法によりウレタン化反応させてポリウレタンを合成し、必要に応じて該ポリウレタンを中和剤で中和した後、得られた該反応液を強攪拌しているところに水を滴下し、滴下終了後必要に応じて溶媒を除去することにより水性ポリウレタン分散体が得られる。また、得られた上記反応液を水中に攪拌しながら添加し分散させたのち、必要に応じて溶媒を除去して水性ポリウレタン分散体を得ることも可能である。
本実施形態の水性塗料組成物は、上述の水性ポリウレタン分散体を含有する。
本実施形態のエラストマーは、上述したポリカーボネートジオールとイソシアネート化合物とを反応させて得られる。
本実施形態のエラストマーの製造に使用されるイソシアネート化合物としては、1分子中にイソシアネート基を2つ以上含有するイソシアネート化合物であれば特に限定されない。イソシアネート化合物の例としては、MDI、シクロヘキサンジイソシアネート、TDI、HDI、トリメチルヘキサンジイソシアネート、NDI、XDI、2,6-ジイソシアネートメチルカプロエート、IPDI、メチルシクロヘキサン-2,4-(又は2,6-)ジイソシアネート、水添MDIなどの芳香族、脂肪族、脂環族系有機ジイソシアネート、又はこれらのビュレット体、イソシアヌレート体等の多官能イソシアネート基を含有する多量体、又はこれらのイソシアネートの単独又は混合物が挙げられる。
また、本実施形態のエラストマー製造は、共重合成分として鎖延長剤を用いてもよい。鎖延長剤としては、水、低分子ポリオール、ポリアミン、高分子ポリオールを併用してもよい。
本実施形態のエラストマーを製造する過程で、必要に応じて公知のウレタン化反応触媒を用いることができる。ウレタン化反応触媒としては、特に限定されないが、例えば、アミン触媒(例えばトリエチルアミン、N-エチルモルホリン、トリエチレンジアミン等)、錫系触媒(例えば、ジブチル錫ジラウリレート、ジオクチル錫ジラウリレート及びオクチル酸錫等)、チタン系触媒(例えば、テトラブチルチタネート等)が挙げられる。
本実施形態のエラストマーを製造する過程で、溶媒を用いてもよい。好ましい溶媒の例として、特に限定されないが、例えば、ジメチルホルムアミド、ジエチルホルムアミド、ジメチルアセトアミド、ジメチルスルホキシド、テトラヒドロフラン、メチルイソブチルケトン、ジオキサン、シクロヘキサノン、メチルエチルケトン、ベンゼン、トルエン、エチルセルソルブ等が挙げられる。
本実施形態のエラストマーは安定剤を含んでもよい。安定剤としては熱安定剤や光安定剤が挙げられる。熱安定剤としては、特に限定されないが、例えば、燐酸や亜燐酸の脂肪族、芳香族又はアルキル基置換芳香族エステルや次亜燐酸誘導体、フェニルホスホン酸、フェニルホスフィン酸、ジフェニルホスホン酸、ポリホスホネート、ジアルキルペンタエリスリトールジホスファイト、ジアルキルビスフェノールA ジホスファイト等のリン化合物; フェノール系誘導体特にヒンダードフェノール化合物、チオエーテル系、ジチオ酸塩系、メルカプトベンズイミダゾール系、チオカルバニリド系、チオジプロピオン酸エステル等のイオウを含む化合物; スズマレート、ジブチルスズモノオキシド等のスズ化合物を用いることができる。
本実施形態のエラストマーは可塑剤を含んでもよい。可塑剤としては、特に限定されないが、例えば、ジオクチルフタレート、ジブチルフタレート、ジエチルフタレート、ブチルベンジルフタレート、ジ-2-エチルヘキシルフタレート、ジイソデシルフタレート、ジウンデシルフタレート、ジイソノニルフタレート等のフタル酸エステル類、トリクレジルホスフェート、トリエチルホスフェート、トリブチルホスフェート、トリ-2-エチルヘキシルホスフェート、トリメチルヘキシルホスフェート、トリス(クロロエチル)ホスフェート、トリス(ジクロロプロピル)ホスフェート等のリン酸エステル類、トリメリット酸オクチルエステル、トリメリット酸イソデシルエステル、トリメリット酸エステル類、ジペンタエリスリトールエステル類、ジオクチルアジペート、ジメチルアジペート、ジ-2-エチルヘキシルアゼレート、ジオクチルアゼレート、ジオクチルセバケート、ジ-2-エチルヘキシルセバケート、メチルアセチルリシノレート等の脂肪酸エステル類、ピロメリット酸オクチルエステル等のピロメリット酸エステル類; エポキシ化大豆油、エポキシ化アマニ油、エポキシ化脂肪酸アルキルエステル等のエポキシ系可塑剤; アジピン酸エーテルエステル、ポリエーテル等のポリエーテル系可塑剤; 液状NBR、液状アクリルゴム、液状ポリブタジエン等の液状ゴム; 非芳香族系パラフィンオイル等を挙げることができる。
本実施形態のエラストマーは添加剤を含んでもよい。添加剤としては、特に限定されないが、例えば、無機充填剤、滑剤、着色剤、シリコンオイル、発泡剤、難燃剤等が挙げられる。具体的には、特に限定されないが、例えば、炭酸カルシウム、タルク、水酸化マグネシウム、マイカ、硫酸バリウム、珪酸(ホワイトカーボン)、酸化チタン、カーボンブラック等が挙げられる。これらの種々の添加剤は、従来のエラストマーに一般に用いる量で用いることができる。
本実施形態のエラストマーの分子量については、ゲルパーミエーションクロマトグラフィー(GPC)分析により測定されるポリスチレン換算数平均分子量(Mn)がそれぞれ5,000~200,000の範囲であることが好ましい。
本実施形態のエラストマーの製造方法は、例えば、特に限定されないが、以下のような方法が挙げられる。分子内に活性水素含有基を含まない有機溶剤(例えば、アセトン、メチルエチルケトン、テトラヒドロフラン、N,N-ジメチルホルムアミド等)の存在下又は非存在下で、1分子中にイソシアネート基を2つ以上含有するイソシアネート化合物と、ポリカーボネートジオールと、鎖延長剤とを(NCO基/活性プロトン基)当量比が、好ましくは0.5~1.5の範囲、より好ましくは0.8~1.2の範囲、さらに好ましくは0.9~1.1の範囲にてワンショット法、又は多段法によりウレタン化反応させる。得られたエラストマー又はエラストマー溶液はペレット状に加工してもよいし、基材に塗布してフィルム状に加工してもよい。安定剤、可塑剤、添加剤はいずれのタイミングで加えてもよい。
[1.OH価]
無水酢酸12.5gをピリジン50mLでメスアップしアセチル化試薬を調製した。100mLナスフラスコに、サンプルを2.5~5.0g精秤した。アセチル化試薬5mLとトルエン10mLとをホールピペットで添加後、冷却管を取り付けて、100℃で1時間撹拌加熱した。蒸留水2.5mLをホールピペットで添加し、更に10分加熱撹拌した。2~3分冷却後、エタノールを12.5mL添加し、指示薬としてフェノールフタレインを2~3滴添加した後に、0.5mol/Lエタノール性水酸化カリウムで滴定した。アセチル化試薬5mL、トルエン10mL、及び蒸留水2.5mLを100mLナスフラスコに入れ、10分間加熱撹拌した後、同様に滴定を行った(空試験)。これらの結果をもとに、下記式(3)で表される式により、OH価を求めた。
c:サンプルの滴定量(mL)
d:空試験の滴定量(mL)
e:サンプル質量(g)
f:滴定液のファクター
各実施例及び比較例で得られたポリカーボネートジオールにおける末端は、13C-NMR(270MHz)の測定により、実質的に全てがヒドロキシル基であった。更に各ポリカーボネートジオール中の酸価をKOHによる滴定により測定したところ、酸価は、0.01以下であった。次に、下記式(4)で表される式により各ポリカーボネートジオールの数平均分子量を求めた。
上記式(A)で表される繰り返し単位の割合は下記の手法で求めた。
1)100mLのナスフラスコにポリカーボネートジオールMg(約1g)、エタノール30g、水酸化カリウム4gを添加して、100℃で1時間反応し、加水分解物を得た。
2)加水分解物を室温まで冷却後、指示薬としてフェノールフタレインを2~3滴添加し、塩酸で中和し、さらに冷蔵庫で1時間冷却した。
3)内標としてジエチレングリコールジエチルエーテルCmol(約0.5g)を加え、沈殿した塩を濾過で除去した。
4)次の条件でガスクロマトグラフィーにより、内標のピーク面積に対する4-オキサ-1,7-ヘプタンジオールのピーク面積比Dを求めた。
装置:ガスクロマトグラフィーGC-2014(島津製作所株式会社製品)
カラム:DB-WAX(J&W会社製品)
検出器:FID
昇温プロファイル:100℃で5分保持した後、250℃まで10℃/分で昇温その後10分保持
5)4-オキサ-1,7-ヘプタンジオール0.1g、内標(ジエチレングリコールジエチルエーテル)0.5g、エタノール30gを混合し、上記4)と同じ条件でガスクロマトグラフィー分析を行い、ファクターfを計算した。
6)ピーク面積値Dとファクターfとから、下記式により、式(A)で表される繰り返し単位の割合を計算した。
式(A)で表される繰り返し単位の割合=(f×C×D×160/M)×100
(注:160は上記式(A)で表される繰り返し単位の分子量)
上記式(B)で表される繰り返し単位の割合は下記の手法で求めた。
1)100mLのナスフラスコにポリカーボネートジオールMg(約1g)、エタノール30g、水酸化カリウム4gを添加して、100℃で1時間反応し、加水分解物を得た。
2)加水分解物を室温まで冷却後、指示薬としてフェノールフタレインを2~3滴添加し、塩酸で中和し、さらに冷蔵庫で1時間冷却した。
3)内標としてジエチレングリコールジエチルエーテルCmol(約0.5g)を加え、沈殿した塩を濾過で除去した。
4)次の条件でガスクロマトグラフィーにより、内標のピーク面積に対する各ジオール(C)のピーク面積比D’をそれぞれ求めた。
装置:ガスクロマトグラフィーGC-2014(島津製作所株式会社製品)
カラム:DB-WAX(J&W会社製品)
検出器:FID
昇温プロファイル:100℃で5分保持した後、250℃まで10℃/分で昇温その後10分保持
5)各ジオール(C)を0.1gずつ、内標(ジエチレングリコールジエチルエーテル)0.5g、エタノール30gを混合し、上記4)と同じ条件でガスクロマトグラフィー分析を行い、ファクターf’をそれぞれ計算した。
6)ピーク面積値D’とファクターf’とから、下記式により、各ジオール(C)に対応する式(B)で表される繰り返し単位の各割合をそれぞれ計算した。
各ジオール(C)に対応する式(B)で表される繰り返し単位の各割合
=(f’×C×D’×Mw/M)×100
(注:Mwは各ジオール(C)に対応する上記式(B)で表される繰り返し単位の分子量)
7)上記式(B)で表される繰り返し単位の割合は上記6)で求めた各ジオール(C)に対応する上記式(B)で表される繰り返し単位の各割合の総和とした。
各実施例及び比較例で得られたポリカーボネートジオールにおける1級水酸基末端比率は下記の手法で求めた。
1級の水酸基末端の割合は、ポリカーボネートジオールをCDCl3(重クロロホルム)に溶解して400MHzにて1H-NMR(JEOL製ECS400)を測定、その積分値より算出した。1級の水酸基末端の割合は、1級の水酸基末端の1プロトン分の積分値と、ポリカーボネートジオールの全水酸基末端及びフェノキシド末端等の炭酸エステル由来末端、それぞれの1プロトン分の積分値の合計との比から求めた。なお、1級の水酸基末端の割合の検出限界はポリカーボネートジオール末端の全構造に対して1.0モル%である。
白板状に作成した厚さ0.04~0.06mmのポリウレタンフィルム又はエラストマーフィルムに赤色の油性ペン(マジックインキ、寺西化学工業株式会社製)にて着色した。1時間後に各フィルムの着色部分をアセトンで洗い流し23度で10分間乾燥させた。各フィルムについて油性ペン着色前と洗浄後との色差ΔE*にて耐汚染性を以下のとおり評価した。ΔE*は試験前後の塗板の色をCIELab表色系に従いカラーメーター(スガ試験機株式会社製、型番:SM-P45)にて測定し、下記式(6)に従い計算した。
○:5<ΔE*≦10
△:10<ΔE*≦30
×:30<ΔE*
ガラス上に厚さ0.04~0.06mmのポリウレタンフィルム又はエラストマーフィルムを形成し、幅10mm、長さ50mmの短冊状に切り出した。このフィルムをUniversal Testing Machine(Zwick Corp.製)を用いて、チャック間20mm、引張速度5mm/分で、温度-20℃の条件下で引っ張り試験を行った。得られた破断伸度から各フィルムの低温柔軟性について以下のとおり評価した。
△:破断伸度が30%以上100%未満
×:破断伸度が30%未満。
ガラス上に厚さ0.04~0.06mmのポリウレタンフィルム又はエラストマーフィルムを形成し、幅10mm、長さ50mmの短冊状に切り出した。このフィルムを120度で1週間加熱した。当該加熱前後のフィルムについて、Universal Testing Machine(Zwick Corp.製)を用いて、チャック間20mm、引張速度5mm/分で、室温条件下で引っ張り試験を行った。得られた破断強度から破断強度保持率を下記式により算出した。
破断強度保持率=加熱後のフィルムの破断強度/加熱前のフィルムの破断強度×100
算出した破断強度保持率から各フィルムの耐熱性について以下のとおり評価した。
○:破断強度保持率:30%以上50%未満
△:破断強度保持率:30%未満
×:溶けて測定できなかった。
実施例及び比較例で得られた水性ポリウレタン分散体のポリウレタンの粒子径は粒度分析計Nanotrac150(Microtrac製)により測定した。
実施例及び比較例で得られたエラストマーの数平均分子量はゲルパーミエーションクロマトグラフィー(GPC)により測定した。GPC装置は東ソー製HLC-8220 GPC装置を用い、RI検出器で検出した。展開溶媒:ジメチルホルムアミド(DMF)、流速:0.5mL/分、操作温度:40℃、ポリスチレン換算で求めた。
攪拌機、温度計、頭頂に還流ヘッドを有する真空ジャケット付きオルダーショウを備えた2Lセパラブルフラスコに、4-オキサ-1,7-ヘプタンジオール2g、1,3-プロパンジオール370g、及びエチレンカーボネート430gを仕込み、触媒としてテトラブドキシチタンを0.08g入れた。フラスコの内温140~180℃、真空度15~3kPaで、還流ヘッドから留分の一部を抜きながら、18時間反応した。その後、フラスコの内温140~180℃で真空度を0.01~3kPaまで落として、セパラブルフラスコ内に残った4-オキサ-1,7-ヘプタンジオール、1,3-プロパンジオール及びエチレンカーボネートを除去した。この反応により、常温で粘稠な液体ポリカーボネートジオール(PCD1)が得られた。
表1に記載の原料の種類及び仕込み量を変更したこと以外は、実施例1と同様にして、常温で粘稠な液体ポリカーボネートジオール(PCD2~PCD12)を得た。
攪拌機、温度計、頭頂に還流ヘッドを有する真空ジャッケト付きオルダーショウを備えた2Lセパラブルフラスコに、4-オキサ-1,7-ヘプタンジオール654g、及びエチレンカーボネート430gを仕込み、触媒としてテトラブドキシチタンを0.08g入れた。フラスコの内温140~180℃、真空度15~3kPaで、還流ヘッドから留分の一部を抜きながら、18時間反応した。その後、フラスコの内温140~180℃で真空度を0.01~3kPaまで落として、セパラブルフラスコ内に残った4-オキサ-1,7-ヘプタンジオール及びエチレンカーボネートを除去した。
この反応により、常温で粘稠な液体ポリカーボネートジオール(PCD13)が得られた。
表1に記載の原料の種類及び仕込み量を変更したこと以外は、比較例1と同様にして、ポリカーボネートジオール(PCD14~PCD15、PCD17~PCD18)を得た。
オイル循環槽、攪拌機、留出液トラップ、及び圧力調整装置を備えた1L反応容器に1,6-ヘキサンジオール(232.9g)、ジプロピレングリコール(113.3g)、ジフェニルカーボネート(553.8g)を入れた後、酢酸マグネシウム4水和物の水溶液(210mg/25mL)をシリンジで1.8mL加えた。その後、反応容器内の窒素置換を3回繰り返した。窒素置換後、まず内温が165℃になるまでオイル循環槽を昇温(190~200℃)し、内容物を加熱溶解させた。昇温及び溶解したら攪拌を開始し、次に圧力を130torrまで5分間で下げ、その後、内温165℃、圧力130torrで90分間、フェノールを留出させながら重合を進めた。そして、90分かけて圧力を60torrまで、その後60分かけて圧力を2torrまでと段階的に反応容器内の圧力を下げながら、フェノール及び未反応のジオールを留出させながら重合を進めた。最後に内温を170℃まで上げて、内温170℃、圧力2torrで120分間反応させ得られた粘稠な液体を20g/分の流量で薄膜蒸留(温度:160℃、圧力:0.027kPa)し、ポリカーボネートジオールPCD16を得た。
撹拌機、温度計、還流冷却管、窒素吹き込み管、滴下ロートを取り付けた4ツ口フラスコ内を窒素雰囲気にし、ヘキサメチレンジイソシアネート600gを仕込み、撹拌下反応器内温度を70℃に保持した。イソシアヌレート化触媒テトラメチルアンモニウムカプリエートを加え、収率が24モル%になった時点でリン酸を添加し反応を停止した。反応液をろ過した後、薄膜蒸発缶を用いて未反応のヘキサメチレンジイソシアネートを除去して製造例のポリイソシアネートを得た。得られたポリイソシアネートの25℃における粘度は1,600mPa・s、イソシアネート基濃度は23.0質量%、数平均分子量は660、残留HDI濃度は0.2質量%であった。
ガラス製のサンプル瓶に、各実施例及び比較例で得たポリカーボネートジオール15gと酢酸ブチル18gと上記で合成したポリイソシアネートとを(NCO基/OH基)当量比が1.05となるように加え、シェイカーにてよく振り混ぜた。溶液が均一になったのを確認し、1モル%のジブチルスズジラウレートを0.2g添加し良く振り混ぜ塗料組成物を調製した。
得られた塗料組成物をガラス板上又はABS板上に流延し、室温で5分間放置して溶剤をとばした後、80℃の乾燥機に1時間入れて乾燥させてポリウレタンフィルムを得た。得られたポリウレタンフィルムを気温23℃湿度50%の環境で一週間養生し各評価(耐汚染性、低温柔軟性及び耐熱性)に使用した。
攪拌機、冷却管、窒素流入管、温度計を備えた2Lの4口フラスコに、窒素雰囲気下、イソホロンジイソシアネート(IPDI)33.3g、ポリカーボネートジオールPCD4を100g、ジメチロールプロピオン酸(DMPA)6.7g、トリエチルアミン(TEA)6.1g、及びメチルエチルケトン(MEK)30mLを加え、80℃で2.5時間反応させてNCO末端のプレポリマー溶液を得た。ついで、脱イオン水342gを添加し、35℃でプレポリマー溶液と混合してプレポリマー分散液を得た。脱イオン水2.0g中にエチレンジアミン(EDA)1.5gを含む溶液をプレポリマー分散液に添加して、30℃で1時間撹拌してポリウレタン分散液を得た。ついで、混合物を80℃に加熱してMEKを除去して、固形分30質量%をもつ水性ポリウレタン分散体(PUD16)を得た。得られた水性ポリウレタン分散体のポリウレタンの粒子径を測定した。測定結果を表2に示す。また、得られた水性ポリウレタン分散体をガラス板上又はABS板上に流延し、室温で5分間放置して養生した後、80℃の乾燥機に1時間入れて乾燥させてポリウレタンフィルムを得た。得られたポリウレタンフィルムを気温23℃湿度50%の環境で一週間養生し各評価(耐汚染性及び耐熱性)に使用した。得られたポリウレタンフィルムの耐汚染性及び耐熱性を表2に示す。
ポリカーボネートジオールPCD4の替わりに、PCD8又はPCD9を用いた以外は、実施例13と同様にして、水性ポリウレタン分散体(PUD17~PUD18)とポリウレタンフィルムとを得て各評価を行った。得られた水性ポリウレタン分散体のポリウレタンの粒子径、並びに、得られたポリウレタンフィルムの耐汚染性及び耐熱性を表2に示す。
ポリカーボネートジオールPCD4の替わりに、PCD14を用いた以外は、実施例13と同様にして、水性ポリウレタン分散体(PUD19)とポリウレタンフィルムとを得て各評価を行った。得られた水性ポリウレタン分散体のポリウレタンの粒子径、並びに、得られたポリウレタンフィルムの耐汚染性及び耐熱性を表2に示す。
攪拌機、冷却管、窒素流入管、温度計を備えた500mLの4口フラスコに、窒素雰囲気下、ポリカーボネートジオールPCD4を30g、ジメチルホルムアミドを150g加え、40℃でPCD4が溶解するまで攪拌した。MDIを7.7g(PCD4の2.05倍モル)加え4時間攪拌しプレポリマーを得た。その後、ジブチルスズジラウリレートをPCD4及びMDIの重量に対して100ppm加え、残存するNCO基に対してOH基が99%となるように1,4-ブタンジオールを加えた。80℃に昇温し攪拌しつつ、1時間ごとにサンプリングしGPCにて目標分子量になったところでエタノール0.1gを加え反応をクエンチしてエラストマー溶液を得た。得られたエラストマーの数平均分子量を測定した。測定結果を表3に示す。得られたエラストマー溶液をガラス板上又は白板上流延し、室温で5分間放置して養生した後、80℃の乾燥機に1時間入れて乾燥させてエラストマーフィルムを得た。得られたエラストマーフィルムを気温23℃湿度50%の環境で一週間養生し評価(耐汚染性及び耐熱性)に使用した。得られたエラストマーフィルム(TPU21)の特性を表3に示す。
ポリカーボネートジオールPCD4の替わりに、PCD8又はPCD9を用いた以外は、実施例16と同様にして、エラストマーフィルム得て各評価を行った。得られたエラストマーの数平均分子量及び得られたエラストマーフィルム(TPU22~TPU23)の特性を表3に示す。
ポリカーボネートジオールPCD4の替わりに、PCD14を用いた以外は、実施例16と同様にして、エラストマーフィルムを得て各評価を行った。得られたエラストマーの数平均分子量及び得られたエラストマーフィルム(TPU24)の特性を表3に示す。
Claims (10)
- 前記式(A)で表される繰り返し単位の割合が、0.1質量%以上50.0質量%以下である、請求項1に記載のポリカーボネートジオール。
- 前記式(B)におけるRの炭素数が3~6である、請求項3に記載のポリカーボネートジオール。
- 数平均分子量が300以上4,000以下である、請求項1~4のいずれか一項に記載のポリカーボネートジオール。
- 1級水酸基末端比率が90%以上である、請求項1~5のいずれか一項に記載のポリカーボネートジオール。
- 請求項1~6に記載のいずれか一項に記載のポリカーボネートジオールを含有する塗料組成物。
- 請求項1~6いずれか一項に記載のポリカーボネートジオールを用いて得られる水分散性ポリウレタンと、水とを含む、水性ポリウレタン分散体。
- 請求項8に記載の水性ポリウレタン分散体を含む水性塗料組成物。
- 請求項1~6に記載のいずれか一項に記載のポリカーボネートジオールとイソシアネート化合物とを反応させて得られるエラストマー。
Priority Applications (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP20767123.1A EP3936552B1 (en) | 2019-03-07 | 2020-02-20 | Polycarbonate diols and their uses |
| CN202080019441.XA CN113544189B (zh) | 2019-03-07 | 2020-02-20 | 聚碳酸酯二醇及其用途 |
| US17/436,391 US20220144997A1 (en) | 2019-03-07 | 2020-02-20 | Polycarbonate diols and their uses |
| JP2021503963A JP7089110B2 (ja) | 2019-03-07 | 2020-02-20 | ポリカーボネートジオール及びその用途 |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2019041555 | 2019-03-07 | ||
| JP2019-041555 | 2019-03-07 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2020179483A1 true WO2020179483A1 (ja) | 2020-09-10 |
Family
ID=72337920
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2020/006909 WO2020179483A1 (ja) | 2019-03-07 | 2020-02-20 | ポリカーボネートジオール及びその用途 |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US20220144997A1 (ja) |
| EP (1) | EP3936552B1 (ja) |
| JP (1) | JP7089110B2 (ja) |
| CN (1) | CN113544189B (ja) |
| WO (1) | WO2020179483A1 (ja) |
Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS63305127A (ja) * | 1987-05-21 | 1988-12-13 | バイエル・アクチエンゲゼルシヤフト | ポリエーテル−ポリカーボネートジオールおよびそれの製造方法並びに使用方法 |
| JPH0529648A (ja) | 1991-07-23 | 1993-02-05 | Sharp Corp | 光学装置 |
| JPH05186631A (ja) * | 1992-01-14 | 1993-07-27 | Asahi Chem Ind Co Ltd | 多孔性構造体およびその製造法 |
| JP2003113237A (ja) * | 2001-10-01 | 2003-04-18 | Kuraray Co Ltd | ポリカーボネートおよびそれを用いたポリウレタンの製造方法 |
| JP2005232447A (ja) * | 2004-01-22 | 2005-09-02 | Ube Ind Ltd | 液状ポリエーテルカーボネートジオール及び該ジオールをジオール成分に持つ熱可塑性ポリウレタン |
| JP2014136783A (ja) | 2013-01-18 | 2014-07-28 | Mitsubishi Chemicals Corp | ポリカーボネートジオールおよびその製造方法、並びにポリカーボネートジオールを用いたポリウレタン |
| JP2019041555A (ja) | 2017-08-29 | 2019-03-14 | 正毅 千葉 | 誘電エラストマートランスデューサー |
Family Cites Families (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR100568492B1 (ko) * | 2001-03-01 | 2006-04-07 | 아사히 가세이 가부시키가이샤 | 코폴리카보네이트 디올 및 이로부터 수득한 열가소성폴리우레탄 |
| WO2006088152A1 (ja) * | 2005-02-18 | 2006-08-24 | Asahi Kasei Chemicals Corporation | ポリカーボネートジオール |
| JP5186631B2 (ja) | 2009-12-16 | 2013-04-17 | 住友電気工業株式会社 | 被膜、切削工具および被膜の製造方法 |
| JP6544889B2 (ja) * | 2013-04-22 | 2019-07-17 | 三菱ケミカル株式会社 | ポリカーボネートジオールおよびその製造方法並びにそれを用いたポリウレタン |
| CN105378988B (zh) * | 2013-08-06 | 2017-09-22 | 第一工业制药株式会社 | 锂二次电池的电极用粘合剂、电极及锂二次电池 |
| JP6663200B2 (ja) * | 2015-10-07 | 2020-03-11 | 旭化成株式会社 | 水性ポリウレタン分散体 |
| JP6650244B2 (ja) * | 2015-10-22 | 2020-02-19 | 旭化成株式会社 | 塗料用硬化性組成物 |
| JP6752022B2 (ja) * | 2016-02-03 | 2020-09-09 | 旭化成株式会社 | ポリカーボネートジオール |
-
2020
- 2020-02-20 WO PCT/JP2020/006909 patent/WO2020179483A1/ja active Application Filing
- 2020-02-20 JP JP2021503963A patent/JP7089110B2/ja active Active
- 2020-02-20 EP EP20767123.1A patent/EP3936552B1/en active Active
- 2020-02-20 US US17/436,391 patent/US20220144997A1/en active Pending
- 2020-02-20 CN CN202080019441.XA patent/CN113544189B/zh active Active
Patent Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS63305127A (ja) * | 1987-05-21 | 1988-12-13 | バイエル・アクチエンゲゼルシヤフト | ポリエーテル−ポリカーボネートジオールおよびそれの製造方法並びに使用方法 |
| JPH0529648A (ja) | 1991-07-23 | 1993-02-05 | Sharp Corp | 光学装置 |
| JPH05186631A (ja) * | 1992-01-14 | 1993-07-27 | Asahi Chem Ind Co Ltd | 多孔性構造体およびその製造法 |
| JP2003113237A (ja) * | 2001-10-01 | 2003-04-18 | Kuraray Co Ltd | ポリカーボネートおよびそれを用いたポリウレタンの製造方法 |
| JP2005232447A (ja) * | 2004-01-22 | 2005-09-02 | Ube Ind Ltd | 液状ポリエーテルカーボネートジオール及び該ジオールをジオール成分に持つ熱可塑性ポリウレタン |
| JP2014136783A (ja) | 2013-01-18 | 2014-07-28 | Mitsubishi Chemicals Corp | ポリカーボネートジオールおよびその製造方法、並びにポリカーボネートジオールを用いたポリウレタン |
| JP2019041555A (ja) | 2017-08-29 | 2019-03-14 | 正毅 千葉 | 誘電エラストマートランスデューサー |
Non-Patent Citations (1)
| Title |
|---|
| See also references of EP3936552A4 |
Also Published As
| Publication number | Publication date |
|---|---|
| JP7089110B2 (ja) | 2022-06-21 |
| EP3936552B1 (en) | 2024-03-27 |
| CN113544189A (zh) | 2021-10-22 |
| EP3936552A4 (en) | 2022-03-16 |
| JPWO2020179483A1 (ja) | 2021-11-04 |
| US20220144997A1 (en) | 2022-05-12 |
| EP3936552A1 (en) | 2022-01-12 |
| CN113544189B (zh) | 2023-02-24 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5401320B2 (ja) | ポリウレタン樹脂 | |
| JP5710065B1 (ja) | 繊維、布帛、不織布、フィルム、シートおよび衣料 | |
| JP5068159B2 (ja) | ポリカーボネートジオール | |
| JP6663200B2 (ja) | 水性ポリウレタン分散体 | |
| JP6663199B2 (ja) | 水系ポリウレタン分散体 | |
| KR20030094269A (ko) | 코폴리카보네이트 디올 및 이로부터 수득한 열가소성폴리우레탄 | |
| JP5570043B2 (ja) | 乾燥速度が速くかつ耐性が改善されたソフトフィール塗料用硬化性組成物 | |
| JP6222101B2 (ja) | ポリエステルポリカーボネートポリオール | |
| JP6988369B2 (ja) | ウレタン樹脂組成物、及びそれを用いたウレタン樹脂成形物 | |
| JP5344852B2 (ja) | ポリカーボネートジオールを含有する硬化性塗料用組成物 | |
| JP7302174B2 (ja) | 高分岐ポリカーボネートポリオール組成物 | |
| JP2008303284A (ja) | 水系ポリウレタン分散体、およびそれを用いたソフトフィール塗料用水系分散体組成物 | |
| TW202112890A (zh) | 聚醚聚碳酸酯二醇及其製造方法 | |
| JP4969175B2 (ja) | コーティング剤組成物 | |
| JP2008037987A (ja) | 水性ポリウレタン組成物 | |
| JP5675011B1 (ja) | 1,4−ビス(イソシアナトメチル)シクロヘキサン、ポリイソシアネート組成物、ポリウレタン樹脂および成形品 | |
| JP7089110B2 (ja) | ポリカーボネートジオール及びその用途 | |
| JP2011190390A (ja) | コーティング剤組成物 | |
| JP2019214646A (ja) | ポリウレタン組成物 | |
| JP2013166852A (ja) | ポリカーボネートジオール | |
| EP3828215B1 (en) | Polyurea resin | |
| JP2019206661A (ja) | ポリウレタンウレア樹脂形成性組成物 | |
| JP2018035309A (ja) | 速硬化型ポリウレタン樹脂組成物 | |
| EP4342927A1 (en) | Polyurethane resin composition, cured product, artificial leather, synthetic leather, and surface treatment agent for leather |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 20767123 Country of ref document: EP Kind code of ref document: A1 |
|
| ENP | Entry into the national phase |
Ref document number: 2021503963 Country of ref document: JP Kind code of ref document: A |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2020767123 Country of ref document: EP |
|
| ENP | Entry into the national phase |
Ref document number: 2020767123 Country of ref document: EP Effective date: 20211007 |