WO2017073481A1 - ポジ型感光性樹脂組成物、感光性シート、硬化膜、層間絶縁膜、半導体保護膜、半導体装置の製造方法、半導体電子部品および半導体装置 - Google Patents
ポジ型感光性樹脂組成物、感光性シート、硬化膜、層間絶縁膜、半導体保護膜、半導体装置の製造方法、半導体電子部品および半導体装置 Download PDFInfo
- Publication number
- WO2017073481A1 WO2017073481A1 PCT/JP2016/081264 JP2016081264W WO2017073481A1 WO 2017073481 A1 WO2017073481 A1 WO 2017073481A1 JP 2016081264 W JP2016081264 W JP 2016081264W WO 2017073481 A1 WO2017073481 A1 WO 2017073481A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- resin composition
- alkali
- photosensitive resin
- film
- positive photosensitive
- Prior art date
Links
Images
Classifications
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/004—Photosensitive materials
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/004—Photosensitive materials
- G03F7/022—Quinonediazides
- G03F7/023—Macromolecular quinonediazides; Macromolecular additives, e.g. binders
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/004—Photosensitive materials
- G03F7/027—Non-macromolecular photopolymerisable compounds having carbon-to-carbon double bonds, e.g. ethylenic compounds
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/20—Exposure; Apparatus therefor
Definitions
- the present invention relates to a positive photosensitive resin composition.
- Polyimide resin has excellent heat resistance, electrical insulation, and mechanical properties. Therefore, surface protection films for semiconductor devices and inductor devices, interlayer insulation films, insulation layers and spacer layers for organic electroluminescence devices, thin film transistor substrates (TFT substrates) It is widely used for flattening layers, insulating layers of organic transistors, and the like.
- Patent Document 1 a photosensitive resin composition using a resin having a flexible aliphatic group in a molecular chain has been proposed so far.
- the aliphatic group has low chemical resistance and heat resistance when formed into a cured film, and when introduced excessively in the molecule, the sensitivity of the aliphatic group is reduced due to a decrease in solubility in an alkali developer. There was a problem of reduction and occurrence of tack and residue after development.
- Patent Document 4 a photosensitive resin composition using an acrylate compound as an additive for improving the mechanical properties and chemical resistance of a cured film has been proposed (for example, Patent Document 4).
- an object of the present invention is to provide a positive photosensitive resin composition having high elongation, high adhesion, and good sensitivity, resolution, and storage stability. .
- the positive photosensitive resin composition of the present invention has the following constitution. That is, (a) an alkali-soluble resin containing at least one selected from a polyimide precursor, a polybenzoxazole precursor, a polyamideimide precursor, a polyimide, and a copolymer thereof, and (b) a photoacid generator, (C) A positive photosensitive resin composition comprising a polyfunctional acrylate compound, wherein the (a) alkali-soluble resin has an aliphatic chain in the molecule.
- the present invention is a photosensitive sheet, a cured film, an interlayer insulating film, a semiconductor protective film, a semiconductor device manufacturing method, a semiconductor electronic component, and a semiconductor device using the positive resin composition.
- a positive photosensitive resin composition having good sensitivity, resolution, and storage stability can be obtained.
- a cured film having high elongation and high adhesion can be obtained.
- the resin composition of the present invention comprises (a) an alkali-soluble resin containing at least one selected from a polyimide precursor, a polybenzoxazole precursor, a polyamideimide precursor, a polyimide, and a copolymer thereof; and (b) light.
- a positive photosensitive resin composition comprising an acid generator and (c) a polyfunctional acrylate compound, wherein the (a) alkali-soluble resin has an aliphatic chain in the molecule.
- the aliphatic chain is an acid dianhydride residue or a diamine residue having a structural unit composed of an aliphatic organic group, and in order to impart flexibility to the alkali-soluble resin, a chain alkyl structure Or an alkyl ether structure.
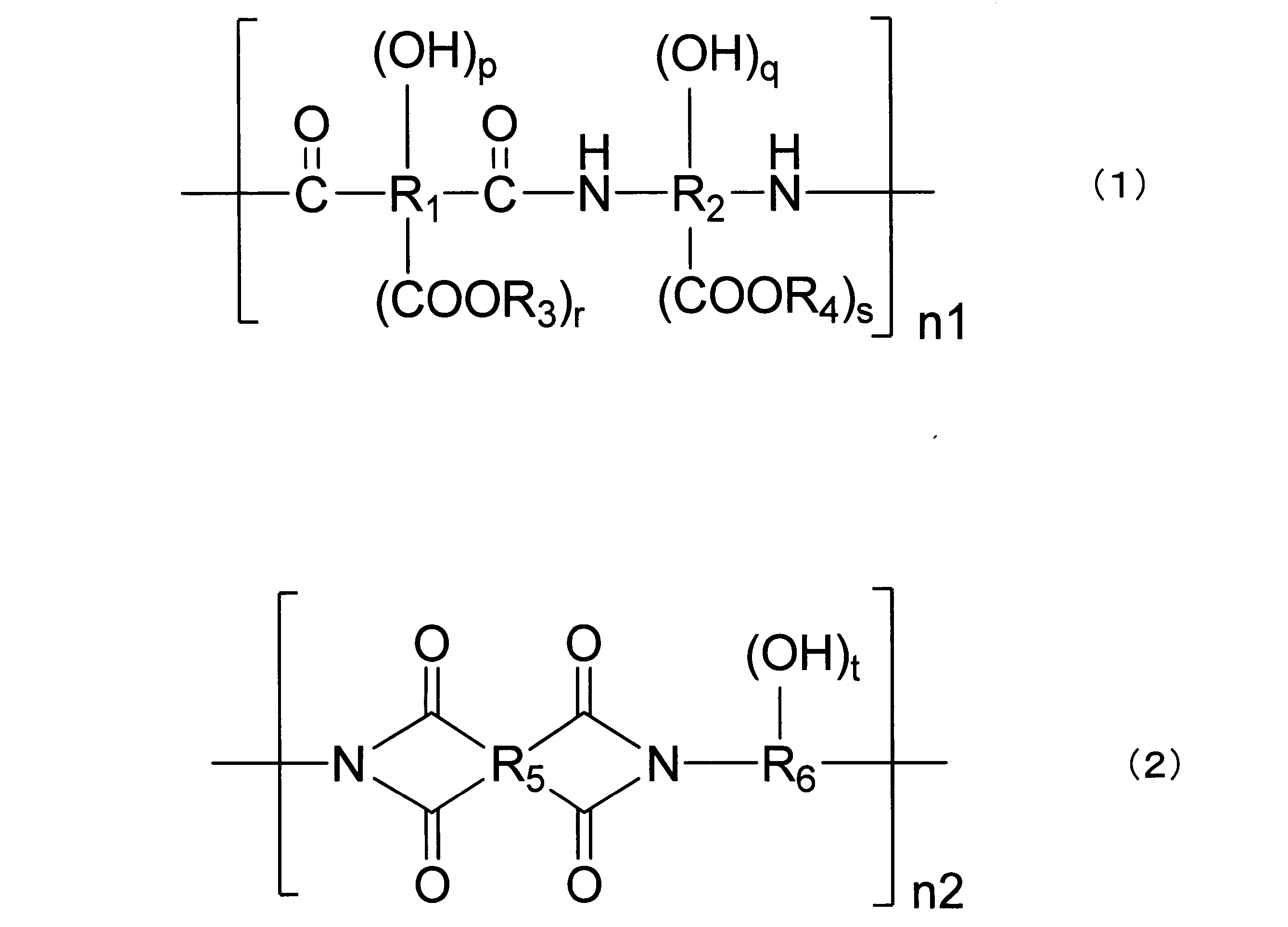
- the structural unit of the (a) alkali-soluble resin preferably has at least one of the general formulas (1) and (2).
- R 1 , R 2 , and R 6 represent a divalent to octavalent organic group having 2 to 200 carbon atoms.
- R 5 has 2 to 200 carbon atoms.
- R 3 and R 4 represent either hydrogen or an organic group having 1 to 20 carbon atoms
- n1 and n2 represent integers in the range of 10 to 100,000
- p, q , R, s, and t are integers satisfying 0 ⁇ p + r ⁇ 6, 0 ⁇ q + s ⁇ 6, and 0 ⁇ t ⁇ 6.
- R 1 and R 5 are organic groups derived from an acid dianhydride.
- acid dianhydride used in the present invention include pyromellitic dianhydride, 3,3 ′, 4,4′-biphenyltetracarboxylic dianhydride, 2,3,3 ′, 4'-biphenyltetracarboxylic dianhydride, 2,2 ', 3,3'-biphenyltetracarboxylic dianhydride, 3,3', 4,4'-benzophenone tetracarboxylic dianhydride, 2,2 ', 3,3'-benzophenonetetracarboxylic dianhydride, 2,2-bis (3,4-dicarboxyphenyl) propane dianhydride, 2,2-bis (2,3-dicarboxyphenyl) propane Anhydride, 1,1-bis (3,4-dicarboxyphenyl) ethane dianhydride, 1,1-bis (2,3-dicarboxyphenyl) ethane dianhydride, bis (3,4-dicarboxyphen
- R 2 and R 6 are organic groups derived from diamine.
- the diamine used in the present invention preferably contains an aliphatic organic group. It is preferable that the aliphatic organic group has a polyether block structural unit represented by the general formula (3).
- R 7 to R 10 each independently represents an alkylene group having 1 to 6 carbon atoms
- R 11 to R 18 each independently represents hydrogen, fluorine, or an alkyl group having 1 to 6 carbon atoms, provided that The structures represented in parentheses are different, and x, y, and z each independently represent an integer of 0 to 35.
- Specific examples of the compound containing an organic group having a polyether block structural unit include “Jeffamine (registered trademark)” HK-511, ED-600, ED-900, ED-2003, EDR-148, EDR-176.
- a polyether structure is preferable because flexibility is imparted, and thus the degree of elongation of the cured film and the adhesion to the substrate are improved, and the elastic modulus is lowered, so that the warpage of the substrate is suppressed. These characteristics are effective in multilayer processing and thick film processing.
- the polyether block structural unit represented by the general formula (3) is 10 mol% or more when R 2 and R 6 in the structure represented by the general formulas (1) and (2) are 100 mol%. High elongation is obtained by imparting flexibility to the resin, and if it is 80 mol% or less, it is preferable from the viewpoint that an appropriate dissolution rate in the developer can be obtained, and more preferably 10 to 40 mol% is contained. preferable.
- R 2 and R 6 may contain a structure derived from a diamine other than a compound containing an organic group having a polyether structure.
- diamines other than compounds containing an organic group having a polyether structure include bis (3-amino-4-hydroxyphenyl) hexafluoropropane, bis (3-amino-4-hydroxyphenyl) sulfone, bis ( 3-amino-4-hydroxyphenyl) propane, bis (3-amino-4-hydroxyphenyl) methylene, bis (3-amino-4-hydroxyphenyl) ether, bis (3-amino-4-hydroxy) biphenyl, bis Hydroxyl group-containing diamines such as (3-amino-4-hydroxyphenyl) fluorene, sulfonic acid-containing diamines such as 3-sulfonic acid-4,4′-diaminodiphenyl ether, thiol group-containing diamines such as dimercaptophenylenediamine, 3, 4'-di
- an aliphatic group having a siloxane structure may be copolymerized within a range where the heat resistance is not lowered, and the adhesion to the substrate can be improved.
- the diamine component include those obtained by copolymerizing 1 to 15 mol% of bis (3-aminopropyl) tetramethyldisiloxane, bis (p-aminophenyl) octamethylpentasiloxane, and the like.
- an aromatic diamine in an amount of 50 mol% or more of the total diamine.
- resin which has at least any one of the structural unit represented by General formula (1) and (2) has a phenolic hydroxyl group component.
- R 1 and R 2 is an organic group having a phenolic hydroxyl group.
- the phenolic hydroxyl group can be appropriately dissolved in an alkali developer, and can interact with the photosensitizer to suppress the solubility of the unexposed area, thereby improving the remaining film ratio and increasing the sensitivity.
- the phenolic hydroxyl group also contributes to the reaction with the cross-linking agent, and thus is preferable in that high mechanical properties and chemical resistance can be obtained.
- aromatic dianhydrides such as acid dianhydrides having an amide group, bis (3-amino-4-hydroxyphenyl) hexafluoropropane, bis (3-amino-4-hydroxyphenyl) sulfone, bis ( 3-amino-4-hydroxyphenyl) propane, bis (3-amino-4-hydroxyphenyl) methylene, bis (3-amino-4-hydroxyphenyl) ether, bis (3-amino-4-hydroxy) biphenyl, bis Hydroxyl group-containing diamines such as (3-amino-4-hydroxyphenyl) fluorene, Alkyl group or a fluoroalkyl group et aromatic ring part having a carbon number of 1
- the resin having the structure represented by the general formulas (1) and (2) is preferably a resin including a structure derived from these compounds. These phenolic hydroxyl group-containing compounds are preferably used in an amount of 10 to 90 mol% of the acid dianhydride component or diamine component in the resin having the structure represented by the general formulas (1) and (2). . By setting the content of the compound having a phenolic hydroxyl group within this range, moderate solubility in an alkali developer can be obtained.
- n1 and n2 represent the degree of polymerization.
- the degree of polymerization n Mw / M.
- the number average molecular weight of the alkali-soluble resin is determined by GPC (gel permeation chromatography) as described in Examples.
- the photosensitive resin composition of the present invention has positive photosensitivity by containing (b) a photoacid generator. That is, the photoacid generator has a characteristic that an acid is generated by light irradiation, and the solubility of the light irradiation portion in an alkaline aqueous solution is increased.
- a quinonediazide compound is mentioned as a photo-acid generator.
- the quinonediazide compound is a compound in which a sulfonic acid of quinonediazide is bonded to a polyhydroxy compound with an ester, a sulfonic acid of quinonediazide is bonded to a polyamino compound in a sulfonamide, and a sulfonic acid of quinonediazide is bonded to a polyhydroxypolyamino compound in an ester bond and / or sulfonamide. Examples include those that are combined.
- All functional groups of these polyhydroxy compounds and polyamino compounds may not be substituted with quinonediazide. It is preferable that 50 mol% or more of the entire functional groups are substituted with quinonediazide. When the substitution with quinonediazide is 50 mol% or more, the solubility in an alkali developer is not excessively high, a contrast with an unexposed portion is obtained, and a desired pattern can be obtained.
- a positive photosensitive resin composition that is sensitive to i-line (365 nm), h-line (405 nm), and g-line (436 nm) of a mercury lamp that is a general ultraviolet ray. it can.
- the quinonediazide compound may be used alone or in combination of two or more.
- polyhydroxy compound used for the quinonediazide compound examples include Bis-Z, BisP-EZ, TekP-4HBPA, TrisP-HAP, TrisP-PA, TrisP-SA, TrisOCR-PA, BisOCHP-Z, BisP-MZ.
- polyamino compound used for the quinonediazide compound examples include 1,4-phenylenediamine, 1,3-phenylenediamine, 4,4′-diaminodiphenyl ether, 4,4′-diaminodiphenylmethane, and 4,4′-diamino. Examples thereof include diphenyl sulfone and 4,4′-diaminodiphenyl sulfide.
- the polyamino compound used for the quinonediazide compound is not limited to these.
- polyhydroxypolyamino compound used for the quinonediazide compound examples include 2,2-bis (3-amino-4- hydroxyphenyl) hexafluoropropane and 3,3′-dihydroxybenzidine.
- the polyhydroxypolyamino compound used for the quinonediazide compound is not limited to these.
- quinonediazide is preferably a 5-naphthoquinonediazidesulfonyl group or a 4-naphthoquinonediazidesulfonyl group.
- 4-Naphthoquinonediazide sulfonyl ester compounds have absorption in the i-line region of mercury lamps and are suitable for i-line exposure.
- the 5-naphthoquinone diazide sulfonyl ester compound has an absorption extending to the g-line region of a mercury lamp and is suitable for g-line exposure.
- a naphthoquinone diazide sulfonyl ester compound can be obtained by using a 4-naphthoquinone diazide sulfonyl group and a 5-naphthoquinone diazide sulfonyl group in the same molecule, or a 4-naphthoquinone diazide sulfonyl ester compound and a 5-naphthoquinone diazide sulfonyl ester compound. Can also be used as a mixture.
- the molecular weight of the quinonediazide compound of the present invention is preferably 300 to 3,000.
- the molecular weight of the quinonediazide compound of the present invention is synthesized from a phenol compound by the following method. For example, there is a method in which 5-naphthoquinonediazide sulfonyl chloride and a phenol compound are reacted in the presence of triethylamine. Examples of the method for synthesizing a phenol compound include a method in which an ⁇ - (hydroxyphenyl) styrene derivative is reacted with a polyhydric phenol compound under an acid catalyst.
- the quinonediazide compound of the present invention is preferably a sulfonium salt, a phosphonium salt or a diazonium salt in order to stabilize the acid component generated by exposure.
- the resin composition obtained from the photosensitive resin composition of the present invention is used as a permanent film, it is environmentally undesirable for phosphorus and the like to remain, and it is necessary to consider the color tone of the film.
- a triarylsulfonium salt which can significantly improve the standing stability after exposure.
- a triarylsulfonium salt represented by the general formula (5) is particularly preferred.
- R 23 indicating any organic group or different and the same respectively wherein R 22 is hydrogen or 1 to 20 carbon atoms is an organic group of from 1 to 20 carbon atoms.
- a, b, and c are each an integer from 0 to 5.
- a quinonediazide compound and a sulfonium salt, phosphonium salt or diazonium salt may be used in combination of two or more.
- the content of the photoacid generator used in the present invention is preferably 0.01 to 50 parts by mass with respect to 100 parts by mass of the resin having a structure represented by the general formula (1) and / or (2).
- the quinonediazide compound is preferably in the range of 3 to 40 parts by mass.
- the total number of compounds selected from sulfonium salts, phosphonium salts, and diazonium salts is 0%.
- the range of 05 to 40 parts by mass is preferable, and the range of 0.1 to 30 parts by mass is more preferable.
- the positive photosensitive resin composition of the present invention contains (c) a polyfunctional acrylate compound.
- the acrylate compound refers to a compound having an acryloyl group or a methacryloyl group.
- acrylic acid ester, methacrylic acid ester, acrylamide, methacrylamide, etc. can be mentioned.
- the polyfunctional acrylate compound refers to a compound having two or more acryloyl groups and / or methacryloyl groups.
- the positive photosensitive resin composition of the present invention is heat-treated after pattern processing.
- the polyfunctional acrylate compound reacts with an acrylate compound by thermal polymerization or an alkali-soluble resin and crosslinks, whereby the elongation of the cured film is improved.
- a monofunctional acrylate compound curing of the film by the crosslinking reaction does not proceed sufficiently, and the effect of improving the elongation is low, so that it is preferably a polyfunctional acrylate.
- “Blemmer (registered trademark)” series manufactured by NOF Corporation GMR-H, GAM, PDE-50, PDE-100, PDE-150, PDE-200, PDE-400, PDE-600, PDE-1000, ADE-200, ADE-400, PDP-400, ADP-200, ADP-400, PDT-650, ADT-250, PDBE-200, PDBE-250, PDBE-450, PDBE-1300, ADBE-200, ADBE- 250, ADBE-450 and the like.
- MBAA manufactured by MRC Unitech Co., Ltd. can be mentioned. You may contain 2 or more types of these compounds.
- acrylate compounds having a molecular weight of 100 or more and 2000 or less are preferable.
- the molecular weight is 100 or more, a highly stretched cured film can be obtained, and when it is 2000 or less, a resin composition having moderate alkali solubility and high compatibility with an alkali-soluble resin can be obtained.
- the acrylate compound which has a polyether block structural unit represented by General formula (4) among the said acrylate compounds is preferable.
- R 19 is an alkyl group having 1 to 6 carbon atoms.
- R 20 and R 21 each independently represents hydrogen, fluorine, or an alkyl group having 1 to 6 carbon atoms.
- N3 is an integer of 1 to 40. Represents.
- These polyfunctional acrylate compounds preferably have 2 to 6 acryloyl groups or methacryloyl groups. Even if it has two or more of either acryloyl group or methacryloyl group, it may have both acryloyl group and methacryloyl group, and the total of these may be 2 to 6.
- the acrylate compounds react with each other by thermal polymerization or an alkali-soluble resin during the heat treatment after pattern processing to form a network structure.
- the content of the polyfunctional acrylate compound is preferably 1 to 50 parts by mass with respect to 100 parts by mass of the (a) alkali-soluble resin, and more preferably 1 from the viewpoint of solubility in alkali. From 20 to 20 parts by weight. If content of an acrylate compound is 1 weight part or more, elongation will improve. If it is 50 parts by weight or less, moderate alkali solubility is maintained, and the storage stability of the resulting composition is improved. Furthermore, if it is 20 parts by weight or less, stable sensitivity can be obtained regardless of the standing time from exposure to development.
- the alkali solubility of the resin composition is increased and the residue in the exposed area is reduced, so that a highly sensitive and high resolution resin composition can be obtained.
- the alkali dissolution rate of the alkali-soluble resin is preferably 100 to 4,000 nm / min with respect to a 2.38% tetramethylammonium (TMAH) aqueous solution.
- the alkali solubility is 100 nm / min or more, it is preferable because a positive pattern can be formed by dissolving the exposed portion during development, and if it is 4,0000 nm / min or less, the unexposed portion after development is This is preferable because the remaining film ratio is high and a pattern with a thick film structure can be formed.
- a dissolution rate of 100 to 20,000 nm / min is more preferable in that a cured film having a higher elongation can be obtained because the amount of the acrylate compound added can be increased, and the contrast between the exposed and unexposed areas is further improved. In order to increase the speed, it is more preferably 100 to 10000 nm / min.
- the alkali-soluble resin of component (a) in addition to the alkali-soluble resin of component (a), it is preferable to contain (d) an alkali-soluble phenol resin as long as the heat resistance of the cured film obtained by heat treatment is not impaired.
- the alkali-soluble phenol resin include phenol novolak resin, cresol novolak resin, resole resin, polyhydroxystyrene, and resins obtained by introducing a cross-linking group such as methylol group, alkoxymethyl group or epoxy group, and copolymerization thereof. Examples thereof include polymers.
- the content thereof is preferably 150 parts by mass or less, more preferably 100 parts by mass or less, with respect to 100 parts by mass of the total amount of the alkali-soluble resin of component (a). More preferably, it is 50 parts by mass or less.
- the dissolution rate of the resin composition of (d) the alkali-soluble phenol resin and the alkali-soluble resin of the component (a) is 100 to 20,000 nm. Therefore, the dissolution rate of the (d) alkali-soluble phenol resin is preferably 100 to 20,000 nm / min.
- the (a) alkali-soluble resin of the present invention preferably has an organic group having an unsaturated bond at the terminal.
- the crosslink density is increased by thermal polymerization with alkali-soluble resins or the polyfunctional acrylate compound of component (c) during heat treatment, and the elongation, heat resistance, and chemical resistance are increased. High cured film is obtained.
- Such an alkali-soluble resin can be obtained by end-capping with a monoamine, an acid anhydride, an acid chloride, a monocarboxylic acid or the like having an organic group having an unsaturated bond at the end.
- the end-capping agent having an organic group having an unsaturated bond include monoamines such as 3-aminophenylacetylene, 4-aminophenylacetylene, 3,5-diethynylaniline, 3-ethynylbenzoic acid, Monocarboxylic acids such as 4-ethynylbenzoic acid, 3,4-diethynylbenzoic acid, 3,5-diethynylbenzoic acid, maleic anhydride, acid anhydrides such as 5-norbornene-2,3-dicarboxylic anhydride, Compound obtained by acid chloride conversion of carboxyl group of monocarboxylic acid, compound obtained by acid chloride conversion of one carboxyl group of dicarboxylic acid such as maleic acid, mono acid
- end-capping agents having no unsaturated bond may be used.
- the end-capping agent is preferably used in an amount of 0.1 to 60 mol%, more preferably 5 to 50 mol%, based on the total acid or total amine component of the resin.
- the content of 50 mol% or less is preferable because a cured film having sufficient mechanical properties can be obtained, and the content of 5 mol% or more is preferable because the effect of the end-capping agent as described above can be obtained.
- the weight average molecular weight of the alkali-soluble resin (a) and the phenol resin (d) is preferably 3,000 to 80,000, more preferably 8,000 to 50 in terms of polystyrene by gel permeation chromatography. , 000. If it is this range, a thick film can be formed easily.
- the resin having the structure represented by the general formulas (1) and (2) can be produced according to a known polyimide precursor and a method for producing a polyimide and a polybenzoxazole precursor.
- a method for reacting a tetracarboxylic dianhydride having an R 1 group with a diamine compound having an R 2 group and a monoamino compound as a terminal blocking agent under low temperature conditions (II) an R 1 group A diester obtained by having a tetracarboxylic dianhydride and an alcohol, and then reacting in the presence of a diamine compound having an R 2 group, a monoamino compound as a terminal blocking agent and a condensing agent, (III) R 1 group Examples include a method in which a diester is obtained from a tetracarboxylic dianhydride having an alcohol and an alcohol, and then the remaining two carboxyl groups are acid chlorideed and reacted with a diamine compound having an R 2 group and
- a diamine compound having an R 2 group is dissolved in a polymerization solvent.
- a tetracarboxylic dianhydride having an R 1 group in a substantially equimolar amount with the diamine compound is gradually added.
- the mixture is stirred at ⁇ 20 to 100 ° C., preferably 10 to 50 ° C. for 0.5 to 100 hours, more preferably 2 to 24 hours.
- an end-capping agent after adding tetracarboxylic dianhydride, stirring at the required temperature and time, the end-capping agent may be added gradually or added all at once to react. You may let them.
- the polymerization solvent is not particularly limited as long as it can dissolve the raw material monomers tetracarboxylic dianhydride and diamine.
- the reaction can be performed without precipitation of raw materials and resins, and if it is 1900 parts by mass or less, the reaction proceeds promptly, 150 to 950 parts by mass is more preferable.
- a compound having a phenolic hydroxyl group may be contained as long as the shrinkage after curing is not reduced.
- the compound having a phenolic hydroxyl group is, for example, Bis-Z, BisOC-Z, BisOPP-Z, BisP-CP, Bis26X-Z, BisOTBP-Z, BisOCHP-Z, BisOCR-CP, BisP-MZ, BisP-EZ Bis26X-CP, BisP-PZ, BisP-IPZ, BisCR-IPZ, BisOCP-IPZ, BisOIPP-CP, Bis26X-IPZ, BisOTBP-CP, TekP-4HBPA (Tetrakis P-DO-BPA), TrisP-HAP, TrisP -PA, TrisP-SA, TrisOCR-PA, BisOFP-Z, BisRS-2P, BisPG-26X, BisRS-3P, BisOC-OCHP, BisPC-OCHP, Bis25X-OCHP, Bis 6X-OCHP, BisOCHP-OC, Bis236T-OCHP, Methylenetris-FR-CR, BisRS-26X, BisRS-OCHP (above,
- preferred compounds having a phenolic hydroxyl group used in the present invention include, for example, Bis-Z, BisP-EZ, TekP-4HBPA, TrisP-HAP, TrisP-PA, BisOCHP-Z, BisP-MZ, BisP-PZ. , BisP-IPZ, BisOCP-IPZ, BisP-CP, BisRS-2P, BisRS-3P, BisP-OCHP, Methylenetris-FR-CR, BisRS-26X, BIP-PC, BIR-PC, BIR-PTBP, BIR- BIPC-F etc. are mentioned.
- particularly preferred compounds having a phenolic hydroxyl group are, for example, Bis-Z, TekP-4HBPA, TrisP-HAP, TrisP-PA, BisRS-2P, BisRS-3P, BIR-PC, BIR-PTBP, BIR-BIPC -F.
- the obtained resin composition is hardly dissolved in an alkali developer before exposure, and is easily dissolved in an alkali developer upon exposure. Development is easy in a short time.
- the content of the compound having a phenolic hydroxyl group is preferably 1 to 50 parts by mass, more preferably 3 to 40 parts by mass with respect to 100 parts by mass of the (a) alkali-soluble resin.
- the positive photosensitive resin composition of the present invention contains a solvent.
- Solvents such as N-methyl-2-pyrrolidone, ⁇ -butyrolactone, N, N-dimethylformamide, N, N-dimethylacetamide, N, N-dimethylformamide, N, N-dimethylisobutyric acid amide, dimethyl sulfoxide, etc.
- Aprotic solvents tetrahydrofuran, dioxane, propylene glycol monomethyl ether, ethers such as diethylene glycol ethyl methyl ether, ketones such as acetone, methyl ethyl ketone, diisobutyl ketone, diacetone alcohol, propylene glycol monomethyl ether acetate, 3-methoxymethyl pro
- esters such as panate, 3-ethoxyethylpropanate, ethyl acetate and ethyl lactate, and aromatic hydrocarbons such as toluene and xylene. Two or more of these may be contained.
- a photosensitive resin composition having an appropriate viscosity is preferable.
- the photosensitive resin composition having positive photosensitivity of the present invention may contain components other than those described above, and preferably contains a compound having an alkoxymethyl group, a methylol group, or an epoxy group as a crosslinking agent. . Since a methylol group and an alkoxymethyl group cause a crosslinking reaction in a temperature range of 100 ° C. or higher, they can be crosslinked by heat treatment to obtain a heat-resistant resin film having excellent mechanical properties.
- the content of the compound having an alkoxymethyl group or a methylol group is preferably 10 to 500 parts by mass with respect to 100 parts by mass of the (c) polyfunctional acrylate compound.
- the epoxy group is thermally cross-linked with the polymer at 200 ° C. or lower and does not cause a film shrinkage because no dehydration reaction occurs due to the cross-linking. Therefore, in addition to mechanical properties, it is effective for low-temperature curing and low warpage.
- the compound having an epoxy group as described above, has high reactivity, there is a risk of lowering the room temperature storage stability and sensitivity of the resin composition. Therefore, the content of the compound having an epoxy group is (c) It is desirable that it is 100 mass parts or less with respect to 100 mass parts of polyfunctional acrylate compounds.
- Examples having an alkoxymethyl group or a methylol group include, for example, DML-PC, DML-PEP, DML-OC, DML-OEP, DML-34X, DML-PTBP, DML-PCHP, DML-OCHP, DML-PFP, DML-PSBP, DML-POP, DML-MBOC, DML-MBPC, DML-MTrisPC, DML-BisOC-Z, DML-BisOCHP-Z, DML-BPC, DML-BisOC-P, DMOM-PC, DMOM-PTBP, DMOM-MBPC, TriML-P, TriML-35XL, TML-HQ, TML-BP, TML-pp-BPF, TML-BPE, TML-BPA, TML-BPAF, TML-BPAP, TMOM-BP, TMOM-BPE, TMOM-BPA, TM M-BPAF, TMOM-BPAP, HML-TPPHBA,
- Examples of the compound having an epoxy group include bisphenol A type epoxy resin, bisphenol F type epoxy resin, propylene glycol diglycidyl ether, polypropylene glycol diglycidyl ether, polymethyl (glycidyloxypropyl) siloxane, and the like, silicone And so on.
- the present invention is not limited to these.
- Epicron 850-S Epicron HP-4032, Epicron HP-7200, Epicron HP-820, Epicron HP-4700, Epicron EXA-4710, Epicron HP-4770, Epicron EXA-859CRP, Epicron EXA-1514, Epicron EXA-4880, Epicron EXA-4850-150, Epicron EXA-4850-1000, Epicron EXA-4816, Epicron EXA-4822 (named above, manufactured by Dainippon Ink & Chemicals, Inc.), Jamaica Resin BEO-60E Trade names, Shin Nippon Chemical Co., Ltd.), EP-4003S, EP-4000S (Adeka Co., Ltd.)
- These compounds having an alkoxymethyl group, a methylol group, or an epoxy group may be contained in two or more kinds.
- the photosensitive resin composition of the present invention can further contain a silane compound.
- a silane compound By containing the silane compound, the adhesion of the heat-resistant resin film is improved.
- the silane compound include N-phenylaminoethyltrimethoxysilane, N-phenylaminoethyltriethoxysilane, N-phenylaminopropyltrimethoxysilane, N-phenylaminopropyltriethoxysilane, N-phenylaminobutyltri Methoxysilane, N-phenylaminobutyltriethoxysilane, vinyltrimethoxysilane, vinyltriethoxysilane, vinyltrichlorosilane, vinyltris ( ⁇ -methoxyethoxy) silane, 3-methacryloxypropyltrimethoxysilane, 3-acryloxypropyltri Examples include methoxysilane, p-styryltrimethoxysilane,
- the photosensitive resin composition having positive photosensitivity of the present invention is optionally provided with a surfactant, an ester such as ethyl lactate or propylene glycol monomethyl ether acetate for the purpose of improving the wettability with the substrate.
- a surfactant such as ethanol, ketones such as cyclohexanone and methyl isobutyl ketone, and ethers such as tetrahydrofuran and dioxane.
- inorganic particles such as silicon dioxide and titanium dioxide, or polyimide powder may be contained for the purpose of suppressing the thermal expansion coefficient, increasing the dielectric constant, and reducing the dielectric constant.
- the viscosity of the positive photosensitive resin composition is preferably 1 to 10,000 mPa ⁇ s.
- the photosensitive resin composition may be filtered through a filter having a pore size of 0.1 ⁇ m to 5 ⁇ m.
- the photosensitive resin composition of the present invention can be formed into a polyimide pattern through a step of coating and drying on a support substrate, a step of exposing, a step of developing, and a step of heat treatment.
- a photosensitive resin composition is applied on a substrate.
- a silicon wafer, ceramics, gallium arsenide, metal, glass, metal oxide insulating film, silicon nitride, ITO, or the like is used as the substrate.
- the substrate is not limited to these.
- the coating method include spin coating using a spinner, spray coating, roll coating, and slit die coating.
- the coating film thickness varies depending on the coating method, the solid content concentration of the positive photosensitive resin composition, the viscosity, and the like. In general, coating is performed so that the film thickness after drying is 0.1 to 150 ⁇ m.
- the substrate coated with the photosensitive resin composition is dried to obtain a photosensitive resin film. Drying is preferably performed using an oven, a hot plate, infrared rays, or the like in the range of 50 ° C. to 150 ° C. for 1 minute to several hours.
- actinic radiation is irradiated on the photosensitive resin film through a mask having a desired pattern.
- actinic rays used for exposure include ultraviolet rays, visible rays, electron beams, and X-rays.
- the exposed portion may be removed using a developer after exposure.
- Developer is tetramethylammonium, diethanolamine, diethylaminoethanol, sodium hydroxide, potassium hydroxide, sodium carbonate, potassium carbonate, triethylamine, diethylamine, methylamine, dimethylamine, dimethylaminoethyl acetate, dimethylaminoethanol, dimethylaminoethyl methacrylate
- An aqueous solution of a compound exhibiting alkalinity, such as cyclohexylamine, ethylenediamine, and hexamethylenediamine is preferred.
- polar aqueous solutions such as N-methyl-2-pyrrolidone, N, N-dimethylformamide, N, N-dimethylacetamide, dimethyl sulfoxide, ⁇ -butyrolactone, dimethylacrylamide, methanol, ethanol, isopropanol are used in these alkaline aqueous solutions.
- alcohols such as ethyl lactate, esters such as propylene glycol monomethyl ether acetate, ketones such as cyclopentanone, cyclohexanone, isobutyl ketone, and methyl isobutyl ketone may be added.
- Rinsing with water is common after development.
- one or more alcohols such as ethanol and isopropyl alcohol
- esters such as ethyl lactate, propylene glycol monomethyl ether acetate, and 3-methoxymethylpropanoate may be added to water.
- the positive photosensitive resin composition of the present invention is a resin composition that can obtain high elongation and high adhesion even at low temperature treatment of 250 ° C. or lower.
- 220 examples thereof include a method of heat treatment at 1 ° C. for 1 hour, a method of linearly raising the temperature from room temperature to 220 ° C. over 1 hour, and heat treating at 220 ° C. for 1 hour.
- the photosensitive resin composition produced as described above is applied onto a substrate, the organic solvent is removed, and a photosensitive sheet is produced.
- PET Polyethylene terephthalate
- a PET film whose surface is coated with a release agent such as a silicone resin is used.
- the photosensitive sheet and the PET film can be easily peeled off, which is preferable.
- the photosensitive resin composition onto the PET film screen printing, spray coater, bar coater, blade coater, die coater, spin coater, or the like can be used.
- the method for removing the organic solvent include heating with an oven or a hot plate, vacuum drying, heating with an electromagnetic wave such as infrared rays or microwaves, and the like.
- the removal of the organic solvent is insufficient, the cured product obtained by the next curing treatment may be in an uncured state or may have poor thermomechanical properties.
- the thickness of the PET film is not particularly limited. From the viewpoint of workability, it is preferably in the range of 30 to 80 ⁇ m. In order to protect the surface of the photosensitive sheet from dust in the atmosphere, a cover film may be bonded to the surface. Moreover, when the solid content concentration of the photosensitive resin composition is low and a photosensitive sheet having a desired film thickness cannot be produced, two or more photosensitive sheets after removal of the organic solvent may be bonded together.
- the photosensitive sheet bonded to the substrate through a mask having a desired pattern is irradiated with actinic radiation and developed. After removing the exposed portion using a liquid, a temperature of 100 ° C. to 400 ° C. is applied to convert it to a heat resistant resin film.
- the heat-resistant resin film formed from the photosensitive resin composition of the present invention can be used for electronic parts such as semiconductor devices and multilayer wiring boards.
- TFT substrate thin film transistor substrate
- the present invention is not limited to this, and can have various structures.
- FIG. 1 is an enlarged cross-sectional view of a pad portion of a semiconductor device having an insulating film of the present invention.
- a passivation film 3 is formed on an input / output Al pad 2 in a silicon wafer 1, and a via hole is formed in the passivation film 3.
- an insulating film 4 is formed as a pattern made of the photosensitive resin composition of the present invention, and a metal (Cr, Ti, etc.) film 5 is formed so as to be connected to the Al pad 2.
- a metal wiring 6 is formed thereon.
- a high-density and high-performance semiconductor device can be manufactured without increasing the chip area. Thereafter, the barrier metal 8 and the solder bump 10 are formed in the opening of the insulating film 7.
- FIG. 2 is an enlarged cross-sectional view of a pad portion of a semiconductor device having an insulating film according to the present invention.
- the silicon wafer 1 on which the Al pad 2 and the passivation film 3 are formed is diced, cut into chips, and sealed with a sealing resin 11.
- an insulating film 4 is formed as a pattern of the photosensitive resin composition of the present invention, and further, a metal (Cr, Ti, etc.) film 5, a metal wiring (Al, Cu, etc.) 6. Is formed.
- a barrier metal 8 and a solder bump 10 are formed in the opening of the insulating film 7 formed on the sealing resin 11 outside the chip.
- FIG. 3 is a cross-sectional view of a coil component having an insulating film of the present invention.
- an insulating film 13 is formed on the substrate 12, and an insulating film 14 is formed thereon as a pattern.
- the photosensitive resin composition of the present invention may be used for either the insulating film 13 or the insulating film 14.
- a metal (Cr, Ti, etc.) film 15 is formed in the opening of this pattern, and a metal wiring (Ag, Cu, etc.) 16 is formed thereon by plating.
- the metal wiring 16 (Ag, Cu, etc.) is formed on the spiral. By repeating the steps 13 to 16 a plurality of times and laminating, the function as a coil can be provided. Finally, the metal wiring (Ag, Cu, etc.) 16 is connected to the electrode 18 by the metal wiring (Ag, Cu, etc.) 17 and sealed with the sealing resin 19.
- the warpage of the wafer is small, exposure and transportation of the wafer can be performed with high accuracy. This is particularly useful when the number of stacked insulating films and wiring layers is increased as in the devices of FIGS.
- a highly durable semiconductor device can be provided.
- the photosensitive resin composition for forming the insulating film 4 and the insulating film 7 in the apparatus as shown in FIG. 1 is processed with a thick film on the scribe line 9, so that the sensitivity is higher and there is no residue in the exposed area. Desirable resin compositions are desirable.
- the insulating film 4 is formed over the silicon wafer and the sealing resin.
- a flexible skeleton is introduced into the photosensitive resin composition and the acrylate compound, a highly stretched film can be obtained, so that stress due to thermal expansion of the sealing resin and twisting of the substrate can be reduced.
- the photosensitive resin composition with small curvature is desirable. From these points, the photosensitive resin composition of the present invention is useful in the apparatus as shown in FIGS.
- the molecular weight of the alkali-soluble resin as component (a) was measured using a GPC (gel permeation chromatography) apparatus Waters 2690-996 (manufactured by Nippon Waters Co., Ltd.), and the developing solvent was N-methyl-2-pyrrolidone.
- the weight average molecular weight (Mw) was calculated in terms of polystyrene.
- Peeling was performed with a 46% by mass hydrofluoric acid aqueous solution to obtain a cured film (heat resistant resin film).
- the cured film obtained by this method was cut out with a single blade so as to be 7 ⁇ 1 cm, and this was pulled at 50 mm / min with a Tensilon universal testing machine (RTM-100 manufactured by Orientec Co., Ltd.). A value obtained by dividing the amount of elongation at this time by the sample length was obtained. This measurement was performed on 10 samples, and the maximum value was defined as the elongation.
- the elongation is preferably 30% or more, and more preferably 60% or more.
- Adhesion evaluation with silicon wafer A varnish is applied on a silicon wafer using a spinner so that the film thickness after pre-baking is 10 ⁇ m, and then a hot plate (coating and developing apparatus D manufactured by Tokyo Electron Co., Ltd.) -SPIN) was used for pre-baking at 120 ° C. for 3 minutes to obtain a photosensitive resin film.
- the prepared photosensitive resin film was heated at 110 ° C. for 30 minutes under a nitrogen stream (oxygen concentration of 20 ppm or less), then heated to 220 ° C. at a rate of 3.5 ° C. per minute, and heat-treated at 220 ° C. for 1 hour.
- a heat-resistant resin film cured film.
- the cured film was cut into a grid with a cutter, 10 ⁇ 10 squares were made, and a peeling test was performed using “Cellotape (registered trademark)”. If there was no peeling in the peeling test, A was given, B was given if slight peeling, and C was given if much peeling was observed.
- Varnish was spin-coated on an 8-inch silicon wafer, and then baked for 3 minutes on a hot plate (using ACT-8) at 120 ° C. to produce a prebaked film having a thickness of 10 ⁇ m.
- the membrane was exposed at 10 mJ / cm 2 steps at 0 ⁇ 1000mJ / cm 2 exposure amount using an i-line stepper (NIKON NSR i9). After the exposure, the film was developed with a 2.38 mass% TMAH aqueous solution for 90 seconds and then rinsed with pure water to obtain a developed film A having a line-and-space pattern.
- the exposure amount (hereinafter referred to as the minimum exposure amount Eth) at which the exposed portion was not completely eluted after exposure and development was defined as sensitivity. If Eth is 400 mJ / cm 2 or less, it can be determined that the sensitivity is high. 300 mJ / cm 2 or less is more preferable.
- the minimum dimension that is resolved by the line and space is defined as the resolution. If the resolution dimension is 10 ⁇ m or less, it can be determined that the resolution is high, and 5 ⁇ m or less is more preferable.
- Synthesis Example 1 Synthesis of quinonediazide compound (a) Under a dry nitrogen stream, 21.22 g (0.05 mol) of a polyhydroxy compound TrisP-PA (trade name, manufactured by Honshu Chemical Industry Co., Ltd.) and 5-naphthoquinonediazidesulfonyl acid chloride 26.86 g (0.10 mol) and 13.43 g (0.05 mol) of 4-naphthoquinone diazide sulfonyl chloride were dissolved in 50 g of 1,4-dioxane and brought to room temperature.
- TrisP-PA trade name, manufactured by Honshu Chemical Industry Co., Ltd.
- Synthesis Example 2 Synthesis of quinonediazide compound (b) In a dry nitrogen stream, 15.31 g (0.05 mol) of a polyhydroxy compound TrisP-HAP (trade name, manufactured by Honshu Chemical Industry Co., Ltd.) and 5-naphthoquinonediazidesulfonyl acid chloride 40.28 g (0.15 mol) was dissolved in 450 g of 1,4-dioxane and brought to room temperature. Using 15.18 g of triethylamine mixed with 50 g of 1,4-dioxane, a quinonediazide compound (b) represented by the following formula was obtained in the same manner as in Synthesis Example 2.
- TrisP-HAP trade name, manufactured by Honshu Chemical Industry Co., Ltd.
- Synthesis Example 3 Synthesis of quinonediazide compound (c) In a dry nitrogen stream, 28.83 g (0.05 mol) of a polyhydroxy compound TekP-4HBPA (trade name, manufactured by Honshu Chemical Industry Co., Ltd.) and 5-naphthoquinonediazidesulfonyl acid chloride 13.43 g (0.125 mol) was dissolved in 450 g of 1,4-dioxane and brought to room temperature. Using 20.24 g of triethylamine mixed with 50 g of 1,4-dioxane, a quinonediazide compound (c) represented by the following formula was obtained in the same manner as in Synthesis Example 2.
- Synthesis Example 5 Synthesis of polyhydroxystyrene (e) 500 ml of tetrahydrofuran and 0.01 mol of sec-butyllithium as an initiator were added to a mixed solution of pt-butoxystyrene and styrene in a molar ratio of 3: 1. 20 g was added and polymerized with stirring for 3 hours. The polymerization termination reaction was performed by adding 0.1 mol of methanol to the reaction solution. Next, in order to purify the polymer, the reaction mixture was poured into methanol, and the precipitated polymer was dried to obtain a white polymer. Further, dissolve in 400 ml of acetone, add a small amount of concentrated hydrochloric acid at 60 ° C.
- polyhydroxystyrene (e) which is a copolymer of purified p-hydroxystyrene and styrene, was obtained.
- GBL was added to the obtained polyhydroxystyrene (e) to obtain a polyhydroxystyrene (e) solution having a solid content concentration of 43% by mass.
- the alkali dissolution rate of this resin was 5,000 um / min.
- Example 1 Under a dry nitrogen stream, 6.20 g (0.020 mol) of ODPA and 13.33 g (0.030 mol) of 6FDA were dissolved in 100 g of NMP. MAP1.09g (0.010mol) was added here with NMP20g. Further, 11.90 g (0.033 mol) of BAHF, 9.00 g (0.010 mol) of ED-900 and 0.62 g (0.003 mol) of SiDA were added together with 20 g of NMP, and reacted at 60 ° C. for 1 hour, and then 180 ° C. For 4 hours. After stirring, the solution was poured into 2 L of water to obtain a white precipitate.
- This precipitate was collected by filtration, washed three times with water, and then dried with a vacuum dryer at 50 ° C. for 72 hours to obtain a powder of a closed ring polyimide alkali-soluble resin (A).
- This resin had a weight average molecular weight of 32,000 and an alkali dissolution rate of 5,000 um / min.
- Table 1 shows components in the alkali-soluble resin (A), and Table 2 shows other resins and photoacid generators in the varnish. As described above, room temperature storage stability evaluation, elongation evaluation, adhesion evaluation, sensitivity evaluation, and resolution evaluation were performed using the obtained varnish. The evaluation results are shown in Table 2.
- Example 2 Under a dry nitrogen stream, 3.92 g (0.020 mol) of CBDA and 13.33 g (0.030 mol) of 6FDA were dissolved in 100 g of NMP. MAP1.09g (0.010mol) was added here with NMP20g. Further, 11.90 g (0.033 mol) of BAHF, 9.00 g (0.010 mol) of ED-900 and 0.62 g (0.003 mol) of SiDA were added together with 20 g of NMP, and reacted at 60 ° C. for 1 hour, and then 180 ° C. For 4 hours. After stirring, the solution was poured into 2 L of water to obtain a white precipitate.
- This precipitate was collected by filtration, washed three times with water, and then dried in a vacuum dryer at 50 ° C. for 72 hours to obtain a powder of a closed ring polyimide alkali-soluble resin (B).
- the resin had a weight average molecular weight of 30,000 and an alkali dissolution rate of 14,000 um / min.
- Table 1 shows components in the alkali-soluble resin (B), and Table 2 shows other resins and photoacid generators in the varnish. As described above, room temperature storage stability evaluation, elongation evaluation, adhesion evaluation, sensitivity evaluation, and resolution evaluation were performed using the obtained varnish. The evaluation results are shown in Table 2.
- Example 3 Under a dry nitrogen stream, 4.65 g (0.020 mol) of ODPA and 13.33 g (0.030 mol) of 6FDA were dissolved in 100 g of NMP. To this, 13.73 g (0.038 mol) of BAHF, 9.00 g (0.010 mol) of ED-900 and 0.62 g (0.003 mol) of SiDA were added together with 20 g of NMP, and reacted at 60 ° C. for 1 hour. After stirring at 4 ° C.
- Table 1 shows components in the alkali-soluble resin (C), and Table 2 shows other resins and photoacid generators in the varnish. As described above, room temperature storage stability evaluation, elongation evaluation, adhesion evaluation, sensitivity evaluation, and resolution evaluation were performed using the obtained varnish. The evaluation results are shown in Table 2.
- Example 4 Under a dry nitrogen stream, 13.73 g (0.038 mol) of BAHF was dissolved in 185 g of NMP. To this, 8.60 g (0.024 mol) of PBOM was added together with 20 g of NMP, and reacted at 85 ° C. for 3 hours. Subsequently, 11.25 g (0.013 mol) of ED-900, 0.62 g (0.003 mol) of SiDA, and 7.53 g (0.021 mol) of PBOM were added together with 30 g of NMP, and reacted at 85 ° C. for 1 hour.
- Table 1 shows components in the alkali-soluble resin (D), and Table 2 shows other resins and photoacid generators in the varnish. As described above, room temperature storage stability evaluation, elongation evaluation, adhesion evaluation, sensitivity evaluation, and resolution evaluation were performed using the obtained varnish. The evaluation results are shown in Table 2.
Landscapes
- Physics & Mathematics (AREA)
- General Physics & Mathematics (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Materials For Photolithography (AREA)
- Exposure And Positioning Against Photoresist Photosensitive Materials (AREA)
- Polymerisation Methods In General (AREA)
Abstract
本発明は、ポジ型感光性樹脂組成物に用いた場合に、高伸度、高密着、高感度、保存安定性良好な樹脂を提供することを目的とする。本発明は、(a)ポリイミド前駆体、ポリベンゾオキサゾール前駆体、ポリアミドイミド前駆体、ポリイミド、およびそれらの共重合体から選ばれる少なくとも一種を含むアルカリ可溶性樹脂と、(b)光酸発生剤と、(c)多官能アクリレート化合物を含有し、(a)アルカリ可溶性樹脂が分子内に脂肪族鎖を有することを特徴とするポジ型感光性樹脂組成物である。
Description
本発明は、ポジ型感光性樹脂組成物に関する。
ポリイミド樹脂は優れた耐熱性や電気絶縁性、機械特性を有することから、半導体素子やインダクタ装置の表面保護膜、層間絶縁膜、有機電界発光素子の絶縁層やスペーサー層、薄膜トランジスタ基板(TFT基板)の平坦化層、有機トランジスタの絶縁層等などに広く用いられている。
ポリイミドを表面保護膜または層間絶縁膜として使用する場合のスルーホール等の形成方法の1つは、ポジ型のフォトレジストを用いるエッチングである。しかし、この方法を用いた工程にはフォトレジストの塗布や剥離が含まれ、煩雑であるという問題がある。そこで作業工程の合理化を目的に感光性を兼ね備えた耐熱性材料の検討がなされてきた。
近年、半導体素子においてパターン加工の微細化、パッケージの小型化と高密度化、高速大容量化により、ポリイミドをバッファコートとして使用するだけでなく、金属配線間の層間絶縁膜として何層にも積層させて使用する再配線用途の需要が高まっている。また、インダクタ装置などの電子部品においても、金属配線とポリイミドを積層させることでコイルを形成するコモンモードフィルタ用途など、多層配線に適応可能な層間絶縁膜に対する需要が高まっている。これらの用途に対し、基板のねじれや膨張に耐え得る高伸度、高密着性、低反り、厚膜加工が可能な高感度、高解像度、といった特性を、デバイスへの負担が小さい低温硬化の条件下で満たす感光性樹脂組成物が求められている。
高密着性、低反りの要求を満たすために、これまでに、分子鎖に柔軟な脂肪族基を有する樹脂を用いた感光性樹脂組成物が提案されている。(例えば、特許文献1)しかし、脂肪族基は硬化膜にしたときの耐薬品性、耐熱性が低く、また分子中に過剰に導入した場合、アルカリ現像液への溶解性の低下による感度の低下や、現像後にタックや残渣が発生するという課題があった。
高い機械特性が得られる感光性樹脂組成物として、エポキシ基やアルコキシメチル基を含有する化合物を架橋剤として用いた感光性樹脂組成物(例えば、特許文献2、3)が提案されている。
一方、硬化膜の機械特性、耐薬品性を向上させるためにアクリレート化合物を添加剤として用いた感光性樹脂組成物が提案されている(例えば、特許文献4)。
しかしながら、エポキシ基を有する化合物は感光性樹脂組成物の室温保存安定性を低下させるという課題があり、アルコキシメチル基を含有する多くの化合物は柔軟性が乏しく、過剰に添加すると伸度を低下させるという課題があった。
また、アクリレート化合物を添加剤として用いた感光性樹脂組成物においては、多くは光重合開始剤を用いてアクリレートを重合させるネガ型の感光性樹脂組成物であり、アクリレートの硬化密度が高い半面、微細なパターン加工性においてポジ型の感光性樹脂組成物に劣っていた。
またポジ型の感光性樹脂組成物にアクリレート化合物を添加したものであっても、これまでの報告例では(例えば、特許文献5)、樹脂の柔軟性が不足していたため、十分な伸度が得られなかった。
以上の理由から、アクリレート化合物を添加剤として用いたこれまでのポジ型感光性樹脂組成物は前述の再配線用途などにおける高解像度、高伸度の要求を十分に満たしていなかった。
そこで、本発明は、上記従来技術の課題に鑑み、高伸度、高密着性を有し、感度、解像度、保存安定性の良好なポジ型感光性樹脂組成物を提供することを目的とする。
上記課題を解決するため、本発明のポジ型感光性樹脂組成物は下記の構成からなる。すなわち、(a)ポリイミド前駆体、ポリベンゾオキサゾール前駆体、ポリアミドイミド前駆体、ポリイミド、およびそれらの共重合体から選ばれる少なくとも1種を含むアルカリ可溶性樹脂と、(b)光酸発生剤と、(c)多官能アクリレート化合物を含有し、前記(a)アルカリ可溶性樹脂が分子内に脂肪族鎖を有することを特徴とするポジ型感光性樹脂組成物である。
また、本発明は、前記ポジ型樹脂組成物を用いた、感光性シート、硬化膜、層間絶縁膜、半導体保護膜、半導体装置の製造方法、半導体電子部品および半導体装置である。
本発明によれば、感度、解像度、および保存安定性が良好なポジ型感光性樹脂組成物を得ることができる。また、本発明のポジ型感光性樹脂組成物によれば、高伸度、高密着性の硬化膜を得ることができる。
本発明の樹脂組成物は、(a)ポリイミド前駆体、ポリベンゾオキサゾール前駆体、ポリアミドイミド前駆体、ポリイミド、およびそれらの共重合体から選ばれる少なくとも一種を含むアルカリ可溶性樹脂と、(b)光酸発生剤と、(c)多官能アクリレート化合物を含有し、前記(a)アルカリ可溶性樹脂が分子内に脂肪族鎖を有することを特徴とするポジ型感光性樹脂組成物である。
前記脂肪族鎖とは、脂肪族の有機基で構成された構造単位を有する酸二無水物残基またはジアミン残基であり、アルカリ可溶性樹脂に柔軟性を付与するために、鎖状のアルキル構造やアルキルエーテル構造を有することが好ましい。
前記(a)アルカリ可溶性樹脂の構造単位は一般式(1)および(2)の少なくともいずれかを有することが好ましい。
(式中、R1 、R2、およびR6は2個以上200個以下の炭素原子を有する2価から8価の有機基を示す。R5は2個以上200個以下の炭素原子を有する4価の有機基を示す。R3およびR4は水素、または炭素数1から20の有機基のいずれかを示す。n1およびn2は10から100,000の範囲の整数を示す。p、q、r、s、およびtは0≦p+r≦6、0≦q+s≦6、0≦t≦6を満たす整数を示す。)
R1およびR5は酸二無水物に由来する有機基である。
R1およびR5は酸二無水物に由来する有機基である。
本発明に使用される酸二無水物としては、具体的には、ピロメリット酸二無水物、3,3’,4,4’-ビフェニルテトラカルボン酸二無水物、2,3,3’,4’-ビフェニルテトラカルボン酸二無水物、2,2’,3,3’-ビフェニルテトラカルボン酸二無水物、3,3’,4,4’-ベンゾフェノンテトラカルボン酸二無水物、2,2’,3,3’-ベンゾフェノンテトラカルボン酸二無水物、2,2-ビス(3,4-ジカルボキシフェニル)プロパン二無水物、2,2-ビス(2,3-ジカルボキシフェニル)プロパン二無水物、1,1-ビス(3,4-ジカルボキシフェニル)エタン二無水物、1,1-ビス(2,3-ジカルボキシフェニル)エタン二無水物、ビス(3,4-ジカルボキシフェニル)メタン二無水物、ビス(2,3-ジカルボキシフェニル)メタン二無水物、1,2,5,6-ナフタレンテトラカルボン酸二無水物、2,3,6,7-ナフタレンテトラカルボン酸二無水物、2,3,5,6-ピリジンテトラカルボン酸二無水物、3,4,9,10-ペリレンテトラカルボン酸二無水物、ビス(3,4-ジカルボキシフェニル)スルホン二無水物、3,3’,4,4’-ジフェニルエーテルテトラカルボン酸二無水物などの芳香族テトラカルボン酸二無水物あるいはこれらの化合物の水素原子をアルキル基やハロゲン原子で置換した化合物や、1,2,3,4-シクロブタンテトラカルボン酸二無水物、1,2-ジメチル-1,2,3,4-シクロブタンテトラカルボン酸二無水物、1,2,3,4-テトラメチル-1,2,3,4-シクロブタンテトラカルボン酸二無水物、1,2,4,5-シクロヘキサンテトラカルボン酸二無水物、5-(2,5-ジオキソテトラヒドロフリル)-3-メチル-3-シクロヘキセン-1,2-ジカルボン酸二無水物、2,3,5-トリカルボキシ-2-シクロペンタン酢酸二無水物、ビシクロ[2.2.2] オクト-7-エン-2,3,5,6-テトラカルボン酸二無水物、2,3,4,5-テトラヒドロフランテトラカルボン酸二無水物、3,5,6-トリカルボキシ-2-ノルボルナン酢酸二無水物、3,4-ジカルボキシ-1,2,3,4-テトラヒドロ-1-ナフタレンコハク酸二無水物の様な脂環式、半脂環式テトラカルボン酸二無水物や、2,2-ビス(3,4-ジカルボキシフェニル)ヘキサフルオロプロパン二無水物のようなフッ素原子を含む化合物あるいはこれらの芳香族環や水素原子をアルキル基やハロゲン原子で置換した化合物、およびアミド基を有する酸二無水物などを挙げることができる。これらは単独で用いても2種以上組み合わせて使用してもよい。
R2、R6はジアミンに由来する有機基である。本発明に使用されるジアミンは、脂肪族
の有機基を含有することが好ましい。脂肪族の有機基として、一般式(3)であらわされるポリエーテルブロック構造単位を有することが好ましい。
の有機基を含有することが好ましい。脂肪族の有機基として、一般式(3)であらわされるポリエーテルブロック構造単位を有することが好ましい。
(式中、R7~R10はそれぞれ独立に炭素数1~6のアルキレン基を表す。R11~R18はそれぞれ独立に水素、フッ素、または炭素数1~6のアルキル基を表す。但し、括弧内に表される構造はそれぞれ異なる。x、y、zはそれぞれ独立に0~35の整数を表す。)
ポリエーテルブロック構造単位を有する有機基を含む化合物としては、具体的には“ジェファーミン(登録商標)”HK-511、ED-600、ED-900、ED-2003、EDR-148、EDR-176、D-200、D-400、D-2000、D-4000、エラスタミンRP-409、RP-2009、RT-1000、HT-1100、HE-1000、HT-1700(以上、HUNTSMAN(株)製) などの脂肪族ジアミンを挙げることができる。
ポリエーテルブロック構造単位を有する有機基を含む化合物としては、具体的には“ジェファーミン(登録商標)”HK-511、ED-600、ED-900、ED-2003、EDR-148、EDR-176、D-200、D-400、D-2000、D-4000、エラスタミンRP-409、RP-2009、RT-1000、HT-1100、HE-1000、HT-1700(以上、HUNTSMAN(株)製) などの脂肪族ジアミンを挙げることができる。
ポリエーテル構造を含有することで柔軟性が付与されるため硬化膜の伸度と基盤との密着性が向上し、また弾性率が低下することで基盤の反りが抑制されるため好ましい。これらの特性は、多層や厚膜加工において有効な特性である。
一般式(3)で表されるポリエーテルブロック構造単位は一般式(1)および(2)で表される構造におけるR2およびR6を100モル%とした場合、10モル%以上であれば樹脂に柔軟性が与えられることにより高伸度が得られ、80モル%以下であれば現像液に対する適切な溶解速度が得られるという点で好ましく、10モル%~40モル%含有することがより好ましい。
また、R2、R6はポリエーテル構造を有する有機基を含む化合物以外のジアミンに由来する構造を含有してもよい。ポリエーテル構造を有する有機基を含む化合物以外のジアミンとしては具体的には、ビス(3-アミノ-4-ヒドロキシフェニル)ヘキサフルオロプロパン、ビス(3-アミノ-4-ヒドロキシフェニル)スルホン、ビス(3-アミノ-4-ヒドロキシフェニル)プロパン、ビス(3-アミノ-4-ヒドロキシフェニル)メチレン、ビス(3-アミノ-4-ヒドロキシフェニル)エーテル、ビス(3-アミノ-4-ヒドロキシ)ビフェニル、ビス(3-アミノ-4-ヒドロキシフェニル)フルオレンなどのヒドロキシル基含有ジアミン、3-スルホン酸-4,4’-ジアミノジフェニルエーテルなどのスルホン酸含有ジアミン、ジメルカプトフェニレンジアミンなどのチオール基含有ジアミン、3,4’-ジアミノジフェニルエーテル、4,4’-ジアミノジフェニルエーテル、3,4’-ジアミノジフェニルメタン、4,4’-ジアミノジフェニルメタン、3,4’-ジアミノジフェニルスルホン、4,4’-ジアミノジフェニルスルホン、3,4’-ジアミノジフェニルスルフィド、4,4’-ジアミノジフェニルスルフィド、1,4-ビス(4-アミノフェノキシ)ベンゼン、ベンジン、m-フェニレンジアミン、p-フェニレンジアミン、1,5-ナフタレンジアミン、2,6-ナフタレンジアミン、ビス(4-アミノフェノキシフェニル)スルホン、ビス(3-アミノフェノキシフェニル)スルホン、ビス(4-アミノフェノキシ)ビフェニル、ビス{4-(4-アミノフェノキシ)フェニル}エーテル、1,4-ビス(4-アミノフェノキシ)ベンゼン、2,2’-ジメチル-4,4’-ジアミノビフェニル、2,2’-ジエチル-4,4’-ジアミノビフェニル、3,3’-ジメチル-4,4’-ジアミノビフェニル、3,3’-ジエチル-4,4’-ジアミノビフェニル、2,2’,3,3’-テトラメチル-4,4’-ジアミノビフェニル、3,3’,4,4’-テトラメチル-4,4’-ジアミノビフェニル、2,2’-ビス(トリフルオロメチル)-4,4’-ジアミノビフェニルなどの芳香族ジアミンや、これらの芳香族環の水素原子の一部を炭素数1~10のアルキル基やフルオロアルキル基、ハロゲン原子などで置換した化合物、シクロヘキシルジアミン、メチレンビスシクロヘキシルアミンなどの脂環式ジアミンなどを挙げることができる。これらのジアミンは、そのまま、あるいは対応するジイソシアネート化合物、トリメチルシリル化ジアミンとして使用できる。また、これら2種以上のジアミン成分を組み合わせて用いてもよい。
これらのジアミンのうち、3,4’-ジアミノジフェニルエーテル、4,4’-ジアミノジフェニルエーテル、3,4’-ジアミノジフェニルスルホン、4,4’-ジアミノジフェニルスルホン、3,4’-ジアミノジフェニルスルヒド、4,4’-ジアミノジフェニルスルヒド、ビス(4-アミノフェノキシフェニル)スルホン、ビス(3-アミノフェノキシフェニル)スルホン、ビス(4-アミノフェノキシ)ビフェニル、ビス{4-(4-アミノフェノキシ)フェニル}エーテル、1,4-ビス(4-アミノフェノキシ)ベンゼン、1,3-ビス(4-アミノフェノキシ)ベンゼン、2,2-ビス[4-(4-アミノフェノキシ)フェニル]ヘキサフルオロプロパン、2,2-ビス[4-(4-アミノフェノキシ)フェニル]プロパン、2,2-ビス(3-アミノ-4-ヒドロキシフェニル)ヘキサフルオロプロパンあるいはこれらの芳香族環をアルキル基やハロゲン原子で置換した化合物、およびアミド基を有するジアミンなどが好ましいものとして挙げられる。これらのジアミンは単独でまたは2種以上を組み合わせて使用される。
また、耐熱性を低下させない範囲で、シロキサン構造を有する脂肪族の基を共重合してもよく、基板との接着性を向上させることができる。具体的には、ジアミン成分として、ビス(3-アミノプロピル)テトラメチルジシロキサン、ビス(p-アミノフェニル)オクタメチルペンタシロキサンなどを1~15モル%共重合したものなどが挙げられる。
耐熱性が要求される用途では、芳香族ジアミンをジアミン全体の50モル%以上使用することが好ましい。
また、一般式(1)および(2)で表される構造単位の少なくともいずれかを有する樹脂は、フェノール性水酸基成分を有することが好ましい。一般式(1)および(2)中において、R1、R2の少なくとも一方が、フェノール性水酸基を有する有機基であることが好ましい。フェノール性水酸基は、アルカリ現像液への適度な溶解性が得られ、また感光剤と相互作用し未露光部の溶解性を抑制するため、残膜率の向上、高感度化が可能になる。また、フェノール性水酸基は、架橋剤との反応にも寄与するため、高機械特性、耐薬品性が得られる点でも好ましい。
フェノール性水酸基を有する化合物としては、具体的には、2,2-ビス(3,4-ジカルボキシフェニル)ヘキサフルオロプロパン二無水物あるいはこれらの芳香族環をアルキル基やハロゲン原子で置換した化合物、およびアミド基を有する酸二無水物などの芳香族酸二無水物や、ビス(3-アミノ-4-ヒドロキシフェニル)ヘキサフルオロプロパン、ビス(3-アミノ-4-ヒドロキシフェニル)スルホン、ビス(3-アミノ-4-ヒドロキシフェニル)プロパン、ビス(3-アミノ-4-ヒドロキシフェニル)メチレン、ビス(3-アミノ-4-ヒドロキシフェニル)エーテル、ビス(3-アミノ-4-ヒドロキシ)ビフェニル、ビス(3-アミノ-4-ヒドロキシフェニル)フルオレンなどのヒドロキシル基含有ジアミンや、これらの芳香族環の水素原子の一部を炭素数1~10のアルキル基やフルオロアルキル基、ハロゲン原子などで置換した化合物、などを挙げることができる。一般式(1)および(2)で表される構造を有する樹脂は、これらの化合物に由来する構造を含む樹脂であることが好ましい。これらのフェノール性水酸基を有する化合物は、一般式(1)および(2)で表される構造を有する樹脂中の酸二無水物成分またはジアミン成分のうち、10~90モル%使用することが好ましい。フェノール性水酸基を有する化合物の含有量をこの範囲とすることにより、アルカリ現像液への適度な溶解性が得られる。
一般式(1)および(2)において、n1およびn2は重合度を表す。一般式(1)および(2)の単位あたりの分子量をM、アルカリ可溶性樹脂の数平均分子量をMnとすると、重合度nはn=Mw/Mの式で求められる。アルカリ可溶性樹脂の数平均分子量は実施例に記載のようにGPC(ゲルパーミエーションクロマトグラフィー)によって求められる。
本発明の感光性樹脂組成物は、(b)光酸発生剤を含有することにより、ポジ型の感光性を有する。すなわち、光酸発生剤は光照射されることにより酸が発生し、光照射部のアルカリ水溶液に対する溶解性が増大する特性を持つ。光酸発生剤としてはキノンジアジド化合物が挙げられる。キノンジアジド化合物は、ポリヒドロキシ化合物にキノンジアジドのスルホン酸がエステルで結合したもの、ポリアミノ化合物にキノンジアジドのスルホン酸がスルホンアミド結合したもの、ポリヒドロキシポリアミノ化合物にキノンジアジドのスルホン酸がエステル結合および/またはスルホンアミド結合したものなどが挙げられる。
これらのポリヒドロキシ化合物やポリアミノ化合物の全ての官能基がキノンジアジドで置換されていなくても良い。官能基全体の50モル%以上がキノンジアジドで置換されていることが好ましい。前記キノンジアジドによる置換が50モル%以上の場合、アルカリ現像液に対する溶解性が高くなり過ぎず、未露光部とのコントラストが得られ、所望のパターンを得ることができる。
このようなキノンジアジド化合物を用いることで、一般的な紫外線である水銀灯のi線(365nm)、h線(405nm)、g線(436nm)に感光するポジ型の感光性樹脂組成物を得ることができる。
キノンジアジド化合物は単独で使用しても良いし、2種以上を混合して使用してもかまわない。
キノンジアジド化合物に用いられるポリヒドロキシ化合物は、具体的には、Bis-Z、BisP-EZ、TekP-4HBPA、TrisP-HAP、TrisP-PA、TrisP-SA、TrisOCR-PA、BisOCHP-Z、BisP-MZ、BisP-PZ、BisP-IPZ、BisOCP-IPZ、BisP-CP、BisRS-2P、BisRS-3P、BisP-OCHP、メチレントリス-FR-CR、BisRS-26X、DML-MBPC、DML-MBOC、DML-OCHP、DML-PCHP、DML-PC、DML-PTBP、DML-34X、DML-EP,DML-POP、ジメチロール-BisOC-P、DML-PFP、DML-PSBP、DML-MTrisPC、TriML-P、TriML-35XL、TML-B P、TML-HQ、TML-pp-BPF、TML-BPA、TMOM-BP、HML-TPPHBA、HML-TPHAP(以上、商品名、本州化学工業(株)製)、BIR-OC、BIP-PC、BIR-PC、BIR-PTBP、BIR-PCHP、BIP-BIOC-F、4PC、BIR-BIPC-F、TEP-BIP-A、46DMOC、46DMOEP、TM-BIP-A(以上、商品名、旭有機材工業(株)製)、2,6-ジメトキシメチル-4-t-ブチルフェノール、2,6-ジメトキシメチル-p-クレゾール、2,6-ジアセトキシメチル-p-クレゾール、ナフトール、テトラヒドロキシベンゾフェノン、没食子酸メチルエステル、ビスフェノールA 、ビスフェノールE、メチレンビスフェノール、BisP-AP(商品名、本州化学工業(株)製)などが挙げられる。キノンジアジド化合物に用いられるポリヒドロキシ化合物はこれらに限定されない。
キノンジアジド化合物に用いられるポリアミノ化合物は、具体的には、1,4-フェニレンジアミン、1,3-フェニレンジアミン、4,4’-ジアミノジフェニルエーテル、4,4’-ジアミノジフェニルメタン、4,4’-ジアミノジフェニルスルホン、4,4’-ジアミノジフェニルスルヒド等が挙げられる。キノンジアジド化合物に用いられるポリアミノ化合物はこれらに限定されない。
また、キノンジアジド化合物に用いられるポリヒドロキシポリアミノ化合物は、具体的には、2,2-ビス(3-アミノ-4- ヒドロキシフェニル)ヘキサフルオロプロパン、3,3’-ジヒドロキシベンジジン等が挙げられる。キノンジアジド化合物に用いられるポリヒドロキシポリアミノ化合物はこれらに限定されない。
本発明においてキノンジアジドは5-ナフトキノンジアジドスルホニル基、4-ナフトキノンジアジドスルホニル基のいずれも好ましく用いられる。
4-ナフトキノンジアジドスルホニルエステル化合物は水銀灯のi線領域に吸収を持っており、i線露光に適している。
5-ナフトキノンジアジドスルホニルエステル化合物は水銀灯のg線領域まで吸収が伸びており、g線露光に適している。
本発明においては、露光する波長によって4-ナフトキノンジアジドスルホニルエステル化合物、5-ナフトキノンジアジドスルホニルエステル化合物を選択することが好ましい。また、同一分子中に4-ナフトキノンジアジドスルホニル基および5-ナフトキノンジアジドスルホニル基を併用した、ナフトキノンジアジドスルホニルエステル化合物を得ることもできるし、4-ナフトキノンジアジドスルホニルエステル化合物と5-ナフトキノンジアジドスルホニルエステル化合物とを混合して使用することもできる。
本発明のキノンジアジド化合物の分子量は300~3,000が好ましい。キノンジアジド化合物の分子量が5000より大きくなると、その後の熱処理においてキノンジアジド化合物が十分に熱分解しないために、得られる膜の耐熱性が低下する、機械特性が低下する、接着性が低下するなどの問題が生じる可能性がある。本発明のキノンジアジド化合物は、フェノール化合物から、次の方法により合成される。例えば5-ナフトキノンジアジドスルホニルクロライドとフェノール化合物をトリエチルアミン存在下で反応させる方法が挙げられる。フェノール化合物の合成方法は、酸触媒下でα-(ヒドロキシフェニル)スチレン誘導体を多価フェノール化合物と反応させる方法などが挙げられる。
本発明のキノンジアジド化合物は、露光によって発生させた酸成分を安定化させるため、スルホニウム塩、ホスホニウム塩またはジアゾニウム塩であることが好ましい。
本発明の感光性樹脂組成物から得られる樹脂組成物は永久膜として使用するため、リン等が残存することは環境上好ましくなく、また膜の色調も考慮する必要があることから、スルホニウム塩が好ましく用いられる。特に好ましくは、トリアリールスルホニウム塩が挙げられ、露光後放置安定性を著しく向上させることができる。特に好ましいものとして、一般式(5)で表されるトリアリールスルホニウム塩が挙げられる。
(式中R22は各々同一であっても異なっていてもよく、水素または炭素数1から20までの有機基のいずれかを示す。R23は炭素数1から20までの有機基を示す。a、b、cはそれぞれ0から5までの整数を示す。)
キノンジアジド化合物とスルホニウム塩、ホスホニウム塩またはジアゾニウム塩は2種以上を混合して使用してもかまわない。
キノンジアジド化合物とスルホニウム塩、ホスホニウム塩またはジアゾニウム塩は2種以上を混合して使用してもかまわない。
本発明で用いられる光酸発生剤の含有量は、一般式(1)および/または(2)で表される構造有する樹脂100質量部に対して、好ましくは0.01~50質量部である。このうち、キノンジアジド化合物は3~40質量部の範囲が好ましい。また、スルホニウム塩、ホスホニウム塩、ジアゾニウム塩から選ばれる化合物は全体で0 .05~40質量部の範囲が好ましく、さらに0.1~30質量部の範囲が好ましい。キノンジアジド化合物の含有量をこの範囲とすることにより、より高感度化を図ることができる。さらに増感剤などを必要に応じて含有してもよい。
本発明のポジ型感光性樹脂組成物は(c)多官能のアクリレート化合物を含有する。
本発明において、アクリレート化合物とは、アクリロイル基またはメタクリロイル基を有する化合物をいう。例えば、アクリル酸エステル、メタクリル酸エステル、アクリルアミド、およびメタクリルアミド等を挙げることができる。また、多官能のアクリレート系化合物とは、アクリロイル基および/またはメタクリロイル基を2以上有する化合物をいう。
本発明のポジ型感光性樹脂組成物は、パターン加工後に熱処理を行う。このとき多官能のアクリレート化合物がアクリレート化合物同士で熱重合またはアルカリ可溶性樹脂と反応し、架橋することにより、硬化膜の伸度が向上する。単官能のアクリレート化合物の場合、架橋反応による膜の硬化が十分には進行せず、伸度の向上効果が低いため、多官能のアクリレートであることが好ましい。
多官能のアクリレート化合物の好ましい例としては、新中村化学工業(株)製NKエステルシリーズ 1G、2G、3G、4G、9G、14G、23G、BG、HD、NPG、9PG、701、BPE-100、BPE-200、BPE-500、BPE-1300、A-200、A-400、A-600、A-HD、A-NPG、APG-200、APG-400、APG-700、A-BPE-4、701A、TMPT、A-TMPT、A-TMM-3、A-TMM-3L、A-TMMT、A-9300、ATM-4E、ATM-35E、ATM-4P、AD-TMP、AD-TMP-L、A-DPH等が挙げられる。また、共栄社化学(株)製ライトエステルシリーズ P-1M、P-2M、EG、2EG、3EG、4EG、9EG、14EG、1.4BG、NP、1.6HX、1.9ND、1.10DC、G-101P、G-201P、DCP-M、BP-2EM、BP-4EM、BP-6EM、TMP等が挙げられる。また、共栄社化学(株)製ライトアクリレートシリーズ 3EG-A、4EG-A、9EG-A、14EG-A、TMGA-250、NP-A、MPD-A、1.6HX-A、BEPG-A、1.9ND-A、MOD-A、DCP-A、BP-4EA、BP-4PA、BA-134、BP-10EA、HPP-A、TMP-A、TMP-3EO-A、TMP-6EO-3A、PE-3A、PE-4A、DPE-6A等が挙げられる。また、共栄社化学(株)製エポキシエステルシリーズ40EM、70PA、200PA、80MFA、3002M、3002A、3000M、3000A等が挙げられる。また、東亜合成(株)製“アロニックス(登録商標)”シリーズ M-203、M-208、M-210、M-211B、M-215、M-220、M-225、M-240、M-243、M-245、M-260、M-270、M-305、M-309、M-310、M-313、M-315、M-320、M-325、M-350、M-360、M-402、M-408、M-450等が挙げられる。また、日本化薬(株)製“KAYARAD(登録商標)”シリーズ R-526、NPGDA、PEG400DA、MANDA、R-167、HX-220、HX-620、R-551、R-712、R-604、R-684、GPO-303、TMPTA、THE-330、TPA-320、TPA-330、PET-30、T-1420(T)、RP-1040等が挙げられる。また、日本油脂(株)製“ブレンマー(登録商標)”シリーズ GMR-H、GAM、PDE-50、PDE-100、PDE-150、PDE-200、PDE-400、PDE-600、PDE-1000、ADE-200、ADE-400、PDP-400、ADP-200、ADP-400、PDT-650、ADT-250、PDBE-200、PDBE-250、PDBE-450、PDBE-1300、ADBE-200、ADBE-250、ADBE-450等が挙げられる。また、MRCユニテック(株)製 MBAA等が挙げられる。これらの化合物を2種以上含有してもよい。
上記多官能アクリレート化合物のうち、分子量が、100以上2000以下であるアクリレート化合物が好ましい。分子量が100以上であることで高伸度の硬化膜を得ることができ、2000以下であることで適度なアルカリ溶解性、アルカリ可溶性樹脂との高い相溶性を持つ樹脂組成物を得ることができる。
また、上記アクリレート化合物のうち、一般式(4)で表されるポリエーテルブロック構造単位を有するアクリレート化合物が好ましい。(a)成分のアルカリ可溶性樹脂だけでなくアクリレート化合物に柔軟骨格を含有することで、アルカリ可溶性樹脂に柔軟骨格を過剰に導入した場合に起こる感度の低下や現像後のタック性、残渣を避けつつ、より伸度、密着性の高い硬化膜を得ることができる。
また、上記アクリレート化合物のうち、一般式(4)で表されるポリエーテルブロック構造単位を有するアクリレート化合物が好ましい。(a)成分のアルカリ可溶性樹脂だけでなくアクリレート化合物に柔軟骨格を含有することで、アルカリ可溶性樹脂に柔軟骨格を過剰に導入した場合に起こる感度の低下や現像後のタック性、残渣を避けつつ、より伸度、密着性の高い硬化膜を得ることができる。
(式中、R19は炭素数1から6のアルキル基である。R20およびR21はそれぞれ独立に水素、フッ素、または炭素数1から6のアルキル基を表す。n3は1~40の整数を表す。)
これらの多官能のアクリレート化合物は、アクリロイル基またはメタクリロイル基が2つから6つであることが好ましい。アクリロイル基、メタクリロイル基のいずれかのみを2つ以上有するものであっても、アクリロイル基およびメタクリロイル基の両方を有し、これらの合計が2つから6つであるものであってもよい。アクリロイル基またはメタクリロイル基を2つから6つ有することにより、パターン加工後の熱処理時にアクリレート化合物同士で熱重合またはアルカリ可溶性樹脂と反応し、網目状構造を形成する。
これらの多官能のアクリレート化合物は、アクリロイル基またはメタクリロイル基が2つから6つであることが好ましい。アクリロイル基、メタクリロイル基のいずれかのみを2つ以上有するものであっても、アクリロイル基およびメタクリロイル基の両方を有し、これらの合計が2つから6つであるものであってもよい。アクリロイル基またはメタクリロイル基を2つから6つ有することにより、パターン加工後の熱処理時にアクリレート化合物同士で熱重合またはアルカリ可溶性樹脂と反応し、網目状構造を形成する。
(c)多官能のアクリレート化合物の含有量は、(a)アルカリ可溶性樹脂100質量部に対し、好ましくは1質量部から50質量部であり、アルカリへの溶解性の点から、より好ましくは1重量部から20重量部である。アクリレート化合物の含有量が1重量部以上であれば、伸度が向上する。50重量部以下であれば、適度なアルカリ溶解性が保たれ、得られる組成物の保存安定性が向上する。さらに、20重量部以下であれば露光後から現像までの放置時間に関係なく、安定した感度が得られる。
本発明の(c)多官能アクリレート化合物を使用した場合、樹脂組成物のアルカリ溶解性が高くなり、露光部の残渣が低減するため、高感度、高解像度の樹脂組成物が得られる。
多官能アクリレート化合物を使用した感光性樹脂組成物において厚膜構造でのパターンを形成するためには、アルカリ可溶性樹脂のアルカリ溶解速度を適度に調整することが必要である。(a)アルカリ可溶性樹脂のアルカリ溶解速度はテトラメチルアンモニウム(TMAH)2.38%水溶液に対し、100~4,0000nm/分であることが望ましい。アルカリ溶解性が100nm/分以上であれば、現像時に露光部が溶解することでポジ型のパターン形成が可能であるため好ましく、4,0000nm/分以下であれば、現像後の未露光部の残膜率が高く、厚膜構造でのパターンを形成することが可能であるため好ましい。溶解速度が100~2,0000nm/分であるとアクリレート化合物の添加量を増やすことができるためより高伸度の硬化膜が得られえる点でより好ましく、さらに露光部と未露光部のコントラストを上げるため、100~1,0000nm/分であることがより好ましい。
また、本発明において、(a)成分のアルカリ可溶性樹脂に加えて、加熱処理によって得られる硬化膜の耐熱性を損なわない範囲で、(d)アルカリ可溶性フェノール樹脂を含有することが好ましい。(d)アルカリ可溶性フェノール樹脂としては、フェノールノボラック樹脂、クレゾールノボラック樹脂、レゾール樹脂、ポリヒドロキシスチレン、またそれらにメチロール基、アルコキシメチル基やエポキシ基などの架橋基を導入した樹脂、それらの共重合ポリマーなどが挙げられる。
これらの(d)アルカリ可溶性フェノール樹脂を含有する場合、その含有量は(a)成分のアルカリ可溶性樹脂の総量100質量部に対して好ましくは150質量部以下であり、より好ましくは100質量部以下であり、さらに好ましくは50質量部以下である。
これらの(d)アルカリ可溶性フェノール樹脂を含有する場合、パターン加工性の点から、(d)アルカリ可溶性フェノール樹脂と(a)成分のアルカリ可溶性樹脂の樹脂組成物の溶解速度が100~2,0000nm/分であることが好ましいため、(d)アルカリ可溶性フェノール樹脂の溶解速度は100~2,0000nm/分であることが好ましい。これらの(d)アルカリ可溶性フェノール樹脂を含有することにより、耐熱性樹脂被膜の密着性や優れた感度を保ちながら、各フェノール樹脂の特性を付与することができる。
さらに、本発明の(a)アルカリ可溶性樹脂は末端に不飽和結合をもつ有機基を有することが好ましい。末端に不飽和結合をもつ有機基を有することで、熱処理時にアルカリ可溶性樹脂同士または(c)成分の多官能アクリレート化合物と熱重合することで架橋密度が上がり、伸度、耐熱性、耐薬品性の高い硬化膜が得られる。
このようなアルカリ可溶性樹脂は末端に不飽和結合をもつ有機基を有するモノアミン、酸無水物、酸クロリド、モノカルボン酸などによって末端封止することで得られる。不飽和結合をもつ有機基を有する末端封止剤としては、具体的には、3-アミノフェニルアセチレン、4-アミノフェニルアセチレン、3,5-ジエチニルアニリンなどのモノアミン、3-エチニル安息香酸、4-エチニル安息香酸、3,4-ジエチニル安息香酸、3,5-ジエチニル安息香酸などのモノカルボン酸、無水マレイン酸、5-ノルボルネン-2,3-ジカルボン酸無水物などの酸無水物、前記モノカルボン酸のカルボキシル基を酸クロリド化した化合物やマレイン酸などのジカルボン酸類のカルボキシル基1つを酸クロリド化した化合物、モノ酸クロリド化合物とN-ヒドロキシ-5-ノルボルネン-2,3-ジカルボキシイミドとの反応により得られる活性エステル化合物などが挙げられる。
その他、不飽和結合をもたない末端封止剤を用いてもよく、具体的には、5-アミノ-8-ヒドロキシキノリン、1-ヒドロキシ-7-アミノナフタレン、1-ヒドロキシ-6-アミノナフタレン、1-ヒドロキシ-5-アミノナフタレン、1-ヒドロキシ-4-アミノナフタレン、2-ヒドロキシ-7-アミノナフタレン、2-ヒドロキシ-6-アミノナフタレン、2-ヒドロキシ-5-アミノナフタレン、1-カルボキシ-7-アミノナフタレン、1-カルボキシ-6-アミノナフタレン、1-カルボキシ-5-アミノナフタレン、2-カルボキシ-7-アミノナフタレン、2-カルボキシ-6-アミノナフタレン、2-カルボキシ-5-アミノナフタレン、2-アミノ安息香酸、3-アミノ安息香酸、4-アミノ安息香酸、4-アミノサリチル酸、5-アミノサリチル酸、6-アミノサリチル酸、2-アミノベンゼンスルホン酸、3-アミノベンゼンスルホン酸、4-アミノベンゼンスルホン酸、3-アミノ-4,6-ジヒドロキシピリミジン、2-アミノフェノール、3-アミノフェノール、4-アミノフェノール、2-アミノチオフェノール、3-アミノチオフェノール、4-アミノチオフェノールなどのモノアミン、無水フタル酸、シクロヘキサンジカルボン酸無水物、3-ヒドロキシフタル酸無水物などの酸無水物、3-カルボキシフェノール、4-カルボキシフェノール、3-カルボキシチオフェノール、4-カルボキシチオフェノール、1-ヒドロキシ-7-カルボキシナフタレン、1-ヒドロキシ-6-カルボキシナフタレン、1-ヒドロキシ-5-カルボキシナフタレン、1-メルカプト-7-カルボキシナフタレン、1-メルカプト-6-カルボキシナフタレン、1-メルカプト-5-カルボキシナフタレン、3-カルボキシベンゼンスルホン酸、4-カルボキシベンゼンスルホン酸などのモノカルボン酸類およびこれらのカルボキシル基が酸クロリド化したモノ酸クロリド化合物、テレフタル酸、フタル酸、シクロヘキサンジカルボン酸、1,5-ジカルボキシナフタレン、1,6-ジカルボキシナフタレン、1,7-ジカルボキシナフタレン、2,6-ジカルボキシナフタレンなどのジカルボン酸類の1つのカルボキシル基だけが酸クロリド化したモノ酸クロリド化合物、モノ酸クロリド化合物とN-ヒドロキシベンゾトリアゾールとの反応により得られる活性エステル化合物が挙げられる。
また、これら不飽和結合をもたない末端封止剤の水素結合をビニル基で置換することで不飽和結合をもつ末端封止剤として用いることができる。
末端封止剤は、樹脂の全酸または全アミン成分に対して0.1~60モル%使用することが好ましく、より好ましくは5~50モル%である。50モル%以下であることで、十分な機械特性を持つ硬化膜が得られるため好ましく、5モル%以上であることで、前述のような末端封止剤の効果を得ることができるため好ましい。
(a)成分のアルカリ可溶性樹脂および(d)成分のフェノール樹脂の重量平均分子量は、ゲルパーミエーションクロマトグラフィーによるポリスチレン換算で3,000~80,000が好ましく、より好ましくは、8,000~50,000である。この範囲であれば、厚膜を容易に形成することができる。
一般式(1)および(2)で表される構造を有する樹脂は、公知のポリイミド前駆体およびポリイミドおよびポリベンゾオキサゾール前駆体の製造方法に準じて製造することができる。例えば、(I)R1基を有するテトラカルボン酸二無水物とR2基を有するジアミン化合物、末端封止剤であるモノアミノ化合物を、低温条件下で反応させる方法、(II)R1基を有するテトラカルボン酸二無水物とアルコールとによりジエステルを得、その後R2基を有するジアミン化合物、末端封止剤であるモノアミノ化合物と縮合剤の存在下で反応させる方法、(III)R1基を有するテトラカルボン酸二無水物とアルコールとによりジエステルを得、その後残りの2つのカルボキシル基を酸クロリド化し、R2基を有するジアミン化合物、末端封止剤であるモノアミノ化合物と反応させる方法などを挙げることができる。
上記の方法で重合させた樹脂は、多量の水やメタノール/水の混合液などに投入し、沈殿させてろ別乾燥し、単離することが望ましい。この沈殿操作によって未反応のモノマーや、2量体や3量体などのオリゴマー成分が除去され、熱硬化後の膜特性が向上する。また、ポリイミド前駆体のイミド化をすすめ、閉環したポリイミドは、上記のポリイミド前駆体を得た後に、公知のイミド化反応させる方法を利用して合成することができる。
以下、(I)の好ましい例として、ポリイミド前駆体の製造方法の例について述べる。まず、R2基を有するジアミン化合物を重合溶媒中に溶解する。この溶液に、実質的にジアミン化合物と等モル量の、R1基を有するテトラカルボン酸二無水物を徐々に添加する。メカニカルスターラーを用い、-20~100℃、好ましくは10~50℃で0.5~100時間、より好ましくは2~24時間撹拌する。末端封止剤を用いる場合には、テトラカルボン酸二無水物を添加後、所要温度、所要時間で撹拌した後、末端封止剤を徐々に添加してもよいし、一度に加えて、反応させてもよい。
重合溶媒は、原料モノマーであるテトラカルボン酸二無水物類とジアミン類を溶解できればよく、その種類は特に限定されない。例えば、N,N-ジメチルホルムアミド、N,N-ジメチルアセトアミド、N-メチル-2-ピロリドンのアミド類、γ-ブチロラクトン、γ-バレロラクトン、δ-バレロラクトン、γ-カプロラクトン、ε-カプロラクトン、α-メチル-γ-ブチロラクトンなどの環状エステル類、エチレンカーボネート、プロピレンカーボネートなどのカーボネート類、トリエチレングリコールなどのグリコール類、m-クレゾール、p-クレゾールなどのフェノール類、アセトフェノン、1,3-ジメチル-2-イミダゾリジノン、スルホラン、ジメチルスルホキシドなどを挙げることができる。
重合溶媒は、得られる樹脂100質量部に対して100質量部以上であれば、原料や樹脂の析出なく反応を行うことができ、1900質量部以下であれば速やかに反応が進行するため好ましく、150~950質量部がより好ましい。
また、感光性樹脂組成物の感度を向上させる目的で、必要に応じて、キュア後の収縮率を小さくしない範囲でフェノール性水酸基を有する化合物を含有してもよい。
このフェノール性水酸基を有する化合物は、たとえば、Bis-Z、BisOC-Z、BisOPP-Z、BisP-CP、Bis26X-Z、BisOTBP-Z、BisOCHP-Z、BisOCR-CP、BisP-MZ、BisP-EZ、Bis26X-CP、BisP-PZ、BisP-IPZ、BisCR-IPZ、BisOCP-IPZ、BisOIPP-CP、Bis26X-IPZ、BisOTBP-CP、TekP-4HBPA(テトラキスP-DO-BPA)、TrisP-HAP、TrisP-PA 、TrisP-SA、TrisOCR-PA、BisOFP-Z、BisRS-2P、BisPG-26X、BisRS-3P、BisOC-OCHP、BisPC-OCHP、Bis25X-OCHP、Bis26X-OCHP、BisOCHP-OC、Bis236T-OCHP、メチレントリス-FR-CR、BisRS-26X、BisRS-OCHP、(以上、商品名、本州化学工業(株) 製) 、BIR-OC、BIP-PC、BIR-PC、BIR-PTBP、BIR-PCHP、BIP-BIOC-F、4PC、BIR-BIPC-F、TEP-BIP-A(以上、商品名、旭有機材工業(株)製) が挙げられる。
これらのうち、本発明で用いる好ましいフェノール性水酸基を有する化合物は、たとえば、Bis-Z、BisP-EZ、TekP-4HBPA、TrisP-HAP、TrisP-PA、BisOCHP-Z、BisP-MZ、BisP-PZ、BisP-IPZ、BisOCP-IPZ、BisP-CP、BisRS-2P、BisRS-3P、BisP-OCHP、メチレントリス-FR-CR、BisRS-26X、BIP-PC、BIR-PC、BIR-PTBP、BIR-BIPC-F等が挙げられる。
これらのうち特に好ましいフェノール性水酸基を有する化合物は、たとえば、Bis-Z、TekP-4HBPA、TrisP-HAP、TrisP-PA、BisRS-2P、BisRS-3P、BIR-PC、BIR-PTBP、BIR-BIPC-Fである。このフェノール性水酸基を有する化合物を含有することで、得られる樹脂組成物は、露光前はアルカリ現像液にほとんど溶解せず、露光すると容易にアルカリ現像液に溶解するために、現像による膜減りが少なく、かつ短時間で現像が容易になる。
フェノール性水酸基を有する化合物の含有量は、(a)アルカリ可溶性樹脂100質量部に対して、好ましくは1~50質量部であり、さらに好ましくは3~40質量部の範囲である。
本発明のポジ型の感光性を有する感光性樹脂組成物は、溶剤を含有する。溶剤としては、N-メチル-2-ピロリドン、γ-ブチロラクトン、N,N-ジメチルホルムアミド、N,N-ジメチルアセトアミド、N,N-ジメチルホルムアミド、N,N-ジメチルイソ酪酸アミド、ジメチルスルホキシドなどの極性の非プロトン性溶媒、テトラヒドロフラン、ジオキサン、プロピレングリコールモノメチルエーテル、ジエチレングリコールエチルメチルエーテルなどのエーテル類、アセトン、メチルエチルケトン、ジイソブチルケトン、ジアセトンアルコールなどのケトン類、プロピレングリコールモノメチルエーテルアセテート、3-メトキシメチルプロパネート、3-エトキシエチルプロパネート、酢酸エチル、乳酸エチルなどのエステル類、トルエン、キシレンなどの芳香族炭化水素類などが挙げられる。これらを2種以上含有してもよい。
溶剤の含有量は、(a)アルカリ可溶性樹脂100質量部に対して、100質量部以上1500質量部以下であれば適切な粘度の感光性樹脂組成物が得られるため好ましい。
本発明のポジ型の感光性を有する感光性樹脂組成物は、前記以外の成分を含有してもよく、アルコキシメチル基、メチロール基、またはエポキシ基を有する化合物を架橋剤として含有することが好ましい。メチロール基、アルコキシメチル基は100℃以上の温度領域で架橋反応を生じるため、熱処理により架橋し、優れた機械特性を有する耐熱性樹脂被膜を得ることができる。アルコキシメチル基、メチロール基を有する化合物の含有量は、(c)多官能アクリレート化合物100質量部に対し10~500質量部であることが望ましい。
エポキシ基は、200℃以下でポリマーと熱架橋し、架橋による脱水反応が起こらないため膜収縮が起きにくく、このため、機械特性に加えて低温硬化、低反り化に効果的である。ただし、前述のようにエポキシ基を有する化合物は反応性の高さから、樹脂組成物の室温保存安定性や感度の低下を招く恐れがあるため、エポキシ基を有する化合物の含有量は(c)多官能アクリレート化合物100質量部に対し100質量部以下であることが望ましい。
アルコキシメチル基またはメチロール基を有する例としては、例えば、DML-PC、DML-PEP、DML-OC、DML-OEP、DML-34X、DML-PTBP、DML-PCHP、DML-OCHP、DML-PFP、DML-PSBP、DML-POP、DML-MBOC、DML-MBPC、DML-MTrisPC、DML-BisOC-Z、DML-BisOCHP-Z、DML-BPC、DML-BisOC-P、DMOM-PC、DMOM-PTBP、DMOM-MBPC、TriML-P、TriML-35XL、TML-HQ、TML-BP、TML-pp-BPF、TML-BPE、TML-BPA、TML-BPAF、TML-BPAP、TMOM-BP、TMOM-BPE、TMOM-BPA、TMOM-BPAF、TMOM-BPAP、HML-TPPHBA、HML-TPHAP、HMOM-TPPHBA、HMOM-TPHAP(以上、商品名、本州化学工業(株)製)、NIKALAC(登録商標)MX-290、NIKALAC MX-280、NIKALAC MX-270、NIKALAC MX-279、NIKALAC MW-100LM、NIKALAC MX-750LM(以上、商品名、(株)三和ケミカル製)が挙げられる。この中でも、アルコキシメチル基を多数含有するHMOM-TPHAP、MW-100LMを添加した場合、架橋効率がよいため好ましい。
エポキシ基を有する化合物しては、例えば、ビスフェノールA型エポキシ樹脂、ビスフェノールF型エポキシ樹脂、プロピレングリコールジグリシジルエーテル、ポリプロピレングリコールジグリシジルエーテル、ポリメチル(グリシジロキシプロピル)シロキサン等のエポキシ基含有、シリコーンなどを挙げることができる。本発明は何らこれらに限定されない。具体的には、エピクロン850-S、エピクロンHP-4032、エピクロンHP-7200、エピクロンHP-820、エピクロンHP-4700、エピクロンEXA-4710、エピクロンHP-4770、エピクロンEXA-859CRP、エピクロンEXA-1514、エピクロンEXA-4880、エピクロンEXA-4850-150、エピクロンEXA-4850-1000、エピクロンEXA-4816、エピクロンEXA-4822(以上商品名、大日本インキ化学工業(株)製)、リカレジンBEO-60E(以下商品名、新日本理化株式会社)、EP-4003S、EP-4000S((株)アデカ)などが挙げられる。
これらアルコキシメチル基、メチロール基、またはエポキシ基を有する化合物は2種以上含有してもよい。
本発明の感光性樹脂組成物は、さらにシラン化合物を含有することができる。シラン化合物を含有することにより、耐熱性樹脂被膜の密着性が向上する。シラン化合物の具体例としては、N-フェニルアミノエチルトリメトキシシラン、N-フェニルアミノエチルトリエトキシシラン、N-フェニルアミノプロピルトリメトキシシラン、N-フェニルアミノプロピルトリエトキシシラン、N-フェニルアミノブチルトリメトキシシラン、N-フェニルアミノブチルトリエトキシシラン、ビニルトリメトキシシラン、ビニルトリエトキシシラン、ビニルトリクロルシラン、ビニルトリス(β-メトキシエトキシ)シラン、3-メタクリロキシプロピルトリメトキシシラン、3-アクリロキシプロピルトリメトキシシラン、p-スチリルトリメトキシシラン、3-メタクリロキシプロピルメチルジメトキシシラン、3-メタクリロキシプロピルメチルジエトキシシランなどを挙げることができる。シラン化合物の含有量は、一般式(1)および(2)で表される構造単位の少なくともいずれかを有する樹脂100質量部に対して、好ましくは0.01質量部以上15質量部以下である。
また、本発明のポジ型の感光性を有する感光性樹脂組成物は、必要に応じて、基材との塗れ性を向上させる目的で界面活性剤、乳酸エチルやプロピレングリコールモノメチルエーテルアセテートなどのエステル類、エタノールなどのアルコール類、シクロヘキサノン、メチルイソブチルケトンなどのケトン類、テトラヒドロフラン、ジオキサンなどのエーテル類を含有してもよい。また、熱膨張係数の抑制や高誘電率化、低誘電率化のなどの目的で、二酸化ケイ素、二酸化チタンなどの無機粒子、あるいはポリイミドの粉末などを含有してもよい。
次に、本発明の感光性樹脂組成物の製造方法を例示する。上記の各成分、および必要によりその他成分をガラス製のフラスコやステンレス製の容器に入れて、メカニカルスターラーなどによって撹拌溶解させる方法、超音波で溶解させる方法、遊星式撹拌脱泡装置で撹拌溶解させる方法などが挙げられる。ポジ型感光性樹脂組成物の粘度は、1~10,000mPa・sが好ましい。また、異物を除去するために感光性樹脂組成物を0.1μm~5μmのポアサイズのフィルターで濾過してもよい。
次に、本発明の感光性樹脂組成物を用いて耐熱性樹脂被膜のパターンを形成する方法について説明する。
本発明の感光性樹脂体組成物は、支持基板上に塗布し乾燥する工程、露光する工程、現像する工程および加熱処理する工程を経て、ポリイミドのパターンとすることができる。
まず、感光性樹脂組成物を基板上に塗布する。基板はシリコンウエハ、セラミックス類、ガリウムヒ素、金属、ガラス、金属酸化絶縁膜、窒化ケイ素、ITOなどが用いられる。基板はこれらに限定されない。塗布方法はスピンナを用いた回転塗布、スプレー塗布、ロールコーティング、スリットダイコーティングなどの方法が挙げられる。塗布膜厚は、塗布手法、ポジ型感光性樹脂組成物の固形分濃度、粘度などによって異なる。乾燥後の膜厚が0.1~150μmになるように塗布することが一般的である。
次に、感光性樹脂組成物を塗布した基板を乾燥して、感光性樹脂膜を得る。乾燥はオーブン、ホットプレート、赤外線などを使用し、50℃~150℃の範囲で1分間~数時間行うことが好ましい。
次に、この感光性樹脂膜上に所望のパターンを有するマスクを通して化学線を照射する。露光に用いられる化学線としては紫外線、可視光線、電子線、X線などが挙げられる。本発明では水銀灯のi線(365nm)、h線(405nm)、g線(436nm)を用いることが好ましい。
感光性樹脂膜からパターンを形成するには、露光後、現像液を用いて露光部を除去すればよい。現像液は、テトラメチルアンモニウム、ジエタノールアミン、ジエチルアミノエタノール、水酸化ナトリウム、水酸化カリウム、炭酸ナトリウム、炭酸カリウム、トリエチルアミン、ジエチルアミン、メチルアミン、ジメチルアミン、酢酸ジメチルアミノエチル、ジメチルアミノエタノール、ジメチルアミノエチルメタクリレート、シクロヘキシルアミン、エチレンジアミン、ヘキサメチレンジアミンなどのアルカリ性を示す化合物の水溶液が好ましい。場合によっては、これらのアルカリ水溶液にN-メチル-2-ピロリドン、N,N-ジメチルホルムアミド、N,N-ジメチルアセトアミド、ジメチルスルホキシド、γ-ブチロラクトン、ジメチルアクリルアミドなどの極性溶媒、メタノール、エタノール、イソプロパノールなどのアルコール類、乳酸エチル、プロピレングリコールモノメチルエーテルアセテートなどのエステル類、シクロペンタノン、シクロヘキサノン、イソブチルケトン、メチルイソブチルケトンなどのケトン類などを1種以上添加してもよい。
現像後は水にてリンス処理をすることが一般的である。リンス処理には、エタノール、イソプロピルアルコールなどのアルコール類、乳酸エチル、プロピレングリコールモノメチルエーテルアセテート、3-メトキシメチルプロパネートなどのエステル類などを1種以上水に添加してもよい。
現像後、100℃~400℃の温度を加えて耐熱性樹脂被膜に変換する。この加熱処理は温度を選び、段階的に昇温するか、ある温度範囲を選び連続的に昇温しながら5分間~5時間実施することが好ましい。本発明のポジ型感光性樹脂組成物は250℃以下の低温処理時においても高伸度、高密着性を得られる樹脂組成物であり、例としては、100℃で30分処理した後、220℃で1時間熱処理する方法や、室温より220℃まで1時間かけて直線的に昇温し、220℃で1時間熱処理する方法などが挙げられる。
次に、本発明の感光性樹脂組成物を感光性シートとして使用する場合の製造方法と加工方法を例示する。
前述のようにして製造した感光性樹脂組成物を基材上に塗布し、有機溶剤を除去し、感光性シートを製造する。
感光性樹脂組成物を塗布する基材にはポリエチレンテレフタレート(PET)などを用いることができる。感光性シートをシリコンウエハなどの基板に貼り合わせて用いる際に、基材であるPETフィルムを剥離除去する必要がある場合は、表面にシリコーン樹脂などの離型剤がコーティングされているPETフィルムを用いると、容易に感光性シートとPETフィルムを剥離できるので好ましい。
感光性樹脂組成物をPETフィルム上へ塗布する方法としては、スクリーン印刷、スプレーコーター、バーコーター、ブレードコーター、ダイコーター、スピンコーターなどを用いることができる。有機溶媒を除去する方法としては、オーブンやホットプレートによる加熱の他、真空乾燥、赤外線やマイクロ波などの電磁波による加熱などが挙げられる。ここで、有機溶媒の除去が不十分である場合、次の硬化処理により得られる硬化物が未硬化状態となったり、熱機械特性が不良となったりすることがある。
PETフィルムの厚みは特に限定されない。作業性の観点から、30~80μmの範囲であることが好ましい。また、感光性シートの表面を大気中のゴミ等から保護するために、表面にカバーフィルムを貼り合わせてもよい。また、感光性樹脂組成物の固形分濃度が低く、所望する膜厚の感光性シートを作製できない場合は、有機溶媒除去後の感光性シートを2枚以上貼り合わせても良い。
上記の方法にて製造した感光性シートを別の基板上に貼り合わせる場合は、ロールラミネーターや真空ラミネーターなどのラミネート装置を使用しても、ホットプレート上で加熱した基板にゴムローラーを用いて手動で貼り合わせても良い。基板へ貼り合わせた後、十分に冷却してからPETフィルムを剥離する。
次に、前述の感光性樹脂組成物を用いて耐熱性樹脂被膜のパターンを形成する方法と同様に、所望のパターンを有するマスクを通して基板へ貼り合わせた感光性シートに化学線を照射し、現像液を用いて露光部を除去した後、100℃~400℃の温度を加えて耐熱性樹脂被膜に変換する。 本発明の感光性樹脂組成物により形成した耐熱性樹脂被膜は、半導体装置や多層配線板等の電子部品に使用することができる。具体的には、半導体のパッシベーション膜、半導体素子の表面保護膜、層間絶縁膜、高密度実装用多層配線の層間絶縁膜、インダクタ装置の表面保護膜、層間絶縁膜、有機電界発光素子の絶縁層やスペーサー層、薄膜トランジスタ基板(TFT基板)の平坦化層、有機トランジスタの絶縁層などの用途に好適に用いられる。本発明はこれに制限されず、様々な構造をとることができる。
次に、本発明の感光性樹脂組成物を用いた、バンプを有する半導体装置への応用例1について図面を用いて説明する。図1は、本発明の絶縁膜を有する半導体装置のパット部分の拡大断面図である。図1に示すように、シリコンウエハ1には入出力用のAlパッド2上にパッシベーション膜3が形成され、そのパッシベーション膜3にビアホールが形成されている。この上に本発明の感光性樹脂組成物によるパターンとして絶縁膜4が形成され、更に、金属(Cr、Ti等)膜5がAlパッド2と接続されるように形成される。この上に金属配線6が形成される。4~6の工程を複数回繰り返し、積層させることで、チップ面積を広げずに、高密度、高性能な半導体装置を作製することができる。その後、絶縁膜7の開口部にバリアメタル8とハンダバンプ10が形成される。
次に、本発明の感光性樹脂組成物を用いた、バンプを有する半導体装置への応用例2について図面を用いて説明する。図2は、本発明の絶縁膜を有する半導体装置のパット部分の拡大断面図である。上記の応用例1と同様にAlパッド2、パッシベーション膜3が形成されたシリコンウエハ1はダイシングされチップごとに切り分けられた後、封止樹脂11で封止される。この封止樹脂11とチップ上に渡り、本発明の感光性樹脂組成物によるパターンとして絶縁膜4が形成され、更に、金属(Cr、Ti等)膜5、金属配線(Al、Cu等)6が形成される。その後、チップ外の封止樹脂11上に形成された絶縁膜7の開口部にバリアメタル8とハンダバンプ10が形成される。
次に、本発明の感光性樹脂組成物を用いた、インダクタ装置のコイル部品への応用例3について図面を用いて説明する。図3は本発明の絶縁膜を有するコイル部品の断面図である。図3に示すように、基板12には絶縁膜13、その上にパターンとして絶縁膜14が形成される。基板12としてはフェライト等が用いられる。本発明の感光性樹脂組成物は絶縁膜13と絶縁膜14のどちらに使用してもよい。このパターンの開口部に金属(Cr、Ti等)膜15が形成され、この上に金属配線(Ag、Cu等)16がめっき形成される。金属配線16(Ag、Cu等)はスパイラル上に形成されている。13~16の工程を複数回繰り返し、積層させることでコイルとしての機能を持たせることができる。最後に金属配線(Ag、Cu等)16は金属配線(Ag、Cu等)17によって電極18に接続され、封止樹脂19により封止される。
感光性樹脂組成物に柔軟成分を導入した場合、ウエハの反りが小さいため、露光やウエハの運搬を高精度に行うことができる。これは図1や図3の装置のように絶縁膜と配線層の積層数を増やしたとき特に有用である。また、実装時も封止樹脂からの応力を緩和することができるため、高耐久性の半導体装置を提供できる。図1のような装置において絶縁膜4や絶縁膜7を形成する感光性樹脂組成物はスクライブライン9において、厚膜加工を行うことになるため、より感度が高く、露光部の残渣がない感光性樹脂組成物が望ましい。
また、図2のような装置において絶縁膜4はシリコンウエハと封止樹脂上に渡って形成される。感光性樹脂組成物およびアクリレート化合物に柔軟骨格を導入した場合、高伸度の膜が得られるため、封止樹脂の熱膨張や基板のねじれによる応力を緩和することができる。また、基板面積が大きくなるため、反りの小さい感光性樹脂組成物が望ましい。これらの点から本発明の感光性樹脂組成物は図1、図2のような装置において有用である。
以下、実施例等をあげて本発明を説明する。本発明はこれらの例によって限定されるものではない。なお、実施例中の樹脂および感光性樹脂組成物の作製および評価は以下の方法により行った。
(1)分子量測定
(a)成分のアルカリ可溶性樹脂の分子量は、GPC(ゲルパーミエーションクロマトグラフィー)装置Waters2690-996(日本ウォーターズ(株)製)を用い、展開溶媒をN-メチル-2-ピロリドン(以降NMPと呼ぶ)として測定し、ポリスチレン換算で重量平均分子量(Mw)を計算した。
(a)成分のアルカリ可溶性樹脂の分子量は、GPC(ゲルパーミエーションクロマトグラフィー)装置Waters2690-996(日本ウォーターズ(株)製)を用い、展開溶媒をN-メチル-2-ピロリドン(以降NMPと呼ぶ)として測定し、ポリスチレン換算で重量平均分子量(Mw)を計算した。
(2)アルカリ溶解速度測定
(a)成分のアルカリ可溶性樹脂のアルカリ溶解速度は、ガンマブチロラクトンに溶解させたアルカリ可溶性樹脂を、東京エレクトロン(株)製の塗布現像装置Mark-7を用いて、120℃で3分プリベークし、2.38質量%のテトラメチルアンモニウム(TMAH)水溶液(三菱ガス化学(株)製、ELM-D)で60秒間現像した後、膜厚の変化量(um/min)を計算した。
(a)成分のアルカリ可溶性樹脂のアルカリ溶解速度は、ガンマブチロラクトンに溶解させたアルカリ可溶性樹脂を、東京エレクトロン(株)製の塗布現像装置Mark-7を用いて、120℃で3分プリベークし、2.38質量%のテトラメチルアンモニウム(TMAH)水溶液(三菱ガス化学(株)製、ELM-D)で60秒間現像した後、膜厚の変化量(um/min)を計算した。
(3)ワニスの室温保存安定性の評価
ワニス調製直後の粘度を測定し、ついでこのワニスを室温(23℃、45%RH)で14日放置後、再び粘度を測定した。ワニスの室温保存安定性は、放置前の粘度に対する、14日放置による粘度の変化量(mPa・s)の比率(%)によって評価した。10%未満を合格、10%以上を不合格とした。
ワニス調製直後の粘度を測定し、ついでこのワニスを室温(23℃、45%RH)で14日放置後、再び粘度を測定した。ワニスの室温保存安定性は、放置前の粘度に対する、14日放置による粘度の変化量(mPa・s)の比率(%)によって評価した。10%未満を合格、10%以上を不合格とした。
(4)伸度評価
8インチシリコンウエハ上に、ワニスをプリベーク後の膜厚T1=11μmとなるように塗布現像装置ACT-8(東京エレクトロン(株)製)を用いてスピンコート法で塗布し、120℃で3分プリベークした後、イナートオーブンCLH-21CD-S(光洋サーモシステム(株)製)を用いて、窒素気流下において酸素濃度20ppm以下で毎分3.5℃の昇温速度で220℃まで昇温し、220℃で1時間加熱処理を行なった。46質量%フッ酸水溶液にて剥離し、キュア膜(耐熱性樹脂膜)を得た。この方法で得たキュア膜を7×1cmになるように片刃で切り出し、これをテンシロン万能試験機(オリエンテック社製 RTM-100)にて50mm/分で引っ張った。このときの伸び量をサンプル長で割った値を求めた。この測定を10個のサンプルについて行い、その最大値を伸度とした。伸度が30%以上であることが好ましく、60%以上であることがより好ましい。
8インチシリコンウエハ上に、ワニスをプリベーク後の膜厚T1=11μmとなるように塗布現像装置ACT-8(東京エレクトロン(株)製)を用いてスピンコート法で塗布し、120℃で3分プリベークした後、イナートオーブンCLH-21CD-S(光洋サーモシステム(株)製)を用いて、窒素気流下において酸素濃度20ppm以下で毎分3.5℃の昇温速度で220℃まで昇温し、220℃で1時間加熱処理を行なった。46質量%フッ酸水溶液にて剥離し、キュア膜(耐熱性樹脂膜)を得た。この方法で得たキュア膜を7×1cmになるように片刃で切り出し、これをテンシロン万能試験機(オリエンテック社製 RTM-100)にて50mm/分で引っ張った。このときの伸び量をサンプル長で割った値を求めた。この測定を10個のサンプルについて行い、その最大値を伸度とした。伸度が30%以上であることが好ましく、60%以上であることがより好ましい。
(5)シリコンウエハとの密着性評価
シリコンウエハ上に、スピンナを用いてプリベーク後の膜厚が10μmとなるようにワニスを塗布し、ついでホットプレート(東京エレクトロン(株)製の塗布現像装置D-SPIN)を用いて、120℃で3分プリベークすることにより、感光性樹脂膜を得た。作製された感光性樹脂膜を窒素気流下(酸素濃度20ppm以下)、110℃で30分、その後毎分3.5℃の昇温速度で220℃まで昇温し、220℃で1時間加熱処理を行い、耐熱性樹脂被膜(キュア膜)を作製した。
シリコンウエハ上に、スピンナを用いてプリベーク後の膜厚が10μmとなるようにワニスを塗布し、ついでホットプレート(東京エレクトロン(株)製の塗布現像装置D-SPIN)を用いて、120℃で3分プリベークすることにより、感光性樹脂膜を得た。作製された感光性樹脂膜を窒素気流下(酸素濃度20ppm以下)、110℃で30分、その後毎分3.5℃の昇温速度で220℃まで昇温し、220℃で1時間加熱処理を行い、耐熱性樹脂被膜(キュア膜)を作製した。
キュア膜にカッターで格子状に切込みを入れ、10×10個のマス目をつくり、“セロテープ(登録商標)”による引き剥がしテストを行った。引き剥がしテストで剥がれが全く無ければA、わずかな剥離であればB、剥離が多く見られればCとし、B以上を合格とした。
(6)現像膜Aの作製
8インチシリコンウエハ上にワニスを回転塗布し、次いで、120℃のホットプレート(ACT-8使用)で3分間ベークし、厚さ10μmのプリベーク膜を作製した。この膜を、i線ステッパー(NIKON NSR i9)を用いて0~1000mJ/cm2の露光量にて10mJ/cm2ステップで露光した。露光後、2.38質量%のTMAH水溶液で90秒間現像し、ついで純水でリンスして、ラインアンドスペースのパターンを有する現像膜Aを得た。
8インチシリコンウエハ上にワニスを回転塗布し、次いで、120℃のホットプレート(ACT-8使用)で3分間ベークし、厚さ10μmのプリベーク膜を作製した。この膜を、i線ステッパー(NIKON NSR i9)を用いて0~1000mJ/cm2の露光量にて10mJ/cm2ステップで露光した。露光後、2.38質量%のTMAH水溶液で90秒間現像し、ついで純水でリンスして、ラインアンドスペースのパターンを有する現像膜Aを得た。
(7)感度評価
現像膜Aにて、露光および現像後、露光部分が完全に溶出してなくなった露光量(最小露光量Ethという)を感度とした。Ethが400mJ/cm2以下であれば高感度であると判断できる。300mJ/cm2以下がより好ましい。
現像膜Aにて、露光および現像後、露光部分が完全に溶出してなくなった露光量(最小露光量Ethという)を感度とした。Ethが400mJ/cm2以下であれば高感度であると判断できる。300mJ/cm2以下がより好ましい。
(8)解像度評価
前記Ethの露光量において、ラインアンドスペースが解像している最小の寸法を解像度とした。解像寸法が10um以下であれば高解像度であると判断でき、5um以下がより好ましい。
前記Ethの露光量において、ラインアンドスペースが解像している最小の寸法を解像度とした。解像寸法が10um以下であれば高解像度であると判断でき、5um以下がより好ましい。
以下の実施例、比較例に示す酸二無水物、ジアミン等の略記号の名称は下記の通りである。
ODPA:3,3’,4,4’-ジフェニルエーテルテトラカルボン酸二無水物
CBDA:シクロブタンテトラカルボン酸二無水物
PBOM:1,1’-(4,4’-オキシベンゾイル)ジイミダゾール
6FDA:4,4’-ヘキサフルオロイソプロピリデンジフタル酸二無水物
SiDA:1,1,3,3-テトラメチル-1,3-ビス(3-アミノプロピル)ジシロキサン
BAHF:2,2-ビス(3-アミノ-4-ヒドロキシフェニル)ヘキサフルオロプロパン
NMP:N-メチル-2-ピロリドン
ED-600:“ジェファーミン(登録商標)”ED-600(商品名、HUNTSMAN(株)製脂肪族ジアミン)
ED-900:“ジェファーミン(登録商標)”ED-900(商品名、HUNTSMAN(株)製脂肪族ジアミン)
MAP:メタアミノフェノール
NA:5-ノルボルネン-2,3-ジカルボン酸無水物
KBM-403:3-グリシドキシプロピルトリメトキシシラン。
ODPA:3,3’,4,4’-ジフェニルエーテルテトラカルボン酸二無水物
CBDA:シクロブタンテトラカルボン酸二無水物
PBOM:1,1’-(4,4’-オキシベンゾイル)ジイミダゾール
6FDA:4,4’-ヘキサフルオロイソプロピリデンジフタル酸二無水物
SiDA:1,1,3,3-テトラメチル-1,3-ビス(3-アミノプロピル)ジシロキサン
BAHF:2,2-ビス(3-アミノ-4-ヒドロキシフェニル)ヘキサフルオロプロパン
NMP:N-メチル-2-ピロリドン
ED-600:“ジェファーミン(登録商標)”ED-600(商品名、HUNTSMAN(株)製脂肪族ジアミン)
ED-900:“ジェファーミン(登録商標)”ED-900(商品名、HUNTSMAN(株)製脂肪族ジアミン)
MAP:メタアミノフェノール
NA:5-ノルボルネン-2,3-ジカルボン酸無水物
KBM-403:3-グリシドキシプロピルトリメトキシシラン。
各実施例、比較例に使用した化合物を下記に示した。
合成例1 キノンジアジド化合物(a)の合成
乾燥窒素気流下、ポリヒドロキシ化合物TrisP-PA(商品名、本州化学工業(株)製)21.22g(0.05モル)と5-ナフトキノンジアジドスルホニル酸クロリド26.86g(0.10モル)、4-ナフトキノンジアジドスルホニル酸クロリド13.43g(0.05モル)を1,4-ジオキサン50gに溶解させ、室温にした。ここに、1,4-ジオキサン50gと混合したトリエチルアミン15.18gを、系内が35℃以上にならないように滴下した。滴下後30℃で2時間撹拌した。トリエチルアミン塩を濾過し、ろ液を水に投入した。その後、析出した沈殿をろ過で集めた。この沈殿を真空乾燥機で乾燥させ、下記式で表されるキノンジアジド化合物(a)を得た。
乾燥窒素気流下、ポリヒドロキシ化合物TrisP-PA(商品名、本州化学工業(株)製)21.22g(0.05モル)と5-ナフトキノンジアジドスルホニル酸クロリド26.86g(0.10モル)、4-ナフトキノンジアジドスルホニル酸クロリド13.43g(0.05モル)を1,4-ジオキサン50gに溶解させ、室温にした。ここに、1,4-ジオキサン50gと混合したトリエチルアミン15.18gを、系内が35℃以上にならないように滴下した。滴下後30℃で2時間撹拌した。トリエチルアミン塩を濾過し、ろ液を水に投入した。その後、析出した沈殿をろ過で集めた。この沈殿を真空乾燥機で乾燥させ、下記式で表されるキノンジアジド化合物(a)を得た。
合成例2 キノンジアジド化合物(b)の合成
乾燥窒素気流下、ポリヒドロキシ化合物TrisP-HAP(商品名、本州化学工業(株)製)15.31g(0.05モル)と5-ナフトキノンジアジドスルホニル酸クロリド40.28g(0.15モル)を1,4-ジオキサン450gに溶解させ、室温にした。1,4-ジオキサン50gと混合したトリエチルアミン15.18gを用い、合成例2と同様にして下記式で表されるキノンジアジド化合物(b)を得た。
乾燥窒素気流下、ポリヒドロキシ化合物TrisP-HAP(商品名、本州化学工業(株)製)15.31g(0.05モル)と5-ナフトキノンジアジドスルホニル酸クロリド40.28g(0.15モル)を1,4-ジオキサン450gに溶解させ、室温にした。1,4-ジオキサン50gと混合したトリエチルアミン15.18gを用い、合成例2と同様にして下記式で表されるキノンジアジド化合物(b)を得た。
合成例3 キノンジアジド化合物(c)の合成
乾燥窒素気流下、ポリヒドロキシ化合物TekP-4HBPA(商品名、本州化学工業(株)製)28.83g(0.05モル)と5-ナフトキノンジアジドスルホニル酸クロリド13.43g(0.125モル)を1,4-ジオキサン450gに溶解させ、室温にした。1,4-ジオキサン50gと混合したトリエチルアミン20.24gを用い、合成例2と同様にして下記式で表されるキノンジアジド化合物(c)を得た。
乾燥窒素気流下、ポリヒドロキシ化合物TekP-4HBPA(商品名、本州化学工業(株)製)28.83g(0.05モル)と5-ナフトキノンジアジドスルホニル酸クロリド13.43g(0.125モル)を1,4-ジオキサン450gに溶解させ、室温にした。1,4-ジオキサン50gと混合したトリエチルアミン20.24gを用い、合成例2と同様にして下記式で表されるキノンジアジド化合物(c)を得た。
合成例4 クレゾールノボラック樹脂(d)の合成
乾燥窒素気流下、m-クレゾール70.2g(0.65モル)、p-クレゾール37.8g(0.35モル)、37質量%ホルムアルデヒド水溶液75.5g(ホルムアルデヒド0.93モル)、シュウ酸二水和物0.63g(0.005モル)、メチルイソブチルケトン264gを仕込んだ後、油浴中に浸し、反応液を還流させながら4時間重縮合反応を行った。その後、油浴の温度を3時間かけて昇温し、その後に、フラスコ内の圧力を40~67hPaまで減圧し、揮発分を除去し、溶解している樹脂を室温まで冷却して、アルカリ可溶性フェノール樹脂のクレゾールノボラック樹脂(d)のポリマー固体を得た。GPCからMwは3,500であった。得られたクレゾールノボラック樹脂(d)にγ-ブチロラクトン(GBL)を加え、固形分濃度43質量%のクレゾールノボラック樹脂(d)溶液を得た。この樹脂のアルカリ溶解速度は12,000um/minであった。
乾燥窒素気流下、m-クレゾール70.2g(0.65モル)、p-クレゾール37.8g(0.35モル)、37質量%ホルムアルデヒド水溶液75.5g(ホルムアルデヒド0.93モル)、シュウ酸二水和物0.63g(0.005モル)、メチルイソブチルケトン264gを仕込んだ後、油浴中に浸し、反応液を還流させながら4時間重縮合反応を行った。その後、油浴の温度を3時間かけて昇温し、その後に、フラスコ内の圧力を40~67hPaまで減圧し、揮発分を除去し、溶解している樹脂を室温まで冷却して、アルカリ可溶性フェノール樹脂のクレゾールノボラック樹脂(d)のポリマー固体を得た。GPCからMwは3,500であった。得られたクレゾールノボラック樹脂(d)にγ-ブチロラクトン(GBL)を加え、固形分濃度43質量%のクレゾールノボラック樹脂(d)溶液を得た。この樹脂のアルカリ溶解速度は12,000um/minであった。
合成例5 ポリヒドロキシスチレン(e)の合成
テトラヒドロフラン500ml、開始剤としてsec-ブチルリチウム0.01モルを加えた混合溶液に、p-t-ブトキシスチレンとスチレンをモル比3:1の割合で合計20gを添加し、3時間撹拌しながら重合させた。重合停止反応は反応溶液にメタノール0.1モルを添加して行った。 次にポリマーを精製するために反応混合物をメタノール中に注ぎ、沈降した重合体を乾燥させたところ白色重合体が得られた。更に、アセトン400mlに溶解し、60℃で少量の濃塩酸を加えて7時間撹拌後、水に注ぎ、ポリマーを沈澱させ、p-t-ブトキシスチレンを脱保護してヒドロキシスチレンに変換し、洗浄乾燥したところ、精製されたp-ヒドロキシスチレンとスチレンの共重合体であるポリヒドロキシスチレン(e)が得られた。得られたポリヒドロキシスチレン(e)にGBLを加え、固形分濃度43質量%のポリヒドロキシスチレン(e)溶液を得た。この樹脂のアルカリ溶解速度は5,000um/minであった。
テトラヒドロフラン500ml、開始剤としてsec-ブチルリチウム0.01モルを加えた混合溶液に、p-t-ブトキシスチレンとスチレンをモル比3:1の割合で合計20gを添加し、3時間撹拌しながら重合させた。重合停止反応は反応溶液にメタノール0.1モルを添加して行った。 次にポリマーを精製するために反応混合物をメタノール中に注ぎ、沈降した重合体を乾燥させたところ白色重合体が得られた。更に、アセトン400mlに溶解し、60℃で少量の濃塩酸を加えて7時間撹拌後、水に注ぎ、ポリマーを沈澱させ、p-t-ブトキシスチレンを脱保護してヒドロキシスチレンに変換し、洗浄乾燥したところ、精製されたp-ヒドロキシスチレンとスチレンの共重合体であるポリヒドロキシスチレン(e)が得られた。得られたポリヒドロキシスチレン(e)にGBLを加え、固形分濃度43質量%のポリヒドロキシスチレン(e)溶液を得た。この樹脂のアルカリ溶解速度は5,000um/minであった。
[実施例1]
乾燥窒素気流下、ODPA6.20g(0.020モル)、6FDA13.33g(0.030モル)をNMP100gに溶解させた。ここにMAP1.09g(0.010モル)をNMP20gとともに加えた。さらにBAHF11.90g(0.033モル)、ED-900 9.00g(0.010モル)、SiDA0.62g(0.003モル)をNMP20gとともに加えて、60℃で1時間反応させ、次いで180℃で4時間撹拌した。撹拌終了後、溶液を水2Lに投入して白色沈殿を得た。この沈殿を濾過で集めて、水で3回洗浄した後、50℃の真空乾燥機で72時間乾燥し既閉環ポリイミドアルカリ可溶性樹脂(A)の粉末を得た。この樹脂の重量平均分子量は32,000、アルカリ溶解速度は5,000um/minであった。
乾燥窒素気流下、ODPA6.20g(0.020モル)、6FDA13.33g(0.030モル)をNMP100gに溶解させた。ここにMAP1.09g(0.010モル)をNMP20gとともに加えた。さらにBAHF11.90g(0.033モル)、ED-900 9.00g(0.010モル)、SiDA0.62g(0.003モル)をNMP20gとともに加えて、60℃で1時間反応させ、次いで180℃で4時間撹拌した。撹拌終了後、溶液を水2Lに投入して白色沈殿を得た。この沈殿を濾過で集めて、水で3回洗浄した後、50℃の真空乾燥機で72時間乾燥し既閉環ポリイミドアルカリ可溶性樹脂(A)の粉末を得た。この樹脂の重量平均分子量は32,000、アルカリ溶解速度は5,000um/minであった。
得られたアルカリ可溶性樹脂(A)21.0g、光酸発生剤として合成例1で得られたキノンジアジド化合物(a)3.0g、アルカリ可溶性フェノール樹脂として合成例4で得られたクレゾールノボラック樹脂(d)12.0g、多官能アクリレート化合物として共栄社化学(株)製ライトエステルBP-6EM(分子量629)3.0g、架橋剤MX-270 3.0g、KBM-403 1.0gをGBL25gに加えてポジ型感光性樹脂組成物のワニスを得た。アルカリ可溶性樹脂(A)中の成分を表1に、ワニス中の他樹脂と光酸発生剤を表2に示す。得られたワニスを用いて前記のように、室温保存安定性評価、伸度評価、密着性評価、感度評価、解像度評価を行った。評価結果を表2に示す。
[実施例2]
乾燥窒素気流下、CBDA3.92g(0.020モル)、6FDA13.33g(0.030モル)をNMP100gに溶解させた。ここにMAP1.09g(0.010モル)をNMP20gとともに加えた。さらにBAHF11.90g(0.033モル)、ED-900 9.00g(0.010モル)、SiDA0.62g(0.003モル)をNMP20gとともに加えて、60℃で1時間反応させ、次いで180℃で4時間撹拌した。撹拌終了後、溶液を水2Lに投入して白色沈殿を得た。この沈殿を濾過で集めて、水で3回洗浄した後、50℃の真空乾燥機で72時間乾燥し既閉環ポリイミドアルカリ可溶性樹脂(B)の粉末を得た。この樹脂の重量平均分子量は30,000、アルカリ溶解速度は14,000um/minであった。
乾燥窒素気流下、CBDA3.92g(0.020モル)、6FDA13.33g(0.030モル)をNMP100gに溶解させた。ここにMAP1.09g(0.010モル)をNMP20gとともに加えた。さらにBAHF11.90g(0.033モル)、ED-900 9.00g(0.010モル)、SiDA0.62g(0.003モル)をNMP20gとともに加えて、60℃で1時間反応させ、次いで180℃で4時間撹拌した。撹拌終了後、溶液を水2Lに投入して白色沈殿を得た。この沈殿を濾過で集めて、水で3回洗浄した後、50℃の真空乾燥機で72時間乾燥し既閉環ポリイミドアルカリ可溶性樹脂(B)の粉末を得た。この樹脂の重量平均分子量は30,000、アルカリ溶解速度は14,000um/minであった。
得られたアルカリ可溶性樹脂(B)21.0g、光酸発生剤として合成例2で得られたキノンジアジド化合物(b)3.0g、アルカリ可溶性フェノール樹脂として合成例5で得られたポリヒドロキシスチレン(e)12.0g、多官能アクリレート化合物として日本油脂(株)製ブレンマーPDE-600(分子量771) 3.0g、架橋剤HMOM-TRHAP3.0g、KBM403 1.0gをGBL 25gに加えてポジ型感光性樹脂組成物のワニスを得た。アルカリ可溶性樹脂(B)中の成分を表1に、ワニス中の他樹脂と光酸発生剤を表2に示す。得られたワニスを用いて前記のように、室温保存安定性評価、伸度評価、密着性評価、感度評価、解像度評価を行った。評価結果を表2に示す。
[実施例3]
乾燥窒素気流下、ODPA4.65g(0.020モル)、6FDA13.33g(0.030モル)をNMP100gに溶解させた。ここにBAHF13.73g(0.038モル)、ED-900 9.00g(0.010モル)、SiDA0.62g(0.003モル)をNMP20gとともに加えて、60℃で1時間反応させ、次いで180℃で4時間撹拌した後、末端封止剤として、5-ノルボルネン-2,3-ジカルボン酸無水物(NA)1.64g(0.010モル)をNMP10gとともに加えて、60℃で1時間反応させた撹拌終了後、溶液を水2Lに投入して白色沈殿を得た。この沈殿を濾過で集めて、水で3回洗浄した後、50℃の真空乾燥機で72時間乾燥し既閉環ポリイミドアルカリ可溶性樹脂(C)の粉末を得た。この樹脂の重量平均分子量は37,000、アルカリ溶解速度は6,000um/minであった。
乾燥窒素気流下、ODPA4.65g(0.020モル)、6FDA13.33g(0.030モル)をNMP100gに溶解させた。ここにBAHF13.73g(0.038モル)、ED-900 9.00g(0.010モル)、SiDA0.62g(0.003モル)をNMP20gとともに加えて、60℃で1時間反応させ、次いで180℃で4時間撹拌した後、末端封止剤として、5-ノルボルネン-2,3-ジカルボン酸無水物(NA)1.64g(0.010モル)をNMP10gとともに加えて、60℃で1時間反応させた撹拌終了後、溶液を水2Lに投入して白色沈殿を得た。この沈殿を濾過で集めて、水で3回洗浄した後、50℃の真空乾燥機で72時間乾燥し既閉環ポリイミドアルカリ可溶性樹脂(C)の粉末を得た。この樹脂の重量平均分子量は37,000、アルカリ溶解速度は6,000um/minであった。
得られたアルカリ可溶性樹脂(C)21.0g、光酸発生剤として合成例2で得られたキノンジアジド化合物(c)3.0g、アルカリ可溶性フェノール樹脂として合成例4で得られたクレゾールノボラック樹脂(d)12.0g、多官能アクリレート化合物として日本油脂(株)製ブレンマーPDBE-450A(分子量805)3.0g、架橋剤MX-270 3.0g、KBM403 1.0gをGBL25gに加えてポジ型感光性樹脂組成物のワニスを得た。アルカリ可溶性樹脂(C)中の成分を表1に、ワニス中の他樹脂と光酸発生剤を表2に示す。得られたワニスを用いて前記のように、室温保存安定性評価、伸度評価、密着性評価、感度評価、解像度評価を行った。評価結果を表2に示す。
[実施例4]
乾燥窒素気流下、BAHF13.73g(0.038モル)をNMP185gに溶解させた。ここに、PBOM8.60g(0.024モル)をNMP20gとともに加えて、85℃で3時間反応させた。続いて、ED-900 11.25g(0.013モル)、SiDA0.62g(0.003モル)、PBOM7.53g(0.021モル)をNMP30gとともに加えて、85℃で1時間反応させた。さらに、末端封止剤として、5-ノルボルネン-2,3-ジカルボン酸無水物(NA)1.64g(0.010モル)をNMP10gとともに加えて、85℃で30分反応させた。反応終了後、室温まで冷却し、酢酸15.01g(0.25モル)をNMP58gとともに加えて、室温で1時間攪拌した。攪拌終了後、溶液を水3Lに投入して白色沈殿を得た。この沈殿を濾過で集めて、水で3回洗浄した後、50℃の通風乾燥機で3日間乾燥し、ポリアミドアルカリ可溶性樹脂(D)の粉末を得た。この樹脂の重量平均分子量は38,000、アルカリ溶解速度は10,000um/minであった。
乾燥窒素気流下、BAHF13.73g(0.038モル)をNMP185gに溶解させた。ここに、PBOM8.60g(0.024モル)をNMP20gとともに加えて、85℃で3時間反応させた。続いて、ED-900 11.25g(0.013モル)、SiDA0.62g(0.003モル)、PBOM7.53g(0.021モル)をNMP30gとともに加えて、85℃で1時間反応させた。さらに、末端封止剤として、5-ノルボルネン-2,3-ジカルボン酸無水物(NA)1.64g(0.010モル)をNMP10gとともに加えて、85℃で30分反応させた。反応終了後、室温まで冷却し、酢酸15.01g(0.25モル)をNMP58gとともに加えて、室温で1時間攪拌した。攪拌終了後、溶液を水3Lに投入して白色沈殿を得た。この沈殿を濾過で集めて、水で3回洗浄した後、50℃の通風乾燥機で3日間乾燥し、ポリアミドアルカリ可溶性樹脂(D)の粉末を得た。この樹脂の重量平均分子量は38,000、アルカリ溶解速度は10,000um/minであった。
得られたアルカリ可溶性樹脂(D)21.0g、光酸発生剤として合成例3で得られたキノンジアジド化合物(a)3.0g、アルカリ可溶性フェノール樹脂として合成例5で得られたポリヒドロキシスチレン(e)12.0g、多官能アクリレート化合物として共栄社化学(株)製ライトアクリレートBP-4PA(分子量569)3.0g、架橋剤HMOM-TRHAP3.0g、KBM-403 1.0gをGBL25gに加えてポジ型感光性樹脂組成物のワニスを得た。アルカリ可溶性樹脂(D)中の成分を表1に、ワニス中の他樹脂と光酸発生剤を表2に示す。得られたワニスを用いて前記のように、室温保存安定性評価、伸度評価、密着性評価、感度評価、解像度評価を行った。評価結果を表2に示す。
[比較例1]
実施例1で得られたアルカリ可溶性樹脂(A)21.0g、光酸発生剤として合成例1で得られたキノンジアジド化合物(a)3.0g、アルカリ可溶性フェノール樹脂として合成例4で得られたクレゾールノボラック樹脂(d)12.0g、架橋剤MX-270 3.0g、KBM-403 1.0gをGBL25gに加えてポジ型感光性樹脂組成物のワニスを得た。アルカリ可溶性樹脂(A)中の成分を表1に、ワニス中の他樹脂と光酸発生剤を表2に示す。得られたワニスを用いて前記のように、室温保存安定性評価、伸度評価、ストレス評価、密着性評価、感度評価、解像度評価を行った。評価結果を表2に示す。
実施例1で得られたアルカリ可溶性樹脂(A)21.0g、光酸発生剤として合成例1で得られたキノンジアジド化合物(a)3.0g、アルカリ可溶性フェノール樹脂として合成例4で得られたクレゾールノボラック樹脂(d)12.0g、架橋剤MX-270 3.0g、KBM-403 1.0gをGBL25gに加えてポジ型感光性樹脂組成物のワニスを得た。アルカリ可溶性樹脂(A)中の成分を表1に、ワニス中の他樹脂と光酸発生剤を表2に示す。得られたワニスを用いて前記のように、室温保存安定性評価、伸度評価、ストレス評価、密着性評価、感度評価、解像度評価を行った。評価結果を表2に示す。
[比較例2]
乾燥窒素気流下、CBDA3.92g(0.020モル)、6FDA13.33g(0.030モル)をNMP100gに溶解させた。ここにMAP1.09g(0.010モル)をNMP20gとともに加えた。さらにBAHF15.57g(0.043モル)、SiDA0.62g(0.003モル)をNMP20gとともに加えて、60℃で1時間反応させ、次いで180℃で4時間撹拌した。撹拌終了後、溶液を水2Lに投入して白色沈殿を得た。この沈殿を濾過で集めて、水で3回洗浄した後、50℃の真空乾燥機で72時間乾燥し既閉環ポリイミドアルカリ可溶性樹脂(E)の粉末を得た。この樹脂の重量平均分子量は24,000、アルカリ溶解速度は5,000um/minであった。
乾燥窒素気流下、CBDA3.92g(0.020モル)、6FDA13.33g(0.030モル)をNMP100gに溶解させた。ここにMAP1.09g(0.010モル)をNMP20gとともに加えた。さらにBAHF15.57g(0.043モル)、SiDA0.62g(0.003モル)をNMP20gとともに加えて、60℃で1時間反応させ、次いで180℃で4時間撹拌した。撹拌終了後、溶液を水2Lに投入して白色沈殿を得た。この沈殿を濾過で集めて、水で3回洗浄した後、50℃の真空乾燥機で72時間乾燥し既閉環ポリイミドアルカリ可溶性樹脂(E)の粉末を得た。この樹脂の重量平均分子量は24,000、アルカリ溶解速度は5,000um/minであった。
得られたアルカリ可溶性樹脂(E)21.0g、光酸発生剤として合成例1で得られたキノンジアジド化合物(a)3.0g、アルカリ可溶性フェノール樹脂として合成例4で得られたクレゾールノボラック樹脂(d)12.0g、多官能アクリレート化合物としてブレンマーPDE-600 3.0g、架橋剤MX-270 3.0g、KBM-403 1.0gをGBL25gに加えてポジ型感光性樹脂組成物のワニスを得た。アルカリ可溶性樹脂(E)中の成分を表1に、ワニス中の他樹脂と光酸発生剤を表2に示す。得られたワニスを用いて前記のように、室温保存安定性評価、伸度評価、密着性評価、感度評価、解像度評価を行った。評価結果を表2に示す。
[比較例3]
実施例3で得られたアルカリ可溶性樹脂(C)21.0g、光酸発生剤として合成例1で得られたキノンジアジド化合物(a)3.0g、アルカリ可溶性フェノール樹脂として合成例4で得られたノボラック樹脂(d)12.0g、架橋剤エピクロンEXA-4822(大日本インキ化学工業(株)製)3.0g、KBM-403 1.0gをGBL25gに加えてポジ型感光性樹脂組成物のワニスを得た。アルカリ可溶性樹脂(C)中の成分を表1に、ワニス中の他樹脂と光酸発生剤を表2に示す。得られたワニスを用いて前記のように、室温保存安定性評価、伸度評価、密着性評価、感度評価、解像度評価を行った。評価結果を表2に示す。
実施例3で得られたアルカリ可溶性樹脂(C)21.0g、光酸発生剤として合成例1で得られたキノンジアジド化合物(a)3.0g、アルカリ可溶性フェノール樹脂として合成例4で得られたノボラック樹脂(d)12.0g、架橋剤エピクロンEXA-4822(大日本インキ化学工業(株)製)3.0g、KBM-403 1.0gをGBL25gに加えてポジ型感光性樹脂組成物のワニスを得た。アルカリ可溶性樹脂(C)中の成分を表1に、ワニス中の他樹脂と光酸発生剤を表2に示す。得られたワニスを用いて前記のように、室温保存安定性評価、伸度評価、密着性評価、感度評価、解像度評価を行った。評価結果を表2に示す。
[比較例4]
乾燥窒素気流下、BAHF17.40g、0.048モル)をNMP185gに溶解させた。ここに、PBOM8.60g(0.024モル)をNMP20gとともに加えて、85℃で3時間反応させた。続いて、SiDA0.62g(0.003モル)、PBOM7.53g(0.021モル)をNMP30gとともに加えて、85℃で1時間反応させた。さらに、末端封止剤として、5-ノルボルネン-2,3-ジカルボン酸無水物(NA)1.64g(0.010モル)をNMP10gとともに加えて、85℃で30分反応させた。反応終了後、室温まで冷却し、酢酸15.01g(0.25モル)をNMP58gとともに加えて、室温で1時間攪拌した。攪拌終了後、溶液を水3Lに投入して白色沈殿を得た。この沈殿を濾過で集めて、水で3回洗浄した後、50℃の通風乾燥機で3日間乾燥し、ポリアミドアルカリ可溶性樹脂(F)の粉末を得た。この樹脂の重量平均分子量は36,000、アルカリ溶解速度は500um/minであった。
乾燥窒素気流下、BAHF17.40g、0.048モル)をNMP185gに溶解させた。ここに、PBOM8.60g(0.024モル)をNMP20gとともに加えて、85℃で3時間反応させた。続いて、SiDA0.62g(0.003モル)、PBOM7.53g(0.021モル)をNMP30gとともに加えて、85℃で1時間反応させた。さらに、末端封止剤として、5-ノルボルネン-2,3-ジカルボン酸無水物(NA)1.64g(0.010モル)をNMP10gとともに加えて、85℃で30分反応させた。反応終了後、室温まで冷却し、酢酸15.01g(0.25モル)をNMP58gとともに加えて、室温で1時間攪拌した。攪拌終了後、溶液を水3Lに投入して白色沈殿を得た。この沈殿を濾過で集めて、水で3回洗浄した後、50℃の通風乾燥機で3日間乾燥し、ポリアミドアルカリ可溶性樹脂(F)の粉末を得た。この樹脂の重量平均分子量は36,000、アルカリ溶解速度は500um/minであった。
得られたアルカリ可溶性樹脂(F)21.0g、光酸発生剤として合成例3で得られたキノンジアジド化合物(a)3.0g、アルカリ可溶性フェノール樹脂として合成例4で得られたクレゾールノボラック樹脂(d)12.0g、多官能アクリレート化合物としてブレンマーPDBE-450A3.0g架橋剤MX-270 4.0g、KBM-403 1.0gをGBL25gに加えてポジ型感光性樹脂組成物のワニスを得た。アルカリ可溶性樹脂(F)中の成分を表1に、ワニス中の他樹脂と光酸発生剤を表2に示す。得られたワニスを用いて前記のように、室温保存安定性評価、伸度評価、密着性評価、感度評価、解像度評価を行った。評価結果を表2に示す。
1 シリコンウエハ
2 Alパッド
3 パッシベーション膜
4 絶縁膜
5 金属(Cr、Ti等)膜
6 金属配線(Al、Cu等)
7 絶縁膜
8 バリアメタル
9 スクライブライン
10 ハンダバンプ
11 封止樹脂
12 基板
13 絶縁膜
14 絶縁膜
15 金属(Cr、Ti等)膜
16 金属配線(Ag、Cu等)
17 金属配線(Ag、Cu等)
18 電極
19 封止樹脂
2 Alパッド
3 パッシベーション膜
4 絶縁膜
5 金属(Cr、Ti等)膜
6 金属配線(Al、Cu等)
7 絶縁膜
8 バリアメタル
9 スクライブライン
10 ハンダバンプ
11 封止樹脂
12 基板
13 絶縁膜
14 絶縁膜
15 金属(Cr、Ti等)膜
16 金属配線(Ag、Cu等)
17 金属配線(Ag、Cu等)
18 電極
19 封止樹脂
Claims (16)
- (a)ポリイミド前駆体、ポリベンゾオキサゾール前駆体、ポリアミドイミド前駆体、ポリイミド、およびそれらの共重合体から選ばれる少なくとも1種を含むアルカリ可溶性樹脂と、(b)光酸発生剤と、(c)多官能アクリレート化合物を含有し、前記(a)アルカリ可溶性樹脂が分子内に脂肪族鎖を有することを特徴とするポジ型感光性樹脂組成物。
- 前記(a)アルカリ可溶性樹脂が一般式(1)および(2)で表される構造単位の少なくともいずれかを有し、前記脂肪族鎖が一般式(3)で表されるポリエーテルブロック構造単位であって、前記一般式(1)におけるR2および一般式(2)におけるR6の少なくともいずれかが、一般式(3)で表されるポリエーテルブロック構造単位を含有する、請求項1に記載のポジ型感光性樹脂組成物。
- 前記(c)多官能アクリレート化合物の分子量が、100以上2000以下である請求項1または2に記載のポジ型感光性樹脂組成物。
- 前記(a)アルカリ可溶性樹脂のアルカリ水溶液に対する溶解速度が100~4,0000nm/分である請求項1~4のいずれかに記載のポジ型感光性樹脂組成物。
- さらに(d)アルカリ可溶性フェノール樹脂を含有する請求項1~5のいずれかに記載のポジ型感光性樹脂組成物。
- 前記(d)アルカリ可溶性フェノール樹脂のアルカリ水溶液に対する溶解速度が100~20,000nm/分である請求項6に記載のポジ型感光性樹脂組成物。
- 前記(a)アルカリ可溶性樹脂が末端に不飽和結合をもつ有機基を有する請求項1~7のいずれかに記載のポジ型感光性樹脂組成物。
- 請求項1~8のいずれかに記載のポジ型感光性樹脂組成物から形成された感光性シート。
- 請求項1~8のいずれかに記載のポジ型感光性樹脂組成物または請求項9に記載の感光性シートを硬化した硬化膜。
- 請求項10に記載の硬化膜が配置された、層間絶縁膜または半導体保護膜。
- 請求項1~8のいずれかに記載のポジ型感光性樹脂組成物を基材上に塗布した後、または請求項9に記載の感光性シートを基材上に貼り合わせた後に紫外線照射工程と現像工程を経てパターンを形成し、さらに加熱して硬化膜のレリーフパターン層を形成する工程を含む、半導体装置の製造方法。
- 請求項10に記載の硬化膜のレリーフパターン層を有する、半導体電子部品または半導体装置。
- 請求項10に記載の硬化膜が再配線間の層間絶縁膜として配置された、半導体電子部品または半導体装置。
- 前記再配線と層間絶縁膜が2~10層繰り返し配置された、請求項14に記載の半導体電子部品または半導体装置。
- 請求項10に記載の硬化膜が、2種以上の材質で構成される隣接する基板の層間絶縁膜として配置された、半導体電子部品または半導体装置。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2016564638A JPWO2017073481A1 (ja) | 2015-10-28 | 2016-10-21 | ポジ型感光性樹脂組成物、感光性シート、硬化膜、層間絶縁膜、半導体保護膜、半導体装置の製造方法、半導体電子部品および半導体装置 |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2015211481 | 2015-10-28 | ||
| JP2015-211481 | 2015-10-28 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2017073481A1 true WO2017073481A1 (ja) | 2017-05-04 |
Family
ID=58630358
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2016/081264 WO2017073481A1 (ja) | 2015-10-28 | 2016-10-21 | ポジ型感光性樹脂組成物、感光性シート、硬化膜、層間絶縁膜、半導体保護膜、半導体装置の製造方法、半導体電子部品および半導体装置 |
Country Status (3)
| Country | Link |
|---|---|
| JP (1) | JPWO2017073481A1 (ja) |
| TW (1) | TW201729001A (ja) |
| WO (1) | WO2017073481A1 (ja) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP3358407A4 (en) * | 2015-09-28 | 2019-05-22 | Toray Industries, Inc. | HARDENED FILM AND METHOD FOR THE PRODUCTION THEREOF |
| CN116149140A (zh) * | 2023-04-19 | 2023-05-23 | 明士(北京)新材料开发有限公司 | 一种高耐化性正性光敏性树脂组合物及其制备方法和应用 |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP7318530B2 (ja) * | 2018-03-22 | 2023-08-01 | 東レ株式会社 | アルカリ可溶性樹脂、感光性樹脂組成物、感光性シート、硬化膜、層間絶縁膜または半導体保護膜、硬化膜のレリーフパターンの製造方法、電子部品または半導体装置 |
Citations (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2009081950A1 (ja) * | 2007-12-26 | 2009-07-02 | Asahi Kasei E-Materials Corporation | 耐熱性樹脂前駆体及びそれを用いた感光性樹脂組成物 |
| US20100167471A1 (en) * | 2008-12-30 | 2010-07-01 | Stmicroelectronics Asia Pacific Pte. Ltd. | Reducing warpage for fan-out wafer level packaging |
| JP2011208025A (ja) * | 2010-03-30 | 2011-10-20 | Asahi Kasei E-Materials Corp | ポリイミド前駆体及びポリイミド前駆体を用いた感光性樹脂組成物 |
| JP2012208360A (ja) * | 2011-03-30 | 2012-10-25 | Toray Ind Inc | ポジ型感光性樹脂組成物 |
| JP2013003310A (ja) * | 2011-06-15 | 2013-01-07 | Hitachi Chemical Dupont Microsystems Ltd | 感光性樹脂組成物、パターン硬化膜の製造方法及び電子部品 |
| JP2013152476A (ja) * | 2008-05-29 | 2013-08-08 | Asahi Kasei E-Materials Corp | 感光性樹脂組成物 |
| JP2014154800A (ja) * | 2013-02-13 | 2014-08-25 | Shinko Electric Ind Co Ltd | 配線基板及びその製造方法 |
| JP2015031724A (ja) * | 2013-07-31 | 2015-02-16 | 日立化成株式会社 | 半導体装置の製造方法及びその製造方法によって得られる半導体装置 |
-
2016
- 2016-10-21 WO PCT/JP2016/081264 patent/WO2017073481A1/ja active Application Filing
- 2016-10-21 JP JP2016564638A patent/JPWO2017073481A1/ja active Pending
- 2016-10-27 TW TW105134668A patent/TW201729001A/zh unknown
Patent Citations (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2009081950A1 (ja) * | 2007-12-26 | 2009-07-02 | Asahi Kasei E-Materials Corporation | 耐熱性樹脂前駆体及びそれを用いた感光性樹脂組成物 |
| JP2013152476A (ja) * | 2008-05-29 | 2013-08-08 | Asahi Kasei E-Materials Corp | 感光性樹脂組成物 |
| US20100167471A1 (en) * | 2008-12-30 | 2010-07-01 | Stmicroelectronics Asia Pacific Pte. Ltd. | Reducing warpage for fan-out wafer level packaging |
| JP2011208025A (ja) * | 2010-03-30 | 2011-10-20 | Asahi Kasei E-Materials Corp | ポリイミド前駆体及びポリイミド前駆体を用いた感光性樹脂組成物 |
| JP2012208360A (ja) * | 2011-03-30 | 2012-10-25 | Toray Ind Inc | ポジ型感光性樹脂組成物 |
| JP2013003310A (ja) * | 2011-06-15 | 2013-01-07 | Hitachi Chemical Dupont Microsystems Ltd | 感光性樹脂組成物、パターン硬化膜の製造方法及び電子部品 |
| JP2014154800A (ja) * | 2013-02-13 | 2014-08-25 | Shinko Electric Ind Co Ltd | 配線基板及びその製造方法 |
| JP2015031724A (ja) * | 2013-07-31 | 2015-02-16 | 日立化成株式会社 | 半導体装置の製造方法及びその製造方法によって得られる半導体装置 |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP3358407A4 (en) * | 2015-09-28 | 2019-05-22 | Toray Industries, Inc. | HARDENED FILM AND METHOD FOR THE PRODUCTION THEREOF |
| CN116149140A (zh) * | 2023-04-19 | 2023-05-23 | 明士(北京)新材料开发有限公司 | 一种高耐化性正性光敏性树脂组合物及其制备方法和应用 |
Also Published As
| Publication number | Publication date |
|---|---|
| JPWO2017073481A1 (ja) | 2018-08-16 |
| TW201729001A (zh) | 2017-08-16 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6982786B2 (ja) | 感光性フィルム | |
| TWI693468B (zh) | 感光性樹脂組成物及電子零件 | |
| JP6724363B2 (ja) | 樹脂および感光性樹脂組成物 | |
| TWI720018B (zh) | 樹脂及感光性樹脂組成物、以及樹脂之製造方法 | |
| KR20170125842A (ko) | 감광성 수지 조성물, 수지 경화막의 제조 방법 및 반도체 장치 | |
| JPWO2018047688A1 (ja) | 樹脂組成物 | |
| JP7247655B2 (ja) | 感光性樹脂組成物 | |
| JP6939553B2 (ja) | 樹脂組成物 | |
| KR101969197B1 (ko) | 포지티브형 감광성 수지 조성물 | |
| JP2018123103A (ja) | ジアミン化合物、それを用いた耐熱性樹脂および樹脂組成物 | |
| WO2017073481A1 (ja) | ポジ型感光性樹脂組成物、感光性シート、硬化膜、層間絶縁膜、半導体保護膜、半導体装置の製造方法、半導体電子部品および半導体装置 | |
| JP2018036329A (ja) | 感光性樹脂組成物 | |
| JP6776772B2 (ja) | 感光性樹脂組成物 | |
| JP2016161894A (ja) | 感光性樹脂組成物 | |
| JPWO2019181782A1 (ja) | アルカリ可溶性樹脂、感光性樹脂組成物、感光性シート、硬化膜、層間絶縁膜または半導体保護膜、硬化膜のレリーフパターンの製造方法、電子部品または半導体装置 | |
| WO2022163335A1 (ja) | 感光性樹脂組成物、硬化膜、電子部品、アンテナ素子、半導体パッケージおよび化合物 | |
| JP2020094194A (ja) | 樹脂組成物、樹脂シート、硬化膜、硬化膜のレリーフパターンの製造方法、保護膜、絶縁膜、電子部品および表示装置 | |
| JP2018095721A (ja) | 樹脂組成物、樹脂シートおよび硬化膜 | |
| KR20230104869A (ko) | 수지 조성물, 경화막, 절연막 또는 보호막, 안테나 소자, 그리고 전자 부품, 표시 장치 또는 반도체 장치 및 그의 제조 방법 | |
| JP2019012181A (ja) | 感光性樹脂組成物、感光性シート、硬化膜、層間絶縁膜、半導体保護膜、半導体装置の製造方法、半導体電子部品および半導体装置 | |
| TW201413387A (zh) | 正型感光性樹脂組成物 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| ENP | Entry into the national phase |
Ref document number: 2016564638 Country of ref document: JP Kind code of ref document: A |
|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 16859711 Country of ref document: EP Kind code of ref document: A1 |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| 122 | Ep: pct application non-entry in european phase |
Ref document number: 16859711 Country of ref document: EP Kind code of ref document: A1 |