WO2015022051A1 - Materialien für elektronische vorrichtungen - Google Patents
Materialien für elektronische vorrichtungen Download PDFInfo
- Publication number
- WO2015022051A1 WO2015022051A1 PCT/EP2014/002031 EP2014002031W WO2015022051A1 WO 2015022051 A1 WO2015022051 A1 WO 2015022051A1 EP 2014002031 W EP2014002031 W EP 2014002031W WO 2015022051 A1 WO2015022051 A1 WO 2015022051A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- formula
- substituted
- radicals
- group
- aromatic
- Prior art date
Links
- 239000000463 material Substances 0.000 title claims description 40
- 150000001875 compounds Chemical class 0.000 claims abstract description 138
- ICPSWZFVWAPUKF-UHFFFAOYSA-N 1,1'-spirobi[fluorene] Chemical group C1=CC=C2C=C3C4(C=5C(C6=CC=CC=C6C=5)=CC=C4)C=CC=C3C2=C1 ICPSWZFVWAPUKF-UHFFFAOYSA-N 0.000 claims abstract description 13
- 125000003118 aryl group Chemical group 0.000 claims description 86
- 125000004432 carbon atom Chemical group C* 0.000 claims description 52
- 239000011159 matrix material Substances 0.000 claims description 39
- 230000005525 hole transport Effects 0.000 claims description 28
- 125000000217 alkyl group Chemical group 0.000 claims description 25
- 229910052739 hydrogen Inorganic materials 0.000 claims description 25
- 229910052731 fluorine Inorganic materials 0.000 claims description 24
- 125000003545 alkoxy group Chemical group 0.000 claims description 23
- 125000006165 cyclic alkyl group Chemical group 0.000 claims description 20
- 125000001072 heteroaryl group Chemical group 0.000 claims description 20
- 229920000642 polymer Polymers 0.000 claims description 19
- 229910052805 deuterium Inorganic materials 0.000 claims description 16
- 239000000203 mixture Substances 0.000 claims description 13
- 229910052760 oxygen Inorganic materials 0.000 claims description 13
- 238000000034 method Methods 0.000 claims description 12
- 229910052799 carbon Inorganic materials 0.000 claims description 10
- 239000000412 dendrimer Substances 0.000 claims description 10
- 229920000736 dendritic polymer Polymers 0.000 claims description 10
- 125000003342 alkenyl group Chemical group 0.000 claims description 9
- 125000000304 alkynyl group Chemical group 0.000 claims description 7
- 229910052710 silicon Inorganic materials 0.000 claims description 7
- 239000002904 solvent Substances 0.000 claims description 7
- 229910052717 sulfur Inorganic materials 0.000 claims description 7
- 125000000609 carbazolyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3NC12)* 0.000 claims description 6
- 238000009472 formulation Methods 0.000 claims description 6
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims description 6
- 125000001769 aryl amino group Chemical group 0.000 claims description 5
- 229910052794 bromium Inorganic materials 0.000 claims description 5
- 229910052801 chlorine Inorganic materials 0.000 claims description 5
- 125000004429 atom Chemical group 0.000 claims description 4
- 238000005859 coupling reaction Methods 0.000 claims description 4
- 125000002524 organometallic group Chemical group 0.000 claims description 4
- 229910052796 boron Inorganic materials 0.000 claims description 3
- 229910052740 iodine Inorganic materials 0.000 claims description 3
- 125000001424 substituent group Chemical group 0.000 claims description 3
- 125000001931 aliphatic group Chemical group 0.000 claims description 2
- 238000009833 condensation Methods 0.000 claims description 2
- 230000005494 condensation Effects 0.000 claims description 2
- 230000005669 field effect Effects 0.000 claims description 2
- 230000003287 optical effect Effects 0.000 claims description 2
- 108091008695 photoreceptors Proteins 0.000 claims description 2
- 238000010791 quenching Methods 0.000 claims description 2
- 239000010409 thin film Substances 0.000 claims description 2
- IANQTJSKSUMEQM-UHFFFAOYSA-N 1-benzofuran Chemical group C1=CC=C2OC=CC2=C1 IANQTJSKSUMEQM-UHFFFAOYSA-N 0.000 abstract description 3
- 238000004519 manufacturing process Methods 0.000 abstract description 2
- 239000010410 layer Substances 0.000 description 104
- 150000003254 radicals Chemical class 0.000 description 51
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 48
- -1 benzocarboline Chemical compound 0.000 description 29
- 230000015572 biosynthetic process Effects 0.000 description 28
- 238000003786 synthesis reaction Methods 0.000 description 28
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 17
- 239000000543 intermediate Substances 0.000 description 15
- ZUOUZKKEUPVFJK-UHFFFAOYSA-N diphenyl Chemical compound C1=CC=CC=C1C1=CC=CC=C1 ZUOUZKKEUPVFJK-UHFFFAOYSA-N 0.000 description 14
- 239000000243 solution Substances 0.000 description 13
- UJOBWOGCFQCDNV-UHFFFAOYSA-N 9H-carbazole Chemical compound C1=CC=C2C3=CC=CC=C3NC2=C1 UJOBWOGCFQCDNV-UHFFFAOYSA-N 0.000 description 12
- IMNFDUFMRHMDMM-UHFFFAOYSA-N N-Heptane Chemical compound CCCCCCC IMNFDUFMRHMDMM-UHFFFAOYSA-N 0.000 description 12
- 238000002347 injection Methods 0.000 description 12
- 239000007924 injection Substances 0.000 description 12
- 230000000903 blocking effect Effects 0.000 description 11
- 229910052751 metal Inorganic materials 0.000 description 11
- 239000002184 metal Substances 0.000 description 11
- 239000012074 organic phase Substances 0.000 description 11
- TXCDCPKCNAJMEE-UHFFFAOYSA-N dibenzofuran Chemical compound C1=CC=C2C3=CC=CC=C3OC2=C1 TXCDCPKCNAJMEE-UHFFFAOYSA-N 0.000 description 10
- IYYZUPMFVPLQIF-UHFFFAOYSA-N dibenzothiophene Chemical compound C1=CC=C2C3=CC=CC=C3SC2=C1 IYYZUPMFVPLQIF-UHFFFAOYSA-N 0.000 description 10
- 239000002019 doping agent Substances 0.000 description 10
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 9
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 9
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 8
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 8
- BASFCYQUMIYNBI-UHFFFAOYSA-N platinum Chemical compound [Pt] BASFCYQUMIYNBI-UHFFFAOYSA-N 0.000 description 8
- 238000006116 polymerization reaction Methods 0.000 description 8
- BBEAQIROQSPTKN-UHFFFAOYSA-N pyrene Chemical compound C1=CC=C2C=CC3=CC=CC4=CC=C1C2=C43 BBEAQIROQSPTKN-UHFFFAOYSA-N 0.000 description 8
- 239000000741 silica gel Substances 0.000 description 8
- 229910002027 silica gel Inorganic materials 0.000 description 8
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 7
- MWPLVEDNUUSJAV-UHFFFAOYSA-N anthracene Chemical compound C1=CC=CC2=CC3=CC=CC=C3C=C21 MWPLVEDNUUSJAV-UHFFFAOYSA-N 0.000 description 7
- 239000004305 biphenyl Substances 0.000 description 7
- 235000010290 biphenyl Nutrition 0.000 description 7
- 150000002739 metals Chemical class 0.000 description 7
- 239000000178 monomer Substances 0.000 description 7
- 239000011541 reaction mixture Substances 0.000 description 7
- BWHDROKFUHTORW-UHFFFAOYSA-N tritert-butylphosphane Chemical compound CC(C)(C)P(C(C)(C)C)C(C)(C)C BWHDROKFUHTORW-UHFFFAOYSA-N 0.000 description 7
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 6
- UFWIBTONFRDIAS-UHFFFAOYSA-N Naphthalene Chemical compound C1=CC=CC2=CC=CC=C21 UFWIBTONFRDIAS-UHFFFAOYSA-N 0.000 description 6
- KDLHZDBZIXYQEI-UHFFFAOYSA-N Palladium Chemical compound [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 6
- 150000001412 amines Chemical class 0.000 description 6
- GVEPBJHOBDJJJI-UHFFFAOYSA-N fluoranthrene Natural products C1=CC(C2=CC=CC=C22)=C3C2=CC=CC3=C1 GVEPBJHOBDJJJI-UHFFFAOYSA-N 0.000 description 6
- 125000005842 heteroatom Chemical group 0.000 description 6
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 6
- 229910052709 silver Inorganic materials 0.000 description 6
- 125000005259 triarylamine group Chemical group 0.000 description 6
- 238000001816 cooling Methods 0.000 description 5
- 239000012043 crude product Substances 0.000 description 5
- NIHNNTQXNPWCJQ-UHFFFAOYSA-N fluorene Chemical compound C1=CC=C2CC3=CC=CC=C3C2=C1 NIHNNTQXNPWCJQ-UHFFFAOYSA-N 0.000 description 5
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 5
- 229910052697 platinum Inorganic materials 0.000 description 5
- 238000002360 preparation method Methods 0.000 description 5
- 238000007639 printing Methods 0.000 description 5
- DXBHBZVCASKNBY-UHFFFAOYSA-N 1,2-Benz(a)anthracene Chemical compound C1=CC=C2C3=CC4=CC=CC=C4C=C3C=CC2=C1 DXBHBZVCASKNBY-UHFFFAOYSA-N 0.000 description 4
- YJTKZCDBKVTVBY-UHFFFAOYSA-N 1,3-Diphenylbenzene Chemical group C1=CC=CC=C1C1=CC=CC(C=2C=CC=CC=2)=C1 YJTKZCDBKVTVBY-UHFFFAOYSA-N 0.000 description 4
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 4
- IDZBFQIPENLMQI-UHFFFAOYSA-N 4-(2-bromophenyl)dibenzofuran Chemical compound BrC1=CC=CC=C1C1=CC=CC2=C1OC1=CC=CC=C21 IDZBFQIPENLMQI-UHFFFAOYSA-N 0.000 description 4
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 4
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 4
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 4
- URLKBWYHVLBVBO-UHFFFAOYSA-N Para-Xylene Chemical group CC1=CC=C(C)C=C1 URLKBWYHVLBVBO-UHFFFAOYSA-N 0.000 description 4
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 4
- SMWDFEZZVXVKRB-UHFFFAOYSA-N Quinoline Chemical compound N1=CC=CC2=CC=CC=C21 SMWDFEZZVXVKRB-UHFFFAOYSA-N 0.000 description 4
- YTPLMLYBLZKORZ-UHFFFAOYSA-N Thiophene Chemical compound C=1C=CSC=1 YTPLMLYBLZKORZ-UHFFFAOYSA-N 0.000 description 4
- 150000004982 aromatic amines Chemical class 0.000 description 4
- IOJUPLGTWVMSFF-UHFFFAOYSA-N benzothiazole Chemical compound C1=CC=C2SC=NC2=C1 IOJUPLGTWVMSFF-UHFFFAOYSA-N 0.000 description 4
- 150000001716 carbazoles Chemical class 0.000 description 4
- 238000006243 chemical reaction Methods 0.000 description 4
- 239000000460 chlorine Substances 0.000 description 4
- 125000004122 cyclic group Chemical group 0.000 description 4
- 150000002148 esters Chemical class 0.000 description 4
- 238000001914 filtration Methods 0.000 description 4
- 238000004128 high performance liquid chromatography Methods 0.000 description 4
- 229910044991 metal oxide Inorganic materials 0.000 description 4
- 150000004706 metal oxides Chemical class 0.000 description 4
- QPJVMBTYPHYUOC-UHFFFAOYSA-N methyl benzoate Chemical compound COC(=O)C1=CC=CC=C1 QPJVMBTYPHYUOC-UHFFFAOYSA-N 0.000 description 4
- 229910052757 nitrogen Inorganic materials 0.000 description 4
- YNPNZTXNASCQKK-UHFFFAOYSA-N phenanthrene Chemical compound C1=CC=C2C3=CC=CC=C3C=CC2=C1 YNPNZTXNASCQKK-UHFFFAOYSA-N 0.000 description 4
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 3
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 3
- MZRVEZGGRBJDDB-UHFFFAOYSA-N N-Butyllithium Chemical compound [Li]CCCC MZRVEZGGRBJDDB-UHFFFAOYSA-N 0.000 description 3
- BQCADISMDOOEFD-UHFFFAOYSA-N Silver Chemical compound [Ag] BQCADISMDOOEFD-UHFFFAOYSA-N 0.000 description 3
- SLGBZMMZGDRARJ-UHFFFAOYSA-N Triphenylene Natural products C1=CC=C2C3=CC=CC=C3C3=CC=CC=C3C2=C1 SLGBZMMZGDRARJ-UHFFFAOYSA-N 0.000 description 3
- 229910052784 alkaline earth metal Inorganic materials 0.000 description 3
- 229910052782 aluminium Inorganic materials 0.000 description 3
- 238000009835 boiling Methods 0.000 description 3
- XJHCXCQVJFPJIK-UHFFFAOYSA-M cesium fluoride Substances [F-].[Cs+] XJHCXCQVJFPJIK-UHFFFAOYSA-M 0.000 description 3
- 229910052802 copper Inorganic materials 0.000 description 3
- 239000010949 copper Substances 0.000 description 3
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 3
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 3
- 150000004985 diamines Chemical class 0.000 description 3
- 125000004986 diarylamino group Chemical group 0.000 description 3
- RAXXELZNTBOGNW-UHFFFAOYSA-N imidazole Natural products C1=CNC=N1 RAXXELZNTBOGNW-UHFFFAOYSA-N 0.000 description 3
- PJULCNAVAGQLAT-UHFFFAOYSA-N indeno[2,1-a]fluorene Chemical compound C1=CC=C2C=C3C4=CC5=CC=CC=C5C4=CC=C3C2=C1 PJULCNAVAGQLAT-UHFFFAOYSA-N 0.000 description 3
- 229910052741 iridium Inorganic materials 0.000 description 3
- GKOZUEZYRPOHIO-UHFFFAOYSA-N iridium atom Chemical compound [Ir] GKOZUEZYRPOHIO-UHFFFAOYSA-N 0.000 description 3
- 150000002576 ketones Chemical class 0.000 description 3
- 239000008204 material by function Substances 0.000 description 3
- MPQXHAGKBWFSNV-UHFFFAOYSA-N oxidophosphanium Chemical class [PH3]=O MPQXHAGKBWFSNV-UHFFFAOYSA-N 0.000 description 3
- 230000001681 protective effect Effects 0.000 description 3
- 238000002390 rotary evaporation Methods 0.000 description 3
- 229920006395 saturated elastomer Polymers 0.000 description 3
- 239000004332 silver Substances 0.000 description 3
- 239000011734 sodium Substances 0.000 description 3
- 238000003756 stirring Methods 0.000 description 3
- 239000000725 suspension Substances 0.000 description 3
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 3
- CXWXQJXEFPUFDZ-UHFFFAOYSA-N tetralin Chemical compound C1=CC=C2CCCCC2=C1 CXWXQJXEFPUFDZ-UHFFFAOYSA-N 0.000 description 3
- 229930192474 thiophene Natural products 0.000 description 3
- 230000007704 transition Effects 0.000 description 3
- 229910052723 transition metal Inorganic materials 0.000 description 3
- 150000003624 transition metals Chemical class 0.000 description 3
- BFIMMTCNYPIMRN-UHFFFAOYSA-N 1,2,3,5-tetramethylbenzene Chemical compound CC1=CC(C)=C(C)C(C)=C1 BFIMMTCNYPIMRN-UHFFFAOYSA-N 0.000 description 2
- UUSUFQUCLACDTA-UHFFFAOYSA-N 1,2-dihydropyrene Chemical compound C1=CC=C2C=CC3=CCCC4=CC=C1C2=C43 UUSUFQUCLACDTA-UHFFFAOYSA-N 0.000 description 2
- CHLICZRVGGXEOD-UHFFFAOYSA-N 1-Methoxy-4-methylbenzene Chemical compound COC1=CC=C(C)C=C1 CHLICZRVGGXEOD-UHFFFAOYSA-N 0.000 description 2
- FCEHBMOGCRZNNI-UHFFFAOYSA-N 1-benzothiophene Chemical compound C1=CC=C2SC=CC2=C1 FCEHBMOGCRZNNI-UHFFFAOYSA-N 0.000 description 2
- QPUYECUOLPXSFR-UHFFFAOYSA-N 1-methylnaphthalene Chemical compound C1=CC=C2C(C)=CC=CC2=C1 QPUYECUOLPXSFR-UHFFFAOYSA-N 0.000 description 2
- DXYYSGDWQCSKKO-UHFFFAOYSA-N 2-methylbenzothiazole Chemical compound C1=CC=C2SC(C)=NC2=C1 DXYYSGDWQCSKKO-UHFFFAOYSA-N 0.000 description 2
- DMEVMYSQZPJFOK-UHFFFAOYSA-N 3,4,5,6,9,10-hexazatetracyclo[12.4.0.02,7.08,13]octadeca-1(18),2(7),3,5,8(13),9,11,14,16-nonaene Chemical group N1=NN=C2C3=CC=CC=C3C3=CC=NN=C3C2=N1 DMEVMYSQZPJFOK-UHFFFAOYSA-N 0.000 description 2
- KDCGOANMDULRCW-UHFFFAOYSA-N 7H-purine Chemical compound N1=CNC2=NC=NC2=C1 KDCGOANMDULRCW-UHFFFAOYSA-N 0.000 description 2
- KWOLFJPFCHCOCG-UHFFFAOYSA-N Acetophenone Chemical compound CC(=O)C1=CC=CC=C1 KWOLFJPFCHCOCG-UHFFFAOYSA-N 0.000 description 2
- HKMTVMBEALTRRR-UHFFFAOYSA-N Benzo[a]fluorene Chemical group C1=CC=CC2=C3CC4=CC=CC=C4C3=CC=C21 HKMTVMBEALTRRR-UHFFFAOYSA-N 0.000 description 2
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 2
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 2
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 2
- YLQBMQCUIZJEEH-UHFFFAOYSA-N Furan Chemical compound C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 2
- LTEQMZWBSYACLV-UHFFFAOYSA-N Hexylbenzene Chemical compound CCCCCCC1=CC=CC=C1 LTEQMZWBSYACLV-UHFFFAOYSA-N 0.000 description 2
- SIKJAQJRHWYJAI-UHFFFAOYSA-N Indole Chemical compound C1=CC=C2NC=CC2=C1 SIKJAQJRHWYJAI-UHFFFAOYSA-N 0.000 description 2
- ZOKXTWBITQBERF-UHFFFAOYSA-N Molybdenum Chemical compound [Mo] ZOKXTWBITQBERF-UHFFFAOYSA-N 0.000 description 2
- SECXISVLQFMRJM-UHFFFAOYSA-N N-Methylpyrrolidone Chemical compound CN1CCCC1=O SECXISVLQFMRJM-UHFFFAOYSA-N 0.000 description 2
- PCLIMKBDDGJMGD-UHFFFAOYSA-N N-bromosuccinimide Chemical compound BrN1C(=O)CCC1=O PCLIMKBDDGJMGD-UHFFFAOYSA-N 0.000 description 2
- CTQNGGLPUBDAKN-UHFFFAOYSA-N O-Xylene Chemical compound CC1=CC=CC=C1C CTQNGGLPUBDAKN-UHFFFAOYSA-N 0.000 description 2
- PWATWSYOIIXYMA-UHFFFAOYSA-N Pentylbenzene Chemical compound CCCCCC1=CC=CC=C1 PWATWSYOIIXYMA-UHFFFAOYSA-N 0.000 description 2
- PCNDJXKNXGMECE-UHFFFAOYSA-N Phenazine Natural products C1=CC=CC2=NC3=CC=CC=C3N=C21 PCNDJXKNXGMECE-UHFFFAOYSA-N 0.000 description 2
- KYQCOXFCLRTKLS-UHFFFAOYSA-N Pyrazine Chemical compound C1=CN=CC=N1 KYQCOXFCLRTKLS-UHFFFAOYSA-N 0.000 description 2
- CZPWVGJYEJSRLH-UHFFFAOYSA-N Pyrimidine Chemical compound C1=CN=CN=C1 CZPWVGJYEJSRLH-UHFFFAOYSA-N 0.000 description 2
- KAESVJOAVNADME-UHFFFAOYSA-N Pyrrole Chemical compound C=1C=CNC=1 KAESVJOAVNADME-UHFFFAOYSA-N 0.000 description 2
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 2
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 2
- DZBUGLKDJFMEHC-UHFFFAOYSA-N acridine Chemical compound C1=CC=CC2=CC3=CC=CC=C3N=C21 DZBUGLKDJFMEHC-UHFFFAOYSA-N 0.000 description 2
- 229910052783 alkali metal Inorganic materials 0.000 description 2
- 150000001340 alkali metals Chemical class 0.000 description 2
- 150000001342 alkaline earth metals Chemical class 0.000 description 2
- RDOXTESZEPMUJZ-UHFFFAOYSA-N anisole Chemical compound COC1=CC=CC=C1 RDOXTESZEPMUJZ-UHFFFAOYSA-N 0.000 description 2
- 125000005577 anthracene group Chemical group 0.000 description 2
- 150000008365 aromatic ketones Chemical class 0.000 description 2
- 229910052788 barium Inorganic materials 0.000 description 2
- 150000001642 boronic acid derivatives Chemical class 0.000 description 2
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 2
- XSIFPSYPOVKYCO-UHFFFAOYSA-N butyl benzoate Chemical compound CCCCOC(=O)C1=CC=CC=C1 XSIFPSYPOVKYCO-UHFFFAOYSA-N 0.000 description 2
- MVPPADPHJFYWMZ-UHFFFAOYSA-N chlorobenzene Chemical compound ClC1=CC=CC=C1 MVPPADPHJFYWMZ-UHFFFAOYSA-N 0.000 description 2
- 238000004587 chromatography analysis Methods 0.000 description 2
- WDECIBYCCFPHNR-UHFFFAOYSA-N chrysene Chemical compound C1=CC=CC2=CC=C3C4=CC=CC=C4C=CC3=C21 WDECIBYCCFPHNR-UHFFFAOYSA-N 0.000 description 2
- 238000010549 co-Evaporation Methods 0.000 description 2
- 230000000052 comparative effect Effects 0.000 description 2
- 238000010276 construction Methods 0.000 description 2
- RWGFKTVRMDUZSP-UHFFFAOYSA-N cumene Chemical compound CC(C)C1=CC=CC=C1 RWGFKTVRMDUZSP-UHFFFAOYSA-N 0.000 description 2
- JHIVVAPYMSGYDF-UHFFFAOYSA-N cyclohexanone Chemical compound O=C1CCCCC1 JHIVVAPYMSGYDF-UHFFFAOYSA-N 0.000 description 2
- NNBZCPXTIHJBJL-UHFFFAOYSA-N decalin Chemical compound C1CCCC2CCCCC21 NNBZCPXTIHJBJL-UHFFFAOYSA-N 0.000 description 2
- MHDVGSVTJDSBDK-UHFFFAOYSA-N dibenzyl ether Chemical compound C=1C=CC=CC=1COCC1=CC=CC=C1 MHDVGSVTJDSBDK-UHFFFAOYSA-N 0.000 description 2
- 239000006185 dispersion Substances 0.000 description 2
- SQNZJJAZBFDUTD-UHFFFAOYSA-N durene Chemical compound CC1=CC(C)=C(C)C=C1C SQNZJJAZBFDUTD-UHFFFAOYSA-N 0.000 description 2
- 238000001194 electroluminescence spectrum Methods 0.000 description 2
- 239000000839 emulsion Substances 0.000 description 2
- MTZQAGJQAFMTAQ-UHFFFAOYSA-N ethyl benzoate Chemical compound CCOC(=O)C1=CC=CC=C1 MTZQAGJQAFMTAQ-UHFFFAOYSA-N 0.000 description 2
- YLQWCDOCJODRMT-UHFFFAOYSA-N fluoren-9-one Chemical compound C1=CC=C2C(=O)C3=CC=CC=C3C2=C1 YLQWCDOCJODRMT-UHFFFAOYSA-N 0.000 description 2
- 229910052737 gold Inorganic materials 0.000 description 2
- 239000010931 gold Substances 0.000 description 2
- 239000005457 ice water Substances 0.000 description 2
- PQNFLJBBNBOBRQ-UHFFFAOYSA-N indane Chemical compound C1=CC=C2CCCC2=C1 PQNFLJBBNBOBRQ-UHFFFAOYSA-N 0.000 description 2
- WUNJCKOTXFSWBK-UHFFFAOYSA-N indeno[2,1-a]carbazole Chemical compound C1=CC=C2C=C3C4=NC5=CC=CC=C5C4=CC=C3C2=C1 WUNJCKOTXFSWBK-UHFFFAOYSA-N 0.000 description 2
- AMGQUBHHOARCQH-UHFFFAOYSA-N indium;oxotin Chemical compound [In].[Sn]=O AMGQUBHHOARCQH-UHFFFAOYSA-N 0.000 description 2
- 238000007641 inkjet printing Methods 0.000 description 2
- PNDPGZBMCMUPRI-UHFFFAOYSA-N iodine Chemical group II PNDPGZBMCMUPRI-UHFFFAOYSA-N 0.000 description 2
- AWJUIBRHMBBTKR-UHFFFAOYSA-N isoquinoline Chemical compound C1=NC=CC2=CC=CC=C21 AWJUIBRHMBBTKR-UHFFFAOYSA-N 0.000 description 2
- 150000003951 lactams Chemical class 0.000 description 2
- IVSZLXZYQVIEFR-UHFFFAOYSA-N m-xylene Chemical compound CC1=CC=CC(C)=C1 IVSZLXZYQVIEFR-UHFFFAOYSA-N 0.000 description 2
- 229910052749 magnesium Inorganic materials 0.000 description 2
- 239000011777 magnesium Substances 0.000 description 2
- 229940095102 methyl benzoate Drugs 0.000 description 2
- 229910052750 molybdenum Inorganic materials 0.000 description 2
- 239000011733 molybdenum Substances 0.000 description 2
- PXHVJJICTQNCMI-UHFFFAOYSA-N nickel Substances [Ni] PXHVJJICTQNCMI-UHFFFAOYSA-N 0.000 description 2
- 150000002894 organic compounds Chemical class 0.000 description 2
- 239000012044 organic layer Substances 0.000 description 2
- 239000011368 organic material Substances 0.000 description 2
- 125000004430 oxygen atom Chemical group O* 0.000 description 2
- HFPZCAJZSCWRBC-UHFFFAOYSA-N p-cymene Chemical compound CC(C)C1=CC=C(C)C=C1 HFPZCAJZSCWRBC-UHFFFAOYSA-N 0.000 description 2
- 229910052763 palladium Inorganic materials 0.000 description 2
- RDOWQLZANAYVLL-UHFFFAOYSA-N phenanthridine Chemical compound C1=CC=C2C3=CC=CC=C3C=NC2=C1 RDOWQLZANAYVLL-UHFFFAOYSA-N 0.000 description 2
- SCVFZCLFOSHCOH-UHFFFAOYSA-M potassium acetate Chemical compound [K+].CC([O-])=O SCVFZCLFOSHCOH-UHFFFAOYSA-M 0.000 description 2
- 238000000746 purification Methods 0.000 description 2
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 2
- XSCHRSMBECNVNS-UHFFFAOYSA-N quinoxaline Chemical compound N1=CC=NC2=CC=CC=C21 XSCHRSMBECNVNS-UHFFFAOYSA-N 0.000 description 2
- 238000010992 reflux Methods 0.000 description 2
- 229910052702 rhenium Inorganic materials 0.000 description 2
- WUAPFZMCVAUBPE-UHFFFAOYSA-N rhenium atom Chemical compound [Re] WUAPFZMCVAUBPE-UHFFFAOYSA-N 0.000 description 2
- 239000004065 semiconductor Substances 0.000 description 2
- 150000004756 silanes Chemical class 0.000 description 2
- 229910052938 sodium sulfate Inorganic materials 0.000 description 2
- 235000011152 sodium sulphate Nutrition 0.000 description 2
- 239000007787 solid Substances 0.000 description 2
- 238000004528 spin coating Methods 0.000 description 2
- 125000003003 spiro group Chemical group 0.000 description 2
- 238000005092 sublimation method Methods 0.000 description 2
- 239000000126 substance Substances 0.000 description 2
- 238000006467 substitution reaction Methods 0.000 description 2
- 239000000758 substrate Substances 0.000 description 2
- 150000003462 sulfoxides Chemical class 0.000 description 2
- ZUHZGEOKBKGPSW-UHFFFAOYSA-N tetraglyme Chemical compound COCCOCCOCCOCCOC ZUHZGEOKBKGPSW-UHFFFAOYSA-N 0.000 description 2
- 150000003918 triazines Chemical class 0.000 description 2
- WFKWXMTUELFFGS-UHFFFAOYSA-N tungsten Chemical compound [W] WFKWXMTUELFFGS-UHFFFAOYSA-N 0.000 description 2
- 229910052721 tungsten Inorganic materials 0.000 description 2
- 239000010937 tungsten Substances 0.000 description 2
- ABDKAPXRBAPSQN-UHFFFAOYSA-N veratrole Chemical compound COC1=CC=CC=C1OC ABDKAPXRBAPSQN-UHFFFAOYSA-N 0.000 description 2
- LHXDLQBQYFFVNW-OIBJUYFYSA-N (-)-Fenchone Chemical compound C1C[C@@]2(C)C(=O)C(C)(C)[C@@H]1C2 LHXDLQBQYFFVNW-OIBJUYFYSA-N 0.000 description 1
- 229930006729 (1R,4S)-fenchone Natural products 0.000 description 1
- CYPYTURSJDMMMP-WVCUSYJESA-N (1e,4e)-1,5-diphenylpenta-1,4-dien-3-one;palladium Chemical compound [Pd].[Pd].C=1C=CC=CC=1\C=C\C(=O)\C=C\C1=CC=CC=C1.C=1C=CC=CC=1\C=C\C(=O)\C=C\C1=CC=CC=C1.C=1C=CC=CC=1\C=C\C(=O)\C=C\C1=CC=CC=C1 CYPYTURSJDMMMP-WVCUSYJESA-N 0.000 description 1
- WUOACPNHFRMFPN-SECBINFHSA-N (S)-(-)-alpha-terpineol Chemical compound CC1=CC[C@@H](C(C)(C)O)CC1 WUOACPNHFRMFPN-SECBINFHSA-N 0.000 description 1
- HQDYNFWTFJFEPR-UHFFFAOYSA-N 1,2,3,3a-tetrahydropyrene Chemical compound C1=C2CCCC(C=C3)C2=C2C3=CC=CC2=C1 HQDYNFWTFJFEPR-UHFFFAOYSA-N 0.000 description 1
- ZFXBERJDEUDDMX-UHFFFAOYSA-N 1,2,3,5-tetrazine Chemical compound C1=NC=NN=N1 ZFXBERJDEUDDMX-UHFFFAOYSA-N 0.000 description 1
- FNQJDLTXOVEEFB-UHFFFAOYSA-N 1,2,3-benzothiadiazole Chemical compound C1=CC=C2SN=NC2=C1 FNQJDLTXOVEEFB-UHFFFAOYSA-N 0.000 description 1
- JYEUMXHLPRZUAT-UHFFFAOYSA-N 1,2,3-triazine Chemical compound C1=CN=NN=C1 JYEUMXHLPRZUAT-UHFFFAOYSA-N 0.000 description 1
- HTJMXYRLEDBSLT-UHFFFAOYSA-N 1,2,4,5-tetrazine Chemical compound C1=NN=CN=N1 HTJMXYRLEDBSLT-UHFFFAOYSA-N 0.000 description 1
- BBVIDBNAYOIXOE-UHFFFAOYSA-N 1,2,4-oxadiazole Chemical compound C=1N=CON=1 BBVIDBNAYOIXOE-UHFFFAOYSA-N 0.000 description 1
- YGTAZGSLCXNBQL-UHFFFAOYSA-N 1,2,4-thiadiazole Chemical compound C=1N=CSN=1 YGTAZGSLCXNBQL-UHFFFAOYSA-N 0.000 description 1
- FYADHXFMURLYQI-UHFFFAOYSA-N 1,2,4-triazine Chemical compound C1=CN=NC=N1 FYADHXFMURLYQI-UHFFFAOYSA-N 0.000 description 1
- UDGKZGLPXCRRAM-UHFFFAOYSA-N 1,2,5-thiadiazole Chemical compound C=1C=NSN=1 UDGKZGLPXCRRAM-UHFFFAOYSA-N 0.000 description 1
- WQONPSCCEXUXTQ-UHFFFAOYSA-N 1,2-dibromobenzene Chemical compound BrC1=CC=CC=C1Br WQONPSCCEXUXTQ-UHFFFAOYSA-N 0.000 description 1
- UXJHQQLYKUVLIE-UHFFFAOYSA-N 1,2-dihydroacridine Chemical class C1=CC=C2N=C(C=CCC3)C3=CC2=C1 UXJHQQLYKUVLIE-UHFFFAOYSA-N 0.000 description 1
- FKASFBLJDCHBNZ-UHFFFAOYSA-N 1,3,4-oxadiazole Chemical compound C1=NN=CO1 FKASFBLJDCHBNZ-UHFFFAOYSA-N 0.000 description 1
- MBIZXFATKUQOOA-UHFFFAOYSA-N 1,3,4-thiadiazole Chemical compound C1=NN=CS1 MBIZXFATKUQOOA-UHFFFAOYSA-N 0.000 description 1
- JIHQDMXYYFUGFV-UHFFFAOYSA-N 1,3,5-triazine Chemical compound C1=NC=NC=N1 JIHQDMXYYFUGFV-UHFFFAOYSA-N 0.000 description 1
- BCMCBBGGLRIHSE-UHFFFAOYSA-N 1,3-benzoxazole Chemical compound C1=CC=C2OC=NC2=C1 BCMCBBGGLRIHSE-UHFFFAOYSA-N 0.000 description 1
- SPPWGCYEYAMHDT-UHFFFAOYSA-N 1,4-di(propan-2-yl)benzene Chemical compound CC(C)C1=CC=C(C(C)C)C=C1 SPPWGCYEYAMHDT-UHFFFAOYSA-N 0.000 description 1
- FLBAYUMRQUHISI-UHFFFAOYSA-N 1,8-naphthyridine Chemical compound N1=CC=CC2=CC=CN=C21 FLBAYUMRQUHISI-UHFFFAOYSA-N 0.000 description 1
- UHXOHPVVEHBKKT-UHFFFAOYSA-N 1-(2,2-diphenylethenyl)-4-[4-(2,2-diphenylethenyl)phenyl]benzene Chemical compound C=1C=C(C=2C=CC(C=C(C=3C=CC=CC=3)C=3C=CC=CC=3)=CC=2)C=CC=1C=C(C=1C=CC=CC=1)C1=CC=CC=C1 UHXOHPVVEHBKKT-UHFFFAOYSA-N 0.000 description 1
- OSIGJGFTADMDOB-UHFFFAOYSA-N 1-Methoxy-3-methylbenzene Chemical compound COC1=CC=CC(C)=C1 OSIGJGFTADMDOB-UHFFFAOYSA-N 0.000 description 1
- LBNXAWYDQUGHGX-UHFFFAOYSA-N 1-Phenylheptane Chemical compound CCCCCCCC1=CC=CC=C1 LBNXAWYDQUGHGX-UHFFFAOYSA-N 0.000 description 1
- HYLLZXPMJRMUHH-UHFFFAOYSA-N 1-[2-(2-methoxyethoxy)ethoxy]butane Chemical compound CCCCOCCOCCOC HYLLZXPMJRMUHH-UHFFFAOYSA-N 0.000 description 1
- SNAQINZKMQFYFV-UHFFFAOYSA-N 1-[2-[2-(2-methoxyethoxy)ethoxy]ethoxy]butane Chemical compound CCCCOCCOCCOCCOC SNAQINZKMQFYFV-UHFFFAOYSA-N 0.000 description 1
- RERATEUBWLKDFE-UHFFFAOYSA-N 1-methoxy-2-[2-(2-methoxypropoxy)propoxy]propane Chemical compound COCC(C)OCC(C)OCC(C)OC RERATEUBWLKDFE-UHFFFAOYSA-N 0.000 description 1
- JCHJBEZBHANKGA-UHFFFAOYSA-N 1-methoxy-3,5-dimethylbenzene Chemical compound COC1=CC(C)=CC(C)=C1 JCHJBEZBHANKGA-UHFFFAOYSA-N 0.000 description 1
- WCOYPFBMFKXWBM-UHFFFAOYSA-N 1-methyl-2-phenoxybenzene Chemical compound CC1=CC=CC=C1OC1=CC=CC=C1 WCOYPFBMFKXWBM-UHFFFAOYSA-N 0.000 description 1
- UDONPJKEOAWFGI-UHFFFAOYSA-N 1-methyl-3-phenoxybenzene Chemical compound CC1=CC=CC(OC=2C=CC=CC=2)=C1 UDONPJKEOAWFGI-UHFFFAOYSA-N 0.000 description 1
- WJFKNYWRSNBZNX-UHFFFAOYSA-N 10H-phenothiazine Chemical compound C1=CC=C2NC3=CC=CC=C3SC2=C1 WJFKNYWRSNBZNX-UHFFFAOYSA-N 0.000 description 1
- TZMSYXZUNZXBOL-UHFFFAOYSA-N 10H-phenoxazine Chemical compound C1=CC=C2NC3=CC=CC=C3OC2=C1 TZMSYXZUNZXBOL-UHFFFAOYSA-N 0.000 description 1
- 238000005160 1H NMR spectroscopy Methods 0.000 description 1
- QWENRTYMTSOGBR-UHFFFAOYSA-N 1H-1,2,3-Triazole Chemical compound C=1C=NNN=1 QWENRTYMTSOGBR-UHFFFAOYSA-N 0.000 description 1
- HYZJCKYKOHLVJF-UHFFFAOYSA-N 1H-benzimidazole Chemical compound C1=CC=C2NC=NC2=C1 HYZJCKYKOHLVJF-UHFFFAOYSA-N 0.000 description 1
- BAXOFTOLAUCFNW-UHFFFAOYSA-N 1H-indazole Chemical compound C1=CC=C2C=NNC2=C1 BAXOFTOLAUCFNW-UHFFFAOYSA-N 0.000 description 1
- LPHIYKWSEYTCLW-UHFFFAOYSA-N 1h-azaborole Chemical compound N1B=CC=C1 LPHIYKWSEYTCLW-UHFFFAOYSA-N 0.000 description 1
- USYCQABRSUEURP-UHFFFAOYSA-N 1h-benzo[f]benzimidazole Chemical compound C1=CC=C2C=C(NC=N3)C3=CC2=C1 USYCQABRSUEURP-UHFFFAOYSA-N 0.000 description 1
- JUUZQMUWOVDZSD-UHFFFAOYSA-N 1h-imidazole;pyrazine Chemical compound C1=CNC=N1.C1=CN=CC=N1 JUUZQMUWOVDZSD-UHFFFAOYSA-N 0.000 description 1
- IGHOZKDBCCFNNC-UHFFFAOYSA-N 1h-imidazole;quinoxaline Chemical compound C1=CNC=N1.N1=CC=NC2=CC=CC=C21 IGHOZKDBCCFNNC-UHFFFAOYSA-N 0.000 description 1
- PLJDGKPRGUMSAA-UHFFFAOYSA-N 2,2',7,7'-tetraphenyl-1,1'-spirobi[fluorene] Chemical compound C12=CC=C(C=3C=CC=CC=3)C=C2C=C(C23C(=CC=C4C5=CC=C(C=C5C=C43)C=3C=CC=CC=3)C=3C=CC=CC=3)C1=CC=C2C1=CC=CC=C1 PLJDGKPRGUMSAA-UHFFFAOYSA-N 0.000 description 1
- 125000004206 2,2,2-trifluoroethyl group Chemical group [H]C([H])(*)C(F)(F)F 0.000 description 1
- VEPOHXYIFQMVHW-XOZOLZJESA-N 2,3-dihydroxybutanedioic acid (2S,3S)-3,4-dimethyl-2-phenylmorpholine Chemical compound OC(C(O)C(O)=O)C(O)=O.C[C@H]1[C@@H](OCCN1C)c1ccccc1 VEPOHXYIFQMVHW-XOZOLZJESA-N 0.000 description 1
- ZNOVTXRBGFNYRX-UHFFFAOYSA-N 2-[[4-[(2-amino-5-methyl-4-oxo-1,6,7,8-tetrahydropteridin-6-yl)methylamino]benzoyl]amino]pentanedioic acid Chemical compound C1NC=2NC(N)=NC(=O)C=2N(C)C1CNC1=CC=C(C(=O)NC(CCC(O)=O)C(O)=O)C=C1 ZNOVTXRBGFNYRX-UHFFFAOYSA-N 0.000 description 1
- UXGVMFHEKMGWMA-UHFFFAOYSA-N 2-benzofuran Chemical compound C1=CC=CC2=COC=C21 UXGVMFHEKMGWMA-UHFFFAOYSA-N 0.000 description 1
- LYTMVABTDYMBQK-UHFFFAOYSA-N 2-benzothiophene Chemical compound C1=CC=CC2=CSC=C21 LYTMVABTDYMBQK-UHFFFAOYSA-N 0.000 description 1
- CRWNQZTZTZWPOF-UHFFFAOYSA-N 2-methyl-4-phenylpyridine Chemical compound C1=NC(C)=CC(C=2C=CC=CC=2)=C1 CRWNQZTZTZWPOF-UHFFFAOYSA-N 0.000 description 1
- 125000004493 2-methylbut-1-yl group Chemical group CC(C*)CC 0.000 description 1
- QCDWFXQBSFUVSP-UHFFFAOYSA-N 2-phenoxyethanol Chemical compound OCCOC1=CC=CC=C1 QCDWFXQBSFUVSP-UHFFFAOYSA-N 0.000 description 1
- LIBHEMBTFRBMOV-UHFFFAOYSA-N 2-phenyl-n-(4-phenylphenyl)aniline Chemical compound C=1C=CC=C(C=2C=CC=CC=2)C=1NC(C=C1)=CC=C1C1=CC=CC=C1 LIBHEMBTFRBMOV-UHFFFAOYSA-N 0.000 description 1
- TVYVQNHYIHAJTD-UHFFFAOYSA-N 2-propan-2-ylnaphthalene Chemical compound C1=CC=CC2=CC(C(C)C)=CC=C21 TVYVQNHYIHAJTD-UHFFFAOYSA-N 0.000 description 1
- VHMICKWLTGFITH-UHFFFAOYSA-N 2H-isoindole Chemical compound C1=CC=CC2=CNC=C21 VHMICKWLTGFITH-UHFFFAOYSA-N 0.000 description 1
- IAWRFMPNMXEJCK-UHFFFAOYSA-N 3-phenyl-9h-carbazole Chemical compound C1=CC=CC=C1C1=CC=C(NC=2C3=CC=CC=2)C3=C1 IAWRFMPNMXEJCK-UHFFFAOYSA-N 0.000 description 1
- ALWNKSOATKGNPM-UHFFFAOYSA-N 4,4,5,5-tetramethyl-3-propan-2-yloxydioxaborolane Chemical compound C(C)(C)OB1OOC(C1(C)C)(C)C ALWNKSOATKGNPM-UHFFFAOYSA-N 0.000 description 1
- HHVGZHHLRBNWAD-UHFFFAOYSA-N 4,6-diphenyltriazine Chemical compound C1=CC=CC=C1C1=CC(C=2C=CC=CC=2)=NN=N1 HHVGZHHLRBNWAD-UHFFFAOYSA-N 0.000 description 1
- NCSVCMFDHINRJE-UHFFFAOYSA-N 4-[1-(3,4-dimethylphenyl)ethyl]-1,2-dimethylbenzene Chemical compound C=1C=C(C)C(C)=CC=1C(C)C1=CC=C(C)C(C)=C1 NCSVCMFDHINRJE-UHFFFAOYSA-N 0.000 description 1
- LVUBSVWMOWKPDJ-UHFFFAOYSA-N 4-methoxy-1,2-dimethylbenzene Chemical compound COC1=CC=C(C)C(C)=C1 LVUBSVWMOWKPDJ-UHFFFAOYSA-N 0.000 description 1
- 229940077398 4-methyl anisole Drugs 0.000 description 1
- NSPMIYGKQJPBQR-UHFFFAOYSA-N 4H-1,2,4-triazole Chemical compound C=1N=CNN=1 NSPMIYGKQJPBQR-UHFFFAOYSA-N 0.000 description 1
- PVFOHMXILQEIHX-UHFFFAOYSA-N 8-[(6-bromo-1,3-benzodioxol-5-yl)sulfanyl]-9-[2-(2-bromophenyl)ethyl]purin-6-amine Chemical compound C=1C=2OCOC=2C=C(Br)C=1SC1=NC=2C(N)=NC=NC=2N1CCC1=CC=CC=C1Br PVFOHMXILQEIHX-UHFFFAOYSA-N 0.000 description 1
- USVZHTBPMMSRHY-UHFFFAOYSA-N 8-[(6-bromo-1,3-benzodioxol-5-yl)sulfanyl]-9-[2-(2-chlorophenyl)ethyl]purin-6-amine Chemical compound C=1C=2OCOC=2C=C(Br)C=1SC1=NC=2C(N)=NC=NC=2N1CCC1=CC=CC=C1Cl USVZHTBPMMSRHY-UHFFFAOYSA-N 0.000 description 1
- SNFCXVRWFNAHQX-UHFFFAOYSA-N 9,9'-spirobi[fluorene] Chemical compound C12=CC=CC=C2C2=CC=CC=C2C21C1=CC=CC=C1C1=CC=CC=C21 SNFCXVRWFNAHQX-UHFFFAOYSA-N 0.000 description 1
- QRMLAMCEPKEKHS-UHFFFAOYSA-N 9,9-dimethyl-n-(4-phenylphenyl)fluoren-2-amine Chemical compound C1=C2C(C)(C)C3=CC=CC=C3C2=CC=C1NC(C=C1)=CC=C1C1=CC=CC=C1 QRMLAMCEPKEKHS-UHFFFAOYSA-N 0.000 description 1
- BPMFPOGUJAAYHL-UHFFFAOYSA-N 9H-Pyrido[2,3-b]indole Chemical compound C1=CC=C2C3=CC=CC=C3NC2=N1 BPMFPOGUJAAYHL-UHFFFAOYSA-N 0.000 description 1
- 239000005964 Acibenzolar-S-methyl Substances 0.000 description 1
- 229910001316 Ag alloy Inorganic materials 0.000 description 1
- 229910016036 BaF 2 Inorganic materials 0.000 description 1
- FMMWHPNWAFZXNH-UHFFFAOYSA-N Benz[a]pyrene Chemical compound C1=C2C3=CC=CC=C3C=C(C=C3)C2=C2C3=CC=CC2=C1 FMMWHPNWAFZXNH-UHFFFAOYSA-N 0.000 description 1
- BMTAFVWTTFSTOG-UHFFFAOYSA-N Butylate Chemical compound CCSC(=O)N(CC(C)C)CC(C)C BMTAFVWTTFSTOG-UHFFFAOYSA-N 0.000 description 1
- 101100394073 Caenorhabditis elegans hil-1 gene Proteins 0.000 description 1
- 101100506090 Caenorhabditis elegans hil-2 gene Proteins 0.000 description 1
- QMPLVXFXWIEGFX-UHFFFAOYSA-N Clc1ccc(I)cc1.Brc1cccc2-c3ccccc3Cc12 Chemical compound Clc1ccc(I)cc1.Brc1cccc2-c3ccccc3Cc12 QMPLVXFXWIEGFX-UHFFFAOYSA-N 0.000 description 1
- 229910052693 Europium Inorganic materials 0.000 description 1
- 238000006736 Huisgen cycloaddition reaction Methods 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- 229910018068 Li 2 O Inorganic materials 0.000 description 1
- 229910000861 Mg alloy Inorganic materials 0.000 description 1
- AHVYPIQETPWLSZ-UHFFFAOYSA-N N-methyl-pyrrolidine Natural products CN1CC=CC1 AHVYPIQETPWLSZ-UHFFFAOYSA-N 0.000 description 1
- 238000005481 NMR spectroscopy Methods 0.000 description 1
- PDXOQFCYGFNAGM-UHFFFAOYSA-N OC(c1ccccc1-c1ccc2)(c1c2N(c(cc1)ccc1-c1ccccc1)c(cc1)ccc1-c1ccccc1)c(cccc1)c1-c1c2[o]c(cccc3)c3c2ccc1 Chemical compound OC(c1ccccc1-c1ccc2)(c1c2N(c(cc1)ccc1-c1ccccc1)c(cc1)ccc1-c1ccccc1)c(cccc1)c1-c1c2[o]c(cccc3)c3c2ccc1 PDXOQFCYGFNAGM-UHFFFAOYSA-N 0.000 description 1
- ZCQWOFVYLHDMMC-UHFFFAOYSA-N Oxazole Chemical compound C1=COC=N1 ZCQWOFVYLHDMMC-UHFFFAOYSA-N 0.000 description 1
- WTKZEGDFNFYCGP-UHFFFAOYSA-N Pyrazole Chemical compound C=1C=NNC=1 WTKZEGDFNFYCGP-UHFFFAOYSA-N 0.000 description 1
- KJTLSVCANCCWHF-UHFFFAOYSA-N Ruthenium Chemical compound [Ru] KJTLSVCANCCWHF-UHFFFAOYSA-N 0.000 description 1
- 101000767160 Saccharomyces cerevisiae (strain ATCC 204508 / S288c) Intracellular protein transport protein USO1 Proteins 0.000 description 1
- 101100457453 Saccharomyces cerevisiae (strain ATCC 204508 / S288c) MNL1 gene Proteins 0.000 description 1
- 229910052772 Samarium Inorganic materials 0.000 description 1
- PJANXHGTPQOBST-VAWYXSNFSA-N Stilbene Natural products C=1C=CC=CC=1/C=C/C1=CC=CC=C1 PJANXHGTPQOBST-VAWYXSNFSA-N 0.000 description 1
- 238000006069 Suzuki reaction reaction Methods 0.000 description 1
- DKGAVHZHDRPRBM-UHFFFAOYSA-N Tert-Butanol Chemical compound CC(C)(C)O DKGAVHZHDRPRBM-UHFFFAOYSA-N 0.000 description 1
- XBDYBAVJXHJMNQ-UHFFFAOYSA-N Tetrahydroanthracene Natural products C1=CC=C2C=C(CCCC3)C3=CC2=C1 XBDYBAVJXHJMNQ-UHFFFAOYSA-N 0.000 description 1
- DHXVGJBLRPWPCS-UHFFFAOYSA-N Tetrahydropyran Chemical compound C1CCOCC1 DHXVGJBLRPWPCS-UHFFFAOYSA-N 0.000 description 1
- DPOPAJRDYZGTIR-UHFFFAOYSA-N Tetrazine Chemical compound C1=CN=NN=N1 DPOPAJRDYZGTIR-UHFFFAOYSA-N 0.000 description 1
- FZWLAAWBMGSTSO-UHFFFAOYSA-N Thiazole Chemical compound C1=CSC=N1 FZWLAAWBMGSTSO-UHFFFAOYSA-N 0.000 description 1
- DGEZNRSVGBDHLK-UHFFFAOYSA-N [1,10]phenanthroline Chemical compound C1=CN=C2C3=NC=CC=C3C=CC2=C1 DGEZNRSVGBDHLK-UHFFFAOYSA-N 0.000 description 1
- XHCLAFWTIXFWPH-UHFFFAOYSA-N [O-2].[O-2].[O-2].[O-2].[O-2].[V+5].[V+5] Chemical compound [O-2].[O-2].[O-2].[O-2].[O-2].[V+5].[V+5] XHCLAFWTIXFWPH-UHFFFAOYSA-N 0.000 description 1
- VGRJHHLDEYYRNF-UHFFFAOYSA-N ac1lasce Chemical compound C1C2=CC=CC=C2C(C=2C3=CC=CC=C3CC=22)=C1C1=C2CC2=CC=CC=C21 VGRJHHLDEYYRNF-UHFFFAOYSA-N 0.000 description 1
- 150000001298 alcohols Chemical class 0.000 description 1
- 239000003513 alkali Substances 0.000 description 1
- 229910001618 alkaline earth metal fluoride Inorganic materials 0.000 description 1
- 125000002947 alkylene group Chemical group 0.000 description 1
- 229910045601 alloy Inorganic materials 0.000 description 1
- 239000000956 alloy Substances 0.000 description 1
- OVKDFILSBMEKLT-UHFFFAOYSA-N alpha-Terpineol Natural products CC(=C)C1(O)CCC(C)=CC1 OVKDFILSBMEKLT-UHFFFAOYSA-N 0.000 description 1
- HSFWRNGVRCDJHI-UHFFFAOYSA-N alpha-acetylene Natural products C#C HSFWRNGVRCDJHI-UHFFFAOYSA-N 0.000 description 1
- LHXDLQBQYFFVNW-UHFFFAOYSA-N alpha-fenchone Natural products C1CC2(C)C(=O)C(C)(C)C1C2 LHXDLQBQYFFVNW-UHFFFAOYSA-N 0.000 description 1
- 229940088601 alpha-terpineol Drugs 0.000 description 1
- AZDRQVAHHNSJOQ-UHFFFAOYSA-N alumane Chemical class [AlH3] AZDRQVAHHNSJOQ-UHFFFAOYSA-N 0.000 description 1
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 1
- 239000010405 anode material Substances 0.000 description 1
- VVLCNWYWKSWJTG-UHFFFAOYSA-N anthracene-1,2-diamine Chemical compound C1=CC=CC2=CC3=C(N)C(N)=CC=C3C=C21 VVLCNWYWKSWJTG-UHFFFAOYSA-N 0.000 description 1
- 150000001454 anthracenes Chemical class 0.000 description 1
- 229940058303 antinematodal benzimidazole derivative Drugs 0.000 description 1
- 229940027991 antiseptic and disinfectant quinoline derivative Drugs 0.000 description 1
- 238000010420 art technique Methods 0.000 description 1
- 125000000732 arylene group Chemical group 0.000 description 1
- 150000001540 azides Chemical class 0.000 description 1
- RFRXIWQYSOIBDI-UHFFFAOYSA-N benzarone Chemical compound CCC=1OC2=CC=CC=C2C=1C(=O)C1=CC=C(O)C=C1 RFRXIWQYSOIBDI-UHFFFAOYSA-N 0.000 description 1
- 150000001556 benzimidazoles Chemical class 0.000 description 1
- WMUIZUWOEIQJEH-UHFFFAOYSA-N benzo[e][1,3]benzoxazole Chemical compound C1=CC=C2C(N=CO3)=C3C=CC2=C1 WMUIZUWOEIQJEH-UHFFFAOYSA-N 0.000 description 1
- 125000000499 benzofuranyl group Chemical group O1C(=CC2=C1C=CC=C2)* 0.000 description 1
- 125000004196 benzothienyl group Chemical group S1C(=CC2=C1C=CC=C2)* 0.000 description 1
- QRUDEWIWKLJBPS-UHFFFAOYSA-N benzotriazole Chemical compound C1=CC=C2N[N][N]C2=C1 QRUDEWIWKLJBPS-UHFFFAOYSA-N 0.000 description 1
- 239000012964 benzotriazole Substances 0.000 description 1
- IPWKHHSGDUIRAH-UHFFFAOYSA-N bis(pinacolato)diboron Chemical compound O1C(C)(C)C(C)(C)OB1B1OC(C)(C)C(C)(C)O1 IPWKHHSGDUIRAH-UHFFFAOYSA-N 0.000 description 1
- UORVGPXVDQYIDP-UHFFFAOYSA-N borane Chemical class B UORVGPXVDQYIDP-UHFFFAOYSA-N 0.000 description 1
- 229910000085 borane Inorganic materials 0.000 description 1
- ZADPBFCGQRWHPN-UHFFFAOYSA-N boronic acid Chemical compound OBO ZADPBFCGQRWHPN-UHFFFAOYSA-N 0.000 description 1
- 125000005620 boronic acid group Chemical class 0.000 description 1
- 125000001246 bromo group Chemical group Br* 0.000 description 1
- 125000004369 butenyl group Chemical group C(=CCC)* 0.000 description 1
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 125000000480 butynyl group Chemical group [*]C#CC([H])([H])C([H])([H])[H] 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- 150000004649 carbonic acid derivatives Chemical class 0.000 description 1
- 150000001732 carboxylic acid derivatives Chemical class 0.000 description 1
- 239000012159 carrier gas Substances 0.000 description 1
- 238000006757 chemical reactions by type Methods 0.000 description 1
- WCZVZNOTHYJIEI-UHFFFAOYSA-N cinnoline Chemical compound N1=NC=CC2=CC=CC=C21 WCZVZNOTHYJIEI-UHFFFAOYSA-N 0.000 description 1
- 239000011248 coating agent Substances 0.000 description 1
- 238000000576 coating method Methods 0.000 description 1
- 239000000470 constituent Substances 0.000 description 1
- 150000001879 copper Chemical class 0.000 description 1
- 239000002537 cosmetic Substances 0.000 description 1
- 230000008878 coupling Effects 0.000 description 1
- 238000010168 coupling process Methods 0.000 description 1
- 238000006352 cycloaddition reaction Methods 0.000 description 1
- 125000001162 cycloheptenyl group Chemical group C1(=CCCCCC1)* 0.000 description 1
- 125000000582 cycloheptyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- HPXRVTGHNJAIIH-UHFFFAOYSA-N cyclohexanol Chemical compound OC1CCCCC1 HPXRVTGHNJAIIH-UHFFFAOYSA-N 0.000 description 1
- 125000000596 cyclohexenyl group Chemical group C1(=CCCCC1)* 0.000 description 1
- HHNHBFLGXIUXCM-GFCCVEGCSA-N cyclohexylbenzene Chemical compound [CH]1CCCC[C@@H]1C1=CC=CC=C1 HHNHBFLGXIUXCM-GFCCVEGCSA-N 0.000 description 1
- 125000000522 cyclooctenyl group Chemical group C1(=CCCCCCC1)* 0.000 description 1
- 125000000640 cyclooctyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C([H])([H])C1([H])[H] 0.000 description 1
- 125000002433 cyclopentenyl group Chemical group C1(=CCCC1)* 0.000 description 1
- JCWIWBWXCVGEAN-UHFFFAOYSA-L cyclopentyl(diphenyl)phosphane;dichloropalladium;iron Chemical compound [Fe].Cl[Pd]Cl.[CH]1[CH][CH][CH][C]1P(C=1C=CC=CC=1)C1=CC=CC=C1.[CH]1[CH][CH][CH][C]1P(C=1C=CC=CC=1)C1=CC=CC=C1 JCWIWBWXCVGEAN-UHFFFAOYSA-L 0.000 description 1
- 150000001987 diarylethers Chemical class 0.000 description 1
- 150000007858 diazaphosphole derivatives Chemical class 0.000 description 1
- ZXHUJRZYLRVVNP-UHFFFAOYSA-N dibenzofuran-4-ylboronic acid Chemical compound C12=CC=CC=C2OC2=C1C=CC=C2B(O)O ZXHUJRZYLRVVNP-UHFFFAOYSA-N 0.000 description 1
- 125000005509 dibenzothiophenyl group Chemical group 0.000 description 1
- 150000001993 dienes Chemical class 0.000 description 1
- 229940028356 diethylene glycol monobutyl ether Drugs 0.000 description 1
- XXPBFNVKTVJZKF-UHFFFAOYSA-N dihydrophenanthrene Natural products C1=CC=C2CCC3=CC=CC=C3C2=C1 XXPBFNVKTVJZKF-UHFFFAOYSA-N 0.000 description 1
- KWKXNDCHNDYVRT-UHFFFAOYSA-N dodecylbenzene Chemical compound CCCCCCCCCCCCC1=CC=CC=C1 KWKXNDCHNDYVRT-UHFFFAOYSA-N 0.000 description 1
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- 125000002534 ethynyl group Chemical group [H]C#C* 0.000 description 1
- OGPBJKLSAFTDLK-UHFFFAOYSA-N europium atom Chemical compound [Eu] OGPBJKLSAFTDLK-UHFFFAOYSA-N 0.000 description 1
- 230000005284 excitation Effects 0.000 description 1
- 230000001747 exhibiting effect Effects 0.000 description 1
- 238000000605 extraction Methods 0.000 description 1
- 150000002220 fluorenes Chemical class 0.000 description 1
- 125000003983 fluorenyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3CC12)* 0.000 description 1
- JKFAIQOWCVVSKC-UHFFFAOYSA-N furazan Chemical compound C=1C=NON=1 JKFAIQOWCVVSKC-UHFFFAOYSA-N 0.000 description 1
- 125000002541 furyl group Chemical group 0.000 description 1
- 238000007429 general method Methods 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 230000009477 glass transition Effects 0.000 description 1
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 1
- 229910052736 halogen Inorganic materials 0.000 description 1
- 230000026030 halogenation Effects 0.000 description 1
- 238000005658 halogenation reaction Methods 0.000 description 1
- 150000002367 halogens Chemical class 0.000 description 1
- 230000009931 harmful effect Effects 0.000 description 1
- KWHDXJHBFYQOTK-UHFFFAOYSA-N heptane;toluene Chemical compound CCCCCCC.CC1=CC=CC=C1 KWHDXJHBFYQOTK-UHFFFAOYSA-N 0.000 description 1
- 125000006038 hexenyl group Chemical group 0.000 description 1
- 125000005980 hexynyl group Chemical group 0.000 description 1
- 239000001257 hydrogen Substances 0.000 description 1
- 229910052738 indium Inorganic materials 0.000 description 1
- PZOUSPYUWWUPPK-UHFFFAOYSA-N indole Natural products CC1=CC=CC2=C1C=CN2 PZOUSPYUWWUPPK-UHFFFAOYSA-N 0.000 description 1
- RKJUIXBNRJVNHR-UHFFFAOYSA-N indolenine Natural products C1=CC=C2CC=NC2=C1 RKJUIXBNRJVNHR-UHFFFAOYSA-N 0.000 description 1
- HOBCFUWDNJPFHB-UHFFFAOYSA-N indolizine Chemical compound C1=CC=CN2C=CC=C21 HOBCFUWDNJPFHB-UHFFFAOYSA-N 0.000 description 1
- VVVPGLRKXQSQSZ-UHFFFAOYSA-N indolo[3,2-c]carbazole Chemical class C1=CC=CC2=NC3=C4C5=CC=CC=C5N=C4C=CC3=C21 VVVPGLRKXQSQSZ-UHFFFAOYSA-N 0.000 description 1
- 239000011229 interlayer Substances 0.000 description 1
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 1
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- ZLTPDFXIESTBQG-UHFFFAOYSA-N isothiazole Chemical compound C=1C=NSC=1 ZLTPDFXIESTBQG-UHFFFAOYSA-N 0.000 description 1
- CTAPFRYPJLPFDF-UHFFFAOYSA-N isoxazole Chemical compound C=1C=NOC=1 CTAPFRYPJLPFDF-UHFFFAOYSA-N 0.000 description 1
- 229910052747 lanthanoid Inorganic materials 0.000 description 1
- 150000002602 lanthanoids Chemical class 0.000 description 1
- 239000003446 ligand Substances 0.000 description 1
- 239000007791 liquid phase Substances 0.000 description 1
- 150000002641 lithium Chemical class 0.000 description 1
- IMKMFBIYHXBKRX-UHFFFAOYSA-M lithium;quinoline-2-carboxylate Chemical compound [Li+].C1=CC=CC2=NC(C(=O)[O-])=CC=C21 IMKMFBIYHXBKRX-UHFFFAOYSA-M 0.000 description 1
- 238000004020 luminiscence type Methods 0.000 description 1
- AUHZEENZYGFFBQ-UHFFFAOYSA-N mesitylene Substances CC1=CC(C)=CC(C)=C1 AUHZEENZYGFFBQ-UHFFFAOYSA-N 0.000 description 1
- 125000001827 mesitylenyl group Chemical group [H]C1=C(C(*)=C(C([H])=C1C([H])([H])[H])C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 229910001092 metal group alloy Inorganic materials 0.000 description 1
- 229910001507 metal halide Inorganic materials 0.000 description 1
- 150000005309 metal halides Chemical class 0.000 description 1
- UZKWTJUDCOPSNM-UHFFFAOYSA-N methoxybenzene Substances CCCCOC=C UZKWTJUDCOPSNM-UHFFFAOYSA-N 0.000 description 1
- 229910003455 mixed metal oxide Inorganic materials 0.000 description 1
- 229910000476 molybdenum oxide Inorganic materials 0.000 description 1
- KTZPDEZASWSSTI-UHFFFAOYSA-N n-(4-chlorophenyl)-2-phenyl-n-(4-phenylphenyl)aniline Chemical compound C1=CC(Cl)=CC=C1N(C=1C(=CC=CC=1)C=1C=CC=CC=1)C1=CC=C(C=2C=CC=CC=2)C=C1 KTZPDEZASWSSTI-UHFFFAOYSA-N 0.000 description 1
- IBHBKWKFFTZAHE-UHFFFAOYSA-N n-[4-[4-(n-naphthalen-1-ylanilino)phenyl]phenyl]-n-phenylnaphthalen-1-amine Chemical compound C1=CC=CC=C1N(C=1C2=CC=CC=C2C=CC=1)C1=CC=C(C=2C=CC(=CC=2)N(C=2C=CC=CC=2)C=2C3=CC=CC=C3C=CC=2)C=C1 IBHBKWKFFTZAHE-UHFFFAOYSA-N 0.000 description 1
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000003136 n-heptyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000001280 n-hexyl group Chemical group C(CCCCC)* 0.000 description 1
- 125000000740 n-pentyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000001624 naphthyl group Chemical group 0.000 description 1
- 125000005244 neohexyl group Chemical group [H]C([H])([H])C(C([H])([H])[H])(C([H])([H])[H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000001971 neopentyl group Chemical group [H]C([*])([H])C(C([H])([H])[H])(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 229910052759 nickel Inorganic materials 0.000 description 1
- 125000004433 nitrogen atom Chemical group N* 0.000 description 1
- QGLKJKCYBOYXKC-UHFFFAOYSA-N nonaoxidotritungsten Chemical compound O=[W]1(=O)O[W](=O)(=O)O[W](=O)(=O)O1 QGLKJKCYBOYXKC-UHFFFAOYSA-N 0.000 description 1
- 125000004365 octenyl group Chemical group C(=CCCCCCC)* 0.000 description 1
- VXNSQGRKHCZUSU-UHFFFAOYSA-N octylbenzene Chemical compound [CH2]CCCCCCCC1=CC=CC=C1 VXNSQGRKHCZUSU-UHFFFAOYSA-N 0.000 description 1
- 125000005069 octynyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C#C* 0.000 description 1
- 238000007645 offset printing Methods 0.000 description 1
- 239000003960 organic solvent Substances 0.000 description 1
- 229910052762 osmium Inorganic materials 0.000 description 1
- SYQBFIAQOQZEGI-UHFFFAOYSA-N osmium atom Chemical compound [Os] SYQBFIAQOQZEGI-UHFFFAOYSA-N 0.000 description 1
- WCPAKWJPBJAGKN-UHFFFAOYSA-N oxadiazole Chemical compound C1=CON=N1 WCPAKWJPBJAGKN-UHFFFAOYSA-N 0.000 description 1
- 150000004866 oxadiazoles Chemical class 0.000 description 1
- 150000002921 oxetanes Chemical class 0.000 description 1
- 230000003647 oxidation Effects 0.000 description 1
- 238000007254 oxidation reaction Methods 0.000 description 1
- 150000002924 oxiranes Chemical class 0.000 description 1
- JCGNDDUYTRNOFT-UHFFFAOYSA-N oxolane-2,4-dione Chemical compound O=C1COC(=O)C1 JCGNDDUYTRNOFT-UHFFFAOYSA-N 0.000 description 1
- PQQKPALAQIIWST-UHFFFAOYSA-N oxomolybdenum Chemical compound [Mo]=O PQQKPALAQIIWST-UHFFFAOYSA-N 0.000 description 1
- NRNFFDZCBYOZJY-UHFFFAOYSA-N p-quinodimethane Chemical class C=C1C=CC(=C)C=C1 NRNFFDZCBYOZJY-UHFFFAOYSA-N 0.000 description 1
- LXNAVEXFUKBNMK-UHFFFAOYSA-N palladium(II) acetate Substances [Pd].CC(O)=O.CC(O)=O LXNAVEXFUKBNMK-UHFFFAOYSA-N 0.000 description 1
- PIBWKRNGBLPSSY-UHFFFAOYSA-L palladium(II) chloride Chemical compound Cl[Pd]Cl PIBWKRNGBLPSSY-UHFFFAOYSA-L 0.000 description 1
- YJVFFLUZDVXJQI-UHFFFAOYSA-L palladium(ii) acetate Chemical compound [Pd+2].CC([O-])=O.CC([O-])=O YJVFFLUZDVXJQI-UHFFFAOYSA-L 0.000 description 1
- SLIUAWYAILUBJU-UHFFFAOYSA-N pentacene Chemical compound C1=CC=CC2=CC3=CC4=CC5=CC=CC=C5C=C4C=C3C=C21 SLIUAWYAILUBJU-UHFFFAOYSA-N 0.000 description 1
- 125000006340 pentafluoro ethyl group Chemical group FC(F)(F)C(F)(F)* 0.000 description 1
- 125000002255 pentenyl group Chemical group C(=CCCC)* 0.000 description 1
- 125000005981 pentynyl group Chemical group 0.000 description 1
- 125000002080 perylenyl group Chemical group C1(=CC=C2C=CC=C3C4=CC=CC5=CC=CC(C1=C23)=C45)* 0.000 description 1
- CSHWQDPOILHKBI-UHFFFAOYSA-N peryrene Natural products C1=CC(C2=CC=CC=3C2=C2C=CC=3)=C3C2=CC=CC3=C1 CSHWQDPOILHKBI-UHFFFAOYSA-N 0.000 description 1
- 150000002987 phenanthrenes Chemical class 0.000 description 1
- 125000001792 phenanthrenyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3C=CC12)* 0.000 description 1
- DLRJIFUOBPOJNS-UHFFFAOYSA-N phenetole Chemical compound CCOC1=CC=CC=C1 DLRJIFUOBPOJNS-UHFFFAOYSA-N 0.000 description 1
- 229950000688 phenothiazine Drugs 0.000 description 1
- 229960005323 phenoxyethanol Drugs 0.000 description 1
- 238000001126 phototherapy Methods 0.000 description 1
- 235000011056 potassium acetate Nutrition 0.000 description 1
- TYJJADVDDVDEDZ-UHFFFAOYSA-M potassium hydrogencarbonate Chemical compound [K+].OC([O-])=O TYJJADVDDVDEDZ-UHFFFAOYSA-M 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 125000004368 propenyl group Chemical group C(=CC)* 0.000 description 1
- 125000002568 propynyl group Chemical group [*]C#CC([H])([H])[H] 0.000 description 1
- CPNGPNLZQNNVQM-UHFFFAOYSA-N pteridine Chemical compound N1=CN=CC2=NC=CN=C21 CPNGPNLZQNNVQM-UHFFFAOYSA-N 0.000 description 1
- 150000003216 pyrazines Chemical class 0.000 description 1
- BUAWIRPPAOOHKD-UHFFFAOYSA-N pyrene-1,2-diamine Chemical class C1=CC=C2C=CC3=C(N)C(N)=CC4=CC=C1C2=C43 BUAWIRPPAOOHKD-UHFFFAOYSA-N 0.000 description 1
- 150000003220 pyrenes Chemical class 0.000 description 1
- PBMFSQRYOILNGV-UHFFFAOYSA-N pyridazine Chemical compound C1=CC=NN=C1 PBMFSQRYOILNGV-UHFFFAOYSA-N 0.000 description 1
- 150000003222 pyridines Chemical class 0.000 description 1
- 229940083082 pyrimidine derivative acting on arteriolar smooth muscle Drugs 0.000 description 1
- 150000003230 pyrimidines Chemical class 0.000 description 1
- HNJBEVLQSNELDL-UHFFFAOYSA-N pyrrolidin-2-one Chemical compound O=C1CCCN1 HNJBEVLQSNELDL-UHFFFAOYSA-N 0.000 description 1
- JWVCLYRUEFBMGU-UHFFFAOYSA-N quinazoline Chemical compound N1=CN=CC2=CC=CC=C21 JWVCLYRUEFBMGU-UHFFFAOYSA-N 0.000 description 1
- 150000003248 quinolines Chemical class 0.000 description 1
- 150000003252 quinoxalines Chemical class 0.000 description 1
- 230000005855 radiation Effects 0.000 description 1
- 239000012429 reaction media Substances 0.000 description 1
- 229910052703 rhodium Inorganic materials 0.000 description 1
- 239000010948 rhodium Substances 0.000 description 1
- MHOVAHRLVXNVSD-UHFFFAOYSA-N rhodium atom Chemical compound [Rh] MHOVAHRLVXNVSD-UHFFFAOYSA-N 0.000 description 1
- 229910052707 ruthenium Inorganic materials 0.000 description 1
- 238000007650 screen-printing Methods 0.000 description 1
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 239000010944 silver (metal) Substances 0.000 description 1
- 125000003808 silyl group Chemical group [H][Si]([H])([H])[*] 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- 239000011780 sodium chloride Substances 0.000 description 1
- MFRIHAYPQRLWNB-UHFFFAOYSA-N sodium tert-butoxide Chemical compound [Na+].CC(C)(C)[O-] MFRIHAYPQRLWNB-UHFFFAOYSA-N 0.000 description 1
- 239000007858 starting material Substances 0.000 description 1
- PJANXHGTPQOBST-UHFFFAOYSA-N stilbene Chemical compound C=1C=CC=CC=1C=CC1=CC=CC=C1 PJANXHGTPQOBST-UHFFFAOYSA-N 0.000 description 1
- 235000021286 stilbenes Nutrition 0.000 description 1
- 238000000859 sublimation Methods 0.000 description 1
- 230000008022 sublimation Effects 0.000 description 1
- 150000003457 sulfones Chemical class 0.000 description 1
- 125000004434 sulfur atom Chemical group 0.000 description 1
- IFLREYGFSNHWGE-UHFFFAOYSA-N tetracene Chemical compound C1=CC=CC2=CC3=CC4=CC=CC=C4C=C3C=C21 IFLREYGFSNHWGE-UHFFFAOYSA-N 0.000 description 1
- 150000003536 tetrazoles Chemical class 0.000 description 1
- 238000001931 thermography Methods 0.000 description 1
- 125000001544 thienyl group Chemical group 0.000 description 1
- 125000004001 thioalkyl group Chemical group 0.000 description 1
- 150000003577 thiophenes Chemical class 0.000 description 1
- 238000010023 transfer printing Methods 0.000 description 1
- 229910000314 transition metal oxide Inorganic materials 0.000 description 1
- 125000002023 trifluoromethyl group Chemical group FC(F)(F)* 0.000 description 1
- YFNKIDBQEZZDLK-UHFFFAOYSA-N triglyme Chemical compound COCCOCCOCCOC YFNKIDBQEZZDLK-UHFFFAOYSA-N 0.000 description 1
- 125000005580 triphenylene group Chemical group 0.000 description 1
- YGPLLMPPZRUGTJ-UHFFFAOYSA-N truxene Chemical compound C1C2=CC=CC=C2C(C2=C3C4=CC=CC=C4C2)=C1C1=C3CC2=CC=CC=C21 YGPLLMPPZRUGTJ-UHFFFAOYSA-N 0.000 description 1
- 229910001930 tungsten oxide Inorganic materials 0.000 description 1
- 238000002061 vacuum sublimation Methods 0.000 description 1
- 229910001935 vanadium oxide Inorganic materials 0.000 description 1
- 238000001947 vapour-phase growth Methods 0.000 description 1
- PXXNTAGJWPJAGM-UHFFFAOYSA-N vertaline Natural products C1C2C=3C=C(OC)C(OC)=CC=3OC(C=C3)=CC=C3CCC(=O)OC1CC1N2CCCC1 PXXNTAGJWPJAGM-UHFFFAOYSA-N 0.000 description 1
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 1
- 150000003751 zinc Chemical class 0.000 description 1
- YVTHLONGBIQYBO-UHFFFAOYSA-N zinc indium(3+) oxygen(2-) Chemical compound [O--].[Zn++].[In+3] YVTHLONGBIQYBO-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/631—Amine compounds having at least two aryl rest on at least one amine-nitrogen atom, e.g. triphenylamine
- H10K85/636—Amine compounds having at least two aryl rest on at least one amine-nitrogen atom, e.g. triphenylamine comprising heteroaromatic hydrocarbons as substituents on the nitrogen atom
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D307/00—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom
- C07D307/94—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom spiro-condensed with carbocyclic rings or ring systems, e.g. griseofulvins
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/04—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- H—ELECTRICITY
- H05—ELECTRIC TECHNIQUES NOT OTHERWISE PROVIDED FOR
- H05B—ELECTRIC HEATING; ELECTRIC LIGHT SOURCES NOT OTHERWISE PROVIDED FOR; CIRCUIT ARRANGEMENTS FOR ELECTRIC LIGHT SOURCES, IN GENERAL
- H05B33/00—Electroluminescent light sources
- H05B33/12—Light sources with substantially two-dimensional radiating surfaces
- H05B33/20—Light sources with substantially two-dimensional radiating surfaces characterised by the chemical or physical composition or the arrangement of the material in which the electroluminescent material is embedded
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/14—Carrier transporting layers
- H10K50/15—Hole transporting layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
- H10K85/624—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene containing six or more rings
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
- H10K85/626—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene containing more than one polycyclic condensed aromatic rings, e.g. bis-anthracene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/631—Amine compounds having at least two aryl rest on at least one amine-nitrogen atom, e.g. triphenylamine
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/631—Amine compounds having at least two aryl rest on at least one amine-nitrogen atom, e.g. triphenylamine
- H10K85/633—Amine compounds having at least two aryl rest on at least one amine-nitrogen atom, e.g. triphenylamine comprising polycyclic condensed aromatic hydrocarbons as substituents on the nitrogen atom
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6572—Polycyclic condensed heteroaromatic hydrocarbons comprising only nitrogen in the heteroaromatic polycondensed ring system, e.g. phenanthroline or carbazole
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6574—Polycyclic condensed heteroaromatic hydrocarbons comprising only oxygen in the heteroaromatic polycondensed ring system, e.g. cumarine dyes
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/17—Carrier injection layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/18—Carrier blocking layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/18—Carrier blocking layers
- H10K50/181—Electron blocking layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/30—Coordination compounds
- H10K85/341—Transition metal complexes, e.g. Ru(II)polypyridine complexes
- H10K85/342—Transition metal complexes, e.g. Ru(II)polypyridine complexes comprising iridium
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E10/00—Energy generation through renewable energy sources
- Y02E10/50—Photovoltaic [PV] energy
- Y02E10/549—Organic PV cells
Definitions
- the present application relates to a compound having spirobifluorene skeleton and benzofluorene moiety fused thereto.
- Compound is suitable for use in electronic devices, in particular in organic electroluminescent devices (OLEDs).
- OLEDs organic electroluminescent devices
- organic electronic devices are understood as meaning so-called organic electronic devices (organic electronic devices) which use organic semiconductor materials
- OLEDs are called electronic
- Devices understood that have one or more layers containing organic compounds and emit light when applying electrical voltage.
- Devices have hole transporting layers such as hole injecting layers, hole transporting layers, electron blocking layers and also emitting layers.
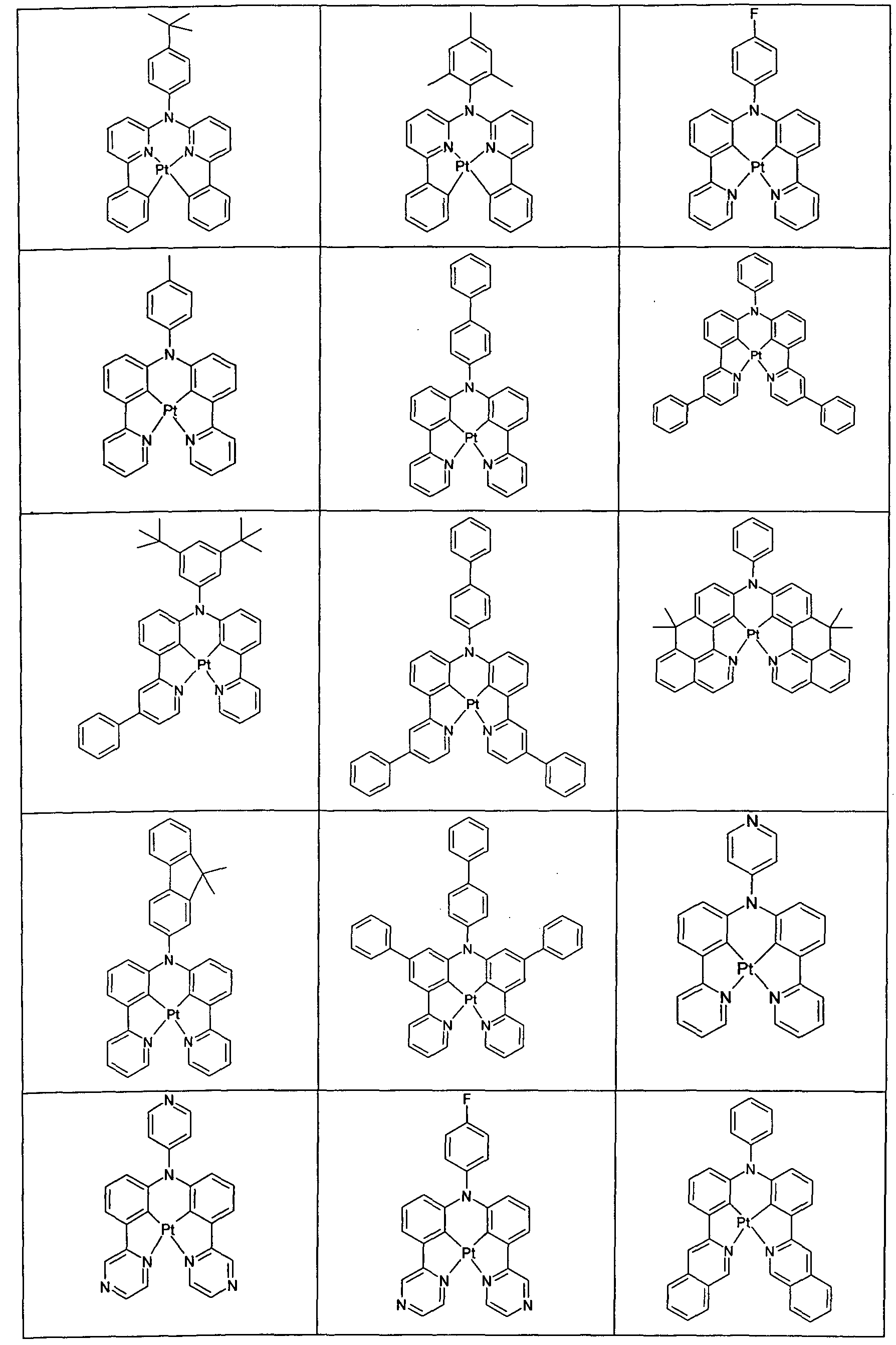
- triarylamines as hole transporting materials in the above-mentioned layers.
- These can represent mono triarylamines, such as for example, in JP 1995/053955, WO 2006/123667 and JP 2010/222268, or represent bis- or other oligoamines, such as
- spirobifluorene derivatives which have a benzofuran unit fused to the spirobifluorene skeleton and which have one or more arylamino groups bonded in position 2 to the spirobifluorene (WO 2013/100467).
- the compounds found have one or more properties selected from very good hole-conducting properties, very good
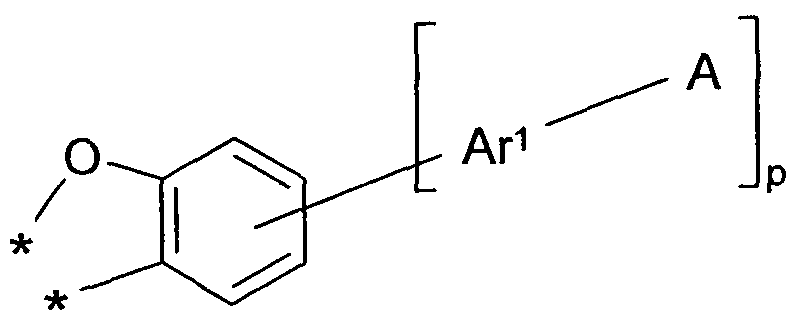
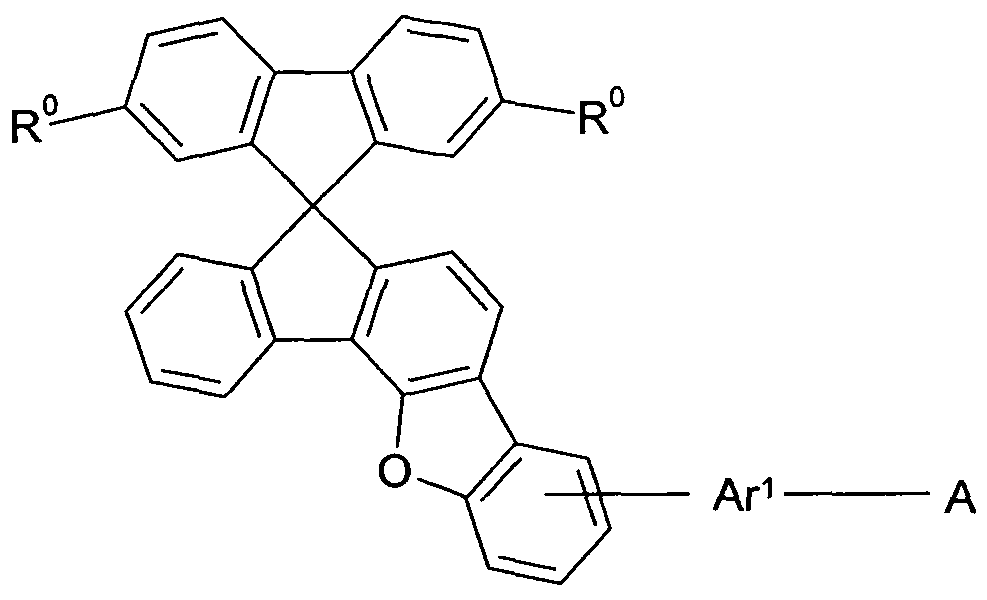
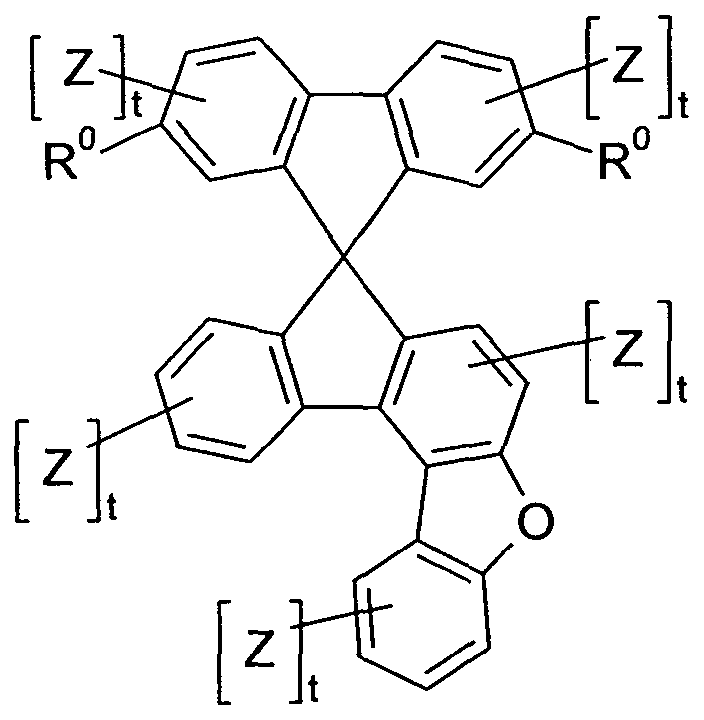
- the present invention therefore relates to a compound of the formula (I)
- A is the same or different on each occurrence and is a group of the formula (A1), (A2) or (A3) which is linked via the bond marked #;
- Formula (A3) is the same or different at each occurrence
- Si (R 3 ) 3 a straight-chain alkyl or alkoxy group having 1 to 20 C atoms or a branched or cyclic alkyl or alkoxy group group of 3 to 20 C atoms or an alkenyl or
- R 4 may be substituted; two or more radicals R 3 may be linked together and form a ring; is identical or different at each occurrence H, D, F, CN or an aliphatic, aromatic or heteroaromatic
- organic radical having 1 to 20 C atoms, in which also one or more H atoms may be replaced by D, F or CN; two or more substituents R 4 may be linked together to form a ring; q is the same or different at each occurrence 0 or 1, wherein at least one q in formula (A2) is 1; i, k, m, n and p are the same or different at each occurrence 0 or 1, wherein at least one of these indices is equal to 1.
- An aryl group in the sense of this invention contains 6 to 60 aromatic ring atoms;
- a heteroaryl group contains 5 to 60 aromatic ring atoms, at least one of which represents a heteroatom.
- the heteroatoms are preferably selected from N, O and S. This is the basic definition. If in the description of the present invention other preferences are given,
- an aryl group or heteroaryl group is either a simple aromatic cycle, ie benzene, or a simpler one
- heteroaromatic cycle for example pyridine, pyrimidine or
- heteroaromatic polycycle for example naphthalene, phenanthrene, Quinoline or carbazole understood.
- a condensed (anneliierter) aromatic or heteroaromatic polycycle consists in the context of the present application of two or more condensed simple aromatic or heteroaromatic cycles.
- aryl or heteroaryl group which may be substituted in each case with the abovementioned radicals and which may be linked via any position on the aromatic or heteroaromatic, are
- benzene in particular groups derived from benzene, naphthalene, anthracene, phenanthrene, pyrene, dihydropyrene, chrysene, perylene, triphenylene, fluoranthene, benzanthracene, benzphenanthrene, tetracene, pentacene, benzpyrene, furan, benzofuran, isobenzofuran, dibenzofuran, thiophene, benzothiophene, Isobenzothiophene, dibenzothiophene, pyrrole, indole, isoindole, carbazole, pyridine, quinoline, isoquinoline, acridine, phenanthridine, benzo-5,6-quinoline, benzo-6,7-quinoline, benzo-7,8-quinoline, phenothiazine, Phenoxazine, pyrazole, indazole, imi
- An aromatic ring system in the sense of this invention contains 6 to 60 carbon atoms in the ring system.
- a heteroaromatic ring system in the context of this invention contains 5 to 60 aromatic ring atoms, at least one of which represents a heteroatom.
- the heteroatoms are preferably selected from N, O and / or S.
- An aromatic or heteroaromatic ring system in the sense of this invention is to be understood as meaning a system which does not necessarily contain only aryl or heteroaryl groups but in which also several aryl or heteroaryl groups a single bond or a non-binding aromatic moiety, such as one or more optionally substituted C, Si, N, O or S atoms.
- the non-aromatic unit preferably comprises less than 10% of the atoms other than H relative to the total number of H atoms
- Systems such as 9,9'-spirobifluorene, 9,9'-diarylfluorene, triarylamine, diaryl ethers and stilbene are understood as aromatic ring systems in the context of this invention, and also systems in which two or more aryl groups, for example by a linear or cyclic alkyl, Alkenyl or alkynyl group or linked by a silyl group. Furthermore, systems in which two or more aryl or
- Heteroaryl groups are linked together via single bonds, as aromatic or heteroaromatic ring systems in the sense of this
- aromatic or heteroaromatic ring system having 5-60 aromatic ring atoms, which may be substituted in each case with radicals as defined above and which may be linked via any positions on the aromatic or heteroaromatic, are understood in particular groups which are derived from those mentioned above Aryl and heteroaryl groups and of biphenyl, terphenyl, quaterphenyl, fluorene, spirobifluorene, dihydrophenanthrene, dihydropyrene, tetrahydropyrene, indenofluorene, truxene, isotruxene, spirotruxene,
- alkoxy or thioalkyl group having 1 to 40 carbon atoms methoxy, trifluoromethoxy, ethoxy, n-propoxy, i-propoxy, n-butoxy, i-butoxy, s-butoxy, t-butoxy, n-pentoxy, s Pentoxy, 2-methylbutoxy, n-hexoxy, cyclohexyloxy, n-heptoxy, cycloheptyloxy, n-octyloxy,
- the two radicals are linked together by a chemical bond, under the formulation that two or more radicals can form a ring with one another.
- the second radical forms a ring to the position to which the hydrogen atom
- A is a group of the formula (A-1) or (A-3), particularly preferably a group of the formula (A-1).
- each occurrence of Ar 1 is the same or different selected from a single bond or a divalent group selected from optionally substituted with radicals R 2 benzene, biphenyl, terphenyl, fluorene, spirobifluorene, indenofluorene, carbazole, dibenzofuran,
- Groups Ar 1 are preferably selected from groups of the following formulas:
- R 2 in the groups of the formulas (Ar 1 -23) and (Ar -24) is preferably the same or different for an alkyl group having 1 to 10 C atoms, in particular methyl, or a phenyl group having one or more radicals R 3 may be substituted and preferred
- Two alkyl groups R 2 can also under
- Forming a spiro group form a ring, preferably one
- each occurrence of Ar 2 is the same or different selected from an aromatic or heteroaromatic ring system having 6 to 25 aromatic ring atoms, which may be substituted by one or more R 2 radicals.
- Particularly preferred are phenyl, biphenyl, terphenyl, fluorenyl, spirobifluorenyl, Indenofluorenyl, naphthyl, phenanthrenyl, furanyl, benzofuranyl, dibenzofuranyl, thiophenyl, benzothiophenyl, dibenzothiophenyl, carbazolyl, Indolocarbazolyl Indenocarbazolyl and which may be substituted with one or more radicals R.sub.2.
- Groups Ar 2 are preferably the same or different at each occurrence selected from groups of the following formulas:
- dashed bond represents the bond to the nitrogen and the groups at the free positions by one or more radicals R 2 may be substituted, but are preferably unsubstituted at the free positions.
- R 2 in the groups of the formulas ( ⁇ ⁇ - ⁇ ) to (Ar * -82) and (Ar 2 to 85) to ( ⁇ ⁇ - ⁇ ) is preferably the same or different for an alkyl group having 1 to 10 C-atoms , in particular methyl, or a phenyl group which may be substituted by one or more radicals R 3 and is preferably unsubstituted.
- Two alkyl groups R 2 can also under
- Forming a spiro group form a ring, preferably one
- Preferred embodiments of the groups Ar 3 correspond to those for groups Ar 2 .
- R ° is preferably the same or different at each occurrence, H, D, F, a straight-chain alkyl or alkoxy group having 1 to 10 C atoms or a branched or cyclic alkyl or alkoxy group having 3 to 10 C atoms, wherein the abovementioned Groups each having one or more radicals R 3 may be substituted, or an aromatic or
- R ° is, identically or differently, H, F, a straight-chain alkyl group having 1 to 10 C atoms or a branched or cyclic alkyl group having 3 to 10 C atoms, the abovementioned groups each having one or more radicals R 3 may be substituted.
- heteroaromatic ring system having 5 to 30 aromatic ring atoms, each of which may be substituted by one or more radicals R 3 , where two or more radicals R 1 and R 2 may be linked together and form a ring. More preferably, R 1 and R 2 each and each occurrence are the same or different H, D, F, CN, a straight-chain alkyl group having 1 to 10 C atoms or a branched or cyclic alkyl group having 3 to 10 C atoms Groups each having one or more radicals R 3 may be substituted, or an aromatic or heteroaromatic ring system having 6 to 25 aromatic ring atoms, which may be substituted in each case with one or more radicals R 3 .
- R 1 is the same or different at each occurrence, H, F, CN, a straight-chain alkyl group having 1 to 10 carbon atoms or a branched or cyclic alkyl group having 3 to 10 carbon atoms, wherein the above-mentioned groups each with one or more R 3 may be substituted, or an aromatic or heteroaromatic
- Ring system having 6 to 25 aromatic ring atoms, each of which may be substituted by one or more R 3 radicals.
- Particularly preferred groups R 1 are H, F, CN, methyl, tert-butyl, phenyl, biphenyl,
- R 1 attached to the skeleton of formula (I) is not H, it is preferably attached to one of the positions 4, 5, 4 'and 5' of the spirobifluorene skeleton, the numbering being as follows:
- R 3 is the same or different at each instance, and is H, D, F, CN, N (Ar 3 ) 2 , or a straight chain one
- p is 1.
- k is 1.
- n is 0. It is furthermore preferred for the sum of the indices i, k, m, n to be equal to 1 or 2, particularly preferably equal to 1.
- the sum of the indices p and m is 1.
- the occurring variables correspond to the embodiments given above as preferred.
- R is the same at each occurrence
- H, F, CN straight-chain alkyl groups having 1 to 10 C atoms or branched or cyclic alkyl groups having 3 to 10 C atoms, where the abovementioned groups may each be substituted by one or more R 3 radicals, or aromatic or heteroaromatic ring systems having 6 to 25 aromatic ring atoms, which may each be substituted by one or more radicals R, more preferably from H, F, CN, methyl, tert-butyl, phenyl, biphenyl, dibenzofuran, dibenzothiophene and carbazole.
- radical R 1 selected from H, F, CN, straight-chain alkyl groups having 1 to 10 C atoms or branched or cyclic alkyl groups having 3 to 10 C atoms, where the abovementioned groups each have one or more radicals R 3 may be substituted, or aromatic or heteroaromatic ring systems having 6 to 25 aromatic ring atoms, each of which may be substituted by one or more radicals R 3 , more preferably from H, F, CN, methyl, tert-butyl, Phenyl, biphenyl, dibenzofuran, dibenzothiophene and carbazole.
- R 1 selected from H, F, CN, straight-chain alkyl groups having 1 to 10 C atoms or branched or cyclic alkyl groups having 3 to 10 C atoms, where the abovementioned groups each have one or more radicals R 3 may be substituted, or aromatic or heteroaromatic ring systems having 6 to 25 aromatic ring atoms, each of which may
- R ° is identical or different on each occurrence H, D, F, a straight-chain alkyl or alkoxy group having 1 to 10 C atoms or a branched or cyclic alkyl or alkoxy group having 3 to 10 C Atoms, wherein the abovementioned groups can each be substituted by one or more radicals R 3 .
- R ° is particularly preferably identical or different at each occurrence, H, F, a straight-chain alkyl group having 1 to 10 C atoms or a branched or cyclic alkyl group having 3 to 10 C atoms, where the abovementioned groups each contain one or more R 3 radicals can be substituted.
- Preferred embodiments of the compounds of the formula (I) correspond to the following formulas (1-1) to (1-18)
- Particularly preferred embodiments of the compounds of the formulas (I-8) and (1-17) correspond to the formulas (I-8-A) and (1-17-A)
- Schemes 1 to 8 show processes for the preparation of compounds of formulas (11-1) to (II-6) which are intermediates in the preparation of compounds of formula (I).
- t is the same or different at each occurrence 0 or 1, wherein at least one index t per formula is equal to 1.
- formulas (11-1) to (II-6) that Z is the same or different at each occurrence from Cl, Br, I and B (OR 3 ) 2 .
- Scheme 1 shows a suitable synthesis for the intermediate of formula (II-6).
- Scheme 2 shows a suitable synthesis for the intermediate of formula (II-5).
- Scheme 3 shows a suitable synthesis for the intermediate of formula (11-4).
- Scheme 4 shows a suitable synthesis for the intermediate of formula (11-3).
- Scheme 5 shows a suitable synthesis for the intermediate of formula (11-2).
- Scheme 7 shows a suitable alternative synthesis for intermediates according to formulas (11-1) and (II-4).
- Scheme 8 shows a suitable alternative synthesis for intermediates according to formulas (II-2) and (II-3).
- the building blocks shown above can be provided at the benzofluorene unit with a reactive group, such as halogen, which shows the following scheme:
- the reactive groups Z provided intermediates according to the formulas (11-1) to (II-6) are versatile building blocks, which can be converted to compounds of formula (I), as shown in the following scheme: chema 10
- the present application therefore also provides a process for the preparation of compounds of the formula (I), which comprises first preparing the spirobifluorene skeleton and, in a later step, using an organometallic coupling reaction, an arylamino or a carbazole group or an aryl group. or
- the organometallic coupling reaction is preferably one
- a cycloaddition such as a 1, 3-dipolar cycloaddition
- Another object of the invention are therefore oligomers, polymers or dendrimers containing one or more compounds according to
- Formula (I), wherein the bond (s) to the polymer, oligomer or dendrimer can be located at any, in formula (I) with R °, R 1 or R 2 substituted positions.
- the compound is part of a side chain of the oligomer or polymer or constituent of the main chain.
- An oligomer in the context of this invention is understood as meaning a compound which is composed of at least three monomer units.
- a polymer in the context of the invention is understood as meaning a compound which is composed of at least ten monomer units.
- the polymers, oligomers or dendrimers according to the invention may be conjugated, partially conjugated or non-conjugated.
- the oligomers or polymers of the invention may be linear, branched or dendritic.
- the units of formula (I) may be directly linked together or may be linked together via a divalent group, for example via a substituted or unsubstituted alkylene group, via a heteroatom or via a divalent aromatic or heteroaromatic group.
- three or more units of formula (I) may be linked via a trivalent or higher valent group, for example via a trivalent or higher valent aromatic or heteroaromatic group, to a branched or dendritic oligomer or polymer.
- the monomers according to the invention are homopolymerized or copolymerized with further monomers.
- Suitable and preferred comonomers are selected from fluorenes (eg according to EP 842208 or WO 2000/22026),
- Spirobifluorenes eg according to EP 707020, EP 894107 or WO 2006/061181
- paraphenylenes eg according to WO 1992/18552
- carbazoles eg according to WO 2004/070772 or WO 2004/113468
- thiophenes eg according to EP 1028136
- dihydrophenanthrenes e.g. B. according to WO
- the polymers, oligomers and dendrimers usually also contain further units, for example emitting (fluorescent or phosphorescent) units, such as. Vinyltriarylamines (for example according to WO 2007/068325) or phosphorescent metal complexes (for example according to WO 2006/003000), and / or charge transport units, especially those based on triarylamines.
- the polymers, oligomers and dendrimers according to the invention have advantageous properties, in particular high lifetimes, high
- the polymers and oligomers according to the invention are generally prepared by polymerization of one or more types of monomer, of which at least one monomer in the polymer leads to repeat units of the formula (I). Suitable polymerization reactions are known in the art and described in the literature. Particularly suitable and preferred polymerization reactions which lead to C-C or C-N linkages are the following:
- formulations of the compounds according to the invention are required. These formulations may be, for example, solutions, dispersions or emulsions. It may be preferable to use mixtures of two or more solvents for this purpose. Suitable and preferred solvents are, for example, toluene, anisole, o-, m- or p-xylene,
- Methyl benzoate mesitylene, tetralin, veratrole, THF, methyl THF, THP, chlorobenzene, dioxane, phenoxytoluene, especially 3-phenoxytoluene, (-) - fenchone, 1,2,3,5-tetramethylbenzene, 1,2,4,5 -Tetramethylbenzene, 1-
- Triethylene glycol dimethyl ether diethylene glycol monobutyl ether
- Tripropylene glycol dimethyl ether Tripropylene glycol dimethyl ether, tetraethylene glycol dimethyl ether, 2-isopropylnaphthalene, pentylbenzene, hexylbenzene, heptylbenzene,
- the invention therefore further provides a formulation, in particular a solution, dispersion or emulsion containing
- Polymer, oligomer or dendrimer comprising at least one unit of the formula (I) and at least one solvent, preferably an organic solvent. How such solutions can be prepared is known to the person skilled in the art and, for example, in WO
- the compounds according to the invention are suitable for use in electronic devices, in particular in organic electrical luminescence devices (OLEDs). Depending on the substitution, the compounds are in different functions and layers
- Another object of the invention is therefore the use of
- the electronic device is preferably selected from the group consisting of organic integrated circuits (OICs), organic field effect transistors (OFETs), organic thin film transistors (OTFTs), organic light emitting transistors (OLETs),
- OICs organic integrated circuits
- OFETs organic field effect transistors
- OTFTs organic thin film transistors
- OLETs organic light emitting transistors
- organic solar cells organic solar cells (OSCs), organic optical detectors, organic photoreceptors, organic field quench devices
- OLEDs organic laser diodes
- O-lasers organic laser diodes
- OLEDs organic electroluminescent devices
- the electronic device is preferably selected from the abovementioned devices.
- OLED organic electroluminescent device
- Hole transport layer or another layer at least one compound according to formula (I) contains.
- the organic electroluminescent device may contain further layers. These are, for example, selected from in each case one or more hole injection layers, hole transport layers, hole blocking layers, electron transport layers, electron injection layers, electron blocking layers, exciton blocking layers, intermediate layers
- the sequence of the layers of the organic electroluminescent device containing the compound of the formula (I) is preferably the following:
- Anode hole injection layer hole transport layer-optionally further hole transport layer-optionally electron-blocking layer-emitting layer-electron transport layer-electron injection layer cathode is not all of the layers mentioned must be present, and additional layers may additionally be present.
- the organic electroluminescent device according to the invention may contain a plurality of emitting layers.
- these emission layers particularly preferably have a total of a plurality of emission maxima between 380 nm and 750 nm, so that overall white emission results, ie. H. in the emitting layers
- Hole transport layer or the electron blocking layer present.
- the compound according to formula (I) is used in an electronic device containing one or more phosphorescent emitters.
- the compound may be contained in different layers, preferably in a hole transport layer, an electron blocking layer, a hole injection layer or in an emitting layer. From the term phosphorescent emitters are typical
- Suitable phosphorescent emitters are, in particular, compounds which emit light, preferably in the visible range, with suitable excitation and also contain at least one atom of atomic number greater than 20, preferably greater than 38 and less than 84, particularly preferably greater than 56 and less than 80.
- Preferred phosphorescent emitters used are compounds containing copper, molybdenum, tungsten, rhenium, ruthenium, osmium, rhodium, iridium, palladium, platinum, silver, gold or europium, in particular compounds containing iridium, platinum or copper.
- luminescent iridium, platinum or copper complexes are regarded as phosphorescent emitters.
- the compound according to formula (I) can also according to the invention in an electronic device containing one or more
- the compounds of the formula (I) are used as hole transport material.
- the compounds are then preferably used in a hole transport layer, an electron blocking layer or a hole injection layer.
- a hole transport layer according to the present application is a hole transporting layer located between the anode and the emissive layer.
- a hole injection layer is in the case of multiple hole transport layers between anode and
- emissive layer has a hole transport layer which connects directly to the anode or is separated from it only by a single coating of the anode.
- An electron blocking layer is, in the case of a plurality of hole transport layers between the anode and the emitting layer, the hole transport layer which adjoins the emitting layer directly on the anode side.
- the organic layer comprising the compound of the formula (I) then additionally contains one or more p-dopants.
- p-dopants preferably those organic electron acceptor compounds are used which can oxidize one or more of the other compounds of the mixture.
- p-dopants are those described in WO 2011/073149, EP 1968131, EP 2276085, EP 2213662, EP 1722602, EP 2045848, DE 102007031220, US 8044390, US 8057712, WO 2009/003455, WO 2010/094378, WO 2011/120709, US 2010/0096600 and WO 2012/095143 disclosed compounds.
- p-dopants are quinodimethane compounds, azaindenofluorendiones, azaphenalens, azatriphenylenes,
- Metal halides preferably transition metal halides, metal oxides, preferably metal oxides containing at least one transition metal or a metal of the 3rd main group, and transition metal complexes, preferably complexes of Cu, Co, Ni, Pd and Pt with ligands containing at least one oxygen atom as a binding site. Preference is still given
- Transition metal oxides as dopants preferably oxides of rhenium, molybdenum and tungsten, particularly preferably Re 2 O 7 , MoO 3) WO 3 and ReO 3 .
- the p-dopants are preferably present largely uniformly distributed in the p-doped layers. This can be achieved, for example, by co-evaporation of the p-dopant and the hole transport material matrix.
- the compound according to formula (I) is used as hole transport material in combination with a hexaazatriphenylene derivative as described in US 2007/0092755.
- a hexaazatriphenylenderivat is used in a separate layer.
- the compound of the formula (I) is used as matrix material in combination with one or more emitters, preferably phosphorescent emitters.
- the proportion of the matrix material in the emitting layer is in this case between 50.0 and 99.9% by volume, preferably between 80.0 and 99.5% by volume and particularly preferred for fluorescent emitting layers between 92.0 and 99.5% by volume and for phosphorescent emitting layers between 85.0 and 97.0 vol.%. Accordingly, the proportion of the emitter is between 0.1 and
- An emitting layer of an organic electroluminescent device may also contain systems comprising a plurality of matrix materials (mixed-matrix systems) and / or a plurality of emitters. Also in this case, the emitters are generally those compounds whose contribution in the system is smaller and the matrix materials are those compounds whose contribution in the system is larger. In individual cases, however, the proportion of a single matrix material in the system may be smaller than the proportion of a single emitter.
- the mixed-matrix systems preferably comprise two or three different ones
- Matrix materials more preferably two different ones
- Matrix materials In this case, one of the two materials preferably constitutes a material with hole-transporting properties and the other material is a material with electron-transporting properties.
- the compound of formula (I) preferably represents the matrix material with hole-transporting properties
- electron-transporting and hole-transporting properties of the mixed-matrix components may also be mainly or completely combined in a single mixed-matrix component, with the further or the further mixed-matrix components fulfilling other functions.
- the two different matrix materials can be present in a ratio of 1:50 to 1: 1, preferably 1:20 to 1: 1, more preferably 1:10 to 1: 1 and most preferably 1: 4 to 1: 1. Preference is given to mixed-matrix systems in
- the mixed-matrix systems may comprise one or more emitters, preferably one or more phosphorescent emitters. In general, mixed-matrix systems are preferably used in phosphorescent organic electroluminescent devices.
- Particularly suitable matrix materials which can be used in combination with the compounds according to the invention as matrix components of a mixed-matrix system are selected from the below-mentioned preferred matrix materials for phosphorescent emitters or the preferred matrix materials for fluorescent
- Emitter depending on which type of emitter is used in the mixed-matrix system.
- Preferred phosphorescent emitters for use in mixed-matrix systems are the phosphorescent emitters listed above.
- the compound of formula (I) can be used as a fluorescent emitter in an emitting layer.
- the compound of the invention is preferably used in combination with one or more matrix materials. Preferred matrix materials for use in combination with the compound of formula (I) as an emitter are given below.
- Preferred phosphorescent emitters are those mentioned above
- Preferred fluorescent emitters are in addition to the compounds of
- Formula (I) selected from the class of arylamines.
- An arylamine or an aromatic amine in the context of this invention is understood as meaning a compound which contains three substituted or unsubstituted aromatic or heteroaromatic ring systems bonded directly to the nitrogen. At least one of these aromatic or heteroaromatic ring systems is preferably a fused ring system, more preferably at least 14 aromatic ring atoms.
- aromatic anthracenediamines aromatic pyrenamines, aromatic pyrenediamines, aromatic chrysenamines or aromatic chrysenediamines.
- aromatic anthracene amine is meant a compound in which a diarylamino group is bonded directly to an anthracene group, preferably in the 9-position.
- aromatic anthracenediamine is meant a compound in which two
- Diarylamino groups are attached directly to an anthracene group, preferably in the 9,10-position.
- Aromatic pyrenamines, pyrenediamines, chrysenamines and chrysenediamines are defined analogously thereto, the diarylamino groups on the pyrene preferably being bonded in the 1-position or in the 1, 6-position.
- Further preferred emitters are indenofluoreneamines or diamines, for example according to WO 2006/108497 or WO 2006/122630, Benzoindenofluorenamine or diamines, for example according to
- pyrene-arylamines disclosed in WO 2012/048780 and in WO 2013/185871. Also preferred are those in WO
- Suitable matrix materials are materials of different substance classes. preferred
- Matrix materials are selected from the classes of the oligoarylenes (for example 2,2 ', 7,7'-tetraphenylspirobifluorene according to EP 676461 or US Pat
- the condensed aromatic groups the oligoarylenevinylenes (eg DPVBi or spiro-DPVBi according to EP 676461), the polypodal metal complexes (eg according to WO 2004/081017), the hole-conducting compounds (eg according to WO 2004/058911) , the electron-conducting compounds, in particular ketones, phosphine oxides, sulfoxides, etc. (for example according to US Pat
- an oligoarylene is to be understood as meaning a compound in which at least three aryl or arylene groups are bonded to one another.
- Preferred matrix materials for phosphorescent emitters are, in addition to the compounds of the formula (I), aromatic ketones, aromatic
- Phosphine oxides or aromatic sulfoxides or sulfones e.g. B. according to WO 2004/013080, WO 2004/093207, WO 2006/005627 or WO 2010/006680, triarylamines, carbazole derivatives, z. B. CBP ( ⁇ , ⁇ -biscarbazolylbiphenyl) or in WO 2005/039246, US 2005/0069729, JP 2004/288381, EP 1205527 or WO 2008/086851 disclosed carbazole derivatives, indolocarbazole derivatives, z. B. according to WO 2007/063754 or WO 2008/056746, indenocarbazole derivatives, for. B.
- CBP ⁇ , ⁇ -biscarbazolylbiphenyl
- EP 1205527 or WO 2008/086851 disclosed carbazole derivatives, indolocarbazole derivatives, z. B. according to WO 2007/06375
- WO 2010/136109 WO 2011/000455 or WO 2013/041176, Azacarbazolderivate, z. B. according to EP 1617710, EP 1617711, EP 1731584, JP 2005/347160, bipolar matrix materials, for. B. according to WO 2007/137725, silanes, z. B. according to WO 2005/111172, azaborole or boronic esters, z. B. according to WO 2006/117052, triazine derivatives, z. B. according to WO 2010/015306, WO 2007/063754 or WO
- Suitable charge transport materials as used in the hole injection or hole transport layer or in the electron blocking layer or in the
- the compounds which can be used are, for example, the compounds disclosed in Y. Shirota et al., Chem. Rev. 2007, 107 (4), 953-1010 or other materials as described in the prior art Technique can be used in these layers.
- materials for the electron transport layer it is possible to use all materials as used in the prior art as electron transport materials in the electron transport layer.
- aluminum complexes for example Alq 3 , are suitable.
- Zirkoniumkomplexe for example Zrq4, lithium complexes, for example Liq, benzimidazole derivatives, triazine derivatives, pyrimidine derivatives, pyridine derivatives, pyrazine derivatives, quinoxaline derivatives, quinoline derivatives,
- Oxadiazole derivatives aromatic ketones, lactams, boranes,
- Diazaphospholderivate and Phosphinoxidderivate are further suitable materials, as disclosed in JP 2000/053957, WO 2003/060956, WO 2004/028217, WO 2004/080975 and WO 2010/072300.
- Hole transport materials which can be used in a hole transport, hole injection or electron blocking layer in the electroluminescent device according to the invention, indenofluorenamine derivatives (for example according to WO 06/122630 or WO 06/100896), which are described in US Pat
- EP 1661888 disclosed amine derivatives, hexaazatriphenylene derivatives (for example according to WO 01/049806), aromatic fused amine derivatives (for example according to US Pat. No. 5,061,569), the amine derivatives disclosed in WO 95/09147, monobenzoindenofluoreneamines (for example according to US Pat WO 08/006449),
- Dibenzoindenofluoreneamines eg according to WO 07/140847
- spirobifluorene amines eg according to WO 2012/034627 or WO 2013/120577
- fluorene amines eg according to WO 2014/015937, WO 2014 / 015938 and WO
- the cathode of the electronic device are low workfunction metals, metal alloys or multilayer structures of various metals, such as alkaline earth metals, alkali metals, main group metals or lanthanides (eg Ca, Ba, Mg, Al, In, Mg, Yb, Sm, Etc.). Also suitable are alloys of an alkali or alkaline earth metal and silver, for example an alloy of magnesium and silver.
- further metals which have a relatively high work function such as, for example, As Ag or Al, which then usually combinations of metals, such as Ca / Ag, Mg / Ag or Ba / Ag are used. It may also be preferable to provide a thin intermediate layer of a high dielectric constant material between a metallic cathode and the organic semiconductor contribute. For this example, come alkali metal or
- Alkaline earth metal fluorides but also the corresponding oxides or
- Carbonates in question eg LiF, Li 2 O, BaF 2 , MgO, NaF, CsF, Cs 2 CO 3 , etc.
- lithium quinolinate (LiQ) can be used for this purpose.
- the layer thickness of this layer is preferably between 0.5 and 5 nm.
- the anode high workfunction materials are preferred.
- the anode has a work function greater than 4.5 eV. Vacuum up.
- metals with a high redox potential such as Ag, Pt or Au, are suitable for this purpose.
- electrodes z. B. AI / Ni / NiO Xl AI / PtO x
- metal / metal oxide may be preferred, metal / metal oxide.
- at least one of the electrodes must be transparent or
- anode materials are conductive mixed metal oxides. Particularly preferred are indium tin oxide (ITO) or indium zinc oxide (IZO). Preference is furthermore given to conductive, doped organic materials, in particular conductive doped polymers.
- the anode can also consist of several layers, for example of an inner layer of ITO and an outer layer of a metal oxide, preferably tungsten oxide,
- Molybdenum oxide or vanadium oxide are examples of Molybdenum oxide or vanadium oxide.
- the device is structured accordingly (depending on the application), contacted and finally sealed to exclude harmful effects of water and air.
- the electronic device is characterized in that one or more layers are coated with a sublimation process. In the process, the materials in the vacuum sublimation plants become smaller at an initial pressure
- Carrier gas sublimation are coated.
- the materials are applied at a pressure between 10 "applied 5 mbar and 1 bar.
- a special case of this method is the OVJP (organic vapor jet printing) method in which the materials are applied directly through a nozzle and patterned (eg. BMS Arnold et al., Appl. Phys. Lett., 2008, 92, 053301) .
- OVJP organic vapor jet printing
- soluble compounds according to formula (I) are necessary. High solubility can be achieved by suitable substitution of the compounds.
- one or more layers of solution and one or more layers are applied by a sublimation method.
- the electronic devices containing one or more compounds of the formula (I) in displays as
- Light sources in lighting applications and as light sources in medical and / or cosmetic applications are used. embodiments
- reaction mixture is heated to boiling for 5 h under a protective atmosphere.
- the mixture is then distributed between toluene and water, the organic phase with three times Washed water and dried over Na 2 SO 4 and concentrated by rotary evaporation.
- the remaining residue from heptane / T oluol is recrystallized and finally in
- inventive OLEDs and OLEDs according to the prior art is carried out according to a general method according to WO 04/058911, which is adapted to the conditions described here (eg materials). ln the following device examples E1 to E13 and E16 to E18
- the OLEDs have the following layer structure: substrate / p-doped hole transport layer (HIL1) /
- HTL Hole transport layer
- HIL2 p-doped hole transport layer
- EBL hole transport layer
- EML emission layer
- the cathode is formed by a 100 nm thick aluminum layer.
- the emission layer always consists of at least one matrix material (host material, host material) and an emitting dopant (dopant, emitter), which is admixed to the matrix material or the matrix materials by co-evaporation in a specific volume fraction.
- the electron transport layer or the hole injection layers may consist of a mixture of two materials.
- the OLEDs are characterized by default. For this, the electroluminescence spectra, the current efficiency (measured in cd / A), the power efficiency (measured in Im / W) and the external quantum efficiency (EQE, measured in percent) as a function of the luminance, calculated from current-voltage-luminance characteristics ( IUL characteristics) assuming a Lambertian radiation characteristic and the
- the electroluminescence spectra are determined at a luminance of 1000 cd / m 2 and from this the CIE 1931 x and y color coordinates are calculated.
- the indication EQE @ 10 mA / cm 2 designates the external quantum efficiency at a current density of 10mA / cm 2 .
- LT80 @ 60 mA / cm 2 is the lifetime until the OLED has dropped to 80% of its initial intensity at a starting current at constant current of 60 mA / cm 2 .
- the compounds HTM1 to HTM5 and HTM8 to HTM10 according to the invention are very suitable for use as OLED materials, as examples E1 to E13 and E 6 to E18 show (E1 to E8: singlet components, E9 to E13 and E16 to E18: triplet components).
- Quantum efficiencies at 10 mA / cm 2 are also present in the samples E1 according to the invention (356 h), E2 (312 h), E4 (403 h), E6 (275 h), E7 (316 h) and E8 (408 h) significantly better than the reference samples V1 (125 h) and V2 (257 h).
- the reference samples V3 (11.7%) and V4 (18.6%) show lower or equal quantum efficiencies at 2 mA / cm 2 than the inventive samples E10 (18.6%), E 2 ( 19.8%), E16 (19.6%), E17 (19.4%) and E8 (18.6%).
- the lifetimes (80%) at 20 mA / cm 2 of the samples according to the invention are E9 (220 h), E10 (96 h), E11 (109 h), E12 (172 h), E13 (111 h), E16 (150 h), E17 (144 h) and E18 (160 h) were larger than for reference samples V3 (80 h) and V4 (84 h).
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Physics & Mathematics (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Optics & Photonics (AREA)
- Electroluminescent Light Sources (AREA)
- Indole Compounds (AREA)
- Plural Heterocyclic Compounds (AREA)
- Furan Compounds (AREA)
- Photovoltaic Devices (AREA)
Abstract
Description
Claims
Priority Applications (8)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP14742471.7A EP3033405B1 (de) | 2013-08-15 | 2014-07-24 | Materialien für elektronische vorrichtungen |
| JP2016533832A JP6567520B2 (ja) | 2013-08-15 | 2014-07-24 | 電子素子のための材料 |
| KR1020167006680A KR102047653B1 (ko) | 2013-08-15 | 2014-07-24 | 전자 소자용 물질 |
| US14/911,359 US9978950B2 (en) | 2013-08-15 | 2014-07-24 | Materials for electronic devices |
| CN201480042646.4A CN105492574B (zh) | 2013-08-15 | 2014-07-24 | 用于电子器件的材料 |
| CN201910197521.3A CN110003155B (zh) | 2013-08-15 | 2014-07-24 | 用于电子器件的材料 |
| US15/638,783 US9837617B2 (en) | 2013-08-15 | 2017-06-30 | Materials for electronic devices |
| US15/959,481 US10665790B2 (en) | 2013-08-15 | 2018-04-23 | Materials for electronic devices |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP13004061 | 2013-08-15 | ||
| EP13004061.1 | 2013-08-15 |
Related Child Applications (3)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| US14/911,359 A-371-Of-International US9978950B2 (en) | 2013-08-15 | 2014-07-24 | Materials for electronic devices |
| US15/638,783 Continuation US9837617B2 (en) | 2013-08-15 | 2017-06-30 | Materials for electronic devices |
| US15/959,481 Continuation US10665790B2 (en) | 2013-08-15 | 2018-04-23 | Materials for electronic devices |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2015022051A1 true WO2015022051A1 (de) | 2015-02-19 |
Family
ID=49033768
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/EP2014/002031 WO2015022051A1 (de) | 2013-08-15 | 2014-07-24 | Materialien für elektronische vorrichtungen |
Country Status (7)
| Country | Link |
|---|---|
| US (3) | US9978950B2 (de) |
| EP (1) | EP3033405B1 (de) |
| JP (1) | JP6567520B2 (de) |
| KR (1) | KR102047653B1 (de) |
| CN (2) | CN105492574B (de) |
| TW (1) | TWI639590B (de) |
| WO (1) | WO2015022051A1 (de) |
Cited By (54)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2015129896A1 (ja) * | 2014-02-28 | 2015-09-03 | 出光興産株式会社 | 化合物、有機エレクトロルミネッセンス素子用材料、有機エレクトロルミネッセンス素子及び電子機器 |
| KR20160081531A (ko) * | 2014-12-31 | 2016-07-08 | 에스에프씨 주식회사 | 고효율과 장수명을 갖는 유기 발광 소자 |
| KR20160088229A (ko) * | 2015-01-13 | 2016-07-25 | 에스에프씨 주식회사 | 고효율과 장수명을 갖는 유기 발광 소자 |
| WO2016017919A3 (ko) * | 2014-07-28 | 2016-10-13 | 에스에프씨 주식회사 | 헤테로고리를 포함하는 축합 플루오렌 유도체 |
| KR20160119904A (ko) * | 2015-04-06 | 2016-10-17 | 삼성디스플레이 주식회사 | 축합환 화합물 및 이를 포함한 유기 발광 소자 |
| CN106188037A (zh) * | 2016-04-25 | 2016-12-07 | 中节能万润股份有限公司 | 一种基于1,8-二氮杂-9-芴酮的化合物及其应用 |
| KR20160146272A (ko) * | 2015-06-12 | 2016-12-21 | 에스에프씨 주식회사 | 고효율을 갖는 유기 발광 소자 |
| US20170012214A1 (en) * | 2015-07-09 | 2017-01-12 | Sfc Co., Ltd. | Organic light-emitting diode with high efficiency and long lifetime |
| KR20170018276A (ko) * | 2015-08-06 | 2017-02-16 | 에스에프씨 주식회사 | 고효율을 갖는 유기 발광 소자 |
| WO2017073932A1 (ko) * | 2015-10-26 | 2017-05-04 | 주식회사 엘지화학 | 아민 화합물 및 이를 포함하는 유기 발광 소자 |
| WO2017082556A1 (ko) * | 2015-11-12 | 2017-05-18 | 에스에프씨 주식회사 | 신규한 유기발광 화합물 및 이를 포함하는 유기 발광 소자 |
| KR20170055411A (ko) * | 2015-11-10 | 2017-05-19 | 에스에프씨 주식회사 | 저전압구동이 가능하며 고효율의 유기 발광 소자 |
| WO2017102063A1 (en) * | 2015-12-16 | 2017-06-22 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2017102064A1 (en) * | 2015-12-16 | 2017-06-22 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2017133829A1 (de) | 2016-02-05 | 2017-08-10 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2017146522A1 (ko) * | 2016-02-25 | 2017-08-31 | 주식회사 엘지화학 | 헤테로고리 화합물 및 이를 포함하는 유기 발광 소자 |
| WO2017207596A1 (en) * | 2016-06-03 | 2017-12-07 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| KR20180030350A (ko) * | 2016-09-13 | 2018-03-22 | 삼성디스플레이 주식회사 | 축합환 화합물 및 이를 포함한 유기 발광 소자 |
| CN107915698A (zh) * | 2016-10-05 | 2018-04-17 | Sfc株式会社 | 新型有机化合物以及包括该有机化合物的有机发光元件 |
| WO2018069167A1 (de) | 2016-10-10 | 2018-04-19 | Merck Patent Gmbh | Elektronische vorrichtung |
| WO2018083053A1 (de) | 2016-11-02 | 2018-05-11 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2018095839A1 (de) | 2016-11-22 | 2018-05-31 | Merck Patent Gmbh | Verbrückte triarylamine für elektronische vorrichtungen |
| WO2018141706A1 (de) | 2017-02-02 | 2018-08-09 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2018157981A1 (de) | 2017-03-02 | 2018-09-07 | Merck Patent Gmbh | Materialien für organische elektronische vorrichtungen |
| JP2018529644A (ja) * | 2015-07-29 | 2018-10-11 | メルク パテント ゲーエムベーハー | 有機エレクトロルミネッセンス素子のための材料 |
| CN108698978A (zh) * | 2016-02-23 | 2018-10-23 | 默克专利有限公司 | 用于有机电致发光器件的材料 |
| WO2018197447A1 (de) | 2017-04-25 | 2018-11-01 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| WO2018234346A1 (en) | 2017-06-23 | 2018-12-27 | Merck Patent Gmbh | MATERIALS FOR ORGANIC ELECTROLUMINESCENT DEVICES |
| WO2019002190A1 (en) | 2017-06-28 | 2019-01-03 | Merck Patent Gmbh | MATERIALS FOR ELECTRONIC DEVICES |
| KR20190006930A (ko) * | 2017-07-11 | 2019-01-21 | 에스에프씨 주식회사 | 고효율을 갖는 유기 발광 소자 |
| US10193076B2 (en) | 2015-10-26 | 2019-01-29 | Lg Chem, Ltd. | Amine compound and organic light emitting element comprising same |
| WO2019020654A1 (en) | 2017-07-28 | 2019-01-31 | Merck Patent Gmbh | SPIROBIFLUORENE DERIVATIVES FOR USE IN ELECTRONIC DEVICES |
| WO2019048443A1 (de) | 2017-09-08 | 2019-03-14 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2019101719A1 (de) | 2017-11-23 | 2019-05-31 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2019115577A1 (en) | 2017-12-15 | 2019-06-20 | Merck Patent Gmbh | Substituted aromatic amines for use in organic electroluminescent devices |
| WO2019175149A1 (en) | 2018-03-16 | 2019-09-19 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| KR20190111855A (ko) * | 2014-05-13 | 2019-10-02 | 에스에프씨 주식회사 | 방향족 아민기를 포함하는 헤테로고리 화합물 및 이를 포함하는 유기 발광 소자 |
| WO2022243403A1 (de) | 2021-05-21 | 2022-11-24 | Merck Patent Gmbh | Verfahren zur kontinuierlichen aufreinigung von mindestens einem funktionalen material und vorrichtung zur kontinuierlichen aufreinigung von mindestens einem funktionalen material |
| WO2023052272A1 (de) | 2021-09-28 | 2023-04-06 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2023052314A1 (de) | 2021-09-28 | 2023-04-06 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2023052377A1 (de) | 2021-09-30 | 2023-04-06 | Merck Patent Gmbh | Organische elektrolumineszierende vorrichtung |
| WO2023052313A1 (de) | 2021-09-28 | 2023-04-06 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2023052275A1 (de) | 2021-09-28 | 2023-04-06 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2023052376A1 (de) | 2021-09-30 | 2023-04-06 | Merck Patent Gmbh | Organische elektrolumineszierende vorrichtung |
| WO2023061998A1 (de) | 2021-10-14 | 2023-04-20 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2023078812A1 (de) | 2021-11-02 | 2023-05-11 | Merck Patent Gmbh | Benzofuro[3,2-d]pyrimidin-2,4-dicarbonitril-derivate und ähnliche verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2023094412A1 (de) | 2021-11-25 | 2023-06-01 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2023099430A1 (de) | 2021-12-02 | 2023-06-08 | Merck Patent Gmbh | Triphenylen-triazin-dibenzofuran/dibenzothiophen-derivate für organische elektrolumineszenzvorrichtungen |
| WO2023117837A1 (de) | 2021-12-21 | 2023-06-29 | Merck Patent Gmbh | Verfahren zur herstellung von deuterierten organischen verbindungen |
| WO2023152346A1 (de) | 2022-02-14 | 2023-08-17 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2023222559A1 (de) | 2022-05-18 | 2023-11-23 | Merck Patent Gmbh | Verfahren zur herstellung von deuterierten organischen verbindungen |
| US11871661B2 (en) | 2015-12-17 | 2024-01-09 | Samsung Display Co., Ltd. | Organic light-emitting device |
| WO2024013004A1 (de) | 2022-07-11 | 2024-01-18 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| US11937502B2 (en) | 2015-04-14 | 2024-03-19 | Samsung Display Co., Ltd. | Condensed cyclic compound and organic light-emitting device comprising the same |
Families Citing this family (19)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP3235892B1 (de) * | 2012-02-14 | 2019-02-27 | Merck Patent GmbH | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2015022051A1 (de) | 2013-08-15 | 2015-02-19 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| KR102148643B1 (ko) * | 2013-09-26 | 2020-08-28 | 롬엔드하스전자재료코리아유한회사 | 신규한 유기 전계 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 |
| WO2016102048A1 (de) * | 2014-12-22 | 2016-06-30 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| JP6925982B2 (ja) * | 2015-02-16 | 2021-08-25 | メルク パテント ゲーエムベーハー | 電子素子のための材料 |
| US10566550B2 (en) * | 2015-05-22 | 2020-02-18 | Merck Patent Gmbh | Formulation containing an organic semiconductor and a metal complex |
| KR102656066B1 (ko) * | 2015-11-13 | 2024-04-09 | 에스에프씨 주식회사 | 신규한 아민 화합물 및 이를 포함하는 유기 발광 소자 |
| KR101964607B1 (ko) * | 2016-09-28 | 2019-04-02 | 주식회사 엘지화학 | 헤테로고리 화합물 및 이를 포함하는 유기 발광 소자 |
| CN107868067B (zh) * | 2016-09-28 | 2021-06-15 | 株式会社Lg化学 | 杂环化合物及包含其的有机发光元件 |
| EP3621957B1 (de) * | 2017-05-09 | 2023-08-23 | Ambient Photonics, Inc. | Kondensierte stilbenderivate als solarzellenfarbstoffe |
| KR102235629B1 (ko) * | 2017-06-05 | 2021-04-02 | 덕산네오룩스 주식회사 | 유기전기 소자용 화합물, 이를 이용한 유기전기소자 및 그 전자 장치 |
| CN108336238B (zh) * | 2017-12-29 | 2020-07-28 | 昱镭光电科技股份有限公司 | 使用螺双芴环化合物的有机发光元件 |
| CN111592464A (zh) * | 2019-02-20 | 2020-08-28 | 常州强力电子新材料股份有限公司 | 含螺二芴结构的有机化合物及其应用 |
| CN111606812B (zh) * | 2020-05-25 | 2021-07-06 | 长春海谱润斯科技股份有限公司 | 一种三芳胺衍生物及其有机电致发光器件 |
| CN111635324B (zh) * | 2020-06-29 | 2021-06-18 | 南京高光半导体材料有限公司 | 一种有机电致发光化合物及有机电致发光器件 |
| CN112457278B (zh) * | 2020-11-24 | 2022-11-08 | 吉林奥来德光电材料股份有限公司 | 一种有机电致发光化合物及其制备方法与应用 |
| KR20220086763A (ko) * | 2020-12-16 | 2022-06-24 | 주식회사 센텀머티리얼즈 | 신규한 스피로플루오렌 화합물 및 이를 포함하는 유기 발광 소자 |
| CN112375053B (zh) * | 2021-01-13 | 2021-04-16 | 南京高光半导体材料有限公司 | 一种化合物及有机电致发光器件 |
| CN112390768B (zh) * | 2021-01-19 | 2021-04-13 | 南京高光半导体材料有限公司 | 一种化合物及有机电致发光器件 |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2006108497A1 (de) * | 2005-04-14 | 2006-10-19 | Merck Patent Gmbh | Verbindungen für organische elektronische vorrichtungen |
| WO2006122630A1 (de) * | 2005-05-20 | 2006-11-23 | Merck Patent Gmbh | Verbindungen für organische elektronische vorrichtungen |
| WO2013100467A1 (ko) * | 2011-12-30 | 2013-07-04 | 제일모직 주식회사 | 유기광전자소자용 화합물, 이를 포함하는 유기발광소자 및 상기 유기발광소자를 포함하는 표시장치 |
| WO2014129846A1 (en) * | 2013-02-21 | 2014-08-28 | Rohm And Haas Electronic Materials Korea Ltd. | Organic electroluminescent compounds and an organic electroluminescent device comprising the same |
Family Cites Families (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE102010013068A1 (de) * | 2010-03-26 | 2011-09-29 | Merck Patent Gmbh | Verbindungen für elektronische Vorrichtungen |
| KR102182270B1 (ko) * | 2013-02-21 | 2020-11-24 | 롬엔드하스전자재료코리아유한회사 | 유기 전계 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 |
| WO2015022051A1 (de) | 2013-08-15 | 2015-02-19 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
-
2014
- 2014-07-24 WO PCT/EP2014/002031 patent/WO2015022051A1/de active Application Filing
- 2014-07-24 EP EP14742471.7A patent/EP3033405B1/de active Active
- 2014-07-24 CN CN201480042646.4A patent/CN105492574B/zh active Active
- 2014-07-24 US US14/911,359 patent/US9978950B2/en active Active
- 2014-07-24 KR KR1020167006680A patent/KR102047653B1/ko active IP Right Grant
- 2014-07-24 CN CN201910197521.3A patent/CN110003155B/zh active Active
- 2014-07-24 JP JP2016533832A patent/JP6567520B2/ja active Active
- 2014-08-12 TW TW103127619A patent/TWI639590B/zh active
-
2017
- 2017-06-30 US US15/638,783 patent/US9837617B2/en active Active
-
2018
- 2018-04-23 US US15/959,481 patent/US10665790B2/en active Active
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2006108497A1 (de) * | 2005-04-14 | 2006-10-19 | Merck Patent Gmbh | Verbindungen für organische elektronische vorrichtungen |
| WO2006122630A1 (de) * | 2005-05-20 | 2006-11-23 | Merck Patent Gmbh | Verbindungen für organische elektronische vorrichtungen |
| WO2013100467A1 (ko) * | 2011-12-30 | 2013-07-04 | 제일모직 주식회사 | 유기광전자소자용 화합물, 이를 포함하는 유기발광소자 및 상기 유기발광소자를 포함하는 표시장치 |
| WO2014129846A1 (en) * | 2013-02-21 | 2014-08-28 | Rohm And Haas Electronic Materials Korea Ltd. | Organic electroluminescent compounds and an organic electroluminescent device comprising the same |
Cited By (105)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US11616200B2 (en) | 2014-02-28 | 2023-03-28 | Idemitsu Kosan Co., Ltd. | Compound, material for organic electroluminescent element, organic electroluminescent element, and electronic apparatus |
| WO2015129896A1 (ja) * | 2014-02-28 | 2015-09-03 | 出光興産株式会社 | 化合物、有機エレクトロルミネッセンス素子用材料、有機エレクトロルミネッセンス素子及び電子機器 |
| KR20190111855A (ko) * | 2014-05-13 | 2019-10-02 | 에스에프씨 주식회사 | 방향족 아민기를 포함하는 헤테로고리 화합물 및 이를 포함하는 유기 발광 소자 |
| KR102230153B1 (ko) | 2014-05-13 | 2021-03-22 | 에스에프씨주식회사 | 방향족 아민기를 포함하는 헤테로고리 화합물 및 이를 포함하는 유기 발광 소자 |
| WO2016017919A3 (ko) * | 2014-07-28 | 2016-10-13 | 에스에프씨 주식회사 | 헤테로고리를 포함하는 축합 플루오렌 유도체 |
| US11683980B2 (en) | 2014-07-28 | 2023-06-20 | Sfc Co., Ltd. | Condensed fluorene derivative comprising heterocyclic ring |
| KR20160081531A (ko) * | 2014-12-31 | 2016-07-08 | 에스에프씨 주식회사 | 고효율과 장수명을 갖는 유기 발광 소자 |
| KR102190108B1 (ko) | 2014-12-31 | 2020-12-11 | 에스에프씨주식회사 | 고효율과 장수명을 갖는 유기 발광 소자 |
| KR20160088229A (ko) * | 2015-01-13 | 2016-07-25 | 에스에프씨 주식회사 | 고효율과 장수명을 갖는 유기 발광 소자 |
| KR102201104B1 (ko) | 2015-01-13 | 2021-01-11 | 에스에프씨주식회사 | 고효율과 장수명을 갖는 유기 발광 소자 |
| KR20160119904A (ko) * | 2015-04-06 | 2016-10-17 | 삼성디스플레이 주식회사 | 축합환 화합물 및 이를 포함한 유기 발광 소자 |
| KR102483949B1 (ko) * | 2015-04-06 | 2023-01-03 | 삼성디스플레이 주식회사 | 축합환 화합물 및 이를 포함한 유기 발광 소자 |
| US11937502B2 (en) | 2015-04-14 | 2024-03-19 | Samsung Display Co., Ltd. | Condensed cyclic compound and organic light-emitting device comprising the same |
| KR102002031B1 (ko) * | 2015-06-12 | 2019-07-23 | 에스에프씨주식회사 | 고효율을 갖는 유기 발광 소자 |
| KR20160146272A (ko) * | 2015-06-12 | 2016-12-21 | 에스에프씨 주식회사 | 고효율을 갖는 유기 발광 소자 |
| US10950802B2 (en) | 2015-06-12 | 2021-03-16 | Sfc Co., Ltd. | Organic light-emitting diode with high efficiency |
| CN107690719A (zh) * | 2015-06-12 | 2018-02-13 | Sfc株式会社 | 具有高效率的有机发光元件 |
| KR20170007688A (ko) * | 2015-07-09 | 2017-01-19 | 에스에프씨 주식회사 | 고효율과 장수명을 갖는 유기 발광 소자 |
| US20170012214A1 (en) * | 2015-07-09 | 2017-01-12 | Sfc Co., Ltd. | Organic light-emitting diode with high efficiency and long lifetime |
| US10790450B2 (en) | 2015-07-09 | 2020-09-29 | Sfc Co., Ltd. | Organic light-emitting diode with high efficiency and long lifetime |
| CN106340593A (zh) * | 2015-07-09 | 2017-01-18 | Sfc株式会社 | 具有高效率和长寿命的有机发光元件 |
| KR102002034B1 (ko) * | 2015-07-09 | 2019-07-22 | 에스에프씨주식회사 | 고효율과 장수명을 갖는 유기 발광 소자 |
| US11538995B2 (en) | 2015-07-29 | 2022-12-27 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| JP2018529644A (ja) * | 2015-07-29 | 2018-10-11 | メルク パテント ゲーエムベーハー | 有機エレクトロルミネッセンス素子のための材料 |
| KR20170018276A (ko) * | 2015-08-06 | 2017-02-16 | 에스에프씨 주식회사 | 고효율을 갖는 유기 발광 소자 |
| US10741768B2 (en) | 2015-08-06 | 2020-08-11 | Sfc Co., Ltd. | Organic light-emitting diode with high efficiency |
| KR102091695B1 (ko) * | 2015-08-06 | 2020-03-24 | 에스에프씨주식회사 | 고효율을 갖는 유기 발광 소자 |
| CN107108498B (zh) * | 2015-10-26 | 2020-08-21 | 株式会社Lg化学 | 胺化合物和包含其的有机发光元件 |
| US10193076B2 (en) | 2015-10-26 | 2019-01-29 | Lg Chem, Ltd. | Amine compound and organic light emitting element comprising same |
| WO2017073932A1 (ko) * | 2015-10-26 | 2017-05-04 | 주식회사 엘지화학 | 아민 화합물 및 이를 포함하는 유기 발광 소자 |
| CN107108498A (zh) * | 2015-10-26 | 2017-08-29 | 株式会社Lg化学 | 胺化合物和包含其的有机发光元件 |
| US11545629B2 (en) | 2015-11-10 | 2023-01-03 | Sfc Co., Ltd. | Organic light-emitting diode with high efficiency and low voltage |
| KR20170055411A (ko) * | 2015-11-10 | 2017-05-19 | 에스에프씨 주식회사 | 저전압구동이 가능하며 고효율의 유기 발광 소자 |
| KR101976408B1 (ko) * | 2015-11-10 | 2019-05-16 | 에스에프씨주식회사 | 저전압구동이 가능하며 고효율의 유기 발광 소자 |
| CN108349922A (zh) * | 2015-11-12 | 2018-07-31 | Sfc株式会社 | 新型有机发光化合物及包括此的有机发光元件 |
| WO2017082556A1 (ko) * | 2015-11-12 | 2017-05-18 | 에스에프씨 주식회사 | 신규한 유기발광 화합물 및 이를 포함하는 유기 발광 소자 |
| KR101817775B1 (ko) * | 2015-11-12 | 2018-01-11 | 에스에프씨주식회사 | 신규한 유기발광 화합물 및 이를 포함하는 유기 발광 소자 |
| CN108368054A (zh) * | 2015-12-16 | 2018-08-03 | 默克专利有限公司 | 用于有机电致发光器件的材料 |
| CN108368082A (zh) * | 2015-12-16 | 2018-08-03 | 默克专利有限公司 | 用于有机电致发光器件的材料 |
| WO2017102063A1 (en) * | 2015-12-16 | 2017-06-22 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2017102064A1 (en) * | 2015-12-16 | 2017-06-22 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| JP2019506369A (ja) * | 2015-12-16 | 2019-03-07 | メルク パテント ゲーエムベーハー | 有機エレクトロルミネッセンス素子のための材料 |
| CN108368054B (zh) * | 2015-12-16 | 2022-09-02 | 默克专利有限公司 | 用于有机电致发光器件的材料 |
| JP2023011548A (ja) * | 2015-12-16 | 2023-01-24 | メルク パテント ゲーエムベーハー | 有機エレクトロルミネッセンス素子のための材料 |
| US11871661B2 (en) | 2015-12-17 | 2024-01-09 | Samsung Display Co., Ltd. | Organic light-emitting device |
| JP7051691B2 (ja) | 2016-02-05 | 2022-04-11 | メルク パテント ゲーエムベーハー | 電子素子のための材料 |
| JP2019507138A (ja) * | 2016-02-05 | 2019-03-14 | メルク パテント ゲーエムベーハー | 電子素子のための材料 |
| WO2017133829A1 (de) | 2016-02-05 | 2017-08-10 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| JP2022031649A (ja) * | 2016-02-23 | 2022-02-22 | メルク パテント ゲーエムベーハー | 有機エレクトロルミネッセントデバイス材料 |
| CN108698978A (zh) * | 2016-02-23 | 2018-10-23 | 默克专利有限公司 | 用于有机电致发光器件的材料 |
| JP2019512466A (ja) * | 2016-02-23 | 2019-05-16 | メルク パテント ゲーエムベーハー | 有機エレクトロルミネッセントデバイス材料 |
| US11538996B2 (en) | 2016-02-23 | 2022-12-27 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| JP7069027B2 (ja) | 2016-02-23 | 2022-05-17 | メルク パテント ゲーエムベーハー | 有機エレクトロルミネッセントデバイス材料 |
| CN113214202A (zh) * | 2016-02-25 | 2021-08-06 | 株式会社Lg化学 | 杂环化合物和包含其的有机发光二极管 |
| CN108026060A (zh) * | 2016-02-25 | 2018-05-11 | 株式会社Lg化学 | 杂环化合物和包含其的有机发光二极管 |
| CN113214202B (zh) * | 2016-02-25 | 2023-11-21 | 株式会社Lg化学 | 杂环化合物和包含其的有机发光二极管 |
| JP2018535185A (ja) * | 2016-02-25 | 2018-11-29 | エルジー・ケム・リミテッド | ヘテロ環化合物およびこれを含む有機発光素子 |
| WO2017146522A1 (ko) * | 2016-02-25 | 2017-08-31 | 주식회사 엘지화학 | 헤테로고리 화합물 및 이를 포함하는 유기 발광 소자 |
| US10822330B2 (en) | 2016-02-25 | 2020-11-03 | Lg Chem, Ltd. | Heterocyclic compound and organic light emitting diode containing same |
| CN108026060B (zh) * | 2016-02-25 | 2020-12-25 | 株式会社Lg化学 | 杂环化合物和包含其的有机发光二极管 |
| CN106188037A (zh) * | 2016-04-25 | 2016-12-07 | 中节能万润股份有限公司 | 一种基于1,8-二氮杂-9-芴酮的化合物及其应用 |
| JP2019523765A (ja) * | 2016-06-03 | 2019-08-29 | メルク パテント ゲーエムベーハー | 有機エレクトロルミネッセントデバイス材料 |
| WO2017207596A1 (en) * | 2016-06-03 | 2017-12-07 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| JP7486921B2 (ja) | 2016-06-03 | 2024-05-20 | メルク パテント ゲーエムベーハー | 有機エレクトロルミネッセントデバイス材料 |
| JP2022116058A (ja) * | 2016-06-03 | 2022-08-09 | メルク パテント ゲーエムベーハー | 有機エレクトロルミネッセントデバイス材料 |
| EP3978477A3 (de) * | 2016-06-03 | 2022-06-22 | Merck Patent GmbH | Materialien für organische elektrolumineszente vorrichtungen |
| KR102643638B1 (ko) | 2016-09-13 | 2024-03-06 | 삼성디스플레이 주식회사 | 축합환 화합물 및 이를 포함한 유기 발광 소자 |
| KR20180030350A (ko) * | 2016-09-13 | 2018-03-22 | 삼성디스플레이 주식회사 | 축합환 화합물 및 이를 포함한 유기 발광 소자 |
| CN107915698A (zh) * | 2016-10-05 | 2018-04-17 | Sfc株式会社 | 新型有机化合物以及包括该有机化合物的有机发光元件 |
| CN107915698B (zh) * | 2016-10-05 | 2024-02-02 | Sfc株式会社 | 新型有机化合物以及包括该有机化合物的有机发光元件 |
| EP4113643A1 (de) | 2016-10-10 | 2023-01-04 | Merck Patent GmbH | Elektronische vorrichtung |
| EP4255151A2 (de) | 2016-10-10 | 2023-10-04 | Merck Patent GmbH | Spiro[fluoren-9,9'-(thio)xanthen] verbindungen |
| WO2018069167A1 (de) | 2016-10-10 | 2018-04-19 | Merck Patent Gmbh | Elektronische vorrichtung |
| WO2018083053A1 (de) | 2016-11-02 | 2018-05-11 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2018095839A1 (de) | 2016-11-22 | 2018-05-31 | Merck Patent Gmbh | Verbrückte triarylamine für elektronische vorrichtungen |
| WO2018141706A1 (de) | 2017-02-02 | 2018-08-09 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2018157981A1 (de) | 2017-03-02 | 2018-09-07 | Merck Patent Gmbh | Materialien für organische elektronische vorrichtungen |
| WO2018197447A1 (de) | 2017-04-25 | 2018-11-01 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| WO2018234346A1 (en) | 2017-06-23 | 2018-12-27 | Merck Patent Gmbh | MATERIALS FOR ORGANIC ELECTROLUMINESCENT DEVICES |
| WO2019002190A1 (en) | 2017-06-28 | 2019-01-03 | Merck Patent Gmbh | MATERIALS FOR ELECTRONIC DEVICES |
| KR20190006930A (ko) * | 2017-07-11 | 2019-01-21 | 에스에프씨 주식회사 | 고효율을 갖는 유기 발광 소자 |
| US11532792B2 (en) | 2017-07-11 | 2022-12-20 | Sfc Co., Ltd. | Organic light emitting diode having high efficiency |
| EP3654395A4 (de) * | 2017-07-11 | 2021-04-07 | SFC Co., Ltd. | Organische leuchtdiode mit hoher effizienz |
| KR102637968B1 (ko) | 2017-07-11 | 2024-02-19 | 에스에프씨 주식회사 | 고효율을 갖는 유기 발광 소자 |
| WO2019020654A1 (en) | 2017-07-28 | 2019-01-31 | Merck Patent Gmbh | SPIROBIFLUORENE DERIVATIVES FOR USE IN ELECTRONIC DEVICES |
| WO2019048443A1 (de) | 2017-09-08 | 2019-03-14 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2019101719A1 (de) | 2017-11-23 | 2019-05-31 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| EP4242286A2 (de) | 2017-11-23 | 2023-09-13 | Merck Patent GmbH | Materialien für elektronische vorrichtungen |
| WO2019115577A1 (en) | 2017-12-15 | 2019-06-20 | Merck Patent Gmbh | Substituted aromatic amines for use in organic electroluminescent devices |
| WO2019175149A1 (en) | 2018-03-16 | 2019-09-19 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2022243403A1 (de) | 2021-05-21 | 2022-11-24 | Merck Patent Gmbh | Verfahren zur kontinuierlichen aufreinigung von mindestens einem funktionalen material und vorrichtung zur kontinuierlichen aufreinigung von mindestens einem funktionalen material |
| WO2023052314A1 (de) | 2021-09-28 | 2023-04-06 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2023052272A1 (de) | 2021-09-28 | 2023-04-06 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2023052313A1 (de) | 2021-09-28 | 2023-04-06 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2023052275A1 (de) | 2021-09-28 | 2023-04-06 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2023052376A1 (de) | 2021-09-30 | 2023-04-06 | Merck Patent Gmbh | Organische elektrolumineszierende vorrichtung |
| WO2023052377A1 (de) | 2021-09-30 | 2023-04-06 | Merck Patent Gmbh | Organische elektrolumineszierende vorrichtung |
| WO2023061998A1 (de) | 2021-10-14 | 2023-04-20 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2023078812A1 (de) | 2021-11-02 | 2023-05-11 | Merck Patent Gmbh | Benzofuro[3,2-d]pyrimidin-2,4-dicarbonitril-derivate und ähnliche verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2023094412A1 (de) | 2021-11-25 | 2023-06-01 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2023099430A1 (de) | 2021-12-02 | 2023-06-08 | Merck Patent Gmbh | Triphenylen-triazin-dibenzofuran/dibenzothiophen-derivate für organische elektrolumineszenzvorrichtungen |
| WO2023117837A1 (de) | 2021-12-21 | 2023-06-29 | Merck Patent Gmbh | Verfahren zur herstellung von deuterierten organischen verbindungen |
| WO2023152346A1 (de) | 2022-02-14 | 2023-08-17 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2023222559A1 (de) | 2022-05-18 | 2023-11-23 | Merck Patent Gmbh | Verfahren zur herstellung von deuterierten organischen verbindungen |
| WO2024013004A1 (de) | 2022-07-11 | 2024-01-18 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
Also Published As
| Publication number | Publication date |
|---|---|
| US9837617B2 (en) | 2017-12-05 |
| US20160190466A1 (en) | 2016-06-30 |
| TW201527292A (zh) | 2015-07-16 |
| US20170301865A1 (en) | 2017-10-19 |
| US9978950B2 (en) | 2018-05-22 |
| KR102047653B1 (ko) | 2019-11-22 |
| US20180240979A1 (en) | 2018-08-23 |
| CN110003155B (zh) | 2023-11-24 |
| US10665790B2 (en) | 2020-05-26 |
| JP2016536323A (ja) | 2016-11-24 |
| CN105492574A (zh) | 2016-04-13 |
| EP3033405B1 (de) | 2018-05-09 |
| CN105492574B (zh) | 2019-03-29 |
| CN110003155A (zh) | 2019-07-12 |
| EP3033405A1 (de) | 2016-06-22 |
| KR20160042132A (ko) | 2016-04-18 |
| TWI639590B (zh) | 2018-11-01 |
| JP6567520B2 (ja) | 2019-08-28 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP3259330B1 (de) | Materialien auf basis von spirobifluorenderivaten für elektronische vorrichtungen | |
| EP3033405B1 (de) | Materialien für elektronische vorrichtungen | |
| EP3238286B1 (de) | Materialien für elektronische vorrichtungen | |
| EP3131901B1 (de) | Materialien für elektronische vorrichtungen | |
| EP3378857B1 (de) | Materialien für elektronische vorrichtungen | |
| EP3341349A1 (de) | 6,9,15,18-tetrahydro-s-indaceno[1,2-b:5,6-b']difluoren- derivate und ihre verwendung in elektronischen vorrichtungen | |
| EP3535240A1 (de) | Materialien für elektronische vorrichtungen | |
| WO2014111269A2 (de) | Materialien für elektronische vorrichtungen | |
| WO2015000549A1 (de) | Materialien für elektronische vorrichtungen | |
| EP3335253A1 (de) | Materialien für elektronische vorrichtungen | |
| WO2015131976A1 (de) | Materialien für elektronische vorrichtungen | |
| EP3523834A1 (de) | Elektronische vorrichtung | |
| WO2013017189A1 (de) | Verbindungen für elektronische vorrichtungen | |
| WO2012150001A1 (de) | Verbindungen für elektronische vorrichtungen | |
| WO2015049022A1 (de) | Triarylamin-substituierte benzo[h]chinolin-derivate als materialien für elektronische vorrichtungen | |
| WO2014079527A1 (de) | Materialien für elektronische vorrichtungen | |
| EP2931698A1 (de) | Materialien für elektronische vorrichtungen | |
| EP2941469A2 (de) | Materialien für elektronische vorrichtungen | |
| WO2018157981A1 (de) | Materialien für organische elektronische vorrichtungen | |
| EP3615542A1 (de) | Verbindungen für elektronische vorrichtungen | |
| EP3544986A1 (de) | Verbrückte triarylamine für elektronische vorrichtungen | |
| WO2019048458A1 (de) | Materialien für elektronische vorrichtungen | |
| EP3394036A1 (de) | Materialien für elektronische vorrichtungen |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| WWE | Wipo information: entry into national phase |
Ref document number: 201480042646.4 Country of ref document: CN |
|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 14742471 Country of ref document: EP Kind code of ref document: A1 |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2014742471 Country of ref document: EP |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 14911359 Country of ref document: US |
|
| ENP | Entry into the national phase |
Ref document number: 2016533832 Country of ref document: JP Kind code of ref document: A |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| ENP | Entry into the national phase |
Ref document number: 20167006680 Country of ref document: KR Kind code of ref document: A |