WO2010010955A1 - ピリピロペンa生合成遺伝子 - Google Patents
ピリピロペンa生合成遺伝子 Download PDFInfo
- Publication number
- WO2010010955A1 WO2010010955A1 PCT/JP2009/063293 JP2009063293W WO2010010955A1 WO 2010010955 A1 WO2010010955 A1 WO 2010010955A1 JP 2009063293 W JP2009063293 W JP 2009063293W WO 2010010955 A1 WO2010010955 A1 WO 2010010955A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- pyripyropene
- nucleotide sequence
- seq
- polynucleotide
- activity
- Prior art date
Links
- 0 C[C@](C(C[C@]1O)[C@](C)(CC2)C([C@]3*)[C@]1(C)OC(C=C(c1cccnc1)O1)=C3C1=O)[C@]2OC(C)=O Chemical compound C[C@](C(C[C@]1O)[C@](C)(CC2)C([C@]3*)[C@]1(C)OC(C=C(c1cccnc1)O1)=C3C1=O)[C@]2OC(C)=O 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N9/00—Enzymes; Proenzymes; Compositions thereof; Processes for preparing, activating, inhibiting, separating or purifying enzymes
- C12N9/10—Transferases (2.)
- C12N9/1025—Acyltransferases (2.3)
- C12N9/1029—Acyltransferases (2.3) transferring groups other than amino-acyl groups (2.3.1)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
- C12N15/52—Genes encoding for enzymes or proenzymes
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
- C12N15/74—Vectors or expression systems specially adapted for prokaryotic hosts other than E. coli, e.g. Lactobacillus, Micromonospora
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N9/00—Enzymes; Proenzymes; Compositions thereof; Processes for preparing, activating, inhibiting, separating or purifying enzymes
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N9/00—Enzymes; Proenzymes; Compositions thereof; Processes for preparing, activating, inhibiting, separating or purifying enzymes
- C12N9/10—Transferases (2.)
- C12N9/1085—Transferases (2.) transferring alkyl or aryl groups other than methyl groups (2.5)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P17/00—Preparation of heterocyclic carbon compounds with only O, N, S, Se or Te as ring hetero atoms
- C12P17/18—Preparation of heterocyclic carbon compounds with only O, N, S, Se or Te as ring hetero atoms containing at least two hetero rings condensed among themselves or condensed with a common carbocyclic ring system, e.g. rifamycin
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P17/00—Preparation of heterocyclic carbon compounds with only O, N, S, Se or Te as ring hetero atoms
- C12P17/18—Preparation of heterocyclic carbon compounds with only O, N, S, Se or Te as ring hetero atoms containing at least two hetero rings condensed among themselves or condensed with a common carbocyclic ring system, e.g. rifamycin
- C12P17/181—Heterocyclic compounds containing oxygen atoms as the only ring heteroatoms in the condensed system, e.g. Salinomycin, Septamycin
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02P—CLIMATE CHANGE MITIGATION TECHNOLOGIES IN THE PRODUCTION OR PROCESSING OF GOODS
- Y02P20/00—Technologies relating to chemical industry
- Y02P20/50—Improvements relating to the production of bulk chemicals
- Y02P20/52—Improvements relating to the production of bulk chemicals using catalysts, e.g. selective catalysts
Abstract
Description
本発明は、ピリピロペンA生合成遺伝子に関する。
ピリピロペンAは、特開平4-360895号公報(特許文献1)およびJournal of Antibiotics(1993),46(7),1168-9(非特許文献1)に開示されるように、ACAT(アシルCoA・コレステロールアシルトランスフェラーゼ)阻害活性を有し、コレステロール蓄積に起因する疾患の治療等への応用が期待されている。
(a)配列番号266のヌクレオチド配列を有するポリヌクレオチド、
(b)配列番号266のヌクレオチド配列と厳密な条件下でハイブリダイズ可能なヌクレオチド配列を有するポリヌクレオチド、または
(c)配列番号267~274から選択される少なくとも一つのアミノ酸配列またはそれと実質的に同等なアミノ酸配列をコードするポリヌクレオチド配列を有するポリヌクレオチド
であることを特徴とするポリヌクレオチドが提供される。
(1)下記(a)-(h)のいずれかに記載されたヌクレオチド配列:
(a) 配列番号266で示されるヌクレオチド配列の3342番から5158番までのヌクレオチド配列
(b) 配列番号266で示されるヌクレオチド配列の5382番から12777番までのヌクレオチド配列
(c) 配列番号266で示されるヌクレオチド配列の13266番から15144番までのヌクレオチド配列
(d) 配列番号266で示されるヌクレオチド配列の16220番から18018番までのヌクレオチド配列
(e) 配列番号266で示されるヌクレオチド配列の18506番から19296番までのヌクレオチド配列
(f) 配列番号266で示されるヌクレオチド配列の19779番から21389番までのヌクレオチド配列
(g) 配列番号266で示されるヌクレオチド配列の21793番から22877番までのヌクレオチド配列
(h) 配列番号266で示されるヌクレオチド配列の23205番から24773番までのヌクレオチド配列
(2)(1)において記載されたヌクレオチド配列と厳密な条件下でハイブリダイズ可能なヌクレオチド配列
が提供される。
プラスミドpCC1-PP1で形質転換された大腸菌(Escherichia coli EPI300TM-T1R)は、2008年10月9日(原寄託日)付で独立行政法人産業技術総合研究所特許生物寄託 センター(〒305-8566 日本国茨城県つくば市東1丁目1番地1 中央第6)に、受託番号がFERM BP-11133(国内寄託FERM P-21704より移管)(寄託者が付した識別のための表示:Escherichia coli EPI300TM-T1R/pCC1-PP1)として寄託されている。
本発明は、単離されたポリヌクレオチドである。本発明による単離されたポリヌクレオチドは、(a)配列番号266のヌクレオチド配列を有するポリヌクレオチド、(b)配列番号266のヌクレオチド配列と厳密な条件下でハイブリダイズ可能なヌクレオチド配列を有するポリヌクレオチド、または(c)配列番号267~274から選択される少なくとも一つのアミノ酸配列またはそれと実質的に同等なアミノ酸配列をコードするポリヌクレオチド配列を有するポリヌクレオチドである。前記単離されたポリヌクレオチドは、ピリピロペンAの生合成に関与する酵素活性を有する少なくとも一種のポリペプチドをコードするヌクレオチド配列を有することが好ましい。
(1)下記(a)-(h)のいずれかに記載されたポリヌクレオチド配列:
(a) 配列番号266で示されるヌクレオチド配列の3342番から5158番までのヌクレオチド配列
(b) 配列番号266で示されるヌクレオチド配列の5382番から12777番までのヌクレオチド配列
(c) 配列番号266で示されるヌクレオチド配列の13266番から15144番までのヌクレオチド配列
(d) 配列番号266で示されるヌクレオチド配列の16220番から18018番までのヌクレオチド配列
(e) 配列番号266で示されるヌクレオチド配列の18506番から19296番までのヌクレオチド配列
(f) 配列番号266で示されるヌクレオチド配列の19779番から21389番までのヌクレオチド配列
(g) 配列番号266で示されるヌクレオチド配列の21793番から22877番までのヌクレオチド配列
(h) 配列番号266で示されるヌクレオチド配列の23205番から24773番までのヌクレオチド配列
(2)(1)において記載されたヌクレオチド配列と厳密な条件下でハイブリダイズ可能なヌクレオチド配列。
本発明による単離ポリヌクレオチドの取得方法は、特に限定されないが、例えば、以下の方法によりペニシリウム コピロビウムPF1169株または糸状菌から単離することができる。
一般に、遺伝子組換えにより二次代謝産物の生産性を向上させる方法として、律速反応となっている生合成反応を触媒するタンパク質をコードする遺伝子の発現増強、生合成遺伝子の発現を制御する遺伝子の発現増強や遺伝子破壊、不必要な二次代謝系の遮断等が挙げられる。よって、生合成遺伝子が特定されれば、適当なベクターに連結し、生産菌に導入することにより、二次代謝産物の生産性を向上させることができる。
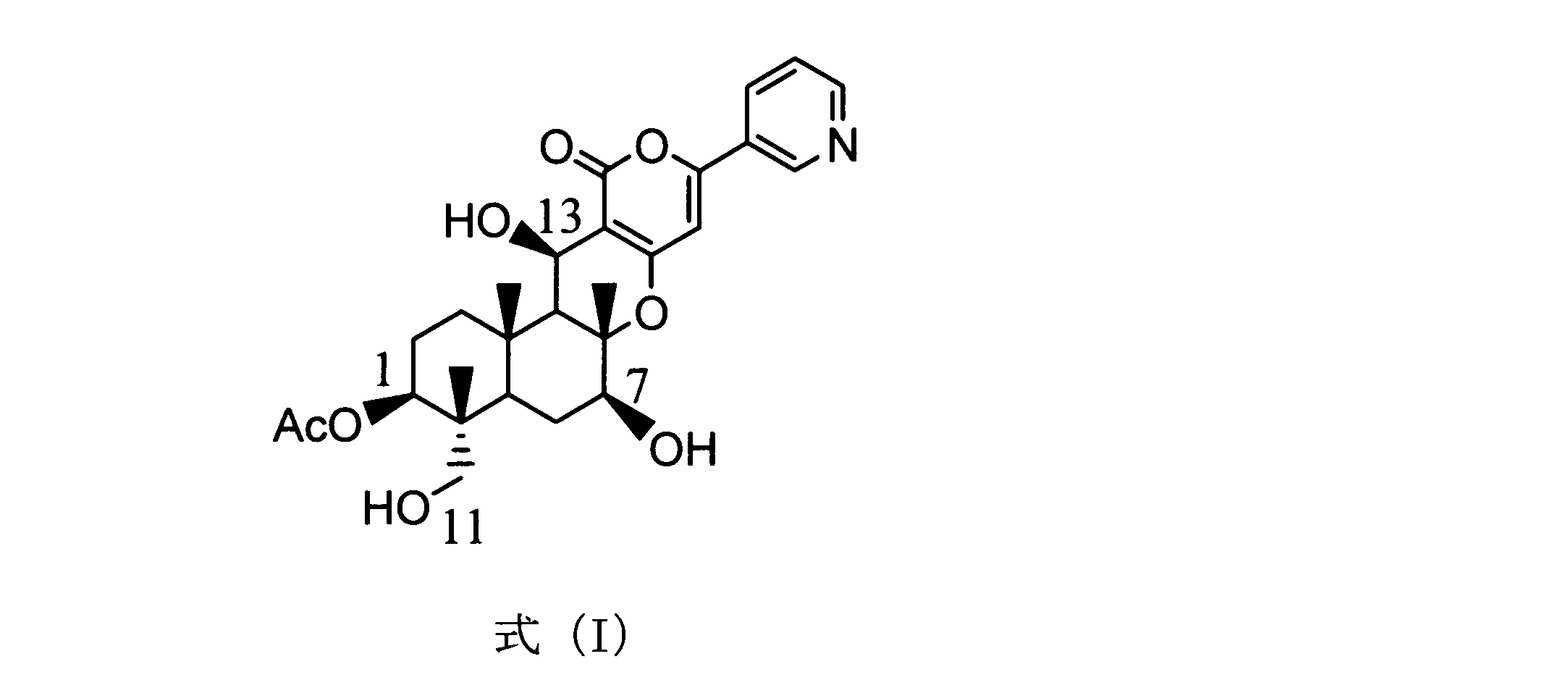
ピリピロペンAを単離するために、ピリピロペンA前駆体から公知の方法を用いてピリピロペンAを単離することができる。公知の方法としては例えば、WO2009/022702号公報の方法が挙げられる。上記一種またはそれ以上を含むベクターを含む微生物とともに培養して、ピリピロペンEからピリピロペンA前駆体を単離することができる。ピリピロペンA前駆体は、例えば、前記式(I)で表される化合物であってもよい。
三角フラスコ(1L)に滅菌したNB培地 500mlを入れ、1/2CMMY寒天培地において、28℃で、4日間前培養していたペニシリウム コピロビウムPF1169株(公開技報2008-500997号(特許文献15))を上記の培地に加え、28℃で、4日間液体培養した。ミラクロスで濾過により、菌体5gを得た。この菌体よりゲノムDNA精製キット Genomic-tip 100/G(キアゲン株式会社製)を、添付のマニュアルに従い、30ugのゲノムDNAを取得した。
種々の糸状菌ポリケチド合成酵素に保存されているアミノ酸配列より増幅用縮重プライマーとして 下記プライマーをデザインし、合成した:
LC1 : GAYCCIMGITTYTTYAAYATG(配列番号1)
LC2c: GTICCIGTICCRTGCATYTC(配列番号2)
(ただし、R=A/G、Y=C/T、M=A/C、I=イノシン)。
この縮重プライマーを使用して、実施例1において調製したゲノムDNAと、ExTaqポリメラーゼ(タカラバイオ株式会社製)とを、添付のマニュアルに従い反応させ、約700bpの増幅断片を検出した(図1参照)。そして、前記増幅断片を解析し、その内部500bpの配列を特定した(配列番号3)。
実施例1において得られたペニシリウム コピロビウムPF1169株のゲノムDNAを大量シークエンスと、アミノ酸配列の相同性検索とに供した。具体的にはゲノムDNA 50ugの一部を前処理の後、Roche社454FLX DNAシークエンサーに供し、約250bp、10.3万本のフラグメント配列(総計49Mbの配列)を取得した。
実施例3において取得したblastxの検索結果より、ポリケチド合成酵素に対して、配列番号227~252に示す13種のプライマー対を合成した。同様に、プレニルトランスフェラーゼに対して、配列番号253~262に示す5種のプライマー対を合成した。これらのプライマーを用いて、ゲノムDNAに対するPCRを行ったところ、全プライマー対について期待される大きさの増幅断片を認めた(図1および図2参照)。
ペニシリウム コピロビウムPF1169株のλファージゲノムライブラリーを、λBlueSTAR Xho I Half-site Arms Kit ( タカラバイオ株式会社製 Cat. No. 69242-3)を用いて、添付のマニュアルに従い、構築した。すなわち、ゲノムDNAを、制限酵素Sau3A1を用いて部分分解し、約20kbのDNA断片0.5ugをキットに添付されたλBlueSTAR DNA0.5ugに連結した。このライゲーション溶液をLambda INN Packaging kit(株式会社ニッポンジーン製)を用い、キットに添付のマニュアルに基づいてin vitroパッケージングを行い、1mlの溶液を取得した。このパッケージングされたファージ溶液10ulを大腸菌ER1647株100ulに感染させ、プラーク形成培地において、37℃で、一晩培養後、約500クローンのプラークを得た。このように感染により10~20kbのペニシリウム コピロビウムPF1169株のゲノム DNA が導入されたファージ約50000クローンからなるゲノムライブラリーを作製した。
実施例5において調製したファージライブラリー10000クローンに対して、上記で調製したLC1-LC2cプライマー対により増幅させたPCR産物をプローブとして、プラークハイブリダイゼーションによる1次スクリーニングを行った。プローブの標識と検出にはAlkPhos Direct Labelling and Detection System with CDP-Star(GEヘルスケア株式会社製 Cat. No. RPN3690)を用いた。前記ハイブリダイゼーションは、添付のマニュアルに従い、実施した。
ペニシリウム コピロビウムPF1169株のゲノムライブラリーは、CopyControl Fosmid Library Production Kit(EPICENTRE社製、Cat. No.CCFOS110)を、添付のマニュアルに従い、構築した。すなわち、約40 kbのゲノムDNA0.25ugのDNA断片を末端の平滑化を行った後、フォスミドベクターpCCFOS(Epicentre社製)に組み込んだ。このライゲーション溶液を同キット添付のMaxPlaxLambda Packaging Extractを用い、キットに添付のマニュアルに基づいて、in vitroパッケージングを行った。このパッケージングされたウィルス溶液10ulを大腸菌EPI300TM-T1R株100ulに感染させ、クロラムフェニコール含有培地において、37℃で、一晩培養し選抜したところ、300クローンのコロニーを得た。このように感染により40kbのペニシリウム コピロビウムPF1169株のゲノムDNA が導入されたフォスミド約30000クローンを取得した。1wellあたり約50クローンとなるように96wellプレートに分注し、つまり、96のプール、約4800クローンからなるゲノムライブラリーを作製した。
フォスミド添付のマニュアルに従い、実施例7において作成したライブラリーの96プールより各プラスミドDNAを調製した。実施例2で合成したポリケチド合成酵素増幅用縮重プライマーを用いて、この96プールのプラスミドDNAサンプルに対して、PCRを行った。その結果、約700bpのDNA断片が、9プールより増幅した。さらにこのポジティブプールから、約300クローン以上のコロニーを含むシャーレを作製し、コロニーハイブリダイゼーションにより再スクリーニングした。その結果、LC1-LC2cプライマー対を用いて、約4800クローンより9種のフォスミドを取得した。
実施例1において得られたペニシリウム コピロビウムPF1169株のゲノムDNAを大量シークエンスと、アミノ酸配列の相同性検索とに供した。具体的にはゲノムDNA 50ugの一部を前処理の後、Roche社454FLX DNAシークエンサーに供し、平均コンティグ長19.621kb、1405本のフラグメント配列(総塩基長27.568160Mbの配列)を取得した。
この配列に対し、ポリケチド合成酵素およびプレニルトランスフェラーゼで既知である配列として、下記の五種の配列(ポリケチド合成酵素: Penicillium(P.) griseofluvum 6-methylsalycilic acid synthase 1744a.a.(P22367) およびAspergillus(A.) fumigatus PKS 2146a.a.(Q4WZA8)、プレニルトランスフェラーゼ:Penicillium(P.) marneffei Prenyltransferase(Q0MRO8)、Aspergillus (A.) fumigatus Prenyltransferase(Q4WBI5)、およびAspergillus(A.) fumigatus Prenyltransferase(4-hydroxybezoate octaprenyltransferase)(Q4WLD0)由来の配列)を選定し、相同配列検索ソフトblastxによる検索を実施した。それぞれ22本(P22367)、21本(Q4WZA8)、2本(Q0MRO8)、3本(Q4WBI5)、および3本(Q4WLD0)の相同配列を取得した。
得られたpCC1-PP1により大腸菌Escherichia coli EPI300TM-T1R株(フォスミドキットに付属)を形質転換することにより大腸菌Escherichia coli EPI300TM-T1R株/pCC1-PP1を得た。
なお、前記配列番266の配列とAdenylate-forming enzyme、LovB-like polyketide synthase、水酸化酵素であるCytochrome P450 monooxygenase、Integral membrane protein、FAD-dependent monooxygenase、UbiA-like prenyltransferase、アセチル化酵素であるAcetyltransferase、Toxin biosynthesis protein Tri7、およびCation transporting ATPase(上記酵素は、いずれもAspergillus fumigatus Af293株由来)との、相同性検索をそれぞれ行ったところ、いずれも70%以上の高い相同性を示した。
配列番号266のヌクレオチド3342-5158は、Adenylate-forming enzymeをコードし、その対応するポリペプチドは、配列番号267に記載したアミノ酸配列で示され、配列番号266のヌクレオチド5382-12777は、LovB-like polyketide synthaseをコードし、対応するポリペプチドは、配列番号268に記載したアミノ酸配列で示され、配列番号266のヌクレオチド13266-15144(以下、このポリヌクレオチド配列(P450-1)によりコードされるタンパク質をCytochrome P450 monooxygenase(1)とする)および16220-18018(以下、このポリヌクレオチド配列(P450-2)によりコードされるタンパク質をCytochrome P450 monooxygenase(2)とする)は、Cytochrome P450 monooxygenaseをコードし、対応するポリペプチドは、それぞれ、配列番号269、270に記載したアミノ酸配列で示され、配列番号266のヌクレオチド18506-19296は、Integral membrane proteinをコードし、対応するポリペプチドは、配列番号271に記載したアミノ酸配列で示され、配列番号266のヌクレオチド19779-21389は、FAD-dependent monooxygenaseをコードし、対応するポリペプチドは、配列番号272に記載したアミノ酸配列で示され、配列番号266のヌクレオチド21793-22877は、UbiA-like prenyltransferaseをコードし、対応するポリペプチドは、配列番号273に記載したアミノ酸配列で示され、配列番号266のヌクレオチド23205-24773は、Acetyltransferaseをコードし、対応するポリペプチドは、配列番号274に記載したアミノ酸配列で示され、配列番号266のヌクレオチド25824-27178は、Toxin biosynthesis protein Tri7をコードし、対応するポリペプチドは、配列番号275に記載したアミノ酸配列で示され、配列番号266のヌクレオチド27798-31855は、Cation transporting ATPaseをコードし、対応するポリペプチドは、配列番
号276に記載したアミノ酸配列で示された。
以下で用いるピリピロペンEは、例えば、特開平8-239385号公報(特許文献4)、WO94/09147号公報、または米国特許5597835号公報に記載される方法に準じた微生物培養法によるか、Tetrahedron Letters, vol. 37, No.36, 6461-6464, 1996に記載される全合成の方法によって製造することができる。また、以下で用いるピリピロペンOは、例えば、J. Antibiotics 49, 292-298, 1996またはWO94/09147号公報に記載される方法に準じた微生物培養法によって製造することができる。
pUSA(図4)とpHSG399(タカラバイオ社)をそれぞれKpnI切断し、連結することにより、pUSA-HSGを取得した。このプラスミドをSmaI、KpnIの順で切断し、ゲル精製することで、KpnIの粘着末端とSmaIの平滑末端を有す線状ベクターDNAを取得した。
Fosmid pCC1-PP1を鋳型として、プライマー対P450-1 with Kpn F(配列番号277)/P450-1 with Swa R(配列番号278)を用いて前記P450-1のポリヌクレオチドを増幅し、精製したDNA断片をpCR-Blunt(Invitorogen社 Cat.No.K2700-20)にクローン化した。得られたプラスミドをKpnIとSwaIで切断し、前記P450-1断片を上述したベクターpUSA-HSGにライゲーションし、図5に示すpPP2のプラスミドを取得した。
Fosmid pCC1-PP1を鋳型としてとして、図6に示す流れに従い、まず、プライマー対F1(配列番号279)/R1(配列番号280)、F2(配列番号281)/R2(配列番号282)、F3(配列番号283)/R3(配列番号284)、F4(配列番号285)/R4(配列番号286)、F5(配列番号287)/R5(配列番号288)、およびF6(配列番号289)/R6(配列番号290)を用い、エキソンのみを増幅し、六つの断片を取得した。次にこれらの断片を鋳型としてF1/R2、F3/R4、およびF5/R6のプライマー対により増幅し、より長い断片を取得した。さらに、F1/R4およびF1/R6のプライマー対により増幅を繰り返すことによって前記P450-2のポリヌクレオチドのイントロンを含まないcDNAを作製した。このcDNA断片をpCR-Blunt(Invitorogen社 Cat.No.K2700-20)に導入し、得られたプラスミドを鋳型として、プライマー対infusion F of P450-2-cDNA(配列番号291)/infusion R of P450-2-cDNA(配列番号292)により増幅した。キットのマニュアルに基づいて、In-Fusion Advantage PCR Cloning Kit(Clontech社)を用い、図7に示すpPP3のプラスミドを取得した。
CD-Met(L-Methionine 40μg/ml含有)寒天培地でA. oryzae(HL-1105株)を30℃で1週間培養した。このシャーレから分生子(>108)を回収し、500ml のフラスコに100mlのYPD液体培地に接種した。20時間培養(30℃、180rpm)後、毬藻状の菌体を取得した。菌体を3G-1 グラスフィルターで集め、0.8M NaClで洗浄し、よく脱水し、TF溶液I(プロトプラスト化溶液)で懸濁後、30℃、60rpmで2時間振盪した。なお、30分間ごとに顕微鏡で観察し、プロトプラストの存在を確認した。その後、培養液を濾過し、遠心(2000rpm、5分間)によりプロトプラストを回収後、TF溶液IIで洗浄した。洗浄後、0.8容量のTF溶液IIおよび0.2容量のTF溶液IIIを加え混和して、プロトプラスト懸濁液を取得した。
化合物名 濃度
ヤタラーゼ(タカラバイオ社製) 20mg/ml
硫安 0.6M
マレイン酸-NaOH 50mM
上記組成を調製後(pH5.5)、ろ過滅菌を行った。
化合物名
1.2M Sorbitol (MW=182.17) 43.72g
50mM CaCl2 10ml 1M CaCl2(1/20)
35mM NaCl 1.4ml 5M NaCl
10mM Tris-HCl 2ml 1M Tris-HCl (1/100)
Up to total volume 200ml
上記組成を調製後、オートクレーブ滅菌を行った。
化合物名
60%PEG4000 6g
50mM CaCl2 500μl 1M CaCl2(1/20)
50mM Tris-HCl 500μl 1M Tris-HCl (1/100)
Up to total volume 10ml
上記組成を調製後、ろ過滅菌を行った。
化合物名 濃度
Sorbitol (MW=182.17) 218.6g 1.2M
NaNO3 3.0g 0.3%(w/v)
KCl 2.0g 0.2%(w/v)
KH2PO4 1.0g 0.1%(w/v)
MgSO4・7H2O 2ml of 1M MgSO4 0.05% 2mM
Trace elements solution 1ml
Glucose 20.0g 2%(w/v)
Up to the total volume 1L
上記組成を調製後(pH 5.5)、オートクレーブ滅菌を行った。
化合物名
FeSO4・7H2O 1.0g
ZnSO4・7H2O 8.8g
CuSO4・5H2O 0.4g
Na2B4O7・10H2O 0.1g
(NH4)6Mo7O24・4H2O 0.05g
Up to the total volume 1L
上記組成を調製後、オートクレーブ滅菌を行った。
1% (w/v)マルトースを含むYPD培地(1% (w/v) Yeast Extract、2% (w/v) Peptone、2% (w/v) Dextrose)に、1/100容のピリピロペンEの2 mg/mLジメチルスルホキシド溶液を添加した培地を培地Aとした。ツァペックドックス寒天培地に培養したAspergillus oryzae PP2-1の菌叢より分生子を採取し、滅菌水に懸濁した。この分生子懸濁液を104 spore/mLに調製し、この調製した分生子懸濁液のうち100 μLを10 mLの培地Aに添加し、25℃で96時間振盪培養した。この培養液に10 mLのアセトンを添加し、よく混合した後、遠心濃縮器を用いてアセトンを留去した。これに10 mLの酢酸エチルを添加し、よく混合した後、酢酸エチル層のみを分取した。遠心濃縮器を用いて酢酸エチルを留去して得られた乾固物を1000 μLのメタノールに溶解した。これをサンプルとして用い、LC-MS(ウォーターズ社、Micromass ZQ、2996PDA、2695 Separation module、Column:Waters XTerra C18 (Φ4.5 x 50 mm、5 μm))、およびLC-NMR (Burker Daltonik社製 Avance500)により分析した。
1.マススペクトラム:ES-MS 468M/Z(M+H)+
2.分子式:C27H33NO6
3.HPLC:カラムWaters XTerra Column C18 (5 μm、4.6mm×50mm)、40℃、移動相20%アセトニトリル水から10分間で100% アセトニトリル(リニアグラジエント)、流速0.8ml/分、検出:UV323nmで保持時間 6.696分
4.1H -NMRスペクトル (CD3CN, 2H:3.134、3.157 H-11)
ピリピロペンEおよび上記4に記載の1H -NMRスペクトルのチャートは、それぞれ、図8および図9に示される通りであった。
1% (w/v)マルトースを含むYPD培地(1% (w/v) Yeast Extract、2%(w/v) Peptone、2%(w/v) Dextrose)に1/100容のピリピロペンEの2mg/mLジメチルスルホキシド溶液を添加した培地を培地B、同じく1/100容のピリピロペンOの2 mg/mLジメチルスルホキシド溶液を添加した培地を培地Cとした。ツァペックドックス寒天培地に培養したAspergillus oryzae PP3-2の菌叢より分生子を採取し、滅菌水に懸濁した。この分生子懸濁液を104 spore/mLに調製し、このうち500μLを50 mLの培地Bまたは培地Cに添加し、25℃で96時間振盪培養した。この培養液に50 mLのアセトンを添加し、よく混合した後、遠心濃縮器を用いてアセトンを留去した。これに50mLの酢酸エチルを添加し、よく混合した後、酢酸エチル層のみを分取した。遠心濃縮器を用いて酢酸エチルを留去して得られた乾固物を1500μLのメタノールに溶解した。これをサンプルとし、LC-MS(ウォーターズ社製 Micromass ZQ、2996PDA、2695 Separation module、Column:Waters XTerra C18 (Φ4.5 x 50mm、5μm))およびLC-MNR(Burker Daltonik社製 Avance500)で分析した。LC-MS測定の結果、培地Bから得られたサンプルから、ピリピロペンEより32分子量の増加した化合物Bを検出した。また、培地Cから得られたサンプルから、ピリピロペンOより32分子量の増加した化合物Cを検出した。さらに、LC-NMR測定の結果、化合物CはピリピロペンOの7位および13位水酸化体であることが確認された。前記Cytochrome P450 monooxygenase(2)は、ピリピロペンEまたはピリピロペンOのそれぞれ7位および13位を水酸化する酵素であることが確認された。
1.マススペクトラム:ES-MS 484M/Z(M+H)+
2.分子式:C27H33NO7
3.HPLC:カラムWaters XTerra Column C18 (5 μm、4.6mm×50mm)、40℃、移動相20%アセトニトリル水から10分間で100% アセトニトリル(リニアグラジエント)、流速0.8ml/分、検出:UV323nmで保持時間 5.614 分
1.マススペクトラム:ES-MS 542M/Z(M+H)+、
2.分子式:C29H35NO9
3.HPLC:カラムWaters XTerra Column C18 (5 μm、4.6mm×50mm)、40℃、移動相20%アセトニトリル水から10分間で100% アセトニトリル(リニアグラジエント)、流速0.8ml/分、検出:UV323nmで保持時間 5.165 分
4.1H -NMRスペクトル (CD3CN, 1H 4.858 H-13)、(CD3CN, 1H 3.65 H-7)
ピリピロペンOおよび上記化合物Cの1H -NMRスペクトルのチャートは、それぞれ、図10および図11に示される通りであった。
FERM BP-11137
FERM BP-11141
Claims (27)
- 単離されたポリヌクレオチドであって、
(a)配列番号266のヌクレオチド配列を有するポリヌクレオチド、
(b)配列番号266のヌクレオチド配列と厳密な条件下でハイブリダイズ可能なヌクレオチド配列を有するポリヌクレオチド、または
(c)配列番号267~274から選択される少なくとも一つのアミノ酸配列またはそれと実質的に同等なアミノ酸配列をコードするポリヌクレオチド配列を有するポリヌクレオチド
であることを特徴とする、ポリヌクレオチド。 - ピリピロペンAの生合成に関与する少なくとも一種のポリペプチドをコードする、請求項1に記載のポリヌクレオチド。
- ポリケチド合成酵素活性、プレニルトランスフェラーゼ活性、水酸化酵素活性、アセチル化酵素活性、またはアデニル酸合成酵素活性のいずれか一つまたはそれ以上の活性を有するポリペプチドをコードする、請求項1または2に記載のポリヌクレオチド。
- ペニシリウム コピロビウムPF1169株由来のものである、請求項1~3のいずれか一項に記載のポリヌクレオチド。
- 単離されたポリヌクレオチドであって、以下の(1)または(2)のいずれかに記載されたヌクレオチド配列から選択された少なくとも1個のヌクレオチド配列を有することを特徴とする、ポリヌクレオチド:
(1)下記(a)-(h)のいずれかに記載されたヌクレオチド配列:
(a) 配列番号266で示されるヌクレオチド配列の3342番から5158番までのヌクレオチド配列
(b) 配列番号266で示されるヌクレオチド配列の5382番から12777番までのヌクレオチド配列
(c) 配列番号266で示されるヌクレオチド配列の13266番から15144番までのヌクレオチド配列
(d) 配列番号266で示されるヌクレオチド配列の16220番から18018番までのヌクレオチド配列
(e) 配列番号266で示されるヌクレオチド配列の18506番から19296番までのヌクレオチド配列
(f) 配列番号266で示されるヌクレオチド配列の19779番から21389番までのヌクレオチド配列
(g) 配列番号266で示されるヌクレオチド配列の21793番から22877番までのヌクレオチド配列
(h) 配列番号266で示されるヌクレオチド配列の23205番から24773番までのヌクレオチド配列
(2)(1)において記載されたヌクレオチド配列と厳密な条件下でハイブリダイズ可能なヌクレオチド配列。 - ピリピロペンAの生合成に関与する少なくとも一種のポリペプチドをコードする、請求項5に記載のポリヌクレオチド。
- ポリケチド合成酵素活性、プレニルトランスフェラーゼ活性、水酸化酵素活性、アセチル化酵素活性、またはアデニル酸合成酵素活性のいずれか一つまたはそれ以上の活性を有するポリペプチドをコードする、請求項5または6に記載のポリヌクレオチド。
- 水酸化酵素活性を有するポリペプチドをコードする、請求項5または6に記載のポリヌクレオチド。
- ペニシリウム コピロビウムPF1169株由来のものである、請求項5~8のいずれか一項に記載のポリヌクレオチド。
- ピリピロペンEまたはOの7位および/または13位を水酸化する活性を有するポリペプチドをコードする、請求項5~9のいずれか一項に記載のポリヌクレオチド。
- ピリピロペンEの11位を水酸化する活性を有するポリペプチドをコードする、請求項5~9のいずれか一項に記載のポリヌクレオチド。
- 請求項1または請求項5に記載のポリヌクレオチドのいずれか一種またはそれ以上を含んでなる、組換えベクター。
- ピリピロペンEまたはOの7位および/または13位を水酸化する活性を有するポリペプチドをコードするポリヌクレオチドを含んでなる、請求項12に記載の組換えベクター。
- ピリピロペンEの11位を水酸化する活性を有するポリペプチドをコードするポリヌクレオチドを含んでなる、請求項12に記載の組換えベクター。
- 前記組換えベクターがプラスミドpCC1-PP1である、請求項12に記載の組換えベクター。
- 前記組換えベクターがプラスミドpPP2である、請求項12に記載の組換えベクター。
- 前記組換えベクターがプラスミドpPP3である、請求項12に記載の組換えベクター。
- 請求項1または請求項5に記載のポリヌクレオチドのいずれか一種またはそれ以上を含んでなる、形質転換体。
- 前記形質転換体がプラスミドpCC1-PP1を含んでなる大腸菌である、請求項18に記載の形質転換体。
- 前記形質転換体がプラスミドpPP2を含んでなるAspergillus oryzaeである、請求項18に記載の形質転換体。
- 前記形質転換体がプラスミドpPP3を含んでなるAspergillus oryzaeである、請求項18に記載の形質転換体。
- 請求項12~17に記載のベクターのいずれか一種またはそれ以上を含む微生物とともに培養して、ピリピロペンEからピリピロペンA前駆体を単離することを特徴とする、ピリピロペンA前駆体の製造法。
- 請求項20に記載の形質転換体および請求項21に記載の形質転換体を同時に、または別々に培養し、ピリピロペンEからピリピロペンA前駆体を単離することを特徴とする、ピリピロペンA前駆体の製造法。
- 請求項12~17に記載のベクターのいずれか一種またはそれ以上を含む微生物とともに培養して、ピリピロペンOからピリピロペンA前駆体を単離することを特徴とする、ピリピロペンA前駆体の製造法。
- 請求項21に記載の形質転換体を培養し、ピリピロペンOからピリピロペンA前駆体を単離することを特徴とする、ピリピロペンA前駆体の製造法。
Priority Applications (17)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US13/055,532 US8557550B2 (en) | 2008-07-24 | 2009-07-24 | Pyripyropene a biosynthetic gene |
| CA2731760A CA2731760C (en) | 2008-07-24 | 2009-07-24 | Pyripyropene a biosynthetic gene |
| DK09800469.0T DK2319923T3 (en) | 2008-07-24 | 2009-07-24 | A PYRIPYROPEN biosynthetic genes |
| ES09800469.0T ES2453665T3 (es) | 2008-07-24 | 2009-07-24 | Genes biosintéticos de piripiropeno A |
| JP2009548252A JP4642922B2 (ja) | 2008-07-24 | 2009-07-24 | ピリピロペンa生合成遺伝子 |
| EP09800469.0A EP2319923B1 (en) | 2008-07-24 | 2009-07-24 | Pyripyropene a biosynthetic genes |
| NZ590795A NZ590795A (en) | 2008-07-24 | 2009-07-24 | Pyripyropene a biosynthetic gene |
| CN200980128891.6A CN102144030B (zh) | 2008-07-24 | 2009-07-24 | 啶南平a生物合成基因 |
| KR1020117001974A KR101690802B1 (ko) | 2008-07-24 | 2009-07-24 | 피리피로펜 a 생합성 유전자 |
| AU2009274832A AU2009274832B2 (en) | 2008-07-24 | 2009-07-24 | Pyripyropene A biosynthetic gene |
| BRPI0916355A BRPI0916355B8 (pt) | 2008-07-24 | 2009-07-24 | Vetor recombinante compreendendo um polinucleotídeo isolado, e, método para produzir um precursor de piripiropeno a |
| MX2011000023A MX2011000023A (es) | 2008-07-24 | 2009-07-24 | Gen biosintetico de piripiropeno a. |
| PL09800469T PL2319923T3 (pl) | 2008-07-24 | 2009-07-24 | Geny biosyntezy pirypiropenu A |
| RU2011106496/10A RU2540017C2 (ru) | 2008-07-24 | 2009-07-24 | Выделенный полинуклеотид, кодирующий полипептид, вовлеченный в биосинтез пирипиропена а, вектор и клетка-хозяин содержащие такой полинуклеотид и способ получения предшественника пирипиропена а (варианты) |
| IL210795A IL210795A (en) | 2008-07-24 | 2011-01-23 | Pyripropene and a biosynthetic gene |
| ZA2011/00709A ZA201100709B (en) | 2008-07-24 | 2011-01-27 | Pyripyropene a biosynthetic gene |
| US14/022,778 US9315785B2 (en) | 2008-07-24 | 2013-09-10 | Pyripyropene a biosynthetic gene |
Applications Claiming Priority (6)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008-190862 | 2008-07-24 | ||
| JP2008190862 | 2008-07-24 | ||
| JP2008270294 | 2008-10-20 | ||
| JP2008-270294 | 2008-10-20 | ||
| JP2009-020591 | 2009-01-30 | ||
| JP2009020591 | 2009-01-30 |
Related Child Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| US13/055,532 A-371-Of-International US8557550B2 (en) | 2008-07-24 | 2009-07-24 | Pyripyropene a biosynthetic gene |
| US14/022,778 Continuation US9315785B2 (en) | 2008-07-24 | 2013-09-10 | Pyripyropene a biosynthetic gene |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2010010955A1 true WO2010010955A1 (ja) | 2010-01-28 |
Family
ID=41570415
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2009/063293 WO2010010955A1 (ja) | 2008-07-24 | 2009-07-24 | ピリピロペンa生合成遺伝子 |
Country Status (17)
| Country | Link |
|---|---|
| US (2) | US8557550B2 (ja) |
| EP (1) | EP2319923B1 (ja) |
| JP (2) | JP4642922B2 (ja) |
| KR (1) | KR101690802B1 (ja) |
| CN (1) | CN102144030B (ja) |
| AU (1) | AU2009274832B2 (ja) |
| BR (1) | BRPI0916355B8 (ja) |
| CA (1) | CA2731760C (ja) |
| DK (1) | DK2319923T3 (ja) |
| ES (1) | ES2453665T3 (ja) |
| IL (1) | IL210795A (ja) |
| MX (1) | MX2011000023A (ja) |
| NZ (1) | NZ590795A (ja) |
| PL (1) | PL2319923T3 (ja) |
| RU (1) | RU2540017C2 (ja) |
| WO (1) | WO2010010955A1 (ja) |
| ZA (1) | ZA201100709B (ja) |
Cited By (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2011093186A1 (ja) * | 2010-01-26 | 2011-08-04 | 明治製菓株式会社 | ピリピロペン生合成遺伝子群およびマーカー遺伝子を含む核酸構築物 |
| WO2011093185A1 (ja) * | 2010-01-26 | 2011-08-04 | 明治製菓株式会社 | ピリピロペンの製造法 |
| WO2011093187A1 (ja) * | 2010-01-26 | 2011-08-04 | 明治製菓株式会社 | 酵素法によるピリピロペン誘導体の製造方法 |
| WO2013073689A1 (ja) * | 2011-11-17 | 2013-05-23 | Meiji Seikaファルマ株式会社 | ピリピロペン生合成遺伝子発現植物体 |
| US9596843B2 (en) | 2012-03-12 | 2017-03-21 | Basf Se | Liquid concentrate formulation containing a pyripyropene insecticide I |
| US9723834B2 (en) | 2010-09-14 | 2017-08-08 | Basf Se | Composition containing a pyripyropene insecticide and a base |
| US9861104B2 (en) | 2012-03-12 | 2018-01-09 | Basf Se | Method for producing an aqueous suspension concentrate formulation of a pyripyropene insecticide |
| US9888689B2 (en) | 2010-09-14 | 2018-02-13 | Basf Se | Compositions containing a pyripyropene insecticide and an adjuvant |
| US9924712B2 (en) | 2012-03-12 | 2018-03-27 | Basf Se | Liquid concentrate formulation containing a pyripyropene insecticide II |
Families Citing this family (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2540017C2 (ru) * | 2008-07-24 | 2015-01-27 | Мейдзи Сейка Фарма Ко,Лтд.,Jp | Выделенный полинуклеотид, кодирующий полипептид, вовлеченный в биосинтез пирипиропена а, вектор и клетка-хозяин содержащие такой полинуклеотид и способ получения предшественника пирипиропена а (варианты) |
| AU2012236099A1 (en) | 2011-03-31 | 2013-10-03 | Moderna Therapeutics, Inc. | Delivery and formulation of engineered nucleic acids |
| EP3682905B1 (en) * | 2011-10-03 | 2021-12-01 | ModernaTX, Inc. | Modified nucleosides, nucleotides, and nucleic acids, and uses thereof |
| US10138507B2 (en) | 2013-03-15 | 2018-11-27 | Modernatx, Inc. | Manufacturing methods for production of RNA transcripts |
| EP2983804A4 (en) | 2013-03-15 | 2017-03-01 | Moderna Therapeutics, Inc. | Ion exchange purification of mrna |
| US10077439B2 (en) | 2013-03-15 | 2018-09-18 | Modernatx, Inc. | Removal of DNA fragments in mRNA production process |
| WO2014152031A1 (en) | 2013-03-15 | 2014-09-25 | Moderna Therapeutics, Inc. | Ribonucleic acid purification |
| HRP20211563T1 (hr) | 2013-07-11 | 2022-01-07 | Modernatx, Inc. | Pripravci koji sadrže sintetske polinukleotide koji kodiraju proteine srodne crispr-u i sintetske sgrna, te postupci njihove uporabe |
| WO2015051169A2 (en) | 2013-10-02 | 2015-04-09 | Moderna Therapeutics, Inc. | Polynucleotide molecules and uses thereof |
| US10286086B2 (en) | 2014-06-19 | 2019-05-14 | Modernatx, Inc. | Alternative nucleic acid molecules and uses thereof |
| AU2015289656A1 (en) | 2014-07-16 | 2017-02-16 | Modernatx, Inc. | Circular polynucleotides |
| WO2017049286A1 (en) | 2015-09-17 | 2017-03-23 | Moderna Therapeutics, Inc. | Polynucleotides containing a morpholino linker |
| US10148618B2 (en) | 2016-06-07 | 2018-12-04 | Abb Schweiz Ag | Network isolation |
| KR102098018B1 (ko) | 2017-12-22 | 2020-04-07 | 주식회사 포스코 | 압력탱크 |
Citations (20)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US500997A (en) | 1893-07-04 | Oar unloadee | ||
| JPH04360895A (ja) | 1991-06-06 | 1992-12-14 | Kitasato Inst:The | Fo−1289a物質およびその製造法 |
| WO1994009147A1 (en) | 1992-10-22 | 1994-04-28 | The Kitasato Institute | Fo-1289 substance and its production |
| JPH08239385A (ja) | 1995-03-03 | 1996-09-17 | Kitasato Inst:The | Fo−1289物質およびその製造法 |
| JPH08259569A (ja) | 1995-03-27 | 1996-10-08 | Kitasato Inst:The | ピリピロペン誘導体 |
| JPH08269062A (ja) | 1995-03-30 | 1996-10-15 | Kitasato Inst:The | ピリピロペン誘導体 |
| JPH08269066A (ja) | 1995-04-03 | 1996-10-15 | Kitasato Inst:The | ピリピロペン誘導体 |
| JPH08269064A (ja) | 1995-04-03 | 1996-10-15 | Kitasato Inst:The | ピリピロペン誘導体 |
| JPH08269065A (ja) | 1995-04-03 | 1996-10-15 | Kitasato Inst:The | ピリピロペン誘導体 |
| JPH08269063A (ja) | 1995-03-28 | 1996-10-15 | Kitasato Inst:The | ピリピロペン誘導体 |
| JPH08291164A (ja) | 1995-04-18 | 1996-11-05 | Kitasato Inst:The | ピリピロペン誘導体 |
| US5597835A (en) | 1993-10-08 | 1997-01-28 | Korea Institute Of Science And Technology | Acyl CoA:cholesterol acyltransferase inhibitors |
| WO2004060065A1 (en) | 2003-01-07 | 2004-07-22 | Korea Research Institute Of Bioscience And Biotechnology | Insecticidal compositions comprising compounds having inhibitory activity versus acyl coa: cholesterol acyltransferase or salts thereof as effective ingredients |
| WO2006129714A1 (ja) | 2005-06-01 | 2006-12-07 | Meiji Seika Kaisha, Ltd. | 害虫防除剤 |
| JP2008500997A (ja) * | 2004-05-28 | 2008-01-17 | シュペーデル・エクスペリメンタ・アーゲー | アロマターゼ阻害剤としての二環式の窒素含有複素環 |
| WO2008066153A1 (fr) | 2006-11-30 | 2008-06-05 | Meiji Seika Kaisha, Ltd. | Agent antiparasitaire |
| JP2008190862A (ja) | 2008-03-26 | 2008-08-21 | Toshiba Corp | 加熱調理器 |
| JP2008270294A (ja) | 2007-04-16 | 2008-11-06 | Sumitomo Electric Ind Ltd | ヒートシンク部材および半導体装置 |
| JP2009020591A (ja) | 2007-07-10 | 2009-01-29 | Canon Inc | プリンタアダプタ装置および制御方法 |
| WO2009022702A1 (ja) | 2007-08-13 | 2009-02-19 | Meiji Seika Kaisha, Ltd. | ピリピロペン誘導体の製造法およびその製造中間体 |
Family Cites Families (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP4360895B2 (ja) | 2003-12-11 | 2009-11-11 | 日立Geニュークリア・エナジー株式会社 | 中性子監視装置 |
| WO2006083411A2 (en) | 2004-12-17 | 2006-08-10 | David Glassel | Methods and compositions of matter for treatment of cellulose |
| US7491738B2 (en) | 2005-06-01 | 2009-02-17 | Meiji Seika Kaisha, Ltd. | Pest control agents |
| RU2540017C2 (ru) * | 2008-07-24 | 2015-01-27 | Мейдзи Сейка Фарма Ко,Лтд.,Jp | Выделенный полинуклеотид, кодирующий полипептид, вовлеченный в биосинтез пирипиропена а, вектор и клетка-хозяин содержащие такой полинуклеотид и способ получения предшественника пирипиропена а (варианты) |
| CA2760078C (en) * | 2009-05-13 | 2016-01-19 | Meiji Seika Pharma Co., Ltd. | Process for producing pyripyropene derivatives |
-
2009
- 2009-07-24 RU RU2011106496/10A patent/RU2540017C2/ru active
- 2009-07-24 CA CA2731760A patent/CA2731760C/en active Active
- 2009-07-24 WO PCT/JP2009/063293 patent/WO2010010955A1/ja active Application Filing
- 2009-07-24 ES ES09800469.0T patent/ES2453665T3/es active Active
- 2009-07-24 DK DK09800469.0T patent/DK2319923T3/en active
- 2009-07-24 KR KR1020117001974A patent/KR101690802B1/ko active IP Right Grant
- 2009-07-24 MX MX2011000023A patent/MX2011000023A/es active IP Right Grant
- 2009-07-24 AU AU2009274832A patent/AU2009274832B2/en active Active
- 2009-07-24 BR BRPI0916355A patent/BRPI0916355B8/pt active IP Right Grant
- 2009-07-24 CN CN200980128891.6A patent/CN102144030B/zh active Active
- 2009-07-24 PL PL09800469T patent/PL2319923T3/pl unknown
- 2009-07-24 EP EP09800469.0A patent/EP2319923B1/en active Active
- 2009-07-24 NZ NZ590795A patent/NZ590795A/xx unknown
- 2009-07-24 JP JP2009548252A patent/JP4642922B2/ja active Active
- 2009-07-24 US US13/055,532 patent/US8557550B2/en active Active
- 2009-11-25 JP JP2009267881A patent/JP2010193878A/ja not_active Withdrawn
-
2011
- 2011-01-23 IL IL210795A patent/IL210795A/en active IP Right Grant
- 2011-01-27 ZA ZA2011/00709A patent/ZA201100709B/en unknown
-
2013
- 2013-09-10 US US14/022,778 patent/US9315785B2/en active Active
Patent Citations (21)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US500997A (en) | 1893-07-04 | Oar unloadee | ||
| JPH04360895A (ja) | 1991-06-06 | 1992-12-14 | Kitasato Inst:The | Fo−1289a物質およびその製造法 |
| WO1994009147A1 (en) | 1992-10-22 | 1994-04-28 | The Kitasato Institute | Fo-1289 substance and its production |
| JPH06184158A (ja) | 1992-10-22 | 1994-07-05 | Kitasato Inst:The | Fo−1289物質およびその製造法 |
| US5597835A (en) | 1993-10-08 | 1997-01-28 | Korea Institute Of Science And Technology | Acyl CoA:cholesterol acyltransferase inhibitors |
| JPH08239385A (ja) | 1995-03-03 | 1996-09-17 | Kitasato Inst:The | Fo−1289物質およびその製造法 |
| JPH08259569A (ja) | 1995-03-27 | 1996-10-08 | Kitasato Inst:The | ピリピロペン誘導体 |
| JPH08269063A (ja) | 1995-03-28 | 1996-10-15 | Kitasato Inst:The | ピリピロペン誘導体 |
| JPH08269062A (ja) | 1995-03-30 | 1996-10-15 | Kitasato Inst:The | ピリピロペン誘導体 |
| JPH08269065A (ja) | 1995-04-03 | 1996-10-15 | Kitasato Inst:The | ピリピロペン誘導体 |
| JPH08269066A (ja) | 1995-04-03 | 1996-10-15 | Kitasato Inst:The | ピリピロペン誘導体 |
| JPH08269064A (ja) | 1995-04-03 | 1996-10-15 | Kitasato Inst:The | ピリピロペン誘導体 |
| JPH08291164A (ja) | 1995-04-18 | 1996-11-05 | Kitasato Inst:The | ピリピロペン誘導体 |
| WO2004060065A1 (en) | 2003-01-07 | 2004-07-22 | Korea Research Institute Of Bioscience And Biotechnology | Insecticidal compositions comprising compounds having inhibitory activity versus acyl coa: cholesterol acyltransferase or salts thereof as effective ingredients |
| JP2008500997A (ja) * | 2004-05-28 | 2008-01-17 | シュペーデル・エクスペリメンタ・アーゲー | アロマターゼ阻害剤としての二環式の窒素含有複素環 |
| WO2006129714A1 (ja) | 2005-06-01 | 2006-12-07 | Meiji Seika Kaisha, Ltd. | 害虫防除剤 |
| WO2008066153A1 (fr) | 2006-11-30 | 2008-06-05 | Meiji Seika Kaisha, Ltd. | Agent antiparasitaire |
| JP2008270294A (ja) | 2007-04-16 | 2008-11-06 | Sumitomo Electric Ind Ltd | ヒートシンク部材および半導体装置 |
| JP2009020591A (ja) | 2007-07-10 | 2009-01-29 | Canon Inc | プリンタアダプタ装置および制御方法 |
| WO2009022702A1 (ja) | 2007-08-13 | 2009-02-19 | Meiji Seika Kaisha, Ltd. | ピリピロペン誘導体の製造法およびその製造中間体 |
| JP2008190862A (ja) | 2008-03-26 | 2008-08-21 | Toshiba Corp | 加熱調理器 |
Non-Patent Citations (20)
| Title |
|---|
| APPLIED AND ENVIRONMENTAL MICROBIOLOGY, vol. 61, no. 12, 1995, pages 4429 - 35 |
| CARRERAS, C.W.; SANTI, D.V., "CURRENT OPINION IN BIOTECHNOLOGY", (UK), vol. 9, 1998, pages 403 - 411 |
| CHEMICAL REVIEW, vol. 105, 2005, pages 4559 - 4580 |
| EUPENICILLIUM RETICULOSPORUM NRRL-3446 STRAIN IS IN APPLIED AND ENVIRONMENTAL MICROBIOLOGY, vol. 61, no. 12, 1995, pages 4429 - 35 |
| FEDOROVA, N.D. ET AL.: "Genomic islands in the pathogenic filamentous fungus Aspergillus fumigatus", PLOS GENET., vol. 4, no. 4, 11 April 2008 (2008-04-11), pages E1000046, XP002544950 * |
| HUTCHINSON, C. R., "BIO/TECHNOLOGY", (USA), vol. 12, 1994, pages 375 - 380 |
| HUTCHINSON, C. R., "CURRENT OPINION IN MICROBIOLOGY", (UK), vol. 1, 1998, pages 319 - 329 |
| IKADA; OHMURA, PROTEIN, NUCLEIC ACID AND ENZYME, vol. 43, 1998, pages 1265 - 1277 |
| J. ANTIBIOTICS, vol. 49, 1996, pages 292 - 298 |
| JOURNAL OF ANTIBIOTICS, vol. 46, no. 7, 1993, pages 1168 - 9 |
| JOURNAL OF ANTIBIOTICS, vol. 50, no. 3, 1997, pages 229 - 36 |
| JOURNAL OF ORGANIC CHEMISTRY, vol. 61, 1996, pages 882 - 886 |
| JOURNAL OF SYNTHETIC ORGANIC CHEMISTRY, JAPAN, vol. 56, no. 6, 1998, pages 478 - 488 |
| KATZ, L.; MCDANIEL, R., "MEDICINAL RESEARCH REVIEWS", (USA), vol. 19, 1999, pages 543 - 558 |
| NIERMAN, W.C. ET AL.: "Genomic sequence of the pathogenic and allergenic filamentous fungus Aspergillus fumigatus", NATURE, vol. 438, no. 7071, 2005, pages 1151 - 1156, XP008139207 * |
| SAMBROOK, J. ET AL.: ""Molecular cloning: a laboratory manual", (USA)", 1989, COLD SPRING HARBOR LABORATORY |
| See also references of EP2319923A4 |
| SUNAZUKA, T. ET AL.: "Total synthesis of alpha- pyrone meroterpenoids, novel bioactive microbial metabolites", CHEM.REV., vol. 105, no. 12, 2005, pages 4559 - 4580, XP008139913 * |
| TETRAHEDRON LETTERS, vol. 37, no. 36, 1996, pages 6461 - 6464 |
| TOMODA, H. ET AL.: "Biosynthesis of Pyripyropene A", J.ORG.CHEM., vol. 61, no. 3, 1996, pages 882 - 886, XP008139912 * |
Cited By (24)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN102762737B (zh) * | 2010-01-26 | 2016-05-04 | 明治制果药业株式会社 | 生产啶南平的方法 |
| TWI633185B (zh) * | 2010-01-26 | 2018-08-21 | 明治製果藥業股份有限公司 | 比利比洛邊(pyripyropene)生物合成基因群及含有標識基因的核酸構築物 |
| WO2011093187A1 (ja) * | 2010-01-26 | 2011-08-04 | 明治製菓株式会社 | 酵素法によるピリピロペン誘導体の製造方法 |
| CN102762737A (zh) * | 2010-01-26 | 2012-10-31 | 明治制果药业株式会社 | 生产啶南平的方法 |
| EP2530149A1 (en) * | 2010-01-26 | 2012-12-05 | Meiji Seika Pharma Co., Ltd. | Nucleic acid structure containing a pyripyropene biosynthesis gene cluster and a marker gene |
| US9090924B2 (en) | 2010-01-26 | 2015-07-28 | Meiji Seika Pharma Co., Ltd. | Nucleic acid construct comprising pyripyropene biosynthetic gene cluster and marker gene |
| EP2530149A4 (en) * | 2010-01-26 | 2014-01-15 | Meiji Seika Pharma Co Ltd | NUCLEIC ACID STRUCTURE CONTAINING GENE FAMILY FOR BIOSYNTHESIS OF PYRIPYROPENE AND A MARKER GENE |
| CN104017839A (zh) * | 2010-01-26 | 2014-09-03 | 明治制果药业株式会社 | 生产啶南平的方法 |
| CN104531726A (zh) * | 2010-01-26 | 2015-04-22 | 明治制果药业株式会社 | 生产啶南平的方法 |
| AU2011210968B2 (en) * | 2010-01-26 | 2015-05-07 | Mitsui Chemicals Crop & Life Solutions, Inc. | Nucleic acid structure containing a pyripyropene biosynthesis gene cluster and a marker gene |
| TWI633190B (zh) * | 2010-01-26 | 2018-08-21 | 明治製菓藥業股份有限公司 | 比利比洛邊(pyripyropene)的製造方法 |
| WO2011093185A1 (ja) * | 2010-01-26 | 2011-08-04 | 明治製菓株式会社 | ピリピロペンの製造法 |
| CN104017839B (zh) * | 2010-01-26 | 2017-01-18 | 明治制果药业株式会社 | 生产啶南平的方法 |
| AU2011210967B2 (en) * | 2010-01-26 | 2016-06-23 | Mitsui Chemicals Crop & Life Solutions, Inc. | Method for manufacturing a pyripyropene |
| WO2011093186A1 (ja) * | 2010-01-26 | 2011-08-04 | 明治製菓株式会社 | ピリピロペン生合成遺伝子群およびマーカー遺伝子を含む核酸構築物 |
| US9169504B2 (en) | 2010-01-26 | 2015-10-27 | Meiji Seika Pharma Co., Ltd. | Method for producing pyripyropene |
| CN104531726B (zh) * | 2010-01-26 | 2017-10-10 | 明治制果药业株式会社 | 生产啶南平的方法 |
| US9723834B2 (en) | 2010-09-14 | 2017-08-08 | Basf Se | Composition containing a pyripyropene insecticide and a base |
| US9888689B2 (en) | 2010-09-14 | 2018-02-13 | Basf Se | Compositions containing a pyripyropene insecticide and an adjuvant |
| CN110294765A (zh) * | 2010-09-14 | 2019-10-01 | 巴斯夫欧洲公司 | 含有啶南平杀虫剂和助剂的组合物 |
| WO2013073689A1 (ja) * | 2011-11-17 | 2013-05-23 | Meiji Seikaファルマ株式会社 | ピリピロペン生合成遺伝子発現植物体 |
| US9861104B2 (en) | 2012-03-12 | 2018-01-09 | Basf Se | Method for producing an aqueous suspension concentrate formulation of a pyripyropene insecticide |
| US9924712B2 (en) | 2012-03-12 | 2018-03-27 | Basf Se | Liquid concentrate formulation containing a pyripyropene insecticide II |
| US9596843B2 (en) | 2012-03-12 | 2017-03-21 | Basf Se | Liquid concentrate formulation containing a pyripyropene insecticide I |
Also Published As
| Publication number | Publication date |
|---|---|
| RU2011106496A (ru) | 2012-08-27 |
| BRPI0916355B1 (pt) | 2021-11-09 |
| AU2009274832A1 (en) | 2010-01-28 |
| DK2319923T3 (en) | 2014-02-24 |
| IL210795A0 (en) | 2011-04-28 |
| CN102144030B (zh) | 2016-05-04 |
| EP2319923A1 (en) | 2011-05-11 |
| JP2010193878A (ja) | 2010-09-09 |
| JP4642922B2 (ja) | 2011-03-02 |
| KR20110038678A (ko) | 2011-04-14 |
| AU2009274832B2 (en) | 2015-07-16 |
| KR101690802B1 (ko) | 2016-12-28 |
| CA2731760C (en) | 2019-09-24 |
| NZ590795A (en) | 2012-11-30 |
| EP2319923B1 (en) | 2013-12-25 |
| JPWO2010010955A1 (ja) | 2012-01-05 |
| PL2319923T3 (pl) | 2014-05-30 |
| US9315785B2 (en) | 2016-04-19 |
| US20120015410A1 (en) | 2012-01-19 |
| BRPI0916355A2 (pt) | 2020-08-18 |
| EP2319923A4 (en) | 2011-12-28 |
| IL210795A (en) | 2014-12-31 |
| ES2453665T3 (es) | 2014-04-08 |
| CA2731760A1 (en) | 2010-01-28 |
| MX2011000023A (es) | 2011-03-30 |
| US20140142289A1 (en) | 2014-05-22 |
| ZA201100709B (en) | 2012-05-01 |
| BRPI0916355B8 (pt) | 2022-12-13 |
| CN102144030A (zh) | 2011-08-03 |
| RU2540017C2 (ru) | 2015-01-27 |
| US8557550B2 (en) | 2013-10-15 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4642922B2 (ja) | ピリピロペンa生合成遺伝子 | |
| JP5898960B2 (ja) | ピリピロペンの製造法 | |
| WO2011093187A1 (ja) | 酵素法によるピリピロペン誘導体の製造方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| WWE | Wipo information: entry into national phase |
Ref document number: 200980128891.6 Country of ref document: CN |
|
| ENP | Entry into the national phase |
Ref document number: 2009548252 Country of ref document: JP Kind code of ref document: A |
|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 09800469 Country of ref document: EP Kind code of ref document: A1 |
|
| WWE | Wipo information: entry into national phase |
Ref document number: MX/A/2011/000023 Country of ref document: MX |
|
| ENP | Entry into the national phase |
Ref document number: 2731760 Country of ref document: CA |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2009274832 Country of ref document: AU |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 13055532 Country of ref document: US Ref document number: 557/DELNP/2011 Country of ref document: IN |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| ENP | Entry into the national phase |
Ref document number: 20117001974 Country of ref document: KR Kind code of ref document: A |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2009800469 Country of ref document: EP |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 590795 Country of ref document: NZ |
|
| ENP | Entry into the national phase |
Ref document number: 2009274832 Country of ref document: AU Date of ref document: 20090724 Kind code of ref document: A |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2011106496 Country of ref document: RU |
|
| ENP | Entry into the national phase |
Ref document number: PI0916355 Country of ref document: BR Kind code of ref document: A2 Effective date: 20110121 |