RU2158656C2 - Агломераты металлического кобальта, способ их получения и их применение - Google Patents
Агломераты металлического кобальта, способ их получения и их применение Download PDFInfo
- Publication number
- RU2158656C2 RU2158656C2 RU97122087/02A RU97122087A RU2158656C2 RU 2158656 C2 RU2158656 C2 RU 2158656C2 RU 97122087/02 A RU97122087/02 A RU 97122087/02A RU 97122087 A RU97122087 A RU 97122087A RU 2158656 C2 RU2158656 C2 RU 2158656C2
- Authority
- RU
- Russia
- Prior art keywords
- cobalt
- agglomerate
- metal
- carbonate
- hydroxide
- Prior art date
Links
Images
Classifications
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B22—CASTING; POWDER METALLURGY
- B22F—WORKING METALLIC POWDER; MANUFACTURE OF ARTICLES FROM METALLIC POWDER; MAKING METALLIC POWDER; APPARATUS OR DEVICES SPECIALLY ADAPTED FOR METALLIC POWDER
- B22F1/00—Metallic powder; Treatment of metallic powder, e.g. to facilitate working or to improve properties
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/48—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides
- H01M4/52—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides of nickel, cobalt or iron
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B22—CASTING; POWDER METALLURGY
- B22F—WORKING METALLIC POWDER; MANUFACTURE OF ARTICLES FROM METALLIC POWDER; MAKING METALLIC POWDER; APPARATUS OR DEVICES SPECIALLY ADAPTED FOR METALLIC POWDER
- B22F9/00—Making metallic powder or suspensions thereof
- B22F9/16—Making metallic powder or suspensions thereof using chemical processes
- B22F9/18—Making metallic powder or suspensions thereof using chemical processes with reduction of metal compounds
- B22F9/20—Making metallic powder or suspensions thereof using chemical processes with reduction of metal compounds starting from solid metal compounds
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B22—CASTING; POWDER METALLURGY
- B22F—WORKING METALLIC POWDER; MANUFACTURE OF ARTICLES FROM METALLIC POWDER; MAKING METALLIC POWDER; APPARATUS OR DEVICES SPECIALLY ADAPTED FOR METALLIC POWDER
- B22F9/00—Making metallic powder or suspensions thereof
- B22F9/16—Making metallic powder or suspensions thereof using chemical processes
- B22F9/18—Making metallic powder or suspensions thereof using chemical processes with reduction of metal compounds
- B22F9/20—Making metallic powder or suspensions thereof using chemical processes with reduction of metal compounds starting from solid metal compounds
- B22F9/22—Making metallic powder or suspensions thereof using chemical processes with reduction of metal compounds starting from solid metal compounds using gaseous reductors
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/10—Energy storage using batteries
Abstract
Описывается агломерат металлического кобальта, состоящий из первичных частиц, имеющих форму ореха арахиса и средний размер в области 0,5-2 мкм, и имеющий вторичную агломерированную структуру. Его получают за счет того, что осуществляют непрерывное взаимодействие соли кобальта общей формулы CoX2, где Х означает Cl-, NO3 - и/или 1/2 SO4 2-, с водным раствором или суспензией карбоната и/или бикарбоната щелочного металла и/или аммония при температуре 40-100°С, предпочтительно 60-90°С, с образованием сферического основного карбоната кобальта, который выделяют и промывают для отделения нейтральных солей и затем восстанавливают до агломерата металлического кобальта, предусмотрен агломерат металлического кобальта, обеспечивающий безупречное качество получаемых с его помощью изделий. 2 с. и 4 з.п. ф-лы, 3 табл., 4 ил.
Description
Изобретение относится к технологии порошковых металлов, в частности к агломерату металлического кобальта и способу его получения.
Известен агломерат металлического кобальта, получаемый путем смешивания порошков, полученных распылением и имеющих размеры 5-150 мкм, и порошков, образующихся путем восстановления водородом, размеры которых составляют 0,9-1,7 мкм. Получаемый таким образом агломерат металлического кобальта состоит из первичных (исходных) частиц порошка кобальта (см. заявку ФРГ N 4 343 594 C1, кл. В 22 F 1/00, 02.02.1995).
Кроме того, известен способ получения агломерата металлического кобальта, согласно которому из соли кобальта общей формулы CoX2, где X означает Cl-, NO3 - и/или 1/2 SO4 -2, получают гидроксид кобальта, затем оксид кобальта и в конечном счете путем его восстановления агломерат металлического кобальта (см. статью "Preparation and Characterization of fine Cobalt metal and Oxide Powders", PMAI News Letter, том 4, N 4, сентябрь 1979, стр. 17-21).
Недостаток известного агломерата металлического кобальта и получаемого известным способом агломерата металлического кобальта заключается в том, что они сорбируют кислород и влагу воздуха, что часто приводит к ухудшению текучести при их использовании в качестве связующего при производстве твердосплавного и режущего инструмента на основе различных твердых веществ, например карбида вольфрама, алмаза, карбида кремния и кубического натрида бора, которое сказывается на качестве инструмента.
Задачей изобретения является разработка агломерата металлического кобальта, обеспечивающего безупречное качество получаемых с его помощью изделий.
Поставленная задача решается предлагаемым агломератом металлического кобальта, состоящим из первичных частиц и имеющим вторичную агломерированную структуру, за счет того, что первичные частицы имеют форму ореха арахиса, их средний размер находится в области 0,5 - 2 мкм, а вторичная агломерированная структура представлена сферами со средними диаметрами от 3 до 50 мкм.
Вторичная агломерированная структура предлагаемого агломерата предпочтительно представлена сферами со средними диаметрами от 5 до 20 мкм.
Предлагаемый агломерат имеет предпочтительную удельную поверхность в диапазоне от 2 до 6 м2/г, в частности 2 - 3,5 м2/г (определенную промышленным стандартом Германии ДИН 66131).
Поставленная задача также решается предлагаемым способом получения агломерата металлического кобальта, включающим взаимодействие соли кобальта общей формулы CoX2, где X означает Cl-, NO3 - и/или 1/2 SO4 2-, с реагентом и восстановление до агломератов металлического кобальта за счет того, что осуществляют непрерывное взаимодействие указанной соли кобальта с водным раствором или суспензией карбоната и/или бикарбоната щелочного металла и/или аммония при температуре от 40 до 100oC, предпочтительно от 60 до 90oC, с образованием сферического основного карбоната кобальта, который выделяют и промывают для отделения нейтральных солей и затем восстанавливают до агломерата металлического кобальта.
Перед восстановлением отмытый от нейтральных солей карбонат кобальта можно превращать в сферический гидроксид кобальта действием раствора гидроксида щелочного металла и/или гидроксида аммония.
Восстановление осуществляют с применением газообразного восстановителя при температуре от 300 до 800oC, предпочтительно от 350 до 650oC.
Предпочтительная средняя длина первичных частиц нерегулярной продолговатой формы составляет от 0,5 до 2 мкм, а их диаметр в общем случае не превышает 0,5 мкм.
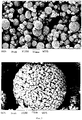
Фиг. 3 демонстрирует полученные на растровом электронном микроскопе снимки соответствующих изобретению агломератов металлического кобальта, полученных по примеру 3, при кратности увеличения, равной 1000 и 5000.
Указанная характеристика по удельной поверхности и небольшие размеры первичных частиц обеспечивают хорошую спекаемость соответствующих изобретению агломератов металлического кобальта, из которых при спекании можно получить изделия с плотностями около 8,5 г/см3 уже при температурах около 700oC.
Предлагаемый способ проводят следующим образом.
На первой стадии в непрерывно действующем проточном реакторе с эффективной мешалкой проводят взаимодействие раствора соли двухвалентного кобальта общей формулы CoX2, где X означает Cl-, NO3 - и/или 1/2 SO4 2-, с водными растворами или с суспензиями карбонатов и/или бикарбонатов щелочных металлов и/или аммония. Температурный интервал, в котором протекает это взаимодействие, лежит предпочтительно в пределах от 60 до 90oC. При этом, в отличие от используемых обычно способов осаждения, образуется не кристаллический карбонат кобальта с кристаллами в виде палочек, а сферический основный карбонат кобальта. Его отфильтровывают и отмывают от нейтральных солей.
Для минимизации содержания примесей, которые могут оказаться критическими при последующем применении, полученный таким образом основный карбонат кобальта может быть превращен на дополнительной стадии в сферический гидроксид двухвалентного кобальта добавлением щелочей или раствора аммиака в воде. Если же для образования карбоната кобальта использовались, соответственно, растворы чистых веществ, то эта стадия становится излишней. Процесс завершается восстановлением полученного таким образом гидроксида двухвалентного кобальта или, соответственно, основного карбоната кобальта газообразным восстановлением, предпочтительно это водород, метан, закись азота и/или монооксид, при вышеуказанных температурах в печи.
В отличие от известных порошков кобальта соответствующие изобретению агломераты металлического кобальта из-за их сферической вторичной структуры показывают очень хорошую текучесть.
Благодаря приведенным здесь свойствам соответствующие изобретению порошки металлического кобальта особенно хорошо подходят в качестве связующих для производства твердосплавного и/или алмазного инструмента. Следует отметить, что соответствующие изобретению агломераты металлического кобальта могут с этой целью применяться как в качестве единственного связующего, так и в комбинации с другими используемыми для этого металлами.
Так, например, они могут применяться для получения спеканием композиционных материалов на основе металлического кобальта и твердых материалов из группы, включающей алмаз, кубический нитрид бора, карбид вольфрама, карбид кремния и оксид алюминия.
Благодаря хорошей текучести и тонкой первичной структуре соответствующие изобретению агломераты порошков металлического кобальта могут быть с успехом использованы для введения в состав содержащих гидроксид никеля электродных масс для положительного полюса перезаряжаемых батарей, основанных на никель-кадмиевых или никель-металлгидридных технологиях.
В так называемых циклах формирования металлический кобальт в соответствии с его потенциалом окисляется в двухвалентный кобальт, который образует в щелочных электролитах, представляющих собой 30%-ный раствор гидроксида калия, растворимые кобальтаты двухвалентного кобальта и в результате этого равномерно распределяется по электродной массе. При последующей зарядке он в конце концов осаждается на частицах гидроксида никеля в виде проводящего электрический ток слоя из CoO(OH) и обеспечивает таким образом желательное высокое использование массы гидроксида никеля в аккумуляторе. Описанное здесь анодное растворение порошка металлического кобальта протекает, естественно, тем скорее и эффективнее, чем тоньше первичная структура и, соответственно, чем более развита поверхность металлического порошка.
Изобретение иллюстрируется примерами.
Пример 1
В проточный реактор с мешалкой загружают 20 л воды, нагревают ее до 80oC и при интенсивном перемешивании непрерывно подают в него дозирующими насосами со скоростью 5 л в час 1,7 молярный раствор хлорида двухвалентного кобальта и со скоростью 19 л в час 0,9 молярный раствор бикарбоната натрия. После выхода реактора на стационарный режим из переливного штуцера реактора отбирают образующийся продукт, отфильтровывают его и отмывают водой от нейтральных солей. Продукт сушат при температуре 80oC до постоянного веса.
В проточный реактор с мешалкой загружают 20 л воды, нагревают ее до 80oC и при интенсивном перемешивании непрерывно подают в него дозирующими насосами со скоростью 5 л в час 1,7 молярный раствор хлорида двухвалентного кобальта и со скоростью 19 л в час 0,9 молярный раствор бикарбоната натрия. После выхода реактора на стационарный режим из переливного штуцера реактора отбирают образующийся продукт, отфильтровывают его и отмывают водой от нейтральных солей. Продукт сушат при температуре 80oC до постоянного веса.
В полученном таким образом карбонате кобальта по данным химического анализа содержится 54,3% кобальта и 32,3% карбонатной составляющей.
Пример 2
В 1,5 л воды суспендируют 500 г полученного по примеру 1 основного карбоната кобальта. К полученной суспензии при интенсивном перемешивании добавляют раствор 200 г гидроксида натрия в 500 мл воды, затем нагревают до 60oC и перемешивают в течение 1 часа. Продукт отфильтровывают, промывают и сушат при температуре 90oC до постоянного веса.
В 1,5 л воды суспендируют 500 г полученного по примеру 1 основного карбоната кобальта. К полученной суспензии при интенсивном перемешивании добавляют раствор 200 г гидроксида натрия в 500 мл воды, затем нагревают до 60oC и перемешивают в течение 1 часа. Продукт отфильтровывают, промывают и сушат при температуре 90oC до постоянного веса.
Выход составляет 426 г сферического агломерированного, чистого по составу фазы гидроксида двухвалентного кобальта с содержанием кобальта 63,3%.
Пример 3
В лодочку из кварца отвешивают 200 г полученного по примеру 2 гидроксида двухвалентного кобальта и восстанавливают его в потоке водорода в течение 1 часа при температуре 700oC. Получают 126 г металлического кобальта в виде сферических агломератов. На фиг. 3 показаны снимки, полученные на растровом электронном микроскопе с кратностью увеличения в 1000 и 5000 раз.
В лодочку из кварца отвешивают 200 г полученного по примеру 2 гидроксида двухвалентного кобальта и восстанавливают его в потоке водорода в течение 1 часа при температуре 700oC. Получают 126 г металлического кобальта в виде сферических агломератов. На фиг. 3 показаны снимки, полученные на растровом электронном микроскопе с кратностью увеличения в 1000 и 5000 раз.
Пример 4
Аналогично примеру 3 проводят обработку 100 г сферического основного карбоната кобальта, полученного по примеру 1. Выход составляет 54 г порошка металлического кобальта в виде частиц сферической формы. На фиг. 4 показаны снимки этого вещества, полученные на растровом электронном микроскопе с кратностью увеличения в 500 и 5000 раз.
Аналогично примеру 3 проводят обработку 100 г сферического основного карбоната кобальта, полученного по примеру 1. Выход составляет 54 г порошка металлического кобальта в виде частиц сферической формы. На фиг. 4 показаны снимки этого вещества, полученные на растровом электронном микроскопе с кратностью увеличения в 500 и 5000 раз.
Пример 5
Опыт по спеканию
Полученные по примеру 3 агломераты металлического кобальта подвергаются термическому прессованию в приведенных ниже условиях:
Используемая аппаратура: DSP 25-ATV (производства др. Фритч ГМБХ)
Нагревание до конечной температуры: 3 минуты
Время выдержки: 3 минуты
Конечное давление: 350 H/мм2
Конечная температура: см. таблицы 1, 2
Размер образцов: 40 х 4 х 10 мм.
Опыт по спеканию
Полученные по примеру 3 агломераты металлического кобальта подвергаются термическому прессованию в приведенных ниже условиях:
Используемая аппаратура: DSP 25-ATV (производства др. Фритч ГМБХ)
Нагревание до конечной температуры: 3 минуты
Время выдержки: 3 минуты
Конечное давление: 350 H/мм2
Конечная температура: см. таблицы 1, 2
Размер образцов: 40 х 4 х 10 мм.
Таблица 1 и фиг. 1 показывают зависимость твердости от температуры спекания для образцов, образующихся из агломерата порошка металлического кобальта, приготовленного соответствующим изобретению способом по примеру 3, в сравнении с образцами, полученными спеканием из известных порошков металлического кобальта. Представленные данные ясно показывают, что использование для спекания соответствующих изобретению порошков металлического кобальта позволяет достигать высоких значений твердости уже при температуре около 700oC и к тому же эти значения твердости остаются постоянными во всем температурном интервале до 980oC.
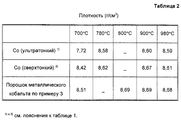
Таблица 2 и фиг. 2 показывают зависимость плотности изделий от температуры для полученных спеканием, образующихся из агломерата порошка металлического кобальта, приготовленного соответствующим изобретению способом по примеру 3, в сравнении с образцами, полученными спеканием из известных порошков металлического кобальта.
В таблице 3 показано сравнение размеров частиц, определенных по методу Фишера и определенных по методу Брюнауэра-Эммета-Теллера удельных поверхностей (определение по одной точке на кривой низкотемпературной адсорбции азота по DIN 66131, БЭТ-поверхности) агломератов порошков кобальта, полученных по примеру 3, и известных порошков кобальта.
Claims (6)
1. Агломерат металлического кобальта, состоящий из первичных частиц и имеющий вторичную агломерированную структуру, отличающийся тем, что первичные частицы имеют форму ореха арахиса, их средний размер находится в области 0,5 - 2 мкм, а вторичная агломерированная структура представлена сферами со средними диаметрами 3 - 50 мкм.
2. Агломерат по п.1, отличающийся тем, что его вторичная агломерированная структура представлена сферами со средними диаметрами 5 - 20 мкм.
3. Агломерат по п.1 или 2, отличающийся тем, что он имеет удельную поверхность в диапазоне 2 - 6 м2/г.
4. Способ получения агломерата металлического кобальта, включающий взаимодействие соли кобальта общей формулы CoX2, где X означает Cl-, NO3 - и/или 1/2 SO4 2-, с реагентом и восстановление до агломерата металлического кобальта, отличающийся тем, что осуществляют непрерывное взаимодействие указанной соли кобальта с водным раствором или суспензией карбоната и/или бикарбоната щелочного металла и/или аммония при температурах 40 - 100oC, предпочтительно 60 - 90oC, с образованием сферического основного карбоната кобальта, который выделяют и промывают для отделения нейтральных солей и затем восстанавливают до агломерата металлического кобальта.
5. Способ по п.4, отличающийся тем, что отмытый от нейтральных солей карбонат кобальта перед восстановлением превращают в сферический гидроксид кобальта действием раствора гидроксида щелочного металла и/или гидроксида аммония.
6. Способ по п.4, отличающийся тем, что восстановление осуществляют с применением газообразного восстановителя при температуре 300 - 800oC, предпочтительно 350 - 650oC.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE19519329.6 | 1995-05-26 | ||
| DE19519329A DE19519329C1 (de) | 1995-05-26 | 1995-05-26 | Kobaltmetallagglomerate, Verfahren zu ihrer Herstellung sowie deren Verwendung |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU97122087A RU97122087A (ru) | 1999-10-10 |
| RU2158656C2 true RU2158656C2 (ru) | 2000-11-10 |
Family
ID=7762916
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU97122087/02A RU2158656C2 (ru) | 1995-05-26 | 1996-05-14 | Агломераты металлического кобальта, способ их получения и их применение |
Country Status (13)
| Country | Link |
|---|---|
| US (1) | US6019813A (ru) |
| EP (1) | EP0828577B1 (ru) |
| JP (1) | JPH11505884A (ru) |
| KR (1) | KR100420605B1 (ru) |
| CN (1) | CN1080155C (ru) |
| AT (1) | ATE175606T1 (ru) |
| AU (1) | AU695628B2 (ru) |
| DE (2) | DE19519329C1 (ru) |
| NO (1) | NO319737B1 (ru) |
| RU (1) | RU2158656C2 (ru) |
| TW (1) | TW402641B (ru) |
| WO (1) | WO1996037325A1 (ru) |
| ZA (1) | ZA964187B (ru) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2560901C1 (ru) * | 2014-07-28 | 2015-08-20 | Общество с ограниченной ответственностью "Завод электрохимических преобразователей" (ООО "ЗЭП") | Способ получения мелкодисперсного металлического порошка |
Families Citing this family (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE19540076C1 (de) * | 1995-10-27 | 1997-05-22 | Starck H C Gmbh Co Kg | Ultrafeines Kobaltmetallpulver, Verfahren zu seiner Herstellung sowie Verwendung des Kobaltmetallpulvers und des Kobaltcarbonates |
| JP4691241B2 (ja) * | 2000-09-29 | 2011-06-01 | ソニー株式会社 | 高純度コバルトの製造方法および塩化コバルトの精製方法 |
| US7442227B2 (en) | 2001-10-09 | 2008-10-28 | Washington Unniversity | Tightly agglomerated non-oxide particles and method for producing the same |
| WO2005023461A1 (ja) | 2003-08-29 | 2005-03-17 | Sumitomo Metal Mining Co., Ltd. | ニッケル粉およびその製造方法 |
| WO2010126424A1 (en) * | 2009-04-27 | 2010-11-04 | Sandvik Intellectual Property Ab | Cemented carbide tools |
| CN103260795B (zh) * | 2010-11-08 | 2015-10-07 | 纳美仕有限公司 | 金属粒子及其制造方法 |
| KR101239086B1 (ko) * | 2011-04-26 | 2013-03-06 | 전자부품연구원 | 구형의 다공성 산화코발트를 이용한 비수계 리튬이차전지용 양극재료 및 그의 제조 방법 |
| KR102327114B1 (ko) * | 2017-03-08 | 2021-11-16 | 유미코아 | 충전식 리튬 이온 배터리용 캐소드 물질의 전구체 |
Family Cites Families (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3855016A (en) * | 1971-03-24 | 1974-12-17 | Graham Magnetics Inc | Acicular cobalt powders having high squarenesss ratios |
| GB1436595A (en) * | 1973-03-30 | 1976-05-19 | Sherritt Gordon Mines Ltd | Process for the production of finely divided cobalt powders |
| CA1089654A (en) * | 1977-03-07 | 1980-11-18 | Barry N. Doyle | Production of ultrafine cobalt powder from dilute solution |
| US4469505A (en) * | 1980-11-19 | 1984-09-04 | Gte Products Corporation | Method for producing cobalt metal powder |
| US4588572A (en) * | 1984-10-12 | 1986-05-13 | Mooney Chemicals, Inc. | Process for preparing aqueous cobalt (II) carbonate slurries, and slurries so produced |
| US4927456A (en) * | 1987-05-27 | 1990-05-22 | Gte Products Corporation | Hydrometallurgical process for producing finely divided iron based powders |
| US4798623A (en) * | 1988-02-19 | 1989-01-17 | Gte Products Corporation | Method for producing fine cobalt metal powder |
| DE4343594C1 (de) * | 1993-12-21 | 1995-02-02 | Starck H C Gmbh Co Kg | Kobaltmetallpulver sowie daraus hergestellte Verbundsinterkörper |
| SE502931C2 (sv) * | 1994-06-10 | 1996-02-26 | Sandvik Ab | Metod för tillverkning av pulver för WC-hårdmaterial |
| HU213130B (en) * | 1994-07-11 | 1997-02-28 | Bank Rt Polgari | Improved information carrying magnetic tape |
-
1995
- 1995-05-26 DE DE19519329A patent/DE19519329C1/de not_active Expired - Fee Related
-
1996
- 1996-04-30 TW TW085105114A patent/TW402641B/zh not_active IP Right Cessation
- 1996-05-14 US US08/952,552 patent/US6019813A/en not_active Expired - Lifetime
- 1996-05-14 EP EP96916063A patent/EP0828577B1/de not_active Expired - Lifetime
- 1996-05-14 JP JP8535334A patent/JPH11505884A/ja not_active Ceased
- 1996-05-14 WO PCT/EP1996/002053 patent/WO1996037325A1/de active IP Right Grant
- 1996-05-14 AU AU58961/96A patent/AU695628B2/en not_active Ceased
- 1996-05-14 CN CN96194173A patent/CN1080155C/zh not_active Expired - Fee Related
- 1996-05-14 KR KR1019970708463A patent/KR100420605B1/ko not_active IP Right Cessation
- 1996-05-14 RU RU97122087/02A patent/RU2158656C2/ru active
- 1996-05-14 DE DE59601152T patent/DE59601152D1/de not_active Expired - Lifetime
- 1996-05-14 AT AT96916063T patent/ATE175606T1/de active
- 1996-05-24 ZA ZA964187A patent/ZA964187B/xx unknown
-
1997
- 1997-11-25 NO NO19975416A patent/NO319737B1/no not_active IP Right Cessation
Non-Patent Citations (1)
| Title |
|---|
| PMAI News Letter. Bd. 4, Nr. 4, September 1979, Sciten 17-21. GB 1:64439 A, 10.04.1980. * |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2560901C1 (ru) * | 2014-07-28 | 2015-08-20 | Общество с ограниченной ответственностью "Завод электрохимических преобразователей" (ООО "ЗЭП") | Способ получения мелкодисперсного металлического порошка |
Also Published As
| Publication number | Publication date |
|---|---|
| ZA964187B (en) | 1996-12-04 |
| EP0828577A1 (de) | 1998-03-18 |
| KR19990021988A (ko) | 1999-03-25 |
| CN1194602A (zh) | 1998-09-30 |
| KR100420605B1 (ko) | 2004-05-20 |
| NO319737B1 (no) | 2005-09-12 |
| CN1080155C (zh) | 2002-03-06 |
| AU695628B2 (en) | 1998-08-20 |
| AU5896196A (en) | 1996-12-11 |
| DE59601152D1 (de) | 1999-02-25 |
| DE19519329C1 (de) | 1996-11-28 |
| NO975416D0 (no) | 1997-11-25 |
| ATE175606T1 (de) | 1999-01-15 |
| US6019813A (en) | 2000-02-01 |
| NO975416L (no) | 1997-11-25 |
| JPH11505884A (ja) | 1999-05-25 |
| EP0828577B1 (de) | 1999-01-13 |
| WO1996037325A1 (de) | 1996-11-28 |
| TW402641B (en) | 2000-08-21 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR100898236B1 (ko) | 인산제1철 함수염 결정, 그의 제조 방법 및 리튬철인계복합 산화물의 제조 방법 | |
| JP3961826B2 (ja) | 高密度及び大きな粒径の水酸化コバルト又はコバルト混合水酸化物の製造方法及びこの方法により製造される製造物 | |
| RU2158656C2 (ru) | Агломераты металлического кобальта, способ их получения и их применение | |
| GB1579313A (en) | Method of preparing electrolyte for use in fuel cells | |
| JP2004359538A (ja) | リン酸リチウム凝集体、その製造方法及びリチウム鉄リン系複合酸化物の製造方法 | |
| JP2003528019A (ja) | 天然グラファイトの表面精製および粉砕および粒度分布に及ぼす不純物の効果 | |
| RU2158657C2 (ru) | Агломераты металлического кобальта, способ их получения и их применение | |
| JP2002158007A (ja) | リチウムマンガンニッケル複合酸化物およびその製造方法 | |
| JP3816305B2 (ja) | 酸化コバルト粉の製造方法 | |
| US4308299A (en) | Lithiated nickel oxide | |
| JP2009093947A (ja) | 球状の電解二酸化マンガンおよびこれを用いたアルカリ一次電池 | |
| JP6999619B2 (ja) | シリコンクラスレートiiを含有する負極活物質 | |
| JP4086551B2 (ja) | 四酸化三コバルトの製造方法及びコバルト酸リチウムの製造方法 | |
| JP2005526680A (ja) | Nh4f及びh2so4の希釈水溶液を用いた不純物を含有する黒鉛の表面精製方法 | |
| RU97122087A (ru) | Агломераты металлического кобальта, способ их получения и их применение | |
| JPH1190219A (ja) | 炭酸ガス吸収材 | |
| CN111115623B (zh) | 一种天然微晶石墨负极材料的制备方法及负极材料与应用 | |
| CN111952561A (zh) | 自模板法合成的CoIn2S4@CPAN微球复合材料及其方法 | |
| JP2006198550A (ja) | 二酸化炭素吸収材料 | |
| CA2221773C (en) | Cobalt metal agglomerates, process for producing the same and their use | |
| JP4652791B2 (ja) | Mg固溶オキシ水酸化コバルト粒子及びその製造方法 | |
| JPH10188975A (ja) | 酸化銀電池用陽極材料とその製造方法 | |
| JP3786457B2 (ja) | 多孔質アルミン酸リチウムの製造方法 | |
| JP3876115B2 (ja) | 金属酸化物の製造方法 | |
| JP2001102054A (ja) | リチウム2次電池用正極活物質の製造方法及びそれを正極に用いた電池 |