RU2073675C1 - Производные 4-пиримидинонов или их органические или минеральные фармацевтические соли, способ их получения и фармацевтическая композиция на их основе - Google Patents
Производные 4-пиримидинонов или их органические или минеральные фармацевтические соли, способ их получения и фармацевтическая композиция на их основе Download PDFInfo
- Publication number
- RU2073675C1 RU2073675C1 SU925010817A SU5010817A RU2073675C1 RU 2073675 C1 RU2073675 C1 RU 2073675C1 SU 925010817 A SU925010817 A SU 925010817A SU 5010817 A SU5010817 A SU 5010817A RU 2073675 C1 RU2073675 C1 RU 2073675C1
- Authority
- RU
- Russia
- Prior art keywords
- alkyl
- group
- methyl
- tetrazol
- methanol
- Prior art date
Links
- 0 *c1ccccc1-c1ccc(CC2=C(*)NC(*)=CC2O)cc1 Chemical compound *c1ccccc1-c1ccc(CC2=C(*)NC(*)=CC2O)cc1 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D239/00—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings
- C07D239/02—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings
- C07D239/24—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings having three or more double bonds between ring members or between ring members and non-ring members
- C07D239/28—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings having three or more double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, directly attached to ring carbon atoms
- C07D239/32—One oxygen, sulfur or nitrogen atom
- C07D239/34—One oxygen atom
- C07D239/36—One oxygen atom as doubly bound oxygen atom or as unsubstituted hydroxy radical
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/02—Drugs for disorders of the urinary system of urine or of the urinary tract, e.g. urine acidifiers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P15/00—Drugs for genital or sexual disorders; Contraceptives
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/12—Antihypertensives
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D239/00—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings
- C07D239/02—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings
- C07D239/24—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings having three or more double bonds between ring members or between ring members and non-ring members
- C07D239/28—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings having three or more double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, directly attached to ring carbon atoms
- C07D239/46—Two or more oxygen, sulphur or nitrogen atoms
- C07D239/52—Two oxygen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/10—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings linked by a carbon chain containing aromatic rings
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Life Sciences & Earth Sciences (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Heart & Thoracic Surgery (AREA)
- Cardiology (AREA)
- Endocrinology (AREA)
- Urology & Nephrology (AREA)
- Ophthalmology & Optometry (AREA)
- Reproductive Health (AREA)
- Pulmonology (AREA)
- Epidemiology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Plural Heterocyclic Compounds (AREA)
- Macromolecular Compounds Obtained By Forming Nitrogen-Containing Linkages In General (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
- Liquid Developers In Electrophotography (AREA)
- Nitrogen And Oxygen Or Sulfur-Condensed Heterocyclic Ring Systems (AREA)
Abstract
Назначение: в медицине. Сущность изобретения: производные 4-пиримидинонов или их органические или минеральные фармацевтические соли в виде трех таутомерных форм. Реагент 1: β - кетоэфир: R1-CH2-CO-CH2-CO-COR4. Реагент II: L-CH2 C6H4-C6H4R5, где L = галоид, R5 = СООR6, защищенная 1Н-тетразол-5-ильная группа; полученное соединение вводят во взаимодействие с амидином: НN = C(R2)NH2, целевой продукт выделяют в свободном виде или в виде органических или минеральных фрамацевтических солей, фармацевтическая композиция, препятствующая фиксации ангиотензина II на своих рецепторах в крови, содержащая наполнители и в качестве активного начала эффективное количество производного 4-пиримидинона. 3 с. и 1 з.п.ф-лы, 2 табл.
Description
Изобретение относится к области синтеза биологически активных соединений.
В частности, настоящее изобретение относится к производным 4-пиримидинонов, способу их получения и их применение в фармкомпозициях.
Соединения по изобретению находятся в виде трех таутомерных форм, отвечающих общим формулам I, I' и I'':
в которых: R1 представляет собой линейную или разветвленную (С1-7)-алкильную группу;
R2 представляет собой линейную (С1-7)-алкильную группу, либо цикло-(С3-7)-алкил-(С1-3)-алкильную группу, фенил-(С1-3)-алкильную группу, замещенную в случае необходимости в кольце галоидом, алкил- или алкокси- или алкилтиогруппой, алкил, алкилсульфенил- или алкилсульфонил группой, содержащей в алкильной части 1-4 атома углерода, трифторметилом, гидроксикарбонилом или метилендиоксигруппой в положении 3,4 кольца, нафтил (С1-C4) алкил, тиенил (С1-C4) алкил, метилтиазол-5-ил-(C1-C4)алкил, пиридинил-(С1-C4)алкил,
R3= -COOH, 1H-тетразол-5-ил.
в которых: R1 представляет собой линейную или разветвленную (С1-7)-алкильную группу;
R2 представляет собой линейную (С1-7)-алкильную группу, либо цикло-(С3-7)-алкил-(С1-3)-алкильную группу, фенил-(С1-3)-алкильную группу, замещенную в случае необходимости в кольце галоидом, алкил- или алкокси- или алкилтиогруппой, алкил, алкилсульфенил- или алкилсульфонил группой, содержащей в алкильной части 1-4 атома углерода, трифторметилом, гидроксикарбонилом или метилендиоксигруппой в положении 3,4 кольца, нафтил (С1-C4) алкил, тиенил (С1-C4) алкил, метилтиазол-5-ил-(C1-C4)алкил, пиридинил-(С1-C4)алкил,
R3= -COOH, 1H-тетразол-5-ил.
Соединения могут находиться в свободном виде или в виде фармацевтически приемлемых органических или неорганических солей.
Известны производные пиримидинонов, общей формулы:
обладающие антагонистическую активность к ангиотензину II (см.заявку WO 91/15209).
обладающие антагонистическую активность к ангиотензину II (см.заявку WO 91/15209).
Новые соединения проявляют аналогичную активность и позволяют расширить ассортимент соединений, обладающих указанной ценной активностью.
Изобретение относится также к способу получения производных 4-пиримидинонов, существующих в виде трех таутомерных форм, отвечающих общим формулам I, I', и I''.
в которых: R1 линейная или разветвленная (С1-C7) алкильная группа;
R2 линейная (С1-C7) алкильная группа, фенил-(С1-C3)-алкил, незамещенный или замещенный в кольце галоидом, алкил или алкокси или алкилтиогруппой, алкилсульфенил или алкилсульфонил группой, содержащей в алкильной части 1 4 атома углерода, трифторметилом, гидроксикарбонилом или метилендиоксигруппой в положении 3,4 кольца, нафтил (С1-C4) алкил, тиенил (С1-C4) алкил, метилтиазол-5-ил-(С1-C4)алкил, пиридинил-(С1-C4)-алкил;
R3 -СООН, 1Н-тетразол-5-ил, а также их органических или минеральных фармацевтических солей, который заключается в том, что β-кетоэфир общей формулы II:
значения R1 указаны выше, R4 метил или этил, вводят во взаимодействие с производным общей формулы III:
где L галоид; R5 СООR6, защищенная 1Н-тетразол-5-ильная группа, причем R6 метил, этил, 1,1-диметилэтил, бензил, полученное соединение общей формулы IV:
значения R1, R4 и R5 определены выше, вводят в реакцию с амидином формулы V:
для получения соединения общей формулы VI:
где R2 имеют значения, указанные в п.1 и затем снимают защиту и/или превращают группу R5 в зависимости от природы этой группы, чтобы после превращения получить соединение общей формулы I, причем, если R5 является трифенилметилен-1Н-тетразол-5-ильной группой или 1,1-диметил-этил-1Н-тетразол-5-ильной группой, снятие защиты проводят в кислой среде, если R5 является сложноэфирной группой карбоновой кислоты, а R1 и R2 являются такими как определено в п.1, подвергают кислотному или основному гидролизу, получая при этом соединения формулы 1, где R3 группа СООН и переводят, при желании, в соответствующую соль.
Реакцию соединения формулы II с соединением формулы III проводят в растворителе, таком как метанол, этанол, 1,1-диметилэтанол или диметилформамид, при температуре, заключенной между -20oC и +80oC, в присутствии основания, такого как метилат натрия, 1,1-диметилэтилат калия или гидрид натрия, и, в случае необходимости, в присутствии катализатора, такого как бромид или иодид лития, магния или цинка.
На второй стадии реакцию β -кетоэфира общей формулы (IV) с амидином общей формулы (V) проводят при нагревании между 40oC и 120oC смеси двух соединений, в случае необходимости, в растворителе, таком как метанол, этанол, бутанол или толуол и, в случае необходимости, в присутствии основания, такого как метилат натрия, ацетат натрия, карбонат калия, пиридин, триэтиламин или 4-диметиламинопиридин.
Последующие примеры иллюстрируют изобретение.
Анализы подтверждают структуру соединений.
Пример 1. 4'-[(6-бутил-2-этил-4-оксо-1,4-дигидро-пиримидин-5-ил)-метил] -[1,1'-бифенил]-2-карбоновая кислота.
1.1 4'-[(2-метоксикарбонил)-4-оксогептил)]-[1,1'-бифенил] -2-карбоксилат метила.
К раствору, содержащему 16 г 3-оксо-гептаноата метила в 145 мл метанола, охлажденному ледяной баней, прибавляют при перемешивании раствор, содержащий 5,57 г метилата натрия (приготовленный, исходя из 2,36 г натрия в 60 мл метанола). По окончании прибавления продолжают перемешивание при комнатной температуре в течение одного часа, затем охлаждают снова при помощи ледяной бани. Добавляют по капле раствор, содержащий 40,12 г 4'-(броммметил)-[1,1'-бифенил]-2-карбоксилата метила в 60 мл метанола. Оставляют реакционную смесь при комнатной температуре с перемешиванием в течение 24 часов. Концентрируют ее при пониженном давлении. Извлекают остаток дихлорметаном. Промывают его при помощи 1н водного раствора хлороводородной кислоты, а затем водой; сушат его на сульфате натрия и выпаривают его под вакуумом, в результате чего получают 42,4 г продукта, используемого в таком виде на следующей стадии.
1.2. 4'-[(6-этил-2-этил-4-оксо-1,4-дигидро-пиримидин-5-ил)-метил] -[1,1'-бифенил]-2-карбоксилат метила.
Нагревают при температуре 90oC в атмосфере аргона смесь, состоящую из 0,48 г пропанимидамида и 2,5 г предыдущего соединения, в течение 7 часов. Очищают полученный продукт методом хроматографии на колонке с силикагелем при элюировании смесью дихлорметана и метанола, в результате чего получают 1,1 г продукта в виде сиропа, используемого в таком виде на следующей стадии.
1.3. 4'-[(6-бутил-2-этил-4-оксо-1,4-дигоидро-пиримидин-5-ил)-метил] -[1,1-бифенил]-2-карбоновая кислота.
Нагревают до образования флегмы в течение 2 часов раствор, содержащий 1,1 г предыдущего соединения и 1,4 г гидроксида натрия в смеси 30 мл метанола и 3 мл воды. Концентрируют при пониженном давлении. Извлекают остаток водой. Промывают водную фазу эфиром, фильтруют ее и подкисляют ее при помощи 3н водного раствора хлороводородной кислоты. Отфильтровывают осадок и перекристаллизовывают его в метаноле, в результате чего получают 0,55 г соединения в виде порошка белого цвета. Температура плавления (Тпл 207oC.
Пример 2. 4'-[6-бутил-2-фенилметил-4-оксо-1,4-дигидро-пиримидин-5-ил)-метил] -[1.1'-бифенил]-2-карбоновая кислота.
В соответствии с примером 1 нагревают при температуре 95oC в атмосфере аргона в течение 4 часов смесь, состоящую из 0,56 г бензолэтанимидамида и 1,7 г 4'-[(2-метоксикарбонил)-3-оксогептил] -[1.1'-фенил]-карбоксилата метила. Полученный продукт очищают методом хроматографии на глиноземе при элюировании смесью дихлорметана и метанола, в результате чего получают 1,0 г продукта. Снова растворяют этот продукт в смеси, состоящей из 30 мл метанола и 3 мл воды в присутствии 1,0 г гидроксида натрия. Нагревают до образования флегмы в течение 3 часов, затем концентрируют при пониженном давлении. Извлекают остаток водой. Промывают водную фазу эфиром, фильтруют ее и подкисляют ее при помощи 3 н водного раствора хлороводородной кислоты. Отфильтровывают осадок и перекристаллизовывают его в метаноле, в результате чего получают 0,60 г соединения в виде порошка белого цвета. Тпл 219oC.
Пример 3. 4'-{[6-бутил-2-(2-фенилэтил)-4-оксо-1,4-дигидро-пиримидин-5-ил] -метил}-[1,1'-бифенил]-2-карбоновая кислота.
В соответствии с примером 1 нагревают при температуре 95oC в течение 6 часов смесь, состоящую из 1,0 г бензолпропанимидамида и 2,4 г 4'-(2-метоксикарбонил-3-оксогептил)-[1,1'-бифенил]-2-карбоксилата метила.
Полученный продукт очищают методом хроматографии на колонке с силикагелем при элюировании смесью дихлорметана и метанола, в результате чего получают 1,0 г продукта в виде сиропа. Снова растворяют этот продукт в смеси, состоящей из 30 мл метанола и 3 мл воды, которая содержит 1,1 г гидроксида натрия. Нагревают до образования флегмы в течение 3 часов, затем концентрируют при пониженном давлении. Извлекают осадок водой. Промывают водную фазу эфиром, потом подкисляют ее при помощи 3н водного раствора хлороводородной кислоты. Отфильтровывают осадок и перекристаллизовывают его в метаноле, в результате чего получают 0,6 г соединения в виде порошка белого цвета. Tпл 194oC.
Пример 4. 6-бутил-2-(2-фенилэтил)-5-{[2'-(1H-тетразол-5-ил)-[1,1'-бифенил] -4-ил]-метил}-пиримидин-4(1Н)-он.
4.1. 3-оксо-2-{[2'-(1-трифенилметил-1Н-тетразол-5-ил) -[1,1'-бифенил]-4-ил]-метил}-гептаноат метила.
К раствору, содержащему 0,97 г 1.1-диметилэтилата калия в 15 мл диметилформамида, охлажденному ледяной баней, в атмосфере аргона прибавляют раствор, содержащий 1,3 г 3-оксогептаноата метила в 13 мл диметилформамида, затем 1,67 г бромида лития, а потом раствор, содержащий 5 г 5-[4'-(бромметил)-[1,1'-бифенил] -2-ил] -1-трифенилметил-1Н-тетразола в 25 мл диметилформамида. Перемешивают реакционную смесь в течение 5 часов при комнатной температуре, затем разбавляют ее в 300 мл эфира. Промывают ее два раза по 100 мл воды, затем при помощи 100 мл насыщенного водного раствора хлорида аммония, сушат ее на сульфате магния и выпаривают ее под вакуумом, в результате чего получают 4,60 г продукта в виде жидкого масла желтого цвета, используемого в таком виде на следующей стадии.
4.2. 6-бутил-2-(2-фенилэтил)-5-{[2'-(1-трифенил метил-1Н- тетразол-5-ил)-[1,1'-бифенил]-4-ил]-метил} -пиримидин-4(1Н)-он.
Нагревают при температуре 90oC в атмосфере аргона в течение 2 часов смесь, состоящую из 0,7 г бензолпропанимидамида и 3 г предыдущего соединения. Извлекают при помощи 120 мл дихлорметана и промывают два раза по 50 мл 1М водного раствора карбоната калия, потом при помощи 50 мл 0,1 н водного раствора хлороводородной кислоты. Сушат на сульфате магния и выпаривают. Очищают остаток методом хроматографии на колонке с силикагелем при элюировании смесью дихлорметана и метанола, в результате чего получают 0,85 г соединения в виде беловатого пенообразного вещества.
4.3. 6-бутил-2-(2-фенилэтил)-5-{ [2'-(1H-тетразол-5-ил)-[1,1' -бифенил] -4-ил]-метил}-пиримидин-4-(1Н)-он.
Растворяют 0,6 г предыдущего соединения в смеси, состоящей из 5 мл метанола и 3 мл диэтилового эфира. Прибавляют 2,7 мл 1,57 М раствора хлороводородной кислоты в диэтиловом эфире. Оставляют на два часа при комнатной температуре, потом выпаривают досуха. Извлекают остаток посредством 70 мл 0,5 н водного раствора гидроксида натрия. Промывают три раза по 30 мл эфира, затем подкисляют при помощи раствора хлороводородной кислоты. Отфильтровывают образованный осадок и перекристаллизовывают в его метаноле, в результате чего получают 0,22 г соединения в виде порошка белого цвета. Тпл 226 228oC.
Пример 5. 4'-[(2,6-дибутил-4-оксо-1,4-дигидро-пиримидин-5-ил) -метил]-[1,1'-бифенил]-2-карбоновая кислота.
В соответствии с примером 1 нагревают при температуре 90oC в атмосфере аргона в течение 10 часов смесь, состоящую из 1,1 г пентанимидамида и 1,5 г 4'-[(2-метоксикарбонил)-3-оксогептил]-[1,1'-бифенил]-2-карбоксилата метила.
Очищают продукт методом хроматографии на колонке с силикагелем при элюировании смесью дихлорметана и метанола, в результате чего получают 1,2 г продукта.
Растворяют 1 г этого продукта в смеси, состоящей из 30 мл метанола и 1 мл воды, в присутствии 1,2 г гидроксида натрия. Нагревают при температуре образования флегмы в течение 4 часов, затем концентрируют при пониженном давлении. Извлекают остаток водой. Промывают водную фазу эфиром и подкисляют ее при помощи 3н водного раствора хлороводородной кислоты. Отфильтровывают полученный осадок и перекристаллизовывают его в смеси метанол/диизопропиловый эфир, в результате чего получают 0,45 г соединения в виде порошка белого цвета. Тпл 119oC.
Пример 6. 4'-{[6-бутил-2-(3,3'-диметил)-бутил-4-оксо-1,4-дигидропирими дин-5-ил]-метил}-[1,1'-бифенил]-2-карбоновая кислота.
В соответствии с примером 1 нагревают при температуре 100oC в атмосфере аргона в течение 8 часов смесь, состоящую из 1,3 г 4,4-диметилпентанимидамида и 2 г 4'-[(2-метоксикар бонил)-3-оксогептил]-[1,1'-бифенил]-2-карбоксилата метила.
Очищают полученный продукт методом хроматографии на колонке с силикагелем при элюировании смесью дихлорметана и метанола, в результате чего получают 1,48 г продукта.
Растворяют этот продукт в смеси, состоящей из 60 мл метанола и 6 мл воды, которая содержит 1,67 г гидроксида натрия. Нагревают при температуре образования флегмы в течение 6 часов, затем концентрируют при пониженном давлении. Извлекают остаток посредством 25 мл воды. Промывают волную фазу при помощи 25 мл эфира и подкисляют ее при помощи 2н водного раствора хлороводородной кислоты. Отфильтровывают полученный осадок, споласкивают его водой и перекристаллизовывают его в метаноле, в результате чего получают 0,6 г соединения. Тпл 222oC.
Пример 7. 4'-{[6-бутил-2-(2-тиофен-3-ил)-этил)-4-оксо-1,4-дигидропиримидин- 5-ил]-метил}-[1,1'-бифенил]-2-карбоновая кислота.
В соответствии с примером 1 нагревают при температуре 110oC в атмосфере аргона в течение 3 часов 30 минут смесь, состоящую из 1,2 г 3-тиофенпронимидамида и 2,2 г 4'-[(2-метоксикарбонил)-3-оксо-гептил]-[1,1'-бифенил]-2-карбоксилата метила.
Очищают полученный продукт методом хроматографии на колонке с силикагелем при элюировании смесью дихлорметана и метанола, в результате чего получают 0,87 г продукта.
Растворяют этот продукт в смеси, состоящей из 20 мл метанола и 2 мл 10 н водного раствора гидроксида натрия. Нагревают при температуре образования флегмы в течение 3 часов, затем концентрируют при пониженном давлении. Извлекают остаток посредством 120 мл воды. Промывают водную фазу 3 раза по 40 мл эфира и подкисляют ее при помощи 6н водного раствора хлороводородной кислоты. Отфильтровывают полученный осадок и перекристаллизовывают его в метаноле, в результате чего получают 0,41 г соединения. Тпл=184 - 185oC.
Пример 8. 4'-{[6-бутил-2-(фенилсульфонил)-метил-4-оксо-1,4-дигидропирими дин-5-ил]-метил}-[1,1'-бифенил]-2-карбоновая кислота.
В соответствии с примером 1 нагревают при температуре 80oC в атмосфере аргона в течение 6 часов смесь, состоящую из 2,6 г 2-фенилсульфонилэтанимидамида и 2 г, 4'-[(2-метоксикарбонил)-3-оксогептил]-[1,1'-бифенил]-2-карбоксилата метила.
Очищают полученный продукт методом хроматографии на колонке с силикагелем при элюировании смесью дихлорметана и метанола, в результате чего получают 0,5 г продукта.
Растворяют этот продукт в смеси, состоящей из 15 мл метанола и 1,5 мл воды, которая содержит 0,5 г гидроксида натрия. Нагревают при температуре образования флегмы в течение 3,5 часов, потом концентрируют при пониженном давлении. Извлекают остаток посредством 150 мл воды. Промывают водную фазу 3 раза по 80 мл эфира, фильтруют ее и подкисляют ее при помощи 3 н водного раствора хлороводородной кислоты. Отфильтровывают полученный осадок, споласкивают его водой и перекристаллизовывают его в этаноле, в результате чего получают 0,19 г соединения. Тпл 210 212oC.
Пример 9. 4'-{[6-бутил-2-(2-хлорфенокси)-метил-4-оксо-1,4-дигидропирими дин-5-ил]-метил}-[1,1'-бифенил]-2-карбоновая кислота.
В соответствии с примером 1 нагревают при температуре 80oC в атмосфере аргона в течение 4 часов смесь, состоящую из 1,2 г 2-(2-хлорфенокси)-этанимидамида и 2 г 4'-[(2-метоксикарбонил)-3-оксогептил]-[1,1'-бифенил]-2-2карбоксилата метила. Добавляют еще 0,5 г 2-(2-хлорфенокси)-этанимидамида, спустя 1 час и спустя 2,5 часа после реакции.
Очищают полученный продукт методом хроматографии на колонке с силикагелем при элюировании смесью дихлорметана и метанола, в результате чего получают 0,8 г продукта.
Растворяют этот продукт в смеси, состоящей из 20 мл метанола и 2 мл воды, которая содержит 0,8 г гидроксида натрия. Нагревают при температуре образования флегмы в течение 4,5 часов, потом концентрируют при пониженном давлении. Извлекают остаток посредством 150 мл воды. Промывают водную фазу 3 раза по 80 мл эфира, фильтруют ее и подкисляют ее при помощи 3 н водного раствора хлороводородной кислоты. Отфильтровывают полученный осадок, споласкивают его водой и перекристаллизовывают его в этаноле, в результате чего получают 0,29 г соединения. Тпл 159 164oC.
Пример 10. 4'-{[6-бутил-2-(2-(4-карбоксифенил)-этил)-4-оксо-1,4-ди гидро-пиримидин-5-ил]-метил}-[1,1'-бифенил]-2-карбоновая кислота.
В соответствии с примером 1 нагревают при температуре 90oC в атмосфере аргона в течение 3 часов смесь, состоящую из 1,4 г 4-метоксикарбонилбензолпропанимидамида и 2 г 4'-[(-2-метоксикарбонил)-3-оксогептил]-[1,1'-бифенил]-2-карбоксилата метила.
Очищают полученный продукт методом хроматографии на колонке с силикагелем при элюировании смесью дихлорметана и метанола, в результате чего получают 1,3 г продукта.
Растворяют 1,1 г этого продукта в смеси, состоящей из 25 мл метанола и 2 мл 10 н водного раствора гидроксида натрия. Нагревают при температуре образования флегмы в течение 3 часов, потом концентрируют при пониженном давлении. Извлекают остаток водой. Промывают водную фазу эфиром и этилацетатом. Подкисляют ее водным раствором хлороводородднодй кислоты. Экстрагируют полученное жидкое масло дихлорметаном и концентрируют вытяжки. Перекристаллизовывают в метаноле в присутствии нескольких капель идизопропилового эфира, в результате чего получают 0,37 г соединения. Тпл 227oC.
Пример 11. 6-бутил-2-[2-(3,4-метилендиоксифенил)-этил]-5-{[2'-(1H-тетра зол-5-ил)-[1,1'-бифенил]-4-ил]-метил}-пиримидин-4(1Н)-он.
В соответствии с примером 4,1 нагревают при температуре образования флегмы в течение 4 часов раствор, содержащий 1,4 г 3,4-метилендиоксибензолпропанимидамида и 2,6 г 3-оксо-2-{[2'-(1-трифенилметил-1Н-тетразол-5-ил)-[1,1'-бифе нил] - 4-ил]-метил}-гептаноата метила в 3 мл толуола. Выпаривают под вакуумом и очищают продукт методом хроматографии на колонке с силикагелем при элюировании смесью дихлорметан-метанол, в результате чего получают 1 г продукта.
Растворяют этот продукт в смеси, состоящей из 15 мл метанола и 5 мл тетрагидрофурана в присутствии 1 мл уксусной кислоты. Нагревают при температуре образования флегмы в течение 5 часов и выпаривают под вакуумом. Извлекают остаток эфиром. Отфильтровывают осадок и споласкивают его 3 раза по 30 мл эфира, в результате чего получают 0,45 г соединения. Тпл 230 - 232oC
Пример 12. 6-бутил-2-[2-(нафт-2-ил)-этил]-5-{[2'-(1Н-тетразол-5-ил) -[1,1'-бифенил]-4-ил]-метил}-пиримидин-4(1Н)-он.
Пример 12. 6-бутил-2-[2-(нафт-2-ил)-этил]-5-{[2'-(1Н-тетразол-5-ил) -[1,1'-бифенил]-4-ил]-метил}-пиримидин-4(1Н)-он.
В соответствии с примером 4.2 нагревают при температуре 100oC в течение 3 часов 30 минут смесь, состоящую из 1,75 г 3-(нафт-2-ил)-пропанимидамида и 3,3 г 3-оксо-2-{ [2'-(1-(1,1-диметилэтил)-1Н-тетразол-5-ил)-[1,1'-бифенил] -4-ил]-метил}-гептаноата метила. Очищают сырой продукт методом фроматографии на колонке с силикагелем при элюировании смесью дихлорметан/метанол, в результате чего получают 2,9 г продукта в виде пастообразного вещества бледно-желтого цвета. Растворяют 1,5 г этого продукта в 30% растворе бромоводородной кислоты в уксусной кислоте. Нагревают при температуре 90oC в течение 5 часов и выпаривают уксусную кислоту. Извлекают остаток дихлорметаном. Промывают органическую фазу водой и сушат ее на сульфате натрия. Выпаривают растворитель, в результате чего получают 1,1 г порошка бежевого цвета. Сырой продукт очищается методом хроматографии на колонке с силикагелем при элюировании смесью дихлорметан/метанол. Получают 0,63 г продукта в виде порошка белого цвета. Tпл 163 166oC.
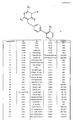
Следующая табл.1 и 2 иллюстрирует структуру и физические свойства некоторых соединений по изобретению.
Пример 67. 2-аминоэтаноловая соль 6-бутил-2-(2-фенилэтил)-5-[[2'-(1H-тетразол-5-ил)[1,1'-бифенил]-4] -метил]пиримидин-4-(1Н)-она.
К суспензии 1,47 н (3 ммол) 6-бутил-2-(2-фенилэтил)-5-[[2'-(1H-тетразол-5-ил) [1,1'-бифенил]-4]-метил]-пиримидин-4(1Н)-она в 10 мл метанола добавляют 0,191 г (3,12 ммол) 2-аминоэтанола в растворе в 5 мл метанола. Оставляют при перемешивании при комнатной температуре в течение нескольких минут, фильтруют через хлопок и выпаривают в вакууме. Растворяют полученную пену в 25 мл дихлорметана и постепенно добавляют при интенсивном перемешивании 20 мл простого диизопропилового эфира. Оставляют реакционную смесь на ночь при комнатной температуре. Фильтруют образованный осадок, прополаскивают 10 мл простого диизопропилового эфира и сушат его в вакууме, при 50oC в присутствии пятиокиси фосфора. Получают 1,6 г продукта. Точка плавления 127 130oC.
Пример 68. 2,2'-иминобисэтаноловая соль 6-бутил-2-(2-фенилэтил)-5-[[2'-(1H-тетразол-5-ил)[[1,1'-би фенил]-4-ил]метил]пиримидин-4-(1Н)-она.
К 1.96 г (4 ммол) 6-бутил-2-(2-фенилэтил)-5-[[2'-(1Н-тетразол-5-ил)[1,1'-би фенил]-4-ил]метил]пиримидин-4(1Н)-она добавляют 0,42 г (4 ммол) 2,2'-иминобисэтанола в растворе в 30 мл метанола. Оставляют при перемешивании при комнатной температуре вс течение нескольких минут, фильтруют через бумагу, прополаскивают 10 мл метанола и выпаривают в вакууме. Снова растворяют в горячем виде остаточную пену в 20 мл изопропанола, затем постепенно добавляют при интенсивном перемешивании 20 мл простого диизопропилового эфира. Фильтруют образованный белый осадок, прополаскивают его 20 мл простого диизопропилового эфира, сушат в вакууме при 55oC в присутствии пятиокиси фосфора. Получают 2,15 г продукта. Точка плавления 124 126oC.
Пример 69. L-(+)-лизиновая соль 6-бутил-2-(2-фееилэтил)-5-[[2'-(1H)-тетразол-5-ил)[1,1'-бифенил] -4-метил]пиримидин-4-(1Н)-она.
К 0,962 г (1,96 ммоль) 6-бутил-2-(2-фенилэтил)-5-[[2'-(1H-тетразол-5-ил)[1,1'-бифенил] -4-ил] метил]пиримидин-4(1Н(-она добавляют 0,287 г (1,96 ммол) L-(+)-лизина в растворе в 15 мл метанола. Оставляют при перемешивании при комнатной температуре в течение нескольких минут, фильтруют через хлопок, прополаскивают 5 мл метанола и выпаривают в вакууме. Снова растворяют в горячем виде остаточный белый порошок в 15 мл дихлорметана и добавляют постепенно, при интенсивном перемешивании, 30 мл простого диизопропилового эфира. Оставляют при комнатной температуре в течение 3 дней, затем фильтруют образованный осадок. Выпаривают маточные растворы, снова растворяют остаточный белый порошок в 5 мл дихлорметана и постепенно добавляют при интенсивном перемешивании 10 мл простого диизопропилового эфира. Фильтруют образованный осадок. Соединяют два осадка, сушат их в вакууме, при 50oC, в присутствии пятиокиси фосфора. Получают 0,7 г продукта. Точка плавления 80 120oC (разложение).
[α] + 5,1 (с 1% метанол).
Пример 70. L-(+)-аргининовая соль 6-бутил-2-(2-фенилэтил)-5-[[2'-(1H-тетразол-5-ил) [1,1'-бифенил]-4-ил]-метил]пиримидин-4(1Н)-она
Перемешивают при комнатной температуре до растворения суспензию 3,63 г (7,4 ммол) 6-бутил-2-(2-фенилэтил)-5-[[2'-(1Н-тетразол-5-ил) [1,1'-бифенил] -4-ил] метил] -пиримидин-4-(1Н)-она и 1,29 г (7,4 ммоль) L-(+)-аргинина в 75 мл метанола. Концентрируют в вакууме, поглощают остаточную пену в 80 мл горячего дихлорметана, фильтруют через бумагу и прополаскивают 10 мл горячего дихлорметана. Добавляют постепенно при интенсивном перемешивании 120 мл простого диизопропилового эфира. Оставляют при комнатной температуре в течение 3 дней, затем фильтруют полученный белый осадок и сушат его в вакууме, при 50oC, в присутствии пятиокиси фосфора. Получают 1,2 г продукта. Точка плавления 120 200oC (разложение).
Перемешивают при комнатной температуре до растворения суспензию 3,63 г (7,4 ммол) 6-бутил-2-(2-фенилэтил)-5-[[2'-(1Н-тетразол-5-ил) [1,1'-бифенил] -4-ил] метил] -пиримидин-4-(1Н)-она и 1,29 г (7,4 ммоль) L-(+)-аргинина в 75 мл метанола. Концентрируют в вакууме, поглощают остаточную пену в 80 мл горячего дихлорметана, фильтруют через бумагу и прополаскивают 10 мл горячего дихлорметана. Добавляют постепенно при интенсивном перемешивании 120 мл простого диизопропилового эфира. Оставляют при комнатной температуре в течение 3 дней, затем фильтруют полученный белый осадок и сушат его в вакууме, при 50oC, в присутствии пятиокиси фосфора. Получают 1,2 г продукта. Точка плавления 120 200oC (разложение).
[α] + 6,1 (с 1% метанол).
Пример 71 DL-лизиновая соль 6-бутил-2(2-фенилэтил)-5-[[2'-(1H-тетразол-5-ил)[1,1'-бифенил]-4 -ил]метил]пиримидин-4-(1Н)-она.
Перемешивают до растворения, при нагревании, суспензию 0,980 г (2 ммол) 6-бутил-2-(2-фенилэтил)-5-[[2'-(1H-тетразол-5-ил)[1,1'-бифенил] -4-ил]метил] пиримидин-4-(1Н)-она и 0,292 г (2 ммол) DL-лизина в 10 мл метанола. Фильтруют через бумагу и прополаскивают 5 мл горячего метанола. Затем постепенно добавляют, при интенсивном перемешивании, 17 мл простого диизопропилового эфира. Оставляют при комнатной температуре в течение ночи, затем фильтруют полученный белый осадок. Прополаскивают последовательно 10 мл смеси метанола: простого диизопропилового эфира (1:1, затем 10 мл простого диизопропилового эфира, и сушат в вакууме, при 60oC, в присутствии пятиокиси фосфора. Получают 0,95 г продукта.
Точка плавления 200 204oC (разложение).
Соединения по изобретению были предметом фармакологических исследований, которые выявили их антагонистические свойства по отношению к ангиотензину II.
Изучение связывания (3H)-ангиотензина II на кордикост ероидном гормоне надпочечника кролика
Используют самцов диких бургундских кроликов весом от 2 до 3 кг. После умерщвления животных путем раздробления (вывиха) шейного позвонка удаляют напочечные железы и быстро препарируют кору надпочечников при температуре 4oC. Гомогенизируют ткань в 10 мл ледяного буферного раствора трис-(гидроксилметил)-аминометана с концентрацией 10 мМ, содержащего 0,33 М сахарозы и 1 мМ этилендиаминтетрауксусной кислоты, рН которого поддерживали при значении 7,4 посредством хлороводородной кислоты, при помощи электрического устройства Поттера со скоростью 1200 оборотов и минуту. Доводят объем препарата до 25 мл при помощи трис-сахарозного буферного раствора перед центрифугированием в течение 15 минут с ускорением 1075 g. Сохраняют всплывшую фазу, снова гомогенизируют остаток после центрифугирования в 10 мл трис-сахарозного буферного раствора, затем центрифугируют, как описано перед этим. Объединяют обе всплывшие фазы и центрифугируют в течение 30 минут с ускорением 47,800 g. Извлекают остаток после центрифегирования посредством 150 объемов/т. е. 100 мг ткани в 15 мл буферного раствора (инкубационного буферного раствора, содержащего 50 мМ Трис-НСl, 150 мМ NaCl, 5 мМ этилендиаминтетрауксусной кислоты, 1,25 мкг на мл бацитрацина, 100 мкМ фенилметилсульфонилфторида и 0,2% бычьей альбуминовой сыворотки (рН 7,4 при 25oC).
Используют самцов диких бургундских кроликов весом от 2 до 3 кг. После умерщвления животных путем раздробления (вывиха) шейного позвонка удаляют напочечные железы и быстро препарируют кору надпочечников при температуре 4oC. Гомогенизируют ткань в 10 мл ледяного буферного раствора трис-(гидроксилметил)-аминометана с концентрацией 10 мМ, содержащего 0,33 М сахарозы и 1 мМ этилендиаминтетрауксусной кислоты, рН которого поддерживали при значении 7,4 посредством хлороводородной кислоты, при помощи электрического устройства Поттера со скоростью 1200 оборотов и минуту. Доводят объем препарата до 25 мл при помощи трис-сахарозного буферного раствора перед центрифугированием в течение 15 минут с ускорением 1075 g. Сохраняют всплывшую фазу, снова гомогенизируют остаток после центрифугирования в 10 мл трис-сахарозного буферного раствора, затем центрифугируют, как описано перед этим. Объединяют обе всплывшие фазы и центрифугируют в течение 30 минут с ускорением 47,800 g. Извлекают остаток после центрифегирования посредством 150 объемов/т. е. 100 мг ткани в 15 мл буферного раствора (инкубационного буферного раствора, содержащего 50 мМ Трис-НСl, 150 мМ NaCl, 5 мМ этилендиаминтетрауксусной кислоты, 1,25 мкг на мл бацитрацина, 100 мкМ фенилметилсульфонилфторида и 0,2% бычьей альбуминовой сыворотки (рН 7,4 при 25oC).
Затем проводят инкубирование аликвотный фракций по 100 мкл суспензии, содержащей микросомы кортикостероидов надпочечников в присутствии 2 нМ (3H)-ангиотензина II (New England Nuclear, удельная активность 61 Ки/ммоль), в конечном объеме инкубационного буферного раствора в течение 30 минут при температуре 25oC. После инкубирования извлекают микросомы путем фильтрации на фильтрах из нитрата целлюлозы Миллипор HAWPTM 0,45 мкм, предварительно обработанный 1% бычьей альбуминовой сывороткой, и промывают их три раза по 5 мл ледяного буферного раствора Трис-СНl. Измеряют количество радиоактивности, связанной тканью и задержанной на фильтрах, методом сцинтилляционной спектрометрии.
Удельное связывание (3H)-ангиотензина II определяется как количество радиоактивности, фиксированной на фильтре, которое может быть ингибировано путем инкубирования в присутствии 1 мкМ нерадиоактивного ангиотензина II. Это удельное связывание составляет от 90 до 95% общего количества радиоактивности, фиксированной на фильтре.
Измеряют удельное связывание (3H)-ангиотензина II в присутствии различных концентраций исследуемых соединений и определяют графически Сl50, т.е. концентрацию исследуемого соединения, которая на 50% ингибирует удельное связывание (3H)-ангиотензина II.
Значения Сl50 соединений по изобретению находятся между 5 нМ и 10 мкМ.
Ингибирование ответной реакции влияния ангиотензина II на артериальное давление крысы.
Используют самцов крыс (Sprague-Dawleg, Charles River Франция), весящих от 250 до 280 г, которых анестезируют пентобарбиталом натрия (55 мг/кг внутрибpюшинным путем) и которым поддерживают искусственное дыхание (респиратор ГарвардаTM: частота дыхания 70 мл в минуту, объем воздуха 1 мл на 100 г веса тела). Удаляют спинной мозг животных при помощи металлического стержня: введенного через орбиту правого глаза и пропущенного вдоль позвоночного столба. Рассекают правый и левый блуждающие нервы (биваготомия), перевязывают правую сонную артерию, причем левая сонная артерия подвергается катетеризации с целью измерения артериального давления при помощи камеры (ячейки) давления (типа StathamTM Р23Дв). Вводят катетер в бедренную вену для введения различных соединений.
Измеряют вариации среднего артериального давления, обусловленного ангоиотензином II, введенным внутривенным путем с дозой 0,5 мкг/кг. Соединения по изобретению или растворитель вводятся за 5 минут (при исследованиях внутривенным путем) или за 60 минут (при исследованиях оральным путем) до введения ангиотензина II. Соединения по изобретению вводятся с дозами, изменяющимися от 0,01 до 100 мг/кг.
Степень ингибирования ответной реакции, контролируемой ангиотензином II, используется для оценки антагонистической способности соединений по изобретению по отношению к ангиотензину II.
Соединения по изобретению могут использоваться для лечения различных форм гипертензивных патологий и коронарной, сердечной, почечной или легочной недостаточности, а также для лечения глаукомы.
Соединения по изобретению могут также использоваться в комбинации с другими веществами, обладающими сердечно-сосудистой активностью, такими как диуретики, α-блокаторы, b-блокаторы, антагонисты кальция или ингибиторы фермента превращения ангиотензина I.
Соединения по изобретению могут находиться в любых фармацевтических формах, пригодных при лечении путем орального, парентерального, внутримышечного или ректального введения: таблетки, капсулы, желатиновые капсулы, стерильные суспензии или растворы, свечи и т.д.
Для лечения глаукомы соединения изобретению могут находиться в виде таблеток, желатиновых капсул, впрыскиваемых растворов или топических (местных) глазных рецептур (капель).
Соединения по изобретению могут вводиться пациентам в количестве, которое может изменяться от 1 до 1000 мг в день для пациента за одну или несколько доз.
Соединения согласно изобретению относятся к малотоксичным.
Так, спустя 1 месяц после лечения перорально соединениями изобретения, доза без токсического эффекта составляет 500 мг/кг/день в случае крысы и 50 мг/кг/день в случае обезъяны.
Ниже даны примеры галогеновых рецептур фармакомпозиций:
Суспензия для приема внутрь
Активное вещество 1 30%
Монопальмитат сахарозы 5%
Cахароза до 100%
Диапазон доз может составлять 1 250 мг продукта в форме основания на флакон пригодной для питья суспензии.
Суспензия для приема внутрь
Активное вещество 1 30%
Монопальмитат сахарозы 5%
Cахароза до 100%
Диапазон доз может составлять 1 250 мг продукта в форме основания на флакон пригодной для питья суспензии.
Желатиновые капсулы
Активное вещество 5 25%
Эксципиент до 100%
Диапазон доз может составлять 4 62 мг продукта в форме основания на взятую единичную дозу.
Активное вещество 5 25%
Эксципиент до 100%
Диапазон доз может составлять 4 62 мг продукта в форме основания на взятую единичную дозу.
В нижеприведенной таблице даны показатели активности некоторых соединений согласно изобретению. Средний процент ингибирования артериального давления представляет собой результат, полученный во втором тесте описания.
Claims (4)
1. Производные 4-пиримидинонов, существующие в виде трех таутомерных форм, отвечающих общим формулам I, I' и I"
где R1 линейная или разветвленная (С1-C7)-алкильная группа;
R2 линейная (С1-С7)-алкильная группа, фенил-(C1-C3)-алкил, незамещенный или замещенный в кольце галоидом, алкил, или алкокси, или алкилтиогруппой, алкилсульфенил или алкилсульфонилгруппой, содержащей в алкильной части 1-4 атома углерода, трифторметилом, гидроксикарбонилом или метилендиоксигруппой в положении 3,4 кольца, нафтил-(С1-С4)-алкил, тиенил(C1-C4)-алкил, метилтиазол-5-ил-(С1-С4)-алкил, пиридинил-(С1-С4)-алкил;
R3 -СООН, 1Н-тетразол-5-ил,
а также их органические или минеральные фармацевтические соли.
где R1 линейная или разветвленная (С1-C7)-алкильная группа;
R2 линейная (С1-С7)-алкильная группа, фенил-(C1-C3)-алкил, незамещенный или замещенный в кольце галоидом, алкил, или алкокси, или алкилтиогруппой, алкилсульфенил или алкилсульфонилгруппой, содержащей в алкильной части 1-4 атома углерода, трифторметилом, гидроксикарбонилом или метилендиоксигруппой в положении 3,4 кольца, нафтил-(С1-С4)-алкил, тиенил(C1-C4)-алкил, метилтиазол-5-ил-(С1-С4)-алкил, пиридинил-(С1-С4)-алкил;
R3 -СООН, 1Н-тетразол-5-ил,
а также их органические или минеральные фармацевтические соли.
2. Производное 4-пиримидинона по п.1, представляющее собой 6-бутил-2-(2-фенилэтил)-5-[[2'-(1Н-тетразол-5-ил)- [1,1'-бифенил] -4-ил]-метил]-пиримидин-4(1Н)-он, а также его органические и минеральные фармацевтические соли.
3. Способ получения производных 4-пиримидинонов, существующих в виде трех таутомерных форм, отвечающих указанным общим формулам I, I' и I", заключающийся в том, что β - кетоэфиры общей формулы II
где R1 линейная или разветвленная (С1 - С7)-алкильная группа,
R4 метил или этил,
вводят во взаимодействие с производным общей формулы III
где L галоген;
R5 COOR6, защищенная 1Н-тетразол-5-ильная группа, причем R6 метил, этил, 1,1-диметилэтил, бензил,
полученное соединение общей формулы IV
где R1, R4 и R5 имеют указанные значения,
вводят в реакцию с амидином формулы V
для получения соединения общей формулы VI
где R2 имеет указанные значения,
и затем снимают защиту и/или превращают группу R5 в зависимости от природы этой группы, чтобы после превращения получить соединение общей формулы I, причем, если R5 -трифенилметил-1H -тетразол-5-ильная группа или 1,1-диметил-этил-1Н-тетразол-5-ильная группа, снятие защиты проводят в кислой среде, если R5 сложноэфирная группа карбоновой кислоты, а R1 и R2 имеют значения, указанные в п.1, подвергают кислотному или основному гидролизу, получая при этом соединения формулы II, где R3 группа СООН, и, при необходимости, полученный продукт переводят в соответствующую соль.
где R1 линейная или разветвленная (С1 - С7)-алкильная группа,
R4 метил или этил,
вводят во взаимодействие с производным общей формулы III
где L галоген;
R5 COOR6, защищенная 1Н-тетразол-5-ильная группа, причем R6 метил, этил, 1,1-диметилэтил, бензил,
полученное соединение общей формулы IV
где R1, R4 и R5 имеют указанные значения,
вводят в реакцию с амидином формулы V
для получения соединения общей формулы VI
где R2 имеет указанные значения,
и затем снимают защиту и/или превращают группу R5 в зависимости от природы этой группы, чтобы после превращения получить соединение общей формулы I, причем, если R5 -трифенилметил-1H -тетразол-5-ильная группа или 1,1-диметил-этил-1Н-тетразол-5-ильная группа, снятие защиты проводят в кислой среде, если R5 сложноэфирная группа карбоновой кислоты, а R1 и R2 имеют значения, указанные в п.1, подвергают кислотному или основному гидролизу, получая при этом соединения формулы II, где R3 группа СООН, и, при необходимости, полученный продукт переводят в соответствующую соль.
4. Фармацевтическая композиция, препятствующая фиксации ангиотензина II в крови к своим рецепторам, включающая активное начало и наполнители, отличающаяся тем, что в качестве активного начала она содержит эффективное количество производного 4-пиримидинона формул I, I' и I", в которых R1- линейная или разветвленная (С1-С7)-алкильная группа; R2 - линейная (С1-С7)-алкильная группа, фенил-(С1-С3)-алкил; R3 1Н-тетразол-5-ил.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| FR9102032A FR2672892B1 (fr) | 1991-02-20 | 1991-02-20 | Derives de 4-pyrimidinones, leur preparation et leur application en therapeutique. |
| FR9102032 | 1991-02-20 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| RU2073675C1 true RU2073675C1 (ru) | 1997-02-20 |
Family
ID=9409925
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| SU925010817A RU2073675C1 (ru) | 1991-02-20 | 1992-02-19 | Производные 4-пиримидинонов или их органические или минеральные фармацевтические соли, способ их получения и фармацевтическая композиция на их основе |
Country Status (23)
| Country | Link |
|---|---|
| EP (1) | EP0500409B1 (ru) |
| JP (1) | JP2529798B2 (ru) |
| KR (1) | KR920016434A (ru) |
| CN (1) | CN1034171C (ru) |
| AT (1) | ATE135695T1 (ru) |
| AU (1) | AU650319B2 (ru) |
| CA (1) | CA2061456A1 (ru) |
| CS (1) | CS49092A3 (ru) |
| DE (1) | DE69209113T2 (ru) |
| DK (1) | DK0500409T3 (ru) |
| ES (1) | ES2086090T3 (ru) |
| FI (1) | FI920720A (ru) |
| FR (1) | FR2672892B1 (ru) |
| GR (1) | GR3019404T3 (ru) |
| HU (2) | HUT60477A (ru) |
| IE (1) | IE76145B1 (ru) |
| IL (1) | IL101014A (ru) |
| MX (1) | MX9200690A (ru) |
| NO (1) | NO920648L (ru) |
| NZ (1) | NZ241659A (ru) |
| PL (1) | PL168617B1 (ru) |
| RU (1) | RU2073675C1 (ru) |
| ZA (1) | ZA921203B (ru) |
Families Citing this family (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| IL102183A (en) * | 1991-06-27 | 1999-11-30 | Takeda Chemical Industries Ltd | The heterocyclic compounds are converted into biphenyl groups, their production and the pharmaceutical compositions containing them |
| FR2700543B1 (fr) * | 1993-01-15 | 1995-03-17 | Synthelabo | Sels de dérivés de 4-pyrimidinone, leur préparation et leur application en thérapeutique. |
| SE9903028D0 (sv) | 1999-08-27 | 1999-08-27 | Astra Ab | New use |
| US8969514B2 (en) | 2007-06-04 | 2015-03-03 | Synergy Pharmaceuticals, Inc. | Agonists of guanylate cyclase useful for the treatment of hypercholesterolemia, atherosclerosis, coronary heart disease, gallstone, obesity and other cardiovascular diseases |
| EA020466B1 (ru) | 2007-06-04 | 2014-11-28 | Синерджи Фармасьютикалз Инк. | Агонисты гуанилатциклазы, пригодные для лечения желудочно-кишечных нарушений, воспаления, рака и других заболеваний |
| EP2810951B1 (en) | 2008-06-04 | 2017-03-15 | Synergy Pharmaceuticals Inc. | Agonists of guanylate cyclase useful for the treatment of gastrointestinal disorders, inflammation, cancer and other disorders |
| ES2624828T3 (es) | 2008-07-16 | 2017-07-17 | Synergy Pharmaceuticals Inc. | Agonistas de la guanilato ciclasa útiles para el tratamiento de trastornos gastrointestinales, inflamación, cáncer y otros |
| MA33071B1 (fr) * | 2009-01-30 | 2012-02-01 | Takeda Pharmaceutical | Compose a noyau condenses et son utilisation |
| US9616097B2 (en) | 2010-09-15 | 2017-04-11 | Synergy Pharmaceuticals, Inc. | Formulations of guanylate cyclase C agonists and methods of use |
| CA2905438A1 (en) | 2013-03-15 | 2014-09-25 | Synergy Pharmaceuticals Inc. | Agonists of guanylate cyclase and their uses |
| CA2905435A1 (en) | 2013-03-15 | 2014-09-25 | Synergy Pharmaceuticals Inc. | Compositions useful for the treatment of gastrointestinal disorders |
| PT3004138T (pt) | 2013-06-05 | 2024-06-18 | Bausch Health Ireland Ltd | Agonistas ultrapuros de guanilato ciclase c, método de produção e utilização dos mesmos |
Family Cites Families (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA1334092C (en) * | 1986-07-11 | 1995-01-24 | David John Carini | Angiotensin ii receptor blocking imidazoles |
| US5064825A (en) * | 1989-06-01 | 1991-11-12 | Merck & Co., Inc. | Angiotensin ii antagonists |
| RU2099330C1 (ru) * | 1989-06-30 | 1997-12-20 | Е.И.Дюпон Де Немур Энд Компани | Замещенные имидазолы или их фармацевтически приемлемые соли и фармацевтическая композиция |
| EP0407342A3 (en) * | 1989-07-06 | 1991-07-10 | Ciba-Geigy Ag | Pyrimidine derivatives |
| EP0424317A3 (en) * | 1989-10-19 | 1991-09-25 | Ciba-Geigy Ag | Pyrimidines |
| EP0435827A3 (en) * | 1989-12-28 | 1991-11-13 | Ciba-Geigy Ag | Diaza compounds |
| JPH05505609A (ja) * | 1990-03-30 | 1993-08-19 | メルク・エンド・カムパニー・インコーポレーテツド | 置換ピリミジン、ピリミジノンおよびピリドリミジン |
| IE912114A1 (en) * | 1990-07-02 | 1992-01-15 | Union Pharma Scient Appl | Novel pyrimidine derivatives which are angiotensin ii¹receptor antagonists, their methods of preparation and¹pharmaceutical compositions in which they are present |
-
1991
- 1991-02-20 FR FR9102032A patent/FR2672892B1/fr not_active Expired - Fee Related
-
1992
- 1992-02-03 DE DE69209113T patent/DE69209113T2/de not_active Expired - Fee Related
- 1992-02-03 AT AT92400269T patent/ATE135695T1/de not_active IP Right Cessation
- 1992-02-03 EP EP92400269A patent/EP0500409B1/fr not_active Expired - Lifetime
- 1992-02-03 DK DK92400269.4T patent/DK0500409T3/da active
- 1992-02-03 ES ES92400269T patent/ES2086090T3/es not_active Expired - Lifetime
- 1992-02-19 AU AU11059/92A patent/AU650319B2/en not_active Ceased
- 1992-02-19 HU HU9200532A patent/HUT60477A/hu unknown
- 1992-02-19 NO NO92920648A patent/NO920648L/no unknown
- 1992-02-19 CN CN92101114A patent/CN1034171C/zh not_active Expired - Fee Related
- 1992-02-19 ZA ZA921203A patent/ZA921203B/xx unknown
- 1992-02-19 MX MX9200690A patent/MX9200690A/es not_active IP Right Cessation
- 1992-02-19 RU SU925010817A patent/RU2073675C1/ru active
- 1992-02-19 CA CA002061456A patent/CA2061456A1/en not_active Abandoned
- 1992-02-19 KR KR1019920002504A patent/KR920016434A/ko not_active Application Discontinuation
- 1992-02-19 IL IL10101492A patent/IL101014A/en not_active IP Right Cessation
- 1992-02-19 CS CS92490A patent/CS49092A3/cs unknown
- 1992-02-19 NZ NZ241659A patent/NZ241659A/xx unknown
- 1992-02-19 FI FI920720A patent/FI920720A/fi unknown
- 1992-02-19 IE IE920525A patent/IE76145B1/en not_active IP Right Cessation
- 1992-02-19 JP JP4031862A patent/JP2529798B2/ja not_active Expired - Lifetime
- 1992-02-19 PL PL92293531A patent/PL168617B1/pl unknown
-
1995
- 1995-06-29 HU HU95P/P00554P patent/HU211886A9/hu unknown
-
1996
- 1996-03-21 GR GR960400758T patent/GR3019404T3/el unknown
Non-Patent Citations (1)
| Title |
|---|
| Патент ФРГ N 2654095, кл. С О7 D 239/32, 1977. Европейский патент N 0153746, кл. С 07 D 239/34, 1985. Патент США N 4046889, кл. С 07 D 205/08, 1977. * |
Also Published As
| Publication number | Publication date |
|---|---|
| CN1034171C (zh) | 1997-03-05 |
| PL168617B1 (pl) | 1996-03-29 |
| HU211886A9 (en) | 1995-12-28 |
| EP0500409B1 (fr) | 1996-03-20 |
| IE920525A1 (en) | 1992-08-26 |
| FI920720A (fi) | 1992-08-21 |
| CS49092A3 (en) | 1992-09-16 |
| FI920720A0 (fi) | 1992-02-19 |
| FR2672892B1 (fr) | 1994-01-14 |
| CA2061456A1 (en) | 1992-08-21 |
| DE69209113T2 (de) | 1996-10-31 |
| ATE135695T1 (de) | 1996-04-15 |
| CN1064269A (zh) | 1992-09-09 |
| ES2086090T3 (es) | 1996-06-16 |
| NO920648L (no) | 1992-08-21 |
| JP2529798B2 (ja) | 1996-09-04 |
| GR3019404T3 (en) | 1996-06-30 |
| DE69209113D1 (de) | 1996-04-25 |
| KR920016434A (ko) | 1992-09-24 |
| HU9200532D0 (en) | 1992-05-28 |
| NO920648D0 (no) | 1992-02-19 |
| AU650319B2 (en) | 1994-06-16 |
| PL293531A1 (en) | 1992-08-24 |
| IE76145B1 (en) | 1997-10-08 |
| HUT60477A (en) | 1992-09-28 |
| MX9200690A (es) | 1992-08-01 |
| IL101014A (en) | 1996-06-18 |
| ZA921203B (en) | 1992-11-25 |
| EP0500409A1 (fr) | 1992-08-26 |
| NZ241659A (en) | 1993-03-26 |
| AU1105992A (en) | 1992-08-27 |
| FR2672892A1 (fr) | 1992-08-21 |
| IL101014A0 (en) | 1992-11-15 |
| JPH04346980A (ja) | 1992-12-02 |
| DK0500409T3 (da) | 1996-07-15 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| FI112217B (fi) | Menetelmä terapeuttisesti käyttökelpoisten N-(4-pyrimidinyyli)bentseenisulfonamidijohdannaisten valmistamiseksi | |
| RU2073675C1 (ru) | Производные 4-пиримидинонов или их органические или минеральные фармацевтические соли, способ их получения и фармацевтическая композиция на их основе | |
| BR112021010871A2 (pt) | Composto agonista do receptor thrb e método de preparação e uso do mesmo | |
| US4879301A (en) | Antiallergic and antiinflammatory benzothiazolinone derivatives | |
| PT95929A (pt) | Processo para a prparacao de derivados de diazina e de composicoes farmaceuticas que os contem | |
| EP0443568A1 (en) | Fused thiophene derivatives, their production and use | |
| CS9100906A2 (en) | Substituted azoles, method of their production, preparations that contain these compounds and their application | |
| EP3144303B1 (en) | 6-substituted phenoxychroman carboxylic acid derivatives | |
| EP0610439A1 (en) | Pyrimidocycloalkanes as angiotensin ii antagonists | |
| JPH05239053A (ja) | キノリン誘導体ならびにその製造方法および治療への応用 | |
| FR2684672A1 (fr) | Derives de pyrimidine, utiles pour le traitement d'etats tels que l'hypertension et l'insuffisance cardiaque, et procede pour leur preparation. | |
| JPH09511238A (ja) | α−拮抗活性を有するキナゾリニル−アミノ誘導体 | |
| US5284661A (en) | Fused thiophene derivatives, their production and use | |
| US5294633A (en) | Imidazolyl-propenoic acid derivatives | |
| HU187337B (en) | Process for producing sbstituted oxo-carboxylic acids and pharmaceutical compositions containing them | |
| US5472967A (en) | 4-pyrimidinone derivatives their preparation and their application in therapy | |
| FR2527608A1 (fr) | Nouveaux composes heterocycliques, leur preparation et leur utilisation comme medicaments | |
| PL184060B1 (pl) | Podstawione związki fenylowe do zastosowania jako środki antagonistyczne endoteliny | |
| EP0686631B1 (en) | Pyrimidine derivatives and pharmaceutical compositions | |
| PL129612B1 (en) | Process for preparing novel derivatives of 2,3,6,7-tetrahydrothiazole/3,2-a/pirymidin-5-one | |
| US5457112A (en) | 3-(6-quinolylmethyl)-4H-imidazol-4-one derivatives, their preparation and their application in therapy | |
| US6303608B1 (en) | 2-{4-[4-(4,5-dichloro-2-methylimidazol-1-yl)butyl]-1-piperazinyl}-5-fluoropyrimidine, its preparation and its therapeutic use | |
| JPS59219268A (ja) | ウラシル誘導体 | |
| JP3059572B2 (ja) | ピロロ[3,2−e]ピラゾロ[1,5−a]ピリミジン誘導体及びこれを有効成分とする高血圧治療剤 | |
| JP2514812B2 (ja) | 3−(1H−テトラゾ−ル−5− イル) チエノ〔2,3−d〕 ピリミジン−4(3H)−オン類 |