RU2012156420A - Левовращающие изовалерил-спирамицины 1, ii, iii, их препараты, способ приготовления и употребление - Google Patents
Левовращающие изовалерил-спирамицины 1, ii, iii, их препараты, способ приготовления и употребление Download PDFInfo
- Publication number
- RU2012156420A RU2012156420A RU2012156420/04A RU2012156420A RU2012156420A RU 2012156420 A RU2012156420 A RU 2012156420A RU 2012156420/04 A RU2012156420/04 A RU 2012156420/04A RU 2012156420 A RU2012156420 A RU 2012156420A RU 2012156420 A RU2012156420 A RU 2012156420A
- Authority
- RU
- Russia
- Prior art keywords
- levoisovalerylspiramycin
- iii
- weight
- preparation
- compound
- Prior art date
Links
- 238000000034 method Methods 0.000 title claims 13
- 238000002360 preparation method Methods 0.000 title claims 13
- 239000004187 Spiramycin Substances 0.000 title claims 3
- 150000001875 compounds Chemical class 0.000 claims abstract 19
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 claims abstract 12
- 238000002844 melting Methods 0.000 claims abstract 6
- 230000008018 melting Effects 0.000 claims abstract 6
- 230000003287 optical effect Effects 0.000 claims abstract 6
- 239000002904 solvent Substances 0.000 claims abstract 6
- 239000000126 substance Substances 0.000 claims abstract 6
- 229910002483 Cu Ka Inorganic materials 0.000 claims abstract 4
- 238000000634 powder X-ray diffraction Methods 0.000 claims abstract 4
- 230000005855 radiation Effects 0.000 claims abstract 4
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 claims 18
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 claims 12
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 claims 10
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims 10
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 claims 9
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 claims 9
- 239000012153 distilled water Substances 0.000 claims 7
- 238000000855 fermentation Methods 0.000 claims 7
- 230000004151 fermentation Effects 0.000 claims 7
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 claims 6
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 claims 6
- WNLRTRBMVRJNCN-UHFFFAOYSA-N adipic acid Chemical compound OC(=O)CCCCC(O)=O WNLRTRBMVRJNCN-UHFFFAOYSA-N 0.000 claims 6
- 238000001816 cooling Methods 0.000 claims 6
- 239000003814 drug Substances 0.000 claims 6
- 229940079593 drug Drugs 0.000 claims 6
- 239000007924 injection Substances 0.000 claims 6
- 238000002347 injection Methods 0.000 claims 6
- 239000000546 pharmaceutical excipient Substances 0.000 claims 6
- 150000003839 salts Chemical class 0.000 claims 6
- 238000003756 stirring Methods 0.000 claims 6
- 241000606125 Bacteroides Species 0.000 claims 5
- 239000000843 powder Substances 0.000 claims 5
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 claims 4
- 241000588724 Escherichia coli Species 0.000 claims 4
- 238000000605 extraction Methods 0.000 claims 4
- 239000012046 mixed solvent Substances 0.000 claims 4
- DKPFZGUDAPQIHT-UHFFFAOYSA-N Butyl acetate Natural products CCCCOC(C)=O DKPFZGUDAPQIHT-UHFFFAOYSA-N 0.000 claims 3
- OFOBLEOULBTSOW-UHFFFAOYSA-N Propanedioic acid Natural products OC(=O)CC(O)=O OFOBLEOULBTSOW-UHFFFAOYSA-N 0.000 claims 3
- 229920002472 Starch Polymers 0.000 claims 3
- 239000001361 adipic acid Substances 0.000 claims 3
- 235000011037 adipic acid Nutrition 0.000 claims 3
- 238000012258 culturing Methods 0.000 claims 3
- 238000001704 evaporation Methods 0.000 claims 3
- 230000008020 evaporation Effects 0.000 claims 3
- 239000000284 extract Substances 0.000 claims 3
- 239000000706 filtrate Substances 0.000 claims 3
- FUZZWVXGSFPDMH-UHFFFAOYSA-N hexanoic acid Chemical compound CCCCCC(O)=O FUZZWVXGSFPDMH-UHFFFAOYSA-N 0.000 claims 3
- 239000008176 lyophilized powder Substances 0.000 claims 3
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 claims 3
- 239000011976 maleic acid Substances 0.000 claims 3
- 239000011259 mixed solution Substances 0.000 claims 3
- 239000000203 mixture Substances 0.000 claims 3
- 239000011780 sodium chloride Substances 0.000 claims 3
- 239000007787 solid Substances 0.000 claims 3
- 239000000243 solution Substances 0.000 claims 3
- 230000000087 stabilizing effect Effects 0.000 claims 3
- 239000008107 starch Substances 0.000 claims 3
- 235000019698 starch Nutrition 0.000 claims 3
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 claims 3
- ACTOXUHEUCPTEW-BWHGAVFKSA-N 2-[(4r,5s,6s,7r,9r,10r,11e,13e,16r)-6-[(2s,3r,4r,5s,6r)-5-[(2s,4r,5s,6s)-4,5-dihydroxy-4,6-dimethyloxan-2-yl]oxy-4-(dimethylamino)-3-hydroxy-6-methyloxan-2-yl]oxy-10-[(2s,5s,6r)-5-(dimethylamino)-6-methyloxan-2-yl]oxy-4-hydroxy-5-methoxy-9,16-dimethyl-2-o Chemical compound O([C@H]1/C=C/C=C/C[C@@H](C)OC(=O)C[C@@H](O)[C@@H]([C@H]([C@@H](CC=O)C[C@H]1C)O[C@H]1[C@@H]([C@H]([C@H](O[C@@H]2O[C@@H](C)[C@H](O)[C@](C)(O)C2)[C@@H](C)O1)N(C)C)O)OC)[C@@H]1CC[C@H](N(C)C)[C@@H](C)O1 ACTOXUHEUCPTEW-BWHGAVFKSA-N 0.000 claims 2
- 229920001817 Agar Polymers 0.000 claims 2
- USFZMSVCRYTOJT-UHFFFAOYSA-N Ammonium acetate Chemical compound N.CC(O)=O USFZMSVCRYTOJT-UHFFFAOYSA-N 0.000 claims 2
- 239000005695 Ammonium acetate Substances 0.000 claims 2
- 241000304886 Bacilli Species 0.000 claims 2
- 241000894006 Bacteria Species 0.000 claims 2
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 claims 2
- 241000607768 Shigella Species 0.000 claims 2
- 108090000992 Transferases Proteins 0.000 claims 2
- 239000008272 agar Substances 0.000 claims 2
- 229940043376 ammonium acetate Drugs 0.000 claims 2
- 235000019257 ammonium acetate Nutrition 0.000 claims 2
- 238000001914 filtration Methods 0.000 claims 2
- 235000013312 flour Nutrition 0.000 claims 2
- 239000012530 fluid Substances 0.000 claims 2
- 230000002538 fungal effect Effects 0.000 claims 2
- 239000008103 glucose Substances 0.000 claims 2
- 239000007788 liquid Substances 0.000 claims 2
- 230000014759 maintenance of location Effects 0.000 claims 2
- 239000003208 petroleum Substances 0.000 claims 2
- 238000000746 purification Methods 0.000 claims 2
- 229960001294 spiramycin Drugs 0.000 claims 2
- 229930191512 spiramycin Natural products 0.000 claims 2
- 235000019372 spiramycin Nutrition 0.000 claims 2
- 241000251468 Actinopterygii Species 0.000 claims 1
- 241000186000 Bifidobacterium Species 0.000 claims 1
- 208000035473 Communicable disease Diseases 0.000 claims 1
- 235000019733 Fish meal Nutrition 0.000 claims 1
- 241000589244 Fluoribacter bozemanae Species 0.000 claims 1
- 241000589282 Fluoribacter dumoffii Species 0.000 claims 1
- 241000589278 Fluoribacter gormanii Species 0.000 claims 1
- 241000605909 Fusobacterium Species 0.000 claims 1
- 235000010469 Glycine max Nutrition 0.000 claims 1
- 241000186660 Lactobacillus Species 0.000 claims 1
- 241000589248 Legionella Species 0.000 claims 1
- 241000589276 Legionella jordanis Species 0.000 claims 1
- 241000589242 Legionella pneumophila Species 0.000 claims 1
- 208000007764 Legionnaires' Disease Diseases 0.000 claims 1
- 241000108664 Nitrobacteria Species 0.000 claims 1
- 241001523956 Parengyodontium album Species 0.000 claims 1
- 206010035664 Pneumonia Diseases 0.000 claims 1
- 241000605861 Prevotella Species 0.000 claims 1
- 241000208474 Protea Species 0.000 claims 1
- 241000589517 Pseudomonas aeruginosa Species 0.000 claims 1
- 240000004808 Saccharomyces cerevisiae Species 0.000 claims 1
- 235000019764 Soybean Meal Nutrition 0.000 claims 1
- 241000295644 Staphylococcaceae Species 0.000 claims 1
- 241000191967 Staphylococcus aureus Species 0.000 claims 1
- 241001505901 Streptococcus sp. 'group A' Species 0.000 claims 1
- 241000589262 Tatlockia micdadei Species 0.000 claims 1
- 102000004357 Transferases Human genes 0.000 claims 1
- 208000037386 Typhoid Diseases 0.000 claims 1
- 239000000654 additive Substances 0.000 claims 1
- DIZPMCHEQGEION-UHFFFAOYSA-H aluminium sulfate (anhydrous) Chemical compound [Al+3].[Al+3].[O-]S([O-])(=O)=O.[O-]S([O-])(=O)=O.[O-]S([O-])(=O)=O DIZPMCHEQGEION-UHFFFAOYSA-H 0.000 claims 1
- 239000003242 anti bacterial agent Substances 0.000 claims 1
- 229940088710 antibiotic agent Drugs 0.000 claims 1
- 239000002518 antifoaming agent Substances 0.000 claims 1
- 239000006286 aqueous extract Substances 0.000 claims 1
- 238000004587 chromatography analysis Methods 0.000 claims 1
- 239000013078 crystal Substances 0.000 claims 1
- 238000010586 diagram Methods 0.000 claims 1
- 238000001035 drying Methods 0.000 claims 1
- 230000008030 elimination Effects 0.000 claims 1
- 238000003379 elimination reaction Methods 0.000 claims 1
- 238000010828 elution Methods 0.000 claims 1
- 230000000369 enteropathogenic effect Effects 0.000 claims 1
- 230000000688 enterotoxigenic effect Effects 0.000 claims 1
- 239000004467 fishmeal Substances 0.000 claims 1
- 239000011521 glass Substances 0.000 claims 1
- 206010022000 influenza Diseases 0.000 claims 1
- 238000011081 inoculation Methods 0.000 claims 1
- 229940115932 legionella pneumophila Drugs 0.000 claims 1
- 238000005259 measurement Methods 0.000 claims 1
- 235000001954 papillon Nutrition 0.000 claims 1
- 244000229285 papillon Species 0.000 claims 1
- 235000011837 pasties Nutrition 0.000 claims 1
- 238000007747 plating Methods 0.000 claims 1
- 230000001376 precipitating effect Effects 0.000 claims 1
- 238000002953 preparative HPLC Methods 0.000 claims 1
- 230000002265 prevention Effects 0.000 claims 1
- 239000000047 product Substances 0.000 claims 1
- 108090000623 proteins and genes Proteins 0.000 claims 1
- 238000002390 rotary evaporation Methods 0.000 claims 1
- 238000010187 selection method Methods 0.000 claims 1
- 238000009331 sowing Methods 0.000 claims 1
- 239000004455 soybean meal Substances 0.000 claims 1
- 235000012424 soybean oil Nutrition 0.000 claims 1
- 239000003549 soybean oil Substances 0.000 claims 1
- 201000008297 typhoid fever Diseases 0.000 claims 1
- 238000000825 ultraviolet detection Methods 0.000 claims 1
- 238000002211 ultraviolet spectrum Methods 0.000 claims 1
- 238000005406 washing Methods 0.000 claims 1
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/04—Antibacterial agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/10—Antimycotics
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N9/00—Enzymes; Proenzymes; Compositions thereof; Processes for preparing, activating, inhibiting, separating or purifying enzymes
- C12N9/10—Transferases (2.)
- C12N9/1025—Acyltransferases (2.3)
- C12N9/1029—Acyltransferases (2.3) transferring groups other than amino-acyl groups (2.3.1)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P19/00—Preparation of compounds containing saccharide radicals
- C12P19/44—Preparation of O-glycosides, e.g. glucosides
- C12P19/60—Preparation of O-glycosides, e.g. glucosides having an oxygen of the saccharide radical directly bound to a non-saccharide heterocyclic ring or a condensed ring system containing a non-saccharide heterocyclic ring, e.g. coumermycin, novobiocin
- C12P19/62—Preparation of O-glycosides, e.g. glucosides having an oxygen of the saccharide radical directly bound to a non-saccharide heterocyclic ring or a condensed ring system containing a non-saccharide heterocyclic ring, e.g. coumermycin, novobiocin the hetero ring having eight or more ring members and only oxygen as ring hetero atoms, e.g. erythromycin, spiramycin, nystatin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7042—Compounds having saccharide radicals and heterocyclic rings
- A61K31/7048—Compounds having saccharide radicals and heterocyclic rings having oxygen as a ring hetero atom, e.g. leucoglucosan, hesperidin, erythromycin, nystatin, digitoxin or digoxin
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07H—SUGARS; DERIVATIVES THEREOF; NUCLEOSIDES; NUCLEOTIDES; NUCLEIC ACIDS
- C07H17/00—Compounds containing heterocyclic radicals directly attached to hetero atoms of saccharide radicals
- C07H17/04—Heterocyclic radicals containing only oxygen as ring hetero atoms
- C07H17/08—Hetero rings containing eight or more ring members, e.g. erythromycins
Landscapes
- Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- Organic Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- General Health & Medical Sciences (AREA)
- Genetics & Genomics (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- Biotechnology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Biochemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Medicinal Chemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Microbiology (AREA)
- General Engineering & Computer Science (AREA)
- Molecular Biology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Oncology (AREA)
- Communicable Diseases (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Biomedical Technology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicinal Preparation (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
- Saccharide Compounds (AREA)
Abstract
1. Левоизовалерилспирамицин, представляющий соединение левоизовалерилспирамицина I, II или III, отличающийся тем, что химическая структурная формула соединения левоизовалерилспирамицина I показана формулой (I), при условии применения хлороформа в качестве растворителя температуры 25°C и концентрации 0,02 г/мл, угол оптического вращения [α]составляет -49°~-62°, предпочтительно -51°~-60°, предпочтительно -60°~-62°, предпочтительно -51°~-58°, предпочтительно -53°~-58°, предпочтительно -55°~-58°, предпочтительно -55°~-57°, предпочтительно -58°~-60°, предпочтительно -51°~-55°, предпочтительно -53°~-55°, предпочтительно -49°~-51°; и температура плавления составляет 116~122°C, предпочтительно 118~~120°C;соединение левоизовалерилспирамицина II, отличающееся тем, что его химическая структурная формула показана формулой (II), при условии применения хлороформа в качестве растворителя, температуры 25°C и концентрации 0,02 г/мл, угол оптического вращения [α]составляет -55°~-61°, предпочтительно -57°~-59°; и температура плавления составляет 120°C~128°C, предпочтительно 123°C~125°C;соединение левоизовалерилспирамицина III, отличающееся тем, что его химическая структурная формула показана формулой (III), при условии применения хлороформа в качестве растворителя, температуры 25°C и концентрации 0,02 г/мл угол оптического вращения [α]составляет -49°~-51°; и температура плавления составляет 116°C~118°C;;;.2. Левоизовалерилспирамицин по п.1, отличающийся тем, что левоизовалерилспирамицин I представляет кристаллическое соединение, дифракция рентгеновских лучей на порошке которого, измеренная с применением излучения Cu-Ka, имеет характерные пики при 2θ=7,6°, 8,0°, 10,0°, 11,4°, 16,4°, 17,0°, 17,5°, 17,9°, 19,5°, 22,7°, 23,7° и 24,4°;ле�
Claims (15)
1. Левоизовалерилспирамицин, представляющий соединение левоизовалерилспирамицина I, II или III, отличающийся тем, что химическая структурная формула соединения левоизовалерилспирамицина I показана формулой (I), при условии применения хлороформа в качестве растворителя температуры 25°C и концентрации 0,02 г/мл, угол оптического вращения [α]D составляет -49°~-62°, предпочтительно -51°~-60°, предпочтительно -60°~-62°, предпочтительно -51°~-58°, предпочтительно -53°~-58°, предпочтительно -55°~-58°, предпочтительно -55°~-57°, предпочтительно -58°~-60°, предпочтительно -51°~-55°, предпочтительно -53°~-55°, предпочтительно -49°~-51°; и температура плавления составляет 116~122°C, предпочтительно 118~~120°C;
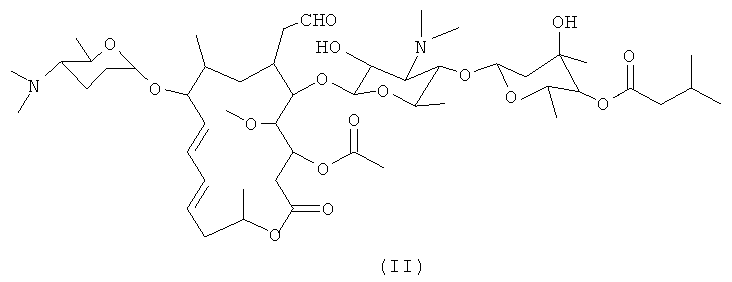
соединение левоизовалерилспирамицина II, отличающееся тем, что его химическая структурная формула показана формулой (II), при условии применения хлороформа в качестве растворителя, температуры 25°C и концентрации 0,02 г/мл, угол оптического вращения [α]D составляет -55°~-61°, предпочтительно -57°~-59°; и температура плавления составляет 120°C~128°C, предпочтительно 123°C~125°C;
соединение левоизовалерилспирамицина III, отличающееся тем, что его химическая структурная формула показана формулой (III), при условии применения хлороформа в качестве растворителя, температуры 25°C и концентрации 0,02 г/мл угол оптического вращения [α]D составляет -49°~-51°; и температура плавления составляет 116°C~118°C;
2. Левоизовалерилспирамицин по п.1, отличающийся тем, что левоизовалерилспирамицин I представляет кристаллическое соединение, дифракция рентгеновских лучей на порошке которого, измеренная с применением излучения Cu-Ka, имеет характерные пики при 2θ=7,6°, 8,0°, 10,0°, 11,4°, 16,4°, 17,0°, 17,5°, 17,9°, 19,5°, 22,7°, 23,7° и 24,4°;
левоизовалерилспирамицин II представляет кристаллическое соединение, дифракция рентгеновских лучей на порошке которого, измеренная с применением излучения Cu-Ka, имеет характерные пики при 2θ=10,0°, 11,6°, 16,4°, 17,3°, 19,1°, 21,2°, 22,1°, 22,7°, 26,4°, 26,9°, 27,5° и 31,5°; объемное соотношение абсолютизированного метанола, безводного ацетона и абсолютного этилового спирта в смешанном растворителе составляет 1:0,1~10:0,5~1, предпочтительно 1:2~8:0,8~1;
левоизовалерилспирамицин III представляет кристаллическое соединение, дифракция рентгеновских лучей на порошке которого, измеренная с применением излучения Cu-Ka, имеет характерные пики при 2θ=8,0°, 10,0°, 11,2°, 11,7°, 16,4°, 19,1°, 19,6°, 20,0°, 21,4°, 22,9°, 23,6° и 29,4°.
3. Препарат по любому из пп.1-2, отличающийся тем, что:
препарат содержит левоизовалерилспирамицин I, фармацевтическую соль левоизовалерилспирамицина I, левоизовалерилспирамицин I и фармацевтически приемлемое вспомогательное вещество или фармацевтическую соль левоизовалерилспирамицина I и фармацевтически приемлемое вспомогательное вещество, чистота
левоизовалерилспирамицина I превышает 90% по массе, предпочтительно более 95% по массе и более предпочтительно превышает 98% по массе; или
препарат содержит левоизовалерилспирамицин II, фармацевтическую соль левоизовалерилспирамицина II, левоизовалерилспирамицин II и фармацевтически приемлемое вспомогательное вещество или фармацевтическую соль левоизовалерилспирамицина II и фармацевтически приемлемое вспомогательное вещество, чистота левоизовалерилспирамицина II превышает 90% по массе, предпочтительно более 95% по массе и более предпочтительно превышает 98% по массе; или
препарат содержит левоизовалерилспирамицин III, фармацевтическую соль левоизовалерилспирамицина III, левоизовалерилспирамицин III и фармацевтически приемлемое вспомогательное вещество или фармацевтическую соль левоизовалерилспирамицина III и фармацевтически приемлемое вспомогательное вещество, чистота левоизовалерилспирамицина III превышает 90% по массе, предпочтительно более 95% по массе и более предпочтительно превышает 98% по массе.
4. Препарат по п.3, отличающийся тем, что препарат содержит следующую стандартную дозу: содержание левоизовалерилспирамицина I, II или III соответственно 10~1500 мг, предпочтительно 50~1000 мг и более предпочтительно 100~500 мг.
5. Препарат по п.3, отличающийся тем, что массовая доля левоизовалерилспирамицина I, II или III соответственно составляет 10~95%, предпочтительно 50~95% и более предпочтительно 75~95%.
6. Препарат по п.3, отличающийся тем, что препарат включает раствор для инъекций, порошок для инъекций или лиофилизированный порошок, содержащий левоизовалерилспирамицин I и, по крайней мере, одно из следующего: лимонная кислота, адипиновая кислота, малеиновая кислота; раствор для инъекций, порошок для инъекций или лиофилизированный порошок, содержащий левоизовалерилспирамицин II и, по крайней мере, одно из следующего: лимонная кислота, адипиновая кислота, малеиновая кислота; раствор для инъекций, порошок для инъекций или лиофилизированный порошок, содержащий, по крайней мере, левоизовалерилспирамицин III и, по крайней мере, одно из следующего: лимонная кислота, адипиновая кислота, малеиновая кислота.
7. Способ приготовления левоизовалерилспирамицина по п.1, отличающийся тем, что способ включает: приготовление левокарримицина и очищение левоизовалерилспирамицина I, II или III, отличающийся тем, что процесс приготовления левокарримицина включает: культивирование и биологическое ферментирование клонированных грибковых штаммов WSP-195, осуществляемое с применением спирамицин-содержащего гена 4″-изовалерилтрансферазы и экстрагирование ферментационной жидкости;
ферментация осуществляется в условиях pH 6,0~9,0, предпочтительно 6,0~8,0 и более предпочтительно 6,0~7,5, кривые изменения pH со временем показывают три непрерывные фазы, отличающиеся тем, что первая фаза удовлетворяет формуле y1=k1x1+6,0, где 0,0227≤k1≤0,1364, 0≤x1≤22; вторая фаза удовлетворяет формуле y2=k2x2+b2, где -0,0735≤k2<0, 6,5<b2≤10,62, 22≤x2≤56; и третья фаза удовлетворяет формуле y3=k3x3+b3, где 0<k3≤0,0078, 6,06≤b3<6,5, 56≤x3≤120.
8. Способ по п.7, отличающийся тем, что: процесс культивирования способа приготовления левокарримицина заключается в культивировании клонированных грибковых штаммов WSP-195, осуществляемом с применением спирамицин-содержащего гена 4″-изовалерилтрансферазы на поверхности среды скошенного агара, содержащей 2% муки соевого жмыха, 1% глюкозы, 3% крахмала, 0,5% CaCO3, 0,4% NaCl и 2% агара в течение 8~15 суток при pH 6,5~7,5 и температуре 28~38°C, последующем посеве на поверхность среды для посева, содержащей 1,5% муки соевого жмыха, 3,0% крахмала, 0,4% NaCl, 0,5% CaCO3, 0,3% рыбного пептона и 0,05% KH2PO4 и культивировании в течение 40~80 часов при pH 6,5~7,5 и температуре 25~30°C, введении в среду ферментации, содержащей 0,5% глюкозы, 6,0% крахмала, 0,5% сухих дрожжей, 2,0% рыбной муки, 0,6% NH4NO3, 1,0% NaCl, 0,5% CaCO3, 0,05% KH2PO4, 0,1% MgSO4, 0,5% соевого масла и 0,02% противовспенивающей добавки и культивировании в течение 72-120 часов при 26-30°C, 0,1-20% количества посева для получения ферментационной жидкости.
9. Способ по п.7, отличающийся тем, что: этап экстрагирования биологической ферментационной жидкости включает: обработку ферментационной жидкости сульфатом алюминия для получения фильтрата, стабилизирование pH фильтрата на уровне 8,5~9,0, применение бутилацетата для экстрагирования, очищение экстракта бутилацетата несоленой водой и раствором 1% NaH2PO4, затем применение воды с pH 2,0~2,5 для экстрагирования с получением водосодержащего экстракта, стабилизирование pH на уровне 4,5~5,5, испарение и устранение остаточного бутилацетата для получения водного экстракта, фильтрацию и стабилизирование pH на уровне 8,5~9,0, осаждение фильтрата и промывание дистиллированной водой для получения влажного продукта и его сушку для получения левокарримицина.
10. Способ по п.7, отличающийся тем, что: этап очищения левоизовалерилспирамицина I, II или III включает: очищение пробы левокарримицина методом хроматографии, выполнение градиентного элюирования и выделение пиков мишеней компонентов левоизовалерилспирамицина I, II или III с применением хроматографической колонки ODS в буферном растворе ацетонитрила и ацетата аммония,
при очищении левоизовалерилспирамицина I, II или III регистрацию диаграммы УФ-спектра левоизовалерилспирамицина I, II или III с применением препаративной высокоэффективной жидкостной хроматографии и УФ-детектирования и отбор пробы левоизовалерилспирамицина I на основании времени удерживания в 44,759 мин, пробы левоизовалерилспирамицина II на основании времени удерживания в 43,34 мин и пробы левоизовалерилспирамицина III на основании времени удерживания в 48,009 мин.
11. Способ по п.10, отличающийся тем, что включает: при очищении левоизовалерилспирамицина I, II или III устранение ацетонитрила в собранном левоизовалерилспирамицине I, II или III, соответственно, с применением метода роторного испарения, затем применение этилацетата для экстрагирования, устранение этилацетата из экстракта путем испарения для получения пастообразной пробы; повторное растворение пробы с применением петролейного эфира, устранение петролейного эфира посредством испарения для получения соответственно белого порошка левоизовалерилспирамицина I, II или III.
12. Способ по п.10, отличающийся тем, что подвижная фаза представляет смешанный растворитель ацетонитрила A и 150 мМ раствора ацетата аммония с pH 8,5,
условия, необходимые для очищения левоизовалерилспирамицина I, II или III являются следующими: линейный градиент: 0~60 минут, A - 25%~65%; и 61~90 минут, A - 65%~90%;
скорость фильтрации: 260 мл/мин;
объем пробы: 10 мл;
концентрация пробы: 0,5 г/мл;
длина волны измерения: 231 нм;
способ отбора: отбор с применением УФ-триггера.
13. Способ по п.11, отличающийся тем, что белый порошок левоизовалерилспирамицина I, II или III образует кристалл, отличающийся тем, что способ для приготовления кристаллического соединения левоизовалерилспирамицина I включает: растворение твердого соединения левоизовалерилспирамицина I в смешанном растворе этилацетата, абсолютного этилового спирта и безводного ацетона, добавление дистиллированной воды при одновременном перемешивании смеси, охлаждение до 5°C~15°C после добавления дистиллированной воды, продолжение перемешивания при охлаждении, затем получение кристаллического соединения левоизовалерилспирамицина I, при этом объемное соотношение этилацетата, абсолютного этилового спирта и безводного ацетона в смешанном растворителе составляет 1:0,1~10:0,5~1, предпочтительно 1:2~8:0,8~1; или
- растворение твердого соединения левоизовалерилспирамицина II в смешанном растворе абсолютного метанола, абсолютного этилового спирта и безводного ацетона, добавление дистиллированной воды при одновременном перемешивании смеси, охлаждение до 5°C~15°C после добавления дистиллированной воды, продолжение перемешивания при охлаждении, затем получение кристаллического соединения левоизовалерилспирамицина II;
- растворение твердого соединения левоизовалерилспирамицина III в смешанном растворе абсолютного метанола, абсолютного этилового спирта и безводного ацетона, добавление дистиллированной воды при одновременном перемешивании смеси, охлаждение до 5°C~15°C после добавления дистиллированной воды, продолжение перемешивания при охлаждении, затем получение кристаллического соединения левоизовалерилспирамицина III, при этом объемное соотношение абсолютного метанола, абсолютного этилового спирта и безводного ацетона в смешанном растворителе составляет 1:0,1~10:0,5~1, предпочтительно, 1:2~8:0,8~1.
14. Применение левоизовалерилспирамицина по п.1 или препарата в соответствии с любым из п.п.2-5 для приготовления лекарственных средств для лечения и/или профилактики инфекционных заболеваний.
15. Применение левоизовалерилспирамицина в соответствии с п.1 или препарата в соответствии с любым из п.п.2~5 для приготовления лекарственных средств, относящихся к антибиотикам, воздействующим на бактерии, включая стрептококки пневмонии, стрептококки группы A, пиогенные стрептококки, энтерококки, золотистые стафилококки, эпидермальные стафилококки, катаральные кокки, гонококки, гриппозные бациллы, кишечные палочки, энтеротоксигенные кишечные палочки, энтеропатогенные кишечные палочки, энтероинвазивные кишечные палочки, синегнойные палочки, палочки Фридлиндера, вульгарный протей, брюшнотифозные палочки, ацинетобактерии, нитробактерии, серрации, шигеллы Зонне, шигеллы Флекснера, грибок Tritirachium album; легионеллы, такие как легионелла pneumophila, легионелла gormanii, легионелла bozemanii, легионелла dumoffii, легионелла jordanis и легионелла micdadei; анаэробы, такие как бактероиды фрагилис, бактероиды thetaiotaomicron, бактероиды vulgatus, бактероиды distasonis, бактероиды prevotella, превотелла asaccharolyticus, превотелла oralis, палочка Плаута, фузобактерии russell, бифидобактерии, лактобациллы, пептострептококки, пропионовые бактерии акне, клостридии перфрингенс и дрожжеподобные грибки.
Applications Claiming Priority (7)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN201010182108.9 | 2010-05-25 | ||
| CN201010182108 | 2010-05-25 | ||
| CN201010182111 | 2010-05-25 | ||
| CN201010182109.3 | 2010-05-25 | ||
| CN201010182109 | 2010-05-25 | ||
| CN201010182111.0 | 2010-05-25 | ||
| PCT/CN2011/074644 WO2011147313A1 (zh) | 2010-05-25 | 2011-05-25 | 左旋异戊酰螺旋霉素i、ii或iii,及其制剂、制备方法及应用 |
Related Child Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2016123980A Division RU2647237C1 (ru) | 2010-05-25 | 2011-05-25 | Левоизовалерилспирамицин iii, препараты, способ приготовления и употребления |
| RU2016123979A Division RU2647236C1 (ru) | 2010-05-25 | 2011-05-25 | Левоизовалерилспирамицин ii, препараты, способ приготовления и употребления |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU2012156420A true RU2012156420A (ru) | 2014-06-27 |
| RU2593498C2 RU2593498C2 (ru) | 2016-08-10 |
Family
ID=45003321
Family Applications (3)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2016123979A RU2647236C1 (ru) | 2010-05-25 | 2011-05-25 | Левоизовалерилспирамицин ii, препараты, способ приготовления и употребления |
| RU2012156420/04A RU2593498C2 (ru) | 2010-05-25 | 2011-05-25 | Левовращающие изовалерил-спирамицины 1, ii, iii, их препараты, способ приготовления и употребление |
| RU2016123980A RU2647237C1 (ru) | 2010-05-25 | 2011-05-25 | Левоизовалерилспирамицин iii, препараты, способ приготовления и употребления |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2016123979A RU2647236C1 (ru) | 2010-05-25 | 2011-05-25 | Левоизовалерилспирамицин ii, препараты, способ приготовления и употребления |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2016123980A RU2647237C1 (ru) | 2010-05-25 | 2011-05-25 | Левоизовалерилспирамицин iii, препараты, способ приготовления и употребления |
Country Status (15)
| Country | Link |
|---|---|
| US (1) | US8778896B2 (ru) |
| EP (3) | EP2578595B1 (ru) |
| JP (1) | JP5945868B2 (ru) |
| KR (2) | KR20130041829A (ru) |
| BR (1) | BR112012029913B1 (ru) |
| CA (3) | CA2800021C (ru) |
| DK (3) | DK3210991T3 (ru) |
| ES (3) | ES2754614T3 (ru) |
| MX (1) | MX340626B (ru) |
| MY (1) | MY164231A (ru) |
| PL (3) | PL2578595T3 (ru) |
| PT (1) | PT3210990T (ru) |
| RU (3) | RU2647236C1 (ru) |
| WO (1) | WO2011147313A1 (ru) |
| ZA (3) | ZA201209738B (ru) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2766176C2 (ru) * | 2017-07-04 | 2022-02-08 | Шенянг Фуянг Фармасьютекал Технолоджи Ко., Лтд. | Применение изовалерил-спирамицина i, ii и/или iii при изготовлении препарата для лечения и/или профилактики опухоли и получения лекарственного препарата |
Families Citing this family (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| ES2633737T3 (es) * | 2010-05-25 | 2017-09-25 | Shenyang Fuyang Pharmaceutical Technology Co., Ltd. | Levocarrimicina, composiciones farmacéuticas, procedimientos de preparación y utilizaciones de la misma |
| CN105497053B (zh) * | 2015-12-31 | 2018-02-13 | 沈阳福洋医药科技有限公司 | 可利霉素在抗结核分枝杆菌感染中的应用 |
| WO2019141254A1 (zh) * | 2018-01-19 | 2019-07-25 | 沈阳福洋医药科技有限公司 | 一种mTOR抑制剂、药物组合物及其应用 |
| CA3088823A1 (en) | 2018-01-19 | 2019-07-25 | Shenyang Fuyang Pharmaceutical Technology Co., Ltd. | Use of carrimycin or active ingredients thereof |
| CN110384710B (zh) * | 2018-04-17 | 2023-01-10 | 沈阳福洋医药科技有限公司 | 一种用于预防和/或治疗疼痛的药物、组合产品及其应用 |
| JP2021533144A (ja) * | 2018-04-17 | 2021-12-02 | 上海同聯製薬有限公司Shanghai Tonglian Pharmaceutical Co., Ltd. | 疼痛及び/又は発熱を予防及び/又は治療するための薬物、組成製品及びその応用 |
| US20220211735A1 (en) * | 2019-05-16 | 2022-07-07 | Shenyang Fuyang Pharmaceutical Technology Co., Ltd. | Medicament and combination product used for preventing, alleviating and/or treating fibrosis, and use thereof |
| CN112239483B (zh) * | 2019-07-18 | 2023-10-27 | 沈阳福洋医药科技有限公司 | 一种化合物及药物组合物 |
| US11351185B2 (en) | 2020-03-11 | 2022-06-07 | Asclea Corporation | Use of isovalerylspiramycins as anti-cancer agents to inhibit metastasis |
Family Cites Families (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS5334788A (en) * | 1976-09-11 | 1978-03-31 | Sanraku Inc | Antibiotics spiramycin derivatives |
| CN1058295C (zh) | 1997-06-03 | 2000-11-08 | 中国医学科学院医药生物技术研究所 | 一种利用基因工程技术制造生技霉素的方法 |
| CN1169947C (zh) * | 2002-11-19 | 2004-10-06 | 中国医学科学院医药生物技术研究所 | 必特螺旋霉素的基因工程菌株螺旋霉素链霉菌wsj-195 |
| CN1237976C (zh) * | 2003-12-23 | 2006-01-25 | 沈阳同联集团有限公司 | 必特螺旋霉素及其在抗感染性疾病中的应用 |
| WO2006018698A2 (en) * | 2004-08-12 | 2006-02-23 | Glaxosmithkline Istrazivacki Centar Zagreb D.O.O. | Use of cell-specific conjugates for treatment of inflammatory diseases of the gastrointestinal tract |
| CN101054553A (zh) * | 2007-04-09 | 2007-10-17 | 中国医学科学院医药生物技术研究所 | 异戊酰螺旋霉素i基因工程菌株的构建 |
| CN101649325B (zh) * | 2009-07-03 | 2011-09-07 | 中国医学科学院医药生物技术研究所 | 一种提高基因工程异戊酰螺旋霉素主组分含量的基因串连技术 |
| CN101773510B (zh) * | 2010-03-09 | 2013-06-05 | 沈阳同联集团有限公司 | 异戊酰螺旋霉素iii的分离制备 |
| CN101785778A (zh) | 2010-03-09 | 2010-07-28 | 沈阳同联集团有限公司 | 异戊酰螺旋霉素i的分离制备及其应用 |
| CN101785779B (zh) * | 2010-03-09 | 2014-03-05 | 沈阳同联集团有限公司 | 异戊酰螺旋霉素ii的分离制备 |
| ES2633737T3 (es) * | 2010-05-25 | 2017-09-25 | Shenyang Fuyang Pharmaceutical Technology Co., Ltd. | Levocarrimicina, composiciones farmacéuticas, procedimientos de preparación y utilizaciones de la misma |
-
2011
- 2011-05-25 RU RU2016123979A patent/RU2647236C1/ru active IP Right Revival
- 2011-05-25 MX MX2012013470A patent/MX340626B/es active IP Right Grant
- 2011-05-25 ES ES17166118T patent/ES2754614T3/es active Active
- 2011-05-25 EP EP11786085.8A patent/EP2578595B1/en active Active
- 2011-05-25 CA CA2800021A patent/CA2800021C/en active Active
- 2011-05-25 JP JP2013511523A patent/JP5945868B2/ja active Active
- 2011-05-25 US US13/699,459 patent/US8778896B2/en active Active
- 2011-05-25 ES ES11786085.8T patent/ES2633723T3/es active Active
- 2011-05-25 DK DK17166118T patent/DK3210991T3/da active
- 2011-05-25 CA CA2915236A patent/CA2915236C/en active Active
- 2011-05-25 WO PCT/CN2011/074644 patent/WO2011147313A1/zh active Application Filing
- 2011-05-25 KR KR1020127033721A patent/KR20130041829A/ko active Application Filing
- 2011-05-25 PL PL11786085T patent/PL2578595T3/pl unknown
- 2011-05-25 PT PT171661176T patent/PT3210990T/pt unknown
- 2011-05-25 KR KR1020167002374A patent/KR101706518B1/ko active IP Right Grant
- 2011-05-25 EP EP17166117.6A patent/EP3210990B1/en active Active
- 2011-05-25 RU RU2012156420/04A patent/RU2593498C2/ru active IP Right Revival
- 2011-05-25 BR BR112012029913-1A patent/BR112012029913B1/pt not_active IP Right Cessation
- 2011-05-25 ES ES17166117T patent/ES2781425T3/es active Active
- 2011-05-25 PL PL17166118T patent/PL3210991T3/pl unknown
- 2011-05-25 PL PL17166117T patent/PL3210990T3/pl unknown
- 2011-05-25 DK DK11786085.8T patent/DK2578595T3/en active
- 2011-05-25 RU RU2016123980A patent/RU2647237C1/ru active IP Right Revival
- 2011-05-25 EP EP17166118.4A patent/EP3210991B1/en active Active
- 2011-05-25 CA CA2915222A patent/CA2915222C/en active Active
- 2011-05-25 MY MYPI2012700969A patent/MY164231A/en unknown
- 2011-05-25 DK DK17166117.6T patent/DK3210990T3/da active
-
2012
- 2012-12-21 ZA ZA2012/09738A patent/ZA201209738B/en unknown
-
2014
- 2014-08-29 ZA ZA2014/06382A patent/ZA201406382B/en unknown
- 2014-08-29 ZA ZA2014/06381A patent/ZA201406381B/en unknown
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2766176C2 (ru) * | 2017-07-04 | 2022-02-08 | Шенянг Фуянг Фармасьютекал Технолоджи Ко., Лтд. | Применение изовалерил-спирамицина i, ii и/или iii при изготовлении препарата для лечения и/или профилактики опухоли и получения лекарственного препарата |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2012156420A (ru) | Левовращающие изовалерил-спирамицины 1, ii, iii, их препараты, способ приготовления и употребление | |
| RU2012156419A (ru) | Лекарственная форма левокарримицина, способ его получения и использования | |
| EP2208732B1 (en) | Deshydroxy vancomycin, the preparation, pharmaceutical composition and the use | |
| JP2016183193A (ja) | フィダキソマイシンの固体状形態およびその調製方法 | |
| CN104356160A (zh) | L-α-甘油磷酰胆碱的纯化工艺 | |
| CN102603524A (zh) | 一种醌类衍生物及其制备方法与作为抗菌剂的应用 | |
| CN110117546B (zh) | 一种海洋真菌来源的萘醌类化合物及其抗炎应用 | |
| CN112111410B (zh) | 二苯并氧杂环庚酮类化合物的制备方法 | |
| CN110863021A (zh) | 一种细胞松弛素类化合物的制备方法和应用 | |
| CN109748838B (zh) | 蒽醌类化合物及其制备方法和在制备酶抑制剂中的应用 | |
| JP2005053782A (ja) | 環状リポペプチド化合物の新規結晶 | |
| CN115724816B (zh) | 红树来源真菌中色原酮晶型及其制备与应用 | |
| EP3617191B1 (en) | Method for manufacturing diastereomer of citric acid derivative | |
| CN108456157B (zh) | 1-取代苯甲酰基-4-脂酰基氨基脲类衍生物、制备方法及作为抗菌药物的用途 | |
| CN112521435B (zh) | 一种罗红霉素类似物在制备抗菌药物中的应用 | |
| CN114989190B (zh) | 一类大环内酯类化合物kongjuemycins及其制备方法和应用 | |
| CN113896752B (zh) | 青龙衣中一种支链醇苷化合物的制备方法和抗菌用途 | |
| JP6856223B2 (ja) | ヒト毛乳頭細胞増殖用組成物 | |
| RU2691997C1 (ru) | Способ получения вещества, обладающего противогрибковой активностью | |
| CN109467546B (zh) | 一种硫代大环内酯化合物及其制备方法和抗水产病害菌活性应用 | |
| CN105061273B (zh) | 酒石酸沃尼妙林多晶型及其制备方法 | |
| DK3137475T3 (en) | Purification of epidaunorubicin | |
| CN111635453A (zh) | 基于多联苯芳烃的多肽缀合物、其制备方法和应用 | |
| PL244025B1 (pl) | Sposób wytwarzania 5,7,4’-trihydroksy-8-metoksyflawonu | |
| JPH06135987A (ja) | フラノン配糖体及びその製造法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PC41 | Official registration of the transfer of exclusive right |
Effective date: 20170413 |
|
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20200526 |
|
| NF4A | Reinstatement of patent |
Effective date: 20210623 |