KR20170067785A - 피복 구리 입자 및 그의 제조 방법 - Google Patents
피복 구리 입자 및 그의 제조 방법 Download PDFInfo
- Publication number
- KR20170067785A KR20170067785A KR1020177010816A KR20177010816A KR20170067785A KR 20170067785 A KR20170067785 A KR 20170067785A KR 1020177010816 A KR1020177010816 A KR 1020177010816A KR 20177010816 A KR20177010816 A KR 20177010816A KR 20170067785 A KR20170067785 A KR 20170067785A
- Authority
- KR
- South Korea
- Prior art keywords
- copper particles
- copper
- carboxylic acid
- aliphatic carboxylic
- coated copper
- Prior art date
Links
Images
Classifications
-
- B22F1/02—
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B22—CASTING; POWDER METALLURGY
- B22F—WORKING METALLIC POWDER; MANUFACTURE OF ARTICLES FROM METALLIC POWDER; MAKING METALLIC POWDER; APPARATUS OR DEVICES SPECIALLY ADAPTED FOR METALLIC POWDER
- B22F1/00—Metallic powder; Treatment of metallic powder, e.g. to facilitate working or to improve properties
- B22F1/10—Metallic powder containing lubricating or binding agents; Metallic powder containing organic material
- B22F1/102—Metallic powder coated with organic material
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B22—CASTING; POWDER METALLURGY
- B22F—WORKING METALLIC POWDER; MANUFACTURE OF ARTICLES FROM METALLIC POWDER; MAKING METALLIC POWDER; APPARATUS OR DEVICES SPECIALLY ADAPTED FOR METALLIC POWDER
- B22F1/00—Metallic powder; Treatment of metallic powder, e.g. to facilitate working or to improve properties
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B22—CASTING; POWDER METALLURGY
- B22F—WORKING METALLIC POWDER; MANUFACTURE OF ARTICLES FROM METALLIC POWDER; MAKING METALLIC POWDER; APPARATUS OR DEVICES SPECIALLY ADAPTED FOR METALLIC POWDER
- B22F9/00—Making metallic powder or suspensions thereof
- B22F9/16—Making metallic powder or suspensions thereof using chemical processes
- B22F9/30—Making metallic powder or suspensions thereof using chemical processes with decomposition of metal compounds, e.g. by pyrolysis
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01B—CABLES; CONDUCTORS; INSULATORS; SELECTION OF MATERIALS FOR THEIR CONDUCTIVE, INSULATING OR DIELECTRIC PROPERTIES
- H01B1/00—Conductors or conductive bodies characterised by the conductive materials; Selection of materials as conductors
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01B—CABLES; CONDUCTORS; INSULATORS; SELECTION OF MATERIALS FOR THEIR CONDUCTIVE, INSULATING OR DIELECTRIC PROPERTIES
- H01B1/00—Conductors or conductive bodies characterised by the conductive materials; Selection of materials as conductors
- H01B1/20—Conductive material dispersed in non-conductive organic material
- H01B1/22—Conductive material dispersed in non-conductive organic material the conductive material comprising metals or alloys
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01B—CABLES; CONDUCTORS; INSULATORS; SELECTION OF MATERIALS FOR THEIR CONDUCTIVE, INSULATING OR DIELECTRIC PROPERTIES
- H01B13/00—Apparatus or processes specially adapted for manufacturing conductors or cables
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01B—CABLES; CONDUCTORS; INSULATORS; SELECTION OF MATERIALS FOR THEIR CONDUCTIVE, INSULATING OR DIELECTRIC PROPERTIES
- H01B5/00—Non-insulated conductors or conductive bodies characterised by their form
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B22—CASTING; POWDER METALLURGY
- B22F—WORKING METALLIC POWDER; MANUFACTURE OF ARTICLES FROM METALLIC POWDER; MAKING METALLIC POWDER; APPARATUS OR DEVICES SPECIALLY ADAPTED FOR METALLIC POWDER
- B22F2301/00—Metallic composition of the powder or its coating
- B22F2301/10—Copper
Landscapes
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Manufacturing & Machinery (AREA)
- Physics & Mathematics (AREA)
- Dispersion Chemistry (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Powder Metallurgy (AREA)
- Conductive Materials (AREA)
- Non-Insulated Conductors (AREA)
Abstract
본 발명은, 구리 입자와, 구리 입자의 표면에 1㎚2당 2.5분자 이상 5.2분자 이하의 밀도로 배치되는 지방족 카르복실산을 포함하는 피복층을 포함하는, 피복 구리 입자를 제공한다.
Description
본 발명은 피복 구리 입자 및 그의 제조 방법에 관한 것이다.
근년의 전자 기기 관련 분야에 있어서, 배선이나 보호막 등의 광 노광에 의한 패터닝을 필요로 하지 않고 마이크로미터급의 미세 배선을 잉크젯이나 인쇄법으로 직접 형성시키는 프린터블 일렉트로닉스라 칭해지는 기술 분야가 주목받고 있다. 애초에는 금이나 은 등의 미립자가 중심이었지만, 금은 비용의 문제가 있고 은은 일렉트로마이그레이션의 문제 및 황화 가스 등에 의한 부식 등의 내식성에 과제가 있다. 이들 문제점을 해결하는 수단으로서 구리계 재료가 주목받고 있다. 구리계 재료는 금이나 은과 마찬가지로 높은 도전성을 나타내고, 일렉트로마이그레이션은 은과 비교하면 몇 단계 우수하며, 내식성도 우수하다.
귀금속인 금이나 은은 비교적 산화되기 어려운 특성을 갖고 있으며, 그로 인하여, 미립자 분산액을 제작했을 때, 함유되는 금속 미립자를 그의 표면에 산화 피막을 형성하지 않으면서 유지하는 것이 용이하다. 그에 반해 구리는 비교적 산화되기 쉬운 특성을 갖고 있으며, 입자 직경이 5㎛ 이하인 구리 입자, 특히 입자 직경이 200㎚ 이하인 미세한 구리 미립자가 되면, 사이즈 효과와 비표면적의 관계에서 그러한 경향은 더욱 현저한 것이 된다. 예를 들어 미립자 분산액을 제작했을 때, 함유되는 미립자는, 단시간에 그의 표면이 산화막으로 덮인 상태가 되고, 나아가 경시적으로 산화막의 두께도 증가하여 미립자의 입자 직경의 대부분이 산화구리의 표면 산화물층으로 변환되는 것도 적지 않다. 또한 200㎚ 이하의 구리 미립자의 경우, 입자 표면의 활성이 매우 높은 상태가 되어 있다. 그 때문에, 질소 가스 등의 불활성 분위기 하 또는 진공 조건 하에서 가열 소성하는 방법에 있어서도, 분위기에 존재하는 미량의 산소로 인하여 산화가 진행되어 미립자끼리의 소결이 저해되는 경우가 있다. 나아가, 소성 중의 표면 산화물층의 증대는, 소성의 최종 단계에서 수소 가스 등을 사용하여 환원 소성을 행하는 경우, 환원 시의 부피 수축을 크게 하여 소성 밀도의 저하로 이어지는 경우가 있다.
한편, 금속 미립자의 기술이 주목되는 이유 중 하나로 사이즈 효과에 의한 융점 강하가 있다. 사이즈 효과에 의한 융점 강하는, 금을 예로 들자면, 융점은 1,064℃이지만 입자 직경이 2㎚가 되면 약 300℃가 되어, 전자 재료 등에서 사용 가능한 온도까지 융점이 저하된다. 그러나 입자 직경이 20㎚를 초과하면 융점 강하는 거의 보이지 않는 것이 보고되어 있다. 따라서 입자 직경이 2㎚ 정도인 싱글 나노 사이즈이면 융점 강하를 충분히 기대할 수 있다. 그러나 구리의 경우, 산화를 방지하는 표면 보호제가 필수적이며, 미립자의 비표면적의 관계로부터 표면 보호제의 필요량은 구리의 부피의 몇 배 이상이 되고, 그 결과, 소결 시에 대폭적인 부피 수축을 야기하여, 고밀도의 소결체를 얻는 것이 곤란해진다. 이에 대하여, 소결 단계에 있어서 환원 분위기 하에서 금속 산화물로부터 싱글 나노 사이즈의 입자를 생성시키고, 사이즈 효과에 의한 융점 강하를 이용하여 300℃ 내지 400℃ 정도의 온도에서 소결을 행하는 방법이 알려져 있다.
상기와 관련하여, 산화구리 입자를 지방족 모노카르복실산의 존재 하에서 환원시켜 얻어지는 지방족 모노카르복실산으로 표면이 피복된 구리 미립자 분산액이 알려져 있으며, 저온에서의 소결성이 우수하다고 되어 있다(예를 들어 일본 특허 공개 제2013-047365호 공보 참조). 또한 구리 분말의 표면에, 지방산의 금속염으로 형성한 표면 처리층을 마련한 표면 처리 구리 분말이 알려져 있으며, 구리 페이스트로 가공했을 때 페이스트 점도를 저하시킬 수 있다고 되어 있다(예를 들어 일본 특허 공개 제2002-332502호 공보 참조). 또한 구리 분말을 카르복실산 함유 유기 용매로 표면 처리하는 구리 페이스트용의 구리 분말의 제조 방법이 알려져 있으며, 구리 페이스트의 점도를 저하시킬 수 있다고 되어 있다(예를 들어 일본 특허 공개 제2004-225122호 공보 참조)
또한 산화구리를 환원시켜 생성한 금속 구리에 지방산 함유 용액을 접촉시켜, 금속 구리의 표면에 지방산의 금속염에 의한 표면 처리층을 형성하는 구리 분말의 제조 방법이 알려져 있다(예를 들어 일본 특허 공개 제2003-342621호 공보 참조).
그러나 일본 특허 공개 제2013-047365호 공보에 기재된 구리 미립자 분산액, 일본 특허 공개 제2002-332502호 공보에 기재된 표면 처리 구리 분말에서는, 구리 입자의 내산화성이 충분히 얻어지지 않는 경향이 있었다. 또한 일본 특허 공개 제2002-332502호 공보, 일본 특허 공개 제2004-225122호 공보 및 일본 특허 공개 제2003-342621호 공보에 기재된 구리 분말에서는, 구리 분말의 입자 직경을 충분히 작게 하는 것이 곤란하여, 충분한 소결성이 얻어지지 않는 경향이 있었다.
본 발명은, 이상의 사정을 감안하여 종래 기술의 문제점을 해소하여, 종래 기술에서는 달성이 곤란했던, 우수한 내산화성과 소결성을 겸비하는 피복 구리 입자 및 그의 제조 방법을 제공하는 것을 목적으로 한다.
본 발명자들은 상기 과제를 해결하고자 검토한 결과, 구리 입자의 표면에 특정한 밀도로 지방족 카르복실산을 배치함으로써, 우수한 내산화성과 소결성을 구비하는 피복 구리 입자가 얻어지는 것을 알아내었다.
본 발명은 이하의 형태를 포함한다.
(1) 구리 입자와, 구리 입자의 표면에 1㎚2당 2.5분자 이상 5.2분자 이하의 밀도로 배치되는 지방족 카르복실산을 포함하는 피복층을 포함하는, 피복 구리 입자이다.
(2) 지방족 카르복실산의 지방족기의 탄소수가 5 내지 17인, (1)에 기재된 피복 구리 입자이다.
(3) 지방족 카르복실산이 구리 표면에 물리적으로 흡착되어 있는, (1) 또는 (2)에 기재된 피복 구리 입자
(4) 피복층이 지방족 카르복실산 구리 착체의 열분해물인, (1) 내지 (3) 중 어느 한 항에 기재된 피복 구리 입자이다.
(5) 구리 산화물 및 구리 수산화물의 총 함유율이 5질량% 이하인, (1) 내지 (4) 중 어느 한 항에 기재된 피복 구리 입자이다.
(6) 구리 입자의 평균 1차 입자 직경이 0.02 내지 5.0㎛인, (1) 내지 (4) 중 어느 한 항에 기재된 피복 구리 입자이다.
(7) 매체 중에서 지방족 카르복실산 구리 착체를 열분해하는 것을 포함하는, (1) 내지 (6) 중 어느 한 항에 기재된 피복 구리 입자의 제조 방법이다.
(8) (1) 내지 (6) 중 어느 한 항에 기재된 피복 구리 입자와, 매체를 포함하는 도전성 조성물이다.
(9) 기재와, 기재 상에 배치되고, (8)에 기재된 도전성 조성물의 열처리물인 배선 패턴 또는 접합층을 구비하는 회로 형성물이다.
본 발명에 의하면, 종래 기술에서는 달성 곤란했던, 우수한 내산화성과 소결성을 겸비한 피복 구리 입자 및 그의 제조 방법을 제공할 수 있다.
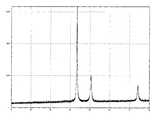
도 1은 실시예 1에서 제작한 피복 구리 입자를 제조 직후에 측정한 XRD 측정의 결과이다.
도 2는 실시예 1에서 제작한 피복 구리 입자의 SEM 관찰 화상이다.
도 3은 실시예 1에서 제작한 피복 구리 입자의 Tof-SIMS 측정의 결과이다.
도 4는 실시예 1에서 제작한 피복 구리 입자의 IR 스펙트럼 측정의 결과이다.
도 5는 실시예 1에서 제작한 피복 구리 입자의 TG-DTA 측정의 결과이다.
도 6은 실시예 2에서 제작한 피복 구리 입자의 SEM 관찰 화상이다.
도 7은 실시예 2에서 제작한 피복 구리 입자의 IR 스펙트럼 측정의 결과이다.
도 8은 실시예 1에서 제작한 피복 구리 입자를 분체의 상태에서 대기 중, 25℃에서 2개월 보관 후에 측정한 XRD 측정의 결과이다.
도 9는 비교예 1에서 제작한 피복 구리 입자의 제조 직후에 측정한 XRD 측정과, 대기 중, 25℃에서 2개월 보관 후에 측정한 XRD 측정의 결과이다.
도 10은 비교예 2에서 제작한 피복 구리 입자의 SEM 관찰 화상이다.
도 2는 실시예 1에서 제작한 피복 구리 입자의 SEM 관찰 화상이다.
도 3은 실시예 1에서 제작한 피복 구리 입자의 Tof-SIMS 측정의 결과이다.
도 4는 실시예 1에서 제작한 피복 구리 입자의 IR 스펙트럼 측정의 결과이다.
도 5는 실시예 1에서 제작한 피복 구리 입자의 TG-DTA 측정의 결과이다.
도 6은 실시예 2에서 제작한 피복 구리 입자의 SEM 관찰 화상이다.
도 7은 실시예 2에서 제작한 피복 구리 입자의 IR 스펙트럼 측정의 결과이다.
도 8은 실시예 1에서 제작한 피복 구리 입자를 분체의 상태에서 대기 중, 25℃에서 2개월 보관 후에 측정한 XRD 측정의 결과이다.
도 9는 비교예 1에서 제작한 피복 구리 입자의 제조 직후에 측정한 XRD 측정과, 대기 중, 25℃에서 2개월 보관 후에 측정한 XRD 측정의 결과이다.
도 10은 비교예 2에서 제작한 피복 구리 입자의 SEM 관찰 화상이다.
본 명세서에 있어서 「공정」라는 단어는, 독립된 공정뿐만 아니라, 다른 공정과 명확히 구별할 수 없는 경우라도 그 공정의 소기의 목적이 달성된다면 본 용어에 포함된다. 또한 조성물 중의 각 성분의 함유량은, 조성물 중에 각 성분에 해당하는 물질이 복수 존재하는 경우, 특별히 언급하지 않는 한, 조성물 중에 존재하는 당해 복수의 물질의 합계량을 의미한다.
이하, 본 발명의 실시 형태에 대하여 상세히 설명한다.
<피복 구리 입자>
본 실시 형태의 피복 구리 입자는, 구리 입자와, 구리 입자의 표면에 1㎚2당 2.5분자 이상 5.2분자 이하의 밀도로 배치되는 지방족 카르복실산을 포함하는 피복층을 포함한다.
구리 입자의 표면에 특정한 범위의 밀도로 지방족 카르복실산이 배치되어 있음으로써, 종래 기술에서는 달성 곤란했던, 우수한 내산화성과 소결성을 양립시켜 달성할 수 있다. 그 이유는 명확하지는 않지만, 예를 들어 이하와 같이 생각할 수 있다. 예를 들어 「에멀션의 과학(Ⅴ) 하나이 데쓰야 저」(조리 과학, 7권, 3호, 1974년)에 기재되어 있는 미리스트산의 단분자 표면막의 표면막압과 분자 면적의 관계 플롯으로부터, 약 3.3 내지 5.4분자/㎚2의 범위는 액체 응집막 영역인 것을 알 수 있다. 따라서 본 실시 형태의 피복 구리 입자의 표면에 있어서는, 지방족 카르복실산이 액체 응집막에 가까운 단분자막을 형성하고 있기 때문에, 우수한 내산화성과 소결성이 달성된다고 생각된다.
본 실시 형태의 피복 구리 입자는, 구리 입자의 표면이, 지방족 카르복실산을 포함하는 피복층으로 피복되어 있다. 구리 입자를 피복하는 지방족 카르복실산은, 구리 입자의 표면에 국재하여 산화나 응집을 억제하는 피복재이며, 소결 시에 입자 표면으로부터 제거되고, 나아가 소결 온도 이하에서 분해 또는 휘발되기 때문에, 소결에 의하여 형성되는 구리 피막 중으로의 잔존이 억제된다고 생각된다. 더욱 바람직한 작용으로서, 지방족 카르복실산이 구리 입자의 표면에서 고밀도로 흡착되어 있기 때문에, 지방족 카르복실산 분자 간에는 견고한 반 데르 발스 힘이 작용하여, 구리 입자 표면 상에서 회합체를 형성하고 있다고 생각된다. 소결 시에는 온도 상승에 수반하여, 피복되어 있는 지방족 카르복실산 간의 반 데르 발스 힘이 감소하기 때문에, 피복 밀도가 저하된다. 그 결과, 흡착되어 있지 않은 피복재인 지방족 카르복실산 분자가 적절히 제거되어, 피복 밀도가 저하된 부분에 있어서 보다 양호한 소결성이 발현된다고 생각된다. 1㎚2당 2.5분자 미만의 저밀도로 지방족 카르복실산으로 피복된 구리 입자의 경우에는, 이러한 반 데르 발스 힘이 작용하기 어렵기 때문에, 소결 시에 지방족 카르복실산이 휘발되기 쉬워 소결 환경의 미량의 산소로 인하여 산화되어 소결이 저해되기 쉽다고 생각된다.
또한 후술하는 제조 방법으로 얻어지는 피복 구리 입자는, 입자 직경이 고르기 때문에 분산성이 우수하다. 또한 피복 구리 입자를 구성하는 구리 입자의 결정자 직경과 SEM 관찰 직경의 차가 작기 때문에, 피복 구리 입자가 복수의 구리 입자의 응집에 의하여 구성되어 있지 않으며, 응집 입자 경계부에 피복재나 불순물, 산화층 등이 존재하여, 소결을 저해하는 것이 억제된다고 생각된다.
피복 구리 입자를 구성하는 구리 입자의 입자 직경은 특별히 제한되지 않으며, 목적 등에 따라 적절히 선택할 수 있다. 예를 들어 구리 입자의 평균 1차 입자 직경은 0.02㎛ 이상 5.0㎛ 이하이며, 0.02㎛ 이상 1.0㎛ 이하로 할 수 있고, 0.02㎛ 이상 0.5㎛ 이하로 할 수 있고, 0.02㎛ 이상 0.2㎛ 이하로 할 수 있다.
구리 입자의 평균 1차 입자 직경은, SEM 관찰에 의한 임의의 20개의 구리 입자의 1차 입자 직경의 산술 평균값으로서 산출된다. 또한 구리 입자의 평균 1차 입자 직경은 피복 구리 입자의 평균 1차 입자 직경과 실질적으로 동일하다고 간주할 수 있다.
구리 입자를 구성하는 구리의 순도는 특별히 제한되지 않으며, 목적 등에 따라 적절히 선택할 수 있다. 구리 입자의 순도는, 예를 들어 95질량% 이상이며, 97질량% 이상인 것이 바람직하다. 또한 구리 입자에 포함되는 구리 산화물 및 구리 수산화물의 총 함유율은, 예를 들어 5질량% 이하이며, 3질량% 이하인 것이 바람직하고, 1질량% 이하인 것이 특히 바람직하다. 또한 구리 산화물은 산화구리(Ⅱ) 및 아산화구리를 포함한다.
구리 입자의 형상은 특별히 제한되지 않으며, 목적 등에 따라 적절히 선택할 수 있다. 구리 입자의 형상은 대략 구상, 판상, 막대상 등을 들 수 있으며, 대략 구상인 것이 바람직하다.
구리 입자의 표면에 배치되는 지방족 카르복실산의 종류는 특별히 제한되지 않으며, 목적 등에 따라 적절히 선택할 수 있다. 지방족 카르복실산이 갖는 카르복시기 수는 특별히 제한되지 않으며, 목적 등에 따라 적절히 선택할 수 있다. 카르복시기 수는, 예를 들어 1 내지 2이며, 1인 것이 바람직하다. 즉, 지방족 모노카르복실산이 바람직하게 사용된다.
지방족 카르복실산은 포화 지방족 카르복실산이어도 불포화 지방족 카르복실산이어도 된다. 지방족 카르복실산이 불포화 지방족 카르복실산인 경우, 불포화 지방족기에 포함되는 불포화 결합 수는, 예를 들어 1 내지 3이며, 1 내지 2가 바람직하다.
지방족 카르복실산에 포함되는 지방족기는 직쇄상이어도 분지쇄상이어도 되며, 직쇄상인 것이 바람직하다. 지방족기의 탄소수는, 예를 들어 5 이상이며, 5 내지 21이 바람직하고, 5 내지 17이 보다 바람직하고, 7 내지 17이 더욱 바람직하고, 9 내지 17이 특히 바람직하다.
지방족 카르복실산의 비점은, 후술하는 제조 방법에 있어서의 열분해 처리의 온도보다도 높은 것이 바람직하다. 구체적으로 지방족 카르복실산의 비점은 120℃ 이상인 것이 바람직하고, 130℃ 이상인 것이 보다 바람직하다. 비점의 상한값은 특별히 제한되지 않으며, 예를 들어 400℃ 이하이다. 비점이 400℃ 이하이면, 피복 구리 입자의 소결성이 보다 향상되는 경향이 있다.
지방족 카르복실산으로서 구체적으로는 올레산, 리놀산 등의 불포화 지방족 카르복실산; 스테아르산, 헵타데칸산, 라우르산, 옥탄산 등의 포화 지방족 카르복실산이 예시되며, 이들로 이루어지는 군에서 선택되는 적어도 1종인 것이 바람직하다. 지방족 카르복실산은 1종 단독이어도, 2종 이상을 조합하여 사용해도 된다.
구리 입자의 표면에는 1㎚2당 2.5분자 이상 5.2분자 이하의 밀도로 지방족 카르복실산이 배치되어 있다. 즉, 구리 입자의 표면은, 지방족 카르복실산을 포함하는 피복층으로 피복되며, 구리 입자 표면에 있어서의 지방족 카르복실산의 피복 밀도가 2.5 내지 5.2분자/㎚2이다. 지방족 카르복실산의 피복 밀도는 내산화성의 관점에서 3.0 내지 5.2분자/㎚2인 것이 바람직하고, 3.5 내지 5.2분자/㎚2인 것이 보다 바람직하다.
구리 입자 표면에 있어서의 지방족 카르복실산의 피복 밀도는 이하와 같이 하여 산출할 수 있다. 피복 구리 입자에 대하여, 일본 특허 공개 제2012-88242호 공보에 기재된 방법에 따라, LC를 이용하여 표면에 부착되어 있는 유기 성분을 추출하여 성분 분석을 한다. 또한 TG-DTA 측정(열중량 측정·시차 열분석)을 행하여, 피복 구리 입자에 포함되는 유기 성분량을 측정한다. 이어서 LC의 분석 결과와 합쳐 피복 구리 입자에 포함되는 지방족 카르복실산량을 산출한다. 또한 SEM 화상 관찰에 의하여 구리 입자의 평균 1차 입자 직경을 측정한다. 이상의 분석 결과로부터, 피복 구리 입자 1g에 포함되는 지방족 카르복실산의 분자수는 하기 식 (a)로 표시된다.
[지방족 카르복실산의 분자수]=Macid/(Mw/NA) … (a)
여기서, Macid는 피복 구리 입자 1g에 포함되는 지방족 카르복실산량(g)이고, Mw는 지방족 카르복실산의 분자량(g/㏖)이고, NA는 아보가드로 상수이다.
구리 입자의 형상을 구체로 근사하고, 피복 구리 입자의 질량에서 유기 성분량을 뺀 구리 입자량 MCu(g)로부터, 피복 구리 입자 1g 중의 구리 입자 수는 아래 식 (b)로 표시된다.
[구리 입자 수]=MCu/[(4πr3/3)×d×10-21] … (b)
여기서, MCu는 피복 구리 입자 1g에 포함되는 구리 입자량(g)이고, r은 SEM 화상 관찰에 의하여 산출된 1차 입자 직경의 반경(㎚)이고, d는 구리의 밀도이다(d=8.94). 피복 구리 입자 1g에 포함되는 구리 입자의 표면적은 식 (b)로부터 아래 식 (c)로 표시된다.
[구리 입자의 표면적(㎚2)]=[구리 입자 수]×4πr2 … (c)
이상으로부터, 지방족 카르복실산에 의한 구리 입자의 피복 밀도(분자/㎚2)는, (a) 식 및 (c) 식을 이용하여 하기 식 (d)로 산출된다.
[피복 밀도]=[지방족 카르복실산의 분자수]/[구리 입자 표면적] … (d)
피복 구리 입자에 있어서의 지방족 카르복실산과 구리 입자의 결합 상태는 특별히 제한되지 않으며, 이온성 결합이어도 물리 흡착이어도 된다. 지방족 카르복실산은, 피복 구리 입자의 소결성의 관점에서 구리 입자의 표면에 물리 흡착되어 있는 것이 바람직하고, 구리 입자의 표면에 카르복시기로 물리 흡착되어 있는 것이 보다 바람직하다.
지방족 카르복실산이 구리 입자에 물리 흡착되어 있는 것은 피복 구리 입자의 표면 조성을 분석함으로써 확인할 수 있다. 구체적으로는, 피복 구리 입자에 대하여 Tof-SIMS 표면 분석을 행하여, 실질적으로 유리된 지방족 카르복실산만이 검출되고, 63Cu 또는 65Cu와 결합해 있는 지방족 카르복실산이 실질적으로 검출되지 않는 것으로 확인할 수 있다. 여기서, 63Cu 또는 65Cu와 결합해 있는 지방족 카르복실산이 실질적으로 검출되지 않는다는 것은, 이들의 검출량이 유리된 지방족 카르복실산만의 검출량에 대하여 5% 이하인 것을 의미하며, 1% 이하인 것이 바람직하다.
또한 지방족 카르복실산이 카르복시기로 구리 입자의 표면에 물리 흡착되어 있는 것은, 피복 구리 입자에 대하여 적외 흡수 스펙트럼 측정을 행하여, 실질적으로 카르복실산-금속염 유래의 신축 진동 피크만이 관측되고, 유리된 카르복실산에서 유래하는 신축 진동 피크가 실질적으로 관측되지 않는 것으로 확인할 수 있다.
피복 구리 입자의 입자 직경은 특별히 제한되지 않으며, 목적 등에 따라 적절히 선택할 수 있다. 피복 구리 입자의 평균 1차 입자 직경은, 예를 들어 0.02㎛ 이상 5.0㎛ 이하이며, 0.02㎛ 이상 1.0㎛ 이하로 할 수 있고, 0.02㎛ 이상 0.5㎛ 이하로 할 수 있고, 0.02㎛ 이상 0.2㎛ 이하로 할 수 있다. 피복 구리 입자의 평균 1차 입자 직경은, SEM 관찰에 의한 임의의 20개의 피복 구리 입자의 1차 입자 직경의 산술 평균값 DSEM으로서 산출된다.
또한 피복 구리 입자의 입도 분포의 변동 계수(표준 편차 SD/평균 1차 입자 직경 DSEM)의 값은, 예를 들어 0.01 내지 0.5이며, 0.05 내지 0.3이 바람직하다. 특히 후술하는 피복 구리 입자의 제조 방법으로 제조되어 있음으로써, 입도 분포의 변동 계수가 작아 입자 직경이 고른 상태로 할 수 있다. 피복 구리 입자의 입도 분포의 변동 계수가 작음으로써, 분산성이 우수하여, 고농도의 분산물을 제작할 수 있다는 효과가 얻어진다.
또한 피복 구리 입자에 있어서는, 분체 X선 측정으로부터 구해지는 결정 입자 직경 DXRD의, SEM 관찰에 의한 평균 1차 입자 직경 DSEM에 대한 비 DXRD/DSEM이, 예를 들어 0.25 내지 1.00이며, 0.5 내지 1.00이 바람직하다. 특히 후술하는 피복 구리 입자의 제조 방법으로 제조되어 있음으로써, 결정 입자 직경과 평균 1차 입자 직경의 차를 작게 할 수 있다. 이것에 의하여, 내산화성이 보다 우수하고 소결성이 보다 향상된다는 효과가 얻어진다
피복 구리 입자는 내산화성이 우수하다. 내산화성이 우수한 것은, 예를 들어 제조하고 나서 소정 시간 후에, 피복 구리 입자 중에 있어서의 구리 산화물 및 구리 수산화물의 생성이 억제되어 있는 것으로 확인할 수 있다. 예를 들어 제조하고 나서 2개월 후의 피복 구리 입자 중의 구리 산화물 및 구리 수산화물의 총 함유율은 5질량% 이하인 것이 바람직하고, 3질량% 이하인 것이 보다 바람직하다. 피복 구리 입자 중에 있어서의 구리 산화물의 생성은 피복 구리 입자의 XRD 측정에 의하여 확인할 수 있다.
본 실시 형태의 피복 구리 입자는 내산화성과 소결성이 우수하기 때문에, 기재 상에 배선 패턴 등을 형성하는 도전성 조성물에 적합하게 사용할 수 있다. 피복 구리 입자를 포함하는 도전성 조성물의 상세에 대해서는 후술한다.
<피복 구리 입자의 제조 방법>
피복 구리 입자의 제조 방법은, 원하는 피복 구리 입자가 얻어지는 한 특별히 한정되지 않는다. 피복 구리 입자의 제조 방법은, 지방족 카르복실산 구리 착체를 열분해 처리하는 것을 포함하는 것이 바람직하다. 피복 구리 입자의 제조 방법에 적용되는 지방족 카르복실산 구리 착체의 구성은, 원하는 피복 구리 입자가 얻어지는 한 특별히 제한되지 않는다. 지방족 카르복실산 구리 착체는 포름산구리, 아미노알코올, 지방족 카르복실산 및 용매를 포함하는 반응액으로부터 형성되는 것이 바람직하고, 포름산구리, 아미노알코올, 탄소수가 5 이상인 지방족기를 갖는 지방족 카르복실산 및 용매를 포함하는 반응액으로부터 형성되는 것이 보다 바람직하다.
지방족 카르복실산 구리 착체를 열분해 처리함으로써 구리 이온이 환원되어 금속 구리 입자가 생성된다. 이어서, 생성된 금속 구리 입자의 표면에 지방족 카르복실산이, 예를 들어 물리적으로 흡착됨으로써, 소정의 피복 밀도의 지방족 카르복실산을 포함하는 피복층이 형성되어, 원하는 피복 구리 입자가 얻어진다.
피복 구리 입자의 제조 방법은, 지방족 카르복실산 구리 착체를 열분해 처리하기에 앞서, 포름산구리, 아미노알코올, 탄소수가 5 이상인 지방족기를 갖는 지방족 카르복실산 및 용매를 포함하는 반응액을 얻는 것을 포함하는 것이 바람직하고, 아미노알코올과 용매와의 SP값의 차인 ΔSP값이 4.2 이상인 것이 보다 바람직하다. 즉, 피복 구리 입자의 제조 방법은, 포름산구리, 아미노알코올, 탄소수가 5 이상인 지방족기를 갖는 지방족 카르복실산 및 용매를 포함하는 반응액을 얻는 것과, 반응액 중에 생성되는 착화합물을 열분해 처리하여 금속 구리를 생성하는 것을 포함하며, 아미노알코올과 용매와의 SP값의 차인 ΔSP값이 4.2 이상인, 지방족 카르복실산으로 표면이 피복된 피복 구리 입자의 제조 방법인 것이 특히 바람직하다.
포름산구리를 출발 원료로 하여 액상 중에 있어서 포름산구리 착체의 열분해 환원 반응을 진행시키고, 반응의 진행에 수반하여 포름산구리 착체로부터 반응 용매 중에 이것과 상용되지 않는 아미노알코올이 방출됨으로써, 유중수 에멀션(Water-in-Oil Emulsion)에 유사한 새로운 반응장을 형성하고, 그 중에서 계속적으로 구리의 금속 핵을 발생시키면서 핵 성장 반응이 진행됨으로써, 내산화성과 소결성이 우수하고, 입자 직경이 제어되어 입도가 고른 환원 구리 입자가 생성된다고 생각된다. 또한 포름산구리 착체의 열분해 속도가 적절히 제어됨으로써 용질의 공급이 제어된다. 이것에 의하여 금속 핵의 성장이 제어되어, 보다 입도가 고른 환원 구리 입자가 생성된다고 생각된다.
더욱이 액상 중에 지방족 카르복실산이 존재함으로써, 물리 흡착에 의하여 지방족 카르복실산이 생성된 환원 구리 입자를 고밀도로 피복한다고 생각된다. 이와 같이 하여 제조되는 피복 구리 입자는, 산화막이 거의 없는 환원 구리 입자로 구성되며, 그의 표면을 물리 흡착에 의하여 지방족 카르복실산이 피복하고 있기 때문에 내산화성과 소결성의 균형이 우수하다. 이것에 의하여, 피복 구리 입자의 소성 공정에 있어서, 구리 입자를 피복하고 있는 유기 보호제인 지방족 카르복실산이 400℃ 이하의 온도에서 제거되어, 수소 가스 등의 환원 분위기를 사용할 것까지도 없이 질소 치환 등의 수단으로 달성할 수 있는 저산소 분위기에 있어서, 피복 구리 입자끼리의 소결을 행할 수 있다. 이로 인하여, 소결에 환원성 분위기를 필요로 하는 종래의 구리 입자에서는 적용이 곤란했던 부위, 예를 들어 수소 취화나 수소와의 반응에 의한 변질이 문제가 되는 부위에도 효과적으로 사용할 수 있다. 또한 질소 치환 리플로우로 등의 기존의 설비를 이용하여 소결시킬 수 있어 경제성의 관점에 있어서도 우수하다.
피복 구리 입자의 제조 방법에 사용되는 반응액은, 포름산구리와, 적어도 1종의 아미노알코올과, 적어도 1종의 지방족 카르복실산(바람직하게는 탄소수가 5 이상인 지방족기를 갖는 지방족 카르복실산)과, 용매를 포함하는 것이 바람직하다. 반응액은 필요에 따라 그 외의 첨가제를 더 포함하고 있어도 된다.
(포름산구리)
포름산구리는 2가의 구리 이온과, 구리 이온 1몰에 대하여 2몰의 포름산 이온으로 구성된다. 포름산구리는 무수물이어도 수화물이어도 된다. 또한 포름산구리는 시판품을 사용해도 되고, 새로이 조제한 것을 사용해도 된다. 포름산구리를 열분해하여 환원 구리의 미립자를 얻는 방법은, 예를 들어 일본 특허 공고 소61-19682호 공보 등에 개시되어 있다. 포름산은 통상의 카르복실산과 달리 환원성을 가지므로, 포름산구리를 열분해하면 2가의 구리 이온을 환원시킬 수 있다. 예를 들어 무수 포름산구리는 불활성 가스 중에서 가열하면 210℃ 내지 250℃에서 열분해되어 금속 구리를 생성하는 것이 알려져 있다.
반응액 중의 포름산구리의 함유량은 특별히 제한되지 않으며, 목적 등에 따라 적절히 선택할 수 있다. 반응액 중의 포름산구리의 함유량은, 예를 들어 제조 효율의 관점에서 1.0몰/리터 이상 2.5몰/리터 이하인 것이 바람직하고, 1.5몰/리터 이상 2.5몰/리터 이하인 것이 보다 바람직하고, 2.0몰/리터 이상 2.5몰/리터 이하인 것이 특히 바람직하다.
(아미노알코올)
아미노알코올은 적어도 하나의 아미노기를 갖는 알코올 화합물이며, 포름산구리와 착화합물을 형성 가능하면 특별히 제한되지 않는다. 반응액 중에 아미노알코올이 존재함으로써 포름산구리로부터 착화합물이 생성되어 용매에 가용화할 수 있다. 아미노알코올은 모노아미노모노알코올 화합물인 것이 바람직하고, 아미노기가 비치환된 모노아미노모노알코올 화합물인 것이 보다 바람직하다. 또한 아미노알코올은 단좌 배위성의 모노아미노모노알코올 화합물인 것도 역시 바람직하다.
아미노알코올의 비점은 특별히 제한되지 않지만, 열분해 처리의 반응 온도보다도 높은 것이 바람직하다. 구체적으로는 아미노알코올의 비점은 120℃ 이상인 것이 바람직하고, 130℃ 이상인 것이 보다 바람직하다. 비점의 상한값은 특별히 제한되지 않으며, 예를 들어 400℃ 이하이고, 300℃ 이하인 것이 바람직하다.
또한 아미노알코올은 극성의 관점에서 SP값이 11.0 이상인 것이 바람직하고, 12.0 이상인 것이 보다 바람직하고, 13.0 이상인 것이 더욱 바람직하다. 아미노알코올의 SP값의 상한값은 특별히 제한되지 않으며, 예를 들어 18.0 이하이고, 17.0 이하인 것이 바람직하다.
여기서 SP값이란, 힐데브란트(Hildebrand)의 정의에 의하면 25℃에서의 시료 1mL당 분자 간 결합 에너지 E1의 제곱근이다. SP값의 계산 방법은 『고에키 샤단 호진 세키유 갓카이 홈페이지』에 기재된 방법(http://sekiyu-gakkai.or.jp/jp/dictionary/petdicsolvent.html#solubility2)을 채용하였다. 구체적으로는 이하와 같이 하여 산출된다.
분자 간 결합 에너지 E1은 증발 잠열에서 기체 에너지를 뺀 값이다. 증발 잠열 Hb는 시료의 비점 Tb로서 아래 식에서 부여된다.
Hb=21×(273+Tb)
이 Hb값으로부터 25℃에서의 몰 증발 잠열 H25가 아래 식에서 구해진다.
H25=Hb×[1+0.175×(Tb-25)/100]
몰 증발 잠열 H25로부터 분자 간 결합 에너지 E가 아래 식에서 구해진다.
E=H25-596
분자 간 결합 에너지 E로부터 시료 1mL당 분자 간 결합 에너지 E1이 아래 식에 의하여 구해진다.
E1=E×D/Mw
여기서, D는 시료의 밀도, Mw는 시료의 분자량이며, E1로부터 SP값이 아래 식에 의하여 구해진다.
SP=(E1)1/2
또한 OH기를 포함하는 용제는 OH기 1기에 대하여 +1의 보정이 필요하다〔예를 들어 미쓰비시 세키유 기술 자료, No. 42, p3, p11(1989) 참조〕.
아미노알코올로서 구체적으로는 2-아미노에탄올(비점: 170℃, SP값: 14.54), 3-아미노-1-프로판올(비점: 187℃, SP값: 13.45), 5-아미노-1-펜탄올(비점: 245℃, SP값: 12.78), DL-1-아미노-2-프로판올(비점: 160℃, SP값: 12.74), N-메틸디에탄올아민(비점: 247℃, SP값: 13.26) 등이 예시되며, 이들로 이루어지는 군에서 선택되는 적어도 1종이 바람직하다.
아미노알코올은 1종 단독이어도, 2종 이상을 조합하여 사용해도 된다. 반응액에 있어서의 아미노알코올의 함유량은 특별히 제한되지 않으며, 목적 등에 따라 적절히 선택할 수 있다. 아미노알코올의 함유량은, 예를 들어 반응액 중의 구리 이온에 대하여 1.5 내지 4.0배 몰의 범위가 바람직하고, 1.5 내지 3.0배 몰의 범위가 보다 바람직하다. 아미노알코올의 함유량이 구리 이온에 대하여 1.5배 몰 이상이면 포름산구리의 용해성이 충분히 얻어져, 반응에 요하는 시간을 단축할 수 있다. 또한 4.0배 몰 이하이면, 생성되는 피복 구리 입자의 오염을 억제할 수 있다.
(지방족 카르복실산)
지방족 카르복실산은 특별히 제한되지 않으며, 목적 등에 따라 적절히 선택할 수 있다. 그 중에서도 내산화성의 관점에서 지방족기의 탄소수가 5 이상인 지방족 카르복실산(이하, 「장쇄 카르복실산」이라고도 함)인 것이 바람직하다. 지방족기는 직쇄상 및 분지쇄상 중 어느 것이어도 되고, 또한 포화 지방족기 및 불포화 지방족기 중 어느 것이어도 된다. 지방족기의 탄소수는 5 이상인데, 5 이상 17 이하인 것이 바람직하고, 7 이상 17 이하인 것이 보다 바람직하다. 지방족기의 탄소수가 5 이상이면, 입도 분포의 지표가 되는 변동률이 작아지는 경향이 있다. 이는, 예를 들어 탄소쇄의 길이가 회합력을 좌우하는 반 데르 발스 힘의 크기와 상관성이 높은 것으로 설명할 수 있다. 즉, 탄소쇄가 긴 카르복실산은 회합력이 강하여, 마이크로 반응장인 유중수 에멀션(Water-in-oil Emulsion)에 유사한 상 안정화에 기여함으로써 입자 직경이 고른 구리 입자를 효율적으로 제조할 수 있다고 생각된다.
또한 지방족 카르복실산의 비점은 열분해 처리의 온도보다도 높은 것이 바람직하다. 구체적으로 지방족 카르복실산의 비점은 120℃ 이상인 것이 바람직하고, 130℃ 이상인 것이 보다 바람직하다. 비점의 상한값은 특별히 제한되지 않으며, 예를 들어 400℃ 이하이다. 비점이 400℃ 이하이면, 피복 구리 입자의 소결성이 보다 향상되는 경향이 있다.
지방족 카르복실산으로서 구체적으로는 올레산, 리놀산, 스테아르산, 헵타데칸산, 라우르산, 옥탄산 등이 예시되며, 이들로 이루어지는 군에서 선택되는 적어도 1종인 것이 바람직하다.
지방족 카르복실산은 1종 단독이어도, 2종 이상을 조합하여 사용해도 된다. 반응액에 있어서의 지방족 카르복실산의 함유량은, 원하는 피복 구리 입자가 얻어지는 한, 특별히 제한되지 않는다. 지방족 카르복실산의 함유량은, 예를 들어 반응액 중의 구리 이온에 대하여 2.5 내지 25몰%의 범위가 바람직하고, 5.0 내지 15몰%의 범위가 보다 바람직하다. 지방족 카르복실산의 함유량이 구리 이온에 대하여 25몰% 이하이면 반응계의 점도 상승을 억제할 수 있는 경향이 있다. 또한 지방족 카르복실산의 함유량이 구리 이온에 대하여 2.5몰% 이상이면, 충분한 반응 속도가 얻어져 생산성이 향상되는 경향이 있고, 입도 분포의 지표가 되는 변동률이 작아지는 경향이 있다.
(용매)
반응액을 구성하는 용매는, 포름산에 의한 환원 반응을 과도하게 저해하지 않고, 아미노알코올과의 SP값의 차인 ΔSP값이 4.2 이상이 되도록 선택되는 것이 바람직하며, 통상 사용되는 유기 용제로부터 적절히 선택할 수 있다. 아미노알코올의 SP값과 용매의 SP값과의 차인 ΔSP값이 4.2 이상이면, 형성되는 피복 구리 입자의 입도 분포 폭이 보다 좁은, 입자 직경이 고른 피복 구리 입자가 얻어진다.
ΔSP값은 반응장의 형성성과 피복 구리 입자의 품질의 관점에서 4.5 이상이 바람직하고, 5.0 이상이 보다 바람직하다. ΔSP값의 상한은 특별히 제한되지 않으며, 예를 들어 ΔSP값은 11.0 이하이고, 10.0 이하가 바람직하다. 용매의 SP값은 아미노알코올보다도 작은 것이 보다 바람직하다. 용매의 SP값은 11.0 이하인 것이 바람직하고, 10.0 이하인 것이 보다 바람직하다. 용매의 SP값의 하한은 특별히 제한되지 않으며, 예를 들어 용매의 SP값은 7.0 이상인 것이 바람직하다.
또한 용매의 비점은 열분해 처리의 온도보다도 높은 것이 바람직하다. 구체적으로 용매의 비점은 120℃ 이상인 것이 바람직하고, 130℃ 이상인 것이 보다 바람직하다. 비점의 상한값은 특별히 제한되지 않으며, 예를 들어 비점은 400℃ 이하이고, 300℃ 이하인 것이 바람직하다. 또한 용매는, 물과 공비 혼합물을 형성 가능한 유기 용제인 것도 역시 바람직하다. 물과 공비 혼합물을 형성 가능하면, 열분해 처리에 의하여 반응액 중에 생성된 물을 용이하게 반응계로부터 제거할 수 있다.
용매로서 구체적으로는 에틸시클로헥산(비점: 132℃, SP값: 8.18), C9계 시클로헥산[마루젠 세키유 제조, 상품명: 스와클린 #150](비점: 149℃, SP값: 7.99), n-옥탄(비점: 125℃, SP값: 7.54) 등이 예시되며, 이들로 이루어지는 군에서 선택되는 적어도 1종인 것이 바람직하다. 용매는 1종 단독이어도, 2종 이상을 조합하여 사용해도 된다.
용매가 2종 이상의 조합인 경우, 아미노알코올과 상용되지 않는 주 용제와, 아미노알코올과 상용 가능한 보조 용제를 포함하는 것이 바람직하다. 주 용제의 구체예는 이미 설명한 바와 같다. 보조 용제의 비점의 바람직한 형태는 주 용제와 마찬가지이다. 보조 용제의 SP값은 주 용제보다도 큰 것이 바람직하고, 아미노알코올과 상용될 정도로 큰 것이 보다 바람직하다. 보조 용제의 구체예로서는 EO계 글리콜에테르, PO계 글리콜에테르, 디알킬글리콜에테르 등의 글리콜에테르를 들 수 있다. 보다 구체적으로는 메틸디글리콜, 이소프로필글리콜, 부틸글리콜 등의 EO계 글리콜에테르; 메틸프로필렌디글리콜, 메틸프로필렌트리글리콜, 프로필프로필렌글리콜, 부틸프로필렌글리콜 등의 PO계 글리콜에테르, 디메틸디글리콜 등의 디알킬 글리콜에테르 등을 들 수 있으며, 이들로 이루어지는 군에서 선택되는 적어도 1종이 바람직하다. 또한 이들 보조 용제는 모두 닛폰 뉴카자이(주) 등으로부터 입수 가능하다.
용매가 2종 이상의 조합인 경우, 용매의 SP값은, 용매에 포함되는 각각의 용매의 SP값과 몰 용적을 고려한 평균 SP값으로서 산출된다. 구체적으로 평균 SP값은, 용매가 용매 1과 용매 2의 2종을 포함하는 경우, 아래 식에 의하여 산출된다.
δ3=〔V1×δ1+V2×δ2〕/(V1+V2)
δ3: 혼합 용매의 평균 SP값, δ1: 용매 1의 SP값, V1: 용매 1의 몰 용적, δ2: 용매 2의 SP값, V2: 용매 2의 몰 용적
반응액에 포함되는 용매량은, 구리 이온의 농도가 1.0 내지 2.5몰/리터가 되도록 선택되는 것이 바람직하고, 1.5 내지 2.5몰/리터가 되도록 선택되는 것이 보다 바람직하다. 반응액 중의 구리 이온 농도가 1.0몰/리터 이상이면 생산성이 보다 향상되고, 2.5몰/리터 이하이면 반응액의 점도 상승이 억제되어 양호한 교반성이 얻어진다.
(착화합물)
포름산구리, 아미노알코올, 지방족 카르복실산(바람직하게는 장쇄 카르복실산) 및 용매를 포함하는 반응액으로부터는, 포름산구리에서 유래하는 착화합물이 생성된다. 착화합물의 구조는 특별히 한정되지 않으며, 1종만을 포함하고 있어도 되고, 2종 이상을 포함하고 있어도 된다. 또한 반응액 중에 존재하는 착화합물은 열분해 처리의 진행에 수반하여 그의 구성이 변화되어도 된다. 즉, 열분해 처리의 초기에 있어서 주로 존재하는 착화합물과, 열분해 처리의 후기에 있어서 주로 존재하는 착화합물은 서로 구성이 상이한 것이어도 된다.
반응액 중에 생성되는 착화합물로서는, 구리 이온과 배위자로서의 포름산 이온 및 아미노알코올을 포함하는 것이 바람직하다. 배위자로서 아미노알코올을 포함함으로써 착화합물의 열분해 온도가 저하된다. 반응액 중에 생성되는 착화합물로서 구체적으로는, 1개의 구리 이온에 2분자의 포름산 이온과 2분자의 아미노알코올이 배위된 착화합물, 1개의 구리 이온에 1분자의 포름산 이온과 1분자의 지방족 카르복실산과 2분자의 아미노알코올이 배위된 착화합물 등을 들 수 있다. 착화합물은 열분해 처리의 적어도 초기에 있어서는, 포름산구리, 아미노알코올 및 지방족 카르복실산으로부터 형성되는 지방족 카르복실산 구리 착체를 포함하는 것이 바람직하다.
반응액 중에 생성된 착화합물은 열분해 처리에 의하여 금속 구리를 생성한다. 열분해 처리의 온도는 착화합물의 구조 등에 따라 적절히 선택하면 된다. 일반적으로 포름산구리의 열분해 온도는 약 220℃이지만, 포름산구리가 아미노알코올과 함께 착화합물을 형성함으로써, 예를 들어 일본 특허 공개 제2008-013466호 공보 등에 기재되어 있는 바와 같이 그의 열분해 온도는 110℃ 내지 120℃ 정도가 된다고 생각된다. 따라서 열분해 처리의 온도는 100℃ 내지 130℃인 것이 바람직하고, 110℃ 내지 130℃인 것이 보다 바람직하다. 열분해 처리의 온도가 130℃ 이하이면, 지방족 카르복실산과 아미노알코올과의 탈수 반응에 의한 산 아미드의 생성이 억제되어, 얻어지는 피복 구리 입자의 세정성이 향상되는 경향이 있다.
착화합물의 열분해 처리에 의하여 금속 구리가 생성되고, 생성된 금속 구리의 표면에, 반응액 중에 존재하는 지방족 카르복실산이 흡착함으로써, 지방족 카르복실산으로 표면이 피복된 피복 구리 입자를 얻을 수 있다. 금속 구리의 표면으로의 지방족 카르복실산의 흡착은 물리 흡착인 것이 바람직하다. 이것에 의하여 피복 구리 입자의 소결성이 향상된다. 착화합물의 열분해 처리에 있어서, 산화구리의 생성을 억제함으로써 지방족 카르복실산의 물리 흡착이 촉진된다.
열분해 처리에 있어서는, 착화합물의 열분해 반응에 수반하여 생성되는 물의 적어도 일부를 제거하는 것이 바람직하다. 열분해 처리에 있어서 물의 제거를 행함으로써 산화구리의 생성을 보다 효율적으로 억제할 수 있다. 물의 제거 방법은 특별히 제한되지 않으며, 통상 이용되는 수분 제거 방법으로부터 적절히 선택할 수 있다. 예를 들어 용매로서 물과 공비 혼합물을 형성할 수 있는 유기 용제를 사용하여, 공비에 의하여 생성되는 물을 제거하는 것이 바람직하다.
열분해 처리의 시간은 열분해 처리의 온도 등에 따라 적절히 선택하면 된다. 예를 들어 30분 간 내지 180분 간으로 할 수 있다. 또한 열분해 처리의 분위기는 질소 분위기 등의 불활성 분위기인 것이 바람직하다.
피복 구리 입자의 제조 방법에 있어서, 생성되는 피복 구리 입자의 입도 분포를 제어하는 인자로서는, 예를 들어 지방족 카르복실산의 종류와 첨가량, 포름산구리 착체의 농도 및 혼합 용매의 비율(주 용제/보조 용제) 등으로 결정된다. 피복 구리 입자의 크기를 제어하는 인자는, 금속 핵 발생 수를 지배하는 승온 속도, 즉, 반응계로의 투입 열량과 마이크로 반응장의 크기와 관계된 교반 속도를 적절히 유지함으로써 고르게 할 수 있다.
피복 구리 입자의 제조 방법은, 포름산구리, 아미노알코올, 지방족 카르복실산 및 용매를 포함하는 반응액을 조제하고 원하는 온도에서 열분해 처리를 행한다는 용이한 조작으로, 입자 직경이 고르고 내산화성과 소결성이 우수한 피복 구리 입자를 효율적으로 제조할 수 있다.
피복 구리 입자의 제조 방법에 있어서는, 입도 분포가 좁은 피복 구리 입자가 얻어진다. 이는, 예를 들어 이하와 같이 생각할 수 있다. 즉, 포름산구리를 반응 용매에 가용화하기 위한 착화제로서의 아미노알코올과 용매와의 SP값의 차인 ΔSP값을, 예를 들어 4.2 이상으로 함으로써, 포름산구리아미노알코올 착체 또는 포름산의 1분자가 지방족 카르복실산으로 치환된 포름산구리아미노알코올 착체의 상태에서는 용해되어 있지만, 착체가 열분해되어 착화제인 아미노알코올이 유리되면, 유리된 아미노알코올은 용매와는 상용될 수 없어 2상을 형성하기 시작한다. 그리고 유리된 아미노알코올은 포름산구리나 포름산구리아미노알코올 착체와 친화성이 높아, 포름산구리가 새로운 착화제 또는 용제로서 거동하여 극성이 높은 내 핵(액적)을 형성하고, 외측을 극성이 낮은 용매가 둘러싸는 유중수 에멀션(Water in oil Emulsion)과 유사한 2상 구조를 취하게 되며, 이것이 마이크로 반응장으로서 기능한다고 추정된다.
또한 반응계 중의 물도, 지방족 카르복실산의 치환으로 탈리된 포름산도 이 마이크로 반응장에 존재하고 있다. 마이크로 반응장 중에 금속 핵, 그의 성장 입자 및 금속 핵의 발생원인 포름산구리아미노알코올 착체, 포름산의 1분자가 지방족 카르복실산으로 치환된 포름산구리아미노알코올 착체, 물 및 포름산이 격리되어 반응이 진행된다. 지방족 카르복실산이 금속 구리 성장 입자의 피복재로서 고정화되어 감소함에 따라 반응 초기에는 포름산구리 착체의 열분해 기구가 후술하는 반응식 1 내지 3으로 진행되고 있었던 것이 점차 반응식 4의 기구로 진행되게 되어, 발생 가스 성분이 변화되게 된다. 마이크로 반응장에서는, 반응식 5에 나타내는 물에 의한 포름산구리아미노알코올 착체의 가수분해로 CuO가 생성되지만 반응식 6 또는 반응식 7을 경유하여 다시 환원되기 때문에, 아산화구리나 산화구리를 포함하지 않는 구리 입자가 제조 가능하게 되어 있다. 또한 마이크로 반응장에 포함되는 구리 원자수가 한정되어 있기 때문에 구리 입자의 입자 직경은 일정하게 제어된다.
(반응식 1)
(HCOO-)(HCOO-)Cu2 +·(H2NC3H6OH)2+C11H23COOH
→ (C11H23COO-)(HCOO-)Cu2 +·(H2NC3H6OH)2+HCOOH
(반응식 2)
(C11H23COO-)(HCOO-)Cu2 +·(H2NC3H6OH)2
→ Cu:C11H23COOH+2H2NC3H6OH+CO2
(반응식 3)
Cu:C11H23COOH
↑↓
Cu+C11H23COOH
(반응식 4)
(HCOO-)(HCOO-)Cu2 +·(H2NC3H6OH)2
→ Cu+2H2NC3H6OH+H2+2CO2
(반응식 5)
(HCOO-)(HCOO-)Cu2 +·(H2NC3H6OH)2+H2O
→ CuO+2H2NC3H6OH+2HCOOH
(반응식 6)
2CuO+2HCOOH → Cu2O+HCOOH+H2O+CO2
→ 2Cu+2H2O+2CO2
(반응식 7)
CuO+2HCOOH
→ (HCOO-)(HCOO-)Cu2 ++H2O
그리고 마이크로 반응장에, 표면에 산화구리가 형성되어 있지 않은 구리 입자가 생성되기 때문에, 마이크로 반응장에 존재하는 지방족 카르복실산이 물리 흡착되기 쉬워져, 입자 직경이 고르고 내산화성과 소결성이 우수한 피복 구리 입자가 효율적으로 얻어진다고 생각할 수 있다. 또한 상기 반응식에서는 편의상 아미노알코올을 프로판올아민, 지방족 카르복실산을 라우르산으로서 기재했지만, 이들에 한정되지 않는 것은 물론이다.
피복 구리 입자의 제조 방법은, 열분해 처리 후에 피복 구리 입자의 세정 공정, 분리 공정, 건조 공정 등을 더 갖고 있어도 된다. 피복 구리 입자의 세정 공정으로서는, 예를 들어 유기 용제에 의한 세정 공정을 들 수 있다. 세정 공정에 사용하는 유기 용제로서는 메탄올 등의 알코올 용제, 아세톤 등의 케톤 용제 등을 들 수 있다. 이들은 1종 단독이어도, 2종 이상을 조합하여 사용해도 된다.
<도전성 조성물>
본 실시 형태의 도전성 조성물은, 이미 설명한 피복 구리 입자 중 적어도 1종과, 매체를 포함한다. 도전성 조성물은 배선 패턴, 접합층 등의 형성에 적합하게 사용할 수 있으며, 저온에서, 도전성이 우수한 배선 패턴, 접합층 등을 용이하게 형성할 수 있다.
도전성 조성물에 포함되는 매체의 구성은 도전성 조성물의 목적 등에 따라 적절히 선택할 수 있다. 예를 들어 도전성 조성물이 스크린 인쇄용인 경우, 매체로서는 탄화수소계 용제, 고급 알코올계 용제, 셀로솔브, 셀로솔브아세테이트계 용제 등을 들 수 있다. 또한 스크린 인쇄용의 도전성 조성물의 고형분 농도는, 예를 들어 40 내지 95질량%로 할 수 있다. 여기서 도전성 조성물의 고형분이란, 불휘발성 성분의 총량을 의미한다.
또한 예를 들어 도전성 조성물이 잉크젯 인쇄용인 경우, 매체로서는 탄화수소계 용제, 고급 알코올계 용제, 셀로솔브, 셀로솔브아세테이트계 용제 등을 들 수 있다. 잉크젯 인쇄용의 도전성 조성물의 고형분 농도는, 예를 들어 40 내지 90질량%로 할 수 있다.
도전성 조성물은 피복 구리 입자 및 매체에 더해, 필요에 따라 기타 첨가제를 더 포함할 수 있다. 기타 첨가제로서는, 예를 들어 실란 커플링제, 티타네이트 커플링제 등의 커플링제, 폴리에스테르계 분산제, 폴리아크릴산계 분산제 등의 분산제 등을 들 수 있다.
<회로 형성물>
본 실시 형태의 회로 형성물은, 기재와, 기재 상에 배치되는 상기 도전성 조성물의 열처리물인 배선 패턴 또는 접합층을 구비한다. 배선 패턴 또는 접합층이 상기 도전성 조성물로 형성됨으로써 배선 패턴 또는 접합층의 도전성이 우수하다. 또한 저온에서 배선 패턴 또는 접합층을 형성할 수 있기 때문에 기재의 선택지의 자유도가 크다.
기재의 재질로서는, 예를 들어 폴리이미드 필름, 유리, 세라믹스, 금속 등을 들 수 있다. 기재의 두께는 특별히 제한되지 않으며, 목적 등에 따라 적절히 선택할 수 있다. 기재의 두께는, 예를 들어 0.01㎜ 이상 5㎜ 이하로 할 수 있다.
배선 패턴의 형성은, 예를 들어 기재 상에 도전성 조성물을 원하는 패턴이 되도록 부여하고, 부여된 도전성 조성물을 열 처리함으로써 행할 수 있다. 도전성 조성물을 사용함으로써, 원하는 패턴을 갖고 도전성이 우수한 배선 패턴을 효율적으로 저온에서 형성할 수 있다. 또한 접합층은, 예를 들어 반도체 소자가 다이 본드 접합으로 배치되는 영역이며, 그의 형상, 크기, 두께 등은 목적 등에 따라 적절히 선택하면 된다. 즉, 회로 형성물은, 예를 들어 기재를 준비하는 공정과, 기재 상에 도전성 조성물을 부여하는 공정과, 도전성 조성물을 열처리하는 공정을 포함하는 제조 방법으로 제조할 수 있다.
도전성 조성물의 부여 방법은 특별히 제한되지 않으며, 예를 들어 잉크젯 인쇄법, 스크린 인쇄법, 플렉소 인쇄법, 디스펜스법 등으로 행할 수 있다. 도전성 조성물의 부여량은 목적 등에 따라 적절히 선택할 수 있으며, 예를 들어 열처리 후의 두께가 1㎛ 이상 100㎛ 이하가 되도록 할 수 있다.
도전성 조성물의 열처리 온도는, 예를 들어 200 내지 600℃로 할 수 있으며, 200 내지 450℃인 것이 바람직하다. 열처리의 시간은, 예를 들어 1 내지 120분 간으로 할 수 있으며, 1 내지 60분 간인 것이 바람직하다. 열처리의 분위기는 저산소 분위기인 것이 바람직하다. 저산소 분위기로서는 질소 분위기, 아르곤 분위기 등을 들 수 있다. 또한 산소 농도가 1,000ppm 이하인 것이 바람직하다.
실시예
이하, 본 발명을 실시예에 의하여 구체적으로 설명하지만, 본 발명은 이들 실시예에 한정되는 것은 아니다.
실시예에서 사용한 시험 방법의 상세를 이하에 나타낸다.
<평균 1차 입자 직경 및 변동률의 계산>
측정 장치: 니혼 덴시 제조의 FE-EPMA JXA-8510F
평균 1차 입자 직경: 샘플 20점의 평균값
변동률: 샘플 20점의 표준 편차/평균값으로 계산되는 값
<SEM 화상 관찰>
측정 장치: 니혼 덴시 제조의 FE-EPMA JXA-8510F
측정 조건: 가속 전압: 6KV 또는 15KV
관찰 배율: ×10,000 내지 ×75,000
<분체 X선 회절(XRD) 측정>
측정기: 시마즈 제조의 XRD-6100
측정 조건: 타깃: Cu
관 전압: 40KV, 관 전류: 30.0㎃
<Tof-SIMS(비행 시간형 2차 이온 질량 분석 장치) 측정>
측정기; 알박파이(ULVAC-PHI) 제조의 PHI TRIFT Ⅳ형
측정 조건: 1차 이온종: Au, 가속 전압: 30KV
<TG-DTA 측정> 유기 잔분 및 금속 함유량의 측정
측정 장치: 리가쿠 제조의 TG8120
승온 속도: 10℃/min
측정 온도 범위: 25℃ 내지 600℃
측정 분위기: 질소: 100ml/min
<LC(액체 크로마토그래피) 측정>
측정기: 워터스(Waters) 제조의 ACQUITY UPLC H-Class System
칼럼: ACQUITY UPLC(R) BEH C18 1.7㎛ 2.1×50㎜
측정 온도: 50℃
측정 용매: 물/아세토니트릴
유량: 0.8mL/min
LC 측정용의 샘플은 이하와 같이 하여 조제하였다.
샘플 병에 피복 구리 입자 1g, 아세토니트릴 9mL를 첨가하였다. 거기에 0.36중량% 염산 수용액 1mL를 첨가하였다. 이 혼합 용액을 30min 초음파 조사 처리하고 교반·혼합하였다. 추출 처리 완료 후 슬러리액을 정치하고 고액 분리한 후, 상청을 채취하였다. 그 상청을 0.2㎛ 필터로 여과하여 LC 측정용의 샘플로 하였다.
<적외 흡수 스펙트럼 측정>
측정기: 퍼킨엘머 AutoIMAGE FT-IR Microscope
(실시예 1)
교반기, 온도계, 환류 냉각관, 75mL 딘스타크관, 질소 도입관을 구비한 3000mL 유리제 4구 플라스크를 오일 배스에 설치하였다. 거기에, 포름산구리 무수물 484g(3.1몰)과, 라우르산(간토 가가쿠사 제조) 34.0g(0.055당량/포름산구리 무수물)과, 반응 용매로서 트리프로필렌글리콜모노메틸에테르(도쿄 가세이 고교사 제조) 150g(0.23당량/포름산구리 무수물) 및 스와클린 150(고도사 제조) 562g(1.42당량/포름산구리 무수물)을 첨가하고, 200rpm으로 교반하면서 혼합하였다. 질소 분위기 하에서 액 온도가 50℃가 되기까지 200rpm으로 가온 교반하였다. 거기에 3-아미노-1-프로판올(도쿄 가세이 고교사 제조) 472g(2.00당량/포름산구리 무수물)을 천천히 적하하였다. 적하 종료 후, 약 1℃/min의 승온 속도로 액 온도가 120℃ 부근이 되기까지 340rpm으로 가온 교반하였다. 딘스타크관에 의하여 포획된 수층은 적시 제거하여 반응계 내에 환류되지 않도록 하였다. 액 온도가 상승함에 따라 반응 용액은 농청색에서 다갈색으로 변화되기 시작하고, 탄산 가스의 발포가 발생하였다. 탄산 가스의 발포가 잦아든 시점을 반응 종점으로 하여 오일 배스 온도 조절을 정지시키고 실온까지 냉각하였다.
실온까지 냉각 후, 메탄올(간토 가가쿠사 제조) 550g을 첨가하고 혼합시켰다. 이 혼합 용액을 30분 이상 정치하고 상청을 데칸테이션하여 침전물을 얻었다. 이 침전물에 메탄올(간토 가가쿠사 제조) 550g, 아세톤(간토 가가쿠사 제조) 300g을 첨가하고 혼합하였다. 이 혼합 용액을 30분 이상 정치하고 상청을 데칸테이션하여 침전물을 얻고, 이 조작을 추가로 1회 더 반복하였다. 이 침전물에 메탄올(간토 가가쿠사 제조) 550g을 사용하여 공세척하면서 500mL 가지형 플라스크로 옮겼다. 30분 이상 정치하고 상청을 데칸테이션하여 얻어진 침전물을 회전식 증발기에 설치하고, 40℃, 1㎪ 이하에서 진공 건조하였다. 진공 건조 종료 후, 실온까지 냉각하고 질소 치환하면서 감압 해제하여 194g의 다갈색의 피복 구리 입자를 얻었다.
(실시예 2)
실시예 1에 있어서, 라우르산 대신 올레산을 사용한 것 이외에는 실시예 1과 마찬가지로 하여 피복 구리 입자 200g을 얻었다.
(실시예 3)
실시예 1에 있어서, 라우르산 대신 스테아르산을 사용한 것 이외에는 실시예 1과 마찬가지로 하여 피복 구리 입자 200g을 얻었다.
(실시예 4)
실시예 1에 있어서, 라우르산을 68.1g, 3-아미노-1-프로판올을 712g으로 변경한 것 이외에는 실시예 1과 마찬가지로 하여 피복 구리 입자 200g을 얻었다.
(실시예 5)
실시예 4에 있어서, 승온 속도를 약 0.5℃/min으로 변경한 것 이외에는 실시예 4와 마찬가지로 하여 피복 구리 입자 200g을 얻었다. 실시예 4보다 평균 1차 입자 직경이 큰 것을 얻었다.
(비교예 1)
일본 특허 공개 제2013-047365호 공보의 실시예 1에 기재된 방법에 준하여, 이하와 같이 하여 피복 구리 입자를 합성하였다.
구리 화합물로서 아산화구리(Ⅰ)(후루카와 케미컬사 제조)를 71.5g(0.5몰), 피복재로서 아세트산 15.0g(250m㏖), 환원제로서 히드라진·1수화물(와코 준야쿠 고교사 제조〕 25.0g(0.5몰), 용매로서 이소프로판올을 500ml 혼합하고 1,000ml의 4구 플라스크에 첨가하였다. 플라스크에는 냉각기, 온도계, 질소 도입관 및 교반 장치를 설치하였다. 질소를 200ml/min을 통기하면서, 교반하면서 70℃까지 승온시키고 2시간 가열·교반을 계속하여 아산화구리(Ⅰ)를 환원시켜, 피복 구리 입자 분산액을 얻었다.
피복 구리 입자 분산액을 기리야마 여과지 No. 5B로 감압 여과하여 분체를 여과 분별하였다. 여과 분별한 분체를 메탄올(간토 가가쿠사 제조)로 3회 세정하고 40℃, 1㎪ 이하에서 감압 건조시키고, 실온까지 냉각 후에 질소 치환을 하여 취출하여 62g의 다갈색 분체를 얻었다.
(비교예 2)
일본 특허 공개 제2002-332502호 공보의 실시예에 준하여, 이하와 같이 하여 표면 처리 구리 분말을 얻었다. 50g의 메탄올(간토 가가쿠사 제조) 중에 평균 1차 입자 직경 672㎚의 구리 분말 25g와 올레산(니치유사 제조) 0.025g을 첨가하고 교반 혼합하여, 구리 분말 표면에 표면 처리층을 형성하였다. 그 후, 기리야마 여과지 No. 5B로 감압 여과하여 분체를 여과 분별하였다. 여과 분별한 분체에 메탄올(간토 가가쿠사 제조) 25g을 적하함으로써 표면 처리 구리 분말을 여과 세정하고, 40℃, 1㎪ 이하에서 감압 건조시키고, 실온까지 냉각 후에 질소 치환을 하여 취출하여 20g의 다갈색 분체를 얻었다.
<평가>
상기에서 제조된 피복 구리 입자를 사용하여 지방족 카르복실산으로 피복된 피복 구리 입자의 조성을 밝히기 위하여, 분체 X선 분석(XRD 측정), SEM 화상 관찰, Tof-SIMS 측정, TG-DTA 측정 및 LC 측정 등을 실시하였다.
실시예 1에서 제조된 피복 구리 입자의 핵의 구조와 입자 직경을 조사하기 위하여 분체 X선 측정을 실시하였다. 분체 X선 측정의 결과를 도 1에 나타낸다. 도 1에 나타낸 바와 같이, 환원 구리에서 유래한 피크(2θ=43.3° 부근)가 검출되고, 산화구리(2θ=35.5° 및 38.7°), 아산화구리(2θ=37.0° 부근)는 검출되지 않았다. 이 결과로부터, 본 실시 형태에 의한 피복 구리 입자는 산화물층이 없고, 환원 구리를 핵으로 하여 형성되어 있는 것을 알 수 있다.
결정 입자 직경을 분체 X선의 회절 각도와 반값 폭으로부터 셰러(Scherrer)의 식으로부터 산출하였다. 셰러(Scherrer)의 식은 식 (1)로 표시된다.
D=Kλ/(βcosθ) … (1)
여기서, D는 결정 입자 직경, K는 셰러(Scherrer) 상수(구체로 가정하고 K=1로서 대입), λ는 측정 X선의 파장(CuKα: 1.5418Å), β는 식 (2)로 표시된다.
β=b-B … (2)
여기서, b는 피크의 반값 폭, B는 장치의 보정 계수(B=0.114)이다.
계산 결과로부터, 피복 구리 입자의 결정자 직경 DXRD는 31.3㎚였다. SEM 관찰 결과(도 2)로부터 산출된 평균 1차 입자 직경 DSEM은 59.2㎚이므로, DXRD/DSEM을 계산하면 0.53이 되어 평균 1차 입자 직경에 대한 결정자 직경이 비교적 큰 것을 알 수 있다.
실시예 1에서 얻어진 피복 구리 입자의 표면 조성을 조사하기 위하여 Tof-SIMS 측정을 실시하였다. Tof-SIMS 측정의 결과(도 3)에 의하면 거의 정량적으로 프리의 라우르산이 검출되었다. 63Cu 및 65Cu와 결합해 있는 라우르산이 검출되지 않은 점에서, 피복 구리 입자 표면에 존재하는 것은 대체로 물리적인 흡착에 의하여 피복되는 라우르산인 것을 알 수 있었다.
실시예 1에서 얻어진 피복 구리 입자에 대하여, 구리 입자의 표면을 피복하고 있는 라우르산이 어떻게 금속 표면에 부착되어 있는 것인지 조사하기 위하여 적외 흡수(IR) 스펙트럼 측정을 행하였다. IR 스펙트럼 측정 결과(도 4)에 의하면 카르복실산-금속염에서 유래한 신축 진동 피크만이 검출되었다. 유리된 카르복실산의 신축 진동 피크가 보이지 않은 점에서, 라우르산은 단분자막을 형성하여 구리 표면에 물리 흡착되어 있는 것이 시사된다.
실시예 1에서 얻어진 피복 구리 입자에 있어서 표면을 피복하고 있는 유기 성분량을 조사하기 위하여 TG-DTA 측정을 실시하였다(도 5). TG-DTA 측정 결과로부터, 가열 감량은 1.79질량%이며, 라우르산의 비점 부근에서는 거의 모두 탈리하고 있는 것을 알 수 있다. 이 결과로부터도, 라우르산이 물리적으로 흡착되어 있는 것이 시사되며, 피복 구리 입자가 저온 소결성을 발현 가능하다고 추측된다.
실시예 1에서 얻어진 피복 구리 입자에 포함되는 유기 성분에 대하여 LC 측정을 행하였다. LC 측정의 결과에 의하면 유기 성분으로서는 라우르산이 주로 검출되었다.
구리 입자의 표면을 피복하고 있는 지방족 카르복실산의 피복 밀도를 이하의 방법으로 산출하였다.
LC 측정의 해석 결과에 따라 가열 감량 성분의 전량을 라우르산으로 하면, 피복 구리 입자에 포함되는 라우르산의 분자수는 식 (3)으로 표시된다.
[라우르산 분자수]=Macid/(MW/NA) … (3)
여기서, Macid는 가열 감량 측정 질량값(g), MW는 라우르산 분자량(g/㏖), NA는 아보가드로 상수(6.02×1023개/㏖)이다.
SEM 관측에 의하여 산출된 1차 입자 직경은 거의 모두 환원 구리 유래로 하고, 그의 형상은 구체라 가정하면, 구리 입자 1g 중의 입자 수는 식 (4)로 표시된다.
[1g 중의 입자 수]=MCu/[(4πr3/3)×d×10-21] … (4)
여기서, MCu는 가열 감량 측정값으로부터 구해지는 질량 계산값(g), r은 SEM 관측에 의하여 산출된 1차 입자 직경의 반경(㎚), d는 밀도이다(구리의 밀도로서 대입하였음; d=8.94). 구리 입자 1g 중의 입자 표면적은 식 (4)를 이용하여 식 (5)로 표시된다.
[1g 중의 구리 입자 표면적(㎚2)]=[1g 중의 입자 수]×4πr2 … (5)
라우르산에 의한 구리 입자의 피복 밀도(분자/㎚2)는 (3) 식 및 (5) 식을 이용하여 식 (6)으로 표시된다.
[피복 밀도]=[라우르산 분자수]/[1g 중의 구리 입자 표면적] … (6)
계산 결과로부터, 피복 구리 입자에 있어서의 라우르산의 피복 밀도는 4.83분자/㎚2였다.
『화학과 교육 40권 2호(1992년) 스테아르산 분자의 단면적을 구하다-실험값과 계산값-』으로부터, 스테아르산 분자의 반 데르 발스(Van der waals) 반경으로부터 최소 면적이 산출되어 있으며, 그 계산값으로부터 환산되는 포화 피복 면적 이론값은 약 5.00분자/㎚2이다. 이 이론값으로부터, 본 실시 형태의 피복 구리 입자는 비교적 고밀도로 라우르산이 입자 표면에 흡착되어 있다고 추측된다. 이 농밀한 피복 효과가, 라우르산 피복이 화학 흡착보다도 약한 물리 흡착임에도 불구하고 내산화성이 우수한 이유라고 생각된다.
다음으로, 실시예 2에서 얻어진 피복 구리 입자에 대하여 상기와 마찬가지로 하여 평가를 행하였다. SEM 관찰(도 6) 및 XRD 측정의 결과로부터, 평균 1차 입자 직경은 65.7㎚이고 결정자 직경은 33.9㎚였다.
또한 IR 스펙트럼 측정 결과(도 7)에 의하면 카르복실산-금속염에서 유래한 신축 진동 피크만이 검출되었다. 유리된 카르복실산의 신축 진동 피크가 보이지 않았던 점에서, 올레산은 단분자막을 형성하여 구리 표면에 물리 흡착되어 있는 것이 시사된다.
TG-DTA 측정 결과로부터, 가열 감량은 1.68질량%이며, 올레산의 비점 부근에서는 거의 모두 탈리하고 있는 것을 알 수 있었다.
LC 측정을 행하였다. LC 측정의 결과에 의하면 유기 성분으로서는 올레산이 주로 검출되었다.
실시예 2에서 얻어진 피복 구리 입자에 대하여, 구리 입자의 표면을 피복하고 있는 올레산의 피복 밀도를 상기와 마찬가지로 하여 산출한바, 3.53분자/㎚2였다.
올레산은 이중 결합을 갖는 불포화 지방산이며, 이 이중 결합의 위치에서 구부러진 분자 구조를 취하고 있다. 라우르산과 같은 포화 지방산과 비교하여, 올레산이 단분자막을 형성할 때, 그의 입체 장애로부터 액체 팽창막을 형성하기 쉽다. 「에멀션의 과학(Ⅴ) 하나이 데쓰야 저」(조리 과학, 7권, 3호, 1974년)로부터, 표면막압 대 분자 면적의 관계 플롯으로부터, 수면 상의 표면막 모델에 있어서의 올레산의 피복 밀도는 약 1.25분자/㎚2라고 산출할 수 있다.
이에 비해, 실시예 2에서 제조된 피복 구리 입자는 비교적 고밀도의 피복 효과가 보이며, 액체 응집막에 가까운 단분자막을 형성하고 있는 것을 알 수 있었다.
비교예 2에서 얻어진 피복 구리 입자에 대하여, 구리 입자의 표면을 피복하고 있는 올레산의 피복 밀도를 상기와 마찬가지로 하여 산출한바, 1.17분자/㎚2였다.
이상의 평가를 실시예 3 내지 5에 대해서도 행하였다. 결과를 하기 표에 정리하여 나타낸다.
(시험예 1) 내산화성의 평가
실시예 1에서 제조된 직후의 분체 X선 측정 결과(도 1)과 25℃, 대기 분위기 하에서 2개월 저장한 후에 마찬가지로 측정하여 산화의 진행의 유무를 확인하였다(도 8). 2개월 후에도 산화 성분은 검출되지 않아, 본 실시 형태의 피복 구리 입자는 우수한 내산화성을 갖는 것이 확인되었다.
한편, 비교예 1에서 제조된 직후의 분체 X선 측정 결과와 25℃, 대기 분위기 하에서 2개월 저장한 후에 마찬가지로 측정한 결과를 도 9에 나타낸다. 도 9에 나타낸 바와 같이, 비교예 1의 조건에서 제조된 피복 구리 입자에서는 2개월 후에 아산화구리에서 유래하는 시그널이 명확히 관측되었다.
일본 특허 출원 제2014-203242호(출원일: 2014년 10월 1일)의 개시는 그의 전체가 참조에 의하여 본 명세서에 도입된다. 본 명세서에 기재된 모든 문헌, 특허출원 및 기술 규격은, 개개의 문헌, 특허출원 및 기술 규격이 참조에 의하여 도입되는 것이 구체적이고도 개별적으로 기재된 경우와 동일한 정도로, 본 명세서에 참조에 의하여 도입된다.
Claims (9)
- 구리 입자와,
구리 입자의 표면에 1㎚2당 2.5분자 이상 5.2분자 이하의 밀도로 배치되는 지방족 카르복실산을 포함하는 피복층을 포함하는, 피복 구리 입자. - 제1항에 있어서, 지방족 카르복실산의 지방족기의 탄소수가 5 내지 17인, 피복 구리 입자.
- 제1항 또는 제2항에 있어서, 지방족 카르복실산이 구리 표면에 물리 흡착되어 있는, 피복 구리 입자.
- 제1항 내지 제3항 중 어느 한 항에 있어서, 피복층이 지방족 카르복실산 구리 착체의 열분해물인, 피복 구리 입자.
- 제1항 내지 제4항 중 어느 한 항에 있어서, 구리 산화물 및 구리 수산화물의 총 함유율이 5질량% 이하인, 피복 구리 입자.
- 제1항 내지 제5항 중 어느 한 항에 있어서, 평균 1차 입자 직경이 0.02㎛ 이상 5.0㎛ 이하인, 피복 구리 입자.
- 매체 중에서 지방족 카르복실산 구리 착체를 열분해하는 것을 포함하는, 제1항 내지 제6항 중 어느 한 항에 기재된 피복 구리 입자의 제조 방법.
- 제1항 내지 제6항 중 어느 한 항에 기재된 피복 구리 입자와, 매체를 포함하는 도전성 조성물.
- 기재와, 기재 상에 배치되고, 제8항에 기재된 도전성 조성물의 열처리물인 배선 패턴 또는 접합층을 구비하는 회로 형성물.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2014203242A JP6368925B2 (ja) | 2014-10-01 | 2014-10-01 | 被覆銅粒子及びその製造方法 |
| JPJP-P-2014-203242 | 2014-10-01 | ||
| PCT/JP2015/076764 WO2016052275A1 (ja) | 2014-10-01 | 2015-09-18 | 被覆銅粒子及びその製造方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20170067785A true KR20170067785A (ko) | 2017-06-16 |
| KR102200822B1 KR102200822B1 (ko) | 2021-01-12 |
Family
ID=55630315
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020177010816A KR102200822B1 (ko) | 2014-10-01 | 2015-09-18 | 피복 구리 입자 및 그의 제조 방법 |
Country Status (5)
| Country | Link |
|---|---|
| JP (1) | JP6368925B2 (ko) |
| KR (1) | KR102200822B1 (ko) |
| CN (1) | CN107073578B (ko) |
| TW (1) | TWI648111B (ko) |
| WO (1) | WO2016052275A1 (ko) |
Families Citing this family (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP3712904A4 (en) | 2017-11-13 | 2021-08-25 | Kyocera Corporation | PASTE COMPOSITION, SEMICONDUCTOR DEVICE AND ELECTRONIC / ELECTRIC COMPONENT |
| JP6892120B2 (ja) * | 2017-11-28 | 2021-06-18 | 協立化学産業株式会社 | 被覆金属粒子、導電性組成物、導電体、接合用積層体、回路形成物及び焼結体の製造方法 |
| JP7006872B2 (ja) * | 2017-11-29 | 2022-01-24 | 国立大学法人北海道大学 | 低温焼結性銅粒子とそれを用いた焼結体の製造方法 |
| WO2019146412A1 (ja) * | 2018-01-26 | 2019-08-01 | 日清エンジニアリング株式会社 | 銀微粒子の製造方法および銀微粒子 |
| WO2019146411A1 (ja) * | 2018-01-26 | 2019-08-01 | 日清エンジニアリング株式会社 | 微粒子の製造方法および微粒子 |
| JP6818359B2 (ja) * | 2018-03-19 | 2021-01-20 | 協立化学産業株式会社 | 導電性ペースト組成物、導電体、導電性ペースト組成物の塗工方法、及び導電体の製造方法 |
| KR20220099976A (ko) | 2019-11-18 | 2022-07-14 | 닛신 엔지니어링 가부시키가이샤 | 미립자의 제조 장치 및 미립자의 제조 방법 |
| JP7380256B2 (ja) * | 2020-01-28 | 2023-11-15 | 三菱マテリアル株式会社 | 接合用シート |
| JP7482214B2 (ja) * | 2020-03-31 | 2024-05-13 | 三井金属鉱業株式会社 | 銅粒子及びその製造方法 |
| JP7121884B1 (ja) * | 2021-03-29 | 2022-08-19 | 三菱マテリアル株式会社 | 銅粒子及びその製造方法 |
Citations (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2002332502A (ja) | 2001-05-10 | 2002-11-22 | Mitsui Mining & Smelting Co Ltd | 銅ペースト用の表面処理銅粉、その表面処理銅粉の製造方法、その表面処理銅粉を用いた銅ペースト及びその銅ペーストを用いたプリント配線板 |
| JP2003342621A (ja) | 2002-05-27 | 2003-12-03 | Mitsui Mining & Smelting Co Ltd | 銅粉の製造方法及びその方法で得られた銅粉 |
| JP2004225122A (ja) | 2003-01-23 | 2004-08-12 | Mitsui Mining & Smelting Co Ltd | 銅ペースト用の銅粉及びその銅粉の製造方法 |
| JP2008013837A (ja) * | 2006-07-10 | 2008-01-24 | Sumitomo Metal Mining Co Ltd | 微小銅粉及びその製造方法 |
| KR20080017457A (ko) * | 2005-07-25 | 2008-02-26 | 스미토모 긴조쿠 고잔 가부시키가이샤 | 구리 미립자 분산액 및 그 제조 방법 |
| KR20100087112A (ko) * | 2007-11-05 | 2010-08-03 | 스미토모 긴조쿠 고잔 가부시키가이샤 | 구리 미립자와 그 제조 방법 및 구리 미립자 분산액 |
| JP2013047365A (ja) | 2011-08-29 | 2013-03-07 | Hitachi Cable Ltd | 銅微粒子分散液およびその製造方法、銅微粒子およびその製造方法、銅微粒子を含む銅ペースト、並びに銅被膜およびその製造方法 |
| JP2013159830A (ja) * | 2012-02-06 | 2013-08-19 | Toyota Central R&D Labs Inc | 表面被覆金属ナノ粒子、およびその製造方法 |
| KR20140037043A (ko) * | 2011-02-04 | 2014-03-26 | 야마가타 유니버시티 | 피복 금속 미립자와 그 제조 방법 |
Family Cites Families (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN1061579C (zh) * | 1995-03-08 | 2001-02-07 | 上海市合成树脂研究所 | 电磁屏蔽导电涂料用铜粉的制备方法 |
| WO2002087809A1 (fr) * | 2001-04-27 | 2002-11-07 | Dowa Mining Co., Ltd. | Poudre de cuivre pour pate electroconductrice a excellente resistance a l'oxydation et procede de preparation |
| CN100542692C (zh) * | 2003-07-09 | 2009-09-23 | 福莱金属公司 | 包覆金属颗粒 |
| JP5205717B2 (ja) * | 2006-07-04 | 2013-06-05 | セイコーエプソン株式会社 | ギ酸銅錯体、銅粒子の製造方法および配線基板の製造方法 |
| KR100814295B1 (ko) * | 2006-10-10 | 2008-03-18 | 삼성전기주식회사 | 구리 나노입자의 제조방법 및 그에 의해 제조된 구리나노입자 |
| CN100556584C (zh) * | 2007-03-26 | 2009-11-04 | 中南大学 | 一种导电浆料用铜粉的表面修饰方法 |
| JP5426270B2 (ja) * | 2009-08-04 | 2014-02-26 | ハリマ化成株式会社 | 金属銅微粒子の製造方法 |
| JP5342597B2 (ja) * | 2011-04-15 | 2013-11-13 | 福田金属箔粉工業株式会社 | 銅超微粒子分散ペーストおよび導電膜の形成方法 |
| CN102601355A (zh) * | 2012-03-20 | 2012-07-25 | 昆明理工大学 | 一种提高铜金粉耐腐蚀性的表面改性方法 |
-
2014
- 2014-10-01 JP JP2014203242A patent/JP6368925B2/ja active Active
-
2015
- 2015-09-18 KR KR1020177010816A patent/KR102200822B1/ko active IP Right Grant
- 2015-09-18 WO PCT/JP2015/076764 patent/WO2016052275A1/ja active Application Filing
- 2015-09-18 CN CN201580053024.6A patent/CN107073578B/zh active Active
- 2015-09-30 TW TW104132187A patent/TWI648111B/zh active
Patent Citations (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2002332502A (ja) | 2001-05-10 | 2002-11-22 | Mitsui Mining & Smelting Co Ltd | 銅ペースト用の表面処理銅粉、その表面処理銅粉の製造方法、その表面処理銅粉を用いた銅ペースト及びその銅ペーストを用いたプリント配線板 |
| JP2003342621A (ja) | 2002-05-27 | 2003-12-03 | Mitsui Mining & Smelting Co Ltd | 銅粉の製造方法及びその方法で得られた銅粉 |
| JP2004225122A (ja) | 2003-01-23 | 2004-08-12 | Mitsui Mining & Smelting Co Ltd | 銅ペースト用の銅粉及びその銅粉の製造方法 |
| KR20080017457A (ko) * | 2005-07-25 | 2008-02-26 | 스미토모 긴조쿠 고잔 가부시키가이샤 | 구리 미립자 분산액 및 그 제조 방법 |
| JP2008013837A (ja) * | 2006-07-10 | 2008-01-24 | Sumitomo Metal Mining Co Ltd | 微小銅粉及びその製造方法 |
| KR20100087112A (ko) * | 2007-11-05 | 2010-08-03 | 스미토모 긴조쿠 고잔 가부시키가이샤 | 구리 미립자와 그 제조 방법 및 구리 미립자 분산액 |
| KR20140037043A (ko) * | 2011-02-04 | 2014-03-26 | 야마가타 유니버시티 | 피복 금속 미립자와 그 제조 방법 |
| JP2013047365A (ja) | 2011-08-29 | 2013-03-07 | Hitachi Cable Ltd | 銅微粒子分散液およびその製造方法、銅微粒子およびその製造方法、銅微粒子を含む銅ペースト、並びに銅被膜およびその製造方法 |
| JP2013159830A (ja) * | 2012-02-06 | 2013-08-19 | Toyota Central R&D Labs Inc | 表面被覆金属ナノ粒子、およびその製造方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| CN107073578B (zh) | 2019-01-15 |
| TWI648111B (zh) | 2019-01-21 |
| KR102200822B1 (ko) | 2021-01-12 |
| TW201617152A (zh) | 2016-05-16 |
| JP6368925B2 (ja) | 2018-08-08 |
| JP2016069716A (ja) | 2016-05-09 |
| WO2016052275A1 (ja) | 2016-04-07 |
| CN107073578A (zh) | 2017-08-18 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR20170067785A (ko) | 피복 구리 입자 및 그의 제조 방법 | |
| KR101743897B1 (ko) | 피복 구리 입자 및 그 제조 방법 | |
| KR101354873B1 (ko) | 금속 나노입자 분산체 | |
| JP6033485B2 (ja) | 被覆銅粒子 | |
| CN103180072B (zh) | 包覆铜微粒及其制造方法 | |
| KR20180126468A (ko) | 피복 은 입자와 그 제조 방법, 도전성 조성물, 및 도전체 | |
| JP2014001443A (ja) | 酸化物被覆銅微粒子及びその製造方法 | |
| KR20090019781A (ko) | 나노입자, 제조 방법 및 용도 | |
| WO2018190246A1 (ja) | 銅粒子混合物及びその製造方法、銅粒子混合物分散液、銅粒子混合物含有インク、銅粒子混合物の保存方法及び銅粒子混合物の焼結方法 | |
| JP6716809B2 (ja) | 銅ペースト組成物の製造方法 | |
| JP2011032558A (ja) | 金属銅微粒子の製造方法 | |
| WO2019106739A1 (ja) | 低温焼結性銅粒子とそれを用いた焼結体の製造方法 | |
| JP6209249B2 (ja) | 酸化物被覆銅微粒子の製造方法 | |
| JP6873510B2 (ja) | 複合粒子、銅ペースト組成物、および導電体 | |
| CN101522928B (zh) | 镍-铼合金粉末和含有其的导体糊 | |
| TW201842989A (zh) | 鎳粉及鎳糊 | |
| JP6892120B2 (ja) | 被覆金属粒子、導電性組成物、導電体、接合用積層体、回路形成物及び焼結体の製造方法 | |
| TWI586462B (zh) | 用於製備可在大氣壓力下被煆燒的銅奈米粒子之方法及其所製備之銅奈米粒子 | |
| JP5512487B2 (ja) | 金微粒子の製造方法 | |
| TWI707052B (zh) | 印刷用導電性糊劑及其調製方法與銀奈米粒子分散液之調製方法 | |
| CN101522929A (zh) | 镍-铼合金粉末及含有其的导体糊 | |
| TW202339875A (zh) | 金屬油墨、金屬油墨之製造方法、及金屬層之製造方法 | |
| JP2011117025A (ja) | 金属微粒子分散体の製造方法及び該製造方法を使用した後に分散媒置換する金属微粒子分散液の製造方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A201 | Request for examination | ||
| A302 | Request for accelerated examination | ||
| E902 | Notification of reason for refusal | ||
| E701 | Decision to grant or registration of patent right | ||
| GRNT | Written decision to grant |