KR101827023B1 - 금속-리간드 착체 및 촉매 - Google Patents
금속-리간드 착체 및 촉매 Download PDFInfo
- Publication number
- KR101827023B1 KR101827023B1 KR1020127024456A KR20127024456A KR101827023B1 KR 101827023 B1 KR101827023 B1 KR 101827023B1 KR 1020127024456 A KR1020127024456 A KR 1020127024456A KR 20127024456 A KR20127024456 A KR 20127024456A KR 101827023 B1 KR101827023 B1 KR 101827023B1
- Authority
- KR
- South Korea
- Prior art keywords
- metal
- formula
- cycloalkyl
- alkyl
- independently
- Prior art date
Links
- 0 C*(C)(*(C(*)C([C@](*1*)C(C)=CC=*(C)*)N)*1OC)I Chemical compound C*(C)(*(C(*)C([C@](*1*)C(C)=CC=*(C)*)N)*1OC)I 0.000 description 5
- RRIWWPGFDIHLER-DARPEHSRSA-N CCCCc(cccc1C(C)C)c1NC1=CCCC/C1=N\CCCC Chemical compound CCCCc(cccc1C(C)C)c1NC1=CCCC/C1=N\CCCC RRIWWPGFDIHLER-DARPEHSRSA-N 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F7/00—Compounds containing elements of Groups 4 or 14 of the Periodic System
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F7/00—Compounds containing elements of Groups 4 or 14 of the Periodic System
- C07F7/003—Compounds containing elements of Groups 4 or 14 of the Periodic System without C-Metal linkages
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F10/00—Homopolymers and copolymers of unsaturated aliphatic hydrocarbons having only one carbon-to-carbon double bond
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F110/00—Homopolymers of unsaturated aliphatic hydrocarbons having only one carbon-to-carbon double bond
- C08F110/02—Ethene
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F4/00—Polymerisation catalysts
- C08F4/42—Metals; Metal hydrides; Metallo-organic compounds; Use thereof as catalyst precursors
- C08F4/44—Metals; Metal hydrides; Metallo-organic compounds; Use thereof as catalyst precursors selected from light metals, zinc, cadmium, mercury, copper, silver, gold, boron, gallium, indium, thallium, rare earths or actinides
- C08F4/60—Metals; Metal hydrides; Metallo-organic compounds; Use thereof as catalyst precursors selected from light metals, zinc, cadmium, mercury, copper, silver, gold, boron, gallium, indium, thallium, rare earths or actinides together with refractory metals, iron group metals, platinum group metals, manganese, rhenium technetium or compounds thereof
- C08F4/62—Refractory metals or compounds thereof
- C08F4/64—Titanium, zirconium, hafnium or compounds thereof
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F4/00—Polymerisation catalysts
- C08F4/42—Metals; Metal hydrides; Metallo-organic compounds; Use thereof as catalyst precursors
- C08F4/72—Metals; Metal hydrides; Metallo-organic compounds; Use thereof as catalyst precursors selected from metals not provided for in group C08F4/44
- C08F4/74—Metals; Metal hydrides; Metallo-organic compounds; Use thereof as catalyst precursors selected from metals not provided for in group C08F4/44 selected from refractory metals
- C08F4/76—Metals; Metal hydrides; Metallo-organic compounds; Use thereof as catalyst precursors selected from metals not provided for in group C08F4/44 selected from refractory metals selected from titanium, zirconium, hafnium, vanadium, niobium or tantalum
Abstract
본 발명은 일반적으로, 금속-리간드 착체, 상기 금속-리간드 착체를 포함하거나 이로부터 제조된 촉매, 상기 촉매를 사용하여 올레핀 중합 반응을 촉진시켜 폴리올레핀을 제조하는 방법, 상기 방법에 의해 제조된 폴리올레핀, 상기 금속-리간드 착체 및 촉매의 제조 방법 및 이에 유용한 중간체 화합물에 관한 것이다.
Description
본 발명은 일반적으로, 금속-리간드 착체, 상기 금속-리간드 착체를 포함하거나 이로부터 제조된 촉매, 상기 촉매를 사용하여 올레핀 중합 반응을 촉진시켜 폴리올레핀을 제조하는 방법, 상기 방법에 의해 제조된 폴리올레핀, 상기 금속-리간드 착체 및 촉매의 제조 방법 및 이에 유용한 중간체 화합물에 관한 것이다.
미국 특허 제 6,096,676 호는 특히, 4족 금속을 포함하는 특정 촉매 및 촉매 전구체를 언급하고 있다.
미국 특허 제 6,114,481 호는 특히, 올레핀-유도된 공중합체를 제조하기 위한 올레핀 중합 반응용 특정 촉매 시스템 및 방법을 언급하고 있다. 촉매 시스템은 4족 금속의 특정 유기금속 착체 및 활성화제를 함유한다. 유기금속 착체는 특히, 케티마이드 리간드(즉, (Sub l)(Sub 2)C=N-)를 함유한다.
미국 특허 제 6,803,433 B2 호는 특히, 니켈, 팔라듐, 백금, 티타늄, 지르코늄, 하프늄, 바나듐 또는 스칸듐 금속을 포함하는 특정 촉매 및 메탈로엔아민 화합물을 언급하고 있다.
미국 특허 제 6,919,413 B2 호, 제 6,919,467 B2 호 및 제 7,199,255 B2 호는 특히, 1족 내지 15족 중 임의의 족의 금속 원소 및 란탄 계열 원소(문헌[Lange's Handbook of Chemistry, McGraw Hill Handbooks, 15th edition, 1999]에 개시된 원소 주기율표 참조)를 포함하는 특정 촉매 및 촉매 전구체를 언급하고 있는 패밀리 특허이다.
문헌[Adams N., et al., Discovery and evaluation of highly active imidotitaniumethylene polymerization catalyst using high throughput catalyst screening, Chemical Communications, 2004:434-435]은 특히, 폴리에틸렌을 제조하기 위한 에틸렌 중합 반응용 특정 촉매 시스템 및 방법을 언급하고 있다. 상기 촉매 시스템은 4족 금속 티타늄의 특정 유기금속 착체 및 활성화제를 함유한다. 일부 유기금속 착체는 단일 케티마이드 리간드(즉, (R)2C=N-)를 함유한다.
PCT 국제 특허 출원 공개 제 WO 2005/123790 Al 호는 특히, 올레핀-유도된 공중합체를 제조하기 위한 올레핀 중합 반응용 촉매 시스템 및 방법을 언급하고 있다. 촉매 시스템은 활성화제에 공유결합된 특정 촉매를 함유한다.
문헌[Nomura K., et al., Nonbridged half-metallocenes containing anionic ancillary donor ligands: New promising candidates as catalysts for precise olefin polymerization, Journal of Molecular Catalysis A: Chemical, 2007; 267:1-29]은 특히, 특정 4족 전이 금속 착체 및 올레핀 중합 반응을 언급하고 있다.
문헌[De Waele P., et al., Synthesis of Hafnium and Zirconium Imino-Amido Complexes from bis-imine Ligands. A New Family of Olefin Polymerization Catalysts, Organometallics, 2007;26:3896-3899]은 특히, 올레핀 중합 반응을 위한 특정 촉매 및 방법을 언급하고 있다.
미국 특허 출원 공개 제 2008/0261804 A1 호는 특히, 올레핀 중합 반응을 촉진하는데 적합한 산소-가교 이종금속(bimetallic) 착체를 언급하고 있다.
화학 산업은, 신규 금속-리간드 착체, 및 상기 착체로부터 제조되고 올레핀 중합 반응 조건(예컨대, 온도) 하에서 개선된 안정성(예컨대, 알킬 기 이동에 대해)을 갖는 촉매를 요구하고 있다. 바람직하게, 신규 촉매는, 신규 조성물(예컨대, 신규 폴리올레핀 조성물)을 제공하는 반응을 촉진시키거나 반응 수율을 개선시키거나 대안적인 기질 선택성을 제공하거나(예컨대, 폴리올레핀 공중합체 제조에서 단량체 및 공단량체에 대한 새로운 상대적 선택성을 제공함), 제조 비용을 낮추거나, 공정 안전성을 개선시키거나, 이러한 특성들의 조합을 제공하는데 유용할 것이다.
제 1 실시양태에서, 본 발명은 하기 화학식 I의 금속-리간드 착체이다:
[화학식 I]
상기 식에서,
LQ는 각각 독립적으로 존재하지 않거나 L이고;
L은 각각 독립적으로 존재하지 않거나, 할로겐 원자, 수소 원자, (C1-C40)하이드로카빌C(O)N(H)-, (C1-C40)하이드로카빌C(O)N((C1-C20)하이드로카빌), (C1-C40)하이드로카빌C(O)O-, (C1-C40)하이드로카빌, (C1-C40)헤테로하이드로카빌, RKRLN-, RLO-, RLS- 또는 RKRLP-이고, 이때 RK 및 RL은 각각 독립적으로 수소, (C1-C40)하이드로카빌, [(C1-C10)하이드로카빌]3Si, [(C1-C10)하이드로카빌]3Si(C1-C10)하이드로카빌(예컨대, 트라이메틸실일에틸) 또는 (C1-C40)헤테로하이드로카빌이거나, RK 및 RL은 함께 (C2-C40)하이드로카빌렌 또는 (C1-C40)헤테로하이드로카빌렌을 형성하거나, L 및 LQ는 함께 (RD)2C=C(RD)-C(RD)=C(RD)2를 형성하고, 이때 RD는 각각 독립적으로 H, 비치환된 (C1-6)알킬, 페닐 또는 나프틸이고,
L은 각각 독립적으로 M1에 결합된 1가 음이온 잔부이고;
n은 0 내지 3의 정수이고,
X는 각각 독립적으로 존재하지 않거나, RXNRKRL, RKORL, RKSRL 또는 RXPRKRL인 중성 루이스 염기 기이되, 이때 RX는 각각 독립적으로 수소, (C1-C40)하이드로카빌, [(C1-C10)하이드로카빌]3Si, [(C1-C10)하이드로카빌]3Si(C1-C10)하이드로카빌 또는 (C1-C40)헤테로하이드로카빌이고, RK 및 RL은 각각 독립적으로 상기 정의된 바와 같고,
J는 하기 화학식 J1 내지 J7 중 임의의 하나의 1가 음이온 잔부이거나:
[화학식 J1]
RKRLRXP=N-
(상기 식에서,
RK, RL 및 RX는 각각 독립적으로 상기 정의된 바와 같다)
[화학식 J2]
RKRLB-O-
(상기 식에서,
RK 및 RL은 각각 독립적으로 상기 정의된 바와 같다)
[화학식 J3]
(상기 식에서,
---은 두 개의 비편재화 파이 결합이고;
RW1 및 RW2는 각각 독립적으로 RX이고;
M2는 Al-RA, Ga-RA 또는 Zn이고, 이때 RA는 각각 독립적으로 (Cl-C40)알킬, RKRLN- 또는 RLO-이고;
RJ는 각각 독립적으로 (C6-C12)아릴이다)
[화학식 J4]
RKRLN-0-
(상기 식에서,
RK 및 RL은 각각 독립적으로 상기 정의된 바와 같다)
[화학식 J5]
(상기 식에서,
RKRLC=N-
RK 및 RL은 각각 독립적으로 상기 정의된 바와 같다)
[화학식 J6]
RK(RLRXN)C=N-
(상기 식에서,
RK, RL 및 RX는 각각 독립적으로 상기 정의된 바와 같다)
[화학식 J7]
(RLRXN)2C=N-
(상기 식에서,
RK, RL 및 RX는 각각 독립적으로 상기 정의된 바와 같다); 또는
n은 1, 2 또는 3이고,
하나의 X 및 J는 함께 하기 화학식 K1 내지 K6 중 임의의 하나의 1가 음이온 바이덴테이트(bidentate) 잔부 XJ-JX를 형성하고:
(상기 식에서,
RK, RL 및 RX는 각각 독립적으로 상기 정의된 바와 같다);
M1은 각각 독립적으로 원소 주기율표의 3족 내지 6족 중 임의의 금속이고(후술됨), 이때 금속은 +2, +3, +4, +5 또는 +6의 형식적 산화 상태로 존재하고;
m은 0 내지 3의 정수이고;
R1은 각각 독립적으로 H, (C1-C40)하이드로카빌 또는 (C1-C40)헤테로하이드로카빌이고,
R2, R3 및 R4는 각각 독립적으로 (C1-C40)하이드로카빌, (C1-C40)하이드로카빌O-, (C1-C40)하이드로카빌S-, (C1-C40)하이드로카빌S(O)-, (C1-C40)하이드로카빌S(O)2-, ((C1-C40)하이드로카빌)2N-, ((C1-C40)하이드로카빌)2P-, 또는 (C1-C40)헤테로하이드로카빌이거나,
R4는 앞서 정의된 바와 같고 R2 및 R3은 하기 화학식 R23의 2가 라디칼로 치환되고(즉, 함께 형성하고):
[화학식 R23]
(상기 식에서,
R2A 및 R3A는 각각 독립적으로 (C1-C40)하이드로카빌, (C1-C40)하이드로카빌O-, (C1-C40)하이드로카빌S-, (C1-C40)하이드로카빌S(O)-, (C1-C40)하이드로카빌S(O)2-, ((C1-C40)하이드로카빌)2N-, ((C1-C40)하이드로카빌)2P-, 또는 (C1-C40)헤테로하이드로카빌이다),
R5는 각각 독립적으로 (C1-C40)하이드로카빌 또는 (C1-C40)헤테로하이드로카빌이거나; 또는
R1 및 R2; R1 및 R4; R1 및 R2A; R2 및 R3; R2 및 R5; R2A 및 R3A; R2A 및 R5; R3 및 R4; R3A 및 R4; R4 및 R5; R1 또는 R5, 및 X 또는 J의 RK; 또는 R1 또는 R5, 및 L 또는 J의 RL은 함께 (C1-C40)하이드로카빌렌 또는 (C1-C40)헤테로하이드로카빌렌을 형성하고, 이의 나머지(즉, X 또는 J의 R1, R2, R2A, R3, R3A, R4, R5, RK, 또는 L 또는 J의 RL의 나머지)는 상기 정의된 바와 같거나; 또는
R1 또는 R5 및 L은 함께 (C1-C40)하이드로카빌렌-C(O)N(H)-, (C1-C40)하이드로카빌렌-C(O)N((C1-C20)하이드로카빌), (C1-C40)하이드로카빌렌-C(O)O-, (C1-C40)하이드로카빌렌 또는 (C1-C40)헤테로하이드로카빌렌을 형성하고, 이의 나머지는 상기 정의된 바와 같거나; 또는
X 또는 J의 R1 내지 R5, R2A, R3A, RK, 및 L 또는 J의 RL 중 3개 또는 4개는 함께 (C1-C40)하이드로카빌렌 또는 (C1-C40)헤테로하이드로카빌렌의 3가 또는 4가 유사체 각각을 형성하고, 이의 나머지는 상기 정의된 바와 같거나; 또는
R1 또는 R5, 및 X 또는 J의 R1 내지 R5, R2A, R3A, RK 및 L 또는 J의 RL의 1개 또는 2개의 나머지는 L과 함께 (C1-C40)하이드로카빌렌-C(O)N(H)-, (C1-C40)하이드로카빌렌-C(O)N((C1-C20)하이드로카빌), (C1-C40)하이드로카빌렌-C(O)O-, (C1-C40)하이드로카빌렌 또는 (C1-C40)헤테로하이드로카빌렌의 3가 또는 4가 유사체 각각을 형성하고, X 또는 J의 R1 내지 R5, R2A, R3A, RK, L 또는 J의 RL, 및 L의 나머지는 상기 정의된 바와 같고;
상기 (C6-C12)아릴, (C1-C10)하이드로카빌, (C1-C20)하이드로카빌, (C1-C40)하이드로카빌, (C1-C40)헤테로하이드로카빌, (C1-C40)하이드로카빌렌, (C2-C40)하이드로카빌렌, 및 (C1-C40)헤테로하이드로카빌렌은 각각 동일하거나 상이하고, 독립적으로 하나 이상의 치환기 RS로 치환되거나 비치환되고;
RS는 각각 독립적으로 할로겐 원자, 폴리플루오로, 퍼플루오로, 비치환된 (C1-C18)하이드로카빌, F3C-, FCH20-, F2HCO-, F3CO-, 옥소(즉, =0), R3Si-, RO-, RS-, RS(O)-, RS(O)2-, R2P-, R2N-, R2C=N-, NC-, RC(O)O-, ROC(O)-, RC(O)N(R)- 또는 R2NC(O)-이고, 이때 R은 각각 독립적으로 비치환된 (C1-C18)하이드로카빌이고;
L, LQ 및 m은 각각, 금속 M1의 형식적 산화 상태에 따라, 화학식 I의 금속-리간드 착체가 총체적으로 중성이 되도록 선택된다(예컨대, LQ가 존재하지 않을 때 m은 0이다).
제 2 실시양태에서, 본 발명은, 하나 이상의 화학식 I의 금속-리간드 착체 및 하나 이상의 활성화 조촉매(co-catalyst) 또는 이들의 반응 생성물을 포함하거나 이로부터 제조된 촉매이며, 이때 상기 하나 이상의 금속-리간드 착체의 총 몰 수 대 상기 하나 이상의 활성화 조촉매의 총 몰 수의 비는 1:10,000 내지 100:1이다.
제 3 실시양태에서, 본 발명은, 하나 이상의 중합성 올레핀의 적어도 일부를 중합하여 이로부터 폴리올레핀을 제조하기에 충분한 올레핀-중합 조건(후술됨) 하에, 하나 이상의 중합성 올레핀(즉, 올레핀 단량체)을 상기 제 2 실시양태의 촉매와 접촉시키는 단계를 포함하는, 폴리올레핀 제조 방법이다.
제 4 실시양태에서, 본 발명은, 상기 제 2 실시양태의 촉매를 제조하기에 충분한 조건 하에, 하나 이상의 화학식 I의 금속-리간드 착체를 하나 이상의 활성화 조촉매와 접촉시키는 단계를 포함하는 촉매 제조 방법이며, 이때 상기 화학식 I의 하나 이상의 금속-리간드 착체의 총 몰 수 대 상기 하나 이상의 활성화 조촉매의 총 몰 수의 비는 1:10,000 내지 100:1이다.
제 5 실시양태에서, 본 발명은, 제 1 실시양태에서 상기된 바와 같이 화학식 I의 금속-리간드 착체를 포함하는 혼합물을 제조하기에 충분한 조건 하에, 하기 화학식 Z의 중간체 금속-리간드 착체를 화학식 J-H의 화합물 또는 XJ-JX-H의 화합물과 접촉시키는 단계를 포함하는, 화학식 I의 금속-리간드 착체 제조 방법이며, 이때 J 및 XJ-JX는 제 1 실시양태에서 정의된 바와 같고, 화학식 J-H의 화합물 또는 XJ-JX-H의 화합물은 각각 기 J 또는 XJ-JX의 공액된 브뢴스테트 산이다:
[화학식 Z]
본 발명의 또 다른 실시양태는 제 3 실시양태의 공정에 따라 제조된 폴리올레핀이다.
화학식 I의 금속-리간드 착체는 제 2 실시양태의 촉매를 제조하는데 유용하다. 제 2 실시양태의 촉매는 폴리올레핀을 제조하기 위한 제 3 실시양태의 공정에서 유용하다. 후술되는 바와 같이, 제 3 실시양태의 발명 공정은 하나 이상의 촉매의 활성, 이로부터 제조된 하나 이상의 폴리올레핀의 성질 또는 이의 조합을 특징으로 한다.
제 3 실시양태의 발명 공정에 의해 제조된 폴리올레핀은 더 높은 Mw 또는 Mn을 가지는 폴리올레핀이 요구되는 물품을 비롯한 예를 들어, 윤활제, 코팅물, 필름, 섬유, 및 성형 물품 및 압출 물품을 제조하는데 유용하다. 이러한 물품의 예는, 주위 서비스 온도보다 높은 온도(예컨대, 약 30 ℃ 초과의 온도)를 요구하는 물품이다. 추가적 예는 합성 윤활제 및 특히, 올레핀 블록 공중합체(OBC), 위생 용도를 위한 탄성 필름(예컨대, 기저귀 커버); 기기, 공구, 소비재(예컨대, 칫솔 손잡이), 스포츠 용품, 빌딩 및 건축물, 자동차 및 의학 용도를 위한 가요성 성형 제품; 기기를 위한 가요성 가스켓 및 프로파일(예컨대, 냉장고 도어 가스켓 및 프로파일), 빌딩 및 건축물, 및 자동차 용도를 위한 가요성 가스켓 및 프로파일; 포장재(예컨대, 골판 카드보드지 박스의 제조에 사용하기 위한 것), 위생 용도, 테이프 및 라벨을 위한 접착제; 및 스포츠 용품(예컨대, 폼 매트), 포장재, 소비재 및 자동차 용도를 위한 폼이다. 다른 예는, 개선된 기계적 특성, 예를 들어 모듈러스(예컨대, 영(Young's) 모듈러스), 아이조드 충격 강도, 항복 강도, 인장 강도, 파단시 신율, 강성, 내열성, 내화학성, 내점화성, 극성 액체 또는 기체에 대한 내확산성, 및 치수 안정성 중 하나 이상을 요구하는 용도이다.
추가적인 비제한적인 실시양태는, 본원에 첨부된 특허청구범위 및 도면을 포함하는 하기 명세서에서 기술된다.
도 1은, 화학식 I의 금속-리간드 착체를 제조하기 위한 반응식 1에서의 대표적인 과정을 도시한 것이다.
도 2는, 화학식 Y-A의 중간체 화합물을 제조하기 위한 반응식 2에서의 대표적인 과정을 도시한 것이다.
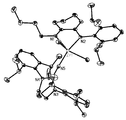
도 3은, 본 발명의 금속-리간드 착체(1)(실시예 1)의, X-선 분석에 의해 유도된 단결정 구조의 오크 리지 열 타원체 플롯(Oak Ridge Thermal Ellipsoid Plot; ORTEP)을 도시한 것이며, 명료함을 위해 수소 원자는 생략되었다.
도 4는, 본 발명의 금속-리간드 착체(2)(실시예 2)의, X-선 분석에 의해 유도된 단결정 구조의 ORTEP를 도시한 것이며, 명료함을 위해 수소 원자는 생략되었다.
도 5는, 본 발명의 금속-리간드 착체(10)(실시예 10)의, X-선 분석에 의해 유도된 단결정 구조의 ORTEP를 도시한 것이며, 명료함을 위해 수소 원자는 생략되었다.
도 6은, 금속-리간드 착체(11)의, X-선 분석에 의해 유도된 단결정 구조의 ORTEP를 도시한 것이며, 명료함을 위해 수소 원자는 생략되었다.
도 7은, 본 발명의 금속-리간드 착체(12)(실시예 12)의, X-선 분석에 의해 유도된 단결정 구조의 ORTEP를 도시한 것이며, 명료함을 위해 수소 원자는 생략되었다.
도 2는, 화학식 Y-A의 중간체 화합물을 제조하기 위한 반응식 2에서의 대표적인 과정을 도시한 것이다.
도 3은, 본 발명의 금속-리간드 착체(1)(실시예 1)의, X-선 분석에 의해 유도된 단결정 구조의 오크 리지 열 타원체 플롯(Oak Ridge Thermal Ellipsoid Plot; ORTEP)을 도시한 것이며, 명료함을 위해 수소 원자는 생략되었다.
도 4는, 본 발명의 금속-리간드 착체(2)(실시예 2)의, X-선 분석에 의해 유도된 단결정 구조의 ORTEP를 도시한 것이며, 명료함을 위해 수소 원자는 생략되었다.
도 5는, 본 발명의 금속-리간드 착체(10)(실시예 10)의, X-선 분석에 의해 유도된 단결정 구조의 ORTEP를 도시한 것이며, 명료함을 위해 수소 원자는 생략되었다.
도 6은, 금속-리간드 착체(11)의, X-선 분석에 의해 유도된 단결정 구조의 ORTEP를 도시한 것이며, 명료함을 위해 수소 원자는 생략되었다.
도 7은, 본 발명의 금속-리간드 착체(12)(실시예 12)의, X-선 분석에 의해 유도된 단결정 구조의 ORTEP를 도시한 것이며, 명료함을 위해 수소 원자는 생략되었다.
상기 요약된 바와 같이, 본 발명은 일반적으로, 금속-리간드 착체, 상기 금속-리간드 착체를 포함하거나 이로부터 제조된 촉매, 상기 촉매를 사용하여 올레핀 중합 반응을 촉진하여 폴리올레핀을 제조하는 방법, 이로부터 제조된 폴리올레핀, 상기 금속-리간드 착체 및 촉매의 제조 방법, 및 이에 유용한 중간체 화합물에 관한 것이다.
바람직하게, 제 2 실시양태의 촉매는 화학식 I의 셋 미만, 더욱 바람직하게는 둘, 더더욱 바람직하게는 하나의 금속-리간드 착체를 포함하거나 이로부터 제조된다. 상기 제 2 실시양태의 본 발명의 바람직한 촉매는 중합 촉매로서 이로운 촉매 효율을 나타내며(예컨대, 본 발명의 촉매를 제조하는 데 사용되는 화학식 I의 금속-리간드 착체 g 당 더 많은 g의 중합체가 제조됨), 통상적인 폴리올레핀의 중량 평균 분자량(Mw) 및 수평균 분자량(Mn)에 비해, 유리하게 더 높은 Mw, Mn 또는 이들 둘 다를 갖는 폴리올레핀(폴리올레핀 공중합체 포함)을 제공한다.
상기 제 3 실시양태의 공정에 의해 제조된 폴리올레핀은 바람직하게, 에틸렌 단독중합체, 에틸렌/알파-올레핀 상호중합체(예컨대, 공중합체) 또는 에틸렌/알파-올레핀/다이엔 상호중합체(예컨대, 삼원공중합체)이다.
상기 제 4 실시양태의 공정은 바람직하게, 비 양성자성 용매(즉, -OH, -NH 및 -SH 작용 기가 존재하지 않는 용매)를 이용한다.
몇몇 실시양태에서, 상기 제 3 실시양태의 공정은 추가로, 올레핀 단량체 및 올레핀 공단량체를 모두 사용하기 위한 또다른 중합성 올레핀(즉, 올레핀 공단량체); 쇄 셔틀링제(CSA, 후술됨); 및 관련 올레핀 중합 촉매(이는, 본 발명의 촉매이거나, 본 발명의 촉매가 아닌 후술되는 촉매일 수 있음)를 이용하고, 바람직한 방법은, 폴리(올레핀 단량체 올레핀 공단량체) 상호중합체(예컨대, 공중합체)를 포함하는 폴리올레핀, 더욱 바람직하게는 폴리(올레핀 단량체 올레핀 공단량체) 블록 공중합체(즉, OBC)를 제공하며, 몇몇 실시양태에서는, 폴리(에틸렌 알파-올레핀) 블록 공중합체를 제공한다. 폴리(에틸렌 알파-올레핀) 블록 공중합체는 바람직하게는, 후술되는 바와 같이 알파-올레핀 및 에틸렌으로부터의 잔기를 포함하는 에틸렌-유도된 경질 분절 및 연질 분절을 포함한다. "폴리(에틸렌 알파-올레핀) 블록 공중합체"라는 용어는, 본원에서 "올레핀 블록 공중합체," "OBC," "에틸렌/알파-올레핀 블록 상호중합체," 및 "에틸렌/알파-올레핀 블록 공중합체"라는 용어와 상호교환적으로 사용된다. "알파-올레핀" 및 "α-올레핀"이라는 용어는 본원에서 상호교환적으로 사용된다.
본원에서, "하나", "적어도 하나" 및 "하나 이상"은 상호교환적으로 사용된다. 본원에 기술된 임의의 실시양태에서, "포함하는", "포함한다" 등(이는, "갖는" 및 "~를 특징으로 하는"과 동의어임)의 개방-종지형(비-배제적) 용어는, "~로 본질적으로 이루어진", "~로 본질적으로 이루어진다" 등의 부분 폐쇄형(부분 배제적) 표현 또는 상응하게 "~로 이루어진", "~로 이루어진다" 등의 폐쇄형(배제적) 표현으로 대체될 수 있다. 구성원의 열거에 사용되는 "또는"이라는 용어는, 달리 언급하지 않는 한, 개별적으로 열거된 구성원뿐만 아니라 이의 임의의 조합도 지칭하고, 개별적인 구성원 중 임의의 하나를 인용하는 추가적인 실시양태를 뒷받침한다(예컨대, 구절 "10 % 이상"을 인용하는 실시양태에서 "또는"은 "10 %"를 인용하는 또 다른 실시양태 및 "10 % 초과"를 인용하는 또 다른 실시양태를 뒷받침한다). 용어 "복수"는 둘 이상을 의미하며, 이때 복수는, 달리 지시되지 않는 한, 각각 독립적으로 선택된다. 용어 "제 1", "제 2" 등은 둘 이상의 요소 사이에서 구별하는 통상적인 의미 또는 제한으로 작용하고(예컨대, 제 1 의자 및 제 2 의자), 특별히 달리 언급하지 않는 한, 양 또는 순서를 의미하지 않는다.
요지의 인용을 허용하는 미국 특허 심사 지침 및 기타 특허 실무 지침을 위해, 달리 언급하지 않는 한, 본 발명의 상세한 설명에서 참조된 각각의 미국 특허, 미국 특허 출원, 미국 특허 출원 공개, 특허 협력 조약(PCT) 국제 특허 출원 및 이의 대응 국제 특허 출원 공개의 전체 내용을 본원에 참고로 인용한다. 가능한 경우, 미국 특허 및 이의 미국 특허 출원 공개 패밀리 일원을, 대응 PCT 국제 특허 출원 또는 WO 공개 대신 참고로 인용할 수 있다. 본 발명의 명세서에 기술된 내용과, 본원에 참고로 인용된 특허, 특허 출원 또는 특허출원 공개 또는 이들의 일부에 기술된 내용이 상충하는 경우, 본 발명의 명세서에 기술된 것이 우선한다.
단어 "임의적으로"는 "가지거나 가지지 않는"을 의미한다. 예를 들어, "임의적으로, 첨가제"는 첨가제를 가지거나 가지지 않음을 의미한다.
괄호 없이 인용된 단위 값[예컨대, 2 인치] 및 괄호 안에 인용된 대응 단위 값[예컨대, (5 cm)]이 서로 상충하는 경우, 괄호 없이 인용된 단위 값이 우선한다.
화합물명과 이의 구조가 상충하는 경우, 그 구조가 우선한다.
본원에서, 특정 범위의 임의의 하한 또는 상기 범위의 임의의 바람직한 하한은, 상기 범위의 임의의 상한 또는 상기 범위의 임의의 바람직한 상한과 조합되어, 상기 범위의 바람직한 실시양태를 정의할 수 있다. 수치들의 각각의 범위는, 상기 범위 내에 포함된 모든 수(유리수 및 무리수 모두)를 포함한다(예를 들면, 약 1 내지 약 5의 범위는 1, 1.5, 2, 2.75, 3, 3.80, 4 및 5를 포함함).
특정 비치환된 화학 기는 최대 40개의 탄소 원자를 갖는 것으로 본원에 기재된다(예컨대, (C1-C40)하이드로카빌 및 (C1-C40)헤테로하이드로카빌). 이러한 기는 탄소 원자의 수가 중요하지 않은 치환기(예컨대, R 기) 및 올레핀 단량체를 포함한다. 이러한 비치환된 화학 기에서 40개의 탄소 원자가 실험적인 상한임에도 불구하고, 몇몇 실시양태에서 본 발명은 40개 보다 더 높은 최대 탄소 원자의 수(예컨대, 100, 1000 또는 그 이상)를 가지는 상기 비치환된 화학 기를 고려한다.
달리 언급하지 않는 한, "원소 주기율표"라는 표현은, 국제 순수 및 응용 화학 연맹(International Union of Pure and Applied Chemistry; IUPAC)에서 발행한 2007년 6월 22일자 버전의 공식적인 주기율표를 지칭한다. 또한, "족"에 대한 임의의 언급은, 상기 원소 주기율표에 반영된 족이다.
몇몇 실시양태에서, M1은 3족 금속이다. 본 발명에 유용한 3족 금속(기호)(란탄족 및 악티늄족 포함)은 스칸듐(Sc), 이트륨(Y), 란탄 계열 원소(종종, 란탄족으로도 불림), 특히 란타늄(La), 세륨(Ce), 프라세오디뮴(Pr), 네오디뮴(Nd), 프로메튬(Pm), 사마륨(Sm), 유로퓸(Eu), 가돌리늄(Gd), 테르븀(Tb), 디스프로슘(Dy), 홀륨(Ho), 에르븀(Er), 툴륨(Tm), 이테르븀(Yb), 및 루테튬(Lu); 및 안정한 악티늄 계열 원소(종종, 악티늄족으로도 불림), 특히 악티늄(Ac), 토륨(Th) 및 우라늄(U)의 안정한 동위 원소이다. 불안정한 악티늄 계열 원소, 예컨대 프로트악티늄(Pa), 넵투늄(Np), 플루토늄(Pu), 아메리슘(Am), 퀴륨(Cm), 버클륨(Bk), 칼리포르늄(Cf), 아인시타이늄(Es), 페르뮴(Fm), 멘델레븀(Md), 노벨륨(No) 및 로렌슘(Lr)은 본 발명의 유용한 악티늄족에서 제외된다. 바람직한 3족 금속은 Sc 및 Y이다. 다른 실시양태에서, M1은 4족 금속이다. 바람직한 4족 금속은, +2, +3 또는 +4, 더욱 바람직하게는 +4의 형식 산화 상태의 금속이다. 본 발명의 목적상, 러더퍼듐(Rf)은 본 발명에 유용한 4족 금속에서 제외된다. 또 다른 실시양태에서, M1은 5족 금속이다. 본 발명에 유용한 5족 금속은 바나듐(V), 니오븀(Nb) 및 탄탈륨(Ta)이다. 본 발명의 목적상, 두브늄(Db)은 본 발명에 유용한 5족 금속에서 제외된다. 또다른 실시양태에서, M1은 6족 금속이다. 본 발명에 유용한 6족 금속은 크롬(Cr), 몰리브덴(Mo) 및 텅스텐(W)이다. 본 발명의 목적상, 시보??(Sg)은 본 발명에 유용한 6족 금속에서 제외된다.
더욱 바람직하게, M1은 4족 금속이고, 이는 M1이 티타늄(Ti), 지르코늄(Zr) 또는 하프늄(Hf)임을 의미하고, 더욱 바람직하게 지르코늄 또는 하프늄이다.
화학 기(예컨대, (C1-C40)알킬)를 기술할 때 사용되는 "(Cx-Cy)" 형태의 괄호 표현은, 상기 화학 기의 비치환된 버전이 x개의 탄소 원자 내지 y개의 탄소 원자를 포함함을 의미하며, 이때 x 및 y는 각각 독립적으로 상기 화학 기에 대해 기술된 바와 같은 정수이다. 따라서, 예를 들어 비치환된 (C1-C40)알킬은 1 내지 40개의 탄소 원자를 함유한다. 상기 화학 기 상의 하나 이상의 치환기가 하나 이상의 탄소 원자를 함유하는 경우, 치환된 (Cx-Cy) 화학 기는 y 초과의 총 탄소 원자를 포함하거나 포함하지 않을 수 있다. 즉, 치환된 (Cx-Cy) 화학 기의 최대 총 탄소 원자 수는, y에 각각의 치환기의 탄소 원자의 수의 합을 더한 것이다. 본원에 명시되지 않은 화학 기의 임의의 원자는 수소 원자로 이해된다.
몇몇 실시양태에서, 본 발명의 화합물(예컨대, 화학식 I의 금속-리간드 착체)은 하나 이상의 치환기 RS를 함유한다. 바람직하게, 본 발명의 화합물에는 20개 이하의 RS, 더욱 바람직하게는 10개 이하의 RS, 더더욱 바람직하게는 5개 이하의 RS가 존재한다. 본 발명의 화합물이 2개 이상의 치환기 RS를 함유하는 경우, RS는 각각 독립적으로 동일하거나 상이한 치환된 화학 기에 결합된다.
몇몇 실시양태에서, 적어도 하나의 RS는 폴리플루오로 또는 퍼플루오로이다. 본 발명의 목적상, "폴리플루오로" 및 "퍼플루오로"는 각각 하나의 RS 치환기로서 간주된다. "폴리플루오로"에서 "폴리"라는 용어는, 대응하는 비치환된 화학 기의 탄소 원자에 결합된 2개 이상의 H(모든 H는 아님)가, 치환된 화학 기에서 플루오로로 대체됨을 의미한다. "퍼플루오로"에서 "퍼"라는 용어는, 대응하는 비치환된 화학 기의 탄소 원자에 결합된 각각의 H가, 치환된 화학 기에서 플루오로로 대체됨을 의미한다.
본원에서 "(C1-C40)하이드로카빌"이라는 용어는, 탄소수 1 내지 40의 탄화수소 라디칼을 의미하며, "(C1-C40)하이드로카빌렌"이라는 용어는, 탄소수 1 내지 40의 탄화수소 2가 라디칼을 의미하고, 이때 탄화수소 라디칼 및 2가 라디칼은 각각 독립적으로 방향족 또는 비방향족, 포화 또는 불포화, 직쇄 또는 분지쇄, 환형(일환형 및 다환형, 및 융합 및 비융합된 다환형 포함) 또는 비환형, 또는 이들 중 2종 이상의 조합이며; 탄화수소 라디칼 및 2가 라디칼은 각각, 또다른 탄화수소 라디칼 및 2가 라디칼과 동일하거나 상이하고, 각각 독립적으로 하나 이상의 RS로 치환되거나 비치환된다.
바람직하게, (C1-C40)하이드로카빌은 독립적으로 치환되거나 비치환된 (C1-C40)알킬, (C3-C40)사이클로알킬, (C3-C20)사이클로알킬-(C1-C20)알킬렌, (C6-C40)아릴 또는 (C6-C20)아릴-(C1-C20)알킬렌이다. 더욱 바람직하게, (C1-C40)하이드로카빌은 독립적으로 치환되거나 비치환된 (C1-C20)하이드로카빌, 예컨대 (C1-C20)알킬, (C3-C20)사이클로알킬, (C3-C10)사이클로알킬-(C1-C10)알킬렌, (C6-C20)아릴 또는 (C6-C18)아릴-(C1-C10)알킬렌이다. 더더욱 바람직하게, (C1-C40)하이드로카빌은 독립적으로 치환되거나 비치환된 (C1-C18)하이드로카빌, 예컨대 (C1-C18)알킬, (C3-C18)사이클로알킬, (C3-C12)사이클로알킬-(C1-C6)알킬렌, (C6-C18)아릴 또는 (C6-C12)아릴-(C1-C6)알킬렌이다. 바람직하게, 임의의 (C3-C18)사이클로알킬은 독립적으로 치환되거나 비치환된 (C3-C10)사이클로알킬이다.
"(C1-C40)알킬"이라는 용어는, 하나 이상의 RS로 치환되거나 비치환된 탄소수 1 내지 40의 포화된 직쇄 또는 분지쇄 탄화수소 라디칼을 의미한다. 비치환된 (C1-C40)알킬의 예는, 비치환된 (C1-C20)알킬; 비치환된 (C1-C10)알킬; 비치환된 (C1-C5)알킬; 메틸; 에틸; 1-프로필; 2-프로필; 1-부틸; 2-부틸; 2-메틸프로필; 1,1-다이메틸에틸; 1-펜틸; 1-헥실; 1-헵틸; 1-노닐; 및 1-데실이다. 치환된 (C1-C40)알킬의 예는, 치환된 (C1-C20)알킬, 치환된 (C1-C10)알킬, 트라이플루오로메틸, 및 (C45)알킬이다. 바람직하게, (C1-C5)알킬은 각각 독립적으로 메틸, 트라이플루오로메틸, 에틸, 1-프로필 또는 2-메틸에틸이다.
"(C1-C20)알킬렌"이라는 용어는, 하나 이상의 RS로 치환되거나 비치환된 탄소수 1 내지 20의 포화된 직쇄 또는 분지쇄 2가 라디칼을 의미한다. 바람직하게, (C1-C20)알킬렌은, 화학식 I의 원자들(이를 통해 (C1-C20)알킬렌이 결합됨)과 함께, 5원 또는 6원 고리를 포함한다. 비치환된 (C1-C20)알킬렌의 예는, 비치환된 (C1-C10)알킬렌, 예컨대 비치환된 1,2-(C1-C10)알킬렌; -CH2-, -CH2CH2-, -(CH2)3-, -CH2 HCH3, -(CH2)4-, -(CH2)5-, -(CH2)6-, -(CH2)7-, -(CH2)8-, 및 -(CH2)4C(H)(CH3)-이다. 치환된 (C1-C20)알킬렌의 예는, 치환된 (C1-C10)알킬렌, -CF2-, -C(O)-, 및 -(CH2)14C(CH3)2(CH2)5-(즉, 6,6-다이메틸 치환된 n-1,20-에이코실렌)이다.
"(C6-C40)아릴"이라는 용어는, (하나 이상의 RS로) 치환되거나 비치환된 탄소수 6 내지 40의 일환형, 이환형 또는 삼환형 방향족 탄화수소 라디칼을 의미하며, 여기서 적어도 6 내지 14개의 탄소 원자가 고리 탄소 원자이고, 상기 일환형, 이환형 또는 삼환형 라디칼은 1, 2 또는 3개의 고리(각각, 제 1, 제 2 및 제 3 고리)를 포함하고, 이때 임의의 제 2 또는 제 3 고리는 독립적으로 제 1 고리 또는 서로의 고리에 융합되거나 비융합되고, 상기 제 1 고리는 방향족이고, 바람직하게는, 임의의 제 2 또는 제 3 고리 중 적어도 하나가 방향족이다. 비치환된 (C6-C40)아릴의 예는, 비치환된 (C6-C20)아릴; 비치환된 (C6-C18)아릴; 비치환된 (C6-C12)아릴; 페닐; 플루오렌일; 테트라하이드로플루오렌일; 인다센일; 헥사하이드로인다센일; 인덴일; 다이하이드로인덴일; 나프틸; 테트라하이드로나프틸; 및 페난트렌이다. 치환된 (C6-C40)아릴의 예는, 치환된 (C6-C20)아릴; 치환된 (C6-C18)아릴; 치환된 (C6-C12)아릴; 2-(C1-C5)알킬-페닐; 2,4-비스[(C1-C5)알킬]-페닐; 2,4-비스[(C20)알킬]-페닐; 폴리플루오로페닐; 펜타플루오로페닐; 및 플루오렌-9-온-1-일이다. 바람직한 치환된 (C6-C12)아릴은 치환된 (C6)아릴, 더욱 바람직하게는 2,6-비스(1-메틸에틸)페닐이다.
"(C3-C40)사이클로알킬"이라는 용어는, 하나 이상의 RS로 치환되거나 비치환된 탄소수 3 내지 40의 포화된 환형 탄화수소 라디칼을 의미한다. 비치환된 (C3-C40)사이클로알킬의 예는, 비치환된 (C3-C20)사이클로알킬, 비치환된 (C3-C10)사이클로알킬, 사이클로프로필, 사이클로부틸, 사이클로펜틸, 사이클로헥실, 사이클로헵틸, 사이클로옥틸, 사이클로노닐, 및 사이클로데실이다. 치환된 (C3-C40)사이클로알킬의 예는, 치환된 (C3-C20)사이클로알킬, 치환된 (C3-C10)사이클로알킬, 사이클로펜탄온-2-일, 및 1-플루오로사이클로헥실이다.
(C1-C40)하이드로카빌렌의 예는, 비치환되거나 치환된 (C6-C40)아릴렌, (C3-C40)사이클로알킬렌, 및 (C1-C40)알킬렌(예컨대, (C1-C20)알킬렌)이다. 몇몇 실시양태에서, 상기 2가 라디칼은 인접 탄소들 원자 상에 존재하거나(즉, 1,2-2가 라디칼), 또는 1개, 2개 또는 그 이상의 개재(intervening) 탄소 원자에 의해 이격된다(예컨대, 각각 1,3-2가 라디칼, 1,4-2가 라디칼, 등). 1,2-, 1,3-, 1,4- 또는 알파,오메가-2가 라디칼(즉, 라디칼 탄소들 사이에 최대 간격을 가짐)이 바람직하고, 더욱 바람직하게는 1,2-2가 라디칼이다. (C6-C18)아릴렌, (C3-C20)사이클로알킬렌, 및 (C2-C20)알킬렌의 1,2-2가 라디칼이 더욱 바람직하다.
"(C1-C40)헤테로하이드로카빌"이라는 용어는, 1 내지 40개의 탄소 원자 및 하나 이상의 헤테로원자 N(특정 질소 함유 헤테로아릴 기(예컨대, 아이속사졸일)에서 -N=을 포함하는 경우); 0; S; S(O); S(O)2; Si(RC)2; P(RP); 및 N(RN)을 갖는 헤테로하이드로카본 라디칼을 의미하며, 이때 RC는 각각 독립적으로 비치환된 (C1-C18)하이드로카빌이고, RP는 각각, 비치환된 (C1-C18)하이드로카빌이고; RN은 각각, 비치환된 (C1-C18)하이드로카빌이다. "(C1-C40)헤테로하이드로카빌렌"이라는 용어는, 1 내지 40개의 탄소 원자, 및 상기 정의된 바와 같은 하나 이상의 헤테로원자 Si(RC)2, P(RP), N(RN), N, O, S, S(O), 및 S(O)2를 갖는 헤테로하이드로카본 2가 라디칼을 의미한다. 상기 헤테로하이드로카본 라디칼 및 각각의 헤테로하이드로카본 2가 라디칼은 독립적으로 이의 탄소 원자 또는 헤테로원자상에 존재한다. 헤테로하이드로카본 라디칼 및 2가 라디칼은 각각 독립적으로 (하나 이상의 RS로) 치환되거나 비치환된, 방향족 또는 비방향족, 포화되거나 불포화된, 직쇄 또는 분지쇄, 환형(일환형 및 다환형, 및 융합 및 비융합된 다환형 포함) 또는 비환형, 또는 이들 중 2종 이상의 조합이고; 헤테로하이드로카본은 각각, 또 다른 헤테로하이드로카본 라디칼 및 2가 라디칼과 동일하거나 상이하다.
바람직하게, (C1-C40)헤테로하이드로카빌은 독립적으로 치환되거나 비치환된 (C1-C40)헤테로알킬, (C2-C40)헤테로사이클로알킬, (C2-C40)헤테로사이클로알킬-(C1-C20)알킬렌, (C3-C40)사이클로알킬-(C1-C20)헤테로알킬렌, (C2-C40)헤테로사이클로알킬-(C1-C20)헤테로알킬렌, (C1-C40)헤테로아릴, (C1-C20)헤테로아릴-(C1-C20)알킬렌, (C6-C20)아릴-(C1-C20)헤테로알킬렌 또는 (C1-C20)헤테로아릴-(C1-C20)헤테로알킬렌이다. 더욱 바람직하게는, (C1-C40)헤테로하이드로카빌은 독립적으로 치환되거나 비치환된 (C1-C20)헤테로하이드로카빌, 예컨대 (C1-C20)헤테로알킬, (C2-C20)헤테로사이클로알킬, (C2-C20)헤테로사이클로알킬-(C1-C20)알킬렌, (C3-C20)사이클로알킬-(C1-C20)헤테로알킬렌, (C2-C20)헤테로사이클로알킬-(C1-C20)헤테로알킬렌, (C1-C20)헤테로아릴, (C1-C20)헤테로아릴(C1-C20)알킬렌, (C6-C20)아릴-(C1-C20)헤테로알킬렌 또는 (C1-C20)헤테로아릴-(C1-C20)헤테로알킬렌이다. 더더욱 바람직하게, (C1-C40)헤테로하이드로카빌은 독립적으로 치환되거나 비치환된 (C1-C18)헤테로하이드로카빌, 예컨대 (C1-C18)헤테로알킬, (C2-C18)헤테로사이클로알킬, (C2-C12)헤테로사이클로알킬-(C1-C6)알킬렌, (C3-C12)사이클로알킬-(C1-C6)헤테로알킬렌, (C2-C12)헤테로사이클로알킬-(C1-C6)헤테로알킬렌, (C1-C12)헤테로아릴, (C1-C12)헤테로아릴-(C1-C6)알킬렌, (C6-C18)아릴-(C1-C6)헤테로알킬렌 또는 (C1-C12)헤테로아릴-(C1-C6)헤테로알킬렌이다. 바람직하게, 임의의 (C2-C18)헤테로사이클로알킬은 독립적으로 치환되거나 비치환된 (C2-C9)헤테로사이클로알킬이다.
(C1-C40)헤테로알킬 및 (C1-C20)헤테로알킬렌의 예는, 각각, 1 내지 40개 또는 1 내지 20개의 탄소 원자, 및 상기 정의된 바와 같은 하나 이상의 헤테로원자 Si(RC)2, P(RP), N(RN), N, O, S, S(O), 및 S(O)2를 갖는 포화된 직쇄 또는 분지쇄 라디칼 또는 2가 라디칼이며, 이때 (C1-C40)헤테로알킬 및 (C1-C20)헤테로알킬렌은 독립적으로 하나 이상의 RS로 치환되거나 비치환된다.
비치환된 (C2-C40)헤테로사이클로알킬의 예는, 비치환된 (C2-C20)헤테로사이클로알킬, 비치환된 (C2-C10)헤테로사이클로알킬, 아지리딘-1-일, 옥세탄-2-일, 테트라하이드로퓨란-3-일, 피롤리딘-1-일, 테트라하이드로티오펜-S,S-다이옥사이드-2-일, 모폴린-4-일, 1,4-다이옥산-2-일, 헥사하이드로아제핀-4-일, 3-옥사-사이클로옥틸, 5-티아-사이클로노닐, 및 2-아자-사이클로데실이다.
비치환된 (C1-C40)헤테로아릴의 예는, 비치환된 (C1-C20)헤테로아릴; 비치환된 (C1-C10)헤테로아릴; 피롤-1-일; 피롤-2-일; 퓨란-3-일; 티오펜-2-일; 피라졸-1-일; 아이속사졸-2-일; 아이소티아졸-5-일; 이미다졸-2-일; 옥사졸-4-일; 티아졸-2-일; 1,2,4-트라이아졸-1-일; 1,3,4-옥사다이아졸-2-일; 1,3,4-티아다이아졸-2-일; 테트라졸-1-일; 테트라졸-2-일; 테트라졸-5-일; 피리딘-2-일; 피리미딘-2-일; 피라진-2-일; 인돌-1-일; 벤즈이미다졸-1-일; 퀴놀린-2-일; 및 아이소퀴놀린-1-일이다.
"할로"라는 용어는, 플루오로(F), 클로로(Cl), 브로모(Br) 또는 요오도(I) 라디칼을 의미한다. 바람직하게, 할로는 플루오로 또는 클로로이고, 더욱 바람직하게는 플루오로이다.
바람직하게, 화학식 I의 금속-리간드 착체에는, S(O) 또는 S(O)2 2가 라디칼 작용 기에서의 O-S 결합 외에는, O-O, S-S 또는 O-S 결합이 존재하지 않는다.
바람직하게, 치환된 (C1-C40)하이드로카빌은 각각, 치환되거나 비치환된 (C1-C40)헤테로하이드로카빌을 제외하고, 이들이 아니며; 바람직하게는, 치환된 (C1-C40)하이드로카빌렌은 각각, 치환되거나 비치환된 (C1-C40)헤테로하이드로카빌렌을 제외하고, 이것이 아니며; 더욱 바람직하게는 이들의 조합이다.
"포화된"이라는 용어는, 탄소-탄소 이중 결합, 탄소-탄소 삼중 결합, 및 (헤테로원자-함유 기 내의) 탄소-질소, 탄소-인, 및 탄소-규소 이중 결합이 없음을 의미한다. 포화된 화학 기가 하나 이상의 치환기 RS로 치환되는 경우, 하나 이상의 이중 및/또는 삼중 결합은 임의적으로, 치환기 RS에 존재하거나 존재하지 않을 수 있다. "불포화된"이라는 용어는, 하나 이상의 탄소-탄소 이중 결합, 탄소-탄소 삼중 결합, 및 (헤테로원자-함유 기 내의) 탄소-질소, 탄소-인, 및 탄소-규소 이중 결합을 함유하되, 치환기 RS(존재하는 경우) 또는 (헤테로)방향족 고리(존재하는 경우)에 존재할 수 있거나 존재할 수 없는 임의의 이중 결합은 포함하지 않음을 의미한다.
몇몇 실시양태는, 2가 라디칼 기의 3가 또는 4가 유사체를 고려한다. 2가 라디칼 기에 적용되는 바와 같이, "3가 또는 4가 유사체"라는 용어는 각각, 각각 상기 2가 라디칼 기로부터의 1개 또는 2개의 수소 원자를 추출함으로써 공식적으로 유도된 3가 라디칼 또는 4가 라디칼을 의미한다. 바람직하게, 추출되는 수소 원자는 각각 독립적으로 C-H 작용 기로부터 얻어진다. 3가 유사체가 4가 유사체에 비해 바람직하다.
몇몇 실시양태에서, R1 내지 R5 중 하나 이상, 더욱 바람직하게는 2개 이상, 더더욱 바람직하게는 이들 모두에서, X, L, LQ 및 J는 독립적으로 비치환된다(즉, 치환기 RS가 없음). 다른 실시양태에서, 치환기 RS는 각각 독립적으로 바람직하게, (C1-C10)알킬이고, 더욱 바람직하게는 (C1-C5)알킬을 가지는 R1 내지 R5 중 하나 이상, 더욱 바람직하게는 2개 이상, 더더욱 바람직하게는 3개 이상에서, X, L, LQ 및 J는 독립적으로 치환된다.
다른 실시양태에서, 화학식 I의 금속-리간드 착체는, 하나의 라디칼 기[예컨대, (C1-C40)하이드로카빌C(O)O-, (C1-C40)하이드로카빌, 또는 (C1-C40)하이드로카빌렌]가 R1 내지 R5, L, LQ 및 J 중 임의의 정의에서 제거되는 것을 제외하고는 상기 제 1 실시양태에서 기술된 바와 같다.
"용매"라는 용어는, 바람직하게는 비양성자성 액체를 의미하며, 이는 상기 제 3, 제 4 및 제 5 실시양태 중 임의의 방법과 혼화성이다. 적합한 용매는 지방족 및 방향족 탄화수소, 에터, 및 환형 에터, 특히 분지쇄 탄화수소, 예컨대 아이소부탄, 부탄, 펜탄, 헥산, 헵탄, 옥탄, 및 이들의 혼합물; 환형 및 지환형 탄화수소, 예컨대 사이클로헥산, 사이클로헵탄, 메틸사이클로헥산, 메틸사이클로헵탄, 및 이들의 혼합물; 벤젠 및 (C1-C5)알킬-치환된 벤젠, 예컨대 톨루엔 및 자일렌; (C1-C5)알킬-O-(C1-C5)알킬; (C4-C5)헤테로사이클로알킬, 예컨대 테트라하이드로퓨란, 테트라하이드로피란, 및 1,4-다이옥산; (폴리)알킬렌 글라이콜의 (C1-C5)알킬 에터; 및 이들의 혼합물을 포함한다.
화학식 I의 금속-리간드 착체는, 이를 활성화 조촉매와 접촉시키거나 배합함으로써, 또는 활성화 기술, 예컨대 금속(예컨대, 4족) 올레핀 중합 반응에 사용하도록 당분야에 공지된 기술을 사용함으로써 촉매적으로 활성이 된다. 본 발명은 비록 활성화 조촉매의 용도가 바람직할지라도, 하나 이상의 활성화 조촉매를 활성화 기술로 대체함에 있어서 호환성이다. 본원에 사용하기 적합한 활성화 조촉매는 알킬 알루미늄; 중합체성 또는 올리고머성 알룸옥산(알루민옥산으로도 공지됨); 중성 루이스 산; 및 비-중합체성, 비-배위성, 이온-형성 화합물(산화 조건 하에 상기 화합물의 사용 포함)을 포함한다. 적합한 활성화 기술은 벌크 전기분해(이후 더 자세히 설명됨)이다. 또한, 하나 이상의 전술된 활성화 조촉매 및 기술의 조합도 고려된다. "알킬 알루미늄"이라는 용어는, 모노알킬 알루미늄 다이하이드라이드 또는 모노알킬알루미늄 다이할라이드, 다이알킬 알루미늄 하이드라이드 또는 다이알킬 알루미늄 할라이드, 또는 트라이알킬알루미늄을 의미한다. 알루민옥산 및 이의 제조 방법은 당분야에 공지되어 있으며, 예를 들어 미국 특허 제 6,103,657 호를 참조한다. 바람직한 중합체성 또는 올리고머성 알룸옥산의 예는 메틸알룸옥산, 트라이아이소부틸알루미늄 개질된 메틸알룸옥산, 및 아이소부틸알룸옥산이다.
바람직한 루이스 산 활성화 조촉매는, 본원에 기술된 바와 같은 하이드로카빌 치환기 1 내지 3개를 함유하는 13족 금속 화합물이다. 더욱 바람직한 13족 금속 화합물은 트라이(하이드로카빌)-치환된-알루미늄 또는 트라이(하이드로카빌)-붕소 화합물이며, 트라이((C1-C10)알킬)알루미늄 또는 트라이((C6-C18)아릴)붕소 화합물 및 이의 할로겐화된(퍼할로겐화되는 것 포함) 유도체가 더더욱 바람직하고, 더더욱 특히 트리스(플루오로치환된 페닐)보란, 더더욱 특히 트리스(펜타플루오로페닐)보란이다.
중성 루이스 산 활성화 조촉매의 바람직한 조합은, 트라이((C1-C4)알킬)알루미늄 및 할로겐화된 트라이((C6-C18)아릴)붕소 화합물, 특히 트리스(펜타플루오로페닐)보란의 조합을 포함하는 혼합물이다. 또한, 상기 중성 루이스 산 혼합물과 중합체성 또는 올리고머성 알루민옥산의 조합, 및 단일 중성 루이스 산, 특히 트리스(펜타플루오로페닐)보란과 중합체성 또는 올리고머성 알루민옥산의 조합이 바람직하다. (금속-리간드 착체):(트리스(펜타플루오로-페닐보란):(알룸옥산)[예컨대 (4족 금속-리간드 착체):(트리스(펜타플루오로-페닐보란):(알룸옥산)]의 몰 수의 바람직한 비는 1:1:1 내지 1:10:30, 더욱 바람직하게는 1:1:1.5 내지 1:5:10이다.
다수의 활성화 조촉매 및 활성화 기술은, 미국 특허 제 5,064,802 호; 미국 특허 제 5,153,157 호; 미국 특허 제 5,296,433 호; 미국 특허 제 5,321,106 호; 미국 특허 제 5,350,723 호; 미국 특허 제 5,425,872 호; 미국 특허 제 5,625,087 호; 미국 특허 제 5,721,185 호; 미국 특허 제 5,783,512 호; 미국 특허 제 5,883,204 호; 미국 특허 제 5,919,983 호; 미국 특허 제 6,696,379 호; 및 미국 특허 제 7,163,907 호에서 다양한 금속-리간드 착체에 대해 이미 교시되었다. 적합한 하이드로카빌옥사이드의 예는 미국 특허 제 5,296,433 호에 개시되어 있다. 부가 중합 촉매를 위한 적합한 브뢴스테드 산 염의 예는 미국 특허 제 5,064,802 호; 미국 특허 제 5,919,983 호; 미국 특허 제 5,783,512 호에 개시되어 있다. 부가 중합 촉매를 위한 활성화 조촉매로서, 양이온성 산화제 및 비-배위성, 혼화성 음이온의 적합한 염은 미국 특허 제 5,321,106 호에 개시되어 있다. 부가 중합 촉매를 위한 활성화 조촉매로서 적합한 카베니움 염은 미국 특허 제 5,350,723 호에 개시되어 있다. 부가 중합 촉매를 위한 활성화 조촉매로서 적합한 실릴륨 염은 미국 특허 제 5,625,087 호에 개시되어 있다. 알코올, 머캅탄, 실란올 및 옥심과 트리스(펜타플루오로페닐)보란의 적합한 착체의 예는 미국 특허 제 5,296,433 호에 개시되어 있다. 또한, 이들 촉매 중 몇몇은, 미국 특허 제 6,515,155 B1 호의 칼럼 50, 39행 내지 칼럼 56, 55행에 개시되어 있으며, 상기 특허의 이 부분을 본원에 참고로 인용한다.
몇몇 실시양태에서, 하나 이상의 전술된 활성화 조촉매는 서로의 조합으로 사용된다. 특히 바람직한 조합은, 트라이((C1-C4)하이드로카빌)알루미늄, 트라이((C1-C4)하이드로카빌)보란 또는 암모늄 보레이트와 올리고머성 또는 중합체성 알룸옥산 화합물의 혼합물이다.
하나 이상의 화학식 I의 금속-리간드 착체의 총 몰 수 대 하나 이상의 활성화 조촉매의 총 몰 수의 비는 1:10,000 내지 100:1이다. 바람직하게, 상기 비는 적어도 1:5000, 더욱 바람직하게는 적어도 1:1000 및 10:1 이하, 더욱 바람직하게는 1:1 이하이다. 알룸옥산이 단독으로 활성화 조촉매로서 사용되는 경우, 바람직하게는, 사용되는 알룸옥산의 몰 수가 화학식 I의 금속-리간드 착체의 총 몰 수보다 100배 이상이다. 트리스(펜타플루오로페닐)이 단독으로 활성화 조촉매로서 사용되는 경우, 바람직하게는, 사용되는 트리스(펜타플루오로페닐)보란의 몰 수 대 하나 이상의 화학식 I의 금속-리간드 착체의 총 몰 수가 0.5:1 내지 10:1, 더욱 바람직하게는 1:1 내지 6:1, 더더욱 바람직하게는 1:1 내지 5:1이다. 나머지 활성화 조촉매는 일반적으로, 하나 이상의 화학식 I의 금속-리간드 착체의 총 몰과 대략적으로 동일한 몰 량으로 사용된다.
화학식 I의 금속-리간드 착체는, 임의적으로는 실질적으로 순수한 형태(즉, 90% 초과) 또는 하나 이상의 다른 화학식 I의 금속-리간드 착체와의 혼합물로서; 임의적으로 용매, 특히 유기 액체, 바람직하게는 비양성자성 용매 중의 용매화된 부가물 형태; 이량체 형태; 또는 이의 킬레이트화된 유도체 형태[이때, 상기 킬레이트화된 유도체는 화학식 I의 금속-리간드 착체 및 킬레이트제를 포함함]로서의 단리된 결정으로서 존재할 수 있다. 바람직하게, 상기 킬레이트제는 유기 루이스 염기(예를 들어, 비양성자성 유기 용매, 예컨대 테트라하이드로퓨란(THF); 또는 비양성자성 아민 염기, 예컨대 트라이에틸아민)이다.
몇몇 실시양태에서, 환원제는, 더 높은 산화 상태(예컨대, +4)의 화학식 I의 금속-리간드 착체로부터 더 낮은 산화 상태(예컨대, +2)의 화학식 I의 금속-리간드 착체를 제조하기 위해 사용된다. 본원에서 "환원제"라는 용어는, 환원 조건 하에 더 높은 산화 상태로부터 더 낮은 산화 상태로(예컨대, +6의 형식적 산화 상태에서 +4의 형식적 산화 상태로) 금속(M1)을 환원시키는 금속-함유 물질 또는 화합물, 유기 환원제 또는 기술(예컨대, 전기 분해)을 의미한다. 적합한 환원제의 예는 알칼리 금속, 알칼리 토금속, 알루미늄 및 아연, 및 알칼리 금속 또는 알칼리 토금속의 합금, 예컨대 나트륨/수은 아말감 및 나트륨/칼륨 합금이다. 또 다른 적합한 환원제의 예는 나트륨 나프탈레나이드, 칼륨 흑연, 리튬 알킬, 리튬 또는 칼륨 알카다이엔일, 및 그리냐르 시약(예컨대, 알킬 마그네슘 할라이드)이다. 가장 바람직한 환원제는 알칼리 금속 또는 알칼리 토금속, 특히 리튬 및 마그네슘 금속이다. 본 발명의 금속-리간드 착체를 제조하기 위해 당업자가 변형할 수 있는 적합한 기술은 공지되어 있으며, 바람직하게는 예를 들어 미국 특허 제 5,866,704 호; 미국 특허 제 5,959,047 호; 및 미국 특허 제 6,268,444 호에 교시된 기술로부터 유도된다.
바람직하게, 화학식 I의 금속-리간드 착체는, 단리된 형태로 수집되고 이때, 이는 실질적으로 용매가 없고, 예컨대 이의 제조에 사용되는 임의의 용매의 총량이 10 중량% 이하이고, 화학식 I의 금속-리간드 착체가 단리된 형태의 70 중량% 이상을 함유함을 의미한다. 더더욱 바람직하게, 화학식 I의 금속-리간드 착체는 단리되고 정제된 형태로 수집된다(즉, 화학식 I의 금속-리간드 착체는 실질적으로 용매가 없고, 80 중량% 이상, 더욱 바람직하게는 90 중량% 이상의 정제된 형태를 포함함). 본원에서 "중량%"는, 형태 또는 혼합물의 총 중량을 기준으로 한다. 바람직하게, 상기 혼합물에서 화학식 I의 금속-리간드 착체의 중량%는 13-탄소 또는 양성자 핵자기 공명(각각, 13C- 또는 1H-NMR) 분광법을 사용하여 결정된다.
화학식 I의 금속-리간드 착체의 몇몇의 더욱 바람직한 실시양태에서, M1은 4가 티타늄이다. 또 다른 실시양태에서, M1은 4가 지르코늄이다. 또 다른 실시양태에서, M1은 4가 하프늄이다.
몇몇 실시양태에서, X는 화학식 I의 금속-리간드 착체에 존재하지 않는다(즉, n은 0이다). 몇몇 실시양태에서, n은 1이다. 몇몇 실시양태에서, n은 2이다. 몇몇 실시양태에서, n은 3이다.
몇몇 실시양태에서, n은 1, 2, 또는 3이고, 하나 이상의 X는, RXNRKRL, RKORL, RKSRL 또는 RXPRKRL의 중성 루이스 염기 기이다. X가 중성 루이스 산 기인 경우, 더욱 바람직하게는 RX, RK 및 RL은 각각 독립적으로 수소, (C1-C40)하이드로카빌, [(C1-C10)하이드로카빌]3Si, [(C1-C10)하이드로카빌]3Si(C1-C10)하이드로카빌 또는 (C1-C40)헤테로하이드로카빌이다. 더더욱 바람직하게는 RX, RK 및 RL은 각각 독립적으로 비치환된 (C1-C20)하이드로카빌이고, 더욱 더 바람직하게는 비치환된 (C1-C10)하이드로카빌이다.
몇몇 실시양태에서, 하나 이상의 L이 존재한다. 이러한 실시양태에서, 두 개의 L이 존재하는 경우(즉, L 및 LQ), L은 각각 동일한 것이 바람직하다. 또 다른 이러한 실시양태에서, L 중 하나는 상이하다. 몇몇 실시양태에서, L은 각각 할로겐 원자, 비치환된 (C1-C20)하이드로카빌, 비치환된 (C1-C20)하이드로카빌C(O)O-, 또는 RKRLN-이고, 이때 RK 및 RL은 각각 독립적으로 비치환된 (C1-C20)하이드로카빌이다. 몇몇 실시양태에서, L은 각각 염소 원자, (C1-C10)하이드로카빌(예컨대, (C1-C6)알킬 또는 벤질), 비치환된 (C1-C10)하이드로카빌C(O)O-, 또는 RKRLN-이고, 이때 RK 및 RL은 각각 독립적으로 비치환된 (C1-C10)하이드로카빌이다.
몇몇 실시양태에서, R4는 이미 정의된 바와 같고, R2 및 R3은 함께 하기 화학식 R23의 2가 라디칼을 형성한다:
화학식 R23
즉, 화학식 I의 금속-리간드 착체는 하기 화학식 II의 금속-리간드 착체이다:
[화학식 II]
상기 식에서,
R1, R2A, R3A, R4, R5, M1, m, n, L, LQ, J 및 X는 화학식 I에 대해 정의된 바와 같다. 바람직하게, R2A, R3A 및 R4는 각각 독립적으로 H 또는 (C1-C20)하이드로카빌이고, 더욱 바람직하게는 H 또는 (C1-C10)알킬, 더더욱 바람직하게는 (C1-C10)알킬이고, 더욱 더 바람직하게는 메틸이다. 또한, 바람직하게 R2A 및 R3A는 함께 (C2-C20)하이드로카빌렌 또는 (C1-C20)헤테로하이드로카빌렌을 형성한다. 또한, 더욱 바람직하게 R5는 (C1-C20)알킬(예컨대, 1-옥틸)이다. 또한, 더욱 바람직하게 R4 및 R5는 함께 (C1-C5)알킬렌, 더더욱 바람직하게는 (C3 또는 C4)알킬렌, 더욱 더 바람직하게는 CH2CH2CH2 또는 CH2CH2CH2CH2를 형성한다.
화학식 II의 더욱 바람직한 금속-리간드 착체는 하기 화학식 II-A의 금속-리간드 착체이다:
[화학식 II-A]
상기 식에서,
R34는 각각 독립적으로 C(R35)2, O, S, S(O), S(O)2, N(RN), Si(RC)2 또는 P(RP)이고,
이때, R35는 각각 독립적으로 H 또는 (C1-C20)하이드로카빌이고,
RN, RC, 및 RP는 각각 독립적으로 (C1-C20)하이드로카빌이고,
M1, m, n, L, LQ, J, X, R1, R2A 및 R5는 상기 화학식 I의 금속-리간드 착체에 대해 정의된 바와 같다.
더더욱 바람직하게는, R34가 각각 CH2이다. 또한, 더더욱 바람직하게는, 3개의 R34 중 내측 R34가 O 또는 N(RN)이고, 외측 R34가 각각 CH2이다(즉, =C(R2A)-R34-R34-R34-가 =C(R2A)-CH2-O-CH2- 또는 =C(R2A)-CH2-N(RN)-CH2-임). 또한, n이 0이고 X가 없는 화학식 II-A의 금속-리간드 착체가 바람직하다. 또한, X의 RK가 R5와 함께 (C1-C20)하이드로카빌렌을 형성하는, 화학식 II-A의 금속-리간드 착체가 바람직하다. 또한, R1 또는 R5가 L의 RL과 함께 (C1-C20)하이드로카빌렌을 형성하는, 화학식 II-A의 금속-리간드 착체가 바람직하다. 또한, R1 또는 R5와 L이 함께, 더욱 바람직하게는 R1과 L이 함께, 더더욱 바람직하게는 R5와 L이 함께 2가 라디칼 잔부 (C1-C40)하이드로카빌렌-C(O)N((C1-C20)하이드로카빌), (C1-C40)하이드로카빌렌-C(O)O-, (C1-C40)하이드로카빌렌 또는 (C1-C40)헤테로하이드로카빌렌을 형성하는, 화학식 II-A의 금속-리간드 착체가 바람직하다.
화학식 II의 또 다른 더욱 바람직한 금속-리간드 착체는 하기 화학식 II-B의 금속-리간드 착체이다:
[화학식 II-B]
상기 식에서,
R34는 각각 독립적으로 상기 화학식 II-A에서 R34에 대해 정의된 바와 같고,
M1, m, n, L, LQ, J, X, R1, R2A 및 R5는 화학식 I의 금속-리간드 착체에서 정의된 바와 같다. 더더욱 바람직하게는, 2개의 R34 중 더 상부의 것이 O 또는 N(RN)이고, 더 하부의 R34는 CH2이다(즉, =C(R2A)-R34-R34-가 =C(R2A)-O-CH2- 또는 =C(R2A)-N(RN)-CH2-임). 더더욱 바람직하게는, R34가 각각 CH2이다. 또한, n은 0이고 X가 없는 화학식 II-B의 금속-리간드 착체가 바람직하다. 또한, X의 RK와 R5가 함께 (C1-C20)하이드로카빌렌을 형성하는, 화학식 II-B의 금속-리간드 착체가 바람직하다. 또한, R1 또는 R5가 L의 RL과 함께 (C1-C20)하이드로카빌렌을 형성하는, 화학식 II-B의 금속-리간드 착체가 바람직하다.
또한, R1 또는 R5가 L과 함께, 더욱 바람직하게는 R1과 L이 함께, 더더욱 바람직하게는 R5와 L이 함께, 2가 라디칼 잔부 (C1-C40)하이드로카빌렌-C(O)N((C1-C20)하이드로카빌), (C1-C40)하이드로카빌렌-C(O)O-, (C1-C40)하이드로카빌렌 또는 (C1-C40)헤테로하이드로카빌렌을 형성하는, 화학식 II-B의 금속-리간드 착체가 바람직하다.
화학식 II의 또 다른 더욱 바람직한 금속-리간드 착체는 하기 화학식 II-C의 금속-리간드 착체이다.
[화학식 II-C]
상기 식에서,
----은 각각, 존재하지 않거나 파이 결합이고,
R34는 각각 독립적으로 상기 화학식 I-A에서 R34에 대해 정의된 바와 같고,
M1, m, n, L, LQ, J, X, R1, R2A 및 R5는 상기 화학식 I의 금속-리간드 착체에 대해 정의된 바와 같다.
더더욱 바람직하게, ----은 각각 존재하지 않고, R34는 CH2이다.
화학식 II의 또 다른 더욱 바람직한 금속-리간드 착체는 하기 화학식 II-D의 금속-리간드 착체이다:
[화학식 II-D]
상기 식에서,
----은 각각, 존재하지 않거나 파이 결합이고,
R34는 존재하지 않거나 독립적으로 화학식 II-A에서 R34에 대해 정의된 바와 같고,
M1, m, n, L, LQ, J, X, R1, R2A 및 R5는 상기 화학식 I의 금속-리간드 착체에 대해 정의된 바와 같다.
더더욱 바람직하게, ----은 각각 파이 결합이고, R34는 O 또는 N(RN)이다. 또한, 더더욱 바람직하게는, ----은 각각 존재하지 않고, R34는 CH2이거나 존재하지 않는다.
화학식 II의 또 다른 더욱 바람직한 금속-리간드 착체는 하기 화학식 II-E의 금속-리간드 착체이다:
[화학식 II-E]
상기 식에서,
----은 각각 파이 결합이거나 존재하지 않고,
M1, m, n, L, LQ, J, X, R1, R2A 및 R5는 상기 화학식 I의 금속-리간드 착체에 대해 정의된 바와 같다.
몇몇 실시양태에서, ----은 각각 파이 결합이고, 다른 경우 ----은 각각 존재하지 않는다.
화학식 II의 또 다른 더욱 바람직한 금속-리간드 착체는 하기 화학식 II-F의 금속-리간드 착체이다:
[화학식 II-F]
상기 식에서, M1, m, n, L, LQ, J, X, R1, R2A 및 R5는 상기 화학식 I의 금속-리간드 착체에 대해 정의된 바와 같다.
몇몇 실시양태에서, R3A, R4 및 R5가 독립적으로 함께 (C1-C40)하이드로카빌렌 또는 (C1-C40)헤테로하이드로카빌렌의 3가 유사체를 형성하고, M1, L, J, n, X, R1, 및 R2A가 상기 화학식 II의 금속-리간드 착체에 대해 정의된 바와 같은, 화학식 II의 금속-리간드 착체가 바람직하다. 화학식 II의 더더욱 바람직한 금속-리간드 착체는 하기 화학식 II-G의 금속-리간드 착체이다:
[화학식 II-G]
상기 식에서, M1, m, n, L, LQ, J, X, R1, R2A는 상기 화학식 I의 금속-리간드 착체에 대해 정의된 바와 같다.
몇몇 실시양태에서, R2A 및 R3A가 각각 H 또는 (C1-C40)하이드로카빌, 바람직하게는 H 또는 (C1-C3)하이드로카빌이고, M1, L, J, n, X, R1, R4 및 R5가 상기 화학식 I의 금속-리간드 착체에 대해 정의된 바와 같은, 화학식 II의 금속-리간드 착체가 바람직하다. 화학식 II의 더더욱 바람직한 금속-리간드 착체는 하기 화학식 II-H의 금속-리간드 착체이다:
[화학식 II-H]
상기 식에서,
R2A는 H 또는 (C1-C40)하이드로카빌(더욱 바람직하게는 H 또는 (C1-C10)하이드로카빌, 더욱 더 바람직하게는 수소)이고, R3A 및 R4는 (C1-C20)하이드로카빌렌(더욱 바람직하게는 (C1-C5)하이드로카빌렌) 또는 (C1-C20)헤테로하이드로카빌렌(더욱 바람직하게는 (C1-C4)하이드로카빌렌)이고, M1, m, n, L, LQ, X, R1 및 R5는 화학식 I의 금속-리간드 착체에 대해 정의된 바와 같다.
몇몇 실시양태에서, R2A 및 R3A는 각각 H 또는 (C1-C40)하이드로카빌, 바람직하게, H 또는 (C1-C3)하이드로카빌인 화학식 II의 금속-리간드 착체가 바람직하고; M1, L, J, n, X, R1, R4 및 R5는 화학식 I의 금속-리간드 착체에 대해 정의된 바와 같다. 하기 화학식 II-I의 금속-리간드 착체인 RKRLC=N-(J5)가 더더욱 바람직하다:
[화학식 II-I]
상기 식에서,
R2A는 H 또는 (C1-C40)하이드로카빌(더욱 바람직하게는 H 또는 (C1-C10)하이드로카빌, 더욱 더 바람직하게는 수소)이고, R3A 및 R4는 (C1-C20)하이드로카빌렌(더욱 바람직하게는 (C1-C5)하이드로카빌렌) 또는 (C1-C20)헤테로하이드로카빌렌(더욱 바람직하게는 (C1-C4)하이드로카빌렌)이고, M1, m, n, L, LQ, X, R1, R5, RK, 및 RL은 화학식 I의 금속-리간드 착체에 대해 정의된 바와 같다. R3A 및 R4가 함께 (C2-C4)하이드로카빌렌을 형성하고, J의 RK 및 RL이 (C1-C3)헤테로하이드로카빌렌(예컨대, (치환된 (C6)아릴)-N(·)-C(H)=C(H)-N(·)-(치환된 (C6)아릴)과 같은 N,N'-2가 치환된-N,N'-(Z)이성질체의 2가 라디칼-에텐-1,2-다이아민)을 형성하는 화학식 II-I의 금속-리간드 착체가 더욱 바람직하다.
하기 구조식 (II-A1), (II-A2), (II-A3), (II-A4), (II-A5) 중 임의의 하나의 화학식 II-A; (II-BI), (II-B2), (II-B3), (II-B4), (II-BS), (II-B6), (II-B7), (II-B8) 중 임의의 하나의 화학식 II-B; (II-C1), (II-C2), (II-C3) 중 임의의 하나의 화학식 C; (II-DI), 및 (II-D2) 중 임의의 하나의 화학식 II-D의 금속-리간드 착체가 더더욱 바람직하다:
상기 식에서,
n은 0이고,
X는 존재하지 않고;
J, R1 및 R5는 화학식 II의 금속-리간드 착체에 대해 정의된 바와 같다.
몇몇 실시양태에서, 화학식 I의 금속-리간드 착체는 하기 화학식 III의 금속-리간드 착체이다:
[화학식 III]
상기 식에서,
R2B, R3B 및 R4는 각각 독립적으로 (C1-C40)하이드로카빌, (C1-C40)하이드로카빌O-, (C1-C40)하이드로카빌S-, (C1-C40)하이드로카빌S(O)-, (C1-C40)하이드로카빌S(O)2-, ((C1-C40)하이드로카빌)2N-, ((C1-C40)하이드로카빌)2P- 또는 (C1-C40)헤테로하이드로카빌이고, R1, R5, M1, m, n, L, LQ, J 및 X는 화학식 I에 대해 정의된 바와 같다.
몇몇 실시양태에서, 화학식 III의 금속-리간드 착체는 J가 RKRLC=N-(J5)인 하기 화학식 III-A의 금속-리간드 착체이다:
[화학식 III-A]
상기 식에서,
R2B, R3B 및 R4는 화학식 III의 금속-리간드 착체에 대해 정의된 바와 같고; M1, L, LQ, n, m, X, R1, 및 R5는 화학식 I의 금속-리간드 착체에 대해 정의된 바와 같다. J의 RK 및 RL이 함께 (C1-C3)헤테로하이드로카빌렌(예컨대, (치환된 (C6)아릴)-N(·)-C(H)=C(H)-N(·)-(치환된 (C6)아릴)과 같은 N,N'-2가 치환된-N,N'-(Z)이성질체의 2가 라디칼-에텐-1,2-다이아민)을 형성하는 화학식 III-A의 금속-리간드 착체가 더욱 바람직하다.
전술한 화학식 중 임의의 금속-리간드 착체의 몇몇의 상기 실시양태에서, J 는 RKRLRxP=N-(J1)이고, 이때 RK, RL, 및 Rx는 각각 독립적으로 화학식 I에 대해 정의된 바와 같다. 더욱 바람직하게, J1은 트리스(1,1-다이메틸에틸)포스핀이미도; 트라이페닐포스핀이미도; 또는 트라이메틸포스핀이미도이다.
화학식 I 내지 III 중 임의의 금속-리간드 착체의 몇몇의 상기 실시양태에서, J는 RKRLB-O-(J2)이고, 이때 RK 및 RL은 각각 독립적으로 상기 정의된 바와 같다. 더욱 바람직하게, J2는 비스(1,1-다이메틸에틸)보라닐-옥사이드; 다이페닐보라닐-옥사이드; 또는 다이메틸보라닐-옥사이드(즉, (CH3)2B-0)이다.
화학식 I 내지 III 중 임의의 금속-리간드 착체의 몇몇의 상기 실시양태에서, J는 하기 화학식 J3이다:
화학식 J3
상기 식에서,
---은 두 개의 비편재화 파이 결합이고;
RW1 및 RW2는 각각 독립적으로 RX이고; M2는 Al-RA, Ga-RA 또는 Zn이고, 이때 RA는 각각 독립적으로 (Cl-C40)알킬, RKRLN- 또는 RLO-이고; RJ는 각각 독립적으로 (C6-C12)아릴이다. 바람직하게 화학식 J3에서 RW1은 각각 메틸이고, RW2는 수소이고; M2는 Al-CH3, Ga-CH3 또는 Zn이고, 더욱 바람직하게 Al-CH3 또는 Zn이고; RJ는 각각 치환된 페닐, 더욱 바람직하게는 2,6-비스(l-메틸에틸)페닐이다. J3 리간드는 미국 특허 제 2008/0261804 A1 호, 문단 [0029], [0043] 및 [0044]와 도 1 및 2a에서 기재된 과정을 적응하여 제조될 수 있다.
화학식 I 내지 III 중 임의의 금속-리간드 착체의 몇몇 상기 실시양태에서, J는 RKRLN-O-(J4)이고, 이때 RK 및 RL은 각각 독립적으로 상기 정의된 바와 같다. 더욱 바람직하게, RKRLN-O-는 2,2,6,6-테트라메틸피페리딘일-l-옥사이드이다.
전술한 화학식 중 임의의 금속-리간드 착체의 몇몇 상기 실시양태에서, J는 RKRLC=N-(J5)이다. 더욱 바람직하게, J5는 1,3-비스((C6-ClO)아릴) 1,3-다이아자-2-이미노 리간드이고, (C6-ClO)아릴은 각각 독립적으로 1 내지 4개의 RS로 치환되거나 비치환된다.
전술한 화학식 중 임의의 금속-리간드 착체의 몇몇 상기 실시양태에서, J는 RK(RLRxN)C=N-(J6)이다.
전술한 화학식 중 임의의 금속-리간드 착체의 몇몇 상기 실시양태에서, J는 (RLRXN)2C=N-(J7)이다.
화학식 J1 내지 J7 중 임의의 하나의 화학식에서, 존재하는 경우, 바람직하게 RK, 및 RL, RX 및 RJ는 각각 독립적으로 (C1-ClO)알킬, (C3-ClO)사이클로알킬, 또는 (C6-ClO)아릴이고; 더욱 바람직하게 (C1-ClO)알킬 또는 (C6)아릴이며, 더더욱 바람직하게 (C1-C4)알킬이다.
화학식 I의 금속-리간드 착체의 몇몇의 상기 실시양태에서, n은 1이고 X 및 J는 함께 하기 화학식 IV의 금속-리간드 착체와 같은 전술한 화학식 K1 내지 K6 중 임의의 1가 음이온 바이덴테이트 잔부 XJ-JX를 형성한다:
[화학식 IV]
몇몇 실시양태에서, R4가 앞서 정의된 바와 같고, R2 및 R3이 함께 하기 화학식 R23의 2가 라디칼을 형성하는 화학식 IV의 금속-리간드 착체가 바람직하다:
화학식 R23
즉, 화학식 IV의 금속-리간드 착체는 하기 화학식 IV-A의 금속-리간드 착체이다:
[화학식 IV-A]
상기 식에서, R1, R2A, R3A, R4, R5, M1, m, L, LQ, 및 Xl-JX는 화학식 IV에 대해 정의된 바와 같다.
몇몇 실시양태에서, 화학식 IV의 금속-리간드 착체는 하기 화학식 IV-B의 금속-리간드 착체이다:
[화학식 IV-B]
상기 식에서,
R2B, R3B 및 R4는 각각 독립적으로 (C1-C40)하이드로카빌, (C1-C40)하이드로카빌O-, (C1-C40)하이드로카빌S-, (C1-C40)하이드로카빌S(O)-, (C1-C40)하이드로카빌S(O)2-, ((C1-C40)하이드로카빌)2N-, ((C1-C40)하이드로카빌)2P- 또는 (C1-C40)헤테로하이드로카빌이고, R1, R5, M1, m, n, L, LQ, XJ-JX는 화학식 IV에 대해 정의된 바와 같다.
화학식 IV, IV-A 또는 IV-B의 금속-리간드 착체의 몇몇 실시양태에서, XJ-JX는 전술한 화학식 K1이다. 화학식 K1의 잔부는 하기 화학식 K1a의 호변 이성질체와 평형으로 존재할 수 있다:
[화학식 K1a]
또한, 호변 이성질체 K1 및 K1a는 탄소-질소 이중 결합에서 파이 전자가 비편재화되는 곳에서 도시될 수 있다(구조는 나타나지 않음).
화학식 IV, IV-A 또는 IV-B의 금속-리간드 착체의 몇몇 실시양태에서, XJ-JX는 전술한 화학식 K2이다. 화학식 K2의 잔부는 하기 화학식 K2a의 호변 이성질체와 평형으로 존재할 수 있다:
[화학식 K2a]
또한, 호변 이성질체 K2 및 K2a는 인-질소 이중 결합에서 파이 전자가 비편재화되는 곳에서 도시될 수 있다(구조는 나타나지 않음).
화학식 IV, IV-A 또는 IV-B의 금속-리간드 착체의 몇몇 실시양태에서, XJ-JX는 전술한 화학식 K3이다.
화학식 IV, IV-A 또는 IV-B의 금속-리간드 착체의 몇몇 실시양태에서, XJ-JX는 전술한 화학식 K4이다.
화학식 IV, IV-A 또는 IV-B의 금속-리간드 착체의 몇몇 실시양태에서, XJ-JX는 전술한 화학식 K5이다.
화학식 IV, IV-A 또는 IV-B의 금속-리간드 착체의 몇몇 실시양태에서, XJ-JX는 전술한 화학식 K6이다.
화학식 K1 내지 K6 중 임의의 XJ-JX에서, 존재하는 경우, 바람직하게 RK, 및 RL 및 RX는 각각 독립적으로 (C1-ClO)알킬, (C4-ClO)사이클로알킬, 더욱 바람직하게 (C1-ClO)알킬이며, 더더욱 바람직하게 (C1-C4)알킬이다.
L을 가지는 전술한 화학식 중 임의의 금속-리간드 착체가 더욱 바람직하고 이때, L(예컨대, LQ)은 각각 독립적으로 (C1-C5)알킬, 트라이메틸실일메틸, 또는 벤질이고; L은 (C1-C5)알킬, 트라이메틸실일메틸, 또는 벤질이다.
R34를 가지는 전술한 화학식 중 임의의 금속-리간드 착체가 더욱 바람직하고 이때, R34는 각각 독립적으로 C(R35)2이고, R35는 각각 H 또는 메틸이다. 또한, 화학식 I의 금속-리간드 착체는 하나의 R34가 O 또는 N(RN)이고 잔여 R34가 존재하는 경우 독립적으로 C(R35)2이고, R35가 각각 H 또는 메틸이다.
전술된 화학식 중 임의의 금속-리간드 착체의 상기 실시양태에서, 더욱 바람직하게 하나 이상의 (C1-C40)헤테로하이드로카빌은 2-[((C1-C5)알킬)2NCH2]-(C6-Cl8)아릴, 더욱 더 바람직하게 2-[((C1-C5)알킬)2NCH2]-페닐이고; 하나 이상의 (C1-C40)헤테로하이드로카빌렌은 2-[((C1-C5)알킬)CH2]-(C6-Cl8)아릴, 더욱 더 바람직하게 2-[((C1-C5)알킬)CH2]-페닐이고; 하나 이상의 (C1-C40)하이드로카빌렌은 2-메틸페닐이다.
몇몇 실시양태에서, 화학식 I, II 내지 II-H, III, 및 IV 내지 IV-B 중 임의의 금속-리간드 착체가 바람직하고, 이때 R3A 및 R4 또는 R3B 및 R4는 각각 (C1-C40)하이드로카빌렌 또는 (C1-C40)헤테로하이드로카빌렌을 함께 형성한다. 더욱 바람직하게, R3A 및 R4 또는 R3B 및 R4는 각각 (C2-C5)하이드로카빌렌 또는 (C1-C4)헤테로하이드로카빌렌, 더더욱 바람직하게 (C2-C5)하이드로카빌렌을 형성하고 바람직하게, R1 및 R5는 각각 독립적으로 (C1-C10)하이드로카빌, 더욱 바람직하게 (C1-C10)알킬, (C3-C10)사이클로알킬, 또는 (C6-C10)아릴이고, 더욱 더 바람직하게 (C1-C10)알킬 또는 (C6)아릴이다. 이러한 실시양태에서, 바람직하게 R2A 또는 R2B는 H 또는 (C1-C10)알킬, 더욱 바람직하게 H 또는 CH3이다.
R1 및 R5를 가지는 전술한 화학식 중 임의의 금속-리간드 착체가 더욱 바람직하고, 이때 R1 및 R5는 각각 독립적으로 (C1-C10)하이드로카빌, 더욱 바람직하게 (C1-C10)알킬, (C3-C10)사이클로알킬, 또는 (C6-C10)아릴이고, 더욱 더 바람직하게 (C1-C10)알킬 또는 (C6)아릴이다. 이러한 실시양태에서, 바람직하게 R2 또는 R2A는 H 또는 (C1-C10)알킬, 더욱 바람직하게 H 또는 CH3이다.
또한, R1을 가지는 전술한 화학식 중 임의의 금속-리간드 착체가 더욱 바람직하고, 이때 R1은 (C1-C40)하이드로카빌이고, 더욱 더 바람직하게 R1은 (C1-C20)하이드로카빌이고, n은 0이고, X는 존재하지 않는다. 또한, R1을 가지는 전술한 화학식 중 임의의 금속-리간드 착체가 더욱 바람직하고, 이때 R1은 (C1-C40)헤테로하이드로카빌이고, 더욱 더 바람직하게 R1은 (C1-C20)헤테로하이드로카빌이고, n은 0이고, X는 존재하지 않는다. 또 다른 실시양태에서, n은 1, 2, 또는 3이고, X의 RK는 함께 (C1-C40)하이드로카빌렌 또는 (C1-C40)헤테로하이드로카빌렌을 형성하고, 더욱 바람직하게 X의 R1 및 RK는 함께 (C1-C40)하이드로카빌렌 또는 (C1-C40)헤테로하이드로카빌을 형성하고, 더욱 바람직하게 X의 R1 및 RK는 함께 (C1-C20)하이드로카빌렌 또는 (C1-C20)헤테로하이드로카빌렌을 형성한다. 또 다른 실시양태에서, L의 R1 및 RL은 함께 (C1-C40)하이드로카빌렌 또는 (C1-C40)헤테로하이드로카빌렌을 형성하고, 더욱 바람직하게 L의 R1 및 RL은 함께 (C1-C20)하이드로카빌렌 또는 (C1-C20)헤테로하이드로카빌렌을 형성하고, n은 0이고, X는 존재하지 않는다. 또 다른 실시양태에서, L의 R1 및 RL은 함께 (C1-C40)하이드로카빌렌 또는 (C1-C40)헤테로하이드로카빌렌을 형성하고, 더욱 바람직하게 L의 R1 및 RL은 함께 (C1-C20)하이드로카빌렌 또는 (C1-C20)헤테로하이드로카빌렌을 형성하고, n은 0이고, X는 존재하지 않는다.
또한, R5를 가지는 전술한 화학식 중 임의의 금속-리간드 착체가 더욱 바람직하고, 이때 R5는 (C1-C40)하이드로카빌이고, 더욱 더 바람직하게 R5는 (C1-C20)하이드로카빌이고, n은 0이고, X는 존재하지 않는다. 또한, R5를 가지는 전술한 화학식 중 임의의 금속-리간드 착체가 더욱 바람직하고, 이때 R5는 (C1-C40)헤테로하이드로카빌이고, 더욱 더 바람직하게 R5는 (C1-C20)헤테로하이드로카빌이고, n은 0이고, X는 존재하지 않는다. 또 다른 실시양태에서, n은 1, 2, 또는 3이고, X의 R5 및 RK는 함께 (C1-C20)하이드로카빌렌 또는 (C1-C20)헤테로하이드로카빌렌을 형성한다. 또 다른 실시양태에서, L의 R5 및 RL는 함께 (C1-C40)하이드로카빌렌 또는 (C1-C40)헤테로하이드로카빌렌을 형성하고, 더욱 바람직하게 L의 R5 및 RL는 함께 (C1-C20)하이드로카빌렌 또는 (C1-C20)헤테로하이드로카빌렌을 형성하고, 임의적으로 n은 0이고, X는 존재하지 않는다. 더더욱 바람직하게는, R5가 1-부틸, 2-프로필, 1,1-다이메틸에틸, 벤질, 페닐, 사이클로헥실, 1-메틸-피페리딘-4-일, 3-(N,N-다이메틸아미노)-프로필, 1,1-다이메틸에틸아미노 또는 피롤-1-일이다.
전술한 화학식 중 R1 및 R5가 각각 독립적으로 (C1-C40)하이드로카빌이고, 더더욱 바람직하게는 R1 및 R5가 각각 독립적으로 (C1-C20)하이드로카빌이고, 임의적으로 n은 0이고, X는 존재하지 않는 임의의 금속-리간드 착체가 더욱 바람직하다. 또한, X, R1 및 R5를 가지는 전술한 화학식 중 임의의 금속-리간드 착체가 더욱 바람직하고, 이때 R1 및 R5 중 하나가 X의 RK와 함께 (C1-C20)하이드로카빌렌 또는 (C1-C20)헤테로하이드로카빌렌을 형성하고, R1 및 R5 중 나머지 하나가 (C1-C20)하이드로카빌 또는 (C1-C20)헤테로하이드로카빌이다. 또한, L, R1 및 R5를 가지는 전술한 화학식 중 임의의 금속-리간드 착체가 더욱 바람직하고, 이때 R1 및 R5 중 하나가 L의 RL과 함께 (C1-C20)하이드로카빌렌 또는 (C1-C20)헤테로하이드로카빌렌을 형성하고, R1 및 R5 중 나머지 하나가 (C1-C20)하이드로카빌 또는 (C1-C20)헤테로하이드로카빌이다.
R1 및 R5를 가지는 전술한 임의의 화학식의 금속-리간드 착체 중에서, R1 및 R5 중 하나가 2,6-비스(다이(C1-C4)알킬-아미노)페닐; 2,6-다이나이트로페닐; 2,6-다이((C1-C4)알킬옥시)페닐; 2-(C1-C4)알킬-페닐; 2,6-다이(C1-C4)알킬-페닐; 3,5-다이(C1-C4)알킬페닐; 2,4,6-트라이(C1-C4)알킬-페닐; 바이페닐-2-일; 2,6-다이페닐페닐; 3,5-다이페닐페닐; 2,4,6-트라이페닐페닐; 3,5-비스(2,6-비스[(C1-C4)알킬]페닐)페닐; 2,6-다이(1-나프틸)페닐; 3,5-다이(1-나프틸)페닐; 사이클로헥실; 다이페닐메틸; 또는 트리틸인 제 1 기이고, 이때 (C1-C4)알킬은 각각 독립적으로 메틸, 에틸, 1-프로필, 1-메틸에틸, 1-부틸, 2-부틸, 2-메틸프로필 또는 1,1-다이메틸에틸인 상기 금속-리간드 착체가 특히 바람직하다. 또한, R1 및 R5 중 하나가, (C1-C20)알킬(예컨대, 1-부틸, 2-프로필, 1,1-다이메틸에틸, 및 1-옥틸), 벤질, 페닐, 사이클로헥실, 1-메틸-피페리딘-4-일, 3-(N,N-다이((C1-C4)알킬)아미노)-프로필, (C1-C4)알킬-아미노 또는 피롤-1-일인 제 2 기인 것이 특히 바람직하다. R1 및 R5 중 하나가 상기 제 1 기에 대해 정의된 바와 같고, R1 및 R5 중 나머지 하나가 상기 제 2 기에 대해 정의된 바와 같은 금속-리간드 착체가 더더욱 바람직하다.
R1이 2,6-비스(1-메틸에틸)페닐, 2-(1-메틸에틸)페닐, 2,4,6-트리스(1,1-다이메틸에틸)페닐, 2-(1,1-다이메틸에틸)페닐, 3,4-비스(1,1-다이메틸에틸)페닐, 2,4,6-트라이페닐페닐, 바이페닐-2-일, 3,5-다이페닐페닐, 사이클로헥실, 다이페닐메틸, 트라이페닐메틸, 3,5-비스(2,6-다이메틸페닐)페닐, 2,6-비스(다이메틸아미노)페닐, 2,6-다이나이트로페닐, 2,6-다이(1-메틸에톡시)페닐, 2,6-다이(1-나프틸)페닐, 또는 3,5-다이(1-나프틸)페닐이고, R5가 1-부틸, 2-프로필, 1,1-다이메틸에틸, 벤질, 페닐, 사이클로헥실, 1-메틸-피페리딘-4-일, 3-(N,N-다이메틸아미노)-프로필, 1,1-다이메틸에틸아미노 또는 피롤-1-일인 전술된 화학식 중 임의의 금속-리간드 착체가 더더욱 바람직하다.
R1이 2,6-비스(1-메틸에틸)페닐, 2-(1-메틸에틸)페닐, 2,4,6-트리스(1,1-다이메틸에틸)페닐, 2-(1,1-다이메틸에틸)페닐, 3,4-비스(1,1-다이메틸에틸)페닐, 2,4,6-트라이페닐페닐, 바이페닐-2-일, 3,5-다이페닐페닐, 사이클로헥실, 다이페닐메틸, 트라이페닐메틸, 3,5-비스(2,6-다이메틸페닐)페닐, 2,6-비스(다이메틸아미노)페닐, 2,6-다이나이트로페닐, 2,6-다이(1-메틸에톡시)페닐, 2,6-다이(1-나프틸)페닐, 또는 3,5-다이(1-나프틸)페닐이고, J가 RKRLRxP=N-(J1)인 전술된 화학식 중 임의의 금속-리간드 착체가 더더욱 바람직하다.
R5가 1-부틸, 2-프로필, 1,1-다이메틸에틸, 벤질, 페닐, 사이클로헥실, 1-메틸-피페리딘-4-일, 3-(N,N-다이메틸아미노)-프로필, 1,1-다이메틸에틸아미노 또는 피롤-1-일이고, J가 RKRLRxP=N-(J1)인 전술된 화학식 중 임의의 금속-리간드 착체가 또한 더더욱 바람직하다.
R1이 2,6-비스(1-메틸에틸)페닐, 2-(1-메틸에틸)페닐, 2,4,6-트리스(1,1-다이메틸에틸)페닐, 2-(1,1-다이메틸에틸)페닐, 3,4-비스(1,1-다이메틸에틸)페닐, 2,4,6-트라이페닐페닐, 바이페닐-2-일, 3,5-다이페닐페닐, 사이클로헥실, 다이페닐메틸, 트라이페닐메틸, 3,5-비스(2,6-다이메틸페닐)페닐, 2,6-비스(다이메틸아미노)페닐, 2,6-다이나이트로페닐, 2,6-다이(1-메틸에톡시)페닐, 2,6-다이(1-나프틸)페닐, 또는 3,5-다이(1-나프틸)페닐이고, J가 RKRLC=N-(J5)인 전술된 화학식 중 임의의 금속-리간드 착체가 또한 더더욱 바람직하다.
R5가 1-부틸, 2-프로필, 1,1-다이메틸에틸, 벤질, 페닐, 사이클로헥실, 1-메틸-피페리딘-4-일, 3-(N,N-다이메틸아미노)-프로필, 1,1-다이메틸에틸아미노 또는 피롤-1-일이고, J가 RKRLC=N-(J5)인 전술된 화학식 중 임의의 금속-리간드 착체가 또한 더더욱 바람직하다.
또한, 후술되는 실시예 중 임의의 화학식 I의 금속-리간드 착체가 더더욱 바람직하다. 몇몇 실시양태에서, 화학식 I의 금속-리간드 착체는 후술되는 실시예 1 내지 4의 임의의 금속-리간드 착체 (1) 내지 (4)중 하나이다. 몇몇 실시양태에서, 화학식 I의 금속-리간드 착체는 후술되는 실시예 5 내지 8의 임의의 금속-리간드 착체 (5) 내지 (8)중 하나이다.
몇몇 실시양태에서, 상기 제 2 실시양태의 촉매는, 바람직한 화학식 I의 금속-리간드 착체 및 바람직한 활성화 조촉매 또는 이들의 반응 생성물을 포함하거나 이로부터 제조된다. 다른 실시양태에서, 상기 제 2 실시양태의 촉매는, 2종 이상의 바람직한 화학식 I의 금속-리간드 착체, 1종 이상의 바람직한 활성화 조촉매 또는 이들의 반응 생성물을 포함하거나 이로부터 제조된다.
몇몇 실시양태에서, 상기 제 2 실시양태의 촉매는 추가로, 하나 이상의 용매, 희석제(후술됨) 또는 이들의 조합물(본원에 기술된 바와 같음)을 포함한다. 다른 실시양태에서, 상기 제 2 실시양태의 촉매는 추가로, 바람직하게는 상기 희석제에 용해된, 분산제, 예컨대 탄성중합체를 포함한다. 이러한 실시양태에서, 상기 제 2 실시양태의 촉매는 바람직하게는 균질 촉매를 포함한다.
몇몇 실시양태에서, 상기 제 2 실시양태의 촉매는 추가로, 무기 또는 유기 미립자화된 고체 지지체를 포함하거나 이로부터 제조되며, 이때 상기 제 2 실시양태의 촉매는 상기 미립자화된 고체 지지체와 지지 조작적으로 접촉하여, 미립자화된 고체-지지된 촉매를 제공한다. 이러한 실시양태에서, 본 발명의 미립자화된 고체-지지된 촉매는 비균질 촉매를 포함한다.
상기 미립자화된 고체 지지체는, 상기 제 2 실시양태의 촉매를 지지할 수 있고 생성된 본 발명의 미립자화된 고체-지지된 촉매가 중합성 올레핀의 중합을 촉진하도록 하는 임의의 물질이다. 미립자화된 고체의 예는 실리카, 실리카 겔, 알루미나, 점토, 팽창된(expanded) 점토(에어로겔), 알루미노실리케이트, 트라이알킬알루미늄 화합물, 및 유기 또는 무기 중합체성 물질, 특히 폴리올레핀, 예컨대, 폴리(테트라플루오로에틸렌)이다. 더욱 바람직하게, 상기 제 2 실시양태의 촉매 및 상기 고체 지지체는, 본 발명의 미립자화된 고체-지지된 촉매에서, (상기 제 2 실시양태의 촉매의 중량(금속 M1 기준)):고체 지지체의 중량)의 비가 1:106 내지 1:103, 더욱 바람직하게는 1:106 내지 1:104가 되게 하는 양으로 사용된다.
"올레핀-중합 조건"이라는 용어는, 5 몰% 이상의 수율로 폴리올레핀을 생성하기에 충분한 반응 매개변수, 예컨대 온도, 압력, 올레핀 단량체의 농도, 용매(존재하는 경우), 반응 시간, 및 반응 압력을 의미한다. 몇몇 실시양태에서, 올레핀 중합은, 지글러-나타(Ziegler-Natta) 또는 카민스키-신(Kaminsky-Sinn) 유형의 올레핀 중합 반응에 대해 공지된 조건을 사용하여 달성된다. 상기 제 3 실시양태로서의 방법은, 하나 이상의 중합성 올레핀의 적어도 일부를 중합시켜 이로부터 폴리올레핀을 생성하기에 충분한 올레핀-중합 조건하에서 수행된다. 상기 방법은, 상기 중합 반응이 일어나는 임의의 온도, 압력 또는 다른 조건(예컨대, 용매, 대기, 및 성분들의 절대량 및 상대량)에서 수행될 수 있다. 바람직하게, 상기 조건은, 약 -100 ℃ 내지 약 300 ℃, 더욱 바람직하게는 약 0 ℃ 이상, 더더욱 바람직하게는 약 20 ℃ 이상, 더더욱 바람직하게는 약 50 ℃ 이상; 및 더욱 바람직하게는 약 250 ℃ 이하, 더더욱 바람직하게는 약 200 ℃ 이하, 더더욱 바람직하게는 약 150 ℃ 이하의 온도; 및 약 0.5 기압(50 kPa) 내지 10,000 기압(1,010,000 kPa), 더욱 바람직하게는 약 1 기압(101 kPa) 이상, 더더욱 바람직하게는 약 10 기압(1010 kPa) 이상; 및 더욱 바람직하게는 1000 기압(101,000 kPa) 이하, 더더욱 바람직하게는 500 기압(50,500 kPa) 이하의 압력을 포함하며; 바람직하게는, 실질적으로 비활성 대기[예컨대, 질소 기체, 희기체(예컨대, 아르곤 기체 및 헬륨 기체) 또는 이들의 2종 이상의 혼합물로 본질적으로 이루어진 건조(즉, 실질적으로 무수) 대기] 하에서; 폴리올레핀을 생성하기에 충분한 시간(예컨대, 반응 혼합물의 분취량을 분석함으로써 결정됨) 동안의 혼합(예컨대, 교반 또는 진탕)을 사용한다.
몇몇 실시양태에서, 본 발명의 금속-리간드 착체는, 본원에 기술된 바와 같은 고체 지지체 상에 지지되고, 슬러리로서 올레핀 중합 공정 또는 기상 중합에 사용된다. 실질적인 한계로서, 슬러리 중합은 바람직하게는, 중합체 생성물이 실질적으로 불용성인 액체 희석제(예컨대, 25 ℃에서, 1.0 mL의 액체 희석제에 50 mg 미만의 중합체 생성물이 용해됨) 내에서 수행된다. 바람직하게, 상기 슬러리 중합을 위한 희석제는, 5개 미만의 탄소 원자를 갖는 하나 이상의 탄화수소이다. 몇몇 실시양태에서, 하나 이상의 포화된 탄화수소, 예컨대 에탄, 프로판 또는 부탄이 상기 희석제의 전체 또는 부분으로서 사용된다. 다른 실시양태에서, 알파-올레핀 단량체 또는 다른 알파-올레핀 단량체들과의 혼합물이 상기 희석제의 전체 또는 부분으로서 사용된다. 가장 바람직하게는, 상기 희석제의 적어도 대부분이, 중합될 알파-올레핀 단량체(들)를 포함한다. 몇몇 실시양태에서, 분산제, 특히 탄성중합체는, 바람직하게는 당분야에 공지된 기술을 사용하여 상기 희석제에 용해된다.
몇몇 실시양태에서, 현탁액, 용액, 슬러리, 기상, 고체 상태 분말 중합 또는 다른 공정 조건이 사용된다. 다른 실시양태에서, 바람직하게는 본 발명의 미립자화된 고체-지지된 촉매가, 기상 중합 공정을 포함하는 제 3 실시양태의 양태에서 사용되는 경우, 미립자화된 고체 지지체는, 전술된 바와 같은 본 발명의 미립자화된 고체-지지된 촉매의 형태로 사용된다. 상기 제 3 실시양태의 대부분의 중합 반응에서, (제 2 실시양태의 촉매의 몰):(사용되는 중합성 화합물의 총 몰)의 비는 10-12:1 내지 10-1:1, 더욱 바람직하게는 10-9:1 내지 10-5:1이다.
상기 제 2 실시양태의 촉매는, 고체 지지체 상에 지지되었는지에 상관 없이, 바람직하게는 중합성 올레핀을 중합하거나 2종 이상의 중합성 올레핀(즉, 올레핀 단량체)을 공중합하여, 폴리올레핀을 제조하는 데 사용된다. "중합성 올레핀"이라는 용어는, 탄소-탄소 이중 결합 또는 삼중 결합-함유 단량체 또는 탄소-탄소 이중 결합 또는 삼중 결합-함유 올리고머 또는 이로부터 제조된 폴리올레핀을 의미하고,독립적으로 2 내지 100,000개의 탄소 원자, 바람직하게는 50,000개 이하의 탄소 원자, 더욱 바람직하게는 10,000개 이하의 탄소 원자를 갖는다. 바람직하게 중합성 올레핀에서 하나 이상의 탄소-탄소 이중 결합이 존재하고, 더욱 바람직하게 중합성 올레핀이 탄소-탄소 이중 결합-함유 단량체가 존재한다. 따라서, 중합성 올레핀은, 연속 용액 중합 반응 동안 동일 반응계에서 형성된 비닐-말단화된 중합체성 잔유물(remnant)인 장쇄 거대분자 알파-올레핀 단위를 포함한다. 상기 제 3 실시양태의 몇몇 양태에서, 상기 장쇄 거대분자 알파-올레핀 단위는, 에틸렌 및 다른 단쇄 올레핀 단량체와 함께 용이하게 중합되어, 장쇄 분지를 갖는 폴리올레핀을 제공한다.
몇몇 실시양태에서, 상기 제 3 실시양태의 방법은, 동일한 반응기 내에서, 또는, 바람직하게는 연속적으로 또는 평행하게 연결된, 개별적인 반응기 내에서, 하나 이상의 상기 제 2 실시양태의 촉매 및 하나 이상의 추가적인 균질 또는 비균질 중합 촉매(이들은 상기 제 2 실시양태의 촉매와 동일하거나 상이한 촉매 또는 예컨대 전술된 바와 같은 선행 기술의 올레핀 중합 촉매일 수 있음)를 사용하여, 목적하는 특성을 갖는 중합체 블렌드를 제공한다. 이러한 방법의 일반적인 기술은 국제 특허 출원 공개 제 WO 94/00500 호에 개시되어 있다.
몇몇 실시양태에서, 상기 제 3 실시양태의 중합 방법은, 회분식 또는 연속식 중합 공정으로 수행된다. 연속식 공정이 바람직하며, 연속식 공정에서는, 예를 들어 상기 제 2 실시양태의 촉매, 에틸렌, 에틸렌 이외의 다른 공단량체 올레핀, 및 임의적으로 용매, 희석제, 분산제 또는 이들의 조합물이 본질적으로 연속적으로 반응 대역에 공급되고, 생성 폴리올레핀 생성물은 본질적으로 연속적으로 이로부터 제거된다.
바람직하게, 상기 폴리올레핀 생성물은, 용액 공정, 가장 바람직하게는 연속 용액 공정으로 제조된다. 본 발명의 범주를 어떠한 방식으로도 제한하고자 하지 않으면서, 이러한 본질적으로 연속적인 중합 공정을 수행하기 위한 예시적인 방법은 다음과 같다. 교반-탱크 반응기 내에서, 중합될 단량체 올레핀을 용매 및 임의적인 쇄 전달제(예컨대, 수소의 스트림)와 함께 연속적으로 반응기로 도입한다. 상기 반응기는, 임의의 용매 또는 추가적인 희석제 및 용해된 중합체와 함께 실질적으로 단량체로 이루어진 액체 상을 함유한다. 다른 실시양태에서는, 소량의 "H"-분지-유도 다이엔, 예컨대 노보나다이엔, 1,7-옥타다이엔 또는 1,9-데카다이엔이 또한 첨가된다. 화학식 I의 금속-리간드 착체 및 활성화 조촉매는 상기 반응기에 액상으로 연속적으로 도입된다. 몇몇 실시양태에서, 반응기 온도 및 압력은, 예를 들어 용매/단량체 비를 조절하거나, 첨가 속도를 조절하거나, 반응기 액상을 냉각 또는 가열하거나(예컨대, 코일, 자켓 또는 이들 둘 다 사용), 이들을 조합하여 제어된다. 몇몇 실시양태에서, 중합 속도는, 상기 제 2 실시양태의 촉매의 첨가 속도를 조절함으로써 제어된다. 몇몇 실시양태에서, 이의 중합체 생성물의 에틸렌 함량은, 반응기 내의 에틸렌 대 공단량체 올레핀 비를 조절함으로써 달라지며, 상기 비는 바람직하게는, 상기 반응기로의 상기 단량체의 각각의 공급 속도를 조절함으로써 제어된다. 몇몇 실시양태에서, 중합체 생성물의 분자량은, 온도를 조절하거나, 단량체 농도를 조절하거나, 상기 언급된 쇄 전달제를 사용함으로써 제어된다. 몇몇 실시양태에서, 반응기 유출물은 촉매 실활제(catalyst kill agent), 예컨대 물과 접촉된다. 생성 폴리올레핀 생성물 용액은 임의적으로 가열되고, 폴리올레핀은 감압 하의 탈휘발화, 예컨대 휘발성 물질(예컨대, 기체 단량체, 잔류 용매 및 희석제)의 플래싱에 의해 회수된다. 몇몇 실시양태에서, 추가의 탈휘발화는 장비, 예컨대 탈휘발화 압출기 내에서 수행된다. 연속식 공정에서, 상기 반응기 내에서 상기 제 2 실시양태의 촉매 및 폴리올레핀 생성물의 평균 체류 시간은 바람직하게는 약 5 분 내지 약 8 시간, 더욱 바람직하게는 약 10 분 내지 약 6 시간이다.
몇몇 실시양태에서, 상기 제 2 실시양태의 촉매는, 높은 수준의 장쇄 분지를 갖는 에틸렌/알파-올레핀 공중합체 및 에틸렌 단독중합체의 제조에 사용된다. 연속식 중합 공정, 특히 연속식 용액 중합 공정에 상기 제 2 실시양태의 촉매를 사용하면, 반응기의 승온이 가능해지며, 이로써 비닐-말단화된 중합체 쇄의 형성이 더 잘 일어난다. 몇몇 실시양태에서, 비닐-말단화된 중합체 쇄는, 성장하는 중합체 내로 혼입되며, 이로써 장쇄 분지를 포함하는 중합체를 제공한다. 상기 제 2 실시양태의 촉매의 사용은 유리하게는, 고압에서 자유 라디칼-생성된 저밀도 폴리에틸렌과 유사한 가공성을 갖는 에틸렌/알파-올레핀 공중합체의 경제적인 제조를 가능하게 한다.
일반적으로, 상기 에틸렌/알파-올레핀 공중합체는 0.85 g/mL 내지 0.96 g/mL의 밀도를 갖는다. 몇몇 실시양태에서, 상기 중합에서 사용되는 에틸렌 단량체의 몰에 대한 알파-올레핀 공단량체의 몰의 공단량체-대-단량체 비는, 생성 에틸렌/알파-올레핀 공중합체의 밀도를 조절하기 위해 변한다. 0.91 g/mL 내지 0.93 g/mL의 바람직한 밀도 범위를 갖는 에틸렌/알파-올레핀 공중합체를 제조하는 경우, 바람직하게는 상기 공단량체-대-단량체 비는 0.2 미만, 더욱 바람직하게는 0.05 미만, 더더욱 바람직하게는 0.02 미만, 더더욱 바람직하게는 0.01 미만이다. 몇몇 실시양태에서, 수소 기체를 사용하면, 생성 에틸렌/알파-올레핀 공중합체의 분자량이 효과적으로 제어되는 것으로 밝혀졌다. 몇몇 실시양태에서, 단량체의 몰에 대한 수소 기체의 몰의 비는 약 0.5 미만, 바람직하게는 0.2 미만, 더욱 바람직하게는 0.05 미만, 더더욱 바람직하게는 0.02 미만, 더더욱 바람직하게는 0.01 미만이다.
바람직하게, 중합성 올레핀은 각각 독립적으로 에틸렌; 탄소수 약 3 내지 약 20의 선형 또는 분지형 알파-올레핀, 예컨대 프로필렌, 아이소부틸렌, 1-부텐, 1-펜텐, 1-헥센, 3-메틸-1-펜텐, 4-메틸-1-펜텐, 1-옥텐, 1-데센, 장쇄 거대분자 알파-올레핀, 및 이들의 혼합물; 비환형 다이엔, 예컨대 1,4-부타다이엔, 1,4-헥사다이엔, 및 1,7-옥타다이엔; 환형 올레핀, 예컨대 사이클로부텐, 사이클로펜텐, 노보넨, 및 5- 및 6-위치에서 (C1-C20)하이드로카빌 기로 치환된 노보넨 유도체; 탄소수 약 4 내지 약 40의 환형 다이엔 탄화수소, 예컨대 사이클로헥사다이엔, 에틸리덴-노보넨, 및 노보나다이엔; 탄소수 8 내지 20의 방향족 고리-치환된 올레핀(예컨대, 스타이렌, (C1-C4)알킬-치환된 스타이렌, 및 4-페닐부텐); 비닐 단량체, 예컨대 4-비닐사이클로헥센, 다이비닐벤젠; 및 이들과, 에틸렌, 아크릴로나이트릴, 말레산 에스터, 비닐 아세테이트, 아크릴레이트 에스터, 메타크릴레이트 에스터 또는 비닐 트라이알킬 실란의 혼합물; 및 이들의 혼합물, 예컨대 에틸렌과 스타이렌의 혼합물, 에틸렌, 프로필렌 및 스타이렌의 혼합물; 에틸렌, 스타이렌 또는 프로필렌, 및 1,4-헥사다이엔 또는 비-공액된 다이엔, 특히 에틸리덴-노보넨의 혼합물이다.
바람직한 실시양태에서, 화학식 I의 금속-리간드 착체 및 상기 제 2 실시양태의 촉매(본 발명의 고체-지지된 촉매 포함)는 각각, 전술된 바와 같은 바람직한 조작 온도에서 가열시 열-유도된 알킬 기 이동이 감소되거나 없음을 나타낸다.
상기 제 2 실시양태의 촉매는, 당분야에 공지된 임의의 관련 공정을 변경함으로써 제조될 수 있으며, 특정 공정이 본 발명의 방법에 중요하지는 않다. 바람직하게, 상기 제 2 실시양태의 촉매는 상기 제 4 실시양태의 방법에 의해 제조된다. 더욱 바람직하게는, 상기 제 4 실시양태의 방법은, 상기 제 2 실시양태의 촉매를 제조하기에 충분한 조건 하에, 화학식 I의 금속-리간드 착체를 활성화 조촉매 및 용매, 바람직하게는 비양성자성 용매와 접촉시키는 것을 포함한다. 바람직하게, 상기 제 2 실시양태의 촉매를 제조하기에 충분한 조건은, 상기 제 3 실시양태의 방법에 대해 전술된 것들을 포함한다. 바람직하게, 상기 제 2 실시양태의 촉매는 동일 반응계에서 제조된다. 더욱 바람직하게, 상기 제 2 실시양태의 촉매는 동일 반응계에서 제조되어, 상기 제 3 실시양태의 방법에 사용된다. 몇몇 실시양태에서, 상기 제 2 실시양태의 촉매는 하나 이상의 중합성 올레핀의 존재 하에 동일 반응계에서 제조되고, 이로써 상기 제 3 실시양태의 방법에서 상기 제 2 실시양태의 촉매는 즉시 하나 이상의 중합성 올레핀과 접촉된다.
몇몇 실시양태에서, 상기 제 2 실시양태의 본 발명의 촉매는, 하나 이상의 화학식 I의 금속-리간드 착체 및 하나 이상의 활성화 조촉매를 용매 또는 희석제에 첨가함으로써 균질 촉매로서 제조되며, 여기서 상기 제 3 실시양태의 중합 방법이 수행될 것이다.
다른 실시양태에서, 상기 제 2 실시양태의 촉매는, 무기 또는 유기 미립자화된 고체 지지체 상에 하나 이상의 화학식 I의 금속-리간드 착체 및 임의적으로 하나 이상의 활성화 조촉매를 흡착, 침착 또는 화학적 부착시켜, 본원에 기술된 바와 같은 본 발명의 미립자화된 고체-지지된 촉매를 제조함으로써 비균질 촉매로서 제조된 고체-지지된 촉매이다. 몇몇 실시양태에서, 상기 금속-리간드 착체는, 상기 활성화 조촉매를 상기 고체 지지체에 첨가하는 것과 순차적으로, 동시에 또는 그 전에 상기 고체 지지체에 첨가된다. 바람직한 실시양태에서, 본 발명의 비균질 촉매는, 무기 고체 지지체, 바람직하게는 트라이((C1-C4)알킬)알루미늄 화합물을 활성화 조촉매와 반응시킴으로써 제조된다. 바람직하게, 상기 활성화 조촉매는, 하이드록시아릴(트리스(펜타플루오로페닐))보레이트의 암모늄 염, 더욱 바람직하게는 (4-하이드록시-3,5-다이-3급-부틸페닐)트리스(펜타플루오로페닐)보레이트 또는 (4-하이드록시페닐)트리스(펜타플루오로페닐)보레이트 중 하나의 암모늄 염이다. 바람직하게, 상기 활성화 조촉매는, 공-침전, 흡수(imbibing), 분무 또는 유사한 기술에 의해 상기 고체 지지체 상에 침착되고, 이후 임의의 용매 또는 희석제는 바람직하게는 제거된다.
화학식 I의 금속-리간드 착체는, 당분야에 공지된 임의의 공정을 변경함으로써 제조될 수 있으며, 특정 공정이 본 발명에 중요하지는 않다. 상기 제 5 실시양태의 방법이 바람직하다. 제 5 실시양태의 공정의 몇몇 실시양태에서, 화학식 Z의 중간체 금속-리간드 착체는 제조 방법에서 이후에 나타날 이의 바람직한 임의의 실시양태 중 하나이다.
몇몇 실시양태에서, 제 5 실시양태의 공정은 추가로 화학식 Z의 중간체 금속-리간드 착체를 제조하는 단계를 포함한다. 화학식 Z의 중간체 금속-리간드 착체는 하기 기술된 바람직한 방법과 같은 다수의 임의의 방법 중 하나에 의해 제조될 수 있다.
상기 제 5 실시양태의 방법에서, 화학식 Z의 바람직한 중간체 금속-리간드 착체는 화학식 Z의 바람직한 중간체 금속-리간드 착체를 제조하기에 충분한 조건 하에, 용매 중의 예컨대 M1(벤질)4 또는 M1(벤질)Cl3[여기서, M1은 화학식 I에 대해 정의된 바와 같음]의 용액을, 용매(예컨대, 톨루엔) 중의, 하기 화학식 Y의 중간체 화합물의 1 몰 당량(예컨대, n = 1) 또는 2 몰 당량(예컨대, n = 2) 또는 이의 공액 염기의 염의 용액과 접촉시킴으로써 제조된다:
[화학식 Y]
상기 식에서, R1 내지 R5는 각각 독립적으로 화학식 I에 대해 정의된 바와 같다.
"화학식 Y의 화합물의 공액 염기의 염"이라는 표현은, 화학식 Y의 화합물의 1가 음이온[예컨대, 단일-탈양자화된(mono-deprotonated)] 유도체(즉, [(Y)-]) 및 총 1가 양이온으로 이루어진 전체적으로 중성인 이온성 분자를 의미한다. 총 1가 양이온의 예는 트리틸 양이온, 테트라((C1-C40)하이드로카빌)암모늄), 나트륨 양이온, 헤미 칼슘 염(예컨대, Ca+2[(Yn)-](대응 1가 음이온)) 중의 칼슘 2가 양이온; 및 헤미 마그네슘 염{Mg+2[(Yn)-](대응 1가 음이온)} 중의 마그네슘 2가 양이온이며, 이때 대응 1가 음이온은, 예를 들어 탄소 음이온, 할라이드, 바이카보네이트(HCO3 -1), 바이설페이트(HSO4 -1) 또는 이수소 포스페이트 (H2PO4 -1)이다. 화학식 Z의 바람직한 중간체 금속 리간드 착체를 제조하기에 충분한 조건은 바람직하게, 제 3 실시양태의 공정에 대해 상기되어 있다.
상기 제 5 실시양태의 또다른 실시양태에서, 화학식 Z의 바람직한 중간체 금속-리간드 착체는, 화학식 Y의 중간체 화합물을 금속 테트라할라이드(예컨대, TiCl4, ZrBr4 및 HfCl4)와 접촉시키고, 이어서 생성 혼합물을 용매 중에서, 예를 들어 (C1-C20)알킬, ((C1-C5)알킬)3Si(C1-C5)알킬, (C3-C10)사이클로알킬, (C3-C10)사이클로알킬-(C1-C3)알킬렌, (C6-C18)아릴 또는 (C6-C18)아릴-(C1-C3)알킬렌의 탄소 음이온과 접촉시켜 화학식 Z의 바람직한 중간체 금속-리간드 착체를 생성함으로써 제조된다. 상기 제 5 실시양태의 또다른 실시양태에서, 화학식 Z의 바람직한 중간체 금속-리간드 착체는, 화학식 Y의 중간체 화합물을 용매 중에서 탄소 음이온과 접촉시켜, 화학식 Y의 중간체 화합물의 공액 염기를 제조하고, 이어서 상기 공액 염기를 금속 테트라할라이드와 접촉시켜 화학식 Z의 바람직한 중간체 금속-리간드 착체를 생성함으로써 제조된다.
상기 제 5 실시양태의 방법의 또다른 대안적 실시양태에서, 상기 화학식 Z의 바람직한 중간체 금속-리간드 착체는, 먼저 화학식 Y의 중간체 화합물을 용매 중에서, 탄소 음이온-함유 염기, 예를 들어 (C1-C4)알킬리튬(예컨대, 1-부틸 리튬) 또는 (C1-C4)알킬 마그네슘 할라이드(예컨대, 메틸 마그네슘 브로마이드)와 접촉시켜 화학식 Y의 중간체 화합물의 공액 염기의 리튬 또는 마그네슘 할라이드 염을 각각 생성하고, 이어서 상기 공액 염기를 트라이알킬실일 할라이드(예컨대, 트라이메틸실일 클로라이드)와 접촉시켜, 화학식 Y의 중간체 화합물의 중간체 N-트라이알킬실일 유사체를 형성함으로써 제조된다. 이어서, 상기 화학식 Y의 중간체 화합물의 N-트라이알킬실일 유사체를 금속 테트라할라이드와 접촉시키고, 이어서 생성 혼합물을 용매 중에서, 예를 들어 (C1-C20)알킬, ((C1-C5)알킬)3Si(C1-C5)알킬, (C3-C10)사이클로알킬, (C3-C10)사이클로알킬-(C1-C3)알킬렌, (C6-C18)아릴 또는 (C6-C18)아릴-(C1-C3)알킬렌의 탄소 음이온과 접촉시켜 화학식 Z의 바람직한 중간체 금속-리간드 착체를 생성한다.
바람직하게, 상기 제 5 실시양태의 방법은 하나 이상의 비양성자성 용매를 사용한다. 더욱 바람직하게, 상기 방법은 하나 이상의 비양성자성 용매를 사용하며, 화학식 I의 금속-리간드 착체는 단리 단계를 통해 단리되고, 더욱 바람직하게는 단리 및 정제 단계를 통해 단리 및 정제되어, 전술된 바와 같은 이의 단리된 형태 또는 단리되고 정제된 형태를 각각 제공한다. 몇몇 실시양태에서, 상기 단리 및 정제 단계는 본질적으로 동시에 수행되며, 즉 본질적으로 단일 단계이다. 단리 단계의 예는, 상기 금속-리간드 착체로부터 용매 및 다른 휘발성 성분의 증발이다. 바람직하게, 상기 증발은, 진공 하에, 실질적으로 비활성 대기 하에 또는 이 두 조건 모두 하에 수행된다. 다른 실시양태에서, 상기 방법은 추가로, 용매로부터 금속-리간드 착체를 단리하고, 상기 단리된 금속-리간드 착체를 통상의 방법에 의해 정제하여, 70 중량% 이상의 순도로 정제된 금속-리간드 착체를 수득한다. 화학식 I의 금속-리간드 착체의 정제의 예는, 금속-리간드 착체를 함유하는 반응 혼합물로부터 용매 및 다른 휘발성 성분을 증발시키고(즉, 화학식 I의 금속-리간드 착체의 단리 및 정제가 동시에 수행됨), 단리된 화학식 I의 금속-리간드 착체를 마쇄하고, 반응 혼합물, 정제 용매 또는 이들의 조합물로부터 화학식 I의 금속-리간드 착체를 침전 또는 결정화시키는 것이다. 바람직하게, 화학식 I의 금속-리간드 착체의 마쇄는, 화학식 I의 금속-리간드 착체가 단지 부분적으로 가용성이거나 불용성인 용매를 사용하여 수행되며, 마쇄물(triturate)은 제거된다. 단리 및 정제를 포함하는 단일 단계의 예는, 반응 혼합물로부터 침전된 화학식 I의 금속-리간드 착체를 여과하고, 임의적으로, 침전된 화학식 I의 금속-리간드 착체의 생성 필터케이크를 용매로 세척하고, 상기 필터케이크를 건조하는 것이며, 이때 침전된 화학식 I의 금속-리간드 착체의 순도는 70 중량% 이상이다.
몇몇 실시양태에서, 화학식 I의 금속-리간드 착체는 동일 반응계에서 제조되어, 상기 제 4 실시양태의 방법에 사용된다. 더욱 바람직하게, 화학식 I의 금속-리간드 착체를 동일 반응계에서 제조하고, 이어서 화학식 I의 금속-리간드 착체를 하나 이상의 활성화 조촉매 및 하나 이상의 중합성 올레핀과 접촉시키며, 또한 상기 제 2 실시양태의 촉매를 상기 제 4 실시양태의 방법에 의해 동일 반응계에서 제조하고, 이어서 상기 제 2 실시양태의 촉매를 상기 제 3 실시양태의 방법에서 하나 이상의 중합성 올레핀과 접촉시켜 폴리올레핀을 제조한다.
화학식 I의 금속-리간드 착체를 제조하는 예시적인 절차를 도 1에 도시한 바와 같은 반응식 1에 도시한다. 도 1에서 반응식 1은, n이 0이고, X가 존재하지 않고, J가 J1 내지 J7 중 임의의 하나이고, M1, R1 내지 R5 및 L이 상기 화학식 I에 대해 정의된 바와 같은 화학식 I의 금속-리간드 착체의 제조를 예시한다. 반응식 1의 선택 A는, R2 및 R3이 화학식 R23의 전술한 2가 라디칼로 치환되지 않는 화학식 Y의 중간체 화합물을 위해 바람직하다. 선택 D는, R2 및 R3이 화학식 R23의 2가 라디칼로 치환된 Y의 중간체 화합물을 위해 바람직하다. 이러한 금속-리간드 착체는 화학식 I 내지 X로서 반응식 1에 도시되어 있고, 이때 반응식 1에서 m은 화학식 I에 대해 정의된 바와 같고, 화학식 I 내지 X의 금속-리간드 착체가 총체적으로 중성인 것으로 선택된다. 반응식 1에서 절차는 화학식 I의 금속-리간드 착체를 제조하기 위해 필요시 변경될 수 있고, 이때 X는 존재(즉, n은 1, 2 또는 3)하거나, 이때 하나의 X 및 J는 X를 화학식 I 내지 X의 화합물과 접촉시킴으로써 또는 화학식 J-H의 화합물을 전술한 화학식 XJ-JX-H로 각각 치환시킴으로써 함께 XJ-JX를 형성한다.
도 1, 반응식 1의 선택 A에서, 화학식 Y의 중간체 화합물(전술됨)은, 비-친핵성 염기를 사용하여 탈보호되어 엔아마이드(도시되지 않음)를 제공하며, 이는 이어서 금속 할라이드, 예컨대 M(Cl)m+1[여기서, m은 화학식 Y에 대해 상기 정의된 바와 같음]과 반응하고, 이어서 생성 금속-리간드 착체는 유기금속 화합물, 예컨대 유기리튬(L-Li) 또는 그리냐르 시약(L-MgBr){또는 유기나트륨(L-Na) 또는 유기칼륨(L-K)}[여기서, L은 상기 화학식 I에 대해 정의된 바와 같음]과 반응하여, 화학식 (Z-X)의 중간체 금속-리간드 착체를 제공한다. 다르게는, 선택 B에서, 화학식 Y의 중간체 화합물은 유기금속 화합물 M1(L)m+1과 반응하여, 화학식 (Z-X)의 중간체 금속-리간드 착체를 제공한다. 또다른 대안으로서, 선택 C에서, 화학식 Y의 중간체 화합물은 금속-아미도 화합물 M1(NRKRL)m+1과 반응하여, 중간체(도시되지 않음)를 생성하고, 이는 이어서 유기금속 화합물(예컨대, 유기리튬 또는 그리냐르 시약)과 반응하여, 화학식 (Z-X)의 중간체 금속-리간드 착체를 생성한다. 또다른 대안으로서, 선택 D에서, 화학식 Y의 중간체 화합물은 상기 금속 할라이드, 예컨대 M1(Cl)m+1과 반응하고, 이어서 생성 금속-리간드 착체는 4 몰 당량의 유기금속 화합물 L-Li 또는 L-MgBr, 예컨대 메틸 리튬 또는 메틸 마그네슘 브로마이드와 반응하여, 화학식 (Z-X)의 중간체 금속-리간드 착체를 생성하고, 이때 L은 (C1-C40)하이드로카빌이다. 이어서, 화학식 (Z-X)의 중간체 금속-리간드 착체는 화학식 (J-H)의 화합물과 반응하여 화학식 (I-X)의 중간체 금속-리간드 착체를 생성한다.
도 1, 반응식 1에서 기술된 반응은 바람직하게는, 실질적으로 비활성 기체 대기 하에서 무수 비양성자성 용매, 예컨대 톨루엔, 자일렌, 테트라하이드로퓨란, 다이에틸렌 글라이콜 다이메틸 에터 또는 이들의 조합물 중에서, 약 -78 ℃ 내지 약 200 ℃ 범위의 온도에서 수행된다. 바람직하게, 상기 반응은 대기압에서 수행된다.
본 발명의 또다른 양태는, 상기 제 3 실시양태의 방법에 따라 제조된 폴리올레핀이다. 몇몇 실시양태에서, 본 발명의 방법에 유용한 중합성 올레핀은, 탄소 및 수소 원자로 이루어지고, 1개 이상, 바람직하게는 3개 이하, 더욱 바람직하게는 2개 이하의 탄소-탄소 이중 결합을 함유하는 (C2-C40)탄화수소이다. 몇몇 실시양태에서, 상기 (C2-C40)탄화수소의 1 내지 4개의 수소 원자가 각각, 할로겐 원자, 바람직하게는 플루오로 또는 클로로로 대체되어, 할로겐 원자-치환된 (C2-C40)탄화수소를 생성한다. 상기 (C2-C40)탄화수소(할로겐 원자-치환되지 않은 것)가 바람직하다. 폴리올레핀을 제조하기에 유용한 바람직한 중합성 올레핀(즉, 올레핀 단량체)은 에틸렌 및 중합성 (C3-C40)올레핀이다. 상기 (C3-C40)올레핀은 알파-올레핀, 환형 올레핀, 스타이렌, 및 환형 또는 비환형 다이엔을 포함한다. 바람직하게, 상기 알파-올레핀은 (C3-C40)알파-올레핀, 더욱 바람직하게는 분지쇄 (C3-C40)알파-올레핀, 더더욱 바람직하게는 직쇄 (C3-C40)알파-올레핀, 더더욱 바람직하게는 CH2=CH2-(CH2)ZCH3(화학식 A)(이때 z는 정수 0 내지 40이다)의 직쇄 (C3-C40)알파-올레핀이고, 더더욱 바람직하게는 직쇄 (C3-C40)알파-올레핀, 즉 1-프로펜, 1-부텐, 1-펜텐, 1-헥센, 1-헵텐, 1-옥텐, 1-노넨, 1-데센, 1-운데센, 1-도데센, 1-트라이데센, 1-테트라데센, 1-펜타데센, 1-헥사데센, 1-헵타데센, 1-옥타데센 또는 직쇄 (C20-C24)알파-올레핀을 포함한다. 바람직하게, 상기 환형 올레핀은 (C3-C40)환형 올레핀이다. 바람직하게, 상기 환형 또는 비환형 다이엔은 (C4-C40)다이엔, 바람직하게는 비환형 다이엔, 더욱 바람직하게는 비환형 공액 (C4-C40)다이엔, 더욱 바람직하게는 비환형 1,3-공액 (C4-C40)다이엔, 더더욱 바람직하게는 1,3-부타다이엔이다.
본 발명의 방법에 의해 제조될 수 있는 폴리올레핀은, 예를 들어 에틸렌 및 하나 이상의 중합성 (C3-C40)올레핀의 잔기를 포함하는 폴리에틸렌 및 상호중합체를 포함한다. 바람직한 단독중합체는 폴리에틸렌, 폴리프로필렌, 및 폴리부틸렌이다. 바람직한 상호중합체는, 2종 이상의 중합성 올레핀의 혼합물, 예컨대 에틸렌/프로필렌, 에틸렌/1-부텐, 에틸렌/1-펜텐, 에틸렌/1-헥센, 에틸렌/4-메틸-1-펜텐, 에틸렌/1-옥텐, 에틸렌/스타이렌, 에틸렌/프로필렌/부타다이엔 및 다른 EPDM 삼원공중합체이다. 바람직하게, 상기 폴리올레핀은 에틸렌 단독중합체, 에틸렌/알파-올레핀 상호중합체(예컨대, 공중합체) 또는 에틸렌/알파-올레핀/다이엔 상호중합체(예컨대, 삼원공중합체)이다.
바람직하게, 상기 폴리올레핀은, 상기 제 3 실시양태의 전술된 바람직한 방법에 따라 제조된 폴리(에틸렌 알파-올레핀) 블록 공중합체를 포함한다. 상기 폴리(에틸렌 알파-올레핀) 블록 공중합체는, 상기 알파-올레핀 및 에틸렌으로부터의 잔기를 포함하는 연질 분절 및 에틸렌-유도된 경질 분절(즉, 폴리에틸렌 경질 분절)을 포함한다. 상기 알파-올레핀 및 에틸렌의 잔기는 전형적으로, 상기 연질 분절 내에 대략적으로 랜덤하게 분포되어 있다.
바람직하게, 상기 폴리에틸렌 경질 분절은, 후술되는 핵자기 공명에 의해 결정시, 내부에 공유결합되어 혼입된 상기 알파-올레핀 잔기를 5 몰% 미만으로 갖는 것을 특징으로 한다.
바람직하게, 상기 폴리(에틸렌 알파-올레핀) 블록 공중합체는, 후술되는 절차를 사용하여 시차 주사 열량계로 결정시, 100 ℃ 초과, 더욱 바람직하게는 120 ℃ 초과의 융점을 갖는 것을 특징으로 한다.
상기 폴리(에틸렌 알파-올레핀) 블록 공중합체는 에틸렌 잔기 및 하나 이상의 공중합성 알파-올레핀 공단량체 잔기(즉, 에틸렌 및 중합된 형태의 하나 이상의 공중합성 알파-올레핀 공단량체)를 포함한다. 상기 폴리(에틸렌 알파-올레핀) 블록 공중합체는, 상이한 화학적 또는 물리적 특성을 갖는 2종 이상의 중합된 단량체 단위의 다중 블록 또는 분절을 특징으로 한다. 즉, 상기 에틸렌/알파-올레핀 상호중합체는 블록 상호중합체, 바람직하게는 다중-블록 상호중합체 또는 공중합체이다.
"상호중합체" 및 공중합체"라는 용어는, 본원에서 상호교환적으로 사용된다. 몇몇 실시양태에서, 상기 다중-블록 공중합체는 하기 구조식으로 제시될 수 있다:
(AB)n
상기 식에서,
n은 1 이상, 바람직하게는 1 초과의 정수, 예컨대 2, 3, 4, 5, 10, 15, 20, 30, 40, 50, 60, 70, 80, 90, 100 또는 그 이상이고,
"A"는 경질 블록 또는 분절을 나타내고,
"B"는 연질 블록 또는 분절을 나타낸다.
바람직하게, A 및 B는, 분지형 또는 스타(star) 방식이 아니라 선형 방식으로 연결된다.
"경질" 분절은, 95 중량% 초과, 바람직하게는 98 중량% 초과의 양으로 상기 폴리(에틸렌 알파-올레핀) 블록 공중합체에 존재하는 에틸렌 잔기의 중합된 단위의 블록을 지칭한다. 달리 말하면, 상기 경질 분절 중의 상기 공단량체(즉, 알파-올레핀) 잔기 함량은 5 중량% 미만, 바람직하게는 2 중량% 미만이다. 몇몇 실시양태에서, 상기 경질 분절은 모든 또는 실질적으로 모든 에틸렌 잔기를 포함한다. "폴리에틸렌 경질 분절" 및 "에틸렌-유도된 경질 분절"이라는 표현은, 폴리(에틸렌 알파-올레핀) 블록 공중합체의 경질 분절 부분을 의미하며, 이와 동의어이다.
"연질" 분절은, 상기 폴리(에틸렌 알파-올레핀) 블록 공중합체에서 상기 공단량체(즉, 알파-올레핀) 잔기 함량이 5 중량% 초과, 바람직하게는 8 중량% 초과, 10 중량% 초과 또는 15 중량% 초과인 중합된 단위의 블록을 지칭한다. 몇몇 실시양태에서, 상기 연질 분절 중의 상기 공단량체 잔기 함량은 20 중량% 초과, 25 중량% 초과, 30 중량% 초과, 35 중량% 초과, 40 중량% 초과, 45 중량% 초과, 50 중량% 초과 또는 60 중량% 초과일 수 있다.
몇몇 실시양태에서, A 블록 및 B 블록은 상기 폴리(에틸렌 알파-올레핀) 블록 공중합체의 중합체 쇄(주쇄)를 따라 랜덤하게 분포된다. 달리 말하면, 상기 폴리(에틸렌 알파-올레핀) 블록 공중합체는 일반적으로 하기 구조를 갖지 않는다:
AAA-AA-BBB-BB
다른 실시양태에서, 상기 폴리(에틸렌 알파-올레핀) 블록 공중합체는 일반적으로, 제 3의 유형의 블록을 갖지 않으며, 즉, A 블록 및 B 블록이 아닌 "C" 블록은 갖지 않는다. 또다른 실시양태에서, 상기 폴리(에틸렌 알파-올레핀) 블록 공중합체의 A 블록 및 B 블록은 각각, 상기 블록 내에 랜덤하게 분포된 단량체 또는 공단량체를 갖는다. 달리 말하면, A 블록 또는 B 블록은, 별개의 조성의 2개 이상의 분절(또는 하위-블록), 예컨대 상기 블록의 나머지와 다른 조성을 갖는 팁(tip) 분절을 갖지 않는다.
몇몇 실시양태에서, 폴리올레핀은 에틸렌/알파-올레핀 상호중합체, 예컨대 미국 특허 가출원 제 61/024,674 호 및 패밀리 일원인 PCT 국제 특허 출원 제PCT/US2009/032699 호에 기술된 것들(상기 출원들을 본원에 참고로 인용함), 바람직하게는 경질 분절 및 연질 분절을 포함하는 블록 공중합체를 포함하며, 약 1.4 내지 약 2.8 범위의 Mw/Mn를 특징으로 하고:
(a) 하나 이상의 Tm(℃), 및 밀도(d)(g/cm3)를 갖되, 상기 Tm 및 d의 수치 값은 하기 관계식에 대응하거나:
Tm > -6553.3 + 13735(d) - 7051.7(d)2
(b) 융해열(ΔH(J/g)), 및 DSC 최대 피크와 결정 분석 분별(CRYSTAF) 최대 피크 사이의 온도 차이로서 정의되는 Δ온도 양(ΔT(℃))을 특징으로 하고, 상기 ΔT 및 ΔH는, ΔH가 0 초과 130 J/g 이하인 경우, ΔT > -0.1299(ΔH) + 62.81이고, ΔH가 130 J/g 초과인 경우, ΔT ≥ 48 ℃인 관계식을 갖되, 상기 CRYSTAF 피크는, 5% 이상의 누적(cumulative) 중합체를 사용하여 결정되며, 상기 중합체의 5% 미만이, 확인가능한 CRYSTAF 피크를 갖는 경우, 상기 CRYSTAF 온도는 30 ℃이거나;
(c) 상기 에틸렌/알파-올레핀 상호중합체의 압축-성형된 필름으로 측정시, 1회 사이클 및 300% 변형에서의 탄성 회복율(elastic recovery; Re)(%)을 특징으로 하고, 밀도(d)(g/cm3)를 갖되, 에틸렌/알파-올레핀 상호중합체가 실질적으로 가교-결합된 상이 없는 경우 Re 및 d의 수치값이 하기 관계식을 만족시키거나:
Re > 1481 - 1629(d);
(d) TREF를 이용하여 분별 시 40 ℃ 내지 130 ℃에서 용출되는 분자 분획을 갖되, 상기 분획은 동일한 온도 사이에서 용출되는 비교용 랜덤 에틸렌 상호중합체 분획의 것보다 5% 이상 더 높은 공단량체 몰 함량을 갖는 것을 특징으로 하며, 상기 비교용 랜덤 에틸렌 상호중합체는 동일한 공단량체(들)를 가지며, 상기 에틸렌/알파-올레핀 상호중합체의 것의 10% 이내의 용융 지수, 밀도 및 공단량체 몰 함량 (전체 중합체 기준)을 갖거나;
(e) 25 ℃에서의 저장 모듈러스 G'(25 ℃), 및 100 ℃에서의 저장 모듈러스 G'(100 ℃)를 갖되, G'(25 ℃) 대 G'(100 ℃)의 비는 약 1:1 내지 약 9:1의 범위이거나;
(f) O 초과 내지 약 1.0 이하의 평균 블록 지수를 특징으로 하거나;
(g) TREF를 사용하여 분별시 40 ℃ 내지 130 ℃에서 용출하는 분자 분획을 갖고, 상기 분획이, (-0.2013)T + 20.07 양 이상, 더욱 바람직하게는 (-0.2013)T + 21.07 양 이상의 공단량체 몰 함량을 갖는 것을 특징으로 하되, 이때 T(℃로 측정됨)는 상기 TREF 분획의 용출 피크 온도의 수치값이고; 상기 에틸렌/알파-올레핀 블록 상호중합체는 메조상 분리된다.
몇몇 실시양태에서, 폴리올레핀은 에틸렌/알파-올레핀 상호중합체, 예컨대 미국 특허 제 7,355,089 호 및 미국 특허 출원 공개 제 2006-0199930 호에 개시된 것들이며, 이때 상호중합체는 바람직하게는 블록 공중합체이고, 경질 분절 및 연질 분절, 및 상기 에틸렌/알파-올레핀 상호중합체를 포함하고:
(a) 약 1.7 내지 약 3.5의 Mw/Mn, 하나 이상의 Tm(℃), 및 밀도(d)(g/cm3)를 갖되, 상기 Tm 및 d의 수치값은 하기 관계식에 대응하거나:
Tm > -2002.9 + 4538.5(d) - 2422.2(d)2;
(b) 약 1.7 내지 약 3.5의 Mw/Mn을 갖고, 융해열(ΔH)(J/g), 및 DSC 최대 피크와 CRYSTAF 최대 피크 사이의 온도 차이로 정의되는 델타 양, ΔT(℃)을 특징으로 하되, 상기 ΔT 및 ΔH의 수치값은, ΔH가 0 초과 내지 130 J/g 이하인 경우, ΔT > -0.1299(LiH) + 62.81이고, ΔH가 130 J/g 초과인 경우, ΔT ≥ 48 ℃인 관계식을 갖고, 상기 CRYSTAF 피크는, 5% 이상의 누적 중합체를 사용하여 결정되며, 상기 중합체의 5% 미만이, 확인가능한 CRYSTAF 피크를 갖는 경우, 상기 CRYSTAF 온도는 30 ℃이거나;
(c) 상기 에틸렌/알파-올레핀 상호중합체의 압축-성형된 필름으로 측정시, 1회 사이클 및 300% 변형에서의 Re를 특징으로 하고, 밀도(d)(g/cm3)를 갖되, 에틸렌/알파-올레핀 상호중합체가 실질적으로 가교-결합된 상이 없는 경우 Re 및 d의 수치값이 하기 관계식을 만족시키거나:
Re > 1481 - 1629(d);
(d) TREF를 이용하여 분별 시 40 ℃ 내지 130 ℃에서 용출되는 분자 분획을 갖되, 상기 분획은 동일한 온도 사이에서 용출되는 비교용 랜덤 에틸렌 상호중합체 분획의 것보다 5% 이상 더 높은 공단량체 몰 함량을 갖는 것을 특징으로 하며, 상기 비교용 랜덤 에틸렌 상호중합체는 동일한 공단량체(들)를 가지며 상기 에틸렌/알파-올레핀 상호중합체의 것의 10% 이내의 용융 지수, 밀도 및 공단량체 몰 함량 (전체 중합체 기준)을 갖거나;
(e) 25 ℃에서의 저장 모듈러스 G'(25 ℃), 및 100 ℃에서의 저장 모듈러스 G'(100 ℃)를 갖되, G'(25 ℃) 대 G'(100 ℃)의 비는 약 1:1 내지 약 9:1의 범위이거나;
(f) TREF를 사용하여 분별시 40 ℃ 내지 130 ℃ 사이에서 용출하는 분자 분획을 갖고, 상기 분획이 0.5 이상 내지 약 1 이하의 블록 지수 및 약 1.3 초과의 Mw/Mn를 갖거나;
(g) O 초과 내지 약 1.0 이하의 평균 블록 지수 및 약 1.3 초과의 Mw/Mn을 갖거나;
(h) TREF를 이용하여 분별 시 40 ℃ 내지 130 ℃에서 용출되는 분자 분획을 갖되, 상기 분획은, (-0.2013)T + 20.07 이상의 양, 더욱 바람직하게는 (-0.2013)T + 21.07 이상의 공단량체 몰 함량을 갖는 것을 특징으로 하되, 상기 T(℃로 측정됨)는 상기 TREF 분획의 피크 용출 온도의 수치 값이다.
다른 실시양태는 중합체 및 방법, 예컨대 국제 특허 출원 공개 제 WO 2005/090425 호, 국제 특허 출원 공개 제 WO 2005/090426 호, 및 국제 특허 출원 공개 제 WO 2005/090427 호에 기술된 것들을 포함한다.
폴리올레핀의 단량체 및 임의의 공단량체 함량은, 임의의 적합한 기술, 예컨대 적외선(IR) 분광법 및 핵자기 공명(NMR) 분광법을 이용하여 측정할 수 있으며, NMR 분광법에 기초한 기술이 바람직하며, 13C NMR이 더욱 바람직하다. 13C NMR 분광법을 사용하기 위해서는, 10 mm NMR 튜브 내에서, 약 3 g의 테트라클로로에탄-d2/오르쏘다이클로로벤젠(50/50 혼합물)을 0.4 g의 상기 중합체 샘플에 가함으로써, 중합체 샘플로부터의 분석 샘플을 제조한다. 상기 튜브 및 이의 내용물을 150 ℃로 가열함으로써, 상기 중합체 샘플을 용해시키고 균질화시킨다. 제올 이클립스(JEOL Eclipse, 상표명) 400MHz 분광기 또는 버라이언 유니티 플러스(Varian Unity Plus, 상표명) 400MHz 분광기를 사용하여 13C NMR 분광법 데이터를 모았으며, 이는 100.5 MHz의 13C 공명 주파수에 해당한다. 6초 펄스 반복 지연을 이용하고 데이터 파일 당 4000 트랜지언트(transients)를 사용하여 13C 데이터를 수득하였다. 정량적 분석을 위한 최소 신호-대-노이즈를 수득하기 위해, 다중 데이터 파일을 함께 더했다. 스펙트럼의 폭은, 32,000 데이터 포인트의 최소 파일 크기를 갖는 25,000 Hz였다. 상기 분석 샘플을 130 ℃에서 10 mm의 넓은 밴드 프로브 내에서 분석하였다. 란달(Randall)의 트라이아드(triad) 방법을 사용하여, 13C 데이터로 공단량체 혼입을 결정하였다(문헌[Randall, J.C.; JMS-Rev. Macromol. Chem. Phys., C29, 201-317 (1989)]참고; 상기 문헌 전체를 본원에 참고로 인용함).
몇몇 실시양태에서, 상기 폴리(올레핀 단량체-올레핀 공단량체) 블록 공중합체 또는 이의 분절에 혼입된 올레핀 공단량체의 양은, 공단량체 혼입 지수를 특징으로 한다. 본원에서 "공단량체 혼입 지수"라는 용어는, 대표적인 올레핀 중합 조건 하에 제조된, 올레핀 단량체/공단량체 공중합체 또는 이의 분절에 혼입된 올레핀 공단량체의 잔기의 몰%를 지칭한다. 바람직하게, 상기 올레핀 단량체는 에틸렌 또는 프로필렌이고, 상기 공단량체는 각각, (C3-C40)알파-올레핀 또는 (C4-C40)알파-올레핀이다. 상기 올레핀 중합 조건은 이상적으로, 정상 상태(steady-state)의, 100 ℃ 및 4.5 MPa 에틸렌(또는 프로필렌) 압력(반응기 압력)에서, 탄화수소 희석제 중에서, 92% 초과(더욱 바람직하게는 95% 초과)의 올레핀 단량체 전환율, 및 0.01% 초과의 올레핀 공단량체 전환율의 연속 용액 중합 조건이다. 올레핀 공단량체 혼입 지수가 많이 다른 촉매 조성물(본 발명의 촉매 포함)의 선택은, 블록 또는 분절 특성, 예컨대 밀도가 많이 다른 2종 이상의 올레핀 단량체로부터의 폴리(올레핀 단량체-올레핀 공단량체) 블록 공중합체를 제공한다.
특정 경우, 상기 공단량체 혼입 지수는, 예를 들어 전술된 바와 같은 NMR 분광 기술 또는 IR 분광법에 의해 직접 결정될 수 있다. NMR 또는 IR 분광 기술을 사용할 수 없는 경우, 공단량체 혼입에서의 임의의 차이가 간접적으로 결정된다. 다중 단량체로부터 형성된 중합체의 경우, 단량체 반응성에 기초한 다양한 기술에 의해 이러한 간접적 결정을 수행할 수 있다.
제시된 촉매에 의해 제조된 공중합체의 경우, 상기 공중합체 및 이에 따른 상기 공중합체 조성물 중의 공단량체 및 단량체의 상대적인 양은, 공단량체 및 단량체의 상대적인 반응 속도에 의해 결정된다. 수학적으로, 단량체에 대한 공단량체의 몰 비는, 미국 특허 제 2007/0167578 A1 호의 단락 [0081] 내지 [0090]에 기술된 식으로 제시된다.
이 모델뿐만 아니라 상기 중합체 조성물은 단지, 온도 의존적 반응성 비 및 반응기 내의 공단량체 몰 분율의 함수이다. 이는 또한, 역(reverse) 공단량체 또는 단량체 삽입이 일어날 수 있거나 2종 이상의 단량체의 상호중합의 경우에 적용된다.
전술된 모델에 사용하기 위한 반응성 비는, 널리 공지된 이론적 기술을 사용하여 예측되거나 실제 중합 데이터로부터 실험적으로 유도될 수 있다. 적합한 이론적 기술은, 예를 들어 문헌[B. G. Kyle, Chemical and Process Thermodynamics, Third Edition, Prentice-Hall, 1999] 및 문헌[Redlich-Kwong-Soave (RKS) Equation of State, Chemical Engineering Science, 1972, pp 1197-1203]에 개시되어 있다. 실험적으로 유도된 데이터로부터 반응성을 유도하는 것을 보조하기 위해, 시판되는 소프트웨어 프로그램이 사용될 수 있다. 이러한 소프트웨어의 하나의 예는 미국 매사추세츠주 02141-2201 캠브리지 텐 캐널 파크 소재의 아스펜 테크놀로지 인코포레이티드(Aspen Technology, Inc.)로부터의 아스펜 플러스(Aspen Plus)이다.
때로는, 쇄 셔틀링을 포함하고 본 발명의 촉매를 사용하는 본 발명의 폴리올레핀 중합 방법의 실시양태에 사용될 수 있는 관련 올레핀 중합 촉매의 예를 참고로 인용하는 것이 편리하다. 편의성 및 일관성을 위해, 본 발명의 촉매 및 관련 올레핀 중합 촉매 중 하나는 종종 본원에서 포괄적인 용어, 예컨대 "제 1 올레핀 중합 촉매"로 지칭되고 다른 하나는 "제 2 올레핀 중합 촉매"로 지칭되거나, 그 반대도 가능하다. 즉, 몇몇 실시양태에서, 상기 제 1 올레핀 중합 촉매는, 본 발명의 촉매와 동일하고, 제 2 올레핀 중합 촉매는 상기 관련 올레핀 중합 촉매와 동일하거나, 다른 실시양태에서는 그 반대도 가능하다. 몇몇 실시양태에서, 상기 제 1 및 제 2 올레핀 중합 촉매는 각각 독립적으로 본 발명의 촉매이다. 본원에서 상기 제 1 올레핀 중합 촉매는, 높은 공단량체 혼입 지수를 갖는 것을 특징으로 하고, 상기 제 2 올레핀 중합 촉매는, 상기 높은 공단량체 혼입 지수의 95% 미만의 공단량체 혼입 지수를 갖는 것을 특징으로 한다. 바람직하게, 상기 제 2 올레핀 중합 촉매는, 상기 제 1 올레핀 중합 촉매의 상기 높은 공단량체 혼입 지수의 90% 미만, 더욱 바람직하게는 50% 미만, 더더욱 바람직하게는 25% 미만, 더더욱 바람직하게는 10% 미만의 공단량체 혼입 지수를 갖는 것을 특징으로 한다.
상기 제 3 실시양태의 바람직한 방법에 따라 폴리(에틸렌 알파-올레핀) 블록 공중합체를 제조할 경우, 상기 제 2 실시양태의 촉매는,
(A) 높은 공단량체 혼입 지수를 갖는 것을 특징으로 하는 제 1 올레핀 중합 촉매;
(B) 상기 제 1 올레핀 중합 촉매의 상기 공단량체 혼입 지수의 90% 미만의 공단량체 혼입 지수를 갖는 것을 특징으로 하는 제 2 올레핀 중합 촉매; 및
(C) 쇄 셔틀링제
의 혼합물 또는 반응 생성물을 포함하는 촉매 시스템의 일부로서 사용되며, 상기 제 2 실시양태의 촉매는 상기 제 1 또는 제 2 올레핀 중합 촉매를 포함한다.
본원에서 일반적으로 사용되는 "촉매"라는 용어는, 금속-리간드 착체의 비활성화된 형태(즉, 전구체)를 지칭하거나, 또는 바람직하게는, 이의 활성화된 형태(예컨대, 상기 비활성화된 형태를 활성화 조촉매와 접촉시킨 후 수득된, 촉매적으로 활성인 이의 혼합물 또는 생성물)를 지칭할 수 있다. 본 발명이 아닌 금속-리간드 착체를 포함하거나 이로부터 제조된 상기 관련 올레핀 중합 촉매의 경우, 본 발명이 아닌 금속-리간드 착체의 금속은 원소 주기율표의 3족 내지 15족, 바람직하게는 4족 중 임의의 족의 금속일 수 있다. 본 발명이 아닌 적합한 금속-리간드 착체의 유형의 예는 메탈로센, 반(half)-메탈로센, 구속된 기하구조(constrained geometry), 및 다가 피리딜아민-, 폴리에터- 또는 다른 폴리-킬레이트화 염기 착체이다. 본 발명이 아닌 이러한 금속-리간드 착체는 국제 특허 출원 공개 제 WO 2008/027283 호 및 대응 미국 특허 출원 제 12/377,034 호에 기술되어 있다. 본 발명이 아닌, 다른 적합한 금속-리간드 착체는, 미국 특허 제 5,064,802 호; 미국 특허 제 5,153,157 호; 미국 특허 제 5,296,433 호; 미국 특허 제 5,321,106 호; 미국 특허 제 5,350,723 호; 미국 특허 제 5,425,872 호; 미국 특허 제 5,470,993 호; 미국 특허 제 5,625,087 호; 미국 특허 제 5,721,185 호; 미국 특허 제 5,783,512 호; 미국 특허 제 5,866,704 호; 미국 특허 제 5,883,204 호; 미국 특허 제 5,919,983 호; 미국 특허 제 6,015,868 호; 미국 특허 제 6,034,022 호; 미국 특허 제 6,103,657 호; 미국 특허 제 6,150,297 호; 미국 특허 제 6,268,444 호; 미국 특허 제 6,320,005 호; 미국 특허 제 6,515,155 호; 미국 특허 제 6,555,634 호; 미국 특허 제 6,696,379 호; 미국 특허 제 7,163,907 호; 및 미국 특허 제 7,355,089 호뿐만 아니라, 국제 특허 출원 공개 제 WO 02/02577 호; 국제 특허 출원 공개 제 WO 02/92610 호; 국제 특허 출원 공개 제 WO 02/38628 호; 국제 특허 출원 공개 제 WO 03/40195 호; 국제 특허 출원 공개 제 WO 03/78480 호; 국제 특허 출원 공개 제 WO 03/78483 호; 국제 특허 출원 공개 제 WO 2009/012215 A2 호; 미국 특허 제 2003/0004286 호; 및 미국 특허 제 04/0220050 호; 미국 특허 제 2006/0199930 A1 호; 미국 특허 제 2007/0167578 A1 호; 및 미국 특허 제 2008/0311812 A1 호에 기술된 것들이다.
본원에서 상기 "제 1 올레핀 중합 촉매"는 "촉매 (A)"로서 상호교환적으로 지칭된다. 본원에서 상기 "제 2 올레핀 중합 촉매"는 "촉매 (B)"로서 상호교환적으로 지칭된다. 공단량체 혼입 지수가 많이 다른 금속 착체 또는 촉매 조성물의 선택은, 블록 또는 분절 특성, 예컨대 밀도가 많이 다른 2종 이상의 단량체로부터의 공중합체를 제공한다.
바람직하게, 상기 촉매 (B)의 공단량체 혼입 지수는 상기 촉매 (A)의 공단량체 혼입 지수의 50% 미만, 더욱 바람직하게는 5% 미만이다. 상기 촉매 (B)의 예는, 전술된 "관련 올레핀 촉매"이다.
몇몇 실시양태에서, 상기 제 2 실시양태의 촉매는 촉매 (A)는 포함하지만, 촉매 (B)는 포함하지 않는다. 이러한 실시양태에서, 바람직하게는 상기 촉매 시스템의 상기 촉매 (B)는, 미국 특허 제 2006/0199930 A1 호; 미국 특허 제 2007/0167578 A1 호; 미국 특허 제 2008/0311812 A1 호; 미국 특허 제 7,355,089 B2 호; 또는 국제 특허 출원 공개 제 WO 2009/012215 A2 호에 기술된 촉매 (B)이다.
몇몇 실시양태에서, 상기 제 2 실시양태의 촉매는 촉매 (B)는 포함하지만, 촉매 (A)는 포함하지 않는다. 이러한 실시양태에서, 바람직하게는 상기 촉매 시스템의 상기 촉매 (A)는, 미국 특허 제 2006/0199930 A1 호; 미국 특허 제 2007/0167578 A1 호; 미국 특허 제 2008/0311812 A1 호; 미국 특허 제 7,355,089 B2 호; 또는 국제 특허 출원 공개 제 WO 2009/012215 A2 호에 기술된 촉매 (A)이다.
미국 특허 제 2006/0199930 A1 호; 미국 특허 제 2007/0167578 A1 호; 미국 특허 제 2008/0311812 A1 호; 미국 특허 제 7,355,089 B2 호; 또는 국제 특허 출원 공개 제 WO 2009/012215 A2 호의 대표적인 촉매 (A) 및 (B)는, 하기 화학식 (A1) 내지 (A5), (B1), (B2), (C1) 내지 (C3) 및 (D1)의 촉매이다.
촉매 (A1)은, 국제 특허 출원 공개 제 WO 03/40195 호, 제 2003/US02/040l7 호, 2003년 5월 2일자로 출원된 미국 특허 출원 제 10/429,024 호, 및 국제 특허 출원 공개 제 WO 04/24740 호의 교시에 따라 제조된 [N-(2,6-다이(1-메틸에틸)페닐)아미도)(2-아이소프로필페닐)((α-나프탈렌-2-다이일(6-피리딘-2-다이일)메탄)]하프늄 다이메틸이며, 하기 구조를 갖는다:
촉매 (A2)는, 국제 특허 출원 공개 제 WO 03/40195 호, 제 2003/US02/040l7 호, 2003년 5월 2일자로 출원된 미국 특허 출원 제 10/429,024 호, 및 국제 특허 출원 공개 제 WO 04/24740 호의 교시에 따라 제조된 [N-(2,6-다이(1-메틸에틸)페닐)아미도)(2-메틸페닐)(1,2-페닐렌-(6-피리딘-2-다이일)메탄)]하프늄 다이메틸이며, 하기 구조를 갖는다:
촉매 (A3)은 비스[N,N'"-(2,4,6-트라이(메틸페닐)아미도)에틸렌다이아민]하프늄 다이벤질이며, 하기 구조를 갖는다:
촉매 (A4)는, 실질적으로 미국 특허 출원 공개 제 2004/0010103 호의 교시에 따라 제조된 비스((2-옥소일-3-(다이벤조-1H-피롤-1-일)-5-(메틸)페닐)-2-페녹시메틸)사이클로헥산-1,2-다이일 지르코늄(IV) 다이벤질이며, 하기 구조를 갖는다:
촉매 (A5)는, 실질적으로 국제 특허 출원 공개 제 WO 2003/051935 호의 교시에 따라 제조된 [η2-2,6-다이아이소프로필-N-(2-메틸-3-(옥틸이미노)부탄-2-일)벤젠아마이드]트라이메틸하프늄이며, 하기 구조를 갖는다:
촉매 (B1)은 1,2-비스-(3,5-다이-3급-부틸페닐렌)(1-(N-(1-메틸에틸)이미노)메틸)(2-옥소일) 지르코늄 다이벤질이며, 하기 구조를 갖는다:
촉매 (B2)는 1,2-비스-(3,5-다이-3급-부틸페닐렌)(1-(N-(2-메틸사이클로헥실)이미노)메틸)(2-옥소일) 지르코늄 다이벤질이며, 하기 구조를 갖는다:
촉매 (C1)은, 실질적으로 미국 특허 제 6,268,444 호의 교시에 따라 제조된 (3급-부틸아미도)다이메틸(3-N-피롤일-1,2,3,3a,7a-η-인덴-1-일)실란티타늄 다이메틸이며, 하기 구조를 갖는다:
촉매 (C2)는, 실질적으로 미국 특허 출원 공개 제 2003/004286 호의 교시에 따라 제조된 (3급-부틸아미도)다이(4-메틸페닐)(2-메틸-1,2,3,3a,7a-η-인덴-1-일)실란티타늄 다이메틸이며, 하기 구조를 갖는다:
촉매 (C3)은, 실질적으로 미국 특허 출원 공개 제 2003/004286 호의 교시에 따라 제조된 (3급-부틸아미도)다이(4-메틸페닐)(2-메틸-1,2,3,3a,8a-η-s-인다센-1-일)실란티타늄 다이메틸이며, 하기 구조를 갖는다:
촉매 (D1)은, 시그마-알드리치(Sigma-Aldrich)로부터 입수가능한 비스(다이메틸다이실록산)(인덴-1-일)지르코늄 다이클로라이드이며, 하기 구조를 갖는다:
전술된 바와 같이, 올레핀을 중합하기 위한 본 발명의 방법의 몇몇 실시양태는 추가로, 쇄 셔틀링제를 사용한다. "쇄 셔틀링제" 및 "CSA"라는 용어는, 본원에서 상호교환적으로 사용되며, 올레핀 중합 조건 하에, 2종의 올레핀 중합 촉매의 2개 이상의 활성 촉매 부위 사이에서 중합체성 쇄(즉, 중합체 쇄 또는 단편)의 교환을 유발할 수 있는 것을 특징으로 하는 화합물을 지칭하며, 상기 2종의 올레핀 중합 촉매는 본 발명의 촉매 및 상기 관련 올레핀 중합 촉매, 예컨대 또다른 본발명의 촉매 또는 본 발명이 아닌, 전술된 바와 같은 촉매 중 하나이다. 즉, 중합체 단편의 전달은 상기 올레핀 중합 촉매의 하나 이상의 활성 부위로, 및 상기 부위로부터 일어난다.
쇄 셔틀링제와 달리, "쇄 전달제"는, 중합체 쇄 성장의 종결을 유발하여, 촉매(예컨대, 본 발명의 촉매)로부터 상기 전달제로 중합체가 1회성으로 전달되게 한다. 몇몇 중합 방법의 실시양태에서, 예컨대 폴리올레핀 단독중합체 및 랜덤 폴리올레핀 공중합체를 제조하기에 유용한 방법에서, 상기 CSA는, 쇄 전달제로서 기능하는 것을 특징으로 한다. 즉, 상기 CSA는, 상기 중합 방법에서 형성된 폴리올레핀 단독중합체 또는 랜덤 폴리올레핀 공중합체 생성물이 상기 올레핀 중합 촉매(예컨대, 본 발명의 촉매)로부터 상기 CSA로 1회성으로 전달되게 하는 방식으로 작용하는 것을 특징으로 한다. 이러한 실시양태에서는, 상기 CSA가 가역적으로 쇄를 셔틀링하는 것이 필요하지 않으며, 이는, 전형적으로 단지 하나의 활성 촉매 부위를 갖거나 사용할 수 있는 단지 하나의 올레핀 중합 촉매를 사용하는 실시양태에서도 마찬가지다.
몇몇 실시양태에서, 상기 쇄 셔틀링제는, 쇄 셔틀링 활성 비 RA -B/RB -A를 갖는 것을 특징으로 한다. 일반적으로, 임의의 2종의 촉매 (A) 및 (B)의 경우, 상기 쇄 셔틀링 활성 비 RA -B/RB -A는, 상기 촉매 (A)의 활성 부위로부터 상기 촉매 (B)의 활성 부위로의 쇄 전달 속도(RA -B)를, 상기 촉매 (B)의 활성 부위로부터 상기 촉매 (A)의 활성 부위로의 쇄 전달 속도(RB -A)로 나눔으로써 계산된다. 바람직하게, 상기 촉매 (A)는 본 발명의 촉매이고, 상기 촉매 (B)는, 상기 전술된 관련 올레핀 중합 촉매이다. 상기 쇄 셔틀링제의 경우, 바람직하게는 상기 쇄 셔틀링 활성 비 RA -B/RB -A는 0.01 내지 100이다. 바람직하게, 상기 쇄 셔틀링제 및 상기 중합체의 쇄 사이에서 형성된 중간체는, 충분히 안정해서 쇄 종결이 비교적 드물다. (폴리올레핀-폴리라디칼)-함유 쇄 셔틀링제가 상기 중간체의 예다.
상이한 공단량체 혼입 속도(본원에 기술된 바와 같음) 및 상이한 반응성을 갖는 올레핀 중합 촉매들의 상이한 조합을 선택함으로써, 2종 이상의 CSA(바람직하게는, 3종 이하의 CSA)를 배합함으로써, 올레핀을 중합하기 위한 본 발명의 방법의 몇몇 실시양태에서, 상이한 폴리(올레핀 단량체-올레핀 공단량체) 다중-블록 공중합체 생성물을 제조할 수 있다. 이러한 상이한 생성물은, 상이한 밀도 또는 공단량체 농도의 분절, 상이한 블록 길이, 상기 분절 또는 블록의 상이한 수 또는 이들의 조합을 가질 수 있다. 예를 들어, 상기 쇄 셔틀링제의 쇄 셔틀링 활성이 하나 이상의 상기 올레핀 중합 촉매의 중합체 쇄 증폭 속도에 비해 낮은 경우, 더 긴 블록 길이의 다중-블록 공중합체 및 중합체 블렌드가 생성물로서 수득될 수 있다. 반대로, 쇄 셔틀링이 중합체 쇄 증폭에 비해 매우 빠른 경우에는, 더 많은 랜덤 쇄 구조 및 더 짧은 블록 길이를 갖는 공중합체 생성물이 수득된다. 일반적으로, 극도로 빠른 쇄 셔틀링제는, 실질적으로 랜덤 공중합체 특성을 갖는 다중-블록 공중합체를 생성할 수 있다. 촉매(들) 및 상기 CSA를 적절히 선택함으로써, 비교적 순수한 블록 공중합체, 비교적 큰 중합체 분절 또는 블록을 함유하는 공중합체, 및/또는 전술된 공중합체와 다양한 에틸렌 또는 프로필렌 단독중합체 및/또는 공중합체와의 블렌드를 생성물로서 수득할 수 있다.
상기 CSA를 사용하여 올레핀을 중합하기 위한 본 발명의 방법의 몇몇 실시양태에서, 본 발명에 사용하기 적합한 상기 쇄 셔틀링제는, 하나 이상의 (C1-C20)하이드로카빌 기를 함유하는 1족, 2족, 12족 또는 13족 금속 화합물 또는 착체, 바람직하게는 (C1-C12)하이드로카빌 치환된 알루미늄, 갈륨 또는 아연 화합물, 및 이들과 양성자 공급원과의 반응 생성물이다. 바람직한 (C1-C20)하이드로카빌 기는 알킬 기, 바람직하게는 선형 또는 분지형 (C1-C8)알킬 기이다. 본 발명에 사용하기에 가장 바람직한 셔틀링제는 트라이알킬 알루미늄 및 다이알킬 아연 화합물, 특히 트라이에틸알루미늄, 트라이(i-프로필) 알루미늄, 트라이(i-부틸)알루미늄, 트라이(n-헥실)알루미늄, 트라이(n-옥틸)알루미늄, 트라이에틸갈륨 또는 다이에틸아연이다. 추가의 적합한 셔틀링제는, 상기 전술된 유기금속 화합물, 바람직하게는 트라이((C1-C8)알킬) 알루미늄 또는 다이((C1-C8)알킬) 아연 화합물, 특히 트라이에틸알루미늄, 트라이(i-프로필) 알루미늄, 트라이(i-부틸)알루미늄, 트라이(n-헥실)알루미늄, 트라이(n-옥틸)알루미늄 또는 다이에틸아연과, (하이드로카빌 기의 수에 대해) 화학량론적 양 미만의 1급 또는 2급 아민, 1급 또는 2급 포스핀, 티올 또는 하이드록실 화합물, 특히 비스(트라이메틸실일)아민, 3급-부틸(다이메틸)실란올, 2-하이드록시메틸피리딘, 다이(n-펜틸)아민, 2,6-다이(3급-부틸)페놀, 에틸(1-나프틸)아민, 비스(2,3,6,7-다이벤조-1-아자사이클로헵탄아민), 다이페닐포스핀, 2,6-다이(3급-부틸)티오펜올 또는 2,6-다이페닐페놀을 배합함으로써 형성된 반응 생성물 또는 혼합물을 포함한다. 바람직하게는, 금속 원자 당 하나 이상의 하이드로카빌 기가 남도록, 충분한 아민, 포스핀, 티올 또는 하이드록실 시약이 사용된다. 셔틀링제로서 본 발명에 사용하기에 가장 바람직한 전술된 조합의 1차 반응 생성물은 n-옥틸알루미늄 다이(비스(트라이메틸실일)아마이드), i-프로필알루미늄 비스(다이메틸(3급-부틸)실록사이드), 및 n-옥틸알루미늄 다이(피리딘일-2-메톡사이드), i-부틸알루미늄 비스(다이메틸(3급-부틸)실록산), i-부틸알루미늄 다이(비스(트라이메틸실일)아마이드), n-옥틸알루미늄 다이(피리딘-2-메톡사이드), i-부틸알루미늄 비스(다이(n-펜틸)아마이드), n-옥틸알루미늄 비스(2,6-다이-3급-부틸페녹사이드), n-옥틸알루미늄 다이(에틸(1-나프틸)아마이드), 에틸알루미늄 비스(3급-부틸다이메틸실록사이드), 에틸알루미늄 다이(비스(트라이메틸실일)아마이드), 에틸알루미늄 비스(2,3,6,7-다이벤조-1-아자사이클로헵탄아마이드), n-옥틸알루미늄 비스(2,3,6,7-다이벤조-1-아자사이클로헵탄아마이드), n-옥틸알루미늄 비스(다이메틸(3급-부틸)실록사이드, 에틸아연 (2,6-다이페닐페녹사이드), 및 에틸아연 (3급-부톡사이드)이다. 본 발명이 아닌, 다른 적합한 쇄 셔틀링제는 국제 특허 출원 공개 제 WO 2005/073283 A1 호; 국제 특허 출원 공개 제 WO 2005/090425 A1 호; 국제 특허 출원 공개 제 WO 2005/090426 A1 호; 국제 특허 출원 공개 제 WO 2005/090427 A2 호; 국제 특허 출원 공개 제 WO 2006/101595 A1 호; 국제 특허 출원 공개 제 WO 2007/035485 A1 호; 국제 특허 출원 공개 제 WO 2007/035492 A1 호; 및 국제 특허 출원 공개 제 WO 2007/035493 A2 호에 기술되어 있다.
특히, 상기 제 3 실시양태의 방법에 의해 제조된 폴리올레핀이 합성 윤활제(합성 자동차 오일)로서 유용하며, 폼, 필름, 코팅, 섬유, 직물, 압출된 물품 및 성형 물품의 제조에 사용하기 위한 물질로서 유용하다.
화학식 Y의 중간체 화합물은 당분야에 공지된 임의의 공정을 변경함으로써 제조될 수 있으며, 특정 공정이 본 발명에 중요하지는 않다. 예를 들어, R2 및 R3이 화학식 R23의 전술된 2가 라디칼에 의해 치환되지 않는 화학식 Y의 중간체 화합물은 미국 특허 제 6,096,676 호 또는 미국 특허 제 6,919,413 B2 호의 방법을 변경함으로써 제조될 수 있다. 예를 들어, 미국 특허 제 6,096,676 호의 방법은 R2 및 R4는 각각 독립적으로 수소, (C1-C40)하이드로카빌 또는 (C1-C40)헤테로하이드로카빌이고; R3은 수소인 화학식 Y의 중간체 화합물을 제조하는데 특히 유용하다. 미국 특허 제 6,096,676 호의 상기 방법은 바람직하게 컬럼 3, 45 행 내지 64 행에 화학식을 가지는 미국 특허 제 6,096,676 호의 헤테로원자-함유 리간드의 제조 방법을 변경시킴을 포함하고, 이때 W는 컬럼 4, 59 행에서 2개의 탄소 연결 기이고, 미국 특허 제 6,096,676 호의 헤테로원자-함유 리간드는 컬럼 6, 1 행 내지 19 행 및 실시예 1, 3 및 6에 예시화되어 있다. 상기 R2 및 R3이 화학식 R23의 전술된 2가 라디칼에 의해 치환되는 화학식 Y의 잔여 중간체 화합물은 바람직하게는 미국 특허 제 6,919,413 B2 호의 방법을 변경함으로써 제조된다. 미국 특허 제 6,919,413 B2 호의 이러한 방법은 컬럼 9, 50 행에서 화학식을 가지는 미국 특허 제 6,919,413 B2 호의 헤테로원자-함유 리간드의 제조 방법을 변경함을 포함하고, 이때 T는 컬럼 4, 20 내지 40 행, 45 내지 47 행(가장 알맞은 기), 및 50 내지 60 행에서 예시화된 바와 같이 2개의 탄소 연결기이다. 미국 특허 제 6,919,413 B2 호의 특정 헤테로원자-함유 리간드의 제조 방법은 컬럼 23, 56 행 내지 컬럼 24, 22 행; 컬럼 25, 55 행 내지 컬럼 26, 67 행; 컬럼 35, 59 행 내지 컬럼 36, 54 행; 및 컬럼 37, 21 행 내지 컬럼 39, 6 행에 기재되어 있다.
R2 및 R3이 화학식 R23의 2가 라디칼로 치환된 화학식 Y의 중간체 화합물은 화학식 Y-A의 화합물이고 도 2에 도시된 반응식 2에서 예시된 공정 중 하나에 따라 제조된다. 도 2의 반응식 2에서는, 바람직하게는 탈수 조건 하에(예컨대, 탈수화제, 예컨대 무수 3Å 분자체 또는 무수 탄산 칼슘의 존재 하에, 또는 예컨대 물의 공비 제거 조건 하에), 에폭사이드(1)(이는, 바람직하게는 대응 2-엔온의 통상적인 에폭사이드화(도시되지 않음)에 의해 제조됨)를 아민 R1-NH2 또는 이의 공액 음이온 R1-N(H)-과 반응시켜, 엔아민(2)을 제조한다. 다르게는, 엔아민(2)은, 바람직하게는 탈수 조건 하에 1,2-다이케톤(3)을 아민 R1-NH2와 반응시킴으로써 제조된다. 다르게는, 엔아민(2)은, 1,2-다이케톤(3)을 비-친핵성 염기(예컨대, 수소화 나트륨, 리튬 다이아이소프로필아마이드, 칼륨 헥사메틸다이실자이드 등)로 탈양성자화시키고, 이어서 생성 에놀레이트 음이온을 설폰일화제(예컨대, 트라이플루오로메탄설폰산 무수물(Tf2O)로 포획하여 케토-엔올(4)을 생성함으로써 제조된다. 이어서, 케토-엔올(4)을, 팔라듐 촉매(예컨대, 팔라듐(II) 아세테이트)의 존재 하에 아민 R1-NH2와 커플링시켜 엔아민(2)을 제조한다. 이어서, 엔아민(2)을, 바람직하게는 탈수 조건 하에 아민 R5-NH2와 반응시켜, 화학식 Y-A의 중간체 화합물을 제조한다. 다르게는, 화학식 Y-A의 중간체 화합물은, 바람직하게는 탈수 조건 하에 1,2-다이케톤(3)과 아민 R1-NH2 및 R5-NH2의 통상적인 축합(도시되지 않음)에 의해 제조된 비스-이민(5)을 비-친핵성 염기를 사용하여 탈양성자화하고, 이어서 생성 엔아마이드를 바람직하게는 1 몰 당량의 바람직하게는 무수 양성자성 산(예컨대, 트라이플루오로아세트산)을 사용하여 소거함으로써 제조된다.
도 2, 반응식 2에 기술된 반응은 바람직하게는, 실질적으로 비활성 기체 대기 하에 무수 비양성자성 용매, 예컨대 톨루엔, 자일렌, 테트라하이드로퓨란, 다이에틸렌 글라이콜 다이메틸 에터 또는 이들의 조합물 중에서, 약 -78 ℃ 내지 약 200℃ 범위의 온도에 수행된다. 바람직하게, 상기 반응은 대기압에서 수행된다.
바람직하게, 상기 화학식 Y의 중간체 화합물은 각각 제조예 1 내지 13(후술됨) 중 임의의 화합물 또는 이들의 공액 염기의 염이다.
재료 및 방법
일반적인 에틸렌/1-옥텐 공중합 절차
2 L 파(Parr) 반응기를 중합에 사용하였다. 모든 공급물은, 상기 반응기에 도입되기 전에 알루미나 및 Q-5(상표명) 촉매(엥겔하르트 케미칼스 인코포레이티드(Englehardt Chemicals Inc.)로부터 입수가능)의 칼럼을 통과하였다. 착체(1) 및 활성화 조촉매(활성화제)의 용액을 글로브 박스 내에서 비활성 대기(예컨대, 질소 기체) 하에 취급하였다. 교반된 2 L 반응기에, 약 533 g의 혼합된 알칸 용매(아이소파르(Isopar) E) 및 250 g의 1-옥텐 공단량체를 채웠다. 300 psi(2070 kPa))에서 75 mL 첨가 탱크로부터의 차등 압력 팽창에 의해 수소 기체(45 psi)를 분자량 제어제로서 가했다. 상기 반응기 내용물을 120 ℃의 중합 온도로 가열하고, 에틸렌을 사용하여 466 psig(3.4 MPa)로 포화시켰다. 금속-리간드 착체(1) 및 활성화 조촉매 (i) 및 (ii)로서, (i) 장쇄 트라이알킬아민("다이(탈로우)메틸아민")의 반응에 의해 제조된, 1.2 몰 당량의 테트라키스(펜타플루오로페닐)보레이트의 메틸다이((C14-C18)알킬)암모늄 염의 혼합물(본원에서 MDATPB로서 약칭됨); 실질적으로 USP 5,919,9883, 실시예 2에 기재된 바와 같이 아크조-노벨 인코포레이티드(Akzo-Nobel, Inc.)로부터 시판중인 알민(ARMEEN(상표명)) M2HT, HCl 및 Li[B(C6F5)4]; 및 (ii) 톨루엔 중에 희석액으로서 변형된 메틸알루미녹산-3Å(MMAO-3A)(10 몰 당량)를 혼합하고 촉매 첨가 탱크로 옮기고, 상기 반응기에 주입하였다. 필요시 에틸렌을 가하면서, 이러한 중합 조건을 15 분 동안 유지하였다. 내부 냉각 코일을 통해, 상기 반응물로부터 열을 연속적으로 제거하였다. 생성 용액을 상기 반응기로부터 제거하고, 아이소프로필 알코올로 반응을 종결시키고, 약 67 mg의 입체장애 페놀 산화방지제(시바 가이기 코포레이션(Ciba Geigy Corporation)으로부터의 이르가녹스(IRGANOX, 상표명) 1010) 및 133 mg의 인 안정화제(시바 가이기 코포레이션으로부터의 이르가포스(IRGAFOS, 상표명) 168)를 함유하는 10 mL의 톨루엔 용액을 가함으로써 안정화시켰다.
중합 작업 사이에, 세척 사이클을 수행하였으며, 이때 850 g의 혼합된 알칸을 상기 반응기에 가하고, 상기 반응기를 150 ℃로 가열하였다. 이어서, 새로운 중합이 시작되기 전에, 상기 반응기에서 가열된 용매를 즉시 제거하였다.
달리 지시하지 않는 한, 중합체의 융점 및 결정화 온도를 DSC(DSC 2910, 티에이 인스트루먼츠 인코포레이티드(TA Instruments, Inc.))로 측정하였다. 먼저, 공중합체의 샘플을 10 ℃/분의 속도로, 실온에서 210 ℃로 가열하였다. 이 온도에서 4 분 동안 유지한 후, 이 샘플을 10 ℃/분의 속도로 -40 ℃로 냉각하고, 이어서 -40 ℃에서 4 분 동안 유지한 후, 10 ℃/분의 속도로 215 ℃로 가열하였다.
달리 지시하지 않는 한, 공중합체의 분자량을 시믹스 테크놀로지 인코포레이티드(Symyx Technologies, Inc.)의 SYMYX(상표명) 고-처리량 겔 투과 크로마토그래피(SHT-GPC) 또는 비스코텍(Viscotek) HT-350 겔 투과 크로마토그래피(V-GPC) 상에서 측정하였다. 상기 SHT-GPC는 160 ℃에서 1,2,4-트라이클로로벤젠 중에서 2개의 폴리머 랩스 피엘겔(Polymer Labs PLgel) 10 μm MIXED-B 칼럼(300 x 10 mm)을 2.5 mL/분의 유속으로 사용하였다. 상기 V-GPC는 낮은-각도/수직-각도 광 산란 검출기, 4-모세관 인라인 점도계 및 굴절률 검출기를 장착했다. V-GPC 분석은, 145 ℃ 또는 160 ℃에서 1,2,4-트라이클로로벤젠 중에서 3개의 폴리머 랩스 피엘겔 10 μm MIXED-B 칼럼(300 mm x 7.5 mm)을 1.0 mL/분의 유속으로 사용하였다.
달리 지시하지 않는 한, SHT-GPC를 위한 샘플을 다음과 같이 제조하였다. 샘플 블록에서, 중합체 샘플을 칭량하여 유리 샘플 튜브(시믹스 테크놀로지스)에 넣고, 1,2,4-트라이클로로벤젠(1,2,4-TCB) 중에서 30 mg/mL로 희석하였다. 유리 교반봉을 각각의 튜브에 넣어, 상기 샘플 블록을, 1 시간 동안 가열된 진탕기로 옮겼다(160 ℃, 220 RPM). 용해/샘플 점도가 달성되었는지 육안으로 검사하여, 완전히 용해되지 않은 경우 또는 SHT-GPC에 사용하기에 너무 점성인 경우에는 용매(1,2,4-TCB)를 가했다. 상기 샘플 블록을 상기 진탕기로 15 분 동안 돌려보내고, 이어서 140 ℃로 가열된 SHT-GPC의 샘플 데크로 옮겼다. 상기 샘플을, 소량의 분취량의 30 mg/mL 용액을 제 2 튜브로 옮기고, 용매(1,2,4-TCB)를 가해, 1 mg/mL의 목적하는 농도에 도달하도록 함으로써 희석하고, 이어서 이 중 500 μL를 GPC에 주입하였다.
달리 지시하지 않는 한, V-GPC를 위한 샘플을 다음과 같이 제조하였다. 중합체를 칭량하여, 비스코텍 인코포레이티드(Viscotek, Inc.)에서 입수된 반-자동화된 샘플 제조(SASP) 프로그램을 사용하여 유리 시험-바이알에 넣었다. 1,2,4-트라이클로로벤젠을 칭량한 후, 상기 SASP 프로그램으로 접속된 컴퓨터-제어된 시린지 펌프에 의해 각각의 샘플에 첨가하여, 1.00 mg/mL 농도를 수득하였다. 테플론-코팅된 교반봉을 각각의 튜브에 넣고, 이 튜브들을 캡핑하고, 알루미늄 블록 내로 담지하고, 육안으로 검사시 완전한 용해가 관찰될 때까지 1 시간 내지 2 시간 동안, 가열된 진탕기 상에 두었다(160 ℃, 220RPM). 이어서, 상기 바이알을 오토-샘플러(145 ℃, 자기 교반)의 가열된 데크로 옮기고, 여기서 주입을 기다렸다. 45 분의 작업 시간 동안 각각의 샘플을 270 μL 주입하였다.
일반적 고찰
모든 용매 및 시약은 상업적 공급원으로부터 수득되었으며, 달리 언급되지 않는 한 입수한 그대로 사용하였다. 톨루엔, 헥산, 벤젠-D6(C6D6) 및 톨루엔-d8은 공지된 절차에 따라 건조하고 탈기하였다. 핵자기 공명(NMR) 스펙트럼은 버라이언 머큐리-Vx-300 및 VNMRS-500 분광기 상에 기록하였다. 화학적 이동(ppm)(δ)은 테트라메틸실란에 대해 보고되며, 중수소화된 용매 중의 잔류 양성자를 기준으로 한다. NMR 피크 및 커플링 상수 지정(coupling constant assignment)을 편의상 제공하지만, 제한적인 것은 아니다. 하기 제조예 및 실시예의 구조에서 몇몇 원자는 지칭하는 것을 용이하게 하기 위해 번호를 매겼다. 모든 금속-리간드 착체는, 진공 대기 및 실질적으로 비활성 대기인 글로브 박스 내에서 건조 질소 대기 하에 또는 표준 슐렌크(Schlenk) 및 진공 라인 기술을 사용함으로써 합성 및 저장되었다.
적외선(IR) 분광법으로 1-옥텐의 혼입% 및 중합체 밀도를 결정하였다.
140 μL의 각각의 중합체 용액을 실리카 웨이퍼 상에 두고, 1,2,4-트라이클로로벤젠(TCB)이 증발할 때까지 140 ℃로 가열하고, 오토프로(AutoPro) 오토 샘플러를 장착한 7.1 버전의 니콜렛 넥서스(Nicolet Nexus) 670 FT-IR을 사용하여 분석하였다.
겔 투과 크로마토그래피(GPC).
중량 평균 분자량(Mw) 및 다분산도를 결정하였다: 폴리머 랩스(Polymer Labs, 상표명) 210 고온 겔 투과 크로마토그래피를 사용하여, Mw 및 Mw/Mn 비(다분산도 또는 PDI)를 결정하였다. 16 mL의 1,2,4-트라이클로로벤젠(부틸화된 하이드록시 톨루엔(BHT)으로 안정화됨)으로 희석시킨 13 mg의 폴리에틸렌 중합체를 사용하여 샘플을 제조하고, 가열하고, 160 ℃로 2 시간 동안 진탕하였다.
시차 주사 열량계(DSC; DSC 2910, 티에이 인스트루먼츠 인코포레이티드)에 의해 융점, 결정화 온도 및 융해열을 결정하였다: 먼저, 샘플을 10 ℃/분의 가열 속도로 실온으로부터 180 ℃로 가열하였다. 이 온도에서 2 내지 4 분 유지한 후, 상기 샘플을 10 ℃/분의 냉각 속도로 -40 ℃로 냉각시키고, 이 온도에서 상기 샘플 2 내지 4 분 유지하고, 이어서 상기 샘플을 160 ℃로 가열하였다.
버라이언 600 MHz NMR 장치 및 중수소화된 테트라클로로에탄을 사용하여, 양성자-핵자기 공명(1H-NMR) 분광법에 의해 말단 기를 분석하였다.
약어(의미): κ(카파); i-Pr(아이소프로필, 즉, 2-프로필); Ph(페닐); Bn(벤질); Me(메틸); nBu, n-Bu 등(n-부틸); CH2C12(다이클로로메탄); CD2C12(다이클로로-중수소화된메탄); THF(테트라하이드로퓨란); p-TsOH·H20(파라-톨루엔설폰산 일수화물); TiCl4(티타늄(IV) 클로라이드); K2CO3(탄산 칼륨); Me(메틸); C6D6(과중수소화된 벤젠); 톨루엔-d8(과중수소화된 톨루엔); Et3N(트라이에틸아민); ZrBn4(지르코늄 테트라벤질); HfBn4 및 Hf(CH2Ph)4(하프늄 테트라벤질); r.t.(실온); ℃ (섭씨); x(횟수(2 x 15 mL에서와 같이)); mmol(밀리몰); psi(lb/in2); psig(lb/in2 게이지); MHz(메가헤르쯔); Hz(헤르쯔) m/z (질량-대-전하); 1H-NMR(양성자 NMR); 13C-NMR(탄소-13 NMR); 19F-NMR(불소-19 NMR); HSQC(헤테로핵 단일 양자 결합성); Anal.(원소 분석); calcd(계산치); br(넓은); sept.(7중항); s(단일항); d(2중항); t(3중항); m(다중항); quat.(4중항); J(커플링 상수); HRMS(고해상도 질량 분광 분석); ESI(전자분무 질량 분광 분석) 및 GC/MS(CI)(기체 크로마토그래피-질량 분광 분석(화학적 이온화)); TLC(박막 크로마토그래피).
벤질 금속 및 다른 유기금속, 예컨대 알킬 금속 및 트라이알킬실일 금속(이때, 상기 금속은 화학식 I에 대해 정의된 바와 같은 M1임)이, 화학식 I의 특정 금속-리간드 착체를 제조하기 위해 화학식 Y의 화합물과 반응시키기에 유용한 출발 물질이다. 상기 유기금속을 어떻게 제조하는지는 중요하지 않다. 몇몇 실시양태에서, 상기 유기금속은, 대응 금속 할라이드(예컨대, 금속 클로라이드 또는 브로마이드) 또는 금속 알콕사이드(예컨대, 금속 테트라부톡사이드) 및 유기 리튬 또는 유기 마그네슘 할라이드로부터 출발하여 제조된다. 예를 들어, 몇몇 실시양태에서, 상기 벤질 금속은, 미국 특허 제 7,067,686 B1 호에 기술된 바와 같이 제조된다. 상기 대응 금속 할라이드는 전형적으로, 예를 들어 미국 미주리주 세인트 루이스 소재의 시그마-알드리치 컴파니 및 독일 레겐스타우프 소재의 케모스 게엠베하(CHEMOS GmbH)로부터 시판된다. 다른 실시양태에서, 상기 벤질 금속은 상업적 공급원으로부터 구입된다(예를 들어, 케모스 게엠베하는 카탈로그 번호 151655로 테트라벤질하프늄을 시판하고, 카탈로그 번호 150405로 테트라벤질지르코늄을 시판한다).
X-선 분석
하기 기술되는 바와 같이 X-선 분석을 수행하였다.
데이터 수집: 적합한 치수의 단일 결정을 오일[파라톤(PARATONE, 등록상표) N(쉐브론 인텔렉츄얼 프라퍼티 엘엘씨)]에 침지하고, 박형 유리 섬유 상에 탑재하였다. 상기 결정을, 단색성 흑연 결정, MoKα 방사선 공급원(λ = 0.71073Å), 및 CCD(전하 커플링된 장치) 영역 검출기를 장착한 브루커 스마트(Bruker SMART, 상표명) 플랫폼 회절기로 옮겼다. 데이터 수집 동안, 상기 결정을 차가운 질소 스트림에 넣었다(-100 ℃).
회절기 제어, 프레임 스캔, 지수화, 배향 매트릭스 계산, 셀 매개변수의 최소 자승 구조분석(refinement), 결정면 측정 및 실제 데이터 수집을 위해 프로그램 스마트(SMARTT, 상표)(미국 위스콘신주 매디슨 소재의 브루커 에이엑스에스 인코포레이티드(Bruker AXS, Inc.)로부터 입수가능)를 사용하였다. 데이터 수집 전략을 수립하기 위해 프로그램 애스트로(ASTRO, 상표명)(미국 위스콘신주 매디슨 소재의 브루커 에이엑스에스 인코포레이티드로부터 입수가능)를 사용하였다.
원 데이터 프레임을 프로그램 세인트(SAINT, 상표명)(미국 위스콘신주 매디슨 소재의 브루커 에이엑스에스 인코포레이티드로부터 입수가능)로 읽고, 3D 프로파일링 알고리즘을 사용하여 적분하였다. 생성 데이터로부터 hkl 반사치 및 이의 강도 및 예상 표준 편차를 생성하였다. 상기 데이터를 로렌츠(Lorentz) 및 분극 효과에 대해 보정하였다. 반사치의 최저 2θ 쉘에서의 2.5%에서 반사치의 최고 2θ 쉘(55°)까지의 3.0%의 Rsym 값 범위로, 1.51 내지 2.16 리던던시(redundancy) 수준의 범위를 나타내기에 충분한 반사치를 수집하였다. 결정 감쇠(decay) 보정을 적용하였으며, 이는 1% 미만이었다. 단위 셀 매개변수는, 반사치의 설정 각의 최소 자승에 의해 분석하였다.
지수화된 측정면 상에 기초한 적분에 의해 흡수 보정을 적용하였다. 프로그램 엑스프렙(XPREP, 상표명)(미국 위스콘신주 매디슨 소재의 브루커 에이엑스에스 인코포레이티드로부터 입수가능)을 사용하여 데이터 제조를 수행하였다. 구조는, SHELXTL5.1(상표명)(미국 위스콘신주 매디슨 소재의 브루커 에이엑스에스 인코포레이티드로부터 입수가능)의 직접 방법에 의해 분석하였으며, 이로부터 모든 비-H 원자의 위치가 수득되었다. 또한, SHELXTL5.1(상표명)에서 풀-매트릭스(full-matrix) 최소 자승 구조분석을 사용하여 구조를 분석하였다. 상기 비-H 원자는, 이방성 열 매개변수를 사용하여 구조분석하였으며, 모든 H 원자는 이상적인 위치로 계산하고, 이의 모(parent) 원자 상에 놓인 것을 구조분석하거나, 차등 퓨리에(Difference Fourier) 맵으로부터 수득되고, 임의의 구속(constraint) 없이 구조분석된다. 2차 소멸(extinction)에 대한 보정은 적용하지 않았다. 최종 구조분석은, F 값보다는 F2를 이용하여 수행하였다. R1은, 통상적인 R 값에 대한 기준치를 제공하기 위해 계산되었지만, 이의 함수는 최소화되지 않는다. 추가적으로, wR2는 최소화된 함수이며, R1이 아니다.
선형 흡수 계수, 원자 산란 인자 및 변칙적-분산 보정치는, 문헌[X-ray Crystallography (1974). Vol. IV, p. 55. Birmingham: Kynoch Press (Present distributor, D. Reidel, Dordrecht.)]에서의 국제적인 표로부터의 값으로부터 계산되었다.
관련 함수는 다음과 같다:
상기 식에서,
n은 반사치의 수이고,
p는 구조분석된 매개변수의 총 수이다.
본원에 기술된 모든 열 타원체는 40% 확률 수준으로 도시된다.
금속 리간드-착체를 제조하거나 사용한 반응은 달리 주지되지 않는 한, 질소 하에 글로브 박스에서 행해진다.
제조예
제조예 1: (E)-N-(2-(2,6-다이아이소프로필페닐아미노)사이클로헥스-2-엔일리덴)-2,6-다이아이소프로필아닐린 (a)의 제조는 2009년 8월 20일에 출원된 미국 정규 특허 출원 제 12/544,581 호의 제조예 1로부터 본원에 참조로 혼입되었고 본원에서 반복하였다.
문헌[Gates, D. P.; Svejda, S. A. Onate, E.; Killian, C. M.; Johnson, L. K.; White, P. S.; Brookhart M. Macromolcules, 2000;33:2320-2334]의 절차에 기초하여 합성하였다. 사이클로헥산-1,2-다이온(2.062 g, 18.39 mmol) 및 2,6-다이아이소프로필아닐린(6.52 g, 36.78 mmol)을 70 mL의 메탄올에 용해시켰다. 이 용액에, 1 mL의 폼산을 가하고, 이 혼합물을 실온에서 3일 동안 교반하였다. 침전된 백색 결정질 고체를 프릿 상에서 수집하고, 메탄올로 세척하고(2 x 15 mL), 감압 하에 건조하여, 4.1 g(51.8% 수율)의 제조예 1의 표제 화합물을 수득하였다.
제조예 2: 2-(모폴린-4-일)-2-사이클로헥센-1-온의 제조는 2009년 8월 20일에 출원된 미국 정규 특허 출원 제 12/544,581 호의 제조예 2로부터 본원에 참조로 혼입되었고 본원에서 반복하였다.
문헌[Ohashi, M.; Takahashi, T.; Inoue, S.; Sato, K. Bulletin Chemical Society of Japan, 1975;48:1892]의 변형된 절차에 기초한 합성. 500 mL 환저 플라스크에 딘 스타크(Dean Stark) 트랩, 응축기, 교반봉 및 기체 주입구(N2 기체 대기)를 장착하였다. 상기 플라스크에, 1,2-사이클로헥산다이온(15.14 g, 135.00 mmol), 모폴린(14.82 g, 170.10 mmol) 및 톨루엔(330 mL)을 채웠다. 생성 황색 용액을 5 시간 동안 가열환류시켰다. 가열을 멈추고, 상기 딘 스타크 트랩 상에 약 3.0 mL의 물을 수집하였다. 이 갈색 용액을 점성 오일로부터 경사 분리하고, 톨루엔으로 세척하였다. 이 용액을 고진공 하에 농축하여, 갈색 고체로서 23.33 g(95.34% 수율)의 제조예 2의 표제 화합물을 수득하였다.
제조예 3: 2-(2,6-다이아이소프로필페닐아미노)사이클로헥스-2-엔온의 제조는 2009년 8월 20일에 출원된 미국 정규 특허 출원 제 12/544,581 호의 제조예 3으로부터 본원에 참조로 혼입되었고 본원에서 반복하였다.
응축기, 기체 주입구 및 격막(septum)을 장착한 250 mL 3구 환저 플라스크를 N2 대기 하에 두었다. 이 플라스크에, 2-(모폴린-4-일)-2사이클로헥센-1-온(7.0046 g, 38.65 mmol; 제조예 2), 톨루엔(74.0 mL) 및 2,6-다이아이소프로필아닐린(6.8521 g, 38.65 mmol)을 채웠다. 이 황색 용액에, p-톨루엔설폰산 일수화물(7.3520 g, 38.65 mmol; p-TsOHoH20)을 가했다. 이 반응 혼합물은 많은 침전물과 함께 매우 점성이 되었다. 이 혼합물을 80 ℃(오일 욕 온도)로 가열하고, 교반하였다. 교반을 용이하게 하기 위해, 또다른 5.0 mL의 톨루엔을 가했다. 이 혼합물을 2 시간 동안 교반하였다. 이 반응 혼합물이 실온에 도달하도록 하였다. 상기 혼합물을 여과하였다. 여액을 고진공 하에 농축하여, 10.09 g의 황색 고체를 수득하였다. 상기 고체를 뜨거운 헥산(약 30 mL)에 용해시키고, 여과하였다. 이 용액을 실온으로 냉각시키고, 시딩하고, 냉장고에 두었다. 이 용액을 여과하면서, 고체의 대부분을 플라스크에 남겼다. 이 플라스크를 얼음 욕에 두었다. 상기 고체를 차가운 헥산의 약 6 mL 분획 2개로 세척하였다. 상기 황색 고체를 건조하고, 바이알로 옮기고, 밤새도록 진공 하에 건조하였다(제 1 수득물(crop): 4.0550 g). 모액을 농축하고, 재결정화를 2회 이상 반복하였다. 제 2 수득물을 5시간 동안 냉장고에 두고(제 2 수득물: 1.0785 g), 제 3 수득물은 밤새도록 두었다(제 3 수득물: 0.6919 g). 제조예 3의 표제 화합물의 합친 수율은 5.8254 g(55.54%)이었다.
제조예 4: 중합체성 n-부틸아미노-티타늄 시약(Ti(N(n-Bu)2)r의 제조는 2009년 8월 20일에 출원된 미국 정규 특허 출원 제 12/544,581 호의 제조예 4로부터 본원에 참조로 혼입되었고 본원에서 반복하였다.
건조 박스 내의 슐렌크 플라스크 내에서 Ti(NMe2)4(26 g, 0.116 mol)를 500 mL의 톨루엔에 용해시켰다. 이 플라스크를 후드에 두었다. 이 용액에, 68.8 mL(0.696 mol)의 n-부틸아민을 가하자, 주황색 고체가 형성되었다. 상기 응축기의 상단에서 질소를 스위핑하면서, 이 혼합물을 매우 약하게 가열환류시켰다. 가열 후 수 분 내에, 황색 용액이 진적색으로 변했다. 6 시간의 환류 후, 이 용액을 실온으로 냉각시키고, 용매를 감압 하에 제거하여, 진한 흑적색 유리질 고체를 수득하였다. 이 생성물을 저장하기 위해 건조 박스로 옮겼다. 23.2933 g의 제조예 4의 표제 시약을 수득하였으며, 이때 r은 Ti(N(n-Bu)2의 반복 단위의 수를 나타낸다.
제조예 5: 2,(2,6-다이아이소프로필페닐아미노)-3,5-다이메틸사이클로펜트-2-엔온의 제조는 2009년 8월 20일에 출원된 미국 정규 특허 출원 제 12/544,581 호의 제조예 6으로부터 본원에 참조로 혼입되었고 본원에서 반복하였다.
제조예 3의 절차와 유사한 절차를 따르되, 3,5-다이메틸-1,2-사이클로펜타다이온(1.5043 g, 11.9237 mmol), 톨루엔(6.0 mL), 2,6-다이아이소프로필아닐린(2.4 mL, 12.7117 mmol) 및 파라-톨루엔설폰산 일수화물(0.4584 g, 2.4098 mmol)을 사용하고; 가열환류시키고(오일 욕 온도: 150 ℃); 생성 혼합물을, 5% 에틸 아세테이트/95% 헥산으로 용리하는 크로마토그래피의 실리카 겔 상에서 직접 정제하여(이의 상대적으로 적은 부피로 인해 허용가능함), 황색 고체로서 2.5156 g(73.9%)의 2-(2,6-다이아이소프로필페닐아미노)-3,5-다이메틸사이클로펜트-2-엔온을 수득하였다.
13C NMR(C6D6, 125 MHz, 30 ℃) 및 HRMS(ESI, (M+H)+) 데이터는 제시되어 있지 않다.
제조예 6: 2-((1,1':3',1"-터페닐)-2'-일아미노)-2-사이클로헥센-1-온의 제조는 2009년 8월 20일에 출원된 미국 정규 특허 출원 제 12/544,581 호의 제조예 7로부터 본원에 참조로 혼입되었고 본원에서 반복하였다.
제조예 2의 절차와 유사한 절차를 따르되, 1,2-사이클로헥산다이온(1.0099 g, 9.0065 mmol); 2,6-다이페닐아닐린(2.2258 g, 9.0731 mmol); 톨루엔(22 mL); p-톨루엔설폰산 일수화물(0.0859 g, 0.4516 mmol)을 사용하고; 2.3 시간 동안 반응 혼합물을 환류시키고; 3.5678 g의 갈색 점성 오일을 단리하였다. 상기 점성 오일을, 바이오테지(Biotage) SNAP 50 g KP-Sil 칼럼을 사용하여, 상기 점성 오일에 소량의 4% 에틸 아세테이트/96% 헥산 및 100% 에틸 아세테이트를 담지하고 헥산 중의 4 내지 8 % 에틸 아세테이트 구배액으로 용리하는 크로마토그래피로 정제하고, 단리한 후, 황색 점성 오일로서 1.1388 g(37.2%)의 2-((1,1':3',1"-터페닐)-2'-일아미노)-2-사이클로헥센-1-온을 수득하였다.
13C NMR(C6D6, 125 MHz, 30 ℃) 및 HSQCAD(C6D6, 500 MHz, 30 ℃) 데이터는 제시되어 있지 않다.
제조예 7: (E)-N-(6-(부틸이미노)사이클로헥스-1-엔일)-2,6-다이아이소프로필아닐린 (B)의 제조는 2009년 8월 20일에 출원된 미국 정규 특허 출원 제 12/544,581 호의 실시예 B로부터 본원에 참조로 혼입되었고 본원에서 반복하였다.
상기 식에서, r은 Ti(N(n-Bu)2의 반복 단위의 수를 나타낸다.
글로브 박스 내에서 N2 대기 하에 반응을 수행하였다. 교반봉을 장착한 20 mL 바이알에, 0.4858 g(1.7900 mmol)의 2-(2,6-다이아이소프로필페닐아미노)사이클로헥스-2-엔온(제조예 3), 톨루엔(6.0 mL) 및 0.3022 g(0.8984 mmol)의 중합체성 n-부틸아미노-티타늄 시약(제조예 4)을 채웠다. 이 혼합물을 밤새도록(24 시간) 교반하였다. 분취물의 1H-NMR에서는, 반응이 완결되지 않은 것으로 나타났다. 약 26%의 출발 물질이 남아 있었다. 따라서, 상기 혼합물에, 46.2 mg의 중합체성 n-부틸아미노-티타늄 시약(제조예 4)을 가했다. 밤새도록 교반한 후, 분취물의 1H-NMR은 출발 물질이 남아 있지 않은 것으로 나타났다. 이 혼합물에 헥산을 가하고, 생성 혼합물을 여과하였다. 또한, 헥산을 사용하여 필터케이크 고체를 세척하였다. 여액(황색 용액)을 감압 하에 농축하여, 황색 오일로서 305.8 mg(52.3%)의 제조예 7의 화합물(B)을 수득하였다.
제조예 8: 화합물 (E)-N-(6-(부틸이미노)사이클로헥스-1-엔일)-2,6-다이아이소프로필아닐린 (N-((6E)-6-(부틸이미노)-1-사이클로헥센-1-일)-2,6-비스(1-메틸에틸)-벤젠아민으로도 명명됨) (B)의 대안적 제조는 2009년 8월 20일에 출원된 미국 정규 특허 출원 제 12/544,581 호의 실시예 C로부터 본원에 참조로 혼입되었고 본원에서 반복하였다.
글로브 박스 내에서 N2 대기 하에 반응을 수행하였다. 40 mL의 톨루엔에 용해된 n-부틸 아민(nBuNH2)에, 5 mL의 톨루엔에 용해된 TiCl4를 45초 내에 가했다. 상기 첨가 동안, 이 반응 혼합물은 적색으로 변했고, 이어서 첨가가 완료되고 약 1 분 후에 주황색으로 변했다. 상기 첨가 동안 온도가 27 ℃에서 49 ℃로 상승했고, 상기 첨가가 완료되고 2 분 후에 감소하기 시작했다.
실온에서 1.5 시간 동안 교반한 후, 2-((2,6-비스(1-메틸에틸)페닐)아미노)-2-사이클로헥센-1-온(제조예 3)을 고체로서 가했다. 생성 반응 혼합물을 주위 온도에서 3.25 시간 동안 교반하였다. 반응 혼합물을 매체 프릿을 통해, 2.1 g의 무수 K2CO3을 함유하는 용기로 여과하고(연황색 여액), 필터케이크(염)를 헥산으로 2회 세척하였다(2 x 15 mL). 이 현탁액을 K2CO3과 함께 2시간 동안 교반하고, 이어서 여과하여(시린지 필터 사용), 무색 용액을 수득하였다(K2CO3은 상기 용액으로부터 황색 색상을 흡수함). 감압 하에 상기 용액으로부터 용매를 제거하여, 무색 오일로서 4.66 g(95.6% 수율)의 제조예 8의 화합물(B)을 수득하였다. 생성물의 1H NMR 및 HRMS는, 제조예 8의 화합물(B)의 1H NMR 및 HRMS 및 제조예 7의 화합물(B)의 1H NMR 및 HRMS와 일치하였다.
제조예 9: N-(2,6-다이아이소프로필페닐)-2-부틸아미노트로폰이민(D)의 제조는 2009년 8월 20일에 출원된 미국 정규 특허 출원 제 12/544,581 호의 실시예 D로부터 본원에 참조로 혼입되었고 본원에서 반복하였다.
2-(2,6-다이아이소프로필아닐리노)트로폰(C)를, 제조예 5의 과정과 유사한 방식으로 p-TsOH의 촉매량을 사용하여 톨루엔 중의 용액 트로폴론(tropolone)(시그마-알드리치 컴파니, 카탈로그 번호 T89702) 및 2,6-비스(1,1-다이메틸에틸)아닐린을 딘-스타크 트랩 상에 환류시킴으로써 제조한다.
Et3OBF4(418 mg, 2.20 mmol)를 CH2Cl2(5 mL)에 용해시켰다. CH2Cl2(15 mL) 중의 2-(2,6-다이아이소프로필아닐리노)트로폰(C)(587 mg, 2.09 mmol)의 용액을 천천히 가했다. 25 ℃에서 3 시간 동안 교반한 후, 이 용액을 약 0 ℃로 냉각시키고, 미리-냉각된(0 ℃) CH2Cl2(5 mL) 중의 n-BuNH2(1.467 g, 20 mmol)의 용액을 가했다. 상기 용액을 25 ℃로 가온하고, 밤새도록 교반하였다. 진공 하에 용매를 제거하고, 잔사를 칼럼 크로마토그래피로 정제하여(용리액: 3 체적%의 Et3N을 함유하는 헥산:Et2O(3:1)), 주황색 고체로서 557 mg(80% 수율)의 본질적으로 순수한 제조예 9의 화합물(D)을 수득하였다.
제조예 10: (E)-N-(5-(부틸이미노)-2,4-다이메틸사이클로펜트-1-엔일)-2,6-다이아이소프로필아닐린(G)의 제조는 2009년 8월 20일에 출원된 미국 정규 특허 출원 제 12/544,581 호의 실시예 G로부터 본원에 참조로 혼입되었고 본원에서 반복하였다.
제조예 8의 절차와 유사한 절차를 따르되, n-부틸아민 (0.3098 g, 4.23 mmol); 톨루엔(5.0 mL); 이어서 톨루엔(2.0 mL) 중의 티타늄(IV) 클로라이드 (0.0841 g, 0.44 mmol)의 용액; 이어서 톨루엔(2 mL) 중의 2-(2,6-다이아이소프로필페닐아미노)-3,5다이메틸사이클로펜트-2-엔온(0.2056 g, 제조예 5)의 용액을 사용하고; 반응 혼합물을 밤새도록 교반하고; 갈색 오일로서 0.2253 g(91.8 %)의 생성물(G)을 수득하였다.
13C NMR(C6D6, 125 MHz, 30 ℃) 및 HSQCAD(C6D6, 500 MHz, 30 ℃) 및 HRMS(ESI, (M+H)+) 데이터는 제시되어 있지 않다.
제조예 11: N2-((1E)-2-((2,6-비스(1-메틸에틸)페닐)아미노)-2-사이클로헥센-1-일리덴)-N1,N1-다이메틸-1,2-에탄다이아민(H)의 제조는 2009년 8월 20일에 출원된 미국 정규 특허 출원 제 12/544,581 호의 실시예 H로부터 본원에 참조로 혼입되었고 본원에서 반복하였다.
1일: 바이알에, N,N-다이메틸에틸렌다이아민(0.58 mL, 5.3098 mmol) 및 톨루엔(7.0 mL)을 채웠다. 이 무색 용액에, 톨루엔(3.0 mL) 중의 티타늄(IV) 클로라이드(0.1001 g, 0.5276 mmol)의 용액을 가했다. 적색 고체가 관찰되었지만, 이어서 강한 교반이 적용되는 동안 용액에 용해되었다. 생성 주황색 용액을 1 시간 동안 교반하였다. 이어서, 톨루엔(2.0 mL) 중의 2-(2,6-다이아이소프로필페닐아미노)-2-사이클로헥센-1-온(0.2437 g, 0.8979 mmol, 제조예 3)의 용액을 가했다. 상기 용액을 함유했던 바이알을 톨루엔(1.0 mL)으로 세척하고, 이 세척액을 상기 반응 혼합물에 가했다.
2일: 바이알에 N,N-다이메틸에틸렌다이아민(0.58 mL, 5.3098 mmol) 및 톨루엔(7.0 mL)을 채움으로써, 티타늄 시약의 모액(1:1.4의 티타늄 대 케토-엔아민의 비를 갖도록)을 개별적으로 제조하였다. 이 무색 용액에, 톨루엔(3.0 mL) 중의 티타늄(IV) 클로라이드(0.1000 g, 0.5271 mmol)의 용액을 가했다. 적색 고체가 관찰되었지만, 강한 교반이 적용되었을 때 용액에 용해되었다. 생성 주황색 용액을 1 시간 동안 교반하였다.
상기 1일로부터의 반응 혼합물을 밤새도록 교반한 후, 이 반응 혼합물에 3.3 mL의 상기 티타늄 시약의 모액(전술된 바와 같이 제조됨)을 가했다. 생성 혼합물을 3 시간 동안 교반하였다. 이 혼합물을 여과하고(시린지 필터), 헥산을 사용하여 고체를 세척하였다. 이 황색 여액 용액을 진공 중에서 농축하여, 황색 오일을 수득하였다. 상기 오일을 헥산(10 mL)에 용해시켜, 고체를 침전시켰다. 이 혼합물을 여과하고(시린지 필터), 고체를 2개 5 mL 분획의 헥산으로 세척하였다. 이 황색 여액 용액을 진공 중에서 농축하여, 황색 오일로서 0.2790 g(90.97%)의 생성물(H)을 수득하였다.
13C NMR(C6D6, 125 MHz, 30 ℃) 데이터는 제시되어 있지 않다.
제조예 12: (6E)-6-(부틸이미노)-N-(1,1':3',1"-터페닐)-2'-일-1-사이클로헥센-1-아민(J)의 제조는 2009년 8월 20일에 출원된 미국 정규 특허 출원 제 12/544,581 호의 실시예 J로부터 본원에 참조로 혼입되었고 본원에서 반복하였다.
제조예 2의 절차와 유사한 절차를 따르되, n-부틸아민(0.53 mL, 5.3406 mmol); 톨루엔(7.0 mL); 톨루엔(3.0 mL) 중의 티타늄(IV) 클로라이드(0.1006 g, 0.5303 mmol)의 용액을 사용하고; 생성 용액을 1 시간 동안 교반하고; 이어서 톨루엔(2.0 mL) 중의 2-((1,1':3',1"-터페닐)-2'-일아미노)-2-사이클로헥센-1-온(0.3062 g, 0.9021 mmol, 제조예 7)의 용액을 가하고; 톨루엔으로 세척하고(1.0 mL); 단리 후에, 갈색 오일로서 0.3352 g(94.18%)의 생성물(J)을 수득하였다.
제조예 13: (E)-2,6-다이아이소프로필-N-(2-(부틸아미노)사이클로헥스-2-엔일리덴)아닐린(L)의 제조는 2009년 8월 20일에 출원된 미국 정규 특허 출원 제 12/544,581 호의 실시예 L로부터 본원에 참조로 혼입되었고 본원에서 반복하였다.
바이알에, N-((6E)-6-(부틸이미노)-1-사이클로헥센-1-일)-2,6-비스(1-메틸에틸)벤젠아민(B)(3.0038 g, 9.1995 mmol, 제조예 7) 및 톨루엔(30.0 mL)을 채웠다. 생성 황색 용액을 교반하고, 다이에틸 에터 중의 1.0M HCl(수성, 0.46 mL, 0.46 mmol)의 용액을 가했다. 생성 반응 혼합물을 3 시간 동안 교반하였다. 이 혼합물에, 헥산(5 mL)을 가하고, 여과하여(시린지 필터) 미세한 고체를 제거하였다. 여과된 고체를 헥산(6 mL)으로 세척하고, 여액을 감압 하에 밤새도록 농축하여, 갈색 점성 오일로서 3.0107 g의 생성물(L)을 수득하였다.
13C NMR(C6D6, 125 MHz, 30 ℃) 데이터는 제시되어 있지 않다.
제조예 14: 금속-리간드 착체(a1), [N-[2-[[2,6-비스(1-메틸에틸)페닐]아미노-κN]-2-사이클로헥센-1-일리덴]-2,6-비스(1-메틸에틸)벤젠아미네이토-κN]트리스(페닐메틸)-하프늄(a1)의 제조는 2009년 8월 20일에 출원된 미국 정규 특허 출원 제 12/544,581 호의 실시예 1로부터 본원에 참조로 혼입되었고 본원에서 반복하였다.
(E)-N-(2-(2,6-다이아이소프로필페닐아미노)사이클로헥스-2-엔일리덴)-2,6-다이아이소프로필아닐린(0.439 g, 1.0 mmol; 제조예 1) 및 테트라벤질 하프늄(0.554 g, 1.0 mmol)을 6 mL의 C6D6에 용해시켰다. 이 용액을 76 ℃로 4일 동안 가열하였다. NMR은, 9:1의 생성물 대 리간드 비로, HfBn4의 완전한 전환을 나타냈다. 용매를 감압 하에 제거하였다. 잔사를 3 mL의 톨루엔에 용해시키고, 여과하였다. 여액에, 8 mL의 헥산을 가했다. 수 분 내에, 황색 결정이 나타났다. 주위 온도에서 3 시간 동안 정치시킨 후, 10 mL의 헥산을 가하고, 용액을 밤새도록 냉장고(-26 ℃)에 두었다. 용매를 경사분리하고, 황색 결정을 헥산(2 x 10 mL)으로 세척하고, 이어서 감압 하에 건조하여, 0.486 mg의 금속-리간드 착체(a1)를 수득하였다. 수율 54%.
X-선 분석에 의해 유도된 단결정 구조의 ORTEP 그림은 도시되어 있지 않다.
제조예 15: 금속-리간드 착체(B1), (N-((6E)-6-(부틸이미노-κN)-1-사이클로헥센-1-일)-2,6-비스(1-메틸에틸)벤젠아미네이토-κN)트리스(페닐메틸)-하프늄의 제조는 2009년 8월 20일에 출원된 미국 정규 특허 출원 제 12/544,581 호의 실시예 3으로부터 본원에 참조로 혼입되었고 본원에서 반복하였다.
실온에서, (E)-N-(6-(부틸이미노)사이클로헥스-1-엔일)-2,6-다이아이소프로필아닐린(0.3005, 0.92 mmol; 제조예 7) 및 테트라벤질 하프늄(0.4997 mmol)을 6 mL의 톨루엔에 용해시켜, 연적색 용액을 수득하였다. 밤새도록 교반한 후(황색 용액), 용매를 감압 하에 제거하여, 고도의 결정질 황색 고체를 수득하였다. 잔사를 2 mL의 톨루엔에 용해시키고, 이어서 8 mL의 헥산을 가했다. 이 용액을 여과하고, 실온에서 밤새도록 두어 큰 황색 결정을 생성하였다. 용액을 경사분리하고, 상기 큰 황색 결정을 차가운 헥산(5 mL)으로 세척하고, 이어서 감압 하에 건조하여, 331 mg의 금속-리간드 착체(B1)를 수득하였다. 용액 및 헥산 세척액을 합치고, 밤새도록 냉장고에 두었다(-20 ℃). 용매를 경사분리하고, 황색 결정을 2 x 2 mL의 차가운 헥산으로 세척하고, 이어서 감압 하에 건조하여, 추가적인 211 mg의 금속-리간드 착체(B1)를 수득하였다. 금속-리간드 착체(B1)의 합친 수율은 0.542 mg,75.8%이었다.
금속-리간드 착체(B1)의 열분해 연구. 금속-리간드 착체(B1)(25 mg)를 0.6 mL의 톨루엔-d8에 용해시키고, 이 용액을 89.3 ℃로 42 시간 동안 가열하였다. 이후, NMR 스펙트럼은 약 4%의 분해를 나타냈다.
X-선 분석에 의해 유도된 단결정 구조의 ORTEP 그림은 도시되어 있지 않다.
제조예 16: 금속-리간드 착체(B2), (N-((6E)-6-(부틸이미노-κN)-1-사이클로헥센-1-일)-2,6-비스(1-메틸에틸)벤젠아미네이토-κN)트리스(페닐메틸)-지르코늄의 제조는 2009년 8월 20일에 출원된 미국 정규 특허 출원 제 12/544,581 호의 실시예 4로부터 본원에 참조로 혼입되었고 본원에서 반복하였다.
실온에서, (E)-N-(6-(부틸이미노)사이클로헥스-1-엔일)-2,6-다이아이소프로필아닐린(0.35 g, 1.07 mmol; 제조예 7) 및 테트라벤질 지르코늄(0.4885 g, 1.07 mmol)을 3 mL의 C6D6에 용해시켜, 연적색 용액을 수득하였다. 1 시간 동안 교반한 후, 양성자 NMR은 완전한 반응이 일어난 것으로 나타났다. NMR 튜브의 함유물을 반응 혼합물로 되돌려 보냈다. 이 반응 혼합물에 8 mL의 헥산을 가하고, 이 용액을 여과하고, 밤새도록 냉장고에 두었다(-45 ℃). 용매를 경사분리하고, 황색 결정을 차가운 헥산(2 x 4 mL)으로 세척하고, 이어서 감압 하에 건조하여, 0.566 g의 금속-리간드 착체(B2)를 수득하였다. 수율 68%.
X-선 분석에 의해 유도된 단결정 구조의 ORTEP 그림은 도시되어 있지 않다.
제조예 17: 금속-리간드 착체(B3): (N-((6E)-6-(부틸이미노-κN)-1-사이클로헥센-1-일)-2,6-비스(1-메틸에틸)벤젠아미네이토-κN)트라이요오도-하프늄의 제조는 2009년 8월 20일에 출원된 미국 정규 특허 출원 제 12/544,581 호의 실시예 13으로부터 본원에 참조로 혼입되었고 본원에서 반복하였다.
실온에서, 20 mL의 CH2Cl2에 용해된 1.5624 g(2.01 mmol)의 (N-((6E)-6-(부틸이미노-κN)-1-사이클로헥센-1-일)-2,6-비스(1-메틸에틸)벤젠아미네이토-κN)트리스(페닐메틸)-하프늄[제조예 15의 금속-리간드 착체(B1)]에, 60 mL의 CH2Cl2.에 용해된 요오드(I2)를 20 분 내에 가했다. 실온에서 10 분 동안 교반한 후, 용매를 감압 하에 제거하였다. 생성 잔사에, 30 mL의 헥산을 가하고, 생성 현탁액을 15 분 동안 교반하였다. 상기 현탁액을 프릿을 사용하여 여과하고, 필터케이크를 15 mL의 헥산으로 세척하고, 감압 하에 건조하여, 1.47 g의 황색 금속-리간드 착체(B3)(82.7% 수율)를 수득하였다.
화학적 이동, 다양성(multiplicity), 및 H3 및 H9에 대한 커플링 상수에 대한 정보는 TOCSY1D 스펙트럼으로부터 수득하였다.
제조예 18: 금속-리간드 착체(B4), (N-((6E)-6-(부틸이미노-κN)-1-사이클로헥센-1-일)-2,6-비스(1-메틸에틸)벤젠아미네이토-κN)트라이메틸-하프늄의 제조는 2009년 8월 20일에 출원된 미국 정규 특허 출원 제 12/544,581 호의 실시예 14로부터 본원에 참조로 혼입되었고 본원에서 반복하였다.
0.7486 g(0.85 mmol)의 (N-((6E)-6-(부틸이미노-κN)-1-사이클로헥센-1-일)-2,6-비스(1-메틸에틸)벤젠아미네이토-κN)트라이요오도-하프늄(제조예 17의 금속-리간드 착체(B3))을 함유하는 30 mL 톨루엔 용액에, 다이에틸 에터 중의 0.88 mL(2.65 mmol)의 3 M 메틸 마그네슘 브로마이드(CH3MgBr)의 용액을 가했다. 생성 반응 혼합물을 20 분 동안 교반하고, 이어서 용매를 감압 하에 제거하였다. 생성 잔사를 30 mL의 헥산으로 추출하고, 여과하였다. 여액으로부터 용매를 제거하여, 황색 결정질 고체로서 0.462 g(99.4% 수율)의 금속-리간드 착체(B4)를 수득하였다.
제조예 19: 금속-리간드 착체(B4), (N-((6E)-6-(부틸이미노-κN)-1-사이클로헥센-1-일)-2,6-비스(1-메틸에틸)벤젠아미네이토-κN)트라이메틸-하프늄의 제조는 2009년 8월 20일에 출원된 미국 정규 특허 출원 제 12/544,581 호의 실시예 15로부터 본원에 참조로 혼입되었고 본원에서 반복하였다.
N-((6E)-6-(부틸이미노)-1-사이클로헥센-1-일)-2,6-비스(1-메틸에틸)-벤젠아민(3.03, 9.28 mol, (B); 제조예 8) 및 HfCl4(2.972 g, 9.28 mmol)의 차가운(-25 ℃) 톨루엔 용액(50 mL)에, 12.68 mL의 3 M CH3MgBr 에터 용액을 가했다. CH3MgBr의 첨가 동안, 기체 발생이 관찰되었다. 생성 반응 혼합물은 따뜻해지지 않았다. 수 분 내에, 반응 혼합물의 색상이 황색에서 흑색으로 변했다. 이 용액을 1 시간 동안 교반하였다. 용매를 감압 하에 제거하였다. 잔사에, 50 mL의 헥산을 가하고, 생성 황색 용액을 여과하였다. 필터케이크(염)를 추가적인 30 mL의 헥산으로 세척하였다. 용매를 감압 하에 제거하여, 황색 고체로서 4.03 g(79.1% 수율)의 금속-리간드 착체(B4)를 수득하였다.
X-선 분석에 의해 유도된 단결정 구조의 ORTEP 그림은 도시되어 있지 않다.
제조예 20: 금속-리간드 착체(D1), [N-(2,6-다이아이소프로필페닐)-2-부틸아미노트로폰이미네이토]트라이벤질하프늄의 제조는 2009년 8월 20일에 출원된 미국 정규 특허 출원 제 12/544,581 호의 실시예 16으로부터 본원에 참조로 혼입되었고 본원에서 반복하였다.
N-(2,6-다이아이소프로필페닐)-2-부틸아미노트로폰이민((D), 제조예 9, 250 mg, 0.74 mmol) 및 HfBn4(403 mg, 0.74 mmol)를 무수 C6D6(3 mL)에 용해시켜, 주황색 용액을 수득하고, 이를 25 ℃에서 교반하였다. 90 분 후에 1H NMR로서, 상기 반응의 완결을 확인하였다. 이 반응 혼합물을 진공 하에 농축하고, 헥산으로 층을 만들고, -45 ℃로 밤새도록 냉각하였다. 생성 황색 결정을 여과하고, 차가운 헥산으로 세척하고, 진공 하에 건조하여, 557 mg(79 % 수율)의 금속-리간드 착체(D1)를 수득하였다.
X-선 분석에 의해 유도된 단결정 구조의 ORTEP 그림은 도시되어 있지 않다.
제조예 21: 금속-리간드 착체(G1), (E)-N-(5-(부틸이미노-κN)-2,4다이메틸사이클로펜트-1-엔일)-2,6-비스(1-메틸에틸) 벤젠아미네이토-κN)트리스(페닐메틸)하프늄의 제조는 2009년 8월 20일에 출원된 미국 정규 특허 출원 제 12/544,581 호의 실시예 21로부터 본원에 참조로 혼입되었고 본원에서 반복하였다.
글로브 박스에서, 바이알에 8 mL의 톨루엔 중의 410 mg(1.2 mmol)의 (E)N-(5-(부틸이미노)-2,4-다이메틸사이클로펜트-1-엔일)-2,6-다이아이소프로필아닐린((G); 제조예 10)을 충전하고; 654 mg(1.2 mmol)의 Hf(CH2Ph)4를 가하고; 생성 반응 혼합물을 2 시간 동안 교반하고(추가적인 리간드를 가하지 않음); 반응 혼합물을 감압하에 농축하여 잔사를 수득하고 3 mL의 톨루엔 및 20 mL의 헥산으로부터 결정화하여 잔사를 용해시켜, 0.335 mg의 금속-리간드 착체(G1)를 수득하였다. 수율 35%. 톨루엔/헥산 용매 혼합물로부터 X-선 품질 결정을 성장시켰다.
13C NMR(C6D6, 125 MHz, 30 ℃) 및 HSQCAD(C6D6, 500 MHz, 30 ℃) 데이터 및 X-선 분석에 의해 유도된 단결정 구조의 ORTEP 그림은 도시되어 있지 않다.
제조예 22: 금속-리간드 착체(H1), (N2-(2-((2,6-비스(1-메틸에틸)페닐)아미노-κN)-2-사이클로헥센-1-일리덴)-N1,N1-다이메틸-1,2-에탄다이아미네이토-κN,κN')트리스(페닐메틸)-하프늄의 제조는 2009년 8월 20일에 출원된 미국 정규 특허 출원 제 12/544,581 호의 실시예 22로부터 본원에 참조로 혼입되었고 본원에서 반복하였다.
제조예 21의 절차와 유사한 절차를 따르되, N2-((1E)-2-((2,6-비스(l 메틸에틸)페닐)아미노)-2-사이클로헥센-1-일리덴)-N1,N1-다이메틸-1,2-에탄다이아민(H)(0.2584 g, 0.7566 mmol; 제조예 11); 톨루엔(3 mL); 톨루엔(2 mL) 중의 하프늄 테트라벤질(0.4103 g, 0.7556 mmol)의 황색 용액을 사용하고; 톨루엔(1 mL)으로 세척하고; 반응 혼합물을 30 분 동안 교반하고; 3 mL의 톨루엔 및 17 mL의 헥산으로부터 결정화하여, 235 mg의 금속-리간드 착체(H1)를 수득하였다. 수율 39.3%.
13C NMR(C6D6, 125 MHz, 30 ℃), HSQCAD(C6D6, 500 MHz, 30 ℃), 원소 분석(C, H, N) 데이터 및 X-선 분석에 의해 유도된 단결정 구조의 ORTEP 그림은 도시되어 있지 않다.
제조예 23: 금속-리간드 착체(J1), (6-(부틸이미노-κN)-N-(1,1':3',1"-터페닐)-2'-일-1-사이클로헥센-1-아미네이토-κN)트리스(페닐메틸)-하프늄의 제조는 2009년 8월 20일에 출원된 미국 정규 특허 출원 제 12/544,581 호의 실시예 23으로부터 본원에 참조로 혼입되었고 본원에서 반복하였다.
제조예 21의 절차와 유사한 절차를 따르되, (6E)-6-(부틸이미노)-N-(1,1':3',1"-터페닐)-2'-일-1-사이클로헥센-1-아민(1)(0.2972 g, 0.7533 mmol; 제조예 12) (추가적인 (J) 첨가 안함); 톨루엔(3 mL); 톨루엔(2 mL) 중의 하프늄 테트라벤질(0.4098 g, 0.7547 mmol)의 용액을 사용하고; 톨루엔으로 세척하고(1 mL); 생성 반응 혼합물을 20 분 동안 교반하고; 이어서 헥산 (2 mL)을 가하고; 단리된 잔사를 2 mL의 톨루엔에 용해시키고, 10 mL의 헥산을 가하고; 여과하고, 농축하여, 황색 점성 오일로서 350 mg의 금속-리간드 착체(J1)를 수득하였다. 수율 55.0%.
13C NMR(C6D6, 125 MHz, 30 ℃) 및 HSQCAD(C6D6, 500 MHz, 30 ℃) 데이터는 도시되어 있지 않다.
제조예 24: 금속-리간드 착체(L1), (2,6-비스(1-메틸에틸)-N-((1E)-2(부틸아미노-κN)-2-사이클로헥센-1-일리덴)벤젠아미네이토-κN)트라이메틸하프늄의 제조는 2009년 8월 20일에 출원된 미국 정규 특허 출원 제 12/544,581 호의 실시예 26으로부터 본원에 참조로 혼입되었고 본원에서 반복하였다.
1.0168 g(3.11 mmol)(E)-2,6-다이아이소프로필-N-(2-(부틸아미노)사이클로헥스-2-엔일리덴)아닐린(L)(제조예 13) 및 0.997 g(3.11 mmol)의 HfCl4를 함유하는 40 mL의 톨루엔 용액에, 4 몰 당량의 3 M MeMgBr 에터 용액을 가했다. MeMgBr의 첨가 동안, 기체 발생이 관찰되었다. 실온에서 2시간 동안 생성 반응 혼합물을 교반한 후, 감압 하에 용매를 제거하였다. 잔사에, 20 mL의 톨루엔 및 이어서 20 mL의 헥산을 가하고, 생성 황색 용액을 여과하였다. 감압 하에 여액으로부터 용매를 제거하여, 황색 결정질 고체를 남겼다. NMR은, 목적하는 생성물(L1)의 형성 및 소량의 불순물을 나타냈다. 상기 고체를 2 mL의 따뜻한 톨루엔에 용해시키고, 18 mL의 헥산을 가했다. 생성 용액을 여과하고, 여액을 밤새도록 냉장고에 두었다(-26 ℃). 침전된 황색 고체를 소결된 유리 깔때기 상에서 수집하고, 3 mL의 차가운 헥산으로 세척하고, 이를 감압 하에 건조하여, 433 mg의 깨끗한 생성물(L1)의 제 1 로트(lot)를 수득하였다. 최종 여액으로부터 용매를 제거하고, 생성 잔사를 15 mL의 헥산에 용해시키고, 이를 냉장고에 넣었다. 냉장고에서 2일 후, 용매를 경사분리하고, 남아있는 큰 결정을 2 mL의 차가운 헥산으로 세척하고, 감압 하에 건조하여, 333 mg의 생성물(L1)의 제 2 로트를 수득하였다. 금속-리간드 착체(L1)의 합친 수율은 766 mg(44.8%)이었다.
13C NMR(C6D6, 125 MHz, 30 ℃), HSQCAD(C6D6, 500 MHz, 30 ℃), 원소 분석(C, H, N) 데이터 및 X-선 분석에 의해 유도된 단결정 구조의 ORTEP 그림은 도시되어 있지 않다.
제조예 25: 금속-리간드 착체(M1), [N-[2-[[2,6-비스(1-메틸에틸)페닐]아미노-κN]-3-메틸부탄-2-일리덴]-2,6-비스(1-메틸에틸)벤젠아미나토-κN])트라이메틸지르코늄의 제조
미국 특허 제 7,199,255 B2 호, 컬럼 37, 43 행 내지 컬럼 38, 32 행에 기재된 바와 같이 (E)-N-(3-(2,6-다이아이소프로필페닐아미노)-3-메틸부탄-2-일리덴)-2,6-다이아이소프로필아닐린(M)을 제조한다.
250 mL의 톨루엔에 용해된 (E)-N-(3-(2,6-다이아이소프로필페닐아미노)-3-메틸부탄-2-일리덴)-2,6-다이아이소프로필아닐린(13.6 g, 32.3 mmol)에 헥산 중 22.4 mL(35.8 mmol)의 1.6 M n-BuLi 용액을 첨가하였다. 2.5 시간 동안 교반한 후, ZrCl4(7.4 g, 32 mmol)를 첨가하고 생성 혼합물을 진갈색 슬러리로서 밤새 교반하였다. 상기 혼합물에 35.5 mL(107 mmol)의 MeMgBr(Et20 중 3M)을 첨가하였다. 주위 온도에서 3 시간 동안 교반한 후, 용매를 진공에서 제거하였다. 생성된 회색 분말을 톨루엔(120 mL)으로 처리하여 생성물을 용해시키고, 여과하여 불용성 염을 제거하였다. 여과된 케익을 추가적인 톨루엔(2 x 40 mL)으로 세척하였다. 톨루엔 분획을 혼합하고 휘발성 성분을 진공에서 제거하여 13.5 g(75%)의 연황갈색 고체를 금속-리간드 착체(M1)로서 수득하였다.
제조예 26: 금속-리간드 착체(M2), [N-[2-[[2,6-비스(1-메틸에틸)페닐]아미노-κN]-3-메틸부탄-2-일리덴]-2,6-비스(1-메틸에틸)벤젠아미나토-κN])트라이메틸하프늄의 제조
60 mL의 톨루엔에 용해된 (E)-N-(3-(2,6-다이아이소프로필페닐아미노)-3-메틸부탄-2-일리덴)-2,6-다이아이소프로필아닐린(3.00 g, 7.13 mmol)에 헥산 중 4.9 mL(7.9 mmol)의 1.6 M n-BuLi 용액을 첨가하였다. 90 분 동안 교반한 후, HfCl4 (2.284 g, 7.132 mmol)를 첨가하고 혼합물을 진갈색 슬러리로서 밤새 교반하였다. 상기 혼합물에 2.61 mL(7.84 mmol)의 MeMgBr(Et20 중 3M)을 첨가하였다. 주위 온도에서 2 시간 동안 교반한 후, 용매를 진공에서 제거하였다. 연갈색 잔사를 톨루엔으로 추출하고, 여과하여 불용성 염을 제거하였다. 여과액을 진공에서 감소시켜 3.04 g(66%)의 황색 고체를 금속-리간드 착체(M2)로서 수득하였다.
제조예 27: 금속-리간드 착체(B5), (N-((6E)-6-(부틸이미노-부틸이미노κN)-1-사이클로헥센-l-일)-2,6-비스(l-메틸에틸)벤젠아미나토-κN)트라이메틸지르코늄의 제조
(6E)-6-(부틸이미노)-N-(1,1':3',1"-터페닐)-2'-일-1-사이클로헥센-1-아민(B)(제조예 7) 및 ZrCl4의 차가운(-25 ℃) 톨루엔 용액(50 mL)에 주위 온도에서 3 M MeMgBr 에터 용액을 첨가했다. MeMgBr의 첨가 동안, 기체 발생이 관찰되었다. 반응 혼합물은 따뜻해지지 않았다. 수 분 내에, 반응 혼합물의 색상이 황색에서 흑색으로 변했다. 이 용액을 2 시간 동안 교반하였다. 용매를 감압 하에 제거하였다. 잔사에, 20 mL의 톨루엔을 가한 후 30 mL의 헥산을 가하고, 용액을 여과하였다. 용매를 감압 하에 제거하여, 1 시간 내에 고도의 결정성 고체로 고체화되는 진한 주황색 오일을 수득하였다. 고체에 20 mL의 헥산을 첨가하고 생성 현탁액을 실온에서 3 시간 동안 교반하였다. 고체를 프릿 상에 수집하고 5 mL의 차가운 헥산으로 세척하고 감압하에 건조시켜 1.44 g의 금속-리간드 착체(B5)를 수득하였다. 여과액을 밤새 냉장고에 놓아두었다. 용매를 경사분리하고 거대한 진한 주황색 결정을 4 mL의 차가운 헥산으로 세척하고 감압하에 건조시켜 680 mg의 금속-리간드 착체(B5)를 수득하였다. 금속-리간드 착체(B5)의 혼합된 수율은 2.12 g(59.1%)이었다.
X-선 분석에 의해 유도된 단결정 구조의 ORTEP 그림은 도시되어 있지 않다.
제조예 28: 1,3-비스(2,6-다이아이소프로필페닐)-lH-이미다졸-2(3H)이민(N)의 제조
1,3-비스[2,6-비스(1-메틸에틸)페닐]-l,3-다이하이드로-2H-이미다졸-2일리덴(4.00 g, 10.3 mmol, 알드리치 케미컬 컴파니) 및 트라이메틸실일아자이드(3.56 g, 30.9 mmol)를 45 mL의 톨루엔에 용해시키고, 생성 혼합물을 117 ℃에서 24 시간 동안 가열하였다. 감압하에 용매를 제거하여 황색 고체를 수득하였다. 황색 고체를 20 mL의 톨루엔 중에 용해시킨 후, 8 mL의 메탄올을 첨가하였다. 생성 혼합물을 실온에서 1 시간 동안 교반한 후, 감압 하에 용매를 제거하였다. 잔사에 10 mL의 헥산을 첨가하고 생성 현탁액을 10 분 동안 교반하고, 이어서 냉장고에 밤새 놓아두었다. 소결된 유리 여과기 상에 고체를 수집하고 수집한 고체를 차가운 헥산(2 x 5 mL)으로 2 회 세척하고, 상기 고체를 감압하에 건조시켜 3.84 g(92.4%)의 생성물(N)을 수득하였다.
본 발명의
실시예
실시예 1: 금속-리간드 착체(1), (N-((6E)-6-(부틸이미노-κN)-1-사이클로헥센-l-일)-2,6-비스(l-메틸에틸)벤젠아미나토-κN)비스(페닐메틸)-트리스(1,1-다이메틸에틸)포스핀이미도-지르코늄의 제조
5 mL의 톨루엔 중에 제조예 16의 금속-리간드 착체(B2)를 용해시켜 황색 용액을 수득하였다. 상기 용액에 1 mL의 톨루엔 중의 1 몰 당량의 트리스(l,1-다이메틸에틸)포스핀이미드(문헌[Rankin D.W.H., et al., Journal of the Chemical Society, Dalton Trans., 1985:827-830])를 첨가하였다. 1 시간 동안 교반한 후, 감압하에 용매를 제거하여 황색 결정 고체를 수득하였다. 고체를 따뜻한 톨루엔(5 mL)에 용해시키고 10 mL의 헥산을 첨가하고, 생성 용액을 냉장고(-26 ℃)에 밤새 놓아두었다. 용매를 경사분리하고 잔여 황색 결정을 헥산(2 x lO mL)으로 세척하고 감압하에 건조시켜 255 mg(66% 수율)의 생성물(1)을 수득하였다.
도 3은, 금속-리간드 착체(1)의 X-선 분석에 의해 유도된 단결정 구조의 ORTEP 그림을 도시한 것이다. 도 3에서, 수소 원자는 명료함을 위해 생략되었다.
실시예 2: 금속-리간드 착체(2), ([N-[2-[[2,6-비스(l-메틸에틸)페닐]아미노-κN]-3-메틸부탄-2-일리덴]-2,6-비스(1-메틸에틸)벤젠아미나토-κN]포스핀이미도-지르코늄의 제조
5 mL의 톨루엔 중에 금속-리간드 착체(M1)(제조예 25)를 용해시키고 고체로서 tBu3P=NH를 첨가한 후, 3 mL의 헥산으로 세척하였다. tBu3P=NH의 첨가 동안 기체 발생을 관찰하였다. 생성 반응 혼합물을 1 시간 동안 실온에서 교반하고, 이어서 감압하에 용매를 제거하여 결정 회백색 생성물(2)을 수득하였다. 생성물(2)을 12 mL의 따뜻한 헥산에 용해시키고 생성 용액을 냉장고(-27 ℃)에 놓아두었다. 2 일 후, 생성된 작은 결정 샘플을 바이알로 이동시켰다. 용매를 경사분리하고 2 mL의 차가운 헥산을 가진 회백색 결정을 생성하고 감압하에 건조시켜 310 mg의 생성물(2)을 수득하였다; 수율 52 %.
도 4는, 금속-리간드 착체(2)의 X-선 분석에 의해 유도된 단결정 구조의 ORTEP 그림을 도시한 것이다. 도 4에서, 수소 원자는 명료함을 위해 생략되었다.
실시예 3: 금속-리간드 착체(3), ([N-[2-[[2,6-비스(l-메틸에틸)페닐]아미노-κN]-3-메틸부탄-2-일리덴]-2,6-비스(1-메틸에틸)벤젠아미나토-κN]포스핀이미도-하프늄의 제조
금속-리간드 착체(M1) 대신에 금속-리간드 착체(M2)(제조예 26)를 사용하는 것을 제외하고 실시예 2의 과정과 유사한 방식으로 81 mg의 생성물(3)을 제조하였다; 수율 60 %.
실시예 4: 금속-리간드 착체(4), (N-((6E)-6-(부틸이미노-κN)-
1-사이클로헥센-l-일)-2,6-비스(1-메틸에틸)벤젠아미나토-κN)비스(페닐메틸)-트리스(1,l-다이메틸에틸)포스핀이미도-하프늄의 제조
15 mL의 톨루엔 중에 제조예 19의 금속-리간드 착체(B4; 0.3128 g, 0.55 밀리몰)를 용해시켜 황색 용액을 수득하였다. -26 ℃로 냉각시켰다. 상기 용액에 8 mL의 헥산 중의 1 몰 당량의 트리스(l,1-다이메틸에틸)포스핀이미드를 첨가하였다. 밤새 교반한 후, 감압하에 용매를 제거하여 황색 고체를 수득하였다. 헥산(3 mL) 중에 고체를 용해시키고 생성 용액을 냉장고(-27 ℃)에 밤새 놓아두었다. 24 시간 후, 용매를 경사분리하고 잔여 결정을 감압하에 건조시켜 289 mg(83% 수율)의 생성물(4)을 수득하였다.
실시예 5 내지 8: 금속-리간드 착체 (5) 내지 (8)의 제조 방법.
별도의 실험에서 하프늄-리간드 착체(B4) 대신에 하프늄-리간드 착체 (Ll), (Gl), (Dl), 및 (HI) 중 상이한 하나를 사용하는 것을 제외하고 실시예 4의 과정과 유사한 방식으로 하기 금속-리간드 착체 (5) 내지 (8)을 각각 제조하였다:
실시예 9: 금속-리간드 착체(9), (N-((6E)-6-(부틸이미노-κN)-1-사이클로헥센-l-일)-2,6-비스(l-메틸에틸)벤젠아미나토-κN)다이메틸-(2,3,4-트라이메틸-3-펜타놀라토)-지르코늄의 제조.
금속-리간드 착체(B5)(제조예 27)를 함유하는 바이알에 0.6 mL의 C6D6에 용해된 다이-i-Pr케톤(2,4-다이메틸펜탄-3-온)의 용액을 첨가하였다. 바이알의 생성된 내용물을 NMR 튜브로 이동시켰다. 15 분 후에 얻은 NMR 스펙트럼은 금속-리간드 착체(9)의 정량적 형성을 나타내었다. 용매를 제거하고 단리되고 순수한 형태로 금속-리간드 착체(9)를 획득하였다.
실시예 10: 금속-리간드 착체(10), (2,6-비스(l,1-다이메틸에틸)페놀레이트)(N-((6E)-6-(부틸이미노-κN)-1-사이클로헥센-1-일)-2,6-비스(1-메틸에틸)벤젠아미나토-κN)다이메틸-하프늄의 제조.
2 mL의 C6D6에 용해된 금속-리간드 착체(B4)(제조예 19)의 용액을 함유하는 바이알에 1 mL의 C6D6에 용해된 57.3 mg의 2,6-비스(1,1-다이메틸에틸)페놀의 용액을 첨가하였다. 기체 발생이 관찰되지 않았다. 반응 혼합물을 주위 온도(약 24 ℃)에서 18 시간 동안 놓아두었다. NMR 스펙트럼은 금속-리간드 착체(10)의 정량적 형성을 나타내었다. 용매를 제거하고 단리되고 순수한 형태로 금속-리간드 착체(10)를 획득하였다.
도 5는, 금속-리간드 착체(10)의 X-선 분석에 의해 유도된 단결정 구조의 ORTEP 그림을 도시한 것이다. 도 5에서, 수소 원자는 명료함을 위해 생략되었다.
실시예 11: 금속-리간드 착체(11), (N-((6E)-6-(부틸이미노-κN)-
1-사이클로헥센-l-일)-2,6-비스(l-메틸에틸)벤젠아미네이토-κN)[N,N'-비스(l-메틸에틸)에탄이미드아미데이토-κN,κN']다이메틸-지르코늄의 제조.
N,N'-메탄테트라일비스-2-프로판아민을 함유하는 바이알에 금속-리간드 착체(B5), 3 mL의 톨루엔에 용해된 (6-(부틸이미노-κN)-N-(1,1':3',1"-터페닐)-2'-일-l-사이클로헥센-1-아미네이토-κN)트라이메틸-지르코늄(제조예 27)을 첨가하였다. 용액을 15 분 동안 교반하고, 이어서 용매를 감압하에 제거하였다. 잔여물을 3 mL의 헥산에 용해시키고 용액을 2 일 동안 냉장고(-30 ℃)에 놓아두었다. 용매를 경사분리하고 매우 큰 주황색-갈색 결정을 2 mL의 차가운 헥산으로 세척하고 감압하에 건조시켜 131 mg의 금속-리간드 착체(11)를 수득하였다. 수율 61.7 %.
도 6은, 금속-리간드 착체(11)의 X-선 분석에 의해 유도된 단결정 구조의 ORTEP 그림을 도시한 것이다. 도 6에서, 수소 원자는 명료함을 위해 생략되었다.
실시예 12: 금속-리간드 착체(12), [(N-((6E)-6-(부틸이미노-κN)-1-사이클로헥센-l-일)-2,6-비스(l-메틸에틸)벤젠아미네이토-κN)][1,3-비스(2,6-다이메틸페닐)-1,3-다이하이드로-2H-이미다졸-2-이미네이토-κN2]다이메틸-지르코늄의 제조.
66.6 mg(0.17 mg)의 금속-리간드 착체(B5)(제조예 27)를 함유하는 바이알에 0.8 mL의 C6D6에 용해된 76.2 mg(0.17 mmol)의 1,3-비스[2,6-비스(1-메틸에틸)페닐]-1,3-다이하이드로-2H-이미다졸-2-이민(N)(제조예 28)을 첨가하였다. 시약의 혼합시 기체 발생이 관찰되었다. 바이알의 내용물을 NMR 튜브로 이동시켰다. 10 분 후 획득한 NMR은 금속-리간드 착체(12)의 깨끗한 형성을 나타내었다. 용매를 감압하에 제거하였다. 잔여물을 4 mL의 따뜻한 헥산에 용해시켰다. 바이알을 냉장고(-30 ℃)에 밤새 놓아두었다. 황색 결정 고체를 소결된 유리 여과기 상에 수집하고 2 mL의 차가운 헥산으로 세척하고 감압하에 건조시켜 75 mg(53.5%)의 금속-리간드 착체(12)를 수득하였다.
도 7은, 금속-리간드 착체(12)의 X-선 분석에 의해 유도된 단결정 구조의 ORTEP 그림을 도시한 것이다. 도 7에서, 수소 원자는 명료함을 위해 생략되었다. 열 타원체는 40% 확률 수준으로 도시된다.
실시예 13: 화학식 I의 금속-리간드 착체의 제조.
화학식 M의 리간드 대신에 제조예 1, 9, 10, 11, 12, 또는 13 중 임의의 화학식 (a), (D), (G), (H), (J), 또는 (L)의 임의의 리간드를 지르코늄 테트라클로라이드 및 4 몰 당량의 메틸 마그네슘 브로마이드와 접촉시키는 것을 제외하고는 제조예 25에서 기재된 것과 유사한 방식으로 상응하는 트라이메틸 지르코늄-리간드 착체를 각각 수득하고, 이어서 트라이메틸 지르코늄-리간드 착체를 화학식 J3-H, J4-H, J5-H, J5-H, J6-H, 또는 J7-H의 화합물(이때 J3, J4, J5, J6 및 J7은 앞서 정의된 바와 같다)에 접촉시켜 트라이메틸 지르코늄-리간드 착체의 메틸(지르코늄에 결합됨) 중 하나가 J3, J4, J5, J6 및 J7로 각각 치환된 화학식 I의 상응하는 금속-리간드 착체를 수득하였다.
실시예 14: 화학식 I의 금속-리간드 착체의 제조.
화학식 M의 리간드 대신에 제조예 1, 9, 10, 11, 12, 또는 13 중 임의의 화학식 (a), (D), (G), (H), (J), 또는 (L) 중 임의의 리간드를 하프늄 테트라클로라이드 및 4 몰 당량의 메틸 마그네슘 브로마이드와 접촉시키는 것을 제외하고는 제조예 26에서 기재된 것과 유사한 방식으로 상응하는 트라이메틸 하프늄-리간드 착체를 각각 수득하고, 이어서 트라이메틸 지르코늄-리간드 착체를 화학식 K1-H, K2-H, K3-H, K4-H, K5-H 또는 K6-H의 화합물(이때 K1,,K2, K3, K4, K5 및 K6은 앞서 정의된 바와 같다)에 접촉시켜 트라이메틸 하프늄-리간드 착체의 메틸(하프늄에 결합됨) 중 둘이 K1, K2, K3, K4, K5 또는 K6으로 각각 치환된 화학식 I의 상응하는 금속-리간드 착체를 수득하였다.
실시예 A 내지 D: 폴리(에틸렌 1-옥텐) 공중합체 (P1) 내지 (P4)의 각각의 제조.
하기 표 1에 요약된 바와 같이, 전술한 일반적인 에틸렌/-1-옥텐 공중합 과정에서 금속-리간드 착체 (1) 또는 (4)의 μM, 활성화 조촉매 MDATPB의 μM, 활성화 조촉매 MMAO의 μM 및 에틸렌의 g을 사용하여 생성물 폴리(에틸렌 1-옥텐) 공중합체 (P1) 내지 (P4)를 수득하되, 각각 140 ℃의 최종 설정 온도로 진공 오븐의 온도를 경사지게 상승시키면서 약 12 시간 동안 건조시킴으로써 회수하였다.
DSC(DSC 2910, 티에이 인스트루먼츠 인코포레이티드(TA Instruments, Inc.))에 의한 각각의 폴리(에틸렌 1-옥텐) 공중합체(예컨대, P1)의 융점 및 결정화 온도를 측정하였다. 별도로, 먼저 폴리(에틸렌 1-옥텐) 공중합체(예컨대, P1)의 샘플을 10 ℃/분의 가열 속도로 실온으로부터 180 ℃로 가열하였다. 이 온도에서 4 분간 유지한 후, 상기 샘플을 10 ℃/분의 냉각 속도로 -40 ℃로 냉각시키고, 상기 샘플을 -40 ℃에서 4 분간 유지하고, 이어서 상기 샘플을 10 ℃/분의 제 2 가열 속도로 160 ℃로 가열하였다.
폴리머 랩스(Polymer Labs, 상표명) 210 고온 겔 투과 크로마토그래피를 사용하여, 폴리(에틸렌 1-옥텐) 공중합체(예컨대, P1)의 각각의 분자량을 측정하였다. 13 mg의 폴리(에틸렌 1-옥텐) 공중합체(예컨대, P1)를 사용하고 이를 16 mL의 1,2,4-트라이클로로벤젠(BHT로 안정화됨)으로 희석시킨 샘플을 제조하고, 가열하고, 희석된 샘플을 160 ℃로 2 시간 동안 진탕하였다. 옥텐의 혼입(몰%) 및 밀도 결정을 위해, 140 μL의 각각의 중합체 용액을 실리카 웨이퍼 상에 별도로 침적시키고, TCB가 건조할 때까지 140 ℃로 가열하고, 건조된 샘플을 오토프로(AutoPro) 오토 샘플러를 장착한 7.1 버전의 니콜렛 넥서스(Nicolet Nexus) 670 FT-IR 소프트웨어를 사용하여 분석하였다.
결과를 하기 표 2에 제시한다. 표 2에서 "g-폴리/g-금속"은, 사용되는 착체 g 당 생성된 중합체의 g을 의미하고, Tm, 중량 평균 분자량 Mw(단위: g), 수 평균 분자량 Mn, 및 Mw/Mn은 상기 정의된 바와 같다.
실시예 E 내지 H: 폴리(에틸렌 1-옥텐) 공중합체 (P5) 내지 (P8)의 각각의 제조.
별도의 실험에서 지그코늄-리간드 착체(1) 대신에 상이한 하프늄-리간드 착체 (Ll), (Gl), (Dl), 및 (H1)을 사용하는 것을 제외하고 실시예 A의 과정과 유사한 방식으로 폴리(에틸렌 1-옥텐) 공중합체 (P5) 내지 (P8)(구조식 도시되지 않음)을 각각 제조하였다.
상기 실시예에 제시한 바와 같이, 상기 제 2 실시양태의 촉매는, 중합 촉매로서 이로운 촉매 효율(예컨대, 상기 제 2 실시양태의 촉매를 제조하기 위해 사용되는 화학식 I의 금속-리간드 착체의 g 당 더 많은 g의 중합체가 생성됨)을 나타내며, 통상적인 폴리올레핀의 Mw 또는 Mn에 비해, 이롭게 더 높은 Mw, Mn 또는 이 둘 모두를 갖는 폴리올레핀(폴리올레핀 공중합체 포함)을 제공한다.
본 발명이 이의 바람직한 실시양태에 따라 상기 기술되었지만, 본 발명은 본 개시내용의 진의 및 범주 내에서 변형될 수 있다. 따라서, 본원은, 본원에 개시된 일반적인 원리를 사용하는 임의의 변화, 용도 또는 변경을 포괄하는 것으로 의도된다. 또한, 본원은, 본 발명과 관련되며 첨부된 특허청구범위의 한계 내에 속하는 당분야의 공지되거나 통상적인 관행 내에 드는, 본 발명의 개시내용으로부터의 이러한 벗어남을 포괄하는 것으로 의도된다.
Claims (12)
- 하기 화학식 I의 금속-리간드 착체:
화학식 I
상기 식에서,
LQ는 각각 존재하지 않거나 L이고;
L은 각각 독립적으로 (C1-C5)알킬, 트라이메틸실일메틸, 또는 벤질이되, L은 각각 독립적으로 M1에 결합된 1가 음이온 잔부이고;
n은 0이고(X는 존재하지 않음),
J는 하기 화학식 J1 또는 J5 중 임의의 하나의 1가 음이온 잔부이고:
화학식 J1
RKRLRXP=N-
(상기 식에서,
RK 및 RL은 각각 독립적으로 수소, (C1-C40)알킬, (C3-C40)사이클로알킬, 또는 (C3-C20)사이클로알킬-(C1-C20)알킬렌이거나, RK 및 RL은 함께 (C6-C40)아릴렌, (C3-C40)사이클로알킬렌, (C1-C40)알킬렌, 또는 (C6-C20)아릴에 의해 치환된, 하나 이상의 질소 원자를 함유하는 (C1-C20)헤테로아릴렌을 형성하고,
RX는 각각 독립적으로 수소, (C1-C40)알킬, (C3-C40)사이클로알킬, 또는 (C3-C20)사이클로알킬-(C1-C20)알킬렌이다)
화학식 J5
RKRLC=N-
(상기 식에서,
RK 및 RL은 각각 독립적으로 상기 정의된 바와 같다)
M1은 각각 독립적으로 4족 금속으로서, +3 또는 +4의 형식적 산화 상태의 금속인 하프늄(Hf), 지르코늄(Zr) 또는 티타늄(Ti)을 의미하고;
m은 0 내지 3의 정수이고;
R1은 각각 독립적으로 2,6-비스(1-메틸에틸)페닐; 2-(1-메틸에틸)페닐; 2,4,6-트리스(1,1-다이메틸에틸)페닐; 2-(1,1-다이메틸에틸)페닐; 3,4-비스(1,1-다이메틸에틸)페닐; 2,4,6-트라이페닐페닐; 바이페닐-2-일; 3,5-다이페닐페닐; 사이클로헥실; 다이페닐메틸; 트라이페닐메틸; 3,5-비스(2,6-다이메틸페닐)페닐; 2,6-비스(다이메틸아미노)페닐; 2,6-다이니트로페닐; 2,6-다이(1-메틸에톡시)페닐; 2,6-다이(1-나프틸)페닐; 또는 3,5-다이(1-나프틸)페닐이고;
R2, R3 및 R4는 각각 독립적으로 (C1-C40)알킬, (C3-C40)사이클로알킬, 또는 (C3-C20)사이클로알킬-(C1-C20)알킬렌이거나; R4는 (C1-C40)알킬, (C3-C40)사이클로알킬, 또는 (C3-C20)사이클로알킬-(C1-C20)알킬렌이고, R2 및 R3은 함께, 화학식 I의 금속-리간드 착체가 하기 화학식 II-B, II-E, II-A, II-H 또는 II-I의 금속-리간드 착체가 되도록, 하기 화학식 R23의 2가 라디칼을 형성하고:
화학식 R23
화학식 II-B
(상기 식에서,
R2A는 H, (C1-C40)알킬, (C3-C40)사이클로알킬, 또는 (C3-C20)사이클로알킬-(C1-C20)알킬렌이고;
R34는 각각 독립적으로 C(R35)2이고;
R35는 각각 독립적으로 H, (C1-C20)알킬, (C3-C20)사이클로알킬, 또는 (C3-C10)사이클로알킬-(C1-C10)알킬렌이다)
화학식 II-E
(상기 식에서,
R2A는 H, (C1-C40)알킬, (C3-C40)사이클로알킬, 또는 (C3-C20)사이클로알킬-(C1-C20)알킬렌이고;
---은 각각 존재하지 않거나 파이 결합이다)
화학식 II-A
(상기 식에서,
R2A는 H, (C1-C40)알킬, (C3-C40)사이클로알킬, 또는 (C3-C20)사이클로알킬-(C1-C20)알킬렌이고;
R34는 각각 독립적으로 C(R35)2이고;
R35는 각각 독립적으로 H, (C1-C20)알킬, (C3-C20)사이클로알킬, 또는 (C3-C10)사이클로알킬-(C1-C10)알킬렌이다)
화학식 II-H
(상기 식에서,
R2A는 H, (C1-C40)알킬, (C3-C40)사이클로알킬, 또는 (C3-C20)사이클로알킬-(C1-C20)알킬렌이고;
R3A 및 R4는 함께 (C6-C20)아릴렌, (C3-C20)사이클로알킬렌 또는 (C1-C20)알킬렌이다)
화학식 II-I
(상기 식에서,
R2A는 H, (C1-C40)알킬, (C3-C40)사이클로알킬, 또는 (C3-C20)사이클로알킬-(C1-C20)알킬렌이고;
R3A 및 R4는 함께 (C6-C20)아릴렌, (C3-C20)사이클로알킬렌 또는 (C1-C20)알킬렌을 형성한다);
R5는 각각 독립적으로 (C1-C40)알킬, (C3-C40)사이클로알킬, 또는 (C3-C20)사이클로알킬-(C1-C20)알킬렌이고;
상기 (C1-C40)알킬, (C1-C20)알킬, (C3-C40)사이클로알킬, (C3-C20)사이클로알킬, (C3-C20)사이클로알킬-(C1-C20)알킬렌, (C3-C10)사이클로알킬-(C1-C10)알킬렌, (C6-C40)아릴렌, (C6-C20)아릴렌, (C3-C40)사이클로알킬렌, (C3-C20)사이클로알킬렌, (C1-C40)알킬렌, (C1-C20)알킬렌, (C6-C20)아릴, 또는 (C1-C20)헤테로아릴렌은 각각 독립적으로 동일하거나 상이하고, 하나 이상의 치환기 RS로 치환되거나 비치환되고;
RS는 각각 독립적으로 (C1-C18)알킬 또는 비치환된 (C1-C18)사이클로알킬이고;
은 각각 독립적으로 결합 단편을 나타내고;
L, LQ 및 m은 각각, 금속 M1의 형식적 산화 상태에 따라, 화학식 I의 금속-리간드 착체가 총체적으로 중성이 되도록 선택된다. - 삭제
- 제 1 항에 있어서,
화학식 II-H 및 II-I에서, R3A 및 R4가 함께 (C2-C5)알킬렌 또는 (C3-C5)사이클로알킬렌을 형성하고; R1 및 R5가 각각 독립적으로 (C1-C10)아릴렌, (C3-C10)사이클로알킬렌, 또는 (C1-C10)알킬렌이고; R2A가 H 또는 (C1-C10)알킬인 금속-리간드 착체. - 삭제
- 삭제
- 제 1 항에 있어서,
RK, RL 및 RX가 각각 독립적으로 (C1-C20)알킬, (C3-C20)사이클로알킬, 또는 (C3-C10)사이클로알킬-(C1-C10)알킬렌인 금속-리간드 착체. - 제 1 항에 있어서,
L 및 LQ가 각각 독립적으로 (C1-C5)알킬, 트라이메틸실일메틸 또는 벤질인 금속-리간드 착체. - 제 1 항, 제 3 항, 제 4 항, 및 제 7 항 내지 제 9 항 중 어느 한 항에 따른 하나 이상의 금속-리간드 착체 및 하나 이상의 활성화 조촉매(co-catalyst) 또는 이들의 반응 생성물을 포함하거나 이로부터 제조된 촉매로서,
상기 하나 이상의 금속-리간드 착체의 총 몰 수 대 상기 하나 이상의 활성화 조촉매의 총 몰 수의 비가 1:10,000 내지 100:1인, 촉매. - 하나 이상의 중합성 올레핀을, 상기 하나 이상의 중합성 올레핀의 적어도 일부를 중합하기에 충분한 올레핀 중합 조건 하에서 제 10 항에 따른 촉매와 접촉시켜 폴리올레핀을 생성하는 단계를 포함하는, 폴리올레핀의 제조 방법.
- 삭제
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US30614710P | 2010-02-19 | 2010-02-19 | |
| US61/306,147 | 2010-02-19 | ||
| PCT/US2011/024012 WO2011102989A1 (en) | 2010-02-19 | 2011-02-08 | Metal-ligand complexes and catalysts |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20130008561A KR20130008561A (ko) | 2013-01-22 |
| KR101827023B1 true KR101827023B1 (ko) | 2018-02-07 |
Family
ID=43743715
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020127024456A KR101827023B1 (ko) | 2010-02-19 | 2011-02-08 | 금속-리간드 착체 및 촉매 |
Country Status (8)
| Country | Link |
|---|---|
| US (1) | US8202954B2 (ko) |
| EP (1) | EP2536735B1 (ko) |
| JP (1) | JP5837514B2 (ko) |
| KR (1) | KR101827023B1 (ko) |
| CN (1) | CN102822180B (ko) |
| BR (1) | BR112012020718A2 (ko) |
| ES (1) | ES2691727T3 (ko) |
| WO (1) | WO2011102989A1 (ko) |
Families Citing this family (27)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2014139861A1 (en) | 2013-03-11 | 2014-09-18 | Universität Bayreuth | Complexes for the catalytic oligomerization of olefins |
| EP2801579B1 (en) * | 2013-05-08 | 2016-10-19 | Arlanxeo Netherlands B.V. | Metal complex with a Lewis base ligand |
| EP3083048B1 (en) | 2013-12-19 | 2021-04-07 | Dow Global Technologies LLC | Metal-ligand complex, olefin polymerization catalyst derived therefrom, and olefin polymerization method utilizing the catalyst |
| CN105732406A (zh) * | 2014-12-10 | 2016-07-06 | 中国科学技术大学 | 含环庚三烯结构的铝化合物催化剂、合成及其用途 |
| EP3596143B1 (en) * | 2017-03-15 | 2023-04-26 | Dow Global Technologies LLC | Catalyst system for multi-block copolymer formation |
| US11078224B2 (en) | 2017-04-07 | 2021-08-03 | Applied Materials, Inc. | Precursors for the atomic layer deposition of transition metals and methods of use |
| JP2021518330A (ja) | 2018-03-19 | 2021-08-02 | ダウ グローバル テクノロジーズ エルエルシー | ケイ素終端テレケリックポリオレフィン組成物およびそれを調製するためのプロセス |
| WO2019182983A1 (en) | 2018-03-19 | 2019-09-26 | Dow Global Technologies Llc | Silicon-terminated organo-metal compounds and processes for preparing the same |
| TW201938570A (zh) | 2018-03-19 | 2019-10-01 | 美商陶氏全球科技有限責任公司 | 矽封端之有機金屬化合物及其製備方法 |
| KR20200135419A (ko) | 2018-03-19 | 2020-12-02 | 다우 글로벌 테크놀로지스 엘엘씨 | 실릴계 작용화제로 오르가노-금속 화합물을 작용화하는 방법 및 이에 의해 제조된 실릴계 작용화제 화합물 |
| BR112020019520A2 (pt) | 2018-03-30 | 2020-12-29 | Dow Global Technologies Llc | Sistema de catalisador, e, processo de polimerização. |
| CN111902439B (zh) | 2018-03-30 | 2023-06-23 | 陶氏环球技术有限责任公司 | 双核烯烃聚合活化剂 |
| SG11202008656PA (en) | 2018-03-30 | 2020-10-29 | Dow Global Technologies Llc | Olefin polymerization activators |
| EP3774942A1 (en) | 2018-03-30 | 2021-02-17 | Dow Global Technologies LLC | Olefin polymerization activators |
| EP3902808A1 (en) | 2018-12-28 | 2021-11-03 | Dow Global Technologies LLC | Curable compositions comprising unsaturated polyolefins |
| WO2020140064A1 (en) | 2018-12-28 | 2020-07-02 | Dow Global Technologies Llc | Organometallic chain transfer agents |
| KR20210121029A (ko) | 2018-12-28 | 2021-10-07 | 다우 글로벌 테크놀로지스 엘엘씨 | 텔레켈릭 폴리올레핀을 포함하는 경화성 조성물 |
| EP3902867A4 (en) | 2018-12-28 | 2022-09-14 | Dow Global Technologies LLC | CURABLE COMPOSITIONS COMPRISING UNSATURATED POLYOLEFINS |
| CN113454130A (zh) | 2018-12-28 | 2021-09-28 | 陶氏环球技术有限责任公司 | 遥爪聚烯烃和用于制备遥爪聚烯烃的方法 |
| CN113631585B (zh) | 2019-03-28 | 2023-10-20 | 陶氏环球技术有限责任公司 | 作为烯烃聚合催化剂活化剂的弱配位阴离子的第iii族阴离子络合物 |
| SG11202111068WA (en) | 2019-04-30 | 2021-11-29 | Dow Global Technologies Llc | Alkene functionalized activators |
| EP4244280A1 (en) | 2020-11-10 | 2023-09-20 | Dow Global Technologies LLC | Preparation of polyolefin-polyacrylate block copolymers additives for increasing surface energy of polyethylene |
| JP2023552056A (ja) | 2020-11-10 | 2023-12-14 | ダウ グローバル テクノロジーズ エルエルシー | ビニル末端ポリオレフィンを介した非極性-極性ブロックコポリマーの調製 |
| WO2022240932A1 (en) | 2021-05-12 | 2022-11-17 | Dow Global Technologies Llc | Rheology modified olefin-based polymer composition and method for making it |
| WO2023039514A1 (en) | 2021-09-10 | 2023-03-16 | Dow Global Technologies Llc | Hydrocarbon soluble borate cocatalysts for olefin polymerization |
| WO2023039515A2 (en) | 2021-09-10 | 2023-03-16 | Dow Global Technologies Llc | Borate cocatalysts for polyolefin production |
| CN115301291B (zh) * | 2022-08-08 | 2024-04-09 | 万华化学集团股份有限公司 | 一种异核双金属配合物自组装型mcm-56分子筛催化剂和制备方法及应用 |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2001524162A (ja) * | 1997-07-02 | 2001-11-27 | ユニオン カーバイド ケミカルズ アンド プラスティックス テクノロジー コーポレイション | オレフィンポリマー製造用触媒 |
| JP2002521500A (ja) * | 1998-07-21 | 2002-07-16 | ノバ ケミカルズ(インターナショナル)ソシエテ アノニム | 唯一つだけの活性化可能な配位子を有するシクロペンタジエニル/ホスフィンイミン触媒 |
| JP2004521168A (ja) * | 2000-12-28 | 2004-07-15 | ユニベーション・テクノロジーズ・エルエルシー | 重合触媒系、重合方法及び得られるポリマー |
| JP2005511867A (ja) * | 2001-12-18 | 2005-04-28 | ユニベーション・テクノロジーズ・エルエルシー | オレフィン重合用イミノ−アミド触媒化合物 |
Family Cites Families (70)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7163907B1 (en) | 1987-01-30 | 2007-01-16 | Exxonmobil Chemical Patents Inc. | Aluminum-free monocyclopentadienyl metallocene catalysts for olefin polymerization |
| US5153157A (en) | 1987-01-30 | 1992-10-06 | Exxon Chemical Patents Inc. | Catalyst system of enhanced productivity |
| US5064802A (en) | 1989-09-14 | 1991-11-12 | The Dow Chemical Company | Metal complex compounds |
| JP2545006B2 (ja) | 1990-07-03 | 1996-10-16 | ザ ダウ ケミカル カンパニー | 付加重合触媒 |
| US5721185A (en) | 1991-06-24 | 1998-02-24 | The Dow Chemical Company | Homogeneous olefin polymerization catalyst by abstraction with lewis acids |
| US5296433A (en) | 1992-04-14 | 1994-03-22 | Minnesota Mining And Manufacturing Company | Tris(pentafluorophenyl)borane complexes and catalysts derived therefrom |
| US5350723A (en) | 1992-05-15 | 1994-09-27 | The Dow Chemical Company | Process for preparation of monocyclopentadienyl metal complex compounds and method of use |
| WO1994000500A1 (en) | 1992-06-26 | 1994-01-06 | Exxon Chemical Patents Inc. | Solution phase polymerization process utilizing metallocene catalyst with production of olefin polymers |
| JP3453160B2 (ja) * | 1993-03-12 | 2003-10-06 | 出光石油化学株式会社 | ポリオレフィンの製造方法 |
| US5470993A (en) | 1993-06-24 | 1995-11-28 | The Dow Chemical Company | Titanium(II) or zirconium(II) complexes and addition polymerization catalysts therefrom |
| US5372682A (en) | 1993-06-24 | 1994-12-13 | The Dow Chemical Company | Electrochemical preparation of addition polymerization catalysts |
| US5625087A (en) | 1994-09-12 | 1997-04-29 | The Dow Chemical Company | Silylium cationic polymerization activators for metallocene complexes |
| CN101182365A (zh) | 1995-01-24 | 2008-05-21 | 纳幕尔杜邦公司 | α-烯烃和烯烃聚合物及其制备方法 |
| CN1214698A (zh) | 1996-03-27 | 1999-04-21 | 陶氏化学公司 | 采用分散的催化剂活化剂进行的溶液聚合方法 |
| BR9708232A (pt) | 1996-03-27 | 1999-08-03 | Dow Chemical Co | Ativador de catalisador sistema de catalisador para polimerização de alfa-olefinas e processo de polimerização |
| JP4050802B2 (ja) * | 1996-08-02 | 2008-02-20 | シチズン電子株式会社 | カラー表示装置 |
| ATE276263T1 (de) | 1996-08-08 | 2004-10-15 | Dow Global Technologies Inc | Metallkomplexe enthaltend ein an position 3 substituierte cyclopentadienylgruppe und ein olefinpolymerisationsverfahren |
| US6015868A (en) | 1996-10-03 | 2000-01-18 | The Dow Chemical Company | Substituted indenyl containing metal complexes and olefin polymerization process |
| US5783512A (en) | 1996-12-18 | 1998-07-21 | The Dow Chemical Company | Catalyst component dispersion comprising an ionic compound and solid addition polymerization catalysts containing the same |
| US5965756A (en) | 1996-12-19 | 1999-10-12 | The Dow Chemical Company | Fused ring substituted indenyl metal complexes and polymerization process |
| JP2001506260A (ja) | 1996-12-19 | 2001-05-15 | ザ ダウ ケミカル カンパニー | 3―アリール置換インデニル含有金属錯体及び重合方法 |
| ATE273329T1 (de) * | 1997-01-14 | 2004-08-15 | Du Pont | Polymerisation von olefinen |
| US6096676A (en) * | 1997-07-02 | 2000-08-01 | Union Carbide Chemicals & Plastics Technology Corporation | Catalyst for the production of olefin polymers |
| JPH1160624A (ja) * | 1997-08-19 | 1999-03-02 | Tosoh Corp | オレフィン重合用触媒およびポリオレフィンの製造方法 |
| CA2215444C (en) * | 1997-09-15 | 2005-08-02 | Stephen John Brown | Catalyst having a ketimide ligand |
| US6150297A (en) | 1997-09-15 | 2000-11-21 | The Dow Chemical Company | Cyclopentaphenanthrenyl metal complexes and polymerization process |
| US6696379B1 (en) | 1997-09-19 | 2004-02-24 | The Dow Chemical Company | Supported modified alumoxane catalyst activator |
| JPH11236409A (ja) * | 1998-02-20 | 1999-08-31 | Nippon Polyolefin Kk | オレフィン重合用触媒成分、オレフィン重合用触媒及びポリオレフィンの製造方法 |
| JP4501872B2 (ja) * | 1998-09-09 | 2010-07-14 | 住友化学株式会社 | 変性アルミニウムオキシ化合物、付加重合用触媒成分、付加重合用触媒、オレフィン重合体の製造方法、アルケニル芳香族炭化水素重合体の製造方法、および共重合体 |
| DE59904565D1 (de) * | 1998-11-25 | 2003-04-17 | Basell Polyolefine Gmbh | Verfahren zur herstellung von monoaryloxy-ansa-metallocenen |
| CA2368111A1 (en) | 1999-05-13 | 2000-11-23 | The Dow Chemical Company | Di- and tri-heteroatom substituted indenyl metal complexes |
| US6340730B1 (en) * | 1999-12-06 | 2002-01-22 | Univation Technologies, Llc | Multiple catalyst system |
| US6825295B2 (en) | 1999-12-10 | 2004-11-30 | Dow Global Technologies Inc. | Alkaryl-substituted group 4 metal complexes, catalysts and olefin polymerization process |
| CN1409729A (zh) | 1999-12-10 | 2003-04-09 | 陶氏环球技术公司 | 取代的第4族金属配合物,催化剂和烯烃聚合方法 |
| US6696380B2 (en) * | 2000-01-12 | 2004-02-24 | Darryl Stephen Williams | Procatalysts, catalyst systems, and use in olefin polymerization |
| US20020034829A1 (en) * | 2000-03-24 | 2002-03-21 | Keith Hall | Combinatorial synthesis and analysis of metal-ligand compositions using soluble metal precursors |
| DE60138708D1 (de) | 2000-06-30 | 2009-06-25 | Dow Global Technologies Inc | Polyzyklische, kondensierte ringverbindungen, meta |
| WO2002046249A2 (en) | 2000-11-07 | 2002-06-13 | Symyx Technologies, Inc. | Methods of copolymerizing ethylene and isobutylene and polymers made thereby |
| WO2002070569A1 (en) * | 2001-03-05 | 2002-09-12 | Stichting Dutch Polymer Institute | Olefin polymerization catalyst component and catalyst system and polymerization process using such a catalyst system |
| US6825147B2 (en) | 2001-05-14 | 2004-11-30 | Dow Global Technologies Inc. | 3-aryl-substituted cyclopentadienyl metal complexes and polymerization process |
| KR100440480B1 (ko) * | 2001-08-31 | 2004-07-14 | 주식회사 엘지화학 | 폴리올레핀 제조용 촉매 및 이를 이용한 폴리올레핀의제조방법 |
| US6960635B2 (en) * | 2001-11-06 | 2005-11-01 | Dow Global Technologies Inc. | Isotactic propylene copolymers, their preparation and use |
| US7199255B2 (en) * | 2001-12-18 | 2007-04-03 | Univation Technologies, Llc | Imino-amide catalysts for olefin polymerization |
| WO2003078483A1 (en) | 2002-03-14 | 2003-09-25 | Dow Global Technologies Inc. | Substituted indenyl metal complexes and polymerization process |
| AU2003216477A1 (en) | 2002-03-14 | 2003-09-29 | Dow Global Technologies Inc. | Polycyclic, fused heteroring compounds, metal complexes and polymerization process |
| AU2003225156A1 (en) | 2002-04-24 | 2003-11-10 | Symyx Technologies, Inc. | Bridged bi-aromatic ligands, complexes, catalysts and processes for polymerizing and poymers therefrom |
| WO2004024740A1 (en) | 2002-09-12 | 2004-03-25 | Dow Global Technologies Inc. | Preparation of metal complexes |
| WO2004074333A2 (en) | 2003-02-18 | 2004-09-02 | Dow Global Technologies Inc. | Process for homo- or copolymerizationof conjugated olefines |
| US6953764B2 (en) | 2003-05-02 | 2005-10-11 | Dow Global Technologies Inc. | High activity olefin polymerization catalyst and process |
| JP5086637B2 (ja) * | 2003-07-09 | 2012-11-28 | ランクセス エラストマーズ ビー.ブイ. | エチレン、α−オレフィン、およびビニルノルボルネンのモノマー単位を含むポリマーの製造方法 |
| WO2005073283A1 (en) | 2004-01-22 | 2005-08-11 | Dow Global Technologies Inc. | Functionalized elastomer compositions |
| CN1954005B (zh) | 2004-03-17 | 2012-10-10 | 陶氏环球技术有限责任公司 | 用于形成高级烯烃多嵌段共聚物的包含梭移剂的催化剂组合物 |
| KR101289564B1 (ko) * | 2004-03-17 | 2013-07-24 | 란세스 엘라스토머즈 비.브이. | 아미딘 리간드를 포함하는 중합촉매 |
| CN1976965B (zh) | 2004-03-17 | 2012-10-10 | 陶氏环球技术有限责任公司 | 用于形成乙烯多嵌段共聚物的包含梭移剂的催化剂组合物 |
| EP1725571A1 (de) * | 2004-03-17 | 2006-11-29 | Georg-August-Universität Göttingen | Sauerstoffverbrückter bimetallischer komplex, dessen herstellung und verwendung für die polymerisations-katalyse |
| US7608668B2 (en) | 2004-03-17 | 2009-10-27 | Dow Global Technologies Inc. | Ethylene/α-olefins block interpolymers |
| US7355089B2 (en) | 2004-03-17 | 2008-04-08 | Dow Global Technologies Inc. | Compositions of ethylene/α-olefin multi-block interpolymer for elastic films and laminates |
| US7915192B2 (en) | 2004-03-17 | 2011-03-29 | Dow Global Technologies Llc | Catalyst composition comprising shuttling agent for ethylene copolymer formation |
| ATE499390T1 (de) | 2004-06-22 | 2011-03-15 | Dsm Ip Assets Bv | Verfahren zur herstellung eines polymers |
| RU2007138504A (ru) | 2005-03-17 | 2009-04-27 | Дау Глобал Текнолоджиз Инк. (Us) | Композиция катализатора, содержащая челночный агент передачи кинетической цепи, предназначенная для получения регионерегулярного многоблочного сополимера |
| US7067686B1 (en) * | 2005-07-21 | 2006-06-27 | Univation Technologies, Llc | Synthesis of benzyl-metal compounds |
| US7301040B2 (en) * | 2005-08-18 | 2007-11-27 | Fina Technology, Inc. | Bidentate catalyst for olefin polymerization, methods of forming such and products therefrom |
| ES2558316T3 (es) | 2005-09-15 | 2016-02-03 | Dow Global Technologies Llc | Control de la arquitectura polimérica y distribución de pesos moleculares por medio de un agente de transporte multicentrado |
| MY157940A (en) | 2005-09-15 | 2016-08-15 | Dow Global Technologies Inc | Catalytic olefin block copolymers with controlled block sequence distribution |
| CA2622720A1 (en) | 2005-09-15 | 2007-03-29 | Dow Global Technologies Inc. | Catalytic olefin block copolymers via polymerizable shuttling agent |
| US8557921B2 (en) | 2006-08-25 | 2013-10-15 | Dow Global Technologies Llc | Production of meta-block copolymers by polymer segment interchange |
| EP2170604B1 (en) | 2007-07-13 | 2019-05-15 | Dow Global Technologies LLC | Ethylene/alpha-olefin interpolymers having low crystallinity hard blocks |
| KR101613165B1 (ko) | 2008-01-30 | 2016-04-18 | 다우 글로벌 테크놀로지스 엘엘씨 | 에틸렌/α-올레핀 블록 혼성중합체 |
| WO2010022228A2 (en) * | 2008-08-21 | 2010-02-25 | Dow Global Technologies, Inc. | Metal-ligand complexes and catalysts |
| EP3549960B1 (en) * | 2010-02-19 | 2021-03-24 | Dow Global Technologies LLC | Process for polymerizing an olefin monomer and catalyst therefor |
-
2011
- 2011-02-08 WO PCT/US2011/024012 patent/WO2011102989A1/en active Application Filing
- 2011-02-08 KR KR1020127024456A patent/KR101827023B1/ko active IP Right Grant
- 2011-02-08 CN CN201180010327.1A patent/CN102822180B/zh active Active
- 2011-02-08 US US13/023,026 patent/US8202954B2/en active Active
- 2011-02-08 EP EP11703565.9A patent/EP2536735B1/en active Active
- 2011-02-08 BR BR112012020718A patent/BR112012020718A2/pt not_active IP Right Cessation
- 2011-02-08 JP JP2012553934A patent/JP5837514B2/ja active Active
- 2011-02-08 ES ES11703565.9T patent/ES2691727T3/es active Active
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2001524162A (ja) * | 1997-07-02 | 2001-11-27 | ユニオン カーバイド ケミカルズ アンド プラスティックス テクノロジー コーポレイション | オレフィンポリマー製造用触媒 |
| JP2002521500A (ja) * | 1998-07-21 | 2002-07-16 | ノバ ケミカルズ(インターナショナル)ソシエテ アノニム | 唯一つだけの活性化可能な配位子を有するシクロペンタジエニル/ホスフィンイミン触媒 |
| JP2004521168A (ja) * | 2000-12-28 | 2004-07-15 | ユニベーション・テクノロジーズ・エルエルシー | 重合触媒系、重合方法及び得られるポリマー |
| JP2005511867A (ja) * | 2001-12-18 | 2005-04-28 | ユニベーション・テクノロジーズ・エルエルシー | オレフィン重合用イミノ−アミド触媒化合物 |
Also Published As
| Publication number | Publication date |
|---|---|
| CN102822180A (zh) | 2012-12-12 |
| CN102822180B (zh) | 2016-06-15 |
| EP2536735B1 (en) | 2018-08-01 |
| EP2536735A1 (en) | 2012-12-26 |
| WO2011102989A1 (en) | 2011-08-25 |
| BR112012020718A2 (pt) | 2016-04-26 |
| ES2691727T3 (es) | 2018-11-28 |
| JP5837514B2 (ja) | 2015-12-24 |
| KR20130008561A (ko) | 2013-01-22 |
| US8202954B2 (en) | 2012-06-19 |
| JP2013520418A (ja) | 2013-06-06 |
| US20110207902A1 (en) | 2011-08-25 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR101827023B1 (ko) | 금속-리간드 착체 및 촉매 | |
| KR101720353B1 (ko) | 금속-리간드 착체 및 촉매 | |
| KR101865645B1 (ko) | 중합성 올레핀의 중합 방법 및 그를 위한 촉매 | |
| EP3160973B1 (en) | Catalyst systems for olefin polymerization | |
| EP3161021B1 (en) | Process for olefin polymerization | |
| KR101854480B1 (ko) | 올레핀 단량체의 중합 방법 및 이를 위한 촉매 | |
| EP2473538B1 (en) | Catalyst and process for polymerizing an olefin and polyolefin prepared thereby | |
| EP3436486B1 (en) | Olefin polymerization catalyst systems and methods of use thereof | |
| KR102592636B1 (ko) | 개선된 용해도를 위한 금속 상에 두 개의 메틸렌트리알킬규소 리간드를 갖는 비스-페닐-페녹시 폴리올레핀 촉매 | |
| JP7053589B2 (ja) | チオ尿素第4族遷移金属触媒および重合系 | |
| US10138257B2 (en) | Transition metal complexes, production and use thereof | |
| KR102590976B1 (ko) | 개선된 용해도를 위한 금속 상에 메틸렌트리알킬규소 리간드를 갖는 비스-페닐-페녹시 폴리올레핀 촉매 | |
| JP7208981B2 (ja) | 溶解度を改善するために金属上にアルコキシ-またはアミド-配位子を有するビス-フェニル-フェノキシポリオレフィン触媒 | |
| JP2023512637A (ja) | 第iii族及びランタニドビス-フェニル-フェノキシ金属-配位子錯体及び連鎖移動剤を含む重合プロセス | |
| JP2019530771A (ja) | チオグアニジン第iv族遷移金属触媒および重合系 | |
| US9598444B2 (en) | Transition metal complexes of tridentate dianionic CNN ligands, production and use thereof | |
| WO2018038880A1 (en) | Transition metal complexes, production and use thereof | |
| CN112533964A (zh) | 双齿唑基氨基金属-配体络合物和烯烃聚合催化剂 | |
| KR20210107735A (ko) | 올레핀 중합을 위한 헤테로고리-헤테로고리계 제iv족 전이 금속 촉매 | |
| WO2017003565A1 (en) | Transition metal complexes of tridentate dianionic cnn ligands, production and use thereof |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A201 | Request for examination | ||
| E701 | Decision to grant or registration of patent right | ||
| GRNT | Written decision to grant |