JP6037486B2 - 非水性電解液及びこれを含むリチウム二次電池 - Google Patents
非水性電解液及びこれを含むリチウム二次電池 Download PDFInfo
- Publication number
- JP6037486B2 JP6037486B2 JP2015520082A JP2015520082A JP6037486B2 JP 6037486 B2 JP6037486 B2 JP 6037486B2 JP 2015520082 A JP2015520082 A JP 2015520082A JP 2015520082 A JP2015520082 A JP 2015520082A JP 6037486 B2 JP6037486 B2 JP 6037486B2
- Authority
- JP
- Japan
- Prior art keywords
- lithium
- aqueous electrolyte
- carbonate
- lithium secondary
- negative electrode
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 229910052744 lithium Inorganic materials 0.000 title claims description 85
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 title claims description 84
- 239000011255 nonaqueous electrolyte Substances 0.000 title claims description 29
- RUOJZAUFBMNUDX-UHFFFAOYSA-N propylene carbonate Chemical compound CC1COC(=O)O1 RUOJZAUFBMNUDX-UHFFFAOYSA-N 0.000 claims description 32
- JBTWLSYIZRCDFO-UHFFFAOYSA-N ethyl methyl carbonate Chemical compound CCOC(=O)OC JBTWLSYIZRCDFO-UHFFFAOYSA-N 0.000 claims description 30
- 239000011356 non-aqueous organic solvent Substances 0.000 claims description 23
- 229910013870 LiPF 6 Inorganic materials 0.000 claims description 21
- FKRCODPIKNYEAC-UHFFFAOYSA-N ethyl propionate Chemical group CCOC(=O)CC FKRCODPIKNYEAC-UHFFFAOYSA-N 0.000 claims description 20
- 239000000203 mixture Substances 0.000 claims description 17
- 229910003002 lithium salt Inorganic materials 0.000 claims description 16
- 159000000002 lithium salts Chemical class 0.000 claims description 16
- 238000002156 mixing Methods 0.000 claims description 11
- 239000008151 electrolyte solution Substances 0.000 claims description 8
- ZPFAVCIQZKRBGF-UHFFFAOYSA-N 1,3,2-dioxathiolane 2,2-dioxide Chemical compound O=S1(=O)OCCO1 ZPFAVCIQZKRBGF-UHFFFAOYSA-N 0.000 claims description 6
- 229910013063 LiBF 4 Inorganic materials 0.000 claims description 5
- IEJIGPNLZYLLBP-UHFFFAOYSA-N dimethyl carbonate Chemical compound COC(=O)OC IEJIGPNLZYLLBP-UHFFFAOYSA-N 0.000 claims description 5
- ZZXUZKXVROWEIF-UHFFFAOYSA-N 1,2-butylene carbonate Chemical compound CCC1COC(=O)O1 ZZXUZKXVROWEIF-UHFFFAOYSA-N 0.000 claims description 4
- OIFBSDVPJOWBCH-UHFFFAOYSA-N Diethyl carbonate Chemical compound CCOC(=O)OCC OIFBSDVPJOWBCH-UHFFFAOYSA-N 0.000 claims description 4
- VUPKGFBOKBGHFZ-UHFFFAOYSA-N dipropyl carbonate Chemical compound CCCOC(=O)OCCC VUPKGFBOKBGHFZ-UHFFFAOYSA-N 0.000 claims description 4
- KKQAVHGECIBFRQ-UHFFFAOYSA-N methyl propyl carbonate Chemical compound CCCOC(=O)OC KKQAVHGECIBFRQ-UHFFFAOYSA-N 0.000 claims description 4
- 150000001875 compounds Chemical class 0.000 claims description 3
- OKVJWADVFPXWQD-UHFFFAOYSA-N difluoroborinic acid Chemical compound OB(F)F OKVJWADVFPXWQD-UHFFFAOYSA-N 0.000 claims description 3
- 125000003431 oxalo group Chemical group 0.000 claims description 3
- 229910015015 LiAsF 6 Inorganic materials 0.000 claims description 2
- 229910013372 LiC 4 Inorganic materials 0.000 claims description 2
- 229910013684 LiClO 4 Inorganic materials 0.000 claims description 2
- 229910012513 LiSbF 6 Inorganic materials 0.000 claims description 2
- ACFSQHQYDZIPRL-UHFFFAOYSA-N lithium;bis(1,1,2,2,2-pentafluoroethylsulfonyl)azanide Chemical compound [Li+].FC(F)(F)C(F)(F)S(=O)(=O)[N-]S(=O)(=O)C(F)(F)C(F)(F)F ACFSQHQYDZIPRL-UHFFFAOYSA-N 0.000 claims description 2
- CYEDOLFRAIXARV-UHFFFAOYSA-N ethyl propyl carbonate Chemical compound CCCOC(=O)OCC CYEDOLFRAIXARV-UHFFFAOYSA-N 0.000 claims 1
- 230000000052 comparative effect Effects 0.000 description 37
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 32
- 229910052799 carbon Inorganic materials 0.000 description 22
- 238000003860 storage Methods 0.000 description 21
- 239000010408 film Substances 0.000 description 17
- HBBGRARXTFLTSG-UHFFFAOYSA-N Lithium ion Chemical compound [Li+] HBBGRARXTFLTSG-UHFFFAOYSA-N 0.000 description 12
- 239000003792 electrolyte Substances 0.000 description 12
- 229910001416 lithium ion Inorganic materials 0.000 description 12
- 239000007773 negative electrode material Substances 0.000 description 11
- PXHVJJICTQNCMI-UHFFFAOYSA-N nickel Substances [Ni] PXHVJJICTQNCMI-UHFFFAOYSA-N 0.000 description 11
- -1 LiPF 6 Chemical class 0.000 description 9
- SECXISVLQFMRJM-UHFFFAOYSA-N N-Methylpyrrolidone Chemical compound CN1CCCC1=O SECXISVLQFMRJM-UHFFFAOYSA-N 0.000 description 9
- 230000014759 maintenance of location Effects 0.000 description 8
- 239000002904 solvent Substances 0.000 description 8
- 238000002474 experimental method Methods 0.000 description 7
- 239000007774 positive electrode material Substances 0.000 description 7
- 238000006243 chemical reaction Methods 0.000 description 6
- 239000006258 conductive agent Substances 0.000 description 6
- 238000000354 decomposition reaction Methods 0.000 description 6
- 230000000694 effects Effects 0.000 description 6
- 229910052782 aluminium Inorganic materials 0.000 description 5
- 239000011230 binding agent Substances 0.000 description 5
- 238000007599 discharging Methods 0.000 description 5
- 239000010410 layer Substances 0.000 description 5
- 238000000034 method Methods 0.000 description 5
- 239000002002 slurry Substances 0.000 description 5
- 239000000126 substance Substances 0.000 description 5
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 4
- VGGSQFUCUMXWEO-UHFFFAOYSA-N Ethene Chemical compound C=C VGGSQFUCUMXWEO-UHFFFAOYSA-N 0.000 description 4
- 239000005977 Ethylene Substances 0.000 description 4
- 239000002033 PVDF binder Substances 0.000 description 4
- RTAQQCXQSZGOHL-UHFFFAOYSA-N Titanium Chemical compound [Ti] RTAQQCXQSZGOHL-UHFFFAOYSA-N 0.000 description 4
- 239000000654 additive Substances 0.000 description 4
- 230000000996 additive effect Effects 0.000 description 4
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 4
- 229920001577 copolymer Polymers 0.000 description 4
- 239000010949 copper Substances 0.000 description 4
- 150000002500 ions Chemical class 0.000 description 4
- 229910021450 lithium metal oxide Inorganic materials 0.000 description 4
- 239000011572 manganese Substances 0.000 description 4
- 238000004519 manufacturing process Methods 0.000 description 4
- 229910052759 nickel Inorganic materials 0.000 description 4
- 229920002981 polyvinylidene fluoride Polymers 0.000 description 4
- 238000007086 side reaction Methods 0.000 description 4
- 229910001220 stainless steel Inorganic materials 0.000 description 4
- 239000010935 stainless steel Substances 0.000 description 4
- 239000002344 surface layer Substances 0.000 description 4
- 239000010936 titanium Substances 0.000 description 4
- 229910052719 titanium Inorganic materials 0.000 description 4
- BVKZGUZCCUSVTD-UHFFFAOYSA-L Carbonate Chemical compound [O-]C([O-])=O BVKZGUZCCUSVTD-UHFFFAOYSA-L 0.000 description 3
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 3
- 239000002000 Electrolyte additive Substances 0.000 description 3
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 3
- 239000011149 active material Substances 0.000 description 3
- 239000006229 carbon black Substances 0.000 description 3
- 229910052802 copper Inorganic materials 0.000 description 3
- 239000000835 fiber Substances 0.000 description 3
- 229910002804 graphite Inorganic materials 0.000 description 3
- 239000010439 graphite Substances 0.000 description 3
- 230000001965 increasing effect Effects 0.000 description 3
- 230000002427 irreversible effect Effects 0.000 description 3
- 239000004745 nonwoven fabric Substances 0.000 description 3
- 238000007254 oxidation reaction Methods 0.000 description 3
- 230000008961 swelling Effects 0.000 description 3
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 2
- 229920002943 EPDM rubber Polymers 0.000 description 2
- KMTRUDSVKNLOMY-UHFFFAOYSA-N Ethylene carbonate Chemical group O=C1OCCO1 KMTRUDSVKNLOMY-UHFFFAOYSA-N 0.000 description 2
- 229910013716 LiNi Inorganic materials 0.000 description 2
- WMFOQBRAJBCJND-UHFFFAOYSA-M Lithium hydroxide Chemical compound [Li+].[OH-] WMFOQBRAJBCJND-UHFFFAOYSA-M 0.000 description 2
- RJUFJBKOKNCXHH-UHFFFAOYSA-N Methyl propionate Chemical compound CCC(=O)OC RJUFJBKOKNCXHH-UHFFFAOYSA-N 0.000 description 2
- BQCADISMDOOEFD-UHFFFAOYSA-N Silver Chemical compound [Ag] BQCADISMDOOEFD-UHFFFAOYSA-N 0.000 description 2
- XLOMVQKBTHCTTD-UHFFFAOYSA-N Zinc monoxide Chemical compound [Zn]=O XLOMVQKBTHCTTD-UHFFFAOYSA-N 0.000 description 2
- 229910003481 amorphous carbon Inorganic materials 0.000 description 2
- 229910021383 artificial graphite Inorganic materials 0.000 description 2
- 239000002131 composite material Substances 0.000 description 2
- 150000002148 esters Chemical class 0.000 description 2
- QKBJDEGZZJWPJA-UHFFFAOYSA-N ethyl propyl carbonate Chemical compound [CH2]COC(=O)OCCC QKBJDEGZZJWPJA-UHFFFAOYSA-N 0.000 description 2
- 238000004299 exfoliation Methods 0.000 description 2
- 239000006260 foam Substances 0.000 description 2
- 239000011888 foil Substances 0.000 description 2
- 230000008014 freezing Effects 0.000 description 2
- 238000007710 freezing Methods 0.000 description 2
- 230000001939 inductive effect Effects 0.000 description 2
- 238000009830 intercalation Methods 0.000 description 2
- MLFHJEHSLIIPHL-UHFFFAOYSA-N isoamyl acetate Chemical compound CC(C)CCOC(C)=O MLFHJEHSLIIPHL-UHFFFAOYSA-N 0.000 description 2
- 229910052751 metal Inorganic materials 0.000 description 2
- 239000002184 metal Substances 0.000 description 2
- TZIHFWKZFHZASV-UHFFFAOYSA-N methyl formate Chemical compound COC=O TZIHFWKZFHZASV-UHFFFAOYSA-N 0.000 description 2
- 229940017219 methyl propionate Drugs 0.000 description 2
- 239000003960 organic solvent Substances 0.000 description 2
- 229920000642 polymer Polymers 0.000 description 2
- 229920006254 polymer film Polymers 0.000 description 2
- 229920000098 polyolefin Polymers 0.000 description 2
- 229910052709 silver Inorganic materials 0.000 description 2
- 239000004332 silver Substances 0.000 description 2
- 239000010409 thin film Substances 0.000 description 2
- HNAGHMKIPMKKBB-UHFFFAOYSA-N 1-benzylpyrrolidine-3-carboxamide Chemical compound C1C(C(=O)N)CCN1CC1=CC=CC=C1 HNAGHMKIPMKKBB-UHFFFAOYSA-N 0.000 description 1
- 229920000049 Carbon (fiber) Polymers 0.000 description 1
- 229920002134 Carboxymethyl cellulose Polymers 0.000 description 1
- 229910000925 Cd alloy Inorganic materials 0.000 description 1
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 1
- 229920002153 Hydroxypropyl cellulose Polymers 0.000 description 1
- JGFBQFKZKSSODQ-UHFFFAOYSA-N Isothiocyanatocyclopropane Chemical compound S=C=NC1CC1 JGFBQFKZKSSODQ-UHFFFAOYSA-N 0.000 description 1
- 229910000733 Li alloy Inorganic materials 0.000 description 1
- 229910003543 Li(Ni0.33Co0.33Mn0.33)O2 Inorganic materials 0.000 description 1
- 229910013733 LiCo Inorganic materials 0.000 description 1
- 229910012851 LiCoO 2 Inorganic materials 0.000 description 1
- 229910015644 LiMn 2 - z Ni Inorganic materials 0.000 description 1
- 229910015643 LiMn 2 O 4 Inorganic materials 0.000 description 1
- 229910015676 LiMn 2-z Co Inorganic materials 0.000 description 1
- 229910014689 LiMnO Inorganic materials 0.000 description 1
- 229910013290 LiNiO 2 Inorganic materials 0.000 description 1
- 229910013872 LiPF Inorganic materials 0.000 description 1
- 101150058243 Lipf gene Proteins 0.000 description 1
- 239000004698 Polyethylene Substances 0.000 description 1
- 229920000265 Polyparaphenylene Polymers 0.000 description 1
- 239000004743 Polypropylene Substances 0.000 description 1
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 1
- XBDQKXXYIPTUBI-UHFFFAOYSA-M Propionate Chemical compound CCC([O-])=O XBDQKXXYIPTUBI-UHFFFAOYSA-M 0.000 description 1
- 229920002125 Sokalan® Polymers 0.000 description 1
- 229920002472 Starch Polymers 0.000 description 1
- GWEVSGVZZGPLCZ-UHFFFAOYSA-N Titan oxide Chemical compound O=[Ti]=O GWEVSGVZZGPLCZ-UHFFFAOYSA-N 0.000 description 1
- VIEVWNYBKMKQIH-UHFFFAOYSA-N [Co]=O.[Mn].[Li] Chemical compound [Co]=O.[Mn].[Li] VIEVWNYBKMKQIH-UHFFFAOYSA-N 0.000 description 1
- KXKVLQRXCPHEJC-UHFFFAOYSA-N acetic acid trimethyl ester Natural products COC(C)=O KXKVLQRXCPHEJC-UHFFFAOYSA-N 0.000 description 1
- 239000006230 acetylene black Substances 0.000 description 1
- AZDRQVAHHNSJOQ-UHFFFAOYSA-N alumane Chemical compound [AlH3] AZDRQVAHHNSJOQ-UHFFFAOYSA-N 0.000 description 1
- OBNCKNCVKJNDBV-UHFFFAOYSA-N butanoic acid ethyl ester Natural products CCCC(=O)OCC OBNCKNCVKJNDBV-UHFFFAOYSA-N 0.000 description 1
- IAQRGUVFOMOMEM-UHFFFAOYSA-N butene Natural products CC=CC IAQRGUVFOMOMEM-UHFFFAOYSA-N 0.000 description 1
- PWLNAUNEAKQYLH-UHFFFAOYSA-N butyric acid octyl ester Natural products CCCCCCCCOC(=O)CCC PWLNAUNEAKQYLH-UHFFFAOYSA-N 0.000 description 1
- 239000004917 carbon fiber Substances 0.000 description 1
- 239000006231 channel black Substances 0.000 description 1
- 239000003610 charcoal Substances 0.000 description 1
- 238000004581 coalescence Methods 0.000 description 1
- 239000011248 coating agent Substances 0.000 description 1
- 238000000576 coating method Methods 0.000 description 1
- 239000004020 conductor Substances 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- 230000007423 decrease Effects 0.000 description 1
- 238000009831 deintercalation Methods 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 238000001035 drying Methods 0.000 description 1
- 239000011267 electrode slurry Substances 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 239000003759 ester based solvent Substances 0.000 description 1
- 229920001973 fluoroelastomer Polymers 0.000 description 1
- 239000006232 furnace black Substances 0.000 description 1
- 239000003365 glass fiber Substances 0.000 description 1
- 229920001519 homopolymer Polymers 0.000 description 1
- 239000001863 hydroxypropyl cellulose Substances 0.000 description 1
- 235000010977 hydroxypropyl cellulose Nutrition 0.000 description 1
- 238000003780 insertion Methods 0.000 description 1
- 230000037431 insertion Effects 0.000 description 1
- 239000012212 insulator Substances 0.000 description 1
- 229940117955 isoamyl acetate Drugs 0.000 description 1
- JMMWKPVZQRWMSS-UHFFFAOYSA-N isopropanol acetate Natural products CC(C)OC(C)=O JMMWKPVZQRWMSS-UHFFFAOYSA-N 0.000 description 1
- 229940011051 isopropyl acetate Drugs 0.000 description 1
- GWYFCOCPABKNJV-UHFFFAOYSA-N isovaleric acid Chemical compound CC(C)CC(O)=O GWYFCOCPABKNJV-UHFFFAOYSA-N 0.000 description 1
- 239000003273 ketjen black Substances 0.000 description 1
- 239000006233 lamp black Substances 0.000 description 1
- 239000001989 lithium alloy Substances 0.000 description 1
- 229910002102 lithium manganese oxide Inorganic materials 0.000 description 1
- FRMOHNDAXZZWQI-UHFFFAOYSA-N lithium manganese(2+) nickel(2+) oxygen(2-) Chemical compound [O-2].[Mn+2].[Ni+2].[Li+] FRMOHNDAXZZWQI-UHFFFAOYSA-N 0.000 description 1
- VGYDTVNNDKLMHX-UHFFFAOYSA-N lithium;manganese;nickel;oxocobalt Chemical compound [Li].[Mn].[Ni].[Co]=O VGYDTVNNDKLMHX-UHFFFAOYSA-N 0.000 description 1
- VLXXBCXTUVRROQ-UHFFFAOYSA-N lithium;oxido-oxo-(oxomanganiooxy)manganese Chemical compound [Li+].[O-][Mn](=O)O[Mn]=O VLXXBCXTUVRROQ-UHFFFAOYSA-N 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 238000002844 melting Methods 0.000 description 1
- 230000008018 melting Effects 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- VNWKTOKETHGBQD-UHFFFAOYSA-N methane Chemical compound C VNWKTOKETHGBQD-UHFFFAOYSA-N 0.000 description 1
- 239000012046 mixed solvent Substances 0.000 description 1
- UUIQMZJEGPQKFD-UHFFFAOYSA-N n-butyric acid methyl ester Natural products CCCC(=O)OC UUIQMZJEGPQKFD-UHFFFAOYSA-N 0.000 description 1
- 229910021382 natural graphite Inorganic materials 0.000 description 1
- 229920003229 poly(methyl methacrylate) Polymers 0.000 description 1
- 229920005569 poly(vinylidene fluoride-co-hexafluoropropylene) Polymers 0.000 description 1
- 239000004584 polyacrylic acid Substances 0.000 description 1
- 229920002239 polyacrylonitrile Polymers 0.000 description 1
- 229920000573 polyethylene Polymers 0.000 description 1
- 229920000139 polyethylene terephthalate Polymers 0.000 description 1
- 239000005020 polyethylene terephthalate Substances 0.000 description 1
- 229920005596 polymer binder Polymers 0.000 description 1
- 239000002491 polymer binding agent Substances 0.000 description 1
- 239000004926 polymethyl methacrylate Substances 0.000 description 1
- 229920001155 polypropylene Polymers 0.000 description 1
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 1
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 1
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 1
- 229910052700 potassium Inorganic materials 0.000 description 1
- 239000011591 potassium Substances 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 229920001384 propylene homopolymer Polymers 0.000 description 1
- 239000004627 regenerated cellulose Substances 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 239000007784 solid electrolyte Substances 0.000 description 1
- 229910052596 spinel Inorganic materials 0.000 description 1
- 239000011029 spinel Substances 0.000 description 1
- 239000008107 starch Substances 0.000 description 1
- 235000019698 starch Nutrition 0.000 description 1
- 229920003048 styrene butadiene rubber Polymers 0.000 description 1
- 229920005608 sulfonated EPDM Polymers 0.000 description 1
- 238000012360 testing method Methods 0.000 description 1
- BFKJFAAPBSQJPD-UHFFFAOYSA-N tetrafluoroethene Chemical group FC(F)=C(F)F BFKJFAAPBSQJPD-UHFFFAOYSA-N 0.000 description 1
- TXEYQDLBPFQVAA-UHFFFAOYSA-N tetrafluoromethane Chemical compound FC(F)(F)F TXEYQDLBPFQVAA-UHFFFAOYSA-N 0.000 description 1
- 239000006234 thermal black Substances 0.000 description 1
- LLZRNZOLAXHGLL-UHFFFAOYSA-J titanic acid Chemical compound O[Ti](O)(O)O LLZRNZOLAXHGLL-UHFFFAOYSA-J 0.000 description 1
- OGIDPMRJRNCKJF-UHFFFAOYSA-N titanium oxide Inorganic materials [Ti]=O OGIDPMRJRNCKJF-UHFFFAOYSA-N 0.000 description 1
- 229920002554 vinyl polymer Polymers 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 1
- 239000011787 zinc oxide Substances 0.000 description 1
Images
Classifications
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/056—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes
- H01M10/0564—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes the electrolyte being constituted of organic materials only
- H01M10/0566—Liquid materials
- H01M10/0567—Liquid materials characterised by the additives
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/052—Li-accumulators
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/056—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes
- H01M10/0564—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes the electrolyte being constituted of organic materials only
- H01M10/0566—Liquid materials
- H01M10/0568—Liquid materials characterised by the solutes
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/056—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes
- H01M10/0564—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes the electrolyte being constituted of organic materials only
- H01M10/0566—Liquid materials
- H01M10/0569—Liquid materials characterised by the solvents
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/10—Energy storage using batteries
Description
[非水性電解液の製造]
プロピレンカーボネート(PC):エチルプロピオネート(EP):ジメチルカーボネート(DMC)=2:4:4(重量比)の組成を有する非水性有機溶媒に、非水性電解液総量を基準にLiPF60.1mole/l及びリチウムビスフルオロスルホニルイミド0.9mole/lを添加して非水性電解液を製造した。
正極活物質として、Li(Ni0.33Co0.33Mn0.33)O2の混合物89重量%、導電剤としてカーボンブラック(carbon black)8重量%、バインダとしてポリビニリデンフルオライド(PVdF)3重量%を溶媒であるN−メチル−2−ピロリドン(NMP)に添加して正極混合物スラリーを製造した。前記正極混合物スラリーを厚さが20μm程度の正極集電体であるアルミニウム(Al)薄膜に塗布し、乾燥して正極を製造した後、ロールプレス(roll press)を行って正極を製造した。
前記リチウム塩を、非水性電解液総量を基準にLiPF60.14mole/l及びリチウムビスフルオロスルホニルイミド0.86mole/l(約1:6のモル比)を用いたことを除いては、実施例1と同一にして非水性電解液及びリチウム二次電池を製造した。
LiPF6 0.17mole/l及びリチウムビスフルオロスルホニルイミド0.83mole/l(約1:5のモル比)を用いたことを除いては、実施例1と同一にして非水性電解液及びリチウム二次電池を製造した。
プロピレンカーボネート(PC):エチルメチルカーボネート(EMC):ジメチルカーボネート(DMC)=3:3:4(重量比)の組成を有する非水性有機溶媒を用いたことを除いては、実施例1と同一にして非水性電解液及びリチウム二次電池を製造した。
エチレンカーボネート(EC):エチルメチルカーボネート(EMC):ジメチルカーボネート(DMC)=3:3:4(重量比)の組成を有する非水性有機溶媒を用いたことを除いては、実施例1と同一にして非水性電解液及びリチウム二次電池を製造した。
リチウム塩としてLiPF6を単独に用いたことを除いては、実施例1と同一に行って非水性電解液及びリチウム二次電池を製造した。
LiPF6及びリチウムビスフルオロスルホニルイミドを約1:0.5のモル比を用いたことを除いては、実施例1と同一にして非水性電解液及びリチウム二次電池を製造した。
<LiPF6及びLiFSIのモル比による低温出力特性の実験>
実施例1から3、及び比較例1、3及び4のリチウム二次電池を、−30℃でSOC(充電深度)別に、0.5Cで10秒間放電して発生する電圧差で低温出力を計算した。その結果を図1に示す。
<リチウム二次電池の高温サイクル特性の実験>
実施例1から3、及び比較例1、3及び4のリチウム二次電池を45℃にける定電流/定電圧(CC/CV)条件で、4.2V/38mAまで1Cで充電した後、定電流(CC)条件で3.03Vまで3Cで放電し、その放電容量を測定した。これを1から1000サイクルで繰り返して行っており、測定した放電容量を図2に示した。
<LiPF6及びLiFSIのモル比による高温貯蔵後の出力特性実験>
実施例1から3、及び比較例1、3及び4のリチウム二次電池を60℃で貯蔵した後に、定電流/定電圧(CC/CV)条件で4.2V/38mAまで1Cで充電した後、定電流(CC)条件で3.0Vまで1Cで放電し、その放電容量を測定した。その結果を図3に示した。
<初期常温出力特性の実験>
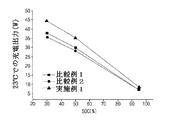
有機溶媒の種類による出力特性試験を評価するため、実施例1、及び比較例1と2のリチウム二次電池を、23℃でSOC(充電深度)別に、0.5Cで10秒間放電して発生する電圧差により常温出力を計算した。その結果を図4a及び図4bに示す。図4aはSOC(%)に応じる23℃での放電出力(W)の結果を示したものであり、図4bはSOC(%)に応じる23℃での充電出力(W)の結果を示したものである。
<高温貯蔵後の容量特性の実験>
実施例1、及び比較例1と2のリチウム二次電池を、定電流/定電圧(CC/CV)条件で4.2V/38mAまで1Cで充電した後、定電流(CC)条件で3.0Vまで1Cで放電し、その放電容量を測定した。その結果を図5に示す。
Claims (7)
- i)プロピレンカーボネート(PC)及びエステル系溶媒を含む非水性有機溶媒;及び
ii)リチウムビスフルオロスルホニルイミド(Lithium bis(fluorosulfonyl)imide;LiFSI)及びリチウム塩を含み、
前記エステル系溶媒はエチルプロピオネート(ethyl propionate)であり、
前記プロピレンカーボネートとエステル系溶媒の混合比は、1:1から2.5重量比であり、
前記リチウム塩とリチウムビスフルオロスルホニルイミドの混合比は、モル比として1:6から9であり、
LiBF 4 、リチウムオキサリルジフルオロボレート(LiODFB)及びエチレンサルフェート(ESa)からなる群より選択される2種以上の化合物をさらに含むことを特徴とする非水性電解液。 - 前記リチウムビスフルオロスルホニルイミドは、非水性電解液中の濃度が0.1mole/lから2mole/lであることを特徴とする請求項1に記載の非水性電解液。
- 前記エステル系溶媒の含量は、非水性有機溶媒100重量部を基準に10重量部から70重量部であることを特徴とする請求項1に記載の非水性電解液。
- 前記エステル系溶媒の含量は、非水性有機溶媒100重量部を基準に20重量部から50重量部であることを特徴とする請求項3に記載の非水性電解液。
- 前記非水性有機溶媒は、ブチレンカーボネート(BC)、ジメチルカーボネート(DMC)、ジエチルカーボネート(DEC)、ジプロピルカーボネート(DPC)、エチルメチルカーボネート(EMC)、メチルプロピルカーボネート(MPC)、及びエチルプロピルカーボネート(EPC)からなる群より選択されるいずれか一つ、またはこれらのうち2種以上の混合物をさらに含むことを特徴とする請求項1に記載の非水性電解液。
- 前記リチウム塩は、LiPF6、LiBF4、LiSbF6、LiAsF6、LiClO4、LiN(C2F5SO2)2、LiN(CF3SO2)2、CF3SO3Li、LiC(CF3SO2)3及びLiC4BO8からなる群より選択されるいずれか一つ、またはこれらのうち2種以上の混合物であることを特徴とする請求項1に記載の非水性電解液。
- 正極、負極、前記正極と前記負極との間に介在されたセパレータ、及び請求項1に記載の非水性電解液を含むリチウム二次電池。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR10-2013-0059920 | 2013-05-27 | ||
| KR20130059920 | 2013-05-27 | ||
| PCT/KR2014/004731 WO2014193148A1 (ko) | 2013-05-27 | 2014-05-27 | 비수성 전해액 및 이를 포함하는 리튬 이차전지 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2015522924A JP2015522924A (ja) | 2015-08-06 |
| JP6037486B2 true JP6037486B2 (ja) | 2016-12-07 |
Family
ID=51989104
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2015520082A Active JP6037486B2 (ja) | 2013-05-27 | 2014-05-27 | 非水性電解液及びこれを含むリチウム二次電池 |
Country Status (6)
| Country | Link |
|---|---|
| EP (1) | EP2846393B1 (ja) |
| JP (1) | JP6037486B2 (ja) |
| KR (1) | KR101605957B1 (ja) |
| CN (1) | CN104604014B (ja) |
| TW (1) | TWI548133B (ja) |
| WO (1) | WO2014193148A1 (ja) |
Families Citing this family (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP6296597B2 (ja) * | 2013-10-16 | 2018-03-20 | 学校法人 関西大学 | リチウムイオン二次電池 |
| JP6750196B2 (ja) * | 2015-07-09 | 2020-09-02 | 株式会社豊田中央研究所 | 非水系リチウム電池及びその使用方法 |
| WO2017057968A1 (ko) * | 2015-09-30 | 2017-04-06 | 주식회사 엘지화학 | 비수성 전해액 및 이를 포함하는 리튬 이차전지 |
| KR101992124B1 (ko) | 2015-09-30 | 2019-06-25 | 주식회사 엘지화학 | 비수성 전해액 및 이를 포함하는 리튬 이차전지 |
| JP6876369B2 (ja) * | 2016-01-15 | 2021-05-26 | 株式会社日本触媒 | リチウムイオン二次電池 |
| WO2017130245A1 (ja) * | 2016-01-25 | 2017-08-03 | パナソニックIpマネジメント株式会社 | リチウム電池 |
| JP2017191740A (ja) * | 2016-04-15 | 2017-10-19 | 国立大学法人 東京大学 | リチウムイオン二次電池 |
| KR102640842B1 (ko) * | 2016-06-09 | 2024-02-27 | 삼성에스디아이 주식회사 | 리튬전지 |
| US11489203B2 (en) * | 2018-07-04 | 2022-11-01 | Lg Energy Solution, Ltd. | Electrolyte for lithium secondary battery and lithium secondary battery including same |
| WO2020158299A1 (ja) * | 2019-01-31 | 2020-08-06 | パナソニックIpマネジメント株式会社 | 非水電解質二次電池およびこれに用いる電解液 |
| JP7152965B2 (ja) * | 2019-02-18 | 2022-10-13 | 株式会社豊田中央研究所 | 蓄電デバイス |
| CN112164826A (zh) * | 2020-09-29 | 2021-01-01 | 中国科学院长春应用化学研究所 | 一种双离子电池低温型电解液以及一种双离子电池 |
| CN113346095A (zh) * | 2021-05-17 | 2021-09-03 | 上海超碳石墨烯产业技术有限公司 | 一种具有耐高温系统的扣式电池 |
Family Cites Families (17)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7709157B2 (en) * | 2002-10-23 | 2010-05-04 | Panasonic Corporation | Non-aqueous electrolyte secondary battery and electrolyte for the same |
| JP4847675B2 (ja) * | 2002-10-23 | 2011-12-28 | パナソニック株式会社 | 非水電解質二次電池およびそれに用いる電解質 |
| US20080057403A1 (en) * | 2006-09-06 | 2008-03-06 | Issaev Nikolai N | Lithium cell |
| KR20090003921A (ko) * | 2007-07-05 | 2009-01-12 | 삼성전자주식회사 | 냉장고 |
| KR101033697B1 (ko) * | 2007-10-17 | 2011-05-09 | 주식회사 엘지화학 | 리튬이차전지용 전해액 첨가제, 상기 전해액 첨가제를포함하는 비수성 전해액 및 리튬이차전지 |
| JP5125559B2 (ja) * | 2008-02-04 | 2013-01-23 | 株式会社Gsユアサ | 非水電解質電池及びその製造方法 |
| FR2948232B1 (fr) * | 2009-07-16 | 2011-08-26 | Commissariat Energie Atomique | Electrolyte liquide pour accumulateur au lithium, comprenant un melange de solvants organiques non aqueux |
| JP5678539B2 (ja) | 2009-09-29 | 2015-03-04 | 三菱化学株式会社 | 非水系電解液電池 |
| WO2011052605A1 (ja) * | 2009-10-27 | 2011-05-05 | 旭硝子株式会社 | 二次電池用非水電解液および二次電池 |
| CN102074734A (zh) * | 2010-09-30 | 2011-05-25 | 张家港市国泰华荣化工新材料有限公司 | 一种含氟磺酰亚胺锂锂盐的电解质溶液及其用途 |
| KR101165535B1 (ko) * | 2010-10-06 | 2012-07-16 | 삼성에스디아이 주식회사 | 리튬 이차전지용 전해액 및 이를 포함하는 리튬 이차전지 |
| US9123973B2 (en) * | 2010-12-22 | 2015-09-01 | Samsung Sdi Co., Ltd. | Electrolyte for lithium secondary battery and lithium secondary battery comprising the same |
| CN102544570A (zh) * | 2010-12-31 | 2012-07-04 | 张家港市国泰华荣化工新材料有限公司 | 一种含氟磺酰亚胺锂的非水电解质溶液的锂硫电池 |
| KR101233325B1 (ko) * | 2011-04-11 | 2013-02-14 | 로베르트 보쉬 게엠베하 | 리튬 이차 전지용 전해액 및 이를 포함하는 리튬 이차 전지 |
| JP6065367B2 (ja) * | 2011-06-07 | 2017-01-25 | ソニー株式会社 | 非水電解質電池、電池パック、電子機器、電動車両、蓄電装置および電力システム |
| CN102952099B (zh) * | 2011-08-30 | 2015-05-06 | 海洋王照明科技股份有限公司 | 吡咯类离子液体及其制备方法和应用 |
| JP2013084592A (ja) * | 2011-09-26 | 2013-05-09 | Nippon Shokubai Co Ltd | アルカリ金属電池 |
-
2014
- 2014-05-27 KR KR1020140063806A patent/KR101605957B1/ko active IP Right Grant
- 2014-05-27 TW TW103118427A patent/TWI548133B/zh active
- 2014-05-27 JP JP2015520082A patent/JP6037486B2/ja active Active
- 2014-05-27 EP EP14795932.4A patent/EP2846393B1/en active Active
- 2014-05-27 CN CN201480001987.7A patent/CN104604014B/zh active Active
- 2014-05-27 WO PCT/KR2014/004731 patent/WO2014193148A1/ko active Application Filing
Also Published As
| Publication number | Publication date |
|---|---|
| CN104604014A (zh) | 2015-05-06 |
| TW201523967A (zh) | 2015-06-16 |
| EP2846393B1 (en) | 2018-10-17 |
| EP2846393A1 (en) | 2015-03-11 |
| KR101605957B1 (ko) | 2016-03-23 |
| KR20140139442A (ko) | 2014-12-05 |
| EP2846393A4 (en) | 2015-05-27 |
| JP2015522924A (ja) | 2015-08-06 |
| CN104604014B (zh) | 2018-03-06 |
| TWI548133B (zh) | 2016-09-01 |
| WO2014193148A1 (ko) | 2014-12-04 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6037486B2 (ja) | 非水性電解液及びこれを含むリチウム二次電池 | |
| JP6095080B2 (ja) | 非水性電解液及びこれを含むリチウム二次電池 | |
| JP6094843B2 (ja) | リチウム二次電池用電解液添加剤、前記電解液添加剤を含む非水性電解液及びリチウム二次電池 | |
| JP5932150B2 (ja) | 非水性電解液及びこれを含むリチウム二次電池 | |
| JP5948660B2 (ja) | 非水性電解液及びこれを含むリチウム二次電池 | |
| KR102167590B1 (ko) | 비수성 전해액 및 이를 포함하는 리튬 이차전지 | |
| KR101582043B1 (ko) | 출력 및 사이클 특성이 우수한 리튬 이차 전지 | |
| JP7038965B2 (ja) | 非水性電解液及びこれを含むリチウム二次電池 | |
| US9806379B2 (en) | Non-aqueous electrolyte solution and lithium secondary battery including the same | |
| US9825335B2 (en) | Non-aqueous electrolyte solution and lithium secondary battery including the same | |
| KR102143100B1 (ko) | 비수성 전해액, 이를 포함하는 리튬 이차전지 및 이의 제조방법 | |
| KR102035247B1 (ko) | 비수성 전해액 및 이를 포함하는 리튬 이차전지 | |
| KR20170038543A (ko) | 비수성 전해액 및 이를 포함하는 리튬 이차전지 | |
| KR101800497B1 (ko) | 비수성 전해액 및 이를 포함하는 리튬 이차전지 | |
| KR102086532B1 (ko) | 비수성 전해액 및 이를 포함하는 리튬 이차전지 | |
| KR102093384B1 (ko) | 비수성 전해액 및 이를 포함하는 리튬 이차전지 | |
| KR20210083098A (ko) | 음극 활물질의 제조방법 | |
| KR102034810B1 (ko) | 비수성 전해액 및 이를 포함하는 리튬 이차전지 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20151130 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20151207 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20160307 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20160530 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20160824 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20161003 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20161027 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6037486 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| S111 | Request for change of ownership or part of ownership |
Free format text: JAPANESE INTERMEDIATE CODE: R313111 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |