JP6015886B2 - リチウムマンガン系複合酸化物およびその製造方法 - Google Patents
リチウムマンガン系複合酸化物およびその製造方法 Download PDFInfo
- Publication number
- JP6015886B2 JP6015886B2 JP2010242064A JP2010242064A JP6015886B2 JP 6015886 B2 JP6015886 B2 JP 6015886B2 JP 2010242064 A JP2010242064 A JP 2010242064A JP 2010242064 A JP2010242064 A JP 2010242064A JP 6015886 B2 JP6015886 B2 JP 6015886B2
- Authority
- JP
- Japan
- Prior art keywords
- lithium
- comparative example
- sample obtained
- valence
- discharge
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/10—Energy storage using batteries
Description
以上の通り、リチウムコバルト系正極材料に代わり得るリチウムマンガン系正極材料について種々の報告がなされているが、より一層の充放電特性改善のためには、遷移金属価数制御を含む正極材料の化学組成や製造条件についての最適化が望まれている。
項2. Li2MnO3型単斜晶層状岩塩型構造の結晶相に加え、立方晶岩塩型構造の結晶相を含む上記項1に記載のリチウムマンガン系複合酸化物。
項3. 上記項1又は2に記載のリチウムマンガン系複合酸化物からなるリチウムイオン二次電池用正極材料。
項4.上記項3に記載のリチウムイオン二次電池用正極材料を構成要素とするリチウム
イオン二次電池。
(1)リチウムマンガン系複合酸化物本発明のリチウムマンガン系複合酸化物は、組成式Li1+x(Mn1-m-nFemTin)1-xO2(但し、0<x<1/3, 0≦m≦0.53, 0≦n≦0.53, 0<m+n≦0.53)で表される化合物であって、酸化物の一般的な結晶構造である岩塩型構造を基本とし、公知物質であるLi2MnO3に類似する単斜晶
マンガンの平均価数
=(MnおよびFeの平均価数×組成式中のFeとMn量の和(1-n)値―(鉄含有量m値×鉄の平均価数))/マンガン含有量(1-m-n)。
本発明の複合酸化物の製造方法については特に限定はないが、例えば、水熱反応を利用した方法によれば、優れた充放電性能を有する複合酸化物を容易に形成できる。以下の項の方法について具体的に説明する。
本発明によるリチウムマンガン系複合酸化物を用いるリチウムイオン二次電池は、公知の手法により製造することができる。例えば、正極材料として、本発明による新規な複合酸化物を使用し、負極材料として、公知の金属リチウム、炭素系材料(活性炭、黒鉛)、珪素、酸化珪素などを使用し、電解液として、公知のエチレンカーボネート、ジメチルカーボネート、ジエチルカーボネートなどからなる混合溶媒に過塩素酸リチウム、LiPF6などのリチウム塩を溶解させた溶液(有機電解液)を使用し、さらにその他の公知の電池構成要素を使用して、常法に従って、リチウムイオン二次電池を組立てればよい。
30%硫酸チタン(IV)水溶液40.00 g、及び塩化マンガン(II)4水和物39.58 g (全量0.25 mol、Ti:Mnモル比=2:8)を500 mlの蒸留水に加え、完全に溶解させた。別のビーカーに水酸化リチウム水溶液(蒸留水1000 mlに無水水酸化リチウム60 gを溶解させた溶液)を作製した。この水酸化リチウム水溶液をチタン製ビーカーに入れ攪拌した。攪拌された水酸化リチウム水溶液に上記金属塩水溶液を2〜3時間かけ、室温にて徐々に滴下して、Ti-Mn沈殿物を形成させた。反応液が完全にアルカリ性(pH11以上)になっていることを確認し、攪拌下に共沈物を含む反応液に室温で1日間空気を吹き込んで湿式酸化処理して、沈殿を熟成させた。
沈殿作製、水熱処理、その後水洗処理・濾過までの工程を実施例1と同様にして行い、、濾過して得た粉末(リチウムマンガン系複合酸化物)を、水酸化リチウム1水和物5.25 gを蒸留水100 mlに溶解させた水酸化リチウム水溶液中に添加して、撹拌しつつ分散・混合し、撹拌後、100 ℃において一晩乾燥し、粉砕して粉末を作製した。
図2に、実施例1および比較例1で得られた各粉末生成物のX線回折(XRD)図を示す。これらのXRDパターンに対して解析プログラムRIETAN-2000(F. Izumi and T. Ikeda, Mater. Sci. Forum, vol.321-324 p.198-203 (2000).)によるリートベルト解析を実施し、表1に示す結晶学パラメーターを算出した。
ICP発光分析およびLi2MnO3を4価標準物質として校正したヨウ素滴定値を用いて、実施例1および比較例1で得られた粉末状生成物の化学組成および遷移金属価数を求めた。結果を表2に示す。なおヨウ素滴定ではTiの価数を見積もることができないため、得られる遷移金属価数はMn価数に対応する。
実施例1および比較例1で得られた各試料をそれぞれ正極活物質としてリチウム二次電池を作製し、以下の電池構成及び充放電試験条件で充放電試験を行った。結果を下記表3及び図3に示す。
電池構成及び充放電試験条件:
正極:活物質5 mg+AB 5mg+PTFE 0.5mgを混合しAlメッシュ上に圧着
負極:金属リチウム
電解液:LiPF6をEC+DMC溶媒中に溶解させたもの
試験温度:30 ℃
電流密度(活物質あたり):40 mA/g、
電位範囲:1.5-4.8 V(初期充電のみ5.0Vまでの定電流―定電圧充電(10 mA/gに下がるまで))
AB:アセチレンブラック、PTFE:ポリテトラフルオロエチレン、EC:エチレンカーボネート、DMC:ジメチルカーボネート
30%硫酸チタン(IV)水溶液を100.00 gと塩化マンガン(II)4水和物を24.74 g (全量0.25mol、Ti:Mnモル比=5:5)用い、水熱処理時に、沈殿物及び水酸化リチウムに、更に、水酸化カリウム309gを加えた水溶液を用いること以外は、実施例1と同様にして、粉末状生成物(リチウムマンガン酸化物)を得た。
沈殿作製、水熱処理、その後水洗処理・濾過までの工程を実施例2と同様にして行い、、濾過して得た粉末(リチウムマンガン系複合酸化物)を、水酸化リチウム1水和物5.25 gを蒸留水100 mlに溶解させた水酸化リチウム水溶液中に添加して、撹拌しつつ分散・混合し、撹拌後、100 ℃において一晩乾燥し、粉砕して粉末を作製した。 次いで、得られた粉末を窒素中で一時間かけて600 ℃まで昇温後、その温度で窒素中において20時間焼成後、炉中で室温付近まで冷却し、過剰のリチウム塩を除去するために焼成物を蒸留水で水洗し、濾過し、乾燥して最終的に粉末状生成物を得た。
図5に、実施例2および比較例2で得られた各粉末生成物のX線回折(XRD)図を示す。これらのXRDパターンに対して解析プログラムRIETAN-2000(F. Izumi and T. Ikeda, Mater. Sci. Forum, vol.321-324 p.198-203 (2000).)によるリートベルト解析を実施し、表5に示す結晶学パラメーターを算出した。
ICP発光分析およびLi2MnO3を4価標準物質として校正したヨウ素滴定値を用いて、実施例2および比較例2で得られた粉末状生成物の化学組成および遷移金属価数を求めた。結果を表6に示す。なおヨウ素滴定ではTiの価数を見積もることができないため、得られる遷移金属価数はMn価数に対応する。
実施例2及び比較例2で得られた各試料をそれぞれ正極活物質としてリチウム二次電池を作製し、充放電試験を行った。電池構成及び充放電条件は、電位範囲を2.0-4.8 Vとしたこと以外は、実施例1における上記充放電試験と同様とした。結果を下記表7及び図6に示す。
実施例2と同様にして、Mn原料およびTi原料の秤量、共沈物作製、及び沈殿熟成処理を行った。
沈殿作製、水熱処理、その後水洗処理・濾過までの工程を実施例3と同様にして行い、濾過して得た粉末(リチウムマンガン系複合酸化物)を、水酸化リチウム1水和物5.25 gを蒸留水100 mlに溶解させた水酸化リチウム水溶液中に添加し、撹拌しつつ分散・混合し、撹拌後、100 ℃において一晩乾燥し、粉砕して粉末を作製した。 次いで得られた粉末を窒素中で一時間かけて600 ℃まで昇温後、その温度で窒素中において20時間焼成後、炉中で室温付近まで冷却し、過剰のリチウム塩を除去するために焼成物を蒸留水で水洗し、濾過し、乾燥して最終的に粉末状生成物を得た。
図7に、実施例3および比較例3で得られた各粉末生成物のX線回折(XRD)図を示す。これらのXRDパターンに対して解析プログラムRIETAN-2000(F. Izumi and T. Ikeda, Mater. Sci. Forum, vol.321-324 p.198-203 (2000).)によるリートベルト解析を実施し、表8に示す結晶学パラメーターを算出した。
ICP発光分析およびLi2MnO3を4価標準物質として校正したヨウ素滴定値を用いて、実施例3よび比較例3で得られた粉末状生成物の化学組成および遷移金属価数を求めた。結果を表9に示す。なおヨウ素滴定ではTiの価数を見積もることができないため、得られる遷移金属価数はMn価数に対応する。
実施例3及び比較例3で得られた各試料をそれぞれ正極活物質としてリチウム二次電池を作製し、充放電試験を行った。電池構成及び充放電条件は、電位範囲を2.0-4.8 Vとしたこと以外は、実施例1における上記充放電試験と同様とした。結果を下記表10及び図8に示す。
塩化鉄(III)6水和物13.52g、及び塩化マンガン(II)4水和物39.58g (全量0.25mol、Fe:Mnモル比=2:8)を500 mlの蒸留水に加え、完全に溶解させた。別のビーカーに水酸化リチウム水溶液(蒸留水1000 mlに無水水酸化リチウム60 gを溶解させた溶液)を作製した。これらの水溶液を用いること以外は、実施例1と同様にして、目的物である粉末状生成物(リチウムマンガン酸化物)を得た。
沈殿作製、水熱処理、その後水洗処理・濾過までの工程を実施例4と同様にして行い、濾過して得た粉末(リチウムマンガン系複合酸化物)を、水酸化リチウム1水和物5.25 gを蒸留水100 mlに溶解させた水酸化リチウム水溶液中に添加して、撹拌しつつ分散・混合し、撹拌後、100 ℃において一晩乾燥し、粉砕して粉末を作製した。 次いで得られた粉末を窒素中で一時間かけて500 ℃まで昇温後、その温度で窒素中において20時間焼成後、炉中で室温付近まで冷却し、過剰のリチウム塩を除去するために焼成物を蒸留水で水洗し、濾過し、乾燥して最終的に粉末状生成物を得た。
図9に、実施例4および比較例4で得られた各粉末生成物のX線回折(XRD)図を示す。これらのXRDパターンに対して解析プログラムRIETAN-2000(F. Izumi and T. Ikeda, Mater. Sci. Forum, vol.321-324 p.198-203 (2000).)によるリートベルト解析を実施し、表11に示す結晶学パラメーターを算出した。
ICP発光分析およびLi2MnO3を4価標準物質として校正したヨウ素滴定値を用いて、実施例4および比較例4で得られた粉末状生成物の化学組成および遷移金属価数を求めた。結果を表12に示す。
=(鉄含有量m値×鉄の価数)+(マンガン含有量(1-m)×マンガンの価数)
故に、マンガンの価数は、下記式となる。
マンガンの価数
=(MnとFeの平均価数―(鉄含有量m値×鉄の価数))/マンガン含有量(1-m)
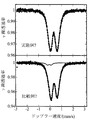
鉄の価数は、実施例4および比較例4で得られた両試料とも、図10に示される57Feメスバウワ分光スペクトルが対照なダブレットを示し、単一の異性体シフト成分で解析可能なことと、得られた異性体シフト値が実施例4で+0.3223(5) mm/s、比較例4で+0.3357(8) mm/sと、典型的な鉄3価の酸化物LiCo0.8Fe0.2O2の値(+0.3212(3) mm/s、V. McLaren, A. West, M. Tabuchi, A. Nakashima, H. Takahara, H. Kobayashi, H. Sakaebe, H. Kageyama, A. Hirano and Y. Takeda, J. Electrochem. Soc., 151 [5] A672-681 (2004).)に近いものであることから、3価と判断できる。
実施例4及び比較例4で得られた各試料をそれぞれ正極活物質としてリチウム二次電池を作製し、充放電試験を行った。電池構成及び充放電条件は、実施例1における充放電試験と同様である(電位範囲を1.5-4.8 V)。結果を下記表13及び図11に示す。
30%硫酸チタン(IV)水溶液60.00g、及び塩化マンガン(II)4水和物34.63g (全量0.25mol、Ti:Mnモル比=3:7)を500mlの蒸留水に加えて、完全に溶解させた。別のビーカーに水酸化リチウム水溶液(蒸留水500mlに水酸化リチウム一水和物50gを溶解させた溶液)を作製した。この水酸化リチウム水溶液をチタン製ビーカーに入れ、200mlのエタノールを加えた後、-10℃に冷却された恒温槽内に静置後、攪拌した。この撹拌された水酸化リチウム水溶液に上記金属塩水溶液を2〜3時間かけて徐々に滴下して、Ti-Mn沈殿物を形成させた。反応液が完全にアルカリ性(pH11以上)になっていることを確認し、撹拌下に共沈物を含む反応液に室温で2日間空気を吹き込んで湿式酸化処理して、沈殿を熟成させた。
沈殿作製、水熱処理、その後の750℃での大気中での焼成までの工程を実施例5と同様にして行い、その後、スクロース粉末の存在下での焼成を行うことなく、そのまま過剰のリチウム塩を除去するために焼成物を蒸留水で水洗し、濾過し、乾燥して最終的に粉末状生成物として得た。
図13に、実施例5および比較例5で得られた各粉末生成物のX線回折(XRD)図を示す。これらのXRDパターンに対して解析プログラムRIETAN-2000(F. Izumi and T. Ikeda, Mater. Sci. Forum, vol.321-324 p.198-203 (2000).)によるリートベルト解析を実施し、表15に示す結晶学パラメーターを算出した。
ICP発光分析およびLi2MnO3を4価標準物質として校正したヨウ素滴定値を用いて、実施例5よび比較例5で得られた粉末状生成物の化学組成および遷移金属価数を求めた。結果を表16に示す。なおヨウ素滴定ではTiの価数を見積もることができないため、得られる遷移金属価数はMn価数に対応する。
実施例5及び比較例5で得られた各試料をそれぞれ正極活物質としてリチウム二次電池を作製し、充放電試験を行った。電池構成及び充放電条件は、実施例1における充放電試験と同様である(電位範囲:1.5-4.8 V)。結果を下記表17及び図14に示す。
硝酸鉄(III)9水和物30.30g、及び塩化マンガン(II)4水和物34.63g (全量0.25mol、Fe:Mnモル比=3:7)を500mlの蒸留水に加えて、完全に溶解させた。別のビーカーに水酸化リチウム水溶液(蒸留水1000mlに無水水酸化リチウム60gを溶解させた溶液)を作製した。この水酸化リチウム水溶液をチタン製ビーカーに入れ、室温で攪拌した。この攪拌された水酸化リチウム水溶液に上記金属塩水溶液を2〜3時間かけて徐々に滴下して、Fe-Mn沈殿物を形成させた。反応液が完全にアルカリ性(pH11以上)になっていることを確認し、攪拌下に共沈物を含む反応液に室温で1日間空気を吹き込んで湿式酸化処理して、沈殿を熟成させた。
沈殿作製、水熱処理、その後の650℃での大気中での焼成までの工程を実施例6と同様にして行い、その後、スクロース粉末の存在下での焼成を行うことなく、そのまま過剰のリチウム塩を除去するために焼成物を蒸留水で水洗し、濾過し、乾燥して最終的に粉末状生成物として得た。
ICP発光分析およびLi2MnO3を4価標準物質として校正したヨウ素滴定値を用いて、実施例6および比較例6で得られた粉末状生成物の化学組成および遷移金属価数を求めた。
実施例6及び比較例6で得られた各試料をそれぞれ正極活物質としてリチウム二次電池を作製し、充放電試験を行った。電池構成及び充放電条件は、実施例1における充放電試験と同様である(電位範囲を1.5-4.8 Vとし、初期充電のみ4.8Vまでの定電流―定電圧充電(10 mA/gに下がるまで)を行った)。結果を下記表20及び図17に示す。
硝酸鉄(III)9水和物及び塩化マンガン(II)4水和物を含む水溶液に代えて、硝酸鉄(III)9水和物20.20g、塩化マンガン(II)4水和物29.69g、及び30%硫酸チタン(IV)溶液40.00g(全量0.25mol、Fe:Mn:Tiモル比=2:6:2)を含む水溶液を用いること以外は、実施例6と同様の操作を行い、目的物である粉末状生成物(リチウムマンガン系複合酸化物)を得た。
沈殿作製、水熱処理、その後の650℃での大気中での焼成までの工程を実施例7と同様にして行い、その後、スクロール粉末の存在下での焼成を行うことなく、そのまま過剰のリチウム塩を除去するために焼成物を蒸留水で水洗し、濾過し、乾燥して最終的に粉末状生成物として得た。
図18に、実施例7および比較例7で得られた各粉末生成物のX線回折(XRD)図を示す。これらのXRDパターンに対して解析プログラムRIETAN-2000(F. Izumi and T. Ikeda, Mater. Sci. Forum, vol.321-324 p.198-203 (2000).)によるリートベルト解析を実施し、表21に示す結晶学パラメーターを算出した。
ICP発光分析およびLi2MnO3を4価標準物質として校正したヨウ素滴定値を用いて、実施例7及び比較例7で得られた粉末状生成物の化学組成および遷移金属価数を求めた。
MnおよびFeの平均価数
=(鉄含有量m値÷組成式中のFeとMn量の和(1-n)値×鉄の価数)+(マンガン含有量(1-m-n)÷組成式中のFeとMn量の和(1-n)値×マンガンの価数)
故に
マンガンの価数
=(MnおよびFeの平均価数×組成式中のFeとMn量の和(1-n)値―(鉄含有量m値×鉄の価数))/マンガン含有量(1-m-n)
尚、鉄の価数は、実施例7の試料が図19に示される57Feメスバウワ分光スペクトルが対照なダブレットを示し、単一の異性体シフト成分で解析可能なことと、得られた異性体シフト値が+0.3273(9) mm/sと典型的な鉄3価の酸化物LiCo0.8Fe0.2O2の値(+0.3212(3) mm/s、V. McLaren, A. West, M. Tabuchi, A. Nakashima, H. Takahara, H. Kobayashi, H. Sakaebe, H. Kageyama, A. Hirano and Y. Takeda, J. Electrochem. Soc., 151 [5] A672-681 (2004).)に近いものであることから、3価と判断できる。一方比較例7の試料は、非対称なダブレット成分を示し、面積比95.2%を占める主成分の異性体シフト値が+0.3457(13) mm/sと上述のような典型的な鉄3価の酸化物の値と一致することから、ほとんどが鉄3価であるが、わずかに残り4.8%の成分があり、その異性体シフト値-0.07(2) mm/sより典型的な鉄4価の酸化物Li0.28Ni0.9Fe0.1O2の値(異性体シフト値-0.11 mm/s, C. Delmas, M. Menetrier, L. Croguennec, I. Saadoune, A. Rougier, C. Pouillerie, G, Prado, M. Grune, and L. Fournes, Electrochim. Acta., 45, 243-253 (1999).)成分と帰属できる。従って両成分の面積比がそのまま価数比と考えると鉄の価数は3.048と推定される。
実施例7及び比較例7で得られた各試料をそれぞれ正極活物質としてリチウム二次電池を作製し、充放電試験を行った。電池構成及び充放電条件は、実施例1における充放電試験と同様である(電位範囲を1.5-4.8 Vとし、初期充電のみ4.8Vまでの定電流―定電圧充電(10 mA/gに下がるまで)を行った)。結果を下記表23及び図20に示す。
Claims (4)
- 組成式:Li1+x(Mn1-m-nFemTin)1-xO2(0<x≦0.194, 0≦m≦0.53, 0≦n≦0.53, 0<m+n≦0.53)で表され、Li2MnO3型単斜晶層状岩塩型構造の結晶相を含むリチウムマンガン系複合酸化物であって、マンガン元素の平均価数が3.67〜3.87価であることを特徴とするリチウムマンガン系複合酸化物。
- Li2MnO3型単斜晶層状岩塩型構造の結晶相に加え、立方晶岩塩型構造の結晶相を含む請求項1に記載のリチウムマンガン系複合酸化物。
- 請求項1又は2に記載のリチウムマンガン系複合酸化物からなるリチウムイオン二次電池用正極材料。
- 請求項3に記載のリチウムイオン二次電池用正極材料を構成要素とするリチウムイオン二次電池。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2010242064A JP6015886B2 (ja) | 2010-07-20 | 2010-10-28 | リチウムマンガン系複合酸化物およびその製造方法 |
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2010163060 | 2010-07-20 | ||
| JP2010163060 | 2010-07-20 | ||
| JP2010242064A JP6015886B2 (ja) | 2010-07-20 | 2010-10-28 | リチウムマンガン系複合酸化物およびその製造方法 |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2015046474A Division JP6119003B2 (ja) | 2010-07-20 | 2015-03-09 | リチウムマンガン系複合酸化物およびその製造方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2012041257A JP2012041257A (ja) | 2012-03-01 |
| JP6015886B2 true JP6015886B2 (ja) | 2016-10-26 |
Family
ID=45897988
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2010242064A Active JP6015886B2 (ja) | 2010-07-20 | 2010-10-28 | リチウムマンガン系複合酸化物およびその製造方法 |
| JP2015046474A Active JP6119003B2 (ja) | 2010-07-20 | 2015-03-09 | リチウムマンガン系複合酸化物およびその製造方法 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2015046474A Active JP6119003B2 (ja) | 2010-07-20 | 2015-03-09 | リチウムマンガン系複合酸化物およびその製造方法 |
Country Status (1)
| Country | Link |
|---|---|
| JP (2) | JP6015886B2 (ja) |
Families Citing this family (15)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP6128303B2 (ja) * | 2012-04-03 | 2017-05-17 | 国立研究開発法人産業技術総合研究所 | リチウムマンガン系複合酸化物およびその製造方法 |
| JP6024220B2 (ja) * | 2012-06-05 | 2016-11-09 | 日本電気株式会社 | リチウムイオン電池およびその製造方法 |
| EP3944374B1 (en) * | 2012-10-02 | 2023-06-21 | Massachusetts Institute Of Technology | High-capacity positive electrode active material |
| JP5962429B2 (ja) * | 2012-10-22 | 2016-08-03 | ソニー株式会社 | 電池、電池パック、電子機器、電動車両、蓄電装置および電力システム |
| KR101513496B1 (ko) | 2013-07-24 | 2015-04-20 | 주식회사 엘지화학 | 리튬 망간계 산화물 및 이를 포함하는 양극 활물질 |
| JP6249270B2 (ja) * | 2013-08-23 | 2017-12-20 | 日本電気株式会社 | リチウム鉄マンガン系複合酸化物およびそれを用いたリチウムイオン二次電池 |
| JP6249269B2 (ja) * | 2013-08-23 | 2017-12-20 | 日本電気株式会社 | リチウム鉄マンガン系複合酸化物およびそれを用いたリチウムイオン二次電池 |
| JP2016122549A (ja) * | 2014-12-24 | 2016-07-07 | トヨタ自動車株式会社 | 正極活物質 |
| EP3595058A1 (en) | 2017-03-06 | 2020-01-15 | Panasonic Intellectual Property Management Co., Ltd. | Positive electrode active material and battery |
| JP6937152B2 (ja) * | 2017-03-31 | 2021-09-22 | 住友化学株式会社 | リチウム複合金属酸化物の製造方法 |
| WO2018198410A1 (ja) * | 2017-04-24 | 2018-11-01 | パナソニックIpマネジメント株式会社 | 正極活物質、および、電池 |
| CN110214389B (zh) | 2017-05-29 | 2023-06-20 | 松下知识产权经营株式会社 | 正极活性物质以及电池 |
| WO2019064816A1 (ja) | 2017-09-27 | 2019-04-04 | パナソニックIpマネジメント株式会社 | 正極活物質、および、電池 |
| JP7094570B2 (ja) * | 2017-10-31 | 2022-07-04 | 国立大学法人横浜国立大学 | リチウムイオン二次電池、電子機器及び車両 |
| JP7228773B2 (ja) | 2018-01-17 | 2023-02-27 | パナソニックIpマネジメント株式会社 | 正極活物質、および、電池 |
Family Cites Families (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP3263725B2 (ja) * | 1997-07-03 | 2002-03-11 | 独立行政法人産業技術総合研究所 | 混合アルカリ水熱法による層状岩塩型リチウムマンガン酸化物の製造方法 |
| JP4519220B2 (ja) * | 1999-07-09 | 2010-08-04 | Agcセイミケミカル株式会社 | リチウム二次電池 |
| JP3461800B2 (ja) * | 2000-11-16 | 2003-10-27 | 株式会社田中化学研究所 | リチウムマンガンニッケル複合酸化物およびその製造方法 |
| JP2002313335A (ja) * | 2001-04-12 | 2002-10-25 | Toyota Central Res & Dev Lab Inc | リチウム二次電池正極活物質用リチウムマンガン複合酸化物およびその製造方法 |
| JP3837469B2 (ja) * | 2001-05-21 | 2006-10-25 | 独立行政法人産業技術総合研究所 | 層状岩塩型リチウム鉄酸化物およびその製造方法 |
| JP4189486B2 (ja) * | 2003-09-22 | 2008-12-03 | 独立行政法人産業技術総合研究所 | リチウム−鉄−マンガン系複合酸化物の製造方法 |
| JP4997609B2 (ja) * | 2006-08-21 | 2012-08-08 | 独立行政法人産業技術総合研究所 | リチウムマンガン系複合酸化物の製造方法 |
| JP5516926B2 (ja) * | 2008-01-30 | 2014-06-11 | 独立行政法人産業技術総合研究所 | 規則構造を有する単斜晶系リチウムマンガン系複合酸化物およびその製造方法 |
| JP5263761B2 (ja) * | 2008-05-19 | 2013-08-14 | 独立行政法人産業技術総合研究所 | 陽イオン規則構造を有する単斜晶系リチウムマンガン系複合酸化物およびその製造方法 |
| JP2010135187A (ja) * | 2008-12-04 | 2010-06-17 | National Institute Of Advanced Industrial Science & Technology | 正極活物質、正極および非水電解質二次電池 |
-
2010
- 2010-10-28 JP JP2010242064A patent/JP6015886B2/ja active Active
-
2015
- 2015-03-09 JP JP2015046474A patent/JP6119003B2/ja active Active
Also Published As
| Publication number | Publication date |
|---|---|
| JP6119003B2 (ja) | 2017-04-26 |
| JP2015144131A (ja) | 2015-08-06 |
| JP2012041257A (ja) | 2012-03-01 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6119003B2 (ja) | リチウムマンガン系複合酸化物およびその製造方法 | |
| JP4963059B2 (ja) | チタン及びニッケル含有リチウムマンガン系複合酸化物 | |
| US8021783B2 (en) | Lithium manganese-based composite oxide and method for preparing the same | |
| JP5263761B2 (ja) | 陽イオン規則構造を有する単斜晶系リチウムマンガン系複合酸化物およびその製造方法 | |
| JP5516926B2 (ja) | 規則構造を有する単斜晶系リチウムマンガン系複合酸化物およびその製造方法 | |
| JP3064655B2 (ja) | 非水電解液二次電池およびその正極活物質の製造法 | |
| JP5958926B2 (ja) | リチウムマンガン系複合酸化物およびその製造方法 | |
| JP3940788B2 (ja) | リチウムフェライト系複合酸化物およびその製造方法 | |
| JP5673932B2 (ja) | 立方晶岩塩型構造を有するリチウムマンガン系複合酸化物およびその製造方法 | |
| JP4997609B2 (ja) | リチウムマンガン系複合酸化物の製造方法 | |
| WO2018169004A1 (ja) | ニッケルマンガン系複合酸化物及びその製造方法 | |
| JP2013073833A (ja) | リチウムイオン二次電池用正極活物質の製造方法 | |
| JP2015166291A (ja) | リチウム複合酸化物 | |
| JP4457213B2 (ja) | リチウムフェライト系複合酸化物の製造方法 | |
| JP7128475B2 (ja) | リチウムマンガン系複合酸化物及びその製造方法 | |
| JP4423391B2 (ja) | リチウムフェライト系複合酸化物およびその製造方法 | |
| WO2018066633A1 (ja) | チタン及び/又はゲルマニウム置換リチウムマンガン系複合酸化物及びその製造方法 | |
| JP4543156B2 (ja) | リチウムフェライト系複合酸化物およびその製造方法 | |
| JP4734672B2 (ja) | リチウム−鉄−マンガン複合酸化物の製造方法 | |
| JP7302826B2 (ja) | リチウムマンガン系複合酸化物及びその製造方法 | |
| WO2018043436A1 (ja) | 異種金属含有リチウムニッケル複合酸化物及びその製造方法 | |
| JP7133215B2 (ja) | ニッケルマンガン系複合酸化物及びその製造方法 | |
| JP3968420B2 (ja) | 立方晶岩塩型リチウムフェライト系複合酸化物およびその製造方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20130307 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20130227 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20140129 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20140304 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20140425 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20141209 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20150309 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20150428 |
|
| A912 | Re-examination (zenchi) completed and case transferred to appeal board |
Free format text: JAPANESE INTERMEDIATE CODE: A912 Effective date: 20150626 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20160629 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20160913 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6015886 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |