JP5564423B2 - D−キシロース利用機能が向上したコリネ型細菌形質転換体 - Google Patents
D−キシロース利用機能が向上したコリネ型細菌形質転換体 Download PDFInfo
- Publication number
- JP5564423B2 JP5564423B2 JP2010517869A JP2010517869A JP5564423B2 JP 5564423 B2 JP5564423 B2 JP 5564423B2 JP 2010517869 A JP2010517869 A JP 2010517869A JP 2010517869 A JP2010517869 A JP 2010517869A JP 5564423 B2 JP5564423 B2 JP 5564423B2
- Authority
- JP
- Japan
- Prior art keywords
- xylose
- corynebacterium glutamicum
- coryneform bacterium
- gene
- arae
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
- C12N15/52—Genes encoding for enzymes or proenzymes
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N1/00—Microorganisms, e.g. protozoa; Compositions thereof; Processes of propagating, maintaining or preserving microorganisms or compositions thereof; Processes of preparing or isolating a composition containing a microorganism; Culture media therefor
- C12N1/20—Bacteria; Culture media therefor
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
- C12N15/74—Vectors or expression systems specially adapted for prokaryotic hosts other than E. coli, e.g. Lactobacillus, Micromonospora
- C12N15/77—Vectors or expression systems specially adapted for prokaryotic hosts other than E. coli, e.g. Lactobacillus, Micromonospora for Corynebacterium; for Brevibacterium
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P7/00—Preparation of oxygen-containing organic compounds
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P7/00—Preparation of oxygen-containing organic compounds
- C12P7/02—Preparation of oxygen-containing organic compounds containing a hydroxy group
- C12P7/04—Preparation of oxygen-containing organic compounds containing a hydroxy group acyclic
- C12P7/06—Ethanol, i.e. non-beverage
- C12P7/065—Ethanol, i.e. non-beverage with microorganisms other than yeasts
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P7/00—Preparation of oxygen-containing organic compounds
- C12P7/02—Preparation of oxygen-containing organic compounds containing a hydroxy group
- C12P7/04—Preparation of oxygen-containing organic compounds containing a hydroxy group acyclic
- C12P7/06—Ethanol, i.e. non-beverage
- C12P7/08—Ethanol, i.e. non-beverage produced as by-product or from waste or cellulosic material substrate
- C12P7/12—Ethanol, i.e. non-beverage produced as by-product or from waste or cellulosic material substrate substrate containing sulfite waste liquor or citrus waste
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P7/00—Preparation of oxygen-containing organic compounds
- C12P7/40—Preparation of oxygen-containing organic compounds containing a carboxyl group including Peroxycarboxylic acids
- C12P7/44—Polycarboxylic acids
- C12P7/46—Dicarboxylic acids having four or less carbon atoms, e.g. fumaric acid, maleic acid
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E50/00—Technologies for the production of fuel of non-fossil origin
- Y02E50/10—Biofuels, e.g. bio-diesel
Description
また、特許文献3では、同様に、ザイモモナス モビリスに、エシェリヒア コリ由来のキシロース イソメラーゼ遺伝子、キシルロキナーゼ遺伝子、トランスケトラーゼ遺伝子及びトランスアルドラーゼ遺伝子の4つの遺伝子を染色体に導入し、発現することにより得られる、導入した遺伝子がより安定な形質転換体ザイモモナス モビリスによるD−キシロース利用技術が開示されている。これらの公知技術においては、ヘキソースに対するペントースの同時利用性はある程度達成されてはいるものの、D−キシロースの消費速度(利用速度)はD−グルコースの消費速度に比し、不十分であり、実用的な意味でのヘキソース及びペントース同時利用性技術としては更なる改良が求められている。
しかしながら、上述したように、D−グルコース及びD−キシロースの両糖の存在下でのD−キシロース利用に対するグルコース抑制が完全に解除され、D−キシロース及びD−グルコースを並行的かつ同時に効率よく利用できるコリネバクテリウム形質転換体は、未だ開発されていない。
具体的には、上述したD−キシロースの利用能を付与したコリネバクテリウム グルタミカムに、コリネバクテリウム グルタミカム(Corynebacterium glutamicum) ATCC31831由来のL−アラビノース輸送系のプロトンシンポーター遺伝子を導入したところ、思いもかけず、基質特異性が発現することもなく、D−キシロース利用速度が大幅に向上すると共に、D−グルコース及びD−キシロースの両糖の存在下での、D−キシロース利用に対するグルコース抑制が完全に解除され、D−グルコース及びD−キシロースの並行的かつ同時利用が可能となることを見出した。
(2) シュガートランスポーター機能を有するタンパク質が、L−アラビノース輸送系のプロトンシンポーターである上記(1)記載のコリネ型細菌形質転換体。
(3) シュガートランスポーター機能を有するタンパク質をコードする外来性遺伝子として、配列番号13で示される塩基配列からなるDNA、又は配列番号13で示される塩基配列と相補的な塩基配列からなるDNAとストリンジェントな条件でハイブリダイズし、かつシュガートランスポーター機能を有するポリペプチドをコードするDNAを用いる上記(1)又は(2)記載のコリネ型細菌形質転換体。
(4) D−キシロース利用能を有するコリネ型細菌が、コリネバクテリウム グルタミカム(Corynebacterium glutamicum) R (FERM P-18976)、セロビオース利用性組換え株もしくは変異株であるFERM P-18979、FERM P-18977及びFERM P-18978、コハク酸生産組換え株であるFERM P-19446及びFERM P-19477、並びにエタノール生産組換え株であるFERM P-17887、FERM P-17888、FERM P-19361及びFERM P-19362からなる群より選択されるいずれか1種の菌株のコリネ型細菌であって、かつD−キシロース利用能が付与されているものであることを特徴とする上記(1)〜(3)のいずれか一項に記載のコリネ型細菌形質転換体。
(5) シュガートランスポーター機能を有するタンパク質をコードする外来性遺伝子として、コリネバクテリウム グルタミカム (Corynebacterium glutamicum) ATCC31831、エシェリヒア コリ (Escherichia coli)、バチラス サブチリス(Bacillus subtilis)、バチラス リチェニフォルミス(Bacillus licheniformis)、バチラス コアグランス(Bacillus coagulans)、ラクトバチルス サケイ(Lactobacillus sakei)、ペディオコッカス ペントサセウス(Pediococcus pentosaceus)、ラクトバチルス レウテリ(Lactobacillus reuteri)、オーシャノバチルス イヘエニス(Oceanobacillus iheyensis)、ラクトコッカス ラクティス(Lactococcus lactis)、ロイコノストック メセンテロイデス(Leuconostoc mesenteroides)、ラクトバチルス プランタリューム(Lactobacillus plantarum)、ラクトバチルス ファーメンタム(Lactobacillus fermentum)、ラクトバチルス ブレビス(Lactobacillus brevis)、ロイコノストック シテリューム(Leuconostoc citreum)、エンテロコッカス フェシウム(Enterococcus faecium)、クレブシエラ オキシトカ(Klebsiella oxytoca)、及びサルモネラ ティフィムリウム(Salmonella typhimurium)からなる群より選ばれる微生物由来のaraE遺伝子を用いる上記(1)又は(2)に記載のコリネ型細菌形質転換体。
(6) D−グルコース及びD−キシロースを並行的かつ同時利用することができる上記(1)〜(5)のいずれか一項に記載のコリネ型細菌形質転換体。
(7) D−グルコース、D−キシロース及びL−アラビノースを並行的かつ同時利用することができる上記(6)記載のコリネ型細菌形質転換体。
(8) コリネ型細菌形質転換体が、コリネバクテリウム グルタミカム (Corynebacterium glutamicum) Ind-araE/pCRA811 (受託番号 NITE BP−576)である上記(1)記載のコリネ型細菌形質転換体。
(9) コリネ型細菌形質転換体が、コリネバクテリウム グルタミカム (Corynebacterium glutamicum) X5-Ind-araE/Plac-araBAD (受託番号 NITE BP−577)である上記(1)記載のコリネ型細菌形質転換体。
(10) コリネ型細菌形質転換体が、コリネバクテリウム グルタミカム(Corynebacterium glutamicum)X5-Ind-araE-Δldh/pEthAra (受託番号 NITE BP−581)である上記(1)記載のコリネ型細菌形質転換体。
(11) D−キシロースを含有する培地中で上記(1)〜(10)のいずれか一項に記載のコリネ型細菌形質転換体を用いて有機化合物を生成させる工程と、同培地より有機化合物を回収する工程とを含む有機化合物の製造方法。
(12) 有機化合物が、エタノール、乳酸、コハク酸、キシリトール、酢酸及びアミノ酸からなる群より選ばれる1種以上であることを特徴とする上記(11)記載の有機化合物の製造方法。
本発明のコリネ型細菌形質転換体は、シュガートランスポーター機能を有するタンパク質をコードする外来性遺伝子を、D−キシロース利用能を有するコリネ型細菌に導入したものである。
D−キシロース利用能を有するコリネ型細菌に、シュガートランスポーター機能を有するタンパク質をコードする外来性遺伝子を導入することにより、該コリネ型細菌のD−キシロース利用能が顕著に向上する。このため、コリネ型細菌形質転換体はD−グルコース及びD−キシロースを並行的かつ同時利用することができるものとなる。
中でも本発明では、エシェリヒア コリ(Escherichia coli)に由来するxylA遺伝子、及びxylB遺伝子の使用が最も好ましい。
マイクロコッカス属菌としては、マイクロコッカス フロイデンライヒ(Micrococcus freudenreichii)NO. 239(FERM P-13221)、マイクロコッカス ルテウス(Micrococcus leuteus)NO. 240(FERM P-13222)、マイクロコッカス ウレアエ(Micrococcus ureae)IAM1010又はマイクロコッカス ロゼウス(Micrococcus roseus)IFO3764等が挙げられる。
本発明において特に好ましいコリネ型細菌は、D−キシロース利用能が付与されたコリネバクテリウム グルタミカムR(FERM P-18976)である。
本発明では、D−キシロース利用能を有するコリネ型細菌に、シュガートランスポーター機能を有するタンパク質をコードする外来性遺伝子(シュガートランスポーター遺伝子ともいう)を導入する。これにより、コリネ型細菌形質転換体のD−キシロース利用能をより向上させることができる。シュガートランスポーター機能を有するタンパク質としては、ヘキソース及びペントースを輸送する機能を有するタンパク質であればよいが、中でも、L−アラビノース輸送系のプロトンシンポーターが好ましい。
本発明において、塩基配列間の相同性は、計算ソフト GENETYX(登録商標) Ver.8(ジェネティックス社製)を用いて計算した値である。
まず、上記のシュガートランスポーター遺伝子、例えば、L−アラビノース輸送系のプロトンシンポーターをコードするDNA(araE、タンパク質をAraEともいう)の配列をPCR (polymerase chain reaction) 法により増幅するためのオリゴヌクレオチドプライマーセットを作製する。このようなプライマーセットとしては、例えば配列番号14、15の塩基配列で示されるものなどが挙げられる。PCR法は、公知のPCR装置、例えばサーマルサイクラーなどを利用することができる。PCRのサイクルは、公知の技術にしたがって行なわれてよく、例えば、変性、アニーリング、伸張を1サイクルとし、通常10〜100サイクル、好ましくは、約20〜50サイクルである。PCRの鋳型としては、シュガートランスポーター遺伝子を有する微生物から単離したDNAを用いて、PCR法によりAraEをコードするDNAのcDNAを合成することができる。PCR法によって得られた遺伝子は、適当なクローニングベクターに導入することができる。クローニング法としては、pGEM-T easy vector system(Promega社製)、TOPO TA-cloning system(Invitrogen社製)、Mighty Cloning Kit(Takara社製)などの商業的に入手可能なPCRクローニングシステムなどを使用することもできる。また、方法の1つの例を実施例で詳記するが、該領域を含むDNA断片を、既知のAraEをコードするDNAの塩基配列に基づいて適当に設計された合成プライマーを鋳型として用いたハイブリダイゼーション法により取得することもできる。
目的遺伝子を含むプラスミドベクターのコリネ型細菌への導入方法としては、電気パルス法(エレクトロポレーション法)、CaC12法等コリネ型細菌への目的遺伝子導入が可能な方法であれば特に限定されるものではない。その具体例として、例えば電気パルス法としては、公知の方法〔Agric. Biol. Chem.、Vol. 54、443-447(1990)〕又は〔Res. Microbiol.、Vol. 144、181-185(1993)〕を用いることができる。
増殖培養工程
本発明のコリネ型細菌形質転換体を用いて有機化合物を製造する場合は、まず上述したコリネ型細菌形質転換体を好気条件下で増殖培養することが好ましい。
上記の如くして得られる培養物から回収分離されたコリネ型細菌形質転換体の培養菌体又はその菌体処理物を用いて、有機化合物を生成させる工程(有機化合物生成工程ともいう)を行う。
有機化合物生成工程においては、D−キシロースを含有する培地(反応培地)中で、上記コリネ型細菌形質転換体を用いて有機化合物を生成させる。このような工程を含む有機化合物の製造方法も、本発明の1つである。
具体的には、糖類としては、(D−又はL−)アラビノース、ガラクトース、フルクトース又はマンノースなどの単糖類;セロビオース、ショ糖、ラクトース、マルトースなどの二糖類;デキストリン又は可溶性澱粉などの多糖類などが挙げられる。特に、C6糖やC5糖などの単糖類が好ましく、中でも、L−アラビノースが好ましい。
培地のpHは、約6〜8が好ましい。
本発明における還元状態とは、反応系(反応培地)の酸化還元電位で規定され、反応培地の酸化還元電位がマイナス(−)の値であることを意味する。還元状態下にある反応培地の酸化還元電位は、好ましくは約−200mV〜−500mV程度、より好ましくは約−250mV〜−500mV程度である。
(1) プラスミドpCRA811構築方法
a) エシェリヒア コリ(Escherichia coli) JM109からの染色体DNAの抽出
エシェリヒア コリ(Escherichia coli) JM109を、L培地(トリプトン 10g、イーストエキストラクト 5g及びNaCl 5gを蒸留水1Lに溶解)に、白金耳を用いて植菌後、対数増殖期まで37℃で振盪培養し、菌体を集めた。DNAゲノム抽出キット(商品名:GenomicPrep Cells and Tissue DNA Isolation Kit、アマシャム社製)を用いて、取扱説明書に従い、集めた菌体から染色体DNAを回収した。
エシェリヒア コリ(Escherichia coli)のキシロースイソメラーゼ遺伝子(以下、xylAと記す)(配列番号1)、及びキシルロキナーゼ遺伝子(以下、xylBと記す)(配列番号2)の2つの遺伝子を含むDNA断片を以下のPCR法により増幅した。
PCRは、パーキンエルマーシータス社製の「DNAサーマルサイクラー」を用い、反応試薬として、DNAポリメラーゼ(商品名:Takara LA Taq HS DNA polymerase、宝酒造株式会社製)を用いて下記の条件で行なった。
デナチュレーション過程: 94℃、1分
アニーリング過程: 55℃、1分
エクステンション過程: 72℃、2分
以上を1サイクルとし、30サイクル行なった。
上記で生成した反応液の一部を用いて1%(W/V)アガロースゲルにより電気泳動を行なったところ、それぞれxylA遺伝子及びxylB遺伝子を含む、約1.4kb及び約1.6kbのDNA断片が検出できた。
該xylA遺伝子を含むプラスミドをpCRA801と命名した。
Ptrc−xylA遺伝子増幅用プライマーセット
Ptrc−xylB遺伝子増幅用プライマーセット
a) コリネバクテリウム グルタミカム(Corynebacterium glutamicum)ATCC31831からの染色体DNAの抽出
コリネバクテリウム グルタミカム(Corynebacterium glutamicum)ATCC31831からの染色体DNA抽出は、培地として表1に示すA液体培地を使用することと、培養温度が30℃であること以外は、上記のエシェリヒア コリ(Escherichia coli)JM109と同様の条件で行なった。
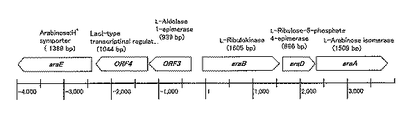
L−アラビノースを単一炭素源として良好な増殖を示したコリネバクテリウム グルタミカム(Corynebacterium glutamicum)ATCC31831よりL−アラビノース代謝に関与する遺伝子のクローニングを試みた。データベースのホモロジー検索の結果より、3種のL−アラビノース代謝酵素L−アラビノースイソメラーゼ、L−リブロキナーゼ、L−リブロース−5−フォスフェイト−4−エピメラーゼをコードする各遺伝子araA、araB、araDの内、araAが最も異種間での保存性が高かった。そこで、このaraAにおける保存領域の配列から以下の一対のプライマーセットを、アプライド・バイオシステムズ社製「394 DNA/RNAシンセサイザー」を用いて合成し、PCRに使用した。
デナチュレーション過程: 94℃、1分
アニーリング過程: 37℃、1分
エクステンション過程: 72℃、1分
以上を1サイクルとし、30サイクル行なった。
PCR増幅産物は、pGEM-T easy vector system(Promega社製)を用いて取扱説明書に従い反応させた。
コリネバクテリウム グルタミカム(Corynebacterium glutamicum)ATCC31831のaraE遺伝子を含むDNA断片を以下のPCR法により増幅した。
araE遺伝子増幅用プライマーセット
尚、いずれのプライマーにもEcoRIサイトが末端に付加されている。
デナチュレーション過程: 98℃、10秒
アニーリング過程: 55℃、30秒
エクステンション過程: 72℃、2分
以上を1サイクルとし、30サイクル行なった。
上述のEcoRI制限酵素で処理した増幅産物と、EcoRIで制限酵素処理をしたpKK223−3(ファルマシア社製)とを混合し、これにMighty Cloning Kit(宝酒造株式会社製)を添加した後、取扱説明書に従い反応させた。
この培地上の生育株を常法により液体培養し、培養液よりaraE遺伝子を含有する長さ約1.7kbのDNA断片が挿入されたプラスミドを、QIAprep Spin Miniprep Kit(キアゲン社製)を用いて抽出した。
該araE遺伝子を含むプラスミドをpKK223−3−araE(図3)と命名した。
次に、araE遺伝子をコリネバクテリウム グルタミカム(Corynebacterium glutamicum)Rにマーカーレスで染色体に導入するために必要なDNA領域を、コリネバクテリウム グルタミカム(Corynebacterium glutamicum)Rの生育に必須でないと報告されている配列〔Appl. Environ. Microbiol.、Vol. 71、3369-3372(2005)〕(SSI領域)を基に決定した。このDNA領域(Indel11領域)を以下のPCR法により増幅した。
araE遺伝子導入用Indel11領域増幅用プライマーセット
尚、いずれのプライマーにもXbaIサイトが末端に付加されている。
デナチュレーション過程: 94℃、30秒
アニーリング過程: 55℃、30秒
エクステンション過程: 72℃、3分
以上を1サイクルとし、30サイクル行なった。
上述の制限酵素XbaIで処理した増幅産物と、XbaIで制限酵素処理をしたマーカーレス遺伝子破壊用プラスミドpCRA725〔J. Mol. Microbiol. Biotechnol.、 Vol. 8、243-254(2004)、(特開2006-124440)〕とを混合し、これにMighty Cloning Kit(宝酒造株式会社製)を添加した後、取扱説明書に従い反応させた。
該araE遺伝子導入用Indel11領域を含むプラスミドをInd11LKS2−4(図3)と命名した。
該araE遺伝子導入用プラスミドをInd11−araE(図3)と命名した。
araE遺伝子導入用プラスミドInd11−araEは、コリネバクテリウム グルタミカム(Corynebacterium glutamicum)R内で複製不可能なプラスミドである。Ind11−araEを、電気パルス法〔Agric. Biol. Chem.、Vol. 54、443-447(1990)及びRes. Microbiol.、Vol. 144、181-185(1993)〕の方法に従って、コリネバクテリウム グルタミカム(Corynebacterium glutamicum)Rへ導入し、カナマイシン50μg/mLを含むA寒天培地〔組成:寒天が1.5%(W/V)含まれていることを除けば上記A液体培地と同一成分組成〕に塗布した。
カナマイシン感受性及びスクロース含有培地生育性を示した株をコリネバクテリウム グルタミカム(Corynebacterium glutamicum) Ind-araEと命名した。
プラスミドpCRA811を上記の実施例1、(4)項に示した電気パルス法に従って、コリネバクテリウム グルタミカム(Corynebacterium glutamicum)Rとコリネバクテリウム グルタミカム(Corynebacterium glutamicum) Ind11-araEへ導入し、クロラムフェニコール5μg/mLを含むA寒天培地〔組成:寒天が1.5%(W/V)含まれていることを除けば上記A液体培地と同一成分組成〕により、形質転換株コリネバクテリウム グルタミカム(Corynebacterium glutamicum)R/pCRA811とコリネバクテリウム グルタミカム(Corynebacterium glutamicum)Ind-araE/pCRA811とを得た。尚、コリネバクテリウム グルタミカム(Corynebacterium glutamicum)Ind-araE/pCRA811は、日本国千葉県木更津市かずさ鎌足2-5-8(郵便番号292-0818)の独立行政法人製品評価技術基盤機構 特許生物寄託センターに寄託した(受託日:2008年5月28日、受託番号:NITE BP−576)。
上記の実施例1、(5)項で作製したコリネバクテリウム グルタミカム(Corynebacterium glutamicum)R/pCRA811とコリネバクテリウム グルタミカム(Corynebacterium glutamicum)Ind-araE/pCRA811をそれぞれ用いて、D−キシロースを唯一の炭素源として含有するBT液体培地におけるD−キシロースの減少と菌の増殖とを検討した。該2菌株をそれぞれ、クロラムフェニコール5μg/mLを含むことを除けば上記A液体培地と同一成分組成培地10mLに一白金耳植菌して33℃、13時間、200rpmの条件で好気的に培養後、上記で示したBT培地で2回洗浄し、単一炭素源として25mM D−キシロースを含有する100mLのBT培地にOD610が0.2になるように植菌した。D−キシロース濃度は、逐次培地の少量をサンプリングして液体クロマトグラフィーによる分析を行い、経時的な消費量の変動を調べた。結果を、図4(1)及び(2)に示す。図4(1)及び(2)において、白丸(○)は、OD610の変化を、黒丸(●)は、培地中のD−キシロース濃度の変化を、それぞれ示す。図4(1)は、araE遺伝子を導入していないコリネバクテリウム グルタミカム(Corynebacterium glutamicum)R/pCRA811による、D−キシロース消費及び増殖の経時変化を示す図である。図4(2)は、araE遺伝子を染色体に導入したコリネバクテリウム グルタミカム(Corynebacterium glutamicum) Ind-araE/pCRA811による、D−キシロース消費及び増殖の経時変化を示す図である。結果、図4(1)及び(2)に示すように、好気条件下において、araE遺伝子を染色体に導入したコリネバクテリウム グルタミカム(Corynebacterium glutamicum)Ind-araE/pCRA811(図4(2))のD−キシロース消費速度と増殖速度は、araE遺伝子を導入していないコリネバクテリウム グルタミカム(Corynebacterium glutamicum)R/pCRA811(図4(1))と比較して、著しく速くなった。
(1)好気培養増殖
冷凍庫にて−80℃で保存してある上記の実施例1、(5)項で作製したコリネバクテリウム グルタミカム(Corynebacterium glutamicum)R/pCRA811とコリネバクテリウム グルタミカム(Corynebacterium glutamicum)Ind-araE/pCRA811を、それぞれプレート培養用培地であるクロラムフェニコール5μg/mLを含むA寒天培地〔組成:寒天が1.5%(W/V)含まれていることを除けば上記A液体培地と同一成分組成〕に塗布し、33℃、12時間暗所に静置した。
上記の実施例3、(1)項の好気培養増殖工程により回収された該2種の菌株それぞれの湿潤菌体 4g(Dry cell換算約0.8g)を、BT−U培地(組成:尿素が含まれていないことを除けば上記BT液体培地と同一成分組成)80mLに懸濁後、100mL容のバイアルに入れ、D−キシロース100mMを利用炭素源として加え、炭酸水素ナトリウム100mMを添加後、密閉した状態で33℃にてゆるく撹拌し、還元条件下の乳酸生成反応を行なった。
反応槽内のD−キシロース及び乳酸濃度は、逐次培地少量をサンプリングして液体クロマトグラフィーによる分析を行い、経時的な消費量及び生成量の変動をそれぞれ調べた。
この結果より、還元条件下においても、araE遺伝子を染色体に導入したコリネバクテリウム グルタミカム(Corynebacterium glutamicum)Ind-araE/pCRA811のD−キシロース消費速度及び乳酸生成速度はいずれも、araE遺伝子を導入していないコリネバクテリウム グルタミカム(Corynebacterium glutamicum)R/pCRA811と比較して、著しく速くなったことが分かった。
上記の実施例2における炭素源をD−キシロースから、D−グルコース及びD−キシロースの混合物(3.6g/L及び3.6g/L;存在比率1:1)に代えて反応を行なう以外は、実施例2と同様の条件及び方法にて、コリネバクテリウム グルタミカム(Corynebacterium glutamicum)R/pCRA811及びコリネバクテリウム グルタミカム(Corynebacterium glutamicum)Ind-araE/pCRA811の好気培養増殖及び糖消費を調べた。
上記の実施例3における基質をD−キシロースから、D−グルコース及びD−キシロースの混合物(40g/L及び20g/L;存在比率2:1)に代えて反応を行なう以外は、実施例3と同様の条件及び方法にて好気培養増殖後、還元条件下での反応を行なった。
(1) Plac−araBADの構築方法
エシェリヒア コリ(Escherichia coli)のL−アラビノースイソメラーゼ(以下araAと記す)、L−リブロキナーゼ(araBと記す)、L−リブロース−5−フォスフェイト−4−エピメラーゼ(araDと記す)の3つの遺伝子はaraB、araA、araDが順に連結したオペロン(araBAD)を形成している(配列番号18)〔Gene、Vol. 47、231-244(1986)〕。araBAD遺伝子を含むDNA断片を以下のPCR法により増幅した。
araBAD遺伝子増幅用プライマーセット
尚、前者にはEcoRIサイトが、後者にはSalIサイトがそれぞれ末端に付加されている。
PCRは、パーキンエルマーシータス社製の「DNAサーマルサイクラー」を用い、反応試薬として、DNAポリメラーゼ(商品名:PrimeSTAR HS DNA polymerase、宝酒造株式会社製)を用いて下記の条件で行なった。
(5×)PCR緩衝液: 10μL
2.5mM dNTP混合液: 4μL
鋳型DNA: 1μL (DNA含有量200ng以下)
上記の2種のプライマー: 各々 1μL(最終濃度0.2μM)
PrimeSTAR HS DNA polymerase: 0.5μL
滅菌蒸留水: 33.5μL
以上を混合し、この50μLの反応液をPCRにかけた。
デナチュレーション過程: 98℃、10秒
アニーリング過程: 55℃、10秒
エクステンション過程: 72℃、5分
以上を1サイクルとし、30サイクル行なった。
上述の制限酵素EcoRI及びSal Iで処理した増幅産物と、EcoRI及びSal Iで制限酵素処理をしたコリネ型細菌−大腸菌シャトルベクターpCRB1(特開2006−124440)とを混合し、これにライゲーションキット(商品名:Mighty Cloning Kit、宝酒造株式会社製)を添加後、取扱説明書に従い反応させた。
該araBAD遺伝子を含むプラスミドをPlac−araBAD(図8)と命名した。
a) コリネバクテリウム グルタミカム(Corynebacterium glutamicum)RからのSSI領域のクローニング
コリネバクテリウム グルタミカム(Corynebacterium glutamicum)RのSSI領域にD−キシロース代謝関連遺伝子xylA及びxylB遺伝子の導入を行なうため、これらのDNA領域を、表3に示したプライマー及びコリネバクテリウム グルタミカム(Corynebacterium glutamicum)Rの染色体DNAを用いたPCR反応により増幅させた。PCRは、Takara LA Taq HS DNA polymeraseを使用し、上記の実施例1、(3)項と同条件で行なった
上記で生成した反応液を用いて1%(W/V)アガロースゲルにより電気泳動を行なったところ、約2.0から3.0kbのDNA断片が検出できた。
表1において、b アンダーラインで示した塩基配列は、クローニング用に作製した制限酵素サイトを示している。
上記の実施例1、(1)項で作製したプラスミドpCRA811をXbaI及びXhoIで処理後、アガロース電気泳動で分離し、ゲルから切り出した約3.3kbのxylA−xylB遺伝子を含むDNA断片をゲル抽出キット(商品名:Minelute Gel Extraction Kit、キアゲン社製)を用いて回収した。得られたDNAを、XbaI及びXhoIで制限酵素処理をした上記実施例6、(2)、a)項で作製したプラスミドと混合し、これにMighty Cloning Kit(宝酒造株式会社製)を添加した後、取扱説明書に従い反応させた。
上記の実施例6、(2)、b)項で作製したxylA−xylB遺伝子導入用プラスミドを上記の実施例1、(3)の方法に従って、コリネバクテリウム グルタミカム(Corynebacterium glutamicum)RのSSI領域にXyl3、7、8、4、1、11、6の順番に導入した。最終的に得られた菌株をコリネバクテリウム グルタミカム(Corynebacterium glutamicum) X5と命名した。
プラスミPlac−araBADを上記の実施例1、(4)項に示した電気パルス法に従って、コリネバクテリウム グルタミカム(Corynebacterium glutamicum)X5及びコリネバクテリウム グルタミカム(Corynebacterium glutamicum)X5-Ind-araEそれぞれへ導入し、クロラムフェニコール5μg/mLを含むA寒天培地〔組成:寒天が1.5%(W/V)含まれていることを除けば上記A液体培地と同一成分組成〕により、形質転換株コリネバクテリウム グルタミカム(Corynebacterium glutamicum)X5/Plac-araBAD及びコリネバクテリウム グルタミカム(Corynebacterium glutamicum) X5-Ind-araE/Plac-araBADを得た。尚、コリネバクテリウム グルタミカム(Corynebacterium glutamicum) X5-Ind-araE/Plac-araBADは、日本国千葉県木更津市かずさ鎌足2-5-8(郵便番号292-0818)の独立行政法人製品評価技術基盤機構 特許生物寄託センターに寄託した(受託日:2008年5月28日、受託番号:NITE BP−577)。
上記の実施例3と同様の条件及び方法にて、コリネバクテリウム グルタミカム(Corynebacterium glutamicum)X5/Plac-araBAD及びコリネバクテリウム グルタミカム(Corynebacterium glutamicum) X5-Ind-araE/Plac-araBADそれぞれを好気培養増殖させた。その後、上記の実施例3における基質をD−キシロースから、D−グルコース、D−キシロース及びL−アラビノースの混合物(それぞれ32g/L、16g/L及び6.4g/L;存在比率5:2.5:1)に代えて行なう以外は、上記の実施例3と同様の条件及び方法にて、還元条件下での反応を行なった。
上記の実施例1、(5)項で作製したコリネバクテリウム グルタミカム(Corynebacterium glutamicum)R/pCRA811及びコリネバクテリウム グルタミカム(Corynebacterium glutamicum)Ind-araE/pCRA811それぞれを、上記の実施例5と同様の条件及び方法にて、好気培養増殖後、還元条件下、コハク酸生成反応を行った。
(1) プラスミドpEthAra構築方法
エタノール生産に必要なザイモモナス モビリス(Zymomonas mobilis)のアルデヒドデヒドロゲナーゼ(以下adhBと記す)及びピルベートデカルボキシラーゼ(pdcと記す)の2つの遺伝子〔Journal Mol Microbiol Biotechnol、Vol. 8、4(2004)〕を含むプラスミドpCRA723〔J. Mol. Microbiol. Biotechnol.、 Vol. 8、243-254(2004)、(特開2006−124440)〕を制限酵素BamHI及びBgl IIで処理後、アガロース電気泳動で分離した。ゲルから切り出した約4.0kbのadhB−pdc遺伝子を含むDNA断片をゲル抽出キット(商品名:Minelute Gel Extraction Kit、キアゲン社製)を用いて回収した。得られたDNAを、平滑末端処理キット(商品名:DNA Blunting Kit、宝酒造株式会社製)を用いて平滑末端処理を行ない、Sal Iで制限酵素処理後、同じく平滑末端処理をした上記の実施例6、(1)項で作製したプラスミドPlac−araBADを混合し、これにMighty Cloning Kit(宝酒造株式会社製)を添加した後、取扱説明書に従い反応させた。
乳酸デヒドロゲナーゼ(ldh)遺伝子をマーカーレス破壊するために、マーカーレスldh遺伝子破壊用プラスミドpCRA728〔J. Mol. Microbiol. Biotechnol.、Vol. 8、243-254(2004)〕を上記の実施例1、(3)の方法に従って、コリネバクテリウム グルタミカム(Corynebacterium glutamicum)X5-Ind11-araEに導入した。最終的に得られた菌株をコリネバクテリウム グルタミカム(Corynebacterium glutamicum)X5-Ind-araE-Δldhと命名した。
上記の実施例9、(1)項で作製したプラスミドpEthAraを、上記の実施例1、(4)項に示した電気パルス法に従って、コリネバクテリウム グルタミカム(Corynebacterium glutamicum)X5-Ind-araE-Δldhへ導入し、クロラムフェニコール5μg/mLを含むA寒天培地〔組成:寒天が1.5%(W/V)含まれていることを除けば上記A液体培地と同一成分組成〕により、形質転換株コリネバクテリウム グルタミカム(Corynebacterium glutamicum)X5-Ind-araE-Δldh/pEthAraを得た。尚、コリネバクテリウム グルタミカム(Corynebacterium glutamicum)X5-Ind-araE-Δldh/pEthAraは、日本国千葉県木更津市かずさ鎌足2-5-8(郵便番号292-0818)の独立行政法人製品評価技術基盤機構 特許生物寄託センターに寄託した(受託日:2008年6月4日、受託番号:NITE BP−581)。
上記の実施例3と同様の条件及び方法にて、コリネバクテリウム グルタミカム(Corynebacterium glutamicum)X5-Ind-araE-Δldh/pEthAraを好気培養増殖後、上記の実施例3における基質をD−キシロースからD−グルコース、D−キシロース及びL−アラビノースの混合物(32g/L、16g/L及び6.4g/L;存在比率5:2.5:1)に代えて行なう以外は、実施例3と同様の条件及び方法にて還元条件下での反応を行なった。
Claims (11)
- シュガートランスポーター機能を有するL−アラビノース輸送系のプロトンシンポーターをコードする外来性遺伝子を、D−キシロース利用能を有するコリネ型細菌に導入したことを特徴とする、コリネ型細菌形質転換体。
- 前記L−アラビノース輸送系のプロトンシンポーターをコードする外来性遺伝子として、配列番号13で示される塩基配列からなるDNA、又は配列番号13で示される塩基配列と90%以上の配列相同性を有し、かつシュガートランスポーター機能を有するポリペプチドをコードするDNAを用いる請求項1に記載のコリネ型細菌形質転換体。
- D−キシロース利用能を有するコリネ型細菌が、コリネバクテリウム グルタミカム(Corynebacterium glutamicum) R (FERM BP-18976)、セロビオース利用性組換え株もしくは変異株であるFERM P-18979、FERM P-18977及びFERM P-18978、コハク酸生産組換え株であるFERM BP-10060及びFERM BP-10061、並びにエタノール生産組換え株であるFERM BP-7621、FERM BP-7622、FERM P-19361及びFERM P-19362からなる群より選択されるいずれか1種の菌株のコリネ型細菌であって、かつD−キシロース利用能が付与されているものであることを特徴とする請求項1又は2に記載のコリネ型細菌形質転換体。
- 前記L−アラビノース輸送系のプロトンシンポーターをコードする外来性遺伝子として、コリネバクテリウム グルタミカム (Corynebacterium glutamicum) ATCC31831、エシェリヒア コリ (Escherichia coli)、バチラス サブチリス(Bacillus subtilis)、バチラス リチェニフォルミス(Bacillus licheniformis)、バチラス コアグランス(Bacillus coagulans)、ラクトバチルス サケイ(Lactobacillus sakei)、ペディオコッカス ペントサセウス(Pediococcus pentosaceus)、ラクトバチルス レウテリ(Lactobacillus reuteri)、オーシャノバチルス イヘエニス(Oceanobacillus iheyensis)、ラクトコッカス ラクティス(Lactococcus lactis)、ロイコノストック メセンテロイデス(Leuconostoc mesenteroides)、ラクトバチルス プランタリューム(Lactobacillus plantarum)、ラクトバチルス ファーメンタム(Lactobacillus fermentum)、ラクトバチルス ブレビス(Lactobacillus brevis)、ロイコノストック シテリューム(Leuconostoc citreum)、エンテロコッカス フェシウム(Enterococcus faecium)、クレブシエラ オキシトカ(Klebsiella oxytoca)、及びサルモネラ ティフィムリウム(Salmonella typhimurium)からなる群より選ばれる微生物由来のaraE遺伝子を用いる請求項1に記載のコリネ型細菌形質転換体。
- D−グルコース及びD−キシロースを並行的かつ同時利用することができる請求項1〜4のいずれか一項に記載のコリネ型細菌形質転換体。
- D−グルコース、D−キシロース及びL−アラビノースを並行的かつ同時利用することができる請求項5記載のコリネ型細菌形質転換体。
- コリネ型細菌形質転換体が、コリネバクテリウム グルタミカム (Corynebacterium glutamicum) Ind-araE/pCRA811 (受託番号 NITE BP−576)である請求項1記載のコリネ型細菌形質転換体。
- コリネ型細菌形質転換体が、コリネバクテリウム グルタミカム (Corynebacterium glutamicum) X5-Ind-araE/Plac-araBAD (受託番号 NITE BP−577)である請求項1記載のコリネ型細菌形質転換体。
- コリネ型細菌形質転換体が、コリネバクテリウム グルタミカム(Corynebacterium glutamicum)X5-Ind-araE-Δldh/pEthAra (受託番号 NITE BP−581)である請求項1記載のコリネ型細菌形質転換体。
- D−キシロースを含有する培地中で請求項1〜9のいずれか一項に記載のコリネ型細菌形質転換体を用いて有機化合物を生成させる工程と、同培地より有機化合物を回収する工程とを含む有機化合物の製造方法。
- 有機化合物が、エタノール、乳酸、コハク酸、キシリトール、酢酸及びアミノ酸からなる群より選ばれる1種以上であることを特徴とする請求項10記載の有機化合物の製造方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2010517869A JP5564423B2 (ja) | 2008-06-17 | 2009-06-10 | D−キシロース利用機能が向上したコリネ型細菌形質転換体 |
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008157409 | 2008-06-17 | ||
| JP2008157409 | 2008-06-17 | ||
| PCT/JP2009/060637 WO2009154122A1 (ja) | 2008-06-17 | 2009-06-10 | D-キシロース利用機能が向上したコリネ型細菌形質転換体 |
| JP2010517869A JP5564423B2 (ja) | 2008-06-17 | 2009-06-10 | D−キシロース利用機能が向上したコリネ型細菌形質転換体 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JPWO2009154122A1 JPWO2009154122A1 (ja) | 2011-12-01 |
| JP5564423B2 true JP5564423B2 (ja) | 2014-07-30 |
Family
ID=41434038
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2010517869A Active JP5564423B2 (ja) | 2008-06-17 | 2009-06-10 | D−キシロース利用機能が向上したコリネ型細菌形質転換体 |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US8685703B2 (ja) |
| EP (1) | EP2287287B1 (ja) |
| JP (1) | JP5564423B2 (ja) |
| KR (1) | KR20110027780A (ja) |
| CN (1) | CN102066553B (ja) |
| WO (1) | WO2009154122A1 (ja) |
Families Citing this family (15)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2010024267A1 (ja) | 2008-09-01 | 2010-03-04 | 国立大学法人信州大学 | 有用物質の製造法 |
| KR101842518B1 (ko) * | 2010-09-08 | 2018-03-27 | 그린 페놀 가이하쓰 가부시키가이샤 | 코리네형 세균 형질 전환체 및 그것을 사용하는 페놀의 제조 방법 |
| EP2639306B1 (en) | 2010-11-10 | 2017-03-29 | Green Phenol Development Co., Ltd. | Coryneform bacterium transformant and method for producing phenol using same |
| WO2012067174A1 (ja) * | 2010-11-18 | 2012-05-24 | グリーンフェノール・高機能フェノール樹脂製造技術研究組合 | コリネ型細菌形質転換体及びそれを用いるフェノールの製造方法 |
| CN103502267A (zh) * | 2011-04-22 | 2014-01-08 | 帝斯曼知识产权资产管理有限公司 | 能转化包括阿拉伯糖和木糖的糖的酵母细胞 |
| CN104245921B (zh) | 2012-01-10 | 2018-09-14 | Cj第一制糖株式会社 | 可利用木糖的棒状杆菌微生物和利用其产生l-赖氨酸的方法 |
| CN102559527B (zh) * | 2012-01-11 | 2013-12-11 | 山东大学 | 一株木糖转运能力高的酿酒酵母菌株及其应用 |
| KR101487810B1 (ko) * | 2013-07-29 | 2015-01-30 | 한국과학기술연구원 | 바이오 화학물질 발효균주의 제조방법 |
| CN104844698B (zh) * | 2014-02-16 | 2020-09-25 | 中国科学院天津工业生物技术研究所 | 一种促进微生物细胞转运葡萄糖、木糖和阿拉伯糖的方法及其在生物基产品发酵中的应用 |
| JP6434704B2 (ja) * | 2014-03-14 | 2018-12-05 | 公益財団法人地球環境産業技術研究機構 | キシロオリゴ糖利用能を付与したコリネ型細菌形質転換体 |
| JP6774494B2 (ja) | 2016-02-19 | 2020-10-21 | インターコンチネンタル グレート ブランズ エルエルシー | バイオマス源から複数の有用なストリームを形成するためのプロセス |
| CN107012161A (zh) * | 2017-04-03 | 2017-08-04 | 天津大学 | 利用秸秆水解液高产琥珀酸的谷氨酸棒杆菌及构建及应用 |
| CN110551648B (zh) * | 2018-05-30 | 2022-03-15 | 天津大学 | 发酵木糖生产琥珀酸的谷氨酸棒杆菌及用途 |
| CN111607601B (zh) * | 2020-04-24 | 2022-10-18 | 天津大学 | 谷氨酸棒杆菌转录调控因子IpsA突变体及应用 |
| CN112458108A (zh) * | 2020-11-24 | 2021-03-09 | 华东理工大学 | 一种在谷氨酸棒状杆菌中利用木糖生成谷氨酸的合成路径的构建方法 |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2001096573A1 (fr) * | 2000-06-16 | 2001-12-20 | Research Institute Of Innovative Technology For The Earth | Procede de production d'ethanol au moyen d'une bacterie coryneforme de recombinaison |
| JP2002338956A (ja) * | 2001-05-16 | 2002-11-27 | Yamagata Public Corp For The Development Of Industry | 紫外線吸収能を有する蛍光体 |
| JP2004089029A (ja) * | 2002-08-29 | 2004-03-25 | Research Institute Of Innovative Technology For The Earth | 新規なセロビオース資化性微生物 |
| WO2005010182A1 (ja) * | 2003-07-29 | 2005-02-03 | Research Institute Of Innovative Technology For The Earth | コリネ型細菌形質転換体及びそれを用いるジカルボン酸の製造方法 |
| JP2008517583A (ja) * | 2004-10-22 | 2008-05-29 | 味の素株式会社 | 腸内細菌科の細菌を用いたl−アミノ酸の製造方法 |
Family Cites Families (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS57183799A (en) | 1981-04-17 | 1982-11-12 | Kyowa Hakko Kogyo Co Ltd | Novel plasmid |
| JPS5867699A (ja) | 1981-10-16 | 1983-04-22 | Ajinomoto Co Inc | プラスミド |
| JPS62166890A (ja) | 1986-01-20 | 1987-07-23 | Asahi Chem Ind Co Ltd | イソクエン酸デヒドロゲナ−ゼ産生遺伝子を含むdna断片 |
| JPS644935A (en) | 1987-06-29 | 1989-01-10 | Toshiba Corp | Information recording medium |
| US5789210A (en) | 1993-11-08 | 1998-08-04 | Purdue Research Foundation | Recombinant yeasts for effective fermentation of glucose and xylose |
| JP2002338596A (ja) * | 1998-12-18 | 2002-11-27 | Ajinomoto Co Inc | 糖トランスポーター及びそれをコードする遺伝子 |
| HUP0203191A3 (en) * | 1999-07-01 | 2009-01-28 | Basf Ag | Corynebacterium glutamicum genes encoding phosphoenolpyruvate: sugar phosphotransferase system proteins |
| US7354755B2 (en) | 2000-05-01 | 2008-04-08 | Midwest Research Institute | Stable zymomonas mobilis xylose and arabinose fermenting strains |
| US6566107B1 (en) | 2000-11-01 | 2003-05-20 | Midwest Research Institute | Recombinant Zymomonas mobilis with improved xylose utilization |
| JP2002252190A (ja) | 2001-02-22 | 2002-09-06 | Toshiba Corp | 半導体基板の研磨方法および半導体基板の研磨装置 |
| JP4294373B2 (ja) | 2003-05-23 | 2009-07-08 | 財団法人地球環境産業技術研究機構 | エタノールの新規製造方法 |
| JP3860189B2 (ja) | 2004-10-27 | 2006-12-20 | 株式会社興人 | 非結晶性ポリエステル樹脂の製造方法 |
| JP2007222439A (ja) | 2006-02-24 | 2007-09-06 | Yamaha Livingtec Corp | 蒸気発生装置 |
| JP5074131B2 (ja) * | 2007-08-29 | 2012-11-14 | 公益財団法人地球環境産業技術研究機構 | L−アラビノース利用機能を有するコリネ型細菌形質転換体 |
-
2009
- 2009-06-10 CN CN2009801231392A patent/CN102066553B/zh active Active
- 2009-06-10 EP EP09766570.7A patent/EP2287287B1/en active Active
- 2009-06-10 KR KR1020117001106A patent/KR20110027780A/ko not_active Application Discontinuation
- 2009-06-10 WO PCT/JP2009/060637 patent/WO2009154122A1/ja active Application Filing
- 2009-06-10 US US12/995,774 patent/US8685703B2/en active Active
- 2009-06-10 JP JP2010517869A patent/JP5564423B2/ja active Active
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2001096573A1 (fr) * | 2000-06-16 | 2001-12-20 | Research Institute Of Innovative Technology For The Earth | Procede de production d'ethanol au moyen d'une bacterie coryneforme de recombinaison |
| JP2002338956A (ja) * | 2001-05-16 | 2002-11-27 | Yamagata Public Corp For The Development Of Industry | 紫外線吸収能を有する蛍光体 |
| JP2004089029A (ja) * | 2002-08-29 | 2004-03-25 | Research Institute Of Innovative Technology For The Earth | 新規なセロビオース資化性微生物 |
| WO2005010182A1 (ja) * | 2003-07-29 | 2005-02-03 | Research Institute Of Innovative Technology For The Earth | コリネ型細菌形質転換体及びそれを用いるジカルボン酸の製造方法 |
| JP2008517583A (ja) * | 2004-10-22 | 2008-05-29 | 味の素株式会社 | 腸内細菌科の細菌を用いたl−アミノ酸の製造方法 |
Non-Patent Citations (2)
| Title |
|---|
| JPN6009032801; KAWAGUCHI H., et al., Engineering of a xylose metabolic pathway in Corynebacterium glutamicum., Appl * |
| JPN6009032802; SA-NOGUEIRA I., et al., Cloning, functional analysis, and transcriptional regulation of the Bacillus * |
Also Published As
| Publication number | Publication date |
|---|---|
| EP2287287B1 (en) | 2015-04-08 |
| CN102066553A (zh) | 2011-05-18 |
| US20110117612A1 (en) | 2011-05-19 |
| EP2287287A4 (en) | 2012-07-11 |
| EP2287287A1 (en) | 2011-02-23 |
| US8685703B2 (en) | 2014-04-01 |
| WO2009154122A1 (ja) | 2009-12-23 |
| KR20110027780A (ko) | 2011-03-16 |
| CN102066553B (zh) | 2013-08-07 |
| JPWO2009154122A1 (ja) | 2011-12-01 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5564423B2 (ja) | D−キシロース利用機能が向上したコリネ型細菌形質転換体 | |
| Sasaki et al. | Xylitol production by recombinant Corynebacterium glutamicum under oxygen deprivation | |
| US10066217B2 (en) | Thermophilic organisms for conversion of lignocellulosic biomass to ethanol | |
| Cirino et al. | Engineering Escherichia coli for xylitol production from glucose‐xylose mixtures | |
| CN105121637B (zh) | 酿酒酵母中替代甘油形成的消耗电子的乙醇生产途径 | |
| CA2664646C (en) | Metabolic engineering of arabinose- fermenting yeast cells | |
| US20110230682A1 (en) | Microorganisms with inactivated lactate dehydrogenase gene (ldh) for chemical production | |
| JP5496356B2 (ja) | アラビノース代謝経路が導入されたキシリトール生産菌株及びそれを用いたキシリトール生産方法 | |
| US20180030482A1 (en) | Use of acetaldehyde in the fermentative production of ethanol | |
| JP5074131B2 (ja) | L−アラビノース利用機能を有するコリネ型細菌形質転換体 | |
| Tamakawa et al. | Construction of a Candida utilis strain with ratio-optimized expression of xylose-metabolizing enzyme genes by cocktail multicopy integration method | |
| JP7181876B2 (ja) | アラビノースを代謝するための高性能酵母株を得ること | |
| EP3274449B1 (en) | Modified 6-phosphofructo-1 -kinases, which enable frementative growth of recombinant yeast saccharomyces cerevisiae cells on pentose sugars | |
| EP2397556A1 (en) | Thermophilic organisms for conversion of lignocellulosic biomass to ethanol | |
| CN110760536A (zh) | 甲醇生物转化菌株的构建方法以及构建的菌株和应用 | |
| EP2643466A2 (en) | Compositions and methods for increased ethanol titer from biomass | |
| Yao | Metabolic engineering of ethanol production in Thermoanaerobacter mathranii | |
| JPWO2010095600A1 (ja) | ペントースからのホモ乳酸発酵 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20120308 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20131119 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20140117 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20140610 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20140616 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5564423 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |