JP4635178B2 - 新規なn−スルフェニル置換複素環化合物およびその製造方法 - Google Patents
新規なn−スルフェニル置換複素環化合物およびその製造方法 Download PDFInfo
- Publication number
- JP4635178B2 JP4635178B2 JP2004267279A JP2004267279A JP4635178B2 JP 4635178 B2 JP4635178 B2 JP 4635178B2 JP 2004267279 A JP2004267279 A JP 2004267279A JP 2004267279 A JP2004267279 A JP 2004267279A JP 4635178 B2 JP4635178 B2 JP 4635178B2
- Authority
- JP
- Japan
- Prior art keywords
- compound
- carbon atoms
- group
- sulfenyl
- producing
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Landscapes
- Plural Heterocyclic Compounds (AREA)
Description
たとえば、ゴムの加硫化剤(特許文献1、特許文献2)、発芽前処理用除草剤(特許文献3)、殺菌剤(特許文献4)等が知られている。特に、ピラゾール化合物の窒素上にスルフェニル置換基を有する場合は、抗菌作用(特許文献5、特許文献6、特許論文7)を有する化合物として有効であることが知られている。
ところで、新規なN−スルフェニル置換複素環化合物であるN−スルフェニルピラゾール化合物は、その構造がピラゾール化合物の窒素上にスルフェニル置換基を有する化合物と比較的して構造が複雑でなく、利用しやすいと考えられるにもかかわらず、従来から知られていない。これらの化合物を得ることは、当該技術の背景を考えると、重要なことである。
N−無置換ピラゾール化合物の製造方法において、塩素を用いない方法としてスルフェンアミド化合物とピラゾール化合物以外の複素環化合物を反応させて目的とするN−スルフェニル複素環化合物を製造する方法が開発されている(特許文献8)。これらの製造方法によって得られる化合物は、前記のように複素環化合物としてピラゾール化合物を用いるものではないので、塩素を用いることなく、スルフェンアミド化合物とピラゾール化合物を反応させて得られるN−スルフェニルピラゾール化合物の開発が望まれていた。
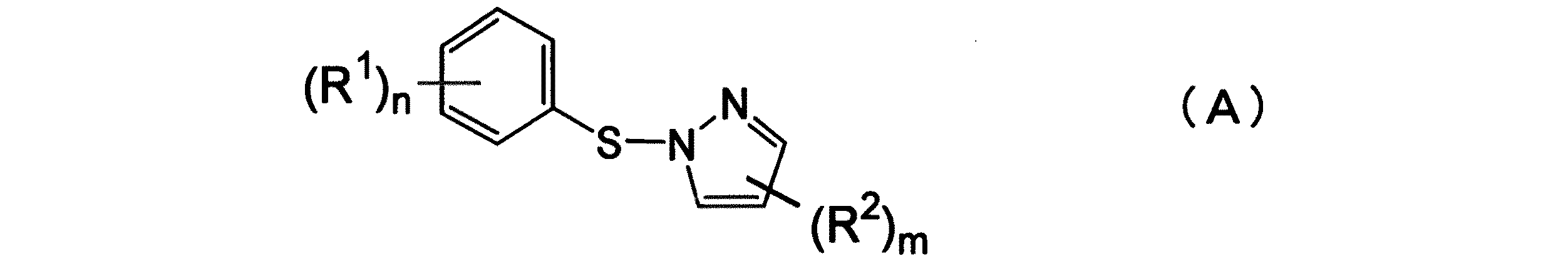
下記一般式(A)で表されるN−スルフェニルピラゾール化合物を製造する方法において、下記一般式(B)で表されるスルフェンアミド化合物と、下記一般式(C)で表されるピラゾール化合物を反応させることを特徴とするN−スルフェニルピラゾール化合物の製造方法。
(式中、R1 は、オルト位に結合している、炭素数2〜12のアルコキシカルボニル基を表す。nは1である。R2は、炭素数1〜8の鎖状あるいは炭素数3〜8の環状のアルキル基、炭素数6〜12の芳香族基、炭素数1〜8のアルコキシル基、ハロゲン原子、ニトロ基から選ばれる基又は原子を表す。R2が複数ある場合は、各R2は、互いに同一であっても異なっていてもよく、mは0または1〜3の整数である。また各R2は連結して環を形成していてもよい。)
(式中、R2は、炭素数1〜8の鎖状あるいは炭素数3〜8の環状のアルキル基、炭素数6〜12の芳香族基、炭素数1〜8のアルコキシル基、ハロゲン原子、及びニトロ基から選ばれる基又は原子を表す。R2が複数ある場合は、各R2は、互いに同一であっても異なっていてもよく、mは、0または1〜3の整数である。また各R2は、連結して環を形成していてもよい。)
本発明のN−スルフェニルピラゾール化合物は、ピラゾール化合物とスルフェンアミド化合物を反応させることにより、収率よく製造することができる。これは、スルフェンアミド化合物の窒素−硫黄結合が比較的開裂しやすいことに注目し、スルフェンアミド化合物と複素環化合物を反応させる新規な製造方法である。この製法には、有毒とされる塩素や臭素を用いることないので、安全にかつ容易にN−スルフェニル置換複素環化合物として製造することができる。従来知られている製造方法として比較して優れた方法である。
前記式中、R1 は、オルト位に結合している、炭素数2〜12のアルコキシカルボニル基を示す。nは1である。
R2は、炭素数1〜8の鎖状あるいは炭素数3〜8の環状のアルキル基、炭素数6〜12の芳香族基、炭素数1〜8のアルコキシル基、ハロゲン原子、ニトロ基から選ばれる基又は原子を示す。
R2が複数ある場合は、各R2は互いに同一であっても異なっていてもよく、mは、0または1〜3の整数である。また各R2は連結して環を形成していてもよい。
前記R 2 のアルコキシル基の具体例としては、メトキシ、エトキシ、プロポキシ、イソプロポキシ、シクロプロポキシ、ブトキシ、イソブトキシ、t−ブトキシ、ペンチロキシ、ヘキシロキシ、シクロヘキシロキシル基等が挙げられる。
前記R1及びR2のアルコキシカルボニル基の具体例としては、メトキシカルボニル、エトキシカルボニル、プロポキシカルボニル、イソプロポキシカルボニル、シクロプロポキシカルボニル、ブトキシカルボニル、イソブトキシカルボニル、t−ブトキシカルボニル、ペンチロキシカルボニル、ヘキシロキシカルボニル、シクロヘキシロキシルカルボニル基等が挙げられる。
前記R 2 のハロゲン原子としては、フッ素、塩素、臭素、ヨウ素が挙げられる。
下記一般式(B)で表されるスルフェンアミド化合物に対し、下記一般式(C)で表されるピラゾール化合物を反応させる。
反応時間は、反応温度により左右され、一概に定めることはできないが、通常は2〜10時間で十分である。
(B)の製法の一例を挙げれば、チオール化合物のアミノ化反応による製造方法を挙げることができる。
(C)の製法の一例を挙げれば、1,3−ジカルボニル化合物とヒドラジンによる製造方法を挙げることができる。
以下に述べる実施例は本発明の理解を容易にするために代表的な化合物の一例をあげたものであり、本発明はこれに限定されるものではない。
下記実施例に記載されているN−スルフェニル置換複素環化合物は、すべて新規化合物である。構造決定に際しては、各種スペクトルと元素分析の結果により同定した。
また、製造された化合物(1)〜(5)は、前記で示した化合物(1)〜(5)に対応するもので、その物性値としては、融点、核磁気共鳴スペクトル(1H−NMR,13C−NMR)、赤外吸収スペクトル(IR)の順にそれぞれ記した。
目的生成物の構造式は、化合物(1)のN−スルフェニル置換複素環化合物であることを以下の結果から確認した。
1H-NMR(CDCl3)δ1.41 (3H, td, J= 7.3, 1.8 Hz), 4.42 (3H, qd, J= 7.3, 1.8 Hz), 5.97 (1H, d, J= 8.2 Hz), 6.47 (1H, d, J=2.1 Hz), 7.17 (1H, t, J= 7.6 Hz), 7.33 (1H, t, J=7.8 Hz), 7.72 (1H, s), 7.81 (1H, s), 8.01 (1H, d, J= 7.6 Hz); 13C-NMR (CDCl3)δ13.9, 61.5, 108.3, 121.9, 123.1, 124.8, 130.0, 133.2, 138.2, 134.8, 146.1, 170.6;IR (neat)νmax 1691, 1311, 1280, 1261, 744 cm-1.
トルエンを減圧下留去させ、粗生成物をシリカゲルクロマトグラフィー(溶出溶媒、塩化メチレン:酢酸エチル=100:1)で精製した。さらにヘキサンで再結晶することにより、目的生成物を得た(収率:51%)。
目的生成物の構造式は、化合物(2)のN−スルフェニル置換複素環化合物であることを以下の結果から確認した。
融点:91.80-93.2 ℃;1H-NMR (CDCl3)δ2.26 (3H, s), 2.30 (3H, s), 3.98 (3H, s), 6.04 (1H, dd, J=8.2, 0.9 Hz), 6.07(1H, s), 7.19 (1H, ddd, J= 7.8, 7.3, 0.9 Hz), 7.37 (1H,ddd, J= 8.2, 7.3, 1.5 Hz), 8.02 (1H, dd, J= 7.8, 1.5 Hz);13C-NMR(CDCl3)δ11.7, 14.0, 52.6, 103.2, 107.6, 122.4, 123.5, 125.0, 130.7, 133.7, 146.5, 147.5, 152.4, 161.1, 167.2;IR (KBr) νmax 1695, 1564, 1462, 1437, 1278, 790, 752 cm-1.
C13H14N2O2Sとしての元素分析値(%)
測定値:C, 59.52; H, 5.38; N, 10.68
計算値:C, 59.61; H, 5.30; N, 10.34
目的生成物の構造式は、化合物(3)のN−スルフェニル置換複素環化合物であることを以下の結果から確認した。
融点:95.2−96.2 ℃;1H-NMR(CDCl3)δ1.45 (3H, t, J= 7.3 Hz), 2.26 (3H, s), 2.30 (3H, s), 4.44 (2H, q, J= 7.0 Hz), 6.04 (1H, dd, J= 8.2, 0.9 Hz), 6.06 (1H, s), 7.19 (1H, ddd, J= 7.9, 7.3, 0.9 Hz), 7.36 (1H, ddd, J=8.2, 7.3, 1.2 Hz), 8.04 (1H, dd, J= 7.9, 1.2 Hz);13C-NMR(CDCl3) δ11.7, 14.0, 14.3, 61.8, 107.5, 122.4, 123.9, 125.0, 130.7, 133.6, 146.4, 147.6, 152.4, 166.8;IR (KBr)νmax 1686, 1562, 1462, 1294, 743 cm-1.
C14H16N2O2Sとしての元素分析値(%)
測定値:C, 60.95; H, 5.79; N, 10.10
計算値:C, 60.85; H, 5.84; N, 10.14
目的生成物の構造式は、化合物(4)のN−スルフェニル置換複素環化合物であることを以下の結果から確認した。
融点:116.7−117.4 ℃;1H-NMR(CDCl3)δ1.42 (3H, td, J= 7.2, 1.8 Hz), 1.98 (3H, s), 2.17 (3H, s), 2.24 (3H, d, J= 1.5 Hz), 4.43 (2H, qd, J= 7.2,1.8 Hz), 6.02 (1H, d, J= 8.2), 7.16 (1H, t, J= 7.6 Hz), 7.34 (1H, t, J= 7.6 Hz), 8.02 (1H, d, J= 7.9 Hz);13C-NMR(CDCl3)δ8.4, 9.9, 12.1, 14.1, 61.4, 113.9, 122.2, 123.6, 124.6, 130.4, 133.3, 143.2, 146.6, 151.6, 166.5;IR (KBr)νmax 1684, 1464, 1298, 1213, 1145, 1101, 746 cm-1.
C15H18N2O2Sとしての元素分析値(%)
測定値:C, 62.22; H, 6.24; N, 9.63
計算値:C, 62.04; H, 6.25; N, 9.65
目的生成物の構造式は、化合物(5)のN−スルフェニル置換複素環化合物であることを以下の結果から確認した。
1H-NMR (CDCl3)δ1.39 (3H, t, J=7.2 Hz), 4.39 (2H, q, J= 7.2 Hz), 6.31 (1H, d, J=8.2 Hz), 6.90 (1H, s), 7.16 (1H, t, J= 7.5 Hz), 7.33-7.38 (6H, m), 7.42 (1H, t, J=7.8 Hz), 7.51-7.54 (2H, m), 7.93 (2H, d, J=7.6 Hz), 8.00 (1H, d, J=7.9 Hz);13C-NMR (CDCl3)δ14.2, 61.7, 105.6, 122.6, 123.7, 125.0, 125.9, 128.3, 128.4, 128.6, 128.8, 129.6, 130.4, 132.3, 133.5, 146.3, 152.3, 154.8, 166.7;IR (neat) νmax 1691, 1311, 1278, 1259, 761, 744, 694 cm-1.
Claims (1)
- 下記一般式(A)で表されるN−スルフェニルピラゾール化合物を製造する方法において、下記一般式(B)で表されるスルフェンアミド化合物と、下記一般式(C)で表されるピラゾール化合物を反応させることを特徴とするN−スルフェニルピラゾール化合物の製造方法。
(式中、R1は、オルト位に結合している、炭素数2〜12のアルコキシカルボニル基を表す。nは1である。R2は、炭素数1〜8の鎖状あるいは炭素数3〜8の環状のアルキル基、炭素数6〜12の芳香族基、炭素数1〜8のアルコキシル基、ハロゲン原子、ニトロ基から選ばれる基又は原子を表す。R2が複数ある場合は、各R2は、互いに同一であっても異なっていてもよく、mは0または1〜3の整数である。また各R2は連結して環を形成していてもよい。)
(式中、R2は、炭素数1〜8の鎖状あるいは炭素数3〜8の環状のアルキル基、炭素数6〜12の芳香族基、炭素数1〜8のアルコキシル基、ハロゲン原子、及びニトロ基から選ばれる基又は原子を表す。R2が複数ある場合は、各R2は互いに同一であっても異なっていてもよく、mは0または1〜3の整数である。また各R2は連結して環を形成していてもよい。)
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2004267279A JP4635178B2 (ja) | 2004-09-14 | 2004-09-14 | 新規なn−スルフェニル置換複素環化合物およびその製造方法 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2004267279A JP4635178B2 (ja) | 2004-09-14 | 2004-09-14 | 新規なn−スルフェニル置換複素環化合物およびその製造方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2006083076A JP2006083076A (ja) | 2006-03-30 |
| JP4635178B2 true JP4635178B2 (ja) | 2011-02-16 |
Family
ID=36161883
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2004267279A Expired - Fee Related JP4635178B2 (ja) | 2004-09-14 | 2004-09-14 | 新規なn−スルフェニル置換複素環化合物およびその製造方法 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP4635178B2 (ja) |
Family Cites Families (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE3118126A1 (de) * | 1981-05-07 | 1982-12-02 | Bayer Ag, 5090 Leverkusen | Sulfenamide zur verwendung in arzneimitteln |
| JP3706904B2 (ja) * | 2001-01-25 | 2005-10-19 | 独立行政法人産業技術総合研究所 | スルフェンアミド化合物の製造方法 |
| JP4041881B2 (ja) * | 2002-07-24 | 2008-02-06 | 独立行政法人産業技術総合研究所 | 新規なn−チオ置換複素環化合物およびその製造方法 |
-
2004
- 2004-09-14 JP JP2004267279A patent/JP4635178B2/ja not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| JP2006083076A (ja) | 2006-03-30 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4731503B2 (ja) | 複素環式化合物のスルフィニル化方法 | |
| JP4635178B2 (ja) | 新規なn−スルフェニル置換複素環化合物およびその製造方法 | |
| JP4041881B2 (ja) | 新規なn−チオ置換複素環化合物およびその製造方法 | |
| JP4639382B2 (ja) | 新規なn−スルフェニルベンゾトリアゾール化合物及びその製造方法 | |
| JP4214220B2 (ja) | 新規なn−スルフェニルピロール化合物およびその製造方法 | |
| JP4296268B2 (ja) | 新規なn−スルフェニル置換複素環化合物およびその製造方法 | |
| JP4296267B2 (ja) | 新規なn−スルフェニル置換複素環化合物およびその製造方法 | |
| JP4761133B2 (ja) | ピリジンスルフェンアミド化合物及びその製造方法 | |
| JP4296266B2 (ja) | 新規なn−スルフェニル置換複素環化合物およびその製造方法 | |
| JP4853911B2 (ja) | イソチアゾロピリジン−3−オン化合物の製造方法 | |
| JP4747359B2 (ja) | 新規なn−スルフェニルピロール化合物およびその製造方法 | |
| JP4853910B2 (ja) | イソチアゾロピリジン−3−オン化合物の製造方法 | |
| JP4002972B2 (ja) | スルフェンアミド化合物の製造方法 | |
| JP4729738B2 (ja) | 新規なn−スルフェニルピロール化合物およびその製造方法 | |
| CN106478508B (zh) | 一种含卤素吡唑甲腈衍生物的合成方法 | |
| JP4238314B2 (ja) | 新規なn−スルフィニル複素環化合物およびその製造方法 | |
| JP4982790B2 (ja) | イソチアゾロピリジン−3−オン化合物の製造方法 | |
| JP4006520B2 (ja) | スルフェンアミド化合物の製造方法 | |
| JP4273224B2 (ja) | N−スルフェニル複素環化合物の製造方法 | |
| US20080319203A1 (en) | Method for Producing 5-Fluoro-1,3-Dialkyl-1H-Pyrazol-4-Carboxylic Acid Chlorides | |
| JP4200209B2 (ja) | 1,2−ベンゾイソチアゾリン−3−オン−1−オキシド化合物の製造方法 | |
| JP4729742B2 (ja) | イソチアゾロピリジン化合物の製造方法 | |
| JP2009132630A (ja) | ベンゾオキサチイン化合物の製造方法 | |
| JP6590406B2 (ja) | 新規なピロロベンゾチアジン化合物とその製造方法 | |
| JP5370990B2 (ja) | 新規なスルフェンアミド化合物とその製造方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20070129 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20100421 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20100427 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20100628 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20100907 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20101004 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20101026 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20101027 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20131203 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20131203 Year of fee payment: 3 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |