JP4162147B2 - アレルギー抑制剤 - Google Patents
アレルギー抑制剤 Download PDFInfo
- Publication number
- JP4162147B2 JP4162147B2 JP2005371005A JP2005371005A JP4162147B2 JP 4162147 B2 JP4162147 B2 JP 4162147B2 JP 2005371005 A JP2005371005 A JP 2005371005A JP 2005371005 A JP2005371005 A JP 2005371005A JP 4162147 B2 JP4162147 B2 JP 4162147B2
- Authority
- JP
- Japan
- Prior art keywords
- kestose
- effect
- allergy
- ige
- bifidobacteria
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 206010020751 Hypersensitivity Diseases 0.000 title abstract description 62
- 208000026935 allergic disease Diseases 0.000 title abstract description 54
- 230000007815 allergy Effects 0.000 title description 45
- VAWYEUIPHLMNNF-OESPXIITSA-N 1-kestose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)OC[C@]1(O[C@@H]2[C@@H]([C@@H](O)[C@H](O)[C@@H](CO)O2)O)[C@@H](O)[C@H](O)[C@@H](CO)O1 VAWYEUIPHLMNNF-OESPXIITSA-N 0.000 claims abstract description 168
- GIUOHBJZYJAZNP-DVZCMHTBSA-N 1-kestose Natural products OC[C@@H]1O[C@](CO)(OC[C@]2(O[C@H]3O[C@H](CO)[C@@H](O)[C@H](O)[C@H]3O)O[C@@H](O)[C@@H](O)[C@@H]2O)[C@@H](O)[C@@H]1O GIUOHBJZYJAZNP-DVZCMHTBSA-N 0.000 claims abstract description 168
- VAWYEUIPHLMNNF-UHFFFAOYSA-N kestotriose Natural products OC1C(O)C(CO)OC1(CO)OCC1(OC2C(C(O)C(O)C(CO)O2)O)C(O)C(O)C(CO)O1 VAWYEUIPHLMNNF-UHFFFAOYSA-N 0.000 claims abstract description 168
- 239000000203 mixture Substances 0.000 claims abstract description 44
- RFSUNEUAIZKAJO-ARQDHWQXSA-N Fructose Chemical class OC[C@H]1O[C@](O)(CO)[C@@H](O)[C@@H]1O RFSUNEUAIZKAJO-ARQDHWQXSA-N 0.000 claims description 11
- 230000000694 effects Effects 0.000 abstract description 65
- 241000186000 Bifidobacterium Species 0.000 abstract description 51
- 238000004519 manufacturing process Methods 0.000 abstract description 40
- 230000000968 intestinal effect Effects 0.000 abstract description 31
- 230000001965 increasing effect Effects 0.000 abstract description 27
- 235000013305 food Nutrition 0.000 abstract description 23
- 238000012360 testing method Methods 0.000 abstract description 19
- 206010012438 Dermatitis atopic Diseases 0.000 abstract description 18
- 201000008937 atopic dermatitis Diseases 0.000 abstract description 18
- 230000002401 inhibitory effect Effects 0.000 abstract description 9
- 230000002265 prevention Effects 0.000 abstract description 9
- 238000011282 treatment Methods 0.000 abstract description 9
- 239000004480 active ingredient Substances 0.000 abstract description 8
- 229940099472 immunoglobulin a Drugs 0.000 abstract description 4
- 230000003213 activating effect Effects 0.000 abstract description 3
- 108060003951 Immunoglobulin Proteins 0.000 abstract description 2
- 102000018358 immunoglobulin Human genes 0.000 abstract description 2
- 230000037406 food intake Effects 0.000 description 28
- 241000894006 Bacteria Species 0.000 description 27
- 235000000346 sugar Nutrition 0.000 description 23
- 241000699670 Mus sp. Species 0.000 description 22
- 239000000843 powder Substances 0.000 description 21
- FTSSQIKWUOOEGC-RULYVFMPSA-N fructooligosaccharide Chemical compound OC[C@H]1O[C@@](CO)(OC[C@@]2(OC[C@@]3(OC[C@@]4(OC[C@@]5(OC[C@@]6(OC[C@@]7(OC[C@@]8(OC[C@@]9(OC[C@@]%10(OC[C@@]%11(O[C@H]%12O[C@H](CO)[C@@H](O)[C@H](O)[C@H]%12O)O[C@H](CO)[C@@H](O)[C@@H]%11O)O[C@H](CO)[C@@H](O)[C@@H]%10O)O[C@H](CO)[C@@H](O)[C@@H]9O)O[C@H](CO)[C@@H](O)[C@@H]8O)O[C@H](CO)[C@@H](O)[C@@H]7O)O[C@H](CO)[C@@H](O)[C@@H]6O)O[C@H](CO)[C@@H](O)[C@@H]5O)O[C@H](CO)[C@@H](O)[C@@H]4O)O[C@H](CO)[C@@H](O)[C@@H]3O)O[C@H](CO)[C@@H](O)[C@@H]2O)[C@@H](O)[C@@H]1O FTSSQIKWUOOEGC-RULYVFMPSA-N 0.000 description 16
- 229940107187 fructooligosaccharide Drugs 0.000 description 16
- FLDFNEBHEXLZRX-DLQNOBSRSA-N Nystose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)OC[C@]1(OC[C@]2(O[C@@H]3[C@@H]([C@@H](O)[C@H](O)[C@@H](CO)O3)O)[C@H]([C@H](O)[C@@H](CO)O2)O)[C@@H](O)[C@H](O)[C@@H](CO)O1 FLDFNEBHEXLZRX-DLQNOBSRSA-N 0.000 description 14
- 238000002474 experimental method Methods 0.000 description 14
- 206010037844 rash Diseases 0.000 description 14
- FLDFNEBHEXLZRX-UHFFFAOYSA-N nystose Natural products OC1C(O)C(CO)OC1(CO)OCC1(OCC2(OC3C(C(O)C(O)C(CO)O3)O)C(C(O)C(CO)O2)O)C(O)C(O)C(CO)O1 FLDFNEBHEXLZRX-UHFFFAOYSA-N 0.000 description 13
- 208000024891 symptom Diseases 0.000 description 13
- ODEHMIGXGLNAKK-OESPXIITSA-N 6-kestotriose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)OC[C@@H]1[C@@H](O)[C@H](O)[C@](CO)(O[C@@H]2[C@@H]([C@@H](O)[C@H](O)[C@@H](CO)O2)O)O1 ODEHMIGXGLNAKK-OESPXIITSA-N 0.000 description 12
- 229920001542 oligosaccharide Polymers 0.000 description 12
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 12
- 230000037396 body weight Effects 0.000 description 11
- 201000005884 exanthem Diseases 0.000 description 11
- 230000006872 improvement Effects 0.000 description 11
- 238000005259 measurement Methods 0.000 description 11
- 230000000172 allergic effect Effects 0.000 description 10
- 150000002482 oligosaccharides Chemical class 0.000 description 10
- 230000001629 suppression Effects 0.000 description 10
- 208000010201 Exanthema Diseases 0.000 description 9
- 208000010668 atopic eczema Diseases 0.000 description 9
- 229940092253 ovalbumin Drugs 0.000 description 9
- 230000003247 decreasing effect Effects 0.000 description 8
- 230000008859 change Effects 0.000 description 7
- 239000003814 drug Substances 0.000 description 7
- 239000000463 material Substances 0.000 description 7
- 238000000034 method Methods 0.000 description 7
- 210000002966 serum Anatomy 0.000 description 7
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 6
- 229930006000 Sucrose Natural products 0.000 description 6
- 230000009471 action Effects 0.000 description 6
- 235000015895 biscuits Nutrition 0.000 description 6
- 239000003795 chemical substances by application Substances 0.000 description 6
- 239000002994 raw material Substances 0.000 description 6
- 239000000126 substance Substances 0.000 description 6
- 239000005720 sucrose Substances 0.000 description 6
- 241000193403 Clostridium Species 0.000 description 5
- 206010012735 Diarrhoea Diseases 0.000 description 5
- 240000003183 Manihot esculenta Species 0.000 description 5
- 235000016735 Manihot esculenta subsp esculenta Nutrition 0.000 description 5
- 108010058846 Ovalbumin Proteins 0.000 description 5
- 229920002472 Starch Polymers 0.000 description 5
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 5
- 239000000306 component Substances 0.000 description 5
- 229940079593 drug Drugs 0.000 description 5
- 210000003608 fece Anatomy 0.000 description 5
- 210000001035 gastrointestinal tract Anatomy 0.000 description 5
- 244000005709 gut microbiome Species 0.000 description 5
- 235000015243 ice cream Nutrition 0.000 description 5
- 210000000987 immune system Anatomy 0.000 description 5
- 230000006058 immune tolerance Effects 0.000 description 5
- 235000011962 puddings Nutrition 0.000 description 5
- 239000008107 starch Substances 0.000 description 5
- 235000019698 starch Nutrition 0.000 description 5
- 239000006188 syrup Substances 0.000 description 5
- 235000020357 syrup Nutrition 0.000 description 5
- 206010003645 Atopy Diseases 0.000 description 4
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 4
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 4
- JVTAAEKCZFNVCJ-UHFFFAOYSA-N lactic acid Chemical compound CC(O)C(O)=O JVTAAEKCZFNVCJ-UHFFFAOYSA-N 0.000 description 4
- 230000002829 reductive effect Effects 0.000 description 4
- 231100000046 skin rash Toxicity 0.000 description 4
- 230000020192 tolerance induction in gut-associated lymphoid tissue Effects 0.000 description 4
- -1 trisaccharide oligosaccharide Chemical class 0.000 description 4
- 229920001817 Agar Polymers 0.000 description 3
- 235000000832 Ayote Nutrition 0.000 description 3
- 240000004244 Cucurbita moschata Species 0.000 description 3
- 235000009854 Cucurbita moschata Nutrition 0.000 description 3
- 235000009804 Cucurbita pepo subsp pepo Nutrition 0.000 description 3
- 208000004262 Food Hypersensitivity Diseases 0.000 description 3
- 108010001336 Horseradish Peroxidase Proteins 0.000 description 3
- 241000186660 Lactobacillus Species 0.000 description 3
- 235000009499 Vanilla fragrans Nutrition 0.000 description 3
- 244000263375 Vanilla tahitensis Species 0.000 description 3
- 235000012036 Vanilla tahitensis Nutrition 0.000 description 3
- 239000008272 agar Substances 0.000 description 3
- 239000012503 blood component Substances 0.000 description 3
- 201000010099 disease Diseases 0.000 description 3
- 239000002552 dosage form Substances 0.000 description 3
- 238000001035 drying Methods 0.000 description 3
- 230000002708 enhancing effect Effects 0.000 description 3
- 235000020932 food allergy Nutrition 0.000 description 3
- 230000006870 function Effects 0.000 description 3
- 239000008187 granular material Substances 0.000 description 3
- 230000016784 immunoglobulin production Effects 0.000 description 3
- 239000004615 ingredient Substances 0.000 description 3
- 235000013336 milk Nutrition 0.000 description 3
- 239000008267 milk Substances 0.000 description 3
- 210000004080 milk Anatomy 0.000 description 3
- 235000015136 pumpkin Nutrition 0.000 description 3
- 230000009467 reduction Effects 0.000 description 3
- 238000005303 weighing Methods 0.000 description 3
- NHBKXEKEPDILRR-UHFFFAOYSA-N 2,3-bis(butanoylsulfanyl)propyl butanoate Chemical compound CCCC(=O)OCC(SC(=O)CCC)CSC(=O)CCC NHBKXEKEPDILRR-UHFFFAOYSA-N 0.000 description 2
- 244000144730 Amygdalus persica Species 0.000 description 2
- 108010074051 C-Reactive Protein Proteins 0.000 description 2
- 102100032752 C-reactive protein Human genes 0.000 description 2
- 235000000378 Caryota urens Nutrition 0.000 description 2
- 240000000163 Cycas revoluta Species 0.000 description 2
- 235000008601 Cycas revoluta Nutrition 0.000 description 2
- 201000004624 Dermatitis Diseases 0.000 description 2
- 229920001353 Dextrin Polymers 0.000 description 2
- 239000004375 Dextrin Substances 0.000 description 2
- 235000016623 Fragaria vesca Nutrition 0.000 description 2
- 240000009088 Fragaria x ananassa Species 0.000 description 2
- 235000011363 Fragaria x ananassa Nutrition 0.000 description 2
- 235000010103 Metroxylon rumphii Nutrition 0.000 description 2
- 235000006040 Prunus persica var persica Nutrition 0.000 description 2
- 238000010521 absorption reaction Methods 0.000 description 2
- 229940024546 aluminum hydroxide gel Drugs 0.000 description 2
- SMYKVLBUSSNXMV-UHFFFAOYSA-K aluminum;trihydroxide;hydrate Chemical compound O.[OH-].[OH-].[OH-].[Al+3] SMYKVLBUSSNXMV-UHFFFAOYSA-K 0.000 description 2
- 238000009835 boiling Methods 0.000 description 2
- 239000002775 capsule Substances 0.000 description 2
- 239000013078 crystal Substances 0.000 description 2
- 235000019425 dextrin Nutrition 0.000 description 2
- LOKCTEFSRHRXRJ-UHFFFAOYSA-I dipotassium trisodium dihydrogen phosphate hydrogen phosphate dichloride Chemical compound P(=O)(O)(O)[O-].[K+].P(=O)(O)([O-])[O-].[Na+].[Na+].[Cl-].[K+].[Cl-].[Na+] LOKCTEFSRHRXRJ-UHFFFAOYSA-I 0.000 description 2
- 210000000624 ear auricle Anatomy 0.000 description 2
- 238000011156 evaluation Methods 0.000 description 2
- 230000002550 fecal effect Effects 0.000 description 2
- 235000011389 fruit/vegetable juice Nutrition 0.000 description 2
- 239000008169 grapeseed oil Substances 0.000 description 2
- 238000010438 heat treatment Methods 0.000 description 2
- 230000003308 immunostimulating effect Effects 0.000 description 2
- 230000006698 induction Effects 0.000 description 2
- 235000014655 lactic acid Nutrition 0.000 description 2
- 239000004310 lactic acid Substances 0.000 description 2
- 229940039696 lactobacillus Drugs 0.000 description 2
- 235000012054 meals Nutrition 0.000 description 2
- 239000002953 phosphate buffered saline Substances 0.000 description 2
- 235000008476 powdered milk Nutrition 0.000 description 2
- 235000013406 prebiotics Nutrition 0.000 description 2
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 2
- 235000017557 sodium bicarbonate Nutrition 0.000 description 2
- 238000003860 storage Methods 0.000 description 2
- 230000002459 sustained effect Effects 0.000 description 2
- 238000010998 test method Methods 0.000 description 2
- OWEGMIWEEQEYGQ-UHFFFAOYSA-N 100676-05-9 Natural products OC1C(O)C(O)C(CO)OC1OCC1C(O)C(O)C(O)C(OC2C(OC(O)C(O)C2O)CO)O1 OWEGMIWEEQEYGQ-UHFFFAOYSA-N 0.000 description 1
- 235000001674 Agaricus brunnescens Nutrition 0.000 description 1
- 208000035285 Allergic Seasonal Rhinitis Diseases 0.000 description 1
- 241000606125 Bacteroides Species 0.000 description 1
- 241001655328 Bifidobacteriales Species 0.000 description 1
- 235000005979 Citrus limon Nutrition 0.000 description 1
- 244000131522 Citrus pyriformis Species 0.000 description 1
- 244000000626 Daucus carota Species 0.000 description 1
- 235000002767 Daucus carota Nutrition 0.000 description 1
- 206010013786 Dry skin Diseases 0.000 description 1
- 238000002965 ELISA Methods 0.000 description 1
- 241000305071 Enterobacterales Species 0.000 description 1
- 108090000790 Enzymes Proteins 0.000 description 1
- 102000004190 Enzymes Human genes 0.000 description 1
- 206010015150 Erythema Diseases 0.000 description 1
- 208000035874 Excoriation Diseases 0.000 description 1
- 241000192125 Firmicutes Species 0.000 description 1
- 229930091371 Fructose Natural products 0.000 description 1
- 239000005715 Fructose Substances 0.000 description 1
- 241000233866 Fungi Species 0.000 description 1
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 1
- 244000068988 Glycine max Species 0.000 description 1
- 235000010469 Glycine max Nutrition 0.000 description 1
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 1
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 1
- GUBGYTABKSRVRQ-PICCSMPSSA-N Maltose Natural products O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@@H]1O[C@@H]1[C@@H](CO)OC(O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-PICCSMPSSA-N 0.000 description 1
- 239000004909 Moisturizer Substances 0.000 description 1
- 241000699666 Mus <mouse, genus> Species 0.000 description 1
- 208000003251 Pruritus Diseases 0.000 description 1
- 206010039085 Rhinitis allergic Diseases 0.000 description 1
- 206010040844 Skin exfoliation Diseases 0.000 description 1
- 210000000447 Th1 cell Anatomy 0.000 description 1
- 235000021307 Triticum Nutrition 0.000 description 1
- 244000098338 Triticum aestivum Species 0.000 description 1
- 230000005856 abnormality Effects 0.000 description 1
- 238000005299 abrasion Methods 0.000 description 1
- 239000013566 allergen Substances 0.000 description 1
- 201000010105 allergic rhinitis Diseases 0.000 description 1
- 238000004458 analytical method Methods 0.000 description 1
- 230000003266 anti-allergic effect Effects 0.000 description 1
- 208000006673 asthma Diseases 0.000 description 1
- 230000001580 bacterial effect Effects 0.000 description 1
- 210000004369 blood Anatomy 0.000 description 1
- 239000008280 blood Substances 0.000 description 1
- 235000014121 butter Nutrition 0.000 description 1
- 150000001720 carbohydrates Chemical group 0.000 description 1
- 210000004027 cell Anatomy 0.000 description 1
- 235000013339 cereals Nutrition 0.000 description 1
- 238000013375 chromatographic separation Methods 0.000 description 1
- 230000000052 comparative effect Effects 0.000 description 1
- 235000009508 confectionery Nutrition 0.000 description 1
- 239000000470 constituent Substances 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- 235000014510 cooky Nutrition 0.000 description 1
- 235000012343 cottonseed oil Nutrition 0.000 description 1
- 238000002425 crystallisation Methods 0.000 description 1
- 235000014113 dietary fatty acids Nutrition 0.000 description 1
- 239000007884 disintegrant Substances 0.000 description 1
- 238000004090 dissolution Methods 0.000 description 1
- 238000009826 distribution Methods 0.000 description 1
- 239000008298 dragée Substances 0.000 description 1
- 239000006196 drop Substances 0.000 description 1
- 230000000857 drug effect Effects 0.000 description 1
- 230000037336 dry skin Effects 0.000 description 1
- 230000002828 effect on organs or tissue Effects 0.000 description 1
- 235000013601 eggs Nutrition 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 238000006911 enzymatic reaction Methods 0.000 description 1
- 231100000321 erythema Toxicity 0.000 description 1
- TVQGDYNRXLTQAP-UHFFFAOYSA-N ethyl heptanoate Chemical compound CCCCCCC(=O)OCC TVQGDYNRXLTQAP-UHFFFAOYSA-N 0.000 description 1
- 230000005713 exacerbation Effects 0.000 description 1
- 238000004299 exfoliation Methods 0.000 description 1
- 239000000284 extract Substances 0.000 description 1
- 229930195729 fatty acid Natural products 0.000 description 1
- 239000000194 fatty acid Substances 0.000 description 1
- 235000021107 fermented food Nutrition 0.000 description 1
- 235000013312 flour Nutrition 0.000 description 1
- 239000013568 food allergen Substances 0.000 description 1
- 239000008103 glucose Substances 0.000 description 1
- 150000004676 glycans Chemical class 0.000 description 1
- 235000021552 granulated sugar Nutrition 0.000 description 1
- 210000003128 head Anatomy 0.000 description 1
- 235000013402 health food Nutrition 0.000 description 1
- 208000030603 inherited susceptibility to asthma Diseases 0.000 description 1
- 239000003112 inhibitor Substances 0.000 description 1
- 210000000936 intestine Anatomy 0.000 description 1
- 239000008101 lactose Substances 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 239000008297 liquid dosage form Substances 0.000 description 1
- 230000003908 liver function Effects 0.000 description 1
- 230000007774 longterm Effects 0.000 description 1
- 210000003141 lower extremity Anatomy 0.000 description 1
- 239000000314 lubricant Substances 0.000 description 1
- 210000002540 macrophage Anatomy 0.000 description 1
- 239000011777 magnesium Substances 0.000 description 1
- 229910052749 magnesium Inorganic materials 0.000 description 1
- 230000001333 moisturizer Effects 0.000 description 1
- 229940126619 mouse monoclonal antibody Drugs 0.000 description 1
- 210000000822 natural killer cell Anatomy 0.000 description 1
- 210000000056 organ Anatomy 0.000 description 1
- 230000000704 physical effect Effects 0.000 description 1
- 239000000419 plant extract Substances 0.000 description 1
- 229920001282 polysaccharide Polymers 0.000 description 1
- 239000005017 polysaccharide Substances 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 230000003449 preventive effect Effects 0.000 description 1
- 239000006041 probiotic Substances 0.000 description 1
- 235000018291 probiotics Nutrition 0.000 description 1
- 239000000047 product Substances 0.000 description 1
- 230000002062 proliferating effect Effects 0.000 description 1
- 108090000623 proteins and genes Proteins 0.000 description 1
- 102000004169 proteins and genes Human genes 0.000 description 1
- 150000003212 purines Chemical class 0.000 description 1
- 238000012552 review Methods 0.000 description 1
- 229940100486 rice starch Drugs 0.000 description 1
- 239000000523 sample Substances 0.000 description 1
- 239000012488 sample solution Substances 0.000 description 1
- 230000003248 secreting effect Effects 0.000 description 1
- 238000004904 shortening Methods 0.000 description 1
- 238000009491 slugging Methods 0.000 description 1
- 239000007909 solid dosage form Substances 0.000 description 1
- 238000007619 statistical method Methods 0.000 description 1
- 150000003431 steroids Chemical class 0.000 description 1
- 238000002563 stool test Methods 0.000 description 1
- 239000006228 supernatant Substances 0.000 description 1
- 239000003826 tablet Substances 0.000 description 1
- 150000004044 tetrasaccharides Chemical class 0.000 description 1
- 229940124597 therapeutic agent Drugs 0.000 description 1
- 230000001225 therapeutic effect Effects 0.000 description 1
- 230000001052 transient effect Effects 0.000 description 1
- 150000004043 trisaccharides Chemical class 0.000 description 1
- 210000001364 upper extremity Anatomy 0.000 description 1
- 235000015112 vegetable and seed oil Nutrition 0.000 description 1
- 235000019871 vegetable fat Nutrition 0.000 description 1
- 239000008158 vegetable oil Substances 0.000 description 1
- 235000013311 vegetables Nutrition 0.000 description 1
- 238000009423 ventilation Methods 0.000 description 1
- 235000013618 yogurt Nutrition 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/702—Oligosaccharides, i.e. having three to five saccharide radicals attached to each other by glycosidic linkages
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23L—FOODS, FOODSTUFFS, OR NON-ALCOHOLIC BEVERAGES, NOT COVERED BY SUBCLASSES A21D OR A23B-A23J; THEIR PREPARATION OR TREATMENT, e.g. COOKING, MODIFICATION OF NUTRITIVE QUALITIES, PHYSICAL TREATMENT; PRESERVATION OF FOODS OR FOODSTUFFS, IN GENERAL
- A23L33/00—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof
- A23L33/10—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof using additives
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/08—Antiallergic agents
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23V—INDEXING SCHEME RELATING TO FOODS, FOODSTUFFS OR NON-ALCOHOLIC BEVERAGES AND LACTIC OR PROPIONIC ACID BACTERIA USED IN FOODSTUFFS OR FOOD PREPARATION
- A23V2002/00—Food compositions, function of food ingredients or processes for food or foodstuffs
Description
実施例1では、1−ケストースがIgAの産生に与える影響を調べる実験を行った。
実施例2では、1−ケストースがIgG1およびIgEの産生に与える影響を調べるため、無菌マウスに1−ケストースを投与し、その投与前後における血清中のIgG1およびIgEの量を測定した。
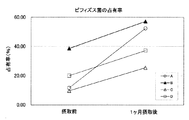
本実施例3では、1−ケストースがヒトの血清中におけるIgEの量に与える影響を調べるため、被験者に1−ケストースを投与し、その投与前後における血清中の非特異的IgEの量を測定した。
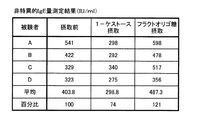
本実施例4では、無菌マウスを使ってフラクトオリゴ糖を構成する各組成物の腸内菌叢の改善効果の強さを比較した。実験に供したマウスは、無菌状態で誕生させた4週齢雄マウス(BALB/c系統)であり、このマウスを一群10〜15匹用いた。これらのマウスにヒト乳児糞便を100倍に希釈したものを0.5ml経口摂取し、無菌状態で2週間育成した。フラクトオリゴ糖の構成物は、3糖類のケストース、4糖類のニストース、5糖類のF−ニストースである。本実施例4で使用したケストースは、1−ケストース99.0%、ニストース0.5%、スクロース0.5%の組成物である。また、ニストースは、ニストース99.0%、1−ケストース0.9%、スクロース0.1%の組成物である。また、F−ニストースは、F−ニストース82.0%、その他の5糖類13.0%、その他の成分5.0%の組成物である。その他、比較のためコントロール群には滅菌水を強制投与したマウスと、一般的なフラクトオリゴ糖(1−ケストース重量35.8%,ニストース50.9重量%,F−ニストース8.5重量%)を投与したマウスについても測定した。図10に各供試糖の組成を示す。各オリゴ糖を無菌マウスに5日間経口投与し、ビフィズス菌の増殖程度として総菌数に対する割合を求めた。
上記実施例4の結果を分析すれば、ビフィズス菌増殖効果は、フラクトオリゴ糖の組成物のうち1−ケストースが最も高い効果を発揮し、フラクトオリゴ糖よりも好結果を示した。このことから腸内環境の改善には純度の高い1−ケストースが効果的であることが認められるところ、さらに直接的なアレルギー抑制効果を確認するため、実施例5では、1−ケストースとフラクトオリゴ糖と摂取することによるIgE抑制効果について実験した。
上記各実施例により、成人に対して1−ケストースのプレバイオティクスとしての効果を示す量は1日3gであることが確認できている。その後、ボランティアによる実験により1日2gで便通改善効果が示されている。そこで、本実施例6では、さらに少量の1日1gで腸内環境の改善効果を示すか否かの確認のため、ボランティアによる試験を行った。被験者は38歳から56歳までの健康成人男性4名であって、各人の体重は被験者Aが67kg、被験者Bが56kg、被験者Cが59kg、被験者Dが63kgである。
上記各実施例により、日常的にアレルギー症状の自覚がある成人に対して、1−ケストースがアレルギー原因であるIgE抗体の産生抑制、IgA抗体の増強、ビフィズス菌の増殖活性等の効果が確認された。そこで、実施例7では、より根本的な対策として、アトピー素因をもつアレルギー疾患患者を乳幼児期に治療することにより、その後の様々なアレルギー発生の予防が期待できることに鑑み、アトピー性皮膚炎の症状をもつ乳幼児を対象とした臨床試験を行った。
[食品製造例1:ビスケット30個分、1−ケストース含量1g/1個]
サクサク粉(サゴヤシでんぷん)100g、タピオカ粉(キャッサバ芋でんぷん)50g、カボチャパウダー(カボチャを蒸して乾燥させ粉状にしたもの)9g、重曹1g、1−ケストース30g、綿実ショートニング(無塩バターの代わりに使用、アレルギー用に辻安全食品から販売されている)12g、ブドウ油(別名グレープシード油、ブドウ種子から取った油でアレルギー用に販売されている)24g、レモン汁少々、バニラエッセンス1滴、以上の原料をパラパラになるまで混合した。その後、沸騰水125ccを少量ずつ加えて耳たぶくらいの固さになるまで捏ねて生地とした。
サクサク粉(サゴヤシでんぷん)100g、タピオカ粉(キャッサバ芋でんぷん)100g、1−ケストース15g、砂糖15g、以上の原料を混合した。その後、沸騰水220ccを少量ずつ加えて耳たぶくらいの固さになるまで捏ねた。これを3等分し、乾燥しないようにそれぞれラップに包んだ。この3等分した1つに抹茶1gを加え、別の1つにいちごジャム7gを加え混ぜ、残りの1つは何も加えない生地とした。上記3種の生地をそれぞれ直径3cmの棒状に延ばして、それぞれ12等分し団子状に丸めた。鍋でたっぷり沸かした湯中に上記団子状に丸めた生地を入れてゆでた。温かいうちにジャム団子、抹茶団子、白団子の順で串に刺し串団子とした。
アレルギー用粉ミルク(森永ニューMA1また明治のびやか)60gを水200ccで溶かしたものにカボチャパウダー(カボチャを蒸して乾燥させ粉状にしたもの)3gを加えて調製ミルクを先に作っておいた。
寒天パウダー9gと1−ケストース20gを混合し、水100ccを加えて混ぜた。これを10分放置した後に加熱して溶かした。これにアレルギー用粉ミルク(森永ニューMA1又は明治のびやか)110gを水200ccで溶いたものと黄桃ピューレ(黄桃の缶詰を汁ごとフードプロセッサーにかけピューレ状にしたもの)100gを加えて加温しながらよく混合し、バニラエッセンス1滴を加えた。これをタッパーに移して、粗熱をとってから冷蔵庫に入れて冷やし固めた。固まったらフードプロセッサーにかけて再度冷やし固めた。アイスデッシャーですくいとり約50gを1人前とした。
大和芋の皮をむいて酢水にさらしたもの80gをすり下ろしながら砂糖60gを2回に分けて混合し、さらに1−ケストース30gを加えよく混合した。これにニンジンのすり下ろし70g、水20cc、重曹1gを合わせたものを少しずつ加えてさらに混合した。次に上新粉90gをふるいにかけながら加えて、よく混合した後、型に入れてそのまま20分休ませた。蒸気の上がった蒸し器に割り箸を2本置き、その上に上記型をのせて20分ほど蒸した。粗熱がとれたら型をはずして切り分けて、約35gを1人前とした。
つぎに、1−ケストースを使用して主にアトピー性皮膚炎治療剤を想定した薬剤の製造例について説明する。
薬剤製造例1では、1−ケストース800g、乳糖200gをよく混合した後、90%エタノール300mLを添加して湿潤させた。湿潤粉末を造粒した後、60℃で16時間通風乾燥した。乾燥後、整粒して適当な細かさの散剤を得た。
薬剤製造例2の錠剤は1−ケストースを含む粉末混合物を作り、顆粒化またはスラグ化し、次いで崩壊剤または滑沢剤を加えた後、打錠することにより製造することができる。具体的には、1−ケストース300g、粉末還元麦芽糖水飴380g、コメデンプン180g、デキストリン100gをよく混合した後、90%エタノール300mLを添加して湿潤させた。湿潤粉末を押し出し造粒した後、60℃で16時間通風乾燥した。乾燥後、顆粒を850μmの篩を用いて整粒し、続いて顆粒470gにショ糖脂肪酸エステル50gを添加し、混合した後、ロータリー打錠機(6B−2、菊水製作所製)を用いて打錠し、直径8mm、重量200mgの錠剤を得た。
Claims (1)
- フラクトオリゴ糖において1−ケストースが最大組成比率の第1組成物であることを特徴とするアレルギー抑制剤。
Priority Applications (8)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2005371005A JP4162147B2 (ja) | 2005-04-21 | 2005-12-22 | アレルギー抑制剤 |
| DK06732082.0T DK1878738T3 (da) | 2005-04-21 | 2006-04-19 | 1-Kestose til behandling af allergi og atopisk dermatitis |
| AT06732082T ATE517907T1 (de) | 2005-04-21 | 2006-04-19 | 1-kestose zur behandlung von allergie und atopischer dermatitis |
| PCT/JP2006/308175 WO2006115136A1 (ja) | 2005-04-21 | 2006-04-19 | アレルギー抑制組成物、アレルギー抑制食品、およびアレルギー抑制剤 |
| EP06732082A EP1878738B1 (en) | 2005-04-21 | 2006-04-19 | 1-kestose for treating allergy and atopic dermatitis |
| SI200631077T SI1878738T1 (sl) | 2005-04-21 | 2006-04-19 | 1-kestoza za zdravljenje alergije in atopiäśnega dermatitisa |
| PT06732082T PT1878738E (pt) | 2005-04-21 | 2006-04-19 | 1-questose para tratar a alergia e a dermatite atópica |
| CY20111100834T CY1112180T1 (el) | 2005-04-21 | 2011-08-30 | 1-κεστοζη για θεραπεια αλλεργιας και ατοπικης δερματιτιδας |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2005123723 | 2005-04-21 | ||
| JP2005371005A JP4162147B2 (ja) | 2005-04-21 | 2005-12-22 | アレルギー抑制剤 |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2008166463A Division JP2008280354A (ja) | 2005-04-21 | 2008-06-25 | アレルギー抑制オリゴ糖 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2006321786A JP2006321786A (ja) | 2006-11-30 |
| JP2006321786A5 JP2006321786A5 (ja) | 2008-08-14 |
| JP4162147B2 true JP4162147B2 (ja) | 2008-10-08 |
Family
ID=37214755
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2005371005A Active JP4162147B2 (ja) | 2005-04-21 | 2005-12-22 | アレルギー抑制剤 |
Country Status (8)
| Country | Link |
|---|---|
| EP (1) | EP1878738B1 (ja) |
| JP (1) | JP4162147B2 (ja) |
| AT (1) | ATE517907T1 (ja) |
| CY (1) | CY1112180T1 (ja) |
| DK (1) | DK1878738T3 (ja) |
| PT (1) | PT1878738E (ja) |
| SI (1) | SI1878738T1 (ja) |
| WO (1) | WO2006115136A1 (ja) |
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2011102529A1 (ja) | 2010-02-22 | 2011-08-25 | 有限会社東海医学検査研究所 | 上皮細胞間接着増強剤およびこれを用いたアレルギー改善、治療または予防剤 |
| WO2011108275A1 (ja) | 2010-03-04 | 2011-09-09 | 株式会社ロッテ | イムノグロブリンa分泌促進剤 |
| WO2015099166A1 (ja) | 2013-12-27 | 2015-07-02 | 物産フードサイエンス株式会社 | 改良型β-フルクトフラノシダーゼ |
| US10240136B2 (en) | 2015-03-11 | 2019-03-26 | B Food Science Co., Ltd. | β-fructofuranosidase |
| KR20210096014A (ko) | 2020-01-27 | 2021-08-04 | 붓산 푸드사이언스 가부시키가이샤 | 1-케스토오스를 함유하는 고체당의 제조방법 및 고체당 |
Families Citing this family (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA2628035A1 (en) * | 2005-10-13 | 2007-04-19 | Meiji Seika Kaisha, Ltd. | Composition for improving intestinal microflora |
| JPWO2009091035A1 (ja) * | 2008-01-18 | 2011-05-26 | 明治製菓株式会社 | 1−ケストース含有焼き菓子およびその製造方法 |
| JP2012176907A (ja) * | 2011-02-25 | 2012-09-13 | Glico Dairy Products Co Ltd | フラクトオリゴ糖を有効成分とするミオシン軽鎖脱リン酸化促進剤、疾患の予防又は治療剤、及び飲食品 |
| JP5923410B2 (ja) * | 2012-08-10 | 2016-05-24 | 花王株式会社 | コラーゲンゲル収縮促進剤 |
| WO2017159643A1 (ja) * | 2016-03-14 | 2017-09-21 | 物産フードサイエンス株式会社 | 腸内酪酸増加剤および酪酸産生菌増殖剤 |
| SG11201807616RA (en) * | 2016-03-14 | 2018-10-30 | B Food Science Co Ltd | Proliferative agent for faecalibacterium |
| GB2548848A (en) * | 2016-03-30 | 2017-10-04 | The Inst Of Food Res | Levan polysaccharide to modulate cell function |
| JP7097259B2 (ja) * | 2018-08-08 | 2022-07-07 | 物産フードサイエンス株式会社 | ハナバチ寿命延長剤 |
| JP6842072B2 (ja) * | 2019-03-07 | 2021-03-17 | 物産フードサイエンス株式会社 | エガセラ属細菌の菌数抑制剤 |
| JP7372112B2 (ja) | 2019-10-29 | 2023-10-31 | 大塚製薬株式会社 | 抗i型アレルギー剤 |
| KR20220097323A (ko) * | 2020-12-31 | 2022-07-07 | 주식회사 삼양사 | 케스토스를 이용한 장내 미생물의 생육 증진용도 |
| CN113461751A (zh) * | 2021-07-15 | 2021-10-01 | 量子高科(广东)生物有限公司 | 一种高蔗果三糖含量低聚果糖及其应用 |
Family Cites Families (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH02235823A (ja) * | 1989-03-09 | 1990-09-18 | Watanabe Mitsuko | 抗アレルギー剤 |
| JPH0670075B2 (ja) * | 1990-08-28 | 1994-09-07 | ホクレン農業協同組合連合会 | 1―ケストース結晶およびその製造方法 |
| US5843922A (en) * | 1994-07-29 | 1998-12-01 | Fuisz Technologies Ltd. | Preparation of oligosaccharides and products therefrom |
| JPH08157379A (ja) | 1994-12-02 | 1996-06-18 | Meiji Seika Kaisha Ltd | アレルギー予防材 |
| JP3257929B2 (ja) * | 1995-06-23 | 2002-02-18 | 明治製菓株式会社 | 機能性低カロリー甘味料 |
| US5827526A (en) * | 1995-07-11 | 1998-10-27 | Abbott Laboratories | Use of indigestible oligosaccharides to prevent gastrointestinal infections and reduce duration of diarrhea in humans |
| JPH0975035A (ja) * | 1995-09-12 | 1997-03-25 | Meiji Seika Kaisha Ltd | 機能性錠菓及び粉末飲料 |
| JP3655965B2 (ja) * | 1996-06-13 | 2005-06-02 | 明治製菓株式会社 | 結晶ケストース含有キャンデー |
| JP2000232878A (ja) * | 1999-02-12 | 2000-08-29 | Hokuren Federation Of Agricult Coop:The | フラクトシル転移酵素、並びに該酵素を用いた1−ケストース及びニストースの分別製造方法 |
| EP1421945A4 (en) * | 2001-08-10 | 2005-06-22 | Hokkaido Tech Licensing Office | ABSORBENT / ADSORBENT OF BILARY ACID |
| JP2003201239A (ja) * | 2001-11-05 | 2003-07-18 | Meiji Milk Prod Co Ltd | 免疫賦活食品組成物 |
| JP4669235B2 (ja) * | 2004-04-21 | 2011-04-13 | ホクレン農業協同組合連合会 | 腸内環境下ビフィズス菌増殖剤 |
| JP4704007B2 (ja) * | 2004-05-12 | 2011-06-15 | ホクレン農業協同組合連合会 | 皮膚水分向上剤 |
-
2005
- 2005-12-22 JP JP2005371005A patent/JP4162147B2/ja active Active
-
2006
- 2006-04-19 AT AT06732082T patent/ATE517907T1/de active
- 2006-04-19 PT PT06732082T patent/PT1878738E/pt unknown
- 2006-04-19 WO PCT/JP2006/308175 patent/WO2006115136A1/ja active Application Filing
- 2006-04-19 SI SI200631077T patent/SI1878738T1/sl unknown
- 2006-04-19 EP EP06732082A patent/EP1878738B1/en not_active Not-in-force
- 2006-04-19 DK DK06732082.0T patent/DK1878738T3/da active
-
2011
- 2011-08-30 CY CY20111100834T patent/CY1112180T1/el unknown
Cited By (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2011102529A1 (ja) | 2010-02-22 | 2011-08-25 | 有限会社東海医学検査研究所 | 上皮細胞間接着増強剤およびこれを用いたアレルギー改善、治療または予防剤 |
| WO2011108275A1 (ja) | 2010-03-04 | 2011-09-09 | 株式会社ロッテ | イムノグロブリンa分泌促進剤 |
| KR20130037672A (ko) | 2010-03-04 | 2013-04-16 | 가부시키가이샤 롯데 | 이뮤노 글로불린 a 분비 촉진제 |
| WO2015099166A1 (ja) | 2013-12-27 | 2015-07-02 | 物産フードサイエンス株式会社 | 改良型β-フルクトフラノシダーゼ |
| KR20160108375A (ko) | 2013-12-27 | 2016-09-19 | 붓산 푸드사이언스 가부시키가이샤 | 개량형 β-프룩토프라노시다아제 |
| US9963691B2 (en) | 2013-12-27 | 2018-05-08 | B Food Science Co., Ltd. | β-fructofuranosidase |
| US10240136B2 (en) | 2015-03-11 | 2019-03-26 | B Food Science Co., Ltd. | β-fructofuranosidase |
| KR20210096014A (ko) | 2020-01-27 | 2021-08-04 | 붓산 푸드사이언스 가부시키가이샤 | 1-케스토오스를 함유하는 고체당의 제조방법 및 고체당 |
Also Published As
| Publication number | Publication date |
|---|---|
| EP1878738A1 (en) | 2008-01-16 |
| ATE517907T1 (de) | 2011-08-15 |
| EP1878738A4 (en) | 2008-09-17 |
| PT1878738E (pt) | 2011-09-02 |
| EP1878738B1 (en) | 2011-07-27 |
| JP2006321786A (ja) | 2006-11-30 |
| DK1878738T3 (da) | 2011-08-29 |
| WO2006115136A1 (ja) | 2006-11-02 |
| SI1878738T1 (sl) | 2011-12-30 |
| CY1112180T1 (el) | 2015-12-09 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4162147B2 (ja) | アレルギー抑制剤 | |
| JP6882931B2 (ja) | プレバイオティック製剤および使用方法 | |
| CA2473209C (en) | Stimulation of the immune system with polydextrose | |
| JP5877902B2 (ja) | バクテロイデス門の胃腸管微生物相対フィルミクテス門の微生物相の比を上昇させるための組成物および製剤の使用 | |
| RU2464995C2 (ru) | Добавка к материнской диете | |
| KR20150118084A (ko) | 비만 및 비만 관련 질환을 치료하기 위한 프로바이오틱 조성물 및 방법 | |
| JP7280069B2 (ja) | 機能性消化管障害予防又は改善用組成物、並びに、該機能性消化管障害予防又は改善用組成物を用いた医薬品組成物及び飲食品組成物 | |
| JP2017095500A (ja) | 精神能力を向上させるためのイソマルツロースの使用 | |
| JP2006512298A (ja) | 水素化形態の縮合パラチノース | |
| JP2008280354A (ja) | アレルギー抑制オリゴ糖 | |
| JP7260903B2 (ja) | 乳糖果糖オリゴ糖(ラクトスクロース)を有効成分として含有するストレス低減用食品組成物 | |
| WO2019170790A1 (en) | Yeast beta glucans | |
| US20210023123A1 (en) | Dietary fiber compositions for curative or prophylactic treatment of obesity and other conditions | |
| JP7257665B2 (ja) | 経口組成物 | |
| JP2019127439A (ja) | 桑葉を含むサプリメント | |
| JP7063514B2 (ja) | 起立性低血圧の予防又は改善用剤及びそれを含む組成物 | |
| JP5420223B2 (ja) | 筋肉量低下抑制剤 | |
| JP2010013395A (ja) | メタボリックシンドローム症状の予防又は改善剤 | |
| ChaMp | Dietary Fibers in Gastroenterology | |
| Haskey | The effect of a prebiotic with a probiotic on symptoms and quality of life in ulcerative colitis | |
| Gavin | Influence of nutrient intake on colonic function and stool composition in enterally fed cystic fibrosis patients | |
| Elbostany | EFFECT OF PRO AND PRE–BIOTIC SUPPLEMENTATIONS IN WEANING FOODS ON SOME MINERAL ABSORPTION | |
| Wagner | Milk-free food | |
| Sawalea et al. | Food Bioscience |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20080625 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20080625 |
|
| A871 | Explanation of circumstances concerning accelerated examination |
Free format text: JAPANESE INTERMEDIATE CODE: A871 Effective date: 20080625 |
|
| A975 | Report on accelerated examination |
Free format text: JAPANESE INTERMEDIATE CODE: A971005 Effective date: 20080710 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20080716 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20080717 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20110801 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 Ref document number: 4162147 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20110801 Year of fee payment: 3 |
|
| S111 | Request for change of ownership or part of ownership |
Free format text: JAPANESE INTERMEDIATE CODE: R313114 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20110801 Year of fee payment: 3 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20110801 Year of fee payment: 3 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20120801 Year of fee payment: 4 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20120801 Year of fee payment: 4 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20120801 Year of fee payment: 4 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20130801 Year of fee payment: 5 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| S111 | Request for change of ownership or part of ownership |
Free format text: JAPANESE INTERMEDIATE CODE: R313117 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |