JP2022166326A - コレスチラミン顆粒、経口コレスチラミン製剤、及びそれらの使用 - Google Patents
コレスチラミン顆粒、経口コレスチラミン製剤、及びそれらの使用 Download PDFInfo
- Publication number
- JP2022166326A JP2022166326A JP2022135754A JP2022135754A JP2022166326A JP 2022166326 A JP2022166326 A JP 2022166326A JP 2022135754 A JP2022135754 A JP 2022135754A JP 2022135754 A JP2022135754 A JP 2022135754A JP 2022166326 A JP2022166326 A JP 2022166326A
- Authority
- JP
- Japan
- Prior art keywords
- cholestyramine
- granules
- formulation
- acid
- colon
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/74—Synthetic polymeric materials
- A61K31/785—Polymers containing nitrogen
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/16—Agglomerates; Granulates; Microbeadlets ; Microspheres; Pellets; Solid products obtained by spray drying, spray freeze drying, spray congealing,(multiple) emulsion solvent evaporation or extraction
- A61K9/1605—Excipients; Inactive ingredients
- A61K9/1629—Organic macromolecular compounds
- A61K9/1635—Organic macromolecular compounds obtained by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyvinyl pyrrolidone, poly(meth)acrylates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/16—Agglomerates; Granulates; Microbeadlets ; Microspheres; Pellets; Solid products obtained by spray drying, spray freeze drying, spray congealing,(multiple) emulsion solvent evaporation or extraction
- A61K9/1605—Excipients; Inactive ingredients
- A61K9/1629—Organic macromolecular compounds
- A61K9/1652—Polysaccharides, e.g. alginate, cellulose derivatives; Cyclodextrin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/50—Microcapsules having a gas, liquid or semi-solid filling; Solid microparticles or pellets surrounded by a distinct coating layer, e.g. coated microspheres, coated drug crystals
- A61K9/5005—Wall or coating material
- A61K9/5021—Organic macromolecular compounds
- A61K9/5026—Organic macromolecular compounds obtained by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyvinyl pyrrolidone, poly(meth)acrylates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/50—Microcapsules having a gas, liquid or semi-solid filling; Solid microparticles or pellets surrounded by a distinct coating layer, e.g. coated microspheres, coated drug crystals
- A61K9/5005—Wall or coating material
- A61K9/5021—Organic macromolecular compounds
- A61K9/5036—Polysaccharides, e.g. gums, alginate; Cyclodextrin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/50—Microcapsules having a gas, liquid or semi-solid filling; Solid microparticles or pellets surrounded by a distinct coating layer, e.g. coated microspheres, coated drug crystals
- A61K9/5073—Microcapsules having a gas, liquid or semi-solid filling; Solid microparticles or pellets surrounded by a distinct coating layer, e.g. coated microspheres, coated drug crystals having two or more different coatings optionally including drug-containing subcoatings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/12—Antidiarrhoeals
Landscapes
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Pharmacology & Pharmacy (AREA)
- Veterinary Medicine (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Epidemiology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Organic Chemistry (AREA)
- Medicinal Preparation (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
Abstract
【解決手段】各顆粒が少なくとも70%w/wのコレスチラミン、並びに、i. 少なくとも6%w/wの結合剤及び少なくとも2%w/wのアクリレートコポリマーの組合せ、又は、ii. 少なくとも5%w/wの結合剤及び少なくとも3%w/wのアクリレートコポリマーの組合せ、又は、iii. 少なくとも6%w/wの結合剤、少なくとも1%w/wのアクリレートコポリマー及び5から15%w/wの微結晶セルロースの組合せを含み、結合剤が、セルロースエーテル、ビニルピロリドン系ポリマー、又はそれらの組合せを含む、顆粒。
【選択図】なし
Description
i.少なくとも7%w/wの結合剤;又は
ii.少なくとも6%w/wの結合剤及び少なくとも2%w/wのアクリレートコポリマーの組合せ;又は
iii.少なくとも5%w/wの結合剤及び少なくとも3%w/wのアクリレートコポリマーの組合せ;又は
iv.少なくとも6%w/wの結合剤、少なくとも1%w/wのアクリレートコポリマー及び5から15%w/wの微結晶セルロースの組合せ;
を含む、顆粒群を提供する。
i.少なくとも7%w/wの結合剤;又は
ii.少なくとも6%w/wの結合剤及び少なくとも2%w/wのアクリレートコポリマーの組合せ;又は
iii.少なくとも5%w/wの結合剤及び少なくとも3%w/wのアクリレートコポリマーの組合せ;又は
iv.少なくとも6%w/wの結合剤、少なくとも1%w/wのアクリレートコポリマー及び5から15%w/wの微結晶セルロースの組合せ;
を含み、
結合剤が、セルロースエーテル、ビニルピロリドン系ポリマー、ショ糖、乳糖、カラギーナン、デンプン、アルギン酸、アルギン酸ナトリウム、ベヘン酸グリセリル、ポリエチレンオキシド、キトサン、カルナウバロウ、ゼラチン、アカシア、グアーガム及びポリビニルアルコール-ポリエチレングリコール-グラフトコポリマー、又はそれらの混合物から成る群から選択される1つの剤を含む、顆粒群に関する。
i.少なくとも7%w/wの結合剤;又は
ii.少なくとも6%w/wの結合剤及び少なくとも2%w/wのアクリレートコポリマーの組合せ;又は
iii.少なくとも5%w/wの結合剤及び少なくとも3%w/wのアクリレートコポリマーの組合せ;又は
iv.少なくとも6%w/wの結合剤、少なくとも1%w/wのアクリレートコポリマー及び5から15%w/wの微結晶セルロースの組合せ;
を含み、結合剤が、セルロースエーテル、ビニルピロリドン系ポリマー、又はそれらの組合せを含む、顆粒群に関する。
a)本明細書に開示の複数の顆粒;及び
b)前記顆粒周囲の結腸放出コーティング
を含む、コレスチラミンの結腸への標的送達のための経口製剤に関する。
a)各顆粒がコレスチラミンを含む、複数の顆粒;及び
b)コーティングが結腸におけるコレスチラミンの標的化放出の能力を有する、前記顆粒周囲のコーティング
を含む経口製剤であって、コレスチラミンの70%超が結腸において放出される経口製剤に関する。
a)各顆粒がコレスチラミンを含む、複数の顆粒;及び
b)コーティングが結腸におけるコレスチラミンの標的化放出の能力を有する、前記顆粒周囲のコーティング
を含む経口製剤であって、コレスチラミンの30%未満が小腸において放出される経口製剤に関する。
a)各顆粒がコレスチラミンを含む、複数の顆粒;及び
b)コーティングが結腸におけるコレスチラミンの標的化放出の能力を有する、前記顆粒周囲のコーティング、
を含む経口製剤であって、顆粒が、欧州薬局方第8版、試験2.9.41を用いて測定したとき3.5%未満の摩損度を呈する経口製剤に関する。
a)各顆粒がコレスチラミンを含む、複数の顆粒;及び
b)コーティングが結腸におけるコレスチラミンの標的化放出の能力を有する、前記顆粒周囲のコーティング、
を含む経口製剤であって、米国薬局方溶解装置2(パドル)、欧州薬局方2.9.3を用いて測定したときpH5.5においてコレスチラミンの30%未満が6時間後に放出される経口製剤に関する。
a)各顆粒がコレスチラミンを含む、複数の顆粒;及び
b)コーティングが結腸におけるコレスチラミンの標的化放出の能力を有する、前記顆粒周囲のコーティング、
を含む経口製剤であって、米国薬局方溶解装置2(パドル)、欧州薬局方2.9.3を用いて測定したときpH5.5において6時間後に、コール酸の30%未満の封鎖を示す経口製剤に関する。
a)各顆粒がコレスチラミンを含む、複数の顆粒;及び
b)コーティングが結腸におけるコレスチラミンの標的化放出の能力を有する、前記顆粒周囲のコーティング、
を含む経口製剤であって、米国薬局方溶解装置2(パドル)、欧州薬局方2.9.3を用いて測定したときpH1で2時間、それに続いてpH6.8で4時間の後に、コール酸の30%超の封鎖を示す経口製剤に関する。
a)各顆粒がコレスチラミンを含む、複数の顆粒;及び
b)コーティングが結腸におけるコレスチラミンの標的化放出の能力を有する、前記顆粒周囲のコーティング、
を含む経口製剤であって、米国薬局方溶解装置2(パドル)、欧州薬局方2.9.3を用いて測定したときpH1で2時間後に、コール酸の30%未満の封鎖を示す経口製剤に関する。
a)各顆粒がコレスチラミンを含む、複数の顆粒;及び
b)コーティングが結腸におけるコレスチラミンの標的化放出の能力を有する、前記顆粒周囲のコーティング、
を含む経口製剤であって、米国薬局方溶解装置2(パドル)、欧州薬局方2.9.3を用いて測定したときpH1で2時間、それに続いてpH7.4で4時間の後に、コール酸の30%超の封鎖を示す経口製剤に関する。
一実施形態において、顆粒周囲の結腸放出コーティングは、結腸におけるコレスチラミンの酵素-制御放出を可能にする。その場合にコーティング層は、結腸内に存在する細菌酵素により分解されるが消化管内に存在するヒト酵素によっては分解されない生分解性ポリマーを含む。顆粒からのコレスチラミンの放出は、細菌環境の変化によって誘発され、実質的には、被覆された顆粒が結腸に到達するまでは妨げられる。
別の一実施形態において、顆粒周囲の結腸放出コーティングは、結腸におけるコレスチラミンのpH-及び拡散-制御放出を可能にする。その場合にコーティングは、顆粒周囲の拡散-制御内部コーティング層及び腸溶性の(pH-制御)外部コーティング層を含む。
a)各顆粒がコレスチラミンを含む、複数の顆粒;及び
b)コーティングが結腸におけるコレスチラミンの標的化放出の能力を有する、各顆粒周囲のコーティング、
を含む経口製剤であって、
本明細書の経口製剤が、Simulator of the Human Intestinal Microbial Ecosystem(SHIME)モデルで測定して、2時間の小腸インキュベーション後に、コール酸、ケノデオキシコール酸、及びデオキシコール酸のうちの1つ又は複数の約30%未満の封鎖を示す経口製剤に関する。
1,1-ジオキソ-3,3-ジブチル-5-フェニル-7-メチルチオ-8-(N-{(R)-α-[N-(カルボキシメチル)カルバモイル]ベンジル}カルバモイルメトキシ)-2,3,4,5-テトラヒドロ-1,2,5-ベンゾチアジアゼピン;
1,1-ジオキソ-3,3-ジブチル-5-フェニル-7-メチルチオ-8-(N-{(R)-α-[N'-((S)-1-カルボキシエチル)カルバモイル]ベンジル}カルバモイルメトキシ)-2,3,4,5-テトラヒドロ-1,5-ベンゾチアゼピン;
1,1-ジオキソ-3,3-ジブチル-5-フェニル-7-メチルチオ-8-(N-{(R)-α-[N-((S)-1-カルボキシプロピル)カルバモイル]ベンジル}カルバモイルメトキシ)-2,3,4,5-テトラヒドロ-1,2,5-ベンゾチアジアゼピン;
1,1-ジオキソ-3,3-ジブチル-5-フェニル-7-メチルチオ-8-(N-{(R)-α-[N-((R)-1-カルボキシ-2-メチルチオエチル)カルバモイル]ベンジル}カルバモイルメトキシ)-2,3,4,5-テトラヒドロ-1,2,5-ベンゾチアジアゼピン;
1,1-ジオキソ-3,3-ジブチル-5-フェニル-7-メチルチオ-8-(N-{(R)-α-[N-((S)-1-カルボキシプロピル)カルバモイル]-4-ヒドロキシベンジル}カルバモイルメトキシ)-2,3,4,5-テトラヒドロ-1,2,5-ベンゾチアジアゼピン;
1,1-ジオキソ-3,3-ジブチル-5-フェニル-7-メチルチオ-8-(N-{(R)-α-[N-((R)-1-カルボキシ-2-メチルチオエチル)カルバモイル]-4-ヒドロキシベンジル}カルバモイルメトキシ)-2,3,4,5-テトラヒドロ-1,2,5-ベンゾチアジアゼピン;
1,1-ジオキソ-3,3-ジブチル-5-フェニル-7-メチルチオ-8-(N-{(R)-α-[N-((S)-1-カルボキシ-2-メチルプロピル)-カルバモイル]ベンジル}カルバモイルメトキシ)-2,3,4,5-テトラヒドロ-1,2,5-ベンゾチアジアゼピン;
1,1-ジオキソ-3,3-ジブチル-5-フェニル-7-メチルチオ-8-(N-{(R)-α-[N-((S)-1-カルボキシ-2-(R)-ヒドロキシプロピル)カルバモイル]-4-ヒドロキシベンジル}カルバモイルメトキシ)-2,3,4,5-テトラヒドロ-1,2,5-ベンゾチアジアゼピン;
1,1-ジオキソ-3,3-ジブチル-5-フェニル-7-メチルチオ-8-(N-{(R)-α-[N-((S)-1-カルボキシブチル)カルバモイル]-4-ヒドロキシベンジル}カルバモイルメトキシ)-2,3,4,5-テトラヒドロ-1,2,5-ベンゾチアジアゼピン;
1,1-ジオキソ-3,3-ジブチル-5-フェニル-7-メチルチオ-8-(N-{(R)-α-[N-((S)-1-カルボキシエチル)カルバモイル]ベンジル}カルバモイルメトキシ)-2,3,4,5-テトラヒドロ-1,2,5-ベンゾチアジアゼピン;
1,1-ジオキソ-3,3-ジブチル-5-フェニル-7-メチルチオ-8-(N-{(R)-α-[N'-((S)-1-カルボキシプロピル)カルバモイル]-4-ヒドロキシベンジル}カルバモイルメトキシ)-2,3,4,5-テトラヒドロ-1,5-ベンゾチアゼピン;
1,1-ジオキソ-3,3-ジブチル-5-フェニル-7-メチルチオ-8-(N-{(R)-α-[N-((S)-1-カルボキシエチル)カルバモイル]-4-ヒドロキシベンジル}カルバモイルメトキシ)-2,3,4,5-テトラヒドロ-1,2,5-ベンゾチアジアゼピン;
1,1-ジオキソ-3,3-ジブチル-5-フェニル-7-メチルチオ-8-(N-{(R)-α-[N-((S)-1-カルボキシ-2-メチルプロピル)カルバモイル]-4-ヒドロキシベンジル}カルバモイルメトキシ)-2,3,4,5-テトラヒドロ-1,2,5-ベンゾチアジアゼピン;及び
1,1-ジオキソ-3,3-ジブチル-5-フェニル-7-メチルチオ-8-(N-{(R)-1'-フェニル-1'-[N'-(カルボキシメチル)カルバモイル]メチル}カルバモイルメトキシ)-2,3,4,5-テトラヒドロ-1,5-ベンゾチアゼピン
から成る群から選択される化合物、
又は医薬品に許容されるその塩である。
1-[4-[4-[(4R,5R)-3,3-ジブチル-7-(ジメチルアミノ)-2,3,4,5-テトラヒドロ-4-ヒドロキシ-1,1-ジオキシド-1-ベンゾチエピン-5-イル]フェノキシ]ブチル]4-アザ-1-アゾニアビシクロ[2.2.2]オクタンメタンスルホネート;
1-[[4-[[4-[3,3-ジブチル-7-(ジメチルアミノ)-2,3,4,5-テトラヒドロ-4-ヒドロキシ-1,1-ジオキシド-1-ベンゾチエピン-5-イル]フェノキシ]メチル]フェニル]メチル]-4-アザ-1-アゾニアザビシクロ[2.2.2]オクタンクロリド;
1-[[5-[[3-[(3S,4R,5R)-3-ブチル-7-(ジメチルアミノ)-3-エチル-2,3,4,5-テトラヒドロ-4-ヒドロキシ-1,1-ジオキシド-1-ベンゾチエピン-5-イル]フェニル]アミノ]-5-オキソペンチル]アミノ]-1-ジオキシ-D-グルシトール;及び
カリウム((2R,3R,4S,5R,6R)-4-ベンジルオキシ-6-{3-[3-((3S,4R,5R)-3-ブチル-7-ジメチルアミノ-3-エチル-4-ヒドロキシ-1,1-ジオキソ-2,3,4,5-テトラヒドロ-1H-ベンゾ[b]チエピン-5-イル)-フェニル]-ウレイド}-3,5-ジヒドロキシ-テトラヒドロ-ピラン-2-イルメチル)サルフェート、エタノレート、ハイドレート、
から成る群から選択される化合物である。
顆粒の調製
全ての実験は200gスケールで行われた。乾燥成分(コレスチラミン及びコポビドン;以下の表1の量を参照)をKenwood Patissierの中で1分間混合した。Eudragit(登録商標) RL 30 D(30%水性分散体)が実験に含まれた場合、適切な量の分散体を水で全質量が最大約300gになるよう希釈した。次いで、水、又は希釈Eudragit分散体を、約100gずつ3回に分けて、乾燥成分に添加し、各添加後に3分間、混合した。その後、追加分の純水(60から100g)を添加し、その結果、添加した水の総量はコレスチラミンの量(w/w)の約2.1倍に等しくなった。1分間、混合を継続した後、湿潤塊をステンレススチールトレイに移し、乾燥オーブン中、50℃で一晩、乾燥した。
コレスチラミン顆粒の崩壊試験
実施例1の顆粒(10g)を、プロペラ撹拌機を用いて300rpmで撹拌しながら、400mLのリン酸緩衝液(50mM、pH6.8)に加える。顆粒が完全に崩壊するまでの時間を測定する。
酵素-制御放出用の製剤A~C
実施例1、エントリー1のコレスチラミン顆粒を、Eudragit(登録商標)FS 30 D及び高アミロース天然トウモロコシデンプンをベースとする結腸放出コーティングにより製剤化した。
pH-及び拡散-制御放出用の製剤D~F
実施例1のコレスチラミン顆粒を、ポリ(アクリル酸エチル-co-メタクリル酸メチル-co-メタクリル酸トリメチルアンモニオエチルクロリド)系拡散制御内部コーティング並びに酢酸コハク酸ヒドロキシプロピルメチルセルロース系腸溶性外部コーティングを含む結腸放出コーティングによって製剤化する。
製剤D:100% Eudragit(登録商標) RL 30 D
製剤E:50% Eudragit(登録商標) RL 30 D+50% Eudragit(登録商標) RS 30 D
製剤F:100% Eudragit(登録商標) RS 30 D
モノステアリン酸グリセロール(GMS)、ポリソルベート80及びクエン酸トリエチル含有のGMSエマルションをEvonik社の一般説明書に従って調製する。エマルションをEudragit(登録商標)RL30D/Eudragit(登録商標)RS30D分散体(30%w/w)と混合する。内部コーティングフィルムの組成を、乾燥質量に基づき、以下に示す。濃度は、適用された分散体乾燥質量に基づいて、19.8%(w/w)である。
7%w/w酢酸コハク酸ヒプロメロース、2.45%w/wクエン酸トリエチル、2.1%w/wタルク、0.21%w/wラウリル硫酸ナトリウム及び88.24%w/w水を<15℃の低温で、オーバーヘッドスターラーを用いて30分間混合することにより、腸溶性コーティングを調製する。外部コーティングフィルムの組成を、乾燥質量に基づき、以下に示す。コーティング液は、コーティング過程の間、15℃未満に維持する。
封鎖アッセイ
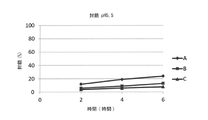
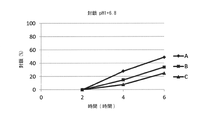
製剤A、B及びCの封鎖能を胃及び小腸のpHを模擬した簡便なアッセイにおいて決定した。封鎖は、水溶液中のコール酸量の減少を測定することによって決定した。米国薬局方溶解装置2(パドル)、欧州薬局方2.9.3を用いた。
250mgコレスチラミンに相当する量の製剤A、B及びCを、500mLのコール酸緩衝溶液(0.192mg/mL)、pH5.5が入った容器に加え、内容物を75rpmで6時間撹拌した。溶液の試料を、種々の時点で採取し、50mm×2.1mm、粒子径1.9μmのThermo Hypersil Goldカラムを用いて、カラム温度60℃、移動相30:70 アセトニトリル:リン酸緩衝液(pH3.0)、流速0.75mL/分で、HPLCによりコール酸の分析を行った。各製剤につき3つの反復用試料を分析し平均値を算出した。
250mgコレスチラミンに相当する量の製剤A、B及びCを、250mLの0.1M塩酸溶液(pH1)が入った容器に加え、内容物を75rpmで2時間撹拌した。次いで、水酸化カリウム/リン酸カリウム緩衝液中コール酸溶液250mLを容器に加え、pH6.8のコール酸の緩衝された溶液(0.192mg/mL)を得た。1分間混合した後、最初の試料を取り出した。その後pHを確認し、必要に応じて、適切な量の0.1M水酸化カリウム溶液を添加して6.8に調整した。その後溶液を更に6時間、混合した。溶液の試料を種々の時点で採取し、50mm×2.1mm、粒子径1.9μmのThermo Hypersil Goldカラムを用いて、カラム温度60℃、移動相30:70 アセトニトリル:リン酸緩衝液(pH3.0)、流速0.75mL/分で、HPLCによりコール酸の分析を行った。各製剤につき3つの反復用試料を分析し平均値を算出した。
消化管の模擬条件下での製剤のコレスチラミン製剤の封鎖能のin vitroでの決定
コレスチラミン製剤の封鎖能を、ProDigest社(ベルギー、ゲント)によって開発されたSimulator of the Human Intestinal Microbial Ecosystem(SHIME(登録商標))を用いて試験する。シミュレーターを、絶食した胃、小腸及び近位結腸の典型的な生理的条件下での、胆汁酸塩を結合する封鎖能を評価するよう適合させる。絶食した胃及び小腸に典型的な液体媒体は、先に、Marzorati他(LWT-Food Sci. Technol. 2015、vol.60、544~551頁)によって記述されている。近位結腸についての液体媒体は、ヒト結腸に典型的な安定な微生物コミュニティを含むSHIME(登録商標)マトリックスを含む。ヒト腸の安定な微生物コミュニティを得るための方法は、Possemiers他(FEMS Microbiol. Ecol. 2004、vol. 49、495~507頁)及びその中の文献によって記述されている。封鎖は、水溶液中の胆汁酸の量の減少を測定することにより決定される。コール酸(CA)、ケノデオキシコール酸(CDCA)及びデオキシコール酸(DCA)の40:40:20(w/w)混合物が、ヒト胆汁酸の典型的混合物として使用される(Carulli他、Aliment. Pharmacol. Ther. 2000、vol.14、issue supplement s2、14~18頁)。
91mgのコレスチラミンに相当する量の製剤A、B及びC、並びに純粋なコレスチラミン(91mg)を、14mLの絶食胃液体媒体(pH1.8)に投与する。消化物を37℃で1時間、インキュベートする。
1時間の胃インキュベーションの後に、胆汁酸塩(46.7mM)の既定の40:40:20混合物を含む5.6mLの膵液(pH 6.8)を添加する。小腸消化物を37℃で2時間、インキュベートし、0、60及び120分後に試料を採取する。
2時間の腸インキュベーションの後に、SHIME(登録商標)システムの上行結腸由来の42mLの完全SHIME(登録商標)マトリックス(pH6.0)を添加する。結腸消化物を37℃で24時間、インキュベートし、最初の6時間は、1時間毎に、その後は19時間後及び24時間後に試料を採取する。
試料中の遊離胆汁酸の濃度を、HPLCを用いて評価する。試料中のCA、CDCA及びDCAの濃度を算出するために、検量線を用いた。1mLの各試料を5000gで2分間、遠心分離した。500μLの上清をメタノール及びリン酸緩衝液の80:20(v:v)混合物500μLと混合し、激しくボルテックスして、0.2μmのPTFEフィルターでろ過し、UV-Vis検出器を搭載したHitachi Chromaster HPLCに注入する。3種の胆汁酸塩を、逆相C18カラム(Synergi Hydro-RP、4μm、80Å、250×4.6mm)によって分離する。分離は、移動相としてメタノール及びリン酸緩衝液の80:20(v:v)混合物を用いて、室温、均一濃度条件下で行う。分析は、0.7mL/分で、23分間で行い、胆汁酸を210nmで検出する。注入量は胃及び小腸の試料については20μLに、結腸試料については50μLに設定する。
Claims (27)
- 各顆粒が少なくとも70%w/wのコレスチラミン、並びに
i.少なくとも6%w/wの結合剤及び少なくとも2%w/wのアクリレートコポリマーの組合せ;又は
ii.少なくとも5%w/wの結合剤及び少なくとも3%w/wのアクリレートコポリマーの組合せ;又は
iii.少なくとも6%w/wの結合剤、少なくとも1%w/wのアクリレートコポリマー及び5から15%w/wの微結晶セルロースの組合せ;
を含み、
結合剤が、セルロースエーテル、ビニルピロリドン系ポリマー、又はそれらの組合せを含む、顆粒。 - 結合剤がセルロースエーテルである、請求項1に記載の顆粒。
- 結合剤が、ビニルピロリドン系ポリマーである、請求項1に記載の顆粒。
- 結合剤が、セルロースエーテル及びビニルピロリドン系ポリマーの組合せを含む、請求項1に記載の顆粒。
- セルロースエーテルが、メチルセルロース、ヒドロキシプロピルセルロース、ヒドロキシプロピルメチルセルロース若しくはカルボキシメチルセルロースナトリウム、又はこれらのセルロースエーテルの2つ以上を含む混合物である、請求項1、2及び4のいずれか一項に記載の顆粒。
- ビニルピロリドン系ポリマーがコポビドンである、請求項1、3及び4のいずれか一項に記載の顆粒。
- アクリレートコポリマーが、メタクリル酸アンモニオコポリマーである、請求項1から6のいずれか一項に記載の顆粒。
- 顆粒が、少なくとも85%w/wのコレスチラミンを含む、請求項1から7のいずれか一項に記載の顆粒。
- 顆粒の直径が、1000から1600μmである、請求項1から8のいずれか一項に記載の顆粒。
- 結腸標的送達のために製剤化されている、請求項1から9のいずれか一項に記載の顆粒。
- 請求項1から10のいずれか一項に記載の複数のコレスチラミン顆粒を含む多粒子薬剤送達システム。
- コレスチラミン顆粒が結腸標的送達のために製剤化されている、請求項11に記載の薬剤送達システム。
- 結腸標的送達が、酵素-制御放出に基づいている、請求項12に記載の薬剤送達システム。
- 結腸標的送達が、pH-及び拡散-制御放出に基づいている、請求項12に記載の薬剤送達システム。
- a)請求項1から9のいずれか一項に記載の複数の顆粒;及び
b)前記顆粒周囲の結腸放出コーティング
を含む、コレスチラミンの結腸への標的送達のための経口製剤。 - 結腸放出コーティングが弾性である、請求項15に記載の製剤。
- 結腸放出コーティングがデンプンを含む、請求項15又は16に記載の製剤。
- デンプンが難消化性デンプンタイプ2(RS2)である、請求項17に記載の製剤。
- 結腸放出コーティングが、拡散-制御内部コーティング層及び腸溶性外部コーティング層を含む、請求項15又は16に記載の製剤。
- 拡散-制御内部コーティング層が、ポリ(アクリル酸エチル-co-メタクリル酸メチル-co-メタクリル酸トリメチルアンモニオエチルクロリド)1:2:0.2、1:2:0.1又はそれらの組合せを含む、請求項19に記載の製剤。
- 腸溶性外部コーティング層が、酢酸コハク酸ヒドロキシプロピルメチルセルロースを含む、請求項19又は20に記載の製剤。
- 胆汁酸吸収不良の治療又は予防における使用のための、請求項15から21のいずれか一項に記載の製剤。
- 胆汁酸吸収不良が、回腸疾患(クローン病等)、回腸切除若しくは回腸バイパスの結果、胆汁酸の過剰産生若しくは肝臓の胆汁酸合成の不完全なフィードバック阻害の結果、又は胆嚢摘出術、迷走神経切離術、小腸内細菌異常増殖(SIBO)、セリアック病、膵機能不全(慢性膵炎、嚢胞性線維症)、膵移植、放射線性腸炎、コラーゲン大腸炎、顕微鏡的大腸炎、リンパ球性大腸炎、潰瘍性大腸炎若しくは過敏性腸症候群(IBS-D)の結果である、請求項22に記載の使用のための製剤。
- 胆汁酸下痢の治療又は予防における使用のための、請求項15から21のいずれか一項に記載の製剤。
- IBAT阻害剤の経口投与時の胆汁酸下痢の治療又は予防における使用のための、請求項15から21のいずれか一項に記載の製剤。
- IBAT阻害剤の経口投与を含む、胆汁うっ滞性肝疾患の治療時の胆汁酸下痢の治療又は予防における使用のための、請求項15から21のいずれか一項に記載の製剤。
- IBAT阻害剤が、
1,1-ジオキソ-3,3-ジブチル-5-フェニル-7-メチルチオ-8-(N-{(R)-α-[N-((S)-1-カルボキシプロピル)カルバモイル]-4-ヒドロキシベンジル}カルバモイルメトキシ)-2,3,4,5-テトラヒドロ-1,2,5-ベンゾチアジアゼピン;若しくは
1,1-ジオキソ-3,3-ジブチル-5-フェニル-7-メチルチオ-8-(N-{(R)-1'-フェニル-1'-[N'-(カルボキシメチル)カルバモイル]メチル}カルバモイルメトキシ)-2,3,4,5-テトラヒドロ-1,5-ベンゾチアゼピン;
又は医薬品に許容されるその塩
である、請求項26に記載の使用のための製剤。
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| SE1750978 | 2017-08-09 | ||
| SE1750978-7 | 2017-08-09 | ||
| PCT/SE2018/050802 WO2019032026A1 (en) | 2017-08-09 | 2018-08-09 | CHOLESTYRAMINE GRANULES, ORAL FORMULATIONS OF CHOLESTYRAMINE AND THEIR USE |
| JP2020506231A JP2020530448A (ja) | 2017-08-09 | 2018-08-09 | コレスチラミン顆粒、経口コレスチラミン製剤、及びそれらの使用 |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2020506231A Division JP2020530448A (ja) | 2017-08-09 | 2018-08-09 | コレスチラミン顆粒、経口コレスチラミン製剤、及びそれらの使用 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2022166326A true JP2022166326A (ja) | 2022-11-01 |
| JP7422827B2 JP7422827B2 (ja) | 2024-01-26 |
Family
ID=63259555
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2020506231A Pending JP2020530448A (ja) | 2017-08-09 | 2018-08-09 | コレスチラミン顆粒、経口コレスチラミン製剤、及びそれらの使用 |
| JP2022135754A Active JP7422827B2 (ja) | 2017-08-09 | 2022-08-29 | コレスチラミン顆粒、経口コレスチラミン製剤、及びそれらの使用 |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2020506231A Pending JP2020530448A (ja) | 2017-08-09 | 2018-08-09 | コレスチラミン顆粒、経口コレスチラミン製剤、及びそれらの使用 |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US10881685B2 (ja) |
| EP (1) | EP3664781A1 (ja) |
| JP (2) | JP2020530448A (ja) |
| CN (1) | CN111032019B (ja) |
| CA (1) | CA3071285A1 (ja) |
| WO (1) | WO2019032026A1 (ja) |
Families Citing this family (36)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| SI3023102T1 (sl) | 2010-11-04 | 2018-11-30 | Albireo Ab | IBAT inhibitorji za zdravljenje jetrnih bolezni |
| WO2015199147A1 (ja) | 2014-06-25 | 2015-12-30 | 味の素株式会社 | 固形製剤及びその着色防止又は着色低減方法 |
| US10441604B2 (en) | 2016-02-09 | 2019-10-15 | Albireo Ab | Cholestyramine pellets and methods for preparation thereof |
| US10441605B2 (en) | 2016-02-09 | 2019-10-15 | Albireo Ab | Oral cholestyramine formulation and use thereof |
| US10786529B2 (en) | 2016-02-09 | 2020-09-29 | Albireo Ab | Oral cholestyramine formulation and use thereof |
| WO2019234077A1 (en) | 2018-06-05 | 2019-12-12 | Albireo Ab | Benzothia(di)azepine compounds and their use as bile acid modulators |
| US10793534B2 (en) | 2018-06-05 | 2020-10-06 | Albireo Ab | Benzothia(di)azepine compounds and their use as bile acid modulators |
| ES3011850T3 (en) | 2018-06-20 | 2025-04-08 | Albireo Ab | Crystal modifications of odevixibat |
| US11801226B2 (en) | 2018-06-20 | 2023-10-31 | Albireo Ab | Pharmaceutical formulation of odevixibat |
| US10722457B2 (en) | 2018-08-09 | 2020-07-28 | Albireo Ab | Oral cholestyramine formulation and use thereof |
| US11549878B2 (en) | 2018-08-09 | 2023-01-10 | Albireo Ab | In vitro method for determining the adsorbing capacity of an insoluble adsorbant |
| US11007142B2 (en) * | 2018-08-09 | 2021-05-18 | Albireo Ab | Oral cholestyramine formulation and use thereof |
| CA3127568A1 (en) | 2019-02-06 | 2020-08-13 | Albireo Ab | Benzothiadiazepine compounds and their use as bile acid modulators |
| US10975045B2 (en) | 2019-02-06 | 2021-04-13 | Aibireo AB | Benzothiazepine compounds and their use as bile acid modulators |
| US10941127B2 (en) | 2019-02-06 | 2021-03-09 | Albireo Ab | Benzothiadiazepine compounds and their use as bile acid modulators |
| CN118834175A (zh) | 2019-02-06 | 2024-10-25 | 阿尔比里奥公司 | 苯并硫氮杂环庚三烯化合物及其用作胆汁酸调节剂的用途 |
| KR20220046623A (ko) | 2019-08-12 | 2022-04-14 | 메사추세츠 인스티튜트 오브 테크놀로지 | 치료제의 투여를 위한 물품 및 방법 |
| TWI867107B (zh) | 2019-12-04 | 2024-12-21 | 瑞典商艾爾比瑞歐公司 | 苯并噻(二)氮呯化合物及其作為膽酸調節劑之用途 |
| US11014898B1 (en) | 2020-12-04 | 2021-05-25 | Albireo Ab | Benzothiazepine compounds and their use as bile acid modulators |
| CN114786772B (zh) | 2019-12-04 | 2024-04-09 | 阿尔比里奥公司 | 苯并硫杂(二)氮杂环庚三烯化合物及其作为胆汁酸调节剂的用途 |
| TWI865673B (zh) | 2019-12-04 | 2024-12-11 | 瑞典商艾爾比瑞歐公司 | 苯并噻(二)氮呯(benzothia(di)azepine)化合物及其作為膽酸調節劑之用途 |
| JP7665620B2 (ja) | 2019-12-04 | 2025-04-21 | アルビレオ・アクチボラグ | ベンゾチアジアゼピン化合物及び胆汁酸モジュレータとしてのそれらの使用 |
| JP7695242B2 (ja) | 2019-12-04 | 2025-06-18 | アルビレオ・アクチボラグ | ベンゾチア(ジ)アゼピン化合物及び胆汁酸モジュレータとしてのそれらの使用 |
| CN114761080B (zh) | 2019-12-04 | 2024-07-23 | 阿尔比里奥公司 | 苯并硫杂(二)氮杂环庚三烯化合物及其作为胆汁酸调节剂的用途 |
| AR120674A1 (es) | 2019-12-04 | 2022-03-09 | Albireo Ab | Compuestos de benzotiazepina y su uso como ácido biliar |
| TWI877263B (zh) | 2019-12-04 | 2025-03-21 | 瑞典商艾爾比瑞歐公司 | 苯并噻二氮呯化合物及其作為膽酸調節劑之用途 |
| TWI871392B (zh) | 2019-12-04 | 2025-02-01 | 瑞典商艾爾比瑞歐公司 | 苯并噻(二)氮呯(benzothia(di)azepine)化合物及其作為膽酸調節劑之用途 |
| WO2022029101A1 (en) | 2020-08-03 | 2022-02-10 | Albireo Ab | Benzothia(di)azepine compounds and their use as bile acid modulators |
| CA3196488A1 (en) | 2020-11-12 | 2022-05-19 | Albireo Ab | Odevixibat for treating progressive familial intrahepatic cholestasis (pfic) |
| CA3198216A1 (en) | 2020-12-04 | 2022-06-09 | Albireo Ab | Benzothia(di)azepine compounds and their use as bile acid modulators |
| TW202313579A (zh) | 2021-06-03 | 2023-04-01 | 瑞典商艾爾比瑞歐公司 | 苯并噻(二)氮呯(benzothia(di)azepine)化合物及其作為膽酸調節劑之用途 |
| CN114146184A (zh) * | 2021-12-03 | 2022-03-08 | 成都施桂行医药科技有限责任公司 | 阳离子聚合物在制备药物中的应用 |
| WO2023154547A1 (en) * | 2022-02-14 | 2023-08-17 | Axial Therapeutics, Inc. | Colon targeted drug delivery |
| US20240067617A1 (en) | 2022-07-05 | 2024-02-29 | Albireo Ab | Benzothia(di)azepine compounds and their use as bile acid modulators |
| WO2025146508A1 (en) | 2024-01-05 | 2025-07-10 | Albireo Ab | Benzothia(di)azepine compounds and their use as bile acid modulators |
| WO2025146507A1 (en) | 2024-01-05 | 2025-07-10 | Albireo Ab | Benzothia(di)azepine compounds and their use as bile acid modulators |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS63290822A (ja) * | 1987-02-09 | 1988-11-28 | ザ ダウ ケミカル カンパニー | コレスティラミン組成物およびその製法 |
| WO2001076635A1 (en) * | 2000-04-10 | 2001-10-18 | Shionogi & Co., Ltd. | Preparations for preventing bile acid diarrhea |
| JP2005536502A (ja) * | 2002-07-13 | 2005-12-02 | アストラゼネカ アクチボラグ | 下痢の処置用のibat阻害剤および金属塩の組合せ |
Family Cites Families (160)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| BE514901A (ja) * | 1951-10-07 | |||
| US3539380A (en) | 1968-01-08 | 1970-11-10 | Upjohn Co | Methylcellulose and polyalkylene glycol coating of solid medicinal dosage forms |
| GB1566609A (en) | 1977-03-10 | 1980-05-08 | Reckitt & Colmann Prod Ltd | Pharmaceutical compositions containing cholestyramine and alginic acid |
| GB1573487A (en) | 1977-05-23 | 1980-08-28 | Bristol Myers Co | Bile acid binding composition |
| DE3061586D1 (en) | 1979-04-30 | 1983-02-17 | Max Planck Gesellschaft | Pancreozymin-cholezystokinin active peptides, process for their preparation and pharmaceutical compositions containing them |
| JPS62290822A (ja) * | 1986-06-09 | 1987-12-17 | Kawasaki Steel Corp | 厚肉鋼管の製造方法 |
| US5167965A (en) * | 1987-02-09 | 1992-12-01 | The Dow Chemical Company | Palatable cholestyramine granules, tablets and methods for preparation thereof |
| US4900757A (en) | 1988-12-08 | 1990-02-13 | Merrell Dow Pharmaceuticals Inc. | Hypocholesterolemic and antiatherosclerotic uses of bix(3,5-di-tertiary-butyl-4-hydroxyphenylthio)methane |
| IL95574A (en) | 1989-09-09 | 1994-11-11 | Knoll Ag | Colestyramine preparation |
| DE3930168A1 (de) * | 1989-09-09 | 1991-03-14 | Knoll Ag | Verbesserte verabreichungsform fuer colestyramin |
| GB8926639D0 (en) | 1989-11-24 | 1990-01-17 | Agricultural & Food Res | Delayed release formulations |
| FI106800B (fi) | 1990-12-06 | 2001-04-12 | Hoechst Ag | Menetelmä uusien terapeuttisesti käyttökelpoisten dimeeristen sappihappojohdannaisten valmistamiseksi |
| NZ245503A (en) | 1991-12-20 | 1995-11-27 | Hoechst Ag | Polymers containing bile acids; pharmaceuticals and preparatory methods |
| JPH05186357A (ja) | 1991-12-31 | 1993-07-27 | Shigeo Ochi | 飲食物消化分解産物吸収抑制手段 |
| GB9203347D0 (en) | 1992-02-17 | 1992-04-01 | Wellcome Found | Hypolipidaemic compounds |
| IT1257793B (it) | 1992-05-18 | 1996-02-13 | Composizione farmaceutica a base di acidi biliari in microgranuli a rilascio controllato | |
| CA2137265C (en) | 1992-06-04 | 2003-10-28 | Sanjay Bhardwaj | Palatable pharmaceutical compositions |
| DK0573848T3 (da) | 1992-06-12 | 1998-08-10 | Hoechst Ag | Galdesyrederivater, fremgangsmåde til deres fremstilling og anvendelse af disse forbindelser som lægemidler |
| US5350584A (en) | 1992-06-26 | 1994-09-27 | Merck & Co., Inc. | Spheronization process using charged resins |
| IL108634A0 (en) | 1993-02-15 | 1994-05-30 | Wellcome Found | Hypolipidaemic heterocyclic compounds, their prepatation and pharmaceutical compositions containing them |
| IL108633A (en) | 1993-02-15 | 1998-07-15 | Wellcome Found | History of Benzothiazepine Hypolipidemic Preparation and Pharmaceutical Preparations Containing Them |
| ES2149250T3 (es) | 1993-04-23 | 2000-11-01 | Novartis Ag | Dispositivo para la administracion de medicamentos con liberacion controlada. |
| EP0624593A3 (de) | 1993-05-08 | 1995-06-07 | Hoechst Ag | Gallensäurederivate, Verfahren zu ihrer Herstellung und Verwendung dieser Verbindungen als Arzneimittel. |
| TW289020B (ja) | 1993-05-08 | 1996-10-21 | Hoechst Sktiengesellschaft | |
| TW289021B (ja) | 1993-05-08 | 1996-10-21 | Hoechst Ag | |
| TW289757B (ja) | 1993-05-08 | 1996-11-01 | Hoechst Ag | |
| ZA956647B (en) | 1994-08-10 | 1997-02-10 | Wellcome Found | Hypolipidaemic compounds. |
| US6262277B1 (en) | 1994-09-13 | 2001-07-17 | G.D. Searle And Company | Intermediates and processes for the preparation of benzothiepines having activity as inhibitors of ileal bile acid transport and taurocholate uptake |
| US5994391A (en) | 1994-09-13 | 1999-11-30 | G.D. Searle And Company | Benzothiepines having activity as inhibitors of ileal bile acid transport and taurocholate uptake |
| BR9508916A (pt) | 1994-09-13 | 1997-12-30 | Monsanto Co | "Novas benzotiepinas tendo atividade como inibidores de transporte do ácido biliar ileal e absorção de taurocolato" |
| US6642268B2 (en) | 1994-09-13 | 2003-11-04 | G.D. Searle & Co. | Combination therapy employing ileal bile acid transport inhibiting benzothipines and HMG Co-A reductase inhibitors |
| GB9423172D0 (en) | 1994-11-17 | 1995-01-04 | Wellcom Foundation The Limited | Hypolipidemic benzothiazepines |
| US5811388A (en) | 1995-06-07 | 1998-09-22 | Cibus Pharmaceutical, Inc. | Delivery of drugs to the lower GI tract |
| WO1997025864A1 (en) | 1996-01-16 | 1997-07-24 | University Technology Corporation | Use of antioxidant agents to treat cholestatic liver disease |
| DE19608592A1 (de) | 1996-03-06 | 1997-09-11 | Hoechst Ag | Antikörper zur selektiven immunologischen Bestimmung von Gallensäuren in biologischen Matrices |
| CA2248586A1 (en) | 1996-03-11 | 1997-09-18 | G.D. Searle & Co. | Novel benzothiepines having activity as inhibitors of ileal bile acid transport and taurocholate uptake |
| ATE394107T1 (de) | 1996-05-23 | 2008-05-15 | Novartis Pharma Gmbh | Vorbeugung und behandlung von kolonadenom oder kolonmikroadenom mit 6-fluorursodeoxycholsäure |
| WO1998003818A1 (de) | 1996-07-24 | 1998-01-29 | Zumtobel Staff Gmbh | Adapter für ein haltemittel, welches zum befestigen einer einbauleuchte in einer einbauöffnung bestimmt ist, oder haltemittel oder einbauleuchte mit einem solchen adapter |
| DE19633268A1 (de) | 1996-08-19 | 1998-02-26 | Hoechst Ag | Polymere Gallensäure-Resorptionsinhibitoren mit gleichzeitiger Gallensäure-Adsorberwirkung |
| GB9704208D0 (en) | 1997-02-28 | 1997-04-16 | Glaxo Group Ltd | Chemical compounds |
| CN1255864A (zh) | 1997-03-11 | 2000-06-07 | G·D·瑟尔公司 | 使用回肠胆汁酸传输抑制苯并硫杂环庚三烯和HMGCo-A还原酶抑制剂的组合疗法 |
| DE69815180T2 (de) | 1997-03-14 | 2004-04-29 | Aventis Pharma Deutschland Gmbh | Hypolipidemische 1,4-Benzothiazepin-1,1-dioxide |
| EP0998271B3 (en) | 1997-06-06 | 2014-10-29 | Depomed, Inc. | Gastric-retentive oral drug dosage forms for controlled release of highly soluble drugs |
| US6635280B2 (en) | 1997-06-06 | 2003-10-21 | Depomed, Inc. | Extending the duration of drug release within the stomach during the fed mode |
| AU7552198A (en) | 1997-06-11 | 1998-12-30 | Sankyo Company Limited | Benzylamine derivatives |
| AUPO763197A0 (en) | 1997-06-30 | 1997-07-24 | Sigma Pharmaceuticals Pty Ltd | Health supplement |
| US5900233A (en) | 1997-10-16 | 1999-05-04 | Day; Charles E. | Epichlorohydrin and 1-(3-aminopropyl) imidazole copolymer and its use in treating irritable bowel syndrome |
| US20030153541A1 (en) | 1997-10-31 | 2003-08-14 | Robert Dudley | Novel anticholesterol compositions and method for using same |
| US6369220B1 (en) | 1997-12-19 | 2002-04-09 | Jinglin (James T.) Li | Method of preparing enantiomerically-enriched tetrahydrobenzothiepine oxides |
| GB9800428D0 (en) | 1998-01-10 | 1998-03-04 | Glaxo Group Ltd | Chemical compounds |
| EP1073650A1 (en) | 1998-04-24 | 2001-02-07 | Fujisawa Pharmaceutical Co., Ltd. | Guanidine derivatives |
| DE19825804C2 (de) | 1998-06-10 | 2000-08-24 | Aventis Pharma Gmbh | 1,4-Benzothiepin-1,1-dioxidderivate, Verfahren zu deren Herstellung und diese Verbindungen enthaltende Arzneimittel |
| US6221897B1 (en) | 1998-06-10 | 2001-04-24 | Aventis Pharma Deutschland Gmbh | Benzothiepine 1,1-dioxide derivatives, a process for their preparation, pharmaceuticals comprising these compounds, and their use |
| AU5194999A (en) | 1998-08-07 | 2000-02-28 | Takeda Chemical Industries Ltd. | Benzothiepin derivatives, process for the preparation of the same and uses thereof |
| PL348508A1 (en) | 1998-12-23 | 2002-05-20 | Searle Llc | Combinations of ileal bile acid transport inhibitors and cholesteryl ester transfer protein inhibitors for cardiovascular indications |
| ES2200588T3 (es) | 1998-12-23 | 2004-03-01 | G.D. Searle Llc | Combinacion de inhibidores del transporte de oxido biliar ileal y de derivados de acido fibrico para indicaciones cardiovasculares. |
| DK1140191T3 (da) | 1998-12-23 | 2003-02-24 | Searle Llc | Kombinationer af ileumgaldesyretransportinhibitorer og nicotinsyrederivater til cardiovaskulære indikationer |
| EP1354604A1 (en) | 1998-12-23 | 2003-10-22 | G.D. Searle LLC. | Combinations for cardiovascular indications |
| DK1140190T3 (da) | 1998-12-23 | 2002-12-23 | Searle Llc | Kombinationer af ileumgaldesyretransport-inhibitorer og galdesyre-sekvestreringsmidler til cardiovaskulære indikatorer |
| CN1195748C (zh) | 1999-02-12 | 2005-04-06 | G.D.瑟尔有限公司 | 具有作为回肠胆汁酸转运和牛磺胆酸摄取抑制剂活性的新的1,2-苯并硫氮杂 |
| DE19915420A1 (de) | 1999-04-06 | 2000-10-12 | Basf Ag | Stabilisierte Polyvinylpyrrolidon-Zubereitungen |
| DE19916108C1 (de) | 1999-04-09 | 2001-01-11 | Aventis Pharma Gmbh | Mit Zuckerresten substituierte 1,4-Benzothiazepin-1,1-dioxidderivate, Verfahren zu deren Herstellung und deren Verwendung |
| SE9901387D0 (sv) | 1999-04-19 | 1999-04-19 | Astra Ab | New pharmaceutical foromaulations |
| US6287609B1 (en) | 1999-06-09 | 2001-09-11 | Wisconsin Alumni Research Foundation | Unfermented gel fraction from psyllium seed husks |
| US20020054903A1 (en) | 1999-10-19 | 2002-05-09 | Joseph Tyler | Direct compression polymer tablet core |
| AU1302301A (en) | 1999-11-08 | 2001-06-06 | Sankyo Company Limited | Nitrogenous heterocycle derivatives |
| GB9927088D0 (en) | 1999-11-17 | 2000-01-12 | Secr Defence | Use of poly(diallylamine) polymers |
| WO2001060807A1 (en) | 2000-02-18 | 2001-08-23 | Merck & Co. Inc. | Aryloxyacetic acids for diabetes and lipid disorders |
| SE0000772D0 (sv) | 2000-03-08 | 2000-03-08 | Astrazeneca Ab | Chemical compounds |
| AU2001247331A1 (en) | 2000-03-10 | 2001-09-24 | Pharmacia Corporation | Combination therapy for the prophylaxis and treatment of hyperlipidemic conditions and disorders |
| WO2001068637A2 (en) | 2000-03-10 | 2001-09-20 | Pharmacia Corporation | Method for the preparation of tetrahydrobenzothiepines |
| US6638498B2 (en) | 2000-06-30 | 2003-10-28 | Semorex Inc. | Molecularly imprinted polymers for the treatment and diagnosis of medical conditions |
| US20020183307A1 (en) | 2000-07-26 | 2002-12-05 | Tremont Samuel J. | Novel 1,4-benzothiazephine and 1,5-benzothiazepine compounds as inhibitors of apical sodium co-dependent bile acid transport and taurocholate uptake |
| EP1307264B1 (en) * | 2000-07-28 | 2004-10-20 | F. Hoffmann-La Roche Ag | New pharmaceutical composition |
| FR2812886B1 (fr) | 2000-08-08 | 2002-11-08 | Assist Publ Hopitaux De Paris | Depistage d'un nouveau syndrome hepatique et ses applications |
| SE0003766D0 (sv) | 2000-10-18 | 2000-10-18 | Astrazeneca Ab | Novel formulation |
| EG26979A (en) | 2000-12-21 | 2015-03-01 | Astrazeneca Ab | Chemical compounds |
| WO2002053548A1 (fr) | 2000-12-27 | 2002-07-11 | Banyu Pharmaceutical Co.,Ltd. | Derives de la benzothiazepine |
| US6506921B1 (en) | 2001-06-29 | 2003-01-14 | Virginia Tech Intellectual Properties, Inc. | Amine compounds and curable compositions derived therefrom |
| US20040077625A1 (en) | 2001-07-25 | 2004-04-22 | Tremont Samuel J. | Novel 1,4-benzothiazepine and 1,5-benzothiazepine compounds as inhibitors of apical sodium codependent bile acid transport abd taurocholate uptake |
| US20040038862A1 (en) | 2001-07-30 | 2004-02-26 | Goodwin Bryan James | Identification of new therapeutic targets for modulating bile acid synthesis |
| GB0121337D0 (en) | 2001-09-04 | 2001-10-24 | Astrazeneca Ab | Chemical compounds |
| GB0121622D0 (en) | 2001-09-07 | 2001-10-31 | Astrazeneca Ab | Chemical compounds |
| GB0121621D0 (en) | 2001-09-07 | 2001-10-31 | Astrazeneca Ab | Chemical compounds |
| WO2003022286A1 (en) | 2001-09-08 | 2003-03-20 | Astrazeneca Ab | Benzothiazepine and benzothiadiazepine derivatives with ileal bile acid transport (ibat) inhibitory activity for the treatment hyperlipidaemia |
| JP2005502702A (ja) | 2001-09-12 | 2005-01-27 | ジー.ディー. サール エルエルシー | 結晶テトラヒドロベンゾチエピンの調製法 |
| US6740663B2 (en) | 2001-11-02 | 2004-05-25 | G.D. Searle, Llc | Mono- and di-fluorinated benzothiepine compounds as inhibitors of apical sodium co-dependent bile acid transport (ASBT) and taurocholate uptake |
| TW200300349A (en) | 2001-11-19 | 2003-06-01 | Sankyo Co | A 4-oxoqinoline derivative |
| GB0314079D0 (en) | 2003-06-18 | 2003-07-23 | Astrazeneca Ab | Therapeutic agents |
| SE0104334D0 (sv) | 2001-12-19 | 2001-12-19 | Astrazeneca Ab | Therapeutic agents |
| GB0229931D0 (en) | 2002-12-21 | 2003-01-29 | Astrazeneca Ab | Therapeutic agents |
| WO2003059378A2 (en) | 2001-12-29 | 2003-07-24 | Novo Nordisk A/S | Combined use of a glp-1 compound and another drug for treating dyslipidemia |
| GB0201850D0 (en) | 2002-01-26 | 2002-03-13 | Astrazeneca Ab | Therapeutic treatment |
| US20040014806A1 (en) | 2002-03-08 | 2004-01-22 | Pharmacia Corporation | Methods and compositions for lowering levels of blood lipids |
| AU2002244881A1 (en) | 2002-03-22 | 2003-10-08 | Ranbaxy Laboratories Limited | Controlled release drug delivery system of pravastatin |
| GB0209467D0 (en) | 2002-04-25 | 2002-06-05 | Astrazeneca Ab | Chemical compounds |
| GB0213669D0 (en) | 2002-06-14 | 2002-07-24 | Astrazeneca Ab | Chemical compounds |
| WO2004020421A1 (ja) | 2002-08-28 | 2004-03-11 | Asahi Kasei Pharma Corporation | 新規な4級アンモニウム化合物 |
| US7312208B2 (en) | 2002-08-28 | 2007-12-25 | Asahi Kasei Pharma Corporation | Quaternary ammonium compounds |
| GB0304194D0 (en) | 2003-02-25 | 2003-03-26 | Astrazeneca Ab | Chemical compounds |
| CA2517245C (en) | 2003-02-28 | 2009-01-20 | Mcgill University | Cell and enzyme compositions for modulating bile acids, cholesterol and triglycerides |
| US20060210633A1 (en) | 2003-04-03 | 2006-09-21 | Sun Pharmaceutical Industries Limited | Programmed drug delivery system |
| GB0307918D0 (en) | 2003-04-05 | 2003-05-14 | Astrazeneca Ab | Therapeutic use |
| CN1852659B (zh) | 2003-10-16 | 2011-02-09 | 泰克康姆集团公司 | 具有降低的血糖应答的可消化性降低的碳水化合物食物 |
| CA2557576C (en) | 2004-02-27 | 2010-02-09 | Asahi Kasei Pharma Corporation | Novel benzothiazepine and benzothiepine compounds |
| US20050197376A1 (en) | 2004-03-02 | 2005-09-08 | Fujisawa Pharmaceutical Co. Ltd. | Concomitant drugs |
| EP1593671A1 (en) | 2004-03-05 | 2005-11-09 | Graffinity Pharmaceuticals AG | DPP-IV inhibitors |
| TWI415635B (zh) | 2004-05-28 | 2013-11-21 | 必治妥施貴寶公司 | 加衣錠片調製物及製備彼之方法 |
| JP4896480B2 (ja) | 2004-10-01 | 2012-03-14 | 第一三共ヘルスケア株式会社 | 陰イオン交換樹脂の粒子状組成物 |
| US9149439B2 (en) | 2005-03-21 | 2015-10-06 | Sandoz Ag | Multi-particulate, modified-release composition |
| US20090131395A1 (en) | 2005-05-05 | 2009-05-21 | Microbia, Inc. | Biphenylazetidinone cholesterol absorption inhibitors |
| US20080193543A1 (en) | 2005-05-17 | 2008-08-14 | Brown University Research Foundation | Drug Delivery Formulations For Targeted Delivery |
| US20070237818A1 (en) | 2005-06-02 | 2007-10-11 | Malcolm Bruce A | Controlled-release formulation of HCV protease inhibitor and methods using the same |
| DE102005033099A1 (de) | 2005-07-15 | 2007-01-18 | Sanofi-Aventis Deutschland Gmbh | Neues 1,4-Benzothiazepin-1,1-Dioxidderivat mit verbesserten Eigenschaften, Verfahren zu dessen Herstellung, diese Verbindung enthaltende Arzneimittel und dessen Verwendung |
| DE102005033100B3 (de) | 2005-07-15 | 2007-01-25 | Sanofi-Aventis Deutschland Gmbh | Neues 1,4-Benzothiazepin-1,1-Dioxidderivat mit verbesserten Eigenschaften, diese Verbindung enthaltene Arzneimittel und Verfahren zu deren Herstellung |
| WO2007035665A1 (en) | 2005-09-20 | 2007-03-29 | Novartis Ag | Use of a dpp-iv inhibitor to reduce hypoglycemic events |
| US20100286122A1 (en) | 2006-04-10 | 2010-11-11 | Kevin Belyk | CGRP Antagonist Salt |
| GB0607534D0 (en) | 2006-04-13 | 2006-05-24 | Univ London Pharmacy | Colonic drug delivery formulation |
| US8048413B2 (en) | 2006-05-17 | 2011-11-01 | Helene Huguet | Site-specific intestinal delivery of adsorbents, alone or in combination with degrading molecules |
| DE102006053637B4 (de) | 2006-11-14 | 2011-06-30 | Sanofi-Aventis Deutschland GmbH, 65929 | Neue mit Fluor substituierte 1,4-Benzothiepin-1,1-Dioxidderivate, diese Verbindungen enthaltende Arzneimittel und deren Verwendung |
| DE102006053635B4 (de) | 2006-11-14 | 2011-06-30 | Sanofi-Aventis Deutschland GmbH, 65929 | Neue mit Benzylresten substituierte 1,4-Benzothiepin-1,1-Dioxidderivate, diese Verbindungen enthaltende Arzneimittel und deren Verwendung |
| DE102006053636B4 (de) | 2006-11-14 | 2008-09-18 | Sanofi-Aventis Deutschland Gmbh | Neue mit Cyclohexylresten substituierte 1,4-Benzothiepin-1,1-Dioxidderivate und deren Verwendung |
| EP2083832B1 (de) | 2006-11-14 | 2011-01-05 | Sanofi-Aventis Deutschland GmbH | Neue 1,4-benzothiepin-1,1-dioxidderivate mit verbesserten eigenschaften, verfahren zu deren herstellung, diese verbindungen enthaltende arzneimittel und deren verwendung |
| US8410083B2 (en) | 2007-01-19 | 2013-04-02 | Intercept Pharmaceuticals, Inc. | 23-substituted bile acids as TGR5 modulators and methods of use thereof |
| US10888521B2 (en) | 2007-03-02 | 2021-01-12 | Farnam Companies, Inc. | Sustained release compositions using wax-like materials |
| DK2200588T3 (da) | 2007-09-25 | 2019-07-01 | Solubest Ltd | Sammensætninger, som omfatter lipofile aktive forbindelser, og fremgangsmåde til fremstilling deraf |
| US9295677B2 (en) | 2008-02-26 | 2016-03-29 | Qing Bile Therapeutics Inc. | Polyhydroxylated bile acids for treatment of biliary disorders |
| BRPI0918499A2 (pt) * | 2008-09-02 | 2015-12-01 | Usv Ltd | polímeros reticulados |
| EP2367554A4 (en) | 2008-11-26 | 2020-03-25 | Satiogen Pharmaceuticals, Inc. | Bile acid reflux inhibitor for the treatment of obesity and diabetes |
| US20110152204A1 (en) | 2009-12-18 | 2011-06-23 | Satiogen Pharmaceuticals, Inc. | Treatment of Obesity or Diabetes with Bile Acid Sequestrants |
| ES2586135T3 (es) | 2010-02-23 | 2016-10-11 | Da Volterra | Formulaciones para el suministro oral de adsorbentes en el intestino |
| JO3131B1 (ar) | 2010-04-27 | 2017-09-20 | Glaxosmithkline Llc | مركبات كيميائية |
| WO2011150286A2 (en) | 2010-05-26 | 2011-12-01 | Satiogen Pharmaceuticals,Inc. | Bile acid recycling inhibitors and satiogens for treatment of diabetes, obesity, and inflammatory gastrointestinal conditions |
| SI3023102T1 (sl) | 2010-11-04 | 2018-11-30 | Albireo Ab | IBAT inhibitorji za zdravljenje jetrnih bolezni |
| US20120114588A1 (en) | 2010-11-08 | 2012-05-10 | Albireo Ab | Ibat inhibitors for treatment of metabolic disorders and related conditions |
| AU2011326873B2 (en) | 2010-11-08 | 2015-02-19 | Albireo Ab | IBAT inhibitors for treatment of metabolic disorders and related conditions |
| CN103228270B (zh) | 2010-11-08 | 2016-02-10 | 阿尔比里奥公司 | 含ibat抑制剂和胆汁酸结合剂的药物组合 |
| BR112014010228B1 (pt) | 2011-10-28 | 2020-09-29 | Lumena Pharmaceuticals Llc | Uso de inibidores de reciclagem de ácido biliar para o tratamento de hipercolemia e doença hepática colestática |
| JP6217938B2 (ja) | 2011-10-28 | 2017-10-25 | ルメナ ファーマシューティカルズ エルエルシー | 小児の胆汁うっ滞性肝疾患の処置のための胆汁酸再循環阻害剤 |
| RU2015139731A (ru) | 2013-03-15 | 2017-04-20 | ЛУМЕНА ФАРМАСЬЮТИКАЛС ЭлЭлСи | Ингибиторы рециркуляции желчных кислот для лечения первичного склерозирующего холангита и воспалительного заболевания кишечника |
| JO3301B1 (ar) | 2013-04-26 | 2018-09-16 | Albireo Ab | تعديلات بلورية على إيلوبيكسيبات |
| WO2015131152A1 (en) | 2014-02-27 | 2015-09-03 | Nusirt Sciences Inc. | Compositions and methods for the reduction or prevention of hepatic steatosis |
| US20170143743A1 (en) | 2014-06-16 | 2017-05-25 | Valpharma International S.P.A. | Formulation for oral administration containing mesalazine |
| CA2952405A1 (en) | 2014-06-25 | 2015-12-30 | Ea Pharma Co., Ltd. | Solid formulation and method for stabilizing the same |
| WO2015199147A1 (ja) | 2014-06-25 | 2015-12-30 | 味の素株式会社 | 固形製剤及びその着色防止又は着色低減方法 |
| EP3012252A1 (en) | 2014-10-24 | 2016-04-27 | Ferring BV | Crystal modifications of elobixibat |
| US9684018B2 (en) | 2014-11-19 | 2017-06-20 | Texas Instruments Incorporated | Current sense circuit that operates over a wide range of currents |
| CN105985254B (zh) | 2015-02-17 | 2018-03-16 | 上海中科绿碳化工科技有限公司 | 一种制备甲酰胺类化合物的方法 |
| CN108601744B (zh) * | 2016-02-09 | 2022-01-04 | 阿尔比里奥公司 | 口服考来烯胺制剂及其用途 |
| US10786529B2 (en) | 2016-02-09 | 2020-09-29 | Albireo Ab | Oral cholestyramine formulation and use thereof |
| CA3011595C (en) | 2016-02-09 | 2024-01-02 | Albireo Ab | Cholestyramine pellets and methods for preparation thereof |
| ES2874546T3 (es) * | 2016-02-09 | 2021-11-05 | Albireo Ab | Formulación oral de colestiramina y uso de la misma |
| US10441605B2 (en) | 2016-02-09 | 2019-10-15 | Albireo Ab | Oral cholestyramine formulation and use thereof |
| US10441604B2 (en) | 2016-02-09 | 2019-10-15 | Albireo Ab | Cholestyramine pellets and methods for preparation thereof |
| CA3071182A1 (en) | 2017-08-09 | 2019-02-14 | Albireo Ab | Cholestyramine pellets, oral cholestyramine formulations and use thereof |
| US20200046758A1 (en) | 2018-08-09 | 2020-02-13 | Albireo Ab | Oral cholestyramine formulation and use thereof |
| US11007142B2 (en) | 2018-08-09 | 2021-05-18 | Albireo Ab | Oral cholestyramine formulation and use thereof |
| US10722457B2 (en) | 2018-08-09 | 2020-07-28 | Albireo Ab | Oral cholestyramine formulation and use thereof |
| US11549878B2 (en) | 2018-08-09 | 2023-01-10 | Albireo Ab | In vitro method for determining the adsorbing capacity of an insoluble adsorbant |
| US20200046757A1 (en) | 2018-08-09 | 2020-02-13 | Albireo Ab | Cholestyramine pellets, oral cholestyramine formulations, and uses thereof |
-
2018
- 2018-08-09 WO PCT/SE2018/050802 patent/WO2019032026A1/en not_active Ceased
- 2018-08-09 JP JP2020506231A patent/JP2020530448A/ja active Pending
- 2018-08-09 EP EP18756513.0A patent/EP3664781A1/en not_active Withdrawn
- 2018-08-09 CN CN201880051581.8A patent/CN111032019B/zh active Active
- 2018-08-09 CA CA3071285A patent/CA3071285A1/en active Pending
- 2018-09-07 US US16/125,358 patent/US10881685B2/en active Active
-
2022
- 2022-08-29 JP JP2022135754A patent/JP7422827B2/ja active Active
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS63290822A (ja) * | 1987-02-09 | 1988-11-28 | ザ ダウ ケミカル カンパニー | コレスティラミン組成物およびその製法 |
| WO2001076635A1 (en) * | 2000-04-10 | 2001-10-18 | Shionogi & Co., Ltd. | Preparations for preventing bile acid diarrhea |
| JP2005536502A (ja) * | 2002-07-13 | 2005-12-02 | アストラゼネカ アクチボラグ | 下痢の処置用のibat阻害剤および金属塩の組合せ |
Also Published As
| Publication number | Publication date |
|---|---|
| RU2020109469A3 (ja) | 2022-01-14 |
| WO2019032026A1 (en) | 2019-02-14 |
| JP7422827B2 (ja) | 2024-01-26 |
| CN111032019A (zh) | 2020-04-17 |
| US20190070217A1 (en) | 2019-03-07 |
| CA3071285A1 (en) | 2019-02-14 |
| RU2020109469A (ru) | 2021-09-10 |
| EP3664781A1 (en) | 2020-06-17 |
| JP2020530448A (ja) | 2020-10-22 |
| CN111032019B (zh) | 2022-07-05 |
| US10881685B2 (en) | 2021-01-05 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7422827B2 (ja) | コレスチラミン顆粒、経口コレスチラミン製剤、及びそれらの使用 | |
| JP7328207B2 (ja) | コレスチラミンペレット、経口コレスチラミン製剤、及びそれらの使用 | |
| JP6954926B2 (ja) | 経口コレスチラミン製剤及びその使用 | |
| JP6954927B2 (ja) | 経口コレスチラミン製剤及びその使用 | |
| US10493096B2 (en) | Oral cholestyramine formulation and use thereof | |
| US10799527B2 (en) | Oral cholestyramine formulation and use thereof | |
| US11007142B2 (en) | Oral cholestyramine formulation and use thereof | |
| US10722457B2 (en) | Oral cholestyramine formulation and use thereof | |
| RU2783157C2 (ru) | Гранулы холестирамина, пероральные композиции холестирамина и их применение | |
| RU2782016C9 (ru) | Пеллеты холестирамина, пероральные композиции холестирамина и их применение | |
| RU2782016C2 (ru) | Пеллеты холестирамина, пероральные композиции холестирамина и их применение | |
| HK40001803B (en) | Oral cholestyramine formulation and use thereof |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20220829 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20230731 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20231026 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20231218 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20240116 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7422827 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |