JP2015160964A - ニッケル粉末とその製造方法 - Google Patents
ニッケル粉末とその製造方法 Download PDFInfo
- Publication number
- JP2015160964A JP2015160964A JP2014035261A JP2014035261A JP2015160964A JP 2015160964 A JP2015160964 A JP 2015160964A JP 2014035261 A JP2014035261 A JP 2014035261A JP 2014035261 A JP2014035261 A JP 2014035261A JP 2015160964 A JP2015160964 A JP 2015160964A
- Authority
- JP
- Japan
- Prior art keywords
- nickel
- water
- nickel powder
- particles
- organic solvent
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Landscapes
- Manufacture Of Metal Powder And Suspensions Thereof (AREA)
- Powder Metallurgy (AREA)
Abstract
Description
上記積層セラミック部品である積層セラミックコンデンサは、次のように製造されている。
まず、ニッケル粉末とエチルセルロース等の樹脂とターピネオール等の有機溶剤等とを混練した導電ペーストを、誘電体グリーンシート上にスクリーン印刷する。印刷された導電ペーストが交互に重なるように、誘電体グリーンシートを積層し、圧着する。
その後、積層体を所定の大きさにカットし、有機バインダとして使用したエチルセルロース等の樹脂の燃焼、除去を行う脱バインダ処理を行って、1300℃まで高温焼成する。そして、このセラミック体に外部電極を取り付けて積層セラミックコンデンサとする。
こうした薄層化に用いられるニッケル粉末は、粒径が均一であるとともに、触媒活性の低いニッケル粉末が求められている。その理由としては、触媒活性の高いニッケル粉末を用いた場合、脱バインダ処理時に急激な樹脂分解とともに多量のガスが発生し、コンデンサ内に滞留する問題が発現しやすくなるためである。この問題は、ニッケル自体に樹脂の加熱分解を促進する作用があることに起因しており、ニッケル粉末の触媒活性と呼ばれている。しかし、ニッケル粉末を用いていない誘電体層などの樹脂は、この温度では分解されないため、部分的樹脂分解にて発生したガスがコンデンサ内部に閉じ込められるため、内部電極の不連続性やデラミネーションといった問題が発現しやすくなる。
更には、ニッケル粉末には、酸素含有量が低いものが求められている。その理由は、酸素含有値が高いニッケル粉末を用いて1300℃まで高温焼成した際には、熱収縮量が大きくなり、その結果、セラミック体の応力が大きくなり、クラックやデラミネーションといった問題点が発現しやすいためである。
この特許文献2によれば、ニッケル表面の硫黄の形態が、硫化ニッケルが50%以上になるので触媒活性を制御できるが、硫化ニッケルと硫酸ニッケルの両方で存在しており、ニッケル表面の硫化物形態へ完全には制御できておらず、触媒活性の制御がまだ十分ではない。硫酸ニッケルができる理由としては、水中の溶存酸素等により硫化物が硫酸形態になってしまうことが影響していると考えられる。
しかしながら、ニッケル粉が微細になると、湿式解粒処理後の乾燥において、再凝集や酸化する問題が生じる。また、不活性ガス又は還元性ガス雰囲気中で乾式解粒処理しても、酸化を十分に抑制できないという問題があった。
また、真空下で130〜300℃の温度範囲で熱乾燥するニッケル粉の製造方法が提案されている(例えば、特許文献4参照。)。この方法においても、微細なニッケル粉では、乾燥凝集や酸化を十分に抑制できないという問題があった。
(A)水溶液系中のニッケル塩から還元剤を用いた湿式還元反応により、ニッケル粒子を生成させ、ニッケル粒子と反応後液との混合物を得る第1工程、
(B)得られた混合物に水を添加して、反応後液を希釈除去して水と置換する第2工程、
(C)反応後液を希釈除去した混合物に、沸点が120℃以下の水溶性有機溶媒を添加して、混合物に含まれる液体成分中の水を希釈除去して水溶性有機溶媒と置換する第3工程、
(D)水溶性有機溶媒と置換することで得られたニッケルスラリーに有機硫黄化合物を添加して、ニッケル表面に有機硫黄化合物を付着させる第4工程、
(E)水溶性有機溶媒と置換した混合物から、ニッケル粒子を固液分離する第5工程、及び、
(F)固液分離後のニッケル粒子に残留している水溶性有機溶媒を気化除去する第6工程、
を含むことを特徴とするニッケル粉末の製造方法が提供される。
さらに、本発明の第3の発明によれば、第2の発明の前記第4工程(D)において、前記有機硫黄化合物は、トリアジン環を有するチオール類、チオグリコール酸、及びこれらの誘導体から選ばれる1種以上であることを特徴とするニッケル粉末の製造方法が提供される。
また、本発明の第4の発明によれば、第1〜3のいずれかの発明の前記第4工程(D)において、前記有機硫黄化合物は、前記第3工程(C)で用いられた沸点が120℃以下の水溶性有機溶媒に溶解されていることを特徴とするニッケル粉末の製造方法が提供される。
また、本発明の第5の発明によれば、第1〜4のいずれかの発明の前記第4工程(D)において、前記有機硫黄化合物を、20〜50℃でニッケルスラリーに添加して、0.5〜24時間攪拌することを特徴とするニッケル粉末の製造方法が提供される。
また、本発明の第7の発明によれば、第6の発明の前記第3工程(C)における水溶性有機溶媒として、メタノール、エタノール、1−プロパノール、又は2−プロパノールから選択される1種類以上を用いることを特徴とするニッケル粉末の製造方法が提供される。
また、本発明の第8の発明によれば、第1〜7のいずれかの発明の前記第3工程(C)において、ニッケル粒子に対する水の残留分の比率が1質量%以下になるまで希釈除去することを特徴とするニッケル粉末の製造方法が提供される。
さらに、本発明の第10の発明によれば、第1〜9のいずれかの発明の前記第2工程(B)における水として、溶存酸素を除去した純水を用いることを特徴とするニッケル粉末の製造方法が提供される。
また、本発明の第11の発明によれば、第1〜10のいずれかの発明の前記第5工程(E)において、ニッケル粒子の固液分離は、不活性ガス雰囲気中で行うことを特徴とするニッケル粉末の製造方法が提供される。
さらに、本発明の第12の発明によれば、第1〜11のいずれかの発明において、前記第6工程(F)において、ニッケル粒子に残留している水溶性有機溶媒を、真空雰囲気中または不活性ガス雰囲気中で、加熱することにより除去することを特徴とするニッケル粉末の製造方法が提供される。
また、本発明の第14の発明によれば、第13の発明において、前記ニッケル粉末の硫黄含有量が0.1〜1.0質量%であることを特徴とするニッケル粉末が提供される。
さらに、本発明の第15の発明によれば、第13又は14の発明において、前記ニッケル粉末の粒子平均径が0.05〜0.3μmの範囲にあることを特徴とするニッケル粉末が提供される。
本発明のニッケル粉末の製造方法は、水溶液中のニッケル塩を還元してニッケル粒子を得る湿式還元反応によるニッケル粉末の製造方法であって、
(A)水溶液系中のニッケル塩から還元剤を用いた湿式還元反応により、ニッケル粒子を生成させ、ニッケル粒子と反応後液との混合物を得る第1工程、
(B)得られた混合物に水を添加して、反応後液を希釈除去して水と置換する第2工程、
(C)反応後液を希釈除去した混合物に、沸点が120℃以下の水溶性有機溶媒を添加して、混合物に含まれる液体成分中の水を希釈除去して水溶性有機溶媒と置換する第3工程、
(D)水溶性有機溶媒と置換することで得られたニッケルスラリーに有機硫黄化合物を添加して、ニッケル表面に有機硫黄化合物を付着させる第4工程、
(E)水溶性有機溶媒と置換した混合物から、ニッケル粒子を固液分離する第4工程、及び、
(F)固液分離後のニッケル粒子に残留している水溶性有機溶媒を気化除去する第5工程、
を含むことを特徴とする。
これにより、上記酸化ニッケルや水酸化ニッケルの生成反応を抑制して、ニッケル粉末の酸素含有量を低減するとともに、ニッケル粒子の凝集を抑制することができるが、本発明では、さらに、ニッケル粒子表面を沸点が120℃以下の水溶性有機溶媒で被覆した後で、沸点が120℃以下の水溶性有機溶媒に溶解した有機硫黄化合物を添加してニッケル粒子表面に有機硫黄化合物を付着させることで、触媒活性が低下したニッケル粒子が得られるようにした。
第1工程(A)は、水溶液系中のニッケル塩から還元剤を用いた湿式還元反応により、ニッケル粒子を生成させ、ニッケル粒子と反応後液の混合物を得る工程である。
ニッケル粒子を生成させることが可能な湿式還元反応による方法であれば、特に制限なく採用することができるが、微細で均一な粒径のニッケル粒子を得るためには、貴金属のコロイド粒子と還元剤を含むアルカリ性コロイド溶液に、ニッケル塩水溶液を添加して、ニッケル粒子を生成させ、反応後液を得る方法を用いることが好ましい。
貴金属コロイド粒子を利用したニッケル粉末の製造には、公知の製造方法を利用することができ、例えば、特開2007−138291号公報に記載された方法を利用することができる。
(i)パラジウムと銀とからなる複合コロイド粒子が分散したコロイド溶液と、還元剤と、アルカリ性物質とを混合して、アルカリ性コロイド溶液を作製する。
(ii)パラジウムと銀とからなる複合コロイド粒子が分散したコロイド溶液を作製し、該コロイド溶液に還元剤とアルカリ性物質を添加して、アルカリ性コロイド溶液を作製する。
(iii)パラジウムと銀とからなる複合コロイド粒子が分散したコロイド溶液と、還元剤を含有するアルカリ性溶液とをそれぞれ作製し、前記コロイド溶液と前記アルカリ性溶液を混合して、アルカリ性コロイド溶液を作製する。
前記アルカリ性コロイド溶液中のパラジウムの量は、後にニッケル塩水溶液として添加されるニッケルの量に対して、10〜500質量ppmとすること好ましく、銀の量は、後にニッケル塩水溶液として添加されるニッケルの量に対して0.1〜5質量ppmとすることが好ましい。
また、前記保護コロイド剤の添加量は、後にニッケル塩水溶液として添加されるニッケルの量に対して、0.02〜1質量%とすることが好ましく、保護コロイド剤としては、特にゼラチンが好ましいが、その他、ポリビニルピロリドン、アラビアゴム、ヘキサメタリン酸ナトリウム、ポリビニルアルコールを用いることもできる。
さらに、前記アルカリ性物質は、特に限定されるものではないが、例えば、水酸化ナトリウム、水酸化カリウム、アンモニア等の水溶性のアルカリ性物質であればよく、アルカリ性コロイド溶液としては、特にpHが10以上に調整された水酸化ナトリウムとヒドラジン水和物を含む混合水溶液であることが好ましい。
第2工程(B)は、第1工程(A)で得られた混合物に、水を添加して、反応後液を希釈除去して水と置換する工程である。
反応後液中には、ニッケル粉末に有害な塩基やアルカリなどが多量に含まれるため、これらの有害成分を除去する必要がある。通常は、固液分離と洗浄を繰り返して除去するが、第2工程(B)においては、ニッケル粒子を液体成分が被覆した状態、すなわち、液体成分によってニッケル粒子が外気雰囲気中の酸素と遮断されている状態を維持して、混合物に水を加えて希釈し、希釈された反応後液を除去する希釈除去を繰り返すことにより、上記有害成分を除去する。
ここで、第1工程(A)で得られた混合物は、スラリー状態であるため、そのままの状態で水を添加すると、反応後液が多いため、希釈除去に用いる水が大量に必要となる。したがって、希釈除去する前に、ニッケル粒子が外気雰囲気と接触しない程度まで、反応後液を減じておくことが好ましい。具体的には、前記混合物を静置沈降させ、上澄み液となっている反応後液を除去する、すなわち、ニッケル粒子が反応後液に浸って外気雰囲気中の酸素と遮断されている状態を保持できる程度まで、反応後液を除去することが好ましい。
さらに、反応後液を減じるためには、ニッケル粒子と反応後液の合計に対して、反応後液が60質量%以上となるように、固液分離してもよい。反応後液が60質量%以上残存する状態であれば、ニッケル粒子は、反応後液に覆われて、酸素との接触を抑制することができる。
反応後液の残留分は、乾燥後に上述のようにニッケル粉末に対して不純物となるので、反応後液の残留分を極力除去することが好ましい。このため、上記希釈と除去を繰り返して行うことが好ましく、ニッケル粒子に対する反応後液の残留分の比率が1質量%以下になるまで、希釈と除去を繰り返して、水と置換することが好ましい。ここで、反応後液の残留分の比率は、例えば、使用した原料から得られるニッケル粒子と反応後液の質量を算出し、除去した反応後液量を除去前の反応後液量から差し引いて残留分を算出し、その残留分をニッケル粒子量で除することで求めることができる。
反応後液の残留分の比率が1質量%を超えると、最終的に得られるニッケル粉末の不純物が多くなり、このニッケル粉末を用いて得られる積層セラミックコンデンサなどの電子機器の特性が低下することがある。
ニッケル粒子の酸化を抑制するためには、不活性ガス雰囲気などの酸素を含まない雰囲気中で上記希釈除去を行うことが好ましいが、酸素とニッケル粒子の接触の低減に配慮して上記操作を行うことにより、得られるニッケル粉末の酸素含有量を低減することが可能である。
第3工程(C)は、ニッケル粒子と反応後液が希釈除去されて置換された水とからなる混合物に、沸点が120℃以下の水溶性有機溶媒を添加して、混合物に含まれる液体成分中の水を希釈除去して、水溶性有機溶媒と置換する工程である。
これにより、乾燥、すなわち、水溶性有機溶媒を気化除去時に残留する水の量を大幅に減らし、酸化ニッケルや水酸化ニッケルの生成を抑制して、ニッケル粉末の酸素含有量や粒子の凝集を大幅に抑制することができる。
第2工程(B)終了後の混合物に、前記水溶性有機溶媒を添加してもよいが、混合物に含まれる水が多くスラリー状態となっている場合は、第2工程(B)と同様に、ニッケル粒子を静置沈降させ、上澄み液となっている水を除去する。その後、第2工程における水を前記水溶性有機溶媒に変更して、第2工程(B)と同様の操作を行い、水を希釈除去して、水溶性有機溶媒と置換する。第3工程(C)においても、ニッケル粒子と酸素の接触を抑制するため、酸素を巻き込まないように水溶性有機溶媒を添加することが好ましい。また、不活性ガス雰囲気中で上記希釈除去を行うことが好ましい。
ニッケル粒子を静置沈降させる際、さらに水を減じるため、第2工程(B)と同様に、ニッケル粒子と水の合計に対して水が60質量%以上となるように、固液分離した後、希釈除去を行ってもよい。
上記水溶性有機溶媒による希釈除去は、ニッケル粒子に対する水の残留分の比率が1質量%以下になるまで、行うことが好ましい。水の残留分の比率が1質量%を超えると、後工程で前記水溶性有機溶媒を気化除去する際に、ニッケル粒子表面に残留する水が増加するため、酸化ニッケルや水酸化ニッケルの形成が増加し、得られるニッケル粉末の酸素含有量や粒子の凝集が多くなることがある。
第4工程(D)は、水溶性有機溶媒と置換することで得られたニッケルスラリーに有機硫黄化合物を添加して、ニッケル表面に有機硫黄化合物を付着させる工程である。
ニッケル粉末の硫黄含有量が0.1質量%より少ないと、ニッケル粉末表面の反応性を抑制し、積層セラミックコンデンサ製造時に脱バインダ工程にてクラックが発生することが多くなる。また、硫黄含有量が1.0質量%を超えると、ニッケル粉末表面の反応性を抑制する効果が向上しなくなることと、積層セラミックコンデンサ製造時に硫黄過多による別の不具合を生じる可能性や、脱バインダ工程やその後の焼成工程にて発生する硫黄含有ガスがコンデンサ製造装置を腐食する可能性がある。
なお、上記ニッケル粉末の硫黄含有量範囲内となる第4工程(D)での有機硫黄化合物の濃度範囲は、その有機硫黄化合物の種類により異なるので、有機硫黄化合物を選択時に調整することになる。
第5工程(E)は、第4工程(D)で得られた有機硫黄化合物が付着したニッケル粒子と水溶性有機溶媒を含む混合物から、該ニッケル粒子を固液分離する工程である。
第5工程(E)においても、ニッケル粒子が酸素と接触することを抑制するため、ニッケル粒子と水溶性有機溶媒の合計に対して、水溶性有機溶媒が60質量%以上となるように、固液分離することが好ましい。
固液分離の方法は、ニッケル粒子が水溶性有機溶媒で覆われた状態を維持できれば、粉末の製造において通常に行われる方法でよく、例えば、吸引ろ過、遠心分離機等による固液分離方法を用いことができる。固液分離する際にも、残留する水が多い場合には、ニッケル粒子の酸化が進行することがあるため、不活性ガス雰囲気で行うことが好ましい。これにより酸素による酸化をさらに抑制することができる。
第6工程(F)は、固液分離後のニッケル粒子に残留している前記水溶性有機溶媒を気化除去する工程である。
本発明では沸点が120℃以下の水溶性有機溶媒用いるので、室温程度でも短時間で気化させることが可能であるが、微量に残留している水分を蒸発させるためには、加温された雰囲気とすることが好ましい。具体的には、50℃以下の範囲で加温することで、短時間で水溶性有機溶媒とともに残留している微量の水分を気化させることができ、ニッケル粉末の酸素含有量や粒子の凝集をさらに抑制することができる。50℃を超える温度まで加熱すると、水溶性有機溶媒の気化に対する効果が向上しないばかりか、過度に加熱すると、熱による粒子の凝集が進行することがある。
上記本発明のニッケル粉末の製造方法によって、ニッケル粒子の凝集を防止して、ニッケル粒子の分散性に優れ、また、微細で粒径の均一性に優れ、触媒活性が抑制され、酸素含有量が少ない本発明の硫黄を含有するニッケル粉末を得ることができる。
また、樹脂の分解速度のピーク温度が300℃未満であると、ニッケル粉末の触媒活性が充分に抑制されておらず、ニッケル粉末を用いていない誘電体層の樹脂が分解する前に、ニッケル粉末近傍の樹脂が分解し、発生したガスがコンデンサ内部に閉じ込められるため、内部電極の不連続性やデラミネーションが発生する。
以上のように、本発明のニッケル粉末は、微細で粒径の均一性に優れ、酸素含有量が少なく、表面に硫黄を含有し触媒活性が抑制されるので、電子部品の電極用、特に積層セラミックコンデンサの内部電極用として好適である。
なお、実施例及び比較例で用いたニッケル粉末の粒径、樹脂の分解速度のピーク温度、酸素含有量、硫黄含有量の測定方法または評価方法は、以下の通りである。
平均粒径は、走査型電子顕微鏡(日本電子社製、JSM−5510)を用いて、倍率20,000倍の写真(縦19.2μm×横25.6μm)を撮影し、写真中の粒子形状の全様が見える100個以上粒子の面積を測定し、面積から各粒子の粒径を求め、個数平均値により求めた。
まず、有機バインダであるエチルセルロース(以下、ECと略記する場合がある。)をニッケル粉末に対して5質量%物理混合した混合物と、ニッケル粉末のみを、それぞれTG測定装置(マックサイエンス社製、2000SA)を用いて、窒素ガス中、5℃/minの昇温速度で重量変化を測定した。
その後、ECとニッケル粉末を混合したニッケル粉末の重量変化からニッケル粉末のみの重量変化を引き去り、ニッケル粉末中のECの重量変化を求めた。これらの結果を用いて、ECの重量変化を温度で一次微分して、EC分解速度を求め、ニッケル粉末の触媒活性を評価した。EC分解速度が最大を示す温度を、EC分解温度とした。
ニッケル粉末の酸素含有量は、酸素分析装置(LECO社製、型番TC−436AR)にて測定した。また、硫黄含有量は、炭素、硫黄同時分析装置(LECO社製、型番CS−600)にて測定した。
1.第1工程:
10Lビーカーに純水6.5Lを入れ、撹拌しながら75℃まで昇温し保持した。その後、ゼラチン0.025gを溶解してゼラチン溶液を作製し、パラジウム0.0025g、銀0.000025gを含む溶液を滴下した後に、60質量%ヒドラジン水溶液0.1gを混合して、複合コロイド溶液を得た。
この複合コロイド溶液に水酸化ナトリウム顆粒50gを添加した後、60質量%ヒドラジン水溶液を185ml加え、ニッケルを還元するためのアルカリ性コロイド溶液とした。
次に、上記アルカリ性コロイド溶液に、100g/L塩化ニッケル水溶液500mlを滴下して、ニッケル粒子を還元析出させ、平均粒径が0.2μmのニッケル粉末を含む混合物を得た。
還元反応が終了した後、攪拌を停止し、混合物からニッケル粉末を静置沈降し反応後液を除去した。除去後の混合物(反応後液量とニッケル粉末)の総量は350gであった。この時点でニッケル粉末量は50g、反応後液量は300gであった。
次に、純水5.7Lをゆっくりと添加して撹拌し、反応後液を希釈した。
その後、静置沈降して、純水と反応後液の混合溶液を5.7kg除去した。更に純水5.7Lをゆっくりと添加した後、撹拌して希釈した。
その後、静置沈降させ、純水と反応後液の混合溶液を5.7kg除去することを繰り返し、ニッケル量に対して反応後液の残留分重量が理論値で1質量%以下になるまで純水で置換した。この時点で混合物(純水量とニッケル粉末)の総量は350gであり、ニッケル粉末量は50g、純水量は300gとなる。
次に、混合物にエタノール5.7kgをゆっくりと添加して撹拌し、純水を希釈した。
その後、静置沈降して、純水とエタノールの混合溶液を5.7kg除去した。更にエタノール5.7kgをゆっくりと添加して撹拌し、純水を希釈した。
その後、静置沈降させ、純水とエタノールの混合溶液を5.7kg除去することを繰り返し、ニッケル量に対して純水の残留分量が1質量%以下になるまでエタノールで置換した。
その後、ニッケル粒子を静置沈降させ、エタノールを5.85kg除去し、残ったエタノールとニッケル粒子を500mlビーカーへ移し替え、50gエタノールを加えてエタノール量200g、ニッケル粉末量50gのニッケルスラリーとした。
また、有機硫黄化合物として2−4−6トリメルカプト―s−トリアジンを用い、硫黄量がニッケル粉末に対し0.5質量%になる量をエタノール50gに溶解させ、有機硫黄化合物溶液を作製した。
引き続き、有機硫黄化合物溶液を、撹拌したニッケルスラリーへ添加し、20℃で30分撹拌をおこなって、有機硫黄化合物が付着したニッケル粒子を含むスラリーを得た。
次に、有機硫黄化合物が付着したニッケル粒子を含むスラリーに対して減圧濾過を行い、エタノールを除去し、ニッケル粉末ケーキとした。
ニッケル粉末ケーキを真空雰囲気中で40℃に加温し、ニッケル粉末ケーキに残っているエタノールを、気化除去した。
その後、徐酸化を行わず、空気を導入し、大気圧まで戻し大気暴露させ、ニッケル粉末を得た。
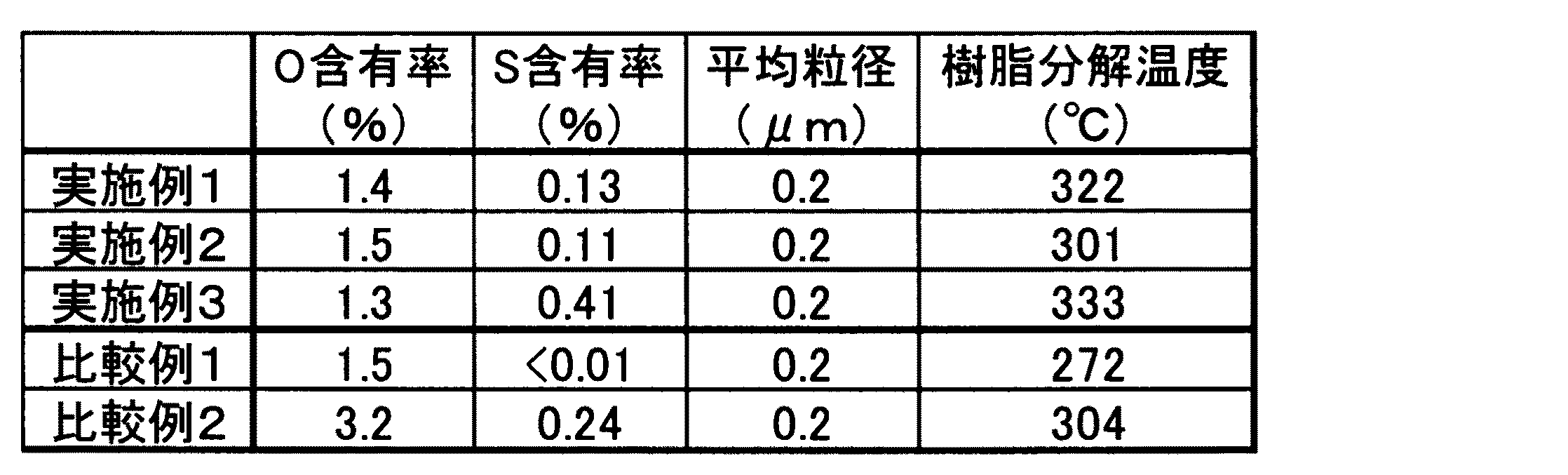
得られたニッケル粉末の酸素含有量、硫黄含有量、樹脂分解温度を測定し、表1に示す。得られたニッケル粉末のSEM観察では、ニッケル粒子が凝集した粗大粒子は、観察されなかった。
実施例1の第4工程で、有機硫黄化合物としてメルカプト酢酸を用いた以外は、実施例1と同様にして、ニッケル粉末を得るとともに、その物性を評価した。得られたニッケル粉末の粒径は0.2μmであった。
得られたニッケル粉末の酸素含有量、硫黄含有量、樹脂分解温度を表1に示す。得られたニッケル粉末のSEM観察では、ニッケル粒子が凝集した粗大粒子は、観察されなかった。
実施例1の第4工程で、有機硫黄化合物として3−メルカプトプロパン酸オクタデシルを用いた以外は、実施例1と同様にして、ニッケル粉末を得るとともに評価した。得られたニッケル粉末の粒径は0.2μmであった。
得られたニッケル粉末の酸素含有量、硫黄含有量、樹脂分解温度を表1に示す。得られたニッケル粉末のSEM観察では、ニッケル粒子が凝集した粗大粒子は、観察されなかった。
実施例1において、第4工程を除外した以外は、実施例1と同様にして実験した。すなわち、水溶液系中のニッケル塩から還元剤を用いた湿式還元反応により、ニッケル粒子を生成させ、得られたニッケル粒子と反応後液との混合物に水を添加して、反応後液を希釈除去して水と置換し、この混合物に、水溶性有機溶媒(エタノール)を添加して、混合物に含まれる液体成分中の水を希釈除去して水溶性有機溶媒と置換した。その後、有機硫黄化合物を添加することなく、スラリーからエタノールを除去しニッケル粉末を得るとともに評価した。得られたニッケル粉末の粒径は0.2μmであった。
得られたニッケル粉末の酸素含有量、硫黄含有量、樹脂分解温度を表1に示す。得られたニッケル粉末のSEM観察では、ニッケル粒子が凝集した粗大粒子は、観察されなかった。
実施例1において、第2工程まで同様に行って得られたニッケル粉末を500mlビーカーに移し、純水200g中に分散させ、ニッケル水スラリーを得た後、水を水溶性有機溶媒(エタノール)に置換することなく、有機硫黄化合物溶液を撹拌したニッケル水スラリーに添加し、30分撹拌した。有機硫黄化合物としては、メルカプト酢酸を用い、硫黄量がニッケル粉末に対し0.5質量%になる量を純水50gに溶解させ、有機硫黄化合物溶液とした。
その後、有機硫黄化合物が付着ニッケル粒子を含むスラリーに対して、減圧濾過を行い、純水を除去し、真空雰囲気中で150℃に加温し、ニッケル粉末ケーキに残っている純水を、気化除去し、ニッケル粉末を得るとともに評価した。得られたニッケル粉末の粒径は0.2μmであった。
得られたニッケル粉末の酸素含有量、樹脂分解温度を表1に示す。得られたニッケル粉末のSEM観察では、ニッケル粒子が凝集した粗大粒子は、観察されなかった。
Claims (15)
- 水溶液中のニッケル塩を還元してニッケル粒子を得る湿式還元反応によるニッケル粉末の製造方法であって、
(A)水溶液系中のニッケル塩から還元剤を用いた湿式還元反応により、ニッケル粒子を生成させ、ニッケル粒子と反応後液との混合物を得る第1工程、
(B)得られた混合物に水を添加して、反応後液を希釈除去して水と置換する第2工程、
(C)反応後液を希釈除去した混合物に、沸点が120℃以下の水溶性有機溶媒を添加して、混合物に含まれる液体成分中の水を希釈除去して水溶性有機溶媒と置換する第3工程、
(D)水溶性有機溶媒と置換することで得られたニッケルスラリーに有機硫黄化合物を添加して、ニッケル表面に有機硫黄化合物を付着させる第4工程、
(E)水溶性有機溶媒と置換した混合物から、ニッケル粒子を固液分離する第5工程、及び、
(F)固液分離後のニッケル粒子に残留している水溶性有機溶媒を気化除去する第6工程、
を含むことを特徴とするニッケル粉末の製造方法。 - 前記第4工程(D)において、前記有機硫黄化合物はチオール基を含有していることを特徴とする請求項1に記載のニッケル粉末の製造方法。
- 前記第4工程(D)において、前記有機硫黄化合物はトリアジン環を有するチオール類、チオグリコール酸、及びこれらの誘導体から選ばれる1種以上であることを特徴とする請求項2に記載のニッケル粉末の製造方法。
- 前記第4工程(D)において、前記有機硫黄化合物は、前記第3工程(C)で用いられた沸点が120℃以下の水溶性有機溶媒に溶解されていることを特徴とする請求項1〜3のいずれか1項に記載のニッケル粉末の製造方法。
- 前記第4工程(D)において、前記有機硫黄化合物は、20〜50℃でニッケルスラリーに添加して、0.5〜24時間攪拌することを特徴とする請求項1〜4のいずれか1項に記載のニッケル粉末の製造方法。
- 前記第3工程(C)における水溶性有機溶媒として、アルコールを用いることを特徴とする請求項1〜5のいずれか1項に記載のニッケル粉末の製造方法。
- 前記第3工程(C)における水溶性有機溶媒として、メタノール、エタノール、1−プロパノール、又は2−プロパノールから選択される1種類以上を用いることを特徴とする請求項6に記載のニッケル粉末の製造方法。
- 前記第3工程(C)において、ニッケル粒子に対する水の残留分の比率が1質量%以下になるまで希釈除去することを特徴とする請求項1〜7のいずれか1項に記載のニッケル粉末の製造方法。
- 前記第1工程(A)において、貴金属のコロイド粒子と還元剤を含むアルカリ性コロイド溶液にニッケル塩水溶液を添加して、ニッケル粒子を生成させ、混合物を得ることを特徴とする請求項1〜8のいずれか1項に記載のニッケル粉末の製造方法。
- 前記第2工程(B)における水として、溶存酸素を除去した純水を用いることを特徴とする請求項1〜9のいずれか1項に記載のニッケル粉末の製造方法。
- 前記第5工程(E)において、ニッケル粒子の固液分離は、不活性ガス雰囲気中で行うことを特徴とする請求項1〜10のいずれか1項に記載のニッケル粉末の製造方法。
- 前記第6工程(F)において、ニッケル粒子に残留している水溶性有機溶媒を、真空雰囲気中または不活性ガス雰囲気中で、加熱することにより除去することを特徴とする請求項1〜11のいずれか1項に記載のニッケル粉末の製造方法。
- 請求項1〜12のいずれか1項に記載のニッケル粉末の製造方法で得られるニッケル粉末であって、
該ニッケル粉末と共存下で測定したエチルセルロースの分解温度が300℃以上であり、該ニッケル粉末の酸素含有量が0.8〜1.5質量%であることを特徴とするニッケル粉末。 - 前記ニッケル粉末の硫黄含有量が0.1〜1.0質量%であることを特徴とする請求項13に記載のニッケル粉末。
- 前記ニッケル粉末の粒子平均径が0.05〜0.3μmの範囲にあることを特徴とする請求項13又は14に記載のニッケル粉末。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2014035261A JP6213301B2 (ja) | 2014-02-26 | 2014-02-26 | ニッケル粉末の製造方法 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2014035261A JP6213301B2 (ja) | 2014-02-26 | 2014-02-26 | ニッケル粉末の製造方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2015160964A true JP2015160964A (ja) | 2015-09-07 |
| JP6213301B2 JP6213301B2 (ja) | 2017-10-18 |
Family
ID=54184287
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2014035261A Active JP6213301B2 (ja) | 2014-02-26 | 2014-02-26 | ニッケル粉末の製造方法 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP6213301B2 (ja) |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2017159659A1 (ja) * | 2016-03-18 | 2017-09-21 | 住友金属鉱山株式会社 | ニッケル粉末、ニッケル粉末の製造方法、およびニッケル粉末を用いた内部電極ペーストならびに電子部品 |
| JP2019044268A (ja) * | 2017-09-06 | 2019-03-22 | 住友金属鉱山株式会社 | 湿式ニッケル粉末の粗大粒子低減方法 |
| KR20190084078A (ko) * | 2016-12-05 | 2019-07-15 | 스미토모 긴조쿠 고잔 가부시키가이샤 | 니켈 분말의 제조 방법 |
| JP7573378B2 (ja) | 2020-05-29 | 2024-10-25 | 日鉄ケミカル&マテリアル株式会社 | ニッケルナノ粒子凝集体、その製造方法及びニッケルナノ粒子複合基板 |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2004068090A (ja) * | 2002-08-07 | 2004-03-04 | Murata Mfg Co Ltd | 導電性粉末の製造方法、導電性粉末、導電性ペーストおよび積層セラミック電子部品 |
| JP2007138291A (ja) * | 2005-10-20 | 2007-06-07 | Sumitomo Metal Mining Co Ltd | ニッケル粉末およびその製造方法 |
| JP2008095145A (ja) * | 2006-10-12 | 2008-04-24 | Sumitomo Metal Mining Co Ltd | 積層セラミックコンデンサの内部電極用ニッケル粉末及びその製造方法 |
| WO2011037150A1 (ja) * | 2009-09-24 | 2011-03-31 | 住友金属鉱山株式会社 | ニッケル微粉及びその製造方法 |
-
2014
- 2014-02-26 JP JP2014035261A patent/JP6213301B2/ja active Active
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2004068090A (ja) * | 2002-08-07 | 2004-03-04 | Murata Mfg Co Ltd | 導電性粉末の製造方法、導電性粉末、導電性ペーストおよび積層セラミック電子部品 |
| JP2007138291A (ja) * | 2005-10-20 | 2007-06-07 | Sumitomo Metal Mining Co Ltd | ニッケル粉末およびその製造方法 |
| JP2008095145A (ja) * | 2006-10-12 | 2008-04-24 | Sumitomo Metal Mining Co Ltd | 積層セラミックコンデンサの内部電極用ニッケル粉末及びその製造方法 |
| WO2011037150A1 (ja) * | 2009-09-24 | 2011-03-31 | 住友金属鉱山株式会社 | ニッケル微粉及びその製造方法 |
Cited By (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2017159659A1 (ja) * | 2016-03-18 | 2017-09-21 | 住友金属鉱山株式会社 | ニッケル粉末、ニッケル粉末の製造方法、およびニッケル粉末を用いた内部電極ペーストならびに電子部品 |
| JP2017171957A (ja) * | 2016-03-18 | 2017-09-28 | 住友金属鉱山株式会社 | ニッケル粉末、ニッケル粉末の製造方法、およびニッケル粉末を用いた内部電極ペーストならびに電子部品 |
| CN108602129A (zh) * | 2016-03-18 | 2018-09-28 | 住友金属矿山株式会社 | 镍粉、镍粉的制造方法以及使用镍粉的内部电极膏和电子部件 |
| TWI701345B (zh) * | 2016-03-18 | 2020-08-11 | 日商住友金屬礦山股份有限公司 | 鎳粉末、鎳粉末的製造方法及使用鎳粉末的內部電極用糊及電子零件 |
| CN113976905A (zh) * | 2016-03-18 | 2022-01-28 | 住友金属矿山株式会社 | 镍粉、镍粉的制造方法以及使用镍粉的内部电极膏和电子部件 |
| US11376658B2 (en) | 2016-03-18 | 2022-07-05 | Sumitomo Metal Mining Co., Ltd. | Nickel powder, method for manufacturing nickel powder, internal electrode paste using nickel powder, and electronic component |
| US11772160B2 (en) | 2016-03-18 | 2023-10-03 | Sumitomo Metal Mining Co., Ltd. | Nickel powder, method for manufacturing nickel powder, internal electrode paste using nickel powder, and electronic component |
| KR20190084078A (ko) * | 2016-12-05 | 2019-07-15 | 스미토모 긴조쿠 고잔 가부시키가이샤 | 니켈 분말의 제조 방법 |
| KR102253292B1 (ko) * | 2016-12-05 | 2021-05-20 | 스미토모 긴조쿠 고잔 가부시키가이샤 | 니켈 분말의 제조 방법 |
| JP2019044268A (ja) * | 2017-09-06 | 2019-03-22 | 住友金属鉱山株式会社 | 湿式ニッケル粉末の粗大粒子低減方法 |
| JP7183504B2 (ja) | 2017-09-06 | 2022-12-06 | 住友金属鉱山株式会社 | 湿式ニッケル粉末の粗大粒子低減方法 |
| JP7573378B2 (ja) | 2020-05-29 | 2024-10-25 | 日鉄ケミカル&マテリアル株式会社 | ニッケルナノ粒子凝集体、その製造方法及びニッケルナノ粒子複合基板 |
Also Published As
| Publication number | Publication date |
|---|---|
| JP6213301B2 (ja) | 2017-10-18 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5574154B2 (ja) | ニッケル粉末およびその製造方法 | |
| JP6224933B2 (ja) | 銀被覆銅合金粉末およびその製造方法 | |
| JP7090511B2 (ja) | 銀粉およびその製造方法 | |
| JP5067312B2 (ja) | ニッケル粉末とその製造方法 | |
| JP6213301B2 (ja) | ニッケル粉末の製造方法 | |
| JP6679312B2 (ja) | 銀被覆銅粉およびその製造方法 | |
| JP6727922B2 (ja) | 銀粉およびその製造方法、ならびに導電性ペースト | |
| JP4879473B2 (ja) | フレーク銅粉及びフレーク銅粉の製造方法並びにフレーク銅粉を含む導電性スラリー | |
| JP5958749B2 (ja) | 金属粉末の製造方法 | |
| WO2014148098A1 (ja) | ニッケル粉末とその製造方法 | |
| WO2016031210A1 (ja) | 銀被覆銅粉およびその製造方法 | |
| JP5526856B2 (ja) | ニッケル粉末およびその製造方法 | |
| JP2007220332A (ja) | 銀粉とその製造方法及びこれを用いたペースト、電子回路部品、電気製品 | |
| JP2012140661A (ja) | 扁平銅粒子 | |
| JP6424104B2 (ja) | 導電性ペースト用銅粉およびその製造方法 | |
| CN110114175B (zh) | 高温烧结型银粉末及其制造方法 | |
| JP7136970B2 (ja) | りんを含有する銀粉および該銀粉を含む導電性ペースト | |
| JP6065699B2 (ja) | ニッケル粉末の製造方法 | |
| JP5785433B2 (ja) | 低炭素銅粒子 | |
| JP2017071851A (ja) | ニッケル粉末 | |
| JP2009024204A (ja) | 炭化物被覆ニッケル粉末およびその製造方法 | |
| JP6131773B2 (ja) | ニッケル粉とその製造方法、及びそれを用いたニッケルペースト | |
| WO2017179524A1 (ja) | 銀被覆銅粉およびその製造方法 | |
| JP6083295B2 (ja) | ニッケル粉末の製造方法 | |
| JP2004183060A (ja) | ポリアニリン系樹脂コート銅粉並びにそのポリアニリン系樹脂コート銅粉の製造方法及びそのポリアニリン系樹脂コート銅粉を用いた導電性ペースト |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20150608 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20160601 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20170307 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20170404 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20170525 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20170822 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20170904 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6213301 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |