JP2009505966A - セリンプロテアーゼのインヒビター - Google Patents
セリンプロテアーゼのインヒビター Download PDFInfo
- Publication number
- JP2009505966A JP2009505966A JP2008525128A JP2008525128A JP2009505966A JP 2009505966 A JP2009505966 A JP 2009505966A JP 2008525128 A JP2008525128 A JP 2008525128A JP 2008525128 A JP2008525128 A JP 2008525128A JP 2009505966 A JP2009505966 A JP 2009505966A
- Authority
- JP
- Japan
- Prior art keywords
- optionally substituted
- mixture
- group
- membered
- compounds according
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 239000003112 inhibitor Substances 0.000 title claims description 36
- 108010022999 Serine Proteases Proteins 0.000 title claims description 34
- 102000012479 Serine Proteases Human genes 0.000 title claims description 34
- 239000000203 mixture Substances 0.000 claims abstract description 176
- 150000003839 salts Chemical class 0.000 claims abstract description 20
- 229910052799 carbon Inorganic materials 0.000 claims abstract description 13
- 150000001875 compounds Chemical class 0.000 claims description 222
- 125000001931 aliphatic group Chemical group 0.000 claims description 167
- 125000001072 heteroaryl group Chemical group 0.000 claims description 113
- -1 n- propyl Chemical group 0.000 claims description 106
- 125000003118 aryl group Chemical group 0.000 claims description 78
- 125000000217 alkyl group Chemical group 0.000 claims description 64
- 238000000034 method Methods 0.000 claims description 52
- 125000004429 atom Chemical group 0.000 claims description 48
- 125000002619 bicyclic group Chemical group 0.000 claims description 41
- 125000000623 heterocyclic group Chemical group 0.000 claims description 38
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 claims description 35
- 125000004122 cyclic group Chemical group 0.000 claims description 34
- 125000001424 substituent group Chemical group 0.000 claims description 31
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims description 26
- 125000000753 cycloalkyl group Chemical group 0.000 claims description 23
- 125000003342 alkenyl group Chemical group 0.000 claims description 20
- 125000005842 heteroatom Chemical group 0.000 claims description 20
- 239000008194 pharmaceutical composition Substances 0.000 claims description 20
- 125000003107 substituted aryl group Chemical group 0.000 claims description 20
- 230000000694 effects Effects 0.000 claims description 19
- 125000002950 monocyclic group Chemical group 0.000 claims description 19
- 210000004369 blood Anatomy 0.000 claims description 18
- 239000008280 blood Substances 0.000 claims description 18
- 102000006992 Interferon-alpha Human genes 0.000 claims description 17
- 108010047761 Interferon-alpha Proteins 0.000 claims description 17
- 102000035195 Peptidases Human genes 0.000 claims description 17
- 108091005804 Peptidases Proteins 0.000 claims description 17
- 239000003443 antiviral agent Substances 0.000 claims description 15
- 239000004365 Protease Substances 0.000 claims description 14
- 239000003795 chemical substances by application Substances 0.000 claims description 13
- 101800001838 Serine protease/helicase NS3 Proteins 0.000 claims description 12
- 239000002552 dosage form Substances 0.000 claims description 12
- 208000015181 infectious disease Diseases 0.000 claims description 12
- 125000003710 aryl alkyl group Chemical group 0.000 claims description 11
- 229910052739 hydrogen Inorganic materials 0.000 claims description 11
- IWUCXVSUMQZMFG-AFCXAGJDSA-N Ribavirin Chemical group N1=C(C(=O)N)N=CN1[C@H]1[C@H](O)[C@H](O)[C@@H](CO)O1 IWUCXVSUMQZMFG-AFCXAGJDSA-N 0.000 claims description 10
- 125000000392 cycloalkenyl group Chemical group 0.000 claims description 10
- 125000004432 carbon atom Chemical group C* 0.000 claims description 9
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 claims description 8
- 229960000329 ribavirin Drugs 0.000 claims description 8
- HZCAHMRRMINHDJ-DBRKOABJSA-N ribavirin Natural products O[C@@H]1[C@H](O)[C@@H](CO)O[C@H]1N1N=CN=C1 HZCAHMRRMINHDJ-DBRKOABJSA-N 0.000 claims description 8
- 125000001313 C5-C10 heteroaryl group Chemical group 0.000 claims description 7
- 239000002955 immunomodulating agent Substances 0.000 claims description 7
- 229910052760 oxygen Inorganic materials 0.000 claims description 7
- 239000000137 peptide hydrolase inhibitor Substances 0.000 claims description 7
- 125000006376 (C3-C10) cycloalkyl group Chemical group 0.000 claims description 6
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 claims description 6
- 229940121354 immunomodulator Drugs 0.000 claims description 6
- 125000006717 (C3-C10) cycloalkenyl group Chemical group 0.000 claims description 5
- 229940124158 Protease/peptidase inhibitor Drugs 0.000 claims description 5
- NCDNCNXCDXHOMX-UHFFFAOYSA-N Ritonavir Natural products C=1C=CC=CC=1CC(NC(=O)OCC=1SC=NC=1)C(O)CC(CC=1C=CC=CC=1)NC(=O)C(C(C)C)NC(=O)N(C)CC1=CSC(C(C)C)=N1 NCDNCNXCDXHOMX-UHFFFAOYSA-N 0.000 claims description 5
- 239000012472 biological sample Substances 0.000 claims description 5
- 125000006317 cyclopropyl amino group Chemical group 0.000 claims description 5
- 230000002401 inhibitory effect Effects 0.000 claims description 5
- 229960000311 ritonavir Drugs 0.000 claims description 5
- NCDNCNXCDXHOMX-XGKFQTDJSA-N ritonavir Chemical group N([C@@H](C(C)C)C(=O)N[C@H](C[C@H](O)[C@H](CC=1C=CC=CC=1)NC(=O)OCC=1SC=NC=1)CC=1C=CC=CC=1)C(=O)N(C)CC1=CSC(C(C)C)=N1 NCDNCNXCDXHOMX-XGKFQTDJSA-N 0.000 claims description 5
- 239000000523 sample Substances 0.000 claims description 5
- 229910052717 sulfur Inorganic materials 0.000 claims description 5
- 125000000041 C6-C10 aryl group Chemical group 0.000 claims description 4
- 102000003996 Interferon-beta Human genes 0.000 claims description 4
- 108090000467 Interferon-beta Proteins 0.000 claims description 4
- 102000008070 Interferon-gamma Human genes 0.000 claims description 4
- 108010074328 Interferon-gamma Proteins 0.000 claims description 4
- 108060004795 Methyltransferase Proteins 0.000 claims description 4
- 108010046075 Thymosin Proteins 0.000 claims description 4
- 102000007501 Thymosin Human genes 0.000 claims description 4
- 229910052736 halogen Inorganic materials 0.000 claims description 4
- 150000002367 halogens Chemical class 0.000 claims description 4
- 125000006239 protecting group Chemical group 0.000 claims description 4
- KAIODGZZEANQLB-UHFFFAOYSA-N 1,2,3,3a,4,5,6,6a-octahydrocyclopenta[c]pyrrole-3-carboxamide Chemical compound C1CCC2C(C(=O)N)NCC21 KAIODGZZEANQLB-UHFFFAOYSA-N 0.000 claims description 3
- 208000003311 Cytochrome P-450 Enzyme Inhibitors Diseases 0.000 claims description 3
- DKNWSYNQZKUICI-UHFFFAOYSA-N amantadine Chemical compound C1C(C2)CC3CC2CC1(N)C3 DKNWSYNQZKUICI-UHFFFAOYSA-N 0.000 claims description 3
- 229960003805 amantadine Drugs 0.000 claims description 3
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 claims description 3
- 229940044627 gamma-interferon Drugs 0.000 claims description 3
- 125000002911 monocyclic heterocycle group Chemical group 0.000 claims description 3
- 125000006574 non-aromatic ring group Chemical group 0.000 claims description 3
- SNOOUWRIMMFWNE-UHFFFAOYSA-M sodium;6-[(3,4,5-trimethoxybenzoyl)amino]hexanoate Chemical compound [Na+].COC1=CC(C(=O)NCCCCCC([O-])=O)=CC(OC)=C1OC SNOOUWRIMMFWNE-UHFFFAOYSA-M 0.000 claims description 3
- LCJVIYPJPCBWKS-NXPQJCNCSA-N thymosin Chemical compound SC[C@@H](N)C(=O)N[C@H](CO)C(=O)N[C@H](CC(O)=O)C(=O)N[C@@H](C)C(=O)N[C@@H](C)C(=O)N[C@H](C(C)C)C(=O)N[C@H](CC(O)=O)C(=O)N[C@H](C(C)C)C(=O)N[C@H](CO)C(=O)N[C@H](CO)C(=O)N[C@H](CCC(O)=O)C(=O)N[C@H]([C@@H](C)CC)C(=O)N[C@H]([C@H](C)O)C(=O)N[C@H](C(C)C)C(=O)N[C@H](CCCCN)C(=O)N[C@H](CC(O)=O)C(=O)N[C@H](CC(C)C)C(=O)N[C@H](CCCCN)C(=O)N[C@H](CCC(O)=O)C(=O)N[C@H](CCCCN)C(=O)N[C@H](CCCCN)C(=O)N[C@H](CCC(O)=O)C(=O)N[C@H](C(C)C)C(=O)N[C@H](C(C)C)C(=O)N[C@H](CCC(O)=O)C(=O)N[C@H](CCC(O)=O)C(=O)N[C@@H](C)C(=O)N[C@H](CCC(O)=O)C(O)=O LCJVIYPJPCBWKS-NXPQJCNCSA-N 0.000 claims description 3
- 125000002618 bicyclic heterocycle group Chemical group 0.000 claims description 2
- 125000000464 thioxo group Chemical group S=* 0.000 claims description 2
- 210000001124 body fluid Anatomy 0.000 claims 4
- 239000010839 body fluid Substances 0.000 claims 4
- 239000002671 adjuvant Substances 0.000 claims 3
- 230000002584 immunomodulator Effects 0.000 claims 3
- 229940122280 Cytochrome P450 inhibitor Drugs 0.000 claims 2
- 238000011109 contamination Methods 0.000 claims 2
- RZVAJINKPMORJF-UHFFFAOYSA-N Acetaminophen Chemical compound CC(=O)NC1=CC=C(O)C=C1 RZVAJINKPMORJF-UHFFFAOYSA-N 0.000 claims 1
- 102000005741 Metalloproteases Human genes 0.000 claims 1
- 108010006035 Metalloproteases Proteins 0.000 claims 1
- IQFYYKKMVGJFEH-UHFFFAOYSA-N beta-L-thymidine Natural products O=C1NC(=O)C(C)=CN1C1OC(CO)C(O)C1 IQFYYKKMVGJFEH-UHFFFAOYSA-N 0.000 claims 1
- 125000004446 heteroarylalkyl group Chemical group 0.000 claims 1
- IQFYYKKMVGJFEH-CSMHCCOUSA-N telbivudine Chemical compound O=C1NC(=O)C(C)=CN1[C@H]1O[C@@H](CO)[C@H](O)C1 IQFYYKKMVGJFEH-CSMHCCOUSA-N 0.000 claims 1
- 229960005311 telbivudine Drugs 0.000 claims 1
- 239000000126 substance Substances 0.000 abstract description 8
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 abstract description 5
- 125000002915 carbonyl group Chemical group [*:2]C([*:1])=O 0.000 description 45
- 125000006297 carbonyl amino group Chemical group [H]N([*:2])C([*:1])=O 0.000 description 36
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 28
- 235000002639 sodium chloride Nutrition 0.000 description 26
- XSQUKJJJFZCRTK-UHFFFAOYSA-N Urea Natural products NC(N)=O XSQUKJJJFZCRTK-UHFFFAOYSA-N 0.000 description 23
- 238000006243 chemical reaction Methods 0.000 description 22
- UMGDCJDMYOKAJW-UHFFFAOYSA-N thiourea Chemical compound NC(N)=S UMGDCJDMYOKAJW-UHFFFAOYSA-N 0.000 description 22
- 241000711549 Hepacivirus C Species 0.000 description 21
- 102000014150 Interferons Human genes 0.000 description 21
- 108010050904 Interferons Proteins 0.000 description 21
- 150000001408 amides Chemical class 0.000 description 21
- 125000000592 heterocycloalkyl group Chemical group 0.000 description 21
- 125000001820 oxy group Chemical group [*:1]O[*:2] 0.000 description 21
- 125000003545 alkoxy group Chemical group 0.000 description 20
- 125000003917 carbamoyl group Chemical group [H]N([H])C(*)=O 0.000 description 17
- 125000005843 halogen group Chemical group 0.000 description 16
- 229940079322 interferon Drugs 0.000 description 16
- 241000700159 Rattus Species 0.000 description 15
- 125000000304 alkynyl group Chemical group 0.000 description 15
- 125000004397 aminosulfonyl group Chemical group NS(=O)(=O)* 0.000 description 15
- 125000003396 thiol group Chemical group [H]S* 0.000 description 15
- 125000004093 cyano group Chemical group *C#N 0.000 description 14
- 208000005176 Hepatitis C Diseases 0.000 description 13
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 13
- 125000002252 acyl group Chemical group 0.000 description 13
- 238000003556 assay Methods 0.000 description 13
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 13
- 125000004043 oxo group Chemical group O=* 0.000 description 13
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 13
- 0 CC(C(C1C(N[Cn](*)CCIN*)=O)I)NC(*)N1*(*)=O Chemical compound CC(C(C1C(N[Cn](*)CCIN*)=O)I)NC(*)N1*(*)=O 0.000 description 12
- 239000002253 acid Substances 0.000 description 12
- 125000004453 alkoxycarbonyl group Chemical group 0.000 description 12
- BDAGIHXWWSANSR-UHFFFAOYSA-N methanoic acid Natural products OC=O BDAGIHXWWSANSR-UHFFFAOYSA-N 0.000 description 12
- 241000700605 Viruses Species 0.000 description 11
- 238000004458 analytical method Methods 0.000 description 11
- 125000003435 aroyl group Chemical group 0.000 description 11
- 239000000872 buffer Substances 0.000 description 11
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 11
- 235000019419 proteases Nutrition 0.000 description 11
- 125000000475 sulfinyl group Chemical group [*:2]S([*:1])=O 0.000 description 11
- 125000004104 aryloxy group Chemical group 0.000 description 10
- 239000003814 drug Substances 0.000 description 10
- 239000007787 solid Substances 0.000 description 10
- NVBFHJWHLNUMCV-UHFFFAOYSA-N sulfamide Chemical compound NS(N)(=O)=O NVBFHJWHLNUMCV-UHFFFAOYSA-N 0.000 description 10
- 125000000472 sulfonyl group Chemical group *S(*)(=O)=O 0.000 description 10
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 9
- 102100040018 Interferon alpha-2 Human genes 0.000 description 9
- 125000004390 alkyl sulfonyl group Chemical group 0.000 description 9
- 238000003776 cleavage reaction Methods 0.000 description 9
- 125000001188 haloalkyl group Chemical group 0.000 description 9
- 125000005553 heteroaryloxy group Chemical group 0.000 description 9
- 210000004185 liver Anatomy 0.000 description 9
- 239000000243 solution Substances 0.000 description 9
- 230000001225 therapeutic effect Effects 0.000 description 9
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 8
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 8
- 108010079944 Interferon-alpha2b Proteins 0.000 description 8
- 108010076039 Polyproteins Proteins 0.000 description 8
- 210000004027 cell Anatomy 0.000 description 8
- 108090000765 processed proteins & peptides Proteins 0.000 description 8
- 230000007017 scission Effects 0.000 description 8
- 239000002904 solvent Substances 0.000 description 8
- 239000000758 substrate Substances 0.000 description 8
- DBMJMQXJHONAFJ-UHFFFAOYSA-M Sodium laurylsulphate Chemical compound [Na+].CCCCCCCCCCCCOS([O-])(=O)=O DBMJMQXJHONAFJ-UHFFFAOYSA-M 0.000 description 7
- 125000004448 alkyl carbonyl group Chemical group 0.000 description 7
- 125000005196 alkyl carbonyloxy group Chemical group 0.000 description 7
- 125000002768 hydroxyalkyl group Chemical group 0.000 description 7
- 238000002347 injection Methods 0.000 description 7
- 239000007924 injection Substances 0.000 description 7
- 238000001990 intravenous administration Methods 0.000 description 7
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 7
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 7
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 7
- 108090000623 proteins and genes Proteins 0.000 description 7
- 239000011780 sodium chloride Substances 0.000 description 7
- 235000019333 sodium laurylsulphate Nutrition 0.000 description 7
- 241000701161 unidentified adenovirus Species 0.000 description 7
- 230000003612 virological effect Effects 0.000 description 7
- 108091032973 (ribonucleotides)n+m Proteins 0.000 description 6
- OSWFIVFLDKOXQC-UHFFFAOYSA-N 4-(3-methoxyphenyl)aniline Chemical compound COC1=CC=CC(C=2C=CC(N)=CC=2)=C1 OSWFIVFLDKOXQC-UHFFFAOYSA-N 0.000 description 6
- WVDDGKGOMKODPV-UHFFFAOYSA-N Benzyl alcohol Chemical compound OCC1=CC=CC=C1 WVDDGKGOMKODPV-UHFFFAOYSA-N 0.000 description 6
- 102000004190 Enzymes Human genes 0.000 description 6
- 108090000790 Enzymes Proteins 0.000 description 6
- 241001465754 Metazoa Species 0.000 description 6
- 101800001020 Non-structural protein 4A Proteins 0.000 description 6
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 6
- RWRDLPDLKQPQOW-UHFFFAOYSA-N Pyrrolidine Chemical compound C1CCNC1 RWRDLPDLKQPQOW-UHFFFAOYSA-N 0.000 description 6
- 125000003806 alkyl carbonyl amino group Chemical group 0.000 description 6
- 125000005126 aryl alkyl carbonyl amino group Chemical group 0.000 description 6
- 125000002102 aryl alkyloxo group Chemical group 0.000 description 6
- 125000005605 benzo group Chemical group 0.000 description 6
- 239000004202 carbamide Substances 0.000 description 6
- 125000004966 cyanoalkyl group Chemical group 0.000 description 6
- 201000010099 disease Diseases 0.000 description 6
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 6
- 235000019253 formic acid Nutrition 0.000 description 6
- 238000009472 formulation Methods 0.000 description 6
- 125000002541 furyl group Chemical group 0.000 description 6
- 208000006454 hepatitis Diseases 0.000 description 6
- 125000004475 heteroaralkyl group Chemical group 0.000 description 6
- 125000005224 heteroarylcarbonylamino group Chemical group 0.000 description 6
- 239000001257 hydrogen Substances 0.000 description 6
- 229940047124 interferons Drugs 0.000 description 6
- 125000000449 nitro group Chemical class [O-][N+](*)=O 0.000 description 6
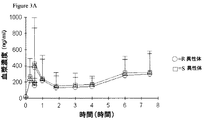
- 230000036470 plasma concentration Effects 0.000 description 6
- 238000012545 processing Methods 0.000 description 6
- 239000000725 suspension Substances 0.000 description 6
- 208000024891 symptom Diseases 0.000 description 6
- DTQVDTLACAAQTR-UHFFFAOYSA-N trifluoroacetic acid Substances OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 description 6
- GBXQPDCOMJJCMJ-UHFFFAOYSA-M trimethyl-[6-(trimethylazaniumyl)hexyl]azanium;bromide Chemical compound [Br-].C[N+](C)(C)CCCCCC[N+](C)(C)C GBXQPDCOMJJCMJ-UHFFFAOYSA-M 0.000 description 6
- NWGPLYYBECWONP-UHFFFAOYSA-N (carbamoylamino) hydrogen sulfate Chemical compound NC(=O)NOS(O)(=O)=O NWGPLYYBECWONP-UHFFFAOYSA-N 0.000 description 5
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 5
- 108010078049 Interferon alpha-2 Proteins 0.000 description 5
- JGFZNNIVVJXRND-UHFFFAOYSA-N N,N-Diisopropylethylamine (DIPEA) Chemical compound CCN(C(C)C)C(C)C JGFZNNIVVJXRND-UHFFFAOYSA-N 0.000 description 5
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 5
- 239000004480 active ingredient Substances 0.000 description 5
- 125000004414 alkyl thio group Chemical group 0.000 description 5
- 125000003368 amide group Chemical group 0.000 description 5
- 230000000840 anti-viral effect Effects 0.000 description 5
- 125000004181 carboxyalkyl group Chemical group 0.000 description 5
- 239000000969 carrier Substances 0.000 description 5
- 125000001316 cycloalkyl alkyl group Chemical group 0.000 description 5
- 229940079593 drug Drugs 0.000 description 5
- 206010073071 hepatocellular carcinoma Diseases 0.000 description 5
- 125000004366 heterocycloalkenyl group Chemical group 0.000 description 5
- 125000005885 heterocycloalkylalkyl group Chemical group 0.000 description 5
- 238000004128 high performance liquid chromatography Methods 0.000 description 5
- 208000019423 liver disease Diseases 0.000 description 5
- 239000000463 material Substances 0.000 description 5
- 108010092853 peginterferon alfa-2a Proteins 0.000 description 5
- 238000002360 preparation method Methods 0.000 description 5
- 102000004169 proteins and genes Human genes 0.000 description 5
- 239000003001 serine protease inhibitor Substances 0.000 description 5
- 238000002560 therapeutic procedure Methods 0.000 description 5
- 125000004178 (C1-C4) alkyl group Chemical group 0.000 description 4
- QGZKDVFQNNGYKY-UHFFFAOYSA-N Ammonia Chemical compound N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 description 4
- 241000282472 Canis lupus familiaris Species 0.000 description 4
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 4
- 241000124008 Mammalia Species 0.000 description 4
- MUBZPKHOEPUJKR-UHFFFAOYSA-N Oxalic acid Chemical compound OC(=O)C(O)=O MUBZPKHOEPUJKR-UHFFFAOYSA-N 0.000 description 4
- 125000004457 alkyl amino carbonyl group Chemical group 0.000 description 4
- 229940024606 amino acid Drugs 0.000 description 4
- 150000001413 amino acids Chemical class 0.000 description 4
- 125000005100 aryl amino carbonyl group Chemical group 0.000 description 4
- 125000004658 aryl carbonyl amino group Chemical group 0.000 description 4
- 230000003197 catalytic effect Effects 0.000 description 4
- 125000000000 cycloalkoxy group Chemical group 0.000 description 4
- 125000005169 cycloalkylcarbonylamino group Chemical group 0.000 description 4
- 231100000844 hepatocellular carcinoma Toxicity 0.000 description 4
- NPZTUJOABDZTLV-UHFFFAOYSA-N hydroxybenzotriazole Substances O=C1C=CC=C2NNN=C12 NPZTUJOABDZTLV-UHFFFAOYSA-N 0.000 description 4
- 238000011534 incubation Methods 0.000 description 4
- 230000005764 inhibitory process Effects 0.000 description 4
- 230000035772 mutation Effects 0.000 description 4
- 125000001400 nonyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 4
- 229940002988 pegasys Drugs 0.000 description 4
- 230000007030 peptide scission Effects 0.000 description 4
- 230000008569 process Effects 0.000 description 4
- 125000006413 ring segment Chemical group 0.000 description 4
- 238000000926 separation method Methods 0.000 description 4
- 238000009097 single-agent therapy Methods 0.000 description 4
- 238000013222 sprague-dawley male rat Methods 0.000 description 4
- 239000011550 stock solution Substances 0.000 description 4
- 125000001544 thienyl group Chemical group 0.000 description 4
- 230000000699 topical effect Effects 0.000 description 4
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 4
- 125000004169 (C1-C6) alkyl group Chemical group 0.000 description 3
- LMDZBCPBFSXMTL-UHFFFAOYSA-N 1-ethyl-3-(3-dimethylaminopropyl)carbodiimide Chemical compound CCN=C=NCCCN(C)C LMDZBCPBFSXMTL-UHFFFAOYSA-N 0.000 description 3
- JKMHFZQWWAIEOD-UHFFFAOYSA-N 2-[4-(2-hydroxyethyl)piperazin-1-yl]ethanesulfonic acid Chemical compound OCC[NH+]1CCN(CCS([O-])(=O)=O)CC1 JKMHFZQWWAIEOD-UHFFFAOYSA-N 0.000 description 3
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 3
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 3
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 3
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical compound OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 description 3
- 239000007995 HEPES buffer Substances 0.000 description 3
- 108010037165 Hepatitis C virus NS3-4A serine protease Proteins 0.000 description 3
- 206010019799 Hepatitis viral Diseases 0.000 description 3
- 241000282412 Homo Species 0.000 description 3
- 101710200424 Inosine-5'-monophosphate dehydrogenase Proteins 0.000 description 3
- OFOBLEOULBTSOW-UHFFFAOYSA-N Malonic acid Chemical compound OC(=O)CC(O)=O OFOBLEOULBTSOW-UHFFFAOYSA-N 0.000 description 3
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 3
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 3
- WHNWPMSKXPGLAX-UHFFFAOYSA-N N-Vinyl-2-pyrrolidone Chemical compound C=CN1CCCC1=O WHNWPMSKXPGLAX-UHFFFAOYSA-N 0.000 description 3
- 229920003081 Povidone K 30 Polymers 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- 108700010756 Viral Polyproteins Proteins 0.000 description 3
- 125000004183 alkoxy alkyl group Chemical group 0.000 description 3
- 150000001412 amines Chemical class 0.000 description 3
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 3
- 125000001164 benzothiazolyl group Chemical group S1C(=NC2=C1C=CC=C2)* 0.000 description 3
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 3
- 239000012620 biological material Substances 0.000 description 3
- 230000015572 biosynthetic process Effects 0.000 description 3
- 230000008859 change Effects 0.000 description 3
- 230000001684 chronic effect Effects 0.000 description 3
- 125000005390 cinnolyl group Chemical group N1=NC(=CC2=CC=CC=C12)* 0.000 description 3
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 3
- 125000005167 cycloalkylaminocarbonyl group Chemical group 0.000 description 3
- 238000007865 diluting Methods 0.000 description 3
- 239000003085 diluting agent Substances 0.000 description 3
- 239000002270 dispersing agent Substances 0.000 description 3
- 239000003937 drug carrier Substances 0.000 description 3
- 239000011521 glass Substances 0.000 description 3
- 231100000283 hepatitis Toxicity 0.000 description 3
- 208000010710 hepatitis C virus infection Diseases 0.000 description 3
- 125000005222 heteroarylaminocarbonyl group Chemical group 0.000 description 3
- 230000002519 immonomodulatory effect Effects 0.000 description 3
- 238000000338 in vitro Methods 0.000 description 3
- 238000001727 in vivo Methods 0.000 description 3
- 125000001041 indolyl group Chemical group 0.000 description 3
- 125000000904 isoindolyl group Chemical group C=1(NC=C2C=CC=CC12)* 0.000 description 3
- 125000002183 isoquinolinyl group Chemical group C1(=NC=CC2=CC=CC=C12)* 0.000 description 3
- 238000004949 mass spectrometry Methods 0.000 description 3
- 230000001404 mediated effect Effects 0.000 description 3
- 238000012986 modification Methods 0.000 description 3
- 230000004048 modification Effects 0.000 description 3
- 239000003921 oil Substances 0.000 description 3
- 235000019198 oils Nutrition 0.000 description 3
- 210000000056 organ Anatomy 0.000 description 3
- 108010092851 peginterferon alfa-2b Proteins 0.000 description 3
- 229940106366 pegintron Drugs 0.000 description 3
- 229920001223 polyethylene glycol Polymers 0.000 description 3
- 235000019833 protease Nutrition 0.000 description 3
- 125000002294 quinazolinyl group Chemical group N1=C(N=CC2=CC=CC=C12)* 0.000 description 3
- 150000003254 radicals Chemical class 0.000 description 3
- 230000002829 reductive effect Effects 0.000 description 3
- 210000002966 serum Anatomy 0.000 description 3
- 125000002023 trifluoromethyl group Chemical group FC(F)(F)* 0.000 description 3
- 239000003981 vehicle Substances 0.000 description 3
- 230000029812 viral genome replication Effects 0.000 description 3
- 201000001862 viral hepatitis Diseases 0.000 description 3
- 230000009385 viral infection Effects 0.000 description 3
- PUPZLCDOIYMWBV-UHFFFAOYSA-N (+/-)-1,3-Butanediol Chemical compound CC(O)CCO PUPZLCDOIYMWBV-UHFFFAOYSA-N 0.000 description 2
- XMAYWYJOQHXEEK-OZXSUGGESA-N (2R,4S)-ketoconazole Chemical compound C1CN(C(=O)C)CCN1C(C=C1)=CC=C1OC[C@@H]1O[C@@](CN2C=NC=C2)(C=2C(=CC(Cl)=CC=2)Cl)OC1 XMAYWYJOQHXEEK-OZXSUGGESA-N 0.000 description 2
- 102000040650 (ribonucleotides)n+m Human genes 0.000 description 2
- UWYZHKAOTLEWKK-UHFFFAOYSA-N 1,2,3,4-tetrahydroisoquinoline Chemical compound C1=CC=C2CNCCC2=C1 UWYZHKAOTLEWKK-UHFFFAOYSA-N 0.000 description 2
- WJFKNYWRSNBZNX-UHFFFAOYSA-N 10H-phenothiazine Chemical compound C1=CC=C2NC3=CC=CC=C3SC2=C1 WJFKNYWRSNBZNX-UHFFFAOYSA-N 0.000 description 2
- GOJUJUVQIVIZAV-UHFFFAOYSA-N 2-amino-4,6-dichloropyrimidine-5-carbaldehyde Chemical group NC1=NC(Cl)=C(C=O)C(Cl)=N1 GOJUJUVQIVIZAV-UHFFFAOYSA-N 0.000 description 2
- YEDUAINPPJYDJZ-UHFFFAOYSA-N 2-hydroxybenzothiazole Chemical compound C1=CC=C2SC(O)=NC2=C1 YEDUAINPPJYDJZ-UHFFFAOYSA-N 0.000 description 2
- VSCBATMPTLKTOV-UHFFFAOYSA-N 2-tert-butylimino-n,n-diethyl-1,3-dimethyl-1,3,2$l^{5}-diazaphosphinan-2-amine Chemical compound CCN(CC)P1(=NC(C)(C)C)N(C)CCCN1C VSCBATMPTLKTOV-UHFFFAOYSA-N 0.000 description 2
- VHYFNPMBLIVWCW-UHFFFAOYSA-N 4-Dimethylaminopyridine Chemical compound CN(C)C1=CC=NC=C1 VHYFNPMBLIVWCW-UHFFFAOYSA-N 0.000 description 2
- GJCOSYZMQJWQCA-UHFFFAOYSA-N 9H-xanthene Chemical compound C1=CC=C2CC3=CC=CC=C3OC2=C1 GJCOSYZMQJWQCA-UHFFFAOYSA-N 0.000 description 2
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 description 2
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 2
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 2
- 206010008909 Chronic Hepatitis Diseases 0.000 description 2
- 229920002261 Corn starch Polymers 0.000 description 2
- PMATZTZNYRCHOR-CGLBZJNRSA-N Cyclosporin A Chemical compound CC[C@@H]1NC(=O)[C@H]([C@H](O)[C@H](C)C\C=C\C)N(C)C(=O)[C@H](C(C)C)N(C)C(=O)[C@H](CC(C)C)N(C)C(=O)[C@H](CC(C)C)N(C)C(=O)[C@@H](C)NC(=O)[C@H](C)NC(=O)[C@H](CC(C)C)N(C)C(=O)[C@H](C(C)C)NC(=O)[C@H](CC(C)C)N(C)C(=O)CN(C)C1=O PMATZTZNYRCHOR-CGLBZJNRSA-N 0.000 description 2
- 108010036949 Cyclosporine Proteins 0.000 description 2
- 102000002004 Cytochrome P-450 Enzyme System Human genes 0.000 description 2
- ULGZDMOVFRHVEP-RWJQBGPGSA-N Erythromycin Chemical compound O([C@@H]1[C@@H](C)C(=O)O[C@@H]([C@@]([C@H](O)[C@@H](C)C(=O)[C@H](C)C[C@@](C)(O)[C@H](O[C@H]2[C@@H]([C@H](C[C@@H](C)O2)N(C)C)O)[C@H]1C)(C)O)CC)[C@H]1C[C@@](C)(OC)[C@@H](O)[C@H](C)O1 ULGZDMOVFRHVEP-RWJQBGPGSA-N 0.000 description 2
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 2
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 2
- 229940122604 HCV protease inhibitor Drugs 0.000 description 2
- OAKJQQAXSVQMHS-UHFFFAOYSA-N Hydrazine Chemical compound NN OAKJQQAXSVQMHS-UHFFFAOYSA-N 0.000 description 2
- AVXURJPOCDRRFD-UHFFFAOYSA-N Hydroxylamine Chemical compound ON AVXURJPOCDRRFD-UHFFFAOYSA-N 0.000 description 2
- 241000283891 Kobus Species 0.000 description 2
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 2
- 241000699666 Mus <mouse, genus> Species 0.000 description 2
- 241000699670 Mus sp. Species 0.000 description 2
- 101800000515 Non-structural protein 3 Proteins 0.000 description 2
- 101710144111 Non-structural protein 3 Proteins 0.000 description 2
- 241000282579 Pan Species 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 2
- 229920002565 Polyethylene Glycol 400 Polymers 0.000 description 2
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 2
- 229940122055 Serine protease inhibitor Drugs 0.000 description 2
- 101710102218 Serine protease inhibitor Proteins 0.000 description 2
- 108091027544 Subgenomic mRNA Proteins 0.000 description 2
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 2
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 2
- 208000036142 Viral infection Diseases 0.000 description 2
- 150000007513 acids Chemical class 0.000 description 2
- DZBUGLKDJFMEHC-UHFFFAOYSA-N acridine Chemical compound C1=CC=CC2=CC3=CC=CC=C3N=C21 DZBUGLKDJFMEHC-UHFFFAOYSA-N 0.000 description 2
- 230000009471 action Effects 0.000 description 2
- 230000001154 acute effect Effects 0.000 description 2
- 125000005073 adamantyl group Chemical group C12(CC3CC(CC(C1)C3)C2)* 0.000 description 2
- 108010080374 albuferon Proteins 0.000 description 2
- 125000004171 alkoxy aryl group Chemical group 0.000 description 2
- 125000003282 alkyl amino group Chemical group 0.000 description 2
- 125000004103 aminoalkyl group Chemical group 0.000 description 2
- 125000005001 aminoaryl group Chemical group 0.000 description 2
- 229910021529 ammonia Inorganic materials 0.000 description 2
- MWPLVEDNUUSJAV-UHFFFAOYSA-N anthracene Chemical compound C1=CC=CC2=CC3=CC=CC=C3C=C21 MWPLVEDNUUSJAV-UHFFFAOYSA-N 0.000 description 2
- 230000036436 anti-hiv Effects 0.000 description 2
- 239000007864 aqueous solution Substances 0.000 description 2
- 239000007900 aqueous suspension Substances 0.000 description 2
- 239000002585 base Substances 0.000 description 2
- 230000008901 benefit Effects 0.000 description 2
- 125000003785 benzimidazolyl group Chemical group N1=C(NC2=C1C=CC=C2)* 0.000 description 2
- 125000004618 benzofuryl group Chemical group O1C(=CC2=C1C=CC=C2)* 0.000 description 2
- 235000019445 benzyl alcohol Nutrition 0.000 description 2
- 230000037396 body weight Effects 0.000 description 2
- 150000001649 bromium compounds Chemical class 0.000 description 2
- 239000002775 capsule Substances 0.000 description 2
- 150000001721 carbon Chemical group 0.000 description 2
- 239000001768 carboxy methyl cellulose Substances 0.000 description 2
- 239000003153 chemical reaction reagent Substances 0.000 description 2
- 229960001265 ciclosporin Drugs 0.000 description 2
- 239000008120 corn starch Substances 0.000 description 2
- 230000008878 coupling Effects 0.000 description 2
- 238000010168 coupling process Methods 0.000 description 2
- 238000005859 coupling reaction Methods 0.000 description 2
- CISNNLXXANUBPI-UHFFFAOYSA-N cyano(nitro)azanide Chemical compound [O-][N+](=O)[N-]C#N CISNNLXXANUBPI-UHFFFAOYSA-N 0.000 description 2
- 125000002433 cyclopentenyl group Chemical group C1(=CCCC1)* 0.000 description 2
- 229930182912 cyclosporin Natural products 0.000 description 2
- WHBIGIKBNXZKFE-UHFFFAOYSA-N delavirdine Chemical compound CC(C)NC1=CC=CN=C1N1CCN(C(=O)C=2NC3=CC=C(NS(C)(=O)=O)C=C3C=2)CC1 WHBIGIKBNXZKFE-UHFFFAOYSA-N 0.000 description 2
- NKLCNNUWBJBICK-UHFFFAOYSA-N dess–martin periodinane Chemical compound C1=CC=C2I(OC(=O)C)(OC(C)=O)(OC(C)=O)OC(=O)C2=C1 NKLCNNUWBJBICK-UHFFFAOYSA-N 0.000 description 2
- 238000001514 detection method Methods 0.000 description 2
- 239000008121 dextrose Substances 0.000 description 2
- 235000014113 dietary fatty acids Nutrition 0.000 description 2
- 229940042399 direct acting antivirals protease inhibitors Drugs 0.000 description 2
- 238000010494 dissociation reaction Methods 0.000 description 2
- VHJLVAABSRFDPM-QWWZWVQMSA-N dithiothreitol Chemical compound SC[C@@H](O)[C@H](O)CS VHJLVAABSRFDPM-QWWZWVQMSA-N 0.000 description 2
- 239000003995 emulsifying agent Substances 0.000 description 2
- 239000003623 enhancer Substances 0.000 description 2
- 239000002532 enzyme inhibitor Substances 0.000 description 2
- 229940125532 enzyme inhibitor Drugs 0.000 description 2
- 235000019439 ethyl acetate Nutrition 0.000 description 2
- 230000029142 excretion Effects 0.000 description 2
- 235000019197 fats Nutrition 0.000 description 2
- 239000000194 fatty acid Substances 0.000 description 2
- 229930195729 fatty acid Natural products 0.000 description 2
- 150000004665 fatty acids Chemical class 0.000 description 2
- 239000012091 fetal bovine serum Substances 0.000 description 2
- RIKMMFOAQPJVMX-UHFFFAOYSA-N fomepizole Chemical compound CC=1C=NNC=1 RIKMMFOAQPJVMX-UHFFFAOYSA-N 0.000 description 2
- 229960004285 fomepizole Drugs 0.000 description 2
- 239000012458 free base Substances 0.000 description 2
- 210000001035 gastrointestinal tract Anatomy 0.000 description 2
- 125000005456 glyceride group Chemical group 0.000 description 2
- 229940093915 gynecological organic acid Drugs 0.000 description 2
- 108700012707 hepatitis C virus NS3 Proteins 0.000 description 2
- XMBWDFGMSWQBCA-UHFFFAOYSA-N hydrogen iodide Chemical compound I XMBWDFGMSWQBCA-UHFFFAOYSA-N 0.000 description 2
- 125000002883 imidazolyl group Chemical group 0.000 description 2
- 229960002751 imiquimod Drugs 0.000 description 2
- DOUYETYNHWVLEO-UHFFFAOYSA-N imiquimod Chemical compound C1=CC=CC2=C3N(CC(C)C)C=NC3=C(N)N=C21 DOUYETYNHWVLEO-UHFFFAOYSA-N 0.000 description 2
- 230000028993 immune response Effects 0.000 description 2
- 125000003453 indazolyl group Chemical group N1N=C(C2=C1C=CC=C2)* 0.000 description 2
- 125000003387 indolinyl group Chemical group N1(CCC2=CC=CC=C12)* 0.000 description 2
- 229960003521 interferon alfa-2a Drugs 0.000 description 2
- 108010006088 interferon alfa-n1 Proteins 0.000 description 2
- 108700027921 interferon tau Proteins 0.000 description 2
- 150000004694 iodide salts Chemical class 0.000 description 2
- 125000005956 isoquinolyl group Chemical group 0.000 description 2
- 229960004125 ketoconazole Drugs 0.000 description 2
- 238000012933 kinetic analysis Methods 0.000 description 2
- 239000008101 lactose Substances 0.000 description 2
- QDLAGTHXVHQKRE-UHFFFAOYSA-N lichenxanthone Natural products COC1=CC(O)=C2C(=O)C3=C(C)C=C(OC)C=C3OC2=C1 QDLAGTHXVHQKRE-UHFFFAOYSA-N 0.000 description 2
- 230000000670 limiting effect Effects 0.000 description 2
- 239000007788 liquid Substances 0.000 description 2
- 238000004811 liquid chromatography Methods 0.000 description 2
- 230000007774 longterm Effects 0.000 description 2
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 2
- 230000014759 maintenance of location Effects 0.000 description 2
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 description 2
- 238000004519 manufacturing process Methods 0.000 description 2
- 238000013507 mapping Methods 0.000 description 2
- 238000005259 measurement Methods 0.000 description 2
- 230000004060 metabolic process Effects 0.000 description 2
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 2
- 239000002480 mineral oil Substances 0.000 description 2
- 235000010446 mineral oil Nutrition 0.000 description 2
- 150000007522 mineralic acids Chemical class 0.000 description 2
- 238000010369 molecular cloning Methods 0.000 description 2
- 238000010172 mouse model Methods 0.000 description 2
- 125000004971 nitroalkyl group Chemical group 0.000 description 2
- 239000000346 nonvolatile oil Substances 0.000 description 2
- 125000002868 norbornyl group Chemical group C12(CCC(CC1)C2)* 0.000 description 2
- 239000002674 ointment Substances 0.000 description 2
- 150000007524 organic acids Chemical class 0.000 description 2
- 235000005985 organic acids Nutrition 0.000 description 2
- 230000008520 organization Effects 0.000 description 2
- 125000002971 oxazolyl group Chemical group 0.000 description 2
- 230000036961 partial effect Effects 0.000 description 2
- JLFNLZLINWHATN-UHFFFAOYSA-N pentaethylene glycol Chemical compound OCCOCCOCCOCCOCCO JLFNLZLINWHATN-UHFFFAOYSA-N 0.000 description 2
- 235000019271 petrolatum Nutrition 0.000 description 2
- 229950000688 phenothiazine Drugs 0.000 description 2
- 125000005542 phthalazyl group Chemical group 0.000 description 2
- 239000013612 plasmid Substances 0.000 description 2
- 229920001451 polypropylene glycol Polymers 0.000 description 2
- 229910052700 potassium Inorganic materials 0.000 description 2
- 239000011591 potassium Substances 0.000 description 2
- BWHMMNNQKKPAPP-UHFFFAOYSA-L potassium carbonate Chemical compound [K+].[K+].[O-]C([O-])=O BWHMMNNQKKPAPP-UHFFFAOYSA-L 0.000 description 2
- 230000003389 potentiating effect Effects 0.000 description 2
- 230000002265 prevention Effects 0.000 description 2
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 2
- 125000003226 pyrazolyl group Chemical group 0.000 description 2
- 125000004076 pyridyl group Chemical group 0.000 description 2
- LDNSHTVNGGHGQJ-UHFFFAOYSA-N pyrrole-1-carboxamide Chemical compound NC(=O)N1C=CC=C1 LDNSHTVNGGHGQJ-UHFFFAOYSA-N 0.000 description 2
- 125000000168 pyrrolyl group Chemical group 0.000 description 2
- 125000002943 quinolinyl group Chemical group N1=C(C=CC2=CC=CC=C12)* 0.000 description 2
- 125000005493 quinolyl group Chemical group 0.000 description 2
- 125000001567 quinoxalinyl group Chemical group N1=C(C=NC2=CC=CC=C12)* 0.000 description 2
- 238000012552 review Methods 0.000 description 2
- YGSDEFSMJLZEOE-UHFFFAOYSA-N salicylic acid Chemical compound OC(=O)C1=CC=CC=C1O YGSDEFSMJLZEOE-UHFFFAOYSA-N 0.000 description 2
- 229920006395 saturated elastomer Polymers 0.000 description 2
- 125000006296 sulfonyl amino group Chemical group [H]N(*)S(*)(=O)=O 0.000 description 2
- 239000000375 suspending agent Substances 0.000 description 2
- 238000003786 synthesis reaction Methods 0.000 description 2
- 239000003826 tablet Substances 0.000 description 2
- 125000003831 tetrazolyl group Chemical group 0.000 description 2
- 125000000335 thiazolyl group Chemical group 0.000 description 2
- 230000036964 tight binding Effects 0.000 description 2
- 229960005041 troleandomycin Drugs 0.000 description 2
- LQCLVBQBTUVCEQ-QTFUVMRISA-N troleandomycin Chemical compound O1[C@@H](C)[C@H](OC(C)=O)[C@@H](OC)C[C@@H]1O[C@@H]1[C@@H](C)C(=O)O[C@H](C)[C@H](C)[C@H](OC(C)=O)[C@@H](C)C(=O)[C@@]2(OC2)C[C@H](C)[C@H](O[C@H]2[C@@H]([C@H](C[C@@H](C)O2)N(C)C)OC(C)=O)[C@H]1C LQCLVBQBTUVCEQ-QTFUVMRISA-N 0.000 description 2
- 239000001993 wax Substances 0.000 description 2
- 238000005303 weighing Methods 0.000 description 2
- LSPHULWDVZXLIL-UHFFFAOYSA-N (+/-)-Camphoric acid Chemical compound CC1(C)C(C(O)=O)CCC1(C)C(O)=O LSPHULWDVZXLIL-UHFFFAOYSA-N 0.000 description 1
- INWOAUUPYIXDHN-ZETCQYMHSA-N (2s)-2-[(2-methylpropan-2-yl)oxycarbonylamino]pentanoic acid Chemical compound CCC[C@@H](C(O)=O)NC(=O)OC(C)(C)C INWOAUUPYIXDHN-ZETCQYMHSA-N 0.000 description 1
- NAWXUBYGYWOOIX-SFHVURJKSA-N (2s)-2-[[4-[2-(2,4-diaminoquinazolin-6-yl)ethyl]benzoyl]amino]-4-methylidenepentanedioic acid Chemical compound C1=CC2=NC(N)=NC(N)=C2C=C1CCC1=CC=C(C(=O)N[C@@H](CC(=C)C(O)=O)C(O)=O)C=C1 NAWXUBYGYWOOIX-SFHVURJKSA-N 0.000 description 1
- MEJYDZQQVZJMPP-ULAWRXDQSA-N (3s,3ar,6r,6ar)-3,6-dimethoxy-2,3,3a,5,6,6a-hexahydrofuro[3,2-b]furan Chemical compound CO[C@H]1CO[C@@H]2[C@H](OC)CO[C@@H]21 MEJYDZQQVZJMPP-ULAWRXDQSA-N 0.000 description 1
- WRIDQFICGBMAFQ-UHFFFAOYSA-N (E)-8-Octadecenoic acid Natural products CCCCCCCCCC=CCCCCCCC(O)=O WRIDQFICGBMAFQ-UHFFFAOYSA-N 0.000 description 1
- RTHCYVBBDHJXIQ-MRXNPFEDSA-N (R)-fluoxetine Chemical compound O([C@H](CCNC)C=1C=CC=CC=1)C1=CC=C(C(F)(F)F)C=C1 RTHCYVBBDHJXIQ-MRXNPFEDSA-N 0.000 description 1
- BJEPYKJPYRNKOW-REOHCLBHSA-N (S)-malic acid Chemical compound OC(=O)[C@@H](O)CC(O)=O BJEPYKJPYRNKOW-REOHCLBHSA-N 0.000 description 1
- GNMCGMFNBARSIY-UHFFFAOYSA-N 1,2,3,4,4a,4b,5,6,7,8,8a,9,10,10a-tetradecahydrophenanthrene Chemical compound C1CCCC2C3CCCCC3CCC21 GNMCGMFNBARSIY-UHFFFAOYSA-N 0.000 description 1
- 125000004520 1,3,4-thiadiazolyl group Chemical group 0.000 description 1
- FTNJQNQLEGKTGD-UHFFFAOYSA-N 1,3-benzodioxole Chemical compound C1=CC=C2OCOC2=C1 FTNJQNQLEGKTGD-UHFFFAOYSA-N 0.000 description 1
- BDNKZNFMNDZQMI-UHFFFAOYSA-N 1,3-diisopropylcarbodiimide Chemical compound CC(C)N=C=NC(C)C BDNKZNFMNDZQMI-UHFFFAOYSA-N 0.000 description 1
- JPRPJUMQRZTTED-UHFFFAOYSA-N 1,3-dioxolanyl Chemical group [CH]1OCCO1 JPRPJUMQRZTTED-UHFFFAOYSA-N 0.000 description 1
- HKDFRDIIELOLTJ-UHFFFAOYSA-N 1,4-dithianyl Chemical group [CH]1CSCCS1 HKDFRDIIELOLTJ-UHFFFAOYSA-N 0.000 description 1
- ASOKPJOREAFHNY-UHFFFAOYSA-N 1-Hydroxybenzotriazole Chemical group C1=CC=C2N(O)N=NC2=C1 ASOKPJOREAFHNY-UHFFFAOYSA-N 0.000 description 1
- VFWCMGCRMGJXDK-UHFFFAOYSA-N 1-chlorobutane Chemical class CCCCCl VFWCMGCRMGJXDK-UHFFFAOYSA-N 0.000 description 1
- VUQPJRPDRDVQMN-UHFFFAOYSA-N 1-chlorooctadecane Chemical class CCCCCCCCCCCCCCCCCCCl VUQPJRPDRDVQMN-UHFFFAOYSA-N 0.000 description 1
- VIAUXFYJOFICQB-UHFFFAOYSA-N 1-hydroxybenzotriazole;piperidine Chemical group C1CCNCC1.C1CCNCC1.C1=CC=C2N(O)N=NC2=C1 VIAUXFYJOFICQB-UHFFFAOYSA-N 0.000 description 1
- IIZPXYDJLKNOIY-JXPKJXOSSA-N 1-palmitoyl-2-arachidonoyl-sn-glycero-3-phosphocholine Chemical compound CCCCCCCCCCCCCCCC(=O)OC[C@H](COP([O-])(=O)OCC[N+](C)(C)C)OC(=O)CCC\C=C/C\C=C/C\C=C/C\C=C/CCCCC IIZPXYDJLKNOIY-JXPKJXOSSA-N 0.000 description 1
- 238000005160 1H NMR spectroscopy Methods 0.000 description 1
- 125000005955 1H-indazolyl group Chemical group 0.000 description 1
- YBYIRNPNPLQARY-UHFFFAOYSA-N 1H-indene Natural products C1=CC=C2CC=CC2=C1 YBYIRNPNPLQARY-UHFFFAOYSA-N 0.000 description 1
- YQTCQNIPQMJNTI-UHFFFAOYSA-N 2,2-dimethylpropan-1-one Chemical group CC(C)(C)[C]=O YQTCQNIPQMJNTI-UHFFFAOYSA-N 0.000 description 1
- CHHHXKFHOYLYRE-UHFFFAOYSA-M 2,4-Hexadienoic acid, potassium salt (1:1), (2E,4E)- Chemical compound [K+].CC=CC=CC([O-])=O CHHHXKFHOYLYRE-UHFFFAOYSA-M 0.000 description 1
- VHVPQPYKVGDNFY-DFMJLFEVSA-N 2-[(2r)-butan-2-yl]-4-[4-[4-[4-[[(2r,4s)-2-(2,4-dichlorophenyl)-2-(1,2,4-triazol-1-ylmethyl)-1,3-dioxolan-4-yl]methoxy]phenyl]piperazin-1-yl]phenyl]-1,2,4-triazol-3-one Chemical compound O=C1N([C@H](C)CC)N=CN1C1=CC=C(N2CCN(CC2)C=2C=CC(OC[C@@H]3O[C@](CN4N=CN=C4)(OC3)C=3C(=CC(Cl)=CC=3)Cl)=CC=2)C=C1 VHVPQPYKVGDNFY-DFMJLFEVSA-N 0.000 description 1
- 125000004974 2-butenyl group Chemical group C(C=CC)* 0.000 description 1
- 125000006040 2-hexenyl group Chemical group 0.000 description 1
- 229940080296 2-naphthalenesulfonate Drugs 0.000 description 1
- LEACJMVNYZDSKR-UHFFFAOYSA-N 2-octyldodecan-1-ol Chemical compound CCCCCCCCCCC(CO)CCCCCCCC LEACJMVNYZDSKR-UHFFFAOYSA-N 0.000 description 1
- WMPPDTMATNBGJN-UHFFFAOYSA-N 2-phenylethylbromide Chemical class BrCCC1=CC=CC=C1 WMPPDTMATNBGJN-UHFFFAOYSA-N 0.000 description 1
- 125000003903 2-propenyl group Chemical group [H]C([*])([H])C([H])=C([H])[H] 0.000 description 1
- 125000001494 2-propynyl group Chemical group [H]C#CC([H])([H])* 0.000 description 1
- LQJBNNIYVWPHFW-UHFFFAOYSA-N 20:1omega9c fatty acid Natural products CCCCCCCCCCC=CCCCCCCCC(O)=O LQJBNNIYVWPHFW-UHFFFAOYSA-N 0.000 description 1
- 125000001698 2H-pyranyl group Chemical group O1C(C=CC=C1)* 0.000 description 1
- BMYNFMYTOJXKLE-UHFFFAOYSA-N 3-azaniumyl-2-hydroxypropanoate Chemical compound NCC(O)C(O)=O BMYNFMYTOJXKLE-UHFFFAOYSA-N 0.000 description 1
- ZRPLANDPDWYOMZ-UHFFFAOYSA-N 3-cyclopentylpropionic acid Chemical compound OC(=O)CCC1CCCC1 ZRPLANDPDWYOMZ-UHFFFAOYSA-N 0.000 description 1
- XMIIGOLPHOKFCH-UHFFFAOYSA-M 3-phenylpropionate Chemical compound [O-]C(=O)CCC1=CC=CC=C1 XMIIGOLPHOKFCH-UHFFFAOYSA-M 0.000 description 1
- PXACTUVBBMDKRW-UHFFFAOYSA-N 4-bromobenzenesulfonic acid Chemical compound OS(=O)(=O)C1=CC=C(Br)C=C1 PXACTUVBBMDKRW-UHFFFAOYSA-N 0.000 description 1
- 229960000549 4-dimethylaminophenol Drugs 0.000 description 1
- MBBZMMPHUWSWHV-UHFFFAOYSA-N 6-(methylamino)hexane-1,2,3,4,5-pentol Chemical compound CNCC(O)C(O)C(O)C(O)CO MBBZMMPHUWSWHV-UHFFFAOYSA-N 0.000 description 1
- FHVDTGUDJYJELY-UHFFFAOYSA-N 6-{[2-carboxy-4,5-dihydroxy-6-(phosphanyloxy)oxan-3-yl]oxy}-4,5-dihydroxy-3-phosphanyloxane-2-carboxylic acid Chemical compound O1C(C(O)=O)C(P)C(O)C(O)C1OC1C(C(O)=O)OC(OP)C(O)C1O FHVDTGUDJYJELY-UHFFFAOYSA-N 0.000 description 1
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical compound [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 1
- HBAQYPYDRFILMT-UHFFFAOYSA-N 8-[3-(1-cyclopropylpyrazol-4-yl)-1H-pyrazolo[4,3-d]pyrimidin-5-yl]-3-methyl-3,8-diazabicyclo[3.2.1]octan-2-one Chemical class C1(CC1)N1N=CC(=C1)C1=NNC2=C1N=C(N=C2)N1C2C(N(CC1CC2)C)=O HBAQYPYDRFILMT-UHFFFAOYSA-N 0.000 description 1
- QSBYPNXLFMSGKH-UHFFFAOYSA-N 9-Heptadecensaeure Natural products CCCCCCCC=CCCCCCCCC(O)=O QSBYPNXLFMSGKH-UHFFFAOYSA-N 0.000 description 1
- PQJUJGAVDBINPI-UHFFFAOYSA-N 9H-thioxanthene Chemical compound C1=CC=C2CC3=CC=CC=C3SC2=C1 PQJUJGAVDBINPI-UHFFFAOYSA-N 0.000 description 1
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 1
- 102100024321 Alkaline phosphatase, placental type Human genes 0.000 description 1
- 239000004475 Arginine Substances 0.000 description 1
- 108010017640 Aspartic Acid Proteases Proteins 0.000 description 1
- 102000004580 Aspartic Acid Proteases Human genes 0.000 description 1
- 239000005711 Benzoic acid Substances 0.000 description 1
- LSNNMFCWUKXFEE-UHFFFAOYSA-M Bisulfite Chemical compound OS([O-])=O LSNNMFCWUKXFEE-UHFFFAOYSA-M 0.000 description 1
- 108010017384 Blood Proteins Proteins 0.000 description 1
- 102000004506 Blood Proteins Human genes 0.000 description 1
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 1
- FERIUCNNQQJTOY-UHFFFAOYSA-M Butyrate Chemical compound CCCC([O-])=O FERIUCNNQQJTOY-UHFFFAOYSA-M 0.000 description 1
- FERIUCNNQQJTOY-UHFFFAOYSA-N Butyric acid Natural products CCCC(O)=O FERIUCNNQQJTOY-UHFFFAOYSA-N 0.000 description 1
- QAGYKUNXZHXKMR-UHFFFAOYSA-N CPD000469186 Natural products CC1=C(O)C=CC=C1C(=O)NC(C(O)CN1C(CC2CCCCC2C1)C(=O)NC(C)(C)C)CSC1=CC=CC=C1 QAGYKUNXZHXKMR-UHFFFAOYSA-N 0.000 description 1
- SLBLRZQZQJHXJW-GFCCVEGCSA-N C[C@H](C1CCCCC1)N(C)Cc1nccnc1 Chemical compound C[C@H](C1CCCCC1)N(C)Cc1nccnc1 SLBLRZQZQJHXJW-GFCCVEGCSA-N 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- 229920002134 Carboxymethyl cellulose Polymers 0.000 description 1
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 description 1
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 1
- PCLITLDOTJTVDJ-UHFFFAOYSA-N Chlormethiazole Chemical compound CC=1N=CSC=1CCCl PCLITLDOTJTVDJ-UHFFFAOYSA-N 0.000 description 1
- 208000006154 Chronic hepatitis C Diseases 0.000 description 1
- KRKNYBCHXYNGOX-UHFFFAOYSA-K Citrate Chemical compound [O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O KRKNYBCHXYNGOX-UHFFFAOYSA-K 0.000 description 1
- 108020004705 Codon Proteins 0.000 description 1
- 206010010144 Completed suicide Diseases 0.000 description 1
- 108010015742 Cytochrome P-450 Enzyme System Proteins 0.000 description 1
- 108010002156 Depsipeptides Proteins 0.000 description 1
- YZCKVEUIGOORGS-OUBTZVSYSA-N Deuterium Chemical group [2H] YZCKVEUIGOORGS-OUBTZVSYSA-N 0.000 description 1
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 1
- XBPCUCUWBYBCDP-UHFFFAOYSA-N Dicyclohexylamine Chemical class C1CCCCC1NC1CCCCC1 XBPCUCUWBYBCDP-UHFFFAOYSA-N 0.000 description 1
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 1
- 241000792859 Enema Species 0.000 description 1
- 208000031969 Eye Hemorrhage Diseases 0.000 description 1
- 206010016654 Fibrosis Diseases 0.000 description 1
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 description 1
- 239000004471 Glycine Substances 0.000 description 1
- 108091006905 Human Serum Albumin Proteins 0.000 description 1
- 102000008100 Human Serum Albumin Human genes 0.000 description 1
- 241000725303 Human immunodeficiency virus Species 0.000 description 1
- CPELXLSAUQHCOX-UHFFFAOYSA-N Hydrogen bromide Chemical compound Br CPELXLSAUQHCOX-UHFFFAOYSA-N 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- 102000002227 Interferon Type I Human genes 0.000 description 1
- 108010014726 Interferon Type I Proteins 0.000 description 1
- 102000013462 Interleukin-12 Human genes 0.000 description 1
- 108010065805 Interleukin-12 Proteins 0.000 description 1
- 102000000588 Interleukin-2 Human genes 0.000 description 1
- 108010002350 Interleukin-2 Proteins 0.000 description 1
- 102000004889 Interleukin-6 Human genes 0.000 description 1
- 108090001005 Interleukin-6 Proteins 0.000 description 1
- OWYWGLHRNBIFJP-UHFFFAOYSA-N Ipazine Chemical compound CCN(CC)C1=NC(Cl)=NC(NC(C)C)=N1 OWYWGLHRNBIFJP-UHFFFAOYSA-N 0.000 description 1
- KJHKTHWMRKYKJE-SUGCFTRWSA-N Kaletra Chemical compound N1([C@@H](C(C)C)C(=O)N[C@H](C[C@H](O)[C@H](CC=2C=CC=CC=2)NC(=O)COC=2C(=CC=CC=2C)C)CC=2C=CC=CC=2)CCCNC1=O KJHKTHWMRKYKJE-SUGCFTRWSA-N 0.000 description 1
- CKLJMWTZIZZHCS-REOHCLBHSA-N L-aspartic acid Chemical compound OC(=O)[C@@H](N)CC(O)=O CKLJMWTZIZZHCS-REOHCLBHSA-N 0.000 description 1
- JVTAAEKCZFNVCJ-UHFFFAOYSA-M Lactate Chemical compound CC(O)C([O-])=O JVTAAEKCZFNVCJ-UHFFFAOYSA-M 0.000 description 1
- 239000012097 Lipofectamine 2000 Substances 0.000 description 1
- KDXKERNSBIXSRK-UHFFFAOYSA-N Lysine Natural products NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 description 1
- 239000004472 Lysine Substances 0.000 description 1
- BYBLEWFAAKGYCD-UHFFFAOYSA-N Miconazole Chemical compound ClC1=CC(Cl)=CC=C1COC(C=1C(=CC(Cl)=CC=1)Cl)CN1C=NC=C1 BYBLEWFAAKGYCD-UHFFFAOYSA-N 0.000 description 1
- MBBZMMPHUWSWHV-BDVNFPICSA-N N-methylglucamine Chemical class CNC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO MBBZMMPHUWSWHV-BDVNFPICSA-N 0.000 description 1
- 125000001429 N-terminal alpha-amino-acid group Chemical group 0.000 description 1
- 101710198130 NADPH-cytochrome P450 reductase Proteins 0.000 description 1
- 206010028980 Neoplasm Diseases 0.000 description 1
- PVNIIMVLHYAWGP-UHFFFAOYSA-N Niacin Chemical compound OC(=O)C1=CC=CN=C1 PVNIIMVLHYAWGP-UHFFFAOYSA-N 0.000 description 1
- 101800001019 Non-structural protein 4B Proteins 0.000 description 1
- 101800001014 Non-structural protein 5A Proteins 0.000 description 1
- 239000005642 Oleic acid Substances 0.000 description 1
- ZQPPMHVWECSIRJ-UHFFFAOYSA-N Oleic acid Natural products CCCCCCCCC=CCCCCCCCC(O)=O ZQPPMHVWECSIRJ-UHFFFAOYSA-N 0.000 description 1
- 229910019142 PO4 Inorganic materials 0.000 description 1
- 229920002230 Pectic acid Polymers 0.000 description 1
- 208000037581 Persistent Infection Diseases 0.000 description 1
- 239000004264 Petrolatum Substances 0.000 description 1
- 108091000041 Phosphoenolpyruvate Carboxylase Proteins 0.000 description 1
- 229920003171 Poly (ethylene oxide) Polymers 0.000 description 1
- 239000004698 Polyethylene Substances 0.000 description 1
- 239000002202 Polyethylene glycol Substances 0.000 description 1
- 229920001214 Polysorbate 60 Polymers 0.000 description 1
- XBDQKXXYIPTUBI-UHFFFAOYSA-M Propionate Chemical compound CCC([O-])=O XBDQKXXYIPTUBI-UHFFFAOYSA-M 0.000 description 1
- 102000007327 Protamines Human genes 0.000 description 1
- 108010007568 Protamines Proteins 0.000 description 1
- YZCKVEUIGOORGS-IGMARMGPSA-N Protium Chemical compound [1H] YZCKVEUIGOORGS-IGMARMGPSA-N 0.000 description 1
- 101800001554 RNA-directed RNA polymerase Proteins 0.000 description 1
- 108010012770 Rebetron Proteins 0.000 description 1
- 241000220010 Rhode Species 0.000 description 1
- 238000011579 SCID mouse model Methods 0.000 description 1
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 1
- UIIMBOGNXHQVGW-DEQYMQKBSA-M Sodium bicarbonate-14C Chemical compound [Na+].O[14C]([O-])=O UIIMBOGNXHQVGW-DEQYMQKBSA-M 0.000 description 1
- 239000005708 Sodium hypochlorite Substances 0.000 description 1
- HVUMOYIDDBPOLL-XWVZOOPGSA-N Sorbitan monostearate Chemical compound CCCCCCCCCCCCCCCCCC(=O)OC[C@@H](O)[C@H]1OC[C@H](O)[C@H]1O HVUMOYIDDBPOLL-XWVZOOPGSA-N 0.000 description 1
- 108020005719 Species specific proteins Proteins 0.000 description 1
- 102000007397 Species specific proteins Human genes 0.000 description 1
- KDYFGRWQOYBRFD-UHFFFAOYSA-N Succinic acid Natural products OC(=O)CCC(O)=O KDYFGRWQOYBRFD-UHFFFAOYSA-N 0.000 description 1
- 230000005867 T cell response Effects 0.000 description 1
- ZMZDMBWJUHKJPS-UHFFFAOYSA-M Thiocyanate anion Chemical compound [S-]C#N ZMZDMBWJUHKJPS-UHFFFAOYSA-M 0.000 description 1
- 239000007983 Tris buffer Substances 0.000 description 1
- YZCKVEUIGOORGS-NJFSPNSNSA-N Tritium Chemical group [3H] YZCKVEUIGOORGS-NJFSPNSNSA-N 0.000 description 1
- 108010067390 Viral Proteins Proteins 0.000 description 1
- 208000003152 Yellow Fever Diseases 0.000 description 1
- 241000710772 Yellow fever virus Species 0.000 description 1
- 101900322197 Yellow fever virus Serine protease NS3 Proteins 0.000 description 1
- GYCPCOJTCINIFZ-JXFKEZNVSA-N [(2s)-1-cyanobutan-2-yl] n-[(1s)-1-[3-[[3-methoxy-4-(1,3-oxazol-5-yl)phenyl]carbamoylamino]phenyl]ethyl]carbamate Chemical compound N#CC[C@H](CC)OC(=O)N[C@@H](C)C1=CC=CC(NC(=O)NC=2C=C(OC)C(C=3OC=NC=3)=CC=2)=C1 GYCPCOJTCINIFZ-JXFKEZNVSA-N 0.000 description 1
- 238000002835 absorbance Methods 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- DPXJVFZANSGRMM-UHFFFAOYSA-N acetic acid;2,3,4,5,6-pentahydroxyhexanal;sodium Chemical compound [Na].CC(O)=O.OCC(O)C(O)C(O)C(O)C=O DPXJVFZANSGRMM-UHFFFAOYSA-N 0.000 description 1
- 125000002777 acetyl group Chemical group [H]C([H])([H])C(*)=O 0.000 description 1
- 230000002378 acidificating effect Effects 0.000 description 1
- 239000013543 active substance Substances 0.000 description 1
- 125000005354 acylalkyl group Chemical group 0.000 description 1
- WNLRTRBMVRJNCN-UHFFFAOYSA-L adipate(2-) Chemical compound [O-]C(=O)CCCCC([O-])=O WNLRTRBMVRJNCN-UHFFFAOYSA-L 0.000 description 1
- 108010062065 albumin interferon Proteins 0.000 description 1
- 229940072056 alginate Drugs 0.000 description 1
- 235000010443 alginic acid Nutrition 0.000 description 1
- 229920000615 alginic acid Polymers 0.000 description 1
- 229910052783 alkali metal Inorganic materials 0.000 description 1
- 229910052784 alkaline earth metal Inorganic materials 0.000 description 1
- 125000005082 alkoxyalkenyl group Chemical group 0.000 description 1
- 125000005078 alkoxycarbonylalkyl group Chemical group 0.000 description 1
- 150000003973 alkyl amines Chemical class 0.000 description 1
- 125000002877 alkyl aryl group Chemical group 0.000 description 1
- 125000005197 alkyl carbonyloxy alkyl group Chemical group 0.000 description 1
- 125000005157 alkyl carboxy group Chemical group 0.000 description 1
- 150000001350 alkyl halides Chemical class 0.000 description 1
- 125000004644 alkyl sulfinyl group Chemical group 0.000 description 1
- AEMOLEFTQBMNLQ-BKBMJHBISA-N alpha-D-galacturonic acid Chemical compound O[C@H]1O[C@H](C(O)=O)[C@H](O)[C@H](O)[C@H]1O AEMOLEFTQBMNLQ-BKBMJHBISA-N 0.000 description 1
- AWUCVROLDVIAJX-UHFFFAOYSA-N alpha-glycerophosphate Natural products OCC(O)COP(O)(O)=O AWUCVROLDVIAJX-UHFFFAOYSA-N 0.000 description 1
- BJEPYKJPYRNKOW-UHFFFAOYSA-N alpha-hydroxysuccinic acid Natural products OC(=O)C(O)CC(O)=O BJEPYKJPYRNKOW-UHFFFAOYSA-N 0.000 description 1
- PNEYBMLMFCGWSK-UHFFFAOYSA-N aluminium oxide Inorganic materials [O-2].[O-2].[O-2].[Al+3].[Al+3] PNEYBMLMFCGWSK-UHFFFAOYSA-N 0.000 description 1
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 1
- CEGOLXSVJUTHNZ-UHFFFAOYSA-K aluminium tristearate Chemical compound [Al+3].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O CEGOLXSVJUTHNZ-UHFFFAOYSA-K 0.000 description 1
- 229940063655 aluminum stearate Drugs 0.000 description 1
- 150000001414 amino alcohols Chemical class 0.000 description 1
- 125000003277 amino group Chemical group 0.000 description 1
- 125000005021 aminoalkenyl group Chemical group 0.000 description 1
- 125000005214 aminoheteroaryl group Chemical group 0.000 description 1
- 150000003863 ammonium salts Chemical class 0.000 description 1
- 229960001830 amprenavir Drugs 0.000 description 1
- YMARZQAQMVYCKC-OEMFJLHTSA-N amprenavir Chemical compound C([C@@H]([C@H](O)CN(CC(C)C)S(=O)(=O)C=1C=CC(N)=CC=1)NC(=O)O[C@@H]1COCC1)C1=CC=CC=C1 YMARZQAQMVYCKC-OEMFJLHTSA-N 0.000 description 1
- 125000002178 anthracenyl group Chemical group C1(=CC=CC2=CC3=CC=CC=C3C=C12)* 0.000 description 1
- 230000000845 anti-microbial effect Effects 0.000 description 1
- 230000000798 anti-retroviral effect Effects 0.000 description 1
- 238000013459 approach Methods 0.000 description 1
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 description 1
- 125000001769 aryl amino group Chemical group 0.000 description 1
- 125000005129 aryl carbonyl group Chemical group 0.000 description 1
- 125000005160 aryl oxy alkyl group Chemical group 0.000 description 1
- 125000004391 aryl sulfonyl group Chemical group 0.000 description 1
- 235000010323 ascorbic acid Nutrition 0.000 description 1
- 239000011668 ascorbic acid Substances 0.000 description 1
- 229960005070 ascorbic acid Drugs 0.000 description 1
- 229940009098 aspartate Drugs 0.000 description 1
- 125000002393 azetidinyl group Chemical group 0.000 description 1
- 235000013871 bee wax Nutrition 0.000 description 1
- 239000012166 beeswax Substances 0.000 description 1
- 229940077388 benzenesulfonate Drugs 0.000 description 1
- SRSXLGNVWSONIS-UHFFFAOYSA-M benzenesulfonate Chemical compound [O-]S(=O)(=O)C1=CC=CC=C1 SRSXLGNVWSONIS-UHFFFAOYSA-M 0.000 description 1
- 229940050390 benzoate Drugs 0.000 description 1
- 235000010233 benzoic acid Nutrition 0.000 description 1
- MJSHDCCLFGOEIK-UHFFFAOYSA-N benzyl (2,5-dioxopyrrolidin-1-yl) carbonate Chemical compound O=C1CCC(=O)N1OC(=O)OCC1=CC=CC=C1 MJSHDCCLFGOEIK-UHFFFAOYSA-N 0.000 description 1
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 1
- XMIIGOLPHOKFCH-UHFFFAOYSA-N beta-phenylpropanoic acid Natural products OC(=O)CCC1=CC=CC=C1 XMIIGOLPHOKFCH-UHFFFAOYSA-N 0.000 description 1
- 150000001602 bicycloalkyls Chemical group 0.000 description 1
- 238000004166 bioassay Methods 0.000 description 1
- 230000004071 biological effect Effects 0.000 description 1
- 230000036765 blood level Effects 0.000 description 1
- 210000001772 blood platelet Anatomy 0.000 description 1
- 210000001185 bone marrow Anatomy 0.000 description 1
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 1
- 229910052794 bromium Inorganic materials 0.000 description 1
- 239000006172 buffering agent Substances 0.000 description 1
- KDYFGRWQOYBRFD-NUQCWPJISA-N butanedioic acid Chemical compound O[14C](=O)CC[14C](O)=O KDYFGRWQOYBRFD-NUQCWPJISA-N 0.000 description 1
- 125000000480 butynyl group Chemical group [*]C#CC([H])([H])C([H])([H])[H] 0.000 description 1
- AIYUHDOJVYHVIT-UHFFFAOYSA-M caesium chloride Chemical compound [Cl-].[Cs+] AIYUHDOJVYHVIT-UHFFFAOYSA-M 0.000 description 1
- 239000011575 calcium Substances 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- 159000000007 calcium salts Chemical class 0.000 description 1
- 238000004364 calculation method Methods 0.000 description 1
- 201000011510 cancer Diseases 0.000 description 1
- 125000003739 carbamimidoyl group Chemical group C(N)(=N)* 0.000 description 1
- 125000002837 carbocyclic group Chemical group 0.000 description 1
- BVKZGUZCCUSVTD-UHFFFAOYSA-N carbonic acid Chemical compound OC(O)=O BVKZGUZCCUSVTD-UHFFFAOYSA-N 0.000 description 1
- 125000005708 carbonyloxy group Chemical group [*:2]OC([*:1])=O 0.000 description 1
- 235000010948 carboxy methyl cellulose Nutrition 0.000 description 1
- 239000008112 carboxymethyl-cellulose Substances 0.000 description 1
- 238000012754 cardiac puncture Methods 0.000 description 1
- 210000001715 carotid artery Anatomy 0.000 description 1
- 239000012876 carrier material Substances 0.000 description 1
- 239000004359 castor oil Substances 0.000 description 1
- 235000019438 castor oil Nutrition 0.000 description 1
- 238000006555 catalytic reaction Methods 0.000 description 1
- 230000004663 cell proliferation Effects 0.000 description 1
- 230000003833 cell viability Effects 0.000 description 1
- 238000003570 cell viability assay Methods 0.000 description 1
- 108091092328 cellular RNA Proteins 0.000 description 1
- 239000001913 cellulose Substances 0.000 description 1
- 229920002678 cellulose Polymers 0.000 description 1
- 210000003169 central nervous system Anatomy 0.000 description 1
- 238000005119 centrifugation Methods 0.000 description 1
- 229940081733 cetearyl alcohol Drugs 0.000 description 1
- 238000012512 characterization method Methods 0.000 description 1
- 239000013626 chemical specie Substances 0.000 description 1
- 238000002512 chemotherapy Methods 0.000 description 1
- 239000000460 chlorine Substances 0.000 description 1
- 229910052801 chlorine Inorganic materials 0.000 description 1
- 238000013375 chromatographic separation Methods 0.000 description 1
- 208000020403 chronic hepatitis C virus infection Diseases 0.000 description 1
- 229960001380 cimetidine Drugs 0.000 description 1
- CCGSUNCLSOWKJO-UHFFFAOYSA-N cimetidine Chemical compound N#CNC(=N/C)\NCCSCC1=NC=N[C]1C CCGSUNCLSOWKJO-UHFFFAOYSA-N 0.000 description 1
- 230000007882 cirrhosis Effects 0.000 description 1
- 208000019425 cirrhosis of liver Diseases 0.000 description 1
- 235000015165 citric acid Nutrition 0.000 description 1
- 229960004414 clomethiazole Drugs 0.000 description 1
- 229940110456 cocoa butter Drugs 0.000 description 1
- 235000019868 cocoa butter Nutrition 0.000 description 1
- 239000008119 colloidal silica Substances 0.000 description 1
- 239000003086 colorant Substances 0.000 description 1
- 230000006957 competitive inhibition Effects 0.000 description 1
- 239000002299 complementary DNA Substances 0.000 description 1
- 230000009918 complex formation Effects 0.000 description 1
- 239000000470 constituent Substances 0.000 description 1
- 239000006071 cream Substances 0.000 description 1
- 125000001995 cyclobutyl group Chemical group [H]C1([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 125000001162 cycloheptenyl group Chemical group C1(=CCCCCC1)* 0.000 description 1
- 125000000582 cycloheptyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- 125000000596 cyclohexenyl group Chemical group C1(=CCCCC1)* 0.000 description 1
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- 125000000522 cyclooctenyl group Chemical group C1(=CCCCCCC1)* 0.000 description 1
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 231100000135 cytotoxicity Toxicity 0.000 description 1
- 230000003013 cytotoxicity Effects 0.000 description 1
- 238000007405 data analysis Methods 0.000 description 1
- 125000004856 decahydroquinolinyl group Chemical group N1(CCCC2CCCCC12)* 0.000 description 1
- 125000002704 decyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 229960005319 delavirdine Drugs 0.000 description 1
- 238000000432 density-gradient centrifugation Methods 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 238000010511 deprotection reaction Methods 0.000 description 1
- 238000013461 design Methods 0.000 description 1
- 229910052805 deuterium Inorganic materials 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 238000011026 diafiltration Methods 0.000 description 1
- 125000004663 dialkyl amino group Chemical group 0.000 description 1
- 150000008050 dialkyl sulfates Chemical class 0.000 description 1
- 235000005911 diet Nutrition 0.000 description 1
- 230000037213 diet Effects 0.000 description 1
- 125000004177 diethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- BGRWYRAHAFMIBJ-UHFFFAOYSA-N diisopropylcarbodiimide Natural products CC(C)NC(=O)NC(C)C BGRWYRAHAFMIBJ-UHFFFAOYSA-N 0.000 description 1
- GXGAKHNRMVGRPK-UHFFFAOYSA-N dimagnesium;dioxido-bis[[oxido(oxo)silyl]oxy]silane Chemical compound [Mg+2].[Mg+2].[O-][Si](=O)O[Si]([O-])([O-])O[Si]([O-])=O GXGAKHNRMVGRPK-UHFFFAOYSA-N 0.000 description 1
- 125000000118 dimethyl group Chemical group [H]C([H])([H])* 0.000 description 1
- GAFRWLVTHPVQGK-UHFFFAOYSA-N dipentyl sulfate Chemical class CCCCCOS(=O)(=O)OCCCCC GAFRWLVTHPVQGK-UHFFFAOYSA-N 0.000 description 1
- ZPWVASYFFYYZEW-UHFFFAOYSA-L dipotassium hydrogen phosphate Chemical compound [K+].[K+].OP([O-])([O-])=O ZPWVASYFFYYZEW-UHFFFAOYSA-L 0.000 description 1
- 229910000396 dipotassium phosphate Inorganic materials 0.000 description 1
- 235000019797 dipotassium phosphate Nutrition 0.000 description 1
- BNIILDVGGAEEIG-UHFFFAOYSA-L disodium hydrogen phosphate Chemical compound [Na+].[Na+].OP([O-])([O-])=O BNIILDVGGAEEIG-UHFFFAOYSA-L 0.000 description 1
- 239000006185 dispersion Substances 0.000 description 1
- 230000005593 dissociations Effects 0.000 description 1
- 208000018459 dissociative disease Diseases 0.000 description 1
- 239000012153 distilled water Substances 0.000 description 1
- 238000009826 distribution Methods 0.000 description 1
- 125000003438 dodecyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- MOTZDAYCYVMXPC-UHFFFAOYSA-N dodecyl hydrogen sulfate Chemical compound CCCCCCCCCCCCOS(O)(=O)=O MOTZDAYCYVMXPC-UHFFFAOYSA-N 0.000 description 1
- 229940043264 dodecyl sulfate Drugs 0.000 description 1
- 239000000890 drug combination Substances 0.000 description 1
- 238000007876 drug discovery Methods 0.000 description 1
- 230000036267 drug metabolism Effects 0.000 description 1
- 235000013601 eggs Nutrition 0.000 description 1
- 239000003792 electrolyte Substances 0.000 description 1
- 230000001804 emulsifying effect Effects 0.000 description 1
- 239000008387 emulsifying waxe Substances 0.000 description 1
- 239000000839 emulsion Substances 0.000 description 1
- 239000007920 enema Substances 0.000 description 1
- 229940095399 enema Drugs 0.000 description 1
- 238000001952 enzyme assay Methods 0.000 description 1
- 229960003276 erythromycin Drugs 0.000 description 1
- CCIVGXIOQKPBKL-UHFFFAOYSA-M ethanesulfonate Chemical compound CCS([O-])(=O)=O CCIVGXIOQKPBKL-UHFFFAOYSA-M 0.000 description 1
- BEFDCLMNVWHSGT-UHFFFAOYSA-N ethenylcyclopentane Chemical compound C=CC1CCCC1 BEFDCLMNVWHSGT-UHFFFAOYSA-N 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- 238000001704 evaporation Methods 0.000 description 1
- 230000008020 evaporation Effects 0.000 description 1
- 230000005284 excitation Effects 0.000 description 1
- 238000002474 experimental method Methods 0.000 description 1
- 239000013604 expression vector Substances 0.000 description 1
- 239000000796 flavoring agent Substances 0.000 description 1
- RFHAOTPXVQNOHP-UHFFFAOYSA-N fluconazole Chemical compound C1=NC=NN1CC(C=1C(=CC(F)=CC=1)F)(O)CN1C=NC=N1 RFHAOTPXVQNOHP-UHFFFAOYSA-N 0.000 description 1
- 229960004884 fluconazole Drugs 0.000 description 1
- 239000012530 fluid Substances 0.000 description 1
- 125000003983 fluorenyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3CC12)* 0.000 description 1
- 238000001506 fluorescence spectroscopy Methods 0.000 description 1
- 229910052731 fluorine Inorganic materials 0.000 description 1
- 239000011737 fluorine Substances 0.000 description 1
- 229960002464 fluoxetine Drugs 0.000 description 1
- CJOFXWAVKWHTFT-XSFVSMFZSA-N fluvoxamine Chemical compound COCCCC\C(=N/OCCN)C1=CC=C(C(F)(F)F)C=C1 CJOFXWAVKWHTFT-XSFVSMFZSA-N 0.000 description 1
- 229960004038 fluvoxamine Drugs 0.000 description 1
- 125000002485 formyl group Chemical group [H]C(*)=O 0.000 description 1
- MLBVMOWEQCZNCC-OEMFJLHTSA-N fosamprenavir Chemical compound C([C@@H]([C@H](OP(O)(O)=O)CN(CC(C)C)S(=O)(=O)C=1C=CC(N)=CC=1)NC(=O)O[C@@H]1COCC1)C1=CC=CC=C1 MLBVMOWEQCZNCC-OEMFJLHTSA-N 0.000 description 1
- 229960003142 fosamprenavir Drugs 0.000 description 1
- 239000012634 fragment Substances 0.000 description 1
- 239000001530 fumaric acid Substances 0.000 description 1
- 235000011087 fumaric acid Nutrition 0.000 description 1
- 230000006870 function Effects 0.000 description 1
- 230000004927 fusion Effects 0.000 description 1
- 230000002068 genetic effect Effects 0.000 description 1
- ZEMPKEQAKRGZGQ-XOQCFJPHSA-N glycerol triricinoleate Natural products CCCCCC[C@@H](O)CC=CCCCCCCCC(=O)OC[C@@H](COC(=O)CCCCCCCC=CC[C@@H](O)CCCCCC)OC(=O)CCCCCCCC=CC[C@H](O)CCCCCC ZEMPKEQAKRGZGQ-XOQCFJPHSA-N 0.000 description 1
- 229960002449 glycine Drugs 0.000 description 1
- 150000002343 gold Chemical class 0.000 description 1
- ZRALSGWEFCBTJO-UHFFFAOYSA-N guanidine group Chemical group NC(=N)N ZRALSGWEFCBTJO-UHFFFAOYSA-N 0.000 description 1
- 150000004820 halides Chemical class 0.000 description 1
- 125000000262 haloalkenyl group Chemical group 0.000 description 1
- 125000003106 haloaryl group Chemical group 0.000 description 1
- 230000036541 health Effects 0.000 description 1
- 210000002216 heart Anatomy 0.000 description 1
- 208000005252 hepatitis A Diseases 0.000 description 1
- MNWFXJYAOYHMED-UHFFFAOYSA-N heptanoic acid Chemical compound CCCCCCC(O)=O MNWFXJYAOYHMED-UHFFFAOYSA-N 0.000 description 1
- 125000005114 heteroarylalkoxy group Chemical group 0.000 description 1
- FUZZWVXGSFPDMH-UHFFFAOYSA-N hexanoic acid Chemical compound CCCCCC(O)=O FUZZWVXGSFPDMH-UHFFFAOYSA-N 0.000 description 1
- 239000004030 hiv protease inhibitor Substances 0.000 description 1
- 150000002431 hydrogen Chemical class 0.000 description 1
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 1
- ZMZDMBWJUHKJPS-UHFFFAOYSA-N hydrogen thiocyanate Natural products SC#N ZMZDMBWJUHKJPS-UHFFFAOYSA-N 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-M hydrogensulfate Chemical compound OS([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-M 0.000 description 1
- 229940071870 hydroiodic acid Drugs 0.000 description 1
- 230000007062 hydrolysis Effects 0.000 description 1
- 238000006460 hydrolysis reaction Methods 0.000 description 1
- 125000005020 hydroxyalkenyl group Chemical group 0.000 description 1
- 125000003454 indenyl group Chemical group C1(C=CC2=CC=CC=C12)* 0.000 description 1
- 229960001936 indinavir Drugs 0.000 description 1
- CBVCZFGXHXORBI-PXQQMZJSSA-N indinavir Chemical compound C([C@H](N(CC1)C[C@@H](O)C[C@@H](CC=2C=CC=CC=2)C(=O)N[C@H]2C3=CC=CC=C3C[C@H]2O)C(=O)NC(C)(C)C)N1CC1=CC=CN=C1 CBVCZFGXHXORBI-PXQQMZJSSA-N 0.000 description 1
- LPAGFVYQRIESJQ-UHFFFAOYSA-N indoline Chemical compound C1=CC=C2NCCC2=C1 LPAGFVYQRIESJQ-UHFFFAOYSA-N 0.000 description 1
- 230000002458 infectious effect Effects 0.000 description 1
- 229940090438 infergen Drugs 0.000 description 1
- 238000001802 infusion Methods 0.000 description 1
- 229940102223 injectable solution Drugs 0.000 description 1
- 229940102213 injectable suspension Drugs 0.000 description 1
- 229910052500 inorganic mineral Inorganic materials 0.000 description 1
- 230000002452 interceptive effect Effects 0.000 description 1
- 229950000038 interferon alfa Drugs 0.000 description 1
- 108010010648 interferon alfacon-1 Proteins 0.000 description 1
- 229960003130 interferon gamma Drugs 0.000 description 1
- 239000002799 interferon inducing agent Substances 0.000 description 1
- 229960001388 interferon-beta Drugs 0.000 description 1
- 229940117681 interleukin-12 Drugs 0.000 description 1
- 229940100601 interleukin-6 Drugs 0.000 description 1
- 238000007917 intracranial administration Methods 0.000 description 1
- 238000007918 intramuscular administration Methods 0.000 description 1
- 238000007919 intrasynovial administration Methods 0.000 description 1
- 238000007913 intrathecal administration Methods 0.000 description 1
- 239000011630 iodine Substances 0.000 description 1
- 229910052740 iodine Inorganic materials 0.000 description 1
- 150000002500 ions Chemical class 0.000 description 1
- SUMDYPCJJOFFON-UHFFFAOYSA-N isethionic acid Chemical compound OCCS(O)(=O)=O SUMDYPCJJOFFON-UHFFFAOYSA-N 0.000 description 1
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 1
- 238000002955 isolation Methods 0.000 description 1
- QXJSBBXBKPUZAA-UHFFFAOYSA-N isooleic acid Natural products CCCCCCCC=CCCCCCCCCC(O)=O QXJSBBXBKPUZAA-UHFFFAOYSA-N 0.000 description 1
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 125000001786 isothiazolyl group Chemical group 0.000 description 1
- 125000000842 isoxazolyl group Chemical group 0.000 description 1
- 229960004130 itraconazole Drugs 0.000 description 1
- 210000003734 kidney Anatomy 0.000 description 1
- 239000000787 lecithin Substances 0.000 description 1
- 235000010445 lecithin Nutrition 0.000 description 1
- 229940067606 lecithin Drugs 0.000 description 1
- 238000012417 linear regression Methods 0.000 description 1
- 229940057995 liquid paraffin Drugs 0.000 description 1
- 239000012280 lithium aluminium hydride Substances 0.000 description 1
- 208000018191 liver inflammation Diseases 0.000 description 1
- 229960004525 lopinavir Drugs 0.000 description 1
- 239000006210 lotion Substances 0.000 description 1
- 239000000314 lubricant Substances 0.000 description 1
- 210000004072 lung Anatomy 0.000 description 1
- 210000004324 lymphatic system Anatomy 0.000 description 1
- 159000000003 magnesium salts Chemical class 0.000 description 1
- 239000000391 magnesium silicate Substances 0.000 description 1
- 235000019359 magnesium stearate Nutrition 0.000 description 1
- 229940099273 magnesium trisilicate Drugs 0.000 description 1
- 229910000386 magnesium trisilicate Inorganic materials 0.000 description 1
- 235000019793 magnesium trisilicate Nutrition 0.000 description 1
- 238000012423 maintenance Methods 0.000 description 1
- 239000011976 maleic acid Substances 0.000 description 1
- 239000001630 malic acid Substances 0.000 description 1
- 235000011090 malic acid Nutrition 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- 239000000155 melt Substances 0.000 description 1
- QLOAVXSYZAJECW-UHFFFAOYSA-N methane;molecular fluorine Chemical compound C.FF QLOAVXSYZAJECW-UHFFFAOYSA-N 0.000 description 1
- 229940098779 methanesulfonic acid Drugs 0.000 description 1
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 description 1
- GDOPTJXRTPNYNR-UHFFFAOYSA-N methyl-cyclopentane Natural products CC1CCCC1 GDOPTJXRTPNYNR-UHFFFAOYSA-N 0.000 description 1
- 229960002509 miconazole Drugs 0.000 description 1
- HPNSFSBZBAHARI-UHFFFAOYSA-N micophenolic acid Natural products OC1=C(CC=C(C)CCC(O)=O)C(OC)=C(C)C2=C1C(=O)OC2 HPNSFSBZBAHARI-UHFFFAOYSA-N 0.000 description 1
- 235000010755 mineral Nutrition 0.000 description 1
- 239000011707 mineral Substances 0.000 description 1
- 229940042472 mineral oil Drugs 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 125000006578 monocyclic heterocycloalkyl group Chemical group 0.000 description 1
- 125000002757 morpholinyl group Chemical group 0.000 description 1
- 239000004570 mortar (masonry) Substances 0.000 description 1
- HPNSFSBZBAHARI-RUDMXATFSA-N mycophenolic acid Chemical compound OC1=C(C\C=C(/C)CCC(O)=O)C(OC)=C(C)C2=C1C(=O)OC2 HPNSFSBZBAHARI-RUDMXATFSA-N 0.000 description 1
- 229960000951 mycophenolic acid Drugs 0.000 description 1
- 125000001421 myristyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- VMESOKCXSYNAKD-UHFFFAOYSA-N n,n-dimethylhydroxylamine Chemical compound CN(C)O VMESOKCXSYNAKD-UHFFFAOYSA-N 0.000 description 1
- PSHKMPUSSFXUIA-UHFFFAOYSA-N n,n-dimethylpyridin-2-amine Chemical compound CN(C)C1=CC=CC=N1 PSHKMPUSSFXUIA-UHFFFAOYSA-N 0.000 description 1
- BEENTKNKPLFNKS-UHFFFAOYSA-N n-ethyl-n'-(3-pyrrolidin-1-ylpropyl)methanediimine Chemical compound CCN=C=NCCCN1CCCC1 BEENTKNKPLFNKS-UHFFFAOYSA-N 0.000 description 1
- 125000003136 n-heptyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- KCXYZMFPZHYUFO-UHFFFAOYSA-N n-methyl-n-phosphanylmethanamine Chemical compound CN(C)P KCXYZMFPZHYUFO-UHFFFAOYSA-N 0.000 description 1
- 125000000740 n-pentyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- KVBGVZZKJNLNJU-UHFFFAOYSA-M naphthalene-2-sulfonate Chemical compound C1=CC=CC2=CC(S(=O)(=O)[O-])=CC=C21 KVBGVZZKJNLNJU-UHFFFAOYSA-M 0.000 description 1
- 125000001624 naphthyl group Chemical group 0.000 description 1
- 239000007922 nasal spray Substances 0.000 description 1
- VRBKIVRKKCLPHA-UHFFFAOYSA-N nefazodone Chemical compound O=C1N(CCOC=2C=CC=CC=2)C(CC)=NN1CCCN(CC1)CCN1C1=CC=CC(Cl)=C1 VRBKIVRKKCLPHA-UHFFFAOYSA-N 0.000 description 1
- 229960001800 nefazodone Drugs 0.000 description 1
- QAGYKUNXZHXKMR-HKWSIXNMSA-N nelfinavir Chemical compound CC1=C(O)C=CC=C1C(=O)N[C@H]([C@H](O)CN1[C@@H](C[C@@H]2CCCC[C@@H]2C1)C(=O)NC(C)(C)C)CSC1=CC=CC=C1 QAGYKUNXZHXKMR-HKWSIXNMSA-N 0.000 description 1
- 229960000884 nelfinavir Drugs 0.000 description 1
- 235000001968 nicotinic acid Nutrition 0.000 description 1
- 239000011664 nicotinic acid Substances 0.000 description 1
- 229910052757 nitrogen Inorganic materials 0.000 description 1
- QJGQUHMNIGDVPM-UHFFFAOYSA-N nitrogen group Chemical group [N] QJGQUHMNIGDVPM-UHFFFAOYSA-N 0.000 description 1
- 231100000344 non-irritating Toxicity 0.000 description 1
- 125000005187 nonenyl group Chemical group C(=CCCCCCCC)* 0.000 description 1
- 231100000252 nontoxic Toxicity 0.000 description 1
- 230000003000 nontoxic effect Effects 0.000 description 1
- GLDOVTGHNKAZLK-UHFFFAOYSA-N octadecan-1-ol Chemical compound CCCCCCCCCCCCCCCCCCO GLDOVTGHNKAZLK-UHFFFAOYSA-N 0.000 description 1
- 125000005889 octahydrochromenyl group Chemical group 0.000 description 1
- 125000005060 octahydroindolyl group Chemical group N1(CCC2CCCCC12)* 0.000 description 1
- 125000002347 octyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- ZQPPMHVWECSIRJ-KTKRTIGZSA-N oleic acid Chemical compound CCCCCCCC\C=C/CCCCCCCC(O)=O ZQPPMHVWECSIRJ-KTKRTIGZSA-N 0.000 description 1
- 239000004006 olive oil Substances 0.000 description 1
- 235000008390 olive oil Nutrition 0.000 description 1
- 230000003287 optical effect Effects 0.000 description 1
- 238000003305 oral gavage Methods 0.000 description 1
- 150000007530 organic bases Chemical class 0.000 description 1
- 235000006408 oxalic acid Nutrition 0.000 description 1
- 239000007800 oxidant agent Substances 0.000 description 1
- 230000003647 oxidation Effects 0.000 description 1
- 238000007254 oxidation reaction Methods 0.000 description 1
- LVSJDHGRKAEGLX-UHFFFAOYSA-N oxolane;2,2,2-trifluoroacetic acid Chemical compound C1CCOC1.OC(=O)C(F)(F)F LVSJDHGRKAEGLX-UHFFFAOYSA-N 0.000 description 1
- 230000020477 pH reduction Effects 0.000 description 1
- 229910052763 palladium Inorganic materials 0.000 description 1
- FJKROLUGYXJWQN-UHFFFAOYSA-N papa-hydroxy-benzoic acid Natural products OC(=O)C1=CC=C(O)C=C1 FJKROLUGYXJWQN-UHFFFAOYSA-N 0.000 description 1
- 229960003930 peginterferon alfa-2a Drugs 0.000 description 1
- 230000035515 penetration Effects 0.000 description 1
- 230000000737 periodic effect Effects 0.000 description 1
- JRKICGRDRMAZLK-UHFFFAOYSA-L peroxydisulfate Chemical compound [O-]S(=O)(=O)OOS([O-])(=O)=O JRKICGRDRMAZLK-UHFFFAOYSA-L 0.000 description 1
- 229940066842 petrolatum Drugs 0.000 description 1
- 239000000546 pharmaceutical excipient Substances 0.000 description 1
- 238000002732 pharmacokinetic assay Methods 0.000 description 1
- 230000000144 pharmacologic effect Effects 0.000 description 1
- XDJOIMJURHQYDW-UHFFFAOYSA-N phenalene Chemical compound C1=CC(CC=C2)=C3C2=CC=CC3=C1 XDJOIMJURHQYDW-UHFFFAOYSA-N 0.000 description 1
- NONJJLVGHLVQQM-JHXYUMNGSA-N phenethicillin Chemical compound N([C@@H]1C(N2[C@H](C(C)(C)S[C@@H]21)C(O)=O)=O)C(=O)C(C)OC1=CC=CC=C1 NONJJLVGHLVQQM-JHXYUMNGSA-N 0.000 description 1
- ISWSIDIOOBJBQZ-UHFFFAOYSA-N phenol group Chemical group C1(=CC=CC=C1)O ISWSIDIOOBJBQZ-UHFFFAOYSA-N 0.000 description 1
- 235000021317 phosphate Nutrition 0.000 description 1
- 239000002367 phosphate rock Substances 0.000 description 1
- 229960004838 phosphoric acid Drugs 0.000 description 1
- 150000003013 phosphoric acid derivatives Chemical class 0.000 description 1
- OJMIONKXNSYLSR-UHFFFAOYSA-N phosphorous acid Chemical compound OP(O)O OJMIONKXNSYLSR-UHFFFAOYSA-N 0.000 description 1
- 229940075930 picrate Drugs 0.000 description 1
- OXNIZHLAWKMVMX-UHFFFAOYSA-M picrate anion Chemical compound [O-]C1=C([N+]([O-])=O)C=C([N+]([O-])=O)C=C1[N+]([O-])=O OXNIZHLAWKMVMX-UHFFFAOYSA-M 0.000 description 1
- 125000005936 piperidyl group Chemical group 0.000 description 1
- 229950010765 pivalate Drugs 0.000 description 1
- IUGYQRQAERSCNH-UHFFFAOYSA-N pivalic acid Chemical compound CC(C)(C)C(O)=O IUGYQRQAERSCNH-UHFFFAOYSA-N 0.000 description 1
- 108010031345 placental alkaline phosphatase Proteins 0.000 description 1
- 229920000058 polyacrylate Polymers 0.000 description 1
- 229920000728 polyester Polymers 0.000 description 1
- 229920000573 polyethylene Polymers 0.000 description 1
- 229920000642 polymer Polymers 0.000 description 1
- 239000001818 polyoxyethylene sorbitan monostearate Substances 0.000 description 1
- 235000010989 polyoxyethylene sorbitan monostearate Nutrition 0.000 description 1
- 229920000136 polysorbate Polymers 0.000 description 1
- 229940113124 polysorbate 60 Drugs 0.000 description 1
- XAEFZNCEHLXOMS-UHFFFAOYSA-M potassium benzoate Chemical compound [K+].[O-]C(=O)C1=CC=CC=C1 XAEFZNCEHLXOMS-UHFFFAOYSA-M 0.000 description 1
- 229910000027 potassium carbonate Inorganic materials 0.000 description 1
- NNFCIKHAZHQZJG-UHFFFAOYSA-N potassium cyanide Chemical compound [K+].N#[C-] NNFCIKHAZHQZJG-UHFFFAOYSA-N 0.000 description 1
- 239000004302 potassium sorbate Substances 0.000 description 1
- 235000010241 potassium sorbate Nutrition 0.000 description 1
- 229940069338 potassium sorbate Drugs 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 239000003755 preservative agent Substances 0.000 description 1
- 230000000750 progressive effect Effects 0.000 description 1
- 230000000069 prophylactic effect Effects 0.000 description 1
- 229950008679 protamine sulfate Drugs 0.000 description 1
- 230000007026 protein scission Effects 0.000 description 1
- 230000002797 proteolythic effect Effects 0.000 description 1
- 230000006337 proteolytic cleavage Effects 0.000 description 1
- 238000000425 proton nuclear magnetic resonance spectrum Methods 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- 125000000561 purinyl group Chemical group N1=C(N=C2N=CNC2=C1)* 0.000 description 1
- 125000004309 pyranyl group Chemical group O1C(C=CC=C1)* 0.000 description 1
- 125000005412 pyrazyl group Chemical group 0.000 description 1
- 125000005495 pyridazyl group Chemical group 0.000 description 1
- 125000000714 pyrimidinyl group Chemical group 0.000 description 1
- 230000035484 reaction time Effects 0.000 description 1
- 238000011084 recovery Methods 0.000 description 1
- 229940100618 rectal suppository Drugs 0.000 description 1
- 239000006215 rectal suppository Substances 0.000 description 1
- 210000000664 rectum Anatomy 0.000 description 1
- 230000000306 recurrent effect Effects 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- 230000010076 replication Effects 0.000 description 1
- 238000002165 resonance energy transfer Methods 0.000 description 1
- 238000003757 reverse transcription PCR Methods 0.000 description 1
- 238000004007 reversed phase HPLC Methods 0.000 description 1
- 230000002441 reversible effect Effects 0.000 description 1
- 230000006965 reversible inhibition Effects 0.000 description 1
- OHRURASPPZQGQM-GCCNXGTGSA-N romidepsin Chemical compound O1C(=O)[C@H](C(C)C)NC(=O)C(=C/C)/NC(=O)[C@H]2CSSCC\C=C\[C@@H]1CC(=O)N[C@H](C(C)C)C(=O)N2 OHRURASPPZQGQM-GCCNXGTGSA-N 0.000 description 1
- 229960004889 salicylic acid Drugs 0.000 description 1
- 229960001852 saquinavir Drugs 0.000 description 1
- QWAXKHKRTORLEM-UGJKXSETSA-N saquinavir Chemical compound C([C@@H]([C@H](O)CN1C[C@H]2CCCC[C@H]2C[C@H]1C(=O)NC(C)(C)C)NC(=O)[C@H](CC(N)=O)NC(=O)C=1N=C2C=CC=CC2=CC=1)C1=CC=CC=C1 QWAXKHKRTORLEM-UGJKXSETSA-N 0.000 description 1
- 238000012216 screening Methods 0.000 description 1
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 238000013207 serial dilution Methods 0.000 description 1
- VGKDLMBJGBXTGI-SJCJKPOMSA-N sertraline Chemical compound C1([C@@H]2CC[C@@H](C3=CC=CC=C32)NC)=CC=C(Cl)C(Cl)=C1 VGKDLMBJGBXTGI-SJCJKPOMSA-N 0.000 description 1
- 229960002073 sertraline Drugs 0.000 description 1
- AWUCVROLDVIAJX-GSVOUGTGSA-N sn-glycerol 3-phosphate Chemical compound OC[C@@H](O)COP(O)(O)=O AWUCVROLDVIAJX-GSVOUGTGSA-N 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- 235000019812 sodium carboxymethyl cellulose Nutrition 0.000 description 1
- 229920001027 sodium carboxymethylcellulose Polymers 0.000 description 1
- SUKJFIGYRHOWBL-UHFFFAOYSA-N sodium hypochlorite Chemical compound [Na+].Cl[O-] SUKJFIGYRHOWBL-UHFFFAOYSA-N 0.000 description 1
- 159000000000 sodium salts Chemical class 0.000 description 1
- 239000007962 solid dispersion Substances 0.000 description 1
- 239000004334 sorbic acid Substances 0.000 description 1
- 235000010199 sorbic acid Nutrition 0.000 description 1
- 229940075582 sorbic acid Drugs 0.000 description 1
- 239000001587 sorbitan monostearate Substances 0.000 description 1
- 235000011076 sorbitan monostearate Nutrition 0.000 description 1
- 229940035048 sorbitan monostearate Drugs 0.000 description 1
- 239000007921 spray Substances 0.000 description 1
- 238000001694 spray drying Methods 0.000 description 1
- 238000010561 standard procedure Methods 0.000 description 1
- 230000004936 stimulating effect Effects 0.000 description 1
- 230000000638 stimulation Effects 0.000 description 1
- 238000007920 subcutaneous administration Methods 0.000 description 1
- 125000005017 substituted alkenyl group Chemical group 0.000 description 1
- 125000000547 substituted alkyl group Chemical group 0.000 description 1
- 238000006467 substitution reaction Methods 0.000 description 1
- KDYFGRWQOYBRFD-UHFFFAOYSA-L succinate(2-) Chemical compound [O-]C(=O)CCC([O-])=O KDYFGRWQOYBRFD-UHFFFAOYSA-L 0.000 description 1
- 125000000020 sulfo group Chemical group O=S(=O)([*])O[H] 0.000 description 1
- 125000005420 sulfonamido group Chemical group S(=O)(=O)(N*)* 0.000 description 1
- 229940032330 sulfuric acid Drugs 0.000 description 1
- RMCMCFUBWGCJLE-UHFFFAOYSA-N sulfuric acid;4,7,7-trimethylbicyclo[2.2.1]heptan-3-one Chemical compound OS(O)(=O)=O.C1CC2(C)C(=O)CC1C2(C)C RMCMCFUBWGCJLE-UHFFFAOYSA-N 0.000 description 1
- 239000000829 suppository Substances 0.000 description 1
- 239000004094 surface-active agent Substances 0.000 description 1
- 239000003765 sweetening agent Substances 0.000 description 1
- 238000004885 tandem mass spectrometry Methods 0.000 description 1
- 229940095064 tartrate Drugs 0.000 description 1
- 230000002123 temporal effect Effects 0.000 description 1
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 238000012360 testing method Methods 0.000 description 1
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 1
- 125000003718 tetrahydrofuranyl group Chemical group 0.000 description 1
- 125000001712 tetrahydronaphthyl group Chemical group C1(CCCC2=CC=CC=C12)* 0.000 description 1
- 125000001412 tetrahydropyranyl group Chemical group 0.000 description 1
- 229940124597 therapeutic agent Drugs 0.000 description 1
- 238000004809 thin layer chromatography Methods 0.000 description 1
- NLVFBUXFDBBNBW-PBSUHMDJSA-N tobramycin Chemical compound N[C@@H]1C[C@H](O)[C@@H](CN)O[C@@H]1O[C@H]1[C@H](O)[C@@H](O[C@@H]2[C@@H]([C@@H](N)[C@H](O)[C@@H](CO)O2)O)[C@H](N)C[C@@H]1N NLVFBUXFDBBNBW-PBSUHMDJSA-N 0.000 description 1
- 229960000707 tobramycin Drugs 0.000 description 1
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 1
- 239000012049 topical pharmaceutical composition Substances 0.000 description 1
- 230000014616 translation Effects 0.000 description 1
- 125000006168 tricyclic group Chemical group 0.000 description 1
- 125000004385 trihaloalkyl group Chemical group 0.000 description 1
- 229910052722 tritium Chemical group 0.000 description 1
- 230000024275 uncoating of virus Effects 0.000 description 1
- ZDPHROOEEOARMN-UHFFFAOYSA-N undecanoic acid Chemical compound CCCCCCCCCCC(O)=O ZDPHROOEEOARMN-UHFFFAOYSA-N 0.000 description 1
- 229960005486 vaccine Drugs 0.000 description 1
- 235000013311 vegetables Nutrition 0.000 description 1
- 230000007444 viral RNA synthesis Effects 0.000 description 1
- 230000008478 viral entry into host cell Effects 0.000 description 1
- 230000006514 viral protein processing Effects 0.000 description 1
- 230000017613 viral reproduction Effects 0.000 description 1
- 239000000080 wetting agent Substances 0.000 description 1
- 239000003871 white petrolatum Substances 0.000 description 1
- 210000002268 wool Anatomy 0.000 description 1
- 229940051021 yellow-fever virus Drugs 0.000 description 1
- 150000003751 zinc Chemical class 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K7/00—Peptides having 5 to 20 amino acids in a fully defined sequence; Derivatives thereof
- C07K7/04—Linear peptides containing only normal peptide links
- C07K7/06—Linear peptides containing only normal peptide links having 5 to 11 amino acids
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N37/00—Biocides, pest repellants or attractants, or plant growth regulators containing organic compounds containing a carbon atom having three bonds to hetero atoms with at the most two bonds to halogen, e.g. carboxylic acids
- A01N37/44—Biocides, pest repellants or attractants, or plant growth regulators containing organic compounds containing a carbon atom having three bonds to hetero atoms with at the most two bonds to halogen, e.g. carboxylic acids containing at least one carboxylic group or a thio analogue, or a derivative thereof, and a nitrogen atom attached to the same carbon skeleton by a single or double bond, this nitrogen atom not being a member of a derivative or of a thio analogue of a carboxylic group, e.g. amino-carboxylic acids
- A01N37/46—N-acyl derivatives
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/4965—Non-condensed pyrazines
- A61K31/497—Non-condensed pyrazines containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/50—Pyridazines; Hydrogenated pyridazines
- A61K31/501—Pyridazines; Hydrogenated pyridazines not condensed and containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/005—Enzyme inhibitors
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/04—Peptides having up to 20 amino acids in a fully defined sequence; Derivatives thereof
- A61K38/08—Peptides having 5 to 11 amino acids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K5/00—Peptides containing up to four amino acids in a fully defined sequence; Derivatives thereof
- C07K5/04—Peptides containing up to four amino acids in a fully defined sequence; Derivatives thereof containing only normal peptide links
- C07K5/06—Dipeptides
- C07K5/06139—Dipeptides with the first amino acid being heterocyclic
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K5/00—Peptides containing up to four amino acids in a fully defined sequence; Derivatives thereof
- C07K5/04—Peptides containing up to four amino acids in a fully defined sequence; Derivatives thereof containing only normal peptide links
- C07K5/10—Tetrapeptides
- C07K5/1024—Tetrapeptides with the first amino acid being heterocyclic
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N9/00—Enzymes; Proenzymes; Compositions thereof; Processes for preparing, activating, inhibiting, separating or purifying enzymes
- C12N9/99—Enzyme inactivation by chemical treatment
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
Abstract
Description
本特許出願は2005年8月2日に出願した米国仮特許出願番号60/704,772(言及することにより本明細書の一部とする)の利益を主張するものである。
本発明はセリンプロテアーゼ活性、とりわけ、C型肝炎ウイルスNS3−NS4Aプロテアーゼの活性を阻害する化合物に関する。それらはそれ自体C型肝炎ウイルスのライフサイクルに干渉することにより作用し、抗ウイルス剤として有用である。本発明は、さらにエキソビボ使用のための、またはHCV感染に罹患する患者に投与するための、これらの化合物を含有してなる組成物に関する。また、本発明は本発明化合物を投与することによって、患者のHCV感染を処置する方法にも関する。
C型肝炎ウイルス(“HCV”)による感染は、注目せざるを得ないヒトの医学的問題である。HCVは非A、非B肝炎の殆どの事例の原因因子として認知されており、世界的規模で3%の人々に広がっているとされている[A. Alberti et al., “Natural History of Hepatitis C(C型肝炎のナチュラル・ヒストリー),” J. Hepatology, 31., (Suppl. 1), pp. 17-24 (1999)]。米国単独でもほぼ400万の個々人が感染している可能性がある[M.J. Alter et al., “The Epidemiology of Viral Hepatitis in the United States(合衆国におけるウイルス感染の疫学), Gastroenterol. Clin. North Am., 23, pp. 437-455 (1994); M. J. Alter “Hepatitis C Virus Infection in the United States(合衆国におけるC型肝炎ウイルス感染),” J. Hepatology, 31., (Suppl. 1), pp. 88-91 (1999)]。
図1A−Bは、C*位置でのR異性体が50%を超える式(I)の化合物と、C*位置でのR異性体が50%以下である化合物との平均(±SD)血漿濃度を、該化合物の経口投与後に経時的にプロットしたものである。
I.定義
本発明の目的上、元素は理化学事典(Handbook of Chemistry and Physics, 75th Ed.)CAS版の周期律表に従って同定される。さらに、有機化学の一般原理は、“Organic Chemistry”, Thomas Sorrell, University Science Books, Sausalito: 1999、および“March's Advanced Organic Chemistry”, 5th Ed., Ed.: Smith, M.B. and March, J., John Wiley & Sons, New York: 2001 (言及することによりその全文を本明細書の一部とする)に記載されている。
本明細書にて使用される場合、「スルホ」基は、末端基として使用される場合には−SO3Hまたは−SO3RXをいい、または内部基として使用される場合には、−S(O)3−をいう。
本明細書にて使用される場合、「オキソ」とは=Oをいう。
本明細書にて使用される場合、「アミノアルキル」は、構造 (RX)2N−アルキルをいう。
本明細書にて使用される場合、「シアノアルキル」は、構造 (NC)−アルキル−をいう。
BEMP=2−tert−ブチルイミノ−2−ジエチルアミノ−1,3−ジメチルペルヒドロ−1,3,2−ジアザホスホリン
Boc=t−ブトキシカルボニル
BOP=ヘキサフルオロリン酸ベンゾトリアゾール−1−イルオキシ−トリス(ジメチルアミノ)ホスホニウム
bd=幅広いダブレット
bs=幅広いシングレット
d=ダブレット
dd=二重のダブレット
DIC=ジイソプロピルカルボジイミド
DMF=ジメチルホルムアミド
DMAP=ジメチルアミノピリジン
DMSO=ジメチルスルホキシド
EDC=エチル−1−(3−ジメチルアミノプロピル)カルボジイミド
eq. =当量
EtOAc=酢酸エチル
g=グラム
HOBT=1−ヒドロキシベンゾトリアゾール
DIPEA=ヒューニッヒ塩基=ジイソプロピルエチルアミン
L=リットル
m=マルチプレット
M=モル濃度
max=最大値
meq=ミリ当量
mg=ミリグラム
mL=ミリリットル
mm=ミリメートル
mmol=ミリモル
MOC=メトキシオキシカルボニル
N=規定
ng=ナノグラム
nm=ナノメートル
OD=吸光度
PEPC=1−(3−(1−ピロリジニル)プロピル)−3−エチルカルボジイミド
PP−HOBT=ピペリジン−ピペリジン−1−ヒドロキシベンゾトリアゾール
psi=平方インチあたりのポンド
Ph=フェニル
q=カルテット
quin.=クインテット
rpm=1分あたりの回転数
s=シングレット
t=トリプレット
TFA=トリフルオロ酢酸
THF=テトラヒドロフラン
tlc=薄層クロマトグラフィー
μL=マイクロリットル
UV=紫外線
本発明化合物は、C*位置でのR異性体が混合物の50%(例えば、約60%、約70%、約80%、約85%、約90%、約95%、または約98%)を超える場合に、それらがより大きなバイオアベイラビリティーを有することが観察されたことから、望ましい治療処置を提供する。予期しないことに、C*位置でのR異性体は、C*位置でのS異性体よりも約2倍バイオアベイラビリティーが高い。さらに、C*位置でのR異性体は、インビボで、C*位置でのSよりもより高い割合でC*位置でのS異性体に変換する。これらの性質は、C型肝炎ウイルスNS3−NS4Aプロテアーゼの活性を阻害するなど、セリンプロテアーゼ活性のインヒビターとして、50%を超えるC*位置でのR異性体を含有する式(I)の化合物の治療効果を高める。例えば、C*での50%を超えるR異性体である本発明の一部の態様では、3μM未満のKi(app)(例えば、約2μM、約1.5μM、または約1.190μM)、約0.9μM未満のIC50(例えば、約0.883μM)、および100μMを超えるCC50を測定値として示した。
C*はジアステレオマー炭素原子を表す;そして
C*位置でのR異性体はS異性体に比較して、混合物の50%を超える;
R1は、RW−、P3−、またはP4−L2−P3−である;
Rは、所望により置換されている脂肪族基、所望により置換されている環状脂肪族基、所望により置換されているヘテロ環状脂肪族基、所望により置換されているアリール基、または所望により置換されているヘテロアリール基である;
Wは結合、−NR4−、−O−、または−S−である;
R4は、H、所望により置換されている脂肪族基、所望により置換されている環状脂肪族基、所望により置換されているヘテロ環状脂肪族基、所望により置換されているアリール基、または所望により置換されているヘテロアリール基である;
Tは、−C(O)−、−OC(O)−、−NHC(O)−、−C(O)C(O)−、または−SO2−である;
R5およびR5'はそれぞれ独立して、H、所望により置換されている脂肪族基、所望により置換されている環状脂肪族基、所望により置換されているヘテロ環状脂肪族基、所望により置換されているフェニル、または所望により置換されているヘテロアリール基である;
R6は、所望により置換されている脂肪族基、所望により置換されているヘテロアリール基、所望により置換されているフェニルである;または
R5およびR6は、それらが結合している原子と一体となって、5員ないし7員の所望により置換されている単環式へテロ環状脂肪族基、または6員ないし12員の所望により置換されている二環式へテロ環状脂肪族基を形成してもよく、各へテロ環状脂肪族環は所望により−O−、−S−または−NR50−から選択されるさらなるヘテロ原子を含む;
P4−L2−P3は
R7およびR7'はそれぞれ独立して、H、所望により置換されている脂肪族基、所望により置換されている環状脂肪族基、所望により置換されているヘテロ環状脂肪族基、所望により置換されているフェニル、または所望により置換されているヘテロアリール基である;または、
R7およびR7'は、それらが結合している原子と一体となって、3員ないし7員の環状脂肪族またはヘテロ環状脂肪族環を形成してもよい;または、
R7およびR6は、それらが結合している原子と一体となって、5員ないし7員の所望により置換されている単環式へテロ環状脂肪族基、5員ないし7員の所望により置換されている単環式へテロアリール基、6員ないし12員の所望により置換されている二環式へテロ環状脂肪族基、または6員ないし12員の所望により置換されている二環式へテロアリール基を形成してもよく、各へテロ環状脂肪族またはヘテロアリール環は、所望により−O−、−S−または−NR50−から選択されるさらなるヘテロ原子を含む;または、R5およびR6が、それらが結合している原子と一体となって環を形成し得る場合、R7およびR5とR6により形成される環系は、8員ないし14員の所望により置換されている二環式縮合環系を形成してもよく、ここで、該二環式縮合環系は、さらに所望により置換されているフェニルと縮合して、所望により置換されている10員ないし16員の三環式縮合環系を形成してもよい;
R8はHまたは保護基である;
R3は、H、所望により置換されている脂肪族基、所望により置換されている環状脂肪族基、所望により置換されているヘテロ環状脂肪族基、所望により置換されているアリール基、または所望により置換されているヘテロアリール基である;
Lは結合、−CF2−、−C(O)−、または−SO2−である;
J1、J2、J'2、およびJ3はそれぞれ独立して、ハロゲン、−OR'、−OC(O)N(R')2、−NO2、−CN、−CF3、−OCF3、−R'、オキソ、チオキソ、−N(R')2、−SR'、−COR'、−SO2R'、−SO2N(R')2、−SO3R'、−C(O)R'、−C(O)C(O)R'、−C(O)CH2C(O)R'、−C(S)R'、−C(O)OR'、−OC(O)R'、−C(O)N(R')2、−OC(O)N(R')2、−C(S)N(R')2、−(CH2)0−2NHC(O)R'、−N(R')N(R')COR'、−N(R')N(R')C(O)OR'、−N(R')N(R')CON(R')2、−N(R')SO2R'、−N(R')SO2N(R')2、−N(R')C(O)OR'、−N(R')C(O)R'、−N(R')C(S)R'、−N(R')C(O)N(R')2、−N(R')C(S)N(R')2、−N(COR')COR'、−N(OR')R'、−C(=NH)N(R')2、−C(O)N(OR')R'、−C(=NOR')R'、−OP(O)(OR')2、−P(O)(R')2、−P(O)(OR')2、または−P(O)(H)(OR')であるか、またはJ2およびJ'2から選択される1つがHであり、
ここで、2つのR'基は、それらが結合している原子と一体となって、N、O、またはSから独立して選択される3個までのヘテロ原子を有する3員ないし10員の芳香族または非芳香族環系を形成してもよく、該環は所望によりC6−C10アリール、C5−C10ヘテロアリール、C3−C10シクロアルキル、またはC3−C10ヘテロ環状脂肪族基に縮合しており、そして全ての環がそれぞれ独立してJ2から選択される3個までの置換基を有するか、またはJ2またはJ'2の1つが水素である;
各R'は独立して、H、C1−C12脂肪族基、C3−C10シクロアルキル、またはC3−C10シクロアルケニル、C3−C10シクロアルキル−C1−C12脂肪族基、C3−C10シクロアルケニル−C1−C12脂肪族基、C6−C10アリール基、C6−C10アリール−C1−C12脂肪族基、3員ないし10員のヘテロ環状脂肪族基、6員ないし10員のヘテロ環状脂肪族−C1−C12脂肪族基、5員ないし10員のヘテロアリール基、または5員ないし10員のヘテロアリール−C1−C12脂肪族基から選択され、ここで、R'はそれぞれ独立してJ2から選択される3個までの置換基を有する]
で示される化合物、または医薬的に許容されるその塩またはそれらの混合物を提供する。
R10は独立して、H、(C1−C12)−脂肪族基、(C6−C10)−アリール、(C6−C10)−アリール−(C1−C12)脂肪族基、(C3−C10)−シクロアルキルもしくは−シクロアルケニル、[(C3−C10)−シクロアルキルもしくは−シクロアルケニル]−(C1−C12)−脂肪族基、(3員ないし10員)−へテロ環状脂肪族−、(6員ないし10員)−へテロ環状脂肪族−(C1−C12)脂肪族−、(5員ないし10員)−ヘテロアリール−、または(5員ないし10員)−へテロアリール−(C1−C12)−脂肪族−である;
各Kは、結合、(C1−C12)−脂肪族基、−O−、−S−、−NR9−、−C(O)−、または−C(O)NR9−である(ここで、R9は水素または(C1−C12)−脂肪族基である);そして
mは1〜3である]
である。
Z2は独立して、O、S、NR10、またはC(R10)2である;
各R10は水素、(C1−C12)−脂肪族基、(C6−C10)−アリール、(C6−C10)−アリール−(C1−C12)脂肪族基、(C3−C10)−シクロアルキルもしくは−シクロアルケニル、[(C3−C10)−シクロアルキルもしくは−シクロアルケニル]−(C1−C12)−脂肪族基、(3員ないし10員)−へテロ環状脂肪族−、(6員ないし10員)−へテロ環状脂肪族−(C1−C12)脂肪族−、(5員ないし10員)−ヘテロアリール−、または(5員ないし10員)−へテロアリール−(C1−C12)−脂肪族−である;
pは独立して1または2である;そして
----- は独立して単結合または二重結合である]
である。
幾つかの実施態様において、Tは−OC(O)−である。
幾つかの実施態様において、Tは−NHC(O)−である。
幾つかの実施態様において、Tは−S(O)2−である。
R7およびR7'はそれぞれ独立して、H、所望により置換されている脂肪族基、所望により置換されているヘテロアリール基、または所望により置換されているフェニルである;または
R7およびR7'は、それらが結合している原子と一体となって、3員ないし7員の環状脂肪族またはヘテロ環状脂肪族環を形成してもよい;または
R7およびR6は、それらが結合している原子と一体となって、5員ないし7員の所望により置換されている単環式へテロ環状脂肪族基、5員ないし7員の所望により置換されている単環式へテロアリール基、6員ないし12員の所望により置換されている二環式へテロ環状脂肪族基、または6員ないし12員の所望により置換されている二環式へテロアリール基を形成してもよく、各へテロ環状脂肪族またはヘテロアリール環は、所望により−O−、−S−または−NR50−から選択されるさらなるヘテロ原子を含む;または
R5およびR6が、それらが結合している原子と一体となって環を形成し得る場合、R7およびR5とR6により形成される環系は、8員ないし14員の所望により置換されている二環式縮合環系を形成してもよく、ここで、該二環式縮合環系は、さらに所望により置換されているフェニルと縮合して、所望により置換されている10員ないし16員の三環式縮合環系を形成してもよい;
R8はHまたは保護基である;
R50は、H、所望により置換されている脂肪族基、所望により置換されているヘテロアリール基、または所望により置換されているフェニルである]
である上記のジアステレオマー化合物の混合物。
幾つかの実施態様において、R3は所望により置換されている(C1−C6)−アルキルまたは所望により置換されている(C1−C6)−シクロアルキルである。
幾つかの実施態様において、C*でのR異性体とS異性体の比が70対30を超える。
幾つかの実施態様において、C*でのR異性体とS異性体の比が90対10を超える。
幾つかの実施態様において、C*でのR異性体とS異性体の比が98対2を超える。
幾つかの実施態様において、C*でのR異性体とS異性体の比が99対1を超える。
で示される化合物のRおよびS異性体を含む混合物の特異的分離は、表1に従って実施した。保持時間は、表2に示すように、C*でのR異性体の場合、8分27秒であり、C*でのS異性体の場合、6分35秒と測定された。
本発明化合物は、それらがC*位置でのR異性体が混合物の50%(例えば、約60%、約70%、約80%、約85%、約90%、約95%、または約99%)を超える場合に、より高いバイオアベイラビリティーを有することが観察されたことから、望ましい治療薬であり得る。C*位置でのR異性体が50%を超える混合物では、C*位置でのS異性体よりも約2倍バイオアベイラビリティーが高い。具体的には、総計バイオアベイラビリティーは、2つの異性体を組合わせて投与されることによって示される場合に、経口投与したC*でのR異性体について約98%であり、経口投与したC*でのS異性体について50%であった。さらに、経口投与後、C*位置でのR異性体からC*位置でのS異性体への変換は、C*でのS異性体からC*でのR異性体への変換よりも顕著であった。相互変換は、IV投与後に比較して、経口投与後により広範に起こった。
「レフェロン」は、ホフマン−ラ・ロシュ(ナットレイ、ニュージャージー)から入手し得るROFERON(登録商標)、組換えインターフェロン・アルファ−2aを意味する;
ウエルフェロン(WELLFERON;登録商標)は、グラクソ・ウエルカム(株)(英国)から入手し得るインターフェロン・アルファn1である;
(a) イントロン(INTRON-A;登録商標)(インターフェロン−アルファ2B、シェリング・プラウ)、
(b) ペグ−イントロン(PEG-INTRON;登録商標)、
(c) ペガシス(PEGASYS;登録商標)、
(d) ロフェロン(ROFERON;登録商標)、
(e) ベレフォア(BEREFOR;登録商標)、
(f) スミフェロン(SUMIFERON;登録商標)、
(g) ウエルフェロン(WELLFERON;登録商標)、
(h) コンセンサス・アルファ・インターフェロン、アムジェン・インク(ニューバリー・パーク、カリフォルニア)から入手可能、
(i) アルフェロン(ALFERON;登録商標)、
(j) ビラフェロン(VIRAFERON;登録商標)、
(k) インフェグレン(INFERGEN;登録商標)および
(l) アルブフェロン(ALBUFERON;商標)。
実施例1:式(I)で示される化合物のC * 位置でのRおよびS異性体のバイオアベイラビリティー
オスのスプラーグ・ドーレーラット(n=6〜7/1群)3群に、式(I)で示される化合物(ここで、混合物はC*位置でのR異性体約92%およびC*位置でのS異性体約8%からなる);C*位置でのR異性体約7%およびC*位置でのS異性体約93%からなる混合物;または式(I)で示される化合物(ここで、混合物はC*位置でのR異性体約54%およびC*位置でのS異性体約45%からなる)を名目30mg/kgで経口投与した。投与後24時間まで、連続血液サンプルを収集した。誘導した血漿サンプル(100μL)はインビトロでの相互変換を防止するために、ギ酸5μLを加えることにより酸性とした。
FSSはC*でのS異性体投与後のC*でのS異性体のバイオアベイラビリティーを表す;
FR+SRはR異性体投与後の(C*位置での)RおよびS異性体に対する組合わせ接触にもとづく予測される合計のバイオアベイラビリティーを表す;
FSRはC*でのR異性体投与後のC*でのS異性体のバイオアベイラビリティーを表す;これはR異性体経口投与後の用量−標準化AUCSと、対するR異性体のIV投与後のAUCSとの相対比である;そして
b n=2、残りのラットではAUCINFが評価できず。
注記:より少ないジアステレオマーのAUCINFへの寄与は無視し得ると仮定した。
5AB基質と生成物の分離のためのHPLCミクロボア法
基質:
NH2-Glu-Asp-Val-Val-(アルファ)Abu-Cys-Ser-Met-Ser-Tyr-COOH
20mM5ABの保存液は、DMSOw/0.2M−DTTで調製した。これを分割して−20℃で保存した。
50mM HEPES、pH7.8;20%グリセロール;100mM NaCl
適切な濃度の試験化合物2.5μLをDMSO(対照についてはDMSOのみ)に溶かし、各ウェルに加えた。これを室温で15分間インキュベートした。
250μM−5AB基質(25μM濃度は5ABのKmに等価であるか、またはそれよりわずかに低い)20μLを添加して反応を開始した。
30℃で20分間インキュベートした。
10%TFA25μLを加えて反応を終結させた。
120μ部分をHPLCバイアルに移した。
ミクロボア分離法:
機器化:エイジレント1100
脱気装置G1322A
二進ポンプG1312A
自動試料採取器G1313A
カラム恒温化チャンバーG1316A
ダイオードアレイ検出器
カラム:フェノメネックス・ジュピター;5ミクロンC18;300Å;150×2mm;P/O00F−4053−B0
カラム恒温器:40℃
注入容量:100μL
実施例3:HCV NS3プロテアーゼ用蛍光ペプチド開裂アッセイ
式(I)で示される幾つかの化合物の定常状態阻害定数Ki*は、Taliani, M., E. Bianchi, F. Narjes, M. Fossatelli, A. Rubani, C. Steinkuhler, R. De Francesco, and A. Pessi. 1996. A Continuous Assay of Hepatitis C Virus Protease Based on Resonance Energy Transfer Depsipeptide Substrates(共鳴エネルギー転移デプシペプチド基質に基づくC型肝炎ウイルスプロテアーゼの連続アッセイ). Anal. Biochem. 240:60-67 (言及することにより本明細書の一部とする)に記載された蛍光ペプチド開裂アッセイを少し改変したアッセイ法により決定した。
F(t)=Vs×t+(Vi−Vs)×(1−exp(-kobs×t))/kobs+C
対照の割合は正味のDMSOを含む反応から決定した。これらの実験条件下、kobsはkoffの20%内である。複合体の半減期(t1/2)は次の等式:t1/2=0.693/koffから計算した。
本アッセイ法は、Landro, J. A., S. A. Raybuck, Y. P. Luong, E. T. O'Malley, S. L. Harbeson, K. A. Morgenstern, G. Rao, and D. J. Livingston. 1997. Mechanistic Role of an NS4A Peptide Cofactor with the Truncated NS3 Protease of Hepatitis C Virus: Elucidation of the NS4A Stimulatory Effect via Kinetic Analysis and Inhibitor Mapping(C型肝炎ウイルスの末端切除NS3プロテアーゼによるNS4Aペプチド補助因子の機構的役割;速度論的分析およびインヒビターマッピングを解してのNS4A刺激作用の解明) Biochemistry 36:9340-9348 (言及することにより本明細書の一部とする)に記載された方法のわずかに改変した方法である。
式(I)で示される数種の化合物は、レプリコン細胞においてHCV RNAレベルを50%(IC50)もしくは90%(IC90)低下させるか、または細胞生存度を50%(CC50)低下させる濃度を有し、その濃度は4パラメータ曲線フィッティング(ソフトマックス・プロ)を用いて、HCV Con1サブゲノム・レプリコン細胞にて決定した (Lohmann, V., F. Korner, J. Koch, U. Herian, L. Theilmann, and R. Bartenschlager. 1999. Replication of subgenomic hepatitis C virus RNAs in a hepatoma cell line(肝細胞癌細胞株におけるサブゲノムC型肝炎ウイルスRNAのレプリコン)、Science 285:110-3.16; 言及することにより本明細書の一部とする)。簡単に説明すると、レプリコン細胞は2%ウシ胎児血清(FBS)および0.5%DMSOを含有する培地に希釈した化合物と、37℃でインキュベートした。全細胞性RNAをRNイージー−96キット(キアゲン、バレンシア、カリフォルニア)で抽出し、HCV RNAのコピー数を定量的実時間多重逆転写−PCR(QRT−PCRまたはタックマン(Taqman))アッセイにより決定した。HCVレプリコン細胞における化合物の細胞毒性は、すでに記載したテトラゾリウムによる細胞生存度アッセイ法を用いて、同じ実験設定条件下に測定した。参照:Lin, C., K. Lin, Y. P. Luong, B. G. Rao, Y. Y. Wei, D. L. Brennan, J. R. Fulghum, H. M. Hsiao, S. Ma, J. P. Maxwell, K. M. Cottrell, R. B. Perni, C. A. Gates, and A. D. Kwong. 2004。C型肝炎ウイルス・セリンプロテアーゼ・インヒビター、(1S,3aR,6aS)−2−[(2S)−2−[[(2S)−2−シクロヘキシル−1−オキソ−2−[(ピラジニルカルボニル)アミノ]エチル]アミノ]−3,3−ジメチル−1−オキソブチル]−N−[(1R)−1−[2−(シクロプロピルアミノ)−1,2−ジオキソエチル]ブチル]オクタヒドロ−シクロペンタ[c]ピロール−1−カルボキサミドのインビトロ耐性研究。
式(I)で示される化合物の静脈内薬物動態は、ラットおよびイヌにおいて評価した。体重250〜300gの3匹のオス・スプラグ−ドーリー系ラット1群に、15%エタノール、10%ジメチルイソソルビド、35%PEG400および40%D5W(5%デキストロース/水)からなるビークル中、式(I)のS−ジアステレオマー0.95mg/kgの静脈内ボーラス用量を投与した。連続血液サンプルは、ヘパリン添加チューブ中に、0時(投与前)、投与処置後、0.083、0.167、0.25、0.5、1、1.5、2、3、4、6、および8時間後に採取した。3頭のオス・ビーグル犬(8〜12kg;チャールス・リバー、マサチューセッツ)の1群に、10%エタノール、40%PEG400および50%D5W中、該ジアステレオマー3.5mg/kgの静脈内ボーラス用量を投与した。連続血液サンプルは、ヘパリン添加チューブ中に、投与前、および投与処置後、0.083、0.167、0.25、0.5、1、1.5、2、4、6、8、12および24時間後に採取した。ラットおよびイヌでの経口研究のために、式(I)で示されるS−ジアステレオマー化合物をポリビニルピロリドン(PVP)K30プラス2%ラウリル硫酸ナトリウム中で製剤化し、次いで経口チューブにより投与した。3匹のオス・スプラグ−ドーリー系ラット(250〜300g、ハーラン、メリーランド)1群に、該化合物40mg/kgを経口投与し、また3頭のオス・ビーグル犬(10.9〜12.0kg;チャールス・リバー、マサチューセッツ)の1群に、該化合物13.2mg/kgの経口用量を投与した。両方の経口研究において、血液サンプルは、投与前、および投与処置後、0.25、0.5、1、1.5、2、3、4、6、8、12および24時間後に採取した。静脈内および経口研究の両方において、血漿サンプルは遠心分離により入手し、分析時まで、−70℃に保存した。ラットの静脈内研究から得られたサンプルは、キラル液体クロマトグラフィー/質量分析(LC/MS/MS)分析に付し、一方、他のすべての研究のサンプルは、非キラルLC/MS/MS法を用いて分析した。標準的技法を用いて、データの非区画分析を実施した;その際、以下の薬物動態パラメータ、すなわち、CmaxまたはCminまたはCavg(それぞれ血清中薬物の最大または最小または平均濃度)、AUCO-8またはAUCO-inf(それぞれ0ないし8時間または0ないし無限時間からの濃度曲線下の合計面積)、t1/2(除去の半減期)、CL(合計体クリアランス)、およびVss(定常状態での分布容量)などの計算のために、ウインノンリン・エンタープライズ/プロ(WinNonlin Enterprise/Pro)バージョン4.0.1(ファーサイト・コーポレーション、マウンテンビュー、カリフォルニア)を使用した。
式(I)の化合物のジアステレオマーの肝臓/血漿比は、ラットにおいて、プロピレングリコール中の化合物の溶液を経口投与した後に評価した。オスのフィッシャーラット6群(1群3匹)に、式(I)の化合物のジアステレオマーの名目用量30mg/kgを経口投与した。投与処置後、0時(投与前)、0.5、1、2、4または8時間目に、1群3匹の動物を各時点ごとに殺し、1匹は血液を、また対応する肝臓サンプルは各動物から得た。血漿は血液サンプルを遠心分離することにより得た。全肝臓を動物から取り出し、正常食塩水で灌流して微量の血液を除去した。重量測定した後、肝臓を小片に切断し、等容量の水でホモジネートとした。血漿および肝臓サンプルは、非キラルLC/MS/MS法を用いる分析時まで、−70℃で保存した。
HCV NS3−4Aセリンプロテアーゼについてのこのマウスモデルの詳細は別に記載する。このモデルの簡単な説明をここに示す。開始Metコドン、His-tag(SHHHHHHAM)、HCV NS3タンパク質の全長631個のアミノ酸、HCV NS4Aタンパク質の全長54残基、およびHCV NS4Bタンパク質のN−末端の6個(ASHLPY)のアミノ酸をエンコードするHCV cDNAフラグメントを、pYes2-NS3-4Aプラスミドおよび pSEAP2(クロンテック、パロアルト、カリフォルニア)からの重複PCRによる全長分泌型胎盤アルカリホスファターゼ(SEAP)遺伝子に融合し、次いで、アデノウイルス発現ベクター、pアデノウイルス(クロンテック)にサブクローンし、pAd-WT-HCVpro-SEAPを生成させた。HCV NS3−4Aセリンプロテアーゼの活性三つ組み構造における触媒的Ser−139のAla置換をもつこの融合遺伝子の対応するバージョン、pAd-MT-HCVpro-SEAPは、Ser139のAlaへの突然変異を含むpYes2/NS3-4Aを用いる同様の重複PCRとサブクローニング法により生成させた。アデノウイルスは、リポフェクタミン2000(インビトロゲン)の存在下、PacI−直線化pアデノウイルスプラスミド、pAd-WT-HCVpro-SEAPまたはpAd-MT-HCVpro-SEAPにより、HEK293細胞(ATCC、ロックビル、メリーランド)のトランスフェクションにより詰め込んだ。組換えアデノウイルスは、塩化セシウム密度勾配遠心分離により精製し、セントリプレップYM−50フィルター(ミリポア、レッドフォード、マサチューセッツ)でのダイアフィルトレーションにより脱塩した。アデノウイルス・ラピッドタイターキット(クロンテック)を用い、組換えアデノウイルス保存株の感染単位(IFU)の量を定量した。6週令のSCIDマウス(≒20g、チャールス・リバー、ウイルミントン、マサチューセッツ)に、経口強制チューブにより、R異性体が50%以下である式(I)の化合物またはビークルのみを投与した。投与2時間後、組換えアデノウイルス、Ad-WT-HCVpro-SEAPまたはAd-MT-HCVpro-SEAPをマウスの側尾部血管に注射した。
本発明のジアステレオマー化合物の混合物は、該化合物の混合物の治療有効量を被験対象(例:哺乳動物)に送達するために、適当な方法で製剤化することができる。一部の実施態様において、式(I)で示されるジアステレオマー化合物の混合物は、ポリビニルピロリドン(PVP)K−30とラウリル硫酸ナトリウム(SLS)にて製剤化することができる。
ジアステレオマー化合物の混合物:49.5%
PVP K30:49.5%
SLS:1%
本発明について、その詳細な説明と関連して記載してきたが、前記の説明は説明を意図するものであって、本発明の範囲を限定するものではないこと、その範囲は別添の請求項の範囲により限定されるものであることを理解すべきである。その他の側面、有益性、および改変は請求項の範囲内のものである。
Claims (68)
- 式(I):
C*はジアステレオマー炭素原子を表す;そして
C*位置でのR異性体はS異性体に比較して、混合物の50%を超える;
R1は、RW−、P3−、またはP4−L2−P3−である;
Rは所望により置換されている脂肪族基、所望により置換されている環状脂肪族基、所望により置換されているヘテロ環状脂肪族基、所望により置換されているアリール基、または所望により置換されているヘテロアリール基である;
Wは結合、−NR4−、−O−、または−S−である;
R4は、H、所望により置換されている脂肪族基、所望により置換されている環状脂肪族基、所望により置換されているヘテロ環状脂肪族基、所望により置換されているアリール基、または所望により置換されているヘテロアリール基である;
P3−は
Tは、−C(O)−、−OC(O)−、−NHC(O)−、−C(O)C(O)−、または−SO2−である;
R5およびR5'はそれぞれ独立して、H、所望により置換されている脂肪族基、所望により置換されている環状脂肪族基、所望により置換されているヘテロ環状脂肪族基、所望により置換されているフェニル、または所望により置換されているヘテロアリール基である;
R6は、所望により置換されている脂肪族基、所望により置換されているヘテロアリール基、所望により置換されているフェニルである;または
R5およびR6は、それらが結合している原子と一体となって、5員ないし7員の所望により置換されている単環式へテロ環状脂肪族基、または6員ないし12員の所望により置換されている二環式へテロ環状脂肪族基を形成してもよく、各へテロ環状脂肪族環は所望により−O−、−S−または−NR50−から選択されるさらなるヘテロ原子を含む;
R50は、H、所望により置換されている脂肪族基、所望により置換されているヘテロアリール基、または所望により置換されているフェニルである;
P4−L2−P3は
R7およびR7'はそれぞれ独立して、H、所望により置換されている脂肪族基、所望により置換されている環状脂肪族基、所望により置換されているヘテロ環状脂肪族基、所望により置換されているフェニル、または所望により置換されているヘテロアリール基である;または
R7およびR7'は、それらが結合している原子と一体となって、3員ないし7員の環状脂肪族またはヘテロ環状脂肪族環を形成してもよい;または
R7およびR6は、それらが結合している原子と一体となって、5員ないし7員の所望により置換されている単環式へテロ環状脂肪族基、5員ないし7員の所望により置換されている単環式へテロアリール基、6員ないし12員の所望により置換されている二環式へテロ環状脂肪族基、または6員ないし12員の所望により置換されている二環式へテロアリール基を形成してもよく、各へテロ環状脂肪族またはヘテロアリール環は、所望により−O−、−S−または−NR50−から選択されるさらなるヘテロ原子を含む;または
R5およびR6が、それらが結合している原子と一体となって環を形成し得る場合、R7およびR5とR6により形成される環系は、8員ないし14員の所望により置換されている二環式縮合環系を形成してもよく、ここで、該二環式縮合環系は、さらに所望により置換されているフェニルと縮合して、所望により置換されている10員ないし16員の三環式縮合環系を形成してもよい;
R8はHまたは保護基である;そして
R2は所望により置換されている脂肪族基、所望により置換されている環状脂肪族基、所望により置換されているヘテロ環状脂肪族基、所望により置換されているヘテロアリール基、または所望により置換されているフェニルである;
R3は、H、所望により置換されている脂肪族基、所望により置換されている環状脂肪族基、所望により置換されているヘテロ環状脂肪族基、所望により置換されているアリール、または所望により置換されているヘテロアリール基である;
Lは結合、−CF2−、C(O)−、または−SO2−である;
J1、J2、J'2、およびJ3はそれぞれ独立して、ハロゲン、−OR'、−OC(O)N(R')2、−NO2、−CN、−CF3、−OCF3、−R'、オキソ、チオキソ、−N(R')2、−SR'、−COR'、−SO2R'、−SO2N(R')2、−SO3R'、−C(O)R'、−C(O)C(O)R'、−C(O)CH2C(O)R'、−C(S)R'、−C(O)OR'、−OC(O)R'、−C(O)N(R')2、−OC(O)N(R')2、−C(S)N(R')2、−(CH2)0−2NHC(O)R'、−N(R')N(R')COR'、−N(R')N(R')C(O)OR'、−N(R')N(R')CON(R')2、−N(R')SO2R'、−N(R')SO2N(R')2、−N(R')C(O)OR'、−N(R')C(O)R'、−N(R')C(S)R'、−N(R')C(O)N(R')2、−N(R')C(S)N(R')2、−N(COR')COR'、−N(OR')R'、−C(=NH)N(R')2、−C(O)N(OR')R'、−C(=NOR')R'、−OP(O)(OR')2、−P(O)(R')2、−P(O)(OR')2、または−P(O)(H)(OR')であるか、またはJ2およびJ'2の1つはHであり、
ここで、2つのR'基は、それらが結合している原子と一体となって、N、O、またはSから独立して選択される3個までのヘテロ原子を有する3員ないし10員の芳香族または非芳香族環系を形成してもよく、該環は所望によりC6−C10アリール、C5−C10ヘテロアリール、C3−C10シクロアルキル、またはC3−C10ヘテロ環状脂肪族基に縮合しており、そして全ての環がそれぞれ独立してJ2から選択される3個までの置換基を有する;
各R'は独立して、H、C1−C12脂肪族基、C3−C10シクロアルキル基、またはC3−C10シクロアルケニル基、C3−C10シクロアルキル−C1−C12脂肪族基、C3−C10シクロアルケニル−C1−C12脂肪族基、C6−C10アリール基、C6−C10アリール−C1−C12脂肪族基、3員ないし10員のヘテロ環状脂肪族基、6員ないし10員のヘテロ環状脂肪族−C1−C12脂肪族基、5員ないし10員のヘテロアリール基、または5員ないし10員のヘテロアリール−C1−C12脂肪族基から選択され、ここで、R'はそれぞれ独立してJ2から選択される3個までの置換基を有する;または
J1およびJ2は、それらが結合している原子と一体となって、C8ないしC12の所望により置換されている二環式環を形成してもよい;
J1およびJ3は、それらが結合している原子と一体となって、C8ないしC12の所望により置換されている二環式環を形成してもよい;
J2およびJ'2は、それらが結合している原子と一体となって、所望により置換されている5〜10員の環状脂肪族基、または所望により置換されている5〜10員のヘテロ環状脂肪族環を形成してもよい;または
J2およびJ3は、それらが結合している原子と一体となって、C8ないしC12の所望により置換されている二環式環を形成してもよい]
で示されるジアステレオマー化合物の混合物または医薬的に許容されるその塩またはそれらの混合物。 - Lが−C(O)−である請求項6記載のジアステレオマー化合物の混合物。
- R1がRWである請求項1記載のジアステレオマー化合物の混合物。
- Rが所望により置換されている脂肪族基、所望により置換されている環状脂肪族基、所望により置換されているヘテロ環状脂肪族基、所望により置換されているアリール基、または所望により置換されているヘテロアリール基であり、Wが結合、−O−、−S−、または−NR4−である請求項9記載のジアステレオマー化合物の混合物。
- Rが所望により置換されているアリール基または所望により置換されているヘテロアリール基であり、Wが−O−である請求項10記載のジアステレオマー化合物の混合物。
- Rが所望により置換されている脂肪族基または所望により置換されている環状脂肪族基である請求項10記載のジアステレオマー化合物の混合物。
- Rが所望により置換されているアリールアルキルまたは所望により置換されているヘテロアリールアルキルである請求項12記載のジアステレオマー化合物の混合物。
- R1がP3であり、P3が
R6が所望により置換されている脂肪族基、所望により置換されている環状脂肪族基、所望により置換されているヘテロアリール基、所望により置換されているフェニルであるか;または
R5およびR6が、それらが結合している原子と一体となって、5員ないし7員の所望により置換されている単環式へテロ環状基、または6員ないし12員の所望により置換されている二環式へテロ環状基を形成してもよく、ここで、へテロ環状環はそれぞれ、所望により−O−、−S−または−NR50−から選択されるさらなるヘテロ原子を含む;そして
Tが−C(O)−、−OC(O)−、−NHC(O)−、−C(O)C(O)−、または−SO2−である、
請求項6記載のジアステレオマー化合物の混合物。 - Tが−C(O)−である請求項15記載のジアステレオマー化合物の混合物。
- Tが−OC(O)−である請求項15記載のジアステレオマー化合物の混合物。
- Tが−NHC(O)−である請求項15記載のジアステレオマー化合物の混合物。
- Tが−C(O)C(O)−である請求項15記載のジアステレオマー化合物の混合物。
- Tが−SO2−である請求項15記載のジアステレオマー化合物の混合物。
- R1がP4−L2−P3−であり、P4−L2−P3が
R7およびR7'はそれぞれ独立して、H、所望により置換されている脂肪族基、所望により置換されているヘテロアリール基、または所望により置換されているフェニルである;または
R7およびR7'は、それらが結合している原子と一体となって、3員ないし7員の環状脂肪族またはヘテロ環状脂肪族環を形成してもよい;または
R7およびR6は、それらが結合している原子と一体となって、5員ないし7員の所望により置換されている単環式へテロ環状脂肪族基、5員ないし7員の所望により置換されている単環式へテロアリール基、6員ないし12員の所望により置換されている二環式へテロ環状脂肪族基、または6員ないし12員の所望により置換されている二環式へテロアリール基を形成してもよく、各へテロ環状脂肪族またはヘテロアリール環は、所望により−O−、−S−または−NR50−から選択されるさらなるヘテロ原子を含む;または
R5およびR6が、それらが結合している原子と一体となって環を形成し得る場合、R7およびR5とR6により形成される環系は、8員ないし14員の所望により置換されている二環式縮合環系を形成してもよく、ここで、該二環式縮合環系は、さらに所望により置換されているフェニルと縮合して、所望により置換されている10員ないし16員の三環式縮合環系を形成してもよい;
R8はHまたは保護基である;
R50は、H、所望により置換されている脂肪族基、所望により置換されているヘテロアリール基、または所望により置換されているフェニルである]
である請求項6記載のジアステレオマー化合物の混合物。 - R7'がHであり;R7がC1−C6アルキル、C3−C10シクロアルキル、C3−C10シクロアルキル−C1−C12アルキル、C6−C10アリール、C6−C10アリール−C1−C6アルキル、3員ないし10員のヘテロ環状脂肪族基、6員ないし10員のヘテロ環状脂肪族−C1−C12アルキル、5員ないし10員のヘテロアリール、または5員ないし10員のヘテロアリール−C1−C12アルキルである請求項21記載のジアステレオマー化合物の混合物。
- R7およびR7'が、それらが結合している原子と一体となって、3員ないし7員の所望により置換されている環状脂肪族環を形成する請求項21記載のジアステレオマー化合物の混合物。
- Rが、
R10はH、C1−12脂肪族基、C6−10アリール、C6−10アリール−C1−12脂肪族基、C3−10シクロアルキル、C3−10シクロアルケニル、C3−10シクロアルキル−C1−12脂肪族基、C3−10シクロアルケニル−C1−12脂肪族基、3員ないし10員のヘテロ環状脂肪族基、6員ないし10員のヘテロ環状脂肪族−C1−12脂肪族基、5員ないし10員のヘテロアリール、または5員ないし10員のヘテロアリール−C1−12脂肪族基である;
Kは結合、C1−12脂肪族基、−O−、−S−、−NR9−、−C(O)−、または−C(O)NR9−である(ここで、R9はHまたはC1−12脂肪族基である);そして
mは1、2、または3である]
である請求項22記載のジアステレオマー化合物の混合物。 - Rが、
Z2はO、S、NR10、またはC(R10)2である;
R10はそれぞれ独立して、H、C1−12脂肪族基、C6−10アリール、C6−10アリール−C1−12脂肪族基、C3−10シクロアルキル、C3−10シクロアルケニル、C3−10シクロアルキル−C1−12脂肪族基、C3−10シクロアルケニル−C1−12脂肪族基、3員ないし10員のヘテロ環状脂肪族基、6員ないし10員のヘテロ環状脂肪族−C1−12脂肪族基、5員ないし10員のヘテロアリール、または5員ないし10員のヘテロアリール−C1−12脂肪族基である;
pは1または2である;そして
----- は単結合または二重結合である]
である請求項22記載のジアステレオマー化合物の混合物。 - Tが結合であり、Rが所望により置換されている(ヘテロ環状脂肪族)脂肪族基である請求項21記載のジアステレオマー化合物の混合物。
- Tが結合であり、Rが所望により置換されているアリールまたは所望により置換されているヘテロアリールである請求項21記載のジアステレオマー化合物の混合物。
- Tが−C(O)−であり、Rが−NR4−である請求項21記載のジアステレオマー化合物の混合物。
- R2が所望により置換されている脂肪族基、所望により置換されているフェニル、所望により置換されている環状脂肪族基、または所望により置換されているヘテロ環状脂肪族基である請求項1記載のジアステレオマー化合物の混合物。
- R2がn−プロピルである請求項34記載のジアステレオマー化合物の混合物。
- R3が所望により置換されているC1−C7脂肪族基、所望により置換されている環状脂肪族基、所望により置換されているアリール、または所望により置換されているヘテロアリールである請求項1記載のジアステレオマー化合物の混合物。
- R3が所望により置換されているC1−C6アルキルまたは所望により置換されているC1−C6シクロアルキルである請求項37記載のジアステレオマー化合物の混合物。
- R3がシクロプロピルである請求項39記載のジアステレオマー化合物の混合物。
- 該混合物中のR異性体の割合が60%を超えるものである請求項41記載のジアステレオマー化合物の混合物。
- 該混合物中のR異性体の割合が70%を超えるものである請求項42記載のジアステレオマー化合物の混合物。
- 該混合物中のR異性体の割合が80%を超えるものである請求項43記載のジアステレオマー化合物の混合物。
- 該混合物中のR異性体の割合が90%を超えるものである請求項44記載のジアステレオマー化合物の混合物。
- 該混合物中のR異性体の割合が95%を超えるものである請求項45記載のジアステレオマー化合物の混合物。
- 該混合物中のR異性体の割合が98%を超えるものである請求項46記載のジアステレオマー化合物の混合物。
- 該混合物中のR異性体の割合が99%を超えるものである請求項47記載のジアステレオマー化合物の混合物。
- セリンプロテアーゼを阻害するのに有効な量の請求項1に記載のジアステレオマー化合物の混合物と、許容される担体、アジュバントまたはビークルとを含有してなる医薬組成物。
- セリンプロテアーゼを阻害するのに有効な量の請求項41に記載のジアステレオマー化合物の混合物と、許容される担体、アジュバントまたはビークルとを含有してなる医薬組成物。
- 当該組成物が患者に投与するために製剤化したものである請求項50に記載の組成物。
- 免疫調節剤、抗ウイルス剤、HCVプロテアーゼの第二インヒビター、HCVライフサイクルにおける別の標的のインヒビター、およびシトクロームP−450インヒビター、またはそのいずれかの組合わせをさらに含有してなる請求項50に記載の組成物。
- 当該免疫調節剤がα−、β−、もしくはγ−インターフェロンまたはチモシンであり;当該抗ウイルス剤がリバビリン、アマンタジン、またはテルビブジンであり;または当該HCVライフサイクルにおける別の標的のインヒビターがHCVヘリカーゼ、ポリメラーゼ、またはメタロプロテアーゼのインヒビターである請求項51に記載の組成物。
- 当該シトクロームP−450インヒビターがリトナビルである請求項52に記載の組成物。
- セリンプロテアーゼの活性を阻害する方法であって、当該セリンプロテアーゼと、請求項1に記載のジアステレオマー化合物の混合物または請求項49に記載の組成物の医薬的に有効な量とを接触させるステップを含む方法。
- セリンプロテアーゼの活性を阻害する方法であって、当該セリンプロテアーゼと、請求項41に記載のジアステレオマー化合物の混合物または請求項50に記載の組成物の医薬的に有効な量とを接触させるステップを含む方法。
- 当該セリンプロテアーゼがHCV NS3プロテアーゼである請求項56に記載の方法。
- 患者のHCV感染を処置する方法であって、請求項1に記載のジアステレオマー化合物の混合物または請求項49に記載の組成物の医薬的に有効な量を当該患者に投与するステップを含む方法。
- 患者のHCV感染を処置する方法であって、請求項41に記載のジアステレオマー化合物の混合物または請求項50に記載の組成物の医薬的に有効な量を当該患者に投与するステップを含む方法。
- さらに、免疫調節剤、抗ウイルス剤、HCVプロテアーゼの第二インヒビター、HCVライフサイクルにおける別の標的のインヒビター、またはその組合わせから選択されるさらなる薬剤を当該患者に投与するさらなるステップ(ここで、当該さらなる薬剤を請求項49に記載の当該組成物の一部として、または別個の投与形態として当該患者に投与する)を含む請求項59に記載の方法。
- 当該免疫調節剤がα−、β−、もしくはγ−インターフェロンまたはチモシンであり;当該抗ウイルス剤がリバビリンまたはアマンタジンであり;または当該HCVライフサイクルにおける別の標的のインヒビターがHCVヘリカーゼ、ポリメラーゼ、またはメタロプロテアーゼのインヒビターである請求項60に記載の方法。
- 生体サンプルまたは医療用もしくは実験用機器のHCV汚染を除去または低減する方法であって、当該生体サンプルまたは医療用もしくは実験用機器を、請求項1に記載のジアステレオマー化合物の混合物または請求項49に記載の組成物と接触させるステップを含む方法。
- 生体サンプルまたは医療用もしくは実験用機器のHCV汚染を除去または低減する方法であって、当該生体サンプルまたは医療用もしくは実験用機器を、請求項41に記載のジアステレオマー化合物の混合物または請求項50に記載の組成物と接触させるステップを含む方法。
- 当該サンプルまたは器具が、血液、他の体液、生体組織、手術器具、手術着、実験用機器、実験着、血液または他の体液の収集用具、血液または他の体液の貯蔵用具から選択されるものである請求項63に記載の方法。
- 当該体液が血液である請求項64に記載の方法。
- 化合物 (1S,3aR,6aS)−2−[(2S)−2−[[(2S)−2−シクロヘキシル−1−オキソ−2−[(ピラジニルカルボニル)アミノ]エチル]アミノ]−3,3−ジメチル−1−オキソブチル]−N−[(1R)−1−[2−(シクロプロピルアミノ)−1,2−ジオキソエチル]ブチル]オクタヒドロ−シクロペンタ[c]ピロール−1−カルボキサミド。
- セリンプロテアーゼを阻害するのに有効な量の請求項66に記載の化合物、および許容される担体、アジュバントまたはビークルを含有してなる医薬組成物。
- セリンプロテアーゼの活性を阻害する方法であって、当該セリンプロテアーゼと、請求項66に記載の化合物または請求項67に記載の組成物とを接触させるステップを含む方法。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US70477205P | 2005-08-02 | 2005-08-02 | |
| PCT/US2006/029988 WO2007016589A2 (en) | 2005-08-02 | 2006-08-01 | Inhibitors of serine proteases |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2009505966A true JP2009505966A (ja) | 2009-02-12 |
| JP2009505966A5 JP2009505966A5 (ja) | 2009-12-24 |
Family
ID=37654834
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2008525128A Pending JP2009505966A (ja) | 2005-08-02 | 2006-08-01 | セリンプロテアーゼのインヒビター |
Country Status (17)
| Country | Link |
|---|---|
| US (4) | US20070105781A1 (ja) |
| EP (3) | EP1910341B1 (ja) |
| JP (1) | JP2009505966A (ja) |
| KR (1) | KR20080033481A (ja) |
| CN (1) | CN101277950B (ja) |
| AR (1) | AR057716A1 (ja) |
| AU (1) | AU2006275413B2 (ja) |
| CA (1) | CA2617679A1 (ja) |
| ES (1) | ES2401661T3 (ja) |
| IL (1) | IL189192A0 (ja) |
| MX (1) | MX2008001528A (ja) |
| NO (1) | NO20081012L (ja) |
| NZ (1) | NZ565540A (ja) |
| RU (2) | RU2441020C2 (ja) |
| TW (1) | TW200740813A (ja) |
| WO (1) | WO2007016589A2 (ja) |
| ZA (1) | ZA200801114B (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2018092724A1 (ja) * | 2016-11-15 | 2018-05-24 | 学校法人東京理科大学 | 分子動態評価方法及びスクリーニング方法 |
Families Citing this family (54)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| PL192280B1 (pl) * | 1996-10-18 | 2006-09-29 | Vertex Pharma | Inhibitory proteaz serynowych, a zwłaszcza proteazy wirusa NS3 zapalenia wątroby C, kompozycja farmaceutyczna i zastosowania |
| SV2003000617A (es) * | 2000-08-31 | 2003-01-13 | Lilly Co Eli | Inhibidores de la proteasa peptidomimetica ref. x-14912m |
| UY28500A1 (es) * | 2003-09-05 | 2005-04-29 | Vertex Pharma | Inhibidores de proteasas de serina, en particular proteasa ns3-ns4a del vhc. |
| CN101263156A (zh) | 2005-07-25 | 2008-09-10 | 因特蒙公司 | C型肝炎病毒复制的新颖大环抑制剂 |
| EP1910341B1 (en) * | 2005-08-02 | 2013-01-02 | Vertex Pharmaceuticals Incorporated | Inhibitors of serine proteases |
| US8399615B2 (en) | 2005-08-19 | 2013-03-19 | Vertex Pharmaceuticals Incorporated | Processes and intermediates |
| AR055395A1 (es) * | 2005-08-26 | 2007-08-22 | Vertex Pharma | Compuestos inhibidores de la actividad de la serina proteasa ns3-ns4a del virus de la hepatitis c |
| US7964624B1 (en) * | 2005-08-26 | 2011-06-21 | Vertex Pharmaceuticals Incorporated | Inhibitors of serine proteases |
| EP2340836A1 (en) * | 2006-02-27 | 2011-07-06 | Vertex Pharmceuticals Incorporated | Co-crystals comprising VX-950 and their pharmaceutical compositions |
| CA2646229A1 (en) | 2006-03-16 | 2007-09-27 | Vertex Pharmaceuticals Incorporated | Deuterated hepatitis c protease inhibitors |
| CA2647158C (en) * | 2006-03-23 | 2012-07-31 | Schering Corporation | Combinations of hcv protease inhibitor(s) and cyp3a4 inhibitor(s), and methods of treatment related thereto |
| WO2007133865A2 (en) | 2006-04-11 | 2007-11-22 | Novartis Ag | Hcv/hiv inhibitors an their uses |
| CA2679426A1 (en) * | 2007-02-27 | 2008-09-04 | Luc Farmer | Inhibitors of serine proteases |
| AP2009004960A0 (en) * | 2007-02-27 | 2009-08-31 | Vertex Pharma | Co-crystals and pharmaceutical compositions comprising the same |
| JP5443360B2 (ja) * | 2007-08-30 | 2014-03-19 | バーテックス ファーマシューティカルズ インコーポレイテッド | 共結晶体およびそれを含む医薬組成物 |
| CN104016970A (zh) | 2007-10-10 | 2014-09-03 | 诺华股份有限公司 | 螺环吡咯烷类与其对抗hcv和hiv感染的应用 |
| ES2437147T3 (es) * | 2008-02-04 | 2014-01-09 | Idenix Pharmaceuticals, Inc. | Inhibidores de serina proteasa macrocíclicos |
| CA2740728A1 (en) * | 2008-10-15 | 2010-04-22 | Intermune, Inc. | Therapeutic antiviral peptides |
| AR074670A1 (es) * | 2008-12-19 | 2011-02-02 | Gilead Sciences Inc | Inhibidores de la proteasa ns3 del vhc virus de la hepatitis c |
| US8102720B2 (en) * | 2009-02-02 | 2012-01-24 | Qualcomm Incorporated | System and method of pulse generation |
| TWI519530B (zh) | 2009-02-20 | 2016-02-01 | 艾伯維德國有限及兩合公司 | 羰醯胺化合物及其作為鈣蛋白酶(calpain)抑制劑之用途 |
| EP2403860B1 (en) | 2009-03-04 | 2015-11-04 | IDENIX Pharmaceuticals, Inc. | Phosphothiophene and phosphothiazole as hcv polymerase inhibitors |
| CA2758072A1 (en) | 2009-04-08 | 2010-10-14 | Idenix Pharmaceuticals, Inc. | Macrocyclic serine protease inhibitors |
| US8512690B2 (en) | 2009-04-10 | 2013-08-20 | Novartis Ag | Derivatised proline containing peptide compounds as protease inhibitors |
| US8236798B2 (en) | 2009-05-07 | 2012-08-07 | Abbott Gmbh & Co. Kg | Carboxamide compounds and their use as calpain inhibitors |
| US20120244122A1 (en) * | 2009-05-28 | 2012-09-27 | Masse Craig E | Peptides for the Treatment of HCV Infections |
| TW201117812A (en) | 2009-08-05 | 2011-06-01 | Idenix Pharmaceuticals Inc | Macrocyclic serine protease inhibitors |
| CN105001302A (zh) * | 2009-09-28 | 2015-10-28 | 英特穆恩公司 | C型肝炎病毒复制的环肽抑制剂 |
| WO2011041551A1 (en) * | 2009-10-01 | 2011-04-07 | Intermune, Inc. | Therapeutic antiviral peptides |
| US20110117055A1 (en) | 2009-11-19 | 2011-05-19 | Macdonald James E | Methods of Treating Hepatitis C Virus with Oxoacetamide Compounds |
| US8362068B2 (en) | 2009-12-18 | 2013-01-29 | Idenix Pharmaceuticals, Inc. | 5,5-fused arylene or heteroarylene hepatitis C virus inhibitors |
| US9051304B2 (en) | 2009-12-22 | 2015-06-09 | AbbVie Deutschland GmbH & Co. KG | Carboxamide compounds and their use as calpain inhibitors V |
| US8598211B2 (en) | 2009-12-22 | 2013-12-03 | Abbvie Inc. | Carboxamide compounds and their use as calpain inhibitors IV |
| CA2819087A1 (en) | 2010-12-09 | 2012-06-14 | AbbVie Deutschland GmbH & Co. KG | Carboxamide compounds and their use as calpain inhibitors v |
| SG191844A1 (en) | 2011-01-04 | 2013-08-30 | Novartis Ag | Indole compounds or analogues thereof useful for the treatment of age-related macular degeneration (amd) |
| AR085352A1 (es) | 2011-02-10 | 2013-09-25 | Idenix Pharmaceuticals Inc | Inhibidores macrociclicos de serina proteasa, sus composiciones farmaceuticas y su uso para tratar infecciones por hcv |
| US20120252721A1 (en) | 2011-03-31 | 2012-10-04 | Idenix Pharmaceuticals, Inc. | Methods for treating drug-resistant hepatitis c virus infection with a 5,5-fused arylene or heteroarylene hepatitis c virus inhibitor |
| SE1450130A1 (sv) | 2011-10-21 | 2014-05-07 | Abbvie Inc | Förfaranden för att behandla hcv innefattande minst två direktverkande antivirala agenser, ribavirin men inte interferon |
| AU2013201532B2 (en) | 2011-10-21 | 2014-10-02 | Abbvie Ireland Unlimited Company | Methods for treating HCV |
| US8466159B2 (en) | 2011-10-21 | 2013-06-18 | Abbvie Inc. | Methods for treating HCV |
| US8492386B2 (en) | 2011-10-21 | 2013-07-23 | Abbvie Inc. | Methods for treating HCV |
| WO2013072328A1 (en) | 2011-11-14 | 2013-05-23 | Sanofi | Use of telaprevir and related compounds in atherosclerosis, heart failure, renal diseases, liver diseases or inflammatory diseases |
| CN104364247A (zh) | 2012-04-03 | 2015-02-18 | 艾伯维德国有限责任两合公司 | 甲酰胺化合物及它们作为钙蛋白酶抑制剂v的用途 |
| US9464081B2 (en) | 2012-06-28 | 2016-10-11 | Novartis Ag | Pyrrolidine derivatives and their use as complement pathway modulators |
| ES2644700T3 (es) | 2012-06-28 | 2017-11-30 | Novartis Ag | Derivados de pirrolidina y su uso como moduladores de la ruta del complemento |
| EP2867225B1 (en) | 2012-06-28 | 2017-08-09 | Novartis AG | Pyrrolidine derivatives and their use as complement pathway modulators |
| US9815819B2 (en) | 2012-06-28 | 2017-11-14 | Novartis Ag | Complement pathway modulators and uses thereof |
| EP2867227B1 (en) | 2012-06-28 | 2018-11-21 | Novartis AG | Complement pathway modulators and uses thereof |
| EP2872503B1 (en) | 2012-07-12 | 2018-06-20 | Novartis AG | Complement pathway modulators and uses thereof |
| WO2014053533A1 (en) | 2012-10-05 | 2014-04-10 | Sanofi | Use of substituted 3-heteroaroylamino-propionic acid derivatives as pharmaceuticals for prevention/treatment of atrial fibrillation |
| WO2015042375A1 (en) | 2013-09-20 | 2015-03-26 | Idenix Pharmaceuticals, Inc. | Hepatitis c virus inhibitors |
| US20170135990A1 (en) | 2014-03-05 | 2017-05-18 | Idenix Pharmaceuticals Llc | Pharmaceutical compositions comprising a 5,5-fused heteroarylene flaviviridae inhibitor and their use for treating or preventing flaviviridae infection |
| US20170066779A1 (en) | 2014-03-05 | 2017-03-09 | Idenix Pharmaceuticals Llc | Solid forms of a flaviviridae virus inhibitor compound and salts thereof |
| CA3022119A1 (en) | 2016-04-28 | 2017-11-02 | Emory University | Alkyne containing nucleotide and nucleoside therapeutic compositions and uses related thereto |
Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1996011697A1 (en) * | 1994-10-12 | 1996-04-25 | Merck & Co., Inc. | Thrombin inhibitors |
| WO2002008244A2 (en) * | 2000-07-21 | 2002-01-31 | Schering Corporation | Peptides as ns3-serine protease inhibitors of hepatitis c virus |
| WO2002018369A2 (en) * | 2000-08-31 | 2002-03-07 | Eli Lilly And Company | Peptidomimetic protease inhibitors |
| WO2003087092A2 (en) * | 2002-04-11 | 2003-10-23 | Vertex Pharmaceuticals Incorporated | Inhibitors of serine proteases, particularly hepatitis c virus ns3 - ns4 protease |
| WO2005007681A2 (en) * | 2003-07-18 | 2005-01-27 | Vertex Pharmaceuticals Incorporated | Inhibitors of serine proteases, particularly hcv ns3-ns4a protease |
| WO2005035525A2 (en) * | 2003-09-05 | 2005-04-21 | Vertex Pharmaceuticals Incorporated | 2-amido-4-aryloxy-1-carbonylpyrrolidine derivatives as inhibitors of serine proteases, particularly hcv ns3-ns4a protease |
| WO2005042570A1 (en) * | 2003-10-27 | 2005-05-12 | Vertex Pharmaceuticals Incorporated | Hcv ns3-ns4a protease resistance mutants |
Family Cites Families (101)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4499082A (en) * | 1983-12-05 | 1985-02-12 | E. I. Du Pont De Nemours And Company | α-Aminoboronic acid peptides |
| FR2575753B1 (fr) * | 1985-01-07 | 1987-02-20 | Adir | Nouveaux derives peptidiques a structure polycyclique azotee, leur procede de preparation et les compositions pharmaceutiques qui les contiennent |
| US5496927A (en) * | 1985-02-04 | 1996-03-05 | Merrell Pharmaceuticals Inc. | Peptidase inhibitors |
| US5736520A (en) * | 1988-10-07 | 1998-04-07 | Merrell Pharmaceuticals Inc. | Peptidase inhibitors |
| EP0604182B1 (en) * | 1992-12-22 | 2000-10-11 | Eli Lilly And Company | Inhibitors of HIV protease useful for the treatment of Aids |
| ATE230402T1 (de) | 1992-12-29 | 2003-01-15 | Abbott Lab | Hemmer der retroviralen protease |
| US5384410A (en) * | 1993-03-24 | 1995-01-24 | The Du Pont Merck Pharmaceutical Company | Removal of boronic acid protecting groups by transesterification |
| IL110752A (en) * | 1993-09-13 | 2000-07-26 | Abbott Lab | Liquid semi-solid or solid pharmaceutical composition for an HIV protease inhibitor |
| US5559158A (en) * | 1993-10-01 | 1996-09-24 | Abbott Laboratories | Pharmaceutical composition |
| IL111991A (en) | 1994-01-28 | 2000-07-26 | Abbott Lab | Liquid pharmaceutical composition of HIV protease inhibitors in organic solvent |
| US5756466A (en) * | 1994-06-17 | 1998-05-26 | Vertex Pharmaceuticals, Inc. | Inhibitors of interleukin-1β converting enzyme |
| US5716929A (en) * | 1994-06-17 | 1998-02-10 | Vertex Pharmaceuticals, Inc. | Inhibitors of interleukin-1β converting enzyme |
| US5861267A (en) * | 1995-05-01 | 1999-01-19 | Vertex Pharmaceuticals Incorporated | Methods, nucleotide sequences and host cells for assaying exogenous and endogenous protease activity |
| US6037157A (en) | 1995-06-29 | 2000-03-14 | Abbott Laboratories | Method for improving pharmacokinetics |
| US6060469A (en) * | 1995-11-23 | 2000-05-09 | Merck Sharp & Dohme Ltd. | Spiro-piperidine derivatives and their use as tachykinin antagonists |
| US5807876A (en) * | 1996-04-23 | 1998-09-15 | Vertex Pharmaceuticals Incorporated | Inhibitors of IMPDH enzyme |
| US6054472A (en) | 1996-04-23 | 2000-04-25 | Vertex Pharmaceuticals, Incorporated | Inhibitors of IMPDH enzyme |
| ZA972195B (en) * | 1996-03-15 | 1998-09-14 | Du Pont Merck Pharma | Spirocycle integrin inhibitors |
| CN1515248A (zh) | 1996-04-23 | 2004-07-28 | ��̩��˹ҩ��ɷ�����˾ | 用作肌苷-5'-一磷酸脱氢酶抑制剂的脲衍生物 |
| AU2933797A (en) | 1996-05-10 | 1997-12-05 | Schering Corporation | Synthetic inhibitors of hepatitis c virus ns3 protease |
| US6046195A (en) * | 1996-09-25 | 2000-04-04 | Merck Sharp & Dohme Ltd. | Spiro-azacyclic derivatives, their preparation and their use as tachykinin antagonists |
| US6348608B1 (en) * | 1996-10-08 | 2002-02-19 | Yian Shi | Catalytic asymmetric epoxidation |
| PL192280B1 (pl) | 1996-10-18 | 2006-09-29 | Vertex Pharma | Inhibitory proteaz serynowych, a zwłaszcza proteazy wirusa NS3 zapalenia wątroby C, kompozycja farmaceutyczna i zastosowania |
| GB9623908D0 (en) | 1996-11-18 | 1997-01-08 | Hoffmann La Roche | Amino acid derivatives |
| DE19648011A1 (de) * | 1996-11-20 | 1998-05-28 | Bayer Ag | Cyclische Imine |
| PT966465E (pt) | 1997-03-14 | 2003-11-28 | Vertex Pharma | Inibidores do enzima imfdh |
| GB9707659D0 (en) | 1997-04-16 | 1997-06-04 | Peptide Therapeutics Ltd | Hepatitis C NS3 Protease inhibitors |
| GB9708484D0 (en) * | 1997-04-25 | 1997-06-18 | Merck Sharp & Dohme | Therapeutic agents |
| GB9711114D0 (en) * | 1997-05-29 | 1997-07-23 | Merck Sharp & Dohme | Therapeutic agents |
| IL134233A0 (en) | 1997-08-11 | 2001-04-30 | Boehringer Ingelheim Ca Ltd | Hepatitis c inhibitor peptide analogues |
| AU757783B2 (en) | 1997-08-11 | 2003-03-06 | Boehringer Ingelheim (Canada) Ltd. | Hepatitis C inhibitor peptides |
| US6767991B1 (en) * | 1997-08-11 | 2004-07-27 | Boehringer Ingelheim (Canada) Ltd. | Hepatitis C inhibitor peptides |
| US6183121B1 (en) * | 1997-08-14 | 2001-02-06 | Vertex Pharmaceuticals Inc. | Hepatitis C virus helicase crystals and coordinates that define helicase binding pockets |
| US20040058982A1 (en) * | 1999-02-17 | 2004-03-25 | Bioavailability System, Llc | Pharmaceutical compositions |
| US20020017295A1 (en) * | 2000-07-07 | 2002-02-14 | Weers Jeffry G. | Phospholipid-based powders for inhalation |
| AU1416099A (en) * | 1997-11-28 | 1999-06-16 | Schering Corporation | Single-chain recombinant complexes of hepatitis c virus ns3 protease and ns4a cofactor peptide |
| IT1299134B1 (it) | 1998-02-02 | 2000-02-29 | Angeletti P Ist Richerche Bio | Procedimento per la produzione di peptidi con proprieta' inibitrici della proteasi ns3 del virus hcv, peptidi cosi' ottenibili e peptidi |
| JP4690545B2 (ja) * | 1998-03-31 | 2011-06-01 | バーテックス ファーマシューティカルズ インコーポレイテッド | セリンプロテアーゼ、特にc型肝炎ウイルスns3プロテアーゼの阻害因子 |
| US6251583B1 (en) * | 1998-04-27 | 2001-06-26 | Schering Corporation | Peptide substrates for HCV NS3 protease assays |
| GB9812523D0 (en) | 1998-06-10 | 1998-08-05 | Angeletti P Ist Richerche Bio | Peptide inhibitors of hepatitis c virus ns3 protease |
| US6323180B1 (en) * | 1998-08-10 | 2001-11-27 | Boehringer Ingelheim (Canada) Ltd | Hepatitis C inhibitor tri-peptides |
| DE19836514A1 (de) | 1998-08-12 | 2000-02-17 | Univ Stuttgart | Modifikation von Engineeringpolymeren mit N-basischen Gruppe und mit Ionenaustauschergruppen in der Seitenkette |
| US6117639A (en) * | 1998-08-31 | 2000-09-12 | Vertex Pharmaceuticals Incorporated | Fusion proteins, DNA molecules, vectors, and host cells useful for measuring protease activity |
| US6025516A (en) * | 1998-10-14 | 2000-02-15 | Chiragene, Inc. | Resolution of 2-hydroxy-3-amino-3-phenylpropionamide and its conversion to C-13 sidechain of taxanes |
| GB9825946D0 (en) | 1998-11-26 | 1999-01-20 | Angeletti P Ist Richerche Bio | Pharmaceutical compounds for the inhibition of hepatitis C virus NS3 protease |
| ATE400251T1 (de) * | 1999-02-09 | 2008-07-15 | Pfizer Prod Inc | Zusammensetzungen basischer arzneistoffe mit verbesserter bioverfügbarkeit |
| US20020042046A1 (en) * | 1999-02-25 | 2002-04-11 | Vertex Pharmaceuticals, Incorporated | Crystallizable compositions comprising a hepatitis C virus NS3 protease domain/NS4A complex |
| AP1498A (en) | 1999-03-19 | 2005-11-21 | Vertex Pharma | Inhibitors of impdh enzyme. |
| US6608027B1 (en) * | 1999-04-06 | 2003-08-19 | Boehringer Ingelheim (Canada) Ltd | Macrocyclic peptides active against the hepatitis C virus |
| UA74546C2 (en) | 1999-04-06 | 2006-01-16 | Boehringer Ingelheim Ca Ltd | Macrocyclic peptides having activity relative to hepatitis c virus, a pharmaceutical composition and use of the pharmaceutical composition |
| US7122627B2 (en) * | 1999-07-26 | 2006-10-17 | Bristol-Myers Squibb Company | Lactam inhibitors of Hepatitis C virus NS3 protease |
| CA2376961A1 (en) | 1999-07-26 | 2001-02-01 | Bristol-Myers Squibb Pharma Company | Lactam inhibitors of hepatitis c virus ns3 protease |
| EP1261611A2 (en) * | 2000-02-29 | 2002-12-04 | Bristol-Myers Squibb Pharma Company | Inhibitors of hepatitis c virus ns3 protease |
| EP1268519B1 (en) * | 2000-04-03 | 2005-06-15 | Vertex Pharmaceuticals Incorporated | Inhibitors of serine proteases, particularly hepatitis c virus ns3 protease |
| JP4748911B2 (ja) * | 2000-04-05 | 2011-08-17 | シェーリング コーポレイション | N−環状p2部分を含むc型肝炎ウイルスの大環状ns3‐セリンプロテアーゼ阻害剤 |
| RU2002131163A (ru) | 2000-04-19 | 2004-06-27 | Шеринг Корпорейшн (US) | Макроциклические ингибиторы ns3-серинпротезы вируса гепатита с, содержащие алкил- и арилаланиновые p2 фрагменты |
| AR034127A1 (es) | 2000-07-21 | 2004-02-04 | Schering Corp | Imidazolidinonas como inhibidores de ns3-serina proteasa del virus de hepatitis c, composicion farmaceutica, un metodo para su preparacion, y el uso de las mismas para la manufactura de un medicamento |
| JP4452441B2 (ja) | 2000-07-21 | 2010-04-21 | シェーリング コーポレイション | C型肝炎ウイルスのns3−セリンプロテアーゼ阻害剤としての新規ペプチド |
| AR029851A1 (es) | 2000-07-21 | 2003-07-16 | Dendreon Corp | Nuevos peptidos como inhibidores de ns3-serina proteasa del virus de hepatitis c |
| CA2418199A1 (en) * | 2000-07-21 | 2002-01-31 | Corvas International, Inc. | Peptides as ns3-serine protease inhibitors of hepatitis c virus |
| GB0021286D0 (en) | 2000-08-30 | 2000-10-18 | Gemini Genomics Ab | Identification of drug metabolic capacity |
| US6846806B2 (en) * | 2000-10-23 | 2005-01-25 | Bristol-Myers Squibb Company | Peptide inhibitors of Hepatitis C virus NS3 protein |
| MXPA03004299A (es) | 2000-11-20 | 2004-02-12 | Bristol Myers Squibb Co | Inhibidores de tripeptido de hepatitis c. |
| US6653295B2 (en) * | 2000-12-13 | 2003-11-25 | Bristol-Myers Squibb Company | Inhibitors of hepatitis C virus NS3 protease |
| WO2002048157A2 (en) | 2000-12-13 | 2002-06-20 | Bristol-Myers Squibb Pharma Company | Imidazolidinones and their related derivatives as hepatitis c virus ns3 protease inhibitors |
| WO2002048116A2 (en) | 2000-12-13 | 2002-06-20 | Bristol-Myers Squibb Pharma Company | Inhibitors of hepatitis c virus ns3 protease |
| US6777395B2 (en) * | 2001-01-22 | 2004-08-17 | Merck & Co., Inc. | Nucleoside derivatives as inhibitors of RNA-dependent RNA viral polymerase of hepatitis C virus |
| GB0102342D0 (en) * | 2001-01-30 | 2001-03-14 | Smithkline Beecham Plc | Pharmaceutical formulation |
| GB0107924D0 (en) * | 2001-03-29 | 2001-05-23 | Angeletti P Ist Richerche Bio | Inhibitor of hepatitis C virus NS3 protease |
| JP2005500322A (ja) * | 2001-07-03 | 2005-01-06 | アルタナ ファルマ アクチエンゲゼルシャフト | 3−フェニルイソセリンの製法 |
| US6909000B2 (en) | 2001-07-11 | 2005-06-21 | Vertex Pharmaceuticals Incorporated | Bridged bicyclic serine protease inhibitors |
| US6824769B2 (en) * | 2001-08-28 | 2004-11-30 | Vertex Pharmaceuticals Incorporated | Optimal compositions and methods thereof for treating HCV infections |
| NZ531681A (en) * | 2001-10-24 | 2007-05-31 | Vertex Pharma | Inhibitors of serine protease, particularly hepatitis C virus NS3-NS4A protease, incorporating a fused ring system |
| CA2465597A1 (en) * | 2001-11-14 | 2003-06-12 | Ben Zion Dolitzky | Amorphous and crystalline forms of losartan potassium and process for their preparation |
| AU2003257157C1 (en) * | 2002-08-01 | 2010-03-18 | Pharmasset Inc. | Compounds with the bicyclo[4.2.1] nonane system for the treatment of Flaviviridae infections |
| WO2004013298A2 (en) * | 2002-08-01 | 2004-02-12 | Pharmasset Ltd. | 2',3'-dideoxynucleoside analogues for the treatment or prevention of flavivitridae infections |
| US20050075279A1 (en) * | 2002-10-25 | 2005-04-07 | Boehringer Ingelheim International Gmbh | Macrocyclic peptides active against the hepatitis C virus |
| CA2413705A1 (en) * | 2002-12-06 | 2004-06-06 | Raul Altman | Use of meloxicam in combination with an antiplatelet agent for treatment of acute coronary syndrome and related conditions |
| CN1771050A (zh) | 2003-02-07 | 2006-05-10 | 益安药业 | 丙型肝炎丝氨酸蛋白酶的大环抑制剂 |
| US20040180815A1 (en) * | 2003-03-07 | 2004-09-16 | Suanne Nakajima | Pyridazinonyl macrocyclic hepatitis C serine protease inhibitors |
| WO2004092161A1 (en) * | 2003-04-11 | 2004-10-28 | Vertex Pharmaceuticals Incorporated | Inhibitors of serine proteases, particularly hcv ns3-ns4a protease |
| EP1636208B1 (en) * | 2003-04-11 | 2012-02-29 | Vertex Pharmaceuticals Incorporated | Inhibitors of serine proteases, particularly hcv ns3-ns4a protease |
| MY143076A (en) * | 2003-05-21 | 2011-02-28 | Boehringer Ingelheim Int | Hepatitis c inhibitors compounds |
| WO2005018330A1 (en) * | 2003-08-18 | 2005-03-03 | Pharmasset, Inc. | Dosing regimen for flaviviridae therapy |
| TW200518669A (en) * | 2003-09-12 | 2005-06-16 | Vertex Pharma | Animal model for protease activity and liver damage |
| AR045769A1 (es) * | 2003-09-18 | 2005-11-09 | Vertex Pharma | Inhibidores de las serina proteasas, particularmente, la proteasa ns3-ns4a del vhc (virus hepatitis c) |
| US6933760B2 (en) * | 2003-09-19 | 2005-08-23 | Intel Corporation | Reference voltage generator for hysteresis circuit |
| CA2536182C (en) * | 2003-09-22 | 2012-07-24 | Boehringer Ingelheim International Gmbh | Macrocyclic peptides active against the hepatitis c virus |
| EP2361925A1 (en) * | 2003-10-10 | 2011-08-31 | Vertex Pharmaceuticals Incorporated | Inhibitors of serine proteases, particularly HCV NS3-NS4A protease |
| AR045870A1 (es) * | 2003-10-11 | 2005-11-16 | Vertex Pharma | Terapia de combinacion para la infeccion de virus de hepatitis c |
| PT1677827E (pt) * | 2003-10-27 | 2009-03-13 | Vertex Pharma | Associações para o tratamento do vhc |
| WO2005043118A2 (en) * | 2003-10-27 | 2005-05-12 | Vertex Pharmaceuticals Incorporated | Drug discovery method |
| US20050119318A1 (en) * | 2003-10-31 | 2005-06-02 | Hudyma Thomas W. | Inhibitors of HCV replication |
| AR049635A1 (es) | 2004-05-06 | 2006-08-23 | Schering Corp | (1r,2s,5s)-n-((1s)-3-amino-1-(ciclobutilmetil)-2,3-dioxopropil)-3-((2s)-2-((((1,1-dimetiletil)amino)carbonil)amino)-3,3-dimetil-1-oxobutil)-6,6-dimetil-3-azabiciclo(3.1.0)hexan-2-carboxamida como inhibidor de la ns3/ns4a serina proteasa del virus de la hepatitis c |
| CN102512372A (zh) | 2004-06-08 | 2012-06-27 | 沃泰克斯药物股份有限公司 | 药物组合物 |
| ATE513844T1 (de) * | 2004-08-27 | 2011-07-15 | Schering Corp | Acylsulfonamidverbindungen als inhibitoren der ns3-serinprotease des hepatitis-c-virus |
| TWI437990B (zh) * | 2004-10-29 | 2014-05-21 | Vertex Pharma | Vx-950之醫藥用途 |
| EP1910341B1 (en) * | 2005-08-02 | 2013-01-02 | Vertex Pharmaceuticals Incorporated | Inhibitors of serine proteases |
| NZ604087A (en) * | 2005-08-19 | 2014-07-25 | Vertex Pharma | Processes and intermediates for the preparation of protease inhibitors |
| RU2446800C2 (ru) * | 2006-05-31 | 2012-04-10 | Вертекс Фармасьютикалз Инкорпорейтед | Препаративные формы с контролируемым высвобождением |
| US8402690B2 (en) | 2010-09-09 | 2013-03-26 | Sterling International Inc. | Bedbug trap |
-
2006
- 2006-08-01 EP EP06800633A patent/EP1910341B1/en not_active Revoked
- 2006-08-01 CN CN2006800365288A patent/CN101277950B/zh not_active Expired - Fee Related
- 2006-08-01 RU RU2008108024/04A patent/RU2441020C2/ru not_active IP Right Cessation
- 2006-08-01 ES ES06800633T patent/ES2401661T3/es active Active
- 2006-08-01 EP EP10171186A patent/EP2256113A1/en not_active Withdrawn
- 2006-08-01 US US11/497,087 patent/US20070105781A1/en not_active Abandoned
- 2006-08-01 WO PCT/US2006/029988 patent/WO2007016589A2/en active Application Filing
- 2006-08-01 MX MX2008001528A patent/MX2008001528A/es not_active Application Discontinuation
- 2006-08-01 NZ NZ565540A patent/NZ565540A/en not_active IP Right Cessation
- 2006-08-01 JP JP2008525128A patent/JP2009505966A/ja active Pending
- 2006-08-01 CA CA002617679A patent/CA2617679A1/en not_active Abandoned
- 2006-08-01 AU AU2006275413A patent/AU2006275413B2/en not_active Ceased
- 2006-08-01 KR KR1020087005022A patent/KR20080033481A/ko not_active Application Discontinuation
- 2006-08-01 EP EP11160049A patent/EP2402331A1/en not_active Withdrawn
- 2006-08-02 AR ARP060103374A patent/AR057716A1/es not_active Application Discontinuation
- 2006-08-02 TW TW095128293A patent/TW200740813A/zh unknown
-
2008
- 2008-02-01 ZA ZA200801114A patent/ZA200801114B/xx unknown
- 2008-02-03 IL IL189192A patent/IL189192A0/en unknown
- 2008-02-26 NO NO20081012A patent/NO20081012L/no not_active Application Discontinuation
-
2011
- 2011-03-18 US US13/051,557 patent/US20110171175A1/en not_active Abandoned
- 2011-10-13 RU RU2011141559/04A patent/RU2011141559A/ru not_active Application Discontinuation
-
2013
- 2013-02-28 US US13/780,373 patent/US20130177531A1/en not_active Abandoned
- 2013-11-01 US US14/069,638 patent/US20140056847A1/en not_active Abandoned
Patent Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1996011697A1 (en) * | 1994-10-12 | 1996-04-25 | Merck & Co., Inc. | Thrombin inhibitors |
| WO2002008244A2 (en) * | 2000-07-21 | 2002-01-31 | Schering Corporation | Peptides as ns3-serine protease inhibitors of hepatitis c virus |
| WO2002018369A2 (en) * | 2000-08-31 | 2002-03-07 | Eli Lilly And Company | Peptidomimetic protease inhibitors |
| WO2003087092A2 (en) * | 2002-04-11 | 2003-10-23 | Vertex Pharmaceuticals Incorporated | Inhibitors of serine proteases, particularly hepatitis c virus ns3 - ns4 protease |
| WO2005007681A2 (en) * | 2003-07-18 | 2005-01-27 | Vertex Pharmaceuticals Incorporated | Inhibitors of serine proteases, particularly hcv ns3-ns4a protease |
| WO2005035525A2 (en) * | 2003-09-05 | 2005-04-21 | Vertex Pharmaceuticals Incorporated | 2-amido-4-aryloxy-1-carbonylpyrrolidine derivatives as inhibitors of serine proteases, particularly hcv ns3-ns4a protease |
| WO2005042570A1 (en) * | 2003-10-27 | 2005-05-12 | Vertex Pharmaceuticals Incorporated | Hcv ns3-ns4a protease resistance mutants |
Non-Patent Citations (3)
| Title |
|---|
| JPN6011066010; Bioorg. Med. Chem. Lett., 2000, Vol.10, p.711-713 * |
| JPN6011066012; Bioorg. Med. Chem. Lett., 2004, Vol.14, p.1441-1446 * |
| JPN6011066015; Bioorg. Med. Chem. Lett., 2004, Vol.14, p.5007-5011 * |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2018092724A1 (ja) * | 2016-11-15 | 2018-05-24 | 学校法人東京理科大学 | 分子動態評価方法及びスクリーニング方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| KR20080033481A (ko) | 2008-04-16 |
| US20070105781A1 (en) | 2007-05-10 |
| CA2617679A1 (en) | 2007-02-08 |
| AU2006275413A1 (en) | 2007-02-08 |
| RU2011141559A (ru) | 2013-04-20 |
| ZA200801114B (en) | 2008-11-26 |
| EP1910341A2 (en) | 2008-04-16 |
| AR057716A1 (es) | 2007-12-12 |
| US20130177531A1 (en) | 2013-07-11 |
| WO2007016589A3 (en) | 2007-03-29 |
| EP2256113A1 (en) | 2010-12-01 |
| AU2006275413B2 (en) | 2012-07-19 |
| ES2401661T3 (es) | 2013-04-23 |
| RU2008108024A (ru) | 2009-09-10 |
| US20140056847A1 (en) | 2014-02-27 |
| EP1910341B1 (en) | 2013-01-02 |
| IL189192A0 (en) | 2008-06-05 |
| MX2008001528A (es) | 2008-04-04 |
| NZ565540A (en) | 2011-06-30 |
| EP2402331A1 (en) | 2012-01-04 |
| RU2441020C2 (ru) | 2012-01-27 |
| US20110171175A1 (en) | 2011-07-14 |
| TW200740813A (en) | 2007-11-01 |
| CN101277950A (zh) | 2008-10-01 |
| NO20081012L (no) | 2008-04-25 |
| CN101277950B (zh) | 2013-03-27 |
| WO2007016589A2 (en) | 2007-02-08 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2441020C2 (ru) | Ингибиторы серинпротеазы | |
| JP4745230B2 (ja) | セリンプロテアーゼ、特に、hcvns3−ns4aプロテアーゼの阻害剤 | |
| JP4685775B2 (ja) | セリンプロテアーゼ、とりわけhcvns3−ns4aプロテアーゼの阻害剤 | |
| JP4767852B2 (ja) | セリンプロテアーゼ、特にhcvns3‐ns4aの阻害剤 | |
| EP1692157B1 (en) | Inhibitors of serine proteases, particularly hcv ns3-ns4a protease | |
| US8536136B2 (en) | Inhibitors of serine proteases, particularly HCV NS3-NS4A protease | |
| JP2010519329A (ja) | セリンプロテアーゼ阻害剤 | |
| CN1906208B (zh) | 丝氨酸蛋白酶、特别是hcv ns3-ns4a蛋白酶的抑制剂 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20090730 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20090730 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20091104 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20111220 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20120319 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20120327 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20120518 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20120525 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20120619 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20130122 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20130522 |