JP2007530706A - N−複素環カルベンリガンドを含有する高活性潜伏オレフィン複分解触媒 - Google Patents
N−複素環カルベンリガンドを含有する高活性潜伏オレフィン複分解触媒 Download PDFInfo
- Publication number
- JP2007530706A JP2007530706A JP2007506479A JP2007506479A JP2007530706A JP 2007530706 A JP2007530706 A JP 2007530706A JP 2007506479 A JP2007506479 A JP 2007506479A JP 2007506479 A JP2007506479 A JP 2007506479A JP 2007530706 A JP2007530706 A JP 2007530706A
- Authority
- JP
- Japan
- Prior art keywords
- heteroatom
- substituted
- hydrocarbyl
- hydrocarbylene
- alkyl
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
- 239000003054 catalyst Substances 0.000 title claims abstract description 166
- 239000003446 ligand Substances 0.000 title claims abstract description 75
- 238000005865 alkene metathesis reaction Methods 0.000 title claims abstract description 31
- ADLVDYMTBOSDFE-UHFFFAOYSA-N 5-chloro-6-nitroisoindole-1,3-dione Chemical compound C1=C(Cl)C([N+](=O)[O-])=CC2=C1C(=O)NC2=O ADLVDYMTBOSDFE-UHFFFAOYSA-N 0.000 title claims abstract description 18
- 238000006798 ring closing metathesis reaction Methods 0.000 claims abstract description 24
- 238000007152 ring opening metathesis polymerisation reaction Methods 0.000 claims abstract description 21
- 125000002524 organometallic group Chemical group 0.000 claims abstract description 17
- 229910052723 transition metal Inorganic materials 0.000 claims abstract description 13
- 125000005842 heteroatom Chemical group 0.000 claims description 94
- 125000001183 hydrocarbyl group Chemical group 0.000 claims description 91
- 125000003118 aryl group Chemical group 0.000 claims description 89
- 125000000217 alkyl group Chemical group 0.000 claims description 80
- 125000000743 hydrocarbylene group Chemical group 0.000 claims description 51
- 238000006243 chemical reaction Methods 0.000 claims description 38
- 125000000304 alkynyl group Chemical group 0.000 claims description 31
- 125000004435 hydrogen atom Chemical class [H]* 0.000 claims description 21
- 239000001257 hydrogen Substances 0.000 claims description 20
- 229910052739 hydrogen Inorganic materials 0.000 claims description 20
- 125000000524 functional group Chemical group 0.000 claims description 18
- 125000003358 C2-C20 alkenyl group Chemical group 0.000 claims description 17
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims description 17
- 238000000034 method Methods 0.000 claims description 16
- 239000005977 Ethylene Chemical group 0.000 claims description 12
- 125000004429 atom Chemical group 0.000 claims description 12
- 230000007935 neutral effect Effects 0.000 claims description 12
- 150000003624 transition metals Chemical class 0.000 claims description 12
- 125000000623 heterocyclic group Chemical group 0.000 claims description 11
- 150000001336 alkenes Chemical class 0.000 claims description 9
- 125000000129 anionic group Chemical group 0.000 claims description 9
- VGGSQFUCUMXWEO-UHFFFAOYSA-N Ethene Chemical compound C=C VGGSQFUCUMXWEO-UHFFFAOYSA-N 0.000 claims description 7
- JRZJOMJEPLMPRA-UHFFFAOYSA-N olefin Natural products CCCCCCCC=C JRZJOMJEPLMPRA-UHFFFAOYSA-N 0.000 claims description 7
- 239000000376 reactant Substances 0.000 claims description 7
- 125000000325 methylidene group Chemical group [H]C([H])=* 0.000 claims description 6
- 230000008569 process Effects 0.000 claims description 6
- 125000001118 alkylidene group Chemical group 0.000 claims description 3
- 238000011534 incubation Methods 0.000 claims description 3
- -1 acrylic olefins Chemical class 0.000 abstract description 49
- HZVOZRGWRWCICA-UHFFFAOYSA-N methanediyl Chemical compound [CH2] HZVOZRGWRWCICA-UHFFFAOYSA-N 0.000 abstract description 14
- 238000006317 isomerization reaction Methods 0.000 abstract description 6
- 230000009257 reactivity Effects 0.000 abstract description 6
- 230000000977 initiatory effect Effects 0.000 abstract description 4
- OFBQJSOFQDEBGM-UHFFFAOYSA-N Pentane Chemical compound CCCCC OFBQJSOFQDEBGM-UHFFFAOYSA-N 0.000 description 38
- 239000007787 solid Substances 0.000 description 35
- 125000004432 carbon atom Chemical group C* 0.000 description 29
- 125000001424 substituent group Chemical group 0.000 description 28
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 24
- 230000000694 effects Effects 0.000 description 23
- 125000003342 alkenyl group Chemical group 0.000 description 22
- 125000003710 aryl alkyl group Chemical group 0.000 description 21
- 125000002877 alkyl aryl group Chemical group 0.000 description 19
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 18
- 229910052707 ruthenium Inorganic materials 0.000 description 17
- KJTLSVCANCCWHF-UHFFFAOYSA-N Ruthenium Chemical compound [Ru] KJTLSVCANCCWHF-UHFFFAOYSA-N 0.000 description 16
- 238000003786 synthesis reaction Methods 0.000 description 16
- 238000005481 NMR spectroscopy Methods 0.000 description 15
- LYUUVYQGUMRKOV-UHFFFAOYSA-N Diethyl diallylmalonate Chemical compound CCOC(=O)C(CC=C)(CC=C)C(=O)OCC LYUUVYQGUMRKOV-UHFFFAOYSA-N 0.000 description 14
- XYFCBTPGUUZFHI-UHFFFAOYSA-N Phosphine Chemical compound P XYFCBTPGUUZFHI-UHFFFAOYSA-N 0.000 description 14
- 230000015572 biosynthetic process Effects 0.000 description 14
- 125000004122 cyclic group Chemical group 0.000 description 14
- 239000000203 mixture Substances 0.000 description 13
- HECLRDQVFMWTQS-RGOKHQFPSA-N 1755-01-7 Chemical compound C1[C@H]2[C@@H]3CC=C[C@@H]3[C@@H]1C=C2 HECLRDQVFMWTQS-RGOKHQFPSA-N 0.000 description 12
- 229910052799 carbon Inorganic materials 0.000 description 12
- 238000005649 metathesis reaction Methods 0.000 description 12
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 11
- 239000003039 volatile agent Substances 0.000 description 11
- 238000001035 drying Methods 0.000 description 10
- 241000894007 species Species 0.000 description 10
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 9
- 125000004104 aryloxy group Chemical group 0.000 description 9
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 9
- 238000006116 polymerization reaction Methods 0.000 description 9
- RTZKZFJDLAIYFH-UHFFFAOYSA-N ether Substances CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 8
- 150000004820 halides Chemical class 0.000 description 8
- 229910000073 phosphorus hydride Inorganic materials 0.000 description 8
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 description 7
- 125000003917 carbamoyl group Chemical group [H]N([H])C(*)=O 0.000 description 7
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 7
- 229910052762 osmium Inorganic materials 0.000 description 7
- 238000005160 1H NMR spectroscopy Methods 0.000 description 6
- UJHRXZWERCGWQW-UHFFFAOYSA-N 2-but-3-enylpyridine Chemical compound C=CCCC1=CC=CC=N1 UJHRXZWERCGWQW-UHFFFAOYSA-N 0.000 description 6
- 125000004414 alkyl thio group Chemical group 0.000 description 6
- 150000001721 carbon Chemical group 0.000 description 6
- 125000004093 cyano group Chemical group *C#N 0.000 description 6
- ZUOUZKKEUPVFJK-UHFFFAOYSA-N diphenyl Chemical compound C1=CC=CC=C1C1=CC=CC=C1 ZUOUZKKEUPVFJK-UHFFFAOYSA-N 0.000 description 6
- 125000005843 halogen group Chemical group 0.000 description 6
- 150000002466 imines Chemical class 0.000 description 6
- SYQBFIAQOQZEGI-UHFFFAOYSA-N osmium atom Chemical compound [Os] SYQBFIAQOQZEGI-UHFFFAOYSA-N 0.000 description 6
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 6
- 239000011541 reaction mixture Substances 0.000 description 6
- YLQBMQCUIZJEEH-UHFFFAOYSA-N Furan Chemical compound C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 5
- 125000004423 acyloxy group Chemical group 0.000 description 5
- 125000004450 alkenylene group Chemical group 0.000 description 5
- 125000003545 alkoxy group Chemical group 0.000 description 5
- 125000004453 alkoxycarbonyl group Chemical group 0.000 description 5
- 125000002947 alkylene group Chemical group 0.000 description 5
- 125000004419 alkynylene group Chemical group 0.000 description 5
- 125000000649 benzylidene group Chemical group [H]C(=[*])C1=C([H])C([H])=C([H])C([H])=C1[H] 0.000 description 5
- 125000000753 cycloalkyl group Chemical group 0.000 description 5
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 5
- 229910052736 halogen Inorganic materials 0.000 description 5
- 229910052751 metal Inorganic materials 0.000 description 5
- 238000012360 testing method Methods 0.000 description 5
- XKRFYHLGVUSROY-UHFFFAOYSA-N Argon Chemical compound [Ar] XKRFYHLGVUSROY-UHFFFAOYSA-N 0.000 description 4
- 125000002252 acyl group Chemical group 0.000 description 4
- 125000002723 alicyclic group Chemical group 0.000 description 4
- 125000000732 arylene group Chemical group 0.000 description 4
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 4
- 125000001309 chloro group Chemical group Cl* 0.000 description 4
- 238000005686 cross metathesis reaction Methods 0.000 description 4
- 125000004404 heteroalkyl group Chemical group 0.000 description 4
- 125000004474 heteroalkylene group Chemical group 0.000 description 4
- 125000001072 heteroaryl group Chemical group 0.000 description 4
- 125000005549 heteroarylene group Chemical group 0.000 description 4
- 125000000018 nitroso group Chemical group N(=O)* 0.000 description 4
- GJVFBWCTGUSGDD-UHFFFAOYSA-L pentamethonium bromide Chemical compound [Br-].[Br-].C[N+](C)(C)CCCCC[N+](C)(C)C GJVFBWCTGUSGDD-UHFFFAOYSA-L 0.000 description 4
- 125000003367 polycyclic group Chemical group 0.000 description 4
- 125000003107 substituted aryl group Chemical group 0.000 description 4
- 238000006467 substitution reaction Methods 0.000 description 4
- UBBDYHXPSVQEJR-ZETCQYMHSA-N (2s)-6-amino-2-(1h-imidazol-2-ylamino)hexanoic acid Chemical compound NCCCC[C@@H](C(O)=O)NC1=NC=CN1 UBBDYHXPSVQEJR-ZETCQYMHSA-N 0.000 description 3
- 125000004642 (C1-C12) alkoxy group Chemical group 0.000 description 3
- 125000003860 C1-C20 alkoxy group Chemical group 0.000 description 3
- RWRDLPDLKQPQOW-UHFFFAOYSA-N Pyrrolidine Chemical compound C1CCNC1 RWRDLPDLKQPQOW-UHFFFAOYSA-N 0.000 description 3
- 239000004809 Teflon Substances 0.000 description 3
- 229920006362 Teflon® Polymers 0.000 description 3
- 125000003302 alkenyloxy group Chemical group 0.000 description 3
- 125000004448 alkyl carbonyl group Chemical group 0.000 description 3
- 125000004644 alkyl sulfinyl group Chemical group 0.000 description 3
- 125000005133 alkynyloxy group Chemical group 0.000 description 3
- 125000005161 aryl oxy carbonyl group Chemical group 0.000 description 3
- 125000005163 aryl sulfanyl group Chemical group 0.000 description 3
- 125000005110 aryl thio group Chemical group 0.000 description 3
- 125000002619 bicyclic group Chemical group 0.000 description 3
- 235000010290 biphenyl Nutrition 0.000 description 3
- 239000004305 biphenyl Substances 0.000 description 3
- 229910052794 bromium Inorganic materials 0.000 description 3
- 230000003197 catalytic effect Effects 0.000 description 3
- 238000006555 catalytic reaction Methods 0.000 description 3
- 229910052801 chlorine Inorganic materials 0.000 description 3
- 239000013078 crystal Substances 0.000 description 3
- 238000010586 diagram Methods 0.000 description 3
- GDWAYKGILJJNBB-UHFFFAOYSA-N diethyl 2-prop-2-enylpropanedioate Chemical compound CCOC(=O)C(CC=C)C(=O)OCC GDWAYKGILJJNBB-UHFFFAOYSA-N 0.000 description 3
- 125000001033 ether group Chemical group 0.000 description 3
- 125000002485 formyl group Chemical group [H]C(*)=O 0.000 description 3
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 3
- 125000001841 imino group Chemical group [H]N=* 0.000 description 3
- RKJUIXBNRJVNHR-UHFFFAOYSA-N indolenine Natural products C1=CC=C2CC=NC2=C1 RKJUIXBNRJVNHR-UHFFFAOYSA-N 0.000 description 3
- 229910052740 iodine Inorganic materials 0.000 description 3
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 3
- 239000002184 metal Substances 0.000 description 3
- 125000002950 monocyclic group Chemical group 0.000 description 3
- 239000000178 monomer Substances 0.000 description 3
- 229910052757 nitrogen Inorganic materials 0.000 description 3
- 238000005192 partition Methods 0.000 description 3
- 238000000425 proton nuclear magnetic resonance spectrum Methods 0.000 description 3
- 125000004076 pyridyl group Chemical group 0.000 description 3
- 239000000523 sample Substances 0.000 description 3
- 229920006395 saturated elastomer Polymers 0.000 description 3
- 239000002904 solvent Substances 0.000 description 3
- 239000007858 starting material Substances 0.000 description 3
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 3
- 125000006735 (C1-C20) heteroalkyl group Chemical group 0.000 description 2
- IANQTJSKSUMEQM-UHFFFAOYSA-N 1-benzofuran Chemical compound C1=CC=C2OC=CC2=C1 IANQTJSKSUMEQM-UHFFFAOYSA-N 0.000 description 2
- MGADZUXDNSDTHW-UHFFFAOYSA-N 2H-pyran Chemical compound C1OC=CC=C1 MGADZUXDNSDTHW-UHFFFAOYSA-N 0.000 description 2
- KDCGOANMDULRCW-UHFFFAOYSA-N 7H-purine Chemical compound N1=CNC2=NC=NC2=C1 KDCGOANMDULRCW-UHFFFAOYSA-N 0.000 description 2
- UJOBWOGCFQCDNV-UHFFFAOYSA-N 9H-carbazole Chemical compound C1=CC=C2C3=CC=CC=C3NC2=C1 UJOBWOGCFQCDNV-UHFFFAOYSA-N 0.000 description 2
- NLHHRLWOUZZQLW-UHFFFAOYSA-N Acrylonitrile Chemical compound C=CC#N NLHHRLWOUZZQLW-UHFFFAOYSA-N 0.000 description 2
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 2
- 239000004215 Carbon black (E152) Substances 0.000 description 2
- SIKJAQJRHWYJAI-UHFFFAOYSA-N Indole Chemical compound C1=CC=C2NC=CC2=C1 SIKJAQJRHWYJAI-UHFFFAOYSA-N 0.000 description 2
- YNAVUWVOSKDBBP-UHFFFAOYSA-N Morpholine Chemical compound C1COCCN1 YNAVUWVOSKDBBP-UHFFFAOYSA-N 0.000 description 2
- 240000007817 Olea europaea Species 0.000 description 2
- PCNDJXKNXGMECE-UHFFFAOYSA-N Phenazine Natural products C1=CC=CC2=NC3=CC=CC=C3N=C21 PCNDJXKNXGMECE-UHFFFAOYSA-N 0.000 description 2
- GLUUGHFHXGJENI-UHFFFAOYSA-N Piperazine Chemical compound C1CNCCN1 GLUUGHFHXGJENI-UHFFFAOYSA-N 0.000 description 2
- NQRYJNQNLNOLGT-UHFFFAOYSA-N Piperidine Chemical compound C1CCNCC1 NQRYJNQNLNOLGT-UHFFFAOYSA-N 0.000 description 2
- KYQCOXFCLRTKLS-UHFFFAOYSA-N Pyrazine Chemical compound C1=CN=CC=N1 KYQCOXFCLRTKLS-UHFFFAOYSA-N 0.000 description 2
- KAESVJOAVNADME-UHFFFAOYSA-N Pyrrole Chemical compound C=1C=CNC=1 KAESVJOAVNADME-UHFFFAOYSA-N 0.000 description 2
- SMWDFEZZVXVKRB-UHFFFAOYSA-N Quinoline Chemical compound N1=CC=CC2=CC=CC=C21 SMWDFEZZVXVKRB-UHFFFAOYSA-N 0.000 description 2
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 2
- XSQUKJJJFZCRTK-UHFFFAOYSA-N Urea Chemical compound NC(N)=O XSQUKJJJFZCRTK-UHFFFAOYSA-N 0.000 description 2
- DZBUGLKDJFMEHC-UHFFFAOYSA-N acridine Chemical compound C1=CC=CC2=CC3=CC=CC=C3N=C21 DZBUGLKDJFMEHC-UHFFFAOYSA-N 0.000 description 2
- 238000010535 acyclic diene metathesis reaction Methods 0.000 description 2
- 125000005248 alkyl aryloxy group Chemical group 0.000 description 2
- 125000005196 alkyl carbonyloxy group Chemical group 0.000 description 2
- 125000004390 alkyl sulfonyl group Chemical group 0.000 description 2
- 150000001412 amines Chemical class 0.000 description 2
- 229910052786 argon Inorganic materials 0.000 description 2
- 125000002102 aryl alkyloxo group Chemical group 0.000 description 2
- 125000005129 aryl carbonyl group Chemical group 0.000 description 2
- 125000005199 aryl carbonyloxy group Chemical group 0.000 description 2
- 125000005135 aryl sulfinyl group Chemical group 0.000 description 2
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 2
- ZADPBFCGQRWHPN-UHFFFAOYSA-N boronic acid Chemical compound OBO ZADPBFCGQRWHPN-UHFFFAOYSA-N 0.000 description 2
- 125000001626 borono group Chemical group [H]OB([*])O[H] 0.000 description 2
- 125000000707 boryl group Chemical group B* 0.000 description 2
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 2
- 150000007942 carboxylates Chemical class 0.000 description 2
- 238000004440 column chromatography Methods 0.000 description 2
- 125000006165 cyclic alkyl group Chemical group 0.000 description 2
- 238000011161 development Methods 0.000 description 2
- 230000018109 developmental process Effects 0.000 description 2
- TXCDCPKCNAJMEE-UHFFFAOYSA-N dibenzofuran Chemical compound C1=CC=C2C3=CC=CC=C3OC2=C1 TXCDCPKCNAJMEE-UHFFFAOYSA-N 0.000 description 2
- USIUVYZYUHIAEV-UHFFFAOYSA-N diphenyl ether Chemical compound C=1C=CC=CC=1OC1=CC=CC=C1 USIUVYZYUHIAEV-UHFFFAOYSA-N 0.000 description 2
- DMBHHRLKUKUOEG-UHFFFAOYSA-N diphenylamine Chemical compound C=1C=CC=CC=1NC1=CC=CC=C1 DMBHHRLKUKUOEG-UHFFFAOYSA-N 0.000 description 2
- 238000005516 engineering process Methods 0.000 description 2
- 125000005678 ethenylene group Chemical group [H]C([*:1])=C([H])[*:2] 0.000 description 2
- 125000002573 ethenylidene group Chemical group [*]=C=C([H])[H] 0.000 description 2
- 150000002367 halogens Chemical class 0.000 description 2
- 229930195733 hydrocarbon Natural products 0.000 description 2
- 150000002430 hydrocarbons Chemical group 0.000 description 2
- JCYWCSGERIELPG-UHFFFAOYSA-N imes Chemical group CC1=CC(C)=CC(C)=C1N1C=CN(C=2C(=CC(C)=CC=2C)C)[C]1 JCYWCSGERIELPG-UHFFFAOYSA-N 0.000 description 2
- IQZZFVDIZRWADY-UHFFFAOYSA-N isocoumarin Chemical compound C1=CC=C2C(=O)OC=CC2=C1 IQZZFVDIZRWADY-UHFFFAOYSA-N 0.000 description 2
- 125000002462 isocyano group Chemical group *[N+]#[C-] 0.000 description 2
- AWJUIBRHMBBTKR-UHFFFAOYSA-N isoquinoline Chemical compound C1=NC=CC2=CC=CC=C21 AWJUIBRHMBBTKR-UHFFFAOYSA-N 0.000 description 2
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 description 2
- 239000003921 oil Substances 0.000 description 2
- 125000001181 organosilyl group Chemical group [SiH3]* 0.000 description 2
- 229910052760 oxygen Inorganic materials 0.000 description 2
- 239000001301 oxygen Substances 0.000 description 2
- 125000000951 phenoxy group Chemical group [H]C1=C([H])C([H])=C(O*)C([H])=C1[H] 0.000 description 2
- 125000000394 phosphonato group Chemical group [O-]P([O-])(*)=O 0.000 description 2
- 229920000642 polymer Polymers 0.000 description 2
- 150000003222 pyridines Chemical class 0.000 description 2
- 239000011347 resin Substances 0.000 description 2
- 229920005989 resin Polymers 0.000 description 2
- 150000003303 ruthenium Chemical class 0.000 description 2
- 238000003756 stirring Methods 0.000 description 2
- 239000000126 substance Substances 0.000 description 2
- 125000000547 substituted alkyl group Chemical group 0.000 description 2
- 230000002194 synthesizing effect Effects 0.000 description 2
- 229920002994 synthetic fiber Polymers 0.000 description 2
- 150000003568 thioethers Chemical class 0.000 description 2
- 125000003396 thiol group Chemical group [H]S* 0.000 description 2
- ITMCEJHCFYSIIV-UHFFFAOYSA-M triflate Chemical compound [O-]S(=O)(=O)C(F)(F)F ITMCEJHCFYSIIV-UHFFFAOYSA-M 0.000 description 2
- 125000004739 (C1-C6) alkylsulfonyl group Chemical group 0.000 description 1
- 125000006710 (C2-C12) alkenyl group Chemical group 0.000 description 1
- 125000006711 (C2-C12) alkynyl group Chemical group 0.000 description 1
- JZTKNVMVUVSGJF-UHFFFAOYSA-N 1,2,3,5-oxatriazole Chemical compound C=1N=NON=1 JZTKNVMVUVSGJF-UHFFFAOYSA-N 0.000 description 1
- JYEUMXHLPRZUAT-UHFFFAOYSA-N 1,2,3-triazine Chemical compound C1=CN=NN=C1 JYEUMXHLPRZUAT-UHFFFAOYSA-N 0.000 description 1
- BBVIDBNAYOIXOE-UHFFFAOYSA-N 1,2,4-oxadiazole Chemical compound C=1N=CON=1 BBVIDBNAYOIXOE-UHFFFAOYSA-N 0.000 description 1
- FYADHXFMURLYQI-UHFFFAOYSA-N 1,2,4-triazine Chemical compound C1=CN=NC=N1 FYADHXFMURLYQI-UHFFFAOYSA-N 0.000 description 1
- WTPCCFHCHCMJIT-UHFFFAOYSA-N 1,2,5-oxathiazine Chemical compound O1SC=CN=C1 WTPCCFHCHCMJIT-UHFFFAOYSA-N 0.000 description 1
- VCZQYTJRWNRPHF-UHFFFAOYSA-N 1,2-dioxin Chemical compound O1OC=CC=C1 VCZQYTJRWNRPHF-UHFFFAOYSA-N 0.000 description 1
- FKASFBLJDCHBNZ-UHFFFAOYSA-N 1,3,4-oxadiazole Chemical compound C1=NN=CO1 FKASFBLJDCHBNZ-UHFFFAOYSA-N 0.000 description 1
- JIHQDMXYYFUGFV-UHFFFAOYSA-N 1,3,5-triazine Chemical compound C1=NC=NC=N1 JIHQDMXYYFUGFV-UHFFFAOYSA-N 0.000 description 1
- BCMCBBGGLRIHSE-UHFFFAOYSA-N 1,3-benzoxazole Chemical compound C1=CC=C2OC=NC2=C1 BCMCBBGGLRIHSE-UHFFFAOYSA-N 0.000 description 1
- XZDYFCGKKKSOEY-UHFFFAOYSA-N 1,3-bis[2,6-di(propan-2-yl)phenyl]-4,5-dihydro-2h-imidazol-1-ium-2-ide Chemical group CC(C)C1=CC=CC(C(C)C)=C1N1CCN(C=2C(=CC=CC=2C(C)C)C(C)C)[C]1 XZDYFCGKKKSOEY-UHFFFAOYSA-N 0.000 description 1
- OHOXMCCFSFSRMD-UHFFFAOYSA-N 1,3-oxathiole Chemical compound C1OC=CS1 OHOXMCCFSFSRMD-UHFFFAOYSA-N 0.000 description 1
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 1
- FLBAYUMRQUHISI-UHFFFAOYSA-N 1,8-naphthyridine Chemical compound N1=CC=CC2=CC=CN=C21 FLBAYUMRQUHISI-UHFFFAOYSA-N 0.000 description 1
- WJFKNYWRSNBZNX-UHFFFAOYSA-N 10H-phenothiazine Chemical compound C1=CC=C2NC3=CC=CC=C3SC2=C1 WJFKNYWRSNBZNX-UHFFFAOYSA-N 0.000 description 1
- TZMSYXZUNZXBOL-UHFFFAOYSA-N 10H-phenoxazine Chemical compound C1=CC=C2NC3=CC=CC=C3OC2=C1 TZMSYXZUNZXBOL-UHFFFAOYSA-N 0.000 description 1
- QWENRTYMTSOGBR-UHFFFAOYSA-N 1H-1,2,3-Triazole Chemical compound C=1C=NNN=1 QWENRTYMTSOGBR-UHFFFAOYSA-N 0.000 description 1
- HYZJCKYKOHLVJF-UHFFFAOYSA-N 1H-benzimidazole Chemical compound C1=CC=C2NC=NC2=C1 HYZJCKYKOHLVJF-UHFFFAOYSA-N 0.000 description 1
- BAXOFTOLAUCFNW-UHFFFAOYSA-N 1H-indazole Chemical compound C1=CC=C2C=NNC2=C1 BAXOFTOLAUCFNW-UHFFFAOYSA-N 0.000 description 1
- LFHLEABTNIQIQO-UHFFFAOYSA-N 1H-isoindole Chemical compound C1=CC=C2CN=CC2=C1 LFHLEABTNIQIQO-UHFFFAOYSA-N 0.000 description 1
- VWSZWVLPNPRXTP-UHFFFAOYSA-N 2,2-dimethyl-n-phenylpent-4-en-1-imine Chemical compound C=CCC(C)(C)C=NC1=CC=CC=C1 VWSZWVLPNPRXTP-UHFFFAOYSA-N 0.000 description 1
- ZMBFSJVNWOSYHA-UHFFFAOYSA-N 2,2-dimethyl-n-propan-2-ylpent-4-en-1-imine Chemical compound CC(C)N=CC(C)(C)CC=C ZMBFSJVNWOSYHA-UHFFFAOYSA-N 0.000 description 1
- XBNGYFFABRKICK-UHFFFAOYSA-N 2,3,4,5,6-pentafluorophenol Chemical compound OC1=C(F)C(F)=C(F)C(F)=C1F XBNGYFFABRKICK-UHFFFAOYSA-N 0.000 description 1
- VEPOHXYIFQMVHW-XOZOLZJESA-N 2,3-dihydroxybutanedioic acid (2S,3S)-3,4-dimethyl-2-phenylmorpholine Chemical compound OC(C(O)C(O)=O)C(O)=O.C[C@H]1[C@@H](OCCN1C)c1ccccc1 VEPOHXYIFQMVHW-XOZOLZJESA-N 0.000 description 1
- AZUHIVLOSAPWDM-UHFFFAOYSA-N 2-(1h-imidazol-2-yl)-1h-imidazole Chemical compound C1=CNC(C=2NC=CN=2)=N1 AZUHIVLOSAPWDM-UHFFFAOYSA-N 0.000 description 1
- ZIVYADMFPMNVMV-UHFFFAOYSA-N 2-but-3-enyl-4-methylpyridine Chemical compound CC1=CC=NC(CCC=C)=C1 ZIVYADMFPMNVMV-UHFFFAOYSA-N 0.000 description 1
- 125000000094 2-phenylethyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000004105 2-pyridyl group Chemical group N1=C([*])C([H])=C([H])C([H])=C1[H] 0.000 description 1
- ZPSJGADGUYYRKE-UHFFFAOYSA-N 2H-pyran-2-one Chemical compound O=C1C=CC=CO1 ZPSJGADGUYYRKE-UHFFFAOYSA-N 0.000 description 1
- JZIBVTUXIVIFGC-UHFFFAOYSA-N 2H-pyrrole Chemical compound C1C=CC=N1 JZIBVTUXIVIFGC-UHFFFAOYSA-N 0.000 description 1
- KGWNRZLPXLBMPS-UHFFFAOYSA-N 2h-1,3-oxazine Chemical compound C1OC=CC=N1 KGWNRZLPXLBMPS-UHFFFAOYSA-N 0.000 description 1
- YHWMFDLNZGIJSD-UHFFFAOYSA-N 2h-1,4-oxazine Chemical compound C1OC=CN=C1 YHWMFDLNZGIJSD-UHFFFAOYSA-N 0.000 description 1
- ACVSHQGHCWUJFU-UHFFFAOYSA-N 2h-imidazole Chemical compound C1N=CC=N1 ACVSHQGHCWUJFU-UHFFFAOYSA-N 0.000 description 1
- BCHZICNRHXRCHY-UHFFFAOYSA-N 2h-oxazine Chemical compound N1OC=CC=C1 BCHZICNRHXRCHY-UHFFFAOYSA-N 0.000 description 1
- GOLORTLGFDVFDW-UHFFFAOYSA-N 3-(1h-benzimidazol-2-yl)-7-(diethylamino)chromen-2-one Chemical compound C1=CC=C2NC(C3=CC4=CC=C(C=C4OC3=O)N(CC)CC)=NC2=C1 GOLORTLGFDVFDW-UHFFFAOYSA-N 0.000 description 1
- OJNYWHSZTYNGPE-UHFFFAOYSA-N 3-[(4-chlorophenyl)methylsulfanyl]-5-(methylcarbamoylamino)-1,2-thiazole-4-carboxamide Chemical compound NC(=O)C1=C(NC(=O)NC)SN=C1SCC1=CC=C(Cl)C=C1 OJNYWHSZTYNGPE-UHFFFAOYSA-N 0.000 description 1
- 125000004975 3-butenyl group Chemical group C(CC=C)* 0.000 description 1
- 125000006201 3-phenylpropyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- VXIKDBJPBRMXBP-UHFFFAOYSA-N 3H-pyrrole Chemical compound C1C=CN=C1 VXIKDBJPBRMXBP-UHFFFAOYSA-N 0.000 description 1
- BWCDLEQTELFBAW-UHFFFAOYSA-N 3h-dioxazole Chemical compound N1OOC=C1 BWCDLEQTELFBAW-UHFFFAOYSA-N 0.000 description 1
- RELAJOWOFXGXHI-UHFFFAOYSA-N 3h-oxathiole Chemical compound C1SOC=C1 RELAJOWOFXGXHI-UHFFFAOYSA-N 0.000 description 1
- MSTDXOZUKAQDRL-UHFFFAOYSA-N 4-Chromanone Chemical compound C1=CC=C2C(=O)CCOC2=C1 MSTDXOZUKAQDRL-UHFFFAOYSA-N 0.000 description 1
- UQRONKZLYKUEMO-UHFFFAOYSA-N 4-methyl-1-(2,4,6-trimethylphenyl)pent-4-en-2-one Chemical group CC(=C)CC(=O)Cc1c(C)cc(C)cc1C UQRONKZLYKUEMO-UHFFFAOYSA-N 0.000 description 1
- 125000000590 4-methylphenyl group Chemical group [H]C1=C([H])C(=C([H])C([H])=C1*)C([H])([H])[H] 0.000 description 1
- NSPMIYGKQJPBQR-UHFFFAOYSA-N 4H-1,2,4-triazole Chemical compound C=1N=CNN=1 NSPMIYGKQJPBQR-UHFFFAOYSA-N 0.000 description 1
- MRUWJENAYHTDQG-UHFFFAOYSA-N 4H-pyran Chemical compound C1C=COC=C1 MRUWJENAYHTDQG-UHFFFAOYSA-N 0.000 description 1
- UCZQXJKDCHCTAI-UHFFFAOYSA-N 4h-1,3-dioxine Chemical compound C1OCC=CO1 UCZQXJKDCHCTAI-UHFFFAOYSA-N 0.000 description 1
- BMRPOOWUTVUBRI-UHFFFAOYSA-N 4h-oxazine Chemical compound C1C=CON=C1 BMRPOOWUTVUBRI-UHFFFAOYSA-N 0.000 description 1
- CLRIMWMVEVYXAK-UHFFFAOYSA-N 5-ethylcyclopenta-1,3-diene Chemical compound CCC1C=CC=C1 CLRIMWMVEVYXAK-UHFFFAOYSA-N 0.000 description 1
- MAQAGRJURDEYDQ-UHFFFAOYSA-N 6-methylpyridine Chemical compound CC1=C=CC=C[N]1 MAQAGRJURDEYDQ-UHFFFAOYSA-N 0.000 description 1
- GJCOSYZMQJWQCA-UHFFFAOYSA-N 9H-xanthene Chemical compound C1=CC=C2CC3=CC=CC=C3OC2=C1 GJCOSYZMQJWQCA-UHFFFAOYSA-N 0.000 description 1
- KYNSBQPICQTCGU-UHFFFAOYSA-N Benzopyrane Chemical compound C1=CC=C2C=CCOC2=C1 KYNSBQPICQTCGU-UHFFFAOYSA-N 0.000 description 1
- ROFVEXUMMXZLPA-UHFFFAOYSA-N Bipyridyl Chemical compound N1=CC=CC=C1C1=CC=CC=N1 ROFVEXUMMXZLPA-UHFFFAOYSA-N 0.000 description 1
- KITLNWPOKPGMRQ-UHFFFAOYSA-N C(=C)[Ru]=C Chemical compound C(=C)[Ru]=C KITLNWPOKPGMRQ-UHFFFAOYSA-N 0.000 description 1
- 125000000882 C2-C6 alkenyl group Chemical group 0.000 description 1
- 125000003601 C2-C6 alkynyl group Chemical group 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 description 1
- WRYCSMQKUKOKBP-UHFFFAOYSA-N Imidazolidine Chemical compound C1CNCN1 WRYCSMQKUKOKBP-UHFFFAOYSA-N 0.000 description 1
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 1
- ZOKXTWBITQBERF-UHFFFAOYSA-N Molybdenum Chemical compound [Mo] ZOKXTWBITQBERF-UHFFFAOYSA-N 0.000 description 1
- PSRJCFCDVXSLIJ-UHFFFAOYSA-N N1=C2C=C(C=C1)C=C2 Chemical compound N1=C2C=C(C=C1)C=C2 PSRJCFCDVXSLIJ-UHFFFAOYSA-N 0.000 description 1
- ZCQWOFVYLHDMMC-UHFFFAOYSA-N Oxazole Chemical compound C1=COC=N1 ZCQWOFVYLHDMMC-UHFFFAOYSA-N 0.000 description 1
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical compound [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 description 1
- CVQUWLDCFXOXEN-UHFFFAOYSA-N Pyran-4-one Chemical compound O=C1C=COC=C1 CVQUWLDCFXOXEN-UHFFFAOYSA-N 0.000 description 1
- WTKZEGDFNFYCGP-UHFFFAOYSA-N Pyrazole Chemical compound C=1C=NNC=1 WTKZEGDFNFYCGP-UHFFFAOYSA-N 0.000 description 1
- CZPWVGJYEJSRLH-UHFFFAOYSA-N Pyrimidine Chemical compound C1=CN=CN=C1 CZPWVGJYEJSRLH-UHFFFAOYSA-N 0.000 description 1
- XUIMIQQOPSSXEZ-UHFFFAOYSA-N Silicon Chemical compound [Si] XUIMIQQOPSSXEZ-UHFFFAOYSA-N 0.000 description 1
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 1
- FZWLAAWBMGSTSO-UHFFFAOYSA-N Thiazole Chemical compound C1=CSC=N1 FZWLAAWBMGSTSO-UHFFFAOYSA-N 0.000 description 1
- 238000002441 X-ray diffraction Methods 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 125000005115 alkyl carbamoyl group Chemical group 0.000 description 1
- 125000005277 alkyl imino group Chemical group 0.000 description 1
- HSFWRNGVRCDJHI-UHFFFAOYSA-N alpha-acetylene Natural products C#C HSFWRNGVRCDJHI-UHFFFAOYSA-N 0.000 description 1
- 125000005427 anthranyl group Chemical group 0.000 description 1
- 238000013459 approach Methods 0.000 description 1
- 125000005116 aryl carbamoyl group Chemical group 0.000 description 1
- 125000004467 aryl imino group Chemical group 0.000 description 1
- 125000004391 aryl sulfonyl group Chemical group 0.000 description 1
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 1
- RWCCWEUUXYIKHB-UHFFFAOYSA-N benzophenone Chemical compound C=1C=CC=CC=1C(=O)C1=CC=CC=C1 RWCCWEUUXYIKHB-UHFFFAOYSA-N 0.000 description 1
- 239000012965 benzophenone Substances 0.000 description 1
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 1
- 125000001246 bromo group Chemical group Br* 0.000 description 1
- 239000004202 carbamide Substances 0.000 description 1
- 235000013877 carbamide Nutrition 0.000 description 1
- 239000011203 carbon fibre reinforced carbon Substances 0.000 description 1
- 238000003421 catalytic decomposition reaction Methods 0.000 description 1
- 239000000919 ceramic Substances 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 239000007809 chemical reaction catalyst Substances 0.000 description 1
- 150000001805 chlorine compounds Chemical class 0.000 description 1
- QZHPTGXQGDFGEN-UHFFFAOYSA-N chromene Chemical compound C1=CC=C2C=C[CH]OC2=C1 QZHPTGXQGDFGEN-UHFFFAOYSA-N 0.000 description 1
- WCZVZNOTHYJIEI-UHFFFAOYSA-N cinnoline Chemical compound N1=NC=CC2=CC=CC=C21 WCZVZNOTHYJIEI-UHFFFAOYSA-N 0.000 description 1
- 229940052810 complex b Drugs 0.000 description 1
- 150000001875 compounds Chemical class 0.000 description 1
- 230000008878 coupling Effects 0.000 description 1
- 238000010168 coupling process Methods 0.000 description 1
- 238000005859 coupling reaction Methods 0.000 description 1
- 125000001651 cyanato group Chemical group [*]OC#N 0.000 description 1
- 125000000392 cycloalkenyl group Chemical group 0.000 description 1
- 125000004956 cyclohexylene group Chemical group 0.000 description 1
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 125000003493 decenyl group Chemical group [H]C([*])=C([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 125000002704 decyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 230000002950 deficient Effects 0.000 description 1
- 238000006731 degradation reaction Methods 0.000 description 1
- 238000013461 design Methods 0.000 description 1
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- 125000002534 ethynyl group Chemical group [H]C#C* 0.000 description 1
- 229910052731 fluorine Inorganic materials 0.000 description 1
- 239000011737 fluorine Substances 0.000 description 1
- 125000001153 fluoro group Chemical group F* 0.000 description 1
- 239000012634 fragment Substances 0.000 description 1
- 238000004817 gas chromatography Methods 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 125000004997 halocarbonyl group Chemical group 0.000 description 1
- 230000020169 heat generation Effects 0.000 description 1
- PZOUSPYUWWUPPK-UHFFFAOYSA-N indole Natural products CC1=CC=CC2=C1C=CN2 PZOUSPYUWWUPPK-UHFFFAOYSA-N 0.000 description 1
- 125000002346 iodo group Chemical group I* 0.000 description 1
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 1
- MKHHKAFWMAYADE-UHFFFAOYSA-N isochromen-3-one Chemical compound C1=CC=CC2=COC(=O)C=C21 MKHHKAFWMAYADE-UHFFFAOYSA-N 0.000 description 1
- 125000000555 isopropenyl group Chemical group [H]\C([H])=C(\*)C([H])([H])[H] 0.000 description 1
- CTAPFRYPJLPFDF-UHFFFAOYSA-N isoxazole Chemical compound C=1C=NOC=1 CTAPFRYPJLPFDF-UHFFFAOYSA-N 0.000 description 1
- QDLAGTHXVHQKRE-UHFFFAOYSA-N lichenxanthone Natural products COC1=CC(O)=C2C(=O)C3=C(C)C=C(OC)C=C3OC2=C1 QDLAGTHXVHQKRE-UHFFFAOYSA-N 0.000 description 1
- 229920002521 macromolecule Polymers 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- RIFHJAODNHLCBH-UHFFFAOYSA-N methanethione Chemical group S=[CH] RIFHJAODNHLCBH-UHFFFAOYSA-N 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 229910052750 molybdenum Inorganic materials 0.000 description 1
- 239000011733 molybdenum Substances 0.000 description 1
- MEYIFNOHQMJVSK-UHFFFAOYSA-N n,2,2-trimethylpent-4-en-1-imine Chemical compound CN=CC(C)(C)CC=C MEYIFNOHQMJVSK-UHFFFAOYSA-N 0.000 description 1
- SYSQUGFVNFXIIT-UHFFFAOYSA-N n-[4-(1,3-benzoxazol-2-yl)phenyl]-4-nitrobenzenesulfonamide Chemical class C1=CC([N+](=O)[O-])=CC=C1S(=O)(=O)NC1=CC=C(C=2OC3=CC=CC=C3N=2)C=C1 SYSQUGFVNFXIIT-UHFFFAOYSA-N 0.000 description 1
- 125000004370 n-butenyl group Chemical group [H]\C([H])=C(/[H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- IYVQMNNHQGDUDH-UHFFFAOYSA-N n-cyclohexyl-2,2-dimethylpent-4-en-1-imine Chemical compound C=CCC(C)(C)C=NC1CCCCC1 IYVQMNNHQGDUDH-UHFFFAOYSA-N 0.000 description 1
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- NBIHPISJSSXWAS-UHFFFAOYSA-N n-tert-butyl-2,2-dimethylpent-4-en-1-imine Chemical compound CC(C)(C)N=CC(C)(C)CC=C NBIHPISJSSXWAS-UHFFFAOYSA-N 0.000 description 1
- 125000001624 naphthyl group Chemical group 0.000 description 1
- 125000004957 naphthylene group Chemical group 0.000 description 1
- 125000004365 octenyl group Chemical group C(=CCCCCCC)* 0.000 description 1
- 125000002347 octyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- CQDAMYNQINDRQC-UHFFFAOYSA-N oxatriazole Chemical compound C1=NN=NO1 CQDAMYNQINDRQC-UHFFFAOYSA-N 0.000 description 1
- ATYBXHSAIOKLMG-UHFFFAOYSA-N oxepin Chemical compound O1C=CC=CC=C1 ATYBXHSAIOKLMG-UHFFFAOYSA-N 0.000 description 1
- XLFDEQZWKMCBSH-UHFFFAOYSA-N pent-4-enyl(diphenyl)phosphane Chemical compound C=1C=CC=CC=1P(CCCC=C)C1=CC=CC=C1 XLFDEQZWKMCBSH-UHFFFAOYSA-N 0.000 description 1
- 229950000688 phenothiazine Drugs 0.000 description 1
- 125000000843 phenylene group Chemical group C1(=C(C=CC=C1)*)* 0.000 description 1
- FVZVCSNXTFCBQU-UHFFFAOYSA-N phosphanyl Chemical group [PH2] FVZVCSNXTFCBQU-UHFFFAOYSA-N 0.000 description 1
- 125000001476 phosphono group Chemical group [H]OP(*)(=O)O[H] 0.000 description 1
- 229910052698 phosphorus Inorganic materials 0.000 description 1
- 239000011574 phosphorus Substances 0.000 description 1
- 239000002685 polymerization catalyst Substances 0.000 description 1
- FLTFWLUOHKERMJ-UHFFFAOYSA-N pyrano[3,4-b]pyrrole Chemical compound C1=COC=C2N=CC=C21 FLTFWLUOHKERMJ-UHFFFAOYSA-N 0.000 description 1
- USPWKWBDZOARPV-UHFFFAOYSA-N pyrazolidine Chemical compound C1CNNC1 USPWKWBDZOARPV-UHFFFAOYSA-N 0.000 description 1
- PBMFSQRYOILNGV-UHFFFAOYSA-N pyridazine Chemical compound C1=CC=NN=C1 PBMFSQRYOILNGV-UHFFFAOYSA-N 0.000 description 1
- JWVCLYRUEFBMGU-UHFFFAOYSA-N quinazoline Chemical compound N1=CN=CC2=CC=CC=C21 JWVCLYRUEFBMGU-UHFFFAOYSA-N 0.000 description 1
- SBYHFKPVCBCYGV-UHFFFAOYSA-N quinuclidine Chemical compound C1CC2CCN1CC2 SBYHFKPVCBCYGV-UHFFFAOYSA-N 0.000 description 1
- 230000035484 reaction time Effects 0.000 description 1
- 229930195734 saturated hydrocarbon Natural products 0.000 description 1
- 229910052710 silicon Inorganic materials 0.000 description 1
- 239000010703 silicon Substances 0.000 description 1
- 238000004611 spectroscopical analysis Methods 0.000 description 1
- 125000005017 substituted alkenyl group Chemical group 0.000 description 1
- 125000004426 substituted alkynyl group Chemical group 0.000 description 1
- 125000000020 sulfo group Chemical group O=S(=O)([*])O[H] 0.000 description 1
- 125000001273 sulfonato group Chemical group [O-]S(*)(=O)=O 0.000 description 1
- 229910052717 sulfur Inorganic materials 0.000 description 1
- 239000011593 sulfur Substances 0.000 description 1
- 125000005063 tetradecenyl group Chemical group C(=CCCCCCCCCCCCC)* 0.000 description 1
- 125000000858 thiocyanato group Chemical group *SC#N 0.000 description 1
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 1
- 230000009466 transformation Effects 0.000 description 1
- 238000000844 transformation Methods 0.000 description 1
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G61/00—Macromolecular compounds obtained by reactions forming a carbon-to-carbon link in the main chain of the macromolecule
- C08G61/02—Macromolecular compounds containing only carbon atoms in the main chain of the macromolecule, e.g. polyxylylenes
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C67/00—Preparation of carboxylic acid esters
- C07C67/30—Preparation of carboxylic acid esters by modifying the acid moiety of the ester, such modification not being an introduction of an ester group
- C07C67/333—Preparation of carboxylic acid esters by modifying the acid moiety of the ester, such modification not being an introduction of an ester group by isomerisation; by change of size of the carbon skeleton
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D493/00—Heterocyclic compounds containing oxygen atoms as the only ring hetero atoms in the condensed system
- C07D493/02—Heterocyclic compounds containing oxygen atoms as the only ring hetero atoms in the condensed system in which the condensed system contains two hetero rings
- C07D493/10—Spiro-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F15/00—Compounds containing elements of Groups 8, 9, 10 or 18 of the Periodic Table
- C07F15/0006—Compounds containing elements of Groups 8, 9, 10 or 18 of the Periodic Table compounds of the platinum group
- C07F15/0046—Ruthenium compounds
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F132/00—Homopolymers of cyclic compounds containing no unsaturated aliphatic radicals in a side chain, and having one or more carbon-to-carbon double bonds in a carbocyclic ring system
- C08F132/08—Homopolymers of cyclic compounds containing no unsaturated aliphatic radicals in a side chain, and having one or more carbon-to-carbon double bonds in a carbocyclic ring system having condensed rings
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G61/00—Macromolecular compounds obtained by reactions forming a carbon-to-carbon link in the main chain of the macromolecule
- C08G61/02—Macromolecular compounds containing only carbon atoms in the main chain of the macromolecule, e.g. polyxylylenes
- C08G61/04—Macromolecular compounds containing only carbon atoms in the main chain of the macromolecule, e.g. polyxylylenes only aliphatic carbon atoms
- C08G61/06—Macromolecular compounds containing only carbon atoms in the main chain of the macromolecule, e.g. polyxylylenes only aliphatic carbon atoms prepared by ring-opening of carbocyclic compounds
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G2261/00—Macromolecular compounds obtained by reactions forming a carbon-to-carbon link in the main chain of the macromolecule
- C08G2261/10—Definition of the polymer structure
- C08G2261/11—Homopolymers
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G2261/00—Macromolecular compounds obtained by reactions forming a carbon-to-carbon link in the main chain of the macromolecule
- C08G2261/30—Monomer units or repeat units incorporating structural elements in the main chain
- C08G2261/33—Monomer units or repeat units incorporating structural elements in the main chain incorporating non-aromatic structural elements in the main chain
- C08G2261/332—Monomer units or repeat units incorporating structural elements in the main chain incorporating non-aromatic structural elements in the main chain containing only carbon atoms
- C08G2261/3325—Monomer units or repeat units incorporating structural elements in the main chain incorporating non-aromatic structural elements in the main chain containing only carbon atoms derived from other polycyclic systems
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G2261/00—Macromolecular compounds obtained by reactions forming a carbon-to-carbon link in the main chain of the macromolecule
- C08G2261/40—Polymerisation processes
- C08G2261/41—Organometallic coupling reactions
- C08G2261/418—Ring opening metathesis polymerisation [ROMP]
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Medicinal Chemistry (AREA)
- Polymers & Plastics (AREA)
- Catalysts (AREA)
- Polyoxymethylene Polymers And Polymers With Carbon-To-Carbon Bonds (AREA)
Abstract
Description
オレフィン複分解触媒作用は、強力な技術であり、これは、最近では、炭素−炭素結合を形成する汎用方法として、極めて注目されており、そして有機合成および高分子化学において、多数の用途がある(非特許文献1)。オレフィン複分解反応の系統には、閉環複分解(RCM)、交差複分解(CM)、開環複分解重合(ROMP)、および非環式ジエン複分解重合(ADMET)が挙げられる。オレフィン複分解の成功は、いくつかの明確な遷移金属錯体(例えば、Schrockモリブデン触媒ならびにGrubbsルテニウムおよびオスミウム触媒の開発に由来している(例えば、非特許文献2;非特許文献3;非特許文献4;非特許文献5;非特許文献6を参照のこと)。これらの錯体の発見に続いて、オレフィン複分解研究のかなりの部分は、それらの活性、選択性および/または安定性を高めるために、ルテニウムおよびオスミウムカルベン触媒を調整することに集中している。最も一般的な方策は、モノ−デンテート(mono−dentate)リガンドを他のモノ−デンテートリガンドで置き換えて新しい有用な特性を有する触媒錯体を提供することが関与している。
本発明は、NHCリガンドおよびキレート化カルベンリガンドを含む新規な高活性の潜伏オレフィン複分解触媒に関する。このキレート化カルベンリガンドを慎重に選択することにより、数分間から数時間またはそれ以上の潜伏期間を有する触媒が得られる。また、驚くべきことに、これらの錯体の簡単な異性化によって、これらの触媒のいくつかの開始は、相当に変えることができ、また、異なる異性体の割合を制御することにより、その反応性は、広範囲に調整できることが発見された。これらの触媒は、アクリル系オレフィンのRCMおよび環状オレフィンのROMPで特に有用である。
点線で示しαおよびβとして命名した結合は、単結合または不飽和(例えば、二重)結合を表わすが、但し、αおよびβは、両方共に不飽和結合ではあり得ない;
Mは、第8族遷移金属、一般に、ルテニウム(Ru)またはオスミウム(Os)である;
R1およびR2は、別個に、水素、ヒドロカルビル、置換ヒドロカルビル、ヘテロ原子含有ヒドロカルビル、ヘテロ原子含有置換ヒドロカルビル、および官能基から選択される;
Qは、有機ジラジカル、すなわち、ヒドロカルビレン、置換ヒドロカルビレン、ヘテロ原子含有ヒドロカルビレンまたはヘテロ原子含有置換ヒドロカルビレンリンカーであり、さらに、ここで、Q内の隣接原子上の2個またはそれ以上の置換基は、結合されて、追加環状基を形成し得る;
X1およびX2は、アニオン性リガンドであり、そして同一または異なり得る;
L1は、中性電子供与リガンドであり、そしてpは、0または1である;
αが単結合であるとき、L2は、NR7R8、PR7R8、N=CR7R8、およびR7C=NR8から選択され、ここで、R7およびR8は、別個に、置換および/またはヘテロ原子含有C1〜C20アルキル、C2〜C20アルケニル、C2〜C20アルキニル、およびC5〜C24アリールから選択されるか、またはR7およびR8は、一緒になって、複素環を形成できる;
αが不飽和結合(例えば、二重結合)であるとき、L2は、NR7およびPR7から選択され、ここで、R7は、先に定義したとおりである;
YおよびZは、ヒドロカルビレン、置換ヒドロカルビレン、ヘテロ原子含有ヒドロカルビレン、ヘテロ原子含有置換ヒドロカルビレン、−O−、−S−、−NR9−、および−PR9−から別個に選択される連鎖であり、ここで、R9は、ヒドロカルビル、置換ヒドロカルビル、ヘテロ原子含有ヒドロカルビル、およびヘテロ原子含有置換ヒドロカルビルから選択され、さらに、ここで、YおよびZ、またはL2およびZは、芳香環内の隣接原子を表わし得る;
mは、0または1である;そして
nは、0または1である。
特に明記しない限り、本発明は、特定の反応物、反応条件などには限定されず、これらは変えられ得ることが理解できるはずである。また、本明細書中で使用する専門用語は、特定の実施態様を説明する目的のためにのみ提示され、限定する意図はないことが理解できるはずである。
「式を有する」または「構造を有する」との語句は、限定されるとは解釈されず、「含む」との用語が一般に使用されるのと同じ様式で、使用される。
点線で示しαおよびβとして命名した結合は、単結合または不飽和(例えば、二重)結合を表わすが、但し、αおよびβは、両方共に不飽和結合ではあり得ない;
Mは、第8族遷移金属である;
R1およびR2は、別個に、水素、ヒドロカルビル、置換ヒドロカルビル、ヘテロ原子含有ヒドロカルビル、ヘテロ原子含有置換ヒドロカルビル、および官能基から選択される;
Qは、有機ジラジカル、すなわち、ヒドロカルビレン、置換ヒドロカルビレン、ヘテロ原子含有ヒドロカルビレンまたはヘテロ原子含有置換ヒドロカルビレンリンカーであり、さらに、ここで、Q内の隣接原子上の2個またはそれ以上の置換基は、結合されて、追加環状基を形成し得る;
X1およびX2は、アニオン性リガンドであり、そして同一または異なり得る;
L1は、中性電子供与リガンドであり、そしてpは、0または1である;
αが単結合であるとき、L2は、NR7R8、PR7R8、N=CR7R8、およびR7C=NR8から選択され、ここで、R7およびR8は、別個に、置換および/またはヘテロ原子含有C1〜C20アルキル、C2〜C20アルケニル、C2〜C20アルキニル、およびC5〜C24アリールから選択されるか、またはR7およびR8は、一緒になって、複素環を形成できる;
αが不飽和結合(例えば、二重結合)であるとき、L2は、NR7およびPR7から選択され、ここで、R7は、先に定義したとおりである;
YおよびZは、ヒドロカルビレン、置換ヒドロカルビレン、ヘテロ原子含有ヒドロカルビレン、ヘテロ原子含有置換ヒドロカルビレン、−O−、−S−、−NR9−、および−PR9−から別個に選択される連鎖であり、ここで、R9は、ヒドロカルビル、置換ヒドロカルビル、ヘテロ原子含有ヒドロカルビル、およびヘテロ原子含有置換ヒドロカルビルから選択され、さらに、ここで、YおよびZ、またはL2およびZは、芳香環内の隣接原子を表わし得る;
mは、0または1である;そして
nは、0または1である。
Mとして指定される金属は、第8族遷移金属、好ましくは、ルテニウムまたはオスミウムである。特に好ましい実施態様では、Mは、ルテニウムである。
C1〜C20アルコキシ、C5〜C24アリールオキシ、ハロ、カルボキシ(−COOH)、アシル(C2〜C20アルキルカルボニル(−CO−アルキル)およびC6〜C24アリールカルボニル(−CO−アリール)を含めて)、ホルミル(−(CO)−H)、ニトロ(−NO2)、シアノ(−C≡N)、イソシアノ(−N+≡C−)、ヒドロキシル、アシルオキシ(−O−アシル、C2〜C20アルキルカルボニルオキシ(−O−CO−アルキル)およびC6〜C24アリールカルボニルオキシ(−O−CO−アリール)を含めて)、C2〜C20アルコキシカルボニル(−(CO)−O−アルキル)、C6〜C24アリールオキシカルボニル(−(CO)−O−アリール)、C1〜C20アルコキシ置換C1〜C20アルキル、C1〜C20アルコキシ置換C5〜C24アリール、C5〜C24アリールオキシ置換C1〜C20アルキル、C5〜C24アリールオキシ置換C5〜C24アリール、アミノ(−NH2)、イミノ(−CR=NHであって、ここで、R=水素、C1〜C20アルキル、C5〜C24アリール、C6〜C24アルカリール、C6〜C24アラルキルなどである)、C2〜C20アルキルアミド(−NH−(CO)−アルキル)、C6〜C24アリールアミド(−NH−(CO)−アリール)、C1〜C20アルキルスルファニル(−S−アルキル;これはまた、「アルキルチオ」とも称する)、C5〜C24アリールスルファニル(−S−アリール;これはまた、「アリールチオ」とも称する)、C1〜C20アルキルジチオ(−S−S−アルキル)、C5〜C24アリールジチオ(−S−S−アリール)、カルバモイル(−(CO)−NH2);C2〜C20アルキルカルバモイル、(−(CO)−NH−アルキル)、C6〜C20アリールカルバモイル(−(CO)−NH−アリール)、シリル(−SiR3であって、ここで、Rは、水素またはヒドロカルビルである)、シリルオキシ(−O−シリル)、ホスフィノ(−PH2)、ホスホナト(−P(O)(O−)2)、ボリル(−BH2)、ボロノ(−B(OH)2)、またはボロナト(−B(OR)2であって、ここで、Rは、アルキルまたは他のヒドロカルビルである)。
窒素含有複素環、例えば、ピリジン、ビピリジン、ピリダジン、ピリミジン、ビピリダミン、ピラジン、1,3,5−トリアジン、1,2,4−トリアジン、1,2,3−トリアジン、ピロール、2H−ピロール、3H−ピロール、ピラゾール、2H−イミダゾール、1,2,3−トリアゾール、1,2,4−トリアゾール、インドール、3H−インドール、1H−イソインドール、シクロペンタ(ビ)ピリジン、インダゾール、キノリン、ビスキノリン、イソキノリン、ビスイソキノリン、シンノリン、キナゾリン、ナフチリジン、ピペリジン、ピペラジン、ピロリジン、ピラゾリジン、キヌクリジン、イミダゾリジン、ピロリルイミン、プリン、ベンゾイミダゾール、ビスイミダゾール、フェナジン、アクリジン、およびカルバゾール;
酸素含有複素環、例えば、2H−ピラン、4H−ピラン、2−ピロン、4−ピロン、1,2−ジオキシン、1,3−ジオキシン、オキセピン、フラン、2H−1−ベンゾピラン、クマリン、クマロン、クロメン、クロマン−4−オン、イソクロメン−1−オン、イソクロメン−3−オン、キサンテン、テトラヒドロフラン、1,4−ジオキサン、およびジベンゾフラン;および
混合複素環、例えば、イソオキサゾール、オキサゾール、チアゾール、イソチアゾール、1,2,3−オキサジアゾール、1,2,4−オキサジアゾール、1,3,4−オキサジアゾール、1,2,3,4−オキサトリアゾール、1、2,3,5−オキサトリアゾール、3H−1,2,3−ジオキサゾール、3H−1,2−オキサチオール、1,3−オキサチオール、4H−1,2−オキサジン、2H−1,3−オキサジン、1,4−オキサジン、1,2,5−オキサチアジン、o−イソキサジン、フェノキサジン、フェノチアジン、ピラノ[3,4−b]ピロール、インドキサジン、ベンゾオキサゾール、アントラニル、およびモルホリン。
(触媒2aの合成:方法A)
250mL丸底シュリンク(Schlenk)フラスコ(これには、撹拌棒を備え付けた)に、錯体1、(sIMes)(PCy3)(Cl)2Ru=CHPh、(10.0g;11.8mmol)を充填した。このフラスコに蓋をし、15分間にわたってアルゴンを散布し、そしてカニューレを経由して、無水CH2Cl2(118mL)を充填した。次いで、注射器を経由して、2−(3−ブテニル)ピリジン(2.4g、17.7mmol)を加え、その反応混合物を、5〜6時間にわたって、40℃まで加熱した。この反応混合物を乾燥状態まで濃縮し、その残渣を、脱気した冷メタノールで倍散した。フリットにて固形物を集め、そして冷メタノール(2×25mL)で洗浄して、乾燥時に淡緑色固形物として、触媒2a、(sIMes)(Cl)2Ru(CH(CH2)2−C、N−2−C5H4N)−Cs(5.6g;9.4mmol)を得た。収率:80%。
(触媒2aの合成:方法B)
グローブボックスにて、バイアルに、2−(3−ブテニル)ピリジン(24mg、0.18mmol)およびCH2Cl2(2mL)を充填した。次いで、固形物として、錯体3、(sIMes)(py)2(Cl)2Ru=CHPh、(86mg;0.12mmol)を加え、その反応物を、室温で、30分間撹拌した。真空下にて揮発性物質を除去し、その残渣をヘキサンで倍散した。固形物を集め、ヘキサン(2×1mL)で洗浄し、そして真空乾燥して、乾燥時に淡緑色固形物として、触媒2a、(sIMes)(Cl)2Ru(CH(CH2)2−C、N−2−C5H4N)−Cs、(60mg;0.10mmol)を得た。収率:85%。
(触媒2aの触媒2bへの変換)
グローブボックスにて、触媒2aの0.1M CD2Cl2溶液を調製し、そしてNMRチューブに移し、これに蓋を付け、そしてグローブボックスから取り出した。このNMRチューブを、油浴中にて、40℃で放置し、その反応を1H NMR分光法でモニターした。混合物中の2bと2aとの比率は、24時間後、30/70;48時間後、60/40;72時間後、70/30;そして96時間後、78/22であった。
(触媒2bの触媒2aへの変換)
グローブボックスにて、触媒2bの0.1M CD2Cl2溶液を調製し、そしてNMRチューブに移し、これに蓋を付け、そしてグローブボックスから取り出した。このNMRチューブを、油浴中にて、40℃で放置し、その反応を1H NMR分光法でモニターした。混合物中の2bと2aとの比率は、24時間後、83/17であった。1H NMR分光法により、また、2bの異性化がある程度の触媒分解を伴うことが明らかとなり、このことにより、この反応混合物を24時間を超えて分析することが困難となった。
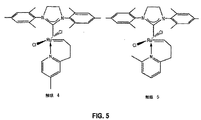
(触媒4の合成)
グローブボックスにて、フラスコに、2−(3−ブテニル)−4−メチルピリジン(40mg、0.27mmol)およびCH2Cl2(5mL)を充填した。次いで、固形物として、錯体3、(sIMes)(py)2(Cl)2Ru=CHPh、(114mg;0.16mmol)を加え、その反応物を、室温で、30分間撹拌した。真空下にて揮発性物質を除去し、その残渣をC6H6(1mL)に再溶解し、そしてペンタン(10mL)で沈殿させた。固形物を集め、ペンタン(3×5mL)で洗浄し、そして真空乾燥して、乾燥時に淡褐色固形物として、触媒4、(sIMes)(Cl)2Ru(CH(CH2)2−C、N−2−(4−Me)−C5H3N)−Cs(80mg;0.13mmol)を得た。収率:84%。
(触媒5の合成)
グローブボックスにて、フラスコに、2−(3−ブテニル)−6−メチルピリジン(50mg、0.34mmol)およびCH2Cl2(5mL)を充填した。次いで、固形物として、錯体3、(sIMes)(py)2(Cl)2Ru=CHPh、(98mg;0.14mmol)を加え、その反応物を、室温で、30分間撹拌した。真空下にて揮発性物質を除去し、その残渣をC6H6(1mL)に再溶解し、そしてペンタン(10mL)で沈殿させた。固形物を集め、ペンタン(3×5mL)で洗浄し、そして真空乾燥して、乾燥時に淡褐色固形物として、触媒5、(sIMes)(Cl)2Ru(CH(CH2)2−C、N−2−(6−Me)−C5H3N)−Cs(57mg;0.094mmol)を得た。収率:69%。
(触媒2bの合成)
220mL丸底シュリンク(Schlenk)フラスコ(これには、撹拌棒を備え付けた)に、錯体1、(sIMes)(PCy3)(Cl)2Ru=CHPh、(5.0g;5.9mmol)を充填した。このフラスコに蓋をし、15分間にわたってアルゴンを散布し、そしてカニューレを経由して、無水CH2Cl2(60mL)を充填した。次いで、注射器を経由して、2−(3−ブテニル)ピリジン(1.2g、8.9mmol)を加え、その反応混合物を、3〜4日間にわたって、40℃まで加熱した。この反応混合物を乾燥状態まで濃縮し、その残渣を、脱気した冷メタノール(15mL)で倍散した。フリットにて固形物を集め、そしてメタノール(2×10mL)で洗浄して、乾燥時に橙色から褐色の固形物として、触媒2b、(sIMes)(Cl)2Ru(CH(CH2)2−C、N−2−C5H4N)−C1、(1.3g;2.2mmol)を得た。収率:37%。
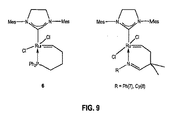
(触媒Ru(C4−PPh2)(6)の合成)
グローブボックスにて、フラスコに、(4−ペンテニル)ジフェニルホスフィン(49mg、0.19mmol)およびCH2Cl2(5mL)を充填した。次いで、固形物として、触媒3、RuCl2(sIMes)(py)2(CHPh)、(127mg;0.17mmol)を加え、その反応物を、室温で、30分間撹拌した。真空下にて揮発性物質を除去し、その残渣をペンタン(2×2mL)で洗浄した。固形物をCH2Cl2(5mL)で再洗浄し、そして12時間にわたって、40℃まで加熱し、その後、真空下にて揮発性物質を除去した。固形物をカラムクロマトグラフィー(5%Et2O/ペンタンに次いで、25%Et2O/ペンタン)で精製し、そして真空乾燥して、乾燥時に淡褐色固形物として、触媒6(59mg;0.082mmol)を得た。収率:47%。
(触媒Ru(Ph−Im)(7)の合成)
グローブボックスにて、フラスコに、触媒3、RuCl2(sIMes)(py)2(CHPh)、(154.7mg;0.21mmol)およびCH2Cl2(5mL)を充填した。次いで、注射器を経由して、(2,2−ジメチル−ペンタ−4−エニリデン)−フェニル−アミン(60mg、0.32mmol)を加え、その反応物を、室温で、15分間撹拌した。真空下にて揮発性物質を除去し、その残渣をペンタン(2×2mL)で洗浄した。固形物をC6H6(2mL)に再溶解し、そしてペンタン(20mL)で沈殿させた。固形物を集め、ペンタン(3×5mL)で洗浄し、そして真空乾燥して、乾燥時にオリーブ緑色固形物として、触媒7(115.6mg;0.18mmol)を得た。収率:83%。
(触媒Ru(Cy−Im)(8)の合成)
グローブボックスにて、フラスコに、触媒3、RuCl2(sIMes)(py)2(CHPh)、(191.5mg;0.26mmol)およびCH2Cl2(5mL)を充填した。次いで、注射器を経由して、(2,2−ジメチル−ペンタ−4−エニリデン)−シクロヘキシル−アミン(74mg、0.38mmol)を加え、その反応物を、室温で、15分間撹拌した。真空下にて揮発性物質を除去し、その残渣をペンタン(2×2mL)で洗浄した。固形物をC6H6(2mL)に再溶解し、そしてペンタン(20mL)で沈殿させた。固形物を集め、ペンタン(3×5mL)で洗浄し、そして真空乾燥して、乾燥時にオリーブ緑色固形物として、触媒8(146.1mg;0.22mmol)を得た。収率:84%。
(触媒Ru(iPr−Im)(9)の合成)
グローブボックスにて、フラスコに、触媒3、触媒3、RuCl2(sIMes)(py)2(CHPh)(239mg;0.33mmol)およびCH2Cl2(5mL)を充填した。次いで、注射器を経由して、(2,2−ジメチル−ペンタ−4−エニリデン)−イソプロピル−アミン(76mg、0.38mmol)を加え、その反応物を、室温で、15分間撹拌した。真空下にて揮発性物質を除去し、その残渣をC6H6(2mL)に再溶解し、そしてペンタン(20mL)で沈殿させた。固形物を集め、ペンタン(3×5mL)で洗浄し、そして真空乾燥して、乾燥時に淡緑色固形物として、触媒9(162mg;0.26mmol)を得た。収率:80%。
(触媒Ru(tBu−Im)(10)の合成)
グローブボックスにて、フラスコに、触媒3、RuCl2(sIMes)(py)2(CHPh)(188mg;0.26mmol)およびCH2Cl2(5mL)を充填した。次いで、注射器を経由して、(2,2−ジメチル−ペンタ−4−エニリデン)−第三級ブチル−アミン(56mg、0.34mmol)を加え、その反応物を、室温で、15分間撹拌した。真空下にて揮発性物質を除去し、その残渣をC6H6(2mL)に再溶解し、そしてペンタン(20mL)で沈殿させた。固形物を集め、ペンタン(3×5mL)で洗浄し、そして真空乾燥して、乾燥時に淡緑色固形物として、触媒10(91mg;0.14mmol)を得た。収率:56%。
(触媒Ru(Me−Im)(11)の合成)
グローブボックスにて、フラスコに、触媒3、RuCl2(sIMes)(py)2(CHPh)(143mg;0.20mmol)およびCH2Cl2(5mL)を充填した。次いで、注射器を経由して、(2,2−ジメチル−ペンタ−4−エニリデン)−メチル−アミン(30mg、0.24mmol)を加え、その反応物を、室温で、30分間撹拌した。真空下にて揮発性物質を除去し、その残渣をC6H6(2mL)に再溶解し、そしてペンタン(20mL)で沈殿させた。固形物を集め、ペンタン(3×5mL)で洗浄し、そして真空乾燥して、乾燥時に緑色−褐色固形物として、触媒11(93mg;0.16mmol)を得た。収率:84%。
(触媒12の合成)
グローブボックスにて、フラスコに、触媒3、RuCl2(sIMes)(PCy3)(CHPh)(5.0g;5.9mmol)およびCH2Cl2(60mL)を充填した。オルト−(N,N)−ジメチルアミノスチレン(1.7g;11.8mmol;2当量)(これは、文献手順(J.Chem.Soc.1958,2302を参照のこと)に従って、調製した)を加え、その反応混合物を、40℃で、不活性雰囲気下にて、24時間撹拌した。真空下にて揮発性物質を除去し、その残渣をメタノール(10mL)で倍散し、そしてフリット付きガラス製漏斗上で固形物を集めた。次いで、この固形物を追加メタノール(2×10mL)およびヘキサン(2×10mL)で洗浄した後、真空乾燥して、緑色固形物として、触媒12(2.8g;4.6mmol)を得た。収率:78%。
(触媒1、2a、2bおよび12の活性:マロン酸ジエチルジアリルのRCM)
異なる触媒を比較する試験反応として、マロン酸ジエチルジアリルの閉環複分解を使用した。触媒1、2a、2bおよび12の比較について:マロン酸ジエチルジアリルの0.1Mジクロロメタン溶液に1mol%の触媒を加え、その反応を25℃で進行させ、そしてガスクロマトグラフィーでモニターした(図10)。図10で示すように、2aは、1よりずっと遅く(使用した条件下にて、100分後、それぞれ、約100%の転化率に対して、20%未満の転化率)、2bは、2aよりずっと遅く(使用した条件下にて、100分後、2%未満の転化率)、そして12は、2bよりずっと遅い。
(触媒2a、4および5の活性:マロン酸ジエチルアリルのRCM)
触媒2a、4および5の活性を比較する試験反応として、マロン酸ジエチルジアリルの閉環複分解を使用した。ドライボックスにて、テフロン(登録商標)隔壁のネジ蓋を取り付けたNMRチューブで、2.5mol%の触媒(0.0052mmol)をC6D6(0.65mL)に溶解した。得られた溶液を、NMRプローブにて、40°Cで、平衡にした。このNMRチューブに、純粋状態で、マロン酸ジエチルジアリル(50μL、0.207mmol、0.30M)を注入し、その反応物を1H NMR分光法でモニターした(図11)。内部標準として使用した残留プロシオ(protio)溶媒ピークを使って、出発物質に対する生成物のオレフィン共鳴積分を測定した。図11で示すように、2aおよび4は、RCMにおいて類似の反応性を示すが、5は、おそらく、そのピリジンリガンド上のオルトメチル基が立体的に混み合っていることが原因で、2aおよび4よりも速く開始することが判明した。
(触媒2a、7および8の活性:マロン酸ジエチルアリルのRCM)
実施例16と同様に、触媒2a、7および8の活性を比較する試験反応として、マロン酸ジエチルジアリルの閉環複分解を使用した。ドライボックスにて、テフロン(登録商標)隔壁のネジ蓋を取り付けたNMRチューブで、2.5mol%の触媒(0.0052mmol)をC6D6(0.65mL)に溶解した。得られた溶液を、NMRプローブにて、40°Cで、平衡にした。このNMRチューブに、純粋状態で、マロン酸ジエチルジアリル(50μL、0.207mmol、0.30M)を注入し、その反応物を1H NMR分光法でモニターした(図12)。内部標準として使用した残留プロシオ(protio)溶媒ピークを使って、出発物質に対する生成物のオレフィン共鳴積分を測定した。図12で示すように、触媒7は、RCMにおいて2aよりも速いのに対して、8は、2aよりも遅い。次いで、前述の試験反応を再度実行して、触媒7、8、9、10および11を比較し、その結果を図13で示す。
(触媒6および8の活性:マロン酸ジエチルアリルのRCM)
実施例16と同様に、触媒6および8の活性を比較する試験反応として、マロン酸ジエチルジアリルの閉環複分解を使用した。ドライボックスにて、テフロン(登録商標)隔壁のネジ蓋を取り付けたNMRチューブで、2.5mol%の触媒(0.0052mmol)をC6D6(0.65mL)に溶解した。得られた溶液を、NMRプローブにて、60°Cで、平衡にした。このNMRチューブに、純粋状態で、マロン酸ジエチルジアリル(50μL、0.207mmol、0.30M)を注入し、その反応物を1H NMR分光法でモニターした(図14)。内部標準として使用した残留プロシオ(protio)溶媒ピークを使って、出発物質に対する生成物のオレフィン共鳴積分を測定した。
(触媒2aおよび2bを使用するジシクロペンタジエン(DCPD)のROMP)
30℃で、触媒(モノマー/触媒=30,000:1 mole:mole)を加えることにより、3.5%のトリシクロペンタジエンを含有するジシクロペンタジエン(100g)を重合させた。触媒2aおよび2bで触媒した重合についての重合発熱を測定し、図15で示す。RCMにおいて触媒2bが2aよりも遅いのと同じ様式で、2bはまた、2aよりもずっとゆっくりと、DCPDのROMPを開始する。2aを使用するDCPDのROMPは、3分以内に、その発熱に達するに対して、2bにより触媒された同じ重合は、25分より長い時間が必要である。
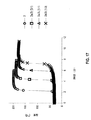
(触媒2aと2bとの混合物を使用するジシクロペンタジエン(DCPD)のROMP)
30℃で、触媒(モノマー/触媒=40,000:1 mole:mole)を加えることにより、3.5%のトリシクロペンタジエンを含有するジシクロペンタジエン(100g)を重合させた。触媒2aと2bとの種々の割合での混合物で触媒した重合についての重合発熱を測定し、図17で示す。
(触媒2a、7および8を使用するジシクロペンタジエン(DCPD)のROMP)
30℃で、触媒(モノマー/触媒=40,000:1 mole:mole)を加えることにより、3.5%のトリシクロペンタジエンを含有するジシクロペンタジエン(100g)を重合させた。触媒2a、Ru(Ph−IM)およびRu(Cy−Im)で触媒した重合についての重合発熱を測定し、図18で示す。
Claims (15)
- 環状構造内にN−複素環カルベンリガンドおよびアルキリデン基を含有させた第8族遷移金属を含む有機金属錯体であって、該錯体は、少なくとも2分間の潜伏期間で、オレフィン複分解反応を触媒できる、有機金属錯体。
- 少なくとも5分間の潜伏期間でオレフィン複分解反応を触媒できる、請求項1に記載の有機金属錯体。
- 前記オレフィン複分解反応が、閉環複分解である、請求項1に記載の有機金属錯体。
- 前記オレフィン複分解反応が、開環複分解重合である、請求項1に記載の有機金属錯体。
- 前記オレフィン複分解反応が、閉環複分解である、請求項2に記載の有機金属錯体。
- 前記オレフィン複分解反応が、開環複分解重合である、請求項2に記載の有機金属錯体。
- 式(I)の構造:
ここで:
αおよびβは、単結合または不飽和結合を表わすが、但し、αおよびβは、両方共に不飽和結合ではあり得ず;
Mは、第8族遷移金属であり;
R1およびR2は、別個に、水素、ヒドロカルビル、置換ヒドロカルビル、ヘテロ原子含有ヒドロカルビル、ヘテロ原子含有置換ヒドロカルビル、および官能基から選択され;
Qは、有機ジラジカルであり;
X1およびX2は、アニオン性リガンドであり、そして同一または異なり得;
L1は、中性電子供与リガンドであり、そしてpは、0または1であり;
αが単結合であるとき、L2は、NR7R8、PR7R8、N=CR7R8、およびR7C=NR8から選択され、ここで、R7およびR8は、別個に、置換および/またはヘテロ原子含有C1〜C20アルキル、C2〜C20アルケニル、C2〜C20アルキニル、およびC5〜C24アリールから選択されるか、またはR7およびR8は、一緒になって、複素環を形成でき;
αが不飽和結合であるとき、L2は、NR7およびPR7から選択され、ここで、R7は、先に定義したとおりであるか、またはL2およびZは、芳香環内の隣接原子を表わし;
YおよびZは、ヒドロカルビレン、置換ヒドロカルビレン、ヘテロ原子含有ヒドロカルビレン、ヘテロ原子含有置換ヒドロカルビレン、−O−、−S−、−NR9−、および−PR9−から別個に選択される結合であり、ここで、R9は、ヒドロカルビル、置換ヒドロカルビル、ヘテロ原子含有ヒドロカルビル、およびヘテロ原子含有置換ヒドロカルビルから選択され、さらに、ここで、YおよびZは、芳香環内の隣接原子を表わし得;
mは、0または1であり;そして
nは、0または1である、
錯体およびそれらの異性体。 - 式(II)の構造:
ここで:
βは、単結合または不飽和結合を表わし;
Mは、第8族遷移金属であり;
R1およびR2は、別個に、水素、ヒドロカルビル、置換ヒドロカルビル、ヘテロ原子含有ヒドロカルビル、ヘテロ原子含有置換ヒドロカルビル、および官能基から選択され;
Qは、有機ジラジカルであり;
X1およびX2は、アニオン性リガンドであり、そして同一または異なり得;
L1は、中性電子供与リガンドであり、そしてpは、0または1であり;
R7およびR8は、別個に、置換および/またはヘテロ原子含有C1〜C20アルキル、C2〜C20アルケニル、C2〜C20アルキニル、およびC5〜C24アリールから選択されるか、またはR7およびR8は、一緒になって、複素環を形成でき;
YおよびZは、ヒドロカルビレン、置換ヒドロカルビレン、ヘテロ原子含有ヒドロカルビレン、ヘテロ原子含有置換ヒドロカルビレン、−O−、−S−、−NR9−、および−PR9−から別個に選択される結合であり、ここで、R9は、ヒドロカルビル、置換ヒドロカルビル、ヘテロ原子含有ヒドロカルビル、およびヘテロ原子含有置換ヒドロカルビルから選択され、さらに、ここで、YおよびZは、芳香環内の隣接原子を表わし得る、
錯体およびそれらの異性体。 - R7およびR8が、C1〜C12アルキルまたはC5〜C12アリールであり、そしてYが、置換または非置換メチレンまたはエチレン結合である、請求項8に記載の錯体。
- 式(III)の構造:
ここで:
βは、単結合または不飽和結合を表わし;
Mは、第8族遷移金属であり;
R1およびR2は、別個に、水素、ヒドロカルビル、置換ヒドロカルビル、ヘテロ原子含有ヒドロカルビル、ヘテロ原子含有置換ヒドロカルビル、および官能基から選択され;
Qは、有機ジラジカルであり;
X1およびX2は、アニオン性リガンドであり、そして同一または異なり得;
L1は、中性電子供与リガンドであり、そしてpは、0または1であり;
R7およびR8は、別個に、置換および/またはヘテロ原子含有C1〜C20アルキル、C2〜C20アルケニル、C2〜C20アルキニル、およびC5〜C24アリールから選択されるか、またはR7およびR8は、一緒になって、複素環を形成でき;
YおよびZは、ヒドロカルビレン、置換ヒドロカルビレン、ヘテロ原子含有ヒドロカルビレン、ヘテロ原子含有置換ヒドロカルビレン、−O−、−S−、−NR9−、および−PR9−から別個に選択される結合であり、ここで、R9は、ヒドロカルビル、置換ヒドロカルビル、ヘテロ原子含有ヒドロカルビル、およびヘテロ原子含有置換ヒドロカルビルから選択され、さらに、ここで、YおよびZは、芳香環内の隣接原子を表わし得る、
錯体およびそれらの異性体。 - R7およびR8が、C1〜C12アルキルまたはC5〜C12アリールであり、そしてYが、置換または非置換メチレンまたはエチレン結合である、請求項10に記載の錯体。
- R7およびR8が、フェニルであり、そしてYが、エチレンである、請求項11に記載の錯体。
- 式(IV)の構造:
ここで:
Mは、第8族遷移金属であり;
R1およびR2は、別個に、水素、ヒドロカルビル、置換ヒドロカルビル、ヘテロ原子含有ヒドロカルビル、ヘテロ原子含有置換ヒドロカルビル、および官能基から選択され;
Qは、有機ジラジカルであり;
X1およびX2は、アニオン性リガンドであり、そして同一または異なり得;
L1は、中性電子供与リガンドであり、そしてpは、0または1であり;
Yは、ヒドロカルビレン、置換ヒドロカルビレン、ヘテロ原子含有ヒドロカルビレン、ヘテロ原子含有置換ヒドロカルビレン、−O−、−S−、−NR9−、および−PR9−から選択される結合であり、ここで、R9は、ヒドロカルビル、置換ヒドロカルビル、ヘテロ原子含有ヒドロカルビル、およびヘテロ原子含有置換ヒドロカルビルから選択される、
錯体およびそれらの異性体。 - 式(V)の構造:
ここで:
Mは、第8族遷移金属であり;
R1およびR2は、別個に、水素、ヒドロカルビル、置換ヒドロカルビル、ヘテロ原子含有ヒドロカルビル、ヘテロ原子含有置換ヒドロカルビル、および官能基から選択され;
Qは、有機ジラジカルであり;
X1およびX2は、アニオン性リガンドであり、そして同一または異なり得;
L1は、中性電子供与リガンドであり、そしてpは、0または1であり;
R7は、置換および/またはヘテロ原子含有C1〜C20アルキル、C2〜C20アルケニル、C2〜C20アルキニル、およびC5〜C24アリールから選択され;
YおよびZは、ヒドロカルビレン、置換ヒドロカルビレン、ヘテロ原子含有ヒドロカルビレン、ヘテロ原子含有置換ヒドロカルビレン、−O−、−S−、−NR9−、および−PR9−から別個に選択される結合であり、ここで、R9は、ヒドロカルビル、置換ヒドロカルビル、ヘテロ原子含有ヒドロカルビル、およびヘテロ原子含有置換ヒドロカルビルから選択される、
錯体およびそれらの異性体。 - オレフィン複分解反応を触媒する方法であって、オレフィン複分解を可能にするように選択された反応条件下で、オレフィン性反応物を、請求項1、7、8、9、10、11、12、13または14のいずれか1項に記載の前記触媒錯体と接触させる工程を包含する、方法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US55774204P | 2004-03-29 | 2004-03-29 | |
| US60415804P | 2004-08-23 | 2004-08-23 | |
| PCT/US2005/010548 WO2005094345A2 (en) | 2004-03-29 | 2005-03-29 | Latent, high-activity olefin metathesis catalysts containing an n-heterocyclic carbene ligand |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2011269459A Division JP5622711B2 (ja) | 2004-03-29 | 2011-12-08 | N−複素環カルベンリガンドを含有する高活性潜伏オレフィン複分解触媒 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2007530706A true JP2007530706A (ja) | 2007-11-01 |
Family
ID=35064307
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2007506479A Withdrawn JP2007530706A (ja) | 2004-03-29 | 2005-03-29 | N−複素環カルベンリガンドを含有する高活性潜伏オレフィン複分解触媒 |
| JP2011269459A Active JP5622711B2 (ja) | 2004-03-29 | 2011-12-08 | N−複素環カルベンリガンドを含有する高活性潜伏オレフィン複分解触媒 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2011269459A Active JP5622711B2 (ja) | 2004-03-29 | 2011-12-08 | N−複素環カルベンリガンドを含有する高活性潜伏オレフィン複分解触媒 |
Country Status (8)
| Country | Link |
|---|---|
| US (3) | US20050261451A1 (ja) |
| EP (1) | EP1735352B1 (ja) |
| JP (2) | JP2007530706A (ja) |
| AU (1) | AU2005228434A1 (ja) |
| BR (1) | BRPI0509322A (ja) |
| MX (1) | MXPA06011302A (ja) |
| PL (1) | PL1735352T3 (ja) |
| WO (1) | WO2005094345A2 (ja) |
Cited By (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2009123209A1 (ja) * | 2008-03-31 | 2009-10-08 | 日本ゼオン株式会社 | 重合性組成物、樹脂成形体、及び架橋樹脂成形体 |
| JP2011521069A (ja) * | 2008-05-22 | 2011-07-21 | リミテッド・ライアビリティ・カンパニー・”ユナイテッド・リサーチ・アンド・デベロップメント・センター” | ジシクロペンタジエンのメタセシス重合触媒、その製造方法および重合方法 |
| JP2012525960A (ja) * | 2009-05-07 | 2012-10-25 | ユミコア・アクチエンゲゼルシャフト・ウント・コムパニー・コマンディットゲゼルシャフト | キレート化アルキリデン配位子を有するルテニウムベースのメタセシス触媒の製造方法 |
| JP2012532954A (ja) * | 2009-07-09 | 2012-12-20 | リミテッド・ライアビリティ・カンパニー・”ユナイテッド・リサーチ・アンド・デベロップメント・センター” | ポリジシクロペンタジエンおよびそれに基づく材料を製造する方法 |
| JP2015516868A (ja) * | 2012-03-14 | 2015-06-18 | ユミコア・アクチエンゲゼルシャフト・ウント・コムパニー・コマンディットゲゼルシャフトUmicore AG & Co.KG | ルテニウムベースのメタセシス触媒およびそれらの製造用前駆体 |
| JP2016511789A (ja) * | 2013-02-27 | 2016-04-21 | マテリア, インコーポレイテッド | 金属カルベンオレフィンメタセシス2種の触媒組成物 |
Families Citing this family (42)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE19815275B4 (de) | 1998-04-06 | 2009-06-25 | Evonik Degussa Gmbh | Alkylidenkomplexe des Rutheniums mit N-heterozyklischen Carbenliganden und deren Verwendung als hochaktive, selektive Katalysatoren für die Olefin-Metathese |
| CN1802341A (zh) * | 2003-01-13 | 2006-07-12 | 卡吉尔公司 | 制备工业化学品的方法 |
| US7037987B2 (en) | 2004-03-26 | 2006-05-02 | Rohn And Haas Company | Olefin polymerization catalyst and polymerization process |
| WO2007081987A2 (en) * | 2006-01-10 | 2007-07-19 | Elevance Renewable Sciences, Inc. | Method of making hydrogenated metathesis products |
| PL379879A1 (pl) | 2006-06-07 | 2007-12-10 | Umicore Ag & Co.Kg. | Kompleksy rutenu i osmu, sposób ich wytwarzania oraz ich zastosowanie jako (pre)katalizatorów reakcji metatezy |
| DE602007002199D1 (de) * | 2006-06-30 | 2009-10-08 | Hoffmann La Roche | Neue rutheniumkomplexe als katalysatoren für metathesereaktionen |
| CN101563315B (zh) | 2006-07-12 | 2013-08-14 | 埃莱文斯可更新科学公司 | 环烯烃与种子油等的开环交叉复分解反应 |
| US8067610B2 (en) | 2006-07-13 | 2011-11-29 | Yann Schrodi | Synthesis of terminal alkenes from internal alkenes and ethylene via olefin metathesis |
| WO2008048520A2 (en) | 2006-10-13 | 2008-04-24 | Elevance Renewable Sciences, Inc. | Methods of making organic compounds by metathesis and hydrocyanation |
| CN102123979A (zh) * | 2006-10-13 | 2011-07-13 | 埃莱文斯可更新科学公司 | 通过烯烃复分解由内烯烃合成末端烯烃的方法 |
| EP3281931A1 (en) * | 2006-10-13 | 2018-02-14 | Elevance Renewable Sciences, Inc. | Methods of making organic compounds by metathesis |
| US8039566B2 (en) | 2006-11-21 | 2011-10-18 | California Institute Of Technology | Olefin metathesis initiators bearing thiazol-2-ylidene ligands |
| DE102007020694A1 (de) | 2007-05-03 | 2008-11-06 | Evonik Degussa Gmbh | Schwefelhaltige Metathesekatalysatoren |
| JP5547631B2 (ja) * | 2007-06-20 | 2014-07-16 | エージェンシー フォー サイエンス, テクノロジー アンド リサーチ | N−複素環式カルベンメタラサイクル触媒およびその方法 |
| JP2012518040A (ja) * | 2009-02-18 | 2012-08-09 | ヘンケル コーポレイション | 熱スイッチ可能なルテニウム開始剤 |
| CN102803433A (zh) * | 2009-05-05 | 2012-11-28 | 斯特潘公司 | 用于提高石油采收率的磺化内烯烃表面活性剂 |
| WO2011043893A2 (en) * | 2009-10-08 | 2011-04-14 | The Regents Of The University Of California | Molecular metal-oxo catalysts for generating hydrogen from water |
| RU2436801C1 (ru) * | 2010-05-27 | 2011-12-20 | Закрытое Акционерное Общество "Сибур Холдинг" | Рутениевый катализатор метатезисной полимеризации дициклопентадиена (варианты) и способ получения полидициклопентадиена (варианты) |
| WO2012121342A1 (ja) * | 2011-03-08 | 2012-09-13 | 日本ゼオン株式会社 | 重合性組成物、樹脂成形体、及び積層体 |
| US8993819B2 (en) | 2011-07-12 | 2015-03-31 | Basf Se | Process for preparing cycloheptene |
| EP2742074A4 (en) * | 2011-08-12 | 2015-04-01 | Exxonmobil Chem Patents Inc | POLYMERS MANUFACTURED BY RING OPENING / CROSS METETHESES |
| US9181360B2 (en) | 2011-08-12 | 2015-11-10 | Exxonmobil Chemical Patents Inc. | Polymers prepared by ring opening / cross metathesis |
| EP2838359A4 (en) | 2012-03-05 | 2015-12-09 | California Inst Of Techn | SYNTHESIS OF Z-OLEFIN-CONTAINING PHEROMONES OF LEPIDOPTERA INSECTS |
| US9598531B2 (en) | 2013-02-27 | 2017-03-21 | Materia, Inc. | Olefin metathesis catalyst compositions comprising at least two metal carbene olefin metathesis catalysts |
| AU2014285077B2 (en) | 2013-07-03 | 2017-09-14 | Materia, Inc. | Liquid molding compositions |
| WO2015076958A1 (en) * | 2013-11-22 | 2015-05-28 | Exxonmobil Chemical Patents Inc. | Novel polyesters containing polyolefin arms |
| US9382354B2 (en) | 2013-11-22 | 2016-07-05 | Exxonmobil Chemical Patents Inc. | Polyesters containing polyolefin arms |
| RU2560151C1 (ru) * | 2014-01-29 | 2015-08-20 | Открытое акционерное общество "Нефтяная компания Роснефть" | Рутениевый катализатор метатезисной полимеризации дициклопентадиена в форме катионного комплекса и способ его получения |
| RU2545176C1 (ru) * | 2014-01-29 | 2015-03-27 | Открытое акционерное общество "Нефтяная компания "Роснефть" | Катализатор метатезисной полимеризации дициклопентадиена и способ его получения |
| RU2545179C1 (ru) * | 2014-01-29 | 2015-03-27 | Открытое акционерное общество "Нефтяная компания "Роснефть" | Катализатор метатезисной полимеризации дициклопентадиена в форме рутениевого комплекса и способ его получения |
| US10501488B2 (en) | 2015-09-24 | 2019-12-10 | Umicore Ag & Co. Kg | Metal carbene olefin metathesis catalysts |
| EP3868890A1 (en) | 2015-11-18 | 2021-08-25 | Provivi, Inc. | Microorganisms for the production of insect pheromones and related compounds |
| WO2017087710A2 (en) | 2015-11-18 | 2017-05-26 | Provivi, Inc. | Production of fatty olefin derivatives via olefin metathesis |
| MX2018006987A (es) * | 2015-12-10 | 2019-05-16 | Umicore Ag & Co Kg | Catalizadores de la metatesis de olefinas. |
| WO2017214133A2 (en) | 2016-06-06 | 2017-12-14 | Provivi, Inc. | Semi-biosynthetic production of fatty alcohols and fatty aldehydes |
| CN109862963B (zh) * | 2016-10-19 | 2022-05-24 | 优美科股份公司及两合公司 | Ru亚烷基络合物的合成与表征 |
| BR112019024258A2 (pt) | 2017-05-17 | 2020-08-18 | Provivi, Inc. | Microorganismos yarrowia lipolytica recombinante e método para produzir um c6-c24 álcool graxo mono- ou poliinsaturado a partir de uma fonte endógena ou exógena de c6-c24 ácidograxo saturado |
| US11242363B2 (en) | 2017-12-01 | 2022-02-08 | University Of Florida Research Foundation, Inc. | Compositions and methods for stereoregular ring expansion metathesis polymerization |
| CN109794292B (zh) * | 2019-01-10 | 2021-12-07 | 天津大学 | Z-选择性钌卡宾烯烃复分解催化剂及其制备方法与应用 |
| PL429476A1 (pl) | 2019-04-02 | 2020-10-05 | Apeiron Synthesis Spółka Akcyjna | Nowe zastosowanie kompleksów metali posiadających ligandy organiczne do aktywacji rutenowych (pre)katalizatorów metatezy olefin |
| EP4157813A1 (en) | 2020-05-29 | 2023-04-05 | ExxonMobil Chemical Patents Inc. | Processes for producing cyclic olefins from polymers and re-polymerization thereof |
| CN111777647A (zh) * | 2020-07-31 | 2020-10-16 | 山东京博中聚新材料有限公司 | 一种共轭二烯烃聚合物中碳-碳双键的连续氢化生产装置和方法 |
Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6107420A (en) * | 1998-07-31 | 2000-08-22 | California Institute Of Technology | Thermally initiated polymerization of olefins using Ruthenium or osmium vinylidene complexes |
| JP2001525417A (ja) * | 1997-12-04 | 2001-12-11 | チバ スペシャルティ ケミカルズ ホールディング インコーポレーテッド | ルテニウム及びオスミウム触媒を含有するヘテロシクリルリガンド |
| JP2002506455A (ja) * | 1997-06-27 | 2002-02-26 | チバ スペシャルティ ケミカルズ ホールディング インコーポレーテッド | 新しい触媒 |
| US20020198426A1 (en) * | 2001-03-30 | 2002-12-26 | Morgan John P. | Selective ring-opening cross-metathesis of cycloolefins |
| WO2003093215A1 (en) * | 2002-04-29 | 2003-11-13 | Dow Global Technologies Inc. | Intergrated chemical processes for industrial utilization of seed oils |
| JP2004506755A (ja) * | 2000-08-10 | 2004-03-04 | トラスティーズ オブ ボストン カレッジ | リサイクル可能メタセシス触媒 |
Family Cites Families (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5312940A (en) | 1992-04-03 | 1994-05-17 | California Institute Of Technology | Ruthenium and osmium metal carbene complexes for olefin metathesis polymerization |
| CA2196061C (en) | 1992-04-03 | 2000-06-13 | Robert H. Grubbs | High activity ruthenium or osmium metal carbene complexes for olefin metathesis reactions and synthesis thereof |
| US5831108A (en) * | 1995-08-03 | 1998-11-03 | California Institute Of Technology | High metathesis activity ruthenium and osmium metal carbene complexes |
| AU6399798A (en) | 1997-03-06 | 1998-09-22 | Ciba Specialty Chemicals Holding Inc. | New catalysts |
| DE19815275B4 (de) | 1998-04-06 | 2009-06-25 | Evonik Degussa Gmbh | Alkylidenkomplexe des Rutheniums mit N-heterozyklischen Carbenliganden und deren Verwendung als hochaktive, selektive Katalysatoren für die Olefin-Metathese |
| KR100823365B1 (ko) | 1999-05-24 | 2008-04-17 | 캘리포니아 인스티튜트 오브 테크놀로지 | 이미다졸리딘계 금속 카르벤 복분해 촉매 |
| US6759537B2 (en) | 2001-03-23 | 2004-07-06 | California Institute Of Technology | Hexacoordinated ruthenium or osmium metal carbene metathesis catalysts |
| JP4295096B2 (ja) * | 2001-08-29 | 2009-07-15 | カリフォルニア インスティチュート オブ テクノロジー | 2個以上のヘテロ原子を含有する架橋された二環式および多環式のオレフィンの開環メタセシス重合 |
-
2005
- 2005-03-29 MX MXPA06011302A patent/MXPA06011302A/es active IP Right Grant
- 2005-03-29 AU AU2005228434A patent/AU2005228434A1/en not_active Abandoned
- 2005-03-29 EP EP05743168.6A patent/EP1735352B1/en active Active
- 2005-03-29 US US11/094,102 patent/US20050261451A1/en not_active Abandoned
- 2005-03-29 PL PL05743168T patent/PL1735352T3/pl unknown
- 2005-03-29 WO PCT/US2005/010548 patent/WO2005094345A2/en active Application Filing
- 2005-03-29 JP JP2007506479A patent/JP2007530706A/ja not_active Withdrawn
- 2005-03-29 BR BRPI0509322-8A patent/BRPI0509322A/pt not_active Application Discontinuation
-
2011
- 2011-12-08 JP JP2011269459A patent/JP5622711B2/ja active Active
-
2013
- 2013-02-27 US US13/779,190 patent/US8871879B2/en active Active
-
2014
- 2014-09-26 US US14/497,387 patent/US9238709B2/en active Active
Patent Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2002506455A (ja) * | 1997-06-27 | 2002-02-26 | チバ スペシャルティ ケミカルズ ホールディング インコーポレーテッド | 新しい触媒 |
| JP2001525417A (ja) * | 1997-12-04 | 2001-12-11 | チバ スペシャルティ ケミカルズ ホールディング インコーポレーテッド | ルテニウム及びオスミウム触媒を含有するヘテロシクリルリガンド |
| US6107420A (en) * | 1998-07-31 | 2000-08-22 | California Institute Of Technology | Thermally initiated polymerization of olefins using Ruthenium or osmium vinylidene complexes |
| JP2004506755A (ja) * | 2000-08-10 | 2004-03-04 | トラスティーズ オブ ボストン カレッジ | リサイクル可能メタセシス触媒 |
| US20020198426A1 (en) * | 2001-03-30 | 2002-12-26 | Morgan John P. | Selective ring-opening cross-metathesis of cycloolefins |
| WO2003093215A1 (en) * | 2002-04-29 | 2003-11-13 | Dow Global Technologies Inc. | Intergrated chemical processes for industrial utilization of seed oils |
Cited By (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2009123209A1 (ja) * | 2008-03-31 | 2009-10-08 | 日本ゼオン株式会社 | 重合性組成物、樹脂成形体、及び架橋樹脂成形体 |
| JP5365625B2 (ja) * | 2008-03-31 | 2013-12-11 | 日本ゼオン株式会社 | 重合性組成物、樹脂成形体、及び架橋樹脂成形体 |
| JP2011521069A (ja) * | 2008-05-22 | 2011-07-21 | リミテッド・ライアビリティ・カンパニー・”ユナイテッド・リサーチ・アンド・デベロップメント・センター” | ジシクロペンタジエンのメタセシス重合触媒、その製造方法および重合方法 |
| JP2012525960A (ja) * | 2009-05-07 | 2012-10-25 | ユミコア・アクチエンゲゼルシャフト・ウント・コムパニー・コマンディットゲゼルシャフト | キレート化アルキリデン配位子を有するルテニウムベースのメタセシス触媒の製造方法 |
| US8846938B2 (en) | 2009-05-07 | 2014-09-30 | Umicore Ag & Co. Kg | Method for preparation of ruthenium-based metathesis catalysts with chelating alkylidene ligands |
| US9562116B2 (en) | 2009-05-07 | 2017-02-07 | Umicore Ag & Co. Kg | Method for preparation of ruthenium-based metathesis catalysts with chelating alkylidene ligands |
| JP2012532954A (ja) * | 2009-07-09 | 2012-12-20 | リミテッド・ライアビリティ・カンパニー・”ユナイテッド・リサーチ・アンド・デベロップメント・センター” | ポリジシクロペンタジエンおよびそれに基づく材料を製造する方法 |
| JP2015516868A (ja) * | 2012-03-14 | 2015-06-18 | ユミコア・アクチエンゲゼルシャフト・ウント・コムパニー・コマンディットゲゼルシャフトUmicore AG & Co.KG | ルテニウムベースのメタセシス触媒およびそれらの製造用前駆体 |
| JP2016511789A (ja) * | 2013-02-27 | 2016-04-21 | マテリア, インコーポレイテッド | 金属カルベンオレフィンメタセシス2種の触媒組成物 |
| JP2018087338A (ja) * | 2013-02-27 | 2018-06-07 | マテリア, インコーポレイテッド | 金属カルベンオレフィンメタセシス2種の触媒組成物 |
Also Published As
| Publication number | Publication date |
|---|---|
| US20130296511A1 (en) | 2013-11-07 |
| JP2012082435A (ja) | 2012-04-26 |
| US8871879B2 (en) | 2014-10-28 |
| EP1735352A2 (en) | 2006-12-27 |
| EP1735352A4 (en) | 2011-05-11 |
| EP1735352B1 (en) | 2019-08-21 |
| BRPI0509322A (pt) | 2007-09-04 |
| WO2005094345A2 (en) | 2005-10-13 |
| PL1735352T3 (pl) | 2020-06-29 |
| AU2005228434A1 (en) | 2005-10-13 |
| WO2005094345A3 (en) | 2006-06-22 |
| JP5622711B2 (ja) | 2014-11-12 |
| US20150141603A1 (en) | 2015-05-21 |
| MXPA06011302A (es) | 2007-01-16 |
| US20050261451A1 (en) | 2005-11-24 |
| US9238709B2 (en) | 2016-01-19 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5622711B2 (ja) | N−複素環カルベンリガンドを含有する高活性潜伏オレフィン複分解触媒 | |
| JP5081620B2 (ja) | オレフィン複分解反応の触媒としてのカチオン性置換基を含む遷移金属カルベン錯体 | |
| KR101835170B1 (ko) | Z-선택적 올레핀 복분해 촉매 및 이들의 합성 절차 | |
| KR100497024B1 (ko) | 고복분해 활성 루테늄 및 오스뮴 금속 카르벤 착화합물 | |
| Wu et al. | Reactions of ruthenium carbenes of the type (PPh3) 2 (X) 2Ru: CH-CH: CPh2 (X= Cl and CF3COO) with strained acyclic olefins and functionalized olefins | |
| US6613910B2 (en) | One-pot synthesis of group 8 transition metal carbene complexes useful as olefin metathesis catalysts | |
| EP2506972B1 (en) | Supported olefin metathesis catalysts | |
| US20030236377A1 (en) | Synthesis of A,B-alternating copolymers by olefin metathesis reactions of cyclic olefins or olefinic polymers with an acyclic diene | |
| JP4922558B2 (ja) | 環状オレフィンモノマーの環挿入重合による大環状ポリマーの合成 | |
| US20030236427A1 (en) | Cross-metathesis of olefins directly substituted with an electron-withdrawing group using transition metal carbene catalysts | |
| AU2012206966A1 (en) | Z-selective olefin metathesis catalysts and their synthetic procedure | |
| CA2442368A1 (en) | Cross-metathesis reaction of functionalized and substituted olefins using group 8 transition metal carbene complexes as metathesis catalysts | |
| JP2009102384A (ja) | シクロオレフィンの選択的開環クロス−メタセシス | |
| JP2005534777A5 (ja) | ||
| WO2017100585A1 (en) | Olefin metathesis catalysts | |
| JP2019526439A (ja) | メタセシス触媒の合成および特性決定 | |
| WO2019158485A1 (en) | Reactions of olefin derivatives in the presence of metathesis catalysts | |
| AU2011205218B2 (en) | Latent, high-activity olefin metathesis catalysts containing an N-heterocyclic carbene ligand | |
| CN101090915A (zh) | 含有n-杂环卡宾配体的潜伏的高活性烯烃置换催化剂 | |
| WO2018191373A1 (en) | Synthesis and characterization of metathesis catalysts |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20080328 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20101214 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20101215 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20110314 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20110322 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20110808 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20111208 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20111216 |
|
| A912 | Re-examination (zenchi) completed and case transferred to appeal board |
Free format text: JAPANESE INTERMEDIATE CODE: A912 Effective date: 20120120 |
|
| A761 | Written withdrawal of application |
Free format text: JAPANESE INTERMEDIATE CODE: A761 Effective date: 20121107 |