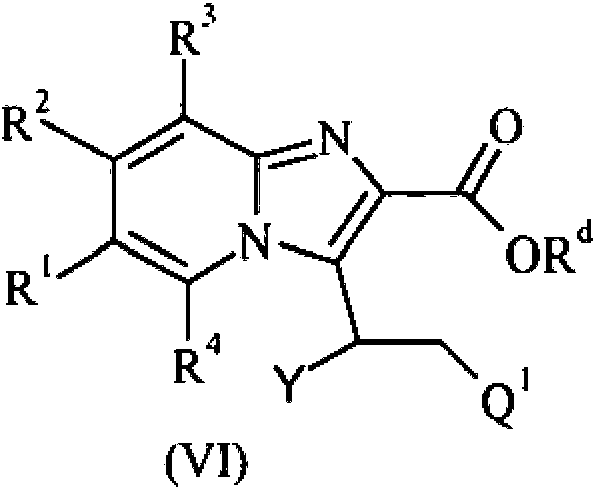
ES2755335T3 - Derivados de imidazoles tricíclicos fusionados como moduladores de la actividad del TNF - Google Patents
Derivados de imidazoles tricíclicos fusionados como moduladores de la actividad del TNF Download PDFInfo
- Publication number
- ES2755335T3 ES2755335T3 ES14808658T ES14808658T ES2755335T3 ES 2755335 T3 ES2755335 T3 ES 2755335T3 ES 14808658 T ES14808658 T ES 14808658T ES 14808658 T ES14808658 T ES 14808658T ES 2755335 T3 ES2755335 T3 ES 2755335T3
- Authority
- ES
- Spain
- Prior art keywords
- alkyl
- hydroxy
- optionally substituted
- heteroaryl
- methyl
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 230000000694 effects Effects 0.000 title description 8
- 150000002460 imidazoles Chemical class 0.000 title description 5
- -1 alkylcarbonyl-C2-6 Chemical group 0.000 claims abstract description 1571
- 150000001875 compounds Chemical class 0.000 claims abstract description 316
- 125000000217 alkyl group Chemical group 0.000 claims abstract description 266
- 125000001424 substituent group Chemical group 0.000 claims abstract description 191
- 229910052739 hydrogen Inorganic materials 0.000 claims abstract description 167
- 239000001257 hydrogen Substances 0.000 claims abstract description 166
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims abstract description 131
- 125000002023 trifluoromethyl group Chemical group FC(F)(F)* 0.000 claims abstract description 129
- 229910052736 halogen Inorganic materials 0.000 claims abstract description 127
- 150000002367 halogens Chemical class 0.000 claims abstract description 116
- 125000004093 cyano group Chemical group *C#N 0.000 claims abstract description 83
- 125000001072 heteroaryl group Chemical group 0.000 claims abstract description 72
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 claims abstract description 68
- 125000003118 aryl group Chemical group 0.000 claims abstract description 64
- 125000004043 oxo group Chemical group O=* 0.000 claims abstract description 60
- 125000004453 alkoxycarbonyl group Chemical group 0.000 claims abstract description 54
- 125000000753 cycloalkyl group Chemical group 0.000 claims abstract description 46
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 claims abstract description 44
- 239000011737 fluorine Substances 0.000 claims abstract description 40
- 229910052731 fluorine Inorganic materials 0.000 claims abstract description 40
- 150000003839 salts Chemical class 0.000 claims abstract description 35
- 125000006272 (C3-C7) cycloalkyl group Chemical group 0.000 claims abstract description 34
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 claims abstract description 33
- 229910052799 carbon Inorganic materials 0.000 claims abstract description 33
- 125000004448 alkyl carbonyl group Chemical group 0.000 claims abstract description 32
- 125000004739 (C1-C6) alkylsulfonyl group Chemical group 0.000 claims abstract description 30
- 125000004397 aminosulfonyl group Chemical group NS(=O)(=O)* 0.000 claims abstract description 30
- 239000000460 chlorine Substances 0.000 claims abstract description 30
- 125000003917 carbamoyl group Chemical group [H]N([H])C(*)=O 0.000 claims abstract description 29
- 229910052801 chlorine Inorganic materials 0.000 claims abstract description 28
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 claims abstract description 27
- 125000002915 carbonyl group Chemical group [*:2]C([*:1])=O 0.000 claims abstract description 25
- 125000003282 alkyl amino group Chemical group 0.000 claims abstract description 24
- 125000004205 trifluoroethyl group Chemical group [H]C([H])(*)C(F)(F)F 0.000 claims abstract description 23
- 125000002485 formyl group Chemical group [H]C(*)=O 0.000 claims abstract description 21
- 125000001028 difluoromethyl group Chemical group [H]C(F)(F)* 0.000 claims abstract description 19
- 125000000876 trifluoromethoxy group Chemical group FC(F)(F)O* 0.000 claims abstract description 17
- 125000004890 (C1-C6) alkylamino group Chemical group 0.000 claims abstract description 15
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical group [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 claims abstract description 15
- 125000005196 alkyl carbonyloxy group Chemical group 0.000 claims abstract description 15
- 125000004663 dialkyl amino group Chemical group 0.000 claims abstract description 15
- 125000004786 difluoromethoxy group Chemical group [H]C(F)(F)O* 0.000 claims abstract description 12
- 125000004473 dialkylaminocarbonyl group Chemical group 0.000 claims abstract description 10
- 125000004971 nitroalkyl group Chemical group 0.000 claims abstract description 9
- 125000002813 thiocarbonyl group Chemical group *C(*)=S 0.000 claims abstract description 9
- 125000003652 trifluoroethoxy group Chemical group FC(CO*)(F)F 0.000 claims abstract description 8
- 125000006700 (C1-C6) alkylthio group Chemical group 0.000 claims abstract description 6
- 125000000472 sulfonyl group Chemical group *S(*)(=O)=O 0.000 claims abstract description 6
- 150000001204 N-oxides Chemical class 0.000 claims abstract description 5
- 125000004966 cyanoalkyl group Chemical group 0.000 claims abstract description 3
- 125000000325 methylidene group Chemical group [H]C([H])=* 0.000 claims abstract 2
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims description 106
- 125000000592 heterocycloalkyl group Chemical group 0.000 claims description 63
- 238000011282 treatment Methods 0.000 claims description 60
- 125000003545 alkoxy group Chemical group 0.000 claims description 42
- 125000004390 alkyl sulfonyl group Chemical group 0.000 claims description 31
- 125000004366 heterocycloalkenyl group Chemical group 0.000 claims description 26
- 125000005115 alkyl carbamoyl group Chemical group 0.000 claims description 22
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims description 17
- 150000001602 bicycloalkyls Chemical group 0.000 claims description 16
- 229910052717 sulfur Inorganic materials 0.000 claims description 16
- 125000003806 alkyl carbonyl amino group Chemical group 0.000 claims description 15
- 125000002757 morpholinyl group Chemical group 0.000 claims description 15
- XEEYBQQBJWHFJM-UHFFFAOYSA-N Iron Chemical compound [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 claims description 14
- 208000035475 disorder Diseases 0.000 claims description 14
- 125000003386 piperidinyl group Chemical group 0.000 claims description 14
- 125000005842 heteroatom Chemical group 0.000 claims description 13
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 claims description 13
- 229910052760 oxygen Inorganic materials 0.000 claims description 13
- 125000003107 substituted aryl group Chemical group 0.000 claims description 13
- 125000003831 tetrazolyl group Chemical group 0.000 claims description 13
- 125000004644 alkyl sulfinyl group Chemical group 0.000 claims description 12
- 125000006216 methylsulfinyl group Chemical group [H]C([H])([H])S(*)=O 0.000 claims description 12
- 125000004193 piperazinyl group Chemical group 0.000 claims description 11
- 125000004181 carboxyalkyl group Chemical group 0.000 claims description 10
- 125000005144 cycloalkylsulfonyl group Chemical group 0.000 claims description 10
- 125000004568 thiomorpholinyl group Chemical group 0.000 claims description 8
- 125000004414 alkyl thio group Chemical group 0.000 claims description 7
- 230000001363 autoimmune Effects 0.000 claims description 7
- 125000002541 furyl group Chemical group 0.000 claims description 7
- AQYSYJUIMQTRMV-UHFFFAOYSA-N hypofluorous acid Chemical group FO AQYSYJUIMQTRMV-UHFFFAOYSA-N 0.000 claims description 7
- 208000027866 inflammatory disease Diseases 0.000 claims description 7
- UXAWXZDXVOYLII-UHFFFAOYSA-N tert-butyl 2,5-diazabicyclo[2.2.1]heptane-2-carboxylate Chemical compound C1C2N(C(=O)OC(C)(C)C)CC1NC2 UXAWXZDXVOYLII-UHFFFAOYSA-N 0.000 claims description 7
- CYRMSUTZVYGINF-UHFFFAOYSA-N trichlorofluoromethane Chemical compound FC(Cl)(Cl)Cl CYRMSUTZVYGINF-UHFFFAOYSA-N 0.000 claims description 7
- 208000024172 Cardiovascular disease Diseases 0.000 claims description 6
- 208000012902 Nervous system disease Diseases 0.000 claims description 6
- 208000030533 eye disease Diseases 0.000 claims description 6
- 125000004029 hydroxymethyl group Chemical group [H]OC([H])([H])* 0.000 claims description 6
- 208000030159 metabolic disease Diseases 0.000 claims description 6
- 208000015122 neurodegenerative disease Diseases 0.000 claims description 6
- 230000000926 neurological effect Effects 0.000 claims description 6
- 230000000771 oncological effect Effects 0.000 claims description 6
- 230000002265 prevention Effects 0.000 claims description 6
- QLXUYKCTEVOUMZ-UHFFFAOYSA-N 2-methylcyclobutane-1,1-diol Chemical compound CC1CCC1(O)O QLXUYKCTEVOUMZ-UHFFFAOYSA-N 0.000 claims description 5
- 208000002193 Pain Diseases 0.000 claims description 5
- 230000003040 nociceptive effect Effects 0.000 claims description 5
- 125000003342 alkenyl group Chemical group 0.000 claims description 4
- 239000003937 drug carrier Substances 0.000 claims description 4
- 239000008194 pharmaceutical composition Substances 0.000 claims description 4
- PXBRQCKWGAHEHS-UHFFFAOYSA-N dichlorodifluoromethane Chemical compound FC(F)(Cl)Cl PXBRQCKWGAHEHS-UHFFFAOYSA-N 0.000 claims description 3
- 238000002560 therapeutic procedure Methods 0.000 claims description 3
- 125000004694 alkoxyaminocarbonyl group Chemical group 0.000 claims description 2
- 125000001188 haloalkyl group Chemical group 0.000 claims description 2
- 125000004356 hydroxy functional group Chemical group O* 0.000 claims 11
- 230000009182 swimming Effects 0.000 claims 3
- 125000001475 halogen functional group Chemical group 0.000 claims 1
- UAEPNZWRGJTJPN-UHFFFAOYSA-N methylcyclohexane Chemical compound CC1CCCCC1 UAEPNZWRGJTJPN-UHFFFAOYSA-N 0.000 claims 1
- 125000002887 hydroxy group Chemical group [H]O* 0.000 abstract description 117
- 125000004169 (C1-C6) alkyl group Chemical group 0.000 abstract description 32
- 125000000882 C2-C6 alkenyl group Chemical group 0.000 abstract description 20
- 125000004457 alkyl amino carbonyl group Chemical group 0.000 abstract description 14
- 125000002768 hydroxyalkyl group Chemical group 0.000 abstract description 13
- 125000004738 (C1-C6) alkyl sulfinyl group Chemical group 0.000 abstract description 12
- 125000004191 (C1-C6) alkoxy group Chemical group 0.000 abstract description 11
- 125000005352 carboxycycloalkyl group Chemical group 0.000 abstract description 11
- 125000004845 (C1-C6) alkylsulfonylamino group Chemical group 0.000 abstract description 6
- 125000004103 aminoalkyl group Chemical group 0.000 abstract description 4
- 125000000171 (C1-C6) haloalkyl group Chemical group 0.000 abstract description 3
- 150000002431 hydrogen Chemical group 0.000 abstract 4
- 125000005094 alkyl carbonyl amino alkyl group Chemical group 0.000 abstract 1
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 103
- 239000000543 intermediate Substances 0.000 description 78
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 71
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 68
- 239000000203 mixture Substances 0.000 description 68
- 239000000243 solution Substances 0.000 description 58
- 238000000034 method Methods 0.000 description 55
- 238000006243 chemical reaction Methods 0.000 description 53
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 51
- 235000019439 ethyl acetate Nutrition 0.000 description 51
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 44
- 238000004895 liquid chromatography mass spectrometry Methods 0.000 description 41
- 239000002904 solvent Substances 0.000 description 41
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 37
- 125000000714 pyrimidinyl group Chemical group 0.000 description 37
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 37
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 35
- 239000007787 solid Substances 0.000 description 35
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 33
- 238000002360 preparation method Methods 0.000 description 32
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 29
- 239000011541 reaction mixture Substances 0.000 description 29
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 28
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 28
- 229910052794 bromium Inorganic materials 0.000 description 28
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 27
- IMNFDUFMRHMDMM-UHFFFAOYSA-N N-Heptane Chemical compound CCCCCCC IMNFDUFMRHMDMM-UHFFFAOYSA-N 0.000 description 26
- 108700012920 TNF Proteins 0.000 description 26
- 239000003921 oil Substances 0.000 description 25
- 235000019198 oils Nutrition 0.000 description 25
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 24
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 24
- 125000003601 C2-C6 alkynyl group Chemical group 0.000 description 24
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 24
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 23
- 239000002253 acid Substances 0.000 description 23
- 125000004170 methylsulfonyl group Chemical group [H]C([H])([H])S(*)(=O)=O 0.000 description 23
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 22
- 239000002585 base Substances 0.000 description 22
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 description 22
- 125000003754 ethoxycarbonyl group Chemical group C(=O)(OCC)* 0.000 description 22
- 229910052757 nitrogen Inorganic materials 0.000 description 22
- 229910052938 sodium sulfate Inorganic materials 0.000 description 22
- 235000011152 sodium sulphate Nutrition 0.000 description 22
- 230000002829 reductive effect Effects 0.000 description 21
- 125000004076 pyridyl group Chemical group 0.000 description 20
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 19
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 19
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 19
- 239000012267 brine Substances 0.000 description 19
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical compound O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 19
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical group N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 18
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 18
- 125000001153 fluoro group Chemical group F* 0.000 description 18
- 238000005160 1H NMR spectroscopy Methods 0.000 description 17
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 17
- 238000003818 flash chromatography Methods 0.000 description 17
- 125000001160 methoxycarbonyl group Chemical group [H]C([H])([H])OC(*)=O 0.000 description 17
- 239000012044 organic layer Substances 0.000 description 17
- 125000002947 alkylene group Chemical group 0.000 description 16
- 238000005481 NMR spectroscopy Methods 0.000 description 15
- 239000013078 crystal Substances 0.000 description 15
- 125000001995 cyclobutyl group Chemical group [H]C1([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 15
- 125000005843 halogen group Chemical group 0.000 description 15
- 239000000725 suspension Substances 0.000 description 15
- 125000002777 acetyl group Chemical group [H]C([H])([H])C(*)=O 0.000 description 14
- 125000000392 cycloalkenyl group Chemical group 0.000 description 14
- CSJLBAMHHLJAAS-UHFFFAOYSA-N diethylaminosulfur trifluoride Chemical compound CCN(CC)S(F)(F)F CSJLBAMHHLJAAS-UHFFFAOYSA-N 0.000 description 14
- 229910052943 magnesium sulfate Inorganic materials 0.000 description 14
- 235000019341 magnesium sulphate Nutrition 0.000 description 14
- 238000003756 stirring Methods 0.000 description 14
- 150000001721 carbon Chemical group 0.000 description 13
- 238000000746 purification Methods 0.000 description 13
- 239000012453 solvate Substances 0.000 description 13
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 12
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 12
- BWHMMNNQKKPAPP-UHFFFAOYSA-L potassium carbonate Chemical compound [K+].[K+].[O-]C([O-])=O BWHMMNNQKKPAPP-UHFFFAOYSA-L 0.000 description 12
- 125000001544 thienyl group Chemical group 0.000 description 12
- 150000001732 carboxylic acid derivatives Chemical class 0.000 description 11
- 239000003054 catalyst Substances 0.000 description 11
- 239000000651 prodrug Substances 0.000 description 11
- 229940002612 prodrug Drugs 0.000 description 11
- UBQKCCHYAOITMY-UHFFFAOYSA-N pyridin-2-ol Chemical class OC1=CC=CC=N1 UBQKCCHYAOITMY-UHFFFAOYSA-N 0.000 description 11
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 11
- 208000023275 Autoimmune disease Diseases 0.000 description 10
- 229910004298 SiO 2 Inorganic materials 0.000 description 10
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 10
- 108060008682 Tumor Necrosis Factor Proteins 0.000 description 10
- 125000004432 carbon atom Chemical group C* 0.000 description 10
- 210000004027 cell Anatomy 0.000 description 10
- 239000007924 injection Substances 0.000 description 10
- 238000002347 injection Methods 0.000 description 10
- 125000003226 pyrazolyl group Chemical group 0.000 description 10
- 125000000335 thiazolyl group Chemical group 0.000 description 10
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical group [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 9
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical group [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 9
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 9
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 9
- 238000001816 cooling Methods 0.000 description 9
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 9
- IXCSERBJSXMMFS-UHFFFAOYSA-N hydrogen chloride Substances Cl.Cl IXCSERBJSXMMFS-UHFFFAOYSA-N 0.000 description 9
- 229910000041 hydrogen chloride Inorganic materials 0.000 description 9
- 239000010410 layer Substances 0.000 description 9
- 239000001301 oxygen Substances 0.000 description 9
- 230000008569 process Effects 0.000 description 9
- 239000000047 product Substances 0.000 description 9
- 125000003373 pyrazinyl group Chemical group 0.000 description 9
- 239000011593 sulfur Chemical group 0.000 description 9
- 125000001412 tetrahydropyranyl group Chemical group 0.000 description 9
- 102000003390 tumor necrosis factor Human genes 0.000 description 9
- GQHTUMJGOHRCHB-UHFFFAOYSA-N 2,3,4,6,7,8,9,10-octahydropyrimido[1,2-a]azepine Chemical compound C1CCCCN2CCCN=C21 GQHTUMJGOHRCHB-UHFFFAOYSA-N 0.000 description 8
- 125000004182 2-chlorophenyl group Chemical group [H]C1=C([H])C(Cl)=C(*)C([H])=C1[H] 0.000 description 8
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 8
- 206010028980 Neoplasm Diseases 0.000 description 8
- 125000004655 dihydropyridinyl group Chemical group N1(CC=CC=C1)* 0.000 description 8
- 150000007529 inorganic bases Chemical class 0.000 description 8
- BDAGIHXWWSANSR-UHFFFAOYSA-N methanoic acid Natural products OC=O BDAGIHXWWSANSR-UHFFFAOYSA-N 0.000 description 8
- 125000001570 methylene group Chemical group [H]C([H])([*:1])[*:2] 0.000 description 8
- 150000007530 organic bases Chemical class 0.000 description 8
- 239000012071 phase Substances 0.000 description 8
- 125000000719 pyrrolidinyl group Chemical group 0.000 description 8
- 229910000104 sodium hydride Inorganic materials 0.000 description 8
- 229910052723 transition metal Inorganic materials 0.000 description 8
- 150000003624 transition metals Chemical class 0.000 description 8
- NLXLAEXVIDQMFP-UHFFFAOYSA-N Ammonium chloride Substances [NH4+].[Cl-] NLXLAEXVIDQMFP-UHFFFAOYSA-N 0.000 description 7
- JGFZNNIVVJXRND-UHFFFAOYSA-N N,N-Diisopropylethylamine (DIPEA) Chemical compound CCN(C(C)C)C(C)C JGFZNNIVVJXRND-UHFFFAOYSA-N 0.000 description 7
- 125000004656 alkyl sulfonylamino group Chemical group 0.000 description 7
- 125000002393 azetidinyl group Chemical group 0.000 description 7
- 125000004618 benzofuryl group Chemical group O1C(=CC2=C1C=CC=C2)* 0.000 description 7
- 201000011510 cancer Diseases 0.000 description 7
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 7
- 125000004446 heteroarylalkyl group Chemical group 0.000 description 7
- 125000001041 indolyl group Chemical group 0.000 description 7
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 7
- 239000002244 precipitate Substances 0.000 description 7
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 6
- IAZDPXIOMUYVGZ-WFGJKAKNSA-N Dimethyl sulfoxide Chemical compound [2H]C([2H])([2H])S(=O)C([2H])([2H])[2H] IAZDPXIOMUYVGZ-WFGJKAKNSA-N 0.000 description 6
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 6
- KEAYESYHFKHZAL-UHFFFAOYSA-N Sodium Chemical compound [Na] KEAYESYHFKHZAL-UHFFFAOYSA-N 0.000 description 6
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 6
- 239000012300 argon atmosphere Substances 0.000 description 6
- JFDZBHWFFUWGJE-UHFFFAOYSA-N benzonitrile Chemical compound N#CC1=CC=CC=C1 JFDZBHWFFUWGJE-UHFFFAOYSA-N 0.000 description 6
- 125000001246 bromo group Chemical group Br* 0.000 description 6
- NXQGGXCHGDYOHB-UHFFFAOYSA-L cyclopenta-1,4-dien-1-yl(diphenyl)phosphane;dichloropalladium;iron(2+) Chemical compound [Fe+2].Cl[Pd]Cl.[CH-]1C=CC(P(C=2C=CC=CC=2)C=2C=CC=CC=2)=C1.[CH-]1C=CC(P(C=2C=CC=CC=2)C=2C=CC=CC=2)=C1 NXQGGXCHGDYOHB-UHFFFAOYSA-L 0.000 description 6
- 125000004472 dialkylaminosulfonyl group Chemical group 0.000 description 6
- 239000000706 filtrate Substances 0.000 description 6
- 238000002875 fluorescence polarization Methods 0.000 description 6
- 125000004216 fluoromethyl group Chemical group [H]C([H])(F)* 0.000 description 6
- 229930182480 glucuronide Natural products 0.000 description 6
- 150000008134 glucuronides Chemical class 0.000 description 6
- 238000010438 heat treatment Methods 0.000 description 6
- 239000005457 ice water Substances 0.000 description 6
- 125000002883 imidazolyl group Chemical group 0.000 description 6
- 230000002757 inflammatory effect Effects 0.000 description 6
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 description 6
- 239000012299 nitrogen atmosphere Substances 0.000 description 6
- 125000004433 nitrogen atom Chemical group N* 0.000 description 6
- NFHFRUOZVGFOOS-UHFFFAOYSA-N palladium;triphenylphosphane Chemical compound [Pd].C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 NFHFRUOZVGFOOS-UHFFFAOYSA-N 0.000 description 6
- 229910000027 potassium carbonate Inorganic materials 0.000 description 6
- 235000011181 potassium carbonates Nutrition 0.000 description 6
- 125000002943 quinolinyl group Chemical group N1=C(C=CC2=CC=CC=C12)* 0.000 description 6
- 235000017557 sodium bicarbonate Nutrition 0.000 description 6
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 6
- 239000012312 sodium hydride Substances 0.000 description 6
- 125000005931 tert-butyloxycarbonyl group Chemical group [H]C([H])([H])C(OC(*)=O)(C([H])([H])[H])C([H])([H])[H] 0.000 description 6
- 125000003718 tetrahydrofuranyl group Chemical group 0.000 description 6
- APOYTRAZFJURPB-UHFFFAOYSA-N 2-methoxy-n-(2-methoxyethyl)-n-(trifluoro-$l^{4}-sulfanyl)ethanamine Chemical compound COCCN(S(F)(F)F)CCOC APOYTRAZFJURPB-UHFFFAOYSA-N 0.000 description 5
- HBAQYPYDRFILMT-UHFFFAOYSA-N 8-[3-(1-cyclopropylpyrazol-4-yl)-1H-pyrazolo[4,3-d]pyrimidin-5-yl]-3-methyl-3,8-diazabicyclo[3.2.1]octan-2-one Chemical class C1(CC1)N1N=CC(=C1)C1=NNC2=C1N=C(N=C2)N1C2C(N(CC1CC2)C)=O HBAQYPYDRFILMT-UHFFFAOYSA-N 0.000 description 5
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 description 5
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 5
- 125000004466 alkoxycarbonylamino group Chemical group 0.000 description 5
- 125000003710 aryl alkyl group Chemical group 0.000 description 5
- 125000000480 butynyl group Chemical group [*]C#CC([H])([H])C([H])([H])[H] 0.000 description 5
- 238000004440 column chromatography Methods 0.000 description 5
- 125000006254 cycloalkyl carbonyl group Chemical group 0.000 description 5
- 125000005215 cycloalkylheteroaryl group Chemical group 0.000 description 5
- 239000003480 eluent Substances 0.000 description 5
- 150000002148 esters Chemical group 0.000 description 5
- 239000000284 extract Substances 0.000 description 5
- 238000001914 filtration Methods 0.000 description 5
- 239000011521 glass Substances 0.000 description 5
- 125000000623 heterocyclic group Chemical group 0.000 description 5
- 125000003453 indazolyl group Chemical group N1N=C(C2=C1C=CC=C2)* 0.000 description 5
- 125000000842 isoxazolyl group Chemical group 0.000 description 5
- 239000000463 material Substances 0.000 description 5
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 5
- IUBQJLUDMLPAGT-UHFFFAOYSA-N potassium bis(trimethylsilyl)amide Chemical compound C[Si](C)(C)N([K])[Si](C)(C)C IUBQJLUDMLPAGT-UHFFFAOYSA-N 0.000 description 5
- 125000002098 pyridazinyl group Chemical group 0.000 description 5
- 108020003175 receptors Proteins 0.000 description 5
- 102000005962 receptors Human genes 0.000 description 5
- 239000012279 sodium borohydride Substances 0.000 description 5
- 229910000033 sodium borohydride Inorganic materials 0.000 description 5
- 125000003944 tolyl group Chemical group 0.000 description 5
- KZPYGQFFRCFCPP-UHFFFAOYSA-N 1,1'-bis(diphenylphosphino)ferrocene Chemical compound [Fe+2].C1=CC=C[C-]1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=C[C-]1P(C=1C=CC=CC=1)C1=CC=CC=C1 KZPYGQFFRCFCPP-UHFFFAOYSA-N 0.000 description 4
- QWVOLCQYBXARGY-UHFFFAOYSA-N 1-chloropyridin-2-one Chemical compound ClN1C=CC=CC1=O QWVOLCQYBXARGY-UHFFFAOYSA-N 0.000 description 4
- GYHSISZNKKTKGW-UHFFFAOYSA-N 2-methylcyclohexane-1,1-diol Chemical compound CC1CCCCC1(O)O GYHSISZNKKTKGW-UHFFFAOYSA-N 0.000 description 4
- OSWFIVFLDKOXQC-UHFFFAOYSA-N 4-(3-methoxyphenyl)aniline Chemical compound COC1=CC=CC(C=2C=CC(N)=CC=2)=C1 OSWFIVFLDKOXQC-UHFFFAOYSA-N 0.000 description 4
- QGZKDVFQNNGYKY-UHFFFAOYSA-N Ammonia Chemical compound N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 description 4
- GAWIXWVDTYZWAW-UHFFFAOYSA-N C[CH]O Chemical group C[CH]O GAWIXWVDTYZWAW-UHFFFAOYSA-N 0.000 description 4
- XTHFKEDIFFGKHM-UHFFFAOYSA-N Dimethoxyethane Chemical compound COCCOC XTHFKEDIFFGKHM-UHFFFAOYSA-N 0.000 description 4
- 206010025323 Lymphomas Diseases 0.000 description 4
- 239000012359 Methanesulfonyl chloride Substances 0.000 description 4
- YNAVUWVOSKDBBP-UHFFFAOYSA-N Morpholine Chemical compound C1COCCN1 YNAVUWVOSKDBBP-UHFFFAOYSA-N 0.000 description 4
- 102000003945 NF-kappa B Human genes 0.000 description 4
- 108010057466 NF-kappa B Proteins 0.000 description 4
- 208000025966 Neurological disease Diseases 0.000 description 4
- KDLHZDBZIXYQEI-UHFFFAOYSA-N Palladium Chemical compound [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 4
- HEDRZPFGACZZDS-MICDWDOJSA-N Trichloro(2H)methane Chemical compound [2H]C(Cl)(Cl)Cl HEDRZPFGACZZDS-MICDWDOJSA-N 0.000 description 4
- DTQVDTLACAAQTR-UHFFFAOYSA-N Trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 description 4
- 125000002877 alkyl aryl group Chemical group 0.000 description 4
- 238000003556 assay Methods 0.000 description 4
- 230000009286 beneficial effect Effects 0.000 description 4
- 125000003236 benzoyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C(*)=O 0.000 description 4
- 230000015572 biosynthetic process Effects 0.000 description 4
- 125000006001 difluoroethyl group Chemical group 0.000 description 4
- 125000006263 dimethyl aminosulfonyl group Chemical group [H]C([H])([H])N(C([H])([H])[H])S(*)(=O)=O 0.000 description 4
- 235000019253 formic acid Nutrition 0.000 description 4
- 238000009472 formulation Methods 0.000 description 4
- 230000006870 function Effects 0.000 description 4
- 125000001841 imino group Chemical group [H]N=* 0.000 description 4
- 208000032839 leukemia Diseases 0.000 description 4
- 239000007788 liquid Substances 0.000 description 4
- 230000014759 maintenance of location Effects 0.000 description 4
- QARBMVPHQWIHKH-UHFFFAOYSA-N methanesulfonyl chloride Chemical compound CS(Cl)(=O)=O QARBMVPHQWIHKH-UHFFFAOYSA-N 0.000 description 4
- 125000006261 methyl amino sulfonyl group Chemical group [H]N(C([H])([H])[H])S(*)(=O)=O 0.000 description 4
- 125000004458 methylaminocarbonyl group Chemical group [H]N(C(*)=O)C([H])([H])[H] 0.000 description 4
- 239000002480 mineral oil Substances 0.000 description 4
- 235000010446 mineral oil Nutrition 0.000 description 4
- 238000002156 mixing Methods 0.000 description 4
- 239000012074 organic phase Substances 0.000 description 4
- 125000003566 oxetanyl group Chemical group 0.000 description 4
- XHXFXVLFKHQFAL-UHFFFAOYSA-N phosphoryl trichloride Chemical compound ClP(Cl)(Cl)=O XHXFXVLFKHQFAL-UHFFFAOYSA-N 0.000 description 4
- IVDFJHOHABJVEH-UHFFFAOYSA-N pinacol Chemical compound CC(C)(O)C(C)(C)O IVDFJHOHABJVEH-UHFFFAOYSA-N 0.000 description 4
- SCVFZCLFOSHCOH-UHFFFAOYSA-M potassium acetate Chemical compound [K+].CC([O-])=O SCVFZCLFOSHCOH-UHFFFAOYSA-M 0.000 description 4
- 238000002953 preparative HPLC Methods 0.000 description 4
- 125000006239 protecting group Chemical group 0.000 description 4
- 238000010992 reflux Methods 0.000 description 4
- 239000000377 silicon dioxide Substances 0.000 description 4
- 125000000547 substituted alkyl group Chemical group 0.000 description 4
- 238000003786 synthesis reaction Methods 0.000 description 4
- 238000012360 testing method Methods 0.000 description 4
- FPGGTKZVZWFYPV-UHFFFAOYSA-M tetrabutylammonium fluoride Chemical compound [F-].CCCC[N+](CCCC)(CCCC)CCCC FPGGTKZVZWFYPV-UHFFFAOYSA-M 0.000 description 4
- 125000001984 thiazolidinyl group Chemical group 0.000 description 4
- AQRLNPVMDITEJU-UHFFFAOYSA-N triethylsilane Chemical compound CC[SiH](CC)CC AQRLNPVMDITEJU-UHFFFAOYSA-N 0.000 description 4
- 239000003981 vehicle Substances 0.000 description 4
- 239000003643 water by type Substances 0.000 description 4
- BANWBNLRSDINSG-UHFFFAOYSA-N 1-fluoropyridin-2-one Chemical compound FN1C=CC=CC1=O BANWBNLRSDINSG-UHFFFAOYSA-N 0.000 description 3
- DVVGIUUJYPYENY-UHFFFAOYSA-N 1-methylpyridin-2-one Chemical compound CN1C=CC=CC1=O DVVGIUUJYPYENY-UHFFFAOYSA-N 0.000 description 3
- 125000004214 1-pyrrolidinyl group Chemical group [H]C1([H])N(*)C([H])([H])C([H])([H])C1([H])[H] 0.000 description 3
- RAXXELZNTBOGNW-UHFFFAOYSA-N 1H-imidazole Chemical compound C1=CNC=N1 RAXXELZNTBOGNW-UHFFFAOYSA-N 0.000 description 3
- 125000001731 2-cyanoethyl group Chemical group [H]C([H])(*)C([H])([H])C#N 0.000 description 3
- NHQDETIJWKXCTC-UHFFFAOYSA-N 3-chloroperbenzoic acid Chemical compound OOC(=O)C1=CC=CC(Cl)=C1 NHQDETIJWKXCTC-UHFFFAOYSA-N 0.000 description 3
- GGHBRLQYBZMEPV-UHFFFAOYSA-N 5-bromo-4-fluoropyridin-2-amine Chemical compound NC1=CC(F)=C(Br)C=N1 GGHBRLQYBZMEPV-UHFFFAOYSA-N 0.000 description 3
- BZTDTCNHAFUJOG-UHFFFAOYSA-N 6-carboxyfluorescein Chemical compound C12=CC=C(O)C=C2OC2=CC(O)=CC=C2C11OC(=O)C2=CC=C(C(=O)O)C=C21 BZTDTCNHAFUJOG-UHFFFAOYSA-N 0.000 description 3
- WFDIJRYMOXRFFG-UHFFFAOYSA-N Acetic anhydride Chemical compound CC(=O)OC(C)=O WFDIJRYMOXRFFG-UHFFFAOYSA-N 0.000 description 3
- 208000030760 Anaemia of chronic disease Diseases 0.000 description 3
- 239000004215 Carbon black (E152) Substances 0.000 description 3
- WSFSSNUMVMOOMR-UHFFFAOYSA-N Formaldehyde Chemical compound O=C WSFSSNUMVMOOMR-UHFFFAOYSA-N 0.000 description 3
- 206010018364 Glomerulonephritis Diseases 0.000 description 3
- WMFOQBRAJBCJND-UHFFFAOYSA-M Lithium hydroxide Chemical compound [Li+].[OH-] WMFOQBRAJBCJND-UHFFFAOYSA-M 0.000 description 3
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 3
- GLUUGHFHXGJENI-UHFFFAOYSA-N Piperazine Chemical compound C1CNCCN1 GLUUGHFHXGJENI-UHFFFAOYSA-N 0.000 description 3
- KWYUFKZDYYNOTN-UHFFFAOYSA-M Potassium hydroxide Chemical compound [OH-].[K+] KWYUFKZDYYNOTN-UHFFFAOYSA-M 0.000 description 3
- 208000006664 Precursor Cell Lymphoblastic Leukemia-Lymphoma Diseases 0.000 description 3
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 3
- 210000001744 T-lymphocyte Anatomy 0.000 description 3
- 230000004913 activation Effects 0.000 description 3
- 201000011040 acute kidney failure Diseases 0.000 description 3
- 150000001350 alkyl halides Chemical class 0.000 description 3
- 125000005213 alkyl heteroaryl group Chemical group 0.000 description 3
- 235000019270 ammonium chloride Nutrition 0.000 description 3
- 208000022400 anemia due to chronic disease Diseases 0.000 description 3
- 206010003246 arthritis Diseases 0.000 description 3
- 239000012298 atmosphere Substances 0.000 description 3
- 125000004429 atom Chemical group 0.000 description 3
- 125000004566 azetidin-1-yl group Chemical group N1(CCC1)* 0.000 description 3
- 125000002057 carboxymethyl group Chemical group [H]OC(=O)C([H])([H])[*] 0.000 description 3
- 238000009903 catalytic hydrogenation reaction Methods 0.000 description 3
- 239000003153 chemical reaction reagent Substances 0.000 description 3
- 239000003795 chemical substances by application Substances 0.000 description 3
- 125000000068 chlorophenyl group Chemical group 0.000 description 3
- 239000012043 crude product Substances 0.000 description 3
- 125000000596 cyclohexenyl group Chemical group C1(=CCCCC1)* 0.000 description 3
- 125000004210 cyclohexylmethyl group Chemical group [H]C([H])(*)C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C1([H])[H] 0.000 description 3
- 238000001514 detection method Methods 0.000 description 3
- 125000002147 dimethylamino group Chemical group [H]C([H])([H])N(*)C([H])([H])[H] 0.000 description 3
- 201000010099 disease Diseases 0.000 description 3
- 125000003005 eta(1)-cyclopentadienyl group Chemical group [H]C1([*])C([H])=C([H])C([H])=C1[H] 0.000 description 3
- VEEVHDVCAUZBBT-UHFFFAOYSA-N ethyl 6-bromo-3-[chloro(phenyl)methyl]-7-fluoroimidazo[1,2-a]pyridine-2-carboxylate Chemical compound CCOC(=O)C1=C(C(Cl)C2=CC=CC=C2)N2C=C(Br)C(F)=CC2=N1 VEEVHDVCAUZBBT-UHFFFAOYSA-N 0.000 description 3
- IBKYSHHPPXLSJK-UHFFFAOYSA-N ethyl 6-bromo-7-fluoro-3-formylimidazo[1,2-a]pyridine-2-carboxylate Chemical compound CCOC(=O)C1=C(C=O)N2C=C(Br)C(F)=CC2=N1 IBKYSHHPPXLSJK-UHFFFAOYSA-N 0.000 description 3
- 229930195733 hydrocarbon Natural products 0.000 description 3
- 238000005984 hydrogenation reaction Methods 0.000 description 3
- 230000005764 inhibitory process Effects 0.000 description 3
- 229910052500 inorganic mineral Inorganic materials 0.000 description 3
- IUYHWZFSGMZEOG-UHFFFAOYSA-M magnesium;propane;chloride Chemical compound [Mg+2].[Cl-].C[CH-]C IUYHWZFSGMZEOG-UHFFFAOYSA-M 0.000 description 3
- 230000036210 malignancy Effects 0.000 description 3
- 235000010755 mineral Nutrition 0.000 description 3
- 239000011707 mineral Substances 0.000 description 3
- 125000004573 morpholin-4-yl group Chemical group N1(CCOCC1)* 0.000 description 3
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 3
- 210000000056 organ Anatomy 0.000 description 3
- 125000004194 piperazin-1-yl group Chemical group [H]N1C([H])([H])C([H])([H])N(*)C([H])([H])C1([H])[H] 0.000 description 3
- 125000000587 piperidin-1-yl group Chemical group [H]C1([H])N(*)C([H])([H])C([H])([H])C([H])([H])C1([H])[H] 0.000 description 3
- 239000003755 preservative agent Substances 0.000 description 3
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 3
- 125000006513 pyridinyl methyl group Chemical group 0.000 description 3
- 238000003571 reporter gene assay Methods 0.000 description 3
- 229920006395 saturated elastomer Polymers 0.000 description 3
- 238000000926 separation method Methods 0.000 description 3
- 229910000029 sodium carbonate Inorganic materials 0.000 description 3
- 235000017550 sodium carbonate Nutrition 0.000 description 3
- 239000011780 sodium chloride Substances 0.000 description 3
- FVAUCKIRQBBSSJ-UHFFFAOYSA-M sodium iodide Chemical compound [Na+].[I-] FVAUCKIRQBBSSJ-UHFFFAOYSA-M 0.000 description 3
- 239000003826 tablet Substances 0.000 description 3
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 3
- 125000001425 triazolyl group Chemical group 0.000 description 3
- DNIAPMSPPWPWGF-VKHMYHEASA-N (+)-propylene glycol Chemical compound C[C@H](O)CO DNIAPMSPPWPWGF-VKHMYHEASA-N 0.000 description 2
- CYPYTURSJDMMMP-WVCUSYJESA-N (1e,4e)-1,5-diphenylpenta-1,4-dien-3-one;palladium Chemical compound [Pd].[Pd].C=1C=CC=CC=1\C=C\C(=O)\C=C\C1=CC=CC=C1.C=1C=CC=CC=1\C=C\C(=O)\C=C\C1=CC=CC=C1.C=1C=CC=CC=1\C=C\C(=O)\C=C\C1=CC=CC=C1 CYPYTURSJDMMMP-WVCUSYJESA-N 0.000 description 2
- 125000004916 (C1-C6) alkylcarbonyl group Chemical group 0.000 description 2
- 125000006642 (C1-C6) cyanoalkyl group Chemical group 0.000 description 2
- DYLIWHYUXAJDOJ-OWOJBTEDSA-N (e)-4-(6-aminopurin-9-yl)but-2-en-1-ol Chemical compound NC1=NC=NC2=C1N=CN2C\C=C\CO DYLIWHYUXAJDOJ-OWOJBTEDSA-N 0.000 description 2
- YPFDHNVEDLHUCE-UHFFFAOYSA-N 1,3-propanediol Substances OCCCO YPFDHNVEDLHUCE-UHFFFAOYSA-N 0.000 description 2
- NDOVLWQBFFJETK-UHFFFAOYSA-N 1,4-thiazinane 1,1-dioxide Chemical compound O=S1(=O)CCNCC1 NDOVLWQBFFJETK-UHFFFAOYSA-N 0.000 description 2
- LMDZBCPBFSXMTL-UHFFFAOYSA-N 1-ethyl-3-(3-dimethylaminopropyl)carbodiimide Chemical compound CCN=C=NCCCN(C)C LMDZBCPBFSXMTL-UHFFFAOYSA-N 0.000 description 2
- LTMRRSWNXVJMBA-UHFFFAOYSA-L 2,2-diethylpropanedioate Chemical compound CCC(CC)(C([O-])=O)C([O-])=O LTMRRSWNXVJMBA-UHFFFAOYSA-L 0.000 description 2
- HBEDSQVIWPRPAY-UHFFFAOYSA-N 2,3-dihydrobenzofuran Chemical compound C1=CC=C2OCCC2=C1 HBEDSQVIWPRPAY-UHFFFAOYSA-N 0.000 description 2
- QPBNHDFPMRENBC-UHFFFAOYSA-N 2-(difluoromethoxy)benzaldehyde Chemical compound FC(F)OC1=CC=CC=C1C=O QPBNHDFPMRENBC-UHFFFAOYSA-N 0.000 description 2
- JWYOAMOZLZXDER-UHFFFAOYSA-N 2-azaniumylcyclopentane-1-carboxylate Chemical compound NC1CCCC1C(O)=O JWYOAMOZLZXDER-UHFFFAOYSA-N 0.000 description 2
- 125000004204 2-methoxyphenyl group Chemical group [H]C1=C([H])C(*)=C(OC([H])([H])[H])C([H])=C1[H] 0.000 description 2
- 125000004179 3-chlorophenyl group Chemical group [H]C1=C([H])C(*)=C([H])C(Cl)=C1[H] 0.000 description 2
- MUZTUTPHGAUQBX-UHFFFAOYSA-N 6-bromo-3-[2-carboxy-1-[2-(trifluoromethoxy)phenyl]ethyl]-7-fluoroimidazo[1,2-a]pyridine-2-carboxylic acid Chemical compound OC(=O)CC(C1=C(N=C2C=C(F)C(Br)=CN12)C(O)=O)C1=C(OC(F)(F)F)C=CC=C1 MUZTUTPHGAUQBX-UHFFFAOYSA-N 0.000 description 2
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical group [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 2
- 208000024893 Acute lymphoblastic leukemia Diseases 0.000 description 2
- 208000031261 Acute myeloid leukaemia Diseases 0.000 description 2
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 description 2
- 125000006577 C1-C6 hydroxyalkyl group Chemical group 0.000 description 2
- 108010029697 CD40 Ligand Proteins 0.000 description 2
- 102100032937 CD40 ligand Human genes 0.000 description 2
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 description 2
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 2
- 229910021595 Copper(I) iodide Inorganic materials 0.000 description 2
- 208000011231 Crohn disease Diseases 0.000 description 2
- 238000006646 Dess-Martin oxidation reaction Methods 0.000 description 2
- ZAFNJMIOTHYJRJ-UHFFFAOYSA-N Diisopropyl ether Chemical compound CC(C)OC(C)C ZAFNJMIOTHYJRJ-UHFFFAOYSA-N 0.000 description 2
- 208000017701 Endocrine disease Diseases 0.000 description 2
- 108010008165 Etanercept Proteins 0.000 description 2
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical compound OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 description 2
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 2
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 2
- 208000035490 Megakaryoblastic Acute Leukemia Diseases 0.000 description 2
- BAPJBEWLBFYGME-UHFFFAOYSA-N Methyl acrylate Chemical compound COC(=O)C=C BAPJBEWLBFYGME-UHFFFAOYSA-N 0.000 description 2
- 101000574441 Mus musculus Alkaline phosphatase, germ cell type Proteins 0.000 description 2
- 208000033776 Myeloid Acute Leukemia Diseases 0.000 description 2
- SECXISVLQFMRJM-UHFFFAOYSA-N N-Methylpyrrolidone Chemical compound CN1CCCC1=O SECXISVLQFMRJM-UHFFFAOYSA-N 0.000 description 2
- PCLIMKBDDGJMGD-UHFFFAOYSA-N N-bromosuccinimide Chemical compound BrN1C(=O)CCC1=O PCLIMKBDDGJMGD-UHFFFAOYSA-N 0.000 description 2
- DFPAKSUCGFBDDF-UHFFFAOYSA-N Nicotinamide Chemical compound NC(=O)C1=CC=CN=C1 DFPAKSUCGFBDDF-UHFFFAOYSA-N 0.000 description 2
- 208000015914 Non-Hodgkin lymphomas Diseases 0.000 description 2
- 208000036576 Obstructive uropathy Diseases 0.000 description 2
- 235000019502 Orange oil Nutrition 0.000 description 2
- 239000004264 Petrolatum Substances 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 2
- SMWDFEZZVXVKRB-UHFFFAOYSA-N Quinoline Chemical compound N1=CC=CC2=CC=CC=C21 SMWDFEZZVXVKRB-UHFFFAOYSA-N 0.000 description 2
- 208000017442 Retinal disease Diseases 0.000 description 2
- 206010038923 Retinopathy Diseases 0.000 description 2
- WQDUMFSSJAZKTM-UHFFFAOYSA-N Sodium methoxide Chemical compound [Na+].[O-]C WQDUMFSSJAZKTM-UHFFFAOYSA-N 0.000 description 2
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 2
- 239000007983 Tris buffer Substances 0.000 description 2
- 206010067584 Type 1 diabetes mellitus Diseases 0.000 description 2
- XSQUKJJJFZCRTK-UHFFFAOYSA-N Urea Chemical compound NC(N)=O XSQUKJJJFZCRTK-UHFFFAOYSA-N 0.000 description 2
- 239000004480 active ingredient Substances 0.000 description 2
- 239000008186 active pharmaceutical agent Substances 0.000 description 2
- 208000013593 acute megakaryoblastic leukemia Diseases 0.000 description 2
- 208000020700 acute megakaryocytic leukemia Diseases 0.000 description 2
- 206010064930 age-related macular degeneration Diseases 0.000 description 2
- 150000001299 aldehydes Chemical class 0.000 description 2
- 150000008044 alkali metal hydroxides Chemical class 0.000 description 2
- 125000005090 alkenylcarbonyl group Chemical group 0.000 description 2
- 125000005091 alkenylcarbonylamino group Chemical group 0.000 description 2
- 125000000033 alkoxyamino group Chemical group 0.000 description 2
- 125000004949 alkyl amino carbonyl amino group Chemical group 0.000 description 2
- 125000005278 alkyl sulfonyloxy group Chemical group 0.000 description 2
- 125000005530 alkylenedioxy group Chemical group 0.000 description 2
- 150000001408 amides Chemical class 0.000 description 2
- 125000004202 aminomethyl group Chemical group [H]N([H])C([H])([H])* 0.000 description 2
- 229910021529 ammonia Inorganic materials 0.000 description 2
- 238000004458 analytical method Methods 0.000 description 2
- 125000003725 azepanyl group Chemical group 0.000 description 2
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 2
- 125000000051 benzyloxy group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])O* 0.000 description 2
- MUALRAIOVNYAIW-UHFFFAOYSA-N binap Chemical compound C1=CC=CC=C1P(C=1C(=C2C=CC=CC2=CC=1)C=1C2=CC=CC=C2C=CC=1P(C=1C=CC=CC=1)C=1C=CC=CC=1)C1=CC=CC=C1 MUALRAIOVNYAIW-UHFFFAOYSA-N 0.000 description 2
- 238000004166 bioassay Methods 0.000 description 2
- 230000037396 body weight Effects 0.000 description 2
- 229910052796 boron Inorganic materials 0.000 description 2
- IAQRGUVFOMOMEM-UHFFFAOYSA-N but-2-ene Chemical group CC=CC IAQRGUVFOMOMEM-UHFFFAOYSA-N 0.000 description 2
- QNRMTGGDHLBXQZ-UHFFFAOYSA-N buta-1,2-diene Chemical group CC=C=C QNRMTGGDHLBXQZ-UHFFFAOYSA-N 0.000 description 2
- FJDQFPXHSGXQBY-UHFFFAOYSA-L caesium carbonate Chemical compound [Cs+].[Cs+].[O-]C([O-])=O FJDQFPXHSGXQBY-UHFFFAOYSA-L 0.000 description 2
- 229910000024 caesium carbonate Inorganic materials 0.000 description 2
- IJOOHPMOJXWVHK-UHFFFAOYSA-N chlorotrimethylsilane Chemical compound C[Si](C)(C)Cl IJOOHPMOJXWVHK-UHFFFAOYSA-N 0.000 description 2
- DQLATGHUWYMOKM-UHFFFAOYSA-L cisplatin Chemical compound N[Pt](N)(Cl)Cl DQLATGHUWYMOKM-UHFFFAOYSA-L 0.000 description 2
- 229960004316 cisplatin Drugs 0.000 description 2
- 238000007796 conventional method Methods 0.000 description 2
- LSXDOTMGLUJQCM-UHFFFAOYSA-M copper(i) iodide Chemical compound I[Cu] LSXDOTMGLUJQCM-UHFFFAOYSA-M 0.000 description 2
- OPQARKPSCNTWTJ-UHFFFAOYSA-L copper(ii) acetate Chemical compound [Cu+2].CC([O-])=O.CC([O-])=O OPQARKPSCNTWTJ-UHFFFAOYSA-L 0.000 description 2
- 238000005859 coupling reaction Methods 0.000 description 2
- 238000002425 crystallisation Methods 0.000 description 2
- 230000008025 crystallization Effects 0.000 description 2
- 125000001047 cyclobutenyl group Chemical group C1(=CCC1)* 0.000 description 2
- 125000006637 cyclobutyl carbonyl group Chemical group 0.000 description 2
- 125000001162 cycloheptenyl group Chemical group C1(=CCCCCC1)* 0.000 description 2
- 125000000582 cycloheptyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 2
- 125000002433 cyclopentenyl group Chemical group C1(=CCCC1)* 0.000 description 2
- 230000001419 dependent effect Effects 0.000 description 2
- NKLCNNUWBJBICK-UHFFFAOYSA-N dess–martin periodinane Chemical compound C1=CC=C2I(OC(=O)C)(OC(C)=O)(OC(C)=O)OC(=O)C2=C1 NKLCNNUWBJBICK-UHFFFAOYSA-N 0.000 description 2
- 125000004188 dichlorophenyl group Chemical group 0.000 description 2
- HPNMFZURTQLUMO-UHFFFAOYSA-N diethylamine Chemical compound CCNCC HPNMFZURTQLUMO-UHFFFAOYSA-N 0.000 description 2
- 238000010790 dilution Methods 0.000 description 2
- 239000012895 dilution Substances 0.000 description 2
- 125000005805 dimethoxy phenyl group Chemical group 0.000 description 2
- 125000006222 dimethylaminomethyl group Chemical group [H]C([H])([H])N(C([H])([H])[H])C([H])([H])* 0.000 description 2
- 150000002009 diols Chemical class 0.000 description 2
- MKRTXPORKIRPDG-UHFFFAOYSA-N diphenylphosphoryl azide Chemical compound C=1C=CC=CC=1P(=O)(N=[N+]=[N-])C1=CC=CC=C1 MKRTXPORKIRPDG-UHFFFAOYSA-N 0.000 description 2
- 239000002552 dosage form Substances 0.000 description 2
- 239000003814 drug Substances 0.000 description 2
- AFEHIDBGTQYTEB-UHFFFAOYSA-N ethyl 6-bromo-7-fluoro-3-iodoimidazo[1,2-a]pyridine-2-carboxylate Chemical compound CCOC(=O)C1=C(I)N2C=C(Br)C(F)=CC2=N1 AFEHIDBGTQYTEB-UHFFFAOYSA-N 0.000 description 2
- SXMPAXHNNFSQFY-UHFFFAOYSA-N ethyl 6-bromo-7-fluoroimidazo[1,2-a]pyridine-2-carboxylate Chemical compound BrC=1C(=CC=2N(C1)C=C(N2)C(=O)OCC)F SXMPAXHNNFSQFY-UHFFFAOYSA-N 0.000 description 2
- PQJJJMRNHATNKG-UHFFFAOYSA-N ethyl bromoacetate Chemical compound CCOC(=O)CBr PQJJJMRNHATNKG-UHFFFAOYSA-N 0.000 description 2
- 238000001704 evaporation Methods 0.000 description 2
- 230000008020 evaporation Effects 0.000 description 2
- 125000000524 functional group Chemical group 0.000 description 2
- 108020001507 fusion proteins Proteins 0.000 description 2
- 102000037865 fusion proteins Human genes 0.000 description 2
- 239000007789 gas Substances 0.000 description 2
- 125000005191 hydroxyalkylamino group Chemical group 0.000 description 2
- 125000004464 hydroxyphenyl group Chemical group 0.000 description 2
- VRZXJLHKXVOHJE-UHFFFAOYSA-N imidazo[1,2-a]pyridin-3-ol Chemical compound C1=CC=CN2C(O)=CN=C21 VRZXJLHKXVOHJE-UHFFFAOYSA-N 0.000 description 2
- 150000005232 imidazopyridines Chemical class 0.000 description 2
- 238000001727 in vivo Methods 0.000 description 2
- 229940079865 intestinal antiinfectives imidazole derivative Drugs 0.000 description 2
- 230000000366 juvenile effect Effects 0.000 description 2
- 210000003734 kidney Anatomy 0.000 description 2
- 229910052744 lithium Inorganic materials 0.000 description 2
- KWGKDLIKAYFUFQ-UHFFFAOYSA-M lithium chloride Chemical compound [Li+].[Cl-] KWGKDLIKAYFUFQ-UHFFFAOYSA-M 0.000 description 2
- 210000004185 liver Anatomy 0.000 description 2
- 208000003747 lymphoid leukemia Diseases 0.000 description 2
- 208000002780 macular degeneration Diseases 0.000 description 2
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 2
- NUJOXMJBOLGQSY-UHFFFAOYSA-N manganese dioxide Chemical compound O=[Mn]=O NUJOXMJBOLGQSY-UHFFFAOYSA-N 0.000 description 2
- 125000000250 methylamino group Chemical group [H]N(*)C([H])([H])[H] 0.000 description 2
- 125000002950 monocyclic group Chemical group 0.000 description 2
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 2
- SLCVBVWXLSEKPL-UHFFFAOYSA-N neopentyl glycol Chemical compound OCC(C)(C)CO SLCVBVWXLSEKPL-UHFFFAOYSA-N 0.000 description 2
- 239000002674 ointment Substances 0.000 description 2
- 239000010502 orange oil Substances 0.000 description 2
- 239000011368 organic material Substances 0.000 description 2
- 239000003960 organic solvent Substances 0.000 description 2
- JMJRYTGVHCAYCT-UHFFFAOYSA-N oxan-4-one Chemical compound O=C1CCOCC1 JMJRYTGVHCAYCT-UHFFFAOYSA-N 0.000 description 2
- 239000007800 oxidant agent Substances 0.000 description 2
- 125000004430 oxygen atom Chemical group O* 0.000 description 2
- LXNAVEXFUKBNMK-UHFFFAOYSA-N palladium(II) acetate Substances [Pd].CC(O)=O.CC(O)=O LXNAVEXFUKBNMK-UHFFFAOYSA-N 0.000 description 2
- YJVFFLUZDVXJQI-UHFFFAOYSA-L palladium(ii) acetate Chemical compound [Pd+2].CC([O-])=O.CC([O-])=O YJVFFLUZDVXJQI-UHFFFAOYSA-L 0.000 description 2
- 238000007911 parenteral administration Methods 0.000 description 2
- 235000019271 petrolatum Nutrition 0.000 description 2
- 229940066842 petrolatum Drugs 0.000 description 2
- SIOXPEMLGUPBBT-UHFFFAOYSA-N picolinic acid Chemical compound OC(=O)C1=CC=CC=N1 SIOXPEMLGUPBBT-UHFFFAOYSA-N 0.000 description 2
- 229960005235 piperonyl butoxide Drugs 0.000 description 2
- 229920000166 polytrimethylene carbonate Polymers 0.000 description 2
- 235000011056 potassium acetate Nutrition 0.000 description 2
- LPNYRYFBWFDTMA-UHFFFAOYSA-N potassium tert-butoxide Chemical compound [K+].CC(C)(C)[O-] LPNYRYFBWFDTMA-UHFFFAOYSA-N 0.000 description 2
- ZRLVQFQTCMUIRM-UHFFFAOYSA-N potassium;2-methylbutan-2-olate Chemical compound [K+].CCC(C)(C)[O-] ZRLVQFQTCMUIRM-UHFFFAOYSA-N 0.000 description 2
- 230000003389 potentiating effect Effects 0.000 description 2
- 239000000843 powder Substances 0.000 description 2
- 239000002243 precursor Substances 0.000 description 2
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 2
- AOJFQRQNPXYVLM-UHFFFAOYSA-N pyridin-1-ium;chloride Chemical compound [Cl-].C1=CC=[NH+]C=C1 AOJFQRQNPXYVLM-UHFFFAOYSA-N 0.000 description 2
- HNJBEVLQSNELDL-UHFFFAOYSA-N pyrrolidin-2-one Chemical compound O=C1CCCN1 HNJBEVLQSNELDL-UHFFFAOYSA-N 0.000 description 2
- 125000004621 quinuclidinyl group Chemical group N12C(CC(CC1)CC2)* 0.000 description 2
- 210000000664 rectum Anatomy 0.000 description 2
- 206010039073 rheumatoid arthritis Diseases 0.000 description 2
- VUPQHSHTKBZVML-UHFFFAOYSA-J rhodium(3+);tetraacetate Chemical compound [Rh+3].[Rh+3].CC([O-])=O.CC([O-])=O.CC([O-])=O.CC([O-])=O VUPQHSHTKBZVML-UHFFFAOYSA-J 0.000 description 2
- 230000028327 secretion Effects 0.000 description 2
- NDVLTYZPCACLMA-UHFFFAOYSA-N silver oxide Chemical compound [O-2].[Ag+].[Ag+] NDVLTYZPCACLMA-UHFFFAOYSA-N 0.000 description 2
- 239000011734 sodium Substances 0.000 description 2
- 229910052708 sodium Inorganic materials 0.000 description 2
- RMBAVIFYHOYIFM-UHFFFAOYSA-M sodium methanethiolate Chemical compound [Na+].[S-]C RMBAVIFYHOYIFM-UHFFFAOYSA-M 0.000 description 2
- JQWHASGSAFIOCM-UHFFFAOYSA-M sodium periodate Chemical compound [Na+].[O-]I(=O)(=O)=O JQWHASGSAFIOCM-UHFFFAOYSA-M 0.000 description 2
- 230000002269 spontaneous effect Effects 0.000 description 2
- 229960002317 succinimide Drugs 0.000 description 2
- 125000004434 sulfur atom Chemical group 0.000 description 2
- 238000004808 supercritical fluid chromatography Methods 0.000 description 2
- 239000000375 suspending agent Substances 0.000 description 2
- 230000009885 systemic effect Effects 0.000 description 2
- 201000000596 systemic lupus erythematosus Diseases 0.000 description 2
- 125000004213 tert-butoxy group Chemical group [H]C([H])([H])C(O*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 2
- DYHSDKLCOJIUFX-UHFFFAOYSA-N tert-butoxycarbonyl anhydride Chemical compound CC(C)(C)OC(=O)OC(=O)OC(C)(C)C DYHSDKLCOJIUFX-UHFFFAOYSA-N 0.000 description 2
- 238000004809 thin layer chromatography Methods 0.000 description 2
- 125000004571 thiomorpholin-4-yl group Chemical group N1(CCSCC1)* 0.000 description 2
- BRNULMACUQOKMR-UHFFFAOYSA-N thiomorpholine Chemical compound C1CSCCN1 BRNULMACUQOKMR-UHFFFAOYSA-N 0.000 description 2
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 2
- WJKHJLXJJJATHN-UHFFFAOYSA-N triflic anhydride Chemical compound FC(F)(F)S(=O)(=O)OS(=O)(=O)C(F)(F)F WJKHJLXJJJATHN-UHFFFAOYSA-N 0.000 description 2
- CSRZQMIRAZTJOY-UHFFFAOYSA-N trimethylsilyl iodide Chemical compound C[Si](C)(C)I CSRZQMIRAZTJOY-UHFFFAOYSA-N 0.000 description 2
- LWIHDJKSTIGBAC-UHFFFAOYSA-K tripotassium phosphate Chemical compound [K+].[K+].[K+].[O-]P([O-])([O-])=O LWIHDJKSTIGBAC-UHFFFAOYSA-K 0.000 description 2
- COIOYMYWGDAQPM-UHFFFAOYSA-N tris(2-methylphenyl)phosphane Chemical compound CC1=CC=CC=C1P(C=1C(=CC=CC=1)C)C1=CC=CC=C1C COIOYMYWGDAQPM-UHFFFAOYSA-N 0.000 description 2
- 229910052721 tungsten Inorganic materials 0.000 description 2
- 201000002327 urinary tract obstruction Diseases 0.000 description 2
- UKSZBOKPHAQOMP-SVLSSHOZSA-N (1e,4e)-1,5-diphenylpenta-1,4-dien-3-one;palladium Chemical compound [Pd].C=1C=CC=CC=1\C=C\C(=O)\C=C\C1=CC=CC=C1.C=1C=CC=CC=1\C=C\C(=O)\C=C\C1=CC=CC=C1 UKSZBOKPHAQOMP-SVLSSHOZSA-N 0.000 description 1
- YTCIHPTZKKWKKC-UHFFFAOYSA-N (2-chloropyrimidin-5-yl)boronic acid Chemical compound OB(O)C1=CN=C(Cl)N=C1 YTCIHPTZKKWKKC-UHFFFAOYSA-N 0.000 description 1
- BTAJUHXJOOODNT-UHFFFAOYSA-N (2-ethoxy-2-oxoethylidene)-iminoazanium Chemical compound CCOC(=O)C=[N+]=N BTAJUHXJOOODNT-UHFFFAOYSA-N 0.000 description 1
- BDANRNLGQOQZSM-VIFPVBQESA-N (3S)-11-bromo-10-fluoro-3-[2-(trifluoromethoxy)phenyl]-1,7-diazatricyclo[6.4.0.02,6]dodeca-2(6),7,9,11-tetraen-5-one Chemical compound BrC=1C(=CC=2N(C=1)C1=C(N=2)C(C[C@H]1C1=C(C=CC=C1)OC(F)(F)F)=O)F BDANRNLGQOQZSM-VIFPVBQESA-N 0.000 description 1
- QJIMTLTYXBDJFC-UHFFFAOYSA-N (4-methylphenyl)-diphenylphosphane Chemical compound C1=CC(C)=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 QJIMTLTYXBDJFC-UHFFFAOYSA-N 0.000 description 1
- 125000004769 (C1-C4) alkylsulfonyl group Chemical group 0.000 description 1
- 125000004750 (C1-C6) alkylaminosulfonyl group Chemical group 0.000 description 1
- 239000001211 (E)-4-phenylbut-3-en-2-one Substances 0.000 description 1
- 125000004605 1,2,3,4-tetrahydroisoquinolinyl group Chemical group C1(NCCC2=CC=CC=C12)* 0.000 description 1
- 125000004607 1,2,3,4-tetrahydroquinolinyl group Chemical group N1(CCCC2=CC=CC=C12)* 0.000 description 1
- DDMOUSALMHHKOS-UHFFFAOYSA-N 1,2-dichloro-1,1,2,2-tetrafluoroethane Chemical compound FC(F)(Cl)C(F)(F)Cl DDMOUSALMHHKOS-UHFFFAOYSA-N 0.000 description 1
- QPPLBCQXWDBQFS-UHFFFAOYSA-N 1,4-diazepan-5-one Chemical compound O=C1CCNCCN1 QPPLBCQXWDBQFS-UHFFFAOYSA-N 0.000 description 1
- MJQJJFZHAQFTDZ-UHFFFAOYSA-N 1-(azaniumylmethyl)cyclopropane-1-carboxylate Chemical compound NCC1(C(O)=O)CC1 MJQJJFZHAQFTDZ-UHFFFAOYSA-N 0.000 description 1
- FVHCSISUKCWWMA-UHFFFAOYSA-N 1-[(2,5-dimethylphenyl)methyl]-6-[4-(piperazin-1-ylmethyl)phenyl]-2-(pyridin-4-ylmethyl)benzimidazole Chemical compound CC1=C(CN2C(=NC3=C2C=C(C=C3)C3=CC=C(C=C3)CN3CCNCC3)CC3=CC=NC=C3)C=C(C=C1)C FVHCSISUKCWWMA-UHFFFAOYSA-N 0.000 description 1
- ZZAKLGGGMWORRT-UHFFFAOYSA-N 1-methylsulfonylpiperazine Chemical compound CS(=O)(=O)N1CCNCC1 ZZAKLGGGMWORRT-UHFFFAOYSA-N 0.000 description 1
- RTBFRGCFXZNCOE-UHFFFAOYSA-N 1-methylsulfonylpiperidin-4-one Chemical compound CS(=O)(=O)N1CCC(=O)CC1 RTBFRGCFXZNCOE-UHFFFAOYSA-N 0.000 description 1
- DNDJHEWLYGJJCY-UHFFFAOYSA-N 1-pyridin-3-ylpiperazine Chemical compound C1CNCCN1C1=CC=CN=C1 DNDJHEWLYGJJCY-UHFFFAOYSA-N 0.000 description 1
- BDANRNLGQOQZSM-UHFFFAOYSA-N 11-bromo-10-fluoro-3-[2-(trifluoromethoxy)phenyl]-1,7-diazatricyclo[6.4.0.02,6]dodeca-2(6),7,9,11-tetraen-5-one Chemical compound BrC=1C(=CC=2N(C=1)C1=C(N=2)C(CC1C1=C(C=CC=C1)OC(F)(F)F)=O)F BDANRNLGQOQZSM-UHFFFAOYSA-N 0.000 description 1
- QNANPZLXXXZPDL-UHFFFAOYSA-N 11-bromo-10-fluoro-3-phenyl-1,7-diazatricyclo[6.4.0.02,6]dodeca-2(6),7,9,11-tetraen-5-one Chemical compound BrC=1C(=CC=2N(C=1)C1=C(N=2)C(CC1C1=CC=CC=C1)=O)F QNANPZLXXXZPDL-UHFFFAOYSA-N 0.000 description 1
- ZCTNXUMIEDJLPG-UHFFFAOYSA-N 11-bromo-3-(2-chlorophenyl)-10-fluoro-1,7-diazatricyclo[6.4.0.02,6]dodeca-2(6),7,9,11-tetraen-5-one Chemical compound BrC=1C(=CC=2N(C1)C1=C(N2)C(CC1C1=C(C=CC=C1)Cl)=O)F ZCTNXUMIEDJLPG-UHFFFAOYSA-N 0.000 description 1
- LHWQVMFQLBIVMT-UHFFFAOYSA-N 11-bromo-3-[2-(difluoromethoxy)phenyl]-10-fluoro-1,7-diazatricyclo[6.4.0.02,6]dodeca-2(6),7,9,11-tetraen-5-ol Chemical compound BrC=1C(=CC=2N(C=1)C1=C(N=2)C(CC1C1=C(C=CC=C1)OC(F)F)O)F LHWQVMFQLBIVMT-UHFFFAOYSA-N 0.000 description 1
- ZHXUWDPHUQHFOV-UHFFFAOYSA-N 2,5-dibromopyridine Chemical compound BrC1=CC=C(Br)N=C1 ZHXUWDPHUQHFOV-UHFFFAOYSA-N 0.000 description 1
- LIHDYIAAKPQZSN-UHFFFAOYSA-N 2,5-dihydroxy-5-methyl-3-(morpholin-4-ylamino)cyclopent-2-en-1-one Chemical compound O=C1C(C)(O)CC(NN2CCOCC2)=C1O LIHDYIAAKPQZSN-UHFFFAOYSA-N 0.000 description 1
- CPHXLFKIUVVIOQ-UHFFFAOYSA-N 2-(trifluoromethoxy)benzaldehyde Chemical compound FC(F)(F)OC1=CC=CC=C1C=O CPHXLFKIUVVIOQ-UHFFFAOYSA-N 0.000 description 1
- IZXIZTKNFFYFOF-UHFFFAOYSA-N 2-Oxazolidone Chemical compound O=C1NCCO1 IZXIZTKNFFYFOF-UHFFFAOYSA-N 0.000 description 1
- NGNBDVOYPDDBFK-UHFFFAOYSA-N 2-[2,4-di(pentan-2-yl)phenoxy]acetyl chloride Chemical compound CCCC(C)C1=CC=C(OCC(Cl)=O)C(C(C)CCC)=C1 NGNBDVOYPDDBFK-UHFFFAOYSA-N 0.000 description 1
- VLAPDEKXZLRRKV-UHFFFAOYSA-N 2-chloro-5-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)pyrimidine Chemical compound O1C(C)(C)C(C)(C)OB1C1=CN=C(Cl)N=C1 VLAPDEKXZLRRKV-UHFFFAOYSA-N 0.000 description 1
- 125000004198 2-fluorophenyl group Chemical group [H]C1=C([H])C(F)=C(*)C([H])=C1[H] 0.000 description 1
- ASUDFOJKTJLAIK-UHFFFAOYSA-N 2-methoxyethanamine Chemical compound COCCN ASUDFOJKTJLAIK-UHFFFAOYSA-N 0.000 description 1
- LEACJMVNYZDSKR-UHFFFAOYSA-N 2-octyldodecan-1-ol Chemical compound CCCCCCCCCCC(CO)CCCCCCCC LEACJMVNYZDSKR-UHFFFAOYSA-N 0.000 description 1
- DIQOUXNTSMWQSA-UHFFFAOYSA-N 2-oxa-5-azabicyclo[2.2.1]heptane Chemical compound C1OC2CNC1C2 DIQOUXNTSMWQSA-UHFFFAOYSA-N 0.000 description 1
- ZZRODMZSMBWYDR-UHFFFAOYSA-N 2-piperazin-1-ium-1-ylpropanoate Chemical compound OC(=O)C(C)N1CCNCC1 ZZRODMZSMBWYDR-UHFFFAOYSA-N 0.000 description 1
- 125000003903 2-propenyl group Chemical group [H]C([*])([H])C([H])=C([H])[H] 0.000 description 1
- 125000001494 2-propynyl group Chemical group [H]C#CC([H])([H])* 0.000 description 1
- LPHWCAUEPAUFHZ-UHFFFAOYSA-N 3,6-Dihydropyridine Chemical compound C1C=CCN=C1 LPHWCAUEPAUFHZ-UHFFFAOYSA-N 0.000 description 1
- MLLSSTJTARJLHK-UHFFFAOYSA-N 3-aminocyclopentane-1-carboxylic acid Chemical compound NC1CCC(C(O)=O)C1 MLLSSTJTARJLHK-UHFFFAOYSA-N 0.000 description 1
- 125000004180 3-fluorophenyl group Chemical group [H]C1=C([H])C(*)=C([H])C(F)=C1[H] 0.000 description 1
- MCSXGCZMEPXKIW-UHFFFAOYSA-N 3-hydroxy-4-[(4-methyl-2-nitrophenyl)diazenyl]-N-(3-nitrophenyl)naphthalene-2-carboxamide Chemical compound Cc1ccc(N=Nc2c(O)c(cc3ccccc23)C(=O)Nc2cccc(c2)[N+]([O-])=O)c(c1)[N+]([O-])=O MCSXGCZMEPXKIW-UHFFFAOYSA-N 0.000 description 1
- 125000003349 3-pyridyl group Chemical group N1=C([H])C([*])=C([H])C([H])=C1[H] 0.000 description 1
- ACZGCWSMSTYWDQ-UHFFFAOYSA-N 3h-1-benzofuran-2-one Chemical compound C1=CC=C2OC(=O)CC2=C1 ACZGCWSMSTYWDQ-UHFFFAOYSA-N 0.000 description 1
- FNVMYJMQMQSCHW-UHFFFAOYSA-N 4-(2h-tetrazol-5-yl)piperidine Chemical compound C1CNCCC1C1=NN=NN1 FNVMYJMQMQSCHW-UHFFFAOYSA-N 0.000 description 1
- 125000001255 4-fluorophenyl group Chemical group [H]C1=C([H])C(*)=C([H])C([H])=C1F 0.000 description 1
- WCCFLOQQACDOAX-UHFFFAOYSA-N 4-fluoropyridin-2-amine Chemical compound NC1=CC(F)=CC=N1 WCCFLOQQACDOAX-UHFFFAOYSA-N 0.000 description 1
- 125000000339 4-pyridyl group Chemical group N1=C([H])C([H])=C([*])C([H])=C1[H] 0.000 description 1
- WGOLHUGPTDEKCF-UHFFFAOYSA-N 5-bromopyridin-2-amine Chemical compound NC1=CC=C(Br)C=N1 WGOLHUGPTDEKCF-UHFFFAOYSA-N 0.000 description 1
- IZDRSEBCBNFCJA-UHFFFAOYSA-N 6-sulfonylcyclohexa-2,4-dien-1-ol Chemical compound OC1C=CC=CC1=S(=O)=O IZDRSEBCBNFCJA-UHFFFAOYSA-N 0.000 description 1
- XGWFJBFNAQHLEF-UHFFFAOYSA-N 9-anthroic acid Chemical compound C1=CC=C2C(C(=O)O)=C(C=CC=C3)C3=CC2=C1 XGWFJBFNAQHLEF-UHFFFAOYSA-N 0.000 description 1
- 208000009304 Acute Kidney Injury Diseases 0.000 description 1
- 208000014697 Acute lymphocytic leukaemia Diseases 0.000 description 1
- 208000036762 Acute promyelocytic leukaemia Diseases 0.000 description 1
- 206010001052 Acute respiratory distress syndrome Diseases 0.000 description 1
- 208000026872 Addison Disease Diseases 0.000 description 1
- 208000024827 Alzheimer disease Diseases 0.000 description 1
- 206010002556 Ankylosing Spondylitis Diseases 0.000 description 1
- 206010003827 Autoimmune hepatitis Diseases 0.000 description 1
- 208000010839 B-cell chronic lymphocytic leukemia Diseases 0.000 description 1
- 208000032791 BCR-ABL1 positive chronic myelogenous leukemia Diseases 0.000 description 1
- 229910015900 BF3 Inorganic materials 0.000 description 1
- 239000005711 Benzoic acid Substances 0.000 description 1
- 208000008439 Biliary Liver Cirrhosis Diseases 0.000 description 1
- 208000033222 Biliary cirrhosis primary Diseases 0.000 description 1
- 208000020084 Bone disease Diseases 0.000 description 1
- KMWKPKKVTIUFLA-UHFFFAOYSA-N BrC=1C(=CC=2N(C1)C(=CN2)C(CC(=O)O)C2=CC=CC=C2)F Chemical compound BrC=1C(=CC=2N(C1)C(=CN2)C(CC(=O)O)C2=CC=CC=C2)F KMWKPKKVTIUFLA-UHFFFAOYSA-N 0.000 description 1
- 208000011691 Burkitt lymphomas Diseases 0.000 description 1
- 206010006895 Cachexia Diseases 0.000 description 1
- 101100080643 Caenorhabditis elegans ran-4 gene Proteins 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- 206010007572 Cardiac hypertrophy Diseases 0.000 description 1
- 208000006029 Cardiomegaly Diseases 0.000 description 1
- 206010062746 Carditis Diseases 0.000 description 1
- 206010008685 Chondritis Diseases 0.000 description 1
- 208000006545 Chronic Obstructive Pulmonary Disease Diseases 0.000 description 1
- 206010009900 Colitis ulcerative Diseases 0.000 description 1
- 206010010904 Convulsion Diseases 0.000 description 1
- 229920002261 Corn starch Polymers 0.000 description 1
- 206010012438 Dermatitis atopic Diseases 0.000 description 1
- YZCKVEUIGOORGS-OUBTZVSYSA-N Deuterium Chemical compound [2H] YZCKVEUIGOORGS-OUBTZVSYSA-N 0.000 description 1
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 1
- 208000007342 Diabetic Nephropathies Diseases 0.000 description 1
- 206010012688 Diabetic retinal oedema Diseases 0.000 description 1
- 206010012689 Diabetic retinopathy Diseases 0.000 description 1
- 239000004338 Dichlorodifluoromethane Substances 0.000 description 1
- 206010013801 Duchenne Muscular Dystrophy Diseases 0.000 description 1
- 208000032928 Dyslipidaemia Diseases 0.000 description 1
- 208000010228 Erectile Dysfunction Diseases 0.000 description 1
- 208000031637 Erythroblastic Acute Leukemia Diseases 0.000 description 1
- 208000036566 Erythroleukaemia Diseases 0.000 description 1
- 108090000371 Esterases Proteins 0.000 description 1
- 206010057671 Female sexual dysfunction Diseases 0.000 description 1
- 201000010915 Glioblastoma multiforme Diseases 0.000 description 1
- 206010018374 Glomerulonephritis minimal lesion Diseases 0.000 description 1
- 208000024869 Goodpasture syndrome Diseases 0.000 description 1
- 208000003807 Graves Disease Diseases 0.000 description 1
- 208000015023 Graves' disease Diseases 0.000 description 1
- 206010019196 Head injury Diseases 0.000 description 1
- 206010019280 Heart failures Diseases 0.000 description 1
- 208000017604 Hodgkin disease Diseases 0.000 description 1
- 208000021519 Hodgkin lymphoma Diseases 0.000 description 1
- 208000010747 Hodgkins lymphoma Diseases 0.000 description 1
- 208000023105 Huntington disease Diseases 0.000 description 1
- WTDHULULXKLSOZ-UHFFFAOYSA-N Hydroxylamine hydrochloride Chemical compound Cl.ON WTDHULULXKLSOZ-UHFFFAOYSA-N 0.000 description 1
- 206010020772 Hypertension Diseases 0.000 description 1
- 206010021245 Idiopathic thrombocytopenic purpura Diseases 0.000 description 1
- 208000022559 Inflammatory bowel disease Diseases 0.000 description 1
- 206010059176 Juvenile idiopathic arthritis Diseases 0.000 description 1
- 229930194542 Keto Natural products 0.000 description 1
- ONIBWKKTOPOVIA-BYPYZUCNSA-N L-Proline Chemical compound OC(=O)[C@@H]1CCCN1 ONIBWKKTOPOVIA-BYPYZUCNSA-N 0.000 description 1
- 239000002211 L-ascorbic acid Substances 0.000 description 1
- 235000000069 L-ascorbic acid Nutrition 0.000 description 1
- FBOZXECLQNJBKD-ZDUSSCGKSA-N L-methotrexate Chemical compound C=1N=C2N=C(N)N=C(N)C2=NC=1CN(C)C1=CC=C(C(=O)N[C@@H](CCC(O)=O)C(O)=O)C=C1 FBOZXECLQNJBKD-ZDUSSCGKSA-N 0.000 description 1
- 229930182821 L-proline Natural products 0.000 description 1
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 1
- 208000017170 Lipid metabolism disease Diseases 0.000 description 1
- 208000004883 Lipoid Nephrosis Diseases 0.000 description 1
- 208000005777 Lupus Nephritis Diseases 0.000 description 1
- 208000031422 Lymphocytic Chronic B-Cell Leukemia Diseases 0.000 description 1
- 208000028018 Lymphocytic leukaemia Diseases 0.000 description 1
- 101150113681 MALT1 gene Proteins 0.000 description 1
- 208000001344 Macular Edema Diseases 0.000 description 1
- 206010025415 Macular oedema Diseases 0.000 description 1
- 208000001145 Metabolic Syndrome Diseases 0.000 description 1
- 208000029725 Metabolic bone disease Diseases 0.000 description 1
- 206010027476 Metastases Diseases 0.000 description 1
- BPSLZWSRHTULGU-UHFFFAOYSA-N Methylpipecolic acid Chemical compound CN1CCCCC1C(O)=O BPSLZWSRHTULGU-UHFFFAOYSA-N 0.000 description 1
- 229920000168 Microcrystalline cellulose Polymers 0.000 description 1
- 102000057613 Mucosa-Associated Lymphoid Tissue Lymphoma Translocation 1 Human genes 0.000 description 1
- 108700026676 Mucosa-Associated Lymphoid Tissue Lymphoma Translocation 1 Proteins 0.000 description 1
- 208000034578 Multiple myelomas Diseases 0.000 description 1
- 201000003793 Myelodysplastic syndrome Diseases 0.000 description 1
- 208000009525 Myocarditis Diseases 0.000 description 1
- HSHXDCVZWHOWCS-UHFFFAOYSA-N N'-hexadecylthiophene-2-carbohydrazide Chemical compound CCCCCCCCCCCCCCCCNNC(=O)c1cccs1 HSHXDCVZWHOWCS-UHFFFAOYSA-N 0.000 description 1
- KWYHDKDOAIKMQN-UHFFFAOYSA-N N,N,N',N'-tetramethylethylenediamine Chemical compound CN(C)CCN(C)C KWYHDKDOAIKMQN-UHFFFAOYSA-N 0.000 description 1
- MBBZMMPHUWSWHV-BDVNFPICSA-N N-methylglucamine Chemical class CNC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO MBBZMMPHUWSWHV-BDVNFPICSA-N 0.000 description 1
- 206010029113 Neovascularisation Diseases 0.000 description 1
- 206010029260 Neuroblastoma Diseases 0.000 description 1
- 208000033755 Neutrophilic Chronic Leukemia Diseases 0.000 description 1
- 239000012425 OXONE® Substances 0.000 description 1
- 206010049088 Osteopenia Diseases 0.000 description 1
- 208000001132 Osteoporosis Diseases 0.000 description 1
- 208000018737 Parkinson disease Diseases 0.000 description 1
- 241000721454 Pemphigus Species 0.000 description 1
- 208000031845 Pernicious anaemia Diseases 0.000 description 1
- 108091000080 Phosphotransferase Proteins 0.000 description 1
- 206010035226 Plasma cell myeloma Diseases 0.000 description 1
- 208000007452 Plasmacytoma Diseases 0.000 description 1
- 206010035664 Pneumonia Diseases 0.000 description 1
- 206010035742 Pneumonitis Diseases 0.000 description 1
- 229920003171 Poly (ethylene oxide) Polymers 0.000 description 1
- 229920001213 Polysorbate 20 Polymers 0.000 description 1
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 1
- 208000012654 Primary biliary cholangitis Diseases 0.000 description 1
- 208000033826 Promyelocytic Acute Leukemia Diseases 0.000 description 1
- OFOBLEOULBTSOW-UHFFFAOYSA-N Propanedioic acid Natural products OC(=O)CC(O)=O OFOBLEOULBTSOW-UHFFFAOYSA-N 0.000 description 1
- 206010060862 Prostate cancer Diseases 0.000 description 1
- 208000000236 Prostatic Neoplasms Diseases 0.000 description 1
- 201000004681 Psoriasis Diseases 0.000 description 1
- 208000036824 Psoriatic arthropathy Diseases 0.000 description 1
- 206010037660 Pyrexia Diseases 0.000 description 1
- LCTONWCANYUPML-UHFFFAOYSA-M Pyruvate Chemical compound CC(=O)C([O-])=O LCTONWCANYUPML-UHFFFAOYSA-M 0.000 description 1
- 208000006265 Renal cell carcinoma Diseases 0.000 description 1
- 208000033626 Renal failure acute Diseases 0.000 description 1
- 108700008625 Reporter Genes Proteins 0.000 description 1
- 208000013616 Respiratory Distress Syndrome Diseases 0.000 description 1
- 206010038933 Retinopathy of prematurity Diseases 0.000 description 1
- 206010038934 Retinopathy proliferative Diseases 0.000 description 1
- 206010039491 Sarcoma Diseases 0.000 description 1
- 206010039710 Scleroderma Diseases 0.000 description 1
- 206010040047 Sepsis Diseases 0.000 description 1
- 208000021386 Sjogren Syndrome Diseases 0.000 description 1
- UIIMBOGNXHQVGW-DEQYMQKBSA-M Sodium bicarbonate-14C Chemical compound [Na+].O[14C]([O-])=O UIIMBOGNXHQVGW-DEQYMQKBSA-M 0.000 description 1
- DBMJMQXJHONAFJ-UHFFFAOYSA-M Sodium laurylsulphate Chemical compound [Na+].CCCCCCCCCCCCOS([O-])(=O)=O DBMJMQXJHONAFJ-UHFFFAOYSA-M 0.000 description 1
- HVUMOYIDDBPOLL-XWVZOOPGSA-N Sorbitan monostearate Chemical compound CCCCCCCCCCCCCCCCCC(=O)OC[C@@H](O)[C@H]1OC[C@H](O)[C@H]1O HVUMOYIDDBPOLL-XWVZOOPGSA-N 0.000 description 1
- 208000006011 Stroke Diseases 0.000 description 1
- KDYFGRWQOYBRFD-UHFFFAOYSA-N Succinic acid Natural products OC(=O)CCC(O)=O KDYFGRWQOYBRFD-UHFFFAOYSA-N 0.000 description 1
- 201000009594 Systemic Scleroderma Diseases 0.000 description 1
- 206010042953 Systemic sclerosis Diseases 0.000 description 1
- FEWJPZIEWOKRBE-UHFFFAOYSA-N Tartaric acid Natural products [H+].[H+].[O-]C(=O)C(O)C(O)C([O-])=O FEWJPZIEWOKRBE-UHFFFAOYSA-N 0.000 description 1
- 208000031981 Thrombocytopenic Idiopathic Purpura Diseases 0.000 description 1
- 208000007536 Thrombosis Diseases 0.000 description 1
- 240000007313 Tilia cordata Species 0.000 description 1
- YZCKVEUIGOORGS-NJFSPNSNSA-N Tritium Chemical compound [3H] YZCKVEUIGOORGS-NJFSPNSNSA-N 0.000 description 1
- 102000000852 Tumor Necrosis Factor-alpha Human genes 0.000 description 1
- 101710187743 Tumor necrosis factor receptor superfamily member 1A Proteins 0.000 description 1
- 102100033732 Tumor necrosis factor receptor superfamily member 1A Human genes 0.000 description 1
- 101710187830 Tumor necrosis factor receptor superfamily member 1B Proteins 0.000 description 1
- 102100033733 Tumor necrosis factor receptor superfamily member 1B Human genes 0.000 description 1
- 201000006704 Ulcerative Colitis Diseases 0.000 description 1
- 206010046851 Uveitis Diseases 0.000 description 1
- 206010047115 Vasculitis Diseases 0.000 description 1
- ZUSWDTWYONAOPH-UHFFFAOYSA-N [2-(trifluoromethyl)phenyl]hydrazine;hydrochloride Chemical group [Cl-].[NH3+]NC1=CC=CC=C1C(F)(F)F ZUSWDTWYONAOPH-UHFFFAOYSA-N 0.000 description 1
- LMWRUVZWLBOLRD-UHFFFAOYSA-M [Cl-].[Mg+]C1=CC=CC=C1Cl Chemical compound [Cl-].[Mg+]C1=CC=CC=C1Cl LMWRUVZWLBOLRD-UHFFFAOYSA-M 0.000 description 1
- KEXBLKHKABOPSR-UHFFFAOYSA-N [K]C=C.FB(F)F Chemical compound [K]C=C.FB(F)F KEXBLKHKABOPSR-UHFFFAOYSA-N 0.000 description 1
- 201000000690 abdominal obesity-metabolic syndrome Diseases 0.000 description 1
- 125000000738 acetamido group Chemical group [H]C([H])([H])C(=O)N([H])[*] 0.000 description 1
- WETWJCDKMRHUPV-UHFFFAOYSA-N acetyl chloride Chemical compound CC(Cl)=O WETWJCDKMRHUPV-UHFFFAOYSA-N 0.000 description 1
- 239000012346 acetyl chloride Substances 0.000 description 1
- 150000008065 acid anhydrides Chemical class 0.000 description 1
- 230000002378 acidificating effect Effects 0.000 description 1
- 239000013543 active substance Substances 0.000 description 1
- 230000001154 acute effect Effects 0.000 description 1
- 208000021841 acute erythroid leukemia Diseases 0.000 description 1
- 229960002964 adalimumab Drugs 0.000 description 1
- YKIOKAURTKXMSB-UHFFFAOYSA-N adams's catalyst Chemical compound O=[Pt]=O YKIOKAURTKXMSB-UHFFFAOYSA-N 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 230000002411 adverse Effects 0.000 description 1
- 239000000443 aerosol Substances 0.000 description 1
- 230000001476 alcoholic effect Effects 0.000 description 1
- 229910052783 alkali metal Inorganic materials 0.000 description 1
- 229910000288 alkali metal carbonate Inorganic materials 0.000 description 1
- 150000008041 alkali metal carbonates Chemical class 0.000 description 1
- 229910052784 alkaline earth metal Inorganic materials 0.000 description 1
- 125000004471 alkyl aminosulfonyl group Chemical group 0.000 description 1
- 239000002168 alkylating agent Substances 0.000 description 1
- 229940100198 alkylating agent Drugs 0.000 description 1
- HSFWRNGVRCDJHI-UHFFFAOYSA-N alpha-acetylene Natural products C#C HSFWRNGVRCDJHI-UHFFFAOYSA-N 0.000 description 1
- PNEYBMLMFCGWSK-UHFFFAOYSA-N aluminium oxide Inorganic materials [O-2].[O-2].[O-2].[Al+3].[Al+3] PNEYBMLMFCGWSK-UHFFFAOYSA-N 0.000 description 1
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 1
- 238000005576 amination reaction Methods 0.000 description 1
- 150000001412 amines Chemical class 0.000 description 1
- VZTDIZULWFCMLS-UHFFFAOYSA-N ammonium formate Chemical compound [NH4+].[O-]C=O VZTDIZULWFCMLS-UHFFFAOYSA-N 0.000 description 1
- 235000011114 ammonium hydroxide Nutrition 0.000 description 1
- 150000003863 ammonium salts Chemical class 0.000 description 1
- 206010002026 amyotrophic lateral sclerosis Diseases 0.000 description 1
- 208000007502 anemia Diseases 0.000 description 1
- JFCQEDHGNNZCLN-UHFFFAOYSA-N anhydrous glutaric acid Natural products OC(=O)CCCC(O)=O JFCQEDHGNNZCLN-UHFFFAOYSA-N 0.000 description 1
- 230000000844 anti-bacterial effect Effects 0.000 description 1
- 230000003110 anti-inflammatory effect Effects 0.000 description 1
- 230000000118 anti-neoplastic effect Effects 0.000 description 1
- 239000000010 aprotic solvent Substances 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 239000008135 aqueous vehicle Substances 0.000 description 1
- 125000001769 aryl amino group Chemical group 0.000 description 1
- 229960005070 ascorbic acid Drugs 0.000 description 1
- 208000006673 asthma Diseases 0.000 description 1
- 201000008937 atopic dermatitis Diseases 0.000 description 1
- 201000003710 autoimmune thrombocytopenic purpura Diseases 0.000 description 1
- CBHOOMGKXCMKIR-UHFFFAOYSA-N azane;methanol Chemical compound N.OC CBHOOMGKXCMKIR-UHFFFAOYSA-N 0.000 description 1
- 239000003899 bactericide agent Substances 0.000 description 1
- 235000013871 bee wax Nutrition 0.000 description 1
- 239000012166 beeswax Substances 0.000 description 1
- 235000010233 benzoic acid Nutrition 0.000 description 1
- 125000001164 benzothiazolyl group Chemical group S1C(=NC2=C1C=CC=C2)* 0.000 description 1
- 125000004196 benzothienyl group Chemical group S1C(=CC2=C1C=CC=C2)* 0.000 description 1
- 125000003354 benzotriazolyl group Chemical group N1N=NC2=C1C=CC=C2* 0.000 description 1
- 125000004622 benzoxazinyl group Chemical group O1NC(=CC2=C1C=CC=C2)* 0.000 description 1
- 125000004541 benzoxazolyl group Chemical group O1C(=NC2=C1C=CC=C2)* 0.000 description 1
- 229930008407 benzylideneacetone Natural products 0.000 description 1
- 125000002619 bicyclic group Chemical group 0.000 description 1
- 239000011230 binding agent Substances 0.000 description 1
- 230000004071 biological effect Effects 0.000 description 1
- 230000036983 biotransformation Effects 0.000 description 1
- 210000000988 bone and bone Anatomy 0.000 description 1
- WTEOIRVLGSZEPR-UHFFFAOYSA-N boron trifluoride Substances FB(F)F WTEOIRVLGSZEPR-UHFFFAOYSA-N 0.000 description 1
- 210000004556 brain Anatomy 0.000 description 1
- 210000000481 breast Anatomy 0.000 description 1
- 125000004799 bromophenyl group Chemical group 0.000 description 1
- 235000019846 buffering salt Nutrition 0.000 description 1
- KDYFGRWQOYBRFD-NUQCWPJISA-N butanedioic acid Chemical compound O[14C](=O)CC[14C](O)=O KDYFGRWQOYBRFD-NUQCWPJISA-N 0.000 description 1
- XJHCXCQVJFPJIK-UHFFFAOYSA-M caesium fluoride Chemical compound [F-].[Cs+] XJHCXCQVJFPJIK-UHFFFAOYSA-M 0.000 description 1
- 239000011575 calcium Substances 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- FUFJGUQYACFECW-UHFFFAOYSA-L calcium hydrogenphosphate Chemical compound [Ca+2].OP([O-])([O-])=O FUFJGUQYACFECW-UHFFFAOYSA-L 0.000 description 1
- 239000002775 capsule Substances 0.000 description 1
- 239000004202 carbamide Substances 0.000 description 1
- 239000001569 carbon dioxide Substances 0.000 description 1
- 229910002092 carbon dioxide Inorganic materials 0.000 description 1
- 150000001244 carboxylic acid anhydrides Chemical class 0.000 description 1
- 210000000845 cartilage Anatomy 0.000 description 1
- 230000030833 cell death Effects 0.000 description 1
- 229960003115 certolizumab pegol Drugs 0.000 description 1
- 210000003679 cervix uteri Anatomy 0.000 description 1
- 229940081733 cetearyl alcohol Drugs 0.000 description 1
- 239000007795 chemical reaction product Substances 0.000 description 1
- 239000003638 chemical reducing agent Substances 0.000 description 1
- 238000004296 chiral HPLC Methods 0.000 description 1
- 229960002152 chlorhexidine acetate Drugs 0.000 description 1
- 125000001309 chloro group Chemical group Cl* 0.000 description 1
- 125000003016 chromanyl group Chemical group O1C(CCC2=CC=CC=C12)* 0.000 description 1
- 238000004587 chromatography analysis Methods 0.000 description 1
- 230000001684 chronic effect Effects 0.000 description 1
- 208000024207 chronic leukemia Diseases 0.000 description 1
- 208000032852 chronic lymphocytic leukemia Diseases 0.000 description 1
- 201000010903 chronic neutrophilic leukemia Diseases 0.000 description 1
- 208000025302 chronic primary adrenal insufficiency Diseases 0.000 description 1
- 229940090100 cimzia Drugs 0.000 description 1
- 208000019425 cirrhosis of liver Diseases 0.000 description 1
- 229940110456 cocoa butter Drugs 0.000 description 1
- 235000019868 cocoa butter Nutrition 0.000 description 1
- 229910052681 coesite Inorganic materials 0.000 description 1
- 210000001072 colon Anatomy 0.000 description 1
- 239000003086 colorant Substances 0.000 description 1
- 239000012230 colorless oil Substances 0.000 description 1
- 238000013270 controlled release Methods 0.000 description 1
- 239000008120 corn starch Substances 0.000 description 1
- 230000008878 coupling Effects 0.000 description 1
- 238000010168 coupling process Methods 0.000 description 1
- 229910052906 cristobalite Inorganic materials 0.000 description 1
- 239000013058 crude material Substances 0.000 description 1
- 125000004850 cyclobutylmethyl group Chemical group C1(CCC1)C* 0.000 description 1
- WEIMJSIRDZDHAH-UHFFFAOYSA-N cyclopent-3-en-1-ol Chemical compound OC1CC=CC1 WEIMJSIRDZDHAH-UHFFFAOYSA-N 0.000 description 1
- 125000004851 cyclopentylmethyl group Chemical group C1(CCCC1)C* 0.000 description 1
- 125000006255 cyclopropyl carbonyl group Chemical group [H]C1([H])C([H])([H])C1([H])C(*)=O 0.000 description 1
- 125000004186 cyclopropylmethyl group Chemical group [H]C([H])(*)C1([H])C([H])([H])C1([H])[H] 0.000 description 1
- 230000001086 cytosolic effect Effects 0.000 description 1
- 230000006378 damage Effects 0.000 description 1
- 230000007850 degeneration Effects 0.000 description 1
- 239000003405 delayed action preparation Substances 0.000 description 1
- 238000013461 design Methods 0.000 description 1
- 229910052805 deuterium Inorganic materials 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 206010012601 diabetes mellitus Diseases 0.000 description 1
- 208000033679 diabetic kidney disease Diseases 0.000 description 1
- 201000011190 diabetic macular edema Diseases 0.000 description 1
- 125000005959 diazepanyl group Chemical group 0.000 description 1
- 125000004987 dibenzofuryl group Chemical group C1(=CC=CC=2OC3=C(C21)C=CC=C3)* 0.000 description 1
- 125000004988 dibenzothienyl group Chemical group C1(=CC=CC=2SC3=C(C21)C=CC=C3)* 0.000 description 1
- 235000019700 dicalcium phosphate Nutrition 0.000 description 1
- 235000019404 dichlorodifluoromethane Nutrition 0.000 description 1
- WBKFWQBXFREOFH-UHFFFAOYSA-N dichloromethane;ethyl acetate Chemical compound ClCCl.CCOC(C)=O WBKFWQBXFREOFH-UHFFFAOYSA-N 0.000 description 1
- 229940087091 dichlorotetrafluoroethane Drugs 0.000 description 1
- MXFYYFVVIIWKFE-UHFFFAOYSA-N dicyclohexyl-[2-[2,6-di(propan-2-yloxy)phenyl]phenyl]phosphane Chemical compound CC(C)OC1=CC=CC(OC(C)C)=C1C1=CC=CC=C1P(C1CCCCC1)C1CCCCC1 MXFYYFVVIIWKFE-UHFFFAOYSA-N 0.000 description 1
- KMSRNCVLMYPKJJ-UHFFFAOYSA-N diethyl 2-[(6-bromo-2-ethoxycarbonyl-7-fluoroimidazo[1,2-a]pyridin-3-yl)-phenylmethyl]propanedioate Chemical compound CCOC(=O)C(C(C1=C(N=C2C=C(F)C(Br)=CN12)C(=O)OCC)C1=CC=CC=C1)C(=O)OCC KMSRNCVLMYPKJJ-UHFFFAOYSA-N 0.000 description 1
- 125000004177 diethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- 125000004212 difluorophenyl group Chemical group 0.000 description 1
- 125000004582 dihydrobenzothienyl group Chemical group S1C(CC2=C1C=CC=C2)* 0.000 description 1
- KZNICNPSHKQLFF-UHFFFAOYSA-N dihydromaleimide Natural products O=C1CCC(=O)N1 KZNICNPSHKQLFF-UHFFFAOYSA-N 0.000 description 1
- 125000005043 dihydropyranyl group Chemical group O1C(CCC=C1)* 0.000 description 1
- 125000005072 dihydrothiopyranyl group Chemical group S1C(CCC=C1)* 0.000 description 1
- IPZJQDSFZGZEOY-UHFFFAOYSA-N dimethylmethylene Chemical group C[C]C IPZJQDSFZGZEOY-UHFFFAOYSA-N 0.000 description 1
- GPAYUJZHTULNBE-UHFFFAOYSA-N diphenylphosphine Chemical compound C=1C=CC=CC=1PC1=CC=CC=C1 GPAYUJZHTULNBE-UHFFFAOYSA-N 0.000 description 1
- 239000007884 disintegrant Substances 0.000 description 1
- 239000002270 dispersing agent Substances 0.000 description 1
- 238000004821 distillation Methods 0.000 description 1
- UZZWBUYVTBPQIV-UHFFFAOYSA-N dme dimethoxyethane Chemical compound COCCOC.COCCOC UZZWBUYVTBPQIV-UHFFFAOYSA-N 0.000 description 1
- 239000008298 dragée Substances 0.000 description 1
- 229940079593 drug Drugs 0.000 description 1
- 238000007876 drug discovery Methods 0.000 description 1
- 238000010828 elution Methods 0.000 description 1
- 239000003995 emulsifying agent Substances 0.000 description 1
- 239000008387 emulsifying waxe Substances 0.000 description 1
- 239000000839 emulsion Substances 0.000 description 1
- 229940073621 enbrel Drugs 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 150000002085 enols Chemical class 0.000 description 1
- 230000002255 enzymatic effect Effects 0.000 description 1
- 206010015037 epilepsy Diseases 0.000 description 1
- 230000003628 erosive effect Effects 0.000 description 1
- 239000003759 ester based solvent Substances 0.000 description 1
- 238000010931 ester hydrolysis Methods 0.000 description 1
- 229960000403 etanercept Drugs 0.000 description 1
- VICYTAYPKBLQFB-UHFFFAOYSA-N ethyl 3-bromo-2-oxopropanoate Chemical compound CCOC(=O)C(=O)CBr VICYTAYPKBLQFB-UHFFFAOYSA-N 0.000 description 1
- 125000004494 ethyl ester group Chemical group 0.000 description 1
- 125000004672 ethylcarbonyl group Chemical group [H]C([H])([H])C([H])([H])C(*)=O 0.000 description 1
- 125000002534 ethynyl group Chemical group [H]C#C* 0.000 description 1
- KTWOOEGAPBSYNW-UHFFFAOYSA-N ferrocene Chemical compound [Fe+2].C=1C=C[CH-]C=1.C=1C=C[CH-]C=1 KTWOOEGAPBSYNW-UHFFFAOYSA-N 0.000 description 1
- 239000000945 filler Substances 0.000 description 1
- 238000013100 final test Methods 0.000 description 1
- 239000000796 flavoring agent Substances 0.000 description 1
- 125000001207 fluorophenyl group Chemical group 0.000 description 1
- 201000003444 follicular lymphoma Diseases 0.000 description 1
- 235000013355 food flavoring agent Nutrition 0.000 description 1
- 235000003599 food sweetener Nutrition 0.000 description 1
- 239000012634 fragment Substances 0.000 description 1
- 238000004108 freeze drying Methods 0.000 description 1
- 239000001530 fumaric acid Substances 0.000 description 1
- 239000000417 fungicide Substances 0.000 description 1
- 206010017758 gastric cancer Diseases 0.000 description 1
- 208000010749 gastric carcinoma Diseases 0.000 description 1
- 230000014509 gene expression Effects 0.000 description 1
- 208000005017 glioblastoma Diseases 0.000 description 1
- 229960001743 golimumab Drugs 0.000 description 1
- 208000007475 hemolytic anemia Diseases 0.000 description 1
- 230000002949 hemolytic effect Effects 0.000 description 1
- 125000005885 heterocycloalkylalkyl group Chemical group 0.000 description 1
- UBHWBODXJBSFLH-UHFFFAOYSA-N hexadecan-1-ol;octadecan-1-ol Chemical compound CCCCCCCCCCCCCCCCO.CCCCCCCCCCCCCCCCCCO UBHWBODXJBSFLH-UHFFFAOYSA-N 0.000 description 1
- 125000004051 hexyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 238000004128 high performance liquid chromatography Methods 0.000 description 1
- 229940048921 humira Drugs 0.000 description 1
- 150000004677 hydrates Chemical class 0.000 description 1
- 150000002430 hydrocarbons Chemical class 0.000 description 1
- 239000001866 hydroxypropyl methyl cellulose Substances 0.000 description 1
- 235000010979 hydroxypropyl methyl cellulose Nutrition 0.000 description 1
- 229920003088 hydroxypropyl methyl cellulose Polymers 0.000 description 1
- 150000005234 imidazo[1,2-a]pyridines Chemical class 0.000 description 1
- 125000002632 imidazolidinyl group Chemical group 0.000 description 1
- 125000002636 imidazolinyl group Chemical group 0.000 description 1
- 239000007943 implant Substances 0.000 description 1
- 201000001881 impotence Diseases 0.000 description 1
- 238000011534 incubation Methods 0.000 description 1
- 125000003392 indanyl group Chemical group C1(CCC2=CC=CC=C12)* 0.000 description 1
- 208000027138 indeterminate colitis Diseases 0.000 description 1
- 125000003387 indolinyl group Chemical group N1(CCC2=CC=CC=C12)* 0.000 description 1
- 125000006301 indolyl methyl group Chemical group 0.000 description 1
- 208000000509 infertility Diseases 0.000 description 1
- 230000036512 infertility Effects 0.000 description 1
- 231100000535 infertility Toxicity 0.000 description 1
- 208000021646 inflammation of heart layer Diseases 0.000 description 1
- 229960000598 infliximab Drugs 0.000 description 1
- 238000001802 infusion Methods 0.000 description 1
- 239000003112 inhibitor Substances 0.000 description 1
- 230000002401 inhibitory effect Effects 0.000 description 1
- 238000010255 intramuscular injection Methods 0.000 description 1
- 239000007927 intramuscular injection Substances 0.000 description 1
- 239000011630 iodine Substances 0.000 description 1
- 229910052740 iodine Inorganic materials 0.000 description 1
- INQOMBQAUSQDDS-UHFFFAOYSA-N iodomethane Chemical compound IC INQOMBQAUSQDDS-UHFFFAOYSA-N 0.000 description 1
- 229910052742 iron Inorganic materials 0.000 description 1
- 230000001788 irregular Effects 0.000 description 1
- 208000028867 ischemia Diseases 0.000 description 1
- 125000004594 isoindolinyl group Chemical group C1(NCC2=CC=CC=C12)* 0.000 description 1
- XVQUOJBERHHONY-UHFFFAOYSA-N isometheptene Chemical compound CNC(C)CCC=C(C)C XVQUOJBERHHONY-UHFFFAOYSA-N 0.000 description 1
- 125000001972 isopentyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000002183 isoquinolinyl group Chemical group C1(=NC=CC2=CC=CC=C12)* 0.000 description 1
- 125000004628 isothiazolidinyl group Chemical group S1N(CCC1)* 0.000 description 1
- 125000001786 isothiazolyl group Chemical group 0.000 description 1
- 201000002215 juvenile rheumatoid arthritis Diseases 0.000 description 1
- 206010023332 keratitis Diseases 0.000 description 1
- 125000000468 ketone group Chemical group 0.000 description 1
- 150000002576 ketones Chemical class 0.000 description 1
- 239000008101 lactose Substances 0.000 description 1
- 239000003446 ligand Substances 0.000 description 1
- 239000006210 lotion Substances 0.000 description 1
- 239000007937 lozenge Substances 0.000 description 1
- 239000000314 lubricant Substances 0.000 description 1
- 210000004072 lung Anatomy 0.000 description 1
- 210000001165 lymph node Anatomy 0.000 description 1
- 201000011649 lymphoblastic lymphoma Diseases 0.000 description 1
- 201000010230 macular retinal edema Diseases 0.000 description 1
- 229910001623 magnesium bromide Inorganic materials 0.000 description 1
- 159000000003 magnesium salts Chemical class 0.000 description 1
- 235000019359 magnesium stearate Nutrition 0.000 description 1
- NXPHGHWWQRMDIA-UHFFFAOYSA-M magnesium;carbanide;bromide Chemical compound [CH3-].[Mg+2].[Br-] NXPHGHWWQRMDIA-UHFFFAOYSA-M 0.000 description 1
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 description 1
- 239000011976 maleic acid Substances 0.000 description 1
- 201000007924 marginal zone B-cell lymphoma Diseases 0.000 description 1
- 208000021937 marginal zone lymphoma Diseases 0.000 description 1
- 230000001404 mediated effect Effects 0.000 description 1
- 201000001441 melanoma Diseases 0.000 description 1
- 206010027191 meningioma Diseases 0.000 description 1
- 229940098779 methanesulfonic acid Drugs 0.000 description 1
- IZDROVVXIHRYMH-UHFFFAOYSA-N methanesulfonic anhydride Chemical compound CS(=O)(=O)OS(C)(=O)=O IZDROVVXIHRYMH-UHFFFAOYSA-N 0.000 description 1
- 229960000485 methotrexate Drugs 0.000 description 1
- DRASECIURSUJCQ-UHFFFAOYSA-N methyl 11-bromo-10-fluoro-5-oxo-3-phenyl-1,7-diazatricyclo[6.4.0.02,6]dodeca-2(6),7,9,11-tetraene-4-carboxylate Chemical compound COC(=O)C1C(C2=C(N=C3N2C=C(C(=C3)F)Br)C1=O)C1=CC=CC=C1 DRASECIURSUJCQ-UHFFFAOYSA-N 0.000 description 1
- 150000004702 methyl esters Chemical class 0.000 description 1
- 125000002816 methylsulfanyl group Chemical group [H]C([H])([H])S[*] 0.000 description 1
- 125000004372 methylthioethyl group Chemical group [H]C([H])([H])SC([H])([H])C([H])([H])* 0.000 description 1
- 235000019813 microcrystalline cellulose Nutrition 0.000 description 1
- 239000008108 microcrystalline cellulose Substances 0.000 description 1
- 229940016286 microcrystalline cellulose Drugs 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- FYCRNRZIEVLZDO-UHFFFAOYSA-N morpholin-4-ium-2-carboxylate Chemical compound OC(=O)C1CNCCO1 FYCRNRZIEVLZDO-UHFFFAOYSA-N 0.000 description 1
- 201000006417 multiple sclerosis Diseases 0.000 description 1
- 210000003205 muscle Anatomy 0.000 description 1
- 201000006938 muscular dystrophy Diseases 0.000 description 1
- 206010028417 myasthenia gravis Diseases 0.000 description 1
- 208000010125 myocardial infarction Diseases 0.000 description 1
- SYSQUGFVNFXIIT-UHFFFAOYSA-N n-[4-(1,3-benzoxazol-2-yl)phenyl]-4-nitrobenzenesulfonamide Chemical class C1=CC([N+](=O)[O-])=CC=C1S(=O)(=O)NC1=CC=C(C=2OC3=CC=CC=C3N=2)C=C1 SYSQUGFVNFXIIT-UHFFFAOYSA-N 0.000 description 1
- 125000001624 naphthyl group Chemical group 0.000 description 1
- 125000004923 naphthylmethyl group Chemical group C1(=CC=CC2=CC=CC=C12)C* 0.000 description 1
- 125000004593 naphthyridinyl group Chemical group N1=C(C=CC2=CC=CN=C12)* 0.000 description 1
- 239000006199 nebulizer Substances 0.000 description 1
- 230000010807 negative regulation of binding Effects 0.000 description 1
- 125000001971 neopentyl group Chemical group [H]C([*])([H])C(C([H])([H])[H])(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 230000007935 neutral effect Effects 0.000 description 1
- 229960003966 nicotinamide Drugs 0.000 description 1
- 235000005152 nicotinamide Nutrition 0.000 description 1
- 239000011570 nicotinamide Substances 0.000 description 1
- XJLSEXAGTJCILF-UHFFFAOYSA-N nipecotic acid Chemical compound OC(=O)C1CCCNC1 XJLSEXAGTJCILF-UHFFFAOYSA-N 0.000 description 1
- LYGJENNIWJXYER-UHFFFAOYSA-N nitromethane Chemical compound C[N+]([O-])=O LYGJENNIWJXYER-UHFFFAOYSA-N 0.000 description 1
- 231100000344 non-irritating Toxicity 0.000 description 1
- 239000002687 nonaqueous vehicle Substances 0.000 description 1
- 239000013110 organic ligand Substances 0.000 description 1
- 210000001672 ovary Anatomy 0.000 description 1
- 125000001715 oxadiazolyl group Chemical group 0.000 description 1
- LMYJGUNNJIDROI-UHFFFAOYSA-N oxan-4-ol Chemical compound OC1CCOCC1 LMYJGUNNJIDROI-UHFFFAOYSA-N 0.000 description 1
- 125000000160 oxazolidinyl group Chemical group 0.000 description 1
- 125000002971 oxazolyl group Chemical group 0.000 description 1
- 230000003647 oxidation Effects 0.000 description 1
- 238000007254 oxidation reaction Methods 0.000 description 1
- 125000003854 p-chlorophenyl group Chemical group [H]C1=C([H])C(*)=C([H])C([H])=C1Cl 0.000 description 1
- 125000001037 p-tolyl group Chemical group [H]C1=C([H])C(=C([H])C([H])=C1*)C([H])([H])[H] 0.000 description 1
- 210000000496 pancreas Anatomy 0.000 description 1
- 230000001575 pathological effect Effects 0.000 description 1
- 230000037361 pathway Effects 0.000 description 1
- 125000001147 pentyl group Chemical group C(CCCC)* 0.000 description 1
- 239000008177 pharmaceutical agent Substances 0.000 description 1
- 239000000546 pharmaceutical excipient Substances 0.000 description 1
- 239000002831 pharmacologic agent Substances 0.000 description 1
- 230000000144 pharmacologic effect Effects 0.000 description 1
- WVDDGKGOMKODPV-ZQBYOMGUSA-N phenyl(114C)methanol Chemical compound O[14CH2]C1=CC=CC=C1 WVDDGKGOMKODPV-ZQBYOMGUSA-N 0.000 description 1
- 125000000286 phenylethyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])C([H])([H])* 0.000 description 1
- ANRQGKOBLBYXFM-UHFFFAOYSA-M phenylmagnesium bromide Chemical compound Br[Mg]C1=CC=CC=C1 ANRQGKOBLBYXFM-UHFFFAOYSA-M 0.000 description 1
- PDTFCHSETJBPTR-UHFFFAOYSA-N phenylmercuric nitrate Chemical compound [O-][N+](=O)O[Hg]C1=CC=CC=C1 PDTFCHSETJBPTR-UHFFFAOYSA-N 0.000 description 1
- 125000004344 phenylpropyl group Chemical group 0.000 description 1
- 102000020233 phosphotransferase Human genes 0.000 description 1
- 125000004592 phthalazinyl group Chemical group C1(=NN=CC2=CC=CC=C12)* 0.000 description 1
- HXEACLLIILLPRG-UHFFFAOYSA-N pipecolic acid Chemical compound OC(=O)C1CCCCN1 HXEACLLIILLPRG-UHFFFAOYSA-N 0.000 description 1
- IWELDVXSEVIIGI-UHFFFAOYSA-N piperazin-2-one Chemical compound O=C1CNCCN1 IWELDVXSEVIIGI-UHFFFAOYSA-N 0.000 description 1
- 229920001223 polyethylene glycol Polymers 0.000 description 1
- 208000005987 polymyositis Diseases 0.000 description 1
- 239000000256 polyoxyethylene sorbitan monolaurate Substances 0.000 description 1
- 235000010486 polyoxyethylene sorbitan monolaurate Nutrition 0.000 description 1
- 229920001451 polypropylene glycol Polymers 0.000 description 1
- 229920000136 polysorbate Polymers 0.000 description 1
- 229950008882 polysorbate Drugs 0.000 description 1
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 1
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 1
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 1
- 229910052700 potassium Inorganic materials 0.000 description 1
- 239000011591 potassium Substances 0.000 description 1
- OKBMCNHOEMXPTM-UHFFFAOYSA-M potassium peroxymonosulfate Chemical compound [K+].OOS([O-])(=O)=O OKBMCNHOEMXPTM-UHFFFAOYSA-M 0.000 description 1
- 229910000160 potassium phosphate Inorganic materials 0.000 description 1
- 235000011009 potassium phosphates Nutrition 0.000 description 1
- 159000000001 potassium salts Chemical class 0.000 description 1
- 229920001592 potato starch Polymers 0.000 description 1
- OIGNJSKKLXVSLS-VWUMJDOOSA-N prednisolone Chemical compound O=C1C=C[C@]2(C)[C@H]3[C@@H](O)C[C@](C)([C@@](CC4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 OIGNJSKKLXVSLS-VWUMJDOOSA-N 0.000 description 1
- 229960005205 prednisolone Drugs 0.000 description 1
- 230000002335 preservative effect Effects 0.000 description 1
- 230000002062 proliferating effect Effects 0.000 description 1
- 229960002429 proline Drugs 0.000 description 1
- VVWRJUBEIPHGQF-MDZDMXLPSA-N propan-2-yl (ne)-n-propan-2-yloxycarbonyliminocarbamate Chemical compound CC(C)OC(=O)\N=N\C(=O)OC(C)C VVWRJUBEIPHGQF-MDZDMXLPSA-N 0.000 description 1
- 239000003380 propellant Substances 0.000 description 1
- 238000011321 prophylaxis Methods 0.000 description 1
- MCSINKKTEDDPNK-UHFFFAOYSA-N propyl propionate Chemical compound CCCOC(=O)CC MCSINKKTEDDPNK-UHFFFAOYSA-N 0.000 description 1
- 235000013772 propylene glycol Nutrition 0.000 description 1
- 108090000623 proteins and genes Proteins 0.000 description 1
- 102000004169 proteins and genes Human genes 0.000 description 1
- 125000001042 pteridinyl group Chemical group N1=C(N=CC2=NC=CN=C12)* 0.000 description 1
- 208000005069 pulmonary fibrosis Diseases 0.000 description 1
- 125000000561 purinyl group Chemical group N1=C(N=C2N=CNC2=C1)* 0.000 description 1
- JAEIBKXSIXOLOL-UHFFFAOYSA-N pyrrolidin-1-ium-3-carboxylate Chemical compound OC(=O)C1CCNC1 JAEIBKXSIXOLOL-UHFFFAOYSA-N 0.000 description 1
- JHHZLHWJQPUNKB-UHFFFAOYSA-N pyrrolidin-3-ol Chemical compound OC1CCNC1 JHHZLHWJQPUNKB-UHFFFAOYSA-N 0.000 description 1
- 125000000168 pyrrolyl group Chemical group 0.000 description 1
- 150000003242 quaternary ammonium salts Chemical class 0.000 description 1
- 125000002294 quinazolinyl group Chemical group N1=C(N=CC2=CC=CC=C12)* 0.000 description 1
- 125000001567 quinoxalinyl group Chemical group N1=C(C=NC2=CC=CC=C12)* 0.000 description 1
- 239000002287 radioligand Substances 0.000 description 1
- 238000001953 recrystallisation Methods 0.000 description 1
- 230000001105 regulatory effect Effects 0.000 description 1
- 229940116176 remicade Drugs 0.000 description 1
- 210000001957 retinal vein Anatomy 0.000 description 1
- 206010039083 rhinitis Diseases 0.000 description 1
- ITDJKCJYYAQMRO-UHFFFAOYSA-L rhodium(2+);diacetate Chemical compound [Rh+2].CC([O-])=O.CC([O-])=O ITDJKCJYYAQMRO-UHFFFAOYSA-L 0.000 description 1
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 208000012201 sexual and gender identity disease Diseases 0.000 description 1
- 208000015891 sexual disease Diseases 0.000 description 1
- 230000001568 sexual effect Effects 0.000 description 1
- 230000011664 signaling Effects 0.000 description 1
- 235000012239 silicon dioxide Nutrition 0.000 description 1
- 229910001923 silver oxide Inorganic materials 0.000 description 1
- 229940068638 simponi Drugs 0.000 description 1
- 210000003491 skin Anatomy 0.000 description 1
- QDRKDTQENPPHOJ-UHFFFAOYSA-N sodium ethoxide Chemical compound [Na+].CC[O-] QDRKDTQENPPHOJ-UHFFFAOYSA-N 0.000 description 1
- 229940023144 sodium glycolate Drugs 0.000 description 1
- 235000009518 sodium iodide Nutrition 0.000 description 1
- 235000019333 sodium laurylsulphate Nutrition 0.000 description 1
- AKHNMLFCWUSKQB-UHFFFAOYSA-L sodium thiosulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=S AKHNMLFCWUSKQB-UHFFFAOYSA-L 0.000 description 1
- 235000019345 sodium thiosulphate Nutrition 0.000 description 1
- 239000012321 sodium triacetoxyborohydride Substances 0.000 description 1
- 238000005063 solubilization Methods 0.000 description 1
- 230000007928 solubilization Effects 0.000 description 1
- 239000001587 sorbitan monostearate Substances 0.000 description 1
- 235000011076 sorbitan monostearate Nutrition 0.000 description 1
- 229940035048 sorbitan monostearate Drugs 0.000 description 1
- 208000020431 spinal cord injury Diseases 0.000 description 1
- 239000007921 spray Substances 0.000 description 1
- 239000003381 stabilizer Substances 0.000 description 1
- 239000007858 starting material Substances 0.000 description 1
- 230000000638 stimulation Effects 0.000 description 1
- 229910052682 stishovite Inorganic materials 0.000 description 1
- 239000011550 stock solution Substances 0.000 description 1
- 210000002784 stomach Anatomy 0.000 description 1
- 201000000498 stomach carcinoma Diseases 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- YBBRCQOCSYXUOC-UHFFFAOYSA-N sulfuryl dichloride Chemical compound ClS(Cl)(=O)=O YBBRCQOCSYXUOC-UHFFFAOYSA-N 0.000 description 1
- 239000006228 supernatant Substances 0.000 description 1
- 239000000829 suppository Substances 0.000 description 1
- 230000004083 survival effect Effects 0.000 description 1
- 239000003765 sweetening agent Substances 0.000 description 1
- 239000006188 syrup Substances 0.000 description 1
- 235000020357 syrup Nutrition 0.000 description 1
- 239000000454 talc Substances 0.000 description 1
- 229910052623 talc Inorganic materials 0.000 description 1
- 239000011975 tartaric acid Substances 0.000 description 1
- 235000002906 tartaric acid Nutrition 0.000 description 1
- 125000006633 tert-butoxycarbonylamino group Chemical group 0.000 description 1
- WDLJASQZSZLWDL-UHFFFAOYSA-N tert-butyl 2,5-dihydropyridine-6-carboxylate Chemical compound C(C)(C)(C)OC(=O)C1=NCC=CC1 WDLJASQZSZLWDL-UHFFFAOYSA-N 0.000 description 1
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- BCNZYOJHNLTNEZ-UHFFFAOYSA-N tert-butyldimethylsilyl chloride Chemical compound CC(C)(C)[Si](C)(C)Cl BCNZYOJHNLTNEZ-UHFFFAOYSA-N 0.000 description 1
- 125000004853 tetrahydropyridinyl group Chemical group N1(CCCC=C1)* 0.000 description 1
- 125000005958 tetrahydrothienyl group Chemical group 0.000 description 1
- 125000004632 tetrahydrothiopyranyl group Chemical group S1C(CCCC1)* 0.000 description 1
- OSBSFAARYOCBHB-UHFFFAOYSA-N tetrapropylammonium Chemical compound CCC[N+](CCC)(CCC)CCC OSBSFAARYOCBHB-UHFFFAOYSA-N 0.000 description 1
- 125000001113 thiadiazolyl group Chemical group 0.000 description 1
- UREFPUSLYHQDMI-UHFFFAOYSA-N thiazinan-3-one Chemical compound O=C1CCCSN1 UREFPUSLYHQDMI-UHFFFAOYSA-N 0.000 description 1
- XXDOCAGWDUVEAN-UHFFFAOYSA-N thiazinane-3,4-dione Chemical compound O=C1CCSNC1=O XXDOCAGWDUVEAN-UHFFFAOYSA-N 0.000 description 1
- 125000002769 thiazolinyl group Chemical group 0.000 description 1
- 206010043778 thyroiditis Diseases 0.000 description 1
- 238000011200 topical administration Methods 0.000 description 1
- 230000000699 topical effect Effects 0.000 description 1
- BWHOZHOGCMHOBV-BQYQJAHWSA-N trans-benzylideneacetone Chemical compound CC(=O)\C=C\C1=CC=CC=C1 BWHOZHOGCMHOBV-BQYQJAHWSA-N 0.000 description 1
- 125000004306 triazinyl group Chemical group 0.000 description 1
- 229910052905 tridymite Inorganic materials 0.000 description 1
- GGUBFICZYGKNTD-UHFFFAOYSA-N triethyl phosphonoacetate Chemical compound CCOC(=O)CP(=O)(OCC)OCC GGUBFICZYGKNTD-UHFFFAOYSA-N 0.000 description 1
- KIEXGUUJAYEUSM-UHFFFAOYSA-N trifluoromethylsilane Chemical compound FC(F)(F)[SiH3] KIEXGUUJAYEUSM-UHFFFAOYSA-N 0.000 description 1
- MWKJTNBSKNUMFN-UHFFFAOYSA-N trifluoromethyltrimethylsilane Chemical compound C[Si](C)(C)C(F)(F)F MWKJTNBSKNUMFN-UHFFFAOYSA-N 0.000 description 1
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 1
- JEJAMASKDTUEBZ-UHFFFAOYSA-N tris(1,1,3-tribromo-2,2-dimethylpropyl) phosphate Chemical compound BrCC(C)(C)C(Br)(Br)OP(=O)(OC(Br)(Br)C(C)(C)CBr)OC(Br)(Br)C(C)(C)CBr JEJAMASKDTUEBZ-UHFFFAOYSA-N 0.000 description 1
- 229910052722 tritium Inorganic materials 0.000 description 1
- 238000007039 two-step reaction Methods 0.000 description 1
- 208000035408 type 1 diabetes mellitus 1 Diseases 0.000 description 1
- 238000004704 ultra performance liquid chromatography Methods 0.000 description 1
- 210000003932 urinary bladder Anatomy 0.000 description 1
- 210000004291 uterus Anatomy 0.000 description 1
- 229910052720 vanadium Inorganic materials 0.000 description 1
- 229920002554 vinyl polymer Polymers 0.000 description 1
- 239000001993 wax Substances 0.000 description 1
- 239000000080 wetting agent Substances 0.000 description 1
- UGOMMVLRQDMAQQ-UHFFFAOYSA-N xphos Chemical compound CC(C)C1=CC(C(C)C)=CC(C(C)C)=C1C1=CC=CC=C1P(C1CCCCC1)C1CCCCC1 UGOMMVLRQDMAQQ-UHFFFAOYSA-N 0.000 description 1
- 229910052727 yttrium Inorganic materials 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/04—Ortho-condensed systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/4353—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom ortho- or peri-condensed with heterocyclic ring systems
- A61K31/437—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom ortho- or peri-condensed with heterocyclic ring systems the heterocyclic ring system containing a five-membered ring having nitrogen as a ring hetero atom, e.g. indolizine, beta-carboline
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/02—Drugs for skeletal disorders for joint disorders, e.g. arthritis, arthrosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/04—Centrally acting analgesics, e.g. opioids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/06—Immunosuppressants, e.g. drugs for graft rejection
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D519/00—Heterocyclic compounds containing more than one system of two or more relevant hetero rings condensed among themselves or condensed with a common carbocyclic ring system not provided for in groups C07D453/00 or C07D455/00
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Veterinary Medicine (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Immunology (AREA)
- Epidemiology (AREA)
- Rheumatology (AREA)
- Biomedical Technology (AREA)
- Physical Education & Sports Medicine (AREA)
- Pain & Pain Management (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Neurosurgery (AREA)
- Neurology (AREA)
- Transplantation (AREA)
- Obesity (AREA)
- Hematology (AREA)
- Diabetes (AREA)
- Ophthalmology & Optometry (AREA)
- Heart & Thoracic Surgery (AREA)
- Cardiology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
- Heterocyclic Carbon Compounds Containing A Hetero Ring Having Nitrogen And Oxygen As The Only Ring Hetero Atoms (AREA)
- Nitrogen And Oxygen Or Sulfur-Condensed Heterocyclic Ring Systems (AREA)
Abstract
Un compuesto representado por la fórmula (IIA), o un N-óxido del mismo, o una sal farmacéuticamente aceptable del mismo,**Fórmula** R1 representa arilo, , heterocicloalquenilo C3-7, heteroarilo, cicloalquil (C3-7)-heteroarilbicicloalquil (C4-9)-heteroaril-, heterocicloalquil (C3-7)-heteroaril-, heterobicicloalquil (C4-9)-heteroaril- o espiroheterocicloalquil (C4-9)-heteroaril-, cualquiera de tales grupos puede estar opcionalmente sustituido con uno, dos o tres sustituyentes seleccionados entre halógeno, haloalquilo (C1-6), ciano, cianoalquilo (C1-6), nitroalquilo (C1-6), alquilo C1-6, trifluorometilo, trifluoroetilo, alquenilo C2-6, hidroxi, hidroxialquilo (C1-6), alcoxi C1-6, trifluoroetoxi, carboxicicloalquiloxi (C3-7), alquiltio C1-6, alquilsulfonilo C1-6, alquilsulfonil (C1-6)-alquilo (C1-6), oxo, amino, amino-alquilo (C1-6), alquilamino C1- 6, dialquilamino (C1-6), alcoxi (C1-6)alquilamino (C1-6), N-[alquil (C1-6)]-N-[hidroxialquil (C1-6)]amino, alquilcarbonilamino (C2-6)-alquilo(C1-6), alquilsulfonilamino C1-6, N-[alquil (C1-6)]-N-[alquilsulfonil (C1-6)]amino, bis[alquilsulfonil (C1-6)]amino, N-[alquil (C1-6)]-N-[carboxialquil (C1-6)]amino, carboxicicloalquil (C3-7)-amino, carboxicicloalquil (C3-7)alquilamino (C1-6), formilo, alquilcarbonilo C2-6, alquilcarboniloxi (C2-6)alquilo (C1-6), carboxi, carboxialquilo (C1-6), alcoxicarbonilo C2-6, alcoxicarbonil C2-6alquilo (C1-6), morfolinil-alcoxicarbonilo (C1-6), alcoxicarbonil C2-6-metilidenilo, aminocarbonilo, dialquilaminocarbonilo (C1-6), aminosulfonilo, alquilsulfoximinilo (C1-6), [alquil (C1-6)][N-alquil (C1-6)]sulfoximinilo, heteroarilo, difluorometilo, alquilsulfinilo C1-6 y cicloalquil (C3- 7)sulfonilo. R2 representa hidrógeno, halógeno, trifluorometilo o ciano; o alquilo C1-6 opcionalmente sustituido con alcoxicarbonilo C2-6; Y representa arilo o heteroarilo, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes seleccionados entre cloro, flúor, ciano, metoxi, metilsulfonilo, trifluorometoxi y difluorometoxi; Z representa metileno; R5a representa hidrógeno, hidroxi, halógeno o trifluorometilo; o -NRbRc, -NRcC(O)Rd, -S(O)2RaORa-O(CO)-Rd o alquilo C1-6, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes seleccionados entre halógeno, hidroxi, trifluorometilo, alquilo C1-6, alcoxi C1-6, alquilcarbonilo C2-6, alquiloxicarbonilo C2-6, (hidroxi)alquilo C1-6, cicloalquilo (C3-7), alquilsulfonilo C1-6, alquilsulfonil (C1-6)-alquilo (C1-6), dialquilaminocarbonilo (C1-6), oxo y carboxi; y R5b representa hidrógeno, hidroxi, halógeno, ciano, trifluorometilo; o alquilo C1-6, dicho grupo puede estar opcionalmente sustituido con uno o más sustituyentes seleccionados entre halógeno, hidroxi, trifluorometilo, alquilo C1-6, alcoxi C1-6, alquilcarbonilo C2-6, alquiloxicarbonilo C2-6, (hidroxi)alquilo C1-6, cicloalquilo (C3-7), alquilsulfonilo C1-6, alquilsulfonil (C1-6)-alquilo (C1-6), dialquilaminocarbonilo (C1-6), oxo y carboxi; o R5a y R5b, cuando se toman junto con el carbono al que están unidos, representan un carbonilo, tiocarbonilo o - C=N-OH; Ra representa alquilo C1-6, arilalquilo (C1-6) o heteroarilalquilo (C1-6), cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes seleccionados entre alcoxi C1-6, oxo, ciano y alcoxicarbonilo C2-6; Rb representa hidrógeno o alquilo C1-6; Rc representa hidrógeno, alquilo C1-6 o cicloalquilo C3-7; y Rd representa hidrógeno; o alquilo C1-6, arilo o heteroarilo, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes seleccionados entre halógeno, alquilo C1-6, alcoxi C1-6, oxo, alquilcarboniloxi C2-6 y dialquilamino (C1-6).
Description
DESCRIPCIÓN
Derivados de imidazoles tricíclicos fusionados como moduladores de la actividad del TNF
La presente invención se refiere a una clase de derivados de imidazoles tricíclicos fusionados, y a su uso en terapia. Más particularmente, la presente invención se refiere derivados de imidazopiridina fusionados sustituidos farmacológicamente activos. En particular, la presente invención se refiere a derivados de dihidro-1H-ciclopenta[4,5]imidazo[1,2-a]piridina.
Estos compuestos son moduladores de la señalización de TNFa y son en consecuencia beneficiosos como agentes farmacéuticos, especialmente en el tratamiento de trastornos inflamatorios y autoinmunitarios adversos, trastornos neurológicos y neurodegenerativos, trastornos del dolor y nociceptivos, trastornos cardiovasculares, trastornos metabólicos, trastornos oculares y trastornos oncológicos.
TNFa es el miembro prototípico de la superfamilia de proteínas del Factor de necrosis tumoral (TNF) que comparten una función primaria de regular la supervivencia celular y la muerte celular. Una característica estructural común a todos los miembros conocidos de la superfamilia TNF es la formación de complejos triméricos que se unen a y activan, receptores específicos de la superfamilia de TNF. A modo de ejemplo, TNFa existe en formas y señales solubles y transmembrana a través de dos receptores, conocidos como TNFR1 y TNFR2, con criterios de valoración funcionales distintos.
Ya hay disponibles en el mercado diversos productos capaces de modular la actividad de TNFa. Todos están aprobados para el tratamiento de trastornos inflamatorios y autoinmunitarios, tales como artritis reumatoide y enfermedad de Crohn. Todos los productos aprobados en la actualidad son macromoleculares y actúan mediante la inhibición de la unión de TNFa humano con su receptor. Los inhibidores del TNFa macromoleculares típicos incluyen anticuerpos anti-TNFa; y proteínas de fusión de receptores del TNFa solubles. Los ejemplos de anticuerpos anti-TNFa disponibles en el mercado incluyen anticuerpos completamente humanos, tales como adalimumab (Humira®) y golimumab (Simponi®), anticuerpos quiméricos, tales como infliximab (Remicade®), y fragmentos Fab' pegilados, tales como certolizumab pegol (Cimzia®). Un ejemplo de una proteína de fusión de receptor de TNFa soluble disponible en el mercado es etanercept (Enbrel®).
Los miembros de la superfamilia de TNF, incluyendo TNFa en sí mismo, están implicados en una variedad de funciones fisiológicas y patológicas que se cree que juegan un papel en una variedad de afecciones de importancia médica significativa (véase, por ejemplo, M.G. Tansey y D.E. Szymkowski, Drug Discovery Today, 2009, 14, 1082-1088; y F.S. Carneiro et al., J. Sexual Medicine, 2010, 7, 3823-3834).
Los compuestos de acuerdo con la presente invención, que son potentes moduladores de la actividad de TNFa humano, son, por tanto, beneficiosos en el tratamiento y/o la prevención de diversas enfermedades humanas. Estas incluyen trastornos autoinmunitarios e inflamatorios; trastornos neurológicos y neurodegenerativos; trastornos del dolor y nociceptivos; trastornos cardiovasculares; trastornos metabólicos; trastornos oculares; y trastornos oncológicos.
Además, los compuestos de acuerdo con la presente invención pueden resultar beneficiosos como patrones farmacológicos para su uso en el desarrollo de nuevos ensayos biológicos y en la búsqueda de nuevos agentes farmacológicos. Por tanto, en una realización, los compuestos de la presente invención pueden resultar útiles como radioligandos en ensayos para la detección de compuestos farmacológicamente activos. En una realización alternativa, determinados compuestos de la presente invención pueden resultar útiles para el acoplamiento con un fluoróforo para proporcionar conjugados fluorescentes que pueden utilizarse en ensayos (por ejemplo, un ensayo de polarización de fluorescencia) para la detección de compuestos farmacológicamente activos.
Las solicitudes de patente internacionales en trámite junto con la presente WO 2013/186229 (publicada el 19 de diciembre de 2013), WO 2014/009295 (publicada el 16 de enero de 2014) y WO 2014/009296 (también publicada el 16 de enero de 2014) describen derivados de imidazol condensados que son moduladores de la actividad de TNFa humano.
Ninguna de las técnicas anteriores disponibles hasta la fecha, sin embargo, desvela o sugiere la clase estructural precisa de derivados de imidazopiridina fusionados tal como se proporcionan mediante la presente invención.
Los compuestos de acuerdo con la presente invención inhiben potentemente la unión de un conjugado de fluorescencia a TNFa cuando se someten a ensayo en el ensayo de polarización de fluorescencia descrito en el presente documento. De hecho, cuando se someten a ensayo en ese ensayo, los compuestos de la presente invención presentan un valor de CI50 de 50 pM o menos, generalmente de 20 pM o menos, por lo general de 5 pM o menos, normalmente de 1 pM o menos, adecuadamente de 500 nM o menos, idealmente de 100 nM o menos y preferentemente de 20 nM o menos (el experto en la materia apreciará que una cifra de CI50 menor indica un compuesto más activo).
Determinados compuestos de acuerdo con la presente invención neutralizan potentemente la actividad de TNFa en
una línea celular indicadora derivada de HEK-293 disponible en el mercado conocida como HEK-Blue™ CD40L. Esta es una estirpe celular transfectada con HEK-293 estable que expresa SEAP (fosfatasa alcalina embrionaria secretada) con el control del promotor mínimo de IFNp condensado con cinco sitios de unión a NF-kB. La secreción de SEAP por estas células se estimula de una manera dependiente de la concentración mediante TNFa. Cuando se someten a ensayo en el bioensayo HEK-293, también denominado en el presente documento el ensayo de genes indicadores, determinados compuestos de la presente invención presentan un valor de CI50 de 50 pM o menos, generalmente de 20 pM o menos, por lo general de 5 pM o menos, normalmente de 1 pM o menos, adecuadamente de 500 nM o menos, idealmente de l00 nM o menos y preferentemente de 20 nM o menos (como anteriormente, el experto en la materia apreciará que una cifra de CI50 menor indica un compuesto más activo).
El documento W02004014900 trata compuestos que inhiben la p-38 cinasa y son útiles en el tratamiento de metástasis o artritis reumatoide.
La presente invención proporciona un compuesto representado por la fórmula (IIA), o un W-óxido del mismo, o una sal farmacéuticamente aceptable del mismo,
R1 representa arilo, , heterocicloalquenilo C3-7, heteroarilo, -, cicloalquil (C3-7)-heteroarilbicicloalquil (C4-9)-heteroaril-, heterocicloalquil (C3-7)-heteroaril-, heterobicicloalquil (C4-9)-heteroaril- o espiroheterocicloalquil (C4-9)-heteroaril-, cualquiera de tales grupos puede estar opcionalmente sustituido con uno, dos o tres sustituyentes seleccionados entre halógeno, haloalquilo (Ci-a), ciano, cianoalquilo (Ci-a ), nitroalquilo (Ci-e), alquilo C1-6, trifluorometilo, trifluoroetilo, alquenilo C2-6, hidroxi, hidroxialquilo (Ci-a), alcoxi Ci-a , trifluoroetoxi, carboxicicloalquiloxi (C3-7), alquiltio Ci-a , alquilsulfonilo Ci-a , alquilsulfonil (Ci-a )-alquilo (Ci-a), oxo, amino, amino-alquilo (Ci-a), alquilamino C i-6 , dialquilamino (Ci-a), alcoxi (Ci-a)alquilamino (Ci-a), W-[alquil (Ci-a)]-W-[hidroxialquil (Ci-a)]amino, alquilcarbonilamino (C2-a)-alquilo(Ci-a), alquilsulfonilamino Ci-a , W-[alquil (Ci-a)]-W-[alquilsulfonil (Ci-a)]amino, bis[alquilsulfonil (Ci-a )]amino, W-[alquil (Ci -6)]-W-[carboxialquil (Ci-a)]amino, carboxicicloalquil (C3-7)-amino, carboxicicloalquil (C3-7)alquilamino (Ci-a), formilo, alquilcarbonilo C2-a, alquilcarboniloxi (C2-a)alquilo (Ci-a), carboxi, carboxialquilo (Ci-a), alcoxicarbonilo C2-a, alcoxicarbonil C2-aalquilo (Ci-a), morfolinil-alcoxicarbonilo (Ci-a ), alcoxicarbonilmetilidenilo C2-a, aminocarbonilo, dialquilaminocarbonilo (Ci-a), aminosulfonilo, alquilsulfoximinilo (Cia), [alquil (Ci-a)][W-alquil (Ci-a )]sulfoximinilo, heteroarilo, difluorometilo, alquilsulfinilo Ci-a y cicloalquil (C3-7)sulfonilo.
R2 representa hidrógeno, halógeno, trifluorometilo o ciano; o alquilo Ci-a opcionalmente sustituido con alcoxicarbonilo C2-6;
Y representa arilo o heteroarilo, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes seleccionados entre cloro, flúor, ciano, metoxi, metilsulfonilo, trifluorometoxi y difluorometoxi;
Z representa metileno;
R5a representa hidrógeno, hidroxi, halógeno o trifluorometilo; o -NRbRc , -NRcC(O)Rd, -S(O)2RaORa-O(CO)-Rd o alquilo Ci-a , , cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes seleccionados entre halógeno, hidroxi, trifluorometilo, alquilo Ci-a , alcoxi Ci-a , alquilcarbonilo C2-6, alquiloxicarbonilo C2-6, (hidroxi)alquilo Ci-a , cicloalquilo (C3-7), alquilsulfonilo Ci-a , alquilsulfonil (Ci-a)-alquilo (Ci-a ), dialquilaminocarbonilo (Ci-a ), oxo y carboxi; y
R5b representa hidrógeno, hidroxi, halógeno, ciano, trifluorometilo; o alquilo Ci-a , dicho grupo puede estar opcionalmente sustituido con uno o más sustituyentes seleccionados entre halógeno, hidroxi, trifluorometilo, alquilo Ci-a , alcoxi Ci-a , alquilcarbonilo C2-6, alquiloxicarbonilo C2-6, (hidroxi)alquilo Ci-a , cicloalquilo (C3-7), alquilsulfonilo Ci-a , alquilsulfonil (Ci-a)-alquilo (Ci-a ), dialquilaminocarbonilo (Ci-a), oxo y carboxi;
o R5a y R5b, cuando se toman junto con el carbono al que están unidos, representan un carbonilo, tiocarbonilo o -C=N-OH; Ra representa alquilo Ci-a , arilalquilo (Ci-a) o heteroarilalquilo (Ci-a ), cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes seleccionados entre alcoxi Ci-a , oxo, ciano y alcoxicarbonilo C2-a;
Rb representa hidrógeno o alquilo Ci-a ;
Rc representa hidrógeno, alquilo Ci -6 o cicloalquilo C3-7; y
Rd representa hidrógeno; o alquilo C1-6, arilo o heteroarilo, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes seleccionados entre halógeno, alquilo C1-6, alcoxi C1-6, oxo, alquilcarboniloxi C2-6 y dialquilamino (C1-6).
En el presente documento, también se desvela un compuesto de fórmula (I) o un W-óxido del mismo, o una sal o solvato farmacéuticamente aceptable del mismo, o un derivado de glucurónido del mismo o un cocristal del mismo:
en la que
Y representa cicloalquilo C3-7, arilo, heterocicloalquilo C3-7 o heteroarilo, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes;
Z representa un heteroátomo, carbonilo; -S(O)-, -S(O)2-, -S(O)(N-Rd), -NC(O)Rd, -N(CO)-ORd, -NS(O)2Rd o -N(Rd); o una cadena de alquileno C1-4 opcionalmente sustituido, lineal o ramificada;
R1 y R2 representan independientemente hidrógeno, halógeno, ciano, nitro, hidroxi, trifluorometilo, trifluorometoxi, -ORa , -SRa , -SORa , -SO2Ra , -SF5, -NRbRc , -NRcCORd, -NRcCO2Rd, -NHCONRbRc , -NRcSO2Re , -N(SO2Re )2, -NHSO2NRbRc, -CORd, -CO2Rd, -CONRbRc, -CON(ORa)Rb, -SO2NRbRc o -S(O)(N-Rd)Ra ; o alquilo C1-6, alquenilo C2-6 , alquinilo C2-6, cicloalquilo C3-7, cicloalquenilo C4-7, cicloalquil C3-7alquilo (C1-6), arilo, arilalquilo (C1-6), heterocicloalquilo C3-7, heterocicloalquil C3-7alquilo (C1-6), heterocicloalquenilo C3-7, heterobicicloalquilo C4-9, heteroarilo, heteroarilalquilo (C1-6), heterocicloalquil C3-7-alquil C1-6-arilo-, heteroaril-heterocicloalquil (C3-7)-, cicloalquil (C3-7)-heteroaril-, cicloalquil (C3-7)-alquil (C1-6)-heteroaril-, cicloalquenil (C4-7)-heteroaril-, bicicloalquil (C4-9)-heteroaril-, bicicloalquenil (C4-9)-heteroaril-, heterocicloalquil (C3-7)-heteroaril-, heterocicloalquil (C3-7)-alquil (C1-6)-heteroaril-, heterocicloalquenil (C3-7)-heteroaril-, heterobicicloalquil (C4-9)-heteroaril- o espiroheterocicloalquil (C4-9)-heteroaril-, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes;
R3 y R4 representan independientemente hidrógeno, halógeno, ciano, nitro, hidroxi, trifluorometilo, trifluorometoxi u -ORa ; o alquilo C1-6 opcionalmente sustituido con uno o más sustituyentes; y
R5a y R5b representan independientemente hidrógeno, hidroxi, halógeno, trifluorometilo, ciano; o -NRbRc , -NRcC(O)Rd, -(CO)NRcRd, -NHS(O)2Re , -S-Ra , -(SO)-Ra , -S(O)2Ra , -S(O)(N-Rd), -S(O)2(N-Rd), -ORa , -C(O)-ORd, -O(CO)-Rd-; alquilo C1-6, alquinilo C2-6, heteroarilo, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes; o R5a y R5b, cuando se toman junto con el carbono al que están unidos, representan un carbonilo, tiocarbonilo o -C=N-OH; y R6 representa hidrógeno, hidroxi, halógeno, trifluorometilo, ciano; o -NRbRc , -NRcC(O)Rd, -(CO)NRcRd, -NHS(O)2Re , -S-Ra , -(SO)-Ra , -S(O)2Ra , -S(O)(N-Rd), -S(O)2(N-Rd), -ORa , -C(O)-ORd u -O(CO)-Rd-; alquilo C1-6, alquinilo C2-6, heteroarilo, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes; o R6 e Y, junto con el átomo de carbono al que están unidos, forman un cicloalquilo C3-7 o heterocicloalquilo C3-7, opcionalmente sustituido con uno o más sustituyentes; y
Ra representa alquilo C1-6, arilo, arilalquilo (C1-6), cicloalquilo C3-7, heterocicloalquilo C3-7, heteroarilo o heteroarilalquilo (C1-6), cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes;
Rb y Rc representan independientemente hidrógeno o trifluorometilo; o alquilo C1-6, cicloalquilo C3-7, cicloalquil C3-7alquilo (C1-6), arilo, arilalquilo (C1-6), heterocicloalquilo C3-7, heterocicloalquil C3-7alquilo (C1-6), heteroarilo o heteroarilalquilo (C1-6), cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes; o
Rb y Rc , cuando se toman en conjunto con el átomo de nitrógeno al que ambos están unidos, representan azetidin-1-ilo, pirrolidin-1-ilo, oxazolidin-3-ilo, isoxazolidin-2-ilo, tiazolidin-3-ilo, isotiazolidin-2-ilo, piperidin-1-ilo, morfolin-4
ilo, tiomorfolin-4-ilo, piperazin-1-ilo, homopiperidin-1-ilo, homomorfolin-4-ilo, homopiperazin-1-ilo, (imino)(oxo)tiazinan-4-ilo, (oxo)tiazinan-4-ilo o (dioxo)tiazinan-4-ilo, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes;
Rd representa hidrógeno; o alquilo C1-6, cicloalquilo C3-7, arilo, heterocicloalquilo C3-7 o heteroarilo, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes; y
Re representa alquilo C1-6, arilo o heteroarilo, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes.
La presente invención también proporciona un compuesto de fórmula (IIA) como se ha definido anteriormente o un N-óxido del mismo, o una sal farmacéuticamente aceptable del mismo, para su uso en terapia.
Los compuestos de fórmula (IIA) tal como se definen anteriormente o un N-óxido de los mismos, o una sal o solvato farmacéuticamente aceptable de los mismos, puede usarse en el tratamiento y/o la prevención de trastornos para los que se indica la administración de un modulador de la función del TNFa.
En otro aspecto, la presente invención proporciona un compuesto de fórmula (IIA) tal como se define anteriormente, o un N-óxido del mismo, o una sal o solvato farmacéuticamente aceptable del mismo, para su uso en el tratamiento y/o la prevención de un trastorno inflamatorio o autoinmunitario, un trastorno neurológico o neurodegenerativo, dolor o un trastorno nociceptivo, un trastorno cardiovascular, un trastorno metabólico, un trastorno ocular o un trastorno oncológico.
Cuando se indique que cualquiera de los grupos en los compuestos de fórmula (I) anteriores está opcionalmente sustituido, este grupo puede estar sin sustituir o sustituido con uno o más sustituyentes. Normalmente, dichos grupos estarán no sustituidos o sustituidos con uno o dos sustituyentes.
Para su uso en medicina, las sales de los compuestos de fórmula (IIA) serán sales farmacéuticamente aceptables. Otras sales pueden, sin embargo, ser útiles en la preparación de los compuestos de uso en la invención o de sus sales farmacéuticamente aceptables. Se describen los principios convencionales que subyacen a la selección y preparación de sales farmacéuticamente aceptables, por ejemplo, en Handbook of Pharmaceutical Salts: Properties, Selection and Use, ed. P.H. Stahl y C.G. Wermuth, Wiley-VCH, 2002. Las sales farmacéuticamente aceptables adecuadas de los compuestos de uso en la presente invención incluyen sales de adición de ácidos que pueden, por ejemplo, formarse mezclando una solución del compuesto de uso en la invención con una solución de un ácido farmacéuticamente aceptable, tal como ácido clorhídrico, ácido sulfúrico, ácido metanosulfónico, ácido fumárico, ácido maleico, ácido succínico, ácido acético, ácido benzoico, ácido cítrico, ácido tartárico o ácido fosfórico. Además, en los casos en los que los compuestos de uso en la invención portan un resto ácido, por ejemplo, carboxi, las sales farmacéuticamente aceptables adecuadas de los mismos pueden incluir sales de metales alcalinos, por ejemplo, sales de sodio o potasio; sales de metales alcalinotérreos, por ejemplo, sales de calcio o magnesio; sales de amonio; y sales formadas con ligandos orgánicos adecuados, por ejemplo, sales de amonio cuaternario y sales de meglumina.
La presente divulgación incluye dentro de su alcance solvatos de los compuestos de fórmula (I) anterior. Dichos solvatos pueden formarse con disolventes orgánicos comunes, por ejemplo, disolventes de hidrocarburo, tales como benceno o tolueno; disolventes clorados, tales como cloroformo o diclorometano; disolventes alcohólicos, tales como metanol, etanol o isopropanol; disolventes etéreos, tales como éter dietílico o tetrahidrofurano; o disolventes de éster, tales como acetato de etilo. Como alternativa, los solvatos de los compuestos de fórmula (I) pueden formarse con agua, en cuyo caso, serán hidratos.
También se desvelan en el presente documento cocristales de los compuestos de fórmula (I). El término técnico "cocristal" se usa para describir la situación donde hay presentes componentes moleculares neutros dentro de un compuesto cristalino en una proporción estequiométrica definida. La preparación de cocristales farmacéuticos hace posible que se realicen modificaciones en la forma cristalina de un ingrediente farmacéutico activo, que, a su vez, puede alterar sus propiedades fisicoquímicas sin afectar a su actividad biológica prevista (véase Pharmaceutical Salts and Co-crystals, ed. J. Wouters y L. Quere, RSC Publishing, 2012). Los ejemplos típicos de formadores de cocristales, que pueden estar presentes en el cocristal junto con el ingrediente farmacéutico activo, incluyen ácido L-ascórbico, ácido cítrico, ácido glutárico, urea y nicotinamida.
También se desvelan en el presente documento profármacos de los compuestos de fórmula (IIA) anteriores. En general, dichos profármacos serán derivados funcionales de los compuestos de fórmula (IIA) que pueden convertirse fácilmente in vivo en el compuesto requerido de fórmula (IIA). Se describen procedimientos convencionales para la selección y preparación de derivados de profármaco adecuados, por ejemplo, en Design of Prodrugs, ed. H. Bundgaard, Elsevier, 1985.
Los grupos alquilo adecuados que pueden estar presentes en los compuestos de uso en la invención incluyen grupos alquilo C1-6 de cadena lineal o ramificada, por ejemplo grupos alquilo C1-4. Los ejemplos típicos incluyen grupos metilo y etilo, y propilo de cadena lineal o ramificada, grupos butilo y pentilo. Los grupos alquilo particulares incluyen metilo,
etilo, n-propilo, isopropilo, n-butilo, sec-butilo, isobutilo, ferc-butilo, 2,2-dimetilpropilo y 3-metilbutilo. Las expresiones derivadas, tales como "alcoxi Ci-6", "alquiltio CW , "alquilsulfonilo Ci-6" y "alquilamino C W deben interpretarse en consecuencia.
La expresión "cadena de alquileno C1-4" se refiere a una cadena de alquileno divalente lineal o ramificada que contiene de 1 a 4 átomos de carbono. Los ejemplos típicos incluyen metileno, etileno, metilmetileno, etilmetileno y dimetilmetileno.
Los grupos alquenilo C2-6 adecuados incluyen vinilo y alilo.
Los grupos alquinilo C2-6 adecuados incluyen etinilo, propargilo y butinilo.
La expresión "cicloalquilo C3-7", como se usa en el presente documento, se refiere a grupos monovalentes de 3 a 7 átomos de carbono derivados de un hidrocarburo monocíclico saturado y pueden comprender análogos benzocondensados de los mismos. Los grupos cicloalquilo C3-7 adecuados incluyen ciclopropilo, ciclobutilo, benzociclobutenilo, ciclopentilo, indanilo, ciclohexilo y cicloheptilo.
La expresión "cicloalquenilo C4-7", como se usa en el presente documento, se refiere a grupos monovalentes de 4 a 7 átomos de carbono derivados de un hidrocarburo monocíclico parcialmente insaturado. Los grupos cicloalquenilo C4-7 adecuados incluyen ciclobutenilo, ciclopentenilo, ciclohexenilo y cicloheptenilo.
La expresión "bicicloalquilo C4-9", como se usa en el presente documento, se refiere a grupos monovalentes de 4 a 9 átomos de carbono derivados de un hidrocarburo cíclico saturado. Los grupos bicicloalquilo C4-9 típicos incluyen biciclo[3.1.0]hexanilo, biciclo[4.1.0]heptanilo, biciclo[2.2.2]octanilo y biciclo[3.3.1]-nonanilo.
Los grupos bicicloalquenilo (C4-9) típicos incluyen biciclo[3.1.0]hexenilo.
El término "arilo", como se usa en el presente documento, se refiere a grupos aromáticos carbocíclicos monovalentes derivados de un solo anillo aromático o de múltiples anillos aromáticos condensados. Los grupos arilo adecuados incluyen fenilo y naftilo, preferentemente fenilo.
Los grupos arilalquilo (C1-6) adecuados incluyen bencilo, feniletilo, fenilpropilo y naftilmetilo.
La expresión "heterocicloalquilo C3-7", como se usa en el presente documento, se refiere a anillos monocíclicos saturados que contienen de 3 a 7 átomos de carbono y al menos un heteroátomo seleccionado entre oxígeno, azufre y nitrógeno y puede comprender análogos benzocondensados de los mismos. Los grupos heterocicloalquilo adecuados incluyen oxetanilo, azetidinilo, tetrahidrofuranilo, dihidrobenzo-furanilo, dihidrobenzotienilo, pirrolidinilo, indolinilo, dihidroisoindolinilo, isoindolinilo, oxazolidinilo, tiazolidinilo, isotiazolidinilo, imidazolidinilo, tetrahidropiranilo, cromanilo, tetrahidro-tiopiranilo, piperidinilo, 1,2,3,4-tetrahidroquinolinilo, 1,2,3,4-tetrahidroisoquinolinilo, piperazinilo, 1,2,3,4-tetrahidroquinoxalinilo, hexahidro-[1.2.5]tiadiazolo[2,3-a]pirazinilo, homopiperazinilo, morfolinilo, benzoxazinilo, tiomorfolinilo, azepanilo, oxazepanilo, diazepanilo, tiadiazepanilo, azocanilo, (imino)(oxo)tiazinanilo, (oxo)tiazinanilo y (dioxo)tiazinanilo.
La expresión "heterocicloalquenilo C3-7", como se usa en el presente documento, se refiere a anillos monocíclicos monoinsaturados o poliinsaturados que contienen de 3 a 7 átomos de carbono y al menos un heteroátomo seleccionado entre oxígeno, azufre y nitrógeno y puede comprender análogos benzocondensados de los mismos. Los grupos heterocicloalquenilo adecuados incluyen tiazolinilo, imidazolinilo, dihidropiranilo, dihidrotiopiranilo y 1,2,3,6-tetrahidropiridinilo.
La expresión "heterobicicloalquilo C4-9", como se usa en el presente documento, corresponde a bicicloalquilo C4-9 en el que uno o más de los átomos de carbono se han reemplazado por uno o más heteroátomos seleccionados entre oxígeno, azufre y nitrógeno. Los grupos heterobicicloalquilo típicos incluyen 3-azabiciclo[3.1.0]hexanilo, 2-oxa-5-azabiciclo[2.2.1]heptanilo, 6-azabiciclo[3.2.0]heptanilo, 3-azabiciclo[3.1.1]heptanilo, 3-azabiciclo[4.1.0]heptanilo, 2-oxabiciclo[2.2.2]octanilo, quinuclidinilo, 2-oxa-5-azabiciclo-[2.2.2]octanilo, 3-azabiciclo-[3.2.1]octanilo, 8-azabiciclo-[3.2.1]octanilo, 3-oxa-8-azabiciclo[3.2.1]octanilo, 3,8-diazabiciclo[3.2.1]octanilo, 3,6-diazabiciclo[3.2.2]nonanilo, 3-oxa-7-azabiciclo[3.3.1]nonanilo, 3,9-diazabiciclo[4.2.1]nonanilo, 3,7-dioxa-9-diazabiciclo-[3.3.1]nonanilanilheptanilo y 2,5-diazabiciclo-[2.2.1]heptanilo.
La expresión "espiroheterocicloalquilo C4-9", como se usa en el presente documento, se refiere a sistemas de anillo bicíclicos saturados que contienen de 4 a 9 átomos de carbono y al menos un heteroátomo seleccionado entre oxígeno, azufre y nitrógeno, en los que dos anillos están unidos mediante un átomo común. Los grupos espiroheterocicloalquilo adecuados incluyen 5-azaespiro[2,3]hexanilo, 5-azaespiro-[2,4]heptanilo, 2-azaespiro[3,3]heptanilo, 2-oxa-6-azaespiro[3,3]heptanilo, 2-oxa-6-azaespiro-[3,4]octanilo, 2-oxa-6-azaespiro[3,5]nonanilo, 7-oxa-2-azaespiro[3,5]nonanilo, 2-oxa-7-azaespiro[3,5]nonanilo y 2,4,8-triazaespiro[4,5]decanilo.
El término "heteroarilo", como se usa en el presente documento, se refiere a grupos aromáticos monovalentes que
contienen al menos 5 átomos derivados de un solo anillo o múltiples anillos condensados, en los que uno o más átomos de carbono se han reemplazado con uno o más heteroátomos seleccionados entre oxígeno, azufre y nitrógeno. Los grupos heteroarilo adecuados incluyen grupos furilo, benzofurilo, dibenzofurilo, tienilo, benzotienilo, tieno[2,3-c]pirazolilo, tieno[3,4-b][1,4]dioxinilo, dibenzotienilo, pirrolilo, indolilo, pirrolo[2,3-d]piridinilo, pirrolo[3,2-c]piridinilo, pirrolo[3,4-b]piridinilo, pirazolilo, pirazolo[1,5-a]piridinilo, pirazolo[3,4-d]pirimidinilo, indazolilo, 4,5,6,7-tetrahidroindazolilo, oxazolilo, benzoxazolilo, isoxazolilo, tiazolilo, benzotiazolilo, isotiazolilo, imidazolilo, benzoimidazolilo, imidazo[2,1-b]tiazolilo, imidazo[1,2-a]piridinilo, imidazo[4,5-d]piridinilo, purinilo, imidazo[1,2-a]pirimidinilo, imidazo[1,2-a]pirazinilo, oxadiazolilo, tiadiazolilo, triazolilo, [1.2.4]triazolo[1,5-a]pirimidinilo, benzotriazolilo, tetrazolilo, piridinilo, quinolinilo, isoquinolinilo, naftiridinilo, piridazinilo, cinolinilo, ftalazinilo, pirimidinilo, quinazolinilo, pirazinilo, quinoxalinilo, pteridinilo, triazinilo y cromenilo.
El término "halógeno", como se usa en el presente documento, pretende incluir átomos de flúor, cloro, bromo y yodo, normalmente flúor, cloro o bromo.
Cuando los compuestos de fórmula (IIA) tienen uno o más centros asimétricos, estos pueden existir en consecuencia como enantiómeros. Cuando los compuestos de uso en la invención poseen dos o más centros asimétricos, estos pueden existir adicionalmente como diastereómeros. Ha de comprenderse que la invención se extiende al uso de todos los enantiómeros y diastereómeros de este tipo, y a mezclas de los mismos en cualquier proporción, incluyendo racematos.
La fórmula (I) y las fórmulas representadas en lo sucesivo en el presente documento están destinadas a representar todos los estereoisómeros individuales y todas las mezclas posibles de los mismos, a menos que se indique o se demuestre lo contrario. Además, los compuestos de fórmula (I) pueden existir como tautómeros, por ejemplo tautómeros ceto (CH2C=O)^enol (CH=CHOH) o tautómeros de amida (NHC=O)^hidroxiimina (N=COH). La fórmula (I) y las fórmulas representadas en lo sucesivo en el presente documento están destinadas a representar todos los tautómeros individuales y todas las mezclas posibles de los mismos, a menos que se indique o se demuestre lo contrario.
Ha de apreciarse que cada átomo individual presente en la fórmula (I) o en las fórmulas que se representan en lo sucesivo en el presente documento, puede, de hecho, estar presente en forma de cualquiera de sus isótopos de origen natural, prefiriéndose el isótopo o isótopos más abundantes. Por tanto, a modo de ejemplo, cada átomo de hidrógeno individual presente en la fórmula (I), o en las fórmulas que se representan en lo sucesivo en el presente documento, puede estar presente como un átomo de 1H, 2H (deuterio) o 3H (tritio), preferiblemente 1H. De manera similar, a modo de ejemplo, cada átomo de carbono individual presente en la fórmula (I) o en las fórmulas que se representan en lo sucesivo en el presente documento, puede estar presente como un átomo de 12C, 13C o 14C, preferiblemente 12C.
Posteriormente se exponen realizaciones y aspectos adicionales de los compuestos de fórmula (I) desvelados en el presente documento.
En general, Y representa cicloalquilo C3-7, arilo o heteroarilo, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes.
Normalmente, Y representa arilo o heteroarilo, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes.
En una primera realización, Y representa cicloalquilo C3-7 opcionalmente sustituido. En un aspecto de esa realización, Y representa cicloalquilo C3-7 no sustituido. En otro aspecto de esa realización, Y representa cicloalquilo C3-7 monosustituido. En un aspecto adicional de esa realización, Y representa cicloalquilo C3-7 disustituido.
En una segunda realización, Y representa arilo opcionalmente sustituido. En un aspecto de esa realización, Y representa arilo no sustituido. En otro aspecto de esa realización, Y representa arilo monosustituido. En un aspecto adicional de esa realización, Y representa arilo disustituido.
En una tercera realización, Y representa heterocicloalquilo C3-7 opcionalmente sustituido. En un aspecto de esa realización, Y representa heterocicloalquilo C3-7 no sustituido. En otro aspecto de esa realización, Y representa heterocicloalquilo C3-7 monosustituido. En un aspecto adicional de esa realización, Y representa heterocicloalquilo C3-7 disustituido.
En una cuarta realización, Y representa heteroarilo opcionalmente sustituido. En un aspecto de esa realización, Y representa heteroarilo no sustituido. En otro aspecto de esa realización, Y representa heteroarilo monosustituido. En un aspecto adicional de esa realización, Y representa heteroarilo disustituido.
Adecuadamente, Y representa benzociclobutenilo, fenilo, tienilo, tiazolilo, piridinilo, pirimidinilo o pirazolilo, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes.
Adecuadamente, Y representa fenilo, tienilo o tiazolilo, cualquiera de tales grupos puede estar opcionalmente
sustituido con uno o más sustituyentes.
Apropiadamente, Y representa fenilo, que puede estar opcionalmente sustituido con uno o más sustituyentes.
Los ejemplos de sustituyentes opcionales que pueden estar presentes en el resto Y incluyen uno, dos o tres sustituyentes seleccionados independientemente entre halógeno, ciano, nitro, alquilo C1-6, trifluorometilo, hidroxi, alcoxi C1-6, difluorometoxi, trifluorometoxi, alquiltio C1-6, alquilsulfinilo C1-6, alquilsulfonilo C1-6, alquilsulfoniloxi (C1-6), amino, alquil C1-6-amino, dialquilamino (C1-6), arilamino, alquilcarbonilamino C2-6, alquilsulfonilamino C1-6, formilo, alquilcarbonilo C2-6, cicloalquilcarbonilo C3-6, heterocicloalquilcarbonilo C3-6, carboxi, alcoxicarbonilo C2-6, aminocarbonilo, alquilaminocarbonilo C1-6, dialquilaminocarbonilo (C1-6), aminosulfonilo, alquilaminosulfonilo C1-6 y dialquilaminosulfonilo (C1-6).
Los ejemplos de sustituyentes particulares en el resto Y incluyen flúor, cloro, bromo, ciano, nitro, metilo, isopropilo, trifluorometilo, hidroxi, metoxi, difluorometoxi, trifluorometoxi, metiltio, metilsulfinilo, metilsulfonilo, metilsulfoniloxi, amino, metilamino, ferc-butilamino, dimetilamino, fenilamino, acetilamino, metil-sulfonilamino, formilo, acetilo, ciclopropilcarbonilo, azetidinilcarbonilo, pirrolidinilcarbonilo, piperidinilcarbonilo, piperazinilcarbonilo, morfolinilcarbonilo, carboxi, metoxicarbonilo, aminocarbonilo, metilaminocarbonilo, dimetilaminocarbonilo, aminosulfonilo, metilaminosulfonilo y dimetilaminosulfonilo.
Los ejemplos típicos de sustituyentes particulares en el resto Y incluyen cloro, flúor, ciano, metoxi, metilsulfonilo, trifluorometoxi y difluorometoxi.
Los valores típicos de Y incluyen benzociclobutenilo, fenilo, (metilsulfonil)fenilo (incluyendo 4-metilsulfonilfenilo), benzonitrilo (incluyendo 2-benzonitrilo, 3-benzonitrilo y 4-benzonitrilo), fluorofenilo (incluyendo 2-fluorofenilo, 3-fluorofenilo y 4-fluorofenilo), clorofenilo (incluyendo 2-cloro-fenilo, 3-clorofenilo y 4-clorofenilo), difluorofenilo (incluyendo 2,6-difluoro-fenilo), (cloro)(fluoro)fenilo (incluyendo 5-cloro-2-fluorofenilo y 2-cloro-5-fluorofenilo), diclorofenilo (incluyendo 2,5-diclorofenilo y 2,6-diclorofenilo), metilfenilo (incluyendo 4-metilfenilo), dimetilfenilo (incluyendo 2,5-dimetilfenilo y 2,6-dimetilfenilo), (trifluorometil)fenilo [incluyendo 2-(trifluorometil)fenilo], (cloro)(trifluorometil)fenilo [incluyendo 5-cloro-2-(trifluorometil)fenilo], (metil)-(trifluorometil)fenilo [incluyendo 2-metil-5-(trifluorometil)fenilo], bis(trifluorometil)fenilo [incluyendo 2,5-bis(trifluorometil)fenilo], metoxifenilo (incluyendo 2-metoxifenilo), (difluorometoxi)fenilo [incluyendo 2-(difluorometoxi)fenilo, 3-(difluorometoxi)fenilo y 4-(difluorometoxi)fenilo], (bis-(difluorometoxi))fenilo [incluyendo 2,5-(bis-(difluorometoxi))-fenilo e incluyendo 2,6-(bis-(difluorometoxi))-fenilo], (difluorometoxi)(fluoro)fenilo [incluyendo 2-(difluorometoxi)-5-fluorofenilo, 2-(difluorometoxi)-3-fluorofenilo, 2-(difluorometoxi)-6-fluorofenilo 5-(difluorometoxi)-2-fluorofenilo, 2-(difluorometoxi)-4-fluorofenilo y 2-(difluorometoxi)-5-fluorofenilo], (difluorometoxi)(difluoro)fenilo [(incluyendo 2-difluorometoxi-3,5-difluoro-fenilo y 2-difluorometoxi-4,5-difluoro-fenilo)], (cloro)(difluorometoxi)fenilo [incluyendo 2-cloro-5-(difluorometoxi) fenilo, 5-cloro-2-(difluorometoxi)fenilo, 5-cloro-3-(difluorometoxi)fenilo y 6-cloro-2-(difluorometoxi)fenilo], (ciano) (difluorometoxi) [incluyendo 6-ciano-2-(difluorometoxi)-fenilo (trifluorometoxi)fenilo [incluyendo 2-(trifluorometoxi)-fenilo], metilsulfoniloxifenilo], (cloro)(trifluorometoxi)fenilo, [incluyendo 3-cloro-6-trifluorometoxi-fenilo], (amino)(cloro)fenilo [incluyendo 5-amino-2-cloro-fenilo], metiltienilo [incluyendo 3-metiltien-2-ilo], metiltiazolilo [incluyendo 2-metil-1,3-tiazol-4-ilo y 4-metil-1,3-tiazol-4-ilo], (cloro)tiazolilo (incluyendo 4-cloro-1,3-tiazolilo), (cloro)(metil)tiazolilo [incluyendo 5-cloro-2-metil-1,3-tiazol-4-ilo], dimetiltiazolilo [incluyendo 2,4-dimetil-1,3-tiazol-5-ilo], piridinilo [incluyendo piridin-3-ilo y piridin-4-ilo], (metil)(trifluorometil)tiazolilo [incluyendo 2-metil-4-trifluorometil-1,3-tiazolilo], (dimetoxi)pirimidinilo [incluyendo 4,6-dimetoxi-piridin-5-ilo] y (metoxi)pirazinilo (incluyendo 5-metoxipirazinilo).
Los valores seleccionados de Y incluyen fenilo, (metilsulfonil)fenilo, benzonitril clorofenilo, (cloro)(fluoro)fenilo, diclorofenilo, dimetilfenilo, (trifluorometil)fenilo, (difluorometoxi)fenilo, (bis-(difluorometoxi))fenilo, (difluorometoxi)(fluoro)fenilo, (difluorometoxi)(ciano)fenilo, (difluorometoxi)(difluoro)fenilo, (cloro)(difluorometoxi)fenilo, (cloro)(trifluorometoxi)fenilo, (cloro)(metil)tiazolilo, (cloro)tiazolilo, (metil)(trifluorometil)tiazolilo, (dimetoxi)pirimidinilo y (metoxi)pirazinilo. Un valor adicional de Y incluye (metoxi)fenilo.
Los valores definitivos de Y incluyen (difluorometoxi)fenilo, (difluorometoxi)(fluoro)fenilo, (cloro)(difluorometoxi)fenilo y (difluorometoxi)(ciano)fenilo, (metoxi)fenilo, (diflurometoxi)(difluoro)fenilo y (cloro)fenilo.
Los valores particulares de Y incluyen (difluorometoxi)fenilo, (difluorometoxi)(fluoro)fenilo, (cloro)(difluorometoxi)fenilo y (difluorometoxi)(ciano)fenilo.
Los valores ilustrativos de Y incluyen 2-difluorometoxi-fenilo, 2-difluorometoxi-5-cloro-fenilo, 2-difluorometoxi-6-clorofenilo, 2-difluorometoxi-6-fluoro-fenilo y 2-difluorometoxi-6-ciano-fenilo, 2-metoxi-fenilo, 3-cloro-fenilo, 2-difluorometoxi-4,5-difluoro-fenilo, 2-difluorometoxi-5-fluoro-fenilo y 2-difluorometoxi-4-fluoro-fenilo.
Los valores específicos de Y incluyen 2-difluorometoxi-fenilo, 2-difluorometoxi-5-cloro-fenilo, 2-difluorometoxi-6-clorofenilo, 2-difluorometoxi-6-fluoro-fenilo y 2-difluorometoxi-6-ciano-fenilo.
En una realización particular, Y representa 2-(difluorometoxi)fenilo.
En otra realización particular, Y representa 2-difluorometoxi-5-cloro-fenilo.
En general, Z representa un heteroátomo; -S(O), -S(O)2, -S(O)(N-Rd), -NC(O)Rd, -N(CO)-ORd, -NS(O)2Rd o -N(Rd); o una cadena de alquileno C1-4 opcionalmente sustituido, lineal o ramificada;
En particular, Z representa una cadena de alquileno C1-4 opcionalmente sustituido, lineal o ramificada.
En una primera realización, Z representa un heteroátomo. En un aspecto de esa realización, Z representa un oxígeno. En un segundo aspecto de esa realización, Z representa un azufre. En una segunda realización, Z representa -S(O). En una tercera realización, Z representa -S(O)2. En una cuarta realización, Z representa S(O)(N-Rd). En una quinta realización, Z representa -NC(O)Rd. En una sexta realización, Z representa -N(CO)-ORd. En una séptima realización, Z representa -NS(O)2Rd. En una octava realización, Z representa -N(Rd).
En una novena realización, Z representa una cadena de alquileno C1-4 opcionalmente sustituido, lineal o ramificada. Los valores típicos de Z de acuerdo con esta realización incluyen metileno (-CH2-), (metil)metileno, etileno (-CH2CH2-), (etil)metileno, (dimetil)-metileno, (metil)etileno, propileno (-CH2CH2CH2-), (propil)metileno y (dimetil)etileno, cualquiera de estas cadenas puede estar opcionalmente sustituida con uno o más sustituyentes. En un aspecto de esta realización, Z representa una cadena de alquileno C1-4 no sustituida, lineal o ramificada. En un segundo aspecto de esta realización, Z representa una cadena de alquileno C1-4 monosustituida, lineal o ramificada. En un tercer aspecto de esta realización, Z representa una cadena de alquileno C1-4 disustituida, lineal o ramificada.
En una décima realización, Z representa carbonilo.
Los ejemplos de sustituyentes típicos en la cadena de alquileno que puede estar presente en un compuesto de acuerdo con la invención incluyen halógeno, hidroxi, oxo, alcoxi C1-6, arilo, -C(O)Rd, -CO2Rd, -CONRbRc , -S(O)(N-Rd)Ra y -SO2NRbRc
Un valor particular de Z es metileno.
Adecuadamente, R1 y R2 representan independientemente hidrógeno, halógeno, ciano, trifluorometilo; -S(O)2(N-Rd) o -CO2Rd; o alquilo C1-6, alquinilo C2-6, arilo, heterocicloalquilo C3-7, heterocicloalquenilo C3-7, heteroarilo, heterocicloalquil (C3-7)alquilaril (C1-6)-, heteroaril-heterocicloalquil C3-7-, cicloalquil (C3-7)-heteroaril-, cicloalquil (C3-7)-alquil (C1-6)-heteroaril-, cicloalquenil (C4-7)-heteroaril-, bicicloalquil (C4-9)-heteroaril-, heterocicloalquil (C3-7)-heteroaril-, heterocicloalquil (C3-7)-alquil (C1-6)-heteroaril-, heterocicloalquenil (C3-7)-heteroaril-, heterobicicloalquil (C4-9)-heteroarilo espiroheterocicloalquil (C4-9)-heteroaril-, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes.
Normalmente, R2 representa hidrógeno, halógeno, ciano, nitro, hidroxi, trifluorometilo, trifluorometoxi u -ORa ; o alquilo C1-6 opcionalmente sustituido con uno o más sustituyentes.
En general, R3 representa hidrógeno, halógeno, ciano, nitro, hidroxi, trifluorometilo, trifluorometoxi; -ORa , -SRa , -SORa o -SO2Ra ; o alquilo C1-6 opcionalmente sustituido con uno o más sustituyentes.
Normalmente, R3 representa hidrógeno, halógeno, ciano, nitro, hidroxi, trifluorometilo, trifluorometoxi u -ORa ; o alquilo C1-6 opcionalmente sustituido con uno o más sustituyentes.
En general, R4 representa hidrógeno, halógeno, ciano, nitro, hidroxi, trifluorometilo, trifluorometoxi; -ORa , -SRa , -SORa o -SO2Ra ; o alquilo C1-6 opcionalmente sustituido con uno o más sustituyentes.
Normalmente, R4 representa hidrógeno, halógeno, ciano, nitro, hidroxi, trifluorometilo, trifluorometoxi u -ORa ; o alquilo C1-6 opcionalmente sustituido con uno o más sustituyentes.
En general, R5a representa hidrógeno, hidroxi, halógeno, ciano, trifluorometilo; -NRbRc , -NRcC(O)Rd, -(CO)NRcRd, -NHS(O)2Re , -S-Ra , -(SO)-Ra , -S(O)2Ra , -S(O)(N-Rd), -S(O)2(N-Rd), -ORa , -C(O)2Rd u -O(CO)-Rd-; o alquilo C1-6, alquenilo C2-6, alquinilo C2-6, arilo o heteroarilo, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes.
En general, R5b representa hidrógeno, hidroxi, halógeno, ciano, trifluorometilo; -NRbRc , -NRcC(O)Rd, -(CO)NRcRd, -NHS(O)2Re , -S-Ra , -(SO)-Ra , -S(O)2Ra , -S(O)(N-Rd), -S(O)2(N-Rd), -ORa , -C(O)2Rd u -O(CO)-Rd-; o alquilo C1-6, alquenilo C2-6, alquinilo C2-6, arilo o heteroarilo, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes.
Adecuadamente, R5a representa hidrógeno, hidroxi, halógeno, ciano, trifluorometilo; -NRbRc , -NRcC(O)Rd, -(CO)NRcRd, -NHS(O)2Re , -S-Ra , -(SO)-Ra, -S(O)2Ra , -S(O)(N-Rd), -S(O)2(N-Rd), -ORa , -C(O)2Rd u -O(CO)-Rd-; o alquilo C1-6, alquenilo C2-6, alquinilo C2-6, arilo, heteroarilo, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes.
R5b representa hidrógeno, hidroxi, halógeno, ciano o trifluorometilo; o alquilo Ci-6, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes.
Como alternativa, R5a y R5b, cuando se toman junto con el carbono al que están unidos, representan un carbonilo, tiocarbonilo o -C=N-OH.
En general, R6 representa hidrógeno, hidroxi, halógeno, ciano, trifluorometilo; -NRbRc, -NRcC(O)Rd, -(CO)NRcRd, -NHS(O)2Re , -S-Ra , -(SO)-Ra , -S(O)2Ra , -S(O)(N-Rd), -S(O)2(N-Rd), -ORa , -C(O)2Rd u -O(CO)-Rd-; o alquilo C1-6, alquenilo C2-6, alquinilo C2-6, arilo, heteroarilo, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes.
Los ejemplos de sustituyentes opcionales que pueden estar presentes en R1, R2 , R3 , R4 , R5a, R5b y R6 incluyen uno, dos o tres sustituyentes seleccionados independientemente entre halógeno, halo-alquilo C1-6, ciano, cianoalquilo (C1-6), nitro, nitroalquilo (C1-6), alquilo C1-6, cicloalquilo (C3-7), difluorometilo, trifluorometilo, difluoroetilo, trifluoroetilo, alquenilo C2-6, hidroxi, hidroxialquilo (C1-6), alcoxi C1-6, difluorometoxi, trifluorometoxi, trifluoroetoxi, carboxicicloalquil (C3-7)-oxi, alquilendioxi C1-3, alcoxi C1-6alquilo (C1-6), alquiltio C1-6, alquilsulfinilo C1-6, alquilsulfonilo C1-6, alquilsulfonil (C1-e)-alquilo (C1-6), oxo, amino, aminoalquilo (C1-6), alquil C1-6-amino, dialquilamino (C1-6), hidroxialquilamino (C1-6), alcoxiamino C1-6, alcoxi (C1-6)-alquilamino (C1-6), [alcoxi (C1-6)](hidroxi)alquilamino (C1-6), [alquiltio (C1-6)](hidroxi)-alquilamino (C1-6), N-[alquil (C1-6)]-N-[hidroxialquil (C1-6)]amino, dialquilamino (C1-6)-alquilamino (C1-6), ^-[dialquilamino (C1-6)alquil (C1-6)]-W-[hidroxialquil (C1-6)]amino, hidroxialquil (C1-6)-cicloalquilamino (C3-7), (hidroxi)[cicloalquil (C3-7)alquil (C1-6)]amino, heterocicloalquil (C3-7)-alquilamino (C1-6), oxoheterocicloalquil (C3-7)-alquilamino (C1-6), alquilheteroarilamino (C1-6), heteroaril-alquilamino (C1-6), alquilheteroaril (C1-6)alquil (C1-6)-amino, alquilcarbonilamino C2-6, N-[alquil (C1-6)]-N-[alquilcarbonil (C2-6)]amino, alquil (C2-6)-carbonilaminoalquilo (C1-6), alquenilcarbonilamino C3-6, bis[alquenilcarbonil (C3-6)]amino, N-[alquil (C1-6)]-N-[cicloalquilcarbonil (C3-7)]amino, alcoxicarbonilamino C2-6, alcoxicarbonil C2-6alquilamino (C1-6), alquilaminocarbonilamino C1-6, alquilsulfonil C1-6-amino, N-[alquil (C1-6)]-N-[alquilsulfonil (C1-6)]amino, bis[alquilsulfonil (C1-6)]amino, N-[alquil (C1-6)]-N-[carboxialquil (C1-6)]amino, carboxicicloalquilamino (C3-7), carboxicicloalquil (C3-7)-alquilamino (C1-6), formilo, alquilcarbonilo C2-6, cicloalquilcarbonilo (C3-7), fenilcarbonilo, alquilcarboniloxi (C2-6)alquilo (C1-6), carboxi, carboxialquilo (C1-6), alcoxicarbonilo C2-6, alcoxicarbonil C2-6alquilo (C1-6), morfolinil-alcoxicarbonilo (C1-6), alcoxicarbonilmetilidenilo C2-6, un resto de profármaco o isóstero de ácido carboxílico O, -alquil (C1-6)-O, aminocarbonilo, alquilaminocarbonilo C1-6, hidroxialquilaminocarbonilo (C1-6), dialquilaminocarbonilo (C1-6), aminocarbonilalquilo (C1-6), aminosulfonilo, dialquilaminosulfonilo (C1-6), alquilsulfoximinilo (C1-6), [alquil (C1-6)][N-alquil (C1-6)]-sulfoximinilo y heteroarilo. Un ejemplo adicional de sustituyentes incluye cicloalquilsulfonilo C3-7.
Mediante la expresión "resto de profármaco o isóstero de ácido carboxílico" se pretende cualquier grupo funcional, estructuralmente distinto de un resto de ácido carboxílico, que será reconocido como similar por un sistema biológico a, y por tanto capaz de imitar, un resto de ácido carboxílico, o será fácilmente convertible por un sistema biológico in vivo en un resto de ácido carboxílico. Una sinopsis de algunos isósteros de ácido carboxílico comunes se presenta por N.A. Meanwell en J. Med. Chem., 2011, 54, 2529-2591 (véanse, en particular, las Figuras 25 y 26). Un isóstero de ácido carboxílico alternativo se describe por N Pemberton et al. en ACS Med. Chem. Lett., 2012, 3, 574-578. Los ejemplos típicos de restos de profármaco o isóstero de ácido carboxílico adecuados representados por O incluyen los grupos funcionales de fórmula (i) a (xliii):
en la que
el asterisco (*) representa el sitio de unión al resto de la molécula; n es cero, 1 o 2;
X representa oxígeno o azufre;
Rf representa hidrógeno, alquilo C1-6 o -CH2CH(OH)CH2OH;
Rg representa alquilo C1-6, trifluorometilo, -CH2CH2F, -CH2CHF2, -CH2CF3 o -CF2CF3;
Rh representa hidrógeno, ciano o -CO2Rd, en el que Rd es como se ha definido anteriormente; y
Rj representa hidrógeno o halógeno.
En una realización, n es cero. En otra realización, n es 1. En una realización adicional, n es 2.
En una realización, X representa oxígeno. En otra realización, X representa azufre.
En una realización, Rf representa hidrógeno. En otra realización, Rf representa alquilo C1-6, especialmente metilo. En una realización adicional, Rf es -CH2CH(OH)CH2OH.
En una realización, Rg representa alquilo C1-6, especialmente metilo. En otra realización, Rg representa trifluorometilo, -CH2CH2F, -CH2CHF2, -CH2CF3 o -CF2CF3. En un primer aspecto de esa realización, Rg representa trifluorometilo. En un segundo aspecto de esa realización, Rg representa -CH2CH2F. En un tercer aspecto de esa realización, Rg representa -CH2CHF2. En un cuarto aspecto de esa realización, Rg representa -CH2CF3. En un quinto aspecto de esa realización, Rg representa -CF2CF3.
En una realización, Rh es hidrógeno. En otra realización, Rh representa ciano. En una realización adicional, Rh representa -CO2Rd, especialmente metoxicarbonilo.
En una realización, Rj representa hidrógeno. En otra realización, Rj representa halógeno, especialmente cloro. En una realización seleccionada, O representa tetrazolilo, especialmente un resto de tetrazolilo C-enlazado de fórmula (xxiv) o (xxv) como se ha representado anteriormente, en particular, un grupo de fórmula (xxiv), como se ha
representado anteriormente.
En otra realización, O representa alquilsulfonilaminocarbonilo Ci -6, es decir un resto de fórmula (iii) como se ha representado anteriormente, en el que Rg representa alquilo Ci -6.
En otra realización, O representa alquilaminosulfonilo Ci -6, es decir, un resto de fórmula (x) como se ha representado anteriormente, en el que Rg representa alquilo Ci -6.
En una realización adicional, O representa alquilcarbonilaminosulfonilo (Ci -6), es decir, un resto de fórmula (v) como se ha representado anteriormente, en el que Rg representa alquilo Ci -6.
Los ejemplos de sustituyentes particulares en Ri , R2, R3 , R4 , R5a, R5b y R6 incluyen flúor, cloro, bromo, fluorometilo, fluoroisopropilo, ciano, cianoetilo, nitro, nitrometilo, metilo, etilo, isopropilo, isobutilo, tere-butilo, ciclopropilo, ciclobutilo, difluorometilo, trifluorometilo, difluoroetilo, trifluoroetilo, etenilo, hidroxi, hidroximetilo, hidroxiisopropilo, metoxi, isopropoxi, difluorometoxi, trifluorometoxi, trifluoroetoxi, carboxiciclobutiloxi, metilendioxi, etilendioxi, metoximetilo, metoxietilo, metiltio, metilsulfinilo, metilsulfonilo, metilsulfoniletilo, oxo, amino, aminometilo, aminoisopropilo, metilamino, etilamino, dimetilamino, hidroxietilamino, hidroxipropilamino, (hidroxi)(metil)propilamino, metoxiamino, metoxietilamino, (hidroxi)-(metoxi)(metil)propilamino, (hidroxi) (metiltio) butilamino, W-(hidroxietil)-W-(metil)amino, dimetilaminoetilamino, (dimetilamino)(metil)propilamino, W-(dimetilaminoetil)-W-(hidroxietil)amino, hidroximetilciclopentilamino, hidroxiciclobutilmetilamino, (ciclopropil)(hidroxi)propilamino, morfoliniletilamino, oxopirrolidinilmetilamino, etiloxadiazolilamino, metiltiadiazolilamino, tiazolilmetilamino, tiazoliletilamino, pirimidinilmetilamino, metilpirazolilmetilamino, acetilamino, W-acetil-W-metilamino, W-isopropilcarbonil-W-metilamino, acetilaminometilo, etenilcarbonilamino, bis(etenilcarbonil)amino, W-ciclopropilcarbonil-W-metilamino, metoxicarbonilamino, etoxicarbonilamino, fere-butoxicarbonilamino, metoxicarboniletilamino, etilaminocarbonilamino, butilaminocarbonilamino, metilsulfonilamino, W-metil-W-(metilsulfonil)amino, bis(metilsulfonil)amino, W-(carboximetil)-W-metilamino, W-(carboxietil)-W-metilamino, carboxiciclopentilamino, carboxiciclopropilmetilamino, formilo, acetilo, isopropilcarbonilo, ciclobutilcarbonilo, fenilcarbonilo, acetoxiisopropilo, carboxi, carboximetilo, carboxietilo, metoxicarbonilo, etoxicarbonilo, n-butoxicarbonilo, fere-butoxicarbonilo, metoxicarbonilmetilo, etoxicarbonilmetilo, etoxicarboniletilo, morfoliniletoxicarbonilo, etoxicarbonilmetilidenilo, metilsulfonilaminocarbonilo, acetilaminosulfonilo, metoxiaminocarbonilo, tetrazolilo, tetrazolilmetilo, hidroxioxadiazolilo, aminocarbonilo, metilaminocarbonilo, hidroxietilaminocarbonilo, dimetilaminocarbonilo, aminocarbonilmetilo, aminosulfonilo, metilaminosulfonilo, dimetilaminosulfonilo, metilsulfoximinilo, (metil)(W-metil)sulfoximinilo y triazolilo. Los ejemplos adicionales de un sustituyente particular incluyen ciclopropilsulfonilo y fere-butoxi.
Los ejemplos adecuados de sustituyentes opcionales en Ri , R2 , R3 , R4 , R5a, R5b y R6 incluyen flúor, hidroxi, metilsulfonilo, metilo, trifluorometilo, isopropilo, ciclopropilo, metoxi, etoxicarbonilo, metilsulfoximinilo, oxo, carboxi, acetilo, cloro, hidroxiisopropilo, fluoroisopropilo, aminoisopropilo, metilsulfonilo, metilsulfinilo, ciclopropilsulfonilo y ferebutoxi.
Los ejemplos típicos de sustituyentes particulares en R1, R2 , R3 , R4 , R5a, R5b y R6 incluyen flúor, hidroxi, metilsulfonilo, metilo, trifluorometilo, isopropilo, ciclopropilo, metoxi, etoxicarbonilo, metilsulfoximinilo, oxo, carboxi y acetilo.
Normalmente, R1 representa hidrógeno, halógeno, ciano o -CO2Rd; o alquilo Ci -6, alquinilo C2-6, arilo, heterocicloalquilo C3-7, heterocicloalquenilo C3-7, heteroarilo, heterocicloalquil C3-7-alquil Ci -6-arilo-, heteroaril-heterocicloalquil (C3-7)-, cicloalquil (C3-7)-heteroaril-, cicloalquil (C3-7)-alquil (Ci -6)-heteroaril-, cicloalquenil (C4-7)-heteroaril-, bicicloalquilheteroaril C4-9-, heterocicloalquil (C3-7)-heteroaril-, heterocicloalquil (C3-7)-alquil (Ci -6)-heteroaril-, heterocicloalquenilheteroaril (C3-7)-, heterobicicloalquil (C4-9)-heteroaril- o espiroheterocicloalquil (C4-9)-heteroaril-, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes.
Adecuadamente, R1 representa halógeno, ciano o -CO2Rd; o alquilo Ci -6, alquinilo C2-6, arilo, heterocicloalquilo C3-7, heterocicloalquenilo C3-7, heteroarilo, heterocicloalquil (C3-7)-alquil (Ci -6)-aril-, heteroaril-heterocicloalquil (C3-7)-, cicloalquil (C3-7)-heteroaril-, cicloalquil (C3-7)-alquil (Ci -6)-heteroaril-, cicloalquenil (C4-7)-heteroaril-, bicicloalquil (C4-9)-heteroaril-, heterocicloalquil (C3-7)-heteroaril-, heterocicloalquil (C3-7)-alquil (Ci -6)-heteroaril-, heterocicloalquenil (C3-7)-heteroaril-, heterobicicloalquil (C4-9)-heteroaril- o espiroheterocicloalquil (C4-9)-heteroaril-, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes.
En general, R1 representa halógeno o ciano; o alquilo Ci -6, alquinilo C2-6, arilo, heterocicloalquilo C3-7, heterocicloalquenilo C3-7, heteroarilo, heterocicloalquil (C3-7)alquilaril (Ci -6)-, heteroaril-heterocicloalquil (C3-7)-, cicloalquil (C3-7)-heteroaril-, cicloalquil (C3-7)-alquil (Ci -6)-heteroaril-, cicloalquenil (C4-7)-heteroaril-, bicicloalquil (C4-9)-heteroaril-, heterocicloalquil (C3-7)-heteroaril-, heterocicloalquil (C3-7)-alquil (Ci -6)-heteroaril-, heterocicloalquenil (C3-7)-heteroaril-, heterobicicloalquil (C4-9)-heteroaril- o espiroheterocicloalquil (C4-9)-heteroaril-, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes.
Más generalmente, R1 representa arilo, heterocicloalquenilo C3-7, heteroarilo, heterocicloalquil (C3-7)-heteroaril-, heterobicicloalquil (C4-9)-heteroaril-, cicloalquil (C3-7)-heteroaril- o bicicloalquil (C4-9)-heteroaril-, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes.
Oportunamente, R1 representa arilo, heteroarilo o heterocicloalquil (C3-7)-heteroaril-, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes.
En una primera realización, R1 representa hidrógeno.
En una segunda realización, R1 representa halógeno. En un aspecto de esa realización, R1 representa bromo.
En una tercera realización, R1 representa ciano.
En una cuarta realización, R1 representa -CO2Rd.
En una quinta realización, R1 representa alquilo C1-6 opcionalmente sustituido. En un aspecto de esa realización, R1 representa metilo opcionalmente sustituido. En otro aspecto de esa realización, , R1 representa etilo opcionalmente sustituido.
En una sexta realización, R1 representa alquinilo C2-6 opcionalmente sustituido. En un aspecto de esa realización, R1 representa butinilo opcionalmente sustituido.
En una séptima realización, R1 representa arilo opcionalmente sustituido. En un aspecto de esa realización, R1 representa fenilo opcionalmente sustituido.
En una octava realización, R1 representa heterocicloalquilo C3-7 opcionalmente sustituido.
En una novena realización, R1 representa heterocicloalquenilo C3-7 opcionalmente sustituido. En un aspecto de esta realización, R1 representa piridin-2(1H)-ona opcionalmente sustituida.
En una décima realización, R1 representa heteroarilo opcionalmente sustituido. En aspectos seleccionados de esa realización, R1 representa benzofurilo, tienilo, indolilo, pirazolilo, indazolilo, isoxazolilo, tiazolilo, imidazolilo, piridinilo, quinolinilo, piridazinilo, pirimidinilo o pirazinilo, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes. En un primer aspecto particular de esa realización, R1 representa pirimidinilo opcionalmente sustituido. En un segundo aspecto particular de esa realización, R1 representa piridinilo opcionalmente sustituido.
En una decimoprimera realización, R1 representa heterocicloalquil (C3-7)alquil (C1-6)-aril- opcionalmente sustituido. En un primer aspecto de esa realización, R1 representa pirrolidinilmetilfenil- opcionalmente sustituido. En un segundo aspecto de esa realización, R1 representa opcionalmente sustituido piperazinilmetilfenil-.
En una duodécima realización, R1 representa heteroaril (C3-7)-heterocicloalquil- opcionalmente sustituido. En un aspecto de esa realización, R1 representa piridinilpiperazinil- opcionalmente sustituido.
En una decimotercera realización, R1 representa cicloalquil (C3-7)-heteroaril- opcionalmente sustituido. En un primer aspecto de esa realización, R1 representa ciclohexilpirazolil- opcionalmente sustituido. En un segundo aspecto de esa realización, R1 representa ciclohexilpiridinil- opcionalmente sustituido. En un tercer aspecto de esa realización, R1 representa ciclopropilpirimidinil- opcionalmente sustituido. En un cuarto aspecto de esa realización, R1 representa ciclobutilpirimidinil- opcionalmente sustituido. En un quinto aspecto de esa realización, R1 representa ciclopentilpirimidinil- opcionalmente sustituido. En un sexto aspecto de esa realización, R1 representa ciclohexilpirimidinil- opcionalmente sustituido. En un séptimo aspecto de esa realización, R1 representa ciclohexilpirazinil- opcionalmente sustituido. En un octavo aspecto de esa realización, R1 representa ciclopropil piridinilo opcionalmente sustituido. En una decimocuarta realización, R1 representa cicloalquenil (C4-7)-heteroarilopcionalmente sustituido.
En una decimoquinta realización, R1 representa heterocicloalquil (C3-7)-heteroaril- opcionalmente sustituido. En un primer aspecto de esa realización, R1 representa pirrolidinilpiridinil- opcionalmente sustituido. En un segundo aspecto de esa realización, R1 representa tetrahidropiranilpiridinil- opcionalmente sustituido. En un tercer aspecto de esa realización, R1 representa piperidinilpiridinil- opcionalmente sustituido. En un cuarto aspecto de esa realización, R1 representa piperazinilpiridinil- opcionalmente sustituido. En un quinto aspecto de esa realización, R1 representa morfolinilpiridinil- opcionalmente sustituido. En un sexto aspecto de esa realización, R1 representa tiomorfolinilpiridinilopcionalmente sustituido. En un séptimo aspecto de esa realización, R1 representa diazepanilpiridinil- opcionalmente sustituido. En un octavo aspecto de esa realización, R1 representa oxetanilpirimidinil- opcionalmente sustituido. En un noveno aspecto de esa realización, R1 representa azetidinilpirimidinil- opcionalmente sustituido. En un décimo aspecto de esa realización, R1 representa tetrahidrofuranoilpirimidinil- opcionalmente sustituido. En un decimoprimer aspecto de esa realización, R1 representa pirrolidinilpirimidinil- opcionalmente sustituido. En un decimosegundo aspecto de esa realización, R1 representa tetrahidropiranilpirimidinil- opcionalmente sustituido. En un decimotercer aspecto de esa realización, R1 representa piperidinilpirimidinil- opcionalmente sustituido. En un decimocuarto aspecto de esa realización, R1 representa piperazinilpirimidinil- opcionalmente sustituido. En un decimoquinto aspecto de esa realización, R1 representa morfolinilpirimidinil- opcionalmente sustituido. En un decimosexto aspecto de esa
realización, R1 representa opcionalmente sustituido tiomorfolinilpirimidinil-. En un decimoséptimo aspecto de esa realización, R1 representa azepanilpirimidinil- opcionalmente sustituido. En un decimoctavo aspecto de esa realización, R1 representa oxazepanilpirimidinil- opcionalmente sustituido. En un decimonoveno aspecto de esa realización, R1 representa diazepanilpirimidinil- opcionalmente sustituido. En un vigésimo aspecto de esa realización, R1 representa tiadiazepanilpirimidinil- opcionalmente sustituido. En un vigesimoprimer aspecto de esa realización, R1 representa oxetanilpirazinil- opcionalmente sustituido. En un vigesimosegundo aspecto de esa realización, R1 representa piperidinilpirazinil- opcionalmente sustituido. En un vigesimotercer aspecto de esta realización, R1 representa tetrahidropiranilpiridinilo opcionalmente sustituido. En un vigesimocuarto aspecto de esa realización, R1 representa tetrahidro-tiopiranilpirimidinilo. En un vigesimoquinto aspecto de esta realización, R1 representa (imino)(oxo)tiazinanilpirimidinilo. En un vigesimosexto aspecto de esa realización, R1 representa (oxo)tiazinanil-pirimidinilo. En un vigesimoséptimo aspecto de esta realización, R1 representa (dioxo)tiazinanil-pirimidinilo.
En una decimosexta realización, R1 representa heterocicloalquil (C3-7)alquil (C1-6)-heteroaril- opcionalmente sustituido. En un primer aspecto de esa realización, R1 representa morfolinilmetiltienil- opcionalmente sustituido. En un segundo aspecto de esa realización, R1 representa morfoliniletilpirazolil- opcionalmente sustituido.
En una decimoséptima realización, R1 representa heterocicloalquenil (C3-7)-heteroaril- opcionalmente sustituido.
En una decimoctava realización, R1 representa heterobicicloalquil (C4-9)-heteroaril- opcionalmente sustituido. En un primer aspecto de esta realización, R1 representa 3-azabiciclo[3.2.1]octanil-pirimidinilo opcionalmente sustituido. En un segundo aspecto de esta realización, , R1 representa 3-oxa-8-azabiciclo-[3.2.1]octanil-pirimidinilo opcionalmente sustituido. En un tercer aspecto de esta realización, R1 representa 3,7-dioxa-9-azabiciclo[3.3.1]nonanil-pirimidnilo opcionalmente sustituido. En un cuarto aspecto de esta realización, R1 representa 2,5-diazabiciclo[2.2.1]heptanilpirimidnilo opcionalmente sustituido.
En una decimonovena realización, R1 representa espiroheterocicloalquil (C4-9)-heteroaril- opcionalmente sustituido.
En una vigésima realización, R1 representa cicloalquil (C3-7)-alquil (C1-6)-heteroaril- opcionalmente sustituido. En un aspecto de esa realización, R1 representa ciclohexilmetilpirimidinil- opcionalmente sustituido.
En una vigesimoprimera realización, R1 representa bicicloalquil (C4-9)-heteroaril- opcionalmente sustituido. En un aspecto particular de esta realización, R1 representa biciclo[3.1.0]hexanil-pirimidinilo opcionalmente sustituido.
En una vigesimosegunda realización, R1 representa bicicloalquenil (C4-9)-heteroaril- opcionalmente sustituido.
Apropiadamente, R1 representa hidrógeno, bromo, ciano o -CO2Rd; o etilo, butinilo, fenilo, pirrolidinilo, piperidinilo, piperazinilo, morfolinilo, 1,2,3,6-tetrahidropiridinilo, 3,6-dihidropiridinilo, benzofurilo, tienilo, indolilo, pirazolilo, indazolilo, isoxazolilo, tiazolilo, imidazolilo, piridinilo, quinolinilo, piridazinilo, pirimidinilo, pirazinilo, pirrolidinilmetilfenilo, piperazinilmetilfenilo, piridinilpiperazinilo, ciclohexilpirazolilo, ciclohexilpiridinilo, ciclopropilpirimidinilo, ciclobutilpirimidinilo, ciclopentilpirimidinilo, ciclohexil-pirimidinilo, ciclohexilpirazinilo, ciclohexilmetilpirimidinilo, ciclohexenilpiridinilo, ciclopropilpiridinilo, ciclohexenilpirimidinilo, biciclo[3.1.0]hexanilpiridinilo, biciclo[3.1.0]hexanilpirimidinilo, biciclo[3.1.0]hexenil-pirimidinilo, biciclo[4.1.0]heptanilpirimidinilo, biciclo[2.2.2]octanilpirimidinilo, pirrolidinilpiridinilo, tetrahidropiranilpiridinilo, tetrahidro-tiopiranilpirimidinilo, piperidinilpiridinilo, piperazinil-piridinilo, morfolinilpiridinilo, tiomorfolinilpiridinilo, diazepanilpiridinilo, oxetanilpirimidinilo, azetidinilpirimidinilo, tetrahidrofuranilpirimidinilo, pirrolidinil-pirimidinilo, tetrahidropiranilpirimidinilo, piperidinilpirimidinilo, piperazinilpirimidinilo, hexahidro[1.2.5]tiadiazolo[2,3-a]pirazinilpirimidinilo, morfolinil-pirimidinilo, tiomorfolinilpirimidinilo, azepanilpirimidinilo, oxazepanilpirimidinilo, diazepanilpirimidinilo, tiadiazepanilpirimidinilo, oxetanilpirazinilo, piperidinilpirazinilo, morfolinilmetiltienilo, morfoliniletilpirazolilo, 3-azabiciclo[3.1.0]-hexanilpiridinilo, 3-azabiciclo[3.1.0]hexanilpiridazinilo, 3-azabiciclo[3.1.0]hexanil-pirimidinilo, 2-oxa-5-azabiciclo[2.2.1]heptanilpirimidinilo, 3-azabiciclo[3.1.1]heptanil-pirimidinilo, 3-azabiciclo[4.1.0]heptanilpiridinilo, 3-azabiciclo[4.1.0]heptanil-pirimidinilo, 2-oxabiciclo[2.2.2]octanilpirimidinilo, 3-azabiciclo[3.2.1]octanil-pirimidinilo, 8-azabiciclo[3.2.1]octanilpirimidinilo, 3-oxa-8-azabiciclo[3.2.1]octanil-pirimidinilo, 3,6-diazabiciclo[3.2.2]nonanilpirimidinilo, 3-oxa-7-azabiciclo[3.3.1]-nonanilpirimidinilo, 3,7-dioxa-9-azabiciclo[3.3.1]-nonanilpirimidinilo, 5-azaespiro[2,3]hexanilpirimidinilo, 5-azaespiro[2,4]heptanil-pirimidinilo, 2-azaespiro[3,3]heptanilpirimidinilo, 2-oxa-6-azaespiro[3,3]heptanil-pirimidinilo, 2-oxa-6-azaespiro[3,4]octanilpirimidinilo, 2-oxa-6-azaespiro[3,5]nonanil-pirimidinilo, 2-oxa-7-azaespiro[3,5]nonanilpirimidinilo, 2,4,8-triazaespiro[4,5]decanil-pirimidinilo, 3,6-epiminofuro [3,2-b]furanil-pirimidinilo, (imino)(oxo)tiazinanil-pirimidinilo, (oxo)tiazinanil-pirimidinilo o (dioxo)tiazinanil-pirimidinilo, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes. Además, R1 representa 2,5-diazabiciclo[2.2.1]heptanil-pirimidinilo o piridin-2(1H)-ona, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes.
Definitivamente, R1 representa bromo, ciano, fenilo, piridinilo, dihidropiridinilo, pirimidinilo, ciclobutilpirimidinilo, ciclopropilpiridinilo, biciclo[3.1.0]hexanil-pirimidinilo, biciclo[3.1.0]hexenil-pirimidinilo, pirimidinilo, tetrahidropiranilpiridinilo, tetrahidro-tiopiranilpirimidinilo, piperazinil-piridinilo, oxetanilpirimidinilo, azetidinilpirimidinilo, tetrahidrofuranilpirimidinilo, piperidinilpirimidinilo, piperazinil-pirimidinilo, morfolinil-pirimidinilo, tiomorfolinilpirimidinilo, 2-oxa-5-azabiciclo[2.2.1]heptanilpirimidinilo, 3-azabiciclo[3.2.1]octanil-pirimidinilo, 3-oxa-8azabicido[3.2.1]octanilpirimidinilo, 3,7-dioxa-9-azabicido[3.3.1]-nonanilpirimidinilo, epiminofuro [3,2-b]furanilpirimidinilo, (imino)(oxo)tiazinanil-pirimidinilo, (oxo)tiazinanil-pirimidinilo, (dioxo)tiazinanil-pirimidinilo, cidopropilpirimidinilo, 2,5-diazabiciclo[2,2,1 ]heptanil-pirimidinilo o piridin-2(1H)-ona, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes. Adecuadamente, R1 representa bromo, ciano, fenilo, piridinilo, dihidropiridinilo, pirimidinilo, ciclobutilpirimidinilo, ciclopropilpiridinilo, biciclo[3.1.0]hexanil-pirimidinilo, biciclo[3.1.0]hexenil-pirimidinilo, pirimidinilo, tetrahidropiranilpiridinilo, tetrahidro-tiopiranilpirimidinilo, piperazinilpiridinilo, oxetanilpirimidinilo, azetidinilpirimidinilo, tetrahidrofuranilpirimidinilo, piperidinilpirimidinilo, piperazinilpirimidinilo, morfolinil-pirimidinilo, tiomorfolinilpirimidinilo, 2-oxa-5-azabiciclo[2.2.1]heptanilpirimidinilo, 3-azabiciclo[3.2.1]octanil-pirimidinilo, 3-oxa-8-azabiciclo[3.2.1 ]octanil-pirimidinilo, 3,7-dioxa-9-azabiciclo[3.3.1]-nonanilpirimidinilo, epiminofuro [3,2-b]furanil-pirimidinilo, (imino)(oxo)tiazinanil-pirimidinilo, (oxo)tiazinanil-pirimidinilo, (dioxo)tiazinanil-pirimidinilo o cidopropilpirimidinilo, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes. Además, R1 representa 2,5-diazabiciclo[2.2.1]heptanil-pirimidinilo o piridin-2(1H)-ona, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes.
Adecuadamente, R1 representa fenilo, piridinilo, dihidropiridinilo, pirimidinilo, ciclobutilpirimidinilo, ciclopropilpiridinilo, biciclo[3.1.0]hexanil-pirimidinilo, biciclo[3.1.0]hexenil-pirimidinilo, pirimidinilo, tetrahidropiranilpiridinilo, tetrahidrotiopiranilpirimidinilo, piperazinil-piridinilo, oxetanilpirimidinilo, azetidinilpirimidinilo, tetrahidrofuranilpirimidinilo, piperidinilpirimidinilo, piperazinil-pirimidinilo, morfolinil-pirimidinilo, tiomorfolinilpirimidinilo, 2-oxa-5-azabiciclo[2,2,1 ]heptanilpirimidinilo, 3-azabiciclo[3.2.1]octanil-pirimidinilo, 3-oxa-8-azabiciclo[3.2.1]octanil-pirimidinilo, 3,7-dioxa-9-azabiciclo[3.3.1]-nonanilpirimidinilo, epiminofuro [3,2-b]furanil-pirimidinilo, 2,5-diazabiciclo[2,2,1 ]heptanilpirimidinilo o piridin-2(1H)-ona, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes.
De manera ilustrativa, R1 representa fenilo, piridinilo, dihidropiridinilo, pirimidinilo, ciclobutilpirimidinilo, ciclopropilpiridinilo, biciclo[3.1.0]hexanil-pirimidinilo, biciclo[3.1.0]hexenil-pirimidinilo, pirimidinilo, tetrahidropiranilpiridinilo, tetrahidro-tiopiranilpirimidinilo, piperazinil-piridinilo, oxetanilpirimidinilo, azetidinilpirimidinilo, tetrahidrofuranilpirimidinilo, piperidinilpirimidinilo, piperazinilpirimidinilo, morfolinil-pirimidinilo, tiomorfolinilpirimidinilo, 2-oxa-5-azabiciclo[2,2,1 ]heptanilpirimidinilo, 3-azabiciclo[3.2.1]octanil-pirimidinilo, 3-oxa-8-azabiciclo[3.2.1]octanilpirimidinilo, 3,7-dioxa-9-azabiciclo[3.3.1]-nonanilpirimidinilo o epiminofuro [3,2-b]furanil-pirimidinilo, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes.
Los ejemplos típicos de sustituyentes opcionales en R1 incluyen uno, dos o tres sustituyentes seleccionados independientemente entre halógeno, haloalquilo (C1-6), ciano, cianoalquilo (C1-6), nitroalquilo (C1-6), alquilo C1-6, trifluorometilo, trifluoroetilo, alquenilo C2-6, hidroxi, hidroxialquilo (C1-6), alcoxi C1-6, trifluoroetoxi, carboxicicloalquiloxi (C3-7), alquiltio C1-6, alquilsulfonilo C1-6, alquilsulfonil (C1-6)-alquilo (C1-6), oxo, amino, amino-alquilo (C1-6), alquilamino C1-6, dialquilamino (C1-6), alcoxi (C1-6)alquilamino (C1-6), N-[alquil (C1-6)]-N-[hidroxialquil (C1-6)]amino, alquilcarbonilamino (C2-6)-alquilo(C1-6), alquilsulfonilamino C1-6, N-[alquil (C1-6)]-N-[alquilsulfonil (C1-6)]amino, bis[alquilsulfonil (C1-6)]amino, N-[alquil (C1-6)]-N-[carboxialquil (C1-6)]amino, carboxicicloalquilamino (C3-7), carboxicicloalquil (C3-7)alquilamino (C1-6), formilo, alquilcarbonilo C2-6, alquilcarboniloxi (C2-6)alquilo (C1-6), carboxi, carboxialquilo (C1-6), alcoxicarbonilo C2-6, alcoxicarbonil C2-6alquilo (C1-6), morfolinil-alcoxicarbonilo (C1-6), alcoxicarbonilmetilidenilo C2-6, aminocarbonilo, dialquilaminocarbonilo (C1-6), aminosulfonilo, alquilsulfoximinilo (C1-6), [alquil (C1-6)][N-alquil (C1-6)]-sulfoximinilo y heteroarilo. Los ejemplos adicionales de sustituyentes opcionales en R1 incluyen difluorometilo, alquilsulfinilo C1-6 y cicloalquil (C3-7)sulfonilo.
Los ejemplos adecuados de sustituyentes opcionales en R1 incluyen uno, dos o tres sustituyentes seleccionados independientemente entre halógeno, hidroxi, trifluorometilo, alquilo C1-6, alcoxi C1-6, alquilcarbonilo C2-6, alquiloxicarbonilo C2-6, (hidroxi)alquilo C1-6, cicloalquilo (C3-7), alquilsulfonilo C1-6, alquilsulfonil (C1-6)-alquilo (C1-6), dialquilaminocarbonilo (C1-6), alquilsulfoximinilo (C1-6), oxo, carboxi, difluorometilo, alquilsulfinilo C1-6 y cicloalquil (C3-7)sulfonilo. Los ejemplos adecuados de sustituyentes opcionales en R1 incluyen uno, dos o tres sustituyentes seleccionados independientemente entre halógeno, hidroxi, trifluorometilo, alquilo C1-6, alcoxi C1-6, alquilcarbonilo C2-6, alquiloxicarbonilo C2-6, (hidroxi)alquilo C1-6, cicloalquilo (C3-7), alquilsulfonilo C1-6, alquilsulfonil (C1-6)-alquilo (C1-6), dialquilaminocarbonilo (C1-6), alquilsulfoximinilo (C1-6), oxo y carboxi.
Los ejemplos típicos de sustituyentes particulares en R1 incluyen uno, dos o tres sustituyentes seleccionados independientemente entre flúor, cloro, fluorometilo, fluoroisopropilo, ciano, cianoetilo, nitrometilo, metilo, etilo, isopropilo, ciclopropilo, ciclobutilo, isopropilmetilo, trifluorometilo, trifluoroetilo, etenilo, hidroxi, hidroximetilo, hidroxiisopropilo, metoxi, isopropoxi, trifluoroetoxi, carboxiciclobutiloxi, metiltio, metilsulfonilo, metilsulfonilmetilo, metilsulfoniletilo, oxo, amino, aminometilo, aminoisopropilo, metilamino, dimetilamino, metoxietilamino, N-(hidroxietil)-N-(metil)amino, acetilaminometilo, metilsulfonilamino, N-metil-N-(metilsulfonil)amino, bis(metilsulfonil)amino, N-(carboxietil)-N-(metil)amino, carboxiciclopentilamino, carboxiciclopropilmetilamino, formilo, acetilo, acetoxiisopropilo, carboxi, carboximetilo, carboxietilo, metoxicarbonilo, etoxicarbonilo, n-butoxicarbonilo, ferc-butoxicarbonilo, metoxicarbonilmetilo, etoxicarbonilmetilo, etoxicarboniletilo, morfoliniletoxicarbonilo, etoxicarbonilmetilidenilo, metilsulfonilaminocarbonilo, acetilaminosulfonilo, metoxiaminocarbonilo, tetrazolilo, tetrazolilmetilo, hidroxioxadiazolilo, aminocarbonilo, aminosulfonilo, metilsulfoximinilo, (metil)(N-metil)sulfoximinilo y triazolilo.
Los ejemplos particulares adecuados de sustituyentes en R1 incluyen cloro, flúor, metilo, trifluorometilo, hidroxi, hidroximetilo, hidroxiisopropilo, metoxi, metilsulfonilo, oxo, amino, acetilo, metoxicarbonilo, metilsulfoximinilo,
etoxicarbonilo, n-butoxicarbonilo, ferc-butoxicarbonilo, fluoroisopropilo, aminoisopropilo, difluorometilo, metilsulfinilo, terc-butoxi y ciclopropilsulfonilo.
Los ejemplos particulares de sustituyentes en R1 incluyen cloro, flúor, metilo, trifluorometilo, hidroxi, hidroximetilo, hidroxiisopropilo, metoxi, metilsulfonilo, oxo, amino, acetilo, metoxicarbonilo, metilsulfoximinilo, etoxicarbonilo, nbutoxicarbonilo y ferc-butoxicarbonilo.
En una realización particular, R1 está sustituido con hidroxialquilo (C1-6). En un aspecto de esa realización, R1 está sustituido con hidroxiisopropilo, especialmente 2-hidroxiprop-2-ilo.
En una segunda realización particular, R1 está sustituido con alquilsulfonilo C1-6. En un aspecto de esta realización, R1 está sustituido con metilsulfonilo.
En una tercera realización particular, R1 está sustituido con alquilsulfoximinilo (C1-6). En un aspecto de esta realización, R1 está sustituido con un metilsulfoximinilo.
Los valores seleccionados de R1 incluyen hidrógeno, bromo, ciano, -CO2Rd, metoxicarboniletilo, etoxicarboniletilo, hidroxibutinilo, clorofenilo, hidroxifenilo, metilsulfonilfenilo, (metilsulfonil)metilfenilo, (metilsulfonil)etilfenilo, aminometilfenilo, aminoisopropilfenilo, acetilaminometilfenilo, acetilfenilo, metoxicarbonilfenilo, aminocarbonilfenilo, aminosulfonilfenilo, acetilaminosulfonilfenilo, (di-(trifluorometil))(hidroxi)fenilo, (metoxicarbonil)(metil)pirrolidinilo, cloropiridinilo, oxopiperidinilo, etoxicarbonilpiperidinilo, metilsulfonilpiperazinilo, morfolinilo, metilsulfonil-1,2,3,6-tetrahidropiridinilo, acetil-1,2,3,6-tetrahidropiridinilo, ferc-butoxicarbonil-1,2,3,6-tetrahidropiridinilo, metoxicarbonilmetil-1,2,3,6-tetrahidropiridinilo, benzofurilo, tienilo, indolilo, pirazolilo, metilpirazolilo, dimetilpirazolilo, (metil)[W-metil-W-(metilsulfonil)amino]pirazolilo, metilindazolilo, dimetilisoxazolilo, hidroxiisopropiltiazolilo, metilimidazolilo, dimetilimidazolilo, piridinilo, tetrahidropiranilpiridinilo, fluoropiridinilo, cianopiridinilo, metilpiridinilo, (ciano)(metil)piridinilo, dimetilpiridinilo, ciclopropilpiridinilo, trifluorometilpiridinilo, etenilpiridinilo, hidroxiisopropilpiridinilo, hidroximetilpiridinilo, metoxipiridinilo, (metoxi)(metil)piridinilo, isopropoxipiridinilo, trifluoroetoxipiridinilo, (metil)-(trifluoroetoxi)piridinilo, metilsulfonilpiridinilo, metilsulfonilmetilpiridinilo, oxopiridinilo, (metil)(oxo)-piridinilo, (dimetil)(oxo)piridinilo, aminopiridinilo, metilaminopiridinilo, dimetil-aminopiridinilo, metoxietilaminopiridinilo, W-(hidroxietil)-W-(metil)amino-piridinilo, metilsulfonilaminopiridinilo, [bis(metilsulfonil)amino]piridinilo, carboxipiridinilo, quinolinilo, hidroxipiridazinilo, pirimidinilo, isopropilpirimidinilo, fluoroisopropil-pirimidinilo, hidroxiisopropilpirimidinilo, metoxipirimidinilo, carboxiciclobutiloxi-pirimidinilo, metiltiopirimidinilo, metilsulfonilpirimidinilo, oxopirimidinilo, aminopirimidinilo, dimetilaminopirimidinilo, metoxietilaminopirimidinilo, W-(carboxietil)-W-(metil)aminopirimidinilo, carboxiciclopentilaminopirimidinilo, carboxiciclopropilmetilaminopirimidinilo, acetoxiisopropilpirimidinilo, etoxicarboniletilpirimidinilo, hidroxipirazinilo, hidroxiisopropilpirazinilo, pirrolidinilmetilfenilo, piperazinilmetilfenilo, piridinilpiperazinilo, carboxiciclohexilpirazolilo, carboxiciclohexilpiridinilo, fluorometilciclopropilpirimidinilo, acetilaminometilciclopropilpirimidinilo, hidroximetilpirimidinilo, hidroxiciclobutilpirimidinilo, carboxiciclopentilpirimidinilo, carboxiciclohexilpirimidinilo, (carboxi)(metil)ciclohexil-pirimidinilo, (carboxi)(hidroxi)ciclohexilpirimidinilo, carboximetilciclohexil-pirimidinilo, etoxicarbonilciclohexilpirimidinilo, (metoxicarbonil)(metil)-ciclohexilpirimidinilo, (etoxicarbonil)(metil)ciclohexilpirimidinilo, carboxiciclohexilpirazinilo, carboxiciclohexilmetilpirimidinilo, carboxiciclohexenilpiridinilo, carboxiciclohexenilpirimidinilo, etoxicarbonilciclohexenilpirimidinilo, carboxibiciclo[3.1.0]hexanilpiridinilo, carboxibiciclo[3.1.0]hexenilpiridinilo, carboxibiciclo[3.1.0]hexanilpirimidinilo, etoxicarbonilbiciclo[3.1.0]hexanilpirimidinilo, carboxibiciclo[4.1.0]heptanilpirimidinilo, carboxibiciclo[2.2.2]octanilpirimidinilo, pirrolidinilpiridinilo, hidroxipirrolidinilpiridinilo, hidroxitetrahidropiranilpiridinilo, piperidinilpiridinilo, acetilpiperidinilpiridinilo, (carboxi)(metil)piperidinilpiridinilo, [(carboxi)-(metil)-piperidinil](fluoro)piridinilo, [(carboxi)(metil)piperidinil](cloro)piridinilo, piperazinilpiridinilo, (metil)(piperazinil)piridinilo, cianoetilpiperazinilpiridinilo, trifluoroetilpiperazinilpiridinilo, metilsulfonilpiperazinilpiridinilo, metilsulfoniletilpiperazinilpiridinilo, oxopiperazinilpiridinilo, acetilpiperazinilpiridinilo, (terc-butoxicarbonilpiperazinil)(metil)piridinilo, metilpiperazinilpiridinilo, carboximetilpiperazinilpiridinilo, carboxietilpiperazinilpiridinilo, etoxicarbonilmetilpiperazinilpiridinilo, etoxicarboniletilpiperazinilpiridinilo, morfolinilpiridinilo, tiomorfolinil-piridinilo, (ferc-butoxicarbonil)-3,6-dihidropiridina, oxotiomorfolinilpiridinilo, dioxotiomorfolinilpiridinilo, oxodiazepanil-piridinilo, fluorooxetanilpirimidinilo, hidroxioxetanilpirimidinilo, hidroxiazetidinil-pirimidinilo, (hidroxi)(metil)azetidinilpirimidinilo, (hidroxi)(trifluorometil)azetidinilpirimidinilo, carboxiazetidinilpirimidinilo, (terc-butoxicarbonil)(hidroxi)azetidinilpirimidinilo, tetrazolilazetidinilpirimidinilo, hidroxitetrahidrofuranilpirimidinilo, hidroxipirrolidinilpirimidinilo, carboxipirrolidinilpirimidinilo, (carboxi)(metil)pirrolidinilpirimidinilo, carboximetilpirrolidinilpirimidinilo, etoxicarbonilpirrolidinilpirimidinilo, fluorotetrahidropiranilpirimidinilo, hidroxitetrahidropiranilpirimidinilo, (hidroxi)dioxidotetrahidrotiopiranil)pirimidinilo, piperidinilpirimidinilo, difluoropiperidinil-pirimidinilo, (ciano)(metil)piperidinilpirimidinilo, (hidroxi)(nitrometil)piperidinilpirimidinilo, (hidroxi)(metil)piperidinilpirimidinilo, (hidroxi)(trifluorometil)-piperidinilpirimidinilo, (hidroximetil)(metil)piperidinilpirimidinilo, metilsulfonilpiperidinilpirimidinilo, oxopiperidinilpirimidinilo, (formil)(metil)-piperidinilpirimidinilo, carboxipiperidinilpirimidinilo, (carboxi)(fluoro)piperidinilpirimidinilo, (carboxi)(metil)piperidinilpirimidinilo, (carboxi)(etil)piperidinilpirimidinilo, (carboxi)(trifluorometil)piperidinilpirimidinilo, (carboxi)(hidroxi)-piperidinilpirimidinilo, (carboxi)(hidroximetil)piperidinilpirimidinilo, (carboxi)-(metoxi)piperidinilpirimidinilo, (amino)(carboxi)piperidinilpirimidinilo, carboximetilpiperidinilpirimidinilo, metoxicarbonilpiperidinilpirimidinilo, etoxicarbonilpiperidinilpirimidinilo, (etoxicarbonil)(fluoro)piperidinilpirimidinilo,
(metoxicarbonil)(metil)piperidinilpirimidinilo, (etil)(metoxicarbonil)piperidinilpirimidinilo, (isopropil)(metoxicarbonil)piperidinilpirimidinilo, (etoxicarbonil)-(metil)piperidinilpirimidinilo, (nbutoxicarbonil)(metil)piperidinilpirimidinilo, (etoxicarbonil)(trifluorometil)piperidinilpirimidinilo, (etoxicarbonil)-(hidroximetil)piperidinilpirimidinilo, (metoxi)(metoxicarbonil)piperidinilpirimidinilo, (carboxi)(metoxicarbonil)piperidinilpirimidinilo, (metil)-(morfoliniletoxicarbonil)piperidinilpirimidinilo, etoxicarbonilmetilpiperidinilpirimidinilo, metilsulfonilaminocarbonilpiperidinilpirimidinilo, acetilpiperidinilpirimidinilo, acetilamino-sulfonilpiperidinilpirimidinilo, metoxiaminocarbonilpiperidinilpirimidinilo, tetrazolilpiperidinilpirimidinilo, hidroxioxadiazolilpiperidinilpirimidinilo, amino-sulfonilpiperidinilpirimidinilo, piperazinilpirimidinilo, metilsulfonilpiperazinil-pirimidinilo, oxopiperazinilpirimidinilo, carboxipiperazinilpirimidinilo, carboxietilpiperazinilpirimidinilo, terc-butoxicarbonilpiperazinilpirimidinilo, tetrazolilmetilpiperazinilpirimidinilo, trioxohexahidro-[1.2.5]tiadiazolo[2,3-a]pirazinilpirimidinilo, morfolinilpirimidinilo, dimetilmorfolinilpirimidinilo, hidroximetilmorfolinilpirimidinilo, carboximorfolinilpirimidinilo, (carboxi)(metil)morfolinilpirimidinilo, carboximetilmorfolinilpirimidinilo, tiomorfolinilpirimidinilo, oxo-tiomorfolinilpirimidinilo, dioxo-tiomorfolinilpirimidinilo, carboxiazepanilpirimidinilo, carboxioxazepanil-pirimidinilo, oxodiazepanilpirimidinilo, (oxodiazepanil)(trifluorometil)pirimidinilo, (oxodiazepanil)(metoxi)pirimidinilo, (metil)(oxo)diazepanilpirimidinilo, dioxotiadiazepanilpirimidinilo, hidroxioxetanilpirazinilo, (carboxi)(metil)piperidinil-pirazinilo, (etoxicarbonil)(metil)piperidinilpirazinilo, morfolinilmetiltienilo, morfoliniletilpirazolilo, isopropilmetilpirazolilo, carboxi-3-azabiciclo[3.1.0]hexanilpiridinilo, carboxi-3-azabiciclo[3.1.0]hexanilpiridazinilo, carboxi-3-azabiciclo[3.1.0]hexanilpirimidinilo, (carboxi)(metil)-3-azabiciclo[3.1.0]hexanilpirimidinilo, metoxicarbonil-3-azabiciclo[3.1.0]hexanilpirimidinilo, etoxicarbonil-3-azabiciclo[3.1.0]hexanilpirimidinilo, 2-oxa-5-azabiciclo[2.2.1]heptanilpirimidinilo, carboxi-2-oxa-5-azabiciclo-[2.2.1]heptanilpirimidinilo, carboxi-3-azabiciclo[3.1.1]heptanilpirimidinilo, carboxi-3-azabiciclo[4.1.0]heptanilpiridinilo, carboxi-3-azabiciclo[4.1.0]heptanilpirimidinilo, metoxicarbonil-3-azabiciclo[4.1.0]heptanilpirimidinilo, etoxicarbonil-3-azabiciclo-[4.1.0]heptanilpirimidinilo, (hidroxi)(metil)(oxo)-2-oxabiciclo[2.2.2]octanilpirimidinilo, carboxi-3-azabiciclo[3.2.1]octanilpirimidinilo, metoxicarbonil-3-azabiciclo[3.2.1]octanilpirimidinilo, oxo-8-azabiciclo[3.2.1]octanilpirimidinilo, etoxicarbonilmetilidenil-8-azabiciclo[3.2.1]octanilpirimidinilo, 3-oxa-8-azabiciclo-[3.2.1] octanilpirimidinilo, 3-carboxi-8-azabiciclo-[3.2.1]-octanilpirimidinilo, 3-(dimetilaminocarbonil)-8-azabiciclo-[3.2.1] octanilpirimidinilo, oxo-3,6-diazabiciclo[3.2.2]nonanilpirimidinilo, 3,7-dioxa-9-azabiciclo[3.3.1]-nonanilpirimidinilo, carboxi-3-oxa-7-azabiciclo[3.3.1]nonanilpirimidinilo, carboxi-5-azaespiro[2,3]hexanilpirimidinilo, (carboxi)(metil)-5-azaespiro[2,3]hexanilpirimidinilo, carboxi-5-azaespiro[2,4]heptanil-pirimidinilo, carboxi-2-azaespiro[3,3]heptanilpirimidinilo, 2-oxa-6-azaespiro[3,3]heptanil-pirimidinilo, 2-oxa-6-azaespiro[3,4]octanilpirimidinilo, 2- oxa-6-azaespiro[3,5]nonanil-pirimidinilo, 2-oxa-7-azaespiro[3,5]nonanilpirimidinilo, (dioxo)(metil)-2,4,8-triazaespiro[4,5]decanilpirimidinilo, 3,6-epiminofuro[3,2-b]furanil-pirimidinil metilsulfoximinilfenilo, (metil)ciclobutildiolpirimidinilo, (imino)(oxo)tiazinanil-pirimidinilo, (oxo)tiazinanil-pirimidinilo y (dioxo)tiazinanil-pirimidinilo. Los valores adicionales de R1 incluyen difluorociclobutanil-pirimidinilo, difluorometil-pirimidinilo, ciclopropil-pirimidinilo, aminoisopropilpirimidinilo, (hidroxi)ciclopropil-pirimidinilo, (difluoro)(hidroxi)ciclobutilpirimidinilo, (metil)ciclobutanodiol, (hidroxi)(metil)ciclohexil-pirimidinilo, (metil)ciclohexano-diol, (cloro)(metoxi)piridinilo, metilsulfinilfenilo, ciclopropilsulfonil-fenilo, terc-butoxi-piridinilo, metilsulfoximinilpiridinilo, piperazinil-2-ona-pirimidinilo, (metil)piridin-2(1H)-ona, (fluoro)piridin-2(1H)-ona, (cloro)piridin-2(1H)-ona, metilcarboxi-3-azabiciclo[3.2.1]octanilpirimidinilo, 3-oxa-8-azabiciclo[3.2.1]octanilpirimidinilo y 2,5-diazabiciclo[2.2.1]hetanilpirimidinilo.
Los valores adecuados de R1 incluyen bromo, ciano, (metilsulfonil)metilfenilo, (metilsulfonil)etilfenilo, (di-(trifluorometil))(hidroxi)fenilo, cloropiridinilo, tetrahidropiranilpiridinilo, hidroxiisopropilpiridinilo, hidroximetilpiridinilo, metoxipiridinilo, isopropoxipiridinilo, isopropilpirimidinilo, hidroxiisopropilpirimidinilo, hidroximetilpirimidinilo, hidroxiciclobutilpirimidinilo, carboxibiciclo[3.1.0]hexanilpiridinilo, carboxibiciclo[3.1.0]hexenilpiridinilo, piperazinilpiridinilo, (terc-butoxicarbonil)-3,6-dihidropiridina, hidroxioxetanilpirimidinilo, hidroxiazetidinil-pirimidinilo, (hidroxi)(metil)azetidinilpirimidinilo, (hidroxi)(trifluorometil)azetidinilpirimidinilo, (tercbutoxicarbonil)(hidroxi)azetidinilpirimidinilo, hidroxitetrahidrofuranoilpirimidinilo, -hidroxitetrahidropiranilpirimidinilo, (hidroxi)dioxidotetrahidrotiopiranil)pirimidinilo, piperidinilpirimidinilo, (ciano)(metil)piperidinilpirimidinilo, (hidroxi)(metil)piperidinilpirimidinilo, (carboxi)(metil)piperidinilpirimidinilo, acetilpiperidinilpirimidinilo, piperazinilpirimidinilo, carboxipiperazinilpirimidinilo, terc-butoxicarbonilpiperazinilpirimidinilo, morfolinilpirimidinilo, tiomorfolinilpirimidinilo, oxo-tiomorfolinilpirimidinilo, dioxo-tiomorfolinilpirimidinilo, oxodiazepanilpirimidinilo, 2-oxa-5-azabiciclo[2.2.1]heptanilpirimidinilo, carboxi-3-azabiciclo[3.2.1]octanilpirimidinilo, oxo-8-azabiciclo[3.2.1]octanilpirimidinilo, 3-carboxi-8-azabiciclo-[3.2.1]octanilpirimidinilo, 3-(dimetilaminocarbonil)-8-azabiciclo-[3.2.1]octanilpirimidinilo, oxo-3,6-diazabiciclo[3.2.2]nonanilpirimidinilo, 3,7-dioxa-9-azabiciclo[3.3.1]-nonanilpirimidinilo, 3,6-epiminofuro [3,2-b]furanil-pirimidinilo, metilsulfoximinilfenilo, (metil)ciclobutildiol-pirimidinilo, (imino)(oxo)tiazinanilpirimidinilo, (oxo)tiazinanil-pirimidinilo, (dioxo)tiazinanilpirimidinilo, difluorociclobutanil-pirimidinilo, difluorometilpirimidinilo, ciclopropilpirimidinilo, aminoisopropil-pirimidinilo, (hidroxi)ciclopropil-pirimidinilo, (difluoro)(hidroxi)ciclobutil-pirimidinilo, (metil)ciclobutano-diol, (hidroxi)(metil)ciclohexil-pirimidinilo, (metil)ciclohexanodiol, (cloro)(metoxi)piridinilo, metilsulfinil-fenilo, ciclopropilsulfonil-fenilo, terc-butoxi-piridinilo, metilsulfoximinilpiridinilo, piperazinil-2-ona-pirimidinilo, (metil)piridin-2(1H)-ona, (fluoro)piridin-2(1H)-ona, (cloro)piridin-2(1H)-ona, metilcarboxi-3- azabiciclo[3.2.1]octanilpirimidinilo, 3-oxa-8-azabiciclo[3.2.1]octanilpirimidinilo y 2,5-diazabiciclo[2.2.1]hetanilpirimidinilo.
Los valores ilustrativos de R1 incluyen bromo, ciano, (metilsulfonil)metilfenilo, (metilsulfonil)etilfenilo, (di-(trifluorometil))(hidroxi)fenilo, cloropiridinilo, tetrahidropiranilpiridinilo, hidroxiisopropilpiridinilo, hidroximetilpiridinilo,
metoxipiridinilo, isopropoxipiridinilo, isopropilpirimidinilo, hidroxiisopropilpirimidinilo, hidroximetilpirimidinilo, hidroxicidobutilpirimidinilo, carboxibiciclo[3.1.0]hexanilpiridinilo, carboxibiciclo[3.1.0]hexenilpiridinilo, piperazinilpiridinilo, (terc-butoxicarbonil)-3,6-dihidropiridina, hidroxioxetanilpirimidinilo, hidroxiazetidinil-pirimidinilo, (hidroxi)(metil)azetidinilpirimidinilo, (hidroxi)(trifluorometil)azetidinilpirimidinilo, (terc-butoxicarbonil)(hidroxi)azetidinilpirimidinilo, hidroxitetrahidrofuranoilpirimidinilo, -hidroxitetrahidropiranilpirimidinilo, (hidroxi)dioxidotetrahidrotiopiranil)pirimidinilo, piperidinilpirimidinilo, (ciano)(metil)piperidinilpirimidinilo, (hidroxi)(metil)piperidinilpirimidinilo, (carboxi)(metil)piperidinilpirimidinilo, acetilpiperidinilpirimidinilo, piperazinilpirimidinilo, carboxipiperazinilpirimidinilo, terc-butoxicarbonilpiperazinilpirimidinilo, morfolinilpirimidinilo, tiomorfolinilpirimidinilo, oxo-tiomorfolinilpirimidinilo, dioxo-tiomorfolinilpirimidinilo, oxodiazepanilpirimidinilo, 2-oxa-5-azabiciclo[2.2.1]heptanilpirimidinilo, carboxi-3-azabiciclo[3.2.1]octanilpirimidinilo, oxo-8-azabiciclo[3.2.1]octanilpirimidinilo, 3-carboxi-8-azabiciclo-[3.2.1]octanilpirimidinilo, 3-(dimetilaminocarbonil)-8-azabiciclo-[3.2.1]octanilpirimidinilo, oxo-3,6-diazabiciclo[3.2.2]nonanilpirimidinilo, 3,7-dioxa-9-azabiciclo[3.3.1]-nonanilpirimidinilo, 3,6-epiminofuro[3,2-b]furanil-pirimidinilo, metilsulfoximinilfenilo, (metil)ciclobutildiol-pirimidinilo, (imino)(oxo)tiazinanilpirimidinilo, (oxo)tiazinanil-pirimidinilo y (dioxo)tiazinanil-pirimidinilo.
Normalmente, R2 representa hidrógeno, halógeno, ciano, nitro, hidroxi, trifluorometilo, trifluorometoxi; u -ORa; o un alquilo C1-6 opcionalmente sustituido.
Los ejemplos típicos de sustituyentes opcionales en R2 incluyen alcoxicarbonilo C2-6.
Los ejemplos típicos de sustituyentes particulares en R2 incluyen etoxicarbonilo.
En una primera realización, R2 representa hidrógeno. En una segunda realización, R2 representa halógeno. En un aspecto de esa realización, R2 representa flúor. En otro aspecto de esa realización, R2 representa cloro. En una tercera realización, R2 representa ciano. En una cuarta realización, R2 representa nitro. En una quinta realización, R2 representa hidroxi. En una sexta realización, R2 representa trifluorometilo. En una séptima realización, R2 representa trifluorometoxi. En una octava realización, R2 representa -ORa. En una novena realización, R2 representa alquilo C1-6 opcionalmente sustituido. En un aspecto de esa realización, R2 representa metilo no sustituido. En otro aspecto de esa realización, R2 representa etilo no sustituido. En un aspecto adicional de esa realización, R2 representa metilo monosustituido o etilo monosustituido.
Los valores típicos de R2 incluyen hidrógeno, flúor, cloro, trifluorometilo, trifluorometoxi, -ORa, metilo y etoxicarboniletilo.
Los valores particulares de R2 incluyen hidrógeno y flúor.
Normalmente, R3 representa hidrógeno, halógeno o alquilo C1-6.
En una primera realización, R3 representa hidrógeno. En una segunda realización, R3 representa halógeno. En un aspecto de esa realización, R3 representa flúor.
En una tercera realización, R3 representa alquilo C1-6. En un aspecto de esa realización, R3 representa alquilo C1-6 no sustituido. En un segundo aspecto de esa realización, R3 representa alquilo C1-6 sustituido. En un aspecto particular de esta realización, R3 representa metilo. En otro aspecto particular de esta realización, R3 representa etilo.
En una realización particular, R3 representa hidrógeno.
Normalmente, R4 representa hidrógeno, halógeno o alquilo C1-6.
En una primera realización, R4 representa hidrógeno. En una segunda realización, R4 representa halógeno. En un aspecto de esa realización, R4 representa flúor. En una tercera realización, R4 representa alquilo C1-6. En un aspecto de esa realización, R4 representa alquilo C1-6 no sustituido. En un segundo aspecto de esa realización, R4 representa alquilo C1-6 sustituido. En un aspecto particular de esta realización, R4 representa metilo. En otro aspecto particular de esta realización, R4 representa etilo.
En una realización particular, R4 representa hidrógeno.
En general, R5a representa hidrógeno, hidroxi, halógeno, ciano, trifluorometilo; -NRbRc, -NRcC(O)Rd, -(CO)NRcRd, -NHS(O)2Re, -S-Ra, -(SO)-Ra, -S(O)2Ra, -S(O)(N-Rd), -S(O)2(N-Rd), -ORa, -C(O)2Rd u -O(CO)-Rd-; o alquilo C1-6, alquenilo C2-6, alquinilo C2-6, arilo o heteroarilo, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes.
Adecuadamente, R5a representa hidrógeno, hidroxi, halógeno, trifluorometilo; -NRbRc, S(O)2Ra, -ORa, O-(CO)-Rd o -NRcC(O)Rd; o alquilo C1-6, cualquiera de tales grupos puede estar opcionalmente sustituido. Normalmente, R5a representa hidrógeno, hidroxi, halógeno, trifluorometilo; -NRbRc, S(O)2Ra, -ORa u O-(CO)-Rd; o alquilo C1-6, cualquiera de tales grupos puede estar opcionalmente sustituido.
Los ejemplos adecuados de sustituyentes opcionales en R5a incluyen uno, dos o tres sustituyentes seleccionados independientemente entre halógeno, hidroxi, trifluorometilo, alquilo Ci -6, alcoxi Ci -6, alquilcarbonilo C2-6, alquiloxicarbonilo C2-6, (hidroxi)alquilo C1-6, cicloalquilo (C3-7), alquilsulfonilo C1-6, alquilsulfonil (C1-6)-alquilo (C1-6), dialquilaminocarbonilo (C1-6), oxo y carboxi.
Los ejemplos típicos de sustituyentes particulares en R5a incluyen uno, dos o tres sustituyentes seleccionados independientemente entre flúor, cloro, fluorometilo, fluoroisopropilo, ciano, cianoetilo, nitrometilo, metilo, etilo, isopropilo, isopropilmetilo, trifluorometilo, trifluoroetilo, etenilo, hidroxi, hidroximetilo, hidroxiisopropilo, metoxi, isopropoxi, trifluoroetoxi, carboxiciclobutiloxi, metiltio, metilsulfonilo, metilsulfonilmetilo, metilsulfoniletilo, oxo, amino, aminometilo, aminoisopropilo, metilamino, dimetilamino, metoxietilamino, W-(hidroxietil)-W-(metil)amino, acetilaminometilo, metilsulfonilamino, W-metil-W-(metilsulfonil)amino, bis(metilsulfonil)amino, W-(carboxietil)-W-(metil)amino, carboxiciclopentilamino, carboxiciclopropilmetilamino, formilo, acetilo, acetoxiisopropilo, carboxi, carboximetilo, carboxietilo, metoxicarbonilo, etoxicarbonilo, n-butoxicarbonilo, ferc-butoxicarbonilo, metoxicarbonilmetilo, etoxicarbonilmetilo, etoxicarboniletilo, morfoliniletoxicarbonilo, etoxicarbonilmetilidenilo, metilsulfonilaminocarbonilo, acetilaminosulfonilo, metoxiaminocarbonilo, tetrazolilo, tetrazolilmetilo, hidroxioxadiazolilo, aminocarbonilo, aminosulfonilo, metilsulfoximinilo y (metil)(W-metil)sulfoximinilo.
En una primera realización, R5a representa hidrógeno. En una segunda realización, R5a representa hidroxi. En una tercera realización, R5a representa halógeno. En un aspecto de esta realización, R5a representa flúor. En una cuarta realización, R5a representa trifluorometilo. En una quinta realización, R5a representa -NRbRc . En un aspecto de esa realización, R5a representa -NH2. En una sexta realización, R5a representa -NRcC(O)Rd. En una séptima realización, R5a representa -C(O)-NRcRd. En una octava realización, R5a representa -NHS(O)2Re . En una novena realización, R5a representa -S-Ra . En una décima realización, R5a representa -S(O)-Ra . En una decimoprimera realización, R5a representa-S(O)2Ra . En un aspecto particular de esta realización, R5a representa -S(O)2-CH3. En una duodécima realización, R5a representa -S(O)(N-Rd)Ra . En una decimotercera realización, R5a representa -S(O)2(N-Rd). En una decimocuarta realización, R5a representa -ORa . En un aspecto de esta realización, Ra es un alquilo C1-6. En un segundo aspecto de esta realización, Ra es un arilo. En un tercer aspecto de esta realización, Ra es un heteroarilo. En una decimoquinta realización, R5a representa -O-(CO)-Rd. En un aspecto particular de esta realización, R5a representa -O-(CO)-CH3. En una decimosexta realización, R5a representa -C(O)-ORd. En una decimoséptima realización, R5a representa alquilo C1-6 opcionalmente sustituido. En un aspecto de esa realización, R5a representa alquilo C1-6 sustituido. En un segundo aspecto de esta realización, R5a representa alquilo C1-6 no sustituido. En un aspecto particular de esta realización, R5a representa metilo. En una decimoctava realización, R5a representa un alquinilo C2-6 opcionalmente sustituido. En una decimonovena realización, R5a representa un heteroarilo opcionalmente sustituido.
En una vigésima realización, R5a representa un arilo opcionalmente sustituido. En una vigesimoprimera realización, R5a representa un alquenilo C2-6 opcionalmente sustituido.
En una vigesimosegunda realización, R5a representa ciano.
En general, R5b representa hidrógeno, hidroxi, halógeno, ciano, trifluorometil-NRbRc, -NRcC(O)Rd, -(CO)NRcRd, -NHS(O)2Re , -S-Ra , -(SO)-Ra , -S(O)2Ra , -S(O)(N-Rd), -S(O)2(N-Rd), -ORa , -C(O)2Rd u -O(CO)-Rd-; o alquilo C1-6, alquenilo C2-6, alquinilo C2-6, arilo o heteroarilo, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes.
Normalmente, R5b representa hidrógeno, hidroxi, halógeno, trifluorometilo, -NRbRc, S(O)2Ra , -ORa u O-(CO)-Rd; o alquilo C1-6, cualquiera de tales grupos puede estar opcionalmente sustituido.
Los ejemplos adecuados de sustituyentes opcionales en R5b incluyen uno, dos o tres sustituyentes seleccionados independientemente entre halógeno, hidroxi, trifluorometilo, alquilo C1-6, alcoxi C1-6, alquilcarbonilo C2-6, alquiloxicarbonilo C2-6, (hidroxi)alquilo C1-6, cicloalquilo (C3-7), alquilsulfonilo C1-6, alquilsulfonil (C1-6)-alquilo (C1-6), dialquilaminocarbonilo (C1-6), oxo y carboxi.
Los ejemplos típicos de sustituyentes particulares en R5b incluyen uno, dos o tres sustituyentes seleccionados independientemente entre flúor, cloro, fluorometilo, fluoroisopropilo, ciano, cianoetilo, nitrometilo, metilo, etilo, isopropilo, isopropilmetilo, trifluorometilo, trifluoroetilo, etenilo, hidroxi, hidroximetilo, hidroxiisopropilo, metoxi, isopropoxi, trifluoroetoxi, carboxiciclobutiloxi, metiltio, metilsulfonilo, metilsulfonilmetilo, metilsulfoniletilo, oxo, amino, aminometilo, aminoisopropilo, metilamino, dimetilamino, metoxietilamino, W-(hidroxietil)-W-(metil)amino, acetilaminometilo, metilsulfonilamino, W-metil-W-(metilsulfonil)amino, bis(metilsulfonil)amino, W-(carboxietil)-W-(metil)amino, carboxiciclopentilamino, carboxiciclopropilmetilamino, formilo, acetilo, acetoxiisopropilo, carboxi, carboximetilo, carboxietilo, metoxicarbonilo, etoxicarbonilo, n-butoxicarbonilo, ferc-butoxicarbonilo, metoxicarbonilmetilo, etoxi-carbonilmetilo, etoxicarboniletilo, morfoliniletoxicarbonilo, etoxicarbonilmetilidenilo, metilsulfonilaminocarbonilo, acetilaminosulfonilo, metoxiamino-carbonilo, tetrazolilo, tetrazolilmetilo, hidroxioxadiazolilo, aminocarbonilo, amino-sulfonilo, metilsulfoximinilo y (metil)(W-metil)sulfoximinilo.
En una primera realización, R5b representa hidrógeno. En una segunda realización, R5b representa hidroxi. En una
tercera realización, R5b representa halógeno. En un aspecto de esta realización, R5b representa flúor. En una cuarta realización, R5b representa trifluorometilo. En una quinta realización, R5b representa -NRbRc . En un aspecto de esa realización, R5b representa -NH2. En una sexta realización, R5b representa -NRcC(O)Rd. En una séptima realización, R5b representa -C(O)-NRcRd. En una octava realización, R5b representa -NHS(O)2Re . En una novena realización, R5a representa -S-Ra . En una décima realización, R5b representa -S(O)-Ra . En una decimoprimera realización, R5b representa-S(O)2Ra . En un aspecto particular de esta realización, R5b representa -S(O)2-CH3. En una duodécima realización, R5b representa -S(O)(N-Rd)Ra . En una decimotercera realización, R5b representa -S(O)2(N-Rd). En una decimocuarta realización, R5b representa -ORa . En un aspecto de esta realización, Ra es un alquilo C1-6. En un segundo aspecto de esta realización, Ra es un arilo. En un tercer aspecto de esta realización, Ra es un heteroarilo. En una decimoquinta realización, R5b representa -O-(CO)-Rd. En un aspecto particular de esta realización, R5a representa -O-(CO)-CH3. En una decimosexta realización, -C(O)-ORd. En una decimoséptima realización, R5b representa alquilo C1-6 opcionalmente sustituido. En un aspecto de esa realización, R5b representa alquilo C1-6 sustituido. En un segundo aspecto de esta realización, R5b representa alquilo C1-6 no sustituido. En un aspecto particular de esta realización, R5b representa metilo. En una decimoctava realización, R5b representa un alquinilo C2-6 opcionalmente sustituido. En una decimonovena realización, R5b representa un heteroarilo opcionalmente sustituido. En una vigésima realización, R5b representa un arilo opcionalmente sustituido. En una vigesimoprimera realización, R5b representa un alquenilo C2-6 opcionalmente sustituido. En una vigesimosegunda realización, R5b representa ciano.
En particular, R5b representa hidrógeno o metilo.
En una realización alternativa, R5a y R5b, cuando se toman junto con el carbono al que están unidos, representan un carbonilo, tiocarbonilo o -C=N-OH.
En un aspecto de esta realización alternativa, R5a y R5b, cuando se toman junto con el carbono al que están unidos, representan un carbonilo.
En un segundo aspecto de esta realización alternativa, R5a y R5b, cuando se toman junto con el carbono al que están unidos, representan un tiocarbonilo.
En otro aspecto de esta realización alternativa, R5a y R5b, cuando se toman junto con el carbono al que están unidos, representan -C=N-OH.
Los valores ilustrativos de R5a incluyen hidrógeno, hidroxi, flúor, trifluorometilo, -N(CH3)2 , -NH(CO)CH3 , -SO2-CH3, -O-(CO)-CH3 , metilo, metoxi, piridinmetiloxi-, benciloxi, (metoxicarbonil)metiloxi-, (etiloxicarbonil)metiloxi-, (terc-butoxicarbonil)metiloxi-, (hidroxicarbonil)metiloxi y cianometiloxi.
Los valores seleccionados de R5a incluyen hidrógeno, hidroxi, flúor, trifluorometilo, -N(CH3)2 , -NH(CO)CH3 , -SO2-CH3, -O-(CO)-CH3 , metilo y metoxi.
Los valores seleccionados de R5b incluyen hidrógeno, hidroxi, flúor, trifluorometilo, -N(CH3)2 , -NH(CO)CH3 , -SO2-CH3, -O-(CO)-CH3 , metilo y metoxi.
En una realización particular, R5a es como se ha definido anteriormente y R5b representa hidrógeno. En un aspecto particular de esta realización, R5a es hidroxi.
En otra realización particular, R5a es como se ha definido anteriormente y R5b representa alquilo C1-4, preferentemente, metilo. En un aspecto particular de esta realización, R5a es hidroxi.
En general, R6 representa hidrógeno, hidroxi, halógeno, trifluorometilo, -NRbRc, -NRcC(O)Rd, -NHS(O)2Re , -S(O)2Ra, -S(O)(N-Rd)Ra u -O-(CO)-Rd; o alcoxi C1-6, alquilo C1-6, alquinilo C2-6, heteroarilo, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes.
Normalmente, R6 representa hidrógeno, hidroxi, halógeno o trifluorometilo.
En una realización particular, R6 representa hidrógeno.
En una realización alternativa, R6 e Y, junto con el átomo de carbono al que están unidos, forman un cicloalquilo C3-7.
En otra realización alternativa, R6 e Y, junto con el átomo de carbono al que están unidos, forman un heterocicloalquilo C3-7. En un aspecto particular de acuerdo con esta realización, R6 e Y, junto con el átomo de carbono al que están unidos, forman un dihidrobenzofurano. En un segundo aspecto particular de acuerdo con esta realización, R6 e Y, junto con el átomo de carbono al que están unidos, forman un 3H-benzofuranona. En un tercer aspecto particular de acuerdo con esta realización, R6 e Y, junto con el átomo de carbono al que están unidos, forman un dihidroisoindol. En un cuarto aspecto particular de acuerdo con esta realización, R6 e Y, junto con el átomo de carbono al que están unidos, forman una dihidroisoindolona.
Los ejemplos típicos de sustituyentes adecuados en Ra , Rb, Rc, Rd o Re , o en el resto heterocíclico -NRbRc , incluyen halógeno, alquilo Ci -6, alcoxi Ci -6, difluorometoxi, trifluorometoxi, alcoxi Ci -6alquilo (Ci -6), alquiltio Ci -6, alquilsulfinilo Ci-6, alquilsulfonilo C1-6, hidroxi, hidroxialquilo (C1-6), aminoalquilo (C1-6), ciano, trifluorometilo, oxo, alquilcarbonilo C2-6, carboxi, alcoxicarbonilo C2-6, alquilcarboniloxi C2-6, amino, alquilamino C1-6, dialquilamino (C1-6), fenilamino, piridinilamino, alquilcarbonilamino C2-6, alquilcarbonilamino C2-6alquilo (C1-6), alcoxicarbonilamino C2-6, alquilsulfonilamino C1-6, aminocarbonilo, alquilaminocarbonilo C1-6 y dialquilaminocarbonilo (C1-6).
Los ejemplos típicos de sustituyentes específicos en Ra , Rb, Rc, Rd o Re , o en el resto heterocíclico -NRbRc , incluyen flúor, cloro, bromo, metilo, etilo, isopropilo, metoxi, isopropoxi, difluorometoxi, trifluorometoxi, metoximetilo, metiltio, etiltio, metilsulfinilo, metilsulfonilo, hidroxi, hidroximetilo, hidroxietilo, aminometilo, ciano, trifluorometilo, oxo, acetilo, carboxi, metoxicarbonilo, etoxicarbonilo, ferc-butoxicarbonilo, acetoxi, amino, metilamino, etilamino, dimetilamino, fenilamino, piridinilamino, acetilamino, ferc-butoxicarbonilamino, acetilaminometilo, metilsulfonilamino, aminocarbonilo, metilaminocarbonilo y dimetilaminocarbonilo.
Adecuadamente, Ra representa alquilo C1-6, arilalquilo (C1-6) o heteroarilalquilo (C1-6), cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes.
Los valores seleccionados de Ra incluyen metilo, etilo, bencilo e isoindolilpropilo, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes.
Los ejemplos ilustrativos de sustituyentes adecuados en Ra incluyen alcoxi C1-6, oxo, ciano y alcoxicarbonilo C2-6. Los ejemplos seleccionados de sustituyentes adecuados en Ra incluyen alcoxi C1-6 y oxo.
Los ejemplos seleccionados de sustituyentes específicos en Ra incluyen metoxi y oxo.
En una realización, Ra representa alquilo C1-6 opcionalmente sustituido. En un aspecto de esa realización, Ra representa idealmente alquilo C1-6 no sustituido, especialmente metilo. En otro aspecto de esa realización, Ra representa idealmente alquilo C1-6 sustituido. En un primer aspecto particular de esta realización, Ra representa metoxietilo. En un segundo aspecto particular de esta realización, Ra representa metoxicarbonilo. En un tercer aspecto de esta realización, Ra representa etoxicarbonilo. En un cuarto aspecto de esta realización, Ra representa ferc-butoxicarbonilo. En un quinto aspecto de esta realización, Ra representa carboxi-metilo. En otra realización, Ra representa arilo opcionalmente sustituido. En un aspecto de esa realización, Ra representa arilo no sustituido, especialmente fenilo. En otro aspecto de esa realización, Ra representa arilo monosustituido, especialmente metilfenilo. En otra realización, Ra representa arilalquilo (C1-6) opcionalmente sustituido, idealmente arilalquilo (C1-6) sin sustituir, especialmente bencilo. En una realización adicional, Ra representa heteroarilo opcionalmente sustituido. En una realización adicional, Ra representa heteroarilalquilo (C1-6) opcionalmente sustituido, por ejemplo dioxoisoindolilpropilo o piridinil-metilo. En una realización adicional, Ra representa cicloalquilo C3-7. En otra realización adicional, Ra representa heterocicloalquilo C3-7.
Los valores ilustrativos de Ra incluyen metilo, metoxietilo, bencilo, dioxoisoindolilpropilo, piridinilmetilo, metoxicarbonilmetilo, carboximetilo, etoxicarbonilmetilo y ferc-butoxi-carbonilmetilo.
Los valores específicos de Ra incluyen metilo, metoxietilo, bencilo y dioxoisoindolilpropilo.
En un aspecto particular, Rb representa hidrógeno o trifluorometilo; o alquilo C1-6, cicloalquilo C3-7, cicloalquil C3-7alquilo (C1-6), arilo, arilalquilo (C1-6), heterocicloalquilo C3-7, heterocicloalquil C3-7alquilo (C1-6), heteroarilo o heteroarilalquilo (C1-6), cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes.
Los valores seleccionados de Rb incluyen hidrógeno; o alquilo C1-6, arilalquilo (C1-6), heterocicloalquilo C3-7 o heterocicloalquil C3-7alquilo (C1-6), cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes.
Los valores típicos de Rb incluyen hidrógeno y alquilo C1-6.
De manera ilustrativa, Rb representa hidrógeno o trifluorometilo; o metilo, etilo, n-propilo, isopropilo, n-butilo, 2-metilpropilo, ferc-butilo, pentilo, hexilo, ciclopropilo, ciclobutilo, ciclopentilo, ciclohexilo, ciclopropilmetilo, ciclobutilmetilo, ciclopentilmetilo, ciclohexilmetilo, fenilo, bencilo, feniletilo, azetidinilo, tetrahidrofurilo, tetrahidrotienilo, pirrolidinilo, piperidinilo, homopiperidinilo, morfolinilo, azetidinilmetilo, tetrahidrofurilmetilo, pirrolidinilmetilo, pirrolidiniletilo, pirrolidinilpropilo, tiazolidinilmetilo, imidazolidiniletilo, piperidinilmetilo, piperidiniletilo, tetrahidroquinolinilmetilo, piperazinilpropilo, morfolinilmetilo, morfoliniletilo, morfolinilpropilo, piridinilo, indolilmetilo, pirazolilmetilo, pirazoliletilo, imidazolilmetilo, imidazoliletilo, bencimidazolilmetilo, triazolilmetilo, piridinilmetilo o piridiniletilo, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes.
Los valores representativos de Rb incluyen hidrógeno; o metilo, etilo, n-propilo, bencilo, pirrolidinilo o morfolinilpropilo, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes.
Los ejemplos seleccionados de sustituyentes adecuados en Rb incluyen alcoxi Ci -6, alquiltio Ci -6, alquilsulfinilo Ci -6, alquilsulfonilo Ci -6, hidroxi, ciano, alcoxicarbonilo C2-6, di-alquilamino (C1-6) y alcoxicarbonilamino C2-6.
Los ejemplos seleccionados de sustituyentes específicos en Rb incluyen metoxi, metiltio, metilsulfinilo, metilsulfonilo, hidroxi, ciano, terc-butoxicarbonilo, dimetilamino y terc-butoxicarbonilamino.
Los valores específicos de Rb incluyen hidrógeno, metilo, metoxietilo, metiltioetilo, metilsulfiniletilo, metilsulfoniletilo, hidroxietilo, cianoetilo, dimetilaminoetilo, terc-butoxicarbonilaminoetilo, dihidroxipropilo, bencilo, pirrolidinilo, terc-butoxicarbonilpirrolidinilo y morfolinilpropilo.
En una realización, Rb representa hidrógeno. En otra realización, Rb representa alquilo C1-6, especialmente metilo. Los valores seleccionados de Rc incluyen hidrógeno; o alquilo C1-6, cicloalquilo C3-7 o heterocicloalquilo C3-7, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes.
En un aspecto particular, Rc representa hidrógeno, alquilo C1-6 o cicloalquilo C3-7.
Los valores representativos de Rc incluyen hidrógeno; o metilo, ciclobutilo, ciclopentilo, ciclohexilo, tetrahidropiranilo y piperidinilo, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes.
Los ejemplos seleccionados de sustituyentes adecuados en Rc incluyen alquilcarbonilo C2-6 y alcoxicarbonilo C2-6. Los ejemplos seleccionados de sustituyentes específicos en Rc incluyen acetilo y terc-butoxicarbonilo.
Los valores específicos de Rc incluyen hidrógeno, metilo, ciclobutilo, ciclopentilo, ciclohexilo, tetrahidropiranilo, acetilpiperidinilo y terc-butoxicarbonilpiperidinilo.
Adecuadamente, Rc representa hidrógeno o alquilo C1-6. En una realización, Rc es hidrógeno. En otra realización, Rc representa alquilo C1-6, especialmente metilo o etilo, en particular metilo. En una realización adicional, Rc representa cicloalquilo C3-7, por ejemplo, ciclopropilo, ciclobutilo, ciclopentilo o ciclohexilo.
Como alternativa, el resto -NRbRc puede representar adecuadamente azetidin-1-ilo, pirrolidin-1-ilo, oxazolidin-3-ilo, isoxazolidin-2-ilo, tiazolidin-3-ilo, isotiazolidin-2-ilo, piperidin-1-ilo, morfolin-4-ilo, tiomorfolin-4-ilo, piperazin-1-ilo, homopiperidin-1-ilo, homomorfolin-4-ilo, homopiperazin-1-ilo, (imino)(oxo)tiazinan-4-ilo, (oxo)tiazinan-4-ilo o (dioxo)tiazinan-4-ilo, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes. Los ejemplos seleccionados de sustituyentes adecuados en el resto heterocíclico -NRbRc incluyen alquilo C1-6, alquilsulfonilo C1-6, hidroxi, hidroxialquilo (C1-6), aminoalquilo (C1-6), ciano, oxo, alquilcarbonilo C2-6, carboxi, alcoxicarbonilo C2-6, amino, alquilcarbonilamino C2-6, alquilcarbonilamino C2-6alquilo (C1-6), alcoxicarbonilamino C2-6, alquilsulfonilamino C1-6 y aminocarbonilo.
Los ejemplos seleccionados de sustituyentes específicos en el resto heterocíclico -NRbRc incluyen metilo, metilsulfonilo, hidroxi, hidroximetilo, aminometilo, ciano, oxo, acetilo, carboxi, etoxicarbonilo, amino, acetilamino, acetilaminometilo, terc-butoxicarbonilamino, metilsulfonilamino y aminocarbonilo.
Los valores específicos del resto heterocíclico -NRbRc incluyen azetidin-1-ilo, hidroxiazetidin-1-ilo, hidroximetilazetidin-1-ilo, (hidroxi)(hidroximetil)azetidin-1-ilo, aminometil-azetidin-1-ilo, cianoazetidin-1-ilo, carboxiazetidin-1-ilo, aminoazetidin-1-ilo, aminocarbonilazetidin-1-ilo, pirrolidin-1-ilo, aminometilpirrolidin-1-ilo, oxopirrolidin-1-ilo, acetilaminometilpirrolidin-1-ilo, terc-butoxicarbonilaminopirrolidin-1-ilo, oxo-oxazolidin-3-ilo, hidroxiisoxazolidin-2-ilo, tiazolidin-3-ilo, oxotiazolidin-3-ilo, dioxo-isotiazolidin-2-ilo, piperidin-1-ilo, hidroxipiperidin-1-ilo, hidroximetilpiperidin-1-ilo, aminopiperidin-1-ilo, acetilaminopiperidin-1-ilo, terc-butoxicarbonilaminopiperidin-1-ilo, metilsulfonilaminopiperidin-1-ilo, morfolin-4-ilo, piperazin-1-ilo, metilpiperazin-1-ilo, metilsulfonilpiperazin-1-ilo, oxopiperazin-1-ilo, acetilpiperazin-1-ilo, etoxicarbonilpiperazin-1-ilo, oxohomopiperazin-1-ilo, (imino)(oxo)tiazinan-4-ilo, (oxo)tiazinan-4-ilo y (dioxo)tiazinan-4-ilo.
Adecuadamente, Rd representa hidrógeno; o alquilo C1-6, arilo o heteroarilo, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes.
Los ejemplos seleccionados de valores adecuados para Rd incluyen hidrógeno, metilo, etilo, isopropilo, 2-metilpropilo, terc-butilo, ciclopropilo, ciclobutilo, fenilo, tiazolidinilo, tienilo, imidazolilo y tiazolilo, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes.
Los ejemplos seleccionados de sustituyentes adecuados en Rd incluyen halógeno, alquilo C1-6, alcoxi C1-6, oxo, alquilcarboniloxi C2-6 y dialquilamino (C1-6).
Los ejemplos seleccionados de sustituyentes particulares en Rd incluyen flúor, metilo, metoxi, oxo, acetoxi y dimetilamino.
En una realización, Rd representa hidrógeno. En otra realización, Rd representa alquilo C1-6 opcionalmente sustituido. En un aspecto de esa realización, Rd representa idealmente alquilo C1-6 no sustituido, por ejemplo, metilo, etilo, isopropilo, 2-metilpropilo o tere-butilo, especialmente metilo. En otro aspecto de esa realización, Rd representa idealmente alquilo C1-6 sustituido, por ejemplo, metilo sustituido o etilo sustituido, incluyendo acetoximetilo, dimetilaminometilo y trifluoroetilo.
En otra realización, Rd representa arilo opcionalmente sustituido. En un aspecto de esa realización, Rd representa arilo no sustituido, especialmente fenilo. En otro aspecto de esa realización, Rd representa arilo monosustituido, especialmente metilfenilo. En un aspecto adicional de esa realización, Rd representa arilo disustituido, por ejemplo, dimetoxifenilo.
En una realización adicional, Rd representa heteroarilo opcionalmente sustituido, por ejemplo, tienilo, clorotienilo, metiltienilo, metilimidazolilo o tiazolilo. En otra realización, Rd representa cicloalquilo C3-7 opcionalmente sustituido, por ejemplo, ciclopropilo o ciclobutilo.
En una realización adicional, Rd representa heterocicloalquilo C3-7 opcionalmente sustituido, por ejemplo, tiazolidinilo u oxotiazolidinilo.
Los ejemplos seleccionados de valores específicos para Rd incluyen hidrógeno, metilo, acetoximetilo, dimetilaminometilo, etilo, trifluoroetilo, isopropilo, 2-metilpropilo, tere-butilo, ciclopropilo, ciclobutilo, fenilo, dimetoxifenilo, tiazolidinilo, oxotiazolidinilo, tienilo, clorotienilo, metiltienilo, metilimidazolilo y tiazolilo.
Los ejemplos particulares de valores seleccionados para Rd incluyen hidrógeno y metilo.
Adecuadamente, Re representa alquilo C1-6 o arilo, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes.
Los ejemplos seleccionados de sustituyentes adecuados en Re incluyen alquilo C1-6, especialmente metilo.
En una realización, Re representa alquilo C1-6 opcionalmente sustituido, idealmente alquilo C1-6 no sustituido, por ejemplo, metilo o propilo, especialmente metilo. En otra realización, Re representa arilo opcionalmente sustituido. En un aspecto de esa realización, Re representa arilo no sustituido, especialmente fenilo. En otro aspecto de esa realización, Re representa arilo monosustituido, especialmente metilfenilo. En una realización adicional, Re representa heteroarilo opcionalmente sustituido.
Los valores seleccionados de Re incluyen metilo, propilo y metilfenilo.
Una subclase de compuestos de acuerdo con la divulgación se representa por los compuestos de fórmula (IIA) y N-óxidos de los mismos, y sales y solvatos farmacéuticamente aceptables de los mismos, y derivados de glucurónido de los mismos, y cocristales de los mismos:
en la que
R1 representa halógeno o ciano; o alquilo C1-6, alquinilo C2-6, arilo, heterocicloalquilo C3-7, heterocicloalquenilo C3-7 , heteroarilo, heterocicloalquil (C3-7)alquilaril (C1-6)-, heteroaril-heterocicloalquil (C3-7)-, cicloalquil (C3-7)-heteroaril-, cicloalquil (C3-7)-alquil (C1-6)-heteroaril-, cicloalquenil (C4-7)-heteroaril-, bicicloalquil ^ -^-heteroarilheterocicloalquil (C3-7)-heteroaril-, heterocicloalquil (C3-7)-alquil (C1-6)-heteroaril-, heterocicloalquenil (C3-7)-heteroaril-, heterobicicloalquil (C4-9)-heteroaril- o espiroheterocicloalquil (C4-9)-heteroaril-, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes.
R2 representa hidrógeno, halógeno, trifluorometilo o ciano; o un alquilo C1-6 opcionalmente sustituido.
Z representa un átomo de oxígeno un átomo de azufre; o -S(O), -N(Rd); o una cadena de alquileno C1-4 opcionalmente sustituido, lineal o ramificada.
R5a representa hidrógeno, hidroxi, halógeno, ciano o trifluorometilo; o -NRbRc, -NRcC(O)Rd, -(CO)NRcRd, -NHS(O)2Re , -S-Ra , -(SO)-Ra , -S(O)2Ra , -S(O)(N-Rd), -S(O)2(N-Rd), -ORa , -C(O)2Rd, -O(CO)-Rd-; alquilo C1-6, alquenilo C2-6, alquinilo C2-6, arilo o heteroarilo, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes; y
R5b representa hidrógeno, hidroxi, halógeno, ciano, trifluorometilo; o alquilo C1-6, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes;
o R5a y R5b, cuando se toman junto con el carbono al que están unidos, representan un carbonilo, tiocarbonilo o -C=N-OH; e
Y, Ra , Rb, Rc , Rd, Re , son como se han definido anteriormente para compuestos de fórmula (I).
Los ejemplos de sustituyentes opcionales que pueden estar presentes en R1, R2 , R5a y R5b incluyen uno, dos o tres sustituyentes seleccionados independientemente entre halógeno, halo-alquilo C1-6, ciano, cianoalquilo (C1-6), nitro, nitroalquilo (C1-6), alquilo C1-6, cicloalquilo (C3-7), difluorometilo, trifluorometilo, difluoroetilo, trifluoroetilo, alquenilo C2-6, hidroxi, hidroxialquilo (C1-6), alcoxi C1-6, difluorometoxi, trifluorometoxi, trifluoroetoxi, carboxicicloalquil (C3-7)-oxi, alquilendioxi C1-3, alcoxi C1-6alquilo (C1-6), alquiltio C1-6, alquilsulfinilo C1-6, alquilsulfonilo C1-6, alquilsulfonil (C1-6)-alquilo (C1-6), oxo, amino, aminoalquilo (C1-6), alquil C1-6-amino, dialquilamino (C1-6), hidroxialquilamino (C1-6), alcoxiamino C1-6, alcoxi (C1-6)-alquilamino (C1-6), [alcoxi (C1-6)](hidroxi)alquilamino (C1-6), [alquiltio (C1-6)](hidroxi)-alquilamino (C1-6), N-[alquil (C1-6)]-N-[hidroxialquil (C1-6)]amino, dialquilamino (C1-6)-alquilamino (C1-6), N-[dialquilamino (C1-e)alquil (C1-6)]-N-[hidroxialquil (C1-6)]amino, hidroxialquil (C1-6)-cicloalquilamino (C3-7), (hidroxi)[cicloalquil (C3-7)alquil (C1-6)]amino, heterocicloalquil (C3-7)-alquilamino (C1-6), oxoheterocicloalquil (C3-7)-alquilamino (C1-6), alquilheteroarilamino (C1-6), heteroaril-alquilamino (C1-6), alquilheteroaril (C1-6)alquil (C1-6)-amino, alquilcarbonilamino C2-6, N-[alquil (C1-6)]-N-[alquilcarbonil (C2-6)]amino, alquil (C2-6)-carbonilaminoalquilo (C1-6), alquenilcarbonilamino C3-6, bis[alquenilcarbonil (C3-6)]amino, N-[alquil (C1-6)]-N-[cicloalquilcarbonil (C3-7)]amino, alcoxicarbonilamino C2-6, alcoxicarbonil C2-6alquilamino (C1-6), alquilaminocarbonilamino C1-6, alquilsulfonil C1-6-amino, N-[alquil (C1-6)]-N-[alquilsulfonil (C1-6)]amino, bis[alquilsulfonil (C1-6)]amino, N-[alquil (C1-6)]-N-[carboxialquil (C1-6)]amino, carboxicicloalquilamino (C3-7), carboxicicloalquil (C3-7)-alquilamino (C1-6), formilo, alquilcarbonilo C2-6, cicloalquilcarbonilo (C3-7), fenilcarbonilo, alquilcarboniloxi (C2-6)alquilo (C1-6), carboxi, carboxialquilo (C1-6), alcoxicarbonilo C2-6, alcoxicarbonil C2-6alquilo (C1-6), morfolinil-alcoxicarbonilo (C1-6), alcoxicarbonilmetilidenilo C2-6, un resto de profármaco o isóstero de ácido carboxílico O, -alquil (C1-6)-Q, aminocarbonilo, alquilaminocarbonilo C1-6, hidroxialquilaminocarbonilo (C1-6), dialquilaminocarbonilo (C1-6), aminocarbonilalquilo (C1-6), aminosulfonilo, dialquilaminosulfonilo (C1-6), alquilsulfoximinilo (C1-6), [alquil (C1-6)][N-alquil (C1-6)]-sulfoximinilo y heteroarilo. Un ejemplo adicional de sustituyentes incluye cicloalquilsulfonilo C3-7.
Los ejemplos de sustituyentes particulares en R1, R2 , R5a y R5b incluyen flúor, cloro, bromo, fluorometilo, fluoroisopropilo, ciano, cianoetilo, nitro, nitrometilo, metilo, etilo, isopropilo, isobutilo, tere-butilo, ciclopropilo, ciclobutilo, difluorometilo, trifluorometilo, difluoroetilo, trifluoroetilo, etenilo, hidroxi, hidroximetilo, hidroxiisopropilo, metoxi, isopropoxi, difluorometoxi, trifluorometoxi, trifluoroetoxi, carboxiciclobutiloxi, metilendioxi, etilendioxi, metoximetilo, metoxietilo, metiltio, metilsulfinilo, metilsulfonilo, metilsulfoniletilo, oxo, amino, aminometilo, aminoisopropilo, metilamino, etilamino, dimetilamino, hidroxietilamino, hidroxipropilamino, (hidroxi)(metil)propilamino, metoxiamino, metoxietilamino, (hidroxi)-(metoxi)(metil)propilamino, (hidroxi) (metiltio) butilamino, N-(hidroxietil)-N-(metil)amino, dimetilaminoetilamino, (dimetilamino)(metil)propilamino, N-(dimetilaminoetil)-N-(hidroxietil)amino, hidroximetilciclopentilamino, hidroxiciclobutilmetilamino, (ciclopropil)(hidroxi)propilamino, morfoliniletilamino, oxopirrolidinilmetilamino, etiloxadiazolilamino, metiltiadiazolilamino, tiazolilmetilamino, tiazoliletilamino, pirimidinilmetilamino, metilpirazolilmetilamino, acetilamino, N-acetil-N-metilamino, N-isopropilcarbonil-N-metilamino, acetilaminometilo, etenilcarbonilamino, bis(etenilcarbonil)amino, N-ciclopropilcarbonil-N-metilamino, metoxicarbonilamino, etoxicarbonilamino, tere-butoxicarbonilamino, metoxicarboniletilamino, etilaminocarbonilamino, butilaminocarbonilamino, metilsulfonilamino, N-metil-N-(metilsulfonil)amino, bis(metilsulfonil)amino, N-(carboximetil)-N-metilamino, N-(carboxietil)-N-metilamino, carboxiciclopentilamino, carboxiciclopropilmetilamino, formilo, acetilo, isopropilcarbonilo, ciclobutilcarbonilo, fenilcarbonilo, acetoxiisopropilo, carboxi, carboximetilo, carboxietilo, metoxicarbonilo, etoxicarbonilo, n-butoxicarbonilo, tere-butoxicarbonilo, metoxicarbonilmetilo, etoxicarbonilmetilo, etoxicarboniletilo, morfoliniletoxicarbonilo, etoxicarbonilmetilidenilo, metilsulfonilaminocarbonilo, acetilaminosulfonilo, metoxiaminocarbonilo, tetrazolilo, tetrazolilmetilo, hidroxioxadiazolilo, aminocarbonilo, metilaminocarbonilo, hidroxietilaminocarbonilo, dimetilaminocarbonilo, aminocarbonilmetilo, aminosulfonilo, metilaminosulfonilo, dimetilaminosulfonilo, metilsulfoximinilo y (metil)(N-metil)sulfoximinilo. Los ejemplos adicionales de un sustituyente particular incluyen ciclopropilsulfonilo y tere-butoxi.
Los ejemplos adecuados de sustituyentes opcionales en R1, R2 , R5b y R6 incluyen flúor, hidroxi, metil-sulfonilo, metilo, trifluorometilo, isopropilo, ciclopropilo, metoxi, etoxicarbonilo, metilsulfoximinilo, oxo, carboxi, acetilo, cloro, hidroxiisopropilo, fluoroisopropilo, aminoisopropilo, metilsulfonilo, metilsulfinilo, ciclopropilsulfonilo y tere-butoxi.
En general, R1 representa alquilo C1-6, alquinilo C2-6, arilo, heterocicloalquilo C3-7, heterocicloalquenilo C3-7, heteroarilo,
heterocicloalquil C3-7-alquil Ci -6-arilo-, heteroaril-heterocicloalquil (C3-7)-, cicloalquil (C3-7)-heteroaril-, cicloalquil (C3-7)-alquil (Ci -6)-heteroaril-, cicloalquenil (C4-7)-heteroaril-, bicicloalquil (C4-9)-heteroaril-, heterocicloalquil (C3-7)-heteroaril-, heterocicloalquil (C3-7)-alquil (Ci -6)-heteroaril-, heterocicloalquenil (C3-7)-heteroaril-, heterobicicloalquil (C4-9)-heteroarilo espiroheterocicloalquil (C4-9)-heteroaril-, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes.
Adecuadamente, R1 representa arilo, heterocicloalquenilo C3-7, heteroarilo, heterocicloalquil (C3-7)-heteroaril-, heterobicicloalquil (C4-9)-heteroaril-, cicloalquil (C3-7)-heteroaril- o bicicloalquil (C4-9)-heteroaril-, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes.
Normalmente, R1 representa arilo, heteroarilo, cicloalquil (C3-7)-heteroarilo o heterocicloalquil (C3-7)-heteroaril-, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes.
A continuación, se exponen realizaciones y aspectos adicionales de los compuestos de fórmula (IIA) desvelados en el presente documento.
En una primera realización, R1 representa halógeno. En un aspecto de esa realización, R1 representa bromo. En una segunda realización, R1 representa ciano. En una tercera realización, R1 representa alquilo C1-6 opcionalmente sustituido. En un aspecto de esa realización, R1 representa metilo opcionalmente sustituido. En otro aspecto de esa realización, R1 representa etilo opcionalmente sustituido. En una cuarta realización, R1 representa alquinilo C2-6 opcionalmente sustituido. En un aspecto de esa realización, R1 representa butinilo opcionalmente sustituido. En una quinta realización, R1 representa arilo opcionalmente sustituido. En un aspecto de esa realización, R1 representa fenilo opcionalmente sustituido. En una sexta realización, R1 representa heterocicloalquilo C3-7 opcionalmente sustituido. En una séptima realización, R1 representa heterocicloalquenilo C3-7 opcionalmente sustituido. En un aspecto de esta realización, R1 representa piridin-2(1H)-ona opcionalmente sustituida.
En una octava realización, R1 representa heteroarilo opcionalmente sustituido. En aspectos seleccionados de esa realización, R1 representa benzofurilo, tienilo, indolilo, pirazolilo, indazolilo, isoxazolilo, tiazolilo, imidazolilo, piridinilo, quinolinilo, piridazinilo, pirimidinilo o pirazinilo, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes. En un primer aspecto particular de esa realización, R1 representa pirimidinilo opcionalmente sustituido. En un segundo aspecto particular de esa realización, R1 representa piridinilo opcionalmente sustituido.
En una novena realización, R1 representa heterocicloalquil (C3-7)alquil (C1-6)-aril- opcionalmente sustituido. En un primer aspecto de esa realización, R1 representa pirrolidinilmetilfenil- opcionalmente sustituido. En un segundo aspecto de esa realización, R1 representa opcionalmente sustituido piperazinilmetilfenil-.
En una décima realización, R1 representa heteroaril (C3-7)-heterocicloalquil- opcionalmente sustituido. En un aspecto de esa realización, R1 representa piridinilpiperazinil- opcionalmente sustituido.
En una decimoprimera realización, R1 representa cicloalquilheteroaril C3-7- opcionalmente sustituido. En un primer aspecto de esa realización, R1 representa ciclohexilpirazolil- opcionalmente sustituido. En un segundo aspecto de esa realización, R1 representa ciclohexilpiridinil- opcionalmente sustituido. En un tercer aspecto de esa realización, R1 representa ciclopropilpirimidinil- opcionalmente sustituido. En un cuarto aspecto de esa realización, R1 representa ciclobutilpirimidinil- opcionalmente sustituido. En un quinto aspecto de esa realización, R1 representa ciclopentilpirimidinil- opcionalmente sustituido. En un sexto aspecto de esa realización, R1 representa ciclohexilpirimidinil- opcionalmente sustituido. En un séptimo aspecto de esa realización, R1 representa ciclohexilpirazinil- opcionalmente sustituido. En un octavo aspecto de esa realización, R1 representa ciclopropilpiridinilo opcionalmente sustituido.
En una duodécima realización, R1 representa cicloalquil (C3-7)-alquil (C1-6)-heteroaril-.
En una decimotercera realización, R1 representa cicloalquenil (C4-7)-heteroaril- opcionalmente sustituido.
En una decimocuarta realización, R1 representa bicicloalquil (C4-9)-heteroaril- opcionalmente sustituido.
En una decimoquinta realización, R1 representa heterocicloalquil (C3-7)-heteroaril- opcionalmente sustituido. En un primer aspecto de esa realización, R1 representa pirrolidinilpiridinil- opcionalmente sustituido. En un segundo aspecto de esa realización, R1 representa tetrahidropiranilpiridinil- opcionalmente sustituido. En un tercer aspecto de esa realización, R1 representa piperidinilpiridinil- opcionalmente sustituido. En un cuarto aspecto de esa realización, R1 representa piperazinilpiridinil- opcionalmente sustituido. En un quinto aspecto de esa realización, R1 representa morfolinilpiridinil- opcionalmente sustituido. En un sexto aspecto de esa realización, R1 representa tiomorfolinilpiridinilopcionalmente sustituido. En un séptimo aspecto de esa realización, R1 representa diazepanilpiridinil- opcionalmente sustituido. En un octavo aspecto de esa realización, R1 representa oxetanilpirimidinil- opcionalmente sustituido. En un noveno aspecto de esa realización, R1 representa azetidinilpirimidinil- opcionalmente sustituido. En un décimo aspecto de esa realización, R1 representa tetrahidrofuranoilpirimidinil- opcionalmente sustituido. En un decimoprimer aspecto de esa realización, R1 representa pirrolidinilpirimidinil- opcionalmente sustituido. En un decimosegundo aspecto de esa
realización, R1 representa tetrahidropiranilpirimidinil- opcionalmente sustituido. En un decimotercer aspecto de esa realización, R1 representa piperidinilpirimidinil- opcionalmente sustituido. En un decimocuarto aspecto de esa realización, R1 representa piperazinilpirimidinil- opcionalmente sustituido. En un decimoquinto aspecto de esa realización, R1 representa morfolinilpirimidinil- opcionalmente sustituido. En un decimosexto aspecto de esa realización, R1 representa opcionalmente sustituido tiomorfolinilpirimidinil-. En un decimoséptimo aspecto de esa realización, R1 representa azepanilpirimidinil- opcionalmente sustituido. En un decimoctavo aspecto de esa realización, R1 representa oxazepanilpirimidinil- opcionalmente sustituido. En un decimonoveno aspecto de esa realización, R1 representa diazepanilpirimidinil- opcionalmente sustituido. En un vigésimo aspecto de esa realización, R1 representa tiadiazepanilpirimidinil- opcionalmente sustituido. En un vigesimoprimer aspecto de esa realización, R1 representa oxetanilpirazinil- opcionalmente sustituido. En un vigesimosegundo aspecto de esa realización, R1 representa piperidinilpirazinil- opcionalmente sustituido. En un vigesimotercer aspecto de esta realización, R1 representa tetrahidropiranilpiridinilo opcionalmente sustituido. En un vigesimocuarto aspecto de esa realización, R1 representa tetrahidro-tiopiranilpirimidinilo. En un vigesimoquinto aspecto, R1 representa (imino)(oxo)tiazinanilpirimidinilo. En un vigesimosexto aspecto de esa realización, R1 representa (oxo)tiazinanil-pirimidinilo. En un vigesimoséptimo aspecto de esa realización, R1 representa un (dioxo)tiazinanil-pirimidinilo.
En una decimosexta realización, R1 representa heterocicloalquil (C3-7)alquil (C1-6)-heteroaril- opcionalmente sustituido. En un primer aspecto de esa realización, R1 representa morfolinilmetiltienil- opcionalmente sustituido. En un segundo aspecto de esa realización, R1 representa morfoliniletilpirazolil- opcionalmente sustituido.
En una decimoséptima realización, R1 representa heterocicloalquenil (C3-7)-heteroaril- opcionalmente sustituido.
En una decimoctava realización, R1 representa heterobicicloalquil (C4-9)-heteroaril- opcionalmente sustituido. En un primer aspecto de esta realización, R1 representa 3-azabiciclo[3.2.1]octanil-pirimidinilo opcionalmente sustituido. En un segundo aspecto de esta realización, , R1 representa 3-oxa-8-azabiciclo-[3.2.1]octanilpirimidinilo opcionalmente sustituido. En un tercer aspecto de esta realización, R1 representa 3,7-dioxa-9-azabiciclo[3.3.1]nonanil-pirimidnilo opcionalmente sustituido. En un cuarto aspecto de esta realización, R1 representa 2,5-diazabiciclo[2.2.1]heptanilpirimidnilo opcionalmente sustituido.
En una decimonovena realización, R1 representa espiroheterocicloalquil (C4-9)-heteroaril- opcionalmente sustituido.
En una vigésima realización, R1 representa bicicloalquil (C4-9)-heteroaril- opcionalmente sustituido. En un aspecto particular de esta realización, R1 representa biciclo[3.1.0]hexanil-pirimidinilo opcionalmente sustituido.
Apropiadamente, R1 representa bromo, ciano; o etilo, butinilo, fenilo, pirrolidinilo, piperidinilo, piperazinilo, morfolinilo, 1.2.3.6- tetrahidropiridinilo, 3,6-dihidropiridinilo, benzofurilo, tienilo, indolilo, pirazolilo, indazolilo, isoxazolilo, tiazolilo, imidazolilo, piridinilo, quinolinilo, piridazinilo, pirimidinilo, pirazinilo, pirrolidinilmetilfenilo, piperazinilmetilfenilo, piridinilpiperazinilo, ciclohexilpirazolilo, ciclohexilpiridinilo, ciclopropilpirimidinilo, ciclobutilpirimidinilo, ciclopentilpirimidinilo, ciclohexilpirimidinilo, ciclohexilpirazinilo, ciclohexilmetilpirimidinilo, ciclohexenilpiridinilo, ciclopropilpiridinilo, ciclohexenilpirimidinilo, biciclo[3.1.0]hexanilpiridinilo, biciclo[3.1.0]hexanil-pirimidinilo, biciclo[3.1.0]hexenil-pirimidinilo, biciclo[4.1.0]heptanilpirimidinilo, biciclo[2.2.2]octanilpirimidinilo, pirrolidinilpiridinilo, tetrahidropiranilpiridinilo, tetrahidro-tiopiranilpirimidinilo, piperidinilpiridinilo, piperazinil-piridinilo, morfolinilpiridinilo, tiomorfolinilpiridinilo, diazepanilpiridinilo, oxetanilpirimidinilo, azetidinilpirimidinilo, tetrahidrofuranilpirimidinilo, pirrolidinil-pirimidinilo, tetrahidropiranilpirimidinilo, piperidinilpirimidinilo, piperazinil-pirimidinilo, hexahidro[1.2.5]tiadiazolo[2,3-a]pirazinilpirimidinilo, morfolinil-pirimidinilo, tiomorfolinilpirimidinilo, azepanilpirimidinilo, oxazepanilpirimidinilo, diazepanilpirimidinilo, tiadiazepanilpirimidinilo, oxetanilpirazinilo, piperidinilpirazinilo, morfolinilmetiltienilo, morfoliniletilpirazolilo, 3-azabiciclo[3.1.0]-hexanilpiridinilo, 3-azabiciclo[3.1.0]hexanilpiridazinilo, 3-azabiciclo[3.1.0]hexanilpirimidinilo, 2-oxa-5-azabiciclo[2.2.1]heptanilpirimidinilo, 3-azabiciclo[3.1.1]heptanilpirimidinilo, 3-azabiciclo[4.1.0]heptanilpiridinilo, 3-azabiciclo[4.1.0]heptanilpirimidinilo, 2-oxabiciclo[2.2.2]octanilpirimidinilo, 3-azabiciclo[3.2.1]octanilpirimidinilo, 8-azabiciclo[3.2.1]octanilpirimidinilo, 3-oxa-8-azabiciclo[3.2.1]octanilpirimidinilo, 3.6- diazabiciclo[3.2.2]nonanilpirimidinilo, 3-oxa-7-azabiciclo[3.3.1]-nonanilpirimidinilo, 3,7-dioxa-9-azabiciclo[3.3.1]-nonanilpirimidinilo, 5-azaespiro[2,3]hexanilpirimidinilo, 5-azaespiro[2,4]heptanil-pirimidinilo, 2-azaespiro[3,3]heptanilpirimidinilo, 2-oxa-6-azaespiro[3,3]heptanil-pirimidinilo, 2-oxa-6-azaespiro[3,4]octanilpirimidinilo, 2-oxa-6-azaespiro[3,5]nonanil-pirimidinilo, 2-oxa-7-azaespiro[3,5]nonanilpirimidinilo, 2,4,8-triazaespiro[4,5]decanilpirimidinilo, 3,6-epiminofuro [3,2-b]furanil-pirimidinilo, (imino)(oxo)tiazinanil-pirimidinilo, (oxo)tiazinanil-pirimidinilo o (dioxo)tiazinanil-pirimidinilo, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes. Además, R1 representa 2,5-diazabiciclo[2.2.1]heptanil-pirimidinilo o piridin-2(1H)-ona, que puede estar opcionalmente sustituido con uno o más sustituyentes.
Definitivamente, R1 representa bromo, ciano, fenilo, piridinilo, dihidropiridinilo, pirimidinilo, ciclobutilpirimidinilo, ciclopropilpiridinilo, biciclo[3.1.0]hexanilpirimidinilo, biciclo[3.1.0]hexenil-pirimidinilo, pirimidinilo, tetrahidropiranilpiridinilo, tetrahidro-tiopiranilpirimidinilo, piperazinil-piridinilo, oxetanilpirimidinilo, azetidinilpirimidinilo, tetrahidrofuranilpirimidinilo, piperidinilpirimidinilo, piperazinilpirimidinilo, morfolinil-pirimidinilo, tiomorfolinilpirimidinilo, 2oxa-5-azabiciclo[2.2.1]heptanilpirimidinilo, 3-azabiciclo[3.2.1]octanil-pirimidinilo, 3-oxa-8-azabiciclo[3.2.1]octanilpirimidinilo, 3,7-dioxa-9-azabiciclo[3.3.1]-nonanilpirimidinilo, epiminofuro [3,2-b]furanilpirimidinilo, (imino)(oxo)tiazinanil-pirimidinilo, (oxo)tiazinanil-pirimidinilo, (dioxo)tiazinanil-pirimidinilo,
cidopropilpirimidinilo, 2,5-diazabiciclo[2,2,1 ]heptanil-pirimidinilo o piridin-2(1H)-ona, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes. Adecuadamente, R1 representa bromo, ciano, fenilo, piridinilo, dihidropiridinilo, pirimidinilo, ciclobutilpirimidinilo, ciclopropilpiridinilo, biciclo[3.1.0]hexanil-pirimidinilo, biciclo[3.1.0]hexenilpirimidinilo, pirimidinilo, tetrahidropiranilpiridinilo, tetrahidro-tiopiranilpirimidinilo, piperazinilpiridinilo, oxetanilpirimidinilo, azetidinilpirimidinilo, tetrahidrofuranilpirimidinilo, piperidinilpirimidinilo, piperazinilpirimidinilo, morfolinil-pirimidinilo, tiomorfolinilpirimidinilo, 2-oxa-5-azabiciclo[2,2,1 ]heptanilpirimidinilo, 3-azabiciclo[3.2.1]octanil-pirimidinilo, 3-oxa-8-azabiciclo[3.2.1 ]octanil-pirimidinilo, 3,7-dioxa-9-azabiciclo[3.3.1]-nonanilpirimidinilo, epiminofuro [3,2-b]furanil-pirimidinilo, (imino)(oxo)tiazinanil-pirimidinilo, (oxo)tiazinanil-pirimidinilo, (dioxo)tiazinanil-pirimidinilo o ciclopropilpirimidinilo, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes. Además, R1 representa 2,5-diazabiciclo[2.2.1]heptanil-pirimidinilo o piridin-2(1H)-ona, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes.
Adecuadamente, R1 representa fenilo, piridinilo, dihidropiridinilo, pirimidinilo, ciclobutilpirimidinilo, ciclopropilpiridinilo, biciclo[3.1.0]hexanil-pirimidinilo, biciclo[3.1.0]hexenil-pirimidinilo, pirimidinilo, tetrahidropiranilpiridinilo, tetrahidrotiopiranilpirimidinilo, piperazinil-piridinilo, oxetanilpirimidinilo, azetidinilpirimidinilo, tetrahidrofuranilpirimidinilo, piperidinilpirimidinilo, piperazinil-pirimidinilo, morfolinil-pirimidinilo, tiomorfolinilpirimidinilo, 2-oxa-5-azabiciclo[2,2,1 ]heptanilpirimidinilo, 3-azabiciclo[3.2.1]octanil-pirimidinilo, 3-oxa-8-azabiciclo[3.2.1]octanil-pirimidinilo, 3,7-dioxa-9-azabiciclo[3.3.1]-nonanilpirimidinilo, epiminofuro [3,2-b]furanil-pirimidinilo, (imino)(oxo)tiazinanil-pirimidinilo, (oxo)tiazinanil-pirimidinilo, (dioxo)tiazinanil-pirimidinilo, 2,5-diazabiciclo[2.2.1]heptanil-pirimidinilo o piridin-2(1H)-ona, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes. De manera ilustrativa, R1 representa fenilo, piridinilo, dihidropiridinilo, pirimidinilo, ciclobutilpirimidinilo, ciclopropilpiridinilo, biciclo[3.1.0]hexanil-pirimidinilo, biciclo[3.1.0]hexenil-pirimidinilo, pirimidinilo, tetrahidropiranilpiridinilo, tetrahidrotiopiranilpirimidinilo, piperazinil-piridinilo, oxetanilpirimidinilo, azetidinilpirimidinilo, tetrahidrofuranilpirimidinilo, piperidinilpirimidinilo, piperazinil-pirimidinilo, morfolinil-pirimidinilo, tiomorfolinilpirimidinilo, 2-oxa-5-azabiciclo[2.2.1]heptanilpirimidinilo, 3-azabiciclo[3.2.1]octanil-pirimidinilo, 3-oxa-8-azabiciclo[3.2.1]octanil-pirimidinilo, 3,7-dioxa-9-azabiciclo[3.3.1]-nonanilpirimidinilo, epiminofuro [3,2-b]furanil-pirimidinilo, , (imino)(oxo)tiazinanilpirimidinilo, (oxo)tiazinanil-pirimidinilo o (dioxo)tiazinanil-pirimidinilo, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes.
Los ejemplos típicos de sustituyentes opcionales en R1 incluyen uno, dos o tres sustituyentes seleccionados independientemente entre halógeno, haloalquilo (C1-6), ciano, cianoalquilo (C1-6), nitroalquilo (C1-6), alquilo C1-6, cicloalquilo C3-7, trifluorometilo, trifluoroetilo, alquenilo C2-6, hidroxi, hidroxialquilo (C1-6), alcoxi C1-6, trifluoroetoxi, carboxicicloalquiloxi (C3-7), alquiltio C1-6, alquilsulfonilo C1-6, alquilsulfonil (C1-6)-alquilo (C1-6), oxo, amino, amino-alquilo (C1-6), alquilamino C1-6, dialquilamino (C1-6), alcoxi (C1-6)alquilamino (C1-6), ^-[alquil (C1-6)]-Ñ-[hidroxialquil (C1-6)]amino, alquilcarbonilamino (C2-6)-alquilo(C1-6), alquilsulfonilamino C1-6, A/-[alquil (C1-6)]-W-[alquilsulfonil (C1-6)]amino, bis[alquil (C1-6)-sulfonil]amino, ^-[alquil (C1-6)]-W-[carboxialquil (C1-6)]amino, carboxicicloalquil (C3-7)-amino, carboxicicloalquil (C3-7)alquilamino (C1-6), formilo, alquilcarbonilo C1-6, alquil-carboniloxi (C2-6)alquilo (C1-6), carboxi, carboxialquilo (C1-6), alcoxicarbonilo C2-6, alcoxicarbonil C2-6alquilo (C1-6), morfolinil-alcoxicarbonilo (C1-6), alcoxicarbonilmetilidenilo C2-6, alquilsulfoximinilo (C1-6) y [alquil (C1-6)][W-alquil (C1-6)]sulfoximinilo. Los ejemplos adicionales de sustituyentes opcionales en R1 incluyen uno, dos o tres sustituyentes seleccionados independientemente entre difluorometilo, alquilsulfinilo C1-6 y cicloalquil (C3-7)sulfonilo.
Los ejemplos adecuados de sustituyentes opcionales en R1 incluyen uno, dos o tres sustituyentes seleccionados independientemente entre halógeno, hidroxi, trifluorometilo, alquilo C1-6, alcoxi C1-6, alquilcarbonilo C2-6, alquiloxicarbonilo C2-6, (hidroxi)alquilo C1-6, cicloalquilo (C3-7), alquilsulfonilo C1-6, alquilsulfonil (C1-6)-alquilo (C1-6), dialquilaminocarbonilo (C1-6), alquilsulfoximinilo (C1-6), oxo, carboxi, difluorometilo, alquilsulfinilo C1-6 y cicloalquil (C3-7)sulfonilo.
Los ejemplos adecuados de sustituyentes opcionales en R1 incluyen uno, dos o tres sustituyentes seleccionados independientemente entre halógeno, hidroxi, alquilo C1-6, alcoxi C1-6, alquilcarbonilo C1-6, (hidroxi)alquilo C1-6, cicloalquilo (C3-7), alquilsulfonilo C1-6, alquilsulfonil (C1-6)-alquilo (C1-6), alquilsulfoximinilo (C1-6), oxo y carboxi.
Los ejemplos típicos de sustituyentes particulares en R1 incluyen uno, dos o tres sustituyentes seleccionados independientemente entre flúor, cloro, fluorometilo, fluoroisopropilo, ciano, cianoetilo, nitrometilo, metilo, etilo, isopropilo, ciclopropilo, isopropilmetilo, trifluorometilo, trifluoroetilo, etenilo, hidroxi, hidroximetilo, hidroxiisopropilo, metoxi, isopropoxi, trifluoroetoxi, carboxiciclobutiloxi, metiltio, metilsulfonilo, metilsulfonilmetilo, metilsulfoniletilo, oxo, amino, aminometilo, aminoisopropilo, metilamino, dimetilamino, metoxietilamino, W-(hidroxietil)-W-(metil)amino, acetilaminometilo, metilsulfonilamino, W-metil-W-(metilsulfonil)amino, bis(metilsulfonil)amino, W-(carboxietil)-W-(metil)amino, carboxiciclopentilamino, carboxiciclopropilmetilamino, formilo, acetilo, acetoxiisopropilo, carboxi, carboximetilo, carboxietilo, metoxicarbonilo, etoxicarbonilo, n-butoxicarbonilo, ferc-butoxicarbonilo, metoxicarbonilmetilo, etoxicarbonilmetilo, etoxicarboniletilo, morfoliniletoxicarbonilo, etoxicarbonilmetilidenilo, metilsulfonilaminocarbonilo, acetilaminosulfonilo, metoxiaminocarbonilo, tetrazolilo, tetrazolilmetilo, hidroxioxadiazolilo, aminocarbonilo, aminosulfonilo, metilsulfoximinilo y (metil)(W-metil)sulfoximinilo.
Los ejemplos particulares adecuados de sustituyentes en R1 incluyen cloro, flúor, metilo, trifluorometilo, hidroxi, hidroximetilo, hidroxiisopropilo, metoxi, metilsulfonilo, oxo, amino, acetilo, metoxicarbonilo, metilsulfoximinilo,
etoxicarbonilo, n-butoxicarbonilo, ferc-butoxicarbonilo, fluoroisopropilo, aminoisopropilo, difluorometilo, metilsulfinilo, terc-butoxi y ciclopropilsulfonilo. Los ejemplos particulares de sustituyentes en R1 incluyen cloro, flúor, metilo, trifluorometilo, hidroxi, hidroximetilo, hidroxiisopropilo, metoxi, metilsulfonilo, metilsulfoximinilo, oxo, amino, acetilo, metoxicarbonilo, etoxicarbonilo, n-butoxicarbonilo y ferc-butoxicarbonilo.
En una realización particular, R1 está sustituido con hidroxialquilo (C1-6). En un aspecto de esa realización, R1 está sustituido con hidroxiisopropilo, especialmente 2-hidroxiprop-2-ilo.
En una realización particular, R1 está sustituido con hidroxialquilo (C1-6). En un aspecto de esa realización, R1 está sustituido con hidroxiisopropilo, especialmente 2-hidroxiprop-2-ilo.
En una segunda realización particular, R1 está sustituido con alquilsulfonilo C1-6. En un aspecto de esta realización, R1 está sustituido con metilsulfonilo.
En una tercera realización particular, R1 está sustituido con un halógeno. En un aspecto de esta realización, R1 está sustituido con un flúor.
En una cuarta realización particular, R1 está sustituido con alquilsulfoximinilo (C1-6). En un aspecto de esta realización particular, R1 está sustituido con metilsulfoximinilo.
Los valores seleccionados de R1 incluyen bromo, ciano, metoxicarboniletilo, etoxicarboniletilo, hidroxibutinilo, clorofenilo, hidroxifenilo, metilsulfonilfenilo, (metilsulfonil)metilfenilo, (metilsulfonil)etilfenilo, aminometilfenilo, aminoisopropilfenilo, acetilaminometilfenilo, acetilfenilo, metoxicarbonilfenilo, aminocarbonilfenilo, aminosulfonilfenilo, acetilaminosulfonilfenilo, (di-(trifluorometil))(hidroxi)fenilo, (metoxicarbonil)(metil)pirrolidinilo, cloropiridinilo, oxopiperidinilo, etoxicarbonilpiperidinilo, metilsulfonilpiperazinilo, morfolinilo, metilsulfonil-1,2,3,6-tetrahidropiridinilo, acetil-1,2,3,6-tetrahidropiridinilo, ferc-butoxicarbonil-1,2,3,6-tetrahidropiridinilo, metoxicarbonilmetil-1,2,3,6-tetrahidropiridinilo, benzofurilo, tienilo, indolilo, pirazolilo, metilpirazolilo, dimetilpirazolilo, (metil)[W-metil-W-(metilsulfonil)amino]pirazolilo, metilindazolilo, dimetilisoxazolilo, hidroxiisopropiltiazolilo, metilimidazolilo, dimetilimidazolilo, piridinilo, tetrahidropiranilpiridinilo, fluoro-piridinilo, cianopiridinilo, metilpiridinilo, (ciano)(metil)piridinilo, dimetilpiridinilo, ciclopropilpiridinilo, trifluorometilpiridinilo, etenilpiridinilo, hidroxiisopropilpiridinilo, hidroximetilpiridinilo, metoxipiridinilo, (metoxi)(metil)piridinilo, isopropoxipiridinilo, trifluoroetoxipiridinilo, (metil)-(trifluoroetoxi)piridinilo, metilsulfonilpiridinilo, metilsulfonilmetilpiridinilo, oxopiridinilo, (metil)(oxo)-piridinilo, (dimetil)(oxo)piridinilo, aminopiridinilo, metilaminopiridinilo, dimetil-aminopiridinilo, metoxietilaminopiridinilo, W-(hidroxietil)-W-(metil)amino-piridinilo, metilsulfonilaminopiridinilo, [bis(metilsulfonil)amino]piridinilo, carboxipiridinilo, quinolinilo, hidroxipiridazinilo, pirimidinilo, isopropilpirimidinilo, fluoroisopropil-pirimidinilo, hidroxiisopropilpirimidinilo, metoxipirimidinilo, carboxiciclobutiloxi-pirimidinilo, metiltiopirimidinilo, metilsulfonilpirimidinilo, oxopirimidinilo, aminopirimidinilo, dimetilaminopirimidinilo, metoxietilaminopirimidinilo, W-(carboxietil)-W-(metil)aminopirimidinilo, carboxiciclopentilaminopirimidinilo, carboxiciclopropilmetilaminopirimidinilo, acetoxiisopropilpirimidinilo, etoxicarboniletilpirimidinilo, hidroxipirazinilo, hidroxiisopropilpirazinilo, pirrolidinilmetilfenilo, piperazinilmetilfenilo, piridinilpiperazinilo, carboxiciclohexilpirazolilo, carboxiciclohexilpiridinilo, fluorometilciclopropilpirimidinilo, acetilaminometilciclopropilpirimidinilo, hidroximetilpirimidinilo, hidroxiciclobutilpirimidinilo, carboxi-ciclopentilpirimidinilo, carboxiciclohexilpirimidinilo, (carboxi)(metil)ciclohexil-pirimidinilo, (carboxi)(hidroxi)ciclohexilpirimidinilo, carboximetilciclohexil-pirimidinilo, etoxicarbonilciclohexilpirimidinilo, (metoxicarbonil)(metil)-ciclohexilpirimidinilo, (etoxicarbonil)(metil)ciclohexilpirimidinilo, carboxiciclohexilpirazinilo, carboxiciclohexilmetilpirimidinilo, carboxiciclohexenilpiridinilo, carboxiciclohexenilpirimidinilo, etoxicarbonilciclohexenilpirimidinilo, carboxibiciclo[3.1.0]hexanilpiridinilo, carboxibiciclo[3.1.0]hexenilpiridinilo, carboxibiciclo[3.1.0]hexanilpirimidinilo, etoxicarbonilbiciclo[3.1.0]hexanilpirimidinilo, carboxibiciclo[4.1.0]heptanil-pirimidinilo, carboxibiciclo[2.2.2]octanilpirimidinilo, pirrolidinilpiridinilo, hidroxipirrolidinilpiridinilo, hidroxitetrahidropiranilpiridinilo, piperidinilpiridinilo, acetilpiperidinilpiridinilo, (carboxi)(metil)piperidinilpiridinilo, [(carboxi)(metil)-piperidinil](fluoro)piridinilo, [(carboxi)(metil)piperidinil](cloro)piridinilo, piperazinilpiridinilo, (metil)(piperazinil)piridinilo, cianoetilpiperazinilpiridinilo, trifluoroetilpiperazinilpiridinilo, metilsulfonilpiperazinilpiridinilo, metilsulfoniletilpiperazinilpiridinilo, oxopiperazinilpiridinilo, acetilpiperazinilpiridinilo, (tercbutoxicarbonilpiperazinil)(metil)piridinilo, metilpiperazinilpiridinilo, carboximetilpiperazinilpiridinilo, carboxietilpiperazinilpiridinilo, etoxicarbonilmetilpiperazinilpiridinilo, etoxicarboniletilpiperazinilpiridinilo, morfolinilpiridinilo, tiomorfolinil-piridinilo, (ferc-butoxicarbonil)-3,6-dihidropiridina, oxotiomorfolinilpiridinilo, dioxotiomorfolinilpiridinilo, oxodiazepanil-piridinilo, fluorooxetanilpirimidinilo, hidroxioxetanilpirimidinilo, hidroxiazetidinil-pirimidinilo, (hidroxi)(metil)azetidinilpirimidinilo, (hidroxi)(trifluorometil)azetidinilpirimidinilo, carboxiazetidinilpirimidinilo, (ferc-butoxicarbonil)(hidroxi)azetidinilpirimidinilo, tetrazolilazetidinilpirimidinilo, hidroxitetrahidrofuranilpirimidinilo, hidroxipirrolidinilpirimidinilo, carboxipirrolidinilpirimidinilo, (carboxi)(metil)pirrolidinilpirimidinilo, carboximetilpirrolidinilpirimidinilo, etoxicarbonilpirrolidinilpirimidinilo, fluorotetrahidropiranilpirimidinilo, hidroxitetrahidropiranilpirimidinilo, (hidroxi)dioxidotetrahidrotiopiranil)pirimidinilo, piperidinilpirimidinilo, difluoropiperidinil-pirimidinilo, (ciano)(metil)piperidinilpirimidinilo, (hidroxi)(nitrometil)piperidinilpirimidinilo, (hidroxi)(metil)piperidinilpirimidinilo, (hidroxi)(trifluorometil)-piperidinilpirimidinilo, (hidroximetil)(metil)piperidinilpirimidinilo, metilsulfonilpiperidinilpirimidinilo, oxopiperidinilpirimidinilo, (formil)(metil)-piperidinilpirimidinilo, carboxipiperidinilpirimidinilo, (carboxi)(fluoro)piperidinilpirimidinilo,
(carboxi)(metil)piperidinilpirimidinilo, (carboxi)(etil)piperidinilpirimidinilo, (carboxi)(trifluorometil)piperidinilpirimidinilo, (carboxi)(hidroxi)-piperidinilpirimidinilo, (carboxi)(hidroximetil)piperidinilpirimidinilo, (carboxi)-(metoxi)piperidinilpirimidinilo, (amino)(carboxi)piperidinilpirimidinilo, carboximetilpiperidinilpirimidinilo, metoxicarbonilpiperidinilpirimidinilo, etoxicarbonilpiperidinilpirimidinilo, (etoxicarbonil)(fluoro)piperidinilpirimidinilo, (metoxicarbonil)(metil)piperidinilpirimidinilo, (etil)(metoxicarbonil)piperidinilpirimidinilo, (isopropil)(metoxicarbonil)piperidinilpirimidinilo, (etoxicarbonil)-(metil)piperidinilpirimidinilo, (nbutoxicarbonil)(metil)piperidinilpirimidinilo, (etoxicarbonil)(trifluorometil)piperidinilpirimidinilo, (etoxicarbonil)-(hidroximetil)piperidinilpirimidinilo, (metoxi)(metoxicarbonil)piperidinilpirimidinilo, (carboxi)(metoxicarbonil)piperidinilpirimidinilo, (metil)-(morfoliniletoxicarbonil)piperidinilpirimidinilo, etoxicarbonilmetilpiperidinilpirimidinilo, metilsulfonilaminocarbonilpiperidinilpirimidinilo, acetilpiperidinilpirimidinilo, acetilamino-sulfonilpiperidinilpirimidinilo, metoxiaminocarbonilpiperidinilpirimidinilo, tetrazolilpiperidinilpirimidinilo, hidroxioxadiazolilpiperidinilpirimidinilo, amino-sulfonilpiperidinilpirimidinilo, piperazinilpirimidinilo, metilsulfonilpiperazinil-pirimidinilo, oxopiperazinilpirimidinilo, carboxipiperazinilpirimidinilo, carboxietilpiperazinilpirimidinilo, terc-butoxicarbonilpiperazinilpirimidinilo, tetrazolilmetilpiperazinilpirimidinilo, trioxohexahidro-[1.2.5]tiadiazolo[2,3-a]pirazinilpirimidinilo, morfolinilpirimidinilo, dimetilmorfolinilpirimidinilo, hidroximetilmorfolinilpirimidinilo, carboximorfolinilpirimidinilo, (carboxi)(metil)morfolinilpirimidinilo, carboximetilmorfolinilpirimidinilo, tiomorfolinilpirimidinilo, oxo-tiomorfolinilpirimidinilo, dioxotiomorfolinilpirimidinilo, carboxiazepanilpirimidinilo, carboxioxazepanil-pirimidinilo, oxodiazepanilpirimidinilo, (oxodiazepanil)(trifluorometil)pirimidinilo, (oxodiazepanil)(metoxi)pirimidinilo, (metil)(oxo)diazepanilpirimidinilo, dioxotiadiazepanilpirimidinilo, hidroxioxetanilpirazinilo, (carboxi)(metil)piperidinil-pirazinilo, (etoxicarbonil)(metil)piperidinilpirazinilo, morfolinilmetiltienilo, morfoliniletilpirazolilo, isopropilmetilpirazolilo, carboxi-3-azabiciclo[3.1.0]hexanilpiridinilo, carboxi-3-azabiciclo[3.1.0]hexanilpiridazinilo, carboxi-3-azabiciclo[3.1.0]hexanilpirimidinilo, (carboxi)(metil)-3-azabiciclo[3.1.0]hexanilpirimidinilo, metoxicarbonil-3-azabiciclo[3.1.0]hexanilpirimidinilo, etoxicarbonil-3-azabiciclo[3.1.0]hexanilpirimidinilo, 2-oxa-5-azabiciclo[2.2.1]heptanilpirimidinilo, carboxi-2-oxa-5-azabiciclo-[2.2.1]heptanilpirimidinilo, carboxi-3-azabiciclo[3.1.1]heptanilpirimidinilo, carboxi-3-azabiciclo[4.1.0]heptanilpiridinilo, carboxi-3-azabiciclo[4.1.0]heptanilpirimidinilo, metoxicarbonil-3-azabiciclo[4.1.0]heptanilpirimidinilo, etoxicarbonil-3-azabiciclo-[4.1.0]heptanilpirimidinilo, (hidroxi)(metil)(oxo)-2-oxabiciclo[2.2.2]octanilpirimidinilo, carboxi-3-azabiciclo[3.2.1]octanilpirimidinilo, metoxicarbonil-3-azabiciclo[3.2.1]octanilpirimidinilo, oxo-8-azabiciclo[3.2.1]octanilpirimidinilo, etoxicarbonilmetilidenil-8-azabiciclo[3.2.1]octanilpirimidinilo, 3-oxa-8-azabiciclo-[3.2.1] octanilpirimidinilo, 3-carboxi-8-azabiciclo-[3.2.1]octanilpirimidinilo, 3-(dimetilaminocarbonil)-8-azabiciclo-[3.2.1] octanilpirimidinilo, oxo-3,6-diazabiciclo[3.2.2]nonanilpirimidinilo, 3,7-dioxa-9-azabiciclo[3.3.1]-nonanilpirimidinilo, carboxi-3-oxa-7-azabiciclo[3.3.1]nonanilpirimidinilo, carboxi-5-azaespiro[2,3]hexanilpirimidinilo, (carboxi)(metil)-5-azaespiro[2,3]hexanilpirimidinilo, carboxi-5 -azaespiro [2,4]heptanil-pirimidinilo, carboxi-2-azaespiro[3,3]heptanilpirimidinilo, 2-oxa-6-azaespiro[3,3]heptanil-pirimidinilo, 2-oxa-6-azaespiro[3,4]octanilpirimidinilo, 2-oxa-6-azaespiro[3,5]nonanil-pirimidinilo, 2-oxa-7-azaespiro[3,5]nonanilpirimidinilo, (dioxo)(metil)-2,4,8-triazaespiro[4,5]decanilpirimidinilo, 3,6-epiminofuro [3,2-b]fu ranil-pirimidinilo, (metil)ciclobutildiolpirimidinilo, metilsulfoximinilfenilo, (imino)(oxo)tiazinanil-pirimidinilo, (oxo)tiazinanil-pirimidinilo y (dioxo)tiazinanil-pirimidinilo. Los valores adicionales de R1 incluyen difluorociclobutanil-pirimidinilo, difluorometil-pirimidinilo, ciclopropil-pirimidinilo, aminoisopropil-pirimidinilo, (hidroxi)ciclopropil-pirimidinilo, (difluoro)(hidroxi)ciclobutil-pirimidinilo, ((metil)ciclobutanodiol)-pirimidinilo, (hidroxi)(metil)ciclohexil-pirimidinilo, ((metil)ciclohexano-diol)-pirimidinilo, (cloro)(metoxi)piridinilo, metilsulfinil-fenilo, ciclopropilsulfonil-fenilo, ferc-butoxi-piridinilo, metilsulfoximinilpiridinilo, piperazinil-2-ona-pirimidinilo, (metil)piridin-2(1H)-ona, (fluoro)piridin-2(1H)-ona, (cloro)piridin-2(1H)-ona, metilcarboxi-3-azabiciclo[3.2.1]octanilpirimidinilo, 3-oxa-8-azabiciclo[3.2,1]octanilpirimidinilo y 2,5-diazabiciclo[2.2.1]hetanilpirimidinilo.
Los valores adecuados de R1 incluyen bromo, ciano, (metilsulfonil)metilfenilo, (metilsulfonil)etilfenilo, (di-(trifluorometil))(hidroxi)fenilo, cloropiridinilo, tetrahidropiranilpiridinilo, hidroxiisopropilpiridinilo, hidroximetilpiridinilo, metoxipiridinilo, isopropoxipiridinilo, isopropilpirimidinilo, hidroxiisopropilpirimidinilo, hidroximetilpirimidinilo, hidroxiciclobutilpirimidinilo, carboxibiciclo[3.1.0]hexanilpiridinilo, carboxibiciclo[3.1.0]hexenilpiridinilo, piperazinilpiridinilo, (terc-butoxicarbonil)-3,6-dihidropiridina, hidroxioxetanilpirimidinilo, hidroxiazetidinil-pirimidinilo, (hidroxi)(metil)azetidinilpirimidinilo, (hidroxi)(trifluorometil)azetidinilpirimidinilo, (terc-butoxicarbonil)(hidroxi)azetidinilpirimidinilo, hidroxitetrahidrofuranoilpirimidinilo, -hidroxitetrahidropiranilpirimidinilo, (hidroxi)dioxidotetrahidrotiopiranil)pirimidinilo, piperidinilpirimidinilo, (ciano)(metil)piperidinilpirimidinilo, (hidroxi)(metil)piperidinilpirimidinilo, (carboxi)(metil)piperidinilpirimidinilo, acetilpiperidinilpirimidinilo, piperazinilpirimidinilo, carboxipiperazinilpirimidinilo, terc-butoxicarbonilpiperazinilpirimidinilo, morfolinilpirimidinilo, tiomorfolinilpirimidinilo, oxo-tiomorfolinilpirimidinilo, dioxo-tiomorfolinilpirimidinilo, oxodiazepanilpirimidinilo, 2-oxa-5-azabiciclo[2.2.1]heptanilpirimidinilo, carboxi-3-azabiciclo[3.2.1]octanilpirimidinilo, oxo-8-azabiciclo[3.2.1]octanilpirimidinilo, 3-carboxi-8-azabiciclo-[3.2.1]octanilpirimidinilo, 3-(dimetilaminocarbonil)-8-azabiciclo-[3.2.1]octanilpirimidinilo, oxo-3,6-diazabiciclo[3.2.2]nonanilpirimidinilo, 3,7-dioxa-9-azabiciclo[3.3.1]-nonanilpirimidinilo, 3,6-epiminofuro [3,2-b]furanil-pirimidinilo, metilsulfoximinilfenilo, (metil)ciclobutildiol-pirimidinilo, (imino)(oxo)tiazinanilpirimidinilo, (oxo)tiazinanil-pirimidinilo, (dioxo)tiazinanil-pirimidinilo, difluorociclobutanilpirimidinilo, difluorometilpirimidinilo, ciclopropil-pirimidinilo, aminoisopropil-pirimidinilo, (hidroxi)ciclopropil-pirimidinilo, (difluoro)(hidroxi)ciclobutil-pirimidinilo, ((metil)ciclobutano-diol)-pirimidinilo, (hidroxi)(metil)ciclohexil-pirimidinilo, ((metil)ciclohexano-diol)-pirimidinilo, (cloro)(metoxi)piridinilo, metilsulfinil-fenilo, ciclopropilsulfonil-fenilo, ferc-butoxipiridinilo, metilsulfoximinilpiridinilo, piperazinil-2-ona-pirimidinilo, (metil)piridin-2(1H)-ona, (fluoro)piridin-2(1H)-ona,
(cloro)piridin-2(1H)-ona, metilcarboxi-3-azabicido[3.2.1]octanilpirimidinilo, 3-oxa-8-azabicido[3.2.1]octanilpirimidinilo y 2,5-diazabicido[2.2.1]hetanilpirimidinilo.
Los valores ilustrativos de R1 incluyen bromo, ciano, (metilsulfonil)metilfenilo, (metilsulfonil)etilfenilo, (di-(trifluorometil))(hidroxi)fenilo, doropiridinilo, tetrahidropiranilpiridinilo, hidroxiisopropilpiridinilo, hidroximetilpiridinilo, metoxipiridinilo, isopropoxipiridinilo, isopropilpirimidinilo, hidroxiisopropilpirimidinilo, hidroximetilpirimidinilo, hidroxiciclobutilpirimidinilo, carboxibiciclo[3.1.0]hexanilpiridinilo, carboxibiciclo[3.1.0]hexenilpiridinilo, piperazinilpiridinilo, (terc-butoxicarbonil)-3,6-dihidropiridina, hidroxioxetanilpirimidinilo, hidroxiazetidinil-pirimidinilo, (hidroxi)(metil)azetidinilpirimidinilo, (hidroxi)(trifluorometil)azetidinilpirimidinilo, (terc-butoxicarbonil)(hidroxi)azetidinilpirimidinilo, hidroxitetrahidrofuranilpirimidinilo, -hidroxitetrahidropiranilpirimidinilo, (hidroxi)dioxidotetrahidrotiopiranil)pirimidinilo, piperidinilpirimidinilo, (ciano)(metil)piperidinilpirimidinilo, (hidroxi)(metil)piperidinilpirimidinilo, (carboxi)(metil)piperidinilpirimidinilo, acetilpiperidinilpirimidinilo, piperazinilpirimidinilo, carboxipiperazinilpirimidinilo, terc-butoxicarbonilpiperazinilpirimidinilo, morfolinilpirimidinilo, tiomorfolinilpirimidinilo, oxo-tiomorfolinilpirimidinilo, dioxo-tiomorfolinilpirimidinilo, oxodiazepanilpirimidinilo, 2-oxa-5-azabiciclo[2.2.1]heptanilpirimidinilo, carboxi-3-azabiciclo[3.2.1]octanilpirimidinilo, oxo-8-azabiciclo[3.2.1]octanilpirimidinilo, 3-carboxi-8-azabiciclo-[3.2.1]octanilpirimidinilo, 3-(dimetilaminocarbonil)-8-azabiciclo-[3.2.1]octanilpirimidinilo, oxo-3,6-diazabiciclo[3.2.2]nonanilpirimidinilo, 3,7-dioxa-9-azabiciclo[3.3.1]-nonanilpirimidinilo, 3,6-epiminofuro [3,2-b]furanil-pirimidinilo, metilsulfoximinilfenilo, (imino)(oxo)tiazinanil-pirimidinilo, (oxo)tiazinanil-pirimidinilo y (dioxo)tiazinanil-pirimidinilo.
Los ejemplos típicos de sustituyentes opcionales en R2 incluyen alcoxicarbonilo C2-6.
Los ejemplos típicos de sustituyentes particulares en R2 incluyen etoxicarbonilo.
En una primera realización, R2 representa hidrógeno. En una segunda realización, R2 representa halógeno. En un aspecto de esa realización, R2 representa flúor. En otro aspecto de esa realización, R2 representa cloro. En una tercera realización, R2 representa trifluorometilo. En una cuarta realización, R2 representa alquilo C1-6 opcionalmente sustituido. En un aspecto de esa realización, R2 representa metilo no sustituido. En otro aspecto de esa realización, R2 representa etilo no sustituido. En un aspecto adicional de esa realización, R2 representa metilo monosustituido o etilo monosustituido. En una quinta realización, R2 representa ciano.
Los valores típicos de R2 incluyen hidrógeno, flúor, cloro, trifluorometilo, metilo y etoxicarboniletilo.
Los valores particulares de R2 incluyen hidrógeno y flúor.
En una primera realización, Z representa un átomo de oxígeno. En una segunda realización, Z representa un átomo de azufre. En una tercera realización, Z representa -S(O). En una cuarta realización, Z representa -N(Rd). En un aspecto de esta realización, X representa -NH.
En una quinta realización, Z representa una cadena de alquileno C1-4 opcionalmente sustituido, lineal o ramificada. Los valores típicos de Z de acuerdo con esta realización incluyen metileno (-CH2-), (metil)metileno, etileno (-CH2CH2-), (etil)metileno, (dimetil)-metileno, (metil)etileno, propileno (-CH2CH2CH2-), (propil)metileno y (dimetil)etileno, cualquiera de estas cadenas puede estar opcionalmente sustituida con uno o más sustituyentes. En un aspecto de esta realización, Z representa una cadena de alquileno C1-4 no sustituida, lineal o ramificada. En un segundo aspecto de esta realización, Z representa una cadena de alquileno C1-4 monosustituida, lineal o ramificada. En un tercer aspecto de esta realización, Z representa una cadena de alquileno C1-4 disustituida, lineal o ramificada. En un aspecto particular de esta realización, Z representa un metileno no sustituido.
Los ejemplos de sustituyentes típicos en la cadena de alquileno que puede estar presente en un compuesto de acuerdo con la invención incluyen halógeno, hidroxi, oxo, alcoxi C1-6, arilo, -C(O)Rd, -CO2Rd, -CONRbRc , -S(O)(N-Rd)Ra o -SO2NRbRc.
Los valores particulares de Z incluyen metileno, -S(O), oxígeno y azufre.
En una realización específica, Z es metileno.
Adecuadamente, R5a representa hidrógeno, hidroxi, halógeno, trifluorometilo; -NRbRc, S(O)2Ra , -ORa , O-(CO)-Rd o -NRcC(O)Rd; o alquilo C1-6, cualquiera de tales grupos puede estar opcionalmente sustituido.
Normalmente, R5a representa hidrógeno, hidroxi, halógeno o trifluorometilo; o -NRbRc , S(O)2Ra , -ORa u O-(CO)-Rd; o alquilo C1-6, cualquiera de tales grupos puede estar opcionalmente sustituido.
Los ejemplos adecuados de sustituyentes opcionales en R5a incluyen uno, dos o tres sustituyentes seleccionados independientemente entre halógeno, hidroxi, trifluorometilo, alquilo C1-6, alcoxi C1-6, alquilcarbonilo C2-6, alquiloxicarbonilo C2-6, (hidroxi)alquilo C1-6, cicloalquilo (C3-7), alquilsulfonilo C1-6, alquilsulfonil (C1-6)-alquilo (C1-6), dialquilaminocarbonilo (C1-6), oxo y carboxi.
Los ejemplos típicos de sustituyentes particulares en R5a incluyen uno, dos o tres sustituyentes seleccionados independientemente entre flúor, cloro, fluorometilo, fluoroisopropilo, ciano, cianoetilo, nitrometilo, metilo, etilo, isopropilo, isopropilmetilo, trifluorometilo, trifluoroetilo, etenilo, hidroxi, hidroximetilo, hidroxiisopropilo, metoxi, isopropoxi, trifluoroetoxi, carboxiciclobutiloxi, metiltio, metilsulfonilo, metilsulfonilmetilo, metilsulfoniletilo, oxo, amino, aminometilo, aminoisopropilo, metilamino, dimetilamino, metoxietilamino, W-(hidroxietil)-W-(metil)amino, acetilaminometilo, metilsulfonilamino, W-metil-W-(metilsulfonil)amino, bis(metilsulfonil)amino, W-(carboxietil)-W-(metil)amino, carboxiciclopentilamino, carboxiciclopropilmetilamino, formilo, acetilo, acetoxiisopropilo, carboxi, carboximetilo, carboxietilo, metoxicarbonilo, etoxicarbonilo, n-butoxicarbonilo, terc-butoxicarbonilo, metoxicarbonilmetilo, etoxicarbonilmetilo, etoxicarboniletilo, morfoliniletoxicarbonilo, etoxicarbonilmetilidenilo, metilsulfonilaminocarbonilo, acetilaminosulfonilo, metoxiaminocarbonilo, tetrazolilo, tetrazolilmetilo, hidroxioxadiazolilo, aminocarbonilo, aminosulfonilo, metilsulfoximinilo y (metil)(W-metil)sulfoximinilo.
En una primera realización, R5a representa hidrógeno. En una segunda realización, R5a representa hidroxi. En una tercera realización, R5a representa halógeno. En un aspecto de esta realización, R5a representa flúor. En una cuarta realización, R5a representa trifluorometilo. En una quinta realización, R5a representa -NRbRc . En un aspecto de esa realización, R5a representa -NH2. En una sexta realización, R5a representa -NRcC(O)Rd. En una séptima realización, R5a representa -C(O)-NRcRd. En una octava realización, R5a representa -NHS(O)2Re . En una novena realización, R5a representa -S-Ra . En una décima realización, R5a representa -S(O)-Ra . En una decimoprimera realización, R5a representa-S(O)2Ra . En un aspecto particular de esta realización, R5a representa -S(O)2-CH3. En una duodécima realización, R5a representa -S(O)(N-Rd)Ra . En una decimotercera realización, R5a representa -S(O)2(N-Rd). En una decimocuarta realización, R5a representa -ORa . En un aspecto de esta realización, Ra es un alquilo C1-6. En un segundo aspecto de esta realización, Ra es un arilo. En un tercer aspecto de esta realización, Ra es un heteroarilo. En una decimoquinta realización, R5a representa -O-(CO)-Rd. En un aspecto particular de esta realización, R5a representa -O-(CO)-CH3. En una decimosexta realización, -C(O)-ORd. En una decimoséptima realización, R5a representa alquilo C i-6 opcionalmente sustituido. En un aspecto de esa realización, R5a representa alquilo C1-6 sustituido. En un segundo aspecto de esta realización, R5a representa alquilo C1-6 no sustituido. En un aspecto particular de esta realización, R5a representa metilo. En una decimoctava realización, R5a representa un alquinilo C2-6 opcionalmente sustituido. En una decimonovena realización, R5a representa un heteroarilo opcionalmente sustituido.
En una vigésima realización, R5a representa un arilo opcionalmente sustituido. En una vigesimoprimera realización, R5a representa un alquenilo C2-6 opcionalmente sustituido.
En una vigesimosegunda realización, R5a representa ciano.
Normalmente, R5b representa hidrógeno, hidroxi; o alquilo C 1-6 opcionalmente sustituido. alcoxi C1-6, cualquiera de tales grupos puede estar opcionalmente sustituido.
En una primera realización, R5b representa hidrógeno. En una segunda realización, R5b representa hidroxi. En una tercera realización, R5b representa halógeno. En un aspecto de esta realización, R5a representa flúor. En una cuarta realización, R5b representa trifluorometilo. En una quinta realización, R5b representa alquilo C1-6 sustituido o no sustituido. En un aspecto de esa realización, R5b es metilo. En una sexta realización, R5b representa ciano.
Los valores particulares de R5b incluyen hidrógeno y metilo.
En una realización alternativa particular, R5a y R5b, cuando se toman junto con el carbono al que están unidos, representan un carbonilo.
En una segunda realización alternativa particular, R5a y R5b, cuando se toman junto con el carbono al que están unidos, representan un tiocarbonilo.
En una tercera realización alternativa particular, R5a y R5b, cuando se toman junto con el carbono al que están unidos, representan -C=N-OH.
Los valores ilustrativos de R5a incluyen hidrógeno, hidroxi, flúor, trifluorometilo, -N(CH3)2 , -NH(CO)CH3 , -SO2-CH3, -O-(CO)-CH3 , metilo, metoxi, piridinmetiloxi-, benciloxi, (metoxicarbonil)metiloxi-, (etiloxicarbonil)metiloxi-, (terc-butoxicarbonil)metiloxi-, (hidroxicarbonil)metiloxi y cianometiloxi.
Los valores seleccionados de R5a incluyen hidrógeno, hidroxi, flúor, trifluorometilo, -N(CH3)2 , -NH(CO)CH3 , -SO2-CH3, -CO2-CH3, metilo y metoxi.
Los valores seleccionados de R5b incluyen hidrógeno, hidroxi, flúor, trifluorometilo y metilo.
En una realización particular, R5a es como se ha definido anteriormente y R5b representa hidrógeno. En un aspecto particular de esta realización, R5a es hidroxi.
En otra realización particular, R5a es como se ha definido anteriormente y R5b representa alquilo C1-4, preferentemente, metilo. En un aspecto particular de esta realización, R5a es hidroxi.
Un subgrupo particular de los compuestos de fórmula (IIA) anterior se representa mediante los compuestos de fórmula (IIB) y W-óxidos de los mismos, y sales farmacéuticamente aceptables y solvatos de los mismos, y derivados de glucurónido de los mismos, y cocristales de los mismos:
en la que
V representa C-R12 o N;
R9 representa hidrógeno, halógeno, haloalquilo (C1-6), ciano, cianoalquilo (C1-6), nitroalquilo (C1-6), alquilo C1-6, trifluorometilo, trifluoroetilo, alquenilo C2-6, hidroxi, hidroxialquilo (C1-6), alcoxi C1-6, trifluoroetoxi, carboxicicloalquiloxi (C3-7), alquiltio C1-6, alquilsulfonilo C1-6, alquilsulfonil (C1-6)-alquilo (C1-6), oxo, amino, aminoalquilo (C1-6), alquilamino C1-6, dialquilamino (C1-6), alcoxi (C1-6)alquilamino (C1-6), W-[alquil (C1-6)]-W-[hidroxialquil (C1-6)]amino, alquilcarbonilamino (C2-6)-alquilo(C1-6), alquilsulfonilamino C1-6, W-[alquil (C1-e)]-N-[alquilsulfonil (C1-6)]amino, bis[alquilsulfonil (C1-6)]amino, W-[alquil (C1-6)]-W-[carboxialquil (C1-6)]amino, carboxicicloalquil (C3-7)-amino, carboxicicloalquil (C3-7)alquilamino (C1-6), formilo, alquilcarbonilo C2-6, alquil-carboniloxi (C2-6)alquilo (C1-6), carboxi, carboxialquilo (C1-6), alcoxicarbonilo C2-6, alcoxicarbonil C2-6alquilo (C1-6), morfolinil-alcoxicarbonilo (C1-6), alcoxicarbonilmetilidenilo C2-6, aminocarbonilo, dialquilaminocarbonilo (C1-6), aminosulfonilo, alquilsulfoximinilo (C1-6) o [alquil (C1-6)][W-alquil (C1-6)]sulfoximinilo; o R9 representa cicloalquilo C3-7, cicloalquil (C3-7)-alquilo (C1-6), cicloalquenilo (C4-7), bicicloalquilo (C4-9), bicicloalquileno (C4-9), heterocicloalquilo (C3-7), heterocicloalquil (C3-7) alquilo (C1-6), heterocicloalquenilo (C3-7), heterobicicloalquilo (C4-9), espiroheterocicloalquilo (C4-9) o heteroarilo, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes; o R9 representa alquilsulfinilo C1-6, cicloalquilsulfonilo (C3-7) o difluorometilo.
R10 y R11 representan independientemente hidrógeno, halógeno, ciano, trifluorometilo, hidroxi; o -NRbRc, -ORa ; alquilo C1-6 o alquilsulfonilo C1-6.
R12 representa hidrógeno, halógeno o alquilo C1-6; y
Z, Y, R2 , R5a y R5b son como se han definido anteriormente.
A continuación, se exponen realizaciones y aspectos adicionales de los compuestos de fórmula (IIB) desvelados en el presente documento.
En una realización, V representa C-R12. En otra realización, V representa N.
Normalmente, R9 representa hidrógeno, halógeno, haloalquilo (C1-6), ciano, alquilo C1-6, trifluorometilo, alquenilo C2-6, hidroxi, hidroxialquilo (C1-6), alcoxi C1-6, trifluoroetoxi, carboxicicloalquiloxi (C3-7), alquiltio C1-6, alquilsulfonilo C1-6, alquilsulfonil (C1-6)-alquilo (C1-6), amino, alquilamino C1-6, dialquilamino (C1-6), alcoxi (C1-6)alquilamino (C1-6), W-[alquil (C1-6)]-W-[hidroxialquil (C1-6)]-amino, W-[alquil (C1-6)]-W-[carboxialquil (C1-6)]amino, carboxicicloalquilamino (C3-7), carboxicicloalquil (C3-7)alquilamino (C1-6), alquilsulfonilamino C1-6, alquilcarboniloxi (C2-6)alquilo (C1-6), carboxi, morfolinil-alcoxicarbonilo (C1-6), alcoxicarbonil C2-6alquilo (C1-6), alcoxicarbonilmetilidenilo C2-6, dialquilaminocarbonilo (C1-6); o R9 representa cicloalquilo C3-7, cicloalquil (C3-7)-alquilo (C1-6), cicloalquenilo (C4-7), bicicloalquilo (C4-9), heterocicloalquilo (C3-7), heterobicicloalquilo (C4-9), espiroheterocicloalquilo (C4-9), bicicloalquileno (C4-9) o heteroarilo, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes; o R9 representa, aminosulfonilo, alquilsulfinilo C1-6, cicloalquilsulfonilo (C3-7) o difluorometilo.
Normalmente, R9 representa halógeno, hidroxialquilo (C1-6), alquilsulfonilo C1-6, alquilsulfonil (C1-6)-alquilo (C1-6), dialquilaminocarbonilo (C1-6); o R9 representa cicloalquilo C3-7, cicloalquenilo (C4-7), bicicloalquilo (C4-9), heterocicloalquilo (C3-7), heterobicicloalquilo (C4-9) o bicicloalquileno (C4-9), cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes; o R9 representa alcoxi C1-6, aminosulfonilo, alquilsulfinilo C1-6, cicloalquilsulfonilo (C3-7) o difluorometilo. De manera adecuada, R9 representa halógeno, hidroxialquilo (C1-6), alquilsulfonilo C1-6, alquilsulfonil (C1-6)-alquilo (C1-6), dialquilaminocarbonilo (C1-6); o R9 representa cicloalquilo C3-7, cicloalquenilo (C4-7), bicicloalquilo (C4-9), heterocicloalquilo (C3-7), heterobicicloalquilo (C4-9) o bicicloalquileno (C4-9),
cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes.
Cuando R9 representa un grupo cicloalquilo (C3-7) opcionalmente sustituido, los valores típicos incluyen ciclopropilo, ciclobutilo, ciclopentilo, ciclohexilo y cicloheptilo, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes.
Cuando R9 representa un grupo cicloalquil (C3-7)-alquilo (C1-6) opcionalmente sustituido, un valor típico es ciclohexilmetilo, grupo que puede estar opcionalmente sustituido con uno o más sustituyentes.
Cuando R9 representa un grupo cicloalquenilo (C4-7) opcionalmente sustituido, los valores típicos incluyen ciclobutenilo, ciclopentenilo, ciclohexenilo y cicloheptenilo, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes.
Cuando R9 representa un grupo bicicloalquilo (C4-9) opcionalmente sustituido, los valores típicos incluyen biciclo[3.1.0]hexanilo, biciclo[4.1.0]heptanilo y biciclo[2.2.2]octanilo, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes.
Cuando R9 representa un grupo bicicloalquenilo (C4-9) opcionalmente sustituido, un valor típico es biciclo[3.1.0]hexenilo.
Cuando R9 representa un grupo heterocicloalquilo (C3-7) opcionalmente sustituido, los valores típicos incluyen oxetanilo, azetidinilo, tetrahidrofuranilo, pirrolidinilo, tetrahidropiranilo, piperidinilo, piperazinilo, hexahidro-[1.2.5]tiadiazolo[2,3-a]pirazinilo, morfolinilo, tiomorfolinilo, azepanilo, oxazepanilo, diazepanilo, tiadiazepanilo, (imino)(oxo)tiazinanilo, (oxo)tiazinanilo o (dioxo)tiazinanilo, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes.
Cuando R9 representa un grupo heterocicloalquenilo (C3-7) opcionalmente sustituido, un valor típico es 1,2,3,6-tetrahidropiridinilo opcionalmente sustituido o 3,6-dihidropiridina.
Cuando R9 representa un grupo heterobicicloalquilo (C4-9) opcionalmente sustituido, los valores típicos incluyen 3-azabiciclo[3.1.0]hexanilo, 2-oxa-5-azabiciclo[2.2.1]heptanilo, 3-azabiciclo[3.1.1]heptanilo, 3-azabiciclo[4.1.0]heptanilo, 2-oxabiciclo[2.2.2]octanilo, quinuclidinilo, 2-oxa-5-azabiciclo[2.2.2]octanilo, 3-azabiciclo-[3.2.1]octanilo, 8-azabiciclo-[3.2.1] octanilo, 3-oxa-8-azabiciclo[3.2.1]octanilo, 3,8-diazabiciclo[3.2.1]octanilo, 3,6-diazabiciclo[3.2.2]nonanilo, 3-oxa-7-azabiciclo[3.3.1]nonanilo, 3,9-diazabiciclo-[4.2.1]nonanil3,6-epimino[3,2b]-furanilo, 3,7-dioxa-9-diazabiciclo-[3.3.1] nonanilanilheptanilo y 2,5-diazabiciclo-[2.2.1]heptanilo, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes.
Cuando R9 representa un grupo espiroheterocicloalquilo (C4-9) opcionalmente sustituido, los valores típicos incluyen 5-azaespiro[2,3]hexanilo, 5-azaespiro[2,4]heptanilo, 2-azaespiro[3,3]-heptanilo, 2-oxa-6-azaespiro[3,3]heptanilo, 2-oxa-6-azaespiro[3,4]octanilo, 2-oxa-6-azaespiro-[3,5]nonanilo, 2-oxa-7-azaespiro[3,5]nonanilo y 2,4,8-triazaespiro[4,5]-decanilo, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes.
Cuando R9 representa un heteroarilo opcionalmente sustituido, los valores típicos incluyen triazolilo y (metil)triazolilo.
Cuando R9 representa un alquilsulfinilo C1-6, los valores típicos incluyen metilsulfinilo.
Cuando R9 representa cicloalquilsulfonilo (C3-7), los valores típicos incluyen ciclopropilsulfonilo. De manera ilustrativa, R9 representa hidrógeno, isopropilo, isopropilmetilo, hidroxi, hidroximetilo, hidroxiisopropilo, metoxi, carboxiciclobutiloxi, metiltio, metilsulfonilo, metilsulfonilmetilo, metilamino, W-[carboxietil]-W-metilamino, carboxiciclopentilamino, carboxiciclopropilmetilamino o etoxicarboniletilo; o R9 representa ciclopropilo, ciclobutilo, ciclopentilo, ciclohexilo, ciclohexilmetilo, ciclohexenilo, biciclo[3.1.0]hexanilo, biciclo[3.1.0]hexenilo, biciclo[4.1.0]heptanilo, biciclo[2.2.2]-octanilo, oxetanilo, azetidinilo, tetrahidrofuranilo, pirrolidinilo, tetrahidropiranilo, tetrahidro-tiopiranilpirimidinilo, piperidinilo, piperazinilo, hexahidro-[1.2.5]tiadiazolo[2,3-a]pirazinilo, morfolinilo, tiomorfolinilo, azepanilo, oxazepanilo, diazepanilo, tiadiazepanilo, 3-azabiciclo[3.1.0]-hexanilo, 2-oxa-5-azabiciclo[2.2.1]heptanilo, 3-azabiciclo[3.1.1]heptanilo, 3-azabiciclo-[4.1.0]heptanilo, 2-oxabiciclo[2.2.2]octanilo, 3-azabiciclo-[3.2.1]octanilo, 8-azabiciclo-[3.2.1]octanilo, 3-oxa-8-azabiciclo[3.2.1]octanilo, 3,6-diazabiciclo[3.2.2]nonanilo, 3-oxa-7-azabiciclo[3.3.1]nonanilo, 5-azaespiro[2,3]hexanilo, 5-azaespiro[2,4]heptanilo, 2-azaespiro-[3,3]heptanilo, 3,7-dioxa-9-azabiciclo[3.3.1]-nonanilo, epiminofuro [3,2-b]furanilo, (imino)(oxo)tiazinanilo, (oxo)tiazinanilo o (dioxo)tiazinanilo, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes. Además, R9 representa difluorometilo, fluoroisopropilo, aminoisopropilo, aminosulfonilo, terc-butoxi, ciclopropilsulfonilo, metilsulfinilo o metilsulfoximinilo; o 2,5-diazabiciclo-[2.2.1]heptanilo opcionalmente sustituido,
Adecuadamente, R9 representa hidrógeno, ciclopropilo, ciclobutilo, ciclohexilo, metoxi, biciclo[3.1.0]hexanilo, biciclo[3.1.0]hexenilo, tetrahidropiranilo, tiopiranilo, piperazinilo, oxetanilo, azetidinilo, tetrahidrofuranilo, piperidinilo, morfolinilo, tiomorfolinilo, 2-oxa-5-azabiciclo[2.2.1]heptanilo, 3-azabiciclo-[3.2.1]octanilo, 3-oxa-8azabicid o[3.2.1]octanil-pirimidinilo, 3,7-dioxa-9-azabiciclo[3.3.1]-nonanilo, epiminofuro[3,2-b]furanilo; o R9 representa difluorometilo, hidroxiisopropilo, fluoroisopropilo, aminoisopropilo, aminosulfonilo, terc-butoxi, metilsulfonilo, cidopropilmetilsulfonilo, metilsulfinilo o metilsulfoximinilo; o 2,5-diazabicido-[2.2.1]heptanilo opcionalmente sustituido.
Oportunamente, R9 representa hidrógeno, ciclopropilo, ciclobutilo, biciclo[3.1.0]hexanilo, biciclo[3.1.0]hexenilo, tetrahidropiranilo, tiopiranilo, piperazinilo, oxetanilo, azetidinilo, tetrahidrofuranilo, piperidinilo, morfolinilo, tiomorfolinilo, 2-oxa-5-azabiciclo[2.2.1]heptanilo, 3-azabiciclo-[3.2.1]octanilo, 3-oxa-8-azabiciclo[3.2.1]octanil-pirimidinilo, 3,7-dioxa-9-azabiciclo[3.3.1]-nonanilo o epiminofuro [3,2-b]furanilo, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes.
Los ejemplos de sustituyentes opcionales que pueden estar presentes en R9 incluyen uno, dos o tres sustituyentes seleccionados independientemente entre halógeno, haloalquilo (C1-6), ciano, ciano-alquilo (C1-6), nitro, nitroalquilo (C1-6), alquilo C1-6, cicloalquilo C3-7, trifluorometilo, trifluoroetilo, alquenilo C2-6, hidroxi, hidroxialquilo (C1-6), alcoxi C1-6, difluorometoxi, trifluorometoxi, trifluoroetoxi, alquiltio C1-6, alquilsulfonilo C1-6, alquilsulfonil (C1-6)-alquilo (C1-6), oxo, amino, alquilamino C1-6, dialquilamino (C1-6), alquilcarbonilamino C2-6, alquilcarbonilamino (C2-6)-alquilo (C1-6), alcoxicarbonilamino C2-6, alquilsulfonilamino C1-6, formilo, alquilcarbonilo C1-6, carboxi, carboxialquilo (C1-6), alcoxicarbonilo C2-6, morfolinil-alcoxicarbonilo (C1-6), alcoxicarbonil C2-6alquilo (C1-6), alcoxicarbonilmetilidenilo C2-6, amino-carbonilo, alquilaminocarbonilo C1-6, dialquilaminocarbonilo (C1-6), aminosulfonilo, dialquilaminosulfonilo (C1-6), alquilsulfoximinilo (C1-6) y [alquil (C1-6)][N-alquil (C1-6)]-sulfoximinilo.
Los ejemplos seleccionados de sustituyentes opcionales en R9 incluyen uno, dos o tres sustituyentes seleccionados independientemente entre halógeno, ciano, trifluorometilo, hidroxi, alquilo C1-6, cicloalquilo C3-7, alcoxi C1-6, alquilsulfonilo C1-6, alquilsulfoximinilo C1-6, alquilcarbonilo C1-6, alcoxicarbonil C1-6 oxo y carboxi.
Los ejemplos adecuados de sustituyentes particulares en R9 incluyen uno, dos o tres sustituyentes seleccionados independientemente entre flúor, fluorometilo, cloro, bromo, ciano, cianometilo, cianoetilo, nitro, nitrometilo, metilo, etilo, isopropilo, ciclopropilo, trifluorometilo, trifluoroetilo, etenilo, hidroxi, hidroximetilo, metoxi, etoxi, difluorometoxi, trifluorometoxi, trifluoroetoxi, metiltio, metilsulfonilo, metilsulfonilmetilo, metilsulfoniletilo, oxo, amino, metilamino, dimetilamino, acetilamino, acetil-aminometilo, metoxicarbonilamino, etoxicarbonilamino, terc-butoxicarbonilamino, metilsulfonilamino, formilo, acetilo, carboxi, carboximetilo, carboxietilo, metoxicarbonilo, etoxicarbonilo, nbutoxicarbonilo, terc-butoxicarbonilo, morfolinil-etoxicarbonilo, metoxicarbonilmetilo, etoxicarbonilmetilo, etoxicarboniletilo, etoxicarbonilmetilidenilo, acetilaminosulfonilo, metoxiaminocarbonilo, tetrazolilo, tetrazolilmetilo, hidroxioxadiazolilo, aminocarbonilo, metilaminocarbonilo, dimetil-aminocarbonilo, metilsulfonilaminocarbonilo, aminosulfonilo, metilaminosulfonilo, dimetilaminosulfonilo, metilsulfoximinilo y (metil)(N-metil)sulfoximinilo.
Los ejemplos seleccionados de sustituyentes particulares en R9 incluyen uno, dos o tres sustituyentes seleccionados independientemente entre cloro, hidroxi, metilo, isopropilo, trifluorometilo, ferc-butoxicarbonilo, acetilo, oxo y carboxi. Un ejemplo particular de un sustituyente particular en R9 incluye flúor.
Normalmente, R9 representa hidrógeno, flúor, fluoroisopropilo, ciano, metilo, isopropilo, trifluorometilo, etenilo, hidroxi, hidroximetilo, hidroxiisopropilo, metoxi, isopropoxi, trifluoroetoxi, carboxiciclobutiloxi, metiltio, metilsulfonilo, metilsulfonilmetilo, amino, metilamino, dimetilamino, metoxietilamino, W-(hidroxietil)-N-(metil)amino, N-[carboxi-etil]-N-metilamino, carboxiciclopentilamino, carboxiciclopropilmetilamino, metilsulfonilamino, acetoxiisopropilo, carboxi, etoxicarboniletilo, ciclopropilo, fluorometil-ciclopropilo, acetilaminometilciclopropilo, hidroxiciclobutilo, carboxiciclopentilo, carboxiciclohexilo, (carboxi)(metil)ciclohexilo, (carboxi)(hidroxi)ciclohexilo, carboximetilciclohexilo, etoxicarbonilciclohexilo, (metoxicarbonil)(metil)-ciclohexilo, (etoxicarbonil)(metil)ciclohexilo, carboxiciclohexilmetilo, carboxiciclohexenilo, etoxicarbonilciclohexenilo, carboxibiciclo[3.1.0]hexanilo, etoxicarbonilbiciclo[3.1.0]hexanilo, carboxibiciclo[4.1.0]heptanilo, carboxibiciclo-[2.2.2]octanilo, fluorooxetanilo, hidroxioxetanilo, hidroxiazetidinilo, (hidroxi)(metil)-azetidinilo, carboxiazetidinilo, (ferc-butoxicarbonil)(hidroxi)azetidinilo, tetrazolil-azetidinilo, hidroxitetrahidrofuranoílo, pirrolidinilo, hidroxipirrolidinilo, carboxi-pirrolidinilo, (carboxi)(metil)pirrolidinilo, carboximetilpirrolidinilo, etoxicarbonil-pirrolidinilo, fluorotetrahidropiranilo, hidroxitetrahidropiranilo, piperidinilo, difluoropiperidinilo, (ciano)(metil)piperidinilo, (hidroxi)(nitrometil)piperidinilo, (hidroxi)-(metil)piperidinilo, (hidroxi)(trifluorometil)piperidinilo, (hidroximetil)(metil)-p iperidinilo, metilsulfonilpiperidinilo, oxopiperidinilo, (formil)(metil)piperidinilo, acetilpiperidinilo, carboxipiperidinilo, (carboxi)(fluoro)piperidinilo, (carboxi)(metil)-piperidinilo, (carboxi)(etil)piperidinilo, (carboxi)(trifluorometil)piperidinilo, (carboxi)-(hidroxi)piperidinilo, (carboxi)(hidroximetil)piperidinilo, (carboxi)(metoxi)-piperidinilo, (amino)(carboxi)piperidinilo, carboximetilpiperidinilo, metoxicarbonil-piperidinilo, (metoxicarbonil)(metil)piperidinilo, (etil)(metoxicarbonil)piperidinilo, (isopropil)(metoxicarbonil)piperidinilo, (metoxi)(metoxicarbonil}piperidinilo, (carboxi)(metoxicarbonil)piperidinilo, etoxicarbonilpiperidinilo, (etoxicarbonil)-(fluoro)piperidinilo, (etoxicarbonil)(metil)piperidinilo, (etoxicarbonil)(trifluorometil)piperidinilo, (etoxicarbonil)(hidroximetil)piperidinilo, (n-butoxicarbonil)-(metil)piperidinilo, (metil)(morfoliniletoxicarbonil)piperidinilo, etoxicarbonilmetilpiperidinilo, metilsulfonilaminocarbonilpiperidinilo, acetilaminosulfonilpiperidinilo, metoxiaminocarbonilpiperidinilo, tetrazolilpiperidinilo, hidroxioxadiazolilpiperidinilo, aminosulfonilpiperidinilo, piperazinilo, metilpiperazinilo, cianoetilpiperazinilo, trifluoroetil-piperazinilo, metilsulfonilpiperazinilo, metilsulfoniletilpiperazinilo, oxopiperazinilo, acetilpiperazinilo, carboxipiperazinilo, terc-butoxicarbonilpiperazinilo, carboximetilpiperazinilo, carboxietilpiperazinilo, etoxicarbonilmetilpiperazinilo, etoxicarboniletilpiperazinilo, tetrazolilmetilpiperazinilo, trioxohexahidro-[1.2.5]tiadiazolo[2,3-a]pirazinilo, morfolinilo,
dimetilmorfolinilo, hidroximetil-morfolinilo, carboximorfolinilo, (carboxi)(metil)morfolinilo, carboximetil-morfolinilo, tiomorfolinilo, oxotiomorfolinilo, dioxotiomorfolinilo, carboxi-azepanilo, carboxioxazepanilo, oxodiazepanilo, (metil)(oxo)diazepanilo, dioxo-tiadiazepanilo, carboxi-3-azabiciclo[3.1.0]hexanilo, (carboxi)(metil)-3-azabiciclo-[3.1.0]hexanilo, metoxicarbonil-3-azabiciclo[3.1.0]hexanilo, etoxicarbonil-3-azabiciclo[3.1.0]hexanilo, 2-oxa-5-azabiciclo[2.2.1]heptanilo, carboxi-2-oxa-5-azabiciclo[2.2.1]heptanilo, carboxi-3-azabiciclo-[3.1.1]heptanilo, carboxi-3-azabiciclo-[4.1.0]heptanilo, metoxicarbonil-3-azabiciclo[4.1.0]heptanilo, etoxicarbonil-3-azabiciclo[4.1.0]heptanilo, (hidroxi)(metil)(oxo)-2-oxabiciclo[2.2.2]octanilo, carboxi-3-azabiciclo[3.2.1]octanilo, metoxicarbonil-3-azabiciclo[3.2.1]octanilo, oxo-8-azabiciclo[3.2.1]octanilo, etoxicarbonilmetilidenil-8-azabiciclo[3.2.1]octanilo, 3-oxa-8-azabiciclo[3.2.l]octanilo, oxo-3,6-diazabiciclo[3.2.2]nonanilo, carboxi-3-oxa-7-azabiciclo[3.3.1]nonanilo, 3,7-dioxa-9-azabiciclo[3.3.l]nonanilo, carboxi-5-azaespiro[2,3]hexanilo, (carboxi)(metil)-5-azaespiro-[2,3]hexanilo, carboxi-5-azaespiro[2,4]heptanilo, carboxi-2-azaespiro[3,3]heptanilo, 2-oxa-6-azaespiro[3,3]heptanilo, 2-oxa-6-azaespiro[3,4joctanilo, 2-oxa-6-azaespiro[3,5]nonanilo, 2-oxa-7-azaespiro[3,5]nonanilo, (dioxo)(metil)-2,4,8-triazaespiro[4,5]decanilo, 3,6-epiminofuro[3,2-b]furanil-pirimidinilo, (metil)ciclobutildiol, (imino)(oxo)tiazinanilo, (oxo)tiazinanilo o (dioxo)tiazinanilo. Además, R9 representa difluorociclobutanilo, difluorometilo, ferc-butoxi, aminoisopropilo, hidroxiciclopropilo, (difluoro)(hidroxi)ciclobutilo, (metil)ciclobutanodiol, (hidroxil)(metil)ciclohexilo, (metil)ciclohexanodiol, ferc-butoxi, aminosulfonilo, metilsulfinilo, metilsulfoximinilo, ciclopropilsulfonilo, 2,5-diazabiciclo[2.2.1]hetanilo y metilcarboxi-3-azabiciclo[3.2.1]octanilo.
Los valores adecuados de R9 incluyen cloro, tetrahidropiranilo, hidroxiisopropilo, hidroximetilo, metoxi, isopropoxi, isopropilo, hidroxiciclobutilo, carboxibiciclo[3.1.0]hexanilo, carboxibiciclo[3.1.0]hexenilo, piperazinilo, hidroxioxetanilo, hidroxiazetidinilo, (hidroxi)(metil)azetidinilo, (hidroxi)(trifluorometil)azetidinilo, (ferc-butoxicarbonil)(hidroxi)azetidinilo, hidroxitetrahidrofuranoílo, hidroxitetrahidropiranilo, (hidroxi)dioxidotetrahidrotiopiranilo), piperidinilo, (ciano)(metil)piperidinilo, (hidroxi)(metil)piperidinilo, (carboxi)(metil)piperidinilo, acetilpiperidinilo, carboxipiperazinilpirimidinilo, ferc-butoxicarbonilpiperazinilo, morfolinilo, tiomorfolinilo, oxo-tiomorfolinilo, dioxo tiomorfolinilo, oxodiazepanilo, 2-oxa-5-azabiciclo[2.2.1]heptanilo, carboxi-3-azabiciclo[3.2.1]octanilo, oxo-8-azabiciclo[3.2.1]octanilo, 3-carboxi-8-azabiciclo-[3.2.1]octanilo, 3-(dimetilaminocarbonil)-8-azabiciclo-[3.2.1]octanilo, oxo-3,6-diazabiciclo[3.2.2]nonanilo, 3,7-dioxa-9-azabiciclo[3.3.1]-nonanilo y 3,6-epiminofuro [3,2-b]furanilo; o difluorociclobutanilo, difluorometilo, ferc-butoxi, aminoisopropilo, hidroxiciclopropilo, (difluoro)(hidroxi)ciclobutilo, (metil)ciclobutanodiol, (hidroxil)(metil)ciclohexilo, (metil)ciclohexanodiol, aminosulfonilo, metilsulfinilo, metilsulfoximinilo, ciclopropilsulfonilo, 2,5-diazabiciclo[2.2.1]hetanilo y metilcarboxi-3-azabiciclo[3.2.1]octanilo. Los valores ilustrativos de R9 incluyen cloro, tetrahidropiranilo, hidroxiisopropilo, hidroximetilo, metoxi, isopropoxi, isopropilo, hidroxiciclobutilo, carboxibiciclo[3.1.0]hexanilo, carboxibiciclo[3.1.0]hexenilo, piperazinilo, hidroxioxetanilo, hidroxiazetidinilo, (hidroxi)(metil)azetidinilo, (hidroxi)(trifluorometil)azetidinilo, (ferc-butoxicarbonil)(hidroxi)azetidinilo, hidroxitetrahidrofuranoílo, hidroxitetrahidropiranilo, (hidroxi)dioxidotetrahidrotiopiranilo), piperidinilo, (ciano)(metil)piperidinilo, (hidroxi)(metil)piperidinilo, (carboxi)(metil)piperidinilo, acetilpiperidinilo, carboxipiperazinilpirimidinilo, ferc-butoxicarbonilpiperazinilo, morfolinilo, tiomorfolinilo, oxo-tiomorfolinilo, dioxo tiomorfolinilo, oxodiazepanilo, 2-oxa-5-azabiciclo[2.2.1]heptanilo, carboxi-3-azabiciclo[3.2.1]octanilo, oxo-8-azabiciclo[3.2.1]octanilo, 3-carboxi-8-azabiciclo-[3.2.1]octanilo, 3-(dimetilaminocarbonil)-8-azabiciclo-[3.2.1]octanilo, oxo-3,6-diazabiciclo[3.2.2]nonanilo, 3,7-dioxa-9-azabiciclo[3.3.1]-nonanilo y 3,6-epiminofuro [3,2-b]furanilo.
En una realización, R10 representa hidrógeno. En una segunda realización, R10 representa halógeno. En una tercera realización, R10 representa ciano. En una cuarta realización, R10 representa trifluorometilo. En una quinta realización, R10 representa hidroxi. En una sexta realización, R10 representa -NRbRc. En un aspecto de esta realización, R10 representa -NH2. En una séptima realización, R10 representa -ORa. En un aspecto de esa realización, R10 representa metoxi. En una octava realización, R10 representa alquilo C1-6. En un aspecto de esa realización, R10 representa metilo. En una novena realización, R10 representa alquilsulfonilo C1-6. En un aspecto de esa realización, R10 representa metilsulfonilo.
En una realización, R11 representa hidrógeno. En una segunda realización, R11 representa halógeno. En una tercera realización, R11 representa ciano. En una cuarta realización, R11 representa trifluormetilo. En una quinta realización, R11 representa hidroxi. En una sexta realización, R11 representa -NRbRc. En un aspecto de esta realización, R11 representa -NH2. En una séptima realización, R11 representa -ORa. En un aspecto de esa realización, R11 representa metoxi. En una octava realización, R11 representa alquilo C1-6. En un aspecto de esa realización, R11 representa metilo. En una novena realización, R11 representa alquilsulfonilo C1-6. En un aspecto de esa realización, R11 representa metilsulfonilo.
Los valores particulares de R10 y R11 incluyen hidrógeno, metilo y metilsulfonilo.
Los subgrupos particulares de los compuestos de la fórmula (IIB) anterior se representan por los compuestos de fórmula (IIC), (IID), (IIE), (IIF), (IIG), (IIH), (IIJ), (IIK), (IIL), (IIM) y W-óxidos de los mismos, y sales farmacéuticamente aceptables y solvatos de los mismos, y derivados de glucurónido de los mismos, y cocristales de los mismos:
Ċ
en las que
T representa -CH2- o -CH2CH2;
U representa C(O) o S(O)2;
W representa O, S, S(O), S(O)2, N(R14), S(O)(N-Rd) o C(R15)(R16);
-M- representa -CH2-, -CH2CH2- o -CH2-W-CH2-;
Q representa C(R15)(R16);
R13 representa hidrógeno, halógeno, ciano, haloalquilo (C1-6), hidroxi, alcoxi C1-6, alquiltio C1-6, alquilsulfinilo C1-6, alquilsulfonilo C1-6, amino, alquilamino C1-6, dialquil (C1-6)-amino, alquilcarbonilamino (C2-6), alquilcarbonilamino (C2-6)-alquilo(C1-6), alquilsulfonilamino (C1-6) o alquilsulfonilamino (C1-e)alquilo (C1-6);
R14 representa hidrógeno, cianoalquilo (C1-6), alquilo C1-6, trifluorometilo, trifluoroetilo, alquilsulfonilo C1-6, alquilsulfonil (C1-6)-alquilo (C1-6), formilo, alquilcarbonilo C2-6, carboxi, carboxialquilo (C1-6), alcoxicarbonilo C2-6, alcoxicarbonil C2-6alquilo (C1-6), un resto de profármaco o isóstero de ácido carboxílico O como se define en el presente documento, -alquil (C1-6)-O, aminocarbonilo, alquilaminocarbonilo C1-6, dialquilaminocarbonilo (C1-6), aminosulfonilo o dialquilamino (C1-6)-sulfonilo;
R15 representa hidrógeno, halógeno, ciano, hidroxi, hidroxialquilo (C1-6), alquilsulfonilo C1-6, formilo, alquilcarbonilo C2-6, di(alquil C1-6)aminocarbonilo, carboxi, carboxialquilo (C1-6), alcoxicarbonilo C2-6, alcoxicarbonil C2-6alquilo (C1-6), aminosulfonilo, alquil (C1-6)-sulfoximinilo, [alquil (C1-6)][W-alquil (C1-6)]sulfoximinilo, un resto de profármaco o isóstero de ácido carboxílico O como se define en el presente documento o -alquil (C1-6)-O;
R16 representa hidrógeno, halógeno, alquilo C1-6, cicloalquilo C3-7, trifluorometilo, hidroxi, hidroxi-alquilo (C1-6), alcoxi C1-6, amino o carboxi; y
V, Y, Z, R2, R5a, R5b, R10 y R11 son como se han definido anteriormente.
Algunas realizaciones adicionales y aspectos de los compuestos de fórmula (IIC), (IID), (IIE), (IIF), (IIG), (IIH), (IIJ), (IIK), (IIL) y (IIM) se exponen a continuación.
En una realización, T representa -CH2-. En una segunda realización, T representa-CH2CH2;
En una realización, U representa C(O). En otra realización, U representa S(O)2.
En general, W representa O, S(O)2, S(O)(N-Rd), N(R14) o C(R15)(R16).
Normalmente, W representa O, N(R14) o C(R15)(R16).
En una primera realización, W representa O. En una segunda realización, W representa S. En una tercera realización, W representa S(O). En una cuarta realización, W representa S(O)2. En una quinta realización, W representa N(R14). En un aspecto particular de esta realización, W representa -NH. En una sexta realización, W representa C(R15)(R16). En una séptima realización, W representa S(O)(N-Rd). En un aspecto particular de esa realización, W representa S(O)(NH).
En una realización, -M- representa -CH2-. En una segunda realización, -M- representa -CH2CH2-. En una tercera realización, M representa CH2-W-CH2. En un aspecto de esa realización, M representa CH2-O-CH2. En un segundo aspecto de esa realización, M representa CH2-S(O)(N-Rd)-CH2. En un tercer aspecto de esa realización, M representa CH2-S-CH2. En un cuarto aspecto de esa realización, M representa CH2-S(O)-CH2. En un quinto aspecto de esa realización, M representa CH2-S(O)2-CH2. En un sexto aspecto de esa realización, M representa CH2-N(r 14)-CH2. En un séptimo aspecto de esa realización, M representa CH2-C(R15)(R16)-CH2.
En una primera realización, R13 representa hidrógeno. En una segunda realización, R13 representa halógeno. En un aspecto de esa realización, R13 representa flúor. En una tercera realización, R13 representa haloalquilo (C1-6). En un aspecto de esa realización, R13 representa fluorometilo. En otro aspecto de esa realización, R13 representa trifluorometilo. En una cuarta realización, R13 representa hidroxi. En una quinta realización, R13 representa alcoxi C1-6. En un aspecto particular de esa realización, R13 representa metoxi. En una sexta realización, R13 representa alquiltio C1-6. En un aspecto particular de esa realización, R13 representa metiltio. En una séptima realización, R13 representa alquilsulfinilo C1-6. En un aspecto particular de esa realización, R13 representa metilsulfinilo. En una octava realización, R13 representa alquilsulfonilo C1-6. En un aspecto particular de esa realización, R13 representa metilsulfonilo. En una novena realización, R13 representa amino. En una décima realización, R13 representa alquilamino C1-6. En un aspecto particular de esa realización, R13 representa metilamino. En una decimoprimera realización, R13 representa dialquilamino (C1-6). En un aspecto particular de esa realización, R13 representa dimetilamino. En una duodécima
realización, R13 representa alquilcarbonilamino (C2-6). En un aspecto particular de esa realización, R13 representa acetilamino. En una decimotercera realización, R13 representa alquilcarbonilamino (C2-6)alquilo (C1-6). En un aspecto particular de esa realización, R13 representa acetilaminometilo. En una decimocuarta realización, R13 representa alquilsulfonil (C1-6)-amino. En un aspecto particular de esa realización, R13 representa metilsulfonilamino. En una decimoquinta realización, R13 representa alquilsulfonilamino (C1-6)alquilo (C1-6). En un aspecto particular de esa realización, R13 representa metilsulfonilaminometilo. En una decimosexta realización, R13 representa ciano.
Normalmente, R13 representa hidrógeno, halógeno, haloalquilo (C1-6), hidroxi o alquilcarbonilamino (C2-6)alquilo (C1-6). Los valores seleccionados de R13 incluyen hidrógeno, flúor, fluorometilo, hidroxi, metoxi, metiltio, metilsulfinilo, metilsulfonilo, amino, metilamino, dimetilamino y acetilaminometilo.
Los valores particulares de R13 incluyen hidrógeno, flúor, fluorometilo, hidroxi y acetilaminometilo.
Adecuadamente, R13 representa hidrógeno, hidroxi o flúor.
Normalmente, R14 representa hidrógeno, cianoalquilo (C1-6), alquilo C1-6, trifluorometilo, trifluoroetilo, alquilsulfonilo C1-6, alquilsulfonil (C1-6)-alquilo (C1-6), formilo, alquilcarbonilo C2-6, carboxi, carboxialquilo (C1-6), alcoxicarbonilo C2-6, alcoxicarbonil C2-6alquilo (C1-6), tetrazolilalquilo (C1-6), aminocarbonilo, alquilaminocarbonilo C1-6, dialquilaminocarbonilo (C1-6), aminosulfonilo, alquilaminosulfonilo C1-6 o dialquilaminosulfonilo (C1-6).
Adecuadamente, R14 representa hidrógeno, alquilo C1-6 o alquilcarbonilo C2-6.
Los valores típicos de R14 incluyen hidrógeno, cianoetilo, metilo, etilo, isopropilo, trifluorometilo, trifluoroetilo, metilsulfonilo, metilsulfoniletilo, formilo, acetilo, carboxi, carboximetilo, carboxietilo, metoxicarbonilo, etoxicarbonilo, ferc-butoxicarbonilo, etoxicarbonilmetilo, etoxicarboniletilo, tetrazolilmetilo, aminocarbonilo, metilaminocarbonilo, dimetilaminocarbonilo, aminosulfonilo, metilaminosulfonilo y dimetilaminosulfonilo.
Los valores particulares de R14 incluyen hidrógeno, metilo y acetilo.
En una realización particular, R14 representa hidrógeno.
En una realización seleccionada, R14 representa alquilo C1-6.
En otra realización particular más, R14 representa alquilcarbonilo C2-6.
En general, R15 representa halógeno, carboxi, carboxialquilo (C1-6), alcoxicarbonilo C2-6, di(alquil C1-6)aminocarbonilo, alcoxicarbonil C2-6alquilo (C1-6), un resto de profármaco o isóstero de ácido carboxílico O como se define en el presente documento o -alquil (C1-6)-O.
Normalmente, R15 representa hidrógeno, halógeno, ciano, hidroxi, hidroxialquilo (C1-6), alquilsulfonilo C1-6, formilo, carboxi, carboxialquilo (C1-6), alcoxicarbonilo C2-6, alcoxicarbonil C2-6alquilo (C1-6), aminosulfonilo, alquilsulfoximinilo (C1-6), [alquil (C1-6)][N-alquil (C1-6)]sulfoximinilo, alquilsulfonilaminocarbonilo (C1-6), alquilcarbonilaminosulfonilo (C2-6), alcoxiaminocarbonilo (C1-6), tetrazolilo o hidroxioxadiazolilo.
Los valores típicos de R15 incluyen hidrógeno, flúor, ciano, hidroxi, hidroximetilo, metilsulfonilo, formilo, carboxi, carboximetilo, carboxietilo, metoxicarbonilo, etoxicarbonilo, ferc-butoxicarbonilo, metoxicarbonilmetilo, metoxicarboniletilo, etoxicarbonilmetilo, etoxicarboniletilo, aminosulfonilo, metilsulfoximinilo, (metil)(W-metil)sulfoximinilo, metilsulfonilaminocarbonilo, dimetilaminocarbonilo, acetilaminosulfonilo, metoxiaminocarbonilo, tetrazolilo e hidroxioxadiazolilo.
En una realización seleccionada, R15 representa carboxi.
En general, R16 representa hidrógeno, halógeno, cicloalquilo C3-7 o alquilo C1-6.
Adecuadamente, R16 representa hidrógeno o alquilo C1-6.
Los valores seleccionados de R16 incluyen hidrógeno, flúor, metilo, etilo, isopropilo, ciclopropilo, trifluorometilo, hidroxi, hidroximetilo, metoxi, amino y carboxi.
Los valores particulares de R16 incluyen hidrógeno y metilo.
En una primera realización, R16 representa hidrógeno.
En una segunda realización, R16 representa halógeno. En un aspecto de esa realización, R16 representa flúor. En una tercera realización, R16 representa alquilo C1-6. En un primer aspecto de esa realización, R16 representa metilo. En un
segundo aspecto de esa realización, R16 representa etilo. En un tercer aspecto de esa realización, R16 representa isopropilo. En una cuarta realización, R16 representa trifluorometilo. En una quinta realización, R16 representa hidroxi. En una sexta realización, R16 representa hidroxialquilo (C1-6). En un aspecto de esa realización, R16 representa hidroximetilo. En una séptima realización, R16 representa alcoxi C1-6. En un aspecto de esa realización, R16 representa metoxi. En una octava realización, R16 representa amino. En una novena realización, R16 representa carboxi. En una décima realización, R16 representa un cicloalquilo C3-7. En un aspecto de esta realización, R16 representa ciclopropilo.
Una subclase alternativa de compuestos de acuerdo con la divulgación se representa por los compuestos de fórmula (IIN) y W-óxidos de los mismos, y sales y solvatos farmacéuticamente aceptables de los mismos, y derivados de glucurónido de los mismos, y cocristales de los mismos:
Z, R2 , R5a, R5b, R9 , R10 y R11 son como se han definido anteriormente.
A continuación, se exponen aspectos y realizaciones adicionales del compuesto de fórmula (IIN).
En una realización particular de compuestos de fórmula (IIN), Z representa metileno.
En una realización particular de compuestos de fórmula (IIN), Y representa 2-diflurometoxi-fenilo. En otra realización particular de compuestos de fórmula (IIN), Y representa 2-diflurometoxi-5-cloro-fenilo.
En una realización particular de compuestos de fórmula (IIN), R2 representa hidrógeno. En una realización particular de compuestos de fórmula (IIN), R2 representa flúor.
En una realización particular de compuestos de fórmula (IIN), R5a representa hidroxi.
En una realización particular de compuestos de fórmula (IIN), R5b representa hidrógeno.
En una realización particular de compuestos de fórmula (IIN), R9 representa alquilsulfonilo C1-4. En un aspecto particular de esa realización, R9 representa metil sulfonilo. En otra realización particular de compuestos de fórmula (IIN), R9 representa cicloalquilsulfonilo C3-7. En un aspecto particular de esta realización, R9 representa ciclopropilsulfonilo. En una realización particular adicional de un compuesto de fórmula (IIN), R9 representa aminosulfonilo. En otra realización particular adicional de un compuesto de fórmula (IIN), R9 representa metilsulfoximinilo.
En una realización particular de compuestos de fórmula (IIN), R10 representa hidrógeno.
En una realización particular de compuestos de fórmula (IIN), R11 representa hidrógeno.
Una subclase alternativa de compuestos de acuerdo con la divulgación se representa por los compuestos de fórmula (IIP) y W-óxidos de los mismos, y sales y solvatos farmacéuticamente aceptables de los mismos, y derivados de glucurónido de los mismos, y cocristales de los mismos:
W, Z, R2, R5a, R5b y R9 son como se han definido anteriormente.
Los compuestos específicos de acuerdo con la presente divulgación incluyen cada uno de los compuestos cuya
preparación se describe en los Ejemplos adjuntos, y las sales y solvatos farmacéuticamente aceptables de los mismos, y los cocristales de los mismos.
Los compuestos de acuerdo con la presente invención resultan beneficiosos en el tratamiento y/o la prevención de diversas enfermedades humanas. Estas incluyen trastornos autoinmunitarios e inflamatorios; trastornos neurológicos y neurodegenerativos; trastornos del dolor y nociceptivos; trastornos cardiovasculares; trastornos metabólicos; trastornos oculares; y trastornos oncológicos.
Los trastornos inflamatorios y autoinmunitarios incluyen trastornos autoinmunitarios sistémicos, trastornos endocrinos autoinmunitarios y trastornos autoinmunitarios específicos de órgano. Los trastornos autoinmunitarios sistémicos incluyen lupus eritematoso sistémico (LES), psoriasis, artropatía psoriásica, vasculitis, polimiositis, esclerodermia, esclerosis múltiple, esclerosis sistémica, espondilitis anquilosante, artritis reumatoide, artritis inflamatoria no específica, artritis inflamatoria juvenil, artritis idiopática juvenil (incluidas sus formas oligoarticulares y poliarticulares), anemia de enfermedad crónica (AEC), enfermedad de Still (de aparición juvenil y/o en adultos), enfermedad de Behpet y síndrome de Sjogren. Los trastornos endocrinos autoinmunitarios incluyen tiroiditis. Los trastornos autoinmunes específicos de órganos incluyen enfermedad de Addison, anemia hemolítica o perniciosa, lesión de riñón aguda (LRA; incluyendo LRA inducida por cisplatino), nefropatía diabética (ND), uropatía obstructiva (incluyendo uropatía obstructiva inducida por cisplatino), glomerulonefritis (incluyendo síndrome de Goodpasture, glomerulonefritis mediada por inmunocomplejos y anticuerpos citoplasmáticos antineutrófilos (glomerulonefritis asociada a ANCA), nefritis lúpica (NL), enfermedad de cambio mínimo, enfermedad de Graves, púrpura trombocitopénica idiopática, enfermedad inflamatoria intestinal (incluyendo enfermedad de Crohn), colitis ulcerosa, colitis indeterminada y reservoritis), pénfigo, dermatitis atópica, hepatitis autoinmunitaria, cirrosis biliar primaria, neumonitis autoinmunitaria, carditis autoinmunitaria, miastenia grave, infertilidad espontánea, osteoporosis, osteopenia, enfermedad ósea erosiva, condritis, degeneración y/o destrucción de cartílago, trastornos fibrosantes (incluyendo diversas formas de fibrosis hepática y pulmonar), asma, rinitis, enfermedad pulmonar obstructiva crónica (EPOC), síndrome de dificultad respiratoria, septicemia, fiebre, distrofia muscular (incluyendo distrofia muscular de Duchenne) y rechazo de trasplante de órganos (incluyendo rechazo de aloinjerto de riñón).
Los trastornos neurológicos y neurodegenerativos incluyen enfermedad de Alzheimer, enfermedad de Parkinson, enfermedad de Huntington, isquemia, ictus, esclerosis lateral amiotrófica, lesión de la médula espinal, traumatismo craneal, convulsiones y epilepsia.
Los trastornos cardiovasculares incluyen trombosis, hipertrofia cardíaca, hipertensión, contractilidad irregular del corazón (por ejemplo, durante insuficiencia cardíaca) y trastornos sexuales (incluyendo disfunción eréctil y disfunción sexual femenina). Los moduladores de la función de TNFa también pueden usarse en el tratamiento y/o la prevención de infarto de miocardio (véase J.J. Wu et al., JAMA, 2013, 309, 2043-2044).
Los trastornos metabólicos incluyen diabetes (incluyendo diabetes mellitus insulinodependiente y diabetes juvenil), dislipidemia y síndrome metabólico.
Los trastornos oculares incluyen retinopatía (incluyendo retinopatía diabética, retinopatía proliferativa, retinopatía no proliferativa y retinopatía del prematuro), edema macular (incluyendo edema macular diabético), degeneración macular relacionada con la edad (DMRE), vascularización (incluyendo vascularización corneana y neovascularización), oclusión de la vena retiniana y diversas formas de uveítis y queratitis.
Los trastornos oncológicos, que pueden ser agudos o crónicos, incluyen trastornos proliferativos, especialmente cáncer y complicaciones asociadas al cáncer (incluyendo complicaciones esqueléticas, caquexia y anemia). Las categorías particulares del cáncer incluyen neoplasia maligna hemática (incluyendo leucemia y linfoma) y neoplasia maligna no hemática (incluyendo cáncer de tumor sólido, sarcoma, meningioma, glioblastoma multiforme, neuroblastoma, melanoma, carcinoma gástrico y carcinoma de células renales). La leucemia crónica puede ser mieloide o linfoide. Las variedades de leucemia incluyen leucemia linfoblástica de linfocitos T, leucemia mielógena crónica (LMC), leucemia linfocítica/linfoide crónica (LLC), tricoleucemia, leucemia linfoblástica aguda (LLA), leucemia mielógena aguda (LMA), síndrome mielodisplásico, leucemia neutrófila crónica, leucemia linfoblástica aguda de linfocitos T, plasmacitoma, leucemia inmunoblástica de células grandes, leucemia de células del manto, mieloma múltiple, leucemia megacarioblástica aguda, leucemia megacariocítica aguda, leucemia promielocítica y eritroleucemia. Las variedades de linfoma incluyen linfoma maligno, linfoma de Hodgkin, linfoma no de Hodgkin, linfoma linfoblástico de linfocitos T, linfoma de Burkitt, linfoma folicular, linfoma MALT1 y linfoma de zona marginal. Las variedades de neoplasia maligna no hemática incluyen cáncer de próstata, pulmón, mama, recto, colon, ganglio linfático, vejiga, riñón, páncreas, hígado, ovario, útero, cuello del útero, cerebro, piel, hueso, estómago y músculo. También pueden usarse moduladores de la función del TNFa para aumentar la seguridad del efecto antineoplásico potente del TNF (véase F.V. Hauwermeiren et al., J. Clin. Invest., 2013, 123, 2590-2603).
La presente invención también proporciona una composición farmacéutica que comprende un compuesto de acuerdo con la invención como se ha descrito anteriormente o una sal o solvato farmacéuticamente aceptable del mismo, en asociación con uno o más vehículos farmacéuticamente aceptables.
Las composiciones farmacéuticas de acuerdo con la invención pueden adoptar una forma adecuada para la administración oral, bucal, parenteral, nasal, tópica, oftálmica o rectal, o una forma adecuada para la administración por inhalación o insuflación.
Para la administración oral, las composiciones farmacéuticas pueden adoptar la forma de, por ejemplo, comprimidos, pastillas para chupar o cápsulas preparados por medios convencionales con excipientes farmacéuticamente aceptables, tales como agentes aglutinantes (por ejemplo, almidón de maíz pregelatinizado, polivinilpirrolidona o hidroxipropil metil celulosa); cargas (por ejemplo, lactosa, celulosa microcristalina o hidrógeno fosfato de calcio); lubricantes (por ejemplo, estearato de magnesio, talco o sílice); disgregantes (por ejemplo, almidón de patata o glicolato sódico); o agentes humectantes (por ejemplo, laurilsulfato sódico). Los comprimidos pueden recubrirse mediante métodos bien conocidos en la técnica. Las preparaciones líquidas para la administración oral pueden adoptar la forma de, por ejemplo, soluciones, jarabes o suspensiones, o pueden presentarse en forma de un producto seco para su constitución con agua u otro vehículo adecuado antes de su uso. Dichas preparaciones líquidas pueden prepararse por medios convencionales con aditivos farmacéuticamente aceptables, tales como agentes de suspensión, agentes emulsionantes, vehículos no acuosos o conservantes. Las preparaciones también pueden contener sales tamponantes, agentes aromatizantes, agentes colorantes o agentes edulcorantes, según sea adecuado.
Las preparaciones para la administración oral pueden formularse de manera adecuada para proporcionar una liberación controlada del compuesto activo.
Para la administración bucal, las composiciones pueden adoptar la forma de comprimidos o grageas formulados de manera convencional.
Los compuestos de fórmula (I) pueden formularse para la administración parenteral mediante inyección, por ejemplo, mediante inyección o infusión en embolada. Las formulaciones para inyección pueden presentarse en forma de dosificación unitaria, por ejemplo, en ampollas de vidrio o recipientes de múltiples dosis, por ejemplo, viales de vidrio. Las composiciones para inyección pueden adoptar formas, tales como suspensiones, soluciones o emulsiones en vehículos oleosos o acuosos y pueden comprender agentes de formulación, tales como agentes de suspensión, estabilizantes, conservantes y/o dispersantes. Como alternativa, el principio activo puede encontrarse en forma de polvo para su constitución con un vehículo adecuado, por ejemplo, agua estéril apirógena, antes de su uso.
Además de las formulaciones descritas anteriormente, los compuestos de fórmula (I) también pueden formularse como una preparación de depósito. Dichas formulaciones de acción prolongada pueden administrarse mediante implante o mediante inyección intramuscular.
Para la administración nasal o la administración mediante inhalación, los compuestos de acuerdo con la presente invención pueden administrarse convenientemente en forma de una presentación de pulverización en aerosol en envases presurizados o un nebulizador, con el uso de un propulsor adecuado, por ejemplo, diclorodifluorometano, fluorotriclorometano, diclorotetrafluoroetano, dióxido de carbono u otro gas o mezcla de gases adecuados.
Las composiciones pueden, si se desea, presentarse en un envase o dispositivo dosificador que puede contener una o más formas de dosificación unitarias que contienen el principio activo. El envase o dispositivo dosificador puede acompañarse de instrucciones para la administración.
Para la administración tópica, los compuestos de uso en la presente invención pueden formularse convenientemente en una pomada adecuada que contiene el componente activo suspendido o disuelto en uno o más vehículos farmacéuticamente aceptables. Los vehículos particulares incluyen, por ejemplo, aceite mineral, vaselina, propilenglicol, polioxietileno, polioxipropileno, cera emulsionante y agua. Como alternativa, los compuestos de uso en la presente invención pueden formularse en una loción adecuada que contiene el componente activo suspendido o disuelto en uno o más vehículos farmacéuticamente aceptables. Los vehículos particulares incluyen, por ejemplo, aceite mineral, monoestearato de sorbitán, polisorbato 6 0 , cera de ésteres cetílicos, alcohol cetearílico, alcohol bencílico, 2-octildodecanol y agua.
Para administración oftálmica, los compuestos de uso en la presente invención pueden formularse convenientemente como suspensiones micronizadas en isotónicas, solución salina estéril de pH ajustado, con o sin un conservante tal como un agente bactericida o fungicida, por ejemplo, nitrato fenilmercúrico, cloruro de bencilalconio o acetato de clorhexidina. Como alternativa, para la administración oftálmica, los compuestos pueden formularse en una pomada, tal como vaselina.
Para la administración rectal, los compuestos de uso en la presente invención pueden formularse convenientemente como supositorios. Estos pueden prepararse mediante la mezcla del componente activo con un excipiente no irritante adecuado que sea sólido a temperatura ambiente, pero líquido a temperatura rectal y, por tanto, se derretirá en el recto para liberar el componente activo. Dichos materiales incluyen, por ejemplo, manteca de cacao, cera de abeja y polietilenglicoles.
La cantidad de un compuesto de uso en la invención requerida para la profilaxis o el tratamiento de una afección particular variará dependiendo del compuesto elegido y la afección del paciente para tratar. En general, sin embargo, las dosificaciones diarias pueden variar de aproximadamente 10 ng/kg a 1.000 mg/kg, normalmente de 100 ng/kg a 100 mg/kg, por ejemplo, de aproximadamente 0,01 mg/kg a 40 mg/kg de peso corporal, para la administración oral o bucal, de aproximadamente 10 ng/kg a 50 mg/kg de peso corporal para la administración parenteral y de aproximadamente 0,05 mg a aproximadamente 1.000 mg, por ejemplo, de aproximadamente 0,5 mg a aproximadamente 1.000 mg para la administración nasal o administración mediante inhalación o insuflación.
Si se desea, un compuesto de acuerdo con la presente invención puede coadministrarse con otro agente farmacéuticamente activo, por ejemplo, una molécula antiinflamatoria, tal como metotrexato o prednisolona.
Será evidente para el experto en la materia que existen diversas rutas sintéticas que pueden llevar a los compuestos de acuerdo con la invención. Los siguientes procesos tienen como objetivo ilustrar algunas de estas rutas sintéticas, pero no deben interpretarse de ninguna manera como una limitación de cómo se deben preparar los compuestos de acuerdo con la invención.
Los compuestos de fórmula (I) anterior pueden prepararse por un proceso que comprende hacer reaccionar un compuesto de fórmula (III) con un compuesto de fórmula (IV), para proporcionar un compuesto de fórmula (VI):
en la que Y, Rd, R1, R2 , R3 y R4 son como se han definido anteriormente. L1 representa un grupo saliente adecuado. E representa -CH2-Y o hidrógeno.
El grupo saliente L1 es normalmente un átomo de halógeno, por ejemplo, bromo.
La reacción se efectúa convenientemente a temperatura elevada en un disolvente adecuado, por ejemplo un alcanol C1-4, tal como etanol, o un éter, tal como 1,4-dioxano o dimetoxietano, y en presencia de sulfato de magnesio.
Como alternativa, los intermedios de fórmula (V), como se ha definido aquí anteriormente, pueden prepararse de acuerdo con un proceso que comprende hacer reaccionar un intermedio de fórmula (VII), en la que; Rd, R1, R2 , R3 y R4 son como se han definido anteriormente, con un compuesto de fórmula H-(CO)-Y, en la que Y es como se ha definido anteriormente, en presencia de un ácido de Meldrum.
La reacción se realiza conveniente en un disolvente adecuado, por ejemplo acetonitrilo, en presencia de L-prolina y sulfato de magnesio, a temperatura elevada, por ejemplo 80 °C.
Los intermedios de fórmula (VII), en la que R1 es halógeno, pueden prepararse a partir de intermedios de fórmula (VIII), en la que R1, R2, R3 y R4 son como se definen para el intermedio de fórmula (VII) anterior, por reacción con el intermedio de fórmula (IX), en la que, L1 y Rd son como se definen para el intermedio (IV) anterior.
Las condiciones de reacción son análogas a las utilizadas aquí anteriormente para la reacción entre el intermedio (III) y el intermedio (IV). El compuesto de fórmula (V), en la que E es hidrógeno, es decir, el intermedio (VII), puede transformarse adicionalmente en compuestos de fórmula (V), en la que E es -(CO)-H, por ejemplo por tratamiento con cloruro de fosforilo en un disolvente adecuado, por ejemplo, dimetilformamida.
Esta reacción se realiza convenientemente a temperatura elevada en un disolvente adecuado, por ejemplo, dimetilformamida.
El compuesto de fórmula (V), en la que E es -(CO)-H puede transformarse en el compuesto de fórmula (V), en la que E es -CH(OH)-Y, por ejemplo por tratamiento con Y-MgX en un disolvente adecuado, por ejemplo THF. Típicamente, X es halógeno, por ejemplo bromo o cloro.
El compuesto de fórmula (V), en la que E es -CH(OH)-Y puede transformarse, por ejemplo en el compuesto de fórmula (V), en la que E es -CH(C1)-Y por reacción con cloruro de sulfonilo en un disolvente adecuado, por ejemplo diclorometano.
El compuesto de fórmula (V), en la que E es -CH(C1)-Y puede transformarse en el compuesto de fórmula (VI), en la que Y, Q1, Rd, R1, R2 , R3 y R4 son como se han definido anteriormente, por ejemplo en una reacción de tres etapas que incluye (i) reacción con Q1-CH2-L2 en el que Q1 es, por ejemplo, un alcoxicarbonilo C2-6 y L2 es un grupo saliente adecuado, por ejemplo alcoxicarbonilo C2-6, en presencia de una base, por ejemplo hidruro sódico, en un disolvente adecuado, por ejemplo THF, (ii) descarbalcoxilación por tratamiento con un ácido, por ejemplo HCl, a temperatura elevada y (iii) reacción posterior con cloruro de sulfonilo, en un disolvente adecuado, tal como alcanol C1-4, adecuadamente metanol.
Como alternativa, el compuesto de fórmula (V), en la que E es hidrógeno, es decir, el intermedio (VII), puede transformarse en el compuesto de fórmula (V), en la que E es un halógeno, por ejemplo yodo o bromo, por ejemplo, por tratamiento con la N-halo-succinimida correspondiente, N-bromo o N-yodo -succinimida en presencia de un ácido, por ejemplo ácido acético.
El compuesto de fórmula (V), en la que E es halógeno puede transformarse adicionalmente en el compuesto de fórmula (V), en la que E es -CH(OH)-Y, por reacción, por ejemplo, con Y-(CO)H en presencia de una sal de alquilmagnesio, por ejemplo cloruro de isopropilmagnesio, en un disolvente adecuado, por ejemplo THF.
El compuesto de fórmula (V) anterior, en la que E es -CH2-Y, puede transformarse en el compuesto (VI) anterior por reacción con Q1-CH2-L3. Q1 representa un alcoxicarbonilo C2-6 y L3 un grupo saliente adecuado.
L3 es típicamente un halógeno, por ejemplo bromo.
Q1 es típicamente metoxicarbonilo o etilcarbonilo.
Esta reacción se realiza convenientemente en un disolvente adecuado, por ejemplo THF, en presencia de bis(trimetilsilil)amida potásica.
El compuesto de fórmula (VI) puede ciclarse adicionalmente, proporcionando el compuesto de fórmula (I) en la que R5a y R5b, junto con el átomo de carbono al que están unidos, forman un carbonilo y Z es CH-Q1 y Q1 es como se ha definido anteriormente. Dicha reacción se realiza típicamente en un disolvente adecuado, por ejemplo THF en presencia de una base, por ejemplo ferc-butóxido potásico.
El compuesto de fórmula (I) en la que Z es CH-Q1 puede transformarse en compuesto de fórmula (I) en la que Z es -CH2- por ejemplo por tratamiento con un ácido, por ejemplo HCl, a temperatura elevada.
Cuando no están disponibles en el mercado, los compuestos de fórmula (III) y (IV) y otros materiales de partida mencionados anteriormente en el presente documento pueden prepararse por métodos análogos a los descritos en los Ejemplos u otros métodos conocidos para los expertos en la materia.
Se entenderá que cualquier compuesto de fórmula (I) obtenido inicialmente a partir de cualquiera de los procesos anteriores puede, cuando sea adecuado, elaborarse a continuación en un compuesto adicional de fórmula (I) por técnicas conocidas en la materia.
Las referencias a un compuesto de fórmula (I) posterior se entenderán como que incluyen todas las subclases y subgrupos potenciales mencionados aquí anteriormente.
Un compuesto de fórmula (I) que contiene un grupo carbonilo, en particular un compuesto de fórmula (I) en la que R5a y R5b con el átomo de carbono al que están unidos forman un carbonilo, puede transformarse en el compuesto correspondiente en el que R5a es un grupo hidroxi y R5b es un hidrógeno, usando, por ejemplo, borohidruro de litio-trisec-butilo o borohidruro sódico en un disolvente adecuado, por ejemplo THF.
Un compuesto de fórmula (I) que contiene un grupo carbonilo, en particular un compuesto de fórmula (I) en la que R5a y R5b con el átomo de carbono al que están unidos forman un carbonilo, puede transformarse en el compuesto correspondiente en el que R5a es un trifluorometilo y R5b es un hidroxi por tratamiento con trifluormetilsilano a temperatura ambiente, en un disolvente adecuado, por ejemplo dimetoxietano.
Un compuesto de fórmula (I) que contiene un grupo carbonilo, en particular un compuesto de fórmula (I) en la que R5a y R5b con el átomo de carbono al que están unidos forman un carbonilo, puede transformarse en el compuesto correspondiente en el que R5a es un (alquil C1-6)sulfonilariloxi trifluorometilo y R5b es un hidrógeno, por tratamiento con (alquil C1-6)sulfonilfenol, en presencia de €-1,2-diazenodicarboxilato de disiopropilo, en un disolvente adecuado, por ejemplo THF.
Un compuesto de fórmula (I) que contiene un grupo carbonilo, en particular un compuesto de fórmula (I) en la que R5a y R5b, con el átomo de carbono al que están unidos, forman un carbonilo puede transformarse en el compuesto correspondiente en el que R5a y R5b, junto con el carbono al que están unidos, forman un -C=N-OH, por tratamiento, por ejemplo con cloruro de hidroxilamina, en presencia de piridina, en presencia de un disolvente adecuado, tal como etanol.
Un compuesto de fórmula (I) que contiene un grupo hidroxi, en particular un compuesto de fórmula (I) en la que R5a es un grupo hidroxi y R5b es un hidrógeno, puede transformarse en el compuesto correspondiente, en el que R5a y R5b son hidrógeno, por ejemplo por tratamiento con yodotrimetilsilano en un disolvente adecuado, por ejemplo acetonitrilo.
Un compuesto de fórmula (I) que contiene un grupo hidroxi, en particular un compuesto de fórmula (I) en la que R5a es un grupo hidroxi y R5b es un hidrógeno, puede transformarse en una reacción de dos etapas en el compuesto correspondiente en el que R5a es -NH2 y R5b es hidrógeno, por ejemplo por (i) tratamiento con difenilfosforilazida y 1,8-diazabiciclo[5.4.0]undec-7-eno. Esta reacción se realiza convenientemente a 0 °C en THF; (ii) aza-reacción de Wittig posterior usando PPh3 en un disolvente adecuado, por ejemplo una mezcla de agua y tolueno.
Un compuesto de fórmula (I) que contiene un grupo hidroxi, en particular un compuesto de fórmula (I) en la que R5a es un grupo hidroxi y R5b es un hidrógeno, puede transformarse en el compuesto correspondiente en el que R5a es -F y R5b es hidrógeno por tratamiento con trifluoruro de dietilaminoazufre en un disolvente adecuado, por ejemplo THF.
Un compuesto de fórmula (I) que contiene un grupo hidroxi, en particular un compuesto de fórmula (I) en la que R5a es un grupo hidroxi y R5b es un hidrógeno, puede transformarse en el compuesto correspondiente de fórmula (I), en la que R5a es un alquilo C1-4, por ejemplo metilo, y R5b es un hidrógeno, por tratamiento, por ejemplo con un bromuro de alquilmagnesio, en un disolvente adecuado, por ejemplo éter dietílico.
Un compuesto de fórmula (I) que contiene un grupo hidroxi, en particular un compuesto de fórmula (I), en la que R5a es un grupo hidroxi y R5b es un hidrógeno, puede transformarse en el compuesto correspondiente en el que R5a es un alcoxi C1-4, por ejemplo metoxi, y R5b es un hidrógeno, por tratamiento con una base, por ejemplo hidruro sódico, en
un disolvente adecuado, por ejemplo THF, en presencia de un agente de alquilación adecuado, tal como un haluro de alquilo, por ejemplo yoduro de metilo.
Un compuesto de fórmula (I), en la que R5a es un grupo hidroxi, puede convertirse en el compuesto correspondiente de fórmula (I), en la que R5a es ORa y Ra es un alquilo sustituido con un grupo alcoxicarbonilo, por tratamiento con una base, por ejemplo hidruro sódico, y adición del haluro de alcoxicarbonilalquilo correspondiente, en un disolvente adecuado, por ejemplo tetrahidrofurano. Será evidente que puede realizarse una reacción similar para la conversión de un compuesto de fórmula (I), en la que R5a es un grupo hidroxi, en el compuesto correspondiente de fórmula (I), en la que R5a es ORa y Ra es un bencilo o un grupo heteroarilalquilo.
Un compuesto de fórmula (I) que contiene un grupo hidroxi puede alquilarse por tratamiento con el haluro de alquilo adecuado en presencia de una base, por ejemplo, hidruro sódico u óxido de plata. Un compuesto de fórmula (I) que contiene hidroxi puede convertirse en el compuesto sustituido con flúor correspondiente por tratamiento con trifluoruro de dietilaminoazufre (DAST) o trifluoruro de bis(2-metoxietil)aminoazufre (BAST). Un compuesto de fórmula (I) que contiene hidroxi puede convertirse en el compuesto sustituido con diflúor correspondiente a través de un procedimiento de dos etapas que comprende: (i) el tratamiento con un agente de oxidación, por ejemplo, dióxido de manganeso; y (ii) el tratamiento del compuesto que contiene carbonilo obtenido de este modo con DASt .
Un compuesto de fórmula (I) que contiene un resto N-H puede alquilarse mediante el tratamiento con el haluro de alquilo adecuado, normalmente a una temperatura elevada en un disolvente orgánico, tal como acetonitrilo; o a temperatura ambiente en presencia de una base, por ejemplo un carbonato de metal alcalino, tal como carbonato potásico o carbonato de cesio, en un disolvente adecuado, por ejemplo un disolvente aprótico dipolar, tal como N,N-dimetilformamida. Como alternativa, un compuesto de fórmula (I) que contiene un resto N-H puede alquilarse por tratamiento con el tosilato de alquilo adecuado en presencia de una base, por ejemplo, una base inorgánica, tal como hidruro sódico, o una base orgánica, tal como 1,8-diazabiciclo[5.4.0]undec-7-eno (DBU).
Un compuesto de fórmula (I) que contiene un resto N-H puede metilarse mediante tratamiento con formaldehído en presencia de un agente reductor, por ejemplo, triacetoxiborohidruro sódico.
Un compuesto de fórmula (I) que contiene un resto N-H puede acilarse mediante el tratamiento con el cloruro de ácido adecuado, por ejemplo, cloruro de acetilo, o con el anhidro de ácido carboxílico adecuado, por ejemplo, anhídrido acético, normalmente a temperatura ambiente en presencia de una base, por ejemplo, una base orgánica, tal como trietilamina.
Un compuesto de fórmula (I) que contiene un resto N-H puede convertirse en el compuesto correspondiente en el que el átomo de nitrógeno se sustituye por alquilsulfonilo C1-6, por ejemplo, metilsulfonilo, por tratamiento con el cloruro de alquilsulfonilo C1-6 adecuado, por ejemplo, cloruro de metanosulfonilo, o con el anhídrido de ácido alquilsulfónico C1-6 adecuado, por ejemplo, anhídrido metanosulfónico, normalmente a temperatura ambiente en presencia de una base, por ejemplo, una base orgánica, tal como trietilamina o N,N-diisopropiletilamina.
Un compuesto de fórmula (I) sustituido con amino (-NH2) puede convertirse en el compuesto correspondiente sustituido con alquilsulfonilamino C1-6, por ejemplo metilsulfonilamino o bis[alquilsulfonil (C1-6)]amino, por ejemplo, bis(metilsulfonil)amino, por tratamiento con el haluro de alquilsulfonilo C1-6 adecuado, por ejemplo un cloruro de alquilsulfonilo C1-6, tal como cloruro de metanosulfonilo. De manera similar, un compuesto de fórmula (I) sustituido con hidroxi (-OH) puede convertirse en el compuesto correspondiente sustituido con alquilsulfoniloxi C1-6, por ejemplo, metilsulfoniloxi, por tratamiento con el haluro de alquilsulfonilo C1-6 adecuado, por ejemplo un cloruro de alquilsulfonilo C1-6, tal como cloruro de metanosulfonilo.
Un compuesto de fórmula (I) que contiene el resto -S- puede convertirse en el compuesto correspondiente que contiene el resto -S(O)- por tratamiento con ácido 3-cloroperoxibenzoico. De forma análoga, un compuesto de fórmula (I) que contiene el resto -S(O)- puede convertirse en el compuesto correspondiente que contiene el resto -S(O)2- por tratamiento con ácido 3-cloroperoxibenzoico. Como alternativa, un compuesto de fórmula (I) que contiene el resto -S-puede convertirse en el compuesto correspondiente que contiene el resto -S(O)2- por tratamiento con Oxona® (peroximonosulfato potásico).
Un compuesto de fórmula (I) que contiene un átomo de nitrógeno aromático puede convertirse en el derivado de N-óxido correspondiente por tratamiento con ácido 3-cloroperoxibenzoico.
Un compuesto de fórmula (I) que contiene un carbonilo puede convertirse en el alcohol correspondiente por tratamiento con un borohidruro adecuado, por ejemplo borohidruro de litio-tri-sec-butilo o borohidruro sódico, en un disolvente adecuado, por ejemplo THF.
Un derivado de bromofenilo de fórmula (I) puede convertirse en el derivado de 2-oxopirrolidin-1-ilfenilo o 2-oxooxazolidin-3-ilfenilo opcionalmente sustituido correspondiente por tratamiento con pirrolidin-2-ona u oxazolidin-2-ona, o un análogo adecuadamente sustituido de las mismas. La reacción se efectúa convenientemente a una temperatura elevada en presencia de yoduro de cobre(I), frans-N,N'-dimetilc¡clohexano-1,2-d¡am¡na y una base
inorgánica tal como carbonato potásico.
Un compuesto de fórmula (I) en la que R1 representa halógeno, por ejemplo bromo, puede convertirse en el compuesto correspondiente en el que R1 representa un resto arilo o heteroarilo opcionalmente sustituido mediante tratamiento con el ácido aril o heteroaril borónico adecuadamente sustituido o un éster cíclico del mismo formado con un diol orgánico, por ejemplo pinacol, 1,3-propanodiol o neopentilglicol. La reacción se efectúa normalmente en presencia de un catalizador de metal de transición, por ejemplo [1,1'-bis(difenilfosfino)ferroceno]dicloropaladio (II), tetraquis(trifenilfosfina)paladio (0) o complejo de bis[3-(difenilfosfanil)ciclopenta-2,4-dien-1-il]hierro-dicloropaladiodiclorometano, y una base, por ejemplo, una base inorgánica, tal como carbonato sódico o carbonato potásico o fosfato potásico. Esta reacción puede realizarse convenientemente en 1,4-dioxano con o sin el uso de tecnología de microondas.
Un compuesto de fórmula (I) en la que R1 representa halógeno, por ejemplo bromo, puede convertirse en el compuesto correspondiente en el que R1 representa un arilo opcionalmente sustituido, heteroarilo o resto heterocicloalquenilo mediante un procedimiento de dos etapas que comprende: (i) reacción con bis(pinacolato)diboro o bis(glicolato de neopentilo)diboro; y (ii) reacción del compuesto obtenido de este modo con un derivado de arilo, heteroarilo o heterocicloalquenilo sustituido con halo o tosiloxi adecuadamente funcionalizado. La etapa (i) se efectúa convenientemente en presencia de un catalizador de metal de transición, tal como [1,1'-bis-(difenilfosfino)ferroceno]dicloropaladio (II) o complejo de bis[3-(difenilfosfanil)-ciclopenta-2,4-dien-1-il]hierrodicloropaladio-diclorometano. La etapa (ii) se efectúa convenientemente en presencia de un catalizador de metal de transición, tal como tetraquis-(trifenilfosfina)paladio (0) o complejo de bis[3-(difenilfosfanil)ciclopenta-2,4-dien-1-il]hierro-dicloropaladio-diclorometano, y una base, por ejemplo una base inorgánica, tal como carbonato sódico o carbonato potásico.
Un compuesto de fórmula (I) en la que R1 representa halógeno, por ejemplo bromo, puede convertirse en el compuesto correspondiente en el que R1 representa una piridin-2(1H)-ona opcionalmente sustituida, mediante un procedimiento de dos etapas que comprende: (i) reacción con la 4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)piridina opcionalmente sustituida correspondiente, en un disolvente adecuado, por ejemplo 1,4-dioxano, en presencia de una base inorgánica, por ejemplo carbonato sódico, y (ii) adición de (tris)(bencilidenoacetona)dipaladio (0) y tetrafluoroborato de tri-tercbutilfosfonio. La reacción se efectúa conveniente a una alta temperatura en un horno microondas.
Un compuesto de fórmula (I) en la que R1 representa halógeno, por ejemplo bromo, puede convertirse en el compuesto correspondiente en el que R1 representa un resto alquinilo C2-6 opcionalmente sustituido por tratamiento con un derivado de alquilo adecuadamente sustituido, por ejemplo, 2-hidroxibut-3-ina. La reacción se completa convenientemente con la ayuda de un catalizador de metal de transición, por ejemplo tetraquis(trifenilfosfina)paladio (0), típicamente en presencia de yoduro de cobre (I) y una base, por ejemplo, una base orgánica, tal como trietilamina.
Un compuesto de fórmula (I) en la que R1 representa halógeno, por ejemplo bromo, puede convertirse en el compuesto correspondiente en el que R1 representa un resto imidazol-1-ilo opcionalmente sustituido por tratamiento con el derivado de imidazol adecuadamente sustituido, típicamente en presencia de acetato de cobre (II), y una base orgánica, tal como N,N,N',N-tetrametiletilenodiamina (TMEDA).
Un compuesto de fórmula (I) en la que R1 representa halógeno, por ejemplo bromo, puede convertirse en el compuesto correspondiente, en el que R1 representa 2-(metoxicarbonil)-etilo mediante un procedimiento de dos etapas que comprende: (i) la reacción con acrilato de metilo; y (ii) hidrogenación catalítica del derivado de alquenilo obtenido de este modo, normalmente por tratamiento con un catalizador de hidrogenación, por ejemplo, paladio sobre carbón vegetal, en una atmósfera de gas de hidrógeno. La etapa (i) se efectúa normalmente en presencia de un catalizador de metal de transición, por ejemplo acetato de paladio (II) o bis(dibencilidenoacetona)paladio (0), y un reactivo, tal como tri(orto-tolil)fosfina.
En general, un compuesto de fórmula (I) que contiene una funcionalidad -C=C- puede convertirse en el compuesto correspondiente que contiene una funcionalidad -CH-CH- mediante hidrogenación catalítica, normalmente por tratamiento con un catalizador de hidrogenación, por ejemplo, paladio sobre carbón vegetal, en una atmósfera de gas de hidrógeno, opcionalmente en presencia de una base, por ejemplo un hidróxido de metal alcalino, tal como hidróxido sódico.
Un compuesto de fórmula (I) en la que R1 representa 6-metoxipiridin-3-ilo puede convertirse en el compuesto correspondiente en el que R1 representa 2-oxo-1,2-dihidro-piridin-5-ilo por tratamiento con clorhidrato de piridina; o calentando con un ácido mineral, tal como ácido clorhídrico. Mediante la utilización de una metodología similar, un compuesto de fórmula (I) en la que R1 representa 6-metoxi-4-metilpiridin-3-ilo puede convertirse en el compuesto correspondiente en el que R1 representa 4-metil-2-oxo-1,2-dihidropiridin-5-ilo; y un compuesto de fórmula (I), en la que R1 representa 6-metoxi-5-metilpiridin-3-il puede convertirse en el compuesto correspondiente en el que R1 representa 3-metil-2-oxo-1,2-dihidropiridin-5-ilo.
Un compuesto de fórmula (I), en la que R1 representa 2-oxo-1,2-dihidropiridin-5-il puede convertirse en el compuesto correspondiente en el que R1 representa 2-oxopiperidin-5-ilo mediante hidrogenación catalítica, típicamente por
tratamiento con hidrógeno gaseoso en presencia de un catalizador de hidrogenación, tal como óxido de platino (IV).
Un compuesto de fórmula (I), en la que R1 representa 2-metoxi-3-metil-piridin-ilo puede convertirse en el compuesto correspondiente en el que R1 representa 3-metil-piridin-2(H)-ona por tratamiento con yoduro sódico y etil eterato trifluoruro de boro en acetonitrilo.
Un compuesto de fórmula (I) que contiene un resto éster, por ejemplo un grupo alcoxicarbonilo C2-6, tal como metoxicarbonilo o etoxicarbonilo, puede convertirse en el compuesto correspondiente que contiene un resto carboxi (-CO2H) por tratamiento con un ácido, por ejemplo un ácido mineral, tal como ácido clorhídrico.
Un compuesto de fórmula (I) que contiene un resto W-(ferc-butoxicarbonilo) puede convertirse en el compuesto correspondiente que contiene un resto N-H mediante el tratamiento con un ácido, por ejemplo un ácido mineral, tal como ácido clorhídrico, o un ácido orgánico, tal como ácido trifluoroacético. Un compuesto de fórmula (I) que contiene un resto éster, por ejemplo un grupo alcoxicarbonilo C2-6, tal como metoxicarbonilo o etoxicarbonilo, como alternativa, puede convertirse en el compuesto correspondiente que contiene un resto carboxi (-CO2H) por tratamiento con una base, por ejemplo, un hidróxido de metal alcalino seleccionado de hidróxido de litio, hidróxido sódico e hidróxido potásico; o una base orgánica, tal como metóxido sódico o etóxido sódico.
Un compuesto de fórmula (I) que contiene un resto carboxi (-CO2H) puede convertirse en el compuesto correspondiente que contiene un resto amida por tratamiento con la amina adecuada en presencia de un agente de condensación, tal como 1-etil-3-(3-dimetilaminopropil)carbodiimida.
Un compuesto de fórmula (I) que contiene un resto carbonilo (C=O) puede convertirse en el compuesto correspondiente que contiene un resto -C(CH3)(OH)- por tratamiento con bromuro de metilmagnesio. De manera similar, un compuesto de fórmula (I) que contiene un resto carbonilo (C=O) puede convertirse en el compuesto correspondiente que contiene un resto -C(CF3)(OH)- mediante tratamiento con (trifluorometil)trimetilsilano y fluoruro de cesio. Un compuesto de fórmula (I) que contiene un resto carbonilo (C=O) puede convertirse en el compuesto correspondiente que contiene un resto -C(CH2NO2)(OH)- mediante tratamiento con nitrometano.
Un compuesto de fórmula (I) que contiene un resto hidroximetilo puede convertirse en el compuesto correspondiente que contiene un resto formilo (-CHO) mediante tratamiento con un agente de oxidación, tal como peryodinano de Dess-Martin. Un compuesto de fórmula (I) que contiene un resto hidroximetilo puede convertirse en el compuesto correspondiente que contiene un resto carboxi mediante tratamiento con un agente de oxidación, tal como perrutenato de tetrapropilamonio.
Un compuesto de fórmula (I), en la que R1 representa un sustituyente que contiene al menos un átomo de nitrógeno, dicho sustituyente está unido al resto de la molécula mediante un átomo de nitrógeno, puede prepararse haciendo reaccionar un compuesto de fórmula (I) en la que R1 representa halógeno, por ejemplo bromo, con el compuesto adecuado de fórmula R1-H [por ejemplo, 1 -(piridin-3-il)piperazina o morfolina]. La reacción se efectúa convenientemente con la ayuda de un catalizador de metal de transición, por ejemplo tris(dibencilidenoacetona)dipaladio(0), en presencia de un ligando de aminación, tal como 2-diciclohexilfosfino-2',4',6'-triisopropilbifenilo (XPhos) o 2,2'-bis(difenilfosfino)-1,1'-binaftaleno (BINAP) y una base, por ejemplo una base inorgánica, tal como ferc-butóxido sódico. Como alternativa, la reacción puede efectuarse utilizando diacetato de paladio, en presencia de un reactivo, tal como [2',6'-bis(propan-2-iloxi)bifenil-2-il](diciclohexil)fosfano y una base, por ejemplo, una base inorgánica, tal como carbonato de cesio.
Un compuesto de fórmula (I) que contiene un resto oxo puede convertirse en el compuesto correspondiente que contiene un resto etoxicarbonilmetilideno por tratamiento con fosfonoacetato de trietilo en presencia de una base, tal como hidruro sódico.
Los compuestos de fórmula (IIB), (IIN) o (IIP), en las que R9 representa etenilo pueden prepararse haciendo reaccionar un compuesto de (IIB), (IIN) o (IIP), en las que R9 representa halógeno, por ejemplo cloro, con vinil trifluoroborato potásico. La reacción se efectúa normalmente en presencia de un catalizador de metal de transición, por ejemplo [1,1'-bis(difenilfosfino)ferroceno]dicloropaladio (II), y una base, por ejemplo, una base orgánica, tal como trietilamina.
Un compuesto de fórmula (IIB), (IIN) o (IIP), en las que R9 representa halógeno, por ejemplo cloro, puede convertirse en el compuesto correspondiente en el que R9 representa un resto cicloalquenilo C4-7 opcionalmente sustituido mediante tratamiento con el ácido cicloalquenil borónico adecuadamente sustituido o un éster cíclico del mismo formado con un diol orgánico, por ejemplo pinacol, 1,3-propanodiol o neopentilglicol. La reacción se efectúa normalmente en presencia de un catalizador de metal de transición, por ejemplo, complejo de bis[3-(difenilfosfanil)ciclopenta-2,4-dien-1-il]hierro-dicloropaladio-diclorometano, y una base, por ejemplo, una base inorgánica, tal como carbonato potásico.
Un compuesto de fórmula (IIB), (IIN) o (IIP), en las que R9 representa un sustituyente que contiene al menos un átomo de nitrógeno, dicho sustituyente está unido al resto de la molécula mediante un átomo de nitrógeno, puede prepararse haciendo reaccionar un compuesto de fórmula (IIB), (IIN) o (IIP), en las que R9 representa halógeno, por ejemplo cloro,
con el compuesto adecuado de fórmula R9-H [por ejemplo 2-metoxietilamina, W-metil-L-alanina, ácido 2-aminociclopentanocarboxílico, ácido 3-aminociclopentanocarboxílico, ácido 1-(aminometil)ciclopropanocarboxílico, azetidin-3-carboxilato de metilo, pirrolidin-3-ol, ácido pirrolidin-3-carboxílico, ácido piperidin-2-carboxílico, ácido piperidin-3-carboxílico, 4-(1H-tetrazol-5-il)piperidina, piperazina, 1-(metilsulfonil)piperazina, piperazin-2-ona, ácido 2-(piperazin-1-il)propanoico, morfolina, ácido morfolin-2-carboxílico, tiomorfolina, 1,1-dióxido de tiomorfolina, 1,4-diazepan-5-ona, 2-oxa-5-azabiciclo[2.2.1]heptano o un azaespiroalcano adecuadamente sustituido], opcionalmente en presencia de una base, por ejemplo una base orgánica, tal como trietilamina o W,W-diisopropiletilamina y/o 1-metil-2-pirrolidinona o piridina, o una base inorgánica, tal como carbonato potásico.
Será evidente para el experto en la materia que la síntesis de compuestos de fórmula (I) con grupos R1 y R9 específicos o con sustituyentes específicos, síntesis que no se ha detallado aquí anteriormente, puede prepararse de acuerdo con los protocolos específicos descritos aquí más adelante en los Ejemplos.
Cuando se obtiene una mezcla de productos a partir de cualquiera de los procesos descritos anteriormente para la preparación de compuestos de acuerdo con la invención, el producto deseado puede separarse de la misma en cualquier etapa adecuada por métodos convencionales, tales como HPLC preparativa; o cromatografía en columna utilizando, por ejemplo, sílice y/o alúmina junto con un sistema de disolventes adecuado.
Cuando los procesos descritos anteriormente para la preparación de los compuestos de acuerdo con la invención dan lugar a mezclas de estereoisómeros, estos isómeros pueden separarse mediante técnicas convencionales. En particular, cuando se desea obtener un enantiómero particular de un compuesto de fórmula (I), este puede producirse a partir de una mezcla de enantiómeros correspondiente usando cualquier procedimiento convencional adecuado para resolver enantiómeros. Por tanto, por ejemplo, los derivados diastereoméricos, por ejemplo, las sales, pueden producirse mediante la reacción de una mezcla de enantiómeros de fórmula (I), por ejemplo, un racemato y un compuesto quiral adecuado, por ejemplo, una base quiral. Después, los diastereómeros pueden separarse mediante cualquier medio conveniente, por ejemplo mediante cristalización, y el enantiómero puede recuperarse, por ejemplo, por tratamiento con un ácido en el caso donde el diastereómero es una sal. En otro proceso de resolución, un racemato de fórmula (I) puede separarse usando HPLC quiral. Además, si se desea, puede obtenerse un enantiómero particular mediante el uso de un producto intermedio quiral adecuado en uno de los procesos descritos anteriormente. Como alternativa, puede obtenerse un enantiómero particular realizando una biotransformación enzimática enantioespecífica, por ejemplo, una hidrólisis de éster usando una esterasa y, después, mediante la purificación de únicamente el ácido hidrolizado enantioméricamente puro del antípodo de éster sin reaccionar. La cromatografía, la recristalización y otros procedimientos de separación convencionales también pueden usarse con intermedios o productos finales donde se desee obtener un isómero geométrico particular de la invención.
Durante cualquiera de las secuencias de síntesis anteriores, puede resultar necesario y/o deseable proteger grupos sensibles o reactivos en cualquiera de las moléculas implicadas. Esto puede conseguirse por medio de grupos protectores convencionales, tales como los descritos en Protective Groups in Organic Chemistry, ed. J. F. W. McOmie, Plenum Press, 1973; y T.W. Greene y P.G.M. Wuts, Protective Groups in Organic Synthesis, John Wiley & Sons, 3a edición, 1999. Los grupos protectores pueden retirarse en cualquier fase posterior conveniente utilizando métodos conocidos de la técnica.
Los siguientes Ejemplos ilustran la preparación de los compuestos de acuerdo con la invención.
Los compuestos de acuerdo con la presente invención inhiben potentemente el enlace de un conjugado de fluorescencia a TNFa cuando se someten a ensayo en el ensayo de polarización de fluorescencia que se describe a continuación. Además, determinados compuestos de acuerdo con la presente invención inhiben potentemente la activación de NF-kB inducida por TNFa en la prueba de genes indicadores descrita más adelante.
Ensayo de polarización de fluorescencia
Preparación del Compuesto (A)
Puede prepararse 1-(2,5-dimetilbencil)-6-[4-(piperazin-1-ilmetil)fenil]-2-(piridin-4-il-metil)-1H-benzoimidazol - en lo sucesivo denominado "Compuesto (A)" - por el procedimiento descrito en el Ejemplo 499 del documento WO 2013/186229 (publicado el 19 de diciembre de 2013); o mediante un procedimiento análogo al mismo.
Preparación del conjugado de fluorescencia
El Compuesto (A) (27,02 mg, 0,0538 mmol) se disolvió en DMSO (2 ml). Se disolvió éster de succinimilo de 5(-6)carboxi-fluoresceína (24,16 mg, 0,0510 mmol) (número de catálogo de Invitrogen: C1311) en DMSO (1 ml) para dar una solución de color amarillo brillante. Las dos soluciones se mezclaron a temperatura ambiente, volviéndose la mezcla de color rojo. La mezcla se agitó a temperatura ambiente. Poco después de mezclar, se retiró una alícuota de 20 |jl y se diluyó en una mezcla 80:20 de AcOH:H2O para análisis de CL-EM en el sistema de CL-EM 1200RR-6140. El cromatograma mostró dos picos de elusión cercanos en los tiempos de retención de 1,42 y 1,50 minutos, ambos con una masa (M+H)+ = 860,8 uma, que correspondían a los dos productos formados con el grupo carboxifluoresceína
5- y 6 -sustituida. Un pico adicional en el tiempo de retención de 2,21 minutos tenía una masa de (M+H)+ = 502,8 uma, correspondiente al Compuesto (A). No se observó ningún pico para el éster de succinimilo de 5(-6)carboxifluoresceína. Las áreas de pico fueron del 22,0 %, 39,6 % y 31,4 % para las tres señales, lo que indicaba una conversión del 61,6 % en los dos isómeros del conjugado de fluorescencia deseado en ese punto de tiempo. Se extrajeron alícuotas de 20 j l adicionales después de varias horas y, a continuación, después de agitar durante una noche, se diluyeron como anteriormente y se sometieron a análisis de CL-EM. El porcentaje de conversión se determinó que era del 79,8 % y el 88 ,6 %, respectivamente, en estos puntos temporales. La mezcla se purificó en un sistema de HPLC preparativa dirigido por UV. Las fracciones purificadas agrupadas se liofilizaron para retirar el exceso de disolvente. Después de la liofilización, se recuperó un sólido de color naranja (23,3 mg), equivalente a 0,027 mmol de conjugado de fluorescencia, que correspondía a un rendimiento global del 53 % para la reacción y la purificación por HPLC preparativa.
Inhibición del enlace de conjugados de fluorescencia a TNFa
Los compuestos se sometieron a ensayo a 10 concentraciones partiendo de 25 □M en una concentración de ensayo final de DMSO al 5 %, mediante la incubación previa con TNF^ durante 60 minutos a temperatura ambiente en Tris 20 mM, NaCl 150 mM, Tween 20 al 0,05 %, antes de la adición del conjugado de fluorescencia y una incubación adicional durante 20 horas a temperatura ambiente. Las concentraciones finales de TNF^ y el conjugado de fluorescencia fueron 10 nM y 10 nM, respectivamente en un volumen de ensayo total de 25 □l. Las placas se leyeron en un lector de placas capaz de detectar la polarización de fluorescencia (por ejemplo, un lector de placas Analyst HT; o un lector de placas Envision). Se calculó un valor de CI50 usando XLfit™ (modelo logístico de 4 parámetros) en ActivityBase.
Cuando se sometieron a ensayo en el ensayo de polarización de fluorescencia, se halló que todos los compuestos de los Ejemplos adjuntos presentaban valores de CI50 de 50 jM o mejores.
Ensayo de genes indicadores
Inhibición de la activación de NF-kB inducida por TNFa
La estimulación de células HEK-293 mediante TNFa lleva a la activación de la vía de NF-kB. La estirpe celular indicadora usada para determinar la actividad de TNFa se adquirió a través de InvivoGen. HEK-Blue™ CD40L es una estirpe celular transfectada con HEK-293 estable que expresa SEAP (fosfatasa alcalina embrionaria secretada) con el control del promotor mínimo de IFNp condensado con cinco sitios de enlace a NF-kB. La secreción de SEAP mediante estas células se estimula de una manera dependiente de la dos mediante TNFa, con una CE50 de 0,5 ng/ml para TNFa humano. Los compuestos se diluyeron de soluciones madre de DMSO 10 mM (concentración final de ensayo de DMSO al 0,3 %) para generar una curva de dilución seriada 3 veces de 10 puntos (por ejemplo., concentración final 30.000 nM a 2 nM). El compuesto diluido se incubó previamente con TNFa durante 60 minutos antes de la adición a una placa de microtitulación de 384 pocillos y se incubó durante 18 h. La concentración final de TNFa en la placa de prueba fue de 0,5 ng/ml. La actividad SEAP se determinó en el sobrenadante utilizando un sustrato colorimétrico QUANTI-Blue™ o medio de detección HEK-Blue™ (InvivoGen). El porcentaje de inhibiciones para las diluciones de compuestos se calculó entre un control DMSO y una inhibición máxima (por exceso de compuesto de control) y un valor de CI50 calculado usando XLfit ™ (modelo logístico de 4 parámetros) en ActivityBase.
Cuando se sometieron a ensayo en el ensayo de genes indicadores, se descubrió que determinados compuestos de los Ejemplos adjuntos presentaban valores de CI50 de 50 jM o mejores.
Ejemplos
Cualquier ejemplo que no se encuentre dentro de las reivindicaciones se incluye con fines de referencia.
Nomenclatura
Los compuestos se nombraron con la ayuda de ACD/Name Batch (Network) ver. 12.0 o Accelyrs Draw 4.0
Abreviaturas
DCM: Diclorometano EtOAc: Acetato de etilo
DMF: N,N-Dimetilformamida MeOH: Metanol
DMSO: Dimetilsulfóxido SiO2 : Sílice
Et2O: Éter dietílico h: Hora
THF: Tetrahidrofurano AcOH: Ácido acético
t.a.: Temperatura ambiente TR: tiempo de retención a.: Ancho M: Masa
Salmuera: Solución acuosa saturada de cloruro sódico
HPLC: Cromatografía líquida de alto rendimiento
CLEM: Cromatografía líquida-espectrometría de masas
EN+: Ionización por electronebulización positiva
TEA: Trietilamina
DEA: Dietilamina
DIPEA: W,W-di-/so-propiletilamina
DIAD: (E)-1,2-Diazenodicarboxilato de diisopropilo
sa.: singlete ancho
Boc2O: Dicarbonato de di-terc butilo
DME dimetoxi etano
TLC cromatografía de capa fina
sat. Saturado
ac. Acuoso
KHMDS: Bis(trimetilsilil)amida potásica
TBAF: Fluoruro de tetra-n-butilamonio
MeCN: Acetonitrilo
Dppf: 1,1'-Bis(difenilfosfino)ferroceno
EtOH: Etanol
SFC: Cromatografía de fluidos supercríticos
IPA alcohol isopropílico
BAST: trifluoruro de bis(2-metoxietil)aminoazufre (BAST).
DAST: trifluoruro de dietilaminoazufre
La solución de amoniaco metanólico se prepara mezclando 100 ml de una solución acuosa al 37 % p/p de NH4OH en 900 ml de MeOH.
Todas las reacciones que implican reactivos sensibles al aire o la humedad se realizaron en una atmósfera de nitrógeno usando disolventes secados y materiales de vidrio.
Condiciones analíticas
Todas las RMN se obtuvieron a 300 MHz o 400 MHz.
Método 1:
Waters Acquity-SQD, Waters Acquity UPLC BEH C18, 2,1 x 50 mm, columna de 1,7 pm
Fase móvil A: Formiato de amonio 10 mM 0,1 % de amoniaco
Fase móvil B: 95 % de MeCN 5 % de H2O 0,1 % de amoniaco
Programa de gradiente (Caudal 1,0 ml/min, Temperatura de columna 40 °C):
Tiempo % de A % de B
0 ,00 95 5
0,50 95 5
1,75 5 95
2 ,00 5 95
2,25 95 5
Método 1b:
Waters Acquity-SDS, Waters Acquity BEH C18, 2,1 x 50 mm, columna de 1,7 pm
Fase móvil A: agua 0,5 % de ácido fórmico
Fase móvil B: MeCN 0,035 % de ácido fórmico
Programa de gradiente (Caudal 0,9 ml/min, temperatura de columna 55 °C):
Tiempo % de A % de B
0 ,00 95 5
2 ,00 5 95
2,60 5 95
2,70 95 5
3,00 95 5
Método 2: La HPLC preparativa para todos los compuestos para los que se requirió se realizó a pH 2,5 usando una columna Luna C18, 21,2 mm, 5 mm.
Fase móvil A: 99,92 % de agua y 0,08 % de ácido fórmico.
Fase móvil B: 99,92 % de MeCN y 0,08 % de ácido fórmico.
Programa de gradiente (caudal 25 ml/min), temperatura de la columna: ambiente, gradiente variable.
Método 2b:
Columna: Merck Purosphere® STAR-RP18; 25 mm x 250 mm, 10 p a temperatura ambiente
Eluyente: ACN:H2O 0,05 % de TFA (caudal 25 ml/min)
Gradiente: 5:95 (0 min) ^ 95:5 (45 min),
Método 2c:
Columna: Agilent Prep C-18, 21,2 mm x250 mm, 10 p a temperatura ambiente
Eluyente: ACN:H2O (caudal 40 ml/min)
Gradiente: 3:97 (0 min) ^ 90:10 (12,5 min) ^ 90:10 (15 min)
Método 2d:
Columna: Agilent Prep C-18, 30 mm x250 mm, 10 p a temperatura ambiente
Eluyente: ACN:H2O (caudal 75 ml/min)
Gradiente: 10:90 (0 min) ^ 90:10 (12,5 min) ^ 90:10 (15 min)
Método 2e:
Columna: Merck Purosphere® STAR-RP18; 25 mm x 250 mm, 10 p a temperatura ambiente
Eluyente: ACN:H2O 0,05 % de TFA (caudal 25 ml/min)
Gradiente: 10:90 (0 min) ^ 90:10 (45 min),
Método 2f:
Columna: Agilent Prep C-18, 21,2 mm x250 mm, 10 p a temperatura ambiente
Eluyente: ACN:H2O (caudal 40 ml/min)
Gradiente: 10:90 (0 min) ^ 90:10 (12,5 min) ^ 90:10 (15 min)
Será evidente para un experto en la materia que pueden obtenerse tiempos de retención diferentes (TR) para CLEM si se utilizan condiciones analíticas diferentes.
INTERMEDIO 1
4-[2-(d¡fluorometox¡)fen¡l1-2-oxobut-3-enoato de (E)-etilo
Una suspensión de 2-(difluorometoxi)benzaldehído (295 g, 1,714 mmol) y (trifenilfosforanilideno)piruvato de etilo (279,1 g, 742 mmol) se calentó a 100 °C. El aldehido de color rojo oscuro se decoloró inmediatamente y se obtuvo una suspensión de color amarillo, que cambió lentamente a una solución de color pardo oscuro. Se añadió 2-(difluorometoxi)benzaldehído (52,5 g, 305 mmol) a la mezcla de reacción. El aldehido residual se separó de la mezcla de reacción mediante destilación. La mezcla resultante se agitó en heptano (500 ml) y Et2O (500 ml). El precipitado sólido de color pardo se retiró por filtración y se lavó con una mezcla 1:1 de heptano y Et2O (3 x 250 ml). El filtrado se concentró, produciendo un aceite de color pardo (218,5 g). La purificación por cromatografía en columna ultrarrápida (SiO2, EtoAc al 2-20 % en heptano) dio el compuesto del título (91 g) en forma de un aceite de color amarillo. 1H (CDCl3, 300 MHz) 88,13 (d, J 16,3 Hz, 1H), 7,75 (dt, J 7,8, 1,6 Hz, 1H), 7,46 (dt, J 7,8, 1,7 Hz, 1H), 7,38 (d, J 16,3 Hz, 1H), 7,28 (t a, J 7,6 Hz, 1H), 7,20 (dd, J 7,3, 1,0 Hz, 1H), 6,59 (t, J 72,9 Hz, 1H), 4,40 (c, J 7,1 Hz, 2H), 1,42 (t, J 7,1 Hz, 3H). CLEM (EN+) 271 (M+H)+.
INTERMEDIO 2
4-r2-(Difluorometoxi)fenil1-2-r(trietilsilil)oxi1but-2-enoato de etilo
A una solución enjuagada con nitrógeno del Intermedio 1 (50 g, 185 mmol) en DCM (500 ml) se añadió dímero de acetato de rodio (II) (0,818 g, 1,85 mmol) y trietilsilano (35,5 ml, 25,8 g, 222 mmol). La mezcla resultante se agitó a reflujo. Se añadieron más trietilsilano (10 ml, 7,28 g, 62,6 mmol) y dímero de acetato de rodio (II) (0,2 g, 0,453 mmol) después de 4 h. Se continuó calentando a reflujo durante 15 h. La mezcla de reacción se enfrió a t.a. y se filtró sobre un lecho apretado de Kieselguhr. El material resultante se aclaró con DCM y se concentró al vacío para producir el compuesto del título (61 g) en forma de un aceite de color amarillo transparente que se empleó en etapas posteriores sin purificación adicional. mezcla 4:1 de isómeros E/Z. Isómero principal: 1H (CDCb, 300 MHz) 87,33 - 7,02 (m, 4H), 6,51 (t, J 74,1 Hz, 1H), 6,11 (t, J 7,4 Hz, 1H), 4,21 (c, J 7,1 Hz, 2H), 3,57 (d, J 7,4 Hz, 2H), 1,30 (t, J 7,1 Hz, 3H), 1,07 - 0,91 (m, 9H), 0,83 - 0,64 (m, 6H). Isómero menor: 1H (CDCla, 300 MHz) 87,33 - 7,02 (m, 4H), 6,51 (t, J 74,1 Hz, 1H), 5,58 (t, J 8,0 Hz, 1H), 4,25 (c, J 7,1 Hz, 2H), 3,86 (d, J 8,0 Hz, 2H), 1,30 (t, J 7,1 Hz, 3H), 1,07 - 0,91 (m, 9H), 0,83
0,64 (m, 6H).
INTERMEDIO 3
3-Bromo-4-f2-(d¡fluorometoxi)fen¡l1-2-oxobutanoato de etilo
A una solución agitada del Intermedio 2 (69 g, 179 mmol) en THF (700 ml) a t.a. se añadió W-bromosuccimida (35,0 g, 196 mmol). La mezcla resultante se agitó a la temperatura de reflujo durante 2 h antes de enfriarse a t.a. La mezcla de reacción se concentró a aproximadamente un tercio de su volumen original. Se añadió DCM (500 ml) y la mezcla resultante se lavó con una solución ac. sat. de bicarbonato sódico (700 ml), después se extrajo con DCM (250 ml), se secó sobre sulfato sódico y se concentró al vacío, para producir un aceite en bruto de color amarillo (97 g). Después de almacenamiento durante una noche a t.a. en una atmósfera de nitrógeno, el producto se había solidificado parcialmente. El material resultante se trituró en éter diisopropílico (300 ml) durante 1 h a t.a. El precipitado se retiró mediante filtración. El filtrado se concentró al vacío,, produciendo un aceite transparente de color amarillo-pardo (88 g). La purificación por cromatografía en columna (SO 2, EtOAc al 2-20 % en heptano) proporcionó el compuesto del título (58,3 g) en forma de un aceite de color pardo claro. 1H (CDCb , 300 MHz) 87,33-7,26 (m, 2H). 7,19-7,09 (m, 2H), 6,58 (t, J 73,5 Hz, 1H), 5,37 (dd, J 7,8, 7,1 Hz, 1H), 4,36 (c, J 7,1 Hz, 2H), 3,55 (dd, J 14,5, 7,1 Hz, 1H), 3,32 (dd, J 14,5, 7,8 Hz, 1H), 1,38 (t, J 7,1 Hz, 3H). CLEM (EN+) 271 (M-Br)+.
INTERMEDIO 4
6-Bromo-3-[[[2-(d¡fluorometox¡)fen¡l1met¡l1¡m¡dazo[1.2-a1p¡r¡d¡n-2-carbox¡lato de etilo
Se suspendieron 5-bromop¡r¡d¡n-2-am¡na (43,5 g, 251,0 mmol), el Intermedio 3 (40,0 g, 140 mmol) y sulfato de magnesio (50,0 g, 419,0 mmol) en 1,4-dioxano (1 l) y se calentó a 60 °C durante 18 h. La reacción se enfrió y los sólidos se retiraron por filtración y se lavaron con EtOAc. El filtrado se concentró, se redisolvió en EtOAc y se lavó con una solución sat. de bicarbonato sódico. La capa orgánica se lavó con salmuera, se secó sobre sulfato sódico y se concentró al vacío para proporcionar un aceite de color pardo. El aceite se trituró con Et2O durante 1 h, se retiró por filtración y se secó al vacío, produciendo el compuesto del título (27,16 g, 44,9 %). 8h (CDCb , 300 MHz) 8,07 (dd, J 1,8, 0,9 Hz, 1H), 7,58 (dd, J 9,6, 0,9 Hz, 1H), 7,32 - 7,21 (m, 2H), 7,19 - 7,12 (m, 1H), 7,07 (td, J 7,4, 1,3 Hz, 1H), 7,00 (dd, J 7,7, 1,6 Hz, 1H), 6,66 (t, J 73,6 Hz, 1H), 4,73 (s, 2H), 4,47 (c, J 7,1 Hz, 2H), 1,44 (t, J 7,1 Hz, 3H). CLEM (EN+) TR 3,10 min, 271 (M-Br)+.
INTERMEDIO 5
6-bromo-3-^1-í2-(d¡fluorometox¡)fen¡l1-3-etox¡-3-oxo-prop¡l1¡m¡dazo^1.2-a1p¡r¡d¡n-2-carbox¡lato de etilo
El Intermedio 4 (13,0 g, 30,6 mmol) se disolvió en THF (600 ml) y la mezcla se enfrió a -100 °C. Se añadió gota a gota KHMDS 1 M en THF (34 ml, 34,0 mmol) y la mezcla resultante se agitó a -95 °C durante 15 minutos. Se añadió 2-bromoacetato de etilo (7,55 g, 45,2 mmol) y la mezcla resultante se agitó a -95 °C durante 30 minutos. Se añadió EtOAc y la mezcla se lavó con agua, los materiales orgánicos se lavaron con salmuera, se secaron con sulfato sódico y se concentraron al vacío para proporcionar un aceite de color amarillo. El residuo se trituró con Et2O y se filtró, produciendo el compuesto del título en forma de un sólido de color beige (10,8 g, 54 %). 8h (CDCb , 300 MHz) 8,56 (s, 1H), 7,73 (dd, J 7,2, 2,2 Hz, 1H), 7,53 (dd, J 9,6, 0,8 Hz, 1H), 7,29 (dd, J 9,6, 1,8 Hz, 1H), 7,26 - 7,15 (m, 2H), 7,01 -6,94 (m, 1H), 6,37 (t, J 73,5 Hz, 1H), 5,39 (dd, J 9,8, 5,8 Hz, 1H), 4,38 (cd, J 7,1, 0,8 Hz, 2H), 4,01 (cd, J 7,1, 3,4 Hz, 2H), 3,82 (dd, J 16,8, 9,8 Hz, 1H), 3,34 (dd, J 16,8, 5,8 Hz, 1H), 1,38 (t, J 7,1 Hz, 3H), 1,11 (t, J 7,1 Hz, 3H). CLEM (EN+) TR 2,13 min, 511,0/513,0 (M-Br)+.
INTERMEDIO 6
Éster etílico del ácido 7-bromo-1-(2-d¡fluorometox¡-fen¡l)-3-oxo-2.3-d¡h¡dro-1Hc¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-2-carboxílico
En una atmósfera de argón, el Intermedio 5 (4,0 g, 7,7 mmol) se disolvió en THF seco (150 ml). Se añadió terc-butóxido potásico (1,6 g, 14,26 mmol) y la mezcla se agitó a t.a. durante 30 minutos. Se añadió EtOAc y la reacción se repartió
con agua. La capa ac. se extrajo con EtOAc (2 x). Las capas orgánicas combinadas se lavaron con salmuera (x 2), se secaron sobre sulfato sódico y se concentraron al vacío para producir un aceite de color negro. El residuo se trituró con 7:3 de éter diisopropílico/DCM y los sólidos se retiraron por filtración. El filtrado se concentró al vacío y se purificó por HPLC preparativa para proporcionar el compuesto del título en forma de un sólido de color amarillo (792 mg, 22,7 %). mezcla 15:1 de diaestereoisómeros, isómero principal: 8h (CDCb, 300 MHz) 7,76 (dd, J 1,8, 1,0 Hz, 1H), 7,63 (dd, J 9,8, 1,0 Hz, 1H), 7,43 - 7,33 (m, 2H), 7,30 - 7,22 (m, 1H), 7,16 (td, J 7,5, 1,2 Hz, 1H), 6,85 - 6,78 (m, 1H), 6,58 (t, J 70,0 Hz, 1H), 5,48 (d, J 2,6 Hz, 1H), 4,27 (c, J 7,1 Hz, 2H), 3,88 (d, J 2,6 Hz, 1H), 1,31 (t, J 7,1 Hz, 3H). CLEM (EN+) TR 2,07 min, 465,0/467,0 (M+H)+.
INTERMEDIO 7
7-Bromo-6-fluoro-1-fen¡l-1.2-d¡h¡dro-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡rid¡n-3-ona
Etapa 1: Preparación de 2-amino-4-fluoro-5-bromopiridina
A una solución de 2-amino-4-fluoropiridina (75,0 g, 0,67 mol) en MeCN seco (700 ml), se añadió en porciones N-bromosuccinimida (122,8 g, 0,69 mol) tras agitar y enfriar en un baño de hielo-agua. La mezcla de reacción se agitó a t.a. durante 1 h. Después de la evaporación a presión reducida, el residuo se lavó concienzudamente con agua (3 x 300 ml), se recogió con MeCN y se concentró al vacío, produciendo el compuesto del título en forma de un sólido de color blanquecino (124 g, 97 %). CLEM (EN+) TR 0,79 min, 19,0/193,0 (M+H)+.
Etapa 2: preparación de 6-bromo-7-fluoro-imidazo[1,2-a]piridin-2-carboxilato de etilo
A una solución de 2-amino-4-fluoro-5-bromopiridina (87,6 g, 0,459 mol) en DME (750 ml), se añadió bromopiruvato de etilo (116,3 g, 0,596 mol, 1,3 equiv.). La mezcla de reacción se agitó a t.a. durante una noche y el precipitado de color blanco resultante se filtró, se lavó con DME (150 ml), Et2O (150 ml) y se secó al aire a t.a. Una suspensión del sólido de color blanco resultante en i-PrOH (1000 ml) se agitó a 90 °C durante 3 h. El disolvente se retiró por destilación a presión reducida, el residuo se agitó con una solución de KHCO3 (75,0 g, 0,75 mol) en agua (500 ml) a t.a. durante 1 h. El precipitado se filtró, se lavó con agua (3 x 500 ml), se evaporó con MeCN y se concentró al vacío, produciendo el compuesto del título en forma de un sólido de color blanquecino (108 g, 82 %). RMN 1H (400 MHz, DMSO-d6) 89,08 (d, J 7,1 Hz, 1H), 8,45 (s, 1H), 7,75 (d, J 9,8 Hz, 1H), 4,31 (c, J 7,1 Hz, 2H), 1,32 (t, J 7,1 Hz, 3H). CLEM (EN+) TR 1,44 min, 287,0/289,0 (M+H)+.
Etapa 3: preparación de 6-bromo-7-fluoro-3-formil-imidazo[1,2-a]piridin-2-carboxilato de etilo
A una suspensión de 6-bromo-7-fluoro-¡m¡dazo[1,2-a]pir¡d¡n-2-carbox¡lato de etilo (50,0 g, 0,174 mol) en DMF seca (101,6 g, 1,39 mol, 8,0 equiv.), se añadió gota a gota cloruro de fosforilo (213,0 g, 1,39 mol, 8,0 equiv.) durante un periodo de 30-40 minutos con agitación vigorosa y calentamiento a 75-85 °C. La solución de color rojo oscuro resultante se agitó a 85 °C durante 4,5 h, se enfrió a t.a. y después se vertió cuidadosamente en un baño de hieloagua y se dejó en agitación durante 20 minutos. El precipitado se filtró, se lavó concienzudamente con agua y se suspendió en agua (500 ml). Se añadió lentamente una solución ac. 5 M de hidróxido sódico hasta pH~7-8, el precipitado se filtró, se lavó con agua y se concentró al vacío, produciendo el compuesto del título en forma de un sólido de color blanquecino (34,9 g, 63 %). RMN 1H (400 MHz, DMSO-d6) 810,42 (s, 1H), 9,71 (d, J 6,8 Hz, 1H), 8,15 (d, J 9,0 Hz, 1H), 4,43 (c, J 7,1 Hz, 2H), 1,38 (t, J 7,1 Hz, 3H), CLEM (EN+) TR 1,71 min, 315,0/317,0 (M+H)+.
Etapa 4: preparación de 6-bromo-7-fluoro-3-[hidroxi(fenil)metil]imidazo[1,2-a]piridin-2-carboxilato de etilo
A una suspensión de 6-bromo-7-fluoro-3-formil-imidazo[1,2-a]piridin-2-carboxilato de etilo (46,4 g, 0,147 mol) en THF (3000 ml), a -45 °C, se añadió gota a gota bromuro de fenilmagensio (170 ml de una solución 1 M en THF, 0,17 mol, 1,15 equiv.), en una atmósfera de argón. Después de esta adición, la temperatura se elevó a -25 °C durante 1 h y después a t.a. durante 2 h. La reacción se interrumpió mediante la adición de una solución sat. de cloruro de amonio (150 ml) y salmuera (150 ml). La mezcla se concentró a presión reducida y se diluyó con EtOAc (1000 ml). La capa orgánica se separó y la capa ac. se extrajo con EtOAc (500 ml). La capa orgánica combinada se lavó con salmuera (3 x 500 ml), se secó sobre sulfato de magnesio, se filtró y se concentró a presión reducida. El residuo se purificó por cromatografía en columna ultrarrápida (S¡O2, EtOAc al 5-10 % en CHCb ), produciendo el compuesto del título en forma de un sólido de color blanquecino (42,1 g, 73 %). RMN 1H (400 MHz, DMSO-d6) 88,62 (d, J 6,9 Hz, 1H), 7,82 (d, J
9,3 Hz, 1H), 7,32-7,43 (m, 4H), 7,27 (m, 1H), 6,98 (d, J 4,4 Hz, 1H), 6,75 (d, J 4,4 Hz, 1H), 4,37 (c, J 7,1 Hz, 2H), 1,33 (t, J 7,1 Hz, 3H). CLEM (EN+) TR 1,76 min, 393,0/395,0 (M+H)+.
Etapa 5: preparación de 6-bromo-3-[cloro(fenil)metil]-7-fluoro-imidazo[1,2-a]piridin-2-carboxilato de etilo
A una solución de 6-bromo-7-fluoro-3-[hidroxi(fenil)metil]imidazo[1,2-a]piridin-2-carboxilato de etilo (18,0 g, 41,2 mmol) en DCM (400 ml), se añadió con agitación una solución de SOCl2 (31,3 g, 263 mmol, 6,4 equiv.) en DCM (60 ml). La mezcla de reacción se agitó a t.a. durante 2 h. El disolvente se evaporó antes de solubilización y evaporación sucesivas de benceno (2 x 200 ml). El residuo se distribuyó entre DCM (400 ml) y KHCO3 ac. al 10 % (100 ml). Después de agitar a t.a. durante 30 minutos, la capa orgánica se separó y la capa ac. se extrajo con DCM (150 ml). La capa orgánica combinada se secó sobre sulfato sódico, se filtró y se concentró al vacío, produciendo 6-bromo-3-[cloro(fenil)metil]-7-fluoro-imidazo[1,2-a]piridin-2-carboxilato de etilo (15,8 g, 92 %), utilizado en la siguiente etapa sin purificación adicional.
Etapa 6: preparación de 2-[(6-bromo-2-etoxicarbonil-7-fluoro-imidazo[1,2-a]piridin-3-il)-fenil-metil]propanodioato de dietilo
A una suspensión de NaH (1,63 g de una suspensión al 60 % en aceite mineral, 40,3 mmol) en THF (250 ml), en una atmósfera de argón, se añadió gota a gota malonato de dietilo (6,46 g, 40,3 mmol) mientras se enfriaba en un baño de hielo-agua. La mezcla se agitó a t.a. durante 1 h. A la solución transparente resultante, se añadió rápidamente con agitación una solución del 6-bromo-3-[cloro(fenil)metil]-7-fluoro-imidazo[1,2-a]piridin-2-carboxilato de etilo en bruto en THF (400 ml). La mezcla de reacción se agitó a t.a. durante 16 h antes de concentrarse a presión reducida. El residuo se distribuyó entre EtOAc (500 ml) y KHCO3 ac. al 10 % (100 ml); la capa orgánica se separó, se lavó con salmuera (2 x 150 ml), se secó sobre sulfato de magnesio, se filtró y se concentró a presión reducida. El residuo se purificó por cromatografía en columna ultrarrápida (SiO2, EtOAc al 0-7 % en DCM), produciendo el compuesto del título en forma de un sólido de color blanquecino (14,3 g, 69 % en 2 etapas a partir de 6-bromo-3-[cloro(fenil)metil]-7-fluoroimidazo[1,2-a]piridin-2-carboxilato de etilo). RMN 1H (400 MHz, DMSO-d6) 89,20 (s a, 1H), 7,78 (d, J 9,3 Hz, 1H), 7,56 (m, 2H), 7,30 (m, 2H), 7,21 (m, 1H), 5,90 (s a, 1H), 5,47 (d, J 12,2 Hz, 1H), 4,37 (c, J 7,1 Hz, 2H), 4,07 (c, J 7,1 Hz, 2H), 3,82 (c, J 7,1 Hz, 2H), 1,34 (t, J 7,1 Hz, 3H), 1,05 (t, J 7,1 Hz, 3H), 0,78 (t, J 7,1 Hz, 3H), CLEM (EN+) TR 2,04 min, 535,0/537,0 (M+H)+.
Etapa 7: preparación de 6-bromo-7-fluoro-3-(2-metoxi-2-oxo-1-feniletil)imidazo[1,2-a]piridin-2-carboxilato de metilo
Una mezcla de 2-[(6-bromo-2-etoxicarbonil-7-fluoro-imidazo[1,2-a]piridin-3-il)-fenil-metil]propanodioato de dietilo (14,26 g, 26,6 mmol) y HCl ac. 6 M (330 ml) se agitó a 100 °C durante 16 h. La mezcla se evaporó a presión reducida y el residuo (un aceite viscoso) se recogió sucesivamente y los disolventes se evaporaron con MeCN (2 x 200 ml) y benceno (2 x 200 ml), se concentraron al vacío, produciendo ácido 6-bromo-7-fluoro-3-(3-hidroxi-3-oxo-1-fenilpropil)imidazo[1,2-a]piridin-2-carboxílico (13,4 g), utilizado en la siguiente etapa sin purificación adicional.
A MeOH (220 ml), tras agitación y refrigeración en un baño de hielo-agua, se añadió gota a gota SOCb (88,2 g, 0,74 mol). La solución resultante se agitó 30 minutos a ~5 °C y se vertió en el ácido 6-bromo-7-fluoro-3-(3-hidroxi-3-oxo-1-fenilpropil)imidazo[1,2-a]piridin-2-carboxílico en bruto. La mezcla de reacción se puso en un recipiente de vidrio de alta presión y se agitó a 50 °C durante 16 h. Después de enfriar a t.a., el disolvente se evaporó, el residuo se evaporó de nuevo tres veces con benceno y se concentró al vacío a 40-50 °C. El residuo se disolvió en CHCb (250 ml); se lavó con KHCO3 ac. al 10 % (85 ml), se secó sobre sulfato sódico, se filtró y se concentró a presión reducida. El residuo se purificó por cromatografía en columna ultrarrápida (SiO2, EtOAc al 0-20 % en DCM), produciendo el compuesto del título en forma de un sólido de color blanquecino (9,9 g, 64 %). RMN 1H (400 MHz, DMsO-d6) 88,88 (d, J 6,4 Hz, 1H), 7,73 (d, J 9,1 Hz, 1H), 7,20-7,35 (m, 5H), 5,70 (t, J 8,1 Hz, 1H), 3,80 (s, 3H), 3,52 (d, J 8,1 Hz, 2H), 3,50 (s, 3H). CLEM (EN+) TR 1,84 min, 435,0/437,0 (M+H)+.
Etapa 8: preparación de éster metílico del ácido 7-bromo-6-fluoro-3-oxo-1-fenil-2,3-dihidro-1H-ciclopenta[4,5]imidazo[1,2-a]piridin-2-carboxílico
A una solución de 6-bromo-7-fluoro-3-(2-metoxi-2-oxo-1-feniletil)imidazo[1,2-a]piridin-2-carboxilato de metilo (9,90 g, 22,7 mmol) en tolueno (1000 ml), en una atmósfera de argón, se añadió una solución terc-pentóxido potásico (solución al 25 % en tolueno, 21 ml, 40,9 mmol, 1,8 equiv.) mientras se agitaba y enfriaba a -10 °C durante 10-15 minutos. La
mezcla de reacción se agitó a -10 °C durante 1 h y se inactivó añadiendo AcOH (2,5 ml). Después de calentar hasta t.a., se añadió KHCO3 ac. al 10 % (95 ml); la capa orgánica se separó y se concentró a presión reducida. El residuo se purificó por cromatografía en columna ultrarrápida (SO 2, MeOH al 0-5 % en DCM), produciendo el compuesto del título en forma de un sólido de color blanquecino (5,1 g, 55 %). RMN 1H (400 MHz, CDCb ) 6,75 (d, J 6,4 Hz, 1H), 7,43 (d, J 8,8 Hz, 1H), 7,43-7,37 (m, 3H), 7,12-7,18 (m, 2H), 5,17 (d, J 2,7 Hz, 1H), 3,98 (d, J 2,7 Hz, 1H), 3,84 (s, 3H), CLEM (EN+) TR 1,68 min, 403,0/405,0 (M+H)+.
Etapa 8: preparación de 7-bromo-6-fluoro-1-fenil-1,2-dihidrociclopenta[4,5]imidazo[1,2-a]piridin-3-ona
Una mezcla de éster metílico del ácido 7-bromo-6-fluoro-3-oxo-1-fenil-2,3-dihidro-1H-ciclopenta[4,5]imidazo[1,2-a]piridin-2-carboxílico (5,06 g, 12,5 mmol) y HCl ac. 6 M (100 ml) se agitó a 100 °C durante 3 h. La solución transparente resultante se evaporó a presión reducida; el residuo se distribuyó entre CHCl3 (200 ml) y KHCO3 ac. al 10 % (50 ml). La capa ac. se extrajo con CHCb (100 ml). La capa orgánica combinada se secó sobre sulfato sódico, se filtró y se concentró a presión reducida. El residuo se suspendió en CHCb (40 ml); la suspensión se agitó ~15 minutos a t.a. y se filtró. El precipitado resultante se lavó con CHCl3 (5 ml), Et2O (5 ml) y se concentró al vacío (1-2 mm de Hg), produciendo 2,60 g del compuesto del título en forma de un sólido de color blanquecino. El filtrado se concentró a presión reducida; el residuo se purificó por cromatografía en columna ultrarrápida (SO 2, MeOH al 0-5 % en CHCb ), produciendo 0,85 g más en forma de un sólido de color blanquecino. Los dos lotes se combinaron entre sí, produciendo el compuesto del título en forma de un sólido de color blanquecino (3,45 g, 80 %). RMN 1H (400 MHz, DMSO-d6) 8 8,42 (d, J 6,4 Hz, 1H), 7,87 (d, J 9,8 Hz, 1H), 7,38-7,26 (m, 3H), 7,18 (m, 2H), 4,93 (dd, J 18,3 Hz, J 2,0 Hz, 1H), 3,64 (dd, J 18,3 Hz, J 7,1 Hz, 1H), 2,76 (dd, J 1 18,3 Hz, J2 2,0 Hz, 1H). CLEM (EN+) TR 1,71 min, 345,0/347,0 (M+H)+.
INTERMEDIOS 8 Y 9
(R)-7-Bromo-6-fluoro-1-fen¡l-1.2-d¡h¡dro-c¡clopenta[4,51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ona y (S)-7-Bromo-6-fluoro-1-fenil-1,2-d¡h¡dro-c¡clopenta[4,51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ona
Los compuestos del título se aislaron mediante separación quiral del Intermedio 7 (1,1 g) en condiciones de CL en un LUX cell-4 (76 x 265 mm x mm, flujo 200 ml/min, 30 °C, 100 % de MeOH, inyección de 382 ml de solución a una concentración de 1,1 g/l). El primer enantiómero en eluirse (TR 6,09 min) se recogió y las fracciones se evaporaron para producir 460 mg de (S)-7-bromo-6-fluoro-1-fen¡l-1,2-d¡h¡dro-c¡clopenta[4,5]¡midazo[1,2-a]p¡r¡d¡n-3-ona (Intermedio 9). El segundo enantiómero en eluirse (TR 8,35 min) se recogió y las fracciones se evaporaron para producir 485 mg de (R)-7-bromo-6-fluoro-1-fen¡l-1,2-d¡h¡dro-c¡clopenta[4,5]im¡dazo[1,2-a]p¡r¡d¡n-3-ona (Intermedio 8).
INTERMEDIO 10
6-bromo-3-[[2-(d¡fluorometox¡)fen¡l1met¡l1-7-fluoro-¡m¡dazo[1.2-a1p¡r¡d¡n-2-carbox¡lato de etilo
Se suspendieron 5-bromo-4-fluoropiridin-2-amina (125 g, 654,0 mmol), el Intermedio 3 (121,0 g, 344,0 mmol) y sulfato de magnesio (124,0 g, 1033,0 mmol) en 1,4-dioxano (2,5 l) y se calentaron a 80 °C durante 72 h.La reacción se enfrió y los sólidos se retiraron por filtración y se lavaron con EtOAc. La mezcla de reacción se filtró y se enjuagó con EtOAc. El filtrado se diluyó con hidróxido sódico 1 N y EtOAc y las capas se separaron. La capa de agua se extrajo con EtOAc (2 x). Las capas orgánicas se combinaron y se lavaron con HCl 2 N (2 x). La capa ac. ácida se extrajo con EtOAc (x 2). Todas las capas orgánicas se combinaron y se lavaron con salmuera, se secaron con sulfato sódico y se concentraron al vacío. El residuo se trituró con Et2O, se retiró por filtración y se enjuagó con Et2O para proporcionar el compuesto del título en forma de un sólido de color amarillo (111 g, 71 %). 8h (CDCl3, 300 MHz) 8,16 (d, J 6,3 Hz, 1H), 7,40 (d, J 8,4 Hz, 1H), 7,30 - 7,21 (m, 1H), 7,15 (d a, J 8,0 Hz, 1H), 7,11 - 7,02 (m, 2H), 6,66 (t, J 73,5 Hz, 1H), 4,71
(s, 2H), 4,47 (c, J 7,1 Hz, 2H), 1,43 (t, J 7,1 Hz, 3H). CLEM (EN+) TR 2,13 min, 443,0/445,0 (M+H)+.
INTERMEDIO 11
6-bromo-3-[1-[2-(difluorometoxi)fenill-3-etoxi-3-oxo-propill-7-fluoroimidazo[1,2-alpiridin-2-carboxilato de etilo
El Intermedio 10 (30,0,0 g, 67,7 mmol) se disolvió en THF (400 ml) y la mezcla se enfrió a -100 °C. Se añadió gota a gota KHMDS 1 M en THF (75,0 ml, 75,0 mmol) y la mezcla resultante se agitó a -95 °C durante 15 minutos. Se añadió 2-bromoacetato de etilo (11,3 ml, 102 mmol) y la mezcla resultante se agitó a -95 °C durante 30 minutos. Se añadió EtOAc y la mezcla se lavó con agua y los materiales orgánicos se lavaron con salmuera, se secaron con sulfato sódico y se concentraron al vacío para proporcionar un aceite de color negro. El residuo se trituró con Et2O y se filtró, produciendo el compuesto del título en forma de un sólido de color pardo claro (26,5 g, 71 %). 8h (CDCb , 300 MHz) 8,67 (d, J 6,4 Hz, 1H), 7,74 (dd, J 7,3, 2,2 Hz, 1H), 7,33 (dd, J 8,3, 0,5 Hz, 1H), 7,29 - 7,16 (m, 2H), 6,99 - 6,93 (m, 1H), 6,37 (t, J 73,5 Hz, 1H), 5,32 (dd, J 10,1, 5,4 Hz, 1H), 4,37 (c, J 7,1 Hz, 2H), 4,09 - 3,95 (m, 2H), 3,89 (dd, J 16,9, 10,1 Hz, 1H), 3,31 (dd, J 16,9, 5,3 Hz, 1H), 1,37 (t, J 7,1 Hz, 3H), 1,14 (t, J 7,1 Hz, 3H). CLEM (EN+) TR 2,16 min, 529,0/531,0 (M+H)+.
INTERMEDIO 12
Éster etílico del ácido 7-bromo-1-(2-difluorometoxi-fenil)-6-fluoro-3-oxo-2,3-dihidro-1H-ciclopenta[4,5limidazo[1,2-alpiridin-2-carboxílico
En una atmósfera de argón, el Intermedio 11 (15,0 g, 28,3 mmol) se disolvió en THF seco (1 l). Se añadió terc-butóxido potásico (7,95 g, 70,8 mmol) y la mezcla se agitó a t.a. durante 30 minutos. La reacción se diluyó con cloruro de amonio sat., se agitó vigorosamente durante minuto y después se diluyó con DCM. Las capas se separaron y la capa ac. se extrajo con DCM. Las capas orgánicas combinadas se lavaron con salmuera, se secaron con sulfato sódico y se concentraron al vacío para proporcionar un aceite de color pardo. El residuo se cristalizó en tolueno caliente (250 ml). Los cristales se retiraron por filtración, se lavaron con Et2O, produciendo el compuesto del título en forma de cristales de color pardo claro (6,8 g, 50 %). 8h (CDCla, 300 MHz) 7,83 (d, J 6,3 Hz, 1H), 7,46 - 7,35 (m, 2H), 7,32 - 7,24 (m, 1H), 7,18 (td, J 7,5, 1,1 Hz, 1H), 6,83 (s, 1H), 6,58 (t, J 69,3 Hz, 1H), 5,47 (d, J 2,5 Hz, 1H), 4,28 (c, J 7,0 Hz, 2H), 3,89 (d, J 2,5 Hz, 1H), 1,32 (t, J 7,2 Hz, 3H). CLEM (EN+) TR 2,09 min, 483,0/485,0 (M+H)+.
INTERMEDIO 13
Ácido [2-[(1R.5S)-8-metox¡carbon¡l-3-azab¡c¡clo[3.2.1loctan-3-¡llp¡r¡m¡d¡n-5-¡llborón¡co
Se suspendió ácido (1R,5S)-3-terc-butoxicarbonil-3-azabiciclo[3.2.1loctano-8-carboxílico (9,0 g, 35,3 mmol) en una solución de HCl (2,25 M en MeOH) y la reacción se calentó a reflujo durante 4 h. La reacción se dejó enfriar a t.a. y después se concentró al vacío para dar un sólido de color blanco. Se añadió ácido (2-cloropirimidin-5-il)borónico (5,58 g, 35,2 mmol) y la mezcla se suspendió en EtOH (130 ml). Se añadió TEA (9,90 ml, 70,5 mmol) y la reacción se calentó a 80 °C durante 5 h. La reacción se dejó enfriar a t.a. y después se añadió agua (30 ml). La mezcla de reacción se concentró a aproximadamente 1/3 del volumen y después se añadió más cantidad de agua (100 ml). Un sólido de color blanquecino precipitó, el cual se filtró y se lavó con agua (2 x 30 ml) para proporcionar el compuesto del título (8,9 g, rendimiento del 86 %) en forma de un polvo de color blanquecino. RMN 1H (300 MHz, DMSO-d6) 8 ppm 8,59 (s, 2H), 8,02 (s, 2H), 4,45 (dd, J 13,1, 3,4 H, 2H), 3,62 (s, 3H), 2,98 (d a, J 12,4 Hz, 2H), 2,77 (s, 1H), 2,59 (s a, 2H), 1,66-1,63 (m, 2H), 1,38-1,33 (m, 2H). CLEM (EN+) TR 0,97 min, 292,0 (M+H)+.
INTERMEDIOS 14 Y 15
(R)-7-Bromo-6-fluoro-1-(2-tr¡fluorometox¡-fen¡l)-1,2-d¡h¡dro-c¡clope nta[4,5limidazo[1,2-alpiridin-3-ona y (S)-7-Bromo-6-fluoro-1-(2-tr¡fluorometox¡fen¡l)-1.2-d¡h¡dro-c¡clopenta[4.5l¡m¡dazo[1.2-alp¡r¡d¡n-3-ona
Etapa 1: Preparación de 6-bromo-7-fluoro-3-yodoimidazo[1,2-a]piridin-2-carboxilato de etilo
A una solución de 6-bromo-7-fluoroimidazo[1,2-a]piridin-2-carboxilato de etilo (Intermedio 7, etapa 2, 10,3 g, 35,9 mmol, 1 equiv.) en AcOH (80 ml), se añadió Ñ-yodosuccinimida (8,5 g, 37,6 mmol, 1,1 equiv.). La mezcla de reacción se agitó a t.a. durante 1 h para proporcionar una suspensión espesa de color blanco. El disolvente se evaporó a presión reducida, el residuo se evaporó de nuevo con CHCl3 y se disolvió en CHCb (400 ml). La solución de color amarillo resultante se lavó con tiosulfato sódico ac. al 10 % (2 x 200 ml) y salmuera (100 ml), se secó sobre sulfato sódico, se filtró y se concentró al vacío. El residuo se lavó con Et2O (50 ml) y se secó al vacío, produciendo el compuesto del título en forma de un sólido de color blanco (14,0 g, 94 %). RMN 1H (400 MHz, DMSO-d6) 88,71 (d, J 6.6 Hz, 1H). 7,82 (d, J 9,1 Hz, 1H), 4,32 (c, J 7,1 Hz, 2H), 1,34 (t, J 7,1 Hz, 3H). CLEM (EN+) TR 1,69 min, 413,0/415,0 (M+H)+.
Etapa 2: Preparación de 6-bromo-7-fluoro-3-{hidroxi[2-(trifluorometoxi)fenil]metil}imidazo[1,2-a]piridin-2-carboxilato de etilo
A una suspensión de 6-bromo-7-fluoro-3-yodoimidazo[1,2-a]piridin-2-carboxilato de etilo (29,57 g, 71,6 mmol, 1 equiv.) en THF (1 l), en una atmósfera de argón, se añadió gota a gota una solución de cloruro de i-propilmagnesio (36,0 ml, 2 M en THF, 72,0 mmol, 1 equiv.) durante ~3 minutos mientras se agitaba a -60 °C (termómetro interno). La mezcla de reacción se agitó a -60 °C durante 15 min, después se añadió gota a gota una solución de 2-(trifluorometoxi)benzaldehído (13,68 g, 72,0 mmol, 1 equiv.) en THF (50 ml) durante 5 minutos. La agitación se continuó tras calentamiento espontáneo a -5 °C durante 2 h. La mezcla se inactivó con cloruro de amonio ac. sat. (250 ml), se agitó a t.a. durante 15 minutos y se extrajo con EtOAc (2 x 300 ml). La capa orgánica se secó sobre sulfato sódico, se filtró y se concentró al vacío. El residuo se purificó por cromatografía en columna (SiO2, EtOAc al 5-20 % en CHCb ), produciendo el compuesto del título (17,38 g, 52 %). RMN 1H (400 MHz, DMSO-d6) 8 8,61 (d, J 6,6 Hz, 1H). 7,78-7,85 (m, 2H), 7,45-7,49 (m, 2H), 7,29-7,32 (m, 1H), 7,16 (d, J 4,2 Hz, 1H), 6,85 (d, J 4,4 Hz, 1H), 4,31 (c, J 7,1 Hz, 2H), 1,30 (t, J 7,1 Hz, 3H). CLEM (EN+) TR 1,94 min, 477,0/479,0 (M+H)+.
Etapa 3: Preparación de 6-bromo-7-fluoro-3-{cloro[2-(trifluorometoxi)fenil]metil}imidazo[1,2-a]piridin-2-carboxilato de etilo
A una suspensión de 6-bromo-7-fluoro-3-{hidroxi[2-(trifluorometoxi)fenil]metil}imidazo[1,2-a]piridin-2-carboxilato (18,27 g, 38,3 mmol, 1 equiv.) en DCM (440 ml), se añadió una solución de SoCb (39,0 g, 328 mmol, 8,6 equiv.) en DCM (50 ml). La mezcla de reacción se agitó a t.a. durante 3 h y se concentró al vacío. El residuo se evaporó de nuevo con benceno absoluto (200 ml) y se disolvió en DCM (300 ml). La solución resultante se lavó con KHCO3 ac. al 10 % (2 x 100 ml) a 5-10 °C, se secó sobre sulfato sódico, se filtró y se concentró al vacío. El residuo se evaporó de nuevo con benceno (200 ml) y se concentró al vacío a t.a para proporcionar el compuesto del título en forma de un sólido de color amarillo (18,9 g).
Etapa 4: Preparación de {[6-bromo-2-(etoxicarbonil)-7-fluoroimidazo[1,2-a]piridin-3-il][2-(trifluorometoxi)fenil]metil}propanodioato de dietilo
A una suspensión de NaH (1,60 g de 60 % en aceite mineral, 40,0 mmol, 1 equiv.) en THF abs. (40 ml), tras agitación y refrigeración en un baño de hielo-agua, se añadió gota a gota una solución de malonato de dietilo (6,40 g, 40,0 mmol, 1 equiv.) en THF (40 ml). La mezcla de reacción se agitó a t.a. durante 30 minutos. A la solución transparente, se añadió rápidamente una solución de 6-bromo-7-fluoro-3-{cloro[2-(trifluorometoxi)fenil]metil}imidazo[1,2-a]piridin-2-carboxilato de etilo en THF (200 ml) mediante agitación y refrigeración en un baño de agua fría. La mezcla se agitó a t.a. durante 6 h y se concentró al vacío. El residuo se distribuyó entre EtOAc (500 ml) y agua (250 ml); la capa orgánica se lavó con KHCO3 ac. al 10 % (200 ml) y salmuera (200 ml), se secó sobre sulfato de magnesio, se filtró y se concentró al vacío. El residuo se purificó por cromatografía en columna ultrarrápida (SiO2, EtOAc al 0-5 % en DCM), produciendo el compuesto del título (16,4 g, pureza del 80 % según RMN 1H). RMN 1H (400 MHz, DMSO-d6) 88,93 (s a, 1H), 7,97 (s a, 1H), 7,77 (d, J 7,0 Hz, 1H), 7,56-7,66 (m, 1H), 7,37-7,41 (m, 2H), 7,37-7,41 (m, 2H), 7,25-7,28 (m, 1H), 5,43-5,50 (m, 1H), 4,25-4,32 (m, 2H), 4,15-4,08 (m, 2H), 3,81-3,71 (m, 2H), 1,30-1,26 (m, 2H), 1,00 (t, J 6,7 Hz, 3H), 0,75 (t, J 6.6 Hz, 3H). CLEM (EN+) TR 2,21 min, 619,0/621,0 (M+H)+.
Etapa 5: Preparación de ácido 6-bromo-3-{2-carboxi-1-[2-(trifluorometoxi)fenil]etil}-7-fluoroimidazo[1,2-a]piridin-2- carboxílico
Una mezcla de {[6-bromo-2-(etoxicarbonil)-7-fluoroimidazo[1,2-a]piridin-3-il][2-(trifluorometoxi)fenil]metil}propanodioato de dietilo (16,4 g) y HCl ac. 6 M (200 ml) se agitó a 100 °C durante 16 h. La mezcla se concentró al vacío. El residuo se evaporó de nuevo con MeCN (2 x 150 ml), benceno (150 ml) y se secó al vacío, produciendo el compuesto del título en forma de un sólido vítreo de color pardo (12,6 g).
Etapa 6: Preparación de 6-bromo-7-fluoro-3-{3-metoxi-3-oxo-1-[2-(trifluorometoxi)fenil]propil}imidazo[1,2-a]piridin-2-carboxilato de metilo
A MeOH (170 ml), mientras se agitaba y enfriaba en un baño de agua y hielo, se añadió gota a gota SOCb (64,3 g, 0,54 mol, 2,1 equiv.) y la mezcla se agitó a 0 °C durante 30 minutos. A la solución resultante de HCl en MeOH se añadió una solución de ácido 6-bromo-3-{2-carboxi-1-[2-(trifluorometoxi)fenil]etil}-7-fluoroimidazo[1,2-a]piridin-2-carboxílico (12,6 g, 25,7 mmol, 1 equiv.) en una pequeña cantidad de MeOH. La solución se puso en un recipiente de vidrio de alta presión y se agitó a 50-60 °C durante 16 h. Después de enfriar a t.a., la mezcla de reacción se concentró al vacío y el residuo se evaporó de nuevo con benceno (3 x 100 ml). El residuo se disolvió en CHCb (450 ml); se lavó con KHCO3 ac. al 10 % (2 x 200 ml), se secó sobre sulfato sódico, se filtró y se concentró al vacío. El residuo se purificó por cromatografía en columna (SiO2, EtOAc al 0-5 % en CHCb ), produciendo el compuesto del título en forma de un sólido de color amarillo claro (6,21 g, 31 % en 4 etapas). RMN 1H (400 MHz, DMSO-d6) 89,01 (d, J 6,6 Hz, 1H), 7,76-7,78 (m, 1H), 7,72 (d, J 9,0 Hz, 1H), 7,36-7,43 (m, 2H), 7,20-7,23 (m, 1H), 5,69 (t, J 19,6 Hz, 1H), 3,71 (s, 3H), 3,51-3,57 (m, 2H), 3,51 (s, 3H). CLEM (EN+) TR 1,90 min, 519,0/521,0(M+H)+.
Etapa 7: Preparación de éster metílico del ácido 7-bromo-6-fluoro-3-oxo-1-(2-trifluorometoxi-fenil)-2,3-dihidro-1H-ciclopenta[4,5]imidazo[1,2-a]piridin-2-carboxílico
A -10 °C, se añadió lentamente gota a gota una solución de terc-pentóxido potásico (11,0 ml de 25 % en tolueno, 18,8 mmol, 1,6 equiv.) a una solución de 6-bromo-7-fluoro-3-{3-metoxi-3-oxo-1-[2-(trifluorometoxi)fenil]propil}imidazo[1,2-a]piridin-2-carboxilato de metilo (6,20 g, 11,9 mmol, 1 equiv.) en tolueno (700 ml). La mezcla de reacción se agitó a -10 °C durante 30 minutos, se inactivó mediante la adición de AcOH (1,5 ml) y se calentó hasta t.a. La capa orgánica se separó, se lavó con KHCO3 ac. al 10 % (100 ml) y los disolventes se evaporaron. El residuo se purificó por cromatografía en columna ultrarrápida (SiO2, EtOAc al 0-15 % en CHCb ), produciendo el compuesto del título en forma de un sólido de color amarillo claro (3,30 g, 62 %). RMN 1H (400 MHz, DMSO-d6) 88,61 (d, J 6,9 Hz, 1H), 7,93 (d, J 9,8 Hz, 1H), 7,42-7,52 (m, 2H), 7,25-7,33 (m, 1H), 6,95-7,05 (m, 1H), 5,42 (s a, 1H), 3,94 (d, J 2,4 Hz, 1H), 3,72 (s, 3H). CLEM (EN+) TR 1,91 min, 487,0/489,0 (M+H)+.
Etapa 8: Preparación de 7-Bromo-6-fluoro-1-(2-trifluorometoxi-fenil)-1,2-dihidrociclopenta[4,5]imidazo[1,2-a]piridin-3-ona
Una solución de éster metílico del ácido 7-bromo-6-fluoro-3-oxo-1-(2-trifluorometoxi-fenil)-2,3-dihidro-1H-ciclopenta[4,5]imidazo[1,2-a]piridin-2-carboxílico (3,30 g, 6,78 mmol, 1 equiv.) en HCI ac. (60 ml, 6 M) se agitó a 100 °C durante 1 h. Después de enfriar a t.a., el disolvente se evaporó al vacío. El residuo se repartió entre EtOAc (300 ml) y
KHCO3 ac. al 10 % (100 ml). La capa orgánica se lavó con salmuera (150 ml), se secó sobre sulfato de magnesio, se filtró a través de un lecho corto de SO 2 y se concentró al vacío, produciendo el compuesto del título en forma de un sólido de color blanco (2,32 g, 80 %). RMN 1H (400 MHz, DMSO-da) 88,53 (d, J 6,6 Hz, 1H), 7,88 (d, J 9,8 Hz, 1H), 7,40-7,50 (m, 2H), 7,25-7,35 (m, 1H), 6,95-7,05 (m, 1H), 5,15 (dd, Ji 7,1 Hz, J2 1,9 Hz, 1H), 3,62 (dd, Ji 18,0 Hz, J2 7,1 Hz, 1H), 2,70 (dd, J* 18,0, Hz, J2 1,9 Hz, 1H); CLEM (EN+) TR 1,91 min, 429,0/431,0 (M+H)+.
Etapa 9: Preparación de (R)-7-bromo-6-fluoro-1-(2-trifluorometoxi-fenil)-1,2-dihidrociclopenta[4,5]imidazo[1,2-a]piridin-3-ona y (S)-7-bromo-6-fluoro-1-(2-trifluorometoxi-fenil)-1,2-dihidro-ciclopenta[4,5]imidazo[1,2-a]piridin-3-ona
Los compuestos del título se aislaron por purificación quiral del Intermedio 13 en condiciones de SFC en un Lux-Cell-4 (50 x 291 mm'mm, flujo 360 ml/min, 25 °C, 30 % de MeOH -> 10 min 50 % de MeOH ->14 min, inyección de 10 ml de solución a una concentración de 30 g/l). El primer enantiómero en eluirse (TR 7,5 min) se recogió y las fracciones se evaporaron para producir 335 mg del Intermedio 14. El segundo enantiómero en eluirse (TR 12,9 min) se recogió y las fracciones se evaporaron para producir 357 mg del Intermedio 15.
INTERMEDIOS 16 Y 17
í1R)-7-bromo-1-í2-clorofen¡l)-6-fluoro-1.2-d¡h¡dro-3H-c¡clopentar4.51¡m¡dazoH.2-a1p¡rid¡n-3-ona o (1S)-7-bromo-1-(2-clorofen¡l)-6-fluoro-1.2-d¡h¡dro-3H-c¡clopentar4.51¡m¡dazoH.2-a1p¡rid¡n-3-ona
Se preparó 7-bromo-1-(2-clorofen¡l)-6-fluoro-1,2-d¡hidro-3H-c¡clopenta[4,5]¡m¡dazo[1,2-a]p¡r¡d¡n-3-ona a partir de 6-bromo-7-fluoro-3-formil-imidazo[1,2-a]piridin-2-carboxilato de etilo (30,0 g, 95,0 mmol, 1 equiv.) y cloruro de 2-clorofenil magnesio (117 mmol, 1,2 equiv.) mediante el procedimiento por etapas descrito para el Intermedio 7 (3,70 g, rendimiento total del 7,1 % en 6 etapas).
Los compuestos del título se aislaron mediante purificación quiral de 7-bromo-1-(2-clorofenil)-6-fluoro-1,2-dihidro-3H-ciclopenta[4,5]imidazo[1 ,2-a]piridin-3-ona en condiciones de SFC en un Whelko-O1 (R.R) (50 x 227 mm x mm, flujo 360 ml/min, 25 °C, CO2 + 20 % de i-PrOH, inyección de 18 ml de solución a una concentración de 7,35 g/l). El primer enantiómero en eluirse (TR 10,4 min) se recogió y las fracciones se evaporaron para producir el Intermedio 16. El segundo enantiómero en eluirse (TR 12,8 min) se recogió y las fracciones se evaporaron para producir el Intermedio 17. RMN 1H (400 MHz, DMSO-d6) 88,67 (d, J 6,4 Hz, 1H), 7,90 (d, J 9,9 Hz, 1H), 7,56 (d, J 7,3 Hz, 1H), 7,34 (td, J 7,7 Hz, J 1,5 Hz, 1H), 7,22 (t, J 7,3 Hz, 1H), 6,71 (s a, 1H), 5,21 (dd, J 7,1 Hz, J 20 Hz, 1H), 3,71 (dd, J 18,2 Hz, J 7,2 Hz, 1H), 2,65 (d, J 18,1 Hz, 1H). CLEM (EN+) TR 1,83 min, 379,0/381,0 (M+H)+.
INTERMEDIO 18
(R)-7-Bromo-1-(2-cloro-fen¡l)-6-fluoro-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ol
El compuesto del título se preparó a partir del Intermedio 16 (250 mg, 0,659 mmol, 1 equiv.) y borohidruro sódico (25,2 mg, 0,659 mmol 1 equiv.) por el Método C (250 mg, 99 %). La proporción de isómeros cis/trans fue 85/15 basado en UV CLEM. CLEM (EN+) TR 4,56 y 4,64 min, 381,1/383,1 (M+H)+
I N T E R M E D I O 19
(S)-7-Bromo-1-(2-cloro-fen¡l)-6-fluoro-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡rid¡n-3-ol
El compuesto del título se preparó a partir del Intermedio 17 (250 mg, 0,659 mmol, 1 equiv.) y borohidruro sódico (25,2 mg, 0,659 mmol 1 equiv.) por el Método C (250 mg, 99 %). La proporción de isómeros cis/trans fue 85/15 basado en UV CLEM. CLEM (EN+) TR 4,56 y 4,64 min, 381,1/383,1 (M+H)+
I N T E R M E D I O 2 0 -
MÉTODO D
(R)-7-Bromo-1-(2-cloro-fenil)-3,6-difluoro-2,3-dihidro-1H-ciclopentar4,51imidazoH,2-a1piridina
El Intermedio 18 (250 mg, 655 mmol, 1 equiv.) se suspendió en 5 ml de DCM, y a -30 °C, se añadió gota a gota trifluoruro de dietilaminoazufre (127 mg, 0,788 mmol, 1,2 equiv.). La mezcla de reacción se agitó a -30 °C durante 30 minutos antes de la adición cuidadosa de una solución sat. de bicarbonato sódico (10 ml). A t.a., la mezcla en bruto se extrajo con DCM (2 x 30 ml). Las capas orgánicas se secaron sobre sulfato de magnesio y se concentraron al vacío. El residuo se purificó por cromatografía en columna ultrarrápida (SiO2, EtOAc al 100 %), produciendo el compuesto del título en forma de un aceite incoloro (147 mg, 67 %). CLEM (EN+) TR 5,12 y 5,14 min, 383,1/385,1 (M+H)+
I N T E R M E D I O S 21 Y 22
(1R.3R)-7-bromo-1-(2-clorofen¡l)-3.6-d¡fluoro-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡na y (1R,3S)-7-bromo-1-(2-clorofen¡l)-3.6-d¡fluoro-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡na
Los compuestos del título se aislaron mediante purificación quiral del Intermedio 20 en condiciones de SFC en un Whelko-O1 (R,R) (50 x 227 mm x mm, flujo 360 ml/min, 25 °C, CO2 + 20 % de i-PrOH, inyección de 18 ml de solución a una concentración de 7,35 g/l). El primer enantiómero en eluirse (TR 10,4 min) se recogió y las fracciones se evaporaron para producir 50 mg de (1R,3R)-7-bromo-1-(2-clorofenil)-3,6-difluoro-2,3-dihidro-1H-ciclopenta[4,5]imidazo[1,2-a]piridina. El segundo enantiómero en eluirse (TR 12,8 min) se recogió y las fracciones se evaporaron para producir 48 mg de (1R,3S)-7-bromo-1-(2-clorofenil)-3,6-difluoro-2,3-dihidro-1H-ciclopenta[4,5]imidazo[1,2-a]piridina.
INTERMEDIO 23
(S)-7-Bromo-1-(2-cloro-fen¡l)-3.6-d¡fluoro-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1pir¡d¡na
El compuesto del título se preparó a partir del Intermedio 19 (250 mg, 655 mmol, 1 equiv.) y trifluoruro de dietilaminoazufre (127 mg, 0,788 mmol, 1,2 equiv.) por el Método D (255 mg, 99 %). CLEM (EN+) t R 5,10 y 5,12 min, 383,1/385,1(M+H)+
INTERMEDIOS 24 Y 25
(1S.3R)-7-bromo-1-(2-clorofenil)-3.6-difluoro-2,3-dihidro-1H-ciclopenta[4.5limidazo[1.2-alpiridina y (1S,3S)-7-bromo-1-(2-clorofenil)-3.6-difluoro-2,3-dihidro-1H-ciclopenta[4.5limidazo[1.2-alpiridina.
Los compuestos del título se aislaron mediante purificación quiral del Intermedio 23 en condiciones de SFC en un Whelko-O1 (R,R) (50 x 227 mm x mm, flujo 360 ml/min, 25 °C, CO2 + 20 % de rPrOH, inyección de 18 ml de solución a una concentración de 6,4 g/l). El primer enantiómero en eluirse (TR 9 min) se recogió y las fracciones se evaporaron para producir 45 mg de (1S,3R)-7-bromo-1-(2-clorofenil)-3,6-difluoro-2,3-dihidro-1H-ciclopenta[4,5]imidazo[1,2-a]piridina. El segundo enantiómero en eluirse (TR 17 min) se recogió y las fracciones se evaporaron para producir 37 mg de (1S.3S)-7-bromo-1-(2-clorofenil)-3,6-difluoro-2,3-dihidro-1H-ciclopenta[4,5]imidazo[1,2-a]piridina.
INTERMEDIO 26
(1R.3S)-7-Bromo-1-(2-d¡fluorometox¡-fen¡l)-6-fluoro-2.3-d¡h¡dro-1H-c¡clopenta^4.51¡m¡dazô 1.2-a1p¡r¡d¡n-3-ol
El compuesto del título se preparó a partir del Ejemplo 13 (4,64 g, 11,3 mmol, lequiv.) y borohidruro sódico (0,431 g, 1 equiv.) por el Método C para producir 7-bromo-1-(2-difluorometoxi-fenil)-6-fluoro-2,3-dihidro-1H-cidopenta[4,5]imidazo[1,2-a]piridin-3-ol. Los compuestos del título se aislaron mediante purificación quiral de 7-bromo-1-(2-difluorometoxi-fenil)-6-fluoro-2,3-dihidro-1H-ciclopenta[4,5]imidazo[1,2-a]piridin-3-ol en condiciones de SFC en un Lux-Cell-4 (50 x 291 mm x mm, flujo 360 ml/min, 25 °C, CO2 + 20 % de MeOH, inyección de 6,8 ml de solución a una concentración de 100 g/l). El primer diastereómero en eluirse (TR 4,61 min) se recogió y las fracciones se evaporaron para producir (1R,3R)-7-bromo-1-(2-difluorometoxi-fenil)-6-fluoro-2,3-dihidro-1H-ciclopenta[4,5]imidazo[1,2-a]piridin-3-ol (2,08 g, 44,6 %). CLEM (EN+) TR 4,02 min, 413,0/415,0 (M+H)+. El segundo diastereómero en eluirse (TR 8,74 min) se recogió y las fracciones se evaporaron para producir el compuesto del título (0,425 g, 9,1 %). CLEM (EN+) TR 3,98 min, 413,0/415,0 (M+H)+.
INTERMEDIO 27
(1R.3R)-3-Az¡do-7-bromo-1-(2-d¡fluorometox¡-fen¡l)-6-fluoro-2.3-d¡h¡dro-1H-c¡clopenta[4,51¡m¡dazo[1.2-a1p¡r¡d¡na
El Intermedio 26 (0,100 g, 1,0 equiv.) se disolvió en 0,5 ml de tolueno. A 0 °C, se añadió gota a gota difenilfosforilazida (1,3 equiv.), seguido de 1,8-diazabiciclo[5.4.0]undec-7-eno (1,4 equiv.). La mezcla de reacción se agita a 0 °C durante 1 h y a t.a. durante 16 h. La mezcla se recogió en EtOAc y se lavó con agua. La fase orgánica se secó sobre sulfato sódico y se concentró al vacío para proporcionar 110 mg (100 %) del compuesto del título en forma de un aceite de color pardo, que se usó en la siguiente etapa sin purificación adicional. CLEM (EN+) TR 5,12 min, 438,0/440,0 (M+H)+.
INTERMEDIO 28
(1R.3R)-7-Bromo-1-(2-d¡fluorometox¡-fen¡l)-6-fluoro-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-3-¡lam¡na
El Intermedio 27(110 mg, 1,0 equiv.) se disolvió en 1,5 ml de una mezcla (2:1) de tolueno:agua. Se añadió resina de trifenilfosfina (1,5 equiv., 3 mmol/g) y la mezcla de reacción se agitó durante 48 h a t.a. La mezcla se filtró, se lavó con EtOAc y se extrajo con HCl 1 N. La fase ac. se neutralizó con una solución ac. sat. de bicarbonato sódico, se extrajo con EtOAc, se secó sobre sulfato de magnesio y se concentró al vacío para proporcionar 30 mg (29 %) del compuesto del título, que se usó en la siguiente etapa sin purificación adicional. CLEM (EN+) TR 3,40 min, 412,0/414,0 (M+H)+.
I N T E R M E D I O 2 9 -
MÉTODO E
ácido (2-t¡omorfol¡nop¡r¡m¡d¡n-5-¡l)borón¡co
Se d¡solv¡eron ác¡do 2-clorop¡r¡m¡d¡n-5-borón¡co (52,3 mmol, 8,53 g), t¡omorfol¡na (52,3 mmol, 5,3 ml) y TEA (52,3 mmol, 7,3 ml) en EtOH (100 ml) y se calentaron a 80 °C durante 4 h. El d¡solvente se ret¡ró al vacío y el sól¡do resultante se tr¡turó con Et2O, produc¡endo el compuesto del título (8,64 g, 74 %). 8h (300 MHz, DMSO-d6) 8,63 (s, 2H); 8,06 (s, 2H); 4,08 (m, 4H); 2,59 (m, 4H). CLEM (EN+) TR 0,21 m¡n 226,8 (M+H)+.
I N T E R M E D I O 30
Ác¡do [2-[(1R,5S)-7-oxo-3,6-d¡azab¡c¡clo[3.2.21nonan-3-¡l1p¡r¡m¡d¡n-5-¡l1borón¡co; cloruro de tr¡et¡lamon¡o
El compuesto del título se preparó a part¡r de ác¡do 2-clorop¡r¡m¡d¡n-5-borón¡co (1,13 g, 7,14 mmol) y (1S,5R)-3,6-d¡azab¡c¡clo[3.2.21nonan-7-ona (1,00 g, 7,13 mmol) por el Método E (2,70 g, 94,7 %). Este mater¡al se usó en bruto en reacc¡ones de acoplam¡ento poster¡ores s¡n la neces¡dad de ret¡rada o separac¡ón de la sal de TEA asoc¡ada. 8h (300 MHz, DMSO-d6) 8,62 (s, 2H), 8,35 (d, 1H, J 4,7 Hz, NH), 8,08 (s, 2H), 4,88-4,75 (m, 2H). 3,63 (m, 1H), 3,43 (m, 1H), 3,25-3,10 (m, 1H), 3,05 (c, 6H, J 7,1 Hz, TEA), 2,57 (m, 1H), 1,75-1,55 (m, 4H), 1,18 (t, 9H, J 7,1 Hz, tr¡et¡lam¡na).
I N T E R M E D I O 31
4-[5-(4.4.5.5-tetramet¡l-1.3.2-d¡oxaborolan-2-¡l)p¡r¡m¡d¡n-2-¡l1p¡peraz¡n-2-ona
El compuesto del título se preparó a part¡r de 2-cloro-5-(tetramet¡l-1,3,2-d¡oxaborolan-2-¡l)p¡r¡m¡d¡na (3,5 g, 14,5 mmol) y p¡peraz¡n-2-ona (1,6 g, 16,0 mmol) por el Método E (2,0 g, 45 %). 8h (250 MHz, CDCb ) 8,57 (s, 2H), 6,64 (s, 1H), 4,42 (s, 2H), 4,05 (s, 2H), 3,40 (s, 2H), 1,26 (s, 12H). CLEM (EN+) TR 1,12 m¡n, 305,0 (M+H)+.
I N T E R M E D I O 32
(1S.4S)-5-[5-(4.4.5.5-tetramet¡l-1.3.2-d¡oxaborolan-2-¡l)p¡r¡m¡d¡n-2-¡l1-2-oxa-5-azab¡c¡clo[2.2.11heptano
El compuesto del título se preparó a part¡r de clorh¡drato de (1S,4S)-2-oxa-5-azab¡c¡clo[2.2.1]heptano (1:1) (406 mg, 2,99 mmol) y 2-cloro-5-(tetramet¡l-1,3,2-d¡oxaborolan-2-¡l)p¡r¡m¡d¡na (650 mg, 2,70 mmol) por el Método E (580 mg, 70 %). RMN 1H (500 MHz, CDCla) 8 ppm 8,59 (s, 2H), 5,11 (s, 1H), 4,71 (s, 1H), 3,92 - 3,83 (m, 2H), 3,66 - 3,53 (m, 2H), 2,02 - 1,89 (m, 2H), 1,32 (s, 12H).
I N T E R M E D I O
33-MÉTODO F
4-(5-Bromop¡r¡m¡d¡n-2-¡l)tetrah¡drop¡ran-4-ol
Se d¡solv¡ó 5-bromo-2-yodop¡r¡m¡d¡na (2 g, 7,02 mmol) en tolueno seco (30 ml) y se enfr¡ó a -78 °C en una atmósfera de n¡trógeno. Se añad¡ó gota a gota una soluc¡ón 2,5 M de n-BuL¡ en hexano (2,95 ml) y la reacc¡ón se ag¡tó durante 15 m¡nutos antes de la ad¡c¡ón gota a gota de tetrah¡dro-4H-p¡ran-4-ona (0,77 g, 7,72 mmol). La reacc¡ón se ag¡tó a -78 °C durante 30 m¡n y después se dejó calentar a t.a. La mezcla de reacc¡ón se d¡luyó con agua (50 ml) y se extrajo con EtOAc (2 x 50 ml). Los extractos orgán¡cos comb¡nados se secaron sobre sulfato de magnes¡o y el d¡solvente se ret¡ró a pres¡ón reduc¡da para proporc¡onar 1,91 g de producto en bruto en forma de un ace¡te de color naranja. El ace¡te en bruto de color naranja se pur¡f¡có por cromatografía en columna ultrarráp¡da (S¡O2, EtOAc al 10-100 % en heptano) para proporc¡onar 762 mg (42 %) del compuesto del título en forma de un ace¡te de color amar¡llo. RMN 1H (500 MHz, CDCb) 8 ppm 8,79 (s, 2H), 4,24 (s, 1H), 3,99 - 3,89 (m, 4H), 2,37 (td, J 12,3, 11,6, 6,3 Hz, 2H), 1,54 (dd, J 13,6, 2,0 Hz, 2H).
I N T E R M E D I O 3 4 -
MÉTODO G
[4-(5-bromop¡r¡m¡d¡n-2-¡l)tetrah¡drop¡ran-4-¡l1ox¡-tr¡met¡l-s¡lano
Se añad¡ó cloruro de tr¡met¡ls¡l¡lo (277 mg, 2,55 mmol) a una soluc¡ón ag¡tada del Intermedio 33 (85 %, 740 mg, 2,43 mmol) e ¡m¡dazol (198 mg, 2,91 mmol) en DCM (15 ml) y la reacc¡ón se ag¡tó durante 1 h. Se añad¡eron más cant¡dades de cloruro de tr¡met¡ls¡l¡lo (66 mg, 0,61 mmol) e ¡m¡dazol (40 mg, 0,61 mmol) y la mezcla se ag¡tó durante 1 h. La reacc¡ón se lavó con agua (2 x 15 ml) y la fase ac. se extrajo de nuevo con DCM (20 ml). Los extractos orgán¡cos comb¡nados se secaron sobre sulfato de magnes¡o y se concentraron a pres¡ón reduc¡da, el ace¡te de color amar¡llo resultante se pur¡f¡có por cromatografía en columna ultrarráp¡da (SO 2, EtOAc al 0-15 % en heptano) para proporc¡onar 623 mg (77 %) del compuesto del título en forma de un ace¡te de color amar¡llo, que cr¡stal¡zo tras un per¡odo de reposo. RMN 1H (500 MHz, CDCb) 8 ppm 8,80 (s, 2H), 3,90 (td, J 11,0, 2,5 Hz, 2H), 3,74 (dt, J 11,4, 4,1 Hz, 2H), 2,26 (ddd, J 14,1, 10,4, 4,4 Hz, 2H), 1,99 (dt, J 11,6, 2,1 Hz, 2H), 0,00 (s, 9H).
I N T E R M E D I O 3 5 -
MÉTODO H
tr¡met¡l-r4-r5-(4.4.5.5-tetramet¡l-1.3.2-d¡oxaborolan-2-¡l)p¡r¡m¡d¡n-2-¡lltetrah¡drop¡ran-4-¡llox¡-s¡lano
Una soluc¡ón del Intermedio 34 (623 mg. 1.88 mmol) en 1.4-d¡oxano (25 ml) se trató con b¡s-p¡nacolatod¡boro (573 mg.
2.26 mmol) y acetato potás¡co (0.35 ml. 5.64 mmol). La mezcla se desgas¡f¡có con n¡trógeno durante 10 m¡nutos antes de la ad¡c¡ón de aducto de Pd(dppf)Cl2 DCM (77 mg. 0.09 mmol) y después se ag¡tó a 80 °C durante 1 h. La reacc¡ón se concentró. se d¡solv¡ó de nuevo en EtOAc (30 ml) y se lavó con una soluc¡ón al 10 % p/v de ác¡do cítr¡co en agua (30 ml). La fase orgán¡ca se secó sobre sulfato de magnes¡o y el d¡solvente se ret¡ró a pres¡ón reduc¡da. El ace¡te en bruto de color pardo resultante por cromatografía en columna ultrarráp¡da (S¡O2. EtOAc al 10-40 % en heptano). Las fracc¡ones pert¡nentes se comb¡naron para proporc¡onar 228 mg (25 %) del compuesto del título en forma de un ace¡te de color amar¡llo que cr¡stal¡zó tras un per¡odo de reposo. RMN 1H (500 MHz. CDCb) 6 ppm 9.01 (s. 2H). 3.91 (t. J 9.9 Hz. 2H). 3.79 - 3.69 (m. 2H). 2.38 - 2.23 (m. 2H). 1.98 (d. J 13.2 Hz. 2H). 1.36 (s. 12H). 0.00 (s. 9H).
I N T E R M E D I O S 36 y 37
Los s¡gu¡entes ¡ntermed¡os se prepararon por el Método E a part¡r de 2-cloro-5-(tetramet¡l-1.3.2-d¡oxaborolan-2-¡l)p¡r¡m¡d¡na usando la am¡na adecuada.
I N T E R M E D I O S 38 a 43
Los s¡gu¡entes ¡ntermed¡os se prepararon por el Método F a part¡r de 5-bromo-2-yodop¡r¡m¡d¡na usando la cetona sust¡tu¡da adecuada.
I N T E R M E D I O S 44 - 48
Los s¡gu¡entes ¡ntermed¡os se prepararon por el Método G a part¡r de los Intermedios 38 a 43 precursores correspond¡entes.
I N T E R M E D I O S 49 - 53
Los siguientes Intermedios pueden sintetizarse a partir de los Intermedios 44-48 precursores correspondientes por el Método H.
I N T E R M E D I O 54
(R)-7-Bromo-1-(2-difluorometoxi-fenil)-6-fluoro-3-metilsulfanil-2.3-dihidro-1H-ciclopentar4.5limidazor1.2-alpmdina
El Ejemplo 19 (80 mg, 0,19 mmol) se disolvió en DCM (2 ml) en una atmósfera de nitrógeno. Después, la mezcla se enfrió a 0 °C y se añadió TEA (32 pl, 0,23 mmol), seguido de cloruro de metanosulfonilo (18 pl, 0,32 mmol). La mezcla de reacción se agitó a t.a. durante 2 h. La mezcla se enfrió a 0 °C, se diluyó con DCM (5 ml) y después se añadió agua (5 ml). La fase orgánica se lavó con agua (2 x 5 ml), se secó sobre sulfato sódico y se concentró al vacío para proporcionar 95 mg de mesilato en bruto en forma de un residuo de color pardo. El residuo en bruto se disolvió en THF (1 ml) en una atmósfera de nitrógeno. Después, la mezcla se enfrió a 0 °C y se añadió tiometóxido sódico (27 mg, 0,39 mmol). La mezcla de reacción se dejó calentar a t.a. y se agitó durante 24 h. Se añadió 15-Corona-5 (42 mg, 0,19 mmol) a la mezcla de reacción y se agitó a t.a. durante 24 h. Se añadió más cantidad de tiometóxido sódico (27 mg, 0,39 mmol) y la mezcla de reacción se agitó a 50 °C durante 5 h. La mezcla se diluyó con agua (2 ml) y se extrajo con EtOAc (3 x 3 ml). La fase orgánica combinada se lavó con salmuera (5 ml), se secó sobre sulfato sódico y se concentró al vacío. El residuo se purificó por cromatografía en columna ultrarrápida (SiO2, EtOAc al 0-100 % en heptano), para proporcionar 46 mg (47 %) del compuesto del título en forma de un aceite de color naranja pálido. CLEM (EN+) TR 1,99 min, 443,0/445,0 (M+H)+.
I N T E R M E D I O 55
2-{5-[(R)-1-(2-Difluorometoxi-fenil)-6-fluoro-3-metilsulfanil-2,3-dihidro-1H-ciclopenta[4,51imidazo[1,2-a1piridin-7-il1-pirimidin-2-il}-propan-2-ol
El compuesto del título se preparó a partir del Intermedio 54 (45 mg, 0,10 mmol) y éster de boronato de 2-pirimidin-2-il propan-2-ol (40 mg, 0,15 mmol), por el Método A, para dar (10 mg,19 %) del compuesto del título en forma de un aceite de cristalización pálido. CLEM (EN+) TR 1,81 min, 501,0 (M+H)+.
I N T E R M E D I O 56
4-(5-Bromopir¡d¡n-2-¡l)oxan-4-ol
El compuesto del título se preparó a partir de 2,5dibromopiridina (5 g, 21,11 mmol) y tetrahidro-4H-piran-4-ona (2,92 ml, 0,03 mol) por el Método F (2,11 g, 39 %). CLEM (EN+) TR 1,53 min, 258,0/260,0 (M+H)+.
I N T E R M E D I O 57
r4-(5-bromo-2-piridil)tetrahidropiran-4-il1oxi-trimetil-silano
El compuesto del título se preparó a partir del Intermedio 56 (2,11 g, 8,17 mmol) y cloruro de trimetilsililo (1,35 ml, 10,63 mmol) por el Método G (2,55 g, 91 %). RMN 1H (500 MHz, CDCla) 8 ppm 8,60 (d, J 2,0 Hz, 1H), 7,81 (dd, J 8,5, 2,4 Hz, 1H), 7,44 - 7,38 (m, 1H), 3,95 - 3,76 (m, 4H), 2,18 (ddd, J 14,7, 11,0, 4,8 Hz, 2H), 1,89 (dd, J 14,2, 2,5 Hz, 2H), 0,00 (s, 9H).
I N T E R M E D I O 58
tr¡met¡l-[4-[5-(4.4.5.5-tetramet¡l-1.3.2-d¡oxaborolan-2-¡l)-2-p¡r¡d¡l1tetrah¡drop¡ran-4-¡l1ox¡-s¡lano
El compuesto del título se preparó a partir del Intermedio 57 (1 g, 3,03 mmol) y 4,4,4',4',5,5,5',5'-octametil-2,2'-bi-1,3,2-dioxaborolano (923 mg, 3,63 mmol) por el Método H, (1,78 g, rendimiento cuantitativo). RMN 1H (500 MHz, CDCb) 8 8,89 (s, 1H), 8,05 (dd, J 7,9, 1,5 Hz, 1H), 7,48 (d, J 7,9 Hz, 1H), 3,90 (td, J 11,1, 2,2 Hz, 2H), 3,82 (dt, J 11,3, 4,0 Hz, 2H), 2,22 (ddd, J 15,1, 11,3, 4,7 Hz, 2H), 1,91 (d, J 11,9 Hz, 2H), 1,35 (s, 12H), 0,00 (s, 9H).
I N T E R M E D I O 59
4-(5-bromop¡r¡m¡d¡n-2-¡l)-1,1-d¡oxo-t¡an-4-ol
Se añadió peryodato sódico (10,53 g, 49,23 mmol) a una solución del Intermedio 42 (3,46 g, 12,31 mmol) en una mezcla de agua (54 ml) y MeOH (40 ml) a 0 °C. La mezcla de reacción se agitó y se calentó progresivamente durante
3 h antes de calentarse a 70 °C durante 18 h. La mezcla de reacción se dejó enfriar a t.a., se diluyó con agua (50 ml) y se extrajo usando EtOAc (3 x 50 ml). Los extractos orgánicos combinados se lavaron con agua (20 ml), se secaron sobre sulfato sódico y se concentraron al vacío para dar un sólido de color amarillo brillante, que se suspendió en EtOAc caliente (5 ml) y después se diluyó con heptano (15 ml). La mezcla se dejó reposar durante 15 minutos y el sólido resultante se filtró y se concentró al vacío para proporcionar 2,54 g (67 %) del compuesto del título en forma de un sólido de color blanquecino. RMN 1H (500 MHz, CDCI3) 8 ppm 8,82 (s, 2H), 4,48 (s, 1H), 3,60 (td, J 13,9, 3,6 Hz, 2H), 3,10 - 2,97 (m, 2H), 2,89 (td, J 14,2, 3,5 Hz, 2H), 2,08 - 1,99 (m, 2H).
I N T E R M E D I O 60
r4-(5-bromopirimidin-2-iI)-1,1-dioxo-tian-4-iI1oxi-trimetiI-siIano
El compuesto del título se preparó a partir del Intermedio 59 (2,54 g, 8,27 mmol), cloruro de trimetilsililo (1,18 ml, 9,21 mmol) por el Método G (2,7 g, 86 %). RMN 1H (500 MHz, CDCla) 8 ppm 8,81 (s, 2H), 3,44 (td, J 13,5, 3,6 Hz, 2H), 3,04 - 2,90 (m, 2H), 2,75 - 2,53 (m, 4H), 0,00 (s, 9H). CLEM (EN+) TR 2,03 min, 379,0/381,0 (M+H)+.
I N T E R M E D I O 61
r1,1-dioxo-4-r5-(4,4,5,5-tetrametiI-1,3,2-dioxaboroIan-2-iI)pirimidin-2-iI1tian-4-iI1oxi-trimetiI-s¡Iano
El compuesto del título se preparó a partir del Intermedio 60 (2,7 g, 7,12 mmol) y bis(pinacolato)diboro (2,16 g, 8,51 mmol) por el Método H (1,93 g, 59 %). RMN 1H (500 MHz, DMSO-d6) 8 8,99 (s, 2H), 3,28 - 3,20 (m, 2H), 3,14 -3,05 (m, 2H), 2,62 - 2,52 (m, 2H), 2,43 - 2,33 (m, 2H), 1,32 (s, 12H), 0,00 (s, 9H).
I N T E R M E D I O 62
1,1-dióxido de 4-r5-(4,4,5,5-tetrametiI-1,3,2-dioxaboroIan-2-iI)pirimidin-2-iI1-1,4-tiazinano
El compuesto del título se preparó a partir de dióxido de tiomorfolina (562 mg, 4,16 mmol) y 2-cloro-5-(tetrametil-1,3,2-dioxaborolan-2-il)pirimidina (1 g, 4,16 mmol) por el Método E (1,38 g, 85 %). RMN 1H (500 MHz, DMSo-d6) 8 8,55 (s, 2H), 4,33 - 4,16 (m, 4H), 3,25 - 3,12 (m, 4H), 1,28 (s, 12H).
I N T E R M E D I O 63
terc-But¡l-c¡clopent-3-en-1-ilox¡-d¡met¡l-s¡lano
Se disolvió ciclopent-3-en-1-ol (10 g, 118,9 mmol) en DMF (100 ml) a 0 °C, después se añadió 1H-imidazol (17,29 ml, 261,5 mmol), seguido de terc-butil(cloro)dimetilsilano (21,5 g, 142,7 mmol) y se calentó hasta t.a. La mezcla se agitó a t.a. durante 14 h, se diluyó con EtOAc (300 ml) y se lavó con LiCl a 5 % (2 x 100 ml) y salmuera (50 ml), se secó sobre sulfato sódico, se filtró y se concentró a presión reducida. El residuo en bruto se purificó por cromatografía en columna ultrarrápida (S¡O2, EtOAc al 0-10 % en hexanos) para proporcionar 17,2 g (73 %) del producto del título en forma de un líquido incoloro y transparente. RMN 1H (250 MHz, Cd C|3) 8 ppm 5,66 (s, 2H), 4,53 (tt, J 7,0, 3,6 Hz, 1H), 2,57 (dd, J 15,2, 6 ,8 Hz, 2H), 2,27 (dd, J 15,3, 3,6 Hz, 2H), 0,89 (s, 9H), 0,06 (s, 6 H).
I N T E R M E D I O 64
3-rterc-ButiI(dimetiI)siIiI1oxibicicIor3.1.01hexano-6-carboxiIato de etilo
Se añadió lentamente 1-(2-etoxi-2-oxoetilideno)diazenio (6,07 ml, 48,4 mmol) en DCM (4 ml) mediante una bomba de jeringa durante 6 h a la solución agitada del Intermedio 63 (8 g, 40,3 mmol) y acetato de rodio (II) (178,24 mg, 0,4 mmol) en DCM (150 ml) en una atmósfera de nitrógeno a t.a. La mezcla se agitó durante 14 h a t.a., después se filtró a través de celite y se concentró a presión reducida para proporcionar un aceite de color pardo claro. El material en bruto se purificó por cromatografía en columna ultrarrápida (S¡O2, EtOAc al 5-30 % en heptano) para proporcionar 7,15 g (59 %) del compuesto del título como una mezcla de isómeros (exo: endo; 2,5:1) en forma de un aceite incoloro y transparente. RMN 1H (500 MHz, CDCI3) 8 ppm 4,12 - 4,03 (m, 2H), 2,13 (dd, J 13,0, 7,2 Hz, 1H), 2,05 (ddd, J 13,2, 5,8, 3,4 Hz, 1H), 1,88 - 1,69 (m, 4H), 1,51 (d, J 14,7 Hz, 1H), 1,28 - 1,19 (m, 4H), 0,88 - 0,82 (m, 9H), 0,04-0,03 (m, 6 H).
I N T E R M E D I O 65
3-H¡drox¡bic¡cIor3.1.01hexano-6-carbox¡Iato de etilo
Se añadió gota a gota TBAF 1 M (68,13 ml) a la solución agitada del Intermedio 64 (95 % puro, 10,2 g, 34,06 mmol) en THF (100 ml) a t.a., después la mezcla se calentó a 50 °C durante 1 hora. La mezcla se enfrió a t.a. y se concentró a presión reducida para proporcionar un aceite de color parduzco claro. El residuo se diluyó con EtOAc (300 ml) y se lavó con agua (2 x 100 ml) y salmuera (50 ml), se secó sobre sulfato de magnesio y se concentró a presión reducida
para proporcionar 9,4 g (en bruto) del compuesto del título en forma de un aceite de color rojizo claro. RMN 1H (500 MHz, CDCb) 8 ppm 4,15 - 4,05 (m, 2H), 2,26 (dd, J 13,1, 7,1 Hz, 1H), 2,20 - 2,11 (m, 1H), 1,99 - 1,93 (m, 1H), 1,92 - 1,84 (m, 4H), 1,84 - 1,75 (m, 1H), 1,64 - 1,53 (m, 1H), 1,30 - 1,20 (m, 3H).
I N T E R M E D I O 66
(1S.5R)-3-Oxob¡c¡clo[3.1.01hexano-6-carboxilato de etilo
El Intermedio 65 (60 % puro, 9,4 g, 33,14 mmol) se disolvió en DCM (100 ml). peryodinano de Dess-Martin (28,11 g, 0,07 mol) se añadió en forma de un sólido y la mezcla se agitó a t.a durante 15 h. La mezcla se diluyó con DCM (200 ml) y se lavó con bicarbonato sódico sat. (2 x 100 ml), agua (100 ml) y salmuera (50 ml), después se secó sobre sulfato sódico y se concentró a presión reducida para proporcionar un sólido de color blanquecino. El producto en bruto se purificó por cromatografía en columna ultrarrápida (SO 2, EtOAc al 30-100 % en heptano) para proporcionar 3,15 g (56 %) del compuesto del título en forma de un aceite de color pardo claro. RMN 1H (500 MHz, cD cb) 8 ppm 4,15 (c, J 7,1 Hz, 2H), 2,66 (ddt, J 18,5, 3,9, 1,6 Hz, 2H), 2,31 (d, J 1,8 Hz, 1H), 2,27 (d, J 1,7 Hz, 2H), 2,18 (td, J 3,4, 1,6 Hz, 2H), 1,31 - 1,23 (m, 3H).
I N T E R M E D I O 67
(1S,5S,6R)-3-(T rifluorometanosulfoniloxi)biciclo[3.1.01hex-2-eno-6-carboxilato de etilo
El Intermedio 6 6 (3 g, 17,84 mmol) se disolvió en tolueno seco (60 ml), se añadió DIPEA (12,5 ml, 71,35 mmol) y la mezcla de reacción se calentó a 45 °C. Se añadió anhídrido tríflico (12 ml, 71,35 mmol), la temperatura ascendió a 70 °C y la reacción se enfrió de nuevo usando un baño de hielo. La mezcla se agitó durante 1,5 h a 45 °C. La reacción se diluyó con EtOAc (200 ml) y se lavó con bicarbonato sódico sat. (2 x 100 ml). Los lavados ac. se extrajeron con EtOAc (200 ml), los extractos orgánicos se combinaron, se lavaron con salmuera (50 ml), se secaron sobre sulfato sódico y se concentraron. El producto en bruto se purificó por cromatografía en columna ultrarrápida (SO 2, EtOAc al 0-20 % en heptano) para proporcionar 2,73 g (51 %) del producto del título. RMN 1H (250 MHz, CDCb) 8 ppm 5,87 (d, J 1,9 Hz, 1H), 4,14 (c, J 7,1 Hz, 2H), 3,00 (dd, J 17,2, 6,2 Hz, 1H), 2,75 - 2,60 (m, 1H), 2,46 - 2,31 (m, 1H), 2,23 - 2,11 (m, 1H), 1,39 - 1,32 (m, 1H), 1,32 - 1,16 (m, 3H).
I N T E R M E D I O 68
(1S.5S.6R)-3-(Tetramet¡l-1.3.2-d¡oxaborolan-2-¡l)b¡c¡clo[3.1.01hex-2-eno-6-carbox¡lato de etilo
El Intermedio 67 (2,73 g, 9,09 mmol) se disolvió en 1,4-dioxano (60 ml) y se desgasificó usando una atmósfera de nitrógeno durante 5 minutos. Se añadieron bis(pinacolato)diborano (3,46 g, 13,64 mmol), acetato potásico (2,68 g, 27,28 mmol), 1,1'-bis(difenilfosfanil)ferroceno (0,15 g, 0,27 mmol) y aducto de Pd(dppf)Cl2 DCM (0,22 g, 0,27 mmol) y la reacción se calentó en atmósfera de nitrógeno a 90 °C durante 18 h. La reacción se enfrió a t.a., se diluyó con EtOAc (200 ml) y se lavó con una solución ac. sat. de bicarbonato sódico (2 x 100 ml). Los lavados ac. se extrajeron de nuevo con EtOAc (50 ml). Los extractos orgánicos se combinaron, se lavaron con salmuera, se secaron sobre sulfato sódico y se concentraron. El residuo en bruto se purificó por cromatografía en columna ultrarrápida (SiO2, EtOAc al 0-40 % en heptano) para proporcionar 2,0 g (59 %) del compuesto del título. RMN 1H (250 m Hz , CDCb) 8 ppm 6,66 (d, J 1,9 Hz, 1H), 4,11 (c, J 7,1 Hz, 2H), 2,88 - 2,73 (m, 1H), 2,66 - 2,44 (m, 2H), 2,33 - 2,22 (m, 1H), 1,34 - 1,18 (m, 16H).
I N T E R M E D I O 69
2-[4-(5.5-d¡met¡l-1.3.2-d¡oxabor¡nan-2-¡l)fen¡l1-1.1.1.3.3.3-hexafluoro-propan-2-ol
Se disolvieron 2-(4-bromofenil)-1,1,1,3,3,3-hexafluoro-2-propanol (0,93 mmol, 300 mg), bis(glicolato de neopentilo)diboro (1,91 mmol, 450 mg) y acetato potásico (2,88 mmol, 285 mg) en DMSO (5 ml). Esto se desgasificó con tres ciclos vacío y nitrógeno antes de la adición de Pd(dppf)Cl2 (5 mol%). Después, la reacción se calentó durante 1 h a 100 °C. Después de dejarse enfriar a t.a., la solución se filtró a través de celite y se repartió entre EtOAc y agua. La capa ac. se llevó a pH10 con una solución al 10 % de hidróxido sódico y se lavó con EtOAc. Después, la capa básica ac. resultante se redujo a pH 5 usando HCl 2 M y se extrajo con EtOAc. La fase orgánica se secó sobre sulfato sódico, se filtró y se concentró al vacío, produciendo el compuesto del título (255 mg, 77 %). 8h (300 MHz, DMSO-d6) 8,71 (s, 1H); 7,82 (d, J 8,5 Hz, 2H); 7,67 (d, J 8,0 Hz, 2H); 3,77 (s, 4H); 0,96 (s, 6H). CLEM (EN+) TR 1,49 min 287,0 (M-[CH2-C(CHa)2-CH2]+3H)+.
I N T E R M E D I O 70
(1R.3R)-6-Fluoro-7-[4-(1-metanosulfon¡l-et¡l)-fen¡l1-1-fen¡l-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ol
El compuesto del título se preparó a partir del Ejemplo 75 (0,2 g, 0,5794 mmol, 1,0 equiv.) y tri-sec-butilborohidruro de litio (0,8691 ml, 0,8691 mmol, 1,5 equiv.) por el Método B (0,2 g). CLEM (EN+) TR 1,45 min, 451,0 (M+H)+.
I N T E R M E D I O 71
9-[5-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)pinmidin-2-il1-3,7-dioxa-9-azabiciclo[3.3.11nonano
El compuesto del título se preparó a partir de 3,7-dioxa-9-azabiciclo[3.3.1]nonano (2,04 g, 15,8 mmol) y 2-cloro-5-(tetrametil-1,3,2-dioxaborolan-2-il)pirimidina (3,8 g, 15,8 mmol) por el Método E (2,0 g, 76 %). CLEM (EN+) TR 1,80 min, 334,0 (M+H)+.
I N T E R M E D I O 72
(1R.3S)-7-bromo-1-[2-(d¡fluorometox¡)fen¡l1-2.3-d¡h¡dro-1H-c¡clopenta[4,51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ol
El compuesto del titulo se preparó a partir del Ejemplo 2 (0,50 g, 1,2 mmol) y borohidruro sódico (0,05 g, 1,4 mmol) por el Método C para producir (R)-7-bromo-1-[2-(difluorometoxi)fenil1-2,3-dihidro-1H-ciclopenta[4,51¡midazo[1,2-a1piridin-3-ol. El compuesto del título se aisló mediante purificación quiral de (R)-7-bromo-1-[2-(difluorometoxi)fenil1-2,3-dihidro-1H-ciclopenta[4,51¡midazo[1,2-a1piridin-3-ol en condiciones de SFC en un Lux-Cell-4 (50 x 291 mm x mm, flujo 360 ml/min, 25 °C, CO2 + 20 % de MeOH, inyección de 6,8 ml de solución a una concentración de 100 g/l). El primer diastereómero en eluirse (TR 4,61 min) se recogió y las fracciones se evaporaron para producir (1R,3R)-7-bromo-1-[2-(difluorometoxi)fenil1-2,3-dihidro-1H-ciclopenta[4,51¡midazo[1,2-a1piridin-3-ol. El segundo diastereómero en eluirse (TR 8,74 min) se recogió y las fracciones se evaporaron para producir el compuesto del título. CLEM (EN+) TR 1,43 min, 395,0/397,0 (M+H)+.
I N T E R M E D I O 73
A/-r(4-Bromofen¡l)(met¡l)oxo-Á6-sulfan¡l¡denol-2.2.2-tr¡fluoroacetamida
A una suspensión de 1-bromo-4-metanosulfinilbenceno (5 g, 22,8 mmol), MgO (3,68 g, 91,3 mmol), tetraquis(acetato-KO)dirrodio(Rh-Rh) (0,25 g, 0,570 mmol) y 2,2,2-trifluoroacetamida (5,16 g, 45,6 mmol) en DCM anhidro (150 ml) se añadió bis(acetiloxi)(fenil)-lambda~3~-yodano (11,03 g, 34,2 mmol) a temperatura ambiente. La reacción se dejó en agitación a t.a. durante 18 h. La mezcla de reacción se filtró sobre celite y la torta de filtro se lavó con DCM (30 ml). El filtrado se concentró al vacío y se purificó por cromatografía en columna (SiO2, EtOAc al 0-100 % en heptano), produciendo el compuesto del título en forma de un aceite de color amarillo claro (5,7 g, 97 %). RMN 1H (250 MHz, CDCla) 8 ppm 7,92 - 7,75 (m, 4H), 3,45 (s, 3H). CLEM (EN+) TR 1,27 min, 330,0/332,0 (M+H)+.
I N T E R M E D I O 74
(4-bromofenil)-¡m¡no-met¡l-oxo-Á6-sulfano
A una solución del Intermedio 73 (5,7 g, 17,1 mmol) en MeOH (100 ml) se añadió carbonato potásico (11,6 g, 83,7 mmol). La reacción se dejó en agitación a t.a. durante 2 h. La mezcla se redujo al vacío, después se diluyó con agua (50 ml). El producto se extrajo con EtOAc (3 x 100 ml). La fracción orgánica combinada se secó (MgSO4) y se redujo al vacío para producir el compuesto del título en forma de un aceite de color amarillo (4,00 g, 96 %). RMN 1H (500 MHz, CDCla) 8 ppm 7,89 - 7,83 (m, 2H), 7,70 - 7,65 (m, 2H), 3,09 (s, 3H), 2,65 (s, 1H). CLEM (EN+) TR 0,81 min,
234,0/236,0 (M+H)+.
I N T E R M E D I O 75
Im¡no-met¡l-oxo-f4-(4.4.5.5-tetramet¡l-1.3.2-d¡oxaborolan-2-il)fen¡l1-Á-6-sulfano
El compuesto del título se preparó a part¡r del Intermedio 74 (4 g. 15.4 mmol) y 4.4.4'.4'.5.5.5'.5'-octamet¡l-2.2'-b¡-1.3.2-d¡oxaborolano (4.69 g. 18.5 mmol) por el Método H (3.05 g. 60 %). RMN 1H (500 MHz. CDCb) 8 ppm 8.02 - 7.98 (m.
4H). 3.09 (s. 3H). 1.36 (s. 12H).
I N T E R M E D I O 76
1-óx¡do de 4-(5-bromop¡r¡m¡d¡n-2-¡l)-1.4-t¡az¡nano
El compuesto del título se preparó a part¡r de 5-bromo-2-yodop¡r¡m¡d¡na (1.98 g. 6.95 mmol) y 1-óx¡do de t¡omorfol¡na (1.3 g. 8.34 mmol) por el Método E (1.63 g. 85 %). RMN 1H (250 MHz. CDCb) 8 ppm 8.34 (s. 2H). 4.64 - 4.39 (m. 2H).
4.28 - 4.00 (m. 2H). 2.94 - 2.63 (m. 4H). CLEM (EN+) TR 1.13 m¡n. 276/278 (M+H)+.
I N T E R M E D I O 77
N-[4-(5-bromop¡r¡m¡d¡n-2-¡l)-1-oxo-1.4-t¡az¡nan-1-¡l¡deno1-2.2.2-tr¡fluoro-acetam¡da
A una suspens¡ón del Intermedio 76 (600 mg. 2.17 mmol). MgO (350 mg. 8.69 mmol). tetraqu¡s(acetato-KO)d¡rrod¡o(Rh-Rh) (24 mg. 0.05 mmol) y 2.2.2-tr¡fluoroacetam¡da (491 mg. 4.35 mmol) se añad¡ó b¡s(acet¡lox¡)(fen¡l)-lambda~3~-yodano (1.05 g. 3.26 mmol). La reacc¡ón se ag¡tó durante 5 h a t.a. La mezcla de reacc¡ón se f¡ltró sobre cel¡te. se concentró y se pur¡f¡có por cromatografía en columna (S¡O2. EtOAc al 0-100 % en heptano) para produc¡r el compuesto del título en forma de un sól¡do de color blanco (706 mg. 83 %). RMN 1H (250 MHz. CDCl3) 8 ppm 8.41 (s.
2H). 4.76 - 4.50 (m. 2H). 4.21 - 4.01 (m. 2H). 3.83 - 3.66 (m. 2H). 3.44 - 3.22 (m. 2H). CLEM (EN+) TR 1.32 m¡n 387/389 (M+H)+.
I N T E R M E D I O 78
1-óx¡do de 4-(5-bromop¡r¡m¡d¡n-2-¡l)-1-¡m¡no-1.4-t¡az¡nano
El Intermedio 77 (706 mg. 1.81 mmol) se d¡solv¡ó en MeOH (15 ml) y se añad¡ó K2CO3 (1.25 g. 9.03 mmol). La reacc¡ón se ag¡tó a t.a. durante 1 h. La mezcla de reacc¡ón se concentró al vacío y se pur¡f¡có por cromatografía en columna (SO2. EtOAc al 0-100 % en heptano. segu¡do de MeOH al 0-10 % en DCM) para produc¡r el compuesto del título en forma de un sól¡do de color blanco (452 mg. 83 %). RMN 1H (250 MHz. CDCla) 8 ppm 8.36 (s. 2H). 4.47 - 4.36 (m. 2H).
4.29 - 4.18 (m. 2H). 3.08 (t. J 5.3 Hz. 4H). CLEM (EN+) TR 0.91 m¡n. 291.0/293.0 (M+H)+.
I N T E R M E D I O 79
1-óx¡do de 1-¡m¡no-4-r5-(4.4.5.5-tetramet¡l-1.3.2-d¡oxaborolan-2-¡l)p¡r¡m¡d¡n-2-¡l1-1.4-t¡az¡nano
El compuesto del título se preparó a part¡r del Intermedio 78 (0.46 g. 1.57 mmol) y 4.4.4'.4'.5.5.5'.5'-octamet¡l-2.2'-b¡-1.3.2-d¡oxaborolano (0.48 g. 1.88 mmol) por el Método H (0.327 g. 53 %). RMN 1H (500 MHz. CDCb) 8 ppm 8.64 (s.
2H). 4.62 - 4.50 (m. 2H). 4.33 - 4.21 (m. 2H). 3.23 (dd. J 12.4. 3.9 Hz. 2H). 3.11 (ddd. J 12.9. 8.2. 3.0 Hz. 2H). 1.33 (s.
12H). CLEM (EN+) TR 1.13 m¡n. 339.0 (M+H)+.
I N T E R M E D I O 80
Ác¡do r2-(morfol¡n-4-¡l)p¡r¡m¡d¡n-5-¡l1borón¡co
Una soluc¡ón de ác¡do (2-clorop¡r¡m¡d¡n-5-¡l)borón¡co (1 g. 6.32 mmol). morfol¡na (2.19 ml. 25.26 mmol) y tr¡et¡lam¡na (0.9 ml. 6.32 mmol) en etanol (25 ml) se ag¡tó a 20 °C durante 1 h. Se añad¡ó lentamente agua (50 ml) a la mezcla de reacc¡ón para formar un prec¡p¡tado. que se recog¡ó por f¡ltrac¡ón. para proporc¡onar el compuesto del título en forma de un sól¡do de color crema (950 mg. 70 %). 8H (250 MHz. DMSO-d6) 8.63 (s. 2H). 8.05 (s. 2H). 3.68 (ddd. J 23.4. 5.7.
3.9 Hz. 8H). CLEM (EN+) 210.0 (M+H)+.
I N T E R M E D I O 81
6-Bromo-3-r(1 E)-3-etox¡-3-oxoprop-1-en-1-¡l1-7-fluoro¡m¡dazoH.2-a1p¡r¡d¡n-2-carbox¡lato de etilo
Se disolvió 6-bromo-7-fluoro-3-yodoimidazo[1,2-a]piridin-2-carboxilato de etilo (5 g, 11,62 mmol) en DMF (100 ml) en una atmósfera de nitrógeno. Se añadió Na2CO3 (1,36 g, 12,79 mmol) en agua (6,4 ml). Se añadieron prop-2-enoato de etilo (1,36 ml, 12,79 mmol) y bis[3-(difenilfosfanil)ciclopenta-2,4-dien-1-il]hierro; diclorometano; dicloropaladio (0,47 g, 0,58 mmol) y la mezcla se calentó a 100 °C durante 2 h. La mezcla de reacción se enfrió y se vertió sobre hielo y el matraz se lavó con agua (4 x 10 ml). La mezcla acuosa combinada se agitó durante 45 min, se calentó a t.a. La suspensión se recogió por filtración, lavando con agua (x 3). El sólido se secó al vacío. El residuo en bruto se purificó por cromatografía (SiO2, EtOAc al 20-35 % en Heptano) y el compuesto del título se aisló en forma de un sólido de color amarillo (1,60 g, 36 %). RMN 1H (500 MHz, CDCla) 8 ppm 8,61 (d, J 6,2 Hz, 1H), 8,33 (d, J 16,6 Hz, 1H), 7,48 (d, J 8,0 Hz, 1H), 6,76 (d, J 16,6 Hz, 1H), 4,51 (c, J 7,1 Hz, 2H), 4,33 (c, J 7,1 Hz, 2H), 1,47 (t, J 7,1 Hz, 3H), 1,38 (t, J 7,1 Hz, 3H). CLEM (EN+) TR 1,95 min, 385,0/387,0 (M+H)+.
I N T E R M E D I O 82
6- Bromo-3-[3-etox¡-1-(2-metox¡fen¡l)-3-oxoprop¡l1-7-fluoro¡m¡dazo[1,2-a1p¡r¡d¡n-2-carbox¡lato de etilo
Una suspensión de (1Z)-cicloocta-1,5-dieno - clororrodio (1:1) (128 mg, 0,26 mmol) en dioxano seco (15 ml) y agua (3 ml) se sometió a ultrasonidos a temperatura ambiente en una atmósfera de nitrógeno durante 5 min. La solución de color amarillo resultante se agitó a t.a. durante 30 min antes de añadirse a una suspensión del Intermedio 81 (1 g, 2,60 mmol) y ácido (2-metoxifenil)borónico (986 mg, 6,49 mmol) en dioxano seco (15 ml) y K2CO3 (502 mg, 3,63 mmol) en una atmósfera de nitrógeno. La mezcla se calentó en el reactor de microondas (200 W, 100 °C) durante 30 min. La reacción enfriada se filtró a través de una capa de celite, se lavó con EtOAc (3 x 50 ml) y los filtrados combinados se concentraron al vacío. El residuo en bruto se purificó por cromatografía (SO 2, EtOAc al 0-100 % en Heptano) y el compuesto del título se aisló en forma de un sólido de color blanco (0,76 g, 53 %). RMN 1H (500 MHz, CDCb ) 88,75 (d, J 6,5 Hz, 1H), 7,62 (dd, J 7,7, 1,4 Hz, 1H), 7,32 (d, J 8,4 Hz, 1H), 7,24 - 7,16 (m, 1H), 6,96 (td, J 7,6, 0,9 Hz, 1H), 6,82 - 6,75 (m, 1H), 5,34 (dd, J 10,5, 5,1 Hz, 1H), 4,39 (cd, J 7,1, 1,2 Hz, 2H), 4,08 - 3,89 (m, 3H), 3,66 (s, 3H), 3,25 (dd, J 16,9, 5,1 Hz, 1H), 1,38 (td, J 7,1, 2,2 Hz, 3H), 1,13 (t, J 7,1 Hz, 3H). CLEM (EN+) TR 3,76 min, 493,0/495,0 (M+H)+.
I N T E R M E D I O 8 3 ,
MÉTODO L
7- bromo-6-fluoro-1-(2-metox¡fen¡l)-3-oxo-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1,2-a1p¡r¡d¡n-2-carbox¡lato de etilo
El Intermedio 82 (372 mg, 0,75 mmol) se destiló azeotrópicamente con tolueno seco (2 x 5 ml) y después se disolvió en tolueno seco (8 ml) en una atmósfera de nitrógeno. La mezcla de reacción se enfrió a 0 °C, se añadió gota a gota pterc-pentóxido potásico (0,59 ml, solución 2 M en tolueno, 1,2 mmol) a la solución agitada mientras se mantenía la temperatura a 0 °C. La mezcla de reacción se agitó a 0 °C durante 30 min, después se añadió más cantidad de solución de terc-pentóxido potásico (0,2 ml). La mezcla de reacción se agitó durante 10 min más a 0 °C, después se inactivó con ácido acético (0,1 ml). La reacción se diluyó con agua (10 ml) y se extrajo con acetato de etilo (3 x 30 ml). Los extractos orgánicos combinados se lavaron con salmuera (15 ml), se secaron sobre sulfato sódico y se concentraron al vacío. El residuo en bruto se purificó por cromatografía (S¡O2, EtOAc al 0-70 % en Heptano) y el compuesto del título se aisló en forma de un aceite de color amarillo (0,18 g, 46 %). CLEM (EN+) t R 1,97 min, 447,0/449,0 (M+H)+.
I N T E R M E D I O 8 4 ,
MÉTODO M
7-bromo-6-fluoro-1-í2-metox¡fen¡l)-1.2-d¡h¡dro-3H-c¡clopentar4.5l¡m¡dazori.2-alp¡r¡din-3-ona
A una soluc¡ón del Intermedio 83 (180 mg. 0.4 mmol) en 4:1 de DMSO/agua des¡on¡zada (5 ml) se burbujeó n¡trógeno a su través durante 2 m¡n. La mezcla de reacc¡ón se calentó a 100 °C con ag¡tac¡ón durante 36 h en una atmósfera de n¡trógeno. Se añad¡ó agua des¡on¡zada (1 ml) y se calentó de nuevo a 100 °C durante 14 horas. La mezcla de reacc¡ón se diluyó con acetato de et¡lo (50 ml). se lavó con agua (3 x 20 ml) y salmuera (1 x 20 ml). se secó sobre sulfato sód¡co. se f¡ltró y se concentró al vacío. El producto en bruto se pur¡f¡có por cromatografía (S¡O2. EtOAc al 0-80 % en Heptano) para produc¡r el compuesto del título en forma de un sól¡do de color naranja (53 mg. 35 %). RMN 1H (500 MHz. CDCb) 8 7.90 (d. J 6.5 Hz. 1H). 7.41 (d. J 8.8 Hz. 1H). 7.31 (td. J 8.3. 1.6 Hz. 1H). 6.98 (d. J 8.2 Hz. 1H). 6.94 - 6.88 (m. 1H).
6.83 (dd. J 7.5. 1.5Hz. 1H). 5.08 (dd. J 6.9. 2.1 Hz. 1H). 3.89 (s. 3H). 3.60 (dd. J 18.4. 7.0 Hz. 1H). 2.98 (dd. J 18.4.
2.2 Hz. 1H). CLEM (EN+) TR 3.03 m¡n. 375.0/377.0 (M+H)+.
I N T E R M E D I O 85
7-bromo-6-fluoro-1-(2-metox¡fen¡l)-2.3-d¡h¡dro-1H-c¡clopentar4.5l¡m¡dazon.2-alp¡r¡d¡n-3-ol
El compuesto del título se preparó a part¡r del Intermedio 84 (53 mg. 0.14 mmol) y una soluc¡ón 1 M de tr¡-secbut¡lboroh¡druro de l¡t¡o en THF (0.09 ml. 0.7 equ¡v.) por el Método B (42 mg. 60 %). RMN 1H (500 MHz. CDCla) 87.87 (d. J 6.6 Hz. 1H). 7.33 (dd. J 9.1. 1.5 Hz. 1H). 7.28 - 7.23 (m. 1H). 7.15 (d. J 7.5 Hz. 1H). 6.96 (d. J 8.2 Hz. 1H). 6.91 (t. J 7.4 Hz. 1H). 5.38 (dd. J 7.3. 2.9 Hz. 1H). 4.82 (dd. J 8.5. 3.7 Hz. 1H). 3.95 (s. 3H). 3.53 (dt. J 14.2. 8.0 Hz. 1H).
2.44 (dt. J 14.1. 3.4 Hz. 1H). CLEM (EN+) TR 1.08 m¡n. 379.0/381.0 (M+H)+.
I N T E R M E D I O 86
2-(5-bromop¡r¡m¡d¡n-2-¡l)propan-2-ol
El compuesto del título se preparó a partir de n-BuL¡ 2.5 M en hexano (14.7 ml. 36.9 mmol). 5-bromo-2-yodop¡r¡m¡d¡na (10 g. 35.1 mmol). tolueno (200 ml) y acetona (2.83 ml. 38.6 mmol) por el Método F (2.86 g.37 %). RMN 1H (500 MHz. CDCla) 88.77 (s. 2H). 4.31 (s. 1H). 1.59 (s. 6H). CLEM (EN+) TR 1.26 m¡n. 219.0 (M+H)+.
I N T E R M E D I O 87
2-(5-bromop¡r¡m¡d¡n-2-¡l)propan-2-am¡na
El Intermedio 86 (1.00 g. 4.61 mmol) se d¡solv¡ó en aceton¡tr¡lo (10 ml) y se trató con ác¡do sulfúr¡co concentrado (1.28 ml. 8.53 mmol). La mezcla se calentó a 60 °C durante 3 h. Se añad¡ó agua (1 ml) y la mezcla de reacc¡ón se agitó a 60 °C durante 15 h. La mezcla se enfr¡ó. se vert¡ó en h¡elo/agua (60 ml) y el pH se ajustó a 14 usando una soluc¡ón 6 M de h¡dróx¡do sód¡co en agua. La mezcla se extrajo con DCM (3 x 30 ml). los extractos orgán¡cos se comb¡naron. se secaron sobre sulfato sód¡co. se f¡ltraron y se concentraron al vacío. El res¡duo de color amar¡llo resultante (0.92 g) se d¡solv¡ó en d¡oxano (6 ml). la soluc¡ón se cargó en un tubo a pres¡ón. se añad¡ó agua (4 ml) y una soluc¡ón concentrada de cloruro de h¡drógeno (12 M. 5 ml). La mezcla de reacc¡ón se cerró hermét¡camente y se ag¡tó a 100 °C durante 15 h. La mezcla se enfr¡ó. se vert¡ó en h¡elo/agua (60 ml). y el pH se ajustó a 14 usando una soluc¡ón 6 M de
hidróxido sódico en agua. La mezcla se extrajo con una mezcla 1:1 de isopropanol:cloroformo (3 x 30 ml). Los extractos orgánicos se combinaron, se secaron sobre sulfato sódico, se filtraron y se concentraron al vacío, produciendo el compuesto del título en forma de un aceite de cristalización de color pardo (621 mg, 46 %).
RMN 1H (500 MHz, CDCb) 88,73 (s, 2H), 1,78 (s a, 2H), 1,53 (s, 6H).
I N T E R M E D I O 88
N-[2-(5-bromopirimidin-2-il)propan-2-illcarbamato de terc-butilo
Se añadieron dicarbonato de di-terc-butilo (627 mg, 2,87 mmol) y W-etil-W-(propan-2-il)propan-2-amina (994 pl, 5,75 mmol) a una solución del Intermedio 87 (621 mg, 2,87 mmol) en THF. La mezcla de reacción se agitó a temperatura ambiente durante 15 h. La mezcla de reacción se diluyó con acetato de etilo (30 ml) y se lavó con agua (2 x 15 ml). Los lavados acuosos se combinaron, se extrajeron de nuevo con acetato de etilo (2 x 15 ml). Los extractos orgánicos se combinaron, se secaron sobre sulfato sódico, se filtraron y se concentraron al vacío. El aceite de color naranja resultante se purificó por cromatografía (S¡O2, EtOAc al 0-50 % en Heptano) para producir el compuesto del título en forma de un aceite incoloro (300 mg, 33 %). RMN 1H (500 MHz, CDCla) 88,73 (s, 2H), 1,69 (s, 6H), 1,40 (s, 9H). CLEM (EN+) TR 1,35 min, 219,0 (M+H)+.
I N T E R M E D I O 89
N-{2-[5-(tetrametil-1,3,2-dioxaborolan-2-il)pirimidin-2-illpropan-2-il}carbamato de terc-butilo
El compuesto del título se preparó a partir del Intermedio 8 8 (300 mg, 0,95 mmol), pinacol éster de diboro (361 mg, 1,42 mmol) y acetato potásico (279 mg, 2,85 mmol) en dioxano (5 ml) y aducto de dicloro[1,1'-bis(d¡fen¡lfosf¡noferroceno]-paladio diclorometano (39 mg, 0,05 mmol) por el Método H (149 mg, 36 %). RMN 1H (500 MHz, CDCb) 88,97 (s, 2H), 6,17 (s, 1H), 1,72 (s, 6H), 1,42 (s, 9H), 1,35 (s, 12H). CLEM (EN+) TR 1,38 min, 282,0 (M+H)+.
I N T E R M E D I O 90
(Z)-3.3-d¡fluoro-N'-h¡drox¡c¡clobut-1-carbox¡m¡dam¡da
Una solución de 3,3-difluorociclobutano-1-carbonitrilo (1 g, 8,54 mmol) en etanol (15 ml) se trató con hidroxilamina (50 % en agua) (5,25 ml, 86,0 mmol) y se agitó a 80 °C durante 3 h. La mezcla de reacción se dejó enfriar y después se concentró al vacío. El residuo se repartió entre DCM (10 ml) y agua (10 ml). La fase orgánica se separó, la fase acuosa se extrajo con DCM (3 x 5 ml),. El producto se extrajo de nuevo con 1:1 de IPA/CHCb (3 x 60 ml), la capa orgánica se separó y se secó sobre sulfato sódico y se concentró al vacío para proporcionar el compuesto del título en forma de una goma de color naranja (545 mg, 42 %). RMN 1H (500 MHz, DMSO-d6) 89,07 (s, 1H), 5,44 (s, 2H), 2,84 - 2,59 (m, 5H). CLEM (EN+) TR 0,25 min, 151,0 (M+H)+.
I N T E R M E D I O 91
3.3-d¡fluoroc¡clobutano-1-carbox¡m¡dam¡da
El Intermedio 90 (1,1 g, 7,33 mmol) se disolvió en ácido acético (20 ml), se añadió anhídrido acético (1,04 ml, 11 mmol) y la reacción se agitó durante 30 minutos en una atmósfera de nitrógeno. Se añadió polvo de cinc (4,8 g, 73,27 mmol) y la reacción continuó en agitación a t.a. en una atmósfera de nitrógeno durante 18 h. La reacción se filtró a través de Celite y se lavó con ácido acético, el disolvente se concentró al vacío. El ácido acético se destiló azeotrópicamente con tolueno (2 x 30 ml) para proporcionar una goma/sólido. Esto se sometió a ultrasonidos en éter (30 ml) durante 5 min y se filtró. El sólido se secó al aire durante 1,5 h, produciendo el compuesto del título en forma de un sólido de color blanquecino (1,41 g, 64 %). RMN 1H (500 MHz, DMSO-d6) 83,15 (s, 1H), 2,84 (s, 4H). CLEM (EN+) TR 0,15 min, 135,0 (M+H)+.
I N T E R M E D I O 92
5-bromo-2-(3.3-d¡fluoroc¡clobut¡l)p¡r¡m¡d¡na
El Intermedio 91 (75 %, 1 g, 3,86 mmol) y (2Z)-2-bromo-3-(dimetilamino)prop-2-enal (0,825 g, 4,63 mmol) se disolvieron en EtOH (30 ml) y se calentaron a 80 °C durante 2,45 h. La mezcla de reacción se dejó reposar a t.a. durante 18 h y se calentó a 80 °C durante 2 h y después a 90 °C durante 2,5 h. La reacción se enfrió a 80 °C y se agitó durante 18 h. La reacción se concentró al vacío y se añadieron DCM (50 ml) y agua (25 ml). Los extractos orgánicos se filtraron a través de Celite y se secaron sobre sulfato sódico y se concentraron al vacío. El residuo se purificó por cromatografía (SiO2, EtOAc al 0-80 % en heptano), produciendo el compuesto del título en forma de un aceite transparente (130 mg, 13 %). RMN 1H (500 MHz, CDCb) 88,74 (s, 2H), 3,59 (pd, J 8,6, 3,0 Hz, 1H), 2,99 (dt, J 16,6, 8,5 Hz, 4H). CLEM (EN+) TR 1,24 min, 251,0 (M+H)+.
I N T E R M E D I O 93
2-(3.3-d¡fluoroc¡clobut¡l)-5-(tetramet¡l-1.3.2-d¡oxaborolan-2-¡l)p¡r¡m¡d¡na
El compuesto del título se preparó a part¡r del Intermedio 92 (174 mg. 0.7 mmol). 4.4.4'.4',5.5.5'.5'-octamet¡l-2.2'-b¡-1,3,2-d¡oxaborolano (212,89 mg. 0.84 mmol). acetato potás¡co (205.7 mg. 2.1 mmol). d¡oxano (2 ml) y Pd(dppf)Cl2.DCM (28,53 mg. 0.03 mmol) por el Método H (306 mg. 93 %). RMN 1H (500 MHz. CDCb) 88.96 (s. 2H).
3.63 (pd. J 8.7. 3.0 Hz. 1H). 3,11 - 2,88 (m. 5H). CLEM (EN+) TR 0.94 m¡n, 215,0 (M+H)+.
I N T E R M E D I O 94
1-(5-bromop¡r¡m¡d¡n-2-¡l)etan-1-ona
Se d¡solv¡eron 5-bromo-2-yodop¡r¡m¡d¡na (16 g. 56.16 mmol) y tr¡but¡l(1-etox¡eten¡l)estannano (25 g. 69,22 mmol) en tolueno (500 ml) y se purgaron con N2 durante 10 m¡n. Se añad¡ó cloruro de palad¡o (2+) - tr¡fen¡lfosfano (1:2:2) (3.5 g.
4.99 mmol) y la mezcla de reacc¡ón se calentó a 130 °C durante 18 h. La reacc¡ón se dejó enfr¡ar a t.a. Se añad¡eron agua (70 ml) y HCl 6 M (280 ml) y la mezcla de reacc¡ón se dejó en ag¡tac¡ón v¡gorosamente durante 4 h. El pH de la mezcla se ajustó a pH 7 med¡ante la ad¡c¡ón de Na2CO3 acuoso saturado (aprox¡madamente 300 ml) y la mezcla se extrajo con EtOAc (3 x 350 ml). Los extractos orgán¡cos comb¡nados se secaron sobre sulfato de magnes¡o, se f¡ltraron y se concentraron al vacío. El res¡duo se pur¡f¡có por cromatografía (S¡O2. EtOAc al 20-100 % en Heptano) para proporc¡onar el compuesto del título en forma de un sól¡do de color dorado-amar¡llo (7.9 g,70 %). RMN 1H (500 MHz, CDCb) 88,97 (s. 2H). 2,77 (s. 3H).
I N T E R M E D I O 95
5-bromo-2-(1.1-d¡fluoroet¡l)p¡r¡m¡d¡na
Se añad¡ó gota a gota BAST (50 % en tolueno) (28 ml. 75,94 mmol) a una soluc¡ón ag¡tada del Intermedio 94 (3.9 g.
19,4 mmol) en DCM anh¡dro (100 ml) a 0 °C en una atmósfera de N2. La mezcla se dejó en ag¡tac¡ón a t.a. durante 18 h. Se añad¡ó BAST (50 % en tolueno) (6 ml. 16,27 mmol) y la mezcla de reacc¡ón se dejó en ag¡tac¡ón a t.a. durante 5 h. La mezcla de reacc¡ón se añad¡ó gota a gota a h¡elo ag¡tado/NaHCO3 (sat., ac., 50 ml). La capa orgán¡ca se separó y el producto en bruto se extrajo ad¡c¡onalmente con DCM (2 x 75 ml). La fase orgán¡ca comb¡nada se secó sobre sulfato sód¡co y se concentró al vacío. produc¡endo el compuesto del título en forma de una soluc¡ón de color pardo en tolueno (5,51 g. 95,5 %). RMN 1H (500 MHz. CDCla) 88,90 (s. 2H). 2,05 (t. J 18,6 Hz. 3H).
I N T E R M E D I O 96
2-(1.1-d¡fluoroet¡l)-5-(tetramet¡l-1.3.2-d¡oxaborolan-2-¡l)p¡r¡m¡d¡na
El compuesto del título se preparó a part¡r del Intermedio 95 (75 %, 5.5 g. 18,5 mmol). 4.4,4'.4'.5.5.5'.5'-octamet¡l-2.2'-b¡-1,3,2-d¡oxaborolano (5.5 g. 21,66 mmol). acetato potás¡co (3.5 ml. 56,04 mmol). 1,4-d¡oxano (10 ml) y b¡s[3-(d¡fen¡lfosfan¡l)c¡clopenta-2,4-d¡en-1-¡l]h¡erro; d¡clorometano; d¡cloropalad¡o (0,75 g. 0,92 mmol) por el Método H (3.3 g.
42,9 %). RMN 1H (500 MHz. CDCb) 89,09 (d. J 2.9 Hz. 2H). 2,03 (td. J 18,6, 4.2 Hz. 3H). 1,35 (d. J 3.9 Hz. 12H).
I N T E R M E D I O 97
(1S.5S.6R)-3-(5-((1R)-1-[2-(d¡fluorometox¡)fen¡l1-6-fluoro-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a]p¡r¡d¡n-7-¡l)p¡r¡m¡d¡n-2-¡l)b¡c¡clo[3.1.0]hex-2-eno-6-carbox¡lato de et¡lo
El compuesto del titulo se preparó a part¡r del Ejemplo 17 (150 mg. 0,38 mmol). el Intermedio 68 (150 mg. 0,38 mmol). carbonato sód¡co 2 M (0,65 ml). d¡oxano (3 ml). aducto de d¡cloro[1,1'-b¡s(d¡fen¡lfosf¡noferroceno]-palad¡o d¡clorometano (31 mg. 0,04 mmol) por el Método A (150 mg. 72 %). RMN 1H (500 MHz. CDCb) 88,67 (d. J 1.4 Hz.
2H), 7,53 (d, J 7,1 Hz, 1H), 7,39 (d, J 11,1 Hz, 1H), 7,29 - 7,26 (m, 1H), 7,22 - 7,15 (m, 2H), 7,11 (t, J 7,5 Hz, 1H), 6,89 (dd, J 7,7, 1,5 Hz, 1H), 6,62 (dd, J 74,3, 73,1 Hz, 1H), 4,95 (dd, J 8,4, 5,3 Hz, 1H), 4,17 - 4,12 (m, 2H), 3,29 - 3,13 (m, 2H), 3,13 - 2,91 (m, 3H), 2,62 (dc, J 4,8, 2,3 Hz, 1H), 2,43 (dtt, J 13,1, 6,4, 3,9 Hz, 2H), 1,28 - 1,24 (m, 4H). CLEM (EN+) TR 3,05 min, 547,0 (M+H)+.
I N T E R M E D I O 98
(1R,5S,6R)-3-(5-{(1R)-1-[2-(d¡fluorometox¡)fen¡ll-6-fluoro-2,3-d¡h¡dro-1H-c¡clopenta[4,5l¡m¡dazo[1,2-alp¡rid¡n-7-¡l}p¡r¡m¡d¡n-2-¡l)b¡c¡clo[3.1.0lhexano-6-carboxilato de etilo
El compuesto del título se preparó a partir del Intermedio 97 (150 mg, 0,28 mmol), acetato de etilo (12 ml), trietilamina (38 |jl, 0,28 mmol), paladio sobre carbono (10 %, 30 mg, 0,024 mmol) por el procedimiento descrito para el Ejemplo 96, produciendo el compuesto del título en forma de un aceite pálido (105 mg, 70 %). RMN 1H (500 MHz, CDCb) 8 8,69 (d, J 1,5 Hz, 2H), 7,55 (d, J 7,1 Hz, 1H), 7,39 (d, J 11,1 Hz, 1H), 7,30 - 7,26 (m, 1H), 7,19 (d, J 7,9 Hz, 1H), 7,13 (t, J 7,5 Hz, 1H), 6,89 (dd, J 7,7, 1,6 Hz, 1H), 6,63 (dd, J 74,2, 73,2 Hz, 1H), 4,96 (dd, J 8,5, 5,1 Hz, 1H), 4,07 (c, J 7,1 Hz, 2H), 3,77 (tt, J 9,0, 4,3 Hz, 1H), 3,23 (dtd, J 13,3, 8,9, 4,6 Hz, 1H), 3,16 - 3,03 (m, 1H), 2,98 (ddd, J 15,5, 8,7, 5,9 Hz, 1H), 2,54 - 2,49 (m, 3H), 2,47 - 2,37 (m, 1H), 1,98 (s, 2H), 1,55 (dd, J 6,7, 3,7 Hz, 2H), 1,21 (t, J 7,1 Hz, 3H). CLEM (EN+) TR 2,97 min, 549,0 (M+H)+.
I N T E R M E D I O 99
5-bromo-2-(2-fluoropropan-2-il)p¡r¡m¡d¡na
El compuesto del título se preparó a partir del Intermedio 8 6 (6 g, 26,8 mmol) y DAST (5,3 ml, 40,3 mmol) por el Método D. RMN 1H (500 MHz, CDCla) 88,81 (s, 2H), 1,78 (d, J 21,7 Hz, 6H). CLEM (EN+) TR 1,89 min, 293,0 (M+H)+.
I N T E R M E D I O 100
2-(2-fluoropropan-2-¡l)-5-(tetramet¡l-1.3.2-d¡oxaborolan-2-il)p¡r¡m¡d¡na
El compuesto del título se preparó a partir del Intermedio 99 (1,09 g, 4,98 mmol), pinacol éster de diboro (1,9 g, 7,46 mmol), acetato potásico (1,46 g, 14,93 mmol), dioxano (10 ml), aducto de dicloro[1,1'-b¡s(d¡fenilfosf¡noferroceno]-paladio diclorometano (203 mg, 0,25 mmol) por el Método H (945 mg, 22 %). RMN 1H (500 MHz, CDCb) 8 9,03 (s, 2H), 1,79 (d, J 21,7 Hz, 6H), 1,36 (s, 12H). CLEM (EN+) TR 1,02 min, 185,0 (M+H)+.
I N T E R M E D I O 101
5-bromo-2-(1-[(terc-but¡ld¡met¡ls¡lil)ox¡leten¡l}p¡r¡m¡d¡na
Se añadió gota a gota trifluorometanosulfonato de terc-Butil(dimet¡l)s¡l¡lo (16,36 g, 61,88 mmol) a una solución agitada del Intermedio 94 (8,65 g, 43,03 mmol) y trietilamina (8,62 ml, 61,88 mmol) en DCM anhidro (300 ml) a 0 °C. Después de 30 min, la mezcla se dejó calentar hasta t.a. La reacción se interrumpió mediante la adición de agua (300 ml) y la fase orgánica se lavó con salmuera (200 ml), se secó sobre sulfato de magnesio, se filtró y se concentró al vacío. El residuo se purificó por cromatografía (S¡O2, EtOAc al 1-8 % en Heptano) para proporcionar el compuesto del título en forma de un aceite de color amarillo (9,09 g, 84 %). CLEM (EN+) TR 2,37 min, 317,0 (M+H)+.
I N T E R M E D I O 102
5-bromo-2-{1-[(terc-but¡ld¡met¡ls¡l¡l)ox¡lc¡cloprop¡l}p¡r¡m¡d¡na
A una solución agitada de tBuOK (1,21 g, 0,01 mol) en DMSO anhidro (25 ml) se añadió en porciones yoduro de trimetilsulfoxonio (2,51 g, 11,42 mmol) y la mezcla se calentó a 50 °C durante 45 min. Después, se añadió gota a gota
una solución del Intermedio 101 (0,90 g, 2,86 mmol) en DMSO anhidro (25 ml) durante 10 min a la mezcla de reacción. La reacción se agitó a 50 °C durante 2 h. La reacción se trató con una solución acuosa saturada de NH4Cl (100 ml). Después, se añadió EtOAc (125 ml) y las dos fases se separaron. La fase acuosa se extrajo con EtOAc (3 x 125 ml). Los extractos orgánicos combinados se lavaron con agua (2 x 125 ml) y salmuera (1 x 125 ml), se secaron sobre sulfato de magnesio, se filtraron y se concentraron al vacío. El residuo se purificó por cromatografía (SiO2, DCM al 5 40 % en Heptano) para proporcionar el ccompuesto del título en forma de un aceite de color amarillo claro (0,44 g, 47 %). CLEM (EN+) TR 2,38 min, 331,0 (M+H)+.
I N T E R M E D I O 103
2-n-[(terc-butildimetilsilil)oxi1ciclopropil}-5-(tetrametil-1,3,2-dioxaborolan-2-il)pirimidina
El compuesto del título se preparó a partir del Intermedio 102 (0,44 g, 1,32 mmol), bis(pinacolato)diboro (0,4 g, 1,59 mmol), acetato potásico (0,39 g, 3,97 mmol), dioxano (10 ml), aducto de dicloro[1,1'-b¡s(d¡fen¡lfosf¡noferroceno]-paladio diclorometano (54,06 mg, 0,07 mmol) por el Método H (720 mg, 96 %). RMN 1H (500 MHz, CDCb) 88,88 (s, 2H), 1,53 - 1,48 (m, 2H), 1,35 (s, 12H), 1,34 - 1,31 (m, 2H), 0,91 (s, 9H), 0,14 (s, 6H). CLEM (EN+) TR 1,95 min, 377,0 (M+H)+.
I N T E R M E D I O 1 0 4 ,
MÉTODO N
2-(D¡fluorometoxi)-4-fluorobenzaldehído
Se disolvió hidróxido potásico (40,04 g, 713,72 mmol) en agua (100 ml) y se dejó enfriar, después se añadió acetonitrilo (100 ml) y la solución se enfrió a - 20 °C donde se congeló. Se añadió 4-fluoro-2-hidroxibenzaldehído (5 g, 35,69 mmol), seguido gota a gota de [bromo(difluoro)metil]fosfonato de dietilo (12,68 ml, 71,37 mmol) y la reacción se agitó a -20 °C durante 30 min. La reacción se extrajo con acetato de etilo (2 x 100 ml), la capa orgánica se lavó con salmuera (50 ml), se secó sobre sulfato sódico y se concentró al vacío. El residuo se purificó por cromatografía, (S¡O2, EtOAc al 0-40 % en Heptano) para proporcionar el compuesto del título en forma de un aceite transparente (3,5 g, 51 %). RMN 1H (250 MHz, DMSO-d6) 8 10,14 (s, 1H), 7,88 (dd, J 8,7, 6,7 Hz, 1H), 7,37 (t, J 73 Hz, 1H), 7,35 - 7,19 (m, 2H).
I N T E R M E D I O 105
Clorhidrato del ácido 6-bromo-3-{2-carboxi-1-[2-(difluorometoxi)-4-fluorofenil1etil}-7-fluoroimidazo[1,2-a1piridin-2-carboxílico
Se calentaron 6-bromo-7-fluoro-3-yodoimidazo[1,2-a]piridin-2-carboxilato de etilo (2 g, 6,97 mmol), el Intermedio 104 (2,65 g, 13,93 mmol) y L-prolina (80,21 mg, 0,7 mmol) en acetonitrilo (15 ml) a 80 °C en un tubo cerrado herméticamente durante 14 h, seguido de 120 °C hasta la conversión completa. La mezcla de reacción se concentró al vacío y se trituró con NaOH 6 M (50 ml) y se extrajo con acetato de etilo (50 ml x 2). La capa acuosa se acidificó con HCl conc. (pH ~3-4) y se extrajo con IPA: CHCb (1:1) (2 x 50 ml). La capa orgánica se concentró al vacío, produciendo el compuesto del título en forma de un sólido de color beige (3,3 g, 55 %). CLEM (EN+) TR 1,70 min, 491,0/493,0 (M+H)+.
I N T E R M E D I O 1 0 6 ,
MÉTODO O
6-Bromo-3-(1-[2-(d¡fluorometox¡)-4-fluorofenil1-3-etox¡-3-oxoprop¡l}-7-fluoro ¡m¡dazo[1,2-a1p¡r¡d¡n-2-carbox¡lato de etilo
Se añadió gota a gota dicloruro de oxalilo (1,78 ml, 18,76 mmol) a la solución agitada del Intermedio 105 (3,3 g, 3,75 mmol), W,W-dimetilformamida (58,05 pl, 0,75 mmol) en DCM (25 ml), se agitó a t.a. durante 2 h. La mezcla se concentró al vacío y se inactivó con etanol (10 ml) y se agitó durante 30 min. La mezcla se concentró al vacío para proporcionar un aceite de color pardo. Esto se disolvió en acetato de etilo (200 ml) y se lavó con bicarbonato sódico ac. sat. (2 x 25 ml). La capa orgánica combinada se lavó con agua (25 ml) y salmuera (25 ml), se secó sobre sulfato sódico, se filtró y se concentró al vacío. El residuo se purificó por cromatografía, (SiO2, EtOAc al 0-50 % en Heptano) para proporcionar el compuesto del título en forma de un sólido de color pardo claro (950 mg, 46 %). CLEM (EN+) TR 1,49 min, 547,0/549,0 (M+H)+.
I N T E R M E D I O 107
7-bromo-1-[2-(d¡fluorometox¡)-4-fluorofen¡l1-6-fluoro-3-oxo-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-2-carboxilato de etilo
El compuesto del título se preparó a partir del Intermedio 106 (900 mg, 1,64 mmol) y terc-pentóxido potásico (1,48 ml, 2,63 mmol) por el Método L (490 mg, 55 %). CLEM (EN+) TR 2,00 min, 501,0/503,0 (M+H)+.
I N T E R M E D I O 108
7-bromo-1-f2-(d¡fluorometox¡)-4-fluorofen¡l1-6-fluoro-1.2-d¡h¡dro-3H-c¡clopentaf4.51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ona
El compuesto del título se preparó a partir del Intermedio 107 (490 mg, 0,68 mmol), DMSO (8 ml) y agua (2 ml) por el Método M (285 mg, 77 %). CLEM (EN+) TR 1,96 min, 429,0/431,0 (M+H)+.
I N T E R M E D I O 10 9
7-bromo-1-[2-(d¡fluorometox¡)-4-fluorofen¡l1-6-fluoro-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ol
El compuesto del título se preparó a partir del Intermedio 108 (275 mg, 0,64 mmol), tri-sec-butilborohidruro de litio 1 M en THF (0,64 ml) y THF (10 ml) por el Método B (165 mg, 56 %). CLEM (EN+) TR 1,76 min, 431,0/433,0 (M+H)+. I N T E R M E D I O 110
2-(D¡fluorometoxi)-5-fluorobenzaldehído
El compuesto del título se preparó a partir de 5-fluoro-2-hidroxibenzaldehído (4,42 ml, 35,69 mmol, hidróxido potásico (40,04 g, 713,72 mmol), agua (100 ml), acetonitrilo (100 ml), [bromo(difluoro)met¡l]fosfonato de dietilo (12,68 ml,
71,37 mmol) por el Método N (2,4 g, 35 %). RMN 1H (500 MHz, CDCla) 8 10,33 (d, J 3,0 Hz, 1H), 7,61 (dd, J 8,0, 3,1 Hz, 1H), 7,33 (ddd, J 9,0, 7,3, 3,2 Hz, 1H), 7,30 - 7,27 (m, 1H), 6,63 (t, J 72,4 Hz, 1H).
I N T E R M E D I O 111
-MÉTODO P
Ácido 3-[6-broiTio-2-(etox¡carbon¡l)-7-fluoro¡iTi¡dazo[1.2-a1p¡r¡d¡n-3-¡l1-3-[2-(d¡fluoroiTietox¡)-5-fluorofen¡l1propano¡co Se calentaron 6-bromo-7-fluoro-3-yodo¡m¡dazo[1,2-a1p¡r¡d¡n-2-carbox¡lato de etilo (2 g, 6,97 mmol), 2,2-d¡met¡l-1,3-d¡oxano-4,6-d¡ona (2,01 g, 13,93 mmol), el Intermedio 110 (2,65 g, 13,93 mmol) y L-prol¡na (80,21 mg, 0,7 mmol) en aceton¡tr¡lo (15 ml) a 80 °C en un tubo cerrado hermét¡camente durante 14 h, segu¡do de 120 °C hasta la convers¡ón completa. La mezcla de reacc¡ón se concentró al vacío y el res¡duo se lavó con acetato de et¡lo (50 ml). El sól¡do se ret¡ró por f¡ltrac¡ón y el f¡ltrado se concentró al vacío a la m¡tad del volumen y se dejó reposar durante 30 m¡n. El prec¡p¡tado sól¡do se f¡ltró y se lavó con acetato de et¡lo (25 ml) para produc¡r el compuesto del título en forma de un sól¡do de color be¡ge (1,6 g, 33 %). CLEM (EN+) TR 1,85 m¡n, 519,0/521,0 (M+H)+.
I N T E R M E D I O 112
6-Bromo-3-{1-[2-(d¡fluorometox¡)-5-fluorofen¡l1-3-etox¡-3-oxoprop¡l}-7-fluoro ¡m¡dazo[1,2-a1p¡r¡d¡n-2-carbox¡lato de et¡lo El compuesto del título se preparó a partir de cloruro de oxal¡lo (1,17 ml, 12,33 mmol), el Intermedio 111 (1,6 g, 2,47 mmol), N,N-d¡met¡lformam¡da (38,13 pl, 0,49 mmol) y DCM (25 ml) por el Método O (1,3 g, 96 %). CLEM (EN+) TR 2,13 m¡n, 547,0/549,0 (M+H)+.
I N T E R M E D I O 113
7-bromo-1-[2-(d¡fluorometox¡)-5-fluorofen¡l1-6-fluoro-3-oxo-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-2-carbox¡lato de et¡lo
El compuesto del título se preparó a part¡r del Intermedio 112 (1,3 g, 2,38 mmol), tolueno (80 ml) y 2-met¡lbutan-2-olato potás¡co (2,13 ml, 3,8 mmol) por el Método L (380 mg, 25 %). CLEM (EN+) TR 1,98 m¡n, 501,0/503,0 (M+H)+.
I N T E R M E D I O 114
7-bromo-1-[2-(d¡fluorometox¡)-5-fluorofen¡l1-6-fluoro-1.2-d¡h¡dro-3H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ona
El compuesto del título se preparó a part¡r del Intermedio 113 (380 mg, 0,61 mmol), DMSO (8 ml) y agua (2 ml) por el Método M (265 mg, 97 %). CLEM (EN+) TR 1,87 m¡n, 429,0/431,0 (M+H)+.
I N T E R M E D I O 115
7-bromo-1-[2-(d¡fluorometox¡)-5-fluorofen¡l1-6-fluoro-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ol
El compuesto del título se preparó a partir del Intermedio 114 (265 mg, 0.62 mmol). tr¡-sec-but¡lboroh¡druro de l¡t¡o 1 M en THF (0.62 ml) y THF (10 ml) por el Método B (180 mg.65 %). CLEM (EN+) TR 1.73 m¡n. 431.0/433.0 (M+H)+.
I N T E R M E D I O 116
2-(D¡fluorometox¡)-4.5-d¡fluorobenzaldehído
El compuesto del título se preparó a part¡r de h¡dróx¡do potás¡co (67.5 g. 1203 mmol). agua (100 ml). MeCN (50 ml).
4.5-d¡fluoro-2-h¡drox¡benzaldehído (9.5 g. 60.09 mmol) y [bromo(d¡fluoro)met¡l]fosfonato de d¡et¡lo (12.8 ml.
72.10 mmol). de acuerdo con el Método N (3.95 g. 12 %). RMN 1H (500 MHz. CDCla) 810.25 (d. J 3.0 Hz. 1H). 7.83 -7.65 (m. 1H). 7.17 (dd. J 10.2. 6.1 Hz. 1H). 6.68 (t. J 71.8 Hz. 1H).
I N T E R M E D I O 117
Ác¡do 3-[6-bromo-2-(etox¡carbon¡l)-7-fluoro¡m¡dazo[1.2-a1p¡r¡d¡n-3-¡l1-3-[2-(d¡fluorometox¡)-4.5-d¡fluorofen¡l1propano¡co
El compuesto del título se preparó a part¡r de 6-bromo-7-fluoro-3-yodo¡m¡dazo[1.2-a1p¡r¡d¡n-2-carbox¡lato de etilo (2 g.
6.97 mmol). 2.2-d¡met¡l-1.3-d¡oxano-4.6-d¡ona (2.74 g. 18.98 mmol). el Intermedio 1 1 6 (3.95 g. 18.98 mmol) y L-prol¡na (80.21 mg. 0.7 mmol) en aceton¡tr¡lo (15 ml) por el Método P (3 g. 56 %). CLEM (EN+) TR 1.98 m¡n. 537.0/539.0 (M+H)+.
I N T E R M E D I O 118
6-Bromo-3-(1-[2-(d¡fluorometox¡)-4.5-d¡fluorofen¡l1-3-etox¡-3-oxoprop¡l)-7-fluoro¡m¡dazo[1.2-a1p¡r¡d¡n-2-carbox¡lato de et¡lo
El compuesto del título se preparó a partir de cloruro de oxal¡lo (1.86 ml. 19.54 mmol). el Intermedio 117 (-70 %. 3 g.
3.91 mmol). N,N-d¡met¡lformam¡da (60.47 pl. 0.78 mmol) en DCM (25 ml) por el Método O (2.0 g. 89 %). CLEM (EN+) TR 2.16 m¡n. 565.0/567.0 (M+H)+.
I N T E R M E D I O 119
7-bromo-1-[2-(d¡fluorometox¡)-4.5-d¡fluorofen¡l1-6-fluoro-3-oxo-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-2-carbox¡lato de et¡lo
El compuesto del título se preparó a partir del Intermedio 118 (1,96 g, 3,47 mmol), tolueno (70 ml) y 2-met¡lbutan-2-olato potásico (3,11 ml, 5,55 mmol, 25 % p/p en tolueno) por el Método L (1,6 g, 58 %). CLEM (EN+) TR 2,02 min, 519,0/521,0 (M+H)+.
I N T E R M E D I O 120
7-bromo-1-r2-íd¡fluorometox¡)-4.5-d¡fluorofen¡l1-6-fluoro-1.2-d¡h¡dro-3H-c¡clopentar4.51¡m¡dazoH.2-a1p¡r¡d¡n-3-ona
El compuesto del título se preparó a partir del Intermedio 119 (1,6 g, 2 mmol), DMSO (25 ml) y agua (5 ml) por el Método M (512 mg, 51 %). CLEM (EN+) TR 2,02 m¡n, 447,0/449,0 (M+H)+.
I N T E R M E D I O 121
7-bromo-1-[2-(difluorometoxi)-4,5-difluorofenil1-6-fluoro-2,3-dihidro-1H-ciclopenta[4,51imidazo[1,2-a1pirídin-3-ol
El compuesto del título se preparó a partir del Intermedio 120 (512 mg, 1,03 mmol), tr¡-sec-but¡lboroh¡druro de l¡t¡o 1 M en THF (1,03 ml) en THF (15 ml) por el Método B (354 mg, 76 %). CLEM (EN+) TR 1,78 m¡n, 449,0/451,0 (M+H)+. I N T E R M E D I O 122
Ác¡do 3-[6-bromo-2-(etox¡carbon¡l)-7-fluoro¡m¡dazo[1.2-a1p¡r¡d¡n-3-¡l1-3-[2-(d¡fluorometox¡)-6-fluorofen¡l1propano¡co El compuesto del título se preparó a partir de 6-bromo-7-fluoro-3-yodo¡m¡dazo[1,2-a]pmd¡n-2-carbox¡lato de et¡lo (3,8 g, 13,24 mmol), 2,2-d¡met¡l-1,3-d¡oxano-4,6-d¡ona (3,82 g, 26,47 mmol), 2-(d¡fluorometox¡)-6-fluorobenzaldehído (5,03 g, 26,47 mmol) y L-prol¡na (152,39 mg, 1,32 mmol) en aceton¡tr¡lo (30 ml) por el Método P (3,4 g, 33 %). CLEM (EN+) TR
1,78 min, 519,0/521,0 (M+H)+.
I N T E R M E D I O 123
6-Bromo-3-n-[2-(d¡fluorometox¡)-6-fluorofen¡l1-3-etox¡-3-oxoprop¡l)-7-fluoro¡m¡dazo[1,2-a1p¡r¡d¡n-2-carbox¡lato de etilo El compuesto del título se preparó a part¡r de cloruro de oxal¡lo (2,05 ml, 21,61 mmol), el Intermedio 122 (3,4 g, 4,32 mmol), N,N-d¡met¡lformam¡da (66,85 pl, 0,86 mmol) en DCM (25 ml) por el Método O (1,2 g, 44 %). CLEM (EN+) TR 2,16 m¡n, 547,0/549,0 (M+H)+.
I N T E R M E D I O 124
7-bromo-1-r2-(d¡fluorometox¡)-6-fluorofen¡l1-6-fluoro-3-oxo-2,3-d¡l'i¡dro-1H-c¡clopentar4,51¡m¡dazor1,2-a1p¡r¡d¡n-2-carbox¡lato de et¡lo
El compuesto del título se preparó a part¡r del Intermedio 123 (1,2 g, 2,13 mmol), tolueno (50 ml) y 2-met¡lbutan-2-olato potás¡co en tolueno (1,91 ml, 3,4 mmol) por el Método L (0,8 g, 56 %). CLEM (EN+) TR 1,38 m¡n, 501,0/503,0 (M+H)+.
I N T E R M E D I O 125
7-bromo-1-r2-(d¡fluorometox¡)-6-fluorofen¡l1-6-fluoro-1,2-d¡h¡dro-3H-c¡clopentar4,51¡m¡dazor1,2-a1p¡r¡d¡n-3-ona
El compuesto del título se preparó a partir del Intermedio 124 (800 mg, 1,2 mmol), DMSO (8 ml) y agua (2 ml) por el Método M (265 mg, 40 %). CLEM (EN+) TR 1,24 m¡n, 429,0/431,0 (M+H)+.
I N T E R M E D I O 126
7-bromo-1-[2-(d¡fluorometox¡)-6-fluorofen¡l1-6-fluoro-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ol
El compuesto del título se preparó a partir del Intermedio 125 (265 mg, 0,48 mmol), tri-sec-butilborohidruro de litio 1 M en THF (0,48 ml) y THF (10 ml) por el Método B (170 mg, 79 %). CLEM (EN+) TR 1,68 min, 431,0/433,0 (M+H)+. I N T E R M E D I O 127
Ácido 3-[6-bromo-2-(etox¡carbon¡l)-7-fluoro¡m¡dazo[1.2-a1p¡r¡d¡n-3-¡l1-3-(3-clorofen¡l)propanoico
El compuesto del título se preparó a partir de 6-bromo-7-fluoro-3-yodoimidazo[1,2-a1piridin-2-carboxilato de etilo (3 g, 10,45 mmol), 2,2-dimetil-1,3-dioxano-4,6-diona (3,01 g, 20,9 mmol), 3-clorobenzaldehído (2,94 g, 20,9 mmol) y L-prolina (60,15 mg, 0,52 mmol) y MgSO4 (2 g, 16,62 mmol) en acetonitrilo (30 ml) por el Método P (4,6 g, 58 %). CLe M (EN+) TR 1,96 min, 469,0/471,0 (M+H)+.
I N T E R M E D I O 128
6-Bromo-3-[1-(3-clorofen¡l)-3-etox¡-3-oxoprop¡l1-7-fluoro¡m¡dazo[1,2-a1p¡r¡d¡n-2-carbox¡lato de etilo
El compuesto del título se preparó a partir de cloruro de oxalilo (0,66 ml, 9,11 mmol), el Intermedio 127 (4,6 g, 6,07 mmol) en EtOH (50 ml) por el Método O (2,9 g, 96 %). CLEM (EN+) TR 2,23 min, 497,0/499,0 (M+H)+.
I N T E R M E D I O 129
7-bromo-1-(3-clorofen¡l)-6-fluoro-3-oxo-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-2-carbox¡lato de etilo
El compuesto del título se preparó a partir del Intermedio 128 (2,9 g, 5,83 mmol), tolueno (50 ml) y 2-metilbutan-2-olato potásico en tolueno (5,23 ml, 9,32 mmol) por el Método L (540 mg, 15 %). Cl EM (EN+) TR 1,38 min, 451,0/453,0 (M+H)+.
I N T E R M E D I O 130
7-bromo-1-(3-clorofen¡l)-6-fluoro-1.2-d¡h¡dro-3H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ona
El compuesto del título se preparó a partir del Intermedio 129 (540 mg, 0,9 mmol), DMSO (8 ml) y agua (2 ml) por el Método M (360 mg, 97 %). CLEM (EN+) TR 1,29 min, 379,0/381,0 (M+H)+.
I N T E R M E D I O 131
7-bromo-1-(3-clorofen¡l)-6-fluoro-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ol
El compuesto del título se preparó a partir del Intermedio 130 (360 mg, 0,87 mmol), tri-sec-butilborohidruro de litio 1 M en THF (0,87 ml) y THF (10 ml) por el Método B (260 mg, 62 %). CLEM (EN+) TR 1,64 min, 381,0/383,0 (M+H)+. I N T E R M E D I O 132
Ácido 3-[6-bromo-2-(etox¡carbon¡l)-7-fluoro¡m¡dazo[1.2-a1p¡r¡d¡n-3-¡l1-3-[5-cloro-2-(d¡fluorometox¡)fen¡l1propano¡co El compuesto del título se preparó a partir de 6-bromo-7-fluoro-3-yodoimidazo[1,2-a1piridin-2-carboxilato de etilo (3 g, 10,45 mmol), 2,2-dimetil-1,3-dioxano-4,6-diona (3,01 g, 20,9 mmol), 5-cloro-2-(difluorometoxi) benzaldehído (4,96 g, 24,03 mmol) y L-prolina (60,15 mg, 0,52 mmol) y MgSO4 (2 g, 16,62 mmol) en acetonitrilo (30 ml) por el Método P (4,1 g, 53 %). CLEM (EN+) TR 1,98 min, 535,0/537,0 (M+H)+.
I N T E R M E D I O 133
6-Bromo-3-{1-[5-cloro-2-(d¡fluorometox¡)fen¡l1-3-etox¡-3-oxoprop¡l}-7-fluoro ¡m¡dazo[1,2-a1p¡r¡d¡n-2-carbox¡lato de etilo El compuesto del título se preparó a partir de cloruro de oxalilo (0,6 ml, 8,27 mmol), el Intermedio 132 (4,1 g, 5,51 mmol) en EtOH (50 ml) por el Método O (2,0 g, 65 %). CLEM (EN+) TR 2,19 min, 563,0/565,0 (M+H)+.
I N T E R M E D I O 134
7-Bromo-1-[5-cloro-2-(d¡fluorometox¡)fen¡l1-6-fluoro-3-oxo-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-2-carboxilato de etilo
El compuesto del título se preparó a partir del Intermedio 133 (2,01 g, 3,57 mmol), tolueno (50 ml) y 2-metilbutan-2-olato potásico en tolueno (3,2 ml, 5,7 mmol) por el Método L (450 mg, 16 %). Cl Em (EN+) TR 1 ,38 min, 517,0/519,0 (M+H)+.
I N T E R M E D I O 135
7-bromo-1-[5-cloro-2-(d¡fluorometox¡)fen¡l1-6-fluoro-1.2-d¡h¡dro-3H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ona
El compuesto del título se preparó a partir del Intermedio 134 (450 mg, 0,56 mmol), DMSO (8 ml) y agua (2 ml) por el Método M (275 mg, 99 %). CLEM (EN+) TR 1,31 min, 445,0/447,0 (M+H)+.
I N T E R M E D I O 136
7-bromo-1-[5-cloro-2-(d¡fluorometox¡)fen¡l1-6-fluoro-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1pir¡d¡n-3-ol
El compuesto del título se preparó a partir del Intermedio 135 (275 mg, 0,56 mmol), tr¡-sec-but¡lboroh¡druro de l¡t¡o 1 M en THF (0,56 ml) y THF (10 ml) por el Método B (230 mg, 75 %). CLEM (EN+) TR 1,77 m¡n, 447,0/449,0 (M+H)+.
I N T E R M E D I O 137
[(5-((1R,3R)-1-[2-(d¡fluorometox¡)fen¡l1-6-fluoro-3-h¡drox¡-2,3-d¡h¡dro-1H-c¡clopenta[4,51¡m¡dazo[1,2-a1p¡r¡d¡n-7-¡l}p¡r¡m¡d¡n-2-¡l)propan-2-¡l1carbamato de t-but¡lo
El compuesto del título se preparó a part¡r del Ejemplo 16 (150 mg, 0,31 mmol), el Intermedio 89 (145 mg, 0,34 mmol), carbonato sód¡co 2 M (0,46 ml), d¡oxano (3 ml) y aducto de d¡cloro[1,1'-b¡s(d¡fen¡lfosf¡noferroceno]-palad¡o d¡clorometano (25 mg, 0,03 mmol) por el Método A (78 mg, 44 %). RMN 1H (500 MHz, CDCla) 88,73 (d, J 1,4 Hz, 2H), 7,66 (d, J 7,1 Hz, 1H), 7,42 (d, J 10,9 Hz, 1H), 7,32 - 7,27 (m, 1H), 7,24 - 7,14 (m, 3H), 6,66 (dd, J 74,5, 72,9 Hz, 1H), 5,87 (s, 1H), 5,44 (dt, J 6,9, 3,4 Hz, 1H), 4,89 (dd, J 8,5, 4,0 Hz, 1H), 3,70 (d, J 3,8 Hz, 1H), 3,61 (dt, J 14,2, 8,2 Hz, 1H), 2,42 (dt, J 14,1, 3,6 Hz, 1H), 1,73 (s, 6H), 1,40 (s, 9H). CLEM (EN+) TR 1,78 m¡n, 570,0 (M+H)+.
I N T E R M E D I O 138
3-Met¡l-1-[5-(4.4.5.5-tetramet¡l-1.3.2-d¡oxaborolan-2-¡l)p¡r¡m¡d¡n-2-¡l1azet¡d¡n-3-ol
El compuesto del título se preparó a partir de 2-cloro-5-(4,4,5,5-tetramet¡l-1,3,2-d¡oxaborolan-2-¡l)p¡r¡m¡d¡na y 3-met¡lazet¡d¡n-3-ol por el Método E. 1H (400 MHz, DMSO-d6) 8,45 (s, 2H), 5,67 (s, 1H), 3,92 (m, 4H), 1,43 (s, 3H), 1,28 (s, 12H).
I N T E R M E D I O 139
3-(tr¡fluoromet¡l)azet¡d¡n-3-ol
A una soluc¡ón de 1-boc-3-azet¡d¡nona (11,3 g, 58,4 mmol,) y (tr¡fluoromet¡l)tr¡met¡ls¡lano (9,22 g, 64,3 mmol) en THF (100 ml) enfr¡ada a ~ -5 °C en un baño de h¡elo/salmuera se añad¡ó en porc¡ones fluoruro de ces¡o (9,77 g, 64,3 mmol). La mezcla resultante se dejó en ag¡tac¡ón a t.a., el anál¡s¡s de TLC después de 4 h ¡nd¡có el consumo completo del mater¡al de part¡da y un componente menos polar. La reacc¡ón se ¡nterrump¡ó med¡ante la ad¡c¡ón de una soluc¡ón acuosa saturada de cloruro de amon¡o (100 ml) y la fase acuosa se extrajo con EtOAc (3 x 100 ml). La fase orgán¡ca se separó, se secó sobre sulfato sód¡co, se f¡ltró y los volátiles se ret¡raron al vacío para dar un ace¡te en bruto. El ace¡te obten¡do de este modo se d¡solv¡ó en DCM (100 ml) y se añad¡ó ác¡do tr¡fluoroacét¡co (40 ml). La mezcla se agitó a temperatura amb¡ente durante cuatro horas. Los volátiles se ret¡raron al vacío y el res¡duo se dest¡ló
azeotrópicamente con tolueno (3 x 150 ml) para dar la sal trifluoroacetato del compuesto del título en forma de un sólido de color pardo (15 g). RMN 1H (400 MHz, da DMSO): 8/ppm 9,48 (s, 2H), 7,95 (d, J 0,3 Hz, 1H), 4,28 (d, J 13,1 Hz, 2H), 4,06 (m, 2H).
El compuesto obtenido de este modo se usó en la siguiente reacción sin purificación adicional.
I N T E R M E D I O 140
1-[5-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)pirimidin-2-il1-3-(trifluorometil)azetidin-3-ol
A una solución del Intermedio 2(12 g) en MeCN (150 ml) se añadió trietilamina (30 ml) y 2-cloro-5-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)pirimidina (16 g) y la reacción se agitó a 65 °C durante 18 h. Los disolventes se retiraron al vacío y el residuo sólido se trituró y se lavó con agua destilada para dar un sólido de color beige y se secó a alto vacío para dar el compuesto del título en forma de un sólido de color beige (18,5 g). RMN 1H (300 MHz, d6 DMSO): 8/ppm 8,53 (2H, s), 7,46 (1H, s), 4,33-4,31 (2H, m), 4,10-4,08 (2H, m), 1,29 (12H, s). CLEM (EN+) TR 1,14 min, 346,0 (M+H)+. I N T E R M E D I O 141
1-(5-bromop¡r¡m¡d¡n-2-¡l)-3,3-d¡fluoroc¡clobutan-1-ol
El compuesto del título se preparó a partir de n-BuLi 2,5 M en hexano (6,08 ml, 15,20 mmol), 5-bromo-2-yodopirimidina (4,24 g, 14,88 mmol), tolueno (45 ml) y 3,3-difluorociclobutanona (1,74 g, 16,37 mmol) por el Método F (329 mg, 8,3 %). RMN 1H (500 MHz, CDCla) 88,83 (s, 2H), 4,72 (s, 1H), 3,54 - 3,18 (m, 2H), 3,16 - 2,83 (m, 2H). CLEM (EN+) TR 1,50 min, 267,0 (M+H)+.
I N T E R M E D I O 142
5-bromo-2-(3,3-difluoro-1-[(trimetilsilil)oxi1ciclobutil}pirimidina
El compuesto del título se preparó a partir del Intermedio 141, (0,33 g, 1,24 mmol), cloruro de trimetilsililo (0,175 ml, 1,36 mmol), imidazol (0,101 g, 1,49 mmol) en diclorometano (5 ml) por el Método G (349 mg, 83 %). RMN 1H (500 MHz, CDCla) 88,82 (s, 2H), 3,47 (ddd, J 14,7, 12,3, 9,3 Hz, 2H), 2,99 (ddd, J 14,6, 13,6, 12,1 Hz, 2H), 0,00 (s, 9H). CLEM (EN+) TR 2,23 min, 233,0 (M+H)+.
I N T E R M E D I O 143
2-(3,3-difluoro-1-[(trimetilsilil)oxi1ciclobutil}-5-(tetrametil-1,3,2-dioxaborolan-2-il)pirimidina
El compuesto del título se preparó a partir del Intermedio 142 (329 mg, 0,98 mmol), pinacol éster de diboro (372 mg, 1,46 mmol), acetato potásico (287 mg, 2,93 mmol) en dioxano (6 ml), aducto de dicloro[1,1'-bis(d¡fen¡lfosf¡noferroceno]-paladio diclorometano (40 mg, 0,05 mmol) por el Método H (200 mg, 53 %). RMN 1H (500 MHz, CDCb) 89,04 (s, 2H), 3,58 - 3,47 (m, 2H), 2,98 (td, J 14,2, 11,7 Hz, 2H), 1,37 (s, 6H), 1,26 (s, 16H). CLEM (EN+) TR 1,89 min, 302,0 (M+H)+.
I N T E R M E D I O 144
(1R)-7-[2-(1-([terc-butil(dimetil)silil1oxi}-3-hidroxi-3-metilciclobutil)pirimidin-5-il1-1-[2-(difluorometoxi)fenil1-6-fluoro-3-met¡l-2.3-d¡h¡dro-1H-c¡clopenta[4,51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ol
El compuesto del título se preparó a partir del Ejemplo 20 (0,6 g, 1,4 mmol), el Intermedio 165 (0,65 g, 1,54 mmol), PdCl2.dppf (0,11 g, 0,14 mmol), K2CO32 M en agua (2,11 ml) en 1,4-dioxano (12 ml) por el Método A (0,484 g, 54 %). I N T E R M E D I O 145
6-bromo¡midazori.2-a1p¡r¡d¡n-2-carbox¡lato de etilo
Se d¡solv¡ó 5-bromop¡r¡d¡n-2-am¡na (60 g. 347 mmol) en 1,4-d¡oxano (1011 ml) y se añad¡ó sulfato de magnes¡o (125 g.
1040 mmol). segu¡do de 3-bromo-2-oxopropanoato de etilo (84 g. 386 mmol. 54 ml). La mezcla de reacc¡ón se calentó a 80 °C durante 18 h. La mezcla de reacc¡ón se enfr¡ó a t.a. y se añad¡ó tr¡et¡lam¡na (43.7 g. 432 mmol. 60 ml). y la suspens¡ón resultante se d¡luyó con una mezcla de EtOH al 10 % en DCM (500 ml) y se ag¡tó v¡gorosamente durante 10 m¡nutos. El prec¡p¡tado se ret¡ró por f¡ltrac¡ón y se lavó con EtOH al 10 % en DCM (500 ml). hasta que solo quedó MgSO4 en el f¡ltro de cr¡stal. El f¡ltrado se concentró al vacío y se ag¡tó en agua (1.5 l). usando un ag¡tador mecán¡co. El prec¡p¡tado se ret¡ró por f¡ltrac¡ón y se lavó conc¡enzudamente con agua y se secó al vacío. produc¡endo el compuesto del título en forma de un sól¡do de color be¡ge (90.0 g. 93 %). CLEM (EN+) TR 1.71 m¡n. 269.0/271.0 (M+H)+.
I N T E R M E D I O 146
Ác¡do 3-(6-bromo-2-etox¡carbon¡l-¡m¡dazof1.2-a1p¡r¡d¡n-3-¡l)-3-f5-cloro-2-(d¡fluorometox¡)fen¡l1propano¡co
El compuesto del título se preparó a part¡r del Intermedio 145 (76 g. 282 mmol). 2.2-d¡met¡l-1.3-d¡oxano-4.6-d¡ona (81 g. 564 mmol). 5-cloro-2-(d¡fluorometox¡) benzaldehído (131 g. 564 mmol) y L-prol¡na (1.62 g. 14.11 mmol) y MgSO4 (102 g. 847 mmol) en aceton¡tr¡lo (1.0 ml) por el Método P (115 g. 79 %). CLEM (EN+) TR 2.04 m¡n. 517.0/519.0 (M+H)+.
I N T E R M E D I O 147
6-bromo-3-[1-[5-cloro-2-(d¡fluorometox¡)fen¡l1-3-etox¡-3-oxoprop¡l1¡m¡dazo[1.2-a1p¡r¡d¡n-2-carbox¡lato de et¡lo
El compuesto del título se preparó a part¡r de cloruro de t¡on¡lo (50.0 g. 420 mmol). el Intermedio 146 (108.7 g.
210 mmol) en EtOH (1 l) por el Método O (94.5 g. 82 %). CLEM (EN+) TR 2.20 m¡n. 545.0/547.0 (M+H)+.
I N T E R M E D I O 148
7-bromo-1-[5-cloro-2-(d¡fluorometox¡)fen¡l1-3-oxo-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-2-carbox¡lato de et¡lo
El compuesto del título se preparó a part¡r del Intermedio 147 (72 g. 132 mmol). tolueno (860 ml) y terc-butóx¡do sód¡co en tolueno (31.7 g. 330 mmol) por el Método L (31.6 g. 48 %). CLEM (EN+) TR 2.12 m¡n. 499.0/501.0 (M+H)+.
I N T E R M E D I O 149
ác¡do 5-bromo-2-c¡clobut¡lp¡r¡m¡d¡n-4-carboxíl¡co
A una suspens¡ón ag¡tada de clorh¡drato de c¡clobutanocarbox¡m¡dam¡da (1:1) (2 g. 14.9 mmol) en etanol (16 ml) se añad¡ó etóx¡do sód¡co 2 M en etanol (15 ml. 29.7 mmol) a t.a. La suspens¡ón se calentó a 50 °C durante 5 m¡nutos antes de la ad¡c¡ón gota a gota de una soluc¡ón de ác¡do mucobróm¡co (2.68 g. 10.4 mmol) en etanol (8 ml) a 50 °C. La mezcla de reacc¡ón se ag¡tó a 50 °C durante 30 m¡nutos. se añad¡ó más cant¡dad de etóx¡do sód¡co 2 M en etanol (7.5 ml. 14.9 mmol) y la reacc¡ón se ag¡tó durante 15 m¡nutos más a 50 °C. La mezcla de reacc¡ón enfr¡ada se concentró al vacío, el res¡duo resultante se d¡solv¡ó en ác¡do clorhídr¡co 2 N (40 ml) y se extrajo con d¡clorometano (3 x 100 ml). Los extractos orgán¡cos comb¡nados se lavaron con salmuera (100 ml). se secaron (Na2SO4) y se redujeron al vacío. El res¡duo se repart¡ó entre EtOAc (100 ml) y una soluc¡ón 2 N de h¡dróx¡do sód¡co (50 ml). la fase acuosa se separó y se lavó con EtOAc (100 ml). Los extractos acuosos comb¡nados se ac¡d¡f¡caron a pH 4 usando ác¡do clorhídr¡co 2 M y se extrajeron de nuevo en d¡clorometano (3 x 100 ml). Los extractos orgán¡cos comb¡nados se secaron (Na2SO4) y se redujeron al vacío para proporc¡onar el compuesto del título en forma de un sól¡do de color naranja pál¡do (830 mg.
19 %). RMN 1H (250 MHz. MeOD) 8 ppm 8.97 (s. 1H). 3.81 (p. J 8.1 Hz. 1H). 2.55 - 2.35 (m. 4H). 2.18 - 2.05 (m. 1H).
2,01 - 1,86 (m, 1H).
I N T E R M E D I O 150
5-bromo-2-c¡clobut¡lp¡rim¡d¡na
El Intermedio 149 (830 mg, 2,91 mmol) en p-xileno (10 ml) se calentó a 140 °C durante 5 h. La mezcla de reacción enfriada se concentró al vacío. El residuo se purificó por cromatografía, (S¡O2, EtOAc al 0-100 % en Heptano) para proporcionar el compuesto del título en forma de un aceite de color amarillo pálido (250 mg, 40 %). RMN 1H (500 MHz, CDCb) 8 ppm 8,71 (s, 2H), 3,78 (p, J 8,8 Hz, 1H), 2,49 - 2,34 (m, 4H), 2,17 - 2,02 (m, 1H), 2,00 - 1,86 (m, 1H).
I N T E R M E D I O 151
2-c¡clobut¡l-5-(tetramet¡l-1.3.2-dioxaborolan-2-¡l)p¡r¡m¡d¡na
El compuesto del título se preparó a partir del Intermedio 150 (250 mg, 1,17 mmol), pinacol éster de diboro (447 mg, 1,76 mmol), acetato potásico (345 mg, 3,52 mmol) y dioxano (5 ml), aducto de dicloro[1,1'-b¡s(d¡fen¡lfosf¡noferroceno]-paladio diclorometano (48 mg, 0,06 mmol) por el Método H (310 mg, 90 %). RMN 1H (500 MHz, CDCl3) 8 ppm 8,95 (s, 2H), 3,84 (p, J 8,6 Hz, 1H), 2,51 - 2,43 (m, 2H), 2,40 (c, J 9,8, 8,9 Hz, 2H), 2,09 (h, J 9,2 Hz, 1H), 1,94 (c, J 9,1 Hz, 1H), 1,35 (s, 12H).
I N T E R M E D I O 152
8-(5-bromop¡r¡m¡d¡n-2-¡l)-1.4-d¡oxasp¡ro[4.51decan-8-ol
El compuesto del título se preparó a partir de 5-bromo-2-yodopirim¡d¡na (10 g, 34,4 mmol), tolueno (200 ml), n-butillitio 2,5 M en hexano (16 ml, 40 mmol) y 1,4-dioxaspiro[4,5]decan-8-ona (6,14 g, 38,2 mmol) en tolueno seco (40 ml) por el Método F (5,96 g, 38 %). RMN 1H (500 MHz, CDCla) 8 ppm 8,77 (s, 2H), 4,17 (s, 1H), 4,00 (t, J 3,3 Hz, 4H), 2,43 -2,29 (m, 2H), 2,17 - 2,06 (m, 2H), 1,73 (t, J 15,4 Hz, 4H).
I N T E R M E D I O 153
5-bromo-2-n,4-d¡oxasp¡ro[4,5]dec-7-en-8-¡l}p¡rim¡d¡na
El Intermedio 152 (2 g, 4,44 mmol), oxicloruro de fósforo (0,58 ml, 6,23 mmol) y piridina (10 ml) se agitaron a temperatura ambiente durante 4 h. La mezcla de reacción se concentró al vacío. Se añadió cuidadosamente hielo, seguido de una solución acuosa al 10 % de hidróxido sódico (20 ml) y después se extrajo en diclorometano (3 x 40 ml). La capa orgánica combinada se lavó con salmuera (40 ml), se secó (Na2SO4) y se concentró al vacío. El producto en bruto se purificó por cromatografía, (S¡O2, EtOAc al 0-40 % en Heptano), produciendo el compuesto del título en forma de un aceite de color amarillo pálido (1,05 g). RMN 1H (500 m Hz , CDCb) 8 ppm 8,69 (s, 2h ), 7,21 (dt, J 4,1, 2,4 Hz, 1H), 4,02 (s, 4H), 2,81 (ddt, J 6,5, 4,3, 1,9 Hz, 2H), 2,54 (d, J 3,6 Hz, 2H), 1,92 (t, J 6,6 Hz, 2H).
I N T E R M E D I O 154
2-n,4-d¡oxasp¡ror[4,5]dec-7-en-8-¡l}-5-(tetramet¡l-1,3,2-d¡oxaborolan-2-¡l)p¡rim¡d¡na
El compuesto del título se preparó a partir del Intermedio 153 (1,05 g, 3,53 mmol), pinacol éster de diboro (1,35 g, 5,30 mmol), acetato potásico (1,05 g, 10,06 mmol), dioxano (10 ml), aducto de dicloro[1,1'-b¡s(d¡fenilfosf¡noferroceno]-paladio diclorometano (145 mg, 0,17 mmol) por el Método H (1,36 g, 99 %). RMN 1H (500 MHz, CDCb) 8 ppm 8,92 (s, 2H), 7,27 (d, J 4,2 Hz, 1H), 4,02 (s, 4H), 2,86 (ddt, J 6,5, 4,3, 1,9 Hz, 2H), 2,57 (d, J 3,4 Hz, 2H), 1,93 (t, J 6,6 Hz, 2H), 1,35 (s, 12H).
I N T E R M E D I O 155
(1R.3R)-1-[2-(d¡fluorometox¡)fen¡l1-7-[2-(1.4-d¡oxasp¡ro[4.51dec-7-en-8-¡l)p¡r¡m¡d¡n-5-¡l1-6-fluoro-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ol
El compuesto del título se preparó a partir del Ejemplo 16 (300 mg, 0,62 mmol), el Intermedio 154 (286 mg, 0,74 mmol), una solución 2 M de carbonato sódico en agua (0,93 ml, 1,85 mmol), dioxano (3 ml) y aducto de dicloro[1,1'-bis(difenilfosfinoferroceno]-paladio diclorometano (50 mg, 0,06 mmol) por el Método A (146 mg, 40 %). RMN 1H (500 MHz, CDCla) 8 ppm 8,70 (d, J 1,1 Hz, 2H), 7,65 (d, J 7,1 Hz, 1H), 7,41 (d, J 10,9 Hz, 1H), 7,29 (d, J 8,1 Hz, 2H), 7,25 - 7,22 (m, 1H), 7,21 - 7,12 (m, 2H), 6,66 (dd, J 74,6, 72,9 Hz, 1H), 5,44 (d, J 4,6 Hz, 1H), 4,88 (dd, J 8,5, 3,9 Hz, 1H), 4,03 (s, 4H), 3,77 (s, 1H), 3,65 - 3,53 (m, 1H), 2,92 - 2,78 (m, 2H), 2,57 (s, 2H), 2,43 (dt, J 14,1, 3,5 Hz, 1H), 1,94 (t, J 6,5 Hz, 2H).
I N T E R M E D I O 156
(1R.3R)-1-[2-(d¡fluorometox¡)fen¡l1-7-[2-(1.4-d¡oxasp¡ro[4.51dec-8-¡l)p¡r¡m¡d¡n-5-¡l1-6-fluoro-2,3-d¡h¡dro-1H-c¡clopenta[4,51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ol
Una solución 0,05 M del Intermedio 155 (120 mg, 0,22 mmol) en EtOH (4,32 ml) y trietilamina (30 pl, 0,22 mmol) se pasó 10 veces a través del H-cube usando Pd al 10 %/C Cat-cart a 1,0 ml/min, 50 °C y una presión de 100 bar en una atmósfera de hidrógeno controlada. El producto en bruto se purificó por cromatografía, (SiO2, EtOAc al 20-100 % en heptano seguido de MeOH al 1-50 % en EtOAc) para proporcionar el compuesto del título en forma de un sólido de color blanquecino (38 mg, 23 %). CLEM (EN+) TR 1,11 min, 553,0 (M+H)+.
I N T E R M E D I O 157
4-(5-{(1R,3R)-1-[2-(difluorometoxi)fenil1-6-fluoro-3-hidroxi-2,3-dihidro-1H-ciclopenta[4,51imidazo[1,2-a1piridin-7-il}pirimidin-2-il)ciclohexanona
El Intermedio 156 (70 mg, 0,09 mmol, pureza del 70 %), ácido clorhídrico 4 N (0,60 ml) y THF (2,0 ml) se cargaron en un tubo cerrado herméticamente. La mezcla se calentó a 50 °C durante 4 h. La mezcla de reacción se diluyó con una solución acuosa saturada de carbonato sódico (5 ml) y se extrajo con EtOAc (3 x 10 ml). La fase orgánica combinada se lavó con agua (10 ml), seguido de salmuera (10 ml), se secó (Na2SO4) y se redujo al vacío. El residuo se purificó por cromatografía, (SiO2, EtOAc al 20-100 % en heptano, seguido de MeOH al 1-100 % en EtOAc), produciendo el
compuesto del título en forma de un sólido de color amarillo pálido (43 mg, 91 %). RMN 1H (500 MHz, CDCI3) 8 ppm 8,72 (d, J 1,4 Hz, 2H), 7,68 (d, J 7,1 Hz, 1H), 7,44 (d, J 10,9 Hz, 1H), 7,31 - 7,27 (m, 1H), 7,25 (d, J 1,5 Hz, 1H), 7,21 - 7,08 (m, 2H), 6,67 (dd, J 74,8, 72,6 Hz, 1H), 5,46 (dd, J 7,3, 3,0 Hz, 1H), 4,89 (dd, J 8,5, 3,9 Hz, 1H), 4,45 (d, J 23,2 Hz, 1H), 3,67 - 3,55 (m, 1H), 3,41 (tt, J 10,7, 3,6 Hz, 1H), 2,60 - 2,47 (m, 4H), 2,47 - 2,35 (m, 3H), 2,21 (ddt, J 16,8, 11,9, 5,3 Hz, 2H). CLEM (EN+) TR 1,05 min, 509,0 (M+H)+.
I N T E R M E D I O 158
2,2-dimetilpropanoato de 2.2-dicloro-3-oxoc¡clobut¡lo
A una mezcla agitada de pivalato de vinilo (30 g, 234 mmol) y cinc (31 g, 474 mmol) en éter (250 ml) se añadió gota a gota una solución de cloruro de 2,2,2-tricloroacetilo (34 ml, 304 mmol) en éter (250 ml) durante 2,5 h en un baño de agua mientras se mantenía la temperatura de reacción entre 15 - 30 °C. La reacción se filtró a través de Celite y se lavó a su través con acetato de etilo (200 ml). El filtrado se lavó con agua (200 ml) y salmuera (200 ml), se secó sobre sulfato sódico y se concentró al vacío para proporcionar el compuesto del título en forma de un líquido de color naranja. ( 68 g, 97 %). RMN 1H (500 MHz, CDCI3) 8 ppm 5,40 (dd, J 8,4, 6,2 Hz, 1H), 3,70 (dd, J 18,9, 8,4 Hz, 1H), 3,39 (dd, J 18,9, 6,2 Hz, 1H), 1,28 (s, 9H).
I N T E R M E D I O 159
2.2-d¡met¡lpropanoato de 3-oxociclobutilo
Se añadió cinc (74 g, 1,1 mol) a ácido acético (200 ml) con agitación y la suspensión se enfrió en un baño de hielo. Se añadió gota a gota el Intermedio 158 (68 g, 228 mmol) en ácido acético (300 ml) durante 2 h. Después de que se completara la adición, la reacción se calentó a t.a. y se agitó durante 1,5 h. La reacción se filtró y se lavó con DCM (100 ml). El filtrado se diluyó con EtOAc (800 ml) y se lavó secuencialmente con agua (3 x 250 ml), una solución acuosa saturada de NaHCO3 (3 x 250 ml) y salmuera (50 ml). La fase orgánica se secó sobre sulfato sódico y se concentró al vacío. El residuo se purificó por cromatografía (SiO2, EtOAc al 0-10 % en heptano), produciendo el compuesto del título en forma de un aceite incoloro y transparente (11 g, 28 %). RMN 1H (500 MHz, Cd CI3) 5,26 - 5,19 (m, 1H), 3,51 - 3,40 (m, 2H), 3,19 - 3,07 (m, 2H), 1,22 (s, 9H).
I N T E R M E D I O 160
2,2-dimetilpropanoato de 3-(5-bromop¡r¡m¡d¡n-2-¡l)-3-h¡drox¡c¡clobut¡lo
El compuesto del título se preparó a partir de 5-bromo-2-yodopirimidina (16,7 g, 58,8 mmol), DCM (200 ml), n-BuLi 2,5 M en hexano en hexano (23,5 ml), el Intermedio 159 (10 g, 58,8 mmol) en DCM (50 ml) por el Método F, produciendo el compuesto del título en forma de un sólido de color amarillo (7,6 g, 35 %). RMN 1H (500 MHz, CDCI3) 8,78 (s, 2H), 5,22 - 5,14 (m, 1H), 3,03 - 2,93 (m, 2H), 2,67 - 2,58 (m, 2H), 1,22 (s, 9H).
I N T E R M E D I O 161
1-(5-bromop¡r¡m¡d¡n-2-¡l)c¡clobutano-1.3-d¡ol
El Intermedio 160 (6 g, 16,4 mmol) se disolvió en MeOH (120 ml) y se añadió K2CO3 (11,3 g, 82 mmol) y la reacción se agitó durante 18 h a t.a. La reacción se diluyó con DCM (400 ml) y se lavó con agua (150 ml). La fase acuosa se extrajo con DCM (200 ml). Los extractos orgánicos combinados se secaron sobre sulfato sódico y se concentraron al vacío para proporcionar el compuesto del título en forma de un sólido de color blanquecino (2,94 g, 73 %). RMN 1H (500 MHz, DMSO-d6) 8,98 (s, 2H), 5,63 (s, 1H), 5,08 (d, J 6,2 Hz, 1H), 4,09 - 3,92 (m, 1H), 2,87 - 2,79 (m, 2H), 2,28 -2,14 (m, 2H).
I N T E R M E D I O 162
3-(5-bromop¡r¡m¡d¡n-2-¡l)-3-h¡drox¡c¡clobutan-1-ona
A una solución agitada del Intermedio 161 (2 g, 8,1 mmol) en DCM (200 ml) se añadió peryodinano de Dess-Martin (4,1 g, 9,8 mmol). La reacción se agitó durante 18 h y la suspensión resultante se diluyó con DCM (100 ml) y se lavó con una solución acuosa saturada de NaHCO3 (100 ml). La capa acuosa se extrajo de nuevo con DCM (100 ml) y los extractos orgánicos combinados se secaron sobre sulfato sódico y se concentraron al vacío. El residuo en bruto se purificó por cromatografía (SiO2, EtOAc al 0-30 % en heptano) para proporcionar el compuesto del título en forma de un sólido de color blanquecino (1,37 g, 69 %). RMN 1H (500 MHz, DMSO-d6) 9,04 (s, 2H), 6,41 (s, 1H), 3,69 - 3,55 (m, 2H), 3,37 - 3,21 (m, 2H).
I N T E R M E D I O 163
3-(5-bromop¡r¡m¡d¡n-2-¡l)-3-[(terc-but¡ld¡met¡ls¡l¡l)ox¡1c¡clobutan-1-ona
El compuesto del título se preparó a partir del Intermedio 196 (1,37 g, 5,64 mmol), DMF (20 ml), IH-imidazol (1,9 g, 28,18 mmol) y terc-butil(doro)dimetilsilano (2,0 g, 13,5 mmol) por el Método G (1,6 g 79 %). RMN 1H (500 MHz, DMSO-d6) 9,06 (s, 2H), 3,78 - 3,66 (m, 2H), 3,44 - 3,34 (m, 2H), 0,88 (s, 9H), 0,00 (s, 6H).
I N T E R M E D I O 164
3-(5-bromop¡r¡m¡d¡n-2-¡l)-3-[(terc-but¡ld¡met¡ls¡l¡l)ox¡1-1-metilc¡clobutan-1-ol
El Intermedio 163 (1,35 g, 3,78 mmol) se disolvió en éter seco (40 ml) en una atmósfera de N2 con agitación y se enfrió a 0 °C usando un baño de hielo. Se añadió gota a gota MeMgBr 3 M en éter dietílico (2,52 ml) y la reacción se agitó durante 30 minutos a 0 °C. La reacción se interrumpió con una solución acuosa saturada de NH4Cl (20 ml) y después agua (20 ml). La mezcla se extrajo con EtOAc (2 x 50 ml), se secó sobre sulfato sódico y se concentró al vacío. El residuo en bruto se purificó por cromatografía (SO 2, DCM al 0-100 % en heptano) para proporcionar el compuesto del título en forma de un aceite transparente (1,19 g, 84 %). Isómero principal, abundancia de ~70 %: RMN 1H (500 MHz, CDCla) 8,79 (s, 2H), 3,10 - 3,03 (m, 2H), 2,59 - 2,51 (m, 2H), 1,18 (s, 3H), 0,87 (s, 9H), -0,14 (s, 6H).
Isómero menor, abundancia ~30 %: RMN 1H (500 MHz, CDCla) 8,79 (s, 2H), 2,78 - 2,63 (m, 4H), 1,49 (s, 3H), 0,95 (s, 9H), 0,04 (s, 6H).
I N T E R M E D I O 165
3-[(terc-but¡ld¡met¡ls¡l¡l)ox¡1-1-met¡l-3-[5-(tetramet¡l-1.3.2-d¡oxaborolan-2-¡l)p¡r¡m¡d¡n-2-¡l1ciclobutan-1-ol
Se preparó a partir del Intermedio 164 por el Método H. RMN 1H (500 MHz, CDCla) 9,02 (s, 2H), 3,15 - 3,08 (m, 2H), 2,58 - 2,50 (m, 2H), 1,37 (s, 12H), 1,27 (s, 3H), 0,87 (s, 9H), -0,16 (s, 6H).
I N T E R M E D I O 166
(1R,3R)-7-bromo-1-r2-(difluorometoxi)fenil1-6-fluoro-3-metoxi-2,3-dihidro-1H-ciclopentar4,51imidazor1,2-a1piridina
El compuesto del título se preparó a partir del Ejemplo 16 por un procedimiento análogo al Ejemplo 14.
I N T E R M E D I O 167 Y 168
(IR ) -7-bromo-1-r5-cloro-2-(difluorometoxi)fenil1-6-fluoro-1,2-dihidro-3H-ciclopentar4,51imidazoH,2-a1pindin-3-ol y (IS ) -7-bromo-1-r5-cloro-2-(difluorometoxi)fenil1-6-fluoro-1,2-dihidro-3H-ciclopentar4,51imidazoH,2-a1pindin-3-ol
Los compuestos del título se prepararon a partir de los Ejemplos 213 y 214, respectivamente, por el Método B. CLEM (EN+) TR 1,77 min, 447,0/449,0 (M+H)+.
I N T E R M E D I O 169
4-(5-bromop¡r¡mid¡n-2-¡l)-4-h¡drox¡c¡clohexan-1-ona
A una solución agitada del Intermedio 152 (1,11 g, 2,96 mmol) en THF (4,5 ml) se añadió HCl 4 N (1,5 ml). La mezcla se calentó a 50 °C en un tubo a presión durante 6,5 h. La mezcla de reacción enfriada se añadió a una mezcla de EtOAc (20 ml) y NaHCO3 saturado (20 ml). La capa orgánica se separó y la capa acuosa se extrajo de nuevo con EtOAc ( 2 x 5 ml). Las capas orgánicas combinadas se lavaron con una mezcla 1:1 de agua y salmuera (4 ml) y salmuera (4 ml), se secaron sobre sulfato de magnesio, se filtraron y el disolvente se concentró al vacío. El producto en bruto se purificó por cromatografía en columna (SiO2, EtOAc al 0-50 % en heptano), produciendo el compuesto del título en forma de un sólido de color amarillo pálido (537 mg, 64 %). CLEM (EN+) TR 1,36 min, 271,0/273,0 (M+H)+.
I N T E R M E D I O 170
4-(5-bromop¡r¡m¡d¡n-2-¡l)-4-[(tr¡met¡lsil¡l)ox¡lc¡clohexan-1-ona
El compuesto del título se preparó a partir del Intermedio 169 (2,35 g, 8,06 mmol), 1H-imidazol (0,84 g, 12,37 mmol), DCM seco (60 ml) y cloro(trimetil)silano (1,2 ml, 9,27 mmol) por el Método G (2,68 g,94 %). CLEM (EN+) TR 2,28 min, 343,0/345,0 (M+H)+.
I N T E R M E D I O 171
4-(5-bromop¡r¡m¡d¡n-2-¡l)-1-met¡l-4[(tr¡met¡ls¡l¡l)ox¡lc¡clohexan-1-ol
A una solución agitada del Intermedio 170 (482 mg, 1,33 mmol) en THF seco (20 ml) se añadió bromo(metil)magnesio 1,4 M en tolueno/THF (1,5 ml) durante 5 minutos a t.a. La mezcla de reacción se agitó durante 21 h y después se inactivó con NH4Cl saturado (1,0 ml). Después, los volátiles se concentraron al vacío; después se añadieron EtOAc (10 ml) y agua (10 ml), la capa orgánica se separó y la capa acuosa se extrajo de nuevo con EtOAc (2 x 5 ml). Las capas orgánicas combinadas se lavaron con una mezcla 1:1 de agua y salmuera (10 ml) y salmuera (5 ml), se secaron sobre sulfato de magnesio, se filtraron y el disolvente se concentró al vacío para dar el compuesto del título (0,48 g, 100 %). CLEM (EN+) TR 2,20 min, 269,0/270,0 (M+H)+.
I N T E R M E D I O 172 Y 173
Isómero A: cis-1-(5-bromopir¡m¡d¡n-2-¡l)-4 met¡lc¡clohexano-1,4-d¡ol e Isómero B: trans-1-(5-bromopir¡m¡d¡n-2-¡l)-4 met¡lc¡clohexano-1,4-d¡ol
A una solución del Intermedio 171 (27,78 g, 77,31 mmol) en THF seco (1 l) se añadió fluoruro de N,W,W-tributilbutan-1-aminio 1 M en THF (90 ml) durante 10 minutos en una atmósfera de gas de nitrógeno a t.a. La reacción se agitó durante 90 minutos y después los volátiles se concentraron al vacío; después se añadieron EtOAc (200 ml), agua (100 ml) y salmuera (100 ml). La capa orgánica se separó y la capa acuosa se extrajo de nuevo con EtOAc (4 x 100 ml). Después, las capas orgánicas se combinaron y se lavaron con una mezcla 1:1 de agua y salmuera (200 ml) y salmuera (100 ml), se secaron sobre sulfato de magnesio (150 ml), se filtraron y el disolvente se concentró al vacío. El aceite se purificó por cromatografía en columna (S¡O2, EtOAc al 0-100 % en heptano): se disolvieron 5,7 g del primer producto eluído en DCM y se adsorbieron sobre gel de sílice (20 g), después se purificaron por cromatografía en columna (S¡O2, EtOAc al 0-60 % en heptano) para dar (2,90 g, 13 %) del compuesto del título, Isómero A: Intermedio 172 en forma de un sólido de color rosa; se disolvieron 4,5 g del segundo producto eluído en DCM y se adsorbieron sobre gel de sílice (21 g), después se purificaron por cromatografía en columna (S¡O2, EtOAc al 17-100 % en heptano) para dar (3,23 g, 12 %) del compuesto del título, Isómero B: Intermedio 173. Intermedio 172: CLEM (EN+) t R 0,95 min, 287,0/289,0 (M+H)+. Intermedio 173: CLEM (EN+) TR 3,11 min, 287,0/289,0 (M+H)+.
I N T E R M E D I O 174
Isómero A: 1-met¡l-4-[5-(tetramet¡l-1,3,2-d¡oxaborolan-2-¡l)p¡r¡m¡d¡n-2-¡llciclohexano-1,4-d¡ol
El compuesto del título se preparó a partir del Intermedio 172 (2,9 g, 10,1 mmol), 4,4,4',4',5,5,5',5'-octametil-2,2'-b¡-1,3,2-dioxaborolano (3,12 g, 12,29 mmol), acetato potásico (3,20 g, 32,61 mmol), 1,4-dioxano (120 ml), bis[3-(difen¡lfosfan¡l)c¡clopenta-2,4-d¡en-1-¡l]h¡erro; diclorometano; dicloropaladio (0,41 g, 0,51 mmol) por el Método H (1,06 g, 24 %). CLEM (EN+) TR 0,91 min, 253,0 (M+H)+.
I N T E R M E D I O 175
Isómero B: 1-met¡l-4-[5-(tetramet¡l-1.3.2-d¡oxaborolan-2-¡l)p¡r¡m¡d¡n-2-¡llc¡clohexano-1.4-d¡ol
El compuesto del título se preparó a partir del Intermedio 173 (3,23 g, 9 mmol), 4,4,4',4',5,5,5',5'-octametil-2,2'-b¡-1,3,2-dioxaborolano (2,82 g, 11,11 mmol), acetato potásico (2,84 g, 28,94 mmol), 1,4-dioxano (130 ml), bis[3-(difen¡lfosfan¡l)c¡clopenta-2,4-d¡en-1-¡l]h¡erro; diclorometano; dicloropaladio (0,38 g, 0,47 mmol) por el Método H (1,12 g, 28 %). CLEM (EN+) TR 0,80 min, 253,0 (M+H)+.
I N T E R M E D I O 176
2-(((1R.3R)-7-bromo-1-(5-cloro-2-(d¡fluorometox¡)fen¡l)-2.3-d¡h¡dro-1H-c¡clopenta[4.5l¡m¡dazo[1.2-alp¡r¡d¡n-3-¡l)oxi)acetato de terc-butilo
El compuesto del titulo se preparó a partir del Ejemplo 190 (50 mg, 0.116 mmol), THF (4 ml), hidruro sódico (10 mg, 0,256 mmol; 60 % en aceite) y bromoacetato de terc-butilo(93 mg, 0,466 mmol) en THF (0,25 ml) por el Método Q (42 mg, 66 %). CLEM [M 1b] (EN+) TR 1,94 min, 543,1 (M+H)+.
I N T E R M E D I O 177
2-(difluorometox¡)-3-fluorobenzaldehído
El compuesto del título se preparó a partir de hidróxido potásico (80,09 g, 1427,43 mmol) en agua (175 ml), MeCN (175 ml), 3-fluoro-2-hidroxibenzaldehído (10 g, 71,37 mmol), [bromo(difluoro)metil]fosfonato de dietilo (13,95 ml, 78,51 mmol) por el Método N (4,55 g, 45 %). RMN 1H (500 MHz, CDCla) 8 ppm 10,35 (s, 1H), 7,73 (dt, J 7,8, 1,4 Hz, 1H), 7,45 (ddd, J 10,0, 8,2, 1,6 Hz, 1H), 7,37 (td, J 8,0, 4,7 Hz, 1H), 6,90 - 6,57 (m, 1H).
I N T E R M E D I O 178
ácido 3-[6-bromo-2-(etoxicarbonil)-7-fluoroimidazo[1.2-a1piridin-3-il1-3-[2-(difluorometoxi)-3-fluorofenil1propanoico
El compuesto del título se preparó a partir de 6-bromo-7-fluoro-3-yodoimidazo[1,2-a1piridin-2-carboxilato de etilo (3,12 g, 10,88 mmol), 2,2-dimetil-1,3-dioxano-4,6-diona (3,14 g, 21,76 mmol), el Intermedio 177 (4,55 g, 21,76 mmol) y L-prolina (152,39 mg, 1,32 mmol) en acetonitrilo (45 ml) por el Método P (6,5 g). El material se recogió hacia adelante para la siguiente etapa sin purificación.
I N T E R M E D I O 179
6-bromo-3-[1-[2-(d¡fluorometox¡)-3-fluoro-fen¡l1-3-etox¡-3-oxo-prop¡l1-7-fluoro-¡m¡dazo[1.2-a1p¡r¡d¡n-2-carbox¡lato de etilo
El compuesto del título se preparó a partir del Intermedio 178 (6,51 g, 7,53 mmol), EtOH (80m l) y dicloruro de tionilo (1,09 ml, 15,0 mmol) por el Método O (2,13 g, 48,1 %). RMN 1H (500 MHz, CDCla) 8 ppm 8,69 (d, J 6,4 Hz, 1H), 7,56 (d, J 8,0 Hz, 1H), 7,36 (d, J 8,3 Hz, 1H), 7,22 (td, J 8,2, 5,3 Hz, 1H), 7,10 (ddd, J 10,0, 8,4, 1,4 Hz, 1H), 6,68 (dd, J 76,5, 73,7 Hz, 1H), 5,37 (dd, J 10,3, 5,1 Hz, 1H), 4,40 (cd, J 7,1, 4,6 Hz, 2H), 4,10 - 4,00 (m, 2H), 3,94 (dd, J 17,0, 10,3 Hz, 1H), 3,30 (dd, J 17,0, 5,1 Hz, 1H), 1,40 (t, J 7,1 Hz, 3H), 1,16 (t, J 7,1 Hz, 3H). CLEM (EN+) TR 1,42 min, 547,0/549,0 (M+H)+.
I N T E R M E D I O 180
7-bromo-1-[2-(d¡fluorometox¡)-3-fluorofen¡l1-6-fluoro-3-oxo-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-2-carboxilato de etilo
El compuesto del título se preparó a partir del Intermedio 179 (2,13 g, 3,62 mmol), tolueno (40 ml) y 2-met¡lbutan-2-olato potásico (2,74 g, 5,43 mmol) por el Método L (480 mg, 23 %). CLEM (EN+) TR 1,98 min, 501,0/503,0 (M+H)+. I N T E R M E D I O 181
7-bromo-1-f2-(d¡fluorometox¡)-3-fluorofen¡l1-6-fluoro-1.2-d¡h¡dro-3H-c¡clopentaf4.51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ona
El compuesto del título se preparó a partir del Intermedio 180 (0,48 g, 0,83 mmol), DMSO (8 ml) y agua (2 ml) por el Método M (267 mg, 75 %). CLEM (EN+) TR 1,99 m¡n, 429,0/431,0 (M+H)+.
I N T E R M E D I O 182
7-bromo-1-[2-(d¡fluorometox¡)-3-fluorofen¡l1-6-fluoro-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ol
El compuesto del título se preparó a part¡r del Intermedio 181 (0,61 g, 1,27 mmol), tr¡-sec-but¡lboroh¡druro de l¡t¡o 1 M en THF (1,521 ml) y THF (10 ml) por el Método B (460 mg, 65 %). CLEM (EN+) TR 1,17 m¡n, 431,0/433,0 (M+H)+. I N T E R M E D I O 183
ác¡do ^2-^(1S.4S)-2-terc-butox¡carbon¡l-2.5-d¡azab¡c¡clô 2.2.11heptan-5-¡l1p¡r¡m¡d¡n-5-¡l1borón¡co
El compuesto del título se preparó a partir de ácido 2-doropirimidin-5-borónico (1,01 g, 6,38 mmol), (1S,4S)-2-boc-2,5-diazabiciclo[2.2.1]heptano (132 mg, 0,6325 mmol), etanol (30 ml, 510 mmol) y trietilamina (0,9 ml, 6 mmol) por el Método E (1,22 g, 60 %). 8h (300 MHz, DMSO-d6) 8,67 (s, 2 H), 4,86-4,97 (m, 2H), 4,39-4,51 (m, 2H), 3,12-3,59 (m, 2H), 1,86-1,97 (m, 2H), 1,30-1,44 (m, 9H).
I N T E R M E D I O 184
(1R)-7-(2-[(1S,4S)-2-terc-butoxicarbonil-2,5-diazabiciclo[2.2.11hept-2-il1pinmidin-5-il}-1-[2-(difluorometoxi)fenil1-3-met¡l-2.3-d¡h¡dro-1H-c¡clopenta[4,51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ol
El compuesto del título se preparó a partir del Ejemplo 15 (501 mg, 1,22 mmol), el Intermedio 183 (520 mg, 1,63 mmol), 1,4-dioxano (11 ml), carbonato sódico ac. 2 M (2 ml) y dicloruro de 1,1'-bis(difenilfosfino)ferroceno-paladio (II) (47 mg, 0,064 mmol) por el Método A (466 mg, 63 %). 8h (300 MHz, DMSO-d6) 8,54 (s, 2 H), 7,97 (d, 1H, J 1,5 Hz), 7,65 (dd, 1H, J 9,5, 0,8 Hz), 7,50 (dd, 1H, J 9,4, 1,7 Hz), 7,36 (t, 1H, J 74,1 Hz), 7,23-7,34 (m, 2H), 7,10-7,17 (m, 1H), 6,98 (dd, 1H, J 7,7, 1,5 Hz), 5,26 (s, 1H), 4,85-4,91 (m, 1H), 4,79 (dd, 1H, J 8,3, 4,3 Hz), 4,41-4,51 (m, 1H), 3,49-3,58 (m, 1H), 3,33-3,45 (m, 2H), 3,09-3,20 (m, 2H), 2,37 (dd, 1H, J 13,4, 4,5 Hz), 1,88-1,96 (m, 2H), 1,55 (s, 3H), 1,39 (s, 9H). Asignación de RMN para el diastereoisómero principal. El material es una mezcla (83:17) de los dos diaestereoisómeros. CLEM (EN+) 605 (M+H)+, TR 2,34 minutos.
I N T E R M E D I O 185
5-Bromo-2-metanosulfin¡lp¡r¡d¡na
Se añadió NaIO4 (9,56 g, 44,69 mmol) en forma de una suspensión en agua (10 ml) a una solución agitada de 5-bromo-2-(metilsulfanil)piridina (2,4 g, 11,76 mmol) en ácido acético (40 ml) a t.a. La mezcla se agitó a t.a. durante 2 h. Después de este tiempo, se había formado un precipitado incoloro. La mezcla se trató con agua (50 ml), tras lo cual se disolvió el precipitado. La mezcla ácida acuosa se basificó a través de la adición de una solución acuosa saturada de carbonato potásico y el producto se extrajo con EtOAc (3 x 50 ml). La fase orgánica combinada se lavó con una solución acuosa al 10 % de tiosulfato sódico (50 ml), se secó (Na2SO4) y se redujo al vacío para dar el producto en bruto, en forma de un cristal de color ámbar (2,52 g), que se solidificó después de un periodo de reposo. La purificación por cromatografía (S¡O2, EtOAc al 0-100 % en heptano) proporcionó el compuesto del título en forma de un aceite de color amarillo pálido (2,04 g, 79 %). 8h (500 MHz, CDCla) 8,68 (d, J 2,0 Hz, 1H), 8,08 (dd, J 8,3, 2,2 Hz, 1H), 7,93 (d, J 8,3 Hz, 1H), 2,84 (s, 3H).
I N T E R M E D I O S 186 - 188
Los siguientes intermedios se prepararon a partir de los intermedios listados o a partir de materiales de partida disponibles en el mercado usando métodos análogos a los mencionados en la columna de la derecha o para los intermedios de la columna de la derecha.
E j e m p l o 1
7-bromo-1-[2-(d¡fluorometox¡)fen¡l1-1.2-d¡h¡dro-3H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ona
Una soluc¡ón del Intermedio 6 (10.0 g. 21.5 mmol) en DMSO (50 ml) y agua (10 ml) se ag¡tó a 100 °C durante 48 h. La mezcla de reacc¡ón se enfr¡ó y se vert¡ó sobre agua helada. Después. el prec¡p¡tado se retiró por f¡ltrac¡ón y se secó al vacío para produc¡r el compuesto del título en forma de un sól¡do de color crema (8.2 g. 97 %). 5h (DMSO-d6. 400 MHz) 8.27 (d. J 0.7 Hz. 1H). 7.73 (d. J 9.8 Hz. 1H). 7.55 (dd. J 9.8 Hz. J 1.9 Hz. 1H). 7.40 (m. 1H). 7.26 (m. 2H). 7.17 (t. J 7.6 Hz. 1H). 6.92 (d. J 7.4 Hz. 1H). 5.14 (dd. J 7.0 Hz. J 1.9 Hz. 1H). 3.60 (dd. J 18.2 Hz. J 7.1 Hz. 1H). 2.75 (dd. J 18.2 Hz. J 2.1 Hz. 1H). CLEM (EN+) TR 1.42 m¡n. 393.0/395.0 (M+H)+.
E j e m p l o s 2 y 3
(R)-7-Bromo-1-(2-d¡fluorometox¡-fen¡l)-1.2-d¡h¡dro-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ona y (S)-7-Bromo-1-(2-d¡fluorometox¡-fen¡l)-1.2-d¡h¡dro-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ona
Los compuestos del título se a¡slaron med¡ante separac¡ón qu¡ral del Ejemplo 1 en cond¡c¡ones de CL en una Ch¡ralpak AD (100 x 500 mm x mm. flujo 300 ml/m¡n. 30 °C. heptano-EtOH (1:1). ¡nyecc¡ón de 84 ml de una soluc¡ón a una concentrac¡ón de 6.2 g/l). El pr¡mer enant¡ómero en elu¡rse (TR 22 m¡n) se recog¡ó y las fracc¡ones se evaporaron para produc¡r el Ejemplo 2. El segundo enant¡ómero en elu¡rse (TR 32 m¡n) se recog¡ó y las fracc¡ones se evaporaron para produc¡r el Ejemplo 3.
E j e m p l o 4 -
MÉTODO A
1-[2-(d¡fluorometox¡)fen¡l1-7-[2-(5-oxo-1.4-d¡azepan-1-¡l)p¡r¡m¡d¡n-5-¡l1-1.2-d¡h¡dro-3H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ona
Una mezcla del Ejemplo 1 (74 mg. 0.188 mmol). ác¡do [2-(5-oxo-1.4-d¡azepan-1-¡l)p¡r¡m¡d¡n-5-¡l1borón¡co (0.06218 g.
0,2635 mmol), aducto de Pd(dppf)Cl2 DCM (0,00392 g, 0,00470 mmol) y carbonato sódico 2 M (1,5 ml) en 1,4-dioxano (4 ml) se desgasificó y se agitó a 110 °C durante 2,5 h. La reacción se enfrió y se diluyó con EtOAc, se lavó con agua, la capa ac. se extrajo una vez más usando EtOAc, los extractos orgánicos se secaron sobre sulfato de magnesio y se concentraron al vacío. El sólido cristalino se trituró en EtOAc, se filtró, se lavó con más EtOAc, después hexano y se secó para dar el compuesto del título en forma de un sólido de color amarillo pálido (66 mg, 70 %). 8h (DMSO-d6 , 400 MHz) 8,64 (s, 2H), 8,22 (s, 1H), 7,84 (m, 1H), 7,78 (m, 1H), 7,67 (m, 1H), 7,38 (m, 1H), 7,28 (t, J 72, 76 Hz, 1H), 7,15 (m, 1H), 7,27 (m, 1H), 6,89 (m, 1H), 5,17 (d, J 5,4 Hz, 1H), 3,93 (m, 4H), 3,62 (m, 1H), 3,29 (m, 2H), 3,20 (m, 2H), 2,77 (dd, J 18,2 Hz, J 1,6 Hz, 1H). CLEM (EN+) TR 1,25 min, 505,0 (M+H)+.
E j e m p l o 5 ,
MÉTODO B
(1R.3R)-7-bromo-1-[2-(d¡fluorometox¡)fen¡l1-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡din-3-ol
Se añadió tri-sec-butilborohidruro de litio (0,041 ml, 1 M en THF) a una solución agitada del Ejemplo 2 (51 mg, 0,13 mmol) en THF seco (2 ml) a -78 °C en una atmósfera de argón. Después de 30 minutos, la solución se diluyó con MeOH y se añadió una solución ac. 1 M de hidróxido sódico. La solución se extrajo con EtOAc, la capa orgánica se secó sobre sulfato de magnesio, se concentró al vacío y el residuo resultante se purificó por HPLC preparativa dirigida por masas, produciendo el compuesto del título en forma de un sólido de color blanco (16 mg, 31 %). RMN 1H (400 MHz, CDCla) 87,72 (d, J 0,5 Hz, 1H), 7,51 (d, J 9,7 Hz, 1H), 7,29 (ddd, J 8,6 Hz, J 6,7 Hz, J 2,4 Hz, 1H), 7,12 7,23 (m, 4H), 6,67 (dd, J 74,2 Hz, J 73,0 Hz, 1H), 5,87 (s, 1H), 5,47 (dd, J 7,2 Hz, J 2,4 Hz, 1H), 4,84 (dd, J 8,6 Hz, J 4,0 Hz, 1H), 3,60 (dt, J 14,3 Hz, J 7,8 Hz, 1H), 2,41 (dt, J 13,9 Hz, J 3,1 Hz, 1H). CLEM (EN+) TR 3,6 min, 395,0/397,0 (M+H)+.
E j e m p l o 6
(3Z)-7-bromo-1-r2-(difluorometoxi)fenil1-N-hidroxi-1,2-dihidro-3H-ciclopentar4,51imidazor1,2-a1piridin-3-imina
A una solución del Ejemplo 1(0,1 g, 0,25 mmol) en EtOH(2 ml), se añadió piridina (0,2 ml) y clorhidrato de hidroxilamina (0,026 g, 0,38 mmol) y la mezcla de reacción se calentó a 65 °C durante 30 minutos. La mezcla de reacción se enfrió a t.a., se repartió entre EtOAc (50 ml) y agua (50 ml). La fase orgánica se separó y se lavó con agua (10 ml) y salmuera (10 ml), se secó sobre sulfato sódico, se filtró y se concentró al vacío para dar un sólido. El lavado con Et2O dio el compuesto del título en forma de un sólido de color beige (0,094 g, 91 %). CLEM (EN+) TR 1,43 min, 408,0/410,0 (M+H)+.
E j e m p l o 7 ,
MÉTODO C
1-(5-r1-r2-(difluorometoxi)fenil1-3-hidroxi-2,3-dihidro-1H-ciclopentar4,51imidazor1,2-a1piridin-7-il1pirimidin-2-il)-1,4-diazepan-5-ona
A una suspensión del Ejemplo 4 (0,055 g, 0,11 mmol) en MeOH (0,5 ml) a t.a. se añadió THF para dar una solución. A esto se le añadió borohidruro sódico (0,004 g, 0,11 mmol) y la mezcla de reacción se agitó a t.a. durante 1 h. Se añadió cloruro de amonio (2 ml), la mezcla se separó en EtOAc (3 x 5 ml) y los materiales orgánicos se lavaron con salmuera (5 ml), se secaron sobre sulfato sódico, se filtraron y se concentraron al vacío para dar un sólido de color blanco, este se lavó con DCM, produciendo el compuesto del título (0,039 g, 71 %). CLe M (EN+) TR 1,62 min, 507,0 (M+H)+.
E j e m p l o 8
7-bromo-1-[2-(d¡fluorometox¡)fen¡l1-3-met¡l-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ol
Se añadió bromuro de metilmagnesio (0,48 ml, 1,44 mmol) a una solución del Ejemplo 1 (0,24 g, 0,61 mmol) en Et2O (5 ml) a -78 °C. La reacción se agitó a t.a. durante 18 h. La mezcla de reacción se trató con una solución ac. sat. de bicarbonato sódico y se repartió con EtOAc, los materiales orgánicos se extrajeron y se secaron sobre sulfato de magnesio y se concentraron al vacío. El residuo se purificó por HPLC preparativa, produciendo el compuesto del título en forma de un sólido de color blanco (9 mg, 3,6 %). RMN 1H (DMSO-d6) 88,00 (dd, Ji 1,9 Hz, J2 0,7 Hz, 1H), 7,57 (m, 1H), 7,31 (m, 4H), 7,15 (td, Ji 7,6 Hz, J2 1,4 Hz, 1H), 6,92 (dd, Ji 7,7 Hz, J2 1,6 Hz, 1H), 5,29 (s, 1H), 4,76 (dd, Ji 8,5 Hz, J2 4,4 Hz, 1H), 3,11 (dd, Ji 13,3 Hz, J2 8,5 Hz, 1H), 2,33 (dd, Ji 13,4 Hz, J2 4,5 Hz, 1H), 1,53 (s, 3H). CLEM (EN+) TR 1,42 min, 409,0/411,0 (M+H)+.
E j e m p l o 9
7-Bromo-1-(2-d¡fluorometox¡-fen¡l)-6-fluoro-1.2-d¡h¡dro-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ona
Una solución del Intermedio i2 (8,6 g, 17,7 mmol) en DMSO (200 ml) y agua (20 ml) se agitó a 100 °C durante 48 h. La mezcla de reacción se enfrió y se vertió sobre agua helada. El precipitado se retiró por filtración y se secó al vacío
para producir el compuesto del título en forma de un sólido de color crema (6,2 g, 76 %). 8h (CDCI3, 300 MHz) 7,83 (d, J 6,4 Hz, 1H), 7,44 (d, J 8,6 Hz, 1H), 7,41 - 7,31 (m, 1H), 7,29 - 7,23 (m, 1H), 7,18 (t, J 7,5 Hz, 1H), 6,86 (dd, J 7,7, 1,3 Hz, 1H), 6,65 (t, J 73,1 Hz, 1H), 5,12 (dd, J 7,0, 2,2 Hz, 1H), 3,64 (dd, J 18,4, 7,0 Hz, 1H), 2,92 (dd, J 18,4, 2,3 Hz, 1H). CLEM (EN+) TR 2,89 min, 411,0/413,0 (M+H)+.
E j e m p l o 10
(1S.3S)-7-bromo-1-[2-(d¡fluorometox¡)fen¡l1-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡din-3-ol
El compuesto del título se preparó a partir del Ejemplo 3 (2 g, 5,086 mmol, 1 equiv.) y tri-sec-butilborohidruro de litio por el Método B (1,68 g, 83 %). RMN 1H (400 MHz, CDCla) 87,72 (s, 1H), 7,53 (m, J 13,0 Hz, 1H), 7,22 (m, 5H), 6,67 (m, 1H), 5,48 (dd, J 7,3 Hz, J 3,0 Hz, 1H), 4,84 (dd, J 8,5 Hz, J 4,0 Hz, 1H), 3,60 (m, 1H), 2,42 (m, 1H). CLEM (EN+) TR 1,43 min, 395,0/397,0 (M+H)+.
E j e m p l o 11
7-bromo-1-r2-(difluorometoxi)fenil1-2,3-dihidro-1H-ciclopentar4,51imidazoH,2-a1piridin-3-ol
El compuesto del título se preparó a partir del Ejemplo 1(0,05 g, 0,12 mmol) y borohidruro sódico (0,005 g, 0,14 mmol) por el Método C (0,03 g, 64 %). CLEM (EN+) TR 1,43 min, 395,0/397,0 (M+H)+.
E j e m p l o s 12 y 13
(S)-7-Bromo-1-(2-d¡fluorometox¡-fen¡l)-6-fluoro-1.2-d¡h¡dro-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ona; (R)-7-Bromo-1-(2-difluorometoxifenil)-6-fluoro-1,2-dihidro-ciclopentar4,51imidazoH,2-a1piridin-3-ona
Los compuestos del título se aislaron mediante separación quiral del Ejemplo 9 en condiciones de CL en un LUX cell-4 (76 x 265 mm x mm, flujo 200 ml/min, 30 °C, 100 % de MeOH, inyección de 78 ml de solución a una concentración de 25 g/l). El primer enantiómero en eluirse (TR 9 min) se recogió y las fracciones se evaporaron para producir 880 mg del Ejemplo 12. El segundo enantiómero en eluirse (TR 14 min) se recogió y las fracciones se evaporaron para producir 880 mg del Ejemplo 13.
E j e m p l o 14
(1R.3R)-7-Bromo-1-(2-difluorometoxi-fenil)-3-metoxi-2.3-dihidro-1H-ciclopentar4.51imidazor1.2-a1piridina
El Ejemplo 5 (1.33 g. 3.36 mmol) se disolvió en THF (40 ml) en una atmósfera de nitrógeno. Después. la mezcla se enfrió a 0 °C y se añadió NaH (al 60 % en aceite mineral. 296 mg. 7.40 mmol) y la mezcla se agitó durante 20 minutos. Después. se añadió yodometano (0.84 ml. 13.46 mmol) a 0 °C y la mezcla se agitó a t.a. durante 30 minutos. Se añadió más cantidad de yodometano (0.42 ml. 6.73 mmol) a t.a. y la mezcla se agitó durante 30 minutos. La mezcla se diluyó con agua (30 ml) y se extrajo con EtOAc (3 x 50 ml). Las fases orgánicas combinadas se lavaron con salmuera (50 ml). se secaron sobre sulfato sódico y se concentraron al vacío. El residuo se purificó por cromatografía en columna ultrarrápida (SiO2. EtOAc al 20-100 % en heptano) para proporcionar 1.25 g (90 %) del compuesto del título en forma de un sólido de color blanco. RMN 1H (500 MHz. cD cb) 8 ppm 7.79 (s. 1H). 7.63 (d. J 8.9 Hz. 1H). 7.31 (td. J 8.0. 7.2.
2.0 Hz. 2H). 7.24 - 7.11 (m. 3H). 6.69 (dd. J 74.2. 73.1 Hz. 1H). 4.94 (dd. J 7.3. 2.7 Hz. 1H). 4.85 (dd. J 8.7. 3.5 Hz.
1H). 3.67 (s. 3H). 3.57 - 3.46 (m. 1H). 2.41 (dt. J 14.3. 3.1 Hz. 1H). CLEM (EN+) TR 1.90 min. 409.0/411.0 (M+H)+.
E j e m p l o 15
(R)-7-Bromo-1-(2-d¡fluorometox¡-fenil)-3-met¡l-2.3-d¡h¡dro-1H-c¡clo penta[4.51¡m¡dazo[1.2-a1pir¡d¡n-3-ol
A una solución del Ejemplo 2 (500 mg. 1.27 mmol) en tolueno (25 ml) a -78 °C. en una atmósfera de nitrógeno. se introdujo bromuro de metilmagnesio (2.7 ml de una solución 1.4 M en THF/tolueno. 3.8 mmol) durante 5 minutos. Después de 1 h a esta temperatura. la mezcla de reacción se trató de nuevo con bromuro de metilmagnesio (0.7 ml de una solución 1.4 M en THF/tolueno. 1.0 mmol) y se diluyó con THF (10 ml). La mezcla de reacción se calentó a 0 °C durante 1 h. después de lo cual se introdujo gota a gota MeOH (1 ml). Una vez la mezcla de reacción se había calentado a t.a.. esta se concentró a presión reducida y el residuo se suspendió de nuevo en EtOAc (30 ml). La suspensión se lavó con carbonato sódico 2 M (10 ml) y la fase orgánica se secó sobre sulfato sódico. El filtrado se filtró y se concentró para proporcionar 493 mg (79 %) del compuesto del título como una mezcla 78:22 de epímeros en favor del estereoisómero 3r . CLEM (EN+) t R 2.28 min. 409.0/411.0 (M+H)+.
E j e m p l o 16
(1R.3R)-7-Bromo-1-(2-d¡fluorometox¡-fen¡l)-6-fluoro-2.3-d¡h¡dro-1H-c¡clopentar4.51¡m¡dazon.2-a1p¡r¡d¡n-3-ol
El compuesto del título se preparó a partir del Ejemplo 13 (400 mg, 0,97 mmol) y una solución 1 M de tri-secbutilborohidruro de litio en THF (1,4 ml) por el Método B, (97 mg, 24 %). CLEM (EN+) TR 2,52 min, 413,0/415,0 (M+H)+.
E j e m p l o 17
(R)-7-Bromo-1-(2-d¡fluorometox¡-fen¡l)-6-fluoro-2,3-d¡h¡dro-1H-c¡clo pentaf4.51¡m¡dazo[1.2-a1p¡r¡d¡na
El Ejemplo 16 (165 mg, 0,32 mmol) se disolvió en MeCN (8 ml) en una atmósfera de nitrógeno. Después, la mezcla se calentó a 80 °C, se añadió gota a gota yodo(trimetil)silano (0,45 ml, 3,20 mmol) y la mezcla se agitó a 80 °C durante 90 minutos. Se añadió gota a gota más cantidad de yodo(trimetil)silano (0,45 ml, 3,20 mmol) a 80 °C y se agitó durante 90 minutos antes de la adición gota a gota de una porción final de yodo(trimetil)silano (0,45 ml, 3,20 mmol) y se agitó durante 90 minutos. La mezcla se diluyó con agua (5 ml) y se extrajo con DCM (10 ml). La fase orgánica se lavó con agua (5 ml), seguido de una solución sat. de bicarbonato sódico en agua (5 ml), una solución sat. de tiosulfato sódico en agua (5 ml) y salmuera (5 ml), después se secó sobre sulfato sódico y se concentró al vacío. El producto en bruto se purificó por cromatografía en columna ultrarrápida (SiO2, EtOAc al 20-100 % en heptano, después MeOH al 1 100 % en EtOAc) para proporcionar 32 mg (24 %) del compuesto del título en forma de un aceite de color amarillo pálido. CLEM (EN+) TR 1,68 min, 397,0/399,0 (M+H)+.
E j e m p l o 18
(R)-7-Bromo-1-(2-difluorometoxi-fenil)-6-fluoro-3-tnfluorometil-2,3-dihidro-1H-ciclopentar4,51imidazoH,2-a1piridin-3-ol
Se añadió trimetil(trifluorometil)silano (292 pl, 1,94 mmol) a una solución del Ejemplo 13 (200 mg, 0,49 mmol) en DME (2 ml). La mezcla se agitó a t.a. durante 10 minutos, después se añadió fluoruro de cesio (7,4 mg, 0,05 mmol) y la mezcla de reacción se agitó a t.a. durante 36 h. La mezcla de reacción se inactivó con una solución 4 M de HCl ac. (2
ml) y se agitó en un baño de hielo durante 10 minutos antes de calentar a t.a. durante 4 h. La mezcla se diluyó con agua (15 ml) y se extrajo con EtOAc (3 x 20 ml), los extractos orgánicos combinados se lavaron con salmuera (10 ml), se secaron sobre sulfato sódico y se concentraron al vacío. El producto en bruto se purificó por cromatografía en columna ultrarrápida (SiO2, EtOAc al 0-50 % en heptano) para proporcionar 55 mg (22 %) del compuesto del título en forma de una goma de color pardo. CLEM (EN+) TR 1,95 min, 481,0/483,0 (M+H)+.
E j e m p l o 19
(R)-7-Bromo-1-(2-d¡fluorometox¡-fen¡l)-6-fluoro-2,3-d¡h¡dro-1H-c¡clo penta[4.51¡m¡dazo[1.2-a1pir¡d¡n-3-ol
El Ejemplo 13 (800 mg, 1,95 mmol) se disolvió en THF (20 ml) en una atmósfera de nitrógeno. Después, la mezcla se enfrió a -78 °C y se añadió una solución 4 M de borohidruro de litio en THF (0,73 ml). La mezcla de reacción se agitó a -78 °C durante 30 minutos antes de la adición adicional de una solución 4 M de borohidruro de litio en THF (0,73 ml). La mezcla de reacción se agitó a -78 °C durante 30 minutos y después se inactivó con una solución ac. sat. de cloruro de amonio (10 ml). La mezcla resultante se extrajo con EtOAc (3 x 15 ml). Las capas orgánicas combinadas se lavaron con salmuera (30 ml), se secaron sobre sulfato sódico y se concentraron al vacío. El residuo se purificó por cromatografía en columna ultrarrápida (S¡O2 , EtOAc al 50-100 % en heptano, después MeOH al 1-100 % en EtOAc para proporcionar 700 mg (84 %) del compuesto del título (aproximadamente una proporción 2:1 de diaestereoisómeros) en forma de un aceite de cristalización de color naranja pálido. CLEM (EN+) TR 2,49 min, 413,0/415,0 (M+H)+.
E j e m p l o 20
(R)-7-Bromo-1-(2-d¡fluorometox¡-fen¡l)-6-fluoro-3-met¡l-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ol
Una solución del Ejemplo 13 (200 mg, 0,48 mmol) en tolueno (5 ml) se añadió gota a gota a una solución de bromuro de metilmagnesio en THF/tolueno (1,4 M, 1,04 ml, 1,46 mmol) en tolueno (5 ml) a -78 °C. La mezcla de reacción se agitó a -78 °C durante 3 h. Se añadió MeOH (1 ml) a -78 °C y la mezcla de reacción se calentó a t.a. antes de concentrarse al vacío. El residuo de color pardo se suspendió en EtOAc (5 ml) y la mezcla se lavó con una solución ac. 2 M de carbonato sódico (3 x 3 ml). Los lavados ac. se combinaron y se extrajeron con EtOAc (3 x 3 ml). Los extractos orgánicos combinados se secaron sobre sulfato sódico y se concentraron al vacío. El residuo en bruto de color pardo se purificó por cromatografía en columna ultrarrápida (S¡O2, EtOAc al 0-100 % en heptano) para proporcionar 158 mg (51 %) del compuesto del título en forma de un cristal de color naranja. RMN 1H (500 MHz, cD cb) 8 ppm 7,71 (dd, J 48,8, 6,5 Hz, 1H), 7,41 - 7,27 (m, 2H), 7,25 - 7,10 (m, 3H), 6,83 - 6,46 (m, 1H), 4,96 (ddd, J 129,3, 8,2, 4,8 Hz, 1H), 3,29 (ddd, J 29,0, 13,8, 8,3 Hz, 1H), 2,54 (ddd, J 73,0, 13,8, 4,8 Hz, 1H), 1,77 (d, J 4,9 Hz, 3H). CLEM (EN+) TR 2,68 min, 427,0 (M+H)+.
E j e m p l o s 21 a 87
Los siguientes Ejemplos se prepararon por el Método A a partir del precursor dado usando el éster de boronato o ácido borónico adecuado.
(c o n t in u a c ió n )
(c o n t in u a c ió n )
(continuación)
(c o n t in u a c ió n )
(c o n t in u a c ió n )
(c o n t in u a c ió n )
(continuación)
(c o n t in u a c ió n )
(c o n t in u a c ió n )
(c o n t in u a c ió n )
(c o n t in u a c ió n )
(c o n t in u a c ió n )
(c o n t in u a c ió n )
(c o n t in u a c ió n )
(c o n t in u a c ió n )
(continuación)
Ejemplo 88, METODO I
Ácido (1S.5R.8R)-3-{5-[(1S.3S)-1-(2-difluorometoxi-fenil)-3-hidroxi-2.3-dihidro-1H-ciclopenta[4.5limidazo[1.2-alpiridin-7-ill-pirimidin-2-il}-3-aza-biciclo[3.2.1loctano-8-carboxílico
El Ejemplo 24 (140 mg. 0.249 mmol) se disolvió en THF (2 ml). Se añadieron agua (2 ml) y monohidrato de hidróxido de litio (105 mg. 2.47 mmol) y se permitió que la reacción se agitara durante 5 h. Una vez completa. la mezcla de reacción se lavó con EtOAc. Después. la capa ac. se acidificó a pH 4 con AcOH y se extrajo con EtOAc. La fase orgánica combinada se secó. se filtró y se redujo al vacío. La trituración del material en bruto con MeCN dio el compuesto del título (90 mg. 66 %). 5h (300 MHz. DMSO-d6) 12.07 (s a. 1H). 8.53 (s. 2H). 8.00 (m. 1H). 7.66 (dd. J 9.5 Hz. J 0.8 Hz. 1H). 7.51 (dd. J 9.5 Hz. J 1.8 Hz. 1H). 7.37 (t. J 74.1 Hz. 1H). 7.28 (m. 2H). 7.13 (m. 1H). 6.95 (dd. J 7.8 Hz. J 1.5 Hz. 1H). 5.48 (d. J 5.2 Hz. 1H). 5.13 (m. 1H). 4.76 (dd. J 8.3 Hz. J 3.7 Hz. 1H). 4.39 (d. J 12.2 Hz. 2H).
3.45 (m. 1H). 3.00 (d. J 12.3 Hz. 2H). 2.66 (s. 1H). 2.58 (s a. 2H). 2.08 (dt. J 13.8 Hz. J 3.7 Hz. 1H). 1.67 (m. 2H). 1.31 (d. J 8.0 Hz. 2H). CLEM (EN+) TR 1.09 min 548.8 (M+H)+.
Ejemplo 89
É s te r_______te rc -b u tí l ic o ________de j________á c id o ________ 4 - {5 - [1 - (2 -d if lu o ro m e to x i- fe n il) -6 - f lu o ro -3 -h id ro x i-2.3 -d ih id ro -1 H -c ic lo p e n ta [4.5 l im id a z o [1.2 -a lp ir id in -7 - i l l- p ir id in -2 - i l} -p ip e ra z in a -1 -c a rb o x í l ic o
El compuesto del título se preparó a partir del Ejemplo 30 (0,084 g, 0,14 mmol) y borohidruro sódico (0,0059 g, 0,16 mmol) por el Método C, (0,084 g). CLEM (EN+) TR 2,01 min, 596,0 (M+H)+.
E j e m p l o 9 0 ,
MÉTODO J
1-[2-(D¡fluoroiTietox¡)fen¡l1-6-fluoro-7-[6-(p¡peraz¡n-1-¡l)p¡r¡d¡n-3-¡l1-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡iTi¡dazo[1.2-a1p¡r¡d¡n-3-ol
El Ejemplo 89 (0,084 g, 0,14 mmol) se disolvió en HCl (4 mol/l) en 1,4-dioxano (2,00 ml) y se agitó a t.a. durante 1 h.
El precipitado se filtró y se secó al vacío. El sólido se purificó por HPLC preparativa, produciendo el compuesto del título en forma de un sólido de color blanquecino (0,009 g, 10 %). RMN 1H (DMSO-d6) 8: 8,13 (d, J 1,4 Hz, 1H), 7,86 (d, J 7,6 Hz, 1H), 7,58 (m, 2H), 7,28 (m, 3H), 7,14 (td, J 7,6 Hz, J 1,4 Hz, 1H), 6,95 (dd, J 7,7 Hz, J 1,6 Hz, 1H), 6,86 (d, J 9,0 Hz, 1H), 5,48 (d, J 5,3 Hz, 1H), 4,74 (dd, J 8,6 Hz, J 4,0 Hz, 1H), 3,69 (d, J 4,3 Hz, 1H), 3,43 (m, 5H), 2,75 (m, 5H), 2,06 (m, 1H). CLEM (EN+) TR 1,54 min, 496,8 (M+H)+.
E j e m p l o 91
Ácido 1-(5-{1-f2-(d¡fluorometox¡)fen¡l1-3-h¡drox¡-2,3-d¡h¡dro-1 H-ciclopenta[4,51imidazo[1,2-a1pindin-7-il}pirimidin-2-il)-4-metilpiperidin-4-carboxílico
El compuesto del título se preparó a partir del Ejemplo 23 (0,111 g, 0,19 mmol) y monohidrato de hidróxido de litio (0,029 g, 0,39 mmol) por el Método I (0,010 g, 9 %). RMN 1H (DMSO-d6, 400 MHz) 8: 8,53 (m, 2H), 7,99 (s, 1H), 7,65 (m, 1H), 7,51 (m, 1H), 7,31 (m, 3H), 7,13 (m, 1H), 6,95 (dd, J 7,9 Hz, J 1,6 Hz, 1H), 5,48 (m, 1H), 5,12 (m, 1H), 4,76 (dd, J 8,3 Hz, J 3,7 Hz, 1H), 4,23 (m, 2H), 3,43 (m, 1H), 2,27 (m, 2H), 2,08 (m, 1H), 1,98 (m, 2H), 1,28 (m, 2H), 1,12
(s, 3H). CLEM (EN+) TR 1,24 min, 536,8 (M+H)+.
E j e m p l o s 92 y 93
(R)-1-(2-D¡fluorometox¡-fen¡l)-7-[2-(1,1-d¡oxo-t¡omorfol¡n-4-¡l)-p¡r¡m¡d¡n-5-¡l1-1,2-d¡h¡dro-c¡clopenta[4,51¡m¡dazo[1,2-alpiridin-3-ona____________ y____________ (R)-1-(2-D¡fluorometox¡fen¡l)-7[2-(1-oxo-t¡omorfol¡n-4-¡l)-p¡r¡m¡d¡n-5-il1-1,2-d¡h¡droc¡clopentaf4.51¡m¡dazof1.2-a1p¡r¡d¡n-3-ona
El Ejemplo 29 (2,05 mmol, 1,01 g) se diluyó con MeOH (20 ml) y se enfrió a 0 °C. Se añadió Oxona® (3,04 mmol, 1,87 g) en agua (15 ml) y se permitió que la reacción se calentara a t.a. durante 12 h. En este punto, la mezcla de reacción contenía aproximadamente un 25 % de sulfóxido de y 75 % de sulfona. El disolvente se retiró al vacío y se añadió EtOAc. El sólido resultante se retiró por filtración antes de la purificación por cromatografía en columna ultrarrápida (S¡O2, EtOH al 0-20 % en DCM), produciendo ambos ccompuestos del título. Ejemplo 92 (560 mg, 52 %): 5h (300 MHz, DMSO-d6) 8,71 (s, 2H); 8,25 (m, 1H); 7,85 (dd, J 9,7 Hz, J 1,0 Hz, 1H); 7,79 (dd, J 9,7 Hz, J 1,8 Hz, 1H); 7,37 (m, 1H); 7,28 (t, J 73,9 Hz, 1H); 7,27 (m, 1H); 7,14 (td, J 7,5 Hz, J 1,1 Hz, 1H); 6,88 (d, J 7,4 Hz, 1H); 5,17 (dd, J 6,9 Hz, J 1,8 Hz, 1H); 4,24 (m, 4H); 3,63 (dd, J 18,2 Hz, J 7,1 Hz, 1H); 3,17 (m, 4H); 2,77 (dd, J 18,1 Hz, J 2,1 Hz, 1H). CLEM (EN+) TR 1,84 min 526,6 (M+H)+. Ejemplo 93 (150 mg, 15 %): 5h (300 MHz, DMSO-d6) 8,68 (s, 2H); 8,23 (m, 1H); 7,84 (dd, J 9,7 Hz, J 1,0 Hz, 1H); 7,78 (dd, J 9,7 Hz, J 1,8 Hz, 1H); 7,37 (m, 1H); 7,28 (t, J 73,9 Hz, 1H); 7,27 (m, 1H); 7,14 (td, J 7,5 Hz, J 1,1 Hz, 1H); 6,88 (m, 1H); 5,16 (dd, J 6,8 Hz, J 1,8 Hz, 1H); 4,49 (m, 2H); 3,95 (m, 2H); 3,63 (dd, J 18,2 Hz, J 7,2 Hz, 1H); 2,88 (m, 2H); 2,76 (m, 3H). CLEM (EN+) TR 1,64 min 510,6 (M+H)+.
E j e m p l o 94
Ácido_______ (1R,5S,8R)-3-{5-[(1R,1R)-1-(2-d¡fluorometox¡-fen¡l)-3-h¡drox¡-2,3-d¡h¡dro-1H-c¡clopenta[4,51¡midazo[1,2-a1p¡r¡d¡n-7-¡l1-p¡r¡mid¡n-2-¡l}-3-aza-b¡c¡clo[3.2.11octano-8-carboxíl¡co
El compuesto del título se preparó a partir del Ejemplo 25 (178 mg, 0,32 mmol) y monohidrato de hidróxido de litio (53 mg, 1,26 mmol) por el Método I (87 mg, 50 %). 5h (300 MHz, DMSO-d6) 12,07-12,23 (m, 1 H), 8,47 (s, 2H), 7,92 7,95 (m, 1H), 7,59 (dd, J 9,5, 0,8 Hz, 1H), 7,45 (dd, J 9,5, 1,8 Hz, 1H), 7,30 (t, J 74,1 Hz, 1H), 7,23 (dd, J 6,8, 1,6 Hz, 1H), 7,17-7,21 (m, 1H), 7,06 (td, J 7,8, 1,7 Hz, 1H), 6,88 (dd, J 7,8, 1,5 Hz, 1H), 5,41 (d, J 5,2 Hz, 1H), 5,02-5,09 (m, 1H), 4,69 (dd, J 8,4, 3,8 Hz, 1H), 4,29-4,38 (m, 2H), 3,32-3,44 (m, 1H), 2,88-2,97 (m, 2H), 2,58 (s, 1H), 2,48-2,54 (m, 2H), 2,02 (dt, J 13,7, 3,7 Hz, 1H), 1,55-1,67 (m, 2H), 1,24-1,35 (m, 2H). CLEM (EN+) TR 1,08 minutos, 548 (M+H)+.
E j e m p l o 95
(1R.3S)-1-(2-D¡fluorometox¡-fen¡l)-7-(6-metanosulfon¡l-p¡r¡d¡n-3-¡l)-3-met¡l-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡ridin-3-ol
El compuesto del título se obtuvo mediante purificación por cromatografía en columna (EtOAc al 50-100 % en heptano, seguido de MeOH al 0-50 % en DCM) y por HPLC preparativa (método ácido) de la mezcla en bruto obtenida para el Ejemplo 65 (las fracciones combinadas se neutralizaron a pH ~7 con una solución ac. sat. de bicarbonato sódico antes de concentración, se disolvieron en agua (12 ml) y se extrajeron con EtOAc (25 ml)) para proporcionar 16,1 mg (4 %) del compuesto del título en forma de un sólido de color beige. RMN 1H (500 MHz, cDCb) 8 ppm 8,75 (d, J 1,7 Hz, 1H), 8,14 (d, J 8,1 Hz, 1H), 8,00 (dd, J 8,1, 2,2 Hz, 1H), 7,91 (d, J 9,4 Hz, 1H), 7,75 (s, 1H), 7,52 (dd, J 9,4, 1,7 Hz, 1H), 7,36 - 7,28 (m, 1H), 7,24 (d, J 8,4 Hz, 1H), 7,15 (td, J 7,6, 1,0 Hz, 1H), 6,92 (dd, J 7,7, 1,5 Hz, 1H), 6,81 - 6,46 (m, 1H), 5,24 (dd, J 7,9, 5,8 Hz, 1H), 3,37 (dd, J 13,8, 8,0 Hz, 1H), 3,25 (s, 3H), 2,56 (dd, J 13,8, 5,8 Hz, 1H), 1,87 (s, 3H), 1,25 (s, 1H). CLEM (EN+) TR 1,97 min 486,0 (M+H)+.
E j e m p l o 96
(1R,3R,5S,6r)-3-(5-((1R,3R)-1-r2-(Difluorometoxi)fenil1-3-hidroxi-2,3-dihidro-1H-ciclopentar4,51imidazor1,2-a1piridin-7-il}pirimidin-2-il)biciclor3.1.01hexano-6-carboxilato de etilo
El Ejemplo 31 (37 mg, 68 pmol) se disolvió en EtOAc (5 ml) y se añadieron paladio sobre carbono (10 %, 7,5 mg, 10 mol%) y TEA (10 pl, 68 pmol). La suspensión se desgasificó usando vacío/nitrógeno/hidrógeno y la reacción se agitó en una atmósfera de hidrógeno a temperatura ambiente y a presión durante 48 h con 4 retratamientos (la mezcla de reacción se filtró y/o la adición de más catalizador de paladio y TEA). La mezcla de reacción se filtró a través de celite y se concentró al vacío. El residuo en bruto se purificó por HPLC preparativa (Método D) para proporcionar 5,7 mg (13 %) del compuesto del título en forma de un aceite de color pardo. RMN 1H (500 MHz, CDCb) 8 ppm 8,75 (s, 2H), 7,99 - 7,78 (m, 2H), 7,59 - 7,47 (m, 1H), 7,36 - 7,29 (m, 1H), 7,22 (dt, J 21,9, 7,6 Hz, 2H), 7,09 - 6,87 (m, 1H), 6,71 (dd, J 74,6, 72,7 Hz, 1H), 5,53 (dd, J 7,3, 3,2 Hz, 1H), 4,96 (dd, J 8,5, 4,0 Hz, 1H), 4,09 (c, J 7,1 Hz, 2H), 3,80 (ddd, J 13,3, 9,5, 3,7 Hz, 1H), 3,66 (dt, J 14,2, 8,2 Hz, 1H), 3,53 (d, J 21,3 Hz, 1H), 2,94 (s, 1H), 2,61 - 2,47 (m, 4H), 2,02 (d, J 8,6 Hz, 2H), 1,55 (t, J 2,9 Hz, 1H), 1,24 (t, J 7,1 Hz, 3H). CLEM (EN+) TR 1,49 min, 547,0 (M+H)+.
E j e m p l o 97
(1R,3R)-6-Fluoro-7-(4-r(metilsulfonil)metil1fenil}-1-fenil-2,3-dihidro-1H-ciclopentar4,51imidazoH,2-a1piridin-3-ol
El compuesto del título se preparó a partir del Ejemplo 42 (1 equiv., 0,800 mmol) y tri-sec-butil borohidruro de litio (1 M en THF, 1,2 mmol, 1,5 equiv.). Por el Método B (30 mg, 9 %). RMN 1H (400 MHz, CDCla) 87,50 (d, J 7,3 Hz, 1H), 7,45 (d, J 7,8 Hz, 1H), 7,44 (s, 1H), 7,36-7,39 (m, 3H), 7,28-7,34 (m, 5H), 5,45 (m, 1H), 4,42 (m, 1H), 4,27 (s, 2H), 3,59 (m, 1H), 2,81 (s, 3H), 2,47 (m, 1H). CLEM (EN+) TR 1,25 min, 437,0 (M+H)+.
E j e m p l o 98
(1S,3S)-1-(2-Difluorometoxi-fenil)-6-fluoro-7-(4-metanosulfonil-fenil)-2,3-dihidro-1H-ciclopentar4,51imidazoH,2-alpiridin-3-ol
El compuesto del título se preparó a partir del Ejemplo 38 (67 mg, 0,14 mmol) y tri-sec-butilborohidruro de litio (1,0 M en THF, 0,2 ml, 0,2 mmol) por el Método B (36 mg, 54 %). 8h (300 MHz, DMSO-d6) 8,06 (d, J 7,5 Hz, 1H), 8,00 (m, 2H), 7,74 (dd, J 8,6 Hz, J 1,7 Hz, 2H), 7,67 (d, J 11,9 Hz, 1H), 7,33 (t, J 73,9 Hz, 1H), 7,30 (m, 1H), 7,23 (m, 1H), 7,12 (td, J 7,6, J 1,5 Hz, 1H), 6,92 (dd, J 7,7 Hz, J 1,6 Hz, 1H), 5,51 (s a, 1H), 5,12 (m, 1H), 4,76 (dd, J 8,5 Hz, J 3,8 Hz, 1H), 3,45 (m, 1H), 3,24 (s, 3H), 2,06 (dt, J 13,6 Hz, J 3,5 Hz, 1H). CLEM (EN+) TR 1,94 min 489,6 (M+H)+.
E j e m p l o 99
Ácido (1S,5R,8R)-3-{5-[(R)-1-(2-difluorometoxi-fenil)-3-oxo-2,3-dihidro-1H-ciclopenta[4,51imidazo[1,2-a1piridin-7-il1-pirimidin-2-il}-3-aza-biciclo[3.2.11octano-8-carboxílico
El compuesto del título se preparó a partir del Ejemplo 40 (191 mg, 0,34 mmol) y monohidrato de hidróxido de litio (74 mg, 1,81 mmol) por el Método I (92 mg, 49 %). 8h (300 MHz, DMSO-d6) 12,13-12,32 (m, 1H), 8,58 (s, 2H), 8,20 (t, J 1,1 Hz, 1H), 7,83 (dd, J 9,6, 0,9 Hz, 1H), 7,76 (dd, J 9,7, 1,7 Hz, 1H), 7,33-7,41 (m, 1H), 7,24-7,30 (m, 1H), 7,28 (t, J 73,9 Hz, 1H), 7,14 (td, J 7,6, 1,1 Hz, 1H), 6,85-6,92 (m, 1H), 5,13-5,19 (m, 1H), 4,38-4,46 (m, 2H), 3,57-3,67 (m, 1H), 3,01 (d, 2H, J 12,2 Hz), 2,72-2,81 (m, 1H), 2,67 (s, 1H), 2,56-2,62 (m, 2H), 1,63-1,74 (m, 2H), 1,31-1,41 (m, 2H). CLEM (EN+) TR 1,31 min, 546 (M+H)+.
Ejemplo 100
Dimetilamida________de]________ácido________(1S.5R.8R)-3-(5-r(R)-1-(2-difluorometoxi-fenil)-3-oxo-2.3-dihidro-1H-c¡clopentar4.51¡m¡dazori.2-a1p¡r¡d¡n-7-¡l1-p¡r¡m¡d¡n-2-¡l)-3-aza-b¡ciclor3.2.11octano-8-carboxíl¡co
A una solución del Ejemplo 99 (33 mg. 0.06 mmol) en THF (5 ml) se añadió DIPEA (0.06 ml. 0.3 mmol). hidrato de 1-hidroxibenzotriazol (21 mg. 0.14 mmol). clorhidrato de 1-(3-dimetilaminopropil)-3-etilcarboiimida (23 mg. 0.12 mmol) y dimetilamina (0.06 ml. 0.1 mmol) y mezcla de reacción se agitó a t.a. durante 18 h. La mezcla de reacción se concentró al vacío. El residuo se disolvió en agua (25 ml) y se extrajo con EtOAc (3 x 25 ml). Los extractos orgánicos combinados se secaron sobre sulfato sódico. se filtraron y se concentraron al vacío. El residuo se purificó por cromatografía en columna ultrarrápida (SiO2. MeOH al 0-20 % en EtOAc) y el material se criodesecó en MeCN/agua para dar el compuesto del título (25 mg. 72 %) en forma de un sólido de color beige. 6h (300 MHz. DMSO-d6) 8.59 (s. 2H). 8.20 8.22 (m. 1H). 7.83 (dd. J 9.7. 1.1 Hz. 1H). 7.76 (dd. J 9.7. 1.8 Hz. 1H). 7.34-7.41 (m. 1H). 7.24-7.30 (m. 1H). 7.28 (t. J 73.9 Hz. 1H). 7.14 (td. J 7.5. 1.1 Hz. 1H). 6.85-6.92 (m. 1H). 5.13-5.18 (m. 1H). 4.36-4.44 (m. 2H). 3.57-3.68 (m. 1H).
3.11 (s. 1H). 3.08 (s. 3H). 2.94 (s. 1H). 2.81 (s. 3H). 2.71-2.81 (m. 2H). 2.41-2.49 (m. 2H). 1.76-1.84 (m. 2H). 1.29-1.38 (m. 2H). CLEM (EN+) TR 2.10 min. 573 (M+H)+.
E j e m p l o 101
Ácido_____(1S.5R.8R)-3-(5-r(R)-1-(2-difluorometoxi-fenil)-3-hidroxi-3-metil-2.3-dihidro-1H-ciclopentar4.51imidazoH.2-a1piridin-7-il1-pirimidin-2-il}-3-aza-biciclo[3.2.11octano-8-carboxílico
El compuesto del título se preparó a partir del Ejemplo 26 (54 mg. 0.09 mmol) y monohidrato de hidróxido de litio (19 mg. 0.45 mmol) por el Método I (28 mg. 53 %). El material es una mezcla 79:21 de los dos diaestereoisómeros. asignación dada para el diastereoisómero principal; 6h (300 MHz. DMSO-d6) 12.04-12.24 (m. 1H). 8.46 (s. 2H). 7.88 7.92 (m. 1H). 7.58 (dd. J 9.4. 0.9 Hz. 1H). 7.44 (dd. J 9.4. 1.8 Hz. 1H). 7.29 (t. J 74.1 Hz. 1H). 7.21-7.25 (m. 1H). 7.17 7.21 (m. 1H). 7.03-7.10 (m. 1H). 6.91 (dd. J 7.7. 1.5 Hz. 1H). 5.19 (s. 1H). 4.69-4.75 (m. 1H). 4.29-4.38 (m. 2H). 3.01 3.12 (m. 1H). 2.89-2.96 (m. 2H). 2.58 (s. 1H). 2.48-2.54 (m. 2H). 2.30 (dd. J 13.5. 4.4 Hz. 1H). 1.56-1.65 (m. 2H). 1.48 (s. 3H). 1.24-1.33 (m. 2H). CLEM (EN+) TR 1.52 min. 562 (M+H)+.
E j e m p l o 102
(1 S .3 S ) -6 -F lu o ro -3 -m e to x i-7 -(4 -H -(m e t ils u lfo n il)e t i l1 fe n il} -1 - fe n il-2.3 -d ih id ro -1 H -c ic lo p e n ta r4.51 im id a z o r1.2 -a 1 p ir id in a
El Ejemplo 74 (19,5 mg, 0,0447 mmol, 1,0 equiv.) se disolvió en THF (1 ml) y se enfrio a 0 °C. Se anadio en una porción hidróxido sódico (0,00214 g, 0,0536 mmol, 1,2 equiv.). Después de 30 minutos, con agitación a 0 °C, se añadió yodometano (0,00641 g, 0,0447 mmol, 1 equiv.). Después de 1 h, se añadió un segundo equivalente de yodometano y la temperatura se elevó a t.a. durante una noche. Los disolventes se evaporaron y el residuo se purificó por HPLC prep., produciendo el compuesto del título en forma de un sólido de color blanquecino (8 mg, 38 %). CLEM (EN+) TR 1,42 min, 465,0 (M+H)+.
E j e m p l o 103
(1S,3S)-6-Fluoro-7-r2-(morfolin-4-il)pirimidin-5-il1-1-fenil-2,3-dihidro-1H-ciclopentar4,51imidazor1,2-a1piridin-3-ol
El compuesto del título se preparó a partir del Ejemplo 82 (344 mg, 1,0 equiv.) y tri-sec-butilborohidruro de litio (1,5equiv.) por el Método B (130 mg, 38 %). CLEM (EN+) TR 3,32 min, 432 (M+H)+.
E j e m p l o 104
(1S,3S)-6-Fluoro-3-metoxi-7r2-(morfolin-4-il)pirimidin-5-il1-1-fenil-2,3-dihidro-1H-ciclopentar4,51imidazor1,2-a1piridina
El Ejemplo 103 (46,3 mg, 1,0 equiv.) se disolvió en THF (9,3 ml/mmol). A 0 °C, se añadió NaH (al 60 % en aceite mineral, 1,2equiv.) y la mezcla de reacción se agitó durante 10 minutos a 0 °C. Se añadió yodometano (1,2 equiv.) y la mezcla se calentó a 60 °C durante 16 h. La reacción se interrumpió con cloruro de amonio (solución sat.), se extrajo con EtOAc, se secó sobre sulfato de magnesio y se concentró al vacío. El residuo se purificó por cromatografía en columna ultrarrápida (S¡O2, MeOH 0 % en DCM), seguido de cromatografía inversa preparativa dirigida por EM, produciendo el compuesto del título en forma de un sólido de color blanco (3 mg, 6 %). CLEM (EN+) TR 1,45 min, 446,0 (M+H)+.
E j e m p l o 105
(1 R ,3 R ) -6 -F lu o ro -7 - r2 -(m o r fo lin -4 - il)p ir im id in -5 - il1 -1 - fe n il-2 ,3 -d ih id ro -1 H -c ic lo p e n ta r4 ,51 im id a z o H ,2 -a 1 p ir id in -3 -o l
El compuesto del título se preparó a partir del Ejemplo 83 (230 mg, 1,0 equiv.) y tri-sec-butilborohidruro de litio (1,5equiv.) por el Método B (105 mg, 46 %). CLEM (EN+) TR 3,33 min, 432 (M+H)+.
E j e m p l o 106
(1R.3R)-6-Fluoro-3-metox¡-7-f2-(morfol¡n-4-¡l)p¡r¡m¡d¡n-5-¡l1-1-fen¡l-2.3-d¡h¡dro-1H-c¡clopentaf4.51¡m¡dazo[1.2-a1p¡r¡d¡na
El compuesto del título se preparó a partir del Ejemplo 105 (95 mg, 1,2 equiv.), NaH (al 60 % en aceite mineral, 1,3equiv.), yodometano (1,3 equiv.) en THF (9,1 ml/mmol) por el método descrito en el Ejemplo 103. El residuo se purificó por cromatografía en columna ultrarrápida (S¡O2, MeOH al 0-4 % en DCM), produciendo el compuesto del título en forma de un sólido de color amarillo (42 mg, 43 %). CLEM (EN+) TR 1,45 min, 446,0 (M+H)+.
E j e m p l o 107
(1R.3R)-7-Bromo-1-[2-(d¡fluorometox¡)fen¡l1-3-[3-(met¡lsulfon¡l)fenox¡1-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-alpiridina
El Intermedio 72 (100 mg, 1,0 equiv.) y 3-metanosulfonil-fenol (1,0 equiv.) se disolvieron en THF (4 ml/mmol). A 0 °C, se añadió resina de trifenilfosfina (1,1 equiv., 1,88 mmol/g), seguido de una solución de DIAD (1,4 equiv.) en THF (0,5 ml). La mezcla de reacción se agitó a t.a. durante 16 h, se inactivó con bicarbonato sódico (solución sat., 1 ml) y se concentró al vacío. El residuo se recogió con EtOAc, se secó sobre sulfato de magnesio y se evaporó. El residuo se purificó por cromatografía en columna ultrarrápida (SO 2, MeOH al 1- 5 % en DCM), seguido de cromatografía inversa preparativa dirigida por UV (Gradiente básico 50-80), produciendo el compuesto del título en forma de un sólido de color blanquecino (33 mg, 24 %). CLEM (EN+) TR 1,59 min, 550,0 (M+H)+.
E j e m p l o 108
(1R.3R)-1-[2-(D¡fluorometox¡)fen¡l1-3-[3-(met¡lsulfon¡l)fenox¡1-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-7-carbonitrilo
El Ejemplo 107 (56 mg, 1,0 equiv.) se disolvió en DMF (19,6 ml/mmol) y la solución se desgasificó con argón. Se añadieron cianuro de cinc (1,1 equiv.) y tetraquis(trifenilfosfina)paladio (0) (0,3 equiv.) y la mezcla de reacción se calentó a 120 °C durante 3 h. La mezcla se filtró sobre celite, se recogió con Et2O, se lavó con salmuera, se secó sobre sulfato de magnesio y se concentró al vacío. El residuo se purificó por cromatografía preparativa de fase inversa dirigida por EM, produciendo el compuesto del título en forma de un cristal sólido de color blanco (10 mg, 18 %). CLEM (EN+) TR 1,51 min, 496,0 (M+H)+.
E j e m p l o 109
(S)-1-(2-Clorofen¡l)-6-fluoro-7-[2-(2-h¡drox¡propan-2-¡l)p¡r¡m¡d¡n-5-¡l1-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1,2-alpiridin-3-ol
El compuesto del título se preparó a partir del Ejemplo 75 (50 mg, 0,114 mmol, 1 equiv.) y borohidruro sódico (4,3 mg, 0,114 mmol 1 equiv.) por el Método C (32 mg, 21 %). CLEM (EN+) TR 1,32 min, 439,0 (M+H)+.
E j e m p l o 110
(R)-1-(2-Clorofen¡l)-6-fluoro-7-[2-(2-h¡drox¡propan-2-¡l)p¡r¡m¡d¡n-5-¡l1-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1pirid¡n-3-ol
El compuesto del título se preparó a partir del Ejemplo 76 (50 mg, 0,114 mmol, 1 equiv.) y borohidruro sódico (4,3 mg, 0,114 mmol 1 equiv.) por el Método C (11 mg, 10 %). CLEM (EN+) TR 1,32 min, 439,0 (M+H)+.
E j e m p l o 111
(1R.3R)-6-Fluoro-7-r2-(2-h¡drox¡propan-2-¡l)p¡r¡m¡d¡n-5-¡l1-1-r2-(tr¡fluorometox¡)fen¡l1-2.3-d¡h¡dro-1H-c¡clopenta[4,51¡iTi¡dazo[1.2-a1p¡r¡d¡n-3-ol
El co m p u e s to d e l títu lo s e preparó a part¡r del E je m p lo 81 (95,3 mg. 1.0 equ¡v.), MeOH (10.2 ml/mmol) y boroh¡druro sód¡co (1.0 equ¡v.) por el M étod o C. El res¡duo s e prec¡p¡tó en MeOH. s e f¡ltró y s e s e c ó a pres¡ón reduc¡da. El co m p u e s to d e l títu lo s e a¡sló med¡ante pur¡f¡cac¡ón qu¡ral en cond¡c¡ones de S F C en un Ch¡ralpak IA (50 x 266 mm x mm. flujo 360 ml/m¡n. 25 °C. C O 2 + 20 % de MeOH. ¡nyecc¡ón de 5.33 ml de soluc¡ón a una concentrac¡ón de 30 g/l). El pr¡mer enant¡ómero en elu¡rse (TR 6.7 m¡n) s e recog¡ó y las fracc¡ones s e evaporaron para produc¡r el co m p u e s to d e l títu lo en forma de un sól¡do de color blanco (9.2 mg. 10 %). CLEM (EN+) TR 1.38 m¡n. 489.0 (M+H)+.
E j e m p l o 112
(1R.3S)-6-Fluoro-7-r2-(2-h¡drox¡propan-2-¡l)p¡r¡m¡d¡n-5-¡l1-1-r2-(tr¡fluorometox¡)fen¡l1-2.3-d¡h¡dro-1H-c¡clopentar4.51¡m¡dazon.2-a1p¡r¡d¡n-3-ol
S e recog¡ó el seg u n d o enant¡ómero en elu¡rse (TR 9.5 m¡n) de la pur¡f¡cac¡ón descr¡ta en el E je m p lo 111 y las fracc¡ones se evaporaron para produc¡r el co m p u e s to d e l títu lo en forma de un sól¡do de color blanco (12 mg. 12 %). CLEM (EN+) T R 1.38 m¡n. 489.0 (M+H)+.
E j e m p l o 113
(1R.3R)-1-(2-D¡fluorometox¡-fen¡l)-7-r2-(1-oxo-t¡omorfol¡n-4-¡l)-p¡r¡m¡d¡n-5-¡l1-2.3-d¡h¡dro-1H-c¡clopentar4.51¡m¡dazon.2-a1p¡r¡d¡n-3-ol
El co m p u e s to de l títu lo s e preparó a part¡r del E je m p lo 93 (0.24 mmol. 120 mg) y tr¡-sec-but¡lboroh¡druro de l¡t¡o (1.0 M en THF. 0.4 mmol. 0.4 ml) por el M étod o B (76 mg. 62 %). 5 h (300 MHz. DMSO-d6) 8.63 (s. 2H); 8.03 (m. 1H); 7.68 (dd. J 9.5 Hz. J 0.9Hz. 1H); 7.54 (dd. J 9.5 Hz. J 1.8 Hz. 1H); 7.37 (t. J 74.1 Hz. 1H); 7.29 (m. 2H); 7.13 (m. 1H); 6.94
(dd, J 8,0 Hz, J 1,5 Hz, 1H); 5,48 (d, J 5,2 Hz, 1H); 5,13 (m, 1H); 4,77 (m, 1H); 4,48 (m, 2H); 3,95 (m, 2H); 3,45 (m, 1H); 2,88 (m, 2H); 2,73 (m, 2H); 2,08 (m, 1H). CLEM (EN+) TR 1,64 min 512,8 (M+H)+.
E j e m p l o 114
(1R,3R)-1-(2-D¡fluorometox¡-fen¡l)-7-[2-(1,1-d¡oxo-t¡omorfol¡n-4-¡l)-p¡r¡m¡d¡n-5-¡l1-2,3-d¡h¡dro-1H-c¡clopenta[4,51¡m¡dazo[1,2-a1p¡r¡d¡n-3-ol
El co m p u e s to de l títu lo se preparó a part¡r del E je m p lo 92 (0,95 mmol, 500 mg) y tr¡-sec-but¡lboroh¡druro de l¡t¡o (1,0 M en THF, 1,0 mmol, 1,0 ml) por el M étod o B (365 mg, 73 %). 5h (300 MHz, DMSO-d6) 8,66 (s, 2H); 8,04 (dd, J 1,4 Hz, J 0,9 Hz, 1H); 7,69 (dd, J 9,5 Hz, J 0,8 Hz, 1H); 7,55 (dd, J 9,5 Hz, J 1, 8 Hz, 1H); 7,37 (t, J 74,1 Hz, 1H); 7,29 (m, 2H); 7,13 (m, 1H); 6,94 (m, 1H); 5,48 (d, J 5,2 Hz, 1H); 5,13 (m, 1H); 4,77 (dd, J 8,5 Hz, J 3,8 Hz, 1H); 4,23 (m, 4H); 3,45 (m, 1H); 3,16 (m, 4H); 2,08 (dt, J 13,4Hz, J 3,5 Hz, 1H). CLEM (EN+) TR 1,80 m¡n 528,6 (M+H)+.
E j e m p l o 115
(R)-1-(2-D¡fluorometox¡-fen¡l)-6-fluoro-7-r2-(1-h¡drox¡-1-met¡l-et¡l)-1.6-d¡h¡dro-p¡r¡m¡d¡n-5-¡l1-1,2-d¡h¡droc¡clopentar4.51¡m¡dazoH.2-a1p¡r¡d¡n-3-ona
El E je m p lo 85 (0,32 mmol, 150 mg) se d¡solv¡ó en THF (10 ml). Se añad¡eron acetato de amon¡o (0,38 mmol, 30 mg), AcOH (0,35 mmol, 20 pl) y tr¡acetox¡boroh¡druro sód¡co (0,45 mmol, 100 mg) y la reacc¡ón se ag¡tó a t.a. durante 12 h. La reacc¡ón se ¡nterrump¡ó con h¡dróx¡do sód¡co y se extrajo con más cant¡dad de EtOAc. La fase orgán¡ca comb¡nada se secó sobre sulfato sód¡co, se f¡ltró y se concentró al vacío antes de la pur¡f¡cac¡ón por HPLC preparat¡va, produc¡endo el co m p u e s to d e l títu lo (40 mg, 27 %). 5h (400 MHz, DMSO-d6) 7,62 (d, J 13,2 Hz, 1H); 7,57 (d, J 7,7 Hz, 1H); 7,39 (d, J 8,4 Hz, J 1,6 Hz, 1H); 7,28 (m, 1H); 7,27 (t, J 73,9 Hz, 1H); 7,17 (td, J 7,6 Hz, J 1,1 Hz, 1H); 6,94 (m, 1H); 6,76 (s, 1H); 5,13 (dd, J 6,9 Hz, J 2,0 Hz, 1H); 4,16 (m, 1H); 3,99 (m, 1H); 3,58 (dd, J 18,2 Hz, J 7,0 Hz, 1H); 2,77 (dd, J 18,2 Hz, J 2,0 Hz, 1H); 1,26 (s, 6H). CLEM (EN+) TR 1,54 m¡n 471,6 (M+H)+.
E j e m p l o 116
(1R,3S)-1-(2-D¡fluorometox¡-fen¡l)-6-fluoro-7-(4-metanosulfon¡l-fen¡l)-2,3-d¡h¡dro-1H-c¡clopentar4,51¡m¡dazoH,2-a1p¡r¡d¡n-3-¡lam¡na
El E je m p lo 46 (0,20 mmol, 100 mg) se disolvió en THF (10 ml) y se enfrió a 0 °C. Se añadieron difenilfosforMazida (0,27 mmol, 60 |jl) y 1,8-diazabicido[5.4.0]undec-7-eno (0,27 mmol, 40 |jl) y la reacción se agitó durante 12 h. Después, el disolvente se retiró al vacío antes de la purificación por cromatografía en columna ultrarrápida (SiO2 , EtOAc al 40-80 % en hexanos), produciendo la (1R,3S)-3-azido-1-(2-difluorometoxi-fenil)-6-fluoro-7-(4-metanosulfonilfenil)-2,3-dihidro-1H-ciclopenta[4,5]imidazo[1,2-a]piridina (45 mg, 43 %). Esto se disolvió en THF (5 ml) y se añadió resina de trifenilfosfina (0,23 mmol, 150 mg). La reacción se calentó a 60 °C durante 12 h antes de la filtración de la resina. La concentración del disolvente al vacío dio el co m p u e s to d e l títu lo (26 mg, 27 % en dos etapas). 8h (300 MHz, DMSO-d6) 8,12 (d, J 7,6 Hz, 1H); 8,00 (d, J 8,5 Hz, 2H); 7,74 (dd, J 8,5 Hz, J 1,7 Hz, 2H); 7,64 (d, J 12,0 Hz, 1H); 7,30 (t, J 74,1 Hz, 1H); 7,29 (m, 1H); 7,22 (m, 1H); 7,07 (td, J 7,5 Hz, J 1,3 Hz, 1H); 6,64 (dd, J 7,7 Hz, J 1,5 Hz, 1H); 4,98 (dd, J 8,1 Hz, J 3,5 Hz, 1H); 4,40 (m, 1H); 3,24 (s, 3H); 2,72 (m, 1H); 2,59 (m, 1H). CLEM (EN+) TR 1,66 min 488,6 (M+H)+.
E j e m p l o 117
Ácido (8-anti)-3-(5-((1R,3R)-1-[2-(difluorometoxi)fenil1-3-metoxi-2,3-dihidro-1H-ciclopenta[4,51imidazo[1,2-a1piridin-7-il}pirimidin-2-il)-3-azabiciclo[3.2.11octano-8-carboxílico
El c o m p u e s to de l títu lo se preparó a partir del E je m p lo 86 (106 mg, 0,18 mmol) y monohidrato de hidróxido de litio (31 mg, 0,73 mmol) por el M étod o I (55 mg, 53 %). 5h (400 MHz, DMSO-d6) 12,00-12,26 (m, 1H), 8,55 (s, 2H), 8,08 8,10 (m, 1H), 7,70 (dd, J 9,5, 0,8 Hz, 1H), 7,56 (dd, J 9,5, 1,8 Hz, 1H), 7,37 (t, J 74,1 Hz, 1H), 7,30 (dd, J 6,8, 1,4 Hz, 1H), 7,23-7,28 (m, 1H), 7,11 (td, J 7,6, 1,7 Hz, 1H), 6,81 (dd, J 7,7, 1,6 Hz, 1H), 4,77-4,85 (m, 2H), 4,37-4,45 (m, 2H), 3,42-3,47 (m, 4H), 2,96-3,03 (m, 2H), 2,66 (d, J 0,4 Hz, 1H), 2,55-2,61 (m, 2H), 2,14-2,22 (m, 1H), 1,64-1,72 (m, 2H), 1,31-1,41 (m, 2H). CLEM (EN+) TR 1,44 min, 562 (M+H)+.
E j e m p l o 118
7-Bromo-1-[2-(d¡fluorometox¡)fen¡l1-2-(h¡drox¡met¡l)-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ol
El c o m p u e s to d e l títu lo se preparó a partir del In te rm e d io 6 (0,25 g, 0,53 mmol) y borohidruro sódico (0,022 g, 0,59 mmol) por el M étod o C (0,036 g, rendimiento del 16 %). RMN 1H (DMSO-d6) 8: 7,93 (m, 1H), 7,70 (m, 1H), 7,58 (m, 1 H), 7,32 (m, 3H), 7 , 17 (m, 1H), 6,93 (dd, J 7 ,7 Hz, J 1,6 Hz, 1H), 5,51 (d, J 5,7 Hz, 1H), 5,21 (m, 1H), 4,98 (dd, J 5,7 Hz, J 3,0 Hz, 1 H), 4,81 (t, J 5,0 Hz, 1H), 4,55 (d, J 3,8 Hz, 1H), 3,79 (m, 1H), 3,62 (m, 1H). CLEM (EN+) TR 1,20 min 425,0/427,0 (M+H)+.
E j e m p l o 119
(1R,3S)-1-r2-(Difluorometoxi)fenil1-3-metil-7-(2-r(1S,4S)-2-oxa-5-azabiciclor2.2.11hept-5-il1pirimidin-5-il}-2,3-dihidro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1pir¡d¡n-3-ol
El co m p u e s to d e l títu lo s e preparó a partir del E je m p lo 15 (245 mg, 0,60 mmol) y (1 S ,4 S )-5 -[5 -(4 ,4 ,5 ,5 -te tra m e til-1 ,3 ,2 -d io x a b o ro la n -2 - il)p ir im id in -2 - il]-2 -o x a -5 -a z a b ic ic lo [2.2.1 ]h e p ta n o (272 mg, 0,90 mmol) por el M étod o A , para proporcionar el producto com o una m ezcla epimérica 4:1. La separación de los epímeros por cromatografía CL quiral (columna Chiralcel OD-H®, eluyente de 85:15 de heptano/EtOH) proporcionó 23 mg (8 %) del co m p u e s to d e l títu lo en forma de un sólido de color verde. RMN 1H (500 MHz, MeOD-d4) 8 ppm 8,43 (s, 2H), 7 ,79 (s, 1H), 7,68 (d, J 9,5 Hz, 1H), 7,54 (dd, J 9,5, 1,8 Hz, 1H), 7,37 - 7,31 (m, 1H), 7,26 (d, J 8,1 Hz, 1H), 7 ,18 - 7 ,12 (m, 1H), 6,95 (t, J 73,9 Hz, 1H), 6,83 (dd, J 7,7, 1,2 Hz, 1H), 5 ,17 (dd, J 7,9, 5,6 Hz, 1H), 5,02 (s, 1H), 4,70 (s, 1H), 3,87 (dd, J 7,4, 1,3 Hz, 1H), 3,79 (d, J 7,4 Hz, 1H), 3,55 (dd, J 10,8, 1,3 Hz, 1H), 3,50 (d, J 10,9 Hz, 1H), 3,24 (dd, J 13,6, 8,0 Hz, 1H), 2,51 (dd, J 13,6, 5,6 Hz, 1H), 1,98 (s, 2H), 1,71 (s, 3H). CLEM (EN+) TR 1,31 min 506,0 (M+H)+.
E j e m p l o 120
(1R,3R)-1-r2-(Difluorometoxi)fenil1-3-metil-7-(2-r(1S,4S)-2-oxa-5-azabiciclor2.2.11hept-5-il1pirimidin-5-il}-2,3-dihidro-1H-ciclopentar4,51imidazoH,2-a1piridin-3-ol
El compuesto del título, 108 mg (36 %), se aisló en forma de un sólido de color verde pálido por cromatografía CL quiral de la m ezcla de epímeros sep arada en el Ejemplo 119. RMN 1H (500 MHz, MeOD-d4) 8 ppm 8,43 (s, 2H), 7,84 (s, 1H), 7,65 (d, J 9,4 Hz, 1H), 7,51 (d, J 11,2 Hz, 1H), 7,31 (td, J 7,8, 7,3, 1,6 Hz, 1H), 7,26 (d, J 8,0 Hz, 1H), 7 , 17 -7 ,12 (m, 1 H), 7,09 (dd, J 7,7, 1,6 Hz, 1H), 7,00 (t, J 73,9 Hz, 1H), 5,02 (s, 1H), 4,94 (dd, J 8,4, 4,9 Hz, 1H), 4,70 (s, 1H), 3,87 (dd, J 7,4, 1,2 Hz, 1H), 3,78 (d, J 7,4 Hz, 1H), 3,55 (dd, J 10,8, 1,1 Hz, 1H), 3,50 (d, J 10,9 Hz, 1H), 3,28 (d, J 8,4 Hz, 1H), 2,52 (dd, J 13,5, 4,9 Hz, 1H), 1,98 (s, 2H), 1,69 (s, 3H). CLEM (EN+) TR 1,31 min 506,0 (M+H)+.
E j e m p l o 1 2 1 ,
MÉTODO K
(1R.3R)-1-[2-(D¡fluorometox¡)fen¡l1-6-fluoro-7-[2-(4-h¡drox¡tetrah¡dro-2H-p¡ran-4-¡l)p¡r¡m¡d¡n-5-¡l1-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1,2-a1p¡r¡d¡n-3-ol
El Ejemplo 16 (95 mg, 0,23 mmol), el Intermedio 35 (pureza del 89 %, 98 mg, 0,23 mmol), una solución 2 M de carbonato sódico en a gua (0,35 ml, 0,69 mmol) y 1,4-dioxano (2 ml) se pusieron en un tubo de microondas. La mezcla se desgasificó con nitrógeno antes de la adición de aducto de P d (d p p f)C h D C M (19 mg, 0,02 mmol). La reacción se cerró herméticamente en una atmósfera de nitrógeno y s e agitó en el microondas a 120 °C durante 1 h. S e añadió una solución 1 M de TBAF en THF (1,38 ml) a la reacción enfriada y la m ezcla se agitó a t.a. durante 3 días. La m ezcla se diluyó con a g u a (3 ml) y s e extrajo con EtOAc (2 x 5 ml). La fase orgánica combinada s e lavó con a g u a (2 x 5 ml) y salmuera (5 ml), se s e c ó sobre sulfato sódico y s e concentró al vacío. El producto en bruto s e purificó por HPLC preparativa (Método C) para proporcionar 35 mg (29 % ) del compuesto del título en forma de un sólido de color blanquecino. RMN 1H (500 MHz, CDCla) 8 ppm 8,78 (d, J 1,4 Hz, 2H), 7,70 (d, J 7,1 Hz, 1H), 7,46 (d, J 10,9 Hz, 1H), 7,32 - 7 ,27 (m, 1H), 7,26 - 7,23 (m, 1H), 7,21 - 7 ,14 (m, 2H), 6,67 (dd, J 74,7, 72,6 Hz, 1H), 5,46 (dd, J 7,3, 3,1 Hz, 1H), 4,90 (dd, J 8,5, 3,8 Hz, 1H), 4,45 (s, 1H), 3,97 (m, 4H), 3,67 - 3 ,57 (m, 1H), 2,42 (ddd, J 14,8, 11,6, 6,9 Hz, 3H), 1,57 (d, J 11,8 Hz, 2H). CLEM (EN+) TR 1,25 min 513,0 (M+H)+.
E j e m p l o 122
(1R.3S)-1-[2-(D¡fluorometox¡)fen¡l1-7-[2-(2-h¡drox¡propan-2-¡l)p¡r¡m¡d¡n-5-¡l1-3-met¡l-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ol
Una mezcla del E je m p lo 15 (245 mg, 0,599 mmol), 2-[5-(tetrametil-1,3,2-dioxaborolan-2-il)pirimidin-2-il]propan-2-ol (237 mg, 0,897 mmol), carbonato sódico (190 mg, 1,795 mmol) en 1,4-dioxano (5 ml) se desgasificó con nitrógeno durante 10 minutos, después se añadió aducto de Pd(dppf)Cl2 DCM (49 mg, 10 mol%), así como agua (1,5 ml) y la mezcla de reacción se calentó a 120 °C durante 1 h en el reactor de microondas. La mezcla de reacción se pasó a través de una frita hidrófoba y se concentró. El residuo en bruto se purificó por cromatografía en columna ultrarrápida (SiO2 , EtOAc al 0-100 % en heptano, después MeOH al 0-100 % en EtOAc), y después por HPLC preparativa para proporcionar 8,2 mg (3 %) del c o m p u e s to d e l títu lo en forma de un sólido de color blanquecino. RMN 1H (500 MHz, CDCls) 8 ppm 8,68 (s, 2H), 7,71 (d, J 9,4 Hz, 1H), 7,60 (s, 1H), 7,29 (dd, J 9,4, 1,8 Hz, 1H), 7,27 - 7,22 (m, 1H), 7,17 (d, J 8,1 Hz, 1H), 7,09 - 7,04 (m, 1H), 6,81 (dd, J 7,7, 1,5 Hz, 1H), 6,75 - 6,40 (m, 1H), 5,11 (dd, J 7,8, 5,8 Hz, 1H), 4,45 (s, 1H), 3,30 (dd, J 13,7, 8,0 Hz, 1H), 2,45 (dd, J 13,7, 5,8 Hz, 1H), 1,80 (s, 3H), 1,54 (s, 6H). CLEM (EN+) TR 1,32 min 467,0 (M+H)+.
E j e m p l o 123
(1R.3R)-1-[2-(D¡fluorometox¡)fen¡l1-7-[2-(2-h¡drox¡propan-2-¡l)p¡r¡m¡d¡n-5-¡l1-3-met¡l-2,3-d¡h¡dro-1H-c¡clopenta[4,51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ol
Una mezcla del E je m p lo 15 (245 mg, 0,599 mmol), 2-[5-(tetramet¡l-1,3,2-d¡oxaborolan-2-¡l)p¡rim¡d¡n-2-¡l]propan-2-ol (237 mg, 0,897 mmol), carbonato sódico (190 mg, 1,795 mmol) en 1,4-dioxano (5 ml) se purgó con nitrógeno durante 10 minutos, después se añadieron aducto de Pd(dppf)Cl2 DCM (49 mg, 10 mol%) y agua (1,5 ml). La mezcla de reacción se calentó a 120 °C durante 1 h en el reactor de microondas. La mezcla de reacción se pasó a través de una frita hidrófoba y se concentró. El residuo en bruto resultante se purificó por cromatografía en columna ultrarrápida (SiO2 , EtOAc al 0-100 % en heptano, después MeOH al 0-100 % en EtOAc) y después por HPLC preparativa para proporcionar 35 mg (12 %) del co m p u e s to d e l títu lo en forma de un sólido de color blanquecino. RMN 1H (500 MHz, CDCla) 8 ppm 8,71 (s, 2H), 7,76 (d, J 9,3 Hz, 2H), 7,35 (d, J 10,8 Hz, 1H), 7,25 - 7,20 (m, 1H), 7,17 (dd, J 7,8, 1,6 Hz, 1H), 7,13 (d, J 8,1 Hz, 1H), 7,10 - 7,05 (m, 1H), 6,62 (dd, J 74,7, 72,7 Hz, 1H), 4,88 (dd, J 8,4, 4,1 Hz, 1H), 4,43 (d, J 26,7 Hz, 1H), 3,25 (dd, J 13,8, 8,5 Hz, 1H), 2,64 (dd, J 13,8, 4,2 Hz, 2H), 1,78 (s, 3H), 1,55 (s, 6H). CLEM (EN+) TR 1,32 min 467,0 (M+H)+.
E j e m p l o 124
(1 R ,3 R ) -1 -[2 -(D if lu o ro m e to x i) fe n il1 -3 -m e t il-7 - {2 -[(1 R ,5 S ) -3 -o x a -8 -a z a b ic ic lo [3.2.11 o c t-8 - il1 p ir im id in -5 - il) -2 ,3 -d ih id ro -1 H -c ¡c lo p e n ta [4.51 ¡m ¡d a z o [1.2 -a 1 p ¡r¡d ¡n -3 -o l
Una mezcla del E je m p lo 15 (245 mg, 0,587 mmol), el In te rm e d io 36 (280 mg, 0,883 mmol), carbonato sódico (190 mg, 1,795 mmol) en 1,4-dioxano (5 ml) se desgasificó con nitrógeno, después se añadieron aducto de Pd(dppf)Cl2 DCM (49 mg, 10 mol%) y agua (1,5 ml). La mezcla de reacción se calentó a 120 °C durante 1 h en un reactor de microondas. La mezcla de reacción se pasó a través de una frita hidrófoba y se concentró. El residuo en bruto se purificó por cromatografía en columna ultrarrápida (SiO2 , EtOAc al 0-100 % en heptano, después MeOH al 0-100 % en EtOAc) y después por HPLC preparativa quiral (85 % de heptano: 15 % de EtOH en una columna Chiralcel OD-H) para proporcionar 12 mg (4 %) del c o m p u e s to d e l títu lo en forma de un sólido de color verde pálido. RMN 1H (500 MHz, CDCls) 8 ppm 8,38 (s, 2H), 7,93 (d, J 9,3 Hz, 1H), 7,62 (s, 1H), 7,54 (d, J 9,1 Hz, 1H), 7,39 - 7,32 (m, 1H), 7,26 (d, J 8,4 Hz, 1H), 7,18 (t, J 7,5 Hz, 1H), 6,95 (d, J 7,5 Hz, 1H), 6,65 (t, J 73,3 Hz, 1H), 5,31 - 5,19 (m, 1H), 4,70 (s, 2H), 3,78 (d, J 10,8 Hz, 2H), 3,68 (d, J 11,0 Hz, 2H), 3,41 (dd, J 13,8, 8,0 Hz, 1H), 2,56 (dd, J 13,8, 5,6 Hz, 1H), 2,14 (c, J 6,3, 5,7 Hz, 3H), 2,07 - 1,98 (m, 2H), 1,91 (s, 3H). CLEM (EN+) TR 1,44 min 520,0 (M+H)+.
E j e m p l o 125
4-(5-{(1R,3R)-1-[2-(Difluorometoxi)fenill-3-hidroxi-3-metil-2,3-dihidro-1H-ciclopenta[4,5limidazo[1,2-alpiridin-7-il)pirimidin-2-il)piperazin-2-ona
Una mezcla del E je m p lo 15 (245 mg, 0,587 mmol), el In te rm e d io 31 (270 mg, 0,888 mmol), carbonato sódico (190 mg, 1,795 mmol) en 1,4-dioxano (5 ml) se desgasificó con nitrógeno, después se añadieron aducto de Pd(dppf)Cl2 DCM (49 mg, 10 mol%) y agua (1,5 ml). La mezcla de reacción se calentó a 120 °C durante 1 h en un reactor de microondas. La mezcla de reacción se pasó a través de una frita hidrófoba y se concentró. El residuo en bruto se purificó por cromatografía en columna ultrarrápida (S¡O2 , EtOAc al 0-100 % en heptano, después MeOH al 0-100 % en EtOAc) y después por HPLC preparativa para proporcionar 59 mg (19 %) del co m p u e s to d e l títu lo en forma de un sólido de color blanco. RMN 1H (500 MHz, CDCla) 8 ppm 8,34 (s, 2H), 7,73 (d, J 9,4 Hz, 1H), 7,63 (s, 1H), 7,32 (dd, J 9,4, 1,7 Hz, 1H), 7,24 - 7,20 (m, 1H), 7,17 (dd, J 7,8, 1,6 Hz, 1H), 7,13 (d, J 8,2 Hz, 1H), 7,08 (t, J 7,5 Hz, 1H), 6,61 (dd, J 74,7, 72,7 Hz, 1H), 6,25 (s, 1H), 4,86 (dd, J 8,4, 4,2 Hz, 1H), 4,39 (s, 2H), 4,08 - 3,97 (m, 2H), 3,43 (td, J 5,3, 2,8 Hz, 2H), 3,23 (dd, J 13,8, 8,5 Hz, 1H), 2,63 (dd, J 13,8, 4,2 Hz, 1H), 1,94 (s, 1H), 1,77 (s, 3H). CLEM (EN+) TR 1,24 min 507,0 (M+H)+.
E j e m p l o 126
4-(5-{(1R,3S)-1-[2-(Difluorometoxi)fenill-3-hidroxi-3-metil-2,3-dihidro-1H-ciclopenta[4,5limidazo[1,2-alpiridin-7-il)pirimidin-2-il)piperazin-2-ona
Una mezcla del Ejemplo 15 (245 mg, 0,587 mmol), el Intermedio 31 (270 mg, 0,888 mmol), carbonato sódico (190 mg, 1,795 mmol) en 1,4-dioxano (5 ml) se desgasificó con nitrógeno, después se añadieron aducto de Pd(dppf)Cl2 DCM (49 mg, 10 mol%) y agua (1,5 ml). La mezcla de reacción se calentó a 120 °C durante 1 h en un reactor de microondas. La mezcla de reacción se pasó a través de una frita hidrófoba y se concentró. El residuo en bruto se purificó por cromatografía en columna ultrarrápida (SiO2 , EtOAc al 0-100 % en heptano, después MeOH al 0-100 % en EtOAc) y después por HPLC preparativa para proporcionar 17 mg (5 %) del compuesto del título en forma de un sólido de color blanco. RMN 1H (500 MHz, CDCla) 8 ppm 8,33 (s, 2H), 7,89 (d, J 9,4 Hz, 1H), 7,54 (s, 1H), 7,48 (d, J 9,4 Hz, 1H), 7,31 - 7,23 (m, 1H), 7,19 - 7,16 (m, 1H), 7,09 (t, J 7,5 Hz, 1H), 6,85 (d, J 6,4 Hz, 1H), 6,56 (t, J 73,3 Hz, 1H), 6,12 (s, 1H), 5,16 (dd, J 7,9, 5,7 Hz, 1H), 4,39 (s, 2H), 4,02 (d, J 4,4, 4,0 Hz, 2H), 3,42 (dc, J 5,2, 2,8 Hz, 2H), 3,32 (dd, J 13,8, 8,1 Hz, 1H), 2,48 (dd, J 13,8, 5,7 Hz, 1H), 1,81 (s, 3H). CLEM (EN+) TR 1,24 min 507,0 (M+H)+.
Ejemplo 12a 132
Los siguientes compuestos del título se prepararon a partir del precursor asignado por el Método K
(c o n t in u a c ió n )
Ejemplo 133
4-(5-((1R.3R)-1-r2-(d¡fluorometox¡)fen¡l1-3-h¡drox¡-2.3-d¡h¡dro-1H-c¡clopentar4.51¡m¡dazori.2-a1p¡rid¡n-7-¡l)p¡r¡m¡d¡n-2-¡l)p¡per¡d¡n-1-carbox¡lato de terc-but¡lo
Una soluc¡ón del Ejemplo 32 (89 %, 442 mg, 0.68 mmol) en EtOAc (15 ml) y TEA (100 pl. 0.71 mmol) se pasó 14 veces sobre palad¡o al 10 % sobre carbono en un H-cube (50-100 bares. de t.a. a 50 °C). El producto en bruto se pur¡f¡có por cromatografía en columna ultrarráp¡da (S¡O2. MeOH al 0-10 % en EtOAc). Se obtuv¡eron dos lotes del compuesto del título. uno proporc¡onó un sól¡do de color blanco. 163 mg (38 %. pureza del 93 %) y otro proporc¡onó un sól¡do de color blanco. 111 mg (27 %. pureza del 98 %). RMN 1H (500 MHz. CDCla) 8 ppm 8.74 (s. 2H). 7.84 - 7.71 (m. 2H). 7.37 (dd. J 9.4. 1.8 Hz. 1H). 7.31 - 7.27 (m. 1H). 7.25 - 7.11 (m. 3H). 6.68 (dd. J 74.7. 72.7 Hz. 1H). 5.49 (dd. J 7.3. 3.2 Hz. 1H).
4.92 (dd. J 8.5. 4.0 Hz. 1H). 4.23 (s. 2H). 3.68 - 3.58 (m. 1H). 3.06 (tt. J 11.6. 3.7 Hz. 1H). 2.88 (s. 2H). 2.45 (dt. J 14.1.
3.7 Hz. 1H). 2.00 (d. J 9.6 Hz. 2H). 1.82 (cd. J 12.6. 4.3 Hz. 3H). 1.47 (s. 9H). CLEM (EN+) TR 1.78m¡n 578.0 (M+H)+. Ejemplo 134
(1R.3R)-1-r2-(D¡fluorometox¡)fen¡l1-7-r2-(p¡per¡d¡n-4-¡l)p¡r¡m¡d¡n-5-¡l1-2.3-d¡h¡dro-1H-c¡clopentar4.51¡m¡dazon.2-a1p¡r¡d¡n-3-ol
Se añadió una solución 6 M de HCl en DCM (640 |jl) a una solución del E je m p lo 133 (220 mg, 0,38 mmol) en DCM (1 ml). La mezcla se agitó a t.a. durante 1 h. La mezcla de reacción se basificó a pH 10 usando una solución sat. de carbonato sódico en agua, un sólido precipitó, que se filtró y se lavó con agua (6 ml) y Et2 O (6 ml), se secó durante 3 h para proporcionar 150 mg (80 %) del co m p u e s to d e l títu lo en forma de un sólido de color blanco. RMN 1H (500 MHz, DMSO-d6) 8 ppm 8,94 (s, 2H), 8,23 (s, 1H), 7,73 (d, J 9,5 Hz, 1H), 7,63 (dd, J 9,5, 1,8 Hz, 1H), 7,53 - 7,20 (m, 3H), 7,15 - 7,09 (m, 1H), 6,91 (dd, J 7,7, 1,4 Hz, 1H), 5,51 (s, 1H), 5,13 (dd, J 7,1, 3,0 Hz, 1H), 4,77 (dd, J 8,6, 3,8 Hz, 1H), 3,52 - 3,40 (m, 1H), 3,03 (d, J 12,2 Hz, 2H), 2,91 (tt, J 11,6, 3,5 Hz, 1H), 2,69 - 2,55 (m, 2H), 2,08 (dt, J 13,6, 3,5 Hz, 1H), 1,85 (d, J 11,4 Hz, 2H), 1,67 (tdd, J 12,3, 8,0, 3,7 Hz, 2H). CLEM (EN+) TR 1,78 min 478,0 (M+H)+.
E j e m p l o 135
(1R.3R)-7-[2-(1-Acet¡l-p¡per¡d¡n-4-¡l)-p¡r¡m¡d¡n-5-¡l1-1-(2-d¡fluorometox¡fen¡l)-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-alpiridin-3-il éster del ácido acético
A una solución del E je m p lo 134 (100 mg, 0,21 mmol) en DCM (2 ml) se añadió TEA (58,22 jl, 0,42 mmol) y la mezcla se agitó durante 5 minutos, se añadió anhídrido acético (22 jl, 0,23 mmol) y la mezcla se agitó a t.a. durante 2 h. La mezcla de reacción se diluyó con agua (2 ml) y se extrajo con DCM (2 ml), el extracto orgánico se lavó con salmuera (2 ml), se secó sobre sulfato sódico y se concentró al vacío para proporcionar 111 mg (95 %) del co m p u e s to d e l títu lo en forma de una goma de color naranja. RMN 1H (500 MHz, CDCb) 8 ppm 8,74 (s, 2h ), 7,86 - 7,75 (m, 2H), 7,40 (dd, J 9,4, 1,7 Hz, 1H), 7,33 - 7,27 (m, 1H), 7,22 (d, J 8,1 Hz, 1H), 7,17 - 7,12 (m, 1H), 7,06 (dd, J 7,8, 1,6 Hz, 1H), 6,68 (dd, J 74,3, 72,7 Hz, 1H), 6,25 (dd, J 7,4, 3,2 Hz, 1H), 4,96 (dd, J 8,5, 3,9 Hz, 1H), 4,71 (d, J 13,4 Hz, 1H), 3,94 (d, J 13,8 Hz, 1H), 3,82 - 3,69 (m, 1H), 3,32 - 3,04 (m, 3H), 2,83 - 2,70 (m, 1H), 2,39 (dt, J 14,6, 3,6 Hz, 1H), 2,13 (s, 3H), 2,10 (s, 3H), 2,06 (d, J 15,9 Hz, 1H), 1,90 (cd, J 12,5, 4,1 Hz, 1H), 1,80 (cd, J 12,5, 4,3 Hz, 1H). CLEM (EN+) TR 1,80 min 562,0 (M+H)+.
E j e m p l o 136
(1R,3R)-1-r2-(Difluorometoxi)fenil1-6-fluoro-7-r2-(3-hidroxiazetidin-3-il)pirimidin-5-il1-2,3-dihidro-1H-ciclopentar4,51imidazoH,2-a1piridin-3-ol
Se añadió una solución 4 M de HCl en 1,4-dioxano (51 j l , 0,206 mmol) a una solución del E je m p lo 127 (60 mg, 0,103 mmol) en 1,4-dioxano (2 ml) a t.a. La mezcla de reacción se agitó a t.a. durante 1 hora y se concentró en un flujo de nitrógeno. El residuo se disolvió en 1,4-dioxano (2 ml) y se añadió una solución 4 M de HCl en 1,4-dioxano (51 jl, 0,206 mmol) a t.a. La mezcla de reacción se agitó a t.a. durante 5 h y se concentró en un flujo de nitrógeno. El residuo resultante se purificó por HPLC preparativa para proporcionar 8,6 mg (16 %) del co m p u e s to d e l títu lo en forma de un sólido de color blanquecino. RMN 1H (500 MHz, DMSO-d6) 8 ppm 8,97 (s, 2H), 8,37 (s, 2H), 8,22 (d, J 7,5 Hz, 1H), 7,71 (d, J 11,7 Hz, 1H), 7,48 - 7,17 (m, 3H), 7,12 (t, J 7,5 Hz, 1H), 6,93 - 6,90 (m, 1H), 5,54 (s, 1H), 5,12 (dd, J 7,2, 3,0 Hz, 1H), 4,75 (dd, J 8,5, 3,9 Hz, 1H), 4,14 (s, 2H), 3,80 (d, J 9,0 Hz, 3H), 2,12 - 1,98 (m, 2H). CLEM (EN+) 1,14 min, 484,0 (M+H)+.
E j e m p l o 137
(1R.3R)-1-r2-(D¡fluorometox¡)fen¡l1-6-fluoro-7-r2-(3-h¡drox¡-1-met¡lazet¡d¡n-3-¡l)p¡r¡m¡d¡n-5-¡l1-2.3-d¡h¡dro-1H-ciclopenta[4,51¡iTi¡dazo[1.2-a1p¡r¡d¡n-3-ol
S e añad¡ó ác¡do tr¡fluoroacét¡co (135 pl. 1,77 mmol) a una soluc¡ón del Ejemplo 136 (127 mg. 0.16 mmol) en DCM (2 ml) a 0 °C. La m ezcla de reacc¡ón s e ag¡tó a 0 °C durante 30 m¡nutos y t.a. durante 3 h. La mezcla de reacc¡ón se concentró al vac ío para proporc¡onar 130 mg (pureza del 64 % ) de un ace¡te. que s e d¡solv¡ó en EtOH (5 ml) y se añad¡ó una soluc¡ón ac. al 37 % de formaldehído (0.047 ml. 0.62 mmol) a t.a. La mezcla s e ag¡tó durante 20 m¡nutos y s e añad¡ó en una porc¡ón tr¡acetox¡boroh¡druro sód¡co (74 mg. 0.348 mmol). segu¡do de AcOH (0.1 ml). T o d a s la mezcla s e ag¡tó a t.a. en una atmósfera de n¡trógeno durante 3.5 h. S e añad¡eron m ás soluc¡ón ac. al 37 % de formaldehído (0.047 ml. 0.62 mmol) y tr¡acetox¡boroh¡druro sód¡co (74 mg. 0.348 mmol) a t.a. y la mezcla de reacc¡ón se agitó durante una noche. La mezcla de reacc¡ón s e ¡nact¡vó con una soluc¡ón sat. de b¡carbonato sód¡co en a gua (~ 3 ml) y la m ezcla s e extrajo con DCM (3 x 5 ml). Los extractos orgán¡cos s e comb¡naron. s e secaron sobre sulfato sód¡co. s e f¡ltraron y s e concentraron al vacío. El res¡duo resultante se pur¡f¡có por HPLC preparat¡va para proporc¡onar 24 mg (35 %) del compuesto del título en forma de un sól¡do de color blanquec¡no. RMN 1H (500 MHz. CDCl3) 8 ppm 8.84 (d. J 1.4 Hz. 2H). 7.69 (d. J 7.1 Hz. 1H). 7.44 (d. J 10.9 Hz. 1H). 7.32 - 7.27 (m. 1H). 7.26 (s. 1H). 7.22 - 7.14 (m.
2H). 6.67 (dd. J 74.7. 72.7 Hz. 1H). 5.45 (dd. J 7.3. 3.1 Hz. 1H). 4.90 (dd. J 8.5. 3.9 Hz. 1H). 3.98 (d. J 7.9 Hz. 2H).
3.65 - 3.57 (m. 1H). 3.51 (d. J 8.1 Hz. 2H). 2.56 (s. 3H). 2.44 (dt. J 14.1. 3.6 Hz. 1H). 1.71 (d. J 8.6 Hz. 2H). CLEM (EN+) 1.20 m¡n. 498.0 (M+H)+.
E j e m p l o 138
(1R)-1-[2-(D¡fluorometox¡)fen¡l1-3.6-d¡fluoro-7-[6-(met¡lsulfon¡l)p¡r¡d¡n-3-¡l1-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡na
A una solución agitada del Ejemplo 21 (110 mg, 0,225 mmol) en THF (3 ml) s e añadió trifluoruro de dietilaminoazufre (55 □!, 0,341 mmol). La m ezcla de reacción s e agitó a t.a. en una atmósfera de nitrógeno durante 1 h. La m ezcla de reacc¡ón s e diluyó con a g u a (15 ml) y s e ajustó a pH ~ 8 (usando 11 ml de una soluc¡ón ac. sat. de b¡carbonato sód¡co) antes de extraerse con DCM (30 ml). La capa orgán¡ca se pasó a través de una fr¡ta h¡drófoba y s e concentró a pres¡ón reduc¡da. El res¡duo en bruto resultante s e purificó por HPLC preparativa (Método C). segu¡do de cromatografía en columna ultrarrápida. e luyendo con EtOAc del 0 al 100 % en heptano y d e sp u é s MeOH del 0 al 100 % en EtOAc para proporc¡onar 14 mg (12 %) del compuesto del título en forma de un sólido de color blanco. RMN 1H (500 MHz. C D C b) 8 ppm 8.65 (d. J 24.8 Hz. 1H). 8.09 (d. J 8.1 Hz. 1H). 7.96 (tt. J 8.4. 1.8 Hz. 1H). 7.74 (d. J 7.1 Hz. 1H). 7.57 - 7.36 (m.
1H). 7.31 - 7.20 (m. 1H). 7.18 - 7.04 (m. 3H). 6.83 - 6.38 (m. 1H). 6.23 - 5.91 (m. 1H). 5.24 - 4.80 (m. 1H). 3.65 - 3.23 (m. 1H). 3.19 (d. J 5.5 Hz. 3H). 2.84 - 2.53 (m. 1H). CLEM (EN+) 1.46 min. 492.0 (M+H)+.
E j e m p l o 139
1- í4-í5-(í1R.3R)-1-r2-ÍD¡fluorometox¡)fen¡l1-3-h¡drox¡-2.3-d¡h¡dro-1H-c¡clopentar4.51¡m¡dazori.2-a1p¡rid¡n-7-¡l)p¡r¡m¡d¡n-2- ¡l)p¡per¡d¡n-1-¡l1etanona
A una soluc¡ón del E je m p lo 135 (110 mg, 0.19 mmol) en THF (1 ml) y agua (0.5 ml) se añad¡ó una soluc¡ón ac. 2 M de h¡dróx¡do de l¡t¡o (98 pl). La mezcla de reacc¡ón se ag¡tó a t.a. durante 2.5 h. La mezcla se d¡luyó con agua (3 ml) y se extrajo con EtOAc (6 ml) y 1:1 de /-PrOH/CHCb (3 ml). los extractos orgán¡cos comb¡nados se lavaron con una soluc¡ón ac. 2 M de carbonato sód¡co (12 ml) y salmuera (6 ml). se secó sobre sulfato sód¡co y se concentró al vacío para proporc¡onar 58 mg (55 %) del co m p u e s to d e l títu lo en forma de un sól¡do de color blanquec¡no. RMN 1H (500 MHz. DMSO-d6) 8 ppm 8.96 (s. 2H). 8.24 (s. 1H). 7.73 (d. J 9.4 Hz. 1H). 7.64 (dd. J 9.5. 1.8 Hz. 1H). 7.53 - 7.18 (m. 3H).
7.11 (t. J 7.4 Hz. 1H). 6.90 (d. J 7.2 Hz. 1H). 5.51 (d. J 5.1 Hz. 1H). 5.13 (s. 1H). 4.77 (dd. J 8.6. 3.8 Hz. 1H). 4.42 (d, J 13.1 Hz. 1H). 3.88 (d. J 13.6 Hz. 1H). 3.51 - 3.41 (m. 1H). 3.23 - 3.14 (m. 1H). 3.11 (tt. J 11.3. 3.6 Hz. 1H). 2.70 (t. J 11.4 Hz. 1H). 2.12 - 2.05 (m. 1H). 2.02 (s. 3H). 2.00 - 1.90 (m. 2H). 1.79 - 1.66 (m. 1H). 1.63 - 1.52 (m. 1H). CLEM (EN+) 1.25 m¡n. 520.0 (M+H)+.
E j e m p l o 140
2-15-[(1R)-1-[2-(D¡fluorometox¡)fen¡l1-6-fluoro-3-(met¡lsulfon¡l)-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-7-¡l1p¡r¡m¡d¡n-2-¡l1propan-2-ol
El In te rm e d /o 55 (10 mg. 0.02 mmol) se d¡solv¡ó en DCM (1 ml) y se añad¡ó ác¡do 3-clorobencenocarboperoxo¡co (9 mg. 0.04 mmol). La mezcla de reacc¡ón se ag¡tó a t.a. durante 24 h. La mezcla se ¡nact¡vó con una soluc¡ón ac. sat. de carbonato sód¡co (3 ml) y se extrajo con DCM (3 x 3 ml). Las capas orgán¡cas comb¡nadas se lavaron con salmuera (5 ml). se secaron sobre sulfato sód¡co y se concentraron al vacío. El res¡duo se pur¡f¡có por cromatografía en columna ultrarrápida (S¡O2. EtOAc al 50-100 % en heptano) para proporc¡onar 7.5 mg (70 %) del c o m p u e s to d e l títu lo (aprox¡madamente una proporc¡ón 1:1 de d¡aestereo¡sómeros) en forma de un sól¡do de color amar¡llo pálido. RMN 1H (500 MHz. CDCla) 8 ppm 8.74 (s. 2H). 7.63 - 7.45 (m. 2H). 7.39 - 7.30 (m. 1H). 7.26 - 6.89 (m. 3H). 6.85 - 6.44 (m. 1H).
5.26 - 5.01 (m. 1H). 4.82 - 4.68 (m. 1H). 4.44 (s. 1H). 3.89 - 3.56 (m. 1H). 3.31 (d. J 42.9 Hz. 3H). 3.10 - 2.76 (m. 1H).
1.62 (s. 6H). CLEM (EN+) 1.35 m¡n. 533.0 (M+H)+.
E j e m p l o 141
(1R.3S)-1-[2-(D¡fluorometox¡)fen¡l1-6-fluoro-7-[2-(2-h¡drox¡propan-2-¡l)p¡r¡m¡d¡n-5-¡l1-3-met¡l-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ol
El E je m p lo 20 (158 mg, 0,37 mmol) y 2-[5-(tetrametil-1,3,2-dioxaborolan-2-il)pirimidin-2-il]propan-2-ol (146,53 mg, 0,55 mmol) s e disolvieron en 1,4-dioxano (5 ml) antes de añadir una solución ac. 2 M de carbonato sódico (0,55 ml). La mezcla s e desgasificó con nitrógeno antes de añadir aducto de Pd(dppf)Cl2 DCM (30 mg, 0,04 mmol) y la mezcla de reacción se agitó a 80 °C durante 2 h. La mezcla de reacción s e enfrió a t.a., s e diluyó con EtOAc (5 ml) y s e lavó con a gua (3 x 3 ml). Los lavados ac. s e combinaron y s e extrajeron con EtOAc (3 x 3 ml). Los extractos orgánicos se combinaron, s e secaron sobre sulfato sódico y se concentraron al vacío. El residuo de color pardo resultante se purificó por cromatografía en columna ultrarrápida (SiO 2 , MeOH al 0-15 % en DCM). La purificación por HPLC preparativa quiral (85 % de heptano: 15 % de EtOH en una columna Chiral P a k AD) proporcionó 10 mg (5,5 % ) del c o m p u e s to de l títu lo en forma de un sólido de color blanco. RMN 1H (500 MHz, C D C b ) 8 ppm 8,74 (d, J 1,4 Hz, 2H), 7,54 (d, J 7,1 Hz, 1H), 7,46 (d, J 10,9 Hz, 1H), 7,35 - 7,29 (m, 1H), 7,23 (d, J 8,0 Hz, 1H), 7 ,15 (t, J 7,5 Hz, 1H), 6,87 (dd, J 7,7, 1,4 Hz, 1H), 6,81 - 6,45 (m, 1H), 5 ,14 (dd, J 7,7, 5,9 Hz, 1H), 4,48 (s, 1H), 3,34 (dd, J 13,8, 7,9 Hz, 1H), 2,51 (dd, J 13,8, 5,7 Hz, 1H), 2,31 (s, 1H), 1,83 (s, 3H), 1,62 (s, 6H). CLEM (EN+) TR 1,35 min 484,0 (M+H)+.
E j e m p l o 142
(1R.3R)-1-[2-(D¡fluorometox¡)fen¡l1-6-fluoro-7-[2-(2-h¡drox¡propan-2-¡l)p¡r¡m¡d¡n-5-¡l1-3-met¡l-2,3-d¡h¡dro-1H-ciclopenta[4,51imidazo[1.2-a1piridin-3-ol
El co m p u e s to d e l títu lo , 43 mg (24 %), s e aisló en forma de un cristal incoloro mediante HPLC preparativa quiral (85 % de heptano: 15 % de EtOH en columna Chiral Pak AD) de la m ezcla de epímeros sep a ra d a en el E je m p lo 141. RMN 1H (500 MHz, CDCla) 8 ppm 8,75 (d, J 1,4 Hz, 2H), 7 ,67 (d, J 7,1 Hz, 1H), 7,43 (d, J 10,9 Hz, 1H), 7,29 (td, J 7,9, 7,3, 1,7 Hz, 1H), 7,22 - 7 ,12 (m, 3H), 6,66 (dd, J 74,6, 72,7 Hz, 1H), 4,90 (dd, J 8,4, 4,0 Hz, 1H), 4,50 (s, 1H), 3,30 (dd, J 13,8, 8,5 Hz, 1 H), 2,88 (s, 1H), 2,66 (dd, J 13,8, 4,0 Hz, 1H), 1,81 (s, 3H), 1,62 (s, 6H). CLEM (EN+) TR 1,35 min 484,0 (M+H)+.
E j e m p l o 143
(1R.3S)-1-[2-(D¡fluorometox¡)fen¡l1-7-[2-(3.7-d¡oxa-9-azab¡c¡clo[3.3.11non-9-¡l)p¡r¡m¡d¡n-5-¡l1-6-fluoro-3-met¡l-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ol
El Ejemplo 20 (130 mg, 0,29 mmol) se disolvió en 1,4-dioxano (2 ml) en un tubo de microondas y después se añadió el Intermedio 71 (96 mg, 0,29 mmol). Se añadió carbonato sódico (92 mg, 0,62 mmol) y la mezcla se desgasificó con nitrógeno antes de la adición de aducto de Pd(dppf)Cl2 DCM (24 mg, 0,029 mmol) y agua (0,6 ml). La mezcla de reacción se agitó durante 1 h a 120 °C en un reactor de microondas. La mezcla de reacción se pasó a través de una frita hidrófoba y se concentró al vacío. El producto en bruto resultante se purificó usando HPLC preparativa para proporcionar un sólido de color crema. El compuesto racémico se purificó por SFC quiral (30 % de EtOH: 70 % de CO2 en una columna Chiral Pak IC de 25 cm) para proporcionar 10 mg (6 %) del compuesto del título en forma de un aceite de color amarillo. RMN 1H (500 MHz, CDCb) 6 ppm 8,33 (d, J 1,3 Hz, 2H), 7,43 (d, J 7,1 Hz, 1H), 7,39 (d, J 10,8 Hz, 1H), 7,32 - 7,28 (m, 1H), 7,22 (d, J 8,1 Hz, 1H), 7,17 - 7,09 (m, 1H), 6,86 (dd, J 7,7, 1,4 Hz, 1H), 6,62 (t, J 73,1 Hz, 1H), 5,12 (dd, J 7,8, 5,8 Hz, 1H), 4,56 (s, 2H), 4,13 (d, J 11,2 Hz, 4H), 3,92 (dd, J 10,9, 2,1 Hz, 4H), 3,33 (dd, J 13,8, 7,9 Hz, 1H), 2,48 (dd, J 13,7, 5,7 Hz, 1H), 1,82 (s, 3H). CLEM (EN+) TR 1,36 min 554,0 (M+H)+.
E j e m p l o 144
(1R.3R)-1-[2-(D¡fluorometox¡)fen¡l1-7-[2-(3.7-d¡oxa-9-azab¡c¡clo[3.3.11non-9-¡l)p¡r¡m¡d¡n-5-¡l1-6-fluoro-3-met¡l-2,3-dihidro-1H-ciclopentar4,51imidazoH,2-a1piridin-3-ol
El compuesto del título, 48 mg (30 %), se aisló en forma de un sólido de color blanco por SFC quiral (30 % de EtOH: 70 % de CO2 en una columna Chiral Pak IC de 25 cm) de la mezcla de epímeros separada en el Ejemplo 143. RMN 1H (500 MHz, CDCla) 68,34 (d, J 1,4 Hz, 2H), 7,55 (d, J 7,2 Hz, 1H), 7,36 (d, J 10,9 Hz, 1H), 7,29 - 7,24 (m, 1H), 7,21 - 7,16 (m, 2H), 7,15 - 7,11. (m, 1H), 6,65 (dd, J 74,7, 72,7 Hz, 1H), 4,87 (dd, J 8,4, 4,1 Hz, 1H), 4,57 (s, 2H), 4,13 (d, J 11,2 Hz, 4H), 3,93 (dd, J 10,9, 2,1 Hz, 4H), 3,28 (dd, J 13,7, 8,5 Hz, 1H), 2,65 (dd, J 13,8, 4,1 Hz, 1H), 1,81 (s, 3H). CLEM (EN+) TR 1,36 min 554,0 (M+H)+.
E j e m p l o 145
(1R,3R)-1-r2-(Difluorometoxi)fenil1-7-r2-(1,1-dioxidotiomorfolin-4-il)pirimidin-5-il1-6-fluoro-3-metil-2,3-dihidro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ol
El E je m p lo 20(130 mg, 0,29 mmol, 1,0 equiv.) y el In te rm e d io 62 (98 mg, 0,29 mmol, 1,0 equiv.) y carbonato sódico (92 mg, 0,620 mmol) se agitaron en 1,4-dioxano (2 ml), la mezcla se desgasificó con nitrógeno durante 10 minutos antes de añadir aducto de Pd(dppf)Cl2 DCM (24 mg, 10 mol%) así como agua (0,6 ml). La mezcla de reacción se calentó a 120 °C durante 1 h en un reactor de microondas. La mezcla de reacción se filtró a través de celite, se lavó con EtOAc (3 x 5 ml) y se concentró al vacío. El producto en bruto se purificó por cromatografía en columna ultrarrápida (SiO2 , MeOH al 0-10 % en DCM), seguido de HPLC preparativa para proporcionar 62 mg del compuesto racémico. La separación de epímeros por SFC quiral (30 % de MeOH: 70 % de CO2 en una columna Chiral Pak IC de 25 cm) proporcionó 93 mg (64 %) del co m p u e s to d e l títu lo en forma de un sólido de color amarillo. RMN 1H (500 MHz, CDCb ) 8 ppm 8,37 (s, 2H), 7,56 (d, J 6,6 Hz, 1H), 7,35 (d, J 10,6 Hz, 1H), 7,28 - 7,22 (m, 2H), 7,19 - 7,10 (m, 2H), 6,66 (t, J 73,7 Hz, 1H), 5,00 - 4,77 (m, 1H), 4,39 (s, 4H), 3,28 (dd, J 13,3, 8,6 Hz, 1H), 3,05 (s, 4H), 2,67 (d, J 11,7 Hz, 1H), 1,83 (s, 3H). CLEM (EN+) TR 1,34 min 560,0 (M+H)+.
E j e m p l o 146
(1R.3S)-1-[2-(D¡fluorometox¡)fen¡l1-7-[2-(1.1-d¡ox¡dot¡omorfol¡n-4-¡l)p¡r¡m¡d¡n-5-¡l1-6-fluoro-3-met¡l-2.3-d¡h¡dro-1H-c¡clopentar4.51¡m¡dazoH.2-a1p¡r¡d¡n-3-ol
El co m p u e s to d e l títu lo , 17 mg (12 %), se aisló en forma de un sólido de color amarillo por SFC quiral (30 % de MeOH: 70 % de CO2 en una columna Chiral Pak IC de 25 cm) de la mezcla de epímeros separada en el E je m p lo 145. RMN 1H (500 MHz, CDCb ) 8 ppm 8,37 (d, J 1,2 Hz, 2H), 7,42 (dd, J 14,5, 9,0 Hz, 2H), 7,33 - 7,28 (m, 1H), 7,22 (d, J 8,1 Hz, 1H), 7,13 (t, J 7,5 Hz, 1H), 6,86 (dd, J 7,7, 1,3 Hz, 1H), 6,63 (t, J 73,4 Hz, 1H), 5,13 (dd, J 7,7, 5,8 Hz, 1H), 4,40 (s, 4H), 3,33 (dd, J 13,8, 7,9 Hz, 1H), 3,12 - 2,92 (m, 4H), 2,50 (dd, J 13,8, 5,6 Hz, 1H), 1,83 (s, 3H). CLEM (EN+) TR 1,34 min, 560,0 (M+H)+.
E j e m p l o 147
(1R,3R)-1-[2-(Difluorometoxi)fenil1-6-fluoro-7-{2-[(3S o R)-3-hidroxitetrahidrofurano-3-il1pirimidin-5-il)-2,3-dihidro-1H-c¡clopenta[4.51¡m¡dazo[1,2-a1p¡r¡d¡n-3-ol
El E je m p lo 16 (235 mg, 0,42 mmol), el In te rm e d io 53 (372 mg, 0,67 mmol) y una solución ac. 2 M de carbonato sódico (0,63 ml) se agitaron en 1,4-dioxano (4 ml) y se desgasificaron con nitrógeno. Se añadió aducto de Pd(dppf)Cl2 DCM (34 mg, 0,04 mmol) y la mezcla de reacción se calentó a 100 °C durante 1,5 h. La mezcla de reacción se enfrió a t.a. y se añadió TBAF 1 M (2,52 ml). La mezcla se agitó a t.a. durante 3 h. La mezcla de reacción se diluyó con EtOAc (20 ml) y se lavó con agua (20 ml) y salmuera (30 ml). La fase orgánica se secó sobre sulfato sódico y se concentró al vacío para proporcionar una goma de color negro. El producto en bruto se purificó por cromatografía en columna ultrarrápida (SiO2 , EtOAc al 50-100 % en heptano, después MeOH al 0-15 % en EtOAc) para proporcionar un sólido de color blanquecino. Esto se purificó adicionalmente usando HPLC preparativa quiral (MeCN 0,1 % de DEA con una columna Chiralcel OD-H de 25 cm), seguido de trituración usando DCM para proporcionar 8 mg (4 %) del co m p u e s to d e l títu lo en forma de un sólido de color blanco. RMN 1H (500 MHz, CDCb ) 8 ppm 8,79 (d, J 1,4 Hz, 2H), 7,70 (d, J 7,1 Hz, 1H), 7,45 (d, J 10,9 Hz, 1H), 7,32 - 7,26 (m, 1H), 7,24 (d, J 1,7 Hz, 1H), 7,18 (c, J 7 ,8 Hz, 2H), 6,67 (dd, J 74,8, 72,6 Hz, 1H), 5,45 (dd, J 7,2, 3,0 Hz, 1H), 4,96 - 4,82 (m, 2H), 4,27 - 4,17 (m, 3H), 3,99 (d, J 9,0 Hz, 1H), 3,67 - 3,56 (m, 1H), 2,64 (dt, J 12,6, 8,8 Hz, 1H), 2,44 (dt, J 14,1, 3,5 Hz, 1H), 2,26 (dt, J 12,4, 5,2 Hz, 1H). CLEM (EN+) TR 1,23 min 499,0 (M+H)+.
E j e m p l o 148
(1R,3R)-1-[2-(Difluorometoxi)fenil1-6-fluoro-7-{2-[(3R o S)-3-hidroxitetrahidrofurano-3-il1pirimidin-5-il)-2,3-dihidro-1H-c¡clopenta[4.51¡m¡dazo[1,2-a1p¡r¡d¡n-3-ol
El co m p u e s to d e l títu lo , 31 mg (14 %), se aisló en forma de un sólido de color blanquecino por HPLC preparativa quiral (MeCN 0,1 % de DEA con una columna Chiralcel OD-H de 25 cm) de la mezcla de epímeros separada en el E je m p lo 146. RMN 1H (500 MHz, CDCb ) 8 ppm 8,79 (d, J 1,3 Hz, 2H), 7,71 (d, J 6,9 Hz, 1H), 7,46 (d, J 10,7 Hz, 1H), 7,32 -7.27 (m, 2H), 7,22 - 7,14 (m, 2H), 6,68 (dd, J 74,8, 72,6 Hz, 1H), 5,47 (d, J 4,4 Hz, 1H), 4,90 (dd, J 8,4, 3,8 Hz, 1H), 4.28 - 4,16 (m, 3H), 3,99 (d, J 9,0 Hz, 1H), 3,68 - 3,55 (m, 1H), 2,64 (dt, J 12,6, 8,8 Hz, 1H), 2,45 (dt, J 14,1, 3,3 Hz, 1H), 2,26 (dt, J 12,5, 5,1 Hz, 1H). CLEM (EN+) TR 1,23 min 499,0 (M+H)+.
E j e m p l o 149
(R)-1-f2-(D¡fluorometox¡)fen¡ll-7-f4-(met¡lsulfon¡l)fen¡ll-3-deuter¡o-2,3-d¡h¡dro -1H-c¡clopenta[4.5l¡m¡dazo[1.2-alp¡r¡d¡n-3-ol
A una solución del Ejemplo 41 (0,11 g, 0,23 mmol) en MeOH (1 ml) s e añadió borodeuteruro sódico (0,012 g, 0,25 mmol) y la mezcla se agitó a t.a. durante 1 h. La m ezcla de reacción s e repartió entre EtOAc (10 ml) y cloruro de amonio ac. sat. (10 ml). Los extractos orgánicos s e separaron, s e lavaron con a gua (5 ml) y salmuera (5 ml), se secaron sobre sulfato sódico y se concentraron al vacío. El residuo en bruto se purificó por cromatografía (SiO 2 , MeOH al 0 10 % en EtOAc) y el compuesto del título s e aisló en forma de un sólido de color blanco (0,048 g 43 %). RMN 1H (DMSO-da) 5; 8,20 (s, 1H), 7,98 (m, 3H), 7,86 (m, 2H), 7 ,74 (m, 1H), 7,64 (m, 1H), 7,39 (s, 1H), 7,30 (m, 3H), 7 ,12 (m, 1H), 6,94 (dd, J 7,7 Hz, J 1,4 Hz, 1H), 5,48 (s, 1H), 4,82 (dd, J 8,6 Hz, J 3,8 Hz, 1H), 3,47 (dd, J 13 ,7 Hz, J 8,6 Hz, 1H), 3,32 (s, 1H), 2 ,10 (dd, J 13 ,7 Hz, J 3,9 Hz, 1H). CLEM (EN+) TR 1,81 min, 472,0 (M+H)+.
E j e m p l o 150
(1R.3R)-1-í2-(Difluorometoxi)fenill-6-fluoro-7-í4-(S-metilsulfonimidoil)fenill-2.3-dihidro-1H-ciclopentaí4,5limidazoí1.2-alpiridin-3-ol
El compuesto del título s e preparó a partir del Ejemplo 16 (210 mg, 0,43 mmol), el Intermedio 75 (171 mg, 0,52 mmol, pureza del 85 %), por el Método A (128 mg, 60 %). RMN 1H (500 MHz, CDCla) 6 ppm 8,06 (d, J 8,3 Hz, 2H), 7,71 (d, J 7,1 Hz, 1 H), 7 ,57 (d, J 7,3 Hz, 2H), 7,44 (d, J 10,8 Hz, 1H), 7,30 (t, J 7,8 Hz, 2H), 7 , 17 (d, J 7,6 Hz, 2H), 6,67 (dd, J 74,9, 72,5 Hz, 1H), 5,48 (d, J 4,9 Hz, 1H), 4,89 (dd, J 8,4, 3,6 Hz, 1H), 3,62 (dt, J 14,9, 7,9 Hz, 1H), 3 ,14 (s, 3H), 2,46 (d, J 14,1 Hz, 1H). ). CLEM (EN+) TR 1,73 min, 488,0 (M+H)+.
E j e m p l o 151
(1R)-1-f2-(D¡fluorometox¡)fen¡ll-6-fluoro-3-met¡l-7-f4-(S-met¡lsulfon¡m¡do¡l)fen¡ll-2,3-d¡h¡dro-1H-ciclopenta[4.5limidazo[1.2-alpiridin-3-ol
El compuesto del titulo s e preparó a partir del Ejemplo 20 (420 mg, 0,98 mmol) y el Intermedio 75 (390 mg, 1,18 mmol) por el Método A (457 mg, 92 %). RMN 1H (500 MHz, CDCla) 6 ppm 8,06 (d, J 8,3 Hz, 2H), 7,69 (d, J 7,1 Hz, 1H), 7,55
(dd, J 13,2, 7,1 Hz, 2H), 7,42 (d, J 10,1 Hz, 1H), 7,32 - 7 ,27 (m, 1H), 7 , 17 - 7 ,13 (m, 1H), 6,84 - 6,42 (m, 1H), 4,89 (dd, J 8,4, 3,8 Hz, 1 H), 3,29 (dd, J 13,8, 8,5 Hz, 1H), 3 ,13 (s, 3H), 2,68 (dd, J 13,8, 3,8 Hz, 1H), 1,81 (s, 3H). CLEM (EN+) T R 1,88 min, 502,0 (M+H)+.
E j e m p l o 152
(1R,3R)-1-[2-(D¡fluorometox¡)fen¡l1-6-fluoro-7-[2-(1-¡m¡no-1-ox¡do-1lambda~4~,4-t¡az¡nan-4-¡l)p¡r¡m¡d¡n-5-¡l1-2,3-d¡h¡dro-1H-c¡clopenta[4,51¡m¡dazo[1,2-a1p¡r¡d¡n-3-ol
El compuesto del título s e preparó a part¡r del Ejemplo 16 (100 mg, 0,22 mmol), el Intermedio 79 (97 mg, 0,25 mmol), por el Método A (28 mg, 25 %). RMN 1H (500 MHz, MeOD) 8 ppm 8,46 (d, J 1,3 Hz, 2H), 7,84 (d, J 7,3 Hz, 1H), 7,44 (d, J 11,0 Hz, 1 H), 7,36 - 7,29 (m, 1H), 7,25 (d, J 8,0 Hz, 1H), 7 ,19 - 6,82 (m, 3H), 5,29 (dd, J 7,2, 3,6 Hz, 1H), 4,56 (d, J 14,8 Hz, 2H), 4,22 - 4,06 (m, 2H), 3,66 - 3,55 (m, 1H), 3 ,17 (d, J 3,9 Hz, 4H), 2,24 (dt, J 13,8, 4,0 Hz, 1H). CLEM (EN+) TR 1,77 m¡n, 545,0 (M+H)+.
E j e m p l o s 153 a 154
Los s¡gu¡entes Ejemplos se prepararon por el Método A a part¡r del mater¡al de part¡da dado usando el éster de boronato o ác¡do borón¡co adecuado.
E j e m p l o s 155 a 169
Los s¡gu¡entes Ejemplos se prepararon por el Método A a part¡r del mater¡al de part¡da dado usando el éster de boronato o ác¡do borón¡co comerc¡al o s¡ntet¡zado adecuado.
(c o n t in u a c ió n )
(c o n t in u a c ió n )
(continuación)
E j e m p l o 170
(1R.3R)-7-[2-(2-Am¡nopropan-2-¡l)p¡r¡m¡d¡n-5-¡l1-1-[2-(d¡fluorometox¡)fen¡l1-6-fluoro-2.3-d¡h¡dro-1H-c¡clopenta[4,51¡iTi¡dazo[1.2-a1p¡r¡d¡n-3-ol
El compuesto del título s e preparó a part¡r del Intermedio 137 (75 mg. 0.13 mmol) en d¡oxano (1.5 ml) y cloruro de h¡drógeno 4 M en 1.4-d¡oxano (0.33 ml) por el Método J (59 mg. 95 %).
RMN 1H (500 MHz. CDCla) 8 8.72 (d. J 1.4 Hz. 2H). 7.65 (d. J 7.1 Hz. 1H). 7.43 (d. J 10.9 Hz. 1H). 7.31 - 7.27 (m. 1H).
7.23 (dd, J 7.7. 1.7 Hz. 1H). 7.21 - 7.14 (m. 2H). 6.66 (dd. J 74.6. 72.8 Hz. 1H). 5.45 (dd. J 7.3. 3.2 Hz. 1H). 4.89 (dd. J 8.5. 4.0 Hz. 1 H). 3.65 - 3.55 (m. 1H). 2.42 (dt. J 14.1. 3.6 Hz. 1H). 1.57 (s. 6H). CLEM (EN+) TR 1.25 m¡n. 470.0 (M+H)+.
E j e m p l o 171
Ác¡do (1R.5S.6r)-3-(5-{(1R)-1-[2-(d¡fluorometox¡)fen¡l1-6-fluoro-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-7-¡l}p¡r¡m¡d¡n-2-¡l)b¡c¡clo(3.1.01hexano-6-carboxíl¡co
El co m p u e s to d e l titu lo s e preparó a partir del In te rm e d io 98 (100 mg, 0,18 mmol) en dioxano (2 ml) e hidróxido potásico 1 M en a g u a (0,187 ml) por el M étod o I (97 mg, 95 %). RMN 1H (500 MHz, DMSO-da) 8 8,80 (d, J 1,2 Hz, 2H), 8,22 (d, J 7,5 Hz, 1 H), 7,64 (d, J 11 ,7 Hz, 1H), 7,46 - 7 ,13 (m, 3H), 7 ,10 (t, J 7,2 Hz, 1H), 6,65 (d, J 6,4 Hz, 1H), 4,88 (dd, J 8,8, 3,5 Hz, 1H), 3 ,14 (dc, J 14,2, 8,8, 7,2 Hz, 1H), 3,02 - 2 ,77 (m, 3H), 2,28 (tt, J 8,3, 4,1 Hz, 1H), 2 ,11 - 1,97 (m, 4H), 1,46 (s, 2H), 1,13 (s, 1H). CLEM (EN+) TR 1,23 min, 521,0 (M+H)+.
E j e m p l o 172
(1R,3R)-1-[2-(Difluorometoxi)fenil1-6-fluoro-7-[2-(1-hidroxiciclopropil)pirimidin-5-il1-2,3-dihidro-1H-c¡clopenta[4.51¡m¡dazo[1,2-a1p¡r¡d¡n-3-ol
El co m p u e s to d e l títu lo s e preparó a partir del E je m p lo 16 (100 mg, 0,21 mmol) en dioxano (4 ml), el In te rm e d io 103 (147 mg, 0,33 mmol), carbonato sódico 2 M (310 pl) y bis[3-(difenilfosfanil)ciclopenta-2,4-dien-1-il]hierro; diclorometano; dicloropaladio (17 mg, 0,02 mmol), seguido de fluoruro de W,W,W-tributilbutan-1-aminio 1 M (3 ml) de acuerdo con el M étod o K (7,6 mg, 7 %). RMN 1H (500 MHz, CDCla) 8 ppm 8,68 (d, J 1,4 Hz, 2H), 7,66 (d, J 7,1 Hz, 1H), 7,42 (d, J 10,9 Hz, 1H), 7,29 (d, J 6,9 Hz, 1H), 7,23 (dd, J 7,7, 1,6 Hz, 1H), 7,20 - 7 ,13 (m, 2H), 6,67 (dd, J 74,7, 72 ,7 Hz, 1H), 5,43 (dd, J 7,2, 2,9 Hz, 1H), 4,89 (dd, J 8,4, 3,8 Hz, 1H), 4,27 (s, 1H), 3,66 - 3,55 (m, 1H), 3,33 (s, 1H), 2,43 (dt, J 14,2, 3,4 Hz, 1H), 1,50 - 1,40 (m, 4H). CLEM (EN+) TR 1,30 min, 469,0 (M+H)+.
E j e m p l o 173
(1S.3S)-1-[2-(D¡fluorometox¡)-4.5-d¡fluorofen¡l1-6-fluoro-7-[2-(3-h¡drox¡-3-met¡lazet¡d¡n-1-¡l)p¡r¡m¡d¡n-5-¡l1-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ol
El c o m p u e s to d e l títu lo se preparó a partir del In te rm e d io 121 (200 mg, 0,45 mmol) en dioxano (4 ml), el In te rm e d io 138 (142,6 mg, 0,49 mmol), carbonato sódico 2 M (668 pl) y bis[3-(difenilfosfanil)ciclopenta-2,4-dien-1-il]hierro; diclorometano; dicloropaladio (18,18 mg, 0,02 mmol) por el M étod o A. La mezcla racémica s e separó por S F C quiral
(90 % de heptano: 10 % de etanol en una columna ChiralPak AD) para proporcionar el compuesto del título en forma de un sólido de color beige (65 mg, 27 %). RMN 1H (500 MHz, Metanol-d4) 8 8,40 (d, J 1,3 Hz, 2H), 7,92 (d, J 7,2 Hz, 1H), 7,42 (d, J 11,0 Hz, 1H), 7 ,27 (dd, J 10,9, 6,8 Hz, 1H), 7,08 (dd, J 11,2, 8,8 Hz, 1H), 7,00 (t, J 73,3 Hz, 1H), 5,25 (dd, J 7,1, 2,8 Hz, 1H), 4,88 - 4,85 (m, 1H), 4,09 - 3,97 (m, 4H), 3,66 - 3,50 (m, 1H), 2,23 (dt, J 14,0, 3,2 Hz, 1H), 1,54 (s, 3H), 1,29 (s, 1H). CLEM (EN+) TR 1,47 min, 534,0 (M+H)+.
E j e m p l o 174
(1R.3R)-1-[2-(D¡fluorometox¡)-4.5-d¡fluorofen¡l1-6-fluoro-7-[2-(3-h¡drox¡-3-met¡lazet¡d¡n-1-¡l)p¡r¡m¡d¡n-5-¡l1-2.3-d¡h¡dro-1H-ciclopenta[4,51imidazo[1,2-a1piridin-3-ol
El compuesto del título se preparó a partir del Intermedio 121 (200 mg, 0,45 mmol) en dioxano (4 ml), el Intermedio 138 (142,6 mg, 0,49 mmol), carbonato sódico 2 M (668 pl) y b¡s[3-(d¡fen¡lfosfan¡l)c¡clopenta-2,4-d¡en-1-¡l]h¡erro; diclorometano; dicloropaladio (18,18 mg, 0,02 mmol) por el Método A. La mezcla racémica s e separó por S F C quiral (90 % de heptano: 10 % de etanol en una columna ChiralPak AD) para proporcionar el compuesto del título en forma de un sólido de color beige (67 mg, 28 %). RMN 1H (500 MHz, Metanol-d4) 8 8,41 (d, J 1,3 Hz, 2H), 7,92 (d, J 7,2 Hz, 1H), 7,43 (d, J 11,0 Hz, 1H), 7,28 (dd, J 10,9, 6,8 Hz, 1H), 7,08 (dd, J 11,2, 8,8 Hz, 1H), 7,01 (t, J 73,3 Hz, 1H), 5,25 (dd, J 7,1, 2,8 Hz, 1H), 4,89 - 4,86 (m, 1H), 4,09 - 3,99 (m, 4H), 3,63 - 3,53 (m, 1H), 2,24 (dt, J 14,0, 3,2 Hz, 1H), 1,54 (s, 3H), 1,30 (s, 1H). CLEM (EN+) TR 1,46 min, 534,0 (M+H)+.
E j e m p l o 175
(1R.3R)-1-[2-(D¡fluorometox¡)-5-fluorofen¡l1-6-fluoro-7-[2-(3-h¡drox¡-3-met¡lazet¡d¡n-1-¡l)p¡r¡m¡d¡n-5-¡l1-2,3-d¡h¡dro-1H-c¡clopenta[4,51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ol
El compuesto del título se preparó a partir del Intermedio 115 (180 mg, 0,42 mmol) en dioxano (4 ml), el Intermedio 138 (133,7 mg, 0,46 mmol), carbonato sódico 2 M (626 pl) y bis[3-(difenilfosfanil)ciclopenta-2,4-dien-1-il1hierro; diclorometano; dicloropaladio (17,05 mg, 0,02 mmol) por el Método A. La mezcla racémica s e separó por S F C quiral (65 % de CÜ2:35 % de metanol en una columna Chiralpak IC), produciendo el compuesto del título en forma de un sólido de color pardo claro (25 mg, 12 %). RMN 1H (500 MHz, Metanol-d4) 8 8,38 (d, J 1,2 Hz, 2H), 7,89 (d, J 7,2 Hz, 1H), 7,42 (d, J 11,0 Hz, 1H), 7,28 (dd, J 9,0, 4,6 Hz, 1H), 7,04 (td, J 8,9, 8,4, 3,1 Hz, 1H), 6,95 (t, J 73,8 Hz, 1H), 6,89 (dd, J 9,2, 3,1 Hz, 1H), 5,26 (dd, J 7,2, 3,0 Hz, 1H), 4,91-4,87 (m, 1H), 4,58 (s, 1H), 4,09 - 3,97 (m, 4H), 3,64 - 3,52 (m, 1H), 2,25 (dt, J 14,0, 3,4 Hz, 1H), 1,53 (s, 3H). CLEM (EN+) TR 1,25 min, 516,0 (M+H)+.
E j e m p l o 176
(1R.3R)-1-[2-(D¡fluorometox¡)-4-fluorofen¡l1-6-fluoro-7-[2-(3-h¡drox¡-3-met¡lazet¡d¡n-1-¡l)p¡r¡m¡d¡n-5-¡l1-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1,2-a1p¡r¡d¡n-3-ol
El c o m p u e s to d e l títu lo se preparó a part¡r del In te rm e d io 109 (165 mg, 0.38 mmol) en d¡oxano (4 ml), el In te rm e d io 138 (122,56 mg. 0.42 mmol). carbonato sód¡co 2 M (574,01 pl) y b¡s[3-(d¡fen¡lfosfan¡l)c¡clopenta-2,4-d¡en-1-¡l]h¡erro; d¡clorometano; d¡cloropalad¡o (15,63 mg. 0.02 mmol) por el M étod o A. La mezcla racém¡ca se separó por SFC qu¡ral (65 % de CÜ2:35 % de metanol en una columna Ch¡ralpak IC). produc¡endo el c o m p u e s to de l títu lo en forma de un sól¡do de color pardo claro (60 mg. 30 %). RMN 1H (500 MHz, Metanol-d4) 88.38 (d, J 1.1 Hz. 2H). 7.87 (d, J 7.2 Hz.
1H). 7,42 (d, J 11,0 Hz. 1H). 7,21 - 6,86 (m. 4H). 5,26 (dd. J 7.2. 3.3 Hz. 1H). 4,85 - 4,83 (m. 2H). 4.59 (s. 1H). 4,10 -3.94 (m. 4H). 3,66 - 3,51 (m. 1H). 2,21 (dt. J 13.9. 3.7 Hz. 1H). 1,53 (s. 3H). CLEM (EN+) TR 1,26 m¡n, 516,0 (M+H)+.
E j e m p l o 177
(1S.3S)-1-[2-(D¡fluorometox¡)-4-fluorofen¡l1-6-fluoro-7-[2-(3-h¡drox¡-3-met¡lazet¡d¡n-1-¡l)p¡r¡m¡d¡n-5-¡l1-2,3-d¡h¡dro-1H-c¡clopenta[4,51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ol
El c o m p u e s to d e l títu lo se preparó a part¡r del In te rm e d io 109 (165 mg. 0,38 mmol) en d¡oxano (4 ml). el In te rm e d io 138 (122,56 mg. 0,42 mmol). carbonato sód¡co 2 M (574,01 pl) y b¡s[3-(d¡fen¡lfosfan¡l)c¡clopenta-2,4-d¡en-1-¡l1h¡erro; d¡clorometano; d¡cloropalad¡o (15,63 mg. 0,02 mmol) por el M étod o A. La mezcla racém¡ca se separó por SFC qu¡ral (65 % de CÜ2:35 % de metanol en una columna Ch¡ralpak IC). produc¡endo el c o m p u e s to de l títu lo en forma de un sól¡do de color pardo claro (63 mg. 31 %). RMN 1H (500 MHz. Metanol-d4) 88,40 (d. J 1.0 Hz. 2H). 7.89 (d. J 7.2 Hz.
1H). 7,46 (d. J 11,0 Hz. 1H). 7,24 - 6,86 (m. 4H). 5,28 (dd. J 7.2. 3.3 Hz. 1H). 4,86 - 4,84 (m. 2H). 4,60 (s. 1H). 4,10 -3,97 (m. 4H). 3,68 - 3,53 (m. 1H). 2,23 (dt. J 13,9, 3.7 Hz. 1H). 1,55 (s. 3H). CLEM (EN+) TR 1,26 m¡n, 516,0 (M+H)+.
E j e m p l o 178
(1S.3S)-1-[2-(D¡fluorometox¡)-5-fluorofen¡l1-6-fluoro-7-[2-(3-h¡drox¡-3-met¡lazet¡d¡n-1-¡l)p¡r¡m¡d¡n-5-¡l1-2,3-d¡h¡dro-1H-c¡clopenta[4,51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ol
El compuesto del título se preparó a partir del Intermedio 115 (180 mg, 0,42 mmol) en dioxano (4 ml), el Intermedio 138 (133,7 mg, 0,46 mmol), carbonato sódico 2 M (626 j l) y bis[3-(difenilfosfanil)ciclopenta-2,4-dien-1-il]hierro; diclorometano; dicloropaladio (17,05 mg, 0,02 mmol) por el Método A. La mezcla racémica s e separó por S F C quiral (65 % de CÜ2:35 % de metanol en una columna Chiralpak IC), produciendo el compuesto del título en forma de un sólido de color pardo claro (21 mg, 10 %). RMN 1H (500 MHz, Metanol-d4) 8 8,44-8,33 (m, 2H), 7,89 (d, J 7,2 Hz, 1H), 7,43 (d, J 11,0 Hz, 1H), 7,28 (dd, J 9,0, 4,6 Hz, 1H), 7,04 (td, J 8,9, 8,4, 3,1 Hz, 1H), 6,95 (t, J 73,8 Hz, 1H), 6,89 (dd, J 9,2, 3,1 Hz, 1 H), 5,26 (dd, J 7,2, 3,0 Hz, 1H), 4,90-4,87 (m, 1H), 4,58 (s, 1H), 4,08 - 3,96 (m, 4H), 3,59 (dt, J 14,2, 8,1 Hz, 1H), 2,25 (dt, J 14,0, 3,4 Hz, 1H), 1,53 (s, 3H). CLEM (EN+) TR 1,25 min, 516,0 (M+H)+.
E j e m p l o 179
(1R,3S)-1-[2-(Difluorometoxi)fenil1-6-fluoro-7-{2-[3-hidroxi-3-(trifluorometil)azetidin-1-il1pirimidin-5-il}-3-metil-2,3-d¡h¡dro-1H-c¡clopenta[4,51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ol
El compuesto del título s e preparó a partir del Ejemplo 20 (200 mg, 0,47 mmol), el Intermedio 140 (178 mg, 0,52 mmol), carbonato sódico 2 M (0,70 ml), dioxano (4 ml), aducto de dicloro[1,1'-b¡s(d¡fen¡lfosf¡noferroceno]-palad¡o diclorometano (38 mg, 0,05 mmol) por el Método A. Seguido de HPLC preparativa quiral (85 % de CÜ2:15 % de metanol en una columna Chiralpak iC), produciendo el compuesto del título en forma de un sólido de color pardo pálido (28,0 mg, 21 %). RMN 1H (500 MHz, CDCla) 8 8,19 (s, 2H), 7,36 - 7 ,27 (m, 2H), 7,25 - 7 ,16 (m, 2H), 7 ,12 (t, J 7,4 Hz, 1H), 6,86 (d, J 7,4 Hz, 1H), 6,63 (t, J 73,4 Hz, 1H), 5,38 (s, 1H), 5 ,11 (t, J 6,6 Hz, 1H), 4,40 (t, J 9,3 Hz, 2H), 4,08 (dd, J 18,2, 10,1 Hz, 2H), 3,32 (dd, J 13,7, 7,9 Hz, 1H), 3,03 (s, 1H), 2,50 (dd, J 13,7, 5,5 Hz, 1H), 1,81 (s, 3H). CLEM (EN+) TR 1,40 min, 566,0 (M+H)+.
E j e m p l o 180
(1R.3R)-1-[2-(D¡fluorometox¡)fen¡l1-6-fluoro-7-[2-(3-h¡drox¡-3-met¡lazet¡d¡n-1-¡l)p¡r¡m¡d¡n-5-¡l1-3-met¡l-2.3-d¡h¡dro-1H-ciclopenta[4,51imidazo[1,2-a]piridin-3-ol
El c o m p u e s to de l títu lo s e preparó a partir del E je m p lo 20 (200 mg, 0,47 mmol), el In te rm e d io 138 (158 mg, 0,53 mmol), carbonato sódico 2 M (0,70 ml), dioxano (4 ml), aducto de dicloro[1,1'-bis(difenilfosfinoferroceno1-paladio diclorometano (38 mg, 0,05 mmol) por el M étod o A. Seguido de HPLC preparativa quiral (85 % de CO2:15 % de metanol en una columna Chiralpak iC), produciendo el co m p u e s to de l títu lo en forma de un sólido de color pardo pálido (20,0 mg, 13 %). RMN 1H (500 MHz, CDCla) 8 8,24 (s, 2H), 7 ,47 (d, J 7,2 Hz, 1H), 7,28 (dd, J 5,6, 2,8 Hz, 2H), 7,21 -7 ,16 (m, 2H), 7 ,13 (t, J 7,4 Hz, 1H), 6,65 (dd, J 74,5, 72,8 Hz, 1H), 4,86 (dd, J 8,4, 4,0 Hz, 1H), 4 ,12 - 4,05 (m, 2H), 4,05 - 3,94 (m, 2H), 3,31 - 3,24 (m, 1H), 3,09 (d, J 23,8 Hz, 2H), 2,64 (dd, J 13,8, 4,0 Hz, 1H), 1,78 (s, 3H), 1,61 (s, 3H). CLEM (EN+) TR 1,27 min, 512,0 (M+H)+.
E j e m p l o 181
(1R.3R)-1-[2-(Difluorometoxi)fenil1-7-{2-[1-(metilsulfonil)piperidin-4-il1pirimidin-5-il}-2.3-dihidro-1H-ciclopenta[4,51imidazo[1.2-a1piridin-3-ol
A una solución del E je m p lo 134 (87 mg, 0,16 mmol) en DMF (2 ml) s e añadió W,W-dietiletanamina (105 pl, 0,75 mmol) y s e agitó durante 5 minutos, s e añadió metanosulfonato de metanosulfonilo (142 mg, 0,82 mmol) y s e calentó a 60 °C durante 18 horas. La m ezcla de reacción s e enfrió a t.a., con refrigeración adicional en un baño de hielo, s e diluyó con a gua (20 ml) y s e extrajo con EtOAc (25 ml), DCM (25 ml) y 1:1 de IPA/cloroformo (2 x 25 ml). Los extractos orgánicos se secaron sobre sulfato sódico y se concentraron al vacío. El residuo en bruto s e purificó por HPLC preparativa, produciendo el co m p u e s to d e l títu lo en forma de un sólido de color blanquecino (3 mg, 3 %). RMN 1H (500 MHz, DMSO-d6) 8 ppm 8,99 (s, 2H), 8,26 (s, 1H), 7 ,79 - 7,71 (m, 1H), 7,66 (dd, J 9,5, 1,8 Hz, 1H), 7 ,55 - 7,20 (m, 3H), 7 , 17 - 7,09 (m, 1 H), 6,91 (dd, J 7,7, 1,5 Hz, 1H), 5,51 (d, J 5,0 Hz, 1H), 5 ,19 - 5,09 (m, 1H), 4,78 (dd, J 8,5, 3,8 Hz, 1H), 3,70 - 3,59 (m, 2H), 3,53 - 3,41 (m, 1H), 3,00 (ddt, J 11,3 , 7,1, 3,6 Hz, 1H), 2,94 - 2,84 (m, 5H), 2 ,15 - 2,03 (m, 3H), 1,81 (cd, J 12,7, 4,2 Hz, 2H). CLEM (EN+) TR 1,30 min, 556,0 (M+H)+.
E j e m p l o 182
(1R,3R)-1-[2-(Difluorometoxi)fenil1-6-fluoro-7-(2-[3-hidroxi-3-(trifluorometil)azetidin-1-il1pinmidin-5-il}-3-metil-2,3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ol
El compuesto del título s e preparó a partir del Ejemplo 20 (200 mg, 0,47 mmol), el Intermedio 140 (178 mg, 0,52 mmol), carbonato sódico 2 M (0,70 ml), dioxano (4 ml), aducto de dicloro[1,1'-bis(difenilfosfinoferroceno1-paladio diclorometano (38 mg, 0,05 mmol) por el Método A. Seguido de HPLC preparativa quiral (85 % de CO2:15 % de metanol en una columna Chiralpak IC), produciendo el compuesto del título en forma de un sólido de color pardo pálido (28,0 mg, 21 %). RMN 1H (500 MHz, C D C b ) 8 8,20 (s, 2H), 7 ,47 (d, J 7,1 Hz, 1H), 7,30 - 7,26 (m, 1H), 7,23 - 7 , 17 (m, 3H), 7 ,13 (t, J 7,5 Hz, 1H), 6,66 (dd, J 74,5, 72,7 Hz, 1H), 5,58 (s, 1H), 4,87 (dd, J 8,4, 4,1 Hz, 1H), 4,44 (d, J 10,2 Hz, 1H), 4,38 (d, J 10,0 Hz, 1H), 4 ,13 - 4,09 (m, 1H), 4,04 (d, J 10,4 Hz, 1H), 3,29 (dd, J 13,8, 8,5 Hz, 1H), 3,05 (s, 1H), 2,65 (dd, J 13,8, 4,1 Hz, 1H), 1,79 (s, 3H). CLEM (EN+) TR 1,41 min, 566,0 (M+H)+.
E j e m p l o 183
(1R.3R)-7-[2-(3.3-D¡fluoro-1-h¡drox¡c¡clobut¡l)p¡r¡m¡d¡n-5-¡l1-1-[2-(d¡fluorometox¡)fen¡l1-6-fluoro-2,3-d¡h¡dro-1H-ciclopenta[4,51imidazo[1.2-a1piridin-3-ol
El compuesto del título s e preparó a partir del Ejemplo 16 (120 mg, 0,25 mmol), el Intermedio 143 (104 mg, 0,27 mmol), carbonato sódico 2 M (0,37 ml, 0,741 mmol), dioxano (6 ml), Pd(dppf)Cl2 complejo con diclorometano (20,0 mg, 0,025 mmol) y posteriormente una solución 1 M de fluoruro de tetrabutilamonio en t Hf (0,741 ml, 0,741 mmol) por el Método K, produciendo el compuesto del título en forma de un sólido de color blanco (8 mg, 6 %). RMN 1H (500 MHz, CDCla) 8 8,81 (d, J 1,4 Hz, 2H), 7,70 (d, J 7,1 Hz, 1H), 7,45 (d, J 11,0 Hz, 1H), 7,33 - 7 ,27 (m, 1H), 7,24 (dd, J 7,9, 1,8 Hz, 1H), 7,21 - 7 ,14 (m, 2H), 6,67 (dd, J 74,8, 72,6 Hz, 1H), 5,43 (dd, J 6,9, 3,5 Hz, 1H), 4,95 (s, 1H), 4,89 (dd, J 8,5, 3,8 Hz, 1 H), 3,69 - 3,53 (m, 1H), 3,40 (td, J 14,4, 11 ,3 Hz, 2H), 3 ,13 - 2,92 (m, 3H), 2,43 (dt, J 14,2, 3,4 Hz, 1H). CLEM (EN+) TR 1,41 min, 519,0 (M+H)+.
E j e m p l o 184
1-(5-{(1R,3R)-1-[2-(Difluorometoxi)fenil1-6-fluoro-3-hidroxi-2,3-dihidro-1H-ciclopenta[4,51imidazo[1,2-a1piridin-7-il}pirimidin-2-il)-3-metilciclobutano-1,3-diol
El co m p u e s to de l títu lo se preparó a partir del E je m p lo 16 (263 mg, 0,64 mmol), 1,4-dioxano (8 ml), el In te rm e d io 165 (368 mg, 0,7 mmol), K2 CO32 M en agua (950 j l) y PdCb .dppf (53 mg, 0,06 mmol), seguido de TBAF 1 M en THF (5,09 ml) por el M étod o K (7,1 mg, 2,1 %). CLEM (EN+) TR 1,21 min, 513,0 (M+H)+.
E j e m p l o 185
1-(5-((1R)-1-r2-(Difluorometoxi)fenil1-6-fluoro-3-hidroxi-3-metil-2,3-dihidro-1H-ciclopentar4,51imidazoH,2-a1pindin-7-il}pirimidin-2-il)-3-metilciclobutano-1,3-diol
El In te rm e d io 144 (0,48 g, 0,76 mmol) se disolvió en THF anhidro (10 ml) en una atmósfera de N2 (g) y se trató con TBAF 1 M en THF (1,51 ml). La mezcla de reacción se agitó a t.a. durante 18 h y se diluyó con EtOAc (30 ml), se lavó con agua (3 x 25 ml) y salmuera (25 ml) y se pasó sobre un separador de fases hidrófobo Biotage de 50 ml. El filtrado se concentró al vacío y el residuo se purificó por cromatografía (C18, MeCN al 0-25 % en H2 O con ácido fórmico al 0,1 %), produciendo el c o m p u e s to de l títu lo en forma de un sólido cristalino de color amarillo (0,315 g, 80 %). CLEM (EN+) TR 1,30 min, 527,0 (M+H)+.
E j e m p l o 186 , M É T O D O Q
(1R,3R)-7-Bromo-1-r2-(difluorometoxi)fenil1-6-fluoro-3-(pindin-3-ilmetoxi)-2,3-dihidro-1H-ciclopentar4,51imidazor1,2-alpiridina
Se añadió hidruro sódico, dispersión al 60 % en aceite mineral (77,44 mg, 1,936 mmol) a una solución del E je m p lo 16 (A, 400 mg, 0,9681 mmol) en THF (10 ml) a -78 °C. Se añadió bromhidrato de 3-(bromometil)piridina (302,9 mg, 1,162 mmol) y la reacción se dejó calentar a t.a. durante 18 h. La mezcla de reacción se trató con agua (10 ml) y se
repartió con DCM (20 ml), los materiales orgánicos s e extrajeron y s e secaron sobre MgSO4, y se concentraron al vacío. El residuo s e purificó por cromatografía (SiO 2 , EtOAc al 0-100 % en hexano), produciendo el co m p u e s to de l títu lo en forma de un sólido de color amarillo (171 mg, 35 %). RMN 1H (400 MHz, DMSO-da) 8 8,49 (m, 2H), 8,39 (d, J 6,9 Hz, 1H), 7,78 (d, J 10,0 Hz, 1H), 7,69 (dt, J 7,8, 1,8 Hz, 1H), 7,33 (m, 3H), 7,25 (m, 1H), 7 ,11 (m, 1H), 6,80 (dd, J 7 ,7 Hz, 1,6 Hz, 1H), 5,02 (m, 1H), 4,79 (m, 3H), 4,79 (dd, J 8,7 Hz, 3,1 Hz, 1H), 3,47 (m, 1H). CLEM (EN+) TR 1,55 min, 504,0/506,0 (M+H)+.
E j e m p l o 187
-Bromo-1-r5-cloro-2-(d¡fluorometox¡)fen¡l1-1.2-d¡h¡dro-3H-c¡clopentar4.51¡m¡dazon.2-a1p¡r¡d¡n-3-ona
El co m p u e s to d e l títu lo s e preparó a partir del In te rm e d io 148 (31,1 g, 62,2 mmol), dioxano (200 ml) y a gua (200 ml) por el M étod o M (28,3 g, 91 %). RMN 1H (DMSO-d6) 8 8,38 (s, 1H), 7,73 (m, 1H), 7,56 (dd, J 9,8, 1,8 Hz, 1H), 7,44 (m, 1H), 7,28 (d, J 8,7 Hz, 1H), 7,20 (t, J 73,7, Hz, 1H), 7,09 (s, 1H), 5 ,11 (dd, J 7,0, 1,9 Hz, 1H), 3 ,57 (m, 1H), 2,81 (dd, J 18,2, 2,1 Hz, 1H). CLEM (EN+) TR 1,49 min, 427,0/429,0 (M+H)+.
E j e m p l o s 188 y 189
(1S)-7-Bromo-1-r5-cloro-2-(difluorometoxi)fenil1-1,2-dihidro-3H-ciclopentar4,51imidazor1,2-a1piridin-3-ona y (1R)-7-bromo-1-r5-cloro-2-(difluorometoxi)fenil1-1,2-dihidro-3H-ciclopentar4,51imidazor1,2-a1piridin-3-ona
Los co m p u e s to s d e l títu lo s e aislaron mediante purificación del E je m p lo 187 en condiciones de CL en un Lux-Cell-4 (76 x 265 mm x mm, flujo 200 ml/min, 30 °C, 100 % de MeOH, inyección de 27 ml de solución a una concentración de 10 g/l).
El primer enantiómero en eluirse (TR 10 min) s e recogió y las fracciones s e evaporaron para producir el (e n a n tió m e ro 1) (E je m p lo 188). RMN 1H (DMSO-d6) 8: 8,38 (d, J 0,9 Hz, 1H), 7,73 (dd, J 9,8 Hz, 0,6 Hz, 1H), 7,56 (dd, J 9,8 Hz, 1,9 Hz, 1H), 7 ,47 (dd, J 8,8 Hz, 2,6 Hz, 1H), 7,28 (d, J 8,7 Hz, 1H), 7,20 (t, J 73,5 Hz), 5 ,10 (dd, J 7,1 Hz, 2,1 Hz, 1H), 4,33 (d, J 4,2 Hz, 0H), 3 ,57 (dd, J 18,2 Hz, 7,2 Hz, 1H), 2,81 (dd, J 18,2 Hz, 2,2 Hz, 1H), 1,04 (d, J 6,1 Hz, 2H). CLEM (EN+) TR 1,49 min, 427,0/429,0 (M+H)+.
El segun do enantiómero en eluirse (TR 14 min) s e recogió y las fracciones s e evaporaron para producir el (e n a n tió m e ro 2) (E je m p lo 189). RMN 1H (DMSO-d6) 8: 8,38 (d, J 0,9 Hz, 1H), 7,73 (dd, J 9,8 Hz, 0,6 Hz, 1H), 7,56 (dd, J 9,8 Hz,
1,9 Hz, 1H), 7 ,47 (dd, J 8 ,8 Hz, 2,6 Hz, 1H), 7,28 (d, J 8 ,7 Hz, 1H), 7,20 (t, J 73,5 Hz), 5 ,10 (dd, J 7,1 Hz, 2,1 Hz, 1H), 4,33 (d, J 4,2 Hz, 0H), 3 ,57 (dd, J 18,2 Hz, 7,2 Hz, 1H), 2,81 (dd, J 18,2 Hz, 2,2 Hz, 1H), 1,04 (d, J 6,1 Hz, 2H); CLEM (EN+) TR 1,49 min, 427,0/429,0 (M+H)+.
E j e m p l o 190
(1R,3R)-7-Bromo-1-[5-cloro-2-(d¡fluorometox¡)fen¡l1-2,3-d¡h¡dro-1H-c¡clopenta[4,51¡m¡dazo[1,2-a1p¡r¡d¡n-3-ol
El co m p u e s to de l títu lo se preparó a partir del E je m p lo 189 (200 mg, 0,47 mmol), tr¡-sec-but¡lboroh¡druro de l¡t¡o 1 M en THF (0,51 ml) y THF (10 ml) por el M étod o B ( 118 mg, 59 %). CLEM (EN+) TR 1,46 m¡n, 429,0/431,0 (M+H)+. E j e m p l o 191
(1S,3S)-7-Bromo-1-r5-cloro-2-(d¡fluorometox¡)fen¡l1-2,3-d¡h¡dro-1H-c¡clopentar4,51¡m¡dazoH,2-a1p¡r¡d¡n-3-ol
El co m p u e s to de l títu lo se preparó a partir del E je m p lo 188 (250 mg, 0,58 mmol), tr¡-sec-but¡lboroh¡druro de l¡t¡o 1 M en THF (0,51 ml) y THF (10 ml) por el M étod o B (142 mg, 56,54 %). CLEM (EN+) TR 1,46 m¡n, 429,0/431,0 (M+H)+. E j e m p l o s 192 a 196
Los s¡gu¡entes Ejemplos se s¡ntet¡zaron de acuerdo con el Método Q a partir del mater¡al de part¡da dado y usando el bromuro de alquilo comerc¡al adecuado.
(continuación)
E j e m p l o 197
Ácido (((1R.3R)-7-bromo-1-r2-(d¡fluorometox¡)fen¡l1-6-fluoro-2.3-d¡h¡dro-1H-ciclopentar4.51¡m¡dazori.2-a1p¡r¡d¡n-3-¡l)ox¡}acét¡co
A una soluc¡ón del E je m p lo 196 (30 mg, 0.06 mmol) en THF (1 ml) se añad¡ó h¡dróx¡do sód¡co ac. 2 M (120 pl.
0.24 mmol) y la mezcla resultante se ag¡tó a t.a. durante 18 h. La reacc¡ón s e concentró al vacío. El res¡duo resultante s e d¡luyó con a gua (5 ml). se ac¡d¡f¡có med¡ante la ad¡c¡ón de una soluc¡ón ac. 2 M de ác¡do clorhídr¡co y s e extrajo con DCM (2 x 5 ml). Las c a p a s orgán¡cas comb¡nadas s e secaron sobre sulfato sód¡co y s e concentraron al vacío. produc¡endo el c o m p u e s to d e l títu lo en forma de un polvo blanquec¡no (26 mg. 90 %). RMN 1H (CDCb. 500 MHz) 8 7.86 (d. J 6.5 Hz. 1H). 7.71 (d. J 8.5 Hz. 1H). 7.32 (ddd. J 8.5. 7.0. 2.0 Hz. 1H). 7.24 - 7.17 (m. 3H). 6.70 (dd. J 74.5.
73.0 Hz. 1H). 5.37 (dd. J 7.0. 2.0 Hz. 1H). 4.85 (dd. J 8.5. 3.0 Hz. 1H). 4.53 (d. J 17.0 Hz. 1H). 4.36 (d. J 17.0 Hz. 1H).
3.62 - 3.52 (m. 1H). 2.53 (dt. J 14.5. 2.5 Hz. 1H). CLEM (EN+) TR 1.27 m¡n. 471.0/473.0 (M+H)+.
E j e m p l o s 198 a 200
Los s¡gu¡entes Ejemplos s e prepararon a part¡r del mater¡al de part¡da dado usando el éster de boronato o ác¡do borón¡co comerc¡al o s¡ntet¡zado adecuado. por el Método A.
(c o n t in u a c ió n )
E j e m p l o 201
Ácido (8-ant¡)-3-(5-((1R.3R)-1-r2-(d¡fluorometox¡)fen¡l1-6-fluoro-3-h¡drox¡-2.3-dih¡dro-1H-c¡clopentar4.51¡m¡dazor1.2-a1piridin-7-il}piriiTiidin-2-il)-3-azabiciclo[3.2.11octano-8-carboxílico
Los c o m p u e s to s d e l títu lo s e prepararon a partir del E je m p lo 169 (102 mg, 0,18 mmol), 1,4-dioxano (1 ml) e hidróxido potásico 1 M en a gu a (0,26 ml) por el M étod o I (82 mg, 78 %). CLEM (EN+) TR 1 ,13 min 566,0 (M+H)+.
E j e m p l o 202
(8-Anti)-3-(5-((1R)-1-r2-(difluoroiTietoxi)fenil1-6-fluoro-2,3-dihidro-1H-ciclopentar4,51iiTiidazor1,2-a1piridin-7-il}piriiTiidin-2-¡l)-3-azab¡c¡clo[3.2.11octano-8-carbox¡lato potásico
El co m p u e s to d e l títu lo s e preparó a partir del E je m p lo 198 (42 mg, 0,08 mmol), 1,4-dioxano (2 ml), hidróxido potásico 1 M (0,08 ml) por el M étod o I (38 mg, 78 %). CLEM (EN+) TR 1,25min 550,0 (M+H)+.
E j e m p l o 203
(8-Anti)-3-(5-{(1R,3R)-1-[2-(difluorometoxi)fenil1-6-fluoro-3-metoxi-2,3-dihidro-1H-ciclopenta[4,51imidazo[1,2-a1piridin-7-il}pinmidin-2-il)-3-azabiciclo[3.2.11octano-8-carboxilato de metilo
El c o m p u e s to d e l títu lo s e preparó a partir del In te rm e d io 166 (341 mg, 0,78 mmol), 1,4-dioxano (3 ml), ácido 2{2-[(1R,5S,8R)-8-(metoxicarbonil)-3-azabiciclo[3.2.11octan-3-il1pirimidin-5-il}borónico (341 mg, 1 , 17 mmol), carbonato sódico 2 M en a g u a ( 1,17 ml), b¡s[3-(d¡fen¡lfosfan¡l)ciclopenta-2,4-d¡en-1-¡l]h¡erro; diclorometano; dicloropaladio (128 mg, 0,16 mmol) por el M étod o A (70 mg, 17 %). CLEM (EN+) TR 1,71m in 580,0 (M+H)+.
E j e m p l o 204
ácido__________ potasio_________ (8-anti)-3-(5-{(1R,3R)-1-[2-(difluorometoxi)fenil1-6-fluoro-3-metoxi-2,3-dihidro-1H-c¡clopenta[4.5l¡m¡dazo[1.2-alp¡r¡d¡n-7-¡l}p¡r¡m¡d¡n-2-¡l)-3-azab¡c¡clo[3.2.1loctano-8-carboxíl¡co
El co m p u e s to d e l títu lo s e preparó a partir del E je m p lo 203 (85 mg, 0,14 mmol), THF (1 ml), hidróxido potásico 1 M en a gu a (0,18 ml) por el M étod o I (66 mg, 74 %). CLEM (EN+) TR 1,25 min, 580,0 (M+H)+.
E j e m p l o s 205 y 206
(1R.3R)-1-r2-(d¡fluorometox¡)-4.5-d¡fluorofen¡l1-6-fluoro-7-r2-(2-h¡drox¡propan-2-¡l)p¡r¡m¡d¡n-5-¡l1-2.3-d¡h¡dro-1H-c¡clopentar4.51im¡dazori.2-a1p¡r¡d¡n-3-ol______ y______ (1S.3S)-1-r2-(d¡fluorometox¡)-4.5-d¡fluorofen¡l1-6-fluoro-7-r2-(2-h¡drox¡propan-2-¡l)p¡r¡m¡d¡n-5-¡l1-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ol
El E je m p lo 199 (123 mg. 0.24 mmol) s e purifico ad¡c¡onalmente por S F C qu¡ral (25 % de metanol: 75 % de C O 2 con una Ch¡ralpak IC de 25 cm) para proporc¡onar el E je m p lo 205 en forma de un sól¡do de color blanquec¡no (42 mg.
27 %). RMN 1H (500 MHz. DMSO-d6) 8 8.92 (d. J 1.4 Hz. 2H). 8.29 (d. J 7.4 Hz. 1H). 7.71 (d. J 11.6 Hz. 1H). 7.49 (dd. J 11.2. 6.8 Hz. 1H). 7.26 (t. J 73.5 Hz. 1H). 6.97 (dd. J 11.3. 9.0 Hz. 1H). 5.60 (d. J 5.4Hz. 1H). 5.15 (s. 1H). 5.12 - 5.04 (m. 1 H). 4.71 (dd. J 8.5. 3.1 Hz. 1H). 3.47 - 3.38 (m. 1H). 2.05 (dt. J 13.7. 3.1 Hz. 1H). 1.51 (s. 6H). Método S F C (25 % de metanol: 75 % de C O 2 con una Ch¡ralpak IC de 25 cm); CLEM (EN+) TR 4.33 m¡n. 507.0 (M+H)+. La S F C qu¡ral tamb¡én produjo el E je m p lo 206 en forma de un sól¡do de color pardo claro (34 mg. 22 %). RMN 1H (500 MHz. DMSO-d6) 8 8.92 (d. J 1.3 Hz. 2H). 8.29 (d. J 7.4 Hz. 1H). 7.71 (d. J 11.6 Hz. 1H). 7.53 - 7.45 (m. 1H). 7.26 (t. J 73.5 Hz. 1H).
6.97 (dd. J 11.3. 9.0 Hz. 1H). 5.60 (s. 1H). 5.15 (s. 1H). 5.08 (dd. J 6.8. 2.2 Hz. 1H). 4.71 (dd. J 8.5. 2.9 Hz. 1H). 3.46 - 3.40 (m. 1 H). 2.05 (dt. J 13.7. 3.0 Hz. 1H). 1.51 (s. 6H). Método S F C (25 % de metanol: 75 % de C O 2 con una Ch¡ralpak IC de 25 cm). CLEM (EN+) TR 8.28 m¡n. 507.0 (M+H)+.
E j e m p l o s 207 y 208
(1R.3R)-1-[2-(d¡fluorometox¡)-6-fluorofen¡l1-6-fluoro-7-[2-(2-h¡drox¡propan-2-¡l)p¡r¡m¡d¡n-5-¡l1-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ol y (1S.3S)-1-[2-(d¡fluorometox¡)-6-fluorofen¡l1-6-fluoro-7-[2-(2-h¡drox¡propan-2-¡l)p¡r¡m¡d¡n-5-¡l1-2.3-d¡h¡dro-1H-c¡clopentar4.51¡m¡dazoH.2-a1p¡r¡d¡n-3-ol
El E je m p lo 161 ( 119 mg. 0.24 mmol) s e pur¡f¡có ad¡c¡onalmente por S F C qu¡ral (85 % de CO2:15 % de metanol 0.1 % de DE A en una columna Ch¡ralpak IC). produc¡endo el E je m p lo 207 en forma de un sól¡do de color blanquec¡no (35 mg.
21 % ) y el E je m p lo 208 en forma de un sól¡do de color blanquec¡no (30 mg. 18 %). Método de S F C (85 % de c 02:15 % de metanol 0.1 % de DEA en una columna Ch¡ralpak IC); CLEM (EN+) TR 21.00 m¡n. 489.0 (M+H)+ y CLEM (EN+) T R 27.09 m¡n. 489.0 (M+H)+. respectivamente.
E j e m p l o s 209 y 210
Isómero A: (1R.3R)-1-r2-(d¡fluorometox¡)fen¡l1-6-fluoro-7-r2-(trans-4-h¡drox¡-4-met¡lc¡clohex¡l)p¡r¡m¡d¡n-5-¡l1-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ol. Isómero B: (1R.3R)-1-[2-(d¡fluorometox¡)fen¡l1-6-fluoro-7-[2-(c/s-4-h¡drox¡-4-met¡lc¡clohex¡l)p¡r¡m¡d¡n-5-¡l1-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ol
A una solución agitada del In te rm e d io 157 (43 mg, 0,09 mmol) en tetrahidrofurano anhidro (2 ml) s e añadió bromuro de metilmagnesio 1,4 M en tolueno/THF (0,21 ml, 0,30 mmol) a t.a. La m ezcla s e agitó a t.a. durante 18 h. S e añadió m ás cantidad de bromuro de metilmagnesio 1,4 M en tolueno/THF (0,21 ml, 0,30 mmol) a la m ezcla a t.a. y s e agitó durante 2 h. La m ezcla s e inactivó con cloruro de amonio saturado (0,5 ml) y s e repartió entre EtOAc (10 ml) y a gua (5 ml). La capa a cu o sa s e extrajo de nuevo en EtOAc (10 ml). La capa orgánica combinada s e lavó con a gua (10 ml) y salmuera (10 ml), s e s e c ó (Na2SO4) y s e concentró al vacío. El residuo s e purificó por HPLC preparativa para proporcionar el E je m p lo 209 en forma de un sólido de color blanquecino (9 mg, 20 %) y el E je m p lo 210 en forma de un sólido de color blanquecino (41 mg, 30 %). CLEM (EN+) TR 1,28 min, 525,0 (M+H)+ y CLEM (EN+) TR 1,37 min, 525,0 (M+H)+, respectivamente.
E j e m p l o 211
Isómero B: trans-1-(5-((1R,3R)-1-[2-(difluorometoxi)fenil1-6-fluoro-3-hidroxi-2,3-dihidro-1H-ciclopenta[4,51imidazo[1,2-a1piridin-7-il}pirimidin-2-il)-4-metilciclohexano-1,4-diol
El co m p u e s to d e l títu lo s e preparó a partir del E je m p lo 16 120 mg, 0,25 mmol), el In te rm e d io 175 (132 mg, 0,30 mmol), una solución 2 M de carbonato sódico en a gua (0,37 ml, 0,74 mmol), 1,4-dioxano (2 ml), aducto de dicloro[1,1'-bis(d¡fen¡lfosf¡noferroceno]-paladio diclorometano (20 mg, 0,025 mmol) por el M étod o A. CLEM (EN+) TR 1,29 min, 541,0 (M+H)+.
E j e m p l o 212
Isómero A: cis-1-(5-((1R,3R)-1-[2-(difluorometoxi)fenil1-6-fluoro-3-hidroxi-2,3-dihidro-1H-ciclopenta[4,51imidazo[1,2-a1piridin-7-il}pirimidin-2-il)-4-metilciclohexano-1,4-diol
El co m p u e s to d e l títu lo s e preparó a partir del E je m p lo 16 120 mg, 0,25 mmol), el In te rm e d io 174 (132 mg, 0,30 mmol), una solución 2 M de carbonato sódico en a gua (0,37 ml, 0,74 mmol), 1,4-dioxano (2 ml), aducto de dicloro[1,1 ’-bis(difenilfosfinoferroceno]-paladio diclorometano (20 mg, 0,025 mmol) por el M étod o A (41 mg, 30 %). CLEM (EN+) T R 1,24 min, 541,0 (M+H)+.
E j e m p l o s 213 y 214
(IR ) -7-bromo-1-[5-cloro-2-(d¡fluorometox¡)fen¡l1-6-fluoro-1.2-d¡h¡dro-3H-c¡clopenta[4,51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ona y ( I S ) -7-bromo-1-[5-cloro-2-(d¡fluorometox¡)fen¡l1-6-fluoro-1.2-d¡h¡dro-3H-c¡clopenta[4,51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ona
Los co m p u e s to s d e l títu lo s e aislaron mediante purificación del In te rm e d io 135 en condiciones de S F C en una Chiralpak AD (50 x 216 mm x mm, flujo 360 ml/min, 40 °C, CO2/2-PrOH 75/25, inyección de 15 ml de solución a una concentración de 11,22 g/l).
El primer enantiómero en eluirse (TR 2,43 min) s e recogió y las fracciones s e evaporaron para producir el (e n a n tió m e ro 1) (16,26 g, 48,3 %, E je m p lo 213). RMN 1H (400 MHz, DMSO-d6) 8 8,63 (d, J 6,8 Hz, 1H), 7,88 (dd, J 9,8, 0,3 Hz, 1H), 7,46 (dd, J 8,8, 2,6 Hz, 1H), 7,28 (d, J 8,8 Hz, 1H), 7,20 (t, J 73 ,7 Hz, 1H), 7,08-7,12 (m, 1H), 5,08 (dd, J 7 ,1,2,1 Hz, 1H), 3 ,57 (dd, J 18,2, 7,2 Hz, 1H), 2,78 (dd, J 18,2, 2,2 Hz, 1H).
El segun do enantiómero en eluirse (TR 4,23 min) se recogió y las fracciones se evaporaron para producir el (e n a n tió m e ro 2) (15,61 g, 46,4 %, E je m p lo 214). RMN 1H (400 MHz, DMSO-d6) 8 8,63 (d, 1H, J 6,8 Hz), 7,88 (d, 1H, J 9,9 Hz), 7,46 (dd, 1H, J 8,8, 2,6 Hz), 7,28 (d, 1H, J 8,8 Hz), 7,20 (t, 1H, J 73,5 Hz), 7,08-7,13 (m, 1H), 5,08 (dd, 1H, J 7,0, 2,1 Hz), 3 ,57 (dd, 1H, J 18,2, 7,2 Hz), 2,78 (dd, 1H, J 18,1, 2,2 Hz).
E j e m p l o 215
Cis-1-(5-((1R,3R)-1-[5-cloro-2-(difluorometoxi)fenil1-3-hidroxi-2,3-dihidro-1H-ciclopenta[4,51imidazo[1,2-a1pindin-7-il}pirimidin-2-il)-3-metilciclobutano-1,3-diol
El co m p u e s to d e l títu lo s e preparó a partir del E je m p lo 190 y el In te rm e d io 165 por el M étod o K. CLEM (EN+) TR 1,19 min, 529,1 (M+H)+
E j e m p l o 216
Cis-1-(5-{(1R,3R)-1-[5-cloro-2-(difluorometoxi)fenil1-6-fluoro-3-hidroxi-2,3-dihidro-1H-ciclopenta[4,51imidazo[1,2-a1piridin-7-il}pinmidin-2-il)-3-metilciclobutano-1,3-diol
El co m p u e s to d e l títu lo s e preparó a partir del In te rm e d io 167 y el In te rm e d io 165 por el M étod o K. CLEM (EN+) TR 1,23 min, 547,2 (M+H)+
E j e m p l o 217 , M E T O D O R
(1R,3R)-1-[5-cloro-2-(d¡fluorometox¡)fen¡l1-7-[4-(met¡lsulfon¡l)fen¡l1-2,3-d¡h¡dro-1H-c¡clopenta[4,51¡m¡dazo[1,2-a1p¡r¡d¡n-3-ol
En un rec¡p¡ente de m¡croondas (20 ml), el E je m p lo 190 (150 mg, 0,349 mmol), carbonato sód¡co (151 mg, 1,40 mmol), ác¡do 4-(met¡lsulfon¡l)fen¡lborón¡co (143 mg, 0,698 mmol) y complejo de d¡cloruro de 1,1'-b¡s(d¡fen¡lfosf¡no)ferrocenopalad¡o (II) d¡clorometano (57 mg, 70 pmol) s e mezclaron con DME (12 ml) y a g u a (3 ml). D e s p u é s de calentar durante 10 m¡n a 100 °C y de enfr¡ar a t.a., s e añad¡ó a gua y la fase a cu o s a s e extrajo con DCM (3 x). Las fa s e s orgán¡cas comb¡nadas se secaron sobre sulfato sód¡co, se f¡ltraron y se concentraron al vacío. El res¡duo se pur¡f¡có por cromatografía (S¡O 2 , EtOH al 0-90 % en DCM) y s e pur¡f¡có ad¡c¡onalmente por HPLC preparat¡va de fase ¡nversa (M2b), produc¡endo el c o m p u e s to d e l títu lo (93 mg, 53 %). RMN 1H (400 MHz, DMSO-d6) 8 ppm 8,30 (dd, J 1,6 Hz, 0,9 Hz, 1H), 7,99 (m, 2H), 7,88 (m, 2H), 7 ,74 (m, 1H), 7,66 (dd, J 9,5 Hz, 1,8 Hz, 1H), 7,40 (t, J 74 Hz, 1H), 7,38 (m, 1H), 7,30 (m, 1 H), 6,97 (d, J 2,6 Hz, 1H), 5 ,57 (d, J 5,3 Hz, 1H), 5 ,12 (m, 1H), 4,80 (dd, J 8,6 Hz, 3,1 Hz, 1H), 3,45 (m, 1H), 3,24 (3H), 2 ,11 (dt, J 13,9 Hz, 2,9 Hz, 1H). CLEM [M 1b] (EN+) TR 1,40 m¡n, 505,1 (M+H)+.
E j e m p l o s 218 a 227
Los s¡gu¡entes Ejemplos se s¡ntet¡zaron s¡gu¡endo el M étod o R a partir del mater¡al de part¡da dado y usando el éster de boronato o ác¡do borón¡co adecuado.
(c o n t in u a c ió n )
(c o n t in u a c ió n )
(continuación)
E j e m p l o 228 , M É T O D O S
(1R.3R)-1-[5-Cloro-2-(d¡fluorometox¡)fen¡l1-7-(6-metox¡-4-met¡lp¡r¡d¡n-3-¡l)-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡midazo[1.2-alpiridin-3-ol
En un recipiente de microondas (20 ml), el E je m p lo 190 (50 mg, 116 |jmol) s e disolvió en 1.4-dioxano y la solución se purgó con argón. Después. se añadieron carbonato sódico (25 mg. 233 |jmol). 2-metoxi-4-met¡l-5-(4.4.5.5-tetramet¡l-1.3.2-dioxaborolan-2-¡l)p¡r¡d¡na (36 mg. 140 pmol) y a gua (1 ml). Esta mezcla s e purgó de nuevo con argón antes de añadir complejo de tris(d¡benc¡lidenoacetona)d¡palad¡o (0) (11 mg. 12 pmol) y tetrafluoroborato de tri-terc-butilfosfonio (1 mg. 3.5 pmol). D e sp u és de calentar durante 15 minutos a 100 °C en un horno microondas y d e sp u é s de enfriar a t.a.. se añadió la misma cantidad de carbonato sódico. ácido borónico. catalizador y borato para completar la reacción por calentamiento a 100 °C durante 15 min en un horno microondas. D e sp u és de enfriar a t.a.. s e añadieron salmuera y EtOAc y d e sp u é s de la separación de fases . la fase a cu o s a s e extrajo dos v e c e s con EtOAc. Las fa s e s orgánicas com binadas s e secaron sobre sulfato sódico. se filtraron y se concentraron al vacío. El residuo s e purificó por HPLC preparativa de f ase inversa (M2d). produciendo el c o m p u e s to de l títu lo (20 mg. 36 %). CLEM [M 1b] (EN+) TR 1.51 min.
472.2 (M+H)+.
E j e m p l o s 229 a 233
Los siguientes Ejemplos s e sintetizaron por el M étod o S a partir del material de partida dado y usando el éster de boronato o ácido borónico adecuado.
(c o n t in u a c ió n )
E j e m p l o 234
(1R.3R)-1-[5-Cloro-2-(d¡fluorometox¡)fen¡l1-6-fluoro-7-[4-(S-met¡lsulfon¡m¡do¡l)fen¡l1-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ol
El co m p u e s to d e l títu lo s e preparó a part¡r del In te rm e d io 167 (665 mg. 1.49 mmol) y el In te rm e d io 75, s¡gu¡endo el M étod o R (274 mg. 35 %). CLEM [M 1b] (EN+) TR 1.32 m¡n. 522.1 (M+H)+.
E j e m p l o 235
Sal______ clorh¡drato______ de______ 5-((1R.3R)-1-[5-cloro-2-(d¡fluorometox¡)fen¡l1-6-fluoro-3-h¡drox¡-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-7-¡l}p¡r¡d¡n-2(1H)-ona
El com puesto del titulo se preparó a part¡r de 5-(4.4.5.5-tetramet¡l-1.3.2-d¡oxaborolan-2-¡l)p¡r¡d¡n-2-ol (252 mg.
1.14 mmol) y el In te rm e d io 167 (255 mg. 0.57 mmol). s¡gu¡endo el M étod o R, pero s¡n la etapa de pur¡f¡cac¡ón con gel de síl¡ce y en la etapa de pur¡f¡cac¡ón de HPLC s e usó HCl en lugar de T F A para obtener la sal clorh¡drato del com puesto del título. CLEM [M 1b1 (EN+) TR 1.20 m¡n. 462.0 (M+H)+.
E j e m p l o 236
Sal clorh¡drato de 5-((1R.3R)-1-(5-cloro-2-(d¡fluorometox¡)fen¡l)-3-h¡drox¡-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-7-¡l)p¡r¡d¡n-2(1 H)-ona
El com puesto del título s e preparó de acuerdo con un método análogo al descrito para la síntesis del E je m p lo 235 a partir del E je m p lo 190.
CLEM [M 1b] (EN+) TR 1,16 min, 444,1 (M+H)+.
E j e m p l o 237
(1R,3R)-7-(6-(terc-butoxi)piridin-3-il)-1-(5-cloro-2-(difluorometoxi)fenil)-2,3-dihidro-1H-ciclopenta[4,51imidazo[1,2-alpiridin-3-ol
El co m p u e s to d e l títu lo s e preparó a partir de 2-(terc-butoxi)-5-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)piridina (194 mg, 0,698 mmol) y el E je m p lo 190 (150 mg, 0,349 mmol), siguiendo el M étod o R, pero sin la etapa de purificación de gel de sílice y en la etapa de purificación de HPLC no se usó nada de T F A para obtener la sal clorhidrato del com puesto del título. CLEM [M 1b] (EN+) TR 1,72 min, 500,1 (M+H)+.
E j e m p l o 238
(1R.3R)-1-(5-cloro-2-(d¡fluorometox¡)fen¡l)-6-fluoro-7-(6-(S-met¡lsulfon¡m¡do¡l)p¡r¡d¡n-3-¡l)-2.3-d¡h¡dro-1H-ciclopenta[4,51imidazo[1,2-a1piridin-3-ol
En una atmósfera de argón, s e mezclaron 5-bromo-2-(S-metil-W-(2,2,2-trifluoro-acetil)sulfonilimidoil)-piridina (200 mg, 0,604 mmol), 4,4,4',4',5,5,5',5'-octametil-2,2'-bi(1,3,2-dioxaborolano) (184 mg, 0,725 mmol) y acetato potásico con dioxano seco. D espués, s e añadió complejo de dicloruro de 1,1'-bis(difenilfosfino)ferroceno-paladio (II) diclorometano (13 mg, 18 pmol) y la m ezcla s e agitó durante 100 minutos a 100 °C. Para completar la reacción, s e añadió la misma cantidad de catalizador y carbonato potásico com o s e ha descrito anteriormente y la agitación se continuó a 100 °C durante 60 min más.
D e sp u és de enfriar, s e añadieron el In te rm e d io 167 (200 mg, 0,446 mmol), carbonato sódico (95 mg, 0,894 mmol), a gua (2,5 ml), Pd2(dba)3 (12 mg, 13 pM) y tetrafluoroborato de tri-terc-butilfosfinio (13 mg, 45 pM). D e s p u é s de agitar durante 30 minutos a 90 °C, el calentamiento s e detuvo y s e añadieron salmuera y EtOAc. D e s p u é s de la separación de fases, la c a p a a cu o s a s e extrajo dos v e c e s con EtOAc y las c a p a s orgánicas com binadas se lavaron con salmuera, se secaron sobre sulfato sódico, s e filtraron y s e concentraron al vacío. D e sp u és de la purificación por cromatografía (SiO 2 , MeOH al 0-10 % en DCM), seguido de una seg u n d a purificación por HPLC de fase inversa (M2c), produjo el co m p u e s to d e l títu lo d e sp u é s de liofilización (72 mg, 31 %). C l EM [M 1b] (EN+) TR 1,28 min, 523,1 (M+H)+.
E j e m p l o 239
(1R.3R)-1-(5-cloro-2-(d¡fluorometox¡)fen¡l)-7-(6-(S-met¡lsulfon¡m¡do¡l)p¡r¡d¡n-3-¡l)-2.3-d¡h¡dro-1H
c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ol
El co m p u e s to d e l títu lo s e preparó de manera análoga al Ejemplo 238. part¡endo del E je m p lo 190 (205 mg. 477 pmol) (85 mg. 35 %). CLEM [M 1b] (EN+) TR 1,21 m¡n. 505,2 (M+H)+.
E j e m p l o s 240 y 241
(1R.3R)-1-(5-cloro-2-(d¡fluorometox¡)fen¡l)-7-(4-((S)-S-met¡lsulfon¡m¡do¡l)fen¡l)-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ol_________ y_________ (1R.3R)-1-(5-cloro-2-(d¡fluorometox¡)fen¡l)-7-(4-((R)-S-met¡lsulfon¡m¡do¡l)fen¡l)-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ol
Los co m p u e s to s de l títu lo s e a¡slaron med¡ante separac¡ón qu¡ral del E je m p lo 218 (312 mg) en cond¡c¡ones de HPLC en una Ch¡ralcell OJ-H (30 x 250 mm x mm. 5 p. flujo 30 ml/m¡n. temperatura amb¡ente. 5:1:1 de heptano:EtOH:MeOH preacond¡c¡onado con d¡et¡lam¡na. El pr¡mer enant¡ómero en elu¡rse (TR 14.9 m¡n) s e recog¡ó. las fracc¡ones se evaporaron y el res¡duo se l¡of¡l¡zó en MeCN/agua para produc¡r 158 mg del E je m p lo 240.
C l E m [M 1b1 (EN+) TR 1.26 m¡n. 504.1 (M+H)+. cromatografía qu¡ral (Ch¡ralcell OJ-H. 4.6 x 250 mm x mm. flujo 1 ml/m¡n. 30 °C. 5:1:1 de heptano:EtOH:MeOH 0.1 % de d¡et¡lam¡na) TR 9.24 m¡n.
El segun do enant¡ómero en elu¡rse (TR 18.2 m¡n) s e recog¡ó. las fracc¡ones se evaporaron y s e l¡of¡l¡zaron en MeCN/agua para produc¡r 145 mg del E je m p lo 241. CLEM [M 1b1 (EN+) TR 1.25 m¡n. 504.1 (M+H)+. cromatografía qu¡ral (Ch¡ralcell OJ-H. 4.6 x 250 mm x mm. flujo 1 ml/m¡n. 30 °C. 5:1:1 de Hep:EtOH:MeOH 0.1 % de d¡et¡lam¡na) T R 11.03 m¡n.
E j e m p l o s 242 y 243
(1R.3R)-1-(5-cloro-2-(d¡fluorometox¡)fen¡l)-6-fluoro-7-(4-((S)-S-met¡lsulfon¡m¡do¡l)fen¡l)-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ol______ y______(1R.3R)-1-(5-cloro-2-(d¡fluorometox¡)fen¡l)-6-fluoro-7-(4-((R)-S-met¡lsulfon¡m¡do¡l)fen¡l)-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ol
Los co m p u e s to s de l títu lo s e aislaron mediante separación quiral del E je m p lo 234 (260 mg) en condiciones de HPLC en una Chiralpak IC (30 x 250 mm x mm, 5 |j, flujo 30 ml/min, temperatura ambiente, 1:1:1 de heptano:EtOH:MeOH 0,05 % de dietilamina. El primer enantiómero en eluirse (TR 13,3 min) se recogió, las fracciones s e evaporaron y el residuo s e liofilizó en MeCN/agua para producir 90 mg del E je m p lo 242.
CLEM [M 1b] (EN+) TR 1,31 min, 522,1 (m H)+. cromatografía quiral (Chiralpak IC (4,6 x 250 mm x mm, flujo 1 ml/min, 30 °C, 1:1 de EtOH:MeOH 0,1 % de dietilamina) TR 7,27 min.
El segun do enantiómero en eluirse (TR 17 ,3 min) s e recogió, las fracciones se evaporaron y s e liofilizaron en MeCN/agua para producir 98 mg del E je m p lo 243.
CLEM [M 1b] (EN+) TR 1,31 min, 522,1 (M+H)+. cromatografía quiral (Chiralpak IC (4,6 x 250 mm x mm, flujo 1 ml/min, 30 °C, 1:1 de EtOH:MeOH 0,1 % de dietilamina) TR 8,09 min.
E j e m p l o 244
({(1R.3R)-1-[5-Cloro-2-(d¡fluorometox¡)fen¡l1-7-[2-(2-h¡drox¡propan-2-¡l)p¡r¡m¡d¡n-5-¡l1-2,3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-3-¡l}ox¡)acetato de etilo
E tap a 1: S ín tes is de 2 -(( (1 R ,3 R )-7 -b ro m o -1 -(5 -c lo ro -2 -(d iflu o ro m e to x i) fe n il)-2 ,3 -d ih id ro -1 H -c ic lo p e n ta [4 ,5 ]im id a z o [1 ,2 -a ]p ir id in -3 - il)o x i)a ce ta to de e tilo
El E je m p lo 190 (100 mg, 0.233 mmol) s e disolvió en THF (7 ml). La solución s e enfrió a 0 °C y se añadió hidruro sódico (21 mg, 0,51 mmol; 60 % en aceite) con agitación. D e sp u és de agitar durante 15 minutos, se añadió bromoacetato de etilo (159 mg, 0,93 mmol) disuelto en THF (0,2 ml). El baño de hielo se retiró y la agitación s e continuó durante 1 h a t.a. Para completar la reacción, la m ezcla s e enfrió de nuevo a 0 °C y s e añadieron m ás cantidad de hidruro sódico (21 mg, 0,51 mmol; 60 % en aceite) y bromoacetato de etilo (159 mg, 0,93 mmol). Este procedimiento s e repitió dos v e c e s m ás hasta que había desaparecido casi todo el material de partida. S e añadió a g u a y la fase a cu o sa se extrajo tres v e c e s con EtOAc. Las c a p a s orgánicas com binadas s e secaron sobre sulfato sódico, s e filtraron y se concentraron al vacío. El residuo se diluyó con MeCN y s e purificó por HPLC preparativa, produciendo el co m p u e s to d e l títu lo (70 mg,58 %). CLEM [M 1b] (EN+) TR 1,84 min, 515 ,1 (M+H)+.
E tap a 2: S ín tes is de 2 -(((1 R ,3 R )-1 -(5 -c lo ro -2 -(d iflu o ro m e to x i) fe n il)-7 -(2 -(2 -h id ro x ip ro p a n -2 -il)p ir im id in -5 - il)-2 ,3 -d ih id ro -1 H -c ic lo p e n ta [4 ,5 ]im id a zo [1 ,2 -a ]p ir id in -3 - il)o x i)a ce ta to de e tilo
El co m p u e s to d e l títu lo s e preparó a partir del producto obtenido en la etapa 1 (68 mg), siguiendo el M étod o R. (41 mg, 54 %). RMN 1H (400 MHz, DMSO-d6) 6 ppm 9,04 (s, 2H), 8,44 (m, 1H), 7,80 (m, 1H), 7,73 (m, 1H), 7,40 (m, 1H), 7,39 (t, 74 Hz, 1H), 7,31 (m, 1H), 6,95 (d, J 2,6 Hz, 1H), 5,09 (s, 1H), 5,05 (dd, J 7,1 Hz, 1,8 Hz, 1H), 4,83 (dd, J 8,6 Hz, 2,4 Hz, 1H), 4 ,47 (d, J 16,3 Hz, 1H), 4,39 (d, J 16,3 Hz, 1H), 4 ,10 (c, J 7,1 Hz, 2H), 3,49 (m, 1H), 2,30 (m, 1H), 1,51 (s, 6H), 1,16 (t, J 7,1 Hz, 3H); CLEM [M 1b] (EN+) TR 1,68 min, 573,2 (M+H)+.
E j e m p l o s 245 y 246
(1R.3R)-1-[2-(d¡fluorometox¡)fen¡l1-3-met¡l-7-[2-(morfol¡n-4-¡l)p¡r¡m¡d¡n-5-¡l1-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ol______ y______ (1R.3S)-1-[2-(d¡fluorometox¡)fen¡l1-3-met¡l-7-[2-(morfol¡n-4-¡l)p¡r¡m¡d¡n-5-¡l1-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ol
Los c o m p u e s to s de l títu lo s e prepararon a partir de la HPLC preparativa del E je m p lo 154. Ejemplo 245: RMN 1H (400 MHz, DMSO-d6) 8 8,63 (d, J 6,8 Hz, 1H), 7,88 (d, J 9,9 Hz, 1H), 7,46 (dd, J 8,8, 2,6 Hz, 1H), 7,28 (d, J 8,8 Hz, 1H), 7,20 (t, J 73,5 Hz, 1H), 7,08-7,13 (m, 1H), 5,08 (dd, J 7,0, 2,1 Hz, 1H), 3 ,57 (dd, J 18,2, 7,2 Hz, 1H), 2,78 (dd, J 18,1, 2,2 Hz, 1 H). CLEM (EN+) TR 1,32 min 494,0 (M+H)+. Ejemplo 246: RMN 1H (400 MHz, DMSO-d6) 8 8,63 (d, J 6,8 Hz, 1H), 7,88 (d, J 9,9 Hz, 1H), 7,46 (dd, J 8,8, 2,6 Hz, 1H), 7,28 (d, J 8,8 Hz, 1H), 7,20 (t, J 73,5 Hz, 1H), 7,08 7 ,13 (m, 1H), 5,08 (dd, J 7,0, 2,1 Hz, 1H), 3 ,57 (dd, J 18,2, 7,2 Hz, 1H), 2,78 (dd, J 18,1, 2,2 Hz, 1H). CLEM (EN+) TR 1,35 min 494,0 (M+H)+.
E je m p lo s 247-254
Los siguientes Ejemplos se prepararon por el M étod o A a partir del material de partida dado usando el éster de boronato o ácido borónico adecuado.
(c o n t in u a c ió n )
(c o n t in u a c ió n )
E j e m p l o s 255 y 256
(1R,3R)-1-(3-clorofenil)-6-fluoro-7-[2-(2-hidroxipropan-2-il)pirimidin-5-il1-2,3-dihidro-1H-ciclopenta[4,51imidazo[1,2-a1pirid¡n-3-ol_______ y_______ (1S.3S)-1-(3-clorofen¡l)-6-fluoro-7-[2-(2-h¡drox¡propan-2-¡l)p¡r¡m¡d¡n-5-¡l1-2.3-d¡h¡dro-1H-c¡clopentaf4.51¡m¡dazof1.2-a1p¡r¡d¡n-3-ol
Los c o m p u e s to s d e l títu lo s e obtuvieron a partir del E je m p lo 160 mediante S F C quiral (92 % de C O 2 : 8 % de metanol 1 % de DEA en una columna ChiralCel OJ-H), produciendo el E je m p lo 255 en forma de un sólido de color blanquecino. RMN 1H (500 MHz, DMSO-d6) 8 8,90 (d, J 1,3 Hz, 2H), 8,30 (d, J 7,5 Hz, 1H), 7,66 (d, J 11 ,6 Hz, 1H), 7,44 (s, 1H), 7,34 - 7,29 (m, 2H), 7,26 (dt, J 7,1, 2,1 Hz, 1H), 5,64 (d, J 4,9 Hz, 1H), 5 ,15 - 5,06 (m, 2H), 4,49 (dd, J 8,5, 3,1 Hz, 1H), 3,49 - 3,41 (m, 1H), 2 ,14 (dt, J 13,8, 2,9 Hz, 1H), 1,52 (s, 6H). Método (92 % de C O 2 : 8 % de metanol 1 % de DEA en una columna ChiralCel OJ-H); CLEM (EN+) TR 5,75 min, 439,0 (M+H)+. El E je m p lo 256 se obtuvo en forma de un sólido de color blanquecino por el mismo método de S F C . RMN 1H (500 MHz, DMSo-d6) 8 8,90 (d, J 1,3 Hz, 2H), 8,30 (d, J 7,5 Hz, 1H), 7,66 (d, J 11 ,6 Hz, 1H), 7,44 (s, 1H), 7,36 - 7,29 (m, 2H), 7,26 (dt, J 7,1, 2,0 Hz, 1H), 5,64 (d, J 5,1 Hz, 1H), 5 ,15 - 5,08 (m, 2H), 4,49 (dd, J 8,5, 3,1 Hz, 1H), 3,50 - 3,39 (m, 1H), 2 ,14 (dt, J 13,8, 2,9 Hz, 1 h ), 1,52 (s, 6H). Método (92 % de C O 2 : 8 % de metanol 0,1 % de d Ea en una columna ChiralCel OJ-H); CLEM (EN+) TR 12 ,76 min, 439,0 (M+H)+.
E j e m p l o 257
2-(((1R.3R)-1-(5-cloro-2-(d¡fluorometox¡)fen¡l)-7-(2-(2-h¡drox¡propan-2-¡l)p¡r¡m¡d¡n-5-¡l)-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-3-¡l)ox¡)acetato de tere-butilo
El e o m pu es to d e l títu lo (23 mg, 52 %) s e preparó a part¡r del In te rm e d io 176. s¡gu¡endo el M étod o R s¡n la etapa de pur¡f¡cac¡ón con gel de síl¡ce. CLEM [M ib] (EN+) TR 1.80 m¡n. 601.2 (M+H)+.
E j e m p l o 258
ác¡do 2-(((1R.3R)-1-(5-cloro-2-(d¡fluorometox¡)fen¡l)-7-(4-(met¡lsulfon¡l)fen¡l)-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-3-¡l)ox¡)acét¡co
El E je m p lo 224 (25 mg. 40 pM) s e d¡solv¡ó en DCM (2.5 ml). D espués. s e añad¡ó lentamente con ag¡tac¡ón T F A al 80 % en a g u a (0.4 ml). 1 h y 2 h desp ués. s e añad¡ó m ás cant¡dad de T F A al 80 % en a g u a (0.2 ml) y la m ezcla de reacc¡ón s e calentó a 40 °C durante 6 h. La m ezcla de reacc¡ón s e concentró al vac ío y d e sp u é s de neutral¡zar con una soluc¡ón saturada de h¡drogenocarbonato sód¡co. s e concentró a sequedad. El res¡duo s e pur¡f¡có por HPLC de fase ¡nversa (M2f). Las fracc¡ones puras s e comb¡naron y s e l¡of¡l¡zaron para produc¡r 19 mg (83 %) del e o m pu es to de l títu lo . CLEM [M 1b] (EN+) TR 1.47 m¡n. 563.1 (M+H)+.
E j e m p l o 259
ác¡do_________ 2-(((1R.3R)-1-(5-cloro-2-(d¡fluorometox¡)fen¡l)-7-(2-(2-h¡drox¡propan-2-¡l)p¡r¡m¡d¡n-5-¡l)-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-3-¡l)ox¡)acét¡co
Partiendo del E je m p lo 257 (10 mg, 17 |jmol), el c o m p u e s to d e l t itu lo (8,4 mg; 93 %) s e obtuvo de manera análoga al Ejemplo 254. CLEM [M 1b] (EN+) TR 1,46 min, 545,2 (M+H)+.
E j e m p l o 260 , M E T O D O T
5-((1R.3R)-1-(5-cloro-2-(d¡fluorometox¡)fen¡l)-3-h¡drox¡-2.3-d¡h¡dro-1H-c¡clopenta[4,51¡m¡dazo[1.2-a1p¡r¡d¡n-7-¡l)-3-metilpir¡d¡n-2(1H)-ona
S e añadieron yoduro sódico (18 mg, 117 jm ol) y etil eterato trifluoruro de boro (17 mg, 117 jm ol) a una solución agitada del E je m p lo 229 (27 mg, 58 jM ) en MeCN (1 ml) a t.a. La reacción s e agitó durante 2 h. S e añadieron una cantidad adicional de yoduro sódico (18 mg, 117 jm ol) y etil eterato trifluoruro de boro (17 mg, 117 jm ol) y la mezcla se agitó durante 2 h más. S e añadieron EtOAc y una solución saturada de hidrogenocarbonato sódico y d e sp u é s de la separación de las fases , la fase a cu o s a s e extrajo dos v e c e s con EtOAc. Las c a p a s orgánicas com binadas se lavaron con salmuera, se secaron sobre sulfato sódico, s e filtraron y s e concentraron al vacío. El residuo s e purificó por cromatografía (S¡O 2 , MeOH al 0-20 %/DCM), seguido de una seg u n d a purificación de HPLC de fase inversa (M2f) para producir el com puesto del título tras liofilización (11 mg, 40 %). CLEM [M 1b] (EN+) TR 1,24 min, 458,2 (M+H)+. E j e m p l o s 261 - 262
Los siguientes Ejemplos se prepararon aplicando el M étod o T a partir del material de partida dado y usando la metoxipiridina adecuada.
(continuación)
E j e m p l o s 263 - 265
Los siguientes Ejemplos s e prepararon aplicando el M étod o R a partir del material de partida dado y usando el éster de boronato o ácido borónico adecuado.
(1R.3R)-1-[2-(difluorometoxi)fenill-7-{2-[(1s.5s)-3.7-dioxa-9-azabiciclo[3.3.1lnon-9-illpirimidin-5-il}-3-metil-2.3-dihidro-1H-c¡clopentaf4.51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ol_____ y_____ (1R.3S)-1-[2-(difluorometoxi)fenill-7-{2-[(1s.5s)-3.7-dioxa-9-azabiciclo[3.3.1lnon-9-illpirimidin-5-il}-3-metil-2.3-dihidro-1H-ciclopenta[4.5limidazo[1.2-alpiridin-3-ol
Los E je m p lo s 265 y 266 se prepararon a partir del E je m p lo 15 (257 mg, 0,63 mmol), el In te rm e d io 71 (211 mg, 0,63 mmol), 1,4-dioxano (10 ml), carbonato sódico 2 M (2 ml) y complejo de dicloruro de 1,1 '-bis(difenilfosfino)ferroceno-paladio (II) diclorometano (26 mg, 0,032 mmol) por el M é to d o A. El material en bruto se purificó por cromatografía en columna (SiO 2 , MeOH al 0-40 % en EtOAc) y s e liofilizó en acetonitrilo/agua para dar una m ezcla del E je m p lo 265 y 266. Los E je m p lo s 265 y 266 se separaron por purificación de S F C quiral (25 % de metanol:75 % de C O 2 con una Chiralpak iA).
Después, el E je m p lo 265 s e purificó adicionalmente por cromatografía en columna ( S O 2 , MeOH al 0-50 % en EtOAc) para dar el co m p u e s to d e l títu lo en forma de un sólido de color blanco (46 mg, 14 %). 8h (300 MHz, DMSO-d6) 8,61 (s, 2H), 8,01 (dd, 1H, J 1,7, 1,0 Hz), 7,66 (dd, 1H, J 9,5, 0,9 Hz), 7,53 (dd, 1H, J 9,5, 1,8 Hz), 7,36 (t, 1H, J 74,1 Hz), 7,28-7,34 (m, 1H), 7,23-7,28 (m, 1H), 7 ,10 -7 ,17 (m, 1H), 6,97 (dd, 1H, J 7,8, 1,6 Hz), 5,26 (s, 1H), 4,79 (dd, 1H, J 8,4, 4 . 4 Hz), 4,46 (s a, 2H), 4,02 (s a, 2H), 3,98 (s a, 2H), 3,74 (d, 2H, J 2,4 Hz), 3,70 (d, 2H, J 2,4 Hz), 3 ,14 (dd, 1H, J 13,3, 8.5 Hz), 2,36 (dd, 1H, J 13,4, 4,3 Hz), 1,55 (s, 3H). CLEM (EN+) 536 (M+H)+, TR 1,84 minutos.
D espués, el E je m p lo 266 s e purificó adicionalmente por cromatografía en columna (SiO 2 , MeOH al 0-50 % en EtOAc) para dar el co m p u e s to d e l títu lo en forma de un sólido de color blanco (9 mg, 3 %). Sh (300 MHz, DMSO-d6) 8,62 (s, 2H), 8,01 (dd, 1 H, J 1,6, 1,0 Hz), 7,68 (dd, 1H, J 9,5, 0,9 Hz), 7,52-7,57 (m, 1H), 7,29-7,34 (m, 1H), 7,32 (t, 1H, J 74,3 Hz), 7,23-7,28 (m, 1H), 7 ,11 (td, 1H, J 7,6, 1,3 Hz), 6,63 (dd, 1H, J 7,6, 1,4 Hz), 5,21 (s, 1H), 4,97-5,03 (m, 1H), 4,45 (s a, 2H), 4,02 (s a, 2H), 3,98 (s a, 2H), 3,73 (d, 2H, J 2,0 Hz), 3,70 (d, 2H, J 2,2 Hz), 3,10 (dd, 1H, J 13,5, 8,3 Hz), 2,27-2,34 (m, 1H), 1,51 (s, 3H). CLEM (EN+) 536 (M+H)+, TR 1,85 minutos.
E j e m p l o 267
7-bromo-1-r2-(difluorometoxi)fenil1-3-metil-2,3-dihidro-1H-ciclopentar4,51imidazoH,2-a1piridin-3-il}acetamida
A una solución agitada del E je m p lo 15 (99,5 mg, 0,24 mmol) en acetonitrilo (4 ml) se añadió ácido sulfúrico (68,5 pl, 1,22 mmol) y la mezcla de reacción s e calentó a 60 °C durante 50 minutos, tiempo d e sp u é s del cual, la m ezcla de reacción s e enfrió a temperatura ambiente y d e sp u é s s e diluyó con a g u a (25 ml), se basificó con NaOH al 10 % y se extrajo con DCM (4 x 25 ml), los materiales orgánicos com binados s e pasaron a través de un separador de f a s e s y se concentraron al vacío. El residuo s e purificó por cromatografía en columna (S¡O 2 , EtOAc al 20-100 % en hexano,
seguido de MeOH al 0-100 % en EtOAc) y el material s e criodesecó en acetonitrilo/agua para dar el c o m p u e s to de l títu lo (52,4 mg, 48 %) en forma de un sólido de color beige. S h (300 MHz, DMSO-d6) 8,11 (s, 1 H), 8,04 (dd, 1H, J 1,8, 0,7 Hz), 7,52-7,58 (m, 1H), 7,23-7,36 (m, 2H), 7,31 (t, 1H, J 74,1 Hz), 7 , 11 - 7 ,19 (m, 1H), 6,66 (dd, 1H, J 7,6, 1,5 Hz), 4,97 (dd, 1 H, J 8,8, 4,4 Hz), 3,45 (dd, 1H, J 13,4, 9,0 Hz), 2,23 (dd, 1H, J 13,6, 4,8 Hz), 1,78 (s, 3H), 1,51 (s, 3H). Asignación de RMN para el diastereoisómero principal. El material e s una m ezcla (11:9) de los dos diaestereoisómeros. C l E m (EN+) 450/452 (M+H)+, t R 2 ,10 minutos.
E j e m p l o 268
1-r2-(difluorometoxi)fenil1-3-metil-7-r4-(metilsulfonil)fenil1-2,3-dihidro-1H-ciclopentar4,51imidazor1,2-a1piridin-3-¡Dacetamida
El co m p u e s to d e l titu lo se preparó a partir del E je m p lo 267 (48 mg, 0,11 mmol), ácido 4-(metilsulfonil)fenilborónico (30 mg, 0,15 mmol), 1,4-dioxano (5 ml), carbonato sódico ac. 2 M (1 ml) y dicloruro de 1,1'-bis(difenilfosfino)ferrocenopaladio (II) (4 mg, 0,006 mmol) por el M étod o A (19,6 mg, 35 %). El E je m p lo 267 contiene una mezcla 73:27 de diaestereoisómeros. 8h (300 MHz, DMSO-d6) 8,20 (s, 1H), 8,06 (s, 1H), 7,96-7,99 (m, 2H), 7,83 (d, 1H, J 8,5 Hz), 7,69 7 ,74 (m, 1 H), 7,64 (dd, 1H, J 9,4, 1,7 Hz), 7,36 (t, 1H, J 74,0 Hz), 7,30-7,35 (m, 1H), 7 ,27 (s, 1H), 7 , 11 - 7 ,14 (m, 1H), 7,03 (dd, 1 H, J 7,7, 1,5 Hz), 4,92 (dd, 1H, J 8,3, 5,8 Hz), 3,23 (s, 3H), 3,10 (dd, 1H, J 13,1, 8,5 Hz), 2,82 (dd, 1H, J 13,1, 5,8 Hz), 1,75 (s, 3H), 1,59 (s, 3H). - asignación de RMN para el diastereoisómero principal. CLEM (EN+) 526 (M+H)+, TR 1,91 y 1,95 minutos
E j e m p l o 269
(1 R ,3 S o R)-7-bromo-1-[2-(d¡fluorometox¡)fen¡l1-3-et¡n¡l-6-fluoro-2.3-d¡h¡dro-1H-c¡clopenta[4.51¡m¡dazo[1.2-a1p¡r¡d¡n-3-ol
A una solución agitada del E je m p lo 2 (1 g, 2,43 mmol) y LiCl (210 mg, 4,954 mmol) en 2-metil tetrahidrofurano (5 ml) se añadió bromuro de etinilmagnesio (0,5 M en THF) (10,5 ml, 5 mmol) y la m ezcla de reacción se agitó a t.a. durante 18 h. La m ezcla de reacción s e trató con una solución saturada de NaHCO3 (100 ml) y s e repartió con EtOAc (100 ml), las c a p a s s e separaron y la a cu o s a s e extrajo con EtOAc (2 x 100 ml), los materiales orgánicos combinados s e secaron sobre MgSO4 y s e filtraron y concentraron al vacío. El residuo s e purificó por cromatografía en columna (S¡O 2 , EtOAc al 50-100 %/hexano) dando el c o m p u e s to d e l títu lo (686 mg, 64 %). CLEM (EN+) 437,0/439,0 (M+H)+, TR 1,46 minutos E j e m p l o s 270 y 271
(1R)-7-f2-r(1S.4S)-2.5-d¡azab¡c¡clor2.2.11hept-2-¡l1p¡r¡m¡d¡n-5-¡l}-1-r2-(d¡fluorometox¡)fen¡l1-3-met¡l-2.3-d¡h¡dro-1H-c¡clopentar4.51im¡dazori.2-a1p¡r¡d¡n-3-ol y (1R)-7-f2-r(1S.4S)-2.5-d¡azab¡c¡clor2.2.11hept-2-¡l1p¡r¡m¡d¡n-5-¡l}-1-í2-íd¡fluorometox¡)fen¡l1-3-metox¡-3-met¡l-2.3-d¡h¡dro-1H-c¡clopentar4.51¡m¡dazon.2-a1p¡r¡d¡na
El In te rm e d io 184 (465 mg. 0.77 mmol) s e d¡solv¡o en ac¡do clorhidr¡co 4 M en 1.4-d¡oxano (11 ml) y metanol (3 ml) y la reacc¡ón se ag¡tó a t.a. durante 1.5 horas. D e s p u és de este t¡empo. la m ezcla de reacc¡ón s e concentró al vacío, el res¡duo s e d¡solv¡ó en a gua (10 ml) y s e bas¡f¡có con NaOH al 10 % (5 ml). y esto s e extrajo con EtOAc (4 x 25 ml). los mater¡ales organ¡cos comb¡nados s e lavaron con salmuera (50 ml). s e secaron (MgSO4). s e f¡ltraron y s e concentraron al vacío. El res¡duo se pur¡f¡có por cromatografía en columna (S¡O2. 0 % de NH3 / 0 % de MeOH/100 % de DCM - 2.5 % de NH3/2 2 . 5 % de MeOH/75 % de DCM) y el mater¡al s e cr¡odesecó en aceton¡tr¡lo/agua para dar una m ezcla del E je m p lo 270 y el E je m p lo 271. Este mater¡al s e pur¡f¡có ad¡c¡onalmente por HPLC preparat¡va para dar am bos co m p u e s to s d e l títu lo , e l E je m p lo 270 (54 mg. 14 %) en forma de un sól¡do de color blanquec¡no y el E je m p lo 271 (19 mg. 5 % ) en forma de un sól¡do de color amar¡llo pálido.
El E je m p lo 270 cont¡ene una m ezcla 14:11 de d¡aestereo¡sómeros.
Sh (300 MHz. DMSO-d6) 8.51 (s. 2H). 7.95 (s. 1H). 7.64 (dd. 1H. J 3.6. 0.8 Hz). 7.52 (dd. 1H. J 4.3. 1.8 Hz). 7.37 (t.
1H. J 74.1 Hz). 7.24-7.34 (m. 2H). 7.12 (dd. 1H. J 7.1. 1.3 Hz). 6.98 (dd. 1H. J 7.7. 1.5 Hz). 5.29 (s. 1H). 4.78 (dd. J 8.4. 4.3 Hz). 4.75 (s. 1H). 3.62-3.67 (m. 1H). 3.42-3.44 (m. 1H). 3.05-3.18 (m. 2H). 2.86-2.93 (m. 1H). 2.71-2.79 (m.
1H). 2.26-2.40 (m. 1H). 1.72 -1.79 (m. 1H). 1.62-1.68 (m. 1H). 1.54 (s. 3H). As¡gnac¡ón de RMN para el d¡astereo¡sómero pr¡nc¡pal. El mater¡al e s una mezcla (14 :11) de los dos d¡aestereo¡sómeros. CLEM (EN+) 505 (M+H)+. T R 1.54 y 1.59 m¡nutos
E j e m p l o 271
Sh (300 MHz. DMSO-d6) 8.53 y 8.51 (s. 2H. d¡astereo¡somér¡co). 8.06 y 7.95 (s. 1H. d¡astereo¡somér¡co). 7.69 (d. 1H. J 9.5 Hz). 7.51-7.58 (m. 1H). 7.24-7.36 (2H. m). 7.34 (t. 1H. J 74.1 Hz). 7.09-7.16 (m. 1H). 6.80 (dd. J 7.8. 1.5 Hz) y 6.66 (dd. J 8.1. 1.5 Hz) (dd. 1H. d¡astereo¡somér¡co). 4.99 (dd. J 8.4. 5.0 Hz) y 4.81 (dd. 1H. J 8.7. 3.9 Hz) (dd. 1H. d¡astereo¡somér¡co). 4.74 (s. 1H). 3.64 (s. 1H). 3.45-3.48 y 3.42-3.44 (m. 1H. d¡astereo¡somér¡co). 3.22 (dd. 1H. J 14.1.8.4 Hz). 3.11 y 3.09 (s. 3H. d¡astereo¡somér¡co). 2.86-2.92 y 2.71-2.78 (m. 2H. d¡astereo¡somér¡co). 2.71-2 .78 (m.
1H). 2.40 (dd. J 14.0. 4.0 Hz) y 2.26 (dd. J 14.0. 5.4 Hz) (dd. 1H. d¡astereo¡somér¡co). 1.72 -1.78 (m. 1H). 1.62-4.68 (m.
1H). 1.57 y 1.54 (s. 3H. d¡astereo¡somér¡co). CLEM (EN+) 519 (M+H)+. TR 1.19 y 1.89 m¡nutos.
Claims (13)
1. Un com puesto representado por la fórmula (IIA), o un N -ó x id o del mismo, o una sal farmacéuticamente aceptable del mismo,
R 1 representa arilo, , heterocicloalquenilo C 3 - 7 , heteroarilo, cicloalquil (C3-7)-heteroarilbicidoalquil (C4-9)-heteroaril-, heterocicloalquil (C3-7)-heteroaril-, heterobicicloalquil (C4-9)-heteroaril- o espiroheterocicloalquil (C4-9)-heteroaril-, cualquiera de tales grupos puede estar opcionalmente sustituido con uno, dos o tres sustituyentes se leccionados entre halógeno, haloalquilo (C 1 -6 ), ciano, cianoalquilo (C 1 -6 ), nitroalquilo (C 1 -6 ), alquilo C 1 -6 , trifluorometilo, trifluoroetilo, alquenilo C 2 -6 , hidroxi, hidroxialquilo (C 1 -6 ), alcoxi C 1 -6 , trifluoroetoxi, carboxicicloalquiloxi (C 3 -7 ), alquiltio C 1 -6 , alquilsulfonilo C 1 -6 , alquilsulfonil (C 1 -6 )-alquilo (C 1 -6 ), oxo, amino, amino-alquilo (C 1 -6 ), alquilamino C 1-6, dialquilamino (C 1 -6 ), alcoxi (C 1 -6 )alquilamino (C 1 -6 ), N-[alquil (C 1-e)]-N-[hidroxialquil (C 1 -6 )]amino, alquilcarbonilamino (C 2 -6 )-alquilo(C1 -6 ), alquilsulfonilamino C 1 -6 , N-[alquil (C 1 -6 )]-N-[alquilsulfonil (C 1 -6 )]amino, bis[alquilsulfonil (C 1 -6 )]amino, N-[alquil (C 1 -6 )]-N-[carboxialquil (C 1 -6 )]amino, carboxicicloalquil (C3-7)-amino, carboxicicloalquil (C3-7)alquilamino (C 1 -6 ), formilo, alquilcarbonilo C 2 -6 , alquilcarboniloxi (C 2 - 6 )alquilo (C 1 -6 ), carboxi, carboxialquilo (C 1 -6 ), alcoxicarbonilo C 2 -6 , alcoxicarbonil C 2 -6 alquilo (C 1 -6 ), morfolinil-alcoxicarbonilo (C 1 -6 ), alcoxicarbonil C 2 -6 -metilidenilo, aminocarbonilo, dialquilaminocarbonilo (C 1 -6 ), aminosulfonilo, alquilsulfoximinilo (C 1 -6 ), [alquil (C 1 -6 )][N-alquil (C 1 -6 )]sulfoximinilo, heteroarilo, difluorometilo, alquilsulfinilo C 1 -6 y cicloalquil (C 3 -7)sulfonilo.
R2 representa hidrógeno, halógeno, trifluorometilo o ciano; o alquilo C 1 -6 opcionalmente sustituido con alcoxicarbonilo C 2 -6 ;
Y representa arilo o heteroarilo, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o más sustituyentes se lecc io nado s entre cloro, flúor, ciano, metoxi, metilsulfonilo, trifluorometoxi y difluorometoxi;
Z representa metileno;
R5a representa hidrógeno, hidroxi, halógeno o trifluorometilo; o -NRbRc, -NRcC (O )R d, -S(O)2 RaO R a-O (CO )-Rd o alquilo C 1 -6 , cualquiera de tales grupos puede estar opcionalmente sustituido con uno o m ás sustituyentes se lecc io nado s entre halógeno, hidroxi, trifluorometilo, alquilo C 1 -6 , alcoxi C 1 -6 , alquilcarbonilo C 2 -6 , alquiloxicarbonilo C 2 -6 , (hidroxi)alquilo C 1 -6 , cicloalquilo (C 3 - 7 ), alquilsulfonilo C 1 -6 , alquilsulfonil (C 1-e)-alquilo (C 1 -6 ), dialquilaminocarbonilo (C 1 - 6 ), oxo y carboxi; y
R5b representa hidrógeno, hidroxi, halógeno, ciano, trifluorometilo; o alquilo C 1 -6 , dicho grupo puede estar opcionalmente sustituido con uno o m ás sustituyentes se lecc io nado s entre halógeno, hidroxi, trifluorometilo, alquilo C 1 -6 , alcoxi C 1 -6 , alquilcarbonilo C 2 -6 , alquiloxicarbonilo C 2 - 6 , (hidroxi)alquilo C 1 -6 , cicloalquilo (C 3 -7 ), alquilsulfonilo C 1 -6 , alquilsulfonil (C 1 -6 )-alquilo (C 1 -6 ), dialquilaminocarbonilo (C 1 -6 ), oxo y carboxi;
o R5a y R5b, cuando s e toman junto con el carbono al que están unidos, representan un carbonilo, tiocarbonilo o -C=N-OH; Ra representa alquilo C 1 -6 , arilalquilo (C 1 -6 ) o heteroarilalquilo (C 1 -6 ), cualquiera de tales grupos puede estar opcionalmente sustituido con uno o m ás sustituyentes se lecc io nado s entre alcoxi C 1 -6 , oxo, ciano y alcoxicarbonilo C 2 -6 ;
R b representa hidrógeno o alquilo C 1 -6 ;
Rc representa hidrógeno, alquilo C 1 -6 o cicloalquilo C3-7; y
Rd representa hidrógeno; o alquilo C 1 -6 , arilo o heteroarilo, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o m ás sustituyentes se lecc io nado s entre halógeno, alquilo C 1 -6 , alcoxi C 1 -6 , oxo, alquilcarboniloxi C 2 -6 y dialquilamino (C 1 -6 ).
2. Un com puesto de acuerdo con la reivindicación 1 representado por la fórmula (IIB), o un N-óxido del mismo, o una sal farmacéuticamente aceptable,
en la que
V representa C -R 12 o N;
R9 representa hidrógeno, halógeno, ciano, difluorometilo, trifluorometilo, trifluoroetilo o amino; o haloalquilo (C 1 -6 ), cianoalquilo (C 1 -6 ), nitroalquilo (C 1 -6 ), alquilo C 1 -6 , , alquenilo C 2 -6 , hidroxi, hidroxialquilo (C 1 -6 ), alcoxi C 1 -6 , trifluoroetoxi, carboxicicloalquiloxi (C 3 -7 ), alquiltio C 1 -6 , alquilsulfonilo C 1 -6 , alquilsulfonil (C 1-e)-alquilo (C 1 -6 ), oxo, amino-alquilo (C 1 -6 ), alquilamino C 1 -6 , dialquilamino (C 1 -6 ), alcoxi (C 1 -6 )alquilamino (C 1 -6 ), N-[alquil (C 1 -6 )]-N-[hidroxialquil (C 1 -6 )]amino, alquilcarbonilamino (C 2 - 6 )-alquilo(C1 -6 ), alquilsulfonilamino C 1 -6 , N-[alquil (C 1 -6 )]-N-[alquilsulfonil (C 1 -6 )]amino, bis[alquilsulfonil (C 1 -6 )]amino, N-[alquil (C 1 -6 )]-N-[carboxialquil (C 1 -6 )]amino, carboxicicloalquilamino (C 3 -7 ), carboxicicloalquil (C3-7)alquilamino (C 1 -6 ), formilo, alquilcarbonilo C 2 - 6 , alquilcarboniloxi (C 2 -6 )alquilo (C 1 -6 ), carboxi, carboxialquilo (C 1 -6 ), alcoxicarbonilo C 2 - 6 , alcoxicarbonil C 2 -6 alquilo (C 1-6) , morfolinil-alcoxicarbonilo (C 1 -6 ), alcoxicarbonilmetilidenilo C 2 -6 , aminocarbonilo, dialquilaminocarbonilo (C 1 -6 ), aminosulfonilo, alquilsulfoximinilo (C 1 -6 ) o [alquil (C 1 -6 )][N-alquil (C 1 -6 )]sulfoximinilo, cicloalquilo (C 3 - 7 ), cicloalquil (C 3 -7) -alquilo (C 1 -6 ), cicloalquenilo (C 4 - 7 ), bicicloalquilo (C 4 - 9 ), bicicloalquileno (C 4 -9 ), heterocicloalquilo (C 3 -7 ), heterocicloalquil (C3-7)alquilo (C 1 -6 ), heterocicloalquenilo (C 3 - 7 ), heterobicicloalquilo (C 4 - 9 ), espiroheterocicloalquilo (C 4 -9 ), alquilsulfinilo C 1 -6 , cicloalquilsulfonilo (C 3 -7 ) o heteroarilo, cualquiera de tales grupos puede estar opcionalmente sustituido con uno o m ás sustituyentes se lecc io nado s entre halógeno, ciano, trifluorometilo, hidroxi, alquilo C 1 -6 , cicloalquilo C 3 -7 , alcoxi C 1 -6 , alquilsulfonilo C 1 -6 , alquilsulfoximinilo C 1 -6 , alquilcarbonilo C 1 -6 , alcoxicarbonil C 1 -6 oxo y carboxi.
R 10 y R11 representan independientemente hidrógeno, halógeno, ciano, trifluorometilo o hidroxi; o -N RbRc, -O R a; alquilo C 1 -6 o alquilsulfonilo C 1 -6 ;
R 12 representa hidrógeno, halógeno o alquilo C 1 -6 ; y
Z, Y, R2, R5a, R5b, Ra, R b, Rc y Rd son como s e definen en la reivindicación 1.
3. Un com puesto de acuerdo con la reivindicación 2 representado por la fórmula (IIC), (IID), (IIE), (IIF), (IIG), (I1H), (IIJ), (IIK), (IIL) o (IIM), o un N-óxido del mismo, o una sal farmacéuticamente aceptable del mismo,
T representa -CH 2 - o -CH 2 CH 2 ;
U representa C(O) o S(O )2 ;
W representa O, S, S(O), S(O )2 , N(R14), S(O)(N-Rd) o C ( R 15)(R16);
-M- representa -CH 2 -, -CH 2 CH 2 - o -CH 2 -W-CH 2 -;
Q representa C (R 15)(R16);
R 13 representa hidrógeno, halógeno, ciano, haloalquilo (C 1 -6 ), hidroxi o alquilcarbonilamino (C 2 -6 )alquilo (C 1 -6 ); R 14 representa hidrógeno, alquilo C 1 -6 o alquilcarbonilo C 2 -6.
R 15 representa hidrógeno, halógeno, ciano, hidroxi, hidroxialquilo (C 1 -6 ), alquilsulfonilo C 1 -6 , formilo, carboxi, carboxialquilo (C 1 -6 ), alcoxicarbonilo C 2 -6 , alcoxicarbonil C 2 -6 alquilo (C 1 -6 ), aminosulfonilo, alquilsulfoximinilo (C 1 -6 ), [alquil (C 1 -6 )][Ñ-alquil (C 1 -6 )]sulfoximinilo, alquilsulfonilaminocarbonilo (C 1 -6 ), alquilcarbonilaminosulfonilo (C 2 - 6 ), alcoxiaminocarbonilo (C 1 -6 ), tetrazolilo o hidroxioxadiazolilo;
R 16 representa hidrógeno, halógeno, alquilo C 1 -6 o cicloalquilo C 3 -7 ;
Y, Z, R2, R5a y R5b son com o s e definen en la reivindicación 1; y
V, R 10 y R 11 son com o s e definen en la reivindicación 2.
5. Un com puesto de acuerdo con la reivindicación 1 representado por la fórmula (IIP), o un W-óxido del mismo, o una sal farmacéuticamente aceptable del mismo,
en la que Z, Y, R2, R5a y R5b son com o s e definen en la reivindicación 1;
R9 e s com o s e define en la reivindicación 2; y
W e s como se define en la reivindicación 3.
6. Un com puesto de acuerdo con una cualquiera de las reivindicaciones 2, 4 y 5, en el que,
R9 representa cloro, tetrahidropiranilo, hidroxiisopropilo, hidroximetilo, metoxi, isopropoxi, isopropilo, hidroxiciclobutilo, carboxibiciclo[3.1.0]hexanilo, carboxibiciclo[3.1.0]hexenilo, piperazinilo, hidroxioxetanilo, hidroxiazetidinilo, (hidroxi)(metil)azetidinilo, (hidroxi)(trifluorometil)azetidinilo, (ferc-butoxicarbonil)(hidroxi)azetidinilo, hidroxitetrahidrofuranoílo, hidroxitetrahidropiranilo, (hidroxi)dioxidotetrahidrotiopiranilo), piperidinilo, (ciano)(metil)piperidinilo, (hidroxi)(metil)piperidinilo, (carboxi)(metil)piperidinilo, acetilpiperidinilo, carboxipiperazinilpirimidinilo, ferc-butoxicarbonilpiperazinilo, morfolinilo, tiomorfolinilo, oxo-tiomorfolinilo, dioxotiomorfolinilo, oxodiazepanilo, 2-oxa-5-azabiciclo[2.2.1]heptanilo, carboxi-3-azabiciclo[3.2.1]octanilo, oxo-8-azabiciclo[3.2.1]octanilo, 3-carboxi-8-azabiciclo-[3.2.1]octanilo, 3-(dimetilaminocarbonil)-8-azabiciclo-[3.2.1]octanilo, oxo-3,6-diazabiciclo[3.2.2]nonanilo, 3,7-dioxa-9-azabiciclo[3.3.1]-nonanilo y 3,6-epiminofuro [3,2-b]furanilo, difluorociclobutanilo, difluorometilo, ferc-butoxi, aminoisopropilo, hidroxiciclopropilo, (difluoro)(hidroxi)ciclobutilo, (metil)ciclobutanodiol, (hidroxil)(metil)ciclohexilo, (metil)ciclohexanodiol, aminosulfonilo, metilsulfinilo, metilsulfoximinilo, ciclopropilsulfonilo, 2,5-diazabiciclo[2.2.1]hetanilo o metilcarboxi-3-azabiciclo[3.2.1]octanilo.
7. Un com puesto de acuerdo con una cualquiera de las reivindicaciones anteriores, en el que Y representa un arilo opcionalmente sustituido o en el que Y representa (difluorometoxi)fenilo, (difluorometoxi)(fluoro)fenilo, (cloro)(difluorometoxi)fenilo o (difluorometoxi)(ciano)fenilo.
8. Un com puesto de acuerdo con una cualquiera de las reivindicaciones anteriores, en el que R2 representa hidrógeno o halógeno.
9. Un com puesto de acuerdo con una cualquiera de las reivindicaciones anteriores, en el que R5a representa hidrógeno, hidroxi, flúor, trifluorometilo, -N(CH3)2, -NH(CO)CH3, -S O 2 -CH 3 , -C O 2 -CH 3 , metilo o metoxi.
10. Un com puesto de acuerdo con una cualquiera de las reivindicaciones anteriores, en el que
R5b representa hidrógeno o metilo.
11. Un com puesto tal com o s e define en la reivindicación 1, o un W-óxido del mismo, o una sal farmacéuticamente aceptable del mismo, para su uso en terapia.
12. Un com puesto de fórmula (I) tal com o se define en la reivindicación 1 o un W-óxido del mismo, o una sal farmacéuticamente aceptable del mismo, para su uso en el tratamiento y/o la prevención de un trastorno inflamatorio 0 autoinmunitario, un trastorno neurológico o neurodegenerativo, dolor o un trastorno nociceptivo, un trastorno cardiovascular, un trastorno metabólico, un trastorno ocular o un trastorno oncológico. 13
13. Una composición farmacéutica que comprende un com puesto de fórmula (I) tal com o s e define en la reivindicación 1 o un W-óxido del mismo, o una sal farmacéuticamente aceptable del mismo, en asociación con un vehículo farmacéuticamente aceptable.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| GBGB1321729.4A GB201321729D0 (en) | 2013-12-09 | 2013-12-09 | Therapeutic agents |
| PCT/EP2014/076884 WO2015086526A1 (en) | 2013-12-09 | 2014-12-08 | Fused tricyclic imidazole derivatives as modulators of tnf activity |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2755335T3 true ES2755335T3 (es) | 2020-04-22 |
Family
ID=50000412
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES14808658T Active ES2755335T3 (es) | 2013-12-09 | 2014-12-08 | Derivados de imidazoles tricíclicos fusionados como moduladores de la actividad del TNF |
Country Status (10)
| Country | Link |
|---|---|
| US (1) | US10087179B2 (es) |
| EP (1) | EP3080113B1 (es) |
| JP (1) | JP6445560B2 (es) |
| CN (1) | CN105814049B (es) |
| BR (1) | BR112016012990A2 (es) |
| CA (1) | CA2931758C (es) |
| ES (1) | ES2755335T3 (es) |
| GB (1) | GB201321729D0 (es) |
| RU (1) | RU2679914C9 (es) |
| WO (1) | WO2015086526A1 (es) |
Families Citing this family (28)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP5746172B2 (ja) | 2009-08-20 | 2015-07-08 | カルス セラピューティクス リミテッド | ホスホイノシチド3−キナーゼ阻害剤としての三環式複素環化合物 |
| GB201321730D0 (en) * | 2013-12-09 | 2014-01-22 | Ucb Pharma Sa | Therapeutic agents |
| GB201402431D0 (en) | 2014-02-12 | 2014-03-26 | Karus Therapeutics Ltd | Compounds |
| MY181019A (en) | 2014-10-03 | 2020-12-16 | Sanofi Sa | Fused pentacyclic imidazole derivatives |
| JP6800158B2 (ja) | 2015-02-20 | 2020-12-16 | ライジェル ファーマシューティカルズ, インコーポレイテッド | Gdf−8阻害剤 |
| AR104293A1 (es) | 2015-04-17 | 2017-07-12 | Abbvie Inc | Indazolonas como moduladores de la señalización de tnf |
| EP3294726A1 (en) | 2015-04-17 | 2018-03-21 | AbbVie Inc. | Indazolones as modulators of tnf signaling |
| UY36630A (es) | 2015-04-17 | 2016-11-30 | Abbvie Inc | Moduladores tricíclicos de la señalización por tnf |
| TWI696617B (zh) | 2015-04-28 | 2020-06-21 | 大陸商上海復尚慧創醫藥研究有限公司 | 特定蛋白質激酶抑制劑 |
| GB201509888D0 (en) | 2015-06-08 | 2015-07-22 | Ucb Biopharma Sprl | Therapeutic agents |
| GB201510758D0 (en) | 2015-06-18 | 2015-08-05 | Ucb Biopharma Sprl | Novel TNFa structure for use in therapy |
| WO2017024406A1 (en) | 2015-08-11 | 2017-02-16 | Neomed Institute | N-substituted bicyclic lactams, their preparation and their use as pharmaceuticals |
| WO2017024408A1 (en) | 2015-08-11 | 2017-02-16 | Neomed Institute | Aryl-substituted dihydroquinolinones, their preparation and their use as pharmaceuticals |
| JP6912039B2 (ja) | 2015-08-12 | 2021-07-28 | ネオメド インスティテュートNeomed Institute | 置換ベンゾイミダゾール、それらの調製及び医薬品としてのそれらの使用 |
| GB201514758D0 (en) | 2015-08-19 | 2015-09-30 | Karus Therapeutics Ltd | Formulation |
| GB201514754D0 (en) * | 2015-08-19 | 2015-09-30 | Karus Therapeutics Ltd | Compounds |
| US10501459B2 (en) | 2015-10-21 | 2019-12-10 | Neomed Institute | Substituted imidazo[1,2-a]pyridines as bromodomain inhibitors |
| WO2017127930A1 (en) | 2016-01-28 | 2017-08-03 | Neomed Institute | Substituted [1,2,4]triazolo[4,3-a]pyridines, their preparation and their use as pharmaceuticals |
| JP6968089B2 (ja) * | 2016-04-01 | 2021-11-17 | ユーシービー バイオファルマ エスアールエル | Tnf活性のモジュレーターとしての縮合六環式イミダゾール誘導体 |
| CN109195969B (zh) * | 2016-04-01 | 2021-12-21 | Ucb生物制药私人有限公司 | 作为tnf活性调节剂的稠合五环咪唑衍生物 |
| CN109219608B (zh) * | 2016-04-01 | 2021-12-21 | Ucb生物制药私人有限公司 | 作为tnf活性调节剂的稠合五环咪唑衍生物 |
| WO2017167994A1 (en) | 2016-04-01 | 2017-10-05 | Ucb Biopharma Sprl | Fused pentacyclic imidazole derivatives as modulators of tnf activity |
| GB201621907D0 (en) | 2016-12-21 | 2017-02-01 | Ucb Biopharma Sprl And Sanofi | Antibody epitope |
| CN110191709A (zh) | 2017-01-17 | 2019-08-30 | 德州大学系统董事会 | 可用作吲哚胺2,3-双加氧酶和/或色氨酸双加氧酶抑制剂的化合物 |
| US10953019B2 (en) * | 2017-03-15 | 2021-03-23 | UCB Biopharma SRL | Fused pentacyclic imidazole derivatives as modulators of TNF activity |
| EP3823604A4 (en) | 2018-07-17 | 2022-03-16 | Board of Regents, The University of Texas System | COMPOUNDS USEFUL AS INDOLEAMINE 2,3-DIOXYGENASE AND/OR TRYPTOPHANE DIOXYGENASE INHIBITORS |
| WO2020084008A1 (en) * | 2018-10-24 | 2020-04-30 | UCB Biopharma SRL | Fused pentacyclic imidazole derivatives as modulators of tnf activity |
| CN113683505A (zh) * | 2021-09-29 | 2021-11-23 | 厦门大华本安化工安全研究院有限公司 | 一种含氧代环丁基的羧酸酯类化合物的制备方法 |
Family Cites Families (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5563143A (en) * | 1994-09-21 | 1996-10-08 | Pfizer Inc. | Catechol diether compounds as inhibitors of TNF release |
| WO2004014900A1 (en) * | 2002-08-09 | 2004-02-19 | Eli Lilly And Company | Benzimidazoles and benzothiazoles as inhibitors of map kinase |
| RU2441004C1 (ru) * | 2007-12-19 | 2012-01-27 | Дженентек, Инк. | 5-анилиноимидазопиридины и способы их применения |
| BR112014030940B1 (pt) | 2012-06-11 | 2022-09-06 | UCB Biopharma SRL | Benzimidazóis que modulam tnf-alfa e composição farmacêutica compreendendo os mesmos |
| JP6259823B2 (ja) | 2012-07-13 | 2018-01-10 | ユーシービー バイオファルマ エスピーアールエル | Tnf活性の調節物質としてのイミダゾピリジン誘導体 |
| GB201212513D0 (en) | 2012-07-13 | 2012-08-29 | Ucb Pharma Sa | Therapeutic agents |
| GB201321730D0 (en) * | 2013-12-09 | 2014-01-22 | Ucb Pharma Sa | Therapeutic agents |
-
2013
- 2013-12-09 GB GBGB1321729.4A patent/GB201321729D0/en not_active Ceased
-
2014
- 2014-12-08 JP JP2016537474A patent/JP6445560B2/ja not_active Expired - Fee Related
- 2014-12-08 WO PCT/EP2014/076884 patent/WO2015086526A1/en active Application Filing
- 2014-12-08 EP EP14808658.0A patent/EP3080113B1/en active Active
- 2014-12-08 CA CA2931758A patent/CA2931758C/en active Active
- 2014-12-08 RU RU2016126974A patent/RU2679914C9/ru active
- 2014-12-08 CN CN201480067053.3A patent/CN105814049B/zh not_active Expired - Fee Related
- 2014-12-08 BR BR112016012990A patent/BR112016012990A2/pt not_active Application Discontinuation
- 2014-12-08 US US15/101,767 patent/US10087179B2/en active Active
- 2014-12-08 ES ES14808658T patent/ES2755335T3/es active Active
Also Published As
| Publication number | Publication date |
|---|---|
| RU2679914C9 (ru) | 2019-03-19 |
| EP3080113A1 (en) | 2016-10-19 |
| RU2016126974A (ru) | 2018-01-23 |
| JP2016539963A (ja) | 2016-12-22 |
| BR112016012990A2 (pt) | 2017-08-08 |
| CN105814049B (zh) | 2019-03-12 |
| RU2679914C1 (ru) | 2019-02-14 |
| JP6445560B2 (ja) | 2018-12-26 |
| US20160376268A1 (en) | 2016-12-29 |
| GB201321729D0 (en) | 2014-01-22 |
| CA2931758C (en) | 2022-10-25 |
| WO2015086526A1 (en) | 2015-06-18 |
| CA2931758A1 (en) | 2015-06-18 |
| CN105814049A (zh) | 2016-07-27 |
| US10087179B2 (en) | 2018-10-02 |
| EP3080113B1 (en) | 2019-09-18 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2755335T3 (es) | Derivados de imidazoles tricíclicos fusionados como moduladores de la actividad del TNF | |
| JP6484632B2 (ja) | Tnf活性のモジュレーターとしてのテトラヒドロイミダゾピリジン誘導体 | |
| ES2753260T3 (es) | Derivados de bencimidazoles tricíclicos fusionados como moduladores de la actividad del TNF | |
| ES2735750T3 (es) | Derivados de imidazol y pirazol condensados como moduladores de la actividad de TNF | |
| ES2810774T3 (es) | Derivados de imidazopiridina como moduladores de la actividad de TNF | |
| ES2817051T3 (es) | Derivados de imidazopirimidina como moduladores de la actividad de TNF | |
| ES2809533T3 (es) | Derivados de imidazopiridina como moduladores de la actividad de TNF | |
| RU2684641C1 (ru) | Производные пиразолопиридина в качестве модуляторов активности tnf | |
| ES2752144T3 (es) | Derivados de tetrahidrobencimidazol como moduladores de la actividad de TNF | |
| ES2775535T3 (es) | Derivados de benzotriazol como moduladores de la actividad del TNF | |
| ES2759253T3 (es) | Derivados de imidazol tricíclicos condensados como moduladores de la actividad de TNF | |
| ES2817052T3 (es) | Derivados de imidazopiridazina como moduladores de la actividad de TNF | |
| ES2809535T3 (es) | Derivados de imidazopiridina como moduladores de la actividad de TNF | |
| ES2751491T3 (es) | Derivados de purina como moduladores de la actividad de TNF | |
| ES2730942T3 (es) | Derivados de triazolopiridina como moduladores de la actividad de TNF | |
| ES2809534T3 (es) | Derivados de triazolopiridazina como moduladores de la actividad de TNF | |
| ES2809536T3 (es) | Derivados de imidazopiridina como moduladores de la actividad de TNF | |
| BR112017006669B1 (pt) | Derivados de imidazol pentacíclico fundido, composição farmacêutica compreendendo os mesmos e uso dos mesmos | |
| ES2743190T3 (es) | Derivados de imidazotizol como moduladores de la actividad de TNF | |
| JP6968092B2 (ja) | Tnf活性のモジュレーターとしての縮合五環式イミダゾール誘導体 | |
| JP6483698B2 (ja) | Tnf活性のモジュレーターとしてのテトラヒドロイミダゾピリジン誘導体 | |
| ES2807848T3 (es) | Imidazopirazinas tricíclicas fusionadas como moduladores de la actividad de TNF | |
| JP7121033B2 (ja) | Tnf活性のモジュレーターとしての縮合五環式イミダゾール誘導体 | |
| JP6968091B2 (ja) | Tnf活性のモジュレーターとしての縮合五環式イミダゾール誘導体 | |
| JP2019512533A (ja) | Tnf活性のモジュレーターとしての縮合五環式イミダゾール誘導体 |