-
Technisches Gebiet
-
Die
vorliegende Erfindung betrifft eine pharmazeutische Zusammensetzung
zur Anwendung auf der Schleimhaut zur Verwendung in der medikamentösen Therapie,
die eine wasserunlösliche
und/oder gering wasserlösliche
Substanz, ein Medikament und ein wässriges Medium enthält und einen
osmotischen Druck von 150 mOsm oder weniger hat. Mehr im Besonderen
betrifft die vorliegende Erfindung eine pharmazeutische Zusammensetzung
zur Anwendung auf der Schleimhaut, die eine wasserunlösliche und/oder
gering wasserlösliche
Substanz, ein Medikament und ein wässriges Medium enthält und einen
osmotischen Druck von 150 mOsm oder weniger hat, die herkömmlichen
pharmazeutischen Zusammensetzungen zur Anwendung auf der Schleimhaut
aufgrund der effizienten und hohen Permeabilität zum Blut an der Schleimhaut überlegen
ist.
-
Die
vorliegende Erfindung betrifft auch eine pharmazeutische Zusammensetzung
zur Anwendung auf der Schleimhaut, die ein Hämostatikum und ein Medikament
enthält.
Mehr im Besonderen betrifft die vorliegende Erfindung eine pharmazeutische
Zusammensetzung zur Anwendung auf der Schleimhaut, worin ein Medikament
mit einem Hämostatikum
vermischt wurde und die herkömmlichen
pharmazeutischen Zusammensetzungen zur Anwendung auf der Schleimhaut
aufgrund der hohen Permeabilität
und der Retention an der Schleimhaut überlegen ist.
-
Hintergrund der Erfindung
-
Die
Anwendung auf der Schleimhaut als Methode der medikamentösen Therapie
ist als nützliches
Mittel der Medikation anerkannt, weil (1) es die direkte Anwendung
auf dem betroffenen Bereich bei Erkrankungen lokaler Bereiche, wie
Nasenschleimhaut, Mundschleimhaut und Vaginalschleimhaut, erlaubt,
(2) sofortige Wirkungen für
systemische Erkrankungen erwartet werden können, wie im Falle eines Nasensprays
für die
Nasenschleimhaut und eines Suppositoriums für die Rektalschleimhaut, und
(3) die Anwen dung einfach ist im Vergleich zur Injektion, wie das
durch ein orales Medikament, das auf die Darmschleimhaut zielt,
und dergleichen repräsentiert
wird. Beispielsweise sind pharmazeutische Zubereitungen zur Anwendung
auf der Schleimhaut bereits wegen des Grundes (1) im Falle von Nasensprays
zur Behandlung von allergischer Rhinitis und wegen des Grundes (2)
im Falle von Suppositorien zur Schmerzstillung im Handel erhältlich.
-
Als
pharmazeutische Zubereitungen für
lokale Schleimhauterkrankungen geben beispielsweise Saunders et
al. (WO 92-14473) eine Suspensionszubereitung, die Tipredan als
Hauptmedikament enthält,
als pharmazeutische Zubereitung zur Behandlung von allergischer
Rhinitis an. Auch Helzner (WO 97-01337) gibt eine pharmazeutische
Zubereitung, die ein Antihistaminikum, ein Steroid und Wasser enthält, als
pharmazeutische Zubereitung zur Behandlung von allergischer Rhinitis
an. Als pharmazeutische Zubereitung für lokale Schleimhauterkrankungen
geben ferner Kim et al. (WO 98-00178) eine Suspensionszubereitung,
die eine thixotrope Eigenschaft aufweist, als pharmazeutische Zubereitung
zur Anwendung auf der Nasenschleimhaut an. Suzuki et al. (japanische
geprüfte
Patentveröffentlichung
(Kokoku) Nr. 60 (1985)-34925) geben auch eine pharmazeutische Zubereitung
mit gesteuerter Freisetzung zur Anwendung in der Nasenhöhle an,
wodurch eine wirksame Abgabe des Medikaments in einer Konzentration
möglich
ist, die ausreichend ist, um eine therapeutische Wirkung zu erzielen.
-
Als
pharmazeutische Zubereitungen für
systemische Erkrankungen wurden verschiedene Methoden angegeben,
welche die Absorption von Medikamenten durch die Schleimhaut erhöhen. Nagata
et al. (japanische ungeprüfte
Patentveröffentlichung
(Kokai) Nr. 63 (1988)-303931) geben beispielsweise ein Verfahren,
um einen Wachstumshormon-freisetzenden Faktor in flüssiger Form
mit einem osmotischen Druckverhältnis
von 1 (einem osmotischen Druck von 290 mOsm) oder niedriger in der
Nasenhöhle
anzuwenden, als Verfahren zur Ermöglichung einer schnellen und
effizienten Absorption des Wachstumshormon-freisetzenden Faktors
durch die Nasenschleimhaut zum Blutkreislauf an. Ferner geben Ohwaki
et al. (japanische ungeprüfte
Patentveröffentlichung
(Kokai) Nr. 60 (1985)-123426) ein Verfahren zur Anwendung einer
Lösung
von Secretin mit einem osmotischen Druckverhältnis von 1 bis 5 (einem osmotischen
Druck von 290-1450
mOsm) und einem pH von 2 bis 5 in der Nasenhöhle als Methode an, um eine
schnelle und wirksame Absorption von Secretin durch die Nasenschleimhaut
zum Blutkreislauf zu ermöglichen.
Ferner geben Awatsu et al. (Pharm. Res. Vol. 10, Nr. 9, 1372- 1377, 1993) ein Verfahren
zur Anwendung einer pharmazeutischen Lösung, der Polyoxyethylen-9-laurylether
als Absorptionsverstärker
zugesetzt wurde, auf der Nasenschleimhaut als Methode an, um eine
effiziente Absorption eines Granulozyten-Koloniestimulierenden Faktors
durch die Nasenschleimhaut zum Blutkreislauf zu ermöglichen.
-
Wenn
jedoch diese pharmazeutischen Zubereitungen auf der Schleimhaut
angewendet werden, kann es zu einem Tropfen von Flüssigkeit
kommen oder die pharmazeutischen Zubereitungen werden aufgrund der mukoziliären Klärfunktion
schnell von dem Schleimgewebe nach außen abgesondert etc., ehe sie
adäquat zum
Schleimhautgewebe transportiert oder permeiert werden. Deshalb kann
der Transport einer adäquaten Menge
an Medikament in das Blut nicht erfolgen, wenn eine systemische
Verabreichung durch den Transport zum Blutkreislauf versucht wird.
Ferner ist ein Verfahren der Verwendung eines Absorptionsverstärkers noch ausständig, da
der Absorptionsverstärker
das Problem der Reizung der Nasenschleimhaut mit sich bringt. Auf der
anderen Seite kann, wenn eine lokale Verabreichung durch Retention
des Medikaments im Schleimhautgewebe versucht wird, keine adäquate Menge
des Medikaments auf dem Gewebe zurückgehalten werden. Außerdem ist
die Permeation in das Schleimhautgewebe nicht adäquat, selbst wenn das Problem
der Retentivität
gelöst
wurde.
-
Es
besteht daher dringend Bedarf, eine pharmazeutische Zubereitung
zur Anwendung auf der Schleimhaut zu entwickeln, welche den Transport
einer adäquaten
Menge des Medikaments durch die Schleimhaut zum Blutkreislauf nach
der Anwendung auf der Schleimhaut ermöglicht. Alternativ besteht
Bedart an der Entwicklung einer pharmazeutischen Zubereitung zur
Anwendung auf der Schleimhaut, wobei der Transport einer adäquaten Menge
des Medikaments zum und die Retention im Schleimhautgewebe bei Anwendung
auf der Schleimhaut möglich
ist.
-
Offenbarung der Erfindung
-
Das
erste Ziel der vorliegenden Erfindung ist es daher, eine pharmazeutische
Zusammensetzung zur Anwendung auf der Schleimhaut anzugeben, die
eine effiziente und hohe Permeabilität durch die Schleimhaut zum
Blut hat, wenn sie auf der Schleimhaut angewendet wird.
-
Das
zweite Ziel der vorliegenden Erfindung ist es, eine pharmazeutische
Zusammensetzung zur Anwendung auf der Schleimhaut anzugeben, die
eine effiziente und hohe Per meabilität zur Schleimhaut und Retentivität an der
Schleimhaut zeigt, wenn sie auf der Schleimhaut angewendet wird.
-
Nach
umfangreichen Untersuchungen zur Erreichung des obigen ersten Ziels
haben die Erfinder der vorliegenden Erfindung gefunden, dass es
möglich
ist, eine pharmazeutische Zubereitung zur Anwendung auf der Schleimhaut
anzugeben, die herkömmlichen
flüssigen
Zusammensetzung aufgrund der effizienten und hohen Permeabilität durch
die Schleimhaut zum Blut überlegen
ist, indem ein Arzneimittel formuliert wird, das eine wasserunlösliche und/oder
gering wasserlösliche
Substanz enthält
und einen osmotischen Druck von 150 mOsm oder weniger hat, und damit
die vorliegende Erfindung erzielt.
-
Eine
verbesserte Absorption eines Medikaments durch die Schleimhaut durch
Kontrolle des osmotischen Drucks einer pharmazeutischen Zubereitung
wird in einem Patent von Ohwaki offenbart und in einer Publikation
von Awazu et al. (Pharm. Res. Vol. 10, Nr. 9, 1372-1377, 1993) berichtet.
Diese Phänomene
werden jedoch nur in wässrigen
Lösungszubereitungen
beobachtet, die keine wasserunlösliche
und/oder gering wasserlösliche
Substanz enthalten, und sind daher grundlegend verschieden von der
pharmazeutischen Zubereitung gemäß der vorliegenden
Erfindung, worin das Vorhandensein einer wasserunlöslichen
und/oder gering wasserlöslichen
Substanz essentiell ist. Außerdem
wurde in Osadas Patent gezeigt, dass die Absorption von Wachstumshormon-freisetzendem
Faktor durch die Nasenschleimhaut einer Ratte höher ist, wenn die Zubereitung
ein osmotisches Druckverhältnis
von 1 (osmotischer Druck von 290 mOsm) oder weniger hat, und in Ohwakis
Patent ist sie höher,
wenn Secretin ein osmotisches Druckverhältnis von 1 (osmotischen Druck
von 290 mOsm) oder höher
hat, und in Awazus Patent ist die Absorption des Granulozyten-Koloniestimulierenden Faktors
höher,
wenn die Zubereitung einen osmotischen Druck von 285 mOsm als 174
mOsm hat. Diese Beobachtungen legen nahe, dass es nicht einfach
ist, an die vorliegende Erfindung zu denken, die eine verbesserte
Absorption unabhängig
von der Art des verwendeten Medikaments erlaubt. In diesen wässrigen
Lösungszubereitungen
ist das Ausmaß der
Verbesserung bei der Absorption durch Kontrolle des osmotischen Drucks
höchstens
etwa 3-fach im Vergleich zu den isotonischen pharmazeutischen Zubereitungen,
und daher ist das Ausmaß von
10- bis 20-fach gemäß der vorliegenden
Erfindung überraschend.
-
Die
oben beschriebenen Patentanmeldungen von Saunders (WO 92-14473)
und Helzner (WO 97-01337) beschreiben pharmazeutische Zubereitungen,
die eine wasserunlösliche und/oder
gering wasserlösliche
Substanz enthalten. Die Patentanmeldung von Saunders (WO 92-11473)
gibt jedoch keine Beschreibung des osmotischen Drucks der pharmazeutischen
Zubereitungen allgemein im Anspruch und beschreibt nur in der Beschreibung,
dass Isotonie bevorzugt ist, und die Patentanmeldung von Helzner
gibt keine Beschreibung des osmotischen Drucks der pharmazeutischen
Zubereitungen allgemein und beschreibt nur in der Beschreibung,
dass die Zugabe eines isotonischen Mittels bevorzugt ist. Aus diesen
Patenten kann man somit keine drastische Erhöhung der Absorption bei niedrigen
osmotischen Drücken
erwarten.
-
Es
ist daher überraschend,
dass der Effekt der Verbesserung der Absorption eines Medikaments
durch die Schleimhaut drastisch ist, wenn eine wasserunlösliche oder
gering wasserlösliche
Substanz mit vorhanden ist. Das heißt, obwohl es Berichte darüber gibt,
dass der Effekt des niedrigen osmotischen Drucks in manchen wässrigen
Lösungszubereitungen
beobachtet wird, haben wir überraschenderweise
festgestellt, dass der Effekt beobachtet werden kann, indem eine
wasserunlösliche
oder gering wasserlösliche
Substanz zugesetzt wird, und dass der Effekt nicht von der Art des
verwendeten Medikaments abhängt.
-
Im
ersten Aspekt gibt die vorliegende Erfindung also eine wässrige pharmazeutische
Zusammensetzung für
die Anwendung auf der Schleimhaut an, die eine oder mehrere wasserunlösliche Substanzen und/oder
gering wasserlösliche
Substanzen und ein oder mehrere Medikamente enthält und einen osmotischen Druck
von 150 mOsm oder weniger hat. Die Zusammensetzung ist eine pharmazeutische
Zusammensetzung für
die Anwendung auf der Schleimhaut, die den herkömmlichen pharmazeutischen Zusammensetzungen
für die
Anwendung auf der Schleimhaut aufgrund der deutlich effizienten
und hohen Permeabilität
zum Blut an der Schleimhaut überlegen
ist.
-
Nach
intensiven Studien zur Erreichung des obigen zweiten Ziels haben
die Erfinder der vorliegenden Erfindung gefunden, dass durch Formulieren
einer pharmazeutischen Zubereitung, bei der ein Hämostatikum einer
pharmazeutischen Zubereitung, die ein Medikament enthält, zugesetzt
wurde, eine pharmazeutische Zusammensetzung für die Anwendung auf der Schleimhaut
angegeben werden kann, die effiziente und hohe Permeabilität zur und
Retentivität
an der Schleimhaut hat, und damit die vorliegende Erfindung erzielt.
-
Im
zweiten Aspekt gibt die vorliegende Erfindung also eine pharmazeutische
Zusammensetzung zur Anwendung auf der Schleimhaut an, die ein oder
mehrere Hämostatika
und ein oder mehrere Medikamente enthält, und mehr im Besonderen
eine wässrige
pharmazeutische Zusammensetzung zur Anwendung auf der Schleimhaut,
die ein oder mehrere Hämostatika,
ein oder mehrere wasserunlösliche
Substanzen und/oder gering wasserlösliche Substanzen und ein oder
mehrere Medikamente enthält
und einen osmotischen Druck von 150 mOsm oder weniger hat. Die Zusammensetzung
ist eine pharmazeutische Zusammensetzung zur Anwendung auf der Schleimhaut,
die den herkömmlichen
pharmazeutischen Zusammensetzungen zur Anwendung auf der Schleimhaut
aufgrund der deutlich effizienten und hohen Permeabilität und Retentivität an der
Schleimhaut überlegen
ist.
-
Kurzbeschreibung der Zeichnungen
-
1 ist
ein Graph, der die Beziehung zwischen dem osmotischen Druck und
der Bioverfügbarkeit
in dem Ergebnis zeigt, das das Absorptionsvermögen von Fluorescein im Arbeitsbeispiel
1 und Vergleichsbeispiel 1 vergleicht.
-
2 ist
ein Graph, der die Beziehung zwischen dem osmotischen Druck und
der Bioverfügbarkeit
in dem Ergebnis zeigt, das das Absorptionsvermögen von 5-Carboxyfluorescein
im Arbeitsbeispiel 2 und Vergleichsbeispiel 2 vergleicht.
-
3 ist
ein Graph, der die Beziehung zwischen dem osmotischen Druck und
der Bioverfügbarkeit
in dem Ergebnis zeigt, das das Absorptionsvermögen von Lachs-Calcitonin im
Arbeitsbeispiel 3 und Vergleichsbeispiel 3 vergleicht.
-
4 ist
eine Fotografie, die die Ausbreitung der Zusammensetzung zeigt,
wenn die erfindungsgemäße Zusammensetzung
mit einem osmotischen Druck von 10 mOsm (A) oder eine Zusammensetzung
mit einem osmotischen Druck von 290 mOsm (isotonischer Druck) zu
einer physiologischen Kochsalzlösung
mit dem gleichen osmotischen Druck wie der Schleim auf der Schleimhaut
(somit den Schleim simulierend) hinzugefügt wurde.
-
Ausführungsformen zur Durchführung der
Erfindung
-
Als
das Medikament der vorliegenden Erfindung kann jedwedes Mittel angewendet
werden, einschließlich
beispielsweise eines für
sedierende Hypnagoga, eines für
Anxiolytika, eines für
Krampfmittel, eines für
analgetische Antipyretika, eines für Lokalanästhetika, eines für Spasmolytika,
eines für
Kardiaka, eines für Diuretika,
eines für
Vasokonstriktoren, eines für
Vasodilatatoren, eines für
Bronchodilatatoren, eines für
Medikamente bei Ma gen- und Zwölffingerdarmgeschwür, eines
für Analgetika,
eines für
Hormonzubereitungen, eines für
Antidote, eines für
Impfstoffe, eines für
Antibiotika, eines für
Chemotherapeutika, eines für
Anti-Parkinson-Medikamente, eines für Psychoneurotika, eines für Muskelrelaxantien,
eines für
Antiarrhythmiemedikamente, eines für blutdrucksenkende Medikamente,
eines für
lipidsenkende Medikamente, eines für Atemstimulatia, eines für Expektorantia,
eines für
Antiflatulantia, eines für
Vitamine, eines für
Antiallergika und dergleichen. Unter diesen werden relativ fettlösliche Mittel
bevorzugt, und spezielle Beispiele schließen fettlösliche Vitamine, Steroide und
Prostaglandine ein. Unter den gut wasserlöslichen Mitteln werden jene
mit einem hohen Molekulargewicht bevorzugt, und spezielle Beispiele
schließen
Proteine und Peptide ein.
-
Mittel,
die günstige
Effekte entwickeln, wenn sie sich auf der Schleimhaut befinden,
schließen
beispielsweise ein: Antiallergika, wie Tranilast, Amlexanox, Repirinast,
Ibudilast, Tazanolast, Pemirolast, Oxatomid, Azelastinhydrochlorid,
Terfenadin, Astemizol, Natriumcromoglicat, Ketotifenfumarat, Emedastinfumarat, Epinastinhydrochlorid,
Mequitazin, Suplatasttosilat, Ozagrel, Seratorodast, Pranlukast,
5-Lipoxygenaseinhibitoren und Blutplättchen-aktivierende Antagonisten;
Steroide für
Rhinitis und Asthma, wie Beclometasondipropionat, Fluticasonpropionat,
Flunisolid und Mometason; Impfstoffe, wie Influenza-HA-Impfstoff,
und Mittel für die
Gentherapie, wie Antisense, Ribozym und Vektoren.
-
Im
ersten Aspekt der vorliegenden Erfindung ist die wasserunlösliche und/oder
gering wasserlösliche Substanz
eine essentielle Komponente, und im zweiten Aspekt der vorliegenden
Erfindung enthält
die Zusammensetzung vorzugsweise eine wasserunlösliche und/oder gering wasserlösliche Substanz.
Eine solche wasserunlösliche
oder gering wasserlösliche
Substanz kann jedwede Substanz sein, und bevorzugte Beispiele schließen Cellulosen
und bevorzugter kristalline Cellulosen ein.
-
Die
Konzentration der wasserunlöslichen
und/oder gering wasserlöslichen
Substanz, die im ersten Aspekt der vorliegenden Erfindung als feste
Teilchen in einem wässrigen
Medium vorhanden ist, ist vorzugsweise 0,1 Gew.-% oder höher, bezogen
auf die Gesamtmenge der Zubereitung, und bevorzugter 1 bis 10 Gew.-%. Die
Konzentration der wasserunlöslichen
und/oder gering wasserlöslichen
Substanz, die im zweiten Aspekt der vorliegenden Erfindung als feste
Teilchen in einem wässrigen
Medium vorhanden ist, ist vor zugsweise 0,1 Gew.-% oder höher, bezogen
auf die Gesamtmenge der Zubereitung, und bevorzugter 1 bis 10 Gew.-%.
-
In
jedem Aspekt der vorliegenden Erfindung ist die wasserunlösliche oder
gering wasserlösliche
Substanz, die als feste Teilchen in einem wässrigen Medium vorhanden ist,
vorzugsweise homogen in dem wässrigen
Medium dispergiert.
-
In
jedem Aspekt der vorliegenden Erfindung ist ferner vorzugsweise
ein wasserlösliches
Polymer zu der Zusammensetzung zugesetzt. Speziell können Alginsäure, Propylenglykol,
Polyethylenglykol, Glycerin, Polyoxyethylen-polyoxypropylenglykol,
Pektin, Pektin mit niedrigem Methoxylgehalt, Guar Gum, Gummi arabicum,
Carrageen, Methylcellulose, Carboxymethylcellulose-Natrium, Xanthangummi,
Hydroxypropylcellulose, Hydroxypropylmethylcellulose und dergleichen
genannt werden, und vorzugsweise können Carboxymethylcellulose-Natrium,
Xanthangummi und Hydroxypropylcellulose genannt werden. Das obige
Polyoxyethylen-polyoxypropylenglykol ist eine Reihe von Polymeren,
in denen Ethylenoxid mit einem Polypropylenglykol, das durch Polymerisation
von Propylenoxid erhalten wurde, additionspolymerisiert ist, und
sie sind nach dem mittleren Polymerisationsgrad von Propylenoxid
und Ethylenoxid in verschiedene Typen klassifiziert, wobei jeder
Typ in der vorliegenden Erfindung verwendbar ist. Außerdem können als
bevorzugte Kombinationen eines wasserlöslichen Polymers und einer
wasserunlöslichen
und/oder gering wasserlöslichen
Substanz kristalline Cellulose-Carmellose-Natrium, das eine Mischung
aus Carboxymethylcellulose-Natrium und kristalliner Cellulose ist,
genannt werden. Vorzugsweise ist die Konzentration dieser wasserlöslichen
Polymere, wenn sie zugesetzt werden, 1 Gew.-% bis 30 Gew.-%, bezogen
auf die wasserunlösliche
und/oder gering wasserlösliche Substanz.
-
Beim
ersten Aspekt der vorliegenden Erfindung ist es ein essentielles
Erfordernis, dass der osmotische Druck der pharmazeutischen Zubereitung
150 mOsm oder weniger und vorzugsweise 128 mOsm oder weniger ist,
bevorzugter 60 mOsm oder weniger, bevorzugter 30 mOsm oder weniger
und am meisten bevorzugt 10 mOsm oder weniger. Die Kontrolle des
osmotischen Druck ist beim zweiten Aspekt der vorliegenden Erfindung
nicht erforderlich, aber er ist vorzugsweise niedriger als der osmotische
Druck des Schleims auf der Schleimhaut der intendierten Verabreichungsstelle,
speziell ist er 150 mOsm oder weniger, vorzugsweise 128 mOsm oder
weniger, bevorzugter 60 mOsm oder weniger, bevorzugter 30 mOsm oder
weniger und am meisten bevorzugt 10 mOsm oder weniger.
-
In
der vorliegenden Erfindung ist die Zugabe einer Substanz zur Kontrolle
des osmotischen Drucks (den osmotischen Druck regulierendes Mittel)
nicht speziell erforderlich, aber wenn sie zugesetzt wird, kann jedwede
Substanz verwendet werden. Spezielle Beispiele schließen Salze,
wie Natriumchlorid, und wasserlösliche
Zucker, wie Glucose, ein, und von diesen sind Salze, wie Natriumchlorid,
bevorzugt.
-
Das
Hämostatikum
zur Verwendung im zweiten Aspekt der vorliegenden Erfindung kann
jedes Mittel sein, und spezielle Beispiele schließen Tranexamsäure, ε-Aminocapronsäure, Carbazochrom,
Carbazochromsulfonat, Carbazochromnatriumsulfonat, Phytonadion,
Etamsylat, Monoethanolaminoleat, Thrombin, Haemocoagulase und Adrenochrom-monoaminoguanidinmesilat
und dergleichen ein. Wenn das obige wasserlösliche Polymer zugesetzt wird,
ist das Hämostatikum
oder das Medikament vorzugsweise gut fettlöslich, und spezielle Beispiele
schließen
Carbazochrom, Carbazochromsulfonat und Carbazochromnatriumsulfonat
als Hämostatikum
und fettlösliche
Vitamine, Steroide und Prostaglandine als Medikament ein. Als das
gut wasserlösliche
Medikament ist eine Verbindung mit hohem Molekulargewicht bevorzugt,
und spezielle Beispiele schließen Proteine
und Peptide ein.
-
In
der vorliegenden Erfindung kann ein bekanntes grenzflächenaktives
Mittel zugesetzt werden, und spezielle Beispiele schließen Polysorbat
80, Glycerinmonostearat, Polyoxylstearat, Lauromacrogol, Sorbitanoleat,
Saccharosefettsäureester
und dergleichen ein. Unter diesen ist Polysorbat 80 am meisten bevorzugt.
-
Die
Menge des Medikaments zur Verwendung in der vorliegenden Erfindung
ist eine therapeutisch wirksame Menge und kann in Abhängigkeit
von der Art des verabreichten Medikaments, der Art und Schwere der
Erkrankung, dem Alter und Gewicht des Patienten und dergleichen
bestimmt werden. Sie beträgt üblicherweise
zwischen dem Gleichen bis zum 20-fachen der Menge jedes Medikaments,
die üblicherweise
für die
Injektion verwendet wird, bevorzugter vom Gleichen bis zum 10-fachen.
-
Die
Konzentration des Medikaments der vorliegenden Erfindung ist vorzugsweise
0,01 Gew.-% bis 1 Gew.-%, bezogen auf die Gesamtmenge der pharmazeutischen
Zubereitung, und am meisten bevorzugt 0,05 Gew.-% bis 0,5 Gew.-%.
-
Um
die physikalischen Eigenschaften, das Aussehen oder den Geruch der
erfindungsgemäßen Zusammensetzung
zu verbessern, kann ein bekanntes Antiseptikum, ein pH-regulierendes
Mittel, ein Konservierungsmittel, ein Puffer, ein Färbemittel,
ein Geruchsverbesserer und dergleichen auf Wunsch zugesetzt werden.
Beispielsweise können
Benzalkoniumchlorid als Antiseptikum, Salzsäure als pH-regulierendes Mittel,
Ascorbinsäure
als Konservierungsmittel, Citronensäure und Salze davon als Puffer,
Rot Nr. 2 als Färbemittel, Menthol
als Geruchsverbesserer genannt werden.
-
Die
Schleimhaut, auf der die vorliegende Erfindung angewendet wird,
kann jede Schleimhaut sein. Spezielle Beispiele schließen die
Darmschleimhaut, Magenschleimhaut, Nasenschleimhaut, Tracheal-/Bronchial-/Lungenschleimhaut,
Schleimhaut der Mundhöhle,
Rektalschleimhaut, Vaginalschleimhaut und dergleichen ein, und die
Nasenschleimhaut ist am meisten bevorzugt.
-
Die
erfindungsgemäße Zusammensetzung
kann in einer Dosierungsform formuliert werden, die für die Verabreichung
als pharmazeutische Zubereitung geeignet ist. Sie kann eine indirekte
Dosierungsform enthalten, wie eine orale Formulierung zur Verabreichung
an die Magen- und Darmschleimhaut, aber vorzugsweise wird die erfindungsgemäße Zusammensetzung
direkt auf die Schleimhaut appliziert, und am bevorzugtesten hat
sie eine Dosierungsform, die als Nebel gesprüht werden kann. In diesem Fall
kann die erfindungsgemäße Zusammensetzung
z.B. in eine gastrische oder enterische Kapsel gefüllt werden,
und die Zusammensetzung wird an die gewünschte Stelle der Schleimhaut
gebracht. Als andere Dosierungsform kann die vorliegende Erfindung,
wenn sie auf die Rektalschleimhaut gebracht wird, in eine Kapsel
in einer Einheitsdosierungsform gefüllt werden, die als Suppositorium
verabreicht wird. Wenn sie auf die Mundschleimhaut, Nasenschleimhaut oder
Vaginalschleimhaut gebracht wird, kann die erfindungsgemäße Zusammensetzung
in einen Behälter
vom Sprüh-Typ
gefüllt
werden, aus dem eine bestimmte Menge in die Mundhöhle, Nase
oder Vagina gesprüht
wird. Bei Anwendung auf der Tracheal-/Bronchial-/Lungenschleimhaut
kann die vorliegende Erfindung in einen Behälter vom Inhalations-Typ gefüllt werden,
wobei die Inhalation in die Trachea, Bronchien oder Lunge möglich ist.
-
BEISPIELE
-
Die
vorliegende Erfindung wird nun unter Bezugnahme auf die folgenden
Beispiele erläutert.
-
Fluorescein
und Carboxyfluorescein, die in der vorliegenden Erfindung verwendet
werden, sind Substanzen, die im Allgemeinen als Modellmedikament
des fettlöslichen
Medikaments niedrigen Molekulargewichts bzw. des wasserlöslichen
Medikaments niedrigen Molekulargewichts verwendet werden. Als Beispiel des
wasserlöslichen
Medikaments hohen Molekulargewichts wurde Lachs-Calcitonin verwendet.
Fluorescein wurde von Wako Pure Chemicals erhalten, 5-Carboxyfluorescein
war von Molecular Probes, Lachs-Calcitonin war
von Bachem, kristalline Cellulose Carmellose-Natrium war von AvielTM RC-591 NF, hergestellt von Asahi Chemical
Industry, Co., Ltd., Polysorbat 80 war von Wako Pure Chemicals,
Benzalkoniumchlorid war von Nakalai Tesque, Glucose war von Wako
Pure Chemicals, Natriumchlorid war von Wako Pure Chemicals, Carboxymethylcellulose-Natrium
war von Wako Pure Chemicals, Carbazochrom war von Wako Pure Chemicals,
Tranexamsäure
war von Wako Pure Chemicals.
-
Beispiel 1:
-
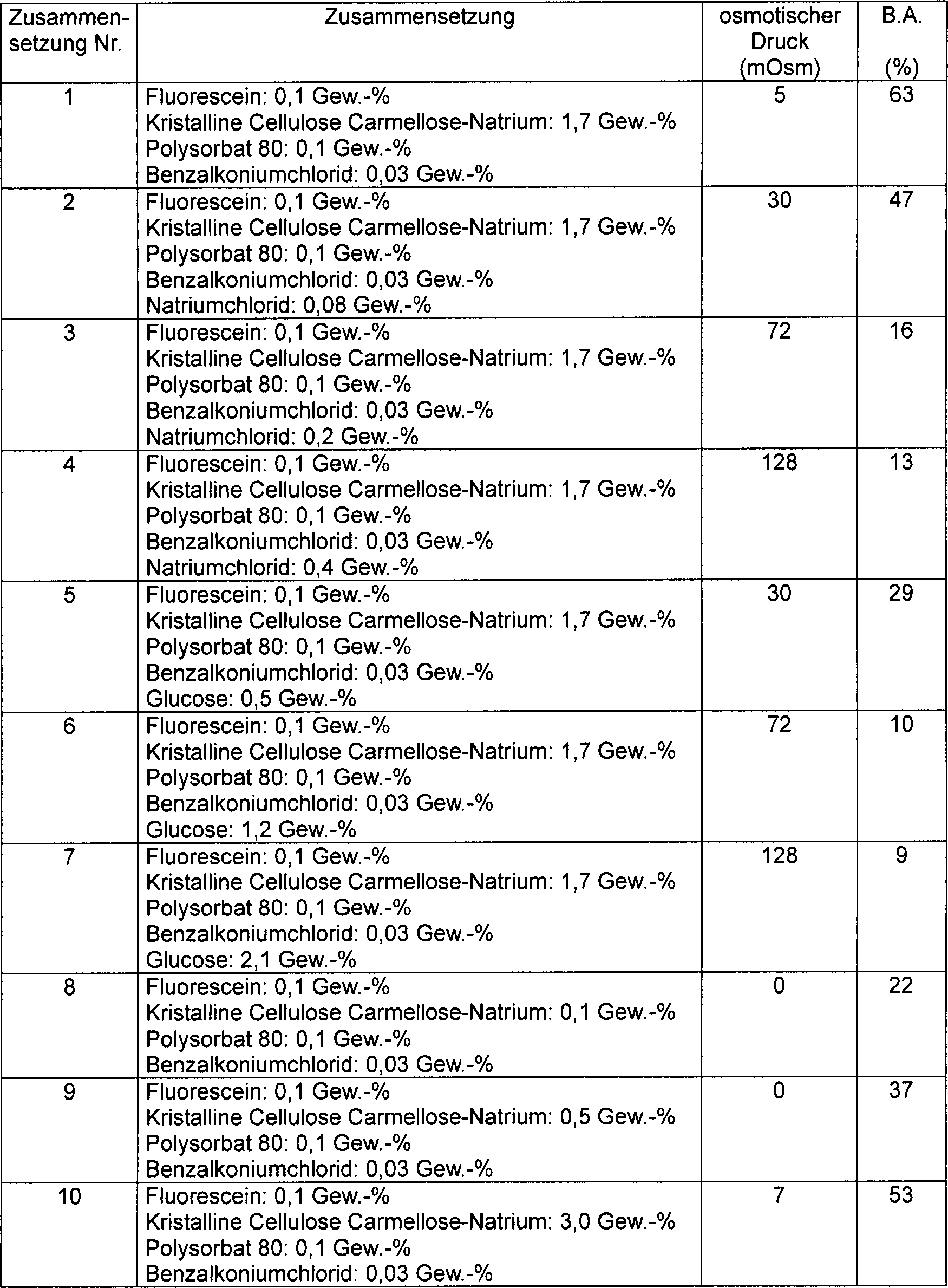
Die
Fluorescein-Zusammensetzungen Nr. 1 bis 10 zur Anwendung auf der
Schleimhaut, die in der folgenden Tabelle 1 beschriebenen Komponenten
enthaltend, wurden hergestellt. Für jede pharmazeutische Zubereitung
wurde der osmotische Druck unter Verwendung des Micro-Osmometer
Model 3MO von Advance Instruments, Inc., gemessen. Das Ergebnis
ist in der Tabelle 1 gezeigt.
-
Jeweils
100 μl der
Zusammensetzungen 1 bis 10 zur Anwendung auf der Nasenschleimhaut
wurden unter Verwendung einer im Handel erhältlichen Suspensionseinrichtung
in die einseitige Nasenhöhle
von Kaninchen (Japanese White, männlich,
3 kg schwer) gesprüht.
5, 10, 15, 30, 60 und 120 Minuten nach der Verabreichung wurden
0,5 ml Blut aus der Ohrvene entnommen, und der Plasmaspiegel von
Fluorescein wurde mittels HPLC bestimmt. Aus der Zeit-Konzentration-Kurve
bis 120 Minuten nach dem Sprühen
wurde AUC0-120min bestimmt, und die Bioverfügbarkeit
(B.A.) für
die intravenöse
Injektion wurde berechnet. Die Mittelwerte von drei Kaninchen sind
in der Tabelle 1 gezeigt.
-
-
Vergleichsbeispiel 1:
-
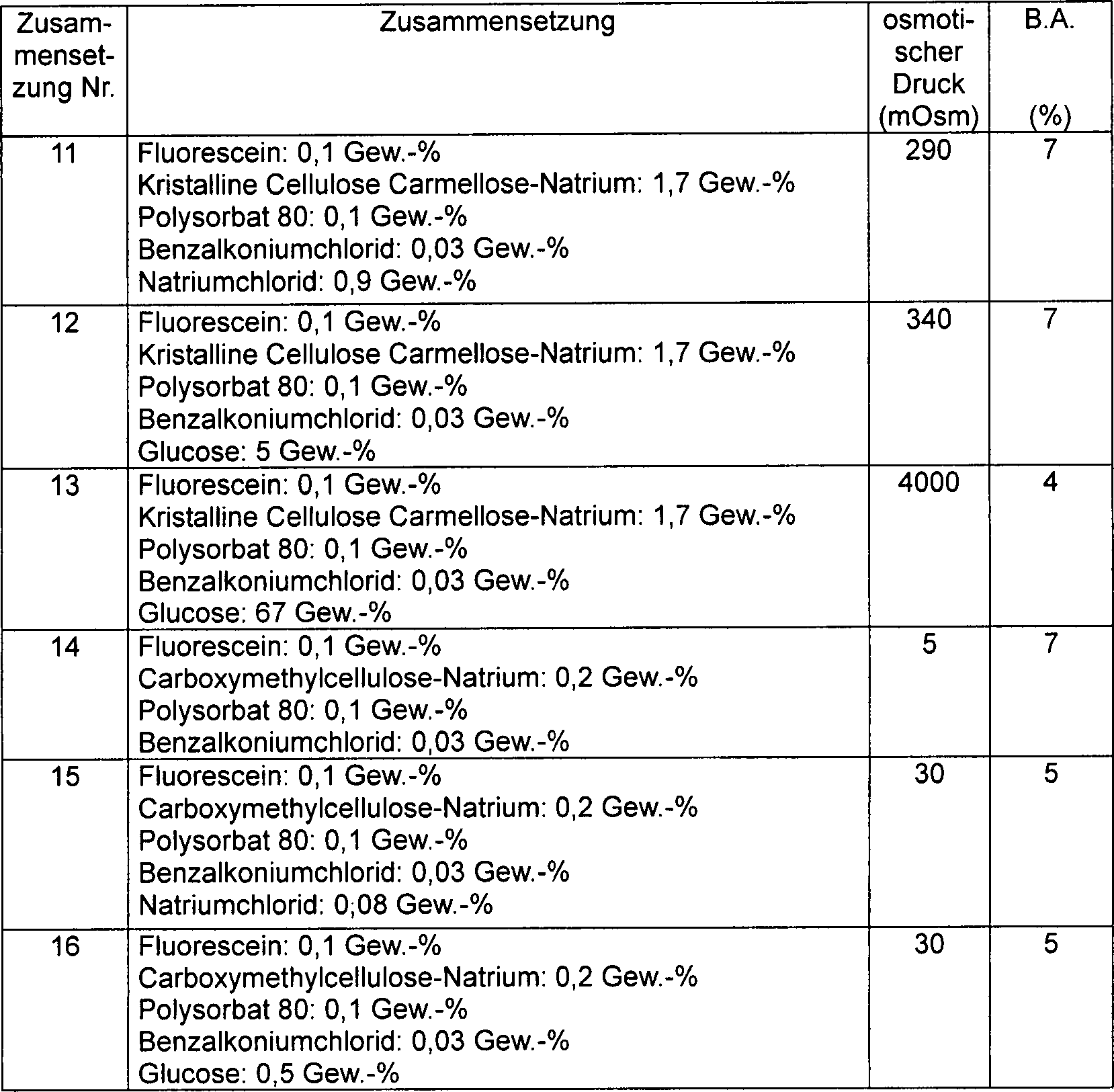
Die
Fluorescein-Zusammensetzungen Nr. 11 bis 16 zur Anwendung auf der
Schleimhaut, die in der folgenden Tabelle 2 beschriebenen Komponenten
enthaltend, wurden hergestellt. Für jede pharmazeutische Zubereitung
wurde der osmotische Druck unter Verwendung des Micro-Osmometer
Model 3MO von Advance Instruments, Inc., gemessen. Das Ergebnis
ist in der Tabelle 2 gezeigt. Die Bioverfügbarkeit (B.A.) der Zusammensetzungen
11 bis 16, bestimmt nach der im Arbeitsbeispiel 1 beschriebenen
Methode, ist ebenfalls in der Tabelle 2 gezeigt.
-
-
Beispiel 2:
-
Die
5-Carboxyfluorescein-Zusammensetzungen Nr. 17 bis 18 zur Anwendung
auf der Schleimhaut, die in der folgenden Tabelle 3 beschriebenen
Komponenten enthaltend, wurden hergestellt. Für jede pharmazeutische Zubereitung
wurde der osmotische Druck unter Verwendung des Micro-Osmometer
Model 3MO von Advance Instruments, Inc., gemessen. Das Ergebnis
ist in der Tabelle 3 gezeigt. Die Bioverfügbarkeit (B.A.) der Zusammensetzungen
17 bis 18, bestimmt nach der im Arbeitsbeispiel 1 beschriebenen
Methode, ist ebenfalls in der Tabelle 3 gezeigt.
-
-
Vergleichsbeispiel 2:
-
Die
5-Carboxyfluorescein-Zusammensetzungen Nr. 19 bis 22 zur Anwendung
auf der Schleimhaut, die in der folgenden Tabelle 4 beschriebenen
Komponenten enthaltend, wurden hergestellt. Für jede pharmazeutische Zubereitung
wurde der osmotische Druck unter Verwendung des Micro-Osmometer
Model 3MO von Advance Instruments, Inc., gemessen. Das Ergebnis
ist in der Tabelle 4 gezeigt. Die Bioverfügbarkeit (B.A.) der Zusammensetzungen
19 bis 22, bestimmt nach der im Arbeitsbeispiel 1 beschriebenen
Methode, ist ebenfalls in der Tabelle 4 gezeigt.
-
-
Beispiel 3:
-
Die
Lachs-Calcitonin-Zusammensetzungen Nr. 23 bis 24 zur Anwendung auf
der Schleimhaut, die in der folgenden Tabelle 5 beschriebenen Komponenten
enthaltend, wurden hergestellt. Für jede pharmazeutische Zubereitung
wurde der osmotische Druck unter Verwendung des Micro-Osmometer
Model 3MO von Advance Instruments, Inc., gemessen. Das Ergebnis
ist in der Tabelle 5 gezeigt. Die Bioverfügbarkeit (B.A.) der Zusammensetzungen
23 bis 24, bestimmt nach der im Arbeitsbeispiel 1 beschriebenen
Methode, ist ebenfalls in der Tabelle 5 gezeigt.
-
-
Vergleichsbeispiel 3:
-
Die
Lachs-Calcitonin-Zusammensetzungen Nr. 25 bis 28 zur Anwendung auf
der Schleimhaut, die in der folgenden Tabelle 6 beschriebenen Komponenten
enthaltend, wurden hergestellt. Für jede pharmazeutische Zubereitung
wurde der osmotische Druck unter Verwendung des Micro-Osmometer
Model 3MO von Advance Instruments, Inc., gemessen. Das Ergebnis
ist in der Tabelle 6 gezeigt. Die Bioverfügbarkeit (B.A.) der Zusammensetzungen
25 bis 28, bestimmt nach der im Arbeitsbeispiel 1 beschriebenen
Methode, ist ebenfalls in der Tabelle 6 gezeigt.
-
-
Wenn
das Modell-Medikament eine fettlösliche
Substanz mit niedrigem Molekulargewicht ist, Fluorescein, waren
die Plasmaspiegel von Fluorescein bei Kaninchen, denen eine pharmazeutische
Zubereitung mit niedrigem osmotischem Druck von 5 mOsm (Zusammensetzung
Nr. 1) auf die Nasenschleimhaut gesprüht wurde, deutlich höher als
jene bei Kaninchen, denen eine pharmazeutische Zubereitung mit einem
nahezu isotonischen osmotischen Druck von 340 mOsm (Zusammensetzung
Nr. 11 und 12) oder eine pharmazeutische Zubereitung mit einem hohen
osmotischen Druck von 4000 mOsm (Zusammensetzung Nr. 13) gesprüht wurde,
und, wie in der Tabelle 1 gezeigt, ist die Bioverfügbarkeit
um das 8- bis 15-fache erhöht.
Die Bioverfügbarkeit
nimmt mit steigendem osmotischem Druck ab, und bei 30 mOsm (Zusammensetzung
Nr. 2) ist sie drei Viertel von der von 5 mOsm (Zusammensetzung
Nr. 1) und bei höheren
72 mOsm (Zusammensetzung Nr. 3) nimmt sie in großem Ausmaß ab. Selbst bei 128 mOsm (Zusammensetzung
Nr. 4) zeigt sich eine Bioverfügbarkeit,
die etwa zweimal so hoch ist wie die der pharmazeutischen Zubereitung
mit 290 mOsm oder mehr (Zusammensetzung Nr. 11 bis 13). Es wurde
auch gezeigt, dass selbst wenn isotonisch bei niedrigem osmotischem
Druck, Salze wie Natriumchlorid (Zusammensetzung Nr. 2 bis 4) eine
höhere
Bioverfügbarkeit
haben als wasserlösliche
Salze wie Glucose (Zusammensetzung Nr. 5 bis 7). Ferner zeigt sich,
dass bis zu etwa 1,5 % je höher
die Konzentration der wasserunlöslichen
oder gering wasserlöslichen
Substanzen ist, desto höher die
Bioverfügbarkeit
ist (Vergleich zwischen Zusammensetzung Nr. 8 und 9 und Zusammensetzung
Nr. 1). Selbst bei den pharmazeutischen Zubereitungen mit einem
niedrigen osmotischen Druck waren die Plasmaspiegel fast gleich
wie bei den pharmazeutischen Zubereitungen mit isotonischem oder
hohem osmotischem Druck, wenn sie keine wasserunlöslichen
oder gering wasserlöslichen
Substanzen enthalten (Zusammensetzung Nr. 14 bis 16). Diese Ergebnisse
zeigen, dass die Wirkung des osmotischen Drucks der pharmazeutischen
Zubereitung, der isotonisch oder niedriger ist, auf die Permeabilität der gering
wasserlöslichen
Substanz zum Blut an der Schleimhaut nur deutlich gezeigt wird,
wenn eine wasserunlösliche
oder gering wasserlösliche Substanz
enthalten ist, und damit wurde die Wirkung der wässrigen pharmazeutischen Zusammensetzung
gemäß der vorliegenden
Erfindung zur Anwendung auf der Schleimhaut gezeigt.
-
Wenn
das Modell-Medikament eine wasserlösliche Substanz mit niedrigem
Molekulargewicht ist, 5-Carboxyfluorescein, sind die Plasmaspiegel
von 5-Carboxyfluorescein bei Kaninchen, denen eine pharmazeutische
Zubereitung mit niedrigem osmotischem Druck von 6 mOsm (Zusammensetzung
Nr. 17) auf die Nasenschleimhaut gesprüht wurde, deutlich höher als
jene bei Kaninchen, denen eine pharmazeutische Zubereitung mit nahezu
isotonischem osmotischem Druck von 340 mOsm (Zusammensetzung Nr.
19) oder eine pharmazeutische Zubereitung mit einem hohen osmotischen
Druck von 4000 mOsm (Zusammensetzung Nr. 20) gesprüht wurde,
und, wie in der Tabelle 3 gezeigt, ist die Bioverfügbarkeit
um das 9- bis 17-fache erhöht.
Ferner sind selbst für
die pharmazeutischen Zubereitungen mit niedrigem osmotischem Druck
die Plasmaspiegel fast gleich wie für die pharmazeutischen Zubereitungen
mit isotonischem oder hohem osmotischem Druck, wenn sie keine wasserunlösliche oder
gering wasserlösliche
Substanz enthalten (Zusammensetzung Nr. 21 bis 22).
-
Diese
Ergebnisse zeigen, dass die Wirkung des osmotischen Drucks der pharmazeutischen
Zubereitung, der isotonisch oder niedriger ist, auf die Permeabilität der gering
wasserlöslichen
Substanz zum Blut an der Schleimhaut nur deutlich gezeigt wird,
wenn eine wasserunlösliche
oder gering wasserlösliche
Substanz enthalten ist, und somit wurde die Wirkung der wässrigen
pharmazeutischen Zusammensetzung der vorliegenden Erfindung zur
Anwendung auf der Schleimhaut gezeigt.
-
Wenn
das Medikament ein wasserlösliches
Lachs-Calcitonin mit hohem Molekulargewicht ist, waren die Plasmaspiegel
von Lachs-Calcitonin bei Kaninchen, denen eine pharmazeutische Zubereitung
mit niedrigem osmotischem Druck von 10 mOsm (Zusammensetzung Nr.
23) auf die Nasenschleimhaut gesprüht wurde, deutlich höher als
jene bei Kaninchen, denen eine pharmazeutische Zubereitung mit einem
nahezu isotonischen osmotischen Druck von 340 mOsm (Zusammensetzung
Nr. 25) oder eine pharmazeutische Zubereitung mit hohem osmotischem
Druck von 4000 mOsm (Zusammensetzung Nr. 26) gesprüht wurde,
und, wie in der Tabelle 5 gezeigt, ist die Bioverfügbarkeit
um das 13- bis 19-fache erhöht.
-
Selbst
für die
pharmazeutischen Zubereitungen mit niedrigem osmotischen Druck waren
die Plasmaspiegel nahezu gleich zu den pharmazeutischen Zubereitungen
mit isotonischem oder hohem osmotischen Druck, wenn sie keine wasserunlösliche oder
gering wasserlösliche
Substanz enthalten (Zusammensetzung Nr. 27 und 28).
-
Diese
Ergebnisse zeigen, dass die Wirkung des osmotischen Drucks der pharmazeutischen
Zubereitung, der isotonisch oder niedriger ist, auf die Permeabilität der gering
wasserlöslichen
Substanz zum Blut an der Schleimhaut nur deutlich gezeigt wird,
wenn eine wasserunlösliche
oder gering wasserlösliche
Substanz enthalten ist, und somit wurde die Wirkung der wässrigen
pharmazeutischen Zusammensetzung der vorliegenden Erfindung zur
Anwendung auf der Schleimhaut gezeigt.
-
In
Bezug auf das Ergebnis, das das Absorptionsvermögen von Fluorescein in Beispiel
1 und Vergleichsbeispiel 1 vergleicht, ist die Beziehung zwischen
dem osmotischen Druck und der Bioverfügbarkeit in 1 gezeigt.
In Bezug auf das Ergebnis, das das Absorptionsvermögen von
5-Carboxyfluorescein in Beispiel 2 und Vergleichsbeispiel 2 vergleicht,
ist die Beziehung zwischen dem osmotischen Druck und der Bioverfügbarkeit
in 2 gezeigt. In Bezug auf das Ergebnis, das das
Absorptionsvermögen
von Lachs-Calcitonin in Beispiel 3 und Vergleichsbeispiel 3 vergleicht,
ist die Beziehung zwischen dem osmotischen Druck und der Bioverfügbarkeit
in 3 gezeigt. Es ist offensichtlich, dass bei jedem
der Medikamente die Bioverfügbarkeit
mit abnehmendem osmotischem Druck zunimmt und dass eine wasserunlösliche und/oder
gering wasserlösliche Substanz,
repräsentiert
durch kristalline Cellulose Carmellose-Natrium, erforderlich ist,
um eine hohe Bioverfügbarkeit
zu erreichen.
-
4 ist
eine Fotografie, die die Ausbreitung der Zusammensetzung zeigt,
wenn die erfindungsgemäße Zusammensetzung
mit einem osmotischen Druck von 10 mOsm und eine Vergleichszusammensetzung
mit einem osmotischen Druck von 290 mOsm (isotonisch) zu der physiologischen
Kochsalzlösung
mit dem gleichen osmotischen Druck wie der Schleim auf der Schleimhaut
(somit Schleim simulierend) hinzugefügt wurde. Die Figur zeigt,
dass die erfindungsgemäße Zusammensetzung
mit einem niedrigen osmotischen Druck an der Zugabestelle bleibt,
während
sich die isotonischen Zusammensetzungen leicht ausbreiten.
-
Beispiel 4:
-
Die
Fluorescein-Zusammensetzungen Nr. 29 bis 33 zur Anwendung auf der
Schleimhaut, die in der folgenden Tabelle 7 beschriebenen Komponenten
enthaltend, wurden hergestellt. Für jede pharmazeutische Zubereitung
wurde der osmotische Druck unter Verwendung des Micro-Osmometer
Model 3MO von Advance Instruments, Inc., gemessen. Das Ergebnis
ist in der Tabelle 7 gezeigt. Die Bioverfügbarkeit (B.A.) der Zusammensetzungen
29 bis 33, bestimmt nach der im Arbeitsbeispiel 1 beschriebenen
Methode, ist ebenfalls in der Tabelle 7 gezeigt. 120 min danach
wurde den Kaninchen Blut entnommen, die Nasenhöhle wurde mit 500 ml 4 mM NaOH-Lösung in
Wasser gewaschen, und dann wurde die Konzentration an Fluorescein
in der Waschlösung
mittels HPLC bestimmt. Die Menge an Fluorescein in der Waschlösung, bezogen
auf die gegebene Menge, wurde als das Restverhältnis in der Nasenhöhle berechnet,
und das mittlere Restverhältnis
in der Nasenhöhle
für drei
Kaninchen ist in der Tabelle 7 gezeigt.
-
-
Vergleichsbeispiel 4:
-
Die
Fluorescein-Zusammensetzungen Nr. 34 bis 38 zur Anwendung auf der
Schleimhaut, die in der folgenden Tabelle 8 beschriebenen Komponenten
enthaltend, wurden hergestellt. Für jede pharmazeutische Zubereitung
wurde der osmotische Druck unter Verwendung des Micro-Osmometer
Model 3MO von Advance Instruments, Inc., gemessen. Die Bioverfügbarkeit
(B.A.) und das Restverhältnis
der Zusammensetzungen 34 bis 38 in der Nasenhöhle, bestimmt nach der im Arbeitsbeispiel
4 beschriebenen Methode, sind ebenfalls in der Tabelle 8 gezeigt.
-
-
Das
Restverhältnis
in der Nasenhöhle
und die Retentivität
in der Nasenschleimhaut sind für
das Modell-Medikament Fluorescein um das 2- bis 3-fache höher in den
erfindungsgemäßen Beispielen
(Zusammensetzung Nr. 29 bis 33), die ein Hämostatikum (Carbazochrom oder
Tranexamsäure)
enthalten, als in den Vergleichsbeispielen (Zusammensetzung Nr.
34 bis 37), die kein Hämostatikum
enthalten. Insbesondere wenn der osmotische Druck so niedrig wie
5 mOsm (Zusammensetzung Nr. 29) oder 7 mOsm (Zusammensetzung Nr. 33)
ist, ist das Restverhältnis
in der Nasenhöhle
sehr hoch bei etwa 50 %. Das Ergebnis zeigt, dass ein Medikament,
das nach einer einzelnen Verabreichung des Medikament in das Blut
permeiert, auf der Schleimhaut bleibt, ohne in das Blut zu permeieren,
wenn es zusammen mit einem Hämostatikum
verabreicht wird, und damit wurde die Nützlichkeit der vorliegenden
Erfindung für
die Medikamente gezeigt, deren Wirksamkeit von der Menge des Medikaments
und der Retentionszeit auf der lokalen Schleimhaut abhängt, was
zu Nebenwirkungen führen
kann. Ferner wurde gezeigt, dass die Menge, die auf der Schleimhaut
bleibt, für
die pharmazeutischen Zubereitungen mit niedrigem osmotischem Druck
höher ist,
für die
die zum Blut permeierte Menge größer ist,
und somit ist die Nützlichkeit
der vorliegenden Erfindung sogar noch größer, wenn die pharmazeutische Zubereitung
einen niedrigen osmotischen Druck hat.
-
Gewerbliche Anwendbarkeit
-
Der
erste Aspekt der vorliegenden Erfindung gibt also eine Zusammensetzung
zur Anwendung auf der Schleimhaut an, die effiziente und hohe Permeabilität des Medikaments
durch die Schleimhaut zum Blut hat. Durch die Verwendung einer solchen
erfindungsgemäßen Zusammensetzung
zur Anwendung auf der Schleimhaut können Effekte, die gleich oder
größer sind
als jene, die mit den herkömmlichen
Zusammensetzungen erreicht werden, sogar bei kleineren Dosen und
geringerer Anwendungshäufigkeit
als bei den herkömmlichen
Methoden erhalten werden. Das kann zu einer Verminderung von Nebenwirkungen
führen.
-
Der
zweite Aspekt der vorliegenden Erfindung gibt eine Zusammensetzung
zur Anwendung auf der Schleimhaut an, die hohe Effizienz und hohe
Permeabilität
zum Blut und Retentivität
an der Schleimhaut hat. Durch die Verwendung einer solchen erfindungsgemäßen Zusammensetzung
zur Anwendung auf der Schleimhaut können Effekte, die gleich oder
größer sind
als jene, die mit herkömmlichen
Zusammensetzungen erhalten werden, sogar bei kleineren Dosen oder
niedrigerer Verabreichungshäufigkeit
als bei den herkömmlichen
Methoden erhalten werden. Das kann zu einer Verminderung von Nebenwirkungen
führen.
-
Somit
ist die vorliegende Erfindung in Bezug auf therapeutische und wirtschaftliche
Effekte außerordentlich
nützlich
für medikamentöse Therapien,
die die Anwendung auf der Schleimhaut beinhalten.