-
Die
vorliegende Erfindung betrifft ein Verfahren zum Polymerisieren
ungesättigter
Fettsäuren,
ungesättigter
Fettsäureester,
ungesättigter
Kohlenwasserstoffe oder ungesättigter
Derivate dieser Produkte durch dielektrische Erwärmung, das heißt, durch
Einsatz von Mikrowellenfrequenzen oder Hochfrequenzen.
-
Die
durch Polymerisieren gewonnenen ungesättigten Fettsäuren oder
ungesättigten
Fettsäureester sind
gut bekannt. Insbesondere sind die aus ungesättigten Pflanzenölen gewonnenen
Polymere anzuführen. Die
Polymerisierungsverfahren verwenden die Doppelverbindungen die Doppelbindungen
von Fettsäuren oder,
nach einer ersten Behandlung (Isomerisierung) die konjugierten Verbindungen.
-
Die
aktuellen Verfahren zur Herstellung dieser Polymere wie z.B. Blasöle oder
Standöle
sind gekennzeichnet durch die Verwendung von Wärme (thermisches Polymerisieren)
in Gegenwart von Katalysatoren (homogener oder heterogener). Die
Verwendung von Katalysatoren wie z.B. Sauerstoff oder Anthrachinon
ermöglicht
es, Polymere von hoher Viskosität
zu erhalten, die aber nach ihrer Herstellung sehr reaktiv sind,
was nur für
Anwendungsbereiche wie Lackieren interessant ist, wo das Produkt
trocknen muss (Vernetzungsphänomen).
-
Hingegen
werden in Bereichen wie Schmierung, Kosmetik oder Pharmazeutik eher
Polymere gewünscht,
die stabil gegenüber
externen Beschränkungen
(Sauerstoff, Wasser, ...) sind. In der Kosmetik und der Pharmazeutik
kommt mitunter noch die Beschränkung
hinzu, dass Spuren von Katalysatoren beseitigt werden müssen.
-
Polymere
sind auf diese Feststellung hin entwickelt worden: sie werden aus
Triglyceriden hergestellt, von denen wenigstens eine Fettsäure wenigsten
eine Ungesättigtheit
(konjugiert oder nicht) aufweist, vorzugsweise ohne Katalysator
und in einer sauerstofflosen Atmosphäre. Diese Entwicklungen verwenden
die thermischen Verfahren wie z.B. die Heizgürtel, die Gilotherme oder die
Widerstände,
die viel Zeit erfordern, was allgemein verhindert, Polymere zu erhalten,
die hohe Viskositäten
aufweisen; im Übrigen
sind sie aufgrund der erheblichen erforderlichen Investitionen teuer.
-
Die
Erfindung ermöglicht
es, diese wesentlichen Nachteile zu beseitigen. Die Verwendung von
Mikrowellen oder Hochfrequenzen ist von zweifachem Interesse: einerseits
wechselwirkt die Mikrowellen- oder Hochfrequenzenergie sofort auf
Molakularebene; andererseits wird weniger Energie benötigt (die
Moleküle selbst,
die durch die elektrischen Felder der Mikrowellen oder Hochfrequenzen
polarisiert werden, wandeln die elektromagnetische Energie in Wärme um).
-
Der
Antragsteller hat gemäß einem
ersten Aspekt der Erfindung entdeckt, dass das Polymerisieren ungesättigter
Fettsäuren,
ungesättigter
Fettsäureester,
ungesättigter
Kohlenwasserstoffe, ungesättigter
Derivate dieser Produkte oder deren Mischungen durch dielektrische
Erwärmung,
das heißt,
mit Hilfe von Mikrowellenfrequenzen oder Hochfrequenzen, vorzugsweise
Mikrowellen, es ermöglicht,
Produkte von hoher Viskosität mit
vorteilhafteren Reaktionszeiten zu erhalten.
-
Die
Erfindung betrifft also das allgemeine Verfahren des Polymerisierens
ungesättigter
Fettsäuren,
ungesättigter
Fettsäureester,
ungesättigter
Kohlenwasserstoffe, ungesättigter
Derivate dieser Produkte oder deren verschiedener Mischungen und
analoger Produkte durch dielektrische Erwärmung, das heißt, mit
Hilfe von Mikrowellenfrequenzen oder Hochfrequenzen, vorzugsweise
Mikrowellen.
-
Die
Verwendung von Mikrowellenenergie ist in der Industrie bereits bekannt,
jedoch in einem anderen Bereich und um auf verschiedene Probleme
einzugehen, insbesondere im Bereich der Epoxidharze und Ähnlichem.
-
Die
Mikrowellen oder Hochfrequenzen sind zum Polymerisieren der Produkte
der oben beschriebenen Art und insbesondere von Squalen nicht beschrieben
worden.
-
Ebenso
wenig ist beschrieben worden, dass das in der Kosmetik verwendete
Squalen sehr vorteilhaft durch ein Squalenpolymer, das auf preiswerte
Weise durch das Verfahren gemäß der Erfindung
gewonnen wurde, ersetzt werden kann.
-
Die
Zeit- und Energiegewinne, kombiniert mit geringeren Investitionskosten,
lassen den Beweis zu, dass das Verfahren durch dielektrische Erwärmung schneller
und wirtschaftlicher ist.
-
Die
vorliegende Erfindung befasst sich mit dem Polymerisieren ungesättigter
Fettsäuren,
ungesättigter Fettsäureester,
ungesättigter
Kohlenwasserstoffe: pflanzliche Öle,
tierische Öle
und Fette sowie deren ungesättigte
Derivate. Diese Produkte können
in roher oder raffinierter Form verwendet werden, nachdem sie eventuell
vorher einer Behandlung unterzogen wurden.
-
Die
Reaktion kann ein einziges Reagens oder ein Gemisch aus Reagenzien
in variablem Verhältnis einsetzen.
-
Das
Polymerisieren erfolgt, indem das Reagens bzw. die Reagenzien einer
dielektrischen Erwärmung unterzogen
werden, das heißt,
einer Erwärmung
unter Frequenzen, die zwischen 30 GHz und ungefähr 3 MHz betragen. Die Mikrowellenfrequenzen,
die bevorzugt werden, betragen zwischen ungefähr 30 GHz und ungefähr 300 MHz,
vorzugsweise 2,45 GHz (zulässige
Frequenz mit einer Toleranz von 2 %) oder 915 MHz (zulässige Frequenz
mit einer Toleranz von 1,4 %). Die Hochfrequenzen betragen zwischen
ungefähr
300 MHz und ungefähr
3 MHz, vorzugsweise 13,56 MHz (zulässige Frequenz mit einer Toleranz
von 0,05 %) oder 27,12 MHz (zulässige
Frequenz mit einer Toleranz von 0,6 %).
-
Die
Reaktionstemperaturen liegen zwischen 200 und 400 °C und besser
noch 230 bis 350 °C,
mit einer Temperaturanstiegszeit von drei bis sechzig Minuten, besser
noch von drei bis zwanzig Minuten, während einer Gesamtreaktionsdauer
von fünfzehn
Minuten bis fünfzehn
Stunden, vorzugsweise von fünfzehn
bis dreihundertsechzig Minuten und besser noch von fünfzehn bis
hundertzwanzig Minuten, mit oder ohne Katalysator, vorzugsweise
ohne Katalysator, unter ständigem
Rühren,
unter inerter oder nicht inerter Atmosphäre, je nachdem, was man erhalten
möchte.
-
Für die vorliegenden
Erfindungen können
das Polymerisierungsreagens oder die Polymerisierungsreagenzien
aus den tierischen oder pflanzlichen Ölen und Fetten und aus den
Polyterpenen, von denen einige von diesen Ölen und Fetten stammen, ausgewählt werden.
-
Als Öle oder
Fette von tierischer Herkunft können
unter anderem Pottwalöl,
Delphinöl,
Walöl,
Seehundöl,
Sardinenöl,
Heringöl,
Haifischöl,
Lebertran, Rindsfußöl, Rinds-,
Schweine-, Pferde-, Schafsfette (Talg) angeführt werden.
-
Als Öle von pflanzlicher
Herkunft können
unter anderem Rapsöl,
Sonnenblumenöl,
Erdnussöl,
Olivenöl,
Nussöl,
Maisöl,
Sojaöl,
Leinöl,
Hanföl,
Traubenkernöl,
Kopraöl,
Palmöl,
Baumwollsamenöl,
Babassuöl,
Jojobaöl,
Sesamöl,
Rizinusöl,
entwässertes
Rizinusöl,
Haselnussöl,
Weizenkeimöl,
Borretschöl,
Nachtkerzenöl, Tallöl angeführt werden.
-
Man
kann ebenfalls Bestandteile tierischer oder pflanzlicher Öle verwenden,
wie z.B. Squalen das aus unverseifbaren pflanzlichen Ölen (Olivenöl, Erdnussöl, Rapsöl, Maiskeimöl, Baumwollöl, Leinöl, Weizenkeimöl, Reiskleieöl) gewonnen
wurde oder in großen
Mengen in Haifischöl
enthalten ist.
-
Als
ungesättigte
Fettsäuren
kann man, allein oder in Mischung, und als nicht einschränkende Beispiele eine
oder mehrere einfach ungesättigte
Fettsäuren
wie zum Beispiel Oleinsäure,
Palmitoleinsäure,
Myristinsäure,
Petroselensäure,
Erucasäure
usw.; eine oder mehrere mehrfach ungesättigte Fettsäuren wie
zum Beispiel Linolsäure,
Alpha- und Gamma-Linolensäuren,
Arachidonsäure;
eine oder mehrere Säuren,
die konjugierte Diene oder konjugierte Triene wie zum Beispiel Licansäure oder
die Isomere der Linol- oder Linolensäuren; eine oder mehrere Säuren, die
eine oder mehrere Hydroxylgruppen umfassen, wie z.B. Rizinolensäure, verwenden.
-
Als
ungesättigte
Fettsäureester
kann man, allein oder in Mischung, und als nicht einschränkende Beispiele
einen oder mehrere der Ester die durch Veresterung zwischen einem
Monoalkohol und/oder einem Polyol (allein oder in Mischung) und
wenigstens einer ungesättigten
Fettsäure
gewonnen wurden, verwenden. Als nicht einschränkende Beispiele kann man für Monoalkohol
Methanol, Ethanol oder Butan; für
Polyole Glycerol, Sorbitol, Neopentylglykol, Trimethylpropan, Pentaerythritol,
Glykol, Ethylenglykol, Polyethylenglykol, anführen. Als Fettsäureester
kann man auch die Wachse und die Phospholipide verwenden.
-
Als
ungesättigte
Kohlenwasserstoffe kann man, allein oder in Mischung, und als nicht
einschränkende Beispiele,
ein Alken, zum Beispiel ein oder mehrere Terpenkohlenwasserstoffe,
mit oder ohne Sauerstoffanreicherung, das heißt, ein oder mehrere Isoprenpolymere
oder ein oder mehrere Isobuten-, Styren-, Ethylen-, Butadien-, Isopren-,
Propenpolymere oder ein oder mehrere Copolymerisate dieser Alkene
verwendet werden.
-
Die
ungesättigten
Derivate dieser Verbindungen können
beispielsweise durch Funktionalisieren der Restungesättigtheiten
durch ein beliebiges, dem Fachmann bekanntes Verfahren gewonnen
werden, zum Beispiel Hydrierung, Hydroxylierung, Epoxidierung oder
Sulfonierung.
-
Vorzugsweise
verwendet man als Reagens oder Reaktionsgemisch einen oder mehrere
ungesättigte Fettsäureester
oder deren Derivate, die wenigstens eine Ungesättigtheit (Amide, teilweise
hydrierte Fettsäureester,
polyoxyethylenierte Fettsäureester
usw.), allein oder in Mischung mit einem oder mehreren ungesättigten
Kohlenwasserstoffen umfassen.
-
Der
Fachmann wird verstehen, dass die Erfindung auch auf analoge Zusammensetzungen
anwendbar ist, das heißt,
deren chemische Struktur dieselbe Funktionalität der Mikrowellen oder Hochfrequenzen
in Bezug auf die Polymerisierung zulässt.
-
Die
Erfindung findet eine besonders interessante Anwendung im Hinblick
auf Squalen oder Spinacene. Es handelt sich um einen Vorläufer von
Cholesterin, der unter anderem in Haifischleber anzutreffen ist.
Er ist für
seine sehr erweichenden, antifungiziden und antibakteriellen Eigenschaften
bekannt. Er fühlt
sich außerdem
nicht fettig an, was im Bereich kosmetischer Produkte einen echten
Vorteil darstellt.
-
Diesbezüglich ist
die Patentschrift
FR 2 576 303 bekannt,
die durch Raffination von Paraffinen arbeitet. Ein weiteres bekanntes
Herstellungsverfahren ist in der Patentschrift
EP 0 228 980 beschrieben.
-
Auch
das Hydrieren der sechs Doppelbindungen von Squalen zur Herstellung
des Squalen ist bekannt, was in der Kosmetologie nützlich ist.
Dieses Verfahren ist jedoch von seiner Art her sehr kostspielig,
was für
die Industrie ein Problem ist.
-
Schließlich ist
bekannt, Unterprodukte, die aus der Raffination von Olivenöl stammen,
zu lösen,
um die Ester zu gewinnen, und die Ester zu destillieren, um das
Squalen zu gewinnen, das man zurückgewinnen kann.
-
Wie
festzustellen ist, sind Squalen und seine Derivate gut untersucht
worden, was dem Wert dieser Produkte für die Industrie angemessen
ist.
-
Wie
oben angegeben sind diese Produkte von großem potenziellem Interesse
in der Kosmetik. Wenn man jedoch das Squalen polymerisieren will,
um ein kosmetisch verwendbares Polymer zu gewinnen, dann verwenden
die zuvor beschriebenen Verfahren eine sehr kostspielige Erwärmung.
-
Die
Verwendung von Mikrowellen- oder Hochfrequenzen gemäß der Erfindung
zum Polymerisieren des Squalen löst
die oben beschriebenen Probleme.
-
Es
folgt eine ausführlichere
Beschreibung der Anwendung der Erfindung auf diese Produkte.
-
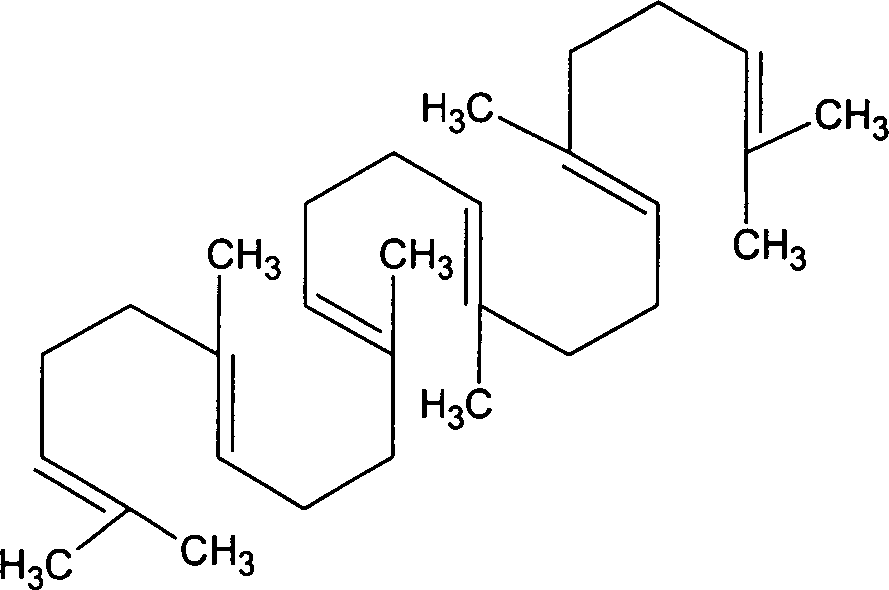
Squalen
oder Spinacene der empirischen Formel C
30H
50' ist
ein Polyterpen, das folgende entwickelte Formel aufweist:
-
Menschliches
Sebum enthält
mehr als 10 % davon, daher sein Interesse in der Dermatologie und
Kosmetologie. Squalen macht die Haut effektiv geschmeidiger (erweichende
Eigenschaft) und trägt
zu ihrem Schutz bei (antibakteriell, antifungizid). Es ist eine
gute Trägersubstanz
für Wirkstoffe
(Anwendung in der Dermatologie). Die Kosmetologen verwenden jedoch
lieber Squalan (hydriertes Squalen), weil es gesättigt und daher stabiler gegen
Oxidation ist. Aber die Hydrierung von Squalen ist teuer und bringt
wenig Differenzierung in Bezug auf die traditionellen Kohlenwasserstoffe
wie z.B. die Paraffinöle
und -wachse mit sich.
-
Vorteilhafterweise
und gemäß einem
zweiten Aspekt der Erfindung schlägt der Antragsteller vor, das Squalen
durch Squalen zu ersetzen, das mit Hilfe von Mikrowellenfrequenzen
oder Hochfrequenzen, allein oder in Kombination mit einer oder mehreren
ungesättigten
Fettsäuren
oder ungesättigten
Fettsäureestern oder
pflanzlichen oder tierischen Ölen
oder sonstigen ungesättigten
Kohlenwasserstoffen polymerisiert wurde. Weil das Squalan gelegentlich
durch ein hydriertes Polyisobuten (ungesättigter Kohlenwasserstoff)
ersetzt wird, kann man, ohne den Rahmen der vorliegenden Erfindung
zu überschreiten,
das Squalen durch ein Polyisobuten ersetzen.
-
Diese Öle und Fette
tierischer oder pflanzlicher Herkunft sowie deren Derivate können vorher
einer Behandlung unterzogen werden, die sie reaktiver oder im Gegenteil
weniger reaktiv machen soll. Die Erfindung betrifft sowohl ein einzelnes
Reagens als auch ein Reaktionsgemisch, das zwei oder mehrere Bestandteile oder
Reagenzien aufweist. Diese Reaktionsgemische können jeden Bestandteil in gleichem
Verhältnis
enthalten oder bestimmte Bestandteile können in der Mehrheit sein.
-
Das
Polymerisieren findet durch dielektrisches Erwärmen des Reagens oder des Reaktionsgemischs statt,
das heißt,
durch Erwärmen
unter Mikrowellenfrequenzen oder Hochfrequenzen. Die gewählte Temperatur
liegt vorzugsweise zwischen 200 und 400 °C, besser noch zwischen 220
und 350 °C.
-
Die
Verwendung von Mikrowellenfrequenzen oder Funkfrequenzen ermöglicht es,
eine Temperaturanstiegszeit (das heißt, die Zeit um von der Umgebungszeit
auf die Polymerisierungstemperatur zu kommen) vorzugeben, ausgewählt zwischen
drei und sechzig Minuten und besser noch zwischen drei und zwanzig
Minuten.
-
Die
Verminderung der Temperaturanstiegszeit ermöglicht es, schnell ideale Bedingungen
für die
Polymerisierung des Reagens zu schaffen und so die Gesamtreaktionszeit
zu reduzieren, was jedoch eine erhebliche Energieleistung über eine
kurze Dauer erfordert.
-
Die
Gesamtreaktionszeit hängt
von dem Reagens oder den Reagenzien, das/die verwendet wird/werden,
und von der Viskosität,
die man erhalten möchte,
ab und beträgt
vorzugsweise zwischen fünfzehn
Minuten und fünfzehn
Stunden, vorzugsweise zwischen fünfzehn
und dreihundertsechzig Minuten und besser noch zwischen fünfzehn und
hundertzwanzig Minuten. Die Gesamtreaktionszeit kann durch die Verwendung
einer höheren
Temperatur reduziert werden. Allerdings können zu hohe Temperaturen zu
einer Qualitätsminderung der
Produkte führen.
-
Man
muss also ein Verhältnis
Reaktionstemperatur/Gesamtreaktionszeit wählen, das eine optimale Polymerisierung
in kurzer Zeit aber ohne übermäßigen Energieverbrauch
und ohne Risiko eines Qualitätsverlusts
des Produkts ermöglicht.
Der Fachmann kann die Optimierung dieser Parameter anhand von Routineversuchen
gemäß den soeben
angegebenen Kriterien vornehmen.
-
Die
Polymerisierung kann mit oder ohne Katalysator stattfinden. Die
Katalysatoren können
homogen oder heterogen sein. Beispiele für einen homogenen Katalysator
sind Anthrachinon, Schwefeldioxid oder lösliche Nickelsalze. Beispiele
für einen
heterogenen Katalysator sind Zeolithe oder Ionenaustauschharze in
Säureform.
Man verwendet vorzugsweise Katalysatoren, die besonders an Hochfrequenzen
oder Mikrowellenfrequenzen angepasst sind, wie z.B. Ton vom Montmorillonit-
oder Bentonittyp, die unter dielektrischer Erwärmung eine erhöhte molekulare
Wechselwirkung bewirken.
-
Man
prüft,
ob die Rührzeit
ausreicht, um eine homogene Temperatur im Reaktor sicherzustellen.
-
Die
Polymerisierung kann unter normaler oder sauerstoffreicher Atmosphäre (zum
Beispiel zur Herstellung von Blasölen) oder vorzugsweise unter
inerter Atmosphäre
(in Gegenwart von Argonstickstoff, Helium oder anderer Edelgase,
allein oder in Mischung) stattfinden. Man arbeitet vorzugsweise
unter reduziertem Druck und achtet darauf, dass die Atmosphäre regelmäßig erneuert
wird.
-
Im
Fall von Squalen besteht die Erfindung darin, die Anzahl ungesättigter
Verbindungen zu reduzieren, indem man diese allein oder in Mischung
mit wenigstens einem der oben genannten Reagenzien mit Hilfe des oben
beschriebenen Verfahrens polymerisiert, um ein oxidationsstabiles
Polymer zu gewinnen, dessen Viskosität sich nach dem Polymerisierungsgrad
richtet. Man versieht so das Squalen mit einer zweiten Funktionalität. So gewinnt
man ein Polymer, das neben seiner erweichenden Eigenschaft ein Konsistenzmittel
für die
Rezepturen kosmetischer Produkte ist. Außerdem ist das oben beschriebene
Polymerisierungsverfahren preiswerter als das Hydrierungsverfahren,
das teure Katalysatoren verwendet.
-
Die
Polymerisierungsvorgänge
können
im "Batch" (diskontinuierlich)
stattfinden, aber vorteilhafterweise verwendet man kontinuierliche
Verfahren, um die Reaktionen zeitlich zu begrenzen.
-
Um
die Polymerisierung zu stoppen genügt es, die Temperatur des Reaktionsgemischs
so zu senken, dass sie unter der Reaktionstemperatur liegt. Diese
hängt im
Wesentlichen vom Reaktionsgemisch ab. Es ist festzuhalten, dass
die Verwendung von Mikrowellen oder Hochfrequenzen an dieser Stelle
des Verfahrens besonders vorteilhaft ist, weil keine Trägheit aufgrund
der Reaktorwände
vorhanden ist.
-
Eine
Reihe zusätzlicher
Schritte ermöglicht
es, das Polymer je nach den Anforderungen der Endanwendung zu raffinieren.
Man kann den Säuregrad
des gewonnenen Polymers reduzieren, es desodorieren, seinen Wasseranteil
reduzieren, es entfärben.
-
Diese
Raffinationsschritte sind dem Fachmann gut bekannt. Einige können angeführt werden.
-
Die
Reduzierung des Säuregrads,
der die Anzahl der freien Carbonsäuren in dem Polymer wiedergibt, erfolgt
durch übermäßiges Hinzufügen von
Mitteln, ausgewählt
aus Alkoholen, Epoxiden, Hydroxiden, Glycidilestern, allein oder
in Kombination. Dann neutralisiert man die Säurestärke, indem man Ester, Salze,
... synthetisiert. Dazu genügt
es, die Temperatur des Reaktionsgemischs bis auf die Reaktionstemperatur
dieser Ester, Salze, ... herabzusetzen.
-
Es
ist festzuhalten, dass man bei diesem Schritt dank der Mikrowellenfrequenzen
oder Hochfrequenzen Zeit gewinnt, denn die Reaktionszeiten betragen
je nach Polymer zwischen drei Minuten und drei Stunden statt durchschnittlich
dem Fünffachen
wie bei den klassischen Erwärmungsverfahren.
-
Die
Desodorierung kann durch Dampfdestillation erfolgen. Dieser Vorgang
findet bei Temperaturen zwischen 50 und 240 °C statt.
-
Nach
diesem Schritt reduziert man den Wasseranteil entweder durch traditionelle
Erwärmungsverfahren
(Erwärmung
nach traditionellem Verfahren, um die Siedetemperatur von Wasser
zu erreichen, und Destillation im Vakuum, oder Verwendung von Entfeuchtungszusammensetzungen)
oder in vorteilhafter Weise durch Verwendung einer dielektrischen
Erwärmung,
das heißt,
durch Verwendung von Mikrowellenfrequenzen oder Hochfrequenzen,
die eine Reaktion der Wassermoleküle bewirken und hier einen
weiteren Zeitgewinn bringen. Der Fachmann kann die geeignete Reduzierung
des Wasseranteils je nach vorgesehener Anwendung ermitteln; zum
Beispiel ist für
Schmiermittel ein Gehalt unter 500 ppm wünschenswert.
-
Falls
der Wasseranteil des Reagens oder des anfänglichen Reaktionsgemischs
als zu hoch erachtet wird, findet die Reduzierung des Wasseranteils
vor dem Polymerisierungsschritt statt; wie oben beschrieben können traditionelle
Erwärmungsverfahren
oder vorteilhafterweise eine dielektrische Erwärmung verwendet werden. Zum
Beispiel mildert man durch eine solche Vorgehensweise bei einem
Reaktionsgemisch, das aus Estern besteht, signifikant die Hydrolysephänomene,
die für
einen hohen Säuregrad
am Ende der Polymerisierung verantwortlich sind.
-
Das
Entfärben
kann mit Hilfe von Wasserstoffperoxid oder durch Verwendung von
entfärbender
Erden oder durch Filtrieren des gewonnenen Polymers mittels Aktivkohlefiltern
erfolgen.
-
Die
gewonnenen Polymere können
beispielsweise und ohne Einschränkung
verwendet werden:
- – zur Herstellung von Lacken,
Klebern, Haftmitteln, wenn man Trockenreagenzien wie Leinöl (Herstellung von
Standölen
oder Blasölen)
oder Trockenreaktionsgemische verwendet;
- – zur
Herstellung von Schmiermitteln oder Performanzadditive für Schmiermittel,
wenn man weniger trocknende Reagenzien wählt, wie zum Beispiel Sonnenblumenöl, Sojaöl oder Canolaöl;
- – zur
Herstellung kosmetischer Produkte, wenn man ein Reaktionsgemisch
wählt,
das beispielsweise zwischen 0 und 100 Gew.-% Squalen oder Polyisobuten
für 100
bis 0 % Fettsäureester
oder ungesättigte Pflanzenöle (Sonnenblumen-,
Soja-, Raps-, Rizinusöl
usw.) umfasst;
- – zur
Herstellung von Kunststoffen, Gummi, ... als Plastifizierungsadditive.
-
Die
folgenden Beispiele, die in keiner Weise einschränkend sind, veranschaulichen
das Interesse und den Umfang der Erfindung. Sie sollen zeigen, dass
die Verwendung von Mikrowellen oder Hochfrequenzen es ermöglicht,
die Polymerisierungsgeschwindigkeit der Reagenzien in eindrucksvoller
Weise zu beschleunigen. Darum wurden keine Raffinationsschritte
hinzugefügt,
die an sich zwar interessant sind aber zur Demonstration wenig beitragen.
-
Wir
haben Polymere unter Verwendung eines Mikrowellenherds Synthewave
(TM) der Firma Prolabo hergestellt. Dieses Gerät ist mit einem Wellenleiter
ausgestattet, der es ermöglicht,
die Mikrowellenenergie auf die Reagenzien zu konzentrieren. Er liefert
300 W Energie für
600 W Leistungsaufnahme. Die Wellenlänge beträgt 2,45 GHz. 100 ml der Versuchsreagenzien
wurden in einen Quarzreaktor von 250 ml eingebracht. Das Gerät wird so
geregelt, dass der Temperaturanstieg mit dem im klassischen Verfahren beobachteten
Temperaturanstieg übereinstimmt.
So lässt
sich nachweisen, dass die Mikrowellen eine katalytische Wirkung
haben. Allerdings ist es im Fall der Mikrowellen möglich, die
Temperaturanstiegszeit auf bis zu 80 % verglichen mit den traditionellen
Erwärmungsverfahren
zu reduzieren.
-
Dasselbe
Experiment wurde mit einer klassischen Erwärmung durchgeführt.
-
100
ml Versuchsreagenzien wurden in einen Reaktor von 250 ml, der von
außen
durch Widerstände erwärmt wurde,
eingebracht.
-
Die
Rührgeschwindigkeit
beträgt
in beiden Fällen
zwischen 60 und 100 U/Min. (Abweichung bei erhöhter Viskosität).
-
-
Bei
der angegebenen Temperatur handelt es sich um eine mittlere Temperatur
nach dem Temperaturanstieg. Es ist festzuhalten, dass das bei der
Erwärmung
durch Mikrowellenfrequenzen beobachtete Temperaturgefälle umgekehrt
zu dem Temperaturgefälle
ist, das bei der Erwärmung
auf klassischem Weg beobachtet wurde. Im ersten Fall liegt die Temperatur
an den Wänden
des Reaktors unter der Temperatur in der Mitte des Reaktionsgemischs.
Im zweiten Fall ist es umgekehrt. Es ist also wichtig, eine mittlere
Temperatur zu nehmen.
-
Die
Viskosität
ist eine dynamische Viskosität
von 40 °C,
die Ergebnisse sind in Pa.s. Die Messungen erfolgten auf einem Rheometer
Carry Mad (TM). Dies ist das Ergebnis, das die Bildung von Polymeren
nachweist.
-
Die
Iodzahl ermöglicht
es, die Ungesättigtheiten,
die reagiert haben, zu messen. Die Norm NF ISO 3961 wurde verwendet.
-
Es
ist erkennbar, dass das Temperaturniveau des Reaktionsgemischs effektiv
die Endviskosität
des Produkts beeinflusst. In allen diesen Fällen stellen wir fest, dass
die Verwendung von Mikrowellenfrequenzen eine signifikante Reduzierung
der Reaktionszeiten ermöglicht.
-
KOSMETISCHE
ANWENDUNG
-
Wir
haben eine Rezeptur für
eine Handpflegecreme verändert,
indem wir die folgenden Zutaten ganz oder teilweise durch ein polymerisiertes
Sonnenblumenöl
(HTP) durch dielektrische Erwärmung
bei 300 °C während einer
Stunde ersetzt haben:
-
Dies
sind die Vorteile der veränderten
Rezeptur:
- – sie
ist weniger seifig bei der Anwendung;
- – sie
ist erweichender (macht die Haut geschmeidig);
- – sie
bildet eine Barriere zur Erhaltung der Hautfeuchtigkeit.
-
Polymerisiertes
Sonnenblumenöl
ist vorteilhaft für
den Rezepturhersteller kosmetischer Produkte, denn:
- – das
Erweichungsvermögen
der Rezeptur ist höher,
während
der Wasseranteil erhöht
wurde;
- – das
http hat eine Viskosewirkung;
- – das
HTP ist ein Coemulgator (Verdicker).
-
ANALYSE DER
POLYMERE
-
Wir
haben durch Hochleistungs-Flüssigchromatographie
(IUPAC 2.508) den Prozentsatz an Triglyceridpolymeren bei vier Proben
von polymerisiertem Sonnenblumenöl
mit derselben Viskosität
(460 cSt bei 40 °C)
aber hergestellt durch dielektrische Erwärmung (DE) gemäß der Erfindung
oder durch traditionelle Erwärmung
(TE) ermittelt.
-
TRIGLYCERIDPOLYMERE
JE CLHP
-
-
Die
Chromatogramme der Proben 107 und 163 weisen auf Höhe der Spitze
der Retentionszeit TR = 6,65 Min.
-
Das
IUPAC 2.508-Verfahren, das zur Dosierung der Triglyceridpolymere
verwendet wurde, ist perfekt auf Triglyceridpolymere, die mittels
traditioneller Erwärmung
hergestellt wurden, abgestimmt aber nicht auf jene, die mittels
dielektrischer Erwärmung
hergestellt wurden.
-
Wir
wiesen hier die Spezifizität
der Polymere, die durch dieses neue Verfahren gewonnen wurden, nach.
-
Die
beigefügten 1 bis 12 stellen
die Chromatogramme dar, die durch Ablesung unter den Bedingungen
erhalten wurden, die auf jeder der Figuren angegeben sind.
-
QUALITATIVER VORTEIL DES
VERFAHRENS
-
"Burn-up" vermeiden:
Bei
traditioneller Erwärmung – durch
Leitung also – wird
eine Wand erwärmt,
die ihrerseits das Produkt erwärmt.
Zwischen der Wand und dem Mittelpunkt bestehen erhebliche Temperaturgefälle, die
selbst unter Rühren
zur Überhitzung
der Moleküle
an den Wänden
führen.
Der Burn-up (Beginn der Verkohlung, der im Fall von Fettkörpern in
der Bildung einer Lackschicht bestehen kann) bei Fettkörpern tritt über dem
Rußpunkt
auf, der vom Produkttyp abhängt.
Die Sonnenblume hat einen Rußpunkt
von 150 °C.
Bei der Polymerisierung pflanzlicher Öle kommt es also zu einer Verrußung des
Reaktors, die einen hohen Reinigungsaufwand verursacht. Bei der
Verwendung dielektrischer Erwärmung
tritt dieses Phänomen
nicht auf. Je mehr man bei der traditionellen Erwärmung versucht,
die Temperaturanstiegszeit herabzusetzen, desto stärker wird
die Verrußung
des Reaktors. Dieses Phänomen
ist bei der dielektrischen Erwärmung
nicht zu beobachten.
-
Trägheit vermeiden:
Jede
traditionelle Erwärmung
weist eine Trägheit
auf, die auf die Kapazität
der Wände,
Wärme zu
speichern, zurückzuführen ist.
Abschalten des Geräts
führt nicht
gleichzeitig zur Senkung der Reagenstemperatur. Es besteht eine
Latenzzeit. Bei der dielektrischen Erwärmung bewirkt das Stoppen der
Wellen ein sofortiges Sinken der Temperatur des Produkts.
-
VORTEIL DES
VERFAHRENS
-
Eines
der Hauptinteressen der Verwendung dielektrischer Erwärmung im
Fall der vorliegenden Erfindung liegt in einer erheblichen Reduzierung
der Temperaturanstiegszeit ohne Auftreten des Burn-up-Phänomens.
-
Folgendes
Experiment wurde durchgeführt:
33 g Sonnenblumenöl
werden unter Rühren
in einen Quarztiegel von 40 mm Durchmesser gegeben, der in einen
Wellenleiter positioniert wird. Mit Hilfe eines Generators von Mikrowellen
mit einer Frequenz von 2,45 GHz wird die Probe einer Leistung von
1000 W ausgesetzt. 45 GHz. Man verwendet ein Fluoroptikthermometer
(welches das Elektromagnetfeld nicht stört) und miss die Temperatur
mit Hilfe einer Faseroptiksonde, die während der Mikrowellenerwärmung in
das Öl
eingetaucht wird. Das Öl
braucht 75 s, um von 20° eine
Temperatur von 320 °C
zu erreichen.
-
Im
zweiten Experiment wird nur das Elektromagnetfeld durch einen Heißluftstrom
ersetzt, der die Tiegelwand mit mehr als 400 °C (474 °C nach 3 Minuten) erreicht.
Nicht nur braucht das Öl
7 Minuten um 320 °C zu
erreichen, man stellt auch ein Verrußen der Tiegelwand fest. Dies
ist darauf zurückzuführen, dass
das Temperaturgefälle
im Inneren des Tiegels sehr hoch ist. Das Experiment wird wiederholt,
wobei 377 °C
nicht überschritten
werden. Dieses Mal braucht das Öl
24 Minuten, um 320 °C
zu erreichen.
-
Zusammenfassende
Tabelle:
-
SONSTIGE ROHSTOFFE, DIE
VON INTERESSE SIND
-
Je
mehr das Pflanzenöl
mehrfach ungesättigt
ist, desto schneller erfolgt die Polymerisierungsreaktion des Öls. Ebenso
kann es vorteilhaft sein, in Mischung mit einfach oder mehrfach
ungesättigten Ölen, Öle zu verwenden,
die einen hohen Anteil konjugierter Fettsäuren (zum Beispiel konjugierte
Diene oder Triene) aufweisen, um die Reaktionszeit zu reduzieren.
Unter diesen Ölen
können
wie Chinaholzöl
oder Tung-Öl
(die 70 bis 80 % α-Eleostearinsäure enthalten), Öle, deren
Linolsäuren
isomerisiert wurden (zum Beispiel Sonnenblumenöl, das durch basische Katalyse
isomerisiert wurde), um einen hohen Anteil konjugierter Linolsäuren zu erhalten, Öle, die
von Samen bestimmter Kürbisgewächse stammen
(ungefähr
20 % Punicinsäure),
Oiticiaöl (ungefähr 80 %
Licansäure),
Calendulaöl
(enthält
mehr als 55 % Calendulasäure
(8t, 10t, 12c – 18
: 3)), oder dehydriertes Rizinusöl
genannt werden.
-
Dehydriertes
Rizinusöl
weist den Vorteil auf, das es aus einem Öl gewonnen wird, das zusätzlich zu seiner
einfachen Beschaffung im Vergleich zur Konjugierung linolsäurereicher Öle, in großen Mengen
im Handel erhältlich
ist (die weltweite Produktion von Rizinusöl beträgt mehrere tausend Tonnen pro
Jahr – Quelle:
Oil World Annual).
-
Dehydriertes
Rizinusöl
wird gewonnen, indem man das Rizinusöl auf Temperaturen im Bereich
von 230-250 °C
in Gegenwart von Säurekatalysatoren
erwärmt.
-
Der
Antragsteller hat entdeckt, dass sich die Reaktionszeiten für die Dehydrierung
von Rizinusöl
durch dielektrische Erwärmung
reduzieren lassen.
-
Die
Zusammensetzung an Fettsäure
von Rizinusöl
sieht folgendermaßen
aus: (%):
-
Sie
enthält
eine Mehrheit von C 18:1(OH) oder Rizinussäure.
-
Die
typischen Merkmale des Öls
sind:
-
Für das Vergleichsexperiment
wurde ein Rizinusöl
mit einer Iodzahl von 85 verwendet.
-
Folgendes
Material wurde verwendet:
-
75
ml Rizinusöl
Nr. 1 werden mit 4 Gew.-% Montmorillonit K10 gemischt. Die Rührgeschwindigkeit
beträgt
120 U/Min. Die Umgebungstemperatur wird in 20 Minuten unter Stickstoffatmosphäre auf 230 °C erhöht, dann
hält man
die Temperatur auf 230 °C,
und zwar 200 Minuten im Vakuum für
die klassische Erwärmung
und 80 Minuten für
die dielektrische Erwärmung.
Die gewonnenen Produkte werden filtriert und analysiert.
-
-
Dehydriert
man das Rizinusöl,
nimmt die Viskosität
ab, und die Iodzahl steigt. Dieses Experiment zeigt, das die Dehydrierung
von Rizinusöl
durch dielektrische Erwärmung
schneller ist als durch traditionelle Erwärmung. Es wurden zwei Stunden
Reaktionszeit gespart, für
ein überragendes
Ergebnis.
-
Dieses
Rizinusöl,
das durch dielektrische Erwärmung
dehydriert wurde, kann anschließend
zum Polymerisieren mit einem ein- oder mehrfach ungesättigten
pflanzlichen Öl
wie zum Beispiel Rapsöl
oder Sonnenblumenöl
verwendet werden. So gewinnt man in einer Stunde unter inerter Atmosphäre Copolymerisate
von sehr hoher Viskosität.
-
Die
Erfindung betrifft außerdem
so gewonnene Polymere und deren Verwendung in der Dermatologie und
Kosmetologie oder zur Herstellung von Additiven, insbesondere für Schmiermittel,
Kunststoffe, Gummi und Ähnliches.
-
Die
Erfindung betrifft ebenfalls die so gewonnenen dermatologischen
oder kosmetischen Produkte oder Produkte, die wenigstens ein solches
Polymer enthalten, sowie die Additive, insbesondere für Schmiermittel,
Kunststoffe, Gummi und Ähnliches.
-
Die
Erfindung betrifft schließlich
die industriellen Produkte, die wenigstens ein solches Additiv enthalten.
-
Die
vorliegende Erfindung wurde erklärend
und nicht einschränkend
beschrieben. Es können
selbstverständlich
alle zweckdienlichen Änderungen
an ihr vorgenommen werden, ohne den Rahmen zu überschreiten.