DE60313292T2 - Oxa- und thiadiazole und ihre verwendung als metalloproteinase-inhibitoren - Google Patents
Oxa- und thiadiazole und ihre verwendung als metalloproteinase-inhibitoren Download PDFInfo
- Publication number
- DE60313292T2 DE60313292T2 DE60313292T DE60313292T DE60313292T2 DE 60313292 T2 DE60313292 T2 DE 60313292T2 DE 60313292 T DE60313292 T DE 60313292T DE 60313292 T DE60313292 T DE 60313292T DE 60313292 T2 DE60313292 T2 DE 60313292T2
- Authority
- DE
- Germany
- Prior art keywords
- alkyl
- phenyl
- compound
- group
- alkenyl
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Lifetime
Links
- 239000003112 inhibitor Substances 0.000 title abstract description 11
- VLLMWSRANPNYQX-UHFFFAOYSA-N thiadiazole Chemical compound C1=CSN=N1.C1=CSN=N1 VLLMWSRANPNYQX-UHFFFAOYSA-N 0.000 title 1
- 150000001875 compounds Chemical class 0.000 claims abstract description 100
- -1 phenacyl group Chemical group 0.000 claims description 197
- 125000004169 (C1-C6) alkyl group Chemical group 0.000 claims description 52
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims description 48
- 238000000034 method Methods 0.000 claims description 32
- 125000000882 C2-C6 alkenyl group Chemical group 0.000 claims description 28
- 125000001072 heteroaryl group Chemical group 0.000 claims description 27
- 102000002274 Matrix Metalloproteinases Human genes 0.000 claims description 24
- 108010000684 Matrix Metalloproteinases Proteins 0.000 claims description 24
- 229910052739 hydrogen Inorganic materials 0.000 claims description 23
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 claims description 22
- 239000001257 hydrogen Substances 0.000 claims description 22
- 125000000623 heterocyclic group Chemical group 0.000 claims description 21
- 125000000753 cycloalkyl group Chemical group 0.000 claims description 20
- 238000006243 chemical reaction Methods 0.000 claims description 19
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 claims description 19
- 125000001424 substituent group Chemical group 0.000 claims description 18
- 239000002253 acid Substances 0.000 claims description 17
- 241001465754 Metazoa Species 0.000 claims description 15
- 125000004432 carbon atom Chemical group C* 0.000 claims description 14
- 125000003601 C2-C6 alkynyl group Chemical group 0.000 claims description 13
- 201000010099 disease Diseases 0.000 claims description 13
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims description 13
- 125000003118 aryl group Chemical group 0.000 claims description 12
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 claims description 12
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 claims description 11
- 229910052799 carbon Inorganic materials 0.000 claims description 11
- 239000003814 drug Substances 0.000 claims description 11
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 claims description 11
- 125000004890 (C1-C6) alkylamino group Chemical group 0.000 claims description 10
- 235000008206 alpha-amino acids Nutrition 0.000 claims description 10
- 125000000392 cycloalkenyl group Chemical group 0.000 claims description 10
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 claims description 9
- 150000002431 hydrogen Chemical class 0.000 claims description 9
- 125000002887 hydroxy group Chemical group [H]O* 0.000 claims description 9
- 210000004185 liver Anatomy 0.000 claims description 9
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims description 9
- 230000008569 process Effects 0.000 claims description 9
- 125000000217 alkyl group Chemical group 0.000 claims description 8
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 claims description 8
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 claims description 8
- 125000006239 protecting group Chemical group 0.000 claims description 8
- 125000004191 (C1-C6) alkoxy group Chemical group 0.000 claims description 7
- 125000003903 2-propenyl group Chemical group [H]C([*])([H])C([H])=C([H])[H] 0.000 claims description 7
- AVXURJPOCDRRFD-UHFFFAOYSA-N Hydroxylamine Chemical compound ON AVXURJPOCDRRFD-UHFFFAOYSA-N 0.000 claims description 7
- 150000001370 alpha-amino acid derivatives Chemical class 0.000 claims description 7
- 208000019425 cirrhosis of liver Diseases 0.000 claims description 7
- 125000004093 cyano group Chemical group *C#N 0.000 claims description 7
- 150000002148 esters Chemical class 0.000 claims description 7
- 125000005842 heteroatom Chemical group 0.000 claims description 7
- 239000000203 mixture Substances 0.000 claims description 7
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 claims description 7
- 150000003839 salts Chemical class 0.000 claims description 7
- 125000002023 trifluoromethyl group Chemical group FC(F)(F)* 0.000 claims description 7
- 125000006552 (C3-C8) cycloalkyl group Chemical group 0.000 claims description 6
- NEAQRZUHTPSBBM-UHFFFAOYSA-N 2-hydroxy-3,3-dimethyl-7-nitro-4h-isoquinolin-1-one Chemical compound C1=C([N+]([O-])=O)C=C2C(=O)N(O)C(C)(C)CC2=C1 NEAQRZUHTPSBBM-UHFFFAOYSA-N 0.000 claims description 6
- XFXPMWWXUTWYJX-UHFFFAOYSA-N Cyanide Chemical compound N#[C-] XFXPMWWXUTWYJX-UHFFFAOYSA-N 0.000 claims description 6
- 125000005843 halogen group Chemical group 0.000 claims description 6
- 238000011282 treatment Methods 0.000 claims description 6
- 125000004400 (C1-C12) alkyl group Chemical group 0.000 claims description 5
- 206010014561 Emphysema Diseases 0.000 claims description 5
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 claims description 5
- 150000001408 amides Chemical class 0.000 claims description 5
- 229940024606 amino acid Drugs 0.000 claims description 5
- 235000001014 amino acid Nutrition 0.000 claims description 5
- 150000001413 amino acids Chemical class 0.000 claims description 5
- 125000001309 chloro group Chemical group Cl* 0.000 claims description 5
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 claims description 5
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 claims description 5
- 125000001153 fluoro group Chemical group F* 0.000 claims description 5
- 229910052736 halogen Inorganic materials 0.000 claims description 5
- 150000002367 halogens Chemical class 0.000 claims description 5
- 230000002757 inflammatory effect Effects 0.000 claims description 5
- 230000001404 mediated effect Effects 0.000 claims description 5
- 201000006417 multiple sclerosis Diseases 0.000 claims description 5
- 125000004076 pyridyl group Chemical group 0.000 claims description 5
- MTCFGRXMJLQNBG-REOHCLBHSA-N (2S)-2-Amino-3-hydroxypropansäure Chemical compound OC[C@H](N)C(O)=O MTCFGRXMJLQNBG-REOHCLBHSA-N 0.000 claims description 4
- 125000003161 (C1-C6) alkylene group Chemical group 0.000 claims description 4
- 125000006554 (C4-C8) cycloalkenyl group Chemical group 0.000 claims description 4
- 125000001494 2-propynyl group Chemical group [H]C#CC([H])([H])* 0.000 claims description 4
- 239000004475 Arginine Substances 0.000 claims description 4
- WHUUTDBJXJRKMK-UHFFFAOYSA-N Glutamic acid Natural products OC(=O)C(N)CCC(O)=O WHUUTDBJXJRKMK-UHFFFAOYSA-N 0.000 claims description 4
- XUJNEKJLAYXESH-REOHCLBHSA-N L-Cysteine Chemical compound SC[C@H](N)C(O)=O XUJNEKJLAYXESH-REOHCLBHSA-N 0.000 claims description 4
- ODKSFYDXXFIFQN-BYPYZUCNSA-P L-argininium(2+) Chemical compound NC(=[NH2+])NCCC[C@H]([NH3+])C(O)=O ODKSFYDXXFIFQN-BYPYZUCNSA-P 0.000 claims description 4
- CKLJMWTZIZZHCS-REOHCLBHSA-N L-aspartic acid Chemical compound OC(=O)[C@@H](N)CC(O)=O CKLJMWTZIZZHCS-REOHCLBHSA-N 0.000 claims description 4
- WHUUTDBJXJRKMK-VKHMYHEASA-N L-glutamic acid Chemical compound OC(=O)[C@@H](N)CCC(O)=O WHUUTDBJXJRKMK-VKHMYHEASA-N 0.000 claims description 4
- HNDVDQJCIGZPNO-YFKPBYRVSA-N L-histidine Chemical compound OC(=O)[C@@H](N)CC1=CN=CN1 HNDVDQJCIGZPNO-YFKPBYRVSA-N 0.000 claims description 4
- KDXKERNSBIXSRK-YFKPBYRVSA-N L-lysine Chemical compound NCCCC[C@H](N)C(O)=O KDXKERNSBIXSRK-YFKPBYRVSA-N 0.000 claims description 4
- AYFVYJQAPQTCCC-GBXIJSLDSA-N L-threonine Chemical compound C[C@@H](O)[C@H](N)C(O)=O AYFVYJQAPQTCCC-GBXIJSLDSA-N 0.000 claims description 4
- QIVBCDIJIAJPQS-VIFPVBQESA-N L-tryptophane Chemical compound C1=CC=C2C(C[C@H](N)C(O)=O)=CNC2=C1 QIVBCDIJIAJPQS-VIFPVBQESA-N 0.000 claims description 4
- OUYCCCASQSFEME-QMMMGPOBSA-N L-tyrosine Chemical compound OC(=O)[C@@H](N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-QMMMGPOBSA-N 0.000 claims description 4
- KDXKERNSBIXSRK-UHFFFAOYSA-N Lysine Natural products NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 claims description 4
- 239000004472 Lysine Substances 0.000 claims description 4
- MTCFGRXMJLQNBG-UHFFFAOYSA-N Serine Natural products OCC(N)C(O)=O MTCFGRXMJLQNBG-UHFFFAOYSA-N 0.000 claims description 4
- AYFVYJQAPQTCCC-UHFFFAOYSA-N Threonine Natural products CC(O)C(N)C(O)=O AYFVYJQAPQTCCC-UHFFFAOYSA-N 0.000 claims description 4
- 239000004473 Threonine Substances 0.000 claims description 4
- QIVBCDIJIAJPQS-UHFFFAOYSA-N Tryptophan Natural products C1=CC=C2C(CC(N)C(O)=O)=CNC2=C1 QIVBCDIJIAJPQS-UHFFFAOYSA-N 0.000 claims description 4
- 125000000539 amino acid group Chemical group 0.000 claims description 4
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 claims description 4
- 235000009697 arginine Nutrition 0.000 claims description 4
- 235000003704 aspartic acid Nutrition 0.000 claims description 4
- UCMIRNVEIXFBKS-UHFFFAOYSA-N beta-alanine Chemical compound NCCC(O)=O UCMIRNVEIXFBKS-UHFFFAOYSA-N 0.000 claims description 4
- OQFSQFPPLPISGP-UHFFFAOYSA-N beta-carboxyaspartic acid Natural products OC(=O)C(N)C(C(O)=O)C(O)=O OQFSQFPPLPISGP-UHFFFAOYSA-N 0.000 claims description 4
- 238000005859 coupling reaction Methods 0.000 claims description 4
- 125000004851 cyclopentylmethyl group Chemical group C1(CCCC1)C* 0.000 claims description 4
- 235000018417 cysteine Nutrition 0.000 claims description 4
- XUJNEKJLAYXESH-UHFFFAOYSA-N cysteine Natural products SCC(N)C(O)=O XUJNEKJLAYXESH-UHFFFAOYSA-N 0.000 claims description 4
- 125000002541 furyl group Chemical group 0.000 claims description 4
- 235000013922 glutamic acid Nutrition 0.000 claims description 4
- 239000004220 glutamic acid Substances 0.000 claims description 4
- 235000014304 histidine Nutrition 0.000 claims description 4
- HNDVDQJCIGZPNO-UHFFFAOYSA-N histidine Natural products OC(=O)C(N)CC1=CN=CN1 HNDVDQJCIGZPNO-UHFFFAOYSA-N 0.000 claims description 4
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims description 4
- 235000018977 lysine Nutrition 0.000 claims description 4
- 238000004519 manufacturing process Methods 0.000 claims description 4
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 claims description 4
- 125000005010 perfluoroalkyl group Chemical group 0.000 claims description 4
- 235000004400 serine Nutrition 0.000 claims description 4
- 125000001544 thienyl group Chemical group 0.000 claims description 4
- 235000008521 threonine Nutrition 0.000 claims description 4
- OUYCCCASQSFEME-UHFFFAOYSA-N tyrosine Natural products OC(=O)C(N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-UHFFFAOYSA-N 0.000 claims description 4
- 235000002374 tyrosine Nutrition 0.000 claims description 4
- 125000006700 (C1-C6) alkylthio group Chemical group 0.000 claims description 3
- 125000004208 3-hydroxyphenyl group Chemical group [H]OC1=C([H])C([H])=C([H])C(*)=C1[H] 0.000 claims description 3
- QNAYBMKLOCPYGJ-REOHCLBHSA-N L-alanine Chemical compound C[C@H](N)C(O)=O QNAYBMKLOCPYGJ-REOHCLBHSA-N 0.000 claims description 3
- AGPKZVBTJJNPAG-WHFBIAKZSA-N L-isoleucine Chemical compound CC[C@H](C)[C@H](N)C(O)=O AGPKZVBTJJNPAG-WHFBIAKZSA-N 0.000 claims description 3
- ROHFNLRQFUQHCH-YFKPBYRVSA-N L-leucine Chemical compound CC(C)C[C@H](N)C(O)=O ROHFNLRQFUQHCH-YFKPBYRVSA-N 0.000 claims description 3
- FFEARJCKVFRZRR-BYPYZUCNSA-N L-methionine Chemical compound CSCC[C@H](N)C(O)=O FFEARJCKVFRZRR-BYPYZUCNSA-N 0.000 claims description 3
- COLNVLDHVKWLRT-QMMMGPOBSA-N L-phenylalanine Chemical compound OC(=O)[C@@H](N)CC1=CC=CC=C1 COLNVLDHVKWLRT-QMMMGPOBSA-N 0.000 claims description 3
- KZSNJWFQEVHDMF-BYPYZUCNSA-N L-valine Chemical compound CC(C)[C@H](N)C(O)=O KZSNJWFQEVHDMF-BYPYZUCNSA-N 0.000 claims description 3
- ROHFNLRQFUQHCH-UHFFFAOYSA-N Leucine Natural products CC(C)CC(N)C(O)=O ROHFNLRQFUQHCH-UHFFFAOYSA-N 0.000 claims description 3
- 206010064996 Ulcerative keratitis Diseases 0.000 claims description 3
- KZSNJWFQEVHDMF-UHFFFAOYSA-N Valine Natural products CC(C)C(N)C(O)=O KZSNJWFQEVHDMF-UHFFFAOYSA-N 0.000 claims description 3
- 208000006673 asthma Diseases 0.000 claims description 3
- 125000001246 bromo group Chemical group Br* 0.000 claims description 3
- 206010006451 bronchitis Diseases 0.000 claims description 3
- 125000001995 cyclobutyl group Chemical group [H]C1([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 claims description 3
- 125000000582 cycloheptyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 claims description 3
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 claims description 3
- 125000000640 cyclooctyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C([H])([H])C1([H])[H] 0.000 claims description 3
- 230000003176 fibrotic effect Effects 0.000 claims description 3
- 208000007565 gingivitis Diseases 0.000 claims description 3
- 150000004820 halides Chemical class 0.000 claims description 3
- 125000002346 iodo group Chemical group I* 0.000 claims description 3
- 229960000310 isoleucine Drugs 0.000 claims description 3
- AGPKZVBTJJNPAG-UHFFFAOYSA-N isoleucine Natural products CCC(C)C(N)C(O)=O AGPKZVBTJJNPAG-UHFFFAOYSA-N 0.000 claims description 3
- 235000014705 isoleucine Nutrition 0.000 claims description 3
- 235000005772 leucine Nutrition 0.000 claims description 3
- 235000006109 methionine Nutrition 0.000 claims description 3
- 229930182817 methionine Natural products 0.000 claims description 3
- 125000002757 morpholinyl group Chemical group 0.000 claims description 3
- 125000001280 n-hexyl group Chemical group C(CCCCC)* 0.000 claims description 3
- 125000000740 n-pentyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 claims description 3
- 125000001624 naphthyl group Chemical group 0.000 claims description 3
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 claims description 3
- 201000008482 osteoarthritis Diseases 0.000 claims description 3
- 125000004043 oxo group Chemical group O=* 0.000 claims description 3
- 229910052760 oxygen Inorganic materials 0.000 claims description 3
- COLNVLDHVKWLRT-UHFFFAOYSA-N phenylalanine Natural products OC(=O)C(N)CC1=CC=CC=C1 COLNVLDHVKWLRT-UHFFFAOYSA-N 0.000 claims description 3
- 235000008729 phenylalanine Nutrition 0.000 claims description 3
- 125000005544 phthalimido group Chemical group 0.000 claims description 3
- 238000011321 prophylaxis Methods 0.000 claims description 3
- 208000037803 restenosis Diseases 0.000 claims description 3
- 206010039073 rheumatoid arthritis Diseases 0.000 claims description 3
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 claims description 3
- 239000012453 solvate Substances 0.000 claims description 3
- 229910052717 sulfur Inorganic materials 0.000 claims description 3
- 239000004474 valine Substances 0.000 claims description 3
- 125000004642 (C1-C12) alkoxy group Chemical group 0.000 claims description 2
- 125000005862 (C1-C6)alkanoyl group Chemical group 0.000 claims description 2
- 125000006569 (C5-C6) heterocyclic group Chemical group 0.000 claims description 2
- ZYVYEJXMYBUCMN-UHFFFAOYSA-N 1-methoxy-2-methylpropane Chemical compound COCC(C)C ZYVYEJXMYBUCMN-UHFFFAOYSA-N 0.000 claims description 2
- 125000006290 2-hydroxybenzyl group Chemical group [H]OC1=C(C([H])=C([H])C([H])=C1[H])C([H])([H])* 0.000 claims description 2
- 125000004204 2-methoxyphenyl group Chemical group [H]C1=C([H])C(*)=C(OC([H])([H])[H])C([H])=C1[H] 0.000 claims description 2
- 125000000175 2-thienyl group Chemical group S1C([*])=C([H])C([H])=C1[H] 0.000 claims description 2
- OKXJJSDTQZSGLY-UHFFFAOYSA-N 3-methylphenol Chemical compound [CH2]C1=CC=CC(O)=C1 OKXJJSDTQZSGLY-UHFFFAOYSA-N 0.000 claims description 2
- 125000001541 3-thienyl group Chemical group S1C([H])=C([*])C([H])=C1[H] 0.000 claims description 2
- 125000003143 4-hydroxybenzyl group Chemical group [H]C([*])([H])C1=C([H])C([H])=C(O[H])C([H])=C1[H] 0.000 claims description 2
- 125000004203 4-hydroxyphenyl group Chemical group [H]OC1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims description 2
- 125000004172 4-methoxyphenyl group Chemical group [H]C1=C([H])C(OC([H])([H])[H])=C([H])C([H])=C1* 0.000 claims description 2
- 208000006386 Bone Resorption Diseases 0.000 claims description 2
- 239000004471 Glycine Substances 0.000 claims description 2
- ZDXPYRJPNDTMRX-VKHMYHEASA-N L-glutamine Chemical compound OC(=O)[C@@H](N)CCC(N)=O ZDXPYRJPNDTMRX-VKHMYHEASA-N 0.000 claims description 2
- 206010027476 Metastases Diseases 0.000 claims description 2
- 208000036110 Neuroinflammatory disease Diseases 0.000 claims description 2
- XAKBSHICSHRJCL-UHFFFAOYSA-N [CH2]C(=O)C1=CC=CC=C1 Chemical group [CH2]C(=O)C1=CC=CC=C1 XAKBSHICSHRJCL-UHFFFAOYSA-N 0.000 claims description 2
- DGYIJVNZSDYBOE-UHFFFAOYSA-N [CH2]C1=CC=NC=C1 Chemical group [CH2]C1=CC=NC=C1 DGYIJVNZSDYBOE-UHFFFAOYSA-N 0.000 claims description 2
- 125000002252 acyl group Chemical group 0.000 claims description 2
- 125000005073 adamantyl group Chemical group C12(CC3CC(CC(C1)C3)C2)* 0.000 claims description 2
- 125000004414 alkyl thio group Chemical group 0.000 claims description 2
- 150000001412 amines Chemical class 0.000 claims description 2
- 125000006620 amino-(C1-C6) alkyl group Chemical group 0.000 claims description 2
- 125000006615 aromatic heterocyclic group Chemical group 0.000 claims description 2
- 125000000051 benzyloxy group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])O* 0.000 claims description 2
- 229940000635 beta-alanine Drugs 0.000 claims description 2
- 230000024279 bone resorption Effects 0.000 claims description 2
- 230000009400 cancer invasion Effects 0.000 claims description 2
- 230000008878 coupling Effects 0.000 claims description 2
- 238000010168 coupling process Methods 0.000 claims description 2
- 125000004210 cyclohexylmethyl group Chemical group [H]C([H])(*)C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C1([H])[H] 0.000 claims description 2
- 125000004186 cyclopropylmethyl group Chemical group [H]C([H])(*)C1([H])C([H])([H])C1([H])[H] 0.000 claims description 2
- 238000006170 formylation reaction Methods 0.000 claims description 2
- 125000000524 functional group Chemical group 0.000 claims description 2
- ZDXPYRJPNDTMRX-UHFFFAOYSA-N glutamine Natural products OC(=O)C(N)CCC(N)=O ZDXPYRJPNDTMRX-UHFFFAOYSA-N 0.000 claims description 2
- 235000004554 glutamine Nutrition 0.000 claims description 2
- 125000004446 heteroarylalkyl group Chemical group 0.000 claims description 2
- 125000005553 heteroaryloxy group Chemical group 0.000 claims description 2
- 150000004677 hydrates Chemical class 0.000 claims description 2
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 claims description 2
- JIQNWFBLYKVZFY-UHFFFAOYSA-N methoxycyclohexatriene Chemical compound COC1=C[C]=CC=C1 JIQNWFBLYKVZFY-UHFFFAOYSA-N 0.000 claims description 2
- 125000004573 morpholin-4-yl group Chemical group N1(CCOCC1)* 0.000 claims description 2
- 125000003136 n-heptyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 claims description 2
- 201000001245 periodontitis Diseases 0.000 claims description 2
- 125000000951 phenoxy group Chemical group [H]C1=C([H])C([H])=C(O*)C([H])=C1[H] 0.000 claims description 2
- 125000003884 phenylalkyl group Chemical group 0.000 claims description 2
- 125000005346 substituted cycloalkyl group Chemical group 0.000 claims description 2
- 125000001412 tetrahydropyranyl group Chemical group 0.000 claims description 2
- 230000004614 tumor growth Effects 0.000 claims description 2
- 201000003883 Cystic fibrosis Diseases 0.000 claims 3
- 125000004344 phenylpropyl group Chemical group 0.000 claims 3
- 125000005913 (C3-C6) cycloalkyl group Chemical group 0.000 claims 2
- 208000006545 Chronic Obstructive Pulmonary Disease Diseases 0.000 claims 2
- 208000011231 Crohn disease Diseases 0.000 claims 2
- 208000028774 intestinal disease Diseases 0.000 claims 2
- 125000004178 (C1-C4) alkyl group Chemical group 0.000 claims 1
- 125000006656 (C2-C4) alkenyl group Chemical group 0.000 claims 1
- RZVAJINKPMORJF-UHFFFAOYSA-N Acetaminophen Chemical compound CC(=O)NC1=CC=C(O)C=C1 RZVAJINKPMORJF-UHFFFAOYSA-N 0.000 claims 1
- 206010053555 Arthritis bacterial Diseases 0.000 claims 1
- 208000023275 Autoimmune disease Diseases 0.000 claims 1
- 206010009900 Colitis ulcerative Diseases 0.000 claims 1
- 206010012438 Dermatitis atopic Diseases 0.000 claims 1
- 206010014989 Epidermolysis bullosa Diseases 0.000 claims 1
- 208000001860 Eye Infections Diseases 0.000 claims 1
- 206010017943 Gastrointestinal conditions Diseases 0.000 claims 1
- 206010018364 Glomerulonephritis Diseases 0.000 claims 1
- 208000004575 Infectious Arthritis Diseases 0.000 claims 1
- 241000124008 Mammalia Species 0.000 claims 1
- 201000004681 Psoriasis Diseases 0.000 claims 1
- 201000001263 Psoriatic Arthritis Diseases 0.000 claims 1
- 208000036824 Psoriatic arthropathy Diseases 0.000 claims 1
- 208000001647 Renal Insufficiency Diseases 0.000 claims 1
- 208000034189 Sclerosis Diseases 0.000 claims 1
- 208000021386 Sjogren Syndrome Diseases 0.000 claims 1
- 206010052779 Transplant rejections Diseases 0.000 claims 1
- 208000025865 Ulcer Diseases 0.000 claims 1
- 201000006704 Ulcerative Colitis Diseases 0.000 claims 1
- 201000008937 atopic dermatitis Diseases 0.000 claims 1
- 125000006297 carbonyl amino group Chemical group [H]N([*:2])C([*:1])=O 0.000 claims 1
- 210000000845 cartilage Anatomy 0.000 claims 1
- 125000001316 cycloalkyl alkyl group Chemical group 0.000 claims 1
- 230000003412 degenerative effect Effects 0.000 claims 1
- 208000011323 eye infectious disease Diseases 0.000 claims 1
- 208000006454 hepatitis Diseases 0.000 claims 1
- 231100000283 hepatitis Toxicity 0.000 claims 1
- 230000004968 inflammatory condition Effects 0.000 claims 1
- 201000006334 interstitial nephritis Diseases 0.000 claims 1
- 208000017169 kidney disease Diseases 0.000 claims 1
- 201000006370 kidney failure Diseases 0.000 claims 1
- 210000000653 nervous system Anatomy 0.000 claims 1
- 201000001119 neuropathy Diseases 0.000 claims 1
- 230000007823 neuropathy Effects 0.000 claims 1
- 125000001400 nonyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 claims 1
- 208000033808 peripheral neuropathy Diseases 0.000 claims 1
- 125000004159 quinolin-2-yl group Chemical group [H]C1=C([H])C([H])=C2C([H])=C([H])C(*)=NC2=C1[H] 0.000 claims 1
- 201000001223 septic arthritis Diseases 0.000 claims 1
- PXQLVRUNWNTZOS-UHFFFAOYSA-N sulfanyl Chemical class [SH] PXQLVRUNWNTZOS-UHFFFAOYSA-N 0.000 claims 1
- 230000036269 ulceration Effects 0.000 claims 1
- 102100030412 Matrix metalloproteinase-9 Human genes 0.000 abstract description 12
- 101000990902 Homo sapiens Matrix metalloproteinase-9 Proteins 0.000 abstract description 7
- 101000577881 Homo sapiens Macrophage metalloelastase Proteins 0.000 abstract description 4
- 102100027998 Macrophage metalloelastase Human genes 0.000 abstract description 4
- 239000011159 matrix material Substances 0.000 abstract 1
- 239000002184 metal Substances 0.000 abstract 1
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 45
- 238000005160 1H NMR spectroscopy Methods 0.000 description 37
- OKKJLVBELUTLKV-VMNATFBRSA-N methanol-d1 Chemical compound [2H]OC OKKJLVBELUTLKV-VMNATFBRSA-N 0.000 description 36
- 239000011734 sodium Substances 0.000 description 33
- 150000002500 ions Chemical class 0.000 description 32
- 230000002829 reductive effect Effects 0.000 description 24
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 22
- HEDRZPFGACZZDS-MICDWDOJSA-N Trichloro(2H)methane Chemical compound [2H]C(Cl)(Cl)Cl HEDRZPFGACZZDS-MICDWDOJSA-N 0.000 description 22
- 238000012360 testing method Methods 0.000 description 22
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 21
- 102000000588 Interleukin-2 Human genes 0.000 description 21
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 18
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 15
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 15
- 239000000243 solution Substances 0.000 description 14
- 239000003981 vehicle Substances 0.000 description 14
- 238000001644 13C nuclear magnetic resonance spectroscopy Methods 0.000 description 13
- 239000012267 brine Substances 0.000 description 13
- 230000005764 inhibitory process Effects 0.000 description 13
- 239000000047 product Substances 0.000 description 13
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical compound O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 13
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 12
- VZGDMQKNWNREIO-UHFFFAOYSA-N tetrachloromethane Chemical compound ClC(Cl)(Cl)Cl VZGDMQKNWNREIO-UHFFFAOYSA-N 0.000 description 12
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 11
- 230000015572 biosynthetic process Effects 0.000 description 11
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 10
- 210000004698 lymphocyte Anatomy 0.000 description 10
- 238000003786 synthesis reaction Methods 0.000 description 10
- 229910052943 magnesium sulfate Inorganic materials 0.000 description 9
- 235000019341 magnesium sulphate Nutrition 0.000 description 9
- KDYFGRWQOYBRFD-UHFFFAOYSA-L succinate(2-) Chemical compound [O-]C(=O)CCC([O-])=O KDYFGRWQOYBRFD-UHFFFAOYSA-L 0.000 description 9
- 108010015302 Matrix metalloproteinase-9 Proteins 0.000 description 8
- 239000012044 organic layer Substances 0.000 description 8
- 238000007920 subcutaneous administration Methods 0.000 description 8
- 230000002354 daily effect Effects 0.000 description 7
- 230000000694 effects Effects 0.000 description 7
- 239000007924 injection Substances 0.000 description 7
- 238000002347 injection Methods 0.000 description 7
- 239000011541 reaction mixture Substances 0.000 description 7
- 239000002904 solvent Substances 0.000 description 7
- 239000000725 suspension Substances 0.000 description 7
- WYURNTSHIVDZCO-UHFFFAOYSA-N tetrahydrofuran Substances C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 7
- FPQQSJJWHUJYPU-UHFFFAOYSA-N 3-(dimethylamino)propyliminomethylidene-ethylazanium;chloride Chemical compound Cl.CCN=C=NCCCN(C)C FPQQSJJWHUJYPU-UHFFFAOYSA-N 0.000 description 6
- 229920002134 Carboxymethyl cellulose Polymers 0.000 description 6
- 102000004190 Enzymes Human genes 0.000 description 6
- 108090000790 Enzymes Proteins 0.000 description 6
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 6
- 150000001721 carbon Chemical group 0.000 description 6
- ZYGHJZDHTFUPRJ-UHFFFAOYSA-N coumarin Chemical compound C1=CC=C2OC(=O)C=CC2=C1 ZYGHJZDHTFUPRJ-UHFFFAOYSA-N 0.000 description 6
- 229940088598 enzyme Drugs 0.000 description 6
- 125000002883 imidazolyl group Chemical group 0.000 description 6
- 238000007912 intraperitoneal administration Methods 0.000 description 6
- ZFFMLCVRJBZUDZ-UHFFFAOYSA-N 2,3-dimethylbutane Chemical group CC(C)C(C)C ZFFMLCVRJBZUDZ-UHFFFAOYSA-N 0.000 description 5
- 102100036475 Alanine aminotransferase 1 Human genes 0.000 description 5
- 108010082126 Alanine transaminase Proteins 0.000 description 5
- 108010003415 Aspartate Aminotransferases Proteins 0.000 description 5
- 102000004625 Aspartate Aminotransferases Human genes 0.000 description 5
- 102000029816 Collagenase Human genes 0.000 description 5
- 108060005980 Collagenase Proteins 0.000 description 5
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 5
- 102000000380 Matrix Metalloproteinase 1 Human genes 0.000 description 5
- 229920001213 Polysorbate 20 Polymers 0.000 description 5
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 5
- 239000001768 carboxy methyl cellulose Substances 0.000 description 5
- 235000010948 carboxy methyl cellulose Nutrition 0.000 description 5
- 239000008112 carboxymethyl-cellulose Substances 0.000 description 5
- 235000019441 ethanol Nutrition 0.000 description 5
- 239000003921 oil Substances 0.000 description 5
- 235000019198 oils Nutrition 0.000 description 5
- 239000000256 polyoxyethylene sorbitan monolaurate Substances 0.000 description 5
- 235000010486 polyoxyethylene sorbitan monolaurate Nutrition 0.000 description 5
- 238000002360 preparation method Methods 0.000 description 5
- 230000007115 recruitment Effects 0.000 description 5
- 229920006395 saturated elastomer Polymers 0.000 description 5
- 235000017557 sodium bicarbonate Nutrition 0.000 description 5
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 5
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 5
- YEDUAINPPJYDJZ-UHFFFAOYSA-N 2-hydroxybenzothiazole Chemical compound C1=CC=C2SC(O)=NC2=C1 YEDUAINPPJYDJZ-UHFFFAOYSA-N 0.000 description 4
- 108010021749 7-methoxycoumarin-4-yl-acetyl-prolyl-leucyl-glycyl-leucyl-(3-(2,4-dinitrophenyl)-2,3-diaminopropanoyl)-alanyl-argininamide Proteins 0.000 description 4
- ZDQWESQEGGJUCH-UHFFFAOYSA-N Diisopropyl adipate Chemical compound CC(C)OC(=O)CCCCC(=O)OC(C)C ZDQWESQEGGJUCH-UHFFFAOYSA-N 0.000 description 4
- 206010016654 Fibrosis Diseases 0.000 description 4
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 4
- 108060008682 Tumor Necrosis Factor Proteins 0.000 description 4
- 102000000852 Tumor Necrosis Factor-alpha Human genes 0.000 description 4
- 239000000872 buffer Substances 0.000 description 4
- 230000004761 fibrosis Effects 0.000 description 4
- 150000002430 hydrocarbons Chemical group 0.000 description 4
- NPZTUJOABDZTLV-UHFFFAOYSA-N hydroxybenzotriazole Substances O=C1C=CC=C2NNN=C12 NPZTUJOABDZTLV-UHFFFAOYSA-N 0.000 description 4
- 238000002955 isolation Methods 0.000 description 4
- 238000007726 management method Methods 0.000 description 4
- 108090000765 processed proteins & peptides Proteins 0.000 description 4
- 239000011780 sodium chloride Substances 0.000 description 4
- 239000000126 substance Substances 0.000 description 4
- 239000000758 substrate Substances 0.000 description 4
- 239000006188 syrup Substances 0.000 description 4
- 235000020357 syrup Nutrition 0.000 description 4
- MZOFCQQQCNRIBI-VMXHOPILSA-N (3s)-4-[[(2s)-1-[[(2s)-1-[[(1s)-1-carboxy-2-hydroxyethyl]amino]-4-methyl-1-oxopentan-2-yl]amino]-5-(diaminomethylideneamino)-1-oxopentan-2-yl]amino]-3-[[2-[[(2s)-2,6-diaminohexanoyl]amino]acetyl]amino]-4-oxobutanoic acid Chemical compound OC[C@@H](C(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCCN=C(N)N)NC(=O)[C@H](CC(O)=O)NC(=O)CNC(=O)[C@@H](N)CCCCN MZOFCQQQCNRIBI-VMXHOPILSA-N 0.000 description 3
- 102100026802 72 kDa type IV collagenase Human genes 0.000 description 3
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 3
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 3
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 3
- WSFSSNUMVMOOMR-UHFFFAOYSA-N Formaldehyde Chemical compound O=C WSFSSNUMVMOOMR-UHFFFAOYSA-N 0.000 description 3
- 108010010803 Gelatin Proteins 0.000 description 3
- 102000013382 Gelatinases Human genes 0.000 description 3
- 108010026132 Gelatinases Proteins 0.000 description 3
- 229940124761 MMP inhibitor Drugs 0.000 description 3
- 108010016113 Matrix Metalloproteinase 1 Proteins 0.000 description 3
- 241000699670 Mus sp. Species 0.000 description 3
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 3
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 3
- 150000007513 acids Chemical class 0.000 description 3
- 150000001371 alpha-amino acids Chemical class 0.000 description 3
- 125000003277 amino group Chemical group 0.000 description 3
- 229960003121 arginine Drugs 0.000 description 3
- 229960005261 aspartic acid Drugs 0.000 description 3
- 238000003556 assay Methods 0.000 description 3
- 239000012131 assay buffer Substances 0.000 description 3
- 125000003785 benzimidazolyl group Chemical group N1=C(NC2=C1C=CC=C2)* 0.000 description 3
- JFDZBHWFFUWGJE-UHFFFAOYSA-N benzonitrile Chemical compound N#CC1=CC=CC=C1 JFDZBHWFFUWGJE-UHFFFAOYSA-N 0.000 description 3
- 210000004369 blood Anatomy 0.000 description 3
- 239000008280 blood Substances 0.000 description 3
- 230000037396 body weight Effects 0.000 description 3
- 125000002837 carbocyclic group Chemical group 0.000 description 3
- 239000003153 chemical reaction reagent Substances 0.000 description 3
- 238000004440 column chromatography Methods 0.000 description 3
- 229960000956 coumarin Drugs 0.000 description 3
- 235000001671 coumarin Nutrition 0.000 description 3
- 229960002433 cysteine Drugs 0.000 description 3
- 229940079593 drug Drugs 0.000 description 3
- 230000003203 everyday effect Effects 0.000 description 3
- 238000002474 experimental method Methods 0.000 description 3
- 238000003818 flash chromatography Methods 0.000 description 3
- 239000008273 gelatin Substances 0.000 description 3
- 229920000159 gelatin Polymers 0.000 description 3
- 235000019322 gelatine Nutrition 0.000 description 3
- 235000011852 gelatine desserts Nutrition 0.000 description 3
- 229960002989 glutamic acid Drugs 0.000 description 3
- 229960002885 histidine Drugs 0.000 description 3
- 125000001041 indolyl group Chemical group 0.000 description 3
- 230000002401 inhibitory effect Effects 0.000 description 3
- 239000007788 liquid Substances 0.000 description 3
- 229960003646 lysine Drugs 0.000 description 3
- 150000002825 nitriles Chemical class 0.000 description 3
- 125000002971 oxazolyl group Chemical group 0.000 description 3
- 239000003755 preservative agent Substances 0.000 description 3
- 229960001153 serine Drugs 0.000 description 3
- 239000000741 silica gel Substances 0.000 description 3
- 229910002027 silica gel Inorganic materials 0.000 description 3
- 239000007787 solid Substances 0.000 description 3
- 239000000600 sorbitol Substances 0.000 description 3
- 235000010356 sorbitol Nutrition 0.000 description 3
- 239000003826 tablet Substances 0.000 description 3
- 125000000335 thiazolyl group Chemical group 0.000 description 3
- 229960002898 threonine Drugs 0.000 description 3
- 210000001519 tissue Anatomy 0.000 description 3
- 230000000699 topical effect Effects 0.000 description 3
- 229960004799 tryptophan Drugs 0.000 description 3
- 229960004441 tyrosine Drugs 0.000 description 3
- 125000001917 2,4-dinitrophenyl group Chemical group [H]C1=C([H])C(=C([H])C(=C1*)[N+]([O-])=O)[N+]([O-])=O 0.000 description 2
- OYIFNHCXNCRBQI-UHFFFAOYSA-N 2-aminoadipic acid Chemical compound OC(=O)C(N)CCCC(O)=O OYIFNHCXNCRBQI-UHFFFAOYSA-N 0.000 description 2
- VHYFNPMBLIVWCW-UHFFFAOYSA-N 4-Dimethylaminopyridine Chemical compound CN(C)C1=CC=NC=C1 VHYFNPMBLIVWCW-UHFFFAOYSA-N 0.000 description 2
- WFDIJRYMOXRFFG-UHFFFAOYSA-N Acetic anhydride Chemical compound CC(=O)OC(C)=O WFDIJRYMOXRFFG-UHFFFAOYSA-N 0.000 description 2
- DCXYFEDJOCDNAF-UHFFFAOYSA-N Asparagine Natural products OC(=O)C(N)CC(N)=O DCXYFEDJOCDNAF-UHFFFAOYSA-N 0.000 description 2
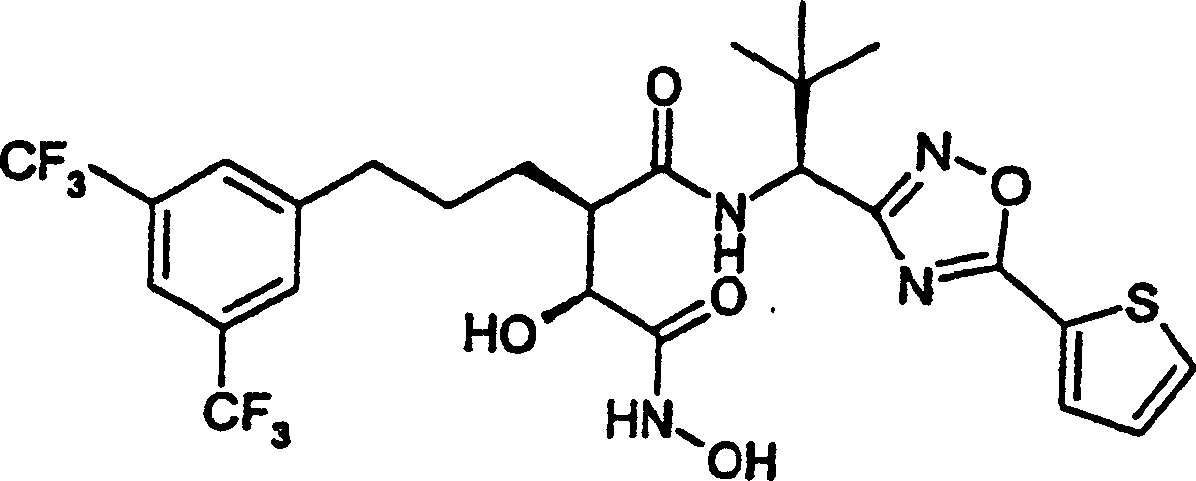
- 0 CCOc1ccc(CCCC([C@@](C(NO)=O)O)C(N[C@@](C(C)(C)C)C2=NOC(c3ccc[s]3)=*C2)=O)cc1 Chemical compound CCOc1ccc(CCCC([C@@](C(NO)=O)O)C(N[C@@](C(C)(C)C)C2=NOC(c3ccc[s]3)=*C2)=O)cc1 0.000 description 2
- 102100027995 Collagenase 3 Human genes 0.000 description 2
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 2
- GKQLYSROISKDLL-UHFFFAOYSA-N EEDQ Chemical compound C1=CC=C2N(C(=O)OCC)C(OCC)C=CC2=C1 GKQLYSROISKDLL-UHFFFAOYSA-N 0.000 description 2
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 2
- 101001013150 Homo sapiens Interstitial collagenase Proteins 0.000 description 2
- 206010061218 Inflammation Diseases 0.000 description 2
- DCXYFEDJOCDNAF-REOHCLBHSA-N L-asparagine Chemical compound OC(=O)[C@@H](N)CC(N)=O DCXYFEDJOCDNAF-REOHCLBHSA-N 0.000 description 2
- WMFOQBRAJBCJND-UHFFFAOYSA-M Lithium hydroxide Chemical compound [Li+].[OH-] WMFOQBRAJBCJND-UHFFFAOYSA-M 0.000 description 2
- 102100030417 Matrilysin Human genes 0.000 description 2
- 108090000855 Matrilysin Proteins 0.000 description 2
- 108010076557 Matrix Metalloproteinase 14 Proteins 0.000 description 2
- 108010016165 Matrix Metalloproteinase 2 Proteins 0.000 description 2
- 102000001776 Matrix metalloproteinase-9 Human genes 0.000 description 2
- 101150101095 Mmp12 gene Proteins 0.000 description 2
- 235000019502 Orange oil Nutrition 0.000 description 2
- 241000700159 Rattus Species 0.000 description 2
- 102100030416 Stromelysin-1 Human genes 0.000 description 2
- 102100028848 Stromelysin-2 Human genes 0.000 description 2
- 102100028847 Stromelysin-3 Human genes 0.000 description 2
- 239000000654 additive Substances 0.000 description 2
- 125000002723 alicyclic group Chemical group 0.000 description 2
- 229960001230 asparagine Drugs 0.000 description 2
- 235000009582 asparagine Nutrition 0.000 description 2
- 239000012298 atmosphere Substances 0.000 description 2
- LUFPJJNWMYZRQE-UHFFFAOYSA-N benzylsulfanylmethylbenzene Chemical compound C=1C=CC=CC=1CSCC1=CC=CC=C1 LUFPJJNWMYZRQE-UHFFFAOYSA-N 0.000 description 2
- SNCZNSNPXMPCGN-UHFFFAOYSA-N butanediamide Chemical compound NC(=O)CCC(N)=O SNCZNSNPXMPCGN-UHFFFAOYSA-N 0.000 description 2
- 239000002775 capsule Substances 0.000 description 2
- 150000001732 carboxylic acid derivatives Chemical class 0.000 description 2
- 230000015556 catabolic process Effects 0.000 description 2
- 229960002424 collagenase Drugs 0.000 description 2
- 239000006071 cream Substances 0.000 description 2
- 230000034994 death Effects 0.000 description 2
- 238000011161 development Methods 0.000 description 2
- 230000018109 developmental process Effects 0.000 description 2
- 238000010790 dilution Methods 0.000 description 2
- 239000012895 dilution Substances 0.000 description 2
- ZUOUZKKEUPVFJK-UHFFFAOYSA-N diphenyl Chemical compound C1=CC=CC=C1C1=CC=CC=C1 ZUOUZKKEUPVFJK-UHFFFAOYSA-N 0.000 description 2
- 238000001035 drying Methods 0.000 description 2
- 150000002170 ethers Chemical class 0.000 description 2
- 239000006260 foam Substances 0.000 description 2
- 238000009472 formulation Methods 0.000 description 2
- 230000004054 inflammatory process Effects 0.000 description 2
- 229960003136 leucine Drugs 0.000 description 2
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 2
- 229960004452 methionine Drugs 0.000 description 2
- 238000013508 migration Methods 0.000 description 2
- 230000005012 migration Effects 0.000 description 2
- 229910052757 nitrogen Inorganic materials 0.000 description 2
- 239000002687 nonaqueous vehicle Substances 0.000 description 2
- 239000002674 ointment Substances 0.000 description 2
- 239000004006 olive oil Substances 0.000 description 2
- 235000008390 olive oil Nutrition 0.000 description 2
- 239000010502 orange oil Substances 0.000 description 2
- 229910052763 palladium Inorganic materials 0.000 description 2
- IZUPBVBPLAPZRR-UHFFFAOYSA-N pentachloro-phenol Natural products OC1=C(Cl)C(Cl)=C(Cl)C(Cl)=C1Cl IZUPBVBPLAPZRR-UHFFFAOYSA-N 0.000 description 2
- 229960005190 phenylalanine Drugs 0.000 description 2
- 238000000746 purification Methods 0.000 description 2
- 125000003226 pyrazolyl group Chemical group 0.000 description 2
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 2
- 125000000714 pyrimidinyl group Chemical group 0.000 description 2
- 125000000168 pyrrolyl group Chemical group 0.000 description 2
- 238000004366 reverse phase liquid chromatography Methods 0.000 description 2
- 210000002966 serum Anatomy 0.000 description 2
- 239000011550 stock solution Substances 0.000 description 2
- 108091007196 stromelysin Proteins 0.000 description 2
- 230000001225 therapeutic effect Effects 0.000 description 2
- 125000001113 thiadiazolyl group Chemical group 0.000 description 2
- 125000003396 thiol group Chemical group [H]S* 0.000 description 2
- DTQVDTLACAAQTR-UHFFFAOYSA-N trifluoroacetic acid Substances OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 description 2
- 229960004295 valine Drugs 0.000 description 2
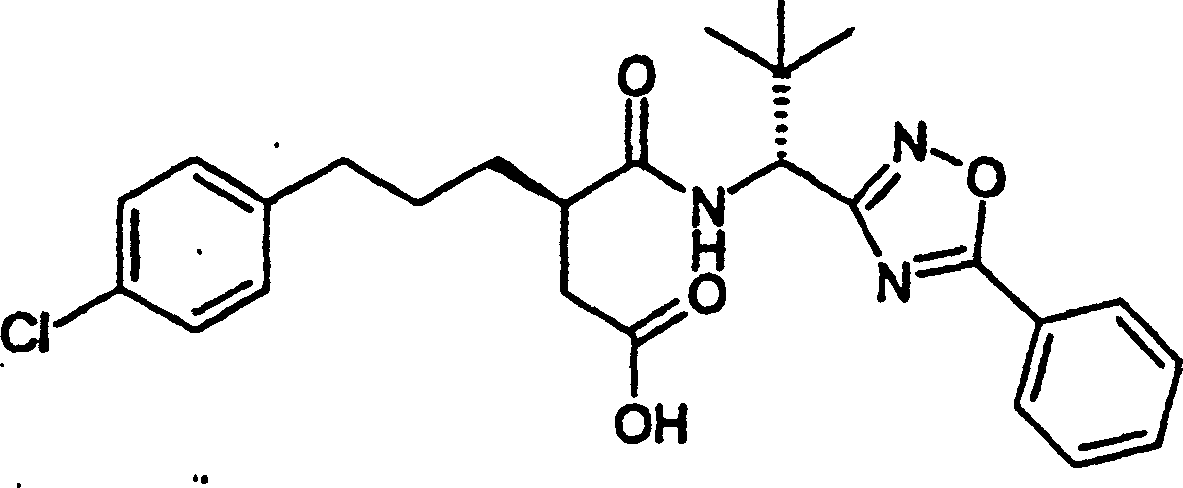
- GGKXLIRIVUXUCE-KNQAVFIVSA-N (3r)-6-(4-chlorophenyl)-3-[[(1r)-2,2-dimethyl-1-(5-phenyl-1,2,4-oxadiazol-3-yl)propyl]carbamoyl]hexanoic acid Chemical compound C([C@@H](C(=O)N[C@H](C(C)(C)C)C=1N=C(ON=1)C=1C=CC=CC=1)CC(O)=O)CCC1=CC=C(Cl)C=C1 GGKXLIRIVUXUCE-KNQAVFIVSA-N 0.000 description 1
- UKAUYVFTDYCKQA-UHFFFAOYSA-N -2-Amino-4-hydroxybutanoic acid Natural products OC(=O)C(N)CCO UKAUYVFTDYCKQA-UHFFFAOYSA-N 0.000 description 1
- ZORQXIQZAOLNGE-UHFFFAOYSA-N 1,1-difluorocyclohexane Chemical compound FC1(F)CCCCC1 ZORQXIQZAOLNGE-UHFFFAOYSA-N 0.000 description 1
- ULVSHNOGEVXRDR-UHFFFAOYSA-N 1,1-dimethoxypropan-2-one Chemical compound COC(OC)C(C)=O ULVSHNOGEVXRDR-UHFFFAOYSA-N 0.000 description 1
- JCIIKRHCWVHVFF-UHFFFAOYSA-N 1,2,4-thiadiazol-5-amine;hydrochloride Chemical compound Cl.NC1=NC=NS1 JCIIKRHCWVHVFF-UHFFFAOYSA-N 0.000 description 1
- PNWCJLFRYRHCFB-UHFFFAOYSA-N 1-(4-methoxyphenyl)-n-[(4-methoxyphenyl)methoxy]methanamine Chemical compound C1=CC(OC)=CC=C1CNOCC1=CC=C(OC)C=C1 PNWCJLFRYRHCFB-UHFFFAOYSA-N 0.000 description 1
- WVUYYXUATWMVIT-UHFFFAOYSA-N 1-bromo-4-ethoxybenzene Chemical compound CCOC1=CC=C(Br)C=C1 WVUYYXUATWMVIT-UHFFFAOYSA-N 0.000 description 1
- 125000004973 1-butenyl group Chemical group C(=CCC)* 0.000 description 1
- 125000004972 1-butynyl group Chemical group [H]C([H])([H])C([H])([H])C#C* 0.000 description 1
- FPIRBHDGWMWJEP-UHFFFAOYSA-N 1-hydroxy-7-azabenzotriazole Chemical compound C1=CN=C2N(O)N=NC2=C1 FPIRBHDGWMWJEP-UHFFFAOYSA-N 0.000 description 1
- DFPYXQYWILNVAU-UHFFFAOYSA-N 1-hydroxybenzotriazole Chemical compound C1=CC=C2N(O)N=NC2=C1.C1=CC=C2N(O)N=NC2=C1 DFPYXQYWILNVAU-UHFFFAOYSA-N 0.000 description 1
- IIZPXYDJLKNOIY-JXPKJXOSSA-N 1-palmitoyl-2-arachidonoyl-sn-glycero-3-phosphocholine Chemical compound CCCCCCCCCCCCCCCC(=O)OC[C@H](COP([O-])(=O)OCC[N+](C)(C)C)OC(=O)CCC\C=C/C\C=C/C\C=C/C\C=C/CCCCC IIZPXYDJLKNOIY-JXPKJXOSSA-N 0.000 description 1
- WUUIYHZKEXDJKH-UHFFFAOYSA-N 1-phenyl-n-phenylmethoxymethanamine Chemical compound C=1C=CC=CC=1CNOCC1=CC=CC=C1 WUUIYHZKEXDJKH-UHFFFAOYSA-N 0.000 description 1
- 125000000530 1-propynyl group Chemical group [H]C([H])([H])C#C* 0.000 description 1
- XBNGYFFABRKICK-UHFFFAOYSA-N 2,3,4,5,6-pentafluorophenol Chemical compound OC1=C(F)C(F)=C(F)C(F)=C1F XBNGYFFABRKICK-UHFFFAOYSA-N 0.000 description 1
- NGNBDVOYPDDBFK-UHFFFAOYSA-N 2-[2,4-di(pentan-2-yl)phenoxy]acetyl chloride Chemical compound CCCC(C)C1=CC=C(OCC(Cl)=O)C(C(C)CCC)=C1 NGNBDVOYPDDBFK-UHFFFAOYSA-N 0.000 description 1
- IEQAICDLOKRSRL-UHFFFAOYSA-N 2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-(2-dodecoxyethoxy)ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethanol Chemical compound CCCCCCCCCCCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCO IEQAICDLOKRSRL-UHFFFAOYSA-N 0.000 description 1
- VKUYLANQOAKALN-UHFFFAOYSA-N 2-[benzyl-(4-methoxyphenyl)sulfonylamino]-n-hydroxy-4-methylpentanamide Chemical compound C1=CC(OC)=CC=C1S(=O)(=O)N(C(CC(C)C)C(=O)NO)CC1=CC=CC=C1 VKUYLANQOAKALN-UHFFFAOYSA-N 0.000 description 1
- QKNYBSVHEMOAJP-UHFFFAOYSA-N 2-amino-2-(hydroxymethyl)propane-1,3-diol;hydron;chloride Chemical compound Cl.OCC(N)(CO)CO QKNYBSVHEMOAJP-UHFFFAOYSA-N 0.000 description 1
- 125000004974 2-butenyl group Chemical group C(C=CC)* 0.000 description 1
- 125000000069 2-butynyl group Chemical group [H]C([H])([H])C#CC([H])([H])* 0.000 description 1
- 125000006022 2-methyl-2-propenyl group Chemical group 0.000 description 1
- CDUUKBXTEOFITR-BYPYZUCNSA-N 2-methyl-L-serine Chemical compound OC[C@@]([NH3+])(C)C([O-])=O CDUUKBXTEOFITR-BYPYZUCNSA-N 0.000 description 1
- 125000004105 2-pyridyl group Chemical group N1=C([*])C([H])=C([H])C([H])=C1[H] 0.000 description 1
- RUROFEVDCUGKHD-UHFFFAOYSA-N 3-bromoprop-1-enylbenzene Chemical compound BrCC=CC1=CC=CC=C1 RUROFEVDCUGKHD-UHFFFAOYSA-N 0.000 description 1
- 125000003349 3-pyridyl group Chemical group N1=C([H])C([*])=C([H])C([H])=C1[H] 0.000 description 1
- 229960000549 4-dimethylaminophenol Drugs 0.000 description 1
- 125000000339 4-pyridyl group Chemical group N1=C([H])C([H])=C([*])C([H])=C1[H] 0.000 description 1
- 229940117976 5-hydroxylysine Drugs 0.000 description 1
- ASIVDOCWODPISQ-UHFFFAOYSA-N 5-thiophen-2-yl-1,2,4-oxadiazole Chemical compound C1=CSC(C=2ON=CN=2)=C1 ASIVDOCWODPISQ-UHFFFAOYSA-N 0.000 description 1
- 101710151806 72 kDa type IV collagenase Proteins 0.000 description 1
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 1
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 1
- 235000019489 Almond oil Nutrition 0.000 description 1
- 241000416162 Astragalus gummifer Species 0.000 description 1
- 201000001320 Atherosclerosis Diseases 0.000 description 1
- KXDHJXZQYSOELW-UHFFFAOYSA-M Carbamate Chemical compound NC([O-])=O KXDHJXZQYSOELW-UHFFFAOYSA-M 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- 208000024172 Cardiovascular disease Diseases 0.000 description 1
- GHXZTYHSJHQHIJ-UHFFFAOYSA-N Chlorhexidine Chemical compound C=1C=C(Cl)C=CC=1NC(N)=NC(N)=NCCCCCCN=C(N)N=C(N)NC1=CC=C(Cl)C=C1 GHXZTYHSJHQHIJ-UHFFFAOYSA-N 0.000 description 1
- 102000008186 Collagen Human genes 0.000 description 1
- 108010035532 Collagen Proteins 0.000 description 1
- 108050005238 Collagenase 3 Proteins 0.000 description 1
- 229910021591 Copper(I) chloride Inorganic materials 0.000 description 1
- 229920002261 Corn starch Polymers 0.000 description 1
- LEVWYRKDKASIDU-QWWZWVQMSA-N D-cystine Chemical compound OC(=O)[C@H](N)CSSC[C@@H](N)C(O)=O LEVWYRKDKASIDU-QWWZWVQMSA-N 0.000 description 1
- FBPFZTCFMRRESA-JGWLITMVSA-N D-glucitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-JGWLITMVSA-N 0.000 description 1
- XUIIKFGFIJCVMT-GFCCVEGCSA-N D-thyroxine Chemical compound IC1=CC(C[C@@H](N)C(O)=O)=CC(I)=C1OC1=CC(I)=C(O)C(I)=C1 XUIIKFGFIJCVMT-GFCCVEGCSA-N 0.000 description 1
- QXNVGIXVLWOKEQ-UHFFFAOYSA-N Disodium Chemical compound [Na][Na] QXNVGIXVLWOKEQ-UHFFFAOYSA-N 0.000 description 1
- 102000005593 Endopeptidases Human genes 0.000 description 1
- 108010059378 Endopeptidases Proteins 0.000 description 1
- 229920000084 Gum arabic Polymers 0.000 description 1
- CPELXLSAUQHCOX-UHFFFAOYSA-N Hydrogen bromide Chemical compound Br CPELXLSAUQHCOX-UHFFFAOYSA-N 0.000 description 1
- PMMYEEVYMWASQN-DMTCNVIQSA-N Hydroxyproline Chemical compound O[C@H]1CN[C@H](C(O)=O)C1 PMMYEEVYMWASQN-DMTCNVIQSA-N 0.000 description 1
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 1
- WTDRDQBEARUVNC-LURJTMIESA-N L-DOPA Chemical compound OC(=O)[C@@H](N)CC1=CC=C(O)C(O)=C1 WTDRDQBEARUVNC-LURJTMIESA-N 0.000 description 1
- WTDRDQBEARUVNC-UHFFFAOYSA-N L-Dopa Natural products OC(=O)C(N)CC1=CC=C(O)C(O)=C1 WTDRDQBEARUVNC-UHFFFAOYSA-N 0.000 description 1
- AHLPHDHHMVZTML-BYPYZUCNSA-N L-Ornithine Chemical compound NCCC[C@H](N)C(O)=O AHLPHDHHMVZTML-BYPYZUCNSA-N 0.000 description 1
- ONIBWKKTOPOVIA-BYPYZUCNSA-N L-Proline Chemical compound OC(=O)[C@@H]1CCCN1 ONIBWKKTOPOVIA-BYPYZUCNSA-N 0.000 description 1
- UKAUYVFTDYCKQA-VKHMYHEASA-N L-homoserine Chemical compound OC(=O)[C@@H](N)CCO UKAUYVFTDYCKQA-VKHMYHEASA-N 0.000 description 1
- HXEACLLIILLPRG-YFKPBYRVSA-N L-pipecolic acid Chemical compound [O-]C(=O)[C@@H]1CCCC[NH2+]1 HXEACLLIILLPRG-YFKPBYRVSA-N 0.000 description 1
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 1
- 235000010643 Leucaena leucocephala Nutrition 0.000 description 1
- 240000007472 Leucaena leucocephala Species 0.000 description 1
- 239000004425 Makrolon Substances 0.000 description 1
- 108010076497 Matrix Metalloproteinase 10 Proteins 0.000 description 1
- 108010076502 Matrix Metalloproteinase 11 Proteins 0.000 description 1
- 108010076503 Matrix Metalloproteinase 13 Proteins 0.000 description 1
- 108010016160 Matrix Metalloproteinase 3 Proteins 0.000 description 1
- 102100030216 Matrix metalloproteinase-14 Human genes 0.000 description 1
- 102000036436 Metzincins Human genes 0.000 description 1
- 108091007161 Metzincins Proteins 0.000 description 1
- 102000006386 Myelin Proteins Human genes 0.000 description 1
- 108010083674 Myelin Proteins Proteins 0.000 description 1
- 238000005481 NMR spectroscopy Methods 0.000 description 1
- 229910002651 NO3 Inorganic materials 0.000 description 1
- 206010028980 Neoplasm Diseases 0.000 description 1
- 208000012902 Nervous system disease Diseases 0.000 description 1
- 208000025966 Neurological disease Diseases 0.000 description 1
- 102100030411 Neutrophil collagenase Human genes 0.000 description 1
- 101710118230 Neutrophil collagenase Proteins 0.000 description 1
- NHNBFGGVMKEFGY-UHFFFAOYSA-N Nitrate Chemical compound [O-][N+]([O-])=O NHNBFGGVMKEFGY-UHFFFAOYSA-N 0.000 description 1
- AHLPHDHHMVZTML-UHFFFAOYSA-N Orn-delta-NH2 Natural products NCCCC(N)C(O)=O AHLPHDHHMVZTML-UHFFFAOYSA-N 0.000 description 1
- UTJLXEIPEHZYQJ-UHFFFAOYSA-N Ornithine Natural products OC(=O)C(C)CCCN UTJLXEIPEHZYQJ-UHFFFAOYSA-N 0.000 description 1
- 229910019142 PO4 Inorganic materials 0.000 description 1
- 239000002202 Polyethylene glycol Substances 0.000 description 1
- ONIBWKKTOPOVIA-UHFFFAOYSA-N Proline Natural products OC(=O)C1CCCN1 ONIBWKKTOPOVIA-UHFFFAOYSA-N 0.000 description 1
- 102000016611 Proteoglycans Human genes 0.000 description 1
- 108010067787 Proteoglycans Proteins 0.000 description 1
- 229940124639 Selective inhibitor Drugs 0.000 description 1
- DBMJMQXJHONAFJ-UHFFFAOYSA-M Sodium laurylsulphate Chemical compound [Na+].CCCCCCCCCCCCOS([O-])(=O)=O DBMJMQXJHONAFJ-UHFFFAOYSA-M 0.000 description 1
- 208000014151 Stomatognathic disease Diseases 0.000 description 1
- 101710108790 Stromelysin-1 Proteins 0.000 description 1
- 101710108792 Stromelysin-2 Proteins 0.000 description 1
- 229920001615 Tragacanth Polymers 0.000 description 1
- HCHKCACWOHOZIP-UHFFFAOYSA-N Zinc Chemical compound [Zn] HCHKCACWOHOZIP-UHFFFAOYSA-N 0.000 description 1
- 235000010489 acacia gum Nutrition 0.000 description 1
- 239000000205 acacia gum Substances 0.000 description 1
- 125000002777 acetyl group Chemical group [H]C([H])([H])C(*)=O 0.000 description 1
- RXSUFCOOZSGWSW-UHFFFAOYSA-M acetyloxy-(4-aminophenyl)mercury Chemical compound CC(=O)O[Hg]C1=CC=C(N)C=C1 RXSUFCOOZSGWSW-UHFFFAOYSA-M 0.000 description 1
- 230000004913 activation Effects 0.000 description 1
- 239000013543 active substance Substances 0.000 description 1
- 229960003767 alanine Drugs 0.000 description 1
- 235000004279 alanine Nutrition 0.000 description 1
- 125000003342 alkenyl group Chemical group 0.000 description 1
- BHELZAPQIKSEDF-UHFFFAOYSA-N allyl bromide Chemical compound BrCC=C BHELZAPQIKSEDF-UHFFFAOYSA-N 0.000 description 1
- 239000008168 almond oil Substances 0.000 description 1
- HSFWRNGVRCDJHI-UHFFFAOYSA-N alpha-acetylene Natural products C#C HSFWRNGVRCDJHI-UHFFFAOYSA-N 0.000 description 1
- QWCKQJZIFLGMSD-UHFFFAOYSA-N alpha-aminobutyric acid Chemical compound CCC(N)C(O)=O QWCKQJZIFLGMSD-UHFFFAOYSA-N 0.000 description 1
- CDUUKBXTEOFITR-UHFFFAOYSA-N alpha-methylserine Natural products OCC([NH3+])(C)C([O-])=O CDUUKBXTEOFITR-UHFFFAOYSA-N 0.000 description 1
- NLBBYLMMDFCTPI-UHFFFAOYSA-N amino tert-butyl carbonate Chemical compound CC(C)(C)OC(=O)ON NLBBYLMMDFCTPI-UHFFFAOYSA-N 0.000 description 1
- 150000008064 anhydrides Chemical class 0.000 description 1
- 230000000844 anti-bacterial effect Effects 0.000 description 1
- 230000003110 anti-inflammatory effect Effects 0.000 description 1
- 239000008135 aqueous vehicle Substances 0.000 description 1
- 150000001499 aryl bromides Chemical class 0.000 description 1
- 239000003899 bactericide agent Substances 0.000 description 1
- 229960000686 benzalkonium chloride Drugs 0.000 description 1
- MXOQNVMDKHLYCZ-UHFFFAOYSA-N benzamidoxime Chemical compound ON=C(N)C1=CC=CC=C1 MXOQNVMDKHLYCZ-UHFFFAOYSA-N 0.000 description 1
- CADWTSSKOVRVJC-UHFFFAOYSA-N benzyl(dimethyl)azanium;chloride Chemical compound [Cl-].C[NH+](C)CC1=CC=CC=C1 CADWTSSKOVRVJC-UHFFFAOYSA-N 0.000 description 1
- 125000001584 benzyloxycarbonyl group Chemical group C(=O)(OCC1=CC=CC=C1)* 0.000 description 1
- 239000011230 binding agent Substances 0.000 description 1
- 239000004305 biphenyl Substances 0.000 description 1
- 235000010290 biphenyl Nutrition 0.000 description 1
- 239000001506 calcium phosphate Substances 0.000 description 1
- 229910000389 calcium phosphate Inorganic materials 0.000 description 1
- 235000011010 calcium phosphates Nutrition 0.000 description 1
- 238000004364 calculation method Methods 0.000 description 1
- 201000011510 cancer Diseases 0.000 description 1
- 150000004657 carbamic acid derivatives Chemical class 0.000 description 1
- 125000004452 carbocyclyl group Chemical group 0.000 description 1
- 230000001413 cellular effect Effects 0.000 description 1
- 239000007795 chemical reaction product Substances 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- 229960003260 chlorhexidine Drugs 0.000 description 1
- 150000001805 chlorine compounds Chemical class 0.000 description 1
- 208000037976 chronic inflammation Diseases 0.000 description 1
- 208000037893 chronic inflammatory disorder Diseases 0.000 description 1
- 235000019504 cigarettes Nutrition 0.000 description 1
- 239000003240 coconut oil Substances 0.000 description 1
- 235000019864 coconut oil Nutrition 0.000 description 1
- 229920001436 collagen Polymers 0.000 description 1
- 239000003086 colorant Substances 0.000 description 1
- 239000012230 colorless oil Substances 0.000 description 1
- 238000010276 construction Methods 0.000 description 1
- 239000012050 conventional carrier Substances 0.000 description 1
- OXBLHERUFWYNTN-UHFFFAOYSA-M copper(I) chloride Chemical compound [Cu]Cl OXBLHERUFWYNTN-UHFFFAOYSA-M 0.000 description 1
- 239000008120 corn starch Substances 0.000 description 1
- 125000001047 cyclobutenyl group Chemical group C1(=CCC1)* 0.000 description 1
- 125000001162 cycloheptenyl group Chemical group C1(=CCCCCC1)* 0.000 description 1
- 125000000596 cyclohexenyl group Chemical group C1(=CCCCC1)* 0.000 description 1
- 125000000522 cyclooctenyl group Chemical group C1(=CCCCCCC1)* 0.000 description 1
- 125000002433 cyclopentenyl group Chemical group C1(=CCCC1)* 0.000 description 1
- 125000000298 cyclopropenyl group Chemical group [H]C1=C([H])C1([H])* 0.000 description 1
- 229960003067 cystine Drugs 0.000 description 1
- 230000006378 damage Effects 0.000 description 1
- DEZRYPDIMOWBDS-UHFFFAOYSA-N dcm dichloromethane Chemical compound ClCCl.ClCCl DEZRYPDIMOWBDS-UHFFFAOYSA-N 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- 230000006735 deficit Effects 0.000 description 1
- YSMODUONRAFBET-UHFFFAOYSA-N delta-DL-hydroxylysine Natural products NCC(O)CCC(N)C(O)=O YSMODUONRAFBET-UHFFFAOYSA-N 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 239000002274 desiccant Substances 0.000 description 1
- UREBDLICKHMUKA-CXSFZGCWSA-N dexamethasone Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@]2(F)[C@@H]1[C@@H]1C[C@@H](C)[C@@](C(=O)CO)(O)[C@@]1(C)C[C@@H]2O UREBDLICKHMUKA-CXSFZGCWSA-N 0.000 description 1
- 229960003957 dexamethasone Drugs 0.000 description 1
- MHDVGSVTJDSBDK-UHFFFAOYSA-N dibenzyl ether Chemical compound C=1C=CC=CC=1COCC1=CC=CC=C1 MHDVGSVTJDSBDK-UHFFFAOYSA-N 0.000 description 1
- 235000005911 diet Nutrition 0.000 description 1
- 230000037213 diet Effects 0.000 description 1
- UXGNZZKBCMGWAZ-UHFFFAOYSA-N dimethylformamide dmf Chemical compound CN(C)C=O.CN(C)C=O UXGNZZKBCMGWAZ-UHFFFAOYSA-N 0.000 description 1
- USIUVYZYUHIAEV-UHFFFAOYSA-N diphenyl ether Chemical compound C=1C=CC=CC=1OC1=CC=CC=C1 USIUVYZYUHIAEV-UHFFFAOYSA-N 0.000 description 1
- PMMYEEVYMWASQN-UHFFFAOYSA-N dl-hydroxyproline Natural products OC1C[NH2+]C(C([O-])=O)C1 PMMYEEVYMWASQN-UHFFFAOYSA-N 0.000 description 1
- 239000002552 dosage form Substances 0.000 description 1
- 239000000890 drug combination Substances 0.000 description 1
- 239000008157 edible vegetable oil Substances 0.000 description 1
- 239000003480 eluent Substances 0.000 description 1
- 239000003995 emulsifying agent Substances 0.000 description 1
- 239000000839 emulsion Substances 0.000 description 1
- 229940066758 endopeptidases Drugs 0.000 description 1
- YSMODUONRAFBET-UHNVWZDZSA-N erythro-5-hydroxy-L-lysine Chemical compound NC[C@H](O)CC[C@H](N)C(O)=O YSMODUONRAFBET-UHNVWZDZSA-N 0.000 description 1
- BEFDCLMNVWHSGT-UHFFFAOYSA-N ethenylcyclopentane Chemical compound C=CC1CCCC1 BEFDCLMNVWHSGT-UHFFFAOYSA-N 0.000 description 1
- 125000002534 ethynyl group Chemical group [H]C#C* 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- 230000005284 excitation Effects 0.000 description 1
- 230000029142 excretion Effects 0.000 description 1
- 239000003925 fat Substances 0.000 description 1
- 235000019197 fats Nutrition 0.000 description 1
- 239000000945 filler Substances 0.000 description 1
- 239000000796 flavoring agent Substances 0.000 description 1
- 239000000417 fungicide Substances 0.000 description 1
- 239000000499 gel Substances 0.000 description 1
- 229960002743 glutamine Drugs 0.000 description 1
- 235000011187 glycerol Nutrition 0.000 description 1
- 239000008187 granular material Substances 0.000 description 1
- 230000036541 health Effects 0.000 description 1
- 206010019692 hepatic necrosis Diseases 0.000 description 1
- XMBWDFGMSWQBCA-UHFFFAOYSA-N hydrogen iodide Chemical compound I XMBWDFGMSWQBCA-UHFFFAOYSA-N 0.000 description 1
- 150000002443 hydroxylamines Chemical class 0.000 description 1
- 229960002591 hydroxyproline Drugs 0.000 description 1
- 239000001866 hydroxypropyl methyl cellulose Substances 0.000 description 1
- 235000010979 hydroxypropyl methyl cellulose Nutrition 0.000 description 1
- 229920003088 hydroxypropyl methyl cellulose Polymers 0.000 description 1
- 229960003943 hypromellose Drugs 0.000 description 1
- 239000005457 ice water Substances 0.000 description 1
- 238000000338 in vitro Methods 0.000 description 1
- 238000001727 in vivo Methods 0.000 description 1
- 208000027866 inflammatory disease Diseases 0.000 description 1
- 239000007928 intraperitoneal injection Substances 0.000 description 1
- DUMSKQUKLVSSII-UHFFFAOYSA-N iodomethylcyclopentane Chemical compound ICC1CCCC1 DUMSKQUKLVSSII-UHFFFAOYSA-N 0.000 description 1
- 125000001786 isothiazolyl group Chemical group 0.000 description 1
- HXEACLLIILLPRG-RXMQYKEDSA-N l-pipecolic acid Natural products OC(=O)[C@H]1CCCCN1 HXEACLLIILLPRG-RXMQYKEDSA-N 0.000 description 1
- 239000008101 lactose Substances 0.000 description 1
- 235000010445 lecithin Nutrition 0.000 description 1
- 239000000787 lecithin Substances 0.000 description 1
- 229940067606 lecithin Drugs 0.000 description 1
- 210000000265 leukocyte Anatomy 0.000 description 1
- 230000000670 limiting effect Effects 0.000 description 1
- YNESATAKKCNGOF-UHFFFAOYSA-N lithium bis(trimethylsilyl)amide Chemical compound [Li+].C[Si](C)(C)[N-][Si](C)(C)C YNESATAKKCNGOF-UHFFFAOYSA-N 0.000 description 1
- 231100000149 liver necrosis Toxicity 0.000 description 1
- 239000003589 local anesthetic agent Substances 0.000 description 1
- 229960005015 local anesthetics Drugs 0.000 description 1
- 239000006210 lotion Substances 0.000 description 1
- 239000007937 lozenge Substances 0.000 description 1
- 239000000314 lubricant Substances 0.000 description 1
- 235000019359 magnesium stearate Nutrition 0.000 description 1
- BCVXHSPFUWZLGQ-UHFFFAOYSA-N mecn acetonitrile Chemical compound CC#N.CC#N BCVXHSPFUWZLGQ-UHFFFAOYSA-N 0.000 description 1
- 210000004379 membrane Anatomy 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- 229920000609 methyl cellulose Polymers 0.000 description 1
- 239000004292 methyl p-hydroxybenzoate Substances 0.000 description 1
- 235000010270 methyl p-hydroxybenzoate Nutrition 0.000 description 1
- 239000001923 methylcellulose Substances 0.000 description 1
- 125000002950 monocyclic group Chemical group 0.000 description 1
- 210000005012 myelin Anatomy 0.000 description 1
- QVWURBTWYBFDQK-UHFFFAOYSA-N n'-hydroxy-n-(1h-imidazol-2-ylmethyl)butanediamide Chemical class ONC(=O)CCC(=O)NCC1=NC=CN1 QVWURBTWYBFDQK-UHFFFAOYSA-N 0.000 description 1
- XHIRWEVPYCTARV-UHFFFAOYSA-N n-(3-aminopropyl)-2-methylprop-2-enamide;hydrochloride Chemical compound Cl.CC(=C)C(=O)NCCCN XHIRWEVPYCTARV-UHFFFAOYSA-N 0.000 description 1
- 125000001971 neopentyl group Chemical group [H]C([*])([H])C(C([H])([H])[H])(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 210000000440 neutrophil Anatomy 0.000 description 1
- MVSMBIBGGPSEHQ-UHFFFAOYSA-N o-[(4-methoxyphenyl)methyl]hydroxylamine Chemical compound COC1=CC=C(CON)C=C1 MVSMBIBGGPSEHQ-UHFFFAOYSA-N 0.000 description 1
- XYEOALKITRFCJJ-UHFFFAOYSA-N o-benzylhydroxylamine Chemical compound NOCC1=CC=CC=C1 XYEOALKITRFCJJ-UHFFFAOYSA-N 0.000 description 1
- AEKHNNJSMVVESS-UHFFFAOYSA-N o-trimethylsilylhydroxylamine Chemical compound C[Si](C)(C)ON AEKHNNJSMVVESS-UHFFFAOYSA-N 0.000 description 1
- 229960003104 ornithine Drugs 0.000 description 1
- 230000002018 overexpression Effects 0.000 description 1
- WCPAKWJPBJAGKN-UHFFFAOYSA-N oxadiazole Chemical group C1=CON=N1 WCPAKWJPBJAGKN-UHFFFAOYSA-N 0.000 description 1
- 125000001715 oxadiazolyl group Chemical group 0.000 description 1
- 125000003854 p-chlorophenyl group Chemical group [H]C1=C([H])C(*)=C([H])C([H])=C1Cl 0.000 description 1
- 239000012188 paraffin wax Substances 0.000 description 1
- 239000003182 parenteral nutrition solution Substances 0.000 description 1
- 125000000538 pentafluorophenyl group Chemical group FC1=C(F)C(F)=C(*)C(F)=C1F 0.000 description 1
- 210000003200 peritoneal cavity Anatomy 0.000 description 1
- 239000008194 pharmaceutical composition Substances 0.000 description 1
- 239000000546 pharmaceutical excipient Substances 0.000 description 1
- 230000000144 pharmacologic effect Effects 0.000 description 1
- 229940096826 phenylmercuric acetate Drugs 0.000 description 1
- UYWQUFXKFGHYNT-UHFFFAOYSA-N phenylmethyl ester of formic acid Natural products O=COCC1=CC=CC=C1 UYWQUFXKFGHYNT-UHFFFAOYSA-N 0.000 description 1
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 1
- 239000010452 phosphate Substances 0.000 description 1
- 230000035790 physiological processes and functions Effects 0.000 description 1
- 125000004193 piperazinyl group Chemical group 0.000 description 1
- 125000003386 piperidinyl group Chemical group 0.000 description 1
- 230000036470 plasma concentration Effects 0.000 description 1
- 229920000515 polycarbonate Polymers 0.000 description 1
- 229920001223 polyethylene glycol Polymers 0.000 description 1
- 235000010482 polyoxyethylene sorbitan monooleate Nutrition 0.000 description 1
- 229920000053 polysorbate 80 Polymers 0.000 description 1
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 1
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 1
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 1
- 239000013641 positive control Substances 0.000 description 1
- 229920001592 potato starch Polymers 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 239000002244 precipitate Substances 0.000 description 1
- 239000002243 precursor Substances 0.000 description 1
- 230000002028 premature Effects 0.000 description 1
- 238000002953 preparative HPLC Methods 0.000 description 1
- 230000002335 preservative effect Effects 0.000 description 1
- 230000000770 proinflammatory effect Effects 0.000 description 1
- 229960002429 proline Drugs 0.000 description 1
- 235000013930 proline Nutrition 0.000 description 1
- 239000004405 propyl p-hydroxybenzoate Substances 0.000 description 1
- 235000010232 propyl p-hydroxybenzoate Nutrition 0.000 description 1
- 235000013772 propylene glycol Nutrition 0.000 description 1
- QELSKZZBTMNZEB-UHFFFAOYSA-N propylparaben Chemical compound CCCOC(=O)C1=CC=C(O)C=C1 QELSKZZBTMNZEB-UHFFFAOYSA-N 0.000 description 1
- 230000001681 protective effect Effects 0.000 description 1
- 125000003373 pyrazinyl group Chemical group 0.000 description 1
- 125000002098 pyridazinyl group Chemical group 0.000 description 1
- 125000000719 pyrrolidinyl group Chemical group 0.000 description 1
- 238000011002 quantification Methods 0.000 description 1
- 238000004445 quantitative analysis Methods 0.000 description 1
- 238000010992 reflux Methods 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 230000033764 rhythmic process Effects 0.000 description 1
- 238000007363 ring formation reaction Methods 0.000 description 1
- 125000006413 ring segment Chemical group 0.000 description 1
- 229930195734 saturated hydrocarbon Natural products 0.000 description 1
- 239000012047 saturated solution Substances 0.000 description 1
- 238000010898 silica gel chromatography Methods 0.000 description 1
- 239000000377 silicon dioxide Substances 0.000 description 1
- 239000000779 smoke Substances 0.000 description 1
- HRZFUMHJMZEROT-UHFFFAOYSA-L sodium disulfite Chemical compound [Na+].[Na+].[O-]S(=O)S([O-])(=O)=O HRZFUMHJMZEROT-UHFFFAOYSA-L 0.000 description 1
- 235000019333 sodium laurylsulphate Nutrition 0.000 description 1
- 229940001584 sodium metabisulfite Drugs 0.000 description 1
- 235000010262 sodium metabisulphite Nutrition 0.000 description 1
- 235000010199 sorbic acid Nutrition 0.000 description 1
- 239000004334 sorbic acid Substances 0.000 description 1
- 229940075582 sorbic acid Drugs 0.000 description 1
- 239000001593 sorbitan monooleate Substances 0.000 description 1
- 235000011069 sorbitan monooleate Nutrition 0.000 description 1
- 229940035049 sorbitan monooleate Drugs 0.000 description 1
- 238000013222 sprague-dawley male rat Methods 0.000 description 1
- 229910001220 stainless steel Inorganic materials 0.000 description 1
- 239000010935 stainless steel Substances 0.000 description 1
- 238000011421 subcutaneous treatment Methods 0.000 description 1
- 239000000375 suspending agent Substances 0.000 description 1
- 239000000454 talc Substances 0.000 description 1
- 229910052623 talc Inorganic materials 0.000 description 1
- AGOSGCWATIJZHQ-UHFFFAOYSA-N tert-butyl [(2-methylpropan-2-yl)oxycarbonylamino] carbonate Chemical compound CC(C)(C)OC(=O)NOC(=O)OC(C)(C)C AGOSGCWATIJZHQ-UHFFFAOYSA-N 0.000 description 1
- IGYIOBZVTSJFSA-UHFFFAOYSA-N tert-butyl [[tert-butyl(dimethyl)silyl]-hydroxyamino] carbonate Chemical compound C(C)(C)(C)OC(=O)ON(O)[Si](C)(C)C(C)(C)C IGYIOBZVTSJFSA-UHFFFAOYSA-N 0.000 description 1
- AJARVVOAVSMPIJ-UHFFFAOYSA-N tert-butyl [hydroxy(oxan-2-yl)amino] carbonate Chemical compound C(C)(C)(C)OC(=O)ON(O)C1OCCCC1 AJARVVOAVSMPIJ-UHFFFAOYSA-N 0.000 description 1
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 1
- WHRNULOCNSKMGB-UHFFFAOYSA-N tetrahydrofuran thf Chemical compound C1CCOC1.C1CCOC1 WHRNULOCNSKMGB-UHFFFAOYSA-N 0.000 description 1
- WROMPOXWARCANT-UHFFFAOYSA-N tfa trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F.OC(=O)C(F)(F)F WROMPOXWARCANT-UHFFFAOYSA-N 0.000 description 1
- 238000002560 therapeutic procedure Methods 0.000 description 1
- 125000005308 thiazepinyl group Chemical group S1N=C(C=CC=C1)* 0.000 description 1
- 239000002562 thickening agent Substances 0.000 description 1
- 125000005301 thienylmethyl group Chemical group [H]C1=C([H])C([H])=C(S1)C([H])([H])* 0.000 description 1
- 150000007970 thio esters Chemical class 0.000 description 1
- 150000003568 thioethers Chemical class 0.000 description 1
- 229940034208 thyroxine Drugs 0.000 description 1
- XUIIKFGFIJCVMT-UHFFFAOYSA-N thyroxine-binding globulin Natural products IC1=CC(CC([NH3+])C([O-])=O)=CC(I)=C1OC1=CC(I)=C(O)C(I)=C1 XUIIKFGFIJCVMT-UHFFFAOYSA-N 0.000 description 1
- 235000010487 tragacanth Nutrition 0.000 description 1
- 239000000196 tragacanth Substances 0.000 description 1
- 229940116362 tragacanth Drugs 0.000 description 1
- 125000004306 triazinyl group Chemical group 0.000 description 1
- 125000001425 triazolyl group Chemical group 0.000 description 1
- QORWJWZARLRLPR-UHFFFAOYSA-H tricalcium bis(phosphate) Chemical compound [Ca+2].[Ca+2].[Ca+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O QORWJWZARLRLPR-UHFFFAOYSA-H 0.000 description 1
- 238000005303 weighing Methods 0.000 description 1
- 239000000080 wetting agent Substances 0.000 description 1
- 239000011701 zinc Substances 0.000 description 1
- 229910052725 zinc Inorganic materials 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D271/00—Heterocyclic compounds containing five-membered rings having two nitrogen atoms and one oxygen atom as the only ring hetero atoms
- C07D271/02—Heterocyclic compounds containing five-membered rings having two nitrogen atoms and one oxygen atom as the only ring hetero atoms not condensed with other rings
- C07D271/06—1,2,4-Oxadiazoles; Hydrogenated 1,2,4-oxadiazoles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/02—Stomatological preparations, e.g. drugs for caries, aphtae, periodontitis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/04—Drugs for disorders of the alimentary tract or the digestive system for ulcers, gastritis or reflux esophagitis, e.g. antacids, inhibitors of acid secretion, mucosal protectants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/16—Drugs for disorders of the alimentary tract or the digestive system for liver or gallbladder disorders, e.g. hepatoprotective agents, cholagogues, litholytics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/06—Antiasthmatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/08—Bronchodilators
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/12—Drugs for disorders of the urinary system of the kidneys
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/02—Drugs for dermatological disorders for treating wounds, ulcers, burns, scars, keloids, or the like
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/06—Antipsoriatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/02—Drugs for skeletal disorders for joint disorders, e.g. arthritis, arthrosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/08—Drugs for skeletal disorders for bone diseases, e.g. rachitism, Paget's disease
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/02—Drugs for disorders of the nervous system for peripheral neuropathies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/04—Antibacterial agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/04—Antineoplastic agents specific for metastasis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/06—Immunosuppressants, e.g. drugs for graft rejection
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D285/00—Heterocyclic compounds containing rings having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by groups C07D275/00 - C07D283/00
- C07D285/01—Five-membered rings
- C07D285/02—Thiadiazoles; Hydrogenated thiadiazoles
- C07D285/04—Thiadiazoles; Hydrogenated thiadiazoles not condensed with other rings
- C07D285/08—1,2,4-Thiadiazoles; Hydrogenated 1,2,4-thiadiazoles
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/04—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/06—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings linked by a carbon chain containing only aliphatic carbon atoms
Description
- Die vorliegende Erfindung bezieht sich auf therapeutisch aktive Hydroxamsäure- und Carbonsäure- Derivate, auf Verfahren zu ihrer Herstellung, auf pharmazeutische Zusammensetzungen, welche diese enthalten, und auf die Verwendung von solchen Verbindungen in der Medizin. Die Verbindungen sind insbesondere Inhibitoren von Matrix-Metalloproteinasen.
- Die Matrix-Metalloproteinasen (MMPs) sind eine Familie von Zink enthaltenden Endopeptidasen, welche in der Lage sind, große Biomoleküle, wie Kollagene, Proteoglycane und Gelatine, zu spalten. Ein gestörtes Gleichgewicht zwischen aktiven MMPs und endogenen Inhibitoren führt zu einer überhöhten Gewebezerstörung. Die Hauptgruppen der MMPs sind die Kollagenasen, die Gelatinasen und die Stromelysinen. Die Kollagenasen umfassen Fibroplastenkollagenase (MMP-1), die neutrophile Kollagenase (MMP-8) und die Kollagenase 3 (MMP-13). Die Gelatinasen umfassen 72 kDa Gelatinase (Gelatinase A; MMP-2) und 93 kDa Gelatinase (Gelatinase B; MMP-9). Die Stromelysine umfassen Stromelysin 1 (MMP-3), Stromelysin 2 (MMP-10) und Matrilysin (MMP-7). Es gibt jedoch MMPs, die nicht eindeutig in die obigen Gruppen passen, zum Beispiel die Metalloelastase (MMP-12), MMP des Membrantyps (MT-MMP oder MMP-14) und Stromelysin 3 (MMP-11).
- Die Überexpression und die Aktivierung von MMPs ist mit einem großen Bereich an Krankheiten verbunden, wie Krebs, rheumatoide Arthritis, Osteoarthritis, chronische Entzündungserkrankungen, wie Asthma, Bronchitis und Emphysem, kardiovaskuläre Erkrankungen, wie Atheriosklerose, Hornhautulceration, dentale Erkrankungen, wie Zahnfleischentzündung und Paradontose, neurologische Erkrankungen, wie multiple Sklerose und Restenose. MMP-12 ist zum Beispiel für die Entwicklung von durch Zigarettenrauch induziertem Emphysem in Mäusen erforderlich (Science, 277,2002 (1997). Die Hemmung von MMPs ist somit eine Strategie für die Behandlung von solchen Krankheitszuständen. Es wurde jedoch gezeigt, dass die nicht-selektive Hemmung der Aktivität der Matrix-Metalloproteinasen die normalen physiologischen Abläufe beeinflussen kann, was zu die Dosis limitierenden Nebenwirkungen führt. Die selektive Hemmung von MMP-12 und/oder MMP-9 kann eine besonders relevante Strategie für die Intervention bei entzündlichen Zuständen sein.
- MMPs können den membrangebundenen Vorläufer des proentzündlichen Cytokin-Tumornekrosefaktors α (TNF-α) hydrolisieren. Diese Spaltung führt zu dem reifen, löslichen TNF-α, und die Hemmstoffe der MMPs können die Bildung von TNF-α sowohl in vitro als auch in vivo blockieren. Diese pharmakologische Wirkung ist wahrscheinlich an der entzündungshemmenden Wirkung von dieser Klasse an Verbindungen beteiligt.
- Für eine neuere Übersicht der MMP-Hemmung, wie sie in der Patentliteratur reflektiert wird, wird verwiesen auf Doherty et. al. Therapeutic Developments in Matrix Metalloproteinase Inhibition; Expert Opinions on Therapeutic Patents, 2002, 12, 665-707.
- Die WO 95 23790 beschreibt insbesondere substituierte N-Hydroxy-N'-(imidazolylmethyl)-succinamide, die als Matrix-Metalloproteinase (MMP)-Inhibitoren nützlich sind.
- Chen et. al. (Bioorganic und Medicinal Chemistry Leiters, Band 6, Nr. 13,9) beschreibt MMP Inhibitoren mit Imidazolyl -oder Benzimidazolyl-Resten.
- Die WO 96 33176 beschreibt MMP Inhibitoren mit einer Reihe von Azolylresten, einschließlich Imidazolyl-, Thiazolyl- und Oxazolyl-Resten.
- Die US 2001/021718 beschreibt MMP Inhibitoren mit Oxazolyl- oder Oxadiazolylresten.
- Die vorliegende Erfindung stellt eine Klasse von Verbindungen bereit, die Inhibitoren von MMPs sind. Die Klasse umfasst Verbindungen, die selektive Inhibitoren von MMP-12 im Verhältnis zu Kollagenasen und Stromelysinen sind. Verbindungen nach der Erfindung können zusätzlich eine selektive Aktivität gegenüber MMP-9 zeigen. Verbindungen nach der Erfindung können somit angezeigt sein für die Behandlung von Krankheiten, die primär durch MMP-9 und/oder MMP-12 vermittelt werden, insbesondere entzündliche Zustände, wie die multiple Sklerose und die Fibrose.
- Gemäß der vorliegenden Erfindung wird eine Verbindung bereitgestellt mit der Formel (IA oder (IB)). wobei
W HO(C=O)-, HONH(C=O)- oder H(C=O)N(OH)- repräsentiert;
X -O- oder -S- repräsentiert;
R1 Wasserstoff;
-OH oder -SH;
Fluoro oder Chloro;
-CF3:
(C1-C6)Alkyl;
(C1-C6)Alkoxy;
(C2-C6)Alkenyl;
Phenyl oder substituiertes Phenyl;
Phenyl(C1-C6)alkyl oder substituiertes Phenyl(C1-C6)alkyl;
Phenyl(C2-C6)alkenyl oder substituiertes Phenyl(C2-C6)alkenyl, Heterocyclyl oder substituiertes Heterocyclyl;
Heterocyclyl(C1-C6)alkyl oder substituiertes Heterocyclyl(C1-C6) alkyl;
eine Gruppe BSOnA-, wobei n 0, 1 oder 2 ist und B Wasserstoff oder ein (C1-C6)Alkyl, Phenyl, substituiertes Phenyl, Heterocyclyl, substituiertes Heterocyclyl, (C1-C6)Acyl, Phenacyl oder eine substituierte Phenacylgruppe ist, und A (C1-C6)Alkylen ist;
-NH2, (C1-C6)Alkylamino oder Di(C1-C6)alkylamino;
Amino(C1-C6)alkyl, (C1-C6)Alkylamino(C1-C6)alkyl, Di(C1-C6)alkylamino(C1-C6)alkyl, Hydroxy(C1-C6)alkyl, Mercapto(C1-C6)alkyl oder Carboxy(C1-C6)alkyl, wobei die Amino-, Hydroxy-, Mercapto- oder Carboxyl- Gruppe optional geschützt sind oder die Carboxylgruppe amidiert ist; oder
Cycloalkyl, Cycloalkenyl oder ein nicht-aromatischer heterocyclischer Ring, welcher bis zu 3 Heteroatome enthält, wobei jeder davon (i) substituiert sein kann mit einem oder mehreren Substituenten, die ausgewählt sind aus C1-C6 Alkyl, C2-C6 Alkenyl, Halogen, Cyano (-CN),
-CO2H, -CO2R, -CONH2, -CONHR, -CON(R)2, -OH, -OR, Oxo-, -SH, -SR, -NHCOR und -NHCO2R, wobei R C1-C6 Alkyl oder Benzyl ist, und/oder (ii) fusioniert an einem Cycloalkyl oder einem heterozyklischen Ring sein kann, repräsentiert;
R2 eine Gruppe R10-(X)n-(ALK)m- repräsentiert, wobei
R10 Wasserstoff oder eine C1-C6 Alkyl-, C2-C6 Alkenyl-, C2-C6 Alkinyl-Cycloalkyl-, Aryl- oder eine Heterocyclyl- Gruppe ist, wobei jede davon unsubstituiert oder substituiert sein kann mit (C1-C12)Alkyl, (C1-C12)Alkoxy, Hydroxy, Mercapto, (C1-C12)Alkylthio, Amino, Halo (einschließlich Fluoro, Chloro, Bromo und lodo), Trifluoromethyl, Cyano, Nitro, Oxo, -COOH, -CONH2, -COORA, -NHCORA, -CONHRA, -NHRA, -NRARB oder -CONRARB, wobei RA und RB unabhängig voneinander eine (C1-C6)Alkylgruppe darstellen und ALK ein geradkettiges oder verzweigtkettiges, divalentes C1-C6 Alkylen, C2-C6 Alkenylen oder ein C2-C6 Alkinylenradikal repräsentiert und durch eine oder mehrere, nicht-benachbarte -NH-, -O- oder -S-Verknüpfungen unterbrochen sein kann,
X eine -NH-, -O-, -S-, -NRC oder -NCORC repräsentiert, wobei RC eine (C1-C12)Alkylgruppe ist, und
m und n unabhängig voneinander 0 oder 1 sind;
R3 die Seitenkette einer natürlichen oder nicht-natürlichen Alpha-Aminosäure repräsentiert;
R4 optional substituiertes
C1-C6 Alkyl,
C2-C6 Alkenyl,
C2-C6 Alkinyl,
C1-C3 Perfluoroalkyl,
Cycloalkyl,
Cycloalkyl(C1-C6 alkyl)-,
Cycloalkenyl,
Cycloalkenyl(C1-C6 alkyl)-,
Phenyl,
Phenyl(C1-C6 alkyl)-,
Naphthyl,
Non-Aryl-Heterocyclyl,
Non-Aryl-Heterocyclyl(C1-C6 alkyl)-,
Heteroaryl, oder
Heteroaryl(C1-C6 alkyl)-repräsentiert;
und pharmazeutisch akzeptable Salze, Hydrate oder Solvate davon. - Wie hier verwendet, bedeutet der Ausdruck „(C1-C6)Alkyl" eine geradkettige oder verzweigtkettige Alkylkomponente mit 1 bis 6 Kohlenstoffatomen, zum Beispiel umfassend Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, Isobutyl, sec-Butyl, t-Butyl, n-Pentyl und n-Hexyl.
- Wie hier verwendet, bedeutet der Ausdruck „divalentes (C1-C6) Alkylenradikal" eine gesättigte Kohlenwasserstoffkette mit 1 bis 6 Kohlenstoffatomen und zwei ungesättigten Valenzen.
- Wie hier verwendet, bedeutet der Ausdruck „(C2-C6)Alkenyl" eine geradkettige oder verzweigtkettige Alkenylkomponente mit 2 bis 6 Kohlenstoffatomen und mit wenigstens einer Doppelbindung mit E- oder Z-Stereochemie, wo anwendbar. Der Ausdruck umfasst zum Beispiel Vinyl, Allyl, 1- und 2-Butenyl und 2-Methyl-2-propenyl.
- Wie hier verwendet, bedeutet der Ausdruck „divalentes (C2-C6) Alkenylenradikal" eine Kohlenwasserstoffkette mit 2 bis 6 Kohlenstoffatomen, wenigstens einer Doppelbindung und mit zwei ungesättigten Valenzen.
- Wie hier verwendet, bezieht sich der Ausdruck „C2-C6 Alkinyl" auf geradkettige oder verzweigtkettige Kohlenwasserstoffgruppen mit 2 bis 6 Kohlenstoffatomen und zusätzlich mit einer Dreifachbindung. Dieser Ausdruck umfasst zum Beispiel Ethinyl, 1-Propinyl, 1- und 2-Butinyl, 2-Methyl-2-propinyl, 2-Pentinyl, 3-Pentinyl, 4-Pentinyl, 2-Hexinyl, 3-Hexinyl, 4-Hexinyl und 5-Hexinyl.
- Wie hier verwendet, bedeutet der Ausdruck „divalentes (C2-C6) Alkinylenradikal" eine Kohlenwasserstoffkette mit 2 bis 6 Kohlenstoffatomen, wenigstens einer Dreifachbindung und zwei ungesättigten Valenzen.
- Wie hier verwendet, bedeutet der Ausdruck „Cycloalkyl" eine gesättigte alicyclische Komponente mit 3-8 Kohlenstoffatomen und umfasst zum Beispiel Cyclopropyl, Cyclobutyl, Cyclopentyl, Cyclohexyl, Cycloheptyl und Cyclooctyl.
- Wie hier verwendet, bedeutet der Ausdruck „Cycloalkenyl" eine ungesättigte alicyclische Komponente mit 3-8 Kohlenstoffatomen und umfasst zum Beispiel Cyclopropenyl, Cyclobutenyl, Cyclopentenyl, Cyclohexenyl, Cycloheptenyl und Cyclooctenyl. Im Falle von Cycloalkenylringen mit 5-8 Kohlenstoffatomen kann der Ring mehr als eine Doppelbindung enthalten.
- Wie hier verwendet, bezieht sich der Ausdruck „Aryl" auf eine mono-, bi- oder tricyclische, carbocyclische, aromatische Gruppe und auf Gruppen, die aus zwei kovalent miteinander verbundenen, monocyclischen, carbocyclischen, aromatischen Gruppen bestehen. Beispiele für solche Gruppen sind Phenyl, Biphenyl und Naphthyl.
- Wie hier verwendet, umfasst der unqualifizierte Ausdruck „Heterocyclyl" oder „heterozyklisch" „Heteroaryl", wie unten definiert, und bedeutet insbesondere einen 5-8 gliedrigen, aromatischen oder nicht-aromatischen, heterozyklischen Ring, der ein oder mehrere Heteroatome enthält, die ausgewählt sind aus S, N und O und die optional an ein Benzyl oder einen sekundären, heterozyklischen Ring kondensiert sind, und der Ausdruck umfasst zum Beispiel Pyrrolyl, Furyl, Thienyl, Piperidinyl, Imidazolyl, Oxazolyl, Thiazolyl, Thiadiazolyl, Thiazepinyl, Pyrazolyl, Pyridinyl, Pyrrolidinyl, Pyrimidinyl, Morpholinyl, Piperazinyl, Indolyl und Benzimidazolylringe.
- Wie hier verwendet, bezieht sich der Ausdruck „Heteroaryl" auf einen 5- oder 6-gliedrigen, aromatischen Ring, der ein oder mehrere Heteroatome enthält und optional an ein Benzyl oder einen Pyridylring kondensiert sein kann, sowie auf Gruppen, die aus zwei kovelent miteinander verbundenen, 5- oder 6-gliedrigen, aromatischen Ringen bestehen, die jeweils ein oder mehrere Heteroatome enthalten, und auf Gruppen, die aus einer monocyclischen, carbocyclischen, aromatischen Gruppe bestehen, welche an 5- oder 6-gliedrige, aromatische Ringe kovalent gebunden sind, welche ein oder mehrere Heteroatome enthalten. Beispiele für solche Gruppen sind Thienyl, Furyl, Pyrrolyl, Imidazolyl, Benzimidazolyl, Thiazolyl, Pyrazolyl, Isoxozolyl, Isothiazolyl, Triazolyl, Thiadiazolyl, Oxadiazolyl, Pyridinyl, Pyridazinyl, Pyrimidinyl, Pyrazinyl, Triazinyl, 4-([1,2,3]-Thiadiazoly-4-yl)phenyl und 5-Isoxazol-3-ylthienyl.
- Wie hier verwendet, bezieht sich der unqualifizierte Ausdruck „Carbocyclyl" oder „carbocyclisch" auf einen 5-8 gliedrigen Ring, dessen Ringatome alle Kohlenstoff darstellen.
- Soweit nicht an anderer Stelle anders spezifiziert, bedeutet der Ausdruck „substituiert", wie er hier auf jede Komponente angewendet wird, substituiert mit bis zu vier Substituenten, wobei jede davon unabhängig voneinander (C1-C6)Alkyl, Phenyl, Benzyl, (C1-C6)Alkoxy, Phenoxy, Hydroxy, Mercapto, (C1-C6)Alkylthio, Amino, Halo (einschließlich Fluoro, Chloro, Bromo und lodo), Trifluoromethyl, Cyano, Nitro, Oxo, -COOH, -CONH2, -CORA, -COORA, -NHCORA, -CONHRA, -NHRA, -NRARB oder -CONRARB sein kann, wobei RA und RB unabhängig voneinander eine (C1-C6)Alkylgruppe sind. In dem Fall, wo „substituiert" mit Benzyl substituiert bedeutet, kann der Phenylring davon selbst mit einem der vorhergehenden Substituenten substituiert sein mit Ausnahme von Phenyl oder Benzyl.
- Wie hier verwendet, bedeuten die Ausdrücke „Seitenkette einer natürlichen Alpha-Aminosäure" und „Seitenkette einer nicht-natürlichen Alpha-Aminosäure" die Gruppe Rx in einer natürlichen bzw. in einer nichtnatürlichen Aminosäure der Formel NH2-CH(Rx)-COOH.
- Beispiele für Seitenketten von natürlichen Alpha-Aminosäuren umfassen solche von Alanin, Arginin, Asparagin, Asparaginsäure, Cystein, Cystin, Glutaminsäure, Histidin, 5-Hydroxylysin, 4-Hydroxyprolin, Isoleucin, Leucin, Lysin, Methionin, Phenylalanin, Prolin, Serin, Threonin, Tryptophan, Tyrosin, Valin, α-Aminoadipinsäure, α-Amino-n-Buttersäure, 3,4-Dihydroxyphenylalanin, Homoserin, α-Methylserin, Ornithin, Pipecolinsäure und Thyroxin.
- In Seitenketten von natürlichen Alpha-Aminosäuren, welche funktionelle Substituenten enthalten, zum Beispiel Amino, Carboxyl, Hydroxy, Mercapto, Guanidyl, Imidazolyl oder Indolylgruppen, wie in Arginin, Lysin, Glutaminsäure, Asparaginsäure, Tryptophan, Histidin, Serin, Threonin, Tyrosin und Cystein, können solche funktionelle Substituenten optional geschützt sein.
- In ähnlicher Weise können die Seitenketten von nicht-natürlichen Alpha-Aminosäuren, welche funktionelle Substituenten enthalten, zum Beispiel Amino-, Carboxyl-, Hydroxy-, Mercapto-, Guanidyl-, Imidazolyl- oder Indolylgruppen, wobei solche funktionelle Substituenten optional geschützt sein können.
- Der Ausdruck „geschützt" bedeutet, wenn er in Beziehung zu einem funktionellen Substituenten in einer Seitenkette einer natürlichen oder nicht-natürlichen Alpha-Aminosäure verwendet wird, ein Derivat von solch einem Substituenten, das im Wesentlichen nicht-funktionell ist. Ein Überblick über dieses Thema bietet das breit genutzte Handbuch von T. W. Greene und P. G. Wuts „Protective Groups in Organic Synthesis" 2. Ausgabe, Wiley, New York, 1991. So können zum Beispiel Carboxylgruppen verestert (z. B. als ein C1-C6 Alkylester) werden; Aminogruppen können zu Amiden (z. B. als ein NHCOC1-C6 Alkylamid) oder zu Carbamaten (z. B. als ein NHC(=O)OC1-C6 Alkyl oder ein NHC(=O)OCH2Ph Carbamat) umgewandelt werden; Hydroxylgruppen können zu Ether (z. B. ein OC1-C6 Alkyl oder ein O(C1-C6 Alkyl)phenylether) oder Ester (z. B. ein OC(=O)C1-C6 Alkylester) umgewandelt werden und Thiolgruppen können umgewandelt werden zu Thioether (z. B. ein tert-Butyl oder Benzylthioether) oder zu Thioester (z. B. ein SC(=O)C1-C6 Alkylthioester).
- Es gibt wenigstens zwei aktuelle oder potentielle chirale Zentren in den Verbindungen gemäß der Erfindung aufgrund der Gegenwart von asymmetrischen Kohlenstoffatomen. Die Gegenwort von verschiedenen asymmetrischen Kohlenstoffatomen führt zu einer Reihe von Diastereomeren mit R- oder S-Stereochemie an jedem chiralen Zentrum. Die Erfindung umfasst alle solche Diastereomere und Mischungen davon. Gegenwärtig ist die bevorzugte Stereokonfiguration an dem Kohlenstoffatom, welches die R2 Gruppe trägt, R. Die bevorzugte Stereokonfiguration an dem Kohlenstoffatom, welches die R1 Gruppe (wenn asymmetrisch) trägt, ist R. Die bevorzugte Stereokonfiguration des Kohlenstoffatoms, welches die R3 Gruppe (wenn asymmetrisch) trägt, ist S.
- Die Gruppe R1
R1 kann zum Beispiel
Wasserstoff, Hydroxy, Methyl, Methoxy, Trifluoromethyl, Ethyl, n-Propyl, Allylphenylpropyl, Cyclopropylmethyl, Phenylprop-2-enyl, Thienylsulphanylmethyl, Thienylsulphinylmethyl, oder Thienylsulphonylmethyl; oder
C1-C4 Alkyl, z. B. Methyl, Ethyl, n-Propyl oder n-Butyl, substituiert durch ein Phthalimido, 1,2-Dimethyl-3,5-dioxo-1,2,4-triazolidin-4-yl, 3-Methyl-2,5-dioxo-1-imidazolidinyl, 3,4,4-Trimethyl-2,5-dioxo-1-imidazolidinyl, 2-Methyl-3,5-dioxo-1,2,4-oxadiazol-4-yl, 3-Methyl-2,4,5-trioxo-1-imidazolidinyl, 2,5-Dioxo-3-phenyl-1-imidazolidinyl, 2-Oxo-1-pyrrolidinyl, 2,5-Dioxo-1-pyrrolidinyl oder 2,6-Dioxopiperidinyl, 5,5-Dimethyl-2,4-dioxo-3-oxazolidinyl, Hexahydro-1,3-dioxopyrazolo[1,2,a][1,2,4]-triazol-2-yl oder ein Naphththalimido (d.h. 1,3-Dihydro-1,3-dioxo-2H-benz[f]isoindol-2-yl), 1,3-Dihydro-1-oxo-2H-benz[f]isoindol-2-yl, 1,3-Dihydro-1,3-dioxo-2H-pyrrolo[3,4-b]chinolin-2-yl oder 2,3-Dihydro-1,3-dioxo-1H-benz[d,e]isochinolin-2-yl Gruppe; oder
Cyclohexyl, Cyclooctyl, Cycloheptyl, Cyclopentyl, Cyclobutyl, Cyclopropyl, Tetrahydropyranyl oder Morpholinyl sein. - Zurzeit bevorzugte R1 Gruppen umfassen Wasserstoff, Hydroxy, Methoxy, Cyclopentyl, n-Propyl und Allyl. Von diesen sind Wasserstoff, Hydroxy, Methoxy und Allyl zur Zeit mehr bevorzugt.
- Die Gruppe R2
R2 kann zum Beispiel
C1-C12 Alkyl, C3-C6 Alkenyl oder C3-C6 Alkinyl; Cycloalkyl(C1-C6 alkyl)-;
Phenyl(C1-C6 alkyl)-, Phenyl(C3-C6 alkenyl)- oder Phenyl(C3-C6 alkinyl)-, optional substituiert in dem Phenylring;
Heteroaryl(C1-C6 alkyl)-, Heteroaryl(C3-C6 alkenyl)- oder Heteroaryl(C3-C6 alkinyl)-, optional substituiert in dem Heteroarylring;
4-Phenylphenyl(C1-C6 alkyl)-, 4-Phenylphenyl(C3-C6 alkenyl)-, 4-Phenylphenyl(C3-C6 alkinyl)-, 4-Heteroarylphenyl(C1-C6 alkyl)-, 4-Heteroarylphenyl(C3-C6 alkenyl)-, 4-Heteroarylphenyl(C3-C6 alkinyl)-, optional substituiert in dem terminalen Phenyl- oder Heteroarylring;
Phenoxy(C1-C6 alkyl)- oder Heteroaryloxy(C1-C6 alkyl)-, optional substituiert in dem Phenyl- oder Heteroarylring. - Spezifische Beispiele für solche Gruppen umfassen Methyl, Ethyl, n- oder iso-Propyl, n-, iso- oder tert-Butyl, n-Pentyl, n-Hexyl, n-Heptyl, n-Nonyl, n-Decyl, Prop-2-yn-1-yl, Cyclohexylethyl, Cyclopentylmethyl, 3- Phenylprop-2-yn-1-yl, 3-(2-Chlorophenyl)prop-2-yn-1-yl, Benzylphenylpropyl, 4-Chlorophenylpropyl, 4-Methylphenylpropyl, 4-Methoxyphenylpropyl, Phenoxybutyl, 3-(4-Pyridylphenyl)propyl-, 3-(4-(4-Pyridyl)phenyl)prop-2-yn-1-yl, 3-(4-Phenylphenyl)propyl-, 3-(4-Phenyl)phenyl)prop-2-yn-1-yl und 3-[(4-Chlorophenyl)phenyl]propyl-.
- Zurzeit bevorzugte R2 Gruppen umfassen Benzyl, n-Butyl, iso-Butyl, n-Hexyl, Ethoxyphenylpropyl, vorzugszweise 4-Ethoxyphenylpropyl, und Cyclopentylmethyl. Von diesen sind zur Zeit Isobutyl und Ethoxyphenylpropyl, insbesondere 4-Ethoxyphenylpropyl, mehr bevorzugt.
- Die Gruppe R3
R3 kann zum Beispiel sein C1-C6 Alkyl, Phenyl, 2-, 3- oder 4-Pyridyl, 2- oder 3-Thienyl, 2-, 3- oder 4-Hydroxyphenyl, 2-, 3- oder 4-Methoxyphenyl, 2-, 3- oder 4-Pyridylmethyl, Benzyl, 2-, 3- oder 4-Hydroxybenzyl, 2-, 3- oder 4-Benzyloxybenzyl, 2-, 3- oder 4-C1-C6 Alkoxybenzyl oder Benzyloxy(C1-C6 alkyl) sein; oder
die charakterisierende Gruppe einer natürlichen α-Aminosäure, wobei jede funktionelle Gruppe geschützt sein kann, jede Aminogruppe kann acyliert und jede vorhandene Carboxylgruppe kann amidiert sein; oder eine Gruppe -[Alk]nR6, wobei Alk eine (C1-C6)Alkyl- oder eine (C2-C6)Alkenylgruppe ist, optional unterbrochen durch ein oder mehrere -O- oder -S- Atome oder -N(R7)- Gruppen [wobei R7 ein Wasserstoffatom oder eine (C1-C6)Alkylgruppe ist), n ist 0 oder 1, und R6 ist eine optional substituierte Cycloalkyl- oder Cycloalkenylgruppe;
oder
eine Benzylgruppe, die in dem Phenylring substituiert ist durch eine Gruppe der Formel -OCH2COR8, wobei R8 ein Hydroxyl, Amino, (C1-C6) Alkoxy, Phenyl(C1-C6)alkoxy, (C1-C6)Alkylamino, Di((C1-C6)alkyl)amino, Phenyl(C1-C6)alkylamino, der Rest einer Aminosäure oder eines Säurehalogenids, Esters oder Amidderivats davon ist, wobei dieser Rest über eine Amidbindung verbunden ist und die Aminosäure ausgewählt wird aus Glycin, α- oder β-Alanin, Valin, Leucin, Isoleucin, Phenylalanin, Tyrosin, Tryptophan, Serin, Threonin, Cystein, Methionin, Asparagin, Glutamin, Lysin, Histidin, Arginin, Glutaminsäure und Asparaginsäure; oder
eine heterozyklische (C1-C6)Alkylgruppe, entweder unsubstituiert oder mono- oder di- substituiert in dem heterozyklischen Ring mit Halogen, Nitro, Carboxy, (C1-C6)Alkoxy, Cyano, (C1-C6)Alkanoyl, Trifluoromethyl(C1-C6)alkyl, Hydroxy, Formyl, Amino, (C1-C6) Alkylamino, Di-(C1-C6)alkylamino, Mercapto, (C1-C6)Alkylthio, Hydroxy (C1-C6)alkyl, Mercapto (C1-C6)alkyl oder (C1-C6) Alkylphenylmethyl; oder
eine Gruppe -CraRbRc, wobei
jeder von Ra, Rb und Rc unabhängig voneinander Wasserstoff, (C1-C6) Alkyl, (C2-C6)Alkenyl, (C2-C6)Alkinyl, Phenyl (C1-C6)alkyl, (C3-C8) Cycloalkyl ist; oder
Rc ist Wasserstoff und Ra und Rb unabhängig voneinander Phenyl oder Heteroaryl sind, wie Pyridyl; oder Rc ist Wasserstoff, (C1-C6)Alkyl, (C2-C6)Alkenyl, (C2-C6)Alkinyl, Phenyl(C1-C6)alkyl oder (C3-C8) Cycloalkyl ist, und Ra und Rb bilden zusammen mit dem Kohlenstoffatom, mit dem sie verbunden sind, einen 3- bis 8-gliedrigen Cycloalkyl- oder einen 5- bis 6-gliedrigen heterozyklischen Ring bilde; oder Ra, Rb und Rc zusammen mit dem Kohlenstoffatom, mit dem sie verbunden sind, einen tricyclischen Ring (z. B. Adamantyl) bilden; oder
Ra und Rb jeweils unabhängig voneinander (C1-C6)Alkyl, (C2-C6) Alkenyl, (C2-C6)Alkinyl, Phenyl (C1-C6)alkyl sind, oder eine Gruppe, wie für Rc unten definiert, verschieden von Wasserstoff, oder Ra und Rb zusammen mit dem Kohlenstoffatom, mit dem sie verbunden sind, einen Cycloalkyl- oder einen heterozyklischen Ring bilden, und Rc Wasserstoff, -OH, -SH, Halogen, -CN, -CO2H, (C1-C4)Perfluoroalkyl, -CH2OH, -CO2(C1-C6)Alkyl, -O(C1-C6)Alkyl, -O(C2-C6)Alkenyl, -S(C1-C6) Alkyl, -SO(C1-C6)Alkyl, -SO2(C1-C6)Alkyl, -S(C2-C6)Alkenyl, -SO(C2-C6) Alkenyl, -SO2(C2-C6)Alkenyl ist, oder eine Gruppe -Q-W, wobei Q eine Bindung oder -O-, -S-, -SO- oder -SO2- repräsentiert und W ein Phenyl, Phenylalkyl, (C3-C8)Cycloalkyl, (C3-C8)Cycloalkylolkyl, (C4-C8)Cycloalkenyl, (C4-C8)Cycloalkenylalkyl, eine Heteroaryl- oder eine Heteroarylalkylgruppe repräsentiert, wobei die Gruppe W optional substituiert sein kann mit einem oder mehreren Substituenten, die unabhängig ausgewählt sind aus Hydroxyl, Halogen, -CN, -CO2H, -CO2(C1-C6)Alkyl, -CONH2, -CONH(C1-C6)Alkyl, -CONH(C1-C6alkyl)2, -CHO, -CH2OH, (C1-C4)Perfluoroalkyl, -O(C1-C6)Alkyl, -S(C1-C6)Alkyl, -SO(C1-C6)Alkyl, -SO2(C1-C6)Alkyl, -NO2, -NH2, -NH(C1-C6)Alkyl, -N((C1-C6)alkyl)2, -NHCO(C1-C6)Alkyl, (C1-C6)Alkyl, (C2-C6)Alkenyl, (C2-C6)Alkinyl, (C3-C8)Cycloalkyl, (C4-C8)Cycloalkenyl, Phenyl oder Benzyl. - Beispiele für besondere R3 Gruppen umfassen Benzyl, Phenyl, Cyclohexylmethyl, Pyridin-3-ylmethyl, tert-Butoxymethyl, iso-Propyl, iso-Butyl, sec-Butyl, tert-Butyl, 1-Benzylthio-1-methylethyl, 1-Methylthio-1-methylethyl und 1-Mercapto-1-methylethyl.
- Besonders bevorzugte R3 Gruppen umfassen zurzeit Phenyl, Benzyl, tert-Butoxymethyl, iso-Propyl, tert-Butyl und iso-Butyl. Von diesen sind zurzeit tert-Butyl und Benzyl mehr bevorzugt.
- Die Gruppe R4
R4 kann zum Beispiel (C1-C6)Alkyl sein, wie Methyl, Ethyl, n- oder iso-Propyl, Prop-2-yl und tert-Butyl; (C3-C8)Cycloalkyl, wie Cyclopropyl, Cyclopentyl; Phenyl; Phenyl(C1-C6alkyl)-, wie Benzyl; Heteroaryl(C1-C6alkyl)-, wie Thienylmethyl; monocyclische Heterocyclic, wie Morpholino; oder monozyklisches Heteroaryl, wie Thienyl oder Furanyl. Jede der vorangegangenen Gruppen kann optional substituiert sein, zum Beispiel mit Methyl, Trifluoromethyl, Hydroxy, Mercapto, Amino oder Carboxy. - Wie oben erwähnt, sind die vorliegenden Verbindungen nützlich in der Humanmedizin oder in der Veterinärmedizin, da sie aktiv sind als Inhibitoren von MMPs. Gemäß einem anderen Aspekt betrifft diese Erfindung:
- (i) eine Verbindung, die ein Mitglied der oben definierten Gruppe ist, zur Verwendung in der Humanmedizin oder der Veterinärmedizin, insbesondere bei dem Management (damit ist die Behandlung oder die Prophylaxe gemeint) von Krankheiten oder Zuständen, die durch MMP vermittelt werden; und
- (ii) die Verwendung einer Verbindung, die ein Mitglied der oben definierten Gruppe ist, bei der Herstellung eines Mittels für das Management (mit dem die Behandlung oder die Prophylaxe gemeint ist) von Krankheiten oder Zuständen, welche durch MMPs vermittelt werden.
- Krankheiten oder Zustände, die durch MMPs vermittelt werden, umfassen solche, die bei einem Gewebezusammenbruch beteiligt sind, wie Knochenresorption, entzündliche Erkrankungen, dermatologische Zustände und Tumorwachstum oder Invasion durch sekundäre Metastasen, insbesondere rheumatoide Arthritis, Osteoarthritis, Periodontitis, Gingivitis, Hornhautulceration, neuroentzündliche Erkrankungen, einschließlich solche, die einen Myelinabbau umfassen, zum Beispiel Multiple Sklerose; Restenose, Emphysem, Bronchitis und Asthma.
- Gemäß einem weiteren Aspekt der Erfindung wird eine pharmazeutische oder Veterinärzusammensetzung bereitgestellt, die eine Verbindung umfasst, welche ein Mitglied der oben definierten Gruppe ist, zusammen mit einem pharmazeutisch oder veterinär akzeptablen Bindemittel oder Trägerstoff.
- Es ist zu verstehen, dass die spezifische Dosierung für jeden einzelnen Patienten von einer Reihe von Faktoren abhängig sein wird, einschließlich der Aktivität der verwendeten spezifischen Verbindung, dem Alter, dem Körpergewicht, dem allgemeinen Gesundheitszustand, dem Geschlecht, der Ernährung, Zeitpunkt der Verabreichung, Route der Verabreichung, Rate der Exkretion, Arzneimittelkombination und Stärke der besonderen zugrunde liegenden Krankheitstherapie. Die optimale Dosierung und die Häufigkeit der Dosierung werden in klinischen Studien bestimmt werden.
- Die Verbindungen, auf die sich die Erfindung bezieht, können für die Verabreichung über jede Route hergestellt werden, der mit seinen pharmakokinetischen Eigenschaften konsistent ist. Oral verabreichbare Zusammensetzungen können in der Form von Tabletten, Kapseln, Pulvern, Körnern, Pastillen, flüssige oder Gel-Zubereitungen, wie orale, topische oder sterile parenterale Lösungen oder Suspensionen, vorliegen. Tabletten und Kapseln für die orale Verabreichung können in einer Einzeldosis-Darreichungsform vorliegen und können konventionelle Trägerstoffe, wie Bindemittel, zum Beispiel Sirup, Akaziengummi, Gelatine, Sorbit, Tragant oder Polyvinylpyrrolidon, enthalten; Füllstoffe, zum Beispiel Laktose, Zucker, Maisstärke, Calciumphosphat, Sorbit oder Glycin; Tablettierschmiermittel, zum Beispiel Magnesiumstearat, Talk, Polyethylenglykol oder Kieselerde; Desintegratoren, zum Beispiel Kartoffelstärke oder akzeptable Benetzungsmittel, wie Natriumlaurylsulfat. Die Tabletten können durch Verfahren beschichtet sein, welche in der normalen pharmazeutischen Praxis bekannt sind. Orale flüssige Zubereitungen können in der Form von beispielsweise wässrigen oder öligen Suspensionen, Lösungen, Emulsionen, Sirups oder Elixier vorliegen, oder können als Trockenprodukt für die Wiederherstellung mit Wasser oder einem anderen geeigneten Vehikel vor der Verwendung präsentiert werden. Solche flüssigen Zubereitungen können konventionelle Additive enthalten, wie Suspendiermittel, zum Beispiel Sorbit, Sirup, Methylcellulose, Glycosesirup, Gelatine, hydrierte essbare Fette; Emulgiermittel, zum Beispiel Lecitin, Sorbitanmonooleat oder Akaziengummi; nicht-wässrige Vehikel (die essbare Öle umfassen), zum Beispiel Mandelöl, fraktioniertes Kokosnussöl, ölige Ester, wie Glycerin, Propylenglykol oder Ethylalkohol; Konservierungsmittel, zum Beispiel Methyl- oder Propyl-p-hydroxybenzoat oder Sorbinsäure, und, falls gewünscht, konventionelle Geschmacks- oder Farbmittel.
- Für die topische Applikation auf die Haut kann das Arzneimittel in eine Creme, Lotion oder Salbe eingebracht werden. Creme- oder Salbenformulierungen, die für das Arzneimittel verwendet werden können, sind konventionelle Formulierungen, die im Stand der Technik gut bekannt sind, zum Beispiel gemäß den Beschreibungen in Standardlehrbüchern der Pharmazeutik, wie British Pharmacopoeia.
- Für die topische Anwendung in das Auge kann das Arzneimittel in eine Lösung oder eine Suspension in einem geeigneten sterilen, wässrigen oder nicht-wässrigen Vehikel eingebracht werden. Additive, zum Beispiel Puffer, wie Natriummetabisulfit oder Dinatriumedeat; Konservierungsmittel, einschließlich bakterizide und fungizide Mittel, wie Phenylquecksilberacetat oder -nitrat, Benzalkoniumchlorid oder Chlorhexidin; und Verdickungsmittel, wie Hypromellose, können auch umfasst sein.
- Der Wirkstoff kann auch parenteral in einem sterilen Medium verabreicht werden. In Abhängigkeit von dem Vehikel und der verwendeten Konzentration kann der Arzneistoff entweder suspendiert oder gelöst in dem Vehikel vorliegen. In vorteilhafter Weise können Hilfsmittel, wie lokale Betäubungsmittel, Konservierungsmittel und Puffer in dem Vehikel gelöst werden.
- Verbindungen gemäß der vorliegenden Erfindung, bei denen W eine Hydroxamsäure-Gruppe HONH(C=O)- ist, können aus entsprechenden Verbindungen der Erfindung hergestellt werden, bei denen W eine Carboxylgruppe -COOH ist, oder von entsprechend geschützten Hydroxamsäure-Derivaten. Das Verfahren, welches einen anderen Aspekt der Erfindung darstellt, umfasst die Erzeugung einer Reaktion einer Säure der allgemeinen Formel (IIA) oder (IIB) oder eines aktivierten Derivates davon mit Hydroxylamin, O-geschütztem Hydroxylamin oder einem N,O-digeschützen Hydroxylamin oder einem Salz davon, wobei X, R1, R2, R3 und R4 den Definitionen in den allgemeinen Formeln (IA) oder (IB) entsprechen, außer, dass alle Substituenten in R1, R2, R3 und R4, welche potentiell reaktiv sind mit Hydroxylamin, O-geschütztem Hydroxylamin, N,O-digeschützem Hydroxylamin oder deren Salzen, selbst vor solch einer Reaktion geschützt sind, und anschließend alle Schutzgruppen von der erzielten Hydroxamsäure-Komponente und von allen geschützten Substituenten in R1, R2, R3 und R4 entfernt werden.
- Die Umwandlung von (IIA) oder (IIB) zu einem aktivierten Derivat, wie das Pentafluorophenyl-, Hydroxysuccinyl- oder Hydroxybenzotriazolylester, kann bewirkt werden durch die Reaktion mit einem geeigneten Alkohol in Gegenwart eines Trockenmittels, wie Dicyclohexyldicarbodiimid (DCC), N,N-Dimethylaminopropyl-N-ethylcarbodiimid (EDC) oder 2-Ethoxy-1-ethoxycarbonyl-1,2-dihydrochinolin (EEDQ).
- Die oben erwähnten Schutzgruppen sind per se gut bekannt, zum Beispiel von Techniken der Peptidchemie. Aminogruppen können oft durch Benzyloxycarbonyl, t-Butoxycarbonyl oder Acetylgruppen oder in Form einer Phthalimidogruppe geschützt werden. Hydroxygruppen können oft geschützt werden als fertig spaltbare Ether, wie t-Butyl- oder Benzylether, oder als fertig spaltbare Ester, wie das Acetat. Carboxylgruppen können oft durch fertig spaltbare Ester geschützt werden, wie t-Butyl- oder Benzylester.
- Beispiele für O-geschützte Hydroxylamine zur Verwendung bei dem obigen Verfahren (a) umfassen O-Benzylhydroxylamin, O-4-Methoxybenzylhydroxylamin, O-Trimethylsilylhydroxylamin und O-tert-Butoxycarbonylhydroxylamin.
- Beispiele für O,N-digeschützte Hydroxylamine zur Verwendung bei dem obigen Verfahren (a) umfassen N,O-Bis(benzyl)hydroxylamin, N,O-Bis(4-methoxybenzyl)hydroxylamin, N-tert-Butoxycarbonyl-O-tert-butyldimethylsilylhydroxylamin, N-tert-Butoxycarbonyl-O-tetrahydropyranylhydroxylamin und N,O-Bis(tert-butoxycarbonyl)hydroxylamin.
- Verbindungen nach der Erfindung, wobei W eine N-Formylhydroxylaminogruppe H(C=O)NH(OH)- ist, können durch eine N-Formylierung der entsprechenden O-geschützten Verbindung, bei der W -NH(OH) ist, und anschließender Entfernung der O-Schutzgruppe hergestellt werden.
- Verbindungen gemäß der vorliegenden Erfindung, bei denen W eine Carboxylsäuregruppe -COOH ist, das heißt, Verbindungen der Formeln (IIA) oder (IIB) können durch ein Verfahren hergestellt werden, welches die folgenden Schritte umfasst: Koppeln einer Säure der Formel (III) oder eines aktivierten Derivats davon mit einem Amin der Formel (IVA) oder (IVB) wobei X, R1, R2, R3 und R4 den Definitionen in den allgemeinen Formeln (IA) und (IB) entsprechen, außer, dass alle Substituenten in R1, R2, R3 und R4, welche potentiell in der Kopplungsreaktion reaktiv sind, selbst vor solch einer Reaktion geschützt sein können und R11 eine Hydroxy-Schutzgruppe darstellt; und die anschließende Entfernung der Schutzgruppe R11 und der anderen Schutzgruppen von R1, R2, R3 und R4.
- Aktive Derivate der Säuren (III) umfassen aktivierte Ester, wie der Pentafluorophenylester, Säureanhydride und Säurehalogenide, zum Beispiel Chloride. Geeignete Hydroxy-Schutzgruppen können aus denen im Stand der Technik bekannten ausgewählt werden.
- Verbindungen der Formeln (IVA) und (IVB) können mittels Verfahren hergestellt werden, die analog zu den allgemeinen Verfahren für die Oxadiazol-Ringbildung sind, die in den Schemata 1 und 2 in den folgenden Beispielen 1 und 2 erläutert sind.
- Die folgenden präparativen Beispiele beschreiben die Herstellung von Verbindungen, die gemäß der Erfindung nützlich sind.
- Die folgenden Abkürzungen werden bei den Beispielen verwendet:
- DCM
- – Dichlormethan
- DMF
- – N,N-Dimethylformamid
- HOBT
- – 1-Hydroxybenzotriazol
- Pfp
- – Pentafluorphenol
- WSCD
- – N-(3-Dimethylaminopropyl)-N'-ethylcarbodiimidhydrochlorid
- HCl
- – Salzsäure
- THF
- – Tetrahydrofuran
- TFA
- – Trifluoressigsäure
- P(O-Tol)3
- – Tri-O-tolylphosphin
- AcOEt
- – Ethylacetat
- CH3CN
- – Acetonitril
- Beispiel 1
- Reagenzien und Bedingungen: A. HOBT, WSC, NH3, DMF. B. OPCl3, Pyridin. C. Aq.NH2OH, Ethanol, 70° C. D. RCOCl, DMAP, Pyridin, DMF, 100° C. E. HBr/Essigsäure. F. chirales Succinat, DMF. G. Aq.NH2OH, Methanol. H. Pfp, WSC, DMF. I. 1M HCl, THF.
- Beispiel 1 wurde, wie in Schema 1 dargestellt, hergestellt unter Verwendung der im Folgenden beschriebenen Verfahren.
- Schritt A. (1S-Carbamoyl-2,2-dimethyl-propyl)-carbamidsäurebenzylester.
- N-Benzyloxycarbonyl-L-tert-butylglycin (50 g, 189 mMol) wurde in DMF (500 ml) gelöst und in einem Eiswasserbad vor Zugabe von HOBT (28,05 g; 208 mMol) und WSCDI (39,8 g; 208 mMol) gekühlt. Die Reaktion wurde bei 0° C für 1 Stunde vor der Zugabe von 0,880 Ammoniaklösung (21 ml; 377 mMol) gerührt. Die Reaktion erwärmte sich auf Zimmertemperatur und wurde für 18 Stunden gerührt. Unter reduziertem Druck wurde das DMF entfernt und der Rest zwischen Ethylacetat und 1M HCl aufgeteilt. Die organische Schicht wurde abgetrennt und mit 1M HCl, gesättigter wässriger Natriumbicarbonat-Lösung und Sole vor Trocknung über Magnesiumsulfat gewaschen, dann filtriert und unter reduziertem Druck konzentriert, um (1S-Carbamolyl-2,2-dimethyl-propyl)-carbamidsäurebenzylester als weißer Feststoff (44,1 g; 89%) zu erhalten.
1H-NMR; delta (CDCl3), 7,32 (5H, m); 6,05 (1H, bs); 5,71 (1H, bs); 5,60(1H, d, J = 6,5 Hz); 5,08 (2H,s); 4,01 (1H, d, J = 6,5 Hz) und 1,00 (9H, s).
LRMS; +ve lon 265 (M+H), 287 (M+Na). - Schritt B. (1S-Cyano-2,2-dimethyl-propyl)-carbamidsäurebenzylester. (1S-carbamoyl-2,2-dimethyl-propyl)-carbamidsäurebenzylester (44,1 g; 167 mMol) wurde in wasserfreiem Pyridin (203 ml; 2,5 Mol) unter einer inerten Atmosphäre gelöst und in einem Eiswasserbad gekühlt.
- Phosphoroxychlorid (21,8 ml; 234 mMol) wurde über einen Zeitraum von 15 Minuten langsam zugesetzt und es wurde in einem Eiswasserbad für 2 Stunden die Reaktion gekühlt, bevor sie auf Raumtemperatur erwärmt und für 12 Stunden gerührt wurde. Die Reaktionsmischung wurde mit Eiswasser (400 ml) behandelt und mit Ethylacetat (2 × 300 ml) extrahiert. Die organische Schicht wurde abgetrennt und mit 1M HCl, gesättigter wässriger Natriumbicarbonat-Lösung und mit Sole vor Trocknung mit Magnesiumsulfat gewaschen, dann filtriert und unter reduziertem Druck konzentriert. Eine Säulenchromatographie auf Kieselgel unter Verwendung von Ethylacetat/hexan als Eluent führte zu der Isolierung des gewünschten Produktes als ein orangenes Öl (36,72 g; 89%).
1H-NMR; delta (CDCl3), 7,42 (5H, m), 5,28 (2H, m), 4,55 (2H, d, J = 6,5 Hz) und 1,11 (9H, s).
LRMS; +ve lon 269 (M+Na), 247,2 (M+H). - Schritt C. [1S-(N-Hydroxycarbamimidoyl)-2,2-dimethyl-propyl]-carbamidsäurebenzylester.
- (1S-Cyano-2,2-dimethyl-propyl)-carbamidsäurebenzylester (37,60 g; 153 mMol) wurde in Ethanol (300 ml) gelöst und tropfenweise mit 50 wässrigem Hydroxylamin (51 ml; 764 mMol) behandelt. Die Reaktion wurde unter Rückfluss erhitzt und für 3 Stunden gerührt. Die Reaktion wurde dann abgekühlt und unter reduziertem Druck konzentriert, um das gewünschte Produkt als einen weißen Schaum/Gummi (41,5 g; 97%) zu erzielen.
1H-NMR; delta (CDCl3), 7,32 (5H, m), 6,21 (1H, bs), 5,95 (1H, bs), 5,81(1H, d, J = 6,4 Hz), 5,08 (2H, m), 4,79 (1H, bs), 4,05 (1H, d, J = 6,5 Hz) und 0,95 (9H, s).
LRMS; +ve lon 279,8 (M+H) - Schritt D. [2,2-Dimethyl-1S-(5-phenyl-[1,2,4]oxadiazol-3-yl)-propyl]-carbamidsäurebenzylester.
- [1S-(N-Hydroxycarbamimidoyl)-2,2-dimethyl-propyl]-carbamidsäurebenzylester (0,21 g; 0,75 mMol) wurde in DMF (5 ml) gelöst und mit Pyridin (0,1 ml; 128 mMol), Benzoylchlorid (0,13 ml; 1,1 mMol) und DMAP (katalytisch) behandelt. Die Reaktionsmischung wurde bei Raumtemperatur für 4 Stunden gerührt, bevor sie auf 100° C erhitzt und für 16 Stunden gerührt wurde. Die Reaktion wurde auf Raumtemperatur abgekühlt und unter reduziertem Druck konzentriert. Die Reaktion wurde mit Ethylacetat verdünnt und mit 1M HCl, gesättigter wässriger Natriumbicarbonat-Lösung und mit Sole gewaschen, über Magnesiumsulfat getrocknet und dann filtriert und unter reduziertem Druck konzentriert wurde. Das gewünschte Produkt wurde als ein orangenes Öl isoliert (0,22 g; 78%).
1H-NMR; delta (CDCl3), 8,12 (2H, m), 7,55 (3H, m), 7,32 (5H, m), 5,55 (1H, d, J = 6,4 Hz), 5,12 (2H, m), 4,95 (1H, d, J = 6,5 Hz) und 1,10 (9H, s).
LRMS; +ve lon 366,2 (M+H), 388,2 (M+Na). - Schritt E. 2,2-Dimethyl-1S-(5-phenyl-[1,2,4]oxadiazol-3-yl)-propylamin.
- [2,2-Dimethyl-1S-(5-phenyl-[1,2,4]oxadiazol-3-yl)-propyl]-carbamidsäurebenzylester (0,2 g; 0,5 mMol) wurde mit 48 Bromwasserstoffsäure in Essigsäure (10 ml) behandelt. Die Reaktionsmischung rührte bei Raumtemperatur für 3 Stunden. Die Reaktion wurde unter reduziertem Druck konzentriert und zwischen Ethylacetat und 1M Na2CO3 aufgeteilt. Die organische Schicht wurde weiter mit 1M Na2CO3 und Sole gewaschen und anschließend über Magnesiumsulfat getrocknet, filtriert und unter reduziertem Druck konzentriert. Das Produkt wurde als ein gelbes Öl isoliert (0,13 g; 98%).
LRMS; +ve lon 232 (M+H). - Schritt F. 2R-(2,2-Dimethyl-5-oxo-[1,3]dioxolan-4S-yl)-4-methylpentansäure[2,2-dimethyl-1S-(5-phenyl-[1,2,4]oxadiazol-3-yl)-propyl]amid.
- 2,2-Dimethyl-1S-(5-phenyl-[1,2,4]oxadiazol-3-yl)-propylamin (0,13 g; 0,6 mMol) wurde in DMF (5 ml) gelöst und in Eiswasser gekühlt vor der Zugabe von 2R-(2,2-Dimethyl-5S-oxo-[1,3]dioxolan-4-yl)-4-methylpentansäure-pentafluorophenylester (0,22 g: 0,6 mMol). Die Reaktion erwärmte sich auf Raumtemperatur und wurde für 15 Stunden gerührt. Unter reduziertem Druck wurde DMF entfernt und die Reaktion wurde mit Ethylacetat verdünnt und mit 1M HCl, gesättigter wässriger Natriumbicarbonat-Lösung und mit Sole gewaschen, über Magnesiumsulfat getrocknet, filtriert und unter reduziertem Druck konzentriert. Eine Säulenchromatographie über Kieselgel unter Verwendung von Ethylacetat und Hexan (1:1) führte zur Isolierung des gewünschten Produktes als einen weißen Feststoff (0,16 g; 64%).
1H-NMR; delta (CDCl3), 8,12 (2H, m), 7,55 (3H, m), 6,65 (1H, d, J = 6,4 Hz), 5,25 (1H, d, J = 6,5 Hz), 4,55 (1H, d, J = 5,9 Hz), 2,75 (1H, m), 1,64 (3H, s), 1,55 (3H, s), 1,04 (9H, s) und 0,88 (6H, m).
LRMS; +ve lon 444 (M-H). - Schritt G. 3R-[2,2-Dimethyl-1S-(5-phenyl-[1,2,4]oxadiazol-3-yl)-propylcarbamoyl]-2S-hydroxy-5-methyl-hexanohydroxamsäure.
- 2R-(2,2-Dimethyl-5S-oxo-[1,3]dioxolan-4-yl)-4-methyl-pentansäure [2,2-dimethyl-1S-(5-penyl-[1,2,4]oxadiazol-3-yl)-propyl]-amide (0,55 g; 0,11 mMol) wurde in Methanol (2 ml) gelöst und mit 50% wässrigem Hydroxylamin (0,04 ml; 0,5 mMol) behandelt. Die Reaktion wurde für 2 Stunden bei Raumtemperatur gerührt und dann unter reduziertem Druck verdampft. Das Reaktionsprodukt wurde durch präparative Umkehrphasenchromatographie aufgetrennt, um das gewünschte Produkt als einen weißen Feststoff zu erzielen (0,02 g; 44%).
1H-NMR; delta (CH3OD), 8,13 (2H, m), 7,65 (1H, m), 7,58 (2H, m), 5,14 (1H, s), 4,01 (1H, d, J = 7,1 Hz), 2,94 (1H, m), 1,60 (1H, m), 1,45 (1H, m), 1,16 (1H, m), 1,07 (9H, s), 0,89 (3H, d, J = 6,5 Hz) und 0,86 (3H, d, J = 6,6 Hz).
13C-NMR, delta (CH3OD), 177,1; 176,3; 172,0; 171,6; 134,6; 130,8; 129,4; 125,7; 73,7; 55,8; 49,6; 39,7; 36,2; 27,4; 27,2; 24,2 und 22,5.
LRMS; +ve lon 419 (M+H); -ve lon 417 (M+H). - Schritt H. 2R-(2,2-Dimethyl-5-oxo-[1,3]dioxolan-4S-yl)-4-methylpentansäurepentafluorphenylester.
- 2R-(2,2-Dimethyl-5-oxo-[1,3]dioxolan-4S-yl)-4-methylpentansäure (hergestellt gemäß WO 94/02447) (30 g; 130 mMol) wurde in Ethylacetat (300 ml) gelöst und mit Pentafluorphenol (28,8 g; 156 mMol) und mit WSCDI (30 g; 156 mMol) behandelt. Die Reaktion wurde für 2 Stunden unter Rückfluss erhitzt und dann bei Raumtemperatur für 12 Stunden gerührt. Die Reaktionsmischung wurde mit 1M Na2CO3 und mit Sole gewaschen, über Magnesiumsulfat getrocknet, filtriert und unter reduziertem Druck konzentriert. Das Produkt wurde aus Ethylacetat/Hexan umkristallisiert, um das gewünschte Produkt als einen einzelnen Diastereomer (21,2 g; 42%) zu erzielen.
1H-NMR; delta (CDCl3), 4,55 (1H, d, J = 6,7 Hz), 3,31 (1H, m), 1,85 (3H, bm), 1,65 (3H, s), 1,58 (3H, s), 1,05 (3H, d, J = 6,5 Hz) und 0,99 (3H, d, J = 6,5 Hz). -
- M+H = 420,0; M+Na = 441,5; M-H = 417,5.
- Die korrespondierende Carboxylsäure wurde gemäß dem Schema 1 und dem unten angegebenen Verfahren hergestellt.
- Schritt I. 3R-[1S-(5-Furan-2-yl-[1,2,4]oxadiazol-3-yl)-2,2-dimethylpropylcarbamoyl]-2S-hydroxy-5-methylhexansäure.
- 2R-(2,2-Dimethyl-5S-oxo-[1,3]dioxolan-4-yl)-4-methylpentansäure[2,2-dimethyl-1S-(5-Furan-2-yl-[1,2,4]oxadiazol-3-yl)-propyl]-amid (0,05 g; 0,12 mMol) wurde in Tetrahydrofuran (5 ml) gelöst und während der Zugabe von 1M Salzsäure (5 ml) auf 4° C abgekühlt. Die Lösung erwärmte sich auf Raumtemperatur und wurde dann für 18 Stunden gerührt. Die Masse des Lösungsmittels wurde unter reduziertem Druck entfernt und unter Hochvakuum zu einem weißen Schaum getrocknet (0,045 g; ca. quant).
1H-NMR; delta (CH3OD), 7,88 (1H, s), 7,45 (1H, d, J = 3,6 Hz), 6,74 (1H, m), 5,15 (1H, s), 4,18 (2H, d, J = 6,4 Hz), 2,91 (1H, m), 1,65 (1H, m), 1,50 (1H, m), 1,31 (1H, m), 1,06 (9H, s), 0,88 (3H, d, J = 6,4 Hz) und 0,82 (3H, d, J = 6,5 Hz).
LRMS; -ve lon 392,2 (M-H). - Beispiel 2
- Reagenzien und Bedingungen: A. HOBT, WSCDI, DMF. B. Toluol, 100° C. C. AqNH2OH, Ethanol, 70° C. D. TFA, DCM. E. HOBT, WSCDI, DMF. F. AqNH2OH, Methanol.
- Das Beispiel 2 wurde gemäß dem Schema 2 unter Verwendung der unten beschriebenen Verfahren hergestellt.
- Schritt A. 2S-tert-Butoxycarbonylamino-3,3-dimethyl-buttersäurebenzo-triazol-1-yl-ester.
- Eine Lösung von N-tert-Butoxycarbonyl-L-tert-butylglycin (5 g; 21,6 mMol) in Ethylacetat (80 ml) wurde in einem Eiswasserbad gekühlt. HOBT (3,22 g; 23,8 mMol) und WSDCI (4,56 g; 23,8 mMol) wurden hinzugefügt und die Reaktion rührte bei Raumtemperatur für 12 Stunden. Die Reaktionsmischung wurde mit 1M Na2CO3 und mit Sole gewaschen, über Magnesiumsulfat getrocknet, filtriert und zu einem weißen Schaum konzentriert (5,74 g; 76%).
1H-NMR; delta (CDCl3), 8,05 (1H, m), 7,65 (2H, m), 7,41 (1H, m), 5,10 (1H, d, J = 6,7 Hz), 4,45 (1H, d, J = 6,5 Hz), 1,55 (9H, s) und 1,21 (9H, s).
LRMS; +ve lon 349 (M+H). - Schritt B. [2,2-Dimethyl-1S-(3-phenyl-[1,2,4]oxadiazol-5-yl)-propyl]-carbamidsäure-tert-butylester
- 2S-tert-Butoxycarbonylamino-3,3-dimethyl-buttersäurebenzotriazol-1-yl-ester (3,7 g; 10,7 mMol) wurde in Toluol (80 ml) gelöst und mit N-Hydroxybenzamidin (2,9 g; 21,3 mMol) behandelt. Die Reaktionsmischung rührte bei 110° C für 18 Stunden. Die Lösung wurde unter reduziertem Druck konzentriert und zwischen Ethylacetat und 1M Na2CO3 aufgeteilt. Die organische Schicht wurde weiter mit 1M Na2CO3 und mit Sole gewaschen, über Magnesiumsulfat getrocknet, filtriert und unter reduziertem Druck konzentriert. Eine Säulenchromatographie auf Kieselgel unter Verwendung von Acetylacetat und Hexan (1:4) führte zu der Isolierung des gewünschten Produktes (2,58 g; 73%).
1H-NMR; delta (CDCl3), 8,10 (2H, m), 7,50 (3H, m), 5,30 (1H, bd), 4,95 (1H, d, J = 6,5 Hz), 1,44 (9H, s) und 1,03 (9H, s).
LRMS; +ve lon 354,2 (M+Na). - Schritt C: N-Hydroxybenzamidin
- Benzonitril (5 g, 48 mMol) wurde in Ethanol (100 ml) gelöst und mit 50 wässrigem Hydroxylamin (16 ml; 242 mMol) behandelt. Die Reaktion wurde unter Rückfluss für 3 Stunden erhitzt und unter reduziertem Druck konzentriert, um einen klaren Schaum zu erzielen (4,5 g; 68%).
LRMS; +ve lon 137 (M+H). - Schritt D: 2,2-Dimethyl-1S-(3-phenyl-[1,2,4]oxadiazol-S-yl)-propylamin.
- [2,2-Dimethyl-1S-(3phenyl-[1,2,4]oxadiazol-5-yl)-propyl]carbamidsäure-tert-butylester (1g; 3,0 mMol) wurde in DCM (5 ml) gelöst und mit TFA (5 ml) behandelt. Die Reaktion rührte bei Raumtemperatur für 3 Stunden. Die Reaktion wurde unter reduziertem Druck konzentriert und zwischen Ethylacetat und 1M Na2CO3 aufgeteilt. Die organische Schicht wurde weiter mit 1M Na2CO3 und mit Sole gewaschen, über Magnesiumsulfat getrocknet, filtriert und unter reduziertem Druck konzentriert, um das gewünschte Produkt zu erzielen (0,65 g; 93%).
1H-NMR; delta (CH3OD), 8,10 (2H, m), 7,55 (3H, m), 481 (1H, s) und 1,19 (9H, s).
LRMS; +ve lon 232 (M+H). - Schritt E: 2R-(2,2-Dimethyl-5-oxo-[1,3]dioxolan-4S-yl]-4-methylpentansäure-[2,2-dimethyl-1S-(3-phenyl-[1,2,4]oxadiazol-5-yl)-propyl]amid.
- 2R-(2,2-Dimethyl-5-oxo-[1,3]dioxolan-4S-yl)-4-methyl-pentansäure (0,27 g; 1,17 mMol) wurde in DMF (5 ml) gelöst und in einem Eiswasserbad abgekühlt vor der Zugabe von HOBT (0,17 g; 1,29 mMol) und WSCDI (0,25 g; 1,29 mMol). Die Reaktion wurde bei 0° C für 1 Stunde gerührt, bevor 2,2-Dimethyl-1S-(3-phenyl-[1,2,4]oxadiazol-S-yl)-propylamin (0,3 g; 1,29 mMol) hinzugegeben wurde. Die Reaktion wurde auf Raumtemperatur erwärmt und für 18 Stunden gerührt. DMF wurde unter reduziertem Druck entfernt und der Rest zwischen Ethylacetat und 1M HCl aufgeteilt. Die organische Schicht wurde abgetrennt und mit 1M HCl, gesättigter wässriger Natriumbicarbonatlösung und mit Sole gewaschen, über Magnesiumsulfat getrocknet, filtriert und unter reduziertem Druck konzentriert. Eine Säulenchromatographie auf Kieselgel unter Verwendung von Ethylacetat und Hexan (1:4) führte zur Isolierung des gewünschten Produktes (0,26 g; 46%).
1H-NMR; delta (CDCl3), 8,10 (2H, m), 7,50 (3H, m), 6,80 (1H, d, J = 9,3 Hz), 5,24 (1H, d, J = 9,3 Hz), 4,55 (1H, d, J = 5,1 Hz), 2,81 (1H, m), 1,63 (3H, s), 1,55 (3H, s), 0,92 (3H, d, J = 6,1 Hz) und 0,89 (3H, d, J = 6,2 Hz).
LRMS; +ve lon 444 (M+H). - Schritt F: 3R-[2,2-Dimethyl-1S-(3-phenyl-[1,2,4]oxadiazol-5-yl)-propylcarbamoyl]-2S-hydroxy-5-methyl-hexanohydroxamsäure.
- 2R-(2,2-Dimethyl-5-oxo-[1,3]dioxolan-4S-yl)-4-methyl-pentansäure-[2,2-dimethyl-1S-(3-phenyl-[1,2,4]oxadiazol-5-yl)-propyl]-amid (0,26 g; 0,6 mMol) wurde in Methanol (5 ml) gelöst und mit 50% wässrigem Hydroxylamin (0,2 ml; 2,95 mMol) behandelt. Die Reaktion rührte bei Raumtemperatur für 3 Stunden und wurde dann unter reduziertem Druck konzentriert. Das Produkt wurde aus Ethylacetat/Hexan umkristallisiert, um das gewünschte Produkt zu erzielen (0,11 g; 41%).
1H-NMR; delta (CH3OD), 8,06 (2H, m), 7,53 (3H, m), 5,21 (1H, s), 4,01 (1H, d, J = 7,5 Hz), 2,99 (1H, m), 1,60 (1H, m), 1,50 (1H, m), 1,15 (1H, m), 1,10 (9H, s), 0,92 (3H, d, J = 6,6 Hz) und 0,81 (3H, d, J = 6,5 Hz).
13C-NMR; delta (CH3OD), 180,3; 176,7; 172,0; 169,7; 132,9; 130,5; 128,8; 128,4; 73,7; 57,1; 49,5; 39,5; 36,5; 27,3; 24,3 und 22,5.
LRMS; +ve lon 419 (M+H); -ve lon 417 (M-1). - Beispiel 3
- Reagenzien und Bedingungen: A. LiHMDS, AlIBr, THF, –78 bis RT; B. 4-OEt-PhenylBr, P(o-Tol)3, Pd(OAc)2, Net3, CH3CN; C. 10% Pd/C, H2, MeOH; D. LiOH, MeOH, H2O; E. CuCl2, Dimethoxyaceton, Aceton; F. Pentafluorphenol, WSC, HOAt, CH2Cl2; G. Amin (wie detailliert in Schritt E, Schema 1), DMF; H. aq.NH2OH, iPrOH Beispiel 3 wurde gemäß dem Schema 3 unter Verwendung der unten beschriebenen Verfahren hergestellt.
- Schritt A: 2R-Allyl-3S-hydroxylbernsteinsäure-diisopropylester.
- Zu einer kalten (-78° C) Lösung von 2S-Hydroxylbernsteinsäurediisopropylester (19,70 ml; 95 mMol) in THF (35 ml) wurde LiNMDS (200 ml; 0,2 Mol; 2,1 eq.) tropfenweise zugegeben. Die Reaktion rührte bei –78° C für 2 Stunden und dann bei –30° C für 30 Minuten. Die Reaktionsmischung wurde auf –78° C abgekühlt und Allylbromid (12,36 ml, 0,14 Mol; 1,5 eq.) wurde tropfenweise zugesetzt. Die Reaktionstemperatur erwärmte sich über Nacht auf Raumtemperatur. Sie wurde dann in eine gesättigte Lösung von NH4Cl/Eis (200 ml) gegossen. Es wurde mit AcOEt (3 × 200 ml) extrahiert und anschließend erfolgte ein Waschgang mit Wasser (50 ml) und mit Sole (50 ml), wodurch nach Entfernung der Lösungsmittel unter Vakuum ein gelbes Öl erzielt wurde. Eine Reinigung mit Flash-Chromatographie ergab 2R-Allyl-3S-hydroxybernsteinsäurediisopropylester als ein farbloses Öl (7,76 g, de = 80%; 40% Ausbeute).
1H-NMR; delta (CDCl3), 5,77-5,88 (1H, m), 4,98-5,21 (4H, m), 4,22 (1H, brs), 3,18 (1H, bs), 2,87-2,94 (1H, m), 2,56-2,65 (1H, m), 2,40-2,48 (1H, m), 1,29 (6H, d, J = 6,3 Hz) und 1,22 (6H, d, J = 6,3 Hz).
LRMS: +ve lon 281 (M+Na). - Schritt B: 2R-[3-(4-Ethoxy-phenyl)-allyl)-3S-hydroxybernsteinsäurediisopropylester.
- Zu einer Lösung von 2R-Allyl-3S-hydroxybernsteinsäurediisopropylester (4,79 g; 18,5 mMol), 4-Bromphenetol (3,19 ml; 22,1 mMol; 1,2 eq.) und NEt3 (6,22 ml; 44,6 mMol; 2,4 eq.) in CH3CN (40 ml) wurde eine beschallte (für 2 Minuten) Suspension von P(O-Tol)3 (0,57 g; 2,22 mMol; 0,1 eq.) und Pd(OAc)3 (209 mg; 5%) in CH3CN (5 ml) zugesetzt. Die Reaktionsmischung wurde für 2 Stunden unter Rückfluss erhitzt. CH3CN wurde unter Vakuum entfernt. Der Rohstoff wurde mit AcOEt (3 × 200 ml) extrahiert, mit Wasser (50 ml) und mit Sole (50 ml) gewaschen. Eine Reinigung mit Flash-Chromatographie ergab den gewünschten 2R-[3-(4-Ethoxy-phenyl)-allyl)-3S-hydroxybernsteinsäurediisopropylester (5,92 g; 84% Ausbeute).
1H-NMR; delta (CDCl3), 7,28 (2H, d, J = 8,8 Hz), 6,83 (2H, d, J = 8,8 Hz), 6,46 (1H, d, J = 15,7 Hz), 6,02-6,12 (1H, m), 4,98-5,13 (2H, m), 4,26 (1H, dd, J = 7,1, 3,0 Hz), 4,02 (2H, q, J = 7,0 Hz), 3,23 (1H, d, J = 7,1 Hz), 2,92-2,97 (1H, m), 2,68-2,79 (1H, m), 2,49-2,62 (1H, m), 1,41 (3H, t, J = 7,0 Hz) und 1,19-1,30 (12H, m).
LRMS: +ve lon 400 (M+Na). - Schritt C: 2R-[3-(4-Ethoxy-phenyl)-propyl]-3S-hydroxysuccinsäurediisopropylester.
- Zu einer Lösung von 2R-[3-(4-Ethoxy-phenyl)-allyl)-3S-hydroxysuccinsäurediisopropylester (129 mg; 0,34 mMol) in MeOH (10 ml) wurde unter einer inerten Atmosphäre 10%Pd/C (13 mg) zugesetzt. H2 wurde durch die erzielte Suspension für 30 Minuten geblasen. Die Reaktionsmischung wurde dann unter 1 Atmosphäre von H2 für 16 Stunden gerührt. Pd/C wurde abfiltriert und das Lösungsmittel wurde unter reduziertem Druck entfernt, wodurch 2R-[3-(4-Ethoxy-phenyl)-propyl]-3S- hydroxybernsteinsäurediisopropylester (115 mg; 88% Ausbeute) erzielt wurde.
1H-NMR; delta (CDCl3), 7,08 (2H, d, J = 8,6 Hz), 6,81 (2H, d, J = 8,6 Hz), 4,97-5,14 (2H, m), 4,20 (1H, dd, J = 7,3, 3,5 Hz), 4,01 (2H, q, J = 7,0 Hz), 3,18 (1H, d, J = 7,3 Hz), 2,77-2,83 (1 H, m), 2,55-2,62 (2H, m), 1,45-1,94 (4H, m), 1,40 (3H, t, J = 7,0 Hz) und 1,12-1,30 (12H, m).
LRMS: +ve lon 402,0 (M+Na). - Schritt D: 2R-[3-(4-Ethoxy-phenyl)-propyl]-3S-hydroxysuccinsäure.
- Zu einer Lösung von 2R-(3-(4-Ethoxy-phenyl)-propyl)-3S-hydroxysuccinsäurediisopropylester (4,78 g; 12,6 mMol) in THF/Wasser (3 1, 120 ml) wurde NaOH (1,66 g; 41,5 mMol; 5,5 eq.) hinzugefügt. Die Reaktionsmischung wurde dann für 16 Stunden bei Raumtemperatur gerührt. Die Mischung wurde unter reduziertem Druck konzentriert und durch Zugabe von 1N HCl auf einen pH = 3 angesäuert. Das Hydroxydiacid wurde mit AcOEt extrahiert. Die organische Schicht wurde über MgSO4 getrocknet und das Lösungsmittel wurde unter reduziertem Druck entfernt, wodurch die gewünschte 2R-[3-(4-Ethoxy-phenyl)-propyl]-3S-hydroxybernsteinsäure (3,66 g; 85% Ausbeute) erzielt wurde.
1H-NMR; delta (CH3OD), 7,07 (2H, d, J = 8,6 Hz), 6,79 (2H, d, J = 8,6 Hz), 4,23 (1H, d, J = 5,8 Hz), 3,98 (2H, q, J = 7,0 Hz), 2,76-2,81 (1H, m), 2,53-2,59 (2H, m), 1,55-1,72 (4H, m), 1,35 (3H, t, J = 7,0 Hz).
LRMS: +ve lon 319 (M-Na); -ve lon 295 (M-H). - Schritt E: 2R-(2,2-Dimethyl-5-oxo-[1,3]dioxolan-4S-yl)-5-(4-ethoxyphenyl)-pentansäure.
- Zu einer Lösung von 2R-[3-(4-Ethoxy-phenyl)-propyl]-3S-hydroxysuccinsäure (3,66 g; 12,3 mMol) in Aceton (50 ml) wurde unter einer inerten Atmosphäre Dimethoxypropan (2,58 ml; 21 mMol; 1,7 eq.) und Kupferchlorid (165 mg; 1,2 mMol; 0,1 eq.) hinzugefügt. Die Reaktionsmischung rührte bei Raumtemperatur für 16 Stunden. Das Lösungsmittel wurde unter Vakuum entfernt, wodurch 2R-(2,2-Dimethyl-5-oxo-[1,3]dioxolan-4S-yl)-5-(4-ethoxy-phenyl)-pentansäure (4,03 g; 97 Ausbeute) erzielt wurde.
1H-NMR; delta (CDCl3), 7,08 (2H, d, J = 8,5 Hz), 6,82 (2H, d, J = 8,5 Hz), 4,48 (1H, d, J = 4,8 Hz), 4,01 (2H, q, J = 7,0 Hz), 2,91-2,98 (1H, m), 2,54-2,64 (3H, m), 1,23-2,20 (4H, m), 1,58 (3H, s), 1,53 (3H, s) und 1,40 (3H, t, J = 7,0 Hz).
LRMS: +ve lon 359 (M+Na); -ve lon 335 (M-H). - Schritt F: 2R-(2,2-Dimethyl-5-oxo-[1,3]dioxolan-4S-yl)-5-(4-ethoxyphenyl)-pentansäurepentafluorphenylester.
- Zu einer kalten Lösung von 2R-(2,2-Dimethyl-5-oxo-[1,3]dioxolan-4S-yl)-5-(4-ethoxy-phenyl)-pentansäure (4,03 g; 12 mMol) und Pentafluorphenol (2,43 g; 13,2 mMol; 1,1 eq.) in CH2Cl2 (50 ml) wurde WSC (2,54 g; 13,2 mMol; 1,1 eq.) hinzugefügt. Die Reaktionsmischung erwärmte sich über Nacht auf Raumtemperatur. CH2Cl2 wurde unter Vakuum entfernt und die erzielte Rohreaktionsmischung wurde in AcOEt (200 ml) gelöst. Die organische Schicht wurde mit Wasser (50 ml), NaHCO3 sat (20 ml) und abschließend mit Sole (20 ml) gewaschen. Das Lösungsmittel wurde unter reduziertem Druck entfernt, wodurch sich ein Öl ergab, welches mit Flash-Chromatographie gereinigt wurde, was zu dem erwarteten 2R-(2,2-Dimethyl-5-oxo-[1,3]dioxolan-4S-yl)-5-(4-ethoxyphenyl)-pentansäurepentafluorphenylester (3,94 g; 65% Ausbeute) führte.
1H-NMR; delta (CDCl3), 7,09 (2H, d, J = 8,4 Hz), 6,83 (2H, d, J = 8,4 Hz), 4,56 (1H, d, J = 6,0 Hz), 4,01 (2H, q, J = 7,0 Hz), 3,20-3,28 (1H, m), 2,64 (2H, t, J = 7,6 Hz), 1,98-2,08 (2H, m), 1,70-1,86 (2H, m), 1,62 (3H, s), 1,57 (3H, s) und 1,40 (3H, t, J = 7,0 Hz). - Schritt G: 2R-[3-(4-Ethoxy-phenyl)-propyl]-N1-(5-thiophen-2-yl)-[1,2,4]oxadiazol-3-yl)-2,2-dimethyl-propyl]-[1,3]dioxolan-4S-on
- Zu einer Lösung von 2R-(2,2-Dimethyl-5-oxo-[1,3]dioxolan-4S-yl)-5-(4-ethoxy-phenyl)-pentansäurepentafluorphenylester (150 mg; 0,30 mMol) in CH2Cl2 (10 ml) wurde 2,2-Dimethyl-1S-(5-thiophen-2-yl)-[1,2,4]oxadiazol-3-yl)-propylamin (100 mg; 0,42 mMol; 1,4 eq.) zugesetzt. Die Reaktionsmischung wurde für 16 Stunden gerührt und das Lösungsmittel wurde unter Vakuum entfernt. Der Rohstoff wurde in AcOEt (70 ml) aufgenommen, mit Wasser (10 ml) gewaschen und dann mit No2CO3 (10 ml) und abschließend mit Sole (10 ml). Das Lösungsmittel wurde über MgSO4 getrocknet und unter reduziertem Druck entfernt, wodurch sich die gewünschte Verbindung 2R-(3-(4-Ethoxy-phenyl)-propyl]-N1-(1S-(5-thiophen-2-yl)-[1,2,4]oxadiazol-3-yl)-2,2-dimethyl-propyl]-[1,3]dioxolan-4S-on (82 mg; 33% Rohstoff) ergab.
1H-NMR; delta (CDI3), 7,88 (1H, m), 7,62 (1H, m), 7,20 (1H, m), 6,95 (2H, d, J = 8,4 Hz), 6,71 (2H, d, J = 8,4 Hz), 6,55 (1H, d, J = 9,7 Hz), 5,19 (1H, d, J = 9,7 Hz), 4,56 (1H, d, J = 6,4 Hz), 3,95 (2H, q, J = 7,0 Hz), 2,64 (3H, bm), 1,84 (2H, m), 1,70 (2H, m), 1,62 (3H, s), 1,54 (3H, s), 1,38 (3H, t, J = 6,9 Hz) und 1,02 (9H, s).
LRMS: +ve lon 556,0 (M+H). - Schritt H: 2R-[3-(4-Ethoxy-phenyl)-propyl]-N1-[1S-(5-thiophen-2-yl)-[1,2,4]oxadiazol-3-yl)-2,2-dimethyl-propyl]-3S,N4-dihydroxy-succinamid.
- Zu einer Lösung von 2R-[3-(4-Ethoxy-phenyl)-propyl]-N1-[1S-(5-thiophen-2-yl)-[1,2,4]oxadiazol-3-yl)-2,2-dimethyl-propyl]-[1,3]dioxolan-4S-on (82 mg; 0,15 mMol) in i-PrOH (5 ml) wurde eine wässrige Lösung von Hydroxylamin (50%; 48 μl; 0,7 mMol; 5 eq.) zugesetzt. Die Reaktionsmischung rührte bei Raumtemperatur für 16 Stunden. Das Lösungsmittel wurde unter reduziertem Druck entfernt, wodurch sich ein Öl ergab, das mit präparativer Umkehrphasenchromatographie gereinigt wurde, um das gewünschte Produkt zu erzielen (25,3 mg; 32%).
1H-NMR; delta (CH3OD), 1H-NMR; delta (CH3OD), 7,86 (2H, m), 7,25 (1H, dd, J = 3,8 Hz), 6,83 (2H, d, J = 8,6 Hz), 6,54 (2H, d, J = 8,6 Hz), 5,14 (1H, s), 4,03 (1H, d, J = 7,6 Hz), 3,87 (2H, q, J = 6,96), 2,88 (1H, m), 2,45 (2H, bm), 1,53 (4H, bm), 1,33 (3H, t, J = 7,0 Hz) und 1,06 (9H, s).
LRMS: +ve lon 553,2 (M+Na); -ve lon 529,2 (M-H). - Die Verbindungen der Beispiele 4-17 wurden gemäß dem Verfahren von Beispiel 1 durch Parallelsynthese unter Verwendung des geeigneten Säurechlorids in Schritt D synthetisiert. Die Produkte wurden mit präparativer HPLC gereinigt.
- Beispiel 4
-
- LRMS; +ve lon 407 (M+Na); -ve lon 383 (M-H)
- Beispiel 5
-
- LRMS; +ve lon 431 (M+Na), -ve lon 407 (M-H).
- Beispiel 6
-
- LRMS; +ve lon 425 (M+H), -ve lon 423 (M-H).
- Beispiel 7
-
- LRMS; +ve lon 461 (M+Na), -ve lon 437 (M-H).
- Beispiel 8
-
- LRMS; +ve lon 393 (M+Na), -ve lon 369 (M-H).
- Beispiel 9
-
- LRMS; +ve lon 411 (M+H), -ve lon 409 (M-H).
- Beispiel 10
-
- LRMS; +ve lon 433 (M+H), -ve lon 431 (M-H).
- Beispiel 11
-
- LRMS; +ve lon 421 (M+Na), -ve lon 397 (M-H).
- Beispiel 12
-
- LRMS; +ve lon 421 (M+Na), -ve lon 397 (M-H).
- Beispiel 13
-
- LRMS; +ve lon 425 (M+H), -ve lon 423 (M-H).
- Das Diastereomer 2R-Hydroxy-3R-[1S-(5-thiophen-2-yl-[1,2,4]oxadiazol-3-yl)-2,2-dimethyl-propylcarbamoylJ-S-methyl-hexanohydroxamsäure wurde auch hergestellt.
-
- M+H = 425,1; M+Na = 447,1; M-H = 423,0.
- Beispiel 14
-
- LRMS; +ve lon 435 (M+Na), -ve lon 411 (M-H).
- Beispiel 15
-
- LRMS; +ve lon 433 (M+H), -ve lon 431 (M-H).
- Beispiel 16
-
- LRMS; +ve lon 405 (M+Na), -ve lon 381 (M-H).
- Beispiel 17
-
- 1H-NMR; delta (CH3OD), 8,26 (1H, d, J = 9,4 Hz), 5,02 (1H, d, J = 9,5 Hz), 4,02 (1H, d, J = 6,4 Hz), 2,89 (1H, m), 2,57 (3H, s), 1,61 (1H, m), 1,44 (1H, m), 1,22 (1H, m), 1,00 (9H, s).
- 13C-NMR; delta (CH3OD), 178,6; 176,1; 171,9; 170,7; 73,5; 55,6; 49,5; 39,9; 36,2; 27,6; 26,6; 24,2; 22,7 und 12,4.
- LRMS; +ve lon 379 (M+Na), -ve lon 355 (M-H).
- Die Verbindungen der Beispiele 18-19 wurden mit dem Verfahren nach Beispiel 2 unter Verwendung des geeigneten Nitrils in Schritt C und/oder des geeigneten Aminosäurerestes in Schritt A hergestellt.
- Beispiel 18
-
- 1H-NMR; delta (CH3OD), 5,12 (1H, s), 3,98 (1H, d, J = 7,5 Hz), 3,06 (1H, m), 2,92 (1H, m), 1,61 (1H, m), 1,43 (1H, m), 1,31 (6H, d, J = 6,9 Hz), 1,14 (1H, m), 1,03 (9H, s), 0,89 (3H, d, J = 6,7 Hz), 0,81 (3H, d, J = 6,8 Hz).
- 13C-NMR; delta (CH3OD), 179,7; 176,6; 176,5; 172,0; 73,7; 56,9; 49,2; 39,5; 36,5; 28,3; 27,3; 24,5; 22,3; 21,2 und 21,1.
- LRMS; +ve lon 385 (M+H), -ve lon 383 (M-H).
- Beispiel 19
-
- 1H-NMR; delta (CH3OD), 8,05 (2H, m), 7,52 (3H, m), 5,14 (1H, d, J = 7,2 Hz), 4,00 (1H, d, J = 7,7 Hz), 2,91 (1H, m), 2,36 (1H, m), 1,63 (1H, m), 1,54 (1H, m), 1,16 (1H, m), 1,09 (3H, d, J = 6,8 Hz), 1,00 (3H, d, J = 6,8 Hz), 0,95 (3H, d, J = 6,3 Hz), 0,84 (3H, d, J = 6,3 Hz).
- 13C-NMR; delta (CH3OD), 181,0; 176,8; 172,0; 169,9; 132,9; 130,5; 128,7; 128,4; 73,7; 54,3; 49,6; 39,5; 33,3; 27,2; 24,4; 22,5; 19,8 und 19,4.
- LRMS; +ve lon 427 (M+Na), -ve lon 403 (M-H).
- Die Verbindungen der Beispiele 20-23 wurden mit dem Verfahren nach Beispiel 2 unter Verwendung des geeigneten Nitrils in Schritt C und/oder des geeigneten Aminosäurerestes in Schritt A hergestellt. Die Synthese des geeigneten chiralen Succinats in Schritt E ist in der WO 94/21625 erläutert.
- Beispiel 20
-
- 1H-NMR; delta (CH3OD), 9,13 (1H, d, J = 8,26 Hz), 8,05 (2H, m), 7,55 (3H, m), 7,25 (5H, m), 5,66 (1H, m), 5,45 (1H, m), 4,90 (2H, m), 4,50 (1H, s), 3,51 (1H, dd, J = 13,92, 4,84 Hz), 3,17 (1H, dd, J = 13,92, 10,90 Hz), 2,50 (1H, m), 2,0 (2H, m), 1,50 (3H, m), 1,0 (3H, d, J = 6,5 Hz), 0,96 (3H, d, J = 6,6 Hz).
- 13C-NMR; delta (CH3OD), 181,0; 177,0; 172,7; 138,0; 136,5; 133,0; 130,8; 130,6; 130,1; 128,7; 128,7; 117,7; 48,4; 48,3; 42,1; 39,5; 36,2; 27,1; 24,9 und 22,0.
- Beispiel 21
-
- 1H-NMR; delta (DMSO), 10,28 (1H, s), 8,64 (1H, d, J = 6,2 Hz), 8,64 (1H, br, s), 7,25 (5H, m), 5,45 (2H, m), 4,51 (1H, m), 4,30 (2H, m), 3,15 (1H, m), 2,85 (2H, m), 2,20 (1H, dt, J = 10,6, 3,12 Hz), 1,70 (2H, m), 1,25 (6H, d, J = 6,91 Hz), 0,70 (1H, m), 0,52 (3H, d, J = 6,4 Hz), 0,48 (3H, d, J = 6,4 Hz).
- 13C-NMR; delta (MEOD), 179,0; 175,6; 175,5; 171,3; 136,6; 135,0; 129,2; 128,6; 127,3; 116,4; 48,7; 46,9; 40,6; 38,1; 34,8; 26,9; 25,6; 23,5; 20,7 und 19,9.
- Beispiel 22
-
- 1H-NMR; delta (CH3OD), 8,98 (1H, d, J = 8,41 Hz), 7,27 (5H, m), 5,51 (2H, m), 4,85 (2H, m), 3,41 (1H, dd, J = 14,0, 5,0 Hz), 3,14 (1H, dd, J = 14,0, 10,97 Hz), 2,47 (1H, dt, J = 11,0, 3,25 Hz), 2,16 (3H, s), 2,00 (1H, dt, J = 11,40, 3,30 Hz), 1,80 (1H, m), 1,15 (1H, m}, 0,98 (3H, d, J = 6,6 Hz), 0,92 (3H, d, J = 6,6 Hz).
- 13C-NMR; delta (CH3OD), 172,62; 168,27; 133,59; 132,07; 126,34; 125,66; 124,28; 113,36; 45,19; 44,04; 43,95; 37,61; 35,15; 31,75; 22,72; 20,44; 17,59 und 7,36.
- Beispiel 23
-
- 1H-NMR; delta (CH3OD), 8,81 (1H, d, J = 8,59 Hz), 7,65 (1H, m), 5,70 (1H, m), 5,15 (1H, d, J = 8,62 Hz), 4,95 (2H, m), 2,60 (1H, dt, J = 11,10, 3,16 Hz), 2,39 (3H, s), 1,38 (1H, dt, J = 13,10, 3,33 Hz), 1,31 (1H, m), 0,98 (1H, m), 0,98 (9H, s), 0,86 (3H, d, J = 6,6 Hz), 0,84 (3H, d, J = 6,6 Hz).
- Die Verbindung des Beispiels 24 wurde mit dem Verfahren nach Beispiel 2 hergestellt. Die Synthese des geeigneten chiralen Succinats in Schritt E ist in der WO 95/19956 erläutert.
- Beispiel 24
-
- LRMS; +ve lon 403,5 (M+H), -ve lon 401,3 (M-H).
- Die Verbindung des Beispiels 25 wurde mit dem Verfahren nach Beispiel 2 unter Verwendung des geeigneten Nitrils in Schritt C und/oder des geeigneten Aminosäurerestes in Schritt A hergestellt. Die Synthese des geeigneten chiralen Succinats in Schritt E ist in der WO 97/02239 erläutert.
- Beispiel 25
-
- 1H-NMR; delta (CH3OD), 7,14 (5H, m), 5,34 (1H, m), 3,38 (1H, d, J = 9,68 Hz), 3,20 (2H, m), 3,02 (3H, s), 2,65 (1H, m), 2,22 (3H, s), 1,35 (2H, m), 0,90 (1H, m), 0,73 (3H, d, J = 6,55 Hz) und 0,70 (3H, d, J = 6,57 Hz).
- Die Verbindungen von Beispiel 26 und 27 wurden durch das Verfahren nach Beispiel 2 hergestellt. Die Synthese des geeigneten chiralen Succinats in Schritt E ist in der WO 92/13831 unter Verwendung von Verfahren, die analog zu denen sind, die in der WO 95/32944 beschrieben sind, erläutert.
- Beispiel 26
-
- 1H-NMR; delta (CH3OD), 8,05 (2H, m), 7,49 (3H, m), 5,22 (1H, s), 2,93 (1H, m), 2,65 (1H, dd, J = 9,8, 16,7 Hz), 2,38 (1H, dd, J = 4,6, 16,6 Hz), 1,52 (1H, m), 1,43 (1H, m), 1,26 (24H, m), 1,10 (9H, s) und 0,89 (3H, m).
- LRMS; +ve lon 528,4 (M+H).
- Beispiel 27
-
- LRMS; +ve lon 556,2 (M+H).
- Die Verbindung des Beispiels 28 wurde hergestellt durch das Verfahren nach Beispiel 1. Die Synthese des geeigneten chrialen Succinats in Schritt H ist in der WO 92/13831 erläutert, wobei Verfahren verwendet werden, die analog zu denen sind, die in der WO 95/32944 beschrieben sind.
- Beispiel 28
-
- 1H-NMR; delta (CH3OD), 8,07 (2H, m), 7,61 (3H, m), 6,93 (4H, m), 5,15 (1H, s), 2,94 (1 H, m), 2,5 (4H, m), 1,5 (4H, m) und 1,07 (9H, s).
- 13C-NMR; delta (CH3OD), 178,0; 177,1; 142,6; 134,6; 132,7; 131,0; 130,8; 129,5; 129,4; 125,7; 55,7; 43,8; 39,0; 36,3; 36,1; 34,1; 30,3 und 27,4. LRMS; +ve lon 506,2 (M+Na), -ve lon 482,4 (M-H).
-
- M+H = 485; M+Na = 507,2; M-H = 482,6.
- Die Verbindungen der Beispiele 29 und 30 wurden mit dem Verfahren nach Beispiel 1 hergestellt.
- Beispiel 29
-
- 1H-NMR; delta (CH3OD), 7,95 (1H, m), 7,87 (1H, d, J = 5,0 Hz), 7,28 (1H, m), 5,15 (1H, s), 4,18 (2H, d, J = 6,4 Hz), 2,94 (1H, m), 1,68 (1H, m), 1,48 (1H, m), 1,31 (1H, m), 1,06 (9H, s), 0,88 (3H, d, J = 6,4 Hz) und 0,82 (3H, d, J = 6,5 Hz).
- LRMS; -ve lon 408,2 (M-H).
- Beispiel 30
-
- 1H-NMR; delta (CH3OD), 7,88 (1H, s), 7,45 (1H, d, J = 3,6 Hz), 6,74 (1H, m), 5,15 (1H, s), 4,18 (2H, d, J = 6,4 Hz), 2,91 (1H, m), 1,65 (1H, m), 1,50 (1H, m), 1,31 (1H, m), 1,06 (9H, s), 0,88 (3H, d, J = 6,4 Hz) und 0,82 (3H, d, J = 6,5 Hz).
- LRMS; -ve lon 392,2 (M-H).
- Die Verbindungen der Beispiele 31 und 32 wurden durch das Verfahren nach Beispiel 2 hergestellt. Die Synthese des geeigneten chiralen Succinats in Schritt E ist in der WO 94/02446 erläutert, wobei das geeignete Cinnamylbromid oder das Cyclopentylmethyliodid anstelle des Methylallyliodids verwendet wurde, wie dies in dem zuvor erwähnten Patent erläutert ist.
- Beispiel 31
-
- 1H-NMR; delta (CH3OD), 7,95 (2H, d, J = 7,2 Hz), 7,53 (1H, m), 7,48 (2H, m), 7,09 (2H, d, J = 6,4 Hz), 6,91 (3H, m), 6,31 (1H, d, J = 15,8 Hz), 6,04 (1H, m), 5,26 (1H, s), 4,14 (1H, d, J = 7,6 Hz), 3,02 (1H, m), 2,46 (1H, m), 2,37 (1H, m) und 1,07 (9H, s).
- 13C-NMR; delta (CH3OD), 179,8; 175,9; 172,0; 169,6; 138,8; 134,0; 132,8; 130,4; 129,7; 128,9; 128,4; 128,4; 127,3; 73,2; 56,5; 51,3; 36,8 und 34,0.
- LRMS; +ve lon 501,2 (M+Na), -ve lon 477,4 (M-H).
- Beispiel 32
-
- 1H-NMR; delta (CH3OD), 5,13 (1H, s), 3,99 (1H, d, J = 7,7 Hz), 3,06 (1H, m), 2,87 (1H, m), 1,83 (1H, m), 1,72 (1H, m), 1,63-1,39 (6H, bm), 1,31 (6H, d, J = 6,9 Hz), 1,27 (1H, m), 1,03 (9H, s) und 1,02 (2H, m).
- 13C-NMR; delta (CH3OD), 179,6; 176,6; 176,5; 172,0; 73,6; 56,8; 50,8; 39,6; 36,7; 36,5; 34,7; 33,6; 28,3; 27,2; 26,5 und 21,2.
- LRMS; +ve lon 411,2 (M+H), -ve lon 409,6 (M-H).
- Die Verbindungen der Beispiele 33-35 wurden mit dem Verfahren nach Beispiel 3 unter Verwendung des geeigneten Arylbromids in Schritt B hergestellt.
- Beispiel 33
-
- 1H-NMR; delta (CH3OD), 8,38 (1H, d, J = 9,4 Hz), 7,86 (1H, s), 7,75 (3H, bs), 7,4 (1H, d, J = 3,5 Hz), 6,7 (1H, m), 5,12 (1H, d, J = 9,4 Hz), 4,26 (1H, d, J = 4,0 Hz), 2,8 (3H, bm), 1,8 (4H, bm) und 1,0 (9H, s).
- LRMS; +ve lon 623,2 (M+H), -ve lon 621,0 (M-H).
- Beispiel 34
-
- 1H-NMR; delta (CH3OD), 8,38 (1H, d, J = 9,4 Hz), 7,86 (1H, s), 7,75 (3H, bs), 7,4 (1H, d, J = 3,5 Hz), 6,7 (1H, m), 5,12 (1H, d, J = 9,4 Hz), 4,26 (1H, d, J = 4,0 Hz), 2,8 (3H, bm), 1,8 (4H, bm) und 1,0 (9H, s).
- LRMS; +ve lon 629,4 (M+Na), -ve lon 605,4 (M-H).
- Beispiel 35
-
- 1H-NMR; delta (CH3OD), 7,86 (2H, m), 7,25 (1H, dd, J = 3,8 Hz), 6,83 (2H, d, J = 8,6 Hz), 6,54 (2H, d, J = 8,6 Hz), 5,14 (1H, s), 4,03 (1H, d, J = 7,6 Hz), 3,87 (2H, q, J = 6,96, 14,0 Hz), 2,88 (1H, m), 2,45 (2H, bm), 1,53 (4H, bm), 1,33 (3H, t, J = 7,0 Hz) und 1,06 (9H, s).
- LRMS; +ve lon 515,2 (M+H), -ve lon 513,2 (M-H).
- Die Verbindung des Beispiels 36 wurde mit dem Verfahren nach Beispiel 2 hergestellt. Die Synthese des geeigneten chiralen Succinats in Schritt E ist in der WO 01/10834 erläutert.
- Beispiel 36
-
- 1H-NMR; delta (CH3OD), 8,26 (0,3H, s), 8,05 (2H, d, J = 6,9 Hz), 7,84 (0,7H, s), 7,52 (3H, m), 5,20 (1H, m), 3,75 (1H, m), 3,63 (0,3H, dd, J = 13,9, 5,5 Hz), 3,43 (0,7H, dd, J = 14,2, 4,6 Hz), 3,18 (0,7H, m), 3,00 (0,3H, m), 1,92 (1H, m), 1,47 (8H, m), 1,10 (3H, s), 1,08 (6H, s) und 0,98 (2H, m).
- 13C-NMR; delta (CH3OD), 179,9; 176,9; 176,6; 169,3; 163,8; 159,2; 132,5; 130,0; 129,6; 128,9; 128,3; 127,9; 56,8; 56,7; 53,9; 50,3; 44,8; 44,6; 39,1; 38,9; 37,9; 37,7; 35,9; 35,8; 34,1; 33,4; 33,3; 26,9; 26,1 und 25,9.
- LRMS; +ve lon 451 (M+Na), -ve lon 427 (M-H).
- Die Verbindung von Beispiel 37 wurde mit dem Verfahren nach Beispiel 1 hergestellt. Die Synthese des geeigneten chiralen Succinats in Schritt E ist in der WO 01/10834 erläutert.
- Beispiel 37
-
- 1H-NMR; delta (CH3DO), 8,49 (0,6H, d, J = 8,7 Hz), 8,37 (0,4H, d, J = 8,1 Hz), 8,28 (0,4H, s), 8,14 (2H, m), 7,85 (0,6H, s), 7,65 (1H, m), 7,59 (2H, m), 4,81 (1H, s), 3,79 (1H, m), 3,63 (0,4H, m) 3,43 (0,6H, m), 3,13 (0,6H, m), 2,97 (0,4H, m), 1,55 (9H, m), 1,08 (3H, s), 1,07 (6H, s) und 1,04 (2H, m).
- 13C-NMR; delta (CH3OD), 176,6; 171,6; 164,2; 159,7; 134,6; 132,8; 130,8; 130,3; 129,4; 125,7; 69,5; 56,0; 54,3; 50,8; 45,4; 45,3; 40,6; 39,5; 38,3; 38,2; 35,9; 34,5; 33,8; 33,7; 32,0; 27,5; 26,4 und 26,3.
- LRMS; +ve lon 429 (M+H).
- Biologische Ergebnisse
- A. Tests auf Enzymhemmung
- Verbindungen nach der Erfindung wurden getestet, um ihre Aktivitäten als Inhibitoren von MMP9 und MMP12 zu bestimmen.
- MMP9 Testprotokoll
- Verbindungen wurden auf ihre hemmende Aktivität gegenüber 92 kDa Gelatinase (MMP9) in einem Test unter Verwendung eines mit Cumarin markierten Peptidsubstrates (7-Methoxycumarin-4-yl)acetyl-Pro-Leu-Gly-Leu(3-[2,4-dinitrophenyl)-L-2,3-diaminopropionyl)-Ala-Arg-NH2 (McaPLGLDpaAR) (Knight et al, FEBS Lett. 1992; 263-266) getestet.
- Die Stammlösungen wurden wie folgt hergestellt:
Testpuffer: 100 mM Tris-HCl; pH 7,6; enthaltend 100 mM NaCl, 10 mM CaCl2 und 0,05% Brij 35.
Substrat: 0,4 mM McaPLGLDpaAR (von Bachem) (0,437 mg/ml) Stammlösung in 100% DMSO (gelagert bei –20° C). Verdünnt auf 8 μM in dem Testpuffer.
Enzym: Rekombinante, humane 92 kDa Gelatinase (MMP-9; APMA (4-aminophenylquecksilber(II)-acetat) -aktiviert, falls notwendig), passend verdünnt im Testpuffer. - Die Testverbindungen wurden anfangs als 10 mM Verbindungslösung in 100% DMSO hergestellt, in 100% DMSO auf 1 mM verdünnt, dann nacheinander 3-fach in 100% DMSO über die Säulen 1-10 einer Mikrotiterplatte mit 96 Vertiefungen verdünnt. Bereich der Testkonzentration: 100 μM (Säule 1) bis 5,1 nM (Säule 10).
- Der Test wurde mit einem Gesamtvolumen von 100 μl pro Vertiefung in den Mikrotiterplatten mit 96 Vertiefungen durchgeführt. Aktiviertes Enzym (20 μl) wurde den Vertiefungen zugefügt und anschließend 20 μl des Testpuffers. Geeignete Konzentrationen der Testverbindungen, die in 10 μl DMSO gelöst waren, wurden dann hinzugegeben und anschließend 50 μl von McaPLGLDpaAR (8 μM, hergestellt durch Verdünnung der DMSO-Stammlösung im Testpuffer). Für jeden Test wurden zehn Konzentrationen der Testverbindung in zweifacher Ausführung geprüft. In den Kontrollvertiefungen fehlte entweder das Enzym oder die Testverbindung. Die Reaktionen wurden bei 37° C für 2 Stunden inkubiert. Die Fluoreszenz bei 405 nm wurde sofort mit einem SLT Fluostar-Fluorometer (SLT Labinstruments GmbH, Grödig, Österreich) unter Verwendung von 320 nm Anregung ohne Stopp der Reaktion gemessen.
- Die Wirkung der Testverbindung wurde aus der Dosis-Effekt-Kurve bestimmt, welche durch die 10 Zweifachkonzentrationen des Inhibitors erzeugt wurde. Der IC50 (die Konzentration der Verbindung, die für eine 50 Abnahme der Enzymaktivität erforderlich ist) wurde erzielt durch Einfügen der Daten in die folgende Gleichung: Y = a + ((b – a)/(1 + (c/X)d)). Y = erzielte Hemmung für eine bestimmte Dosis; X = die Dosis in nM; a = Minimum y oder Null% Hemmung; b = Maximum y oder 100 Hemmung; c = ist der IC50; d = ist die Neigung. Das Ergebnis wurde auf eine signifikante Zahl gerundet.
- MMP 12 Testprotokoll
- Die Verbindungen wurden auf ihre hemmende Aktivität gegenüber Metalloelastase (MMP12) in einem Test unter Verwendung eines mit Cumarin markierten Peptidsubstrates (7-Methoxycumarin-4-yl)acetyl-Pro-Leu-Gly-Lev-(3-[2,4-dinitrophenyl]-L-2,3-diaminopropionyl)-Ala-Arg-NH2 (McaPLGLDpaAR) (Knight et al, FEBS Lett. 1992; 263-266). Das Protokoll für diesen Test war entsprechend dem Protokoll für den obigen MMP9 Test getestet.
- MMP1 Testprotokoll
- Die Verbindungen wurden auf ihre hemmende Aktivität gegenüber Kollagenase (MMP1) in einem Test unter Verwendung eines mit Cumarin markierten Peptidsubstrates getestet (7-Methoxycumarin-4-yl)acetyl-Pro-Leu-Gly-Leu-(3-[2,4-dinitrophenyl]-L-2,3-diaminopropionyl)-Ala-Arg-NH2 (McaPLGLDpaAR) (Knight et al, FEBS Lett. 1992; 263-266). Das Protokoll für diesen Test entsprach dem Protokoll für den obigen MMP9 Test.
-
- Diese Ergebnisse zeigen allgemein, dass die getesteten Verbindungen aktiv als Inhibitoren von MMP12 sind, wobei einige Beispiele eine selektive Hemmung von MMP-9 und 12 relativ zu MMP-1 zeigen.
- B. CCl4-induziertes Leberfibrosemodell
- Tetrachlorkohlenstoff (CCl4) induziert Leberfibrose, wenn eine intraperitoneale Verabreichung erfolgt (Bulbena O, Culat J. Bravo ML., inflammation 1997 Oct; 21 (5):475-88). Die Verbindungen nach der Erfindung können auf ihre Fähigkeit überprüft werden, die CCl4-induzierte Bildung von fibrotischem Gewebe zu verhindern.
- Tiere
- Männliche Sprague-Dawley-Ratten, 7 Wochen alt, Gewicht etwa 300 g von Charles River/Iffa-Credo, St-Germain/I'Arbresle, Frankreich.
- Vor Beginn der Experimente wurden die Ratten 5 Tage in einem klimatisierten Raum akklimatisiert; zwei Tiere pro Käfig; Temperatur: 22° C ± 2; relative Feuchtigkeit: 55% ± 10; Licht: 12 Stundenrhythmus (7 morgens – 19 abends); Käfig: Makrolon®-Käfig, 42,5 × 26,6 × 15, ausgerüstet mit einer Abdeck-Vorschubzahnstange aus rostfreiem Stahl.
- Bei der Studie wurden die folgenden Gruppen von jeweils 8 Tieren verwendet.
- Gruppe 1: „Schein"-Tiere erhielten CCl4 Vehikel (i.p.) und einmal täglich das Vehikel der Testsubstanz (s.c.).
- Gruppe 2: Positive Kontrollgruppe erhielt CCl4 (i.p.) und einmal täglich das Vehikel der Testsubstanz (s.c.).
- Gruppe 3: Experimentelle Gruppe erhielt CCl4 (i.p.) und einmal täglich 2 mg/Kilo s.c. der Verbindung von Beispiel 13.
- Gruppe 4: Experimentelle Gruppe erhielt CCl4 (i.p.) und einmal täglich 10 mg/Kilo s.c. der Verbindung von Beispiel 13.
- Gruppe 5: Experimentelle Gruppe erhielt CCl4 (i.p.) und einmal täglich 20 mg/Kilo s.c. der Verbindung nach Beispiel 13.
- Die Ratten wurden an ihren Schwänzen markiert. Die Markierungen wurden überprüft und erneuert, falls notwendig, nach jeder CCl4 Injektion.
- Verfahren
- CCl4 (Prolabo) in Olivenöl wurde jeden dritten Tag für 3 Wochen durch intraperitoneale Injektion verabreicht (0,25 ml CCl4/kg Körpergewicht, verdünnt in Öl 1:1 (Vol.:Vol.) auf ein Gesamtvolumen von 0,5 ml/Kilo). Die Tiere wurden täglich gewogen. Falls das Körpergewicht um mehr als 10% des Anfangsgewichtes abnahm, wurden die Tiere aus der Studie ausgeschlossen.
- Die Vehikel und die Verbindungen waren die folgenden:
CCl4 wurde in Ölivenöl (Prolabo) in einer 1:1 Verdünnung verabreicht. - Die Verbindung nach Beispiel 13 wurde in 0,25% Tween-80 und 0,25% Carboxymethylcellulose in sterilem 0,9% NaCl suspendiert.
- Die Lösung wurde bei 4° C über die Dauer des Experimentes gehalten und jeden Tag verwendet, um die Suspensionen herzustellen.
- Die Verbindung nach Beispiel 13 wurde täglich durch subkutane (s.c.) Injektion mit einem Verabreichungsvolumen von 5 ml/kg verabreicht. Die Gruppen 1 und 2 wurden s.c. dosiert mit 5 ml/Kilo Vehikel. Frisch zubereitete Lösungen wurden an jedem Tag des Experimentes verwendet. Die Verabreichungen wurden jeden Tag zur selben Zeit durchgeführt.
- Die Behandlung der Gruppen bei dieser Studie startete für jedes Tier zum Zeitpunkt der ersten CCl4 Verabreichung und wurde für 21 nachfolgende Tage fortgeführt. Die letzte Verabreichung der Testsubstanzen oder des Vehikels erfolgte einen Tag vor Tötung der Tiere.
- Ergebnisse
- Bei 16 Tieren wurde ein frühzeitiger Tod festgestellt. Datum und die vermutliche Ursache sind in der Tabelle 1 dargelegt.
- Serumenzym-Spiegel
- Die Tiere wurden 21 Tage nach der ersten CCl4 Verabreichung durch Isofuran-Inhalation getötet. Blut wurde individuell zum Todeszeitpunkt entnommen, das heißt, einen Tag nach der letzten Verabreichung der Testsubstanz oder des Vehikels. Das Blut wurde bei 4° C zentrifugiert. Das Plasma wurde vorsichtig gesammelt und in drei Fraktionen aufgeteilt. Die Plasmaspiegel der Aspartataminotransferase (ASAT) und der Alaninaminotransferase (ALAT) wurden gemessen, um eine Lebernekrose zu bestimmen. Erhöhte Spiegel von ASAT und ALAT im Serum sind mit einer Leberbeeinträchtigung assoziiert. Die durchschnittlichen Spiegel für ASAT und ALAT für die Kontrolltiere und solche, die mit der Verbindung nach Beispiel 13 mit den drei unterschiedlichen Dosierungen behandelt wurden, sind in der
1 gezeigt (Y-Achse zeigt die Einheiten der Enzymaktivität pro Liter Blut, IU/L). Die subkutane Behandlung mit der Verbindung nach Beispiel 13 führte zu einer deutlichen Abnahme der Spiegel von ASAT und ALAT im Vergleich zu den Tieren, die nur mit dem Vehikel behandelt wurden. Dies zeigt, dass die Verbindung nach Beispiel 13 eine schützende Wirkung auf die Leber hat. - Histologische Auswertung der Leberfibrose
- Die Leberfibrose wurde bestimmt durch Messung des Bereiches der Fibrose in der Leber unter Verwendung der Mikrochotomie. Die Ergebnisse sind dargestellt als der Prozentbereich, der fibrotisch war.
- Die Leber wurde entfernt und es wurden drei Lappen präpariert. Die Proben wurden entfernt und entweder in 10% Formaldehyd fixiert oder bei –80° C eingefroren.
- Die Leberabschnitte wurden in Paraffinblocks eingebettet. Es wurde eine Zerlegung in Abschnitte und einer Anfärbung mit Sirius-Rot durchgeführt. Die Quantifizierung der Fibrose in der Leber wurde mit einem Minimum von drei Abschnitten durchgeführt, die von verschiedenen Orten in der Leber entnommen wurden. Die quantitative Analyse wurde unter Verwendung eines Bildabtasters (Imstar) und der Software Morphostar durchgeführt.
- Die durchschnittlichen Prozentbereiche von Fibrose in den Lebern der Tiere von den verschiedenen Gruppen wurden berechnet und die Ergebnisse sind in der
2 gezeigt. - B. IL2-induzierte peritoneale Rekrutierung von Lymphozyten
- Die Verabreichung von IL2 intraperitoneal führt zu einer Migration der Lymphozyten in die intraperitoneale Höhle. Dies ist ein Modell für die zelluläre Migration, die während einer Entzündung auftritt.
- Verbindungen nach der Erfindung hemmen die IL2-induzierte Lymphozytenrekrutierung.
- Protokoll
- C3H/HEN Mäusen (Elevage Janvier, Frankreich) wurde intraperitoneal IL2 (Serono Pharmaceutical Research Institute, 20 μg/kg, in Kochsalzlösung) injiziert.
- Die Verbindungen nach der Erfindung wurden in 0,5 Carboxymethylcellulose (CMC)/0,25% Tween-20 suspendiert und über die sc oder po Route (10 ml/kg) 15 Minuten vor der Verabreichung von IL2 verabreicht.
- 24 Stunden vor der Verabreichung von IL2 wurden peritoneale weiße Blutzellen gesammelt durch 3 aufeinander folgende Spülungen der peritonealen Höhle mit 5 ml gepufferter Phosphatsalzlösung (PBS)-1 mM EDTA (+4° C). Die Suspension wurde zentrifugiert (1700 g × 10 Minuten bei +4° C). Der erzielte Niederschlag wurde in 1 ml PBS-1 mM EDTA suspendiert.
- Die Lymphozyten wurden identifiziert und mit einem Beckman/Coulter Counter gezählt.
- Experimenteller Aufbau
- Die Tiere wurden in fünf Gruppen eingeteilt (sechs Mäuse pro Gruppe).
- Gruppe 1: (Basislinie) erhielt 0,5% CMC/0,25% Tween-20 (Vehikel der Verbindung nach der Erfindung) und Salzlösung (Vehikel von IL2).
- Gruppe 2: (Kontrolle IL2) erhielt 0,5% CMC/0,25% Tween-20 und Injektion von IL2.
- Gruppe 3: Experimentelle Gruppe (Verbindung nach der Erfindung, Dosierung 1) erhielt eine Verbindung nach der Erfindung und eine Injektion von IL2.
- Gruppe 4: Experimentelle Gruppe (Verbindung nach der Erfindung, Dosierung 2) erhielt eine Verbindung nach der Erfindung und eine Injektion von IL2.
- Gruppe 5: Experimentelle Gruppe (Verbindung nach der Erfindung, Dosierung 3) erhielt eine Verbindung nach der Erfindung und eine Injektion von IL2.
- Gruppe 6: Die Referenzgruppe erhielt die Referenzverbindung Dexamethason und eine Injektion von IL2.
- Berechnung
-
- Ly 1 = Zahl der Lymphozyten in der Gruppe 1 (E3/μl); Ly 2 = Zahl der Lymphozyten in der Gruppe 2 (E3/μl); Ly X = Zahl der Lymphozyten in der Gruppe X (3-5) (E3/μl).
- Die Dosierung der Verbindung nach der Erfindung, welche für eine 50 % (ID50) Hemmung der Lymphozytenrekrutierung erforderlich ist, wurde unter Verwendung eines Kurvenanpassungsprogramms berechnet. Die Ergebnisse sind in der Tabelle 1 aufgelistet. Tabelle 1: ID50 für die Hemmung der IL2-induzierten peritonealen Rekrutierung von Lymphozyten durch Verbindungen nach der Erfindung
Claims (38)
- Eine Verbindung der Formel (IA) oder (IB) wobei W HO(C=O)-, HONH(C=O)- oder H(C=O)N(OH)- repräsentiert; X -O- oder -S- repräsentiert; R1 Wasserstoff; -OH oder -SH; Fluoro oder Chloro; -CF3; (C1-C6)Alkyl; (C1-C6)Alkoxy; (C2-C6)Alkenyl; Phenyl oder substituiertes Phenyl; Phenyl (C1-C6)alkyl oder substituiertes Phenyl(C1-C6)alkyl; Phenyl (C2-C6)alkenyl oder substituiertes Phenyl(C2-C6)alkenyl Heterocyclyl oder substituiertes Heterocyclyl; Heterocyclyl(C1-C6)alkyl oder substituiertes Heterocyclyl(C1-C6)alkyl; eine Gruppe BSOnA-, wobei n is 0, 1 oder 2 ist, und B Wasserstoff oder ein (C1-C6)Alkyl, Phenyl, substituiertes Phenyl, Heterocyclyl, substituiertes Heterocyclyl, (C1-C6)acyl, Phenacyl oder eine substituierte Phenacylgruppe ist, und A (C1-C6)Alkylen; -NH2, (C1-C6)Alkylamino oder Di(C1-C6)alkylamino; amino(C1-C6)alkyl, (C1-C6)Alkylamino(C1-C6)alkyl, Di(C1-C6)alkylamino(C1-C6)alkyl, Hydroxy(C1-C6)alkyl, Mercapto(C1-C6)alkyl oder Carboxy(C1-C6)alkyl, wobei die Amino-, Hydroxy-, Mercapto- oder Carboxylgruppe optional geschützt sind, oder die Carboxylgruppe amidiert ist, repräsentiert; oder ein Cycloalkyl, Cycloalkenyl oder einen nicht-aromatischer heterozyklischer Ring, welcher bis zu 3 Heteroatome enthält, wobei jeder davon (i) substituiert sein kann mit einem oder mehreren Substituenten ausgewählt aus C1-C6 Alkyl, C2-C6 Alkenyl, Halo, Cyano (-CN), -CO2H, -CO2R, -CONH2, -CONHR, -CON(R)2, -OH, -OR, oxo-, -SH, -SR, -NHCOR, und -NHCO2R, wobei R gleich C1-C6 Alkyl oder Benzyl ist und/oder (ii) fusioniert an einem Cycloalkyl oder Heterocyclylring sein kann, repräsentiert; R2 eine Gruppe R10-(X)n-(ALK)m- repräsentiert, wobei R10 Wasserstoff repräsentiert, oder eine C1-C6 Alkyl-, C2-C6 Alkenyl-, C2-C6 Alkinyl-, Cycloalkyl-, Aryl-, oder Heterocyclyl-Gruppe, wobei jede davon unsubstituiert oder substituiert sein kann mit (C1-C12)Alkyl, (C1-C12)Alkoxy, Hydroxy, Mercapto, (C1-C12)Alkylthio, Amino, Halo (einschließend Fluoro, Chloro, Bromo und lodo), Trifluoromethyl, Cyano, Nitro, oxo, -COOH, -CONH2, -COORA, -NHCORA, -CONHRA, -NHRA, -NRARB, oder -CONRARB wobei RA und RB unabhängig voneinander eine (C1-C12)Alkylgruppe darstellen und ALK ein geradkettiges oder verzweigtkettiges divalentes C1-C6 Alkylen, C2-C6 Alkenylen, oder C2-C6 Alkinylenradikal repräsentiert und unterbrochen sein kann mit einem oder mehreren nicht benachbarten -NH-, -O- oder -S-Verknüpfungen, X ein -NH-, -O- oder -S-, -NRc oder -NCORc repräsentiert, wobei Rc eine (C1-C12)Alkylgruppe ist, und m und n unabhängig voneinander 0 oder 1 sind; R3 die Seitenkette einer natürlichen oder nicht natürlichen Alphaaminosäure repräsentiert; R4 optional substituiertes C1-C6 alkyl, C2-C6 alkenyl, C2-C6 alkinyl, C1-C3 perfluoroalkyl, Cycloalkyl, Cycloalkyl(C1-C6 alkyl)-, Cycloalkenyl, Cycloalkenyl(C1-C6 alkyl)-, Phenyl, Phenyl(C1-C6 alkyl)-, Naphthyl, Non-aryl heterocyclyl, Non-aryl heterocyclyl(C1-C6 alkyl)-, Heteroaryl; oder Heteroaryl(C1-C6 alkyl)-; repräsentiert; oder ein pharmazeutisch verträgliches Salz, Hydrat oder Solvat davon.
- Eine Verbindung, wie in Anspruch 1 beansprucht, wobei die Verbindung die Formel (IA) aufweist.
- Eine Verbindung, wie in Anspruch 1 beansprucht, wobei die Verbindung die Formel (IB) aufweist.
- Eine Verbindung, wie in irgendeinem der vorangegangenen Ansprüche beansprucht, wobei W gleich HONH(C=O)- ist.
- Eine Verbindung, wie in irgendeinem der vorangegangenen Ansprüche beansprucht, wobei X gleich -O- ist.
- Eine Verbindung, wie in irgendeinem der vorangegangenen Ansprüche beansprucht, wobei R1 gleich Hydrogen, Hydroxy, Fluoro, Chloro, Methyl, Methoxy, Trifluoromethyl, Ethyl, N-propyl, Allyl, Phenylpropyl, Cyclopropylmethyl, Phenylprop-2-enyl, Thienylsulphanylmethyl, Thienylsulphinylmethyl, oder Thienylsulphonylmethyl; oder C1-C4 alkyl, z.B. Methyl, Ethyl n-Propyl oder n-Butyl, substituiert durch eine Phthalimido-, 1,2-Dimethyl-3,5-dioxo-1,2,4triazolidin-4-yl-, 3-Methyl-2,5-dioxo-1-imidazolidinyl-, 3,4,4-Trimethyl-2,5-dioxo-1-imidazolidinyl-, 2-Methyl-3,5-dioxo-1,2,4-oxadiazol-4-yl, 3-Methyl-2,4,5-trioxo-1-imidazolidinyl-, 2,5-Dioxo-3-phenyl-1-imidazolidinyl-, 2-Oxo-1-pyrrolidinyl-, 2,5-Dioxo-1-pyrrolidinyl- oder 2,6-Dioxopiperidinyl-, 5,5-Dimethyl-2,4-dioxo-3-oxazolidinyl-, Hexahydro-1,3-dioxopyrazolo[1,2,a][1,2,4]-triazol-2-yl-, oder einer Naphththalimido-(z.B. 1,3-dihydro-1,3-dioxo-2H-benz[f]isoindol-2-yl)-, 1,3-Dihydro-1-oxo-2H-benz[f]isoindol-2-yl-, 1,3-Dihydro-1,3-dioxo-2H-pyrrolo[3,4b]quinolin-2-yl-, oder 2,3-dihydro-1,3-dioxo-1H-benz[d,e]isoquinolin-2-yl-Gruppe; oder Cyclohexyl, Cyclooctyl, Cycloheptyl, Cycopentyl, Cyclobutyl, Cyclopropyl, Tetrahydropyranyl oder Morpholinyl ist.
- Eine Verbindung wie in irgendeinem der Ansprüche 1 bis 5 beansprucht, wobei R1 Wasserstoff, Hydroxy, C2-C4 Alkenyl oder C1-C4 Alkoxy ist.
- Eine Verbindung wie in irgendeinem der Ansprüche 1 bis 5 beansprucht, wobei R1 Wasserstoff, Hydroxy, Fluoro, Methoxy, Cyclopentyl, n-Propyl, oder Allyl ist.
- Eine Verbindung wie in irgendeinem der Ansprüche 1 bis 8 beansprucht, wobei R2 gleich C1-C12 Alkyl, C3-C6 Alkenyl oder C3-C6 Alkinyl; Cycloalkyl(C1-C6 alkyl)-; Phenyl(C1-C6 alkyl)-, Phenyl(C3-C6 alkenyl)- oder Penyl(C3-C6 alkinyl)-, optional substituiert in dem Phenylring; Heteroaryl(C1-C6 alkyl)-, Heteroaryl(C3-C6 alkenyl)- oder Heteroaryl(C3-C6 alkinyl)-, optional substituiert in dem Heteroarylring; 4-Phenylphenyl(C1-C6 alkyl)-, 4-Phenylphenyl(C3-C6 alkenyl)-, 4-Phenylphenyl(C3-C6 alkinyl)-, 4-Heteroarylphenyl(C1-C6 alkyl)-, 4-Heteroarylphenyl(C3-C6 alkenyl)-, 4-Heteroarylphenyl(C3-C6 alkinyl)-, optional substituiert in dem Heteroarylring; oder Phenoxy(C1-C6 alkyl)- oder Heteroaryloxy(C1-C6 alkyl)-, optional substituiert in dem terminalen Phenyl- oder Heteroarylring; ist.
- Eine Verbindung wie in irgendeinem der Ansprüche 1 bis 8 beansprucht, wobei R2 gleich Methyl, Ethyl, n- oder iso-Propyl, n-, iso- oder tert-Butyl, n-Pentyl, n-Hexyl, n-Heptyl, n-Nonyl, n-Decyl, Prop-2-yn-1-yl, Cyclohexylethyl, Cyclopentylmethyl, 3-Phenylprop-2-yn-1-yl, 3-(2-Chlorophenyl)prop-2-yn-1-yl, Benzylphenylpropyl, 4-Chlorophenylpropyl, 4-Methylphenylpropyl, 4-Methoxyphenylpropyl, Phenoxybutyl, 3-(4-Pyridylphenyl)propyl-, 3-(4-(4-Pyridyl)phenyt)prop-2-yn-1-yl, 3-(4-Phenylphenyl)propyl-, 3-(4-Phenyl)phenyl)prop-2-yn-1-yl oder 3-[(4-Chlorophenyl)phenyl]propyl- ist.
- Eine Verbindung wie in irgendeinem der Ansprüche 1 bis 8 beansprucht, wobei R2 gleich C1-C4 Alkyl, 3-8 gliedriges Cycloalkyl-C1-C4 Alkyl-, optional enthaltend 1-3 Heteroatome in dem Ring, ausgewählt aus N, O and S, oder Aryl-C1-C4 Alkyl ist.
- Eine Verbindung wie in irgendeinem der Ansprüche 1 to 8 beansprucht, wobei R2 gleich Benzyl, n-Butyl, iso-Butyl, n-Hexyl, Cyclopentylmethyl, 4-Ethoxyphenylpropyl oder Phenylpropyl.
- Eine Verbindung wie in irgendeinem der vorangegangenen Ansprüche beansprucht, wobei R3 gleich C1-C6 Alkyl, Phenyl, 2,- 3-, oder 4-Pyndyl, 2- oder 3-Thienyl, 2,- 3-, oder 4-Hydroxyphenyl, 2,- 3-, or 4-Methoxyphenyl, 2,- 3-, or 4-Pyridylmethyl, Benzyl, 2,- 3-, oder 4-Hydroxybenzyl, 2,- 3-, oder 4-Benzyloxybenzyl, 2,- 3-, oder 4-C1-C6 Alkoxybenzyl, oder Benzyloxy(C1-C6alkyl)- ist; oder die charakteristische Gruppe einer natürlichen α-Aminosäure, in welcher irgendeine funktionelle Gruppe geschützt sein kann, irgendeine Aminosäuregruppe acyliert sein kann und irgendeine Carboxylgruppe, die vorliegt, amidiert sein kann; oder eine Gruppe -[Alk]nR6, wobei Alk gleich einer (C1-C6)Alkyl- oder (C2-C6)Alkenylgruppe ist, optional unterbrochen durch ein oder mehrere -O-, oder -S- Atome, oder -N(R7)-Gruppen, [wobei R7 gleich ein Wasserstoffatom ist, oder eine (C1-C6)Alkylgruppe], n gleich 0 oder 1 ist, und R6 eine optional substituierte Cycloalkyl- oder Cycloalkenylgruppe ist; oder eine Benzylgruppe, substituiert in dem Phenylring mit einer Gruppe der Formel -OCH2COR8, wobei R8 ein Hydroxyl, Amino, (C1-C6)Alkoxy, Phenyl(C1-C6)Alkoxy, (C1-C6)Alkylamino, Di((C1-C6)alkyl)amino, Phenyl(C1-C6)alkylamino, der Rest einer Aminosäure oder eines Säurehalids, Esters oder Amidderivats davon ist, wobei besagter Rest über eine Amid-Bindung verknüpft ist, und besagte Aminosäure ausgewählt ist aus Glycin, α oder β Alanin, Valin, Leucin, Isoleucin, Phenylalanin, Tyrosin, Tryptophan, Serin, Threonin, Cystein, Methionin, Asparagin, Glutamin, Lysin, Histidin, Arginin, Glutaminsäure, und Aspartensäure; oder eine heterozyklische (C1-C6)Alkylgruppe ist, entweder unsubstituiert oder mono- oder di-substituiert in dem heterozyklischen Ring mit Halo, Nitro, Carboxy, (C1-C6)Alkoxy, Cyano, (C1-C6)Alkanoyl, Trifluoromethyl (C1-C6)alkyl, Hydroxy, Formyl, Amino, (C1-C6)Alkylamino, Di-(C1-C6)Alkylamino, Mercapto, (C1-C6)Alkylthio, Hydroxy(C1-C6)alkyl, Mercapto(C1-C6)alkyl oder (C1-C6)Alkylphenylmethyl; oder eine Gruppe -CRaRbRc ist, in welcher: ein jeder von Ra, Rb und Rc unabhängig voneinander Wasserstoff, (C1-C6)Alkyl, (C2-C6)Alkenyl, (C2-C6)Alkinyl, Phenyl(C1-C6)alkyl, (C3-C6)Cycloalkyl ist; oder Rc Wasserstoff ist und Ra and Rb unabhängig voneinander Phenyl oder Heteroaryl, sind, wie z.B. Pyridyl; oder Rc gleich Wasserstoff, (C1-C6)Alkyl, (C2-C6)Alkenyl, (C2-C6)Alkinyl, Phenyl(C1-C6)alkyl, oder (C3-C6)Cycloalkyl ist, und Ra and Rb zusammen mit dem Kohlenstoffatom, an welches sie angebunden sind, einen 3 bis 8-gliedrigen Cycloalkyl- oder einen 5- bis 6-gliedrigen heterozyklischen Ring ausbilden; oder Ra, Rb und Rc zusammen mit dem Kohlenstoffatom, an welches sie angebunden sind einen trizyklischen Ring (beispielsweise Adamantyl) ausbilden; oder Ra und Rb jeweils unabhängig voneinander (C1-C6)Alkyl, (C2-C6)Alkenyl, (C2-C6)Alkinyl, Phenyl(C1-C6)Alkyl sind, oder eine Gruppe, wie für Rc unten definiert, verschieden von Wasserstoff, oder Ra and Rb zusammen mit dem Kohlenstoffatom, an welches sie angebunden sind, einen Cycloalkyl- oder einen heterozyklischen Ring ausbilden, und Rc gleich Wasserstoff, -OH, -SH, Halogen, -CN, -CO2H, (C1-C4)Perfluoroalkyl, -CH2OH, -CO2(C1-C6)Alkyl, -O(C1-C6)Alkyl, -O(C2-C6)Alkenyl, -S(C1-C6)Alkyl, -SO(C1-C6)Alkyl, -SO2(C1-C6)Alkyl, -S(C2-C6)Alkenyl, -SO(C2-C6)Alkenyl, -SO2(C2-C6)Alkenyl ist, oder eine Gruppe -Q-W, wobei Q eine Bindung repräsentiert, oder -O-, -S-, -SO- oder -SO2 und W ein Phenyl, Phenylalkyl, (C3-C8)Cycloalkyl, (C3-C8)Cycloalkylalkyl, (C4-C8)Cycloalkenyl, (C4-C8)Cycloalkenylalkyl, Heteroaryl- oder eine Heteroarylalkyl-Gruppe repräsentiert, wobei die Gruppe W optional substituiert sein kann mit einem oder mehreren Substituenten, unabhängig voneinander ausgewählt aus Hydroxyl, Halogen, -CN, -CO2H, -CO2(C1-C6)Alkyl, -CONH2, -CONH(C1-C6)Alkyl, -CONH(C1-C6alkyl)2, -CHO, -CH2OH, (C1-C4)perfluoroalkyl, -O(C1-C6)Alkyl, -S(C1-C6)Alkyl, -SO(C1-C6)Alkyl, -SO2(C1-C6)Alkyl, -NO2, -NH2, -NH(C1-C6)Alkyl, -N((C1-C6)Alkyl)2, -NHCO(C1-C6)Alkyl, (C1-C6)Alkyl, (C2-C6)Alkenyl, (C2-C6)Alkinyl, (C3-C8)Cycloalkyl, (C4-C8)cycloalkenyl, Phenyl oder Benzyl ist.
- Eine Verbindung wie in irgendeinem der Ansprüche 1 bis 12 beansprucht, wobei R3 gleich Benzyl, Phenyl, Cyclohexylmethyl, Pyridin-3-ylmethyl, tert-Butoxymethyl, iso-Propyl, iso-Butyl, sec-Butyl, tert-Butyl, 1-Benzylthio-1-Methylethyl, 1-Methylthio-1-methylethyl, oder 1-Mercapto-1-methylethyl ist.
- Eine Verbindung wie in irgendeinem der Ansprüche 1 to 12 beansprucht, wobei R3 gleich (C1-C4)Alkyl oder Aryl ist.
- Eine Verbindung wie in irgendeinem der Ansprüche 1 bis 12 beansprucht, wobei R3 gleich Benzyl, tert-Butoxymethyl, iso-Propyl, tert-Butyl, oder iso-Butyl ist.
- Eine Verbindung wie in irgendeinem der vorangegangenen Ansprüche beansprucht, wobei R4 gleich optional substituiertes (C1-C6)Alkyl; (C3-C8)Cycloalkyl; Phenyl; monozyklisches heterozyklisches; oder monozyklisches Heteroaryl ist.
- Eine Verbindung wie in irgendeinem der vorangegangenen Ansprüche 1 to 16 beansprucht, wobei R4 gleich C1-C4 Alkyl, Aryl, Heteroaryl, 3-8 gliedriges Cycloalkyl optional enthaltend 1-3 Heteroatome in dem Ring, ausgewählt aus N, O und S, Aryl-C1-C4 Alkyl oder Heteroaryl-C1-C4 alkyl ist.
- Eine Verbindung wie in irgendeinem der Ansprüche 1 bis 16 beansprucht, wobei R4 gleich optional substituiertes Methyl, Ethyl, n- oder iso-Propyl, Prop-2-yl, tert-Butyl, Cyclopropyl, Cyclopentyl; Phenyl; Morpholino; Thienyl oder Furanyl ist.
- Eine Verbindung wie in Anspruch 2 beansprucht, wobei R1 gleich -OH ist; W- gleich C(=O)NHOH ist; X gleich -O- ist und R3 gleich tert-Butyl ist.
- Eine Verbindung wie in Anspruch 2 beansprucht, wobei R1 gleich -OH ist; W gleich -C(=O)NHOH ist; X gleich -O- ist, R3 gleich tert-butyl ist, und R2 gleich C1-C12 Alkyl, oder Phenyl(C1-C12)alkyl- oder Heteroaryl(C1-C6)alkyl- ist, welche optional substituiert in dem Phenyl oder Heteroarylring sind.
- Eine Verbindung wie in Anspruch 2 beansprucht, wobei R1 gleich -OH ist; W gleich -C(=O)NHOH ist; X gleich -O-, R3 gleich tert-butyl, und R2 gleich Phenylpropyl- oder Ethoxyphenylpropyl ist.
- Eine Verbindung wie in Anspruch 2, wobei R1 gleich -OH ist; W gleich -C(=O)NHOH ist; X gleich -O- ist, R3 gleich tert-Butyl ist; und R4 gleich verzweigtes C1-C12 Alkyl, Cycloalkyl, Phenyl, Heteroaryl, Phenyl(C1-C6 alkyl)- oder Heteroaryl(C1-C6)alkyl)- ist.
- Eine Verbindung wie in Anspruch 2, wobei R1 is -OH ist; W gleich -C(=O)NHOH ist, X gleich -O- ist, R3 gleich tert-Butyl ist, R2 gleich Ethoxyphenylpropyl ist, und R4 gleich Phenyl oder Heteroaryl ist.
- Eine Verbindung wie in Anspruch 3 beansprucht, wobei W gleich -C(=O)NHOH und X gleich -O- ist.
- Eine Verbindung wie in Anspruch 3 beansprucht, wobei W gleich -C(=O)NHOH ist, X gleich -O- ist, und R3 gleich tert-Butyl ist.
- Eine Verbindung wie in Anspruch 3 beansprucht, wobei W gleich -C(=O)NHOH ist, X gleich -O- ist, und R1 gleich -OH, C2-C6 Alkoxy, oder C2-C6 Alkenyl ist.
- 2S-Hydroxy-3R-[1S-(5-thiophen-2-yl-[1,2,4]oxadiazol-3-yl)-2,2-dimethylpropylcarbamoyl]-5-methylhexanohydroxamsäure oder 2S-Hydroxy-3R-[1S-(5-furan-2-yl-[1,2,4]oxadiazol-3-yl]-2,2-dimethyl-propylcarbamoyl]-5-methylhexanohydroxamsäure oder ihre pharmazeutisch verträglichen Salze, Hydrate und Solvate.
- Eine Verbindung wie in irgendeinem der Ansprüche 1 bis 28 beansprucht zur Verwendung in der menschlichen oder Tier-Medizin.
- Eine pharmazeutische oder tiermedizinische Zusammensetzung umfassend eine Verbindung, wie in irgendeinem der vorangegangenen Ansprüche beansprucht.
- Verwendung einer Verbindung wie in irgendeinem der Ansprüche 1 bis 29 beansprucht in der Herstellung eines Medikaments zur Behandlung oder Prophylaxe von Erkrankungen mediatisiert durch MMPs.
- Verwendung gemäß Anspruch 31, wobei das Medikament zur Verwendung in Säugetieren ist.
- Die Verwendung gemäß Anspruch 31 oder 32, wobei die Erkrankung Knochenresorption ist, Tumorwachstum oder Invasion durch sekundäre Metastasen; rheumatoide Arthritis, septische Arthritis, Osteoarthritis, Periodontitis, Gingivitis, Cornealulceration, neuroentzündliche Erkrankungen, beispielsweise Multiple Sklerose; Restenosis; Emphysemie; fibrotische Erkrankung, beispielsweise Leberfibrose und zystische Fibrose; chronisch obstruktive pulmonäre Erkrankung; Bronchitis; Asthma; Autoimmunerkrankung; Transplantabstoßung (beispielsweise Transplant-Wirtserkrankung); zystische Fibrose; Psoriasis; psoriasische Arthritis; degenerativer Knorpel-Verlust; entzündliche Magenzustände; z.B. Crohn-Erkrankung, entzündliche Darmerkrankung und ulcerative Colitis; atopische Dermatitis, Epidermolysis Bullosa; epidermische Ulceration; eine Neuropathie oder Nephropathie, beispielsweise interstitielle Nephritis, Glomerulonephritis und Nierenversagen; Augenentzündung; Leberzirrhose, Sjoegren's Syndrom; oder ein Entzündungszustand des Nervensystems.
- Die Verwendung gemäß irgendeinem der Ansprüche 31 oder 32, wobei die Erkrankung Multiple Sklerose, Emphysemie, Leberfibrose, zystische Fibrose, chronisch obstruktive pulmonäre Erkrankung, Crohn's-Erkrankung, entzündliche Darmerkrankung oder Lebersklerose ist.
- Die Verwendung gemäß Anspruch 32, wobei die Erkrankung Hepatitis ist.
- Ein Prozess zur Herstellung einer Verbindung wie in Anspruch 1 beansprucht, welche W eine Hydroxamsäure-Gruppe HONH(C=O)- ist, wobei der Prozess verursacht, dass eine Säure der allgemeinen Formel (IIA) oder (IIB) oder ein aktiviertes Derivat davon mit Hydroxylamin, O-geschütztem Hydroxylamine, oder einem N,O-digeschützten Hydroxylamin, oder einem Salz davon reagieren, wobei X, R1, R2, R3, und R4 wie in Anspruch 1 definiert sind, außer, dass jegliche Substituenten in R1, R2, R3, und R4, welche potentiell reaktiv sind mit Hydroxylamin, O-geschütztem Hydroxylamin, dem N,O-digeschützten Hydroxylamin oder deren Salzen optional selbst geschützt sind gegen solch eine Reaktion, anschließend Entfernen von irgendwelchen Schutzgruppen von der resultierenden Hydroxamsäure-Gruppe und von irgendeinem geschützten Substituenten in R1, R2, R3, und R4.
- Ein Prozess zur Herstellung einer Verbindung wie in Anspruch 1 beansprucht, wobei W eine N-Formylhydroxylamino-Gruppe H(C=O)NH(OH)- ist, wobei der Prozess die N-Formylierung der korrespondierenden Verbindung umfasst, in welcher W gleich -NH(OP) ist, wobei P eine O-Schutzgruppe ist, anschließend Entfernen der O-Schutzgruppe P.
- Ein Prozess zur Herstellung einer Verbindung wie in Anspruch 1 beansprucht, wobei W eine Karbonsäuregruppe -COOH ist, wobei der Prozess folgendes umfasst: Koppeln einer Säure der Formel (III) oder eines aktivierten Derivats davon mit einem Amin der Formel (IVA) oder (IVB) wobei X, R1 R2, R3, und R4 wie in Anspruch 1 definiert sind, außer, dass irgendwelche Substituenten in R1, R2, R3, und R4 welche potentiell reaktiv sind in der Kopplungsreaktion selbst geschützt sein können gegen solch eine Reaktion und R11 eine Hydroxy-Schutzgruppe repräsentiert, und nachfolgend Entfernen der Schutzgruppe R11 sowie jeglicher Schutzgruppen von R1 R2, R3, und R4.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| GB0204159 | 2002-02-22 | ||
| GBGB0204159.8A GB0204159D0 (en) | 2002-02-22 | 2002-02-22 | Metalloproteinase inhibitors |
| PCT/GB2003/000741 WO2003070711A1 (en) | 2002-02-22 | 2003-02-20 | Oxa- and thiadiazoles and their use as metalloproteinase inhibitors |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| DE60313292D1 DE60313292D1 (de) | 2007-05-31 |
| DE60313292T2 true DE60313292T2 (de) | 2007-12-27 |
Family
ID=9931543
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| DE60313292T Expired - Lifetime DE60313292T2 (de) | 2002-02-22 | 2003-02-20 | Oxa- und thiadiazole und ihre verwendung als metalloproteinase-inhibitoren |
Country Status (27)
| Country | Link |
|---|---|
| US (4) | US7358265B2 (de) |
| EP (1) | EP1476438B1 (de) |
| JP (1) | JP4615864B2 (de) |
| KR (1) | KR101098614B1 (de) |
| CN (1) | CN100351245C (de) |
| AT (1) | ATE360007T1 (de) |
| AU (1) | AU2003205910B2 (de) |
| BR (1) | BR0307899A (de) |
| CA (1) | CA2475867C (de) |
| CY (1) | CY1106730T1 (de) |
| DE (1) | DE60313292T2 (de) |
| DK (1) | DK1476438T3 (de) |
| EA (1) | EA007609B1 (de) |
| ES (1) | ES2286404T3 (de) |
| GB (1) | GB0204159D0 (de) |
| HK (1) | HK1078583A1 (de) |
| HR (1) | HRP20040725A2 (de) |
| IL (1) | IL163413A (de) |
| MX (1) | MXPA04008132A (de) |
| NO (1) | NO330772B1 (de) |
| PL (1) | PL210773B1 (de) |
| PT (1) | PT1476438E (de) |
| RS (1) | RS51354B (de) |
| SI (1) | SI1476438T1 (de) |
| UA (1) | UA78275C2 (de) |
| WO (1) | WO2003070711A1 (de) |
| ZA (1) | ZA200406755B (de) |
Families Citing this family (18)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2004101537A1 (en) * | 2003-05-17 | 2004-11-25 | British Biotech Pharmaceuticals Ltd | Metalloproteinase inhibitors |
| DE602004032548D1 (de) * | 2003-08-23 | 2011-06-16 | Merck Serono Sa | Derivate von hydroxamsäure als metalloproteinaseinhibitoren |
| US7838522B2 (en) | 2004-11-17 | 2010-11-23 | Ares Trading S.A. | Benzothiazole formulations and use thereof |
| JP5021488B2 (ja) | 2004-12-21 | 2012-09-05 | メルク セローノ ソシエテ アノニム | スルホニルアミノ環式誘導体及びその使用 |
| DK1844032T3 (da) | 2005-01-31 | 2011-10-24 | Merck Serono Sa | N-hydroxyamid-derivater og deres anvendelse |
| KR20080044836A (ko) | 2005-07-15 | 2008-05-21 | 라보라뚜와르 세로노 에스. 에이. | 자궁내막증 치료용 jnk 억제제 |
| BRPI0613042A2 (pt) | 2005-07-15 | 2010-12-14 | Serono Lab | inibidores de jnk para o tratamento de endometriose |
| CA2616479A1 (en) | 2005-09-01 | 2007-03-08 | Ares Trading S.A. | Treatment of optic neuritis |
| US8153166B2 (en) * | 2006-06-08 | 2012-04-10 | Chih-Hsiung Lin | Composition for prophylaxis or treatment of urinary system infection and method thereof |
| SG11201601682RA (en) | 2013-09-06 | 2016-04-28 | Aurigene Discovery Tech Ltd | 1,2,4-oxadiazole derivatives as immunomodulators |
| AU2016230759A1 (en) * | 2015-03-10 | 2017-09-07 | Aurigene Discovery Technologies Limited | 3-substituted-1,2,4-oxadiazole and thiadiazole compounds as immunomodulators |
| MY196130A (en) | 2015-03-10 | 2023-03-16 | Aurigene Discovery Tech Ltd | 1,2,4-Oxadiazole and Thiadiazole Compounds as Immunomodulators |
| CN105384736B (zh) * | 2015-10-28 | 2018-11-02 | 南昌大学 | 一种ⅳ型胶原酶抑制剂及合成方法 |
| WO2019061324A1 (en) | 2017-09-29 | 2019-04-04 | Curis Inc. | CRYSTALLINE FORMS OF IMMUNOMODULATORS |
| KR20200068659A (ko) | 2017-10-11 | 2020-06-15 | 오리진 디스커버리 테크놀로지스 리미티드 | 3-치환된 1,2,4-옥사다이아졸의 결정질 형태 |
| JP7378394B2 (ja) | 2017-11-03 | 2023-11-13 | オーリジーン オンコロジー リミテッド | Tim-3およびpd-1経路の二重阻害剤 |
| EP3706798A1 (de) | 2017-11-06 | 2020-09-16 | Aurigene Discovery Technologies Limited | Gemeinsame therapien zur immunmodulation |
| CN108530378B (zh) * | 2018-05-29 | 2021-09-14 | 济南大学 | 一类含有噁二唑结构的氮原子双取代异羟肟酸类化合物、用途及其制备方法 |
Family Cites Families (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB9404046D0 (en) * | 1994-03-03 | 1994-04-20 | Smithkline Beecham Corp | Novel compounds |
| US5665753A (en) * | 1994-03-03 | 1997-09-09 | Smithkline Beecham Corporation | Cytokine inhibiting imidazole substituted hydroxamic acid derivatives |
| US5703092A (en) | 1995-04-18 | 1997-12-30 | The Dupont Merck Pharmaceutical Company | Hydroxamic acid compounds as metalloprotease and TNF inhibitors |
| PT946166E (pt) * | 1996-12-17 | 2004-06-30 | Warner Lambert Co | Utilizacao de inibidores das metaloproteinases da matriz para tratar disturbios neurologicos e promover a cicatrizacao de feridas |
| CA2319493A1 (en) * | 1998-03-18 | 1999-09-23 | Regine Bohacek | Heterocyclic signal transduction inhibitors, compositions containing them |
| JP2001031637A (ja) * | 1999-05-17 | 2001-02-06 | Fuji Chemical Industries Ltd | 新規なヒドロキサム酸誘導体 |
| GB9930570D0 (en) * | 1999-12-23 | 2000-02-16 | Pfizer Ltd | Therapy |
| US6448278B2 (en) | 1999-12-23 | 2002-09-10 | Pfizer Inc. | Procollagen C-proteinase inhibitors |
-
2002
- 2002-02-22 GB GBGB0204159.8A patent/GB0204159D0/en not_active Ceased
-
2003
- 2003-02-20 CA CA2475867A patent/CA2475867C/en not_active Expired - Fee Related
- 2003-02-20 DE DE60313292T patent/DE60313292T2/de not_active Expired - Lifetime
- 2003-02-20 MX MXPA04008132A patent/MXPA04008132A/es active IP Right Grant
- 2003-02-20 US US10/504,317 patent/US7358265B2/en not_active Expired - Fee Related
- 2003-02-20 AT AT03702791T patent/ATE360007T1/de active
- 2003-02-20 UA UA20040806941A patent/UA78275C2/uk unknown
- 2003-02-20 PT PT03702791T patent/PT1476438E/pt unknown
- 2003-02-20 BR BR0307899-0A patent/BR0307899A/pt not_active IP Right Cessation
- 2003-02-20 AU AU2003205910A patent/AU2003205910B2/en not_active Ceased
- 2003-02-20 RS YUP-716/04A patent/RS51354B/sr unknown
- 2003-02-20 ES ES03702791T patent/ES2286404T3/es not_active Expired - Lifetime
- 2003-02-20 WO PCT/GB2003/000741 patent/WO2003070711A1/en active IP Right Grant
- 2003-02-20 JP JP2003569618A patent/JP4615864B2/ja not_active Expired - Fee Related
- 2003-02-20 EA EA200401095A patent/EA007609B1/ru not_active IP Right Cessation
- 2003-02-20 CN CNB038089122A patent/CN100351245C/zh not_active Expired - Fee Related
- 2003-02-20 PL PL372268A patent/PL210773B1/pl unknown
- 2003-02-20 SI SI200330870T patent/SI1476438T1/sl unknown
- 2003-02-20 EP EP03702791A patent/EP1476438B1/de not_active Expired - Lifetime
- 2003-02-20 DK DK03702791T patent/DK1476438T3/da active
- 2003-02-20 KR KR1020047012821A patent/KR101098614B1/ko not_active IP Right Cessation
-
2004
- 2004-08-09 IL IL163413A patent/IL163413A/en not_active IP Right Cessation
- 2004-08-10 HR HR20040725A patent/HRP20040725A2/hr not_active Application Discontinuation
- 2004-08-25 ZA ZA200406755A patent/ZA200406755B/en unknown
- 2004-09-14 NO NO20043846A patent/NO330772B1/no not_active IP Right Cessation
-
2006
- 2006-01-26 HK HK06101230A patent/HK1078583A1/xx not_active IP Right Cessation
-
2007
- 2007-07-13 CY CY20071100937T patent/CY1106730T1/el unknown
-
2008
- 2008-02-08 US US12/028,275 patent/US20080227833A1/en not_active Abandoned
-
2009
- 2009-10-14 US US12/588,372 patent/US20100035943A1/en not_active Abandoned
-
2010
- 2010-10-07 US US12/900,262 patent/US20110086893A1/en not_active Abandoned
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| DE60313292T2 (de) | Oxa- und thiadiazole und ihre verwendung als metalloproteinase-inhibitoren | |
| KR100418808B1 (ko) | 금속단백질분해효소억제제 | |
| EP0371876B1 (de) | Isoxazole und Isoxazolin-Derivate mit Antikonvulsiva und pharmazeutische Zusammensetzungen, die sie enthalten | |
| DE69633003T2 (de) | Verbindungen mit wachstumshormon-freisetzenden eigenschaften | |
| EP2268625B1 (de) | Oxo-heterocyclisch substituierte carbonsäure-derivate und ihre verwendung | |
| DE69928667T2 (de) | Nicht-peptidische Inhibitoren von VLA-4-abhängiger Zellbindung für die Behandlung von entzündlichen, autoimmun-und respiratorischen Krankheiten und Atemstörungen | |
| EP0608759B1 (de) | Piperazinderivate | |
| JP2001508811A (ja) | cGMP−ホスホジエステラーゼ阻害剤としてのアントラニル酸誘導体 | |
| JPH04230681A (ja) | 1,4‐ベンゾチアゼピン誘導体 | |
| EP0031104A1 (de) | Thiazolidin-Verbindungen, Verfahren zu ihrer Herstellung und sie enthaltende pharmazeutische Zusammensetzungen | |
| DE19726427A1 (de) | Pyrimidin-2,4,6-trion-Derivate, Verfahren zu deren Herstellung und diese Verbindungen enthaltende Arzneimittel | |
| FR2842523A1 (fr) | Derives d'acylaminothiazole, leur preparation et leur application en therapeutique | |
| US4925968A (en) | N-acyl-N-naphthoylglycines as aldose reductase inhibitors | |
| JP3093419B2 (ja) | 1,4‐ベンゾチアゼピン誘導体 | |
| DE2952594A1 (de) | Disulfidverbindungen | |
| US4499102A (en) | Thiazolidine and pyrrolidine compounds and pharmaceutical compositions containing them | |
| DE69825281T2 (de) | Neue sulfonamid-derivate | |
| DE69912639T2 (de) | N-formyl hydroxylamin derivate als antibakterielle mittel | |
| WO1998023588A1 (en) | Metalloproteinase inhibitors | |
| US5103013A (en) | Dithioketene derivatives, pharmaceutical compositions containing the same and uses thereof | |
| EP0764637B1 (de) | 2-Cyano-3-mercaptocrotonsäureamide | |
| DE60118780T2 (de) | Zur verwendung als procollagen-c-proteinase-inhibitoren geeignete 3-ox(adi)azolylpropanohydroxamsäuren | |
| DE3413876A1 (de) | Arzneimittel | |
| WO2004101537A1 (en) | Metalloproteinase inhibitors | |
| US4473577A (en) | 2-Thiazolamine derivatives, process for preparing same, and pharmaceutical compositions comprising same |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 8364 | No opposition during term of opposition | ||
| 8327 | Change in the person/name/address of the patent owner |
Owner name: MERCK SERONO SA, COINSINS, VAUD, CH Owner name: VERNALIS (R&D) LTD., ABINGTON, CAMBRIDGE, GB |