-
Gebiet und
Hintergrund der Erfindung
-
Die
vorliegende Erfindung betrifft im Allgemeinen die katalytische Polymerisation
und im Besonderen die taktische katalytische Polymerisation von
Alpha-Olefinmonomeren unter Verwendung eines aktiven nicht-Metallocen
Präkatalysators,
der einen Diamindiphenolatkomplex aufweist, und ein entsprechendes
Verfahren, das den offenbarten Präkatalysator verwendet.
-
Gegenwärtig gibt
es ein erhebliches Interesse in Bezug auf Verfahren und Systeme
von katalytischer Polymerisation von Alpha-Olefinmonomeren, die
auf einem "Präkatalysator" basieren, der ein
Metall, das an einen oder mehrere Zuschauerliganden gebunden ist,
aufweist, wobei der Präkatalysator
in einem Flüssigphasenlösungsmittel
löslich
ist oder auf einer festen Oberfläche
absorbiert ist und wobei der Alpha-Olefinmonomerreaktant flüssig oder
in der Gasphase sein kann. Bei diesen Verfahren und Systemen wird
der Präkatalysator
typischerweise durch mindestens einen "Cokatalysator" aktiviert, wobei die Kombination des
aktivierten Präkatalysators
und des mindestens einen Cokatalysators als eine einzelne chemische
Einheit oder als Komplex-"Katalysator" für die Polymerisation
des Alpha-Olefinmonomers
wirkt. Das Gebiet der katalytischen Polymerisation von Alpha-Olefinmonomeren
ist von erheblicher industrieller Bedeutung, da mehr als 50 Millionen Tonnen
von Poly(Alpha-Olefin)-Produkten, wie zum Beispiel Polyethylene
und Polypropylene, jedes Jahr hergestellt werden, was Metall-basierende katalytische
Verfahren und Systeme einschließt.
-
Nachstehend
betrifft der Begriff "Präkatalysator" im Allgemeinen eine
chemische Einheit und im Besonderen eine chemische Verbindung, die,
wenn durch mindestens einen Cokatalysator aktiviert, Teil eines "Katalysator" wird, der für die katalytische
Polymerisation eines Alpha-Olefinmonomers
unter echten Polymerisations-reaktionsbedingungen
funktionell ist. Im Allgemeinen ist ein Präkatalysator ohne die Gegenwart
mindestens eines Cokatalysators für die katalytische Polymerisation
eines Alpha-Olefinmonomers unwirksam und zeigt konsequenterweise
im Wesentlichen keine katalytische Aktivität für die Polymerisation eines
Alpha-Olefinmonomers. Wenn hier auf die katalytische Aktivität während einer
Polymerisationsreaktion Bezug genommen wird, bezieht sich die Bezugnahme
auf die katalytische Aktivität
eines Präkatalysators
und es sollte verständlich
sein, dass der Präkatalysator
zusammen mit mindestens einem Cokatalysator wirkt, um die katalytische
Polymerisation eines Alpha-Olefinmonomers zu bewirken. Es sei jedoch
angemerkt, dass es seltene Ausnahmen eines bestimmten Präkatalysators
gibt, der wirkt, ohne zuerst durch einen Cokatalysator aktiviert
zu werden, um die katalytische Polymerisation eines Alpha-Olefinmonomers
zu bewirken. Somit fokussiert sich die vorliegende Erfindung auf
einen im Vergleich zu Präkatalysatoren,
die gegenwärtig
für die
katalytische Polymerisation von Alpha-Olefinmonomeren verwendet
werden, neuen und neuartigen Präkatalysator.
-
Gegenwärtig ist
eines der Hauptziele auf diesem Gebiet eine Vielzahl neuer Typen
von Poly(Alpha-Olefin)-Produkten, zum Beispiel taktische Polymere,
die aus Alpha-Olefinmonomeren hergestellt sind, die mehr als zwei
Kohlenstoffatome aufweisen, mit gut definierten Massen- oder globalen physiochemischen
Eigenschaften, wie zum Beispiel mechanische Festigkeit, Elastizität, Schmelzpunkt
und chemischer Beständigkeit,
herzustellen, die für
die Herstellung einer Vielzahl von Endprodukten anwendbar sind.
Dies kann durch Kontrollieren der Polymertaktizität und durch
Polymerisieren verschiedener Arten von Alpha-Olefinmonomeren erreicht
werden, um eine Vielzahl von Homopolymeren oder Co-Polymeren mit
variierendem Grad an Monomereinschluss herzustellen.
-
Massen-
oder globale physiochemische Eigenschaften der Polymere sind direkt
mit molekularen oder lokalen physiochemischen Charakteristika der
Polymereinheiten, die das Massenpolymer bilden, verbunden und sind
dadurch kontrollierbar. Drei bemerkenswerte molekulare physiochemische
Charakteristika sind das Molekulargewicht des Polymers, die Molekulargewichtsverteilung
des Polymers und die Polymertaktizität.
-
Das
Molekulargewicht des Polymers und die Molekulargewichtsverteilung
des Polymers sind äußerst relevant
in Bezug auf die Herstellung verschiedener Arten von Polymeren.
Zum Beispiel hat Polyethylen mit ultra-hohem Molekulargewicht (UHMWPE)
mit einem durchschnittlichen Molekulargewicht oberhalb 3.000.000 die
höchste
Abriebfestigkeit von Thermoplasten und einen geringen Reibungskoeffizienten.
Im Gegensatz zur Synthese von kleinen Molekülen schließen Polymerisationsreaktionen
jedoch zufällige
Ereignisse ein, die durch Bildung von Polymerketten, die eher einen
Bereich von Molekulargewichten als ein einzelnes Molekulargewicht
haben, charakterisiert werden. Typischerweise sind Polymere besser
definiert und charakterisiert in Bezug auf enge Molekulargewichtsbereiche.
-
Der
akzeptierte Parameter zur Definition der Molekulargewichtsverteilung
eines Polymers ist der Polydispersitätsindex (PDI), welcher das
massengemittelte Molekulargewicht Mw, geteilt
durch das Molekulargewicht-Zahlenmittel
Mn oder Mw/Mn ist. Abhängig von der tatsächlichen
Anwendung weist ein katalytisches Polymerisationssystem idealerweise
eine "lebende" Polymerisation auf,
bei der die Initiationsgeschwindigkeit höher ist als die Geschwindigkeit
der Propagation, die zu einem PDI nahe 1 führt und schließt eine
einzelne katalytisch aktive Stelle ein und die Geschwindigkeit der
Beendigung der Reaktionen ist vernachlässigbar, relativ zur Propagation.
Dies ist in sehr wenigen Systemen für die katalytische Polymerisation
von Alpha-Olefinmonomeren erreicht worden. Ein PDI von 2.0, der "nicht lebende" Polymerisation kennzeichnet,
wird oft in katalytischen Systemen von Metallocen gefunden, die
ebenfalls eine einzelne katalytisch aktive Stelle beinhalten. Klassische
heterogene Ziegler-Natta Katalysatorsysteme führen gewöhnlich zu einem breiteren Bereich
von Molekulargewichten mit einem PDI von ungefähr 5. Ein gegenwärtiger Versuch
ist es, Alpha-Olefin-Polymersationspräkatalysatoren und katalytische
Systeme, die diese Präkatalysatoren
beinhalten, zu entwerfen, was zu Poly(Alpha-Olefin)-Produkten mit
niedrigen Werten an PDI führt.
-
Eine
andere gegenwärtige
Herausforderung auf dem Gebiet der katalytischen Polymerisation
von Alpha-Olefinen ist es, Alpha-Olefin-Polymersationspräkatalysatoren
und katalytischen Systemen zu entwerfen, die diese Präkatalysatoren
beinhalten, was zu Poly(Alpha-Olefin)-Produkten mit kontrollierbarem
und klassifizierbarem Grad an Polymertaktizität führt. Polymertaktizität ist eine
andere sehr wesentliche molekulare physiochemische Charakteristik
eines Polymers, die die physiochemischen Masseneigenschaften eines
Polymers, wie zum Beispiel eines Poly(Alpha-Olefin)-Polymers, dramatisch
bestimmen und beeinflussen kann. Der Begriff "Polymertaktizität" betrifft die besondere Mikro- oder
lokale Strukturkonfiguration der Substituenten auf dem Polymerrückgrad oder äquivalent
die Stereoregularität
der Polymerkette, ob ein Polymer zum Beispiel isotaktisch, syndiotaktisch
oder ataktisch ist. Polymertaktizität wird typischerweise in Bezug
auf ein Kohlenwasserstoffpolymer, das sich von der Polymerisation
eines Monomers mit mehr als 2 Kohlenstoffatomen ableitet, verwendet,
so dass das Polymer eine Seitenkette an jedem anderen Kohlenstoffatom
des Polymerrückgrads hat.
Außerdem
gibt es verschiedene besondere Formen oder Arten der "Polymertaktizität" gemäß der besonderen
Mikro- oder lokalen Struktur in Bezug auf die relativen Orientierungen
der Seitenketten, die an das Polymerrückgrad gebunden sind.
-
Ein
Polymer, bei dem alle Seitenketten sich von derselben Seite oder
Ebene des Polymerrückgrads erstrecken
oder herausragen, wird als ein "isotaktisches
Polymer" bezeichnet,
welches aus einem "isotaktischen" oder entsprechend
einem "isospezifischen" Polymerisationsprozess
erhalten wird. Ein Polymer, bei dem sich die Seitenketten alternierend
von gegenüberliegenden
Seiten des Polymerrückgrads
erstrecken oder herausragen, wird als ein "syndiotaktisches Polymer" bezeichnet, das
aus einem "syndiotaktischen" oder entsprechend
einem "syndiospezifischen" Polymerisationsprozess
erhalten wird. Ein Polymer, bei dem sich die Seitenketten zufällig von
jeder Seite des Polymerrückgrads
erstrecken oder hervorragen, wird als ein "ataktisches Polymer" bezeichnet, das aus einem "ataktischen" Polymerisationsprozess
erhalten wird. Des Weiteren wird das Ausmaß oder der Grad einer besonderen
Form oder Art an Polymertaktizität
ebenfalls in Bezug auf die Polymertaktizität verwendet. Zum Beispiel kann
ein Polymer als 80% isotaktisch und 20% ataktisch klassifiziert
werden. Ein anderes Beispiel ist ein hemi-isotaktisches Polymer,
bei dem sich jede zweite Seitenkette von derselben Seite oder Ebene
des Polymerrückgrads
erstreckt oder hervorragt, wohingegen der Rest der Seitenketten
sich zufällig
von beiden Seiten des Polymerrückgrads
erstreckt oder herausragt. Typischerweise wird das Ausmaß oder der
Grad an Taktizität
eines Polymers oder eines Polymerisationsprozesses bestimmt, indem
das Polymer oder die Produkte des Polymerisationsprozesses NMR spektroskopischen
Analysen, insbesondere 13C NMR, unterzogen
werden.
-
Ein
illustratives Beispiel, das den dramatischen Einfluss zeigt, den
die Polymertaktizität
auf die physiochemischen Masseneigenschaften eines Polymers hat,
ist die taktische Polymerisation von Propylen. Isotaktisches Polypropylen
ist fest und halb transparent bei Raumtemperatur mit einem Schmelzpunkt
im Bereich von 150–165°C, syndiotaktisches
Polypropylen ist ein transparenter Feststoff bei Raumtemperatur
mit einem Schmelzpunkt von ungefähr
145°C und
ataktisches Polypropylen ist bei Raumtemperatur ein viskoses Öl.
-
Metallocen-Präkatalysatoren,
die einen Metallkomplex aufweisen, der ein Metallatom, zum Beispiel aus Übergangselementen
der Gruppe IV, wie zum Beispiel Titan, Zirkonium und Hafnium, beinhaltet,
das an zwei Liganden der gut bekannten Cyclopentadienyl (Cp) Ligandfamilie,
zum Beispiel Pentamethylcyclopentadienyl, Indenyl oder Fluorenyl,
bindet, wurden während
der letzten zwei Dekaden zum Zweck der katalytischen Polymerisation
von Alpha-Olefinmonomeren eingeführt.
Die allgemeinste Art von Metallocenpräkatalysatoren ist ein neutraler
Komplex, der ein Metall im Oxidationszustand von +4, das zusätzlich zu
zwei Standard Cp-Liganden
an zwei anionische Liganden gebunden ist, beinhaltet, zum Beispiel
Bis(cyclopentadienyl)titandichlorid, ebenfalls als Titanocendichlorid
bekannt. Eine besondere Gruppe von Metallocenpräkatalysatoren ist als Ansa-Metallocenkomplexe
bekannt, bei denen die zwei Cp-Liganden kovalent aneinander gebunden
sind. Eine verwandte Gruppe von Komplexen sind Präkatalysatoren
mit "eingeschränkter Geometrie", die ein Metall aufweisen,
das sowohl an einen einzelnen Liganden vom Cp-Typ als auch an eine
zweite anionische Gruppe gebunden ist, wobei der Cp-Ligand und die
zweite anionische Gruppe kovalent aneinander gebunden sind.
-
Die
Verwendung von Metallocenpräkatalysatoren
und Präkatalysatoren
vom Metallocentyp in katalytischen Verfahren und Systemen zur Polymerisation
von Alpha-Olefinmonomeren erfordert eine bessere Kontrolle des Molekulargewichts
und eine engere Molekulargewichtsverteilung, was mit niedrigeren
Werten des PDI verbunden ist, relativ zur klassischen Ziegler-Natta
Familie von Präkatalysatoren,
wie zum Beispiel Titantrichlorid, das einen Trialkylaluminium-Cokatalysator
verwendet. Außerdem
ist die Gruppe der Ansa-Metallocenpräkatalysatoren
zur Herstellung von Polymeren mit einem kontrollierbaren und klassifizierbaren
Grad an Polymertaktizität
verwendbar. Metallocenpräkatalysatoren
und Präkatalysatoren
vom Metallocentyp, Verfahren und Systeme sind gut bekannt und im
Stand der Technik beschrieben. Diese Präkatalysatoren, Verfahren und
Systeme sind jedoch in vielerlei Hinsicht in Bezug auf die oben
genannte Diskussion begrenzt.
-
Zuerst
zeigen Präkatalysatoren
vom Metallocentyp in Bezug auf die katalytische Aktivität typischerweise
eine relativ moderate Aktivität
zur Polymerisierung einer kleinen Vielzahl von Alpha-Olefinmonomeren.
In Bezug auf Poly(Alpha-Olefin)-Produkttypen
und Verschiedenheit sind Alpha-Olefinmonomere, die durch Metallocenpräkatalysatoren
polymerisiert wurden, häufig
kurzkettiges Ethylen und Propylen, welche bereits gut beschrieben
sind. Metallocenpräkatalysatoren
sind in Bezug auf die Verfügbarkeit
und Vielseitigkeit begrenzt. Präkatalysatoren
vom Metallocentyp sind relativ schwierig zu synthetisieren, eine
Tatsache, die die Möglichkeit der
Entwicklung neuer Varianten von Alpha-Olefin Polymerisationspräkatalysatoren
vom Metallocentyp beschränkt.
-
Aufgrund
der anhaltenden Suche für
neue Poly(Alpha-Olefin)-Produkte,
die ausgewählte,
gut definierte physiochemische Masseneigenschaften und molekulare,
physiochemische Charakteristika zeigen, verbunden mit den oben genannten
Beschränkungen,
die mit Metallocenpräkatalysatoren
verbunden sind, gibt es ein wachsendes Interesse an der Entwicklung
von nicht-Metallocen Alpha-Olefin-Polymerisationspräkatalysatoren und
betreffende katalytische Verfahren und Systeme. Der Hauptschwerpunkt
liegt auf dem Erhalten neuer Alpha-Olefin-Polymerisationspräkatalysatoren, welche leicht
erhältlich
sind, eine relativ hohe Stabilität
zeigen und zur verbesserten Kontrolle gegenüber industriell wichtigen Polymerparametern,
wie zum Beispiel Molekulargewicht, Molekulargewichtsverteilung,
Produkttypen und Vielzahl und kontrollierbare und klassifizierbare Polymertaktizität, verwendet
werden können.
-
Das
Prinzip der Kontrolle der Polymertaktizität durch Ligandendesign wurde
zuerst für
verschiedene katalytische Systeme gezeigt, die eine Gruppe von Ansa-Metallocenkomplexpräkatalysatoren
aufweisen, wie von Brintzinger, H. H, et. al. in Angew. Chem., Int.
Ed. Engl. 34, 1143, 1995 rezensiert. Die dort beschriebenen katalytischen
Systeme führen
gewöhnlich
zu einem PDI von nicht weniger als 2.0 und leiden an den oben beschriebenen
Nachteilen und Beschränkungen
von Metallocensystemen.
-
Ein
Beispiel eines "Halbsandwich" Präkatalysators,
der einen Komplex aufweist, der einen Liganden vom Cp-Typ und einen
Heteroatomdonor beinhaltet, wird von Sita, L. R., in J. Am. Chem.
Soc. 122, 958, 2000 beschrieben. Dieses katalytische Halbmetallocen-System
ist in Bezug auf Polymerisospezifität und lebende Polymerisation
von Alpha-Olefinmonomeren aktiv. Dieses System schließt jedoch
das Arbeiten bei kommerziell unerwünschten Reaktionsbedingungen,
wie zum Beispiel –10°C, ein.
-
Ein
nicht-Metallocen Alpha-Olefinpolymerisationskatalysesystem ist in
US Patent Nr. 5,852,146 offenbart und weist einen Bis(hydroxyaromatischen
Stickstoffligand)-Übergangsmetallpräkatalysator
auf, der mit einem aktivierenden Methylaluminoxan (MAO) Cokatalysator
arbeitet. Eine relativ hohe katalytische Aktivität von ungefähr 4.000 Gramm/(mmol-pre-cat.hr)
wird nur für
die Polymerisation von Ethylen berichtet. Außerdem wird MAO in großen Mengen
als Cokatalysator benötigt,
was im Allgemeinen beachtliche Beschränkungen in Bezug auf Kosten
und Verschmutzung bewirkt. MAO, das in großen Mengen verwendet wird,
ist teuer und muss sauber entsorgt werden in Bezug auf Umweltüberlegungen.
-
Lebende
Polymerisation von 1-Hexen wird von Schrock, R. R., in J. Am. Chem.
Soc. 119, 3830, 1997 beschrieben und ist in US Patent Nr. 5,889,128
offenbart. Eine der dort beschriebenen nicht-Metallocen Präkatalysatorzusammensetzungen
umfasst einen Dimethylkomplex, bei dem das Metallatom zu einem dreizähnigen Zuschauerligand
chelatisiert ist, welcher durch einen nicht-MAO Borsalz-Cokatalysator
aktiviert wird. Es werden jedoch nur ataktische Polymerprodukte
von diesem System erhalten.
-
Die
lebende Polymerisation von 1-Hexen wird ebenfalls von McConville,
D. H., in J. Am. Chem. Soc. 118, 10008, 1996 beschrieben. Sie beschreiben
einen aktiven nicht-Metallocen Polymerisationspräkatalysator, der die Aktivierung
eines Präkatalysator
mit einschließt,
der einen Dimetallkomplex eines Bis(amid)-Liganden beinhaltet, mit
einer nicht-MAO Bor-Lewis-Säure als
Cokatalysator unter Raumtemperatur zur Herstellung ataktischer Polymere.
-
Einen
anderen aktiven lebenden nicht-Metallocen 1-Hexen-Polymerisationspräkatalysator,
der mit einem nicht-MAO Cokatalysator arbeitet, wird von Kim, K.,
in Organometallics 17, 3161, 1998 berichtet. Ähnlich zu den anderen Lehren
ergibt das beschriebene katalytische System nur ataktische Polymere.
-
Ein
nicht-Metallocen Diphenolatpräkatalysator
wird von Schaverien, C. J., in J. Am. Chem. Soc. 117, 3008, 1995
berichtet. Die Verwendung des offenbarten Präkatalysators führt zu hoch
isotaktischem Poly(1-hexen), wobei der Polymerisationsprozess jedoch
nicht lebend ist.
-
Die
Publikation HINSHAW C J ET AL: "Molybdenum(VI)-dioxo
complexes with linear and tripodal tetradentate ligands: models
for the molybdenum (VI/V) centers of the molybdenum hydroxylases
and relates enzymes 1. Syntheses and structures" INORGANIC CHEMISTRY, Vol 28, Nr. 25,
1989, Seiten 4483–4496, XP002935342
ISSN: 0020-1669 ist auf neue Mo(VI)-Dioxokomplexe als Modelle für Molybdän (VI/V)
Zentren von Molybdänhydroxylasen
und verwandten Enzymen fokussiert. Sie offenbart Komplexe von nur
einem bestimmten Metallatom, Molybdän. Darin sind alle Molybdänkomplexe
1–5, die
in Bezug auf die Tabellen I und II beschrieben sind, vom Dioxo-Typ,
d.h. jeder weist zwei Sauerstoffliganden auf, die doppelt an das
Molybdänatom
gebunden sind. Außerdem
ist das Molybdän
in jedem dort beschriebenen Molybdänkomplex in demselben besonderen
Oxidationszustand von VI(+6).
-
Die
Publikation BANDOLI G ET Al: "Preparation
and crystal and molecular structure of [N,N'-o-phenylene-bis(salicylideneiminato)UO2(EtOH)]' JOURNAL OF THE CHEMICAL
SOCIETY, SECTION D, 1971, pages 1330–1331, XP009025789 offenbart
die Synthese und die Molekülstrucktur
von [N,N'-o-Phenylen-bis(salicylideniminato)UO2(EtOH)]'.
Dies ist ein Urankomplex, der durch einen Diamin-bis(phenolat)-Liganden
charakterisiert wird.
-
Die
Publikation DATABASE CROSSFIRE BEILSTEIN [Online] Beilstein Institut
zur Förderung
der Chemischen Wissenschaften, Frankfurt am Main, DE; 26. Februar
1991 (1991-02-26) Datenbankzugang Nr. 3869282 (BRN) XP002270891
offenbart einen Kupfermetallkomplex, der als N,N'-Bis-(2-hydroxy-α-ureido-benzyl)harnstoff-Kupfer-(II)-Verbindung
mit einem Liganden eines Harnstoffderivats bezeichnet wird. Die zwei
zentralen Stickstoffe, die an die Carbonyleinheit gebunden sind,
binden nicht notwendigerweise an das Metall, um einen Metallkomplex
zu bilden.
-
Kürzlich offenbarten
die vorliegenden Erfinder in US-A-6,333,423, eingereicht am 20. September 1999,
einen Nicht-Metallocen
Präkatalysator
von äußerst hoher
Aktivität,
der einen Amindiphenolatkomplex beinhaltet, und ein entsprechendes
Verfahren zur katalytischen Polymerisation von Alpha-Olefinmonomeren unter
Verwendung dieses Präkatalysators.
Es werden jedoch nur ataktische Polymere unter Verwendung des offenbarten
Präkatalysators
unter den aufgezeigten Polymersiationsbedingungen erhalten.
-
In
Hinblick auf die oben diskutierten Beschränkungen für die Polymerisation von Alpha-Olefinen,
gibt es somit einen Bedarf für
einen Durchschnittsfachmann und wäre es äußerst vorteilhaft einen aktiven
nicht-Metallocen Präkatalysator
und ein entsprechendes Verfahren zur katalytischen Polymerisation
von Alpha-Olefinmonomeren zu haben, der/das nicht auf die Aktivierung
durch große
Mengen eines Cokatalysators, wie zum Beispiel MAO, beschränkt ist
und ebenfalls durch eine hohe Stabilität charakterisiert ist, schnell
erhalten oder synthetisiert werden kann, und verschiedene Arten
und eine Vielzahl von Poly(Alpha-Olefin)-Produkte mit einem hohen
Molekulargewicht und einer niedrigen Molekulargewichtsverteilung
herstellen kann und einen kontrollierbaren und klassifizierbaren
Grad an Polymertaktizität
hat. Außerdem
gibt es einen Bedarf für
einen solchen Präkatalysator
und von Verfahren zur Herstellung von Alpha-Olefinpolymeren mit
Ausnahme von Polyethylenen und Polypropylenen, der/das industriell
einsetzbare Eigenschaften und Charakteristika hat.
-
Zusammenfassung
der Erfindung
-
Die
vorliegende Erfindung betrifft im Allgemeinen die katalytische Polymerisation
und im Besonderen die taktische katalytische Polymerisation von
Alpha-Olefinmonomeren unter Verwendung eines aktiven nicht-Metallocen
Präkatalysators,
der einen Diamindiphenolatkomplex aufweist. Außerdem weist die vorliegende
Erfindung ein allgemeines Verfahren für die katalytische Polymerisation,
einschließlich
eines besonderen Verfahrens für
die taktische katalytische Polymerisation von Alpha-Olefinpolymeren
unter Verwendung des offenbarten Diamindiphenolatpräkatalysators
auf.
-
Es
ist deshalb ein Gegenstand der vorliegenden Erfindung allgemeine
Strukturen und allgemeine Formeln eines aktiven nicht-Metallocen
Präkatalysators
im Allgemeinen für
die katalytische Polymerisation und insbesondere für die taktische
katalytische Polymerisation von Alpha-Olefinpolymeren bereitzustellen.
-
Es
ist weiter ein Gegenstand der vorliegenden Erfindung allgemeine
Strukturen und allgemeine Formeln eines aktiven nicht-Metallocen
Präkatalysators
im Allgemeinen für
die katalytische Polymerisation und im Besonderen für die taktische
katalytische Polymerisation von Alpha-Olefinpolymeren bereitzustellen, wobei der
Präkatalysator
ein Diamindiphenolatkomplex ist, der die Variabilität des Metallatoms,
der Liganden, der aromatischen Gruppen, der Substituenten der aromatischen
Gruppe, einer verbrückenden
Gruppe und von Substituenten einer verbrückenden Gruppe aufweist.
-
Es
ist ein anderer Gegenstand der vorliegenden Erfindung ein Verfahren
im Allgemeinen für
die katalytische Polymerisation und im Besonderen für die taktische
katalytische Polymerisation von Alpha-Olefinpolymeren bereitzustellen,
dass die Verwendung eines aktiven Diamindiphenolatpräkatalysators
aufweist, wobei der Präkatalysator
die Variabilität
des Metallatoms, der Liganden, der aromatischen Gruppen, der Substituenten
der aromatischen Gruppe, einer verbrückenden Gruppe und von Substituenten
der verbrückenden
Gruppe aufweist.
-
Es
ist ein anderer Gegenstand der vorliegenden Erfindung ein Verfahren
für die
katalytische Polymerisation einschließlich taktischer katalytischer
Polymerisation von Alpha-Olefinpolymeren
bereitzustellen, das die Verwendung eines aktiven Diamindiphenolatkomplexes
aufweist, wobei das Polymerisationsverfahren im Wesentlichen ein
lebendes System ist.
-
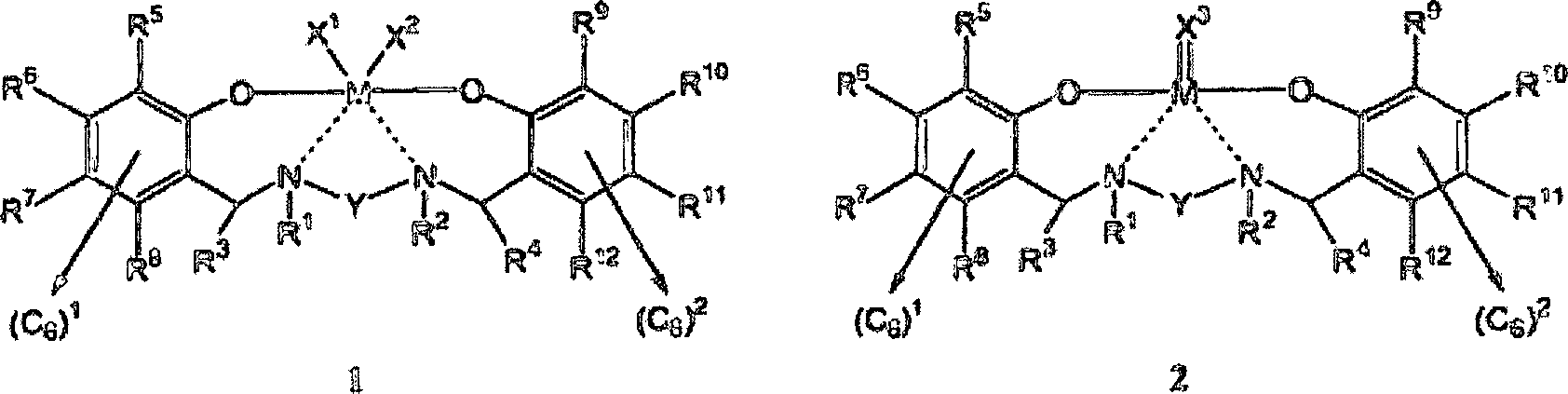
Somit
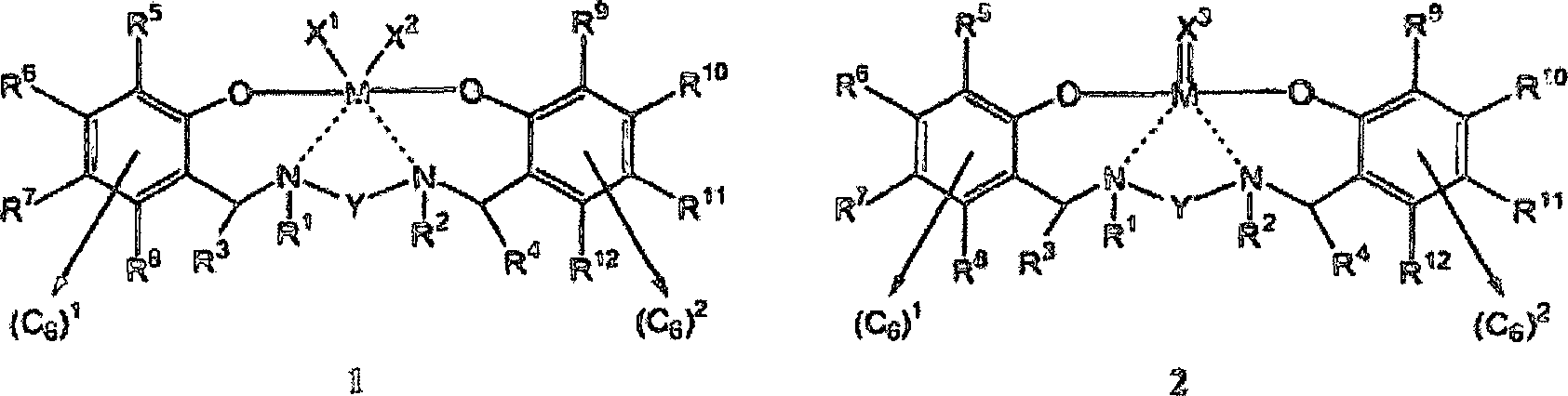
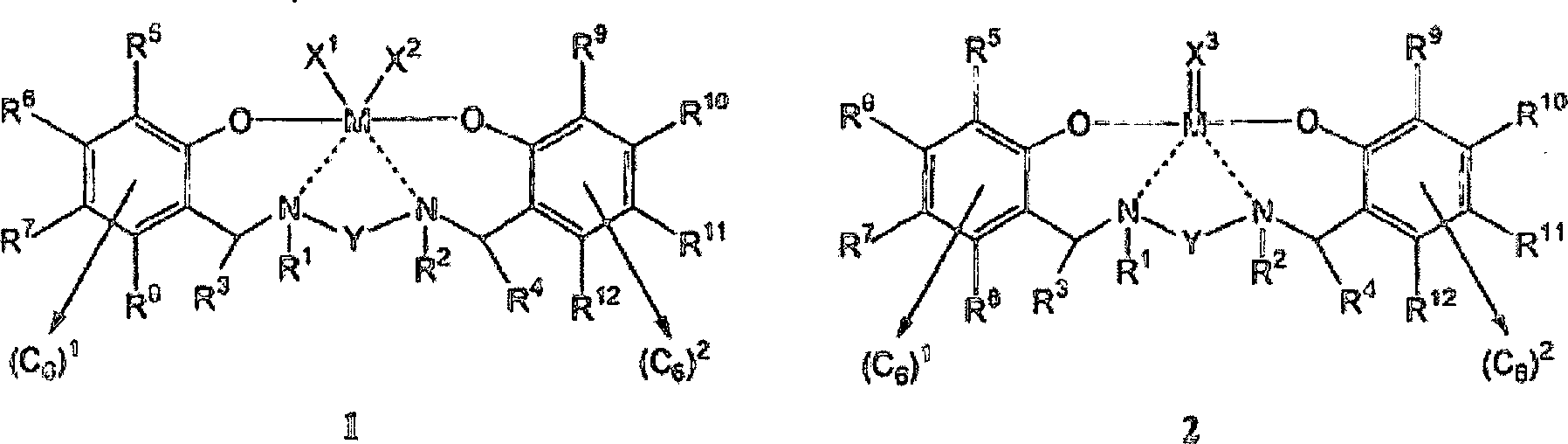
wird gemäß der vorliegenden
Erfindung eine Verbindung mit einer allgemeinen Struktur, die aus der
Gruppe, die aus Struktur 1 und Struktur 2 besteht, ausgewählt wird,
bereitgestellt:
worin
in jeder Struktur 1 und Struktur 2: jede einzelne durchgezogene
Linie eine kovalente Bindung darstellt; jede doppelte durchgezogene
Linie eine Bindung mit variierenden Graden der Kovalenz darstellt;
jede gestrichelte Linie eine Bindung mit einem variierenden Grad
an Kovalenz und einem variierenden Grad der Koordination darstellt;
M ein Metallatom ist, das an jedes O Sauerstoffatom kovalent gebunden
ist und mit variierenden Graden der Kovalenz und Koordination an
jedes N Stickstoffatom gebunden ist; X
1 und
X
2 jeweils ein univalenter anionischer Ligand
ist, der an das Metallatom kovalent gebunden ist; X
3 ein
einzelner anionischer Ligand ist, der an das Metallatom kovalent
gebunden ist; R
1 und R
2 jeweils
ein univalenter Radikal ist, der an ein unterschiedliches der N
Stickstoffatome kovalent gebunden ist; R
3 ein
univalenter Radikal ist, der an das C-Kohlenstoffatom des -CHR
3-
der (C
6)
1-CHR
3-N-Verknüpfungs-Einheit kovalent
gebunden ist; R
4 ein univalenter Radikal
ist, der an das C-Kohlenstoffatom des -CHR
4-
der -N-CHR
4-(C
6)
2-Verknüpfungs-Einheit
kovalent gebunden ist; jedes R
5 bis R
8 ein univalenter Radikal ist, der an ein
unterschiedliches der C-Kohlenstoffatome der ersten aromatischen
Gruppe (C
6)
1 kovalent
gebunden ist; jedes R
9 bis R
12 ein
univalenter Radikal ist, der an ein unterschiedliches der C-Kohlenstoffatome
der zweiten aromatischen Gruppe (C
6)
2 kovalent gebunden ist; und Y ein divalenter
Radikal ist, der an beide der IV Stickstoffatome kovalent gebunden
ist und zwischen ihnen verknüpft.
-
Gemäß eines
anderen Aspekts der vorliegenden Erfindung wird eine Verbindung
einer allgemeinen Formel bereitgestellt, die aus der Gruppe, die
aus: [{OR5R6R7R8(C6)1(CHR3)NR1YNR2(CHR4)(C6)2R9R10R11R12O}MX1X2]
und [{OR5R6R7R8(C6)1(CHR3)NR1YNR2(CHR4)(C6)2R9R10R11R12O}MX3] besteht,
ausgewählt
wird, wobei in jeder allgemeinen Formel: M ein Metallatom ist, das
an jedes O Sauerstoffatom kovalent gebunden ist und mit variierenden
Graden der Kovalenz und Koordination an jedes N Stickstoffatom gebunden
ist; X1 und X2 jeweils
ein univalenter anionischer Ligand ist, der an das Metallatom kovalent
gebunden ist; X3 ein einzelner anionischer Ligand
ist, der an das Metallatom kovalent gebunden ist; R1 und
R2 jeweils ein univalenter Radikal ist,
der an ein unterschiedliches der N Stickstoffatome kovalent gebunden
ist; R3 ein univalenter Radikal ist, der
an das C-Kohlenstoffatom
des -CHR3- der (C6)1-CHR3-N-Verknüpfungs-Einheit kovalent
gebunden ist; R4 ein univalenter Radikal
ist, der an das C-Kohlenstoffatom des -CHR4-
der -N-CHR4-(C6)2-Verknüpfungs-Einheit
kovalent gebunden ist; jedes R5 bis R8 ein univalenter Radikal ist, der an ein
unterschiedliches der C-Kohlenstoffatome der ersten aromatischen
Gruppe (C6)1 kovalent
gebunden ist; jedes R9 bis R12 ein
univalenter Radikal ist, der an ein unterschiedliches der C-Kohlenstoffatome
der zweiten aromatischen Gruppe (C6)2 kovalent gebunden ist; und Y ein divalenter
Radikal ist, der an beide der N Stickstoffatome kovalent gebunden
ist und zwischen ihnen verknüpft.
-
Gemäß eines
anderen Aspekts der vorliegenden Erfindung wird ein Verfahren zur
katalytischen Polymerisation eines Alpha-Olefinmonomers bereitgestellt, wobei
das Verfahren die Schritte umfasst:
(a) Bereitstellen eines
Diamindiphenolat-Präkatalysators
mit einer allgemeinen Struktur, die aus der Gruppe, die aus
besteht,
ausgewählt
wird, wobei in jeder Struktur 1 und Struktur 2: jede einzelne durchgezogene
Linie eine kovalente Bindung darstellt; jede doppelt durchgezogene
Linie eine Bindung mit variierenden Graden der Kovalenz darstellt;
jede gestrichelte Linie eine Bindung mit einem variierenden Grad
der Kovalenz und einem variierenden Grad der Koordination darstellt;
M ein Metallatom ist, das an jedes O Sauerstoffatom kovalent gebunden
ist und mit variierenden Graden der Kovalenz und Koordination an
jedes N Stickstoffatom gebunden ist; X
1 und
X
2 jeweils ein univalenter anionischer Ligand
ist, der an das Metallatom kovalent gebunden ist; X
3 ein einzelner
anionischer Ligand ist, der an das Metallatom kovalent gebunden
ist; R
1 und R
2 jeweils
ein univalenter Radikal ist, der an ein unterschiedliches der N
Stickstoffatome kovalent gebunden ist; R
3 ein
univalenter Radikal ist, der an das C Kohlenstoffatom des -CHR
3- der (C
6)
1-CHR
3-N-Verknüpfungs-Einheit kovalent
gebunden ist; R
4 ein univalenter Radikal
ist, der an das C Kohlenstoffatom des -CHR
4-
der -N-CHR
4-(C
6)
2-Verknüpfungs-Einheit
kovalent gebunden ist; jedes R
5 bis R
8 ein univalenter Radikal ist, der an ein
unterschiedliches der C-Kohlenstoffatome der ersten aromatischen
Gruppe (C
6)
1 kovalent
gebunden ist; jedes R
9 bis R
12 ein
univalenter Radikal ist, der an ein unterschiedliches der C-Kohlenstoffatome
der zweiten aromatischen Gruppe (C
6)
2 kovalent gebunden ist; und Y ein divalenter
Radikal ist, der an beide der N Stickstoffatome kovalent gebunden
ist und zwischen ihnen verknüpft;
(b) Herstellen einer ersten chemischen Einheit, die eine bestimmte Form
des Präkatalysators
aus Schritt (a) aufweist; (c) Bereitstellen eines Cokatalysators,
der zum Aktivieren des Präkatalysators
aus Schritt (a) geeignet ist; (d) Herstellen einer zweiten chemischen
Einheit, die den Cokatalysator aus Schritt (c) aufweist; (e) Bilden
eines katalytischen Polymerisationsreaktionssystems für die katalytische
Polymerisation des Alpha-Olefinmonomers durch Mischen der ersten
chemischen Einheit, die den Präkatalysator
aufweist, mit der zweiten chemischen Einheit, die den Cokatalysator
aufweist, mit dem zu polymerisierenden Alpha-Olefinmonomer, wobei
der Cokatalysator den Präkatalysator
zu einem Katalysator aktiviert, der die katalytische Polymerisation
des Alpha-Olefinmonomers zum Herstellen wenigstens einer Art eines
Poly(alpha-Olefin)produkts bewirkt; (f) Beenden der katalytischen
Polymerisation des Alpha-Olefinmonomers; und (g) Isolieren der wenigstens
einen Art des Poly(alpha-Olefin)produkts.
-
Gemäß eines
anderen Aspekts der vorliegenden Erfindung wird ein Verfahren zur
katalytische Polymerisation eines Alpha-Olefinmonomers bereitgestellt, wobei
das Verfahren die Schritte umfasst:
(a) Bereitstellen eines
Diamindiphenolat-Katalysators mit einer allgemeinen Struktur, die
aus der Gruppe, die aus
besteht,
ausgewählt
wird, wobei in jeder Struktur 1 und Struktur 2: jede einzelne durchgezogene
Linie eine kovalente Bindung darstellt; jede doppelt durchgezogene
Linie eine Bindung mit variierenden Graden der Kovalenz darstellt;
jede gestrichelte Linie eine Bindung mit einem variierenden Grad
der Kovalenz und einem variierenden Grad der Koordination darstellt;
M ein Metallatom ist, das an jedes O Sauerstoffatom kovalent gebunden
ist und mit variierenden Graden der Kovalenz und Koordination an
jedes N Stickstoffatom gebunden ist; X
1 und
X
2 jeweils ein univalenter anionischer Ligand
ist, der an das Metallatom kovalent gebunden ist; X
3 ein einzelner
anionischer Ligand ist, der an das Metallatom kovalent gebunden
ist; R
1 und R
2 jeweils
ein univalenter Radikal ist, der an ein unterschiedliches der IV
Stickstoffatome kovalent gebunden ist; R
3 ein
univalenter Radikal ist, der an das C Kohlenstoffatom des -CHR
3- der (C
6)
1-CHR
3-N-Verknüpfungs-Einheit kovalent
gebunden ist; R
4 ein univalenter Radikal
ist, das an das C Kohlenstoffatom des -CHR
4-
der -N-CHR
4-(C
6)
2-Verknüpfungs-Einheit
kovalent gebunden ist; jedes R
5 bis R
8 ein univalenter Radikal ist, der an ein
unterschiedliches der C Kohlenstoffatome der ersten aromatischen
Gruppe (C
6)
1 kovalent
gebunden ist; jedes R
9 bis R
12 ein
univalenter Radikal ist, der an ein unterschiedliches der C-Kohlenstoffatome
der zweiten aromatischen Gruppe (C
6)
2 kovalent gebunden ist; und Y ein divalenter
Radikal ist, der an beide der N Stickstoffatome kovalent gebunden
ist und zwischen ihnen verknüpft;
(b) Herstellen einer ersten chemischen Einheit, die eine bestimmte Form
des Katalysators aus Schritt (a) aufweist; (c) Bilden eines katalytischen
Polymerisationsreaktionssystems für die katalytische Polymerisation
des Alpha-Olefinmonomers durch Mischen der ersten chemischen Einheit,
die den Katalysator aufweist, mit dem zu polymerisierenden Alpha-Olefinmonomer,
wobei der Katalysator die katalytische Polymerisation des Alpha-Olefinmonomers zum
Herstellen wenigstens einer Art eines Poly(alpha-Olefin)produkts
bewirkt; (d) Beenden der katalytischen Polymerisation des Alpha-Olefinmonomers; und
(e) Isolieren der wenigstens einen Art des Poly(alpha-Olefin)produkts.
-
Gemäß eines
anderen Aspekts der vorliegenden Erfindung wird ein Verfahren für die isotaktische
und lebende katalytische Polymerisation eines 1-Hexen-Monomers zur
Bildung eines isotaktischen Poly(1-hexen)-Produkts bereitgestellt,
wobei das Verfahren die Schritte umfasst:
(a) Bereitstellen
eines Diamindiphenolat-Präkatalysators
[{N,N'-Bis(3,5-di-tert-butyl-2-hydroxyphenylmethyl)-N,N'-dimethylethylendiamin}zirkoniumdibenzyl];
(b) Herstellen einer ersten chemischen Einheit, die den Diamindiphenolat-Präkatalysator
aus Schritt (a) aufweist; (c) Bereitstellen eines Bor-Lewis-Säure Cokatalysators
[B(C6F5)3], der zum Aktivieren des Präkatalysators
aus Schritt (a) geeignet ist; (d) Herstellen einer zweiten chemischen
Einheit, die den Bor-Lewis-Säure Cokatalysator
aus Schritt (c) aufweist; (e) Bilden eines isotaktischen und lebenden
katalytischen Polymerisationsreaktionssystems für die isotaktische und lebende
katalytische Polymerisation des 1-Hexenmonomers durch Mischen der
ersten chemischen Einheit, die den Präkatalysator aufweist, mit der
zweiten chemischen Einheit, die den Cokatalysator aufweist, mit
dem zu polymerisierenden 1-Hexenmonomer,
wobei der Cokatalysator den Präkatalysator
zu einem Katalysator aktiviert, der die isotaktische und lebende
katalytische Polymerisation des 1-Hexenmonomers zum Herstellen des
isotaktischen Poly(1-hexen)produkts bewirkt; (f) Beenden der katalytischen
Polymerisation des 1-Hexenmonomers;
und (g) Isolieren des isotaktischen Poly(1-hexen)produkts.
-
Die
vorliegende Erfindung führt
mehrere Vorzüge
in das Gebiet der katalytischen Polymerisation von Alpha-Olefinmonomeren
ein, welche bis jetzt unerreichbar waren. Zum Beispiel ermöglichen
bestimmte Formen des Diamindiphenolat-Präkatalysators
der vorliegenden Erfindung, wenn durch einen Cokatalysator unter milden
Reaktionsbedingungen aktiviert, das Erreichen einer isotaktischen
(isospezifischen) Polymerisation einer Vielzahl von Alpha-Olefinmonomeren,
wie zum Beispiel die Polymerisation von langkettigen Alpha-Olefinmonomeren,
zum Beispiel 1-Hexen oder 1-Okten, zur Bildung einer Vielzahl von
Poly(Alpha-Olefin)-Produkten, wie zum Beispiel Poly(1-hexen) oder
Poly(1-okten) mit hohem Molekulargewicht und einer niedrigen Molekulargewichtsverteilung.
Außerdem
können
diese katalytischen Systeme zusätzlich
als lebend bezeichnet werden. Des Weiteren können diese isotaktischen und
lebenden katalytischen Polymerisationssysteme bei praktischen kommerziellen
Reaktionsbedingungen, einschließlich
insbesondere dem Arbeiten bei Raumtemperatur, ausgeführt werden.
-
Der
Diamindiphenolatpräkatalysator
der vorliegenden Erfindung ist unter kommerziell anwendbaren Bedingungen
für Polymerisation
von Alpha-Olefinmonomeren relativ stabil. Außerdem ist der Präkatalysator und
verwandte Formen des Präkatalysators
der vorliegenden Erfindung relativ einfach zu synthetisieren, hauptsächlich aufgrund
einfacher Synthesen der entsprechenden Diamin-di(2-hydroxyarylmethyl)-Ligandprecursor aus
einer Vielzahl kommerziell erhältlicher
billiger Anfangsmaterialien, verglichen zu Synthesen von Präkatalysatoren
vom Metallocentyp.
-
Kurze Beschreibung
der Zeichnungen
-
Die
Erfindung ist hier mit Bezugnahme auf die beigefügten Zeichnungen nur beispielhaft
beschrieben, wobei:
-
1 eine
Darstellung einer Röntgenstruktur
eines sechsfach koordinierten Dialkyldiamindiphenolatpräkatalysators
[{N,N'-Bis(3,5-di-tert-butyl-2-hydroxyphenylmethyl)-N,N'-dimethylethylendiamin}zirkoniumdibenzyl]
16 ist;
-
2 eine
Darstellung des 13C NMR Spektrums des isotaktischen
Poly(1-hexen)-Produkts ist, dass in Übereinstimmung mit der vorliegenden
Erfindung durch katalytische Polymerisation eines 1-Hexenmonomers unter
Verwendung des Dialkyldiamindiphenolatpräkatalysators [{N,N'-Bis(3,5-di-tert-butyl-2-hydroxyphenylmethyl)-N,N'-dimethylethylendiamin}zirkoniumdibenzyl]
16 ist;
-
3 eine
Darstellung der Abhängigkeit
des massegemittelten Molekulargewichts Mw von
Poly(1-hexen) ist, das durch katalytische Polymerisation eines 1-Hexenmonomers
unter Verwendung des Dialkyldiamindiphenolatpräkatalysators [{N,N'- Bis(3,5-di-tert-butyl-2-hydroxyphenylmethyl)-N,N'-dimethylethylendiamin}zirkoniumdibenzyl]
16 durch Verbrauch des 1-Hexenmonomers erhalten wird;
-
4 eine
Darstellung des 13C NMR Spektrums des ataktischen
Poly(1-hexens) ist, dass durch katalytische Polymerisation eines
1-Hexenmonomers unter Verwendung des Dialkyldiamindiphenolatpräkatalysators
[{N,N'-Bis(3,5-dimethyl-2-hydroxyphenylmethyl)-N,N'-dimethylethylendiamin}zirkoniumdibenzyl]
17 erhalten wird.
-
Beschreibung
der bevorzugten Ausführungsformen
-
Die
vorliegende Erfindung betrifft im Allgemeinen die katalytische Polymerisation
und im Besonderen die taktische katalytische Polymerisation von
Alpha-Olefinmonomeren unter Verwendung eines aktiven nicht-Metallocen
Präkatalysators,
der einen Diamindiphenolatkomplex aufweist, und ein entsprechendes
Verfahren, das den offenbarten Präkatalysator verwendet. Der
Diamindiphenolatpräkatalysator
der vorliegenden Erfindung ist, wenn durch einen Cokatalysator unter
milden Reaktionsbedingungen aktiviert, für isotaktische (isospezifische)
und lebende Polymerisation einer Vielzahl von Alpha-Olefinmonomeren
aktiv. Der Diamindiphenolatpräkatalysator
polymerisiert langkettige Alpha-Olefinmonomere, wie zum Beispiel
1-Hexen oder 1-Okten, zur Bildung einer Vielzahl von Poly(Alpha-Olefin)-Produkten,
wie zum Beispiel Poly(1-hexen) oder Poly(1-Okten) mit einem klassifizierbaren
Ausmaß oder
Grad an Taktizität,
hohem Molekulargewicht und niedriger Molekulargewichtsverteilung.
Der Diamindiphenolatpräkatalysator
ist unter kommerziell anwendbaren Bedingungen für die Polymerisation von Alpha-Olefinmonomeren relativ
stabil. Außerdem
ist dieser Präkatalysator
relativ einfach zu synthetisieren, und ist verglichen mit Präkatalysatoren
vom Metallocentyp, die momentan verwendet werden, besser erhältlich.
-
Es
ist verständlich,
dass die Erfindung in ihrer Anwendung in Bezug auf die Details der
beispielhaften bevorzugten Ausführungsformen
der chemischen Strukturen, Formeln und Verfahren, die in der folgenden
Beschreibung, Zeichnungen oder Beispielen dargelegt sind, nicht
beschränkt
ist. Die Erfindung ist für
andere Ausführungsformen
geeignet oder kann auf verschiedene Art und Weisen praktiziert oder
durchgeführt
werden. Es sollte ebenfalls verständlich sein, dass die hier
verwendete Ausdrucksweise und Terminologie zum Zweck der Beschreibung
dienen und nicht als beschränkend
angesehen werden sollten.
-
Der
Diamindiphenolatpräkatalysator
und das entsprechende Verfahren zur Verwendung dieses Präkatalysators
für die
katalytische Polymerisation von Alpha-Olefinmonomeren der vorliegenden
Erfindung sind hier zum ersten Mal offenbart und sind nicht durch
den nicht-Metallocen Präkatalysator
mit äußerst großer Aktivität, der einen
Amindiphenolatkomplex aufweist, und entsprechender Verfahren zur
Verwendung dieses Präkatalysators
für die
katalytische Polymerisation von Alpha-Olefinmonomeren, wie in US-A-6,333,423,
eingereicht am 20. September 1999 von Kol et al. offenbart, offensichtlich
und auch nicht vorweggenommen. Außerdem ist der Diamindiphenolatpräkatalysator
der vorliegenden Erfindung nicht offensichtlich und auch nicht durch
irgendeine der Amindiphenolatligandprecursor, die zuvor in US-A-6,333,423
offenbart wurden, vorweggenommen.
-
Des
Weiteren sind die Diamindiphenolatligandprecursor, die für die Synthese
des Präkatalysators
der vorliegenden Erfindung verwendet werden, entweder neu oder sind
aus dem Stand der Technik bekannt, aber werden durch neue Verfahren
synthetisiert und werden nicht unter Verwendung irgendwelcher Amindiphenolatligandprecursor,
die zuvor in US-A-6,333,423 offenbart wurde, synthetisiert.
-
Allgemeine
Strukturen und Formeln des Diamindiphenolatpräkatalysators
-
Die
bevorzugte Ausführungsform
des Diamindiphenolatpräkatalysators
der vorliegenden Erfindung ist entweder die allgemeine Struktur
1 oder die allgemeine Struktur 2:
wobei
eine einzelne durchgezogene Linie eine kovalente Bindung darstellt,
eine doppelt durchgezogene Linie eine Bindung mit variierenden Graden
der Kovalenz darstellt und eine gestrichelte Linie eine koordinative
Bindung zwischen den angezeigten Atomen darstellt; M ein Metallatom
ist, das an jedes O Sauerstoffatom kovalent gebunden ist und koordinativ
an jedes Stickstoffatom N gebunden ist, wie in den Strukturen 1
und 2 durch die gestrichelte Linie zwischen dem Metallatom M und
dem Stickstoffatom N gezeigt, wobei M eine Übergangsmetallatomzusammensetzung
darstellt, bevorzugt, aber nicht darauf beschränkt, ein einzelnes Übergangsmetallatom,
das aus der Gruppe, die aus Zirkonium, Hafnium, Titan und einem
Lanthanid besteht, ausgewählt wird;
X
1 und X
2 (Struktur
1) jeweils ein univalenter anionischer Ligand ist, der an das Metallatom
M kovalent gebunden ist, wie zum Beispiel ein Halogenid, ein Hydrid,
ein gesättigtes
oder ungesättigtes
Hydrocarbyl, ein Alkoxid, ein Aryloxid, ein Dialkylamid oder ein
Arylamid; X
3 (Struktur 2) ein einzelner
univalenter oder divalenter anionischer Ligand ist, der kovalent
an das Metallatom M entweder durch eine Einfachbindung oder eine
Doppelbindung gebunden ist, wie zum Beispiel ein cyclometalliertes
Hydrocarbyl oder ein Radikal, wie zum Beispiel ein Alkyl oder ein
Alkyliden; R
1 und R
2 jeweils
ein univalenter Radikal ist, der kovalent an ein unterschiedliches
der beiden Stickstoffatome N gebunden ist, wie zum Beispiel Wasserstoff,
Hydrocarbyl oder jeder andere univalente Radikal, wie zum Beispiel
Trimethylsilyl; R
3 ein univalenter Radikal
ist, der kovalent an das Kohlenstoffatom des -CHR
3-
der (C
6)
1-CHR
3-N-Verknüpfungseinheit
gebunden ist, wie zum Beispiel ein Wasserstoff, ein Hydrocarbyl
oder irgendein anderer univalenter Radikal, wie zum Beispiel ein
Benzyl; R
4 ein univalenter Radikal ist,
der kovalent an das Kohlenstoffatom des -CHR
4-
der -N-CHR
4-(C
6)
2 Verbrückungseinheit
gebunden ist, wie zum Beispiel ein Wasserstoff, ein Hydrocarbyl
oder irgendein anderer univalenter Radikal, wie zum Beispiel Benzyl;
R
5 bis R
8 jeweils
ein univalenter Radikal ist, der kovalent an ein unterschiedliches
Kohlenstoffatom in der ersten aromatischen Gruppe (C
6)
1 gebunden ist, wie zum Beispiel ein Wasserstoff,
ein Hydrocarbyl oder irgendein anderer univalenter Radikal, wie
zum Beispiel ein Alkoxid; R
9 bis R
12 jeweils ein univalenter Radikal ist, der
kovalent an ein unterschiedliches Kohlenstoffatom in der zweiten
aromatischen Gruppe (C
6)
2 gebunden
ist, wie zum Beispiel ein Wasserstoff, ein Hydrocarbyl oder irgendein
anderer univalenter Radikal, wie zum Beispiel ein Alkoxid; und Y
ein divalenter Radikal ist, der kovalent an die zwei Stickstoffatome N
gebunden ist und zwischen diesen verbrückt, wie zum Beispiel ein Dihydrocarbyl
oder irgendein anderer divalenter Radikal, wie zum Beispiel ein
Cycloalkandiyl.
-
Die
allgemeinen Formeln, die den allgemeinen Strukturen 1 und 2 des
Diamindiphenolatpräkatalysators
der vorliegenden Erfindung entsprechen, sind wie folgt: [{OR5R6R7R8(C6)1(CHR3)NR1YNR2(CHR4)(C6)2R9R10R11R12O}MX1X2]
bzw. [{OR5R6R7R8(C6)1(CHR3)NR1YNR2(CHR4)(C6)2R9R10R11R12O}MX3].
-
Entsprechend
zu den zuvor veranschaulichten und beschriebenen allgemeinen Strukturen
1 und 2 des Präkatalysators
der vorliegenden Erfindung ist M hier ein Metallatom, das kovalent
an jedes Sauerstoffatom O gebunden ist und koordinativ an jedes
Stickstoffatom N gebunden ist, wie in den allgemeinen Strukturen
1 und 2 durch die gestrichelte Linie zwischen dem Metallatom M und
jedem Stickstoffatom N gezeigt, wobei M eine Übergangsmetallatomzusammensetzung
aufweist, bevorzugt, aber nicht darauf beschränkt, ein einzelnes Übergangsmetallatom,
das aus der Gruppe, die aus Zirkonium, Hafnium, Titan und einem
Lanthanid besteht, ausgewählt
wird; X1 und X2 (Struktur
1) sind jeweils ein univalenter anionischer Ligand, der kovalent
an das Metallatom M gebunden ist, wie zum Beispiel ein Halogenid,
ein Hydrid, ein gesättigtes
oder ungesättigtes
Hydrocarbyl, ein Alkoxid, ein Aryloxid, ein Dialkylamid oder ein
Arylamid; X3 (Struktur 2) ist ein einzelner
univalenter oder ein divalenter anionischer Ligand, der kovalent
an das Metallatom M entweder durch eine Einfachbindung oder eine
Doppelbindung gebunden ist, wie zum Beispiel ein cyclometalliertes
Hydrocarbyl oder ein Radikal, wie zum Beispiel ein Alkyl oder ein
Alkyliden; R1 und R2 jeweils
ein univalenter Radikal ist, der kovalent an ein anderes der zwei
Stickstoffatome N gebunden ist, wie zum Beispiel ein Wasserstoff,
Hydrocarbyl oder irgendein anderer univalenter Radikal, wie zum
Beispiel ein Trimethylsilyl; R3 ist ein
univalenter Radikal, der kovalent an das Kohlenstoffatom des -CHR3- der (C6)1-CHR3-N-Verbrückungseinheit
gebunden ist, wie zum Beispiel ein Wasserstoff, ein Hydrocarbyl
oder irgendein anderer univalenter Radikal, wie zum Beispiel ein Benzyl;
R4 ist ein univalenter Radikal, der kovalent
an das Kohlenstoffatom des -CHR4- der -N-CHR4-(C6)2 Verbrückungseinheit
gebunden ist, wie zum Beispiel ein Wasserstoff, ein Hydrocarbyl
oder irgendein anderer univalenter Radikal, wie zum Beispiel ein
Benzyl; R5 bis R8 ist
jeweils ein univalenter Radikal, der kovalent an ein unterschiedliches
Kohlenstoffatom in der ersten aromatischen Gruppe (C6)1 gebunden ist, wie zum Beispiel ein Wasserstoff,
ein Hydrocarbyl oder irgendein anderer univalenter Radikal, wie
zum Beispiel ein Alkoxid; R9 bis R12 ist jeweils ein univalenter Radikal, der
kovalent an ein unterschiedliches Kohlenstoffatom in der zweiten aromatischen
Gruppe (C6)2 gebunden
ist, wie zum Beispiel ein Wasserstoff, ein Hydrocarbyl oder irgendein
anderer univalenter Radikal, wie zum Beispiel ein Alkoxid; und Y
ist ein divalenter Radikal, der kovalent an die zwei Stickstoffatome
N gebunden ist und diese verbrückt,
wie zum Beispiel ein Dihydrocarbyl oder irgendein anderer divalenter
Radikal, wie zum Beispiel ein Cycloalkandiyl.
-
Synthese eines allgemeinen
Diamindi(2-yydroxarylmethyl)-Ligandprecursors
-
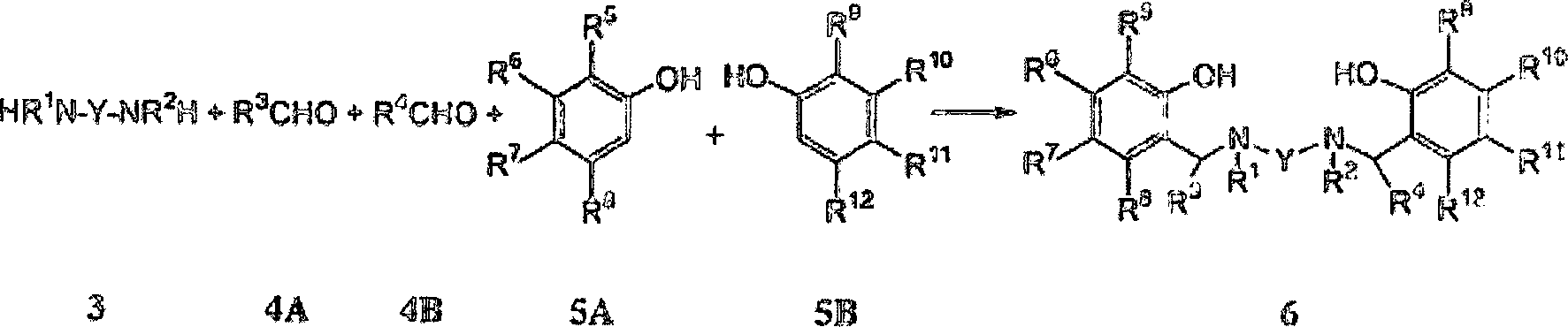
Die
Synthese von unterschiedlichen aber verbundenen besonderen Formen
des allgemeinen Ligandprecursors Diamindi(2-hydroxarylmethyl) 6,
wird unten beschrieben, welcher dann für die Synthese unterschiedlicher,
aber verbundener besonderer Formen des Diamindiphenolatpräkatalysators
der vorliegenden Erfindung, der mit den Strukturen 1 und 2 und den
davon korrespondierenden Formeln übereinstimmt, verwendet wird.
Diamin 3, das aus der Gruppe, die aus einem N,N'-Di-primären Amin, einem N,N'-Di-sekundären Amin und
einem N-primären-N'-sekundären Diamin
besteht, ausgewählt
wird, reagiert mit Aldehyden 4A und 4B und den substituierten Phenolen
5A und 5B durch eine modifizierte Mannich-Reaktion unter variablen
Reaktionsbedingungen in variablen Lösungsmitteln, wie zum Beispiel
Methanol und Ethanol, um verschiedene besondere Formen des allgemeinen
Ligandprecursors 6 zu ergeben.
-
-
Die
Struktur des allgemeinen Diamindi(2-hydroxarylmethyl)-Ligandprecursors
6 weist zwei Hydroxarylringe auf, wobei die Hydroxarylringe eine
Vielzahl von Substituenten R5 bis R12 beinhalten. Die Substituenten R5 bis R8 sind jeweils
ein univalenter Radikal, der an den ersten Hydroxarylring kovalent
gebunden ist, wie zum Beispiel ein Wasserstoff, ein Hydrocarbyl
oder irgendein anderer univalenter Radikal, wie zum Beispiel ein
Alkoxid, und die Substituenten R9 bis R12 sind jeweils ein univalenter Radikal,
der kovalent an den zweiten Hydroxarylring gebunden ist, wie zum
Beispiel ein Wasserstoff, ein Hydrocarbyl oder irgendein anderer
univalenter Radikal, wie zum Beispiel ein Alkoxid.
-
Die
zwei Hydroxarylringe werden durch eine Verknüpfungseinheit -CHR3-NR1-Y-NR2-CHR4- verbrückt, wobei
wie oben beschrieben R1 und R2 jeweils
ein univalenter Radikal ist, der kovalent an eines der beiden Stickstoffatome
N gebunden ist, wie zum Beispiel ein Wasserstoff, ein Hydrocarbyl
oder irgendein anderer univalenter Radikal, wie zum Beispiel ein
Alkoxid; R3 ein univalenter Radikal ist,
der kovalent an das Kohlenstoffatom des -CHR3-
der (C6)1-CHR3-N Verbrückungseinheit
gebunden ist, wie zum Beispiel ein Wasserstoff, ein Hydrocarbyl
oder irgendein anderer univalenter Radikal, wie zum Beispiel ein
Benzyl; R4 ein univalenter Radikal ist,
der kovalent an das Kohlenstoffatom des -CHR4-
der -N-CHR4-(C6)2 Verbrückungseinheit
gebunden ist, wie zum Beispiel ein Wasserstoff, ein Hydrocarbyl
oder irgendein anderer univalenter Radikal, wie zum Beispiel ein
Benzyl; und Y ein divalenter Radikal ist, der kovalent an die zwei
Stickstoffatome N gebunden ist und diese verbrückt, wie zum Beispiel ein Dihydrocarbyl
oder irgendein anderer divalenter Radikal, wie zum Beispiel ein
Cycloalkandiyl.
-
Die
Synthesen von acht beispielhaften oder besonderen Formen des allgemeinen
Diamindi(2-hydroxarylmethyl)-Ligandprecursors 6 der vorliegenden
Erfindung sind hier beschrieben. Die ersten sechs beispielhaften
oder besonderen Formen des allgemeinen Diamindi(2-hydroxarylmethyl)-Ligandprecursors
6, entsprechend die besonderen Ligandprecursor 7, 8, 10, 11 und
12 und ihre entsprechenden Synthesen sind hier das erste Mal offenbart.
Die letzten beiden beispielhaften oder besonderen Formen des allgemeinen
Diamindi(2-hydroxarylmethyl)-Ligandprecursors
6, entsprechend der besonderen Ligandprecursor 13 und 14, sind im Stand
der Technik bekannt, aber ihre entsprechenden Synthesen sind hier
das erste Mal offenbart.
-
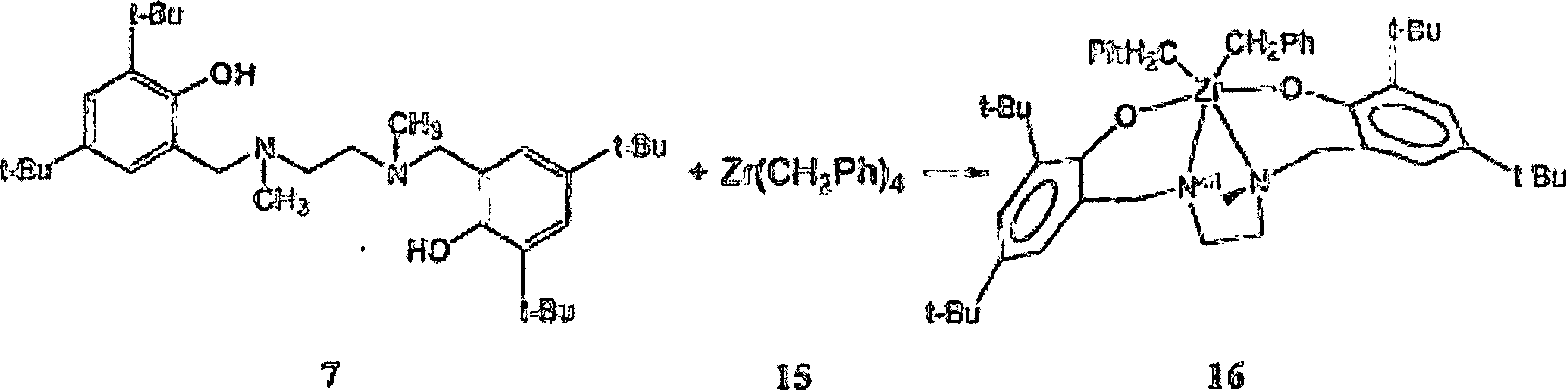
Synthese des ersten beispielhaften
Ligandprecursors [{N,N'-Bis(3,5-di-tert-butyl-2-hydroxyphenylmethyl)-N,N'-dimethylethylendiamin] 7
-
Die
erste beispielhafte oder besondere Form des allgemeinen Ligandprecursors
6, der spezifische Diamindi(2-hydroxarylmethyl)-Ligandprecursor
7, hier im Anschluss als Ligandprecursor [{N,N'-Bis(3,5-di-tert-butyl-2-hydroxyphenylmethyl)-N,N'-dimethylethylendiamin]
7 (neu) bezeichnet, leitet sich von der Umsetzung (nicht gezeigt)
von N,N'-Dimethylethylendiamin
als eine besondere Form eines Di-sekundären Amins
3 mit Formaldehyd als eine besondere Form von Aldehyden 4A und 4B
und 2,4-Di-tert-butylphenol als eine besondere Form substituierter
Phenole 5A und 5B in refluxierendem Methanol für 2 Stunden und Isolation durch
Filtration ab. Der Ligandprecursor [{N,N'-Bis(3,5-di-tert-butyl-2-hydroxyphenylmethyl)-N,N'-dimethylethylendiamin]
7 ist eine besondere Form des allgemeinen Diamindi(2-hydroxarylmethyl)-Ligandprecursors
6, wobei R1 und R2 Methylgruppen
(CH3) sind, R3,
R4, R6, R8, R10 und R12 Wasserstoffatome sind, R5,
R7, R9 und R11 tert-Butyl Gruppen sind und Y ein divalenter
Dihydrocarbylradikal -CH2CH2-
ist. Weitere Details der Synthese und spektroskopische Daten werden
unten in Beispiel 1 bereitgestellt.
-
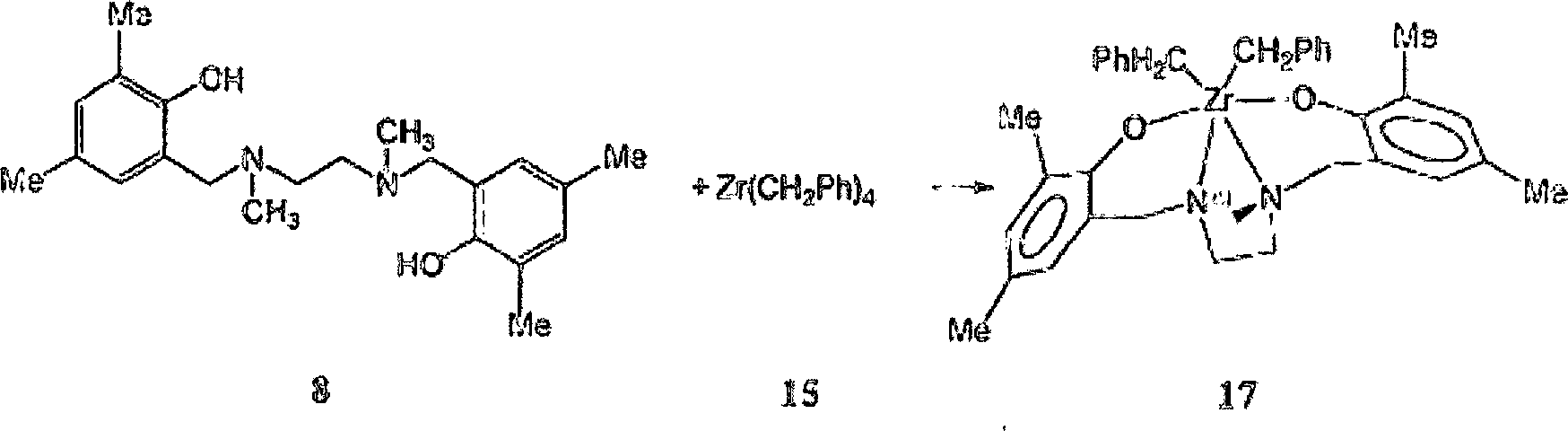
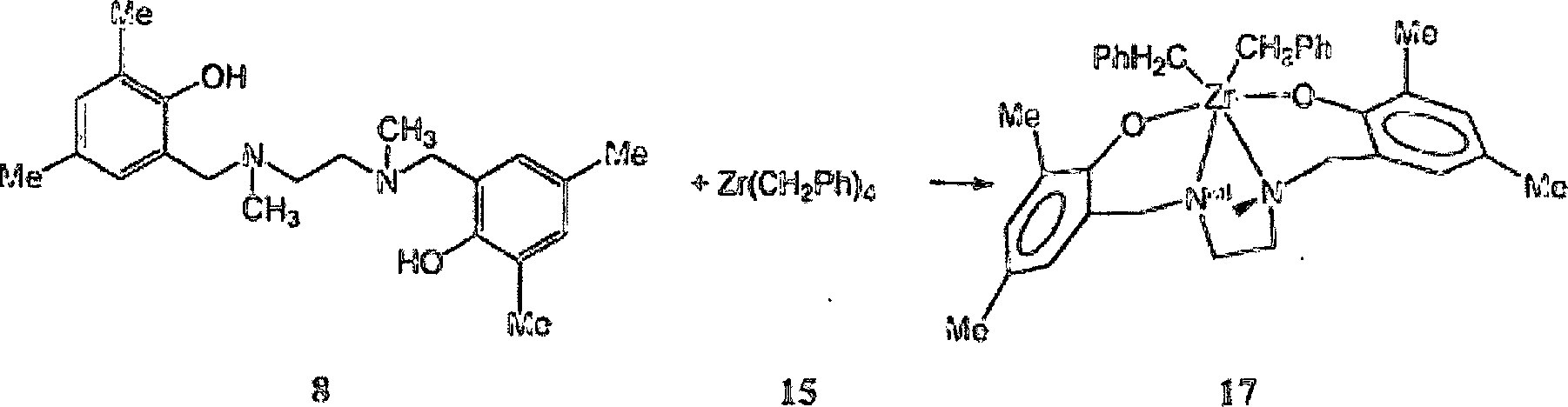
Synthese des zweiten exemplarischen
Ligandprecursors [{N,N'-Bis(3,5-dimethyl-2-hydroxyphenylmethyl)-N,N'-dimethylethylendiamin] 8
-
Die
zweite beispielhafte oder besondere Form des allgemeinen Ligandprecursors
6, der spezifische Diamindi(2-hydroxarylmethyl)-Ligandprecursor
8, hier im Anschluss als Ligandprecursor [{N,N'-Bis(3,5-dimethyl-2-hydroxyphenylmethyl)-N,N'-dimethylethylendiamin]
8 (neu) bezeichnet, leitet sich von der Umsetzung (nicht gezeigt)
von N,N'-Dimethylethylendiamin
als eine besondere Form eines Di-sekundären Amins
3 mit Formaldehyd als eine besondere Form von Aldehyden 4A und 4B
und 2,4-Dimethylphenol als eine besondere Form substituierter Phenole
5A und 5B in refluxierendem Methanol für 2 Stunden und Isolation durch
Filtration ab. Der Ligandprecursor [{N,N'-Bis(3,5-dimethyl-2-hydroxyphenylmethyl)-N,N'-dimethylethylendiamin]
8 ist eine besondere Form des allgemeinen Diamindi(2-hydroxarylmethyl)-Ligandprecursors
6, wobei R1, R2,
R5, R7, R9 und R11 Methylgruppen
(CH3) sind, R3,
R4, R6, R8, R10 und R12 Wasserstoffatome sind und Y ein divalenter Dihydrocarbylradikal
-CH2CH2- ist. Weitere
Details der Synthese und spektroskopische Daten werden unten in Beispiel
2 bereitgestellt.
-
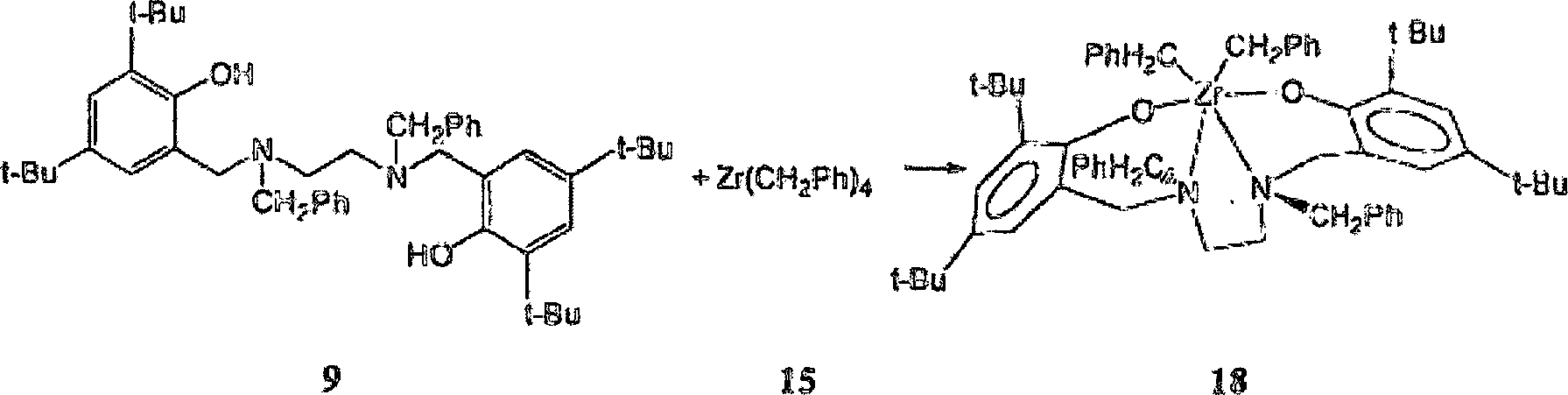
Synthese des dritten exemplarischen
Ligandprecursors [{N,N'-Bis(3,5-di-tert-butyl-2-hydroxyphenylmethyl)-N,N'-dibenzylethylendiamin] 9
-
Die
dritte beispielhafte oder besondere Form des allgemeinen Ligandprecursors
6, der spezifische Diamindi(2-hydroxarylmethyl)-Ligandprecursor
9, hier im Anschluss als Ligandprecursor [{N,N'-Bis(3,5-di-tert-butyl-2-hydroxyphenylmethyl)-N,N'-dibenzylethylendiamin]
9 (neu) bezeichnet, leitet sich von der Umsetzung (nicht gezeigt)
von N,N'-Dibenzylethylendiamin
als eine besondere Form eines Di-sekundären Amins
3 mit Formaldehyd als eine besondere Form von Aldehyden 4A und 4B
und 2,4-Di-tert-butylphenol als eine besondere Form substituierter
Phenole 5A und 5B in refluxierendem Methanol für 2 Stunden und Isolation durch
Filtration nach Ausfällung
unter Verwendung von Hexanlösungsmitteln
ab. Der Ligandprecursor [{N,N'-Bis(3,5-di-tert-butyl-2-hydroxyphenylmethyl)-N,N'-dibenzylethylendiamin] 9 ist eine besondere
Form des allgemeinen Diamindi(2-hydroxarylmethyl)-Ligandprecursors
6, wobei R1 und R2 Benzylgruppen
(CH2Ph) sind, R3,
R4, R6, R8, R10 und R12 Wasserstoffatome sind, R5,
R7, R9 und R11 tert-Butyl-Gruppen sind und Y ein divalenter Dihydrocarbylradikal
-CH2CH2- ist. Weitere
Details der Synthese werden unten in Beispiel 3 bereitgestellt.
-
Synthese des vierten exemplarischen
Ligandprecursors [{N,N'-Bis(3,5-di-tert-butyl-2-hydroxyphenylmethyl)-N,N'-diethylethylendiamin] 10
-
Die
vierte beispielhafte oder besondere Form des allgemeinen Ligandprecursors
6, der spezifische Diamindi(2-hydroxarylmethyl)-Ligandprecursor
10, hier im Anschluss als Ligandprecursor [{N,N'-Bis(3,5-ditert-butyl-2-hydroxyphenylmethyl)-N,N'-diethylethylendiamin]
10 (neu) bezeichnet, leitet sich von der Umsetzung (nicht gezeigt)
von N,N'-Diethylethylendiamin
als eine besondere Form eines Di-sekundären Amins
3 mit Formaldehyd als eine besondere Form von Aldehyden 4A und 4B
und 2,4-Di-tert-butylphenol als eine besondere Form substituierter
Phenole 5A und 5B in refluxierendem Methanol für 2 Stunden und Isolation durch
Filtration ab. Der Ligandprecursor [{N,N'-Bis(3,5-di-tert-butyl-2-hydroxyphenylmethyl)-N,N'-diethylethylendiamin] 10
ist eine besondere Form des allgemeinen Diamindi(2-hydroxarylmethyl)-Ligandprecursors
6, wobei R1 und R2 Ethylgruppen
(CH2CH3) sind, R3, R4, R6,
R8, R10 und R12 Wasserstoffatome sind, R5,
R7, R9 und R11 tert-Butylgruppen sind und Y ein divalenter
Dihydrocarbylradikal -CH2CH2-
ist. Weitere Details der Synthese werden unten in Beispiel 4 bereitgestellt.
-
Synthese des fünften exemplarischen
Ligandprecursors [{N,N'-Bis(4,5-dimethyl-2-hydroxyphenylmethyl)-N,N'-dimethylethylendiamin] 11
-
Die
fünfte
beispielhafte oder besondere Form des allgemeinen Ligandprecursors
6, der spezifische Diamindi(2-hydroxarylmethyl)-Ligandprecursor
11, hier im Anschluss als Ligandprecursor [{N,N'-Bis(4,5-dimethyl-2-hydroxyphenylmethyl)-N,N'-dimethylethylendiamin]
11 (neu) bezeichnet, leitet sich von der Umsetzung (nicht gezeigt)
von N,N'-Dimethylethylendiamin
als eine besondere Form eines Di-sekundären Amins
3 mit Formaldehyd als eine besondere Form von Aldehyden 4A und 4B
und 3,4-Dimethylphenol als eine besondere Form substituierter Phenole
5A und 5B in refluxierendem Methanol für 2 Stunden und Isolation durch
Filtration ab. Der Ligandprecursor [{N,N'-Bis(4,5-dimethyl-2-hydroxyphenylmethyl)-N,N'-dimethylethylendiamin]
11 ist eine besondere Form des allgemeinen Diamindi(2-hydroxarylmethyl)-Ligandprecursors
6, wobei R1, R2,
R6, R7, R10 und R11 Methylgruppen
(CH3) sind, R3,
R4, R5, R8, R9 und R12 Wasserstoffatome sind und Y ein divalenter Dihydrocarbylradikal
-CH2CH2- ist. weitere
Details der Synthese werden unten in Beispiel 5 bereitgestellt.
-
Synthese des sechsten
exemplarischen Ligandprecursors [{N,N'-Bis(3,5-di-tert-butyl-2-hydroxyphenylmethyl)-N,N'-dimethyl-1,3-propandiamin]
12
-
Die
sechste beispielhafte oder besondere Form des allgemeinen Ligandprecursors
6, der spezifische Diamindi(2-hydroxarylmethyl)-Ligandprecursor
12, hier im Anschluss als Ligandprecursor [{N,N'-Bis(3,5-di-tert-butyl-2-hydroxyphenylmethyl)-N,N'-dimethyl-1,3-propandiamin]
12 (neu) bezeichnet, leitet sich von der Umsetzung (nicht gezeigt)
von N,N'-Dimethylpropan-1,3-diamin
als eine besondere Form eines Di-sekundären Amins 3 mit Formaldehyd
als eine besondere Form von Aldehyden 4A und 4B und 2,4-Di-tert-butylphenol
als eine besondere Form substituierter Phenole 5A und 5B in refluxierendem
Methanol für
12 Stunden und Isolation durch Filtration ab. Der Ligandprecursor
[{N,N'-Bis(3,5-di-tert-butyl-2-hydroxyphenylmethyl)-N,N'-dimethyl-1,3-propandiamin]
12 ist eine besondere Form des allgemeinen Diamindi(2-hydroxarylmethyl)-Ligandprecursors
6, wobei R1 und R2 Methylgruppen
(CH3) sind, R3,
R4, R6, R8, R10 und R12 Wasserstoffatome sind, R5,
R7, R9 und R11 tert-Butylgruppen und Y ein divalenter
Dihydrocarbylradikal -CH2CH2CH2- ist. Weitere Details der Synthese werden
unten in Beispiel 6 bereitgestellt.
-
Synthese des siebten exemplarischen
Ligandprecursors [{N,N'-Bis(3,5-di-tert-butyl-2-hydroxophenylmethyl)-ethylendiamin]
13
-
Die
siebte beispielhafte oder besondere Form des allgemeinen Ligandprecursors
6, der spezifische Diamindi(2-hydroxarylmethyl)-Ligandprecursor
13, hier im Anschluss als Ligandprecursor [{N,N'-Bis(3,5-di-tert-butyl-2-hydroxophenylmethyl)-ethylendiamin]
13 (im Stand der Technik bekannt) bezeichnet, leitet sich von der
Umsetzung (nicht gezeigt) von Ethylendiamin als eine besondere Form
eines Di- primären Amins
3 mit Formaldehyd als eine besondere Form von Aldehyden 4A und 4B
und 2,4-Di-tert-butylphenol als eine besondere Form substituierter
Phenole 5A und 5B in refluxierendem Methanol für 2 Stunden und Isolation durch
Filtration ab. Der Ligandprecursor [{N,N'-Bis(3,5-di-tert-butyl-2-hydroxophenylmethyl)-ethylendiamin]
13 ist eine besondere Form des allgemeinen Diamindi(2-hydroxarylmethyl)-Ligandprecursors
6, wobei R1, R2,
R3, R4, R6, R8, R10 und
R12 Wasserstoffatome sind, R5,
R7, R9, und R11 tert-Butylgruppen sind und Y ein divalenter
Dihydrocarbylradikal -CH2CH2-
ist. Weitere Details der Synthese werden unten in Beispiel 7 bereitgestellt.
-
Synthese des achten exemplarischen
Ligandprecursors [{N,N'-Bis(3,5-di-tert-butyl-2-hydroxophenylmethyl)-1,3-propandiamin] 14
-
Die
achte beispielhafte oder besondere Form des allgemeinen Ligandprecursors
6, der spezifische Diamindi(2-hydroxarylmethyl)-Ligandprecursor
14, hier im Anschluss als Ligandprecursor [{N,N'-Bis(3,5-di-tert-butyl-2-hydroxophenylmethyl)-1,3-propandiamin]
14 (im Stand der Technik bekannt) bezeichnet, leitet sich von der
Umsetzung (nicht gezeigt) von Propan-1,3-diamin als eine besondere
Form eines Di-primären
Amins 3 mit Formaldehyd als eine besondere Form von Aldehyden 4A
und 4B und 2,4-Di-tert-butylphenol als eine besondere Form substituierter
Phenole 5A und 5B in refluxierendem Methanol für 2 Stunden und Isolation durch
Filtration ab. Der Ligandprecursor [{N,N'-Bis(3,5-di-tert-butyl-2-hydroxophenylmethyl)-1,3-propandiamin]
14 ist eine besondere Form des allgemeinen Diamindi(2-hydroxarylmethyl)-Ligandprecursors
6, wobei R1, R2,
R3, R4, R6, R8, R10 und
R12 Wasserstoffatome sind, R5,
R7, R9, und R11 tert-Butylgruppen sind und Y ein divalenter
Dihydrocarbylradikal -CH2CH2CH2- ist.
Weitere Details der Synthese werden unten in Beispiel 8 bereitgestellt.
-
Synthese von
Diamindiphenolatpräkatalysatoren
-
Der
allgemeine Diamindi(2-hydroxarylmethyl)-Ligandprecursor 6 zielt
auf die Bindung an ein Metall, wie zum Beispiel eine Übergangsmetallatomzusammensetzung,
bevorzugt, aber nicht darauf beschränkt, ein einzelnes Übergangsmetallatom,
das aus der Gruppe, die aus Zirkonium, Hafnium, Titan und einem
Lanthanid besteht, ausgewählt
wird, zur Synthese unterschiedlicher besonderer Formen des Diamindiphenolatpräkatalysators
1 oder 2 in Übereinstimmung
mit den obigen Beschreibungen, ab.
-
Der
allgemeine Diamindi(2-hydroxarylmethyl)-Ligandprecursor 6 reagiert
unter variablen Reaktionsbedingungen mit einem Äquivalent eines Übergangsmetallkomplexes,
wie zum Beispiel Zirkoniumtetra(benzyl), Zirkoniumtetrakis(dimethylamid),
Hafniumtetra(chlorid), Titantetra(isopropoxid) oder ein Lanthanidkomplex,
um den Diphenolatzirkoniumdibenzylkomplex, den Diphenolatzirkonium-bis(dimethylamid)komplex,
den Diphenolathafniumdichloridkomplex, den Diphenolattitan-bis(isopropoxid)komplex
bzw. den Diphenolatlanthanidkomplex zu ergeben. Jeder so gebildete
Komplex kann direkt als ein Präkatalysator
für die
Polymerisation eines Alpha-Olefinmonomers
verwendet werden oder kann durch chemische Umwandlung, wie zum Beispiel Umwandlung
von Diamindiphenolattitan-bis(isopropoxid) in Diamindiphenolattitandichlorid
unter Verwendung einer Vielzahl von Chlorierungsmitteln, wie zum
Beispiel Trimethylsilylchlorid oder Triethylaminhydrochlorid, in einen
Präkatalysator umgewandelt
werden. Das Diamindiphenolattitandichlorid kann weiter in ein Diamindiphenolattitandialkyl
unter Verwendung einer Vielzahl von Alkylierungsmitteln, wie zum
Beispiel Benzylmagnesiumchlorid oder Methylmagnesiumbromid, umgewandelt
werden.
-
Die
Synthese von vier beispielhaften oder besonderen Formen des Diamindiphenolatpräkatalysators 1
der vorliegenden Erfindung werden hier allgemein beschrieben.
-
Synthese des ersten beispielhaften
Präkatalysators
[{N,N'-Bis(3,5-di-tert-butyl-2-hydroxyphenylmethyl)-N,N'-dimethylethylendiamin}zirkoniumdibenzyl]
16
-
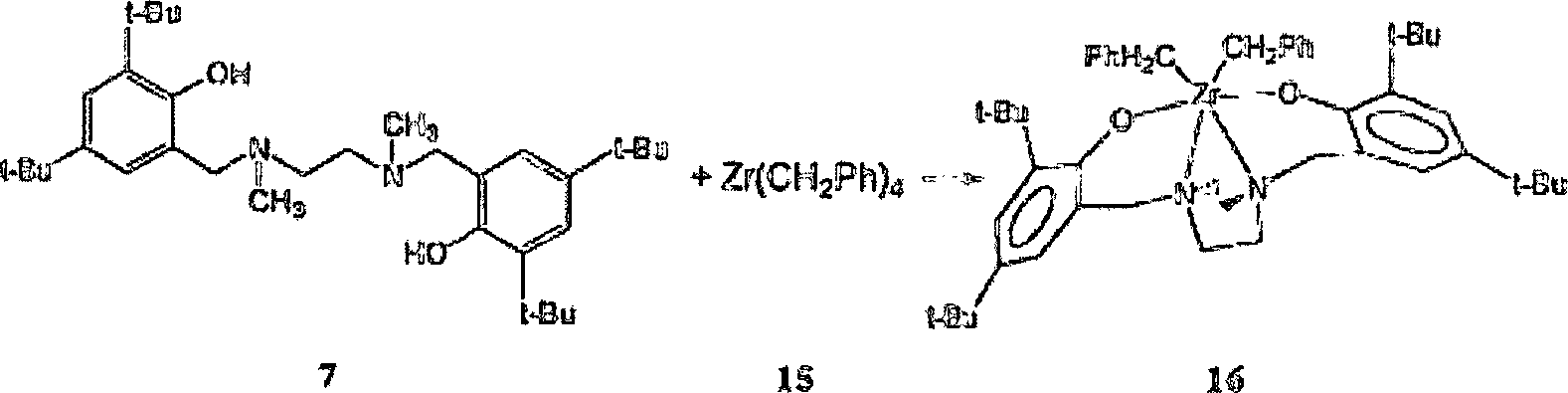
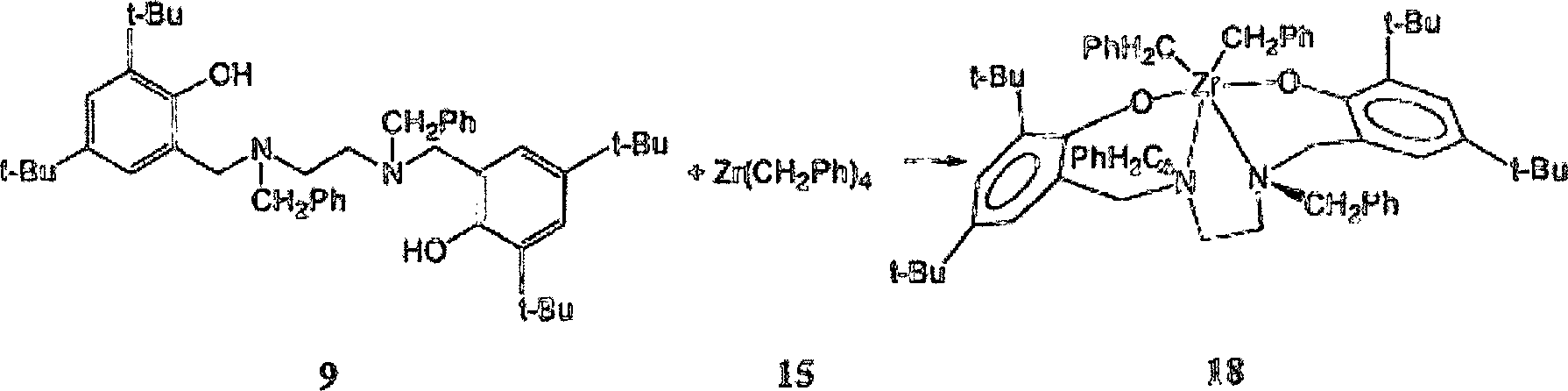
Der
Ligandprecursor [{N,N'-Bis(3,5-di-tert-butyl-2-hydroxyphenylmethyl)-N,N'-dimethylethylendiamin] 7
reagiert sauber mit einem Äquivalent
Zirkoniumtetra(benzyl), Zr(CH2Ph)4 15, bei 65°C, was den hexakoordinierten
Dialkyldiamindiphenolatpräkatalysator
16 quantitativ als einen gelben kristallinen Feststoff ergibt, der ebenfalls
als [{N,N'-Bis(3,5-di-tert-butyl-2-hydroxyphenylmethyl)-N,N'-dimethylethylendiamin}zirkoniumdibenzyl]
16 bezeichnet wird.
-
-
Die
spektroskopischen Daten des Präkatalysators
16 stimmen mit einem einzelnen Stereoisomer überein, das symmetrisch verwandte
Phenolatringe, symmetrisch verwandte Benzylgruppen und drei AX-Spinsysteme
aufweist. Dies deutet auf einen Chelat mit C2-Symmetrie
auf der NMR Zeitskala hin. Die (Röntgen)-Kristallstruktur des
Präkatalysators
16, die in 1 gezeigt ist, unterstützt die
spektroskopischen Daten und zeigt an, dass die zwei Benzylgruppen
in cis Konfiguration stehen. Weitere Details der Synthese und der spektroskopischen
Daten werden unten in Beispiel 9 bereitgestellt.
-
Synthese des zweiten beispielhaften
Präkatalysators
[{N,N'-Bis(3,5-dimethyl-2-hydroxyphenylmethyl)-N,N'-dimethylethylendiamin}zirkoniumdibenzyl]
17
-
Der
Ligandprecursor [{N,N'-Bis(3,5-dimethyl-2-hydroxyphenylmethyl)-N,N'-dimethylethylendiamin]
8 reagiert sauber mit einem Äquivalent
Zirkoniumtetra(benzyl), Zr(CH2Ph)4 15, bei 65°C, was den hexakoordinierten
Dialkyldiamindiphenolatpräkatalysator
17 quantitativ als einen gelben kristallinen Feststoff ergibt, der ebenfalls
als [{N,N'-Bis(3,5-dimethyl-2-hydroxyphenylmethyl)-N,N'-dimethylethylendiamin}zirkoniumdibenzyl] 17
bezeichnet wird.
-
-
Die
spektroskopischen Daten des Präkatalysators
17 stimmen mit einem einzelnen Stereoisomer überein, das symmetrisch verwandte
Phenolatringe, symmetrisch verwandte Benzylgruppen und drei AX-Spinsysteme
aufweist. Dies deutet auf einen Chelat mit C2-Symmetrie
auf der NMR Zeitskala hin. Weitere Details der Synthese und der
spektroskopischen Daten werden unten in Beispiel 10 bereitgestellt.
-
Synthese des dritten beispielhaften
Präkatalysators
[{N,N'-Bis(3,5-di-tert-butyl-2-hydroxyphenylmethyl)-N,N'-dibenzylethylendiamin}zirkoniumdibenzyl]
18
-
Der
Ligandprecursor [{N,N'-Bis(3,5-di-tert-butyl-2-hydroxyphenylmethyl)-N,N'-dibenzylethylendiamin] 9
reagiert sauber mit einem Äquivalent
Zirkoniumtetra(benzyl), Zr(CH2Ph)4 15, bei 65°C, was den hexakoordinierten
Dialkyldiamindiphenolatpräkatalysator
18 quantitativ als einen gelben kristallinen Feststoff ergibt, der ebenfalls
als [{N,N'-Bis(3,5-di-tert-butyl-2-hydroxyphenylmethyl)-N,N'-dibenzylethylendiamin}zirkoniumdibenzyl]
18 bezeichnet wird.
-
-
Die
spektroskopischen Daten des Präkatalysators
18 stimmen mit einem einzelnen Stereoisomer überein, das symmetrisch verwandte
Phenolatringe, symmetrisch verwandte Benzylgruppen und drei AX-Spinsysteme
aufweist. Dies deutet auf einen Chelat mit C2-Symmetrie
auf der NMR Zeitskala hin. Weitere Details der Synthese werden unten
in Beispiel 11 bereitgestellt.
-
Synthese des vierten beispielhaften
Präkatalysators
[{N,N-Bis(3,5-di-tert-butyl-2-hydroxyphenylmethyl)-N,N'-diethylethylendiamin}zirkoniumdibenzyl]
19
-
Der
Ligandprecursor [{N,N'-Bis(3,5-di-tert-butyl-2-hydroxyphenylmethyl)-N,N'-diethylethylendiamin] 10
reagiert sauber mit einem Äquivalent
Zirkoniumtetra(benzyl), Zr(CH2Ph)4 15, bei 65°C, was den hexakoordinierten
Dialkyldiamindiphenolatpräkatalysator
19 quantitativ als einen gelben kristallinen Feststoff ergibt, der ebenfalls
als [{N,N'-Bis(3,5-di-tert-butyl-2-hydroxyphenylmethyl)-N,N'-diethylethylendiamin}zirkoniumdibenzyl] 19
bezeichnet wird.
-
-
Die
spektroskopischen Daten des Präkatalysators
19 stimmen mit einem einzelnen Stereoisomer überein, das symmetrisch verwandte
Phenolatringe, symmetrisch verwandte Benzylgruppen und drei AX-Spinsysteme
aufweist. Dies deutet auf einen Chelat mit C2-Symmetrie
auf der NMR Zeitskala hin. Weitere Details der Synthese werden unten
in Beispiel 12 bereitgestellt.
-
Verfahren
für die
katalytische Polymerisation von Alpha-Olefinmonomeren
-
Die
bevorzugte Ausführungsform
des Verfahrens zur katalytischen Polymerisation von Alpha-Olefinmonomeren
gemäß der vorliegenden
Erfindung wird hier allgemein in Bezug auf die Verwendung irgendeiner besonderen
Form des Diamindiphenolatpräkatalysators
1 oder 2 beschrieben, die die vier beispielhaften besonderen Formen
des Präkatalysators
1, wie oben beschrieben, nämlich
Dialkyldiamindiphenolatpräkatalysator
[{N,N'-Bis(3,5-(di-tert-butyl-2-hydroxophenylmethyl)-N,N'-dimethylethylendiamin)zirkoniumdibenzyl]
16, Dialkyldiamindiphenolatpräkatalysator
[{N,N'-Bis(3,5-dimethyl-2-hydroxophenylmethyl)-N,N'-dimethylethylendiamin}zirkoniumdibenzyl]
17, Dialkyldiamindiphenolatpräkatalysator
[{N,N'-Bis(3,5-di-tert-butyl-2-hydroxophenylmethyl)-N,N'-dibenzylethylendiamin)zirkoniumdibenzyl]
18 oder Dialkyldiamindiphenolyatpräkatalysator [{N,N'-Bis(3,5-di-tert-butyl-2-hydroxophenylmethyl)-N,N'-diethylethylendiamin)zirkoniumdibenzyl]
19 einschließen.
-
Basierend
auf der Ausführung
des folgenden beschriebenen allgemeinen Verfahrens werden Details zweier
beispielhafter katalytischer Polymerisationsreaktionen, der ersten
isotaktischen katalytischen Polymerisation und der zweiten ataktischen
katalytischen Polymerisation, die jeweils die Verwendung eines beispielhaften
Alpha-Olefinmonomers, 1-Hexen,
beinhalten und die die besondere Form 16 bzw. die besondere Form 17
des Diamindiphenolatpräkatalysators
1 zur Bildung eines Poly(1-hexen)-Produktes beinhalten, und die
betreffenden empirischen Daten davon unten in den Beispielen 13
bzw. 14 bereitgestellt.
-
Das
hier beschriebene Verfahren für
die katalytische Polymerisation von Alpha-Olefinmonomeren gemäß der vorliegenden
Erfindung ist allgemein auf jede Art und Größe eines chemischen Reaktors
und/oder chemischen Prozesses anwendbar. Insbesondere können die
folgenden Schritte des Verfahrens der vorliegenden Erfindung unter
Verwendung eines chemischen Reaktors, der aus der Gruppe, die aus
einem chemischen Reaktor mit kontinuierlichem Fluss, einem chemischen
Batch-Reaktor und einem chemischen Plug-Flow-Reaktor besteht, ausgewählt wird,
ausgeführt
werden, wobei die Größe des chemischen
Reaktors aus der Gruppe, die aus einem chemischen Laborreaktor in
Mikromaßstab,
einem chemischen Reaktor im Produkt/Prozessentwicklungsmaßstab und
einem kommerziellen chemischen Reaktor im Großmaßstab besteht, ausgewählt wird.
Zusätzlich
können
die folgenden Schritte des Verfahrens der vorliegenden Erfindung
in einem chemischen Prozess ausgeführt werden, der aus der Gruppe,
die aus einem chemischen Verfahren mit kontinuierlichem Fluss, einem
chemischen Batch-Verfahren, einem chemischen Plug-Flow-Verfahren und einer
Kombination eines chemischen Verfahrens, das eine Kombination dieser
chemischen Verfahren aufweist, besteht, ausgewählt wird, wobei die Größe des chemischen
Verfahrens aus der Gruppe, die aus einem chemischen Laborprozess
im Mikromaßstab,
einem chemischen Prozess im Produkt/Prozessentwicklungsmaßstab und
einem kommerziellen chemischen Verfahren im Großmaßstab besteht, ausgewählt wird.
-
In
Schritt (a) des Verfahrens zur katalytischen Polymerisation eines
Alpha-Olefinmonomers wird eine besondere Form eines Diamindiphenolatpräkatalysators
1 oder 2 bereitgestellt.
-
In
Schritt (b) wird eine erste chemische Einheit, die die besondere
Form des Diamindiphenolatpräkatalysators
1 oder 2 von Schritt (a) aufweist, für die Verwendung in der katalytischen
Polymerisation eines Alpha-Olefinmonomers hergestellt.
-
Bevorzugt
wird eine Menge der besonderen Form des Diamindiphenolatpräkatalysators
1 oder 2 mit einem organischen Lösungsmittel
gemischt. Jedes nicht-protische organische Lösungsmittel kann verwendet werden,
welches den Präkatalysator
1 oder 2 ohne Zersetzung suspendieren oder auflösen kann. Bevorzugter ist das
organische Lösungsmittel
die flüssige
Form des zu polymerisierenden Alpha-Olefinmonomers, zum Beispiel ein organisches
Lösungsmittel,
das aus der Gruppe, die aus 1-Penten, 1-Hexen und 1-Okten besteht, ausgewählt wird.
Alternativ ist das organische Lösungsmittel
die flüssige
Form des zu polymerisierenden Alpha-Olefinmonomers, zum Beispiel
ein organisches Lösungsmittel,
das aus der Gruppe, die aus 1-Penten, 1-Hexen und 1-Okten besteht,
ausgewählt
wird, gemischt mit mindestens einem zusätzlichen organischen Lösungsmittel,
das nicht das zu polymerisierende Alpha-Olefinmonomer beinhaltet,
zum Beispiel mindestens ein zusätzliches
organisches Lösungsmittel,
das aus der Gruppe, die aus Pentan, Heptan, Toluol, Methylenchlorid und
Chlorbenzol besteht, ausgewählt
wird. Alternativ ist das organische Lösungsmittel mindestens ein
organisches Lösungsmittel,
das nicht das zu polymerisierende Alpha-Olefinmonomer beinhaltet,
zum Beispiel mindestens ein organisches Lösungsmittel, das aus der Gruppe,
die aus Pentan, Heptan, Toluol, Methylenchlorid und Chlorbenzol
besteht, ausgewählt
wird.
-
Alternativ
wird die erste chemische Einheit, die die besondere Form des Diamindiphenolatpräkatalysators
1 oder 2 wie sie unten beschrieben ist aufweist, ohne den Präkatalysator
1 oder 2 in einem Lösungsmittel
vor dem nachfolgenden Schritt (e) zu suspendieren oder aufzulösen, hergestellt,
zur Bildung eines katalytischen Polymerisationsreaktionssystems
zur katalytischen Polymerisation des Alpha-Olefinmonomers.
-
Gewöhnlich ist
ein geeigneter Cokatalysator für
die Aktivierung des Präkatalysators
1 oder 2 erforderlich, um die katalytische Polymerisation des Alpha-Olefinmonomers
zu bewirken, es existieren jedoch bestimmte Formen des Präkatalysators
1 oder 2, zum Beispiel Diphenolatlanthanidkomplexe, die die katalytische Polymerisation
des Alpha-Olefinmonomers, wie zum Beispiel 1-Penten, 1-Hexen oder 1-Okten, ohne durch
einen Cokatalysator aktiviert zu werden, bewirken können. Somit
wirken in diesen katalytischen Polymerisationssystemen der Präkatalysator
1 oder 2 wirksam als ein "unabhängiger" Katalysator, wobei
es keinen Bedarf zur Durchführung
der folgenden Schritte (c) und (d) gibt und das Verfahren zur katalytischen
Polymerisation des Alpha-Olefinmonomers geht mit dem alternativen
Schritt (e), wie unten beschrieben, weiter.
-
Optional
beinhaltet Schritt (b) des Weiteren das Aussetzen irgendeiner der
oben beschriebenen bevorzugten oder alternativen Formen der ersten
chemischen Einheit, die die besondere Form des Diamindiphenolatpräkatalysators
1 oder 2 aufweist, gegenüber
der Oberfläche
eines festen Trägers,
wie zum Beispiel Siliziumdioxid, Aluminiumoxid oder Magnesiumoxid,
um einen adsorbierten Zustand der ersten chemischen Einheit des
Präkatalysators
1 oder 2 herzustellen.
-
Im
Schritt (c) wird ein Cokatalysator, der für die Aktivierung einer bestimmten
Form des Diamindiphenolatpräkatalysators
1 oder 2 geeignet ist, für
die Verwendung bei der katalytischen Polymerisation des Alpha-Olefinmonomers
bereitgestellt. Der Cokatalysator wird aus der Gruppe ausgewählt, die
zum Beispiel eine Bor-Lewis-Säure, wie
zum Beispiel Tris(pentafluorphenyl)bor, B(C6F5)3, ein Borsalz,
wie zum Beispiel N,N'-Dimethylaniliniumtetrakis(pentafluorphenyl)borat,
[PhNH(CH3)2][B(C6F5)4]
und eine Aluminiumverbindung, wie zum Beispiel Methylaluminoxan
(MAO) beinhaltet, aber nicht darauf beschränkt ist.
-
In
Schritt (d) wird eine zweite chemische Einheit, die den ausgewählten Cokatalysator
von Schritt (c) aufweist, für
die Verwendung bei der katalytischen Polymerisation des Alpha-Olefinmonomers hergestellt.
-
Bevorzugt
wird der ausgewählte
Cokatalysator, der für
die Aktivierung des Präkatalysators
1 oder 2 benötigt
wird, mit einem organischen Lösungsmittel
gemischt. Jedes organische Lösungsmittel
kann verwendet werden, das den ausgewählten Cokatalysator ohne Zersetzung
suspendieren oder auflösen
kann. Bevorzugter ist das organische Lösungsmittel die flüssige Form
des zu polymerisierenden Alpha-Olefinmonomers, zum Beispiel ein
organisches Lösungsmittel,
das aus der Gruppe, die aus 1-Penten, 1-Hexen und 1-Okten besteht,
ausgewählt
wird. Alternativ ist das organische Lösungsmittel die flüssige Form
des zu polymerisierenden Alpha-Olefinmonomers,
zum Beispiel ein organisches Lösungsmittel,
das aus der Gruppe, die aus 1-Penten, 1-Hexen und 1-Okten besteht,
ausgewählt
wird, das mit mindestens einem zusätzlichen organischen Lösungsmittel
gemischt wird, das nicht das zu polymerisierenden Alpha-Olefinmonomer
enthält,
zum Beispiel mindestens ein zusätzliches
organisches Lösungsmittel,
das aus der Gruppe, die aus Pentan, Heptan, Toluol, Methylenchlorid
und Chlorbenzol besteht, ausgewählt
wird. Alternativ ist das organische Lösungsmittel mindestens ein
organisches Lösungsmittel,
das das zu polymerisierenden Alpha-Olefinmonomer nicht beinhaltet,
zum Beispiel mindestens ein organisches Lösungsmittel, das aus der Gruppe,
die aus Pentan, Heptan, Toluol, Methylenchlorid und Chlorbenzol
besteht, ausgewählt
wird.
-
Alternativ
wird die zweite chemische Einheit, die den ausgewählten Cokatalysator,
wie er unten beschrieben ist aufweist, ohne das ausgewählte Lösungsmittel
vor dem folgenden Schritt (e) in einem Lösungsmittel zu suspendieren
oder aufzulösen
zur Bildung eines katalytischen Polymerisationsreaktionssystems
zur katalytischen Polymerisation des Alpha-Olefinmonomers hergestellt.
-
Optional
beinhaltet Schritt (d) weiter das Aussetzen irgendeiner der oben
beschriebenen bevorzugten oder alternativen Formen der zweiten chemischen
Einheit, die den ausgewählten
Cokatalysator aufweist, gegenüber
der Oberfläche
eines festen Trägers,
wie zum Beispiel Siliziumdioxid, Aluminiumoxid oder Magnesiumoxid,
um einen adsorbierten Zustand der zweiten chemischen Einheit des
ausgewählten
Cokatalysators herzustellen.
-
In
Bezug auf den oben genannten Schritt (b) und Schritt (d) hängen das
spezifische Lösungsmittel oder
die Lösungsmittel,
die für
die Suspendierung oder das Auflösen
des Diamindiphenolatpräkatalysators
1 oder 2 und/oder für
das Suspendieren oder Auslösen
des ausgewählten
Cokatalysators verwendet werden, von der gewünschten Poly(Alpha-Olefin)-Produktverteilung
ab, insbesondere in Bezug auf die Bildung verschiedener Homopolymere
oder Co-Polymere, wobei jedes einen unterschiedlichen Grad an Alpha-Olefin-Einbettung
hat. Typischerweise ist, wenn das zu polymerisierende Monomer die flüssige Phase
ist, mindestens eines der für
die Suspendierung oder das Auflösen
des Diamindiphenolatpräkatalysators
1 oder 2 und/oder des ausgewählten
Cokatalysators verwendeten Lösungsmittel
das Alpha-Olefinmonomer, das als das gewünschte Poly(Alpha-Olefin)-Produkt ausgewählt wird.
-
In
Schritt (e) wird ein katalytisches Polymerisationsreaktionssystem
für die
katalytische Polymerisation des Alpha-Olefinmonomers durch Mischen
(i) der ersten chemischen Einheit, die die besondere Form des Diamindiphenolatpräkatalysators
1 oder 2 von Schritt (b) aufweist, mit (ii) der zweiten chemischen
Einheit des ausgewählten
Cokatalysators von Schritt (d) mit (iii) dem zu polymerisierenden
Alpha-Olefinmonomer gebildet.
-
Es
gibt zwei Kategorien, Kategorie (A) und Kategorie (B), zur Bildung
des katalytischen Polymerisationsreaktionssystems, die das Mischen
der ersten und der zweiten chemischen Einheiten mit dem Alpha-Olefinmonomer
betrifft, gemäß des Vorhandenseins
oder des Fehlens des zu polymerisierenden Alpha-Olefinmonomers in
mindestens einer der ersten und zweiten chemischen Einheiten. Zusätzlich zum
Vorhandensein oder dem Fehlen des zu polymerisierenden Alpha-Olefinmonomers
wird in jedem alternativen Verfahren von Kategorie (A) und Kategorie
(B) die erste chemische Einheit in einem Zustand, der aus der Gruppe,
die aus einem nicht adsorbierten Zustand der ersten chemischen Einheit
und einem absorbierten Zustand der ersten chemischen Einheit besteht,
ausgewählt
wird, mit der zweiten chemischen Einheit in einem Zustand, der aus der
Gruppe, die aus einem nicht absorbierten Zustand der zweiten chemischen
Einheit und einem absorbierten Zustand der zweiten chemischen Einheit
besteht, ausgewählt
wird, gemischt.
-
In
Kategorie (A), bei der das zu polymerisierende Alpha-Olefinmonomer in
mindestens einer der chemischen Einheiten vorliegt, die aus der
Gruppe, die aus der ersten chemischen Einheit, die den Präkatalysator 1
oder 2 aufweist, und der zweiten chemischen Einheit, die den ausgewählten Cokatalysator
aufweist, besteht, ausgewählt
werden, wird die erste chemische Einheit, die den Präkatalysator
1 oder 2 aufweist, mit der zweiten chemischen Einheit, die den ausgewählten Cokatalysator
aufweist, gemischt.
-
Kategorie
(A) zur Bildung des katalytischen Polymerisationssystems beinhaltet
die folgenden fünf
alternativen Verfahren zum Mischen der ersten chemischen Einheit,
die den Präkatalysator
1 oder 2 aufweist, mit der zweiten chemischen Einheit, die den ausgewählten Cokatalysator
aufweist: (1) Mischen der ersten chemischen Einheit, die den Präkatalysator
1 oder 2 aufweist, der in dem Alpha-Olefinmonomer suspendiert oder aufgelöst ist,
in einem nicht absorbierten Zustand oder in einem absorbierten Zustand
mit der zweiten chemischen Einheit, die den ausgewählten Cokatalysator
aufweist, der in dem Alpha-Olefinmonomer suspendiert oder aufgelöst ist,
in einem nicht absorbierten Zustand oder in einem absorbierten Zustand,
(2) Mischen der ersten chemischen Einheit, die den Präkatalysator
1 oder 2 aufweist, der in dem Alpha-Olefinmonomer suspendiert oder
aufgelöst
ist, in einem nicht absorbierten Zustand oder in einem absorbierten
Zustand mit der zweiten chemischen Einheit, die den ausgewählten Cokatalysator
aufweist, der in einem organischen Lösungsmittel, das das Alpha-Olefinmonomer
nicht beinhaltet, suspendiert oder aufgelöst ist, in einem nicht absorbierten
Zustand oder in einem absorbierten Zustand, (3) Mischen der ersten
chemischen Einheit, die den Präkatalysator
1 oder 2 aufweist, der in einem organischen Lösungsmittel, das nicht das
Alpha-Olefinmonomer beinhaltet, suspendiert oder aufgelöst ist,
in einem nicht absorbierten Zustand oder in einem absorbierten Zustand
mit der zweiten chemischen Einheit, die den ausgewählten Cokatalysator
aufweist, der in dem Alpha-Olefinmonomer suspendiert oder aufgelöst ist,
in einem nicht absorbierten Zustand oder in einem absorbierten Zustand,
(4) Mischen der ersten chemischen Einheit, die den Präkatalysator
1 oder 2 aufweist, der in dem Alpha-Olefinmonomer suspendiert oder
aufgelöst
ist, in einem nicht absorbierten Zustand oder in einem absorbierten
Zustand mit der zweiten chemischen Einheit, die den ausgewählten Cokatalysator
aufweist, der nicht in einem organischen Lösungsmittel suspendiert oder
aufgelöst
ist, in einem nicht absorbierten Zustand oder in einem absorbierten
Zustand und (5) Mischen der ersten chemischen Einheit, die den Präkatalysator
1 oder 2 aufweist, der nicht in einem organischen Lösungsmittel
suspendiert oder aufgelöst
ist, in einem nicht absorbierten Zustand oder in einem absorbierten
Zustand mit der zweiten chemischen Einheit, die den ausgewählten Cokatalysator
aufweist, der in dem Alpha-Olefinmonomer
suspendiert oder aufgelöst
ist, in einem nicht absorbierten Zustand oder in einem absorbierten
Zustand.
-
In
Kategorie (B), wo das zu polymerisierende Alpha-Olefinmonomer allen chemischen Einheiten
fehlt, die aus der Gruppe, die aus der ersten chemischen Einheit,
die den Präkatalysator
1 oder 2 aufweist, und der zweiten chemischen Einheit, die den ausgewählten Cokatalysator
aufweist, besteht, ausgewählt
werden, wird die erste chemische Einheit, die den Präkatalysator
1 oder 2 aufweist, mit der zweiten chemischen Einheit, die den ausgewählten Cokatalysator aufweist,
gemischt, gefolgt von Mischen mit dem gewünschten oder Ziel-Alpha-Olefinmonomer,
das polymerisiert werden soll.
-
Die
Kategorie (B) zur Bildung des katalytischen Polymerisationssystems
beinhaltet die folgenden vier alternativen Verfahren zum Mischen
der ersten chemischen Einheit, die den Präkatalysator 1 oder 2 aufweist, mit
der zweiten chemischen Einheit, die den ausgewählten Cokatalysator aufweist,
gefolgt von Mischen mit dem Alpha-Olefinmonomer: (1) Mischen der ersten
chemischen Einheit, die den Präkatalysator
1 oder 2 aufweist, die in einem organischen Lösungsmittel, das das Alpha-Olefinmonomer
nicht beinhaltet, suspendiert oder aufgelöst ist, in einem nicht absorbierten
Zustand oder in einem absorbierten Zustand mit der zweiten chemischen
Einheit, die den ausgewählten
Cokatalysator aufweist, die nicht in einem organischen Lösungsmittel
suspendiert oder aufgelöst
ist, in einem nicht absorbierten Zustand oder in einem absorbierten
Zustand, gefolgt von Mischen mit dem Alpha-Olefinmonomer, (2) Mischen
der ersten chemischen Einheit, die den Präkatalysator 1 oder 2 aufweist,
die in einem organischen Lösungsmittel,
das nicht das Alpha-Olefinmonomer beinhaltet, suspendiert oder aufgelöst ist,
in einem nicht absorbierten Zustand oder in einem absorbierten Zustand
mit der zweiten chemischen Einheit, die den ausgewählten Cokatalysator
aufweist, die in einem organischen Lösungsmittel, das nicht das
Alpha-Olefinmonomer
beinhaltet, suspendiert oder aufgelöst ist, in einem nicht absorbierten
Zustand oder in einem absorbierten Zustand, gefolgt von Mischen
mit dem Alpha-Olefinmonomer, (3) Mischen der ersten chemischen Einheit,
die den Präkatalysator
1 oder 2 aufweist, die nicht in einem organischen Lösungsmittel
suspendiert oder aufgelöst
ist, in einem nicht absorbierten Zustand oder in einem absorbierten
Zustand mit der zweiten chemischen Einheit, die den ausgewählten Cokatalysator
aufweist, der in einem organischen Lösungsmittel, das nicht das
Alpha-Olefinmonomer beinhaltet, suspendiert oder aufgelöst ist,
in einem nicht absorbierten Zustand oder in einem absorbierten Zustand,
gefolgt von Mischen mit dem Alpha-Olefinmonomer, und (4) Mischen
der ersten chemischen Einheit, die den Präkatalysator 1 oder 2 aufweist,
die nicht in einem organischen Lösungsmittel
suspendiert oder aufgelöst
ist, in einem nicht absorbierten Zustand oder in einem absorbierten
Zustand mit der zweiten chemischen Einheit, die den ausgewählten Cokatalysator
aufweist, die nicht in einem organischen Lösungsmittel suspendiert oder
aufgelöst
ist, in einem nicht absorbierten Zustand oder in einem absorbierten
Zustand, gefolgt von Mischen mit dem Alpha-Olefinmonomer.
-
In
Kategorie (B) zur Bildung des katalytischen Polymerisationssystems
gemäß den oben
beschriebenen vier alternativen Verfahren ist das Alpha-Olefinmonomer
entweder eine flüssige
Phase oder eine Gasphase zum Mischen mit der anfänglich gebildeten Flüssigphasenmischung
oder der Festphasenmischung der ersten chemischen Einheit, die den
Präkatalysator
1 oder 2 aufweist, und der zweiten chemischen Einheit, die den ausgewählten Cokatalysator
aufweist. Entsprechend wird das Flüssigphasen-Alpha-Olefinmonomer
zu der anfänglich
gebildeten Flüssigphasenmischung
oder der Festphasenmischung der ersten chemischen Einheit, die den
Präkatalysator
1 oder 2 aufweist, und der zweiten chemischen Einheit, die den ausgewählten Cokatalysator
aufweist, hinzugegeben. Alternativ wird das Gasphasen-Alpha-Olefinmonomer in
und/oder durch die anfänglich
gebildete Flüssigphasenmischung
oder Festphasenmischung der ersten chemischen Einheit, die den Präkatalysator
1 oder 2 aufweist, und der zweiten chemischen Einheit, die den ausgewählten Cokatalysator aufweist,
hindurch geblubbert.
-
Gemäß des zuvor
beschriebenen Schritt (b) gibt es besondere Formen des Präkatalysators
1 oder 2, zum Beispiel Diphenylatlanthanidkomplexe, die die katalytische
Polymerisation des Alpha-Olefinmonomers bewirken können, ohne
durch einen Cokatalysator aktiviert zu werden, wobei es der Herstellung
der ersten chemischen Einheit, die die besondere Form des Diamindiphenolatpräkatalysators
1 oder 2 gemäß dem zuvor beschriebenen
Schritt (b) aufweist, folgend keinen Bedarf zur Herstellung der
zweiten chemischen Einheit, die den ausgewählten Cokatalysator aufweist,
gemäß den zuvor
beschriebenen Schritte (c) und (d) gibt. Somit wird im alternativen
Schritt (e) ein katalytisches Polymerisationsreaktionssystem für die katalytische
Polymerisation des Alpha-Olefinmonomers durch Mischen (i) der ersten
chemischen Einheit, die die besondere Form des Diamindiphenolatpräkatalysators
1 oder 2 aufweist, die in flüssiger
Phase oder in flüssiger
oder fester Phase in einem nicht-adsorbierten Zustand oder in einem
adsorbierten Zustand suspendiert oder aufgelöst ist, ohne das Alpha-Olefinmonomer
zu enthalten, gemäß dem zuvor
beschriebenen Schritt (b), mit (ii) dem zu polymerisierenden Alpha-Olefinmonomer
gebildet. Entsprechend wird Flüssigphasen-Alpha-Olefinmonomer
zu der anfänglich
hergestellten Flüssigphase
oder Festphase der ersten chemischen Einheit, die den Präkatalysator
1 oder 2 in einem nicht-adsorbierten Zustand oder in einem adsorbierten
Zustand aufweist, hinzugegeben. Alternativ wird das Gasphasen-Alpha-Olefinmonomer
in und/oder durch die anfänglich
hergestellte Flüssigphase
oder Festphase der ersten chemischen Einheit, die den Präkatalysator
1 oder 2 in einem nicht adsorbierten Zustand oder in einem adsorbierten
Zustand aufweist, hindurch geblubbert.
-
Unabhängig von
der tatsächlichen
Reihenfolge oder Sequenz des Mischens der chemischen Einheiten resultiert
die Vervollständigung
von Schritt (e) in der Bildung des katalytischen Polymerisationsreaktionssystems
für die
katalytische Polymerisation des Alpha-Olefinmonomers, einschließlich (i)
der ersten chemischen Einheit, die die besondere Form des Diamindiphenolatpräkatalysators
1 oder 2 von Schritt (b) in einem nicht adsorbierten Zustand oder
in einem adsorbierten Zustand aufweist, (ii) der zweiten chemische
Einheit, die den ausgewählten
Cokatalysator von Schritt (d) in einem nicht adsorbierten Zustand
oder in einem adsorbierten Zustand aufweist, und (iii) des zu polymerisierenden
Alpha-Olefinmonomers. Alternativ resultiert die Vervollständigung
von Schritt (e) in der Bildung des katalytischen Polymerisationsreaktionssystems
für die
katalytische Polymerisation des Alpha-Olefinmonomers, einschließlich (i)
der ersten chemischen Einheit, die die besondere Form des Diamindiphenolatpräkatalysators
1 oder 2 von Schritt (b) in einem nicht adsorbierten Zustand oder
in einem adsorbierten Zustand aufweist, und (ii) des zu polymerisierenden
Alpha-Olefinmonomers.
-
Die
Bedingungen zur Durchführung
von Schritt (a) bis Schritt (e) sind bevorzugt Raumtemperatur unter Ausschluss
von Feuchtigkeit und Sauerstoff, um Hydrolyse oder Oxidation entweder
des Präkatalysators
1 oder 2 oder des ausgewählten
Cokatalysators zu verhindern.
-
In
der Praxis beinhaltet die Ausführung
des Verfahrens zur katalytischen Polymerisation eines Alpha-Olefinmonomers
gemäß der vorliegenden
Erfindung bevorzugt die Durchführung
des oben beschriebenen Schritt (e) zur Bildung eines katalytischen
Polymerisationsreaktionssystems zur katalytischen Polymerisation des
Alpha-Olefinmonomers durch Mischen (i) der ersten chemischen Einheit,
die die besondere Form des Diamindiphenolatpräkatalysators 1 oder 2 von Schritt
(b) aufweist, mit (ii) der zweiten chemische Einheit des ausgewählten Cokatalysators
von Schritt (d) mit (iii) dem Alpha-Olefinmonomer, welches polymerisiert
werden soll, gemäß einem
besonderen Verfahren, das aus Kategorie (A) oder Kategorie (B) ausgewählt wird.
-
Im
Prinzip kann die komplexe chemische Einheit, die als Ergebnis des
Mischens der ersten chemischen Einheit, die den Präkatalysators
1 oder 2 in Abwesenheit des Alpha-Olefinmonomers in einem nicht adsorbierten
Zustand oder in einem adsorbierten Zustand aufweist, mit der zweiten
chemischen Einheit, die den ausgewählten Cokatalysators ebenfalls
in Abwesenheit des Alpha-Olefinmonomers in einem nicht adsorbierten
Zustand oder in einem adsorbierten Zustand aufweist, gebildet wird,
isoliert werden und so wie sie ist, kurzfristig oder langfristig,
gemäß der Stabilität einer
solchen komplexen chemischen Einheit ohne die komplexe chemische
Einheit sofort einem Alpha-Olefinmonomer zur Bildung eines katalytischen
Polymerisationsreaktionssystems zur katalytischen Polymerisation
eines Alpha-Olefinmonomers auszusetzen, gehalten werden. In diesem
Fall wird die komplexe chemische Einheit, die durch Aktivieren des
Präkatalysators
1 oder 2 mit dem ausgewählten
Cokatalysator in Abwesenheit des Alpha-Olefinmonomers als ein "aktivier" Katalysator für die katalytische
Polymerisation eines Alpha-Olefinmonomers
wirksam angesehen werden, so dass durch separates Hinzufügen eines
Alpha-Olefinmonomers zu der komplexen chemischen Einheit ein katalytisches
Polymerisationsreaktionssystem für
die katalytischen Polymerisation des Alpha-Olefinmonomers in Übereinstimmung mit
der zuvor beschriebenen Kategorie (B) von Schritt (e) gebildet wird.
-
In
Schritt (f) wird das katalytische Polymerisationsreaktionssystem
für eine
Dauer im Bereich von ungefähr
5 Sekunden bis ungefähr
12 Stunden gerührt.
Ausgehend von der Initiierung der Polymerisationsreaktion und einschließlich der
Dauer des Rührens
des Reaktionssystems kann exotherme Wärme aus dem Reaktionssystem
freigesetzt werden, begleitet von einer möglichen Farbänderung
des Reaktionssystems. Die katalytische Polymerisation kann bei verschiedenen
Temperaturen durchgeführt
werden. Externes Kühlen
zum Beispiel herunter auf ungefähr
0°C kann
zur Verlangsamung der katalytischen Polymerisation verwendet werden.
Erwärmen,
zum Beispiel auf Rückflusstemperatur,
beschleunigt die Reaktion.
-
Zusätzlich wird
in Schritt (f) mindestens eine andere Art und Menge eines chemischen
Reagenzes zur Verbesserung der Polymerisationsreaktion zu dem katalytischen
Polymerisationsreaktionssystem hinzugegeben. Zum Beispiel wird manchmal
Wasserstoffgas zu dem katalytischen Polymerisationsreaktionssystem
zur Verbesserung der Kontrolle des Molekulargewichtes der resultierenden
Poly(Alpha-Olefin)-Produkte
hinzugegeben.
-
In
Schritt (g) wir die katalytische Polymerisationsreaktion durch Verwenden
von Reaktionsbedingungen, die aus der Gruppe, die aus (i) Hinzufügen eines
externen Quenchers, wie zum Beispiel ein protisches Lösungsmittel,
(ii) vollständiger Verbrauch
des Monomers und (iii) Deaktivieren des Katalysators, der zuvor
gemäß dem oben
geschriebenen Schritt (e) gebildet wurde, besteht, ausgewählt wird,
die einen Komplex der ersten chemischen Einheit, die die besondere
Form des Diamindiphenolatpräkatalysators
1 oder 2 von Schritt (b) aufweist, der mit der zweiten chemischen
Einheit des ausgewählten
Cokatalysators von Schritt (d) gemischt wird, beendet.
-
In
Schritt (h) wird das Polymerprodukt durch das folgende Verfahren
isoliert. Überschüssiger Präkatalysator
1 oder 2 und/oder der ausgewählte
Cokatalysator können
hydrolysiert werden. Die Isolierung des Polymerprodukts aus dem
Lösungsmittel
und/oder dem restlichen Alpha-Olefinmonomer in der Lösung hängt von der
Löslichkeit
des Polymerproduktes ab. Im Falle eines unlöslichen Polymerproduktes, zum
Beispiel Polyethylen, beinhaltet das Isolierungsverfahren die Filtration
und Trocknung, wohingegen im Falle eines löslichen Polymerproduktes flüchtige Spezies
durch Destillation entfernt werden und das Polymerprodukt dann getrocknet
wird. Verunreinigungen, wie zum Beispiel Zersetzungsprodukte des
Präkatalysator
1 oder 2 und/oder des ausgewählten
Cokatalysators, werden typischerweise weggewaschen.
-
In
Schritt (i) werden die physiochemischen Eigenschaften und Charakteristika
der Poly(Alpha-Olefin)-Produkte, die durch das katalytische Polymerisationsreaktionssystem
hergestellt wurden, durch verschiedene Techniken gemessen und analysiert,
zum Beispiel der Schmelzpunkt, Spektroskopie, wie zum Beispiel NMR,
Röntgenkristallographie,
mechanische Festigkeit, wie zum Beispiel Elastizität, etc.
Strukturinformation und Molekulargewichtsinformation, die die molekulare
Gewichtsverteilung des Polymers betreffen, werden über den
Polydispersitätsindex
(PDI) ebenfalls bestimmt.
-
Um
das große
Potential des Diamindiphenolatpräkatalysators
1 der vorliegenden Erfindung für
die taktische katalytische Polymerisation von Alpha-Olefinmonomeren
zu veranschaulichen, werden Glanzpunkte des in den Beispielen 13
und 14 beschriebenen katalytischen Polymerisationsreaktionssystem
hier bereitgestellt.
-
Der
Diamindiphenolatpräkatalysator
1, in der ersten beispielhaften besonderen Form, die oben beschrieben
ist, nämlich
hexakoordinierter Dialkyldiamindiphenolatpräkatalysator 1 [{N,N'-Bis(3,5-di-tert-butyl-2-hydroxyphenylmethyl)-N,N'-dimethylethylendiamin}zirkoniumdibenzyl]
16, wird durch Bor-Lewis-Säure, B(C6F5)3 in
Gegenwart von wenig 1-Hexen bei Raumtemperatur unter Stickstoffgasineratmosphäre aktiviert, wobei
1-Hexen sowohl als das zu polymerisierende Ziel-Alpha-Olefinmonomer als
auch als Auflösungslösungsmittel
für den
Präkatalysator
16 und für
den Bor-Cokatalysator fungiert.
-
Bei
diesen Reaktionsbedingungen wird Poly(1-hexen) gebildet, welches
interessanterweise hoch isotaktisch ist, wobei es zu einem Ausmaß oder Grad
größer als
95% klassifizierbar ist, wie durch 13C NMR
Spektrum des resultierenden Polymers, wie in 2 gezeigt,
abgeleitet wird. Das nach 30 min erhaltene Polymer hat ein Gewichtsmittelwert
des Molekulargewichts vom MW = 12.000 Gramm/Mol
und einen PDI von 1.15. Der enge PDI und die lineare Abhängigkeit
des Gewichtsmittelwert des Molekulargewichts von dem Verbrauch des Monomers,
die in 3 gezeigt ist, zeigt, dass dieses besondere katalytische
Polymerisierungssystem als lebend klassifizierbar ist.
-
In
einem anderen Beispiel wird hexakoordinierter Dialkyldiamindiphenolatpräkatalysator [{N,N'-Bis(3,5-dimethyl-2-hydroxyphenylmethyl)-N,N'-dimethylethylendiamin}zirkoniumdibenzyl]
17 durch Bor-Lewis-Säure Cokatalysator,
B(C6F5)3,
in Gegenwart von reinen 1-Hexen bei Raumtemperatur unter Stickstoffgasineratmosphäre aktiviert,
wobei erneut 1-Hexen sowohl als das zu polymerisierende Ziel-Alpha-Olefinmonomer
als auch als Lösungsmittel
für den
Präkatalysator
17 und für
den Bor-Cokatalysator
fungiert. Das in diesem Falle erhaltene Polymer hat ein Gewichtsmittelwert
des Molekulargewichts von MW = 23.000 Gramm/Mol
und einen PDI von 1.57. Dieses Polymer ist gemäß seines 13C
NMR Spektrums, was in 4 gezeigt ist, als ataktisch
klassifizierbar.
-
Die
katalytische Aktivität
des Diamindiphenolatpräkatalysators
1 der vorliegenden Erfindung, die teilweise veranschaulicht wird
durch besondere Formen des sechsfach koordinierten Diamindiphenolatkomplexes,
den Präkatalysator
[{N,N'-Bis(3,5-di-tert-butyl-2-hydroxyphenylmethyl)-N,N'-dimethylethylendiamin}zirkoniumdibenzyl]
16, die unter den oben beschriebenen Reaktionsbedingungen arbeitet,
ist das erste Beispiel eines nicht-Metallocen Katalysators, der
sowohl isospezifische als auch lebende Polymerisation von Alpha-Olefinmonomeren
erzeugt.
-
Zusätzliche
Gegenstände,
Vorteile und neue Merkmale der vorliegenden Erfindung werden dem Durchschnittsfachmann
nach Prüfen
der folgenden Beispiele, welche nicht als beschränkend anzusehen sind, offensichtlich
werden. Zusätzlich
finden alle verschiedenen Ausführungsformen
und Aspekte der vorliegenden Erfindung, wie hier beschrieben und
unten im Anspruchsteil beansprucht, experimentelle Unterstützung in
den folgenden Beispielen.
-
Bezug
wird nun auf die folgenden Beispiele genommen, welche zusammen mit
der obigen Beschreibung die Erfindung in einer nicht beschränkenden
Art und Weise veranschaulichen. Details der Synthesen von acht unterschiedlichen
besonderen Formen des allgemeinen Diamindi(2-hydroxyarylmethyl)-Ligandprecursors 6
sind unten in den Beispielen 1 bis 8 bereitgestellt. Details der
Synthesen und spektroskopische und Röntgendaten der resultierenden
Strukturen der entsprechenden Beispielformen des Diamindiphenolatpräkatalysators
1 der vorliegenden Erfindung sind in den Beispielen 9 bis 12 unten
bereitgestellt.
-
Details
der katalytischen Polymerisation eines beispielhaften Alpha-Olefinmonomers,
1-Hexen, unter Verwendung der besonderen Form 16 oder der besonderen
Form 17 des Diamindiphenolatpräkatalysators
1, die der isotaktischen katalytischen Polymerisation oder der ataktischen
katalytischen Polymerisation in Übereinstimmung
mit dem Verfahren der vorliegenden Erfindung entsprechen, zur Bildung
von isotaktischem Poly(1-hexen) bzw. ataktischen Poly(1-hexen) und die betreffenden
empirischen Daten davon werden hier in den Beispielen 13 bzw. 14
bereitgestellt. Die Referenznummern der chemischen Spezies und Strukturen,
die in den folgenden Beispielen auftauchen, sind denen, die in der
obigen Beschreibung der bevorzugten Ausführungsformen angegeben sind,
identisch.
-
Beispiel 1
-
Synthese des Diamindi(2-hydroxyarylmethyl)-Ligandprecursors
[{N,N'-Bis(3,5-di-tert-butyl-2-hydroxyphenylmethyl)-N,N'-dimethylethylendiamin] 7.
-
Eine
Mischung von 2,4-Di-tert-butylphenol (50 mmol), N,N'-Dimethylethylendiamin (25 mmol) und
37% wässriges
Formaldehyd (50 mmol) wurden für
2 h in refluxierendem Methanol gerührt. Die Mischung wurde auf
Raumtemperatur abgekühlt
und der Feststoff wurde abfiltriert und mit Methanol gewaschen,
was den Ligandprecursor 7 in 70% ergab.
Schmelzpunkt des Ligandprecursors
7 war 150–151°C.
Spektroskopische
Daten des Ligandprecursors 7. 1H NMR (200 MHz, CDCl3) δ 10.70 (s,
2H, OH), 7.20 (d, J = 2.3 Hz, 2H, Ar), 6.80 (d, J = 2.3 Hz, 2H,
Ar), 3.66 (s, 4H, Ar-CH2-N), 2.63 (s, 4H,
N-CH2), 2.26 (s, 6H NCH3), 1.40
(s, 18H, C(CH3)3),
1.27 (s, 18H, C(CH3)3). 13C NMR (50.4 MHz, CDCl3) δ 154.2, 140.6,
135.7, 123.3, 123.0, 121.0, 62.7 (Ar-CH2-N),
53.8 (N-CH2), 41.6 (NCH3),
34.7 (C(CH3)3),
34.1 (C(CH3)3),
31.7 (C(CH3)3),
29.6 (C(CH3)3).
HRMS
(Hochauflösende
Massenspektrometrie) des Ligandprecursor 7: berechnet 524.43418
und beobachtet 524.43413.
-
Beispiel 2
-
Synthese des Diamindi(2-hydroxyarylmethyl)-Ligandprecursors
[{N,N'-Bis(3,5-dimethyl-2-hydroxyphenylmethyl)-N,N'-dimethylethylendiamin] 8.
-
Eine
Mischung von 2,4-Dimethylphenyl (50 mmol), N,N'-Dimethylethylendiamin
(25 mmol) und 37% wässriges
Formaldehyd (50 mmol) wurden für
2 h in refluxierendem Methanol gerührt. Die Mischung wurde auf
Raumtemperatur abgekühlt
und der Feststoff wurde filtriert und mit Methanol gewaschen, was
den Ligandprecursor 8 in 50% ergab.
Schmelzpunkt des Ligandprecursors
8 war 120–121°C.
Spektroskopische
Daten des Ligandprecursors 8. 1NMR (200
MHz, CDCl3) δ 10.57 (s, 2H, OH), 6.87 (s,
2H, Ar), 6.62 (s, 2H, Ar), 3.63 (s, 4H, Ar-CH2-N),
2.66 (s, 4H, N-CH2), 2.27 (s, 6H, NCH3), 2.22 (s, 6H, CH3),
2.20 (s, 6H, CH3). 13C
NMR (50.4 MHz, CDCl3) δ 153.4, 130.6, 127.5, 126.6,
124.6, 120.6, 61.8 (CH2), 54.1 (CH2), 50.1 (CH3), 20.4
(CH3), 15.5 (CH3).
HRMS
(Hochauflösende
Massenspektrometrie) des Ligandprecursors 8: berechnet 356.24638
und beobachtet 356.24642.
-
Beispiel 3
-
Synthese des Diamindi(2-hydroxyarylmethyl)-Ligandprecursors
[{N,N'-Bis(3,5-di-tert-butyl-2-hydroxyphenylmethyl)-N,N'-dibenzylethylendiamin] 9.
-
Eine
Mischung von 2,4-Di-tert-butylphenol (50 mmol), N,N'-Dibenzylethylendiamin (25 mmol) und
37% wässriges
Formaldehyd (50 mmol) wurden für
2 h in refluxierendem Methanol gerührt. Die Mischung wurde auf
Raumtemperatur abgekühlt
und das resultierende Öl
wurde von der wässrigen
Schicht, welche verworfen wurde, getrennt und verdampft. Das Produkt
wurde dann mit Hexan ausgefällt,
filtriert und mit Hexan gewaschen, was den Ligandprecursor 9 in
40% ergab. Die spektroskopische Daten (nicht gezeigt) unterstützen die Bildung
des Ligandprecursors 9.
-
Beispiel 4
-
Synthese des Diamindi(2-hydroxyarylmethyl)-Ligandprecursors
[{N,N'-Bis(3,5-di-tert-butyl-2-hydroxyphenylmethyl)-N,N'-diethylethylendiamin] 10.
-
Eine
Mischung von 2,4-Di-tert-butylphenol (50 mmol), N,N'-Diethylethylendiamin (25 mmol) und 37% wässriges
Formaldehyd (50 mmol) wurden in refluxierendem Methanol für 2 h gerührt. Die
Mischung wurde auf Raumtemperatur abgekühlt und der Feststoff wurde
abfiltriert und mit Methanol gewaschen, was 10 zu 40% ergab. Die
spektroskopischen Daten (nicht gezeigt) unterstützen die Bildung des Ligandprecursors
10.
-
Beispiel 5
-
Synthese des Diamindi(2-hydroxyarylmethyl)-Ligandprecursors
[{N,N'-Bis(4,5-dimethyl-2-hydroxyphenylmethyl)-N,N'-dimethylethylendiamin] 11.
-
Eine
Mischung von 3,4-Dimethylphenol (50 mmol), N,N'-Dimethylethylendiamin
(25 mmol) und 37% wässriges
Formaldehyd (50 mmol) wurden für
2 h in refluxierendem Methanol gerührt. Die Mischung wurde auf
Raumtemperatur abgekühlt
und der Feststoff wurde filtriert und mit Methanol gewaschen, was
11 zu 45% ergab. Die spektroskopischen Daten (nicht gezeigt) unterstützen die
Bildung des Ligandprecursors 11.
-
Beispiel 6
-
Synthese des Diamindi(2-hydroxyarylmethyl)-Ligandprecursors
[{N,N'-Bis(3,5-di-tert-butyl-2-hydroxyphenylmethyl)-N,N'-dimethyl-1,3-propandiamin] 12.
-
Eine
Mischung von 2,4-Di-tert-butylphenol (50 mmol), N,N'-Dimethyl-1,3-propandiamin (25 mmol)
und 37% wässriges
Formaldehyd (50 mmol) wurden für
12 h in refluxierendem Methanol gerührt. Die Mischung wurde auf
Raumtemperatur abgekühlt
und der Feststoff wurde filtriert und mit Methanol gewaschen, was
12 zu 40% ergab. Die spektroskopischen Daten (nicht gezeigt) unterstützen die
Bildung des Ligandprecursors 12.
-
Beispiel 7
-
Synthese des Diamindi(2-hydroxyarylmethyl)-Ligandprecursors
[{N,N'-Bis(3,5-di-tert-butyl-2-hydroxyphenylmethyl)ethylendiamin]
13.
-
Eine
Mischung von 2,4-Di-tert-butylphenol (50 mmol), Ethylendiamin (25
mmol) und 37% wässriges Formaldehyd
(50 mmol) wurden für
2 h in refluxierendem Methanol gerührt. Die Mischung wurde auf
Raumtemperatur abgekühlt
und der Feststoff wurde abfiltriert und mit Methanol gewaschen,
was 13 zu 45% ergab. Die spektroskopischen Daten (nicht gezeigt)
unterstützen
die Bildung des Ligandprecursors 13.
-
Beispiel 8
-
Synthese des Diamindi(2-hydroxyarylmethyl)-Ligandprecursors
[{N,N'-Bis(3,5-di-tert-butyl-2-hydroxyphenylmethyl)-1,3-propandiamin] 14.
-
Eine
Mischung von 2,4-Di-tert-butylphenol (50 mmol), Propan-1,3-diamin (25 mmol)
und 37% wässriges
Formaldehyd (50 mmol) wurden für
2 h in refluxierendem Methanol gerührt. Die Mischung wurde auf Raumtemperatur
abgekühlt
und der Feststoff wurde filtriert und mit Methanol gewaschen, was
14 zu 10% ergab. Die spektroskopischen Daten (nicht gezeigt) unterstützen die
Bildung des Ligandprecursors 14.
-
Beispiel 9
-
Synthese des Diamindiphenolatpräkatalysators
[{N,N'-Bis(3,5-di-tert-butyl-2-hydroxyphenylmethyl)-N,N'-dimethylethylendiamin}zirkoniumdibenzyl]
16
-
Eine
Lösung
des Diamindi(2-hydroxyarylmethyl)-Ligandprecursors [{N,N'-Bis(3,5-di-tert-butyl-2-hydroxyphenylmethyl)-N,N'-dimethylethylendiamin]
7, wie gemäß Beispiel
1 hergestellt, (200 mg, 0.38 mmol) in Toluol (10 ml) wurden tropfenweise
zu einer Lösung
von Tetra(benzyl)zirkonium 15 (0.38 mmol) in Toluol (10 ml) bei
Raumtemperatur unter Stickstoffgasinertatmosphäre hinzugegeben. Die Reaktionsmischung
wurde dann auf 65°C
erwärmt
und für
2 Stunden gerührt.
Das Toluol wurde aus der Reaktionsmischung unter geringem Druck
entfernt, um reinen Präkatalysator
16 quantitativ als einen gelben Feststoff zu ergeben.
Spektroskopische
Daten des Präkatalysators
16.
1NMR (200 MHz, C
6D
6) δ 7.62
(d, J = 2.4 Hz, 2H), 7.20 (d, J = 7.5 Hz, 4H), 7.04 (t, J = 7.4
Hz, 4H), 6.77 (t, J = 7.2 Hz, 2H), 6.76 (d, J = 2.2 Hz, 2H), 3.69
(d, J = 13.7 Hz, 2H, CH
2 AX System 1), 2.82
(d, J = 10.3, 2H, CH
2 AX System 2), 2.63
(d, J = 9.3 Hz, 2H, CH
2 AX System 3), 2.43
(d, J = 10.0 Hz, 2H, CH
2 AX System 2), 2.36
(d, J = 13.6 Hz, 2H, CH
2 AX System 1), 1.82
(s, 18H, CH
3), 1.70 (s, 6H, NCH
3),
1.34 (s, 18H, CH
3), 0.83 (d, J = 9.4 Hz,
2H, CH
2 AX System 3).
13C
NMR (126 MHz, C
6D
6) δ 157.7, 149.2,
141.9, 138.1, 129.3, 127.9, 126.1, 125.8, 125.0, 122.2, 69.6 (CH
2), 65.0 (CH
2), 53.5
(CH
3), 46.3 (CH
2),
36.4 (C(CH
3)
3),
35.1 (C(CH
3)
3),
32.6 (C(CH
3)
3, 31.1
(C(CH
3)
3).
-
Die
spektroskopischen Daten des Präkatalysators
16 stimmen mit einem einzelnen Stereoisomer überein, das symmetrisch verwandte
Phenolatringe, zwei symmetrisch verwandte Benzylgruppen und drei
AX Spinsysteme aufweist. Dies deutet auf einen Chelat mit C2 Symmetrie auf der NMR Zeitskala hin.
-
(Röntgen)-Kristallographische
Daten für
den Präkatalysator
2(C48H68N2O2Zr)·3 (C7H8) 16: M = 1868.93,
monokline Raumgruppe P21/c, a = 31.0080
(5), b = 11.9200 (3), c = 29.7910 (7) Å, β = 107.994 (1)°, U = 10472.6
(4) Å3, Z = 4, Dc = 1.185 g cm–3 μ(Mo-Kα) = 0.252 mm–1,
T = 115 K, Enraf-Nonius Kappa-CCD, 19001 rReflexion wurde gemessen
(Rint = 0.000). Die Endverfeinerung konvergierte bei R1 = 0.0493
and wR2 = 0.1157 zur Beobachtung mit [I > 2σ(I)]
und R1 = 0.0852 and wR2 = 0.1323 für alle Daten.
-
Die
(Röntgen)-Kristallographischen
Daten unterstützen
die spektroskopischen Daten, was auf einen Komplex mit einer C2 Symmetrie hindeutet. Die Röntgenstruktur
des Präkatalysators [(2,4-Di-t-Bu-Ar-O)CH2-N(CH3)]2-(CH2)2-Zr(CH2Ph)2 16, in 1 gezeigt,
deutet auf eine Struktur hin, die einen mononuklearen Zirkoniumchelat
mit einer leicht fehlgeordneten oktahedralen Geometrie, einschließlich zweier koordinativer
Bindungen zwischen Zr und jedem der zwei Stickstoffatome aufweist.
Die zwei Benzylgruppen sind in einer cis Konfiguration, wie für die Alpha-Olefinpolymerisationskatalyse
erforderlich.
-
Beispiel 10
-
Synthese des Diamindiphenolatpräkatalysators
[{N,N'-Bis(3,5-dimethyl-2-hydroxyphenylmethyl)-N,N'-dimethylethylendiamin}zirkoniumdibenzyl]
17.
-
Eine
Lösung
des Diamindi(2-hydroxyarylmethyl)-Ligandprecursors [(2,4-Di-Me-Ar-O)CH
2-N(CH
3)]
2-(CH
2)
2 8,
wie gemäß Beispiel
2 2 synthetisiert, (135 mg, 0.38 mmol) in Toluol (10 ml) wurde tropfenweise
zu einer Lösung
von Tetra(benzyl)zirkonium 15 (0.38 mmol) in Toluol (10 ml) bei Raumtemperatur
unter Stickstoffgasinertatmosphäre
hinzugegeben. Die Reaktionsmischung wurde dann auf 65°C erwärmt und
für 2 h
gerührt.
Das Toluol wurde aus der Reaktionsmischung unter verringertem Druck
entfernt, um reinen Präkatalysator
17 quantitativ als einen gelben Feststoff zu ergeben.
Spektroskopische
Daten des Präkatalysators
17.
1H NMR (200 MHz, C
6D
6) δ 7.12
(m, 8H), 6.96 (d, J = 1.3 Hz, 2H), 6.87 (t, J = 7.0 Hz, 2H), 6.42
(d, J = 1.3 Hz, 2H), 3.95 (d, J = 13.6 Hz, 2H, CH
2 AX
System 1), 2.51 (d, J = 9.1 Hz, 2H, CH
2 AX
System 2), 2.43 (s, 6H, CH
3), 2.34 (d, J
= 14.0 Hz, 2H, CH
2 AX System 1), 2.32 (d,
J = 11.5 Hz, 2H, CH
2 AX System 3), 2.21
(s, 6H, CH
3), 2.12 (d, J = 10.9 Hz, 2H,
CH
2 AX System 3), 1.73 (s, 6H, CH
3), 0.81 (d, J = 9.0, 2H, CH
2 AX
System 2).
13C NMR (126 MHz, C
6D
6) δ 157.0,
147.7, 132.4, 129.7, 129.3, 129.1, 127.3, 127.1, 125.2, 122.9, 69.6
(CH
2), 64.2 (CH
2),
63.5 (CH
2), 53.6 (CH
2),
45.0 (CH
3) 21.4 (CH
3),
17.9 (CH
3).
-
Beispiel 11
-
Synthese des Diamindiphenolatpräkatalysators
[{N,N'-Bis(3,5-di-tert-butyl-2-hydroxyphenylmethyl)-N,N'-dibenzylethylendiamin}zirkoniumdibenzyl]
18.
-
Eine
Lösung
des Diamindi(2-hydroxyarylmethyl)-Ligandprecursors [(2,4-Di-t-Bu-Ar-O)CH2-N(CH2Ph)]2-(CH2)2 9,
wie gemäß Beispiel
3 synthetisiert, (257 mg, 0.38 mmol) in Toluol (10 ml) wurde tropfenweise
zu einer Lösung
von Tetra(benzyl)zirkonium 15 (0.38 mmol) in Toluol (10 ml) bei Raumtemperatur
unter Stickstoffgasinertatmosphäre
hinzugegeben. Die Reaktionsmischung wurde dann auf 65°C erwärmt und
für 2 Stunden
gerührt.
Das Toluol wurde aus der Reaktionsmischung unter verringertem Druck
entfernt, um reinen Präkatalysator
18 quantitativ als einen gelben Feststoff zu ergeben.
-
-
Die
spektroskopischen Daten (nicht gezeigt) unterstützen die Bildung des Präkatalysators
18.
-
Beispiel 12
-
Synthese des Diamindiphenolatpräkatalysators
[{N,N'-Bis(3,5-di-tert-butyl-2-hydroxyphenylmethyl)-N,N'-diethylethylendiamin}zirkoniumdibenzyl]
19.
-
Eine
Lösung
des Diamindi(2-hydroxyarylmethyl)-Ligandprecursors [(2,4-Di-t-Bu-Ar-O)CH2-N(CH2CH3)]2-(CH2)2 10, wie gemäß Beispiel 4 synthetisiert,
(210 mg, 0.38 mmol) in Toluol (10 ml) wurde tropfenweise zu einer
Lösung
von Tetra(benzyl)zirkonium 15 (0.38 mmol) in Toluol (10 ml) bei
Raumtemperatur unter Stickstoffgasinertatmosphäre hinzugegeben. Die Reaktionsmischung
wurde dann auf 65°C
erwärmt
und für
2 Stunden gerührt.
Das Toluol wurde aus der Reaktionsmischung unter verringertem Druck
entfernt, um reinen Präkatalysator
19 quantitativ als einen gelben Feststoff zu ergeben.
-
Die
spektroskopischen Daten (nicht gezeigt) unterstützen die Bildung des Präkatalysators
19.
-
-
Beispiel 13
-
Isotaktische und lebende
Polymerisation eines 1-Hexenmonomers unter Verwendung des Diamindiphenolatpräkatalysators
[{N,N'-Bis(3,5-di-tert-butyl-2-hydroxyphenylmethyl)-N,N'-dimethylethylendiamin}zirkoniumdibenzyl]
16.
-
Die
Daten, die mit diesem katalytischen Polymerisationsreaktionssystem
verbunden sind, weisen klar auf ein isotaktisches und im wesentlichen
lebendes Polymerisationssystem hin. Zu einer Lösung des Präkatalysators 16 (0.032 mmol)
in 1-Hexen (1 ml) wurde eine Lösung
des Cokatalysators B(C6F5)3 (1.1 Äquivalente) in
1-Hexen (1 ml) bei
Raumtemperatur unter Stickstoffgasinertatmosphäre hinzugegeben. Die Reaktionsmischung
wurde für
30 Minuten gerührt.
Der restliche 1-Hexenmonomerreaktant/Lösungsmittel wurde aus der Reaktionsmischung
unter verringertem Druck entfernt, um stark isotaktisches Poly(1-hexen)
als ein farbloses Öl
zu erhalten, welches zu einen Ausmaß oder Grad von mehr als 95%
klassifizierbar ist.
-
Die
aus diesen Reaktionsdaten berechnete katalytische Aktivität: (18 g
hergestelltes Poly(1-hexen))/(mmol-pre-cat.hr).
-
Erhaltender
Gewichtsmittelwert des Molekulargewichts: MW =
12.000 Gramm/Mol mit einen PDI von 1.15, der relativ nah einem PDI
von 1 ist, was für
ein lebendes System charakteristisch ist. Die Abhängigkeit des
massengemittelten Molekulargewichts Mw von
dem Verbrauch des Monomer (mg) ist in 3 veranschaulicht.
-
Spektroskopische
Daten des isotaktischen Poly(1-hexen) Produkts. 1H
NMR (500 MHz, CDCl3): 1.21 (m, 8H, CH2), 0.99 (br, 1H, CH), 0.84 (t, J = 7.1 Hz,
3H, CH3), 13C NMR
(126 MHz, CDCl3) (siehe 2):
41.21 (CH2), 35.56 (CH2),
33.36 (CH), 29.67 (CH2), 24.17 (CH2), 15.10 (CH3).
-
Beispiel 14
-
Ataktische Polymerisation
des 1-Hexenmonomers unter Verwendung des Diamindiphenolatpräkatalysators [{N,N'-Bis(3,5-dimethyl-2-hydroxyphenylmethyl)-N,N'-dimethylethylendiamin}zirkoniumdibenzyl]
17.
-
Die
Daten, die mit diesem katalytischen Polymerisationsreaktionssystem
verbunden sind, weisen klar auf ein ataktisches und im Wesentlichen
nicht lebendes Polymerisationssystem hin. Zu einer Lösung des
Präkatalysators
17 (0.032 mmol) in 1-Hexen (1 ml) wurde eine Lösung des Cokatalysators B(C6F5)3 (1.1 Äquivalente)
in 1-Hexen (1 ml)
bei Raumtemperatur unter Stickstoffatmosphäre hinzugegeben. Die Reaktionsmischung
wurde für
30 Minuten gerührt.
Der restliche 1-Hexenmonomerreaktant/Lösungsmittel wurde aus der Reaktionsmischung
unter verringertem Druck entfernt, um ataktisches Poly(1-hexen)
als ein farbloses Öl
zu erhalten.
-
Aus
den Reaktionsdaten berechnete katalytische Aktivität: (35 g
hergestelltes Poly(1-hexen))/(mmol-pre-cat.hr).
-
Erhaltender
Gewichtsmittelwert des Molekulargewichts: MW =
23.000 Gramm/Mol mit einem PDI von 1.57, der für ein im Wesentlichen nicht
lebendes System charakteristisch ist.
-
Spektroskopische
Daten des ataktischen Poly(1-hexen) Produkts. 1H
NMR (500 MHz, CDCl3): 1.23 (m, 8H, CH2), 1.06 (m, 1H, CH), 0.85 (t, J = 6.6 Hz,
3H, CH3), 13C NMR
(126 MHz, CDCl3) (siehe 4):
41.24 (m, CH2), 35.17–34.62 (m, CH2),
32.27 (CH), 29.63 (CH2), 29.29 (CH2), 24.19 (CH2),
15.10 (CH3).
-
Während die
Erfindung zusammen mit spezifischen Ausführungsformen und Beispielen
davon beschrieben worden ist, ist es offensichtlich, dass viele
Alternativen, Modifikationen und Variationen dem Durchschnittsfachmann
offensichtlich sein werden. Entsprechend ist es beabsichtigt, all
diese Alternativen, Modifikationen und Variationen, die in den breiten
Umfang der angehängten
Ansprüche
fallen, umfasst sind.