WO2023058761A1 - エチレン-ビニルアルコール共重合体を含有するペレット及びその製造方法 - Google Patents
エチレン-ビニルアルコール共重合体を含有するペレット及びその製造方法 Download PDFInfo
- Publication number
- WO2023058761A1 WO2023058761A1 PCT/JP2022/037692 JP2022037692W WO2023058761A1 WO 2023058761 A1 WO2023058761 A1 WO 2023058761A1 JP 2022037692 W JP2022037692 W JP 2022037692W WO 2023058761 A1 WO2023058761 A1 WO 2023058761A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- pellet
- pellets
- particles
- group
- evoh
- Prior art date
Links
- 239000008188 pellet Substances 0.000 title claims abstract description 284
- 229920000219 Ethylene vinyl alcohol Polymers 0.000 title claims abstract description 88
- 238000004519 manufacturing process Methods 0.000 title claims description 28
- 239000002245 particle Substances 0.000 claims abstract description 103
- 239000004715 ethylene vinyl alcohol Substances 0.000 claims abstract description 83
- 238000002844 melting Methods 0.000 claims abstract description 42
- 230000008018 melting Effects 0.000 claims abstract description 42
- 230000005484 gravity Effects 0.000 claims abstract description 40
- 238000007127 saponification reaction Methods 0.000 claims abstract description 32
- 239000000178 monomer Substances 0.000 claims description 62
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims description 46
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims description 38
- 125000004432 carbon atom Chemical group C* 0.000 claims description 32
- 238000001035 drying Methods 0.000 claims description 28
- 125000002887 hydroxy group Chemical group [H]O* 0.000 claims description 28
- 150000003839 salts Chemical class 0.000 claims description 17
- 239000000194 fatty acid Substances 0.000 claims description 15
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims description 15
- 125000002947 alkylene group Chemical group 0.000 claims description 14
- 235000014113 dietary fatty acids Nutrition 0.000 claims description 14
- 229930195729 fatty acid Natural products 0.000 claims description 14
- 150000004665 fatty acids Chemical class 0.000 claims description 14
- 125000005529 alkyleneoxy group Chemical group 0.000 claims description 13
- 125000002252 acyl group Chemical group 0.000 claims description 11
- 229910052751 metal Inorganic materials 0.000 claims description 10
- 239000002184 metal Substances 0.000 claims description 10
- 125000003545 alkoxy group Chemical group 0.000 claims description 9
- 125000002485 formyl group Chemical group [H]C(*)=O 0.000 claims description 9
- 125000005843 halogen group Chemical group 0.000 claims description 9
- 238000005520 cutting process Methods 0.000 claims description 8
- 229910052809 inorganic oxide Inorganic materials 0.000 claims description 7
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 claims description 6
- 229910052814 silicon oxide Inorganic materials 0.000 claims description 6
- 150000002894 organic compounds Chemical class 0.000 claims description 5
- 229910044991 metal oxide Inorganic materials 0.000 claims description 4
- 150000004706 metal oxides Chemical class 0.000 claims description 4
- 125000004029 hydroxymethyl group Chemical group [H]OC([H])([H])* 0.000 claims description 3
- 150000004671 saturated fatty acids Chemical class 0.000 claims description 3
- 150000004670 unsaturated fatty acids Chemical class 0.000 claims description 3
- 235000021122 unsaturated fatty acids Nutrition 0.000 claims description 3
- RZXDTJIXPSCHCI-UHFFFAOYSA-N hexa-1,5-diene-2,5-diol Chemical compound OC(=C)CCC(O)=C RZXDTJIXPSCHCI-UHFFFAOYSA-N 0.000 claims 2
- 229920000642 polymer Polymers 0.000 claims 2
- UFRKOOWSQGXVKV-UHFFFAOYSA-N ethene;ethenol Chemical compound C=C.OC=C UFRKOOWSQGXVKV-UHFFFAOYSA-N 0.000 abstract description 154
- 230000000903 blocking effect Effects 0.000 abstract description 35
- 238000001125 extrusion Methods 0.000 abstract description 16
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 66
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 63
- 238000000034 method Methods 0.000 description 39
- -1 unmodified EVOH (modified EVOH Chemical class 0.000 description 32
- VGGSQFUCUMXWEO-UHFFFAOYSA-N Ethene Chemical compound C=C VGGSQFUCUMXWEO-UHFFFAOYSA-N 0.000 description 31
- 239000005977 Ethylene Substances 0.000 description 31
- 229920001567 vinyl ester resin Polymers 0.000 description 30
- 239000000243 solution Substances 0.000 description 28
- 229910019142 PO4 Inorganic materials 0.000 description 26
- 235000021317 phosphate Nutrition 0.000 description 26
- 239000010452 phosphate Substances 0.000 description 25
- 239000002904 solvent Substances 0.000 description 25
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 24
- 238000006116 polymerization reaction Methods 0.000 description 24
- 150000001875 compounds Chemical class 0.000 description 18
- 239000004593 Epoxy Substances 0.000 description 15
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 15
- 125000000217 alkyl group Chemical group 0.000 description 15
- 239000000203 mixture Substances 0.000 description 15
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 14
- 230000004888 barrier function Effects 0.000 description 14
- XTXRWKRVRITETP-UHFFFAOYSA-N Vinyl acetate Chemical compound CC(=O)OC=C XTXRWKRVRITETP-UHFFFAOYSA-N 0.000 description 12
- 229920005989 resin Polymers 0.000 description 12
- 239000011347 resin Substances 0.000 description 12
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 11
- 238000011156 evaluation Methods 0.000 description 11
- 239000000047 product Substances 0.000 description 11
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical class OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 10
- 239000007864 aqueous solution Substances 0.000 description 10
- 238000006243 chemical reaction Methods 0.000 description 10
- 238000003756 stirring Methods 0.000 description 10
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 9
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 9
- 239000000654 additive Substances 0.000 description 9
- 229910052783 alkali metal Inorganic materials 0.000 description 9
- 150000002148 esters Chemical group 0.000 description 9
- 239000003999 initiator Substances 0.000 description 9
- 229910052708 sodium Inorganic materials 0.000 description 9
- 239000011734 sodium Substances 0.000 description 9
- 230000015572 biosynthetic process Effects 0.000 description 8
- 238000004806 packaging method and process Methods 0.000 description 8
- 238000003786 synthesis reaction Methods 0.000 description 8
- 235000010338 boric acid Nutrition 0.000 description 7
- 238000010438 heat treatment Methods 0.000 description 7
- 238000005259 measurement Methods 0.000 description 7
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 7
- ZWEHNKRNPOVVGH-UHFFFAOYSA-N 2-Butanone Chemical compound CCC(C)=O ZWEHNKRNPOVVGH-UHFFFAOYSA-N 0.000 description 6
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 6
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 6
- KWYUFKZDYYNOTN-UHFFFAOYSA-M Potassium hydroxide Chemical compound [OH-].[K+] KWYUFKZDYYNOTN-UHFFFAOYSA-M 0.000 description 6
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 6
- KGBXLFKZBHKPEV-UHFFFAOYSA-N boric acid Chemical compound OB(O)O KGBXLFKZBHKPEV-UHFFFAOYSA-N 0.000 description 6
- 229920001577 copolymer Polymers 0.000 description 6
- 125000004185 ester group Chemical group 0.000 description 6
- 239000000155 melt Substances 0.000 description 6
- 125000001570 methylene group Chemical group [H]C([H])([*:1])[*:2] 0.000 description 6
- 239000002356 single layer Substances 0.000 description 6
- FKAKGSJLTBVQOP-UHFFFAOYSA-N 2-(acetyloxymethyl)prop-2-enyl acetate Chemical compound CC(=O)OCC(=C)COC(C)=O FKAKGSJLTBVQOP-UHFFFAOYSA-N 0.000 description 5
- IMROMDMJAWUWLK-UHFFFAOYSA-N Ethenol Chemical group OC=C IMROMDMJAWUWLK-UHFFFAOYSA-N 0.000 description 5
- 238000005481 NMR spectroscopy Methods 0.000 description 5
- 150000001298 alcohols Chemical class 0.000 description 5
- 229960002645 boric acid Drugs 0.000 description 5
- 150000001639 boron compounds Chemical class 0.000 description 5
- 239000003054 catalyst Substances 0.000 description 5
- 230000000052 comparative effect Effects 0.000 description 5
- 238000007334 copolymerization reaction Methods 0.000 description 5
- 230000000694 effects Effects 0.000 description 5
- 239000007789 gas Substances 0.000 description 5
- 239000012046 mixed solvent Substances 0.000 description 5
- 238000002156 mixing Methods 0.000 description 5
- 238000000465 moulding Methods 0.000 description 5
- 229910052757 nitrogen Inorganic materials 0.000 description 5
- 239000003505 polymerization initiator Substances 0.000 description 5
- 238000005406 washing Methods 0.000 description 5
- 238000005160 1H NMR spectroscopy Methods 0.000 description 4
- WQDUMFSSJAZKTM-UHFFFAOYSA-N Sodium methoxide Chemical compound [Na+].[O-]C WQDUMFSSJAZKTM-UHFFFAOYSA-N 0.000 description 4
- 125000002777 acetyl group Chemical group [H]C([H])([H])C(*)=O 0.000 description 4
- 239000002253 acid Substances 0.000 description 4
- 238000000576 coating method Methods 0.000 description 4
- 230000006835 compression Effects 0.000 description 4
- 238000007906 compression Methods 0.000 description 4
- 125000000753 cycloalkyl group Chemical group 0.000 description 4
- 230000007423 decrease Effects 0.000 description 4
- 230000006866 deterioration Effects 0.000 description 4
- WMFOQBRAJBCJND-UHFFFAOYSA-M Lithium hydroxide Chemical compound [Li+].[OH-] WMFOQBRAJBCJND-UHFFFAOYSA-M 0.000 description 3
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 3
- XBDQKXXYIPTUBI-UHFFFAOYSA-M Propionate Chemical compound CCC([O-])=O XBDQKXXYIPTUBI-UHFFFAOYSA-M 0.000 description 3
- 235000010724 Wisteria floribunda Nutrition 0.000 description 3
- KXKVLQRXCPHEJC-UHFFFAOYSA-N acetic acid trimethyl ester Natural products COC(C)=O KXKVLQRXCPHEJC-UHFFFAOYSA-N 0.000 description 3
- 239000003377 acid catalyst Substances 0.000 description 3
- 150000007513 acids Chemical class 0.000 description 3
- 239000003513 alkali Substances 0.000 description 3
- 239000004327 boric acid Substances 0.000 description 3
- 150000001642 boronic acid derivatives Chemical class 0.000 description 3
- 229910052799 carbon Inorganic materials 0.000 description 3
- 239000012986 chain transfer agent Substances 0.000 description 3
- 239000011248 coating agent Substances 0.000 description 3
- 238000010528 free radical solution polymerization reaction Methods 0.000 description 3
- 230000004927 fusion Effects 0.000 description 3
- 229910052736 halogen Inorganic materials 0.000 description 3
- 150000002367 halogens Chemical class 0.000 description 3
- 150000002484 inorganic compounds Chemical class 0.000 description 3
- 229910010272 inorganic material Inorganic materials 0.000 description 3
- 150000002576 ketones Chemical class 0.000 description 3
- 230000014759 maintenance of location Effects 0.000 description 3
- 238000001000 micrograph Methods 0.000 description 3
- 239000003921 oil Substances 0.000 description 3
- 150000002978 peroxides Chemical class 0.000 description 3
- 238000001556 precipitation Methods 0.000 description 3
- BDERNNFJNOPAEC-UHFFFAOYSA-N propan-1-ol Chemical compound CCCO BDERNNFJNOPAEC-UHFFFAOYSA-N 0.000 description 3
- 238000000746 purification Methods 0.000 description 3
- 159000000000 sodium salts Chemical class 0.000 description 3
- 239000000126 substance Substances 0.000 description 3
- 238000012546 transfer Methods 0.000 description 3
- BEQKKZICTDFVMG-UHFFFAOYSA-N 1,2,3,4,6-pentaoxepane-5,7-dione Chemical compound O=C1OOOOC(=O)O1 BEQKKZICTDFVMG-UHFFFAOYSA-N 0.000 description 2
- 150000000185 1,3-diols Chemical group 0.000 description 2
- UZKWTJUDCOPSNM-UHFFFAOYSA-N 1-ethenoxybutane Chemical compound CCCCOC=C UZKWTJUDCOPSNM-UHFFFAOYSA-N 0.000 description 2
- OVGRCEFMXPHEBL-UHFFFAOYSA-N 1-ethenoxypropane Chemical compound CCCOC=C OVGRCEFMXPHEBL-UHFFFAOYSA-N 0.000 description 2
- LIKMAJRDDDTEIG-UHFFFAOYSA-N 1-hexene Chemical compound CCCCC=C LIKMAJRDDDTEIG-UHFFFAOYSA-N 0.000 description 2
- OZAIFHULBGXAKX-UHFFFAOYSA-N 2-(2-cyanopropan-2-yldiazenyl)-2-methylpropanenitrile Chemical compound N#CC(C)(C)N=NC(C)(C)C#N OZAIFHULBGXAKX-UHFFFAOYSA-N 0.000 description 2
- WYGWHHGCAGTUCH-UHFFFAOYSA-N 2-[(2-cyano-4-methylpentan-2-yl)diazenyl]-2,4-dimethylpentanenitrile Chemical compound CC(C)CC(C)(C#N)N=NC(C)(C#N)CC(C)C WYGWHHGCAGTUCH-UHFFFAOYSA-N 0.000 description 2
- XHALKWMTKWHQLO-UHFFFAOYSA-N 2-tert-butyl-4-(3-tert-butyl-4-hydroxyphenyl)sulfanylphenol Chemical compound C1=C(O)C(C(C)(C)C)=CC(SC=2C=C(C(O)=CC=2)C(C)(C)C)=C1 XHALKWMTKWHQLO-UHFFFAOYSA-N 0.000 description 2
- IKHGUXGNUITLKF-UHFFFAOYSA-N Acetaldehyde Chemical compound CC=O IKHGUXGNUITLKF-UHFFFAOYSA-N 0.000 description 2
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 description 2
- NIQCNGHVCWTJSM-UHFFFAOYSA-N Dimethyl phthalate Chemical compound COC(=O)C1=CC=CC=C1C(=O)OC NIQCNGHVCWTJSM-UHFFFAOYSA-N 0.000 description 2
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical compound OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 description 2
- CTKINSOISVBQLD-UHFFFAOYSA-N Glycidol Chemical compound OCC1CO1 CTKINSOISVBQLD-UHFFFAOYSA-N 0.000 description 2
- MHAJPDPJQMAIIY-UHFFFAOYSA-N Hydrogen peroxide Chemical compound OO MHAJPDPJQMAIIY-UHFFFAOYSA-N 0.000 description 2
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 2
- 241000209094 Oryza Species 0.000 description 2
- 235000007164 Oryza sativa Nutrition 0.000 description 2
- ISWSIDIOOBJBQZ-UHFFFAOYSA-N Phenol Chemical compound OC1=CC=CC=C1 ISWSIDIOOBJBQZ-UHFFFAOYSA-N 0.000 description 2
- NBBJYMSMWIIQGU-UHFFFAOYSA-N Propionic aldehyde Chemical compound CCC=O NBBJYMSMWIIQGU-UHFFFAOYSA-N 0.000 description 2
- GOOHAUXETOMSMM-UHFFFAOYSA-N Propylene oxide Chemical compound CC1CO1 GOOHAUXETOMSMM-UHFFFAOYSA-N 0.000 description 2
- VMHLLURERBWHNL-UHFFFAOYSA-M Sodium acetate Chemical compound [Na+].CC([O-])=O VMHLLURERBWHNL-UHFFFAOYSA-M 0.000 description 2
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 2
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 2
- 239000004809 Teflon Substances 0.000 description 2
- 229920006362 Teflon® Polymers 0.000 description 2
- XLOMVQKBTHCTTD-UHFFFAOYSA-N Zinc monoxide Chemical compound [Zn]=O XLOMVQKBTHCTTD-UHFFFAOYSA-N 0.000 description 2
- 239000006096 absorbing agent Substances 0.000 description 2
- 230000000996 additive effect Effects 0.000 description 2
- 239000003905 agrochemical Substances 0.000 description 2
- 150000001299 aldehydes Chemical class 0.000 description 2
- 229910052782 aluminium Inorganic materials 0.000 description 2
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 2
- 239000002216 antistatic agent Substances 0.000 description 2
- 230000008901 benefit Effects 0.000 description 2
- 125000005619 boric acid group Chemical class 0.000 description 2
- WTEOIRVLGSZEPR-UHFFFAOYSA-N boron trifluoride Chemical compound FB(F)F WTEOIRVLGSZEPR-UHFFFAOYSA-N 0.000 description 2
- 238000012662 bulk polymerization Methods 0.000 description 2
- CJZGTCYPCWQAJB-UHFFFAOYSA-L calcium stearate Chemical compound [Ca+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O CJZGTCYPCWQAJB-UHFFFAOYSA-L 0.000 description 2
- 239000008116 calcium stearate Substances 0.000 description 2
- 235000013539 calcium stearate Nutrition 0.000 description 2
- 125000002091 cationic group Chemical group 0.000 description 2
- 239000007810 chemical reaction solvent Substances 0.000 description 2
- 239000003795 chemical substances by application Substances 0.000 description 2
- 239000003086 colorant Substances 0.000 description 2
- 238000000354 decomposition reaction Methods 0.000 description 2
- 230000007547 defect Effects 0.000 description 2
- 230000018044 dehydration Effects 0.000 description 2
- 238000006297 dehydration reaction Methods 0.000 description 2
- ZQMIGQNCOMNODD-UHFFFAOYSA-N diacetyl peroxide Chemical compound CC(=O)OOC(C)=O ZQMIGQNCOMNODD-UHFFFAOYSA-N 0.000 description 2
- FLKPEMZONWLCSK-UHFFFAOYSA-N diethyl phthalate Chemical compound CCOC(=O)C1=CC=CC=C1C(=O)OCC FLKPEMZONWLCSK-UHFFFAOYSA-N 0.000 description 2
- 238000000635 electron micrograph Methods 0.000 description 2
- 238000010556 emulsion polymerization method Methods 0.000 description 2
- FJKIXWOMBXYWOQ-UHFFFAOYSA-N ethenoxyethane Chemical compound CCOC=C FJKIXWOMBXYWOQ-UHFFFAOYSA-N 0.000 description 2
- 239000005038 ethylene vinyl acetate Substances 0.000 description 2
- OXZOLXJZTSUDOM-UHFFFAOYSA-N fluoro 2,2,2-trifluoroacetate Chemical compound FOC(=O)C(F)(F)F OXZOLXJZTSUDOM-UHFFFAOYSA-N 0.000 description 2
- 235000013305 food Nutrition 0.000 description 2
- 239000000446 fuel Substances 0.000 description 2
- 239000000499 gel Substances 0.000 description 2
- 230000001771 impaired effect Effects 0.000 description 2
- 239000003317 industrial substance Substances 0.000 description 2
- 239000010954 inorganic particle Substances 0.000 description 2
- 239000011229 interlayer Substances 0.000 description 2
- 239000000314 lubricant Substances 0.000 description 2
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 2
- 125000001434 methanylylidene group Chemical group [H]C#[*] 0.000 description 2
- 230000004048 modification Effects 0.000 description 2
- 238000012986 modification Methods 0.000 description 2
- 239000002808 molecular sieve Substances 0.000 description 2
- 238000005453 pelletization Methods 0.000 description 2
- 238000009512 pharmaceutical packaging Methods 0.000 description 2
- KJFMBFZCATUALV-UHFFFAOYSA-N phenolphthalein Chemical compound C1=CC(O)=CC=C1C1(C=2C=CC(O)=CC=2)C2=CC=CC=C2C(=O)O1 KJFMBFZCATUALV-UHFFFAOYSA-N 0.000 description 2
- 125000002467 phosphate group Chemical group [H]OP(=O)(O[H])O[*] 0.000 description 2
- 239000004014 plasticizer Substances 0.000 description 2
- 229920001200 poly(ethylene-vinyl acetate) Polymers 0.000 description 2
- 230000000379 polymerizing effect Effects 0.000 description 2
- 229920000098 polyolefin Polymers 0.000 description 2
- 239000000843 powder Substances 0.000 description 2
- 239000002244 precipitate Substances 0.000 description 2
- 238000002360 preparation method Methods 0.000 description 2
- 238000012545 processing Methods 0.000 description 2
- 238000000425 proton nuclear magnetic resonance spectrum Methods 0.000 description 2
- 238000010791 quenching Methods 0.000 description 2
- 230000000171 quenching effect Effects 0.000 description 2
- 229920005604 random copolymer Polymers 0.000 description 2
- 230000009257 reactivity Effects 0.000 description 2
- 239000012966 redox initiator Substances 0.000 description 2
- 238000010992 reflux Methods 0.000 description 2
- 235000009566 rice Nutrition 0.000 description 2
- 239000001632 sodium acetate Substances 0.000 description 2
- 235000017281 sodium acetate Nutrition 0.000 description 2
- URGAHOPLAPQHLN-UHFFFAOYSA-N sodium aluminosilicate Chemical compound [Na+].[Al+3].[O-][Si]([O-])=O.[O-][Si]([O-])=O URGAHOPLAPQHLN-UHFFFAOYSA-N 0.000 description 2
- 229910001220 stainless steel Inorganic materials 0.000 description 2
- 239000010935 stainless steel Substances 0.000 description 2
- CZDYPVPMEAXLPK-UHFFFAOYSA-N tetramethylsilane Chemical compound C[Si](C)(C)C CZDYPVPMEAXLPK-UHFFFAOYSA-N 0.000 description 2
- 238000003856 thermoforming Methods 0.000 description 2
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 2
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 2
- 229920002554 vinyl polymer Polymers 0.000 description 2
- JHPBZFOKBAGZBL-UHFFFAOYSA-N (3-hydroxy-2,2,4-trimethylpentyl) 2-methylprop-2-enoate Chemical group CC(C)C(O)C(C)(C)COC(=O)C(C)=C JHPBZFOKBAGZBL-UHFFFAOYSA-N 0.000 description 1
- BQCIDUSAKPWEOX-UHFFFAOYSA-N 1,1-Difluoroethene Chemical compound FC(F)=C BQCIDUSAKPWEOX-UHFFFAOYSA-N 0.000 description 1
- QMMJWQMCMRUYTG-UHFFFAOYSA-N 1,2,4,5-tetrachloro-3-(trifluoromethyl)benzene Chemical compound FC(F)(F)C1=C(Cl)C(Cl)=CC(Cl)=C1Cl QMMJWQMCMRUYTG-UHFFFAOYSA-N 0.000 description 1
- RBACIKXCRWGCBB-UHFFFAOYSA-N 1,2-Epoxybutane Chemical compound CCC1CO1 RBACIKXCRWGCBB-UHFFFAOYSA-N 0.000 description 1
- ICCVOKMKWYGITK-UHFFFAOYSA-N 1-(2-methylprop-2-enoylamino)propane-1-sulfonic acid Chemical compound CCC(S(O)(=O)=O)NC(=O)C(C)=C ICCVOKMKWYGITK-UHFFFAOYSA-N 0.000 description 1
- IAUGBVWVWDTCJV-UHFFFAOYSA-N 1-(prop-2-enoylamino)propane-1-sulfonic acid Chemical compound CCC(S(O)(=O)=O)NC(=O)C=C IAUGBVWVWDTCJV-UHFFFAOYSA-N 0.000 description 1
- VXNZUUAINFGPBY-UHFFFAOYSA-N 1-Butene Chemical compound CCC=C VXNZUUAINFGPBY-UHFFFAOYSA-N 0.000 description 1
- BPGQBXWSUSDSQY-UHFFFAOYSA-N 1-butanoyloxypropyl butanoate Chemical compound CCCC(=O)OC(CC)OC(=O)CCC BPGQBXWSUSDSQY-UHFFFAOYSA-N 0.000 description 1
- LAYAKLSFVAPMEL-UHFFFAOYSA-N 1-ethenoxydodecane Chemical compound CCCCCCCCCCCCOC=C LAYAKLSFVAPMEL-UHFFFAOYSA-N 0.000 description 1
- QJJDJWUCRAPCOL-UHFFFAOYSA-N 1-ethenoxyoctadecane Chemical compound CCCCCCCCCCCCCCCCCCOC=C QJJDJWUCRAPCOL-UHFFFAOYSA-N 0.000 description 1
- MEZZCSHVIGVWFI-UHFFFAOYSA-N 2,2'-Dihydroxy-4-methoxybenzophenone Chemical compound OC1=CC(OC)=CC=C1C(=O)C1=CC=CC=C1O MEZZCSHVIGVWFI-UHFFFAOYSA-N 0.000 description 1
- KGRVJHAUYBGFFP-UHFFFAOYSA-N 2,2'-Methylenebis(4-methyl-6-tert-butylphenol) Chemical compound CC(C)(C)C1=CC(C)=CC(CC=2C(=C(C=C(C)C=2)C(C)(C)C)O)=C1O KGRVJHAUYBGFFP-UHFFFAOYSA-N 0.000 description 1
- JZODKRWQWUWGCD-UHFFFAOYSA-N 2,5-di-tert-butylbenzene-1,4-diol Chemical compound CC(C)(C)C1=CC(O)=C(C(C)(C)C)C=C1O JZODKRWQWUWGCD-UHFFFAOYSA-N 0.000 description 1
- STMDPCBYJCIZOD-UHFFFAOYSA-N 2-(2,4-dinitroanilino)-4-methylpentanoic acid Chemical compound CC(C)CC(C(O)=O)NC1=CC=C([N+]([O-])=O)C=C1[N+]([O-])=O STMDPCBYJCIZOD-UHFFFAOYSA-N 0.000 description 1
- SMZOUWXMTYCWNB-UHFFFAOYSA-N 2-(2-methoxy-5-methylphenyl)ethanamine Chemical compound COC1=CC=C(C)C=C1CCN SMZOUWXMTYCWNB-UHFFFAOYSA-N 0.000 description 1
- JAHNSTQSQJOJLO-UHFFFAOYSA-N 2-(3-fluorophenyl)-1h-imidazole Chemical compound FC1=CC=CC(C=2NC=CN=2)=C1 JAHNSTQSQJOJLO-UHFFFAOYSA-N 0.000 description 1
- OEPOKWHJYJXUGD-UHFFFAOYSA-N 2-(3-phenylmethoxyphenyl)-1,3-thiazole-4-carbaldehyde Chemical compound O=CC1=CSC(C=2C=C(OCC=3C=CC=CC=3)C=CC=2)=N1 OEPOKWHJYJXUGD-UHFFFAOYSA-N 0.000 description 1
- NGVUURZMTYCUAE-UHFFFAOYSA-N 2-(hydroxymethyl)cyclopropan-1-ol Chemical group OCC1CC1O NGVUURZMTYCUAE-UHFFFAOYSA-N 0.000 description 1
- DIBCJRYCOGXPAM-UHFFFAOYSA-N 2-(propanoyloxymethyl)prop-2-enyl propanoate Chemical compound CCC(=O)OCC(=C)COC(=O)CC DIBCJRYCOGXPAM-UHFFFAOYSA-N 0.000 description 1
- NIXOWILDQLNWCW-UHFFFAOYSA-N 2-Propenoic acid Natural products OC(=O)C=C NIXOWILDQLNWCW-UHFFFAOYSA-N 0.000 description 1
- PFHOSZAOXCYAGJ-UHFFFAOYSA-N 2-[(2-cyano-4-methoxy-4-methylpentan-2-yl)diazenyl]-4-methoxy-2,4-dimethylpentanenitrile Chemical compound COC(C)(C)CC(C)(C#N)N=NC(C)(C#N)CC(C)(C)OC PFHOSZAOXCYAGJ-UHFFFAOYSA-N 0.000 description 1
- MWWXARALRVYLAE-UHFFFAOYSA-N 2-acetyloxybut-3-enyl acetate Chemical compound CC(=O)OCC(C=C)OC(C)=O MWWXARALRVYLAE-UHFFFAOYSA-N 0.000 description 1
- PGYJSURPYAAOMM-UHFFFAOYSA-N 2-ethenoxy-2-methylpropane Chemical compound CC(C)(C)OC=C PGYJSURPYAAOMM-UHFFFAOYSA-N 0.000 description 1
- BAASKFPCFXDLJB-UHFFFAOYSA-N 2-methylidenebutane-1,3-diol Chemical compound CC(O)C(=C)CO BAASKFPCFXDLJB-UHFFFAOYSA-N 0.000 description 1
- JFFYKITVXPZLQS-UHFFFAOYSA-N 2-methylidenepropane-1,3-diol Chemical compound OCC(=C)CO JFFYKITVXPZLQS-UHFFFAOYSA-N 0.000 description 1
- 125000003903 2-propenyl group Chemical group [H]C([*])([H])C([H])=C([H])[H] 0.000 description 1
- XDVOLDOITVSJGL-UHFFFAOYSA-N 3,7-dihydroxy-2,4,6,8,9-pentaoxa-1,3,5,7-tetraborabicyclo[3.3.1]nonane Chemical compound O1B(O)OB2OB(O)OB1O2 XDVOLDOITVSJGL-UHFFFAOYSA-N 0.000 description 1
- HRPVXLWXLXDGHG-UHFFFAOYSA-N Acrylamide Chemical compound NC(=O)C=C HRPVXLWXLXDGHG-UHFFFAOYSA-N 0.000 description 1
- NLHHRLWOUZZQLW-UHFFFAOYSA-N Acrylonitrile Chemical compound C=CC#N NLHHRLWOUZZQLW-UHFFFAOYSA-N 0.000 description 1
- OSDWBNJEKMUWAV-UHFFFAOYSA-N Allyl chloride Chemical compound ClCC=C OSDWBNJEKMUWAV-UHFFFAOYSA-N 0.000 description 1
- 229910015900 BF3 Inorganic materials 0.000 description 1
- ZOXJGFHDIHLPTG-UHFFFAOYSA-N Boron Chemical compound [B] ZOXJGFHDIHLPTG-UHFFFAOYSA-N 0.000 description 1
- NLZUEZXRPGMBCV-UHFFFAOYSA-N Butylhydroxytoluene Chemical compound CC1=CC(C(C)(C)C)=C(O)C(C(C)(C)C)=C1 NLZUEZXRPGMBCV-UHFFFAOYSA-N 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- 229910052684 Cerium Inorganic materials 0.000 description 1
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 1
- MQIUGAXCHLFZKX-UHFFFAOYSA-N Di-n-octyl phthalate Natural products CCCCCCCCOC(=O)C1=CC=CC=C1C(=O)OCCCCCCCC MQIUGAXCHLFZKX-UHFFFAOYSA-N 0.000 description 1
- RWSOTUBLDIXVET-UHFFFAOYSA-N Dihydrogen sulfide Chemical class S RWSOTUBLDIXVET-UHFFFAOYSA-N 0.000 description 1
- GDFCSMCGLZFNFY-UHFFFAOYSA-N Dimethylaminopropyl Methacrylamide Chemical compound CN(C)CCCNC(=O)C(C)=C GDFCSMCGLZFNFY-UHFFFAOYSA-N 0.000 description 1
- IAYPIBMASNFSPL-UHFFFAOYSA-N Ethylene oxide Chemical compound C1CO1 IAYPIBMASNFSPL-UHFFFAOYSA-N 0.000 description 1
- SIKJAQJRHWYJAI-UHFFFAOYSA-N Indole Chemical compound C1=CC=C2NC=CC2=C1 SIKJAQJRHWYJAI-UHFFFAOYSA-N 0.000 description 1
- VQTUBCCKSQIDNK-UHFFFAOYSA-N Isobutene Chemical group CC(C)=C VQTUBCCKSQIDNK-UHFFFAOYSA-N 0.000 description 1
- HETCEOQFVDFGSY-UHFFFAOYSA-N Isopropenyl acetate Chemical compound CC(=C)OC(C)=O HETCEOQFVDFGSY-UHFFFAOYSA-N 0.000 description 1
- 239000002211 L-ascorbic acid Substances 0.000 description 1
- 235000000069 L-ascorbic acid Nutrition 0.000 description 1
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 1
- CERQOIWHTDAKMF-UHFFFAOYSA-N Methacrylic acid Chemical compound CC(=C)C(O)=O CERQOIWHTDAKMF-UHFFFAOYSA-N 0.000 description 1
- RJUFJBKOKNCXHH-UHFFFAOYSA-N Methyl propionate Chemical compound CCC(=O)OC RJUFJBKOKNCXHH-UHFFFAOYSA-N 0.000 description 1
- GYCMBHHDWRMZGG-UHFFFAOYSA-N Methylacrylonitrile Chemical compound CC(=C)C#N GYCMBHHDWRMZGG-UHFFFAOYSA-N 0.000 description 1
- ZOKXTWBITQBERF-UHFFFAOYSA-N Molybdenum Chemical compound [Mo] ZOKXTWBITQBERF-UHFFFAOYSA-N 0.000 description 1
- FXHOOIRPVKKKFG-UHFFFAOYSA-N N,N-Dimethylacetamide Chemical compound CN(C)C(C)=O FXHOOIRPVKKKFG-UHFFFAOYSA-N 0.000 description 1
- SECXISVLQFMRJM-UHFFFAOYSA-N N-Methylpyrrolidone Chemical compound CN1CCCC1=O SECXISVLQFMRJM-UHFFFAOYSA-N 0.000 description 1
- GRYLNZFGIOXLOG-UHFFFAOYSA-N Nitric acid Chemical compound O[N+]([O-])=O GRYLNZFGIOXLOG-UHFFFAOYSA-N 0.000 description 1
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical compound [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 description 1
- 229920003171 Poly (ethylene oxide) Polymers 0.000 description 1
- 239000004698 Polyethylene Substances 0.000 description 1
- 239000004743 Polypropylene Substances 0.000 description 1
- OFOBLEOULBTSOW-UHFFFAOYSA-N Propanedioic acid Natural products OC(=O)CC(O)=O OFOBLEOULBTSOW-UHFFFAOYSA-N 0.000 description 1
- NRCMAYZCPIVABH-UHFFFAOYSA-N Quinacridone Chemical compound N1C2=CC=CC=C2C(=O)C2=C1C=C1C(=O)C3=CC=CC=C3NC1=C2 NRCMAYZCPIVABH-UHFFFAOYSA-N 0.000 description 1
- DWAQJAXMDSEUJJ-UHFFFAOYSA-M Sodium bisulfite Chemical compound [Na+].OS([O-])=O DWAQJAXMDSEUJJ-UHFFFAOYSA-M 0.000 description 1
- IYFATESGLOUGBX-YVNJGZBMSA-N Sorbitan monopalmitate Chemical compound CCCCCCCCCCCCCCCC(=O)OC[C@@H](O)[C@H]1OC[C@H](O)[C@H]1O IYFATESGLOUGBX-YVNJGZBMSA-N 0.000 description 1
- FEWJPZIEWOKRBE-UHFFFAOYSA-N Tartaric acid Natural products [H+].[H+].[O-]C(=O)C(O)C(O)C([O-])=O FEWJPZIEWOKRBE-UHFFFAOYSA-N 0.000 description 1
- GWEVSGVZZGPLCZ-UHFFFAOYSA-N Titan oxide Chemical compound O=[Ti]=O GWEVSGVZZGPLCZ-UHFFFAOYSA-N 0.000 description 1
- RTAQQCXQSZGOHL-UHFFFAOYSA-N Titanium Chemical compound [Ti] RTAQQCXQSZGOHL-UHFFFAOYSA-N 0.000 description 1
- WYGWHHGCAGTUCH-ISLYRVAYSA-N V-65 Substances CC(C)CC(C)(C#N)\N=N\C(C)(C#N)CC(C)C WYGWHHGCAGTUCH-ISLYRVAYSA-N 0.000 description 1
- BZHJMEDXRYGGRV-UHFFFAOYSA-N Vinyl chloride Chemical compound ClC=C BZHJMEDXRYGGRV-UHFFFAOYSA-N 0.000 description 1
- HCHKCACWOHOZIP-UHFFFAOYSA-N Zinc Chemical compound [Zn] HCHKCACWOHOZIP-UHFFFAOYSA-N 0.000 description 1
- QCWXUUIWCKQGHC-UHFFFAOYSA-N Zirconium Chemical compound [Zr] QCWXUUIWCKQGHC-UHFFFAOYSA-N 0.000 description 1
- 150000008360 acrylonitriles Chemical class 0.000 description 1
- 150000007933 aliphatic carboxylic acids Chemical class 0.000 description 1
- 150000008044 alkali metal hydroxides Chemical class 0.000 description 1
- 150000001340 alkali metals Chemical class 0.000 description 1
- 229910052784 alkaline earth metal Inorganic materials 0.000 description 1
- 125000000746 allylic group Chemical group 0.000 description 1
- 150000001412 amines Chemical class 0.000 description 1
- ROOXNKNUYICQNP-UHFFFAOYSA-N ammonium peroxydisulfate Substances [NH4+].[NH4+].[O-]S(=O)(=O)OOS([O-])(=O)=O ROOXNKNUYICQNP-UHFFFAOYSA-N 0.000 description 1
- VAZSKTXWXKYQJF-UHFFFAOYSA-N ammonium persulfate Chemical compound [NH4+].[NH4+].[O-]S(=O)OOS([O-])=O VAZSKTXWXKYQJF-UHFFFAOYSA-N 0.000 description 1
- 229910001870 ammonium persulfate Inorganic materials 0.000 description 1
- 238000004458 analytical method Methods 0.000 description 1
- 150000001450 anions Chemical class 0.000 description 1
- 239000003963 antioxidant agent Substances 0.000 description 1
- 235000006708 antioxidants Nutrition 0.000 description 1
- 238000000149 argon plasma sintering Methods 0.000 description 1
- 150000004945 aromatic hydrocarbons Chemical class 0.000 description 1
- 229960005070 ascorbic acid Drugs 0.000 description 1
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 1
- 125000000751 azo group Chemical group [*]N=N[*] 0.000 description 1
- 239000004305 biphenyl Substances 0.000 description 1
- BJQHLKABXJIVAM-UHFFFAOYSA-N bis(2-ethylhexyl) phthalate Chemical compound CCCCC(CC)COC(=O)C1=CC=CC=C1C(=O)OCC(CC)CCCC BJQHLKABXJIVAM-UHFFFAOYSA-N 0.000 description 1
- 239000002981 blocking agent Substances 0.000 description 1
- 229910021538 borax Inorganic materials 0.000 description 1
- 229910052796 boron Inorganic materials 0.000 description 1
- OCWYEMOEOGEQAN-UHFFFAOYSA-N bumetrizole Chemical compound CC(C)(C)C1=CC(C)=CC(N2N=C3C=C(Cl)C=CC3=N2)=C1O OCWYEMOEOGEQAN-UHFFFAOYSA-N 0.000 description 1
- DQXBYHZEEUGOBF-UHFFFAOYSA-N but-3-enoic acid;ethene Chemical class C=C.OC(=O)CC=C DQXBYHZEEUGOBF-UHFFFAOYSA-N 0.000 description 1
- ZTQSAGDEMFDKMZ-UHFFFAOYSA-N butyric aldehyde Natural products CCCC=O ZTQSAGDEMFDKMZ-UHFFFAOYSA-N 0.000 description 1
- 125000004063 butyryl group Chemical group O=C([*])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 238000004364 calculation method Methods 0.000 description 1
- 150000001721 carbon Chemical group 0.000 description 1
- 239000006229 carbon black Substances 0.000 description 1
- BVKZGUZCCUSVTD-UHFFFAOYSA-N carbonic acid Chemical class OC(O)=O BVKZGUZCCUSVTD-UHFFFAOYSA-N 0.000 description 1
- 150000004649 carbonic acid derivatives Chemical class 0.000 description 1
- 150000007942 carboxylates Chemical class 0.000 description 1
- DBUPOCYLUHVFHU-UHFFFAOYSA-N carboxyoxy 2,2-diethoxyethyl carbonate Chemical compound CCOC(OCC)COC(=O)OOC(O)=O DBUPOCYLUHVFHU-UHFFFAOYSA-N 0.000 description 1
- ZMIGMASIKSOYAM-UHFFFAOYSA-N cerium Chemical compound [Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce] ZMIGMASIKSOYAM-UHFFFAOYSA-N 0.000 description 1
- 229910000420 cerium oxide Inorganic materials 0.000 description 1
- 239000007809 chemical reaction catalyst Substances 0.000 description 1
- 239000003638 chemical reducing agent Substances 0.000 description 1
- 238000004040 coloring Methods 0.000 description 1
- 239000002131 composite material Substances 0.000 description 1
- 230000008602 contraction Effects 0.000 description 1
- 230000002596 correlated effect Effects 0.000 description 1
- 239000003431 cross linking reagent Substances 0.000 description 1
- BSVQJWUUZCXSOL-UHFFFAOYSA-N cyclohexylsulfonyl ethaneperoxoate Chemical compound CC(=O)OOS(=O)(=O)C1CCCCC1 BSVQJWUUZCXSOL-UHFFFAOYSA-N 0.000 description 1
- 239000002274 desiccant Substances 0.000 description 1
- GDVKFRBCXAPAQJ-UHFFFAOYSA-A dialuminum;hexamagnesium;carbonate;hexadecahydroxide Chemical class [OH-].[OH-].[OH-].[OH-].[OH-].[OH-].[OH-].[OH-].[OH-].[OH-].[OH-].[OH-].[OH-].[OH-].[OH-].[OH-].[Mg+2].[Mg+2].[Mg+2].[Mg+2].[Mg+2].[Mg+2].[Al+3].[Al+3].[O-]C([O-])=O GDVKFRBCXAPAQJ-UHFFFAOYSA-A 0.000 description 1
- 150000001991 dicarboxylic acids Chemical class 0.000 description 1
- 238000001938 differential scanning calorimetry curve Methods 0.000 description 1
- FBSAITBEAPNWJG-UHFFFAOYSA-N dimethyl phthalate Natural products CC(=O)OC1=CC=CC=C1OC(C)=O FBSAITBEAPNWJG-UHFFFAOYSA-N 0.000 description 1
- 229960001826 dimethylphthalate Drugs 0.000 description 1
- 229910001873 dinitrogen Inorganic materials 0.000 description 1
- POLCUAVZOMRGSN-UHFFFAOYSA-N dipropyl ether Chemical compound CCCOCCC POLCUAVZOMRGSN-UHFFFAOYSA-N 0.000 description 1
- 239000006185 dispersion Substances 0.000 description 1
- 238000004090 dissolution Methods 0.000 description 1
- 238000009826 distribution Methods 0.000 description 1
- ILRSCQWREDREME-UHFFFAOYSA-N dodecanamide Chemical compound CCCCCCCCCCCC(N)=O ILRSCQWREDREME-UHFFFAOYSA-N 0.000 description 1
- MCPKSFINULVDNX-UHFFFAOYSA-N drometrizole Chemical compound CC1=CC=C(O)C(N2N=C3C=CC=CC3=N2)=C1 MCPKSFINULVDNX-UHFFFAOYSA-N 0.000 description 1
- 125000003700 epoxy group Chemical group 0.000 description 1
- UAUDZVJPLUQNMU-KTKRTIGZSA-N erucamide Chemical compound CCCCCCCC\C=C/CCCCCCCCCCCC(N)=O UAUDZVJPLUQNMU-KTKRTIGZSA-N 0.000 description 1
- ZJOLCKGSXLIVAA-UHFFFAOYSA-N ethene;octadecanamide Chemical compound C=C.CCCCCCCCCCCCCCCCCC(N)=O.CCCCCCCCCCCCCCCCCC(N)=O ZJOLCKGSXLIVAA-UHFFFAOYSA-N 0.000 description 1
- YCUBDDIKWLELPD-UHFFFAOYSA-N ethenyl 2,2-dimethylpropanoate Chemical compound CC(C)(C)C(=O)OC=C YCUBDDIKWLELPD-UHFFFAOYSA-N 0.000 description 1
- WNMORWGTPVWAIB-UHFFFAOYSA-N ethenyl 2-methylpropanoate Chemical compound CC(C)C(=O)OC=C WNMORWGTPVWAIB-UHFFFAOYSA-N 0.000 description 1
- MEGHWIAOTJPCHQ-UHFFFAOYSA-N ethenyl butanoate Chemical compound CCCC(=O)OC=C MEGHWIAOTJPCHQ-UHFFFAOYSA-N 0.000 description 1
- GFJVXXWOPWLRNU-UHFFFAOYSA-N ethenyl formate Chemical compound C=COC=O GFJVXXWOPWLRNU-UHFFFAOYSA-N 0.000 description 1
- LZWYWAIOTBEZFN-UHFFFAOYSA-N ethenyl hexanoate Chemical compound CCCCCC(=O)OC=C LZWYWAIOTBEZFN-UHFFFAOYSA-N 0.000 description 1
- UIWXSTHGICQLQT-UHFFFAOYSA-N ethenyl propanoate Chemical compound CCC(=O)OC=C UIWXSTHGICQLQT-UHFFFAOYSA-N 0.000 description 1
- NKSJNEHGWDZZQF-UHFFFAOYSA-N ethenyl(trimethoxy)silane Chemical compound CO[Si](OC)(OC)C=C NKSJNEHGWDZZQF-UHFFFAOYSA-N 0.000 description 1
- 150000002170 ethers Chemical class 0.000 description 1
- XUCNUKMRBVNAPB-UHFFFAOYSA-N fluoroethene Chemical compound FC=C XUCNUKMRBVNAPB-UHFFFAOYSA-N 0.000 description 1
- 239000001530 fumaric acid Substances 0.000 description 1
- 125000000524 functional group Chemical group 0.000 description 1
- 238000001879 gelation Methods 0.000 description 1
- 239000012760 heat stabilizer Substances 0.000 description 1
- FEEPBTVZSYQUDP-UHFFFAOYSA-N heptatriacontanediamide Chemical compound NC(=O)CCCCCCCCCCCCCCCCCCCCCCCCCCCCCCCCCCCC(N)=O FEEPBTVZSYQUDP-UHFFFAOYSA-N 0.000 description 1
- HSEMFIZWXHQJAE-UHFFFAOYSA-N hexadecanamide Chemical compound CCCCCCCCCCCCCCCC(N)=O HSEMFIZWXHQJAE-UHFFFAOYSA-N 0.000 description 1
- 229920001903 high density polyethylene Polymers 0.000 description 1
- 239000004700 high-density polyethylene Substances 0.000 description 1
- 229910052739 hydrogen Inorganic materials 0.000 description 1
- 239000001257 hydrogen Substances 0.000 description 1
- 150000004679 hydroxides Chemical class 0.000 description 1
- 125000004356 hydroxy functional group Chemical group O* 0.000 description 1
- 125000002768 hydroxyalkyl group Chemical group 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 229910052738 indium Inorganic materials 0.000 description 1
- APFVFJFRJDLVQX-UHFFFAOYSA-N indium atom Chemical compound [In] APFVFJFRJDLVQX-UHFFFAOYSA-N 0.000 description 1
- 229910052500 inorganic mineral Inorganic materials 0.000 description 1
- JEIPFZHSYJVQDO-UHFFFAOYSA-N iron(III) oxide Inorganic materials O=[Fe]O[Fe]=O JEIPFZHSYJVQDO-UHFFFAOYSA-N 0.000 description 1
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 1
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 238000004898 kneading Methods 0.000 description 1
- 239000010410 layer Substances 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 229940057995 liquid paraffin Drugs 0.000 description 1
- 239000011777 magnesium Substances 0.000 description 1
- 229910052749 magnesium Inorganic materials 0.000 description 1
- 239000000395 magnesium oxide Substances 0.000 description 1
- CPLXHLVBOLITMK-UHFFFAOYSA-N magnesium oxide Inorganic materials [Mg]=O CPLXHLVBOLITMK-UHFFFAOYSA-N 0.000 description 1
- 235000019359 magnesium stearate Nutrition 0.000 description 1
- AXZKOIWUVFPNLO-UHFFFAOYSA-N magnesium;oxygen(2-) Chemical compound [O-2].[Mg+2] AXZKOIWUVFPNLO-UHFFFAOYSA-N 0.000 description 1
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 description 1
- 239000011976 maleic acid Substances 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 150000002739 metals Chemical class 0.000 description 1
- FQPSGWSUVKBHSU-UHFFFAOYSA-N methacrylamide Chemical compound CC(=C)C(N)=O FQPSGWSUVKBHSU-UHFFFAOYSA-N 0.000 description 1
- 229940098779 methanesulfonic acid Drugs 0.000 description 1
- 229940017219 methyl propionate Drugs 0.000 description 1
- XJRBAMWJDBPFIM-UHFFFAOYSA-N methyl vinyl ether Chemical compound COC=C XJRBAMWJDBPFIM-UHFFFAOYSA-N 0.000 description 1
- LVHBHZANLOWSRM-UHFFFAOYSA-N methylenebutanedioic acid Natural products OC(=O)CC(=C)C(O)=O LVHBHZANLOWSRM-UHFFFAOYSA-N 0.000 description 1
- 239000011707 mineral Substances 0.000 description 1
- 235000010755 mineral Nutrition 0.000 description 1
- 239000011259 mixed solution Substances 0.000 description 1
- 229910052750 molybdenum Inorganic materials 0.000 description 1
- 239000011733 molybdenum Substances 0.000 description 1
- 229910000476 molybdenum oxide Inorganic materials 0.000 description 1
- 229910000402 monopotassium phosphate Inorganic materials 0.000 description 1
- 235000019796 monopotassium phosphate Nutrition 0.000 description 1
- 229910000403 monosodium phosphate Inorganic materials 0.000 description 1
- 235000019799 monosodium phosphate Nutrition 0.000 description 1
- WFKDPJRCBCBQNT-UHFFFAOYSA-N n,2-dimethylprop-2-enamide Chemical compound CNC(=O)C(C)=C WFKDPJRCBCBQNT-UHFFFAOYSA-N 0.000 description 1
- 229940088644 n,n-dimethylacrylamide Drugs 0.000 description 1
- YLGYACDQVQQZSW-UHFFFAOYSA-N n,n-dimethylprop-2-enamide Chemical compound CN(C)C(=O)C=C YLGYACDQVQQZSW-UHFFFAOYSA-N 0.000 description 1
- OMNKZBIFPJNNIO-UHFFFAOYSA-N n-(2-methyl-4-oxopentan-2-yl)prop-2-enamide Chemical compound CC(=O)CC(C)(C)NC(=O)C=C OMNKZBIFPJNNIO-UHFFFAOYSA-N 0.000 description 1
- RKISUIUJZGSLEV-UHFFFAOYSA-N n-[2-(octadecanoylamino)ethyl]octadecanamide Chemical compound CCCCCCCCCCCCCCCCCC(=O)NCCNC(=O)CCCCCCCCCCCCCCCCC RKISUIUJZGSLEV-UHFFFAOYSA-N 0.000 description 1
- ADTJPOBHAXXXFS-UHFFFAOYSA-N n-[3-(dimethylamino)propyl]prop-2-enamide Chemical compound CN(C)CCCNC(=O)C=C ADTJPOBHAXXXFS-UHFFFAOYSA-N 0.000 description 1
- ZIWDVJPPVMGJGR-UHFFFAOYSA-N n-ethyl-2-methylprop-2-enamide Chemical compound CCNC(=O)C(C)=C ZIWDVJPPVMGJGR-UHFFFAOYSA-N 0.000 description 1
- SWPMNMYLORDLJE-UHFFFAOYSA-N n-ethylprop-2-enamide Chemical compound CCNC(=O)C=C SWPMNMYLORDLJE-UHFFFAOYSA-N 0.000 description 1
- YPHQUSNPXDGUHL-UHFFFAOYSA-N n-methylprop-2-enamide Chemical compound CNC(=O)C=C YPHQUSNPXDGUHL-UHFFFAOYSA-N 0.000 description 1
- 238000006386 neutralization reaction Methods 0.000 description 1
- 229910017604 nitric acid Inorganic materials 0.000 description 1
- QGLKJKCYBOYXKC-UHFFFAOYSA-N nonaoxidotritungsten Chemical compound O=[W]1(=O)O[W](=O)(=O)O[W](=O)(=O)O1 QGLKJKCYBOYXKC-UHFFFAOYSA-N 0.000 description 1
- LYRFLYHAGKPMFH-UHFFFAOYSA-N octadecanamide Chemical compound CCCCCCCCCCCCCCCCCC(N)=O LYRFLYHAGKPMFH-UHFFFAOYSA-N 0.000 description 1
- SSDSCDGVMJFTEQ-UHFFFAOYSA-N octadecyl 3-(3,5-ditert-butyl-4-hydroxyphenyl)propanoate Chemical compound CCCCCCCCCCCCCCCCCCOC(=O)CCC1=CC(C(C)(C)C)=C(O)C(C(C)(C)C)=C1 SSDSCDGVMJFTEQ-UHFFFAOYSA-N 0.000 description 1
- WGOROJDSDNILMB-UHFFFAOYSA-N octatriacontanediamide Chemical compound NC(=O)CCCCCCCCCCCCCCCCCCCCCCCCCCCCCCCCCCCCC(N)=O WGOROJDSDNILMB-UHFFFAOYSA-N 0.000 description 1
- FATBGEAMYMYZAF-KTKRTIGZSA-N oleamide Chemical compound CCCCCCCC\C=C/CCCCCCCC(N)=O FATBGEAMYMYZAF-KTKRTIGZSA-N 0.000 description 1
- 239000003960 organic solvent Substances 0.000 description 1
- TWNQGVIAIRXVLR-UHFFFAOYSA-N oxo(oxoalumanyloxy)alumane Chemical compound O=[Al]O[Al]=O TWNQGVIAIRXVLR-UHFFFAOYSA-N 0.000 description 1
- BMMGVYCKOGBVEV-UHFFFAOYSA-N oxo(oxoceriooxy)cerium Chemical compound [Ce]=O.O=[Ce]=O BMMGVYCKOGBVEV-UHFFFAOYSA-N 0.000 description 1
- VGTPKLINSHNZRD-UHFFFAOYSA-N oxoborinic acid Chemical compound OB=O VGTPKLINSHNZRD-UHFFFAOYSA-N 0.000 description 1
- PQQKPALAQIIWST-UHFFFAOYSA-N oxomolybdenum Chemical compound [Mo]=O PQQKPALAQIIWST-UHFFFAOYSA-N 0.000 description 1
- DXGLGDHPHMLXJC-UHFFFAOYSA-N oxybenzone Chemical compound OC1=CC(OC)=CC=C1C(=O)C1=CC=CC=C1 DXGLGDHPHMLXJC-UHFFFAOYSA-N 0.000 description 1
- 229910052760 oxygen Inorganic materials 0.000 description 1
- 239000001301 oxygen Substances 0.000 description 1
- RVTZCBVAJQQJTK-UHFFFAOYSA-N oxygen(2-);zirconium(4+) Chemical compound [O-2].[O-2].[Zr+4] RVTZCBVAJQQJTK-UHFFFAOYSA-N 0.000 description 1
- 230000000737 periodic effect Effects 0.000 description 1
- 150000003013 phosphoric acid derivatives Chemical class 0.000 description 1
- PJNZPQUBCPKICU-UHFFFAOYSA-N phosphoric acid;potassium Chemical compound [K].OP(O)(O)=O PJNZPQUBCPKICU-UHFFFAOYSA-N 0.000 description 1
- 229910052698 phosphorus Inorganic materials 0.000 description 1
- 239000011574 phosphorus Substances 0.000 description 1
- IEQIEDJGQAUEQZ-UHFFFAOYSA-N phthalocyanine Chemical compound N1C(N=C2C3=CC=CC=C3C(N=C3C4=CC=CC=C4C(=N4)N3)=N2)=C(C=CC=C2)C2=C1N=C1C2=CC=CC=C2C4=N1 IEQIEDJGQAUEQZ-UHFFFAOYSA-N 0.000 description 1
- 239000000049 pigment Substances 0.000 description 1
- 239000003880 polar aprotic solvent Substances 0.000 description 1
- 229920000573 polyethylene Polymers 0.000 description 1
- 229920001223 polyethylene glycol Polymers 0.000 description 1
- 229920001155 polypropylene Polymers 0.000 description 1
- USHAGKDGDHPEEY-UHFFFAOYSA-L potassium persulfate Chemical compound [K+].[K+].[O-]S(=O)(=O)OOS([O-])(=O)=O USHAGKDGDHPEEY-UHFFFAOYSA-L 0.000 description 1
- 159000000001 potassium salts Chemical class 0.000 description 1
- 230000008569 process Effects 0.000 description 1
- BWJUFXUULUEGMA-UHFFFAOYSA-N propan-2-yl propan-2-yloxycarbonyloxy carbonate Chemical compound CC(C)OC(=O)OOC(=O)OC(C)C BWJUFXUULUEGMA-UHFFFAOYSA-N 0.000 description 1
- 125000001325 propanoyl group Chemical group O=C([*])C([H])([H])C([H])([H])[H] 0.000 description 1
- QQONPFPTGQHPMA-UHFFFAOYSA-N propylene Natural products CC=C QQONPFPTGQHPMA-UHFFFAOYSA-N 0.000 description 1
- 125000004805 propylene group Chemical group [H]C([H])([H])C([H])([*:1])C([H])([H])[*:2] 0.000 description 1
- 239000002994 raw material Substances 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- XWGJFPHUCFXLBL-UHFFFAOYSA-M rongalite Chemical compound [Na+].OCS([O-])=O XWGJFPHUCFXLBL-UHFFFAOYSA-M 0.000 description 1
- LIVNPJMFVYWSIS-UHFFFAOYSA-N silicon monoxide Chemical class [Si-]#[O+] LIVNPJMFVYWSIS-UHFFFAOYSA-N 0.000 description 1
- 235000017557 sodium bicarbonate Nutrition 0.000 description 1
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 1
- AJPJDKMHJJGVTQ-UHFFFAOYSA-M sodium dihydrogen phosphate Chemical compound [Na+].OP(O)([O-])=O AJPJDKMHJJGVTQ-UHFFFAOYSA-M 0.000 description 1
- 229940079827 sodium hydrogen sulfite Drugs 0.000 description 1
- 235000010267 sodium hydrogen sulphite Nutrition 0.000 description 1
- KOUDKOMXLMXFKX-UHFFFAOYSA-N sodium oxido(oxo)phosphanium hydrate Chemical compound O.[Na+].[O-][PH+]=O KOUDKOMXLMXFKX-UHFFFAOYSA-N 0.000 description 1
- 239000004328 sodium tetraborate Chemical class 0.000 description 1
- 235000010339 sodium tetraborate Nutrition 0.000 description 1
- 235000011071 sorbitan monopalmitate Nutrition 0.000 description 1
- 229940031953 sorbitan monopalmitate Drugs 0.000 description 1
- 239000001570 sorbitan monopalmitate Substances 0.000 description 1
- 241000894007 species Species 0.000 description 1
- 239000003381 stabilizer Substances 0.000 description 1
- 230000000087 stabilizing effect Effects 0.000 description 1
- 230000001629 suppression Effects 0.000 description 1
- 239000002344 surface layer Substances 0.000 description 1
- 239000004094 surface-active agent Substances 0.000 description 1
- 238000010558 suspension polymerization method Methods 0.000 description 1
- 239000011975 tartaric acid Substances 0.000 description 1
- 235000002906 tartaric acid Nutrition 0.000 description 1
- ISIJQEHRDSCQIU-UHFFFAOYSA-N tert-butyl 2,7-diazaspiro[4.5]decane-7-carboxylate Chemical compound C1N(C(=O)OC(C)(C)C)CCCC11CNCC1 ISIJQEHRDSCQIU-UHFFFAOYSA-N 0.000 description 1
- NMOALOSNPWTWRH-UHFFFAOYSA-N tert-butyl 7,7-dimethyloctaneperoxoate Chemical compound CC(C)(C)CCCCCC(=O)OOC(C)(C)C NMOALOSNPWTWRH-UHFFFAOYSA-N 0.000 description 1
- 229920005992 thermoplastic resin Polymers 0.000 description 1
- 239000010936 titanium Substances 0.000 description 1
- 229910052719 titanium Inorganic materials 0.000 description 1
- OGIDPMRJRNCKJF-UHFFFAOYSA-N titanium oxide Inorganic materials [Ti]=O OGIDPMRJRNCKJF-UHFFFAOYSA-N 0.000 description 1
- 238000004448 titration Methods 0.000 description 1
- AJSTXXYNEIHPMD-UHFFFAOYSA-N triethyl borate Chemical compound CCOB(OCC)OCC AJSTXXYNEIHPMD-UHFFFAOYSA-N 0.000 description 1
- ITMCEJHCFYSIIV-UHFFFAOYSA-N triflic acid Chemical compound OS(=O)(=O)C(F)(F)F ITMCEJHCFYSIIV-UHFFFAOYSA-N 0.000 description 1
- WRECIMRULFAWHA-UHFFFAOYSA-N trimethyl borate Chemical compound COB(OC)OC WRECIMRULFAWHA-UHFFFAOYSA-N 0.000 description 1
- WFKWXMTUELFFGS-UHFFFAOYSA-N tungsten Chemical compound [W] WFKWXMTUELFFGS-UHFFFAOYSA-N 0.000 description 1
- 229910052721 tungsten Inorganic materials 0.000 description 1
- 239000010937 tungsten Substances 0.000 description 1
- 229910001930 tungsten oxide Inorganic materials 0.000 description 1
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 1
- UKRDPEFKFJNXQM-UHFFFAOYSA-N vinylsilane Chemical class [SiH3]C=C UKRDPEFKFJNXQM-UHFFFAOYSA-N 0.000 description 1
- 239000001993 wax Substances 0.000 description 1
- 238000005303 weighing Methods 0.000 description 1
- 229910052725 zinc Inorganic materials 0.000 description 1
- 239000011701 zinc Substances 0.000 description 1
- 239000011787 zinc oxide Substances 0.000 description 1
- 229910052726 zirconium Inorganic materials 0.000 description 1
- 229910001928 zirconium oxide Inorganic materials 0.000 description 1
- 239000004711 α-olefin Substances 0.000 description 1
- DGVVWUTYPXICAM-UHFFFAOYSA-N β‐Mercaptoethanol Chemical compound OCCS DGVVWUTYPXICAM-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F8/00—Chemical modification by after-treatment
- C08F8/10—Acylation
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08J—WORKING-UP; GENERAL PROCESSES OF COMPOUNDING; AFTER-TREATMENT NOT COVERED BY SUBCLASSES C08B, C08C, C08F, C08G or C08H
- C08J3/00—Processes of treating or compounding macromolecular substances
- C08J3/20—Compounding polymers with additives, e.g. colouring
- C08J3/205—Compounding polymers with additives, e.g. colouring in the presence of a continuous liquid phase
- C08J3/21—Compounding polymers with additives, e.g. colouring in the presence of a continuous liquid phase the polymer being premixed with a liquid phase
- C08J3/215—Compounding polymers with additives, e.g. colouring in the presence of a continuous liquid phase the polymer being premixed with a liquid phase at least one additive being also premixed with a liquid phase
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08K—Use of inorganic or non-macromolecular organic substances as compounding ingredients
- C08K3/00—Use of inorganic substances as compounding ingredients
- C08K3/18—Oxygen-containing compounds, e.g. metal carbonyls
- C08K3/20—Oxides; Hydroxides
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08K—Use of inorganic or non-macromolecular organic substances as compounding ingredients
- C08K3/00—Use of inorganic substances as compounding ingredients
- C08K3/34—Silicon-containing compounds
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08K—Use of inorganic or non-macromolecular organic substances as compounding ingredients
- C08K5/00—Use of organic ingredients
- C08K5/04—Oxygen-containing compounds
- C08K5/09—Carboxylic acids; Metal salts thereof; Anhydrides thereof
- C08K5/098—Metal salts of carboxylic acids
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08K—Use of inorganic or non-macromolecular organic substances as compounding ingredients
- C08K5/00—Use of organic ingredients
- C08K5/16—Nitrogen-containing compounds
- C08K5/20—Carboxylic acid amides
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08L—COMPOSITIONS OF MACROMOLECULAR COMPOUNDS
- C08L29/00—Compositions of homopolymers or copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and at least one being terminated by an alcohol, ether, aldehydo, ketonic, acetal or ketal radical; Compositions of hydrolysed polymers of esters of unsaturated alcohols with saturated carboxylic acids; Compositions of derivatives of such polymers
- C08L29/02—Homopolymers or copolymers of unsaturated alcohols
- C08L29/04—Polyvinyl alcohol; Partially hydrolysed homopolymers or copolymers of esters of unsaturated alcohols with saturated carboxylic acids
Definitions
- the present invention relates to pellets containing ethylene-vinyl alcohol copolymer and a method for producing the same.
- Ethylene-vinyl alcohol copolymer (hereinafter sometimes abbreviated as EVOH) is excellent in gas barrier properties, transparency, aroma retention properties, solvent resistance, oil resistance, etc., and is used in food packaging by taking advantage of these properties. It is used in a wide range of applications, including various packaging containers such as containers, pharmaceutical packaging containers, industrial chemical packaging containers, agricultural chemical packaging containers, and fuel containers. When producing such a molded product, secondary processing is often performed after EVOH is melt-molded. For example, stretching to improve mechanical strength and thermoforming of a film or sheet containing an EVOH layer to form a container shape are widely practiced.
- Patent Document 1 2-methylene-1,3-propanediol units obtained by copolymerizing ethylene, vinyl acetate and 2-methylene-1,3-propanediol diacetate and then saponifying are copolymerized.
- a modified EVOH is described.
- the modified EVOH is described as having excellent barrier properties, flexibility and secondary workability.
- there is a problem of blocking in which the molded articles adhere to each other when the obtained molded articles such as films or sheets are stacked or rolled and stored.
- Patent Document 2 describes a modified EVOH containing an antiblocking agent composed of inorganic particles having an average particle size of more than 0.3 ⁇ m and 20 ⁇ m or less.
- the modified EVOH was found to improve the blocking of the film, the improvement of the blocking between pellets was insufficient.
- the present invention has been made to solve the above problems, and provides EVOH-containing pellets with excellent secondary workability, flexibility and blocking resistance, and a method for producing the same.
- the present inventors have made intensive studies to improve the flexibility and blocking resistance of pellets containing EVOH.
- the problem was solved by forming a predetermined recess in the .
- the above problem is a pellet containing EVOH and particles having a degree of saponification of 90 mol% or more and cut into a cylindrical shape, wherein the enthalpy of fusion ⁇ Hm (J/g) of the pellet is 65 (J/g) or less.
- the pellet contains 5 to 5000 ppm of particles having an average particle diameter R of 1 to 30 ⁇ m, the length of the pellet is L (mm), and a recess is formed on the side or cut surface of the pellet,
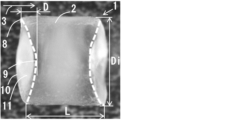
- the number n of the recesses is 2 to 5, and at least 1 perpendicular to the flow direction of the pellets at a position L / 4 (mm) or less from the center of gravity of the pellets.
- the distances ⁇ 1 to ⁇ n from the center of gravity of the cross section to the edge of the recess formed on the side surface and the distances ⁇ 1 to ⁇ n from the center of gravity of the cross section to the bottom of the recess formed on the side surface are calculated by the following formula ( 1) is satisfied, ( ⁇ 1+ ⁇ 2...+ ⁇ n)/( ⁇ 1+ ⁇ 2...+ ⁇ n) ⁇ 0.8 (1)
- the ratio D / L of the depth D (mm) of the recess formed in the cut surface to the length L (mm) of the pellet is 0.1 or more
- the problem is solved by providing a pellet in which projections having a height H of 0.1 to 15 ⁇ m are formed on the surface of the pellet, the projections contain the particles, and the particles are coated with the EVOH.
- the melting enthalpy ⁇ Hm (J/g) of the pellet is preferably 64 (J/g) or less.
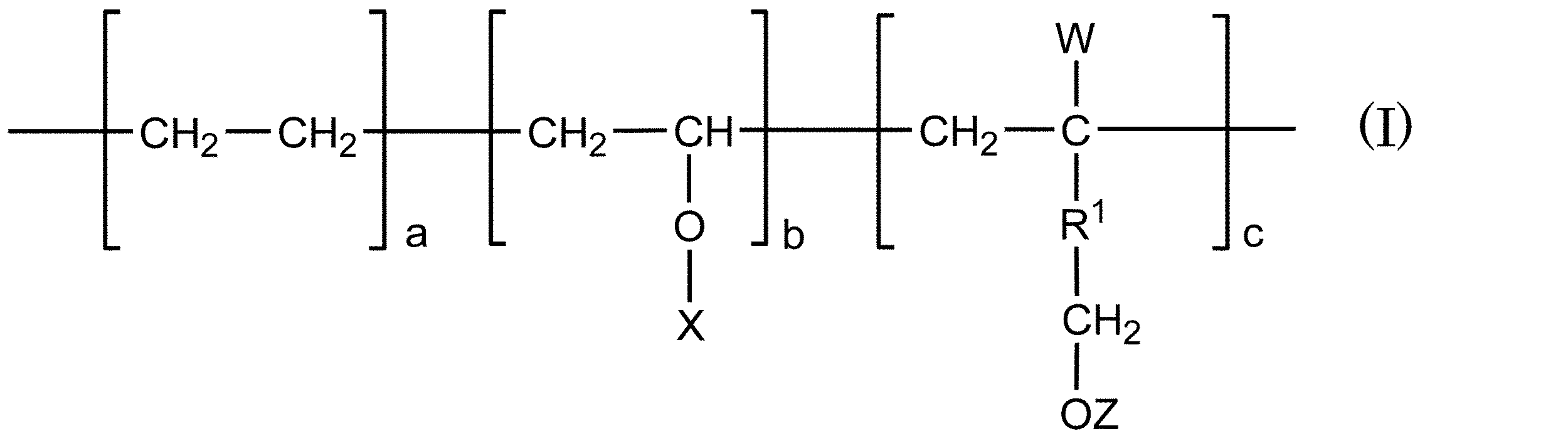
- the EVOH is represented by the following formula (I) and is a modified EVOH in which the content ratios (mol%) of a, b and c with respect to the total monomer units satisfy the following formulas (2) to (4). preferable.
- W represents a hydrogen atom, a methyl group or a group represented by R 2 -OY
- X, Y and Z each independently represent a hydrogen atom, a formyl group or a represents an alkanoyl group.
- R 1 and R 2 each independently represent a single bond, an alkylene group having 1 to 9 carbon atoms, or an alkyleneoxy group having 1 to 9 carbon atoms, and the alkylene group and the alkyleneoxy group are a hydroxyl group, an alkoxy group, or a halogen atom.
- R 1 in the above formula (I) is a single bond and W is a hydroxymethyl group.
- the melting enthalpy ⁇ Hm (J/g) of the pellets and the content A (ppm) of the particles satisfy the following formula (6). 1 ⁇ Hm/100+A/500 ⁇ 10 (6)
- the average particle diameter R ( ⁇ m) of the particles and the height H ( ⁇ m) of the protrusions satisfy the following formula (7). 0.1 ⁇ H/R ⁇ 0.9 (7)
- the particles are inorganic oxide particles. More preferably, the inorganic oxide particles are silicon oxide particles or metal oxide particles.
- the particles are organic compound particles containing at least one selected from the group consisting of saturated fatty acid amides, unsaturated fatty acid amides, bis fatty acid amides and fatty acid metal salts.
- the above problem is to manufacture the pellets, which includes the step of cutting the strands containing the EVOH, the particles and water to obtain cylindrical hydrous pellets, and the step of drying the hydrous pellets to form the recesses. It is also solved by providing a method.
- the above object is a pellet containing modified EVOH and particles and cut into a cylindrical shape, wherein the pellet contains 5 to 5000 ppm of particles having an average particle diameter R of 1 to 30 ⁇ m, and the modified EVOH is Represented by the following formula (I), the content ratio (mol%) of a, b and c with respect to the total monomer units satisfies the following formulas (2) to (4), and is defined by the following formula (8)
- the degree of saponification (DS) is 90 mol% or more
- W represents a hydrogen atom, a methyl group or a group represented by R 2 -OY
- X, Y and Z each independently represent a hydrogen atom, a formyl group or a represents an alkanoyl group.
- R 1 and R 2 each independently represent a single bond, an alkylene group having 1 to 9 carbon atoms, or an alkyleneoxy group having 1 to 9 carbon atoms, and the alkylene group and the alkyleneoxy group are a hydroxyl group, an alkoxy group, or a halogen atom.
- L (mm) a recess is formed in the side surface or cut surface of the pellet, and the recess is formed in the side surface, the number n of the recesses is 2 to 5, and the pellet In at least one cross section perpendicular to the flow direction of the pellet at a position L / 4 (mm) or less from the center of gravity of the distance ⁇ 1 to ⁇ n from the center of gravity of the cross section to the edge of the recess formed on the side surface and the distance ⁇ 1 to ⁇ n from the center of gravity of the cross section to the bottom of the recess formed on the side surface satisfies the following formula (1)
- the pellets of the present invention have excellent blocking resistance and can be molded into products with excellent secondary workability and flexibility. Moreover, the pellets are excellent in extrusion stability. Therefore, the pellet can be suitably used as a barrier material or the like. Moreover, according to the production method of the present invention, such pellets can be produced easily.
- FIG. 1 is an appearance photograph of a side surface of a pellet obtained in Example 1.
- FIG. 2 is an electron micrograph of a cross section obtained by cutting the pellet perpendicularly to the flow direction at a position of L/4 (mm) or less from the center of gravity of the pellet obtained in Example 1.
- FIG. It is an example of an appearance photograph of the pellet side surface of the present invention in which a recess is formed in the cut surface.
- 1 is an electron microscope image of the surface of a pellet obtained in Example 1.
- the pellets of the present invention contain EVOH and particles having a degree of saponification of 90 mol% or more, are cylindrically cut pellets, and have a melting enthalpy ⁇ Hm (J/g) of 65 (J/g ) or less, the pellet contains 5 to 5000 ppm of particles having an average particle diameter R of 1 to 30 ⁇ m, the length of the pellet is L (mm), and a recess is formed on the side or cut surface of the pellet and when recesses are formed on the side surface, the number n of the recesses is 2 to 5, and the pellet is perpendicular to the flow direction at a position L / 4 (mm) or less from the center of gravity of the pellet.
- the distances ⁇ 1 to ⁇ n from the center of gravity of the cross section to the edge of the recess formed on the side surface, and the distances ⁇ 1 to ⁇ n from the center of gravity of the cross section to the bottom of the recess formed on the side surface are as follows.
- the ratio D / L of the depth D (mm) of the recess formed in the cut surface to the length L (mm) of the pellet is 0.1 or more, Projections having a height H of 0.1 to 15 ⁇ m are formed on the surface of the pellet, and the projections contain the particles and are coated with the EVOH.
- the pellets of the present invention have excellent flexibility and blocking resistance. Moreover, the pellets are excellent in extrusion stability.
- modified EVOH has been known in which flexibility and the like are improved by copolymerizing predetermined units.
- Modified EVOH containing an anti-blocking agent composed of inorganic particles having a predetermined average particle size has also been known, but the modified EVOH pellets sometimes block each other, which still poses a problem.
- the present invention by forming the protrusions on the surface of the pellets and forming the recesses on the side surfaces or cut surfaces, the contact area between the pellets is reduced, and the blocking resistance is considered to be improved. .
- the flexibility is improved and the concave portions are easily formed by setting the melting enthalpy ⁇ Hm (J/g) of the pellet within a predetermined range.
- the contact area between the pellets is reduced, the discharge rate during melt extrusion is stabilized, and the extrusion stability is also improved.
- the EVOH contained in the pellets of the present invention is usually obtained by saponifying an ethylene-vinyl ester copolymer obtained by polymerizing ethylene and vinyl ester.
- the ethylene unit content a (mol %) relative to the total monomer units in the EVOH satisfies the following formula (2), that is, 24 to 55 mol %. If the ethylene unit content a is less than 24 mol %, the melt moldability of the EVOH may deteriorate.
- the ethylene unit content a is more preferably 26 mol % or more, and even more preferably 30 mol % or more. On the other hand, if the ethylene unit content a exceeds 55 mol %, the barrier properties of the EVOH may be insufficient.
- the ethylene unit content a is more preferably 52 mol % or less, and even more preferably 49 mol % or less. 24 ⁇ a ⁇ 55 (2)
- the EVOH contained in the pellets of the present invention has a degree of saponification (DS) of 90 mol% or more.
- the degree of saponification refers to the ratio (mol%) of the number of moles of the hydroxyl group to the total number of moles of the hydroxyl group and the ester group that can be converted to a hydroxyl group by saponification in the EVOH. If the degree of saponification (DS) is less than 90 mol %, not only is sufficient barrier performance not obtained, but also the thermal stability of the EVOH is insufficient, and gels and lumps are likely to occur during melt molding.
- the degree of saponification (DS) is preferably 95 mol% or more, more preferably 98 mol% or more, still more preferably 99 mol% or more.
- the degree of saponification (DS) is preferably 99 mol% or more, more preferably 99.5 mol% or more, and even more preferably It is 99.8 mol% or more.
- the degree of saponification (DS) can be obtained by the nuclear magnetic resonance (NMR) method.
- the ethylene unit content a and the monomer unit content b and c in the modified EVOH represented by formula (I) described later can also be obtained by NMR.
- the preferred melt flow rate (MFR) of the EVOH (190° C., under 2160 g load) is 0.1 to 30 g/10 min, more preferably 0.3 to 25 g/10 min, still more preferably 0.5 to 20 g. /10 minutes. However, if the melting point is near or above 190°C, the measurement is performed at multiple temperatures above the melting point under a load of 2160 g. Expressed as a value extrapolated to 190°C.
- the MFR of the obtained pellets is also preferably within the above range.
- the EVOH contained in the pellets of the present invention may have a saponification degree (DS) within the above range, and the type is not particularly limited, but is represented by the following formula (I),
- the modified EVOH is preferably one in which the contents (mol %) of b and c satisfy the above formula (2) and the following formulas (3) and (4).
- This modified EVOH contains, in addition to ethylene units and vinyl alcohol units, a monomer unit having a primary hydroxyl group (the rightmost monomer unit containing W, Z and R1 in formula (I)). , the crystallinity is lower than that of EVOH that does not contain the monomer unit, so flexibility and secondary workability can be further improved.
- this modified EVOH can reduce the deterioration of the barrier properties caused by the deterioration of the crystallinity due to the strong hydrogen bonding force of the primary hydroxyl group. In other words, it is possible to further improve flexibility and secondary workability while minimizing deterioration in barrier performance. Furthermore, since the modified EVOH containing the monomer unit having a primary hydroxyl group has low crystallinity, the hydrous pellets tend to shrink unevenly when dried.
- W represents a hydrogen atom, a methyl group or a group represented by R 2 -OY
- X, Y and Z each independently represent a hydrogen atom, a formyl group or a represents an alkanoyl group.
- R 1 and R 2 each independently represent a single bond, an alkylene group having 1 to 9 carbon atoms, or an alkyleneoxy group having 1 to 9 carbon atoms, and the alkylene group and the alkyleneoxy group are a hydroxyl group, an alkoxy group, or a halogen atom.
- R 1 and R 2 each independently represent a single bond, an alkylene group having 1 to 9 carbon atoms or an alkyleneoxy group having 1 to 9 carbon atoms.
- the alkylene group and alkyleneoxy group may contain a hydroxyl group, an alkoxy group, or a halogen atom.
- the number of carbon atoms in the alkylene group is preferably 5 or less, more preferably 3 or less, and even more preferably 2 or less.
- the number of carbon atoms in the alkyleneoxy group is preferably 5 or less, more preferably 3 or less, and even more preferably 2 or less.
- W is preferably a hydrogen atom or a group represented by R 2 --OH, more preferably a group represented by R 2 --OH.
- the group represented by R 2 —OH is preferably a hydroxyalkyl group (R 2 is an alkylene group).
- monomer units having a primary hydroxyl group in the formula (I) include monomer units represented by the following formulas (II) to (IV). Structural units represented are preferred.
- R 3 and R 4 each independently represent a hydrogen atom or an alkyl group having 1 to 8 carbon atoms, and the alkyl group may contain a hydroxyl group, an alkoxy group or a halogen atom. ]
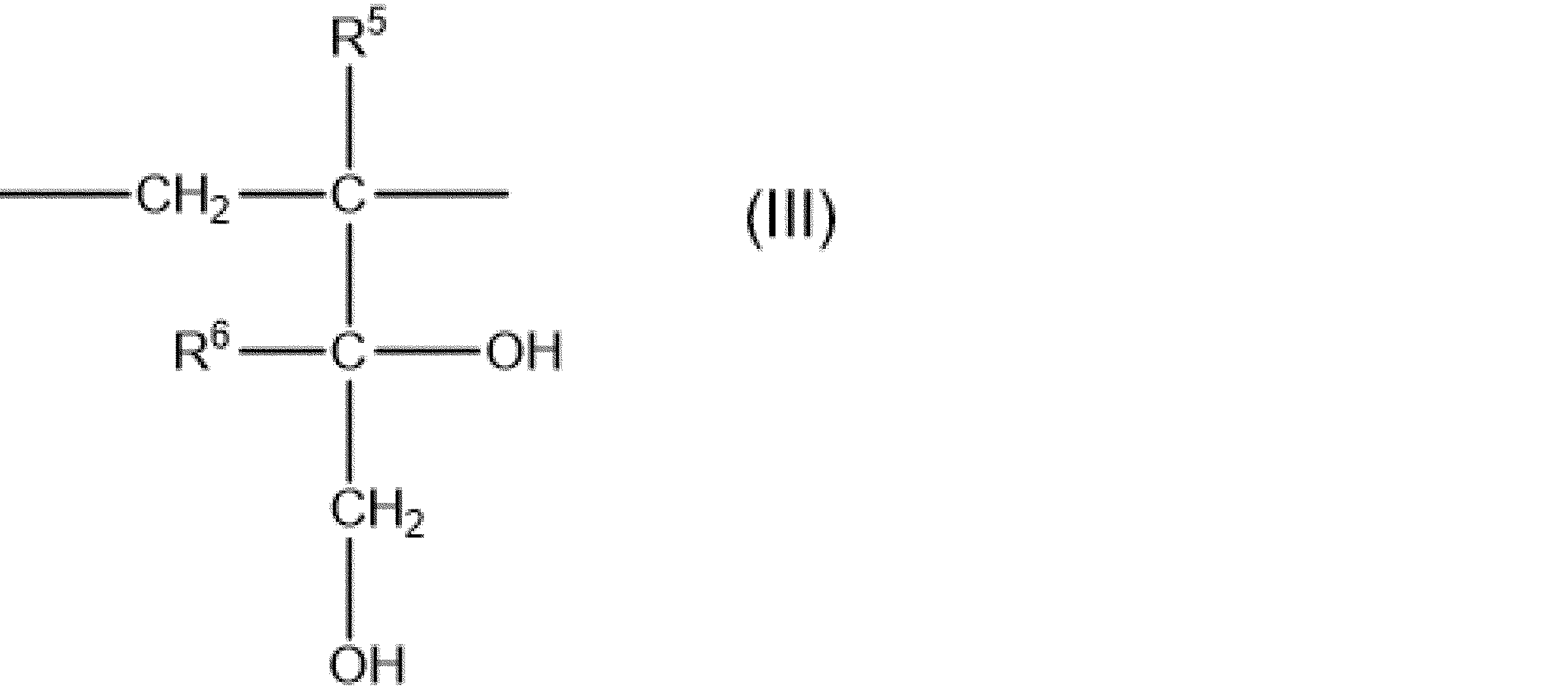
- R 5 has the same definition as W in formula (I).
- R 6 represents a hydrogen atom or an alkyl group having 1 to 8 carbon atoms, and the alkyl group may contain a hydroxyl group, an alkoxy group or a halogen atom.
- R 7 and R 8 each independently represent a hydrogen atom, an alkyl group having 1 to 8 carbon atoms, a cycloalkyl group having 3 to 8 carbon atoms or a hydroxyl group, and the alkyl group and the A cycloalkyl group may contain a hydroxyl group, an alkoxy group or a halogen atom.
- R 1 is a single bond
- W is a hydroxymethyl group
- R 3 and R 4 in formula (II) above are hydrogen atoms
- R 1 is hydroxy A methylene group
- W is a hydrogen atom
- R 5 and R 6 in the above formula (III) are hydrogen atoms
- R 1 is a methylmethyleneoxy group
- W is a hydrogen atom
- one of R 7 and R 8 is preferably a methyl group and the other is a hydrogen atom, and (1) is particularly preferable.
- X, Y and Z each independently represent a hydrogen atom, a formyl group or an alkanoyl group having 2 to 10 carbon atoms.
- the above formula (I) has a hydroxyl group
- the above formula (I) is an ester group
- the alkanoyl group is preferably an alkanoyl group having 2 to 5 carbon atoms, more preferably an acetyl group, a propanoyl group, a butanoyl group, etc., and more preferably an acetyl group.
- Each of X, Y and Z is preferably a hydrogen atom or a mixture containing a hydrogen atom.
- a monomeric unit containing X is usually obtained by saponifying a vinyl ester. Therefore, X is preferably a mixture of a hydrogen atom and a formyl group or an alkanoyl group having 2 to 10 carbon atoms. Considering the availability of the monomer (vinyl acetate) and production costs, X is more preferably a mixture of a hydrogen atom and an acetyl group.
- the monomer unit containing Y and Z can also be produced by copolymerizing a monomer having an ester group such as an unsaturated monomer having a 1,3-diester structure and then saponifying it. , 1,3-diol structure, or the like, by directly copolymerizing a monomer having a hydroxyl group. Therefore, both Y and Z may be only a hydrogen atom, or a mixture of a hydrogen atom and a formyl group or an alkanoyl group having 2 to 10 carbon atoms, more preferably a mixture of a hydrogen atom and an acetyl group. may be
- c represents the content (mol%) of monomer units having a primary hydroxyl group shown on the right end with respect to all monomer units in the modified EVOH, and 0 It is preferably from 0.01 to 10 mol %. If c is less than 0.01 mol %, the moldability and secondary workability of the modified EVOH may be insufficient. c is more preferably 0.05 mol % or more, still more preferably 0.1 mol % or more, and particularly preferably 0.5 mol % or more. On the other hand, if c exceeds 10 mol %, the barrier properties of the modified EVOH may deteriorate. c is more preferably 5 mol % or less.
- b represents the content (mol %) of vinyl alcohol units and vinyl ester units with respect to all monomer units in the modified EVOH. It is preferable that this satisfies the above formula (4). Satisfying the above formula (4) means that in the modified EVOH, 90% of the monomer units other than the ethylene unit and the monomer unit having a primary hydroxyl group shown on the right end in the above formula (I) It means that the above are vinyl alcohol units or vinyl ester units. If the above formula (4) is not satisfied, the gas barrier properties may be insufficient. More preferably, the following formula (4') is satisfied, and more preferably the following formula (4'') is satisfied. [100-(a+c)] ⁇ 0.95 ⁇ b ⁇ [100-(a+c)](4′) [100-(a+c)] ⁇ 0.98 ⁇ b ⁇ [100-(a+c)](4′′)
- the EVOH contained in the pellets of the present invention has a degree of saponification (DS) of 90 mol % or more.
- the degree of saponification (DS) is determined by the following formula (8).
- DS [(Total number of moles of hydrogen atoms among X, Y and Z)/(Total number of moles of X, Y and Z)] ⁇ 100 (8)
- the "total number of moles of hydrogen atoms among X, Y and Z" indicates the number of moles of hydroxyl groups
- the “total number of moles of X, Y and Z” is the total number of moles of hydroxyl groups and ester groups.
- the modified EVOH represented by formula (I) above is usually a random copolymer.
- the fact that it is a random copolymer can be confirmed from the measurement results of NMR and melting point.
- a and c in the above formula (I) satisfy the following formula (5). If “1.2a+8c” is less than 29, the moldability and secondary workability of the modified EVOH may be insufficient. "1.2a+8c” is preferably 40 or more, more preferably 50 or more, still more preferably 55 or more. On the other hand, when “1.2a+8c” exceeds 100, the barrier properties of the modified EVOH may deteriorate. "1.2a+8c” is preferably 90 or less, more preferably 85 or less, still more preferably 80 or less. 29 ⁇ 1.2a+8c ⁇ 100 (5)
- the EVOH contained in the pellets may be a mixture of modified EVOH represented by the formula (I) and unmodified EVOH.
- the mass ratio of the modified EVOH and unmodified EVOH (modified EVOH/unmodified EVOH) in the mixture is preferably 1/9 to 9/1.
- the mass ratio (modified EVOH/unmodified EVOH) preferably exceeds 9/1, and substantially no unmodified EVOH is contained. more preferred.
- the EVOH contained in the pellet is a mixture of two or more different modified EVOH or a mixture of modified EVOH and unmodified EVOH
- the content of each monomer unit, saponification degree and MFR are An average value calculated from the mass ratio is used.
- the manufacturing method of the EVOH is not particularly limited.
- a method for producing a modified EVOH containing a monomer unit represented by the above formula (II) as a monomer unit having a primary hydroxyl group shown on the right end of the above formula (I), ethylene the following After obtaining a modified ethylene-vinyl ester copolymer represented by the following formula (VII) by radically polymerizing a vinyl ester represented by the formula (V) and an unsaturated monomer represented by the following formula (VI), There is a method of saponifying it.
- the manufacturing method will be described below.
- An unmodified EVOH can be obtained in the same manner as in the above method, except that the unsaturated monomer represented by the following formula (VI) is not used.
- R 9 represents a hydrogen atom or an alkyl group having 1 to 9 carbon atoms.
- the number of carbon atoms in the alkyl group is preferably 1-4.
- Examples of the vinyl ester represented by formula (V) include vinyl formate, vinyl acetate, vinyl propionate, vinyl butyrate, vinyl isobutyrate, vinyl pivalate, vinyl versatate, and vinyl caproate. Vinyl acetate is more preferred from an economic point of view.
- R3 and R4 are the same as in formula (II).
- R 10 and R 11 each independently represent a hydrogen atom or an alkyl group having 1 to 9 carbon atoms. The number of carbon atoms in the alkyl group is preferably 1-4.
- unsaturated monomers represented by formula (VI) include 2-methylene-1,3-propanediol diacetate, 2-methylene-1,3-propanediol dipropionate, 2-methylene-1,3- and propanediol dibutyrate. Among them, 2-methylene-1,3-propanediol diacetate is preferably used because of its easy production. In the case of 2-methylene-1,3-propanediol diacetate, R 3 and R 4 are hydrogen atoms and R 10 and R 11 are methyl groups.
- R 3 , R 4 , R 9 , R 10 and R 11 are the same as in formulas (II), (V) and (VI).
- a, b, and c are ethylene units, vinyl ester units, and the content (mol%) of units derived from unsaturated monomers represented by formula (VI), respectively, relative to all monomer units. show. The modified ethylene-vinyl ester copolymer thus obtained is then saponified.
- an unsaturated monomer represented by the above formula (VI) may be copolymerized. Only vinyl ester units containing will be saponified.
- R3 and R4 are the same as in formula (II).
- Unsaturated monomers represented by formula (VIII) include 2-methylene-1,3-propanediol and 2-methylene-1,3-butanediol.
- the unsaturated monomers represented by the above formulas (VI) and (VIII) have high copolymerization reactivity with vinyl ester monomers, so the copolymerization reaction proceeds easily. Therefore, it is easy to increase the degree of modification and the degree of polymerization of the resulting modified ethylene-vinyl ester copolymer. Moreover, even if the polymerization reaction is stopped at a low polymerization rate, the amount of the unreacted unsaturated monomer remaining at the end of the polymerization is small, so that it is excellent in terms of environment and cost.
- the unsaturated monomers represented by formulas (VI) and (VIII) are those having one carbon atom having a functional group at the allylic position, such as allyl glycidyl ether and 3,4-diacetoxy-1-butene. superior to other monomers that are only Here, the unsaturated monomer represented by formula (VI) has higher reactivity than the unsaturated monomer represented by formula (V).
- a modified ethylene-vinyl ester copolymer is produced by copolymerizing ethylene, a vinyl ester represented by the above formula (V), and an unsaturated monomer represented by the above formula (VI) or (VIII).
- the polymerization system may be batch polymerization, semi-batch polymerization, continuous polymerization, or semi-continuous polymerization.
- known methods such as bulk polymerization method, solution polymerization method, suspension polymerization method and emulsion polymerization method can be employed.
- a bulk polymerization method or a solution polymerization method, in which polymerization is carried out without solvent or in a solvent such as alcohol, is usually employed.
- the solvent used in the solution polymerization method is not particularly limited, but examples include alcohols, and lower alcohols such as methanol, ethanol, and propanol are more preferable.
- the amount of the solvent used in the polymerization reaction solution may be selected in consideration of the desired viscosity-average degree of polymerization of the modified EVOH and the chain transfer of the solvent. (solvent/total monomers) is usually in the range of 0.01-10, preferably in the range of 0.03-3, more preferably in the range of 0.05-1.
- the polymerization initiator used in copolymerizing ethylene, the vinyl ester represented by the above formula (V), and the unsaturated monomer represented by the above formula (VI) or (VIII) is a known polymerization initiator.
- the initiator is selected from azo initiators, peroxide initiators and redox initiators, depending on the polymerization method.
- azo initiators include 2,2′-azobisisobutyronitrile, 2,2′-azobis(2,4-dimethylvaleronitrile), 2,2′-azobis(4-methoxy-2,4 -dimethylvaleronitrile).
- peroxide-based initiators include peroxydicarbonate-based compounds such as diisopropyl peroxydicarbonate, di-2-ethylhexyl peroxydicarbonate, and diethoxyethyl peroxydicarbonate; t-butyl peroxyneodecanate, ⁇ - perester compounds such as cumyl peroxyneodecanate and acetyl peroxide; acetylcyclohexylsulfonyl peroxide; 2,4,4-trimethylpentyl-2-peroxyphenoxyacetate and the like. Potassium persulfate, ammonium persulfate, hydrogen peroxide and the like may be combined with the above initiators.
- the redox initiator is, for example, a polymerization initiator obtained by combining the above peroxide initiator with a reducing agent such as sodium hydrogensulfite, sodium hydrogencarbonate, tartaric acid, L-ascorbic acid, or Rongalite.
- the amount of the polymerization initiator used is adjusted according to the polymerization rate.
- the amount of polymerization initiator to be used is preferably 0.01 to 0.2 mol, more preferably 0.02 to 0.15 mol, per 100 mol of vinyl ester monomer.
- the polymerization temperature is not particularly limited, but room temperature to about 150°C is suitable, preferably 40°C or higher and 100°C or lower.
- Copolymerization may be carried out in the presence of a chain transfer agent.
- chain transfer agents include aldehydes such as acetaldehyde and propionaldehyde; ketones such as acetone and methyl ethyl ketone; mercaptans such as 2-hydroxyethanethiol; and phosphinates such as sodium phosphinate monohydrate. . Among them, aldehydes and ketones are preferred.
- the amount of the chain transfer agent added to the polymerization reaction solution is determined according to the chain transfer coefficient of the chain transfer agent and the degree of polymerization of the desired modified ethylene-vinyl ester copolymer. 0.1 to 10 parts by mass is preferable.
- the modified ethylene-vinyl ester copolymer thus obtained can be saponified to obtain modified EVOH.
- the vinyl ester units in the copolymer are converted to vinyl alcohol units.
- an ester bond derived from the unsaturated monomer represented by formula (VI) is also hydrolyzed and converted to a 1,3-diol structure.
- different types of ester groups can be hydrolyzed simultaneously by one saponification reaction.
- a known method can be employed as a method for saponifying the modified ethylene-vinyl ester copolymer.
- the saponification reaction is usually carried out in an alcohol or hydroalcoholic solution.
- Alcohols preferably used at this time are lower alcohols such as methanol and ethanol, and more preferably methanol.
- the alcohol or hydroalcohol used in the saponification reaction may contain other solvents such as acetone, methyl acetate, ethyl acetate, benzene, etc., as long as it is 40% by weight or less of its weight.
- Catalysts used for saponification are, for example, alkali metal hydroxides such as potassium hydroxide and sodium hydroxide, alkali catalysts such as sodium methylate, and acid catalysts such as mineral acids.
- the temperature for saponification is not limited, a range of 20 to 120°C is preferable.
- the modified EVOH is copolymerizable with ethylene, the vinyl ester represented by the above formula (V), and the unsaturated monomer represented by the above formula (VI) or (VIII) as long as the effects of the present invention are not impaired. , may contain structural units derived from other ethylenically unsaturated monomers.
- Examples of such other ethylenically unsaturated monomers include ⁇ -olefins such as propylene, n-butene, isobutylene and 1-hexene; acrylic acid and its salts; methacrylic acid and its salts; unsaturated monomers having a methacrylic ester group; acrylamide, N-methylacrylamide, N-ethylacrylamide, N,N-dimethylacrylamide, diacetoneacrylamide, acrylamidopropanesulfonic acid and its salts, acrylamidopropyldimethylamine and its salts (e.g.,
- methacrylamide, N-methylmethacrylamide, N-ethylmethacrylamide, methacrylamidopropanesulfonic acid and its salts, methacrylamidopropyldimethylamine and its salts e.g.
- quaternary salt methyl vinyl ether, ethyl vinyl ether, n-propyl vinyl ether, i-propyl vinyl ether, n-butyl vinyl ether, i-butyl vinyl ether, t-butyl vinyl ether, dodecyl vinyl ether, stearyl vinyl ether, 2,3-diacetoxy-1- vinyl ethers such as vinyloxypropane; vinyl cyanides such as acrylonitrile and methacrylonitrile; vinyl halides such as vinyl chloride and vinyl fluoride; vinylidene halides such as vinylidene chloride and vinylidene fluoride; , 3-diacetoxy-1-allyloxypropane, allyl compounds such as allyl chloride; unsaturated dicarboxylic acids such as maleic acid, itaconic acid and fumaric acid and their salts or esters; vinylsilane compounds such as vinyltrimethoxysilane; isopropenyl acetate
- the method for producing the modified EVOH containing the monomer unit represented by the formula (III) as the monomer unit having a primary hydroxyl group shown on the right end of the formula (I) is not particularly limited.
- a method of saponifying a copolymer obtained by copolymerizing 3,4-diol-1-butene, a vinyl ester monomer and ethylene A method of saponifying a copolymer obtained by copolymerization
- a method of saponifying a copolymer obtained by copolymerizing 3-acyloxy-4-ol-1-butene, a vinyl ester monomer and ethylene , 4-acyloxy-3-ol-1-butene, a method of saponifying a copolymer obtained by copolymerizing a vinyl ester monomer and ethylene, 3,4-diacyloxy-2-methyl-1-butene A method of saponifying a copolymer obtained by copolymerizing a vinyl ester monomer and ethylene can be
- a modified EVOH containing a monomer unit represented by the formula (III) can be obtained in the same manner as for EVOH.
- Such 3,4-diol-1-butene is represented by the following formula (IX)
- 3,4-diacyloxy-1-butene is represented by the following formula (X)
- 3-acyloxy-4-ol-1-butene is represented by the following formula.
- Formula (XI) and 4-acyloxy-3-ol-1-butene are represented by the following formula (XII).
- R 12 is an alkyl group, preferably a methyl group.
- R 13 is an alkyl group, preferably a methyl group.
- R 14 is an alkyl group, preferably a methyl group.
- the method for producing a modified EVOH containing a monomer unit represented by the formula (IV) as the monomer unit having a primary hydroxyl group shown on the right end of the formula (I) is not particularly limited.
- a method of reacting EVOH having an ethylene unit content of 24 to 55 mol % with a monovalent epoxy compound described later is not particularly limited.
- the reaction method is not particularly limited, but suitable methods include a production method in which EVOH and a monovalent epoxy compound are reacted in a solution, and a production method in which EVOH and a monovalent epoxy compound are reacted in an extruder.
- modified EVOH is obtained by reacting a monovalent epoxy compound with an EVOH solution in the presence of an acid or alkali catalyst.
- Modified EVOH can also be produced by dissolving EVOH and a monovalent epoxy compound in a reaction solvent and performing heat treatment.
- the reaction solvent polar aprotic solvents such as dimethylsulfoxide, dimethylformamide, dimethylacetamide and N-methylpyrrolidone, which are good solvents for EVOH, are preferred.
- Reaction catalysts include acid catalysts such as p-toluenesulfonic acid, methanesulfonic acid, trifluoromethanesulfonic acid, sulfuric acid and boron trifluoride, and alkali catalysts such as sodium hydroxide, potassium hydroxide, lithium hydroxide and sodium methoxide. is mentioned. Among these, it is preferable to use an acid catalyst.
- a suitable amount of the catalyst is about 0.0001 to 10 parts by mass with respect to 100 parts by mass of EVOH.
- a suitable reaction temperature is from room temperature to 150°C.
- the extruder to be used is not particularly limited, but single-screw extruders, twin-screw extruders, or multi-screw extruders with two or more screws can be mentioned. Also, it is preferable to react EVOH with the monovalent epoxy compound at a temperature of about 200°C to 300°C. When using a twin-screw extruder or a multi-screw extruder with two or more screws, it is easy to increase the pressure in the reaction section by changing the screw configuration, and the reaction between EVOH and the monovalent epoxy compound can be performed efficiently. .
- a single-screw extruder two or more extruders are connected, and a valve is arranged in the resin flow path between them to increase the pressure in the reaction section.
- two or more twin-screw extruders or multi-screw extruders having two or more screws may be connected to manufacture.
- a monovalent epoxy compound is an epoxy compound that has only one epoxy group in the molecule.
- the monovalent epoxy compound used in the present invention is not particularly limited, specifically, compounds represented by the following formulas (XIII) to (XV) are preferably used.
- R 15 , R 16 and R 17 represent a hydrogen atom, an alkyl group having 1 to 7 carbon atoms, or a cycloalkyl group having 3 to 7 carbon atoms.
- R 16 and R 17 each represent a hydrogen atom, an alkyl group having 1 to 6 carbon atoms, or a cycloalkyl group having 3 to 6 carbon atoms.
- i represents an integer of 1-7.
- the number of carbon atoms in the monovalent epoxy compound is particularly preferably 2 to 8.
- the monovalent epoxy compound is more preferably 1,2-epoxybutane, epoxypropane, epoxyethane and glycidol, and still more preferably epoxypropane and glycidol.
- a modified EVOH is obtained by reacting EVOH with a monovalent epoxy compound.
- the mixing ratio of the monovalent epoxy compound to 100 parts by mass of EVOH is preferably 1 to 50 parts by mass.
- the content of the EVOH in the pellets of the present invention is usually 50% by mass or more, preferably 60% by mass or more, more preferably 70% by mass or more, and still more preferably 80% by mass or more, Especially preferably 90% by mass or more, most preferably 95% by mass or more.
- the type of particles contained in the pellets of the present invention is not particularly limited, and may be inorganic compound particles or organic compound particles, but inorganic compound particles are preferred. As the particles, one type may be used alone, or two or more types may be used in combination.
- the inorganic compound particles are preferably inorganic oxide particles, more preferably silicon oxide particles or metal oxide particles.
- the metal constituting the metal oxide particles is preferably at least one selected from the group consisting of aluminum, magnesium, zirconium, cerium, tungsten, molybdenum, titanium and zinc.
- Specific examples of inorganic oxides constituting the inorganic oxide particles include silicon oxide, aluminum oxide, zirconium oxide, magnesium oxide, cerium oxide, tungsten oxide, molybdenum oxide, titanium oxide, zinc oxide, and composites thereof.
- silicon oxide is preferred.
- amorphous silica is particularly preferred.
- organic compound particles include, but are not limited to, fatty acid amides, fatty acid metal salts (such as calcium stearate), and low-molecular-weight polyolefins (such as low-molecular-weight polyethylene or low-molecular-weight polypropylene having a molecular weight of about 500 to 10,000).
- fatty acid amides such as calcium stearate
- low-molecular-weight polyolefins such as low-molecular-weight polyethylene or low-molecular-weight polypropylene having a molecular weight of about 500 to 10,000.
- fatty acid amides are more preferable.
- the fatty acid amide examples include saturated fatty acid amides (e.g., stearic acid amide, palmitic acid amide, lauric acid amide, etc.), unsaturated fatty acid amides (e.g., oleic acid amide, erucic acid amide, etc.), bis fatty acid amides (e.g., ethylenebisstearic acid amide, methylenebisstearic acid amide, etc.).
- the number of carbon atoms in the fatty acid amide and the fatty acid metal salt is preferably 6 or more, more preferably 10 or more.
- bis-fatty acid amides are preferred, and ethylene bis-stearic acid amide is more preferred.
- the average particle diameter R of the particles is 1 to 30 ⁇ m. If the average particle size R is less than 1 ⁇ m, blocking resistance will be insufficient.
- the average particle diameter R is preferably 2 ⁇ m or more, more preferably 3.5 ⁇ m or more. On the other hand, when the average particle size R exceeds 30 ⁇ m, the flexibility of the obtained molded article becomes insufficient.
- the average particle diameter R of the particles is a median diameter measured by a light scattering method while circulating a dispersion obtained after the particles are dispersed in water or an organic solvent and sufficiently stirred.
- the content A of the particles in the pellet of the present invention is 5-5000 ppm. When the content is less than 5 ppm, the pellets are blocked.
- the content A is preferably 50 ppm or more, more preferably 200 ppm or more, still more preferably 500 ppm or more, particularly preferably 800 ppm or more, and most preferably 1000 ppm or more.
- the content A of the pellets exceeds 5000 ppm, the flexibility of the obtained molded article becomes insufficient.
- the content A is preferably 4000 ppm or less, more preferably 3000 ppm or less, still more preferably 2700 ppm or less, and particularly preferably 1800 ppm or less.
- the pellets may contain additives other than the EVOH and the particles as long as they do not impair the effects of the present invention.
- additives include plasticizers, lubricants, stabilizers, surfactants, colorants, ultraviolet absorbers, antistatic agents, desiccants, cross-linking agents, and metal salts.
- the pellets of the present invention contain an alkali metal salt.
- the cationic species of the alkali metal salt is not particularly limited, sodium salts and/or potassium salts are preferred.
- the anion species of the alkali metal salt is also not particularly limited. They can be added as carboxylates, carbonates, hydrogen carbonates, phosphates, hydrogen phosphates, borates, hydroxides, and the like.
- the content of the alkali metal salt is preferably 10 to 500 ppm in terms of alkali metal element.
- the interlayer adhesion may become insufficient, and it is more preferably 50 ppm or more.
- the melt stability may be insufficient, and it is more preferably 300 ppm or less.
- the pellets of the present invention contain a phosphate compound.
- the phosphoric acid compound is not particularly limited, and various acids such as phosphoric acid and phosphorous acid, salts thereof, and the like can be used.
- the phosphate may be contained in any form of primary phosphate, secondary phosphate, and tertiary phosphate, but primary phosphate is preferred.
- the cationic species is not particularly limited, it is preferably an alkali metal salt. Among these, sodium dihydrogen phosphate and potassium dihydrogen phosphate are preferred.
- the content of the phosphate compound is preferably 5 to 200 ppm in terms of phosphate root.
- the content of the phosphoric acid compound is less than 5 ppm, the coloration resistance during melt molding may be insufficient.
- the content of the phosphoric acid compound exceeds 200 ppm, the melt stability may be insufficient, and it is more preferably 160 ppm or less.
- the pellet of the present invention may contain a boron compound.
- the boron compound is not particularly limited, and examples thereof include boric acids, borate esters, borates, and borohydrides.
- boric acids include orthoboric acid, metaboric acid, and tetraboric acid.
- boric acid esters include triethyl borate and trimethyl borate.
- orthoboric acid hereinafter sometimes simply referred to as boric acid
- the content of the boron compound is preferably 20 to 2000 ppm or less in terms of boron element.
- the content of the boron compound is less than 20 ppm, the suppression of torque fluctuation during heating and melting may be insufficient, and the content is more preferably 50 ppm or more.
- the content of the boron compound exceeds 2000 ppm, gelation tends to occur, and moldability may deteriorate.
- hydrotalcite compounds hindered phenol-based and hindered amine-based heat stabilizers, metal salts of higher aliphatic carboxylic acids (for example, calcium stearate, magnesium stearate, etc.) may be contained in the pellets in an amount of 0.001 to 1% by mass.
- specific examples of other additives include the following.
- Antioxidants 2,5-di-t-butyl-hydroquinone, 2,6-di-t-butyl-p-cresol, 4,4'-thiobis-(6-t-butylphenol), 2,2'- methylene-bis-(4-methyl-6-t-butylphenol), octadecyl-3-(3′,5′-di-t-butyl-4′-hydroxyphenyl)propionate, 4,4′-thiobis-(6 -t-butylphenol) and the like.
- UV absorber ethylene-2-cyano-3',3'-diphenyl acrylate, 2-(2'-hydroxy-5'-methylphenyl)benzotriazole, 2-(2'-hydroxy-3'-t-butyl -5′-methylphenyl)5-chlorobenzotriazole, 2-hydroxy-4-methoxybenzophenone, 2,2′-dihydroxy-4-methoxybenzophenone and the like.
- Plasticizers dimethyl phthalate, diethyl phthalate, dioctyl phthalate, wax, liquid paraffin, phosphate ester, etc.
- Antistatic agents pentaerythrityl monostearate, sorbitan monopalmitate, sulfated polyolefins, polyethylene oxide, carbowax, etc.
- Lubricants ethylene bisstearamide, butyl stearate, etc.
- Coloring agents carbon black, phthalocyanine, quinacridone, indoline, azo pigments, red iron oxide, etc.
- the method for producing the pellets of the present invention is not particularly limited, but includes a step of cutting the strand containing the EVOH, the particles and water to obtain cylindrical hydrous pellets, and drying the hydrous pellets to form the recesses.
- a manufacturing method having a step of forming is preferred. According to this method, as will be described later, predetermined protrusions can be formed on the pellet surface, and predetermined recesses can be formed on the side surface or cut surface of the pellet.
- the method of mixing the EVOH and the particles includes a method of mixing the EVOH dissolved in a good solvent such as a water/alcohol mixed solvent and the particles, and a method of mixing the EVOH and the particles in the good solvent, followed by mixing the EVOH and the particles.
- a method of dissolving EVOH and the like can be mentioned.
- other additives may be mixed as necessary.
- Methanol, ethanol, propanol and the like are used as the alcohol contained in the mixed solvent, and methanol is industrially preferred.
- the mass ratio (EVOH/good solvent) is usually 20/80 to 60/40.
- the mass ratio of water to alcohol in the mixed solvent is usually 10/90 to 60/40.
- the EVOH solution obtained in this way is extruded through a nozzle or the like into a poor solvent for precipitation to obtain strands containing the EVOH, the particles, water and, if necessary, other additives.
- protrusions are formed in a state where the particles are coated with EVOH. At this time, since the particles are coated with EVOH, the projections can be maintained without the particles slipping down.
- some projections are initially formed on the surface of the strands due to contraction of the strands when the EVOH solution is extruded into the poor solvent for precipitation. After that, when the hydrous pellets are dried, the pellets shrink further as the solvent volatilizes, so that the projections on the surface of the pellets become higher.
- the poor solvent examples include water or water/alcohol mixed solvents, aromatic hydrocarbons such as benzene, ketones such as acetone and methyl ethyl ketone, ethers such as dipropyl ether, methyl acetate, ethyl acetate, methyl propionate and the like.
- Organic acid esters and the like are used, but water or a water/alcohol mixed solvent is preferable in terms of ease of handling.
- Alcohols such as methanol, ethanol and propanol are used as the alcohol, and methanol is industrially preferred.
- the mass ratio (water/alcohol) when water/alcohol is mixed may be appropriately adjusted according to the composition of the EVOH solution, the bath temperature during pelletizing, which will be described later, and the like, but is usually 70/30 to 95/5. be.
- the mass ratio of the poor solvent to the strands (poor solvent/strand) is not particularly limited, but is preferably 50 to 10,000 from the viewpoint of easily obtaining hydrous pellets with a uniform size distribution.
- the temperature at which the EVOH solution containing the EVOH, the particles, etc. is brought into contact with the poor solvent is preferably ⁇ 10° C. or higher, more preferably 0° C. or higher.
- the temperature is preferably 40° C. or lower, more preferably 20° C. or lower, even more preferably 15° C. or lower, and even more preferably 10° C. or lower.
- the solution is extruded into the poor solvent in the form of a strand through a nozzle or the like.
- the shape of the outlet of such a nozzle is preferably circular.
- the inner diameter of the nozzle is preferably 1 to 10 mm. In this way, the solution is extruded in a strand from the nozzle.
- the number of strands does not necessarily have to be one, and any number between several to several hundred can be extruded.
- the extruded strands are then cut after the EVOH has sufficiently solidified to obtain cylindrical hydrous pellets.
- the length of the hydrous pellets at this time is usually 1 to 10 mm.
- Examples of the method for washing the water-containing pellets include a method of immersing the water-containing pellets in water or the like.
- the water may contain acetic acid, in which case the content of acetic acid is usually 0.1-5 g/l.
- the water content of the water-containing pellets after washing is usually 30 to 60% by mass.
- additives may be added to the water-containing pellets after washing.
- Examples of the method at this time include a method of immersing the water-containing pellets in an aqueous solution in which an additive is dissolved.
- Suitable methods for drying the water-containing pellets include a stationary drying method and a fluidized drying method, and it is also possible to adopt a multi-stage drying process that combines several drying methods.
- the drying temperature is 50-120° C. and the drying time is 0.5-30 hours. At this time, the drying temperature may be raised stepwise.
- the moisture content of the water-containing pellets before drying is usually 30 to 60% by mass, and the moisture content of the pellets after drying is usually 0 to 9% by mass.
- At least one of the side surface and the cut surface of the pellet of the present invention obtained in this way must be formed with a predetermined concave portion, which will be described later.
- These recesses can be formed by drying cylindrical wet pellets. By forming recesses in the pellets, the contact area between the pellets is reduced, thereby improving the blocking resistance, stabilizing the discharge amount during melt extrusion, and improving the extrusion stability.
- the recess may be formed only on one of the side surface and the cut surface of the pellet, or may be formed on both. Among them, it is preferable that the recess is formed at least on the side surface of the pellet.
- FIG. 1 is an appearance photograph of the pellet 1 side surface 2 obtained in Example 1, which will be described later.
- FIG. 2 is an electron micrograph of a cross section 4 obtained by cutting the pellet 1 perpendicularly to the flow direction 3 (extrusion direction when forming strands).
- the recess 5 formed in the side surface 2 of the pellet 1 of the present invention will be described using these figures.
- Four recesses 5 are formed in the side 2 of the pellet 1 shown in FIGS.
- the recesses 5 formed in the side surface 2 are generally arranged in a line circumferentially of the cylindrical pellet 1 .
- the number n of the recesses 5 should be 2-5.
- the number n of the concave portions 5 is preferably 3 or more. On the other hand, the number of concave portions 5 is preferably four or less.
- FIG. 1 two cross-sections perpendicular to the flow direction 3 of the pellets 1 at a distance of L/4 (mm) from the center of gravity 6 of the pellets 1 are indicated by broken lines.
- the distances ⁇ 1 to ⁇ n and the distances ⁇ 1 to ⁇ n obtained by measuring at least one cross section 4 at positions between them must satisfy the above formula (1).
- the cross section 4 shown in FIG. 2 is obtained by cutting perpendicularly to the flow direction 3 of the pellet 1 at a position L/4 (mm) or less from the center of gravity 6 of the pellet 1 .
- the distances ⁇ 1 to ⁇ n from the center of gravity 7 of the cross section 4 to the edge 8 of the concave portion 5 are defined by the center of gravity 7 at each edge 8 from the center of gravity 7 of the cross section 4 as shown by the solid line in FIG. means the distance to the furthest point from Further, the distances ⁇ 1 to ⁇ n from the center of gravity 7 of the cross section 4 to the bottom 9 of the recess 5 are the distances from the center of gravity 7 of the cross section 4 to the center of gravity 7 of each bottom 9, as shown by the broken lines in FIG. Means the distance to the nearest point.
- the left side of equation (1) is the distance ⁇ 1 to ⁇ n from the center of gravity 7 to the bottom 9 of the recess 5 ( dashed line).
- the ratio is 1, and when the recess 5 is formed by deformation, the ratio decreases.
- a cylindrical water-containing pellet is dried, it shrinks uniformly, so that the cross section of the dried pellet perpendicular to the flow direction becomes circular.
- (1) changing the ethylene unit content a (2) changing the melting enthalpy ⁇ Hm, and (3) using the modified EVOH represented by the above formula (I) as the EVOH.
- the left side of the above formula (1) is preferably 0.7 or less (that is, satisfying the following formula (1')), more preferably 0.65 or less, further preferably 0.55 or less, and 0.52 or less. Especially preferred.
- the left side of the above formula (1) is preferably 0.2 or more (that is, satisfying the following formula (1'')), more preferably 0.3 or more, further preferably 0.35 or more, and 0 .4 or more is particularly preferred. ( ⁇ 1+ ⁇ 2...+ ⁇ n)/( ⁇ 1+ ⁇ 2...+ ⁇ n) ⁇ 0.7 (1') 0.2 ⁇ ( ⁇ 1+ ⁇ 2...+ ⁇ n)/( ⁇ 1+ ⁇ 2...+ ⁇ n) (1'')
- the ratio (Di/L) of the diameter Di to the length L (mm) of the pellet 1 is preferably 1 or less.
- the ratio (Di/L) is more preferably 0.9 or less, even more preferably 0.8 or less.
- the ratio (Di/L) is preferably 0.2 or more, more preferably 0.3 or more, and even more preferably 0.5 or more.
- FIG. 3 is an example of an appearance photograph of the side surface 2 of the pellet 1 of the present invention in which the recess 11 is formed in the cut surface 10. As shown in FIG. Two dashed lines indicate the shape of each concave portion 11 formed on both cut surfaces 10 viewed from the side surface 2 of the cylindrical pellet 1 .
- the depth D (mm) of the recess 11 means the distance in the flow direction 3 between the two most distant points in the flow direction 3 of the recess 11 formed in the cut surface 10 .
- the ratio D/L is usually 0.4 or less.
- the ratio (Di/L) of the diameter Di to the length L (mm) of the pellet 1 preferably exceeds 1.
- the ratio (Di/L) is preferably 3 or less, more preferably 2 or less, and even more preferably 1.75 or less.
- projections containing the particles and coated with the EVOH must be formed on the surface of the pellet. Blocking resistance is improved by forming such protrusions. It is considered that such an effect is produced by coating the surface of the particles with the EVOH. Such coatings can be formed by the methods described above. It is believed that the projections are formed by pushing up the EVOH pellet surface layer by the added particles. Therefore, the height H ( ⁇ m) and the number per unit area of the projections can be adjusted by the amount of the particles added and their average particle diameter R ( ⁇ m).
- the number of protrusions formed on the surface of the pellet of the present invention is preferably 1 to 100000/mm 2 . When the number of protrusions is within this range, the contact area between the pellets 1 is further reduced, thereby further improving blocking resistance and extrusion stability.
- the height H of the protrusion is 0.1 to 15 ⁇ m. If the height H is less than 0.1 ⁇ m, blocking resistance will be insufficient.
- the height H is preferably 0.2 ⁇ m or more, more preferably 0.3 ⁇ m or more, still more preferably 0.4 ⁇ m or more, and particularly preferably 0.5 ⁇ m or more. On the other hand, if the height H exceeds 15 ⁇ m, the flexibility of the resulting molded product will be insufficient.
- the height H is preferably 10 ⁇ m or less, more preferably 7.5 ⁇ m or less, even more preferably 5 ⁇ m or less, even more preferably 3 ⁇ m or less, particularly preferably 2.5 ⁇ m or less, most preferably 2 ⁇ m or less.
- the height of the protrusions is calculated by the method described in Examples.
- the average particle diameter R ( ⁇ m) of the particles and the height H ( ⁇ m) of the protrusions satisfy the following formula (7). If H/R is less than 0.1, blocking resistance may be insufficient. H/R is more preferably 0.11 or more, still more preferably 0.12 or more. On the other hand, when H/R exceeds 0.9, the resulting molded article may have insufficient flexibility. H/R is more preferably 0.85 or less, still more preferably 0.8 or less. 0.1 ⁇ H/R ⁇ 0.9 (7)
- the melting enthalpy ⁇ Hm of the pellets is preferably 10 to 100 J/g. If the melting enthalpy ⁇ Hm is less than 10 J/g, blocking resistance may be insufficient.
- the melting enthalpy ⁇ Hm is more preferably 20 J/g or more. On the other hand, if the melting enthalpy ⁇ Hm exceeds 100 J/g, the drawability may be insufficient.
- the melting enthalpy ⁇ Hm is 100 J/g or less, the crystallinity of the EVOH is lowered. The decrease in crystallinity makes it easier for the water-containing pellets to shrink unevenly, so that predetermined recesses are likely to be formed on the side surfaces of the pellets.
- the melting enthalpy ⁇ Hm is more preferably 90 J/g or less, still more preferably 80 J/g or less, still more preferably 65 J/g or less, and particularly preferably 64 J/g or less.
- the melting enthalpy ⁇ Hm of the pellet is calculated by the method described in Examples.
- the melting enthalpy ⁇ Hm (J/g) of the pellets and the content A (ppm) of the particles satisfy the following formula (6). If “ ⁇ Hm/100+A/500" is less than 1, blocking resistance may be insufficient. “ ⁇ Hm/100+A/500” is more preferably 2 or more, and still more preferably 2.5 or more. On the other hand, when ⁇ Hm/100+A/500 is greater than 10, stretchability may be insufficient. ⁇ Hm/100+A/500 is more preferably 9 or less, still more preferably 8 or less. 1 ⁇ Hm/100+A/500 ⁇ 10 (6)
- the melting point of the pellets is not particularly limited, it is usually 110-200°C. If the melting point is lower than 110°C, blocking resistance may be insufficient.
- the melting point is preferably 120° C. or higher, more preferably 130° C. or higher, still more preferably 140° C. or higher, and particularly preferably 145° C. or higher. On the other hand, when the melting point exceeds 200° C., the thermal stability during molding is deteriorated.
- the melting point is preferably 190° C. or lower, more preferably 185° C. or lower, still more preferably 180° C. or lower, and particularly preferably 175° C. or lower.
- the pellets may be used alone, or may be used as mixed pellets together with other resin pellets.
- other resin pellets include EVOH pellets other than the pellets of the present invention, pellets of various thermoplastic resins, and the like.
- the content of the pellets of the present invention in the mixed pellets is not particularly limited, but is usually 50% by mass or more, preferably 70% by mass or more, more preferably 80% by mass or more, and further preferably 90% by mass or more.
- the pellets of the present invention have excellent blocking resistance and can be molded into products with excellent flexibility.
- the pellets also have excellent extrusion stability. Furthermore, since the pellets have a high dissolution rate in a solvent, the coating solution preparation process time can be shortened, and the coating film production rate can be increased. Therefore, the pellets can be used as food packaging containers, pharmaceutical packaging containers, industrial chemical packaging containers, and agricultural chemical packaging containers by taking advantage of the gas barrier properties, transparency, aroma retention, solvent resistance, oil resistance, etc. inherent in the EVOH. It is used in a wide range of applications, including various packaging containers such as fuel containers, transport pipes, and resin wallpaper.
- a pellet containing modified EVOH and particles and cut into a cylindrical shape wherein the pellet contains 5 to 5000 ppm of particles having an average particle diameter R of 1 to 30 ⁇ m, and the modified EVOH is represented by the following formula (I ), the content ratio (mol%) of a, b and c with respect to the total monomer units satisfies the following formulas (2) to (4), and the degree of saponification defined by the following formula (8) (DS) is 90 mol% or more,
- W represents a hydrogen atom, a methyl group or a group represented by R 2 -OY
- X, Y and Z each independently represent a hydrogen atom, a formyl group or a represents an alkanoyl group.
- R 1 and R 2 each independently represent a single bond, an alkylene group having 1 to 9 carbon atoms, or an alkyleneoxy group having 1 to 9 carbon atoms, and the alkylene group and the alkyleneoxy group are a hydroxyl group, an alkoxy group, or a halogen atom.
- L the length of the pellet
- a recess is formed in the side surface or cut surface of the pellet, and the recess is formed in the side surface, the number n of the recesses is 2 to 5, and the pellet In at least one cross section perpendicular to the flow direction of the pellet at a position L / 4 (mm) or less from the center of gravity of the distance ⁇ 1 to ⁇ n from the center of gravity of the cross section to the edge of the recess formed on the side surface and the distance ⁇ 1 to ⁇ n from the center of gravity of the cross section to the bottom of the recess formed on the side surface satisfies the following
- the ethylene-vinyl acetate copolymer may be referred to as EVAc.
- Synthesis example 1 (1) Synthesis of EVAc Into a 250 L pressurized reactor equipped with a jacket, a stirrer, a nitrogen inlet, an ethylene inlet, and an initiator addition port, 90 kg of vinyl acetate (in formula (V), R 9 is a methyl group; hereinafter referred to as VAc), 9 kg of methanol (hereinafter sometimes referred to as MeOH), 2-methylene-1,3-propanediol diacetate (in formula (VI), R 3 and R 4 are hydrogen atoms, R 10 and R 11 are methyl 1.9 kg of a group: hereinafter referred to as MPDAc) was charged, the temperature was raised to 60° C., and nitrogen was bubbled for 30 minutes to replace the inside of the reaction vessel with nitrogen.
- V vinyl acetate
- R 9 is a methyl group; hereinafter referred to as VAc
- MeOH 9 kg of methanol
- ethylene pressure was 5.8 MPa.
- 72 g of 2,2′-azobis(2,4-dimethylvaleronitrile) (manufactured by Wako Pure Chemical Industries, Ltd. “V-65”) was added as a methanol solution as an initiator. to initiate polymerization.
- the ethylene pressure was maintained at 5.8 MPa and the polymerization temperature at 60° C. during the polymerization. After 6 hours, when the conversion of VAc reached 40%, the mixture was cooled to stop the polymerization. After the reactor was opened to deethyleneize, nitrogen gas was bubbled through to completely deethylenize.
- modified EVAc ethylene-vinyl acetate copolymer
- MPDAc structural unit derived from MPDAc
- modified EVOH ion-exchanged water was added to distill MeOH out of the reaction vessel to precipitate modified EVOH.
- the precipitated modified EVOH was collected and pulverized with a mixer.
- the obtained modified EVOH powder was put into a 1 g/L aqueous solution of acetic acid (bath ratio: 20: ratio of 20 L of aqueous solution to 1 kg of powder) and washed with stirring for 2 hours. This was deliquored, further put into a 1 g/L acetic acid aqueous solution (bath ratio: 20), and washed with stirring for 2 hours.
- the deliquored product was put into ion-exchanged water (bath ratio: 20), stirred and washed for 2 hours, and the deliquoring operation was repeated three times for purification. Next, it was immersed in 10 L of an aqueous solution containing 0.5 g/L of acetic acid and 0.1 g/L of sodium acetate with stirring for 4 hours, deliquored, and dried at 60° C. for 16 hours to obtain a roughly dried modified EVOH. got
- modified EVAc was precipitated in ion-exchanged water. The precipitate was collected and dried under vacuum at 60° C. to obtain a dry product of modified EVAc.
- the resulting dry product of modified EVAc was dissolved in dimethyl sulfoxide (DMSO)-d6 containing tetramethylsilane as an internal standard substance, and 1 H-NMR at 500 MHz (manufactured by JEOL Ltd.: “GX-500” ) at 80°C.
- DMSO dimethyl sulfoxide
- x is the integrated value of 0.6 to 1.0 ppm
- y is the integrated value of 1.0 to 1.85 ppm
- z is the integrated value of 3.7 to 4.1 ppm
- 4.4 to 5 When the integrated value of 3 ppm is w, the content of ethylene units (a: mol%), the content of vinyl ester units (b: mol%), and the content of structural units derived from MPDAc (c: mol%) are , are calculated according to the following equations.
- the ethylene unit content (a) of the modified EVAc in Example 1 was 44.0 mol%
- the vinyl ester unit content (b) was 54.5 mol%
- the structural unit derived from MPDAc content (c) was 1.5 mol %.
- the values of a, b and c in modified EVAc are the same as the values of a, b and c in modified EVOH after saponification treatment.
- Synthesis Examples 2-10 EVAc and EVOH were prepared and analyzed in the same manner as in Synthesis Example 1, except that the polymerization conditions in Synthesis Example 1 were changed as shown in Table 1. Table 1 shows the results.
- Silysia 310P manufactured by Fuji Silysia Chemical Co., Ltd.
- Water-containing pellets of modified EVOH were obtained by cutting into cylindrical pellets having a height of 4 mm and a diameter of 3 mm.
- the moisture content of the resulting hydrous pellets of modified EVOH was measured with a halogen moisture meter "HR73" manufactured by Mettler Co., Ltd., and found to be 60% by mass.
- Moist pellets of modified EVOH were obtained from which residues were removed.
- the moisture content of the resulting hydrous pellets of modified EVOH was measured with a halogen moisture meter "HR73" manufactured by Mettler Co., Ltd., and found to be 55% by mass.
- This solution was analyzed for contained metals by an ICP emission spectrometer (“Avio500” manufactured by PerkinElmer) to determine the contents of elemental sodium and elemental phosphorus.
- the sodium salt content was 150 ppm in terms of sodium element, and the phosphate compound content was 40 ppm in terms of phosphate root.
- FIG. 1 is a photograph of the appearance of the sides of the pellets obtained in (3) above.
- the diameter Di (mm) and the length L (mm) in the flow direction of the pellets were obtained by measuring with vernier calipers.
- FIG. 2 is an electron microscope image of a cross section 4 obtained by cutting perpendicularly to the flow direction 3 of the pellet 1 at a position L/4 (mm) or less from the center of gravity 6 of the pellet 1 .
- Four recesses 5 were formed on the side surface of the pellet.
- FIG. 4 is an electron microscope image of the pellet surface obtained in (3) above. As shown in FIG. 4, protrusions were formed on the surface of pellet 1 . The height H ( ⁇ m) and the number of protrusions (pieces/mm 2 ) were determined from the images (two images on the right side of FIG. 4) observed from the direction parallel to the pellet surface. Table 3 shows the results. Images observed from the perpendicular direction to the surface of the pellet 1 (two on the left side of FIG. 4) and a scanning electron microscope "S-3000N" with an EDX (energy dispersive X-ray spectrometer) manufactured by Hitachi, Ltd. Since the carbon element component and the oxygen element component were detected in the analysis, it was confirmed that the surface of the protrusions was modified EVOH.
- EDX energy dispersive X-ray spectrometer
- the temperature conditions of the extruder were set as follows according to the melting point of the modified EVOH.
- Supply part 150°C (120°C in Example 11 and Comparative Example 7)
- Compressed part Melting point of modified EVOH +20°C
- Weighing part Melting point of modified EVOH +20°C
- Die temperature Melting point of modified EVOH +20°C
- the heat-degraded resin adhering to the lip part tends to cause defects such as gels and lumps in the resulting film, and the small amount of accumulated resin means that it is possible to stably melt and mold over a long period of time. means. Table 3 shows the results.
- Examples 2-13, 16, Comparative Examples 1-2, 4, 7, 8 Pellets were produced and evaluated in the same manner as in Example 1, except that the type of EVOH and the type and content of particles were changed. Results are shown in Tables 2 and 3. In all pellets, the elemental sodium content was 150 ppm, the phosphate compound content was 40 ppm in terms of phosphate root, and the acetic acid content was 100 ppm.
- Example 14 Pellets were produced and evaluated in the same manner as in Example 2, except that the water and methanol charged during the production of hydrous pellets were changed to 37 parts by mass and 149 parts by mass, respectively.
- the sodium element content was 150 ppm
- the phosphate compound content was 40 ppm in terms of phosphate root
- the acetic acid content was 100 ppm.
- the obtained pellets had recesses formed on both cut surfaces, and their D/L was 0.22. Results are shown in Tables 2 and 3.
- Example 15 The solution into which 1 part by mass of the water-containing pellets is added during pellet production is an aqueous solution with a sodium acetate concentration of 0.5 g/L, an acetic acid concentration of 0.4 g/L, a phosphoric acid concentration of 0.05 g/L, and a boric acid concentration of 0.2 g/L.
- Pellets were produced and evaluated in the same manner as in Example 2, except that the content was changed to 18.5 parts by mass (bath ratio: 20). Results are shown in Tables 2 and 3.
- the obtained pellets had an elemental sodium content of 150 ppm, a phosphate compound content of 40 ppm in terms of phosphate radical, an acetic acid content of 100 ppm, and a boric acid content of 1000 ppm.
- the melt flow rate (MFR) of the obtained modified EVOH (190° C., under 2160 g load) was 3.7 g/10 minutes.
- Example 17 Pellets were produced and evaluated in the same manner as in Example 2, except that the roughly dried EVOH obtained in Synthesis Example 9 was used. Results are shown in Tables 2 and 3. The obtained pellets had a sodium element content of 150 ppm, a phosphate compound content of 40 ppm in terms of phosphate radical, and an acetic acid content of 100 ppm.
- Example 18 100 parts by mass of the crude dried EVOH obtained in Synthesis Example 10, 0.12 parts by mass of Silysia 350 (manufactured by Fuji Silysia Chemical Co., Ltd.), 70 parts by mass of water, and 163 parts by mass of MeOH were charged to produce hydrous pellets. Pellets were produced and evaluated in the same manner as in Example 2. The obtained pellets had a sodium element content of 150 ppm, a phosphate compound content of 40 ppm in terms of phosphate radical, and an acetic acid content of 100 ppm. Results are shown in Tables 2 and 3.
- Comparative example 3 Pellets were obtained by carrying out the above (1) to (3) in the same manner as in Example 2, except that no particles were added. Also, based on (4) to (7), the melting point, sodium element content, phosphate compound content, and acetic acid content were measured. The melting point was 152° C., the sodium element content was 150 ppm, the phosphate compound content was 40 ppm in terms of phosphate radical, the acetic acid content was 100 ppm, and the melting enthalpy ⁇ Hm was 55 (J/g). rice field. When the cut surface of the pellet obtained as described in (8) was observed with an electron microscope, four concave portions 5 were formed on the side surface of the pellet.
- Electron microscope observation of the cut surface of the pellet after kneading with the twin-screw extruder revealed that no depressions were formed. Further, when the surface of the pellet was observed with an electron microscope, no projections were formed on the surface of the pellet.
- Comparative Examples 5 and 6 Pellets were produced and evaluated in the same manner as in Example 1, except that in the production of hydrous pellets, the particles to be added were changed to molecular sieve 4A (manufactured by Union Showa Co., Ltd.). Molecular sieve 4A was pulverized in a mixer to have the average particle size shown in Tables 2 and 3. Table 2 shows the results.
Landscapes
- Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Medicinal Chemistry (AREA)
- Polymers & Plastics (AREA)
- Organic Chemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Addition Polymer Or Copolymer, Post-Treatments, Or Chemical Modifications (AREA)
Abstract
Description
(β1+β2・・・+βn)/(α1+α2・・・+αn)≦0.8 (1)
前記切断面に凹部が形成される場合、前記ペレットの長さL(mm)に対する、切断面に形成される凹部の深さD(mm)の比D/Lが0.1以上であり、前記ペレットの表面に高さHが0.1~15μmの突起が形成され、該突起が、前記粒子を含むとともに、該粒子が前記EVOHで被覆されてなる、ペレットを提供することによって解決される。
24≦a≦55 (2)
0.01≦c≦10 (3)
[100-(a+c)]×0.9≦b≦[100-(a+c)] (4)
29≦1.2a+8c≦100 (5)
1≦ΔHm/100+A/500≦10 (6)
0.1≦H/R≦0.9 (7)
24≦a≦55 (2)
0.01≦c≦10 (3)
[100-(a+c)]×0.9≦b≦[100-(a+c)] (4)
DS=[(X、Y及びZのうち水素原子であるものの合計モル数)/(X、Y及びZの合計モル数)]×100 (8)
前記ペレットの長さがL(mm)であり、前記ペレットの側面又は切断面に凹部が形成され、前記側面に凹部が形成される場合、該凹部の数nが2~5であり、前記ペレットの重心からL/4(mm)以下の位置における、前記ペレットの流れ方向に対して垂直な少なくとも1つの断面において、該断面の重心から、側面に形成される凹部の縁までの距離α1~αnと、該断面の重心から、側面に形成される凹部の底までの距離β1~βnが下記式(1)を満たし、
(β1+β2・・・+βn)/(α1+α2・・・+αn)≦0.8 (1)
前記切断面に凹部が形成される場合、前記ペレットの長さL(mm)に対する、切断面に形成される凹部の深さD(mm)の比D/Lが0.1以上であり、前記ペレットの表面に高さHが0.1~15μmの突起が形成され、該突起が、前記粒子を含むとともに、該粒子が前記変性EVOHで被覆されてなるペレットを提供することによっても解決される。
(β1+β2・・・+βn)/(α1+α2・・・+αn)≦0.8 (1)
前記切断面に凹部が形成される場合、前記ペレットの長さL(mm)に対する、切断面に形成される凹部の深さD(mm)の比D/Lが0.1以上であり、前記ペレットの表面に高さHが0.1~15μmの突起が形成され、該突起が、前記粒子を含むとともに、該粒子が前記EVOHで被覆されてなるものである。
24≦a≦55 (2)
0.01≦c≦10 (3)
[100-(a+c)]×0.9≦b≦[100-(a+c)] (4)
[100-(a+c)]×0.95≦b≦[100-(a+c)](4’)
[100-(a+c)]×0.98≦b≦[100-(a+c)](4”)
DS=[(X、Y及びZのうち水素原子であるものの合計モル数)/(X、Y及びZの合計モル数)]×100 (8)
ここで、「X、Y及びZのうち水素原子であるものの合計モル数」は、水酸基のモル数を示し、「X、Y及びZの合計モル数」は、水酸基とエステル基の合計モル数を示す。
29≦1.2a+8c≦100 (5)
(β1+β2・・・+βn)/(α1+α2・・・+αn)≦0.8 (1)
(β1+β2・・・+βn)/(α1+α2・・・+αn)≦0.7 (1’)
0.2≦(β1+β2・・・+βn)/(α1+α2・・・+αn) (1’’)
0.1≦H/R≦0.9 (7)
1≦ΔHm/100+A/500≦10 (6)
24≦a≦55 (2)
0.01≦c≦10 (3)
[100-(a+c)]×0.9≦b≦[100-(a+c)] (4)
DS=[(X、Y及びZのうち水素原子であるものの合計モル数)/(X、Y及びZの合計モル数)]×100 (4)
前記ペレットの長さがL(mm)であり、前記ペレットの側面又は切断面に凹部が形成され、前記側面に凹部が形成される場合、該凹部の数nが2~5であり、前記ペレットの重心からL/4(mm)以下の位置における、前記ペレットの流れ方向に対して垂直な少なくとも1つの断面において、該断面の重心から、側面に形成される凹部の縁までの距離α1~αnと、該断面の重心から、側面に形成される凹部の底までの距離β1~βnが下記式(5)を満たし、
(β1+β2・・・+βn)/(α1+α2・・・+αn)≦0.8 (8)
前記切断面に凹部が形成される場合、前記ペレットの長さL(mm)に対する、切断面に形成される凹部の深さD(mm)の比D/Lが0.1以上であり、前記ペレットの表面に高さHが0.1~15μmの突起が形成され、該突起が、前記粒子を含むとともに、該粒子が前記変性EVOHで被覆されてなるペレットも好適に用いられる。当該ペレットは、EVOHとして、上記式(I)で表されるものが用いられること及び融解エンタルピーΔHmが限定されないこと以外は初めに説明したペレットと同じであり、同等の性能を有する。
(1)EVAcの合成
ジャケット、攪拌機、窒素導入口、エチレン導入口及び開始剤添加口を備えた250L加圧反応槽に、酢酸ビニル(式(V)において、R9がメチル基:以下、VAcと称する)を90kg、メタノール(以下、MeOHと称することがある)を9kg、2-メチレン-1,3-プロパンジオールジアセテート(式(VI)において、R3及びR4が水素原子で、R10及びR11がメチル基:以下、MPDAcと称する)を1.9kg仕込み、60℃に昇温した後、30分間窒素バブリングして反応槽内を窒素置換した。次いで反応槽圧力(エチレン圧力)が5.8MPaとなるようにエチレンを導入した。反応槽内の温度を60℃に調整した後、開始剤として72gの2,2’-アゾビス(2,4-ジメチルバレロニトリル)(和光純薬工業株式会社製「V-65」)をメタノール溶液として添加し、重合を開始した。重合中はエチレン圧力を5.8MPaに、重合温度を60℃に維持した。6時間後にVAcの重合率が40%となったところで冷却して重合を停止した。反応槽を開放して脱エチレンした後、窒素ガスをバブリングして脱エチレンを完全に行った。次いで減圧下で未反応のVAcを除去した後、MPDAc由来の構造単位が共重合により導入された変性エチレン-酢酸ビニル共重合体(以下、変性EVAcと称することがある)にMeOHを添加して20質量%MeOH溶液とした。
ジャケット、攪拌機、窒素導入口、還流冷却器及び溶液添加口を備えた500L反応槽に(1)で得た変性EVAcの20質量%MeOH溶液を仕込んだ。この溶液に窒素を吹き込みながら60℃に昇温し、変性EVAc中の酢酸ビニルユニットに対し0.5等量の水酸化ナトリウムを2規定のMeOH溶液として添加した。水酸化ナトリウムMeOH溶液の添加終了後、系内温度を60℃に保ち、酢酸メチルとMeOHを留去させながら2時間攪拌してケン化反応を進行させた。その後酢酸を添加してケン化反応を停止した。その後、60~80℃で加熱攪拌しながら、イオン交換水を添加し、反応槽外にMeOHを留出させ、変性EVOHを析出させた。析出した変性EVOHを収集し、ミキサーで粉砕した。得られた変性EVOH粉末を1g/Lの酢酸水溶液(浴比20:粉末1kgに対して水溶液20Lの割合)に投入して2時間攪拌洗浄した。これを脱液し、さらに1g/Lの酢酸水溶液(浴比20)に投入して2時間攪拌洗浄した。これを脱液したものを、イオン交換水(浴比20)に投入して攪拌洗浄を2時間行い脱液する操作を3回繰り返して精製を行った。次いで、酢酸0.5g/L及び酢酸ナトリウム0.1g/Lを含有する水溶液10Lに4時間攪拌浸漬してから脱液し、これを60℃で16時間乾燥させることで変性EVOHの粗乾燥物を得た。
変性EVAc中の、エチレン単位含有率(式(VII)におけるaモル%)、酢酸ビニル由来の構造単位の含有量(式(VII)におけるbモル%)及びMPDAc由来の構造単位の含有量(式(VII)におけるcモル%)は、ケン化前の変性EVAcを1H-NMR測定して算出した。
・0.6~1.0ppm:末端部位エチレン単位のメチレンプロトン(4H)
・1.0~1.85ppm:中間部位エチレン単位のメチレンプロトン(4H)、MPDAc由来の構造単位の主鎖部位メチレンプロトン(2H)、酢酸ビニル単位のメチレンプロトン(2H)
・1.85~2.1ppm:MPDAc由来の構造単位のメチルプロトン(6H)と酢酸ビニル単位のメチルプロトン(3H)
・3.7~4.1ppm:MPDAc由来の構造単位の側鎖部位メチレンプロトン(4H)
・4.4~5.3ppm:酢酸ビニル単位のメチンプロトン(1H)
a=(2x+2y-z-4w)/(2x+2y+z+4w)×100
b=8w/(2x+2y+z+4w)×100
c=2z/(2x+2y+z+4w)×100
ケン化後の変性EVOHについても同様に1H-NMR測定を行った。上記(2)で得られた変性EVOHの粗乾燥物を、内部標準物質としてテトラメチルシラン、添加剤としてテトラフルオロ酢酸(TFA)を含むジメチルスルホキシド(DMSO)-d6に溶解し、500MHzの1H-NMR(日本電子株式会社製:「GX-500」)を用いて80℃で測定した。1H-NMR測定の結果、1.85~2.1ppmのピーク強度が大幅に減少していることから、変性EVOH中の酢酸ビニル由来のエステル基に加え、MPDAc由来の構造単位に含まれるエステル基もケン化されて水酸基になっていることが明らかである。実施例1で得られた1H-NMRスペクトルからもこのような1.85~2.1ppmのピーク強度の減少が見られた。ケン化度は酢酸ビニル単位等のメチルプロトン(1.85~2.1ppm)と、ビニルアルコール単位等のメチンプロトン(3.15~4.15ppm)のピーク強度比より式(8)を用いて算出した。実施例1の変性EVOHのケン化度は99.9モル%以上であった。
合成例1における重合条件を表1に示すとおりに変更した以外は合成例1と同様にして、EVAc及びEVOHの作製及び分析を行った。結果を表1に示す。
(1)含水ペレットの製造
ジャケット、攪拌機及び還流冷却器を備えた80L攪拌槽に、合成例1で得た変性EVOHの粗乾燥物100質量部、サイリシア310P(富士シリシア化学株式会社製)0.12質量部、水56質量部、MeOH130質量部を仕込み、80℃に昇温して溶解させた。この溶解液を開口部が内径4mmの円状のノズルを通して5℃に冷却した水/MeOH=90/10の混合液中に押し出してストランド状に析出させ、このストランドをストランドカッターで押し出し方向の長さ4mm、直径3mmの円柱状のペレットにカットすることで変性EVOHの含水ペレットを得た。得られた変性EVOHの含水ペレットの含水率をメトラー社製ハロゲン水分計「HR73」で測定したところ、60質量%であった。
上記(1)で得た変性EVOHの含水ペレットを1g/Lの酢酸水溶液(浴比20)に投入して2時間攪拌洗浄した。これを脱液し、さらに1g/Lの酢酸水溶液(浴比20)に投入して2時間攪拌洗浄した。脱液後、酢酸水溶液を更新し同様の操作を行った。酢酸水溶液で洗浄してから脱液したものを、イオン交換水(浴比20)に投入して攪拌洗浄を2時間行い脱液する操作を3回繰り返して精製を行い、ケン化反応時の触媒残渣が除去された、変性EVOHの含水ペレットを得た。得られた変性EVOHの含水ペレットの含水率をメトラー社製ハロゲン水分計「HR73」で測定したところ、55質量%であった。
(2)で得られた含水率55質量%の含水ペレット1質量部を酢酸ナトリウム濃度0.5g/L、酢酸濃度0.4g/L、リン酸濃度0.05g/Lの水溶液18.5質量部(浴比20)に投入し、定期的に攪拌しながら4時間浸漬させた。これを遠心脱水して表面の水分を除去した後、含水状態のペレットをペレット同士が重ならないようにテフロンシート上に並べ、60℃で3時間、80℃で3時間、及び110℃で20時間乾燥させることによって、変性EVOHを含むペレットを得た。得られたペレットの含水率をメトラー社製ハロゲン水分計「HR73」で測定したところ、0.2質量%であった。また、得られたペレット(変性EVOH)のメルトフローレート(MFR)(190℃、2160g荷重下)は6.0g/10分であった。
上記(3)で得られたペレットについて、JIS K 7121に準じて、30℃から200℃まで10℃/分の速度にて昇温した後10℃/分で0℃まで急冷して再度0℃から200℃まで10℃/分の昇温速度にて測定を実施した(TA Instruments社製示差走査熱量計(DSC)「Q2000」)。温度の校正にはインジウムを用いた。2ndランのチャートから前記JISにしたがって融解ピーク温度(Tpm)を求め、これを変性EVOHを含むペレットの融点とした。融点は152℃であった。
上記(3)で得られたペレット0.5gをテフロン(登録商標)製圧力容器に入れ、ここに濃硝酸5mLを加えて室温で30分間分解させた。30分後蓋をし、湿式分解装置(株式会社アクタック製:「speedwave4」)により150℃で10分間、次いで180℃で5分間加熱することで分解を行い、その後室温まで冷却した。この処理液を50mLのメスフラスコ(TPX製)に移し純水でメスアップした。この溶液について、ICP発光分光分析装置(パーキンエルマー社製「Avio500」)により含有金属の分析を行い、ナトリウム元素及びリン元素の含有量を求めた。ナトリウム塩含有量は、ナトリウム元素換算値で150ppmであり、リン酸化合物含有量は、リン酸根換算値で40ppmであった。
上記(3)で得られたペレット20gをイオン交換水100mlに投入し、95℃で6時間加熱抽出した。フェノールフタレインを指示薬として、1/50規定のNaOHで抽出液を中和滴定し、酢酸含有量を定量したところ、100ppmであった。なお、酢酸含有量の算出については、リン酸の含有量を考慮して行った。
上記(3)で得られたペレットから切り取った3mgのサンプルをアルミニウム製パン(TA Instrument社製)に封入し、30℃から200℃まで10℃/分の速度にて昇温した後10℃/分で0℃まで急冷して再度0℃から200℃まで10℃/分の昇温速度にてDSC測定を実施した。得られたDSC曲線における2回目の昇温時における融解開始から終了までの温度範囲のピーク面積により、変性EVOHを含むペレットの融解エンタルピー(ΔHm:J/g)を求めた。結果を表3に示す。
図1は、上記(3)で得られたペレット側面の外観写真である。前記ペレットの直径Di(mm)及び流れ方向の長さL(mm)はノギスで計測することにより求めた。図2は、前記ペレット1の重心6からL/4(mm)以下の位置において、前記ペレット1の流れ方向3に対して垂直に切断して得られた断面4の電子顕微鏡画像である。当該ペレット側面には、4つの凹部5が形成されていた。当該断面4から、断面4の重心7から、凹部5の縁8までの距離α1~α4(断面4の重心7から、各縁8において重心7から最も遠い点までの距離)と、断面4の重心7から、凹部5の底9までの距離β1~β4(断面4の重心7から、各底9において重心7から最も近い点までの距離)を求めた。得られた値を上記式(1)に代入して、左辺の値を求めた。結果を表3に示す。
(9-1)乾燥温度70℃での含水ペレットの乾燥時ブロッキング耐性評価
上記(3)で得られた遠心脱水後の含水ペレット3kgを30cm四方のステンレス製網かごに入れ、ヤマト科学株式会社製精密恒温器「DH410」にて70℃で2時間乾燥させた。乾燥後のペレットを目開き5mmの篩に1分間かけ、篩中に残留していたペレットをブロッキングが発生したペレットとしてその質量を測定し、70℃でのブロッキング発生率を下記式(9)にて算出し、以下の基準で評価した。結果を表3に示す。
ブロッキング発生率(質量%)=(篩中に残留していたペレットの質量(kg))/3kg×100 (9)
A:ブロッキング率が10質量%未満
B:ブロッキング率が10質量%以上20質量%未満
C:ブロッキング率が20質量%以上
(9-1)の評価に用いたペレット全量を再度30cm四方のステンレス製網かごに入れ、ヤマト科学株式会社製精密恒温器「DH410」にて90℃で2時間乾燥させた。(9-1)と同様の操作を行い、90℃でのブロッキング発生率を算出した。結果を表3に示す。
(9-2)の評価に用いたペレット全量を再度30cm四方のステンレス製網かごに入れ、ヤマト科学株式会社製精密恒温器「DH410」にて110℃で2時間乾燥させた。(9-1)と同様の操作を行い、110℃でのブロッキング発生率を算出した。結果を表3に示す。
株式会社東洋精機製作所製20mm押出機「D2020」(D(mm)=20、L/D=20、圧縮比=3.5、スクリュー:フルフライト)を用いて以下の条件にて、上記(3)で得られたペレットの単層製膜を行い、欠点数を評価した。
シリンダー温度:供給部150℃、圧縮部172℃、計量部172℃
ダイ温度:172℃
スクリュー回転数:40rpm
吐出量:1.2kg/時間
引取りロール温度:80℃
引取りロール速度:3.0m/分
フィルム厚み:20μm
供給部:150℃(実施例11と比較例7は120℃)
圧縮部:変性EVOHの融点+20℃
計量部:変性EVOHの融点+20℃
ダイ温度:変性EVOHの融点+20℃
判定:基準
A:50個/100cm2以下
B:50個/100cm2超、100個/100cm2以下
C:100個/100cm2超、200個/100cm2以下
D:200個/100cm2超
ダイ温度を250℃としたこと以外は「(10)押出安定性評価」と同様にして、上記(3)で得られたペレットの単層製膜を8時間行った後、スクリュー回転数を50rpmに変更し、500gの高密度ポリエチレンで押出機内をパージ(洗浄)した。次に、ダイスを分解し、リップ部に付着している熱劣化樹脂を採取して秤量し、加工時のロングラン性(ダイリップ付着量)を評価した。なお、リップ部に付着している熱劣化樹脂は、得られるフィルム中のゲルやブツなどの欠点の原因になりやすく、その蓄積量が小さいことは長時間にわたって安定に溶融成形可能であることを意味する。結果を表3に示す。
上記(3)で得られたペレットを用いて、株式会社東洋精機製作所製20mm押出機「D2020」(D(mm)=20、L/D=20、圧縮比=3.5、スクリュー:フルフライト)を用いて以下の条件にて単層製膜を行い、単層フィルムを得た。
シリンダー温度:供給部170℃、圧縮部200℃、計量部200℃
ダイ温度:200℃
スクリュー回転数:100rpm
吐出量:3.0kg/時間
引取りロール温度:80℃
引取りロール速度:1.5m/分
フィルム厚み:100μm
得られた厚み100μmの単層フィルムをエトー株式会社製パンタグラフ式二軸延伸装置にて80℃で3.75×3.75倍の延伸倍率において同時二軸延伸を行い、以下の基準で延伸性を評価した。
A:延伸後フィルムに延伸ムラ及び局部的偏肉が認められず、外観が良好であった。
B:延伸後フィルムに破れは生じなかったが、わずかに延伸ムラ又は局部的偏肉が生じた。
C:延伸後フィルムに破れは生じなかったが、全面積の半分以下に明らかな延伸ムラ又は局部的偏肉が生じた。
D:延伸後フィルムに破れは生じなかったが、全面積の半分超に延伸ムラ又は局部的偏肉が生じた。
E:延伸後フィルムの全面に延伸ムラ又は局部的偏肉が生じたうえに、フィルムに破れが生じた。
上記(3)で得られたペレット10gをジメチルスルホキシド100gに入れ、80℃に昇温撹拌した。1時間後の溶液を20番手の金属メッシュ(目開き0.98mm)を用いて濾過した後に、不溶分を採取した。ジメチルスルホキシドに添加したペレット10gに対する不溶分(g)の割合を計算し、以下の基準で評価した。結果を表3に示す。
A:不溶分1%未満
B:不溶分1%以上10%未満
C:不溶分10%以上
EVOHの種類、粒子の種類や含有量を変更した以外は、実施例1と同様にして、ペレットの作製及び評価を行った。結果を表2及び3に示す。なお、いずれのペレットについても、ナトリウム元素含有量は150ppmであり、リン酸化合物含有量はリン酸根換算で40ppmであり、酢酸含有量は100ppmであった。
含水ペレットの製造時に仕込む水とメタノールをそれぞれ37質量部、149質量部に変更した以外は、実施例2と同様にして、ペレットの作製及び評価を行った。ナトリウム元素含有量は150ppmであり、リン酸化合物含有量はリン酸根換算で40ppmであり、酢酸含有量は100ppmであった。得られたペレットは両切断面に凹部が形成されており、そのD/Lはいずれも0.22であった。結果を表2及び3に示す。
ペレットの製造時に含水ペレット1質量部を投入する溶液を酢酸ナトリウム濃度0.5g/L、酢酸濃度0.4g/L、リン酸濃度0.05g/L、ホウ酸濃度0.2g/Lの水溶液18.5質量部(浴比20)に変更した以外は、実施例2と同様にして、ペレットの作製及び評価を行った。結果を表2及び3に示す。得られたペレットのナトリウム元素含有量は150ppmであり、リン酸化合物含有量はリン酸根換算で40ppmであり、酢酸含有量は100ppm、ホウ酸含有量は1000ppmであった。また、得られた変性EVOHのメルトフローレート(MFR)(190℃、2160g荷重下)は3.7g/10分であった。
合成例9で得たEVOH粗乾燥物を用いた以外は、実施例2と同様にして、ペレットの作製及び評価を行った。結果を表2及び3に示す。なお、得られたペレットのナトリウム元素含有量は150ppmであり、リン酸化合物含有量はリン酸根換算で40ppmであり、酢酸含有量は100ppmであった。
合成例10で得たEVOH粗乾燥物100質量部、サイリシア350(富士シリシア化学株式会社製)0.12質量部、水70質量部、MeOH163質量部を仕込んで含水ペレットを製造した以外は、実施例2と同様にしてペレットの作製及び評価を行った。なお、得られたペレットのナトリウム元素含有量は150ppmであり、リン酸化合物含有量はリン酸根換算で40ppmであり、酢酸含有量は100ppmであった。結果を表2及び3に示す。
粒子を添加しなかったこと以外は実施例2と同様にして上記(1)~(3)を行うことにより、ペレットを得た。また、(4)~(7)に基づいて、融点、ナトリウム元素含有量、リン酸化合物含有量、酢酸含有量を測定した。融点は152℃であり、ナトリウム元素含有量は150ppmであり、リン酸化合物含有量はリン酸根換算で40ppmであり、酢酸含有量は100ppmであり、融解エンタルピーΔHmは55(J/g)であった。(8)の通り得られたペレットの切断面を電子顕微鏡観察したところ、当該ペレット側面には、4つの凹部5が形成されていた。また、当該ペレットの表面を電子顕微鏡観察したところ、ペレット表面に突起が形成されていなかった。さらに、(3)ペレットの製造で得られた遠心脱水後の含水ペレットを用いて、(9)乾燥時のブロッキング耐性を評価した。結果を表2及び3に示す。
なお、二軸押出機にて混錬した後のペレットの切断面を電子顕微鏡観察したところ、凹部が形成されていなかった。また、当該ペレットの表面を電子顕微鏡観察したところ、ペレット表面に突起も形成されていなかった。
含水ペレットの製造において、添加する粒子をモレキュラーシーブ4A(ユニオン昭和株式会社製)に変更した以外は、実施例1と同様にして、ペレットの作製及び評価を行った。モレキュラーシーブ4Aは表2及び3に記載した平均粒子径となるよう、ミキサーで粉砕した。結果を表2に示す。
2 側面
3 流れ方向
4 断面
5、11 凹部
6 ペレットの重心
7 断面の重心
8 縁
9 底
10 切断面
Claims (11)
- ケン化度90モル%以上のエチレン-ビニルアルコール共重合体及び粒子を含有し、円筒状に切断されてなるペレットであって、
前記ペレットの融解エンタルピーΔHm(J/g)が65(J/g)以下であり、
前記ペレットが、平均粒子径Rが1~30μmの粒子を5~5000ppm含有し、
前記ペレットの長さがL(mm)であり、
前記ペレットの側面又は切断面に凹部が形成され、
前記側面に凹部が形成される場合、該凹部の数nが2~5であり、前記ペレットの重心からL/4(mm)以下の位置における、前記ペレットの流れ方向に対して垂直な少なくとも1つの断面において、該断面の重心から、側面に形成される凹部の縁までの距離α1~αnと、該断面の重心から、側面に形成される凹部の底までの距離β1~βnが下記式(1)を満たし、
(β1+β2・・・+βn)/(α1+α2・・・+αn)≦0.8 (1)
前記切断面に凹部が形成される場合、前記ペレットの長さL(mm)に対する、切断面に形成される凹部の深さD(mm)の比D/Lが0.1以上であり、
前記ペレットの表面に高さHが0.1~15μmの突起が形成され、
該突起が、前記粒子を含むとともに、該粒子が前記エチレン-ビニルアルコール共重合体で被覆されてなる、ペレット。 - 前記ペレットの融解エンタルピーΔHm(J/g)が64(J/g)以下である、請求項1に記載のペレット。
- 前記エチレン-ビニルアルコール重合体が、下記式(I)で表され、全単量体単位に対するa、b及びcの含有率(モル%)が下記式(2)~(4)を満足するものである、請求項1又は2に記載のペレット。
24≦a≦55 (2)
0.01≦c≦10 (3)
[100-(a+c)]×0.9≦b≦[100-(a+c)] (4) - 式(I)中のa及びcが下記式(5)を満たす、請求項3に記載のペレット。
29≦1.2a+8c≦100 (5) - 式(I)中のR1が単結合で、Wがヒドロキシメチル基である、請求項3又は4に記載のペレット。
- 前記ペレットの融解エンタルピーΔHm(J/g)と前記粒子の含有量A(ppm)が下記式(6)を満たす、請求項1~5のいずれかに記載のペレット。
1≦ΔHm/100+A/500≦10 (6) - 前記粒子の平均粒子径R(μm)と前記突起の高さH(μm)が、下記式(7)を満たす、請求項1~6のいずれかに記載のペレット。
0.1≦H/R≦0.9 (7) - 前記粒子が無機酸化物粒子である、請求項1~7のいずれかに記載のペレット。
- 前記無機酸化物粒子が酸化ケイ素粒子又は金属酸化物粒子である、請求項8に記載のペレット。
- 前記粒子が飽和脂肪酸アミド、不飽和脂肪酸アミド、ビス脂肪酸アミド及び脂肪酸金属塩からなる群から選択される少なくとも一種からなる有機化合物粒子である、請求項1~7のいずれかに記載のペレット。
- 前記エチレン-ビニルアルコール重合体、前記粒子及び水を含有するストランドを切断して円筒状の含水ペレットを得る工程と、該含水ペレットを乾燥させることにより前記凹部を形成させる工程とを有する、請求項1~10のいずれかに記載のペレットの製造方法。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2021-166524 | 2021-10-08 | ||
| JP2021166524 | 2021-10-08 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2023058761A1 true WO2023058761A1 (ja) | 2023-04-13 |
Family
ID=85804372
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2022/037692 WO2023058761A1 (ja) | 2021-10-08 | 2022-10-07 | エチレン-ビニルアルコール共重合体を含有するペレット及びその製造方法 |
Country Status (1)
| Country | Link |
|---|---|
| WO (1) | WO2023058761A1 (ja) |
Citations (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2000265025A (ja) * | 1999-03-16 | 2000-09-26 | Nippon Synthetic Chem Ind Co Ltd:The | 水酸基含有熱可塑性樹脂改質用の樹脂組成物およびその使用法 |
| JP2002284887A (ja) * | 2001-01-22 | 2002-10-03 | Kuraray Co Ltd | エチレン−ビニルアルコール共重合体樹脂組成物の製造方法 |
| JP2008208327A (ja) * | 2007-01-31 | 2008-09-11 | Nippon Synthetic Chem Ind Co Ltd:The | 樹脂複合体およびその製造方法 |
| WO2010001471A1 (ja) * | 2008-07-02 | 2010-01-07 | 日本合成化学工業株式会社 | Evoh複合体の製造方法 |
| WO2014024912A1 (ja) | 2012-08-09 | 2014-02-13 | 株式会社クラレ | 変性エチレン-ビニルアルコール共重合体、その製造方法及びその用途 |
| WO2018124295A1 (ja) * | 2016-12-29 | 2018-07-05 | 株式会社クラレ | 樹脂組成物及びその用途 |
| WO2019194318A1 (ja) * | 2018-04-06 | 2019-10-10 | 株式会社クラレ | ジオメンブレン並びにそれを用いたランドフィルシート及びラドンバリアフィルム |
| JP2019182947A (ja) | 2018-04-04 | 2019-10-24 | 株式会社クラレ | 樹脂組成物及びその用途 |
| JP2022016088A (ja) * | 2020-07-10 | 2022-01-21 | 株式会社クラレ | 樹脂組成物、その製造方法及びそれを用いた多層構造体 |
-
2022
- 2022-10-07 WO PCT/JP2022/037692 patent/WO2023058761A1/ja active Application Filing
Patent Citations (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2000265025A (ja) * | 1999-03-16 | 2000-09-26 | Nippon Synthetic Chem Ind Co Ltd:The | 水酸基含有熱可塑性樹脂改質用の樹脂組成物およびその使用法 |
| JP2002284887A (ja) * | 2001-01-22 | 2002-10-03 | Kuraray Co Ltd | エチレン−ビニルアルコール共重合体樹脂組成物の製造方法 |
| JP2008208327A (ja) * | 2007-01-31 | 2008-09-11 | Nippon Synthetic Chem Ind Co Ltd:The | 樹脂複合体およびその製造方法 |
| WO2010001471A1 (ja) * | 2008-07-02 | 2010-01-07 | 日本合成化学工業株式会社 | Evoh複合体の製造方法 |
| WO2014024912A1 (ja) | 2012-08-09 | 2014-02-13 | 株式会社クラレ | 変性エチレン-ビニルアルコール共重合体、その製造方法及びその用途 |
| WO2018124295A1 (ja) * | 2016-12-29 | 2018-07-05 | 株式会社クラレ | 樹脂組成物及びその用途 |
| JP2019182947A (ja) | 2018-04-04 | 2019-10-24 | 株式会社クラレ | 樹脂組成物及びその用途 |
| WO2019194318A1 (ja) * | 2018-04-06 | 2019-10-10 | 株式会社クラレ | ジオメンブレン並びにそれを用いたランドフィルシート及びラドンバリアフィルム |
| JP2022016088A (ja) * | 2020-07-10 | 2022-01-21 | 株式会社クラレ | 樹脂組成物、その製造方法及びそれを用いた多層構造体 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5909811B2 (ja) | 変性エチレン−ビニルアルコール共重合体及び多層構造体 | |
| JP6110678B2 (ja) | ヒドロキシメチル基含有ビニルアルコール系重合体 | |
| JP2019182947A (ja) | 樹脂組成物及びその用途 | |
| WO2015115511A1 (ja) | エチレン-ビニルアルコール共重合体樹脂組成物及びその製造方法 | |
| TWI637969B (zh) | 改性聚乙烯醇及其製造方法 | |
| JP6029143B2 (ja) | 変性エチレン−ビニルアルコール共重合体及びその製造方法 | |
| JP2015034262A (ja) | 変性ビニルアルコール系重合体 | |
| JP5971173B2 (ja) | 熱収縮フィルム | |
| JP6218177B2 (ja) | 樹脂組成物及びその製造方法 | |
| JP6890125B2 (ja) | 樹脂組成物、押出成形品、射出成形品及びブロー成形品 | |
| EP2407491B1 (en) | Process for manufacturing composition of solvolysis product of ethylene-vinyl ester copolymer | |
| WO2023058761A1 (ja) | エチレン-ビニルアルコール共重合体を含有するペレット及びその製造方法 | |
| JP2011202052A (ja) | 変性エチレン−ビニルアルコール共重合体およびそれを含有する組成物 | |
| JP2024034799A (ja) | 変性エチレン-ビニルアルコール共重合体を含むペレットの製造方法 | |
| JP7157760B2 (ja) | 樹脂組成物、積層体及び包装体 | |
| WO2021210555A1 (ja) | 変性ビニルアルコール系重合体 | |
| JP5715025B2 (ja) | 変性ビニルアルコール系重合体 | |
| US6646087B2 (en) | Method of manufacturing ethylene-vinyl acetate copolymer | |
| JP7339742B2 (ja) | 多層フィルム | |
| JP2024002234A (ja) | 変性エチレン-ビニルアルコール共重合体を含むペレット及びその製造方法 | |
| JP7318153B1 (ja) | 変性エチレン-ビニルアルコール共重合体の製造方法 | |
| JP2023023159A (ja) | 変性エチレン―ビニルアルコール共重合体 | |
| JP6203038B2 (ja) | 成形品及びその製造方法 | |
| WO2018124296A1 (ja) | 熱水殺菌処理された包装体及びその製造方法 | |
| JP2016050241A (ja) | ビニルアルコール系共重合体および成形物 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 22878628 Country of ref document: EP Kind code of ref document: A1 |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2023552971 Country of ref document: JP |
|
| REG | Reference to national code |
Ref country code: BR Ref legal event code: B01A Ref document number: 112024005405 Country of ref document: BR |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2022878628 Country of ref document: EP |
|
| ENP | Entry into the national phase |
Ref document number: 2022878628 Country of ref document: EP Effective date: 20240508 |