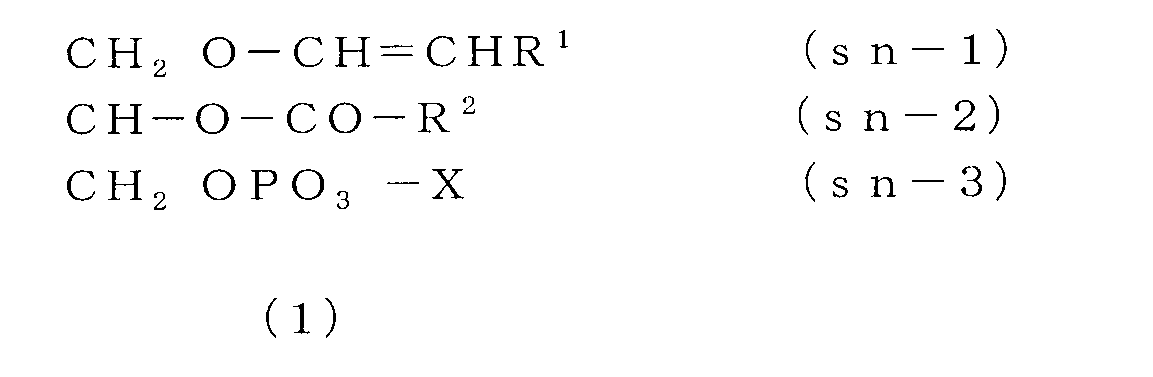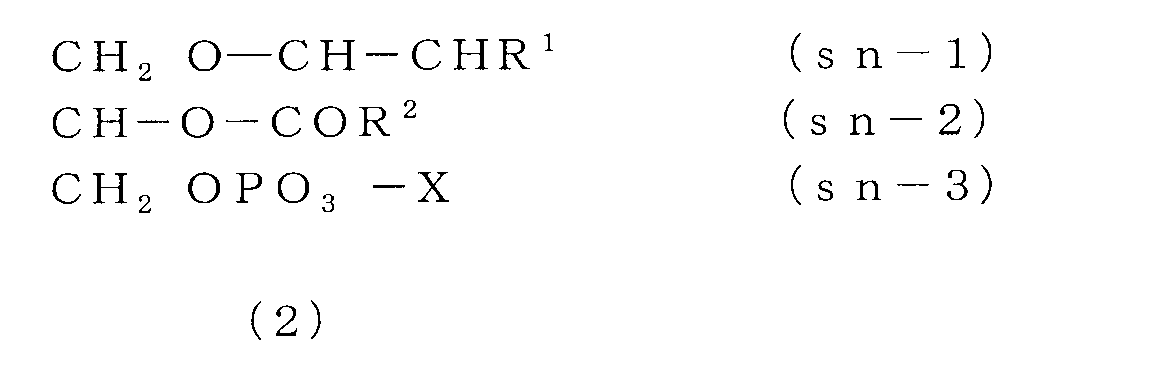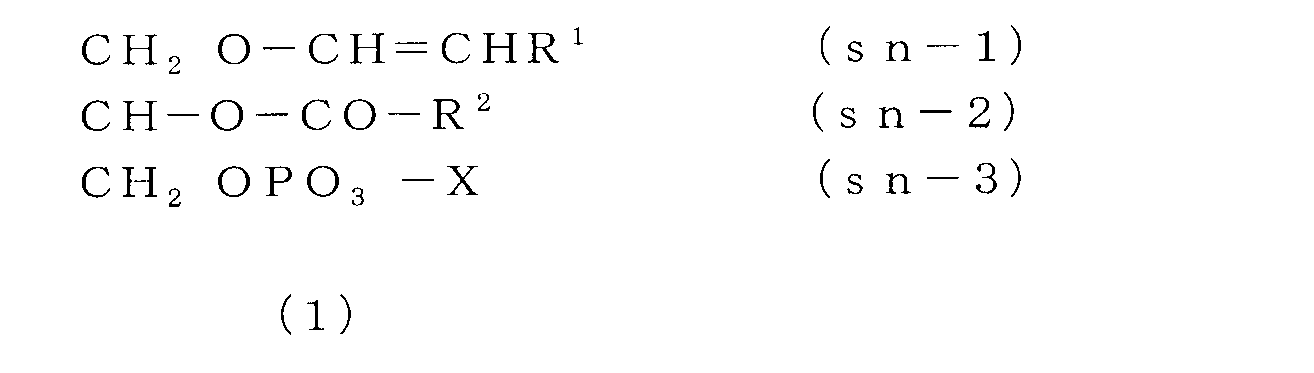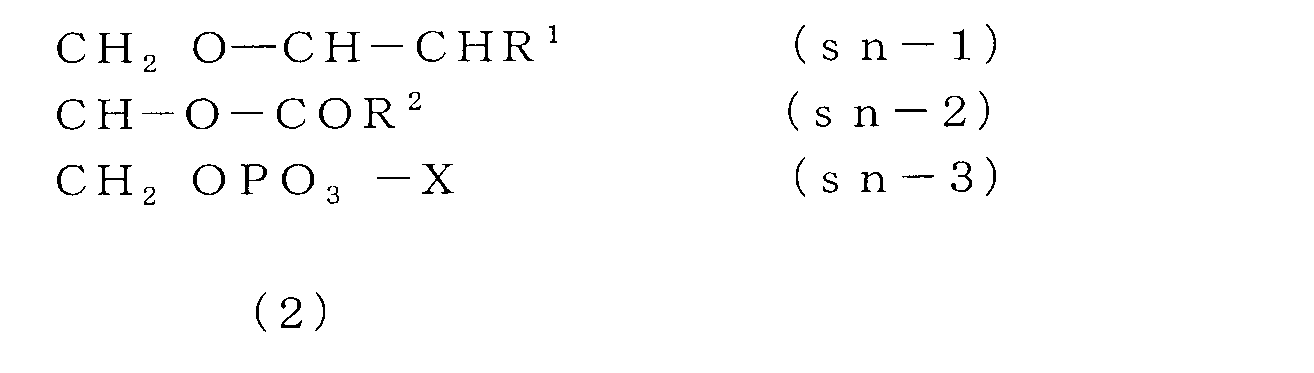WO2016092878A1 - エーテルリン脂質およびその製造方法 - Google Patents
エーテルリン脂質およびその製造方法 Download PDFInfo
- Publication number
- WO2016092878A1 WO2016092878A1 PCT/JP2015/063740 JP2015063740W WO2016092878A1 WO 2016092878 A1 WO2016092878 A1 WO 2016092878A1 JP 2015063740 W JP2015063740 W JP 2015063740W WO 2016092878 A1 WO2016092878 A1 WO 2016092878A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- ether
- bivalve
- phospholipid
- ether phospholipid
- tissue
- Prior art date
Links
- RTZKZFJDLAIYFH-UHFFFAOYSA-N ether Substances CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 title claims abstract description 132
- -1 Ether phospholipid Chemical class 0.000 title claims abstract description 121
- 238000004519 manufacturing process Methods 0.000 title claims abstract description 22
- 238000000605 extraction Methods 0.000 claims abstract description 17
- 150000002327 glycerophospholipids Chemical class 0.000 claims description 47
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical group CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 claims description 41
- 150000002632 lipids Chemical class 0.000 claims description 40
- 150000003904 phospholipids Chemical class 0.000 claims description 31
- 238000000034 method Methods 0.000 claims description 28
- YZXBAPSDXZZRGB-DOFZRALJSA-N arachidonic acid Chemical compound CCCCC\C=C/C\C=C/C\C=C/C\C=C/CCCC(O)=O YZXBAPSDXZZRGB-DOFZRALJSA-N 0.000 claims description 24
- 108010013563 Lipoprotein Lipase Proteins 0.000 claims description 21
- 102100022119 Lipoprotein lipase Human genes 0.000 claims description 21
- 235000013305 food Nutrition 0.000 claims description 17
- JAZBEHYOTPTENJ-JLNKQSITSA-N all-cis-5,8,11,14,17-icosapentaenoic acid Chemical compound CC\C=C/C\C=C/C\C=C/C\C=C/C\C=C/CCCC(O)=O JAZBEHYOTPTENJ-JLNKQSITSA-N 0.000 claims description 16
- 235000020673 eicosapentaenoic acid Nutrition 0.000 claims description 16
- 229960005135 eicosapentaenoic acid Drugs 0.000 claims description 16
- JAZBEHYOTPTENJ-UHFFFAOYSA-N eicosapentaenoic acid Natural products CCC=CCC=CCC=CCC=CCC=CCCCC(O)=O JAZBEHYOTPTENJ-UHFFFAOYSA-N 0.000 claims description 16
- 239000002904 solvent Substances 0.000 claims description 14
- HZAXFHJVJLSVMW-UHFFFAOYSA-N 2-Aminoethan-1-ol Chemical compound NCCO HZAXFHJVJLSVMW-UHFFFAOYSA-N 0.000 claims description 12
- 235000021342 arachidonic acid Nutrition 0.000 claims description 12
- 229940114079 arachidonic acid Drugs 0.000 claims description 12
- 239000000203 mixture Substances 0.000 claims description 11
- 239000003960 organic solvent Substances 0.000 claims description 11
- 235000019197 fats Nutrition 0.000 claims description 9
- 230000008569 process Effects 0.000 claims description 9
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 claims description 7
- 230000002209 hydrophobic effect Effects 0.000 claims description 7
- 150000002576 ketones Chemical class 0.000 claims description 7
- 230000007935 neutral effect Effects 0.000 claims description 7
- MBMBGCFOFBJSGT-KUBAVDMBSA-N all-cis-docosa-4,7,10,13,16,19-hexaenoic acid Chemical compound CC\C=C/C\C=C/C\C=C/C\C=C/C\C=C/C\C=C/CCC(O)=O MBMBGCFOFBJSGT-KUBAVDMBSA-N 0.000 claims description 6
- 229960001231 choline Drugs 0.000 claims description 6
- 238000000638 solvent extraction Methods 0.000 claims description 6
- 125000001931 aliphatic group Chemical group 0.000 claims description 5
- OEYIOHPDSNJKLS-UHFFFAOYSA-N choline Chemical compound C[N+](C)(C)CCO OEYIOHPDSNJKLS-UHFFFAOYSA-N 0.000 claims description 5
- 235000020669 docosahexaenoic acid Nutrition 0.000 claims description 5
- 239000008194 pharmaceutical composition Substances 0.000 claims description 5
- 125000004432 carbon atom Chemical group C* 0.000 claims description 3
- 229940090949 docosahexaenoic acid Drugs 0.000 claims description 3
- 239000003208 petroleum Substances 0.000 claims description 3
- 125000001033 ether group Chemical group 0.000 claims 1
- 208000024827 Alzheimer disease Diseases 0.000 abstract description 11
- 208000001145 Metabolic Syndrome Diseases 0.000 abstract description 11
- 201000000690 abdominal obesity-metabolic syndrome Diseases 0.000 abstract description 11
- 230000000694 effects Effects 0.000 abstract description 11
- 208000035473 Communicable disease Diseases 0.000 abstract description 9
- 208000018737 Parkinson disease Diseases 0.000 abstract description 9
- 201000000980 schizophrenia Diseases 0.000 abstract description 9
- 206010012601 diabetes mellitus Diseases 0.000 abstract description 8
- 208000019736 Cranial nerve disease Diseases 0.000 abstract description 7
- 230000009390 immune abnormality Effects 0.000 abstract description 4
- 241000271566 Aves Species 0.000 abstract description 3
- 208000020401 Depressive disease Diseases 0.000 abstract 1
- 241000620877 Ruditapes philippinarum Species 0.000 abstract 1
- 239000013505 freshwater Substances 0.000 abstract 1
- 230000001225 therapeutic effect Effects 0.000 abstract 1
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 60
- 210000001519 tissue Anatomy 0.000 description 35
- 238000004128 high performance liquid chromatography Methods 0.000 description 28
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 20
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 14
- 235000020639 clam Nutrition 0.000 description 12
- 235000014113 dietary fatty acids Nutrition 0.000 description 11
- 239000000194 fatty acid Substances 0.000 description 11
- 229930195729 fatty acid Natural products 0.000 description 11
- 150000004665 fatty acids Chemical class 0.000 description 11
- 241000237519 Bivalvia Species 0.000 description 10
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 9
- 239000007788 liquid Substances 0.000 description 9
- 239000000243 solution Substances 0.000 description 9
- 235000020777 polyunsaturated fatty acids Nutrition 0.000 description 8
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 7
- 239000000872 buffer Substances 0.000 description 7
- 235000021588 free fatty acids Nutrition 0.000 description 7
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 6
- 102000004190 Enzymes Human genes 0.000 description 6
- 108090000790 Enzymes Proteins 0.000 description 6
- 235000013330 chicken meat Nutrition 0.000 description 6
- 238000006460 hydrolysis reaction Methods 0.000 description 6
- 238000000746 purification Methods 0.000 description 6
- 229920002472 Starch Polymers 0.000 description 5
- 230000007062 hydrolysis Effects 0.000 description 5
- 230000006872 improvement Effects 0.000 description 5
- 239000000047 product Substances 0.000 description 5
- 235000019698 starch Nutrition 0.000 description 5
- 239000008107 starch Substances 0.000 description 5
- 239000000126 substance Substances 0.000 description 5
- VTYYLEPIZMXCLO-UHFFFAOYSA-L Calcium carbonate Chemical compound [Ca+2].[O-]C([O-])=O VTYYLEPIZMXCLO-UHFFFAOYSA-L 0.000 description 4
- 241000287828 Gallus gallus Species 0.000 description 4
- 206010034203 Pectus Carinatum Diseases 0.000 description 4
- 239000004698 Polyethylene Substances 0.000 description 4
- 241000269959 Xiphias gladius Species 0.000 description 4
- 238000006243 chemical reaction Methods 0.000 description 4
- 238000001816 cooling Methods 0.000 description 4
- 238000009826 distribution Methods 0.000 description 4
- 208000026278 immune system disease Diseases 0.000 description 4
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 4
- 239000002244 precipitate Substances 0.000 description 4
- 235000021335 sword fish Nutrition 0.000 description 4
- ZWEHNKRNPOVVGH-UHFFFAOYSA-N 2-Butanone Chemical compound CCC(C)=O ZWEHNKRNPOVVGH-UHFFFAOYSA-N 0.000 description 3
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 3
- JZNWSCPGTDBMEW-UHFFFAOYSA-N Glycerophosphorylethanolamin Natural products NCCOP(O)(=O)OCC(O)CO JZNWSCPGTDBMEW-UHFFFAOYSA-N 0.000 description 3
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 3
- 241000124008 Mammalia Species 0.000 description 3
- 239000004480 active ingredient Substances 0.000 description 3
- 238000004458 analytical method Methods 0.000 description 3
- 239000001913 cellulose Substances 0.000 description 3
- 229920002678 cellulose Polymers 0.000 description 3
- 150000001875 compounds Chemical class 0.000 description 3
- 235000009508 confectionery Nutrition 0.000 description 3
- 239000003814 drug Substances 0.000 description 3
- 238000005516 engineering process Methods 0.000 description 3
- 238000006911 enzymatic reaction Methods 0.000 description 3
- 235000013376 functional food Nutrition 0.000 description 3
- 239000008101 lactose Substances 0.000 description 3
- 239000012528 membrane Substances 0.000 description 3
- 235000013336 milk Nutrition 0.000 description 3
- 239000008267 milk Substances 0.000 description 3
- 210000004080 milk Anatomy 0.000 description 3
- 238000002156 mixing Methods 0.000 description 3
- 239000000546 pharmaceutical excipient Substances 0.000 description 3
- WTJKGGKOPKCXLL-RRHRGVEJSA-N phosphatidylcholine Chemical compound CCCCCCCCCCCCCCCC(=O)OC[C@H](COP([O-])(=O)OCC[N+](C)(C)C)OC(=O)CCCCCCCC=CCCCCCCCC WTJKGGKOPKCXLL-RRHRGVEJSA-N 0.000 description 3
- 150000008104 phosphatidylethanolamines Chemical class 0.000 description 3
- 239000000843 powder Substances 0.000 description 3
- 238000002360 preparation method Methods 0.000 description 3
- DVSZKTAMJJTWFG-SKCDLICFSA-N (2e,4e,6e,8e,10e,12e)-docosa-2,4,6,8,10,12-hexaenoic acid Chemical compound CCCCCCCCC\C=C\C=C\C=C\C=C\C=C\C=C\C(O)=O DVSZKTAMJJTWFG-SKCDLICFSA-N 0.000 description 2
- GZJLLYHBALOKEX-UHFFFAOYSA-N 6-Ketone, O18-Me-Ussuriedine Natural products CC=CCC=CCC=CCC=CCC=CCC=CCCCC(O)=O GZJLLYHBALOKEX-UHFFFAOYSA-N 0.000 description 2
- 244000215068 Acacia senegal Species 0.000 description 2
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 description 2
- 229920002261 Corn starch Polymers 0.000 description 2
- 229920000084 Gum arabic Polymers 0.000 description 2
- 241001465754 Metazoa Species 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 2
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 2
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 2
- 229930006000 Sucrose Natural products 0.000 description 2
- 235000010489 acacia gum Nutrition 0.000 description 2
- 239000000205 acacia gum Substances 0.000 description 2
- 230000009471 action Effects 0.000 description 2
- 125000003342 alkenyl group Chemical group 0.000 description 2
- 125000000217 alkyl group Chemical group 0.000 description 2
- 239000007864 aqueous solution Substances 0.000 description 2
- 239000011230 binding agent Substances 0.000 description 2
- 229910000019 calcium carbonate Inorganic materials 0.000 description 2
- 239000002775 capsule Substances 0.000 description 2
- 210000004027 cell Anatomy 0.000 description 2
- HVYWMOMLDIMFJA-DPAQBDIFSA-N cholesterol Chemical compound C1C=C2C[C@@H](O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@H]([C@H](C)CCCC(C)C)[C@@]1(C)CC2 HVYWMOMLDIMFJA-DPAQBDIFSA-N 0.000 description 2
- 239000007979 citrate buffer Substances 0.000 description 2
- 239000008120 corn starch Substances 0.000 description 2
- 210000003792 cranial nerve Anatomy 0.000 description 2
- 230000009849 deactivation Effects 0.000 description 2
- 239000007857 degradation product Substances 0.000 description 2
- 238000001514 detection method Methods 0.000 description 2
- 239000003085 diluting agent Substances 0.000 description 2
- 239000007884 disintegrant Substances 0.000 description 2
- KAUVQQXNCKESLC-UHFFFAOYSA-N docosahexaenoic acid (DHA) Natural products COC(=O)C(C)NOCC1=CC=CC=C1 KAUVQQXNCKESLC-UHFFFAOYSA-N 0.000 description 2
- 230000002255 enzymatic effect Effects 0.000 description 2
- 210000002615 epidermis Anatomy 0.000 description 2
- 239000000706 filtrate Substances 0.000 description 2
- 235000003599 food sweetener Nutrition 0.000 description 2
- 239000008187 granular material Substances 0.000 description 2
- 230000036541 health Effects 0.000 description 2
- 230000003301 hydrolyzing effect Effects 0.000 description 2
- 239000000314 lubricant Substances 0.000 description 2
- 235000019359 magnesium stearate Nutrition 0.000 description 2
- 235000013372 meat Nutrition 0.000 description 2
- 239000011259 mixed solution Substances 0.000 description 2
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 2
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 2
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 2
- 230000002265 prevention Effects 0.000 description 2
- 150000003180 prostaglandins Chemical class 0.000 description 2
- 239000002994 raw material Substances 0.000 description 2
- 150000003333 secondary alcohols Chemical class 0.000 description 2
- 238000000926 separation method Methods 0.000 description 2
- 229910001467 sodium calcium phosphate Inorganic materials 0.000 description 2
- 239000005720 sucrose Substances 0.000 description 2
- 238000000967 suction filtration Methods 0.000 description 2
- 239000003765 sweetening agent Substances 0.000 description 2
- 239000006188 syrup Substances 0.000 description 2
- 235000020357 syrup Nutrition 0.000 description 2
- 239000003826 tablet Substances 0.000 description 2
- 239000000454 talc Substances 0.000 description 2
- 229910052623 talc Inorganic materials 0.000 description 2
- 235000013618 yogurt Nutrition 0.000 description 2
- MTCFGRXMJLQNBG-REOHCLBHSA-N (2S)-2-Amino-3-hydroxypropansäure Chemical group OC[C@H](N)C(O)=O MTCFGRXMJLQNBG-REOHCLBHSA-N 0.000 description 1
- JSPNNZKWADNWHI-PNANGNLXSA-N (2r)-2-hydroxy-n-[(2s,3r,4e,8e)-3-hydroxy-9-methyl-1-[(2r,3r,4s,5s,6r)-3,4,5-trihydroxy-6-(hydroxymethyl)oxan-2-yl]oxyoctadeca-4,8-dien-2-yl]heptadecanamide Chemical compound CCCCCCCCCCCCCCC[C@@H](O)C(=O)N[C@H]([C@H](O)\C=C\CC\C=C(/C)CCCCCCCCC)CO[C@@H]1O[C@H](CO)[C@@H](O)[C@H](O)[C@H]1O JSPNNZKWADNWHI-PNANGNLXSA-N 0.000 description 1
- TZCPCKNHXULUIY-RGULYWFUSA-N 1,2-distearoyl-sn-glycero-3-phosphoserine Chemical compound CCCCCCCCCCCCCCCCCC(=O)OC[C@H](COP(O)(=O)OC[C@H](N)C(O)=O)OC(=O)CCCCCCCCCCCCCCCCC TZCPCKNHXULUIY-RGULYWFUSA-N 0.000 description 1
- IXPNQXFRVYWDDI-UHFFFAOYSA-N 1-methyl-2,4-dioxo-1,3-diazinane-5-carboximidamide Chemical compound CN1CC(C(N)=N)C(=O)NC1=O IXPNQXFRVYWDDI-UHFFFAOYSA-N 0.000 description 1
- IIZPXYDJLKNOIY-JXPKJXOSSA-N 1-palmitoyl-2-arachidonoyl-sn-glycero-3-phosphocholine Chemical compound CCCCCCCCCCCCCCCC(=O)OC[C@H](COP([O-])(=O)OCC[N+](C)(C)C)OC(=O)CCC\C=C/C\C=C/C\C=C/C\C=C/CCCCC IIZPXYDJLKNOIY-JXPKJXOSSA-N 0.000 description 1
- IKRZCYCTPYDXML-UHFFFAOYSA-N 2-hydroxypropane-1,2,3-tricarboxylic acid;hydrochloride Chemical compound Cl.OC(=O)CC(O)(C(O)=O)CC(O)=O IKRZCYCTPYDXML-UHFFFAOYSA-N 0.000 description 1
- 240000006439 Aspergillus oryzae Species 0.000 description 1
- 235000002247 Aspergillus oryzae Nutrition 0.000 description 1
- YDNKGFDKKRUKPY-JHOUSYSJSA-N C16 ceramide Natural products CCCCCCCCCCCCCCCC(=O)N[C@@H](CO)[C@H](O)C=CCCCCCCCCCCCCC YDNKGFDKKRUKPY-JHOUSYSJSA-N 0.000 description 1
- 108010055167 CD59 Antigens Proteins 0.000 description 1
- 102100022002 CD59 glycoprotein Human genes 0.000 description 1
- 229920002134 Carboxymethyl cellulose Polymers 0.000 description 1
- 206010051288 Central nervous system inflammation Diseases 0.000 description 1
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 1
- 229920001353 Dextrin Polymers 0.000 description 1
- 239000004375 Dextrin Substances 0.000 description 1
- 235000021294 Docosapentaenoic acid Nutrition 0.000 description 1
- 241000196324 Embryophyta Species 0.000 description 1
- 108010010803 Gelatin Proteins 0.000 description 1
- ZWZWYGMENQVNFU-UHFFFAOYSA-N Glycerophosphorylserin Natural products OC(=O)C(N)COP(O)(=O)OCC(O)CO ZWZWYGMENQVNFU-UHFFFAOYSA-N 0.000 description 1
- SQUHHTBVTRBESD-UHFFFAOYSA-N Hexa-Ac-myo-Inositol Chemical group CC(=O)OC1C(OC(C)=O)C(OC(C)=O)C(OC(C)=O)C(OC(C)=O)C1OC(C)=O SQUHHTBVTRBESD-UHFFFAOYSA-N 0.000 description 1
- 206010061218 Inflammation Diseases 0.000 description 1
- 229930195725 Mannitol Natural products 0.000 description 1
- CRJGESKKUOMBCT-VQTJNVASSA-N N-acetylsphinganine Chemical compound CCCCCCCCCCCCCCC[C@@H](O)[C@H](CO)NC(C)=O CRJGESKKUOMBCT-VQTJNVASSA-N 0.000 description 1
- 208000012902 Nervous system disease Diseases 0.000 description 1
- 208000036110 Neuroinflammatory disease Diseases 0.000 description 1
- 208000025966 Neurological disease Diseases 0.000 description 1
- 241000237502 Ostreidae Species 0.000 description 1
- 229910019142 PO4 Inorganic materials 0.000 description 1
- 241000237503 Pectinidae Species 0.000 description 1
- MTCFGRXMJLQNBG-UHFFFAOYSA-N Serine Chemical group OCC(N)C(O)=O MTCFGRXMJLQNBG-UHFFFAOYSA-N 0.000 description 1
- QYKIQEUNHZKYBP-UHFFFAOYSA-N Vinyl ether Chemical compound C=COC=C QYKIQEUNHZKYBP-UHFFFAOYSA-N 0.000 description 1
- 230000005856 abnormality Effects 0.000 description 1
- DPXJVFZANSGRMM-UHFFFAOYSA-N acetic acid;2,3,4,5,6-pentahydroxyhexanal;sodium Chemical compound [Na].CC(O)=O.OCC(O)C(O)C(O)C(O)C=O DPXJVFZANSGRMM-UHFFFAOYSA-N 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 210000000577 adipose tissue Anatomy 0.000 description 1
- 150000001338 aliphatic hydrocarbons Chemical class 0.000 description 1
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 1
- 239000003963 antioxidant agent Substances 0.000 description 1
- 230000003078 antioxidant effect Effects 0.000 description 1
- 125000002886 arachidonoyl group Chemical group O=C([*])C([H])([H])C([H])([H])C([H])([H])/C([H])=C([H])\C([H])([H])/C([H])=C([H])\C([H])([H])/C([H])=C([H])\C([H])([H])/C([H])=C([H])\C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- HJJPJSXJAXAIPN-UHFFFAOYSA-N arecholine Natural products COC(=O)C1=CCCN(C)C1 HJJPJSXJAXAIPN-UHFFFAOYSA-N 0.000 description 1
- 125000003118 aryl group Chemical group 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- 235000013361 beverage Nutrition 0.000 description 1
- 230000037396 body weight Effects 0.000 description 1
- 210000004556 brain Anatomy 0.000 description 1
- 235000008429 bread Nutrition 0.000 description 1
- 235000012970 cakes Nutrition 0.000 description 1
- 239000001506 calcium phosphate Substances 0.000 description 1
- 235000011010 calcium phosphates Nutrition 0.000 description 1
- 229910052799 carbon Inorganic materials 0.000 description 1
- 239000001768 carboxy methyl cellulose Substances 0.000 description 1
- 235000010948 carboxy methyl cellulose Nutrition 0.000 description 1
- 229920003123 carboxymethyl cellulose sodium Polymers 0.000 description 1
- 239000008112 carboxymethyl-cellulose Substances 0.000 description 1
- 229940105329 carboxymethylcellulose Drugs 0.000 description 1
- 229940084030 carboxymethylcellulose calcium Drugs 0.000 description 1
- 229940063834 carboxymethylcellulose sodium Drugs 0.000 description 1
- 230000007910 cell fusion Effects 0.000 description 1
- 210000003169 central nervous system Anatomy 0.000 description 1
- 238000005119 centrifugation Methods 0.000 description 1
- 229940106189 ceramide Drugs 0.000 description 1
- ZVEQCJWYRWKARO-UHFFFAOYSA-N ceramide Natural products CCCCCCCCCCCCCCC(O)C(=O)NC(CO)C(O)C=CCCC=C(C)CCCCCCCCC ZVEQCJWYRWKARO-UHFFFAOYSA-N 0.000 description 1
- 229930183167 cerebroside Natural products 0.000 description 1
- RIZIAUKTHDLMQX-UHFFFAOYSA-N cerebroside D Natural products CCCCCCCCCCCCCCCCC(O)C(=O)NC(C(O)C=CCCC=C(C)CCCCCCCCC)COC1OC(CO)C(O)C(O)C1O RIZIAUKTHDLMQX-UHFFFAOYSA-N 0.000 description 1
- 235000015218 chewing gum Nutrition 0.000 description 1
- 229940112822 chewing gum Drugs 0.000 description 1
- 235000012000 cholesterol Nutrition 0.000 description 1
- 230000006835 compression Effects 0.000 description 1
- 238000007906 compression Methods 0.000 description 1
- 239000000470 constituent Substances 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- 229940099112 cornstarch Drugs 0.000 description 1
- 235000013365 dairy product Nutrition 0.000 description 1
- 238000000354 decomposition reaction Methods 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- 235000019425 dextrin Nutrition 0.000 description 1
- 150000001982 diacylglycerols Chemical class 0.000 description 1
- 150000002009 diols Chemical class 0.000 description 1
- 201000010099 disease Diseases 0.000 description 1
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 1
- 239000006185 dispersion Substances 0.000 description 1
- YEKFYCQGYMVFKR-UHFFFAOYSA-N docosa-2,4,6,8,10-pentaenoic acid Chemical class CCCCCCCCCCCC=CC=CC=CC=CC=CC(O)=O YEKFYCQGYMVFKR-UHFFFAOYSA-N 0.000 description 1
- 239000002552 dosage form Substances 0.000 description 1
- 239000008298 dragée Substances 0.000 description 1
- 229940079593 drug Drugs 0.000 description 1
- 239000003937 drug carrier Substances 0.000 description 1
- 239000003995 emulsifying agent Substances 0.000 description 1
- 201000002491 encephalomyelitis Diseases 0.000 description 1
- 229940031098 ethanolamine Drugs 0.000 description 1
- 150000002170 ethers Chemical class 0.000 description 1
- 239000000945 filler Substances 0.000 description 1
- 239000007941 film coated tablet Substances 0.000 description 1
- 239000000796 flavoring agent Substances 0.000 description 1
- 235000019634 flavors Nutrition 0.000 description 1
- 235000011194 food seasoning agent Nutrition 0.000 description 1
- 235000015203 fruit juice Nutrition 0.000 description 1
- 235000011389 fruit/vegetable juice Nutrition 0.000 description 1
- 150000002270 gangliosides Chemical class 0.000 description 1
- 239000008273 gelatin Substances 0.000 description 1
- 229920000159 gelatin Polymers 0.000 description 1
- 239000007903 gelatin capsule Substances 0.000 description 1
- 235000019322 gelatine Nutrition 0.000 description 1
- 235000011852 gelatine desserts Nutrition 0.000 description 1
- 150000002339 glycosphingolipids Chemical class 0.000 description 1
- 210000002149 gonad Anatomy 0.000 description 1
- 235000013402 health food Nutrition 0.000 description 1
- 210000001320 hippocampus Anatomy 0.000 description 1
- 150000002430 hydrocarbons Chemical group 0.000 description 1
- 230000036039 immunity Effects 0.000 description 1
- 239000003701 inert diluent Substances 0.000 description 1
- 230000004054 inflammatory process Effects 0.000 description 1
- CDAISMWEOUEBRE-GPIVLXJGSA-N inositol Chemical group O[C@H]1[C@H](O)[C@@H](O)[C@H](O)[C@H](O)[C@@H]1O CDAISMWEOUEBRE-GPIVLXJGSA-N 0.000 description 1
- 229960000367 inositol Drugs 0.000 description 1
- 230000037427 ion transport Effects 0.000 description 1
- 235000015110 jellies Nutrition 0.000 description 1
- 239000008274 jelly Substances 0.000 description 1
- 239000005453 ketone based solvent Substances 0.000 description 1
- 239000000787 lecithin Substances 0.000 description 1
- 235000010445 lecithin Nutrition 0.000 description 1
- 229940067606 lecithin Drugs 0.000 description 1
- 210000000265 leukocyte Anatomy 0.000 description 1
- 150000002617 leukotrienes Chemical class 0.000 description 1
- 125000003473 lipid group Chemical group 0.000 description 1
- 150000004668 long chain fatty acids Chemical class 0.000 description 1
- 239000000594 mannitol Substances 0.000 description 1
- 235000010355 mannitol Nutrition 0.000 description 1
- 230000000873 masking effect Effects 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 244000005700 microbiome Species 0.000 description 1
- 210000003205 muscle Anatomy 0.000 description 1
- 210000004165 myocardium Anatomy 0.000 description 1
- 229920001206 natural gum Polymers 0.000 description 1
- 230000009707 neogenesis Effects 0.000 description 1
- 230000004770 neurodegeneration Effects 0.000 description 1
- 208000015122 neurodegenerative disease Diseases 0.000 description 1
- 210000004498 neuroglial cell Anatomy 0.000 description 1
- 230000003959 neuroinflammation Effects 0.000 description 1
- VVGIYYKRAMHVLU-UHFFFAOYSA-N newbouldiamide Natural products CCCCCCCCCCCCCCCCCCCC(O)C(O)C(O)C(CO)NC(=O)CCCCCCCCCCCCCCCCC VVGIYYKRAMHVLU-UHFFFAOYSA-N 0.000 description 1
- 235000015097 nutrients Nutrition 0.000 description 1
- 230000036542 oxidative stress Effects 0.000 description 1
- 229940094443 oxytocics prostaglandins Drugs 0.000 description 1
- 235000020636 oyster Nutrition 0.000 description 1
- 238000005192 partition Methods 0.000 description 1
- 230000002688 persistence Effects 0.000 description 1
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 1
- 239000010452 phosphate Substances 0.000 description 1
- 239000006187 pill Substances 0.000 description 1
- 229940093429 polyethylene glycol 6000 Drugs 0.000 description 1
- CASUWPDYGGAUQV-UHFFFAOYSA-M potassium;methanol;hydroxide Chemical compound [OH-].[K+].OC CASUWPDYGGAUQV-UHFFFAOYSA-M 0.000 description 1
- 239000008213 purified water Substances 0.000 description 1
- 229920006395 saturated elastomer Polymers 0.000 description 1
- 229930195734 saturated hydrocarbon Natural products 0.000 description 1
- 235000020637 scallop Nutrition 0.000 description 1
- CDAISMWEOUEBRE-UHFFFAOYSA-N scyllo-inosotol Chemical group OC1C(O)C(O)C(O)C(O)C1O CDAISMWEOUEBRE-UHFFFAOYSA-N 0.000 description 1
- 229960001153 serine Drugs 0.000 description 1
- 210000002027 skeletal muscle Anatomy 0.000 description 1
- 210000003491 skin Anatomy 0.000 description 1
- 235000010413 sodium alginate Nutrition 0.000 description 1
- 239000000661 sodium alginate Substances 0.000 description 1
- 229940005550 sodium alginate Drugs 0.000 description 1
- 229910000029 sodium carbonate Inorganic materials 0.000 description 1
- RYYKJJJTJZKILX-UHFFFAOYSA-M sodium octadecanoate Chemical compound [Na+].CCCCCCCCCCCCCCCCCC([O-])=O RYYKJJJTJZKILX-UHFFFAOYSA-M 0.000 description 1
- 239000001488 sodium phosphate Substances 0.000 description 1
- 239000007901 soft capsule Substances 0.000 description 1
- 150000003408 sphingolipids Chemical class 0.000 description 1
- 229940032147 starch Drugs 0.000 description 1
- 238000003756 stirring Methods 0.000 description 1
- 235000000346 sugar Nutrition 0.000 description 1
- 239000007940 sugar coated tablet Substances 0.000 description 1
- 150000008163 sugars Chemical class 0.000 description 1
- 239000006228 supernatant Substances 0.000 description 1
- 239000013589 supplement Substances 0.000 description 1
- 239000004094 surface-active agent Substances 0.000 description 1
- 150000003509 tertiary alcohols Chemical class 0.000 description 1
- QORWJWZARLRLPR-UHFFFAOYSA-H tricalcium bis(phosphate) Chemical compound [Ca+2].[Ca+2].[Ca+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O QORWJWZARLRLPR-UHFFFAOYSA-H 0.000 description 1
- RYFMWSXOAZQYPI-UHFFFAOYSA-K trisodium phosphate Chemical compound [Na+].[Na+].[Na+].[O-]P([O-])([O-])=O RYFMWSXOAZQYPI-UHFFFAOYSA-K 0.000 description 1
- DCXXMTOCNZCJGO-UHFFFAOYSA-N tristearoylglycerol Chemical compound CCCCCCCCCCCCCCCCCC(=O)OCC(OC(=O)CCCCCCCCCCCCCCCCC)COC(=O)CCCCCCCCCCCCCCCCC DCXXMTOCNZCJGO-UHFFFAOYSA-N 0.000 description 1
- 210000001835 viscera Anatomy 0.000 description 1
- 230000003245 working effect Effects 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/56—Materials from animals other than mammals
- A61K35/618—Molluscs, e.g. fresh-water molluscs, oysters, clams, squids, octopus, cuttlefish, snails or slugs
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic System
- C07F9/02—Phosphorus compounds
- C07F9/06—Phosphorus compounds without P—C bonds
- C07F9/08—Esters of oxyacids of phosphorus
- C07F9/09—Esters of phosphoric acids
- C07F9/10—Phosphatides, e.g. lecithin
- C07F9/103—Extraction or purification by physical or chemical treatment of natural phosphatides; Preparation of compositions containing phosphatides of unknown structure
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23J—PROTEIN COMPOSITIONS FOR FOODSTUFFS; WORKING-UP PROTEINS FOR FOODSTUFFS; PHOSPHATIDE COMPOSITIONS FOR FOODSTUFFS
- A23J1/00—Obtaining protein compositions for foodstuffs; Bulk opening of eggs and separation of yolks from whites
- A23J1/04—Obtaining protein compositions for foodstuffs; Bulk opening of eggs and separation of yolks from whites from fish or other sea animals
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23J—PROTEIN COMPOSITIONS FOR FOODSTUFFS; WORKING-UP PROTEINS FOR FOODSTUFFS; PHOSPHATIDE COMPOSITIONS FOR FOODSTUFFS
- A23J7/00—Phosphatide compositions for foodstuffs, e.g. lecithin
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23L—FOODS, FOODSTUFFS, OR NON-ALCOHOLIC BEVERAGES, NOT COVERED BY SUBCLASSES A21D OR A23B-A23J; THEIR PREPARATION OR TREATMENT, e.g. COOKING, MODIFICATION OF NUTRITIVE QUALITIES, PHYSICAL TREATMENT; PRESERVATION OF FOODS OR FOODSTUFFS, IN GENERAL
- A23L2/00—Non-alcoholic beverages; Dry compositions or concentrates therefor; Their preparation
- A23L2/52—Adding ingredients
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23L—FOODS, FOODSTUFFS, OR NON-ALCOHOLIC BEVERAGES, NOT COVERED BY SUBCLASSES A21D OR A23B-A23J; THEIR PREPARATION OR TREATMENT, e.g. COOKING, MODIFICATION OF NUTRITIVE QUALITIES, PHYSICAL TREATMENT; PRESERVATION OF FOODS OR FOODSTUFFS, IN GENERAL
- A23L33/00—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof
- A23L33/10—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof using additives
- A23L33/115—Fatty acids or derivatives thereof; Fats or oils
- A23L33/12—Fatty acids or derivatives thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/66—Phosphorus compounds
- A61K31/683—Diesters of a phosphorus acid with two hydroxy compounds, e.g. phosphatidylinositols
- A61K31/685—Diesters of a phosphorus acid with two hydroxy compounds, e.g. phosphatidylinositols one of the hydroxy compounds having nitrogen atoms, e.g. phosphatidylserine, lecithin
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic System
- C07F9/02—Phosphorus compounds
- C07F9/06—Phosphorus compounds without P—C bonds
- C07F9/08—Esters of oxyacids of phosphorus
- C07F9/09—Esters of phosphoric acids
- C07F9/091—Esters of phosphoric acids with hydroxyalkyl compounds with further substituents on alkyl
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic System
- C07F9/02—Phosphorus compounds
- C07F9/06—Phosphorus compounds without P—C bonds
- C07F9/08—Esters of oxyacids of phosphorus
- C07F9/09—Esters of phosphoric acids
- C07F9/10—Phosphatides, e.g. lecithin
-
- C—CHEMISTRY; METALLURGY
- C11—ANIMAL OR VEGETABLE OILS, FATS, FATTY SUBSTANCES OR WAXES; FATTY ACIDS THEREFROM; DETERGENTS; CANDLES
- C11B—PRODUCING, e.g. BY PRESSING RAW MATERIALS OR BY EXTRACTION FROM WASTE MATERIALS, REFINING OR PRESERVING FATS, FATTY SUBSTANCES, e.g. LANOLIN, FATTY OILS OR WAXES; ESSENTIAL OILS; PERFUMES
- C11B11/00—Recovery or refining of other fatty substances, e.g. lanolin or waxes
-
- C—CHEMISTRY; METALLURGY
- C11—ANIMAL OR VEGETABLE OILS, FATS, FATTY SUBSTANCES OR WAXES; FATTY ACIDS THEREFROM; DETERGENTS; CANDLES
- C11B—PRODUCING, e.g. BY PRESSING RAW MATERIALS OR BY EXTRACTION FROM WASTE MATERIALS, REFINING OR PRESERVING FATS, FATTY SUBSTANCES, e.g. LANOLIN, FATTY OILS OR WAXES; ESSENTIAL OILS; PERFUMES
- C11B7/00—Separation of mixtures of fats or fatty oils into their constituents, e.g. saturated oils from unsaturated oils
- C11B7/0008—Separation of mixtures of fats or fatty oils into their constituents, e.g. saturated oils from unsaturated oils by differences of solubilities, e.g. by extraction, by separation from a solution by means of anti-solvents
- C11B7/0025—Separation of mixtures of fats or fatty oils into their constituents, e.g. saturated oils from unsaturated oils by differences of solubilities, e.g. by extraction, by separation from a solution by means of anti-solvents in solvents containing oxygen in their molecule
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23V—INDEXING SCHEME RELATING TO FOODS, FOODSTUFFS OR NON-ALCOHOLIC BEVERAGES AND LACTIC OR PROPIONIC ACID BACTERIA USED IN FOODSTUFFS OR FOOD PREPARATION
- A23V2002/00—Food compositions, function of food ingredients or processes for food or foodstuffs
Definitions
- the present invention relates to an ether phospholipid and a method for producing the ether phospholipid. More specifically, ether phospholipids effective for the treatment and improvement of Alzheimer's disease, Parkinson's disease, depression, cranial nerve diseases such as schizophrenia, metabolic syndrome such as diabetes, various infectious diseases and immune disorders, and the ether phospholipids
- the present invention relates to a method for producing a large amount easily.
- a lipid refers to a substance having a long-chain fatty acid or a similar hydrocarbon chain in a molecule and existing in a living body or derived from an organism. These lipids can be classified into simple lipids and complex lipids. Simple lipids are composed of C, H, and O and are generally soluble in acetone. The simple lipid triacylglycerol exists in the animal body as a reservoir of energy in adipose tissue.
- the complex lipid is a lipid group containing P of phosphate, N of base and the like. Therefore, the complex lipid is composed of a hydrophobic portion (fatty acid portion) and a hydrophilic portion (phosphoric acid or base portion), and exhibits amphipathic properties.
- the simple lipid is soluble in acetone, while the complex lipid is insoluble in acetone.
- Such complex lipids are constituents of biological membranes.
- the complex lipid is 1) Glycerophospholipid; phosphatidylcholine (also known as lecithin), phosphatidylethanolamine and the like belong. 2) Sphingophospholipids; sphingomyelin, ceramide serialine and the like belong. 3) Glycosphingolipid; cerebroside, sulfatide, ganglioside and the like belong. And 4) Groseroglycolipids: those obtained by binding various sugars to diacylglycerols present in microorganisms and higher plants. Can be broadly classified. The 2) sphingophospholipid and the 3) sphingoglycolipid are collectively referred to as sphingolipids.
- the glycerophospholipid is a general term for phospholipids having glycerol as a skeleton, and includes phosphatidylcholine, phosphatidylethanolamine, phosphatidylserine, and the like. Many of these glycerophospholipids have an ester bond (acyl bond) with a nonpolar moiety, but some have a vinyl ether bond (alkenyl bond) or an ether bond (alkyl bond) at the 1-position (sn-1) of glycerol. . Those bonded with vinyl ether are also called plasmalogen.
- the glycerophospholipid having a vinyl ether bond and an ether bond is collectively called an ether phospholipid.
- Phospholipids are important as components of biological membranes.
- plasmalogens which are ether phospholipids, account for about 18% of phospholipids in mammalian biological membranes. Especially in cranial nerves, myocardium, skeletal muscle leukocytes and sperm.
- Plasmalogens are bound to many polyunsaturated fatty acids such as docosahexaenoic acid and arachidonic acid. Therefore, it not only serves as a reservoir for secondary messengers of interstitial signals such as prostaglandins and leukotrienes produced from these polyunsaturated fatty acids, but also plays an important role in cell fusion and ion transport. Yes.
- the vinyl ether bond (alkenyl bond) of plasmalogen is particularly sensitive to oxidative stress, and thus also serves as an antioxidant for cells.
- ether phospholipids having an alkyl bond are present in a small amount.
- phosphatidylcholine and phosphatidylethanolamine with alkyl bonds were identified in the hippocampus of rat brain.
- ingested phospholipids having ether bonds (alkyl bonds) are converted into plasmalogens in mammals.
- Non-Patent Document 1 plasmalogen-type glycerophospholipid has been reported to have a cranial nerve cell neogenesis effect as shown in, for example, International Publication No. 2011/083827 (Patent Document 1). Furthermore, as shown in International Publication No. 2012/039472 (Patent Document 2) and Ifuku et al., Journalof Neuroinflammation, 9: 197 (2012) (Non-Patent Document 1), the plasmalogen-type glycerophospholipid is a central nervous system. It has the effect of suppressing the increase of glial cells, which is considered to be one of the causes of inflammation, and improving central nervous system inflammation, and is particularly effective in the prevention and treatment of neurodegenerative diseases such as Alzheimer's disease It has been pointed out.
- Patent Documents 1 to 7 are intended to produce plasmalogen-type glycerophospholipid easily and in large quantities from bird tissues such as chicken epidermis and chicken fillet.
- the production method described in Patent Document 4 is intended to produce plasmalogen-type glycerophospholipid easily and in large quantities from chicken breast meat rather than conventional chicken skin.
- the present invention has been studied for the purpose of providing a method for easily and mass-producing plasmalogen-type glycerophospholipids or ether phospholipids that are extremely excellent in the above effects.
- the invention according to claim 1 of the present invention is An ether phospholipid obtained by extraction from bivalve tissue.
- the invention according to claim 2 of the present invention is The ether phospholipid according to claim 1,
- the ether phospholipid is What is shown by following formula (1) and / or (2) is included, It is characterized by the above-mentioned.
- R 1 is an aliphatic hydrocarbon group having 14 to 18 carbon atoms.
- R 2 is mainly eicosapentaenoic acid, docosahexaenoic acid or arachidonic acid, and preferably these three fatty acids account for 50% or more of the total fatty acids.
- X is mainly ethanolamine or choline, and these preferably occupy 90% or more of the total phospholipid.
- the invention according to claim 3 of the present invention is I.
- Step a. A step of obtaining a glycerophospholipid by extraction treatment with a hydrophobic organic solvent from the de-neutral fat bivalve phospholipid obtained in 1) and c.
- Step b. After phospholipase A1 was allowed to act on the glycerophospholipid obtained in step 1 to decompose the mixed diacylglycerophospholipid, it was purified by solution partitioning (for example, extraction of lipid into hexane and partitioning with acetone or water).
- a method for producing an ether phospholipid derived from bivalve tissue, comprising a step of obtaining an ether phospholipid.
- the invention according to claim 4 of the present invention is in the method for producing a bivalve tissue-derived ether phospholipid according to claim 3,
- the hydrophobic organic solvent is It is characterized by being ether or petroleum ether.
- the invention according to claim 5 of the present invention is in the method for producing a bivalve tissue-derived ether phospholipid according to claim 3 or 4,
- the water-soluble ketone solvent is It is characterized by being acetone.
- the invention according to claim 6 of the present invention is D.
- the phospholipase A1 is allowed to act on the total lipid obtained in step 1 to decompose mixed diacyl phospholipids, and then a step of obtaining purified ether phospholipids by solvent partitioning or the like is included. It is a manufacturing method.
- the invention according to claim 7 of the present invention is A bivalve tissue-derived ether phospholipid obtained by the method for producing a bivalve tissue-derived ether phospholipid according to any one of claims 3 to 6.
- invention according to claim 8 of the present invention is A food or drink comprising the bivalve tissue-derived ether phospholipid according to any one of claims 1, 2, and 7.
- the invention according to claim 9 of the present invention provides A medicinal composition comprising the bivalve tissue-derived ether phospholipid according to claim 1, 2 or 7.
- the ether phospholipid obtained from the bivalve tissue of the present invention is excellent in the treatment and improvement of Alzheimer's disease, Parkinson's disease, depression, cranial nerve diseases such as schizophrenia, metabolic syndrome such as diabetes, various infectious diseases and immune abnormalities. It has a working effect.
- Ether phospholipids having such action and effects can be produced in large quantities from bivalves by simple operations.
- FIG. 1 is an HPLC chart
- FIG. 1 (a) is a HPLC chart of total phospholipids derived from bivalves (clams)
- FIG. 1 (b) is a purified ether phospholipid derived from clams (clams).
- the HPLC chart of is shown.
- Fig. 2 is an HPLC chart
- Fig. 2 (a) is a HPLC chart of total phospholipids derived from bivalves (shijimi)
- Fig. 2 (b) is an ether phospholipid derived from purified bivalves (shijimi).
- the HPLC chart of is shown.
- FIG. 3 is an HPLC chart
- FIG. 3 is an HPLC chart
- FIG. 3 is an HPLC chart
- FIG. 3 (a) is an HPLC chart showing the content of polyunsaturated fatty acids in all fatty acids of ether phospholipids derived from chicken breast
- FIG. 3 (b) is a HPLC chart showing the content of polyunsaturated fatty acids in the total fatty acids of clams-derived ether phospholipids
- Fig. 3 (c) is a polyunsaturated fatty acid in the total fatty acids of etheric phospholipids derived from clams.
- the HPLC chart which shows the content rate of is shown.
- the ether phospholipid of the present invention is obtained by extraction from bivalve tissue.
- the ether phospholipid refers to a glycerophospholipid having a vinyl ether bond (alkenyl bond) or an ether bond (alkyl bond) at the 1-position (sn-1) of the glycerol skeleton.
- the general formula of ether phospholipid is shown below.
- the compound represented by the formula (1) is an alkenyl phospholipid (plasmalogen), and the compound represented by the formula (2) is an alkyl phospholipid.
- R 1 represents an aliphatic hydrocarbon group.
- R 1 is usually an aliphatic hydrocarbon group having 14 to 18 carbon atoms.
- R 2 is an aliphatic hydrocarbon group, and, for example, polyunsaturated fatty acids such as arachidonic acid (ARA), docosahesaenoic acid (DHA), and eicosapentaenoic acid (EPA) are often bonded.
- ARA arachidonic acid
- DHA docosahesaenoic acid
- EPA eicosapentaenoic acid
- X represents a polar group. X is preferably ethanolamine, choline, serine, inositol and the like.
- ethanolamine plasmalogen in which X in the formula is ethanolamine and choline plasmalogen that is choline are main ether phospholipids present in mammals.
- the ingested glycerophospholipid having an ether bond (alkyl bond) is absorbed as it is and used in each tissue, or converted into an alkenyl-linked phospholipid (plasmalogen) in the body.
- bivalve used in the present invention examples include clams, swordfish, clams, scallops and oysters.
- bivalve tissues include viscera, gonads and muscles.
- the method for extracting ether phospholipid from bivalve tissue is not particularly limited as long as the ether phospholipid can be extracted (and purified if necessary).
- Step a A step of further extracting total glycerophospholipid with a hydrophobic organic solvent from the de-neutral fat bivalve phospholipid obtained in Step 1, and concentrating as necessary.
- Step b
- phospholipase A1 is allowed to act on the total glycerophospholipid obtained in step 1, hydrolyzing the mixed diacylglycerophospholipid, solution decomposition (solvent distribution method) is used to remove degradation products (for example, lyso-type phospholipids and free fatty acids)
- solvent distribution method solvent distribution method
- Extraction and purification of ether phospholipids can be performed by a method comprising the steps of:
- the steps c. Is a process for purifying ether phospholipids.
- a purification step may not necessarily be included, but it is more preferable to obtain a purified and concentrated ether phospholipid because it has a more excellent effect.
- Step a In, neutral lipids are removed from the total lipids of bivalve tissues.
- the bivalve tissue it is preferable to mince or pulverize it in advance.
- the water-soluble ketone solvent include acetone and / or methyl ethyl ketone, and preferably acetone is selected.
- there is no particular difficulty in obtaining total lipid and total lipid can be obtained by performing an extraction process according to a conventional method using a solvent such as isopropanol or hexane.
- Step b Is the process a. Is a step of extracting total glycerophospholipids from the de-neutral fat bivalve phospholipids obtained in step 1 with a hydrophobic organic solvent. Ether or petroleum ether is selected as the organic solvent.
- the process c. Is the process b. This is a step of removing diacyl phospholipids by hydrolyzing diacyl glycerophospholipids mixed from the total glycerophospholipids obtained in 1.
- PLA1 phospholipase A1
- This PLA1 specifically hydrolyzes the sn-1 acyl bond of the diacyl phospholipid. Therefore, since sn-1 of ether phospholipid is an ether bond, PLA1 does not act.
- the diacylglycerophospholipid is decomposed into free fatty acid and lysophospholipid. Free fatty acids and lysophospholipids can be removed by taking advantage of their relatively water solubility.
- the PLA1 is not particularly limited in its origin as long as the effect can be obtained.
- PLA1 include PLA1 derived from Aspergillus oryzae. Such PLA1 can be purchased from, for example, Mitsubishi Chemical Foods Corporation.
- the usage-amount of the said PLA1 it can select suitably according to the quantity of the said total glycerophospholipid.
- the amount is 0.15 to 0.45 g, more preferably 0.2 to 0.3 g, based on 1 g of total glycerophospholipid.
- the enzyme reaction with PLA1 can be performed in a buffer, and such a buffer can be appropriately selected according to PLA1 to be used.
- a buffer can be appropriately selected according to PLA1 to be used.
- PLA1 may be added to the total glycerophospholipid after the buffer is added and dissolved.
- the amount of the buffer used is not particularly limited as long as the enzyme reaction can proceed, but is preferably 1 to 30 mL, more preferably 5 to 15 mL, per 1 g of total glycerophospholipid.
- reaction conditions it can choose suitably.
- the reaction is preferably performed at a temperature of 30 to 70 ° C., more preferably at a temperature of 45 to 55 ° C., and even more preferably at a temperature of 50 ° C., preferably for 1 to 5 hours, more preferably 1 to 2 hours.
- the pH at that time is preferably pH 3.5 to 5.5, more preferably pH 4 to 5.
- the enzyme reaction may be stopped by cooling.
- an enzyme deactivation treatment may be performed.
- the deactivation treatment can be performed by raising the temperature to about 70 ° C. after the hydrolysis reaction.
- the process liquid (hydrolysis process liquid) by which the diacyl type
- the enzyme buffer and enzyme protein can be removed by adding, for example, 2 to 3 times the amount of hexane to the hydrolysis treatment liquid, and then collecting the liquid layer.
- ether phospholipids dissolve in hexane, but are poorly soluble in water-soluble ketone solvents such as acetone. Therefore, these solvents and water are appropriately combined for distribution, and further solution distribution is performed with water or aqueous solution.
- solvent partition method lysophospholipid can be removed and ether phospholipid can be purified. That is, neutral lipids other than phospholipids can be removed with a water-soluble ketone solvent such as acetone, and ether phospholipids and lysophospholipids can be separated by aqueous solution partitioning.
- Step d D. (B) extracting the total lipid from bivalve tissue with a nonpolar organic solvent / branched alcohol mixture; Step d.
- the nonpolar organic solvent include saturated aliphatic hydrocarbons, preferably linear saturated hydrocarbons, more preferably hexane.
- the branched alcohol includes a secondary alcohol and a tertiary alcohol, preferably a secondary alcohol, more preferably isopropanol.
- a treatment liquid in which the diacyl phospholipid is decomposed is obtained.
- lipid degradation products free fatty acid, lysophospholipid
- enzyme protein and enzyme buffer
- the bivalve tissue-derived ether phospholipid of the present invention mainly contains ethanolamine phospholipid and choline phospholipid.
- the structure of such lipids can be analyzed and confirmed by high performance liquid chromatography (HPLC) for bivalve tissue-derived ether phospholipids.
- the bivalve tissue-derived ether phospholipid in the present invention is bound to many docosapentaenoic acids (DHA), arachidonic acid (ARA), and eicosapentaenoic acid (EPA) in sn-2. That is, it contains as a residue many one or more selected from the group consisting of docosahexaenoyl group, arachidonoyl group and eicosapentaenoyl group.
- DHA docosapentaenoic acids
- ARA arachidonic acid
- EPA eicosapentaenoic acid
- the bivalve tissue-derived ether phospholipid of the present invention is used to treat Alzheimer's disease, Parkinson's disease, depression, cranial nerve diseases such as schizophrenia, metabolic syndrome such as diabetes, various infectious diseases and immune disorders, and It is extremely effective for improvement.
- the bivalve tissue-derived ether phospholipid of the present invention can be used as a raw material for foods and drinks and as a raw material for pharmaceuticals.
- This ether phospholipid is effective for the treatment and improvement of Alzheimer's disease, Parkinson's disease, depression, cranial nerve diseases such as schizophrenia, metabolic syndrome such as diabetes, various infectious diseases and immune abnormalities. By doing so, these effects can be exhibited.
- bivalve tissue-derived ether phospholipid of the present invention can appropriately adopt various forms of foods and drinks known or developed in the future as described above.
- the form of functional food or food for specified health use can be similarly adopted.
- Examples of various food and drink products include various products such as confectionery (frozen confectionery, jelly, cake, candy, chewing gum, etc.), bread, dairy products such as milk and yogurt. It can also be used in the form of a drink as a solution using a seasoning or sweetener that can be used as a food or drink.
- the functional food or the food for specified health use (including a nutrient) contains the bivalve tissue-derived ether phospholipid of the present invention, as described above, but generally not only in the form of beverages and foods, It is configured to be orally ingested in the form of preparations such as tablets (including sugar-coated tablets and film-coated tablets), powders, granules, capsules (including soft capsules), syrups, and liquids (such as juice).
- such a food can be produced by adding the ether phospholipid to a general health food material such as fruit juice, milk products such as milk and yogurt, and excipients such as lactose and dextrin.
- a general health food material such as fruit juice, milk products such as milk and yogurt, and excipients such as lactose and dextrin.
- excipients such as lactose and dextrin.
- it is not limited to these.
- a supplement form which is an embodiment of a functional food it may be produced according to a known method.
- the ether phospholipid which is an active ingredient, excipient (lactose, sucrose, starch, etc.), disintegrant (starch, calcium carbonate, etc.), binder (starch, gum arabic, carboxymethylcellulose, polyvinylpyrrolidone, hydroxypropyl) (Such as cellulose) or a lubricant (talc, magnesium stearate, polyethylene glycol 6000, etc.) is added and compression molded. Then, if necessary, it can be coated by a known method for the purpose of taste masking, enteric property or persistence.
- excipient lactose, sucrose, starch, etc.
- disintegrant starch, calcium carbonate, etc.
- binder starch, gum arabic, carboxymethylcellulose, polyvinylpyrrolidone, hydroxypropyl
- talc magnesium stearate, polyethylene glycol 6000, etc.
- Such foods also contain the ether phospholipids, so that when taken orally, Alzheimer's disease, Parkinson's disease, depression, schizophrenia and other cranial nerve diseases, diabetes and other metabolic syndrome, various infectious diseases and immunity It works to treat and improve abnormalities.
- the ether phospholipid is easy to use in a mixture with the product to be used, but it should be understood that an effective amount of the ether phospholipid should be contained to achieve the above action.
- the ether phospholipid can be contained in a food or drink, preferably about 0.01 to 80% by mass, more preferably about 0.05 to 20% by mass.
- the intake of the ether phospholipid which is an active ingredient, may be appropriately selected according to the subject's age, weight, constitution, physical condition, form, intake period, and the like.
- the foods and drinks are used for prevention, not only for healthy people but also for people with various diseases, from severe patients to mild patients, especially without limiting to those with metabolic syndrome, Alzheimer's disease, etc. Can do.
- the bivalve tissue-derived ether phospholipid of the present invention can be orally administered to a patient as a drug dissolved or suspended in a diluent mixed with a pharmaceutically acceptable carrier as necessary.
- the pharmaceutical composition comprises suitable additives such as Excipients such as lactose, sucrose, mannitol, corn starch, synthetic or natural gum, crystalline cellulose, Binding agents such as starch, cellulose derivatives, gum arabic, gelatin, polyvinylpyrrolidone, Disintegrants such as carboxymethylcellulose calcium, carboxymethylcellulose sodium, starch, corn starch, sodium alginate, Lubricants such as talc, magnesium stearate, sodium stearate, Tablets, powders (powder), pills, granules, and the like can be obtained by appropriately mixing with fillers or diluents such as calcium carbonate, sodium carbonate, calcium phosphate, and sodium phosphate. Note that a hard or soft gelatin capsule can be used to form a capsule.
- Excipients such as lactose, sucrose, mannitol, corn starch, synthetic or natural gum, crystalline cellulose
- Binding agents such as starch, cellulose derivatives, gum arab
- the pharmaceutical composition is dissolved in a generally used inert diluent such as purified water, and if necessary, this solution is infiltrated, emulsifier, dispersion aid, surfactant, Liquid preparations such as syrups and elixirs can be obtained by appropriately adding sweeteners, flavors, aromatic substances and the like. These preparations can be made by a conventionally known method.
- the dosage when the obtained pharmaceutical composition is administered to a human as a medicine, the dosage is determined by the dosage of the specific compound as an active ingredient.
- the dose depends on the dosage form, the age of the patient, etc., but is in the range of 1 mg to 1,000 mg per day, and preferably 10 mg to 500 mg per day for an adult with a body weight of 50 kg.
- forms such as a feed, a pharmaceutical, and a pharmaceutical composition, also to animals other than a human.
- Example 1 Manufacture of bivalve-derived ether-type glycerophospholipids (1) Extraction of bivalve total lipids To 100 g of bivalve clams, 200 mL of isopropanol and 300 mL of hexane were added, pulverized using a blender, and allowed to stand at room temperature for 1 hour. Thereafter, suction filtration was performed, and the filtrate was transferred to a separatory funnel. To the separatory funnel, 360 mL of water was added and mixed. The upper hexane layer was collected and dried to obtain bivalve total lipids.
- Example 2 Manufacture of bivalve-derived ether phospholipids (1) Separation of de-neutral fat bivalve crushed tissue and extraction of total glycerophospholipid Total glycerophospholipid was obtained by the same method as in Example 1 except that swordfish was used instead of clams as a bivalve.
- Example 4 (Production and analysis of total glycerophospholipids derived from various bivalve tissues) Total glycerophospholipids were obtained from various bivalves by the same method as in Example 1. The obtained total glycerophospholipid was subjected to HPLC analysis under the same conditions as in Example 1. The results are shown in Table 2.
- glycerophospholipid was ethanolamine phospholipid (PE) and about 90% of this PE was plasmalogen (alkenyl PE).
- PE ethanolamine phospholipid
- plasmalogen alkenyl PE
- about 50% of total glycerophospholipids are choline phospholipids (PC) and about 35% of the PC is alkyl PCs.
- PC choline phospholipids
- about 30-55% of the total glycerophospholipid is composed of ether phospholipids.
- Example 5 (Analysis of polyunsaturated fatty acids in total fatty acids of ether phospholipids) The ratio of polyunsaturated fatty acids (EPA, DHA and ARA) in the total fatty acids contained in bivalve-derived ether phospholipids and chicken tissue-derived ether phospholipids was analyzed using HPLC according to the following method. . The results are shown in Tables 4 and 5 and FIG.
- the bivalve-derived ether phospholipid binds a large amount of eicosapentaenoic acid (EPA), docosahexaenoic acid (DHA), and arachidonic acid (ARA) in its sn-2.
- EPA eicosapentaenoic acid
- DHA docosahexaenoic acid
- ARA arachidonic acid
- EPA and DHA are decreased in Alzheimer's disease, Parkinson's disease, depression, cranial nerve diseases such as schizophrenia, metabolic syndrome such as diabetes, various infectious diseases and immune abnormalities, EPA is prostaglandin, DHA is neuro It serves to store protectin.
- the bivalve-derived ether phospholipid contains a large amount of such EPA and DHA, but chicken breast-derived ether phospholipid does not contain EPA at all, and a small amount of DHA is contained. It is.
- the bivalve-derived ether phospholipid of the present invention contains a large amount of eicosapentaenoic acid (EPA), docosahexaenoic acid (DHA), and arachidonic acid (ARA), and therefore has an effect superior to conventional ether phospholipids. Be expected.
- EPA eicosapentaenoic acid
- DHA docosahexaenoic acid
- ARA arachidonic acid
- an ether phospholipid effective in treating and improving various neurological diseases such as Alzheimer's disease, Parkinson's disease, depression, schizophrenia, metabolic syndrome such as diabetes, and various infectious diseases and immune disorders can be easily and Since it can be produced in large quantities, it is widely used in the pharmaceutical industry.
Abstract
【課題】 アルツハイマー病、パーキンソン病、うつ病、統合失調症などの脳神経病、糖尿病などのメタボリックシンドローム、種々の感染症や免疫異常の治療、および改善の効果において、従来品よりも優れたエーテルリン脂質を、容易にかつ大量に製造することを可能とする。 【解決手段】 エーテルリン脂質を、アサリ、シジミなどの二枚貝の組織から抽出処理によって得る。 このエーテルリン脂質は、前記効果において、従来の鳥組織由来のエーテルリン脂質を遥かに凌ぐものである。
Description
この発明は、エーテルリン脂質と、その製造方法に関するものである。
より詳しくは、アルツハイマー病、パーキンソン病、うつ病、統合失調症などの脳神経病、糖尿病などのメタボリックシンドローム、種々の感染症や免疫異常の治療および改善に有効なエーテルリン脂質と、このエーテルリン脂質を容易に、かつ大量に製造する方法に関するものである。
より詳しくは、アルツハイマー病、パーキンソン病、うつ病、統合失調症などの脳神経病、糖尿病などのメタボリックシンドローム、種々の感染症や免疫異常の治療および改善に有効なエーテルリン脂質と、このエーテルリン脂質を容易に、かつ大量に製造する方法に関するものである。
脂質とは、分子中に長鎖脂肪酸又は類似の炭化水素鎖を有し、生体内に存在するか、生物に由来する物質を指す。
この脂質は、単純脂質と複合脂質に分類することができる。
単純脂質は、C、HおよびOより構成され、一般にアセトンに可溶で、単純脂質のトリアシルグリセロールは、動物体では、脂肪組織にエネルギーの貯蔵体として存在する。
この脂質は、単純脂質と複合脂質に分類することができる。
単純脂質は、C、HおよびOより構成され、一般にアセトンに可溶で、単純脂質のトリアシルグリセロールは、動物体では、脂肪組織にエネルギーの貯蔵体として存在する。
一方、複合脂質は、リン酸のPや塩基のNなどを含む脂質群である。
したがって、複合脂質は、疎水性部分(脂肪酸部分)と親水性部分(リン酸や塩基の部分)からなり、両親媒性を示す。
一般的には、前記単純脂質がアセトンに可溶であるのに対し、複合脂質はアセトンに不溶である。
このような複合脂質は、生体膜の構成成分となっている。
したがって、複合脂質は、疎水性部分(脂肪酸部分)と親水性部分(リン酸や塩基の部分)からなり、両親媒性を示す。
一般的には、前記単純脂質がアセトンに可溶であるのに対し、複合脂質はアセトンに不溶である。
このような複合脂質は、生体膜の構成成分となっている。
前記複合脂質は、
1)グリセロリン脂質;ホスファチジルコリン(別名レシチン)、ホスファチジルエタノールアミンなどが属する。
2)スフィンゴリン脂質;スフィンゴミエリン、セラミドシリアチンなどが属する。
3)スフィンゴ糖脂質;セレブロシド、スルファチド、ガングリオシドなどが属する。
および
4)グロセロ糖脂質;微生物や高等植物に存在するジアシルグリセロールに種々の糖が結合したものなどがある。
に大別することができる。
なお、前記2)スフィンゴリン脂質および3)のスフィンゴ糖脂質を総称して、スフィンゴ脂質と呼ばれる。
1)グリセロリン脂質;ホスファチジルコリン(別名レシチン)、ホスファチジルエタノールアミンなどが属する。
2)スフィンゴリン脂質;スフィンゴミエリン、セラミドシリアチンなどが属する。
3)スフィンゴ糖脂質;セレブロシド、スルファチド、ガングリオシドなどが属する。
および
4)グロセロ糖脂質;微生物や高等植物に存在するジアシルグリセロールに種々の糖が結合したものなどがある。
に大別することができる。
なお、前記2)スフィンゴリン脂質および3)のスフィンゴ糖脂質を総称して、スフィンゴ脂質と呼ばれる。
前記グリセロリン脂質は、グリセロールを骨格にもつリン脂質の総称で、ホスファチジルコリン、ホスファチジルエタノールアミン、ホスファチジルセリンなどがある。
このグリセロリン脂質は、非極性部分とエステル結合(アシル結合)しているものが多いが、グリセロールの1位(sn-1)にビニルエーテル結合(アルケニル結合)あるいはエーテル結合(アルキル結合)したものがある。
ビニルエーテル結合したものは、プラズマローゲンとも呼ばれている。
ビニルエーテル結合およびエーテル結合を持つグリセロリン脂質を合わせて、エーテルリン脂質と呼ばれている。
このグリセロリン脂質は、非極性部分とエステル結合(アシル結合)しているものが多いが、グリセロールの1位(sn-1)にビニルエーテル結合(アルケニル結合)あるいはエーテル結合(アルキル結合)したものがある。
ビニルエーテル結合したものは、プラズマローゲンとも呼ばれている。
ビニルエーテル結合およびエーテル結合を持つグリセロリン脂質を合わせて、エーテルリン脂質と呼ばれている。
リン脂質は生体膜の構成成分として重要であるが、なかでもエーテルリン脂質であるプラズマローゲンは、哺乳動物の生体膜のリン脂質の約18%を占めている。
特に、脳神経、心筋、骨格筋 白血球、精子に多い。
プラズマローゲンは、ドコサヘキサエン酸やアラキドン酸などの多価不飽和脂肪酸と多く結合している。
したがって、これらの多価不飽和脂肪酸から産生するプロスタグランヂンやロイコトリエンなどの細胞間シグナルの、2次メッセンジャーの貯留所となっているだけでなく、細胞融合、イオン移送など重要な働きをしている。
さらに、プラズマローゲンのビニルエーテル結合(アルケニル結合)が、特に酸化ストレスに敏感であるため細胞の抗酸化の役目もしている。
哺乳動物においても少量ではあるがアルキル結合を有するエーテルリン脂質が存在する。特にラットの脳の海馬にはアルキル結合を持つホスファチジルコリン、フォスファチジルエタノラミンを確認した。
さらに、摂取されたエーテル結合(アルキル結合)を持つリン脂質は、哺乳動物ではプラズマローゲンに転化されることが知られている。
特に、脳神経、心筋、骨格筋 白血球、精子に多い。
プラズマローゲンは、ドコサヘキサエン酸やアラキドン酸などの多価不飽和脂肪酸と多く結合している。
したがって、これらの多価不飽和脂肪酸から産生するプロスタグランヂンやロイコトリエンなどの細胞間シグナルの、2次メッセンジャーの貯留所となっているだけでなく、細胞融合、イオン移送など重要な働きをしている。
さらに、プラズマローゲンのビニルエーテル結合(アルケニル結合)が、特に酸化ストレスに敏感であるため細胞の抗酸化の役目もしている。
哺乳動物においても少量ではあるがアルキル結合を有するエーテルリン脂質が存在する。特にラットの脳の海馬にはアルキル結合を持つホスファチジルコリン、フォスファチジルエタノラミンを確認した。
さらに、摂取されたエーテル結合(アルキル結合)を持つリン脂質は、哺乳動物ではプラズマローゲンに転化されることが知られている。
最近、プラズマローゲン型グリセロリン脂質は、例えば、国際公開第2011/083827号(特許文献1)に示されるように、脳神経細胞新生効果を有することが報告されている。
さらに、国際公開第2012/039472号(特許文献2)や、Ifukuら,Journalof Neuroinflammagtion,9:197(2012)(非特許文献1)に示されるように、プラズマローゲン型グリセロリン脂質は、中枢神経系炎症を引き起こす原因の一つと考えられているグリア細胞の増加を抑制し、中枢神経系炎症を改善する効果を有し、特にアルツハイマー病などの神経変性疾患の予防および治療に効果的であることが指摘されている。
さらに、国際公開第2012/039472号(特許文献2)や、Ifukuら,Journalof Neuroinflammagtion,9:197(2012)(非特許文献1)に示されるように、プラズマローゲン型グリセロリン脂質は、中枢神経系炎症を引き起こす原因の一つと考えられているグリア細胞の増加を抑制し、中枢神経系炎症を改善する効果を有し、特にアルツハイマー病などの神経変性疾患の予防および治療に効果的であることが指摘されている。
さらに、このようなプラズマローゲン型グリセロリン脂質は、例えば、特許文献1~7に示されるように、ニワトリ表皮、鶏ムネ肉などの鳥組織から容易にかつ大量に得られることが報告されている。
Ifuku ら,Journal of Neuroinflammagtion, 9: 197 (2012)
前記特許文献1~7に記載されている製造方法は、ニワトリ表皮、鶏ムネ肉などの鳥組織から、プラズマローゲン型グリセロリン脂質を容易かつ大量に製造するものである。
特に、特許文献4に記載されている製造方法は、鶏ムネ肉から、従来の鶏皮よりも、プラズマローゲン型グリセロリン脂質を、容易かつ大量に製造するものである。
特に、特許文献4に記載されている製造方法は、鶏ムネ肉から、従来の鶏皮よりも、プラズマローゲン型グリセロリン脂質を、容易かつ大量に製造するものである。
このように、アルツハイマー病、パーキンソン病、うつ病、統合失調症などの脳神経病、糖尿病などのメタボリックシンドロームや、種々の感染症や免疫異常の治療および改善の効果において、従来品よりも優れたプラズマローゲン型グリセロリン脂質ないしエーテルリン脂質を、容易にかつ大量に製造できる方法が求められている。
この発明はかかる現状に鑑み、前記効果に極めて優れたプラズマローゲン型グリセロリン脂質ないしエーテルリン脂質を、容易かつ大量に製造する方法を提供することを目的として検討を行なった。
その結果、二枚貝組織から、好ましくは特定の工程を施すことによって得られるエーテルリン脂質が、前記効果において、従来の鳥組織由来のプラズマローゲン型グリセロリン脂質を遥かに凌ぐものであることを見出して、この発明を完成させたものである。
すなわち、この発明の請求項1に記載の発明は、
二枚貝組織から抽出処理によって得られること
を特徴とするエーテルリン脂質である。
二枚貝組織から抽出処理によって得られること
を特徴とするエーテルリン脂質である。
この発明の請求項2に記載の発明は、
請求項1に記載のエーテルリン脂質において、
前記エーテルリン脂質は、
下記式(1)及び/又は(2)で示されるものを含むこと
を特徴とするものである。
請求項1に記載のエーテルリン脂質において、
前記エーテルリン脂質は、
下記式(1)及び/又は(2)で示されるものを含むこと
を特徴とするものである。
但し、前記式において、
R1は炭素数14~18の脂肪族炭化水素基である。
R2は、主としてエイコサペンタエン酸、ドコサヘキサエン酸又はアラキドン酸であり、好ましくはこれらの3種の脂肪酸が全脂肪酸の50%以上を占める。
Xは、主としてエタノールアミン又はコリンであり、好ましくはこれらが合計して全リン脂質の90%以上を占める。
R1は炭素数14~18の脂肪族炭化水素基である。
R2は、主としてエイコサペンタエン酸、ドコサヘキサエン酸又はアラキドン酸であり、好ましくはこれらの3種の脂肪酸が全脂肪酸の50%以上を占める。
Xは、主としてエタノールアミン又はコリンであり、好ましくはこれらが合計して全リン脂質の90%以上を占める。
この発明の請求項3に記載の発明は、
イ.二枚貝組織の総脂質を水溶性ケトン系溶媒で処理して脱中性脂肪二枚貝リン脂質を得る工程
ロ.前記工程イ.で得られた脱中性脂肪二枚貝リン脂質から疎水性有機溶媒で抽出処理してグリセロリン脂質を得る工程
ならびに
ハ.前記工程ロ.で得られたグリセロリン脂質にホスホリパーゼA1を作用させて、混在するジアシルグリセロリン脂質を分解した後、溶液分配(例えば、脂質をヘキサンに抽出して、アセトンや水による分配法)などにより、精製されたエーテルリン脂質を得る工程
を含むこと
を特徴とする二枚貝組織由来エーテルリン脂質の製造方法である。
イ.二枚貝組織の総脂質を水溶性ケトン系溶媒で処理して脱中性脂肪二枚貝リン脂質を得る工程
ロ.前記工程イ.で得られた脱中性脂肪二枚貝リン脂質から疎水性有機溶媒で抽出処理してグリセロリン脂質を得る工程
ならびに
ハ.前記工程ロ.で得られたグリセロリン脂質にホスホリパーゼA1を作用させて、混在するジアシルグリセロリン脂質を分解した後、溶液分配(例えば、脂質をヘキサンに抽出して、アセトンや水による分配法)などにより、精製されたエーテルリン脂質を得る工程
を含むこと
を特徴とする二枚貝組織由来エーテルリン脂質の製造方法である。
この発明の請求項4に記載の発明は、
請求項3に記載の二枚貝組織由来エーテルリン脂質の製造方法において、
前記疎水性有機溶媒は、
エーテル又は石油エーテルであること
を特徴とするものである。
請求項3に記載の二枚貝組織由来エーテルリン脂質の製造方法において、
前記疎水性有機溶媒は、
エーテル又は石油エーテルであること
を特徴とするものである。
この発明の請求項5に記載の発明は、
請求項3又は4に記載の二枚貝組織由来エーテルリン脂質の製造方法において、
前記水溶性ケトン系溶媒は、
アセトンであること
を特徴とするものである。
請求項3又は4に記載の二枚貝組織由来エーテルリン脂質の製造方法において、
前記水溶性ケトン系溶媒は、
アセトンであること
を特徴とするものである。
この発明の請求項6に記載の発明は、
ニ.二枚貝組織から、その総脂質を非極性有機溶媒・分岐アルコール混合液で抽出する工程
ならびに
ホ.前記工程ニ.で得られた総脂質にホスホリパーゼA1を作用させて、混在するジアシルリン脂質を分解した後、溶媒分配などにより、精製されたエーテルリン脂質を得る工程
を含むこと
を特徴とする二枚貝組織由来エーテルリン脂質の製造方法である。
ニ.二枚貝組織から、その総脂質を非極性有機溶媒・分岐アルコール混合液で抽出する工程
ならびに
ホ.前記工程ニ.で得られた総脂質にホスホリパーゼA1を作用させて、混在するジアシルリン脂質を分解した後、溶媒分配などにより、精製されたエーテルリン脂質を得る工程
を含むこと
を特徴とする二枚貝組織由来エーテルリン脂質の製造方法である。
この発明の請求項7に記載の発明は、
請求項3~6のいずれかに記載の二枚貝組織由来エーテルリン脂質の製造方法で得られたこと
を特徴とする二枚貝組織由来エーテルリン脂質である。
請求項3~6のいずれかに記載の二枚貝組織由来エーテルリン脂質の製造方法で得られたこと
を特徴とする二枚貝組織由来エーテルリン脂質である。
さらに、この発明の請求項8に記載の発明は、
請求項1、2又は7のいずれかに記載の二枚貝組織由来エーテルリン脂質を含むこと
を特徴とする飲食品である。
請求項1、2又は7のいずれかに記載の二枚貝組織由来エーテルリン脂質を含むこと
を特徴とする飲食品である。
さらにまた、この発明の請求項9に記載の発明は、
請求項1、2又は7にいずれかに記載の二枚貝組織由来エーテルリン脂質を含むこと
を特徴とする医薬用組成物である。
請求項1、2又は7にいずれかに記載の二枚貝組織由来エーテルリン脂質を含むこと
を特徴とする医薬用組成物である。
この発明の二枚貝組織から得られるエーテルリン脂質は、アルツハイマー病、パーキンソン病、うつ病、統合失調症などの脳神経病、糖尿病などのメタボリックシンドローム、種々の感染症や免疫異常の治療および改善に極めて優れ作用効果を有するものである。
かかる作用効果を有するエーテルリン脂質は、二枚貝から簡単な操作で、大量に製造することができる。
以下、この発明にかかるエーテルリン脂質およびその製造方法の実施の形態について、説明する。
なお、この発明について、好ましい代表的な例を中心に説明するが、この発明はこのような代表例に限定されるものではない。
なお、この発明について、好ましい代表的な例を中心に説明するが、この発明はこのような代表例に限定されるものではない。
この発明のエーテルリン脂質は、二枚貝組織から抽出処理によって得られるものである。
ここで、エーテルリン脂質とは、グリセロール骨格の1位(sn-1)に、ビニルエーテル結合(アルケニル結合)あるいはエーテル結合(アルキル結合)をもつグリセロリン脂質をいう。
以下に、エーテルリン脂質の一般式を示す。式(1)で示される化合物がアルケニルリン脂質(プラズマローゲン)であり、式(2)で示される化合物がアルキルリン脂質である。
以下に、エーテルリン脂質の一般式を示す。式(1)で示される化合物がアルケニルリン脂質(プラズマローゲン)であり、式(2)で示される化合物がアルキルリン脂質である。
前記式中、R1 は脂肪族炭化水素基を示す。
R1 は通常、炭素数14~18の脂肪族炭化水素基である。
R2 は脂肪族炭化水素基で、例えば、アラキドン酸(ARA)、ドコサヘサエン酸(DHA)、エイコサペンタエン酸(EPA)などの多価不飽和脂肪酸が結合している場合が多い。
さらに、式中、Xは極性基を示す。
Xは、好ましくはエタノールアミン、コリン、セリン、イノシトールなどである。
R1 は通常、炭素数14~18の脂肪族炭化水素基である。
R2 は脂肪族炭化水素基で、例えば、アラキドン酸(ARA)、ドコサヘサエン酸(DHA)、エイコサペンタエン酸(EPA)などの多価不飽和脂肪酸が結合している場合が多い。
さらに、式中、Xは極性基を示す。
Xは、好ましくはエタノールアミン、コリン、セリン、イノシトールなどである。
特に、前記式中Xが、エタノールアミンであるエタノールアミンプラズマローゲンと、コリンであるコリンプラズマローゲンは、哺乳動物に存在するエーテルリン脂質として主要である。
摂取されたエーテル結合(アルキル結合)をもつグリセロリン脂質は、そのまま吸収されて各組織で利用されるか、体内でアルケニル結合型リン脂質(プラズマローゲン)に転化する。
摂取されたエーテル結合(アルキル結合)をもつグリセロリン脂質は、そのまま吸収されて各組織で利用されるか、体内でアルケニル結合型リン脂質(プラズマローゲン)に転化する。
この発明において使用する二枚貝としては、例えば、アサリ、シジミ、ハマグリ、ホタテ、カキなどである。
二枚貝の組織としては、例えば、内臓、性腺、筋肉などが挙げられる。
二枚貝の組織としては、例えば、内臓、性腺、筋肉などが挙げられる。
この発明において、二枚貝組織からエーテルリン脂質を抽出する方法としては、エーテルリン脂質が抽出(および必要に応じて精製)できる限り、特に制限されない。
好ましくは、
イ.二枚貝組織の総脂質を水溶性ケトン系溶媒で処理して、中性脂質を除いて脱中性脂肪二枚貝リン脂質を得る工程、
ロ.前記工程イ.で得られた脱中性脂肪二枚貝リン脂質から、総グリセロリン脂質を疎水性有機溶媒でさらに抽出し、必要により濃縮する工程、
ならびに
ハ.前記工程ロ.で得られた総グリセロリン脂質に、ホスホリパーゼA1を作用させ、混在するジアシルグリセロリン脂質を加水分解したのち、溶液分配(溶媒分配法)によって、分解産物(例えば、リゾ型リン脂質や遊離脂肪酸)を除去する工程
を含む方法で、エーテルリン脂質の抽出および精製を行うことができる。
イ.二枚貝組織の総脂質を水溶性ケトン系溶媒で処理して、中性脂質を除いて脱中性脂肪二枚貝リン脂質を得る工程、
ロ.前記工程イ.で得られた脱中性脂肪二枚貝リン脂質から、総グリセロリン脂質を疎水性有機溶媒でさらに抽出し、必要により濃縮する工程、
ならびに
ハ.前記工程ロ.で得られた総グリセロリン脂質に、ホスホリパーゼA1を作用させ、混在するジアシルグリセロリン脂質を加水分解したのち、溶液分配(溶媒分配法)によって、分解産物(例えば、リゾ型リン脂質や遊離脂肪酸)を除去する工程
を含む方法で、エーテルリン脂質の抽出および精製を行うことができる。
なお、前記方法において、前記工程ハ.は、エーテルリン脂質の精製工程である。
このような精製工程は必ずしも含まれてなくてもよいが、精製濃縮されたエーテルリン脂質を得ることが、より優れた効果を有するものとなるため、より好ましい。
このような精製工程は必ずしも含まれてなくてもよいが、精製濃縮されたエーテルリン脂質を得ることが、より優れた効果を有するものとなるため、より好ましい。
前記工程イ.においては、二枚貝組織の総脂質から中性脂質を除去する。
前記二枚貝組織を用いる際には、予めミンチ化や、粉砕をしておくことが好ましい。
前記水溶性ケトン系溶剤としては、例えば、アセトンおよび/またはメチルエチルケトンが挙げられ、好ましくはアセトンが選択される。
なお、総脂質を得ることには特に困難はなく、イソプロパノール、ヘキサンなどの溶剤を用いて常法に従って抽出処理を行うことによって総脂質を得ることができる。
前記二枚貝組織を用いる際には、予めミンチ化や、粉砕をしておくことが好ましい。
前記水溶性ケトン系溶剤としては、例えば、アセトンおよび/またはメチルエチルケトンが挙げられ、好ましくはアセトンが選択される。
なお、総脂質を得ることには特に困難はなく、イソプロパノール、ヘキサンなどの溶剤を用いて常法に従って抽出処理を行うことによって総脂質を得ることができる。
前記工程ロ.は、前記工程イ.で得られた脱中性脂肪二枚貝リン脂質から疎水性有機溶媒で、総グリセロリン脂質を抽出する工程である。
前記有機溶媒として、エーテルまたは石油エーテルが選択される。
前記有機溶媒として、エーテルまたは石油エーテルが選択される。
前記工程ハ.は、前記工程ロ.で得られた総グリセロリン脂質から混在するジアシル型グリセロリン脂質を加水分解することで、ジアシル型リン脂質を除く工程である。
前記加水分解には、ホスホリパーゼA1(PLA1)が使用される。
このPLA1は、ジアシル型リン脂質のsn-1のアシル結合を、特異的に加水分解する。
したがって、エーテルリン脂質のsn-1はエーテル結合であるので、PLA1は作用しない。
このPLA1は、ジアシル型リン脂質のsn-1のアシル結合を、特異的に加水分解する。
したがって、エーテルリン脂質のsn-1はエーテル結合であるので、PLA1は作用しない。
PLA1処理によって、ジアシルグリセロリン脂質は、遊離脂肪酸とリゾリン脂質に分解される。
遊離脂肪酸とリゾリン脂質は、比較的水溶性であることなどを利用して除去することができる。
遊離脂肪酸とリゾリン脂質は、比較的水溶性であることなどを利用して除去することができる。
前記PLA1については、前記効果が得られるものであれば、その由来などは特に制限されない。
前記PLA1として、例えば、アスペルギルス・オリゼ由来のPLA1が挙げられる。
かかるPLA1は、例えば、三菱化学フーズ株式会社などから購入可能である。
前記PLA1として、例えば、アスペルギルス・オリゼ由来のPLA1が挙げられる。
かかるPLA1は、例えば、三菱化学フーズ株式会社などから購入可能である。
前記PLA1の使用量については、前記総グリセロリン脂質の量に応じて適宜選択され得る。
好ましくは、総グリセロリン脂質1gに対して、0.15~0.45g、より好ましくは0.2~0.3gである。
好ましくは、総グリセロリン脂質1gに対して、0.15~0.45g、より好ましくは0.2~0.3gである。
前記PLA1による酵素反応を、バッファー中で行うことができるが、このようなバッファーは、使用するPLA1に応じて適宜選択され得る。
例えば、0.1Mクエン酸-HClバッファー(pH4.5)を用いることができる。
この場合、総グリセロリン脂質に前記バッファーを加えて溶解させてから、これにPLA1を加えればよい。
前記バッファーの使用量については、酵素反応が進行し得るものであればよく、特に制限はないが、好ましくは総グリセロリン脂質1g当たり1~30mL、より好ましくは5~15mLである。
例えば、0.1Mクエン酸-HClバッファー(pH4.5)を用いることができる。
この場合、総グリセロリン脂質に前記バッファーを加えて溶解させてから、これにPLA1を加えればよい。
前記バッファーの使用量については、酵素反応が進行し得るものであればよく、特に制限はないが、好ましくは総グリセロリン脂質1g当たり1~30mL、より好ましくは5~15mLである。
反応条件については、適宜選択できる。
好ましくは温度30~70℃、より好ましくは温度45~55℃、さらに好ましくは温度50℃で撹拌しながら、好ましくは1~5時間、より好ましくは1~2時間反応させる。
その際のpHは、好ましくはpH3.5~5.5、より好ましくはpH4~5である。
好ましくは温度30~70℃、より好ましくは温度45~55℃、さらに好ましくは温度50℃で撹拌しながら、好ましくは1~5時間、より好ましくは1~2時間反応させる。
その際のpHは、好ましくはpH3.5~5.5、より好ましくはpH4~5である。
なお、酵素反応を、冷却により止めてもよい。
さらに、酵素の失活処理を行ってもよい。
例えば、前記失活処理は、加水分解反応後、温度を70℃程度まで上昇させることによって行うことができる。
さらに、酵素の失活処理を行ってもよい。
例えば、前記失活処理は、加水分解反応後、温度を70℃程度まで上昇させることによって行うことができる。
このようにして、ジアシル型グリセロリン脂質が分解された処理液(加水分解処理液)を得ることができる。
この加水分解処理液に、例えば、2~3倍量のヘキサンを加え、その後、液層を回収することで、酵素バッファーおよび酵素タンパク質を除去することができる。
この加水分解処理液に、例えば、2~3倍量のヘキサンを加え、その後、液層を回収することで、酵素バッファーおよび酵素タンパク質を除去することができる。
さらに、エーテルリン脂質は、ヘキサンに溶解するが、アセトンなどの水溶性ケトン系溶剤には難溶性であることから、これらの溶媒および水を適宜組み合わせて分配を行い、さらに水又は水溶液により溶液分配すること(溶媒分配法)で、リゾリン脂質を除去してエーテルリン脂質を精製することができる。
すなわち、アセトンなどの水溶性ケトン系溶媒によりリン脂質以外の中性脂質を除去でき、水系溶液分配によりエーテルリン脂質とリゾリン脂質を分離できる。
すなわち、アセトンなどの水溶性ケトン系溶媒によりリン脂質以外の中性脂質を除去でき、水系溶液分配によりエーテルリン脂質とリゾリン脂質を分離できる。
この発明において、
ニ.二枚貝組織から、その総脂質を非極性有機溶媒・分岐アルコール混合液で抽出する工程
ならびに
ホ.前記工程ニ.で得られた総脂質にホスホリパーゼA1を作用させて、混在するジアシルリン脂質を分解した後、溶媒分配などにより、精製されたエーテルリン脂質をうる工程
を含む方法でも、エーテルリン脂質の抽出および精製を行うことができる。
この発明では、簡便であることから、このような方法を採用することが、より好ましい。
前記非極性有機溶媒としては、飽和脂肪族炭化水素類が挙げられ、好ましくは直鎖状の飽和炭化水素、より好ましくはヘキサンが選択される。
前記分岐アルコールには、二級アルコールおよび三級アルコールが含まれ、好ましくは二級アルコール、より好ましくはイソプロパノールが選択される。
この場合において、この方法の前記工程ホ.で、ジアシルリン脂質が分解された処理液が得られる。例えば、この加水分解処理液に、5~10倍溶のヘキサン・イソプロパノール混合液(3:2)を加えて分液ロートに移し、その約3分の2の水を加えて、2層に分け、上層(ヘキサン層)を回収することで、脂質分解産物(遊離脂肪酸、リゾリン脂質)、酵素タンパク質、酵素バッファーを除去できる。
なお、この方法については、前述のエーテルリン脂質の抽出および精製方法を参考にして容易に実施することができる。
ニ.二枚貝組織から、その総脂質を非極性有機溶媒・分岐アルコール混合液で抽出する工程
ならびに
ホ.前記工程ニ.で得られた総脂質にホスホリパーゼA1を作用させて、混在するジアシルリン脂質を分解した後、溶媒分配などにより、精製されたエーテルリン脂質をうる工程
を含む方法でも、エーテルリン脂質の抽出および精製を行うことができる。
この発明では、簡便であることから、このような方法を採用することが、より好ましい。
前記非極性有機溶媒としては、飽和脂肪族炭化水素類が挙げられ、好ましくは直鎖状の飽和炭化水素、より好ましくはヘキサンが選択される。
前記分岐アルコールには、二級アルコールおよび三級アルコールが含まれ、好ましくは二級アルコール、より好ましくはイソプロパノールが選択される。
この場合において、この方法の前記工程ホ.で、ジアシルリン脂質が分解された処理液が得られる。例えば、この加水分解処理液に、5~10倍溶のヘキサン・イソプロパノール混合液(3:2)を加えて分液ロートに移し、その約3分の2の水を加えて、2層に分け、上層(ヘキサン層)を回収することで、脂質分解産物(遊離脂肪酸、リゾリン脂質)、酵素タンパク質、酵素バッファーを除去できる。
なお、この方法については、前述のエーテルリン脂質の抽出および精製方法を参考にして容易に実施することができる。
この発明の二枚貝組織由来エーテルリン脂質は、主にエタノールアミンリン脂質とコリンリン脂質を含むものである。
このような脂質の構成は、二枚貝組織由来エーテルリン脂質を、高速液体クロマトグラフィー(HPLC)で解析・確認することができる。
このような脂質の構成は、二枚貝組織由来エーテルリン脂質を、高速液体クロマトグラフィー(HPLC)で解析・確認することができる。
この発明における二枚貝組織由来エーテルリン脂質は、そのsn-2において、多くのドコサペンタエン酸(DHA)や、アラキドン酸(ARA)、エイコサペンタエン酸(EPA)と結合している。
すなわち、ドコサヘキサエノイル基、アラキドノイル基およびエイコサペンタエノイル基からなる群から選択される1種以上を残基として多く含む。
すなわち、ドコサヘキサエノイル基、アラキドノイル基およびエイコサペンタエノイル基からなる群から選択される1種以上を残基として多く含む。
このような構成によって、この発明の二枚貝組織由来エーテルリン脂質は、アルツハイマー病、パーキンソン病、うつ病、統合失調症などの脳神経病、糖尿病などのメタボリックシンドローム、種々の感染症や免疫異常の治療および改善にきわめて有効である。
この発明の二枚貝組織由来エーテルリン脂質は、飲食品の素材として、医薬の原料として、利用することができるものである。
このエーテルリン脂質は、アルツハイマー病、パーキンソン病、うつ病、統合失調症などの脳神経病、糖尿病などのメタボリックシンドローム、種々の感染症や免疫異常の治療および改善に有効であるので、生体内に摂取されることによって、これらの効果が発揮され得る。
このエーテルリン脂質は、アルツハイマー病、パーキンソン病、うつ病、統合失調症などの脳神経病、糖尿病などのメタボリックシンドローム、種々の感染症や免疫異常の治療および改善に有効であるので、生体内に摂取されることによって、これらの効果が発揮され得る。
さらに、この発明の二枚貝組織由来エーテルリン脂質は、前述の如く公知の、又は将来開発される様々な飲食品の形態を適宜採用することができる。
この場合において、機能性食品又は特定保健用食品の形態についても、同様に採用することができる。
この場合において、機能性食品又は特定保健用食品の形態についても、同様に採用することができる。
様々な飲食品の製品の形態として、例えば、菓子(冷菓、ゼリー、ケーキ、キャンディー、チューインガムなど)、パン、牛乳やヨーグルトなどの乳製品などの各種製品を挙げることができる。
飲食品として使用できる調味剤や甘味剤を使用し、溶液としてドリンクの形態で使用することもできる。
飲食品として使用できる調味剤や甘味剤を使用し、溶液としてドリンクの形態で使用することもできる。
前記機能性食品又は特定保健用食品(栄養剤を含む)は、前記同様、この発明の二枚貝組織由来エーテルリン脂質を含有するものであるが、一般に飲料品や、食料品の形態のみならず、錠剤(糖衣錠、フィルムコーティング錠を含む)、散剤、顆粒剤、カプセル剤(ソフトカプセルを含む)、シロップ剤、液剤(ジュースなど)などの製剤の形態で経口摂取できるように構成される。
例えば、このような食品は、前記エーテルリン脂質を果汁、牛乳やヨーグルトなどの乳製品、乳糖やデキストリンなどの賦形剤などの、一般的な健康食品用の素材に添加することによって製造され得るが、これらに限定されるものではない。
機能性食品の一態様であるサプリメントの形態を選択する場合であっても、公知の方法に従って製造すればよい。
機能性食品の一態様であるサプリメントの形態を選択する場合であっても、公知の方法に従って製造すればよい。
例えば、有効成分である前記エーテルリン脂質に、賦形剤(乳糖、白糖、デンプンなど)、崩壊剤(デンプン、炭酸カルシウムなど)、結合剤(デンプン、アラビアゴム、カルボキシメチルセルロース、ポリビニルピロリドン、ヒドロキシプロピルセルロースなど)又は滑沢剤(タルク、ステアリン酸マグネシウム、ポリエチレングリコール 6000など)などを添加して圧縮成形する。
ついで、必要によって、味のマスキング、腸溶性あるいは持続性の目的のため、公知の方法でコーティングすることができる。
ついで、必要によって、味のマスキング、腸溶性あるいは持続性の目的のため、公知の方法でコーティングすることができる。
このような食品もまた、前記エーテルリン脂質を含有するので、経口摂取した時に、アルツハイマー病、パーキンソン病、うつ病、統合失調症などの脳神経病、糖尿病などのメタボリックシンドローム、種々の感染症や免疫異常の治療および改善の作用を発揮する。
なお、前記エーテルリン脂質は、使用される製品に混合して使用することが簡便であるが、前記作用を奏するに有効な量のエーテルリン脂質を含有すべきことは当然のことである。
例えば、前記エーテルリン脂質を、飲食品に、好ましくは0.01~80質量%程度、より好ましくは0.05~20質量%程度含有することができる。
例えば、前記エーテルリン脂質を、飲食品に、好ましくは0.01~80質量%程度、より好ましくは0.05~20質量%程度含有することができる。
飲食品に関し、有効成分である前記エーテルリン脂質の摂取量については、被検者の年齢、体重、体質、体調、形態、摂取期間などに応じて適宜選択すればよい。
前記飲食品は、予防用として、健常者は勿論、各種の疾患を有する者で、重症患者から軽症の患者まで、特にメタボリックシンドロームや、アルツハイマー病などの疾患者に限定することなく、使用することができる。
この発明の二枚貝組織由来エーテルリン脂質は、必要に応じて薬剤的に許容できる担体と配合し、希釈剤に溶解もしくは懸濁した薬剤として、経口的に患者に投与できる。
この発明において、医薬用組成物は、適当な添加剤、例えば、
乳糖、ショ糖、マンニット、トウモロコシデンプン、合成もしくは天然ガム、結晶セルロースなどの賦形剤、
デンプン、セルロース誘導体、アラビアゴム、ゼラチン、ポリビニルピロリドンなどの結合剤、
カルボシキメチルセルロースカルシウム、カルボシキメチルセルロースナトリウム、デンプン、コーンスターチ、アルギン酸ナトリウムなどの崩壊剤、
タルク、ステアリン酸マグネシウム、ステアリン酸ナトリウムなどの滑沢剤、
炭酸カルシウム、炭酸ナトリウム、リン酸カルシウム、リン酸ナトリウムなどの充填剤又は希釈剤
などと、適宜混合し、錠剤、散剤(粉末)、丸剤及び顆粒剤などとすることができる。
なお、硬質又は軟質のゼラチンカプセルなどを用い、カプセル剤とすることもできる。
乳糖、ショ糖、マンニット、トウモロコシデンプン、合成もしくは天然ガム、結晶セルロースなどの賦形剤、
デンプン、セルロース誘導体、アラビアゴム、ゼラチン、ポリビニルピロリドンなどの結合剤、
カルボシキメチルセルロースカルシウム、カルボシキメチルセルロースナトリウム、デンプン、コーンスターチ、アルギン酸ナトリウムなどの崩壊剤、
タルク、ステアリン酸マグネシウム、ステアリン酸ナトリウムなどの滑沢剤、
炭酸カルシウム、炭酸ナトリウム、リン酸カルシウム、リン酸ナトリウムなどの充填剤又は希釈剤
などと、適宜混合し、錠剤、散剤(粉末)、丸剤及び顆粒剤などとすることができる。
なお、硬質又は軟質のゼラチンカプセルなどを用い、カプセル剤とすることもできる。
さらに、この発明において、医薬用組成物は、精製水などの一般的に用いられる不活性希釈剤に溶解させ、必要に応じて、この溶液に浸潤剤、乳化剤、分散助剤、界面活性剤、甘味料、フレーバー、芳香物質などを適宜添加することによって、シロップ剤、エリキシル剤などの液状製剤とすることもできる。
なお、これらの製剤化は、従来公知の方法で可能である。
なお、これらの製剤化は、従来公知の方法で可能である。
この発明において、得られた医薬用組成物を、医薬としてヒトに投与する場合における投与量は、有効成分である特定化合物の投与量により定められる。
その投与量は、剤型や患者の年齢などに依存するが、一日当たり1mg~1,000mgの範囲内であって、体重50kgの成人に対する投与量では、一日当たり10mg~500mgが好ましい。
その投与量は、剤型や患者の年齢などに依存するが、一日当たり1mg~1,000mgの範囲内であって、体重50kgの成人に対する投与量では、一日当たり10mg~500mgが好ましい。
なお、ヒト以外の動物に対しても、飼料、医薬品および医薬用組成物などの形態で適用することができる。
以下に、実施例を挙げて、この発明のエーテルリン脂質およびその製造方法を詳細に説明するが、この発明は、これら実施例により制限されることはない。
<実施例1>
(二枚貝由来エーテル型グリセロリン脂質の製造)
(1)二枚貝総脂質の抽出
二枚貝アサリ100gにイソプロパノール200mL、ヘキサン300mLを加えて、ブレンダーを用いて粉砕し、室温で1時間静置した。
その後、吸引ろ過し、ろ液を分液ロートに移した。
分液ロートに水360mLを加えて混和した。
上層のヘキサン層を回収、乾固して二枚貝総脂質を得た。
(二枚貝由来エーテル型グリセロリン脂質の製造)
(1)二枚貝総脂質の抽出
二枚貝アサリ100gにイソプロパノール200mL、ヘキサン300mLを加えて、ブレンダーを用いて粉砕し、室温で1時間静置した。
その後、吸引ろ過し、ろ液を分液ロートに移した。
分液ロートに水360mLを加えて混和した。
上層のヘキサン層を回収、乾固して二枚貝総脂質を得た。
(2)総脂質から総リン脂質の抽出
得られた総脂質にアセトン200mLを加えて撹拌し、氷冷後、1000g、10分間、4℃で遠心した。沈殿を回収して脱中性脂肪二枚貝総リン脂質を得た。
得られた総脂質にアセトン200mLを加えて撹拌し、氷冷後、1000g、10分間、4℃で遠心した。沈殿を回収して脱中性脂肪二枚貝総リン脂質を得た。
(3)アサリ由来総リン脂質のHPLC解析
得られた総リン脂質について、下記条件でHPLCを行った。
その結果を、図1(a)に示す。
得られた総リン脂質について、下記条件でHPLCを行った。
その結果を、図1(a)に示す。
<HPLCの条件>
使用機器:HPLC Agilent 1100 system(Agilent Technologies,Tokyo)
カラム :Lichrosphere 100Diol (250×3mm,5μm)(Agilent Technologies)
流 量 :0.8ml/分
検 出 :ELSD(蒸発光検出器)(Agilent Technologies)
移動相 :
(A)ヘキサン/イソプロパノール/酢酸(82:17:1,v/v,0.08%TEA*)
(B)イソプロパノール/水/酢酸(85:14:1,0.08%TEA*)
*TEA:トリエチルアミン
なお、時間帯と移動相(A)と(B)の液組成を、表1に示す。
使用機器:HPLC Agilent 1100 system(Agilent Technologies,Tokyo)
カラム :Lichrosphere 100Diol (250×3mm,5μm)(Agilent Technologies)
流 量 :0.8ml/分
検 出 :ELSD(蒸発光検出器)(Agilent Technologies)
移動相 :
(A)ヘキサン/イソプロパノール/酢酸(82:17:1,v/v,0.08%TEA*)
(B)イソプロパノール/水/酢酸(85:14:1,0.08%TEA*)
*TEA:トリエチルアミン
なお、時間帯と移動相(A)と(B)の液組成を、表1に示す。
(4)総グリセロリン脂質の分離
得られた総リン脂質(アセトン沈殿)をエーテル50mLに溶解し、混和した後、1000g、4℃、10分間遠心し、上清(エーテル層)を乾固して、総グリセロリン脂質を得た。
得られた総リン脂質(アセトン沈殿)をエーテル50mLに溶解し、混和した後、1000g、4℃、10分間遠心し、上清(エーテル層)を乾固して、総グリセロリン脂質を得た。
(5)総グリセロリン脂質の酵素処理と抽出によるエーテルリン脂質の精製
得られた総グリセロリン脂質を、ホスホリパーゼA1(三菱化学フーズ(株)製)溶液(20mg/mL クエン酸緩衝液(pH4.5))20mL中に分散させ、超音波などで、充分混和し、温度50℃、2時間反応させた。
その後、冷却し、反応を止めた。
ヘキサン/イソプロパノール(3:2)400mLを加えて、分液ロートに移し、混和後、水240mLを加えて、静置し、水層を除いた。
残存しているリゾ型リン脂質を除くために、残ったヘキサン層に200mLの水を加えて混和し、ヘキサン層を回収し乾固した。
残留している中性脂質を除くため、これに、アセトン100mLを加えて混和し、冷却後、遠心して沈殿を回収し、精製された二枚貝由来エーテル型グリセロリン脂質を得た。
得られた総グリセロリン脂質を、ホスホリパーゼA1(三菱化学フーズ(株)製)溶液(20mg/mL クエン酸緩衝液(pH4.5))20mL中に分散させ、超音波などで、充分混和し、温度50℃、2時間反応させた。
その後、冷却し、反応を止めた。
ヘキサン/イソプロパノール(3:2)400mLを加えて、分液ロートに移し、混和後、水240mLを加えて、静置し、水層を除いた。
残存しているリゾ型リン脂質を除くために、残ったヘキサン層に200mLの水を加えて混和し、ヘキサン層を回収し乾固した。
残留している中性脂質を除くため、これに、アセトン100mLを加えて混和し、冷却後、遠心して沈殿を回収し、精製された二枚貝由来エーテル型グリセロリン脂質を得た。
(6)精製された二枚貝由来エーテルリン脂質(エーテル型グリセロリン脂質)のHPLC解析
得られた二枚貝(アサリ)由来エーテル型グリセロリン脂質について、前記HPLC条件でHPLC解析を行った。
その結果を、図1(b)に示す。
得られた二枚貝(アサリ)由来エーテル型グリセロリン脂質について、前記HPLC条件でHPLC解析を行った。
その結果を、図1(b)に示す。
<実施例2>
(二枚貝由来エーテルリン脂質の製造)
(1)脱中性脂肪二枚貝粉砕組織の分離と総グリセロリン脂質の抽出
二枚貝としてアサリに代えてシジミを用いること以外、実施例1と同様の方法により、総グリセロリン脂質を得た。
(二枚貝由来エーテルリン脂質の製造)
(1)脱中性脂肪二枚貝粉砕組織の分離と総グリセロリン脂質の抽出
二枚貝としてアサリに代えてシジミを用いること以外、実施例1と同様の方法により、総グリセロリン脂質を得た。
(2)シジミ由来総リン脂質のHPLC解析のHPLC解析
得られた総リン脂質について、実施例1と同様の条件でHPLC解析を行った。
その結果を、図2(a)に示す。
得られた総リン脂質について、実施例1と同様の条件でHPLC解析を行った。
その結果を、図2(a)に示す。
(3)総グリセロリン脂質の酵素処理と抽出によるエーテルリン脂質の精製
実施例1と同様の方法によって、総グリセロリン脂質からシジミ由来エーテル型グリセロリン脂質を調製し、このエーテル型グリセロリン脂質を精製した。
実施例1と同様の方法によって、総グリセロリン脂質からシジミ由来エーテル型グリセロリン脂質を調製し、このエーテル型グリセロリン脂質を精製した。
(4)精製された二枚貝由来エーテルリン脂質のHPLC解析
得られた二枚貝由来エーテルリン脂質について、実施例1と同様の条件でHPLC解析を行った。
その結果を、図2(b)に示す。
得られた二枚貝由来エーテルリン脂質について、実施例1と同様の条件でHPLC解析を行った。
その結果を、図2(b)に示す。
<実施例3>
(二枚貝由来エーテルリン脂質の製造)
(1)二枚貝総脂質の抽出
二枚貝アサリ100gにヘキサン・イソプロパノール混合液(3:2)500mLを加えて、ブレンダーを用いて粉砕し、攪拌しながら室温に1時間置いた。
その後、吸引ろ過し、残渣を200mLのヘキサン・イソプロパノール混合液(3:2)で洗い、合わせた、ろ液を分液ロートに移した。
分液ロートに水400mLを加えて混和後、静置した。
2層に分離した下層を捨てて、上層のヘキサン層を回収した。
得られたヘキサン層を乾固して、二枚貝総脂質を得た。
(二枚貝由来エーテルリン脂質の製造)
(1)二枚貝総脂質の抽出
二枚貝アサリ100gにヘキサン・イソプロパノール混合液(3:2)500mLを加えて、ブレンダーを用いて粉砕し、攪拌しながら室温に1時間置いた。
その後、吸引ろ過し、残渣を200mLのヘキサン・イソプロパノール混合液(3:2)で洗い、合わせた、ろ液を分液ロートに移した。
分液ロートに水400mLを加えて混和後、静置した。
2層に分離した下層を捨てて、上層のヘキサン層を回収した。
得られたヘキサン層を乾固して、二枚貝総脂質を得た。
(2)総脂質の酵素処理と抽出によるエーテルリン脂質の精製
得られた総脂質を、ホスホリパーゼA1(三菱化学フーズ(株)製)溶液(20mg/mL クエン酸緩衝液(pH4.5))20mL中に分散させ、超音波などで、充分混和し、温度50℃、2時間反応させた。
その後、冷却し、反応を止めた。
ヘキサン/イソプロパノール(3:2)360mLを加えて、分液ロートに移し、混和後、水220mLを加えて、静置し、水層を除いた。
ヘキサン層を回収し乾固した。
その後、残留しているコレステロールなどの中性脂質を除くため、これに、アセトン20mLを加えて混和し、氷冷後、温度4℃、10分間で遠心して沈殿を回収し、精製された二枚貝由来エーテルリン脂質を得た。
得られた総脂質を、ホスホリパーゼA1(三菱化学フーズ(株)製)溶液(20mg/mL クエン酸緩衝液(pH4.5))20mL中に分散させ、超音波などで、充分混和し、温度50℃、2時間反応させた。
その後、冷却し、反応を止めた。
ヘキサン/イソプロパノール(3:2)360mLを加えて、分液ロートに移し、混和後、水220mLを加えて、静置し、水層を除いた。
ヘキサン層を回収し乾固した。
その後、残留しているコレステロールなどの中性脂質を除くため、これに、アセトン20mLを加えて混和し、氷冷後、温度4℃、10分間で遠心して沈殿を回収し、精製された二枚貝由来エーテルリン脂質を得た。
<実施例4>
(各種二枚貝組織由来の総グリセロリン脂質の製造・解析)
各種二枚貝から、実施例1と同様の方法により、総グリセロリン脂質を得た。
得られた総グリセロリン脂質について、前記実施例1と同様の条件でHPLC解析を行った。
その結果を、表2に示す。
(各種二枚貝組織由来の総グリセロリン脂質の製造・解析)
各種二枚貝から、実施例1と同様の方法により、総グリセロリン脂質を得た。
得られた総グリセロリン脂質について、前記実施例1と同様の条件でHPLC解析を行った。
その結果を、表2に示す。
総グリセロリン脂質の約30%がエタノールアミンリン脂質(PE)で、このPEの約90%がプラズマローゲン(アルケニルPE)であることが分かった。
さらに、総グリセロリン脂質の約50%がコリンリン脂質(PC)で、そのPCの約35%がアルキルPCである。
二枚貝組織において、その総グリセロリン脂質の約30~55%が、エーテルリン脂質で構成されている。
さらに、総グリセロリン脂質の約50%がコリンリン脂質(PC)で、そのPCの約35%がアルキルPCである。
二枚貝組織において、その総グリセロリン脂質の約30~55%が、エーテルリン脂質で構成されている。
<実施例5>
(エーテルリン脂質の全脂肪酸中の多価不飽和脂肪酸の分析)
二枚貝由来エーテルリン脂質および鶏組織由来のエーテルリン脂質に含まれている全脂肪酸中の多価不飽和脂肪酸(EPA、DHAおよびARA)の割合について、下記方法に従い、HPLCを用いて、分析をした。
その結果を、表4および5、ならびに図3に示す。
(エーテルリン脂質の全脂肪酸中の多価不飽和脂肪酸の分析)
二枚貝由来エーテルリン脂質および鶏組織由来のエーテルリン脂質に含まれている全脂肪酸中の多価不飽和脂肪酸(EPA、DHAおよびARA)の割合について、下記方法に従い、HPLCを用いて、分析をした。
その結果を、表4および5、ならびに図3に示す。
(各種二枚貝由来のエーテルリン脂質の加水分解)
各種二枚貝由来のエーテルリン脂質を分取し、乾固したものを0.5規定水酸化カリウムのメタノール溶液で加水分解し、遊離脂肪酸を得た。
各種二枚貝由来のエーテルリン脂質を分取し、乾固したものを0.5規定水酸化カリウムのメタノール溶液で加水分解し、遊離脂肪酸を得た。
(各種エーテルリン脂質からの遊離脂肪酸のラベル)
上記エーテルリン脂質から加水分解で産生した、遊離脂肪酸を0.05% 9-アントレルヂアゾメタン(ADAM)でラベルした。
上記エーテルリン脂質から加水分解で産生した、遊離脂肪酸を0.05% 9-アントレルヂアゾメタン(ADAM)でラベルした。
(脂肪酸の分析)
前記ラベルした脂肪酸を、下記条件のHPLCで分析した。
前記ラベルした脂肪酸を、下記条件のHPLCで分析した。
[HPLCの条件]
使用機器:アジレント HPLC 1100 シリーズ(アジレント社)
カラム :Ultrasphere 100 RP-18e (メルク社)
流 量 :0.8ml/分
検 出 :蛍光検出器
移動相:
(A)アセトニトリル
(B)エタノール
(C)ヘキサン
なお、時間帯と移動相(A)、(B)、(C)の液組成を、表3に示す。
使用機器:アジレント HPLC 1100 シリーズ(アジレント社)
カラム :Ultrasphere 100 RP-18e (メルク社)
流 量 :0.8ml/分
検 出 :蛍光検出器
移動相:
(A)アセトニトリル
(B)エタノール
(C)ヘキサン
なお、時間帯と移動相(A)、(B)、(C)の液組成を、表3に示す。
表4および5ならびに図3から、二枚貝由来のエーテルリン脂質は、そのsn-2において、エイコサペンタエン酸(EPA)、ドコサヘキサエン酸(DHA)およびアラキドン酸(ARA)を多量に結合していることが分かる。
一方、二枚貝由来エーテルリン脂質と同時に同じ方法で分析した鶏胸肉由来のエーテルリン脂質では、PE,PCともにアルケニルリン脂質であり、アルキルPCは存在していない。
したがって、脂肪酸の構成を比較すると、二枚貝由来エーテルリン脂質には、EPAおよびDHAが多く含まれることが示された。
アルツハイマー病、パーキンソン病、うつ病、統合失調症などの脳神経病、糖尿病などのメタボリックシンドローム、種々の感染症や免疫異常において、EPAおよびDHAが減少し、また、EPAはプロスタグランジン、DHAはノイロプロテクチンを貯蔵する役目をするものである。
二枚貝由来のエーテルリン脂質には、このようなEPAおよびDHAが多数含まれているが、鶏胸肉由来のエーテルリン脂質には、EPAは全く含まれておらず、含まれているDHAも少量である。
よって、この発明の二枚貝由来のエーテルリン脂質は、エイコサペンタエン酸(EPA)、ドコサヘキサエン酸(DHA)およびアラキドン酸(ARA)を多く含むため、従来のエーテルリン脂質よりも優れた効果を奏することが期待される。
一方、二枚貝由来エーテルリン脂質と同時に同じ方法で分析した鶏胸肉由来のエーテルリン脂質では、PE,PCともにアルケニルリン脂質であり、アルキルPCは存在していない。
したがって、脂肪酸の構成を比較すると、二枚貝由来エーテルリン脂質には、EPAおよびDHAが多く含まれることが示された。
アルツハイマー病、パーキンソン病、うつ病、統合失調症などの脳神経病、糖尿病などのメタボリックシンドローム、種々の感染症や免疫異常において、EPAおよびDHAが減少し、また、EPAはプロスタグランジン、DHAはノイロプロテクチンを貯蔵する役目をするものである。
二枚貝由来のエーテルリン脂質には、このようなEPAおよびDHAが多数含まれているが、鶏胸肉由来のエーテルリン脂質には、EPAは全く含まれておらず、含まれているDHAも少量である。
よって、この発明の二枚貝由来のエーテルリン脂質は、エイコサペンタエン酸(EPA)、ドコサヘキサエン酸(DHA)およびアラキドン酸(ARA)を多く含むため、従来のエーテルリン脂質よりも優れた効果を奏することが期待される。
この発明によれば、アルツハイマー病、パーキンソン病、うつ病、統合失調症などの脳神経病、糖尿病などのメタボリックシンドローム、種々の感染症や免疫異常の治療および改善に有効なエーテルリン脂質を、容易かつ大量に製造することが可能となるので、医薬業界において幅広く利用されるものである。
Claims (9)
- 二枚貝組織から抽出処理によって得られること
を特徴とするエーテルリン脂質。 - 下記工程を含むことを特徴とする二枚貝組織由来エーテルリン脂質の製造方法:
イ.二枚貝組織の総脂質を水溶性ケトン系溶媒で処理して脱中性脂肪二枚貝リン脂質を得る工程
ロ.前記工程イ.で得られた脱中性脂肪二枚貝リン脂質から疎水性有機溶媒で抽出処理してグリセロリン脂質を得る工程
ならびに
ハ.前記工程ロ.で得られたグリセロリン脂質にホスホリパーゼA1を作用させて、混在するジアシルグリセロリン脂質を分解した後、溶液分配などにより、精製されたエーテルリン脂質を得る工程。 - 前記疎水性有機溶媒は、
エーテル又は石油エーテルであること
を特徴とする請求項3に記載の二枚貝組織由来エーテルリン脂質の製造方法。 - 前記水溶性ケトン系溶媒は、
アセトンであること
を特徴とする請求項3又は4に記載の二枚貝組織由来エーテルリン脂質の製造方法。 - 下記工程を含むことを特徴とする二枚貝組織由来エーテルリン脂質の製造方法:
ニ.二枚貝組織から、その総脂質を非極性有機溶媒・分岐アルコール混合液で抽出する工程
ならびに
ホ.前記工程ニ.で得られた総脂質にホスホリパーゼA1を作用させて、混在するジアシルリン脂質を分解した後、溶媒分配などにより、精製されたエーテルリン脂質を得る工程。 - 請求項3~6のいずれかに記載の二枚貝組織由来エーテルリン脂質の製造方法で得られたこと
を特徴とする二枚貝組織由来エーテルリン脂質。 - 請求項1、2又は7のいずれかに記載の二枚貝組織由来エーテルリン脂質を含むこと
を特徴とする飲食品。 - 請求項1、2又は7にいずれかに記載の二枚貝組織由来エーテルリン脂質を含むこと
を特徴とする医薬用組成物。
Priority Applications (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP15867632.0A EP3241884B1 (en) | 2014-12-08 | 2015-05-13 | Method for producing ether phospholipid |
| US15/533,528 US11066432B2 (en) | 2014-12-08 | 2015-05-13 | Ether phospholipids and method for producing the same |
| CN201580067010.XA CN107001980A (zh) | 2014-12-08 | 2015-05-13 | 醚磷脂及其制备方法 |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2014-247792 | 2014-12-08 | ||
| JP2014247792A JP6349532B2 (ja) | 2014-12-08 | 2014-12-08 | エーテルリン脂質およびその製造方法 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2016092878A1 true WO2016092878A1 (ja) | 2016-06-16 |
Family
ID=56107082
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2015/063740 WO2016092878A1 (ja) | 2014-12-08 | 2015-05-13 | エーテルリン脂質およびその製造方法 |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US11066432B2 (ja) |
| EP (1) | EP3241884B1 (ja) |
| JP (1) | JP6349532B2 (ja) |
| CN (1) | CN107001980A (ja) |
| WO (1) | WO2016092878A1 (ja) |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP6242532B1 (ja) * | 2017-07-13 | 2017-12-06 | 佐々木食品工業株式会社 | 新規化合物、脂肪肝の予防又は治療剤、血中コレステロール低下剤及び血中コレステロール低下用食品組成物 |
| US10324100B2 (en) | 2017-04-04 | 2019-06-18 | Institute of Rheological Functions of Food | Method for quantifying plasmalogens using PLA1 processing |
| WO2021221066A1 (ja) * | 2020-04-28 | 2021-11-04 | 株式会社レオロジー機能食品研究所 | 免疫機能亢進用組成物 |
Families Citing this family (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP6349532B2 (ja) | 2014-12-08 | 2018-07-04 | 志郎 馬渡 | エーテルリン脂質およびその製造方法 |
| US20180127680A1 (en) * | 2015-05-12 | 2018-05-10 | Institute of Rheological Functions of Food | Method for producing ether phospholipids |
| US10653708B2 (en) | 2017-06-16 | 2020-05-19 | Institute of Rheological Functions of Food | Uses of ether phospholipids in treating diseases |
| JP6664638B1 (ja) * | 2018-04-27 | 2020-03-13 | 株式会社 レオロジー機能食品研究所 | 新規プラズマローゲン誘導体 |
| WO2023089986A1 (ja) * | 2021-11-22 | 2023-05-25 | 株式会社 レオロジー機能食品研究所 | 化合物、そのラセミ体、それらの塩、組成物、抗炎症剤、認知症治療剤及びRett症候群治療剤 |
Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2006124488A (ja) * | 2004-10-28 | 2006-05-18 | Asahi Kasei Chemicals Corp | 高度不飽和脂肪酸含有リン脂質の水分散液 |
| JP2009227765A (ja) * | 2008-03-21 | 2009-10-08 | Adeka Corp | プラスマローゲン含有脂質の製造方法 |
| JP2009538366A (ja) * | 2006-05-24 | 2009-11-05 | インダストリアル リサーチ リミテッド | 液体ジメチルエーテルによる高度不飽和脂質の抽出 |
| WO2012039472A1 (ja) * | 2010-09-24 | 2012-03-29 | 医療法人社団ブックス | 抗中枢神経系炎症剤 |
| JP2013053109A (ja) * | 2011-09-05 | 2013-03-21 | Teikyo Univ | リン脂質結合型dha増加剤 |
| JP2013053110A (ja) * | 2011-09-05 | 2013-03-21 | Teikyo Univ | 経口投与剤 |
Family Cites Families (15)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP5062873B2 (ja) | 2005-02-24 | 2012-10-31 | 有限会社梅田事務所 | 複合脂質画分、それから単離されたヒト型スフィンゴミエリンとプラズマローゲンならびにこれらを含む機能性食品素材、医薬品素材および化粧品素材 |
| JP2007262024A (ja) | 2006-03-29 | 2007-10-11 | Tohoku Univ | プラズマローゲン含有脂質の抽出方法及びプラズマローゲン含有脂質、並びに機能性飲食品 |
| JP5185539B2 (ja) | 2007-01-26 | 2013-04-17 | 有限会社梅田事務所 | スフィンゴミエリンおよびプラズマローゲン型グリセロリン脂質の製造方法 |
| CA2679660A1 (en) | 2007-02-21 | 2008-09-12 | Umeda Jimusho Ltd. | Process for producing functional material, the functional material and continuous heating apparatus for obtaining the same |
| JP5774816B2 (ja) | 2007-05-28 | 2015-09-09 | 有限会社梅田事務所 | リン脂質含有機能性素材の製造方法およびプラズマローゲン型グリセロリン脂質の製造方法 |
| JP2009263518A (ja) | 2008-04-25 | 2009-11-12 | Mitsumaru Kagaku Kk | プラズマローゲン含有脂質の抽出方法及び分離方法 |
| JP5430566B2 (ja) | 2008-06-20 | 2014-03-05 | 有限会社梅田事務所 | 高純度リン脂質の製造方法およびその方法で得られた高純度のスフィンゴミエリンとプラズマローゲン型グリセロリン脂質 |
| JP5489439B2 (ja) | 2008-09-11 | 2014-05-14 | 丸大食品株式会社 | プラズマローゲン型リン脂質及びスフィンゴ脂質の製造方法 |
| WO2010047404A1 (ja) | 2008-10-24 | 2010-04-29 | 有限会社梅田事務所 | 常温保存安定化機能性乾燥物またはその粉砕物とその抽出画分の製造方法、およびそれらの用途 |
| EP2522353A4 (en) | 2010-01-06 | 2013-06-19 | Marudai Food Co Ltd | Active substance for brain nerve cell genesis |
| WO2012043481A1 (ja) * | 2010-09-30 | 2012-04-05 | 国立大学法人東京海洋大学 | 2-アシル-リゾホスファチジルセリン含有組成物及びその製造方法 |
| JP6025568B2 (ja) | 2010-12-28 | 2016-11-16 | 株式会社藤野ブレインリサーチ | 認知症を血液サンプルで判定するための検査方法 |
| AU2012321073B2 (en) | 2011-11-17 | 2015-02-26 | Med-Life Discoveries Lp | Methods for the synthesis of plasmalogens and plasmalogen derivatives, and therapeutic uses thereof |
| JP6349532B2 (ja) | 2014-12-08 | 2018-07-04 | 志郎 馬渡 | エーテルリン脂質およびその製造方法 |
| US20180127680A1 (en) | 2015-05-12 | 2018-05-10 | Institute of Rheological Functions of Food | Method for producing ether phospholipids |
-
2014
- 2014-12-08 JP JP2014247792A patent/JP6349532B2/ja active Active
-
2015
- 2015-05-13 WO PCT/JP2015/063740 patent/WO2016092878A1/ja active Application Filing
- 2015-05-13 CN CN201580067010.XA patent/CN107001980A/zh active Pending
- 2015-05-13 US US15/533,528 patent/US11066432B2/en active Active
- 2015-05-13 EP EP15867632.0A patent/EP3241884B1/en active Active
Patent Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2006124488A (ja) * | 2004-10-28 | 2006-05-18 | Asahi Kasei Chemicals Corp | 高度不飽和脂肪酸含有リン脂質の水分散液 |
| JP2009538366A (ja) * | 2006-05-24 | 2009-11-05 | インダストリアル リサーチ リミテッド | 液体ジメチルエーテルによる高度不飽和脂質の抽出 |
| JP2009227765A (ja) * | 2008-03-21 | 2009-10-08 | Adeka Corp | プラスマローゲン含有脂質の製造方法 |
| WO2012039472A1 (ja) * | 2010-09-24 | 2012-03-29 | 医療法人社団ブックス | 抗中枢神経系炎症剤 |
| JP2013053109A (ja) * | 2011-09-05 | 2013-03-21 | Teikyo Univ | リン脂質結合型dha増加剤 |
| JP2013053110A (ja) * | 2011-09-05 | 2013-03-21 | Teikyo Univ | 経口投与剤 |
Non-Patent Citations (19)
| Title |
|---|
| E.BOSELLI ET AL.: "Characterization of Phospholipid Molecular Species in the Edible Parts of Bony Fish and Shellfish", JOURNAL OF AGRICULTURAL AND FOOD CHEMISTRY, vol. 60, no. 12, 2012, pages 3234 - 3245, XP055454209 * |
| E.KRAFFE ET AL.: "Cis-4,7,10,trans-13-22:4 fatty acid distribution in phospholipids of pectinid species Aequipecten opercularis and Pecten maximus", LIPIDS, vol. 41, no. 5, 2006, pages 491 - 497, XP009503732 * |
| E.KRAFFE ET AL.: "Fatty acids of serine, ethanolamine, and choline plasmalogens in some marine bivalves", LIPIDS, vol. 39, no. 1, 2004, pages 59 - 66, XP009503737 * |
| E.KREPS ET AL.: "Phospholipids in the nervous system of molluscs", JOURNAL OF NEUROCHEMISTRY, vol. 15, no. 4, 1968, pages 285 - 291, XP055454186 * |
| F.L.GRAND ET AL.: "Altered membrane lipid composition and functional parameters of circulating cells in cockles (Cerastoderma edule) affected by disseminated neoplasia", CHEMISTRY AND PHYSICS OF LIPIDS, vol. 167, no. 168, 2013, pages 9 - 20, XP055454182 * |
| F.L.GRAND ET AL.: "Disseminated Neoplasia in the Soft-Shell Clam Mya arenaria: Membrane Lipid Composition and Functional Parameters of Circulating Cells", LIPIDS, vol. 49, no. 8, August 2014 (2014-08-01), pages 807 - 818, XP055454235 * |
| F.L.GRAND ET AL.: "Membrane phospholipid composition of hemocytes in the Pacific oyster Crassostrea gigas and the Manila clam Ruditapes philippin arum", COMPARATIVE BIOCHEMISTRY AND PHYSIOLOGY, PART A: MOLECULAR & INTEGRATIVE PHYSIOLOGY, vol. 159A, no. 4, 2011, pages 383 - 391 * |
| J.C.NEVENZEL ET AL.: "Plasmalogens in the gill lipids of aquatic animals", COMPARATIVE BIOCHEMISTRY AND PHYSIOLOGY, PART B: BIOCHEMISTRY & MOLECULAR BIOLOGY, vol. 82B, no. 2, 1985, pages 293 - 297, XP023528392, DOI: doi:10.1016/0305-0491(85)90244-5 * |
| L.O.HANUS ET AL.: "Plasmalogens, fatty acids and alkyl glyceryl ethers of marine and freshwater clams and mussels", FOOD CHEMISTRY, vol. 116, no. 2, 2009, pages 491 - 498, XP026098333, DOI: doi:10.1016/j.foodchem.2009.03.004 * |
| M.A.CHEBOTAREVA ET AL.: "Limit of change in unsaturation index of fatty acid composition of phospholipids at adaptation of molluscs to biogenic and abiogenic environmental factors", JOURNAL OF EVOLUTIONARY BIOCHEMISTRY AND PHYSIOLOGY, vol. 47, no. 5, 2011, pages 448 - 453, XP019984828, DOI: doi:10.1134/S0022093011050069 * |
| P.MENESES ET AL.: "High resolution 31P NMR of extracted phospholipids", JOURNAL OF LIPID RESEARCH, vol. 29, no. 5, 1988, pages 679 - 689, XP055454240 * |
| S.HIGASHI ET AL.: "Role of phospholipids in the aerobic endogenous metabolism of freshwater mussel spermatozoa", JOURNAL OF CELLULAR PHYSIOLOGY, vol. 72, no. 1, 1968, pages 55 - 63, XP055454206 * |
| S.MAWATARI ET AL.: "Simultaneous preparation of purified plasmalogens and sphingomyelin in human erythrocytes with phospholipase A1 from Aspergillus orizae", BIOSCIENCE, BIOTECHNOLOGY, AND BIOCHEMISTRY, vol. 73, no. 12, 2009, pages 2621 - 2625, XP055330963 * |
| S.MISRA ET AL.: "Naturally occurring ether- linked phosphatidylcholine activates phosphatidylinositol 3-kinase and stimulates cell growth", JOURNAL OF CELLULAR BIOCHEMISTRY, vol. 55, no. 1, 1994, pages 146 - 153, XP055454177 * |
| S.YASUDA ET AL.: "Studies on the Lipids of Japanese Littleneck, Tapes japonica Deshayes. II.", COMPOSITION OF PHOSPHOLIPIDS, YUKAGAKU, vol. 16, no. 11, 1967, pages 596 - 600 * |
| See also references of EP3241884A4 * |
| V.P.CHELOMIN ET AL.: "Alterations of microsomal lipid synthesis in gill cells of bivalve mollusc Mizuhopecten yessoensis in response to cadmium accumulation", COMPARATIVE BIOCHEMISTRY AND PHYSIOLOGY, PART C: PHARMACOLOGY, TOXICOLOGY & ENDOCRINOLOGY, vol. 99C, no. 1-2, 1991, pages 1 - 5, XP025903762, DOI: doi:10.1016/0742-8413(91)90065-2 * |
| V.P.CHELOMIN ET AL.: "Lipid composition and some aspects of aminophospholipid organization in erythrocyte membrane of the marine bivalve mollusc Scapharca broughtoni", COMPARATIVE BIOCHEMISTRY AND PHYSIOLOGY, PART B: BIOCHEMISTRY & MOLECULAR BIOLOGY, vol. 69B, no. 3, 1981, pages 599 - 604, XP025749333, DOI: doi:10.1016/0305-0491(81)90355-2 * |
| Y.G.JOH ET AL.: "Studies on the lipids of abalone (II) The aldehyde composition of plasmalogen from abalone and some marine molluscs", BULLETIN OF THE KOREAN FISHERIES SOCIETY, vol. 12, no. 3, 1979, pages 181 - 189, XP009503743 * |
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US10324100B2 (en) | 2017-04-04 | 2019-06-18 | Institute of Rheological Functions of Food | Method for quantifying plasmalogens using PLA1 processing |
| JP6242532B1 (ja) * | 2017-07-13 | 2017-12-06 | 佐々木食品工業株式会社 | 新規化合物、脂肪肝の予防又は治療剤、血中コレステロール低下剤及び血中コレステロール低下用食品組成物 |
| JP2019019063A (ja) * | 2017-07-13 | 2019-02-07 | 佐々木食品工業株式会社 | 新規化合物、脂肪肝の予防又は治療剤、血中コレステロール低下剤及び血中コレステロール低下用食品組成物 |
| WO2021221066A1 (ja) * | 2020-04-28 | 2021-11-04 | 株式会社レオロジー機能食品研究所 | 免疫機能亢進用組成物 |
| JP7033263B1 (ja) * | 2020-04-28 | 2022-03-10 | 株式会社 レオロジー機能食品研究所 | 免疫機能亢進用組成物 |
Also Published As
| Publication number | Publication date |
|---|---|
| US11066432B2 (en) | 2021-07-20 |
| JP6349532B2 (ja) | 2018-07-04 |
| EP3241884A4 (en) | 2018-06-06 |
| JP2016108466A (ja) | 2016-06-20 |
| CN107001980A (zh) | 2017-08-01 |
| US20180327433A1 (en) | 2018-11-15 |
| EP3241884B1 (en) | 2019-12-18 |
| EP3241884A1 (en) | 2017-11-08 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6349532B2 (ja) | エーテルリン脂質およびその製造方法 | |
| JP6626099B2 (ja) | エーテルリン脂質の製造方法 | |
| US8524282B2 (en) | Method for production of highly pure phospholipid, and highly pure sphingomyelin and plasmalogen-type glycerophospholipid produced by the method | |
| JP6016363B2 (ja) | 脳神経細胞新生剤 | |
| JP2021508343A (ja) | リゾホスファチジルコリン組成物 | |
| KR20130141460A (ko) | 건강 유지 및 급성 및 만성 장애의 치료를 위한 지질 보충제 | |
| CN108276438B (zh) | 一种epa缩醛磷脂的制备方法及其应用 | |
| JP5997887B2 (ja) | 経口投与剤 | |
| JP6207545B2 (ja) | 学習記憶能力増強剤 | |
| JP7190598B2 (ja) | 多価不飽和脂肪酸が結合したリン脂質を含む魚卵脂質組成物 | |
| JP2013216654A (ja) | 脳萎縮抑制剤 | |
| JP2009269865A (ja) | 経口投与剤 | |
| WO2020213132A1 (ja) | プラズマローゲンを含む機能性素材の製造方法 | |
| JP7021953B2 (ja) | エーテル型グリセロリン脂質の製造方法 | |
| JP2009269864A (ja) | リン脂質結合型アラキドン酸増加剤 | |
| JP6824506B2 (ja) | 脂質組成物 | |
| JP6842093B2 (ja) | 学習記憶能力増強剤 | |
| JP2018177711A (ja) | Hdl機能改善剤及びhdl機能改善食品組成物 | |
| JP2022067965A (ja) | プラズマローゲン含有組成物、プラズマローゲン吸収促進用組成物、及びプラズマローゲン吸収促進方法 | |
| JP2022067969A (ja) | プラズマローゲン含有組成物、プラズマローゲン吸収促進用組成物、及びプラズマローゲン吸収促進方法 | |
| JP2023119096A (ja) | 間葉系細胞活性化剤、創傷治療剤、間葉系細胞活性化用経口組成物及び創傷治療用経口組成物 | |
| JP2017165785A (ja) | 学習記憶能力増強剤 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 15867632 Country of ref document: EP Kind code of ref document: A1 |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 15533528 Country of ref document: US |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| REEP | Request for entry into the european phase |
Ref document number: 2015867632 Country of ref document: EP |