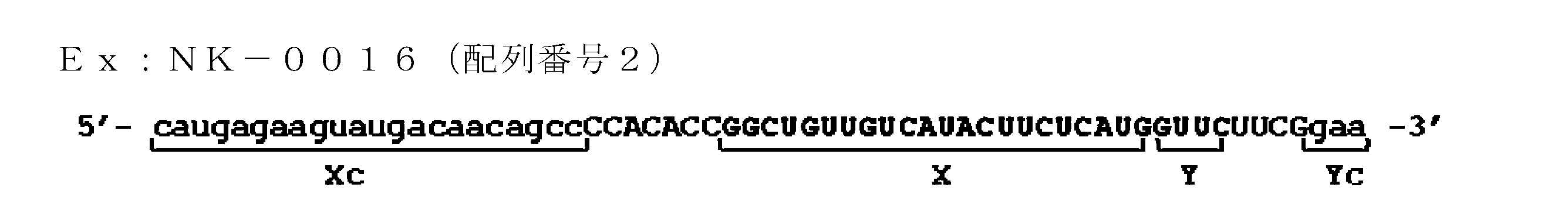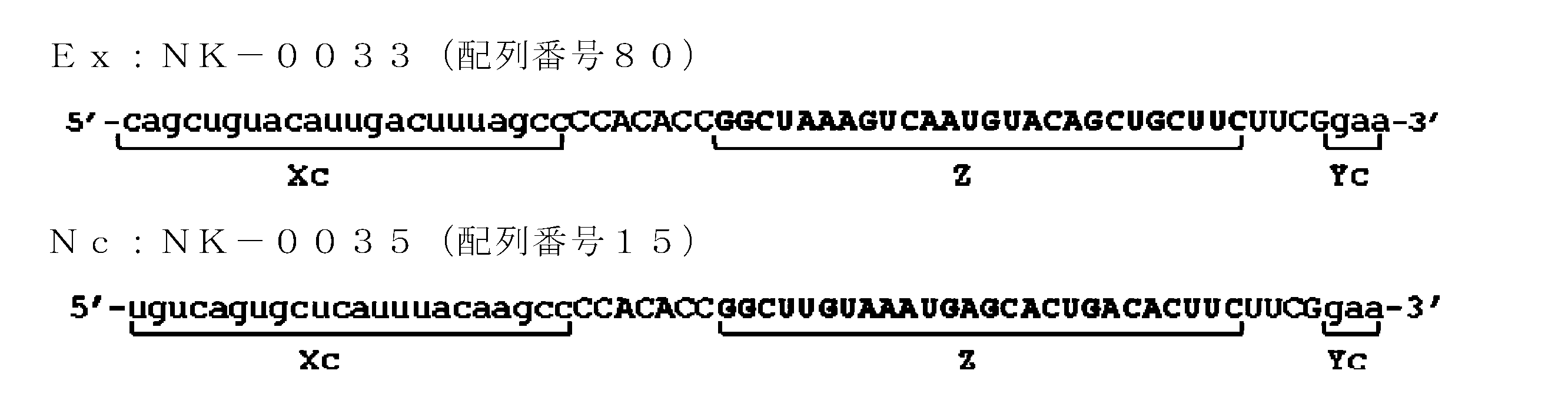WO2012005368A1 - 遺伝子発現制御のための一本鎖核酸分子 - Google Patents
遺伝子発現制御のための一本鎖核酸分子 Download PDFInfo
- Publication number
- WO2012005368A1 WO2012005368A1 PCT/JP2011/065737 JP2011065737W WO2012005368A1 WO 2012005368 A1 WO2012005368 A1 WO 2012005368A1 JP 2011065737 W JP2011065737 W JP 2011065737W WO 2012005368 A1 WO2012005368 A1 WO 2012005368A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- region
- bases
- nucleic acid
- acid molecule
- side region
- Prior art date
Links
- 0 *CC(CCC1)N1C(C(F)(F)F)=O Chemical compound *CC(CCC1)N1C(C(F)(F)F)=O 0.000 description 3
- MJLRPTJLURGFSY-UHFFFAOYSA-N OCC(CCC1)N1C(C(F)(F)F)=O Chemical compound OCC(CCC1)N1C(C(F)(F)F)=O MJLRPTJLURGFSY-UHFFFAOYSA-N 0.000 description 2
- STSCVKRWJPWALQ-UHFFFAOYSA-N CCOC(C(F)(F)F)=O Chemical compound CCOC(C(F)(F)F)=O STSCVKRWJPWALQ-UHFFFAOYSA-N 0.000 description 1
- UOXWXIOMPFEAET-UHFFFAOYSA-N COc1ccc(C(c2ccccc2)(c(cc2)ccc2[O](C)CCOc2ccc(C(c3ccccc3)(c(cc3)ccc3OC)Cl)cc2)OCC(CCC2)N2C(C(F)(F)F)=O)cc1 Chemical compound COc1ccc(C(c2ccccc2)(c(cc2)ccc2[O](C)CCOc2ccc(C(c3ccccc3)(c(cc3)ccc3OC)Cl)cc2)OCC(CCC2)N2C(C(F)(F)F)=O)cc1 UOXWXIOMPFEAET-UHFFFAOYSA-N 0.000 description 1
- HVVNJUAVDAZWCB-UHFFFAOYSA-N OCC1NCCC1 Chemical compound OCC1NCCC1 HVVNJUAVDAZWCB-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
- C12N15/113—Non-coding nucleic acids modulating the expression of genes, e.g. antisense oligonucleotides; Antisense DNA or RNA; Triplex- forming oligonucleotides; Catalytic nucleic acids, e.g. ribozymes; Nucleic acids used in co-suppression or gene silencing
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
- C12N15/111—General methods applicable to biologically active non-coding nucleic acids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K48/00—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/10—Type of nucleic acid
- C12N2310/11—Antisense
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/10—Type of nucleic acid
- C12N2310/14—Type of nucleic acid interfering N.A.
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/31—Chemical structure of the backbone
- C12N2310/318—Chemical structure of the backbone where the PO2 is completely replaced, e.g. MMI or formacetal
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/50—Physical structure
- C12N2310/53—Physical structure partially self-complementary or closed
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/50—Physical structure
- C12N2310/53—Physical structure partially self-complementary or closed
- C12N2310/531—Stem-loop; Hairpin
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/50—Physical structure
- C12N2310/53—Physical structure partially self-complementary or closed
- C12N2310/533—Physical structure partially self-complementary or closed having a mismatch or nick in at least one of the strands
Definitions
- the present invention relates to a single-stranded nucleic acid molecule that suppresses gene expression, a composition containing the same, and use thereof.
- RNA interference is known as a technique for suppressing gene expression (Non-patent Document 1). Inhibition of gene expression by RNA interference is generally performed, for example, by administering a short double-stranded RNA molecule to a cell or the like.
- the double-stranded RNA molecule is usually referred to as siRNA (small interfering RNA).
- siRNA small interfering RNA
- gene expression can also be suppressed by an RNA molecule that is a circular RNA molecule and partially forms a double strand by intramolecular annealing (Patent Document 1).
- Patent Document 1 RNA molecules that induce gene expression suppression have the following problems.
- an object of the present invention is to provide a new nucleic acid molecule that can suppress gene expression and can be easily and efficiently produced.
- the single-stranded nucleic acid molecule of the present invention is a single-stranded nucleic acid molecule comprising an expression suppressing sequence that suppresses the expression of a target gene, From the 5 ′ side to the 3 ′ side, the 5 ′ side region (Xc), the inner region (Z), and the 3 ′ side region (Yc) are included in the above order,
- the internal region (Z) is configured by connecting an internal 5 ′ side region (X) and an internal 3 ′ side region (Y),
- the 5 ′ side region (Xc) is complementary to the internal 5 ′ side region (X);
- the 3 ′ side region (Yc) is complementary to the inner 3 ′ side region (Y);
- At least one of the internal region (Z), the 5 ′ side region (Xc), and the 3 ′ side region (Yc) includes the expression suppression sequence.
- composition of the present invention is a composition for suppressing the expression of a target gene, and is characterized by containing the single-stranded nucleic acid molecule of the present invention.
- composition of the present invention is a pharmaceutical composition, and is characterized by containing the single-stranded nucleic acid molecule of the present invention.
- the expression suppression method of the present invention is a method of suppressing the expression of a target gene, characterized in that the single-stranded nucleic acid molecule of the present invention is used.
- the method for treating a disease of the present invention includes a step of administering the single-stranded nucleic acid molecule of the present invention to a patient, wherein the single-stranded nucleic acid molecule serves as the expression-suppressing sequence of a gene causing the disease. It has a sequence that suppresses expression.
- the single-stranded nucleic acid molecule of the present invention gene expression can be suppressed, and since it is not circular, its synthesis is easy, and since it is single-stranded, a double-stranded annealing step And can be manufactured efficiently.
- the present inventors are the first to find that the structure of the single-stranded nucleic acid molecule of the present invention can suppress gene expression.
- the gene expression suppression effect of the single-stranded nucleic acid molecule of the present invention is presumed to be due to the same phenomenon as RNA interference, but gene expression suppression in the present invention is not limited or limited to RNA interference.
- FIG. 1 is a schematic diagram showing an example of a single-stranded nucleic acid molecule of the present invention.
- FIG. 2 is a schematic diagram showing another example of the single-stranded nucleic acid molecule of the present invention.
- FIG. 3 is a schematic diagram showing another example of the single-stranded nucleic acid molecule of the present invention.
- FIG. 4 is a graph showing the relative value of GAPDH gene expression level in the examples of the present invention.
- FIG. 5 is a graph showing the relative value of GAPDH gene expression level in the examples of the present invention.
- FIG. 6 is a graph showing the relative value of the GAPDH gene expression level of A549 cells in the examples of the present invention.
- FIG. 1 is a schematic diagram showing an example of a single-stranded nucleic acid molecule of the present invention.
- FIG. 2 is a schematic diagram showing another example of the single-stranded nucleic acid molecule of the present invention.
- FIG. 3 is a schematic
- FIG. 7 is a graph showing the relative value of GAPDH gene expression level of 293 cells in the examples of the present invention.
- FIG. 8 is a graph showing the relative value of the expression level of TGF- ⁇ 1 gene in the examples of the present invention.
- FIG. 9 is a graph showing the expression level of TGF- ⁇ 1 gene per unit weight of lung in each administration group in the examples of the present invention.
- FIG. 10 is a graph showing the number of cells in the BAFL sample in each administration group in the examples of the present invention.
- FIG. 11 is a graph showing the number of neutrophil cells in the BALF sample in each administration group in the examples of the present invention.
- FIG. 12 is a photograph showing the result of Giemsa staining of cells in a BALF sample in the example of the present invention,
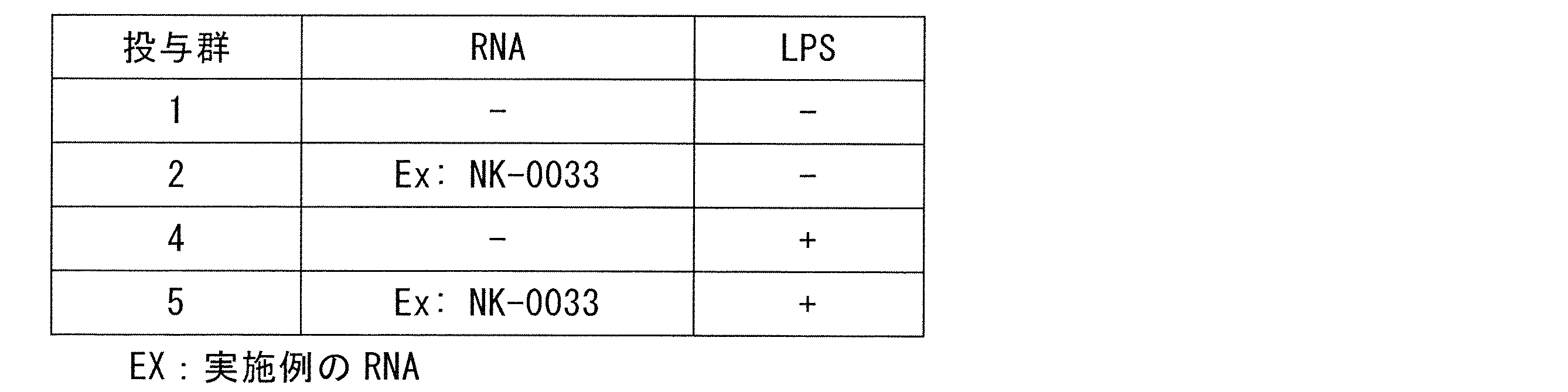
- A is the result of administration group 4 of LPS (+) / RNA ( ⁇ );
- B) is the result of LPS (+) / negative control NK-0035 (+) administration group 6, and
- C) is the result of LPS (+) / NK-0033 (+) example administration group 5.
- FIG. 13 is a photograph showing the result of HE staining of lung tissue in the example of the present invention
- (A) is the result of LPS (+) / RNA ( ⁇ ) administration group 4
- (B) is , LPS (+) / negative control NK-0035 (+) administration group 6 results
- (C) shows LPS (+) / NK-0033 (+) Example administration group 5 results.
- FIG. 14 (A) shows the result showing the expression level of the TGF- ⁇ 1 gene in the example of the present invention
- FIG. 14 (B) shows the result showing the expression level of the IFN- ⁇ gene in the example of the present invention
- FIG. 14C shows the results showing the expression level of the IFN- ⁇ gene in the examples of the present invention.
- FIG. 14A shows the result showing the expression level of the TGF- ⁇ 1 gene in the example of the present invention
- FIG. 14 (B) shows the result showing the expression level of the IFN- ⁇ gene in the example of the present invention
- FIG. 14C shows the results
- FIG. 15 is a graph showing the relative value of the expression level of the TGF- ⁇ 1 gene in the examples of the present invention.
- FIG. 16 is a graph showing the relative value of TGF- ⁇ 1 gene expression level in the examples of the present invention.
- FIG. 17 is a graph showing the expression level of TGF- ⁇ 1 per lung per unit weight in each administration group in the examples of the present invention.
- FIG. 18 (A) is a graph showing the amount of TNF- ⁇ in the BALF sample of each administration group in the example of the present invention
- FIG. 18 (B) is the BALF sample of each administration group in the example of the present invention.
- 2 is a graph showing the amount of IFN- ⁇ in the medium.
- FIG. 19 is a graph showing the relative value of the expression level of the LAMA gene in 293 cells in the examples of the present invention.
- FIG. 20 is a graph showing the relative value of the expression level of the LMNA gene in A549 cells in the examples of the present invention.
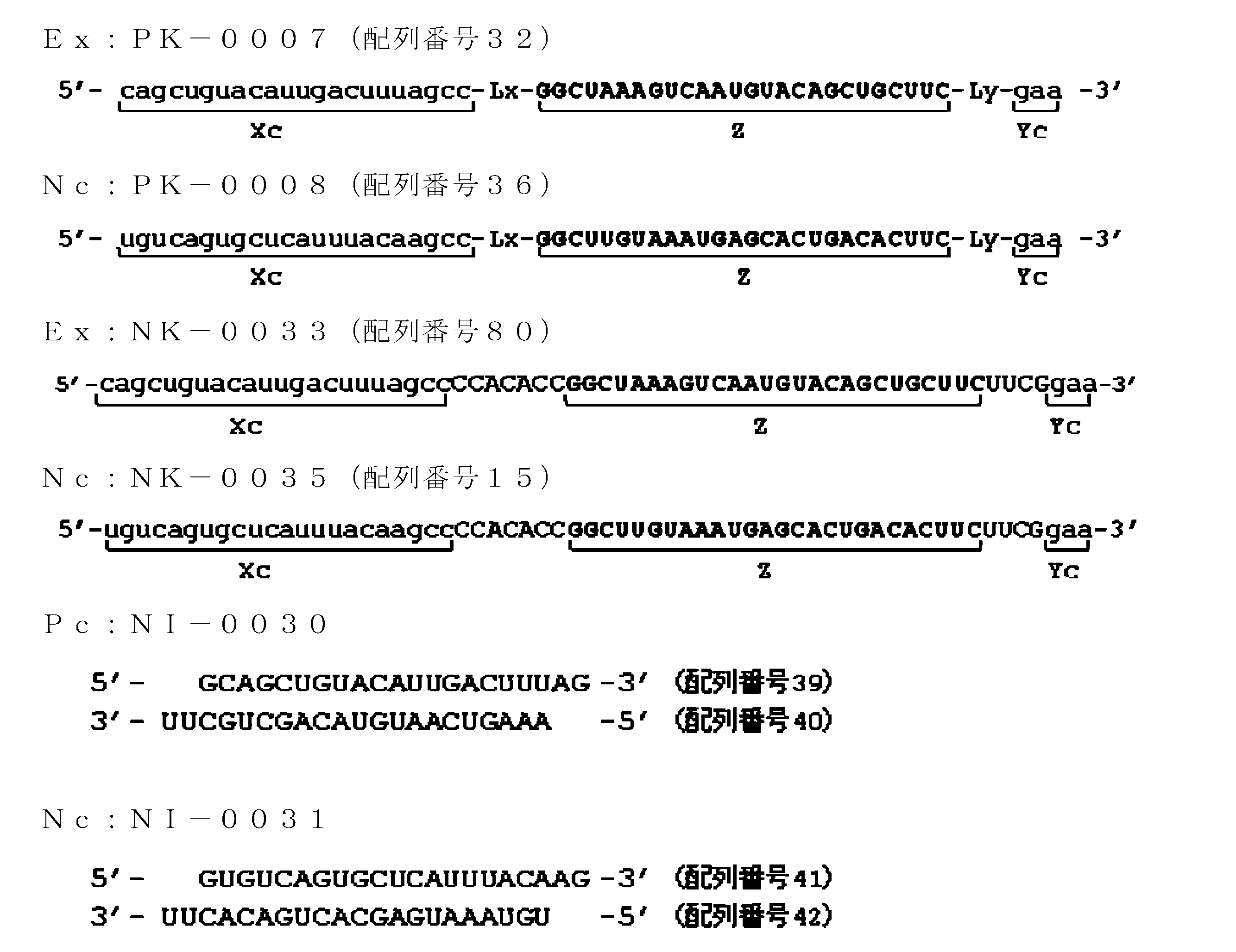
- FIG. 21 is a diagram showing ssRNA used in Examples of the present invention.
- FIG. 22 is a graph showing relative values of GAPDH gene expression levels in the examples of the present invention.
- FIG. 23 is a diagram showing ssRNA used in Examples of the present invention.
- FIG. 24 is a graph showing the relative value of GAPDH gene expression level in the examples of the present invention.
- FIG. 25 is a diagram showing ssRNA used in Examples of the present invention.
- FIG. 26 is a graph showing relative values of GAPDH gene expression levels in the examples of the present invention.
- FIG. 27 is a diagram showing ssRNA used in Examples of the present invention.
- FIG. 28 is a graph showing the relative values of GAPDH gene expression levels in the examples of the present invention.
- FIG. 29 is a graph showing relative values of GAPDH gene expression levels in the examples of the present invention.
- FIG. 30 is a graph showing the relative value of the GAPDH gene expression level of HCT116 cells in Examples of the present invention.
- FIG. 31 is an electrophoretogram showing ribonuclease resistance in the examples of the present invention.
- FIG. 32 is an electrophoretogram showing S7 nuclease resistance in the examples of the present invention.
- the single-stranded nucleic acid molecule of the present invention is a single-stranded nucleic acid molecule comprising an expression suppressing sequence that suppresses the expression of a target gene, as described above, From the 5 ′ side to the 3 ′ side, the 5 ′ side region (Xc), the inner region (Z), and the 3 ′ side region (Yc) are included in the above order,
- the internal region (Z) is configured by connecting an internal 5 ′ side region (X) and an internal 3 ′ side region (Y),
- the 5 ′ side region (Xc) is complementary to the internal 5 ′ side region (X);
- the 3 ′ side region (Yc) is complementary to the inner 3 ′ side region (Y); At least one of the internal region (Z), the 5 ′ side region (Xc), and the 3 ′ side region (Yc) includes the expression suppression sequence.
- suppression of target gene expression means, for example, inhibiting the expression of the target gene.
- the suppression mechanism is not particularly limited, and may be, for example, down regulation or silencing.
- the suppression of the expression of the target gene can be achieved, for example, by reducing the production amount of the transcription product from the target gene, reducing the activity of the transcription product, reducing the production amount of the translation product from the target gene, or activity of the translation product. It can be confirmed by decrease of Examples of the protein include a mature protein or a precursor protein before undergoing processing or post-translational modification.
- the single-stranded nucleic acid molecule of the present invention is also referred to as “ssNc molecule” of the present invention.
- the ssNc molecule of the present invention can be used, for example, in vivo or in vitro to suppress the expression of a target gene, it is also referred to as “target gene expression suppression ssNc molecule” or “target gene expression inhibitor”.
- target gene expression suppression ssNc molecule target gene expression inhibitor
- the ssNc molecule of the present invention can suppress the expression of the target gene by, for example, RNA interference, “ssNc molecule for RNA interference”, “RNA interference induction molecule”, “RNA interference agent” or “RNA interference induction” It is also called “agent”.
- the ssNc molecule of the present invention can suppress side effects such as interferon induction.
- the ssNc molecule of the present invention has an unlinked 5 'end and 3' end, and can also be referred to as a linear single-stranded nucleic acid molecule.
- the ssNc molecule of the present invention for example, in the inner region (Z), the inner 5 'region (X) and the inner 3' region (Y) are directly linked.
- the 5 ′ side region (Xc) is complementary to the internal 5 ′ side region (X), and the 3 ′ side region (Yc) is the internal 3 ′ side region (Y ). Therefore, on the 5 ′ side, the region (Xc) is folded toward the region (X), and the region (Xc) and the region (X) can form a double chain by self-annealing. In addition, on the 3 ′ side, the region (Yc) is folded toward the region (Y), and the region (Yc) and the region (Y) can form a double chain by self-annealing. . In this way, the ssNc molecule of the present invention can form a double strand within the molecule. For example, as in the case of siRNA used for conventional RNA interference, two separated single-stranded RNAs are doubled by annealing. The structure that forms a single-stranded RNA is clearly different.
- the expression suppressing sequence is, for example, a sequence exhibiting an activity of suppressing the expression of the target gene when the ssNc molecule of the present invention is introduced into a cell in vivo or in vitro. is there.
- the expression suppression sequence is not particularly limited, and can be appropriately set according to the type of target gene of interest.
- a sequence involved in RNA interference by siRNA can be appropriately applied.
- RNA interference In RNA interference, generally, a long double-stranded RNA (dsRNA) is cleaved by a dicer into a double-stranded RNA (siRNA: small interfering RNA) of about 19 to 21 base pairs with a 3 ′ end protruding in a cell.
- siRNA double-stranded RNA
- siRNA small interfering RNA
- This is a phenomenon in which one of the single-stranded RNAs binds to the target mRNA and degrades the mRNA, thereby suppressing the translation of the mRNA.
- Various types of single-stranded RNA sequences in the siRNA that bind to the target mRNA have been reported, for example, depending on the type of target gene.
- a single-stranded RNA sequence of the siRNA can be used as the expression suppression sequence.
- the present invention relates to the structure of a nucleic acid molecule for allowing the expression suppression activity of the target gene by the expression suppression sequence to function in the cell, for example, not the point of the sequence information of the expression suppression sequence for the target gene. . Therefore, in the present invention, for example, in addition to the siRNA single-stranded RNA sequence known at the time of filing, a sequence that will become clear in the future can be used as the expression-suppressing sequence.
- the expression suppressing sequence preferably has 90% or more complementarity with respect to a predetermined region of the target gene, more preferably 95%, still more preferably 98%, Preferably it is 100%.
- complementarity for example, off-target can be sufficiently reduced.
- the target gene when the target gene is a GAPDH gene, for example, the 19-base long sequence shown in SEQ ID NO: 1 can be used as the expression suppression sequence.
- the expression suppression sequence is, for example,
- the expression-suppressing sequence can be, for example, the 19-base sequence shown in SEQ ID NO: 5
- the target gene is the LMNA gene.
- a 19-base sequence shown in SEQ ID NO: 6 can be used.
- Inhibition of the expression of the target gene by the ssNc molecule of the present invention can be achieved by, for example, expressing the expression suppressing sequence in at least one of the internal region (Z), the 5 ′ side region (Xc) and the 3 ′ side region (Yc)
- RNA interference or a phenomenon similar to RNA interference an RNA interference-like phenomenon
- the ssNc molecule of the present invention is not introduced into a cell or the like as a dsRNA consisting of a double-stranded single-stranded RNA, for example, so-called siRNA. , Not necessarily required. For this reason, it can also be said that the ssNc molecule of the present invention has an RNA interference-like function, for example.
- the expression suppressing sequence is contained in at least one of the internal region (Z), the 5 'side region (Xc), and the 3' side region (Yc) as described above.
- the ssNc molecule of the present invention may have, for example, one or more than two of the expression suppression sequences.
- the ssNc molecule of the present invention may have two or more of the same expression suppression sequences for the same target gene, or may have two or more different expression suppression sequences for the same target gene. Two or more different expression suppression sequences for different target genes may be included.
- the location of each expression suppression sequence is not particularly limited, and the internal region (Z), the 5 ′ side region (Xc), and the Any one of the 3 ′ side regions (Yc) may be used, or a different region may be used.
- the ssNc molecule of the present invention has two or more of the expression suppression sequences for different target genes, for example, the expression of two or more different target genes can be suppressed by the ssNc molecule of the present invention.
- the inner region (Z) is connected to the inner 5 'region (X) and the inner 3' region (Y).
- the region (X) and the region (Y) are directly connected, for example, and do not have an intervening sequence therebetween.
- the inner region (Z) is defined as “the inner 5 ′ side region (X) and the inner 3 ′ side in order to indicate the arrangement relationship between the 5 ′ side region (Xc) and the 3 ′ side region (Xc)”.
- the region (Y) is connected to each other ”, and in the inner region (Z), the 5 ′ side region (Xc) and the 3 ′ side region (Xc) are, for example,
- the use of ssNc molecules is not limited to being a separate and independent region. That is, for example, when the internal region (Z) has the expression suppression sequence, the expression suppression sequence is arranged across the region (X) and the region (Y) in the internal region (Z). Also good.
- the 5 'side region (Xc) is complementary to the internal 5' side region (X).
- the region (Xc) may have a sequence complementary to the entire region of the region (X) or a partial region thereof.
- the region (Xc) It is preferable that the entire region or a partial region thereof includes a complementary sequence or consists of the complementary sequence.
- the region (Xc) may be, for example, completely complementary to the entire region complementary to the region (X) or the complementary partial region, and one or several bases may be non-complementary. However, it is preferably completely complementary.
- the 3 'side region (Yc) is complementary to the internal 3' side region (Y).
- the region (Yc) may have a sequence complementary to the entire region of the region (Y) or a partial region thereof. Specifically, for example, the entire region (Y) Alternatively, it preferably includes a sequence complementary to the partial region, or consists of the complementary sequence.
- the region (Yc) may be, for example, completely complementary to the entire region complementary to the region (Y) or the complementary partial region, and one or several bases may be non-complementary. However, it is preferably completely complementary.
- the one base or several bases is, for example, 1 to 3 bases, preferably 1 base or 2 bases.
- the 5 'side region (Xc) and the internal 5' side region (X) may be directly connected or indirectly connected, for example.
- direct linkage includes, for example, linkage by a phosphodiester bond.
- a linker region (Lx) is provided between the region (Xc) and the region (X), and the region (Xc) and the region ( And X) are linked together.
- the 3 ′ side region (Yc) and the inner 3 ′ side region (Y) may be directly connected or indirectly connected, for example.
- direct linkage includes, for example, linkage by a phosphodiester bond.
- a linker region (Ly) is provided between the region (Yc) and the region (Y), and the region (Yc) and the region ( And Y) are linked.
- the ssNc molecule of the present invention may have, for example, both the linker region (Lx) and the linker region (Ly), or one of them.
- the linker region (Lx) is provided between the 5 ′ side region (Xc) and the inner 5 ′ side region (X), and the 3 ′ side region (Yc) and the inner 3 'The linker region (Ly) is not present between the side region (Y), that is, the region (Yc) and the region (Y) are directly linked.
- the linker region (Ly) is provided between the 3 ′ side region (Yc) and the inner 3 ′ side region (Y), and the 5 ′ side region (Xc) and the The linker region (Lx) is not provided between the internal 5′-side region (X), that is, the region (Xc) and the region (X) are directly linked.
- the linker region (Lx) and the linker region (Ly) each preferably have a structure that does not cause self-annealing within its own region.
- FIG. 1A is a schematic diagram showing an outline of the order of each region from the 5 ′ side to the 3 ′ side of the ssNc molecule.
- FIG. 1B shows the ssNc molecule. It is a schematic diagram which shows the state which forms the double chain
- FIG. 1 merely shows the order of connection of the regions and the positional relationship of the regions forming the double chain.
- the length of each region is not limited to this.
- FIG. 2 (A) is a schematic diagram showing an outline of the order of each region from the 5 ′ side to the 3 ′ side of the ssNc molecule as an example
- FIG. 2 (B) shows the ssNc molecule.
- FIG. 2 is a schematic diagram showing a state in which a double chain is formed in the molecule.
- the ssNc molecule is located between the 5 ′ side region (Xc) and the inner 5 ′ side region (X), and between the inner 3 ′ side region (Y) and the 3 ′ side.
- a double chain is formed with the side region (Yc), and the Lx region and the Ly region have a loop structure.
- FIG. 2 merely shows the connection order of the regions and the positional relationship of the regions forming the double chain.
- the length of each region is not limited to this.
- the number of bases in the 5 ′ side region (Xc), the internal 5 ′ side region (X), the internal 3 ′ side region (Y) and the 3 ′ side region (Yc) is particularly For example, it is as follows.
- “the number of bases” means, for example, “length” and can also be referred to as “base length”.
- the 5′-side region (Xc) may be complementary to the entire region of the inner 5′-side region (X), for example.
- the region (Xc) has the same base length as the region (X), and is composed of a base sequence complementary to the entire region from the 5 ′ end to the 3 ′ end of the region (X).
- the region (Xc) has the same base length as the region (X), and all bases in the region (Xc) are complementary to all bases in the region (X). That is, for example, it is preferably completely complementary.
- the present invention is not limited to this, and for example, as described above, one or several bases may be non-complementary.
- the 5′-side region (Xc) may be complementary to a partial region of the inner 5′-side region (X), for example.
- the region (Xc) has, for example, the same base length as the partial region of the region (X), that is, consists of a base sequence having a base length shorter by one base or more than the region (X). preferable. More preferably, the region (Xc) has the same base length as the partial region of the region (X), and all the bases of the region (Xc) are included in the partial region of the region (X). It is preferred that it is complementary to all bases, that is, for example, completely complementary.
- the partial region of the region (X) is preferably, for example, a region (segment) having a base sequence continuous from the 5 ′ terminal base (first base) in the region (X).
- the 3′-side region (Yc) may be complementary to the entire region of the inner 3′-side region (Y), for example.
- the region (Yc) has, for example, the same base length as the region (Y) and is composed of a base sequence complementary to the entire region from the 5 ′ end to the 3 ′ end of the region (Y).
- the region (Yc) has the same base length as the region (Y), and all bases in the region (Yc) are complementary to all bases in the region (Y). That is, for example, it is preferable to be completely complementary.
- the present invention is not limited to this, and for example, as described above, one or several bases may be non-complementary.
- the 3′-side region (Yc) may be complementary to a partial region of the inner 3′-side region (Y), for example.
- the region (Yc) has, for example, the same base length as the partial region of the region (Y), that is, consists of a base sequence having a base length shorter by one base or more than the region (Y). preferable. More preferably, the region (Yc) has the same base length as the partial region of the region (Y), and all the bases of the region (Yc) are included in the partial region of the region (Y). It is preferred that it is complementary to all bases, that is, for example, completely complementary.
- the partial region of the region (Y) is preferably, for example, a region (segment) having a base sequence continuous from the base at the 3 'end (first base) in the region (Y).
- the number of bases (Z) in the inner region (Z), the number of bases (X) in the inner 5 ′ side region (X), and the number of bases in the inner 3 ′ side region (Y) ( Y), the number of bases (Z) in the internal region (Z), the number of bases (X) in the internal 5 ′ side region (X), and the number of bases (Xc) in the 5 ′ side region (Xc) For example, the following conditions (1) and (2) are satisfied.
- Z X + Y (1)
- the relationship between the number of bases (X) in the inner 5 ′ side region (X) and the number of bases (Y) in the inner 3 ′ side region (Y) is not particularly limited, For example, any condition of the following formula may be satisfied.
- X Y (19) X ⁇ Y (20) X> Y (21)
- the number of bases (X) in the inner 5 ′ side region (X), the number of bases (Xc) in the 5 ′ side region (Xc), the number of bases in the inner 3 ′ side region (Y) satisfies, for example, the following conditions (a) to (d).
- (A) Satisfy the conditions of the following formulas (3) and (4). X> Xc (3) Y Yc (4)
- the difference between the number of bases (X) in the inner 5 ′ side region (X) and the number of bases (Xc) in the 5 ′ side region (Xc), the inner 3 ′ side region ( The difference between the number of bases (Y) of Y) and the number of bases (Yc) of the 3 ′ side region (Yc) preferably satisfies the following condition, for example.
- A The conditions of the following formulas (11) and (12) are satisfied.
- FIG. 3 shows ssNc containing the linker region (Lx) and the linker region (Ly), (A) is the ssNc molecule of (a), (B) is the ssNc molecule of (b), ( C) is an example of the ssNc molecule of (c), and (D) is an example of the ssNc molecule of (d).
- a dotted line shows the state which has formed the double chain
- FIG. 3 is merely the relationship between the inner 5 ′ side region (X) and the 5 ′ side region (Xc), and the relationship between the inner 3 ′ side region (Y) and the 3 ′ side region (Yc).
- the length and shape of each region are not limited thereto, and the presence or absence of the linker region (Lx) and the linker region (Ly) is not limited thereto.
- the ssNc molecules of (a) to (c) include, for example, the 5 ′ side region (Xc) and the inner 5 ′ side region (X), and the 3 ′ side region (Yc) and the inner 3 ′ side.
- the region (Y) has a base that cannot be aligned with any of the 5 ′ side region (Xc) and the 3 ′ side region (Yc) in the internal region (Z) by forming a double chain, respectively. It can be said that the structure has a base that does not form a double chain.
- the base that cannot be aligned also referred to as a base that does not form a double chain
- free base In FIG.
- the free base region is indicated by “F”.
- the number of bases in the region (F) is not particularly limited.
- the number of bases (F) in the region (F) is, for example, the number of bases “X—Xc” in the case of the ssNc molecule of (a), and “Y—Yc” in the case of the ssNc molecule of (b). In the case of the ssNc molecule of (c), it is the total number of bases “X-Xc” and “Y-Yc”.
- the ssNc molecule of (d) is, for example, a structure in which the entire region of the internal region (Z) is aligned with the 5 ′ side region (Xc) and the 3 ′ side region (Yc), It can also be said that the entire region (Z) forms a double chain.
- the 5 'end of the 5' side region (Xc) and the 3 'end of the 3' side region (Yc) are unlinked.
- the length of each region is exemplified below, but the present invention is not limited thereto.
- the numerical range of the number of bases discloses all positive integers belonging to the range.
- the description “1 to 4 bases” includes “1, 2, 3, 4 bases”. "Means all disclosures (the same applies hereinafter).
- the total number of bases of the free base (F) in the 5 ′ side region (Xc), the 3 ′ side region (Yc), and the internal region (Z) is, for example, the number of bases in the internal region (Z) It becomes.
- the lengths of the 5 ′ side region (Xc) and the 3 ′ side region (Yc) depend on, for example, the length of the internal region (Z), the number of free bases (F), and the position thereof. Can be determined as appropriate.
- the number of bases in the internal region (Z) is, for example, 19 bases or more.
- the lower limit of the number of bases is, for example, 19 bases, preferably 20 bases, and more preferably 21 bases.
- the upper limit of the number of bases is, for example, 50 bases, preferably 40 bases, and more preferably 30 bases.
- Specific examples of the number of bases in the internal region (Z) include, for example, 19 bases, 20 bases, 21 bases, 22 bases, 23 bases, 24 bases, 25 bases, 26 bases, 27 bases, 28 bases, 29 bases, or , 30 bases.
- the internal region (Z) may be, for example, a region composed only of the expression suppression sequence or a region including the expression suppression sequence.
- the number of bases in the expression suppressing sequence is, for example, 19 to 30 bases, and preferably 19, 20 or 21 bases.
- the internal region (Z) may further have an additional sequence on the 5 'side and / or 3' side of the expression suppression sequence.
- the number of bases of the additional sequence is, for example, 1 to 31 bases, preferably 1 to 21 bases, more preferably 1 to 11 bases, and further preferably 1 to 7 bases.
- the number of bases in the 5 ′ side region (Xc) is, for example, 1 to 29 bases, preferably 1 to 11 bases, more preferably 1 to 7 bases, and further preferably 1 to 4 bases. Particularly preferred are 1 base, 2 bases and 3 bases.
- the internal region (Z) or the 3 'side region (Yc) includes the expression suppression sequence, for example, such a base number is preferable.
- the number of bases in the internal region (Z) is 19 to 30 bases (for example, 19 bases)
- the number of bases in the 5 ′ side region (Xc) is, for example, 1 to 11 bases
- the number is preferably 1 to 7 bases, more preferably 1 to 4 bases, and still more preferably 1 base, 2 bases, and 3 bases.
- the 5′-side region (Xc) may be, for example, a region composed only of the expression suppression sequence, or a region including the expression suppression sequence But you can.
- the length of the expression suppression sequence is, for example, as described above.
- the 5 'region (Xc) contains the expression suppression sequence, it may further have an additional sequence on the 5' side and / or 3 'side of the expression suppression sequence.
- the number of bases of the additional sequence is, for example, 1 to 11 bases, and preferably 1 to 7 bases.
- the number of bases in the 3 ′ side region (Yc) is, for example, 1 to 29 bases, preferably 1 to 11 bases, more preferably 1 to 7 bases, and further preferably 1 to 4 bases. Particularly preferred are 1 base, 2 bases and 3 bases.
- the internal region (Z) or the 5 'side region (Xc) includes the expression suppression sequence, for example, such a base number is preferable.
- the number of bases in the internal region (Z) is 19 to 30 bases (for example, 19 bases)
- the number of bases in the 3 ′ side region (Yc) is, for example, 1 to 11 bases
- the number is preferably 1 to 7 bases, more preferably 1 to 4 bases, and still more preferably 1 base, 2 bases, and 3 bases.
- the 3 ′ side region (Yc) may be, for example, a region composed only of the expression suppression sequence, or a region including the expression suppression sequence But you can.
- the length of the expression suppression sequence is, for example, as described above.
- the 3 'side region (Yc) includes the expression suppression sequence, it may further have an additional sequence on the 5' side and / or 3 'side of the expression suppression sequence.
- the number of bases of the additional sequence is, for example, 1 to 11 bases, and preferably 1 to 7 bases.
- the number of bases in the internal region (Z), the 5′-side region (Xc), and the 3′-side region (Yc) is expressed by, for example, “Z ⁇ Xc + Yc” in the formula (2). Can do.
- the number of bases “Xc + Yc” is, for example, the same as or smaller than the inner region (Z).
- “Z ⁇ (Xc + Yc)” is, for example, 1 to 10, preferably 1 to 4, more preferably 1, 2 or 3.
- the “Z ⁇ (Xc + Yc)” corresponds to, for example, the number of bases (F) in the free base region (F) in the internal region (Z).
- the length of the linker region (Lx) and the linker region (Ly) is not particularly limited.
- the linker region (Lx) preferably has, for example, a length that allows the internal 5 ′ side region (X) and the 5 ′ side region (Xc) to form a double chain, and the linker region (Ly) ) Is, for example, preferably a length such that the inner 3 ′ side region (Y) and the 3 ′ side region (Yc) can form a double chain.
- the number of bases of the linker region (Lx) and the linker region (Ly) may be the same or different.
- the base sequence may be the same or different.
- the lower limit of the number of bases in the linker region (Lx) and the linker region (Ly) is, for example, 1 base, preferably 2 bases, more preferably 3 bases, and the upper limit thereof is, for example, 100 bases, preferably 80 bases, more preferably 50 bases.
- Specific examples of the number of bases in each linker region include 1 to 50 bases, 1 to 30 bases, 1 to 20 bases, 1 to 10 bases, 1 to 7 bases, and 1 to 4 bases. This is not a limitation.
- the total length of the ssNc molecule of the present invention is not particularly limited.
- the lower limit of the total number of bases (total number of bases) is, for example, 38 bases, preferably 42 bases, more preferably 50 bases, and even more preferably 51 bases.
- the upper limit is, for example, 300 bases, preferably 200 bases, more preferably 150 bases, still more preferably 100 bases, particularly preferably 80 bases. It is.
- the lower limit of the total number of bases excluding the linker region (Lx) and the linker region (Ly) is, for example, 38 bases, preferably 42 bases, more preferably 50 bases. Yes, more preferably 51 bases, particularly preferably 52 bases, and the upper limit is, for example, 300 bases, preferably 200 bases, more preferably 150 bases, still more preferably 100 bases Particularly preferred is 80 bases.
- the structural unit of the ssNc molecule of the present invention is not particularly limited, and examples thereof include nucleotide residues.
- the nucleotide residue include a ribonucleotide residue and a deoxyribonucleotide residue.
- the nucleotide residue include an unmodified unmodified nucleotide residue and a modified modified nucleotide residue.
- the ssNc molecule of the present invention can improve nuclease resistance and stability by including, for example, the modified nucleotide residue.
- the ssNc molecule of the present invention may further contain a non-nucleotide residue in addition to the nucleotide residue, for example. Details of the nucleotide residue and the non-nucleotide residue will be described later.
- each of the structural units of the internal region (Z), the 5 ′ side region (Xc) and the 3 ′ side region (Yc) is preferably the nucleotide residue.
- Each region is composed of the following residues (1) to (3), for example. (1) Unmodified nucleotide residue (2) Modified nucleotide residue (3) Unmodified nucleotide residue and modified nucleotide residue
- the structural units of the linker region (Lx) and the linker region (Ly) are not particularly limited, and examples thereof include the nucleotide residue and the non-nucleotide residue.
- the linker region may be composed of, for example, only the nucleotide residue, may be composed of only the non-nucleotide residue, or may be composed of the nucleotide residue and the non-nucleotide residue.
- the linker region is composed of the following residues (1) to (7), for example.
- both structural units may be the same or different.
- Specific examples include, for example, a form in which the constituent units of both linker regions are the nucleotide residues, a form in which the constituent units of both linker regions are the non-nucleotide residues, and the constituent units of one region are the nucleotide residues.
- the other linker region is a non-nucleotide residue.
- the ssNc molecule of the present invention examples include a molecule composed only of the nucleotide residue, a molecule containing the non-nucleotide residue in addition to the nucleotide residue, and the like.
- the nucleotide residue may be, for example, only the unmodified nucleotide residue, only the modified nucleotide residue, or the unmodified nucleotide residue and the modification. Both nucleotide residues may be present.
- the number of the modified nucleotide residue is not particularly limited, and is, for example, “one or several”, specifically For example, 1 to 5, preferably 1 to 4, more preferably 1 to 3, and most preferably 1 or 2.
- the number of the non-nucleotide residue is not particularly limited, and is, for example, “one or several”, specifically, for example, 1 to Eight, one to six, one to four, one, two or three.
- the nucleotide residue is preferably, for example, a ribonucleotide residue.
- the ssNc molecule of the present invention is also referred to as “RNA molecule” or “ssRNA molecule”, for example.
- RNA molecule or “ssRNA molecule”
- examples of the ssRNA molecule include a molecule composed only of the ribonucleotide residue, and a molecule containing the non-nucleotide residue in addition to the ribonucleotide residue.
- the ribonucleotide residue may be, for example, only the unmodified ribonucleotide residue, only the modified ribonucleotide residue, or the unmodified ribonucleotide residue and Both of the modified ribonucleotide residues may be included.
- the number of the modified ribonucleotide residue is not particularly limited. For example, “1 or several” Specifically, for example, 1 to 5, preferably 1 to 4, more preferably 1 to 3, and most preferably 1 or 2.
- the modified ribonucleotide residue relative to the unmodified ribonucleotide residue may be, for example, the deoxyribonucleotide residue in which a ribose residue is replaced with a deoxyribose residue.
- the number of the deoxyribonucleotide residue is not particularly limited, and is, for example, “one or several”. Specifically, for example, 1 to 5, preferably 1 to 4, more preferably 1 to 3, and most preferably 1 or 2.
- the ssNc molecule of the present invention may contain, for example, a labeling substance and may be labeled with the labeling substance.
- the labeling substance is not particularly limited, and examples thereof include fluorescent substances, dyes, isotopes and the like.
- the labeling substance include fluorophores such as pyrene, TAMRA, fluorescein, Cy3 dye, and Cy5 dye, and examples of the dye include Alexa dye such as Alexa488.
- the isotope include a stable isotope and a radioactive isotope, and preferably a stable isotope.
- the stable isotope has a low risk of exposure and does not require a dedicated facility, so that it is easy to handle and the cost can be reduced.
- the stable isotope does not change the physical properties of the labeled compound, for example, and is excellent in properties as a tracer.
- the stable isotope is not particularly limited, and examples thereof include 2 H, 13 C, 15 N, 17 O, 18 O, 33 S, 34 S, and 36 S.
- the ssNc molecule of the present invention can suppress the expression of the target gene. Therefore, the ssNc molecule of the present invention can be used as a therapeutic agent for diseases caused by genes, for example.
- the ssNc molecule of the present invention includes, for example, a sequence that suppresses the expression of a gene causing the disease as the expression suppression sequence, the disease can be treated by suppressing the expression of the target gene, for example.
- “treatment” includes, for example, the meanings of preventing the disease, improving the disease, and improving the prognosis.
- the method of using the ssNc molecule of the present invention is not particularly limited, and for example, the ssNc molecule may be administered to an administration subject having the target gene.
- Examples of the administration target include cells, tissues or organs.
- Examples of the administration subject include non-human animals such as humans and non-human mammals other than humans.
- the administration may be, for example, in vivo or in vitro.
- the cells are not particularly limited, and examples thereof include various cultured cells such as HeLa cells, 293 cells, NIH3T3 cells, and COS cells, stem cells such as ES cells and hematopoietic stem cells, and cells isolated from living bodies such as primary cultured cells. can give.
- the target gene to be subject to expression suppression is not particularly limited, and a desired gene can be set. Then, as described above, the expression suppression sequence may be appropriately designed according to the type of the target gene.
- the present invention is not limited thereto.
- the base sequence of the ssNc molecule include the base sequences of SEQ ID NOs: 2, 7, 8, 13, 14, 29-35, 37, 43, 44, 47, 48, and 51-80. In the sequence, for example, it may be a base sequence in which one or several deletions, substitutions and / or additions are made.
- the target gene is a GAPDH gene, for example, the nucleotide sequences of SEQ ID NOs: 2, 7, 8, 13, 37, and 51-80 are listed.
- the target gene is TGF- ⁇ 1, for example, SEQ ID NOs: 14 and 29-
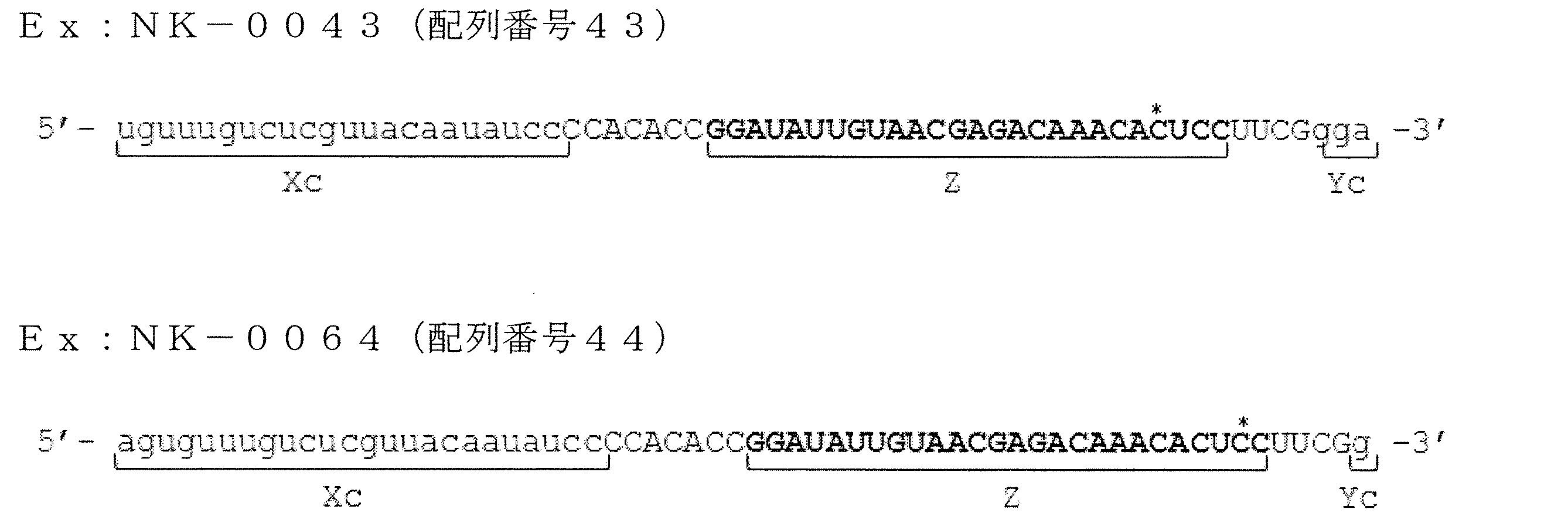
- the target gene is the LAMA1 gene, for example, the base sequences of SEQ ID NOS: 43 and 44 are listed.
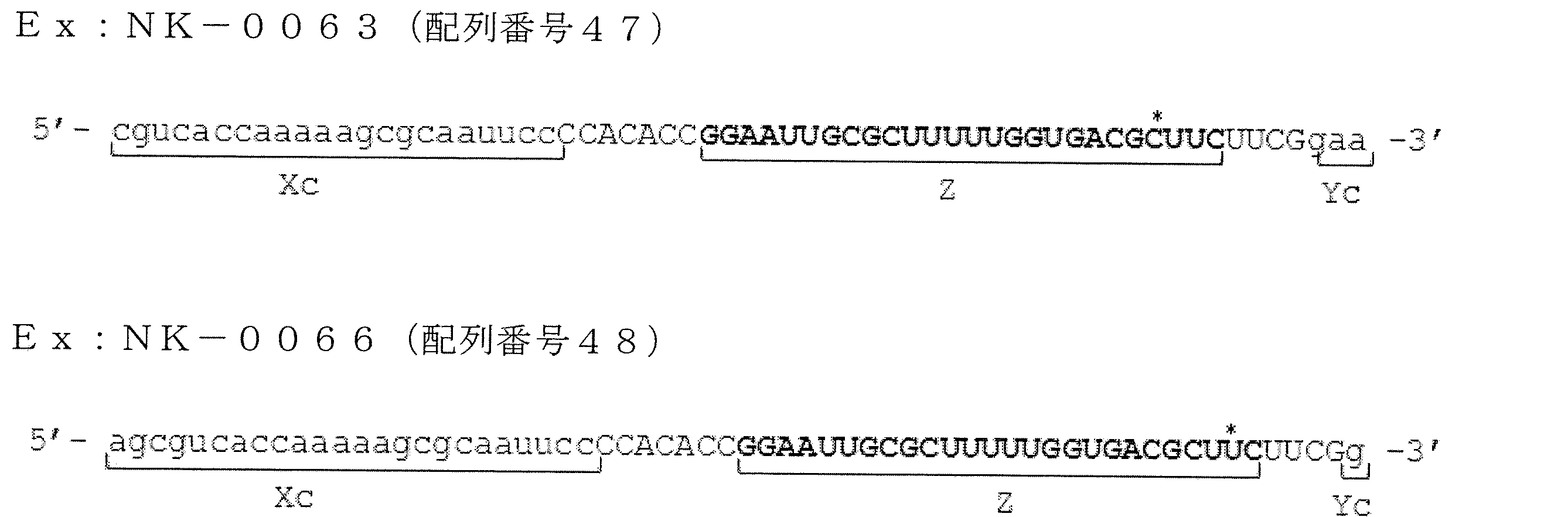
- the target gene is the LMNA gene, for example, the base sequences of SEQ ID NOS: 47 and 48 are listed. Can be given.
- the ssNc molecule of the present invention can suppress the expression of a target gene as described above, it is useful as a research tool for, for example, pharmaceuticals, diagnostic agents and agricultural chemicals, and agricultural chemicals, medicine, and life sciences.
- nucleotide residues include, for example, sugars, bases and phosphates as constituent elements.
- examples of the nucleotide residue include a ribonucleotide residue and a deoxyribonucleotide residue as described above.
- the ribonucleotide residue has, for example, a ribose residue as a sugar, and has adenine (A), guanine (G), cytosine (C) and U (uracil) as bases
- the deoxyribose residue is For example, it has a deoxyribose residue as a sugar and has adenine (A), guanine (G), cytosine (C) and thymine (T) as bases.
- the nucleotide residue includes an unmodified nucleotide residue and a modified nucleotide residue.
- each of the constituent elements is, for example, the same or substantially the same as that existing in nature, and preferably the same or substantially the same as that naturally occurring in the human body. .
- the modified nucleotide residue is, for example, a nucleotide residue obtained by modifying the unmodified nucleotide residue.
- the modified nucleotide residue for example, any of the constituent elements of the unmodified nucleotide residue may be modified.
- “modification” refers to, for example, substitution, addition and / or deletion of the component, substitution, addition and / or deletion of atoms and / or functional groups in the component, and is referred to as “modification”. be able to.
- modified nucleotide residue include naturally occurring nucleotide residues, artificially modified nucleotide residues, and the like. For example, Limbac et al.
- modified nucleosides of RNA Nucleic Acids Res. 22: 2183-2196
- the modified nucleotide residue may be, for example, a residue of the nucleotide substitute.
- ribophosphate skeleton examples include modification of a ribose-phosphate skeleton (hereinafter referred to as ribophosphate skeleton).
- a ribose residue can be modified.
- the ribose residue can be modified, for example, at the 2′-position carbon.
- a hydroxyl group bonded to the 2′-position carbon can be replaced with hydrogen or a halogen such as fluoro.
- the ribose residue can be replaced with deoxyribose.
- the ribose residue can be substituted with, for example, a stereoisomer, and can be substituted with, for example, an arabinose residue.
- the ribophosphate skeleton may be substituted with a non-ribophosphate skeleton having a non-ribose residue and / or non-phosphate, for example.
- the non-ribophosphate skeleton include uncharged ribophosphate skeletons.
- the substitute for the nucleotide substituted with the non-ribophosphate skeleton include morpholino, cyclobutyl, pyrrolidine and the like.
- Other examples of the substitute include artificial nucleic acid monomer residues. Specific examples include PNA (peptide nucleic acid), LNA (Locked Nucleic Acid), ENA (2'-O, 4'-C-Ethylenebridged Nucleic Acid), and PNA is preferable.
- a phosphate group can be modified.
- the phosphate group closest to the sugar residue is called an ⁇ -phosphate group.
- the ⁇ -phosphate group is negatively charged, and the charge is evenly distributed over two oxygen atoms that are not bound to a sugar residue.
- the four oxygen atoms in the ⁇ -phosphate group in the phosphodiester bond between nucleotide residues, the two oxygen atoms that are non-bonded to the sugar residue are hereinafter referred to as “non-linking oxygen”.
- the two oxygen atoms bonded to the sugar residue are hereinafter referred to as “linking oxygen”.
- the ⁇ -phosphate group is preferably subjected to, for example, a modification that makes it uncharged or a modification that makes the charge distribution in the unbound oxygen asymmetric.
- the phosphate group may replace the non-bonded oxygen, for example.
- the oxygen is, for example, one of S (sulfur), Se (selenium), B (boron), C (carbon), H (hydrogen), N (nitrogen), and OR (R is an alkyl group or an aryl group).
- R is an alkyl group or an aryl group.
- the non-bonded oxygen for example, both are preferably substituted, and more preferably, both are substituted with S.
- the modified phosphate group include phosphorothioate, phosphorodithioate, phosphoroselenate, boranophosphate, boranophosphate ester, phosphonate hydrogen, phosphoramidate, alkyl or arylphosphonate, and phosphotriester. Among them, phosphorodithioate in which the two non-bonded oxygens are both substituted with S is preferable.
- the phosphate group may substitute, for example, the bonded oxygen.
- the oxygen can be substituted with any atom of S (sulfur), C (carbon) and N (nitrogen), for example.
- Examples of the modified phosphate group include a bridged phosphoramidate substituted with N, a bridged phosphorothioate substituted with S, and a bridged methylenephosphonate substituted with C.
- the binding oxygen substitution is preferably performed, for example, on at least one of the 5 ′ terminal nucleotide residue and the 3 ′ terminal nucleotide residue of the ssNc molecule of the present invention, and in the case of the 5 ′ side, substitution with C is preferable. For the 'side, substitution with N is preferred.
- the phosphate group may be substituted with, for example, the phosphorus-free linker.
- the linker include siloxane, carbonate, carboxymethyl, carbamate, amide, thioether, ethylene oxide linker, sulfonate, sulfonamide, thioformacetal, formacetal, oxime, methyleneimino, methylenemethylimino, methylenehydrazo, and methylenedimethyl. Hydrazo, methyleneoxymethylimino and the like, preferably methylenecarbonylamino group and methylenemethylimino group.
- the ssNc molecule of the present invention for example, at least one nucleotide residue at the 3 'end and the 5' end may be modified.
- the modification may be, for example, either the 3 'end or the 5' end, or both.
- the modification is, for example, as described above, and is preferably performed on the terminal phosphate group.
- the phosphate group may be modified entirely, or one or more atoms in the phosphate group may be modified. In the former case, for example, the entire phosphate group may be substituted or deleted.
- Examples of the modification of the terminal nucleotide residue include addition of other molecules.
- Examples of the other molecule include functional molecules such as a labeling substance and a protecting group as described above.
- Examples of the protecting group include S (sulfur), Si (silicon), B (boron), ester-containing groups, and the like.
- the functional molecule such as the labeling substance can be used for, for example, detection of the ssNc molecule of the present invention.
- the other molecule may be added to the phosphate group of the nucleotide residue, for example, or may be added to the phosphate group or the sugar residue via a spacer.
- the terminal atom of the spacer can be added or substituted, for example, to the binding oxygen of the phosphate group or O, N, S or C of the sugar residue.
- the binding site of the sugar residue is preferably, for example, C at the 3 'position or C at the 5' position, or an atom bonded thereto.
- the spacer can be added or substituted at a terminal atom of a nucleotide substitute such as PNA.
- the spacer is not particularly limited.
- n is a positive integer
- n 3 or 6 is preferable.
- the molecule to be added to the terminal includes, for example, a dye, an intercalating agent (for example, acridine), a crosslinking agent (for example, psoralen, mitomycin C), a porphyrin (TPPC4, texaphyrin, suffirin), a polycyclic Aromatic hydrocarbons (eg phenazine, dihydrophenazine), artificial endonucleases (eg EDTA), lipophilic carriers (eg cholesterol, cholic acid, adamantaneacetic acid, 1-pyrenebutyric acid, dihydrotestosterone, 1,3-bis- O (hexadecyl) glycerol, geranyloxyhexyl group, hexadecylglycerol, borneol, menthol, 1,3-propanediol, heptadecyl group, palmitic acid, myristic acid, O3- (oleoy
- the 5 ′ end may be modified with, for example, a phosphate group or a phosphate group analog.
- the phosphate group is, for example, 5 ′ monophosphate ((HO) 2 (O) PO-5 ′), 5 ′ diphosphate ((HO) 2 (O) POP (HO) (O) —O— 5 '), 5' triphosphate ((HO) 2 (O) PO- (HO) (O) POP (HO) (O) -O-5 '), 5'-guanosine cap (7-methylated or Unmethylated, 7m-GO-5 '-(HO) (O) PO- (HO) (O) POP (HO) (O) -O-5'), 5'-adenosine cap (Appp), optional Modified or unmodified nucleotide cap structure (NO-5 '-(HO) (O) PO- (HO) (O) POP (HO) (O) -O-5'), 5 'monophosphate (NO-5 '-(HO
- the base is not particularly limited.
- the base may be, for example, a natural base or a non-natural base.
- the base may be, for example, naturally derived or a synthetic product.
- As the base for example, a general base or a modified analog thereof can be used.
- Examples of the base include purine bases such as adenine and guanine, and pyrimidine bases such as cytosine, uracil and thymine.
- Other examples of the base include inosine, thymine, xanthine, hypoxanthine, nubalarine, isoguanisine, and tubercidine.
- the base examples include alkyl derivatives such as 2-aminoadenine and 6-methylated purine; alkyl derivatives such as 2-propylated purine; 5-halouracil and 5-halocytosine; 5-propynyluracil and 5-propynylcytosine; -Azouracil, 6-azocytosine and 6-azothymine; 5-uracil (pseudouracil), 4-thiouracil, 5-halouracil, 5- (2-aminopropyl) uracil, 5-aminoallyluracil; 8-halogenated, aminated, Thiolated, thioalkylated, hydroxylated and other 8-substituted purines; 5-trifluoromethylated and other 5-substituted pyrimidines; 7-methylguanine; 5-substituted pyrimidines; 6-azapyrimidines; N-2, N -6 and O-6 substituted purines (2-aminopropyladenyl 5-
- the modified nucleotide residue may include, for example, a residue lacking a base, that is, an abasic ribophosphate skeleton.
- the modified nucleotide residues are, for example, US Provisional Application No. 60 / 465,665 (filing date: April 25, 2003) and International Application No. PCT / US04 / 07070 (filing date: 2004/3). The residues described on the 8th of May) can be used, and the present invention can incorporate these documents.
- Non-nucleotide residue is not particularly limited.
- the ssNc molecule of the present invention may have, for example, a non-nucleotide structure containing a pyrrolidine skeleton or a piperidine skeleton as the non-nucleotide residue.
- the non-nucleotide residue is preferably present in at least one of the linker region (Lx) and the linker region (Ly).
- the non-nucleotide residue may be included in the linker region (Lx), may be included in the linker region (Ly), or may be included in both the linker regions.
- the linker region (Lx) and the linker region (Ly) may be the same or different, for example.
- the pyrrolidine skeleton may be, for example, a skeleton of a piperidine derivative in which one or more carbons constituting the five-membered ring of pyrrolidine are substituted.
- a carbon atom other than C-2 carbon is used. It is preferable.
- the carbon may be substituted with, for example, nitrogen, oxygen, or sulfur.
- the pyrrolidine skeleton may include, for example, a carbon-carbon double bond or a carbon-nitrogen double bond in the 5-membered ring of pyrrolidine.
- the carbon and nitrogen constituting the 5-membered ring of pyrrolidine may be bonded to, for example, a hydrogen group or a substituent as described later.
- the linker region (Lx) may be bonded to the region (X) and the region (Xc) through, for example, any group of the pyrrolidine skeleton, preferably any one of the 5-membered rings Carbon atoms and nitrogen, preferably carbon (C-2) and nitrogen at the 2-position of the 5-membered ring.
- Examples of the pyrrolidine skeleton include a proline skeleton and a prolinol skeleton.
- the proline skeleton, prolinol skeleton, and the like are excellent in safety because they are, for example, in-vivo substances and their reduced forms.
- the piperidine skeleton may be, for example, a skeleton of a piperidine derivative in which one or more carbons constituting the six-membered ring of piperidine are substituted, and when substituted, for example, a carbon atom other than C-2 carbon. It is preferable.
- the carbon may be substituted with, for example, nitrogen, oxygen, or sulfur.
- the piperidine skeleton may contain, for example, a carbon-carbon double bond or a carbon-nitrogen double bond in the six-membered ring of piperidine.
- the carbon and nitrogen constituting the piperidine 6-membered ring may be bonded to, for example, a hydrogen group or a substituent as described later.
- the linker region (Lx) may be bonded to the region (X) and the region (Xc), for example, via any group of the piperidine skeleton, and preferably any one of the six-membered rings Of the 6-membered ring, and carbon (C-2) and nitrogen are preferred. The same applies to the linker region (Ly).
- the linker region may be, for example, only a non-nucleotide residue consisting of the non-nucleotide structure, or may include a non-nucleotide residue consisting of the non-nucleotide structure and a nucleotide residue.
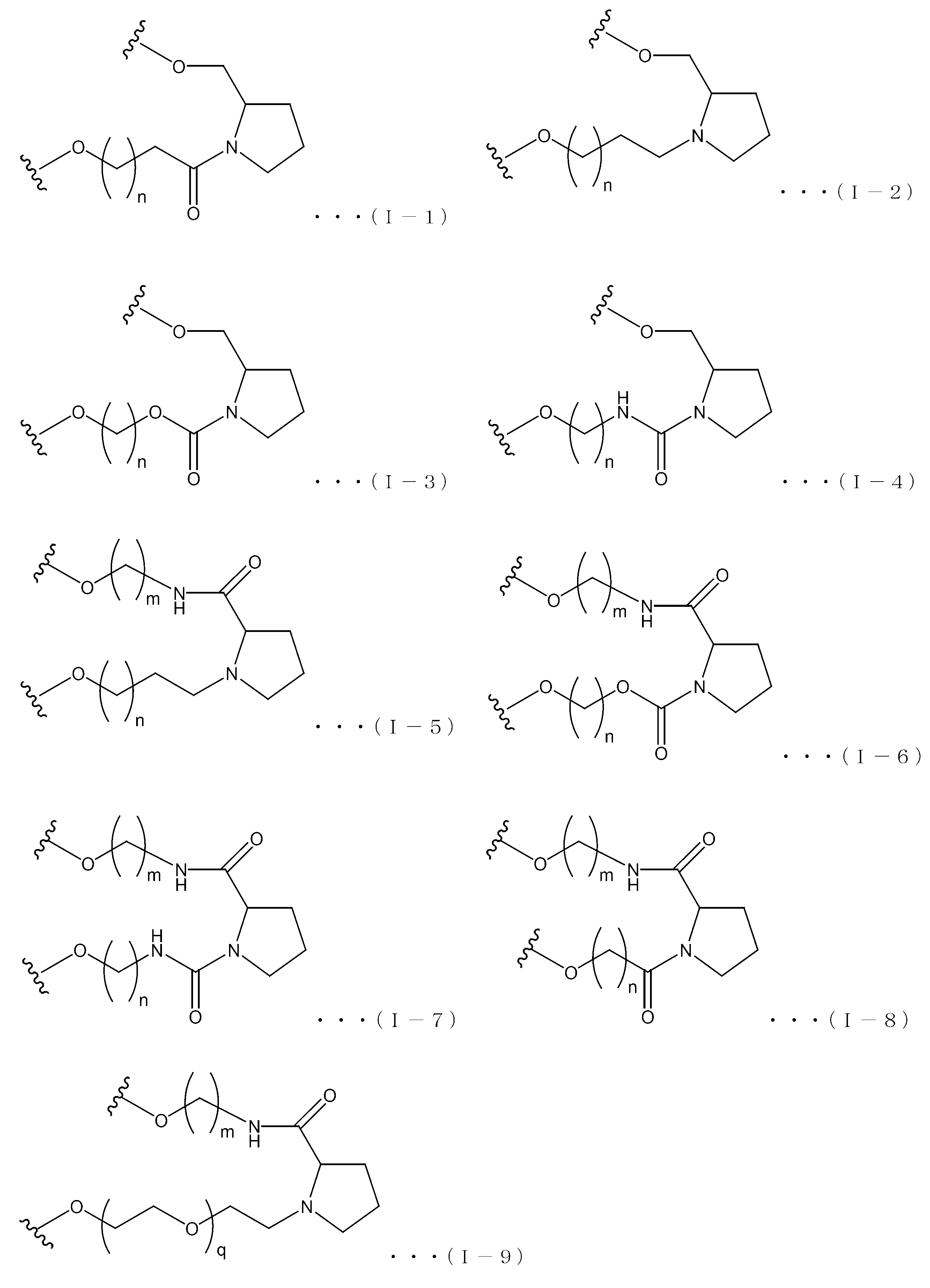
- the linker region is represented by the following formula (I), for example.
- X 1 and X 2 are each independently H 2 , O, S or NH; Y 1 and Y 2 are each independently a single bond, CH 2 , NH, O or S; R 3 is a hydrogen atom or substituent bonded to C-3, C-4, C-5 or C-6 on ring A; The substituent is OH, OR 4 , NH 2 , NHR 4 , NR 4 R 5 , SH, SR 4 or an oxo group ( ⁇ O); When R 3 is the substituent, the substituent R 3 may be one, plural or absent, and in plural cases, may be the same or different; R 4 and R 5 are substituents or protecting groups and may be the same or different; L 1 is an alkylene chain consisting of n atoms, wherein the hydrogen atom on the alkylene carbon atom is substituted with OH, OR a , NH 2 , NHR a , NR a R b , SH or SR a May not be substituted,
- the ring A may contain a carbon-carbon double bond or a carbon-nitrogen double bond.
- linker region (Lx) is represented by the formula (1)
- the region (Xc) and the region (X) are each linked to the linker region (Lx) via —OR 1 — or —OR 2 —.
- the linker region (Ly) is represented by the formula (1)
- the region (Yc) and the region (Y) are each linked to the linker region via —OR 1 — or —OR 2 —. It binds to (Ly).
- R 1 and R 2 may be present or absent, and when present, R 1 and R 2 are each independently a nucleotide residue or the structure (I).
- X 1 and X 2 are each independently, for example, H 2 , O, S or NH.
- X 1 being H 2 means that X 1 together with the carbon atom to which X 1 is bonded forms CH 2 (methylene group). The same is true for X 2.
- l 1 or 2.
- ring A is a 5-membered ring, for example, the pyrrolidine skeleton.
- the pyrrolidine skeleton include a proline skeleton and a prolinol skeleton, and examples thereof include a bivalent structure.
- ring A is a 6-membered ring, for example, the piperidine skeleton.
- one carbon atom other than C-2 on ring A may be substituted with nitrogen, oxygen or sulfur.
- Ring A may contain a carbon-carbon double bond or a carbon-nitrogen double bond in ring A.
- Ring A may be, for example, either L-type or D-type.
- Y 1 and Y 2 are each independently a single bond, CH 2 , NH, O or S.
- R 3 is a hydrogen atom or a substituent bonded to C-3, C-4, C-5 or C-6 on the ring A.
- the substituent is OH, OR 4 , NH 2 , NHR 4 , NR 4 R 5 , SH, SR 4 or an oxo group ( ⁇ O).
- R 3 is the above-described substituent, the substituent R 3 may be one, plural, or absent, and when plural, it may be the same or different.
- R 4 and R 5 are substituents or protecting groups, and may be the same or different.
- substituents examples include halogen, alkyl, alkenyl, alkynyl, haloalkyl, aryl, heteroaryl, arylalkyl, cycloalkyl, cycloalkenyl, cycloalkylalkyl, cyclylalkyl, hydroxyalkyl, alkoxyalkyl, aminoalkyl, heterocyclylalkenyl. , Heterocyclylalkyl, heteroarylalkyl, silyl, silyloxyalkyl and the like. The same applies hereinafter.
- the protecting group is, for example, a functional group that converts a highly reactive functional group to inert, and examples thereof include known protecting groups.
- the description of the literature J. F. W. McOmie, “Protecting Groups in Organic Chemistry”, Prenum Press, London and New York, 1973) can be cited as the protecting group.
- the protecting group is not particularly limited, and examples thereof include tert-butyldimethylsilyl (TBDMS) group, bis (2-acetoxyethyloxy) methyl (ACE) group, triisopropylsilyloxymethyl (TOM) group, 1- (2 -Cyanoethoxy) ethyl (CEE) group, 2-cyanoethoxymethyl (CEM) group and tolylsulfonylethoxymethyl (TEM) group, dimethoxytrityl (DMTr) and the like.
- TDMS tert-butyldimethylsilyl
- ACE (2-acetoxyethyloxy) methyl
- TOM triisopropylsilyloxymethyl
- CEE 2-Cyanoethoxymethyl
- CEM 2-cyanoethoxymethyl
- TEM dimethoxytrityl
- the protecting group is not particularly limited, and examples thereof include a TBDMS group, an ACE group, a TOM group, a CEE group, a CEM group, and a TEM group.
- silyl-containing groups described later are also included. The same applies hereinafter.
- L 1 is an alkylene chain composed of n atoms.
- the hydrogen atom on the alkylene carbon atom may be substituted with, for example, OH, OR a , NH 2 , NHR a , NR a R b , SH or SR a , or may not be substituted.
- L 1 may be a polyether chain in which one or more carbon atoms of the alkylene chain are substituted with an oxygen atom.
- the polyether chain is, for example, polyethylene glycol.
- L 2 is an alkylene chain composed of m atoms.
- the hydrogen atom on the alkylene carbon atom may be substituted with, for example, OH, OR c , NH 2 , NHR c , NR c R d , SH or SR c , or may not be substituted.
- L 2 may be a polyether chain in which one or more carbon atoms of the alkylene chain are substituted with an oxygen atom.
- Y 2 is NH, O or S
- the L 2 atom bonded to Y 2 is carbon
- the L 2 atom bonded to OR 2 is carbon
- oxygen atoms are not adjacent to each other. That is, for example, when Y 2 is O, the oxygen atom and the oxygen atom of L 2 are not adjacent, and the oxygen atom of OR 2 and the oxygen atom of L 2 are not adjacent.
- N in L 1 and m in L 2 are not particularly limited, and the lower limit is, for example, 0, and the upper limit is not particularly limited.
- n and m can be appropriately set depending on, for example, the desired length of the linker region (Lx).
- n and m are each preferably 0 to 30, more preferably 0 to 20, and still more preferably 0 to 15 from the viewpoint of production cost and yield.
- n + m is, for example, 0 to 30, preferably 0 to 20, and more preferably 0 to 15.
- R a , R b , R c and R d are each independently a substituent or a protecting group.
- the substituent and the protecting group are the same as described above, for example.
- hydrogen atoms may be independently substituted with halogens such as Cl, Br, F and I, for example.
- the linker region (Lx) is represented by the formula (I)
- the region (Xc) and the region (X) are, for example, linked to the linker via —OR 1 — or —OR 2 —, respectively.
- R 1 and R 2 may or may not exist.
- R 1 and R 2 are each independently a nucleotide residue or the structure of formula (I) above.
- the linker region (Lx) is, for example, the non-nucleotide residue having the structure of the formula (I) excluding the nucleotide residue R 1 and / or R 2. And a nucleotide residue.
- the linker region (Lx) has, for example, two or more non-nucleotide residues having the structure of the formula (I) linked to each other. It becomes a structure.
- the structure of the formula (I) may include 1, 2, 3, or 4, for example.
- the linker region (Lx) is formed only from the non-nucleotide residue having the structure of the formula (I), for example.
- the linker region (Ly) is represented by the formula (I), for example, the region (Yc), the region (Y), and the linker region (Ly) are described in the linker region (Lx). Can be used.
- the combination of the region (Xc) and the region (X), the region (Yc) and the region (Y), and the —OR 1 — and —OR 2 — is not particularly limited.
- One of the following conditions can be given.
- Condition (1) The region (Xc) is bonded to the structure of the formula (I) through —OR 2 —, and the region (X) is bonded through —OR 1 —.
- the region (Yc) is bonded to the structure of the formula (I) through —OR 1 —, and the region (Y) is bonded through —OR 2 —.
- Condition (2) The region (Xc) is bonded to the structure of the formula (I) through —OR 2 —, and the region (X) is bonded through —OR 1 —.
- the region (Yc) is bonded to the structure of the formula (I) through —OR 2 —, and the region (Y) is bonded through —OR 1 —.
- Condition (3) The region (Xc) is bonded to the structure of the formula (I) through —OR 1 —, and the region (X) is bonded through —OR 2 —.
- the region (Yc) is bonded to the structure of the formula (I) through —OR 1 —, and the region (Y) is bonded through —OR 2 —.
- Condition (4) The region (Xc) is bonded to the structure of the formula (I) through —OR 1 —, and the region (X) is bonded through —OR 2 —.
- the region (Yc) is bonded to the structure of the formula (I) through —OR 2 —, and the region (Y) is bonded through —OR 1 —.
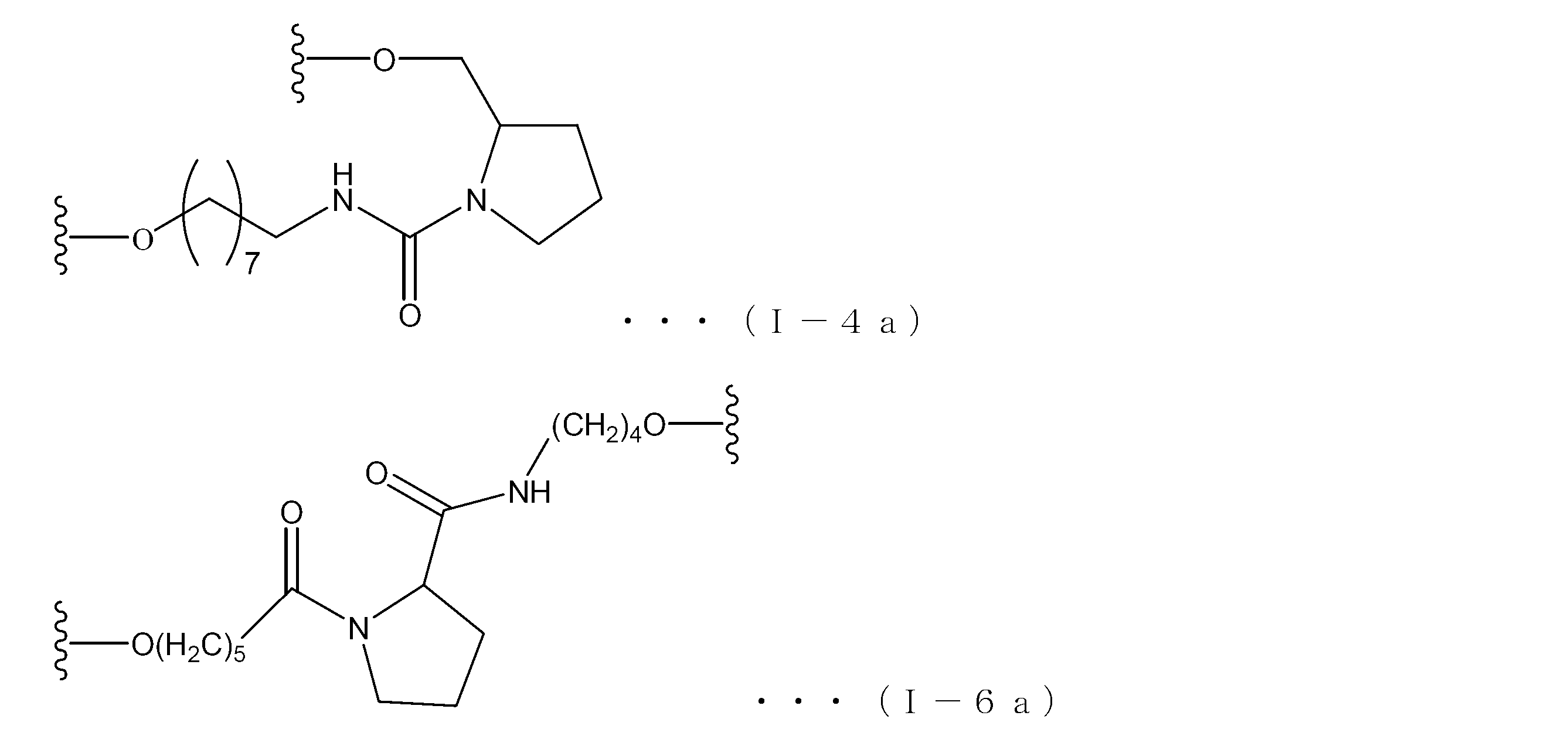
- Examples of the structure of the formula (I) include the following formulas (I-1) to (I-9), in which n and m are the same as those in the formula (I).
- q is an integer of 0 to 10.
- n, m and q are not particularly limited and are as described above.
- alkyl includes, for example, a linear or branched alkyl group.
- the number of carbon atoms of the alkyl is not particularly limited, and is, for example, 1 to 30, preferably 1 to 6 or 1 to 4.
- Examples of the alkyl group include methyl, ethyl, n-propyl, isopropyl, n-butyl, isobutyl, sec-butyl, tert-butyl, n-pentyl, isopentyl, neopentyl, n-hexyl, isohexyl, n-heptyl, Examples thereof include n-octyl, n-nonyl, n-decyl and the like.
- Preferred examples include methyl, ethyl, n-propyl, isopropyl, n-butyl, isobutyl, sec-butyl, tert-butyl, n-pentyl, isopentyl, neopentyl, n-hexyl, isohexyl and the like.
- alkenyl includes, for example, linear or branched alkenyl.
- alkenyl include those having one or more double bonds in the alkyl.
- the number of carbon atoms of the alkenyl is not particularly limited, and is the same as, for example, the alkyl, preferably 2 to 8.
- alkenyl include vinyl, 1-propenyl, 2-propenyl, 1-butenyl, 2-butenyl, 3-butenyl, 1,3-butadienyl, 3-methyl-2-butenyl and the like.
- alkynyl includes, for example, linear or branched alkynyl.
- alkynyl include those having one or more triple bonds in the alkyl.
- the number of carbon atoms of the alkynyl is not particularly limited, and is the same as, for example, the alkyl, preferably 2 to 8.
- examples of the alkynyl include ethynyl, propynyl, butynyl and the like.
- the alkynyl may further have one or more double bonds, for example.
- aryl includes, for example, a monocyclic aromatic hydrocarbon group and a polycyclic aromatic hydrocarbon group.
- the monocyclic aromatic hydrocarbon group include phenyl and the like.
- the polycyclic aromatic hydrocarbon group include 1-naphthyl, 2-naphthyl, 1-anthryl, 2-anthryl, 9-anthryl, 1-phenanthryl, 2-phenanthryl, 3-phenanthryl, 4-phenanthryl, 9- Examples include phenanthryl.
- Preferable examples include naphthyl such as phenyl, 1-naphthyl and 2-naphthyl.
- heteroaryl includes, for example, a monocyclic aromatic heterocyclic group and a condensed aromatic heterocyclic group.
- heteroaryl include furyl (eg, 2-furyl, 3-furyl), thienyl (eg, 2-thienyl, 3-thienyl), pyrrolyl (eg, 1-pyrrolyl, 2-pyrrolyl, 3-pyrrolyl), Imidazolyl (eg, 1-imidazolyl, 2-imidazolyl, 4-imidazolyl), pyrazolyl (eg, 1-pyrazolyl, 3-pyrazolyl, 4-pyrazolyl), triazolyl (eg, 1,2,4-triazol-1-yl, 1,2,4-triazol-3-yl, 1,2,4-triazol-4-yl), tetrazolyl (eg 1-tetrazolyl, 2-tetrazolyl, 5-tetrazolyl), oxazolyl (eg 2-
- cycloalkyl is, for example, a cyclic saturated hydrocarbon group, and the number of carbons is, for example, 3-15.
- the cycloalkyl include cyclopropyl, cyclobutyl, cyclopentyl, cyclohexyl, cycloheptyl, cyclooctyl, a bridged cyclic hydrocarbon group, a spiro hydrocarbon group, and the like, preferably cyclopropyl, cyclobutyl, cyclopentyl, cyclohexyl. And a bridged cyclic hydrocarbon group.
- the “bridged cyclic hydrocarbon group” includes, for example, bicyclo [2.1.0] pentyl, bicyclo [2.2.1] heptyl, bicyclo [2.2.2] octyl and bicyclo [3. 2.1] octyl, tricyclo [2.2.1.0] heptyl, bicyclo [3.3.1] nonane, 1-adamantyl, 2-adamantyl and the like.
- examples of the “spiro hydrocarbon group” include spiro [3.4] octyl and the like.
- cycloalkenyl includes, for example, a cyclic unsaturated aliphatic hydrocarbon group, and has, for example, 3 to 7 carbon atoms.
- examples of the group include cyclopropenyl, cyclobutenyl, cyclopentenyl, cyclohexenyl, cycloheptenyl, and the like, preferably cyclopropenyl, cyclobutenyl, cyclopentenyl, cyclohexenyl, and the like.
- the cycloalkenyl includes, for example, a bridged cyclic hydrocarbon group and a spiro hydrocarbon group having an unsaturated bond in the ring.
- arylalkyl includes, for example, benzyl, 2-phenethyl, naphthalenylmethyl and the like
- cycloalkylalkyl or “cyclylalkyl” includes, for example, cyclohexylmethyl, adamantylmethyl and the like.
- hydroxyalkyl include hydroxymethyl and 2-hydroxyethyl.
- alkoxy includes the alkyl-O— group, and examples thereof include methoxy, ethoxy, n-propoxy, isopropoxy, and n-butoxy.
- Alkoxyalkyl includes, for example, methoxymethyl
- aminoalkyl include 2-aminoethyl and the like.
- heterocyclyl is, for example, 1-pyrrolinyl, 2-pyrrolinyl, 3-pyrrolinyl, 1-pyrrolidinyl, 2-pyrrolidinyl, 3-pyrrolidinyl, pyrrolidinone, 1-imidazolinyl, 2-imidazolinyl, 4-imidazolinyl, 1 -Imidazolidinyl, 2-imidazolidinyl, 4-imidazolidinyl, imidazolidinone, 1-pyrazolinyl, 3-pyrazolinyl, 4-pyrazolinyl, 1-pyrazolidinyl, 3-pyrazolidinyl, 4-pyrazolidinyl, piperidinone, piperidinyl, 2-piperidinyl 4-piperidinyl, 1-piperazinyl, 2-piperazinyl, piperazinone, 2-morpholinyl, 3-morpholinyl, morpholino, tetrahydropyranyl, tetra
- heterocyclylalkyl includes, for example, piperidinylmethyl, piperazinylmethyl and the like
- heterocyclylalkenyl includes, for example, 2-piperidinylethenyl and the like
- heteroarylalkyl Examples include pyridylmethyl and quinolin-3-ylmethyl.
- sil includes a group represented by the formula R 3 Si—, and R can be independently selected from the above alkyl, aryl and cycloalkyl, for example, trimethylsilyl group, tert-butyldimethylsilyl
- the “silyloxy” includes, for example, a trimethylsilyloxy group
- the “silyloxyalkyl” includes, for example, trimethylsilyloxymethyl.
- alkylene includes, for example, methylene, ethylene, propylene and the like.
- the various groups described above may be substituted.
- substituents include hydroxy, carboxy, halogen, alkyl halide (eg, CF 3 , CH 2 CF 3 , CH 2 CCl 3 ), nitro, nitroso, cyano, alkyl (eg, methyl, ethyl, isopropyl, tert -Butyl), alkenyl (eg vinyl), alkynyl (eg ethynyl), cycloalkyl (eg cyclopropyl, adamantyl), cycloalkylalkyl (eg cyclohexylmethyl, adamantylmethyl), cycloalkenyl (eg cyclopropenyl) , Aryl (eg phenyl, naphthyl), arylalkyl (eg benzyl, phenethyl), heteroaryl (eg pyridyl, furyl), hetero
- alkoxy e.g. OCF 3
- alkenyloxy e.g. vinyloxy, allyloxy
- aryloxy e.g. phenyloxy
- alkyloxycarbonyl eg : Methoxycarbonyl, ethoxycarbonyl, tert-butoxycarbonyl
- arylalkyloxy eg, benzyloxy
- amino [alkylamino eg, methylamino, ethylamino, dimethylamino
- acylamino eg, acetylamino, benzoylamino
- Arylalkylamino eg benzylamino, tritylamino
- hydroxyamino] alkylaminoalkyl eg diethylaminomethyl
- sulfamoyl oxo and the like.
- Method for synthesizing ssNc molecule of the present invention is not particularly limited, and conventionally known methods can be adopted.
- the synthesis method include a synthesis method using a genetic engineering technique, a chemical synthesis method, and the like.
- genetic engineering techniques include in vitro transcription synthesis, a method using a vector, and a method using a PCR cassette.
- the vector is not particularly limited, and examples thereof include non-viral vectors such as plasmids and viral vectors.
- the chemical synthesis method is not particularly limited, and examples thereof include a phosphoramidite method and an H-phosphonate method.
- a commercially available automatic nucleic acid synthesizer can be used.
- amidite is generally used.
- the amidite is not particularly limited, and commercially available amidites include, for example, RNA Phosphoramidates (2′-O-TBDMSi, trade name, Michisato Pharmaceutical), ACE amidite, TOM amidite, CEE amidite, CEM amidite, TEM amidite, etc. Is given.
- composition for suppressing expression of the present invention is a composition for suppressing the expression of a target gene, and is characterized by containing the ssNc molecule of the present invention.
- the composition of the present invention is characterized by containing the ssNc molecule of the present invention, and other configurations are not limited at all.
- the expression suppressing composition of the present invention can also be referred to as an expression suppressing reagent, for example.
- expression of the target gene can be suppressed by administration to a subject in which the target gene exists.
- the pharmaceutical composition of the present invention is characterized by containing the ssNc molecule of the present invention.
- the composition of the present invention is characterized by containing the ssNc molecule of the present invention, and other configurations are not limited at all.
- the pharmaceutical composition of the present invention can also be referred to as a pharmaceutical product, for example.
- treatment includes, for example, the meanings of prevention of the above-mentioned diseases, improvement of the diseases, and improvement of the prognosis.
- the disease to be treated is not particularly limited, and examples thereof include diseases caused by gene expression.
- a gene that causes the disease is set as the target gene, and the expression suppression sequence may be set as appropriate according to the target gene.
- the target gene is set to the TGF- ⁇ 1 gene and an expression suppression sequence for the gene is arranged in the ssNc molecule, for example, for treatment of inflammatory diseases, specifically acute lung injury, etc. Can be used.
- composition for suppressing expression and the pharmaceutical composition (hereinafter referred to as composition) of the present invention is not particularly limited.
- composition for example, if the ssNc molecule is administered to an administration subject having the target gene. Good.
- Examples of the administration target include cells, tissues or organs.
- Examples of the administration subject include non-human animals such as humans and non-human mammals other than humans.
- the administration may be, for example, in vivo or in vitro.
- the cells are not particularly limited, and examples thereof include various cultured cells such as HeLa cells, 293 cells, NIH3T3 cells, and COS cells, stem cells such as ES cells and hematopoietic stem cells, and cells isolated from living bodies such as primary cultured cells. can give.
- the administration method is not particularly limited, and can be appropriately determined according to the administration subject, for example.
- the administration subject is a cultured cell
- examples thereof include a method using a transfection reagent and an electroporation method.
- composition of the present invention may contain, for example, only the ssNc molecule of the present invention, or may further contain other additives.
- the additive is not particularly limited, and for example, a pharmaceutically acceptable additive is preferable.
- the type of the additive is not particularly limited, and can be appropriately selected depending on, for example, the type of administration target.
- the ssNc molecule may form a complex with the additive, for example.
- the additive can also be referred to as a complexing agent, for example.
- the complex formation for example, the ssNc molecule can be efficiently delivered.
- the bond between the ssNc molecule and the complexing agent is not particularly limited, and examples thereof include non-covalent bonds. Examples of the complex include an inclusion complex.
- the complexing agent is not particularly limited, and examples thereof include a polymer, cyclodextrin, adamantine and the like.
- examples of the cyclodextrin include a linear cyclodextrin copolymer and a linear oxidized cyclodextrin copolymer.
- Examples of the additive include a carrier, a binding substance to a target cell, a condensing agent, a fusing agent, an excipient, and the like.
- the carrier is preferably a polymer, and more preferably a biopolymer, for example.
- the carrier is preferably biodegradable, for example.
- the carrier include proteins such as human serum albumin (HSA), low density lipoprotein (LDL), and globulin; carbohydrates such as dextran, pullulan, chitin, chitosan, inulin, cyclodextrin, and hyaluronic acid; lipids and the like Can be given.
- a synthetic polymer such as a synthetic polyamino acid can also be used.
- polyamino acid examples include polylysine (PLL), poly L-aspartic acid, poly L-glutamic acid, styrene-maleic anhydride copolymer, poly (L-lactide-co-glycolide) copolymer, divinyl ether-maleic anhydride. Copolymer, N- (2-hydroxypropyl) methacrylamide copolymer (HMPA), polyethylene glycol (PEG), polyvinyl alcohol (PVA), polyurethane, poly (2-ethylacrylic acid), N-isopropylacrylamide polymer, or polyphosphazine ) Etc.
- PLL polylysine
- poly L-aspartic acid poly L-glutamic acid
- styrene-maleic anhydride copolymer poly (L-lactide-co-glycolide) copolymer
- divinyl ether-maleic anhydride divinyl ether-maleic anhydride.
- binding substance examples include thyroid stimulating hormone, melanocyte stimulating hormone, lectin, glycoprotein, surfactant protein A, mucin carbohydrate, polyvalent lactose, polyvalent galactose, N-acetylgalactosamine, N-acetylglucosamine, polyvalent mannose.
- PEI polyethyleneimine
- PEI polyethyleneimine
- the fusing agent and condensing agent include polyamino chains such as polyethyleneimine (PEI).
- PEI may be, for example, linear or branched, and may be either a synthetic product or a natural product.
- the PEI may be alkyl-substituted or lipid-substituted, for example.
- polyhistidine, polyimidazole, polypyridine, polypropyleneimine, melittin, polyacetal substance (for example, cationic polyacetal) and the like can be used as the fusion agent.
- the fusion agent may have an ⁇ helical structure, for example.
- the fusion agent may be a membrane disrupting agent such as melittin.
- composition of the present invention can use, for example, US Pat. No. 6,509,323, US Patent Publication No. 2003/0008818, PCT / US04 / 07070, and the like for the formation of the complex.
- amphiphilic molecules include amphiphilic molecules.
- the amphiphilic molecule is, for example, a molecule having a hydrophobic region and a hydrophilic region.
- the molecule is preferably a polymer, for example.
- the polymer is, for example, a polymer having a secondary structure, and a polymer having a repetitive secondary structure is preferable.
- a polypeptide is preferable, and an ⁇ -helical polypeptide is more preferable.
- the amphiphilic polymer may be a polymer having two or more amphiphilic subunits, for example.
- the subunit include a subunit having a cyclic structure having at least one hydrophilic group and one hydrophobic group.
- the subunit may have, for example, a steroid such as cholic acid, an aromatic structure, or the like.
- the polymer may have both a cyclic structure subunit such as an aromatic subunit and an amino acid.
- the expression suppression method of the present invention is a method of suppressing the expression of a target gene, characterized by using the ssNc molecule of the present invention.
- the expression suppression method of the present invention is characterized by using the ssNc molecule of the present invention, and other processes and conditions are not limited at all.
- the gene expression suppression mechanism is not particularly limited, and examples thereof include expression suppression by RNA interference or RNA interference-like phenomenon.
- the expression suppression method of the present invention is, for example, a method of inducing RNA interference that suppresses the expression of the target gene, and can also be said to be an expression induction method characterized by using the ssNc molecule of the present invention.
- the expression suppression method of the present invention includes, for example, a step of administering the ssNc molecule to a subject in which the target gene is present.
- the administration step for example, the ssNc molecule is brought into contact with the administration subject.
- the administration subject include cells, tissues, and organs.
- the administration subject include non-human animals such as humans and non-human mammals other than humans.
- the administration may be, for example, in vivo or in vitro.
- the ssNc molecule may be administered alone, or the composition of the present invention containing the ssNc molecule may be administered.
- the administration method is not particularly limited, and can be appropriately selected depending on, for example, the type of administration target.
- the treatment method for a disease of the present invention includes the step of administering the ssNc molecule of the present invention to a patient as described above, and the ssNc molecule serves as the gene that causes the disease as the expression-suppressing sequence. It has a sequence that suppresses the expression of.
- the treatment method of the present invention is characterized by using the ssNc molecule of the present invention, and other steps and conditions are not limited at all.
- the expression suppression method of the present invention can be used.
- the administration method is not particularly limited, and may be, for example, oral administration or parenteral administration.
- ssNc molecule The use of the present invention is the use of the ssNc molecule of the present invention for suppressing the expression of the target gene. The use of the present invention is also the use of the ssNc molecule of the present invention for the induction of RNA interference.
- the nucleic acid molecule of the present invention is a nucleic acid molecule for use in the treatment of a disease, wherein the nucleic acid molecule is the ssNc molecule of the present invention, and the ssNc molecule serves as the cause of the disease as the expression suppression sequence. It has a sequence that suppresses the expression of the gene to be
- RNA (Example A1) Synthesis of RNA
- the following ssRNA (NK-0016) was synthesized as the RNA (Ex) of the Example.
- the NK-0016 has a 19-base long expression suppressing sequence (SEQ ID NO: 1) that suppresses the expression of the GAPDH gene.
- SEQ ID NO: 1 a region between the region (Xc) and the region (X) is a linker region (Lx), and a region between the region (Y) and the region (Yc) is a linker region (Ly).
- the 5 ′ region (Xc) and the 3 ′ region (Yc) are each represented by lower case letters (the same applies hereinafter).
- GAPDH gene expression suppression sequence (SEQ ID NO: 1) 5'-GUUGUCAAUACUCUCAUGG-3 '
- RNAi positive control (Pc) dsRNA (NI-0011) was synthesized.
- NI-0011 has an overhang of 2 bases at the 3 ′ end of each single strand, and the single strand of SEQ ID NO: 4 has the 19-base long expression-suppressing sequence as in NK-0016. ing.
- RNA was synthesized by a nucleic acid synthesizer (trade name: ABI Expedite (registered trademark) 8909 Nucleic Acid Synthesis System, Applied Biosystems) based on the phosphoramidite method.
- RNA Phosphoramidites (2'-O-TBDMSi, trade name, Michisato Pharmaceutical) was used as an RNA amidite (hereinafter the same).
- the deprotection of the amidite followed a conventional method.
- the synthesized RNA was purified by HPLC. Each purified RNA was lyophilized. In the following examples, RNA synthesis was performed in the same manner as in this example unless otherwise indicated.
- RNA was dissolved to a desired concentration using distilled water for injection (Otsuka Pharmaceutical, the same applies hereinafter).
- Example A2 GAPDH gene expression suppression effect in HCT116 cells Using the ssRNA of the present invention, in vitro suppression of GAPDH gene expression was confirmed.
- RNA (Ex) of the example the ssRNA (NK-0016) of Example A1 was used.
- RNA was dissolved in distilled water for injection to a desired concentration to prepare an RNA solution.
- the cells used were HCT116 cells (DS Pharma Biomedical), the medium was McCoy's 5A (Invitrogen) medium containing 10% FBS, and the culture conditions were 37 ° C. and 5% CO 2 .
- HCT116 cells were cultured in the above medium, and the culture solution was dispensed into a 24-well plate at 400 ⁇ L in an amount of 2 ⁇ 10 4 cells / well. Furthermore, after culturing the cells in the well for 24 hours, the RNA was transfected using the transfection reagent Lipofectamine 2000 (trade name, Invitrogen) according to the attached protocol. Specifically, the composition per well was set as follows, and transfection was performed. In the wells, the final RNA concentration was 5 nmol / L, 10 nmol / L, 20 nmol / L, and 40 nmol / L.
- GAPDH gene primer set 5'-GGAGAAGGCTGGGGCTCATTTGC-3 '(SEQ ID NO: 9) 5'-TGGCCAGGGGTGCTAAGCAGTTG-3 '(SEQ ID NO: 10) Primer set for ⁇ -actin gene 5'-GCCACGGCTGCTTCCAGCTCCTC-3 '(SEQ ID NO: 11) 5'-AGGTCTTTGCGGATGTCCACGTCAC-3 '(SEQ ID NO: 12)
- the amount of gene expression was also measured for cells to which only 100 ⁇ L of (B) was added ( ⁇ ).
- the RNA solution was not added, and the cells treated in the same manner except that (A) 1.5 ⁇ L and (B) were added in total 100 ⁇ L were also used for gene expression. The amount was measured (mock).
- the expression level of the control (-) was set to 1, and the relative value of the expression level of each cell into which each RNA was introduced was determined.
- FIG. 4 is a graph showing the relative value of the GAPDH gene expression level. As shown in FIG. 4, it was found that NK-0016 had a lower expression level than the control ( ⁇ ) to which no RNA was added, and suppressed the expression of the GAPHD gene. Moreover, as shown in FIG. 4, it turned out that a gene expression suppression effect is shown depending on dosage.
- Example A3 GAPDH gene expression suppression effect in HCT116 cells Using the ssRNA of the present invention, in vitro suppression of GAPDH gene expression was confirmed.
- RNA (Ex) of the example, the ssRNA (NK-0016) of Example A1 was used.
- the comparative RNA the dsRNA (NI-0011) of RNAi positive control (Pc) was used.
- the RNA was dissolved in distilled water for injection so as to be 40 ⁇ mol / L to prepare an RNA solution.
- the expression level of the GAPDH gene in HCT116 cells was confirmed in the same manner as in Example A2 except that the RNA solution was used.
- the RNA concentration at the time of transfection was 40 nmol / L.
- FIG. 5 is a graph showing the relative value of the GAPDH gene expression level, and the vertical axis represents the relative gene expression level.
- NK-0016 of the above example showed extremely strong gene expression suppression activity compared to NI-0011 of the comparative example.
- Example A4 GAPDH gene expression suppression effect in A549 cells and 293 cells Using the ssRNA of the present invention, suppression of GAPDH gene expression in vitro was confirmed.
- RNA (Ex) of the example NK-0016 of Example A1 and the following Ex-ssRNA (PK-0004) were used.
- the linker region (Lx) and the linker region (Ly) are separated between Xc and X and between Yc and Y by the compound 10 (L-proline diamide amidite shown in Example B). ).
- the chemical formulas of both linkers are shown below.
- the NK-0016 and the PK-0004 have the same sequence except that the linker region (Lx) between Xc and X and the linker region (Ly) between Yc and Y are different.
- RNA was dissolved in distilled water for injection so as to be 20 ⁇ mol / L to prepare an RNA solution.
- As the cells A549 cells and 293 cells (DS Pharma Biomedical) were used.
- the former medium was DMEM (Invitrogen) containing 10% FBS, and the latter medium was MEM (Invitrogen) medium containing 10% FBS.
- the culture conditions were 37 ° C. and 5% CO 2 .
- the cells were cultured in the medium, and the culture solution was dispensed into a 24-well plate in 400 ⁇ L portions at 5 ⁇ 10 4 cells / well. Furthermore, after culturing the cells in the well for 24 hours, the RNA was transfected using the transfection reagent Lipofectamine 2000 (trade name, Invitrogen) according to the attached protocol. Specifically, transfection was performed on A549 cells and 293 cells with the composition per well set as follows. In the following composition, (B) is Opti-MEM (trade name, Invitrogen), and (C) is 20 ⁇ mol / L of the RNA solution, and 98.5 ⁇ L or 99 ⁇ L of both were added together. In the wells, the final concentration of the RNA was 1 nmol / L, 3 nmol / L, 10 nmol / L.
- the cells were cultured for 48 hours, and RNA recovery, cDNA synthesis and PCR were performed in the same manner as in Example A2, and the relative expression level of the GAPDH gene was measured.
- FIGS. 6 and 7 are graphs showing the relative values of the GAPDH gene expression level. As shown in FIGS. 6 and 7, it was found that NK-0016 and PK-0004 of Examples showed strong gene expression suppression activity and showed an effect in a concentration-dependent manner.
- Example A5 TGF- ⁇ 1 gene expression inhibitory effect in Hepa1-6 cells
- the in vitro TGF- ⁇ 1 gene expression inhibitory effect of the ssRNA of the present invention was confirmed.
- ssRNA As RNA (Ex) in the examples, ssRNA (NK-0033) shown below was used.
- the NK-0033 has the following sequence of 21 bases that suppresses the expression of the TGF- ⁇ 1 gene. This sequence was designed based on the siRNA used by Cheng et al. (Mol. Pharm., 2009, 6, 772-779).
- TGF- ⁇ 1 gene expression suppressing sequence SEQ ID NO: 16) 5'-AAAGUCAAUGUACAGCUUGCUU-3 '
- RNA of the comparative example ssRNA (NK-0035) of RNAi negative control (Nc) shown below was used.
- NK-0035 incorporates a scrambled sequence that is not involved in expression suppression, not the expression suppression sequence.
- RNA was dissolved in distilled water for injection to prepare an RNA solution.
- Hepa1-6 cells RIKEN BioResource Center
- DMEM Invitrogen
- FBS FBS
- RNA concentrations were 10 nmol / L, 25 nmol / L, 50 nmol / L, and 100 nmol / L.
- the following PCR primer set for TGF- ⁇ 1 gene and primer set for ⁇ -actin gene were prepared as follows. PCR was performed in the same manner as in Example A2 except that it was used, and the expression level of the TGF- ⁇ 1 gene and the expression level of the internal standard ⁇ -actin gene were measured. This was corrected by the expression level of the ⁇ -actin gene.
- Primer set for TGF- ⁇ 1 gene 5′-CCATTGCTGTCCCGTGCAGAGCTG-3 ′ (SEQ ID NO: 17) 5'-ATGGTAGCCCTTGGGCTCGTGGATC-3 '(SEQ ID NO: 18)
- Primer set for ⁇ -actin gene amplification 5'-GTCGTACCACAGGCATTGTGATGG-3 '(SEQ ID NO: 19) 5'-GCAATGCCTGGGTACATGGTGG-3 '(SEQ ID NO: 20)
- Example A2 the gene expression level was measured for the control ( ⁇ ) and the control (mock). Then, with respect to the corrected TGF- ⁇ 1 gene expression level, the expression level of the control ( ⁇ ) cell was taken as 1, and the relative value of the expression level of the cell into which each RNA was introduced was determined.
- FIG. 8 is a graph showing the relative value of the expression level of TGF- ⁇ 1 gene.
- NK-0033 of the above example suppressed the expression of TGF- ⁇ 1 gene in vitro.
- the negative control NK-0035 did not suppress the expression of the TGF- ⁇ 1 gene.
- Example A6 In vivo TGF- ⁇ 1 gene expression-suppressing effect and acute lung injury-suppressing effect
- the ssRNA of the present invention was confirmed to suppress gene expression and suppress acute lung injury in vivo. The effect was confirmed according to the method described in Takagi et al. (J. Thromb Hemost 2009; 7: 2053-2063).
- Example A5 Materials and method (1.1) Administration of ssRNA to mice with acute lung injury
- the ssRNA (NK-0033) of Example A5 was used as the RNA (Ex) of the example.
- RNA (Ex) of the example As the RNA of the comparative example, the RNAi negative control (Nc) ssRNA (NK-0035) shown in Example A5 was used.
- RNA solution was prepared by dissolving 100 ⁇ g of the RNA in 80 ⁇ L of sterile physiological saline (Nippon Kayaku Co., Ltd., hereinafter the same). On the other hand, 100 ⁇ g of lipopolysaccharide (LPS) was dissolved in 50 ⁇ L of sterile physiological saline to prepare an LPS solution.
- LPS lipopolysaccharide
- RNA solution 80 ⁇ L was dropped into the trachea of a mouse.
- 50 ⁇ L of the LPS solution was dropped into the trachea of the mouse to induce lung injury.
- Each administration group is shown below. Four to six mice were used in each treatment group.
- ⁇ Administration group 1 One hour after administration of 80 ⁇ L of sterile physiological saline, 50 ⁇ L of sterile physiological saline was administered / administered group 2
- One hour after administration of 80 ⁇ L of RNA solution (NK-0033) 50 ⁇ L of sterile physiological saline was administered / administered group 3
- 50 ⁇ L of sterile physiological saline was administered / administered group 4
- One hour after administration of 80 ⁇ L of sterile physiological saline, 50 ⁇ L of the LPS solution was administered / administered group 5
- 50 ⁇ L of LPS solution was administered / administered group 6
- the mouse heart was punctured and a blood sample was collected and added to a test tube containing a 3.8% aqueous sodium citrate solution.
- the amount (volume) of the aqueous sodium citrate solution was 1/10 of the blood sample.
- a BALF sample was recovered from this mixture according to the description of Yasui et al. (Am J Respir Crit Care Med 2001: 163: 1660-8). Then, the total number of cells in the BALF sample was measured using NucleoCounter (trade name, Chemomeded).
- the BALF sample was subjected to centrifugation, and the supernatant of the BALF sample was collected and stored at ⁇ 80 ° C. until biochemical analysis was performed.
- the BALF sample was centrifuged using cytospin, and the separated cells were subjected to May-Grunwald-Giemsa (trade name, Merck). And Giemsa staining.
- lung tissue was collected from the mouse and subjected to HE staining.
- FIG. 9 is a graph showing the expression level of TGF- ⁇ 1 gene per unit weight of lung in each administration group.
- LPS (+) / RNA ( ⁇ ) administration group 4 compared to LPS ( ⁇ ) / RNA ( ⁇ ) administration group 1, the expression level of the gene increased as a result of LPS treatment.
- Example 5 administration group of LPS (+) / NK-0033 (+), an increase in the expression level of the gene was suppressed as compared with administration group 4 of LPS (+) / RNA ( ⁇ ). .
- This inhibitory effect was not observed in the administration group 6 of LPS (+) / negative control NK-0035 (+). From this result, it was found that the expression of TGF- ⁇ 1 gene can be effectively suppressed by NK-0033 of the above Example.
- Acute lung injury inhibitory effect Inflammation in acute lung injury occurs when cells such as neutrophils infiltrate the lung. Therefore, a drug that suppresses infiltration of cells such as neutrophils into the lung is a therapeutic agent for inflammation in acute lung injury. Therefore, the pharmacological effect of the ssRNA of the present invention was confirmed using the number of cells in bronchoalveolar lavage fluid (BALF) as an index of the number of cells infiltrating into the lung.
- BALF bronchoalveolar lavage fluid
- FIG. 10 is a graph showing the number of cells in the BAFL sample in each administration group.
- LPS (+) / RNA ( ⁇ ) administration group 4 as a result of LPS treatment, the number of cells in the BALF sample increased as compared to LPS ( ⁇ ) / RNA ( ⁇ ) administration group 1. This indicates that LPS induced an inflammatory effect, resulting in cells infiltrating the lungs.
- Example 5 administration group of LPS (+) / NK-0033 (+), an increase in the cell number was suppressed as compared with administration group 4 of LPS (+) / RNA ( ⁇ ). This indicates that inflammation in acute lung injury was suppressed by the NK-0033. This inhibitory effect was not observed in the administration group 6 of LPS (+) / negative control NK-0035 (+). From this result, it was found that the inflammation in acute lung injury can be effectively suppressed by NK-0033 of the above example.
- FIG. 11 shows the measurement results of the neutrophil count in the BALF sample.
- FIG. 11 is a graph showing the number of neutrophil cells in the BALF sample in each administration group.
- LPS (+) / RNA ( ⁇ ) administration group 4 increased the number of neutrophils in the BALF sample as a result of LPS treatment compared to LPS ( ⁇ ) / RNA ( ⁇ ) administration group 1 . This indicates that LPS induced an inflammatory effect, and as a result, neutrophils infiltrated the lungs.
- Example 5 administration group 5 of LPS (+) / NK-0033 (+) the number of neutrophils in the BALF sample was increased as compared to administration group 4 of LPS (+) / ssRNA ( ⁇ ). Was suppressed.
- FIG. 12 is a photograph showing the results of Giemsa staining of the cells in the BALF sample (magnification 100 times).
- A shows the results of LPS (+) / RNA ( ⁇ ) administration group 4
- B shows LPS (+) / negative control NK-0035 (+) administration group 6 results.
- C shows the results of Example administration group 5 of LPS (+) / NK-0033 (+).
- Example administration group 5 (C) of LPS (+) / NK-0033 (+) was administered to LPS (+) / RNA ( ⁇ ) administration group 4 (A) and LPS (+). / The number of cells infiltrating into the lung was remarkably small as compared with the negative control NK-0035 (+) administration group 6 (B). This histological observation is consistent with the cell count results in the BALF sample described above.
- FIG. 13 is a photograph showing the result of HE staining of the lung tissue (magnification 10 times).
- A shows the results of LPS (+) / RNA ( ⁇ ) administration group 4
- B shows LPS (+) / negative control NK-0035 (+) administration group 6 results.
- C shows the results of Example administration group 5 of LPS (+) / NK-0033 (+). From FIG. 13, it was found that the infiltration of cells such as neutrophils around the blood vessels, in the alveolar cavity, the alveolar wall, and around the bronchus was reduced, and the lung tissue injury was reduced.
- Example A7 Evaluation of side effect using interferon induction as an index It is known that conventional iRNA agents induce interferon as a side effect in a sequence-independent manner, and this side effect is regarded as a problem. Therefore, the side effect of interferon induction was evaluated for the ssRNA of the present invention.
- Example A6 Materials and Method According to the same method and conditions as in Example A6, ssRNA was administered to acute lung injury mice. Then, in the same manner as in Example A6, 24 hours after the LPS solution or sterile physiological saline (negative control for LPS) was dropped, the mouse was euthanized and lung tissue was collected.
- RNA was isolated using TRIZOL (trade name, Invitrogen) in order to measure the expression level of each gene.
- cDNA was synthesized from the RNA using reverse transcriptase (trade name SuperScriptII, Invitrogen) according to the attached protocol. Then, PCR was performed using the synthesized cDNA as a template, and the expression levels of the TGF- ⁇ 1 gene, IFN- ⁇ gene, and IFN- ⁇ gene were measured.
- Primer set for TGF- ⁇ 1 gene 5'-ACTCCACGTGGAAATCAACGG-3 '(SEQ ID NO: 23) 5'-TAGTAGACGATGGGCAGTGG-3 '(SEQ ID NO: 24)
- the obtained PCR product was subjected to agarose electrophoresis. Further, the agarose after electrophoresis was subjected to density analysis using NIH imaging system to confirm the expression level of each gene.
- the expression levels of the TGF- ⁇ 1 gene, the IFN- ⁇ gene, and the IFN- ⁇ gene were relatively evaluated using the expression level of the GAPDH gene as a standard. Specifically, with the measurement intensity of the PCR product using the GAPDH gene primer set as standard 1, the relative value of the measurement intensity of the PCR product using each gene primer set was determined and evaluated.
- FIG. 14 (A) shows the result of the expression level of the TGF- ⁇ 1 gene.
- the administration group 5 in which NK-0033 was administered showed an increase in TGF- ⁇ 1 gene expression induced by LPS, compared with the administration group 4 in RNA ( ⁇ ). Suppressed. This result correlates with the measurement result of the expression level of TGF- ⁇ 1 shown in FIG. 8 of Example A5.
- FIG. 14 (B) shows the expression level of the IFN- ⁇ gene
- FIG. 14 (C) shows the expression level of the IFN- ⁇ gene.
- RNA ( ⁇ ) administration group 1 and RNA (+) administration group 2 were compared. Expression induction of IFN- ⁇ gene and IFN- ⁇ gene, which are type I interferons, did not occur.
- FIGS. 14 (B) and 14 (C) in the case of addition of LPS, the results of comparing RNA ( ⁇ ) administration group 4 and NK-0033 (+) administration group 5 were the same.
- expression of the IFN- ⁇ gene and the IFN- ⁇ gene was not induced by the addition of ssRNA.
- Example A8 TGF- ⁇ 1 gene expression inhibitory effect in Hepa1-6 cells
- the in vitro TGF- ⁇ 1 gene expression inhibitory effect of the ssRNA of the present invention was confirmed.
- NK-0033 of Example A5 NK-0061, NK-0055 and NK-0062 shown below were used as the RNA (Ex) of the Example. In the following sequences, “*” indicates a free base.
- RNA The following PK-0007, PK-0026, PK-0027, and PK-0028 were used as RNA (Ex) in the examples.
- the linker region (Lx) and linker region (Ly) are between Xc and X, between Yc and Y, compound 10 of Scheme 3 (L-proline diamide amidite) shown in Example B. was used to bind.
- NK-0033, NK-0061, NK-0055 and NK-0062 and PK-0007, PK-0026, PK-0027 and PK-0028 are the first linker (L1) and the second linker (L2). Except for differences, the sequences are the same, and all have a sequence (SEQ ID NO: 16) that suppresses the expression of the TGF- ⁇ 1 gene.
- RNA concentration at the time of transfection was 1 nmol / L.
- FIGS. FIG. 15 and FIG. 16 are graphs showing the relative values of the expression level of TGF- ⁇ 1 gene, respectively.
- FIG. 15 shows the results using NK-0033, NK-0061, NK-0055, and NK-0062.
- FIG. 16 shows the results using PK-0007, PK-0026, PK-0027, and PK-0028. is there. As shown in FIGS. 15 and 16, all ssRNAs showed strong gene expression inhibitory activity.
- RNA administration to acute lung injury mice was performed in the same manner as in Example A6 unless otherwise specified.
- RNA (Ex) of Example PK-0007 and NK0033 in Example A8 were used. Further, as RNAs of comparative examples, RNAi negative control (Nc) PK-0008 and NK-0035, RNAi positive control (Pc) dsRNA (NI-0030) and RNAi negative control (Nc) dsRNA (shown below) NI-0031) was used.
- the negative control PK-0008 has the same linkers Lx and Ly derived from the amidite (said compound 10 of Scheme 3: L-proline diamide amidite) as PK-0007.
- RNA 100 ⁇ g of the RNA was dissolved in 75 ⁇ L of sterile physiological saline to prepare an RNA solution.
- lipopolysaccharide 100 ⁇ g of lipopolysaccharide (LPS) was dissolved in 50 ⁇ L of sterile physiological saline to prepare an LPS solution.
- Each administration group is shown below. Unless otherwise indicated, administration was performed in the same manner as in Example A6. Four to six mice were used in each treatment group. ⁇ Administration group 1 5 minutes after administration of 75 ⁇ L of sterile physiological saline, 50 ⁇ L of sterile physiological saline was administered / administered group 2 5 minutes after administration of 75 ⁇ L of sterile physiological saline, 50 ⁇ L of LPS solution was administered / administration group 3 5 minutes after administration of 75 ⁇ L of RNA solution (PK-0007), 50 ⁇ L of LPS solution was administered / administered group 4 5 minutes after administration of 75 ⁇ L of RNA solution (PK-0008), 50 ⁇ L of LPS solution was administered / administered group 5 Five minutes after administration of 75 ⁇ L of RNA solution (NK-0033), 50 ⁇ L of LPS solution was administered / administered group 6 Five minutes after administration of 75 ⁇ L of RNA solution (NK-0035), 50 ⁇ L of LPS solution was administered / administered group 7 Five minutes after administration
- Example A6 a lung sample was prepared in the same manner as in Example A6, and the expression level of TGF- ⁇ 1 per unit weight of lung was measured.
- FIG. 17 is a graph showing the expression level of TGF- ⁇ 1 per lung per unit weight in each administration group.
- LPS (+) / PK-0007 (+) administration group 3 and LPS (+) / NK-0033 (+) administration group 5 were compared with LPS (+) / ssRNA ( ⁇ ) administration group 2, respectively.
- This inhibitory effect was found to be stronger than that of the administration group 7 of LPS (+) / positive control NI-0030.
- the administration group 3 of LPS (+) / PK-0007 (+) showed a remarkable inhibitory effect. No inhibitory effect was observed in administration group 4 (PK-0008), administration group 6 (NK-0035), and administration group 8 (NI-0031) to which negative control RNA was administered.
- RNA of the example As the RNA of the example, the ssRNA (PK-0007) of Example A8 was used.
- the RNA of the comparative example was the RNAi negative control (Nc) ssRNA (PK-0008), RNAi positive control (Pc) dsRNA (NI-0030) and RNAi negative control dsRNA (NI) shown in Example A9-1. -0031) was used. Then, 100 ⁇ g of the RNA was dissolved in 75 ⁇ L of sterile physiological saline to prepare an RNA solution.
- Each administration group is shown below. Two to four mice were used in each treatment group. ⁇ Administration group 1 Administration of administration of sterile physiological saline 75 ⁇ L 2 Administration of RNA solution (PK-0007) 75 ⁇ L and administration group 3 Administration of 75 ⁇ L of RNA solution (PK-0008)
- the BALF sample was collected from the mouse in the same manner as in Example A6, and the supernatant of the BALF sample was obtained. With respect to the supernatant, the amount of TNF- ⁇ and the amount of IFN- ⁇ were measured.
- the amount of TNF- ⁇ was quantified using the trade name Mouse TNF set II (Beckton Dickinson and Company) according to the instructions for use.
- the amount of IFN- ⁇ was determined using ELISA plates prepared using the trade name Rabbit Anti-Mouse Interferon ⁇ (PBL InterferonSource) and the trade name Biotin Labeling Kit-NH2 (Dojindo Laboratories). Quantified according to
- FIG. 18 (A) is a graph showing the amount of TNF- ⁇ in the BALF sample of each administration group
- FIG. 18 (B) is a graph showing the amount of IFN- ⁇ in the BALF sample of each administration group.
- the horizontal axis indicates the respective amounts.
- the PK-0007 (+) administration group 2 did not induce the expression of TNF- ⁇ and IFN- ⁇ as compared to the RNA ( ⁇ ) administration group 1.
- Example A10 LAMA1 gene expression suppression effect in 293 cells Using the ssRNA of the present invention, in vitro suppression of the LAMA1 gene expression was confirmed.
- NK-0043 and NK-0064 were used as RNA (Ex) in the examples.
- “*” represents a free base (hereinafter the same).
- RNA recovery was carried out in the same manner as in Example A2, and the expression level of LAMA1 gene and ⁇ -actin as an internal standard were used.
- the expression level of the gene was measured.
- the expression level of the LAMA1 gene was corrected by the expression level of the ⁇ -actin gene which is an internal standard.
- Example A2 the expression level was also measured for control 1 ( ⁇ ) and control 2 (mock). Then, with respect to the corrected LAMA1 gene expression level, the expression level of the control ( ⁇ ) cell was taken as 1, and the relative value of the expression level of the cell into which each RNA was introduced was determined.
- FIG. 19 is a graph showing the relative value of the expression level of the LAMA1 gene in 293 cells. As shown in FIG. 19, it was found that NK-0043 and NK-0064 of Example showed strong gene expression inhibitory activity.
- Example A11 Inhibition of LMNA gene expression in A549 cells Using the ssRNA of the present invention, in vitro suppression of the expression of the LMNA gene due to the RNA interference effect was confirmed.
- NK-0063 and NK-0066 shown below were used as RNA (Ex) in the examples. In the following sequences, “*” indicates a free base.
- A549 cells were transfected as in Example A4 except that the RNA was used, and the cells were cultured for 48 hours. The RNA concentration at the time of transfection was 3 nmol / L. Then, except that the following primer set for LMNA gene was used as a primer, RNA recovery, cDNA synthesis and PCR were carried out in the same manner as in Example A2, and the expression level of LMNA gene and ⁇ -actin as an internal standard were used. The expression level of the gene was measured. The expression level of the LMNA gene was corrected by the expression level of ⁇ -actin gene which is an internal standard. LMNA gene primer set 5'-CTGGACATCAAGCTGGCCCTGGAC-3 '(SEQ ID NO: 49) 5'-CACCAGCTTGCGCATGGCCACTTC-3 '(SEQ ID NO: 50)
- control 1 ⁇
- control 2 mock
- the control ( ⁇ ) cell expression level was set to 1, and the relative value of the expression level of the cells into which each RNA was introduced was determined.
- FIG. 20 is a graph showing the relative value of the expression level of the LMNA gene in A549 cells. As shown in FIG. 20, it was found that NK-0063 and NK-0066 of the examples showed strong gene expression suppressing activity.
- RNA of an Example ssRNA shown in FIG. 21 was used.
- the number at the right end indicates the sequence number.
- the lower case underlined region indicates the region (Xc)
- the upper case underlined region indicates the internal region (Z)
- the lower case underlined region indicates the region (Yc).
- Between Xc and Z is a linker region (Lx)
- between Z and Yc is a linker region (Ly).
- “Xc / Yc” indicates a ratio between the base length (Xc) of the region (Xc) and the base length (Yc) of the region (Yc).
- “*” indicates a free base.
- the base length of the internal region (Z) was 26 bases
- the base length of the linker region (Lx) was 7 bases
- the base length of the linker region (Ly) was 4 bases.
- the total number of bases (Xc + Yc) of the region (Xc) and the region (Yc) is 26 bases. Otherwise, the region (Xc) and the region (Yc) The total number of bases (Xc + Yc) was 25 bases. Under these conditions, the base lengths of the region (Xc) and the region (Yc) were changed.
- NK-0036 and NK-0040 were molecules having no free base.
- each ssRNA other than these has all the free bases that do not form a double strand in the internal region (Z) as one base, and the position of the free base in the internal region (Z) from the 3 ′ side. Fluctuated 5 'side.
- RNA concentration at the time of transfection was 10 nmol / L.
- FIG. 22 is a graph showing the relative value of the GAPDH gene expression level when RNA having a final concentration of 10 nmol / L is used. As shown in FIG. 22, GAPDH gene expression suppression was confirmed for any ssRNA in which the lengths of the 5 ′ region (Xc) and the 3 ′ region (Yc) were changed.
- the gene expression level decreased relatively and the expression suppression activity increased. That is, it was found that the expression suppression activity can be improved as the position of the free base in the inner region (Z) is arranged 5 'or 3' from the center of the inner region.
- Example A2 NK-0016 has been confirmed to have a very strong expression suppression activity.
- NK-0025 and NK-0037 were found to have a higher activity than NK-0016.
- Example A8 TGF- ⁇ 1 gene
- Example A10 LAMA1 gene
- Example A11 LMNA gene
- Example A8 As shown in the aforementioned sequence, both NK-0033 and NK-0055 have one free base, and the former is the fourth from the 3 ′ end of the internal region (Z). The latter is located second from the 3 ′ end of the internal region (Z).
- NK-0055 in which the free base is located on the 3′-end side, showed high expression suppression. Similar results were obtained between NK-0061 and NK-0062, which have two free bases.
- Example A9 and Example 10 the position of the free base was changed under the same conditions as in Example 8. Similarly, the ssRNA in which the free base is located on the 3 ′ end side is High expression suppression was shown.
- the ssRNA of the present invention can be said to be an applicable tool regardless of the type of target gene.
- RNA of the example ssRNA shown in FIG. 23 was used.
- the number at the right end indicates a sequence number.
- the lower case underlined area indicates the area (Xc)
- the upper case underlined area indicates the internal area (Z)
- the lowercase underlined area indicates the area (Yc).
- Xc + Yc / X + Y indicates a ratio of the total base length of the region (Xc) and the region (Yc) to the total base length of the region (X) and the region (Y).
- “*” indicates a free base.
- Each ssRNA has a base length of the linker region (Lx) of 7 bases, a base length of the linker region (Ly) of 4 bases, a base length of the region (Yc) of 1 base, and the internal region (Z).
- the second base from the 3 ′ side of was used as a free base. Then, the base length of the internal region (Z) and the base length of the region (Xc) were varied.
- Example A2 the RNA was subjected to transfection into HCT116 cells, culture, RNA recovery, cDNA synthesis and PCR, and the expression level of the GAPDH gene was measured.
- the composition per well was set as follows. In the following composition, (B) is Opti-MEM (trade name, Invitrogen), and (C) is 20 ⁇ mol / L of the RNA solution, and 98.5 ⁇ L of both were added together. In the well, the final concentration of RNA was 1 nmol / L. Correction by the internal standard and calculation of the relative value of the expression level were performed in the same manner as in Example A2.
- FIG. 24 is a graph showing the relative value of GAPDH gene expression level when RNA with a final concentration of 1 nmol / L is used.
- the suppression of GAPDH gene expression was confirmed for any ssRNA in which the length of the region (X), the region (Xc), the region (Y), and the region (Yc) was changed. did it.
- NK-0016 has been confirmed to have a very strong expression suppressing activity. In this example, all ssRNAs other than NK-0016 were found to have an activity even higher than that of NK-0016.
- RNA of an Example ssRNA shown in FIG. 25 was used.
- the lower case underlined region indicates the region (Xc)
- the upper case underlined region indicates the internal 5 ′ region (X)
- the lower case underlined region indicates the region (Yc).
- “Xc / Yc” represents the ratio between the base length (Xc) of the region (Xc) and the base length (X) of the region (X).
- “*” indicates a free base.
- SEQ ID NOs: 74 to 76 The following RNA sequences are shown in SEQ ID NOs: 74 to 76.
- each ssRNA the base length of the internal region (Z) is 26 bases, the region (X) is 25 bases, the region (Y) is 1 base, the region (Yc) is 1 base, the linker region (Lx ) Was 7 bases, and the linker region (Ly) was 4 bases long. Under this condition, the base length of the region (Xc) was changed. Thereby, each ssRNA changed the presence and number of free bases that do not form a double strand in the internal region (Z). NK-0001 has no free base.
- RNA was used, transfection into HCT116 cells, culture, RNA recovery, cDNA synthesis and PCR were carried out in the same manner as in Example A13, and the expression level of the GAPDH gene was measured. Correction by the internal standard and calculation of the relative value of the expression level were performed in the same manner as in Example A13.
- FIG. 26 is a graph showing the relative value of GAPDH gene expression level when RNA with a final concentration of 1 nmol / L is used.
- the suppression of GAPDH gene expression could be confirmed for any ssRNA in which the length of the 5 ′ side region (Xc) was changed.
- Xc 5 ′ side region
- NK-0016 has been confirmed to have a very strong expression suppressing activity.
- all ssRNAs other than NK-0016 were found to have an activity even higher than that of NK-0016.
- Example A8 TGF- ⁇ 1 gene targeting a gene different from this example. That is, in Example A8, as shown in the above-mentioned sequence, the free bases of NK-0033 and NK-0061 are one base in the former and two bases in the latter. As shown in FIG. 15 described above, NK-0033 with less free base showed high expression suppression. As described in Example A12, NK-0055 and NK-0062 are different from NK-0033 and NK-0061 in that the position of the free base is changed to the 3 ′ side of the internal region (Z). It showed high expression suppression. From these results, it is clear that the same behavior is exhibited regardless of the type of the target gene and the expression suppression sequence thereto. For this reason, the ssRNA of the present invention can be said to be an applicable tool regardless of the type of target gene.
- RNA of an Example ssRNA shown in FIG. 27 was used.
- the lower case underline region is the 5 ′ side region (Xc)
- the upper case underline region is the internal region (Z)
- the lower case underline region is the 3 ′ side region (Yc).
- the sequence between X and Xc is a linker region (Lx)
- the sequence between Y and Yc is a linker region (Ly).
- the ratio (Lx / Ly) between the base length (Lx) of the linker region (Lx) and the base length (Ly) of the linker region (Ly) is shown.
- “*” indicates a free base.
- RNA was used, transfection into HCT116 cells, culture, RNA recovery, cDNA synthesis and PCR were carried out in the same manner as in Example A13, and the expression level of the GAPDH gene was measured. Correction by the internal standard and calculation of the relative value of the expression level were performed in the same manner as in Example A13.
- FIG. 28 is a graph showing the relative value of the GAPDH gene expression level when RNA having a final concentration of 1 nmol / L is used.
- the GAPDH gene is similarly applied to any ssRNA in which the conditions of the linker regions (Lx) and (Ly), that is, the length, the ratio of the lengths between them, the sequence, and the like are changed. Suppression of the expression was confirmed. From this result, it was found that the conditions of the linker regions (Lx) and (Ly) are not particularly limited, and can be designed in various lengths, sequences, and the like.
- Example A16 GAPDH gene expression inhibitory effect in HCT116 cells Using ssRNA substituted with a linker having proline or prolinol, the GAPDH expression inhibitory effect in HCT116 cells was confirmed.
- RNA (Ex ssRNA) shown below was synthesized as RNA (Ex) in the examples. Moreover, Nc ssRNA of RNAi negative control (Nc) shown below was synthesized as RNA of Comparative Example.
- the linker region (Lx) and the linker region (Ly) are bound to XcX and to YcY using amidite (see Example B) having proline or prolinol in the following table. I let you.
- RNA was used, transfection into HCT116 cells, culture, RNA recovery, cDNA synthesis and PCR were carried out in the same manner as in Example A13, and the expression level of the GAPDH gene was measured. Correction by the internal standard and calculation of the relative value of the expression level were performed in the same manner as in Example A13.
- FIG. 29 is a graph showing the relative value of GAPDH gene expression level.
- the Ex ssRNA containing proline or prolinol as the linker region (Lx) and the linker region (Ly) can confirm a strong gene expression inhibitory activity and show an effect in a concentration-dependent manner. all right.
- the negative control ssRNA did not show an inhibitory effect.
- Example A17 GAPDH gene expression inhibitory effect in HCT116 cells Using ssRNA substituted with a proline-containing linker, the GAPDH expression inhibitory effect in HCT116 cells was confirmed.
- RNA (Ex ssRNA) shown below was synthesized as RNA (Ex) in the examples. Moreover, Nc ssRNA of RNAi negative control (Nc) shown below was synthesized as RNA of Comparative Example.
- the linker region (Lx) and the linker region (Ly) use amidite (see Example B) having proline or prolinol between Xc and X and YcY. And combined.
- RNA was used, transfection into HCT116 cells, culture, RNA recovery, cDNA synthesis and PCR were carried out in the same manner as in Example A13, and the expression level of the GAPDH gene was measured. Correction by the internal standard and calculation of the relative value of the expression level were performed in the same manner as in Example A13.
- FIG. 30 is a graph showing the relative value of GAPDH gene expression level in HCT116 cells. As shown in FIG. 30, it was found that Ex ssRNA containing proline as a linker region (Lx) and a linker region (Ly) showed strong gene expression inhibitory activity and showed an effect in a concentration-dependent manner. On the other hand, the negative control ssRNA did not show an inhibitory effect.
- RNA (Ex) Materials and Methods NK-0033 in Example A5 and PK-0007 in Example A8 were used as RNA (Ex) in the examples. Further, as the RNA of the comparative example, dsRNA (NI-0030) of positive control (Pc) in Example A9 was used.
- FIG. 31 is an electrophoresis photograph showing resistance to ribonuclease.
- lane “M” is a molecular weight marker, and min indicates an incubation time.
- RNA and Method The same RNA as in Example A18 was used. First, 60 pmol of the RNA and 0.5 unit of S7 nuclease (Roche) were mixed with 50 mmol / L Tris-HCl (pH 8) containing 5 mmol / L CaCl 2 and incubated at 37 ° C. 0.5 hours after the start of incubation (0 h), the reaction of S7 nuclease was stopped according to a conventional method. Then, the reaction solution was electrophoresed on a 7M urea-15% polyacrylamide gel according to a conventional method, then stained with SYBR Green II (trade name, Lonza), and E-BOX-VX2 (trade name, MS Instruments). Was used for analysis.
- SYBR Green II trade name, Lonza
- E-BOX-VX2 trade name, MS Instruments
- FIG. 32 is an electrophoresis photograph showing resistance to S7 nuclease.
- lane “M” is a molecular weight marker.
- H represents the incubation time.
- NI-0030 of the comparative example was almost completely decomposed after 0.5 hours of incubation.
- NK-0033 and PK-0007 of the example remained even after 0.5 hours of incubation. From this result, it was found that the ssRNA of the present invention is superior to dsRNA in S7 nuclease resistance.
- the ssRNA of the present invention can be constructed without depending on, for example, the type of target gene.
- the ssRNA includes, for example, the length of the duplex formed by the region (X) and the region (Xc) and the duplex formed by the region (Y) and the region (Yc).
- the internal region (Z) the presence / absence of free base that does not form a double chain, the number and position, and the presence / absence, type and length of the linker region (Lx) and linker region (Ly), It was found that it can be modified. From this, it can be said that the ssRNA of the present invention is a highly versatile new tool that can be used in gene expression suppression without depending on the type of target gene.
- Example B1 Synthesis of Prolinol Prolinol protected with a dimethoxytrityl group was synthesized according to Scheme 1 shown in the following formula.
- Fmoc-L-prolinol (compound 2)
- L-prolinol (Compound 1) (0.61 g, 6.0 mmol) was dissolved in 70 mL of pure water to prepare an L-prolinol aqueous solution.
- N- (9-fluorenylmethoxycarbonyloxy) succinimide (Fmoc-OSu) (2.0 g, 6.0 mmol) was dissolved in 10 mL of THF. This THF solution was added to the L-prolinol aqueous solution and stirred for 1 hour to react both. This reaction solution was separated into a liquid fraction and a precipitate fraction, and each fraction was extracted with ethyl acetate, and the organic layer was recovered.
- DMTr-amide-L-prolinol (compound 5)
- the DMTr-L-prolinol (compound 4) (0.80 g, 2.0 mmol), EDC (0.46 g, 2.4 mmol) and DMAP (0.29 g, 2.4 mmol) were dissolved in 20 mL of dichloromethane. Stir. To this solution, 10-hydroxydecanoic acid (0.45 g, 2.4 mmol) was added and stirred. The reaction was monitored by TLC with ethyl acetate and allowed to react for 20 hours until the DMTr-L-prolinol spot disappeared. And after adding dichloromethane to the said reaction liquid, the organic layer was collect
- DMTr-alkyl-L-prolinol (Compound 6)
- the DMTr-L-prolinol (compound 4) (0.80 g, 2.0 mmol) was dissolved in 15 mL of methanol, and 5-hydroxypentanal (0.31 g, 3.0 mmol) was added and stirred.
- sodium cyanoborohydride (0.25 g, 4.0 mmol) was added and further stirred.
- the reaction was monitored by TLC of ethyl acetate / hexane and allowed to react for 24 hours until the DMTr-L-prolinol spot disappeared. And the ethyl acetate was added to the said reaction liquid, and the organic layer was collect
- DMTr-Ureido-L-prolinol (Compound 8)
- the DMTr-L-prolinol (Compound 4) (0.50 g, 1.2 mmol) and triphosgene (0.12 g, 0.40 mmol) were dissolved in 8 mL of dichloromethane and stirred in an ice bath under argon. Then, N, N-diisopropylethylamine (0.31 g, 2.4 mmol) was added to the solution and stirred for 1 hour.
- the amount of 5-benzylthio-1H-tetrazole used was 0.15 g (0.78 mmol) for compounds 5 to 7 and 54 mg (0.15 mmol) for compound 8.
- 2-cyanoethyl N, N, N ′, N′-tetraisopropyl phosphorodiamidite was added under argon and stirred for 2 hours.
- the addition amount of the 2-cyanoethyl N, N, N ′, N′-tetraisopropyl phosphorodiamidite was 0.54 g (1.8 mmol) in the system using the compounds 5 to 7, and the compound 8 was used. In this system, it was 0.19 g (0.64 mmol).
- DMTr-amidoureido-L-proline amidite (Compound 17)
- the obtained DMTr-hydroxyamidoureido-L-proline (Compound 16) (0.62 g, 0.94 mmol) was mixed with anhydrous acetonitrile and azeotropically dried at room temperature.
- Diisopropylammonium tetrazolide (192 mg, 1.12 mmol) was added to the resulting residue, degassed under reduced pressure, and filled with argon gas.
- Example B3 Synthesis of Proline Diamide Amidite L-proline diamide amidite and D-proline diamide amidite were synthesized according to Scheme 3 above to generate the nucleic acid molecule of the present invention containing a linker having a proline skeleton.
- the mixture was diluted with dichloromethane (100 mL), washed with saturated aqueous sodium hydrogen carbonate (150 mL), and the organic layer was separated. The organic layer was dried over sodium sulfate, and then the organic layer was filtered. About the obtained filtrate, the solvent was distilled off under reduced pressure. To the resulting crude residue, anhydrous dimethylformamide (39 mL) and piperidine (18.7 mL, 189 mmol) were added and stirred at room temperature for 1 hour. After completion of the reaction, the solvent was distilled off from the mixed solution at room temperature under reduced pressure.
- DMTr-Diamide-L-proline amidite (Compound 10)
- the obtained DMTr-hydroxydiamide-L-proline (Compound 8) (8.55 g, 14.18 mmol) was mixed with anhydrous acetonitrile and dried azeotropically three times at room temperature.
- Diisopropylammonium tetrazolide (2.91 g, 17.02 mmol) was added to the resulting residue, degassed under reduced pressure, and filled with argon gas.
- the mixture was diluted with dichloromethane and washed with saturated aqueous sodium hydrogen carbonate, and the organic layer was separated. The organic layer was dried over sodium sulfate, and then the organic layer was filtered. About the obtained filtrate, the solvent was distilled off under reduced pressure. To the resulting crude residue, anhydrous dimethylformamide (5 mL) and piperidine (2.4 mL, 24 mmol) were added and stirred at room temperature for 1 hour. After completion of the reaction, the solvent was distilled off from the mixed solution at room temperature under reduced pressure.
- Example B4 In order to generate the nucleic acid molecule of the present invention including a linker having a proline skeleton, L-proline diamide amidite type B was synthesized according to the following scheme 4.
- Fmoc-t-butyl-dimethylsiloxyamide-L-proline (Compound 18) Fmoc-hydroxyamide-L-proline (compound 4) (2.00 g, 30 mmol), t-butyl-dimethylsilyl chloride (1.11 g, 35 mmol) and imidazole (10.90 g, 71 mmol) were mixed. The mixture was degassed under reduced pressure and filled with argon gas. To the mixture was added anhydrous acetonitrile (20 mL) at room temperature, and the mixture was stirred overnight at room temperature under an argon atmosphere.
- the mixture was diluted with dichloromethane and washed with saturated aqueous sodium hydrogen carbonate.
- the organic layer was collected and dried over sodium sulfate, and then the organic layer was filtered. About the obtained filtrate, the solvent was distilled off under reduced pressure.
- To the obtained residue were added anhydrous acetonitrile (5 mL) and 1 mol / L tetrabutylammonium fluoride-containing tetrahydrofuran solution (1.42 mL, tetrabutylammonium fluoride 1.42 mmol), and the mixture was stirred at room temperature overnight.
- DMTr-diamide-L-proline amidite type B (Compound 22)
- the obtained DMTr-hydroxydiamide-L-proline type B (Compound 21) (637 mg, 1.06 mmol) was mixed with anhydrous acetonitrile and azeotropically dried at room temperature.
- Diisopropylammonium tetrazolide (201 mg, 1.16 mmol) was added to the obtained residue, degassed under reduced pressure, and filled with argon gas.
- Example B5 In order to generate the nucleic acid molecule of the present invention including a linker having a proline skeleton, DMTr-amidoethyleneoxyethylamino-L-proline amidite (hereinafter referred to as PEG spacer type) was synthesized according to Scheme 5 below.
- PEG spacer type DMTr-amidoethyleneoxyethylamino-L-proline amidite
- the filtrate was concentrated and the obtained residue was subjected to silica gel column chromatography.
- the NMR results of the above compound are shown below.
- Example B6 Synthesis of Protected Prolinol Prolinol (compound 3) protected with a dimethoxytrityl group was synthesized according to Scheme 6 shown below.
- Trifluoroacetyl-L-prolinol (Compound 1) L-prolinol (2.0 g, 20 mmol) was dissolved in 20 mL of THF. On the other hand, ethyl trifluoroacetate (3.0 g, 21 mmol) was dissolved in 20 mL of THF. The latter THF solution was added dropwise to the former L-prolinol-containing THF solution and stirred for 12 hours. The reaction solution was concentrated under reduced pressure to obtain Compound 1 (3.7 g, yield 97%). The NMR results of the above compound are shown below.
- Trifluoroacetyl-DMTr-L-prolinol (Compound 2)
- the obtained trifluoroacetyl-L-prolinol (Compound 1) (3.7 g, 19 mmol) was dissolved in pyridine and dried azeotropically three times at room temperature. The obtained residue was dissolved in 15 mL of pyridine, and 4,4′-dimethoxytrityl chloride (DMTr—Cl) (8.1 g, 24 mmol) was added while stirring in an ice bath under argon. Reacted for hours. Then, in order to quench excess DMTr-Cl, 10 mL of methanol was further added to the reaction solution and stirred for 10 minutes.
- DMTr—Cl 4,4′-dimethoxytrityl chloride
- the organic layer was filtered, the obtained filtrate was concentrated under reduced pressure, and the residue was purified by reverse phase silica gel column chromatography.
- a mixed solvent of acetone and water containing 0.1% pyridine was used, and the mixing ratio of the acetone and water was stepwise. Specifically, the molar ratio of acetone: water The ratio was changed in the order of 2: 8, 3: 7, 4: 6 and 5: 5.
- the fraction containing the target compound 5 was extracted with dichloromethane, and the organic layer was dried over anhydrous sodium sulfate. The organic layer was filtered, and the obtained filtrate was concentrated under reduced pressure to obtain Compound 5 (prolinol urea amidite) (0.9 g, yield 49%).
- 2-cyanoethyl N, N, N ′, N′-tetraisopropyl phosphorodiamidite (0.50 g, 1.7 mmol) was dissolved in 1 mL of acetonitrile. This was added to the reaction solution and stirred at room temperature for 4 hours. Dichloromethane was added to the reaction solution, and the mixture was washed with a saturated aqueous sodium hydrogen carbonate solution and saturated brine. The collected organic layer after washing was dried over anhydrous sodium sulfate, the organic layer was filtered, and the obtained filtrate was concentrated under reduced pressure.
- the single-stranded nucleic acid molecule of the present invention gene expression can be suppressed, and since it is not circular, its synthesis is easy, and since it is single-stranded, a double-stranded annealing step And can be manufactured efficiently. Since the ssNc molecule of the present invention can suppress the expression of a target gene as described above, it is useful as a research tool for, for example, pharmaceuticals, diagnostic agents and agricultural chemicals, and agricultural chemicals, medicine, and life sciences.
Abstract
Description
5’側から3’側にかけて、5’側領域(Xc)、内部領域(Z)および3’側領域(Yc)を、前記順序で含み、
前記内部領域(Z)が、内部5’側領域(X)および内部3’側領域(Y)が連結して構成され、
前記5’側領域(Xc)が、前記内部5’側領域(X)と相補的であり、
前記3’側領域(Yc)が、前記内部3’側領域(Y)と相補的であり、
前記内部領域(Z)、前記5’側領域(Xc)および前記3’側領域(Yc)の少なくとも一つが、前記発現抑制配列を含むことを特徴とする。
本発明の一本鎖核酸分子は、前述のように、標的遺伝子の発現を抑制する発現抑制配列を含む一本鎖核酸分子であって、
5’側から3’側にかけて、5’側領域(Xc)、内部領域(Z)および3’側領域(Yc)を、前記順序で含み、
前記内部領域(Z)が、内部5’側領域(X)および内部3’側領域(Y)が連結して構成され、
前記5’側領域(Xc)が、前記内部5’側領域(X)と相補的であり、
前記3’側領域(Yc)が、前記内部3’側領域(Y)と相補的であり、
前記内部領域(Z)、前記5’側領域(Xc)および前記3’側領域(Yc)の少なくとも一つが、前記発現抑制配列を含むことを特徴とする。
5’-GUUGUCAUACUUCUCAUGG-3’(配列番号1)
5’-AAAGUCAAUGUACAGCUGCUU-3’(配列番号16)
5’-AUUGUAACGAGACAAACAC-3’(配列番号5)
5’-UUGCGCUUUUUGGUGACGC-3’(配列番号6)
Z=X+Y ・・・(1)
Z≧Xc+Yc ・・・(2)
X=Y ・・・(19)
X<Y ・・・(20)
X>Y ・・・(21)
(a)下記式(3)および(4)の条件を満たす。
X>Xc ・・・(3)
Y=Yc ・・・(4)
(b)下記式(5)および(6)の条件を満たす。
X=Xc ・・・(5)
Y>Yc ・・・(6)
(c)下記式(7)および(8)の条件を満たす。
X>Xc ・・・(7)
Y>Yc ・・・(8)
(d)下記式(9)および(10)の条件を満たす。
X=Xc ・・・(9)
Y=Yc ・・・(10)
(a)下記式(11)および(12)の条件を満たす。
X-Xc=1~10、好ましくは1、2、3または4、
より好ましくは1、2または3 ・・・(11)
Y-Yc=0 ・・・(12)
(b)下記式(13)および(14)の条件を満たす。
X-Xc=0 ・・・(13)
Y-Yc=1~10、好ましくは1、2、3または4、
より好ましくは1、2または3 ・・・(14)
(c)下記式(15)および(16)の条件を満たす。
X-Xc=1~10、好ましくは、1、2または3、
より好ましくは1または2 ・・・(15)
Y-Yc=1~10、好ましくは、1、2または3、
より好ましくは1または2 ・・・(16)
(d)下記式(17)および(18)の条件を満たす。
X-Xc=0 ・・・(17)
Y-Yc=0 ・・・(18)
(1)非修飾ヌクレオチド残基
(2)修飾ヌクレオチド残基
(3)非修飾ヌクレオチド残基および修飾ヌクレオチド残基
(1)非修飾ヌクレオチド残基
(2)修飾ヌクレオチド残基
(3)非修飾ヌクレオチド残基および修飾ヌクレオチド残基
(4)非ヌクレオチド残基
(5)非ヌクレオチド残基および非修飾ヌクレオチド残基
(6)非ヌクレオチド残基および修飾ヌクレオチド残基
(7)非ヌクレオチド残基、非修飾ヌクレオチド残基および修飾ヌクレオチド残基
前記ヌクレオチド残基は、例えば、構成要素として、糖、塩基およびリン酸を含む。前記ヌクレオチド残基は、前述のように、例えば、リボヌクレオチド残基およびデオキシリボヌクレオチド残基があげられる。前記リボヌクレオチド残基は、例えば、糖としてリボース残基を有し、塩基として、アデニン(A)、グアニン(G)、シトシン(C)およびU(ウラシル)を有し、前記デオキシリボース残基は、例えば、糖としてデオキシリボース残基を有し、塩基として、アデニン(A)、グアニン(G)、シトシン(C)およびチミン(T)を有する。
前記非ヌクレオチド残基は、特に制限されない。本発明のssNc分子は、例えば、前記非ヌクレオチド残基として、ピロリジン骨格またはピペリジン骨格を含む非ヌクレオチド構造を有してもよい。前記非ヌクレオチド残基は、例えば、前記リンカー領域(Lx)および前記リンカー領域(Ly)の少なくとも一方に有することが好ましい。前記非ヌクレオチド残基は、例えば、前記リンカー領域(Lx)に有してもよいし、前記リンカー領域(Ly)に有してもよいし、両方の前記リンカー領域に有してもよい。前記リンカー領域(Lx)および前記リンカー領域(Ly)は、例えば、同じでもよいし、異なってもよい。
X1およびX2は、それぞれ独立して、H2、O、SまたはNHであり;
Y1およびY2は、それぞれ独立して、単結合、CH2、NH、OまたはSであり;
R3は、環A上のC-3、C-4、C-5またはC-6に結合する水素原子または置換基であり、
前記置換基は、OH、OR4、NH2、NHR4、NR4R5、SH、SR4またはオキソ基(=O)であり;
R3が前記置換基の場合、置換基R3は、1でも複数でも、存在しなくてもよく、複数の場合、同一でも異なってもよく;
R4およびR5は、置換基または保護基であり、同一でも異なってもよく;
L1は、n個の原子からなるアルキレン鎖であり、ここで、アルキレン炭素原子上の水素原子は、OH、ORa、NH2、NHRa、NRaRb、SHもしくはSRaで置換されても置換されていなくてもよく、または、
L1は、前記アルキレン鎖の一つ以上の炭素原子が、酸素原子で置換されたポリエーテル鎖であり、
ただし、Y1が、NH、OまたはSの場合、Y1に結合するL1の原子は炭素であり、OR1に結合するL1の原子は炭素であり、酸素原子同士は隣接せず;
L2は、m個の原子からなるアルキレン鎖であり、ここで、アルキレン炭素原子上の水素原子は、OH、ORc、NH2、NHRc、NRcRd、SHもしくはSRcで置換されても置換されていなくてもよく、または、
L2は、前記アルキレン鎖の一つ以上の炭素原子が、酸素原子で置換されたポリエーテル鎖であり、
ただし、Y2が、NH、OまたはSの場合、Y2に結合するL2の原子は炭素であり、OR2に結合するL2の原子は炭素であり、酸素原子同士は隣接せず;
Ra、Rb、RcおよびRdは、それぞれ独立して、置換基または保護基であり;
lは、1または2であり;
mは、0~30の範囲の整数であり;
nは、0~30の範囲の整数であり;
環Aは、前記環A上のC-2以外の1個の炭素原子が、窒素、酸素、または硫黄で置換されてもよく、
前記環A内に、炭素-炭素二重結合、または、炭素-窒素二重結合を含んでもよい。前記リンカー領域(Lx)が前記式(1)で表わされる場合、前記領域(Xc)および前記領域(X)は、それぞれ、-OR1-または-OR2-を介して、前記リンカー領域(Lx)に結合する。また、前記リンカー領域(Ly)が前記式(1)で表わされる場合、前記領域(Yc)および前記領域(Y)は、それぞれ、-OR1-または-OR2-を介して、前記リンカー領域(Ly)に結合する。ここで、R1およびR2は、存在しても存在しなくてもよく、存在する場合、R1およびR2は、それぞれ独立して、ヌクレオチド残基または前記構造(I)である。
条件(1)
前記領域(Xc)は、-OR2-を介して、前記領域(X)は、-OR1-を介して、前記式(I)の構造と結合し、
前記領域(Yc)は、-OR1-を介して、前記領域(Y)は、-OR2-を介して、前記式(I)の構造と結合する。
条件(2)
前記領域(Xc)は、-OR2-を介して、前記領域(X)は、-OR1-を介して、前記式(I)の構造と結合し、
前記領域(Yc)は、-OR2-を介して、前記領域(Y)は、-OR1-を介して、前記式(I)の構造と結合する。
条件(3)
前記領域(Xc)は、-OR1-を介して、前記領域(X)は、-OR2-を介して、前記式(I)の構造と結合し、
前記領域(Yc)は、-OR1-を介して、前記領域(Y)は、-OR2-を介して、前記式(I)の構造と結合する。
条件(4)
前記領域(Xc)は、-OR1-を介して、前記領域(X)は、-OR2-を介して、前記式(I)の構造と結合し、
前記領域(Yc)は、-OR2-を介して、前記領域(Y)は、-OR1-を介して、前記式(I)の構造と結合する。
本発明のssNc分子の合成方法は、特に制限されず、従来公知の方法が採用できる。前記合成方法は、例えば、遺伝子工学的手法による合成法、化学合成法等があげられる。遺伝子工学的手法は、例えば、インビトロ転写合成法、ベクターを用いる方法、PCRカセットによる方法があげられる。前記ベクターは、特に制限されず、プラスミド等の非ウイルスベクター、ウイルスベクター等があげられる。前記化学合成法は、特に制限されず、例えば、ホスホロアミダイト法およびH-ホスホネート法等があげられる。前記化学合成法は、例えば、市販の自動核酸合成機を使用可能である。前記化学合成法は、一般に、アミダイトが使用される。前記アミダイトは、特に制限されず、市販のアミダイトとして、例えば、RNA Phosphoramidites(2’-O-TBDMSi、商品名、三千里製薬)、ACEアミダイトおよびTOMアミダイト、CEEアミダイト、CEMアミダイト、TEMアミダイト等があげられる。
本発明の発現抑制用組成物は、前述のように、標的遺伝子の発現を抑制するための組成物であり、前記本発明のssNc分子を含むことを特徴とする。本発明の組成物は、前記本発明のssNc分子を含むことが特徴であり、その他の構成は、何ら制限されない。本発明の発現抑制用組成物は、例えば、発現抑制用試薬ということもできる。
本発明の発現抑制方法は、前述のように、標的遺伝子の発現を抑制する方法であって、前記本発明のssNc分子を使用することを特徴とする。本発明の発現抑制方法は、前記本発明のssNc分子を使用することが特徴であって、その他の工程および条件は、何ら制限されない。
本発明の疾患の治療方法は、前述のように、前記本発明のssNc分子を、患者に投与する工程を含み、前記ssNc分子が、前記発現抑制配列として、前記疾患の原因となる遺伝子の発現を抑制する配列を有することを特徴とする。本発明の治療方法は、前記本発明のssNc分子を使用することが特徴であって、その他の工程および条件は、何ら制限されない。
本発明の使用は、前記標的遺伝子の発現抑制のための、前記本発明のssNc分子の使用である。また、本発明の使用は、RNA干渉の誘導のための、前記本発明のssNc分子の使用である。
実施例のRNA(Ex)として、以下に示すssRNA(NK-0016)を合成した。前記NK-0016は、GAPDH遺伝子の発現を抑制する19塩基長の発現抑制配列(配列番号1)を有する。NK-0016の配列において、領域(Xc)と領域(X)との間が、リンカー領域(Lx)であり、領域(Y)と領域(Yc)との間が、リンカー領域(Ly)である(以下、同様)。配列において、5’領域(Xc)および3’領域(Yc)は、それぞれ小文字で表わす(以下、同様)。
GAPDH遺伝子発現抑制配列(配列番号1)
5’-GUUGUCAUACUUCUCAUGG-3’
本発明のssRNAを用いて、in vitroにおけるGAPDH遺伝子の発現抑制を確認した。
GAPDH遺伝子用プライマーセット
5’-GGAGAAGGCTGGGGCTCATTTGC-3’(配列番号9)
5’-TGGCCAGGGGTGCTAAGCAGTTG-3’(配列番号10)
β-アクチン遺伝子用プライマーセット
5’-GCCACGGCTGCTTCCAGCTCCTC-3’(配列番号11)
5’-AGGTCTTTGCGGATGTCCACGTCAC-3’(配列番号12)
これらの結果を、図4に示す。図4は、GAPDH遺伝子発現量の相対値を示すグラフである。図4に示すように、前記NK-0016は、RNA未添加のコントロール(-)よりも低い発現量であり、GAPHD遺伝子の発現を抑制したことがわかった。また、図4に示すように、投与量依存的に遺伝子発現抑制効果を示すことがわかった。
本発明のssRNAを用いて、in vitroにおけるGAPDH遺伝子の発現抑制を確認した。
実施例のRNA(Ex)として、前記実施例A1のssRNA(NK-0016)を使用した。比較例のRNAとして、RNAiポジティブコントロール(Pc)の前記dsRNA(NI-0011)を使用した。前記RNAを、40μmol/Lとなるように、注射用蒸留水に溶解し、RNA溶液を調製した。
これらの結果を、図5に示す。図5は、GAPDH遺伝子発現量の相対値を示すグラフであり、縦軸は、相対遺伝子発現量である。図5に示すように、前記実施例のNK-0016は、比較例のNI-0011と比較して、極めて強い遺伝子発現抑制活性を示した。
本発明のssRNAを用いて、in vitroにおけるGAPDH遺伝子の発現抑制を確認した。
実施例のRNA(Ex)として、前記実施例A1のNK-0016および以下のEx-ssRNA(PK-0004)を使用した。前記PK-0004において、リンカー領域(Lx)およびリンカー領域(Ly)は、XcとXとの間、YcとYとの間を、実施例Bに示すスキーム3の化合物10(L-プロリンジアミドアミダイト)を用いて結合させた。前記両リンカーの化学式を以下に示す。前記NK-0016と前記PK-0004は、XcとXとの間のリンカー領域(Lx)、およびYcとYとの間のリンカー領域(Ly)が異なる以外は、同じ配列とした。
これらの結果を、図6および7に示す。図6は、A549細胞の結果であり、図7は、293細胞の結果である。図6および7は、GAPDH遺伝子発現量の相対値を示すグラフである。図6および7に示すように、実施例のNK-0016およびPK-0004は、強い遺伝子発現抑制活性を示し、濃度依存的に効果を示すことがわかった。
本発明のssRNAについて、in vitroでのTGF-β1遺伝子の発現抑制効果を確認した。
実施例のRNA(Ex)として、以下に示すssRNA(NK-0033)を使用した。前記NK-0033は、TGF-β1遺伝子の発現を抑制する21塩基長の下記配列を有している。この配列は、Chengらが用いたsiRNA(Mol.Pharm.,2009,6,772-779)に基づいて、設計した。
TGF-β1遺伝子発現抑制配列(配列番号16)
5’-AAAGUCAAUGUACAGCUGCUU-3’
TGF-β1遺伝子用プライマーセット
5’-CCATTGCTGTCCCGTGCAGAGCTG-3’(配列番号17)
5’-ATGGTAGCCCTTGGGCTCGTGGATC-3’(配列番号18)
β-アクチン遺伝子増幅用プライマーセット
5’-GTCGTACCACAGGCATTGTGATGG-3’(配列番号19)
5’-GCAATGCCTGGGTACATGGTGG-3’(配列番号20)
これらの結果を、図8に示す。図8は、TGF-β1遺伝子発現量の相対値を示すグラフである。図8に示すように、前記実施例のNK-0033は、in vitroにおいて、TGF-β1遺伝子の発現を抑制した。他方、ネガティブコントロールのNK-0035は、TGF-β1遺伝子の発現を抑制しなかった。
本発明のssRNAについて、in vivoでの遺伝子発現抑制および急性肺傷害抑制の効果を確認した。前記効果の確認は、Takagiら(J.Thromb Hemost 2009;7:2053-2063)に記載の方法に従って行った。
(1.1)急性肺傷害マウスへのssRNAの投与
実施例のRNA(Ex)は、前記実施例A5のssRNA(NK-0033)を使用した。比較例のRNAは、前記実施例A5に示す、RNAiネガティブコントロール(Nc)のssRNA(NK-0035)を使用した。
・投与群1
滅菌生理食塩水80μLの投与から1時間後、滅菌生理食塩水50μLを投与
・投与群2
RNA溶液(NK-0033)80μLの投与から1時間後、滅菌生理食塩水50μLを投与
・投与群3
RNA溶液(NK-0035)80μLの投与から1時間後、滅菌生理食塩水50μLを投与
・投与群4
滅菌生理食塩水80μLの投与から1時間後、前記LPS溶液50μLを投与
・投与群5
RNA溶液(NK-0033)80μLの投与から1時間後、前記LPS溶液50μLを投与
・投与群6
RNA溶液(NK-0035)80μLの投与から1時間後、前記LPS溶液50μLを投与
前記LPS溶液を滴下してから24時間後、前記マウスの腹腔に、過剰量のペントバルビタールを投与して安楽死させ、生化学的解析および組織学的解析のサンプルとした。ネガティブコントロールは、前記LPS溶液に代えて、滅菌生理食塩水を添加した。
(2.1)肺におけるTGF-β1遺伝子発現の抑制
前記マウスの肺サンプルについて、TGF-β1 Quantikine Colorimetric Sandwich ELISA(商品名、R&D Systems社)を用いて、単位重量の肺あたりのTGF-β1発現量を測定した。
急性肺傷害における炎症は、好中球等の細胞が肺に浸潤することによって生じる。このため、肺に対する好中球等の細胞の浸潤を抑制する薬物は、急性肺傷害における炎症の治療薬となる。そこで、気管支肺胞洗浄液(BALF)中の細胞数を、肺へ浸潤した細胞数の指標として、本発明のssRNAの薬理効果を確認した。
ギムザ染色の結果を、図12に示す。図12は、前記BALFサンプル中の細胞のギムザ染色の結果を示す写真である(倍率100倍)。図12において、(A)は、LPS(+)/RNA(-)の投与群4の結果であり、(B)は、LPS(+)/ネガティブコントロールNK-0035(+)の投与群6の結果であり、(C)は、LPS(+)/NK-0033(+)の実施例投与群5の結果を示す。
HE染色の結果を、図13に示す。図13は、前記肺組織のHE染色の結果を示す写真である(倍率10倍)。図13において、(A)は、LPS(+)/RNA(-)の投与群4の結果であり、(B)は、LPS(+)/ネガティブコントロールNK-0035(+)の投与群6の結果であり、(C)は、LPS(+)/NK-0033(+)の実施例投与群5の結果を示す。図13から、血管周囲、肺胞腔内、肺胞壁および気管支周辺への、好中球等の細胞の浸潤が減少し、肺組織の傷害性が低減していることがわかった。
従来法のiRNA剤は、副作用としてインターフェロンを配列非依存的に誘導することが知られており、この副作用が問題視されている。そこで、本発明のssRNAについて、インターフェロン誘導の副作用を評価した。
前記実施例A6と同じ方法および条件により、急性肺傷害マウスへのssRNAの投与を行った。そして、前記実施例A6と同様にして、前記LPS溶液または滅菌生理食塩水(LPSに対するネガティブコントロール)を滴下してから24時間後、マウスを安楽死させ、肺組織を採取した。
GAPDH遺伝子用プライマーセット
5’-CCCTTATTGACCTCAACTACATGGT-3’(配列番号21)
5’-GAGGGGCCATCCACAGTCTTCTG-3’(配列番号22)
TGF-β1遺伝子用プライマーセット
5’-ACTCCACGTGGAAATCAACGG-3’(配列番号23)
5’-TAGTAGACGATGGGCAGTGG-3’(配列番号24)
IFN-α遺伝子用プライマーセット
5’-ATGGCTAGRCTCTGTGCTTCCT-3’(配列番号25)
5’-AGGGCTCTCCAGAYTTCTGCTCTG-3’(配列番号26)
IFN-β遺伝子用プライマーセット
5’-CATCAACTATAAGCAGCTCCA-3’(配列番号27)
5’-TTCAAGTGGAGAGCAGTTCAG-3(配列番号28)
前記TGF-β1遺伝子、IFN-α遺伝子およびIFN-β遺伝子の発現量に関する定量的解析結果を、それぞれ、図14(A)~(C)のグラフに示す。各投与群は、前記実施例A6と同様に以下の通りである。
本発明のssRNAについて、in vitroでのTGF-β1遺伝子の発現抑制効果を確認した。
凍結保存した前記RNAを、20μmol/Lとなるように、注射用蒸留水に溶解し、RNA溶液を調製した。そして、前記RNA溶液を使用した以外は、前記実施例A5と同様にして、Hepal-6細胞への前記ssRNAのトランスフェクション、RNA回収、cDNA合成およびPCRを行い。TGF-β1遺伝子の相対的発現量を測定した。トランスフェクション時のRNA濃度は、1nmol/Lとした。
これらの結果を、図15および16に示す。図15および図16は、それぞれ、TGF-β1遺伝子発現量の相対値を示すグラフである。図15は、NK-0033、NK-0061、NK-0055およびNK-0062を使用した結果であり、図16は、PK-0007、PK-0026、PK-0027およびPK-0028を使用した結果である。図15および図16に示すように、いずれのssRNAも、強い遺伝子発現抑制活性を示した。
in vivoでのTGF-β1遺伝子発現抑制効果および急性肺傷害抑制効果
本発明のssRNAを用いて、in vivoでのTGF-β1遺伝子の発現抑制効果を確認した。
急性肺傷害マウスへのRNAの投与は、特に示さない限り、前記実施例A6と同様にして行った。
・投与群1
滅菌生理食塩水75μLの投与から5分後、滅菌生理食塩水50μLを投与
・投与群2
滅菌生理食塩水75μLの投与から5分後、LPS溶液50μLを投与
・投与群3
RNA溶液(PK-0007)75μLの投与から5分後、LPS溶液50μLを投与
・投与群4
RNA溶液(PK-0008)75μLの投与から5分後、LPS溶液50μLを投与
・投与群5
RNA溶液(NK-0033)75μLの投与から5分後、LPS溶液50μLを投与
・投与群6
RNA溶液(NK-0035)75μLの投与から5分後、LPS溶液50μLを投与
・投与群7
RNA溶液(NI-0030)75μLの投与から5分後、LPS溶液50μLを投与
・投与群8
RNA溶液(NI-0031)50μLの投与から5分後、LPS溶液50μLを投与
本発明のssRNAを用いて、in vivoでのオフターゲット効果を確認し、副作用を評価した。
・投与群1
滅菌生理食塩水75μLを投与
・投与群2
RNA溶液(PK-0007)75μLを投与
・投与群3
RNA溶液(PK-0008)75μLを投与
本発明のssRNAを用いて、in vitroにおけるLAMA1遺伝子の発現抑制を確認した。
LAMA1遺伝子用プライマーセット
5’-AAAGCTGCCAATGCCCCTCGACC-3’(配列番号45)
5’-TAGGTGGGTGGCCCTCGTCTTG-3’(配列番号46)
これらの結果を、図19に示す。図19は、293細胞におけるLAMA1遺伝子の発現量の相対値を示すグラフである。図19に示すように、実施例のNK-0043およびNK-0064は、強い遺伝子発現抑制活性を示すことがわかった。
本発明のssRNAを用いて、RNA干渉効果による、in vitroにおけるLMNA遺伝子の発現抑制を確認した。
LMNA遺伝子用プライマーセット
5’-CTGGACATCAAGCTGGCCCTGGAC-3’(配列番号49)
5’-CACCAGCTTGCGCATGGCCACTTC-3’(配列番号50)
これらの結果を、図20に示す。図20は、A549細胞におけるLMNA遺伝子の発現量の相対値を示すグラフである。図20に示すように、実施例のNK-0063およびNK-0066は、強い遺伝子発現抑制活性を示すことがわかった。
本発明のssRNAについて、前記内部5’側領域(X)に相補的な前記5’側領域(Xc)の長さ、および、前記内部3’側領域(Y)に相補的な前記3’側領域(Yc)の長さを変化させ、in vitroにおけるGAPDH遺伝子の発現抑制を確認した。
実施例のRNAとして、図21に示すssRNAを使用した。図21において、右端の番号は、配列番号を示す。図21において、5’側から、小文字下線の領域は、前記領域(Xc)、大文字下線の領域は、前記内部領域(Z)、小文字下線の領域は、前記領域(Yc)を示す。前記Xcと前記Zとの間が、リンカー領域(Lx)であり、前記Zと前記Ycとの間が、リンカー領域(Ly)である。また、「Xc/Yc」は、前記領域(Xc)の塩基長(Xc)と、前記領域(Yc)の塩基長(Yc)との比を示す。図21において、「*」は、フリー塩基を示す。
これらの結果を、図22に示す。図22は、終濃度10nmol/LのRNAを使用した場合におけるGAPDH遺伝子発現量の相対値を示すグラフである。図22に示すように、前記5’側領域(Xc)および前記3’側領域(Yc)の長さを変化させたいずれのssRNAについても、GAPDH遺伝子の発現抑制が確認できた。
本発明のssRNAについて、前記内部5’側領域(X)、前記5’側領域(Xc)、前記内部3’側領域(Y)および前記3’側領域(Yc)の各長さを変化させ、in vitroにおけるGAPDH遺伝子の発現抑制を確認した。
実施例のRNAとして、図23に示すssRNAを使用した。図23において、右端の番号は、配列番号を示す。図23において、5’側から、小文字下線の領域は、前記領域(Xc)、大文字下線の領域は、前記内部領域(Z)、小文字下線の領域は、前記領域(Yc)を示す。また、「Xc+Yc/X+Y」は、前記領域(Xc)と前記領域(Yc)の塩基長の合計と、前記領域(X)と前記領域(Y)の塩基長の合計との比を示す。図23において、「*」は、フリー塩基を示す。
これらの結果を、図24に示す。図24は、終濃度1nmol/LのRNAを使用した場合におけるGAPDH遺伝子発現量の相対値を示すグラフである。図24に示すように、前記領域(X)、前記領域(Xc)、前記領域(Y)および前記領域(Yc)の長さを変化させたいずれのssRNAについても、GAPDH遺伝子の発現抑制が確認できた。また、前記実施例A2において、NK-0016は、極めて強い発現抑制活性が確認されている。本実施例において、NK-0016以外のssRNAは、全てNK-0016をさらに上回る活性が認められた。
本発明のssRNAについて、前記内部5’側領域(X)に相補的な前記5’側領域(Xc)の長さを変化させ、in vitroにおけるGAPDH遺伝子の発現抑制を確認した。
実施例のRNAとして、図25に示すssRNAを使用した。図25において、5’側から、小文字下線の領域は、前記領域(Xc)、大文字下線の領域は、前記内部5’領域(X)、小文字下線の領域は、前記領域(Yc)を示す。また、「Xc/Yc」は、前記領域(Xc)の塩基長(Xc)と、前記領域(X)の塩基長(X)との比を示す。図25において、「*」は、フリー塩基を示す。下記RNAの配列は、配列番号74~76に示す。
これらの結果を、図26に示す。図26は、終濃度1nmol/LのRNAを使用した場合におけるGAPDH遺伝子発現量の相対値を示すグラフである。図26に示すように、前記5’側領域(Xc)の長さを変化させたいずれのssRNAについても、GAPDH遺伝子の発現抑制が確認できた。特に、フリー塩基を有する場合、その数が少ない程、前記発現抑制活性を向上できると考えられる。また、前記実施例A2において、NK-0016は、極めて強い発現抑制活性が確認されている。本実施例において、NK-0016以外のssRNAは、全てNK-0016をさらに上回る活性が認められた。
本発明のssRNAについて、前記内部5’側領域(X)と前記5’側領域(Xc)との間のリンカー領域(Lx)および前記内部3’側領域(Y)と前記3’側領域(Yc)との間のリンカー領域(Ly)を変化させ、in vitroにおけるGAPDH遺伝子の発現抑制を確認した。
実施例のRNAとして、図27に示すssRNAを使用した。図27において、5’側から、小文字下線の領域は、前記5’側領域(Xc)、大文字下線の領域は、前記内部領域(Z)、小文字下線の領域は、前記3’側領域(Yc)を示す。前記Xと前記Xcとの間の配列が、リンカー領域(Lx)であり、前記Yと前記Ycとの間の配列が、リンカー領域(Ly)である。また、各RNAについて、リンカー領域(Lx)の塩基長(Lx)と、リンカー領域(Ly)の塩基長(Ly)との比(Lx/Ly)を示す。図27において、「*」は、フリー塩基を示す。
これらの結果を、図28に示す。図28は、終濃度1nmol/LのRNAを使用した場合におけるGAPDH遺伝子発現量の相対値を示すグラフである。図28に示すように、前記リンカー領域(Lx)および(Ly)の条件、すなわち、長さ、両者間の長さの比、配列等を変化させたいずれのssRNAについても、同様に、GAPDH遺伝子の発現抑制が確認できた。この結果から、前記リンカー領域(Lx)および(Ly)の条件は、特に制限されず、様々な長さ、配列等に設計可能であることがわかった。
プロリンまたはプロリノールを有するリンカーで置換したssRNAを用いて、HCT116細胞でのGAPDH発現抑制効果を確認した。
実施例のRNA(Ex)として、以下に示すRNA(Ex ssRNA)を合成した。また、比較例のRNAとして、以下に示す、RNAiのネガティブコントロール(Nc)のNc ssRNAを合成した。下記式において、リンカー領域(Lx)およびリンカー領域(Ly)は、XcXとの間、および、YcYとの間を、プロリンまたはプロリノールを有する下記表のアミダイト(実施例B参照)を用いて結合させた。
これらの結果を、図29に示す。図29は、GAPDH遺伝子発現量の相対値を示すグラフである。図29に示すように、リンカー領域(Lx)およびリンカー領域(Ly)としてプロリンまたはプロリノールを含むEx ssRNAは、いずれも、強い遺伝子発現抑制活性が確認でき、濃度依存的に効果を示すことがわかった。他方、ネガティブコントロールのssRNAは、抑制効果が観察されなかった。
プロリンを有するリンカーで置換したssRNAを用いて、HCT116細胞でのGAPDH発現抑制効果を確認した。
実施例のRNA(Ex)として、以下に示すRNA(Ex ssRNA)を合成した。また、比較例のRNAとして、以下に示す、RNAiのネガティブコントロール(Nc)のNc ssRNAを合成した。下記式において、リンカー領域(Lx)およびリンカー領域(Ly)は、XcとXとの間、および、YcYとの間を、プロリンまたはプロリノールを有する下記表のアミダイト(実施例B参照)を用いて結合させた。
これらの結果を、図30に示す。図30は、HCT116細胞のGAPDH遺伝子発現量の相対値を示すグラフである。図30に示すように、リンカー領域(Lx)およびリンカー領域(Ly)としてプロリンを含むEx ssRNAは、強い遺伝子発現抑制活性を示し、濃度依存的に効果を示すことがわかった。他方、ネガティブコントロールのssRNAは、抑制効果が観察されなかった。
本発明のssRNAについて、リボヌクレアーゼ耐性を確認した。
実施例のRNA(Ex)として、実施例A5におけるNK-0033および実施例A8におけるPK-0007を使用した。また、比較例のRNAとして、実施例A9におけるポジティブコントロール(Pc)のdsRNA(NI-0030)を使用した。
この結果を図31に示す。図31は、リボヌクレアーゼ耐性を示す電気泳動写真である。図31において、レーン「M」は、分子量マーカーであり、minは、インキュベート時間を示す。
本発明のssRNAについて、ヌクレアーゼ耐性を確認した。
前記実施例A18と同じRNAを使用した。まず、5mmol/L CaCl2を含む50mmol/L Tris-HCl(pH8)に、60pmolの前記RNA、0.5ユニットのS7ヌクレアーゼ(Roche)を混合し、37℃にてインキュベートした。インキュベート開始(0h)から0.5時間後に、定法に従ってS7ヌクレアーゼの反応を停止させた。そして、そして、前記反応液を定法に従い、7M尿素-15%ポリアクリルアミドゲルで電気泳動した後、SYBR Green II(商品名、Lonza)で染色し、E-BOX-VX2(商品名、エムエス機器)を用いて分析した。
この結果を図32に示す。図32は、S7ヌクレアーゼ耐性を示す電気泳動写真である。図32において、レーン「M」は、分子量マーカーである。また、hは、インキュベート時間を示す。
1.プロリノールの合成
下記式に示すスキーム1に従い、ジメトキシトリチル基で保護されたプロリノールを合成した。
L-プロリノール(化合物1)(0.61g、6.0mmol)を、純水70mLに溶解し、L-プロリノール水溶液を調製した。N-(9-フルオレニルメトキシカルボニロキシ)スクシンイミド(Fmoc-OSu)(2.0g、6.0mmol)を、THF10mLに溶解した。このTHF溶液を、前記L-プロリノール水溶液に加え、1時間撹拌して、両者を反応させた。この反応液を、液体画分と沈殿画分とに分離し、それぞれの画分を酢酸エチルで抽出し、それぞれ有機層を回収した。そして、それぞれの有機層を合わせた後、無水硫酸ナトリウムを添加して、水分を吸収させた(以下、乾燥という)。前記有機層をろ過して、ろ液を回収し、前記ろ液を減圧濃縮した。得られた残渣を、シリカゲルカラムクロマトグラフィー(展開溶媒 ヘキサン:酢酸エチル=1:1)により精製し、化合物2を得た(1.4g、収率74%)。以下に、化合物のNMRの結果を示す。
1H-NMR(CDCl3): δ7.77(2H,d,J=7.7Hz,Ar-H),7.60(2H,d,J=7.3Hz,Ar-H),7.40(2H,t,J=7.5Hz,Ar-H),7.31(2H,t,J=7.6Hz,Ar-H),4.40-4.50(2H,m,COOCH2),4.22(1H,t,J=6.5Hz,Ar-CH),3.20-3.80(5H,m,H-5,H-6),1.75(3H,m,H-3,H-4),1.40(1H,m,H-3).
前記Fmoc-L-プロリノール(化合物2)(1.4g、4.3mmol)を、ピリジン20mLに溶解して、3回共沸した。得られた残留物を、ピリジン20mLに溶解した。この溶液を、アルゴン下、氷浴中で、撹拌しながら、4,4’-ジメトキシトリチルクロリド(DMTr-Cl)(1.8g、5.3mmol)を添加した。この反応液について、クロロホルム/メタノールのTLCにより反応を追跡し、Fmoc-L-プロリノールのスポットが消えるまで、4時間反応させた。そして、過剰のDMTr-Clをクエンチするために、前記反応液に、メタノール3mLを加えて10分撹拌した。前記反応液に、さらに、クロロホルムを加えた後、有機層を回収した。回収した前記有機層に、飽和食塩水による洗浄、5%炭酸水素ナトリウム水溶液による洗浄を行い、もう一度、飽和食塩水による洗浄を行った。洗浄後の有機層を、無水硫酸ナトリウムで乾燥させた。前記有機層をろ過して、得られたろ液を減圧濃縮した。得られた残渣を、シリカゲルカラムクロマトグラフィー(展開溶媒 クロロホルム、1%ピリジン)により精製し、化合物3を得た(2.0g、収率74%)。以下に、化合物のNMRの結果を示す。
1H-NMR(CDCl3): δ7.77(2H,d,J=7.7Hz,Ar-H),7.60(2H,d,J=7.3Hz,Ar-H),7.40-7.18(13H,m,Ar-H),6.89(4H,d,J=8.6Hz,Ar-H),4.20-4.40(2H,m,COOCH2),4.02(1H,t,J=6.5Hz,Ar-CH),3.80-3.10(5H,m,H-5,H-6),3.73(s,6H,OCH3),1.84(3H,m,H-3,H-4),1.58(1H,m,H-3).
前記Fmoc-DMTr-L-プロリノール(化合物3)(2.0g、3.2mmol)を、20%ピペリジンを含むDMF溶液25mLに溶解し、12時間撹拌した。この溶液を減圧濃縮し、得られた残渣を、シリカゲルカラムクロマトグラフィー(クロロホルム:メタノール=85:15、1%ピリジン含有)で精製し、化合物4を得た(1.0g、収率78%)。以下に、化合物のNMRの結果を示す。
1H-NMR(CDCl3): δ7.40-7.14(9H,m,Ar-H),6.82(4H,d,J=8.6Hz,Ar-H),3.78(6H,s,OCH3),3.31(1H,m,H-6), 3.07(2H,m,H-2,H-6),2.90(2H,m,H-5),1.84(3H,m,H-3,H-4),1.40(1H,m,H-3).
つぎに、下記式に示すスキーム2に従い、プロリノールを有するアミダイト誘導体を合成した。以下、1-エチル-3-(3-ジメチルアミノプロピル)カルボジイミド塩酸塩を、「EDC」、N,N-ジメチルアミノピリジン(4-ジメチルアミノピリジン)を「DMAP」という。
前記DMTr-L-プロリノール(化合物4)(0.80g、2.0mmol)、EDC(0.46g、2.4mmol)およびDMAP(0.29g、2.4mmol)を、ジクロロメタン20mLに溶解して撹拌した。この溶液に、10-ヒドロキシデカン酸(0.45g、2.4mmol)を添加し、撹拌した。この反応液について、酢酸エチルのTLCにより反応を追跡し、DMTr-L-プロリノールのスポットが消えるまで、20時間反応させた。そして、前記反応液に、ジクロロメタンを加えた後、有機層を回収した。回収した前記有機層を、飽和食塩水で洗浄した後、無水硫酸ナトリウムで乾燥させた。前記有機層をろ過して、得られたろ液を減圧濃縮し、その残渣を、シリカゲルカラムクロマトグラフィー(酢酸エチル、1%ピリジン含有)により精製し、化合物5を得た(0.71g,収率62%)。以下に、化合物のNMRの結果を示す。
1H-NMR(CDCl3): δ7.40-7.14(9H,m,Ar-H), 6.82(4H,d,J=8.6Hz,Ar-H),3.78(6H,s,OCH3),3.68-2.93(7H,m,H-2,H-5,H-6),2.27-1.72(6H,m,アルキル,H-3,H-4),1.58(4H,s,アルキル),1.30(10H,s,アルキル).
前記DMTr-L-プロリノール(化合物4)(0.80g、2.0mmol)を、メタノール15mLに溶解し、5-ヒドロキシペンタナール(0.31g、3.0mmol)を加えて撹拌した。この溶液に、シアノ水素化ホウ素ナトリウム(0.25g、4.0mmol)を加え、さらに撹拌した。この反応液について、酢酸エチル/ヘキサンのTLCにより反応を追跡し、DMTr-L-プロリノールのスポットが消えるまで、24時間反応させた。そして、前記反応液に、酢酸エチルを加え、有機層を回収した。回収した前記有機層を、飽和食塩水で洗浄した後、無水硫酸ナトリウムで乾燥させた。前記有機層をろ過して、得られたろ液を減圧濃縮し、その残渣を、シリカゲルカラムクロマトグラフィー(ヘキサン:酢酸エチル=1:1、1%ピリジン含有)により精製し、化合物6を得た(0.62g、収率63%)。以下に、化合物のNMRの結果を示す。
1H-NMR(CDCl3): δ7.40-7.14(9H,m,Ar-H),6.82(4H,d,J=8.6Hz,Ar-H),3.78(6H,s,OCH3),3.70-2.86(4H,m,CH2OH,H-6),2.06-1.79(5H,m,アルキル,H-2,H-5),1.74-1.49(6H,m,アルキル,H-3,H-4),1.45-1.27(4H,m,アルキル).
1,4-ブタンジオール(0.90g、10mmol)を、ジクロロメタン30mLに溶解し、さらに、カルボニルジイミダゾール(1.4g、8.6mmol)を加え、3時間撹拌した。この反応液の有機層を、飽和食塩水で洗浄した後、無水硫酸ナトリウムで乾燥させた。前記有機層をろ過して、得られたろ液を減圧濃縮し、その残渣を、シリカゲルカラムクロマトグラフィー(クロロホルム:メタノール=9:1)により精製した。これによって、1,4-ブタンジオールの一方の末端がカルボニルジイミダゾールで活性化された化合物を得た(0.25g,1.5mmol)。この化合物をジクロロメタン15mLに溶解し、前記DMTr-L-プロリノール(化合物4)(0.6g、1.5mmol)を添加し、24時間撹拌した。この混合液に、さらに、酢酸エチルを加え、有機層を回収した。回収した前記有機層を、飽和食塩水で洗浄した後、無水硫酸ナトリウムで乾燥させた。前記有機層をろ過して、得られたろ液を減圧濃縮し、その残渣を、シリカゲルカラムクロマトグラフィー(ヘキサン:酢酸エチル=1:1、1%ピリジン含有)により精製し、化合物7を得た(0.61g、収率77%)。以下に、化合物のNMRの結果を示す。
1H-NMR(CDCl3): δ7.40-7.14(9H,m,Ar-H),6.82(4H,d,J=8.6Hz,Ar-H),4.24-3.94(2H,m,COOCH2),3.78(s,6H,OCH3),3.72-2.96(7H,m,アルキル,H-2,H-5,H-6),2.10-1.30(8H,m,アルキル,H-3,H-4).
前記DMTr-L-プロリノール(化合物4)(0.50g、1.2mmol)およびトリホスゲン(0.12g、0.40mmol)を、ジクロロメタン8mLに溶解し、アルゴン下、氷浴中で、撹拌した。そして、前記溶液に、N,N-ジイソプロピルエチルアミン(0.31g、2.4mmol)を添加し、1時間撹拌した。さらに、前記溶液に、8-アミノ-1-オクタノール(0.17g、1.2mmol)を添加し、同様にして氷浴中で30分撹拌した後、室温で20時間撹拌した。前記溶液に、ジクロロメタンを加え、有機層を回収した。回収した前記有機層を、飽和食塩水で洗浄した後、無水硫酸ナトリウムで乾燥させた。前記有機層をろ過して、得られたろ液を減圧濃縮し、その残渣を、シリカゲルカラムクロマトグラフィー(ヘキサン:酢酸エチル=4:1、1%トリエチルアミン含有)により精製し、化合物8を得た(0.44g、収率62%)。以下に、化合物のNMRの結果を示す。
1H-NMR(CDCl3): δ7.40-7.14(9H,m,Ar-H),6.82(4H,m,Ar-H),3.78(s,6H,OCH3),3.68-3.25(9H,m,CH2NH,CH2OH,H-2,H-5,H-6),1.74-1.18(16H,m,アルキル,H-3,H-4).
前記修飾プロリノール(化合物5~8)を、それぞれ原料として、以下に示す方法により、化合物9~12を合成した。前記修飾プロリノールおよび5-ベンジルチオ-1H-テトラゾールを、アセトニトリル3mLに溶解した。前記修飾プロリノールの使用量は、化合物5の場合、0.69g(1.2mmol)、化合物6の場合、0.60g(1.2mmol)、化合物7の場合、0.60g(1.2mmol)、化合物8の場合、0.25g(0.43mmol)とした。また、5-ベンジルチオ-1H-テトラゾールの使用量は、化合物5~7に対しては、0.15g(0.78mmol)、化合物8に対しては、54mg(0.15mmol)とした。前記溶液に、アルゴン下、2-シアノエチルN,N,N’,N’-テトライソプロピルホスホロジアミダイトを添加し、2時間撹拌した。前記2-シアノエチルN,N,N’,N’-テトライソプロピルホスホロジアミダイトの添加量は、前記化合物5~7を使用した系では、0.54g(1.8mmol)とし、前記化合物8を使用した系では、0.19g(0.64mmol)とした。そして、前記溶液に、飽和炭酸水素ナトリウム水溶液を添加し、さらに、ジクロロメタンで抽出し、有機層を回収した。回収した前記有機層を、無水硫酸ナトリウムで乾燥させた。前記有機層をろ過して、得られたろ液を減圧濃縮し、その残渣を、シリカゲルカラムクロマトグラフィー(ヘキサン:酢酸エチル=1:1、1%トリエチルアミン含有)により精製し、化合物9~12を得た。以下に、各化合物のNMRの結果を示す。
1H-NMR(CDCl3)δ7.40-7.14(9H,m,Ar-H),6.82(4H,d,J=8.6Hz,Ar-H),3.78(6H,s,OCH3),3.68-2.93(11H,m,CH2O,POCH2,CHCH3,H-2,H-5,H-6),2.58(2H,m,CH2CN),2.27-1.72(6H,m,アルキル,H-3,H-4),1.58(4H,s,アルキル),1.30(22H,s,アルキル,CHCH3).
1H-NMR(CDCl3): δ7.40-7.14(9H,m,Ar-H),6.82(4H,d,J=8.6Hz,Ar-H),3.78(6H,s,OCH3),3.70-2.86(8H,m,CH2O,POCH2,CHCH3,H-6),2.58(2H,m,CH2CN),2.06-1.79(5H,m,アルキル,H-2,H-5),1.74-1.49(6H,m,アルキル,H-3,H-4),1.37-1.10(16H,m,アルキル,CHCH3).
1H-NMR(CDCl3): δ7.40-7.14(9H,m,Ar-H),6.82(4H,d,J=8.6Hz,Ar-H),4.24-3.94(2H,m,COOCH2),3.78(s,6H,OCH3),3.72-2.96(11H,m,CH2O,POCH2,CHCH3,H-2,H-5,H-6),2.58(2H,m,CH2CN),2.10-1.46(8H,m,アルキル,H-3,H-4),1.34-1.10(12H,m,CHCH3).
1H-NMR(CDCl3): δ7.40-7.14(9H,m,Ar-H),6.82(4H,m,Ar-H),3.78(s,6H,OCH3),3.65-3.25(13H,m,CH2O,POCH2,CHCH3,H-2,CH2NH,CH2OH,H-2,H-5,H-6),2.73(2H,m,CH2CN),2.10-1.48(16H,m,アルキル,H-3,H-4),1.35-1.10(12H,m,CHCH3).
つぎに、下記式に示すスキーム3に従い、L-プロリンを有するアミダイト誘導体を合成した。
DMTr-アミド-L-プロリン(化合物6)(1.00g、2.05mmol)および5-ヒドロキシペンタナール(0.33g、3.07mmol)を含むエタノール溶液(7mL)に、氷冷下、酢酸緩衝液(7mL)を加えた。この混合液を、氷冷下、20分撹拌した後、シアノ化ホウ素ナトリウム(0.77g、12.28mmol)を加え、さらに、室温下、7時間撹拌した。前記混合液をジクロロメタンで希釈し、水で洗浄した後、さらに飽和食塩水で洗浄した。そして、前記有機層を回収し、硫酸ナトリウムで乾燥させた。前記有機層をろ過し、ろ液について、減圧下で溶媒を留去した。得られた残渣を、シリカゲルカラムクロマトグラフィー(展開溶媒 CH2Cl2:CH3OH=98:2、0.05%ピリジン含有)に供した。ついで、得られた生成物を、シリカゲルカラムクロマトグラフィー(展開溶媒 CH2Cl2:CH3OH=98:2、0.05%ピリジン含有)に供し、さらに、得られた生成物を、シリカゲルカラムクロマトグラフィー(展開溶媒 ジクロロメタン:アセトン=7:3、0.05%ピリジン含有)に供した。これによって、無色シロップ状の化合物11を得た(0.49g、収率41%)。
Ms (FAB+): m/z 575 (M+)、303 (DMTr+)
得られた前記DMTr-ヒドロキシアミドアミノ-L-プロリン(化合物11)(0.50g、0.87mmol)を無水アセトニトリルと混合し、室温で共沸乾燥した。得られた残留物に、ジイソプロピルアンモニウムテトラゾリド(178mg、1.04mmol)を加え、減圧下で脱気し、アルゴンガスを充填した。前記混合物に対し、無水アセトニトリル(1mL)を加え、さらに、2-シアノエトキシ-N,N,N’,N’-テトライソプロピルホスホロジアミダイト(313mg、1.04mmol)の無水アセトニトリル溶液(1mL)を加えた。この混合物を、アルゴン雰囲気下、室温で4時間撹拌した。そして、前記混合物をジクロロメタンで希釈し、飽和重曹水および飽和食塩水で、順次洗浄した。有機層を回収し、硫酸ナトリウムで乾燥した後、前記有機層をろ過した。得られた前記ろ液について、減圧下で溶媒を留去した。得られた残渣を、充填剤としてアミノシリカを用いたカラムクロマトグラフィー(展開溶媒 ヘキサン:アセトン=7:3、0.05%ピリジン含有)に供し、無色シロップ状の化合物12(0.57g、純度93%、収率79%)を得た。前記純度は、HPLCにより測定した(以下、同様)。以下に、化合物のNMRの結果を示す。
1H-NMR (CDCl3): δ7.41-7.43 (m,2H,Ar-H)、7.28-7.32(m,4H,Ar-H)、7.25-7.27(m,2H,Ar-H)、7.18-7.21(m,1H,Ar-H)、6.80-6.84(m,4H,Ar-H)、3.73-3.84(m,1H)、3.79(s,6H,OCH3)、3.47-3.64(m,3H)、3.12-3.26(m,2H)、3.05(t,J=6.4Hz,2H,CH2)、2.98-2.02(m,2H)、2.61(t,J=5.8Hz,2H,CH2)、2.55-2.63(m,2H)、2.27-2.42(m,1H,CH)、2.31(t,7.8Hz,2H,CH2)、2.03-2.19(m,1H,CH)、1.40-1.90(m,8H)、1.23-1.33(m,5H)、1.14-1.20(m,12H,CH3);
P-NMR(CDCl3): δ146.91;
Ms(FAB+): m/z 774(M+)、303(DMTr+),201(C8H19N2OP+).
DMTr-アミド-L-プロリン(化合物6)(1.00g、2.05mmol)を溶解した無水アセトニトリル溶液(10mL)に、1-イミダゾカルボニルオキシ-8-ヒドロキシオクタン(1.12g,4.92mmol)を溶解した無水アセトニトリル溶液(20mL)を、アルゴン雰囲気下、室温で加えた。この混合液を、40~50℃で2日間加熱した後、5日間室温で放置した。前記混合液について、減圧下で溶媒を留去した。得られた残渣を、シリカゲルカラムクロマトグラフィー(展開溶媒 ジクロロメタン:アセトン=4:1、0.05%ピリジン含有)に供した。これによって、無色シロップ状の化合物13を得た(0.68g、収率50%)。以下に、化合物のNMRの結果を示す。
1H-NMR (CDCl3): δ7.40-7.42(m,2H,Ar-H)、7.27-7.31(m,6H,Ar-H)、7.17-7.21(m,1H,Ar-H)、6.79-6.82(m,4H,Ar-H)、4.23-4.30(m,1H)、4.05-4.10(m,2H)、3.79(s,6H,OCH3)、3.60-3.65(m,2H)、3.32-3.55(m,2H)、3.16-3.29(m,2H),3.01-3.07(m,2H)、2.38-2.40(m,1H,CH)、1.83-1.90(m,2H)、1.57-1.69(m,8H)、1.26-1.36(m,2H);
Ms (FAB+): m/z 602(M+)、303(DMTr+).
得られた前記DMTr-ヒドロキシアミドカルバモイル-L-プロリン(化合物13)(0.63g、1.00mmol)を無水ピリジンと混合し、室温で共沸乾燥した。得られた残留物に、ジイソプロピルアンモニウムテトラゾリド(206mg、1.20mmol)を加え、減圧下に脱気し、アルゴンガスを充填した。前記混合物に対し、無水アセトニトリル(1mL)を加え、さらに、2-シアノエトキシ-N,N,N’,N’-テトライソプロピルホスホロジアミダイト(282mg、1.12mmol)の無水アセトニトリル溶液(1mL)を加えた。この混合物を、アルゴン雰囲気下、室温で4時間撹拌した。そして、前記混合物をジクロロメタンで希釈し、飽和重曹水および飽和食塩水で順次洗浄した。有機層を回収し、硫酸ナトリウムで乾燥した後、前記有機層をろ過した。得られたろ液について、減圧下で溶媒を留去した。得られた残渣を、充填剤としてアミノシリカを用いたカラムクロマト(展開溶媒 ヘキサン:アセトン=7:3、0.5%ピリジン含有)に供し、無色シロップ状の化合物14(0.74g、純度100%、収率87%)を得た。以下に、化合物のNMRの結果を示す。
P-NMR (CDCl3): δ147.19;
Ms(FAB+): m/z 860(M+)、303(DMTr+),201(C8H19N2OP+).
トリホスゲン(1.22g、4.10mmol)に、アルゴン雰囲気および氷冷下、無水テトラヒドロフラン溶液(10mL)を加えた。この混合液に、アルゴン雰囲気および氷冷下、DMTr-アミド-L-プロリン(化合物6)(1.00g、2.05mmol)およびDIEA(9.80g、75.8mmol)を溶解した無水テトラヒドロフラン溶液(10mL)を、30分間で滴下し、その後、室温で1時間撹拌した。前記混合液に、アルゴン雰囲気および氷冷下、10-アミノ-1-t-ブチルジメチルシロキシデカン(2.66g、10.25mmol)およびDIEA(3.20g、24.76mmol)を溶解した無水テトラヒドロフラン溶液(20mL)を、45分間で滴下した。そして、前記混合物を、アルゴン雰囲気下、室温で一晩撹拌した。この混合液を酢酸エチル(200mL)で希釈し、有機層を回収した。前記有機層を、飽和重曹水で洗浄した後、さらに、飽和食塩水で洗浄した。そして、有機層を回収し、硫酸ナトリウムで乾燥させた。前記有機層をろ過し、ろ液について、減圧下で溶媒を留去した。得られた残渣を、シリカゲルカラムクロマトグラフィー(展開溶媒 ジクロロメタン:アセトン=4:1、0.05%ピリジン含有)に供した。これによって、無色シロップ状の化合物15を得た(0.87g、収率55%)。
得られた前記DMTr-t-ブチルジメチルシロキシアミドウレイド-L-プロリン(15)(0.87g、1.12mmol)に、アルゴン雰囲気下、無水テトラヒドロフランジクロロメタン溶液(10mL)を室温で加えた。前記混合液に、アルゴン雰囲気下、1mol/Lテトラブチルアンモニウムフルオリド含有テトラヒドロフラン溶液(4.69mL、東京化成)を加え、室温で3日間撹拌した。前記混合液をジクロロメタン(150mL)で希釈し、水で洗浄した後、さらに飽和食塩水で洗浄した。有機層を回収し、硫酸ナトリウムで乾燥した後、前記有機層をろ過した。得られたろ液について、減圧下で溶媒を留去した。得られた残渣を、シリカゲルカラムクロマトグラフィー(展開溶媒 ジクロロメタン:アセトン=1:1、0.05%ピリジン含有)に供し、無色シロップ状の化合物16を得た(0.68g、収率92%)。以下に、化合物のNMRの結果を示す。
1H-NMR (CDCl3): δ7.41-7.43(m,2H,Ar-H)、7.27-7.31(m,4H,Ar-H)、7.19-7.26(m,2H,Ar-H)、7.19-7.21(m,1H,Ar-H)、6.80-6.83(m,4H,Ar-H)、4.34(t,2H,CH2)、3.79(s,6H,OCH3)、3.63(d,1H,J=6.4Hz,CH2)、3.61(d,1H,J=6.4Hz,CH2)、3.34-3.37(m,1H,CH)、3.16-3.27(m,5H),3.04(t,J=5.9Hz,2H,CH2)、2.38-2.45(m,1H,CH)、1.83-2.05(m,3H)、1.45-1.64(m,8H)、1.25-1.38(m,7H).
得られた前記DMTr-ヒドロキシアミドウレイド-L-プロリン(化合物16)(0.62g、0.94mmol)を無水アセトニトリルと混合し、室温で共沸乾燥した。得られた残留物に、ジイソプロピルアンモニウムテトラゾリド(192mg、1.12mmol)を加え、減圧下で脱気し、アルゴンガスを充填した。前記混合液に対し、無水アセトニトリル(1mL)を加え、さらに、2-シアノエトキシ-N,N,N’,N’-テトライソプロピルホスホロジアミダイト(282mg、1.12mmol)の無水アセトニトリル溶液(1mL)を加えた。この混合物を、アルゴン雰囲気下、室温で4時間撹拌した。そして、前記混合物をジクロロメタンで希釈し、飽和重曹水および飽和食塩水で、順次洗浄した。有機層を回収し、硫酸ナトリウムで乾燥した後、前記有機層をろ過した。得られた前記ろ液について、減圧下で溶媒を留去した。得られた残渣を、充填剤としてアミノシリカを用いたカラムクロマト(展開溶媒 ヘキサン:アセトン=1:1、0.05%ピリジン含有)に供し、無色シロップ状の化合物17を得た(0.77g、純度88%、収率84%)。以下に、化合物のNMRの結果を示す。
P-NMR (CDCl3): δ147.27;
Ms (FAB+): m/z 860(M++1)、303(DMTr+),201(C8H19N2OP+).
プロリン骨格を有するリンカーを含む本発明の核酸分子を生成するため、前記スキーム3により、L-プロリンジアミドアミダイトおよびD-プロリンジアミドアミダイトを合成した。
(1)Fmoc-ヒドロキシアミド-L-プロリン(化合物4)
前記スキーム3の化合物2(Fmoc-L-プロリン)を開始原料とした。前記化合物2(10.00g、29.64mmol)、4-アミノ-1-ブタノール(3.18g、35.56mmol)および1-ヒドロキシベンゾトリアゾール(10.90g、70.72mmol)を混合し、前記混合物に対し、減圧下で脱気し、アルゴンガスを充填した。前記混合物に、無水アセトニトリル(140mL)を室温で加え、さらに、ジシクロヘキシルカルボジイミド(7.34g、35.56mmol)の無水アセトニトリル溶液(70mL)を添加した後、アルゴン雰囲気下、室温で15時間撹拌した。反応終了後、生成した沈殿をろ別し、回収したろ液について、減圧下で溶媒を留去した。得られた残渣にジクロロメタン(200mL)を加え、飽和重曹水(200mL)で洗浄した。そして、有機層を回収し、硫酸マグネシウムで乾燥した後、前記有機層をろ過した。得られたろ液について、減圧下で溶媒を留去し、その残渣にジエチルエーテル(200mL)を加え、粉末化した。生じた粉末を濾取することにより、無色粉末状の化合物4(10.34g、収率84%)を得た。以下に、前記化合物のNMRの結果を示す。
1H-NMR(CDCl3): δ7.76-7.83(m,2H,Ar-H)、7.50-7.63(m,2H,Ar-H)、7.38-7.43(m,2H,Ar-H)、7.28-7.33(m,2H,Ar-H),4.40-4.46(m,1H,CH),4.15-4.31(m,2H,CH2),3.67-3.73(m,2H,CH2)、3.35-3.52(m,2H,CH2)、3.18-3.30(m,2H,CH2)、2.20-2.50(m,4H)、1.81-2.03(m,3H)、1.47-1.54(m,2H);
Ms (FAB+): m/z 409(M+H+).
Fmoc-ヒドロキシアミド-L-プロリン(化合物4)(7.80g、19.09mmol)を無水ピリジン(5mL)と混合し、室温で2回共沸乾燥した。得られた残留物に、4,4’-ジメトキシトリチルクロリド(8.20g、24.20mmol)、DMAP(23mg、0.19mmol)および無水ピリジン(39mL)を加えた。この混合物を、室温で1時間撹拌した後、メタノール(7.8mL)を加え、室温で30分撹拌した。この混合物を、ジクロロメタン(100mL)で希釈し、飽和重曹水(150mL)で洗浄後、有機層を分離した。前記有機層を、硫酸ナトリウムで乾燥した後、前記有機層をろ過した。得られたろ液について、減圧下で溶媒を留去した。得られた未精製の残渣に、無水ジメチルホルムアミド(39mL)およびピペリジン(18.7mL、189mmol)を加え、室温で1時間撹拌した。反応終了後、前記混合液について、減圧下、室温で、溶媒を留去した。得られた残渣をシリカゲルカラムクロマトグラフィー(商品名Wakogel C-300、展開溶媒 CH2Cl2:CH3OH=9:1、0.05%ピリジン含有に供し、淡黄色油状の化合物6(9.11g、収率98%)を得た。以下に、前記化合物のNMRの結果を示す。
1H-NMR (CDCl3): δ7.39-7.43(m,2H,Ar-H)、7.30(d,J=8.8Hz,4H,Ar-H)、7,21(tt,1H,4.9,1.3Hz,Ar-H)、6.81(d,J=8.8Hz,4H,Ar-H)、3.78(s,6H,OCH3)、3.71(dd,H,J=6.3Hz,5.4Hz,CH)、3.21(2H,12.9,6.3Hz,2H,CH2)、3.05(t,J=6.3Hz,2H,CH2)、2.85-2.91(m,2H,CH2)、2.08-2.17(m,1H,CH)、1.85-2.00(m,3H)、1.55-1.65(m,5H):
Ms (FAB+); m/z 489(M+H+)、303(DMTr+).
得られた前記DMTr-アミド-L-プロリン(化合物6)(6.01g、12.28mmol)、EDC(2.83g、14.74mmol)、1-ヒドロキシベンゾトリアゾール(3.98g、29.47mmol)およびトリエチルアミン(4.47g、44.21mmol)の無水ジクロロメタン溶液(120mL)を混合した。この混合液に、さらに、アルゴン雰囲気下、室温で、6-ヒドロキシヘキサン酸(1.95g、14.47mmol)を加え、その後、アルゴン雰囲気下、室温で、1時間撹拌した。前記混合液をジクロロメタン(600mL)で希釈し、飽和食塩水(800mL)で3回洗浄した。有機層を回収し、前記有機層を、硫酸ナトリウムで乾燥した後、前記有機層をろ過した。得られたろ液について、減圧下で溶媒を留去した。これにより、淡黄色泡状の前記化合物8(6.29g、収率85%)を得た。以下に、前記化合物のNMRの結果を示す。
1H-NMR (CDCl3): δ7.41-7.43(m,2H,Ar-H)、7.27-7.31(m,4H,Ar-H)、7.19-7.26(m,2H,Ar-H)、7.17-7.21(m,1H,Ar-H)、6.79-6.82(m,4H,Ar-H)、4.51-4.53(m,1H,CH)、3.79(s,6H,OCH3)、3.61(t,2H,J=6.4Hz,CH2)、3.50-3.55(m,1H,CH)、3.36-3.43(m,1H,CH),3.15-3.24(m,2H,CH2),3.04(t,J=6.3Hz,2H,CH2)、2.38-2.45(m,1H,CH)、2.31(t,6.8Hz,2H,CH2)、2.05-2.20(m,1H,CH)、1.92-2.00(m,1H,CH)、1.75-1.83(m,1H,CH)、1.48-1.71(m,8H)、1.35-1.44(m,2H,CH2);
Ms (FAB+): m/z 602(M+)、303(DMTr+).
得られた前記DMTr-ヒドロキシジアミド-L-プロリン(化合物8)(8.55g、14.18mmol)を無水アセトニトリルと混合し、室温で3回共沸乾燥した。得られた残留物に、ジイソプロピルアンモニウムテトラゾリド(2.91g、17.02mmol)を加え、減圧下で脱気し、アルゴンガスを充填した。前記混合物に対し、無水アセトニトリル(10mL)を加え、さらに、2-シアノエトキシ-N,N,N’,N’-テトライソプロピルホスホロジアミダイト(5.13g、17.02mmol)の無水アセトニトリル溶液(7mL)を加えた。この混合物を、アルゴン雰囲気下、室温で2時間撹拌した。そして、前記混合物をジクロロメタンで希釈し、飽和重曹水(200mL)で3回洗浄した後、飽和食塩水(200mL)で洗浄した。有機層を回収し、硫酸ナトリウムで乾燥した後、前記有機層をろ過した。得られた前記ろ液について、減圧下に溶媒を留去した。得られた残渣を、充填剤としてアミノシリカゲルを用いたカラムクロマトグラフィー(展開溶媒 ヘキサン:酢酸エチル=1:3、0.05%ピリジン含有)に供し、無色シロップ状の化合物10(10.25g、純度92%、収率83%)を得た。以下に、前記化合物のNMRの結果を示す。
1H-NMR (CDCl3): δ7.40-7.42(m,2H,Ar-H)、7.29-7.31(m,4H,Ar-H)、7.25-7.27(m,2H,Ar-H)、7.17-7.21(m,1H,Ar-H)、6.80-6.82(m,4H,Ar-H)、4.51-4.53(m,1H,CH)、3.75-3.93(m,4H)、3.79(s,6H,OCH3)、3.45-3.60(m,4H)、3.35-3.45(m,1H,CH)、3.20-3.29(m,1H)、3.04(t,J=6.4Hz,2H,CH2)、2.62(t,J=5.8Hz,2H,CH2)、2.40-2.44(m,1H,CH)、2.31(t,7.8Hz,2H,CH2)、2.03-2.19(m,1H,CH)、1.92-2.02(m,1H,CH)、1.70-1.83(m,1H,CH)、1.51-1.71(m,8H)、1.35-1.44(m,2H,CH2)、1.18(d,J=6.8Hz,6H,CH3)、1.16(d,J=6.8Hz,6H,CH3);
P-NMR (CDCl3): Msδ147.17;
Ms(FAB+): m/z 802(M+)、303(DMTr+),201(C8H19N2OP+).
(1)Fmoc-ヒドロキシアミド-D-プロリン(化合物3)
前記スキーム3の化合物1(Fmoc-D-プロリン)を開始原料とした。前記化合物1(1.5g、4.45mmol)、ジシクロヘキシルカルボジイミド(1.1g、5.34mmol)および1-ヒドロキシベンゾトリアゾール(1.5g、10.69mmol)の混合物に対し、減圧下で脱気し、アルゴンガスを充填した。前記混合物に、無水アセトニトリル(24mL)を室温で加え、さらに、4-アミノ-1-ブタノール(0.48g、5.34mmol)の無水アセトニトリル溶液(6mL)添加した後、アルゴン雰囲気下、室温で15時間撹拌した。反応終了後、生成した沈殿をろ別し、回収したろ液について、減圧下で溶媒を留去した。得られた残渣にジクロロメタンを加え、酢酸緩衝液(pH4.0)で3回、飽和重曹水で3回洗浄した。そして、有機層を回収し、硫酸マグネシウムで乾燥した後、前記有機層をろ過した。得られたろ液について、減圧下で溶媒留去し、その残渣にジエチルエーテル(50mL)を加え、粉末化した。生じた粉末を濾取することにより、白色粉末状の化合物3を得た。以下に、前記化合物のNMRの結果を示す。
1H-NMR (400MHz,CDCl3): δ7.77(d,J=7.3Hz,2H);7.58(br,2H);7.41(t,J=7.3Hz,2H);7.32(t,J=7.3Hz,2H); 4.25-4.43(m,4H);3.25-3.61(m,6H);1.57-1.92(m,8H).
MS(FAB+): m/z 409(M+H+).
Fmoc-ヒドロキシアミド-D-プロリン(化合物3)(1.0g、2.45mmol)を無水ピリジン(5mL)と混合し、室温で2回共沸乾燥した。得られた残留物に、4,4’-ジメトキシトリチルクロリド(1.05g、3.10mmol)、DMAP(3mg、0.024mmol)および無水ピリジン(5mL)を加えた。この混合物を、室温で1時間撹拌した後、メタノール(1mL)を加え、室温で30分撹拌した。この混合物を、ジクロロメタンで希釈し、飽和重曹水で洗浄後、有機層を分離した。前記有機層を、硫酸ナトリウムで乾燥した後、前記有機層をろ過した。得られたろ液について、減圧下で溶媒を留去した。得られた未精製の残渣に、無水ジメチルホルムアミド(5mL)およびピペリジン(2.4mL、24mmol)を加え、室温で1時間撹拌した。反応終了後、前記混合液について、減圧下、室温で、溶媒を留去した。得られた残渣をシリカゲルカラムクロマトグラフィー(商品名Wakogel C-300、展開溶媒 CH2Cl2:CH3OH=9:1、0.05%ピリジン含有)に供し、淡黄色油状の化合物5(1.26g、収率96%)を得た。以下に、前記化合物のNMRの結果を示す。
1H-NMR(400MHz, CDCl3): δ7.62(br,1H);7.41-7.44(m,2H);7.26-7.33(m,6H);7.17-7.22(m,1H);6.80-6.84(m,4H);3.78(s,6H);3.71(dd,J=8.8,5.4Hz,1H);3.22 (q,6.5Hz,2H);3.07(t, J=6.1Hz,2H);2.97-3.03(m,1H);2.85-2.91(m,1H);1.85-2.15(m,3H);1.55-1.73(m,6H).
MS (FAB+): m/z 489 (M+H+), 303(DMTr+).
得られた前記DMTr-アミド-D-プロリン(化合物5)(1.2g、2.45mmol)、EDC(566mg、2.95mmol)、1-ヒドロキシベンゾトリアゾール(796mg、5.89mmol)、およびトリエチルアミン(1.2mL、8.84mmol)の無水ジクロロメタン溶液(24mL)を混合した。この混合液に、さらに、アルゴン雰囲気下、室温で、6-ヒドロキシヘキサン酸(390mg、2.95mmol)を加え、その後、アルゴン雰囲気下、室温で1時間撹拌した。前記混合液をジクロロメタンで希釈し、飽和重曹水で3回洗浄した。有機層を回収し、前記有機層を、硫酸ナトリウムで乾燥した後、前記有機層をろ過した。得られたろ液について、減圧下で溶媒を留去した。これにより、淡黄色油状の化合物7(1.4g、収率95%)を得た。以下に、前記化合物のNMRの結果を示す。
1H-NMR(400MHz,CDCl3): δ7.40-7.43(m,2H);7.25-7.32(m,6H);7.17-7.22(m,1H);6.79-6.83(m,4H);3.79(s,6H);3.58-3.63(m,2H);3.49-3.55(m,1H);3.15-3.26(m,2H);3.02-3.07(m,2H);2.30-2.33(m,2H);2.11-2.20(m,1H);1.50-1.99(m,13H);1.36-1.43(m,2H).
MS(FAB+): m/z 602(M+),303(DMTr+).
得られた前記DMTr-ヒドロキシジアミド-D-プロリン(化合物7)(1.2g、1.99mmol)を無水アセトニトリルと混合し、室温で3回共沸乾燥した。得られた残留物に、ジイソプロピルアンモニウムテトラゾリド(410mg、2.40mmol)を加え、減圧下で脱気し、アルゴンガスを充填した。前記混合物に対し、無水アセトニトリル(2.4mL)を加え、さらに、2-シアノエトキシ-N,N,N’,N’-テトライソプロピルホスホロジアミダイト(722mg、2.40mmol)を加えた。この混合物を、アルゴン雰囲気下、室温で2時間撹拌した。そして、前記混合物をジクロロメタンで希釈し、飽和重曹水で3回洗浄後、飽和食塩水で洗浄した。有機層を回収し、硫酸ナトリウムで乾燥した後、前記有機層をろ過した。得られたろ液について、減圧下で溶媒を留去した。得られた残渣を、充填剤としてアミノシリカゲルを用いたカラムクロマトグラフィー(展開溶媒 ヘキサン:酢酸エチル=1:3)に供し、無色油状の化合物9(1.4g、純度95%、収率83%)を得た。以下に、前記化合物のNMRの結果を示す。
1H-NMR(400MHz,CDCl3): δ7.40-7.43(m,2H);7.25-7.32(m,6H);7.14-7.21(m,1H);6.80-6.83(m,4H);3.80-3.85(m,2H);3.79(s,6H);3.49-3.65(m,5H);3.02-3.06(m,2H);2.60-2.63(m,2H);2.29-2.33(m,2H);1.77-1.82(m,2H);1.56-1.68(m,8H);1.38-1.43(m,2H);1.15-1.29(m,18H).
31P-NMR (162MHz,CDCl3): δ146.94.
MS (FAB+): m/z 802(M+),303(DMTr+),201(C8H19N2OP+).
プロリン骨格を有するリンカーを含む本発明の核酸分子を生成するため、下記スキーム4により、L-プロリンジアミドアミダイトタイプBを合成した。
Fmoc-ヒドロキシアミド-L-プロリン(化合物4)(2.00g、30mmol)、t-ブチル-ジメチルシリルクロリド(1.11g、35mmol)およびイミダゾール(10.90g、71mmol)を混合した。前記混合物に対し、減圧下に脱気し、アルゴンガスを充填した。前記混合物に、無水アセトニトリル(20mL)を室温で加え、アルゴン雰囲気下、室温で終夜撹拌した。反応終了後、前記混合物にジクロロメタン(150mL)を加え、水で3回洗浄し、飽和食塩水で洗浄した。有機層を回収し、硫酸マグネシウムで乾燥した後、前記有機層をろ過した。得られたろ液について、減圧下で溶媒を留去し、その残渣をシリカゲルカラムクロマトグラフィー(展開溶媒 CH2Cl2:CH3OH=95:5)に供し、無色シロップ状の化合物18(2.35g、収率92%)を得た。以下に、前記化合物のNMRの結果を示す。
1H-NMR(CDCl3): δ7.76-7.78(m,2H,Ar-H)、7.50-7.63(m,2H,Ar-H)、7.38-7.42(m,2H,Ar-H)、7.29-7.34(m,2H,Ar-H),4.10-4.46(m,4H,CH2),3.47-3.59(m,4H,CH2)、3.20-3.26(m,2H,CH)、1.85-1.95(m,2H)、1.42-1.55(m,6H)、0.96(s,9H,t-Bu)、0.02(s,6H,SiCH3);
Ms(FAB+): m/z 523(M+H+).
得られた前記Fmoc-t-ブチル-ジメチルシロキシアミド-L-プロリン(化合物18)(1.18g、2.5mmol)に対し、無水アセトニトリル(5mL)およびピペリジン(2.4mL)を加え、室温で1時間撹拌した。反応終了後、前記混合物にアセトニトリル(50mL)を加え、不溶物をろ別した。得られたろ液について、減圧下で溶媒を留去し、得られた残渣をシリカゲルカラムクロマトグラフィー(展開溶媒 CH2Cl2:CH3OH=9:1)に供し、無色シロップ状の化合物19(0.61g、収率90%)を得た。以下に、前記化合物のNMRの結果を示す。
1H-NMR(CDCl3): δ3.71(dd,1H,J=9.0Hz,5.2Hz,CH)、3.61-3.64 (m,2H,CH2)、3.22-3.28(m,2H,CH2)、2.98-3.04(m,1H,CH)、2.86-2.91(m,1H,CH)、2.08-2.17(m,1H,CH)、1.86-1.93(m,1H,CH)、1.66-1.75(m,2H,CH2)、1.52-1.57(m,4H)、0.89(s,9H,t-Bu)、0.05(s,6H,SiCH3):
Ms(FAB+); m/z 301 (M+H+).
得られた前記t-ブチル-ジメチルシロキシアミド-L-プロリン(化合物19)(550mg、1.8mmol)、6-ヒドロキシヘキサン酸(300mg、2.3mmol)、EDC(434mg、2.3mmol)、および1-ヒドロキシベンゾトリアゾール(695mg、4.5mmol)の無水ジクロロメタン溶液(20mL)を混合した。前記混合物に、アルゴン雰囲気下、室温で、トリエチルアミン(689mg、6.8mmol)を加え、その後、アルゴン雰囲気下、室温で、終夜撹拌した。前記混合液を飽和食塩水で洗浄した。有機層を回収し、前記を硫酸ナトリウムで乾燥した後、前記有機層をろ過した。得られたろ液について、減圧下で溶媒を留去した。得られた残渣をシリカゲルカラムクロマトグラフィー(展開溶媒 CH2Cl2:CH3OH=9:1)に供し、無色シロップ状の化合物20(696mg、収率92%)を得た。以下に、前記化合物のNMRの結果を示す。
1H-NMR(CDCl3): δ4.54(d,1H,CH)、3.58-3.67(m,5H)、3.52-3.56(m,1H,CH),3.32-3.39(m,1H),3.20-3.25(m,2H)、2.40-2.43(m,1H,CH)、2.33(t,J=7.3Hz,2H,CH2)、2.05-2.25(m,2H)、1.93-2.03(m,1H,CH)、1.75-1.85(m,1H,CH)、1.50-1.73(m,8H)、1.37-1.46(m,2H,CH2)、0.87(s, 9H,t-Bu)、0.04(s,6H,SiCH3);
Ms(FAB+): m/z 415(M++1).
得られた前記t-ブチル-ジメチルシロキシアミドヒドロキシアミド-L-プロリン(化合物20)(640mg、1.54mmol)を無水ピリジン(1mL)と混合し、室温で共沸乾燥した。得られた残留物に、4,4’-ジメトキシトリチルクロリド(657mg、1.85mmol)、DMAP(2mg)および無水ピリジン(5mL)を加え、室温で4時間撹拌した後、メタノール(1mL)を加え、30分室温で撹拌した。前記混合物をジクロロメタンで希釈し、飽和重曹水で洗浄した。有機層を回収し、硫酸ナトリウムで乾燥した後、前記有機層をろ過した。得られたろ液について、減圧下で溶媒を留去した。得られた残渣に、無水アセトニトリル(5mL)および1mol/Lテトラブチルアンモニウムフルオリド含有テトラヒドロフラン溶液(1.42mL、テトラブチルアンモニウムフルオリド1.42mmol)を加え、室温で終夜撹拌した。反応終了後、前記混合物に酢酸エチル(100mL)を加え、水で洗浄した後、飽和食塩水で洗浄した。有機層を回収し、硫酸ナトリウムで乾燥した後、前記有機層をろ過した。得られたろ液について、減圧下に溶媒を留去した。得られた残渣を、シリカゲルカラムクロマトグラフィー(展開溶媒 CH2Cl2:CH3OH=95:5、0.05%ピリジン含有)に供し、無色シロップ状の化合物21(680mg、収率73%)を得た。以下に、前記化合物のNMRの結果を示す。
1H-NMR(CDCl3): δ7.41-7.44(m,2H,Ar-H)、7.26-7.33(m,4H,Ar-H)、7.18-7.21(m,2H,Ar-H)、7.17-7.21(m,1H,Ar-H)、6.80-6.84(m,4H,Ar-H)、4.51-4.53(d,6.8Hz,1H,CH)、3.79(s,6H,OCH3)、3.61(dd,2H,J=11Hz,5.4Hz,CH2)、3.50-3.54(m,1H,CH)、3.36-3.43(m,1H,CH),3.20-3.26(m,2H,CH2),3.05(t,J=6.4Hz,2H,CH2)、2.38-2.45(m,1H,CH)、2.30(t,J=7.8Hz,2H,CH2)、2.05-2.25(m,1H,CH)、1.92-2.00(m,1H,CH)、1.75-1.83(m,1H,CH)、1.52-1.67(m,8H)、1.35-1.45(m,2H,CH2);
Ms(FAB+): m/z 602(M+)、303(DMTr+).
得られた前記DMTr-ヒドロキシジアミド-L-プロリン タイプB(化合物21)(637mg、1.06mmol)を無水アセトニトリルと混合し、室温で共沸乾燥した。得られた残留物に、ジイソプロピルアンモニウムテトラゾリド(201mg、1.16mmol)を加え、減圧下で脱気し、アルゴンガスを充填した。前記混合物に対し、無水アセトニトリル(1mL)を加え、さらに、2-シアノエトキシ-N,N,N’,N’-テトライソプロピルホスホロジアミダイト(350mg、1.16mmol)の無水アセトニトリル溶液(1mL)を加えた。この混合物を、アルゴン雰囲気下、室温で4時間撹拌した。前記混合物をジクロロメタンで希釈し、飽和重曹水および飽和食塩水で洗浄した。有機層を回収し、硫酸ナトリウムで乾燥した後、前記有機層をろ過した。得られたろ液について、減圧下で溶媒を留去した。得られた残渣を、充填剤としてアミノシリカゲルを用いたカラムクロマトグラフィー(展開溶媒 ヘキサン:アセトン=7:3)に供し、無色シロップ状の化合物22(680mg、純度95%、収率76%)を得た。以下に、前記化合物のNMRの結果を示す。
1H-NMR(CDCl3): δ7.41-7.43(m,2H,Ar-H)、7.25-7.32(m,4H,Ar-H)、7.17-7.22(m,2H,Ar-H)、6.80-6.83(m,4H,Ar-H)、4.53(d,J=7.8Hz,1H,CH)、3.75-3.93(m,3H)、3.79(s,6H,OCH3)、3.46-3.68(m,5H)、3.34-3.41(m,1H,CH)、3.10-3.31(m,1H,CH)、3.05(t,J=6.3Hz,2H,CH2)、2.62(t,J=6.3Hz,2H,CH2)、2.39-2.46(m,1H,CH)、2.29(t,7.3Hz,2H,CH2)、2.03-2.19(m,1H,CH)、1.90-2.00(m,1H,CH)、1.70-1.83(m,1H,CH)、1.51-1.71(m,8H)、1.35-1.45(m,2H,CH2)、1.18(d,J=6.4Hz,6H,CH3)、1.16(d,J=6.4 Hz,6H,CH3);
P-NMR(CH3CN): δ146.90;
Ms(FAB+): m/z 803(M++1)、303(DMTr+).
プロリン骨格を有するリンカーを含む本発明の核酸分子を生成するため、下記スキーム5により、DMTr-アミドエチレンオキシエチルアミノ-L-プロリンアミダイト(以下、PEGスペーサータイプという)を合成した。
DMTr-アミド-L-プロリン(化合物6)(1.00g、2.05mmol)、4-トルエンスルホン酸2-(2-ヒドロキシエトキシ)エチルエステル(3.10g、12.30mmol)、および炭酸カリウム(0.85g、6.15mmol)の無水ジメチルホルムアミド溶液(10mL)を混合し、アルゴン雰囲気下、室温で4日間撹拌した。前記混合物について、減圧化、室温で溶媒を留去した後、ジクロロメタン(20mL)を加え、ろ過した。ろ液を濃縮し、得られた残渣をシリカゲルカラムクロマトグラフィーに供した。前記シリカゲルカラムクロマトグラフィーの添加溶媒は、まず、0.05%ピリジンを含む酢酸エチルを使用した後、0.05%ピリジンを含むCH2Cl2とCH3OHの混合液(CH2Cl2:CH3OH=9::1)を使用した。その結果、無色シロップ状の化合物23(1.15g、収率97%)を得た。以下に、前記化合物のNMRの結果を示す。
1H-NMR(CDCl3): δ7.41-7.45(m,2H,Ar-H)、7.27-7.31(m,6H,Ar-H)、7.17-7.21(m,1H,Ar-H)、6.79-6.82(m,4H,Ar-H)、3.79(s,6H,OCH3)、3.60-3.70(m,2H)、3.39-3.57(m,4H),3.13-3.27(m,3H),3.07-3.08(m,2H)、2.71-2.84(m,1H)、2.38-2.46(m,1H)、2.14-2.19(m,1H)、1.84-1.87(m,1H)、1.57-1.76 (m,8H).
得られた前記DMTr-アミドヒドロキシエトキシエチルアミノ-L-プロリン(化合物23)(0.63g、1.00mmol)を無水ピリジンと混合し、室温で共沸乾燥した。得られた残留物に、ジイソプロピルアンモニウムテトラゾリド(206mg、1.20mmol)を加え、減圧下で脱気し、アルゴンガスを充填した。前記混合物に対し、無水アセトニトリル(1mL)を加え、さらに、2-シアノエトキシ-N,N,N’,N’-テトライソプロピルホスホロジアミダイト(282mg、1.12mmol)の無水アセトニトリル溶液(1mL)を加えた。この混合物を、アルゴン雰囲気下、室温で4時間撹拌した。そして、前記混合物をジクロロメタンで希釈し、飽和重曹水および飽和食塩水で洗浄した。有機層を回収し、硫酸ナトリウムで乾燥した後、前記有機層をろ過した。得られた前記ろ液について、減圧下で溶媒を留去した。得られた残渣を、充填剤としてアミノシリカゲルを用いたカラムクロマトグラフィー(展開溶媒 ヘキサン:アセトン=7:3、0.05%ピリジン含有)に供し、無色シロップ状の化合物24(0.74g、純度100%、収率87%)を得た。以下に、前記化合物のNMRの結果を示す。
1H-NMR(CD3CN): δ7.41-7.43(m,2H,Ar-H)、7.28-7.31(m,6H,Ar-H)、7.18-7.22(m,1H,Ar-H)、6.84-6.86(m,4H, Ar-H)、3.73-3.84(m,2H,CH2)、3.79(s,6H,OCH3)、3.47-3.64(m,7H)、3.15-3.23(m,1H)、3.11(t,J=6.4Hz,2H,CH2)、3.01(t,J=5.9Hz,2H,CH2)、2.95-2.99(m,1H)、2.58-2.63(m,2H)、2.31-2.35(m,1H,CH)、2.03-2.19(m,1H,CH)、1.48-1.78(m,10H)、1.12-1.57(m,12H,CH3);
P-NMR(CD3CN) :δ148.00;
Ms(FAB+): m/z 776(M+)、303(DMTr+) 201(C8H19N2OP+).
1.保護プロリノールの合成
以下に示すスキーム6に従い、ジメトキシトリチル基で保護されたプロリノール(化合物3)を合成した。
L-プロリノール(2.0g、20mmol)をTHF20mLに溶解した。他方、トリフルオロ酢酸エチル(3.0g、21mmol)をTHF20mLに溶解した。そして、後者のTHF溶液を、前者のL-プロリノール含有THF溶液に滴下し、12時間撹拌した。この反応液を減圧濃縮し、化合物1を得た(3.7g、収率97%)。以下に、前記化合物のNMRの結果を示す。
1H-NMR(CDCl3): δ4.28-4,23(1.0H,m,OH),3.90-3.41(5H,H-2,H-5,H-6,m), 2.27-1.77(4H,H-3,H-4,m).
得られた前記トリフルオロアセチル-L-プロリノール(化合物1)(3.7g、19mmol)をピリジンに溶解して、3回、室温で共沸乾燥した。得られた残留物をピリジン15mLに溶かし、アルゴン下、氷浴中で撹拌しながら、4,4’-ジメトキシトリチルクロリド(DMTr-Cl)(8.1g、24mmol)を加え、さらに、室温で4時間反応させた。そして、過剰のDMTr-Clをクエンチするために、前記反応液に、さらに、メタノール10mLを加え10分撹拌した。その後、前記反応液に、ジクロロメタンを加え飽和炭酸水素ナトリウム水溶液と飽和食塩水で洗浄した。洗浄後の回収した有機層を、硫酸ナトリウムで乾燥させた。前記有機層をろ過して、得られたろ液を減圧濃縮し、その残渣を、シリカゲルカラムクロマトグラフィー(展開溶媒CH2Cl2:CH3OH=95:5、0.1%ピリジン含有)に供し、精製した化合物2を得た(8.5g、収率89%)。以下に、前記化合物のNMRの結果を示す。
1H-NMR(CDCl3): δ7.39-7.18(9H,m,Ar-H),6.82(4H,d,J=8.6Hz,Ar-H),3.78(6H,s,OCH3),3.70-3.41(5H,H-2,H-5,H-6, m),2.19-1.85(4H,H-3,H-4,m).
得られた前記トリフルオロアセチル-DMTr-L-プロリノール(化合物2)(5g、10mmol)をTHF100mLに溶解した。このTHF溶液に5%水酸化ナトリウム水溶液100mLを加え、撹拌した。この溶液に、1M フッ化テトラ-n-ブチルアンモニウム(TBAF)溶液5mL加え、室温で12時間撹拌した。この反応液を、飽和炭酸水素ナトリウム水溶液と飽和食塩水で洗浄した。洗浄後の回収した有機層を、硫酸ナトリウムで乾燥させた。前記有機層をろ過して、得られたろ液を減圧濃縮し、化合物3を得た(3.6g、収率90%)。以下に、前記化合物のNMRの結果を示す。
1H-NMR(CDCl3): δ7.40-7.14(9H,m,Ar-H),6.82(4H,d,J=8.6Hz,Ar-H),3.78(6H,s,OCH3),3.31(1H,m,H-6),3.07(2H,m,H-2,H-6),2.90(2H,m,H-5),1.84(3H,m,H-3,H-4),1.40(1H,m,H-3).
前記「1.」で合成した保護プロリノール(化合物3)を用いて、下記スキーム7により、結合形式が異なる、プロリノールを有するアミダイト誘導体を合成した。
1,8-オクタンジオール(9.0g、62mmol)をTHF90mLに溶解し、アルゴン下に置いた。他方、カルボニルジイミダゾール(2.0g、12mmol)をTHF10mLに溶解した。後者のTHF溶液を、前者のTHF溶液に加え、室温で1時間撹拌した。この反応液を、1,8-オクタンジオールのTLCスポットが消えるまで、水で洗浄した。さらに、洗浄後に回収した有機層を、飽和食塩水で洗浄し、回収した有機層を、無水硫酸ナトリウムで乾燥させた。前記有機層をろ過し、得られたろ液を減圧濃縮した。その残渣を、シリカゲルカラムクロマトグラフィー(展開溶媒 CH2Cl2:CH3OH=95:5)に供し、精製した化合物を得た。この化合物は、1,8-オクタンジオールの片末端がカルボニルジイミダゾールで活性化された化合物であった(2.3g、収率77%)。
1H-NMR(CDCl3): δ7.40-7.14(9H,m,Ar-H),6.82(4H,d,J=8.6Hz,Ar-H),4.24-3.94(2H,m,COOCH2),3.78(s,6H,OCH3),3.72-2.96(7H,m,alkyl,H-2,H-5,H-6),2.10-1.30(16H,m,alkyl,H-3,H-4).
FAB-MS:576 [M+H]+.
アルゴン下、トリホスゲン(2.0g、6.7mmol)をTHF10mLに溶解し、0℃で撹拌した。他方、DMTr-L-プロリノール(化合物3)(1.3g、3.2mmol)およびN,N-ジイソプロピルエチルアミン(16g、124mmol)をTHF10mLに溶解し、前記トリホスゲンのTHF溶液に滴下した。この反応液を、0℃で1時間、続いて、室温で2時間撹拌した。そして、8-アミノ-1-オクタノール(2.3g、16mmol)およびN,N-ジイソプロピルエチルアミン(5.0g、38mmol)をTHF30mLに溶解した。このTHF溶液に、前記撹拌後の反応液を滴下し、0℃で1時間、続いて、室温で48時間撹拌した。この反応液を減圧濃縮し、その残渣をジクロロメタンに溶解した。この溶液を、飽和炭酸水素ナトリウム水溶液と飽和食塩水で洗浄し、回収した有機層を、無水硫酸ナトリウムで乾燥させた。前記有機層をろ過して、得られたろ液を減圧濃縮し、その残渣を、逆相シリカゲルカラムクロマトグラフィーに供して、精製した。この際、展開溶媒は、0.1%ピリジンを含有するアセトンと水との混合溶媒を使用し、前記アセトンと水との混合割合は、ステップワイズとし、具体的には、アセトン:水のモル比を、2:8、3:7、4:6および5:5の順に変化させた。目的の化合物5を含むフラクションを、ジクロロメタンで抽出し、この有機層を無水硫酸ナトリウムで乾燥させた。前記有機層をろ過し、得られたろ液を減圧濃縮し、化合物5(プロリノールウレイドアミダイト)を得た(0.9g、収率49%)。以下に、前記化合物のNMRの結果を示す。
1H-NMR(CDCl3): δ7.40-7.14(9H,m,Ar-H),6.82(4H,m,Ar-H),3.78(s,6H,OCH3),3.68-3.25(9H,m,CH2NH,CH2OH,H-2,H-5,H-6),1.74-1.18(16H,m,alkyl,H-3,H-4).
FAB-MS :575 [M+H]+.
修飾プロリノールとして、得られた前記化合物4(0.80g、1.4mmol)をアセトニトリルに溶解し、室温で3回共沸乾燥した。得られた残留物をアセトニトリル1mLに溶解し、アルゴン下においた。このアセトニトリル溶液に、ジイソプロピルアンモニウムテトラゾリド(0.24g,1.4mmol)を添加し、反応液とした。他方、2-シアノエチルN,N,N’,N’-テトライソプロピルホスホロジアミダイト(0.50g、1.7mmol)をアセトニトリル1mLに溶解した。これを、前記反応液に添加し、室温で4時間撹拌した。前記反応液に、ジクロロメタンを加え、飽和炭酸水素ナトリウム水溶液と飽和食塩水で洗浄した。洗浄後の回収した有機層を無水硫酸ナトリウムで乾燥させ、前記有機層をろ過して、得られたろ液を減圧濃縮した。その残渣を、アミノシリカゲルカラムクロマトグラフィー(展開溶媒ヘキサン:アセトン=10:1、0.1%ピリジン含有)に供し、精製した化合物6(DMTr-ウレタン-L-プロリノールアミダイト)(0.90g、収率83%)を得た。以下に、前記化合物のNMRの結果を示す。
1H-NMR(CDCl3): δ7.40-7.14(9H,m,Ar-H),6.82(4H,d,J=8.6Hz,Ar-H),4.24-3.94(2H,m,COOCH2),3.78(s,6H,OCH3),3.72-2.96(11H,m,CH2O,POCH2,CHCH3,H-2,H-5,H-6),2.58(2H,m,CH2CN),2.10-1.46(16H,m,alkyl,H-3,H-4),1.34-1.10(12H,m,CHCH3)。31P-NMR(CD3CN)δ 146.82.
FAB-MS:776 [M+H]+.
1H-NMR(CDCl3): δ7.40-7.14(9H,m,Ar-H),6.82(4H,m,Ar-H),3.78(s,6H,OCH3),3.65-3.25(13H,m,CH2O,POCH2,CHCH3,H-2,CH2NH,CH2OH,H-2,H-5,H-6),2.73(2H,m,CH2CN),2.10-1.48(16H,m,alkyl,H-3,H-4),1.35-1.10(12H,m,CHCH3).
31P-NMR(CD3CN)δ 146.83.
FAB-MS:775 [M+H]+.
Claims (37)
- 標的遺伝子の発現を抑制する発現抑制配列を含む一本鎖核酸分子であって、
5’側から3’側にかけて、5’側領域(Xc)、内部領域(Z)および3’側領域(Yc)を、前記順序で含み、
前記内部領域(Z)が、内部5’側領域(X)および内部3’側領域(Y)が連結して構成され、
前記5’側領域(Xc)が、前記内部5’側領域(X)と相補的であり、
前記3’側領域(Yc)が、前記内部3’側領域(Y)と相補的であり、
前記内部領域(Z)、前記5’側領域(Xc)および前記3’側領域(Yc)の少なくとも一つが、前記発現抑制配列を含むことを特徴とする一本鎖核酸分子。 - 前記5’側領域(Xc)と前記内部5’側領域(X)との間に、リンカー領域(Lx)を有し、
前記リンカー領域(Lx)を介して、前記5’側領域(Xc)と前記内部5’側領域(X)とが連結している、請求項1記載の一本鎖核酸分子。 - 前記3’側領域(Yc)と前記内部3’側領域(Y)との間に、リンカー領域(Ly)を有し、
前記リンカー領域(Ly)を介して、前記3’側領域(Yc)と前記内部3’側領域(Y)とが連結している、請求項1または2記載の一本鎖核酸分子。 - 前記5’側領域(Xc)と前記内部5’側領域(X)との間に、リンカー領域(Lx)を有し、
前記リンカー領域(Lx)を介して、前記5’側領域(Xc)と前記内部5’側領域(X)とが連結し、
前記3’側領域(Yc)と前記内部3’側領域(Y)との間に、リンカー領域(Ly)を有し、
前記リンカー領域(Ly)を介して、前記3’側領域(Yc)と前記内部3’側領域(Y)とが連結している、請求項1記載の一本鎖核酸分子。 - 前記内部領域(Z)の塩基数(Z)、前記内部5’側領域(X)の塩基数(X)、前記内部3’側領域(Y)の塩基数(Y)、前記5’側領域(Xc)の塩基数(Xc)および前記3’側領域(Yc)の塩基数(Yc)が、下記式(1)および(2)の条件を満たす、請求項1から4のいずれか一項に記載の一本鎖核酸分子。
Z=X+Y ・・・(1)
Z≧Xc+Yc ・・・(2) - 前記内部5’側領域(X)の塩基数(X)、前記5’側領域(Xc)の塩基数(Xc)、前記内部3’側領域(Y)の塩基数(Y)および前記3’側領域(Yc)の塩基数(Yc)が、下記(a)~(d)のいずれかの条件を満たす、請求項1から5のいずれか一項に記載の一本鎖核酸分子。
(a)下記式(3)および(4)の条件を満たす。
X>Xc ・・・(3)
Y=Yc ・・・(4)
(b)下記式(5)および(6)の条件を満たす。
X=Xc ・・・(5)
Y>Yc ・・・(6)
(c)下記式(7)および(8)の条件を満たす。
X>Xc ・・・(7)
Y>Yc ・・・(8)
(d)下記式(9)および(10)の条件を満たす。
X=Xc ・・・(9)
Y=Yc ・・・(10) - 前記(a)~(d)において、前記内部5’側領域(X)の塩基数(X)と前記5’側領域(Xc)の塩基数(Xc)の差、前記内部3’側領域(Y)の塩基数(Y)と前記3’側領域(Yc)の塩基数(Yc)の差が、下記条件を満たす、請求項6記載の一本鎖核酸分子。
(a)下記式(11)および(12)の条件を満たす。
X-Xc=1、2または3 ・・・(11)
Y-Yc=0 ・・・(12)
(b)下記式(13)および(14)の条件を満たす。
X-Xc=0 ・・・(13)
Y-Yc=1、2または3 ・・・(14)
(c)下記式(15)および(16)の条件を満たす。
X-Xc=1、2または3 ・・・(15)
Y-Yc=1、2または3 ・・・(16)
(d)下記式(17)および(18)の条件を満たす。
X-Xc=0 ・・・(17)
Y-Yc=0 ・・・(18) - 前記内部領域(Z)の塩基数(Z)が、19塩基以上である、請求項1から7のいずれか一項に記載の一本鎖核酸分子。
- 前記内部領域(Z)の塩基数(Z)が、19塩基~30塩基である、請求項8記載の一本鎖核酸分子。
- 前記5’側領域(Xc)の塩基数(Xc)が、1~11塩基である、請求項1から9のいずれか一項に記載の一本鎖核酸分子。
- 前記5’側領域(Xc)の塩基数(Xc)が、1~7塩基である、請求項10記載の一本鎖核酸分子。
- 前記5’側領域(Xc)の塩基数(Xc)が、1~3塩基である、請求項10記載の一本鎖核酸分子。
- 前記3’側領域(Yc)の塩基数(Yc)が、1~11塩基である、請求項1から12のいずれか一項に記載の一本鎖核酸分子。
- 前記3’側領域(Yc)の塩基数(Yc)が、1~7塩基である、請求項13記載の一本鎖核酸分子。
- 前記3’側領域(Yc)の塩基数(Yc)が、1~3塩基である、請求項13記載の一本鎖核酸分子。
- 少なくとも1つの修飾された残基を含む、請求項1から15のいずれか一項に記載の一本鎖核酸分子。
- 標識物質を含む、請求項1から16のいずれか一項に記載の一本鎖核酸分子。
- 安定同位体を含む、請求項1から17のいずれか一項に記載の一本鎖核酸分子。
- RNA分子である、請求項1から18のいずれか一項に記載の一本鎖核酸分子。
- 前記リンカー領域(Lx)および/または前記リンカー領域(Ly)が、
ヌクレオチド残基および非ヌクレオチド残基の少なくとも一つから構成される、請求項2から19のいずれか一項に記載の一本鎖核酸分子。 - 前記ヌクレオチド残基が、非修飾ヌクレオチド残基および/または修飾ヌクレオチド残基である、請求項20記載の一本鎖核酸分子。
- 前記リンカー領域(Lx)および/または前記リンカー領域(Ly)が、下記(1)~(7)のいずれかの残基で構成される、請求項20または21記載の一本鎖核酸分子。
(1)非修飾ヌクレオチド残基
(2)修飾ヌクレオチド残基
(3)非修飾ヌクレオチド残基および修飾ヌクレオチド残基
(4)非ヌクレオチド残基
(5)非ヌクレオチド残基および非修飾ヌクレオチド残基
(6)非ヌクレオチド残基および修飾ヌクレオチド残基
(7)非ヌクレオチド残基、非修飾ヌクレオチド残基および修飾ヌクレオチド残基 - 前記一本鎖核酸分子において、塩基数の合計が、50塩基以上である、請求項1から22のいずれか一項に記載の一本鎖核酸分子。
- 前記遺伝子の発現抑制が、RNA干渉による発現抑制である、請求項1から23のいずれか一項に記載の一本鎖核酸分子。
- 前記一本鎖核酸分子の塩基配列が、
配列番号2、7、8、13、14、29-35、37、43、44、47、48および51-80のいずれかの塩基配列である、請求項1から24のいずれか一項に記載の一本鎖核酸分子。 - 標的遺伝子の発現を抑制するための組成物であって、
請求項1から25のいずれか一項に記載の一本鎖核酸分子を含むことを特徴とする、発現抑制用組成物。 - 請求項1から25のいずれか一項に記載の一本鎖核酸分子を含むことを特徴とする、薬学的組成物。
- 炎症治療用である、請求項27記載の薬学組成物。
- 標的遺伝子の発現を抑制する方法であって、
請求項1から25のいずれか一項に記載の一本鎖核酸分子を使用することを特徴とする発現抑制方法。 - 前記一本鎖核酸分子を、細胞、組織または器官に投与する工程を含む、請求項29記載の発現抑制方法。
- 前記一本鎖核酸分子を、in vivoまたはin vitroで投与する、請求項30記載の発現抑制方法。
- 前記遺伝子の発現抑制が、RNA干渉による発現抑制である、請求項29から31のいずれか一項に記載の発現抑制方法。
- 標的遺伝子の発現を抑制するRNA干渉を誘導する方法であって、
請求項1から25のいずれか一項に記載の一本鎖核酸分子を使用することを特徴とする発現誘導方法。 - 疾患の治療方法であって、
請求項1から25のいずれか一項に記載の一本鎖核酸分子を、患者に投与する工程を含み、
前記一本鎖核酸分子が、前記発現抑制配列として、前記疾患の原因となる遺伝子の発現を抑制する配列を有することを特徴とする治療方法。 - 標的遺伝子の発現抑制のための、請求項1から25のいずれか一項に記載の一本鎖核酸分子の使用。
- RNA干渉の誘導のための、請求項1から25のいずれか一項に記載の一本鎖核酸分子の使用。
- 疾患の治療に使用するための核酸分子であって、
前記核酸分子は、請求項1から25のいずれか一項に記載の一本鎖核酸分子であり、
前記一本鎖核酸分子が、前記発現抑制配列として、前記疾患の原因となる遺伝子の発現を抑制する配列を有することを特徴とする核酸分子。
Priority Applications (17)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020127033429A KR101849798B1 (ko) | 2010-07-08 | 2011-07-08 | 유전자 발현 제어를 위한 일본쇄 핵산 분자 |
| JP2011537086A JP4968811B2 (ja) | 2010-07-08 | 2011-07-08 | 遺伝子発現制御のための一本鎖核酸分子 |
| CA2804511A CA2804511C (en) | 2010-07-08 | 2011-07-08 | Single-stranded nucleic acid molecule for controlling gene expression |
| CN201180027223.1A CN102918156B (zh) | 2010-07-08 | 2011-07-08 | 用于控制基因表达的单链核酸分子 |
| DK11746147.5T DK2431466T3 (en) | 2010-07-08 | 2011-07-08 | Single-stranded nucleic acid molecule for the control of gene expression |
| MX2013000315A MX352568B (es) | 2010-07-08 | 2011-07-08 | Molecula de acido nucleico de cadena simple para el control de la expresion de genes. |
| ES11746147.5T ES2550487T3 (es) | 2010-07-08 | 2011-07-08 | Molécula de ácido nucleico monocatenario para controlar la expresión génica |
| AU2011274854A AU2011274854B2 (en) | 2010-07-08 | 2011-07-08 | Single-strand nucleic acid molecule for controlling gene expression |
| NZ606232A NZ606232A (en) | 2010-07-08 | 2011-07-08 | Single-stranded nucleic acid molecule for controlling gene expression |
| EP11746147.5A EP2431466B1 (en) | 2010-07-08 | 2011-07-08 | Single-strand nucleic acid molecule for controlling gene expression |
| US13/254,150 US8785121B2 (en) | 2010-07-08 | 2011-07-08 | Single-stranded nucleic acid molecule for controlling gene expression |
| BR112013000481-9A BR112013000481A2 (ja) | 2010-07-08 | 2011-07-08 | The 1 chain nucleic acid molecule for gene expression control |
| RU2013105329A RU2628311C2 (ru) | 2010-07-08 | 2011-07-08 | Молекула одноцепочечной нуклеиновой кислоты для контроля экспрессии генов |
| SG2013000211A SG186899A1 (en) | 2010-07-08 | 2011-07-08 | Single-strand nucleic acid molecule for controlling gene expression |
| HK13108676.9A HK1181423A1 (zh) | 2010-07-08 | 2013-07-24 | 用於控制基因表達的單鏈核酸分子 |
| US14/303,315 US20150011605A1 (en) | 2010-07-08 | 2014-06-12 | Single-Stranded Nucleic Acid Molecule for Controlling Gene Expression |
| US14/927,270 US20160108400A1 (en) | 2010-07-08 | 2015-10-29 | Single-Stranded Nucleic Acid Molecule for Controlling Gene Expression |
Applications Claiming Priority (12)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2010-156122 | 2010-07-08 | ||
| JP2010156122 | 2010-07-08 | ||
| JP2010-174915 | 2010-08-03 | ||
| JP2010174915 | 2010-08-03 | ||
| JP2010-230808 | 2010-10-13 | ||
| JP2010230808 | 2010-10-13 | ||
| JP2010-230806 | 2010-10-13 | ||
| JP2010230806 | 2010-10-13 | ||
| JP2010269824 | 2010-12-02 | ||
| JP2010-269823 | 2010-12-02 | ||
| JP2010-269824 | 2010-12-02 | ||
| JP2010269823 | 2010-12-02 |
Related Child Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| US13/254,150 A-371-Of-International US8785121B2 (en) | 2010-07-08 | 2011-07-08 | Single-stranded nucleic acid molecule for controlling gene expression |
| US14/303,315 Continuation US20150011605A1 (en) | 2010-07-08 | 2014-06-12 | Single-Stranded Nucleic Acid Molecule for Controlling Gene Expression |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2012005368A1 true WO2012005368A1 (ja) | 2012-01-12 |
Family
ID=45441339
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2011/065737 WO2012005368A1 (ja) | 2010-07-08 | 2011-07-08 | 遺伝子発現制御のための一本鎖核酸分子 |
Country Status (18)
| Country | Link |
|---|---|
| EP (2) | EP2431466B1 (ja) |
| JP (3) | JP4968811B2 (ja) |
| KR (1) | KR101849798B1 (ja) |
| CN (2) | CN102918156B (ja) |
| AU (1) | AU2011274854B2 (ja) |
| BR (1) | BR112013000481A2 (ja) |
| CA (1) | CA2804511C (ja) |
| DK (2) | DK2431466T3 (ja) |
| ES (2) | ES2670017T3 (ja) |
| HK (1) | HK1181423A1 (ja) |
| HU (2) | HUE026520T2 (ja) |
| MX (1) | MX352568B (ja) |
| NZ (2) | NZ606232A (ja) |
| PT (2) | PT2933333T (ja) |
| RU (1) | RU2628311C2 (ja) |
| SG (2) | SG196779A1 (ja) |
| TW (2) | TWI573870B (ja) |
| WO (1) | WO2012005368A1 (ja) |
Cited By (30)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2013077446A1 (ja) * | 2011-11-26 | 2013-05-30 | 株式会社ボナック | 遺伝子発現制御のための一本鎖核酸分子 |
| WO2013133393A1 (ja) * | 2012-03-07 | 2013-09-12 | 学校法人東京医科大学 | Vegf遺伝子の発現抑制用一本鎖核酸分子 |
| WO2013147140A1 (ja) | 2012-03-29 | 2013-10-03 | 国立大学法人九州大学 | ペリオスチン遺伝子の発現抑制核酸分子、ペリオスチン遺伝子の発現抑制方法、およびその用途 |
| WO2013180038A1 (ja) | 2012-05-26 | 2013-12-05 | 株式会社ボナック | デリバリー機能を有する遺伝子発現制御用の一本鎖核酸分子 |
| US9200278B2 (en) | 2010-08-03 | 2015-12-01 | Bonac Corporation | Single-stranded nucleic acid molecule having nitrogen-containing alicyclic skeleton |
| WO2017115872A1 (ja) | 2015-12-29 | 2017-07-06 | 国立大学法人北海道大学 | プロレニン遺伝子またはプロレニン受容体遺伝子の発現を抑制する一本鎖核酸分子およびその用途 |
| KR20180066250A (ko) | 2015-10-30 | 2018-06-18 | 가부시키가이샤 보낙 | TGF-β1 유전자의 발현을 억제하는 단일-가닥 핵산 분자를 안정적으로 함유하는 조성물 |
| KR20180100692A (ko) | 2016-01-30 | 2018-09-11 | 가부시키가이샤 보낙 | 인공 단일 가이드 rna 및 이의 용도 |
| WO2018182008A1 (ja) | 2017-03-31 | 2018-10-04 | 株式会社ボナック | 遺伝子発現制御機能を有する環状型核酸分子 |
| WO2018199338A1 (ja) * | 2017-04-27 | 2018-11-01 | 国立大学法人広島大学 | B型肝炎治療用核酸分子 |
| WO2019022257A1 (ja) | 2017-07-28 | 2019-01-31 | 杏林製薬株式会社 | 線維症治療剤 |
| WO2019074071A1 (ja) | 2017-10-11 | 2019-04-18 | 日東電工株式会社 | 核酸分子発現の調節 |
| WO2019074110A1 (ja) | 2017-10-13 | 2019-04-18 | 株式会社ボナック | 一本鎖核酸分子およびその製造方法 |
| US10337009B2 (en) | 2014-12-15 | 2019-07-02 | Bonac Corporation | Single-stranded nucleic acid molecule for inhibiting TGF-β1 expression |
| WO2019189591A1 (ja) | 2018-03-30 | 2019-10-03 | 住友化学株式会社 | 一本鎖rnaの製造方法 |
| US10612020B2 (en) | 2013-12-26 | 2020-04-07 | Tokyo Medical University | Artificial mimic miRNA for controlling gene expression, and use of same |
| WO2020071407A1 (ja) * | 2018-10-02 | 2020-04-09 | 東レ株式会社 | ヘアピン型一本鎖rna分子の製造方法 |
| WO2020152869A1 (ja) | 2019-01-25 | 2020-07-30 | 杏林製薬株式会社 | 線維症治療剤 |
| JP2020182461A (ja) * | 2018-02-09 | 2020-11-12 | 住友化学株式会社 | 核酸分子の製造方法 |
| JP2020536506A (ja) * | 2017-09-15 | 2020-12-17 | コモンウェルス サイエンティフィック アンド インダストリアル リサーチ オーガナイゼーション | Rna分子 |
| US10934542B2 (en) | 2013-12-27 | 2021-03-02 | Bonac Corporation | Artificial match-type miRNA for controlling gene expression and use therefor |
| WO2021070494A1 (ja) | 2019-10-11 | 2021-04-15 | 住友化学株式会社 | 核酸オリゴマーの製造方法 |
| US11027023B2 (en) | 2014-12-27 | 2021-06-08 | Bonac Corporation | Natural type miRNA for controlling gene expression, and use of same |
| WO2021153770A1 (en) | 2020-01-29 | 2021-08-05 | Sumitomo Chemical Company, Limited | Process of preparing nucleic acid oligomer |
| WO2021153047A1 (ja) | 2020-01-29 | 2021-08-05 | 住友化学株式会社 | 核酸オリゴマーの製造方法 |
| EP3885434A1 (en) | 2020-03-25 | 2021-09-29 | Ajinomoto Co., Inc. | Ligase mutant |
| WO2021193954A1 (ja) | 2020-03-27 | 2021-09-30 | 住友化学株式会社 | 核酸オリゴマーの製造方法 |
| US11142769B2 (en) | 2015-03-27 | 2021-10-12 | Bonac Corporation | Single-stranded nucleic acid molecule having delivery function and gene expression regulating ability |
| WO2022009959A1 (ja) | 2020-07-09 | 2022-01-13 | 住友化学株式会社 | 核酸オリゴマーの製造方法 |
| WO2022064908A1 (ja) | 2020-09-24 | 2022-03-31 | 住友化学株式会社 | 核酸オリゴマーの製造方法 |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP3778886A4 (en) | 2018-03-30 | 2022-11-02 | Toray Industries, Inc. | METHOD FOR PRODUCING A HAIRPIN SINGLE-STRANDED RNA MOLECULE |
Citations (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3687808A (en) | 1969-08-14 | 1972-08-29 | Univ Leland Stanford Junior | Synthetic polynucleotides |
| US20030008818A1 (en) | 2000-12-19 | 2003-01-09 | California Institute Of Technology And Insert Therapeutics, Inc | Compositions containing inclusion complexes |
| US6509323B1 (en) | 1998-07-01 | 2003-01-21 | California Institute Of Technology | Linear cyclodextrin copolymers |
| JP2008278784A (ja) | 2007-05-09 | 2008-11-20 | Institute Of Physical & Chemical Research | 1本鎖環状rnaおよびその製造方法 |
| WO2009102081A1 (ja) * | 2008-02-15 | 2009-08-20 | Riken | 環状1本鎖核酸複合体およびその製造方法 |
| JP2010156122A (ja) | 2008-12-26 | 2010-07-15 | Marubeni Construction Material Lease Co Ltd | 掘削機の泥土飛散防止装置 |
| JP2010174915A (ja) | 2009-01-27 | 2010-08-12 | Toyota Motor Corp | 高圧ガスタンク |
| JP2010230808A (ja) | 2009-03-26 | 2010-10-14 | Funai Electric Co Ltd | 液晶モジュール |
| JP2010230806A (ja) | 2009-03-26 | 2010-10-14 | Sumitomo Chemical Co Ltd | 偏光板の製造方法、偏光板および液晶表示装置 |
| JP2010269824A (ja) | 2009-05-21 | 2010-12-02 | Fp Corp | 包装用容器 |
| JP2010269823A (ja) | 2009-05-21 | 2010-12-02 | British American Tobacco Japan Kk | 喫煙品用容器 |
Family Cites Families (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5631148A (en) * | 1994-04-22 | 1997-05-20 | Chiron Corporation | Ribozymes with product ejection by strand displacement |
| FR2790757B1 (fr) * | 1999-03-09 | 2003-08-01 | Bioalliance Pharma | Oligonucleotides contenant une sequence antisens stabilises par une structure secondaire et compositions pharmaceutiques les contenant. |
| US20060111312A1 (en) * | 2002-02-22 | 2006-05-25 | The John Hopkins University | Antigene locks and therapeutic uses thereof |
| AU2003260370B2 (en) * | 2002-08-05 | 2008-05-22 | Silence Therapeutics Gmbh | Further novel forms of interfering RNA molecules |
| US20040058886A1 (en) * | 2002-08-08 | 2004-03-25 | Dharmacon, Inc. | Short interfering RNAs having a hairpin structure containing a non-nucleotide loop |
| WO2005030960A1 (ja) * | 2003-09-30 | 2005-04-07 | Anges Mg, Inc. | ステイプル型オリゴヌクレオチドおよびそれからなる医薬 |
| EP1789553B1 (en) * | 2004-06-30 | 2014-03-26 | Alnylam Pharmaceuticals Inc. | Oligonucleotides comprising a non-phosphate backbone linkage |
| EP1838875A4 (en) * | 2004-12-30 | 2010-08-25 | Todd M Hauser | COMPOSITIONS AND METHODS FOR MODULATING GENE EXPRESSION USING SELF-PROTECTED OLIGONUCLEOTIDES |
| KR100848666B1 (ko) * | 2006-03-17 | 2008-07-28 | (주)바이오니아 | NF-k B의 발현을 억제하는 s i RNA |
| WO2009074076A1 (fr) * | 2007-11-29 | 2009-06-18 | Suzhou Ribo Life Science Co., Ltd | Molécule complexe interférant avec l'expression de gènes cibles, et ses méthodes de préparation |
| US20110159586A1 (en) * | 2007-12-07 | 2011-06-30 | Halo-Bio Rnai Therapeutics, Inc. | Compositions and methods for modulating gene expression using asymmetrically-active precursor polynucleotides |
-
2011
- 2011-07-08 SG SG2013097233A patent/SG196779A1/en unknown
- 2011-07-08 DK DK11746147.5T patent/DK2431466T3/en active
- 2011-07-08 CA CA2804511A patent/CA2804511C/en active Active
- 2011-07-08 BR BR112013000481-9A patent/BR112013000481A2/ja not_active Application Discontinuation
- 2011-07-08 RU RU2013105329A patent/RU2628311C2/ru active
- 2011-07-08 KR KR1020127033429A patent/KR101849798B1/ko active IP Right Grant
- 2011-07-08 JP JP2011537086A patent/JP4968811B2/ja active Active
- 2011-07-08 HU HUE11746147A patent/HUE026520T2/en unknown
- 2011-07-08 NZ NZ606232A patent/NZ606232A/en not_active IP Right Cessation
- 2011-07-08 PT PT151699337T patent/PT2933333T/pt unknown
- 2011-07-08 NZ NZ704812A patent/NZ704812A/en unknown
- 2011-07-08 EP EP11746147.5A patent/EP2431466B1/en active Active
- 2011-07-08 EP EP15169933.7A patent/EP2933333B1/en active Active
- 2011-07-08 ES ES15169933.7T patent/ES2670017T3/es active Active
- 2011-07-08 SG SG2013000211A patent/SG186899A1/en unknown
- 2011-07-08 PT PT117461475T patent/PT2431466E/pt unknown
- 2011-07-08 ES ES11746147.5T patent/ES2550487T3/es active Active
- 2011-07-08 TW TW104143857A patent/TWI573870B/zh active
- 2011-07-08 CN CN201180027223.1A patent/CN102918156B/zh active Active
- 2011-07-08 MX MX2013000315A patent/MX352568B/es active IP Right Grant
- 2011-07-08 CN CN201510226685.6A patent/CN104818276B/zh active Active
- 2011-07-08 AU AU2011274854A patent/AU2011274854B2/en active Active
- 2011-07-08 WO PCT/JP2011/065737 patent/WO2012005368A1/ja active Application Filing
- 2011-07-08 DK DK15169933.7T patent/DK2933333T3/en active
- 2011-07-08 TW TW100124393A patent/TWI527901B/zh active
- 2011-07-08 HU HUE15169933A patent/HUE037500T2/hu unknown
-
2012
- 2012-01-20 JP JP2012009515A patent/JP5804642B2/ja active Active
-
2013
- 2013-07-24 HK HK13108676.9A patent/HK1181423A1/zh not_active IP Right Cessation
-
2015
- 2015-07-29 JP JP2015150156A patent/JP6162182B2/ja active Active
Patent Citations (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3687808A (en) | 1969-08-14 | 1972-08-29 | Univ Leland Stanford Junior | Synthetic polynucleotides |
| US6509323B1 (en) | 1998-07-01 | 2003-01-21 | California Institute Of Technology | Linear cyclodextrin copolymers |
| US20030008818A1 (en) | 2000-12-19 | 2003-01-09 | California Institute Of Technology And Insert Therapeutics, Inc | Compositions containing inclusion complexes |
| JP2008278784A (ja) | 2007-05-09 | 2008-11-20 | Institute Of Physical & Chemical Research | 1本鎖環状rnaおよびその製造方法 |
| WO2009102081A1 (ja) * | 2008-02-15 | 2009-08-20 | Riken | 環状1本鎖核酸複合体およびその製造方法 |
| JP2010156122A (ja) | 2008-12-26 | 2010-07-15 | Marubeni Construction Material Lease Co Ltd | 掘削機の泥土飛散防止装置 |
| JP2010174915A (ja) | 2009-01-27 | 2010-08-12 | Toyota Motor Corp | 高圧ガスタンク |
| JP2010230808A (ja) | 2009-03-26 | 2010-10-14 | Funai Electric Co Ltd | 液晶モジュール |
| JP2010230806A (ja) | 2009-03-26 | 2010-10-14 | Sumitomo Chemical Co Ltd | 偏光板の製造方法、偏光板および液晶表示装置 |
| JP2010269824A (ja) | 2009-05-21 | 2010-12-02 | Fp Corp | 包装用容器 |
| JP2010269823A (ja) | 2009-05-21 | 2010-12-02 | British American Tobacco Japan Kk | 喫煙品用容器 |
Non-Patent Citations (15)
| Title |
|---|
| "Concise Encyclopedia of Polymer Science and Engineering", 1990, JOHN WILEY & SONS, pages: 858 - 859 |
| ABE, NAOKO ET AL.: "Dumbbell-shaped nanocircular RNAs for RNA interference.", J. AM. CHEM. SOC., vol. 129, 2007, pages 15108 - 15109, XP008120979 * |
| BRAMSEN, JESPER B. ET AL.: "Improved silencing properties using small internally segmented interfering RNAs.", NUCLEIC ACIDS RES., vol. 35, no. 17, 2007, pages 5886 - 5897, XP002458184 * |
| CHENG ET AL., MOL. PHARM., vol. 6, 2009, pages 772 - 779 |
| ENGLISCH ET AL.: "Angewandte Chemie", vol. 30, 1991, pages: 613 |
| FIRE. ET AL., NATURE, vol. 391, 1998, pages 806 - 811 |
| HOSOYA, TAKESHI ET AL.: "Sequence-specific inhibition of a transcription factor by circular dumbbell DNA oligonucleotides.", FEBS LETT., vol. 461, 1999, pages 136 - 140, XP004260536 * |
| J. F. W MCOMIE: "Protecting Groups in Organic Chemistry", 1973, PLENUM PRESS |
| KUNUGIZA, YASUO ET AL.: "Inhibitory effect of ribbon-type NF-kappaB decoy oligodeoxynucleotides on osteoclast induction and activity in vitro and in vivo.", ARTHRITIS RES. THER., vol. 8, no. 4, 2006, pages 1 - 10, XP021020579 * |
| LEIRDAL, MARIANNE ET AL.: "Gene silencing in mammalian cells by preformed small RNA duplexes.", BIOCHEM. BIOPHYS. RES. COMMUN., vol. 295, 2002, pages 744 - 748, XP002953281 * |
| LIMBACH ET AL.: "Summary: the modified nucleosides of RNA", NUCLEIC ACIDS RES., vol. 22, 1994, pages 2183 - 2196 |
| See also references of EP2431466A4 * |
| TAKAGI ET AL., J. THROMB HEMOST, vol. 7, 2009, pages 2053 - 2063 |
| YAMAKAWA, HIDEFUMI ET AL.: "Properties and anti-HIV activity of nicked dumbbell oligonucleotides.", NUCLEOSIDES NUCLEOTIDES, vol. 15, no. 1-3, 1996, pages 519 - 529, XP002975792 * |
| YASUI ET AL., AM J RESPIR CRIT CARE MED, vol. 163, 2001, pages 1660 - 8 |
Cited By (43)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9200278B2 (en) | 2010-08-03 | 2015-12-01 | Bonac Corporation | Single-stranded nucleic acid molecule having nitrogen-containing alicyclic skeleton |
| US9206422B2 (en) | 2010-08-03 | 2015-12-08 | Bonac Corporation | Single-stranded nucleic acid molecule having nitrogen-containing alicyclic skeleton |
| WO2013077446A1 (ja) * | 2011-11-26 | 2013-05-30 | 株式会社ボナック | 遺伝子発現制御のための一本鎖核酸分子 |
| WO2013133393A1 (ja) * | 2012-03-07 | 2013-09-12 | 学校法人東京医科大学 | Vegf遺伝子の発現抑制用一本鎖核酸分子 |
| WO2013147140A1 (ja) | 2012-03-29 | 2013-10-03 | 国立大学法人九州大学 | ペリオスチン遺伝子の発現抑制核酸分子、ペリオスチン遺伝子の発現抑制方法、およびその用途 |
| WO2013180038A1 (ja) | 2012-05-26 | 2013-12-05 | 株式会社ボナック | デリバリー機能を有する遺伝子発現制御用の一本鎖核酸分子 |
| CN104379744A (zh) * | 2012-05-26 | 2015-02-25 | 株式会社博纳克 | 具有递送功能的基因表达调控用单链核酸分子 |
| JPWO2013180038A1 (ja) * | 2012-05-26 | 2016-01-21 | 株式会社ボナック | デリバリー機能を有する遺伝子発現制御用の一本鎖核酸分子 |
| EP2857513A4 (en) * | 2012-05-26 | 2016-05-25 | Bonac Corp | SINGLE STRANDED NUCLEIC ACID MOLECULE FOR CONTROLLING THE EXPRESSION OF A GENE HAVING AN ADMINISTRATION FUNCTION |
| US9663784B2 (en) | 2012-05-26 | 2017-05-30 | Bonac Corporation | Single-stranded nucleic acid molecule for regulating expression of gene having delivering function |
| US10238752B2 (en) | 2012-05-26 | 2019-03-26 | Bonac Corporation | Single-stranded nucleic acid molecule for regulating expression of gene having delivering function |
| JP2017148057A (ja) * | 2012-05-26 | 2017-08-31 | 株式会社ボナック | デリバリー機能を有する遺伝子発現制御用の一本鎖核酸分子 |
| CN109810977A (zh) * | 2012-05-26 | 2019-05-28 | 株式会社博纳克 | 具有递送功能的基因表达调控用单链核酸分子 |
| US10612020B2 (en) | 2013-12-26 | 2020-04-07 | Tokyo Medical University | Artificial mimic miRNA for controlling gene expression, and use of same |
| US10934542B2 (en) | 2013-12-27 | 2021-03-02 | Bonac Corporation | Artificial match-type miRNA for controlling gene expression and use therefor |
| US10337009B2 (en) | 2014-12-15 | 2019-07-02 | Bonac Corporation | Single-stranded nucleic acid molecule for inhibiting TGF-β1 expression |
| US11027023B2 (en) | 2014-12-27 | 2021-06-08 | Bonac Corporation | Natural type miRNA for controlling gene expression, and use of same |
| US11142769B2 (en) | 2015-03-27 | 2021-10-12 | Bonac Corporation | Single-stranded nucleic acid molecule having delivery function and gene expression regulating ability |
| KR20180066250A (ko) | 2015-10-30 | 2018-06-18 | 가부시키가이샤 보낙 | TGF-β1 유전자의 발현을 억제하는 단일-가닥 핵산 분자를 안정적으로 함유하는 조성물 |
| US10751426B2 (en) | 2015-10-30 | 2020-08-25 | Bonac Corporation | Composition stably containing single-stranded nucleic acid molecule that suppresses expression of TGF-β1 gene |
| WO2017115872A1 (ja) | 2015-12-29 | 2017-07-06 | 国立大学法人北海道大学 | プロレニン遺伝子またはプロレニン受容体遺伝子の発現を抑制する一本鎖核酸分子およびその用途 |
| KR20180100692A (ko) | 2016-01-30 | 2018-09-11 | 가부시키가이샤 보낙 | 인공 단일 가이드 rna 및 이의 용도 |
| US11518994B2 (en) | 2016-01-30 | 2022-12-06 | Bonac Corporation | Artificial single guide RNA and use thereof |
| WO2018182008A1 (ja) | 2017-03-31 | 2018-10-04 | 株式会社ボナック | 遺伝子発現制御機能を有する環状型核酸分子 |
| WO2018199338A1 (ja) * | 2017-04-27 | 2018-11-01 | 国立大学法人広島大学 | B型肝炎治療用核酸分子 |
| WO2019022257A1 (ja) | 2017-07-28 | 2019-01-31 | 杏林製薬株式会社 | 線維症治療剤 |
| JP2020536506A (ja) * | 2017-09-15 | 2020-12-17 | コモンウェルス サイエンティフィック アンド インダストリアル リサーチ オーガナイゼーション | Rna分子 |
| WO2019074071A1 (ja) | 2017-10-11 | 2019-04-18 | 日東電工株式会社 | 核酸分子発現の調節 |
| US11298371B2 (en) | 2017-10-11 | 2022-04-12 | Nitto Denko Corporation | Regulation of nucleic acid molecule expression |
| WO2019074110A1 (ja) | 2017-10-13 | 2019-04-18 | 株式会社ボナック | 一本鎖核酸分子およびその製造方法 |
| JP2020182461A (ja) * | 2018-02-09 | 2020-11-12 | 住友化学株式会社 | 核酸分子の製造方法 |
| WO2019189591A1 (ja) | 2018-03-30 | 2019-10-03 | 住友化学株式会社 | 一本鎖rnaの製造方法 |
| JPWO2019189591A1 (ja) * | 2018-03-30 | 2020-10-01 | 住友化学株式会社 | 一本鎖rnaの製造方法 |
| WO2020071407A1 (ja) * | 2018-10-02 | 2020-04-09 | 東レ株式会社 | ヘアピン型一本鎖rna分子の製造方法 |
| US11891602B2 (en) | 2018-10-02 | 2024-02-06 | Toray Industries, Inc. | Method of producing hairpin single-stranded RNA molecules |
| WO2020152869A1 (ja) | 2019-01-25 | 2020-07-30 | 杏林製薬株式会社 | 線維症治療剤 |
| WO2021070494A1 (ja) | 2019-10-11 | 2021-04-15 | 住友化学株式会社 | 核酸オリゴマーの製造方法 |
| WO2021153770A1 (en) | 2020-01-29 | 2021-08-05 | Sumitomo Chemical Company, Limited | Process of preparing nucleic acid oligomer |
| WO2021153047A1 (ja) | 2020-01-29 | 2021-08-05 | 住友化学株式会社 | 核酸オリゴマーの製造方法 |
| EP3885434A1 (en) | 2020-03-25 | 2021-09-29 | Ajinomoto Co., Inc. | Ligase mutant |
| WO2021193954A1 (ja) | 2020-03-27 | 2021-09-30 | 住友化学株式会社 | 核酸オリゴマーの製造方法 |
| WO2022009959A1 (ja) | 2020-07-09 | 2022-01-13 | 住友化学株式会社 | 核酸オリゴマーの製造方法 |
| WO2022064908A1 (ja) | 2020-09-24 | 2022-03-31 | 住友化学株式会社 | 核酸オリゴマーの製造方法 |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6162182B2 (ja) | 遺伝子発現制御のための一本鎖核酸分子 | |
| JP5555346B2 (ja) | 含窒素脂環式骨格を有する一本鎖核酸分子 | |
| JP5876890B2 (ja) | アミノ酸骨格を有する一本鎖核酸分子 | |
| US9206422B2 (en) | Single-stranded nucleic acid molecule having nitrogen-containing alicyclic skeleton | |
| US8785121B2 (en) | Single-stranded nucleic acid molecule for controlling gene expression | |
| WO2013077446A1 (ja) | 遺伝子発現制御のための一本鎖核酸分子 | |
| JP2013153736A (ja) | ペプチド骨格を有する一本鎖核酸分子 | |
| JP2013055913A (ja) | 遺伝子発現制御のための一本鎖rna分子 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| WWE | Wipo information: entry into national phase |
Ref document number: 201180027223.1 Country of ref document: CN |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2011746147 Country of ref document: EP |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2011537086 Country of ref document: JP Ref document number: 13254150 Country of ref document: US |
|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 11746147 Country of ref document: EP Kind code of ref document: A1 |
|
| ENP | Entry into the national phase |
Ref document number: 20127033429 Country of ref document: KR Kind code of ref document: A |
|
| ENP | Entry into the national phase |
Ref document number: 2804511 Country of ref document: CA |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| WWE | Wipo information: entry into national phase |
Ref document number: MX/A/2013/000315 Country of ref document: MX |
|
| ENP | Entry into the national phase |
Ref document number: 2013105329 Country of ref document: RU Kind code of ref document: A |
|
| ENP | Entry into the national phase |
Ref document number: 2011274854 Country of ref document: AU Date of ref document: 20110708 Kind code of ref document: A |
|
| REG | Reference to national code |
Ref country code: BR Ref legal event code: B01A Ref document number: 112013000481 Country of ref document: BR |
|
| ENP | Entry into the national phase |
Ref document number: 112013000481 Country of ref document: BR Kind code of ref document: A2 Effective date: 20130108 |
|
| ENPC | Correction to former announcement of entry into national phase, pct application did not enter into the national phase |
Ref country code: BR Free format text: ANULADA A PUBLICACAO CODIGO 1.3 NA RPI NO 2430 DE 01/08/2017 POR TER SIDO INDEVIDA. |
|
| REG | Reference to national code |
Ref country code: BR Ref legal event code: B01E Ref document number: 112013000481 Country of ref document: BR Kind code of ref document: A2 Free format text: 1) COM BASE NA RESOLUCAO 228/09, SOLICITA-SE QUE SEJA APRESENTADO, EM ATE 60 (SESSENTA) DIAS, NOVO CONTEUDO DE LISTAGEM DE SEQUENCIA NOS MOLDES DA RESOLUCAO NO 187 DE 27/04/2017, POIS OS CD'S/DVD'S APRESENTADOS NA PETICAO NO 016130000074 DE 08/01/2013 NAO ESTAO EM LINGUA VERNACULA.2) APRESENTAR A TRADUCAO SIMPLES DA FOLHA DE ROSTO DA CERTIDAO DE DEPOSITO DAS PRIORIDADES JP 2010-156122 DE 08/07/2010, JP 2010-174915 DE 03/08/2010, JP 2010-230806 DE 13/10/2010, JP 2010-230808, JP 2010-269823 DE 02/12/2010 E JP 2010-269824 DE 02/12/2010 OU DECLARACAO CONTENDO, OBRIGATORIAMENTE, TODOS OS DADOS IDENTIFICADORES DESTA (DEPOSITANTE(S), INVENTOR(ES), NUMERO DE REGISTRO, DATA DE DEPOSITO E TITULO), CON |
|
| ENP | Entry into the national phase |
Ref document number: 112013000481 Country of ref document: BR Kind code of ref document: A2 Effective date: 20130108 |