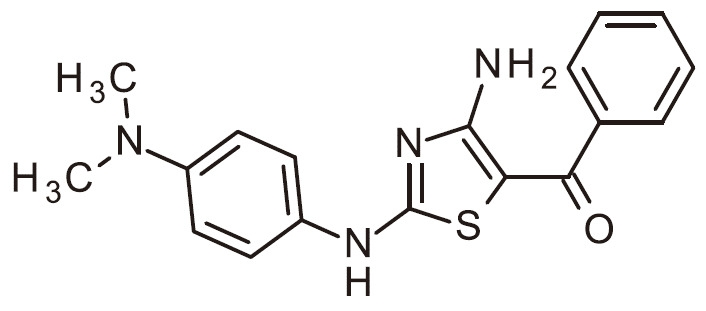
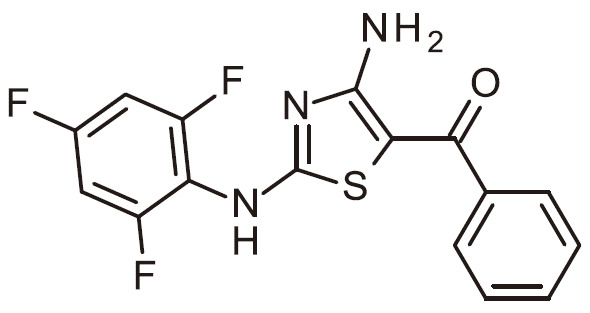
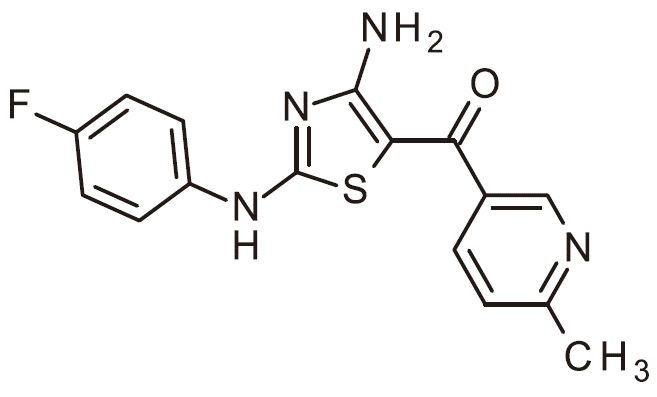
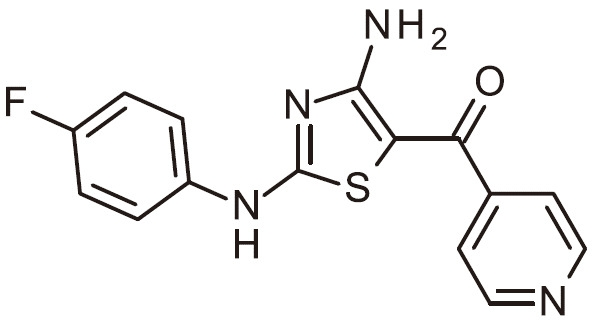
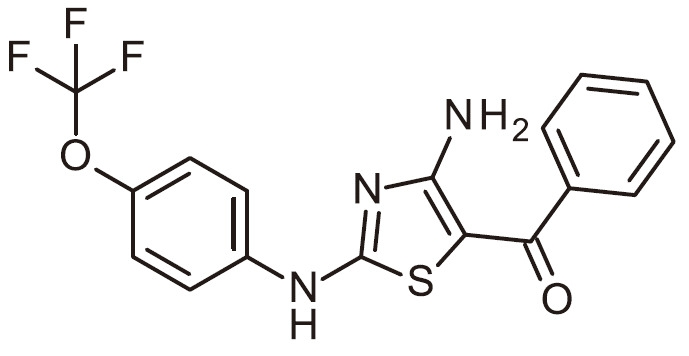
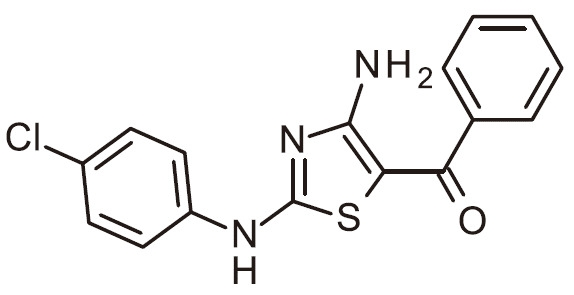
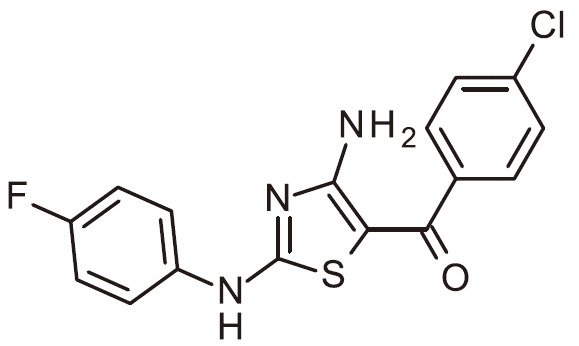
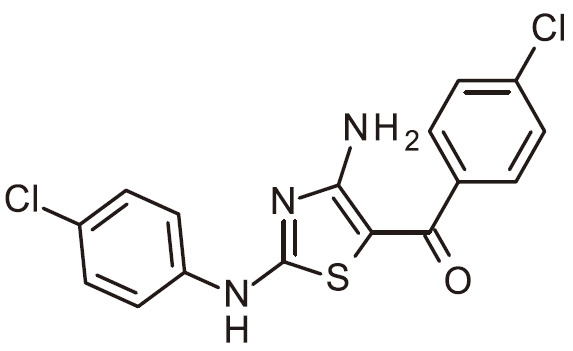
TW202200552A - 作為用於免疫活化之DGKζ抑制劑之經取代胺基噻唑 - Google Patents
作為用於免疫活化之DGKζ抑制劑之經取代胺基噻唑 Download PDFInfo
- Publication number
- TW202200552A TW202200552A TW110114675A TW110114675A TW202200552A TW 202200552 A TW202200552 A TW 202200552A TW 110114675 A TW110114675 A TW 110114675A TW 110114675 A TW110114675 A TW 110114675A TW 202200552 A TW202200552 A TW 202200552A
- Authority
- TW
- Taiwan
- Prior art keywords
- amino
- group
- anilino
- thiazol
- alkyl
- Prior art date
Links
- 239000003112 inhibitor Substances 0.000 title claims description 14
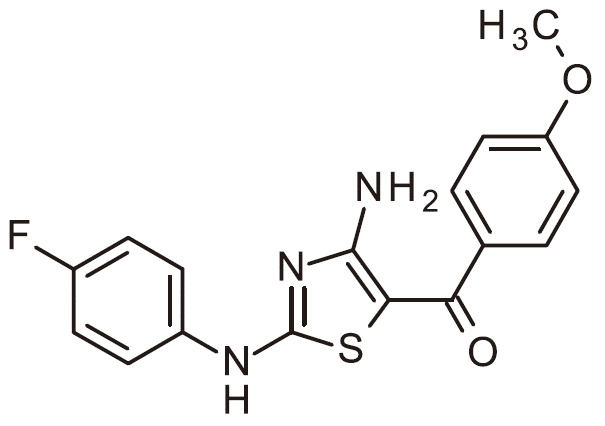
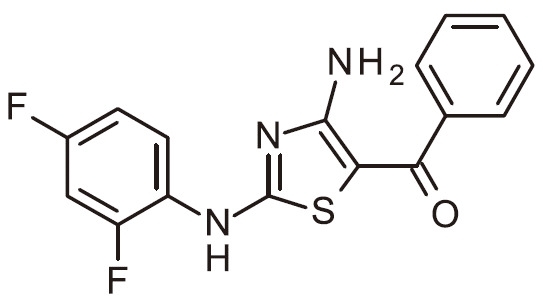
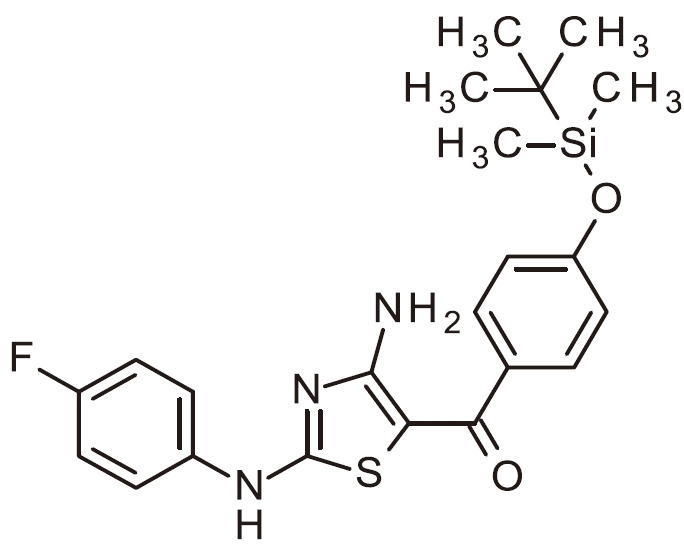
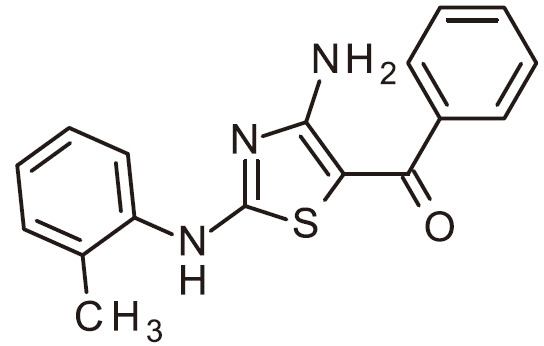
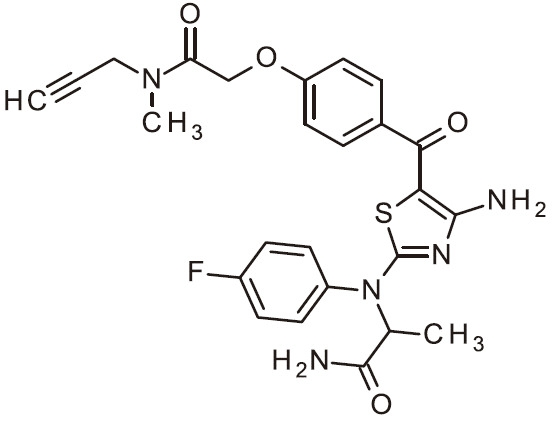
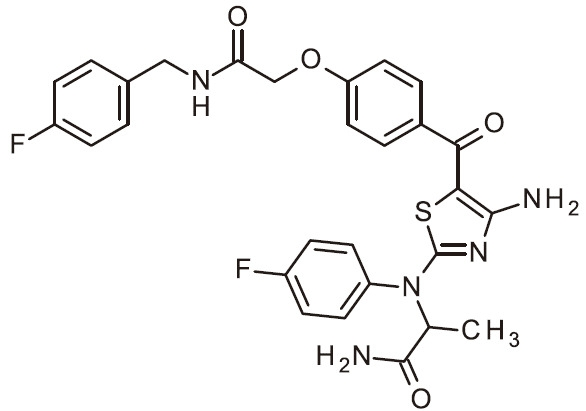
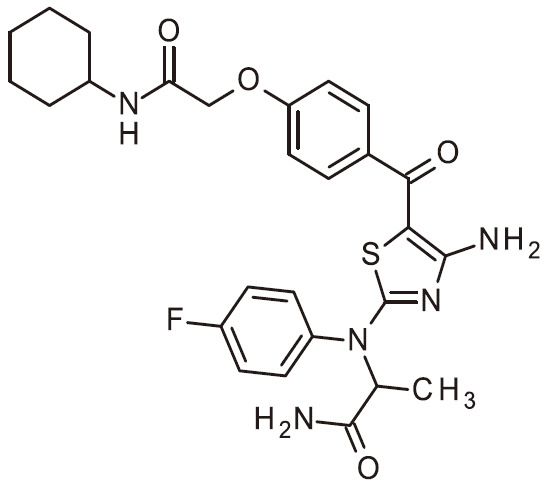
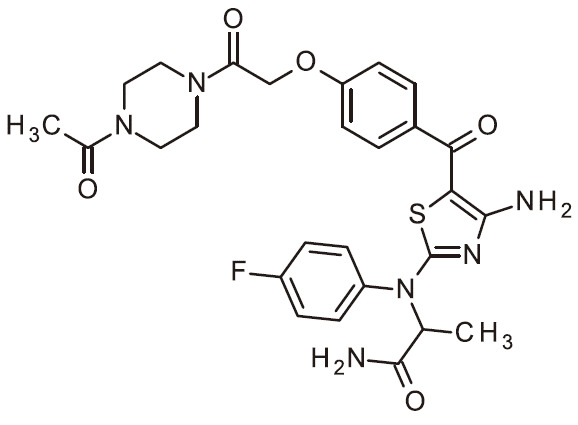
- RAIPHJJURHTUIC-UHFFFAOYSA-N 1,3-thiazol-2-amine Chemical class NC1=NC=CS1 RAIPHJJURHTUIC-UHFFFAOYSA-N 0.000 title abstract description 7
- 230000005934 immune activation Effects 0.000 title 1
- 150000001875 compounds Chemical class 0.000 claims abstract description 333
- 238000011282 treatment Methods 0.000 claims abstract description 21
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims abstract description 19
- 239000008194 pharmaceutical composition Substances 0.000 claims abstract description 9
- 201000010099 disease Diseases 0.000 claims abstract description 6
- 239000004480 active ingredient Substances 0.000 claims abstract description 5
- 238000011321 prophylaxis Methods 0.000 claims abstract description 4
- 125000001424 substituent group Chemical group 0.000 claims description 451
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims description 388
- -1 cyano, methyl Chemical group 0.000 claims description 382
- 239000000203 mixture Substances 0.000 claims description 243
- 229910052731 fluorine Inorganic materials 0.000 claims description 235
- 150000003839 salts Chemical class 0.000 claims description 233
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims description 227
- 125000001153 fluoro group Chemical group F* 0.000 claims description 224
- 239000012453 solvate Substances 0.000 claims description 212
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims description 210
- 125000000592 heterocycloalkyl group Chemical group 0.000 claims description 202
- 150000004677 hydrates Chemical class 0.000 claims description 201
- 125000005843 halogen group Chemical group 0.000 claims description 194
- 150000001204 N-oxides Chemical class 0.000 claims description 184
- 229910052801 chlorine Inorganic materials 0.000 claims description 182
- 125000001309 chloro group Chemical group Cl* 0.000 claims description 176
- 229910052757 nitrogen Inorganic materials 0.000 claims description 173
- 125000004433 nitrogen atom Chemical group N* 0.000 claims description 168
- 125000004093 cyano group Chemical group *C#N 0.000 claims description 166
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 claims description 138
- 229910052799 carbon Inorganic materials 0.000 claims description 121
- 125000002023 trifluoromethyl group Chemical group FC(F)(F)* 0.000 claims description 112
- 125000002950 monocyclic group Chemical group 0.000 claims description 108
- 125000002887 hydroxy group Chemical group [H]O* 0.000 claims description 99
- 125000004076 pyridyl group Chemical group 0.000 claims description 99
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 claims description 95
- XEEYBQQBJWHFJM-UHFFFAOYSA-N Iron Chemical compound [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 claims description 90
- CYRMSUTZVYGINF-UHFFFAOYSA-N trichlorofluoromethane Chemical compound FC(Cl)(Cl)Cl CYRMSUTZVYGINF-UHFFFAOYSA-N 0.000 claims description 89
- 125000002619 bicyclic group Chemical group 0.000 claims description 85
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 claims description 76
- PXBRQCKWGAHEHS-UHFFFAOYSA-N dichlorodifluoromethane Chemical compound FC(F)(Cl)Cl PXBRQCKWGAHEHS-UHFFFAOYSA-N 0.000 claims description 70
- 125000004432 carbon atom Chemical group C* 0.000 claims description 68
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical group [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 claims description 65
- 125000005073 adamantyl group Chemical group C12(CC3CC(CC(C1)C3)C2)* 0.000 claims description 60
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 claims description 60
- 125000001313 C5-C10 heteroaryl group Chemical group 0.000 claims description 53
- 125000000876 trifluoromethoxy group Chemical group FC(F)(F)O* 0.000 claims description 53
- 125000000951 phenoxy group Chemical group [H]C1=C([H])C([H])=C(O*)C([H])=C1[H] 0.000 claims description 48
- 239000011737 fluorine Substances 0.000 claims description 46
- 125000004765 (C1-C4) haloalkyl group Chemical group 0.000 claims description 43
- 239000000460 chlorine Substances 0.000 claims description 42
- 125000006645 (C3-C4) cycloalkyl group Chemical group 0.000 claims description 33
- 125000001028 difluoromethyl group Chemical group [H]C(F)(F)* 0.000 claims description 29
- 125000001072 heteroaryl group Chemical group 0.000 claims description 29
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 claims description 28
- 150000003254 radicals Chemical class 0.000 claims description 26
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 claims description 25
- 125000005913 (C3-C6) cycloalkyl group Chemical group 0.000 claims description 24
- 206010028980 Neoplasm Diseases 0.000 claims description 24
- 125000002915 carbonyl group Chemical group [*:2]C([*:1])=O 0.000 claims description 24
- 125000001624 naphthyl group Chemical group 0.000 claims description 24
- 229910052760 oxygen Inorganic materials 0.000 claims description 23
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 claims description 20
- 125000004767 (C1-C4) haloalkoxy group Chemical group 0.000 claims description 18
- 125000002853 C1-C4 hydroxyalkyl group Chemical group 0.000 claims description 17
- 201000011510 cancer Diseases 0.000 claims description 17
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical group C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 claims description 14
- 239000001301 oxygen Substances 0.000 claims description 13
- 125000000171 (C1-C6) haloalkyl group Chemical group 0.000 claims description 12
- 125000006273 (C1-C3) alkyl group Chemical group 0.000 claims description 11
- 125000003226 pyrazolyl group Chemical group 0.000 claims description 11
- 125000004178 (C1-C4) alkyl group Chemical group 0.000 claims description 9
- 125000006163 5-membered heteroaryl group Chemical group 0.000 claims description 9
- 125000006570 (C5-C6) heteroaryl group Chemical group 0.000 claims description 8
- 125000004429 atom Chemical group 0.000 claims description 8
- 239000003814 drug Substances 0.000 claims description 8
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 claims description 7
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 claims description 7
- 238000002360 preparation method Methods 0.000 claims description 7
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Chemical group COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 claims description 7
- 229910052794 bromium Inorganic materials 0.000 claims description 6
- 125000004737 (C1-C6) haloalkoxy group Chemical group 0.000 claims description 5
- 125000006164 6-membered heteroaryl group Chemical group 0.000 claims description 5
- 230000028993 immune response Effects 0.000 claims description 5
- 230000011664 signaling Effects 0.000 claims description 5
- FZWLAAWBMGSTSO-UHFFFAOYSA-N Thiazole Chemical compound C1=CSC=N1 FZWLAAWBMGSTSO-UHFFFAOYSA-N 0.000 claims description 4
- 229910052739 hydrogen Inorganic materials 0.000 claims description 4
- 239000001257 hydrogen Substances 0.000 claims description 4
- 125000006677 (C1-C3) haloalkoxy group Chemical group 0.000 claims description 3
- 239000007983 Tris buffer Substances 0.000 claims description 3
- 230000001594 aberrant effect Effects 0.000 claims description 3
- 125000004785 fluoromethoxy group Chemical group [H]C([H])(F)O* 0.000 claims description 3
- 238000006467 substitution reaction Methods 0.000 claims description 3
- YZCKVEUIGOORGS-UHFFFAOYSA-N Hydrogen atom Chemical compound [H] YZCKVEUIGOORGS-UHFFFAOYSA-N 0.000 claims description 2
- 230000006806 disease prevention Effects 0.000 claims description 2
- QLNJFJADRCOGBJ-UHFFFAOYSA-N propionamide Chemical compound CCC(N)=O QLNJFJADRCOGBJ-UHFFFAOYSA-N 0.000 claims 125
- 229940080818 propionamide Drugs 0.000 claims 125
- 125000000437 thiazol-2-yl group Chemical group [H]C1=C([H])N=C(*)S1 0.000 claims 100
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 claims 24
- 125000002490 anilino group Chemical group [H]N(*)C1=C([H])C([H])=C([H])C([H])=C1[H] 0.000 claims 23
- LKJPYSCBVHEWIU-UHFFFAOYSA-N N-[4-cyano-3-(trifluoromethyl)phenyl]-3-[(4-fluorophenyl)sulfonyl]-2-hydroxy-2-methylpropanamide Chemical compound C=1C=C(C#N)C(C(F)(F)F)=CC=1NC(=O)C(O)(C)CS(=O)(=O)C1=CC=C(F)C=C1 LKJPYSCBVHEWIU-UHFFFAOYSA-N 0.000 claims 11
- 125000000250 methylamino group Chemical group [H]N(*)C([H])([H])[H] 0.000 claims 8
- 125000001301 ethoxy group Chemical group [H]C([H])([H])C([H])([H])O* 0.000 claims 7
- 125000005825 oxyethoxy group Chemical group [H]C([H])(O[*:1])C([H])([H])O[*:2] 0.000 claims 7
- FZZMTSNZRBFGGU-UHFFFAOYSA-N 2-chloro-7-fluoroquinazolin-4-amine Chemical compound FC1=CC=C2C(N)=NC(Cl)=NC2=C1 FZZMTSNZRBFGGU-UHFFFAOYSA-N 0.000 claims 6
- KXDAEFPNCMNJSK-UHFFFAOYSA-N Benzamide Chemical compound NC(=O)C1=CC=CC=C1 KXDAEFPNCMNJSK-UHFFFAOYSA-N 0.000 claims 6
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 claims 6
- WGQKYBSKWIADBV-UHFFFAOYSA-N benzylamine Chemical compound NCC1=CC=CC=C1 WGQKYBSKWIADBV-UHFFFAOYSA-N 0.000 claims 6
- ATUOYWHBWRKTHZ-UHFFFAOYSA-N dimethylmethane Natural products CCC ATUOYWHBWRKTHZ-UHFFFAOYSA-N 0.000 claims 5
- 239000001294 propane Substances 0.000 claims 5
- 125000002252 acyl group Chemical group 0.000 claims 4
- MTZQAGJQAFMTAQ-UHFFFAOYSA-N ethyl benzoate Chemical compound CCOC(=O)C1=CC=CC=C1 MTZQAGJQAFMTAQ-UHFFFAOYSA-N 0.000 claims 4
- 125000000031 ethylamino group Chemical group [H]C([H])([H])C([H])([H])N([H])[*] 0.000 claims 4
- 229940076838 Immune checkpoint inhibitor Drugs 0.000 claims 3
- 102000037984 Inhibitory immune checkpoint proteins Human genes 0.000 claims 3
- 108091008026 Inhibitory immune checkpoint proteins Proteins 0.000 claims 3
- 125000002777 acetyl group Chemical group [H]C([H])([H])C(*)=O 0.000 claims 3
- 239000012274 immune-checkpoint protein inhibitor Substances 0.000 claims 3
- ZHNUHDYFZUAESO-UHFFFAOYSA-N Formamide Chemical compound NC=O ZHNUHDYFZUAESO-UHFFFAOYSA-N 0.000 claims 2
- AHLPHDHHMVZTML-BYPYZUCNSA-N L-Ornithine Chemical compound NCCC[C@H](N)C(O)=O AHLPHDHHMVZTML-BYPYZUCNSA-N 0.000 claims 2
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 claims 2
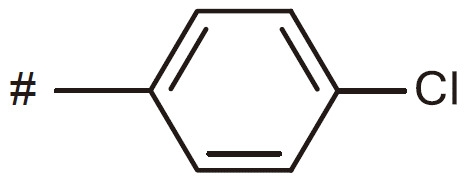
- 125000003854 p-chlorophenyl group Chemical group [H]C1=C([H])C(*)=C([H])C([H])=C1Cl 0.000 claims 2
- 125000004182 2-chlorophenyl group Chemical group [H]C1=C([H])C(Cl)=C(*)C([H])=C1[H] 0.000 claims 1
- 125000004198 2-fluorophenyl group Chemical group [H]C1=C([H])C(F)=C(*)C([H])=C1[H] 0.000 claims 1
- 125000004204 2-methoxyphenyl group Chemical group [H]C1=C([H])C(*)=C(OC([H])([H])[H])C([H])=C1[H] 0.000 claims 1
- 125000004179 3-chlorophenyl group Chemical group [H]C1=C([H])C(*)=C([H])C(Cl)=C1[H] 0.000 claims 1
- 125000004207 3-methoxyphenyl group Chemical group [H]C1=C([H])C(*)=C([H])C(OC([H])([H])[H])=C1[H] 0.000 claims 1
- 125000001255 4-fluorophenyl group Chemical group [H]C1=C([H])C(*)=C([H])C([H])=C1F 0.000 claims 1
- 125000004172 4-methoxyphenyl group Chemical group [H]C1=C([H])C(OC([H])([H])[H])=C([H])C([H])=C1* 0.000 claims 1
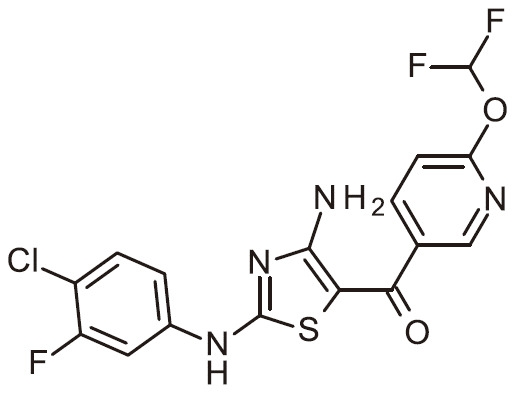
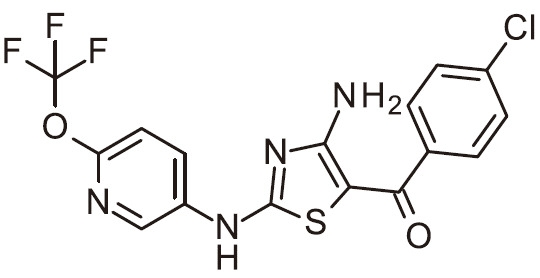
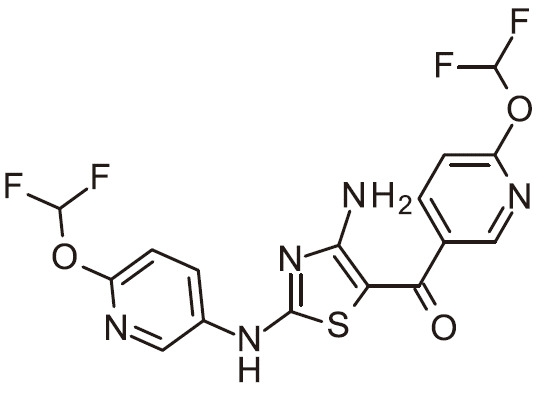
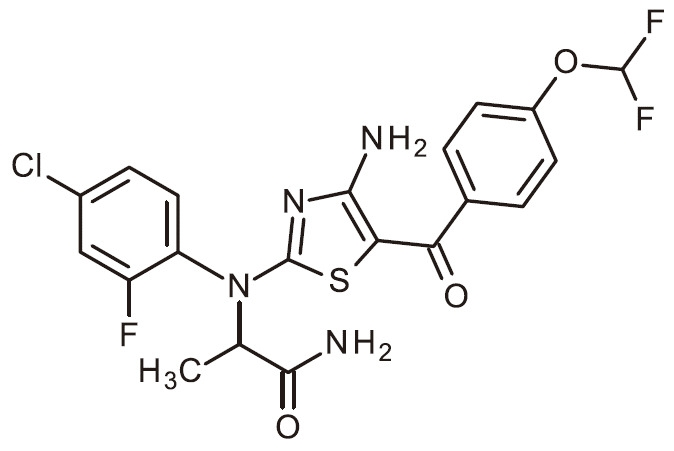
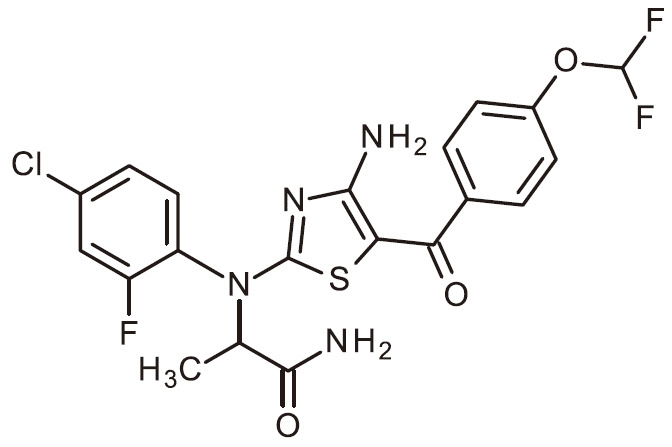
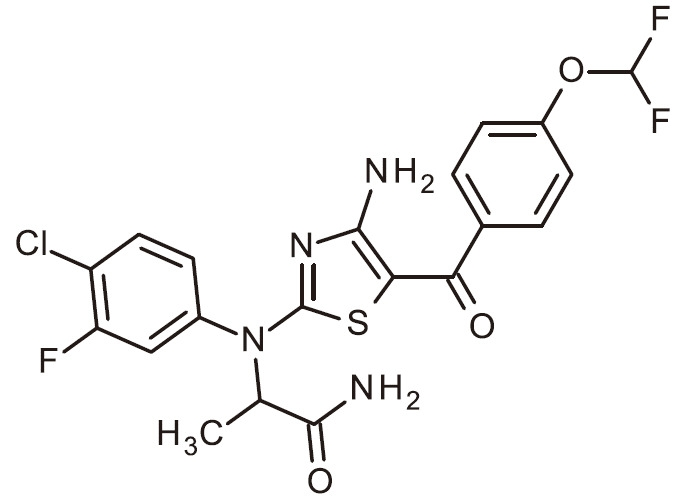
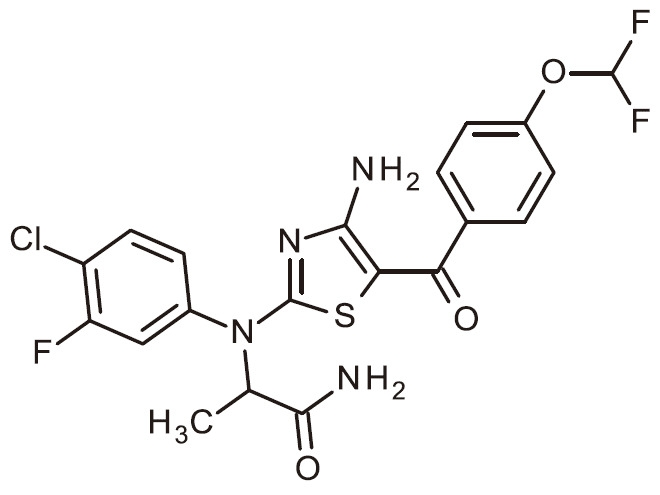
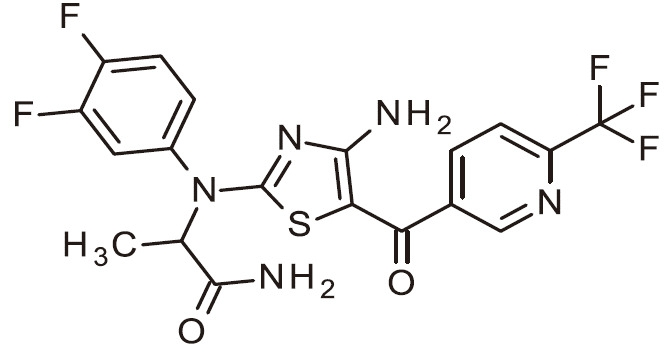
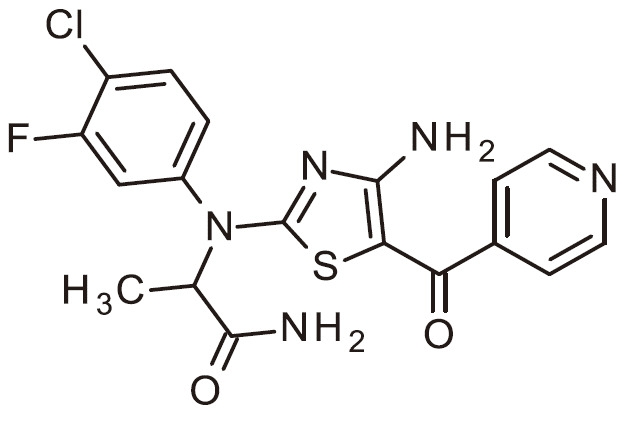
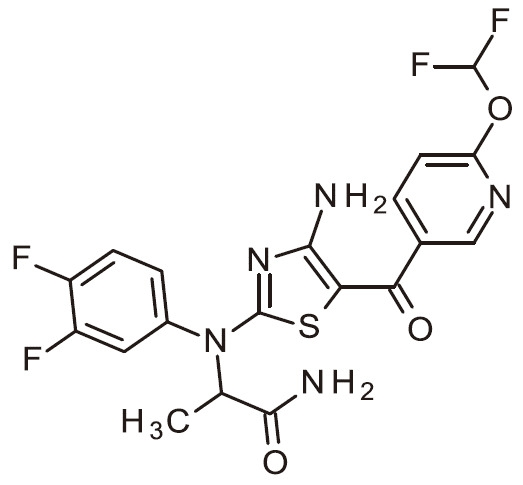
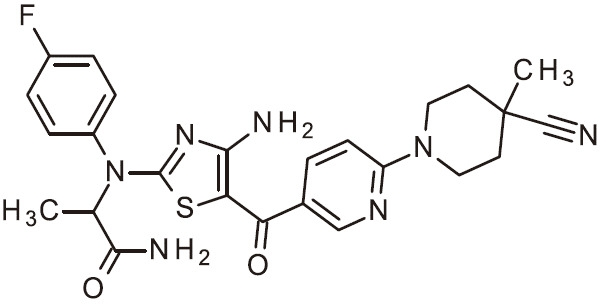
- FJKJWNDFKBCKQU-SECBINFHSA-N C[C@H](C(N)=O)N(C1=NC(N)=C(C(C2=CC=NC=C2)=O)S1)C(C=C1)=CC(Cl)=C1F Chemical compound C[C@H](C(N)=O)N(C1=NC(N)=C(C(C2=CC=NC=C2)=O)S1)C(C=C1)=CC(Cl)=C1F FJKJWNDFKBCKQU-SECBINFHSA-N 0.000 claims 1
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 claims 1
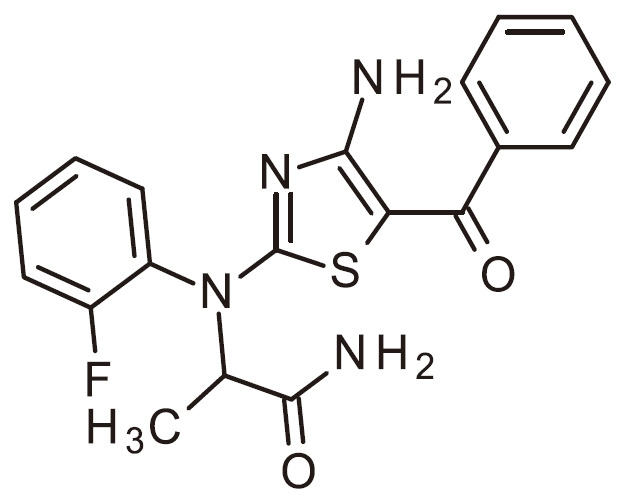
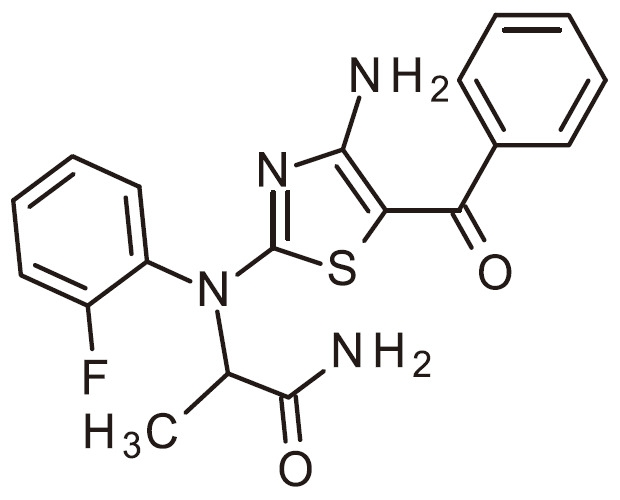
- HCQNTLGGZRFSKW-UHFFFAOYSA-N NC=1N=C(SC=1C(=O)C1=CC(=NC=C1)C(F)F)N(C1=CC=C(C=C1)F)C(C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C1=CC(=NC=C1)C(F)F)N(C1=CC=C(C=C1)F)C(C(=O)N)C HCQNTLGGZRFSKW-UHFFFAOYSA-N 0.000 claims 1
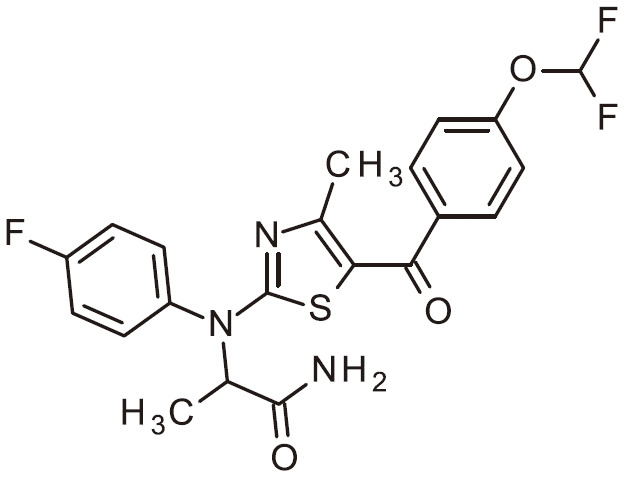
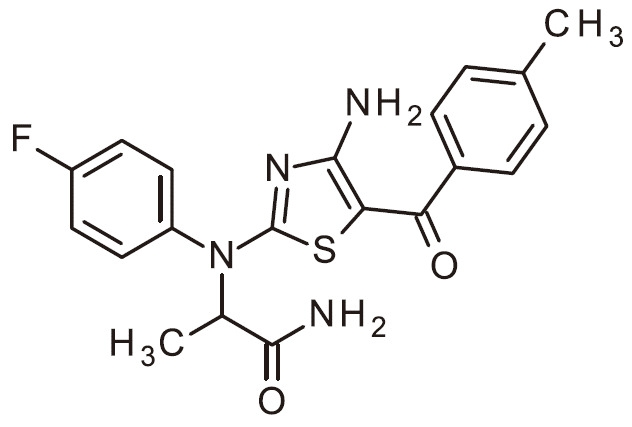
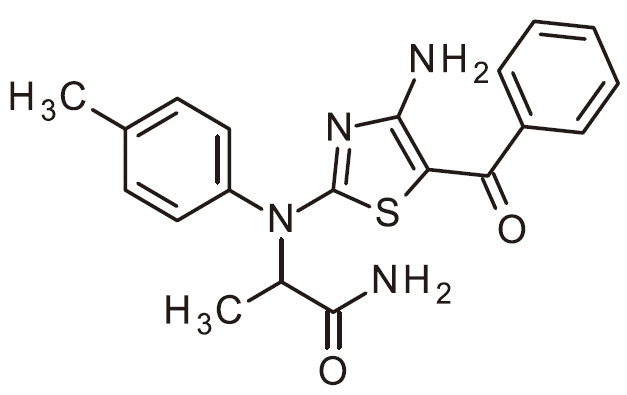
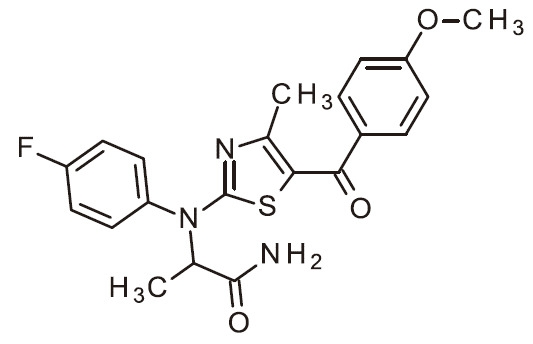
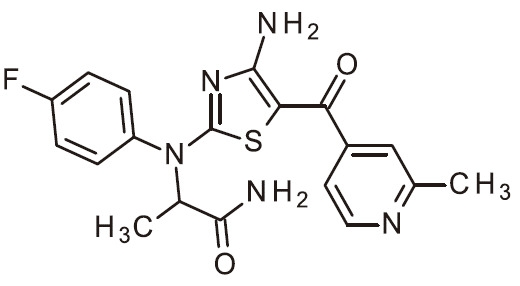
- NUKUFDBSXQTZTO-UHFFFAOYSA-N NC=1N=C(SC=1C(=O)C1=CC(=NC=C1)C)N(C1=CC=C(C=C1)F)C(C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C1=CC(=NC=C1)C)N(C1=CC=C(C=C1)F)C(C(=O)N)C NUKUFDBSXQTZTO-UHFFFAOYSA-N 0.000 claims 1
- NUKUFDBSXQTZTO-LLVKDONJSA-N NC=1N=C(SC=1C(=O)C1=CC(=NC=C1)C)N(C1=CC=C(C=C1)F)[C@@H](C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C1=CC(=NC=C1)C)N(C1=CC=C(C=C1)F)[C@@H](C(=O)N)C NUKUFDBSXQTZTO-LLVKDONJSA-N 0.000 claims 1
- NUKUFDBSXQTZTO-NSHDSACASA-N NC=1N=C(SC=1C(=O)C1=CC(=NC=C1)C)N(C1=CC=C(C=C1)F)[C@H](C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C1=CC(=NC=C1)C)N(C1=CC=C(C=C1)F)[C@H](C(=O)N)C NUKUFDBSXQTZTO-NSHDSACASA-N 0.000 claims 1
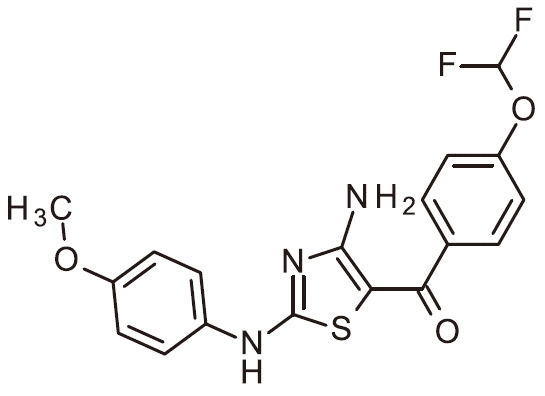
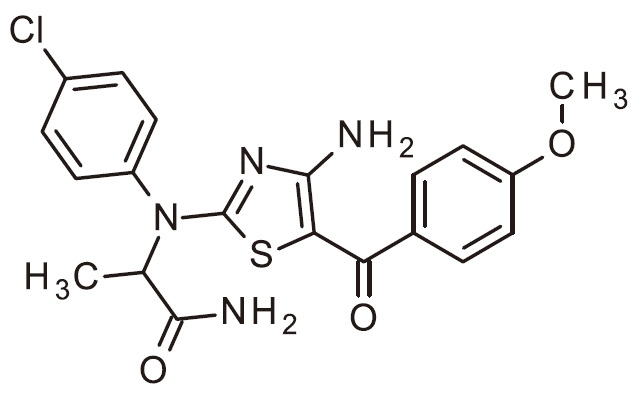
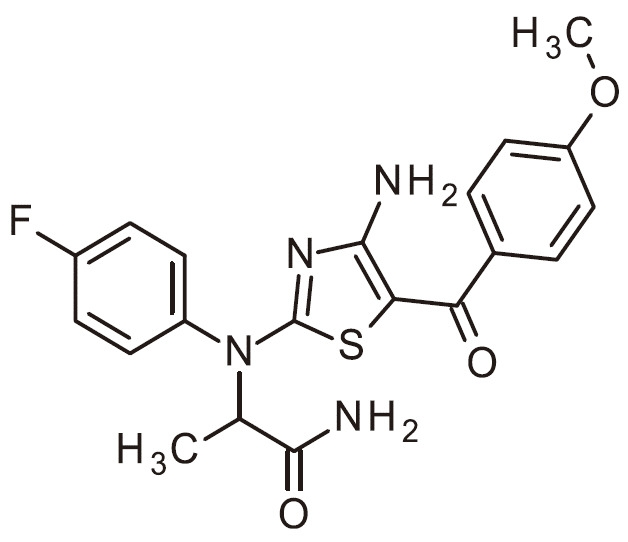
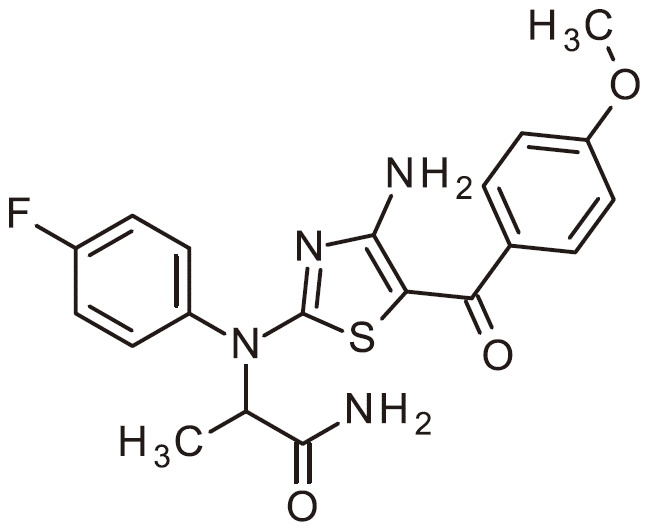
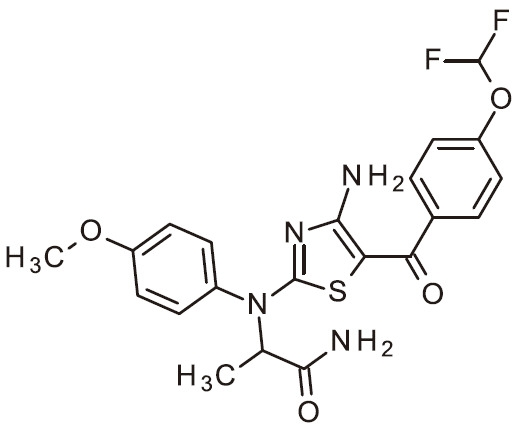
- UIPQNDNKPARBFM-UHFFFAOYSA-N NC=1N=C(SC=1C(=O)C1=CC(=NC=C1)OC)N(C1=CC=C(C=C1)F)C(C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C1=CC(=NC=C1)OC)N(C1=CC=C(C=C1)F)C(C(=O)N)C UIPQNDNKPARBFM-UHFFFAOYSA-N 0.000 claims 1
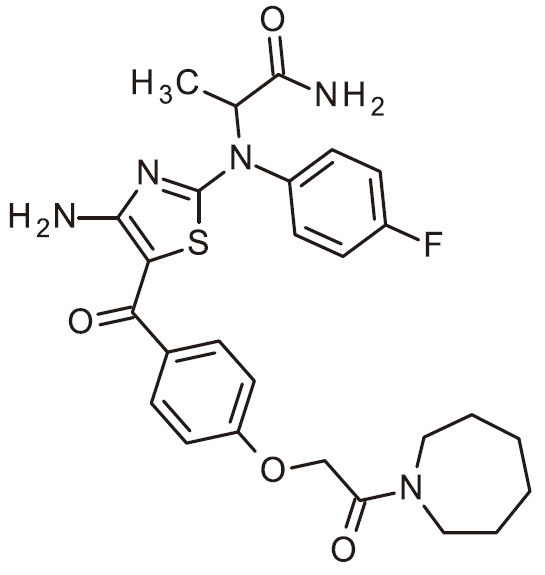
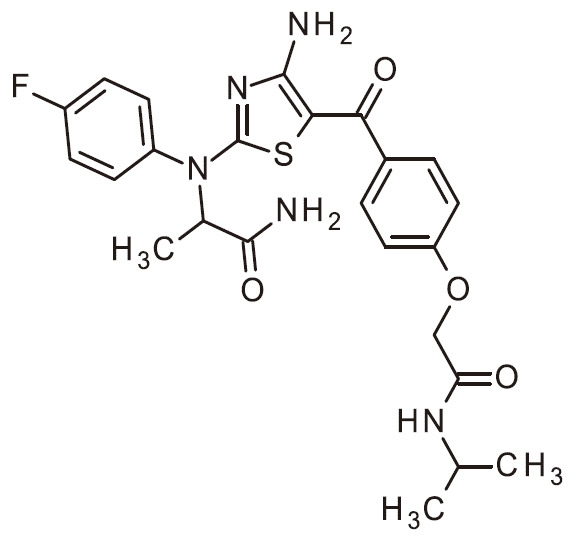
- JLDUOHKKWYKZJT-UHFFFAOYSA-N NC=1N=C(SC=1C(=O)C1=CC=C(C(=O)NC2CCCCC2)C=C1)N(C1=CC=C(C=C1)F)C(C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C1=CC=C(C(=O)NC2CCCCC2)C=C1)N(C1=CC=C(C=C1)F)C(C(=O)N)C JLDUOHKKWYKZJT-UHFFFAOYSA-N 0.000 claims 1
- PGXGRZXFBHHISM-PZORYLMUSA-N NC=1N=C(SC=1C(=O)C1=CC=C(C(=O)NC[C@@H](C)O)C=C1)N(C1=CC=C(C=C1)F)C(C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C1=CC=C(C(=O)NC[C@@H](C)O)C=C1)N(C1=CC=C(C=C1)F)C(C(=O)N)C PGXGRZXFBHHISM-PZORYLMUSA-N 0.000 claims 1
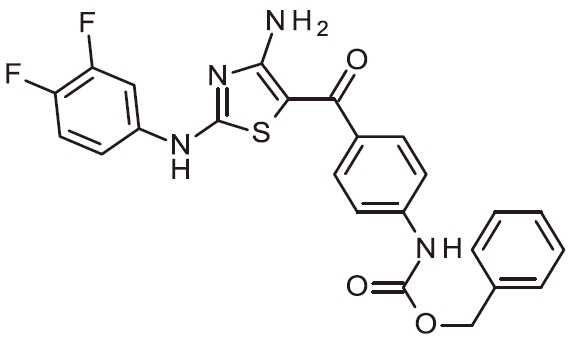
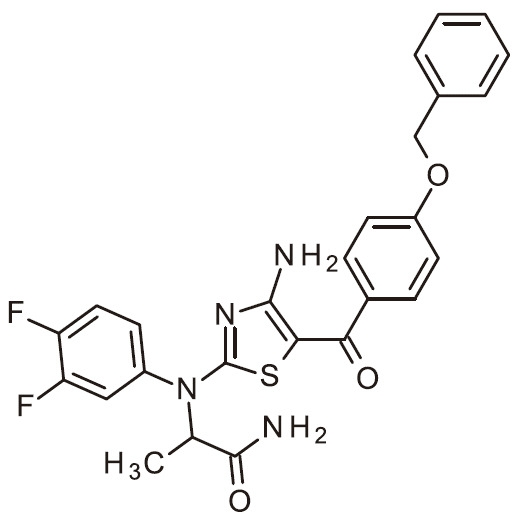
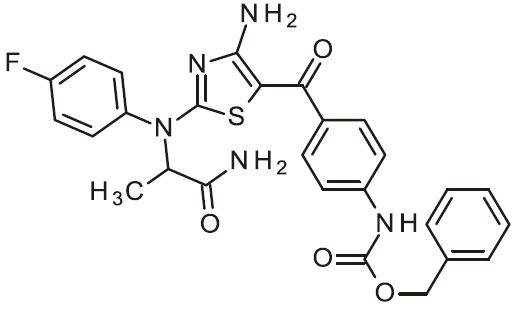
- QVXAWMPZFCEVDL-INIZCTEOSA-N NC=1N=C(SC=1C(=O)C1=CC=C(C=C1)NC(OCC1=CC=CC=C1)=O)N(C1=CC=C(C=C1)F)[C@H](C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C1=CC=C(C=C1)NC(OCC1=CC=CC=C1)=O)N(C1=CC=C(C=C1)F)[C@H](C(=O)N)C QVXAWMPZFCEVDL-INIZCTEOSA-N 0.000 claims 1
- BYNAUJSSCAFXLO-UHFFFAOYSA-N NC=1N=C(SC=1C(=O)C1=CC=C(OCC(=O)O)C=C1)N(C1=CC=C(C=C1)F)C(C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C1=CC=C(OCC(=O)O)C=C1)N(C1=CC=C(C=C1)F)C(C(=O)N)C BYNAUJSSCAFXLO-UHFFFAOYSA-N 0.000 claims 1
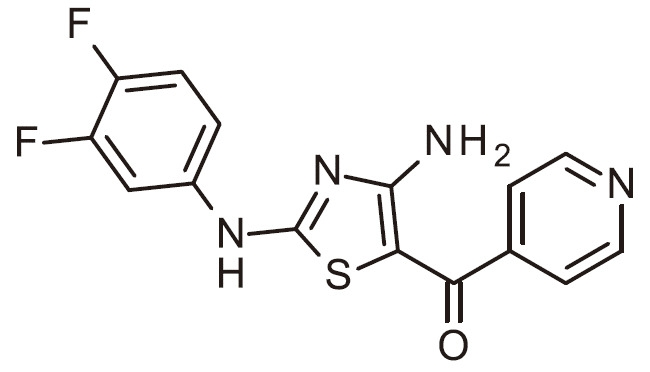
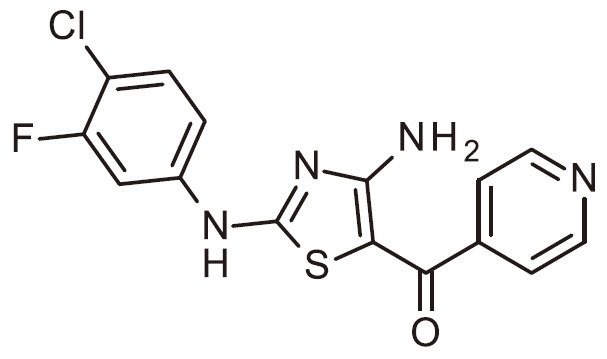
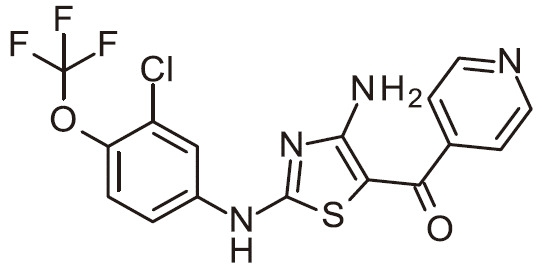
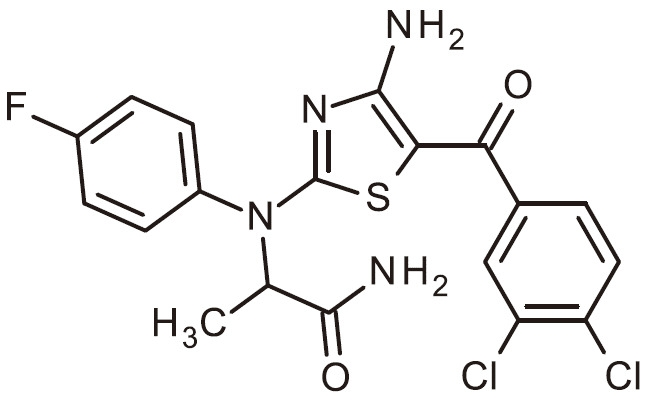
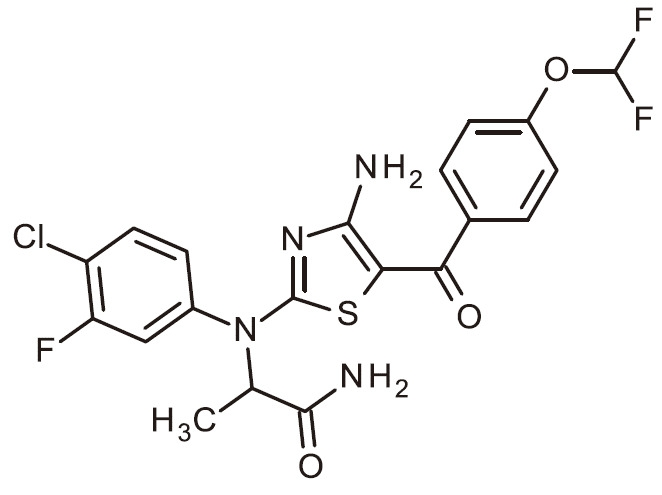
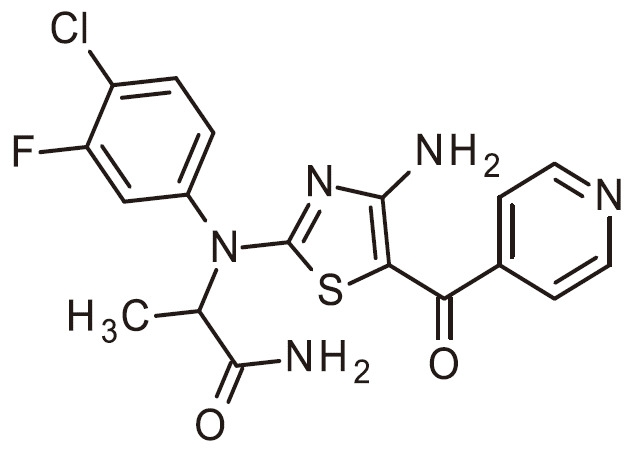
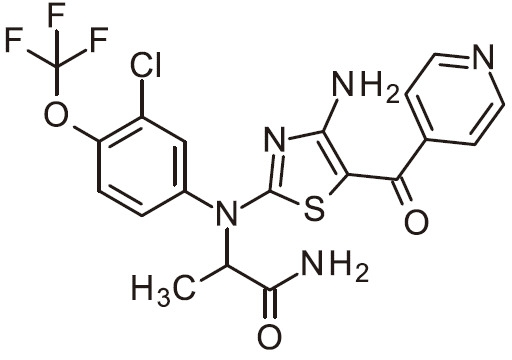
- NQZAVLBRQZIWEM-UHFFFAOYSA-N NC=1N=C(SC=1C(=O)C1=CC=NC=C1)N(C1=CC(=C(C=C1)Cl)F)C(C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C1=CC=NC=C1)N(C1=CC(=C(C=C1)Cl)F)C(C(=O)N)C NQZAVLBRQZIWEM-UHFFFAOYSA-N 0.000 claims 1
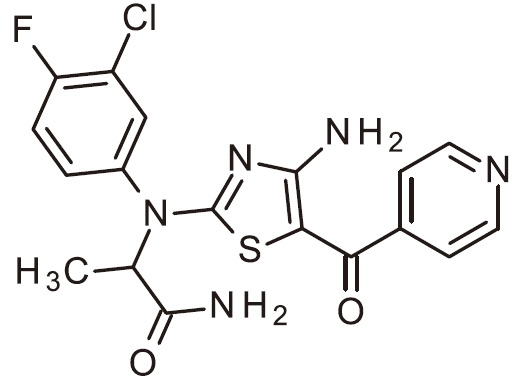
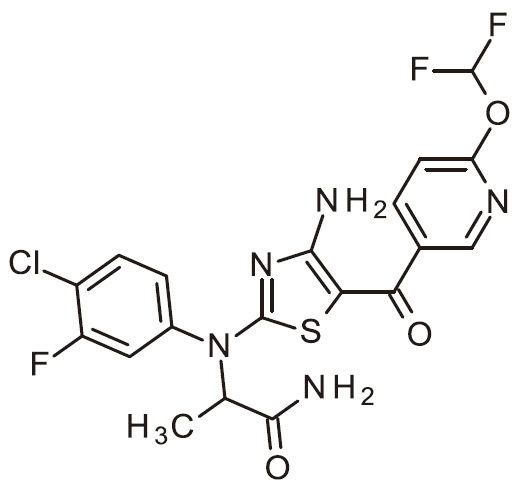
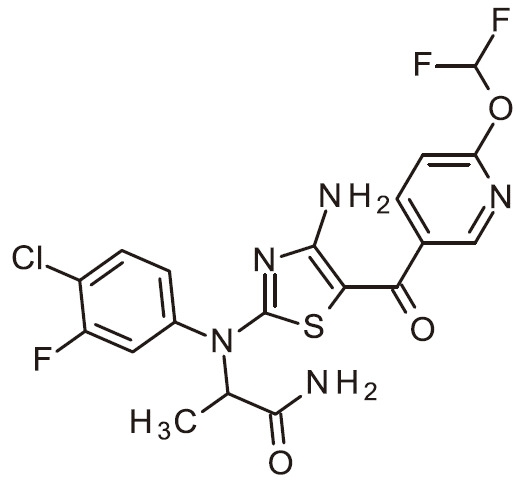
- FJKJWNDFKBCKQU-UHFFFAOYSA-N NC=1N=C(SC=1C(=O)C1=CC=NC=C1)N(C1=CC(=C(C=C1)F)Cl)C(C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C1=CC=NC=C1)N(C1=CC(=C(C=C1)F)Cl)C(C(=O)N)C FJKJWNDFKBCKQU-UHFFFAOYSA-N 0.000 claims 1
- FJKJWNDFKBCKQU-VIFPVBQESA-N NC=1N=C(SC=1C(=O)C1=CC=NC=C1)N(C1=CC(=C(C=C1)F)Cl)[C@H](C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C1=CC=NC=C1)N(C1=CC(=C(C=C1)F)Cl)[C@H](C(=O)N)C FJKJWNDFKBCKQU-VIFPVBQESA-N 0.000 claims 1
- TYGGQIPKCUJTGS-VIFPVBQESA-N NC=1N=C(SC=1C(=O)C1=CC=NC=C1)N(C1=CC(=C(C=C1)F)F)[C@H](C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C1=CC=NC=C1)N(C1=CC(=C(C=C1)F)F)[C@H](C(=O)N)C TYGGQIPKCUJTGS-VIFPVBQESA-N 0.000 claims 1
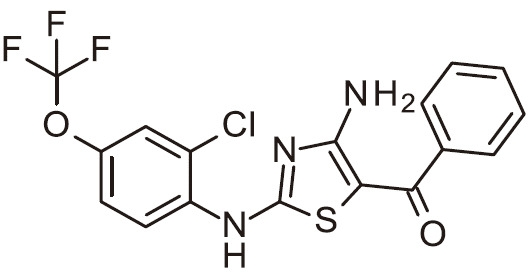
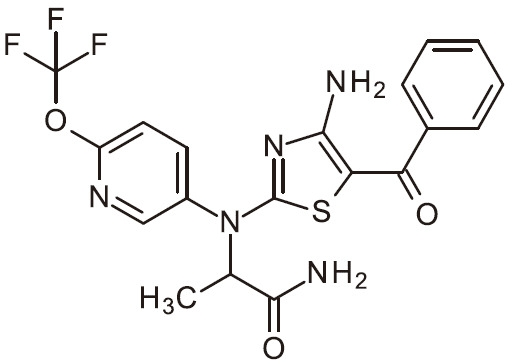
- JUWLQASUMOJISE-UHFFFAOYSA-N NC=1N=C(SC=1C(=O)C1=CC=NC=C1)N(C1=CC(=C(C=C1)OC(F)(F)F)Cl)C(C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C1=CC=NC=C1)N(C1=CC(=C(C=C1)OC(F)(F)F)Cl)C(C(=O)N)C JUWLQASUMOJISE-UHFFFAOYSA-N 0.000 claims 1
- DTSLZZSVLSYCNC-UHFFFAOYSA-N NC=1N=C(SC=1C(=O)C1=CC=NC=C1)N(C1=CC(=C(C=C1)OC(F)(F)F)F)C(C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C1=CC=NC=C1)N(C1=CC(=C(C=C1)OC(F)(F)F)F)C(C(=O)N)C DTSLZZSVLSYCNC-UHFFFAOYSA-N 0.000 claims 1
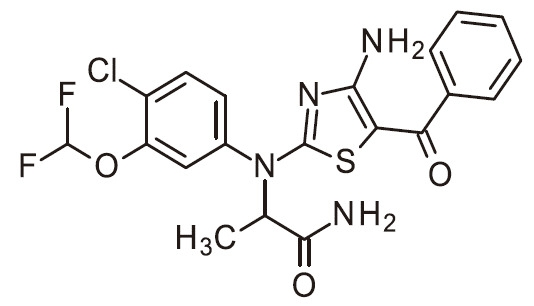
- ZFMHBTVEKUSADO-UHFFFAOYSA-N NC=1N=C(SC=1C(=O)C1=CC=NC=C1)N(C1=CC(=C(C=C1)OC(F)F)Cl)C(C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C1=CC=NC=C1)N(C1=CC(=C(C=C1)OC(F)F)Cl)C(C(=O)N)C ZFMHBTVEKUSADO-UHFFFAOYSA-N 0.000 claims 1
- XWSMVTOMGPLVJL-UHFFFAOYSA-N NC=1N=C(SC=1C(=O)C1=CC=NC=C1)N(C1=CC(=C(C=C1)OC(F)F)F)C(C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C1=CC=NC=C1)N(C1=CC(=C(C=C1)OC(F)F)F)C(C(=O)N)C XWSMVTOMGPLVJL-UHFFFAOYSA-N 0.000 claims 1
- JHZVQYFLJUHJKM-UHFFFAOYSA-N NC=1N=C(SC=1C(=O)C1=CC=NC=C1)N(C1=CC2=C(OC(O2)(F)F)C=C1)C(C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C1=CC=NC=C1)N(C1=CC2=C(OC(O2)(F)F)C=C1)C(C(=O)N)C JHZVQYFLJUHJKM-UHFFFAOYSA-N 0.000 claims 1
- CVUONGSFVJCHJG-UHFFFAOYSA-N NC=1N=C(SC=1C(=O)C1=CC=NC=C1)N(C1=CC=C(C=C1)Cl)C(C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C1=CC=NC=C1)N(C1=CC=C(C=C1)Cl)C(C(=O)N)C CVUONGSFVJCHJG-UHFFFAOYSA-N 0.000 claims 1
- CVUONGSFVJCHJG-SNVBAGLBSA-N NC=1N=C(SC=1C(=O)C1=CC=NC=C1)N(C1=CC=C(C=C1)Cl)[C@@H](C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C1=CC=NC=C1)N(C1=CC=C(C=C1)Cl)[C@@H](C(=O)N)C CVUONGSFVJCHJG-SNVBAGLBSA-N 0.000 claims 1
- CVUONGSFVJCHJG-JTQLQIEISA-N NC=1N=C(SC=1C(=O)C1=CC=NC=C1)N(C1=CC=C(C=C1)Cl)[C@H](C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C1=CC=NC=C1)N(C1=CC=C(C=C1)Cl)[C@H](C(=O)N)C CVUONGSFVJCHJG-JTQLQIEISA-N 0.000 claims 1
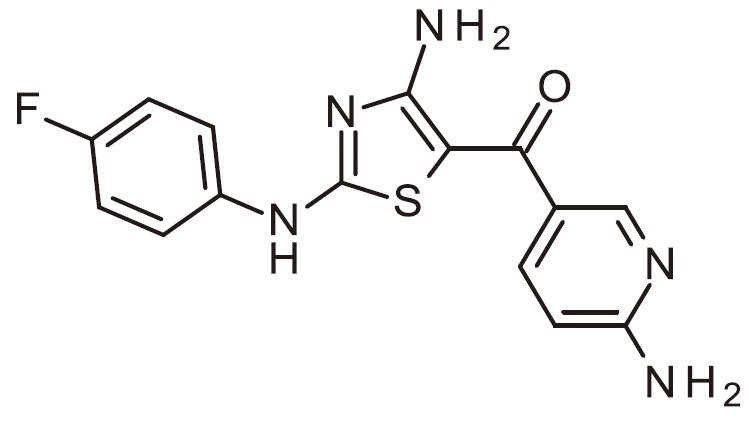
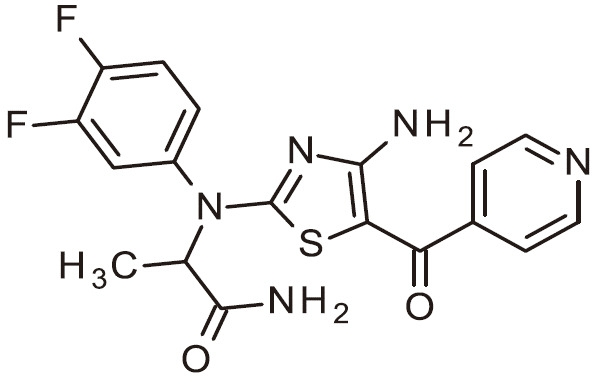
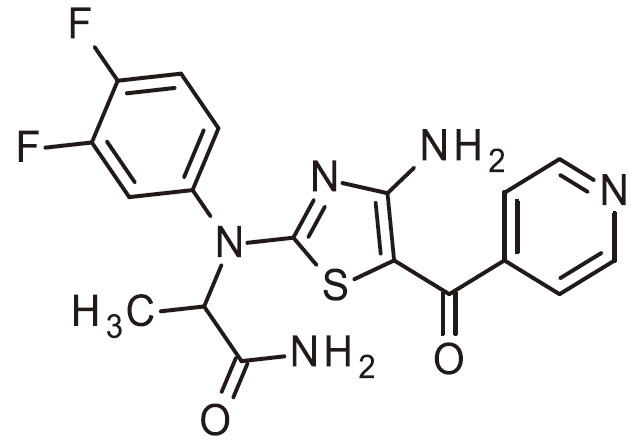
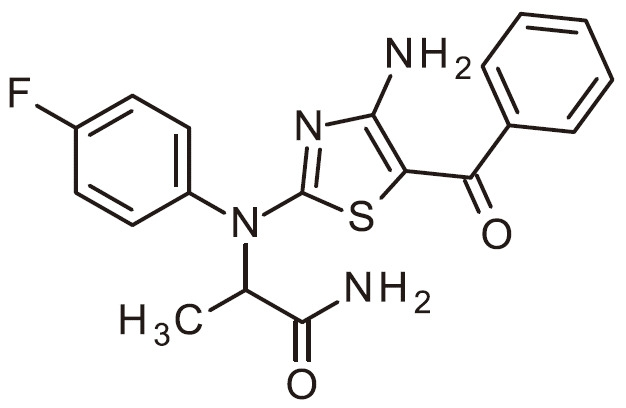
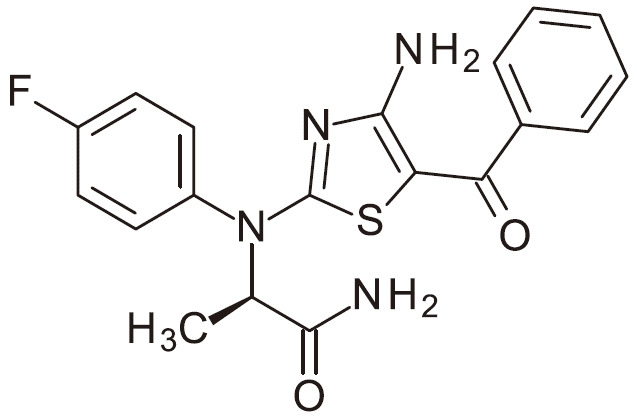
- ZLOPVRGPKHYVNC-UHFFFAOYSA-N NC=1N=C(SC=1C(=O)C1=CC=NC=C1)N(C1=CC=C(C=C1)F)C(C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C1=CC=NC=C1)N(C1=CC=C(C=C1)F)C(C(=O)N)C ZLOPVRGPKHYVNC-UHFFFAOYSA-N 0.000 claims 1
- PLVDRVQQRZQDHR-UHFFFAOYSA-N NC=1N=C(SC=1C(=O)C=1C=C2CCCC2=CC=1)N(C1=CC=C(C=C1)F)C(C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C=1C=C2CCCC2=CC=1)N(C1=CC=C(C=C1)F)C(C(=O)N)C PLVDRVQQRZQDHR-UHFFFAOYSA-N 0.000 claims 1
- OGIUCELXXSGFKR-UHFFFAOYSA-N NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)Br)N(C1=CC=C(C=C1)F)C(C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)Br)N(C1=CC=C(C=C1)F)C(C(=O)N)C OGIUCELXXSGFKR-UHFFFAOYSA-N 0.000 claims 1
- CBUQYHJELJLGFB-UHFFFAOYSA-N NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)C(F)(F)F)N(C1=CC(=C(C=C1)F)F)C(C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)C(F)(F)F)N(C1=CC(=C(C=C1)F)F)C(C(=O)N)C CBUQYHJELJLGFB-UHFFFAOYSA-N 0.000 claims 1
- CBUQYHJELJLGFB-MRVPVSSYSA-N NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)C(F)(F)F)N(C1=CC(=C(C=C1)F)F)[C@@H](C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)C(F)(F)F)N(C1=CC(=C(C=C1)F)F)[C@@H](C(=O)N)C CBUQYHJELJLGFB-MRVPVSSYSA-N 0.000 claims 1
- CBUQYHJELJLGFB-QMMMGPOBSA-N NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)C(F)(F)F)N(C1=CC(=C(C=C1)F)F)[C@H](C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)C(F)(F)F)N(C1=CC(=C(C=C1)F)F)[C@H](C(=O)N)C CBUQYHJELJLGFB-QMMMGPOBSA-N 0.000 claims 1
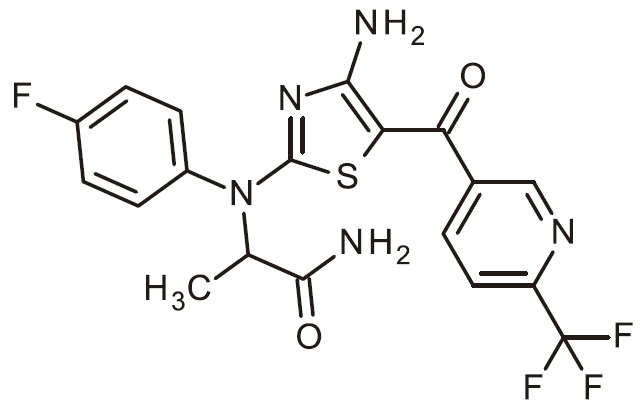
- XCBONNCKWYRONX-UHFFFAOYSA-N NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)C(F)(F)F)N(C1=CC=C(C=C1)F)C(C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)C(F)(F)F)N(C1=CC=C(C=C1)F)C(C(=O)N)C XCBONNCKWYRONX-UHFFFAOYSA-N 0.000 claims 1
- XCBONNCKWYRONX-SECBINFHSA-N NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)C(F)(F)F)N(C1=CC=C(C=C1)F)[C@@H](C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)C(F)(F)F)N(C1=CC=C(C=C1)F)[C@@H](C(=O)N)C XCBONNCKWYRONX-SECBINFHSA-N 0.000 claims 1
- XCBONNCKWYRONX-VIFPVBQESA-N NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)C(F)(F)F)N(C1=CC=C(C=C1)F)[C@H](C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)C(F)(F)F)N(C1=CC=C(C=C1)F)[C@H](C(=O)N)C XCBONNCKWYRONX-VIFPVBQESA-N 0.000 claims 1
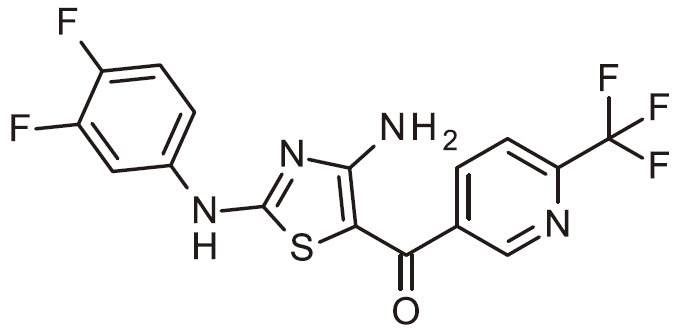
- WLQLJMQPNZYHGO-UHFFFAOYSA-N NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)C(F)F)N(C1=CC=C(C=C1)F)C(C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)C(F)F)N(C1=CC=C(C=C1)F)C(C(=O)N)C WLQLJMQPNZYHGO-UHFFFAOYSA-N 0.000 claims 1
- WUTAOWAQLYGSJN-UHFFFAOYSA-N NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)C)N(C1=CC=C(C=C1)F)C(C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)C)N(C1=CC=C(C=C1)F)C(C(=O)N)C WUTAOWAQLYGSJN-UHFFFAOYSA-N 0.000 claims 1
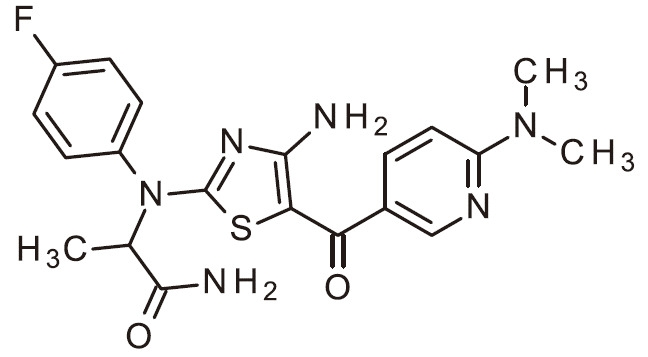
- PBKIUQJUTRXOJA-UHFFFAOYSA-N NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)N(C)C)N(C1=CC=C(C=C1)F)C(C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)N(C)C)N(C1=CC=C(C=C1)F)C(C(=O)N)C PBKIUQJUTRXOJA-UHFFFAOYSA-N 0.000 claims 1
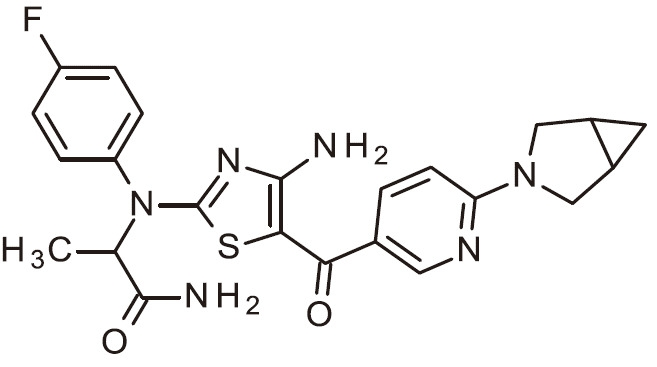
- DEWNJSAEJPGVNV-UHFFFAOYSA-N NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)N1CC2CC2C1)N(C1=CC=C(C=C1)F)C(C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)N1CC2CC2C1)N(C1=CC=C(C=C1)F)C(C(=O)N)C DEWNJSAEJPGVNV-UHFFFAOYSA-N 0.000 claims 1
- JDBVRJOZCUUBBI-UHFFFAOYSA-N NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)N1CC2CCC(C1)C2)N(C1=CC=C(C=C1)F)C(C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)N1CC2CCC(C1)C2)N(C1=CC=C(C=C1)F)C(C(=O)N)C JDBVRJOZCUUBBI-UHFFFAOYSA-N 0.000 claims 1
- OUOWQEYAAGSTMH-UHFFFAOYSA-N NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)N1CCC(CC1)(C)C#N)N(C1=CC=C(C=C1)F)C(C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)N1CCC(CC1)(C)C#N)N(C1=CC=C(C=C1)F)C(C(=O)N)C OUOWQEYAAGSTMH-UHFFFAOYSA-N 0.000 claims 1
- OUOWQEYAAGSTMH-OAHLLOKOSA-N NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)N1CCC(CC1)(C)C#N)N(C1=CC=C(C=C1)F)[C@@H](C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)N1CCC(CC1)(C)C#N)N(C1=CC=C(C=C1)F)[C@@H](C(=O)N)C OUOWQEYAAGSTMH-OAHLLOKOSA-N 0.000 claims 1
- PSUROJDOEHBQFF-UHFFFAOYSA-N NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)N1CCC(CC1)(F)F)N(C1=CC=C(C=C1)F)C(C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)N1CCC(CC1)(F)F)N(C1=CC=C(C=C1)F)C(C(=O)N)C PSUROJDOEHBQFF-UHFFFAOYSA-N 0.000 claims 1
- OFMKKGGLWMGCRM-UHFFFAOYSA-N NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)N1CCC(CC1)C(F)(F)F)N(C1=CC=C(C=C1)F)C(C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)N1CCC(CC1)C(F)(F)F)N(C1=CC=C(C=C1)F)C(C(=O)N)C OFMKKGGLWMGCRM-UHFFFAOYSA-N 0.000 claims 1
- XAJORIZXDUWHQT-UHFFFAOYSA-N NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)N1CCC(CC1)C1COC1)N(C1=CC=C(C=C1)F)C(C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)N1CCC(CC1)C1COC1)N(C1=CC=C(C=C1)F)C(C(=O)N)C XAJORIZXDUWHQT-UHFFFAOYSA-N 0.000 claims 1
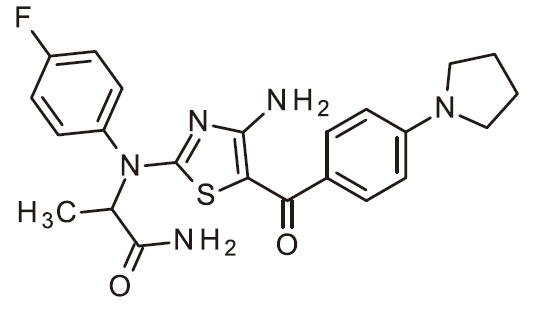
- AIYRSEPQZJXUED-UHFFFAOYSA-N NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)N1CCCCC1)N(C1=CC=C(C=C1)F)C(C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)N1CCCCC1)N(C1=CC=C(C=C1)F)C(C(=O)N)C AIYRSEPQZJXUED-UHFFFAOYSA-N 0.000 claims 1
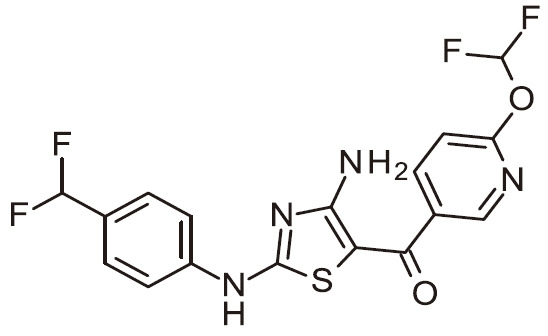
- JEVNKWFVOCUTNZ-UHFFFAOYSA-N NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)OC(F)F)N(C(C(=O)N)C)C1=CC2=C(OC(O2)(F)F)C=C1 Chemical compound NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)OC(F)F)N(C(C(=O)N)C)C1=CC2=C(OC(O2)(F)F)C=C1 JEVNKWFVOCUTNZ-UHFFFAOYSA-N 0.000 claims 1
- GEIUOTKSGDTINF-UHFFFAOYSA-N NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)OC(F)F)N(C(C(=O)N)C)C=1C=NC(=CC=1)OC(F)F Chemical compound NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)OC(F)F)N(C(C(=O)N)C)C=1C=NC(=CC=1)OC(F)F GEIUOTKSGDTINF-UHFFFAOYSA-N 0.000 claims 1
- PXMCGYNIQWLKKC-UHFFFAOYSA-N NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)OC(F)F)N(C1=CC(=C(C=C1)Cl)F)C(C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)OC(F)F)N(C1=CC(=C(C=C1)Cl)F)C(C(=O)N)C PXMCGYNIQWLKKC-UHFFFAOYSA-N 0.000 claims 1
- PXMCGYNIQWLKKC-MRVPVSSYSA-N NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)OC(F)F)N(C1=CC(=C(C=C1)Cl)F)[C@@H](C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)OC(F)F)N(C1=CC(=C(C=C1)Cl)F)[C@@H](C(=O)N)C PXMCGYNIQWLKKC-MRVPVSSYSA-N 0.000 claims 1
- PXMCGYNIQWLKKC-QMMMGPOBSA-N NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)OC(F)F)N(C1=CC(=C(C=C1)Cl)F)[C@H](C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)OC(F)F)N(C1=CC(=C(C=C1)Cl)F)[C@H](C(=O)N)C PXMCGYNIQWLKKC-QMMMGPOBSA-N 0.000 claims 1
- ACERZSPTEWPRIN-UHFFFAOYSA-N NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)OC(F)F)N(C1=CC(=C(C=C1)F)F)C(C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)OC(F)F)N(C1=CC(=C(C=C1)F)F)C(C(=O)N)C ACERZSPTEWPRIN-UHFFFAOYSA-N 0.000 claims 1
- ACERZSPTEWPRIN-QMMMGPOBSA-N NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)OC(F)F)N(C1=CC(=C(C=C1)F)F)[C@H](C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)OC(F)F)N(C1=CC(=C(C=C1)F)F)[C@H](C(=O)N)C ACERZSPTEWPRIN-QMMMGPOBSA-N 0.000 claims 1
- JRFUBNBHCRPWTA-UHFFFAOYSA-N NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)OC(F)F)N(C1=CC(=C(C=C1)OC(F)(F)F)Cl)C(C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)OC(F)F)N(C1=CC(=C(C=C1)OC(F)(F)F)Cl)C(C(=O)N)C JRFUBNBHCRPWTA-UHFFFAOYSA-N 0.000 claims 1
- GLSWXQDXCIAAPT-UHFFFAOYSA-N NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)OC(F)F)N(C1=CC(=C(C=C1)OC(F)F)Cl)C(C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)OC(F)F)N(C1=CC(=C(C=C1)OC(F)F)Cl)C(C(=O)N)C GLSWXQDXCIAAPT-UHFFFAOYSA-N 0.000 claims 1
- BEOHNFNAOOKTGL-UHFFFAOYSA-N NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)OC(F)F)N(C1=CC(=C(C=C1)OC(F)F)F)C(C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)OC(F)F)N(C1=CC(=C(C=C1)OC(F)F)F)C(C(=O)N)C BEOHNFNAOOKTGL-UHFFFAOYSA-N 0.000 claims 1
- NOBATSAWXRLMCR-UHFFFAOYSA-N NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)OC(F)F)N(C1=CC=C(C=C1)C(F)F)C(C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)OC(F)F)N(C1=CC=C(C=C1)C(F)F)C(C(=O)N)C NOBATSAWXRLMCR-UHFFFAOYSA-N 0.000 claims 1
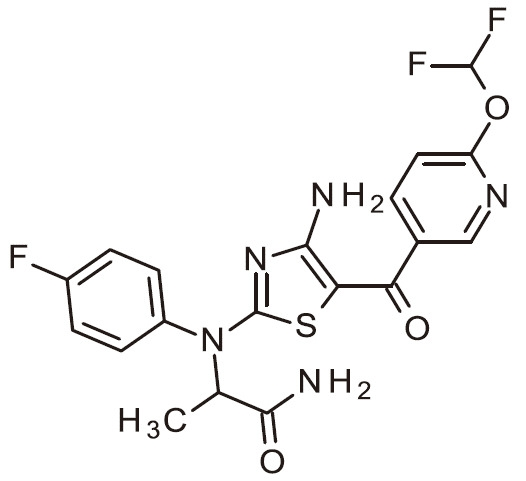
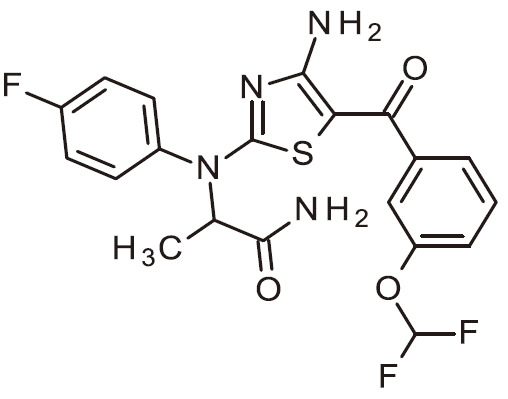
- VSBANMWETSOHLA-UHFFFAOYSA-N NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)OC(F)F)N(C1=CC=C(C=C1)F)C(C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)OC(F)F)N(C1=CC=C(C=C1)F)C(C(=O)N)C VSBANMWETSOHLA-UHFFFAOYSA-N 0.000 claims 1
- VSBANMWETSOHLA-SECBINFHSA-N NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)OC(F)F)N(C1=CC=C(C=C1)F)[C@@H](C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)OC(F)F)N(C1=CC=C(C=C1)F)[C@@H](C(=O)N)C VSBANMWETSOHLA-SECBINFHSA-N 0.000 claims 1
- VSBANMWETSOHLA-VIFPVBQESA-N NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)OC(F)F)N(C1=CC=C(C=C1)F)[C@H](C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)OC(F)F)N(C1=CC=C(C=C1)F)[C@H](C(=O)N)C VSBANMWETSOHLA-VIFPVBQESA-N 0.000 claims 1
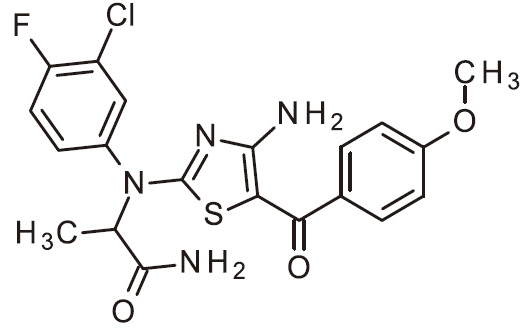
- UZCMBISSLYTBJM-SECBINFHSA-N NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)OC)N(C1=CC(=C(C=C1)Cl)F)[C@@H](C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)OC)N(C1=CC(=C(C=C1)Cl)F)[C@@H](C(=O)N)C UZCMBISSLYTBJM-SECBINFHSA-N 0.000 claims 1
- UZCMBISSLYTBJM-VIFPVBQESA-N NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)OC)N(C1=CC(=C(C=C1)Cl)F)[C@H](C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)OC)N(C1=CC(=C(C=C1)Cl)F)[C@H](C(=O)N)C UZCMBISSLYTBJM-VIFPVBQESA-N 0.000 claims 1
- GIPRRYZHOWUKAY-UHFFFAOYSA-N NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)OC)N(C1=CC(=C(C=C1)F)F)C(C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)OC)N(C1=CC(=C(C=C1)F)F)C(C(=O)N)C GIPRRYZHOWUKAY-UHFFFAOYSA-N 0.000 claims 1
- GIPRRYZHOWUKAY-SECBINFHSA-N NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)OC)N(C1=CC(=C(C=C1)F)F)[C@@H](C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)OC)N(C1=CC(=C(C=C1)F)F)[C@@H](C(=O)N)C GIPRRYZHOWUKAY-SECBINFHSA-N 0.000 claims 1
- GIPRRYZHOWUKAY-VIFPVBQESA-N NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)OC)N(C1=CC(=C(C=C1)F)F)[C@H](C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)OC)N(C1=CC(=C(C=C1)F)F)[C@H](C(=O)N)C GIPRRYZHOWUKAY-VIFPVBQESA-N 0.000 claims 1
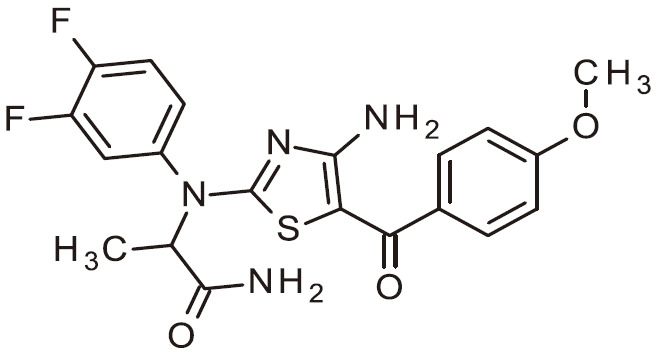
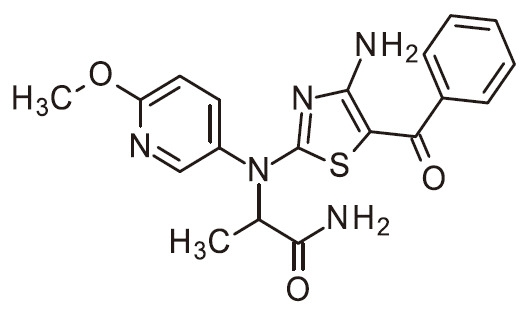
- ANOQCMYOPATPOV-UHFFFAOYSA-N NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)OC)N(C1=CC=C(C=C1)F)C(C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C=1C=NC(=CC=1)OC)N(C1=CC=C(C=C1)F)C(C(=O)N)C ANOQCMYOPATPOV-UHFFFAOYSA-N 0.000 claims 1
- RUGSRCZNVBTWQV-UHFFFAOYSA-N NC=1N=C(SC=1C(=O)C=1C=NC=CC=1)N(C1=CC(=C(C=C1)F)F)C(C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C=1C=NC=CC=1)N(C1=CC(=C(C=C1)F)F)C(C(=O)N)C RUGSRCZNVBTWQV-UHFFFAOYSA-N 0.000 claims 1
- RUGSRCZNVBTWQV-VIFPVBQESA-N NC=1N=C(SC=1C(=O)C=1C=NC=CC=1)N(C1=CC(=C(C=C1)F)F)[C@H](C(=O)N)C Chemical compound NC=1N=C(SC=1C(=O)C=1C=NC=CC=1)N(C1=CC(=C(C=C1)F)F)[C@H](C(=O)N)C RUGSRCZNVBTWQV-VIFPVBQESA-N 0.000 claims 1
- UHWPLNHRROQPMB-UHFFFAOYSA-N [4-(difluoromethoxy)phenyl]methanamine Chemical compound NCC1=CC=C(OC(F)F)C=C1 UHWPLNHRROQPMB-UHFFFAOYSA-N 0.000 claims 1
- PRDBLLIPPDOICK-UHFFFAOYSA-N [4-(trifluoromethyl)phenyl]methanamine Chemical compound NCC1=CC=C(C(F)(F)F)C=C1 PRDBLLIPPDOICK-UHFFFAOYSA-N 0.000 claims 1
- 229910001573 adamantine Inorganic materials 0.000 claims 1
- 239000005557 antagonist Substances 0.000 claims 1
- JPYQFYIEOUVJDU-UHFFFAOYSA-N beclamide Chemical compound ClCCC(=O)NCC1=CC=CC=C1 JPYQFYIEOUVJDU-UHFFFAOYSA-N 0.000 claims 1
- JFDZBHWFFUWGJE-UHFFFAOYSA-N benzenecarbonitrile Natural products N#CC1=CC=CC=C1 JFDZBHWFFUWGJE-UHFFFAOYSA-N 0.000 claims 1
- BSEXNZMHLUMQKR-UHFFFAOYSA-N cyclopropanecarboxamide Chemical compound NC(=O)C1CC1.NC(=O)C1CC1 BSEXNZMHLUMQKR-UHFFFAOYSA-N 0.000 claims 1
- 239000007788 liquid Substances 0.000 claims 1
- PYLWMHQQBFSUBP-UHFFFAOYSA-N monofluorobenzene Chemical compound FC1=CC=CC=C1 PYLWMHQQBFSUBP-UHFFFAOYSA-N 0.000 claims 1
- 239000000546 pharmaceutical excipient Substances 0.000 claims 1
- VLJNHYLEOZPXFW-UHFFFAOYSA-N pyrrolidine-2-carboxamide Chemical compound NC(=O)C1CCCN1 VLJNHYLEOZPXFW-UHFFFAOYSA-N 0.000 claims 1
- 238000000034 method Methods 0.000 abstract description 13
- 238000004519 manufacturing process Methods 0.000 abstract description 4
- 101710192015 Diacylglycerol kinase zeta Proteins 0.000 abstract description 2
- 102100030220 Diacylglycerol kinase zeta Human genes 0.000 abstract description 2
- 230000001105 regulatory effect Effects 0.000 abstract description 2
- YCKRFDGAMUMZLT-UHFFFAOYSA-N Fluorine atom Chemical compound [F] YCKRFDGAMUMZLT-UHFFFAOYSA-N 0.000 description 39
- 229910052805 deuterium Inorganic materials 0.000 description 25
- YZCKVEUIGOORGS-OUBTZVSYSA-N Deuterium Chemical compound [2H] YZCKVEUIGOORGS-OUBTZVSYSA-N 0.000 description 23
- 239000002585 base Substances 0.000 description 21
- 125000001246 bromo group Chemical group Br* 0.000 description 20
- 150000001721 carbon Chemical group 0.000 description 20
- 125000001400 nonyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 20
- 239000002253 acid Substances 0.000 description 18
- 125000002347 octyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 18
- 125000003003 spiro group Chemical group 0.000 description 18
- 125000006413 ring segment Chemical group 0.000 description 17
- 125000005842 heteroatom Chemical group 0.000 description 15
- 125000002704 decyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 14
- 125000003187 heptyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 14
- 210000001744 T-lymphocyte Anatomy 0.000 description 13
- 208000035475 disorder Diseases 0.000 description 12
- 230000000694 effects Effects 0.000 description 12
- 230000002829 reductive effect Effects 0.000 description 12
- 229920006395 saturated elastomer Polymers 0.000 description 12
- 229910052717 sulfur Chemical group 0.000 description 12
- 125000006568 (C4-C7) heterocycloalkyl group Chemical group 0.000 description 11
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 11
- 150000002430 hydrocarbons Chemical group 0.000 description 11
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 10
- 230000002349 favourable effect Effects 0.000 description 10
- 230000000155 isotopic effect Effects 0.000 description 10
- 125000000051 benzyloxy group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])O* 0.000 description 8
- 238000007254 oxidation reaction Methods 0.000 description 8
- 239000000126 substance Substances 0.000 description 8
- 102000011107 Diacylglycerol Kinase Human genes 0.000 description 7
- 108010062677 Diacylglycerol Kinase Proteins 0.000 description 7
- 241000699670 Mus sp. Species 0.000 description 7
- 208000036142 Viral infection Diseases 0.000 description 7
- 150000007513 acids Chemical class 0.000 description 7
- 230000002950 deficient Effects 0.000 description 7
- 239000002207 metabolite Substances 0.000 description 7
- QJGQUHMNIGDVPM-UHFFFAOYSA-N nitrogen group Chemical group [N] QJGQUHMNIGDVPM-UHFFFAOYSA-N 0.000 description 7
- 230000009385 viral infection Effects 0.000 description 7
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 6
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 6
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 6
- 125000000217 alkyl group Chemical group 0.000 description 6
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 6
- 239000003153 chemical reaction reagent Substances 0.000 description 6
- 229940079593 drug Drugs 0.000 description 6
- 229930195733 hydrocarbon Natural products 0.000 description 6
- 235000018102 proteins Nutrition 0.000 description 6
- 102000004169 proteins and genes Human genes 0.000 description 6
- 108090000623 proteins and genes Proteins 0.000 description 6
- 150000007979 thiazole derivatives Chemical class 0.000 description 6
- 150000003557 thiazoles Chemical class 0.000 description 6
- 125000004169 (C1-C6) alkyl group Chemical group 0.000 description 5
- 230000015572 biosynthetic process Effects 0.000 description 5
- 125000000623 heterocyclic group Chemical group 0.000 description 5
- 230000001965 increasing effect Effects 0.000 description 5
- 230000005764 inhibitory process Effects 0.000 description 5
- 208000001072 type 2 diabetes mellitus Diseases 0.000 description 5
- MSWZFWKMSRAUBD-IVMDWMLBSA-N 2-amino-2-deoxy-D-glucopyranose Chemical compound N[C@H]1C(O)O[C@H](CO)[C@@H](O)[C@@H]1O MSWZFWKMSRAUBD-IVMDWMLBSA-N 0.000 description 4
- 239000004215 Carbon black (E152) Substances 0.000 description 4
- 229920000858 Cyclodextrin Polymers 0.000 description 4
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 4
- 208000030289 Lymphoproliferative disease Diseases 0.000 description 4
- 108091008874 T cell receptors Proteins 0.000 description 4
- 102000016266 T-Cell Antigen Receptors Human genes 0.000 description 4
- DZBUGLKDJFMEHC-UHFFFAOYSA-N acridine Chemical compound C1=CC=CC2=CC3=CC=CC=C3N=C21 DZBUGLKDJFMEHC-UHFFFAOYSA-N 0.000 description 4
- MSWZFWKMSRAUBD-UHFFFAOYSA-N beta-D-galactosamine Natural products NC1C(O)OC(CO)C(O)C1O MSWZFWKMSRAUBD-UHFFFAOYSA-N 0.000 description 4
- 210000004027 cell Anatomy 0.000 description 4
- 239000003795 chemical substances by application Substances 0.000 description 4
- 239000002131 composite material Substances 0.000 description 4
- 125000004431 deuterium atom Chemical group 0.000 description 4
- 150000001982 diacylglycerols Chemical class 0.000 description 4
- 229960002442 glucosamine Drugs 0.000 description 4
- 125000004051 hexyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 4
- 208000032839 leukemia Diseases 0.000 description 4
- 230000002503 metabolic effect Effects 0.000 description 4
- 108020003175 receptors Proteins 0.000 description 4
- 102000005962 receptors Human genes 0.000 description 4
- 210000004881 tumor cell Anatomy 0.000 description 4
- 125000006699 (C1-C3) hydroxyalkyl group Chemical group 0.000 description 3
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 3
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 3
- KZBUYRJDOAKODT-UHFFFAOYSA-N Chlorine Chemical compound ClCl KZBUYRJDOAKODT-UHFFFAOYSA-N 0.000 description 3
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 3
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 3
- 206010022489 Insulin Resistance Diseases 0.000 description 3
- OFOBLEOULBTSOW-UHFFFAOYSA-N Malonic acid Chemical compound OC(=O)CC(O)=O OFOBLEOULBTSOW-UHFFFAOYSA-N 0.000 description 3
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 3
- MUBZPKHOEPUJKR-UHFFFAOYSA-N Oxalic acid Chemical compound OC(=O)C(O)=O MUBZPKHOEPUJKR-UHFFFAOYSA-N 0.000 description 3
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 3
- 230000003213 activating effect Effects 0.000 description 3
- 125000003342 alkenyl group Chemical group 0.000 description 3
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 3
- 238000010348 incorporation Methods 0.000 description 3
- 229910052500 inorganic mineral Inorganic materials 0.000 description 3
- 239000000543 intermediate Chemical class 0.000 description 3
- 230000000670 limiting effect Effects 0.000 description 3
- 230000004060 metabolic process Effects 0.000 description 3
- 235000010755 mineral Nutrition 0.000 description 3
- 239000011707 mineral Substances 0.000 description 3
- 150000007524 organic acids Chemical class 0.000 description 3
- 239000012071 phase Substances 0.000 description 3
- 230000026731 phosphorylation Effects 0.000 description 3
- 238000006366 phosphorylation reaction Methods 0.000 description 3
- 125000003386 piperidinyl group Chemical group 0.000 description 3
- 230000002265 prevention Effects 0.000 description 3
- 229940002612 prodrug Drugs 0.000 description 3
- 239000000651 prodrug Substances 0.000 description 3
- 238000000746 purification Methods 0.000 description 3
- UBQKCCHYAOITMY-UHFFFAOYSA-N pyridin-2-ol Chemical group OC1=CC=CC=N1 UBQKCCHYAOITMY-UHFFFAOYSA-N 0.000 description 3
- 125000000719 pyrrolidinyl group Chemical group 0.000 description 3
- 125000002943 quinolinyl group Chemical group N1=C(C=CC2=CC=CC=C12)* 0.000 description 3
- 238000000926 separation method Methods 0.000 description 3
- 238000003786 synthesis reaction Methods 0.000 description 3
- 230000009885 systemic effect Effects 0.000 description 3
- 230000001225 therapeutic effect Effects 0.000 description 3
- 125000002948 undecyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 3
- MIOPJNTWMNEORI-GMSGAONNSA-N (S)-camphorsulfonic acid Chemical compound C1C[C@@]2(CS(O)(=O)=O)C(=O)C[C@@H]1C2(C)C MIOPJNTWMNEORI-GMSGAONNSA-N 0.000 description 2
- PORPENFLTBBHSG-MGBGTMOVSA-N 1,2-dihexadecanoyl-sn-glycerol-3-phosphate Chemical compound CCCCCCCCCCCCCCCC(=O)OC[C@H](COP(O)(O)=O)OC(=O)CCCCCCCCCCCCCCC PORPENFLTBBHSG-MGBGTMOVSA-N 0.000 description 2
- 125000005962 1,4-oxazepanyl group Chemical group 0.000 description 2
- PAMIQIKDUOTOBW-UHFFFAOYSA-N 1-methylpiperidine Chemical compound CN1CCCCC1 PAMIQIKDUOTOBW-UHFFFAOYSA-N 0.000 description 2
- CNWINRVXAYPOMW-FCNJXWMTSA-N 1-stearoyl-2-arachidonoyl-sn-glycero-3-phospho-1D-myo-inositol 4,5-biphosphate Chemical compound CCCCC\C=C/C\C=C/C\C=C/C\C=C/CCCC(=O)O[C@H](COC(=O)CCCCCCCCCCCCCCCCC)COP(O)(=O)O[C@@H]1[C@H](O)[C@H](O)[C@@H](OP(O)(O)=O)[C@H](OP(O)(O)=O)[C@H]1O CNWINRVXAYPOMW-FCNJXWMTSA-N 0.000 description 2
- 125000003903 2-propenyl group Chemical group [H]C([*])([H])C([H])=C([H])[H] 0.000 description 2
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical group [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 2
- QGZKDVFQNNGYKY-UHFFFAOYSA-N Ammonia Chemical compound N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 description 2
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 description 2
- 239000005711 Benzoic acid Substances 0.000 description 2
- FERIUCNNQQJTOY-UHFFFAOYSA-N Butyric acid Chemical compound CCCC(O)=O FERIUCNNQQJTOY-UHFFFAOYSA-N 0.000 description 2
- 125000006577 C1-C6 hydroxyalkyl group Chemical group 0.000 description 2
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 2
- 108010019670 Chimeric Antigen Receptors Proteins 0.000 description 2
- 206010009944 Colon cancer Diseases 0.000 description 2
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 2
- 108010052167 Dihydroorotate Dehydrogenase Proteins 0.000 description 2
- 102100032823 Dihydroorotate dehydrogenase (quinone), mitochondrial Human genes 0.000 description 2
- 102000004190 Enzymes Human genes 0.000 description 2
- 108090000790 Enzymes Proteins 0.000 description 2
- QUSNBJAOOMFDIB-UHFFFAOYSA-N Ethylamine Chemical compound CCN QUSNBJAOOMFDIB-UHFFFAOYSA-N 0.000 description 2
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical compound OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 description 2
- 241000701044 Human gammaherpesvirus 4 Species 0.000 description 2
- SIKJAQJRHWYJAI-UHFFFAOYSA-N Indole Chemical compound C1=CC=C2NC=CC2=C1 SIKJAQJRHWYJAI-UHFFFAOYSA-N 0.000 description 2
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 2
- FXHOOIRPVKKKFG-UHFFFAOYSA-N N,N-Dimethylacetamide Chemical compound CN(C)C(C)=O FXHOOIRPVKKKFG-UHFFFAOYSA-N 0.000 description 2
- 102000012064 NLR Proteins Human genes 0.000 description 2
- 108091005686 NOD-like receptors Proteins 0.000 description 2
- PVNIIMVLHYAWGP-UHFFFAOYSA-N Niacin Chemical compound OC(=O)C1=CC=CN=C1 PVNIIMVLHYAWGP-UHFFFAOYSA-N 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 2
- NQRYJNQNLNOLGT-UHFFFAOYSA-N Piperidine Chemical compound C1CCNCC1 NQRYJNQNLNOLGT-UHFFFAOYSA-N 0.000 description 2
- 108010029485 Protein Isoforms Proteins 0.000 description 2
- 102000001708 Protein Isoforms Human genes 0.000 description 2
- LCTONWCANYUPML-UHFFFAOYSA-N Pyruvic acid Chemical compound CC(=O)C(O)=O LCTONWCANYUPML-UHFFFAOYSA-N 0.000 description 2
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 2
- 229940126530 T cell activator Drugs 0.000 description 2
- 102000003567 TRPV4 Human genes 0.000 description 2
- 101150098315 TRPV4 gene Proteins 0.000 description 2
- FEWJPZIEWOKRBE-UHFFFAOYSA-N Tartaric acid Natural products [H+].[H+].[O-]C(=O)C(O)C(O)C([O-])=O FEWJPZIEWOKRBE-UHFFFAOYSA-N 0.000 description 2
- DTQVDTLACAAQTR-UHFFFAOYSA-N Trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 description 2
- 208000033779 X-linked lymphoproliferative disease Diseases 0.000 description 2
- 230000002378 acidificating effect Effects 0.000 description 2
- 230000009471 action Effects 0.000 description 2
- WNLRTRBMVRJNCN-UHFFFAOYSA-N adipic acid Chemical compound OC(=O)CCCCC(O)=O WNLRTRBMVRJNCN-UHFFFAOYSA-N 0.000 description 2
- 229910052783 alkali metal Inorganic materials 0.000 description 2
- 229910052784 alkaline earth metal Inorganic materials 0.000 description 2
- 239000000010 aprotic solvent Substances 0.000 description 2
- 125000003118 aryl group Chemical group 0.000 description 2
- 208000006673 asthma Diseases 0.000 description 2
- 125000003725 azepanyl group Chemical group 0.000 description 2
- 230000008901 benefit Effects 0.000 description 2
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 2
- 239000011575 calcium Substances 0.000 description 2
- 229910052791 calcium Inorganic materials 0.000 description 2
- 239000003054 catalyst Substances 0.000 description 2
- 238000006243 chemical reaction Methods 0.000 description 2
- 238000004587 chromatography analysis Methods 0.000 description 2
- JBDSSBMEKXHSJF-UHFFFAOYSA-N cyclopentanecarboxylic acid Chemical compound OC(=O)C1CCCC1 JBDSSBMEKXHSJF-UHFFFAOYSA-N 0.000 description 2
- 125000004855 decalinyl group Chemical group C1(CCCC2CCCCC12)* 0.000 description 2
- 238000012217 deletion Methods 0.000 description 2
- 230000037430 deletion Effects 0.000 description 2
- 238000001212 derivatisation Methods 0.000 description 2
- 150000001975 deuterium Chemical class 0.000 description 2
- XBDQKXXYIPTUBI-UHFFFAOYSA-N dimethylselenoniopropionate Natural products CCC(O)=O XBDQKXXYIPTUBI-UHFFFAOYSA-N 0.000 description 2
- POULHZVOKOAJMA-UHFFFAOYSA-N dodecanoic acid Chemical compound CCCCCCCCCCCC(O)=O POULHZVOKOAJMA-UHFFFAOYSA-N 0.000 description 2
- 238000003821 enantio-separation Methods 0.000 description 2
- 230000002708 enhancing effect Effects 0.000 description 2
- 229940088598 enzyme Drugs 0.000 description 2
- 208000030533 eye disease Diseases 0.000 description 2
- 125000003709 fluoroalkyl group Chemical group 0.000 description 2
- 125000004216 fluoromethyl group Chemical group [H]C([H])(F)* 0.000 description 2
- 239000007789 gas Substances 0.000 description 2
- 125000001475 halogen functional group Chemical group 0.000 description 2
- FUZZWVXGSFPDMH-UHFFFAOYSA-N hexanoic acid Chemical compound CCCCCC(O)=O FUZZWVXGSFPDMH-UHFFFAOYSA-N 0.000 description 2
- 238000004128 high performance liquid chromatography Methods 0.000 description 2
- 125000002632 imidazolidinyl group Chemical group 0.000 description 2
- 210000000987 immune system Anatomy 0.000 description 2
- 208000015181 infectious disease Diseases 0.000 description 2
- SUMDYPCJJOFFON-UHFFFAOYSA-N isethionic acid Chemical compound OCCS(O)(=O)=O SUMDYPCJJOFFON-UHFFFAOYSA-N 0.000 description 2
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 2
- 238000002955 isolation Methods 0.000 description 2
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 2
- JVTAAEKCZFNVCJ-UHFFFAOYSA-N lactic acid Chemical compound CC(O)C(O)=O JVTAAEKCZFNVCJ-UHFFFAOYSA-N 0.000 description 2
- 230000021633 leukocyte mediated immunity Effects 0.000 description 2
- 150000002632 lipids Chemical class 0.000 description 2
- BDAGIHXWWSANSR-UHFFFAOYSA-N methanoic acid Natural products OC=O BDAGIHXWWSANSR-UHFFFAOYSA-N 0.000 description 2
- 150000007522 mineralic acids Chemical class 0.000 description 2
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 2
- NQDJXKOVJZTUJA-UHFFFAOYSA-N nevirapine Chemical compound C12=NC=CC=C2C(=O)NC=2C(C)=CC=NC=2N1C1CC1 NQDJXKOVJZTUJA-UHFFFAOYSA-N 0.000 description 2
- 230000003287 optical effect Effects 0.000 description 2
- FJKROLUGYXJWQN-UHFFFAOYSA-N papa-hydroxy-benzoic acid Natural products OC(=O)C1=CC=C(O)C=C1 FJKROLUGYXJWQN-UHFFFAOYSA-N 0.000 description 2
- 239000002245 particle Substances 0.000 description 2
- 125000001147 pentyl group Chemical group C(CCCC)* 0.000 description 2
- 230000003285 pharmacodynamic effect Effects 0.000 description 2
- 239000002798 polar solvent Substances 0.000 description 2
- 230000002062 proliferating effect Effects 0.000 description 2
- 230000035755 proliferation Effects 0.000 description 2
- 230000001737 promoting effect Effects 0.000 description 2
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 2
- 125000003072 pyrazolidinyl group Chemical group 0.000 description 2
- 230000002441 reversible effect Effects 0.000 description 2
- YGSDEFSMJLZEOE-UHFFFAOYSA-N salicylic acid Chemical compound OC(=O)C1=CC=CC=C1O YGSDEFSMJLZEOE-UHFFFAOYSA-N 0.000 description 2
- FSYKKLYZXJSNPZ-UHFFFAOYSA-N sarcosine Chemical compound C[NH2+]CC([O-])=O FSYKKLYZXJSNPZ-UHFFFAOYSA-N 0.000 description 2
- GAJDDVONBAWAGB-UHFFFAOYSA-N spiro[2.6]nonyl Chemical group [CH]1CC11CCCCCC1 GAJDDVONBAWAGB-UHFFFAOYSA-N 0.000 description 2
- LMUMMJCCZMWLEN-UHFFFAOYSA-N spiro[3.3]heptyl Chemical group [CH]1CCC11CCC1 LMUMMJCCZMWLEN-UHFFFAOYSA-N 0.000 description 2
- 230000000638 stimulation Effects 0.000 description 2
- 125000004434 sulfur atom Chemical group 0.000 description 2
- 230000004083 survival effect Effects 0.000 description 2
- 229940042055 systemic antimycotics triazole derivative Drugs 0.000 description 2
- 230000008685 targeting Effects 0.000 description 2
- 235000002906 tartaric acid Nutrition 0.000 description 2
- 239000011975 tartaric acid Substances 0.000 description 2
- 125000001544 thienyl group Chemical group 0.000 description 2
- ZMZDMBWJUHKJPS-UHFFFAOYSA-N thiocyanic acid Chemical compound SC#N ZMZDMBWJUHKJPS-UHFFFAOYSA-N 0.000 description 2
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 2
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 2
- 238000012546 transfer Methods 0.000 description 2
- ZDPHROOEEOARMN-UHFFFAOYSA-N undecanoic acid Chemical compound CCCCCCCCCCC(O)=O ZDPHROOEEOARMN-UHFFFAOYSA-N 0.000 description 2
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 2
- WWUZIQQURGPMPG-UHFFFAOYSA-N (-)-D-erythro-Sphingosine Natural products CCCCCCCCCCCCCC=CC(O)C(N)CO WWUZIQQURGPMPG-UHFFFAOYSA-N 0.000 description 1
- YZOUYRAONFXZSI-SBHWVFSVSA-N (1S,3R,5R,6R,8R,10R,11R,13R,15R,16R,18R,20R,21R,23R,25R,26R,28R,30R,31S,33R,35R,36R,37S,38R,39S,40R,41S,42R,43S,44R,45S,46R,47S,48R,49S)-5,10,15,20,25,30,35-heptakis(hydroxymethyl)-37,39,40,41,42,43,44,45,46,47,48,49-dodecamethoxy-2,4,7,9,12,14,17,19,22,24,27,29,32,34-tetradecaoxaoctacyclo[31.2.2.23,6.28,11.213,16.218,21.223,26.228,31]nonatetracontane-36,38-diol Chemical compound O([C@@H]([C@H]([C@@H]1OC)OC)O[C@H]2[C@@H](O)[C@@H]([C@@H](O[C@@H]3[C@@H](CO)O[C@@H]([C@H]([C@@H]3O)OC)O[C@@H]3[C@@H](CO)O[C@@H]([C@H]([C@@H]3OC)OC)O[C@@H]3[C@@H](CO)O[C@@H]([C@H]([C@@H]3OC)OC)O[C@@H]3[C@@H](CO)O[C@@H]([C@H]([C@@H]3OC)OC)O3)O[C@@H]2CO)OC)[C@H](CO)[C@H]1O[C@@H]1[C@@H](OC)[C@H](OC)[C@H]3[C@@H](CO)O1 YZOUYRAONFXZSI-SBHWVFSVSA-N 0.000 description 1
- QBYIENPQHBMVBV-HFEGYEGKSA-N (2R)-2-hydroxy-2-phenylacetic acid Chemical compound O[C@@H](C(O)=O)c1ccccc1.O[C@@H](C(O)=O)c1ccccc1 QBYIENPQHBMVBV-HFEGYEGKSA-N 0.000 description 1
- MTCFGRXMJLQNBG-REOHCLBHSA-N (2S)-2-Amino-3-hydroxypropansäure Chemical compound OC[C@H](N)C(O)=O MTCFGRXMJLQNBG-REOHCLBHSA-N 0.000 description 1
- DNISEZBAYYIQFB-PHDIDXHHSA-N (2r,3r)-2,3-diacetyloxybutanedioic acid Chemical compound CC(=O)O[C@@H](C(O)=O)[C@H](C(O)=O)OC(C)=O DNISEZBAYYIQFB-PHDIDXHHSA-N 0.000 description 1
- FWIVDMJALNEADT-SFTDATJTSA-N (2s)-n-(1-cyanocyclopropyl)-4-fluoro-4-methyl-2-[[(1s)-2,2,2-trifluoro-1-[4-(4-methylsulfonylphenyl)phenyl]ethyl]amino]pentanamide Chemical compound C1=CC([C@H](N[C@@H](CC(C)(F)C)C(=O)NC2(CC2)C#N)C(F)(F)F)=CC=C1C1=CC=C(S(C)(=O)=O)C=C1 FWIVDMJALNEADT-SFTDATJTSA-N 0.000 description 1
- KWMLJOLKUYYJFJ-GASJEMHNSA-N (2xi)-D-gluco-heptonic acid Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@@H](O)C(O)C(O)=O KWMLJOLKUYYJFJ-GASJEMHNSA-N 0.000 description 1
- 125000004191 (C1-C6) alkoxy group Chemical group 0.000 description 1
- BJEPYKJPYRNKOW-REOHCLBHSA-N (S)-malic acid Chemical compound OC(=O)[C@@H](O)CC(O)=O BJEPYKJPYRNKOW-REOHCLBHSA-N 0.000 description 1
- WBYWAXJHAXSJNI-VOTSOKGWSA-M .beta-Phenylacrylic acid Natural products [O-]C(=O)\C=C\C1=CC=CC=C1 WBYWAXJHAXSJNI-VOTSOKGWSA-M 0.000 description 1
- FIARMZDBEGVMLV-UHFFFAOYSA-N 1,1,2,2,2-pentafluoroethanolate Chemical group [O-]C(F)(F)C(F)(F)F FIARMZDBEGVMLV-UHFFFAOYSA-N 0.000 description 1
- 125000005918 1,2-dimethylbutyl group Chemical group 0.000 description 1
- 125000005960 1,4-diazepanyl group Chemical group 0.000 description 1
- ZFPGARUNNKGOBB-UHFFFAOYSA-N 1-Ethyl-2-pyrrolidinone Chemical compound CCN1CCCC1=O ZFPGARUNNKGOBB-UHFFFAOYSA-N 0.000 description 1
- 125000004972 1-butynyl group Chemical group [H]C([H])([H])C([H])([H])C#C* 0.000 description 1
- 125000006218 1-ethylbutyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C([H])([H])[H] 0.000 description 1
- VUQMOERHEHTWPE-UHFFFAOYSA-N 1-ethylpiperidin-2-one Chemical compound CCN1CCCCC1=O VUQMOERHEHTWPE-UHFFFAOYSA-N 0.000 description 1
- 125000004066 1-hydroxyethyl group Chemical group [H]OC([H])([*])C([H])([H])[H] 0.000 description 1
- GGYVTHJIUNGKFZ-UHFFFAOYSA-N 1-methylpiperidin-2-one Chemical compound CN1CCCCC1=O GGYVTHJIUNGKFZ-UHFFFAOYSA-N 0.000 description 1
- 102100026205 1-phosphatidylinositol 4,5-bisphosphate phosphodiesterase gamma-1 Human genes 0.000 description 1
- 125000001462 1-pyrrolyl group Chemical group [*]N1C([H])=C([H])C([H])=C1[H] 0.000 description 1
- POXWDTQUDZUOGP-UHFFFAOYSA-N 1h-1,4-diazepine Chemical group N1C=CC=NC=C1 POXWDTQUDZUOGP-UHFFFAOYSA-N 0.000 description 1
- UJIBOGAQJRDRES-UHFFFAOYSA-N 1h-pyridin-2-one Chemical compound OC1=CC=CC=N1.O=C1C=CC=CN1 UJIBOGAQJRDRES-UHFFFAOYSA-N 0.000 description 1
- IAAQUOVTPAMQCR-UHFFFAOYSA-N 1h-pyrido[3,2-d]pyrimidin-2-one Chemical compound C1=CC=C2NC(=O)N=CC2=N1 IAAQUOVTPAMQCR-UHFFFAOYSA-N 0.000 description 1
- 125000004206 2,2,2-trifluoroethyl group Chemical group [H]C([H])(*)C(F)(F)F 0.000 description 1
- 125000004778 2,2-difluoroethyl group Chemical group [H]C([H])(*)C([H])(F)F 0.000 description 1
- JAHNSTQSQJOJLO-UHFFFAOYSA-N 2-(3-fluorophenyl)-1h-imidazole Chemical compound FC1=CC=CC(C=2NC=CN=2)=C1 JAHNSTQSQJOJLO-UHFFFAOYSA-N 0.000 description 1
- HZAXFHJVJLSVMW-UHFFFAOYSA-N 2-Aminoethan-1-ol Chemical compound NCCO HZAXFHJVJLSVMW-UHFFFAOYSA-N 0.000 description 1
- WXHLLJAMBQLULT-UHFFFAOYSA-N 2-[[6-[4-(2-hydroxyethyl)piperazin-1-yl]-2-methylpyrimidin-4-yl]amino]-n-(2-methyl-6-sulfanylphenyl)-1,3-thiazole-5-carboxamide;hydrate Chemical compound O.C=1C(N2CCN(CCO)CC2)=NC(C)=NC=1NC(S1)=NC=C1C(=O)NC1=C(C)C=CC=C1S WXHLLJAMBQLULT-UHFFFAOYSA-N 0.000 description 1
- NHNCENSIZAIPGZ-UHFFFAOYSA-N 2-aminoethanol;n-ethylethanamine Chemical compound NCCO.CCNCC NHNCENSIZAIPGZ-UHFFFAOYSA-N 0.000 description 1
- KJJPLEZQSCZCKE-UHFFFAOYSA-N 2-aminopropane-1,3-diol Chemical compound OCC(N)CO KJJPLEZQSCZCKE-UHFFFAOYSA-N 0.000 description 1
- 125000004974 2-butenyl group Chemical group C(C=CC)* 0.000 description 1
- 125000000069 2-butynyl group Chemical group [H]C([H])([H])C#CC([H])([H])* 0.000 description 1
- BFSVOASYOCHEOV-UHFFFAOYSA-N 2-diethylaminoethanol Chemical compound CCN(CC)CCO BFSVOASYOCHEOV-UHFFFAOYSA-N 0.000 description 1
- 125000006176 2-ethylbutyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(C([H])([H])*)C([H])([H])C([H])([H])[H] 0.000 description 1
- 125000004777 2-fluoroethyl group Chemical group [H]C([H])(F)C([H])([H])* 0.000 description 1
- 125000000954 2-hydroxyethyl group Chemical group [H]C([*])([H])C([H])([H])O[H] 0.000 description 1
- 125000004493 2-methylbut-1-yl group Chemical group CC(C*)CC 0.000 description 1
- 125000005916 2-methylpentyl group Chemical group 0.000 description 1
- 125000001494 2-propynyl group Chemical group [H]C#CC([H])([H])* 0.000 description 1
- 125000004105 2-pyridyl group Chemical group N1=C([*])C([H])=C([H])C([H])=C1[H] 0.000 description 1
- 125000000175 2-thienyl group Chemical group S1C([*])=C([H])C([H])=C1[H] 0.000 description 1
- SLRMQYXOBQWXCR-UHFFFAOYSA-N 2154-56-5 Chemical compound [CH2]C1=CC=CC=C1 SLRMQYXOBQWXCR-UHFFFAOYSA-N 0.000 description 1
- ALKYHXVLJMQRLQ-UHFFFAOYSA-N 3-Hydroxy-2-naphthoate Chemical compound C1=CC=C2C=C(O)C(C(=O)O)=CC2=C1 ALKYHXVLJMQRLQ-UHFFFAOYSA-N 0.000 description 1
- ZCNBZFRECRPCKU-UHFFFAOYSA-N 3-[2-[4-[bis(4-fluorophenyl)methylidene]-1-piperidinyl]ethyl]-2-sulfanylidene-1H-quinazolin-4-one Chemical compound C1=CC(F)=CC=C1C(C=1C=CC(F)=CC=1)=C1CCN(CCN2C(C3=CC=CC=C3NC2=S)=O)CC1 ZCNBZFRECRPCKU-UHFFFAOYSA-N 0.000 description 1
- KQIGMPWTAHJUMN-UHFFFAOYSA-N 3-aminopropane-1,2-diol Chemical compound NCC(O)CO KQIGMPWTAHJUMN-UHFFFAOYSA-N 0.000 description 1
- BMYNFMYTOJXKLE-UHFFFAOYSA-N 3-azaniumyl-2-hydroxypropanoate Chemical compound NCC(O)C(O)=O BMYNFMYTOJXKLE-UHFFFAOYSA-N 0.000 description 1
- 125000004975 3-butenyl group Chemical group C(CC=C)* 0.000 description 1
- QOXOZONBQWIKDA-UHFFFAOYSA-N 3-hydroxypropyl Chemical group [CH2]CCO QOXOZONBQWIKDA-UHFFFAOYSA-N 0.000 description 1
- 125000003542 3-methylbutan-2-yl group Chemical group [H]C([H])([H])C([H])(*)C([H])(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 125000005917 3-methylpentyl group Chemical group 0.000 description 1
- 125000003349 3-pyridyl group Chemical group N1=C([H])C([*])=C([H])C([H])=C1[H] 0.000 description 1
- 125000001541 3-thienyl group Chemical group S1C([H])=C([*])C([H])=C1[H] 0.000 description 1
- OSWFIVFLDKOXQC-UHFFFAOYSA-N 4-(3-methoxyphenyl)aniline Chemical compound COC1=CC=CC(C=2C=CC(N)=CC=2)=C1 OSWFIVFLDKOXQC-UHFFFAOYSA-N 0.000 description 1
- WIFPJDJJFUSIFP-UHFFFAOYSA-N 4-aminobutane-1,2,3-triol Chemical compound NCC(O)C(O)CO WIFPJDJJFUSIFP-UHFFFAOYSA-N 0.000 description 1
- SXIFAEWFOJETOA-UHFFFAOYSA-N 4-hydroxy-butyl Chemical group [CH2]CCCO SXIFAEWFOJETOA-UHFFFAOYSA-N 0.000 description 1
- 229940090248 4-hydroxybenzoic acid Drugs 0.000 description 1
- 125000000339 4-pyridyl group Chemical group N1=C([H])C([H])=C([*])C([H])=C1[H] 0.000 description 1
- AWQSAIIDOMEEOD-UHFFFAOYSA-N 5,5-Dimethyl-4-(3-oxobutyl)dihydro-2(3H)-furanone Chemical compound CC(=O)CCC1CC(=O)OC1(C)C AWQSAIIDOMEEOD-UHFFFAOYSA-N 0.000 description 1
- TVEXGJYMHHTVKP-UHFFFAOYSA-N 6-oxabicyclo[3.2.1]oct-3-en-7-one Chemical compound C1C2C(=O)OC1C=CC2 TVEXGJYMHHTVKP-UHFFFAOYSA-N 0.000 description 1
- HBAQYPYDRFILMT-UHFFFAOYSA-N 8-[3-(1-cyclopropylpyrazol-4-yl)-1H-pyrazolo[4,3-d]pyrimidin-5-yl]-3-methyl-3,8-diazabicyclo[3.2.1]octan-2-one Chemical class C1(CC1)N1N=CC(=C1)C1=NNC2=C1N=C(N=C2)N1C2C(N(CC1CC2)C)=O HBAQYPYDRFILMT-UHFFFAOYSA-N 0.000 description 1
- WDJHALXBUFZDSR-UHFFFAOYSA-N Acetoacetic acid Natural products CC(=O)CC(O)=O WDJHALXBUFZDSR-UHFFFAOYSA-N 0.000 description 1
- 229920001450 Alpha-Cyclodextrin Polymers 0.000 description 1
- QGZKDVFQNNGYKY-UHFFFAOYSA-O Ammonium Chemical compound [NH4+] QGZKDVFQNNGYKY-UHFFFAOYSA-O 0.000 description 1
- 239000004475 Arginine Substances 0.000 description 1
- 208000023275 Autoimmune disease Diseases 0.000 description 1
- 206010006187 Breast cancer Diseases 0.000 description 1
- 208000026310 Breast neoplasm Diseases 0.000 description 1
- 206010006482 Bronchospasm Diseases 0.000 description 1
- 238000011740 C57BL/6 mouse Methods 0.000 description 1
- HNUALPPJLMYHDK-UHFFFAOYSA-N C[CH]C Chemical compound C[CH]C HNUALPPJLMYHDK-UHFFFAOYSA-N 0.000 description 1
- LSPHULWDVZXLIL-UHFFFAOYSA-N Camphoric acid Natural products CC1(C)C(C(O)=O)CCC1(C)C(O)=O LSPHULWDVZXLIL-UHFFFAOYSA-N 0.000 description 1
- 108091007741 Chimeric antigen receptor T cells Proteins 0.000 description 1
- 206010008761 Choriomeningitis lymphocytic Diseases 0.000 description 1
- WBYWAXJHAXSJNI-SREVYHEPSA-N Cinnamic acid Chemical compound OC(=O)\C=C/C1=CC=CC=C1 WBYWAXJHAXSJNI-SREVYHEPSA-N 0.000 description 1
- 208000001333 Colorectal Neoplasms Diseases 0.000 description 1
- 102000018832 Cytochromes Human genes 0.000 description 1
- 108010052832 Cytochromes Proteins 0.000 description 1
- 102000004127 Cytokines Human genes 0.000 description 1
- 108090000695 Cytokines Proteins 0.000 description 1
- RGHNJXZEOKUKBD-SQOUGZDYSA-N D-gluconic acid Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@@H](O)C(O)=O RGHNJXZEOKUKBD-SQOUGZDYSA-N 0.000 description 1
- RGHNJXZEOKUKBD-UHFFFAOYSA-N D-gluconic acid Natural products OCC(O)C(O)C(O)C(O)C(O)=O RGHNJXZEOKUKBD-UHFFFAOYSA-N 0.000 description 1
- 208000001490 Dengue Diseases 0.000 description 1
- 206010012310 Dengue fever Diseases 0.000 description 1
- XBPCUCUWBYBCDP-UHFFFAOYSA-N Dicyclohexylamine Chemical compound C1CCCCC1NC1CCCCC1 XBPCUCUWBYBCDP-UHFFFAOYSA-N 0.000 description 1
- XPOQHMRABVBWPR-UHFFFAOYSA-N Efavirenz Natural products O1C(=O)NC2=CC=C(Cl)C=C2C1(C(F)(F)F)C#CC1CC1 XPOQHMRABVBWPR-UHFFFAOYSA-N 0.000 description 1
- PIICEJLVQHRZGT-UHFFFAOYSA-N Ethylenediamine Chemical compound NCCN PIICEJLVQHRZGT-UHFFFAOYSA-N 0.000 description 1
- 108010087894 Fatty acid desaturases Proteins 0.000 description 1
- 208000032612 Glial tumor Diseases 0.000 description 1
- 206010018338 Glioma Diseases 0.000 description 1
- 108050008339 Heat Shock Transcription Factor Proteins 0.000 description 1
- 102000000039 Heat Shock Transcription Factor Human genes 0.000 description 1
- SQUHHTBVTRBESD-UHFFFAOYSA-N Hexa-Ac-myo-Inositol Natural products CC(=O)OC1C(OC(C)=O)C(OC(C)=O)C(OC(C)=O)C(OC(C)=O)C1OC(C)=O SQUHHTBVTRBESD-UHFFFAOYSA-N 0.000 description 1
- 241000282412 Homo Species 0.000 description 1
- 101000691599 Homo sapiens 1-phosphatidylinositol 4,5-bisphosphate phosphodiesterase gamma-1 Proteins 0.000 description 1
- 101000979342 Homo sapiens Nuclear factor NF-kappa-B p105 subunit Proteins 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- 206010061598 Immunodeficiency Diseases 0.000 description 1
- 208000029462 Immunodeficiency disease Diseases 0.000 description 1
- 108050003558 Interleukin-17 Proteins 0.000 description 1
- 102000013691 Interleukin-17 Human genes 0.000 description 1
- 108010002350 Interleukin-2 Proteins 0.000 description 1
- 108010063738 Interleukins Proteins 0.000 description 1
- 102000015696 Interleukins Human genes 0.000 description 1
- 206010022998 Irritability Diseases 0.000 description 1
- ODKSFYDXXFIFQN-BYPYZUCNSA-P L-argininium(2+) Chemical compound NC(=[NH2+])NCCC[C@H]([NH3+])C(O)=O ODKSFYDXXFIFQN-BYPYZUCNSA-P 0.000 description 1
- CKLJMWTZIZZHCS-REOHCLBHSA-N L-aspartic acid Chemical compound OC(=O)[C@@H](N)CC(O)=O CKLJMWTZIZZHCS-REOHCLBHSA-N 0.000 description 1
- KDXKERNSBIXSRK-YFKPBYRVSA-N L-lysine Chemical compound NCCCC[C@H](N)C(O)=O KDXKERNSBIXSRK-YFKPBYRVSA-N 0.000 description 1
- 239000005639 Lauric acid Substances 0.000 description 1
- KDXKERNSBIXSRK-UHFFFAOYSA-N Lysine Natural products NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 description 1
- 239000004472 Lysine Substances 0.000 description 1
- 102000019149 MAP kinase activity proteins Human genes 0.000 description 1
- 108040008097 MAP kinase activity proteins Proteins 0.000 description 1
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 1
- 241000124008 Mammalia Species 0.000 description 1
- 206010027406 Mesothelioma Diseases 0.000 description 1
- 241001529936 Murinae Species 0.000 description 1
- JGFZNNIVVJXRND-UHFFFAOYSA-N N,N-Diisopropylethylamine (DIPEA) Chemical compound CCN(C(C)C)C(C)C JGFZNNIVVJXRND-UHFFFAOYSA-N 0.000 description 1
- SUAKHGWARZSWIH-UHFFFAOYSA-N N,N‐diethylformamide Chemical compound CCN(CC)C=O SUAKHGWARZSWIH-UHFFFAOYSA-N 0.000 description 1
- SECXISVLQFMRJM-UHFFFAOYSA-N N-Methylpyrrolidone Chemical compound CN1CCCC1=O SECXISVLQFMRJM-UHFFFAOYSA-N 0.000 description 1
- UEEJHVSXFDXPFK-UHFFFAOYSA-N N-dimethylaminoethanol Chemical compound CN(C)CCO UEEJHVSXFDXPFK-UHFFFAOYSA-N 0.000 description 1
- 108050002826 Neuropeptide Y Receptor Proteins 0.000 description 1
- 102000012301 Neuropeptide Y receptor Human genes 0.000 description 1
- GRYLNZFGIOXLOG-UHFFFAOYSA-N Nitric acid Chemical compound O[N+]([O-])=O GRYLNZFGIOXLOG-UHFFFAOYSA-N 0.000 description 1
- 102100023050 Nuclear factor NF-kappa-B p105 subunit Human genes 0.000 description 1
- 206010061902 Pancreatic neoplasm Diseases 0.000 description 1
- 102100020749 Pantetheinase Human genes 0.000 description 1
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical compound [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 description 1
- 108091000080 Phosphotransferase Proteins 0.000 description 1
- 102100040678 Programmed cell death protein 1 Human genes 0.000 description 1
- 206010060862 Prostate cancer Diseases 0.000 description 1
- 208000000236 Prostatic Neoplasms Diseases 0.000 description 1
- 108010015499 Protein Kinase C-theta Proteins 0.000 description 1
- 102100021566 Protein kinase C theta type Human genes 0.000 description 1
- 102000016971 Proto-Oncogene Proteins c-kit Human genes 0.000 description 1
- 108010014608 Proto-Oncogene Proteins c-kit Proteins 0.000 description 1
- 102000000874 Pyrin Domain-Containing 3 Protein NLR Family Human genes 0.000 description 1
- 108010001946 Pyrin Domain-Containing 3 Protein NLR Family Proteins 0.000 description 1
- IWYDHOAUDWTVEP-UHFFFAOYSA-N R-2-phenyl-2-hydroxyacetic acid Natural products OC(=O)C(O)C1=CC=CC=C1 IWYDHOAUDWTVEP-UHFFFAOYSA-N 0.000 description 1
- 208000002200 Respiratory Hypersensitivity Diseases 0.000 description 1
- 208000007135 Retinal Neovascularization Diseases 0.000 description 1
- 208000017442 Retinal disease Diseases 0.000 description 1
- 206010038923 Retinopathy Diseases 0.000 description 1
- 108010077895 Sarcosine Proteins 0.000 description 1
- MTCFGRXMJLQNBG-UHFFFAOYSA-N Serine Natural products OCC(N)C(O)=O MTCFGRXMJLQNBG-UHFFFAOYSA-N 0.000 description 1
- 235000021355 Stearic acid Nutrition 0.000 description 1
- 102000016553 Stearoyl-CoA Desaturase Human genes 0.000 description 1
- KDYFGRWQOYBRFD-UHFFFAOYSA-N Succinic acid Natural products OC(=O)CCC(O)=O KDYFGRWQOYBRFD-UHFFFAOYSA-N 0.000 description 1
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 1
- 230000024932 T cell mediated immunity Effects 0.000 description 1
- GSEJCLTVZPLZKY-UHFFFAOYSA-N Triethanolamine Chemical compound OCCN(CCO)CCO GSEJCLTVZPLZKY-UHFFFAOYSA-N 0.000 description 1
- DTQVDTLACAAQTR-UHFFFAOYSA-M Trifluoroacetate Chemical compound [O-]C(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-M 0.000 description 1
- YZCKVEUIGOORGS-NJFSPNSNSA-N Tritium Chemical compound [3H] YZCKVEUIGOORGS-NJFSPNSNSA-N 0.000 description 1
- 108060008682 Tumor Necrosis Factor Proteins 0.000 description 1
- 102000000852 Tumor Necrosis Factor-alpha Human genes 0.000 description 1
- 108010037584 Type 4 Cyclic Nucleotide Phosphodiesterases Proteins 0.000 description 1
- 102000014384 Type C Phospholipases Human genes 0.000 description 1
- 108010079194 Type C Phospholipases Proteins 0.000 description 1
- 241000607479 Yersinia pestis Species 0.000 description 1
- QBCRLDPMQHPGIM-QGZVFWFLSA-N [2-fluoro-4-[2-(4-methoxyphenyl)ethynyl]phenyl]-[(3r)-3-hydroxypiperidin-1-yl]methanone Chemical compound C1=CC(OC)=CC=C1C#CC(C=C1F)=CC=C1C(=O)N1C[C@H](O)CCC1 QBCRLDPMQHPGIM-QGZVFWFLSA-N 0.000 description 1
- 239000012190 activator Substances 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 230000000996 additive effect Effects 0.000 description 1
- 239000001361 adipic acid Substances 0.000 description 1
- 235000011037 adipic acid Nutrition 0.000 description 1
- 230000010085 airway hyperresponsiveness Effects 0.000 description 1
- 208000037883 airway inflammation Diseases 0.000 description 1
- 235000010443 alginic acid Nutrition 0.000 description 1
- 229920000615 alginic acid Polymers 0.000 description 1
- 239000000783 alginic acid Substances 0.000 description 1
- 229960001126 alginic acid Drugs 0.000 description 1
- 150000004781 alginic acids Chemical class 0.000 description 1
- 150000001340 alkali metals Chemical class 0.000 description 1
- HFHDHCJBZVLPGP-RWMJIURBSA-N alpha-cyclodextrin Chemical compound OC[C@H]([C@H]([C@@H]([C@H]1O)O)O[C@H]2O[C@@H]([C@@H](O[C@H]3O[C@H](CO)[C@H]([C@@H]([C@H]3O)O)O[C@H]3O[C@H](CO)[C@H]([C@@H]([C@H]3O)O)O[C@H]3O[C@H](CO)[C@H]([C@@H]([C@H]3O)O)O3)[C@H](O)[C@H]2O)CO)O[C@@H]1O[C@H]1[C@H](O)[C@@H](O)[C@@H]3O[C@@H]1CO HFHDHCJBZVLPGP-RWMJIURBSA-N 0.000 description 1
- 229940043377 alpha-cyclodextrin Drugs 0.000 description 1
- AWUCVROLDVIAJX-UHFFFAOYSA-N alpha-glycerophosphate Natural products OCC(O)COP(O)(O)=O AWUCVROLDVIAJX-UHFFFAOYSA-N 0.000 description 1
- BJEPYKJPYRNKOW-UHFFFAOYSA-N alpha-hydroxysuccinic acid Natural products OC(=O)C(O)CC(O)=O BJEPYKJPYRNKOW-UHFFFAOYSA-N 0.000 description 1
- 229910052782 aluminium Inorganic materials 0.000 description 1
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 1
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 1
- 125000003277 amino group Chemical group 0.000 description 1
- 229910021529 ammonia Inorganic materials 0.000 description 1
- 150000003863 ammonium salts Chemical class 0.000 description 1
- 230000000844 anti-bacterial effect Effects 0.000 description 1
- 230000002924 anti-infective effect Effects 0.000 description 1
- 230000000259 anti-tumor effect Effects 0.000 description 1
- 230000005809 anti-tumor immunity Effects 0.000 description 1
- 230000006907 apoptotic process Effects 0.000 description 1
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 description 1
- 150000001491 aromatic compounds Chemical class 0.000 description 1
- 235000010323 ascorbic acid Nutrition 0.000 description 1
- 239000011668 ascorbic acid Substances 0.000 description 1
- 229960005070 ascorbic acid Drugs 0.000 description 1
- 235000003704 aspartic acid Nutrition 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- 229960001716 benzalkonium Drugs 0.000 description 1
- SRSXLGNVWSONIS-UHFFFAOYSA-N benzenesulfonic acid Chemical compound OS(=O)(=O)C1=CC=CC=C1 SRSXLGNVWSONIS-UHFFFAOYSA-N 0.000 description 1
- 229940092714 benzenesulfonic acid Drugs 0.000 description 1
- 125000003785 benzimidazolyl group Chemical group N1=C(NC2=C1C=CC=C2)* 0.000 description 1
- 125000004603 benzisoxazolyl group Chemical group O1N=C(C2=C1C=CC=C2)* 0.000 description 1
- CYDRXTMLKJDRQH-UHFFFAOYSA-N benzododecinium Chemical compound CCCCCCCCCCCC[N+](C)(C)CC1=CC=CC=C1 CYDRXTMLKJDRQH-UHFFFAOYSA-N 0.000 description 1
- 125000000499 benzofuranyl group Chemical group O1C(=CC2=C1C=CC=C2)* 0.000 description 1
- 235000010233 benzoic acid Nutrition 0.000 description 1
- 125000001164 benzothiazolyl group Chemical group S1C(=NC2=C1C=CC=C2)* 0.000 description 1
- 125000004196 benzothienyl group Chemical group S1C(=CC2=C1C=CC=C2)* 0.000 description 1
- QRUDEWIWKLJBPS-UHFFFAOYSA-N benzotriazole Chemical compound C1=CC=C2N[N][N]C2=C1 QRUDEWIWKLJBPS-UHFFFAOYSA-N 0.000 description 1
- 239000012964 benzotriazole Substances 0.000 description 1
- 125000004541 benzoxazolyl group Chemical group O1C(=NC2=C1C=CC=C2)* 0.000 description 1
- YOUGRGFIHBUKRS-UHFFFAOYSA-N benzyl(trimethyl)azanium Chemical compound C[N+](C)(C)CC1=CC=CC=C1 YOUGRGFIHBUKRS-UHFFFAOYSA-N 0.000 description 1
- OQFSQFPPLPISGP-UHFFFAOYSA-N beta-carboxyaspartic acid Natural products OC(=O)C(N)C(C(O)=O)C(O)=O OQFSQFPPLPISGP-UHFFFAOYSA-N 0.000 description 1
- WHGYBXFWUBPSRW-FOUAGVGXSA-N beta-cyclodextrin Chemical compound OC[C@H]([C@H]([C@@H]([C@H]1O)O)O[C@H]2O[C@@H]([C@@H](O[C@H]3O[C@H](CO)[C@H]([C@@H]([C@H]3O)O)O[C@H]3O[C@H](CO)[C@H]([C@@H]([C@H]3O)O)O[C@H]3O[C@H](CO)[C@H]([C@@H]([C@H]3O)O)O[C@H]3O[C@H](CO)[C@H]([C@@H]([C@H]3O)O)O3)[C@H](O)[C@H]2O)CO)O[C@@H]1O[C@H]1[C@H](O)[C@@H](O)[C@@H]3O[C@@H]1CO WHGYBXFWUBPSRW-FOUAGVGXSA-N 0.000 description 1
- 229960004853 betadex Drugs 0.000 description 1
- 230000004071 biological effect Effects 0.000 description 1
- 230000000903 blocking effect Effects 0.000 description 1
- 230000007885 bronchoconstriction Effects 0.000 description 1
- KDYFGRWQOYBRFD-NUQCWPJISA-N butanedioic acid Chemical compound O[14C](=O)CC[14C](O)=O KDYFGRWQOYBRFD-NUQCWPJISA-N 0.000 description 1
- 102100029168 cAMP-specific 3',5'-cyclic phosphodiesterase 4B Human genes 0.000 description 1
- LSPHULWDVZXLIL-QUBYGPBYSA-N camphoric acid Chemical compound CC1(C)[C@H](C(O)=O)CC[C@]1(C)C(O)=O LSPHULWDVZXLIL-QUBYGPBYSA-N 0.000 description 1
- 230000003197 catalytic effect Effects 0.000 description 1
- 230000009134 cell regulation Effects 0.000 description 1
- 210000003169 central nervous system Anatomy 0.000 description 1
- 239000013000 chemical inhibitor Substances 0.000 description 1
- OEYIOHPDSNJKLS-UHFFFAOYSA-N choline Chemical compound C[N+](C)(C)CCO OEYIOHPDSNJKLS-UHFFFAOYSA-N 0.000 description 1
- 229960001231 choline Drugs 0.000 description 1
- 235000013985 cinnamic acid Nutrition 0.000 description 1
- 229930016911 cinnamic acid Natural products 0.000 description 1
- 235000015165 citric acid Nutrition 0.000 description 1
- 208000029742 colonic neoplasm Diseases 0.000 description 1
- 239000013078 crystal Substances 0.000 description 1
- JEVCWSUVFOYBFI-UHFFFAOYSA-N cyanyl Chemical compound N#[C] JEVCWSUVFOYBFI-UHFFFAOYSA-N 0.000 description 1
- 125000000753 cycloalkyl group Chemical group 0.000 description 1
- 125000001995 cyclobutyl group Chemical group [H]C1([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 125000000582 cycloheptyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 description 1
- 231100000135 cytotoxicity Toxicity 0.000 description 1
- 230000003013 cytotoxicity Effects 0.000 description 1
- 229960002887 deanol Drugs 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- 230000007812 deficiency Effects 0.000 description 1
- 208000025729 dengue disease Diseases 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- WOWBFOBYOAGEEA-UHFFFAOYSA-N diafenthiuron Chemical compound CC(C)C1=C(NC(=S)NC(C)(C)C)C(C(C)C)=CC(OC=2C=CC=CC=2)=C1 WOWBFOBYOAGEEA-UHFFFAOYSA-N 0.000 description 1
- HPNMFZURTQLUMO-UHFFFAOYSA-N diethylamine Chemical compound CCNCC HPNMFZURTQLUMO-UHFFFAOYSA-N 0.000 description 1
- 230000004069 differentiation Effects 0.000 description 1
- MGHPNCMVUAKAIE-UHFFFAOYSA-N diphenylmethanamine Chemical compound C=1C=CC=CC=1C(N)C1=CC=CC=C1 MGHPNCMVUAKAIE-UHFFFAOYSA-N 0.000 description 1
- 238000009826 distribution Methods 0.000 description 1
- 125000005883 dithianyl group Chemical group 0.000 description 1
- MOTZDAYCYVMXPC-UHFFFAOYSA-N dodecyl hydrogen sulfate Chemical compound CCCCCCCCCCCCOS(O)(=O)=O MOTZDAYCYVMXPC-UHFFFAOYSA-N 0.000 description 1
- 230000007783 downstream signaling Effects 0.000 description 1
- XPOQHMRABVBWPR-ZDUSSCGKSA-N efavirenz Chemical compound C([C@]1(C2=CC(Cl)=CC=C2NC(=O)O1)C(F)(F)F)#CC1CC1 XPOQHMRABVBWPR-ZDUSSCGKSA-N 0.000 description 1
- 229960003804 efavirenz Drugs 0.000 description 1
- 239000012636 effector Substances 0.000 description 1
- 210000002472 endoplasmic reticulum Anatomy 0.000 description 1
- 230000002255 enzymatic effect Effects 0.000 description 1
- CCIVGXIOQKPBKL-UHFFFAOYSA-M ethanesulfonate Chemical compound CCS([O-])(=O)=O CCIVGXIOQKPBKL-UHFFFAOYSA-M 0.000 description 1
- 230000017188 evasion or tolerance of host immune response Effects 0.000 description 1
- 230000001747 exhibiting effect Effects 0.000 description 1
- 230000008622 extracellular signaling Effects 0.000 description 1
- 235000019253 formic acid Nutrition 0.000 description 1
- 238000009472 formulation Methods 0.000 description 1
- 238000001640 fractional crystallisation Methods 0.000 description 1
- 239000012458 free base Substances 0.000 description 1
- 239000001530 fumaric acid Substances 0.000 description 1
- 229960002598 fumaric acid Drugs 0.000 description 1
- 125000000524 functional group Chemical group 0.000 description 1
- 125000002541 furyl group Chemical group 0.000 description 1
- GDSRMADSINPKSL-HSEONFRVSA-N gamma-cyclodextrin Chemical compound OC[C@H]([C@H]([C@@H]([C@H]1O)O)O[C@H]2O[C@@H]([C@@H](O[C@H]3O[C@H](CO)[C@H]([C@@H]([C@H]3O)O)O[C@H]3O[C@H](CO)[C@H]([C@@H]([C@H]3O)O)O[C@H]3O[C@H](CO)[C@H]([C@@H]([C@H]3O)O)O[C@H]3O[C@H](CO)[C@H]([C@@H]([C@H]3O)O)O[C@H]3O[C@H](CO)[C@H]([C@@H]([C@H]3O)O)O3)[C@H](O)[C@H]2O)CO)O[C@@H]1O[C@H]1[C@H](O)[C@@H](O)[C@@H]3O[C@@H]1CO GDSRMADSINPKSL-HSEONFRVSA-N 0.000 description 1
- 229940080345 gamma-cyclodextrin Drugs 0.000 description 1
- 238000003209 gene knockout Methods 0.000 description 1
- 210000004602 germ cell Anatomy 0.000 description 1
- 208000005017 glioblastoma Diseases 0.000 description 1
- 235000012208 gluconic acid Nutrition 0.000 description 1
- 229950006191 gluconic acid Drugs 0.000 description 1
- 230000036252 glycation Effects 0.000 description 1
- 230000012010 growth Effects 0.000 description 1
- 229940093915 gynecological organic acid Drugs 0.000 description 1
- 125000001188 haloalkyl group Chemical group 0.000 description 1
- 229910052736 halogen Inorganic materials 0.000 description 1
- 150000002367 halogens Chemical class 0.000 description 1
- 208000010710 hepatitis C virus infection Diseases 0.000 description 1
- NAQMVNRVTILPCV-UHFFFAOYSA-N hexane-1,6-diamine Chemical compound NCCCCCCN NAQMVNRVTILPCV-UHFFFAOYSA-N 0.000 description 1
- XMBWDFGMSWQBCA-UHFFFAOYSA-N hydrogen iodide Chemical compound I XMBWDFGMSWQBCA-UHFFFAOYSA-N 0.000 description 1
- 229940071870 hydroiodic acid Drugs 0.000 description 1
- 230000007062 hydrolysis Effects 0.000 description 1
- 238000006460 hydrolysis reaction Methods 0.000 description 1
- 125000004029 hydroxymethyl group Chemical group [H]OC([H])([H])* 0.000 description 1
- 230000003463 hyperproliferative effect Effects 0.000 description 1
- 125000002883 imidazolyl group Chemical group 0.000 description 1
- 210000002865 immune cell Anatomy 0.000 description 1
- 208000026278 immune system disease Diseases 0.000 description 1
- 230000007813 immunodeficiency Effects 0.000 description 1
- 230000001976 improved effect Effects 0.000 description 1
- 238000000338 in vitro Methods 0.000 description 1
- 238000011503 in vivo imaging Methods 0.000 description 1
- 125000003453 indazolyl group Chemical group N1N=C(C2=C1C=CC=C2)* 0.000 description 1
- PZOUSPYUWWUPPK-UHFFFAOYSA-N indole Natural products CC1=CC=CC2=C1C=CN2 PZOUSPYUWWUPPK-UHFFFAOYSA-N 0.000 description 1
- RKJUIXBNRJVNHR-UHFFFAOYSA-N indolenine Natural products C1=CC=C2CC=NC2=C1 RKJUIXBNRJVNHR-UHFFFAOYSA-N 0.000 description 1
- 125000001041 indolyl group Chemical group 0.000 description 1
- 230000002458 infectious effect Effects 0.000 description 1
- 208000027866 inflammatory disease Diseases 0.000 description 1
- 230000002401 inhibitory effect Effects 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 238000011081 inoculation Methods 0.000 description 1
- CDAISMWEOUEBRE-GPIVLXJGSA-N inositol Chemical compound O[C@H]1[C@H](O)[C@@H](O)[C@H](O)[C@H](O)[C@@H]1O CDAISMWEOUEBRE-GPIVLXJGSA-N 0.000 description 1
- 229960000367 inositol Drugs 0.000 description 1
- 229940047122 interleukins Drugs 0.000 description 1
- 230000009545 invasion Effects 0.000 description 1
- PNDPGZBMCMUPRI-UHFFFAOYSA-N iodine Chemical compound II PNDPGZBMCMUPRI-UHFFFAOYSA-N 0.000 description 1
- 229910052740 iodine Inorganic materials 0.000 description 1
- 125000000904 isoindolyl group Chemical group C=1(NC=C2C=CC=CC12)* 0.000 description 1
- 125000001972 isopentyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000002183 isoquinolinyl group Chemical group C1(=NC=CC2=CC=CC=C12)* 0.000 description 1
- 125000001786 isothiazolyl group Chemical group 0.000 description 1
- 125000000842 isoxazolyl group Chemical group 0.000 description 1
- 238000011813 knockout mouse model Methods 0.000 description 1
- 235000014655 lactic acid Nutrition 0.000 description 1
- 239000004310 lactic acid Substances 0.000 description 1
- 239000003446 ligand Substances 0.000 description 1
- 239000011777 magnesium Substances 0.000 description 1
- 229910052749 magnesium Inorganic materials 0.000 description 1
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 description 1
- 239000011976 maleic acid Substances 0.000 description 1
- 235000011090 malic acid Nutrition 0.000 description 1
- 239000001630 malic acid Substances 0.000 description 1
- 238000007726 management method Methods 0.000 description 1
- 229960002510 mandelic acid Drugs 0.000 description 1
- 238000004949 mass spectrometry Methods 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 230000001404 mediated effect Effects 0.000 description 1
- 201000001441 melanoma Diseases 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- 230000037323 metabolic rate Effects 0.000 description 1
- 229910052751 metal Inorganic materials 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- LVWZTYCIRDMTEY-UHFFFAOYSA-N metamizole Chemical compound O=C1C(N(CS(O)(=O)=O)C)=C(C)N(C)N1C1=CC=CC=C1 LVWZTYCIRDMTEY-UHFFFAOYSA-N 0.000 description 1
- 229940098779 methanesulfonic acid Drugs 0.000 description 1
- WBYWAXJHAXSJNI-UHFFFAOYSA-N methyl p-hydroxycinnamate Natural products OC(=O)C=CC1=CC=CC=C1 WBYWAXJHAXSJNI-UHFFFAOYSA-N 0.000 description 1
- IZXGZAJMDLJLMF-UHFFFAOYSA-N methylaminomethanol Chemical compound CNCO IZXGZAJMDLJLMF-UHFFFAOYSA-N 0.000 description 1
- LVHBHZANLOWSRM-UHFFFAOYSA-N methylenebutanedioic acid Natural products OC(=O)CC(=C)C(O)=O LVHBHZANLOWSRM-UHFFFAOYSA-N 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 125000006578 monocyclic heterocycloalkyl group Chemical group 0.000 description 1
- LNOPIUAQISRISI-UHFFFAOYSA-N n'-hydroxy-2-propan-2-ylsulfonylethanimidamide Chemical compound CC(C)S(=O)(=O)CC(N)=NO LNOPIUAQISRISI-UHFFFAOYSA-N 0.000 description 1
- AJFDBNQQDYLMJN-UHFFFAOYSA-N n,n-diethylacetamide Chemical compound CCN(CC)C(C)=O AJFDBNQQDYLMJN-UHFFFAOYSA-N 0.000 description 1
- SYSQUGFVNFXIIT-UHFFFAOYSA-N n-[4-(1,3-benzoxazol-2-yl)phenyl]-4-nitrobenzenesulfonamide Chemical class C1=CC([N+](=O)[O-])=CC=C1S(=O)(=O)NC1=CC=C(C=2OC3=CC=CC=C3N=2)C=C1 SYSQUGFVNFXIIT-UHFFFAOYSA-N 0.000 description 1
- 125000001298 n-hexoxy group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])O* 0.000 description 1
- YZMHQCWXYHARLS-UHFFFAOYSA-N naphthalene-1,2-disulfonic acid Chemical compound C1=CC=CC2=C(S(O)(=O)=O)C(S(=O)(=O)O)=CC=C21 YZMHQCWXYHARLS-UHFFFAOYSA-N 0.000 description 1
- KVBGVZZKJNLNJU-UHFFFAOYSA-N naphthalene-2-sulfonic acid Chemical compound C1=CC=CC2=CC(S(=O)(=O)O)=CC=C21 KVBGVZZKJNLNJU-UHFFFAOYSA-N 0.000 description 1
- 210000000822 natural killer cell Anatomy 0.000 description 1
- 125000001971 neopentyl group Chemical group [H]C([*])([H])C(C([H])([H])[H])(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 230000001613 neoplastic effect Effects 0.000 description 1
- 230000004770 neurodegeneration Effects 0.000 description 1
- 208000015122 neurodegenerative disease Diseases 0.000 description 1
- 229960000689 nevirapine Drugs 0.000 description 1
- 229960003512 nicotinic acid Drugs 0.000 description 1
- 239000011664 nicotinic acid Substances 0.000 description 1
- 235000001968 nicotinic acid Nutrition 0.000 description 1
- 229910017604 nitric acid Inorganic materials 0.000 description 1
- 125000002868 norbornyl group Chemical group C12(CCC(CC1)C2)* 0.000 description 1
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 1
- OQCDKBAXFALNLD-UHFFFAOYSA-N octadecanoic acid Natural products CCCCCCCC(C)CCCCCCCCC(O)=O OQCDKBAXFALNLD-UHFFFAOYSA-N 0.000 description 1
- 229950009755 odanacatib Drugs 0.000 description 1
- 235000005985 organic acids Nutrition 0.000 description 1
- 201000008968 osteosarcoma Diseases 0.000 description 1
- 125000001715 oxadiazolyl group Chemical group 0.000 description 1
- 235000006408 oxalic acid Nutrition 0.000 description 1
- 150000007978 oxazole derivatives Chemical class 0.000 description 1
- 125000005968 oxazolinyl group Chemical group 0.000 description 1
- 125000002971 oxazolyl group Chemical group 0.000 description 1
- 125000003566 oxetanyl group Chemical group 0.000 description 1
- 230000003647 oxidation Effects 0.000 description 1
- 125000001820 oxy group Chemical group [*:1]O[*:2] 0.000 description 1
- 125000004430 oxygen atom Chemical group O* 0.000 description 1
- 229910052763 palladium Inorganic materials 0.000 description 1
- KDLHZDBZIXYQEI-UHFFFAOYSA-N palladium Substances [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 1
- WLJNZVDCPSBLRP-UHFFFAOYSA-N pamoic acid Chemical compound C1=CC=C2C(CC=3C4=CC=CC=C4C=C(C=3O)C(=O)O)=C(O)C(C(O)=O)=CC2=C1 WLJNZVDCPSBLRP-UHFFFAOYSA-N 0.000 description 1
- 201000002528 pancreatic cancer Diseases 0.000 description 1
- 108010029648 pantetheinase Proteins 0.000 description 1
- 244000052769 pathogen Species 0.000 description 1
- 125000006340 pentafluoro ethyl group Chemical group FC(F)(F)C(F)(F)* 0.000 description 1
- 125000003538 pentan-3-yl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])C([H])([H])[H] 0.000 description 1
- 230000002085 persistent effect Effects 0.000 description 1
- WTJKGGKOPKCXLL-RRHRGVEJSA-N phosphatidylcholine Chemical compound CCCCCCCCCCCCCCCC(=O)OC[C@H](COP([O-])(=O)OCC[N+](C)(C)C)OC(=O)CCCCCCCC=CCCCCCCCC WTJKGGKOPKCXLL-RRHRGVEJSA-N 0.000 description 1
- 229910052698 phosphorus Inorganic materials 0.000 description 1
- 239000011574 phosphorus Substances 0.000 description 1
- 102000020233 phosphotransferase Human genes 0.000 description 1
- IUGYQRQAERSCNH-UHFFFAOYSA-N pivalic acid Chemical compound CC(C)(C)C(O)=O IUGYQRQAERSCNH-UHFFFAOYSA-N 0.000 description 1
- 229910052697 platinum Inorganic materials 0.000 description 1
- XAEFZNCEHLXOMS-UHFFFAOYSA-M potassium benzoate Chemical compound [K+].[O-]C(=O)C1=CC=CC=C1 XAEFZNCEHLXOMS-UHFFFAOYSA-M 0.000 description 1
- 150000003141 primary amines Chemical class 0.000 description 1
- 230000009290 primary effect Effects 0.000 description 1
- MFDFERRIHVXMIY-UHFFFAOYSA-N procaine Chemical compound CCN(CC)CCOC(=O)C1=CC=C(N)C=C1 MFDFERRIHVXMIY-UHFFFAOYSA-N 0.000 description 1
- 229960004919 procaine Drugs 0.000 description 1
- 230000002035 prolonged effect Effects 0.000 description 1
- 125000006238 prop-1-en-1-yl group Chemical group [H]\C(*)=C(/[H])C([H])([H])[H] 0.000 description 1
- 230000000069 prophylactic effect Effects 0.000 description 1
- 235000019260 propionic acid Nutrition 0.000 description 1
- FVSKHRXBFJPNKK-UHFFFAOYSA-N propionitrile Chemical compound CCC#N FVSKHRXBFJPNKK-UHFFFAOYSA-N 0.000 description 1
- ODLMAHJVESYWTB-UHFFFAOYSA-N propylbenzene Chemical compound CCCC1=CC=CC=C1 ODLMAHJVESYWTB-UHFFFAOYSA-N 0.000 description 1
- 230000004063 proteosomal degradation Effects 0.000 description 1
- 208000008128 pulmonary tuberculosis Diseases 0.000 description 1
- 125000000561 purinyl group Chemical group N1=C(N=C2N=CNC2=C1)* 0.000 description 1
- WKSAUQYGYAYLPV-UHFFFAOYSA-N pyrimethamine Chemical compound CCC1=NC(N)=NC(N)=C1C1=CC=C(Cl)C=C1 WKSAUQYGYAYLPV-UHFFFAOYSA-N 0.000 description 1
- 229960000611 pyrimethamine Drugs 0.000 description 1
- 229940083082 pyrimidine derivative acting on arteriolar smooth muscle Drugs 0.000 description 1
- 150000003230 pyrimidines Chemical class 0.000 description 1
- 125000000714 pyrimidinyl group Chemical group 0.000 description 1
- 125000000168 pyrrolyl group Chemical group 0.000 description 1
- 229940107700 pyruvic acid Drugs 0.000 description 1
- 125000001453 quaternary ammonium group Chemical group 0.000 description 1
- 125000002294 quinazolinyl group Chemical group N1=C(N=CC2=CC=CC=C12)* 0.000 description 1
- IUVKMZGDUIUOCP-BTNSXGMBSA-N quinbolone Chemical compound O([C@H]1CC[C@H]2[C@H]3[C@@H]([C@]4(C=CC(=O)C=C4CC3)C)CC[C@@]21C)C1=CCCC1 IUVKMZGDUIUOCP-BTNSXGMBSA-N 0.000 description 1
- 230000002285 radioactive effect Effects 0.000 description 1
- 239000011541 reaction mixture Substances 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 230000002207 retinal effect Effects 0.000 description 1
- 229910052703 rhodium Inorganic materials 0.000 description 1
- RZJQGNCSTQAWON-UHFFFAOYSA-N rofecoxib Chemical compound C1=CC(S(=O)(=O)C)=CC=C1C1=C(C=2C=CC=CC=2)C(=O)OC1 RZJQGNCSTQAWON-UHFFFAOYSA-N 0.000 description 1
- 229960000371 rofecoxib Drugs 0.000 description 1
- 229960004889 salicylic acid Drugs 0.000 description 1
- 229940043230 sarcosine Drugs 0.000 description 1
- HFHDHCJBZVLPGP-UHFFFAOYSA-N schardinger α-dextrin Chemical compound O1C(C(C2O)O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC(C(O)C2O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC2C(O)C(O)C1OC2CO HFHDHCJBZVLPGP-UHFFFAOYSA-N 0.000 description 1
- CDAISMWEOUEBRE-UHFFFAOYSA-N scyllo-inosotol Natural products OC1C(O)C(O)C(O)C(O)C1O CDAISMWEOUEBRE-UHFFFAOYSA-N 0.000 description 1
- 125000003548 sec-pentyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 150000003335 secondary amines Chemical class 0.000 description 1
- 229960001153 serine Drugs 0.000 description 1
- 150000003384 small molecules Chemical class 0.000 description 1
- AWUCVROLDVIAJX-GSVOUGTGSA-N sn-glycerol 3-phosphate Chemical compound OC[C@@H](O)COP(O)(O)=O AWUCVROLDVIAJX-GSVOUGTGSA-N 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- 159000000000 sodium salts Chemical class 0.000 description 1
- 239000002904 solvent Substances 0.000 description 1
- 241000894007 species Species 0.000 description 1
- WWUZIQQURGPMPG-KRWOKUGFSA-N sphingosine Chemical compound CCCCCCCCCCCCC\C=C\[C@@H](O)[C@@H](N)CO WWUZIQQURGPMPG-KRWOKUGFSA-N 0.000 description 1
- 238000010561 standard procedure Methods 0.000 description 1
- 239000007858 starting material Substances 0.000 description 1
- 239000008117 stearic acid Substances 0.000 description 1
- 210000004500 stellate cell Anatomy 0.000 description 1
- 210000000130 stem cell Anatomy 0.000 description 1
- 159000000008 strontium salts Chemical class 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- 125000000446 sulfanediyl group Chemical group *S* 0.000 description 1
- 239000011593 sulfur Substances 0.000 description 1
- 239000013589 supplement Substances 0.000 description 1
- 108010017101 telaprevir Proteins 0.000 description 1
- BBAWEDCPNXPBQM-GDEBMMAJSA-N telaprevir Chemical compound N([C@H](C(=O)N[C@H](C(=O)N1C[C@@H]2CCC[C@@H]2[C@H]1C(=O)N[C@@H](CCC)C(=O)C(=O)NC1CC1)C(C)(C)C)C1CCCCC1)C(=O)C1=CN=CC=N1 BBAWEDCPNXPBQM-GDEBMMAJSA-N 0.000 description 1
- 229960002935 telaprevir Drugs 0.000 description 1
- 125000001973 tert-pentyl group Chemical group [H]C([H])([H])C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 150000003512 tertiary amines Chemical class 0.000 description 1
- DZLFLBLQUQXARW-UHFFFAOYSA-N tetrabutylammonium Chemical compound CCCC[N+](CCCC)(CCCC)CCCC DZLFLBLQUQXARW-UHFFFAOYSA-N 0.000 description 1
- CBXCPBUEXACCNR-UHFFFAOYSA-N tetraethylammonium Chemical compound CC[N+](CC)(CC)CC CBXCPBUEXACCNR-UHFFFAOYSA-N 0.000 description 1
- 125000003718 tetrahydrofuranyl group Chemical group 0.000 description 1
- 125000001412 tetrahydropyranyl group Chemical group 0.000 description 1
- 125000004632 tetrahydrothiopyranyl group Chemical group S1C(CCCC1)* 0.000 description 1
- QEMXHQIAXOOASZ-UHFFFAOYSA-N tetramethylammonium Chemical compound C[N+](C)(C)C QEMXHQIAXOOASZ-UHFFFAOYSA-N 0.000 description 1
- 125000003831 tetrazolyl group Chemical group 0.000 description 1
- 229940124597 therapeutic agent Drugs 0.000 description 1
- 125000001113 thiadiazolyl group Chemical group 0.000 description 1
- 125000002769 thiazolinyl group Chemical group 0.000 description 1
- 125000000335 thiazolyl group Chemical group 0.000 description 1
- 125000002053 thietanyl group Chemical group 0.000 description 1
- 125000001166 thiolanyl group Chemical group 0.000 description 1
- 210000001519 tissue Anatomy 0.000 description 1
- 239000003053 toxin Substances 0.000 description 1
- ODLHGICHYURWBS-LKONHMLTSA-N trappsol cyclo Chemical compound CC(O)COC[C@H]([C@H]([C@@H]([C@H]1O)O)O[C@H]2O[C@@H]([C@@H](O[C@H]3O[C@H](COCC(C)O)[C@H]([C@@H]([C@H]3O)O)O[C@H]3O[C@H](COCC(C)O)[C@H]([C@@H]([C@H]3O)O)O[C@H]3O[C@H](COCC(C)O)[C@H]([C@@H]([C@H]3O)O)O[C@H]3O[C@H](COCC(C)O)[C@H]([C@@H]([C@H]3O)O)O3)[C@H](O)[C@H]2O)COCC(O)C)O[C@@H]1O[C@H]1[C@H](O)[C@@H](O)[C@@H]3O[C@@H]1COCC(C)O ODLHGICHYURWBS-LKONHMLTSA-N 0.000 description 1
- 125000001425 triazolyl group Chemical group 0.000 description 1
- ITMCEJHCFYSIIV-UHFFFAOYSA-N triflic acid Chemical compound OS(=O)(=O)C(F)(F)F ITMCEJHCFYSIIV-UHFFFAOYSA-N 0.000 description 1
- 125000000102 trisulfanyl group Chemical group [*]SSS[H] 0.000 description 1
- 229910052722 tritium Inorganic materials 0.000 description 1
- 230000004614 tumor growth Effects 0.000 description 1
- 230000007306 turnover Effects 0.000 description 1
- 230000029812 viral genome replication Effects 0.000 description 1
- 238000012447 xenograft mouse model Methods 0.000 description 1
- 150000003751 zinc Chemical class 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D277/00—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings
- C07D277/02—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings not condensed with other rings
- C07D277/20—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members
- C07D277/32—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D277/38—Nitrogen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D277/00—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings
- C07D277/02—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings not condensed with other rings
- C07D277/20—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members
- C07D277/32—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D277/38—Nitrogen atoms
- C07D277/42—Amino or imino radicals substituted by hydrocarbon or substituted hydrocarbon radicals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/425—Thiazoles
- A61K31/426—1,3-Thiazoles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/425—Thiazoles
- A61K31/427—Thiazoles not condensed and containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/4427—Non condensed pyridines; Hydrogenated derivatives thereof containing further heterocyclic ring systems
- A61K31/4439—Non condensed pyridines; Hydrogenated derivatives thereof containing further heterocyclic ring systems containing a five-membered ring with nitrogen as a ring hetero atom, e.g. omeprazole
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/445—Non condensed piperidines, e.g. piperocaine
- A61K31/4523—Non condensed piperidines, e.g. piperocaine containing further heterocyclic ring systems
- A61K31/454—Non condensed piperidines, e.g. piperocaine containing further heterocyclic ring systems containing a five-membered ring with nitrogen as a ring hetero atom, e.g. pimozide, domperidone
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/47—Quinolines; Isoquinolines
- A61K31/4709—Non-condensed quinolines and containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/47—Quinolines; Isoquinolines
- A61K31/472—Non-condensed isoquinolines, e.g. papaverine
- A61K31/4725—Non-condensed isoquinolines, e.g. papaverine containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/496—Non-condensed piperazines containing further heterocyclic rings, e.g. rifampin, thiothixene or sparfloxacin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/519—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim ortho- or peri-condensed with heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/535—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with at least one nitrogen and one oxygen as the ring hetero atoms, e.g. 1,2-oxazines
- A61K31/5375—1,4-Oxazines, e.g. morpholine
- A61K31/5377—1,4-Oxazines, e.g. morpholine not condensed and containing further heterocyclic rings, e.g. timolol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/55—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having seven-membered rings, e.g. azelastine, pentylenetetrazole
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D277/00—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings
- C07D277/02—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings not condensed with other rings
- C07D277/20—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members
- C07D277/32—Heterocyclic compounds containing 1,3-thiazole or hydrogenated 1,3-thiazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D277/38—Nitrogen atoms
- C07D277/44—Acylated amino or imino radicals
- C07D277/46—Acylated amino or imino radicals by carboxylic acids, or sulfur or nitrogen analogues thereof
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings
- C07D417/06—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings linked by a carbon chain containing only aliphatic carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings
- C07D417/10—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings linked by a carbon chain containing aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings
- C07D417/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/08—Bridged systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D487/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00
- C07D487/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00 in which the condensed system contains two hetero rings
- C07D487/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2803—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily
- C07K16/2818—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily against CD28 or CD152
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2803—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily
- C07K16/2827—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily against B7 molecules, e.g. CD80, CD86
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2300/00—Mixtures or combinations of active ingredients, wherein at least one active ingredient is fully defined in groups A61K31/00 - A61K41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07B—GENERAL METHODS OF ORGANIC CHEMISTRY; APPARATUS THEREFOR
- C07B2200/00—Indexing scheme relating to specific properties of organic compounds
- C07B2200/07—Optical isomers
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Epidemiology (AREA)
- Immunology (AREA)
- Biophysics (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Molecular Biology (AREA)
- Genetics & Genomics (AREA)
- Biochemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Plural Heterocyclic Compounds (AREA)
- Thiazole And Isothizaole Compounds (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
Abstract
Description
本發明涵蓋如本文所描述及定義之通式(I)的經取代胺基噻唑化合物;製備該等化合物、適用於製備該等化合物之中間化合物、包含該等化合物之醫藥組合物及組合的方法;及該等化合物作為單一藥劑或與其他活性成分組合用於製備用於治療或預防疾病,特定言之二醯基甘油激酶澤塔(DGKzeta,DGKζ)調節病症之醫藥組合物的用途。
通式(I)化合物抑制DGKζ,且藉此增強T細胞介導之免疫反應。此為一種新穎策略,其使用患者自身之免疫系統來克服由許多贅生性病症(個別地,癌症)所利用之免疫逃避策略且藉此增強抗腫瘤免疫性。此外,該等化合物尤其用於治療病症,諸如病毒感染或具有失調免疫反應之病狀或與異常DGKζ信號傳導相關之其他病症。
本發明進一步係關於一種通式(I)化合物之用途,其用於製備用於增強T細胞介導之免疫反應之醫藥組合物。
本發明進一步係關於一種通式(I)化合物用途用途,其用於製備用於治療癌症之醫藥組合物。
本發明進一步係關於一種通式(I)化合物之用途,其用於製備用於治療或預防病毒感染、淋巴增生病症、哮喘、眼病及2型糖尿病/胰島素抗性之醫藥組合物。
二醯基甘油激酶(DGK)表示催化膜脂質sn-1,2二醯基甘油(DAG)磷酸化以形成磷脂酸(PA)之酶家族(T.O. Eichmann及A. Lass, Cell. Mol. Life Sci. 2015, 72, 3931-3952)。在T細胞中,在活化磷脂酶C之γ1同功型(PLCγ1)且將磷脂醯肌醇4,5-二磷酸(PIP2)裂解成DAG及額外第二信使肌醇1,4,5-三磷酸(IP3)之後,在T細胞受體(TCR)下游形成DAG (S. Krishna及X.-P. Zhong, Front. Immunol. 2013, 4, 178)。儘管,IP3在促進自內質網釋放鈣方面至關重要,但DAG與TCR信號轉導中重要的其他蛋白質(諸如蛋白激酶Cθ (E. J. Quann等人, Nat. Immunol. 2011, 12 (7), 647-654)及Ras活化蛋白RasGRP1 (S. Krishna及X.-P. Zhong, Front. Immunol. 2013, 4, 178)相互作用。儘管已知三種DGK同功型[DGKα(DGKalpha)、DGKδ(DGKdelta)及DGKζ(DGKzeta)]存在於T細胞內,但認為僅DGKα及DGKζ兩者在促進TCR下游之DAG代謝方面起重要作用(R. P. Joshi及G. A. Koretzky, Int. J. Mol. Sci. 2013, 14 (4), 6649-6673)。
藉由生殖系缺失或利用化學抑制劑靶向T細胞中之DGKζ之活性引起T細胞之增強且持久的下游信號傳導,作為藉由下游分子之延長磷酸化評定,該等下游分子諸如胞外信號相關激酶1/2 (ERK1/2)及NFκB (X.-P.-Zhong等人, Nat. Immunol. 2003, 4, 882-890;B. A. Olenchock等人, Nat. Immunol. 2006, 7 (11), 1174-1181;M. J. Riese等人, J. Biol. Chem. 2011, 286, 5254-5265;E. M. Wesley等人, ImmunoHorizons 2018, 2 (4), 107-118)。
T細胞中DGKζ之缺失導致效應細胞介素(諸如IL2、IFNγ)之產生增強及增殖增強(X.-P. Zhong等人, Nat. Immunol. 2003, 4, 882-890;B. A. Olenchock等人, Nat. Immunol. 2006, 7 (11), 1174-1181;E. M. Riese等人, J. Biol. Chem. 2011, 286, 5254-5264)。
相較於對照,在接種C1498.SIY白血病細胞之後,DGKζ缺陷型T細胞之授受性轉移降低白血病負荷。此外,DGKζ缺陷型T細胞至少部分地對PD1介導之抑制性信號具有抗性(W. Jing等人, Cancer Res. 2017, 77 (20), 5676-5686)。另外,相較於對照,在胰臟腫瘤模型之原位腫瘤注射之後,DGKζ缺陷型小鼠的腫瘤大小減小(E. M. Wesley等人, ImmunoHorizons, 2018, 2 (4), 107-118)。此外,S. Wee等人用各種同基因型腫瘤細胞株(MC38結腸癌、B16F1黑色素瘤及C1498白血病)接種C57BL/6小鼠,且分析在存在或不存在抗PD1處理下DGKζ缺陷型小鼠之間的存活期及腫瘤生長。在三個模型系統中,DGKζ-/-小鼠抑制皮下植入的腫瘤細胞之生長,且在腫瘤對照中DGKζ缺陷及抗PD1之組合為相加性的(S. Wee等人, 美國癌症研究協會2019年度會議會議論文(Proceedings of the American Association for CancerResearch Annual Meeting 2019);Cancer Res. 2019, 79 (13增刊):摘要編號936)。
此等發現表明,DGKζ可充當用於增強T細胞抗腫瘤活性之適用目標。
另外,嵌合抗原受體(chimeric antigen receptor;CAR)-DGKζ缺陷型T細胞之授受性轉移表明相較於野生型CAR T細胞,在與DGKα基因剔除組合治療鼠類間皮瘤(M. J. Riese等人, Cancer Res. 2013, 73 (12), 3566-3577)及神經膠母細胞瘤異種移植小鼠模型(I.-Y. Jung等人, Cancer Res. 2018, 78 (16), 4692-4703)方面之功效增加。
此外,DGKζ缺陷型小鼠裝設比野生型小鼠對於淋巴球性脈絡叢腦膜炎病毒感染更穩固的免疫反應(X.-P. Zhong等人, Nat. Immunol. 2003, 4, 882-890)。
DGKζ亦與自然殺手(NK)細胞有關。在經由多種活化受體刺激後,來自缺乏DGKζ之小鼠之NK細胞呈現呈ERK依賴性方式的增加的細胞介素產生及去顆粒。另外,其針對腫瘤細胞株具有改良的細胞毒性功能。(E. Yang等人J. Immunol. 2016, 197(3), 934-41。)
除免疫細胞調節以外,DGKζ亦在癌症方面起作用,調節癌細胞進展之多種態樣,包括增殖、細胞凋亡、存活期、侵襲及致瘤性,例如在骨肉瘤、大腸癌、乳癌、前列腺癌、神經膠質瘤及白血病模型中(W. Yu等人, Front. Oncol. 2019, 8:655;K. Cai等人, BMC Cancer 2014, 14:208;J. Diao等人, Mol. Neurobiol. 2016; 53, 5425-35;H. Li等人Pharmazie 2019, 74(7): 418-422)。
另外,DGKζ基因剔除減少小鼠中之氣道炎症及氣道高反應性且亦藉由阻斷T輔助細胞2 (TH2)分化活體外減少人類氣道樣品之支氣管收縮(B. A. Singh等人, Sci. Signal. 2019, 12: eaax3332)。
總之,來自此等研究之發現說明,限制T細胞及腫瘤細胞中之DGKζ活性可證明在產生針對病原體及腫瘤之更劇烈的免疫反應及在緩解Th2驅動的(自體)免疫疾病(在再平衡免疫系統中)方面有價值。
此外,DGKα之抑制具有逆轉X性聯淋巴增生性疾病(XLP-1)患者中出現的危及生命之埃-巴二氏病毒(Epstein-Barr virus;EBV)-相關免疫病理學的潛能(E. Ruffo等人, Sci. Transl. Med. 2016, 8: (321):321ra7;S. Velnati等人, Eur. J. Med. Chem. 2019, 164, 378-390)。基於基本作用模式,可假定DGKζ之抑制將具有類似效果。
在氧誘導的視網膜病變模型中,DGKα-抑制劑II (R59949)可抑制視網膜新血管生成且保護視網膜星狀細胞(L. Yang等人, J. Mol. Neurosci. 2015, 56, 78-88)。此外,基於基本作用模式,可假定DGKζ之抑制將具有類似效果。
在DGKζ基因剔除小鼠中,顯示DGKζ缺陷增加針對胰島素抗性之保護(B. Benziane等人, J. Lipid Res. 2017, 58 (12), 2324-2333)。
總體而言,抑制DGKζ活性在直接靶向腫瘤以及處理病毒感染、淋巴增生病症、哮喘、眼病及2型糖尿病/胰島素抗性方面具有治療潛能。
先前技術
WO2020/006016及WO2020/006018描述作為用於治療病毒感染及增生性病症(諸如癌症)之T細胞活化因子之萘啶酮化合物,其抑制DGKα及/或DGKζ之活性。WO2021/041588描述作為用於治療病毒感染及增生性病症(諸如癌症)之T細胞活化因子之吡啶并嘧啶酮基化合物,其抑制DGKα及/或DGKζ之活性。
具有與噻唑核心之C-2連接之經取代胺基之2,4,5-三取代三唑衍生物已揭示於在各種技術情況下但不在DGK抑制之情況下的公開專利申請案中。
WO 2014/181287揭示作為介白素17及腫瘤壞死因子α之抑制劑之雜環基化合物。
WO 2014/173904揭示具有抗菌活性之化合物。
WO 2009/149054揭示用於治療或預防登革熱感染(Dengue fever infection)之小分子抑制劑。
WO 2007/130075揭示作為人類硬脂醯基-CoA去飽和酶抑制劑之胺基噻唑衍生物。
WO 2012/064715揭示關於活化化合物及其目標之熱休克轉錄因子之組合物及方法。
WO 2005/103022揭示作為黑皮素原受體調節劑之經取代噻唑及嘧啶衍生物。
CN 106109467揭示芳族化合物(包括噻唑)在治療吡𠯤甲醯胺抗性肺結核方面之醫療應用。
WO 2015/199206揭示作為TRPV4抑制劑之衍生自六員環之化合物。
WO 2015/046193揭示作為TRPV4抑制劑之芳族雜環胺衍生物。
CN 103159695揭示能夠限制人類免疫缺乏症(HIV)病毒複製且有效針對抗藥性HIV病毒株之噻唑化合物。
WO 2013/056684揭示作為二氫乳清酸去氫酶(DHODH)抑制劑之噻唑衍生物。
WO 2013/033037揭示作為抗傳染性蛋白顆粒化合物之各種化學型之化合物,尤其噻唑衍生物。
WO 2012/075393揭示作為蛋白酶體降解之活化因子之各種化學型之化合物,尤其噻唑衍生物。
JP 2011032254揭示作為有害生物控制劑之各種化學型之化合物,尤其噻唑衍生物。
WO 2009/041790揭示作為用於治療炎性疾病之鞘胺醇磷脂醯膽鹼(SPC)受體之抑制劑之2,4,5-三取代噻唑衍生物。
WO 2008/090382揭示用於治療傳染性蛋白顆粒疾病、癌症及中樞神經系統病狀以及用於調節幹細胞之噻唑及㗁唑衍生物。
WO 2007/022415揭示用於治療神經退化性疾病之經取代2-胺基噻唑。
WO 2006/122011揭示用於治療病毒感染,特定言之C型肝炎病毒感染之噻唑化合物及方法。
WO 2006/078287揭示作為磷酸二酯酶4B之抑制劑之各種5員雜芳烴之衍生物,尤其噻唑。
WO 2005/102318、WO 2005/102325、WO 2005/102326、WO 2005/102346、WO 2005/102455、WO 2005/112920、WO 2005/115304、WO 2005/115385全部涉及各種化學型之c-Kit抑制劑(包括2-胺基噻唑衍生物)及其各種用途。
EP 1543824及US 2005/0137239揭示用於逆糖化之噻唑衍生物。
WO 2004/014884揭示作為神經肽Y受體配體之噻唑衍生物。
WO 2019/133445揭示作為Vanin-1之抑制劑之胺基噻唑衍生物。
WO 2021/043966揭示作為NOD樣受體(NLR)家族含有膿素域之蛋白質3 (NLRP3)之抑制劑之經取代五員含氮雜芳化合物。
結構上與本發明化合物相關但結構上又不同之2,4,5-三取代三唑衍生物亦已揭示於若干科學公開案中。
D. Kikelj及U. Urleb, Science of Synthesis (2002), 11, 627-833為關於噻唑合成之一般綜述。迄今為止,除具有與本發明化合物相同的噻唑核心以外,大部分所揭示之特定化合物結構上遠遠不同於此等。其中揭示之若干個別化合物,即在第651、681-683及719頁揭示之化合物且包括{4-甲基-2-[甲基(苯基)胺基]-1,3-噻唑-5-基}(苯基)甲酮,結構上略微與本發明化合物相關但結構上又不同。
結構上與本發明化合物相關但結構上又不同之2,4,5-三取代三唑衍生物亦已揭示於若干雜誌論文中。
下文所列之雜誌論文(其亦揭示結構上略微與本發明化合物相關但結構上又不同之一些化合物)中無一者揭示其中揭示之化合物之醫藥應用的療法。
S. Titus等人, Tetrahedron Lett. 2014, 55, 5465-5467揭示4-肼基噻唑衍生物之四組分合成。
T. N. Birkinshaw等人, J. Chem. Soc. Perkin Trans. 1, 1988, 2209-2212揭示關於5-醯基及5-亞硝基-2-(N,N-二取代胺基)噻唑之光譜及化學研究。
R. A. Funnell等人, J. Chem. Soc. Perkin Trans. 1, 1987, 2311-2315揭示關於異構2-(N,N-二取代胺基)噻唑-5-基酮類之形成之研究。
J. C. Brindley等人, J. Chem. Soc. Perkin Trans. 1, 1987, 1153-1158揭示將N'-取代N-醯基及N-醯亞胺基硫脲轉化為2-(N,N-二取代胺基)噻唑-5-基酮類。
G. D. Meakins等人, J. Chem. Soc. Chem. Comm. 1984, 837-838揭示出乎意料地產生5-苯甲醯基-4-甲基-2-(N-甲基-N-苯胺基)噻唑之化學反應。
K. Akiba等人, Tetrahedron Lett. 1975, 7, 459-462揭示藉由4-芳基-3-芳基亞胺基-5-亞胺基-1,2-4-噻二唑啶(亦稱為赫克特氏鹼(Hector's base))及乙炔之1,3-環加成合成某些2-芳基胺基噻唑。
最後,結構上略微與本發明化合物相關但結構上又不同之三種結構揭示於資料庫化學文摘註冊(CAS Registry®)中,所有均無參考且無技術申請,具有CAS註冊號1349635-19-3、1349215-57-1及1348293-02-6。
然而,目前最佳技術未描述:
● 如本文所描述及定義之本發明之通式(I)之特定經取代胺基噻唑化合物,亦即具有攜帶以下之2-胺基噻唑核心之化合物:
● 與C-5連接之視情況經取代苯甲醯基或6員雜芳醯基,
● 與C-4連接之-NH2
或甲基,
● 及(i)視情況經取代苯基或5或6員雜芳基及(ii)側向經基團-S(=O)2
-NH2
或特定言之-C(=O)-NH2
取代之烷基,(i)及(ii)與連接C-2之氮原子連接,該側向經取代烷基為DGKζ之強效抑制所必需的,如比較實驗中所示,見下文,
或如本文所描述及定義之其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物、鹽或其混合物,且如下文稱為「通式(I)化合物」或「本發明化合物」,
● 或其藥理學活性。
關於根據式(I)及摘要之不同化學型([1,2,4]三唑并[1.5-c]喹唑啉-5-胺化合物)之WO 2021/028382揭示單一化合物,名稱為N2
-(4-胺基-5-苯甲醯基-1,3-噻唑-2-基)-N2
-(3-甲基苯基)丙胺醯胺,不提供合成方案且無關於該化合物名稱之生物學資料。
期望提供具有預防及治療特性之新穎化合物。
因此,本發明之一個目的在於提供用於以T細胞免疫刺激或免疫修飾方式預防及治療DGKζ調節病症之化合物及包含此等化合物之醫藥組合物。DGKζ調節病症包含具有失調免疫反應(特定言之在癌症中之免疫學抑制的腫瘤微環境中)之病狀、自體免疫疾病、病毒感染以及其他與異常DGKζ信號傳導相關之病症。該等化合物可以作為單獨藥劑或與其他活性成分組合使用。
現已發現本發明化合物具有出人意料且有利之特性,且此構成本發明之基礎。
特定言之,已出乎意料地發現本發明化合物有效地抑制DGKζ蛋白且藉此增強T細胞介導之免疫。因此,其提供用於治療哺乳動物(包括人類)之疾病,特定言之癌症之新穎結構,且可因此用於治療或預防過度增生病症,舉例而言,諸如癌症。
根據一第一態樣,本發明涵蓋通式(I)化合物:
其中:
R1
表示視情況經取代一次、兩次或三次之苯基或6員雜芳基,各取代基獨立地選自鹵素原子或選自以下之基團:羥基、氰基、硝基、C1
-C6
-烷基、(苯基)-(C1
-C3
-烷基)-、C1
-C6
-鹵烷基、C1
-C6
-烷氧基、(苯基)-(C1
-C3
-烷氧基)-、C1
-C6
-鹵烷氧基、-N(R5
)(R6
),
其中該(苯基)-(C1
-C3
-烷基)-基團及該(苯基)-(C1
-C3
-烷氧基)-基團中之苯基視情況經取代一次或兩次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、甲基、乙基、三氟甲基、甲氧基、乙氧基、二甲胺基及三氟甲氧基,
或與該苯基或6員雜芳基之相鄰碳原子連接之兩個取代基一起形成選自以下之二價基團:-(CH2
)3
-、-(CH2
)4
-、-(CH2
)2
-O-、-(CH2
)3
-O-、-CH2
-O-CH2
-、-(CH2
)2
-O-CH2
-、-O-CH2
-O-、-O-CH2
-CH2
-O-、-O-CF2
-O-、-O-CH2
-CF2
-O-及-O-CF2
-CF2
-O-,
或
R1
表示視情況經取代一次或兩次之5員雜芳基,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、C1
-C3
-烷基及C1
-C3
-烷氧基;
R2
表示基團,
其中「*」指示與連接R2
之氮原子連接之點;
R3
表示選自甲基及-NH2
之基團;
R4
表示視情況經取代一次、兩次或三次之苯基或6員雜芳基,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、硝基、C1
-C6
-烷基、(苯基)-(C1
-C3
-烷基)-、(5或6員雜芳基)-(C1
-C3
-烷基)-、(C3
-C7
-環烷基)-(C1
-C3
-烷基)-、((R9
)O)-(C1
-C6
-烷基)-、C1
-C6
-鹵烷基、C3
-C7
-環烷基、-OR9
、-N(R10
)(R11
)、((R10
)(R11
)N)-(C1
-C3
-烷基)-、-C(=O)-N(R12
)(R13
)、-S(=O)n
-R14
、-C(=O)R14
、-C(=O)-OR17
,及自身視情況經一或兩個選自鹵素原子及甲基之取代基取代的5或6員雜芳基,
或與該苯基或6員雜芳基之相鄰碳原子連接之兩個取代基一起形成選自以下之二價基團:-(CH2
)3
-、-(CH2
)4
-、-(CH2
)2
-O-、-(CH2
)3
-O-、-CH2
-O-CH2
-、-(CH2
)2
-O-CH2
-、-O-CH2
-O-、-O-CH2
-CH2
-O-、-O-CF2
-O-、-O-CH2
-CF2
-O-及-O-CF2
-CF2
-O-;
R5
及R6
在每次出現時獨立地表示氫原子或選自以下之基團:C1
-C4
-烷基、(C1
-C4
-烷基)-C(=O)-、C3
-C4
-環烷基及(苯基)-(C1
-C3
-烷基)-,
或
R5
及R6
連同其所連接之氮原子一起表示視情況經取代一次、兩次或三次之單環含氮4至7員雜環烷基,各取代基獨立地選自鹵素原子或選自以下之基團:側氧基、羥基、C1
-C4
-烷基、(C1
-C4
-烷基)-C(=O)-、C3
-C4
-環烷基及C1
-C4
-烷氧基;
R7
表示氫原子或C1
-C2
-烷基;
R8
表示選自-C(=O)-NH2
及-S(=O)2
-NH2
之基團;
R9
表示氫原子或選自以下之基團:C1
-C6
-烷基、(5或6員雜芳基)-(C1
-C3
-烷基)-、(苯基)-(C1
-C3
-烷基)-、C1
-C6
-鹵烷基、C2
-C4
-羥烷基、(C1
-C3
-烷氧基)-C2
-C3
-烷基-、((C1
-C3
-烷基)-C(=O)-O)-C2
-C3
-烷基-、-C(R18
)(R19
)-C(=O)-OR17
、-C(R18
)(R19
)-C(=O)-N(R20
)(R21
)、-C(=O)-N(R20
)(R21
)、苯基及5或6員雜芳基,
其中該(苯基)-(C1
-C3
-烷基)-基團內之苯基及該苯基自身以及該(5或6員雜芳基)-(C1
-C3
-烷基)-基團內之5或6員雜芳基及該5或6員雜芳基自身視情況經取代一次或兩次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、甲基、乙基、三氟甲基、甲氧基、乙氧基、二甲胺基及三氟甲氧基;
R10
及R11
在每次出現時獨立地表示氫原子或選自以下之基團:C1
-C4
-烷基、C1
-C4
-鹵烷基、C2
-C4
-羥烷基、(C1
-C3
-烷氧基)-C2
-C3
-烷基-、((R22
)(R23
)N)-C2
-C3
-烷基、(C3
-C7
-環烷基)-(C1
-C3
-烷基)-、(C1
-C4
-烷基)-C(=O)-、C3
-C7
-環烷基、(C3
-C7
-環烷基)-C(=O)-、(苯基)-(C1
-C3
-烷基)-、(苯基)-(C1
-C3
-烷基)-C(=O)-、(苯基)-(C1
-C3
-烷基)-O-C(=O)-、苯基及5或6員雜芳基,
其中C3
-C7
-環烷基以及該(C3
-C7
-環烷基)-(C1
-C3
-烷基)-基團及(C3
-C7
-環烷基)-C(=O)-基團內之C3
-C7
-環烷基視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自氰基、C1
-C2
-烷基及C1
-C2
-鹵烷基之基團,
且其中該苯基及該5或6員雜芳基、以及該(苯基)-(C1
-C3
-烷基)-基團、(苯基)-(C1
-C3
-烷基)-C(=O)-基團及(苯基)-(C1
-C3
-烷基)-O-C(=O)-基團內之苯基視情況經取代一次或兩次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、甲基、乙基、三氟甲基、甲氧基、乙氧基、二甲胺基及三氟甲氧基,
或
R10
及R11
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基或雙環含氮5至11員雜環烷基,其視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、側氧基、羥基、C1
-C4
-烷基、C1
-C4
-鹵烷基、(C1
-C4
-烷基)-C(=O)-、C3
-C7
-環烷基、C1
-C4
-烷氧基、-N(R22
)(R23
)及單環4至7員雜環烷基;
R12
及R13
在每次出現時獨立地表示氫原子或選自以下之基團:C1
-C4
-烷基、C1
-C4
-鹵烷基、C1
-C4
-羥烷基、(C1
-C4
-烷氧基)-C2
-C3
-烷基-、(C1
-C4
-鹵烷氧基)-C2
-C3
-烷基-、(苯氧基)-C2
-C3
-烷基-、C3
-C7
-環烷基、單環4至7員雜環烷基及(苯基)-(C1
-C3
-烷基)-,
其中C3
-C7
-環烷基及單環4至7員雜環烷基視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、側氧基、羥基、C1
-C4
-烷基、(C1
-C4
-烷基)-C(=O)-、C3
-C4
-環烷基及C1
-C4
-烷氧基,
且其中該(苯氧基)-C2
-C3
-烷基-基團及該(苯基)-(C1
-C3
-烷基)-基團內之苯基視情況經取代一次或兩次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、甲基、乙基、三氟甲基、甲氧基、乙氧基、二甲胺基及三氟甲氧基,
或
R12
及R13
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、側氧基、羥基、C1
-C4
-烷基、(C1
-C4
-烷基)-C(=O)-、C3
-C4
-環烷基及C1
-C4
-烷氧基;
R14
表示選自C1
-C4
-烷基、C1
-C4
-鹵烷基及苯基之基團,
其中苯基視情況經取代一次或兩次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、甲基、乙基、三氟甲基、甲氧基、乙氧基、二甲胺基及三氟甲氧基;
R17
表示C1
-C4
-烷基;
R18
及R19
在每次出現時獨立地表示氫原子或C1
-C4
-烷基;
R20
表示氫原子或選自以下之基團:C1
-C6
-烷基、C3
-C4
-烯基、C3
-C4
-炔基、C1
-C3
-烷氧基、C3
-C7
-環烷基、雙環C5
-C11
-環烷基、金剛烷基、單環4至7員雜環烷基、雙環5至11員雜環烷基、苯基、萘基及5至10員雜芳基,
其中該C1
-C6
-烷基視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:羥基、氰基、C1
-C3
-烷氧基、-N(R22
)(R23
)、C3
-C7
-環烷基、雙環C5
-C11
-環烷基、金剛烷基、單環4至7員雜環烷基、雙環5至11員雜環烷基、苯基及5至10員雜芳基,該苯基取代基及該5至10員雜芳基取代基自身視情況經取代一次或兩次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、甲基、乙基、三氟甲基、甲氧基、乙氧基、二甲胺基及三氟甲氧基,
且其中C3
-C7
-環烷基、雙環C5
-C11
-環烷基、金剛烷基、單環4至7員雜環烷基及雙環5至11員雜環烷基視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、側氧基、羥基、C1
-C4
-烷基、(C1
-C4
-烷基)-C(=O)-、C3
-C4
-環烷基及C1
-C4
-烷氧基,
且其中該苯基、該萘基及該5至10員雜芳基視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、C1
-C4
-烷基、C1
-C4
-鹵烷基、C1
-C4
-烷氧基、C1
-C4
-鹵烷氧基、-N(R22
)(R23
)及-C(=O)-N(R24
)(R25
),
R21
表示氫原子或C1
-C4
-烷基,
或
R20
及R21
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況為苯并縮合的且其視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、側氧基、羥基、C1
-C4
-烷基、C1
-C4
-鹵烷基、(苯基)-(C1
-C3
-烷基)-、(C1
-C4
-烷基)-C(=O)-、C3
-C4
-環烷基、C1
-C4
-烷氧基、C1
-C3
-鹵烷氧基、-N(R22
)(R23
)及-C(=O)-N(R24
)(R25
);
R22
及R23
在每次出現時獨立地表示氫原子或選自C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-之基團;
R24
及R25
在每次出現時獨立地表示氫原子或C1
-C4
-烷基,及
n 表示整數0、1或2,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
定義
術語「經取代」意謂指定原子或基團上之一或多個氫原子經來自指定基團之選項置換,其限制條件為不超過指定原子在現有情形下之正常原子價。容許取代基及/或變數之組合。
術語「視情況經取代」意謂取代基之數目可等於或不同於零。除非另外指明,否則視情況經取代基團有可能經視情況存在之許多取代基取代,只要可藉由在任何可用之碳或氮等原子上用非氫取代基置換氫原子來容納即可。通常,視情況存在之取代基(若存在)的數目有可能為1、2、3或4,特定言之1、2或3。
除非另外說明,否則當本發明化合物中之基團經取代時,該等基團有可能經取代基單取代或多取代。在本發明之範疇內,重複出現之所有基團之含義為彼此獨立的。本發明化合物中之基團有可能經一個、兩個或三個相同或不同取代基取代,特定言之經一個取代基取代。
如本文中所使用,側氧基取代基表示經由雙鍵鍵結至碳原子或硫原子之氧原子。
若複合取代基由超過一個部分構成,例如(C1
-C2
-烷氧基)-(C1
-C6
-烷基)-,給定部分可能連接在該複合取代基之任何合適位置,例如C1
-C2
-烷氧基部分可能連接至該(C1
-C2
-烷氧基)-(C1
-C6
-烷基)-基團之C1
-C6
-烷基部分的任何合適碳原子。該種複合取代基之開頭或末尾處之連字符指示該複合取代基與分子之其餘部分之連接點。若包含碳原子及視情況存在之一或多個雜原子(諸如氮、氧或硫原子)之環例如經取代基取代,則該取代基有可能在該環之任何適合位置處鍵結,其鍵結至適合碳原子及/或適合雜原子。
術語「包含」當用於本說明書中時包括「由……組成」。
若在本發明文本內任一項被稱為「如本文所提及」,則其意謂其可在本發明文本中之任何位置提及。
如本發明文本中所提及之術語具有以下含義:
術語「鹵素原子」意謂氟、氯、溴或碘原子,尤其氟、氯或溴原子。
術語「C1
-C6
-烷基」意謂具有1、2、3、4、5或6個碳原子之直鏈或分支鏈的飽和一價烴基,例如甲基、乙基、丙基、異丙基、丁基、二級丁基、異丁基、三級丁基、戊基、異戊基、2-甲基丁基、1-甲基丁基、1-乙基丙基、1,2-二甲基丙基、新戊基、1,1-二甲基丙基、己基、1-甲基戊基、2-甲基戊基、3-甲基戊基、4-甲基戊基、1-乙基丁基、2-乙基丁基、1,1-二甲基丁基、2,2-二甲基丁基、3,3-二甲基丁基、2,3-二甲基丁基、1,2-二甲基丁基或1,3-二甲基丁基或其異構物。特定言之,該基團具有1、2、3或4個碳原子(「C1
-C4
-烷基」),例如甲基、乙基、丙基、異丙基、丁基、二級丁基、異丁基或三級丁基;更特定言之1、2或3個碳原子(「C1
-C3
-烷基」),例如甲基、乙基、正丙基或異丙基;更特定言之1或2個碳原子(「C1
-C2
-烷基」),例如甲基或乙基。
術語「C1
-C4
-羥烷基」意謂直鏈或分支鏈的飽和一價烴基,其中術語「C1
-C4
-烷基」如上文所定義,且其中1或2個氫原子經羥基置換,例如羥甲基、1-羥乙基、2-羥乙基、1,2-二羥基乙基、3-羥丙基、2-羥丙基、1-羥丙基、1-羥基丙-2-基、2-羥基丙-2-基、2,3-二羥基丙基、1,3-二羥基丙-2-基、3-羥基-2-甲基-丙基、2-羥基-2-甲基-丙基、1-羥基-2-甲基-丙基、1-羥丁基、2-羥丁基、3-羥丁基、4-羥丁基或其異構物。
術語「C1
-C6
-鹵烷基」意謂直鏈或分支鏈的飽和一價烴基,其中術語「C1
-C6
-烷基」如上文所定義,且其中一或多個氫原子經鹵素原子相同或不同地置換。特定言之,該鹵素原子為氟原子。該C1
-C6
-鹵烷基為例如氟甲基、二氟甲基、三氟甲基、2-氟乙基、2,2-二氟乙基、2,2,2-三氟乙基、五氟乙基、3,3,3-三氟丙基或1,3-二氟丙-2-基。
術語「C1
-C6
-烷氧基」意謂式(C1
-C6
-烷基)-O-之直鏈或分支鏈的飽和一價基團,其中術語「C1
-C6
-烷基」如上文所定義,例如甲氧基、乙氧基、正丙氧基、異丙氧基、正丁氧基、二級丁氧基、異丁氧基、三級丁氧基、戊氧基、異戊氧基或正己氧基,或其異構物。
術語「C1
-C6
-鹵烷氧基」意謂如上文所定義之直鏈或分支鏈的飽和一價C1
-C6
-烷氧基,其中一或多個氫原子經鹵素原子相同或不同地置換。特定言之,該鹵素原子為氟原子。該C1
-C6
-鹵烷氧基為例如氟甲氧基、二氟甲氧基、三氟甲氧基、2,2,2-三氟乙氧基或五氟乙氧基。
術語「C3
-C4
-烯基」意謂含有一個或兩個雙鍵且具有3或4個碳原子之直鏈或分支鏈的一價烴基。該烯基為例如丙-2-烯-1-基(或「烯丙基」)、丙-1-烯-1-基、丁-3-烯基、丁-2-烯基或丁-1-烯基。
術語「C3
-C4
-炔基」意謂含有一個三鍵且含有3或4個碳原子之直鏈或分支鏈的一價烴基。該C3
-C4
-炔基為例如丙-1-炔基、丙-2-炔基(或「炔丙基」)、丁-1-炔基、丁-2-炔基或丁-3-炔基。
術語「C3
-C7
-環烷基」意謂含有3、4、5、6或7個碳環原子之飽和一價單環烴環(「C3
-C7
-環烷基」)。該C3
-C7
-環烷基為例如環丙基、環丁基、環戊基、環己基或環庚基。
術語「雙環C6
-C11
-環烷基」意謂如下文所定義之螺環烷基、稠合C6
-C10
-環烷基或橋聯C7
-C10
-環烷基:
術語「螺環烷基」意謂雙環飽和一價C5
-C11
烴基,其中兩個環共用一個共同環碳原子,且其中該雙環烴基含有5、6、7、8、9、10或11個碳原子,該螺環烷基有可能經由除螺碳原子以外之任一碳原子與分子之其餘部分連接。該螺環烷基為例如螺[2.6]壬基、螺[3.3]庚基、螺[3.4]辛基、螺[3.5]壬基、螺[3.6]癸基、螺[4.4]壬基、螺[4.5]癸基、螺[4.6]十一基或螺[5.5]十一基。
術語「稠合C6
-C10
-環烷基」意謂雙環飽和一價烴基,其中兩個環共用兩個相鄰環原子,諸如雙環[4.2.0]辛基、八氫并環戊二烯基或十氫萘基。
術語「橋聯C7
-C10
-環烷基」意謂雙環飽和一價烴基,其中兩個環共用兩個不相鄰之共有環原子,例如雙環[2.2.1]庚基(亦稱為降莰基)。
術語「雙環C5
-C11
-環烷基」意謂如下文所定義之螺環烷基、稠合C5
-C10
-環烷基或橋聯C5
-C10
-環烷基:
術語「螺環烷基」意謂雙環飽和一價C5
-C11
烴基,其中兩個環共用一個共同環碳原子,且其中該雙環烴基含有5、6、7、8、9、10或11個碳原子,該螺環烷基有可能經由除螺碳原子以外之任一碳原子與分子之其餘部分連接。該螺環烷基為例如螺[2.6]壬基、螺[3.3]庚基、螺[3.4]辛基、螺[3.5]壬基、螺[3.6]癸基、螺[4.4]壬基、螺[4.5]癸基、螺[4.6]十一基或螺[5.5]十一基。
術語「稠合C5
-C10
-環烷基」意謂雙環飽和一價烴基,其中兩個環共用兩個相鄰環原子,諸如雙環[4.2.0]辛基、八氫并環戊二烯基或十氫萘基。
術語「橋聯C5
-C10
-環烷基」意謂雙環飽和一價烴基,其中兩個環共用兩個不相鄰之共有環原子,例如雙環[1.1.1]戊基或雙環[2.2.1]庚基(亦稱為降莰基)。
術語「單環4至7員雜環烷基」意謂總共具有4、5、6或7個環原子之單環飽和雜環,其含有一個或兩個來自組N、O及S之相同或不同環雜原子。
該單環雜環烷基可為(但不限於)例如4員環,諸如吖呾基、氧環丁基或硫雜環丁基;或例如5員環,諸如四氫呋喃基、1,3-二氧戊環基、硫雜環戊基、吡咯啶基、咪唑啶基、吡唑啶基、1,1-二氧離子基硫雜環戊基、1,2-㗁唑啶基、1,3-㗁唑啶基或1,3-噻唑啶基;或例如6員環,諸如四氫哌喃基、四氫硫代哌喃基、哌啶基、𠰌啉基、二噻烷基、硫代𠰌啉基、哌𠯤基、1,3-二㗁烷基、1,4-二㗁烷基或1,2-氧氮雜環己基;例如7員環,諸如氮雜環庚烷基、1,4-二氮𠰢基或1,4-氧氮雜環庚烷基。
術語「單環含氮4至7員雜環烷基」意謂總共具有4、5、6或7個環原子之單環飽和雜環,其含有一個環氮原子及視情況存在之來自組N、O及S之另一環雜原子。
該單環含氮4至7員雜環烷基可為(但不限於)例如4員環,諸如吖呾基;或例如5員環,諸如吡咯啶基、咪唑啶基、吡唑啶基、1,2-㗁唑啶基、1,3-㗁唑啶基或1,3-噻唑啶基;或例如6員環,諸如哌啶基、𠰌啉基、硫代𠰌啉基、哌𠯤基或1,2-氧氮雜環己基;或例如7員環,諸如氮雜環庚烷基、1,4-二氮𠰢基或1,4-氧氮雜環庚烷基。
術語「視情況為苯并縮合的單環含氮4至7員雜環烷基」意謂總共具有4、5、6或7個環原子之單環飽和雜環,其含有一個環氮原子及視情況存在之來自組N、O及S之另一環雜原子,其中兩個相鄰環碳原子可與視情況與其稠合之苯環共用,此類基團為前述單環含氮4至7員雜環烷基中之一者,諸如吡咯啶基、哌啶基及其類似者,或苯并縮合基團,例如3,4-二氫喹啉-1(2H)-基、3,4-二氫異喹啉-2(1H)-基、1,3-二氫-2H-異吲哚-2-基或2,3-二氫-1H-吲哚-1-基。
術語「雙環6-11員雜環烷基」意謂如下文所定義之6至11員雜螺環烷基、6至10員稠合雜環烷基或7至10員橋聯雜環烷基:
術語「6至11員雜螺環烷基」意謂總共具有6、7、8、9、10或11個環原子之雙環飽和雜環,其中兩個環共用一個共有環碳原子,該「雜螺環烷基」含有一或兩個來自組N、O、S之相同或不同環雜原子;該雜螺環烷基有可能經由除螺碳原子以外之任一碳原子或經由氮原子(若存在)與分子之其餘部分連接。
該雜螺環烷基為例如氮雜螺[2.3]己基、氮雜螺[3.3]庚基、氧雜氮雜螺[3.3]庚基、硫雜氮雜螺[3.3]庚基、氧雜螺[3.3]庚基、氧雜氮雜螺[5.3]壬基、氧雜氮雜螺[4.3]辛基、氮雜螺[4,5]癸基、氧雜氮雜螺[5.5]十一基、二氮雜螺[3.3]庚基、硫雜氮雜螺[3.3]庚基、硫雜氮雜螺[4.3]辛基、氮雜螺[5.5]十一基或諸如以下的其他同系架構之一:螺[3.4]-、螺[4.4]-、螺[2.4]-、螺[2.5]-、螺[2.6]-、螺[3.5]-、螺[3.6]-、螺[4.5]-及螺[4.6]-。
術語「6至10員稠合雜環烷基」意謂總共具有6、7、8、9或10個環原子之雙環飽和雜環,其中兩個環共用兩個相鄰環原子,該「稠合雜環烷基」含有一或兩個來自組N、O、S之相同或不同環雜原子;該稠合雜環烷基有可能經由任一碳原子或氮原子(若存在)與分子之其餘部分連接。
該稠合雜環烷基為例如氮雜雙環[3.3.0]辛基、氮雜雙環[4.3.0]壬基、二氮雜雙環[4.3.0]壬基、氧氮雜雙環[4.3.0]壬基、硫氮雜雙環[4.3.0]壬基或氮雜雙環[4.4.0]癸基。
術語「7至10員橋聯雜環烷基」意謂總共具有7、8、9或10個環原子之雙環飽和雜環,其中兩個環共用兩個不相鄰之共有環原子,該「橋聯雜環烷基」含有一個或兩個來自組N、O、S之相同或不同環雜原子;該橋聯雜環烷基有可能經由除螺碳原子以外之任一碳原子或氮原子(若存在)與分子之其餘部分連接。
該橋聯雜環烷基為例如氮雜雙環[2.2.1]庚基、氧氮雜雙環[2.2.1]庚基、硫氮雜雙環[2.2.1]庚基、二氮雜雙環[2.2.1]庚基、氮雜雙環[2.2.2]辛基、二氮雜雙環[2.2.2]辛基、氧氮雜雙環[2.2.2]辛基、硫氮雜雙環[2.2.2]辛基、氮雜雙環[3.2.1]辛基、二氮雜雙環[3.2.1]辛基、氧氮雜雙環[3.2.1]辛基、硫氮雜雙環[3.2.1]辛基、氮雜雙環[3.3.1]壬基、二氮雜雙環[3.3.1]壬基、氧氮雜雙環[3.3.1]壬基、硫氮雜雙環[3.3.1]壬基、氮雜雙環[4.2.1]壬基、二氮雜雙環[4.2.1]壬基、氧氮雜雙環[4.2.1]壬基、硫氮雜雙環[4.2.1]壬基、氮雜雙環[3.3.2]癸基、二氮雜雙環[3.3.2]癸基、氧氮雜雙環[3.3.2]癸基、硫氮雜雙環[3.3.2]癸基或氮雜雙環[4.2.2]癸基。
術語「雙環含氮6-11員雜環烷基」意謂如上文所定義之6至11員雜螺環烷基、6至10員稠合雜環烷基或7至10員橋聯雜環烷基,但含有一個環氮原子及視情況存在之一個或兩個來自組N、O及S之其他環雜原子;該雙環含氮6-11員雜環烷基有可能經由氮原子或除螺碳原子以外之任一碳原子與分子之其餘部分連接。
術語「雙環5-11員雜環烷基」意謂如下文所定義之5-11員雜螺環烷基、5-11員稠合雜環烷基或5-11員橋聯雜環烷基:
術語「5-11員雜螺環烷基」意謂總共具有5、6、7、8、9、10或11個環原子之雙環飽和雜環,其中兩個環共用一個共有環碳原子,該「雜螺環烷基」含有一或兩個來自組N、O、S之相同或不同環雜原子;該雜螺環烷基有可能經由除螺碳原子以外之任一碳原子或經由氮原子(若存在)與分子之其餘部分連接。
該雜螺環烷基為例如氮雜螺[2.2]戊基、氮雜螺[2.3]己基、氮雜螺[3.3]庚基、氧雜氮雜螺[3.3]庚基、硫雜氮雜螺[3.3]庚基、氧雜螺[3.3]庚基、氧雜氮雜螺[5.3]壬基、氧雜氮雜螺[4.3]辛基、氮雜螺[4.5]癸基、氧雜氮雜螺[5.5]十一基、二氮雜螺[3.3]庚基、硫雜氮雜螺[3.3]庚基、硫雜氮雜螺[4.3]]辛基、氮雜螺[5.5]十一基或諸如以下的其他同系架構之一:螺[3.4]-、螺[4.4]-、螺[2.4]-、螺[2.5]-、螺[2.6]-、螺[3.5]-、螺[3.6]-、螺[4.5]-及螺[4.6]-。
術語「5-11員稠合雜環烷基」意謂總共具有5、6、7、8、9或10個環原子之雙環飽和雜環,其中兩個環共用兩個相鄰環原子,該「稠合雜環烷基」含有一或兩個來自組N、O、S之相同或不同環雜原子;該稠合雜環烷基有可能經由任一碳原子或氮原子(若存在)與分子之其餘部分連接。
該稠合雜環烷基為例如氮雜雙環[3.1.0]己基、氮雜雙環[3.3.0]辛基、氮雜雙環[4.3.0]壬基、二氮雜雙環[4.3.0]壬基、氧雜氮雜雙環[4.3.0]壬基、硫氮雜雙環[4.3.0]壬基或氮雜雙環[4.4.0]癸基。
術語「5-11員橋聯雜環烷基」意謂總共具有5、6、7、8、9或10個環原子之雙環飽和雜環,其中兩個環共用兩個不相鄰之共有環原子,該「橋聯雜環烷基」含有一個或兩個來自組N、O、S之相同或不同環雜原子;該橋聯雜環烷基有可能經由除螺碳原子以外之任一碳原子或氮原子(若存在)與分子之其餘部分連接。
該橋聯雜環烷基為例如氮雜雙環[2.2.1]庚基、氧氮雜雙環[2.2.1]庚基、硫氮雜雙環[2.2.1]庚基、二氮雜雙環[2.2.1]庚基、氮雜雙環[2.2.2]辛基、二氮雜雙環[2.2.2]辛基、氧氮雜雙環[2.2.2]辛基、硫氮雜雙環[2.2.2]辛基、氮雜雙環[3.2.1]辛基、二氮雜雙環[3.2.1]辛基、氧氮雜雙環[3.2.1]辛基、硫氮雜雙環[3.2.1]辛基、氮雜雙環[3.3.1]壬基、二氮雜雙環[3.3.1]壬基、氧氮雜雙環[3.3.1]壬基、硫氮雜雙環[3.3.1]壬基、氮雜雙環[4.2.1]壬基、二氮雜雙環[4.2.1]壬基、氧氮雜雙環[4.2.1]壬基、硫氮雜雙環[4.2.1]壬基、氮雜雙環[3.3.2]癸基、二氮雜雙環[3.3.2]癸基、氧氮雜雙環[3.3.2]癸基、硫氮雜雙環[3.3.2]癸基或氮雜雙環[4.2.2]癸基。
術語「雙環含氮5-11員雜環烷基」意謂如上文所定義之5-11員雜螺環烷基、5-11員稠合雜環烷基或5-11員橋聯雜環烷基,但含有一個環氮原子及視情況存在之一個或兩個來自組N、O及S之其他環雜原子;該雙環含氮5-11員雜環烷基有可能經由氮原子或除螺碳原子以外之任一碳原子與分子之其餘部分連接。
術語「雜芳基」意謂具有5、6、8、9或10個環原子之一價單環或雙環芳族環(「5至10員雜芳基」),其含有至少一個環雜原子及視情況存在之一個、兩個或三個來自組N、O及/或S之其他環雜原子,且其經由環碳原子或氮原子(如原子價允許,如例如在吡咯-1-基中)結合。
該雜芳基可為:5員雜芳基,諸如噻吩基、呋喃基、吡咯基、㗁唑基、噻唑基、咪唑基、吡唑基、異㗁唑基、異噻唑基、㗁二唑基、三唑基、噻二唑基或四唑基;或6員雜芳基,諸如吡啶基(pyridinyl) (本文中亦稱為吡啶基(pyridyl))、嗒𠯤基、嘧啶基、吡𠯤基或三𠯤基;或9員雜芳基,諸如苯并呋喃基、苯并噻吩基、苯并㗁唑基、苯并異㗁唑基、苯并咪唑基、苯并噻唑基、苯并三唑基、噻唑并吡啶基、吲唑基、吲哚基、異吲哚基、吲基或嘌呤基;或10員雜芳基,諸如喹啉基、喹唑啉基、異喹啉基、㖕啉基、呔𠯤基、喹㗁啉基或喋啶基。
一般而言,且除非另有提及,否則雜芳基或伸雜芳基包括其所有可能的異構形式,例如關於與分子之其餘部分之連接點的互變異構物及位置異構物。因此,對於一些說明性非限制性實例而言,術語吡啶基包括吡啶-2-基、吡啶-3-基及吡啶-4-基;或術語噻吩基包括噻吩-2-基及噻吩-3-基。
如本發明文本中所用,例如在「C1
-C6
-烷基」、「C1
-C6
-鹵烷基」、「C1
-C6
-羥烷基」、「C1
-C6
-烷氧基」或「C1
-C6
-鹵烷氧基」定義之上下文中所用,術語「C1
-C6
」意謂具有1至6有限數目個碳原子(亦即1、2、3、4、5或6個碳原子)之烷基。
此外,如本文所用,如在本發明文本中所用,例如在「C3
-C7
-環烷基」的定義之情形下,術語「C3
-C7
」意謂具有3至7有限數目個碳原子,亦即3、4、5、6或7個碳原子之環烷基。
當給出值之範圍時,該範圍涵蓋該範圍內之各值及子範圍。
舉例而言:
「C1
-C6
」涵蓋C1
、C2
、C3
、C4
、C5
、C6
、C1
-C6
、C1
-C5
、C1
-C4
、C1
-C3
、C1
-C2
、C2
-C6
、C2
-C5
、C2
-C4
、C2
-C3
、C3
-C6
、C3
-C5
、C3
-C4
、C4
-C6
、C4
-C5
及C5
-C6
;
「C2
-C6
」涵蓋C2
、C3
、C4
、C5
、C6
、C2
-C6
、C2
-C5
、C2
-C4
、C2
-C3
、C3
-C6
、C3
-C5
、C3
-C4
、C4
-C6
、C4
-C5
及C5
-C6
;
「C3
-C6
」涵蓋C3
、C4
、C5
、C6
、C3
-C6
、C3
-C5
、C3
-C4
、C4
-C6
、C4
-C5
及C5
-C6
。
如本文所用,術語「離去基」意謂在化學反應中與鍵結之電子一起置換為穩定物種之原子或原子基團。特定言之,此類離去基選自包含以下各者之群:鹵素原子,特定言之氟原子、氯原子、溴原子或碘原子,作為鹵基(特定言之氟基、氯基、溴基或碘基)經置換;(甲磺醯基)氧基、[(三氟甲基)磺醯基]氧基、[(九氟丁基)-磺醯基]氧基、(苯磺醯基)氧基、[(4-甲基苯基)磺醯基]氧基、[(4-溴苯基)磺醯基]氧基、[(4-硝基苯基)磺醯基]氧基、[(2-硝基苯基)磺醯基]氧基、[(4-異丙基苯基)磺醯基]氧基、[(2,4,6-三異丙基苯基)磺醯基]氧基、[(2,4,6-三甲基苯基)磺醯基]氧基、[(4-三級丁基-苯基)磺醯基]氧基及[(4-甲氧基苯基)磺醯基]氧基。
如本文所用,術語「偶極非質子性溶劑」意謂選自以下之溶劑:丙酮、乙腈、丙腈、二甲基亞碸、二乙基亞碸、N,N-二甲基甲醯胺、N,N-二甲基乙醯胺、N,N-二乙基甲醯胺、N,N-二乙基乙醯胺、1-甲基-2-吡咯啶酮、1-乙基-2-吡咯啶酮、1-甲基-2-哌啶酮及1-乙基-2-哌啶酮,或其混合物。特定言之,該偶極非質子性溶劑為乙腈、二甲基亞碸、N,N-二甲基甲醯胺、N,N-二甲基乙醯胺或1-甲基-2-吡咯啶酮。
如本文所用,術語「室溫」意謂在15℃至25℃範圍內之溫度。
通式(I)化合物有可能以同位素變體之形式存在。因此,本發明包括通式(I)化合物之一或多種同位素變體,特定言之,含氘之通式(I)化合物。
術語化合物或試劑之「同位素變體」定義為如下化合物,其具有非天然比例的構成此類化合物之同位素中之一或多者。
術語「通式(I)化合物之同位素變體」定義為如下通式(I)化合物,其具有非天然比例的構成此類化合物之同位素中之一或多者。
表述「非天然比例」意謂此類同位素之比例高於其天然豐度之比例。在此情況下,待應用之同位素之天然豐度描述於「Isotopic Compositions of the Elements 1997」, Pure Appl. Chem., 70(1), 217-235, 1998中。
此類同位素之實例包括氫、碳、氮、氧、磷、硫、氟、氯、溴及碘之穩定及放射性同位素,分別諸如2
H (氘)、3
H (氚)、11
C、13
C、14
C、15
N、17
O、18
O、32
P、33
P、33
S、34
S、35
S、36
S、18
F、36
Cl、82
Br、123
I、124
I、125
I、129
I及131
I。
關於本文所規定病症之治療及/或預防,通式(I)化合物之同位素變體較佳含有氘(「含氘之通式(I)化合物」)。其中併入有一或多種放射性同位素(諸如3
H或14
C)之通式(I)化合物之同位素變體適用於例如藥物及/或受質組織分佈研究中。為方便同位素之併入及可偵測性,此等同位素為尤其較佳的。可將諸如18
F或11
C之正電子發射同位素併入通式(I)化合物中。通式(I)之化合物之此等同位素變體適用於活體內成像應用中。含氘及含13
C之通式(I)化合物可以在臨床前或臨床研究之情形下用於質譜分析中。
通式(I)化合物之同位素變體通常可以藉由熟習此項技術者已知之方法製備,諸如本文流程及/或實例中所描述之方法,藉由用試劑之同位素變體,較佳含氘試劑取代該試劑。視所要氘化位點而定,在一些情況下,來自D2
O之氘可直接併入化合物中或併入適用於合成此類化合物之試劑中。氘氣亦為適用於將氘併入分子中之試劑。烯鍵及炔鍵之催化氘化為併入氘之快速途徑。在氘氣存在下,金屬催化劑(亦即Pd、Pt及Rh)可用於將含有官能基之烴中的氫直接交換為氘。各種氘化試劑及合成建構單元可購自各公司,諸如C/D/N Isotopes, Quebec, Canada;Cambridge Isotope Laboratories Inc., Andover, MA, USA;及CombiPhos Catalysts, Inc., Princeton, NJ, USA。
術語「含氘之通式(I)化合物」定義為其中一或多個氫原子經一或多個氘原子置換且其中通式(I)化合物之各氘化位置處之氘的豐度高於氘之天然豐度(其為約0.015%)的通式(I)化合物。特定言之,在含氘之通式(I)化合物中,通式(I)化合物之各氘化位置處之氘的豐度高於10%、20%、30%、40%、50%、60%、70%或80%,較佳高於90%、95%、96%或97%,甚至更佳地,在該(等)位置處高於98%或99%。應瞭解,各氘化位置處之氘豐度獨立於其他氘化位置處之氘豐度。
將一或多個氘原子選擇性併入通式(I)化合物中可以改變分子之物理化學特性(諸如酸性[C. L. Perrin等人, J. Am. Chem. Soc., 2007, 129, 4490]、鹼性[C. L. Perrin等人, J. Am. Chem. Soc., 2005, 127, 9641]、親脂性[B. Testa等人, Int. J. Pharm., 1984, 19(3), 271])及/或代謝概況,且可引起親本化合物與代謝物之比率或所形成代謝物之量變化。此類變化可以產生某些治療優勢且因此在一些情況下可為較佳的。已報導代謝及代謝轉換之速率降低,其中代謝物比率變化(A. E. Mutlib等人,Toxicol. Appl. Pharmacol., 2000, 169, 102)。在暴露於親本藥物及代謝物時此等改變可具有關於含氘之通式(I)化合物之藥效學、耐受性及功效的重要結果。在一些情況下,氘取代減少或消除非所需或毒性代謝物之形成且增強所需代謝物(例如奈韋拉平(Nevirapine):A. M. Sharma等人,Chem. Res. Toxicol., 2013, 26, 410;依法韋侖(Efavirenz):A. E. Mutlib等人,Toxicol. Appl. Pharmacol., 2000, 169, 102)之形成。在其他情況下,氘化之主要作用為降低全身清除速率。因此,化合物之生物半衰期增加。潛在臨床益處包括能夠經由降低峰值含量及增加最低含量來維持類似的全身暴露。此可導致副作用減少及功效增強,視特定化合物之藥物動力學/藥效學關係而定。ML-337 (C. J. Wenthur等人, J. Med. Chem., 2013, 56, 5208)及奧當卡替(Odanacatib) (K. Kassahun等人, WO2012/112363)為此氘效果之實例。另外報導有其他情況,其中代謝速率降低導致在不改變全身清除速率之情況下藥物之暴露量增加(例如羅非考昔(Rofecoxib):F. Schneider等人,Arzneim. Forsch./Drug.Res., 2006, 56, 295;特拉匹韋(Telaprevir):F. Maltais等人,J. Med. Chem., 2009, 52, 7993)。顯示此效果之氘化藥物可具有降低的給藥要求(例如,用於達成所需效果之劑量數目減少或劑量降低)及/或可產生較低之代謝物負荷。
通式(I)化合物可具有多個潛在的代謝攻擊位點。為了使對物理化學特性及代謝概況之上述影響最佳化,可選擇具有特定的一或多個氘-氫交換模式的含氘之通式(I)化合物。特定言之,含氘之通式(I)化合物之氘原子與碳原子連接及/或位於通式(I)化合物之彼等位置處,該等位置為用於代謝諸如細胞色素P450
之酶的攻擊位點。
在另一實施例中,本發明係關於一種具有1、2、3或4個氘原子,特定言之,具有1、2或3個氘原子之含氘之通式(I)化合物。
在本文使用複數形式之措詞化合物、鹽、多形體、水合物、溶劑合物及其類似物時,係亦意謂單一化合物、鹽、多形體、異構物、水合物、溶劑合物或其類似物。
「穩定化合物」或「穩定結構」意謂足夠穩固以經受住自反應混合物分離至適用純度且調配成有效治療劑之化合物。
視各種所需取代基之位置及性質而定,本發明化合物視情況含有一或多個不對稱中心。一或多個不對稱碳原子有可能以(R)或(S)組態存在,此可在單一不對稱中心之情況下產生外消旋混合物且在多個不對稱中心之情況下產生非鏡像異構物混合物。在某些情況下,不對稱性亦有可能由於圍繞既定鍵(例如與規定化合物之兩個經取代芳環鄰接之中心鍵)限制性旋轉而存在。
較佳異構物為產生較理想生物活性之異構物。本發明化合物之此等經分離的、純的或部分純化的異構物或外消旋混合物亦包括在本發明之範疇內。此類物質之純化及分離可藉由此項技術中已知之標準技術實現。
光學異構物可藉由根據習知方法解析外消旋混合物來獲得,例如藉由使用光學活性酸或鹼形成非鏡像異構物鹽,或形成共價非鏡像異構物來獲得。適當酸之實例為酒石酸、二乙醯基酒石酸、二甲苯醯基酒石酸及樟腦磺酸。非鏡像異構物之混合物可藉由此項技術中已知之方法(例如層析或分步結晶)、基於其物理及/或化學差異分離成其個別非鏡像異構物。隨後自經分離之非對映異構鹽釋放光活性鹼或酸。分離光學異構物之不同方法涉及在進行或不進行習知衍生之情況下使用對掌性層析(例如使用對掌相之HPLC管柱),最佳選擇習知衍生以使鏡像異構物之分離最大化。適合的使用對掌性相之HPLC管柱為可商購的,諸如由Daicel製造之管柱,例如Chiracel OD及Chiracel OJ,例如以及許多其他管柱,其均可常規地選擇。使用或不使用衍生法的酶分離亦為適用的。本發明之光學活性化合物同樣可藉由利用光學活性起始物質之對掌性合成來獲得。
為了將不同類型的異構物彼此區分開,參考IUPAC規則E部分(Pure Appl Chem 45, 11-30, 1976)。
本發明包括本發明化合物之所有可能立體異構物,其呈單一立體異構物形式或呈該等立體異構物(例如(R)-異構物或(S)-異構物)之任何比率之任何混合物形式。本發明化合物之單一立體異構物(例如單一鏡像異構物或單一非鏡像異構物)的分離例如藉由任何適合的目前最佳技術方法(諸如層析,尤其對掌性層析)達成。
本發明包括本發明化合物之所有可能互變異構物,其呈單一互變異構物形式或該等互變異構物的任何比率之任何混合物形式。
此外,本發明化合物可以N-氧化物形式存在,其定義為本發明化合物之至少一個氮經氧化。本發明包括所有此類可能的N-氧化物。
本發明亦涵蓋本發明化合物之有用形式,諸如代謝物、水合物、溶劑合物、前藥、鹽(尤其醫藥學上可接受之鹽)及/或共沈澱物。
本發明化合物可以水合物或溶劑合物之形式存在,其中本發明化合物含有極性溶劑(特定言之,例如水、甲醇或乙醇)作為化合物晶格的結構元素。極性溶劑,特定言之水之量有可能以化學計量或非化學計量比率存在。在化學計量溶劑合物(例如水合物)之情況下,半-(hemi-/semi-)、單-、倍半-(sesqui-)、二-、三-、四-、五-等溶劑合物或水合物分別為可能的。本發明包括所有此類水合物或溶劑合物。
此外,本發明化合物有可能以游離形式(例如以游離鹼形式、或以游離酸形式、或以兩性離子形式)存在,或以鹽形式存在。該鹽可為慣用於藥劑學中或用於(例如)分離或純化本發明化合物之任何鹽,有機或無機加成鹽(特定言之,任何醫藥學上可接受之有機或無機加成鹽)。
術語「醫藥學上可接受之鹽」係指本發明化合物之無機或有機酸加成鹽。舉例而言,參見S. M. Berge等人, 「Pharmaceutical Salts,」 J. Pharm. Sci. 1977, 66, 1-19。
本發明化合物之適合的醫藥學上可接受之鹽可為例如本發明化合物之在鏈或環中攜帶氮原子且例如呈足夠鹼性的酸加成鹽,諸如與無機酸或「礦物酸(mineral acid)」之酸加成鹽,該無機酸諸如鹽酸、氫溴酸、氫碘酸、硫酸、胺磺酸、重硫酸、磷酸或硝酸,例如與有機酸之酸加成鹽,該有機酸諸如甲酸、乙酸、乙醯乙酸、丙酮酸、三氟乙酸、丙酸、丁酸、己酸、庚酸、十一烷酸、月桂酸、苯甲酸、水楊酸、2-(4-羥基苯甲醯基)-苯甲酸、樟腦酸、肉桂酸、環戊丙酸、二葡萄糖酸、3-羥基-2-萘甲酸、菸鹼酸、雙羥萘酸、果膠酯酸、3-苯基丙酸、特戊酸、2-羥基乙磺酸、衣康酸(itaconic)、三氟甲磺酸、十二基硫酸、乙磺酸、苯磺酸、對甲苯磺酸、甲磺酸、2-萘磺酸、萘二磺酸、樟腦磺酸、檸檬酸、酒石酸、硬脂酸、乳酸、乙二酸、丙二酸、丁二酸、蘋果酸、己二酸、海藻酸、順丁烯二酸、反丁烯二酸、D-葡萄糖酸、杏仁酸、抗壞血酸、葡糖庚酸、甘油磷酸、天冬胺酸、磺基柳酸或硫氰酸。
此外,呈足夠酸性之本發明化合物的另一適合的醫藥學上可接受之鹽為鹼金屬鹽,例如鈉或鉀鹽;鹼土金屬鹽,例如鈣、鎂或鍶鹽;或鋁或鋅鹽;或衍生自氨或具有1至20個碳原子的有機一級、二級或三級胺之銨鹽,該胺諸如乙胺、二乙胺、三乙胺、乙基二異丙胺、單乙醇胺、二乙醇胺、三乙醇胺、二環己胺、二甲胺基乙醇、二乙胺基乙醇、參(羥甲基)胺基甲烷、普魯卡因(procaine)、二苯甲基胺、N
-甲基𠰌啉、精胺酸、離胺酸、1,2-乙二胺、N
-甲基哌啶、N
-甲基-還原葡糖胺、N,N
-二甲基-還原葡糖胺、N
-乙基-還原葡糖胺、1,6-己二胺、葡糖胺、肌胺酸、絲胺醇、2-胺基-1,3-丙二醇、3-胺基-1,2-丙二醇、4-胺基-1,2,3-丁三醇;或與具有1至20個碳原子的四級銨離子之鹽,該銨離子諸如四甲銨、四乙銨、四(正丙基)銨、四(正丁基)銨、N
-苯甲基-N,N,N
-三甲銨、膽鹼或苯甲烴銨。
熟習此項技術者應進一步瞭解,所主張化合物之酸加成鹽有可能藉由使化合物與適當無機酸或有機酸經由多種已知方法中之任一者反應而製備。替代地,本發明之酸性化合物之鹼金屬鹽及鹼土金屬鹽藉由使本發明化合物與適當鹼經由多種已知方法反應而製備。
本發明包括本發明化合物之所有可能鹽,其呈單一鹽或任何比率之該等鹽之任何混合物形式。
在本發明正文中,尤其在「實驗章節」中,對於本發明之中間物及實例之合成,當以與對應鹼或酸形成之鹽形式提及化合物時,如藉由各別製備及/或純化方法獲得之該鹽形式的精確化學計量組成在大多數情況下為未知的。
除非另外規定,否則關於鹽之化學名稱或結構式之後綴,諸如「鹽酸鹽」、「三氟乙酸鹽」、「鈉鹽」或「x HCl」、「x CF3
COOH」、「x Na+
」意謂鹽形式,該鹽形式之化學計量未指定。
此類似地應用於其中已藉由所描述製備及/或純化方法以(若定義)未知化學計量組成的溶劑合物(諸如水合物)形式獲得合成中間物或實例化合物或其鹽的情況。
此外,本發明包括本發明化合物之所有可能結晶形式或多形體,其呈單一多形體或超過一種多形體之任何比率的混合物形式。
此外,本發明亦包括本發明化合物之前藥。術語「前藥」在此表示自身可以具有生物活性或無活性,但其在體內滯留時間期間轉化(例如以代謝或水解方式)為本發明化合物的化合物。
本發明進一步包括所有可能環糊精晶籠化合物,亦即α-、β-或γ-環糊精,羥丙基-β-環糊精、甲基β環糊精。
根據第一態樣之第二實施例,本發明涵蓋上文通式(I)化合物,其中:
R1
表示視情況經取代一次、兩次或三次之苯基或吡啶基,各取代基獨立地選自鹵素原子或選自以下之基團:羥基、氰基、硝基、C1
-C4
-烷基、(苯基)-(C1
-C2
-烷基)-、C1
-C4
-鹵烷基、C1
-C4
-烷氧基、(苯基)-(C1
-C2
-烷氧基)-、C1
-C4
-鹵烷氧基、-N(R5
)(R6
),
其中該(苯基)-(C1
-C2
-烷基)-基團及該(苯基)-(C1
-C2
-烷氧基)-基團中之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及溴原子或選自甲基、三氟甲基及甲氧基之基團,
或與該苯基或吡啶基之相鄰碳原子連接之兩個取代基一起形成選自以下之二價基團:-(CH2
)3
-、-(CH2
)4
-、-(CH2
)2
-O-、-(CH2
)3
-O-、-CH2
-O-CH2
-、-O-CH2
-O-、-O-CH2
-CH2
-O-及-O-CF2
-O-,
或
R1
表示視情況經取代一次或兩次之吡唑基,各取代基獨立地選自鹵素原子或選自氰基、C1
-C2
-烷基及C1
-C2
-烷氧基之基團;
R2
表示基團,
其中「*」指示與連接R2
之氮原子連接之點;
R3
表示選自甲基及-NH2
之基團;
R4
表示視情況經取代一次、兩次或三次之苯基或吡啶基,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、硝基、C1
-C4
-烷基、(苯基)-(C1
-C2
-烷基)-、(5員雜芳基)-(C1
-C2
-烷基)-、(C3
-C7
-環烷基)-(C1
-C2
-烷基)-、((R9
)O)-(C1
-C4
-烷基)-、C1
-C4
-鹵烷基、C3
-C7
-環烷基、-OR9
、-N(R10
)(R11
)、((R10
)(R11
)N)-(C1
-C3
-烷基)-、-C(=O)-N(R12
)(R13
)、S(=O)n
-R14
、-C(=O)R14
、-C(=O)-OR17
及自身視情況經一或兩個甲基取代5員雜芳基,
或與該苯基或吡啶基之相鄰碳原子連接之兩個取代基一起形成選自以下之二價基團:-(CH2
)3
-、-(CH2
)4
-、-(CH2
)2
-O-、-(CH2
)3
-O-、-CH2
-O-CH2
-、-O-CH2
-O-、-O-CH2
-CH2
-O-及-O-CF2
-O-;
R5
及R6
在每次出現時獨立地表示氫原子或選自C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-之基團,
或
R5
及R6
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:側氧基、羥基、C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-;
R7
表示氫原子或C1
-C2
-烷基;
R8
表示-C(=O)-NH2
基團;
R9
表示氫原子或選自以下之基團:C1
-C4
-烷基、(苯基)-(C1
-C2
-烷基)-、C1
-C4
-鹵烷基、C2
-C3
-羥烷基、(C1
-C2
-烷氧基)-C2
-烷基-、((C1
-C2
-烷基)-C(=O)-O)-C2
-烷基-、-C(R18
)(R19
)-C(=O)-OR17
、-C(R18
)(R19
)-C(=O)-N(R20
)(R21
)、-C(=O)-N(R20
)(R21
)及苯基,
其中該(苯基)-(C1
-C2
-烷基)-基團內之苯基及該苯基自身視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:氰基、甲基、三氟甲基及甲氧基;
R10
及R11
在每次出現時獨立地表示氫原子或選自以下之基團:C1
-C2
-烷基、C1
-C2
-鹵烷基、C2
-C3
-羥烷基、(C1
-C2
-烷氧基)-C2
-烷基-、((R22
)(R23
)N)-C2
-烷基、(C3
-C7
-環烷基)-(C1
-C2
-烷基)-、(C1
-C2
-烷基)-C(=O)-、C3
-C7
-環烷基、(C3
-C7
-環烷基)-C(=O)-、(苯基)-(C1
-C2
-烷基)-、(苯基)-(C1
-C2
-烷基)-C(=O)-及(苯基)-(C1
-C2
-烷基)-O-C(=O)-,
其中C3
-C7
-環烷基以及該(C3
-C7
-環烷基)-(C1
-C2
-烷基)-基團及該(C3
-C7
-環烷基)-C(=O)-基團內之C3
-C7
-環烷基視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自以下之基團:氰基、C1
-C2
-烷基及C1
-C2
-鹵烷基,
且其中該(苯基)-(C1
-C2
-烷基)-基團、該(苯基)-(C1
-C2
-烷基)-C(=O)-基團及該(苯基)-(C1
-C2
-烷基)-C(=O)-基團內之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:甲基、三氟甲基及甲氧基,
或
R10
及R11
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基或雙環含氮5至10員雜環烷基,其視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、側氧基、羥基、C1
-C2
-烷基、C1
-C2
-鹵烷基、(C1
-C2
-烷基)-C(=O)-、C1
-C2
-烷氧基、-N(R22
)(R23
)及單環4至7員雜環烷基;
R12
及R13
在每次出現時獨立地表示氫原子或選自以下之基團:C1
-C4
-烷基、C1
-C4
-鹵烷基、C1
-C4
-羥烷基、(C1
-C4
-烷氧基)-C2
-C3
-烷基-、(C1
-C4
-鹵烷氧基)-C2
-C3
-烷基-、(苯氧基)-C2
-C3
-烷基-、C3
-C7
-環烷基、單環4至7員雜環烷基及(苯基)-(C1
-C3
-烷基)-,
其中C3
-C7
-環烷基及單環4至7員雜環烷基視情況經取代一次或兩次,各取代基獨立地選自鹵素原子或選自以下之基團:側氧基、C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-,
且其中該(苯氧基)-C2
-C3
-烷基-基團及該(苯基)-(C1
-C3
-烷基)-基團內之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:氰基、甲基、三氟甲基及甲氧基,
或
R12
及R13
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況經取代一次或兩次,各取代基獨立地選自鹵素原子或選自以下之基團:側氧基、C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-;
R14
表示選自以下之基團:C1
-C2
-烷基、C1
-C2
-鹵烷基及苯基,
其中苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:甲基、三氟甲基及甲氧基;
R17
表示C1
-C4
-烷基;
R18
及R19
在每次出現時獨立地表示氫原子或C1
-C2
-烷基;
R20
表示氫原子或選自以下之基團:C1
-C6
-烷基、C3
-C4
-烯基、C3
-C4
-炔基、C1
-C3
-烷氧基、C3
-C7
-環烷基、雙環C5
-C11
-環烷基、金剛烷基、單環4至7員雜環烷基、雙環5至10員雜環烷基、苯基、萘基及5至10員雜芳基,
其中該C1
-C6
-烷基視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:羥基、氰基、C1
-C3
-烷氧基、-N(R22
)(R23
)、C3
-C7
-環烷基、雙環C5
-C11
-環烷基、金剛烷基、單環4至7員雜環烷基、雙環5至10員雜環烷基、苯基及5至10員雜芳基,該苯基取代基及該5至10員雜芳基取代基自身視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:甲基、三氟甲基及甲氧基,
且其中C3
-C7
-環烷基、雙環C5
-C11
-環烷基、金剛烷基、單環4至7員雜環烷基、雙環5至10員雜環烷基視情況經取代一次或兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、側氧基、羥基、C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-,
且其中該苯基、該萘基及該5至10員雜芳基視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、C1
-C2
-烷基、C1
-C2
-鹵烷基、C1
-C2
-烷氧基、C1
-C2
-鹵烷氧基、-N(R22
)(R23
)及-C(=O)-N(R24
)(R25
),
R21
表示氫原子或C1
-C2
-烷基,
或
R20
及R21
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況為苯并縮合的且其視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、側氧基、羥基、C1
-C2
-烷基、C1
-C2
-鹵烷基、(苯基)-(C1
-C2
-烷基)-、(C1
-C2
-烷基)-C(=O)-、C3
-C4
-環烷基、C1
-C2
-烷氧基、C1
-C2
-鹵烷氧基、-N(R22
)(R23
)及-C(=O)-N(R24
)(R25
);
R22
及R23
在每次出現時獨立地表示氫原子或選自C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-之基團;
R24
及R25
在每次出現時獨立地表示氫原子或C1
-C2
-烷基,及
n 表示整數0、1或2,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
根據第一態樣之第三實施例,本發明涵蓋上文通式(I)化合物,其中:
R1
表示視情況經取代一次、兩次或三次之苯基或吡啶基,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:羥基、氰基、C1
-C4
-烷基、C1
-C2
-氟烷基、C1
-C2
-烷氧基、(苯基)-(C1
-C2
-烷氧基)-、C1
-C2
-氟烷氧基及-N(R5
)(R6
),
或與該苯基或吡啶基之相鄰碳原子連接之兩個取代基一起形成選自以下之二價基團:-(CH2
)3
-、-O-CH2
-O-及-O-CF2
-O-,
或
R1
表示視情況經一個甲基取代之吡唑基;
R2
表示基團,
其中「*」指示與連接R2
之氮原子連接之點;
R3
表示選自甲基及-NH2
之基團;
R4
表示視情況經取代一次、兩次或三次之苯基或吡啶基,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、C1
-C3
-烷基、((R9
)O)-(C1
-C3
-烷基)-、C1
-C3
-氟烷基、-OR9
、-N(R10
)(R11
)、-C(=O)-N(R12
)(R13
)、S(=O)n
-R14
及-C(=O)-OR17
,
或與該苯基或吡啶基之相鄰碳原子連接之兩個取代基一起形成選自以下之二價基團:-(CH2
)3
-、-O-CH2
-O-及-O-CF2
-O-;
R5
及R6
在每次出現時獨立地表示氫原子或C1
-C2
-烷基,
或
R5
及R6
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自以下之基團:羥基及C1
-C2
-烷基;
R7
表示氫原子或C1
-C2
-烷基;
R8
表示-C(=O)-NH2
基團;
R9
表示氫原子或選自以下之基團:C1
-C2
-烷基、苯甲基、C1
-C2
-氟烷基、C2
-羥烷基、(C1
-C2
-烷氧基)-C2
-烷基-、((C1
-C2
-烷基)-C(=O)-O)-C2
-烷基-、-C(R18
)(R19
)-C(=O)-OR17
、-C(R18
)(R19
)-C(=O)-N(R20
)(R21
)、-C(=O)-N(R20
)(R21
)及苯基,
其中該苯甲基內之苯基及該苯基自身視情況經取代一次或兩次,各取代基獨立地選自氟原子及氯原子或選自以下之基團:氰基及甲基;
R10
及R11
在每次出現時獨立地表示氫原子或選自以下之基團:C1
-C2
-烷基、C1
-C2
-氟烷基、(C3
-C5
-環烷基)-(C1
-C2
-烷基)-(C1
-C2
-烷基)-C(=O)-、C3
-C7
-環烷基、C3
-C7
-環烷基-(C=O)-、(苯基)-(C1
-C2
-烷基)-、(苯基)-(C1
-C2
-烷基)-C(=O)-及(苯基)-(C1
-C2
-烷基)-O-C(=O)-,
其中C3
-C7
-環烷基、及該(C3
-C5
-環烷基)-(C1
-C2
-烷基)-內之C3
-C5
-環烷基以及C3
-C7
-環烷基-(C=O)-基團內之C3
-C7
-環烷基視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自以下之基團:氰基、C1
-C2
-烷基及C1
-C2
-氟烷基,
且其中該(苯基)-(C1
-C2
-烷基)-基團、該(苯基)-(C1
-C2
-烷基)-C(=O)-基團及該(苯基)-(C1
-C2
-烷基)-O-C(=O)-基團內之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及甲基,
或
R10
及R11
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自以下之基團:氰基、側氧基、C1
-C2
-烷基、C1
-C2
-氟烷基及(C1
-C2
-烷基)-C(=O)-;
R12
及R13
在每次出現時獨立地表示氫原子或選自以下之基團:C1
-C4
-烷基、C1
-C4
-氟烷基、C1
-C4
-羥烷基、(C1
-C4
-烷氧基)-C2
-C3
-烷基-、(C1
-C2
-氟烷氧基)-C2
-C3
-烷基-、(苯氧基)-C2
-C3
-烷基-、C3
-C7
-環烷基、單環4至7員雜環烷基及(苯基)-(C1
-C2
-烷基)-,
其中C3
-C7
-環烷基及單環4至7員雜環烷基視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自以下之基團:側氧基、C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-,
且其中該(苯氧基)-C2
-C3
-烷基-基團及該(苯基)-(C1
-C2
-烷基)-基團內之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子及氯原子或選自以下之基團:甲基、三氟甲基及甲氧基,
或
R12
及R13
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況經取代一次或兩次,各取代基獨立地選自鹵素原子或選自以下之基團:側氧基、C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-;
R14
表示選自甲基及三氟甲基之基團;
R17
表示C1
-C2
-烷基;
R18
及R19
在每次出現時獨立地表示氫原子或甲基;
R20
表示氫原子或選自以下之基團:視情況經取代C1
-C3
-烷基、未經取代C4
-C6
-烷基、丙-2-炔基、甲氧基、C3
-C6
-環烷基、金剛烷基、單環4至7員雜環烷基、苯基及5至10員雜芳基,
其中該C1
-C3
-烷基視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:羥基、氰基、C1
-C3
-烷氧基、-N(R22
)(R23
)、C3
-C6
-環烷基、金剛烷基、單環4至7員雜環烷基、苯基及5至10員雜芳基,該苯基取代基及該5至10員雜芳基取代基自身視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及甲基,
且其中該C3
-C6
-環烷基、該金剛烷基及該單環4至7員雜環烷基視情況經取代一次或兩次或三次,各取代基獨立地選自氟原子或選自以下之基團:側氧基、C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-,
且其中該苯基及該5至10員雜芳基視情況經取代一次、兩次或三次,各取代基獨立地選自氟原子及氯原子或選自以下之基團:氰基、C1
-C2
-烷基、C1
-C2
-氟烷基、C1
-C2
-烷氧基、C1
-C2
-氟烷氧基、-N(R22
)(R23
)及-C(=O)-N(R24
)(R25
),
R21
表示氫原子或C1
-C2
-烷基,
或
R20
及R21
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況為苯并縮合的且其視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、側氧基、羥基、C1
-C2
-烷基、C1
-C2
-氟烷基、苯甲基、(C1
-C2
-烷基)-C(=O)-、C3
-C4
-環烷基、C1
-C2
-烷氧基、C1
-C2
-氟烷氧基、-N(R22
)(R23
)及-C(=O)-N(R24
)(R25
);
R22
及R23
在每次出現時獨立地表示氫原子或選自C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-之基團;
R24
及R25
在每次出現時獨立地表示氫原子或C1
-C2
-烷基,及
n 表示整數2,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
根據第一態樣之第四實施例,本發明涵蓋上文通式(I)化合物,其中:
R1
表示視情況經取代一次或兩次之苯基或吡啶基,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:氰基、甲基、二氟甲基、三氟甲基、甲氧基、苯甲氧基、二氟甲氧基及三氟甲氧基,
或與該苯基或吡啶基之相鄰碳原子連接之兩個取代基一起形成二價基團-O-CF2
-O-;
R2
表示基團,
其中「*」指示與連接R2
之氮原子連接之點;
R3
表示選自甲基及-NH2
之基團;
R4
表示視情況經取代一次或兩次之苯基或吡啶基,各取代基獨立地選自鹵素原子或選自以下之基團:C1
-C2
-烷基、C1
-C2
-氟烷基、-OR9
, -N(R10
)(R11
)、-C(=O)-N(R12
)(R13
)及-C(=O)-OR17
;
R7
表示氫原子或C1
-C2
-烷基;
R8
表示-C(=O)-NH2
基團;
R9
表示氫原子或選自以下之基團:C1
-C2
-烷基、苯甲基、C1
-C2
-氟烷基、(C1
-C2
-烷氧基)-C2
-烷基-、((C1
-C2
-烷基)-C(=O)-O)-C2
-烷基-、-C(R18
)(R19
)-C(=O)-N(R20
)(R21
)、-C(=O)-N(R20
)(R21
)及苯基,
其中該苯甲基內之苯基及該苯基自身視情況經取代一次或兩次,各取代基獨立地選自氟原子及氯原子或選自以下之基團:氰基及甲基;
R10
及R11
在每次出現時獨立地表示氫原子或選自以下之基團:C1
-C2
-烷基、(C3
-C5
-環烷基)-(C1
-C2
-烷基)-、C3
-C7
-環烷基及(苯基)-(C1
-C2
-烷基)-O-C(=O)-,
其中C3
-C7
-環烷基及該(C3
-C5
-環烷基)-(C1
-C2
-烷基)-基團內之C3
-C5
-環烷基視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自以下之基團:氰基、甲基及C1
-氟烷基,
且其中該(苯基)-(C1
-C2
-烷基)-O-C(=O)-基團內之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及甲基,
或
R10
及R11
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自以下之基團:氰基、甲基及C1
-氟烷基;
R12
及R13
在每次出現時獨立地表示氫原子或選自以下之基團:C1
-C4
-烷基、C1
-C2
-氟烷基、C1
-C2
-羥烷基、(C1
-C4
-烷氧基)-C2
-C3
-烷基-、(C1
-C2
-氟烷氧基)-C2
-C3
-烷基-、(苯氧基)-C2
-C3
-烷基-、C3
-C7
-環烷基及(苯基)-(C1
-C2
-烷基)-,
其中C3
-C7
-環烷基視情況經取代一次或兩次,各取代基獨立地選自氟原子或甲基,
且其中該(苯氧基)-C2
-C3
-烷基-基團及該(苯基)-(C1
-C2
-烷基)-基團內之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子及氯原子或選自以下之基團:甲基、三氟甲基及甲氧基;
R17
表示C1
-C2
-烷基;
R18
及R19
在每次出現時獨立地表示氫原子或甲基;
R20
表示氫原子或選自以下之基團:C1
-C3
-烷基及苯基,
其中該C1
-C3
-烷基視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自羥基、C1
-C3
-烷氧基及苯基之基團,該苯基自身視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及甲基,
且其中該苯基視情況經取代一次、兩次或三次,各取代基獨立地選自氟原子及氯原子或選自以下之基團:甲基、三氟甲基、甲氧基及三氟甲氧基,及
R21
表示氫原子或C1
-C2
-烷基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
根據第一態樣之第五實施例,本發明涵蓋上文通式(I)化合物,其中:
R1
表示視情況經取代一次或兩次苯基或吡啶基,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:氰基、二氟甲基、三氟甲基、甲氧基、苯甲氧基、二氟甲氧基及三氟甲氧基,
或與該苯基或吡啶基之相鄰碳原子連接之兩個取代基一起形成二價基團-O-CF2
-O-;
R2
表示基團,
其中「*」指示與連接R2
之氮原子連接之點;
R3
表示選自甲基及-NH2
之基團;
R4
表示視情況經取代一次或兩次之苯基或吡啶基,各取代基獨立地選自鹵素原子或選自以下之基團:C1
-C2
-烷基、C1
-C2
-氟烷基、-OR9
, -N(R10
)(R11
)、-C(=O)-N(R12
)(R13
)及-C(=O)-OR17
;
R7
表示氫原子或C1
-C2
-烷基;
R8
表示-C(=O)-NH2
基團;
R9
表示氫原子或選自以下之基團:C1
-C2
-烷基、苯甲基、C1
-C2
-氟烷基、(C1
-C2
-烷氧基)-C2
-烷基-、((C1
-C2
-烷基)-C(=O)-O)-C2
-烷基-、-C(R18
)(R19
)-C(=O)-N(R20
)(R21
)、-C(=O)-N(R20
)(R21
)及苯基,
其中該苯甲基內之苯基及該苯基自身視情況經取代一次或兩次,各取代基獨立地選自氟原子及氯原子或選自以下之基團:氰基及甲基;
R10
及R11
在每次出現時獨立地表示氫原子或選自以下之基團:C1
-C2
-烷基、(C3
-C5
-環烷基)-(C1
-C2
-烷基)-、C3
-C7
-環烷基及(苯基)-(C1
-C2
-烷基)-O-C(=O)-,
其中C3
-C7
-環烷基及該(C3
-C5
-環烷基)-(C1
-C2
-烷基)-基團內之C3
-C5
-環烷基視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自以下之基團:氰基、甲基及C1
-氟烷基,
且其中該(苯基)-(C1
-C2
-烷基)-O-C(=O)-基團內之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及甲基,
或
R10
及R11
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自以下之基團:氰基、甲基及C1
-氟烷基;
R12
及R13
在每次出現時獨立地表示氫原子或選自以下之基團:C1
-C4
-烷基、C1
-C2
-氟烷基、C1
-C2
-羥烷基、(C1
-C4
-烷氧基)-C2
-C3
-烷基-、(C1
-C2
-氟烷氧基)-C2
-C3
-烷基-、(苯氧基)-C2
-C3
-烷基-、C3
-C7
-環烷基及(苯基)-(C1
-C2
-烷基)-,
其中C3
-C7
-環烷基視情況經取代一次或兩次,各取代基獨立地選自氟原子或甲基,
且其中該(苯氧基)-C2
-C3
-烷基-基團及該(苯基)-(C1
-C2
-烷基)-基團內之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子及氯原子或選自以下之基團:甲基、三氟甲基及甲氧基;
R17
表示C1
-C2
-烷基;
R18
及R19
在每次出現時獨立地表示氫原子或甲基;
R20
表示氫原子或選自以下之基團:C1
-C3
-烷基及苯基,
其中該C1
-C3
-烷基視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自羥基、C1
-C3
-烷氧基及苯基之基團,該苯基自身視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及甲基,
且其中該苯基視情況經取代一次、兩次或三次,各取代基獨立地選自氟原子及氯原子或選自以下之基團:甲基、三氟甲基、甲氧基及三氟甲氧基,及
R21
表示氫原子或C1
-C2
-烷基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
根據第一態樣之第六實施例,本發明涵蓋上文通式(I)化合物,其中:
R1
表示基團,
其中「**」指示與連接R1
之氮原子連接之點;
R2
表示基團,
其中「*」指示與連接R2
之氮原子連接之點;
R3
表示選自甲基及-NH2
之基團;
R4
表示基團
其中「#」指示與連接R4
之羰基連接之點;
R7
表示氫原子或C1
-C2
-烷基;
R8
表示-C(=O)-NH2
基團;
R9
表示氫原子或選自以下之基團:C1
-C2
-烷基、苯甲基、C1
-C2
-氟烷基、(C1
-C2
-烷氧基)-C2
-烷基-、((C1
-C2
-烷基)-C(=O)-O)-C2
-烷基-、-C(R18
)(R19
)-C(=O)-N(R20
)(R21
)、-C(=O)-N(R20
)(R21
)及苯基,
其中該苯甲基內之苯基及該苯基自身視情況經取代一次或兩次,各取代基獨立地選自氟原子及氯原子或選自以下之基團:氰基及甲基;
R10
及R11
在每次出現時獨立地表示氫原子或選自以下之基團:C1
-C2
-烷基、C3
-C7
-環烷基及(苯甲基)-O-C(=O)-,
其中C3
-C7
-環烷基視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自以下之基團:甲基及三氟甲基,
且其中該(苯甲基)-O-C(=O)-基團內之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及甲基,
或
R10
及R11
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自以下之基團:氰基、甲基及三氟甲基;
R12
及R13
在每次出現時獨立地表示氫原子或選自以下之基團:C1
-C4
-烷基、C1
-C2
-氟烷基、C1
-C2
-羥烷基、(C1
-C4
-烷氧基)-C2
-烷基-、(C1
-C2
-氟烷氧基)-C2
-烷基-、(苯氧基)-C2
-烷基-、C3
-C7
-環烷基及(苯基)-(C1
-C2
-烷基)-,
其中該(苯氧基)-C2
-烷基-基團及該(苯基)-(C1
-C2
-烷基)-基團內之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子及氯原子或選自以下之基團:甲基、三氟甲基及甲氧基,
R17
表示C1
-C2
-烷基;
R18
及R19
在每次出現時獨立地表示氫原子或甲基;
R20
表示選自苯甲基及苯基之基團,
其中該苯基及該苯甲基內之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及甲基,
R21
表示氫原子或甲基,
Y1
表示-C(H)=、-C(F)=、-C(Cl)=、-C(CN)=或-N=;
Y2
表示-C(H)=或-N=;
Y3
表示-C(R27
)=或-N=,
其限制條件為,若Y2
表示-N=,則Y3
表示-C(R27
)=;且若Y3
表示-N=,則Y2
表示-C(H)=;
R26
表示氟原子、氯原子或溴原子或選自以下之基團:甲基、二氟甲基、三氟甲基、甲氧基、苯甲氧基、二氟甲氧基及三氟甲氧基,及
R27
表示鹵素原子或選自以下之基團:C1
-C2
-烷基、C1
-C2
-氟烷基、-OR9
、-N(R10
)(R11
)、-C(=O)-N(R12
)(R13
)及-C(=O)-OR17
,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
根據第一態樣之第七實施例,本發明涵蓋上文通式(I)化合物,其中:
R1
表示基團,
其中「**」指示與連接R1
之氮原子連接之點;
R2
表示基團,
其中「*」指示與連接R2
之氮原子連接之點;
R3
表示選自甲基及-NH2
之基團;
R4
表示基團
其中「#」指示與連接R4
之羰基連接之點;
R7
表示氫原子或C1
-C2
-烷基;
R8
表示-C(=O)-NH2
基團;
R9
表示氫原子或選自以下之基團:C1
-C2
-烷基、苯甲基、C1
-C2
-氟烷基及苯基,
其中該苯甲基內之苯基及該苯基自身視情況經取代一次或兩次,各取代基獨立地選自氟原子及氯原子或選自以下之基團:氰基及甲基;
R10
及R11
在每次出現時獨立地表示氫原子或選自以下之基團:C1
-C2
-烷基及(苯甲基)-O-C(=O)-,
且其中該(苯甲基)-O-C(=O)-基團內之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及甲基,
或
R10
及R11
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自以下之基團:氰基、甲基及三氟甲基;
R12
及R13
在每次出現時獨立地表示氫原子或選自以下之基團:C1
-C2
-烷基、(C1
-C4
-烷氧基)-C2
-烷基-、(C1
-C2
-氟烷氧基)-C2
-烷基-、(苯氧基)-C2
-烷基-、C3
-C7
-環烷基及(苯基)-(C1
-C2
-烷基)-;
Y1
表示-C(H)=、-C(F)=、-C(Cl)=或-N=;
Y2
表示-C(H)=或-N=;
Y3
表示-C(R27
)=或-N=,
其限制條件為,若Y2
表示-N=,則Y3
表示-C(R27
)=;且若Y3
表示-N=,則Y2
表示-C(H)=;
R26
表示氟原子、氯原子或溴原子或選自以下之基團:二氟甲基、甲氧基、苯甲氧基、二氟甲氧基及三氟甲氧基,及
R27
表示鹵素原子或選自以下之基團:-OR9
、-N(R10
)(R11
)及-C(=O)-N(R12
)(R13
),
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
根據第一態樣之第八實施例,本發明涵蓋通式(I)化合物:
其中:
R1
表示視情況經取代一次、兩次或三次之苯基或6員雜芳基,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、硝基、C1
-C6
-烷基、(苯基)-(C1
-C3
-烷基)-、C1
-C6
-鹵烷基、C1
-C6
-烷氧基、(苯基)-(C1
-C3
-烷氧基)-、C1
-C6
-鹵烷氧基、-N(R5
)(R6
),
其中該(苯基)-(C1
-C3
-烷基)-基團及該(苯基)-(C1
-C3
-烷氧基)-基團中之苯基視情況經取代一次或兩次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、甲基、乙基、三氟甲基、甲氧基、乙氧基、二甲胺基及三氟甲氧基,
或與該苯基或6員雜芳基之相鄰碳原子連接之兩個取代基一起形成選自以下之二價基團:-(CH2
)3
-、-(CH2
)4
-、-(CH2
)2
-O-、-(CH2
)3
-O-、-CH2
-O-CH2
-、-(CH2
)2
-O-CH2
-、-O-CH2
-O-、-O-CH2
-CH2
-O-、-O-CF2
-O-、-O-CH2
-CF2
-O-及-O-CF2
-CF2
-O-,
或
R1
表示視情況經取代一次或兩次之5員雜芳基,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、C1
-C3
-烷基及C1
-C3
-烷氧基;
R2
表示基團,
其中「*」指示與連接R2
之氮原子連接之點;
R3
表示選自甲基及-NH2
之基團;
R4
表示視情況經取代一次、兩次或三次之苯基或6員雜芳基,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、硝基、C1
-C6
-烷基、(苯基)-(C1
-C3
-烷基)-、(5員雜芳基)-(C1
-C3
-烷基)-、C1
-C6
-羥烷基、C1
-C6
-鹵烷基、-OR9
、-N(R10
)(R11
)、-C(=O)-N(R12
)(R13
)、S(=O)n
-R14
及自身視情況經一個或兩個甲基取代之5員雜芳基,
或與該苯基或6員雜芳基之相鄰碳原子連接之兩個取代基一起形成選自以下之二價基團:-(CH2
)3
-、-(CH2
)4
-、-(CH2
)2
-O-、-(CH2
)3
-O-、-CH2
-O-CH2
-、-(CH2
)2
-O-CH2
-、-O-CH2
-O-、-O-CH2
-CH2
-O-、-O-CF2
-O-、-O-CH2
-CF2
-O-及-O-CF2
-CF2
-O-;
R5
及R6
在每次出現時獨立地表示氫原子或選自以下之基團:C1
-C4
-烷基、(C1
-C4
-烷基)-C(=O)-、C3
-C4
-環烷基及(苯基)-(C1
-C3
-烷基)-,
或
R5
及R6
連同其所連接之氮原子一起表示視情況經取代一次、兩次或三次之單環含氮4至7員雜環烷基,各取代基獨立地選自鹵素原子或選自以下之基團:側氧基、羥基、C1
-C4
-烷基、(C1
-C4
-烷基)-C(=O)-、C3
-C4
-環烷基及C1
-C4
-烷氧基;
R7
表示氫原子或C1
-C2
-烷基;
R8
表示選自-C(=O)-NH2
及-S(=O)2
-NH2
之基團;
R9
表示氫原子或選自以下之基團:C1
-C6
-烷基、(苯基)-(C1
-C3
-烷基)-、C1
-C6
-鹵烷基、C2
-C4
-羥烷基、(C1
-C3
-烷氧基)-C2
-C3
-烷基-、((C1
-C3
-烷基)-C(=O)-O)-C2
-C3
-烷基-、-C(R18
)(R19
)-C(=O)-OR17
、-C(R18
)(R19
)-C(=O)-N(R20
)(R21
)及苯基,
其中該(苯基)-(C1
-C3
-烷基)-基團內之苯基及該苯基自身視情況經取代一次或兩次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、甲基、乙基、三氟甲基、甲氧基、乙氧基、二甲胺基及三氟甲氧基;
R10
及R11
在每次出現時獨立地表示氫原子或選自以下之基團:C1
-C4
-烷基、C1
-C4
-鹵烷基、C2
-C4
-羥烷基、(C1
-C3
-烷氧基)-C2
-C3
-烷基-、((R22
)(R23
)N)-C2
-C3
-烷基、(C1
-C4
-烷基)-C(=O)-、C3
-C7
-環烷基、(C3
-C7
-環烷基)-C(=O)-、(苯基)-(C1
-C3
-烷基)-、(苯基)-(C1
-C3
-烷基)-C(=O)-及(苯基)-(C1
-C3
-烷基)-O-C(=O)-,
其中該(苯基)-(C1
-C3
-烷基)-基團、該(苯基)-(C1
-C3
-烷基)-C(=O)-基團及該(苯基)-(C1
-C3
-烷基)-O-C(=O)-基團內之苯基視情況經取代一次或兩次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、甲基、乙基、三氟甲基、甲氧基、乙氧基、二甲胺基及三氟甲氧基,
或
R10
及R11
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基或雙環含氮6至11員雜環烷基,其視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、側氧基、羥基、C1
-C4
-烷基、C1
-C4
-鹵烷基、(C1
-C4
-烷基)-C(=O)-、C3
-C7
-環烷基、C1
-C4
-烷氧基、-N(R22
)(R23
)及單環4至7員雜環烷基;
R12
及R13
在每次出現時獨立地表示氫原子或選自以下之基團:C1
-C4
-烷基、C1
-C4
-鹵烷基、C1
-C4
-羥烷基、(C1
-C3
-烷氧基)-C2
-C3
-烷基-、C3
-C7
-環烷基、單環4至7員雜環烷基及(苯基)-(C1
-C3
-烷基)-,
其中C3
-C7
-環烷基及單環4至7員雜環烷基視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:側氧基、羥基、C1
-C4
-烷基、(C1
-C4
-烷基)-C(=O)-、C3
-C4
-環烷基及C1
-C4
-烷氧基,
或
R12
及R13
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:側氧基、羥基、C1
-C4
-烷基、(C1
-C4
-烷基)-C(=O)-、C3
-C4
-環烷基及C1
-C4
-烷氧基;
R14
表示選自C1
-C4
-烷基及C1
-C4
-鹵烷基之基團;
R17
表示C1
-C4
-烷基;
R18
及R19
在每次出現時獨立地表示氫原子或C1
-C4
-烷基;
R20
表示氫原子或選自以下之基團:C1
-C6
-烷基、C3
-C4
-烯基、C3
-C4
-炔基、C1
-C3
-烷氧基、C3
-C7
-環烷基、雙環C6
-C11
-環烷基、金剛烷基、單環4至7員雜環烷基、雙環6至11員雜環烷基、苯基、萘基及5至10員雜芳基,
其中該C1
-C6
-烷基視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:羥基、氰基、C1
-C3
-烷氧基、-N(R22
)(R23
)、C3
-C7
-環烷基、雙環C6
-C11
-環烷基、金剛烷基、單環4至7員雜環烷基、雙環6至11員雜環烷基、苯基及5至10員雜芳基,該苯基取代基及該5至10員雜芳基取代基自身視情況經取代一次或兩次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、甲基、乙基、三氟甲基、甲氧基、乙氧基、二甲胺基及三氟甲氧基,
其中C3
-C7
-環烷基、雙環C6
-C11
-環烷基、金剛烷基、單環4至7員雜環烷基及雙環6至11員雜環烷基視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、側氧基、羥基、C1
-C4
-烷基、(C1
-C4
-烷基)-C(=O)-、C3
-C4
-環烷基及C1
-C4
-烷氧基,
且其中該苯基、該萘基及該5至10員雜芳基視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、C1
-C4
-烷基、C1
-C4
-鹵烷基、C1
-C4
-烷氧基、C1
-C4
-鹵烷氧基、-N(R22
)(R23
)及-C(=O)-N(R24
)(R25
),
R21
表示氫原子或C1
-C4
-烷基,
或
R20
及R21
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況為苯并縮合的且其視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、側氧基、羥基、C1
-C4
-烷基、C1
-C4
-鹵烷基、(苯基)-(C1
-C3
-烷基)-、(C1
-C4
-烷基)-C(=O)-、C3
-C4
-環烷基、C1
-C4
-烷氧基、C1
-C3
-鹵烷氧基、-N(R22
)(R23
)及-C(=O)-N(R24
)(R25
);
R22
及R23
在每次出現時獨立地表示氫原子或選自C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-之基團;
R24
及R25
在每次出現時獨立地表示氫原子或C1
-C4
-烷基,及
n 表示整數0、1或2,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
根據第一態樣之第九實施例,本發明涵蓋上文通式(I)化合物,其中:
R1
表示視情況經取代一次、兩次或三次之苯基或吡啶基,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、硝基、C1
-C4
-烷基、(苯基)-(C1
-C2
-烷基)-、C1
-C4
-鹵烷基、C1
-C4
-烷氧基、(苯基)-(C1
-C2
-烷氧基)-、C1
-C4
-鹵烷氧基、-N(R5
)(R6
),
其中該(苯基)-(C1
-C2
-烷基)-基團及該(苯基)-(C1
-C2
-烷氧基)-基團中之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及溴原子或選自甲基、三氟甲基及甲氧基之基團,
或與該苯基或吡啶基之相鄰碳原子連接之兩個取代基一起形成選自以下之二價基團:-(CH2
)3
-、-(CH2
)4
-、-(CH2
)2
-O-、-(CH2
)3
-O-、-CH2
-O-CH2
-、-O-CH2
-O-、-O-CH2
-CH2
-O-及-O-CF2
-O-,
或
R1
表示視情況經取代一次或兩次之吡唑基,各取代基獨立地選自鹵素原子或選自氰基、C1
-C2
-烷基及C1
-C2
-烷氧基之基團;
R2
表示基團,
其中「*」指示與連接R2
之氮原子連接之點;
R3
表示選自甲基及-NH2
之基團;
R4
表示視情況經取代一次、兩次或三次之苯基或吡啶基,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、硝基、C1
-C4
-烷基、(苯基)-(C1
-C2
-烷基)-、(5員雜芳基)-(C1
-C2
-烷基)-、C1
-C4
-羥烷基、C1
-C4
-鹵烷基、-OR9
、-N(R10
)(R11
)、-C(=O)-N(R12
)(R13
)、S(=O)n
-R14
及自身視情況經一個或兩個甲基取代之5員雜芳基,
或與該苯基或吡啶基之相鄰碳原子連接之兩個取代基一起形成選自以下之二價基團:-(CH2
)3
-、-(CH2
)4
-、-(CH2
)2
-O-、-(CH2
)3
-O-、-CH2
-O-CH2
-、-O-CH2
-O-、-O-CH2
-CH2
-O-及-O-CF2
-O-;
R5
及R6
在每次出現時獨立地表示氫原子或選自C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-之基團,
或
R5
及R6
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:側氧基、羥基、C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-;
R7
表示氫原子或C1
-C2
-烷基;
R8
表示-C(=O)-NH2
基團;
R9
表示氫原子或選自以下之基團:C1
-C4
-烷基、(苯基)-(C1
-C2
-烷基)-、C1
-C4
-鹵烷基、C2
-C3
-羥烷基、(C1
-C2
-烷氧基)-C2
-烷基-、((C1
-C2
-烷基)-C(=O)-O)-C2
-烷基-、-C(R18
)(R19
)-C(=O)-OR17
、-C(R18
)(R19
)-C(=O)-N(R20
)(R21
)及苯基,
其中該(苯基)-(C1
-C2
-烷基)-基團內之苯基及該苯基自身視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:甲基、三氟甲基及甲氧基;
R10
及R11
在每次出現時獨立地表示氫原子或選自以下之基團:C1
-C2
-烷基、C1
-C2
-鹵烷基、C2
-C3
-羥烷基、(C1
-C2
-烷氧基)-C2
-烷基-、((R22
)(R23
)N)-C2
-烷基、(C1
-C2
-烷基)-C(=O)-、C3
-C5
-環烷基、(C3
-C5
-環烷基)-C(=O)-、(苯基)-(C1
-C2
-烷基)-、(苯基)-(C1
-C2
-烷基)-C(=O)-及(苯基)-(C1
-C2
-烷基)-O-C(=O)-,
其中該(苯基)-(C1
-C2
-烷基)-基團、該(苯基)-(C1
-C2
-烷基)-C(=O)-基團及該(苯基)-(C1
-C2
-烷基)-O-C(=O)-基團內之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:甲基、三氟甲基及甲氧基,
或
R10
及R11
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基或雙環含氮6至10員雜環烷基,其視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、側氧基、羥基、C1
-C2
-烷基、C1
-C2
-鹵烷基、(C1
-C2
-烷基)-C(=O)-、C1
-C2
-烷氧基、-N(R22
)(R23
)及單環4至7員雜環烷基;
R12
及R13
在每次出現時獨立地表示氫原子或選自以下之基團:C1
-C4
-烷基、C1
-C4
-鹵烷基、C1
-C4
-羥烷基、(C1
-C2
-烷氧基)-C2
-C3
-烷基-、C3
-C7
-環烷基、單環4至7員雜環烷基及(苯基)-(C1
-C3
-烷基)-,
其中C3
-C7
-環烷基及單環4至7員雜環烷基視情況經取代一次或兩次,各取代基獨立地選自鹵素原子或選自以下之基團:側氧基、C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-,
或
R12
及R13
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況經取代一次或兩次,各取代基獨立地選自鹵素原子或選自以下之基團:側氧基、C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-;
R14
表示選自C1
-C2
-烷基及C1
-C2
-鹵烷基之基團;
R17
表示C1
-C4
-烷基;
R18
及R19
在每次出現時獨立地表示氫原子或C1
-C2
-烷基;
R20
表示氫原子或選自以下之基團:C1
-C6
-烷基、C3
-C4
-烯基、C3
-C4
-炔基、C1
-C3
-烷氧基、C3
-C7
-環烷基、雙環C6
-C11
-環烷基、金剛烷基、單環4至7員雜環烷基、雙環6至10員雜環烷基、苯基、萘基及5至10員雜芳基,
其中該C1
-C6
-烷基視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:羥基、氰基、C1
-C3
-烷氧基、-N(R22
)(R23
)、C3
-C7
-環烷基、雙環C6
-C11
-環烷基、金剛烷基、單環4至7員雜環烷基、雙環6至10員雜環烷基、苯基及5至10員雜芳基,該苯基取代基及該5至10員雜芳基取代基自身視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:甲基、三氟甲基及甲氧基,
其中C3
-C7
-環烷基、雙環C6
-C11
-環烷基、金剛烷基、單環4至7員雜環烷基、雙環6至10員雜環烷基視情況經取代一次或兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、側氧基、羥基、C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-,
且其中該苯基、該萘基及該5至10員雜芳基視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、C1
-C2
-烷基、C1
-C2
-鹵烷基、C1
-C2
-烷氧基、C1
-C2
-鹵烷氧基、-N(R22
)(R23
)及-C(=O)-N(R24
)(R25
),
R21
表示氫原子或C1
-C2
-烷基,
或
R20
及R21
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況為苯并縮合的且其視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、側氧基、羥基、C1
-C2
-烷基、C1
-C2
-鹵烷基、(苯基)-(C1
-C2
-烷基)-、(C1
-C2
-烷基)-C(=O)-、C3
-C4
-環烷基、C1
-C2
-烷氧基、C1
-C2
-鹵烷氧基、-N(R22
)(R23
)及-C(=O)-N(R24
)(R25
);
R22
及R23
在每次出現時獨立地表示氫原子或選自C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-之基團;
R24
及R25
在每次出現時獨立地表示氫原子或C1
-C2
-烷基,及
n 表示整數0、1或2,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
根據第一態樣之第十實施例,本發明涵蓋上文通式(I)化合物,其中:
R1
表示視情況經取代一次、兩次或三次之苯基或吡啶基,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:氰基、C1
-C4
-烷基、C1
-C2
-氟烷基、C1
-C2
-烷氧基、C1
-C2
-氟烷氧基及-N(R5
)(R6
),
或與該苯基或吡啶基之相鄰碳原子連接之兩個取代基一起形成選自以下之二價基團:-(CH2
)3
-、-O-CH2
-O-及-O-CF2
-O-,
或
R1
表示視情況經一個甲基取代之吡唑基,
R2
表示基團,
其中「*」指示與連接R2
之氮原子連接之點;
R3
表示選自甲基及-NH2
之基團;
R4
表示視情況經取代一次、兩次或三次之苯基或吡啶基,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:氰基、C1
-C3
-烷基、C1
-C3
-羥烷基、C1
-C3
-氟烷基、-OR9
、-N(R10
)(R11
)、-C(=O)-N(R12
)(R13
)及S(=O)n
-R14
,
或與該苯基或吡啶基之相鄰碳原子連接之兩個取代基一起形成選自以下之二價基團:-(CH2
)3
-、-O-CH2
-O-及-O-CF2
-O-;
R5
及R6
在每次出現時獨立地表示氫原子或C1
-C2
-烷基,
或
R5
及R6
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自以下之基團:羥基及C1
-C2
-烷基;
R7
表示氫原子或C1
-C2
-烷基;
R8
表示-C(=O)-NH2
基團;
R9
表示氫原子或選自以下之基團:C1
-C2
-烷基、苯甲基、C1
-C2
-氟烷基、(C1
-C2
-烷氧基)-C2
-烷基-、((C1
-C2
-烷基)-C(=O)-O)-C2
-烷基-、-C(R18
)(R19
)-C(=O)-OR17
、-C(R18
)(R19
)-C(=O)-N(R20
)(R21
)及苯基,
其中該苯甲基內之苯基及該苯基自身視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及甲基;
R10
及R11
在每次出現時獨立地表示氫原子或選自以下之基團:C1
-C2
-烷基、C1
-C2
-氟烷基、(C1
-C2
-烷基)-C(=O)-、(苯基)-(C1
-C2
-烷基)-、(苯基)-(C1
-C2
-烷基)-C(=O)-及(苯基)-(C1
-C2
-烷基)-O-C(=O)-,
其中該(苯基)-(C1
-C2
-烷基)-基團、該(苯基)-(C1
-C2
-烷基)-C(=O)-基團及該(苯基)-(C1
-C2
-烷基)-O-C(=O)-基團內之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及甲基,
或
R10
及R11
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自以下之基團:側氧基、C1
-C2
-烷基、C1
-C2
-氟烷基及(C1
-C2
-烷基)-C(=O)-;
R12
及R13
在每次出現時獨立地表示氫原子或選自以下之基團:C1
-C4
-烷基、C1
-C4
-氟烷基、C3
-C7
-環烷基、單環4至7員雜環烷基及(苯基)-(C1
-C2
-烷基)-,
其中C3
-C7
-環烷基及單環4至7員雜環烷基視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自以下之基團:側氧基、C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-,
或
R12
及R13
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況經取代一次或兩次,各取代基獨立地選自鹵素原子或選自以下之基團:側氧基、C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-;
R14
表示選自甲基及三氟甲基之基團;
R17
表示C1
-C2
-烷基;
R18
及R19
在每次出現時獨立地表示氫原子或甲基;
R20
表示氫原子或選自以下之基團:視情況經取代C1
-C3
-烷基、未經取代C4
-C6
-烷基、丙-2-炔基、甲氧基、C3
-C6
-環烷基、金剛烷基、單環4至7員雜環烷基、苯基及5至10員雜芳基,
其中該C1
-C3
-烷基視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:羥基、氰基、C1
-C3
-烷氧基、-N(R22
)(R23
)、C3
-C6
-環烷基、金剛烷基、單環4至7員雜環烷基、苯基及5至10員雜芳基,該苯基取代基及該5至10員雜芳基取代基自身視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及甲基,
其中該C3
-C6
-環烷基、該金剛烷基及該單環4至7員雜環烷基視情況經取代一次或兩次或三次,各取代基獨立地選自氟原子或選自以下之基團:側氧基、C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-,
且其中該苯基及該5至10員雜芳基視情況經取代一次、兩次或三次,各取代基獨立地選自氟原子及氯原子或選自以下之基團:氰基、C1
-C2
-烷基、C1
-C2
-氟烷基、C1
-C2
-烷氧基、C1
-C2
-鹵烷氧基、-N(R22
)(R23
)及-C(=O)-N(R24
)(R25
),
R21
表示氫原子或C1
-C2
-烷基,
或
R20
及R21
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況為苯并縮合的,且其視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、側氧基、羥基、C1
-C2
-烷基、C1
-C2
-氟烷基、苯甲基、(C1
-C2
-烷基)-C(=O)-、C3
-C4
-環烷基、C1
-C2
-烷氧基、C1
-C2
-鹵烷氧基、-N(R22
)(R23
)及-C(=O)-N(R24
)(R25
);
R22
及R23
在每次出現時獨立地表示氫原子或選自C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-之基團;
R24
及R25
在每次出現時獨立地表示氫原子或C1
-C2
-烷基,及
n 表示整數2,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
根據第一態樣之第十一實施例,本發明涵蓋上文通式(I)化合物,其中:
R1
表示視情況經取代一次或兩次之苯基或吡啶基,各取代基獨立地選自氟原子及氯原子或選自以下之基團:氰基、C1
-C2
-烷基、C1
-C2
-氟烷基、C1
-C2
-烷氧基、C1
-C2
-氟烷氧基;
R2
表示基團,
其中「*」指示與連接R2
之氮原子連接之點;
R3
表示選自甲基及-NH2
之基團;
R4
表示視情況經取代一次或兩次之苯基或吡啶基,各取代基獨立地選自氟原子及氯原子或選自以下之基團:C1
-C2
-烷基、C1
-C2
-氟烷基、-OR9
;
R7
表示氫原子或C1
-C2
-烷基;
R8
表示-C(=O)-NH2
基團,及
R9
表示選自以下之基團:C1
-C2
-烷基、苯甲基、C1
-C2
-氟烷基、(C1
-C2
-烷氧基)-C2
-烷基-及苯基,
其中該苯甲基內之苯基及該苯基自身視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及甲基;
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
根據第一態樣之第十二實施例,本發明涵蓋上文通式(I)化合物,其中:
R1
表示視情況經取代一次或兩次之苯基或吡啶基,各取代基獨立地選自氟原子及氯原子或選自以下之基團:氰基、C1
-C2
-氟烷基、C1
-C2
-烷氧基、C1
-C2
-氟烷氧基;
R2
表示基團,
其中「*」指示與連接R2
之氮原子連接之點;
R3
表示選自甲基及-NH2
之基團;
R4
表示視情況經取代一次或兩次之苯基或吡啶基,各取代基獨立地選自氟原子及氯原子或選自以下之基團:C1
-C2
-烷基、C1
-C2
-氟烷基、-OR9
;
R7
表示氫原子或C1
-C2
-烷基;
R8
表示-C(=O)-NH2
基團,及
R9
表示選自以下之基團:C1
-C2
-烷基、苯甲基、C1
-C2
-氟烷基、(C1
-C2
-烷氧基)-C2
-烷基-及苯基,
其中該苯甲基內之苯基及該苯基自身視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及甲基;
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
根據第一態樣之第十三實施例,本發明涵蓋上文通式(I)化合物,其中:
R1
表示基團
其中「**」指示與連接R1
之氮原子連接之點;
R2
表示基團,
其中「*」指示與連接R2
之氮原子連接之點;
R3
表示選自甲基及-NH2
之基團;
R4
表示基團
其中「#」指示與連接R4
之羰基連接之點;
R7
表示氫原子或C1
-C2
-烷基;
R8
表示-C(=O)-NH2
基團;
Y1
表示-C(H)=、-C(F)=、-C(Cl)=、-C(CN)=或-N=;
Y2
表示-C(H)=及-N=;
Y3
表示-C(R27
)=及-N=,
其限制條件為,若Y2
表示-N=,則Y3
表示-C(R27
)=;且若Y3
表示-N=,則Y2
表示-C(H)=;
R26
表示氟原子、氯原子或選自以下之基團:C1
-C2
-烷基、C1
-C2
-氟烷基、C1
-C2
-烷氧基及C1
-C2
-氟烷氧基,及
R27
表示氟原子、氯原子或選自以下之基團:C1
-C2
-烷氧基、苯甲氧基及C1
-C2
-氟烷氧基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
根據第一態樣之第十四實施例,本發明涵蓋上文通式(I)化合物,其中:
R1
表示基團
其中「**」指示與連接R1
之氮原子連接之點;
R2
表示基團,
其中「*」指示與連接R2
之氮原子連接之點;
R3
表示選自甲基及-NH2
之基團;
R4
表示基團
其中「#」指示與連接R4
之羰基連接之點;
R7
表示氫原子或C1
-C2
-烷基;
R8
表示-C(=O)-NH2
基團;
Y1
表示-C(H)=、-C(F)=、-C(Cl)=、-C(CN)=或-N=;
Y2
表示-C(H)=或-N=;
Y3
表示-C(R27
)=或-N=,
其限制條件為,若Y2
表示-N=,則Y3
表示-C(R27
)=;且若Y3
表示-N=,則Y2
表示-C(H)=;
R26
表示氟原子、氯原子或選自以下之基團:C1
-C2
-烷基、C1
-C2
-氟烷基、C1
-C2
-烷氧基及C1
-C2
-氟烷氧基,及
R27
表示氟原子、氯原子或選自以下之基團:C1
-C2
-烷氧基、苯甲氧基及C1
-C2
-氟烷氧基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
根據第一態樣之第十五實施例,本發明涵蓋上文通式(I)化合物,其中:
R1
表示基團
其中「**」指示與連接R1
之氮原子連接之點;
R2
表示基團,
其中「*」指示與連接R2
之氮原子連接之點;
R3
表示選自甲基及-NH2
之基團;
R4
表示基團
其中「#」指示與連接R4
之羰基連接之點;
R7
表示氫原子或C1
-C2
-烷基;
R8
表示-C(=O)-NH2
基團;
Y1
表示-C(H)=、-C(F)=或-N=;
Y2
表示-C(H)=及-N=;
Y3
表示-C(R27
)=及-N=,
其限制條件為,若Y2
表示-N=,則Y3
表示-C(R27
)=;且若Y3
表示-N=,則Y2
表示-C(H)=;
R26
表示氟原子、氯原子或選自以下之基團:甲基、二氟甲基、三氟甲基、甲氧基、二氟甲氧基及三氟甲氧基,及
R27
表示氯原子或選自以下之基團:甲氧基、苯甲氧基、二氟甲氧基及三氟甲氧基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
根據第一態樣之第十六實施例,本發明涵蓋上文通式(I)化合物,其中:
R1
表示基團
其中「**」指示與連接R1
之氮原子連接之點;
R2
表示基團,
其中「*」指示與連接R2
之氮原子連接之點;
R3
表示選自甲基及-NH2
之基團;
R4
表示基團
其中「#」指示與連接R4
之羰基連接之點;
R7
表示氫原子或C1
-C2
-烷基;
R8
表示-C(=O)-NH2
基團;
Y1
表示-C(H)=、-C(F)=或-N=;
Y2
表示-C(H)=或-N=;
Y3
表示-C(R27
)=或-N=,
其限制條件為,若Y2
表示-N=,則Y3
表示-C(R27
)=;且若Y3
表示-N=,則Y2
表示-C(H)=;
R26
表示氟原子、氯原子或選自以下之基團:甲基、二氟甲基、三氟甲基、甲氧基、二氟甲氧基及三氟甲氧基,及
R27
表示氯原子或選自以下之基團:甲氧基、苯甲氧基、二氟甲氧基及三氟甲氧基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
根據第一態樣之第十七實施例,本發明涵蓋上文通式(I)化合物,其中:
R1
表示基團
其中「**」指示與連接R1
之氮原子連接之點;
R2
表示基團,
其中「*」指示與連接R2
之氮原子連接之點;
R3
表示-NH2
基團;
R4
表示基團
其中「#」指示與連接R4
之羰基連接之點;
R7
表示氫原子或C1
-C2
-烷基;
R8
表示-C(=O)-NH2
基團;
Y1
表示-C(H)=、-C(F)=、-C(Cl)=、-C(CN)=或-N=;
Y2
表示-C(H)=及-N=;
Y3
表示-C(R27
)=及-N=,
其限制條件為,若Y2
表示-N=,則Y3
表示-C(R27
)=;且若Y3
表示-N=,則Y2
表示-C(H)=;
R26
表示氟原子、氯原子或選自以下之基團:C1
-C2
-烷基、C1
-C2
-氟烷基、C1
-C2
-烷氧基及C1
-C2
-氟烷氧基,及
R27
表示氟原子、氯原子或選自以下之基團:C1
-C2
-烷氧基、苯甲氧基及C1
-C2
-氟烷氧基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
根據第一態樣之第十八實施例,本發明涵蓋上文通式(I)化合物,其中:
R1
表示基團
其中「**」指示與連接R1
之氮原子連接之點;
R2
表示基團,
其中「*」指示與連接R2
之氮原子連接之點;
R3
表示-NH2
基團;
R4
表示基團
其中「#」指示與連接R4
之羰基連接之點;
R7
表示氫原子或C1
-C2
-烷基;
R8
表示-C(=O)-NH2
基團;
Y1
表示-C(H)=、-C(F)=、-C(Cl)=、-C(CN)=或-N=;
Y2
表示-C(H)=或-N=;
Y3
表示-C(R27
)=或-N=,
其限制條件為,若Y2
表示-N=,則Y3
表示-C(R27
)=;且若Y3
表示-N=,則Y2
表示-C(H)=;
R26
表示氟原子、氯原子或選自以下之基團:C1
-C2
-烷基、C1
-C2
-氟烷基、C1
-C2
-烷氧基及C1
-C2
-氟烷氧基,及
R27
表示氟原子、氯原子或選自以下之基團:C1
-C2
-烷氧基、苯甲氧基及C1
-C2
-氟烷氧基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
根據第一態樣之第十九實施例,本發明涵蓋上文通式(I)化合物,其中:
R1
表示基團
其中「**」指示與連接R1
之氮原子連接之點;
R2
表示基團,
其中「*」指示與連接R2
之氮原子連接之點;
R3
表示-NH2
基團;
R4
表示基團
其中「#」指示與連接R4
之羰基連接之點;
R7
表示氫原子或C1
-C2
-烷基;
R8
表示-C(=O)-NH2
基團;
Y1
表示-C(H)=、-C(F)=或-N=;
Y2
表示-C(H)=及-N=;
Y3
表示-C(R27
)=及-N=,
其限制條件為,若Y2
表示-N=,則Y3
表示-C(R27
)=;且若Y3
表示-N=,則Y2
表示-C(H)=;
R26
表示氟原子、氯原子或選自以下之基團:甲基、二氟甲基、三氟甲基、甲氧基、二氟甲氧基及三氟甲氧基,及
R27
表示氯原子或選自以下之基團:甲氧基、苯甲氧基、二氟甲氧基及三氟甲氧基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
根據第一態樣之第二十實施例,本發明涵蓋上文通式(I)化合物,其中:
R1
表示基團
其中「**」指示與連接R1
之氮原子連接之點;
R2
表示基團,
其中「*」指示與連接R2
之氮原子連接之點;
R3
表示-NH2
基團;
R4
表示基團
其中「#」指示與連接R4
之羰基連接之點;
R7
表示氫原子或C1
-C2
-烷基;
R8
表示-C(=O)-NH2
基團;
Y1
表示-C(H)=、-C(F)=或-N=;
Y2
表示-C(H)=或-N=;
Y3
表示-C(R27
)=或-N=,
其限制條件為,若Y2
表示-N=,則Y3
表示-C(R27
)=;且若Y3
表示-N=,則Y2
表示-C(H)=;
R26
表示氟原子、氯原子或選自以下之基團:甲基、二氟甲基、三氟甲基、甲氧基、二氟甲氧基及三氟甲氧基,及
R27
表示氯原子或選自以下之基團:甲氧基、苯甲氧基、二氟甲氧基及三氟甲氧基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
根據第一態樣之第二十一實施例,本發明涵蓋上文通式(I)化合物,其中:
R1
表示基團,
其中「**」指示與連接R1
之氮原子連接之點,
或
R1
表示基團,
其中「**」指示與連接R1
之氮原子連接之點;
R2
表示基團,
其中「*」指示與連接R2
之氮原子連接之點;
R3
表示選自甲基及-NH2
之基團;
R4
表示選自以下之基團: ,
其中「#」指示與連接R4
之羰基連接之點;
R7
表示甲基;
R8
表示-C(=O)-NH2
基團;
Y1
表示-C(H)=或-C(F)=;
R26
表示氟原子、氯原子或選自以下之基團:二氟甲基、三氟甲基、甲氧基、二氟甲氧基及三氟甲氧基;
R28
表示選自以下之基團:甲基、二氟甲基、三氟甲基、甲氧基、二氟甲氧基及三氟甲氧基;
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
根據第一態樣之第二十二實施例,本發明涵蓋上文通式(I)化合物,其中:
R1
表示基團,
其中「**」指示與連接R1
之氮原子連接之點,
或
R1
表示基團,
其中「**」指示與連接R1
之氮原子連接之點;
R2
表示基團,
其中「*」指示與連接R2
之氮原子連接之點;
R3
表示-NH2
基團;
R4
表示選自以下之基團: ,
其中「#」指示與連接R4
之羰基連接之點;
R7
表示甲基;
R8
表示-C(=O)-NH2
基團;
Y1
表示-C(H)=或-C(F)=;
R26
表示氟原子、氯原子或選自以下之基團:二氟甲基、三氟甲基、甲氧基、二氟甲氧基及三氟甲氧基;
R28
表示選自以下之基團:甲基、二氟甲基、三氟甲基、甲氧基、二氟甲氧基及三氟甲氧基;
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
根據第一態樣之第二十三實施例,本發明涵蓋上文通式(I)化合物,其中:
R1
表示基團,
其中「**」指示與連接R1
之氮原子連接之點,
或
R1
表示基團,
其中「**」指示與連接R1
之氮原子連接之點;
R2
表示基團,
其中「*」指示與連接R2
之氮原子連接之點;
R3
表示甲基;
R4
表示選自以下之基團: ,
其中「#」指示與連接R4
之羰基連接之點;
R7
表示甲基;
R8
表示-C(=O)-NH2
基團;
Y1
表示-C(H)=或-C(F)=;
R26
表示氟原子、氯原子或選自以下之基團:二氟甲基、三氟甲基、甲氧基、二氟甲氧基及三氟甲氧基;
R28
表示選自以下之基團:甲基、二氟甲基、三氟甲基、甲氧基、二氟甲氧基及三氟甲氧基;
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
根據第一態樣之第二十四實施例,本發明涵蓋上文通式(I)化合物,其中:
R1
表示選自以下之基團: ,
其中「**」指示與連接R1
之氮原子連接之點;
R2
表示基團,
其中「*」指示與連接R2
之氮原子連接之點;
R3
表示-NH2
基團;
R4
表示選自以下之基團: ,
其中「#」指示與連接R4
之羰基連接之點;
R7
表示甲基;
R8
表示-C(=O)-NH2
基團;
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
根據第一態樣之第二十五實施例,本發明涵蓋上文通式(I)化合物,其中:
R1
表示選自以下之基團:,
其中「**」指示與連接R1
之氮原子連接之點;
R2
表示基團,
其中「*」指示與連接R2
之氮原子連接之點;
R3
表示甲基;
R4
表示選自以下之基團:,
其中「#」指示與連接R4
之羰基連接之點;
R7
表示甲基;
R8
表示-C(=O)-NH2
基團;
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
本發明之第一態樣之其他實施例 在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R1
表示視情況經取代一次、兩次或三次之苯基或吡啶基,各取代基獨立地選自鹵素原子或選自以下之基團:羥基、氰基、硝基、C1
-C4
-烷基、(苯基)-(C1
-C2
-烷基)-、C1
-C4
-鹵烷基、C1
-C4
-烷氧基、(苯基)-(C1
-C2
-烷氧基)-、C1
-C4
-鹵烷氧基、-N(R5
)(R6
),
其中該(苯基)-(C1
-C2
-烷基)-基團及該(苯基)-(C1
-C2
-烷氧基)-基團中之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及溴原子或選自甲基、三氟甲基及甲氧基之基團,
或與該苯基或吡啶基之相鄰碳原子連接之兩個取代基一起形成選自以下之二價基團:-(CH2
)3
-、-(CH2
)4
-、-(CH2
)2
-O-、-(CH2
)3
-O-、-CH2
-O-CH2
-、-O-CH2
-O-、-O-CH2
-CH2
-O-及-O-CF2
-O-,
或
R1
表示視情況經取代一次或兩次之吡唑基,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、C1
-C2
-烷基及C1
-C2
-烷氧基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R1
表示視情況經取代一次、兩次或三次之苯基或吡啶基,各取代基獨立地選自鹵素原子或選自以下之基團:羥基、氰基、硝基、C1
-C4
-烷基、(苯基)-(C1
-C2
-烷基)-、C1
-C4
-鹵烷基、C1
-C4
-烷氧基、(苯基)-(C1
-C2
-烷氧基)-、C1
-C4
-鹵烷氧基、-N(R5
)(R6
),
其中該(苯基)-(C1
-C2
-烷基)-基團及該(苯基)-(C1
-C2
-烷氧基)-基團中之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及溴原子或選自甲基、三氟甲基及甲氧基之基團,
或與該苯基或吡啶基之相鄰碳原子連接之兩個取代基一起形成選自以下之二價基團:-(CH2
)3
-、-(CH2
)4
-、-(CH2
)2
-O-、-(CH2
)3
-O-、-CH2
-O-CH2
-、-O-CH2
-O-、-O-CH2
-CH2
-O-及-O-CF2
-O-,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R1
表示視情況經取代一次、兩次或三次之苯基或吡啶基,各取代基獨立地選自鹵素原子或選自以下之基團:羥基、氰基、硝基、(苯基)-(C1
-C2
-烷基)-、C1
-C4
-鹵烷基、C1
-C4
-烷氧基、(苯基)-(C1
-C2
-烷氧基)-、C1
-C4
-鹵烷氧基、-N(R5
)(R6
),
其中該(苯基)-(C1
-C2
-烷基)-基團及該(苯基)-(C1
-C2
-烷氧基)-基團中之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及溴原子或選自甲基、三氟甲基及甲氧基之基團,
或與該苯基或吡啶基之相鄰碳原子連接之兩個取代基一起形成選自以下之二價基團:-(CH2
)3
-、-(CH2
)4
-、-(CH2
)2
-O-、-(CH2
)3
-O-、-CH2
-O-CH2
-、-O-CH2
-O-、-O-CH2
-CH2
-O-及-O-CF2
-O-,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R1
表示視情況經取代一次、兩次或三次之苯基或吡啶基,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、硝基、C1
-C4
-烷基、(苯基)-(C1
-C2
-烷基)-、C1
-C4
-鹵烷基、C1
-C4
-烷氧基、(苯基)-(C1
-C2
-烷氧基)-、C1
-C4
-鹵烷氧基、-N(R5
)(R6
),
其中該(苯基)-(C1
-C2
-烷基)-基團及該(苯基)-(C1
-C2
-烷氧基)-基團中之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及溴原子或選自甲基、三氟甲基及甲氧基之基團,
或與該苯基或吡啶基之相鄰碳原子連接之兩個取代基一起形成選自以下之二價基團:-(CH2
)3
-、-(CH2
)4
-、-(CH2
)2
-O-、-(CH2
)3
-O-、-CH2
-O-CH2
-、-O-CH2
-O-、-O-CH2
-CH2
-O-及-O-CF2
-O-,
或
R1
表示視情況經取代一次或兩次之吡唑基,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、C1
-C2
-烷基及C1
-C2
-烷氧基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R1
表示視情況經取代一次、兩次或三次之苯基或吡啶基,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、硝基、C1
-C4
-烷基、(苯基)-(C1
-C2
-烷基)-、C1
-C4
-鹵烷基、C1
-C4
-烷氧基、(苯基)-(C1
-C2
-烷氧基)-、C1
-C4
-鹵烷氧基、-N(R5
)(R6
),
其中該(苯基)-(C1
-C2
-烷基)-基團及該(苯基)-(C1
-C2
-烷氧基)-基團中之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及溴原子或選自甲基、三氟甲基及甲氧基之基團,
或與該苯基或吡啶基之相鄰碳原子連接之兩個取代基一起形成選自以下之二價基團:-(CH2
)3
-、-(CH2
)4
-、-(CH2
)2
-O-、-(CH2
)3
-O-、-CH2
-O-CH2
-、-O-CH2
-O-、-O-CH2
-CH2
-O-及-O-CF2
-O-,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R1
表示視情況經取代一次、兩次或三次之苯基或吡啶基,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、硝基、(苯基)-(C1
-C2
-烷基)-、C1
-C4
-鹵烷基、C1
-C4
-烷氧基、(苯基)-(C1
-C2
-烷氧基)-、C1
-C4
-鹵烷氧基、-N(R5
)(R6
),
其中該(苯基)-(C1
-C2
-烷基)-基團及該(苯基)-(C1
-C2
-烷氧基)-基團中之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及溴原子或選自甲基、三氟甲基及甲氧基之基團,
或與該苯基或吡啶基之相鄰碳原子連接之兩個取代基一起形成選自以下之二價基團:-(CH2
)3
-、-(CH2
)4
-、-(CH2
)2
-O-、-(CH2
)3
-O-、-CH2
-O-CH2
-、-O-CH2
-O-、-O-CH2
-CH2
-O-及-O-CF2
-O-,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R1
表示視情況經取代一次、兩次或三次之苯基或吡啶基,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:羥基、氰基、C1
-C4
-烷基、C1
-C2
-氟烷基、C1
-C2
-烷氧基、(苯基)-(C1
-C2
-烷氧基)-、C1
-C2
-氟烷氧基及-N(R5
)(R6
),
或與該苯基或吡啶基之相鄰碳原子連接之兩個取代基一起形成選自以下之二價基團:-(CH2
)3
-、-O-CH2
-O-及-O-CF2
-O-,
或
R1
表示視情況經一個甲基取代之吡唑基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R1
表示視情況經取代一次、兩次或三次之苯基或吡啶基,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:羥基、氰基、C1
-C4
-烷基、C1
-C2
-氟烷基、C1
-C2
-烷氧基、(苯基)-(C1
-C2
-烷氧基)-、C1
-C2
-氟烷氧基及-N(R5
)(R6
),
或與該苯基或吡啶基之相鄰碳原子連接之兩個取代基一起形成選自以下之二價基團:-(CH2
)3
-、-O-CH2
-O-及-O-CF2
-O-,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R1
表示視情況經取代一次、兩次或三次之苯基或吡啶基,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:羥基、氰基、C1
-C2
-氟烷基、C1
-C2
-烷氧基、(苯基)-(C1
-C2
-烷氧基)-、C1
-C2
-氟烷氧基及-N(R5
)(R6
),
或與該苯基或吡啶基之相鄰碳原子連接之兩個取代基一起形成選自以下之二價基團:-(CH2
)3
-、-O-CH2
-O-及-O-CF2
-O-,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R1
表示視情況經取代一次、兩次或三次之苯基,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:羥基、氰基、C1
-C4
-烷基、C1
-C2
-氟烷基、C1
-C2
-烷氧基、(苯基)-(C1
-C2
-烷氧基)-、C1
-C2
-氟烷氧基及-N(R5
)(R6
),
或與該苯基之相鄰碳原子連接之兩個取代基一起形成選自以下之二價基團:-(CH2
)3
-、-O-CH2
-O-及-O-CF2
-O-,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R1
表示視情況經取代一次、兩次或三次之苯基,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:羥基、氰基、C1
-C2
-氟烷基、C1
-C2
-烷氧基、(苯基)-(C1
-C2
-烷氧基)-、C1
-C2
-氟烷氧基及-N(R5
)(R6
),
或與該苯基之相鄰碳原子連接之兩個取代基一起形成選自以下之二價基團:-(CH2
)3
-、-O-CH2
-O-及-O-CF2
-O-,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R1
表示視情況經取代一次、兩次或三次之吡啶基,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:羥基、氰基、C1
-C4
-烷基、C1
-C2
-氟烷基、C1
-C2
-烷氧基、(苯基)-(C1
-C2
-烷氧基)-、C1
-C2
-氟烷氧基及-N(R5
)(R6
),
或與該吡啶基之相鄰碳原子連接之兩個取代基一起形成選自以下之二價基團:-(CH2
)3
-、-O-CH2
-O-及-O-CF2
-O-,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R1
表示視情況經取代一次、兩次或三次之苯基或吡啶基,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:氰基、C1
-C4
-烷基、C1
-C2
-氟烷基、C1
-C2
-烷氧基、C1
-C2
-氟烷氧基及-N(R5
)(R6
),
或與該苯基或吡啶基之相鄰碳原子連接之兩個取代基一起形成選自以下之二價基團:-(CH2
)3
-、-O-CH2
-O-及-O-CF2
-O-,
或
R1
表示視情況經一個甲基取代之吡唑基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R1
表示視情況經取代一次、兩次或三次之苯基或吡啶基,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:氰基、C1
-C4
-烷基、C1
-C2
-氟烷基、C1
-C2
-烷氧基、C1
-C2
-氟烷氧基及-N(R5
)(R6
),
或與該苯基或吡啶基之相鄰碳原子連接之兩個取代基一起形成選自以下之二價基團:-(CH2
)3
-、-O-CH2
-O-及-O-CF2
-O-,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R1
表示視情況經取代一次、兩次或三次之苯基或吡啶基,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:氰基、C1
-C2
-氟烷基、C1
-C2
-烷氧基、C1
-C2
-氟烷氧基及-N(R5
)(R6
),
或與該苯基或吡啶基之相鄰碳原子連接之兩個取代基一起形成選自以下之二價基團:-(CH2
)3
-、-O-CH2
-O-及-O-CF2
-O-,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R1
表示視情況經取代一次、兩次或三次之苯基,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:氰基、C1
-C4
-烷基、C1
-C2
-氟烷基、C1
-C2
-烷氧基、C1
-C2
-氟烷氧基、-N(R5
)(R6
),
或與該苯基或吡啶基之相鄰碳原子連接之兩個取代基一起形成選自以下之二價基團:-(CH2
)3
-、-O-CH2
-O-及-O-CF2
-O-,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R1
表示視情況經取代一次、兩次或三次之苯基,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:氰基、C1
-C2
-氟烷基、C1
-C2
-烷氧基、C1
-C2
-氟烷氧基、-N(R5
)(R6
),
或與該苯基之相鄰碳原子連接之兩個取代基一起形成選自以下之二價基團:-(CH2
)3
-、-O-CH2
-O-及-O-CF2
-O-,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R1
表示視情況經取代一次、兩次或三次之吡啶基,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:氰基、C1
-C4
-烷基、C1
-C2
-氟烷基、C1
-C2
-烷氧基、C1
-C2
-氟烷氧基、-N(R5
)(R6
),
或與該苯基或吡啶基之相鄰碳原子連接之兩個取代基一起形成選自以下之二價基團:-(CH2
)3
-、-O-CH2
-O-及-O-CF2
-O-,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R1
表示視情況經取代一次或兩次之苯基或吡啶基,各取代基獨立地選自氟原子及氯原子或選自以下之基團:C1
-C2
-烷基、C1
-C2
-氟烷基、C1
-C2
-烷氧基、C1
-C2
-氟烷氧基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R1
表示視情況經取代一次或兩次之苯基或吡啶基,各取代基獨立地選自氟原子及氯原子或選自以下之基團:C1
-C2
-氟烷基、C1
-C2
-烷氧基、C1
-C2
-氟烷氧基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R1
表示視情況經取代一次或兩次之苯基,各取代基獨立地選自氟原子及氯原子或選自以下之基團:氰基、C1
-C2
-烷基、C1
-C2
-氟烷基、C1
-C2
-烷氧基、C1
-C2
-氟烷氧基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R1
表示視情況經取代一次或兩次之苯基,各取代基獨立地選自氟原子及氯原子或選自以下之基團:C1
-C2
-烷基、C1
-C2
-氟烷基、C1
-C2
-烷氧基、C1
-C2
-氟烷氧基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R1
表示視情況經取代一次或兩次之苯基,各取代基獨立地選自氟原子及氯原子或選自以下之基團:氰基、C1
-C2
-氟烷基、C1
-C2
-烷氧基、C1
-C2
-氟烷氧基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R1
表示視情況經取代一次或兩次之苯基,各取代基獨立地選自氟原子及氯原子或選自以下之基團:C1
-C2
-氟烷基、C1
-C2
-烷氧基、C1
-C2
-氟烷氧基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R1
表示視情況經取代一次或兩次之吡啶基,各取代基獨立地選自氟原子及氯原子或選自以下之基團:C1
-C2
-烷基、C1
-C2
-氟烷基、C1
-C2
-烷氧基、C1
-C2
-氟烷氧基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R1
表示視情況經取代一次或兩次之苯基或吡啶基,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:氰基、甲基、二氟甲基、三氟甲基、甲氧基、苯甲氧基、二氟甲氧基及三氟甲氧基,
或與該苯基或吡啶基之相鄰碳原子連接之兩個取代基一起形成二價基團-O-CF2
-O-,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R1
表示視情況經取代一次或兩次苯基或吡啶基,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:氰基、二氟甲基、三氟甲基、甲氧基、苯甲氧基、二氟甲氧基及三氟甲氧基,
或與該苯基或吡啶基之相鄰碳原子連接之兩個取代基一起形成二價基團-O-CF2
-O-,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R1
表示視情況經取代一次或兩次之苯基,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:氰基、甲基、二氟甲基、三氟甲基、甲氧基、苯甲氧基、二氟甲氧基及三氟甲氧基,
或與該苯基之相鄰碳原子連接之兩個取代基一起形成二價基團-O-CF2
-O-,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R1
表示視情況經取代一次或兩次之苯基,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:氰基、二氟甲基、三氟甲基、甲氧基、苯甲氧基、二氟甲氧基及三氟甲氧基,
或與該苯基之相鄰碳原子連接之兩個取代基一起形成二價基團-O-CF2
-O-,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R1
表示視情況經取代一次或兩次之吡啶基,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:氰基、甲基、二氟甲基、三氟甲基、甲氧基、苯甲氧基、二氟甲氧基及三氟甲氧基,
或與該吡啶基之相鄰碳原子連接之兩個取代基一起形成二價基團-O-CF2
-O-,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R1
表示視情況經取代一次或兩次之苯基或吡啶基,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:甲基、二氟甲基、三氟甲基、甲氧基、苯甲氧基、二氟甲氧基及三氟甲氧基,
或與該苯基或吡啶基之相鄰碳原子連接之兩個取代基一起形成二價基團-O-CF2
-O-,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R1
表示視情況經取代一次或兩次苯基或吡啶基,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:二氟甲基、三氟甲基、甲氧基、苯甲氧基、二氟甲氧基及三氟甲氧基,
或與該苯基或吡啶基之相鄰碳原子連接之兩個取代基一起形成二價基團-O-CF2
-O-,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R1
表示視情況經取代一次或兩次之苯基,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:甲基、二氟甲基、三氟甲基、甲氧基、苯甲氧基、二氟甲氧基及三氟甲氧基,
或與該苯基之相鄰碳原子連接之兩個取代基一起形成二價基團-O-CF2
-O-,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R1
表示視情況經取代一次或兩次之苯基,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:二氟甲基、三氟甲基、甲氧基、苯甲氧基、二氟甲氧基及三氟甲氧基,
或與該苯基之相鄰碳原子連接之兩個取代基一起形成二價基團-O-CF2
-O-,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R1
表示視情況經取代一次或兩次之吡啶基,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:甲基、二氟甲基、三氟甲基、甲氧基、苯甲氧基、二氟甲氧基及三氟甲氧基,
或與該吡啶基之相鄰碳原子連接之兩個取代基一起形成二價基團-O-CF2
-O-,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R1
表示基團
其中「**」指示與連接R1
之氮原子連接之點,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R1
表示基團
其中「**」指示與連接R1
之氮原子連接之點;
Y1
表示-C(H)=、-C(F)=、-C(Cl)=、-C(CN)=或-N=;
R26
表示氟原子、氯原子或溴原子或選自以下之基團:甲基、二氟甲基、三氟甲基、甲氧基、苯甲氧基、二氟甲氧基及三氟甲氧基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R1
表示基團
其中「**」指示與連接R1
之氮原子連接之點;
Y1
表示-C(H)=、-C(F)=、-C(Cl)=、-C(CN)=或-N=;
R26
表示氟原子、氯原子或溴原子或選自以下之基團:二氟甲基、三氟甲基、甲氧基、苯甲氧基、二氟甲氧基及三氟甲氧基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R1
表示基團
其中「**」指示與連接R1
之氮原子連接之點;
Y1
表示-C(H)=、-C(F)=或-N=;
R26
表示氟原子、氯原子或選自以下之基團:C1
-C2
-烷基、C1
-C2
-氟烷基、C1
-C2
-烷氧基及C1
-C2
-氟烷氧基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R1
表示基團
其中「**」指示與連接R1
之氮原子連接之點;
Y1
表示-C(H)=、-C(F)=或-N=;
R26
表示氟原子、氯原子或選自以下之基團:C1
-C2
-氟烷基、C1
-C2
-烷氧基及C1
-C2
-氟烷氧基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R1
表示基團
其中「**」指示與連接R1
之氮原子連接之點;
Y1
表示-C(H)=、-C(F)=、-C(Cl)=或-N=;
R26
表示氟原子、氯原子或溴原子或選自以下之基團:二氟甲基、甲氧基、苯甲氧基、二氟甲氧基及三氟甲氧基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R1
表示基團,
其中「**」指示與連接R1
之氮原子連接之點,
Y1
表示-C(H)=或-C(F)=,及
R26
表示氟原子、氯原子或選自以下之基團:二氟甲基、三氟甲基、甲氧基、二氟甲氧基及三氟甲氧基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R1
表示基團,
其中「**」指示與連接R1
之氮原子連接之點,及
R28
表示選自以下之基團:甲基、二氟甲基、三氟甲基、甲氧基、二氟甲氧基及三氟甲氧基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R1
表示選自以下之基團: ,
其中「**」指示與連接R1
之氮原子連接之點,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R1
表示選自以下之基團:,
其中「**」指示與連接R1
之氮原子連接之點,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R2
表示基團,
其中「*」指示與連接R2
之氮原子連接之點;
R7
表示氫原子或C1
-C2
-烷基;
R8
表示-C(=O)-NH2
基團,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R2
表示基團,
其中「*」指示與連接R2
之氮原子連接之點;
R7
表示C1
-C2
-烷基;
R8
表示-C(=O)-NH2
基團,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R2
表示基團,
其中「*」指示與連接R2
之氮原子連接之點;
R7
表示C1
-C2
-烷基;
R8
表示-C(=O)-NH2
基團,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R2
表示基團,
表示基團其中「*」指示與連接R2
之氮原子連接之點;
R7
表示C1
-C2
-烷基;
R8
表示-C(=O)-NH2
基團,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物之異構混合物,其中:
R2
表示基團,比率為約99:1及更高,有利的為,
其中「*」指示與連接R2
之氮原子連接之點;
R7
表示C1
-C2
-烷基;
R8
表示-C(=O)-NH2
基團,
及其互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物之異構混合物,其中:
R2
表示基團,比率為約98:2及更高,有利的為,
其中「*」指示與連接R2
之氮原子連接之點;
R7
表示C1
-C2
-烷基;
R8
表示-C(=O)-NH2
基團,
及其互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物之異構混合物,其中:
R2
表示基團,比率為約95:5及更高,有利的為,
其中「*」指示與連接R2
之氮原子連接之點;
R7
表示C1
-C2
-烷基;
R8
表示-C(=O)-NH2
基團,
及其互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物之異構混合物,其中:
R2
表示基團,比率為約90:10及更高,有利的為,
其中「*」指示與連接R2
之氮原子連接之點;
R7
表示C1
-C2
-烷基;
R8
表示-C(=O)-NH2
基團,
及其互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物之異構混合物,其中:
R2
表示基團,比率為約80:20及更高,有利的為,
其中「*」指示與連接R2
之氮原子連接之點;
R7
表示C1
-C2
-烷基;
R8
表示-C(=O)-NH2
基團,
及其互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物之異構混合物,其中:
R2
表示基團,比率為約50:50,即,在不具有其他對掌性元素之化合物之情況下,為外消旋混合物,
其中「*」指示與連接R2
之氮原子連接之點;
R7
表示C1
-C2
-烷基;
R8
表示-C(=O)-NH2
基團,
及其互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R2
表示基團,
其中「*」指示與連接R2
之氮原子連接之點;
R7
表示甲基;
R8
表示-C(=O)-NH2
基團,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R2
表示基團,
其中「*」指示與連接R2
之氮原子連接之點;
R7
表示甲基;
R8
表示-C(=O)-NH2
基團,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R2
表示基團,
其中「*」指示與連接R2
之氮原子連接之點;
R7
表示甲基;
R8
表示-C(=O)-NH2
基團,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物之異構混合物,其中:
R2
表示基團,比率為約99:1及更高,有利的為,
其中「*」指示與連接R2
之氮原子連接之點;
R7
表示甲基;
R8
表示-C(=O)-NH2
基團,
及其互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物之異構混合物,其中:
R2
表示基團,比率為約98:2及更高,有利的為,
其中「*」指示與連接R2
之氮原子連接之點;
R7
表示甲基;
R8
表示-C(=O)-NH2
基團,
及其互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物之異構混合物,其中:
R2
表示基團,比率為約95:5及更高,有利的為,
其中「*」指示與連接R2
之氮原子連接之點;
R7
表示甲基;
R8
表示-C(=O)-NH2
基團,
及其互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物之異構混合物,其中:
R2
表示基團,比率為約90:10及更高,有利的為,
其中「*」指示與連接R2
之氮原子連接之點;
R7
表示甲基;
R8
表示-C(=O)-NH2
基團,
及其互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物之異構混合物,其中:
R2
表示基團,比率為約80:20及更高,有利的為,
其中「*」指示與連接R2
之氮原子連接之點;
R7
表示甲基;
R8
表示-C(=O)-NH2
基團,
及其互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物之異構混合物,其中:
R2
表示基團,比率為約50:50,即,在不具有其他對掌性元素之化合物之情況下,為外消旋混合物,
其中「*」指示與連接R2
之氮原子連接之點;
R7
表示甲基;
R8
表示-C(=O)-NH2
基團,
及其互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R3
表示選自甲基及-NH2
之基團,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R3
表示-NH2
基團,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R3
表示甲基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R4
表示視情況經取代一次、兩次或三次之苯基或吡啶基,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、硝基、C1
-C4
-烷基、(苯基)-(C1
-C2
-烷基)-、(5員雜芳基)-(C1
-C2
-烷基)-、(C3
-C7
-環烷基)-(C1
-C2
-烷基)-、((R9
)O)-(C1
-C4
-烷基)-、C1
-C4
-鹵烷基、C3
-C7
-環烷基、-OR9
、-N(R10
)(R11
)、((R10
)(R11
)N)-(C1
-C3
-烷基)-、-C(=O)-N(R12
)(R13
)、S(=O)n
-R14
、-C(=O)R14
、-C(=O)-OR17
及自身視情況經一或兩個甲基取代5員雜芳基,
或與該苯基或吡啶基之相鄰碳原子連接之兩個取代基一起形成選自以下之二價基團:-(CH2
)3
-、-(CH2
)4
-、-(CH2
)2
-O-、-(CH2
)3
-O-、-CH2
-O-CH2
-、-O-CH2
-O-、-O-CH2
-CH2
-O-及-O-CF2
-O-,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R4
表示視情況經取代一次、兩次或三次之苯基或吡啶基,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、硝基、C1
-C4
-烷基、(苯基)-(C1
-C2
-烷基)-、(5員雜芳基)-(C1
-C2
-烷基)-、C1
-C4
-羥烷基、C1
-C4
-鹵烷基、-OR9
、-N(R10
)(R11
)、-C(=O)-N(R12
)(R13
)、S(=O)n
-R14
及自身視情況經一個或兩個甲基取代之5員雜芳基,
或與該苯基或吡啶基之相鄰碳原子連接之兩個取代基一起形成選自以下之二價基團:-(CH2
)3
-、-(CH2
)4
-、-(CH2
)2
-O-、-(CH2
)3
-O-、-CH2
-O-CH2
-、-O-CH2
-O-、-O-CH2
-CH2
-O-及-O-CF2
-O-,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R4
表示視情況經取代一次、兩次或三次之苯基或吡啶基,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、C1
-C3
-烷基、((R9
)O)-(C1
-C3
-烷基)-、C1
-C3
-氟烷基、-OR9
、-N(R10
)(R11
)、-C(=O)-N(R12
)(R13
)、S(=O)n
-R14
及-C(=O)-OR17
,
或與該苯基或吡啶基之相鄰碳原子連接之兩個取代基一起形成選自以下之二價基團:-(CH2
)3
-、-O-CH2
-O-及-O-CF2
-O-,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R4
表示視情況經取代一次、兩次或三次之苯基,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、C1
-C3
-烷基、((R9
)O)-(C1
-C3
-烷基)-、C1
-C3
-氟烷基、-OR9
、-N(R10
)(R11
)、-C(=O)-N(R12
)(R13
)、S(=O)n
-R14
及-C(=O)-OR17
,
或與該苯基或吡啶基之相鄰碳原子連接之兩個取代基一起形成選自以下之二價基團:-(CH2
)3
-、-O-CH2
-O-及-O-CF2
-O-,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R4
表示視情況經取代一次、兩次或三次之吡啶基,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、C1
-C3
-烷基、((R9
)O)-(C1
-C3
-烷基)-、C1
-C3
-氟烷基、-OR9
、-N(R10
)(R11
)、-C(=O)-N(R12
)(R13
)、S(=O)n
-R14
及-C(=O)-OR17
,
或與該苯基或吡啶基之相鄰碳原子連接之兩個取代基一起形成選自以下之二價基團:-(CH2
)3
-、-O-CH2
-O-及-O-CF2
-O-,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R4
表示視情況經取代一次、兩次或三次之苯基,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:氰基、C1
-C3
-烷基、C1
-C3
-羥烷基、C1
-C3
-氟烷基、-OR9
、-N(R10
)(R11
)、-C(=O)-N(R12
)(R13
)及S(=O)n
-R14
,
或與該苯基之相鄰碳原子連接之兩個取代基一起形成選自以下之二價基團:-(CH2
)3
-、-O-CH2
-O-及-O-CF2
-O-,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R4
表示視情況經取代一次、兩次或三次之吡啶基,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:氰基、C1
-C3
-烷基、C1
-C3
-羥烷基、C1
-C3
-氟烷基、-OR9
、-N(R10
)(R11
)、-C(=O)-N(R12
)(R13
)及S(=O)n
-R14
,
或與該吡啶基之相鄰碳原子連接之兩個取代基一起形成選自以下之二價基團:-(CH2
)3
-、-O-CH2
-O-及-O-CF2
-O-,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R4
表示視情況經取代一次或兩次之苯基或吡啶基,各取代基獨立地選自氟原子及氯原子或選自以下之基團:C1
-C2
-烷基、C1
-C2
-氟烷基、-OR9
;
R9
表示選自以下之基團:C1
-C2
-烷基、苯甲基、C1
-C2
-氟烷基、(C1
-C2
-烷氧基)-C2
-烷基-及苯基,
其中該苯甲基內之苯基及該苯基自身視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及甲基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R4
表示視情況經取代一次或兩次之苯基或吡啶基,各取代基獨立地選自鹵素原子或選自以下之基團:C1
-C2
-烷基、C1
-C2
-氟烷基、-OR9
, -N(R10
)(R11
)、-C(=O)-N(R12
)(R13
)及-C(=O)-OR17
;
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R4
表示視情況經取代一次或兩次之苯基,各取代基獨立地選自鹵素原子或選自以下之基團:C1
-C2
-烷基、C1
-C2
-氟烷基、-OR9
、-N(R10
)(R11
)、-C(=O)-N(R12
)(R13
)及-C(=O)-OR17
;
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R4
表示視情況經取代一次或兩次之吡啶基,各取代基獨立地選自鹵素原子或選自以下之基團:C1
-C2
-烷基、C1
-C2
-氟烷基、-OR9
、-N(R10
)(R11
)、-C(=O)-N(R12
)(R13
)及-C(=O)-OR17
;
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R4
表示視情況經取代一次或兩次之苯基或吡啶基,各取代基獨立地選自氟原子及氯原子或選自以下之基團:C1
-C2
-烷基、C1
-C2
-氟烷基、-OR9
,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R4
表示視情況經取代一次或兩次之苯基,各取代基獨立地選自氟原子及氯原子或選自以下之基團:C1
-C2
-烷基、C1
-C2
-氟烷基、-OR9
;
R9
表示選自以下之基團:C1
-C2
-烷基、苯甲基、C1
-C2
-氟烷基、(C1
-C2
-烷氧基)-C2
-烷基-及苯基,
其中該苯甲基內之苯基及該苯基自身視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及甲基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R4
表示視情況經取代一次或兩次之苯基,各取代基獨立地選自氟原子及氯原子或選自以下之基團:C1
-C2
-烷基、C1
-C2
-氟烷基、-OR9
,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R4
表示視情況經取代一次或兩次之吡啶基,各取代基獨立地選自氟原子及氯原子或選自以下之基團:C1
-C2
-烷基、C1
-C2
-氟烷基、-OR9
;
R9
表示選自以下之基團:C1
-C2
-烷基、苯甲基、C1
-C2
-氟烷基、(C1
-C2
-烷氧基)-C2
-烷基-及苯基,
其中該苯甲基內之苯基及該苯基自身視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及甲基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R4
表示視情況經取代一次或兩次之吡啶基,各取代基獨立地選自氟原子及氯原子或選自以下之基團:C1
-C2
-烷基、C1
-C2
-氟烷基、-OR9
,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R4
表示基團
其中「#」指示與連接R4
之羰基連接之點;
Y2
表示-C(H)=或-N=;
Y3
表示-C(R27
)=或-N=,
其限制條件為,若Y2
表示-N=,則Y3
表示-C(R27
)=;且若Y3
表示-N=,則Y2
表示-C(H)=;
R27
表示鹵素原子或選自以下之基團:C1
-C2
-烷基、C1
-C2
-氟烷基、-OR9
、-N(R10
)(R11
)、-C(=O)-N(R12
)(R13
)及-C(=O)-OR17
,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R4
表示基團
其中「#」指示與連接R4
之羰基連接之點;
Y2
表示-C(H)=或-N=;
Y3
表示-C(R27
)=或-N=,
其限制條件為,若Y2
表示-N=,則Y3
表示-C(R27
)=;且若Y3
表示-N=,則Y2
表示-C(H)=;
R27
表示氟原子、氯原子或選自以下之基團:C1
-C2
-烷氧基、苯甲氧基及C1
-C2
-氟烷氧基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R4
表示基團
其中「#」指示與連接R4
之羰基連接之點;
Y2
表示-C(H)=及-N=;
Y3
表示-C(R27
)=及-N=,
其限制條件為,若Y2
表示-N=,則Y3
表示-C(R27
)=;且若Y3
表示-N=,則Y2
表示-C(H)=;
R27
表示氟原子、氯原子或選自以下之基團:C1
-C2
-烷氧基、苯甲氧基及C1
-C2
-氟烷氧基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R4
表示基團
其中「#」指示與連接R4
之羰基連接之點;
R27
表示氟原子、氯原子或選自以下之基團:C1
-C2
-烷氧基、苯甲氧基及C1
-C2
-氟烷氧基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R4
表示基團
其中「#」指示與連接R4
之羰基連接之點;
R27
表示氟原子、氯原子或選自以下之基團:C1
-C2
-烷氧基、苯甲氧基及C1
-C2
-氟烷氧基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R4
表示選自以下之基團: ,
其中「#」指示與連接R4
之羰基連接之點,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R4
表示選自以下之基團:,
其中「#」指示與連接R4
之羰基連接之點,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R5
及R6
在每次出現時獨立地表示氫原子或選自C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-之基團,
或
R5
及R6
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:側氧基、羥基、C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R5
及R6
在每次出現時獨立地表示氫原子或選自C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-之基團,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R5
及R6
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:側氧基、羥基、C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R5
及R6
在每次出現時獨立地表示氫原子或C1
-C2
-烷基,
或
R5
及R6
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自以下之基團:羥基及C1
-C2
-烷基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R5
及R6
在每次出現時獨立地表示氫原子或C1
-C2
-烷基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R5
及R6
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自以下之基團:羥基及C1
-C2
-烷基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R7
表示氫原子,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R7
表示甲基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R7
表示乙基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R7
表示氫原子或C1
-C2
-烷基;
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R9
表示氫原子或選自以下之基團:C1
-C4
-烷基、(苯基)-(C1
-C2
-烷基)-、C1
-C4
-鹵烷基、C2
-C3
-羥烷基、(C1
-C2
-烷氧基)-C2
-烷基-、((C1
-C2
-烷基)-C(=O)-O)-C2
-烷基-、-C(R18
)(R19
)-C(=O)-OR17
、-C(R18
)(R19
)-C(=O)-N(R20
)(R21
)、-C(=O)-N(R20
)(R21
)及苯基,
其中該(苯基)-(C1
-C2
-烷基)-基團內之苯基及該苯基自身視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:氰基、甲基、三氟甲基及甲氧基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R9
表示氫原子或選自以下之基團:C1
-C4
-烷基、(苯基)-(C1
-C2
-烷基)-、C1
-C4
-鹵烷基、C2
-C3
-羥烷基、(C1
-C2
-烷氧基)-C2
-烷基-、((C1
-C2
-烷基)-C(=O)-O)-C2
-烷基-、-C(R18
)(R19
)-C(=O)-OR17
、-C(R18
)(R19
)-C(=O)-N(R20
)(R21
)及苯基,
其中該(苯基)-(C1
-C2
-烷基)-基團內之苯基及該苯基自身視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:甲基、三氟甲基及甲氧基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R9
表示氫原子或選自以下之基團:C1
-C2
-烷基、苯甲基、C1
-C2
-氟烷基、C2
-羥烷基、(C1
-C2
-烷氧基)-C2
-烷基-、((C1
-C2
-烷基)-C(=O)-O)-C2
-烷基-、-C(R18
)(R19
)-C(=O)-OR17
、-C(R18
)(R19
)-C(=O)-N(R20
)(R21
)、-C(=O)-N(R20
)(R21
)及苯基,
其中該苯甲基內之苯基及該苯基自身視情況經取代一次或兩次,各取代基獨立地選自氟原子及氯原子或選自以下之基團:氰基及甲基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R9
表示氫原子或選自以下之基團:C1
-C2
-烷基、苯甲基、C1
-C2
-氟烷基、(C1
-C2
-烷氧基)-C2
-烷基-、((C1
-C2
-烷基)-C(=O)-O)-C2
-烷基-、-C(R18
)(R19
)-C(=O)-OR17
、-C(R18
)(R19
)-C(=O)-N(R20
)(R21
)及苯基,
其中該苯甲基內之苯基及該苯基自身視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及甲基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R9
表示選自以下之基團:C1
-C2
-烷基、苯甲基、C1
-C2
-氟烷基、(C1
-C2
-烷氧基)-C2
-烷基-及苯基,
其中該苯甲基內之苯基及該苯基自身視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及甲基;
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R9
表示氫原子或選自以下之基團:C1
-C2
-烷基、苯甲基、C1
-C2
-氟烷基、(C1
-C2
-烷氧基)-C2
-烷基-、((C1
-C2
-烷基)-C(=O)-O)-C2
-烷基-、-C(R18
)(R19
)-C(=O)-N(R20
)(R21
)、-C(=O)-N(R20
)(R21
)及苯基,
其中該苯甲基內之苯基及該苯基自身視情況經取代一次或兩次,各取代基獨立地選自氟原子及氯原子或選自以下之基團:氰基及甲基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R9
表示氫原子或選自以下之基團:C1
-C2
-烷基、苯甲基、C1
-C2
-氟烷基及苯基,
其中該苯甲基內之苯基及該苯基自身視情況經取代一次或兩次,各取代基獨立地選自氟原子及氯原子或選自以下之基團:氰基及甲基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R10
及R11
在每次出現時獨立地表示氫原子或選自以下之基團:C1
-C2
-烷基、C1
-C2
-鹵烷基、C2
-C3
-羥烷基、(C1
-C2
-烷氧基)-C2
-烷基-、((R22
)(R23
)N)-C2
-烷基、(C3
-C7
-環烷基)-(C1
-C2
-烷基)-、(C1
-C2
-烷基)-C(=O)-、C3
-C7
-環烷基、(C3
-C7
-環烷基)-C(=O)-、(苯基)-(C1
-C2
-烷基)-、(苯基)-(C1
-C2
-烷基)-C(=O)-及(苯基)-(C1
-C2
-烷基)-O-C(=O)-,
其中C3
-C7
-環烷基以及該(C3
-C7
-環烷基)-(C1
-C2
-烷基)-基團及該(C3
-C7
-環烷基)-C(=O)-基團內之C3
-C7
-環烷基視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自以下之基團:氰基、C1
-C2
-烷基及C1
-C2
-鹵烷基,
且其中該(苯基)-(C1
-C2
-烷基)-基團、該(苯基)-(C1
-C2
-烷基)-C(=O)-基團及該(苯基)-(C1
-C2
-烷基)-C(=O)-基團內之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:甲基、三氟甲基及甲氧基,
或
R10
及R11
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基或雙環含氮5至10員雜環烷基,其視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、側氧基、羥基、C1
-C2
-烷基、C1
-C2
-鹵烷基、(C1
-C2
-烷基)-C(=O)-、C1
-C2
-烷氧基、-N(R22
)(R23
)及單環4至7員雜環烷基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R10
及R11
在每次出現時獨立地表示氫原子或選自以下之基團:C1
-C2
-烷基、C1
-C2
-鹵烷基、C2
-C3
-羥烷基、(C1
-C2
-烷氧基)-C2
-烷基-、((R22
)(R23
)N)-C2
-烷基、(C3
-C7
-環烷基)-(C1
-C2
-烷基)-、(C1
-C2
-烷基)-C(=O)-、C3
-C7
-環烷基、(C3
-C7
-環烷基)-C(=O)-、(苯基)-(C1
-C2
-烷基)-、(苯基)-(C1
-C2
-烷基)-C(=O)-及(苯基)-(C1
-C2
-烷基)-O-C(=O)-,
其中C3
-C7
-環烷基以及該(C3
-C7
-環烷基)-(C1
-C2
-烷基)-基團及該(C3
-C7
-環烷基)-C(=O)-基團內之C3
-C7
-環烷基視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自以下之基團:氰基、C1
-C2
-烷基及C1
-C2
-鹵烷基,
且其中該(苯基)-(C1
-C2
-烷基)-基團、該(苯基)-(C1
-C2
-烷基)-C(=O)-基團及該(苯基)-(C1
-C2
-烷基)-C(=O)-基團內之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:甲基、三氟甲基及甲氧基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R10
及R11
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基或雙環含氮5至10員雜環烷基,其視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、側氧基、羥基、C1
-C2
-烷基、C1
-C2
-鹵烷基、(C1
-C2
-烷基)-C(=O)-、C1
-C2
-烷氧基、-N(R22
)(R23
)及單環4至7員雜環烷基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R10
及R11
在每次出現時獨立地表示氫原子或選自以下之基團:C1
-C2
-烷基、C1
-C2
-鹵烷基、C2
-C3
-羥烷基、(C1
-C2
-烷氧基)-C2
-烷基-、((R22
)(R23
)N)-C2
-烷基、(C1
-C2
-烷基)-C(=O)-、C3
-C5
-環烷基、(C3
-C5
-環烷基)-C(=O)-、(苯基)-(C1
-C2
-烷基)-、(苯基)-(C1
-C2
-烷基)-C(=O)-及(苯基)-(C1
-C2
-烷基)-O-C(=O)-,
其中該(苯基)-(C1
-C2
-烷基)-基團、該(苯基)-(C1
-C2
-烷基)-C(=O)-基團及該(苯基)-(C1
-C2
-烷基)-O-C(=O)-基團內之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:甲基、三氟甲基及甲氧基,
或
R10
及R11
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基或雙環含氮6至10員雜環烷基,其視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、側氧基、羥基、C1
-C2
-烷基、C1
-C2
-鹵烷基、(C1
-C2
-烷基)-C(=O)-、C1
-C2
-烷氧基、-N(R22
)(R23
)及單環4至7員雜環烷基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R10
及R11
在每次出現時獨立地表示氫原子或選自以下之基團:C1
-C2
-烷基、C1
-C2
-鹵烷基、C2
-C3
-羥烷基、(C1
-C2
-烷氧基)-C2
-烷基-、((R22
)(R23
)N)-C2
-烷基、(C1
-C2
-烷基)-C(=O)-、C3
-C5
-環烷基、(C3
-C5
-環烷基)-C(=O)-、(苯基)-(C1
-C2
-烷基)-、(苯基)-(C1
-C2
-烷基)-C(=O)-及(苯基)-(C1
-C2
-烷基)-O-C(=O)-,
其中該(苯基)-(C1
-C2
-烷基)-基團、該(苯基)-(C1
-C2
-烷基)-C(=O)-基團及該(苯基)-(C1
-C2
-烷基)-O-C(=O)-基團內之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:甲基、三氟甲基及甲氧基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R10
及R11
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基或雙環含氮6至10員雜環烷基,其視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、側氧基、羥基、C1
-C2
-烷基、C1
-C2
-鹵烷基、(C1
-C2
-烷基)-C(=O)-、C1
-C2
-烷氧基、-N(R22
)(R23
)及單環4至7員雜環烷基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R10
及R11
在每次出現時獨立地表示氫原子或選自以下之基團:C1
-C2
-烷基、C1
-C2
-氟烷基、(C3
-C5
-環烷基)-(C1
-C2
-烷基)- (C1
-C2
-烷基)-C(=O)-、C3
-C7
-環烷基、C3
-C7
-環烷基-(C=O)-、(苯基)-(C1
-C2
-烷基)-、(苯基)-(C1
-C2
-烷基)-C(=O)-及(苯基)-(C1
-C2
-烷基)-O-C(=O)-,
其中C3
-C7
-環烷基、及該(C3
-C5
-環烷基)-(C1
-C2
-烷基)-內之C3
-C5
-環烷基以及C3
-C7
-環烷基-(C=O)-基團內之C3
-C7
-環烷基視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自以下之基團:氰基、C1
-C2
-烷基及C1
-C2
-氟烷基,
且其中該(苯基)-(C1
-C2
-烷基)-基團、該(苯基)-(C1
-C2
-烷基)-C(=O)-基團及該(苯基)-(C1
-C2
-烷基)-O-C(=O)-基團內之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及甲基,
或
R10
及R11
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自以下之基團:氰基、側氧基、C1
-C2
-烷基、C1
-C2
-f氟烷基及(C1
-C2
-烷基)-C(=O)-,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R10
及R11
在每次出現時獨立地表示氫原子或選自以下之基團:C1
-C2
-烷基、C1
-C2
-氟烷基、(C3
-C5
-環烷基)-(C1
-C2
-烷基)- (C1
-C2
-烷基)-C(=O)-、C3
-C7
-環烷基、C3
-C7
-環烷基-(C=O)-、(苯基)-(C1
-C2
-烷基)-、(苯基)-(C1
-C2
-烷基)-C(=O)-及(苯基)-(C1
-C2
-烷基)-O-C(=O)-,
其中C3
-C7
-環烷基、及該(C3
-C5
-環烷基)-(C1
-C2
-烷基)-內之C3
-C5
-環烷基以及C3
-C7
-環烷基-(C=O)-基團內之C3
-C7
-環烷基視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自以下之基團:氰基、C1
-C2
-烷基及C1
-C2
-氟烷基,
且其中該(苯基)-(C1
-C2
-烷基)-基團、該(苯基)-(C1
-C2
-烷基)-C(=O)-基團及該(苯基)-(C1
-C2
-烷基)-O-C(=O)-基團內之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及甲基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R10
及R11
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自以下之基團:氰基、側氧基、C1
-C2
-烷基、C1
-C2
-f氟烷基及(C1
-C2
-烷基)-C(=O)-,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R10
及R11
在每次出現時獨立地表示氫原子或選自以下之基團:C1
-C2
-烷基、C1
-C2
-氟烷基、(C1
-C2
-烷基)-C(=O)-、(苯基)-(C1
-C2
-烷基)-、(苯基)-(C1
-C2
-烷基)-C(=O)-及(苯基)-(C1
-C2
-烷基)-O-C(=O)-,
其中該(苯基)-(C1
-C2
-烷基)-基團、該(苯基)-(C1
-C2
-烷基)-C(=O)-基團及該(苯基)-(C1
-C2
-烷基)-O-C(=O)-基團內之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及甲基,
或
R10
及R11
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自以下之基團:側氧基、C1
-C2
-烷基、C1
-C2
-氟烷基及(C1
-C2
-烷基)-C(=O)-,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R10
及R11
在每次出現時獨立地表示氫原子或選自以下之基團:C1
-C2
-烷基、C1
-C2
-氟烷基、(C1
-C2
-烷基)-C(=O)-、(苯基)-(C1
-C2
-烷基)-、(苯基)-(C1
-C2
-烷基)-C(=O)-及(苯基)-(C1
-C2
-烷基)-O-C(=O)-,
其中該(苯基)-(C1
-C2
-烷基)-基團、該(苯基)-(C1
-C2
-烷基)-C(=O)-基團及該(苯基)-(C1
-C2
-烷基)-O-C(=O)-基團內之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及甲基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R10
及R11
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自以下之基團:側氧基、C1
-C2
-烷基、C1
-C2
-氟烷基及(C1
-C2
-烷基)-C(=O)-,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R10
及R11
在每次出現時獨立地表示氫原子或選自以下之基團:C1
-C2
-烷基、(C3
-C5
-環烷基)-(C1
-C2
-烷基)-、C3
-C7
-環烷基及(苯基)-(C1
-C2
-烷基)-O-C(=O)-,
其中C3
-C7
-環烷基及該(C3
-C5
-環烷基)-(C1
-C2
-烷基)-基團內之C3
-C5
-環烷基視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自以下之基團:氰基、甲基及C1
-氟烷基,
且其中該(苯基)-(C1
-C2
-烷基)-O-C(=O)-基團內之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及甲基,
或
R10
及R11
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自以下之基團:氰基、甲基及C1
-氟烷基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R10
及R11
在每次出現時獨立地表示氫原子或選自以下之基團:C1
-C2
-烷基、(C3
-C5
-環烷基)-(C1
-C2
-烷基)-、C3
-C7
-環烷基及(苯基)-(C1
-C2
-烷基)-O-C(=O)-,
其中C3
-C7
-環烷基及該(C3
-C5
-環烷基)-(C1
-C2
-烷基)-基團內之C3
-C5
-環烷基視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自以下之基團:氰基、甲基及C1
-氟烷基,
且其中該(苯基)-(C1
-C2
-烷基)-O-C(=O)-基團內之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及甲基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R10
及R11
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自以下之基團:氰基、甲基及C1
-氟烷基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R10
及R11
在每次出現時獨立地表示氫原子或選自以下之基團:C1
-C2
-烷基、C3
-C7
-環烷基及(苯甲基)-O-C(=O)-,
其中C3
-C7
-環烷基視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自以下之基團:甲基及三氟甲基,
且其中該(苯甲基)-O-C(=O)-基團內之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及甲基,
或
R10
及R11
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自以下之基團:氰基、甲基及三氟甲基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R10
及R11
在每次出現時獨立地表示氫原子或選自以下之基團:C1
-C2
-烷基、C3
-C7
-環烷基及(苯甲基)-O-C(=O)-,
其中C3
-C7
-環烷基視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自以下之基團:甲基及三氟甲基,
且其中該(苯甲基)-O-C(=O)-基團內之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及甲基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R10
及R11
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自以下之基團:氰基、甲基及三氟甲基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R10
及R11
在每次出現時獨立地表示氫原子或選自以下之基團:C1
-C2
-烷基及(苯甲基)-O-C(=O)-,
且其中該(苯甲基)-O-C(=O)-基團內之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及甲基,
或
R10
及R11
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自以下之基團:氰基、甲基及三氟甲基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R10
及R11
在每次出現時獨立地表示氫原子或選自以下之基團:C1
-C2
-烷基及(苯甲基)-O-C(=O)-,
且其中該(苯甲基)-O-C(=O)-基團內之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及甲基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R12
及R13
在每次出現時獨立地表示氫原子或選自以下之基團:C1
-C4
-烷基、C1
-C4
-鹵烷基、C1
-C4
-羥烷基、(C1
-C4
-烷氧基)-C2
-C3
-烷基-、(C1
-C4
-鹵烷氧基)-C2
-C3
-烷基-、(苯氧基)-C2
-C3
-烷基-、C3
-C7
-環烷基、單環4至7員雜環烷基及(苯基)-(C1
-C3
-烷基)-,
其中C3
-C7
-環烷基及單環4至7員雜環烷基視情況經取代一次或兩次,各取代基獨立地選自鹵素原子或選自以下之基團:側氧基、C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-,
且其中該(苯氧基)-C2
-C3
-烷基-基團及該(苯基)-(C1
-C3
-烷基)-基團內之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:氰基、甲基、三氟甲基及甲氧基,
或
R12
及R13
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況經取代一次或兩次,各取代基獨立地選自鹵素原子或選自以下之基團:側氧基、C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R12
及R13
在每次出現時獨立地表示氫原子或選自以下之基團:C1
-C4
-烷基、C1
-C4
-鹵烷基、C1
-C4
-羥烷基、(C1
-C4
-烷氧基)-C2
-C3
-烷基-、(C1
-C4
-鹵烷氧基)-C2
-C3
-烷基-、(苯氧基)-C2
-C3
-烷基-、C3
-C7
-環烷基、單環4至7員雜環烷基及(苯基)-(C1
-C3
-烷基)-,
其中C3
-C7
-環烷基及單環4至7員雜環烷基視情況經取代一次或兩次,各取代基獨立地選自鹵素原子或選自以下之基團:側氧基、C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-,
且其中該(苯氧基)-C2
-C3
-烷基-基團及該(苯基)-(C1
-C3
-烷基)-基團內之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:氰基、甲基、三氟甲基及甲氧基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R12
及R13
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況經取代一次或兩次,各取代基獨立地選自鹵素原子或選自以下之基團:側氧基、C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R12
及R13
在每次出現時獨立地表示氫原子或選自以下之基團:C1
-C4
-烷基、C1
-C4
-鹵烷基、C1
-C4
-羥烷基、(C1
-C2
-烷氧基)-C2
-C3
-烷基-、C3
-C7
-環烷基、單環4至7員雜環烷基及(苯基)-(C1
-C3
-烷基)-,
其中C3
-C7
-環烷基及單環4至7員雜環烷基視情況經取代一次或兩次,各取代基獨立地選自鹵素原子或選自以下之基團:側氧基、C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-,
或
R12
及R13
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況經取代一次或兩次,各取代基獨立地選自鹵素原子或選自以下之基團:側氧基、C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R12
及R13
在每次出現時獨立地表示氫原子或選自以下之基團:C1
-C4
-烷基、C1
-C4
-鹵烷基、C1
-C4
-羥烷基、(C1
-C2
-烷氧基)-C2
-C3
-烷基-、C3
-C7
-環烷基、單環4至7員雜環烷基及(苯基)-(C1
-C3
-烷基)-,
其中C3
-C7
-環烷基及單環4至7員雜環烷基視情況經取代一次或兩次,各取代基獨立地選自鹵素原子或選自以下之基團:側氧基、C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R12
及R13
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況經取代一次或兩次,各取代基獨立地選自鹵素原子或選自以下之基團:側氧基、C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R12
及R13
在每次出現時獨立地表示氫原子或選自以下之基團:C1
-C4
-烷基、C1
-C4
-氟烷基、C1
-C4
-羥烷基、(C1
-C4
-烷氧基)-C2
-C3
-烷基-、(C1
-C2
-氟烷氧基)-C2
-C3
-烷基-、(苯氧基)-C2
-C3
-烷基-、C3
-C7
-環烷基、單環4至7員雜環烷基及(苯基)-(C1
-C2
-烷基)-,
其中C3
-C7
-環烷基及單環4至7員雜環烷基視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自以下之基團:側氧基、C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-,
且其中該(苯氧基)-C2
-C3
-烷基-基團及該(苯基)-(C1
-C2
-烷基)-基團內之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子及氯原子或選自以下之基團:甲基、三氟甲基及甲氧基,
或
R12
及R13
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況經取代一次或兩次,各取代基獨立地選自鹵素原子或選自以下之基團:側氧基、C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R12
及R13
在每次出現時獨立地表示氫原子或選自以下之基團:C1
-C4
-烷基、C1
-C4
-氟烷基、C1
-C4
-羥烷基、(C1
-C4
-烷氧基)-C2
-C3
-烷基-、(C1
-C2
-氟烷氧基)-C2
-C3
-烷基-、(苯氧基)-C2
-C3
-烷基-、C3
-C7
-環烷基、單環4至7員雜環烷基及(苯基)-(C1
-C2
-烷基)-,
其中C3
-C7
-環烷基及單環4至7員雜環烷基視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自以下之基團:側氧基、C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-,
且其中該(苯氧基)-C2
-C3
-烷基-基團及該(苯基)-(C1
-C2
-烷基)-基團內之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子及氯原子或選自以下之基團:甲基、三氟甲基及甲氧基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R12
及R13
在每次出現時獨立地表示氫原子或選自以下之基團:C1
-C4
-烷基、C1
-C4
-氟烷基、C3
-C7
-環烷基、單環4至7員雜環烷基及(苯基)-(C1
-C2
-烷基)-,
其中C3
-C7
-環烷基及單環4至7員雜環烷基視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自以下之基團:側氧基、C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-,
或
R12
及R13
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況經取代一次或兩次,各取代基獨立地選自鹵素原子或選自以下之基團:側氧基、C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R12
及R13
在每次出現時獨立地表示氫原子或選自以下之基團:C1
-C4
-烷基、C1
-C4
-氟烷基、C3
-C7
-環烷基、單環4至7員雜環烷基及(苯基)-(C1
-C2
-烷基)-,
其中C3
-C7
-環烷基及單環4至7員雜環烷基視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自以下之基團:側氧基、C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R12
及R13
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況經取代一次或兩次,各取代基獨立地選自鹵素原子或選自以下之基團:側氧基、C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R12
及R13
在每次出現時獨立地表示氫原子或選自以下之基團:C1
-C4
-烷基、C1
-C2
-氟烷基、C1
-C2
-羥烷基、(C1
-C4
-烷氧基)-C2
-C3
-烷基-、(C1
-C2
-氟烷氧基)-C2
-C3
-烷基-、(苯氧基)-C2
-C3
-烷基-、C3
-C7
-環烷基及(苯基)-(C1
-C2
-烷基)-,
其中C3
-C7
-環烷基視情況經取代一次或兩次,各取代基獨立地選自氟原子或甲基,
且其中該(苯氧基)-C2
-C3
-烷基-基團及該(苯基)-(C1
-C2
-烷基)-基團內之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子及氯原子或選自以下之基團:甲基、三氟甲基及甲氧基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R12
及R13
在每次出現時獨立地表示氫原子或選自以下之基團:C1
-C4
-烷基、C1
-C2
-氟烷基、C1
-C2
-羥烷基、(C1
-C4
-烷氧基)-C2
-烷基-、(C1
-C2
-氟烷氧基)-C2
-烷基-、(苯氧基)-C2
-烷基-、C3
-C7
-環烷基及(苯基)-(C1
-C2
-烷基)-,
其中該(苯氧基)-C2
-烷基-基團及該(苯基)-(C1
-C2
-烷基)-基團內之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子及氯原子或選自以下之基團:甲基、三氟甲基及甲氧基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R12
及R13
在每次出現時獨立地表示氫原子或選自以下之基團:C1
-C2
-烷基、(C1
-C4
-烷氧基)-C2
-烷基-、(C1
-C2
-氟烷氧基)-C2
-烷基-、(苯氧基)-C2
-烷基-、C3
-C7
-環烷基及(苯基)-(C1
-C2
-烷基)-,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R14
表示選自以下之基團:C1
-C2
-烷基、C1
-C2
-鹵烷基及苯基,
其中苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:甲基、三氟甲基及甲氧基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R14
表示選自以下之基團:C1
-C2
-烷基、C1
-C2
-鹵烷基及苯基,
其中苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:甲基、三氟甲基及甲氧基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R14
表示選自C1
-C2
-烷基及C1
-C2
-鹵烷基之基團,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R14
表示選自甲基及三氟甲基之基團,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R14
表示甲基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R17
表示C1
-C4
-烷基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R17
表示C1
-C3
-烷基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R17
表示C1
-C2
-烷基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R17
表示甲基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R17
表示乙基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R18
及R19
在每次出現時獨立地表示氫原子或C1
-C2
-烷基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R18
及R19
在每次出現時獨立地表示氫原子或甲基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R18
及R19
均表示甲基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R18
及R19
均表示氫原子,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R18
表示氫原子且R19
表示甲基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R20
表示氫原子或選自以下之基團:C1
-C6
-烷基、C3
-C4
-烯基、C3
-C4
-炔基、C1
-C3
-烷氧基、C3
-C7
-環烷基、雙環C6
-C11
-環烷基、金剛烷基、單環4至7員雜環烷基、雙環6至10員雜環烷基、苯基、萘基及5至10員雜芳基,
其中該C1
-C6
-烷基視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:羥基、氰基、C1
-C3
-烷氧基、-N(R22
)(R23
)、C3
-C7
-環烷基、雙環C6
-C11
-環烷基、金剛烷基、單環4至7員雜環烷基、雙環6至10員雜環烷基、苯基及5至10員雜芳基,該苯基取代基及該5至10員雜芳基取代基自身視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:甲基、三氟甲基及甲氧基,
其中C3
-C7
-環烷基、雙環C6
-C11
-環烷基、金剛烷基、單環4至7員雜環烷基、雙環6至10員雜環烷基視情況經取代一次或兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、側氧基、羥基、C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-,
且其中該苯基、該萘基及該5至10員雜芳基視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、C1
-C2
-烷基、C1
-C2
-鹵烷基、C1
-C2
-烷氧基、C1
-C2
-鹵烷氧基、-N(R22
)(R23
)及-C(=O)-N(R24
)(R25
),
R21
表示氫原子或C1
-C2
-烷基,
或
R20
及R21
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況為苯并縮合的且其視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、側氧基、羥基、C1
-C2
-烷基、C1
-C2
-鹵烷基、(苯基)-(C1
-C2
-烷基)-、(C1
-C2
-烷基)-C(=O)-、C3
-C4
-環烷基、C1
-C2
-烷氧基、C1
-C2
-鹵烷氧基、-N(R22
)(R23
)及-C(=O)-N(R24
)(R25
);
R22
及R23
在每次出現時獨立地表示氫原子或選自C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-之基團;
R24
及R25
在每次出現時獨立地表示氫原子或C1
-C2
-烷基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R20
表示氫原子或選自以下之基團:C1
-C6
-烷基、C3
-C4
-烯基、C3
-C4
-炔基、C1
-C3
-烷氧基、C3
-C7
-環烷基、雙環C6
-C11
-環烷基、金剛烷基、單環4至7員雜環烷基、雙環6至10員雜環烷基、苯基、萘基及5至10員雜芳基,
其中該C1
-C6
-烷基視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:羥基、氰基、C1
-C3
-烷氧基、-N(R22
)(R23
)、C3
-C7
-環烷基、雙環C6
-C11
-環烷基、金剛烷基、單環4至7員雜環烷基、雙環6至10員雜環烷基、苯基及5至10員雜芳基,該苯基取代基及該5至10員雜芳基取代基自身視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:甲基、三氟甲基及甲氧基,
其中C3
-C7
-環烷基、雙環C6
-C11
-環烷基、金剛烷基、單環4至7員雜環烷基、雙環6至10員雜環烷基視情況經取代一次或兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、側氧基、羥基、C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-,
且其中該苯基、該萘基及該5至10員雜芳基視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、C1
-C2
-烷基、C1
-C2
-鹵烷基、C1
-C2
-烷氧基、C1
-C2
-鹵烷氧基、-N(R22
)(R23
)及-C(=O)-N(R24
)(R25
),
R21
表示氫原子或C1
-C2
-烷基,
R22
及R23
在每次出現時獨立地表示氫原子或選自C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-之基團;
R24
及R25
在每次出現時獨立地表示氫原子或C1
-C2
-烷基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R20
及R21
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況為苯并縮合的且其視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、側氧基、羥基、C1
-C2
-烷基、C1
-C2
-鹵烷基、(苯基)-(C1
-C2
-烷基)-、(C1
-C2
-烷基)-C(=O)-、C3
-C4
-環烷基、C1
-C2
-烷氧基、C1
-C2
-鹵烷氧基、-N(R22
)(R23
)及-C(=O)-N(R24
)(R25
);
R22
及R23
在每次出現時獨立地表示氫原子或選自C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-之基團;
R24
及R25
在每次出現時獨立地表示氫原子或C1
-C2
-烷基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R20
表示氫原子或選自以下之基團:C1
-C6
-烷基、C3
-C4
-烯基、C3
-C4
-炔基、C1
-C3
-烷氧基、C3
-C7
-環烷基、雙環C5
-C11
-環烷基、金剛烷基、單環4至7員雜環烷基、雙環5至10員雜環烷基、苯基、萘基及5至10員雜芳基,
其中該C1
-C6
-烷基視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:羥基、氰基、C1
-C3
-烷氧基、-N(R22
)(R23
)、C3
-C7
-環烷基、雙環C5
-C11
-環烷基、金剛烷基、單環4至7員雜環烷基、雙環5至10員雜環烷基、苯基及5至10員雜芳基,該苯基取代基及該5至10員雜芳基取代基自身視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:甲基、三氟甲基及甲氧基,
且其中C3
-C7
-環烷基、雙環C5
-C11
-環烷基、金剛烷基、單環4至7員雜環烷基、雙環5至10員雜環烷基視情況經取代一次或兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、側氧基、羥基、C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-,
且其中該苯基、該萘基及該5至10員雜芳基視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、C1
-C2
-烷基、C1
-C2
-鹵烷基、C1
-C2
-烷氧基、C1
-C2
-鹵烷氧基、-N(R22
)(R23
)及-C(=O)-N(R24
)(R25
),及
R21
表示氫原子或C1
-C2
-烷基,
或
R20
及R21
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況為苯并縮合的,且其視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、側氧基、羥基、C1
-C2
-烷基、C1
-C2
-鹵烷基、(苯基)-(C1
-C2
-烷基)-、(C1
-C2
-烷基)-C(=O)-、C3
-C4
-環烷基、C1
-C2
-烷氧基、C1
-C2
-鹵烷氧基、-N(R22
)(R23
)及-C(=O)-N(R24
)(R25
),
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R20
表示氫原子或選自以下之基團:C1
-C6
-烷基、C3
-C4
-烯基、C3
-C4
-炔基、C1
-C3
-烷氧基、C3
-C7
-環烷基、雙環C5
-C11
-環烷基、金剛烷基、單環4至7員雜環烷基、雙環5至10員雜環烷基、苯基、萘基及5至10員雜芳基,
其中該C1
-C6
-烷基視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:羥基、氰基、C1
-C3
-烷氧基、-N(R22
)(R23
)、C3
-C7
-環烷基、雙環C5
-C11
-環烷基、金剛烷基、單環4至7員雜環烷基、雙環5至10員雜環烷基、苯基及5至10員雜芳基,該苯基取代基及該5至10員雜芳基取代基自身視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:甲基、三氟甲基及甲氧基,
且其中C3
-C7
-環烷基、雙環C5
-C11
-環烷基、金剛烷基、單環4至7員雜環烷基、雙環5至10員雜環烷基視情況經取代一次或兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、側氧基、羥基、C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-,
且其中該苯基、該萘基及該5至10員雜芳基視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、C1
-C2
-烷基、C1
-C2
-鹵烷基、C1
-C2
-烷氧基、C1
-C2
-鹵烷氧基、-N(R22
)(R23
)及-C(=O)-N(R24
)(R25
),及
R21
表示氫原子或C1
-C2
-烷基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R20
表示氫原子或選自以下之基團:C1
-C6
-烷基、C3
-C4
-烯基、C3
-C4
-炔基、C1
-C3
-烷氧基、C3
-C7
-環烷基、雙環C6
-C11
-環烷基、金剛烷基、單環4至7員雜環烷基、雙環6至10員雜環烷基、苯基、萘基及5至10員雜芳基,
其中該C1
-C6
-烷基視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:羥基、氰基、C1
-C3
-烷氧基、-N(R22
)(R23
)、C3
-C7
-環烷基、雙環C6
-C11
-環烷基、金剛烷基、單環4至7員雜環烷基、雙環6至10員雜環烷基、苯基及5至10員雜芳基,該苯基取代基及該5至10員雜芳基取代基自身視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:甲基、三氟甲基及甲氧基,
其中C3
-C7
-環烷基、雙環C6
-C11
-環烷基、金剛烷基、單環4至7員雜環烷基、雙環6至10員雜環烷基視情況經取代一次或兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、側氧基、羥基、C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-,
且其中該苯基、該萘基及該5至10員雜芳基視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、C1
-C2
-烷基、C1
-C2
-鹵烷基、C1
-C2
-烷氧基、C1
-C2
-鹵烷氧基、-N(R22
)(R23
)及-C(=O)-N(R24
)(R25
),
R21
表示氫原子或C1
-C2
-烷基,
或
R20
及R21
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況為苯并縮合的且其視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、側氧基、羥基、C1
-C2
-烷基、C1
-C2
-鹵烷基、(苯基)-(C1
-C2
-烷基)-、(C1
-C2
-烷基)-C(=O)-、C3
-C4
-環烷基、C1
-C2
-烷氧基、C1
-C2
-鹵烷氧基、-N(R22
)(R23
)及-C(=O)-N(R24
)(R25
);
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R20
表示氫原子或選自以下之基團:C1
-C6
-烷基、C3
-C4
-烯基、C3
-C4
-炔基、C1
-C3
-烷氧基、C3
-C7
-環烷基、雙環C6
-C11
-環烷基、金剛烷基、單環4至7員雜環烷基、雙環6至10員雜環烷基、苯基、萘基及5至10員雜芳基,
其中該C1
-C6
-烷基視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:羥基、氰基、C1
-C3
-烷氧基、-N(R22
)(R23
)、C3
-C7
-環烷基、雙環C6
-C11
-環烷基、金剛烷基、單環4至7員雜環烷基、雙環6至10員雜環烷基、苯基及5至10員雜芳基,該苯基取代基及該5至10員雜芳基取代基自身視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:甲基、三氟甲基及甲氧基,
其中C3
-C7
-環烷基、雙環C6
-C11
-環烷基、金剛烷基、單環4至7員雜環烷基、雙環6至10員雜環烷基視情況經取代一次或兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、側氧基、羥基、C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-,
且其中該苯基、該萘基及該5至10員雜芳基視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、C1
-C2
-烷基、C1
-C2
-鹵烷基、C1
-C2
-烷氧基、C1
-C2
-鹵烷氧基、-N(R22
)(R23
)及-C(=O)-N(R24
)(R25
),
R21
表示氫原子或C1
-C2
-烷基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R20
及R21
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況為苯并縮合的且其視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、側氧基、羥基、C1
-C2
-烷基、C1
-C2
-鹵烷基、(苯基)-(C1
-C2
-烷基)-、(C1
-C2
-烷基)-C(=O)-、C3
-C4
-環烷基、C1
-C2
-烷氧基、C1
-C2
-鹵烷氧基、-N(R22
)(R23
)及-C(=O)-N(R24
)(R25
);
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R20
表示氫原子或選自以下之基團:視情況經取代C1
-C3
-烷基、未經取代C4
-C6
-烷基、丙-2-炔基、甲氧基、C3
-C6
-環烷基、金剛烷基、單環4至7員雜環烷基、苯基及5至10員雜芳基,
其中該C1
-C3
-烷基視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:羥基、氰基、C1
-C3
-烷氧基、-N(R22
)(R23
)、C3
-C6
-環烷基、金剛烷基、單環4至7員雜環烷基、苯基及5至10員雜芳基,該苯基取代基及該5至10員雜芳基取代基自身視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及甲基,
其中該C3
-C6
-環烷基、該金剛烷基及該單環4至7員雜環烷基視情況經取代一次或兩次或三次,各取代基獨立地選自氟原子或選自以下之基團:側氧基、C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-,
且其中該苯基及該5至10員雜芳基視情況經取代一次、兩次或三次,各取代基獨立地選自氟原子及氯原子或選自以下之基團:氰基、C1
-C2
-烷基、C1
-C2
-氟烷基、C1
-C2
-烷氧基、C1
-C2
-鹵烷氧基、-N(R22
)(R23
)及-C(=O)-N(R24
)(R25
),
R21
表示氫原子或C1
-C2
-烷基,
或
R20
及R21
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況為苯并縮合的,且其視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、側氧基、羥基、C1
-C2
-烷基、C1
-C2
-氟烷基、苯甲基、(C1
-C2
-烷基)-C(=O)-、C3
-C4
-環烷基、C1
-C2
-烷氧基、C1
-C2
-鹵烷氧基、-N(R22
)(R23
)及-C(=O)-N(R24
)(R25
);
R22
及R23
在每次出現時獨立地表示氫原子或選自C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-之基團;
R24
及R25
在每次出現時獨立地表示氫原子或C1
-C2
-烷基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R20
表示氫原子或選自以下之基團:視情況經取代C1
-C3
-烷基、未經取代C4
-C6
-烷基、丙-2-炔基、甲氧基、C3
-C6
-環烷基、金剛烷基、單環4至7員雜環烷基、苯基及5至10員雜芳基,
其中該C1
-C3
-烷基視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:羥基、氰基、C1
-C3
-烷氧基、-N(R22
)(R23
)、C3
-C6
-環烷基、金剛烷基、單環4至7員雜環烷基、苯基及5至10員雜芳基,該苯基取代基及該5至10員雜芳基取代基自身視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及甲基,
其中該C3
-C6
-環烷基、該金剛烷基及該單環4至7員雜環烷基視情況經取代一次或兩次或三次,各取代基獨立地選自氟原子或選自以下之基團:側氧基、C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-,
且其中該苯基及該5至10員雜芳基視情況經取代一次、兩次或三次,各取代基獨立地選自氟原子及氯原子或選自以下之基團:氰基、C1
-C2
-烷基、C1
-C2
-氟烷基、C1
-C2
-烷氧基、C1
-C2
-鹵烷氧基、-N(R22
)(R23
)及-C(=O)-N(R24
)(R25
),
R21
表示氫原子或C1
-C2
-烷基,
R22
及R23
在每次出現時獨立地表示氫原子或選自C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-之基團;
R24
及R25
在每次出現時獨立地表示氫原子或C1
-C2
-烷基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R20
及R21
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況為苯并縮合的,且其視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、側氧基、羥基、C1
-C2
-烷基、C1
-C2
-氟烷基、苯甲基、(C1
-C2
-烷基)-C(=O)-、C3
-C4
-環烷基、C1
-C2
-烷氧基、C1
-C2
-鹵烷氧基、-N(R22
)(R23
)及-C(=O)-N(R24
)(R25
);
R22
及R23
在每次出現時獨立地表示氫原子或選自C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-之基團;
R24
及R25
在每次出現時獨立地表示氫原子或C1
-C2
-烷基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R20
表示氫原子或選自以下之基團:視情況經取代C1
-C3
-烷基、未經取代C4
-C6
-烷基、丙-2-炔基、甲氧基、C3
-C6
-環烷基、金剛烷基、單環4至7員雜環烷基、苯基及5至10員雜芳基,
其中該C1
-C3
-烷基視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:羥基、氰基、C1
-C3
-烷氧基、-N(R22
)(R23
)、C3
-C6
-環烷基、金剛烷基、單環4至7員雜環烷基、苯基及5至10員雜芳基,該苯基取代基及該5至10員雜芳基取代基自身視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及甲基,
其中該C3
-C6
-環烷基、該金剛烷基及該單環4至7員雜環烷基視情況經取代一次或兩次或三次,各取代基獨立地選自氟原子或選自以下之基團:側氧基、C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-,
且其中該苯基及該5至10員雜芳基視情況經取代一次、兩次或三次,各取代基獨立地選自氟原子及氯原子或選自以下之基團:氰基、C1
-C2
-烷基、C1
-C2
-氟烷基、C1
-C2
-烷氧基、C1
-C2
-鹵烷氧基、-N(R22
)(R23
)及-C(=O)-N(R24
)(R25
),
R21
表示氫原子或C1
-C2
-烷基,
或
R20
及R21
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況為苯并縮合的,且其視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、側氧基、羥基、C1
-C2
-烷基、C1
-C2
-氟烷基、苯甲基、(C1
-C2
-烷基)-C(=O)-、C3
-C4
-環烷基、C1
-C2
-烷氧基、C1
-C2
-鹵烷氧基、-N(R22
)(R23
)及-C(=O)-N(R24
)(R25
),
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R20
表示氫原子或選自以下之基團:視情況經取代C1
-C3
-烷基、未經取代C4
-C6
-烷基、丙-2-炔基、甲氧基、C3
-C6
-環烷基、金剛烷基、單環4至7員雜環烷基、苯基及5至10員雜芳基,
其中該C1
-C3
-烷基視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:羥基、氰基、C1
-C3
-烷氧基、-N(R22
)(R23
)、C3
-C6
-環烷基、金剛烷基、單環4至7員雜環烷基、苯基及5至10員雜芳基,該苯基取代基及該5至10員雜芳基取代基自身視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及甲基,
其中該C3
-C6
-環烷基、該金剛烷基及該單環4至7員雜環烷基視情況經取代一次或兩次或三次,各取代基獨立地選自氟原子或選自以下之基團:側氧基、C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-,
且其中該苯基及該5至10員雜芳基視情況經取代一次、兩次或三次,各取代基獨立地選自氟原子及氯原子或選自以下之基團:氰基、C1
-C2
-烷基、C1
-C2
-氟烷基、C1
-C2
-烷氧基、C1
-C2
-鹵烷氧基、-N(R22
)(R23
)及-C(=O)-N(R24
)(R25
),
R21
表示氫原子或C1
-C2
-烷基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R20
及R21
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況為苯并縮合的,且其視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、側氧基、羥基、C1
-C2
-烷基、C1
-C2
-氟烷基、苯甲基、(C1
-C2
-烷基)-C(=O)-、C3
-C4
-環烷基、C1
-C2
-烷氧基、C1
-C2
-鹵烷氧基、-N(R22
)(R23
)及-C(=O)-N(R24
)(R25
),
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R20
表示氫原子或選自以下之基團:視情況經取代C1
-C3
-烷基、未經取代C4
-C6
-烷基、丙-2-炔基、甲氧基、C3
-C6
-環烷基、金剛烷基、單環4至7員雜環烷基、苯基及5至10員雜芳基,
其中該C1
-C3
-烷基視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:羥基、氰基、C1
-C3
-烷氧基、-N(R22
)(R23
)、C3
-C6
-環烷基、金剛烷基、單環4至7員雜環烷基、苯基及5至10員雜芳基,該苯基取代基及該5至10員雜芳基取代基自身視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及甲基,
且其中該C3
-C6
-環烷基、該金剛烷基及該單環4至7員雜環烷基視情況經取代一次或兩次或三次,各取代基獨立地選自氟原子或選自以下之基團:側氧基、C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-,
且其中該苯基及該5至10員雜芳基視情況經取代一次、兩次或三次,各取代基獨立地選自氟原子及氯原子或選自以下之基團:氰基、C1
-C2
-烷基、C1
-C2
-氟烷基、C1
-C2
-烷氧基、C1
-C2
-氟烷氧基、-N(R22
)(R23
)及-C(=O)-N(R24
)(R25
),
R21
表示氫原子或C1
-C2
-烷基,
或
R20
及R21
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況為苯并縮合的,且其視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、側氧基、羥基、C1
-C2
-烷基、C1
-C2
-氟烷基、苯甲基、(C1
-C2
-烷基)-C(=O)-、C3
-C4
-環烷基、C1
-C2
-烷氧基、C1
-C2
-氟烷氧基、-N(R22
)(R23
)及-C(=O)-N(R24
)(R25
),
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R20
表示氫原子或選自以下之基團:視情況經取代C1
-C3
-烷基、未經取代C4
-C6
-烷基、丙-2-炔基、甲氧基、C3
-C6
-環烷基、金剛烷基、單環4至7員雜環烷基、苯基及5至10員雜芳基,
其中該C1
-C3
-烷基視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:羥基、氰基、C1
-C3
-烷氧基、-N(R22
)(R23
)、C3
-C6
-環烷基、金剛烷基、單環4至7員雜環烷基、苯基及5至10員雜芳基,該苯基取代基及該5至10員雜芳基取代基自身視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及甲基,
且其中該C3
-C6
-環烷基、該金剛烷基及該單環4至7員雜環烷基視情況經取代一次或兩次或三次,各取代基獨立地選自氟原子或選自以下之基團:側氧基、C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-,
且其中該苯基及該5至10員雜芳基視情況經取代一次、兩次或三次,各取代基獨立地選自氟原子及氯原子或選自以下之基團:氰基、C1
-C2
-烷基、C1
-C2
-氟烷基、C1
-C2
-烷氧基、C1
-C2
-氟烷氧基、-N(R22
)(R23
)及-C(=O)-N(R24
)(R25
),
R21
表示氫原子或C1
-C2
-烷基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R20
及R21
連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況為苯并縮合的,且其視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、側氧基、羥基、C1
-C2
-烷基、C1
-C2
-氟烷基、苯甲基、(C1
-C2
-烷基)-C(=O)-、C3
-C4
-環烷基、C1
-C2
-烷氧基、C1
-C2
-氟烷氧基、-N(R22
)(R23
)及-C(=O)-N(R24
)(R25
),
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R20
表示氫原子或選自以下之基團:C1
-C3
-烷基及苯基,
其中該C1
-C3
-烷基視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自羥基、C1
-C3
-烷氧基及苯基之基團,該苯基自身視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及甲基,
且其中該苯基視情況經取代一次、兩次或三次,各取代基獨立地選自氟原子及氯原子或選自以下之基團:甲基、三氟甲基、甲氧基及三氟甲氧基;
R21
表示氫原子或C1
-C2
-烷基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R20
表示選自苯甲基及苯基之基團,
其中該苯基及該苯甲基內之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及甲基,
R21
表示氫原子或甲基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R22
及R23
在每次出現時獨立地表示氫原子或選自C1
-C2
-烷基及(C1
-C2
-烷基)-C(=O)-之基團,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R22
及R23
在每次出現時獨立地表示氫原子或選自以下之基團:甲基及(CH3
)-C(=O)-,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R24
及R25
在每次出現時獨立地表示氫原子或C1
-C2
-烷基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R24
及R25
在每次出現時獨立地表示氫原子或甲基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R26
表示氟原子、氯原子或選自以下之基團:C1
-C2
-烷基、C1
-C2
-氟烷基、C1
-C2
-烷氧基及C1
-C2
-氟烷氧基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R26
表示氟原子、氯原子或溴原子或選自以下之基團:甲基、二氟甲基、三氟甲基、甲氧基、苯甲氧基、二氟甲氧基及三氟甲氧基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R26
表示氟原子、氯原子或選自以下之基團:甲基、二氟甲基、三氟甲基、甲氧基、二氟甲氧基及三氟甲氧基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R26
表示氟原子、氯原子或溴原子或選自以下之基團:二氟甲基、甲氧基、苯甲氧基、二氟甲氧基及三氟甲氧基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R26
表示氟原子、氯原子或選自以下之基團:二氟甲基、三氟甲基、甲氧基、二氟甲氧基及三氟甲氧基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R27
表示鹵素原子或選自以下之基團:C1
-C2
-烷基、C1
-C2
-氟烷基、-OR9
、-N(R10
)(R11
)、-C(=O)-N(R12
)(R13
)及-C(=O)-OR17
,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R27
表示氟原子、氯原子或選自以下之基團:C1
-C2
-烷氧基、苯甲氧基及C1
-C2
-氟烷氧基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R27
表示鹵素原子或選自以下之基團:-OR9
、-N(R10
)(R11
)及-C(=O)-N(R12
)(R13
),
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
R27
表示氯原子或選自以下之基團:甲氧基、苯甲氧基、二氟甲氧基及三氟甲氧基,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
n 表示整數0、1或2,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
n 表示整數0或2,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
n 表示整數0,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
n 表示整數2,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
Y1
表示-C(H)=、-C(F)=、-C(Cl)=、-C(CN)=或-N=,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
Y1
表示-C(H)=、-C(F)=、-C(Cl)=或-N=;
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
Y1
表示-C(H)=、-C(F)=或-N=,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
Y1
表示-C(H)=或-C(F)=,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
Y1
表示-C(H)=,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
Y1
表示-C(Cl)=,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
Y1
表示-C(F)=,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
Y1
表示-N=,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
Y2
表示-C(H)=或-N=,
Y3
表示-C(R27
)=或-N=,
其限制條件為,若Y2
表示-N=,則Y3
表示-C(R27
)=;且若Y3
表示-N=,則Y2
表示-C(H)=,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
Y2
表示-C(H)=及-N=,
Y3
表示-C(R27
)=及-N=,
其限制條件為,若Y2
表示-N=,則Y3
表示-C(R27
)=;且若Y3
表示-N=,則Y2
表示-C(H)=,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
Y2
表示-N=;
Y3
表示-C(R27
)=,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
Y2
表示-C(H)=;
Y3
表示-N=,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一實施例中,本發明涵蓋上文式(I)化合物,其中:
Y2
表示-C(H)=;
Y3
表示-C(R27
)=,
及其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,及其混合物。
在第一態樣之另一特定實施例中,本發明涵蓋標題「本發明之第一態樣之其他實施例」下之上述實施例中之兩者或更多者的組合。
本發明涵蓋上文通式(I)化合物之本發明之任何實施例或態樣內的任何子組合。
本發明涵蓋下文本文實例章節中所揭示之通式(I)化合物。
本發明之通式(I)化合物可如本文所描述,藉由熟習此項技術者已知之任何方法轉化成任何鹽,較佳為醫藥學上可接受之鹽。類似地,本發明之通式(I)化合物之任何鹽可藉由熟習此項技術者已知之任何方法轉化成游離化合物。
本發明之通式(I)化合物表明尚不可預測到之有價值的藥理學作用範圍。已出乎意料地發現本發明化合物有效地抑制DGKζ,且因此該等化合物有可能用於治療或預防哺乳動物(包括人類)之疾病,較佳具有失調免疫反應之病狀,特定言之癌症或與異常DGKζ信號傳導相關之其他病症。
特別適合於用本發明之DGKζ抑制劑治療之病症及病狀為液體及實體腫瘤,諸如乳癌、呼吸道癌、腦癌、生殖器官癌、消化道癌、泌尿道癌、眼癌、肝癌、皮膚癌、頭頸癌、甲狀腺癌、甲狀旁腺癌及其遠處轉移。彼等病症亦包括淋巴瘤、肉瘤及白血病。
乳癌之實例包括(但不限於)三陰性乳癌、侵襲性乳腺管癌、侵襲性小葉癌、乳腺管原位癌及小葉原位癌。
呼吸道癌之實例包括(但不限於)小細胞肺癌及非小細胞肺癌,以及支氣管腺瘤及胸膜肺母細胞瘤。
腦癌之實例包括(但不限於)腦幹及下丘腦神經膠質瘤、小腦及大腦星形細胞瘤、神經膠母細胞瘤、神經管胚細胞瘤、室管膜瘤,以及神經外胚層及松果體腫瘤。
男性生殖器官腫瘤包括(但不限於)前列腺癌及睾丸癌。
女性生殖器官腫瘤包括(但不限於)子宮內膜癌、子宮頸癌、卵巢癌、陰道癌及外陰癌以及子宮肉瘤。
卵巢癌之實例包括(但不限於)漿液性腫瘤、子宮內膜樣腫瘤、黏液性囊腺癌、粒層細胞腫瘤、塞-萊二氏細胞瘤(Sertoli-Leydig cell tumour)及卵巢男胚瘤。
子宮頸癌之實例包括(但不限於)鱗狀細胞癌、腺癌、腺鱗癌、小細胞癌、神經內分泌腫瘤、玻璃細胞癌及絨毛腺管狀腺癌。
消化道腫瘤包括(但不限於)肛門癌、結腸癌、結腸直腸癌、食道癌、膽囊癌、胃癌、胰臟癌、直腸癌、小腸癌及唾液腺癌。
食道癌之實例包括(但不限於)食道細胞癌及腺癌,以及鱗狀細胞癌、平滑肌肉瘤、惡性黑色素瘤、橫紋肌肉瘤及淋巴瘤。
胃癌之實例包括(但不限於)腸型及彌漫型胃腺癌。
胰臟癌之實例包括(但不限於)乳腺管腺癌、腺鱗癌及胰臟內分泌腫瘤。
泌尿道腫瘤包括(但不限於)膀胱癌、陰莖癌、腎癌、腎盂癌、輸尿管癌、尿道癌及人類乳頭狀腎癌。
腎癌之實例包括(但不限於)腎細胞癌、尿道上皮細胞癌、近腎小球細胞瘤(腎素瘤)、血管肌脂瘤、腎臟嗜酸性腺瘤、貝里尼管癌(Bellini duct carcinoma)、腎透明細胞肉瘤、中胚層腎瘤及威耳姆氏瘤(Wilms' tumour)。
膀胱癌之實例包括(但不限於)移行細胞癌、鱗狀細胞癌、腺癌、肉瘤及小細胞癌。
眼癌包括(但不限於)眼內黑色素瘤及視網膜母細胞瘤。
肝癌之實例包括(但不限於)肝細胞癌瘤(有或無纖維板層變異之肝細胞癌瘤)、膽管癌瘤(肝內膽管癌瘤)及混合型肝細胞膽管癌瘤。
皮膚癌包括(但不限於)鱗狀細胞癌、卡波西氏肉瘤(Kaposi's sarcoma)、惡性黑色素瘤、梅克爾細胞皮膚癌(Merkel cell skin cancer)及非黑色素瘤皮膚癌。
頭頸癌包括(但不限於)頭頸部鱗狀細胞癌、喉癌、下咽癌、鼻咽癌、口咽癌、唾液腺癌、唇及口腔癌及鱗狀細胞癌。
淋巴瘤包括(但不限於) AIDS相關淋巴瘤、非霍奇金氏淋巴瘤(non-Hodgkin's lymphoma)、皮膚T細胞淋巴瘤、伯基特淋巴瘤(Burkitt lymphoma)、霍奇金氏病(Hodgkin's disease)及中樞神經系統淋巴瘤。
肉瘤包括(但不限於)軟組織肉瘤、骨肉瘤、惡性纖維組織細胞瘤、淋巴肉瘤及橫紋肌肉瘤。
白血病包括(但不限於)急性骨髓性白血病、急性淋巴母細胞白血病、慢性淋巴球性白血病、慢性骨髓性白血病及毛細胞白血病。
如遍及本文件所陳述之術語「治療(treating/treatment)」通常用於例如為了對抗、減輕、減少、緩解、改善疾病或病症(諸如癌瘤)之病狀而管理或護理受試者。
本發明化合物尤其可用於治療及預防(亦即防治)腫瘤生長及癌轉移,尤其用於在進行或未進行腫瘤生長之預治療的情況下治療所有適應症及階段之實體腫瘤。
一般而言,使用化學治療劑及/或抗癌劑與本發明化合物或醫藥組合物組合將用以:
1. 相較於單獨投與任一藥劑,產生減少腫瘤生長或甚至消除腫瘤之更佳功效,
2. 使得所投與之化學治療劑的投與量減小,
3. 相較於使用單一藥劑化學療法及某些其他組合療法所觀測,提供患者耐受性良好且有害藥理學併發症更少之化學治療性療法,
4. 對哺乳動物(尤其人類)之廣泛範圍的不同癌症類型提供治療,
5. 在所治療患者中提供較高反應率,
6. 相較於標準化學療法,使得所治療患者中的存活時間更長,
7. 提供更長腫瘤進展時間,及/或
8. 相較於其他癌症藥劑組合產生拮抗作用之已知情形,產生至少與單獨使用之藥劑一樣好的功效及耐受性結果。
另外,本發明之通式(I)化合物亦可與放射療法及/或手術干預組合使用。
在本發明之另一實施例中,本發明之通式(I)化合物與輻射組合使用:亦即輻射治療藉由誘導腫瘤細胞死亡及隨後將腫瘤新抗原呈遞至腫瘤反應性T細胞而使癌症對抗腫瘤免疫反應敏感。由於DGKζ增強T細胞之抗原特異性活化,相較於單獨的放射治療,總體效果引起更強的癌細胞攻擊。
因此,本發明亦提供一種殺死腫瘤之方法,其中在投與一或多種本發明化合物之前採用習知放射療法。
本發明化合物可以單一藥劑之形式或與一或多種其他醫藥學上活性成分組合投與,其中該組合不會引起不可接受之副作用。本發明亦涵蓋此類醫藥組合。舉例而言,本發明化合物可以與以下組合:
131I-chTNT、阿巴瑞克(abarelix)、阿貝力布(abemaciclib)、阿比特龍(abiraterone)、阿卡拉布魯替尼(acalabrutinib)、阿克拉黴素(aclarubicin)、阿達木單抗(adalimumab)、曲妥珠單抗-美坦新偶聯物(ado-trastuzumab emtansine)、阿法替尼(afatinib)、阿柏西普(aflibercept)、阿地介白素(aldesleukin)、艾樂替尼(alectinib)、阿侖單抗(alemtuzumab)、阿侖膦酸(alendronic acid)、亞利崔托寧(alitretinoin)、艾法雷啶(alpharadin)、六甲蜜胺(altretamine)、阿米福汀(amifostine)、胺魯米特(aminoglutethimide)、胺基乙醯丙酸己酯、胺柔比星(amrubicin)、安吖啶(amsacrine)、阿那曲唑(anastrozole)、安西司亭(ancestim)、大茴香腦二硫雜環戊二烯硫酮(anethole dithiolethione)、阿內圖單抗拉夫坦辛(anetumab ravtansine)、血管緊張素II、抗凝血酶III、阿帕魯胺(apalutamide)、阿瑞匹坦(aprepitant)、阿西莫單抗(arcitumomab)、阿格拉賓(arglabin)、三氧化二砷、天冬醯胺酶、阿特珠單抗(atezolizumab)、艾維路單抗(avelumab)、西卡思羅(axicabtagene ciloleucel)、阿西替尼(axitinib)、阿紮胞苷(azacitidine)、巴利昔單抗(basiliximab)、貝洛替康(belotecan)、苯達莫司汀(bendamustine)、貝索單抗(besilesomab)、貝林諾他(belinostat)、貝伐單抗(bevacizumab)、貝沙羅汀(bexarotene)、比卡魯胺(bicalutamide)、比生群(bisantrene)、博萊黴素(bleomycin)、布林莫單抗(blinatumomab)、硼替佐米(bortezomib)、伯舒替尼(bosutinib)、布舍瑞林(buserelin)、貝倫妥單抗維多汀(brentuximab vedotin)、布加替尼(brigatinib)、白消安(busulfan)、卡巴他賽(cabazitaxel)、卡博替尼(cabozantinib)、降鈣素(calcitonine)、亞葉酸鈣、左亞葉酸鈣、卡培他濱(capecitabine)、卡羅單抗(capromab)、卡馬西平卡鉑(carbamazepine carboplatin)、卡波醌(carboquone)、卡非佐米(carfilzomib)、卡莫氟(carmofur)、卡莫司汀(carmustine)、卡托莫西單抗(catumaxomab)、塞內昔布(celecoxib)、西莫介白素(celmoleukin)、西米普利單抗(cemiplimab)、色瑞替尼(ceritinib)、西妥昔單抗(cetuximab)、氯芥苯丁酸(chlorambucil)、氯地孕酮(chlormadinone)、氮芥(chlormethine)、西多福韋(cidofovir)、西那卡塞(cinacalcet)、順鉑(cisplatin)、克拉屈濱(cladribine)、氯膦酸(clodronic acid)、氯法拉濱(clofarabine)、考比替尼(cobimetinib)、考班昔布(copanlisib)、克立他酶(crisantaspase)、克唑替尼(crizotinib)、環磷醯胺(cyclophosphamide)、環丙孕酮(cyproterone)、阿糖胞苷(cytarabine)、達卡巴嗪(dacarbazine)、放線菌素(dactinomycin)、達雷木單抗(daratumumab)、阿法達貝泊汀(darbepoetin alfa)、達拉菲尼(dabrafenib)、達沙替尼(dasatinib)、道諾黴素(daunorubicin)、地西他濱(decitabine)、地加瑞克(degarelix)、地尼介白素迪夫托斯(denileukin diftitox)、德諾單抗(denosumab)、地普奧肽(depreotide)、德舍瑞林(deslorelin)、衛康醇(dianhydrogalactitol)、右雷佐生(dexrazoxane)、二溴螺氯銨(dibrospidium chloride)、衛康醇(dianhydrogalactitol)、雙氯芬酸(diclofenac)、迪奴圖單抗(dinutuximab)、多西他賽(docetaxel)、多拉司瓊(dolasetron)、去氧氟尿苷(doxifluridine)、小紅莓(doxorubicin)、小紅莓+雌酮、屈大麻酚(dronabinol)、德瓦魯單抗(durvalumab)、艾庫組單抗(eculizumab)、依決洛單抗(edrecolomab)、伊利塞替布(elimusertib) (BAY1895344)、依利醋銨(elliptinium acetate)、埃羅妥珠單抗(elotuzumab)、艾曲波帕(eltrombopag)、艾那尼布(enasidenib)、內皮生長抑素(endostatin)、依諾他濱(enocitabine)、恩雜魯胺(enzalutamide)、表柔比星(epirubicin)、環硫雄醇(epitiostanol)、阿法依泊汀(epoetin alfa)、倍他依泊汀(epoetin beta)、澤塔依伯汀(epoetin zeta)、依鉑(eptaplatin)、艾日布林(eribulin)、埃羅替尼(erlotinib)、埃索美拉唑(esomeprazole)、雌二醇(estradiol)、雌氮芥(estramustine)、炔雌醇(ethinylestradiol)、依託泊苷(etoposide)、依維莫司(everolimus)、依西美坦(exemestane)、法屈唑(fadrozole)、芬太尼(fentanyl)、非格司亭(filgrastim)、氟甲睪酮(fluoxymesterone)、氟尿苷(floxuridine)、氟達拉賓(fludarabine)、氟尿嘧啶(fluorouracil)、氟他胺(flutamide)、醛葉酸(folinic acid)、福美司坦(formestane)、福沙匹坦(fosaprepitant)、福莫司汀(fotemustine)、氟維司群(fulvestrant)、釓布醇(gadobutrol)、釓特醇(gadoteridol)、釓特酸酸葡甲胺(gadoteric acid meglumine)、釓弗塞胺(gadoversetamide)、釓塞酸(gadoxetic acid)、硝酸鎵、加尼瑞克(ganirelix)、吉非替尼(gefitinib)、吉西他濱(gemcitabine)、吉妥珠單抗(gemtuzumab)、麩卡匹酶(Glucarpidase)、氧化型穀胱甘肽(glutoxim)、GM-CSF、戈舍瑞林(goserelin)、格拉司瓊(granisetron)、粒細胞群落刺激因子(granulocyte colony stimulating factor)、組織胺二鹽酸鹽(histamine dihydrochloride)、組胺瑞林(histrelin)、羥基脲(羥基carbamide)、I-125種子(I-125 seed)、蘭索拉唑(lansoprazole)、伊班膦酸(ibandronic acid)、替伊莫單抗替歇坦(ibritumomab tiuxetan)、依魯替尼(ibrutinib)、艾達黴素(idarubicin)、異環磷醯胺(ifosfamide)、伊馬替尼(imatinib)、咪喹莫特(imiquimod)、英丙舒凡(improsulfan)、吲地司瓊(indisetron)、英卡膦酸(incadronic acid)、巨大戟醇甲基丁烯酸酯(ingenol mebutate)、奧英妥珠單抗奧佐米星(inotuzumab ozogamicin)、干擾素α、干擾素β、干擾素γ、碘比醇(iobitridol)、碘苄胍(iobenguane) (123I)、碘美普爾(iomeprol)、伊匹單抗(ipilimumab)、伊立替康(irinotecan)、伊曲康唑(Itraconazole)、伊沙匹隆(ixabepilone)、依薩佐米(ixazomib)、蘭瑞肽(lanreotide)、蘭索拉唑(lansoprazole)、拉帕替尼(lapatinib)、艾索膽鹼(Iasocholine)、來那度胺(lenalidomide)、樂伐替尼(lenvatinib)、來格司亭(lenograstim)、磨菇多糖(lentinan)、來曲唑(letrozole)、亮丙瑞林(leuprorelin)、左旋咪唑(levamisole)、左炔諾孕酮(levonorgestrel)、左旋甲狀腺素鈉(levothyroxine sodium)、麥角乙脲(lisuride)、洛鉑(lobaplatin)、洛莫司汀(lomustine)、氯尼達明(lonidamine)、鎦氧奧曲肽(lutetium Lu 177 dotatate)、馬索羅酚(masoprocol)、甲羥孕酮(medroxyprogesterone)、甲地孕酮(megestrol)、美拉胂醇(melarsoprol)、美法侖(melphalan)、美雄烷(mepitiostane)、巰基嘌呤(mercaptopurine)、美司鈉(mesna)、美沙酮(methadone)、甲胺喋呤(methotrexate)、甲氧沙林(methoxsalen)、胺基乙醯丙酸甲酯(methylaminolevulinate)、甲基普賴蘇濃(methylprednisolone)、甲基睪固酮(methyltestosterone)、甲酪胺酸(metirosine)、米哚妥林(midostaurin)、米伐木肽(mifamurtide)、米替福新(miltefosine)、米鉑(miriplatin)、二溴甘露醇(mitobronitol)、丙脒腙(mitoguazone)、二溴衛矛醇(mitolactol)、絲裂黴素(mitomycin)、米托坦(mitotane)、米托蒽醌(mitoxantrone)、莫格利珠單抗(mogamulizumab)、莫拉司亭(molgramostim)、莫哌達醇(mopidamol)、嗎啡鹼鹽酸鹽(morphine hydrochloride)、嗎啡鹼硫酸鹽(morphine sulfate)、美維絲(mvasi)、大麻隆(nabilone)、納比系莫耳(nabiximols)、那法瑞林(nafarelin)、納洛酮+戊唑星(naloxone + pentazocine)、納曲酮(naltrexone)、那托司亭(nartograstim)、萊西單抗(necitumumab)、奈達鉑(nedaplatin)、奈拉濱(nelarabine)、來那替尼(neratinib)、奈立膦酸(neridronic acid)、奈妥吡坦(netupitant)/帕洛諾司瓊(palonosetron)、納武單抗(nivolumab)、噴曲肽(pentetreotide)、尼羅替尼(nilotinib)、尼魯胺(nilutamide)、尼莫唑(nimorazole)、尼妥珠單抗(nimotuzumab)、尼莫司汀(nimustine)、尼達尼布(nintedanib)、尼拉帕尼(niraparib)、二胺硝吖啶(nitracrine)、納武單抗(nivolumab)、阿托珠單抗(obinutuzumab)、奧曲肽(octreotide)、奧伐木單抗(ofatumumab)、奧拉帕尼(olaparib)、奧拉單抗(olaratumab)、高三尖杉酯鹼(omacetaxine mepesuccinate)、奧美拉唑(omeprazole)、昂丹司瓊(ondansetron)、奧普瑞介白素(oprelvekin)、奧古蛋白(orgotein)、奧瑞洛替莫德(orilotimod)、奧希替尼(osimertinib)、奧沙利鉑(oxaliplatin)、羥考酮(oxycodone)、羥次甲氫龍(oxymetholone)、奧佐米星(ozogamicine)、p53基因療法、太平洋紫杉醇(paclitaxel)、帕博西尼(palbociclib)、帕利夫明(palifermin)、鈀-103種子(palladium-103 seed)、帕洛諾司瓊(palonosetron)、帕米膦酸(pamidronic acid)、帕尼單抗(panitumumab)、帕比司他(panobinostat)、泮托拉唑(pantoprazole)、帕佐泮尼(pazopanib)、培門冬酶(pegaspargase)、PEG-倍他依泊汀(methoxyPEG-倍他依泊汀)、帕博利珠單抗(pembrolizumab)、派非格司亭(pegfilgrastim)、聚乙二醇化干擾素α-2b、培美曲塞(pemetrexed)、戊唑星(pentazocine)、噴司他丁(pentostatin)、培洛黴素(peplomycin)、全氟正丁烷、培磷醯胺(perfosfamide)、帕妥珠單抗(Pertuzumab)、畢西巴尼(picibanil)、匹魯卡品(pilocarpine)、吡柔比星(pirarubicin)、匹蒽醌(pixantrone)、普樂沙福(plerixafor)、普卡黴素(plicamycin)、聚胺葡糖(poliglusam)、聚磷酸雌二醇、聚乙烯吡咯啶酮+玻尿酸鈉、多醣-K、泊利度胺(pomalidomide)、普納替尼(ponatinib)、卟吩姆鈉(porfimer sodium)、普拉曲沙(pralatrexate)、潑尼氮芥(prednimustine)、普賴松(prednisone)、丙卡巴肼(procarbazine)、丙考達唑(procodazole)、普萘洛爾(propranolol)、喹高利特(quinagolide)、雷貝拉唑(rabeprazole)、拉克莫單抗(racotumomab)、鐳-223氯化物、拉多替尼(radotinib)、雷洛昔芬(raloxifene)、雷替曲塞(raltitrexed)、拉莫司瓊(ramosetron)、雷莫蘆單抗(ramucirumab)、雷莫司汀(ranimustine)、拉布立酶(rasburicase)、雷佐生(razoxane)、瑞法美替尼(refametinib)、瑞戈非尼(regorafenib)、瑞博西尼(ribociclib)、利塞膦酸(risedronic acid)、錸-186依替膦酸鹽、利妥昔單抗(rituximab)、羅拉吡坦(rolapitant)、羅米地辛(romidepsin)、羅米司亭(romiplostim)、羅莫肽(romurtide)、蘆卡帕尼(rucaparib)、釤(153Sm)來昔決南釤、沙格司亭(sargramostim)、賽瑞單抗(sarilumab)、沙妥莫單抗(satumomab)、腸泌素(secretin)、司妥昔單抗(siltuximab)、西普亮塞-T (sipuleucel-T)、西佐喃(sizofiran)、索布佐生(sobuzoxane)、甘胺雙唑鈉(sodium glycididazole)、索尼得吉(sonidegib)、索拉非尼(sorafenib)、司坦唑醇(stanozolol)、鏈脲黴素(streptozocin)、舒尼替尼(sunitinib)、他拉泊芬(talaporfin)、塔里穆尼拉赫帕雷普韋克(talimogene laherparepvec)、他米巴羅汀(tamibarotene)、他莫昔芬(tamoxifen)、他噴他多(tapentadol)、他索納明(tasonermin)、替西介白素(teceleukin)、鎝(99mTc)諾非單抗美噴坦(nofetumomab merpentan)、99mTc-HYNIC-[Tyr3]-奧曲肽、替加氟(tegafur)、替加氟+吉美拉西(gimeracil)+奧特拉西(oteracil)、替莫泊芬(temoporfin)、替莫唑胺(temozolomide)、替西羅莫司(temsirolimus)、替尼泊苷(teniposide)、睾固酮、替曲膦(tetrofosmin)、沙立度胺(thalidomide)、噻替派(thiotepa)、胸腺法新(thymalfasin)、促甲狀腺激素α (thyrotropin alfa)、硫鳥嘌呤、替沙津魯(tisagenlecleucel)、替雷利珠單抗(tislelizumab)、托西利單抗(tocilizumab)、拓朴替康(topotecan)、托瑞米芬(toremifene)、托西莫單抗(tositumomab)、曲貝替定(trabectedin)、曲美替尼(trametinib)、曲馬多(tramadol)、曲妥珠單抗(trastuzumab)、曲妥珠單抗美坦新、曲奧舒凡(treosulfan)、視網酸(tretinoin)、曲氟尿苷(trifluridine)+替吡嘧啶(tipiracil)、曲洛司坦(trilostane)、曲普瑞林(triptorelin)、曲美替尼(trametinib)、曲洛磷胺(trofosfamide)、血小板生成素(thrombopoietin)、色胺酸、烏苯美司(ubenimex)、伐拉替尼(valatinib)、伐柔比星(valrubicin)、凡德他尼(vandetanib)、伐普肽(vapreotide)、維羅非尼(vemurafenib)、長春鹼(vinblastine)、長春新鹼(vincristine)、長春地辛(vindesine)、長春氟寧(vinflunine)、長春瑞濱(vinorelbine)、維莫德吉(vismodegib)、伏立諾他(vorinostat)、伏羅唑(vorozole)、釔-90玻璃微球、淨司他丁(zinostatin)、淨司他丁司他美(zinostatin stimalamer)、唑來膦酸(zoledronic acid)、左柔比星(zorubicin)。
本發明化合物可進一步與靶向免疫系統之其他試劑組合,諸如免疫檢查點抑制劑,例如aPD-1/-L1軸拮抗劑。
PD-1以及其配體PD-L1及PD-L2充當T細胞活化之負調控劑。PD-L1過度表現於許多癌症中,且PD-1通常同時過度表現於腫瘤浸潤性T細胞中。此導致T細胞活化減弱及逃避免疫監視,其導致抗腫瘤免疫反應受損。(M. E. Keir等人, Annu.Rev. Immunol. 2008, 26, 677-704)。
根據另一態樣,本發明涵蓋包含如本文所描述之通式(I)之化合物中之一或多者或其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽(特定言之,其醫藥學上可接受之鹽)或其混合物及一或多種免疫檢查點抑制劑的組合。
較佳地,免疫檢查點抑制劑為aPD-1/-L1軸拮抗劑。
本發明化合物可進一步與DGKα抑制劑組合,諸如WO2020/006016、WO2020/006018及WO 2021/041588中揭示之DGKα抑制劑。由於T細胞中之DGKα以與DGKζ類似的方式運作,所以雙重抑制相較於任一單獨DGK同功型缺失之細胞或野生型細胞極大地增強T細胞效應功能。(M. J.Riese等人Cancer Res. (2013), 73(12); 第3566-77頁)。
本發明化合物可以進一步與嵌合抗原受體T細胞(CAR-T細胞),諸如Axicabtagen-Ciloleucel或Tisagenlecleucel組合。可藉由腫瘤微環境(TME)抑制CAR-T細胞之活性。已顯示藉由諸如Crispr之技術基因剔除DGK增強抑制性TME中之CAR-T細胞活性(I. Y. Jung等人, Mol. Cells 2018, 41 (8), 717-723)。
根據另一態樣,本發明涵蓋包含一或多種如本文所描述之通式(I)之化合物或其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,尤其其醫藥學上可接受之鹽或其與嵌合抗原受體T細胞、(CAR-T細胞)、CAR-NKT細胞或CAR-NK細胞之混合物的組合。
較佳地,嵌合抗原受體T細胞(CAR-T細胞)為Axicabtagen-Ciloleucel或Tisagenlecleucel。
本發明進一步提供本發明化合物之用途,其用於活體外擴增包括CAR-T細胞及腫瘤浸潤淋巴細胞之T細胞。
根據另一態樣,本發明涵蓋如本文所描述之通式(I)之化合物或其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,尤其其醫藥學上可接受之鹽或其混合物,其用於活體外擴增包括CAR-T細胞、CAR-NKT細胞或CAR-NK細胞及腫瘤浸潤淋巴細胞之T細胞。
因此,本發明亦係關於本發明化合物用於活體外擴增包括CAR-T細胞、CAR-NKT細胞或CAR-NK細胞及腫瘤浸潤淋巴細胞之T細胞的用途。
本發明亦包含一種活體外擴增包括CAR-T細胞、CAR-NKT細胞或CAR-NK細胞及腫瘤浸潤淋巴細胞之T細胞的方法,使該等T細胞與本發明化合物接觸。
本發明化合物可以用於抑制、阻斷、降低或降低DGKζ活性,從而調節失調免疫反應,例如用於阻斷免疫抑制且在癌症及癌症免疫療法之情形下增加免疫細胞活化及浸潤,最終導致腫瘤生長減少。
此方法包含向有需要之哺乳動物(包括人類)投與有效治療病症之量的本發明化合物或其醫藥學上可接受之鹽、異構物、多形體、代謝物、水合物、溶劑合物或酯。
本發明亦提供治療其中涉及DGKζ之各種其他病症之方法,該等病症諸如(但不限於)具有失調免疫反應之病症、炎症、針對感染及癌症之疫苗接種、病毒感染、淋巴增生病症、哮喘、眼病及2型糖尿病/胰島素抗性。
此等病症在人類中已得到良好表徵,且在其他哺乳動物中亦以類似病源學存在,且可藉由投與本發明之醫藥組合物來治療。
根據另一態樣,本發明涵蓋如上文所描述之通式(I)化合物或其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,特定言之其醫藥學上可接受之鹽或其混合物之用途,其用於治療或預防疾病,尤其癌症或具有失調免疫反應之病狀或與異常DGKζ信號傳導相關之其他病症。
根據本發明之化合物的醫藥活性可以藉由其作為DGKζ抑制劑之活性來加以闡述。
根據另一態樣,本發明涵蓋如上文所描述之通式(I)化合物或其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,特定言之其醫藥學上可接受之鹽或其混合物之用途,其用於治療或預防疾病,尤其癌症或具有失調免疫反應之病狀或與異常DGKζ信號傳導相關之其他病症,特定言之液體及實體腫瘤。
根據另一態樣,本發明涵蓋如上文所描述之通式(I)化合物或其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,特定言之其醫藥學上可接受之鹽或其混合物之用途,其用於治療或預防疾病,特定言之癌症或具有失調免疫反應之病狀或與異常DGKζ信號傳導相關之其他病症,特定言之液體及實體腫瘤。
根據另一態樣,本發明涵蓋如上文所描述之通式(I)化合物或其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,特定言之,其醫藥學上可接受之鹽或其混合物之用途,其用於治療或預防疾病,特定言之失調免疫反應之癌症或病狀或與異常DGKζ信號傳導相關之其他病症,特定言之,液體及實體腫瘤的方法中。
根據另一態樣,本發明涵蓋如上文所描述之通式(I)化合物或其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,特定言之,其醫藥學上可接受之鹽或其混合物之用途,其用於治療或預防疾病,特定言之失調免疫反應之癌症或病狀或與異常DGKζ信號傳導相關之其他病症,特定言之,液體及實體腫瘤的方法中。
根據另一態樣,本發明涵蓋如上文所描述之通式(I)化合物或其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,特定言之其醫藥學上可接受之鹽或其混合物之用途,其用於製備醫藥組合物(較佳藥物)以預防或治療疾病,特定言之具有失調免疫反應之癌症或病狀或與異常DGKζ信號傳導相關之其他病症,特定言之液體及實體腫瘤。
根據另一態樣,本發明涵蓋一種使用有效量之如上文所描述之通式(I)化合物或其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物及鹽,特定言之其醫藥學上可接受之鹽或其混合物來治療或預防疾病,特定言之具有失調免疫反應之癌症或病狀或與異常DGKζ信號傳導相關之其他病症(特定言之,液體及實體腫瘤)的方法。
根據另一態樣,本發明涵蓋醫藥組合物,尤其藥劑,其包含如上文所描述之通式(I)化合物或其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物、鹽(特別是醫藥學上可接受之鹽)或其混合物;及一或多種賦形劑,尤其一或多種醫藥學上可接受之賦形劑。可使用將此類醫藥組合物製備成適當劑型之習知程序。
本發明此外涵蓋醫藥組合物,尤其藥物,其包含至少一種根據本發明化合物,習知地連同一或多種醫藥學上適合之賦形劑;及其用於上文所提及目的之用途。
本發明化合物有可能具有全身性及/或局部活性。出於此目的,其可以適合方式投與,諸如經由口服、非經腸、經肺、經鼻、舌下、經舌、經頰、經直腸、經陰道、經由皮膚、經皮、經結膜、經耳途徑或以植入物或血管支架形式。
就此等投與途徑而言,本發明化合物有可能以合適之投與形式投與。
就口服而言,有可能將本發明化合物調配為此項技術中已知的快速及/或以經調節之方式遞送本發明化合物之劑型,諸如錠劑(非包衣或包衣錠劑,例如具有延遲溶解或不可溶之腸溶或控制釋放包衣)、經口崩解錠劑、薄膜/粉片、薄膜/凍乾製劑、膠囊(例如硬或軟明膠膠囊)、糖包衣錠劑、顆粒劑、丸劑、粉劑、乳液、懸浮液、氣霧劑或溶液。可將本發明化合物以結晶及/或非晶型及/或溶解形式併入該等劑型中。
非經腸投予可在避免吸收步驟之情況下(例如靜脈內、動脈內、心內、脊椎內或腰內)或在包括吸收之情況下(例如肌肉內、皮下、皮內、經皮或腹膜內)實現。適用於非經腸投與之投與形式尤其為供注射及輸注用之製劑,其呈溶液、懸浮液、乳液、凍乾製劑或無菌散劑形式。
適合於其他投與途徑之實例為用於吸入之醫藥形式[尤其粉劑吸入器、噴霧器]、滴鼻劑、鼻用溶液、噴鼻劑;用於經舌、舌下或經頰投與之錠劑/膜/粉片/膠囊;栓劑;滴眼劑、眼膏、洗眼液、眼部插入物、滴耳劑、噴耳劑、耳用粉劑、沖耳劑、耳塞;陰道膠囊、水性懸浮液(洗劑、震盪混合物(mixturae agitandae))、親脂性懸浮液、乳液、軟膏、乳膏、透皮治療性系統(諸如貼片)、乳汁、糊劑、泡沫、敷粉、植入物或支架。
可以將本發明化合物併入所描述投與形式中。此可以本身已知之方式藉由與醫藥學上適合之賦形劑混合而實現。醫藥學上可適合的賦形劑尤其包括
● 填充劑及載劑(例如纖維素、微晶纖維素(諸如Avicel®
)、乳糖、甘露醇、澱粉、磷酸鈣(諸如Di-Cafos®
)),
● 軟膏基質(例如石油膏、石蠟、甘油三酯、蠟、毛絨蠟、毛絨蠟醇、羊毛脂、親水性軟膏、聚乙二醇),
● 栓劑用基質(例如聚乙二醇、可可脂、硬脂肪),
● 溶劑(例如水、乙醇、異丙醇、甘油、丙二醇、中鏈長三酸甘油酯脂肪油、液體聚乙二醇、石蠟),
● 界面活性劑、乳化劑、分散劑或潤濕劑(例如十二烷基硫酸鈉)、卵磷脂、磷脂、脂肪醇(諸如Lanette®
)、脫水山梨糖醇脂肪酸酯(諸如Span®
)、聚氧乙烯脫水山梨糖醇脂肪酸酯(諸如Tween®
)、聚氧乙烯脂肪酸甘油酯(諸如Cremophor®
)、聚氧乙烯脂肪酸酯、聚氧乙烯脂肪醇醚、甘油脂肪酸酯、泊洛沙姆(poloxamer) (諸如Pluronic®
),
● 緩衝劑、酸及鹼(例如磷酸鹽、碳酸鹽、檸檬酸、乙酸、鹽酸、氫氧化鈉溶液、碳酸銨、胺丁三醇、三乙醇胺),
● 等滲劑(例如葡萄糖、氯化鈉),
● 吸附劑(例如高分散性二氧化矽),
● 增黏劑、凝膠形成劑、增稠劑及/或黏合劑(例如聚乙烯吡咯啶酮、甲基纖維素、羥丙基甲基纖維素、羥丙基纖維素、羧甲基纖維素鈉、澱粉、卡波姆(carbomer)、聚丙烯酸(諸如Carbopol®
)、褐藻酸鹽、明膠),
● 崩解劑(例如經改質澱粉、羧甲基纖維素鈉、羥基乙酸澱粉鈉(諸如Explotab®
)、交聯聚乙烯吡咯啶酮、交聯羧甲纖維素鈉(諸如AcDiSol®
)),
● 流量調節劑、潤滑劑、滑動劑及脫模劑(例如硬脂酸鎂、硬脂酸、滑石、高分散二氧化矽(諸如Aerosil®
)),
● 包衣材料(例如糖、蟲膠)及快速或以經修改方式溶解之用於薄膜或擴散膜之成膜劑(例如聚乙烯吡咯啶酮(諸如Kollidon®
)、聚乙烯醇、羥丙基甲基纖維素、羥丙基纖維素、乙基纖維素、羥丙基甲基纖維素鄰苯二甲酸酯、乙酸纖維素、鄰苯二甲酸乙酸纖維素、聚丙烯酸酯、聚甲基丙烯酸酯諸如Eudragit®
)),
● 膠囊材料(例如明膠、羥基丙基甲基纖維素),
● 合成聚合物(例如聚乳酸交酯、聚乙交酯、聚丙烯酸酯、聚甲基丙烯酸酯(諸如Eudragit®
)、聚乙烯吡咯啶酮(諸如Kollidon®
)、聚乙烯醇、聚乙酸乙烯酯、聚氧乙烯、聚乙二醇及其共聚物及嵌段共聚物),
● 塑化劑(例如聚乙二醇、丙二醇、丙三醇、三乙酸甘油酯、檸檬酸三乙醯酯、鄰苯二甲酸二丁酯),
● 滲透增強劑,
● 穩定劑(例如抗氧化劑,諸如抗壞血酸、抗壞血酸棕櫚酸酯、抗壞血酸鈉、丁基羥基苯甲醚、丁基羥基甲苯、沒食子酸丙酯),
● 防腐劑(例如對羥基苯甲酸酯、山梨酸、硫柳汞、苯紮氯銨、乙酸氯己定、苯甲酸鈉),
● 著色劑(例如無機顏料,諸如氧化鐵、二氧化鈦),
● 調味劑、甜味劑、香料及/或氣味遮蔽劑。
本發明此外係關於一種醫藥組合物,其包含至少一種根據本發明化合物(習知地連同一或多種醫藥學上適合之賦形劑一起);及其根據本發明之其用途。
根據另一態樣,本發明涵蓋醫藥組合,特定言之藥劑,其包含至少一種本發明之通式(I)化合物及至少一或多種其他活性成分,特定言之用於治療及/或預防具有失調免疫反應之癌症或病狀或與異常DGKζ信號傳導相關之其他病症,特定言之液體及實體腫瘤。
特定言之,本發明涵蓋一種醫藥組合,其包含:
● 一或多種第一活性成分,尤其如上文所定義之通式(I)化合物,及
● 一或多種其他活性成分,特定言之,免疫檢查點抑制劑。
術語「組合」在本發明中的使用如熟習此項技術者所知,該組合可為固定組合、非固定組合或分裝部分之套組。
「固定組合」在本發明中如熟習此項技術者所已知般使用,且定義為其中例如第一活性成分(諸如一或多種本發明之通式(I)化合物)及另一活性成分一起存在於一個單位劑量或一個單一實體中之組合。「固定組合」之一個實例為醫藥組合物,其中第一活性成分與另一種活性成分存在於同時投與的混合物中,諸如調配物。「固定組合」之另一實例為醫藥組合,其中第一活性成分與另一活性成分存在於一個單元中,而非存在於混雜物中。
本發明中之非固定組合或「分裝部分之套組」的使用如熟習此項技術者所知,且定義為組合,其中第一活性成分與另一活性成分存在於超過一個單元中。非固定組合或分裝部分之套組之一個實例為其中第一活性成分與另一種活性成分單獨存在之組合。非固定組合或分裝部分之套組中之各組分可單獨、依序、同時、並行投與或按交錯時間順序投與。
基於已知標準實驗室技術評估可用於治療具有失調免疫反應之癌症或病狀或與異常DGKζ信號傳導相關之其他病症的化合物,藉由標準毒性測試及藉由用於確定哺乳動物之上述經鑑別之病狀之治療的標準藥理學分析,及藉由將此等結果與用於治療此等病狀之已知活性成分或藥劑的結果進行比較,可容易地判定本發明化合物用於治療各所需適應症的有效劑量。治療此等病狀中之一者所投與之活性成分之量可根據諸如以下考慮因素而變化極大:所用特定化合物及劑量單位、投與模式、療程、所治療患者之年齡及性別,及所治療病狀之性質及程度。
待投與之活性成分之總量的範圍一般為每日每公斤體重約0.001 mg至約200 mg且較佳為每日每公斤體重約0.01 mg至約20 mg。臨床上適用之給藥時程之範圍將為一天給藥一至三次至每四週給藥一次。另外,「藥物假期」(其中在一定時段內不向患者給藥)有可能有益於藥理學效應與耐受性之間的整體平衡。單位劑量有可能含有約0.5 mg至約1500 mg活性成分,且可每日投與一或多次或每日投與少於一次。藉由注射(包括靜脈內、肌肉內、皮下及非經腸注射)及使用輸注技術投與之平均日劑量較佳為每公斤總體重0.01至200 mg。直腸平均日劑量方案較佳為每公斤總體重0.01至200 mg。陰道平均日劑量方案較佳為每公斤總體重0.01至200 mg。局部平均日劑量方案較佳為0.1至200 mg,每日投與一次至四次。透皮濃度較佳為維持0.01至200 mg/kg之日劑量所需之濃度。吸入平均日劑量方案較佳為每公斤總體重0.01至100 mg。
當然,各患者之特定初始及連續給藥方案將根據如主治診斷醫師所確定之病狀性質及嚴重程度、所用特定化合物之活性、患者之年齡及一般狀況、投與時間、投與途徑、藥物之排泄速率、藥物組合及其類似因素而變。所需治療模式及本發明化合物或其醫藥學上可接受之鹽或酯或組合物之劑量數可由熟習此項技術者使用習知治療測試來確定。
本發明化合物之一般合成 根據本發明之通式(I)化合物可以根據以下流程1、2、3及4製備。下文所描述之流程及程序說明本發明之通式(I)化合物之合成途徑且並不意欲為限制性的。熟習此項技術者清楚,可以多種方式修改如流程1、2、3及4中所例示之轉化次序。因此,此等流程中所例示之轉化次序並不意欲具有限制性。另外,可在所例示之轉化之前及/或之後達成取代基R1
、R2
、R3
或R4
中之任一者之修飾。此等修飾可為諸如熟習此項技術者已知之引入保護基、保護基裂解、官能基之還原或氧化、鹵化、金屬化、取代或偶合反應,諸如醯胺偶合(羧酸與胺之偶合)或過渡金屬催化之諸如反應(諸如熟知的鈴木偶合(Suzuki coupling))。此等轉化包括引入允許取代基進一步修飾之功能性的修飾。適當保護基及其引入及裂解為熟習此項技術者所熟知(參見例如T.W. Greene及P.G.M. Wuts,Protective Groups in Organic Synthesis
, 第3版, Wiley 1999)。特定實例描述於後續段落中。
用於製備式(I-a)及(I-b)之化合物(其為通式(I)之子集,該集合在其綜合在一起時形成)及用於製備式(I-c)之化合物(其轉而構成式(I-a)之子集)的適合途徑描述於流程1、2、3及4中。 流程 1 :
自式(II)之異硫氰酸酯及式(III)之酮類製備式(I-a)化合物(通式(I)之子集,其中R3
表示胺基)之途徑.
可由式(II)之異硫氰酸酯(其中R1
具有如關於通式(I)給出之含義)及式(III)之酮類(其中R4
具有如關於通式(I)給出之含義,且其中LG1
表示如本文所定義之離去基,較佳氯、溴或碘原子,更佳地溴原子),藉由在非親核鹼(較佳1,8-二氮雜雙環(5.4.0)十一碳-7-烯(本文中亦稱為DBU,CAS-RN 6674-22-2)存在下,在如本文所定義之偶極非質子性溶劑(較佳乙腈)中,在0℃至50℃ (較佳15℃至30℃,更佳地在室溫)範圍內之溫度,與氰胺(IV)反應持續在1小時至100小時(較佳1小時至10小時,更佳地2小時至4小時)範圍內之時間,得到式(V-a)中間化合物,來製備式(I-a)化合物(其構成通式(I)之子集,其中R3
表示胺基)。隨後,該式(V-a)中間化合物可在如本文所定義之偶極非質子性溶劑(較佳N,N-二甲基甲醯胺)中,在60℃至120℃ (較佳80℃至100℃,更佳地90℃)範圍內之溫度,與式(VI)化合物(其中R2
具有如關於通式(I)給出之含義,且其中LG2
表示如本文所定義之離去基,較佳氯、溴或碘原子,或(甲磺醯基)氧基或[(4-甲基苯基)磺醯基]氧基,更佳地溴原子)反應,持續在30分鐘至24小時(較佳1小時至4小時,更佳地2小時)範圍內之時間,得到本發明式(I-a)化合物。藉由與式(VI)化合物反應將式(V-a)中間化合物轉化為本發明式(I-a)化合物之該轉化亦可有利地如下來實現:在如本文所定義之偶極非質子性溶劑(較佳N,N-二甲基甲醯胺)中,在0℃至60℃ (較佳10℃至40℃,更佳地在如本文所定義之室溫)範圍內之溫度,持續在6小時至48小時(較佳12小時至24小時)範圍內之時間。特定實例描述於實驗章節中。如所此章節之介紹性段落中指示,取代基(例如與R1
及R4
連接之取代基)可在此合成途徑期間或在最終步驟,藉由熟習此項技術者已知之各種方法來修飾。特定實例描述於實驗章節中。 流程 2 :
自式(V-a)中間物製備式(I-a)化合物(通式(I)之子集,其中R3
表示胺基)之備用途徑.
式(V-a)中間物與式(VI)化合物之間的反應選擇性地在與噻唑之C-2連接的氮原子(不涉及與C-4連接之-NH2
基團)處進行。如流程2中所示,此亦適用於與二碳酸二三級丁酯之類似反應,該反應得到式(V-c)化合物,但不得到式(V-b)化合物,同樣,在於如本文所定義之偶極非質子性溶劑(較佳N,N-二甲基甲醯胺)中,在60℃至120℃ (較佳80℃至100℃,更佳地90℃)範圍內之溫度,與式(VI)化合物(其中R2
具有如關於通式(I)給出之含義,且其中LG2
表示如本文所定義之離去基,較佳氯、溴或碘原子,更佳地溴原子)反應持續在30分鐘至24小時(較佳1小時至4小時,更佳地2小時)範圍內之時間後,該等式(V-c)化合物轉化為本發明式(I-a)化合物。特定實例描述於實驗章節中。 流程 3 :
自式(II)之異硫氰酸酯及式(III)之酮類製備式(I-b)化合物(通式(I)之子集,其中R3
表示甲基)之途徑.
可由式(II)之異硫氰酸酯(其中R1
具有如關於通式(I)給出之含義)及式(III)之酮類(其中R4
具有如關於通式(I)給出之含義,且其中LG1
表示如本文所定義之離去基,較佳氯、溴或碘原子,更佳地溴原子),藉由在非親核鹼(較佳1,8-二氮雜雙環(5.4.0)十一碳-7-烯(本文中亦稱為DBU,CAS-RN 6674-22-2))存在下,在如本文所定義之偶極非質子性溶劑(較佳乙腈)中,在0℃至50℃ (較佳15℃至30℃,更佳地在室溫)範圍內之溫度,與式(VII)之乙脒鹽(其中X-
表示一價陰離子,較佳氯離子、溴離子、碘離子或乙酸根,更佳地氯離子)反應,持續在1小時至100小時(較佳1小時至10小時,更佳地2小時至4小時)範圍內之時間,得到式(V-d)中間化合物,來製備式(I-b)化合物(其構成通式(I)之子集,其中R3
表示甲基)。隨後,該式(V-d)中間化合物可在如本文所定義之偶極非質子性溶劑(較佳N,N-二甲基甲醯胺)中,在60℃至120℃ (較佳80℃至100℃,更佳地90℃)範圍內之溫度,與式(VI)化合物(其中R2
具有如關於通式(I)給出之含義,且其中LG2
表示如本文所定義之離去基,較佳氯、溴或碘原子,或(甲磺醯基)氧基或[(4-甲基苯基)磺醯基]氧基,更佳地溴原子)反應,持續在30分鐘至24小時(較佳1小時至4小時,更佳地2小時)範圍內之時間,得到本發明式(I-b)化合物。特定實例描述於實驗章節中。
式(II)、(III)、(IV)、(VI)及(VII)之化合物大部分為市售的或可使用熟習此項技術者已知之方法製備,對於式(II)之異硫氰酸酯之製備,參見例如F. Calderon等人Journal of Medicinal Chemistry 2017, 60 (16), 6880 - 6896;對於式(III)之酮類之製備,亦參見實驗章節中之中間物200至208的合成方案或Y. Xing等人European Journal of Organic Chemistry 2017, 2017 (4), 781 - 785,A. Wu等人Tetrahedron 2013, 69 (31), 6392 - 6398;亦參見實驗章節中之中間物198及199的合成方案。
替代地,可由前驅物(其中R4
基團經不涵蓋在R4
定義內之基團(諸如羧基)取代,然而其允許自常見前驅物(諸如式(I-c)之羧醯胺)產生具有不同取代基的R4
基團),來製備式(I-a)化合物(其構成通式(I)之子集,其中R3
表示胺基) (流程4)。 流程 4 :
自式(VIII)之高級中間化合物來製備本發明式(I-c)之其他化合物之途徑.
流程4例示(對於本發明無任何限制)式(VIII)之高級中間物之轉化,其可使用前述流程中所描述之方法與公認方法(諸如羧酸酯之皂化)組合製備,因此,式(VIII)之羧酸衍生物可在偶合劑(諸如HATU)及三級胺(諸如三乙胺或N,N-二異丙基乙胺)存在下及視情況在DMAP存在下,在如本文所定義之偶極非質子性溶劑(較佳N,N-二甲基甲醯胺)中,在0℃至50℃ (較佳在如本文所定義之室溫)範圍內之溫度,在熟知醯胺偶合反應中與胺(R12
)(R13
)NH反應,持續在2小時至24小時(較佳12小時至20小時)範圍內之時間,得到本發明式(I-c)之羧醯胺化合物。特定實例描述於實驗章節中。
根據第二態樣,本發明涵蓋製備式(I-a)及(I-b)之化合物(其為上文通式(I)之子集,該集合在其綜合在一起時形成)之方法。
根據第二態樣之第二實施例,該方法包含以下步驟:使式(V-a)之中間化合物:
其中R1
及R4
如關於如上文所定義之通式(I)化合物所定義,
與式(VI)化合物反應:,
其中R2
如關於如上文所定義之通式(I)化合物所定義,且其中LG2
表示如本文所定義之離去基,
從而得到式(I-a)化合物:,
其中R1
、R2
及R4
如上文所定義。
根據第二態樣之第三實施例,本發明涵蓋製備式(I-a)化合物之方法,該等方法包含以下步驟:使式(V-c)中間化合物:
其中R1
及R4
如關於如上文所定義之通式(I)化合物所定義,
與式(VI)化合物反應:,
其中R2
如關於如上文所定義之通式(I)化合物所定義,且其中LG2
表示如本文所定義之離去基,
從而得到式(I-a)化合物:,
其中R1
、R2
及R4
如上文所定義。
根據第二態樣之第四實施例,本發明涵蓋製備式(I-b)化合物之方法,該等方法包含以下步驟:使式(V-d)中間化合物:
其中R1
及R4
如關於如上文所定義之通式(I)化合物所定義,
與式(VI)化合物反應:,
其中R2
如關於如上文所定義之通式(I)化合物所定義,且其中LG2
表示如本文所定義之離去基,
從而得到式(I-b)化合物:,
其中R1
、R2
及R4
如上文所定義。
根據第三態樣,本發明涵蓋製備式(I-a)及(I-b)之化合物(其為上文通式(I)之子集,該集合在其綜合在一起時形成)之方法。
根據第三態樣之第二實施例,該等方法包含以下步驟:使式(V-a)中間化合物:
其中R1
及R4
如關於如上文所定義之通式(I)化合物所定義,
與式(VI)化合物反應:,
其中R2
如關於如上文所定義之通式(I)化合物所定義,且其中LG2
表示如本文所定義之離去基,
從而得到式(I-a)化合物:,
其中R1
、R2
及R4
如上文所定義,
接著視情況使用對應(i)溶劑及/或(ii)鹼或酸,將該化合物轉化為溶劑合物、鹽及/或此類鹽之溶劑合物。
根據第三態樣之第三實施例,本發明涵蓋製備式(I-a)化合物之方法,該等方法包含以下步驟:使式(V-c)中間化合物:
其中R1
及R4
如關於如上文所定義之通式(I)化合物所定義,
與式(VI)化合物反應:,
其中R2
如關於如上文所定義之通式(I)化合物所定義,且其中LG2
表示如本文所定義之離去基,
從而得到式(I-a)化合物:,
其中R1
、R2
及R4
如上文所定義,
接著視情況使用對應(i)溶劑及/或(ii)鹼或酸,將該化合物轉化為溶劑合物、鹽及/或此類鹽之溶劑合物。
根據第三態樣之第四實施例,本發明涵蓋製備式(I-b)化合物之方法,該等方法包含以下步驟:使式(V-d)中間化合物:
其中R1
及R4
如關於如上文所定義之通式(I)化合物所定義,
與式(VI)化合物反應:,
其中R2
如關於如上文所定義之通式(I)化合物所定義,且其中LG2
表示如本文所定義之離去基,
從而得到式(I-b)化合物:,
其中R1
、R2
及R4
如上文所定義,
接著視情況使用對應(i)溶劑及/或(ii)鹼或酸,將該化合物轉化為溶劑合物、鹽及/或此類鹽之溶劑合物。
本發明涵蓋製備本發明之通式(I)化合物之方法,該等方法包含如本文實驗章節中所描述之步驟。
根據第四態樣,本發明涵蓋中間化合物,其適用於製備式(I-a)及(I-b)之化合物(其為上文通式(I)之子集,該集合在其綜合在一起時形成)。
根據第五態樣,本發明涵蓋中間化合物之用途,其用於製備式(I-a)及(I-b)之化合物(其為上文通式(I)之子集,該集合在其綜合在一起時形成)。
本發明涵蓋本文本之下文實例章節中所揭示之中間化合物。
本發明涵蓋下文本文實例章節中所揭示之中間化合物之用途。
本發明涵蓋上文式(V-a)、(V-c)及(V-d)之中間化合物之本發明之任何實施例或態樣內之任何子組合。
實驗章節——通用部分 規定光譜中所出現的NMR峰形式,尚未考慮可能的高階效應。不考慮高階之NMR譜效應,根據頻譜中出現的信號形式陳述多重性。NMR信號之多重性:s =單峰,d =二重峰,t =三重峰,q =四重峰,quin =五重峰,br =寬峰信號,m =多重峰。NMR信號:以[ppm]為單位之位移。多重性之組合可為例如dd=二重峰之二重峰。
使用軟體程式,諸如來自ACD/Labs之ACD/Name批次版本14.05及BioVia Draw 2019版19.1 NET,生成化學名稱,且若有需要調適化學名稱。在一些情況下,使用市售試劑之一般認可名稱替代使用上述軟體程式生成之化學名稱。
其合成未在實驗部分中描述之所有試劑均商業地購買,或該試劑為已知化合物或可藉由熟習此項技術者已知之方法由已知化合物形成。
表1列出本段及實例章節中所用之縮寫,只要其在本文正文內未加解釋。其他縮寫具有熟習此項技術者本身慣用之含義。
表1:縮寫 CDCl3
氘化氯仿
DAD 二極體陣列偵測器
SQD 單一四極偵測器
Azura UVD 用於HPLC之單一可變波長UV偵測器
DMF N,N-二甲基甲醯胺
DMSO-d6 氘化二甲基亞碸
DMSO 二甲基亞碸
ELSD 蒸發光散射偵測器
ESIpos 正電噴霧電離
Expl. 實例
HATU (7-氮雜-1H-苯并三唑-1-基)-1,1,3,3-四甲基脲鎓六氟磷酸鹽
HPLC 高壓液相層析
LC-MS 液相層析耦聯質譜
mL 毫升
min 分鐘
MTBE 甲基三級丁基醚
RP-HPLC 逆相高壓液相層析
Rt 滯留時間
rt 室溫
sat. 飽和
THF 四氫呋喃
EtOAc 乙酸乙酯
TLC 薄層層析
rac 外消旋
µM 微莫耳
M 莫耳
UPLC 超高效層析
UPLC-MS 超高效層析耦聯質譜
BEH 乙烯橋接雜交
CSH 帶電表面雜交
UV 紫外線
CAS-RN 化學文摘社註冊號
NMR 核磁共振
MHz 百萬赫
分析型UPLC-MS標準程序
方法 1
/酸性
儀器:Waters Acquity UPLC-MS SQD 3001;管柱:Acquity UPLC BEH C18 1.7 50 × 2.1 mm;溶離劑A:水+ 0.1 vol%甲酸,溶離劑B:乙腈;梯度:0-1.6 min 1-99% B,1.6-2.0 min 99% B;流速0.8 mL/min;溫度:60℃;注射:2 µL;DAD掃描:210-400 nm;ELSD
方法 2
/鹼性
儀器:Waters Acquity UPLC-MS SQD 3001;管柱:Acquity UPLC BEH C18 1.7 50×2.1 mm;溶離劑A:水+ 0.2 vol%氨水(32%),溶離劑B:乙腈;梯度:0-1.6 min 1-99% B,1.6-2.0 min 99% B;流速0.8 mL/min;溫度:60℃;注射:2 µL;DAD掃描:210-400 nm;ELSD
方法 3
/鹼性
儀器:Waters Acquity UPLCMS SingleQuad;管柱:Acquity UPLC CSH C18 1.7 µm 50×2.1 mm;溶離劑A:水+ 0.2 vol%氨水(32%),溶離劑B:乙腈;梯度:0-1.6 min 1-99% B,1.6-2.0 min 99% B;流速0.8 mL/min;溫度:60℃;DAD掃描:210-400 nm。
旋光度
使用溶劑及每一種情況在20℃陳述之濃度、波長589 nm、積分時間10 s、層厚度100 mm,用JASCO偏光計2000量測旋光度。
化合物純化——通用
根據本發明方法製成之實例化合物及中間物可能需要純化。有機化合物之純化為熟習此項技術者所熟知且該化合物可存在若干種純化方法。在一些情況下,可不必純化。在一些情況下,可藉由結晶來純化化合物。在一些情況下,雜質可藉由使用適合之溶劑攪拌移除。在一些情況下,化合物可藉由層析,尤其急驟管柱層析,使用例如預填充矽膠筒(例如Biotage SNAP筒KP-Sil®
或KP-NH®
)以及Biotage自動純化器系統(SP4®
或Isolera Four®
)及溶離劑(諸如己烷/乙酸乙酯或二氯甲烷/甲醇之梯度)來純化。在一些情況下,可使用例如配備有二極體陣列偵測器及/或線上電噴霧電離質譜儀之Waters自動純化器以及適合的預填充逆相管柱及溶離劑(諸如水及乙腈之梯度,其可含有諸如三氟乙酸、甲酸或氨水之添加劑),藉由製備型HPLC來純化化合物。
在一些情況下,如上文所描述之純化方法可提供具有足夠鹼性或酸性官能性、呈鹽形式的彼等本發明化合物,諸如在本發明化合物為足夠鹼性之情況下,例如呈三氟乙酸鹽或甲酸鹽形式;或在本發明化合物為足夠酸性之情況下,例如呈銨鹽形式。此類型之鹽可藉由熟習此項技術者已知之多種方法分別轉化為其游離鹼或游離酸形式,或在後續生物學測定中作為鹽來使用。應理解,如所分離且如本文所描述之本發明化合物的特定形式(例如鹽、游離鹼等)未必為該化合物可應用於生物測定以便對具體生物活性進行定量的唯一形式。
具體方法在下文及在描述實例化合物及中間物之製備之各別方案中描述。
製備型HPLC 儀器:泵:Labomatic HD-3000,頭HDK 280,低壓梯度模組ND-B1000;手動噴射閥:Rheodyne 3725i038;偵測器:Knauer Azura UVD 2.15;採集器:Labomatic Labocol Vario-4000;管柱:ChromatorexRP C-18 10 µm,125×30mm;溶離劑;梯度;UV-偵測。溶離劑:溶劑A:水+ 0.1 vol%甲酸(99%;酸性)或0.2 vol%氨水(32%,鹼性),溶劑B:乙腈;流速150 mL/min。
梯度: 方法 A
:0.00-0.50 min 1% B,0.50-6.00 min 1-25% B,6.00-6.10 min 25-100% B,6.10-8.00 min 100% B
方法 B
:0.00-0.50 min 10% B,0.50-6.00 min 10-50% B,6.00-6.10 min 50-100% B,6.10-8.00 min 100% B
方法 C
:0.00-0.50 min 15% B,0.50-6.00 min 15-55% B,6.00-6.10 min 55-100% B,6.10-8.00 min 100% B
方法 D
:0.00-0.50 min 30% B,0.50-6.00 min 30-70% B,6.00-6.10 min 70-100% B,6.10-8.00 min 100% B
方法 E
:0.00-0.50 min 40% B,0.50-6.00 min 40-80% B,6.00-6.10 min 80-100% B,6.10-8.00 min 100% B
方法 F :
儀器:Waters autopurification system;管柱:Waters CSH C18 5µ 100×30 mm;溶離劑A:水+ 0.1 Vol%氨水(32%),溶離劑B:乙腈,DAD掃描:210-400 nm;MS儀器:QDA (Waters);採集器-觸發:DAD-MS,流速:60 mL/min
對掌性HPLC及立體化學指定(assignment)
藉由對掌性HPLC 分離立體異構混合物(諸如外消旋化合物)可導致分離出不知道所分離異構物中之各別立體對稱中心之組態的單一立體異構物。在以下中,獲自異構混合物(包括(R)及(S)組態)之所有此類經分離異構物之完整化學名稱按字母次序連同所有各別中間物或實例編號一起列出,隨後帶有關於其分析、分離及產率之資料之個別異構物,之後為描述詞,諸如「(鏡像異構物1)」、「(立體異構物2)」及其類似者。同樣,獲自未知絕對組態之單一立體異構物之起始材料的實例化合物以類似方式揭示於本文中。完整化學名稱(包括(R)及(S)組態)之次序不能解釋為編碼對於個別中間物或實例編號之任何相關性。
製備型急驟層析
儀器:Biotage Isolera Four;泵:Dual-Piston;流速:1至200 mL/min;內部偵測器:200-400 nm (可變UV偵測器);溶劑入口:4個;料筒:Biotage SNAP UltraTM
,大小:10 g、25 g、50 g、100 g、340 g,介質:Biotage® HP-Sphere - 25微米球形二氧化矽,解析:最小7000 N/m (盤/米),通常10 000 N/m;溶劑A:己烷,溶劑B:乙酸乙酯,溶劑C:二氯甲烷,溶劑D:乙醇;溶劑E:甲醇;UV收集模式:單/雙/λ-所有波長(可變UV );分級分離模式:體積、臨限值、臨限值與體積、低斜度、中等斜度、自定義斜度或經由外部偵測
方法 X
:用溶劑A及B之梯度,λ-所有
方法 Y
:用溶劑C及D之梯度,λ-所有
方法 Z
:用溶劑C及E之梯度,λ-所有
本申請案中所描述之本發明之各種態樣藉由不以任何方式限制本發明之以下實例來說明。
本文所描述之實例測試實驗用以說明本發明且本發明不限於所示出之實例。
實驗章節——中間物之製備
1-(4-羥基苯基)乙-1-酮(2.00 g,14.7 mmol)提供於在0℃之二氯甲烷(25 mL)中。添加4-二甲基胺基吡啶(100 mg,819 µmol;CAS-RN 1122-58-3)及咪唑(2.00 g,29.4 mmol;CAS-RN-288-32-4)。向混合物中逐滴添加三級丁基(氯)二甲基矽烷(3.32 g,22.0 mmol)於二氯甲烷中之溶液。在室溫攪拌反應混合物2 h。將混合物倒入碳酸氫鈉水溶液中且用二氯甲烷萃取。有機層用水洗滌,乾燥且減壓濃縮。藉由急驟層析(矽膠,己烷/乙酸乙酯梯度0-10%)純化殘餘物,得到3.7 g (96%產率)標題化合物。
1
H-NMR (400 MHz, 氯仿-d
): δ ppm = 0.23 (s, 6 H), 0.99 (s, 9 H), 2.55 (s, 3 H), 6.85 - 6.89 (m, 2 H), 7.86 - 7.90 (m, 2 H)
在氬氣下在-70℃提供二異丙胺基鋰於四氫呋喃中之溶液(1.5 mL,2.0 M,3.0 mmol;CAS-RN 4111-54-0),且添加1-(4-{[三級丁基(二甲基)矽基]氧基}苯基)乙-1-酮(500 mg,2.00 mmol,中間物1)。使混合物升溫至0℃且在0℃攪拌30 min。添加三甲基氯矽烷(1.6 mL,13 mmol;CAS-RN 75-77-4),且在室溫攪拌反應混合物4 h。將混合物倒入水/鹽水中且用甲基三級丁基醚萃取。經合併之有機層用鹽水洗滌,乾燥且減壓濃縮,得到700 mg (98%產率)呈黃色油狀之標題化合物。
¹H-NMR (400 MHz, 氯仿-d
): δ ppm = 0.07 (s, 9 H), 0.77 - 0.82 (m, 15 H), 4.13 - 4.15 (m, 1 H), 4.60 (d,J
=1.77 Hz, 1 H), 6.57 - 6.61 (m, 2 H), 7.24 - 7.29 (m, 2 H)。
三級丁基(二甲基)(4-{1-[(三甲基矽基)氧基]乙烯基}苯氧基)矽烷(695 mg,2.15 mmol;中間物2)在0℃提供於四氫呋喃(57 mL)中,且添加N-溴丁二醯亞胺(460 mg,2.59 mmol;CAS-RN 128-08-5)。在室溫攪拌反應混合物隔夜。混合物用水/鹽水處理且用乙酸乙酯萃取。經合併之有機層用鹽水洗滌,乾燥且減壓濃縮。藉由急驟層析(二氧化矽,己烷/乙酸乙酯梯度0-10%)純化殘餘物,得到460 mg (62%產率)標題化合物。
¹H-NMR (400 MHz, 氯仿-d
): δ ppm = 0.24 - 0.26 (m, 6 H), 0.99 (s, 9 H), 4.40 (s, 2 H), 6.90 (d,J
=8.87 Hz, 2 H), 7.91 (d,J
=8.87 Hz, 2 H)。
LC-MS (方法2):Rt
= 1.58 min; MS (ESIpos): m/z = 329.2 [M+H]+
將1-異硫氰基-4-甲氧基-2-甲苯(225.1 mg,1.26 mmol)溶解於乙腈(25 mL)中,隨後添加1,8-二氮雜雙環(5.4.0)十一碳-7-烯(190 mg,1.26 mmol)及氰胺(63.4 mg,1.51 mmol)。在室溫攪拌45 min之後,添加另外1,8-二氮雜雙環(5.4.0)十一碳-7-烯(96 mg,0.62 mmol)及2-溴-1-苯基乙酮(225 mg,1.26 mmol)。在室溫攪拌反應混合物隔夜。懸浮液用水處理,且沈澱藉由過濾分離,用水及一定量的乙酸乙酯洗滌且藉由凍乾乾燥,得到351 mg (78%產率)標題化合物。
1
H-NMR: (400 MHz, DMSO-d
6): δ ppm = 2.19 (s, 3 H), 3.74 (s, 3 H), 6.78 (dd,J
=8.62, 2.79 Hz, 1 H), 6.88 (d,J
=2.79 Hz, 1 H), 7.26 (d,J
=8.62 Hz, 1 H), 7.34 - 7.47 (m, 3 H), 7.50 - 7.62 (m, 2 H), 7.75 - 8.52 (m, 2 H), 9.90 - 10.16 (br s, 1 H)。
LC-MS (方法2)Rt = 1.09 min; MS (ESIpos): m/z = 340.1 [M+H]+
以下中間物由下表2中陳述之商業起始材料,使用關於中間物 4
之程序製備,隨後藉由層析純化(若需要)。若未指明純化,則各別標題化合物作為粗產物分離。
必要時,粗產物藉由RP-HPLC (方法A至D,視極性而定)或藉由製備型急驟層析(方法X、Y或Z,視極性而定)純化。在缺少沈澱之情況下,反應混合物用乙酸乙酯萃取三次。經合併之有機相經硫酸鈉乾燥,過濾且蒸發至乾燥。藉由如表2中所陳述之層析純化粗產物。
表2:中間物5至77
| 中間物編號 | 化學結構 化學名稱 | 起始材料 | 分析/純化/產率 |
| 5 | [4-胺基-2-[4-(二甲基胺基)苯胺基]噻唑-5-基]-苯基-甲酮 | 4-異硫氰基-N,N-二甲基苯胺; 2-溴-1-苯基乙酮 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 2.87 (s, 6 H), 6.72 (d,J =9.13 Hz, 2 H), 7.30 (br d,J= 8.36Hz, 2 H), 7.38 - 7.51 (m, 3 H), 7.61 (dd,J= 7.48, 2.15 Hz, 2 H), 7.82 - 8.55 (m, 2 H), 10.32 - 10.58 (br s, 1 H)。 LC-MS (方法1)Rt = 1.00 min; MS (ESIpos): m/z = 339.3 [M+H]+ RP-HPLC (方法C,酸性) 10%產率 |
| 6 | [4-胺基-2-(4-異丙氧基苯胺基)噻唑-5-基]-苯基-甲酮 | 1-異丙氧基-4-異硫氰基苯; 2-溴-1-苯基乙酮 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.24 (d,J =6.08 Hz, 6 H), 4.56 (spt,J =6.04 Hz, 1 H), 6.88 - 6.95 (m, 2 H), 7.42 - 7.49 (m, 5 H), 7.61 - 7.67 (m, 2 H), 7.89 - 8.41 (m, 2 H), 10.57 - 10.61 (br s, 1 H)。 LC-MS (方法1)Rt = 1.24 min; MS (ESIpos): m/z = 354.8 [M+H]+ RP-HPLC (方法D,酸性) 66%產率 |
| 7 | [4-胺基-2-(2,4,6-三氟苯胺基)噻唑-5-基]-苯基-甲酮 | 1,3,5-三氟-2-異硫氰基苯; 2-溴-1-苯基乙酮 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 7.38 (m, 2 H), 7.43 - 7.52 (m, 3 H), 7.63 (m, 2 H), 7.97 - 8.42 (m, 2 H), 10.22 - 10.38 (br s, 1 H)。 LC-MS (方法2)Rt = 0.81 min; MS (ESIpos): m/z = 350.5 [M+H]+ RP-HPLC (方法C,鹼性) 68%產率 |
| 8 | [4-胺基-2-(2-溴-4-氟-苯胺基)噻唑-5-基]-苯基-甲酮 | 2-溴-4-氟-1-異硫氰基苯; 2-溴-1-苯基乙酮 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 7.33 (td,J =8.55, 2.91 Hz, 1 H), 7.39 - 7.51 (m, 3 H), 7.61 (dd,J =7.48, 1.90 Hz, 2 H), 7.66 - 7.75 (m, 2 H), 7.96 - 8.45 (m, 2 H), 10.20 - 10.49 (br s, 1 H)。 LC-MS (方法2)Rt = 0.81 min; MS (ESIpos): m/z = 350.5 [M+H]+ RP-HPLC (方法C,鹼性) 33%產率 |
| 9 | [4-胺基-2-(4-氟苯胺基)噻唑-5-基]-(6-甲基-3-吡啶基)甲酮 | 1-氟-4-異硫氰基苯; 2-氯-1-(6-甲基吡啶-3-基)乙酮 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 2.52 (s, 3 H), 7.22 (t,J =8.87 Hz, 2 H), 7.36 (d,J =7.86 Hz, 1 H), 7.60 - 7.67 (m, 2 H), 7.92 (dd,J =7.86, 2.28 Hz, 1 H), 8.14 - 8.48 (m, 2 H), 8.72 (d,J =2.03 Hz, 1 H), 10.87 (s, 1 H)。 LC-MS (方法2)Rt = 0.86 min; MS (ESIpos): m/z = 329.2 [M+H]+ 72%產率 |
| 10 | [4-胺基-2-(4-氟苯胺基)噻唑-5-基]-(4-吡啶基)甲酮 | 1-氟-4-異硫氰基苯; 2-溴-1-(4-吡啶基)乙酮氫溴酸鹽(1:1) | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 7.20 - 7.26 (m, 2 H), 7.54 - 7.59 (m, 1 H), 7.56 - 7.58 (m, 1 H), 7.60 - 7.67 (m, 2 H), 8.27 - 8.47 (m, 2 H), 8.70 (d,J =5.83 Hz, 2 H), 10.83 - 11.02 (br s, 1 H)。 LC-MS (方法2)Rt = 0.77 min; MS (ESIpos): m/z = 315.1 [M+H]+ 76%產率 |
| 11 | [4-胺基-2-(4-氟苯胺基)噻唑-5-基]-(2-氟苯基)甲酮 | 1-氟-4-異硫氰基苯; 2-溴-1-(2-氟苯基)乙酮 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 7.21 (t,J =8.87 Hz, 2 H), 7.24 - 7.31 (m, 2 H), 7.44 - 7.53 (m, 2 H), 7.55 - 7.63 (m, 2 H), 8.16 (br s, 2 H), 10.79 (s, 1 H)。 LC-MS (方法2)Rt = 0.97 min; MS (ESIpos): m/z = 332.3 [M+H]+ 92%產率 |
| 12 | 4-[(4-胺基-5-苯甲醯基-噻唑-2-基)胺基]苯甲腈 | 4-異硫氰基苯甲腈; 2-溴-1-苯基乙酮 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 7.45 - 7.52 (m, 3 H), 7.68 (dd,J =7.73, 1.65 Hz, 2 H), 7.81 (s, 4 H), 8.17 - 8.40 (m, 2 H), 11.08 - 11.35 (br s, 1 H)。 LC-MS (方法2)Rt = 0.92 min; MS (ESIpos): m/z = 321.1 [M+H]+ 56%產率 |
| 13 | [4-胺基-2-(4-氟苯胺基)噻唑-5-基]-[4-氯-3-(三氟甲基)苯基]甲酮 | 1-氟-4-異硫氰基苯; 2-溴-1-[4-氯-3-(三氟甲基)苯基]乙酮 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 7.22 (t,J =8.87 Hz, 2 H), 7.66 (br d,J =4.06 Hz, 2 H), 7.87 (s, 1 H), 7.95 - 8.01 (m, 1 H), 8.07 (s, 1 H), 8.28 - 8.49 (m, 2 H), 10.90 - 10.96 (br s, 1 H)。 LC-MS (方法2)Rt = 1.26 min; MS (ESIpos): m/z = 416.2 [M+H]+ RP-HPLC (方法D,鹼性) 31%產率 |
| 14 | [4-胺基-2-(2-氯-4-氟-苯胺基)噻唑-5-基]-苯基-甲酮 | 2-氯-4-氟-1-異硫氰基苯; 2-溴-1-苯基乙酮 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 7.25 - 7.31 (m, 1 H), 7.41 - 7.50 (m, 3 H), 7.58 (dd,J =8.49, 2.91 Hz, 1 H), 7.60 - 7.66 (m, 2 H), 7.81 (dd,J =9.12, 5.83 Hz, 1 H), 8.17 (br s, 2 H), 10.36 (br s, 1 H)。 LC-MS (方法2)Rt = 1.00 min; MS (ESIpos): m/z = 348.5 [M+H]+ RP-HPLC (方法C,鹼性) 67%產率 |
| 15 | 3-[4-胺基-2-(4-氟苯胺基)噻唑-5-羰基]苯甲腈 | 1-氟-4-異硫氰基苯; 3-(溴乙醯基)苯甲腈 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 7.22 (t,J =8.87 Hz, 2 H), 7.61 - 7.66 (m, 2 H), 7.69 (t,J =7.98 Hz, 1 H), 7.97 (dd,J =7.86, 1.77 Hz, 2 H), 8.06 (t,J =1.52 Hz, 1 H), 8.33 (br s, 2 H), 10.81 - 10.97 (m, 1 H)。 LC-MS (方法2)Rt = 0.97 min; MS (ESIpos): m/z = 339.2 [M+H]+ 78%產率 |
| 16 | [4-胺基-2-[3-氯-4-(二甲基胺基)苯胺基]噻唑-5-基]-苯基-甲酮 | 2-氯-4-異硫氰基-N,N-二甲基苯胺; 2-溴-1-苯基乙酮 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 2.68 (s, 6 H), 7.14 (d,J =8.87 Hz, 1 H), 7.34 (dd,J =8.62, 2.53 Hz, 1 H), 7.42 - 7.50 (m, 3 H), 7.60 - 7.69 (m, 2 H), 7.69 - 7.74 (m, 1 H), 8.22 (br s, 2 H), 10.58 (br s, 1 H)。 LC-MS (方法2)Rt = 1.14 min; MS (ESIpos): m/z = 373.2 [M+H]+ RP-HPLC (方法D,鹼性) 66%產率 |
| 17 | [4-胺基-2-(4-氟苯胺基)噻唑-5-基]-(6-甲氧基-3-吡啶基)甲酮 | 1-氟-4-異硫氰基苯; 2-溴-1-(6-甲氧基吡啶-3-基)乙酮 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 3.91 (s, 3 H), 6.91 (dd,J =8.49, 0.63 Hz, 1 H), 7.19 - 7.26 (m, 2 H), 7.62 - 7.66 (m, 2 H), 7.98 (dd,J =8.62, 2.53 Hz, 1 H), 8.24 (br s, 2 H), 8.51 (dd,J =2.53, 0.76 Hz, 1 H), 10.85 (br s, 1 H)。 LC-MS (方法1)Rt = 1.09 min; MS (ESIpos): m/z = 345.2 [M+H]+ 72%產率 |
| 18 | 4-[4-胺基-2-(4-氟苯胺基)噻唑-5-羰基]-N-甲基-苯甲醯胺 | 1-氟-4-異硫氰基苯; 4-(溴乙醯基)-N-甲基苯甲醯胺 | LC-MS (方法2)Rt = 0.79 min; MS (ESIpos): m/z = 371.2 [M+H]+ RP-HPLC (方法C,鹼性) 31%產率 |
| 19 | [4-胺基-2-(4-氟苯胺基)噻唑-5-基]-(3-氟苯基)甲酮 | 1-氟-4-異硫氰基苯; 2-溴-1-(3-氟苯基)乙酮 | LC-MS (方法2)Rt = 1.03 min; MS (ESIpos): m/z = 332.2 [M+H]+ RP-HPLC (方法D,鹼性) 13%產率 |
| 20 | [4-胺基-2-(3-氯-4-甲氧基-苯胺基)噻唑-5-基]-苯基-甲酮 | 2-氯-4-異硫氰基-1-甲氧基苯; 2-溴-1-苯基乙酮 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 3.83 (s, 3 H), 7.15 (d,J =8.87 Hz, 1 H), 7.41 (dd,J =8.87, 2.79 Hz, 1 H), 7.44 - 7.51 (m, 3 H), 7.62 - 7.69 (m, 2 H), 7.82 (d,J =2.03 Hz, 1 H), 8.27 (br s, 2 H), 10.71 (s, 1 H)。 LC-MS (方法2)Rt = 0.98 min; MS (ESIpos): m/z = 360.2 [M+H]+ 39%產率 |
| 21 | [4-胺基-2-(4-甲氧基苯胺基)噻唑-5-基]-(4-氟苯基)甲酮 | 1-異硫氰基-4-甲氧基苯; 2-溴-1-(4-氟苯基)乙酮 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 3.74 (s, 3 H), 6.94 (d,J =8.87 Hz, 2 H), 7.28 (t,J =8.87 Hz, 2 H), 7.45 (br d,J =8.62 Hz, 2 H), 7.67 - 7.73 (m, 2 H), 7.89 - 8.50 (m, 2 H), 10.64 (br s, 1 H)。 LC-MS (方法2)Rt = 1.09 min; MS (ESIpos): m/z = 344.5 [M+H]+ 製備型急驟層析(方法Y,1-10%) 66%產率 |
| 22 | [4-胺基-2-(4-氟苯胺基)噻唑-5-基]-(4-甲磺醯基苯基)甲酮 | 1-氟-4-異硫氰基苯; 2-溴-1-[4-(甲磺醯基)苯基]乙酮 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 3.28 (s, 3 H), 7.22 (t,J =8.87 Hz, 2 H), 7.60 - 7.65 (m, 2 H), 7.88 (d,J =8.62 Hz, 2 H), 8.00 - 8.04 (m, 2 H), 8.31 (br s, 2 H), 9.20 (s, 1 H)。 LC-MS (方法2)Rt = 0.83 min; MS (ESIpos): m/z = 392.2 [M+H]+ 92%產率 |
| 23 | [4-胺基-2-(4-氟苯胺基)噻唑-5-基]-(4-咪唑-1-基苯基)甲酮 | 1-氟-4-異硫氰基苯; 2-溴-1-[4-(1H-咪唑-1-基)苯基]乙酮 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 7.14 - 7.15 (m, 1 H), 7.22 (t,J =8.87 Hz, 2 H), 7.58 - 7.69 (m, 2 H), 7.75 - 7.82 (m, 4 H), 7.84 (t,J =1.39 Hz, 1 H), 8.00 - 8.56 (m, 2 H), 8.37 (t,J =1.14 Hz, 1 H), 10.84 (br s, 1 H)。 LC-MS (方法2)Rt = 0.88 min; MS (ESIpos): m/z = 380.2 [M+H]+ RP-HPLC (方法C,鹼性) 16%產率 |
| 24 | 4-[4-胺基-2-(4-氟苯胺基)噻唑-5-羰基]-2-氟-苯甲腈 | 1-氟-4-異硫氰基苯; 4-(溴乙醯基)-2-氟苯甲腈 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 7.22 (t,J =8.87 Hz, 2 H), 7.58 - 7.63 (m, 2 H), 7.65 (dd,J =7.98, 1.39 Hz, 1 H), 7.72 (dd,J =9.76, 1.39 Hz, 1 H), 8.04 (dd,J =7.86, 6.59 Hz, 1 H), 8.39 (br s, 2 H), 10.92 (br s, 1 H)。 LC-MS (方法2)Rt = 0.92 min; MS (ESIpos): m/z = 357.2 [M+H]+ RP-HPLC (方法C,鹼性) 5%產率 |
| 25 | 4-[4-胺基-2-(4-氟苯胺基)噻唑-5-羰基]-3-氟-苯甲腈 | 1-氟-4-異硫氰基苯; 4-(溴乙醯基)-3-氟苯甲腈 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 7.23 (t,J =8.87 Hz, 2 H), 7.60 - 7.67 (m, 3 H), 7.73 (dd,J =9.89, 1.27 Hz, 1 H), 8.05 (dd,J =7.86, 6.59 Hz, 1 H), 8.41 (br s, 2 H), 10.94 (br s, 1 H)。 LC-MS (方法2)Rt = 0.92 min; MS (ESIpos): m/z = 357.2 [M+H]+ RP-HPLC (方法D,酸性) 13%產率 |
| 26 | [4-胺基-2-(4-氟苯胺基)噻唑-5-基]-(2-氟-4-甲氧基-苯基)甲酮 | 1-氟-4-異硫氰基苯; 2-溴-1-(2-氟-4-甲氧基苯基)乙酮 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 3.81 (s, 3 H), 6.83 (dd,J =8.49, 2.41 Hz, 1 H), 6.89 (dd,J =12.29, 2.41 Hz, 1 H), 7.21 (t,J =8.87 Hz, 2 H), 7.42 (t,J =8.49 Hz, 1 H), 7.56 - 7.63 (m, 2 H), 7.99 - 8.17 (br s, 2 H), 10.77 (br s, 1 H)。 LC-MS (方法1)Rt = 1.13 min; MS (ESIpos): m/z = 362.4 [M+H]+ 81%產率 |
| 27 | [4-胺基-2-[4-(三氟甲氧基)苯胺基]噻唑-5-基]-苯基-甲酮 | 1-異硫氰基-4-(三氟甲氧基)苯; 2-溴-1-苯基乙酮 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 7.38 (d,J =8.36 Hz, 2 H), 7.45 - 7.52 (m, 3 H), 7.67 (dd,J =7.60, 1.77 Hz, 2 H), 7.74 (d,J =9.13 Hz, 2 H), 8.03 - 8.37 (br s, 2 H), 10.94 (br s, 1 H)。 LC-MS (方法1)Rt = 1.13 min; MS (ESIpos): m/z = 380.5 [M+H]+ 製備型急驟層析(方法X,25-90%) 21%產率 |
| 28 | [4-胺基-2-(4-氟苯胺基)噻唑-5-基]-(3,4-二氟苯基)甲酮 | 1-氟-4-異硫氰基苯; 2-氯-1-(3,4-二氟苯基)乙酮 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 7.22 (t,J =8.87 Hz, 2 H), 7.52 - 7.58 (m, 2 H), 7.61 - 7.73 (m, 3 H), 8.06 - 8.52 (br s, 2 H), 10.87 (br s, 1 H)。 LC-MS (方法2)Rt = 1.13 min; MS (ESIpos): m/z = 350.2 [M+H]+ RP-HPLC (方法D,鹼性) 34%產率 |
| 29 | [4-胺基-2-(4-氟苯胺基)噻唑-5-基]-(3,4-二氯苯基)甲酮 | 1-氟-4-異硫氰基苯; 2-溴-1-(3,4-二氯苯基)乙酮 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 7.19 (t,J =8.87 Hz, 2 H), 7.56 (br s, 2 H), 7.63 (dd,J =8.36, 2.03 Hz, 1 H), 7.73 (d,J =8.36 Hz, 1 H), 7.84 (d,J =1.77 Hz, 1 H), 8.03 - 8.58 (m, 2 H), 10.83 (br s, 1 H)。 LC-MS (方法2)Rt = 1.22 min; MS (ESIneg): m/z = 380.3 [M-H]+ RP-HPLC (方法D,鹼性) 32%產率 |
| 30 | [4-胺基-2-[4-(三氟甲氧基)苯胺基]噻唑-5-基]-(4-氟苯基)甲酮 | 1-異硫氰基-4-(三氟甲氧基)苯; 2-溴-1-(4-氟苯基)乙酮 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 7.31 (t,J =8.87 Hz, 2 H), 7.37 (d,J =8.36 Hz, 2 H), 7.70 - 7.77 (m, 4 H), 8.07 - 8.34 (br s, 2 H), 10.98 (br s, 1 H)。 LC-MS (方法2)Rt = 1.20 min; MS (ESIpos): m/z = 398.2 [M+H]+ 89%產率 |
| 31 | [4-胺基-2-[4-(三氟甲基)苯胺基]噻唑-5-基]-苯基-甲酮 | 1-異硫氰基-4-(三氟甲基)苯; 2-溴-1-苯基乙酮 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 7.45 - 7.52 (m, 3 H), 7.66 - 7.73 (m, 4 H), 7.83 (br d,J =8.36 Hz, 2 H), 8.24 (br s, 2 H), 11.13 (br s, 1 H)。 LC-MS (方法2)Rt = 1.14 min; MS (ESIpos): m/z = 364.2 [M+H]+ 85%產率 |
| 32 | [4-胺基-2-(4-氟苯胺基)噻唑-5-基]-[6-(三氟甲基)-3-吡啶基]甲酮 | 1-氟-4-異硫氰基苯; 2-溴-1-[6-(三氟甲基)吡啶-3-基]乙酮 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 7.22 (t,J =8.87 Hz, 2 H), 7.55 - 7.64 (m, 2 H), 8.02 (d,J =7.86 Hz, 1 H), 8.39 (br s, 1 H), 8.29 (dd,J =7.86, 1.77 Hz, 2 H), 8.99 (d,J =1.77 Hz, 1 H), 10.95 (br s, 1 H)。 LC-MS (方法2)Rt = 1.03 min; MS (ESIpos): m/z = 383.1 [M+H]+ RP-HPLC (方法C,鹼性) 97%產率 |
| 33 | [4-胺基-2-(4-氯-2-氟-苯胺基)噻唑-5-基]-苯基-甲酮 | 4-氯-2-氟-1-異硫氰基苯; 2-溴-1-苯基乙酮 | LC-MS (方法2)Rt = 0.97 min; MS (ESIpos): m/z = 348.2 [M+H]+ 94%產率 |
| 34 | [4-胺基-2-(4-氟苯胺基)噻唑-5-基]-茚烷-5-基-甲酮 | 1-氟-4-異硫氰基苯; 2-溴-1-(2,3-二氫-1H-茚-5-基)乙酮 | LC-MS (方法2)Rt = 1.25 min; MS (ESIpos): m/z = 354.5 [M+H]+ 89%產率 |
| 35 | [4-胺基-2-(3,4-二氟苯胺基)噻唑-5-基]-苯基-甲酮 | 1,2-二氟-4-異硫氰基苯; 2-溴-1-苯基乙酮 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 7.21 - 7.28 (m, 1 H), 7.38 - 7.54 (m, 4 H), 7.63 - 7.72 (m, 2 H), 7.90 - 8.02 (m, 1 H), 8.10 - 8.46 (br s, 2 H), 10.86 - 11.07 (br s, 1 H)。 LC-MS (方法2)Rt = 1.05 min; MS (ESIpos): m/z = 332.2 [M+H]+ 76%產率 |
| 36 | 4-[4-胺基-2-(4-氟苯胺基)噻唑-5-羰基]苯甲腈 | 1-氟-4-異硫氰基苯; 4-(溴乙醯基)苯甲腈 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 7.22 (t,J =8.87 Hz, 2 H), 7.62 (br dd,J =8.87, 4.82 Hz, 2 H), 7.80 (d,J =8.36 Hz, 2 H), 7.95 (d,J =1.00 Hz, 2 H), 8.32 (br s, 2 H), 10.84 - 10.95 (br s, 1 H)。 LC-MS (方法2)Rt = 0.97 min; MS (ESIpos): m/z = 339.2 [M+H]+ 84%產率 |
| 37 | [4-胺基-2-(4-氯苯胺基)噻唑-5-基]-苯基-甲酮 | 1-氯-4-異硫氰基苯; 2-溴-1-苯基乙酮 | LC-MS (方法1)Rt = 1.23 min; MS (ESIneg): m/z = 328.3 [M-H]+ 100%產率 |
| 38 | [4-胺基-2-(3,4-二氯苯胺基)噻唑-5-基]-苯基-甲酮 | 1,2-二氯-4-異硫氰基苯; 2-溴-1-苯基乙酮 | LC-MS (方法1)Rt = 1.32 min; MS (ESIneg): m/z = 362.3 [M-H]+ 製備型急驟層析(方法X,10-80%) 65%產率 |
| 39 | [4-胺基-2-(4-氯-3-氟-苯胺基)噻唑-5-基]-苯基-甲酮 | 1-氯-2-氟-4-異硫氰基苯; 2-溴-1-苯基乙酮 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 7.28 (br dt,J =8.87, 1.27 Hz, 1 H), 7.45 - 7.57 (m, 4 H), 7.68 (dd,J =7.60, 1.77 Hz, 2 H), 7.99 (dd,J =11.91, 2.03 Hz, 1 H), 8.27 (br s, 2 H), 11.07 (br s, 1 H)。 LC-MS (方法2)Rt = 1.04 min; MS (ESIpos): m/z = 348.1 [M+H]+ 67%產率 |
| 40 | [4-胺基-2-(4-氯苯胺基)噻唑-5-基]-(4-氟苯基)甲酮 | 1-氟-4-異硫氰基苯; 2-溴-1-(4-氯苯基)乙酮 | LC-MS (方法2)Rt = 1.12 min; MS (ESIpos): m/z = 348.1 [M+H]+ 94%產率 |
| 41 | [4-胺基-2-(4-氟苯胺基)噻唑-5-基]-(4-氯苯基)甲酮 | 1-氟-4-異硫氰基苯; 2-溴-1-(4-氯苯基)乙酮 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 7.21 (t,J =8.87 Hz, 2 H), 7.54 (d,J =8.62 Hz, 2 H), 7.62 (br dd,J =8.87, 5.07 Hz, 2 H), 7.68 (d,J =8.62 Hz, 2 H), 8.28 (br s, 2 H), 10.83 (br s, 1 H)。 LC-MS (方法1)Rt = 1.25 min; MS (ESIneg): m/z = 346.3 [M-H]+ 製備型急驟層析(方法Y,0-15%) 53%產率 |
| 42 | 2-[4-[4-胺基-2-(4-氟苯胺基)噻唑-5-羰基]苯氧基]-2-甲基-丙酸乙酯 | 1-氟-4-異硫氰基苯; 2-[4-(溴乙醯基)苯氧基]-2-甲基丙酸乙酯 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.15 (t,J =7.10 Hz, 3 H), 1.56 (s, 6 H), 4.17 (q,J =7.10 Hz, 2 H), 6.78 (d,J= 8.87 Hz, 2 H), 7.12 (t,J= 8.87 Hz, 2 H), 7.34 - 7.51 (br s, 2 H), 7.58 (d,J= 8.62 Hz, 2 H), 7.62 - 8.80 (m, 2 H), 9.78 - 10.70 (m, 1 H)。 LC-MS (方法2)Rt = 1.25 min; MS (ESIpos): m/z = 444.3 [M+H]+ 93%產率 |
| 43 | [4-胺基-2-(4-氟苯胺基)噻唑-5-基]-[4-(三氟甲氧基)苯基]甲酮 | 1-氟-4-異硫氰基苯; 2-溴-1-[4-(三氟甲氧基)苯基]乙酮 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 7.21 (t,J =8.87 Hz, 2 H), 7.46 (dd,J =8.74, 0.89 Hz, 2 H), 7.55 - 7.66 (m, 2 H), 7.79 (d,J =8.87 Hz, 2 H), 8.36 (br s, 2 H), 10.77 (br s, 1 H)。 LC-MS (方法2)Rt = 1.21 min; MS (ESIpos): m/z = 398.1 [M+H]+ RP-HPLC (方法D,鹼性) 50%產率 |
| 44 | [4-胺基-2-(4-氯苯胺基)噻唑-5-基]-(4-氯苯基)甲酮 | 1-氯-4-異硫氰基苯; 2-溴-1-(4-氯苯基)乙酮 | LC-MS (方法2)Rt = 1.19 min; MS (ESIpos): m/z = 364.1 [M+H]+ 87%產率 |
| 45 | [4-胺基-2-(4-氟苯胺基)噻唑-5-基]-[4-(三氟甲基)苯基]甲酮 | 1-氟-4-異硫氰基苯; 2-溴-1-[4-(三氟甲基)苯基]乙酮 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 7.22 (t,J =8.87 Hz, 2 H), 7.61 - 7.65 (m, 2 H), 7.85 (s, 4 H), 8.36 (br s, 2 H), 10.88 (br s, 1 H)。 LC-MS (方法2)Rt = 1.15 min; MS (ESIpos): m/z = 382.2 [M+H]+ 66%產率 |
| 46 | [4-胺基-2-[4-(三氟甲基)苯胺基]噻唑-5-基]-[4-(二氟甲氧基)苯基]甲酮 | 1-異硫氰基-4-(三氟甲基)苯; 2-溴-1-[4-(二氟甲氧基)苯基]乙酮 | LC-MS (方法2)Rt = 1.15 min; MS (ESIpos): m/z = 430.2 [M+H]+ 87%產率 |
| 47 | [4-胺基-2-(4-氟苯胺基)噻唑-5-基]-[4-(二氟甲氧基)苯基]甲酮 | 1-氟-4-異硫氰基苯; 2-溴-1-[4-(二氟甲氧基)苯基]乙酮 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 7.34 (t,J =74.50 Hz, 1 H), 7.17 - 7.31 (m, 4 H), 7.61 (br dd,J =8.62, 4.82 Hz, 2 H), 7.73 (d,J =8.62 Hz, 2 H), 8.23 (br s, 2 H), 10.82 (br s, 1 H)。 LC-MS (方法2)Rt = 1.11 min; MS (ESIpos): m/z = 380.4 [M+H]+ RP-HPLC (方法D,鹼性) 94%產率 |
| 48 | (4-胺基-2-苯胺基-噻唑-5-基)-(4-羥基苯基)甲酮 | 異硫氰酸苯酯; 2-溴-4'-羥基苯乙酮 | 1 H-NMR (400 MHz, DMSO-d6): δ ppm = 6.78 (d, 2 H), 7.04 (t, 1 H), 7.33 (d, 2H), 7.54 (d, 2 H), 7.57 (d, 2 H), 8.06 (br s, 2 H), 9.95 (br s, 1 H), 10.68 (br s, 1 H) LC-MS (方法2)Rt = 0.61 min; MS (ESIpos): m/z = 312 [M+H]+ 製備型急驟層析(乙酸乙酯/庚烷4/1) 80%產率 |
| 49 | [4-胺基-2-(4-氯-2-氟-苯胺基)噻唑-5-基]-[4-(二氟甲氧基)苯基]甲酮 | 4-氯-2-氟-1-異硫氰基苯; 2-溴-1-[4-(二氟甲氧基)苯基]乙酮 | LC-MS (方法2)Rt = 1.00 min; MS (ESIpos): m/z = 414.2 [M+H]+ 定量產率 |
| 50 | [4-胺基-2-(4-氯苯胺基)噻唑-5-基]-[4-(二氟甲氧基)苯基]甲酮 | 1-氯-4-異硫氰基苯; 2-溴-1-[4-(二氟甲氧基)苯基]乙酮 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 7.35 (t,J =74.77 Hz, 1 H), 7.26 (d,J =8.62 Hz, 2 H), 7.42 (d,J =8.87 Hz, 1 H), 7.66 (d,J =8.87 Hz, 2 H), 7.75 (d,J =8.62 Hz, 2 H), 8.26 (br s, 2 H), 10.92 (br s, 1 H)。 LC-MS (方法2)Rt = 1.19 min; MS (ESIpos): m/z = 396.2 [M+H]+ RP-HPLC (方法D,酸性) 定量產率 |
| 51 | [4-胺基-2-(4-氯-3-氟-苯胺基)噻唑-5-基]-[4-(二氟甲氧基)苯基]甲酮 | 1-氯-2-氟-4-異硫氰基苯; 2-溴-1-[4-(二氟甲氧基)苯基]乙酮 | LC-MS (方法2)Rt = 1.08 min; MS (ESIpos): m/z = 414.2 [M+H]+ 95%產率 |
| 52 | [4-胺基-2-(3,4-二氟苯胺基)噻唑-5-基]-[4-(二氟甲氧基)苯基]甲酮 | 1,2-二氟-4-異硫氰基苯; 2-溴-1-[4-(二氟甲氧基)苯基]乙酮 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 7.35 (t,J =76.04 Hz, 1 H), 7.27 (br d,J =8.62 Hz, 3 H), 7.39 - 7.48 (m, 1 H), 7.75 (d,J =8.87 Hz, 2 H), 7.97 (ddd,J =12.99, 7.29, 2.28 Hz, 1 H), 8.27 (br s, 2 H), 10.99 (br s, 1 H)。 LC-MS (方法2)Rt = 1.06 min; MS (ESIpos): m/z = 398.2 [M+H]+ 87%產率 |
| 53 | [4-胺基-2-(3,4-二氟苯胺基)-1,3-噻唑-5-基](吡啶-4-基)甲酮 | 2-溴-1-(吡啶-4-基)乙-1-酮氫溴酸鹽; 1,2-二氟-4-異硫氰基苯 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 7.22 - 7.28 (m, 1 H), 7.39 - 7.47 (m, 1 H), 7.56 - 7.59 (m, 2 H), 7.91 - 7.99 (m, 1 H), 8.39 (td,J =6.46, 2.79 Hz, 1 H), 8.36 - 8.44 (m, 1 H), 8.68 - 8.74 (m, 2 H), 10.78 - 11.25 (m, 1 H)。 LC-MS (方法1)Rt = 0.89 min; MS (ESIpos): m/z = 333.1 [M+H]+ RP-HPLC (方法C,酸性) 76%產率 |
| 54 | [4-胺基-2-(3,4-二氟苯胺基)-1,3-噻唑-5-基](4-甲氧基苯基)甲酮 | 2-溴-1-(4-甲氧基苯基)乙-1-酮; 1,2-二氟-4-異硫氰基苯 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 3.82 (s, 3 H), 7.02 (d,J =8.87 Hz, 2 H), 7.22 - 7.28 (m, 1 H), 7.38 - 7.47 (m, 1 H), 7.68 (d,J =8.87 Hz, 2 H), 7.91 - 8.03 (m, 1 H), 8.19 (br s, 2 H), 10.81 - 11.06 (m, 1 H)。 LC-MS (方法2)Rt = 1.07 min; MS (ESIpos): m/z = 362.1 [M+H]+ 92%產率 |
| 55 | [4-胺基-2-(3,4-二氟苯胺基)-1,3-噻唑-5-基](6-甲氧基吡啶-3-基)甲酮 | 2-溴-1-(6-甲氧基吡啶-3-基)乙-1-酮; 1,2-二氟-4-異硫氰基苯 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 2.54 (s, 3 H), 6.92 (dd,J =8.62, 0.51 Hz, 1 H), 7.28 (br s, 1 H), 7.40 - 7.49 (m, 1 H), 7.94 - 8.03 (m, 2 H), 8.18 - 8.36 (m, 2 H), 8.53 (dd,J =2.53, 0.76 Hz, 1 H), 10.98 - 11.04 (m, 1 H)。 LC-MS (方法2)Rt = 0.92 min; MS (ESIpos): m/z = 363.2 [M+H]+ 77%產率 |
| 56 | [4-胺基-2-(3,4-二氟苯胺基)-1,3-噻唑-5-基][6-(三氟甲基)吡啶-3-基]甲酮 | 2-溴-1-[6-(三氟甲基)吡啶-3-基]乙-1-酮; 1,2-二氟-4-異硫氰基苯 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 7.21 - 7.27 (m, 1 H), 7.38 - 7.47 (m, 1 H), 7.87 - 7.98 (m, 1 H), 8.03 (d,J =8.36 Hz, 1 H), 8.31 (dd,J =8.11, 2.03 Hz, 1 H), 8.33 - 8.52 (m, 2 H), 9.00 (d,J =1.52 Hz, 1 H), 11.04 - 11.24 (m, 1 H)。 LC-MS (方法2)Rt = 0.96 min; MS (ESIpos): m/z = 401.3 [M+H]+ 74%產率 |
| 57 | [4-胺基-2-(4-氯-3-氟苯胺基)-1,3-噻唑-5-基](吡啶-4-基)甲酮 | 2-溴-1-(吡啶-4-基)乙-1-酮氫溴酸鹽; 1-氯-2-氟-4-異硫氰基苯 | LC-MS (方法2)Rt = 0.77 min; MS (ESIpos): m/z = 349.1 [M+H]+ 69%產率 |
| 58 | [4-胺基-2-(4-氯苯胺基)-1,3-噻唑-5-基](吡啶-4-基)甲酮 | 2-溴-1-(吡啶-4-基)乙-1-酮氫溴酸鹽; 1-氯-4-異硫氰基苯 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 3.78 (d,J =12.42 Hz, 1 H), 4.08 (d,J =12.17 Hz, 1 H), 7.18 - 7.23 (m, 2 H), 7.31 - 7.36 (m, 2 H), 7.56 - 7.60 (m, 2 H), 8.39 (s, 1 H), 8.48 - 8.55 (m, 2 H)。 LC-MS (方法2)Rt = 0.84 min; MS (ESIpos): m/z = 331.1 [M+H]+ 57%產率 |
| 59 | [4-胺基-2-(4-氯苯胺基)-1,3-噻唑-5-基](4-甲氧基苯基)甲酮 | 2-溴-1-(4-甲氧基苯基)乙-1-酮; 1-氯-4-異硫氰基苯 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 3.82 (s, 3 H), 7.01 (d,J =8.87 Hz, 2 H), 7.38 - 7.43 (m, 2 H), 7.61 - 7.70 (m, 4 H), 8.03 - 8.27 (m, 2 H), 10.78 - 10.92 (m, 1 H)。 LC-MS (方法2)Rt = 1.15 min; MS (ESIpos): m/z = 360.1 [M+H]+ 94%產率 |
| 60 | [4-胺基-2-(4-氯-3-氟苯胺基)-1,3-噻唑-5-基](4-甲氧基苯基)甲酮 | 2-溴-1-(4-甲氧基苯基)乙-1-酮; 1-氯-2-氟-4-異硫氰基苯 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 3.82 (s, 3 H), 6.99 - 7.03 (m, 2 H), 7.25 (dd,J =8.74, 1.65 Hz, 1 H), 7.51 (t,J =8.74 Hz, 1 H), 7.68 (d,J =8.87 Hz, 2 H), 7.95 (br d,J =12.17 Hz, 1 H), 8.06 - 8.29 (m, 2 H), 10.92 - 11.16 (m, 1 H)。 LC-MS (方法2)Rt = 1.15 min; MS (ESIpos): m/z = 378.1 [M+H]+ 80%產率 |
| 61 | (4-胺基-2-苯胺基-1,3-噻唑-5-基)(苯基)甲酮 | 2-溴-1-苯基乙-1-酮; 異硫氰基苯 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 7.08 (t,J =7.60 Hz, 1 H), 7.36 (t,J =7.86 Hz, 2 H), 7.44 - 7.51 (m, 3 H), 7.61 (d,J =7.86 Hz, 2 H), 7.64 - 7.69 (m, 2 H), 8.21 (br s, 2 H), 10.78 (br s, 1 H)。 LC-MS (方法2)Rt = 1.05 min; MS (ESIpos): m/z = 296.4 [M+H]+ 14%產率 |
| 62 | [4-胺基-2-(4-氟苯胺基)-1,3-噻唑-5-基](苯基)甲酮 | 2-溴-1-苯基乙-1-酮; 1-氟-4-異硫氰基苯 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 7.21 (t,J =8.87 Hz, 2 H), 7.43 - 7.52 (m, 3 H), 7.59 - 7.69 (m, 4 H), 8.22 (br s, 2 H), 10.79 (br s, 1 H)。 LC-MS (方法2)Rt = 1.04 min; MS (ESIpos): m/z = 314.4 [M+H]+ 製備型急驟層析(方法Z,0-1%) 78%產率 |
| 63 | [4-胺基-2-(4-氟苯胺基)-1,3-噻唑-5-基](4-甲氧基苯基)甲酮 | 2-溴-1-(4-甲氧基苯基)乙-1-酮; 1-氟-4-異硫氰基苯 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 3.81 (s, 3 H), 7.01 (d,J =8.87 Hz, 2 H), 7.21 (t,J =8.87 Hz, 2 H), 7.66 (d,J =8.87 Hz, 4 H), 8.15 (br s, 2 H), 10.77 (br s, 1 H)。 LC-MS (方法2)Rt = 1.09 min; MS (ESIpos): m/z = 344.4 [M+H]+ 製備型急驟層析(方法Z,0-3%) 57%產率 |
| 64 | [4-胺基-2-(4-氟苯胺基)-1,3-噻唑-5-基](4-甲基苯基)甲酮 | 2-溴-1-(4-甲基苯基)乙-1-酮; 1-氟-4-異硫氰基苯 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 2.35 (s, 3 H), 7.21 (t,J =8.87 Hz, 2 H), 7.27 (d,J =7.86 Hz, 2 H), 7.57 (d,J =8.11 Hz, 2 H), 7.63 (dd,J =9.13, 4.82 Hz, 2 H), 8.19 (br s, 2 H), 10.77 (s, 1 H)。 LC-MS (方法2)Rt = 1.14 min; MS (ESIpos): m/z = 328.4 [M+H]+ 製備型急驟層析(方法Z,0-3%) 47%產率 |
| 65 | [4-胺基-2-(4-氟苯胺基)-1,3-噻唑-5-基](4-氟苯基)甲酮 | 2-溴-1-(4-氟苯基)乙-1-酮; 1-氟-4-異硫氰基苯 | 1 H NMR (400 MHz, DMSO-d 6 ): δ ppm = 7.21 (t,J =8.87 Hz, 2 H), 7.30 (t,J =8.87 Hz, 2 H), 7.62 (dd,J =8.87, 4.82 Hz, 2 H), 7.73 (dd,J =8.74, 5.45 Hz, 2 H), 8.22 (br s, 2 H), 10.82 (br s, 1 H)。 LC-MS (方法2)Rt = 1.05 min; MS (ESIpos): m/z = 332.4 [M+H]+ 製備型急驟層析(方法Z,0-2%) 66%產率 |
| 66 | [4-胺基-2-(2,4-二氟苯胺基)-1,3-噻唑-5-基](苯基)甲酮 | 2-溴-1-苯基乙-1-酮; 2,4-二氟-1-異硫氰基苯 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 7.09 - 7.17 (m, 1 H), 7.39 (ddd,J =11.15, 8.74, 2.91 Hz, 1 H), 7.43 - 7.50 (m, 3 H), 7.62 - 7.65 (m, 2 H), 8.01 (br td,J =9.12, 6.34 Hz, 1 H), 8.08 - 8.39 (m, 2 H), 10.50 (br s, 1 H)。 LC-MS (方法2)Rt = 0.88 min; MS (ESIpos): m/z = 332.4 [M+H]+ 製備型急驟層析(方法Z,0-3%) 71%產率 |
| 67 | [4-胺基-2-(4-甲氧基苯胺基)-1,3-噻唑-5-基](苯基)甲酮 | 2-溴-1-苯基乙-1-酮; 1-異硫氰基-4-甲氧基苯 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 3.70 - 3.76 (m, 3 H), 6.92 - 6.96 (m, 2 H), 7.42 - 7.50 (m, 5 H), 7.60 - 7.66 (m, 2 H), 7.93 - 8.48 (m, 2 H), 10.60 (br s, 1 H)。 LC-MS (方法2)Rt = 1.04 min; MS (ESIpos): m/z = 326.4 [M+H]+ 製備型急驟層析(方法Z,0-1%) 76%產率 |
| 68 | [4-胺基-2-(4-氟苯胺基)-1,3-噻唑-5-基](4-{[三級丁基(二甲基)矽基]氧基}苯基)甲酮 | 2-溴-1-(4-{[三級丁基(二甲基)矽基]氧基}苯基)乙-1-酮(中間物3); 1-氟-4-異硫氰基苯 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 0.23 (s, 6 H), 0.96 (s, 9 H), 6.92 (d,J =8.62 Hz, 2 H), 7.21 (t,J =8.87 Hz, 2 H), 7.59 - 7.66 (m, 4 H), 8.15 (br s, 2 H), 10.76 (br s, 1 H)。 LC-MS (方法2)Rt = 1.56 min; MS (ESIpos): m/z = 444.2 [M+H]+ 製備型急驟層析(方法Z,0-3%) 27%產率 |
| 69 | [4-胺基-2-(4-甲基苯胺基)-1,3-噻唑-5-基](苯基)甲酮 | 2-溴-1-苯基乙-1-酮; 1-異硫氰基-4-甲基苯 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 2.27 (s, 3 H), 7.16 (d,J =8.11 Hz, 2 H), 7.44 - 7.49 (m, 5 H), 7.63 - 7.67 (m, 2 H), 7.93 - 8.63 (m, 2 H), 10.69 (br s, 1 H)。 LC-MS (方法2)Rt = 1.15 min; MS (ESIpos): m/z = 310.5 [M+H]+ 製備型急驟層析(方法Z,0-3%) 67%產率 |
| 70 | [4-胺基-2-(3-氟苯胺基)-1,3-噻唑-5-基](苯基)甲酮 | 2-溴-1-苯基乙-1-酮; 1-氟-3-異硫氰基苯 | ¹H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 6.85 - 6.93 (m, 1 H), 7.27 (ddd,J =8.24, 2.03, 0.89 Hz, 1 H), 7.38 (td,J =8.17, 6.72 Hz, 1 H), 7.45 - 7.53 (m, 3 H), 7.66 - 7.70 (m, 2 H), 7.76 (dt,J =11.66, 2.15 Hz, 1 H), 8.26 (br s, 2 H), 10.96 (s, 1 H)。 LC-MS (方法2)Rt = 1.07 min; MS (ESIpos): m/z = 314.4 [M+H]+ 製備型急驟層析(方法Z,0-3%) 53%產率 |
| 71 | [4-胺基-2-(2-氟苯胺基)-1,3-噻唑-5-基](苯基)甲酮 | 2-溴-1-苯基乙-1-酮; 1-氟-2-異硫氰基苯 | ¹H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 7.15 - 7.25 (m, 2 H), 7.27 - 7.34 (m, 1 H), 7.43 - 7.51 (m, 3 H), 7.62 - 7.68 (m, 2 H), 8.04 - 8.11 (m, 1 H), 8.10 - 8.32 (m, 2 H), 10.54 (s, 1 H)。 LC-MS (方法2)Rt = 0.96 min; MS (ESIpos): m/z = 314.5 [M+H]+ 製備型急驟層析(方法Z,0-1%) 36%產率 |
| 72 | [4-胺基-2-(3-甲基苯胺基)-1,3-噻唑-5-基](苯基)甲酮 | 2-溴-1-苯基乙-1-酮; 1-異硫氰基-3-甲基苯 | ¹H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 2.30 (s, 3 H), 6.91 (br d,J =7.35 Hz, 1 H), 7.24 (br t,J =7.73 Hz, 1 H), 7.38 (br s, 1 H), 7.41 - 7.54 (m, 4 H), 7.62 - 7.68 (m, 2 H), 8.20 (br s, 2 H), 10.70 (br s, 1 H)。 LC-MS (方法2)Rt = 1.15 min; MS (ESIpos): m/z = 310.5 [M+H]+ 製備型急驟層析(方法Z,0-3%) 53%產率 |
| 73 | [4-胺基-2-(2-甲基苯胺基)-1,3-噻唑-5-基](苯基)甲酮 | 2-溴-1-苯基乙-1-酮; 1-異硫氰基-2-甲基苯 | ¹H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 2.23 (s, 3 H), 7.14 - 7.26 (m, 2 H), 7.27 - 7.31 (m, 1 H), 7.38 - 7.52 (m, 4 H), 7.57 - 7.62 (m, 2 H), 8.15 (br s, 2 H), 10.18 (br s, 1 H)。 LC-MS (方法2)Rt = 1.10 min; MS (ESIpos): m/z = 310.5 [M+H]+ 製備型急驟層析(方法Z,0-1%) 60%產率 |
| 74 | {4-胺基-2-[(1-甲基-1H-吡唑-4-基)胺基]-1,3-噻唑-5-基}(苯基)甲酮 | 2-溴-1-苯基乙-1-酮; 4-異硫氰基-1-甲基-1H-吡唑 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 3.81 (s, 3 H), 7.41 - 7.52 (m, 4 H), 7.58 - 7.66 (m, 2 H), 7.90 (s, 1 H), 7.94 - 8.50 (m, 2 H), 10.44 - 10.57 (m, 1 H)。 LC-MS (方法2)Rt = 0.78 min; MS (ESIpos): m/z = 300.5 [M+H]+ 製備型急驟層析(方法Z,0-1%) 58%產率 |
| 75 | {4-胺基-2-[(吡啶-3-基)胺基]-1,3-噻唑-5-基}(苯基)甲酮 | 2-溴-1-苯基乙-1-酮; 3-異硫氰基吡啶 | ¹H-NMR (400 MHz, DMSO-d 6): δ ppm = 7.37 - 7.42 (m, 1 H), 7.45 - 7.53 (m, 3 H), 7.65 - 7.69 (m, 2 H), 8.12 (br ddd,J =8.36, 2.53, 1.52 Hz, 1 H), 8.16 - 8.39 (m, 2 H), 8.28 (dd,J =4.69, 1.39 Hz, 1 H), 8.81 (d,J =2.53 Hz, 1 H), 10.95 (br s, 1 H)。 LC-MS (方法2)Rt = 0.70 min; MS (ESIpos): m/z = 297.4 [M+H]+ 製備型急驟層析(方法Z,0-3%) 23%產率 |
| 76 | [4-胺基-2-(4-氟苯胺基)-1,3-噻唑-5-基](4-溴苯基)甲酮 | 2-溴-1-(4-溴苯基)乙-1-酮; 1-氟-4-異硫氰基苯 | ¹H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 7.21 (t,J =8.87 Hz, 2 H), 7.56 - 7.65 (m, 4 H), 7.66 - 7.70 (m, 2 H), 8.26 (br s, 2 H), 10.85 (br s, 1 H)。 LC-MS (方法2)Rt = 1.19 min; MS (ESIpos): m/z = 392.3 [M+H]+ 製備型急驟層析(方法Z,0-1%) 77%產率 |
| 77 | [4-胺基-2-(4-氟苯胺基)-1,3-噻唑-5-基][4-(苯甲氧基)苯基]甲酮 | 1-[4-(苯甲氧基)苯基]-2-溴乙-1-酮; 1-氟-4-異硫氰基苯 | 1 H-NMR (400 MHz, DMSO-d 6): δ ppm = 5.17 (s, 2 H), 7.09 (d,J =8.87 Hz, 2 H), 7.21 (t,J =8.87 Hz, 2 H), 7.31 - 7.37 (m, 1 H), 7.41 (t,J =7.35 Hz, 2 H), 7.45 - 7.49 (m, 2 H), 7.60 - 7.69 (m, 4 H), 7.96 - 8.34 (m, 2 H), 10.71 - 10.79 (m, 1 H)。 LC-MS (方法2)Rt = 1.30 min; MS (ESIpos): m/z = 420.2 [M+H]+ 87%產率 |
將1-氟-4-異硫氰基苯(116 mg,0.755 mmol)溶解於乙腈(7.5 mL)中,隨後添加1,8-二氮雜雙環(5.4.0)十一碳-7-烯(100 mg,0.66 mmol)及乙脒(鹽酸鹽) (86 mg,0.91 mmol)。在室溫攪拌45 min之後,添加另外1,8-二氮雜雙環(5.4.0)十一碳-7-烯(70 mg,0.47 mmol)及2-溴-1-[4-(二氟甲氧基)苯基]乙-1-酮(200 mg,0.755 mmol)。在室溫攪拌反應混合物隔夜。真空濃縮反應混合物,且藉由製備型HPLC (方法D,鹼性)純化殘餘物,得到72 mg (25%產率)標題化合物。
LC-MS (方法2)Rt = 1.30 min; MS (ESIpos): m/z = 379.4 [M+H]+
將1,2-二氟-4-異硫氰基苯(129 mg,0.755 mmol)溶解於乙腈(7.5 mL)中,隨後添加1,8-二氮雜雙環(5.4.0)十一碳-7-烯(100 mg,0.66 mmol)及乙脒(鹽酸鹽) (86 mg,0.91 mmol)。在室溫攪拌45 min之後,添加另外1,8-二氮雜雙環(5.4.0)十一碳-7-烯(70 mg,0.47 mmol)及2-溴-1-[4-(二氟甲氧基)苯基]乙-1-酮(200 mg,0.755 mmol)。在室溫攪拌反應混合物隔夜。真空濃縮反應混合物,且藉由製備型HPLC (方法E,鹼性)純化殘餘物,得到31 mg (10%產率)標題化合物。
LC-MS (方法2)Rt = 1.36 min; MS (ESIpos): m/z = 397.3 [M+H]+
將1-氟-4-異硫氰基苯(8.91 g,58.20 mmol)溶解於乙腈(450 mL)中,隨後添加1,8-二氮雜雙環(5.4.0)十一碳-7-烯(8.86 g,58.20 mmol)及氰胺(2.94 g,69.82 mmol)。在室溫攪拌45 min之後,添加另外1,8-二氮雜雙環(5.4.0)十一碳-7-烯(4.43 g,29.07 mmol)及[4-(溴乙醯基)苯氧基]乙酸乙酯(17.52 g,58.20 mmol)。在室溫攪拌反應混合物隔夜。懸浮液用水處理,且沈澱藉由過濾分離,用水洗滌且藉由凍乾乾燥,得到18.54 g (77%產率)標題化合物。
1
H-NMR (500 MHz, DMSO-d
6): δ ppm = 1.22 (t,J
=7.09 Hz, 3 H), 4.18 (q,J
=7.25 Hz, 2 H), 4.86 (s, 2 H), 7.00 (d,J
=9.14 Hz, 2 H), 7.21 (t,J
=9.14 Hz, 2 H), 7.61 - 7.67 (m, 4 H), 8.21 (br s, 2 H), 10.77 (s, 1 H)。
LC-MS (方法2)Rt = 1.09 min; MS (ESIpos): m/z = 416.3 [M+H]+
將1-氟-4-異硫氰基苯(77 mg,0.50 mmol)溶解於乙腈(5 mL)中,隨後添加1,8-二氮雜雙環(5.4.0)十一碳-7-烯(77 mg,0.50 mmol)及乙脒(鹽酸鹽) (57 mg,0.60 mmol)。在室溫攪拌45 min之後,另外添加1,8-二氮雜雙環(5.4.0)十一碳-7-烯(38 mg,0.25 mmol)及2-溴-1-苯基乙酮(100 mg,0.50 mmol)。在室溫攪拌反應混合物隔夜。溶液經過濾且藉由RP-HPLC (方法D,鹼性)純化。藉由凍乾分離標題化合物(53 mg,33%產率)。
1
H-NMR (400 MHz, DMSO-d6
): δ ppm = 2.28 (s, 3 H), 7.18 (t,J
=8.87 Hz, 2 H), 7.51 (d,J
=7.86 Hz, 2 H), 7.53 - 7.58 (m, 3 H), 7.63 - 7.67 (m, 2 H), 10.67 (br s, 1 H)。
LC-MS (方法2)Rt = 1.22 min; MS (ESIpos): m/z = 313.1 [M+H]+
將外消旋-2-[4-[4-胺基-2-(N-[2-胺基-1-甲基-2-側氧基-乙基]-4-氟-苯胺基)噻唑-5-羰基]苯氧基]-2-甲基-丙酸乙酯(180 mg,349 µmol,實例39)溶解於THF (1.8 ml)中,冷卻至0℃,且添加氫氧化鈉水溶液(350 µl,1.0 M,350 µmol)。在室溫攪拌反應混合物隔夜。添加額外氫氧化鈉水溶液(1.04 mmol),且在室溫攪拌混合物3天。反應混合物用水處理,且添加鹽酸水溶液(1 M)以將pH調整至5,且隨後其用二氯甲烷萃取三次。減壓濃縮有機層,得到36 mg (21%產率)標題化合物。
水層藉由添加鹽酸水溶液(1 M)調整至pH 3,所形成沈澱藉由過濾分離,用水洗滌且藉由凍乾乾燥,得到90 mg (53%產率)標題化合物。
1
H NMR (400 MHz, DMSO-d 6
): δ ppm = 1.15 (d,J
=7.35 Hz, 3 H), 1.51 (s, 6 H), 4.94 - 5.14 (m, 1 H), 6.73 - 6.79 (m, 2 H), 7.22 - 7.26 (m, 1 H), 7.30 - 7.37 (m, 2 H), 7.42 - 7.47 (m, 2 H), 7.58 (br s, 1 H), 7.64 (dd,J
=8.87, 5.07 Hz, 2 H), 7.77 - 8.44 (m, 2 H), 12.81 - 13.47 (m, 1 H)
LC-MS (方法1)Rt = 1.00 min; MS (ESIpos): m/z = 487.5 [M+H]+
(4-胺基-2-苯胺基-1,3-噻唑-5-基)(苯基)甲酮(100 mg,339 µmol,中間物61)提供於在室溫之二氯甲烷中。添加N,N-二異丙基乙基胺(180 µl,1.0 mmol;CAS-RN 7087-68-5), 4-(二甲基胺基)吡啶(8 mg,67.7 µmol;CAS-RN 1122-58-3)及二碳酸二三級丁酯(81 mg,372 µmol;CAS-RN 24424-99-5)。在室溫攪拌反應混合物3 h。混合物用二氯甲烷稀釋,用鹽水洗滌,乾燥且蒸發,得到120 mg (95%純度,85%產率)標題化合物。
1
H-NMR (400 MHz, DMSO-d 6
): δ ppm = 1.32 (s, 9 H), 7.35 - 7.44 (m, 3 H), 7.45 - 7.51 (m, 2 H), 7.52 - 7.58 (m, 3 H), 7.69 - 7.73 (m, 2 H), 7.94 (s, 2 H)。
以下中間物由下表3中陳述之起始材料,使用關於中間物83之程序製備。
必要時,在沈澱、萃取或過濾反應混合物之後,藉由RP-HPLC (方法A至D,視極性而定)或藉由製備型急驟層析(方法X、Y或Z,視極性而定)純化粗產物。
表3:中間物84至96
| 中間物編號 | 化學結構 化學名稱 | 起始材料 | 分析/純化/產率 |
| 84 | N-(4-胺基-5-苯甲醯基-噻唑-2-基)-N-(4-氟苯基)胺基甲酸三級丁酯 | 中間物62; 二碳酸二三級丁酯 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.34 (s, 9 H), 7.31 (t,J =8.87 Hz, 2 H), 7.44 - 7.48 (m, 2 H), 7.50 - 7.59 (m, 3 H), 7.68 - 7.74 (m, 2 H), 7.93 (s, 2 H)。 91%產率 |
| 85 | N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-N-(4-氟苯基)胺基甲酸三級丁酯 | 中間物63; 二碳酸二三級丁酯 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.35 (s, 9 H), 3.84 (s, 3 H), 7.05 - 7.10 (m, 2 H), 7.31 (t,J =8.74 Hz, 2 H), 7.46 (dd,J =8.87, 5.07 Hz, 2 H), 7.73 (d,J =8.87 Hz, 2 H), 7.86 (s, 2 H)。 94%產率 |
| 86 | N-[4-胺基-5-(4-甲基苯甲醯基)噻唑-2-基]-N-(4-氟苯基)胺基甲酸三級丁酯 | 中間物64; 二碳酸二三級丁酯 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.34 (s, 9 H), 2.39 (s, 3 H), 7.31 (s, 4 H), 7.44 - 7.48 (m, 2 H), 7.61 (s, 2 H), 7.89 (s, 2 H)。 79%產率 |
| 87 | N-[4-胺基-5-(4-氟苯甲醯基)噻唑-2-基]-N-(4-氟苯基)胺基甲酸三級丁酯 | 中間物65; 二碳酸二三級丁酯 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.34 (s, 9 H), 7.31 (t,J =8.87 Hz, 2 H), 7.37 (t,J =9.00 Hz, 2 H), 7.46 (dd,J =9.12, 5.07 Hz, 2 H), 7.79 (dd,J =8.87, 5.58 Hz, 2 H), 7.95 (s, 2 H)。 定量產率 |
| 88 | N-(4-胺基-5-苯甲醯基-噻唑-2-基)-N-(2,4-二氟苯基)胺基甲酸三級丁酯 | 中間物66; 二碳酸二三級丁酯 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.35 (s, 9 H), 7.22 - 7.27 (m, 1 H), 7.49 - 7.57 (m, 4 H), 7.67 - 7.74 (m, 3 H), 7.95 (s, 2 H)。 69%產率 |
| 89 | N-(4-胺基-5-苯甲醯基-噻唑-2-基)-N-(4-甲氧基苯基)胺基甲酸三級丁酯 | 中間物67; 二碳酸二三級丁酯 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.34 (s, 9 H), 3.80 (s, 3 H), 6.98 - 7.02 (m, 2 H), 7.25 - 7.30 (m, 2 H), 7.50 - 7.58 (m, 3 H), 7.68 - 7.74 (m, 2 H), 7.93 (s, 2 H)。 91%產率 |
| 90 | N-[4-胺基-5-[4-[三級丁基(二甲基)矽基]氧基苯甲醯基]噻唑-2-基]-N-(4-氟苯基)胺基甲酸三級丁酯 | 中間物68; 二碳酸二三級丁酯 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 0.25 (s, 6 H), 0.96 - 0.99 (m, 9 H), 1.35 (s, 9 H), 6.99 (d,J =8.62 Hz, 2 H), 7.28 - 7.34 (m, 2 H), 7.46 (dd,J =8.87, 5.07 Hz, 2 H), 7.69 (d,J =8.87 Hz, 2 H), 7.88 (s, 2 H)。 92%產率 |
| 91 | N-(4-胺基-5-苯甲醯基-噻唑-2-基)-N-(對甲苯基)胺基甲酸三級丁酯 | 中間物69; 二碳酸二三級丁酯 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.33 (s, 9 H), 2.36 (s, 3 H), 7.25 (d,J =9.38 Hz, 4 H), 7.54 (s, 3 H), 7.69 - 7.74 (m, 2 H), 7.93 (s, 2 H)。 85%產率 |
| 92 | N-(4-胺基-5-苯甲醯基-噻唑-2-基)-N-(3-氟苯基)胺基甲酸三級丁酯 | 中間物70; 二碳酸二三級丁酯 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.34 (s, 9 H), 7.22 - 7.32 (m, 2 H), 7.43 (br dt,J =9.76, 2.22 Hz, 1 H), 7.48 - 7.60 (m, 4 H), 7.69 - 7.74 (m, 2 H), 7.95 (s, 2 H)。 99%產率 |
| 93 | N-(4-胺基-5-苯甲醯基-噻唑-2-基)-N-(2-氟苯基)胺基甲酸三級丁酯 | 中間物71; 二碳酸二三級丁酯 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.34 (s, 9 H), 7.33 (td,J =7.67, 1.39 Hz, 1 H), 7.41 (ddd,J =10.01, 8.49, 1.27 Hz, 1 H), 7.47 - 7.60 (m, 5 H), 7.70 - 7.75 (m, 2 H), 7.95 (s, 2 H)。 88%產率 |
| 94 | N-(4-胺基-5-苯甲醯基-噻唑-2-基)-N-(1-甲基吡唑-4-基)胺基甲酸三級丁酯 | 中間物74; 二碳酸二三級丁酯 | ¹H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.39 (s, 9 H), 3.85 (s, 3 H), 7.49 - 7.57 (m, 4 H), 7.68 - 7.73 (m, 2 H), 7.92 (s, 1 H), 7.98 (s, 2 H)。 89%產率 |
| 95 | N-(4-胺基-5-苯甲醯基-噻唑-2-基)-N-(3-吡啶基)胺基甲酸三級丁酯 | 中間物75; 二碳酸二三級丁酯 | ¹H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.34 (s, 9 H), 7.49 - 7.61 (m, 4 H), 7.68 - 7.75 (m, 2 H), 7.90 - 7.97 (m, 3 H), 8.60 (dd,J =4.56, 1.52 Hz, 1 H), 8.63 (dd,J =2.54, 0.51 Hz, 1 H)。 LC-MS (方法2)Rt = 1.24 min; MS (ESIpos): m/z = 397.5 [M+H]+ 85%產率 |
| 96 | N-[4-胺基-5-(4-溴苯甲醯基)噻唑-2-基]-N-(4-氟苯基)胺基甲酸三級丁酯 | 中間物76; 二碳酸二三級丁酯 | ¹H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.34 (s, 9 H), 7.31 (t,J =8.74 Hz, 2 H), 7.44 - 7.48 (m, 2 H), 7.64 - 7.68 (m, 2 H), 7.73 - 7.77 (m, 2 H), 7.98 (s, 2 H)。 LC-MS (方法2)Rt = 1.53 min; MS (ESIpos): m/z = 492.5 [M+H]+ 製備型急驟層析(方法Z,0-3%) 92%產率 |
4-羥基苯甲醯甲基溴(2.50 g,11.6 mmol)提供於THF (50 mL)中。向此溶液中添加氫化鈉(511 mg,60%於礦物油中,12.8 mmol),且在室溫攪拌懸浮液1 h,其後逐滴添加氯甲基甲基醚(1.1 mL,13.9 mmol)。在室溫攪拌懸浮液72 h。反應藉由添加氯化銨飽和水溶液終止且用二氯甲烷萃取。有機物用鹽水洗滌,經硫酸鎂乾燥,過濾且真空濃縮,得到棕色油。藉由正相管柱層析(10-80% EtOAc/庚烷)純化殘餘物,得到1.161 g (39%產率)呈淺黃色油狀之標題化合物。
1
H-NMR (CDCl3, 400 MHz): δ ppm = 3.48 (s, 3H); 4.40 (s, 2H); 5.23 (s, 2H); 7.09 (d, 2H); 7.96 (d, 2H)
LC-MS (方法2):Rt = 0.79 min; MS(ESIpos) m/z = 260 [M+H]+
提供無水乙腈(65 mL),且添加異硫氰酸苯酯(350 µl,2.9 mmol;CAS-RN 103-72-0)、氰胺(146 mg,3.47 mmol;CAS-RN 420-04-2)及1,8-二氮雜雙環[5.4.0]十一碳-7-烯(0.75 mL,5.1 mmol;CAS-RN 6674-22-2),且在室溫攪拌溶液45 min,其後添加另外1,8-二氮雜雙環(5.4.0)十一碳-7-烯(0.75 mL,5.1 mmol),隨後添加2-溴-1-[4-(甲氧基甲氧基)苯基]乙-1-酮(750 mg,2.89 mmol於10 mL乙腈中;中間物97)。在室溫攪拌溶液1.5 h。將混合物分配於乙酸乙酯與飽和碳酸氫鈉水溶液之間。有機物用鹽水洗滌,且添加二氧化矽。真空濃縮懸浮液。藉由正相管柱層析(10-80% EtOAc/庚烷)純化殘餘物,得到669 mg (65%產率)呈黃色固體狀之標題化合物。
LC-MS (方法2):Rt = 0.81 min; MS(ESIpos) m/z = 356 [M+H]+
1
H-NMR (CDCl3, 400 MHz): δ ppm = 3.49 (s, 3H); 5.20 (s, 2H); 7.05 (d, 2H); 7.19 (t, 1H); 7.33-7.43 (m, 4H); 7.73 (d, 2H); 8.46 (br s, 1H);未觀測到NH2。
提供無水乙腈(25 mL),且添加異硫氰酸4-氟苯酯(296 mg,1.93 mmol)、氰胺(97.4 mg,2.32 mmol;CAS-RN 420-04-2)及1,8-二氮雜雙環(5.4.0)十一碳-7-烯(0.5 mL,3.4 mmol;CAS-RN 6674-22-2),且在室溫攪拌溶液45 min,其後添加另外1,8-二氮雜雙環(5.4.0)十一碳-7-烯(0.5 mL,3.4 mmol),隨後添加2-溴-1-[4-(甲氧基甲氧基)苯基]乙-1-酮(500 mg,1.93 mmol於10 mL乙腈中;中間物98)。在室溫攪拌溶液18 h。將混合物真空蒸發至乾燥,將其分配於水與乙酸乙酯之間且萃取至乙酸乙酯中。將有機層合併且用飽和碳酸氫鈉水溶液及鹽水洗滌,接著經硫酸鎂乾燥,之後過濾。添加二氧化矽,且使懸浮液蒸發。藉由正相管柱層析(15-100% EtOAc/庚烷)純化此物質,得到620 mg (72%產率)標題化合物。
1
H-NMR (DMSO-d6, 400 MHz): δ ppm = 3.43 (s, 3H); 5.29 (s, 2H); 7.12 (d, 2H); 7.25 (2H, t); 7.64-7.72 (m, 4H); 8.20 (br s, 2H); 10.79 (s, 1H)。
LC-MS (方法2):Rt = 0.81 min; MS(ESIpos) m/z = 374 [M+H]+
向外消旋-2-[4-[4-胺基-2-(4-氟-N-[2-胺基-1-甲基-2-側氧基-乙基]苯胺基)噻唑-5-羰基]苯氧基]乙酸乙酯(24 mg,0.05 mmol;實例81)於四氫呋喃(2 mL)中之溶液中,添加氫氧化鈉水溶液(0.1 mL,1 M)。在室溫攪拌反應混合物隔夜。
反應混合物用水稀釋,逐滴添加鹽酸水溶液(1 M)以將pH調整至3,且之後用二氯甲烷萃取混合物。有機層用鹽水洗滌,經由拒水過濾圈(MN 617 WA)過濾且蒸發至乾燥。將殘餘物溶解於乙腈/水(1:1)中且藉由凍乾乾燥,得到15 mg (63%產率)標題化合物。
1
H-NMR (400 MHz, DMSO-d 6
): δ ppm = 1.16 (d,J
=7.35 Hz, 3 H), 4.68 (s, 2 H), 5.05 (br q,J
=7.44 Hz, 1 H), 6.89 (d,J
=8.87 Hz, 2 H), 7.24 (s, 1 H), 7.33 (t,J
=8.74 Hz, 2 H), 7.47 (d,J
=8.87 Hz, 2 H), 7.58 (s, 1 H), 7.64 (dd,J
=8.87, 5.07 Hz, 2 H), 8.08 (br s, 2 H), 13.02 (br s, 1 H)。
LC-MS (方法1)Rt = 0.87 min; MS (ESIpos): m/z = 459.5 [M+H]+
中間物 100.1
及100.2 :
(R)-2-[4-[4-胺基-2-(N-[2-胺基-1-甲基-2-側氧基-乙基]-4-氟-苯胺基)噻唑-5-羰基]苯氧基]乙酸及(S)-2-[4-[4-胺基-2-(N-[2-胺基-1-甲基-2-側氧基-乙基]-4-氟-苯胺基)噻唑-5-羰基]苯氧基]乙酸
向2-[4-[4-胺基-2-(4-氟-N-[2-胺基-1-甲基-2-側氧基-乙基]苯胺基)噻唑-5-羰基]苯氧基]乙酸乙酯(鏡像異構物1) (2.50 g,5.14 mmol,實例81.1)於四氫呋喃(26.3 mL)中之冰冷卻溶液中,添加氫氧化鈉水溶液(5.1 mL,1 M)。在室溫攪拌混合物隔夜。
反應混合物用水稀釋,逐滴添加鹽酸水溶液(1 M)以將pH調整至3,且之後用二氯甲烷處理混合物。所得沈澱藉由過濾分離,用水及一定量的二氯甲烷洗滌且藉由凍乾乾燥,得到1.48 g (62%產率)標題化合物。
向2-[4-[4-胺基-2-(4-氟-N-[2-胺基-1-甲基-2-側氧基-乙基]苯胺基)噻唑-5-羰基]苯氧基]乙酸乙酯(鏡像異構物2) (2.60 g,5.34 mmol;實例81.2)於四氫呋喃(27.3 mL)中之冰冷卻溶液中,添加氫氧化鈉水溶液(5.3 mL,1 M)。在室溫攪拌混合物隔夜。
反應混合物用水稀釋,逐滴添加鹽酸水溶液(1 M)以將pH調整至3,且之後用二氯甲烷處理混合物。所得沈澱藉由過濾分離,用水及一定量的二氯甲烷洗滌且藉由凍乾乾燥,得到0.95 g (37%產率)標題化合物。
分離濾液之有機層,用鹽水洗滌,經由拒水過濾圈(MN 617 WA)過濾且蒸發至乾燥,得到另外695 mg (28%產率)標題化合物。
以下中間物由下表4中陳述之商業起始材料,使用關於中間物4之程序製備,隨後藉由層析純化(若需要)。若未指明純化,則各別標題化合物作為粗產物分離。
必要時,粗產物藉由RP-HPLC (方法A至D,視極性而定)或藉由製備型急驟層析(方法X、Y或Z,視極性而定)純化。在缺少沈澱之情況下,反應混合物用乙酸乙酯萃取三次。經合併之有機相經硫酸鈉乾燥,過濾且蒸發至乾燥。藉由如表4中所陳述之層析純化粗產物。
表4:中間物101至197
| 中間物編號 | 化學結構 化學名稱 | 起始材料 | 分析/純化/產率 |
| 101 | [4-胺基-2-(4-氟苯胺基)噻唑-5-基]-[6-(二氟甲基)-3-吡啶基]甲酮 | 1-氟-4-異硫氰基-苯; 2-溴-1-[6-(二氟甲基)-3-吡啶基]乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 7.03 (t, J=60 Hz, 1 H), 7.23 (t,J =8.87 Hz, 2 H), 7.64 (dd,J =9.12, 4.82 Hz, 2 H), 7.81 (d,J =8.11 Hz, 1 H), 8.22 (dd,J =7.98, 2.15 Hz, 1 H), 8.35 - 8.40 (m, 2 H), 8.92 (d,J =1.52 Hz, 1 H), 10.94 (s, 1 H)。 LC-MS (方法1)Rt = 1.08 min; MS (ESIpos): m/z = 365.2 [M+H]+ 71%產率 |
| 102 | [4-胺基-2-(3-氯-4-氟-苯胺基)噻唑-5-基]-(4-吡啶基)甲酮 | 2-氯-1-氟-4-異硫氰基-苯;2-溴-1-(4-吡啶基)乙酮;氫溴酸鹽 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 7.22 (ddd,J =8.87, 4.56, 2.53 Hz, 1 H), 7.33 - 7.37 (m, 1 H), 7.47 (dd,J =6.84, 2.53 Hz, 1 H), 7.57 - 7.62 (m, 2 H), 8.41 (s, 1 H), 8.50 - 8.55 (m, 2 H)。 LC-MS (方法2)Rt = 0.81 min; MS (ESIpos): m/z = 349.2 [M+H]+ 65%產率 |
| 103 | [4-胺基-2-(3-氯-4-氟-苯胺基)噻唑-5-基]-4-甲氧基苯基)甲酮 | 2-氯-1-氟-4-異硫氰基-苯; 2-溴-1-(4-甲氧基苯基)乙酮 | 1 H NMR (400 MHz, DMSO-d6 ) δ ppm = 3.79 - 3.84 (m, 3 H), 7.00 (d, 2 H), 7.32 - 7.43 (m, 2 H), 7.66 (d, 2 H), 7.88 - 7.98 (m, 1 H), 8.05 - 8.34 (m, 1 H)。 LC-MS (方法2)Rt = 1.14 min; MS (ESIpos): m/z = 378.3 [M+H]+ 96%產率 |
| 104 | [4-胺基-2-(4-氟苯胺基)噻唑-5-基]-[6-(二氟甲氧基)-3-吡啶基]甲酮 | 1-氟-4-異硫氰基苯; 2-溴-1-[6-(二氟甲氧基)吡啶-3-基]乙酮 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 7.15 - 7.26 (m, 3 H), 7.61 - 7.68 (m, 2 H), 7.77 (t, 1H), 8.12 - 8.19 (m, 1 H), 8.21 - 8.40 (m, 2 H), 8.53 - 8.57 (m, 1 H), 10.90 (br s, 1 H)。 LC-MS (方法2)Rt = 1.03 min; MS (ESIpos): m/z = 381.2 [M+H]+ 73%產率 |
| 105 | [4-胺基-2-(3,4-二氟苯胺基)噻唑-5-基]-[6-(二氟甲氧基)-3-吡啶基]甲酮 | 1,2-二氟-4-異硫氰基-苯; 2-溴-1-[6-(二氟甲氧基)吡啶-3-基]乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 7.16 - 7.20 (m, 1 H), 7.24 (br d,J =8.87 Hz, 1 H), 7.43 (d,J =10.39 Hz, 1 H), 7.78 (t,J =72 Hz, 1 H), 7.90 - 7.94 (m, 1 H), 8.17 (dd,J =8.36, 2.53 Hz, 1 H), 8.28 - 8.33 (m, 2 H), 8.56 (d,J =1.77 Hz, 1 H), 11.05 (br s, 1 H)。 LC-MS (方法2)Rt = 1.02 min; MS (ESIpos): m/z = 399.2 [M+H]+ 63%產率 |
| 106 | [4-胺基-2-(4-氯-3-氟-苯胺基)噻唑-5-基]-[6-(二氟甲氧基)-3-吡啶基]甲酮 | 1-氯-2-氟-4-異硫氰基苯;2-溴-1-[6-(二氟甲氧基)吡啶-3-基]乙酮 | LC-MS (方法2)Rt = 1.03 min; MS (ESIpos): m/z = 415.2 [M+H]+ 57%產率 |
| 107 | [4-胺基-2-(3,4-二氟苯胺基)-1,3-噻唑-5-基][4-(苯甲氧基)苯基]甲酮 | 1,2-二氟-4-異硫氰基-苯; 1-[4-(苯甲氧基)苯基]-2-溴乙酮 | LC-MS (方法2)Rt = 1.29 min; MS (ESIpos): m/z = 438.3 [M+H]+ 71%產率 |
| 108 | [4-胺基-2-(4-氯-3-氟-苯胺基)噻唑-5-基]-(4-苯甲氧基苯基)甲酮 | 1-氯-2-氟-4-異硫氰基苯;1-[4-(苯甲氧基)苯基]-2-溴乙酮 | LC-MS (方法2)Rt = 1.35 min; MS (ESIpos): m/z = 454.3 [M+H]+ 94%產率 |
| 109 | (4-{[4-胺基-2-(3,4-二氟苯胺基)-1,3-噻唑-5-基]羰基}苯基)胺基甲酸苯甲酯 | 1,2-二氟-4-異硫氰基-苯;N-[4-(2-溴乙醯基)苯基]胺基甲酸苯甲酯 | LC-MS (方法2)Rt = 1.18 min; MS (ESIpos): m/z = 481.3 [M+H]+ 78%產率 |
| 110 | [4-胺基-2-(4-氟苯胺基)噻唑-5-基]-(4-苯甲氧基苯基)甲酮 | 1-氟-4-異硫氰基苯;1-[4-(苯甲氧基)苯基]-2-溴乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 5.17 (s, 2 H), 7.06 - 7.10 (m, 2 H), 7.19 - 7.23 (m, 2 H), 7.39 - 7.43 (m, 5 H), 7.62 - 7.67 (m, 4 H), 8.11 - 8.15 (m, 2 H), 10.75 (br s, 1 H) LC-MS (方法2)Rt = 1.30 min; MS (ESIpos): m/z = 420.2 [M+H]+ 86%產率 |
| 111 | [4-胺基-2-(4-氟苯胺基)噻唑-5-基]-(4-碘苯基)甲酮 | 1-氟-4-異硫氰基苯;2-溴-1-(4-碘苯基)乙酮 | LC-MS (方法2)Rt = 1.21 min; MS (ESIpos): m/z = 440.1 [M+H]+ 82%產率 |
| 112 | 2-[4-[4-胺基-2-(4-氟苯胺基)噻唑-5-羰基]苯氧基]乙酸乙酯 | 1-氟-4-異硫氰基苯;乙酸2-[4-(溴乙醯基)苯氧基]乙酯(中間物198) | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 3.73 (q,J =5.15 Hz, 2 H), 4.03 - 4.07 (m, 2 H), 4.91 (t,J =5.45 Hz, 1 H), 7.00 - 7.05 (m, 3 H), 7.19 - 7.23 (m, 2 H), 7.60 - 7.65 (m, 5 H), 8.15 - 8.19 (m, 2 H), 10.74 - 10.76 (m, 1 H)。 LC-MS (方法2)Rt = 1.06 min; MS (ESIpos): m/z = 416.3 [M+H]+ 11%產率 |
| 113 | [4-胺基-2-(4-氯-3-氟苯胺基)-1,3-噻唑-5-基](6-甲氧基吡啶-3-基)甲酮 | 1-氯-2-氟-4-異硫氰基苯;2-溴-1-(6-甲氧基-3-吡啶基)乙酮 | LC-MS (方法2)Rt = 1.05 min; MS (ESIpos): m/z = 379.2 [M+H]+ 100%產率 |
| 114 | [4-胺基-2-(4-氟苯胺基)噻唑-5-基]-(4-苯氧基苯基)甲酮 | 1-氟-4-異硫氰基苯;2-溴-1-(4-苯氧基苯基)乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 7.02 - 7.06 (m, 2 H), 7.09 - 7.13 (m, 2 H), 7.19 - 7.23 (m, 3 H), 7.43 - 7.47 (m, 2 H), 7.61 - 7.65 (m, 2 H), 7.69 - 7.71 (m, 2 H), 8.19 - 8.21 (m, 2 H), 10.77 (br s, 1 H) LC-MS (方法2)Rt = 1.27 min; MS (ESIpos): m/z = 406.2 [M+H]+ 84%產率 |
| 115 | 4-胺基-2-(4-甲氧基苯胺基)噻唑-5-基]-[4-(二氟甲氧基)苯基]甲酮 | 1-異硫氰基-4-甲氧基苯;2-溴-1-[4-(二氟甲氧基)苯基]乙酮 | 1 H NMR (500 MHz, DMSO-d 6 ) δ ppm = 3.73 - 3.76 (m, 3 H), 6.93 - 6.96 (m, 2 H), 7.22 - 7.26 (m, 2 H), 7.33 (t, 1 H), 7.45 - 7.48 (m, 2 H), 7.70 - 7.73 (m, 2 H), 8.19 - 8.21 (m, 2 H), 10.63 (m, 1 H) LC-MS (方法2)Rt = 1.27 min; MS (ESIpos): m/z = 406.2 [M+H]+ 57%產率 |
| 116 | [4-胺基-2-(4-氟苯胺基)噻唑-5-基]-(4-硝基苯基)甲酮 | 1-氟-4-異硫氰基苯;2-溴-1-(4-硝基苯基)乙酮 | LC-MS (方法2)Rt = 0.95 min; MS (ESIpos): m/z = 359.1 [M+H]+ 81%產率 |
| 117 | [2-(4-氟苯胺基)-4-甲基-1,3-噻唑-5-基](4-甲氧基苯基)甲酮 | 1-氟-4-異硫氰基苯;乙酸乙脒(1:1);2-溴-1-(4-甲氧基苯基)乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 2.34 (s, 3 H), 3.84 (s, 3 H), 7.05 (m, 2 H), 7.21 (m, 2 H), 7.64 (m, 2 H), 7.71 (m, 2 H), 10.76 (s, 1 H) LC-MS (方法2)Rt = 1.24 min; MS (ESIpos): m/z = 343.2 [M+H]+ 8%產率 |
| 118 | N-[4-[4-胺基-2-(4-氟苯胺基)噻唑-5-羰基]苯基]環丙烷甲醯胺 | 1-氟-4-異硫氰基苯;N-[4-(溴乙醯基)苯基]環丙烷甲醯胺 | LC-MS (方法2)Rt = 0.77 min; MS (ESIpos): m/z = 397.3 [M+H]+ 69%產率 |
| 119 | [4-胺基-2-(4-氟苯胺基)噻唑-5-基]-(4-(N-𠰌啉基)苯基)甲酮 | 1-氟-4-異硫氰基苯;2-溴-1-[4-(𠰌啉-4-基)苯基]乙酮 | LC-MS (方法2)Rt = 1.04 min; MS (ESIpos): m/z = 399.2 [M+H]+ 66%產率 |
| 120 | [4-胺基-2-(4-氟苯胺基)-1,3-噻唑-5-基][4-(1H-吡唑-1-基甲基)苯基]甲酮 | 1-氟-4-異硫氰基苯;2-溴-1-{4-[(1H-吡唑-1-基)甲基]苯基}乙-1-酮,溴化氫 | LC-MS (方法2)Rt = 1.01 min; MS (ESIpos): m/z = 394.3 [M+H]+ 64%產率 |
| 121 | [4-胺基-2-(4-氟苯胺基)-1,3-噻唑-5-基][4-(二甲基胺基)苯基]甲酮 | 1-氟-4-異硫氰基苯;4-(二甲基胺基)苯甲醯甲基溴 | LC-MS (方法2)Rt = 1.16 min; MS (ESIpos): m/z = 357.3 [M+H]+ 86%產率 |
| 122 | [4-胺基-2-(4-氟苯胺基)噻唑-5-基]-(4-吡咯啶-1-基苯基)甲酮 | 1-氟-4-異硫氰基苯;2-溴-1-[4-(吡咯啶-1-基)苯基]乙酮 | LC-MS (方法2)Rt = 1.26 min; MS (ESIpos): m/z = 383.2 [M+H]+ 84%產率 |
| 123 | [4-胺基-2-(4-苯甲氧基苯胺基)噻唑-5-基]-[4-(二氟甲氧基)苯基]甲酮 | 1-(苯甲氧基)-4-異硫氰基苯;2-溴-1-[4-(二氟甲氧基)苯基]乙酮 | LC-MS (方法2)Rt = 1.32 min; MS (ESIpos): m/z = 468.3 [M+H]+ 89%產率 |
| 124 | [4-胺基-2-(4-氟苯胺基)-1,3-噻唑-5-基][3-(二氟甲氧基)苯基]甲酮 | 1-氟-4-異硫氰基苯;2-溴-1-[3-(二氟甲氧基)苯基]乙酮(中間物199) | LC-MS (方法2)Rt = 1.10 min; MS (ESIpos): m/z = 380.2 [M+H]+ 91%產率 |
| 125 | [4-胺基-2-(3,4-二氟苯胺基)-1,3-噻唑-5-基](吡啶-3-基)甲酮 | 1,2-二氟-4-異硫氰基苯;2-溴-1-(吡啶-3-基)乙酮氫溴酸鹽(1:1) | LC-MS (方法2)Rt = 0.77 min; MS (ESIpos): m/z = 333.2 [M+H]+ 88%產率 |
| 126 | N-(4-{[4-胺基-2-(4-氟苯胺基)-1,3-噻唑-5-基]羰基}苯基)乙醯胺 | 1-氟-4-異硫氰基苯;4-乙醯胺基苯甲醯甲基溴 | LC-MS (方法2)Rt = 0.87 min; MS (ESIpos): m/z = 371.3 [M+H]+ 58%產率 |
| 127 | [4-胺基-2-(4-氟苯胺基)-1,3-噻唑-5-基](2-氯吡啶-4-基)甲酮 | 1-氟-4-異硫氰基苯;2-溴-1-(2-氯吡啶-4-基)乙酮 | LC-MS (方法2)Rt = 0.86 min; MS (ESIpos): m/z = 349.2 [M+H]+ 88%產率 |
| 128 | [4-胺基-2-(4-氟苯胺基)噻唑-5-基]-(2-甲基-4-吡啶基)甲酮 | 1-氟-4-異硫氰基苯;2-溴-1-(2-甲基吡啶-4-基)乙酮氫溴酸鹽(1:1) | LC-MS (方法2)Rt = 0.80 min; MS (ESIpos): m/z = 329.2 [M+H]+ 80%產率 |
| 129 | [4-胺基-2-(4-氟苯胺基)-1,3-噻唑-5-基][2-(二氟甲基)吡啶-4-基]甲酮 | 1-氟-4-異硫氰基苯;2-溴-1-[2-(二氟甲基)-4-吡啶基]乙酮 | LC-MS (方法2)Rt = 0.87 min; MS (ESIpos): m/z = 365.2 [M+H]+ 78%產率 |
| 130 | [4-胺基-2-(吡啶-4-基胺基)-1,3-噻唑-5-基](苯基)甲酮 | 4-異硫氰基吡啶;2-溴-1-苯基乙酮 | LC-MS (方法2)Rt = 0.69 min; MS (ESIpos): m/z = 297.2 [M+H]+ 17%產率 |
| 131 | [4-胺基-2-(4-氟苯胺基)噻唑-5-基]-(2-甲氧基-4-吡啶基)甲酮 | 1-氟-4-異硫氰基苯;2-溴-1-(2-甲氧基吡啶-4-基)乙酮 | LC-MS (方法2)Rt = 0.91 min; MS (ESIpos): m/z = 345.2 [M+H]+ 80%產率 |
| 132 | (4-{[4-胺基-2-(4-氟苯胺基)-1,3-噻唑-5-基]羰基}苯基)胺基甲酸苯甲酯 | 1-氟-4-異硫氰基苯;N-[4-(2-溴乙醯基)苯基]胺基甲酸苯甲酯 | LC-MS (方法2)Rt = 1.20 min; MS (ESIpos): m/z = 463.3 [M+H]+ 72%產率 |
| 133 | [4-胺基-2-(3-氟-4-甲氧基苯胺基)-1,3-噻唑-5-基](苯基)甲酮 | 2-氟-4-異硫氰基-1-甲氧基苯;2-溴-1-苯基乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 10.75 (s, 1H), 8.23 (br s, 2H), 7.68-7.75 (m, 1H), 7.64-7.68 (m, 2H), 7.44-7.52 (m, 3H), 7.13-7.22 (m, 2H), 3.82 (s, 3H)。 LC-MS (方法2)Rt = 1.08 min MS (ESIpos): m/z = 344.6 [M+H]+ 96%產率 |
| 134 | 4-[(4-胺基-5-苯甲醯基-1,3-噻唑-2-基)胺基]-2-氟苯甲腈 | 2-氟-4-異硫氰基苯甲腈; 2-溴-1-苯基乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 11.42 (br s, 1H), 8.28 (br s, 2H), 8.10 (dd, J = 12.5, 1.9 Hz, 1H), 7.86 (dd, J = 8.6, 7.9 Hz, 1H), 7.67-7.72 (m, 2H), 7.46-7.56 (m, 3H), 7.39 (dd, J = 8.6, 2.0 Hz, 1H)。 LC-MS (方法2)Rt = 0.9 min MS (ESIpos): m/z = 339.5 [M+H]+ 87%產率 |
| 135 | [4-胺基-2-(4-溴苯胺基)-1,3-噻唑-5-基](苯基)甲酮 | 1-溴-4-異硫氰基苯; 2-溴-1-苯基乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 10.89 (br s, 1H), 8.22 (br s, 2H), 7.64-7.70 (m, 2H), 7.57-7.64 (m, 2H), 7.44-7.57 (m, 5H)。 LC-MS (方法2)Rt = 1.18 min MS (ESIpos): m/z = 375.2 [M+H]+ 100%產率 |
| 136 | {4-胺基-2-[3-氯-4-(二氟甲氧基)苯胺基]-1,3-噻唑-5-基}(苯基)甲酮 | 2-氯-1-(二氟甲氧基)-4-異硫氰基苯; 2-溴-1-苯基乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 10.97 (br s, 1H), 8.26 (br s, 2H), 8.05 (d, J = 2.5 Hz, 1H), 7.64-7.70 (m, 2H), 7.45-7.54 (m, 4H), 7.36 (d, J = 8.9 Hz, 1H), 7.20 (t, J = 73.3 Hz, 1H)。 LC-MS (方法2)Rt = 1.14 min MS (ESIpos): m/z = 396.3 [M+H]+ 92%產率 |
| 137 | [4-胺基-2-(4-乙氧基苯胺基)-1,3-噻唑-5-基](苯基)甲酮 | 1-乙氧基-4-異硫氰基苯; 2-溴-1-苯基乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 10.58 (br s, 1H), 7.69-8.55 (m, 2H), 7.60-7.66 (m, 2H), 7.40-7.51 (m, 5H), 6.88-6.95 (m, 2H), 4.00 (q, J = 7.1 Hz, 2H), 1.31 (t, J = 7.0 Hz, 3H)。 LC-MS (方法2)Rt = 1.14 min MS (ESIpos): m/z = 340.4 [M+H]+ 100%產率 |
| 138 | [4-胺基-2-(1,3-苯并間二氧雜環戊烯-5-基胺基)-1,3-噻唑-5-基](苯基)甲酮 | 5-異硫氰基-1,3-苯并間二氧雜環戊烯; 2-溴-1-苯基乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 10.64 (s, 1H), 8.20 (br s, 2H), 7.62-7.67 (m, 2H), 7.43-7.52 (m, 3H), 7.32-7.37 (m, 1H), 6.88-6.95 (m, 2H), 6.02 (s, 2H)。 LC-MS (方法2)Rt = 0.99 min MS (ESIpos): m/z = 340.2 [M+H]+ 57%產率 |
| 139 | {4-胺基-2-[(2,2-二氟-1,3-苯并間二氧雜環戊烯-5-基)胺基]-1,3-噻唑-5-基}(苯基)甲酮 | 2,2-二氟-5-異硫氰基-1,3-苯并間二氧雜環戊烯; 2-溴-1-苯基乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 10.95 (br s, 1H), 8.24 (br s, 2H), 7.94 (d, J = 2.0 Hz, 1H), 7.64-7.69 (m, 2H), 7.45-7.53 (m, 3H), 7.40 (d, J = 8.6 Hz, 1H), 7.24 (dd, J = 8.7, 2.2 Hz, 1H)。 LC-MS (方法2)Rt = 1.17 min MS (ESIpos): m/z = 376.4 [M+H]+ 78%產率 |
| 140 | {4-胺基-2-[4-(二氟甲氧基)-3-氟苯胺基]-1,3-噻唑-5-基}(苯基)甲酮 | 1-(二氟甲氧基)-2-氟-4-異硫氰基苯; 2-溴-1-苯基乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 11.00 (s, 1H), 8.26 (br s, 2H), 7.97 (dd, J = 12.9, 2.5 Hz, 1H), 7.65-7.70 (m, 2H), 7.45-7.54 (m, 3H), 7.33-7.39 (m, 1H), 7.24-7.29 (m, 1H), 7.18 (t, J = 73.3 Hz, 1H)。 LC-MS (方法2)Rt = 1.08 min MS (ESIpos): m/z = 380.2 [M+H]+ 92%產率 |
| 141 | {4-胺基-2-[4-(苯甲氧基)苯胺基]-1,3-噻唑-5-基}(苯基)甲酮 | 1-(苯甲氧基)-4-異硫氰基苯; 2-溴-1-苯基乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 10.61 (br s, 1H), 8.17 (br s, 2H), 7.64 (dd, J = 7.6, 1.8 Hz, 2H), 7.42-7.50 (m, 7H), 7.36-7.42 (m, 2H), 7.30-7.36 (m, 1H), 6.99-7.04 (m, 2H), 5.09 (s, 2H)。 LC-MS (方法2)Rt = 1.3 min MS (ESIpos): m/z = 402.4 [M+H]+ 98%產率 |
| 142 | {4-胺基-2-[3-氯-4-(二氟甲氧基)苯胺基]-1,3-噻唑-5-基}(4-甲氧基苯基)甲酮 | 2-氯-1-(二氟甲氧基)-4-異硫氰基苯; 2-溴-1-(4-甲氧基苯基)乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 10.94 (br s, 1H), 8.21 (br s, 2H), 8.06 (d, J = 2.5 Hz, 1H), 7.66-7.71 (m, 2H), 7.48 (dd, J = 8.9, 2.5 Hz, 1H), 7.36 (d, J = 8.9 Hz, 1H), 7.20 (t, J = 73.8 Hz, 1H), 7.02-7.05 (m, 1H), 7.00-7.02 (m, 1H), 3.82 (s, 3H)。 LC-MS (方法2)Rt = 1.17 min MS (ESIpos): m/z = 426.2 [M+H]+ 99%產率 |
| 143 | {4-胺基-2-[3-氯-4-(二氟甲氧基)苯胺基]-1,3-噻唑-5-基}[4-(二氟甲氧基)苯基]甲酮 | 2-氯-1-(二氟甲氧基)-4-異硫氰基苯; 2-溴-1-[4-(二氟甲氧基)苯基]乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 11.00 (br s, 1H), 8.14-8.42 (m, 2H), 8.05 (d, J = 2.5 Hz, 1H), 7.73-7.78 (m, 2H), 7.48 (dd, J = 9.0, 2.7 Hz, 1H), 7.38 (d, J = 6.1 Hz, 1H), 7.35 (t, J = 73.8 Hz, 1H), 7.24-7.29 (m, 2H), 7.20 (t, J = 73.3 Hz, 1H)。 LC-MS (方法2)Rt = 1.15 min MS (ESIpos): m/z = 462.2 [M+H]+ 87%產率 |
| 144 | {4-胺基-2-[3-氯-4-(二氟甲氧基)苯胺基]-1,3-噻唑-5-基}(4-氯苯基)甲酮 | 2-氯-1-(二氟甲氧基)-4-異硫氰基苯; 2-溴-1-(4-氯苯基)乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 11.02 (br s, 1H), 8.31 (br s, 2H), 8.05 (d, J = 2.3 Hz, 1H), 7.67-7.72 (m, 2H), 7.53-7.58 (m, 2H), 7.47 (dd, J = 9.0, 2.7 Hz, 1H), 7.36 (d, J = 8.9 Hz, 1H), 7.20 (t, J = 73.5 Hz, 1H)。 LC-MS (方法2)Rt = 1.20 min MS (ESIpos): m/z = 430.2 [M+H]+ 100%產率 |
| 145 | {4-胺基-2-[3-氯-4-(二氟甲氧基)苯胺基]-1,3-噻唑-5-基}(吡啶-4-基)甲酮 | 2-氯-1-(二氟甲氧基)-4-異硫氰基苯; 2-溴-1-(吡啶-4-基)乙酮氫溴酸鹽 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 11.08 (br s, 1H), 8.70-8.74 (m, 2H), 8.42 (br s, 2H), 8.06 (d, J = 2.5 Hz, 1H), 7.56-7.60 (m, 2H), 7.46-7.51 (m, 1H), 7.37 (d, J = 9.1 Hz, 1H), 7.21 (t, J = 73.3 Hz, 1H)。 LC-MS (方法2)Rt = 0.82 min MS (ESIpos): m/z = 397.2 [M+H]+ 45%產率 |
| 146 | {4-胺基-2-[3-氯-4-(二氟甲氧基)苯胺基]-1,3-噻唑-5-基}[6-(二氟甲氧基)吡啶-3-基]甲酮 | 2-氯-1-(二氟甲氧基)-4-異硫氰基苯; 2-溴-1-[6-(二氟甲氧基)吡啶-3-基]乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 11.07 (br s, 1H), 8.55-8.58 (m, 1H), 8.34 (br s, 2H), 8.18 (dd, J = 8.6, 2.5 Hz, 1H), 8.04 (d, J = 2.0 Hz, 1H), 7.78 (t, J = 72.5 Hz, 1H), 7.47 (dd, J = 9.0, 2.7 Hz, 1H), 7.37 (d, J = 8.9 Hz, 1H), 7.21 (t, J = 73.5 Hz, 1H), 7.18-7.21 (m, 1H)。 LC-MS (方法2)Rt = 1.06 min MS (ESIpos): m/z = 463.2 [M+H]+ 92%產率 |
| 147 | {4-胺基-2-[4-(二氟甲氧基)-3-氟苯胺基]-1,3-噻唑-5-基}(4-甲氧基苯基)甲酮 | 1-(二氟甲氧基)-2-氟-4-異硫氰基苯; 2-溴-1-(4-甲氧基苯基)乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 10.99 (br s, 1H), 8.20 (br s, 2H), 7.97 (dd, J = 13.1, 2.4 Hz, 1H), 7.66-7.71 (m, 2H), 7.33-7.39 (m, 1H), 7.24-7.30 (m, 1H), 7.17 (t, J = 73.3 Hz, 1H), 7.00-7.05 (m, 2H), 3.82 (s, 3H)。 LC-MS (方法2)Rt = 1.13 min MS (ESIpos): m/z = 410.2 [M+H]+ 96%產率 |
| 148 | {4-胺基-2-[4-(二氟甲氧基)-3-氟苯胺基]-1,3-噻唑-5-基}(4-氯苯基)甲酮 | 1-(二氟甲氧基)-2-氟-4-異硫氰基苯; 2-溴-1-(4-氯苯基)乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 11.06 (br s, 1H), 8.30 (br s, 2H), 7.96 (dd, J = 12.9, 2.5 Hz, 1H), 7.68-7.72 (m, 2H), 7.53-7.58 (m, 2H), 7.33-7.39 (m, 1H), 7.24-7.29 (m, 1H), 7.18 (t, J = 73.3 Hz, 1H)。 LC-MS (方法2)Rt = 1.18 min MS (ESIpos): m/z = 414.2 [M+H]+ 95%產率 |
| 149 | {4-胺基-2-[4-(二氟甲氧基)-3-氟苯胺基]-1,3-噻唑-5-基}[4-(二氟甲氧基)苯基]甲酮 | 1-(二氟甲氧基)-2-氟-4-異硫氰基苯; 2-溴-1-[4-(二氟甲氧基)苯基]乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 11.03 (br s, 1H), 8.28 (br s, 2H), 7.96 (dd, J = 12.9, 2.3 Hz, 1H), 7.73-7.78 (m, 2H), 7.32-7.55 (m, 2H), 6.99-7.30 (m, 4H)。 LC-MS (方法2)Rt = 1.14 min MS (ESIpos): m/z = 446.2 [M+H]+ 88%產率 |
| 150 | {4-胺基-2-[4-(二氟甲氧基)-3-氟苯胺基]-1,3-噻唑-5-基}(吡啶-4-基)甲酮 | 1-(二氟甲氧基)-2-氟-4-異硫氰基苯; 2-溴-1-(吡啶-4-基)乙酮氫溴酸鹽 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 11.12 (s, 1H), 8.70-8.74 (m, 2H), 8.41 (br s, 2H), 7.97 (dd, J = 12.9, 2.5 Hz, 1H), 7.57-7.60 (m, 2H), 7.34-7.38 (m, 1H), 7.25-7.30 (m, 1H), 7.18 (t, J = 73.3 Hz, 1H)。 LC-MS (方法2)Rt = 0.8 min MS (ESIpos): m/z = 381.2 [M+H]+ 15%產率 |
| 151 | {4-胺基-2-[4-(二氟甲氧基)-3-氟苯胺基]-1,3-噻唑-5-基}[6-(二氟甲氧基)吡啶-3-基]甲酮 | 1-(二氟甲氧基)-2-氟-4-異硫氰基苯; 2-溴-1-[6-(二氟甲氧基)吡啶-3-基]乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 11.02-11.23 (m, 1H), 8.57 (d, J = 2.3 Hz, 1H), 8.25-8.41 (m, 2H), 8.18 (dd, J = 8.5, 2.4 Hz, 1H), 7.92-7.98 (m, 1H), 7.78 (t, J = 72.2 Hz, 1H), 7.33-7.40 (m, 1H), 7.24-7.30 (m, 1H), 7.20 (d, J = 9.1 Hz, 1H), 7.18 (t, J = 73.5 Hz, 1H)。 LC-MS (方法2)Rt = 1.06 min MS (ESIpos): m/z = 447.2 [M+H]+ 86%產率 |
| 152 | {4-胺基-2-[3-氟-4-(三氟甲氧基)苯胺基]-1,3-噻唑-5-基}(苯基)甲酮 | 2-氟-4-異硫氰基-1-(三氟甲氧基)苯(中間物200); 2-溴-1-苯基乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 11.12 (br s, 1H), 8.26 (br s, 2H), 8.08 (dd, J = 12.9, 2.5 Hz, 1H), 7.66-7.70 (m, 2H), 7.45-7.59 (m, 4H), 7.29-7.34 (m, 1H)。 LC-MS (方法2)Rt = 1.21 min MS (ESIpos): m/z = 398.2 [M+H]+ 96%產率 |
| 153 | {4-胺基-2-[3-氯-4-(三氟甲氧基)苯胺基]-1,3-噻唑-5-基}(苯基)甲酮 | 2-氯-4-異硫氰基-1-(三氟甲氧基)苯; 2-溴-1-苯基乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 11.08 (br s, 1H), 8.28 (br s, 2H), 8.16 (d, J = 2.3 Hz, 1H), 7.65-7.72 (m, 2H), 7.45-7.59 (m, 5H)。 LC-MS (方法2)Rt = 1.22 min MS (ESIpos): m/z = 414.2 [M+H]+ 91%產率 |
| 154 | {4-胺基-2-[(2,2-二氟-1,3-苯并間二氧雜環戊烯-5-基)胺基]-1,3-噻唑-5-基}(4-甲氧基苯基)甲酮 | 2,2-二氟-5-異硫氰基-1,3-苯并間二氧雜環戊烯; 2-溴-1-(4-甲氧基苯基)乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 10.92 (br s, 1H), 8.17 (br s, 2H), 7.95 (d, J = 2.0 Hz, 1H), 7.65-7.70 (m, 2H), 7.40 (d, J = 8.6 Hz, 1H), 7.24 (dd, J = 8.7, 2.2 Hz, 1H), 6.99-7.05 (m, 2H), 3.82 (s, 3H)。 LC-MS (方法2)Rt = 1.21 min MS (ESIpos): m/z = 406.2 [M+H]+ 89%產率 |
| 155 | {4-胺基-2-[(2,2-二氟-1,3-苯并間二氧雜環戊烯-5-基)胺基]-1,3-噻唑-5-基}(4-氯苯基)甲酮 | 2,2-二氟-5-異硫氰基-1,3-苯并間二氧雜環戊烯; 2-溴-1-(4-氯苯基)乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 11.00 (br d, J = 1.3 Hz, 1H), 8.28 (br s, 2H), 7.94 (d, J = 2.0 Hz, 1H), 7.66-7.73 (m, 2H), 7.51-7.58 (m, 2H), 7.40 (d, J = 8.6 Hz, 1H), 7.24 (dd, J = 8.9, 2.3 Hz, 1H)。 LC-MS (方法2)Rt = 1.25 min MS (ESIpos): m/z = 410.2 [M+H]+ 93%產率 |
| 156 | {4-胺基-2-[(2,2-二氟-1,3-苯并間二氧雜環戊烯-5-基)胺基]-1,3-噻唑-5-基}[4-(二氟甲氧基)苯基]甲酮 | 2,2-二氟-5-異硫氰基-1,3-苯并間二氧雜環戊烯; 2-溴-1-[4-(二氟甲氧基)苯基]乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 10.98 (br s, 1H), 8.24 (br s, 2H), 7.93 (d, J = 1.5 Hz, 1H), 7.71-7.78 (m, 2H), 7.40 (d, J = 8.6 Hz, 1H), 7.35 (t, J = 73.8 Hz, 1H), 7.21-7.29 (m, 3H)。 LC-MS (方法2)Rt = 1.23 min MS (ESIpos): m/z = 442.2 [M+H]+ 61%產率 |
| 157 | {4-胺基-2-[(2,2-二氟-1,3-苯并間二氧雜環戊烯-5-基)胺基]-1,3-噻唑-5-基}(吡啶-4-基)甲酮 | 2,2-二氟-5-異硫氰基-1,3-苯并間二氧雜環戊烯; 2-溴-1-(吡啶-4-基)乙酮氫溴酸鹽 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 11.06 (s, 1H), 8.69-8.74 (m, 2H), 8.38 (br s, 2H), 7.94 (d, J = 1.8 Hz, 1H), 7.56-7.60 (m, 2H), 7.41 (d, J = 8.9 Hz, 1H), 7.25 (dd, J = 8.7, 2.2 Hz, 1H)。 LC-MS (方法2)Rt = 0.85 min MS (ESIpos): m/z = 377.2 [M+H]+ 13%產率 |
| 158 | {4-胺基-2-[(2,2-二氟-1,3-苯并間二氧雜環戊烯-5-基)胺基]-1,3-噻唑-5-基}[6-(二氟甲氧基)吡啶-3-基]甲酮 | 2,2-二氟-5-異硫氰基-1,3-苯并間二氧雜環戊烯; 2-溴-1-[6-(二氟甲氧基)吡啶-3-基]乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 11.05 (br s, 1H), 8.54-8.58 (m, 1H), 8.31 (br s, 2H), 8.17 (dd, J = 8.6, 2.5 Hz, 1H), 7.94 (d, J = 1.8 Hz, 1H), 7.78 (t, J = 72.5 Hz, 1H), 7.41 (d, J = 8.9 Hz, 1H), 7.25 (dd, J = 8.9, 2.3 Hz, 1H), 7.17-7.22 (m, 1H)。 LC-MS (方法2)Rt = 1.15 min MS (ESIpos): m/z = 443.2 [M+H]+ 85%產率 |
| 159 | {4-胺基-2-[3-氟-4-(三氟甲氧基)苯胺基]-1,3-噻唑-5-基}(4-甲氧基苯基)甲酮 | 2-氟-4-異硫氰基-1-(三氟甲氧基)苯(中間物200); 2-溴-1-(4-甲氧基苯基)乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 11.10 (br s, 1H), 8.20 (br s, 2H), 8.08 (dd, J = 12.9, 2.5 Hz, 1H), 7.66-7.72 (m, 2H), 7.55 (td, J = 8.9, 1.0 Hz, 1H), 7.30-7.35 (m, 1H), 7.00-7.05 (m, 2H), 3.82 (s, 3H)。 LC-MS (方法2)Rt = 1.24 min MS (ESIpos): m/z = 428.2 [M+H]+ 90%產率 |
| 160 | {4-胺基-2-[3-氟-4-(三氟甲氧基)苯胺基]-1,3-噻唑-5-基}(4-氯苯基)甲酮 | 2-氟-4-異硫氰基-1-(三氟甲氧基)苯(中間物200); 2-溴-1-(4-氯苯基)乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 11.10 (br s, 1H), 8.20 (br s, 2H), 8.08 (dd, J = 12.9, 2.5 Hz, 1H), 7.66-7.72 (m, 2H), 7.55 (td, J = 9.0, 1.0 Hz, 1H), 7.30-7.35 (m, 1H), 7.00-7.06 (m, 2H), 3.82 (s, 3H)。 LC-MS (方法2)Rt = 1.23 min MS (ESIpos): m/z = 432.2 [M+H]+ 91%產率 |
| 161 | {4-胺基-2-[3-氟-4-(三氟甲氧基)苯胺基]-1,3-噻唑-5-基}[4-(二氟甲氧基)苯基]甲酮 | 2-氟-4-異硫氰基-1-(三氟甲氧基)苯(中間物200); 2-溴-1-[4-(二氟甲氧基)苯基]乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 11.15 (br s, 1H), 8.28 (br s, 2H), 8.07 (dd, J = 12.9, 2.5 Hz, 1H), 7.73-7.80 (m, 2H), 7.51-7.62 (m, 1H), 7.36 (t, J = 73.8 Hz, 1H), 7.30-7.34 (m, 1H), 7.25-7.30 (m, 2H)。 LC-MS (方法2)Rt = 1.24 min MS (ESIpos): m/z = 464.2 [M+H]+ 86%產率 |
| 162 | {4-胺基-2-[3-氟-4-(三氟甲氧基)苯胺基]-1,3-噻唑-5-基}(吡啶-4-基)甲酮 | 2-氟-4-異硫氰基-1-(三氟甲氧基)苯(中間物200); 2-溴-1-(吡啶-4-基)乙酮氫溴酸鹽 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 11.23 (s, 1H), 8.70-8.75 (m, 2H), 8.42 (br s, 2H), 8.08 (dd, J = 12.9, 2.5 Hz, 1H), 7.53-7.62 (m, 3H), 7.30-7.35 (m, 1H)。 LC-MS (方法2)Rt = 0.89 min MS (ESIpos): m/z = 399.2 [M+H]+ 21%產率 |
| 163 | {4-胺基-2-[3-氟-4-(三氟甲氧基)苯胺基]-1,3-噻唑-5-基}[6-(二氟甲氧基)吡啶-3-基]甲酮 | 2-氟-4-異硫氰基-1-(三氟甲氧基)苯(中間物200); 2-溴-1-[6-(二氟甲氧基)吡啶-3-基]乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 11.22 (br s, 1H), 8.55-8.61 (m, 1H), 8.34 (br s, 2H), 8.19 (dd, J = 8.5, 2.4 Hz, 1H), 8.07 (dd, J = 12.9, 2.5 Hz, 1H), 7.78 (t, J = 72.5 Hz, 1H), 7.56 (td, J = 8.9, 1.0 Hz, 1H), 7.30-7.36 (m, 1H), 7.18-7.22 (m, 1H)。 LC-MS (方法2)Rt = 1.15 min MS (ESIpos): m/z = 465.2 [M+H]+ 84%產率 |
| 164 | {4-胺基-2-[3-氯-4-(三氟甲氧基)苯胺基]-1,3-噻唑-5-基}(4-甲氧基苯基)甲酮 | 2-氯-4-異硫氰基-1-(三氟甲氧基)苯; 2-溴-1-(4-甲氧基苯基)乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 11.06 (br s, 1H), 8.05-8.37 (m, 3H), 7.66-7.72 (m, 2H), 7.50-7.58 (m, 2H), 7.00-7.05 (m, 2H), 3.82 (s, 3H)。 LC-MS (方法2)Rt = 1.22 min MS (ESIpos): m/z = 444.2 [M+H]+ 79%產率 |
| 165 | {4-胺基-2-[3-氯-4-(三氟甲氧基)苯胺基]-1,3-噻唑-5-基}(4-氯苯基)甲酮 | 2-氯-4-異硫氰基-1-(三氟甲氧基)苯; 2-溴-1-(4-氯苯基)乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 7.87-7.99 (m, 1H), 7.64-7.71 (m, 2H), 7.48-7.54 (m, 2H), 7.43 (s, 1H), 7.37 (br d, J = 0.8 Hz, 1H)。 LC-MS (方法2)Rt = 1.3 min MS (ESIpos): m/z = 448.2 [M+H]+ 53%產率 |
| 166 | {4-胺基-2-[3-氯-4-(三氟甲氧基)苯胺基]-1,3-噻唑-5-基}[4-(二氟甲氧基)苯基]甲酮 | 2-氯-4-異硫氰基-1-(三氟甲氧基)苯; 2-溴-1-[4-(二氟甲氧基)苯基]乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 11.11 (br s, 1H), 8.29 (br s, 2H), 8.15 (d, J = 2.5 Hz, 1H), 7.73-7.79 (m, 2H), 7.50-7.58 (m, 2H), 7.36 (t, J = 73.2 Hz, 1H), 7.25-7.30 (m, 2H)。 LC-MS (方法2)Rt = 1.24 min MS (ESIpos): m/z = 480.2 [M+H]+ 71%產率 |
| 167 | {4-胺基-2-[3-氯-4-(三氟甲氧基)苯胺基]-1,3-噻唑-5-基}(吡啶-4-基)甲酮 | 2-氯-4-異硫氰基-1-(三氟甲氧基)苯; 2-溴-1-(吡啶-4-基)乙酮氫溴酸鹽 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 11.19 (s, 1H), 8.70-8.75 (m, 2H), 8.43 (br s, 2H), 8.17 (d, J = 2.3 Hz, 1H), 7.51-7.61 (m, 4H)。 LC-MS (方法2)Rt = 0.93 min MS (ESIpos): m/z = 415.2 [M+H]+ 47%產率 |
| 168 | {4-胺基-2-[3-氯-4-(三氟甲氧基)苯胺基]-1,3-噻唑-5-基}[6-(二氟甲氧基)吡啶-3-基]甲酮 | 2-氯-4-異硫氰基-1-(三氟甲氧基)苯; 2-溴-1-[6-(二氟甲氧基)吡啶-3-基]乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 11.20 (br s, 1H), 8.54-8.59 (m, 1H), 8.21-8.52 (m, 2H), 8.18 (dd, J = 8.4, 2.5 Hz, 1H), 8.11 (br s, 1H), 7.78 (t, J = 72.5 Hz, 1H), 7.46-7.58 (m, 2H), 7.17-7.21 (m, 1H)。 LC-MS (方法2)Rt = 1.19 min MS (ESIpos): m/z = 481.2 [M+H]+ 34%產率 |
| 169 | {4-胺基-2-[(6-甲氧基吡啶-3-基)胺基]-1,3-噻唑-5-基}(苯基)甲酮 | 5-異硫氰基-2-甲氧基吡啶; 2-溴-1-苯基乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 10.69 (br s, 1H), 8.40 (d, J = 2.5 Hz, 1H), 7.96-8.38 (m, 2H), 7.93 (dd, J = 8.9, 2.8 Hz, 1H), 7.62-7.67 (m, 2H), 7.43-7.52 (m, 3H), 6.84-6.88 (m, 1H), 3.83 (s, 3H)。 LC-MS (方法2)Rt = 0.91 min MS (ESIpos): m/z = 327.2 [M+H]+ 87%產率 |
| 170 | (4-胺基-2-{[6-(三氟甲氧基)吡啶-3-基]胺基}-1,3-噻唑-5-基)(苯基)甲酮 | 5-異硫氰基-2-(三氟甲氧基)吡啶(中間物201); 2-溴-1-苯基乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 11.10 (br s, 1H), 8.67 (d, J = 2.8 Hz, 1H), 8.27 (dd, J = 8.9, 2.8 Hz, 3H), 7.66-7.70 (m, 2H), 7.46-7.53 (m, 3H), 7.34 (d, J = 8.9 Hz, 1H)。 LC-MS (方法2)Rt = 0.96 min MS (ESIpos): m/z = 381.2 [M+H]+ 82%產率 |
| 171 | (4-胺基-2-{[6-(二氟甲氧基)吡啶-3-基]胺基}-1,3-噻唑-5-基)(苯基)甲酮 | 2-(二氟甲氧基)-5-異硫氰基吡啶(中間物202); 2-溴-1-苯基乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 10.94 (br s, 1H), 8.56 (d, J = 2.8 Hz, 1H), 8.16 (dd, J = 8.9, 2.8 Hz, 3H), 7.67 (dd, J = 7.6, 1.8 Hz, 2H), 7.65 (t, J = 73.0 Hz, 1H), 7.45-7.53 (m, 3H), 7.14 (d, J = 8.9 Hz, 1H)。 LC-MS (方法2)Rt = 0.93 min MS (ESIpos): m/z = 363.2 [M+H]+ 90%產率 |
| 172 | (4-胺基-2-{[6-(三氟甲基)吡啶-3-基]胺基}-1,3-噻唑-5-基)(苯基)甲酮 | 5-異硫氰基-2-(三氟甲基)吡啶; 2-溴-1-苯基乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 11.26-11.46 (m, 1H), 8.93 (d, J = 2.5 Hz, 1H), 8.40 (dd, J = 8.5, 2.2 Hz, 1H), 8.25 (br s, 2H), 7.89 (d, J = 8.6 Hz, 1H), 7.67-7.72 (m, 2H), 7.46-7.56 (m, 3H)。 LC-MS (方法2)Rt = 0.88 min MS (ESIpos): m/z = 365.2 [M+H]+ 69%產率 |
| 173 | (4-胺基-2-{[6-(二氟甲基)吡啶-3-基]胺基}-1,3-噻唑-5-基)(苯基)甲酮 | 2-(二氟甲基)-5-異硫氰基吡啶(中間物203); 2-溴-1-苯基乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 11.21 (br s, 1H), 8.88 (d, J = 2.3 Hz, 1H), 8.15-8.37 (m, 3H), 7.66-7.72 (m, 3H), 7.46-7.55 (m, 3H), 6.92 (t, J = 55.3 Hz, 1H)。 LC-MS (方法2)Rt = 0.79 min MS (ESIpos): m/z = 347.2 [M+H]+ 66%產率 |
| 174 | {4-胺基-2-[(6-氯吡啶-3-基)胺基]-1,3-噻唑-5-基}(苯基)甲酮 | 2-氯-5-異硫氰基吡啶; 2-溴-1-苯基乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 11.09 (br s, 1H), 8.68 (d, J = 2.5 Hz, 1H), 8.12-8.37 (m, 3H), 7.65-7.71 (m, 2H), 7.45-7.55 (m, 4H)。 LC-MS (方法2)Rt = 0.79 min MS (ESIpos): m/z = 331.2 [M+H]+ 60%產率 |
| 175 | {4-胺基-2-[(6-氟吡啶-3-基)胺基]-1,3-噻唑-5-基}(苯基)甲酮 | 2-氟-5-異硫氰基吡啶; 2-溴-1-苯基乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 10.99 (br s, 1H), 8.52 (dd, J = 2.5, 1.3 Hz, 1H), 7.96-8.46 (m, 3H), 7.65-7.70 (m, 2H), 7.44-7.54 (m, 3H), 7.22 (dd, J = 8.9, 3.0 Hz, 1H)。 LC-MS (方法2)Rt = 0.79 min MS (ESIpos): m/z = 315.2 [M+H]+ 70%產率 |
| 176 | {4-胺基-2-[(6-甲基吡啶-3-基)胺基]-1,3-噻唑-5-基}(苯基)甲酮 | 5-異硫氰基-2-甲基吡啶; 2-溴-1-苯基乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 10.83 (br s, 1H), 8.63 (d, J = 2.5 Hz, 1H), 8.03-8.52 (m, 2H), 8.00 (dd, J = 8.4, 2.5 Hz, 1H), 7.63-7.70 (m, 2H), 7.44-7.53 (m, 3H), 7.25 (d, J = 8.4 Hz, 1H), 2.43 (s, 3H)。 LC-MS (方法2)Rt = 0.81 min MS (ESIpos): m/z = 311.2 [M+H]+ 88%產率 |
| 177 | {4-胺基-2-[4-氟-3-(三氟甲氧基)苯胺基]-1,3-噻唑-5-基}(苯基)甲酮 | 1-氟-4-異硫氰基-2-(三氟甲氧基)苯(中間物204); 2-溴-1-苯基乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 11.01 (br s, 1H), 8.09-8.42 (m, 2H), 7.99 (dd, J = 7.1, 1.3 Hz, 1H), 7.66-7.70 (m, 2H), 7.56-7.61 (m, 1H), 7.45-7.55 (m, 4H)。 LC-MS (方法2)Rt = 1.21 min MS (ESIpos): m/z = 398.2 [M+H]+ 94%產率 |
| 178 | {4-胺基-2-[4-氯-3-(三氟甲氧基)苯胺基]-1,3-噻唑-5-基}(苯基)甲酮 | 1-氯-4-異硫氰基-2-(三氟甲氧基)苯; 2-溴-1-苯基乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 11.12 (br s, 1H), 8.25 (br s, 2H), 8.01 (d, J = 0.8 Hz, 1H), 7.60-7.71 (m, 4H), 7.45-7.55 (m, 3H)。 LC-MS (方法2)Rt = 1.28 min MS (ESIpos): m/z = 414.2 [M+H]+ 90%產率 |
| 179 | {4-胺基-2-[3-(二氟甲氧基)-4-氟苯胺基]-1,3-噻唑-5-基}(苯基)甲酮 | 2-(二氟甲氧基)-1-氟-4-異硫氰基苯(中間物205); 2-溴-1-苯基乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 10.91 (br s, 1H), 8.06-8.43 (m, 2H), 7.74 (dd, J = 6.7, 2.2 Hz, 1H), 7.64-7.70 (m, 2H), 7.45-7.53 (m, 4H), 7.37-7.42 (m, 1H), 7.25 (t, J = 73.0 Hz, 1H)。 LC-MS (方法2)Rt = 1.1 min MS (ESIpos): m/z = 380.2 [M+H]+ 95%產率 |
| 180 | {4-胺基-2-[4-氯-3-(二氟甲氧基)苯胺基]-1,3-噻唑-5-基}(苯基)甲酮 | 1-氯-2-(二氟甲氧基)-4-異硫氰基苯; 2-溴-1-苯基乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 11.03 (br s, 1H), 8.23 (br s, 2H), 7.75 (d, J = 2.0 Hz, 1H), 7.65-7.70 (m, 2H), 7.46-7.58 (m, 5H), 7.27 (t, J = 73.0 Hz, 1H)。 LC-MS (方法2)Rt = 1.12 min MS (ESIpos): m/z = 396.2 [M+H]+ 98%產率 |
| 181 | {4-胺基-2-[2-氟-4-(三氟甲氧基)苯胺基]-1,3-噻唑-5-基}(苯基)甲酮 | 2-氟-1-異硫氰基-4-(三氟甲氧基)苯(中間物206); 2-溴-1-苯基乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 10.69 (br s, 1H), 8.25 (br t, J = 9.0 Hz, 3H), 7.63-7.69 (m, 2H), 7.43-7.56 (m, 4H), 7.28 (dd, J = 9.1, 1.0 Hz, 1H)。 LC-MS (方法2)Rt = 1.02 min MS (ESIpos): m/z = 398.2 [M+H]+ 100%產率 |
| 182 | {4-胺基-2-[2-氯-4-(三氟甲氧基)苯胺基]-1,3-噻唑-5-基}(苯基)甲酮 | 2-氯-1-異硫氰基-4-(三氟甲氧基)苯; 2-溴-1-苯基乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 9.25-9.70 (m, 1H), 8.46 (s, 1H), 7.55-7.68 (m, 3H), 7.32-7.46 (m, 4H), 7.16-7.25 (m, 1H)。 LC-MS (方法2)Rt = 1.05 min MS (ESIpos): m/z = 414.2 [M+H]+ 45%產率 |
| 183 | {4-胺基-2-[4-(二氟甲氧基)-2-氟苯胺基]-1,3-噻唑-5-基}(苯基)甲酮 | 4-(二氟甲氧基)-2-氟-1-異硫氰基苯(中間物207); 2-溴-1-苯基乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 10.25-10.79 (m, 1H), 7.90-8.47 (m, 3H), 7.61-7.66 (m, 2H), 7.40-7.50 (m, 4H), 7.24-7.29 (m, 2H), 7.02-7.09 (m, 1H)。 LC-MS (方法2)Rt = 0.98 min MS (ESIpos): m/z = 380.2 [M+H]+ 100%產率 |
| 184 | {4-胺基-2-[2-氯-4-(二氟甲氧基)苯胺基]-1,3-噻唑-5-基}(苯基)甲酮 | 2-氯-4-(二氟甲氧基)-1-異硫氰基苯(中間物208); 2-溴-1-苯基乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 10.43 (br s, 1H), 7.88-8.41 (m, 2H), 7.84 (d, J = 8.6 Hz, 1H), 7.62 (dd, J = 7.6, 1.8 Hz, 2H), 7.41-7.48 (m, 4H), 7.30 (t, J = 73.8 Hz, 1H), 7.21 (dd, J = 8.7, 2.7 Hz, 1H)。 LC-MS (方法2)Rt = 1.02 min MS (ESIpos): m/z = 396.2 [M+H]+ 99%產率 |
| 185 | {4-胺基-2-[4-(二氟甲基)苯胺基]-1,3-噻唑-5-基}(4-甲氧基苯基)甲酮 | 1-(二氟甲基)-4-異硫氰基苯; 2-溴-1-(4-甲氧基苯基)乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 10.97 (br s, 1H), 8.17 (br s, 2H), 7.77 (d, J = 8.6 Hz, 2H), 7.66-7.71 (m, 2H), 7.56 (d, J = 8.6 Hz, 2H), 7.00-7.05 (m, 2H), 6.98 (t, J = 56.0 Hz, 1H), 3.82 (s, 3H)。 LC-MS (方法2)Rt = 1.07 min MS (ESIpos): m/z = 376.1 [M+H]+ 88%產率 |
| 186 | {4-胺基-2-[4-(二氟甲基)苯胺基]-1,3-噻唑-5-基}(4-氯苯基)甲酮 | 1-(二氟甲基)-4-異硫氰基苯; 2-溴-1-(4-氯苯基)乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 11.06 (br s, 1H), 8.28 (br s, 2H), 7.75 (br d, J = 8.4 Hz, 2H), 7.68-7.72 (m, 2H), 7.52-7.58 (m, 4H), 6.98 (t, J = 56.0 Hz, 1H)。 LC-MS (方法2)Rt = 1.11 min MS (ESIpos): m/z = 380.1 [M+H]+ 94%產率 |
| 187 | {4-胺基-2-[4-(二氟甲基)苯胺基]-1,3-噻唑-5-基}[4-(二氟甲氧基)苯基]甲酮 | 1-(二氟甲基)-4-異硫氰基苯; 2-溴-1-[4-(二氟甲氧基)苯基]乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 11.03 (br s, 1H), 8.24 (br s, 2H), 7.73-7.78 (m, 4H), 7.56 (d, J = 8.6 Hz, 2H), 7.35 (t, J = 73.8 Hz, 1H), 7.24-7.29 (m, 2H), 6.99 (t, J = 56.0 Hz, 1H)。 LC-MS (方法2)Rt = 1.09 min MS (ESIpos): m/z = 412.1 [M+H]+ 91%產率 |
| 188 | {4-胺基-2-[4-(二氟甲基)苯胺基]-1,3-噻唑-5-基}(吡啶-4-基)甲酮 | 1-(二氟甲基)-4-異硫氰基苯; 2-溴-1-(吡啶-4-基)乙酮氫溴酸鹽 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 10.83-11.29 (m, 1H), 8.67-8.76 (m, 2H), 8.39 (br s, 2H), 7.77 (d, J = 8.6 Hz, 2H), 7.53-7.63 (m, 4H), 6.99 (t, J = 55.8 Hz, 1H)。 LC-MS (方法2)Rt = 0.72 min MS (ESIpos): m/z = 347.1 [M+H]+ 39%產率 |
| 189 | {4-胺基-2-[4-(二氟甲基)苯胺基]-1,3-噻唑-5-基}[6-(二氟甲氧基)吡啶-3-基]甲酮 | 1-(二氟甲基)-4-異硫氰基苯; 2-溴-1-[6-(二氟甲氧基)吡啶-3-基]乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 11.10 (br s, 1H), 8.56-8.60 (m, 1H), 8.32 (br s, 2H), 8.18 (dd, J = 8.4, 2.5 Hz, 1H), 7.78 (t, J = 72.5 Hz, 1H), 7.77 (d, J = 8.4 Hz, 2H), 7.57 (d, J = 8.6 Hz, 2H), 7.18-7.22 (m, 1H), 6.99 (t, J = 55.8 Hz, 1H)。 LC-MS (方法2)Rt = 1.04 min MS (ESIpos): m/z = 413 [M+H]+ 89%產率 |
| 190 | (4-胺基-2-{[6-(三氟甲氧基)吡啶-3-基]胺基}-1,3-噻唑-5-基)(4-甲氧基苯基)甲酮 | 5-異硫氰基-2-(三氟甲氧基)吡啶(中間物201); 2-溴-1-(4-甲氧基苯基)乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 11.07 (br s, 1H), 8.67 (d, J = 2.8 Hz, 1H), 8.27 (dd, J = 8.9, 2.8 Hz, 1H), 8.17 (br s, 2H), 7.65-7.71 (m, 2H), 7.34 (d, J = 8.9 Hz, 1H), 7.00-7.05 (m, 2H), 3.82 (s, 3H)。 LC-MS (方法2)Rt = 0.95 min MS (ESIpos): m/z = 411.2 [M+H]+ 63%產率 |
| 191 | (4-胺基-2-{[6-(三氟甲氧基)吡啶-3-基]胺基}-1,3-噻唑-5-基)(4-氯苯基)甲酮 | 5-異硫氰基-2-(三氟甲氧基)吡啶(中間物201); 2-溴-1-(4-氯苯基)乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 11.18 (br s, 1H), 8.64 (d, J = 2.5 Hz, 1H), 8.25 (br dd, J = 8.9, 3.0 Hz, 3H), 7.67-7.73 (m, 2H), 7.53-7.58 (m, 2H), 7.33 (d, J = 8.9 Hz, 1H)。 LC-MS (方法2)Rt = 0.98 min MS (ESIpos): m/z = 415.2 [M+H]+ 68%產率 |
| 192 | (4-胺基-2-{[6-(三氟甲氧基)吡啶-3-基]胺基}-1,3-噻唑-5-基)[4-(二氟甲氧基)苯基]甲酮 | 5-異硫氰基-2-(三氟甲氧基)吡啶(中間物201); 2-溴-1-[4-(二氟甲氧基)苯基]乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 11.13 (br s, 1H), 8.67 (d, J = 2.8 Hz, 1H), 8.27 (dd, J = 8.9, 2.8 Hz, 3H), 7.72-7.79 (m, 2H), 7.16-7.55 (m, 4H)。 LC-MS (方法2)Rt = 0.97 min MS (ESIpos): m/z = 447.4 [M+H]+ 90%產率 |
| 193 | (4-胺基-2-{[6-(三氟甲氧基)吡啶-3-基]胺基}-1,3-噻唑-5-基)[6-(二氟甲氧基)吡啶-3-基]甲酮 | 5-異硫氰基-2-(三氟甲氧基)吡啶(中間物201); 2-溴-1-[6-(二氟甲氧基)吡啶-3-基]乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 11.23 (br s, 1H), 8.65 (d, J = 2.5 Hz, 1H), 8.55-8.59 (m, 1H), 8.21-8.48 (m, 3H), 8.18 (dd, J = 8.6, 2.5 Hz, 1H), 7.78 (t, J = 72.9 Hz, 1H), 7.34 (d, J = 8.9 Hz, 1H), 7.17-7.22 (m, 1H)。 LC-MS (方法2)Rt = 0.85 min MS (ESIpos): m/z = 448.2 [M+H]+ 70%產率 |
| 194 | (4-胺基-2-{[6-(二氟甲氧基)吡啶-3-基]胺基}-1,3-噻唑-5-基)(4-甲氧基苯基)甲酮 | 2-(二氟甲氧基)-5-異硫氰基吡啶(中間物202); 2-溴-1-(4-甲氧基苯基)乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 10.91 (s, 1H), 8.57 (d, J = 2.5 Hz, 1H), 8.17 (dd, J = 8.9, 2.8 Hz, 3H), 7.65-7.70 (m, 2H), 7.65 (t, J = 73.0 Hz, 1H), 7.13 (d, J = 8.9 Hz, 1H), 6.99-7.05 (m, 2H), 3.82 (s, 3H)。 LC-MS (方法2)Rt = 0.94 min MS (ESIpos): m/z = 393.2 [M+H]+ 86%產率 |
| 195 | (4-胺基-2-{[6-(二氟甲氧基)吡啶-3-基]胺基}-1,3-噻唑-5-基)(4-氯苯基)甲酮 | 2-(二氟甲氧基)-5-異硫氰基吡啶(中間物202); 2-溴-1-(4-氯苯基)乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 11.00 (br s, 1H), 8.52 (d, J = 2.5 Hz, 1H), 8.14 (dd, J = 8.9, 2.8 Hz, 3H), 7.66-7.71 (m, 2H), 7.65 (t, J = 73.3 Hz, 1H), 7.54 (d, J = 8.6 Hz, 2H), 7.12 (d, J = 8.9 Hz, 1H)。 LC-MS (方法2)Rt = 0.94 min MS (ESIpos): m/z = 397.1 [M+H]+ 82%產率 |
| 196 | (4-胺基-2-{[6-(二氟甲氧基)吡啶-3-基]胺基}-1,3-噻唑-5-基)[4-(二氟甲氧基)苯基]甲酮 | 2-(二氟甲氧基)-5-異硫氰基吡啶(中間物202); 2-溴-1-[4-(二氟甲氧基)苯基]乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 8.56-10.12 (m, 1H), 7.70-8.09 (m, 2H), 7.65 (d, J = 8.6 Hz, 2H), 7.57 (t, J = 73.8 Hz, 1H), 7.27 (t, J = 74.1 Hz, 1H), 7.14 (d, J = 8.6 Hz, 2H), 6.88 (d, J = 8.9 Hz, 1H)。 LC-MS (方法2)Rt = 1.04 min MS (ESIpos): m/z = 429.1 [M+H]+ 87%產率 |
| 197 | (4-胺基-2-{[6-(二氟甲氧基)吡啶-3-基]胺基}-1,3-噻唑-5-基)[6-(二氟甲氧基)吡啶-3-基]甲酮 | 2-(二氟甲氧基)-5-異硫氰基吡啶(中間物202); 2-溴-1-[6-(二氟甲氧基)吡啶-3-基]乙酮 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1H NMR (400 MHz, DMSO-d6, 22ºC): Shift = 11.04 (br s, 1H), 8.53-8.59 (m, 2H), 8.31 (br s, 2H), 8.14-8.19 (m, 2H), 7.78 (t, J = 72.5 Hz, 1H), 7.65 (t, J = 73.0 Hz, 1H), 7.20 (dd, J = 8.6, 0.8 Hz, 1H), 7.14 (d, J = 8.9 Hz, 1H)。 LC-MS (方法2)Rt = 0.92 min MS (ESIpos): m/z = 430.4 [M+H]+ 86%產率 |
在0℃之含2-(4-乙醯基苯氧基)乙酸乙酯(940 mg,4.23 mmol)之THF (12.5 mL)用三溴化苯基三甲基銨(1.59 g,4.23 mmol)處理。在室溫攪拌反應混合物隔夜,用水稀釋且用二氯甲烷萃取三次。經合併之有機相用鹽水洗滌,經由拒水過濾圈(MN 617 WA)過濾且蒸發至乾燥。藉由Biotage (方法X)純化粗產物,得到237 mg (0.79 mmol,18%產率)標題化合物。
LC-MS (方法1):Rt = 1.05 min; MS(ESIpos) m/z = 300.0 [M+H]+
在0℃之含3'-(二氟甲氧基)苯乙酮(1 g,5.37 mmol)之THF (15 mL)用三溴化苯基三甲基銨(2.02 g,5.37 mmol)處理。在室溫攪拌反應混合物隔夜,用水稀釋且用乙酸乙酯萃取三次。經合併之有機相用鹽水洗滌,經由拒水過濾圈(MN 617 WA)過濾且蒸發至乾燥。粗產物(定量)未經進一步純化即使用。
LC-MS (方法1):Rt = 1.14 min; MS(ESIpos) m/z = 264.9 [M+H]+
將3-氟-4-(三氟甲氧基)苯胺(560 mg,2.81 mmol)懸浮於二氯甲烷(12 mL)中,隨後添加三乙胺(1.76 mL,12.65 mmol)。將混合物冷卻至0℃,且緩慢添加稀釋於二氯甲烷(1.5 mL)中之硫代碳醯氯(356 mg,3.09 mmol)。在移除冰浴之後,在室溫攪拌該批料一小時。添加水(12 mL)及二氯甲烷(7.5 mL),分離有機層,且用二氯甲烷萃取水相。經合併之有機相經由拒水過濾圈(MN 617 WA)過濾且蒸發至乾燥。經由Biotage (己烷/乙酸乙酯)純化粗材料,得到350 mg (1.36 mmol,48%)標題化合物。
1
H NMR (400 MHz, DMSO-d 6
) δ ppm = 7.79 (dd, J = 11.0, 2.4 Hz, 1H), 7.65-7.71 (m, 1H), 7.43 (ddd, J = 8.9, 2.5, 1.5 Hz, 1H)。
以下中間物由下表5中陳述之起始材料,使用關於2-氟-4-異硫氰基-1-(三氟甲氧基)苯/中間物200之程序製備。
表5:中間物201至208
| 中間物編號 | 化學結構 化學名稱 | 起始材料 | 分析/產率 |
| 201 | 5-異硫氰基-2-(三氟甲氧基)吡啶 | 6-(三氟甲氧基)吡啶-3-胺二鹽酸鹽; 硫代碳醯氯 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 8.52 (d, J = 2.8 Hz, 1H), 8.13 (dd, J = 8.7, 2.7 Hz, 1H), 7.39-7.43 (m, 1H)。 79%產率 |
| 202 | 2-(二氟甲氧基)-5-異硫氰基-吡啶 | 6-(二氟甲氧基)吡啶-3-胺; 硫代碳醯氯 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 8.43 (d, J = 2.8 Hz, 1H), 8.05 (dd, J = 8.7, 2.7 Hz, 1H), 7.69 (t, J = 72.5 Hz, 1H), 7.20 (d, J = 8.9 Hz, 1H)。 86%產率 |
| 203 | 2-(二氟甲基)-5-異硫氰基-吡啶 | 6-(二氟甲基)吡啶-3-胺二鹽酸鹽; 硫代碳醯氯 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1H NMR (400 MHz, DMSO-d6, 22ºC): Shift = 8.78 (d, J = 2.0 Hz, 1H), 8.06 (dd, J = 8.4, 2.3 Hz, 1H), 7.78 (d, J = 8.4 Hz, 1H), 7.00 (t, J = 54.8 Hz, 1H)。 77%產率 |
| 204 | 1-氟-4-異硫氰基-2-(三氟甲氧基)-苯 | 4-氟-3-(三氟甲氧基)苯胺; 硫代碳醯氯 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 7.83-7.88 (m, 1H), 7.59-7.65 (m, 2H)。 53%產率 |
| 205 | 2-(二氟甲氧基)-1-氟-4-異硫氰基-苯 | 3-(二氟甲氧基)-4-氟苯胺鹽酸鹽; 硫代碳醯氯 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 7.60 (dd, J = 7.0, 2.4 Hz, 1H), 7.51 (dd, J = 10.4, 8.9 Hz, 1H), 7.39-7.44 (m, 1H), 7.30 (t, J = 72.8 Hz, 1H)。 73%產率 |
| 206 | 2-氟-1-異硫氰基-4-(三氟甲氧基)-苯 | 2-氟-4-(三氟甲氧基)苯胺; 硫代碳醯氯 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 7.70 (dd, J = 10.0, 2.4 Hz, 1H), 7.64 (t, J = 8.7 Hz, 1H), 7.33 (ddt, J = 8.9, 2.4, 1.3 Hz, 1H)。 35%產率 |
| 207 | 4-(二氟甲氧基)-2-氟-1-異硫氰基-苯 | 4-(二氟甲氧基)-2-氟苯胺; 硫代碳醯氯 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 7.58 (t, J = 8.9 Hz, 1H), 7.43 (dd, J = 11.0, 2.7 Hz, 1H), 7.34 (t, J = 73.3 Hz, 1H), 7.07-7.13 (m, 1H)。 70%產率 |
| 208 | 2-氯-4-(二氟甲氧基)-1-異硫氰基-苯 | 2-氯-4-(二氟甲氧基)苯胺; 硫代碳醯氯 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 7.64 (d, J = 8.9 Hz, 1H), 7.57 (d, J = 2.8 Hz, 1H), 7.34 (t, J = 73.3 Hz, 1H), 7.25 (dd, J = 8.9, 2.8 Hz, 1H)。 48%產率 |
在形成2-(4-{[4-胺基-2-(4-氟苯胺基)-1,3-噻唑-5-基]羰基}苯氧基)乙酸乙酯(中間物112)時,分離出作為副產物之標題化合物(36 mg,0.09 mmol,11%產率)。
LC-MS (方法2):Rt = 0.90 min; MS(ESIpos) m/z = 374.3 [M+H]+
將1-氟-4-異硫氰基苯(5.65 g,36.9 mmol)溶解於乙腈(200 mL)中,隨後添加1,8-二氮雜雙環(5.4.0)十一碳-7-烯(5.61 g,36.9 mmol)及氰胺(1.86 g,44.3 mmol)。在室溫攪拌45 min之後,添加另外1,8-二氮雜雙環(5.4.0)十一碳-7-烯(2.8 g,18.5 mmol)及溶解於乙腈(80 mL)中之4-(溴乙醯基)苯甲酸乙酯(10 g,36.9 mmol)。在室溫攪拌反應混合物2.5 h且用水處理。過濾出沈澱,用水洗滌且真空乾燥,得到14.2 g (定量)標題化合物。
1
H NMR (400 MHz, DMSO-d 6
) δ ppm = 1.34 (t,J
=7.1 Hz, 3 H), 4.34 (d,J
=7.1 Hz, 3 H), 7.22 (m, 2 H), 7.61 (m, 1 H), 7.78 (d,J
=8.62 Hz, 2 H), 8.04 (d,J
=8.62 Hz, 2 H), 8.32 (m, 2 H), 10.87 (br s, 1 H)。
LC-MS (方法2):Rt = 1.10 min; MS(ESIpos) m/z = 386.3 [M+H]+
將外消旋-4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氟-苯胺基)噻唑-5-羰基]苯甲酸乙酯(15.47 g,33 mmol,實例257)懸浮於THF (150 mL)中,且用1M氫氧化鈉水溶液(43 mL,43 mmol)處理。攪拌反應混合物隔夜,隨後添加1M鹽酸水溶液直至pH 3。用乙酸乙酯萃取溶液三次。經合併之有機相用鹽水洗滌,經由拒水過濾圈(MN 617 WA)過濾且蒸發至乾燥,得到11.63 g (25 mmol,87%產率)標題化合物。
LC-MS (方法2):Rt = 0.53 min; MS(ESIpos) m/z = 429.4 [M+H]+
將1-氯-2-氟-4-異硫氰基苯(692 mg,3.7 mmol)溶解於乙腈(20 mL)中,隨後添加1,8-二氮雜雙環(5.4.0)十一碳-7-烯(561.5 mg,3.68 mmol)及氰胺(186 mg,4.43 mmol)。在室溫攪拌45 min之後,添加另外1,8-二氮雜雙環(5.4.0)十一碳-7-烯(280.75 mg,1.84 mmol)及溶解於乙腈(14 mL)中之4-(溴乙醯基)苯甲酸乙酯(1 g,3.7 mmol)。在室溫攪拌反應混合物2 h。懸浮液用水處理,且沈澱藉由過濾分離,用水及一定量的乙酸乙酯洗滌且真空乾燥,得到1.24 g (2.52 mmol,68%,85%純度)標題化合物。
LC-MS (方法2):Rt = 1.12 min; MS(ESIpos) m/z = 420.2 [M+H]+
將外消旋-4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氯-3-氟-苯胺基)噻唑-5-羰基]苯甲酸乙酯(830 mg,1.7 mmol,實例258)懸浮於THF (10 mL)中,且用2M氫氧化鈉水溶液(8.5 mL,17 mmol)處理。在室溫攪拌反應混合物隔夜,隨後添加2M鹽酸水溶液直至pH 3。過濾出沈澱,用水洗滌且真空乾燥,得到680 mg (1.47 mmol,88%)標題化合物。
LC-MS (方法1):Rt = 1.07 min; MS(ESIpos) m/z = 463.1 [M+H]+
將1-氟-4-異硫氰基苯(349 mg,2.28 mmol)溶解於乙腈(8 mL)中,隨後添加1,8-二氮雜雙環(5.4.0)十一碳-7-烯(346 mg,2.28 mmol)及氰胺(115 mg,2.7 mmol)。在室溫攪拌45 min之後,添加另外1,8-二氮雜雙環(5.4.0)十一碳-7-烯(173 mg,1.14 mmol)及溶解於乙腈(4 mL)中之2-[4-(2-溴乙醯基)苯氧基]-2-甲基-丙酸乙酯(750 mg,2.28 mmol)。在室溫攪拌反應混合物隔夜。懸浮液用水處理,且沈澱藉由過濾分離,用水洗滌且真空乾燥,得到1.01 g (2.28 mmol,70%)標題化合物。
1
H NMR (400 MHz, DMSO-d 6
) δ ppm = 1.15 (t,J
=7.1 Hz, 3 H), 1.57 (s, 6 H), 4.17 (q,J
=7.1 Hz, 2 H), 6.80 (m, 2 H), 7.15 (m, 2 H), 7.50 (m, 2 H), 7.59 (m, 2 H), 8.12 (m, 2 H), 10.51 (m, 1 H)。
LC-MS (方法2):Rt = 1.24 min; MS(ESIpos) m/z = 444.3 [M+H]+
將外消旋-2-[4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氟-苯胺基)噻唑-5-羰基]苯氧基]-2-甲基-丙酸乙酯(925 mg,1.79 mmol,實例259)懸浮於THF (10 mL)中,且用1M氫氧化鈉水溶液(2.7 mL,2.7 mmol)處理。在室溫攪拌反應混合物隔夜,隨後添加1M鹽酸水溶液直至pH 3。用乙酸乙酯萃取反應混合物三次。經合併之有機相用鹽水洗滌,經由拒水過濾圈(MN 617 WA)過濾且蒸發至乾燥,得到861 mg (1.6 mmol,91%)標題化合物。
1
H NMR (400 MHz, DMSO-d 6
) δ ppm = 1.16 (d,J
=7.35 Hz, 3 H), 1.52 (s, 6 H), 5.06 (m, 1 H), 6.76 (m, 2 H), 7.24 (s, 1 H), 7.33 (t,J
=8.74 Hz, 2 H), 7.45 (m, 2 H), 7.57 (s, 1 H), 7.64 (m, 2 H), 8.10 (m, 2 H), 13.15 (m, 1 H)。
LC-MS (方法2):Rt = 0.63 min; MS(ESIpos) m/z = 487.4 [M+H]+
將1-氟-4-異硫氰基苯(250 mg,1.63 mmol)溶解於乙腈(8 mL)中,隨後添加1,8-二氮雜雙環(5.4.0)十一碳-7-烯(248.5 mg,1.63 mmol)及氰胺(82 mg,1.96 mmol)。在室溫攪拌45 min之後,添加另外1,8-二氮雜雙環(5.4.0)十一碳-7-烯(124.2 mg,0.82 mmol)及溶解於乙腈(7 mL)中之1-(6-胺基-3-吡啶基)-2-溴-乙酮(351 mg,1.63 mmol)。在室溫攪拌反應混合物2.5 h。懸浮液用水處理,且沈澱藉由過濾分離,用水洗滌且真空乾燥,得到350 mg (1.05 mmol,64%)標題化合物。
1
H NMR (400 MHz, DMSO-d 6
) δ ppm = 4.65 (s, 2 H), 6.96 (d,J
=9.63 Hz, 1 H), 7.03 (d,J
=9.38 Hz, 2 H), 8.24 (m, 3 H), 8.62 (d,J
=2.28 Hz, 2 H), 8.82 (d,J
=2.28 Hz, 1 H)。
LC-MS (方法2):Rt = 0.82 min; MS(ESIpos) m/z = 330.2 [M+H]+
將[4-胺基-2-(4-氟苯胺基)噻唑-5-基]-(6-胺基-3-吡啶基)甲酮(205 mg,0.62 mmol,中間物216)懸浮於THF (5 mL)中,且用氯甲酸苯甲酯(106 mg,0.62 mmol)及三乙胺(94 mg,0.93 mmol)處理。在室溫攪拌隔夜反應混合物,隨後添加另外氯甲酸苯甲酯(106 mg,0.62 mmol)、三乙胺(94 mg,0.93 mmol)及DMAP (1 mg)。在4.5 h之後,添加水,且用乙酸乙酯萃取反應混合物三次。經合併之有機相用鹽水洗滌,經由拒水過濾圈(MN 617 WA)過濾且蒸發至乾燥。經由Biotage層析(方法Y)純化殘餘物,得到25 mg (0.05 mmol,9%)標題化合物。
LC-MS (方法2):Rt = 1.11 min; MS(ESIpos) m/z = 464.3 [M+H]+
將1-氟-4-異硫氰基苯(1.29 g,8.43 mmol)溶解於乙腈(65 mL)中,隨後添加1,8-二氮雜雙環(5.4.0)十一碳-7-烯(1.28 g,8.43 mmol)及氰胺(0.43 g,10.1 mmol)。在室溫攪拌45 min之後,添加另外1,8-二氮雜雙環(5.4.0)十一碳-7-烯(0.64 g,4.2 mmol)及溶解於乙腈(15 mL)中之2-溴-1-(6-溴-3-吡啶基)乙酮(2.35 g,8.43 mmol)。在室溫攪拌反應混合物隔夜且用水處理。過濾出沈澱,用水洗滌且真空乾燥,得到2.52 g (6.4 mmol,76%)標題化合物。
LC-MS (方法2):Rt = 0.95 min; MS(ESIpos) m/z = 395.1 [M+H]+
實驗章節——實例化合物之製備
將[4-胺基-2-(4-甲氧基-2-甲基-苯胺基)噻唑-5-基]-苯基-甲酮(100 mg,0.295 mmol;中間物 4
)溶解於N,N-二甲基甲醯胺(3 mL)中,隨後添加碳酸鉀(407 mg,2.95 mmol)及外消旋-2-溴丙醯胺(224 mg,1.47 mmol)。在90℃攪拌反應混合物2 h。過濾反應混合物且藉由RP-HPLC (方法D,鹼性)純化,得到57 mg (47%產率)標題化合物。
1
H-NMR: (400 MHz, DMSO-d 6
): δ ppm = 1.03 (d,J
=7.35 Hz, 3 H), 2.13 (s, 3 H), 3.75 - 3.78 (m, 3 H), 4.93 - 5.13 (m, 1 H), 6.85 - 6.93 (m, 2 H), 7.17 - 7.24 (m, 1 H), 7.34 - 7.42 (m, 3 H), 7.42 - 7.50 (m, 2 H), 7.54 (br s, 1 H), 7.64 (d,J
=8.62 Hz, 1 H), 7.73 - 8.60 (m, 2 H)。
LC-MS (方法2)Rt = 1.08 min; MS (ESIpos): m/z = 411.5 [M+H]+
以下實例由下表6中陳述之起始材料,使用關於實例1之程序製備。
必要時,在沈澱、萃取或過濾反應混合物之後,藉由RP-HPLC (方法A至D,視極性而定)或藉由製備型急驟層析(方法X、Y或Z,視極性而定)純化粗產物。
使用所陳述管柱及溶劑條件藉由對掌性HPLC將鏡像異構物與其外消旋體分離。
表6:實例2至80
| 實例編號 | 化學結構 化學名稱 | 起始材料 | 分析/純化/產率 |
| 2 | 外消旋-2-[N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-(二甲基胺基)苯胺基]丙醯胺 | 中間物5; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.14 (d,J =7.35 Hz, 3 H), 2.93 (s, 6 H), 5.06 (br d,J =6.08 Hz, 1 H), 6.70 (d,J =9.38 Hz, 2 H), 7.15 - 7.20 (m, 1 H), 7.28 (d,J =8.87 Hz, 2 H), 7.34 - 7.41 (m, 3 H), 7.43 - 7.50 (m, 3 H), 7.74 - 8.53 (m, 2 H)。 LC-MS (方法2)Rt = 1.11 min; MS (ESIpos): m/z = 410.6 [M+H]+ RP-HPLC (方法D,鹼性) 51%產率 |
| 3 | 外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-異丙氧基-苯胺基)丙醯胺 | 中間物6; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.15 (d,J =7.35 Hz, 3 H), 1.27 (d,J =6.08 Hz, 6 H), 4.62 (spt,J =6.04 Hz, 1 H), 5.01 - 5.11 (m, 1 H), 6.96 (d,J =9.12 Hz, 2 H), 7.21 (s, 1 H), 7.35 - 7.49 (m, 7 H), 7.52 (s, 1 H), 7.75 - 8.51 (m, 2 H)。 LC-MS (方法1)Rt = 1.18 min; MS (ESIpos): m/z = 425.7 [M+H]+ RP-HPLC (方法D,鹼性) 42%產率 |
| 4 | 外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-2,4,6-三氟-苯胺基)丙醯胺 | 中間物7; 外消旋-2-溴丙醯胺 | 1 H-NMR (500 MHz, DMSO-d6 ): δ ppm = 1.32 (d,J =6.99 Hz, 3 H), 4.95 (q,J =6.57 Hz, 1 H), 7.04 - 7.11 (m, 1 H), 7.33 (br s, 2 H), 7.39 - 7.48 (m, 4 H), 7.56 (dd,J =7.79, 1.75 Hz, 2 H), 7.96 (br s, 2 H) LC-MS (方法2)Rt = 1.08 min; MS (ESIpos): m/z = 421.5 [M+H]+ RP-HPLC (方法D,鹼性) 製備型急驟層析(方法X,40-100%) 33%產率 |
| 5 | 外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-2-溴-4-氟-苯胺基)丙醯胺 | 中間物8; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.03 - 1.15 (m, 3 H), 4.98 - 5.13 (m, 1 H), 7.21 - 7.34 (m, 1 H), 7.34 - 7.55 (m, 6 H), 7.57 - 7.87 (m, 2 H), 7.90 - 8.49 (m, 3 H)。 LC-MS (方法2)Rt = 1.11 min; MS (ESIpos): m/z = 463.2 [M+H]+ RP-HPLC (方法D,鹼性) 83%產率 |
| 6 | 外消旋-2-(N-[4-胺基-5-(6-甲基吡啶-3-羰基)噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物9; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.16 (d,J =7.60 Hz, 3 H), 2.45 (s, 3 H), 5.00 - 5.11 (m, 1 H), 7.24 - 7.28 (m, 2 H), 7.33 (t,J =8.87 Hz, 2 H), 7.59 (s, 1 H), 7.62 - 7.67 (m, 2 H), 7.74 (dd,J =8.11, 2.28 Hz, 1 H), 7.97 - 8.46 (m, 2 H), 8.54 (d,J =2.03 Hz, 1 H)。 LC-MS (方法2)Rt = 0.93 min; MS (ESIpos): m/z = 400.4 [M+H]+ RP-HPLC (方法C,鹼性) 59%產率 |
| 7 | 外消旋-2-(N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物10; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.16 (d,J =7.60 Hz, 3 H), 5.06 (br d,J =7.10 Hz, 1 H), 7.26 (s, 1 H), 7.33 (t,J =8.74 Hz, 2 H), 7.38 - 7.42 (m, 2 H), 7.59 (s, 1 H), 7.61 - 7.67 (m, 2 H), 8.10 - 8.50 (m, 2 H), 8.59 - 8.64 (m, 2 H)。 LC-MS (方法2)Rt = 0.85 min; MS (ESIpos): m/z = 386.3 [M+H]+ RP-HPLC (方法C,酸性) 17%產率 |
| 8 | 外消旋-2-(N-[4-胺基-5-(2-氟苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物11; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.14 (d,J =7.35 Hz, 3 H), 4.89 - 5.13 (m, 1 H), 7.15 - 7.34 (m, 7 H), 7.40 (tdd,J =7.73, 7.73, 5.58, 1.77 Hz, 1 H), 7.53 - 7.66 (m, 3 H), 8.09 (br s, 2 H)。 LC-MS (方法1)Rt = 1.05 min; MS (ESIpos): m/z = 403.4 [M+H]+ RP-HPLC (方法D,鹼性) 71%產率 |
| 9 | 外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-氰基-苯胺基)丙醯胺 | 中間物12; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.18 (d,J =7.35 Hz, 3 H), 5.05 (q,J =7.69 Hz, 1 H), 7.31 (s, 1 H), 7.36 - 7.43 (m, 3 H), 7.48 - 7.52 (m, 2 H), 7.64 (s, 1 H), 7.81 (d,J =8.62 Hz, 2 H), 8.16 (br s, 2 H), 7.99 (d,J =8.36 Hz, 2 H)。 LC-MS (方法1)Rt = 0.99 min; MS (ESIpos): m/z = 392.3 [M+H]+ RP-HPLC (方法C,鹼性) 8%產率 |
| 10 | 外消旋-2-(N-[4-胺基-5-[4-氯-3-(三氟甲基)苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物13; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 5.01 - 5.14 (m, 1 H), 7.27 (s, 1 H), 7.34 (t,J =8.87 Hz, 2 H), 7.59 (s, 1 H), 7.62 - 7.67 (m, 2 H), 7.77 (s, 2 H), 7.89 - 7.91 (m, 1 H), 8.08 - 8.64 (m, 2 H)。 LC-MS (方法2)Rt = 1.30 min; MS (ESIpos): m/z = 487.2 [M+H]+ RP-HPLC (方法D,鹼性) 22%產率 |
| 11 | 外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-2-氯-4-氟-苯胺基)丙醯胺 | 中間物14; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.09 (d,J =7.35 Hz, 3 H), 4.98 - 5.21 (m, 1 H), 7.26 - 7.34 (m, 1 H), 7.36 - 7.55 (m, 6 H), 7.59 - 7.76 (m, 2 H), 7.89 - 8.45 (m, 2 H), 8.03 (dd,J =8.87, 5.83 Hz, 1 H)。 LC-MS (方法2)Rt = 1.13 min; MS (ESIpos): m/z = 419.4 [M+H]+ RP-HPLC (方法D,鹼性) 48%產率 |
| 12 | 外消旋-2-(N-[4-胺基-5-(3-氰基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物15; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 5.01 - 5.10 (m, 1 H), 7.24 - 7.28 (m, 1 H), 7.33 (t,J =8.87 Hz, 2 H), 7.57 - 7.66 (m, 4 H), 7.78 (dt,J =7.79, 1.30 Hz, 1 H), 7.86 - 7.89 (m, 2 H), 8.25 (br s, 2 H)。 LC-MS (方法2)Rt = 1.02 min; MS (ESIpos): m/z = 410.3 [M+H]+ RP-HPLC (方法C,鹼性) 31%產率 |
| 13 | 外消旋-2-[N-(4-胺基-5-苯甲醯基-噻唑-2-基)-3-氯-4-(二甲基胺基)苯胺基]丙醯胺 | 中間物16; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 2.77 (s, 6 H), 4.99 - 5.09 (m, 1 H), 7.18 (d,J =8.62 Hz, 1 H), 7.22 - 7.27 (m, 1 H), 7.35 - 7.46 (m, 4 H), 7.47 - 7.52 (m, 2 H), 7.57 (s, 1 H), 7.63 (d,J =2.28 Hz, 1 H), 8.16 (br s, 2 H)。 LC-MS (方法2)Rt = 0.91 min; MS (ESIpos): m/z = 444.5 [M+H]+ RP-HPLC (方法C,鹼性) 51%產率 |
| 14 | 外消旋-2-(N-[4-胺基-5-(6-甲氧基吡啶-3-羰基)噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物17; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.16 (d,J =7.60 Hz, 3 H), 3.85 (s, 3 H), 5.01 - 5.11 (m, 1 H), 6.83 (dd,J =8.62, 0.51 Hz, 1 H), 7.24 - 7.28 (m, 1 H), 7.34 (t,J =8.87 Hz, 2 H), 7.59 (s, 1 H), 7.62 - 7.68 (m, 2 H), 7.82 (dd,J =8.62, 2.53 Hz, 1 H), 8.17 (br s, 2 H), 8.33 (d,J =2.03 Hz, 1 H)。 LC-MS (方法2)Rt = 1.02 min; MS (ESIpos): m/z = 416.4 [M+H]+ RP-HPLC (方法C,鹼性) 43%產率 |
| 15 | 外消旋-4-[4-胺基-2-(N-[2-胺基-1-甲基-2-側氧基-乙基]-4-氟-苯胺基)噻唑-5-羰基]-N-甲基-苯甲醯胺 | 中間物18; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 2.75 (d,J =4.56 Hz, 3 H), 4.99 - 5.12 (m, 1 H), 7.25 (s, 1 H), 7.32 (t,J =8.87 Hz, 2 H), 7.53 (d,J =8.36 Hz, 2 H), 7.58 (br s, 1 H), 7.60 - 7.66 (m, 2 H), 7.78 (d,J =8.36 Hz, 2 H), 8.17 (br s, 2 H), 8.46 (q,J =4.48 Hz, 1 H)。 LC-MS (方法2)Rt = 0.85 min; MS (ESIpos): m/z = 442.5 [M+H]+ RP-HPLC (方法C,鹼性) 10%產率 |
| 16 | 外消旋-2-(N-[4-胺基-5-(3-氟苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物19; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 4.98 - 5.17 (m, 1 H), 7.22 - 7.29 (m, 3 H), 7.29 - 7.36 (m, 3 H), 7.39 - 7.48 (m, 1 H), 7.58 (s, 1 H), 7.64 (dd,J =8.62, 5.07 Hz, 2 H), 7.97 - 8.59 (m, 2 H)。 LC-MS (方法1)Rt = 1.10 min; MS (ESIpos): m/z = 403.3 [M+H]+ RP-HPLC (方法D,鹼性) 68%產率 |
| 17 | 外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-3-氯-4-甲氧基-苯胺基)丙醯胺 | 中間物20; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 3.89 (s, 3 H), 4.96 - 5.10 (m, 1 H), 7.22 (d,J =8.87 Hz, 1 H), 7.25 (s, 1 H), 7.35 - 7.43 (m, 3 H), 7.46 - 7.54 (m, 3 H), 7.59 (s, 1 H), 7.71 (d,J =2.53 Hz, 1 H), 7.87 - 8.37 (m, 2 H)。 LC-MS (方法2)Rt = 1.10 min; MS (ESIpos): m/z = 431.3 [M+H]+ RP-HPLC (方法D,鹼性) 60%產率 |
| 18 | 外消旋-2-(N-[4-胺基-5-(4-氟苯甲醯基)噻唑-2-基]-4-甲氧基-苯胺基)丙醯胺 | 中間物21; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.14 (d,J =7.35 Hz, 3 H), 3.78 (s, 3 H), 5.01 - 5.10 (m, 1 H), 7.01 (d,J =9.13 Hz, 2 H), 7.17 - 7.24 (m, 3 H), 7.46 (d,J =8.62 Hz, 2 H), 7.51 - 7.58 (m, 3 H), 8.09 (br s, 2 H)。 LC-MS (方法1)Rt = 1.08 min; MS (ESIpos): m/z = 415.6 [M+H]+ RP-HPLC (方法C,酸性) 36%產率 |
| 19 | 外消旋-2-(N-[4-胺基-5-(4-甲磺醯基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物22; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 3.23 (s, 3 H), 4.96 - 5.15 (m, 1 H), 7.26 (s, 1 H), 7.33 (t,J =8.74 Hz, 2 H), 7.59 (s, 1 H), 7.64 (dd,J =8.87, 5.07 Hz, 2 H), 7.70 (d,J =8.36 Hz, 2 H), 7.93 (d,J =8.62 Hz, 2 H), 8.04 - 8.56 (m, 2 H)。 LC-MS (方法1)Rt = 0.91 min; MS (ESIpos): m/z = 463.4 [M+H]+ RP-HPLC (方法C,鹼性) 31%產率 |
| 20 | 外消旋-2-(N-[4-胺基-5-(4-咪唑-1-基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物23; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 5.00 - 5.13 (m, 1 H), 7.10 (s, 1 H), 7.26 (s, 1 H), 7.34 (t,J =8.74 Hz, 2 H), 7.56 - 7.73 (m, 7 H), 7.78 (t,J =1.27 Hz, 1 H), 7.88 - 8.62 (m, 2 H), 8.30 (s, 1 H)。 LC-MS (方法1)Rt = 0.70 min; MS (ESIpos): m/z = 451.5 [M+H]+ RP-HPLC (方法C,鹼性) 68%產率 |
| 21 | 外消旋-2-(N-[4-胺基-5-(4-氰基-3-氟-苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物24; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.15 (d,J =7.35 Hz, 3 H), 5.01 - 5.11 (m, 1 H), 7.25 (s, 1 H), 7.33 (t,J =8.87 Hz, 2 H), 7.45 (dd,J =7.86, 1.27 Hz, 1 H), 7.55 (dd,J =9.89, 1.27 Hz, 1 H), 7.58 - 7.66 (m, 3 H), 7.93 (dd,J =7.86, 6.59 Hz, 1 H), 8.11 - 8.52 (m, 2 H)。 LC-MS (方法1)Rt = 1.08 min; MS (ESIpos): m/z = 428.3 [M+H]+ RP-HPLC (方法C,鹼性) 5%產率 |
| 21.1 及21.2 | (R)-2-(N-[4-胺基-5-(4-氰基-3-氟-苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺及 (S)-2-(N-[4-胺基-5-(4-氰基-3-氟-苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺 | ||
| 21.1 | 2-(N-[4-胺基-5-(4-氰基-3-氟-苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺(鏡像異構物1) | 實例21 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.15 (d,J =7.35 Hz, 3 H), 5.01 - 5.11 (m, 1 H), 7.25 (s, 1 H), 7.33 (t,J =8.87 Hz, 2 H), 7.45 (dd,J =7.86, 1.27 Hz, 1 H), 7.55 (dd,J =9.89, 1.27 Hz, 1 H), 7.58 - 7.66 (m, 3 H), 7.93 (dd,J =7.86, 6.59 Hz, 1 H), 8.11 - 8.52 (m, 2 H)。 LC-MS (方法1)Rt = 1.07 min; MS (ESIpos): m/z = 428.3 [M+H]+ RP-HPLC (方法C,鹼性) 8%產率 |
| 對掌性HPLC實例21.1 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-(4-氰基-3-氟-苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺(實例21,106 mg,0.25 mmol),隨後進行另一製備型HPLC,得到9.2 mg (8%產率) 2-(N-[4-胺基-5-(4-氰基-3-氟-苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺,鏡像異構物1。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:YMC Cellulose SB 5µ,250×30;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:乙醇+ 0.1 vol%二乙胺;等度:80% A+20% B;流速:50 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 5.46 min 儀器:Waters Alliance 2695;管柱:YMC Cellulose SB 3µ,100×4.6; 溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:乙醇;等度:80% A+20% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 21.2 | 2-(N-[4-胺基-5-(4-氰基-3-氟-苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺(鏡像異構物2) | 實例21 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.15 (d,J =7.35 Hz, 3 H), 5.01 - 5.11 (m, 1 H), 7.25 (s, 1 H), 7.33 (t,J =8.87 Hz, 2 H), 7.45 (dd,J =7.86, 1.27 Hz, 1 H), 7.55 (dd,J =9.89, 1.27 Hz, 1 H), 7.58 - 7.66 (m, 3 H), 7.93 (dd,J =7.86, 6.59 Hz, 1 H), 8.11 - 8.52 (m, 2 H)。 LC-MS (方法1)Rt = 1.07 min; MS (ESIpos): m/z = 428.3 [M+H]+ RP-HPLC (方法C,鹼性) 7%產率 |
| 對掌性HPLC實例21.2 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-(4-氰基-3-氟-苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺(實例21,106 mg,0.25 mmol),隨後進行另一製備型HPLC,得到7 mg (6%產率) 2-(N-[4-胺基-5-(4-氰基-3-氟-苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺,鏡像異構物2。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:YMC Cellulose SB 5µ,250×30;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:乙醇+ 0.1 vol%二乙胺;等度:80% A+20% B;流速:50 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 7.71 min 儀器:Waters Alliance 2695;管柱:YMC Cellulose SB 3µ,100×4.6; 溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:乙醇;等度:80% A+20% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 22 | 外消旋-2-(N-[4-胺基-5-(4-氰基-2-氟-苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物25; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 5.01 - 5.11 (m, 1 H), 7.27 (s, 1 H), 7.34 (t,J =8.87 Hz, 2 H), 7.45 (dd,J =8.11, 1.27 Hz, 1 H), 7.56 (dd,J =9.76, 1.14 Hz, 1 H), 7.59 (s, 1 H), 7.64 (dd,J =8.74, 4.94 Hz, 2 H), 7.92 - 7.97 (m, 1 H), 8.18 - 8.50 (m, 2 H)。 LC-MS (方法1)Rt = 1.07 min; MS (ESIpos): m/z = 428.3 [M+H]+ RP-HPLC (方法D,鹼性) 40%產率 |
| 23 | 外消旋-2-(N-[4-胺基-5-(2-氟-4-甲氧基-苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物26; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.14 (d,J =7.60 Hz, 3 H), 3.75 (s, 3 H), 4.98 - 5.09 (m, 1 H), 6.76 (d,J =20.28 Hz, 1 H), 6.78 (br d,J =23.32 Hz, 1 H), 7.22 - 7.27 (m, 2 H), 7.31 (t,J =8.87 Hz, 2 H), 7.57 (s, 1 H), 7.59 - 7.64 (m, 2 H), 8.03 (br s, 2 H)。 LC-MS (方法2)Rt = 1.06 min; MS (ESIpos): m/z = 433.4 [M+H]+ RP-HPLC (方法D,鹼性) 47%產率 |
| 24 | 外消旋-2-[N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-(三氟甲氧基)苯胺基]丙醯胺 | 中間物27; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.17 (d,J =7.35 Hz, 3 H), 5.05 (q,J =7.18 Hz, 1 H), 7.28 (s, 1 H), 7.36 - 7.42 (m, 3 H), 7.45 - 7.52 (m, 4 H), 7.61 (s, 1 H), 7.69 - 7.75 (m, 2 H), 8.16 (br s, 2 H)。 LC-MS (方法2)Rt = 1.20 min; MS (ESIpos): m/z = 451.5 [M+H]+ RP-HPLC (方法D,鹼性) 49%產率 |
| 25 | 外消旋-2-(N-[4-胺基-5-(3,4-二氟苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物28; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 5.02 - 5.10 (m, 1 H), 7.26 (s, 1 H), 7.34 (t,J =8.62 Hz, 3 H), 7.41 - 7.49 (m, 1 H), 7.52 (ddd,J =11.15, 7.98, 2.15 Hz, 1 H), 7.58 (s, 1 H), 7.62 - 7.66 (m, 2 H), 7.98 - 8.50 (m, 2 H)。 LC-MS (方法2)Rt = 1.14 min; MS (ESIpos): m/z = 419.3 [M+H]+ RP-HPLC (方法D,鹼性) 30%產率 |
| 26 | 外消旋-2-(N-[4-胺基-5-(3,4-二氯苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物29, 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 5.00 - 5.11 (m, 1 H), 7.26 (s, 1 H), 7.34 (t,J =8.74 Hz, 2 H), 7.44 (dd,J =8.36, 2.03 Hz, 1 H), 7.57 - 7.61 (m, 1 H), 7.62 - 7.66 (m, 2 H), 7.67 (d,J =11.66 Hz, 1 H), 7.67 (d,J =1.27 Hz, 1 H), 8.03 - 8.48 (m, 2 H)。 LC-MS (方法2)Rt = 1.24 min; MS (ESIpos): m/z = 453.1 [M+H]+ RP-HPLC (方法D,鹼性) 38%產率 |
| 27 | 外消旋-2-[N-[4-胺基-5-(4-氟苯甲醯基)噻唑-2-基]-4-(三氟甲氧基)苯胺基]丙醯胺 | 中間物30; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.15 - 1.19 (m, 3 H), 5.02 - 5.09 (m, 1 H), 7.22 (t,J =8.87 Hz, 2 H), 7.28 (s, 1 H), 7.50 (d,J =8.11 Hz, 2 H), 7.56 (dd,J =8.62, 5.58 Hz, 2 H), 7.61 (s, 1 H), 7.73 (d,J =9.13 Hz, 2 H), 7.90 - 8.49 (m, 2 H)。 LC-MS (方法2)Rt = 1.23 min; MS (ESIpos): m/z = 469.3 [M+H]+ 59%產率 |
| 27.1 及27.2 | (R)-2-[N-[4-胺基-5-(4-氟苯甲醯基)噻唑-2-基]-4-(三氟甲氧基)苯胺基]丙醯胺及 (S)-2-[N-[4-胺基-5-(4-氟苯甲醯基)噻唑-2-基]-4-(三氟甲氧基)苯胺基]丙醯胺 | ||
| 27.1 | 2-[N-[4-胺基-5-(4-氟苯甲醯基)噻唑-2-基]-4-(三氟甲氧基)苯胺基]丙醯胺(鏡像異構物1) | 實例27 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.17 (d,J =7.35 Hz, 3 H), 5.05 (q,J =7.27 Hz, 1 H), 7.22 (t,J =9.00 Hz, 2 H), 7.28 (s, 1 H), 7.48 - 7.53 (m, 2 H), 7.53 - 7.59 (m, 2 H), 7.61 (s, 1 H), 7.70 - 7.75 (m, 2 H), 7.95 - 8.42 (m, 2 H)。 LC-MS (方法1)Rt = 1.23 min; MS (ESIpos): m/z = 469.3 [M+H]+ 39%產率 |
| 對掌性HPLC實例27.1 在對掌性管柱上HPLC分離外消旋-2-[N-[4-胺基-5-(4-氟苯甲醯基)噻唑-2-基]-4-(三氟甲氧基)苯胺基]丙醯胺(1130 mg,2.4 mmol;實例27),得到448 mg (39%產率) 2-[N-[4-胺基-5-(4-氟苯甲醯基)噻唑-2-基]-4-(三氟甲氧基)苯胺基]丙醯胺,鏡像異構物1。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:YMC Cellulose SB 5µ,250×30;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:乙醇+ 0.1 vol%二乙胺;等度:80% A+20% B;流速:60 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 2.99 min 儀器:Waters Alliance 2695;管柱:YMC Cellulose SB 3µ,100×4.6; 溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:乙醇;等度:80% A+20% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 27.2 | 2-[N-[4-胺基-5-(4-氟苯甲醯基)噻唑-2-基]-4-(三氟甲氧基)苯胺基]丙醯胺(鏡像異構物2) | 實例27 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.17 (d,J =7.60 Hz, 3 H), 5.05 (br d,J =7.10 Hz, 1 H), 7.19 - 7.25 (m, 2 H), 7.28 (s, 1 H), 7.47 - 7.53 (m, 2 H), 7.53 - 7.59 (m, 2 H), 7.59 - 7.63 (m, 1 H), 7.70 - 7.76 (m, 2 H), 7.96 - 8.40 (m, 2 H)。 LC-MS (方法1)Rt = 1.23 min; MS (ESIpos): m/z = 469.2 [M+H]+ 37%產率 |
| 對掌性HPLC實例27.2 在對掌性管柱上HPLC分離外消旋-2-[N-[4-胺基-5-(4-氟苯甲醯基)噻唑-2-基]-4-(三氟甲氧基)苯胺基]丙醯胺(1130 mg,2.4 mmol;實例27),得到430 mg (37%產率) 2-[N-[4-胺基-5-(4-氟苯甲醯基)噻唑-2-基]-4-(三氟甲氧基)苯胺基]丙醯胺,鏡像異構物2。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:YMC Cellulose SB 5µ,250×30;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:乙醇+ 0.1 vol%二乙胺;等度:80% A+20% B;流速:60 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 3.81 min 儀器:Waters Alliance 2695;管柱:YMC Cellulose SB 3µ,100×4.6; 溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:乙醇;等度:80% A+20% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 28 | 外消旋-2-[N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-(三氟甲基)苯胺基]丙醯胺 | 中間物31; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.18 (d,J =7.35 Hz, 3 H), 5.06 (q,J =7.52 Hz, 1 H), 7.30 (s, 1 H), 7.36 - 7.44 (m, 3 H), 7.47 - 7.52 (m, 2 H), 7.63 (s, 1 H), 7.80 - 7.91 (m, 4 H), 8.18 (br s, 2 H)。 LC-MS (方法1)Rt = 1.18 min; MS (ESIpos): m/z = 435.3 [M+H]+ RP-HPLC (方法D,鹼性) 29%產率 |
| 29 | 外消旋-2-(N-[4-胺基-5-[6-(三氟甲基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物32; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.16 (d,J =7.60 Hz, 3 H), 5.02 - 5.13 (m, 1 H), 7.25 (s, 1 H), 7.30 - 7.38 (m, 2 H), 7.60 (s, 1 H), 7.64 (dd,J =8.87, 5.07 Hz, 2 H), 7.94 (d,J =7.86 Hz, 1 H), 8.12 (dd,J =8.11, 1.77 Hz, 1 H), 8.23 - 8.46 (m, 2 H), 8.84 (br d,J =1.80 Hz, 1 H)。 LC-MS (方法1)Rt = 1.13 min; MS (ESIpos): m/z = 454.5 [M+H]+ RP-HPLC (方法C,鹼性) 42%產率 |
| 29.1 及29.2 | (R)-2-(N-[4-胺基-5-[6-(三氟甲基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺及 (S)-2-(N-[4-胺基-5-[6-(三氟甲基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | ||
| 29.1 | 2-(N-[4-胺基-5-[6-(三氟甲基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺(鏡像異構物1) | 實例29 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 5.00 - 5.16 (m, 1 H), 7.27 (s, 1 H), 7.33 (t,J =8.74 Hz, 2 H), 7.58 - 7.69 (m, 3 H), 7.93 (d,J =8.11 Hz, 1 H), 8.11 (br d,J =1.77 Hz, 1 H), 8.17 - 8.50 (m, 2 H), 8.84 (d,J =1.27 Hz, 1 H)。 LC-MS (方法1)Rt = 1.13 min; MS (ESIpos): m/z = 454.5 [M+H]+ [α]D 20 = +53.2° (c = 1.00,二甲基亞碸) 13%產率 |
| 對掌性HPLC實例29.1 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-[6-(三氟甲基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺(394 mg,1.0 mmol;實例29),得到163 mg (33%產率) 2-(N-[4-胺基-5-[6-(三氟甲基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺,鏡像異構物1。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:YMC Cellulose SB 10µ,250×50;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:2-丙醇+ 0.1 vol%二乙胺;等度:60% A+40% B;流速:140 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 2.24 min 儀器:Waters Alliance 2695;管柱:YMC Cellulose SB 3µ,100×4.6; 溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:2-丙醇;等度:60% A+40% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 29.2 | 2-(N-[4-胺基-5-[6-(三氟甲基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺(鏡像異構物2) | 實例29 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.17 (d,J =7.35 Hz, 3 H), 5.01 - 5.17 (m, 1 H), 7.28 (s, 1 H), 7.33 (t,J =8.74 Hz, 2 H), 7.54 - 7.72 (m, 3 H), 7.93 (d,J =8.11 Hz, 1 H), 8.12 (dd,J =8.11, 1.77 Hz, 1 H), 8.21 - 8.54 (m, 2 H), 8.84 (d,J =1.27 Hz, 1 H)。 LC-MS (方法1)Rt = 1.12 min; MS (ESIpos): m/z = 454.5 [M+H]+ [α]D 20 = -44.3° (c = 1.00,二甲基亞碸) 13%產率 |
| 對掌性HPLC實例29.2 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-[6-(三氟甲基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺(394 mg,1.0 mmol;實例29),得到164 mg (33%產率) 2-(N-[4-胺基-5-[6-(三氟甲基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺,鏡像異構物2。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:YMC Cellulose SB 10µ,250×50;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:2-丙醇+ 0.1 vol%二乙胺;等度:60% A+40% B;流速:140 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 3.26 min 儀器:Waters Alliance 2695;管柱:YMC Cellulose SB 3µ,100×4.6; 溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:2-丙醇;等度:60% A+40% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 30 | 外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-氯-2-氟-苯胺基)丙醯胺 | 中間物33; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.11 - 1.22 (m, 3 H), 4.92 - 5.22 (m, 1 H), 7.28 - 7.36 (m, 1 H), 7.39 - 7.54 (m, 6 H), 7.59 - 7.76 (m, 2 H), 7.79 - 7.93 (m, 1 H), 7.97 - 8.32 (m, 2 H)。 LC-MS (方法1)Rt = 1.16 min; MS (ESIpos): m/z = 417.2 [M+H]+ RP-HPLC (方法D,鹼性) 37%產率 |
| 31 | 外消旋-2-(N-[4-胺基-5-(茚烷-5-羰基)噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物34; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.15 (d,J =7.35 Hz, 3 H), 1.98 (quin,J =7.41 Hz, 2 H), 2.82 (td,J =7.29, 4.18 Hz, 4 H), 5.04 (br q,J =6.67 Hz, 1 H), 7.18 - 7.23 (m, 2 H), 7.24 (s, 1 H), 7.29 - 7.35 (m, 3 H), 7.56 - 7.59 (m, 1 H), 7.60 - 7.65 (m, 2 H), 7.80 - 8.40 (m, 2 H)。 LC-MS (方法2)Rt = 1.23 min; MS (ESIpos): m/z = 425.6 [M+H]+ RP-HPLC (方法D,鹼性) 24%產率 |
| 32 | 外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-3,4-二氟-苯胺基)丙醯胺 | 中間物35; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.18 (d,J =7.35 Hz, 3 H), 5.02 (q,J =7.69 Hz, 1 H), 7.29 (s, 1 H), 7.36 - 7.44 (m, 3 H), 7.47 - 7.53 (m, 3 H), 7.54 - 7.60 (m, 1 H), 7.61 - 7.65 (m, 1 H), 7.77 (ddd,J =11.47, 7.54, 2.28 Hz, 1 H), 8.15 (br s, 2 H)。 LC-MS (方法1)Rt = 1.11 min; MS (ESIpos): m/z = 403.3 [M+H]+ RP-HPLC (方法C,鹼性) 48%產率 |
| 33 | 外消旋-2-(N-[4-胺基-5-(4-氰基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物36; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 4.90 - 5.24 (m, 1 H), 7.23 - 7.29 (m, 1 H), 7.33 (t,J =8.74 Hz, 2 H), 7.59 (s, 1 H), 7.60 - 7.66 (m, 4 H), 7.86 (d,J =8.36 Hz, 2 H), 8.05 - 8.57 (m, 2 H)。 LC-MS (方法2)Rt = 1.02 min; MS (ESIpos): m/z = 410.3 [M+H]+ RP-HPLC (方法C,鹼性) 78%產率 |
| 33.1 及33.2 | (R)-2-(N-[4-胺基-5-(4-氰基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺及 (S)-2-(N-[4-胺基-5-(4-氰基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺 | ||
| 33.1 | 2-(N-[4-胺基-5-(4-氰基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺(鏡像異構物1) | 實例33 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 5.02 - 5.11 (m, 1 H), 7.24 - 7.28 (m, 1 H), 7.33 (t,J =8.74 Hz, 2 H), 7.58 (s, 1 H), 7.61 - 7.66 (m, 4 H), 7.86 (d,J =8.62 Hz, 2 H), 8.05 - 8.50 (m, 2 H)。 LC-MS (方法2)Rt = 1.02 min; MS (ESIpos): m/z = 410.3 [M+H]+ [α]D 20 = +93.9° (c = 1.00,二甲基亞碸) 31%產率 |
| 對掌性HPLC實例33.1 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-(4-氰基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺(96 mg,0.23 mmol;實例33),得到30 mg (30%產率) 2-(N-[4-胺基-5-(4-氰基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺,鏡像異構物1。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:YMC Cellulose SB 10µ,250×50;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:乙醇;等度:60% A+40% B;流速:150 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 2.26 min 儀器:Waters Alliance 2695;管柱:YMC Cellulose SB 3µ,100×4.6; 溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:乙醇;等度:60% A+40% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 33.2 | 2-(N-[4-胺基-5-(4-氰基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺(鏡像異構物2) | 實例33 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.16 (d,J =7.60 Hz, 3 H), 5.01 - 5.12 (m, 1 H), 7.26 (s, 1 H), 7.33 (t,J =8.87 Hz, 2 H), 7.58 (s, 1 H), 7.63 (d,J =8.36 Hz, 4 H), 7.86 (d,J =8.36 Hz, 2 H), 8.05 - 8.53 (m, 2 H)。 LC-MS (方法2)Rt = 1.02 min; MS (ESIpos): m/z = 410.3 [M+H]+ [α]D 20 = -89.9° (c = 1.00,二甲基亞碸) 30%產率 |
| 對掌性HPLC實例33.2 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-(4-氰基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺(96 mg,0.23 mmol;實例33),得到32 mg (31%產率) 2-(N-[4-胺基-5-(4-氰基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺,鏡像異構物2。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:YMC Cellulose SB 10µ,250×50;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:乙醇;等度:60% A+40% B;流速:150 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 3.05 min 儀器:Waters Alliance 2695;管柱:YMC Cellulose SB 3µ,100×4.6; 溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:乙醇;等度:60% A+40% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 34 | 外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-氯-苯胺基)丙醯胺 | 中間物37; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 5.05 (q,J =7.18 Hz, 1 H), 7.26 (s, 1 H), 7.35 - 7.42 (m, 3 H), 7.47 - 7.50 (m, 2 H), 7.54 - 7.63 (m, 5 H), 8.16 (br s, 2 H)。 LC-MS (方法2)Rt = 1.15 min; MS (ESIpos): m/z = 402.2 [M+H]+ RP-HPLC (方法D,鹼性) 9%產率 |
| 35 | 外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-3,4-二氯-苯胺基)丙醯胺 | 中間物38; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.19 (d,J =7.35 Hz, 3 H), 5.01 (q,J =7.18 Hz, 1 H), 7.31 (s, 1 H), 7.37 - 7.45 (m, 3 H), 7.49 - 7.54 (m, 2 H), 7.62 (dd,J =8.90, 2.53 Hz, 1 H), 7.64 (s, 1 H), 7.79 (d,J =8.36 Hz, 1 H), 7.95 (d,J =2.28 Hz, 1 H), 8.24 (br s, 2 H)。 LC-MS (方法1)Rt = 1.23 min; MS (ESIneg): m/z = 433.4 [M-H]+ RP-HPLC (方法D,鹼性) 27%產率 |
| 36 | 外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-氯-3-氟-苯胺基)丙醯胺 | 中間物39; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.19 (d,J =7.35 Hz, 3 H), 5.02 (q,J =7.35 Hz, 1 H), 7.30 (s, 1 H), 7.38 - 7.45 (m, 3 H), 7.49 - 7.53 (m, 3 H), 7.63 (s, 1 H), 7.72 - 7.77 (m, 2 H), 8.15 (br s, 2 H)。 LC-MS (方法1)Rt = 1.17 min; MS (ESIpos): m/z = 419.3 [M+H]+ RP-HPLC (方法D,鹼性) 39%產率 |
| 37 | 外消旋-2-(N-[4-胺基-5-(4-氟苯甲醯基)噻唑-2-基]-4-氯-苯胺基)丙醯胺 | 中間物40; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.16 (d,J =7.60 Hz, 3 H), 5.02 - 5.11 (m, 1 H), 7.25 (s, 1 H), 7.33 (t,J =8.87 Hz, 2 H), 7.43 - 7.52 (m, 4 H), 7.58 (s, 1 H), 7.64 (dd,J =8.87, 5.07 Hz, 2 H), 7.98 - 8.43 (m, 2 H)。 LC-MS (方法2)Rt = 1.18 min; MS (ESIpos): m/z = 419.2 [M+H]+ 55%產率 |
| 37.1 及37.2 | (R)-2-(N-[4-胺基-5-(4-氟苯甲醯基)噻唑-2-基]-4-氯-苯胺基)丙醯胺及 (S)-2-(N-[4-胺基-5-(4-氟苯甲醯基)噻唑-2-基]-4-氯-苯胺基)丙醯胺 | ||
| 37.1 | 2-(N-[4-胺基-5-(4-氟苯甲醯基)噻唑-2-基]-4-氯-苯胺基)丙醯胺(鏡像異構物1) | 實例37 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.13 - 1.19 (m, 3 H), 5.01 - 5.11 (m, 1 H), 7.25 (s, 1 H), 7.33 (t,J =8.87 Hz, 2 H), 7.43 - 7.53 (m, 4 H), 7.58 (s, 1 H), 7.64 (dd,J =8.87, 5.07 Hz, 2 H), 7.88 - 8.52 (m, 2 H)。 LC-MS (方法1)Rt = 1.19 min; MS (ESIpos): m/z = 419.2 [M+H]+ 31%產率 |
| 對掌性HPLC實例37.1 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-(4-氟苯甲醯基)噻唑-2-基]-4-氯-苯胺基)丙醯胺(170 mg,0.41 mmol,實例37),得到54 mg (31%產率) 2-(N-[4-胺基-5-(4-氟苯甲醯基)噻唑-2-基]-4-氯-苯胺基)丙醯胺,鏡像異構物1。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:YMC Cellulose SB 5µ,250×30;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:乙醇+ 0.1 vol%二乙胺;等度:60% A+40% B;流速:50 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 1.66 min 儀器:Waters Alliance 2695;管柱:YMC Cellulose SB 3µ,100×4.6; 溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:乙醇;等度:60% A+40% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 37.2 | 2-(N-[4-胺基-5-(4-氟苯甲醯基)噻唑-2-基]-4-氯-苯胺基)丙醯胺(鏡像異構物2) | 實例37 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 5.01 - 5.11 (m, 1 H), 7.23 - 7.27 (m, 1 H), 7.33 (t,J =8.87 Hz, 2 H), 7.43 - 7.53 (m, 4 H), 7.58 (s, 1 H), 7.64 (dd,J =8.87, 5.07 Hz, 2 H), 7.92 - 8.37 (m, 2 H)。 LC-MS (方法1)Rt = 1.19 min; MS (ESIpos): m/z = 419.2 [M+H]+ 32%產率 |
| 對掌性HPLC實例37.2 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-(4-氟苯甲醯基)噻唑-2-基]-4-氯-苯胺基)丙醯胺(170 mg,0.41 mmol,實例37),得到57 mg (32%產率) 2-(N-[4-胺基-5-(4-氟苯甲醯基)噻唑-2-基]-4-氯-苯胺基)丙醯胺,鏡像異構物2。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:YMC Cellulose SB 5µ,250×30;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:乙醇+ 0.1 vol%二乙胺;等度:60% A+40% B;流速:50 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 2.20 min 儀器:Waters Alliance 2695;管柱:YMC Cellulose SB 3µ,100×4.6; 溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:乙醇;等度:60% A+40% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 38 | 外消旋-2-(N-[4-胺基-5-(4-氯苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物41; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.16 (d,J =7.60 Hz, 3 H), 5.01 - 5.12 (m, 1 H), 7.25 (s, 1 H), 7.29 - 7.37 (m, 2 H), 7.43 - 7.53 (m, 4 H), 7.58 (s, 1 H), 7.63 (dd,J= 8.87, 5.07 Hz; 2 H), 7.92 - 8.44 (m, 2 H)。 LC-MS (方法1)Rt = 1.19 min; MS (ESIpos): m/z = 419.2 [M+H]+ RP-HPLC (方法C,鹼性) 42%產率 |
| 38.1 及38.2 | (R)-2-(N-[4-胺基-5-(4-氯苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺及 (S)-2-(N-[4-胺基-5-(4-氯苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺 | ||
| 38.1 | 2-(N-[4-胺基-5-(4-氯苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺(鏡像異構物1) | 實例38 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 4.98 - 5.16 (m, 1 H), 7.25 (s, 1 H), 7.33 (t,J =8.87 Hz, 2 H), 7.43 - 7.52 (m, 4 H), 7.58 (s, 1 H), 7.63 (dd,J =8.87, 5.07 Hz, 2 H), 7.92 - 8.50 (m, 2 H)。 LC-MS (方法1)Rt = 1.19 min; MS (ESIpos): m/z = 419.2 [M+H]+ RP-HPLC (方法D,鹼性) 16%產率 |
| 對掌性HPLC實例38.1 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-(4-氯苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺(115 mg,0.27 mmol;實例38),隨後進行額外RP-HPLC,得到19 mg (16%產率) 2-(N-[4-胺基-5-(4-氯苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺,鏡像異構物1。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:YMC Cellulose SB 10µ,250×50;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:2-丙醇+ 0.1 vol%二乙胺;等度:60% A+40% B;流速:140 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 2.23 min 儀器:Waters Alliance 2695;管柱:YMC Cellulose SB 3µ,100×4.6; 溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:2-丙醇;等度:60% A+40% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 38.2 | 2-(N-[4-胺基-5-(4-氯苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺(鏡像異構物2) | 實例38 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 5.02 - 5.10 (m, 1 H), 7.25 (s, 1 H), 7.33 (t,J =8.87 Hz, 2 H), 7.43 - 7.52 (m, 4 H), 7.57 - 7.60 (m, 1 H), 7.63 (dd,J =8.87, 5.07 Hz, 2 H), 7.95 - 8.47 (m, 2 H)。 LC-MS (方法1)Rt = 1.19 min; MS (ESIpos): m/z = 419.2 [M+H]+ RP-HPLC (方法D,鹼性) 38%產率 |
| 對掌性HPLC實例38.2 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-(4-氯苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺(115 mg,0.27 mmol;實例38),隨後進行額外RP-HPLC,得到20 mg (17%產率) 2-(N-[4-胺基-5-(4-氯苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺,鏡像異構物2。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:YMC Cellulose SB 10µ,250×50;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:2-丙醇+ 0.1 vol%二乙胺;等度:60% A+40% B;流速:140 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 3.79 min 儀器:Waters Alliance 2695;管柱:YMC Cellulose SB 3µ,100×4.6; 溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:2-丙醇;等度:60% A+40% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 39 | 外消旋-2-[4-[4-胺基-2-(N-[2-胺基-1-甲基-2-側氧基-乙基]-4-氟-苯胺基)噻唑-5-羰基]苯氧基]-2-甲基-丙酸乙酯 | 中間物42; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.07 (t,J =7.10 Hz, 3 H), 1.15 (d,J =7.35 Hz, 3 H), 1.53 (s, 6 H), 4.12 (q,J =7.01 Hz, 2 H), 5.02 - 5.09 (m, 1 H), 6.72 - 6.76 (m, 2 H), 7.24 (s, 1 H), 7.33 (t,J =8.87 Hz, 2 H), 7.44 (d,J =8.87 Hz, 2 H), 7.58 (s, 1 H), 7.63 (dd,J =9.00, 5.20 Hz, 2 H), 7.88 (br s, 2 H)。 LC-MS (方法1)Rt = 1.21 min; MS (ESIpos): m/z = 515.4 [M+H]+ RP-HPLC (方法D,鹼性) 50%產率 |
| 40 | 外消旋-2-(N-[4-胺基-5-[4-(三氟甲氧基)苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物43; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 5.06 (br d,J =6.84 Hz, 1 H), 7.26 (s, 1 H), 7.33 (t,J =8.74 Hz, 2 H), 7.38 (d,J =7.86 Hz, 2 H), 7.58 (s, 1 H), 7.60 - 7.67 (m, 4 H), 7.95 - 8.56 (m, 2 H)。 LC-MS (方法1)Rt = 1.25 min; MS (ESIpos): m/z = 469.5 [M+H]+ RP-HPLC (方法D,鹼性) 83%產率 |
| 40.1 及40.2 | (R)-2-(N-[4-胺基-5-[4-(三氟甲氧基)苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺及 (S)-2-(N-[4-胺基-5-[4-(三氟甲氧基)苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | ||
| 40.1 | 2-(N-[4-胺基-5-[4-(三氟甲氧基)苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺(鏡像異構物1) | 實例40 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 5.02 - 5.11 (m, 1 H), 7.26 (s, 1 H), 7.33 (t,J =8.74 Hz, 2 H), 7.38 (d,J =8.11 Hz, 2 H), 7.58 (s, 1 H), 7.60 - 7.67 (m, 4 H), 7.95 - 8.46 (m, 2 H)。 LC-MS (方法2)Rt = 1.24 min; MS (ESIpos): m/z = 469.4 [M+H]+ 20%產率 |
| 對掌性HPLC實例40.1 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-[4-(三氟甲氧基)苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺(69 mg,0.15 mmol;實例40),得到20 mg (20%產率) 2-(N-[4-胺基-5-[4-(三氟甲氧基)苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺,鏡像異構物1。 製備型對掌性 HPLC 儀器:Sepiatec:Prep SFC100;管柱:Chiralpak IC 5µ 250×30mm;溶離劑A:CO2 ;溶離劑B:乙醇+ 0.2 vol%氨水(32%);等度:15% B;流速:100 mL/min;溫度:40℃;BPR:150巴;UV:254 nm 分析型對掌性 HPLC : Rt = 2.73 min 儀器:Agilent:1260,Aurora SFC-模組;管柱:Chiralpak IC 5µ 100×4.6mm;溶離劑A:CO2 ;溶離劑B:乙醇+ 0.2 vol%氨水(32%);等度:15% B;流速:4 mL/min;溫度:37.5℃;BPR:100巴;UV:254 nm | |||
| 40.2 | 2-(N-[4-胺基-5-[4-(三氟甲氧基)苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺(鏡像異構物2) | 實例40 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 5.02 - 5.11 (m, 1 H), 7.26 (s, 1 H), 7.33 (t,J =8.87 Hz, 2 H), 7.38 (d,J =8.11 Hz, 2 H), 7.58 (s, 1 H), 7.60 - 7.67 (m, 4 H), 7.95 - 8.48 (m, 2 H)。 LC-MS (方法2)Rt = 1.25 min; MS (ESIpos): m/z = 469.3 [M+H]+ 21%產率 |
| 對掌性HPLC實例40.2 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-[4-(三氟甲氧基)苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺(69 mg,0.15 mmol;實例40),得到20 mg (21%產率) 2-(N-[4-胺基-5-[4-(三氟甲氧基)苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺,鏡像異構物2。 製備型對掌性 HPLC 儀器:Sepiatec:Prep SFC100;管柱:Chiralpak IC 5µ 250×30mm;溶離劑A:CO2 ;溶離劑B:乙醇+ 0.2 vol%氨水(32%);等度:15% B;流速:100 mL/min;溫度:40℃;BPR:150巴;UV:254 nm 分析型對掌性 HPLC : Rt = 3.48 min 儀器:Agilent:1260,Aurora SFC-模組;管柱:Chiralpak IC 5µ 100×4.6mm;溶離劑A:CO2 ;溶離劑B:乙醇+ 0.2 vol%氨水(32%);等度:15% B;流速:4 mL/min;溫度:37.5℃;BPR:100巴;UV:254 nm | |||
| 41 | 外消旋-2-(N-[4-胺基-5-(4-氯苯甲醯基)噻唑-2-基]-4-氯-苯胺基)丙醯胺 | 中間物44; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 5.06 (q,J =7.27 Hz, 1 H), 7.23 - 7.28 (m, 1 H), 7.44 - 7.53 (m, 4 H), 7.55 - 7.63 (m, 5 H), 7.96 - 8.44 (m, 2 H)。 LC-MS (方法2)Rt = 1.27 min; MS (ESIpos): m/z = 435.2 [M+H]+ 47%產率 |
| 41.1 及41.2 | (R)-2-(N-[4-胺基-5-(4-氯苯甲醯基)噻唑-2-基]-4-氯-苯胺基)丙醯胺及 (S)-2-(N-[4-胺基-5-(4-氯苯甲醯基)噻唑-2-基]-4-氯-苯胺基)丙醯胺 | ||
| 41.1 | 2-(N-[4-胺基-5-(4-氯苯甲醯基)噻唑-2-基]-4-氯-苯胺基)丙醯胺(鏡像異構物1) | 實例41 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.14 - 1.19 (m, 3 H), 5.06 (q,J =7.10 Hz, 1 H), 7.27 (s, 1 H), 7.44 - 7.53 (m, 4 H), 7.55 - 7.64 (m, 5 H), 7.99 - 8.41 (m, 2 H)。 LC-MS (方法1)Rt = 1.27 min; MS (ESIpos): m/z = 435.2 [M+H]+ [α]D 20 = +83.8° (c = 1.00,二甲基亞碸) 25%產率 |
| 對掌性HPLC實例41.1 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-(4-氯苯甲醯基)噻唑-2-基]-4-氯-苯胺基)丙醯胺(144 mg,0.33 mmol;實例41),得到36 mg (25%產率) 2-(N-[4-胺基-5-(4-氯苯甲醯基)噻唑-2-基]-4-氯-苯胺基)丙醯胺,鏡像異構物1。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:YMC Cellulose SB 10µ,250×50;溶離劑A:己烷;溶離劑B:乙醇;等度:60% A+40% B;流速:150 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 1.84 min 儀器:Waters Alliance 2695;管柱:YMC Cellulose SB 3µ,100×4.6;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:乙醇;等度:60% A+40% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 41.2 | 2-(N-[4-胺基-5-(4-氯苯甲醯基)噻唑-2-基]-4-氯-苯胺基)丙醯胺(鏡像異構物2) | 實例41 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 5.06 (q,J =7.10 Hz, 1 H), 7.26 - 7.29 (m, 1 H), 7.44 - 7.52 (m, 4 H), 7.55 - 7.63 (m, 5 H), 7.94 - 8.68 (m, 2 H)。 LC-MS (方法1)Rt = 1.27 min; MS (ESIpos): m/z = 435.2 [M+H]+ [α]D 20 = -78.4° (c = 1.00,二甲基亞碸) 18%產率 |
| 對掌性HPLC實例41.2 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-(4-氯苯甲醯基)噻唑-2-基]-4-氯-苯胺基)丙醯胺(144 mg,0.33 mmol;實例41),得到26 mg (18%產率) 2-(N-[4-胺基-5-(4-氯苯甲醯基)噻唑-2-基]-4-氯-苯胺基)丙醯胺,鏡像異構物2。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:YMC Cellulose SB 10µ,250×50;溶離劑A:己烷;溶離劑B:乙醇;等度:60% A+40% B;流速:150 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 2.34 min 儀器:Waters Alliance 2695;管柱:YMC Cellulose SB 3µ,100×4.6;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:乙醇;等度:60% A+40% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 42 | 外消旋-2-(N-[4-胺基-5-[4-(三氟甲基)苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物45; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 5.00 - 5.13 (m, 1 H), 7.26 (s, 1 H), 7.33 (t,J =8.87 Hz, 2 H), 7.59 (s, 1 H), 7.64 (dd,J =8.87, 5.07 Hz, 2 H), 7.72 (dd,J =37.13, 8.24 Hz, 4 H), 7.98 - 8.51 (m, 2 H)。 LC-MS (方法1)Rt = 1.22 min; MS (ESIpos): m/z = 453.4 [M+H]+ RP-HPLC (方法D,鹼性) 71%產率 |
| 43 | 外消旋-2-[N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-(三氟甲基)苯胺基]丙醯胺 | 中間物46; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.18 (d,J =7.35 Hz, 3 H), 5.07 (q,J =7.27 Hz, 1 H), 7.28 (t,J =72.24 Hz, 1 H), 7.18 (d,J =9.38 Hz, 2 H), 7.30 (s, 1 H), 7.57 (d,J =8.87 Hz, 2 H), 7.64 (s, 1 H), 7.86 (dd,J =27.88, 8.36 Hz, 4 H), 8.18 (br s, 2 H)。 LC-MS (方法1)Rt = 1.22 min; MS (ESIpos): m/z = 501.4 [M+H]+ RP-HPLC (方法D,鹼性) 54%產率 |
| 43.1 及43.2 | (R)-2-[N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-(三氟甲基)苯胺基]丙醯胺及 (S)-2-[N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-(三氟甲基)苯胺基]丙醯胺 | ||
| 43.1 | 2-[N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-(三氟甲基)苯胺基]丙醯胺(鏡像異構物1) | 實例43 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.18 (d,J =7.35 Hz, 3 H), 5.07 (q,J =7.35 Hz, 1 H), 7.28 (t,J =74.01 Hz, 1 H), 7.18 (d,J =8.62 Hz, 2 H), 7.31 (s, 1 H), 7.57 (d,J =8.87 Hz, 2 H), 7.63 (s, 1 H), 7.86 (dd,J =27.88, 8.62 Hz, 4 H), 7.99 - 8.36 (m, 2 H)。 LC-MS (方法1)Rt = 1.22 min; MS (ESIpos): m/z = 501.4 [M+H]+ 34%產率 |
| 對掌性HPLC實例43.1 在對掌性管柱上HPLC分離外消旋-2-[N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-(三氟甲基)苯胺基]丙醯胺(280 mg,0.56 mmol;實例43),得到99 mg (35%產率) 2-[N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-(三氟甲基)苯胺基]丙醯胺,鏡像異構物1。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:YMC Cellulose SB 5µ,250×30;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:乙醇+ 0.1 vol%二乙胺;等度:80% A+20% B;流速:50 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 4.50 min 儀器:Waters Alliance 2695;管柱:YMC Cellulose SB 3µ,100×4.6; 溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:乙醇;等度:80% A+20% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 43.2 | 2-[N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-(三氟甲基)苯胺基]丙醯胺(鏡像異構物2) | 實例43 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.18 (d,J =7.35 Hz, 3 H), 5.07 (q,J =7.35 Hz, 1 H), 7.28 (t,J =73.76 Hz, 1 H), 7.18 (d,J =8.62 Hz, 2 H), 7.31 (s, 1 H), 7.57 (d,J =8.87 Hz, 2 H), 7.63 (s, 1 H), 7.86 (dd,J =27.88, 8.62 Hz, 4 H), 8.18 (br s, 2 H)。 LC-MS (方法1)Rt = 1.22 min; MS (ESIpos): m/z = 501.3 [M+H]+ 27%產率 |
| 對掌性HPLC實例43.2 在對掌性管柱上HPLC分離外消旋-2-[N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-(三氟甲基)苯胺基]丙醯胺(280 mg,0.56 mmol;實例43),得到79 mg (27%產率) 2-[N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-(三氟甲基)苯胺基]丙醯胺,鏡像異構物2。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:YMC Cellulose SB 5µ,250×30;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:乙醇+ 0.1 vol%二乙胺;等度:80% A+20% B;流速:50 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 5.44 min 儀器:Waters Alliance 2695;管柱:YMC Cellulose SB 3µ,100×4.6; 溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:乙醇;等度:80% A+20% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 44 | 外消旋-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物47; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 5.06 (q,J =7.10 Hz, 1 H), 7.28 (t,J =73.76 Hz, 1 H), 7.17 (d,J =8.62 Hz, 2 H), 7.25 (br s, 1 H), 7.33 (t,J =8.87 Hz, 2 H), 7.55 (d,J =8.87 Hz, 2 H), 7.58 (br s, 1 H), 7.64 (dd,J =8.87, 5.07 Hz, 2 H), 8.21 (br s, 2 H)。 LC-MS (方法2)Rt = 1.13 min; MS (ESIpos): m/z = 451.6 [M+H]+ RP-HPLC (方法D,鹼性) 87%產率 |
| 44.1 及44.2 | (R)-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺及 (S)-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | ||
| 44.1 | 2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺(鏡像異構物1) | 實例44 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 5.02 - 5.10 (m, 1 H), 7.26 (t,J =74.01 Hz, 1 H), 7.17 (d,J =9.38 Hz, 2 H), 7.25 (s, 1 H), 7.33 (t,J =8.74 Hz, 2 H), 7.55 (d,J =8.87 Hz, 2 H), 7.58 (br s, 1 H), 7.64 (dd,J =8.87, 5.07 Hz, 2 H), 7.86 - 8.45 (m, 2 H)。 LC-MS (方法2)Rt = 1.12 min; MS (ESIpos): m/z = 451.3 [M+H]+ [α]D 20 = +77.2° (c = 1.00,二甲基亞碸) 38%產率 |
| 對掌性HPLC實例44.1 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺(2552 mg,5.61 mmol;實例44),得到1096 mg (35%產率) 2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺,鏡像異構物1。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:YMC Cellulose SB 10µ,250×50;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:2-丙醇+ 0.1 vol%二乙胺;等度:60% A+40% B;流速:140 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 2.81 min 儀器:Waters Alliance 2695;管柱:YMC Cellulose SB 3µ,100×4.6; 溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:2-丙醇;等度:80% A+20% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 44.2 | 2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺(鏡像異構物2) | 實例44 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 5.01 - 5.12 (m, 1 H), 7.28 (t,J =73.76 Hz, 1 H), 7.17 (d,J =8.62 Hz, 2 H), 7.25 (s, 1 H), 7.33 (t,J =8.87 Hz, 2 H), 7.55 (d,J =8.87 Hz, 2 H), 7.58 (br s, 1 H), 7.64 (dd,J =8.87, 5.07 Hz, 2 H), 8.15 (br s, 2 H)。 LC-MS (方法2)Rt = 1.12 min; MS (ESIpos): m/z = 451.4 [M+H]+ [α]D 20 = -79.7° (c = 1.00,二甲基亞碸) 38%產率 |
| 對掌性HPLC實例44.2 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺(2552 mg,5.61 mmol;實例44),得到1139 mg (37%產率) 2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺,鏡像異構物2。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:YMC Cellulose SB 10µ,250×50;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:2-丙醇+ 0.1 vol%二乙胺;等度:60% A+40% B;流速:140 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 4.61 min 儀器:Waters Alliance 2695;管柱:YMC Cellulose SB 3µ,100×4.6; 溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:2-丙醇;等度:80% A+20% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 45 | 2-(N-[4-胺基-5-[4-[2-胺基-1-甲基-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]苯胺基)丙醯胺(立體異構物之混合物) | 中間物48; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 1.41 (d,J =6.59 Hz, 3 H), 4.63 (q,J =6.59 Hz, 1 H), 5.04 - 5.12 (m, 1 H), 6.86 (d,J =8.87 Hz, 2 H), 7.24 (br d,J =3.80 Hz, 2 H), 7.42 - 7.52 (m, 6 H), 7.53 - 7.58 (m, 3 H), 8.08 (br s, 2 H)。 LC-MS (方法2)Rt = 0.85 min; MS (ESIpos): m/z = 454.4 [M+H]+ RP-HPLC (方法C,鹼性) 70%產率 |
| 45.1 、45.2 、45.3 及45.4 | (2R)-(N-[4-胺基-5-[4-[2-胺基-(1R)-甲基-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]苯胺基)丙醯胺, (2R)-(N-[4-胺基-5-[4-[2-胺基-(1S)-甲基-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]苯胺基)丙醯胺, (2S)-(N-[4-胺基-5-[4-[2-胺基-(1R)-甲基-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]苯胺基)丙醯胺,及 (2S)-(N-[4-胺基-5-[4-[2-胺基-(1S)-甲基-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]苯胺基)丙醯胺 | ||
| 45.1 | 2-(N-[4-胺基-5-[4-[2-胺基-1-甲基-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]苯胺基)丙醯胺(立體異構物1) | 實例45 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 1.41 (d,J =6.59 Hz, 3 H), 4.63 (q,J =6.76 Hz, 1 H), 5.08 (q,J =7.35 Hz, 1 H), 6.86 (d,J =8.87 Hz, 2 H), 7.23 (br d,J =3.30 Hz, 2 H), 7.43 - 7.52 (m, 6 H), 7.53 - 7.60 (m, 3 H), 7.75 - 8.37 (m, 2 H)。 LC-MS (方法1)Rt = 0.86 min; MS (ESIpos): m/z = 454.3 [M+H]+ 4%產率 |
| 對掌性HPLC實例45.1 在對掌性管柱上HPLC分離2-(N-[4-胺基-5-[4-[2-胺基-1-甲基-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]苯胺基)丙醯胺(立體異構物之混合物;449 mg,0.99 mmol;實例45),得到29 mg (6%產率) 2-(N-[4-胺基-5-[4-[2-胺基-1-甲基-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]苯胺基)丙醯胺,鏡像異構物1。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:YMC Amylose SA 10µ,250×50;溶離劑A:甲基三級丁基醚;溶離劑B:乙腈;等度:80% A+20% B;流速:100 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 6.48 min 儀器:Waters Alliance 2695;管柱:YMC Amylose SA 3µ,100×4.6;溶離劑A:甲基三級丁基醚;溶離劑B:乙腈;等度:80% A+20% B;流速:1.4 ml/min;溫度:25℃;UV:254 nm | |||
| 45.2 | 2-(N-[4-胺基-5-[4-[2-胺基-1-甲基-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]苯胺基)丙醯胺(立體異構物2) | 實例45 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 1.41 (d,J =6.59 Hz, 3 H), 4.63 (q,J =6.59 Hz, 1 H), 5.08 (q,J =7.27 Hz, 1 H), 6.86 (d,J =8.87 Hz, 2 H), 7.23 (br d,J =4.82 Hz, 2 H), 7.42 - 7.52 (m, 6 H), 7.55 (br d,J =1.27 Hz, 3 H), 8.14 (br s, 2 H)。 LC-MS (方法1)Rt = 0.85 min; MS (ESIpos): m/z = 454.3 [M+H]+ 5%產率 |
| 對掌性HPLC實例45.2 在對掌性管柱上HPLC分離2-(N-[4-胺基-5-[4-[2-胺基-1-甲基-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]苯胺基)丙醯胺(立體異構物之混合物;449 mg,0.99 mmol;實例45),得到36 mg (7%產率) 2-(N-[4-胺基-5-[4-[2-胺基-1-甲基-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]苯胺基)丙醯胺,鏡像異構物2。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:YMC Amylose SA 10µ,250×50;溶離劑A:甲基三級丁基醚;溶離劑B:乙腈;等度:80% A+20% B;流速:100 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 6.48 min 儀器:Waters Alliance 2695;管柱:YMC Amylose SA 3µ,100×4.6;溶離劑A:甲基三級丁基醚;溶離劑B:乙腈;等度:80% A+20% B;流速:1.4 ml/min;溫度:25℃;UV:254 nm | |||
| 45.3 | 2-(N-[4-胺基-5-[4-[2-胺基-1-甲基-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]苯胺基)丙醯胺(立體異構物3) | 實例45 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 1.41 (d,J =6.59 Hz, 3 H), 4.59 - 4.66 (m, 1 H), 5.08 (q,J =7.77 Hz, 1 H), 6.86 (d,J =8.87 Hz, 2 H), 7.23 (br d,J =4.06 Hz, 2 H), 7.42 - 7.52 (m, 6 H), 7.53 - 7.59 (m, 3 H), 8.05 (br s, 2 H)。 LC-MS (方法1)Rt = 0.85 min; MS (ESIpos): m/z = 454.3 [M+H]+ 5%產率 |
| 對掌性HPLC實例45.3 在對掌性管柱上HPLC分離2-(N-[4-胺基-5-[4-[2-胺基-1-甲基-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]苯胺基)丙醯胺(立體異構物之混合物;449 mg,0.99 mmol;實例45),得到36 mg (8%產率) 2-(N-[4-胺基-5-[4-[2-胺基-1-甲基-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]苯胺基)丙醯胺,鏡像異構物3。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:YMC Amylose SA 10µ,250×50;溶離劑A:甲基三級丁基醚;溶離劑B:乙腈;等度:80% A+20% B;流速:100 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 6.48 min 儀器:Waters Alliance 2695;管柱:YMC Amylose SA 3µ,100×4.6;溶離劑A:甲基三級丁基醚;溶離劑B:乙腈;等度:80% A+20% B;流速:1.4 ml/min;溫度:25℃;UV:254 nm | |||
| 45.4 | 2-(N-[4-胺基-5-[4-[2-胺基-1-甲基-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]苯胺基)丙醯胺(立體異構物4) | 實例45 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 1.41 (d,J =6.59 Hz, 3 H), 4.63 (q,J =6.59 Hz, 1 H), 5.08 (q,J =6.93 Hz, 1 H), 6.86 (d,J =8.87 Hz, 2 H), 7.23 (br d,J =3.04 Hz, 2 H), 7.43 - 7.52 (m, 6 H), 7.53 - 7.58 (m, 3 H), 8.04 (br s, 2 H)。 LC-MS (方法2)Rt = 0.86 min; MS (ESIpos): m/z = 454.3 [M+H]+ 5%產率 |
| 對掌性HPLC實例45.4 在對掌性管柱上HPLC分離2-(N-[4-胺基-5-[4-[2-胺基-1-甲基-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]苯胺基)丙醯胺(立體異構物之混合物;449 mg,0.99 mmol;實例45),得到36 mg (8%產率) 2-(N-[4-胺基-5-[4-[2-胺基-1-甲基-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]苯胺基)丙醯胺,鏡像異構物4。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:YMC Amylose SA 10µ,250×50;溶離劑A:甲基三級丁基醚;溶離劑B:乙腈;等度:80% A+20% B;流速:100 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 6.48 min 儀器:Waters Alliance 2695;管柱:YMC Amylose SA 3µ,100×4.6;溶離劑A:甲基三級丁基醚;溶離劑B:乙腈;等度:80% A+20% B;流速:1.4 ml/min;溫度:25℃;UV:254 nm | |||
| 46 | 外消旋-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-氯-2-氟-苯胺基)丙醯胺 | 中間物49; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.17 (s, 3 H), 4.98 - 5.23 (m, 1 H), 7.30 (br t,J =73.76 Hz, 1 H), 7.19 (br d,J =8.36 Hz, 2 H), 7.32 (br s, 1 H), 7.48 (br d,J =8.90 Hz, 1 H), 7.59 (br d,J =7.35 Hz, 2 H), 7.65 (br s, 1 H), 7.71 (br d,J =9.12 Hz, 1 H), 7.80 - 7.91 (m, 1 H), 8.18 (br s, 2 H)。 LC-MS (方法1)Rt = 1.21 min; MS (ESIpos): m/z = 485.3 [M+H]+ RP-HPLC (方法D,鹼性) 40%產率 |
| 46.1 及46.2 | (R)-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-氯-2-氟-苯胺基)丙醯胺及 (S)-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-氯-2-氟-苯胺基)丙醯胺 | ||
| 46.1 | 2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-氯-2-氟-苯胺基)丙醯胺(鏡像異構物1) | 實例46 | 1 H-NMR (400 MHz, DMSO-d6 ) δ ppm = 1.13 - 1.22 (m, 3 H), 5.02 - 5.22 (m, 1 H), 7.19 (br d,J =8.36 Hz, 2 H), 7.30 (t, 1 H), 7.32 (br s, 1 H), 7.47 - 7.50 (m, 1 H), 7.56 - 7.63 (m, 2 H), 7.63 - 7.67 (m, 1 H), 7.68 - 7.75 (m, 1 H), 7.81 - 7.94 (m, 1 H), 8.02 - 8.36 (m, 2 H)。 LC-MS (方法1)Rt = 1.21 min; MS (ESIpos): m/z = 485.3 [M+H]+ 35%產率 |
| 對掌性HPLC實例46.1 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-氯-2-氟-苯胺基)丙醯胺(253 mg,0.52 mmol;實例46),得到90 mg (35%產率) 2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-氯-2-氟-苯胺基)丙醯胺,鏡像異構物1。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:YMC Cellulose SB 5µ,250×30;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:乙醇+ 0.1 vol%二乙胺;等度:70% A+30% B;流速:40 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 2.42 min 儀器:Waters Alliance 2695;管柱:YMC Cellulose SB 3µ,100×4.6;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:乙醇;等度:70% A+30% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 46.2 | 2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-氯-2-氟-苯胺基)丙醯胺(鏡像異構物2) | 實例46 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.12 - 1.22 (m, 3 H), 4.97 - 5.23 (m, 1 H), 7.19 (br d,J =8.36 Hz, 2 H), 7.30 (s, 1 H), 7.32 (br s, 1 H), 7.47 - 7.51 (m, 1 H), 7.59 (br d,J =7.60 Hz, 2 H), 7.65 (br s, 1 H), 7.69 - 7.76 (m, 1 H), 7.82 - 7.92 (m, 1 H), 7.99 - 8.31 (m, 2 H)。 LC-MS (方法1)Rt = 1.21 min; MS (ESIpos): m/z = 485.2 [M+H]+ 52%產率 |
| 對掌性HPLC實例46.2 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-氯-2-氟-苯胺基)丙醯胺(253 mg,0.52 mmol;實例46),得到135 mg (52%產率) 2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-氯-2-氟-苯胺基)丙醯胺,鏡像異構物2。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:YMC Cellulose SB 5µ,250×30;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:乙醇+ 0.1 vol%二乙胺;等度:70% A+30% B;流速:40 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 3.13 min 儀器:Waters Alliance 2695;管柱:YMC Cellulose SB 3µ,100×4.6;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:乙醇;等度:70% A+30% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 47 | 外消旋-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-氯-苯胺基)丙醯胺 | 中間物50; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 5.06 (br q,J =7.27 Hz, 1 H), 7.28 (t,J =73.51 Hz, 1 H), 7.17 (d,J =8.62 Hz, 2 H), 7.26 (s, 1 H), 7.54 - 7.64 (m, 7 H), 8.14 (br s, 2 H)。 LC-MS (方法2)Rt = 1.19 min; MS (ESIpos): m/z = 467.3 [M+H]+ 40%產率 |
| 47.1 及47.2 | (R)-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-氯-苯胺基)丙醯胺及 (S)-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-氯-苯胺基)丙醯胺 | ||
| 47.1 | 2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-氯-苯胺基)丙醯胺(鏡像異構物1) | 實例47 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.17 (d,J =7.35 Hz, 3 H), 5.06 (q,J =7.18 Hz, 1 H), 7.28 (t,J =73.76 Hz, 1 H), 7.18 (d,J =8.62 Hz, 2 H), 7.27 (s, 1 H), 7.54 - 7.64 (m, 7 H), 8.14 (br s, 2 H)。 LC-MS (方法2)Rt = 1.19 min; MS (ESIpos): m/z = 467.2 [M+H]+ [α]D 20 = +73.5° (c = 1.00,二甲基亞碸). RP-HPLC (方法D,鹼性) 11%產率 |
| 對掌性HPLC實例47.1 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-氯-苯胺基)丙醯胺(524 mg,1.12 mmol;實例47),得到147 mg (29%產率) 2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-氯-苯胺基)丙醯胺,鏡像異構物1。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:YMC Cellulose SB 5µ,250×30;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:2-丙醇;等度:60% A+40% B;流速:40 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 2.99 min 儀器:Waters Alliance 2695;管柱:YMC Cellulose SB 3µ,100×4.6;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:2-丙醇;等度:60% A+40% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 47.2 | 2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-氯-苯胺基)丙醯胺(鏡像異構物2) | 實例47 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.17 (d,J =7.35 Hz, 3 H), 5.06 (q,J =7.18 Hz, 1 H), 7.28 (t,J =73.76 Hz, 1 H), 7.18 (d,J =8.62 Hz, 2 H), 7.27 (s, 1 H), 7.54 - 7.64 (m, 7 H), 8.14 (br s, 2 H)。 LC-MS (方法2)Rt = 1.19 min; MS (ESIpos): m/z = 467.2 [M+H]+ [α]D 20 = -67.1° (c = 1.00,二甲基亞碸). RP-HPLC (方法D,鹼性) 13%產率 |
| 對掌性HPLC實例47.2 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-氯-苯胺基)丙醯胺(524 mg,1.12 mmol;實例47),得到178 mg (34%產率) 2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-氯-苯胺基)丙醯胺,鏡像異構物2。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:YMC Cellulose SB 5µ,250×30;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:2-丙醇;等度:60% A+40% B;流速:40 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt =4.37 min 儀器:Waters Alliance 2695;管柱:YMC Cellulose SB 3µ,100×4.6;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:2-丙醇;等度:60% A+40% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 48 | 外消旋-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺 | 中間物51; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.19 (d,J =7.35 Hz, 3 H), 5.00 - 5.07 (m, 1 H), 7.29 (t,J =73.76 Hz, 1 H), 7.19 (d,J =8.62 Hz, 2 H), 7.30 (s, 1 H), 7.49 - 7.54 (m, 1 H), 7.58 (d,J =8.87 Hz, 2 H), 7.63 (s, 1 H), 7.73 - 7.79 (m, 2 H), 8.19 (br s, 2 H)。 LC-MS (方法1)Rt = 1.22 min; MS (ESIpos): m/z = 485.4 [M+H]+ RP-HPLC (方法D,鹼性) 25%產率 |
| 48.1 及48.2 | (R)-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺及 (S)-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺 | ||
| 48.1 | 2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺(鏡像異構物1) | 實例48 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.19 (d,J =7.60 Hz, 3 H), 5.03 (q,J =7.44 Hz, 1 H), 7.29 (t,J =73.76 Hz, 1 H), 7.19 (d,J =8.62 Hz, 2 H), 7.30 (s, 1 H), 7.49 - 7.54 (m, 1 H), 7.58 (d,J =8.87 Hz, 2 H), 7.63 (s, 1 H), 7.73 - 7.78 (m, 2 H), 8.17 (br s, 2 H)。 LC-MS (方法1)Rt = 1.22 min; MS (ESIpos): m/z = 485.2 [M+H]+ 19%產率 |
| 對掌性HPLC實例48.1 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺(144 mg,0.3 mmol;實例48),得到29 mg (20%產率) 2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺,鏡像異構物1。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:YMC Amylose SA 5µ,250×30;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:85% A+15% B;流速:50 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt =1.54 min 儀器:Waters Alliance 2695;管柱:YMC Amylose SA 3µ,100×4.6;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:85% A+15% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 48.2 | 2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺(鏡像異構物2) | 實例48 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.19 (d,J =7.35 Hz, 3 H), 5.03 (q,J =7.10 Hz, 1 H), 7.29 (t,J =73.76 Hz, 1 H), 7.19 (d,J =8.87 Hz, 2 H), 7.30 (s, 1 H), 7.51 (dt,J =8.62, 1.27 Hz, 1 H), 7.58 (d,J =8.62 Hz, 2 H), 7.63 (s, 1 H), 7.73 - 7.79 (m, 2 H), 8.18 (br s, 2 H)。 LC-MS (方法1)Rt = 1.22 min; MS (ESIpos): m/z = 485.3 [M+H]+ 24%產率 |
| 對掌性HPLC實例48.2 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺(144 mg,0.3 mmol;實例48),得到36 mg (24%產率) 2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺,鏡像異構物2。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:YMC Amylose SA 5µ,250×30;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:85% A+15% B;流速:50 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt =2.09 min 儀器:Waters Alliance 2695;管柱:YMC Amylose SA 3µ,100×4.6;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:85% A+15% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 49 | 外消旋-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺 | 中間物52; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.18 (d,J =7.35 Hz, 3 H), 5.03 (q,J =6.76 Hz, 1 H), 7.28 (t,J =73.76 Hz, 1 H), 7.18 (d,J =8.62 Hz, 2 H), 7.30 (s, 1 H), 7.48 - 7.53 (m, 1 H), 7.58 (d,J =8.62 Hz, 4 H), 7.78 (ddd,J =11.34, 7.41, 2.53 Hz, 1 H), 8.13 (br s, 2 H)。 LC-MS (方法1)Rt = 1.16 min; MS (ESIpos): m/z = 469.3 [M+H]+ RP-HPLC (方法D,鹼性) 65%產率 |
| 49.1 及49.2 | (R)-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺及 (S)-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺 | ||
| 49.1 | 2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺(鏡像異構物1) | 實例49 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.18 (d,J =7.35 Hz, 3 H), 5.03 (br q,J =7.18 Hz, 1 H), 7.29 (t,J =73.51 Hz, 3 H), 7.18 (d,J =8.36 Hz, 1 H), 7.30 (s, 1 H), 7.48 - 7.53 (m, 1 H), 7.56 - 7.64 (m, 4 H), 7.78 (ddd,J =11.34, 7.54, 2.41 Hz, 1 H), 8.17 (br s, 2 H)。 LC-MS (方法1)Rt = 1.16 min; MS (ESIpos): m/z = 469.3 [M+H]+ 39%產率 |
| 對掌性HPLC實例49.1 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺(381 mg,0.81 mmol;實例49),得到155 mg (39%產率) 2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺,鏡像異構物1。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:YMC Cellulose SB 5µ,250×30;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:乙醇+ 0.1 vol%二乙胺;等度:80% A+20% B;流速:50 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 4.31 min 儀器:Waters Alliance 2695;管柱:YMC Cellulose SB 3µ,100×4.6;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:乙醇;等度:80% A+20% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 49.2 | 2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺(鏡像異構物2) | 實例49 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.18 (d,J =7.35 Hz, 3 H), 5.03 (q,J =7.35 Hz, 1 H), 7.28 (t,J =74.01 Hz, 1 H), 7.18 (d,J =8.62 Hz, 2 H), 7.30 (s, 1 H), 7.48 - 7.53 (m, 1 H), 7.55 - 7.65 (m, 4 H), 7.78 (ddd,J =11.34, 7.54, 2.41 Hz, 1 H), 8.19 (br s, 2 H)。 LC-MS (方法1)Rt = 1.16 min; MS (ESIpos): m/z = 469.3 [M+H]+ 34%產率 |
| 對掌性HPLC實例49.2 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺(381 mg,0.81 mmol;實例49),得到136 mg (34%產率) 2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺,鏡像異構物2。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:YMC Cellulose SB 5µ,250×30;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:乙醇+ 0.1 vol%二乙胺;等度:80% A+20% B;流速:50 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 5.54 min 儀器:Waters Alliance 2695;管柱:YMC Cellulose SB 3µ,100×4.6;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:乙醇;等度:80% A+20% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 49.2 | 藉助於X射線晶體結構分析,判定實例49.2為(R)-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺。 | ||
| 50 | 外消旋-2-(N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺 | 中間物53; 外消旋-2-溴丙醯胺 | 1 H-NMR (400MHz, DMSO-d6 ): δ ppm = 1.18 (d,J =7.60 Hz, 3 H), 5.03 (q,J =7.35 Hz, 1 H), 7.30 (s, 1 H), 7.40 - 7.44 (m, 2 H), 7.47 - 7.53 (m, 1 H), 7.55 - 7.66 (m, 2 H), 7.77 (ddd,J =11.34, 7.54, 2.41 Hz, 1 H), 8.13 - 8.49 (m, 2 H), 8.60 - 8.66 (m, 2 H)。 LC-MS (方法2)Rt = 0.90 min; MS (ESIpos): m/z = 404.3 [M+H]+ 97%產率 |
| 50.1 及50.2 | (R)-2-(N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺及 (S)-2-(N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺 | ||
| 50.1 | 2-(N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺(鏡像異構物1) | 實例50 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.18 (d,J =7.35 Hz, 3 H), 5.03 (br q,J =7.27 Hz, 1 H), 7.30 (s, 1 H), 7.40 - 7.45 (m, 2 H), 7.47 - 7.53 (m, 1 H), 7.55 - 7.65 (m, 2 H), 7.78 (br ddd,J =11.34, 7.54, 2.41 Hz, 1 H), 8.17 - 8.47 (m, 2 H), 8.60 - 8.66 (m, 2 H)。 LC-MS (方法2)Rt = 0.87 min; MS (ESIpos): m/z = 404.2 [M+H]+ [α]D 20 = -79.8° (c = 1.00,二甲基亞碸) 21%產率 |
| 對掌性HPLC實例50.1 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺(974 mg,2.35 mmol;實例50),得到205 mg (21%產率) 2-(N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺,鏡像異構物1。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:YMC Cellulose SC 10µ,250×50;溶離劑A:甲基三級丁基醚;溶離劑B:乙腈;等度:20% A+80% B;流速:140 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 2.71 min 儀器:Thermo Fisher UltiMate 3000;管柱:YMC Cellulose SC 3µ,100×4.6;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:20% A+80% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 50.2 | 2-(N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺(鏡像異構物2) | 實例50 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.18 (d,J =7.60 Hz, 3 H), 5.03 (q,J =6.67 Hz, 1 H), 7.30 (s, 1 H), 7.40 - 7.44 (m, 2 H), 7.47 - 7.53 (m, 1 H), 7.55 - 7.65 (m, 2 H), 7.77 (ddd,J =11.34, 7.54, 2.41 Hz, 1 H), 8.14 - 8.46 (m, 2 H), 8.60 - 8.66 (m, 2 H)。 LC-MS (方法2)Rt = 0.87 min; MS (ESIpos): m/z = 404.2 [M+H]+ [α]D 20 = +84.9° (c = 1.00,二甲基亞碸) 21%產率 |
| 對掌性HPLC實例50.2 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺(974 mg,2.35 mmol;實例50),得到204 mg (21%產率) 2-(N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺,鏡像異構物2。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:YMC Cellulose SC 10µ,250×50;溶離劑A:甲基三級丁基醚;溶離劑B:乙腈;等度:20% A+80% B;流速:140 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 3.06 min 儀器:Thermo Fisher UltiMate 3000;管柱:YMC Cellulose SC 3µ,100×4.6;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:20% A+80% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 51 | 外消旋-2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺 | 中間物54; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.18 (d,J =7.60 Hz, 3 H), 3.76 (s, 3 H), 5.02 (q,J =7.27 Hz, 1 H), 6.94 (d,J =8.87 Hz, 2 H), 7.29 (s, 1 H), 7.50 (d,J =8.62 Hz, 3 H), 7.56 - 7.65 (m, 2 H), 7.78 (ddd,J =11.41, 7.48, 2.41 Hz, 1 H), 7.89 - 8.45 (m, 2 H) LC-MS (方法2)Rt = 1.09 min; MS (ESIpos): m/z = 433.2 [M+H]+ 85%產率 |
| 51.1 及51.2 | (R)-2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺及 (S)-2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺 | ||
| 51.1 | 2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺(鏡像異構物1) | 實例51 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.19 (d,J =7.35 Hz, 3 H), 3.76 (s, 3 H), 5.03 (q,J =7.18 Hz, 1 H), 6.94 (d,J =8.87 Hz, 2 H), 7.29 (s, 1 H), 7.48 - 7.53 (m, 3 H), 7.55 - 7.64 (m, 2 H), 7.78 (ddd,J =11.47, 7.41, 2.41 Hz, 1 H), 7.87 - 8.36 (m, 2 H)。 LC-MS (方法1)Rt = 1.10 min; MS (ESIpos): m/z = 433.5 [M+H]+ 33%產率 |
| 對掌性HPLC實例51.1 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺(88 mg,0.20 mmol;實例51),得到19 mg (21%產率) 2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺,鏡像異構物1。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:YMC Cellulose SC 10µ,250×50;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:50% A+50% B;流速:100 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt =1.57 min 儀器:Waters Alliance 2695;管柱:YMC Cellulose SC 3µ,100×4.6;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:50% A+50% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 51.2 | 2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺(鏡像異構物2) | 實例51 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.19 (d,J =7.35 Hz, 3 H), 3.76 (s, 3 H), 5.03 (q,J =7.10 Hz, 1 H), 6.94 (d,J =8.87 Hz, 2 H), 7.29 (s, 1 H), 7.48 - 7.53 (m, 3 H), 7.56 - 7.65 (m, 2 H), 7.75 - 7.82 (m, 1 H), 7.89 - 8.38 (m, 2 H)。 LC-MS (方法1)Rt = 1.10 min; MS (ESIpos): m/z = 433.5 [M+H]+ 36%產率 |
| 對掌性HPLC實例51.2 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺(88 mg,0.20 mmol;實例51),得到22 mg (24%產率) 2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺,鏡像異構物2。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:YMC Cellulose SC 10µ,250×50;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:50% A+50% B;流速:100 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 1.84 min 儀器:Waters Alliance 2695;管柱:YMC Cellulose SC 3µ,100×4.6;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:50% A+50% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 52 | 外消旋-2-(N-[4-胺基-5-(6-甲氧基吡啶-3-羰基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺 | 中間物55; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.19 (d,J =7.35 Hz, 3 H), 3.86 (s, 3 H), 5.03 (q,J =7.69 Hz, 1 H), 6.84 (dd,J =8.62, 0.76 Hz, 1 H), 7.30 (s, 1 H), 7.49 - 7.54 (m, 1 H), 7.56 - 7.65 (m, 2 H), 7.79 (ddd,J =11.41, 7.35, 2.53 Hz, 1 H), 7.84 (dd,J =8.62, 2.28 Hz, 1 H), 8.16 (br s, 2 H), 8.36 (dd,J =2.41, 0.63 Hz, 1 H)。 LC-MS (方法1)Rt = 1.07 min; MS (ESIpos): m/z = 434.3 [M+H]+ RP-HPLC (方法C,鹼性) 48%產率 |
| 52.1 及52.2 | (R)-2-(N-[4-胺基-5-(6-甲氧基吡啶-3-羰基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺及 (S)-2-(N-[4-胺基-5-(6-甲氧基吡啶-3-羰基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺 | ||
| 52.1 | 2-(N-[4-胺基-5-(6-甲氧基吡啶-3-羰基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺(鏡像異構物1) | 實例52 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.19 (d,J =7.35 Hz, 3 H), 3.86 (s, 3 H), 5.03 (q,J =6.84 Hz, 1 H), 6.84 (dd,J =8.49, 0.63 Hz, 1 H), 7.30 (s, 1 H), 7.49 - 7.54 (m, 1 H), 7.56 - 7.65 (m, 2 H), 7.79 (ddd,J =11.34, 7.54, 2.41 Hz, 1 H), 7.84 (dd,J =8.62, 2.28 Hz, 1 H), 7.97 - 8.32 (m, 2 H), 8.35 - 8.37 (m, 1 H)。 LC-MS (方法1)Rt = 1.07 min; MS (ESIpos): m/z = 434.3 [M+H]+ 31%產率 |
| 對掌性HPLC實例52.1 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-(6-甲氧基吡啶-3-羰基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺(31 mg,0.07 mmol;實例52),得到9 mg (27%產率) 2-(N-[4-胺基-5-(6-甲氧基吡啶-3-羰基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺,鏡像異構物1。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:YMC Amylose SA 5µ,250×30;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈+ 0.1 vol%二乙胺;等度:50% A+50% B;流速:40 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 1.25 min 儀器:Waters Alliance 2695;管柱:YMC Amylose SA 3µ,100×4.6;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:50% A+50% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 52.2 | 2-(N-[4-胺基-5-(6-甲氧基吡啶-3-羰基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺(鏡像異構物2) | 實例52 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.19 (d,J =7.35 Hz, 3 H), 3.86 (s, 3 H), 5.03 (q,J =6.93 Hz, 1 H), 6.82 - 6.86 (m, 1 H), 7.30 (s, 1 H), 7.49 - 7.54 (m, 1 H), 7.56 - 7.64 (m, 2 H), 7.79 (ddd,J =11.28, 7.48, 2.28 Hz, 1 H), 7.84 (dd,J =8.62, 2.53 Hz, 1 H), 7.96 - 8.31 (m, 2 H), 8.36 (d,J =2.03 Hz, 1 H)。 LC-MS (方法1)Rt = 1.07 min; MS (ESIpos): m/z = 434.3 [M+H]+ 31%產率 |
| 對掌性HPLC實例52.2 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-(6-甲氧基吡啶-3-羰基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺(31 mg,0.07 mmol;實例52),得到7 mg (20%產率) 2-(N-[4-胺基-5-(6-甲氧基吡啶-3-羰基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺,鏡像異構物2。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:YMC Amylose SA 5µ,250×30;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈+ 0.1 vol%二乙胺;等度:50% A+50% B;流速:40 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 1.74 min 儀器:Waters Alliance 2695;管柱:YMC Amylose SA 3µ,100×4.6;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:50% A+50% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 53 | 外消旋-2-(N-[4-胺基-5-[6-(三氟甲基)吡啶-3-羰基]噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺 | 中間物56; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.19 (d,J =7.60 Hz, 3 H), 4.99 - 5.09 (m, 1 H), 7.31 (s, 1 H), 7.47 - 7.54 (m, 1 H), 7.55 - 7.67 (m, 2 H), 7.78 (ddd,J =11.22, 7.54, 2.53 Hz, 1 H), 7.95 (d,J =7.60 Hz, 1 H), 8.15 (dd,J =7.98, 1.90 Hz, 1 H), 8.24 - 8.49 (m, 2 H), 8.86 (d,J =1.77 Hz, 1 H)。 LC-MS (方法1)Rt = 1.16 min; MS (ESIpos): m/z = 472.3 [M+H]+ RP-HPLC (方法C,鹼性) 55%產率 |
| 53.1 及53.2 | (R)-2-(N-[4-胺基-5-[6-(三氟甲基)吡啶-3-羰基]噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺及 (S)-2-(N-[4-胺基-5-[6-(三氟甲基)吡啶-3-羰基]噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺 | ||
| 53.1 | 2-(N-[4-胺基-5-[6-(三氟甲基)吡啶-3-羰基]噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺(鏡像異構物1) | 實例53 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.19 (d,J =7.60 Hz, 3 H), 5.04 (br q,J =6.84 Hz, 1 H), 7.31 (s, 1 H), 7.48 - 7.53 (m, 1 H), 7.55 - 7.66 (m, 2 H), 7.78 (ddd,J =11.28, 7.48, 2.28 Hz, 1 H), 7.95 (dd,J =8.24, 0.63 Hz, 1 H), 8.15 (dd,J =7.98, 1.90 Hz, 1 H), 8.23 - 8.51 (m, 2 H), 8.86 (d,J =1.77 Hz, 1 H)。 LC-MS (方法1)Rt = 1.13 min; MS (ESIpos): m/z = 472.2 [M+H]+ 30%產率 |
| 對掌性HPLC實例53.1 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-[6-(三氟甲基)吡啶-3-羰基]噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺(164 mg,0.35 mmol;實例53),得到51 mg (30%產率) 2-(N-[4-胺基-5-[6-(三氟甲基)吡啶-3-羰基]噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺,鏡像異構物1。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:YMC Amylose SA 5µ,250×30;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:50% A+50% B;流速:50 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 1.05 min 儀器:Waters Alliance 2695;管柱:YMC Amylose SA 3µ,100×4.6;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:50% A+50% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 53.2 | 2-(N-[4-胺基-5-[6-(三氟甲基)吡啶-3-羰基]噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺(鏡像異構物2) | 實例53 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.19 (d,J =7.35 Hz, 3 H), 5.04 (br q,J =7.10 Hz, 1 H), 7.31 (s, 1 H), 7.46 - 7.53 (m, 1 H), 7.55 - 7.66 (m, 2 H), 7.78 (ddd,J =11.34, 7.54, 2.41 Hz, 1 H), 7.95 (dd,J =8.24, 0.63 Hz, 1 H), 8.15 (dd,J =7.98, 1.90 Hz, 1 H), 8.23 - 8.56 (m, 2 H), 8.86 (d,J =1.77 Hz, 1 H)。 LC-MS (方法1)Rt = 1.13 min; MS (ESIpos): m/z = 472.2 [M+H]+ 27%產率 |
| 對掌性HPLC實例53.2 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-[6-(三氟甲基)吡啶-3-羰基]噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺(164 mg,0.35 mmol;實例53),得到47 mg (27%產率) 2-(N-[4-胺基-5-[6-(三氟甲基)吡啶-3-羰基]噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺,鏡像異構物2。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:YMC Amylose SA 5µ,250×30;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:50% A+50% B;流速:50 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 1.36 min 儀器:Waters Alliance 2695;管柱:YMC Amylose SA 3µ,100×4.6;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:50% A+50% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 54 | 外消旋-2-(N-[5-[4-(二氟甲氧基)苯甲醯基]-4-甲基-噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物78; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.16 (d,J =7.60 Hz, 3 H), 2.28 (s, 3 H), 5.11 (q,J =7.10 Hz, 1 H), 7.15 - 7.25 (m, 3 H), 7.33 - 7.39 (m, 3 H), 7.61 - 7.71 (m, 5 H)。 LC-MS (方法1)Rt = 1.20 min; MS (ESIpos): m/z = 449.1 [M+H]+ RP-HPLC (方法D,鹼性) 52%產率 |
| 55 | 外消旋-2-(N-[5-[4-(二氟甲氧基)苯甲醯基]-4-甲基-噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺 | 中間物79; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.19 (d,J =7.35 Hz, 3 H), 2.27 (s, 3 H), 5.09 (q,J =7.27 Hz, 1 H), 7.16 - 7.38 (m, 4 H), 7.51 - 7.56 (m, 1 H), 7.58 - 7.69 (m, 4 H), 7.82 (ddd,J =11.34, 7.54, 2.41 Hz, 1 H)。 LC-MS (方法1)Rt = 1.23 min; MS (ESIpos): m/z = 466.3 [M+H]+ RP-HPLC (方法D,鹼性) 7%產率 |
| 55.1 及55.2 | (R)-2-(N-[5-[4-(二氟甲氧基)苯甲醯基]-4-甲基-噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺及(S)-2-(N-[5-[4-(二氟甲氧基)苯甲醯基]-4-甲基-噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺 | ||
| 55.1 | 2-(N-[5-[4-(二氟甲氧基)苯甲醯基]-4-甲基-噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺(鏡像異構物1) | 實例55 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.19 (d,J =7.35 Hz, 3 H), 2.27 (s, 3 H), 5.08 - 5.10 (m, 1 H), 7.20 - 7.24 (m, 3 H), 7.35 (t, J=72 Hz, 1 H), 7.52 - 7.54 (m, 1 H), 7.60 - 7.66 (m, 4 H), 7.81 - 7.83 (m, 1 H) LC-MS (方法1)Rt = 1.23 min MS (ESIpos): m/z = 468.5 [M+H]+ 35%產率 |
| 對掌性HPLC實例55.1 在對掌性管柱上HPLC分離外消旋-2-(N-[5-[4-(二氟甲氧基)苯甲醯基]-4-甲基-噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺(59 mg,0.13 mmol,實例55),得到21 mg (35%產率) 2-(N-[5-[4-(二氟甲氧基)苯甲醯基]-4-甲基-噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺,鏡像異構物1。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC-2;管柱:Chiralpak AS 5µ,250×20;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:2-丙醇;等度:80% A+20% B;流速:20 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 5.43 min 儀器:Thermo Fisher UltiMate 3000;管柱:Chiralpak AS 3µ,100×4.6;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:2-丙醇;等度:80% A+20% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 55.2 | 2-(N-[5-[4-(二氟甲氧基)苯甲醯基]-4-甲基-噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺丙醯胺(鏡像異構物2) | 實例55 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.19 (d,J =7.35 Hz, 3 H), 2.27 (s, 3 H), 5.08 - 5.10 (m, 1 H), 7.20 - 7.24 (m, 3 H), 7.35 (t, J=72 Hz, 1 H), 7.52 - 7.54 (m, 1 H), 7.60 - 7.66 (m, 4 H), 7.81 - 7.83 (m, 1 H) LC-MS (方法1)Rt = 1.23 min MS (ESIpos): m/z = 468.5 [M+H]+ 17%產率 |
| 對掌性HPLC實例55.2 在對掌性管柱上HPLC分離外消旋-2-(N-[5-[4-(二氟甲氧基)苯甲醯基]-4-甲基-噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺(59 mg,0.13 mmol,實例55),得到10 mg (17%產率) 2-(N-[5-[4-(二氟甲氧基)苯甲醯基]-4-甲基-噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺,鏡像異構物2。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC-2;管柱:Chiralpak AS 5µ,250×20;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:2-丙醇;等度:80% A+20% B;流速:20 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 9.88 min 儀器:Thermo Fisher UltiMate 3000;管柱:Chiralpak AS 3µ,100×4.6;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:2-丙醇;等度:80% A+20% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 56 | 外消旋-2-(N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺 | 中間物57; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.19 (d,J =7.35 Hz, 3 H), 5.03 (q,J =7.35 Hz, 1 H), 7.31 (s, 1 H), 7.43 (br d,J =4.31 Hz, 2 H), 7.49 - 7.53 (m, 1 H), 7.64 (s, 1 H), 7.71 - 7.78 (m, 2 H), 8.13 - 8.48 (m, 2 H), 8.63 (br s, 2 H)。 LC-MS (方法2)Rt = 0.96 min; MS (ESIpos): m/z = 420.3 [M+H]+ RP-HPLC (方法C,鹼性) 33%產率 |
| 56.1 及56.2 | (R)-2-(N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺及 (S)-2-(N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺 | ||
| 56.1 | 2-(N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺(鏡像異構物1) | 實施例56 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.19 (d,J =7.60 Hz, 3 H), 4.98 - 5.08 (m, 1 H), 7.31 (s, 1 H), 7.41 - 7.45 (m, 2 H), 7.48 - 7.53 (m, 1 H), 7.64 (s, 1 H), 7.72 - 7.77 (m, 2 H), 8.07 - 8.45 (m, 2 H), 8.62 - 8.65 (m, 2 H)。 LC-MS (方法2)Rt = 0.94 min; MS (ESIpos): m/z = 420.2 [M+H]+ 19%產率 |
| 對掌性HPLC實例56.1 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺(133 mg,0.32 mmol;實例56),得到26 mg (20%產率) 2-(N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺,鏡像異構物1。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:YMC Cellulose SC 10µ,250×50;溶離劑A:甲基三級丁基醚;溶離劑B:乙腈;等度:60% A+40% B;流速:140 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 3.10 min 儀器:Thermo Fisher UltiMate 3000;管柱:YMC Cellulose SC 3µ,100×4.6;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:60% A+40% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 56.2 | 2-(N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺(鏡像異構物2) | 實施例56 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.19 (d,J =7.60 Hz, 3 H), 5.03 (q,J =7.35 Hz, 1 H), 7.31 (s, 1 H), 7.40 - 7.46 (m, 2 H), 7.49 - 7.53 (m, 1 H), 7.64 (s, 1 H), 7.72 - 7.79 (m, 2 H), 8.12 - 8.47 (m, 2 H), 8.61 - 8.66 (m, 2 H) LC-MS (方法2)Rt = 0.94 min; MS (ESIpos): m/z = 420.2 [M+H]+ 20%產率 |
| 對掌性HPLC實例56.2 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺(133 mg,0.32 mmol;實例56),得到27 mg (20%產率) 2-(N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺,鏡像異構物2。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:YMC Cellulose SC 10µ,250×50;溶離劑A:甲基三級丁基醚;溶離劑B:乙腈;等度:60% A+40% B;流速:140 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt =3.34 min 儀器:Thermo Fisher UltiMate 3000;管柱:YMC Cellulose SC 3µ,100×4.6;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:60% A+40% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 57 | 外消旋-2-(N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-4-氯-苯胺基)丙醯胺 | 中間物58; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 5.06 (q,J =7.27 Hz, 1 H), 7.27 (s, 1 H), 7.41 (d,J =6.08 Hz, 2 H), 7.59 (d,J =10.90 Hz, 5 H), 8.08 - 8.48 (m, 2 H), 8.62 (d,J =6.08 Hz, 2 H)。 LC-MS (方法2)Rt = 0.91 min; MS (ESIpos): m/z = 402.2 [M+H]+ 50%產率 |
| 57.1 及57.2 | (R)-2-(N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-4-氯-苯胺基)丙醯胺及(S)-2-(N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-4-氯-苯胺基)丙醯胺 | ||
| 57.1 | 2-(N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-4-氯-苯胺基)丙醯胺(鏡像異構物1) | 實施例57 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.17 (d,J =7.35 Hz, 3 H), 5.06 (m, 1 H), 7.28 (s, 1 H), 7.41 (m, 2 H), 7.59 (m, 5 H), 8.28 (m, 2 H), 8.62 (m, 2 H) LC-MS (方法1)Rt = 0.85 min MS (ESIpos): m/z = 402.4 [M+H]+ [α]D 20 = -67° c = 8.2 mg/mL於DMSO中 38%產率 |
| 對掌性HPLC實例57.1 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-4-氯-苯胺基)丙醯胺(590 mg,1.47 mmol,實例57),得到234 mg (38%產率) 2-(N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-4-氯-苯胺基)丙醯胺,鏡像異構物1。 製備型對掌性 HPLC 儀器:Sepiatec:Prep SFC100;管柱:Chiralpak IG 5µ 250×30mm;溶離劑A:CO2 ;溶離劑B:乙醇+ 0.2 vol%氨水(32%);等度:30% B;流速:100 mL/min;溫度:40℃;BPR:150巴;UV:254 nm 分析型對掌性 HPLC : Rt = 4.76 min 儀器:Agilent:1260,Aurora SFC-模組;管柱:Chiralpak IG 5µ 100×4.6mm;溶離劑A:CO2 ;溶離劑B:乙醇+ 0.2 vol%氨水(32%);等度:30% B;流速:4 mL/min;溫度:37.5℃;BPR:100巴;UV:254 nm | |||
| 57.2 | 2-(N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-4-氯-苯胺基)丙醯胺(鏡像異構物2) | 實施例57 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.17 (d,J =7.35 Hz, 3 H), 5.06 (m, 1 H), 7.28 (s, 1 H), 7.41 (m, 2 H), 7.59 (m, 5 H), 8.28 (m, 2 H), 8.62 (m, 2 H) LC-MS (方法1)Rt = 0.85 min MS (ESIpos): m/z = 402.4 [M+H]+ [α]D 20 = 76° c = 9.6 mg/mL於DMSO中 36%產率 |
| 對掌性HPLC實例57.2 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-4-氯-苯胺基)丙醯胺(590 mg,1.47 mmol,實例57),得到225 mg (36%產率) 2-(N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-4-氯-苯胺基)丙醯胺,鏡像異構物2。 製備型對掌性 HPLC 儀器:Sepiatec:Prep SFC100;管柱:Chiralpak IG 5µ 250×30mm;溶離劑A:CO2 ;溶離劑B:乙醇+ 0.2 vol%氨水(32%);等度:30% B;流速:100 mL/min;溫度:40℃;BPR:150巴;UV:254 nm 分析型對掌性 HPLC : Rt = 2.59 min 儀器:Agilent:1260,Aurora SFC-模組;管柱:Chiralpak IG 5µ 100×4.6mm;溶離劑A:CO2 ;溶離劑B:乙醇+ 0.2 vol%氨水(32%);等度:30% B;流速:4 mL/min;溫度:37.5℃;BPR:100巴;UV:254 nm | |||
| 58 | 外消旋-2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-4-氯-苯胺基)丙醯胺 | 中間物59; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 3.76 (s, 3 H), 5.05 (q,J =7.18 Hz, 1 H), 6.93 (d,J =8.87 Hz, 2 H), 7.26 (s, 1 H), 7.49 (d,J =8.87 Hz, 2 H), 7.55 - 7.64 (m, 5 H), 7.82 - 8.39 (m, 2 H)。 LC-MS (方法2)Rt = 1.13 min; MS (ESIpos): m/z = 431.2 [M+H]+ 77%產率 |
| 58.1 及58.2 | (R)-2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-4-氯-苯胺基)丙醯胺及(S)-2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-4-氯-苯胺基)丙醯胺 | ||
| 58.1 | 2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-4-氯-苯胺基)丙醯胺(鏡像異構物1) | 實施例58 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 3.76 (s, 3 H), 5.06 (m, 1 H), 6.93 (m, 2 H), 7.25 (m, 1 H), 7.49 (m, 2 H), 7.60 (m, 5 H), 8.04 (m, 2 H) LC-MS (方法1)Rt = 1.14 min MS (ESIpos): m/z = 431.4 [M+H]+ [α]D 20 = - 80° c = 11.1 mg/mL於DMSO中 36%產率 |
| 對掌性HPLC實例58.1 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-4-氯-苯胺基)丙醯胺(2.83 g,6.57 mmol,實例58),得到1.03 g (36%產率) 2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-4-氯-苯胺基)丙醯胺,鏡像異構物1。 製備型對掌性 HPLC 儀器:Labomatic HD3000,Knauer Pump 100,Labcol Vario 4000 Plus,Knauer DAD 2600;管柱:Cellulose SB 5µ 250×50mm Nr.034;溶離劑A:己烷+ 0.1 Vol%二乙胺(99%);溶離劑B:乙醇+ 0.1 Vol%二乙胺(99%);等度:60% A+40% B;流速100.0 mL/min,UV:254 nm 分析型對掌性 HPLC : Rt = 4.15 min 儀器:Agilent HPLC 1260;管柱:Cellulose SB 3µ 100×4.6mm;溶離劑A:己烷+ 0.1 Vol%二乙胺(99%);溶離劑B:乙醇+ 0.1 Vol%二乙胺(99%);等度:60% A+40% B;流速1.0 mL/min;溫度:25℃;DAD 254 nm | |||
| 58.2 | 2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-4-氯-苯胺基)丙醯胺(鏡像異構物2) | 實施例58 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 3.76 (s, 3 H), 5.06 (m, 1 H), 6.93 (m, 2 H), 7.25 (m, 1 H), 7.49 (m, 2 H), 7.60 (m, 5 H), 8.04 (m, 2 H) LC-MS (方法1)Rt = 1.14 min MS (ESIpos): m/z = 431.4 [M+H]+ [α]D 20 = 79° c = 11.1 mg/mL於DMSO中 41%產率 |
| 對掌性HPLC實例58.2 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-4-氯-苯胺基)丙醯胺(2.83 g,6.57 mmol,實例58),得到1.18 g (41%產率) 2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-4-氯-苯胺基)丙醯胺,鏡像異構物2。 製備型對掌性 HPLC 儀器:Labomatic HD3000,Knauer Pump 100,Labcol Vario 4000 Plus,Knauer DAD 2600;管柱:Cellulose SB 5µ 250×50mm Nr.034;溶離劑A:己烷+ 0.1 Vol%二乙胺(99%);溶離劑B:乙醇+ 0.1 Vol%二乙胺(99%);等度:60% A+40% B;流速100.0 mL/min,UV:254 nm 分析型對掌性 HPLC : Rt = 3.40 min 儀器:Agilent HPLC 1260;管柱:Cellulose SB 3µ 100×4.6mm;溶離劑A:己烷+ 0.1 Vol%二乙胺(99%);溶離劑B:乙醇+ 0.1 Vol%二乙胺(99%);等度:60% A+40% B;流速1.0 mL/min;溫度:25℃;DAD 254 nm | |||
| 59 | 外消旋-2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺 | 中間物60; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.20 (d,J =7.35 Hz, 3 H), 3.77 (s, 3 H), 5.03 (q,J =7.35 Hz, 1 H), 6.94 (d,J =8.87 Hz, 2 H), 7.30 (s, 1 H), 7.49 - 7.53 (m, 3 H), 7.63 (s, 1 H), 7.73 - 7.79 (m, 2 H), 7.88 - 8.31 (m, 2 H)。 LC-MS (方法2)Rt = 1.17 min; MS (ESIpos): m/z = 449.3 [M+H]+ 83%產率 |
| 59.1 及59.2 | (R)-2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺及(S)-2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺 | ||
| 59.1 | 2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺(鏡像異構物1) | 實施例59 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.20 (d,J =7.35 Hz, 3 H), 3.76 (s, 3 H), 5.03 (q,J =7.35 Hz, 1 H), 6.94 (m, 2 H), 7.30 (s, 1 H), 7.52 (m, 3 H), 7.63 (s, 1 H), 7.75 (m, 2 H), 8.10 (m, 2 H) LC-MS (方法1)Rt = 1.16 min MS (ESIpos): m/z = 449.4 [M+H]+ [α]D 20 = -82° c = 8.2 mg/mL於DMSO中 29%產率 |
| 對掌性HPLC實例59.1 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺(442 mg,0.98 mmol,實例59),得到132 mg (29%產率) 2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺,鏡像異構物1。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC-4;管柱:YMC Amylose SA 5µ,250×30;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:70% A+30% B;流速:50 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 1.49 min 儀器:Waters Alliance 2695;管柱:YMC Amylose SA 3µ,100×4.6; 溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:70% A+30% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 59.1 | 藉助於X射線晶體結構分析,判定實例59.1為(R)-2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺。 | ||
| 59.2 | 2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺(鏡像異構物2) | 實施例59 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.20 (d,J =7.35 Hz, 3 H), 3.76 (s, 3 H), 5.03 (q,J =7.35 Hz, 1 H), 6.94 (m, 2 H), 7.30 (s, 1 H), 7.52 (m, 3 H), 7.63 (s, 1 H), 7.75 (m, 2 H), 8.10 (m, 2 H) LC-MS (方法1)Rt = 1.16 min MS (ESIpos): m/z = 449.4 [M+H]+ [α]D 20 = 87° c = 7.6 mg/mL於DMSO中 15%產率 |
| 對掌性HPLC實例59.2 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺(442 mg,0.98 mmol,實例59),得到68 mg (15%產率) 2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺,鏡像異構物2。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC-4;管柱:YMC Amylose SA 5µ,250×30;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:70% A+30% B;流速:50 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 2.03 min 儀器:Waters Alliance 2695;管柱:YMC Amylose SA 3µ,100×4.6; 溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:70% A+30% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 60 | 外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)苯胺基)丙醯胺 | 中間物83; 外消旋-2-溴丙醯胺 | 1 H-NMR (600 MHz, DMSO-d 6 ): δ ppm = 1.16 (d,J =7.25 Hz, 3 H), 5.09 (q,J =7.25 Hz, 1 H), 7.24 (s, 1 H), 7.35 - 7.40 (m, 3 H), 7.42 - 7.50 (m, 5 H), 7.54 - 7.57 (m, 3 H), 7.74 - 8.52 (m, 2 H)。 LC-MS (方法2)Rt = 1.02 min; MS (ESIpos): m/z = 367.1 [M+H]+ 製備型急驟層析(方法Z,0-3%) 46%產率 |
| 61 | 外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-氟-苯胺基)丙醯胺 | 中間物84; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 5.00 - 5.10 (m, 1 H), 7.25 (s, 1 H), 7.32 (t,J =8.87 Hz, 2 H), 7.35 - 7.42 (m, 3 H), 7.45 - 7.52 (m, 2 H), 7.58 (s, 1 H), 7.63 (dd,J =9.00, 5.20 Hz, 2 H), 7.80 - 8.46 (m, 2 H)。 LC-MS (方法2)Rt = 1.07 min; MS (ESIpos): m/z = 385.3 [M+H]+ 製備型急驟層析(方法Z,0-3%) 87%產率 |
| 61.1 及61.2 | (R)-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-氟-苯胺基)丙醯胺及 (S)-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-氟-苯胺基)丙醯胺 | ||
| 61.1 | 2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-氟-苯胺基)丙醯胺(鏡像異構物1) | 實例61 | 1 H-NMR (400 MHz, DMSO-d 6): δ ppm = 1.15 (d,J =7.60 Hz, 3 H), 5.02 - 5.09 (m, 1 H), 7.25 (s, 1 H), 7.32 (t,J =8.87 Hz, 2 H), 7.36 - 7.42 (m, 3 H), 7.46 - 7.50 (m, 2 H), 7.58 (s, 1 H), 7.63 (dd,J =8.74, 5.20 Hz, 2 H), 7.80 - 8.50 (m, 2 H)。 LC-MS (方法1)Rt = 1.07 min; MS (ESIpos): m/z = 385.5 [M+H]+ 24%產率 |
| 對掌性HPLC實例61.1 在對掌性管柱上HPLC分離外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-氟-苯胺基)丙醯胺(414 mg,1.08 mmol;實例61),得到139 mg (33%產率) 2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-氟-苯胺基)丙醯胺,鏡像異構物1。 製備型對掌性 HPLC 儀器:Sepiatec:Prep SFC100;管柱:Chiralpak IA 5µ 250×30mm;溶離劑A:CO2 ;溶離劑B:2-丙醇+ 0.4 vol%二乙胺;等度:25% B;流速:100 mL/min;溫度:40℃;BPR:150巴;UV:280 nm 分析型對掌性 HPLC : Rt = 2.10 min 儀器:安捷倫1260,Aurora SFC-模組;管柱Chiralpak IA 5µ 100×4.6mm;溶離劑A:CO2 ;溶離劑B:2-丙醇+ 0.4%二乙胺(99%);等度:25% B;流速:4 mL/min;溫度:37.5℃;BPR:100巴;UV:280 nm | |||
| 61.2 | 2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-氟-苯胺基)丙醯胺(鏡像異構物2) | 實例61 | 1 H-NMR (400 MHz, DMSO-d 6): δ ppm = 1.15 (d,J =7.60 Hz, 3 H), 5.02 - 5.09 (m, 1 H), 7.25 (s, 1 H), 7.32 (t,J =8.87 Hz, 2 H), 7.36 - 7.42 (m, 3 H), 7.46 - 7.50 (m, 2 H), 7.58 (s, 1 H), 7.63 (dd,J =8.74, 5.20 Hz, 2 H), 7.80 - 8.50 (m, 2 H)。 LC-MS (方法1)Rt = 1.07 min; MS (ESIpos): m/z = 385.5 [M+H]+ 26%產率 |
| 對掌性HPLC實例61.2 在對掌性管柱上HPLC分離外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-氟-苯胺基)丙醯胺(414 mg,1.08 mmol;實例61),得到103 mg (24%產率) 2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-氟-苯胺基)丙醯胺,鏡像異構物2。 製備型對掌性 HPLC 儀器:Sepiatec:Prep SFC100;管柱:Chiralpak IA 5µ 250×30mm;溶離劑A:CO2 ;溶離劑B:2-丙醇+ 0.4 vol%二乙胺;等度:25% B;流速:100 mL/min;溫度:40℃;BPR:150巴;UV:280 nm 分析型對掌性 HPLC : Rt = 3.08 min 儀器:Agilent:1260,Aurora SFC-模組;管柱:Chiralpak IA 5µ 100×4.6mm;溶離劑A:CO2 ;溶離劑B:2-丙醇+ 0.4%二乙胺(99%);等度:25% B;流速:4 mL/min;溫度:37.5℃;BPR:100巴;UV:280 nm | |||
| 61.2 | 藉助於X射線晶體結構分析,判定實例61.2為(R)-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-氟-苯胺基)丙醯胺。 | ||
| 62 | 外消旋-2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物85; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d 6): δ ppm = 1.16 (d,J =7.60 Hz, 3 H), 3.75 (s, 3 H), 5.06 (q,J =6.76 Hz, 1 H), 6.93 (d,J =8.87 Hz, 2 H), 7.22 - 7.27 (m, 1 H), 7.34 (t,J =8.87 Hz, 2 H), 7.48 (d,J =8.87 Hz, 2 H), 7.57 (s, 1 H), 7.64 (dd,J =8.87, 5.07 Hz, 2 H), 7.79 - 8.38 (m, 2 H)。 LC-MS (方法2)Rt = 1.06 min; MS (ESIpos): m/z = 415.5 [M+H]+ 製備型急驟層析(方法Z,0-3%) 49%產率 |
| 62.1 及62.2 | (R)-2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺及 (S)-2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺 | ||
| 62.1 | 2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺(鏡像異構物1) | 實例62 | 1 H-NMR (400 MHz, DMSO-d 6): δ ppm = 1.16 (d,J =7.60 Hz, 3 H), 3.75 (s, 3 H), 5.06 (q,J =6.76 Hz, 1 H), 6.93 (d,J =8.87 Hz, 2 H), 7.22 - 7.27 (m, 1 H), 7.34 (t,J =8.87 Hz, 2 H), 7.48 (d,J =8.87 Hz, 2 H), 7.57 (s, 1 H), 7.64 (dd,J =8.87, 5.07 Hz, 2 H), 7.79 - 8.38 (m, 2 H)。 [α]D 20 = -142.9° (c = 1.00,氯仿) 45%產率 |
| 對掌性HPLC實例62.1 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺(350 mg,0.80 mmol;實例62),得到135 mg (45%產率) 2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺,鏡像異構物1。 製備型對掌性 HPLC 儀器:Sepiatec:Prep SFC100;管柱:Chiralpak IA 5µ 250×30mm;溶離劑A:CO2 ;溶離劑B:2-丙醇+ 0.4 vol%二乙胺;等度:30% B;流速:100 mL/min;溫度:40℃;BPR:150巴;UV:254 nm 分析型對掌性 HPLC : Rt = 1.72 min 儀器:Agilent:1260,Aurora SFC-Modul;管柱:Chiralpak IA 5µ 100×4.6mm;溶離劑A:CO2 ;溶離劑B:2-丙醇+ 0.4 vol%二乙胺;等度:30% B;流速:4 mL/min;溫度:37.5℃;BPR:100巴;UV:254 nm | |||
| 62.2 | 2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺(鏡像異構物2) | 實例62 | 1 H-NMR (400 MHz, DMSO-d 6): δ ppm = 1.16 (d,J =7.60 Hz, 3 H), 3.75 (s, 3 H), 5.06 (q,J =6.76 Hz, 1 H), 6.93 (d,J =8.87 Hz, 2 H), 7.22 - 7.27 (m, 1 H), 7.34 (t,J =8.87 Hz, 2 H), 7.48 (d,J =8.87 Hz, 2 H), 7.57 (s, 1 H), 7.64 (dd,J =8.87, 5.07 Hz, 2 H), 7.79 - 8.38 (m, 2 H)。 [α]D 20 = +114.5° (c = 1.00,氯仿) 49%產率 |
| 對掌性HPLC實例62.2 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺(350 mg,0.80 mmol;實例62),得到15 mg (49%產率) 2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺,鏡像異構物2。 製備型對掌性 HPLC 儀器:Sepiatec:Prep SFC100;管柱:Chiralpak IA 5µ 250×30mm;溶離劑A:CO2 ;溶離劑B:2-丙醇+ 0.4 vol%二乙胺;等度:30% B;流速:100 mL/min;溫度:40℃;BPR:150巴;UV:254 nm 分析型對掌性 HPLC : Rt = 2.61 min 儀器:Agilent:1260,Aurora SFC-Modul;管柱:Chiralpak IA 5µ 100×4.6mm;溶離劑A:CO2 ;溶離劑B:2-丙醇+ 0.4 vol%二乙胺;等度:30% B;流速:4 mL/min;溫度:37.5℃;BPR:100巴;UV:254 nm | |||
| 62.2 | 藉助於X射線晶體結構分析,判定實例62.2為(R)-2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺。 | ||
| 63 | 外消旋-2-(N-[4-胺基-5-(4-甲基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物86; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.16 (d,J =7.60 Hz, 3 H), 2.29 (s, 3 H), 5.05 (q,J =6.67 Hz, 1 H), 7.18 (d,J =8.11 Hz, 2 H), 7.24 (s, 1 H), 7.32 (t,J =8.87 Hz, 2 H), 7.38 (d,J =8.11 Hz, 2 H), 7.57 (s, 1 H), 7.63 (dd,J =8.62, 5.07 Hz, 2 H), 8.10 (br s, 2 H)。 LC-MS (方法2)Rt = 1.15 min; MS (ESIpos): m/z = 399.3 [M+H]+ 製備型急驟層析(方法Z,0-3%) 18%產率 |
| 63.1 及63.2 | (R)-2-(N-[4-胺基-5-(4-甲基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺及 (S)-2-(N-[4-胺基-5-(4-甲基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺 | ||
| 63.1 | 2-(N-[4-胺基-5-(4-甲基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺(鏡像異構物1) | 實例63 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.16 (d,J =7.60 Hz, 3 H), 2.29 (s, 3 H), 5.05 (q,J =6.67 Hz, 1 H), 7.18 (d,J =8.11 Hz, 2 H), 7.24 (s, 1 H), 7.32 (t,J =8.87 Hz, 2 H), 7.38 (d,J =8.11 Hz, 2 H), 7.57 (s, 1 H), 7.63 (dd,J =8.62, 5.07 Hz, 2 H), 8.10 (br s, 2 H)。 [α]D 20 = -159.9° (c = 1.00,氯仿) 13%產率 |
| 對掌性HPLC實例63.1 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-(4-甲基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺(1.5 g,3.58 mmol;實例63),得到660 mg (45%產率) 2-(N-[4-胺基-5-(4-甲基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺,鏡像異構物1。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:YMC Cellulose SB 10µ,250×50;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:2-丙醇+ 0.1 vol%二乙胺;等度:60% A+40% B;流速:140 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 2.46 min 儀器:Waters Alliance 2695;管柱:YMC Cellulose SB 3µ,100×4.6;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:2-丙醇;等度:60% A+40% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 63.2 | 2-(N-[4-胺基-5-(4-甲基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺(鏡像異構物2) | 實例63 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.16 (d,J =7.60 Hz, 3 H), 2.29 (s, 3 H), 5.05 (q,J =6.67 Hz, 1 H), 7.18 (d,J =8.11 Hz, 2 H), 7.24 (s, 1 H), 7.32 (t,J =8.87 Hz, 2 H), 7.38 (d,J =8.11 Hz, 2 H), 7.57 (s, 1 H), 7.63 (dd,J =8.62, 5.07 Hz, 2 H), 8.10 (br s, 2 H)。 [α]D 20 = +147.0° (c = 1.00,氯仿) 13%產率 |
| 對掌性HPLC實例63.2 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-(4-甲基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺(1.5 g,3.58 mmol;實例63),得到680 mg (44%產率) 2-(N-[4-胺基-5-(4-甲基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺,鏡像異構物2。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:YMC Cellulose SB 10µ,250×50;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:2-丙醇+ 0.1 vol%二乙胺;等度:60% A+40% B;流速:140 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 3.69 min 儀器:Waters Alliance 2695;管柱:YMC Cellulose SB 3µ,100×4.6;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:2-丙醇;等度:60% A+40% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 64 | 外消旋-2-(N-[4-胺基-5-(4-氟苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物87; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 5.06 (br q,J =6.84 Hz, 1 H), 7.22 (t,J =8.87 Hz, 2 H), 7.25 (s, 1 H), 7.33 (t,J =8.87 Hz, 2 H), 7.55 (dd,J =8.74, 5.45 Hz, 2 H), 7.58 (br s, 1 H), 7.64 (dd,J =8.87, 5.07 Hz, 2 H), 7.86 - 8.56 (m, 2 H)。 LC-MS (方法2)Rt = 1.09 min; MS (ESIpos): m/z = 403.3 [M+H]+ 製備型急驟層析(方法Z,0-3%) 7%產率 |
| 65 | 外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-2,4-二氟-苯胺基)丙醯胺 | 中間物88; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, 氯仿-d ): δ ppm = 1.27 (d,J =7.10 Hz, 3 H), 5.23 (q,J =7.18 Hz, 1 H), 5.39 - 5.48 (m, 1 H), 6.58 - 6.70 (m, 1 H), 6.94 - 7.02 (m, 2 H), 7.33 - 7.43 (m, 4 H), 7.58 - 7.64 (m, 2 H) (NH2 missing). LC-MS (方法2)Rt = 1.08 min; MS (ESIpos): m/z = 403.3 [M+H]+ 製備型急驟層析(方法Z,0-3%) 29%產率 |
| 66 | 外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-甲氧基-苯胺基)丙醯胺 | 中間物89; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.15 (d,J =6.84 Hz, 3 H), 3.78 (s, 3 H), 5.06 (q,J =6.59 Hz, 1 H), 7.00 (d,J =9.12 Hz, 2 H), 7.21 (s, 1 H), 7.35 - 7.42 (m, 3 H), 7.43 - 7.49 (m, 4 H), 7.52 (s, 1 H), 7.65 - 8.49 (m, 2 H)。 LC-MS (方法2)Rt = 1.03 min; MS (ESIpos): m/z = 397.4 [M+H]+ 製備型急驟層析(方法Z,0-3%) 19%產率 |
| 67 | 外消旋-2-[(4-胺基-5-苯甲醯基-1,3-噻唑-2-基)(苯基)胺基]丁醯胺 | 中間物83; 外消旋-2-溴丁醯胺 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 0.84 (t,J =7.35 Hz, 3 H), 1.47 - 1.60 (m, 1 H), 1.69 - 1.81 (m, 1 H), 4.87 - 4.95 (m, 1 H), 7.30 (s, 1 H), 7.34 - 7.51 (m, 8 H), 7.54 - 7.58 (m, 3 H), 7.78 - 8.48 (m, 2 H)。 LC-MS (方法2)Rt = 1.09 min; MS (ESIpos): m/z = 381.3 [M+H]+ 製備型急驟層析(方法Z,0-3%) 43%產率 |
| 68 | 外消旋-2-[(4-胺基-5-苯甲醯基-1,3-噻唑-2-基)(4-氟苯基)胺基]丁醯胺 | 中間物84; 外消旋-2-溴丁醯胺 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 0.84 (t,J =7.35 Hz, 3 H), 1.46 - 1.58 (m, 1 H), 1.68 - 1.79 (m, 1 H), 4.85 - 4.92 (m, 1 H), 7.32 (s, 3 H), 7.37 - 7.42 (m, 3 H), 7.47 - 7.50 (m, 2 H), 7.59 (s, 1 H), 7.64 (dd,J =9.12, 5.07 Hz, 2 H), 7.83 - 8.36 (m, 2 H)。 LC-MS (方法2)Rt = 1.12 min; MS (ESIpos): m/z = 399.3 [M+H]+ 製備型急驟層析(方法Z,0-3%) 29%產率 |
| 69 | 2-(N-[4-胺基-5-[4-(2-胺基-1-甲基-2-側氧基-乙氧基)苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺(立體異構物之混合物) | 中間物90; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 1.41 (d,J =6.59 Hz, 3 H), 4.64 (q,J =6.59 Hz, 1 H), 5.05 (q,J =6.76 Hz, 1 H), 6.87 (d,J =8.87 Hz, 2 H), 7.25 (br s, 2 H), 7.33 (t,J =8.74 Hz, 2 H), 7.46 (d,J =8.62 Hz, 2 H), 7.50 (s, 1 H), 7.57 (s, 1 H), 7.64 (dd,J =9.00, 5.20 Hz, 2 H), 7.78 - 8.35 (m, 2 H)。 LC-MS (方法2)Rt = 0.87 min; MS (ESIpos): m/z = 472.2 [M+H]+ 製備型急驟層析(方法Z,0-8%) 28%產率 |
| 70 | 外消旋-2-{[4-胺基-5-(4-甲氧基苯甲醯基)-1,3-噻唑-2-基](4-氟苯基)胺基}丁醯胺 | 中間物85; 外消旋-2-溴丁醯胺 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 0.84 (t,J =7.22 Hz, 3 H), 1.46 - 1.58 (m, 1 H), 1.67 - 1.78 (m, 1 H), 3.76 (s, 3 H), 4.85 - 4.93 (m, 1 H), 6.93 (d,J =8.87 Hz, 2 H), 7.33 (t,J =8.74 Hz, 2 H), 7.32 (br s, 1 H), 7.49 (d,J =8.87 Hz, 2 H), 7.59 (s, 1 H), 7.65 (dd,J =9.00, 4.94 Hz, 2 H), 8.11 (br s, 2 H)。 LC-MS (方法2)Rt = 1.12 min; MS (ESIpos): m/z = 429.3 [M+H]+ 製備型急驟層析(方法Z,0-3%) 28%產率 |
| 71 | 2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-氟-苯胺基)乙醯胺 | 中間物84; 2-溴乙醯胺 | 1 H-NMR (500 MHz, DMSO-d 6 ): δ ppm = 4.44 (s, 2 H), 7.23 (s, 1 H), 7.32 (t,J =8.67 Hz, 2 H), 7.38 - 7.43 (m, 3 H), 7.50 - 7.53 (m, 2 H), 7.56 (s, 1 H), 7.61 (dd,J =8.83, 5.04 Hz, 2 H), 7.94 - 8.44 (m, 2 H)。 LC-MS (方法2)Rt = 1.00 min; MS (ESIpos): m/z = 371.4 [M+H]+ 製備型急驟層析(方法Z,0-3%) 8%產率 |
| 72 | 2-(N-[4-胺基-5-(4-甲基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)乙醯胺 | 中間物86; 2-溴乙醯胺 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 2.30 (s, 3 H), 4.44 (s, 2 H), 7.18 - 7.24 (m, 3 H), 7.32 (t,J =8.87 Hz, 2 H), 7.42 (d,J =8.11 Hz, 2 H), 7.55 (s, 1 H), 7.61 (dd,J =9.13, 5.07 Hz, 2 H), 7.79 - 8.41 (m, 2 H)。 LC-MS (方法2)Rt = 1.07 min; MS (ESIpos): m/z = 385.5 [M+H]+ 製備型急驟層析(方法Z,0-3%) 6%產率 |
| 73 | 外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-甲基-苯胺基)丙醯胺 | 中間物91; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.15 (d,J =7.35 Hz, 3 H), 2.33 (s, 3 H), 5.07 (q,J =7.01 Hz, 1 H), 7.21 (s, 1 H), 7.27 (d,J =8.11 Hz, 2 H), 7.35 - 7.43 (m, 5 H), 7.44 - 7.48 (m, 2 H), 7.52 (s, 1 H), 8.10 (br s, 2 H)。 LC-MS (方法2)Rt = 1.10 min; MS (ESIpos): m/z = 381.5 [M+H]+ 製備型急驟層析(方法Z,0-3%) 35%產率 |
| 73.1 及73.2 | (R)-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-甲基-苯胺基)丙醯胺及 (S)-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-甲基-苯胺基)丙醯胺 | ||
| 73.1 | 2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-甲基-苯胺基)丙醯胺(鏡像異構物1) | 實例73 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.15 (d,J =7.35 Hz, 3 H), 2.33 (s, 3 H), 5.07 (q,J =7.01 Hz, 1 H), 7.21 (s, 1 H), 7.27 (d,J =8.11 Hz, 2 H), 7.35 - 7.43 (m, 5 H), 7.44 - 7.48 (m, 2 H), 7.52 (s, 1 H), 8.10 (br s, 2 H)。 [α]D 20 = -173.6° (c = 1.00,氯仿) 35%產率 |
| 對掌性HPLC實例73.1 在對掌性管柱上HPLC分離外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-甲基-苯胺基)丙醯胺(440 mg,1.10 mmol;實例73),得到160 mg (36%產率) 2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-甲基-苯胺基)丙醯胺,鏡像異構物1。 製備型對掌性 HPLC 儀器:Sepiatec:Prep SFC100;管柱:Chiralpak IA 5µ 250×30mm;溶離劑A:CO2 ;溶離劑B:2-丙醇+ 0.4 vol%二乙胺;等度:25% B;流速:100 mL/min;溫度:40℃;BPR:150巴;UV:280 nm 分析型對掌性 HPLC : Rt = 2.88 min 儀器:Agilent:1260,Aurora SFC-模組;管柱:Chiralpak IA 5µ 100×4.6mm;溶離劑A:CO2 ;溶離劑B:2-丙醇+ 0.4 vol%二乙胺,等度:25% B;流速:4 mL/min;溫度:37.5℃;BPR:100巴;UV:280 nm | |||
| 73.2 | 2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-甲基-苯胺基)丙醯胺(鏡像異構物2) | 實例73 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.15 (d,J =7.35 Hz, 3 H), 2.33 (s, 3 H), 5.07 (q,J =7.01 Hz, 1 H), 7.21 (s, 1 H), 7.27 (d,J =8.11 Hz, 2 H), 7.35 - 7.43 (m, 5 H), 7.44 - 7.48 (m, 2 H), 7.52 (s, 1 H), 8.10 (br s, 2 H)。 [α]D 20 = +161.4° (c = 1.00,氯仿) 8%產率 |
| 對掌性HPLC實例73.2 在對掌性管柱上HPLC分離外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-甲基-苯胺基)丙醯胺(440 mg,1.10 mmol;實例73),得到100 mg (23%產率) 2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-甲基-苯胺基)丙醯胺,鏡像異構物2。 製備型對掌性 HPLC 儀器:Sepiatec:Prep SFC100;管柱:Chiralpak IA 5µ 250×30mm;溶離劑A:CO2 ;溶離劑B:2-丙醇+ 0.4 vol%二乙胺;等度:25% B;流速:100 mL/min;溫度:40℃;BPR:150巴;UV:280 nm 分析型對掌性 HPLC : Rt = 4.57 min 儀器:Agilent:1260,Aurora SFC-模組;管柱:Chiralpak IA 5µ 100×4.6mm;溶離劑A:CO2 ;溶離劑B:2-丙醇+ 0.4 vol%二乙胺,等度:25% B;流速:4 mL/min;溫度:37.5℃;BPR:100巴;UV:280 nm | |||
| 74 | 外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-3-氟-苯胺基)丙醯胺 | 中間物92; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.18 (d,J =7.35 Hz, 3 H), 5.05 (q,J =7.18 Hz, 1 H), 7.28 (s, 1 H), 7.32 (td,J =8.30, 2.15 Hz, 1 H), 7.37 - 7.46 (m, 4 H), 7.47 - 7.56 (m, 4 H), 7.60 (s, 1 H), 7.85 - 8.35 (m, 2 H)。 LC-MS (方法2)Rt = 1.06 min; MS (ESIpos): m/z = 385.5 [M+H]+ 製備型急驟層析(方法Z,0-3%) 15%產率 |
| 74.1 及74.2 | (R)-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-3-氟-苯胺基)丙醯胺及 (S)-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-3-氟-苯胺基)丙醯胺 | ||
| 74.1 | 2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-3-氟-苯胺基)丙醯胺(鏡像異構物1) | 實例74 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.18 (d,J =7.35 Hz, 3 H), 5.05 (q,J =7.18 Hz, 1 H), 7.28 (s, 1 H), 7.32 (td,J =8.30, 2.15 Hz, 1 H), 7.37 - 7.46 (m, 4 H), 7.47 - 7.56 (m, 4 H), 7.60 (s, 1 H), 7.85 - 8.35 (m, 2 H)。 [α]D 20 = -143.6° (c = 1.00,氯仿) 4%產率 |
| 對掌性HPLC實例74.1 在對掌性管柱上HPLC分離外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-3-氟-苯胺基)丙醯胺(260 mg,0.64 mmol;實例74),得到65 mg (25%產率) 2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-3-氟-苯胺基)丙醯胺,鏡像異構物1。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:YMC Cellulose SC 10µ,250×50;溶離劑A:己烷;溶離劑B:2-丙醇;等度:70% A+30% B;流速:150 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 5.46 min 儀器:Waters Alliance 2695;管柱:YMC Cellulose SC 3µ,100×4.6;溶離劑A:己烷;溶離劑B:2-丙醇;等度:70% A+30% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 74.2 | 2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-3-氟-苯胺基)丙醯胺(鏡像異構物2) | 實例74 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.18 (d,J =7.35 Hz, 3 H), 5.05 (q,J =7.18 Hz, 1 H), 7.28 (s, 1 H), 7.32 (td,J =8.30, 2.15 Hz, 1 H), 7.37 - 7.46 (m, 4 H), 7.47 - 7.56 (m, 4 H), 7.60 (s, 1 H), 7.85 - 8.35 (m, 2 H)。 [α]D 20 = +151.0° (c = 1.00,氯仿) 4%產率 |
| 對掌性HPLC實例74.2 在對掌性管柱上HPLC分離外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-3-氟-苯胺基)丙醯胺(260 mg,0.64 mmol;實例74),得到65 mg (25%產率) 2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-3-氟-苯胺基)丙醯胺,鏡像異構物2。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:YMC Cellulose SC 10µ,250×50;溶離劑A:己烷;溶離劑B:2-丙醇;等度:70% A+30% B;流速:150 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 6.76 min 儀器:Waters Alliance 2695;管柱:YMC Cellulose SC 3µ,100×4.6;溶離劑A:己烷;溶離劑B:2-丙醇;等度:70% A+30% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 75 | 外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-2-氟-苯胺基)丙醯胺 | 中間物93; 外消旋-2-溴丙醯胺 | 1 H-NMR (500 MHz, DMSO-d 6 ): δ ppm = 1.22 (d,J =7.31 Hz, 3 H), 5.04 (q,J =7.10 Hz, 1 H), 6.87 - 7.30 (m, 2 H), 7.32 (td,J =7.63, 1.27 Hz, 1 H), 7.34 - 7.43 (m, 4 H), 7.49 - 7.55 (m, 3 H), 7.77 (td,J =7.95, 1.59 Hz, 1 H), 7.92 (br s, 2 H)。 LC-MS (方法2)Rt = 1.04 min; MS (ESIpos): m/z = 385.4 [M+H]+ 製備型急驟層析(方法Z,0-3%) 52%產率 |
| 75.1 及75.2 | (R)-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-2-氟-苯胺基)丙醯胺及 (S)-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-2-氟-苯胺基)丙醯胺 | ||
| 75.1 | 2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-2-氟-苯胺基)丙醯胺(鏡像異構物1) | 實例75 | 1 H-NMR (500 MHz, DMSO-d 6 ): δ ppm = 1.22 (d,J =7.31 Hz, 3 H), 5.04 (q,J =7.10 Hz, 1 H), 6.87 - 7.30 (m, 2 H), 7.32 (td,J =7.63, 1.27 Hz, 1 H), 7.34 - 7.43 (m, 4 H), 7.49 - 7.55 (m, 3 H), 7.77 (td,J =7.95, 1.59 Hz, 1 H), 7.92 (br s, 2 H)。 [α]D 20 = -116.9° (c = 1.00,氯仿) 13%產率 |
| 對掌性HPLC實例75.1 在對掌性管柱上HPLC分離外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-2-氟-苯胺基)丙醯胺(560 mg,1.38 mmol;實例75),得到135 mg (24%產率) 2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-2-氟-苯胺基)丙醯胺,鏡像異構物1。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:YMC Cellulose SB 5µ,250×30;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:2-丙醇;等度:70% A+30% B;流速:50 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 3.50 min 儀器:Waters Alliance 2695;管柱:YMC Cellulose SB 3µ,100×4.6;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:2-丙醇;等度:70% A+30% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 75.2 | 2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-2-氟-苯胺基)丙醯胺(鏡像異構物2) | 實例75 | 1 H-NMR (500 MHz, DMSO-d 6 ): δ ppm = 1.22 (d,J =7.31 Hz, 3 H), 5.04 (q,J =7.10 Hz, 1 H), 6.87 - 7.30 (m, 2 H), 7.32 (td,J =7.63, 1.27 Hz, 1 H), 7.34 - 7.43 (m, 4 H), 7.49 - 7.55 (m, 3 H), 7.77 (td,J =7.95, 1.59 Hz, 1 H), 7.92 (br s, 2 H)。 [α]D 20 = +109.3° (c = 1.00,氯仿) 15%產率 |
| 對掌性HPLC實例75.2 在對掌性管柱上HPLC分離外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-2-氟-苯胺基)丙醯胺(560 mg,1.38 mmol;實例75),得到165 mg (31%產率) 2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-2-氟-苯胺基)丙醯胺,鏡像異構物2。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:YMC Cellulose SB 5µ,250×30;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:2-丙醇;等度:70% A+30% B;流速:50 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 4.39 min 儀器:Waters Alliance 2695;管柱:YMC Cellulose SB 3µ,100×4.6;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:2-丙醇;等度:70% A+30% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 76 | 外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-3-甲基-苯胺基)丙醯胺 | 中間物72; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 2.31 (s, 3 H), 5.05 (q,J =7.18 Hz, 1 H), 7.22 (s, 1 H), 7.23 - 7.27 (m, 1 H), 7.33 - 7.41 (m, 6 H), 7.45 - 7.50 (m, 2 H), 7.53 (s, 1 H), 7.70 - 8.47 (m, 2 H)。 LC-MS (方法2)Rt = 1.10 min; MS (ESIpos): m/z = 381.5 [M+H]+ 製備型急驟層析(方法Z,0-3%) 71%產率 |
| 76.1 及76.2 | (R)-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-3-甲基-苯胺基)丙醯胺及 (S)-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-3-甲基-苯胺基)丙醯胺 | ||
| 76.1 | 2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-3-甲基-苯胺基)丙醯胺(鏡像異構物1) | 實例76 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 2.31 (s, 3 H), 5.05 (q,J =7.18 Hz, 1 H), 7.22 (s, 1 H), 7.23 - 7.27 (m, 1 H), 7.33 - 7.41 (m, 6 H), 7.45 - 7.50 (m, 2 H), 7.53 (s, 1 H), 7.70 - 8.47 (m, 2 H)。 [α]D 20 = +177.3° (c = 1.00,氯仿) 31%產率 |
| 對掌性HPLC實例76.1 在對掌性管柱上HPLC分離外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-3-甲基-苯胺基)丙醯胺(1170 mg,3.00 mmol;實例76),得到525 mg (44%產率) 2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-3-甲基-苯胺基)丙醯胺,鏡像異構物1。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:YMC Cellulose SC 10µ,250×50;溶離劑A:甲基三級丁基醚;溶離劑B:乙腈;等度:95% A+5% B;流速:150 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 6.56 min 儀器:Waters Alliance 2695;管柱:YMC Cellulose SC 3µ,100×4.6;溶離劑A:甲基三級丁基醚;溶離劑B:乙腈;等度:95% A+5% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 76.2 | 2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-3-甲基-苯胺基)丙醯胺(鏡像異構物2) | 實例76 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 2.31 (s, 3 H), 5.05 (q,J =7.18 Hz, 1 H), 7.22 (s, 1 H), 7.23 - 7.27 (m, 1 H), 7.33 - 7.41 (m, 6 H), 7.45 - 7.50 (m, 2 H), 7.53 (s, 1 H), 7.70 - 8.47 (m, 2 H)。 [α]D 20 = +177.3° (c = 1.00,氯仿) 34%產率 |
| 對掌性HPLC實例76.2 在對掌性管柱上HPLC分離外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-3-甲基-苯胺基)丙醯胺(1170 mg,3.00 mmol;實例76),得到525 mg (45%產率) 2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-3-甲基-苯胺基)丙醯胺,鏡像異構物2。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:YMC Cellulose SC 10µ,250×50;溶離劑A:甲基三級丁基醚;溶離劑B:乙腈;等度:95% A+5% B;流速:150 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 8.91 min 儀器:Waters Alliance 2695;管柱:YMC Cellulose SC 3µ,100×4.6;溶離劑A:甲基三級丁基醚;溶離劑B:乙腈;等度:95% A+5% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 77 | 外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-2-甲基-苯胺基)丙醯胺 | 中間物73; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 0.97 - 1.08 (m, 3 H), 2.17 (s, 3 H), 4.97 - 5.12 (m, 1 H), 7.24 (br s, 1 H), 7.33 - 7.40 (m, 6 H), 7.46 (br d,J =5.32 Hz, 2 H), 7.57 (br s, 1 H), 7.71 - 7.77 (m, 1 H), 7.85 - 8.48 (m, 2 H)。 LC-MS (方法2)Rt = 1.08 min; MS (ESIpos): m/z = 381.4 [M+H]+ 製備型急驟層析(方法Z,0-3%) 56%產率 |
| 77.1 及77.2 | (R)-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-2-甲基-苯胺基)丙醯胺及 (S)-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-2-甲基-苯胺基)丙醯胺 | ||
| 77.1 | 2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-2-甲基-苯胺基)丙醯胺(鏡像異構物1) | 實例77 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 0.97 - 1.08 (m, 3 H), 2.17 (s, 3 H), 4.97 - 5.12 (m, 1 H), 7.24 (br s, 1 H), 7.33 - 7.40 (m, 6 H), 7.46 (br d,J =5.32 Hz, 2 H), 7.57 (br s, 1 H), 7.71 - 7.77 (m, 1 H), 7.85 - 8.48 (m, 2 H)。 [α]D 20 = +166.1° (c = 1.00,氯仿) 23%產率 |
| 對掌性HPLC實例77.1 在對掌性管柱上HPLC分離外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-2-甲基-苯胺基)丙醯胺(1010 mg,2.52 mmol;實例77),得到420 mg (42%產率) 2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-2-甲基-苯胺基)丙醯胺,鏡像異構物1。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:Chiralpak IG 5µ,250×30;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:乙醇+ 0.1 vol%二乙胺;等度:85% A+15% B;流速:60 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 7.09 min 儀器:Waters Alliance 2695;管柱:Chiralpak IG 3µ,100×4.6;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:乙醇;等度:85% A+15% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 77.2 | 2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-2-甲基-苯胺基)丙醯胺(鏡像異構物1) | 實例77 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 0.97 - 1.08 (m, 3 H), 2.17 (s, 3 H), 4.97 - 5.12 (m, 1 H), 7.24 (br s, 1 H), 7.33 - 7.40 (m, 6 H), 7.46 (br d,J =5.32 Hz, 2 H), 7.57 (br s, 1 H), 7.71 - 7.77 (m, 1 H), 7.85 - 8.48 (m, 2 H)。 [α]D 20 = -152.0° (c = 1.00,氯仿) 23%產率 |
| 對掌性HPLC實例77.2 在對掌性管柱上HPLC分離外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-2-甲基-苯胺基)丙醯胺(1010 mg,2.52 mmol;實例77),得到420 mg (42%產率) 2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-2-甲基-苯胺基)丙醯胺,鏡像異構物2。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:Chiralpak IG 5µ,250×30;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:乙醇+ 0.1 vol%二乙胺;等度:85% A+15% B;流速:60 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 10.30 min 儀器:Waters Alliance 2695;管柱:Chiralpak IG 3µ,100×4.6;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:乙醇;等度:85% A+15% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 78 | 外消旋-2-[(4-胺基-5-苯甲醯基-噻唑-2-基)-(1-甲基吡唑-4-基)胺基]丙醯胺 | 中間物94; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.19 (d,J =7.35 Hz, 3 H), 3.83 (s, 3 H), 4.99 - 5.18 (m, 1 H), 7.18 (s, 1 H), 7.37 - 7.44 (m, 3 H), 7.48 (s, 1 H), 7.49 - 7.53 (m, 3 H), 7.80 - 8.48 (m, 2 H), 7.90 (s, 1 H)。 LC-MS (方法2)Rt = 0.80 min; MS (ESIpos): m/z = 371.3 [M+H]+ 製備型急驟層析(方法Z,0-3%) 17%產率 |
| 78.1 及78.2 | (R)-2-[(4-胺基-5-苯甲醯基-噻唑-2-基)-(1-甲基吡唑-4-基)胺基]丙醯胺及 (S)-2-[(4-胺基-5-苯甲醯基-噻唑-2-基)-(1-甲基吡唑-4-基)胺基]丙醯胺 | ||
| 78.1 | 2-[(4-胺基-5-苯甲醯基-噻唑-2-基)-(1-甲基吡唑-4-基)胺基]丙醯胺(鏡像異構物1) | 實施例78 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.19 (d,J =7.35 Hz, 3 H), 3.83 (s, 3 H), 4.99 - 5.18 (m, 1 H), 7.18 (s, 1 H), 7.37 - 7.44 (m, 3 H), 7.48 (s, 1 H), 7.49 - 7.53 (m, 3 H), 7.80 - 8.48 (m, 2 H), 7.90 (s, 1 H)。 [α]D 20 = -82.8° (c = 1.00,氯仿) 6%產率 |
| 對掌性HPLC實例78.1 在對掌性管柱上HPLC分離外消旋-2-[(4-胺基-5-苯甲醯基-噻唑-2-基)-(1-甲基吡唑-4-基)胺基]丙醯胺(240 mg,0.64 mmol;實例78),得到89 mg (36%產率) 2-[(4-胺基-5-苯甲醯基-噻唑-2-基)-(1-甲基吡唑-4-基)胺基]丙醯胺,鏡像異構物1。 製備型對掌性 HPLC 儀器:Sepiatec:Prep SFC100;管柱:Chiralpak IC 5µ 250×30mm;溶離劑A:CO2 ;溶離劑B:甲醇+ 0.2 vol%氨水(32%);等度:40% B;流速:100 mL/min;溫度:40℃;BPR:150巴;UV:254 nm 分析型對掌性 HPLC : Rt = 1.77 min 儀器:Agilent:1260,Aurora SFC-模組;管柱:Chiralpak IC 5µ 100×4.6mm;溶離劑A:CO2 ;溶離劑B:甲醇+ 0.2 vol%氨水(32%);等度:40% B;流速:4 mL/min;溫度:37.5℃;BPR:100巴;UV:254 nm | |||
| 78.2 | 2-[(4-胺基-5-苯甲醯基-噻唑-2-基)-(1-甲基吡唑-4-基)胺基]丙醯胺(鏡像異構物2) | 實施例78 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.19 (d,J =7.35 Hz, 3 H), 3.83 (s, 3 H), 4.99 - 5.18 (m, 1 H), 7.18 (s, 1 H), 7.37 - 7.44 (m, 3 H), 7.48 (s, 1 H), 7.49 - 7.53 (m, 3 H), 7.80 - 8.48 (m, 2 H), 7.90 (s, 1 H)。 [α]D 20 = +72.6° (c = 1.00,氯仿) 6%產率 |
| 對掌性HPLC實例78.2 在對掌性管柱上HPLC分離外消旋-2-[(4-胺基-5-苯甲醯基-噻唑-2-基)-(1-甲基吡唑-4-基)胺基]丙醯胺(240 mg,0.64 mmol;實例78),得到80 mg (33%產率) 2-[(4-胺基-5-苯甲醯基-噻唑-2-基)-(1-甲基吡唑-4-基)胺基]丙醯胺,鏡像異構物2。 製備型對掌性 HPLC 儀器:Sepiatec:Prep SFC100;管柱:Chiralpak IC 5µ 250×30mm;溶離劑A:CO2 ;溶離劑B:甲醇+ 0.2 vol%氨水(32%);等度:40% B;流速:100 mL/min;溫度:40℃;BPR:150巴;UV:254 nm 分析型對掌性 HPLC : Rt = 2.66 min 儀器:Agilent:1260,Aurora SFC-模組;管柱:Chiralpak IC 5µ 100×4.6mm;溶離劑A:CO2 ;溶離劑B:甲醇+ 0.2 vol%氨水(32%);等度:40% B;流速:4 mL/min;溫度:37.5℃;BPR:100巴;UV:254 nm | |||
| 79 | 外消旋-2-[(4-胺基-5-苯甲醯基-噻唑-2-基)-(3-吡啶基)胺基]丙醯胺 | 中間物95; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.17 (d,J =7.35 Hz, 3 H), 5.07 (q,J =7.10 Hz, 1 H), 5.76 (s, 1 H), 7.30 (s, 1 H), 7.35 - 7.43 (m, 3 H), 7.47 - 7.51 (m, 2 H), 7.54 (dd,J =8.11, 4.82 Hz, 1 H), 7.64 (s, 1 H), 7.90 - 8.44 (m, 2 H), 8.04 - 8.08 (m, 1 H), 8.63 (dd,J =4.56, 1.52 Hz, 1 H), 8.74 (d,J =2.03 Hz, 1 H)。 LC-MS (方法2)Rt = 0.84 min; MS (ESIpos): m/z = 368.5 [M+H]+ 製備型急驟層析(方法Z,0-3%) 10%產率 |
| 79.1 及79.2 | (R)-2-[(4-胺基-5-苯甲醯基-噻唑-2-基)-(3-吡啶基)胺基]丙醯胺及 (S)-2-[(4-胺基-5-苯甲醯基-噻唑-2-基)-(3-吡啶基)胺基]丙醯胺 | ||
| 79.1 | 2-[(4-胺基-5-苯甲醯基-噻唑-2-基)-(3-吡啶基)胺基]丙醯胺(鏡像異構物1) | 實例79 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.17 (d,J =7.35 Hz, 3 H), 5.07 (q,J =7.10 Hz, 1 H), 5.76 (s, 1 H), 7.30 (s, 1 H), 7.35 - 7.43 (m, 3 H), 7.47 - 7.51 (m, 2 H), 7.54 (dd,J =8.11, 4.82 Hz, 1 H), 7.64 (s, 1 H), 7.90 - 8.44 (m, 2 H), 8.04 - 8.08 (m, 1 H), 8.63 (dd,J =4.56, 1.52 Hz, 1 H), 8.74 (d,J =2.03 Hz, 1 H)。 [α]D 20 = -119.3° (c = 1.00,氯仿) 3%產率 |
| 對掌性HPLC實例79.1 在對掌性管柱上HPLC分離外消旋-2-[(4-胺基-5-苯甲醯基-噻唑-2-基)-(3-吡啶基)胺基]丙醯胺(200 mg,0.52 mmol;實例79),得到50 mg (25%產率) 2-[(4-胺基-5-苯甲醯基-噻唑-2-基)-(3-吡啶基)胺基]丙醯胺,鏡像異構物1。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:YMC Cellulose SB 10µ,250×50;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:乙醇;等度:60% A+40% B;流速:150 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 2.15 min 儀器:Waters Alliance 2695;管柱:YMC Cellulose SB 3µ,100×4.6;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:乙醇;等度:60% A+40% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 79.2 | 2-[(4-胺基-5-苯甲醯基-噻唑-2-基)-(3-吡啶基)胺基]丙醯胺(鏡像異構物2) | 實例79 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.17 (d,J =7.35 Hz, 3 H), 5.07 (q,J =7.10 Hz, 1 H), 5.76 (s, 1 H), 7.30 (s, 1 H), 7.35 - 7.43 (m, 3 H), 7.47 - 7.51 (m, 2 H), 7.54 (dd,J =8.11, 4.82 Hz, 1 H), 7.64 (s, 1 H), 7.90 - 8.44 (m, 2 H), 8.04 - 8.08 (m, 1 H), 8.63 (dd,J =4.56, 1.52 Hz, 1 H), 8.74 (d,J =2.03 Hz, 1 H)。 [α]D 20 = +138.1° (c = 1.00,氯仿) 3%產率 |
| 對掌性HPLC實例79.2 在對掌性管柱上HPLC分離外消旋-2-[(4-胺基-5-苯甲醯基-噻唑-2-基)-(3-吡啶基)胺基]丙醯胺(200 mg,0.52 mmol;實例79),得到50 mg (25%產率) 2-[(4-胺基-5-苯甲醯基-噻唑-2-基)-(3-吡啶基)胺基]丙醯胺,鏡像異構物2。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:YMC Cellulose SB 10µ,250×50;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:乙醇;等度:60% A+40% B;流速:150 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 2.15 min 儀器:Waters Alliance 2695;管柱:YMC Cellulose SB 3µ,100×4.6;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:乙醇;等度:60% A+40% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 80 | 外消旋-2-(N-[4-胺基-5-(4-溴苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物96; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 5.06 (q,J =6.25 Hz, 1 H), 7.25 (s, 1 H), 7.33 (t,J =8.74 Hz, 2 H), 7.40 - 7.46 (m, 2 H), 7.57 - 7.67 (m, 5 H), 7.82 - 8.54 (m, 2 H)。 LC-MS (方法2)Rt = 1.20 min; MS (ESIpos): m/z = 463.4 [M+H]+ 製備型急驟層析(方法Z,0-3%) 19%產率 |
將2-[4-[4-胺基-2-(4-氟苯胺基)噻唑-5-羰基]苯氧基]乙酸乙酯(18.54 g,44.6 mmol;中間物 80
)溶解於N,N-二甲基甲醯胺(493 mL)中,隨後添加碳酸鉀(30.84 g,223.1 mmol)及外消旋-2-溴丙醯胺(8.14 g,53.6 mmol)。在90℃攪拌反應混合物1 h。在冷卻之後,將反應混合物分配於水與乙酸乙酯之間。分離有機層,且用飽和氯化銨水溶液及鹽水洗滌。之後,有機層藉由拒水過濾圈(MN 617 WA)過濾且蒸發至乾燥。向殘餘物中添加水,且藉由凍乾乾燥所得懸浮液,得到6.16 g (27%產率)外消旋-2-[4-[4-胺基-2-(4-氟-N-[2-胺基-1-甲基-2-側氧基-乙基]苯胺基)噻唑-5-羰基]苯氧基]-乙酸乙酯。
1
H-NMR (400 MHz, DMSO-d6
): δ ppm = 1.16 (d,J
=7.86 Hz, 3 H), 1.18 (t,J
=6.84 Hz, 3 H), 4.15 (q,J
=7.10 Hz, 2 H), 4.80 (s, 2 H), 5.06 (q,J
=6.25 Hz, 1 H), 6.91 (d,J
=8.87 Hz, 2 H), 7.25 (s, 1 H), 7.33 (t,J
=8.74 Hz, 2 H), 7.47 (d,J
=8.87 Hz, 2 H), 7.58 (s, 1 H), 7.64 (dd,J
=8.87, 5.07 Hz, 2 H), 8.15 (br s, 2 H)。
LC-MS (方法2)Rt = 1.09 min; MS (ESIpos): m/z = 487.5 [M+H]+
實例81 1及81.2: (R)-2-[4-[4-胺基-2-(4-氟-N-[2-胺基-1-甲基-2-側氧基-乙基]苯胺基)噻唑-5-羰基]苯氧基]乙酸乙酯及(S)-2-[4-[4-胺基-2-(4-氟-N-[2-胺基-1-甲基-2-側氧基-乙基]苯胺基)噻唑-5-羰基]苯氧基]乙酸乙酯
在對掌性管柱上HPLC分離外消旋-2-[4-[4-胺基-2-(4-氟-N-[2-胺基-1-甲基-2-側氧基-乙基]苯胺基)噻唑-5-羰基]苯氧基]乙酸乙酯(6.16 g,12.66 mmol;實例81),得到2.50 g (39%產率) 2-[4-[4-胺基-2-(4-氟-N-[2-胺基-1-甲基-2-側氧基-乙基]苯胺基)噻唑-5-羰基]苯氧基]乙酸乙酯,鏡像異構物1。
製備型對掌性 HPLC
Labomatic HD3000,Knauer Pump 100,Labcol Vario 4000 Plus,Knauer DAD 2600;管柱:Amylose SB 5µ 250×50mm Nr.34;溶離劑A:己烷;溶離劑B:乙醇;等度:70% A+30% B;流速150.0 mL/min;UV:254 nm
分析型對掌性 HPLC :
Rt = 7.31 min
儀器:Agilent HPLC 1260;管柱:Amylose SB 3µ 100×4.6mm;溶離劑A:己烷;溶離劑B:乙醇;等度:70% A+30% B;流速1.4 mL/min;溫度:25℃;DAD 254 nm
在對掌性管柱上HPLC分離外消旋- 2-[4-[4-胺基-2-(4-氟-N-[2-胺基-1-甲基-2-側氧基-乙基]苯胺基)噻唑-5-羰基]苯氧基]乙酸乙酯(6.16 g,12.66 mmol;實例81),得到2.60 g (40%產率) 2-[4-[4-胺基-2-(4-氟-N-[2-胺基-1-甲基-2-側氧基-乙基]苯胺基)噻唑-5-羰基]苯氧基]乙酸乙酯,鏡像異構物2。
製備型對掌性 HPLC
Labomatic HD3000,Knauer Pump 100,Labcol Vario 4000 Plus,Knauer DAD 2600;管柱:Amylose SB 5µ 250×50mm Nr.34;溶離劑A:己烷;溶離劑B:乙醇;等度:70% A+30% B;流速150.0 mL/min;UV:254 nm
分析型對掌性 HPLC :
Rt = 10.17 min
儀器:Agilent HPLC 1260;管柱:Amylose SB 3µ 100×4.6mm;溶離劑A:己烷;溶離劑B:乙醇;等度:70% A+30% B;流速1.4 mL/min;溫度:25℃;DAD 254 nm
將外消旋-2-[4-[4-胺基-2-(N-[2-胺基-1-甲基-2-側氧基-乙基]-4-氟-苯胺基)噻唑-5-羰基]苯氧基]乙酸(12 mg,26 µmol,中間物100)及異丙基胺(3 mg,51 µmol)溶解於二甲基甲醯胺(0.4 mL)中。添加N,N-二異丙基乙基胺(13 mg,102 µmol)、4-二甲基胺基吡啶(0.2 mg,1 µmol)及HATU (19 mg,51 µmol)。在室溫攪拌反應混合物2 h。
過濾反應混合物且藉由RP-HPLC (方法C,鹼性)純化,得到6 mg (42%產率)標題化合物。
1
H-NMR (400 MHz, DMSO-d6
): δ ppm = 1.04 - 1.07 (m, 6 H), 1.16 (d,J
=7.35 Hz, 3 H), 3.86 - 3.97 (m, 1 H), 4.45 (s, 2 H), 5.05 (q,J
=6.34 Hz, 1 H), 6.92 (d,J
=8.87 Hz, 2 H), 7.24 (s, 1 H), 7.33 (t,J
=8.87 Hz, 2 H), 7.47 (d,J
=8.87 Hz, 2 H), 7.58 (s, 1 H), 7.64 (dd,J
=8.87, 5.07 Hz, 2 H), 7.88 (br d,J
=7.86 Hz, 1 H), 8.13 (br s, 2 H)。
LC-MS (方法2)Rt = 1.00 min; MS (ESIpos): m/z = 500.6 [M+H]+
以下實例由下表7中陳述之起始材料,使用關於實例82之程序製備。
在過濾反應混合物之後,藉由方法F (給出個別梯度,視分析型HPLC中之滯留時間而定)純化粗產物。
表7:實例83至141
| 實例編號 | 化學結構 化學名稱 | 起始材料 | 分析/純化/產率 |
| 83 | 外消旋-2-(N-[4-胺基-5-[4-[2-(間甲苯基甲基胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物100,1-(3-甲基苯基)甲胺 | LC-MS (方法3)Rt = 1.12 min; MS (ESIpos): m/z = 562.2 [M+H]+ 方法F:Prep_30-60% B 11%產率 |
| 84 | 外消旋-2-(N-[4-胺基-5-[4-[2-(鄰甲苯基甲基胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物100,1-(2-甲基苯基)甲胺 | LC-MS (方法3)Rt = 1.11 min; MS (ESIpos): m/z = 562.1 [M+H]+ 方法F:Prep_30-60% B 11%產率 |
| 85 | 外消旋-2-(N-[4-胺基-5-[4-[2-[(3-氯苯基)甲基胺基]-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物100,1-(3-氯苯基)甲胺 | LC-MS (方法3)Rt = 1.13 min; MS (ESIpos): m/z = 582.1 [M+H]+ 方法F:Prep_35-65% B 10%產率 |
| 86 | 外消旋-2-(N-[4-胺基-5-[4-[2-(4-甲基哌𠯤-1-基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物100,1-甲基哌𠯤 | LC-MS (方法3)Rt = 0.88 min; MS (ESIpos): m/z = 541.1 [M+H]+ 方法F:Prep_20-50% B 12%產率 |
| 87 | 外消旋-2-(N-[4-胺基-5-[4-[2-(3-甲基苯胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物100,間甲苯胺 | LC-MS (方法3)Rt = 1.15 min; MS (ESIpos): m/z = 548.1 [M+H]+ 方法F:Prep_40-70% B 12%產率 |
| 88 | 外消旋-2-(N-[4-胺基-5-[4-(2-(N-𠰌啉基)-2-側氧基-乙氧基)苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物100,𠰌啉 | LC-MS (方法3)Rt = 0.90 min; MS (ESIpos): m/z = 528.1 [M+H]+ 方法F:Prep_20-50% B 13%產率 |
| 89 | 外消旋-2-(N-[4-胺基-5-[4-[2-側氧基-2-[2-(1-哌啶基)乙基胺基]乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物100,2-(哌啶-1-基)乙胺 | LC-MS (方法3)Rt = 1.07 min; MS (ESIpos): m/z = 569.2 [M+H]+ 方法F:Prep_30-60% B 5%產率 |
| 90 | 外消旋-2-(N-[4-胺基-5-[4-[2-(4-苯甲基-1-哌啶基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物100,4-苯甲基哌啶 | LC-MS (方法3)Rt = 1.26 min; MS (ESIpos): m/z = 616.2 [M+H]+ 方法F:Prep_45-75% B 5%產率 |
| 91 | 外消旋-2-(N-[4-胺基-5-[4-[2-(2-甲氧基乙基胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物100,2-甲氧基乙胺 | LC-MS (方法3)Rt = 0.90 min; MS (ESIpos): m/z = 516.1 [M+H]+ 方法F:Prep_20-50% B 5%產率 |
| 92 | 外消旋-2-(N-[4-胺基-5-[4-[2-(4-氰基苯胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物100,4-胺基苯甲腈 | LC-MS (方法3)Rt = 1.06 min; MS (ESIpos): m/z = 559.1 [M+H]+ 方法F:Prep_30-60% B 9%產率 |
| 93 | 外消旋-2-(N-[4-胺基-5-[4-[2-[甲基(丙-2-炔基)胺基]-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物100,N-甲基丙-2-炔-1-胺 | LC-MS (方法3)Rt = 0.96 min; MS (ESIpos): m/z = 510.1 [M+H]+ 方法F:Prep_25-55% B 9%產率 |
| 94 | 外消旋-2-(N-[4-胺基-5-[4-[2-[(2-甲氧基苯基)甲基胺基]-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物100,1-(2-甲氧基苯基)甲胺 | LC-MS (方法3)Rt = 1.08 min; MS (ESIpos): m/z = 578.1 [M+H]+ 方法F:Prep_30-60% B 13%產率 |
| 95 | 外消旋-2-(N-[4-胺基-5-[4-[2-[(3-甲氧基苯基)甲基胺基]-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物100,1-(3-甲氧基苯基)甲胺 | LC-MS (方法3)Rt = 1.06 min; MS (ESIpos): m/z = 578.1 [M+H]+ 方法F:Prep_30-60% B 10%產率 |
| 96 | 外消旋-2-(N-[4-胺基-5-[4-[2-[(2-氟苯基)甲基胺基]-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物100,1-(2-氟苯基)甲胺 | LC-MS (方法3)Rt = 1.07 min; MS (ESIpos): m/z = 566.1 [M+H]+ 方法F:Prep_30-60% B 10%產率 |
| 97 | 外消旋-2-(N-[4-胺基-5-[4-[2-[(4-氟苯基)甲基胺基]-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物100,1-(4-氟苯基)甲胺 | LC-MS (方法3)Rt = 1.07 min; MS (ESIpos): m/z = 566.1 [M+H]+ 方法F:Prep_30-60% B 13%產率 |
| 98 | 外消旋-2-(N-[4-胺基-5-[4-[2-(1H-苯并咪唑-2-基甲基胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物100,1-(1H-苯并咪唑-2-基)甲胺 | LC-MS (方法3)Rt = 0.93 min; MS (ESIpos): m/z = 588.1 [M+H]+ 方法F:Prep_25-55% B 7%產率 |
| 99 | 外消旋-2-(N-[4-胺基-5-[4-[2-側氧基-2-(2,2,2-三氟乙基胺基)乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物100,2,2,2-三氟乙胺 | LC-MS (方法3)Rt = 1.00 min; MS (ESIpos): m/z = 540.0 [M+H]+ 方法F:Prep_25-55% B 21%產率 |
| 100 | 外消旋-2-(N-[4-胺基-5-[4-[2-[甲基(2-吡啶基)胺基]-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物100,N-甲基吡啶-2-胺 | LC-MS (方法3)Rt = 0.99 min; MS (ESIpos): m/z = 549.1 [M+H]+ 方法F:Prep_25-55% B 9%產率 |
| 101 | 外消旋-2-(N-[4-胺基-5-[4-[2-[甲基-(1-甲基-4-哌啶基)胺基]-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物100,N,1-二甲基哌啶-4-胺 | LC-MS (方法3)Rt = 0.94 min; MS (ESIpos): m/z = 569.1 [M+H]+ 方法F:Prep_25-55% B 23%產率 |
| 102 | 外消旋-2-(N-[4-胺基-5-[4-[2-(甲氧基胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物100,O-甲基羥基胺 | LC-MS (方法3)Rt = 0.90 min; MS (ESIpos): m/z = 488.1 [M+H]+ 方法F:Prep_20-50% B 22%產率 |
| 103 | 外消旋-2-(N-[4-胺基-5-[4-[2-[(5-甲基異㗁唑-3-基)胺基]-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物100,5-甲基-1,2-㗁唑-3-胺 | LC-MS (方法3)Rt = 0.99 min; MS (ESIpos): m/z = 539.1 [M+H]+ 方法F:Prep_25-55% B 7%產率 |
| 104 | 外消旋-2-(N-[4-胺基-5-[4-[2-(乙基胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物100,乙胺 | LC-MS (方法3)Rt = 0.92 min; MS (ESIpos): m/z = 486.0 [M+H]+ 方法F:Prep_25-55% B 33%產率 |
| 105 | 外消旋-2-(N-[4-胺基-5-[4-[2-(4-甲基苯胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物100,對甲苯胺 | LC-MS (方法3)Rt = 1.15 min; MS (ESIpos): m/z = 548.1 [M+H]+ 方法F:Prep_40-70% B 37%產率 |
| 106 | 外消旋-2-(N-[4-胺基-5-[4-[2-(環己基胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物100,環己胺 | LC-MS (方法3)Rt = 1.12 min; MS (ESIpos): m/z = 540.1 [M+H]+ 方法F:Prep_35-65% B 11%產率 |
| 107 | 外消旋-3-[[2-[4-[4-胺基-2-(N-[2-胺基-1-甲基-2-側氧基-乙基]-4-氟-苯胺基)噻唑-5-羰基]苯氧基]乙醯基]胺基]苯甲醯胺 | 中間物100,3-胺基苯甲醯胺 | LC-MS (方法3)Rt = 0.89 min; MS (ESIpos): m/z = 577.1 [M+H]+ 方法F:Prep_20-50% B 20%產率 |
| 108 | 外消旋-2-(N-[4-胺基-5-[4-[2-側氧基-2-(6-喹啉基胺基)乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物100,喹啉-6-胺 | LC-MS (方法3)Rt = 1.01 min; MS (ESIpos): m/z = 585.1 [M+H]+ 方法F:Prep_25-55% B 30%產率 |
| 109 | 外消旋-4-[[2-[4-[4-胺基-2-(N-[2-胺基-1-甲基-2-側氧基-乙基]-4-氟-苯胺基)噻唑-5-羰基]苯氧基]乙醯基]胺基]苯甲醯胺 | 中間物100,4-胺基苯甲醯胺 | LC-MS (方法3)Rt = 1.01 min; MS (ESIpos): m/z = 577.1 [M+H]+ 方法F:Prep_20-50% B 7%產率 |
| 110 | (2S)-1-[2-[4-[4-胺基-2-(N-[2-胺基-(1RS)-甲基-2-側氧基-乙基]-4-氟-苯胺基)噻唑-5-羰基]苯氧基]乙醯基]吡咯啶-2-甲醯胺(兩種非鏡像異構物之混合物) | 中間物100,L-脯胺醯胺 | LC-MS (方法3)Rt = 0.82 min; MS (ESIpos): m/z = 555.1 [M+H]+ 方法F:Prep_15-45% B 15%產率 |
| 111 | 外消旋-2-(N-[4-胺基-5-[4-[2-[乙基(甲基)胺基]-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物100,N-甲基乙胺 | LC-MS (方法3)Rt = 0.96 min; MS (ESIpos): m/z = 500.1 [M+H]+ 方法F:Prep_25-55% B 23%產率 |
| 112 | 外消旋-2-(N-[4-胺基-5-[4-[2-[(3-甲基異㗁唑-5-基)胺基]-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物100,3-甲基-1,2-㗁唑-5-胺 | LC-MS (方法3)Rt = 0.80 min; MS (ESIpos): m/z = 539.1 [M+H]+ 方法F:Prep_10-40% B 4%產率 |
| 113 | 外消旋-2-(N-[4-胺基-5-[4-[2-[3-(二甲基胺基)丙基-甲基-胺基]-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物100,N,N,N'-三甲基丙烷-1,3-二胺 | LC-MS (方法3)Rt = 1.02 min; MS (ESIpos): m/z = 557.2 [M+H]+ 方法F:Prep_25-55% B 12%產率 |
| 114 | 外消旋-2-(N-[5-[4-[2-(4-乙醯基哌𠯤-1-基)-2-側氧基-乙氧基]苯甲醯基]-4-胺基-噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物100,1-(哌𠯤-1-基)乙酮 | LC-MS (方法3)Rt = 0.84 min; MS (ESIpos): m/z = 569.1 [M+H]+ 方法F:Prep_15-45% B 14%產率 |
| 115 | 外消旋-2-(N-[4-胺基-5-[4-[2-側氧基-2-(3-吡啶基甲基胺基)乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物100,1-(吡啶-3-基)甲胺 | LC-MS (方法3)Rt = 0.90 min; MS (ESIpos): m/z = 549.1 [M+H]+ 方法F:Prep_20-50% B 4%產率 |
| 116 | 2-(N-[4-胺基-5-[4-[2-(2,3-二羥基丙基胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺(立體異構物之混合物) | 中間物100,外消旋-3-胺基丙烷-1,2-二醇 | LC-MS (方法3)Rt = 0.77 min; MS (ESIpos): m/z = 532.0 [M+H]+ 方法F:Prep_10-40% B 12%產率 |
| 117 | 外消旋-2-(N-[4-胺基-5-[4-[2-(4-甲氧基苯胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物100,4-甲氧基苯胺 | LC-MS (方法3)Rt = 1.07 min; MS (ESIpos): m/z = 564.1 [M+H]+ 方法F:Prep_30-60% B 21%產率 |
| 118 | 外消旋-2-(N-[4-胺基-5-[4-[2-[苯甲基(甲基)胺基]-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物100,N-甲基-1-苯基甲胺 | LC-MS (方法3)Rt = 1.10 min; MS (ESIpos): m/z = 562.1 [M+H]+ 方法F:Prep_30-60% B 14%產率 |
| 119 | 外消旋-2-(N-[4-胺基-5-[4-[2-(4-氯苯胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物100,4-氯苯胺 | LC-MS (方法3)Rt = 1.18 min; MS (ESIpos): m/z = 568.1 [M+H]+ 方法F:Prep_40-70% B 22%產率 |
| 120 | 外消旋-2-(N-[4-胺基-5-[4-[2-[(2-氯苯基)甲基胺基]-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物100,1-(2-氯苯基)甲胺 | LC-MS (方法3)Rt = 1.13 min; MS (ESIpos): m/z = 582.1 [M+H]+ 方法F:Prep_35-65% B 12%產率 |
| 121 | 外消旋-2-(N-[4-胺基-5-[4-[2-[(4-氯苯基)甲基胺基]-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物100,1-(4-氯苯基)甲胺 | LC-MS (方法3)Rt = 1.13 min; MS (ESIpos): m/z = 582.1 [M+H]+ 方法F:Prep_35-65% B 15%產率 |
| 122 | 外消旋-2-(N-[4-胺基-5-[4-[2-(4-氟苯胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物100,4-氟苯胺 | LC-MS (方法3)Rt = 1.10 min; MS (ESIpos): m/z = 552.1 [M+H]+ 方法F:Prep_30-60% B 24%產率 |
| 123 | 外消旋-2-(N-[4-胺基-5-[4-[2-(氮𠰢-1-基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物100,氮𠰢 | LC-MS (方法3)Rt = 1.08 min; MS (ESIpos): m/z = 540.1 [M+H]+ 方法F:Prep_30-60% B 6%產率 |
| 124 | 外消旋-2-(N-[4-胺基-5-[4-[2-[(4-甲氧基苯基)甲基胺基]-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物100,1-(4-甲氧基苯基)甲胺 | LC-MS (方法3)Rt = 1.05 min; MS (ESIpos): m/z = 578.1 [M+H]+ 方法F:Prep_30-60% B 8%產率 |
| 125 | 2-(N-[4-胺基-5-[4-[2-側氧基-2-(1-苯基乙基胺基)乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺(立體異構物之混合物) | 中間物100,外消旋-1-苯基乙胺 | LC-MS (方法3)Rt = 1.10 min; MS (ESIpos): m/z = 562.1 [M+H]+ 方法F:Prep_30-60% B 9%產率 |
| 126 | 外消旋-2-(N-[4-胺基-5-[4-[2-側氧基-2-(對甲苯基甲基胺基)乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物100,1-(4-甲基苯基)甲胺 | LC-MS (方法3)Rt = 1.12 min; MS (ESIpos): m/z = 562.1 [M+H]+ 方法F:Prep_35-65% B 13%產率 |
| 127 | 外消旋-2-(N-[4-胺基-5-[4-[2-[甲基(2-苯基乙基)胺基]-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物100,N-甲基-2-苯基乙胺 | LC-MS (方法3)Rt = 1.11 min; MS (ESIpos): m/z = 576.1 [M+H]+ 方法F:Prep_30-60% B 23%產率 |
| 128 | 2-(N-[4-胺基-5-[4-[2-(3-甲基-1-哌啶基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺(立體異構物之混合物) | 中間物100,外消旋-3-甲基哌啶 | LC-MS (方法3)Rt = 1.11 min; MS (ESIpos): m/z = 540.1 [M+H]+ 方法F:Prep_30-60% B 4%產率 |
| 129 | 外消旋-2-(N-[4-胺基-5-[4-[2-(4-甲基-1-哌啶基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物100,4-甲基哌啶 | LC-MS (方法3)Rt = 1.11 min; MS (ESIpos): m/z = 540.1 [M+H]+ 方法F:Prep_30-60% B 5%產率 |
| 130 | 外消旋-2-(N-[5-[4-[2-(4-乙醯胺基苯胺基)-2-側氧基-乙氧基]苯甲醯基]-4-胺基-噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物100,N-(4-胺基苯基)乙醯胺 | LC-MS (方法3)Rt = 0.92 min; MS (ESIpos): m/z = 591.1 [M+H]+ 方法F:Prep_25-55% B 25%產率 |
| 131 | 外消旋-2-(N-[4-胺基-5-[4-[2-側氧基-2-(1H-吡唑并[3,4-d]嘧啶-4-基胺基)乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物100,1H-吡唑并[3,4-d]嘧啶-4-胺 | LC-MS (方法3)Rt = 0.80 min; MS (ESIpos): m/z = 576.1 [M+H]+ 方法F:Prep_10-40% B 7%產率 |
| 132 | 外消旋-2-(N-[4-胺基-5-[4-[2-(環戊基胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物100,環戊胺 | LC-MS (方法3)Rt = 1.06 min; MS (ESIpos): m/z = 526.1 [M+H]+ 方法F:Prep_30-60% B 8%產率 |
| 133 | 外消旋-2-(N-[4-胺基-5-[4-[2-(3,4-二氫-1H-異喹啉-2-基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物100,1,2,3,4-四氫異喹啉 | LC-MS (方法3)Rt = 1.13 min; MS (ESIpos): m/z = 574.1 [M+H]+ 方法F:Prep_35-65% B 8%產率 |
| 134 | 外消旋-2-(N-[4-胺基-5-[4-(2-異吲哚啉-2-基-2-側氧基-乙氧基)苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物100,異吲哚啉 | LC-MS (方法3)Rt = 1.09 min; MS (ESIpos): m/z = 560.1 [M+H]+ 方法F:Prep_30-60% B 6%產率 |
| 135 | 外消旋-2-(N-[4-胺基-5-[4-[2-[2-呋喃基甲基(甲基)胺基]-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物100,1-(2-呋喃基)-N-甲基甲胺 | LC-MS (方法3)Rt = 1.04 min; MS (ESIpos): m/z = 552.1 [M+H]+ 方法F:Prep_30-60% B 12%產率 |
| 136 | 外消旋-2-(N-[4-胺基-5-[4-[2-[4-(二甲基胺基)-1-哌啶基]-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物100,N,N-二甲基哌啶-4-胺 | LC-MS (方法3)Rt = 0.97 min; MS (ESIpos): m/z = 569.2 [M+H]+ 方法F:Prep_25-55% B 13%產率 |
| 137 | 外消旋-2-(N-[4-胺基-5-[4-[2-[甲基(3-吡啶基甲基)胺基]-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物100,N-甲基-1-(吡啶-3-基)甲胺 | LC-MS (方法3)Rt = 0.92 min; MS (ESIpos): m/z = 563.1 [M+H]+ 方法F:Prep_25-55% B 24%產率 |
| 138 | 外消旋-2-(N-[4-胺基-5-[4-[2-(N,2-二甲基苯胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物100,N,2-二甲基苯胺 | LC-MS (方法3)Rt = 1.13 min; MS (ESIpos): m/z = 562.1 [M+H]+ 方法F:Prep_35-65% B 13%產率 |
| 139 | 外消旋-2-(N-[4-胺基-5-[4-[2-(N,4-二甲基苯胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物100,N,4-二甲基苯胺 | LC-MS (方法3)Rt = 1.16 min; MS (ESIpos): m/z = 562.1 [M+H]+ 方法F:Prep_40-70% B 26%產率 |
| 140 | 外消旋-2-(N-[4-胺基-5-[4-[2-(N,3-二甲基苯胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物100,N,3-二甲基苯胺 | LC-MS (方法3)Rt = 1.15 min; MS (ESIpos): m/z = 562.1 [M+H]+ 方法F:Prep_40-70% B 31%產率 |
| 141 | 外消旋-2-(N-[4-胺基-5-[4-[2-(2,2-二甲基丙基胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物100,2,2-二甲基丙-1-胺 | LC-MS (方法3)Rt = 1.08 min; MS (ESIpos): m/z = 528.1 [M+H]+ 方法F:Prep_30-60% B 4%產率 |
將2-[4-[4-胺基-2-(N-[2-胺基-1-甲基-2-側氧基-乙基]-4-氟-苯胺基)噻唑-5-羰基]苯氧基]乙酸(鏡像異構物2) (30 mg,65 µmol;中間物100.2)及金剛烷-1-胺(20 mg,131 µmol)溶解於二甲基甲醯胺(0.5 mL)中。添加N,N-二異丙基乙基胺(25 mg,196 µmol)、4-二甲基胺基吡啶(0.4 mg,3 µmol)及HATU (50 mg,131 µmol)。在室溫攪拌反應混合物隔夜。
過濾反應混合物且藉由RP-HPLC (方法E,鹼性)純化,得到12 mg (29%產率)標題化合物。
1
H-NMR (400 MHz, DMSO-d6
): δ ppm = 1.16 (d,J
=7.60 Hz, 3 H), 1.59 - 1.63 (m, 6 H), 1.92 (d,J
=2.53 Hz, 6 H), 2.00 (br d,J
=1.77 Hz, 3 H), 4.41 (s, 2 H), 5.00 - 5.13 (m, 1 H), 6.89 (d,J
=8.87 Hz, 2 H), 7.24 (s, 1 H), 7.30 - 7.36 (m, 3 H), 7.46 (d,J
=8.87 Hz, 2 H), 7.57 (s, 1 H), 7.64 (dd,J
=9.00, 5.20 Hz, 2 H), 8.11 (br s, 2 H)。
LC-MS (方法2)Rt = 1.32 min; MS (ESIpos): m/z = 592.5 [M+H]+
以下實例由下表8中陳述之起始材料,使用關於實例142之程序製備。
表8:實例143至155
| 實例編號 | 化學結構 化學名稱 | 起始材料 | 分析/純化/產率 |
| 143 | 2-(N-[5-[4-[2-(1-金剛烷基甲基胺基)-2-側氧基-乙氧基]苯甲醯基]-4-胺基-噻唑-2-基]-4-氟-苯胺基)丙醯胺(單一立體異構物) | 中間物100.2; 1-金剛烷基甲胺 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.15 (d,J =7.35 Hz, 3 H), 1.31 (d,J =2.03 Hz, 6 H), 1.44 - 1.48 (m, 3 H), 1.55 - 1.61 (m, 3 H), 1.80 (br s, 3 H), 2.78 (d,J =6.59 Hz, 2 H), 4.54 (s, 2 H), 5.02 - 5.11 (m, 1 H), 6.94 (d,J =8.87 Hz, 2 H), 7.25 (s, 1 H), 7.32 (t,J =8.74 Hz, 2 H), 7.48 (d,J =8.62 Hz, 2 H), 7.57 (s, 1 H), 7.63 (dd,J =8.87, 4.82 Hz, 2 H), 7.82 (t,J =6.21 Hz, 1 H), 8.19 (br s, 2 H)。 LC-MS (方法1)Rt = 1.29 min; MS (ESIpos): m/z = 606.5 [M+H]+ RP-HPLC (方法E,鹼性) 41%產率 |
| 144 | 2-(N-[5-[4-[2-[2-(1-金剛烷基)乙基胺基]-2-側氧基-乙氧基]苯甲醯基]-4-胺基-噻唑-2-基]-4-氟-苯胺基)丙醯胺(單一立體異構物) | 中間物100.2; 2-(1-金剛烷基)乙胺 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.13 - 1.17 (m, 3 H), 1.17 - 1.24 (m, 2 H), 1.44 (d,J =2.03 Hz, 6 H), 1.55 - 1.61 (m, 3 H), 1.62 - 1.68 (m, 3 H), 1.87 - 1.91 (m, 3 H), 3.07 - 3.15 (m, 2 H), 4.45 (s, 2 H), 5.01 - 5.10 (m, 1 H), 6.92 (d,J =8.87 Hz, 2 H), 7.24 (s, 1 H), 7.33 (t,J =8.87 Hz, 2 H), 7.47 (d,J =8.87 Hz, 2 H), 7.57 (s, 1 H), 7.64 (dd,J =8.87, 5.07 Hz, 2 H), 8.30 (br s, 2 H), 7.97 (t,J =5.83 Hz, 1 H)。 LC-MS (方法1)Rt = 1.40 min; MS (ESIpos): m/z = 620.6 [M+H]+ RP-HPLC (方法E,鹼性) |
| 145 | 2-(N-[4-胺基-5-[4-[2-(4-氯苯胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺(單一立體異構物) | 中間物100.2; 4-氯苯胺 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 4.73 (s, 2 H), 5.00 - 5.11 (m, 1 H), 6.98 (d,J =8.87 Hz, 2 H), 7.24 (s, 1 H), 7.33 (t,J =8.87 Hz, 2 H), 7.38 (d,J =8.87 Hz, 2 H), 7.49 (d,J =8.87 Hz, 2 H), 7.57 (s, 1 H), 7.61 - 7.67 (m, 4 H), 8.08 (br s, 2 H), 10.24 (s, 1 H)。 LC-MS (方法1)Rt = 1.20 min; MS (ESIpos): m/z = 568.4 [M+H]+ RP-HPLC (方法D,鹼性) 59%產率 |
| 146 | 4-[[2-[4-[4-胺基-2-(4-氟-N-[2-胺基-1-甲基-2-側氧基-乙基]苯胺基)噻唑-5-羰基]苯氧基]乙醯基]胺基]苯甲醯胺(單一立體異構物) | 中間物100.2; 4-胺基苯甲醯胺 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 4.76 (s, 2 H), 5.01 - 5.09 (m, 1 H), 6.99 (d,J =8.87 Hz, 2 H), 7.24 (s, 1 H), 7.26 (br s, 1 H), 7.33 (t,J =8.74 Hz, 2 H), 7.49 (d,J =8.62 Hz, 2 H), 7.58 (s, 1 H), 7.64 (dd,J =9.00, 5.20 Hz, 2 H), 7.68 (d,J =8.87 Hz, 2 H), 7.84 (d,J =8.87 Hz, 2 H), 7.87 - 7.90 (m, 1 H), 8.10 (br s, 2 H), 10.31 (s, 1 H)。 LC-MS (方法1)Rt = 0.88 min; MS (ESIpos): m/z = 577.4 [M+H]+ RP-HPLC (方法C,鹼性) 48%產率 |
| 147 | 2-(N-[4-胺基-5-[4-[2-((2RS),3-二羥基丙基胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺(兩種非鏡像異構物之混合物) | 中間物100.2; 外消旋-3-胺基丙烷-1,2-二醇 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 2.99 - 3.08 (m, 1 H), 3.24 - 3.30 (m, 4 H), 3.48 - 3.56 (m, 2 H), 4.49 - 4.53 (m, 2 H), 4.55 - 4.60 (m, 1 H), 4.75 - 4.85 (m, 1 H), 5.05 (br d,J =7.10 Hz, 1 H), 6.92 - 6.96 (m, 2 H), 7.24 (s, 1 H), 7.33 (t,J =8.87 Hz, 2 H), 7.48 (d,J =8.62 Hz, 2 H), 7.58 (s, 1 H), 7.61 - 7.67 (m, 2 H), 7.93 - 7.99 (m, 1 H)。 LC-MS (方法1)Rt = 0.78 min; MS (ESIpos): m/z = 532.4 [M+H]+ RP-HPLC (方法B,鹼性) 54%產率 |
| 148 | 2-(N-[4-胺基-5-[4-[2-側氧基-2-[2-(1-哌啶基)乙基胺基]乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺(單一立體異構物) | 中間物100.2; 2-(哌啶-1-基)乙胺(鹽酸鹽) | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.16 (d,J =7.60 Hz, 3 H), 1.28 - 1.46 (m, 7 H), 2.22 - 2.30 (m, 6 H), 3.16 - 3.24 (m, 2 H), 4.42 - 4.56 (m, 2 H), 4.96 - 5.19 (m, 1 H), 6.90 - 6.95 (m, 2 H), 7.23 - 7.26 (m, 1 H), 7.33 (t,J =8.74 Hz, 2 H), 7.45 - 7.50 (m, 2 H), 7.56 - 7.59 (m, 1 H), 7.61 - 7.66 (m, 2 H), 7.87 (t,J =5.32 Hz, 1 H)。 LC-MS (方法1)Rt = 0.77 min; MS (ESIpos): m/z = 569.5 [M+H]+ RP-HPLC (方法C,鹼性) 54%產率 |
| 149 | 2-(N-[4-胺基-5-[4-(2-胺基-2-側氧基-乙氧基)苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺(單一立體異構物) | 中間物100.2; 含氨水之二㗁烷 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 4.44 (s, 2 H), 5.05 (q,J =6.84 Hz, 1 H), 6.92 (d,J =8.87 Hz, 2 H), 7.24 (s, 1 H), 7.33 (t,J =8.87 Hz, 2 H), 7.38 (br s, 1 H), 7.47 (d,J =8.87 Hz, 2 H), 7.52 (br s, 1 H), 7.58 (s, 1 H), 7.64 (dd,J =8.87, 5.07 Hz, 2 H), 8.07 (br s, 2 H)。 LC-MS (方法1)Rt = 0.82 min; MS (ESIpos): m/z = 458.3 [M+H]+ RP-HPLC (方法B,鹼性) 60%產率 |
| 150 及151 | (R)-2-(N-[4-胺基-5-[4-[2-(甲基胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺及 (S)-2-(N-[4-胺基-5-[4-[2-(甲基胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | ||
| 150 | 2-(N-[4-胺基-5-[4-[2-(甲基胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺(鏡像異構物1) | 中間物100.1; 含甲胺之四氫呋喃,2.0M | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.16 (d,J =7.60 Hz, 3 H), 2.63 (d,J =4.82 Hz, 3 H), 4.47 (s, 2 H), 5.05 (q,J =6.00 Hz, 1 H), 6.93 (d,J =8.87 Hz, 2 H), 7.24 (s, 1 H), 7.33 (t,J =8.74 Hz, 2 H), 7.48 (d,J =8.62 Hz, 2 H), 7.58 (s, 1 H), 7.64 (dd,J =8.87, 5.07 Hz, 2 H), 8.15 (br s, 2 H), 8.00 - 8.04 (m, 1 H)。 LC-MS (方法1)Rt = 0.88 min; MS (ESIpos): m/z = 472.3 [M+H]+ RP-HPLC (方法C,鹼性) 64%產率 |
| 151 | 2-(N-[4-胺基-5-[4-[2-(甲基胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺(鏡像異構物2) | 中間物100.2; 含甲胺之四氫呋喃,2.0M | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.16 (d,J =7.60 Hz, 3 H), 2.63 (d,J =4.82 Hz, 3 H), 4.47 (s, 2 H), 5.05 (q,J =7.35 Hz, 1 H), 6.93 (d,J =8.87 Hz, 2 H), 7.25 (s, 1 H), 7.33 (t,J =8.74 Hz, 2 H), 7.48 (d,J =8.62 Hz, 2 H), 7.58 (s, 1 H), 7.64 (dd,J =8.87, 5.07 Hz, 2 H), 8.07 (br s, 2 H), 7.99 - 8.05 (m, 1 H)。 LC-MS (方法1)Rt = 0.88 min; MS (ESIpos): m/z = 472.3 [M+H]+ RP-HPLC (方法C,鹼性) 29%產率 |
| 152 及153 | (R)-2-(N-[4-胺基-5-[4-[2-(異丙基胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺及 (S)-2-(N-[4-胺基-5-[4-[2-(異丙基胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | ||
| 152 | 2-(N-[4-胺基-5-[4-[2-(異丙基胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺(鏡像異構物1) | 中間物100.1; 丙-2-胺 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.04 - 1.08 (m, 6 H), 1.16 (d,J =7.35 Hz, 3 H), 3.86 - 3.96 (m, 1 H), 4.45 (s, 2 H), 5.05 (br q,J =7.10 Hz, 1 H), 6.92 (d,J =8.87 Hz, 2 H), 7.24 (s, 1 H), 7.33 (t,J =8.87 Hz, 2 H), 7.47 (d,J =8.87 Hz, 2 H), 7.57 (s, 1 H), 7.64 (dd,J =9.00, 5.20 Hz, 2 H), 8.08 (br s, 2 H), 7.87 (br d,J =8.11 Hz, 1 H)。 LC-MS (方法1)Rt = 1.00 min; MS (ESIpos): m/z = 500.4 [M+H]+ RP-HPLC (方法C,鹼性) 75%產率 |
| 153 | 2-(N-[4-胺基-5-[4-[2-(異丙基胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺(鏡像異構物2) | 中間物100.2; 丙-2-胺 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.06 (d,J =6.59 Hz, 6 H), 1.16 (d,J =7.35 Hz, 3 H), 3.87 - 3.96 (m, 1 H), 4.45 (s, 2 H), 5.05 (q,J =7.86 Hz, 1 H), 6.92 (d,J =8.87 Hz, 2 H), 7.24 (s, 1 H), 7.33 (t,J =8.87 Hz, 2 H), 7.47 (d,J =8.87 Hz, 2 H), 7.57 (s, 1 H), 7.64 (dd,J =9.00, 5.20 Hz, 2 H), 8.06 (br s, 2 H), 7.87 (br d,J =7.86 Hz, 1 H)。 LC-MS (方法1)Rt = 1.00 min; MS (ESIpos): m/z = 500.4 [M+H]+ RP-HPLC (方法C,鹼性) 72%產率 |
| 154 | 外消旋-2-[4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氟-苯胺基)噻唑-5-羰基]苯氧基]-N-異丙基-2-甲基-丙醯胺 | 中間物82;丙-2-胺 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 0.94 (d,J =6.59 Hz, 6 H), 1.16 (d,J =7.35 Hz, 3 H), 1.43 (s, 6 H), 3.83 - 3.96 (m, 1 H), 4.99 - 5.11 (m, 1 H), 6.79 (d,J =8.62 Hz, 2 H), 7.24 (s, 1 H), 7.32 (t,J =8.87 Hz, 2 H), 7.42 (d,J =8.62 Hz, 2 H), 7.57 (s, 1 H), 7.63 (dd,J =8.74, 5.20 Hz, 2 H), 7.75 (d,J =8.11 Hz, 1 H), 7.80 - 8.50 (m, 2 H)。 LC-MS (方法1)Rt = 1.10 min; MS (ESIpos): m/z = 528.4 [M+H]+ RP-HPLC (方法D,鹼性) 23%產率 |
| 155 | 外消旋-2-[4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氟-苯胺基)噻唑-5-羰基]苯氧基]-2-甲基-丙醯胺 | 中間物82;氨水 | 1 H-NMR (400 MHz, DMSO-d 6 ): δ ppm = 1.15 (d,J =7.35 Hz, 3 H), 1.43 (s, 6 H), 4.99 - 5.11 (m, 1 H), 6.82 (d,J =8.87 Hz, 2 H), 7.25 (br d,J =7.86 Hz, 2 H), 7.33 (t,J =8.87 Hz, 2 H), 7.44 (d,J =8.62 Hz, 2 H), 7.50 - 7.52 (m, 1 H), 7.57 - 7.59 (m, 1 H), 7.64 (dd,J =8.74, 5.20 Hz, 2 H), 7.82 - 8.34 (m, 2 H)。 LC-MS (方法1)Rt = 0.93 min; MS (ESIpos): m/z = 486.3 [M+H]+ RP-HPLC (方法C,鹼性) 42%產率 |
將[2-(4-氟苯胺基)-4-甲基-噻唑-5-基]-苯基-甲酮(40 mg,0.13 mmol;中間物 81
)溶解於N,N-二甲基甲醯胺(1.4 mL)中,隨後添加碳酸鉀(177 mg,1.28 mmol)及外消旋-2-溴丙醯胺(97 mg,0.64 mmol)。在90℃攪拌反應混合物1 h。過濾反應混合物且藉由RP-HPLC (方法D,鹼性)純化,得到24 mg (48%產率)標題化合物。
1
H-NMR (400 MHz, DMSO-d6
): δ ppm = 1.16 (d,J
=7.35 Hz, 3 H), 2.24 - 2.27 (m, 3 H), 5.11 (q,J
=7.35 Hz, 1 H), 7.20 (s, 1 H), 7.36 (t,J
=8.87 Hz, 2 H), 7.43 - 7.48 (m, 2 H), 7.51 - 7.57 (m, 3 H), 7.62 (s, 1 H), 7.67 (dd,J
=9.13, 5.07 Hz, 2 H)。
LC-MS (方法2)Rt = 1.16 min; MS (ESIpos): m/z = 384.4 [M+H]+
將外消旋-2-(N-[4-胺基-5-(4-苯甲氧基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺(100 mg,204 µmol,實例158)溶解於乙醇(2.5 mL)中。在氮氣氛圍下添加鈀/碳(325 mg,10%純度,306 µmol;CAS-RN 7440-05-3),且接著對氮氣氛圍抽真空且用氫氣置換。在室溫在氫氣氛圍下攪拌混合物3.5 h。另外添加鈀/碳(100 µmol),且在室溫在氫氣氛圍下另外攪拌混合物3 h。反應混合物經由矽藻土過濾,用乙醇洗滌,且減壓濃縮濾液。藉由RP-HPLC (方法B,鹼性)純化殘餘物,得到27 mg (31%產率)標題化合物。
LC-MS (方法2)Rt = 0.69 min; MS (ESIpos): m/z = 401.2 [M+H]+
1
H-NMR (400 MHz, DMSO-d
6): δ ppm = 1.16 (d,J
=7.35 Hz, 3 H), 2.08 (s, 1 H), 5.01 - 5.09 (m, 1 H), 6.70 - 6.75 (m, 2 H), 7.24 (s, 1 H), 7.33 (t,J
=8.87 Hz, 2 H), 7.37 - 7.41 (m, 2 H), 7.57 (s, 1 H), 7.64 (dd,J
=9.00, 4.94 Hz, 2 H), 7.76 - 8.21 (m, 2 H), 9.90 (br s, 1 H)
將[4-胺基-2-(4-氟苯胺基)-1,3-噻唑-5-基][4-(苯甲氧基)苯基]甲酮(610 mg,1.45 mmol,中間物77)懸浮於DMF (10 mL)中,添加外消旋-2-溴丙醯胺(265 mg,1.75 mmol)及碳酸鉀(301 mg,2.18 mmol)。在室溫攪拌反應混合物3.5 h。另外添加外消旋-2-溴丙醯胺(265 mg,1.75 mmol)及碳酸鉀(301 mg,2.18 mmol),且在室溫攪拌混合物隔夜。混合物用水處理且攪拌30 min。所得沈澱藉由過濾分離,用水洗滌且乾燥,得到641 mg (98%純度,88%產率)標題化合物。
1
H-NMR (400 MHz, DMSO-d6
): δ ppm = 1.16 (d,J
=7.35 Hz, 3 H), 5.02 - 5.09 (m, 1 H), 5.11 (s, 2 H), 7.00 (d,J
=8.87 Hz, 2 H), 7.25 (s, 1 H), 7.31 - 7.45 (m, 7 H), 7.46 - 7.50 (m, 2 H), 7.57 (s, 1 H), 7.64 (dd,J
=8.87, 5.07 Hz, 2 H), 7.78 - 8.38 (m, 2 H)。
LC-MS (方法2)Rt = 1.25 min; MS (ESIpos): m/z = 491.3 [M+H]+
以下實例由下表9中陳述之起始材料,使用關於實例158之程序製備。
必要時,在沈澱、萃取或過濾反應混合物之後,藉由RP-HPLC (方法A至D,視極性而定)或藉由製備型急驟層析(方法X、Y或Z,視極性而定)純化粗產物。
使用所陳述管柱及溶劑條件藉由對掌性HPLC將鏡像異構物與其外消旋體分離。
表9:實例159至256
| 實例編號 | 化學結構 化學名稱 | 起始材料 | 分析/純化/產率 |
| 159 | 外消旋-2-(N-[4-胺基-5-[6-(二氟甲基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物101; 外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 5.04 - 5.08 (m, 1 H), 6.94 (t,J =60 Hz, 1 H), 7.29 - 7.33 (m, 3 H), 7.60 -7.65 (m, 3 H), 7.72 (d,J =8.11 Hz, 1 H), 8.04 (dd,J =7.98, 2.15 Hz, 1 H), 8.30 8.34 (m, 2 H), 8.76 (d,J =1.52 Hz, 1 H)。 RP-HPLC (方法C鹼性) LC-MS (方法2)Rt = 1.00 min MS (ESIpos): m/z = 436.4 [M+H]+ 48%產率 |
| 160 | 外消旋-2-(N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-3-氯-4-氟-苯胺基)丙醯胺 | 中間物102; 外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.18 (d,J =7.35 Hz, 3 H), 5.00 - 5.04 (m, 1 H), 7.31 (s, 1 H), 7.40 - 7.44 (m, 2 H), 7.55 - 7.58 (m, 1 H), 7.63 - 7.67 (m, 2 H), 7.91 (dd,J =6.84, 2.28 Hz, 1 H), 8.27 -8.31 (m, 2 H), 8.60 - 8.64 (m, 2 H)。 經由沈澱分離 LC-MS (方法2)Rt = 0.94 min MS (ESIpos): m/z = 420.3 [M+H]+ 60%產率 |
| 160.1 及 160.2 | (R)-2-(N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-3-氯-4-氟-苯胺基)丙醯胺及(S)- 2-(N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-3-氯-4-氟-苯胺基)丙醯胺 | ||
| 160.1 | 2-(N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-3-氯-4-氟-苯胺基)丙醯胺(鏡像異構物1) | 實例160 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.18 (d,J =7.35 Hz, 4 H), 5.00 - 5.05 (m, 1 H), 7.31 (s, 1 H), 7.42 (d,J =6.08 Hz, 2 H), 7.57 (m, 1 H), 7.62 - 7.67 (m, 2 H), 7.92 (dd,J =6.84, 2.53 Hz, 1 H), 8.25 - 8.29 (m, 2 H), 8.63 (d,J =5.83 Hz, 2 H)。 LC-MS (方法1)Rt = 0.86 min; MS (ESIpos): m/z = 420.3 [M+H]+ 34%產率 |
| 對掌性HPLC實例160.1 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-3-氯-4-氟-苯胺基)丙醯胺(560 mg,1.33 mmol,實例160),得到190 mg (34%產率) 2-(N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-3-氯-4-氟-苯胺基)丙醯胺,鏡像異構物1。 製備型對掌性 HPLC PrepCon Labomatic HPLC;管柱:YMC Amylose SA 10µ,250×50; 溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:50% A+50% B;流速:120 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 1.23 min Waters Alliance 2695;管柱:YMC Amylose SA 3µ,100×4.6; 溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:50% A+50% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 160.2 | 2-(N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-3-氯-4-氟-苯胺基)丙醯胺(鏡像異構物2) | 實例160 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.18 (d,J =7.35 Hz, 4 H), 5.00 - 5.04 (m, 1 H), 7.31 (s, 1 H), 7.42 (d,J =6.08 Hz, 2 H), 7.55 - 7.59 (m, 1 H), 7.63 - 7.67 (m, 2 H), 7.92 (dd,J =6.84, 2.53 Hz, 1 H), 8.24 - 8.30 (m, 2 H), 8.63 (d,J =5.83 Hz, 2 H)。 LC-MS (方法1)Rt = 0.86 min; MS (ESIpos): m/z = 420.3 [M+H]+ 33%產率 |
| 對掌性HPLC實例160.2 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-3-氯-4-氟-苯胺基)丙醯胺(560 mg,1.33 mmol,實例160),得到185 mg (33%產率) 2-(N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-3-氯-4-氟-苯胺基)丙醯胺,鏡像異構物2。 製備型對掌性 HPLC PrepCon Labomatic HPLC;管柱:YMC Amylose SA 5µ,250×50; 溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:50% A+50% B;流速:120 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 1.67 min Waters Alliance 2695;管柱:YMC Amylose SA 3µ,100×4.6; 溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:50% A+50% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 161 | 外消旋-2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-3-氯-4-氟-苯胺基)丙醯胺 | 中間物103; 外消旋-2-溴丙醯胺 | 1 H NMR (500 MHz, DMSO-d 6 ) δ ppm = 1.18 (d,J =7.57 Hz, 3 H), 3.76 (s, 3 H), 5.00 - 5.04 (m, 1 H), 6.94 (d,J =8.83 Hz, 2 H), 7.29 (s, 1 H), 7.50 (d,J =8.83 Hz, 2 H), 7.57 - 7.59 (m, 1 H), 7.63 (s, 1 H), 7.64 - 7.68 (m, 1 H), 7.92 (m, 1 H), 8.12 - 8.17 (m, 2 H)。 LC-MS (方法2)Rt = 1.17 min 經由沈澱分離 MS (ESIpos): m/z = 449.3 [M+H]+ 70%產率 |
| 161.1 及 161.2 | (R)- 2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-3-氯-4-氟-苯胺基)丙醯胺及 (S)- 2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-3-氯-4-氟-苯胺基)丙醯胺 | ||
| 161.1 | 2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-3-氯-4-氟-苯胺基)丙醯胺(鏡像異構物1) | 實例161 | 1 H NMR (500 MHz, DMSO-d 6 ) δ ppm = 1.18 (d,J =7.57 Hz, 3 H), 3.76 (s, 3 H), 5.00 - 5.04 (m, 1 H), 6.94 (d,J =8.83 Hz, 2 H), 7.29 (s, 1 H), 7.50 (d,J =8.83 Hz, 2 H), 7.55 - 7.59 (m, 1 H), 7.63 (s, 1 H), 7.64 - 7.66 (m, 1 H), 7.90 - 7.94 (m, 1 H), 8.14 (m, 2 H)。 LC-MS (方法1)Rt = 1.13 min MS (ESIpos): m/z = 449.4 [M+H]+ [α]D 20 = 85° c = 10.3 mg/mL於DMSO中 31%產率 |
| 對掌性HPLC實例161.1 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-3-氯-4-氟-苯胺基)丙醯胺(1300 mg,2.9 mmol,實例161),隨後在MTBE中濕磨,得到401 mg (31%產率) 2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-3-氯-4-氟-苯胺基)丙醯胺,鏡像異構物1。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:YMC Cellulose SB 5µ,250×30;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:2-丙醇;等度:60% A+40% B;流速:40 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 2.11 min 儀器:Thermo Fisher UltiMate 3000;管柱:YMC Cellulose SB 3µ,100×4.6;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:2-丙醇;等度:60% B+40% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 161.2 | 2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-3-氯-4-氟-苯胺基)丙醯胺(鏡像異構物2) | 實例161 | 1 H NMR (500 MHz, DMSO-d 6 ) δ ppm = 1.18 (d,J =7.57 Hz, 3 H), 3.76 (s, 3 H), 5.00 - 5.04 (m, 1 H), 6.94 (d,J =8.83 Hz, 2 H), 7.29 (s, 1 H), 7.50 (d,J =8.83 Hz, 2 H), 7.58 (m, 1 H), 7.63 (s, 1 H), 7.66 (m, 1 H), 7.90 - 7.94 (m, 1 H), 8.10 - 8.16 (m, 2 H)。 LC-MS (方法1)Rt = 1.13 min; MS (ESIpos): m/z = 449.4 [M+H]+ [α]D 20 = -89° c = 10.1 mg/mL於DMSO中 29%產率 |
| 對掌性HPLC實例161.2 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-3-氯-4-氟-苯胺基)丙醯胺(1300 mg,2.9 mmol,實例161),隨後在MTBE中濕磨,得到375 mg (29%產率) 2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-3-氯-4-氟-苯胺基)丙醯胺,鏡像異構物2。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC;管柱:YMC Cellulose SB 5µ,250×30;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:2-丙醇;等度:60% A+40% B;流速:40 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 5.48 min 儀器:Thermo Fisher UltiMate 3000;管柱:YMC Cellulose SB 3µ,100×4.6;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:2-丙醇;等度:60% B+40% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 162 | 外消旋-2-(N-[4-胺基-5-[6-(二氟甲氧基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物104; 外消旋-2-溴丙醯胺 | 1 H-NMR (400 MHz, DMSO-d6 ): δ ppm = 1.13 - 1.20 (m, 3 H), 5.00 - 5.12 (m, 1 H), 7.10 (d, J=8.62 Hz, 1 H), 7.23 - 7.28 (m, 1 H), 7.34 (t, J=8.87 Hz, 2 H), 7.52 - 7.68 (m, 3 H), 7.97 - 8.03 (m, 1 H), 8.06 - 8.35 (m, 1 H), 8.35 - 8.42 (m, 1 H)。 LC-MS (方法2)Rt = 1.10 min 經由沈澱分離 MS (ESIpos): m/z = 452.2 [M+H]+ 61%產率 |
| 162.1 及162.2 | (R)-2-(N-[4-胺基-5-[6-(二氟甲氧基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺及 (S)-2-(N-[4-胺基-5-[6-(二氟甲氧基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | ||
| 162.1 | 2-(N-[4-胺基-5-[6-(二氟甲氧基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺(鏡像異構物1) | 實例162 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 5.06 (m, 1 H), 7.11 (d,J =8.62 Hz, 1 H), 7.26 (s, 1 H), 7.34 (m, 2 H), 7.59 (s, 1 H), 7.65 (br d,J =3.80 Hz, 2 H), 7.71 (t,J =72 Hz, 1 H), 8.00 (dd,J =8.49, 2.41 Hz, 1 H), 8.19 (m, 1 H), 8.38 (d,J =2.03 Hz, 1 H), 8.38 (m, 1 H)。 LC-MS (方法2)Rt = 1.13 min; MS (ESIpos): m/z = 452.3 [M+H]+ [α]D 20 = -71° c = 8 mg/mL於DMSO中 37%產率 |
| 對掌性HPLC實例162.1 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-[6-(二氟甲氧基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺(105 mg,0.23 mmol,實例162),得到39 mg (37%產率) 2-(N-[4-胺基-5-[6-(二氟甲氧基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺,鏡像異構物1。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC-4;管柱:YMC Cellulose SB 5µ,250×30; 溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:乙醇+ 0.1 vol%二乙胺;等度:70% A+30% B;流速:50 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 3.07 min 儀器:Waters Alliance 2695;管柱:YMC Cellulose SB 3µ,100×4.6; 溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:乙醇;等度:70% A+30% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 162.2 | 2-(N-[4-胺基-5-[6-(二氟甲氧基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺(鏡像異構物2) | 實例162 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 5.02 - 5.08 (m, 1 H), 7.11 (d,J =8.62 Hz, 1 H), 7.26 (s, 1 H), 7.34 (m, 2 H), 7.59 (s, 1 H), 7.65 (br d,J =3.80 Hz, 2 H), 7.71 (t,J =72 Hz, 1 H), 8.00 (dd,J =8.49, 2.41 Hz, 1 H), 8.17 - 8.21 (m, 1 H), 8.38 (d,J =2.03 Hz, 1 H), 8.38 (m, 1 H)。 LC-MS (方法2)Rt = 1.13 min; MS (ESIpos): m/z = 452.3 [M+H]+ [α]D 20 = 74° c = 8.7 mg/mL於DMSO中 39%產率 |
| 對掌性HPLC實例162.2 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-[6-(二氟甲氧基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺(105 mg,0.23 mmol,實例162),得到41 mg (39%產率) 2-(N-[4-胺基-5-[6-(二氟甲氧基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺,鏡像異構物2。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC-4;管柱:YMC Cellulose SB 5µ,250×30; 溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:乙醇+ 0.1 vol%二乙胺;等度:70% A+30% B;流速:50 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 2.40 min 儀器:Waters Alliance 2695;管柱:YMC Cellulose SB 3µ,100×4.6; 溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:乙醇;等度:70% A+30% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 163 | 外消旋-2-(N-[4-胺基-5-[6-(二氟甲氧基)吡啶-3-羰基]噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺 | 中間物105; 外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.19 (d,J =8 Hz, 3 H), 5.03 (q,J =6.84 Hz, 1 H), 7.09 - 7.12 (m, 1 H), 7.30 (s, 1 H), 7.58 (m, 3 H), 7.71 (t,J =72 Hz, 1 H), 7.79 (m, 1 H), 8.02 (dd,J =8.49, 2.41 Hz, 1 H), 8.19 - 8.23 (m, 2 H), 8.41 (d,J =2.03 Hz, 1 H)。 LC-MS (方法2)Rt = 1.15 min Biotage (方法X) MS (ESIpos): m/z = 470.3 [M+H]+ 56%產率 |
| 163.1 及163.2 | (R)-(N-[4-胺基-5-[6-(二氟甲氧基)吡啶-3-羰基]噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺及(S)-(N-[4-胺基-5-[6-(二氟甲氧基)吡啶-3-羰基]噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺 | ||
| 163.1 | 2-(N-[4-胺基-5-[6-(二氟甲氧基)吡啶-3-羰基]噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺(鏡像異構物1) | 實例163 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 5.02 - 5.06 (m, 1 H), 7.11 (d,J =8.62 Hz, 1 H), 7.26 (s, 1 H), 7.34 (m, 2 H), 7.59 (s, 1 H), 7.65 (br d,J =3.80 Hz, 2 H), 7.71 (t,J =72 Hz, 1 H), 8.00 (dd,J =8.49, 2.41 Hz, 1 H), 8.17 - 8.22 (m, 1 H), 8.38 (d,J =2.03 Hz, 1 H), 8.35 - 8.37 (m, 1 H)。 LC-MS (方法2)Rt = 1.15 min 41%產率 |
| 對掌性HPLC實例163.1 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-[6-(二氟甲氧基)吡啶-3-羰基]噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺(120 mg,0.26 mmol,實例163),得到49 mg (41%產率) 2-(N-[4-胺基-5-[6-(二氟甲氧基)吡啶-3-羰基]噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺,鏡像異構物1。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC-2;管柱:YMC Amylose SA 10µ,250×50;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:95% A+5% B;流速:100 mL/min;溫度:25℃;UV:280 nm 分析型對掌性 HPLC : Rt = 2.42 min 儀器:Thermo Fisher UltiMate 3000;管柱:YMC Amylose SA 3µ,100×4.6;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:95% A+5% B;流速:1.4 mL/min;溫度:25℃;UV:280 nm | |||
| 163.2 | 2-(N-[4-胺基-5-[6-(二氟甲氧基)吡啶-3-羰基]噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺(鏡像異構物2) | 實例163 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.19 (d,J =7.35 Hz, 3 H), 5.02 - 5.06 (m, 1 H), 7.12 (d,J =8.62 Hz, 1 H), 7.30 (s, 1 H), 7.48 - 7.52 (m, 1 H), 7.58 - 7.62 (m, 2 H), 7.72 (t,J =72 Hz, 1 H), 7.77 - 7.82 (m, 1 H), 8.02 (dd,J =8.49, 2.41 Hz, 1 H), 8.20 - 8.25 (m, 2 H), 8.41 (d,J =2.53 Hz, 1 H)。 LC-MS (方法2)Rt = 1.15 min 56%產率 |
| 對掌性HPLC實例163.2 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-[6-(二氟甲氧基)吡啶-3-羰基]噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺(120 mg,0.26 mmol,實例163),得到68 mg (56%產率) 2-(N-[4-胺基-5-[6-(二氟甲氧基)吡啶-3-羰基]噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺,鏡像異構物2。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC-2;管柱:YMC Amylose SA 10µ,250×50;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:95% A+5% B;流速:100 mL/min;溫度:25℃;UV:280 nm 分析型對掌性 HPLC : Rt = 3.72 min 儀器:Thermo Fisher UltiMate 3000;管柱:YMC Amylose SA 3µ,100×4.6;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:95% A+5% B;流速:1.4 mL/min;溫度:25℃;UV:280 nm | |||
| 164 | 外消旋-2-(N-[4-胺基-5-[6-(二氟甲氧基)吡啶-3-羰基]噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺 | 中間物106,外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.20 (d,J =8.11 Hz, 3 H), 5.01 - 5.05 (m, 1 H), 7.12 (d,J =8.62 Hz, 1 H), 7.32 (s, 1 H), 7.53 (m, 1 H), 7.64 (s, 1 H), 7.71 (t,J =72 Hz, 1 H), 7.72 - 7.76 (m, 2 H), 8.03 (dd,J =8.62, 2.53 Hz, 1 H), 8.20 - 8.25 (m, 2 H), 8.41 (d,J =2.28 Hz, 1 H)。 Biotage (方法X) LC-MS (方法2)Rt = 1.21 min MS (ESIpos): m/z = 486.3 [M+H]+ 53%產率 |
| 164.1 及164.2 | (R)-2-(N-[4-胺基-5-[6-(二氟甲氧基)吡啶-3-羰基]噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺及(S)-2-(N-[4-胺基-5-[6-(二氟甲氧基)吡啶-3-羰基]噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺 | ||
| 164.1 | 2-(N-[4-胺基-5-[6-(二氟甲氧基)吡啶-3-羰基]噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺(鏡像異構物1) | 實例164 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.20 (d,J =7.35 Hz, 3 H), 5.01 - 5.05 (m, 1 H), 7.12 (m, 1 H), 7.32 (s, 1 H), 7.53 (m, 1 H), 7.64 (s, 1 H), 7.71 (t,J =72 Hz, 1 H), 7.72 - 7.77 (m, 2 H), 8.03 (dd,J =8.62, 2.53 Hz, 1 H), 8.21 - 8.26 (m, 2 H), 8.39 - 8.42 (m, 1 H)。 45%產率 |
| 對掌性HPLC實例164.1 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-[6-(二氟甲氧基)吡啶-3-羰基]噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺(113 mg,0.23 mmol,實例164),得到51 mg (45%產率) 2-(N-[4-胺基-5-[6-(二氟甲氧基)吡啶-3-羰基]噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺,鏡像異構物1。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC-2;管柱:YMC Amylose SA 10µ,250×50;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:95% A+5% B;流速:100 mL/min;溫度:25℃;UV:280 nm 分析型對掌性 HPLC : Rt = 2.6 min 儀器:Thermo Fisher UltiMate 3000;管柱:YMC Amylose SA 3µ,100×4.6;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:95% A+5% B;流速:1.4 mL/min;溫度:25℃;UV:280 nm | |||
| 164.2 | 2-(N-[4-胺基-5-[6-(二氟甲氧基)吡啶-3-羰基]噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺(鏡像異構物2) | 實例164 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.20 (d,J =7.35 Hz, 3 H), 5.01 - 5.05 (m, 1 H), 7.10 - 7.14 (m, 1 H), 7.32 (s, 1 H), 7.50 - 7.56 (m, 1 H), 7.64 (s, 1 H), 7.71 (t,J =72 Hz, 1 H), 7.70 - 7.78 (m, 2 H), 8.03 (dd,J =8.62, 2.53 Hz, 1 H), 8.20 - 8.25 (m, 2 H), 8.40 - 8.43 (m, 1 H)。 45%產率 |
| 對掌性HPLC實例164.2 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-[6-(二氟甲氧基)吡啶-3-羰基]噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺(113 mg,0.23 mmol,實例164),得到51 mg (45%產率) 2-(N-[4-胺基-5-[6-(二氟甲氧基)吡啶-3-羰基]噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺,鏡像異構物2。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC-2;管柱:YMC Amylose SA 10µ,250×50;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:95% A+5% B;流速:100 mL/min;溫度:25℃;UV:280 nm 分析型對掌性 HPLC : Rt = 3.87 min 儀器:Thermo Fisher UltiMate 3000;管柱:YMC Amylose SA 3µ,100×4.6;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:95% A+5% B;流速:1.4 mL/min;溫度:25℃;UV:280 nm | |||
| 165 | 外消旋-2-(N-[4-胺基-5-(4-苯甲氧基苯甲醯基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺 | 中間物107,外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.18 (d,J =7.35 Hz, 3 H), 5.00 - 5.04 (m, 1 H), 5.12 (s, 2 H), 7.00 - 7.05 (m, 2 H), 7.24 - 7.64 (m, 11 H), 7.77 - 7.81 (m, 1 H), 8.03 - 8.07 (m, 2 H)。 Biotage (方法X) LC-MS (方法2)Rt = 1.32 min MS (ESIpos): m/z = 509.4 [M+H]+ 57%產率 |
| 165.1 及165.2 | (R)-2-(N-[4-胺基-5-(4-苯甲氧基苯甲醯基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺及(S)-2-(N-[4-胺基-5-(4-苯甲氧基苯甲醯基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺 | ||
| 165.1 | 2-(N-[4-胺基-5-(4-苯甲氧基苯甲醯基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺(鏡像異構物1) | 實例165 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.19 (d,J =7.35 Hz, 4 H), 5.00 - 5.04 (m, 1 H), 5.12 (s, 2 H), 7.00 - 7.05 (m, 2 H), 7.28 (s, 1 H), 7.36 - 7.44 (m, 5 H), 7.47 - 7.52 (m, 3 H), 7.59 - 7.63 (m, 2 H), 7.78 (ddd,J =11.34, 7.54, 2.41 Hz, 1 H), 8.02 - 8.06 (m, 2 H) 46%產率 |
| 對掌性HPLC實例165.1 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-(4-苯甲氧基苯甲醯基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺(340 mg,0.67 mmol,實例165),得到155 mg (46%產率) 2-(N-[4-胺基-5-(4-苯甲氧基苯甲醯基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺,鏡像異構物1。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC-4;管柱:YMC Amylose SA 5µ,250×30;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:80% A+20% B;流速:50 mL/min;溫度:25℃;UV:280 nm 分析型對掌性 HPLC : Rt = 1.73 min 儀器:Waters Alliance 2695;管柱:YMC Amylose SA 3µ,100×4.6; 溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:80% A+20% B;流速:1.4 mL/min;溫度:25℃;UV:280 nm | |||
| 165.2 | 2-(N-[4-胺基-5-(4-苯甲氧基苯甲醯基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺(鏡像異構物2) | 實例165 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.19 (d,J =7.35 Hz, 4 H), 5.00 - 5.04 (m, 1 H), 5.12 (s, 2 H), 7.02 (m, 2 H), 7.28 (s, 1 H), 7.35 - 7.45 (m, 5 H), 7.47 - 7.52 (m, 3 H), 7.58 - 7.62 (m, 2 H), 7.78 (ddd,J =11.34, 7.54, 2.41 Hz, 1 H), 8.02 - 8.05 (m, 2 H) 46%產率 |
| 對掌性HPLC實例165.2 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-(4-苯甲氧基苯甲醯基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺(340 mg,0.67 mmol,實例165),得到156 mg (46%產率) 2-(N-[4-胺基-5-(4-苯甲氧基苯甲醯基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺,鏡像異構物2。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC-4;管柱:YMC Amylose SA 5µ,250×30;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:80% A+20% B;流速:50 mL/min;溫度:25℃;UV:280 nm 分析型對掌性 HPLC : Rt = 2.32 min 儀器:Waters Alliance 2695;管柱:YMC Amylose SA 3µ,100×4.6; 溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:80% A+20% B;流速:1.4 mL/min;溫度:25℃;UV:280 nm | |||
| 166 | 外消旋-2-(N-[4-胺基-5-(4-苯甲氧基苯甲醯基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺 | 中間物108,外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.20 (d,J =7.35 Hz, 3 H), 5.00 - 5.04 (m, 1 H), 5.12 (s, 2 H), 7.00 - 7.05 (m, 2 H), 7.30 - 7.42 (m, 6 H), 7.47 - 7.52 (m, 3 H), 7.63 (s, 1 H), 7.73 - 7.77 (m, 2 H), 8.09 - 8.13 (m, 2 H) Biotage (方法X) LC-MS (方法2)Rt = 1.36 min MS (ESIpos): m/z = 525.3 [M+H]+ 57%產率 |
| 166.1 及166.2 | (R)-2-(N-[4-胺基-5-(4-苯甲氧基苯甲醯基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺及(S)-2-(N-[4-胺基-5-(4-苯甲氧基苯甲醯基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺 | ||
| 166.1 | 2-(N-[4-胺基-5-(4-苯甲氧基苯甲醯基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺(鏡像異構物1) | 實例166 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.20 (d,J =7.35 Hz, 3 H), 5.01 - 5.04 (m, 1 H), 5.12 (s, 2 H), 7.00 - 7.05 (m, 2 H), 7.35 - 7.45 (m, 9 H), 7.63 (s, 1 H), 7.73 - 7.77 (m, 2 H), 8.08 - 8.13 (m, 2 H) 39%產率 |
| 對掌性HPLC實例166.1 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-(4-苯甲氧基苯甲醯基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺(790 mg,1.5 mmol,實例166),得到313 mg (39%產率) 2-(N-[4-胺基-5-(4-苯甲氧基苯甲醯基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺,鏡像異構物1。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC-4;管柱:YMC Cellulose SC 10µ,250×50;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:90% A+10% B;流速:100 mL/min;溫度:25℃;UV:325 nm 分析型對掌性 HPLC : Rt = 2.94 min 儀器:Thermo Fisher UltiMate 3000;管柱:YMC Cellulose SC 3µ,100×4.6;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:90% A+10% B;流速:1.4 mL/min;溫度:25℃;UV:325 nm | |||
| 166.2 | 2-(N-[4-胺基-5-(4-苯甲氧基苯甲醯基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺(鏡像異構物2) | 實例166 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.20 (d,J =7.35 Hz, 3 H), 5.01 - 5.05 (m, 1 H), 5.12 (s, 2 H), 7.00 - 7.05 (m, 2 H), 7.35 - 7.45 (m, 9 H), 7.63 (s, 1 H), 7.73 - 7.77 (m, 2 H), 8.08 - 8.13 (m, 2 H) 35%產率 |
| 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-(4-苯甲氧基苯甲醯基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺(790 mg,1.5 mmol,實例166),得到276 mg (35%產率) 2-(N-[4-胺基-5-(4-苯甲氧基苯甲醯基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺,鏡像異構物2。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC-4;管柱:YMC Cellulose SC 10µ,250×50;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:90% A+10% B;流速:100 mL/min;溫度:25℃;UV:325 nm 分析型對掌性 HPLC : Rt = 3.51 min 儀器:Thermo Fisher UltiMate 3000;管柱:YMC Cellulose SC 3µ,100×4.6;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:90% A+10% B;流速:1.4 mL/min;溫度:25℃;UV:325 nm | |||
| 167 | 外消旋-N-[4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-3,4-二氟-苯胺基)噻唑-5-羰基]苯基]胺基甲酸苯甲酯 | 中間物109,外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.18 (d,J =7.60 Hz, 3 H), 5.01 (br d,J =7.35 Hz, 1 H), 5.15 (s, 2 H), 7.28 (s, 1 H), 7.40 (m, 6 H), 7.48 (m, 5 H), 7.57 (m, 1 H), 7.61 (s, 1 H), 7.77 (ddd,J =11.41, 7.48, 2.41 Hz, 1 H), 7.95 (m, 2 H) Biotage (方法X) LC-MS (方法2)Rt = 1.22 min MS (ESIpos): m/z = 552.4 [M+H]+ 64%產率 |
| 167.1 及167.2 | (R)-N-[4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-3,4-二氟-苯胺基)噻唑-5-羰基]苯基]胺基甲酸苯甲酯及(S)-N-[4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-3,4-二氟-苯胺基)噻唑-5-羰基]苯基]胺基甲酸苯甲酯 | ||
| 167.1 | N-[4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-3,4-二氟-苯胺基)噻唑-5-羰基]苯基]胺基甲酸苯甲酯(鏡像異構物1) | 實例167 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.18 (d,J =7.35 Hz, 3 H), 5.01 (q,J =7.35 Hz, 1 H), 5.15 (s, 2 H), 5.76 (s, 1 H), 7.28 (s, 1 H), 7.35 - 7.42 (m, 5 H), 7.46 - 7.52 (m, 5 H), 7.57 (m, 1 H), 7.61 (s, 1 H), 7.78 (m, 1 H), 8.18 (m, 2 H), 10.00 (s, 1 H) 32%產率 |
| 對掌性HPLC實例167.1 在對掌性管柱上HPLC分離外消旋-N-[4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-3,4-二氟-苯胺基)噻唑-5-羰基]苯基]胺基甲酸苯甲酯(385 mg,0.7 mmol,實例167),隨後在MTBE中濕磨,得到123 mg (32%產率) N-[4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-3,4-二氟-苯胺基)噻唑-5-羰基]苯基]胺基甲酸苯甲酯,鏡像異構物1。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC-3;管柱:YMC Amylose SA 10µ,250×50;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:90% A+10% B;流速:100 mL/min;溫度:25℃;UV:280 nm 分析型對掌性 HPLC : Rt = 2.87 min 儀器:Thermo Fisher UltiMate 3000;管柱:YMC Cellulose SC 3µ,100×4.6;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:90% A+10% B;流速:1.4 mL/min;溫度:25℃;UV:325 nm | |||
| 167.2 | N-[4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-3,4-二氟-苯胺基)噻唑-5-羰基]苯基]胺基甲酸苯甲酯(鏡像異構物2) | 實例167 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.18 (d,J =7.35 Hz, 3 H), 5.01 (q,J =7.35 Hz, 1 H), 5.15 (s, 2 H), 5.76 (s, 1 H), 7.28 (s, 1 H), 7.40 (m, 5 H), 7.48 (m, 5 H), 7.57 (m, 1 H), 7.61 (s, 1 H), 7.78 (m, 1 H), 8.18 (m, 2 H), 10.00 (s, 1 H) 34%產率 |
| 對掌性HPLC實例167.2 在對掌性管柱上HPLC分離外消旋-N-[4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-3,4-二氟-苯胺基)噻唑-5-羰基]苯基]胺基甲酸苯甲酯(385 mg,0.7 mmol,實例167),隨後在MTBE中濕磨,得到129 mg (34%產率) N-[4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-3,4-二氟-苯胺基)噻唑-5-羰基]苯基]胺基甲酸苯甲酯,鏡像異構物2。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC-3;管柱:YMC Amylose SA 10µ,250×50;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:90% A+10% B;流速:100 mL/min;溫度:25℃;UV:280 nm 分析型對掌性 HPLC : Rt = 3.90 min 儀器:Thermo Fisher UltiMate 3000;管柱:YMC Cellulose SC 3µ,100×4.6;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:90% A+10% B;流速:1.4 mL/min;溫度:25℃;UV:325 nm | |||
| 168 | 外消旋- 2-[4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氟-苯胺基)噻唑-5-羰基]苯氧基]乙酸乙酯 | 中間物112,外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.15 (d,J =7.60 Hz, 3 H), 2.01 (s, 3 H), 4.18 (dd,J =5.32, 3.55 Hz, 2 H), 4.30 (dd,J =5.45, 3.42 Hz, 2 H), 5.06 (m, 1 H), 6.94 (m, 2 H), 7.23 (s, 1 H), 7.33 (t,J =8.74 Hz, 2 H), 7.47 (d,J =8.87 Hz, 2 H), 7.58 (s, 1 H), 7.63 (m, 2 H), 8.06 (m, 2 H) RP-HPLC (方法C鹼性) LC-MS (方法1)Rt = 1.04 min MS (ESIpos): m/z = 487.6 [M+H]+ 54%產率 |
| 169 | 外消旋-N-[4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氟-苯胺基)噻唑-5-羰基]苯基]胺基甲酸苯甲酯 | 中間物132,外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 5.05 (q,J =7.35 Hz, 1 H), 5.15 (s, 2 H), 7.25 (s, 1 H), 7.40 (m, 11 H), 7.58 (s, 1 H), 7.64 (m, 2 H), 8.12 (m, 2 H), 9.99 (m, 1 H) Biotage (方法X) LC-MS (方法1)Rt = 1.19 min MS (ESIpos): m/z = 534.4 [M+H]+ 65%產率 |
| 169.1 及 169.2 | (R)-N-[4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氟-苯胺基)噻唑-5-羰基]苯基]胺基甲酸苯甲酯及(S)-N-[4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氟-苯胺基)噻唑-5-羰基]苯基]胺基甲酸苯甲酯 | ||
| 169.1 | N-[4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氟-苯胺基)噻唑-5-羰基]苯基]胺基甲酸苯甲酯(鏡像異構物1) | 實例169 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 5.05 (q,J =7.35 Hz, 1 H), 5.15 (s, 2 H), 7.25 (s, 1 H), 7.40 (m, 11 H), 7.58 (s, 1 H), 7.64 (m, 2 H), 8.12 (m, 2 H), 9.99 (m, 1 H) LC-MS (方法1)Rt = 1.19 min MS (ESIpos): m/z = 534.4 [M+H]+ 14%產率 |
| 對掌性HPLC實例169.1 在對掌性管柱上HPLC分離外消旋-N-[4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氟-苯胺基)噻唑-5-羰基]苯基]胺基甲酸苯甲酯(422 mg,0.76 mmol,實例169),隨後在MTBE中濕磨,得到88 mg (14%產率) N-[4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氟-苯胺基)噻唑-5-羰基]苯基]胺基甲酸苯甲酯,鏡像異構物1。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC-3;管柱:YMC Amylose SA 10µ,250×50;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:50% A+50% B;流速:80 mL/min;溫度:25℃;UV:280 nm 分析型對掌性 HPLC : Rt = 1.39 min 儀器:Thermo Fisher UltiMate 3000;管柱:YMC Amylose SA 3µ,100×4.6;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:50% A+50% B;流速:1.4 mL/min;溫度:25℃;UV:280 nm | |||
| 169.2 | N-[4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氟-苯胺基)噻唑-5-羰基]苯基]胺基甲酸苯甲酯(鏡像異構物2) | 實例169 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 5.05 (q,J =7.35 Hz, 1 H), 5.15 (s, 2 H), 7.25 (s, 1 H), 7.40 (m, 11 H), 7.58 (s, 1 H), 7.64 (m, 2 H), 8.12 (m, 2 H), 9.99 (m, 1 H) LC-MS (方法1)Rt = 1.19 min MS (ESIpos): m/z = 534.4 [M+H]+ 16%產率 |
| 對掌性HPLC實例169.2 在對掌性管柱上HPLC分離外消旋-N-[4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氟-苯胺基)噻唑-5-羰基]苯基]胺基甲酸苯甲酯(422 mg,0.76 mmol,實例169),隨後在MTBE中濕磨,得到106 mg (14%產率) N-[4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氟-苯胺基)噻唑-5-羰基]苯基]胺基甲酸苯甲酯,鏡像異構物2。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC-3;管柱:YMC Amylose SA 10µ,250×50;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:50% A+50% B;流速:80 mL/min;溫度:25℃;UV:280 nm 分析型對掌性 HPLC : Rt = 1.80 min 儀器:Thermo Fisher UltiMate 3000;管柱:YMC Amylose SA 3µ,100×4.6;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:50% A+50% B;流速:1.4 mL/min;溫度:25℃;UV:280 nm | |||
| 170 | 外消旋-2-(N-[4-胺基-5-(4-苯甲氧基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物110,外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 5.05 (m, 1 H), 5.11 (s, 2 H), 7.00 (m, 2 H), 7.25 (s, 1 H), 7.37 (m, 7 H), 7.48 (m, 2 H), 7.57 (s, 1 H), 7.64 (m, 2 H), 8.11 (m, 2H) RP-HPLC (方法B鹼性) LC-MS (方法2)Rt = 1.25 min MS (ESIpos): m/z = 491.3 [M+H]+ 88%產率 |
| 170.1 及170.2 | (R)-2-(N-[4-胺基-5-(4-苯甲氧基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺及(S)-2-(N-[4-胺基-5-(4-苯甲氧基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺 | ||
| 170.1 | 2-(N-[4-胺基-5-(4-苯甲氧基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺(鏡像異構物1) | 實例170 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 5.02 - 5.06 (m, 1 H), 5.11 (s, 2 H), 7.00 (m, 2 H), 7.25 (s, 1 H), 7.30 - 7.40 (m, 7 H), 7.46 - 7.50 (m, 2 H), 7.57 (s, 1 H), 7.62 - 7.66 (m, 2 H), 8.08 - 8.12 (m, 2H) LC-MS (方法2)Rt = 1.25 min MS (ESIpos): m/z = 491.3 [M+H]+ 35%產率 |
| 對掌性HPLC實例170.1 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-(4-苯甲氧基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺(150 mg,0.3 mmol,實例170),得到53 mg (35%產率) 2-(N-[4-胺基-5-(4-苯甲氧基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺,鏡像異構物1。 製備型對掌性 HPLC 儀器:Sepiatec:Prep SFC100;管柱:Chiralpak IB 5µ 250×30mm;溶離劑A:CO2 ;溶離劑B:2-丙醇+ 0.4 vol%二乙胺;等度:35% B;流速:100 mL/min;溫度:40℃;BPR:150巴;UV:254 nm 分析型對掌性 HPLC : Rt = 3.08 min 儀器:Agilent:1260,Aurora SFC-Modul;管柱:Chiralpak IB 5µ 100×4.6mm;溶離劑A:CO2 ;溶離劑B:2-丙醇+ 0.4 vol%二乙胺;等度:35% B;流速:4 mL/min;溫度:37.5℃;BPR:100巴;UV:254 nm | |||
| 170.2 | 2-(N-[4-胺基-5-(4-苯甲氧基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺(鏡像異構物2) | 實例170 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 5.04 - 5.07 (m, 1 H), 5.11 (s, 2 H), 6.97 - 7.02 (m, 2 H), 7.25 (s, 1 H), 7.30 - 7.40 (m, 7 H), 7.46 - 7.50 (m, 2 H), 7.57 (s, 1 H), 7.62 - 7.66 (m, 2 H), 8.09 - 8.11 (m, 2H) LC-MS (方法2)Rt = 1.25 min MS (ESIpos): m/z = 491.3 [M+H]+ 34%產率 |
| 對掌性HPLC實例170.2 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-(4-苯甲氧基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺(150 mg,0.3 mmol,實例170),得到51 mg (34%產率) 2-(N-[4-胺基-5-(4-苯甲氧基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺,鏡像異構物2。 製備型對掌性 HPLC 儀器:Sepiatec:Prep SFC100;管柱:Chiralpak IB 5µ 250×30mm;溶離劑A:CO2 ;溶離劑B:2-丙醇+ 0.4 vol%二乙胺;等度:35% B;流速:100 mL/min;溫度:40℃;BPR:150巴;UV:254 nm 分析型對掌性 HPLC : Rt = 4.42 min 儀器:Agilent:1260,Aurora SFC-Modul;管柱:Chiralpak IB 5µ 100×4.6mm;溶離劑A:CO2 ;溶離劑B:2-丙醇+ 0.4 vol%二乙胺;等度:35% B;流速:4 mL/min;溫度:37.5℃;BPR:100巴;UV:254 nm | |||
| 171 | 外消旋-2-(N-[4-胺基-5-(4-碘苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物111,外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 5.07 (q,J =7.35 Hz, 1 H), 7.29 (m, 5 H), 7.58 (m, 1 H), 7.63 (m, 2 H), 7.76 (m, 2 H), 8.21 (m, 2 H) Biotage (方法X) LC-MS (方法2)Rt = 1.21 min MS (ESIpos): m/z = 511.0 [M+H]+ 39%產率 |
| 172 | 外消旋-2-(N-[4-胺基-5-(6-甲氧基吡啶-3-羰基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺 | 中間物113,外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.20 (d,J =7.35 Hz, 3 H), 3.87 (s, 3 H), 5.03 (q,J =7.35 Hz, 1 H), 6.85 (dd,J =8.62, 0.76 Hz, 1 H), 7.31 (s, 1 H), 7.52 (m, 1 H), 7.64 (s, 1 H), 7.76 (m, 2 H), 7.84 (dd,J =8.49, 2.41 Hz, 1 H), 8.14 (m, 2 H), 8.37 (m, 1 H) Biotage (方法Y) LC-MS (方法2)Rt = 1.14 min MS (ESIpos): m/z = 450.3 [M+H]+ 38%產率 |
| 172.1 及172.2 | (R)-2-(N-[4-胺基-5-(6-甲氧基吡啶-3-羰基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺及(S)-2-(N-[4-胺基-5-(6-甲氧基吡啶-3-羰基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺 | ||
| 172.1 | 2-(N-[4-胺基-5-(6-甲氧基吡啶-3-羰基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺(鏡像異構物1) | 實例172 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.20 (d,J =7.35 Hz, 3 H), 3.87 (s, 3 H), 5.03 (q,J =7.35 Hz, 1 H), 6.85 (dd,J =8.62, 0.76 Hz, 1 H), 7.31 (s, 1 H), 7.52 (m, 1 H), 7.64 (s, 1 H), 7.76 (m, 2 H), 7.84 (dd,J =8.49, 2.41 Hz, 1 H), 8.14 (m, 2 H), 8.37 (m, 1 H) LC-MS (方法2)Rt = 1.14 min MS (ESIpos): m/z = 450.3 [M+H]+ 24%產率 |
| 對掌性HPLC實例172.1 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-(6-甲氧基吡啶-3-羰基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺(312 mg,0.69 mmol,實例172),得到78 mg (24%產率) 2-(N-[4-胺基-5-(6-甲氧基吡啶-3-羰基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺,鏡像異構物1。 製備型對掌性 HPLC 儀器:Sepiatec:Prep SFC100;管柱:Chiralpak IG 5µ 250×30mm;溶離劑A:CO2 ;溶離劑B:甲醇+ 0.2 vol%氨水(32%);等度:30% B;流速:100 mL/min;溫度:40℃;BPR:150巴;UV:254 nm 分析型對掌性 HPLC : Rt = 2.61 min 儀器:Agilent:1260,Aurora SFC-模組;管柱:Chiralpak IG 5µ 100×4.6mm;溶離劑A:CO2 ;溶離劑B:甲醇+ 0.2 vol%氨水(32%);等度:30% B;流速:4 mL/min;溫度:37.5℃;BPR:100巴;UV:254 nm | |||
| 172.2 | 2-(N-[4-胺基-5-(6-甲氧基吡啶-3-羰基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺(鏡像異構物2) | 實例172 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.20 (d,J =7.35 Hz, 3 H), 3.87 (s, 3 H), 5.03 (q,J =7.35 Hz, 1 H), 6.85 (dd,J =8.62, 0.76 Hz, 1 H), 7.31 (s, 1 H), 7.52 (m, 1 H), 7.64 (s, 1 H), 7.76 (m, 2 H), 7.84 (dd,J =8.49, 2.41 Hz, 1 H), 8.14 (m, 2 H), 8.37 (m, 1 H) LC-MS (方法2)Rt = 1.14 min MS (ESIpos): m/z = 450.3 [M+H]+ 23%產率 |
| 對掌性HPLC實例172.2 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-(6-甲氧基吡啶-3-羰基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺(312 mg,0.69 mmol,實例172),得到73 mg (23%產率) 2-(N-[4-胺基-5-(6-甲氧基吡啶-3-羰基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺,鏡像異構物2。 製備型對掌性 HPLC 儀器:Sepiatec:Prep SFC100;管柱:Chiralpak IG 5µ 250×30mm;溶離劑A:CO2 ;溶離劑B:甲醇+ 0.2 vol%氨水(32%);等度:30% B;流速:100 mL/min;溫度:40℃;BPR:150巴;UV:254 nm 分析型對掌性 HPLC : Rt = 3.40 min 儀器:Agilent:1260,Aurora SFC-模組;管柱:Chiralpak IG 5µ 100×4.6mm;溶離劑A:CO2 ;溶離劑B:甲醇+ 0.2 vol%氨水(32%);等度:30% B;流速:4 mL/min;溫度:37.5℃;BPR:100巴;UV:254 nm | |||
| 173 | 外消旋-2-(N-[4-胺基-5-(4-苯氧基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物114,外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 5.07 (m, 1 H), 6.94 (m, 2 H), 7.06 (m, 2 H), 7.20 (m, 1 H), 7.25 (s, 1 H), 7.33 (dd,J =8.87 Hz, 2 H), 7.41 (m, 2 H), 7.53 (m, 2 H), 7.58 (s, 1 H), 7.64 (m, 2 H), 8.14 (m, 2 H) Biotage (方法X) LC-MS (方法2)Rt = 1.26 min MS (ESIpos): m/z = 477.2 [M+H]+ 56%產率 |
| 174 | 外消旋-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-甲氧基-苯胺基)丙醯胺 | 中間物115,外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.15 (d,J =7.35 Hz, 3 H), 3.73 (s, 3H), 5.06 (q,J =7.35 Hz, 1 H), 7.01 (d,J =9.13 Hz, 2 H), 7.16 (m, 2 H), 7.21 (s, 1 H), 7.27 (t,J =72 Hz, 1 H), 7.46 (m, 2 H), 7.54 (m, 3 H), 8.15 (m, 2 H) Biotage (方法X) LC-MS (方法2)Rt = 1.08 min MS (ESIpos): m/z = 463.2 [M+H]+ 77%產率 |
| 174.1 及174.2 | (R)-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-甲氧基-苯胺基)丙醯胺及(S)-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-甲氧基-苯胺基)丙醯胺 | ||
| 174.1 | 2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-甲氧基-苯胺基)丙醯胺(鏡像異構物1) | 實例174 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.15 (d,J =7.35 Hz, 3 H), 3.73 (s, 3H), 5.06 (q,J =7.35 Hz, 1 H), 7.01 (d,J =9.13 Hz, 2 H), 7.16 (m, 2 H), 7.21 (s, 1 H), 7.27 (t,J =72 Hz, 1 H), 7.46 (m, 2 H), 7.54 (m, 3 H), 8.15 (m, 2 H) LC-MS (方法2)Rt = 1.08 min MS (ESIpos): m/z = 463.2 [M+H]+ 31%產率 |
| 對掌性HPLC實例174.1 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-甲氧基-苯胺基)丙醯胺(316 mg,0.66 mmol,實例174),得到121 mg (31%產率) 2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-甲氧基-苯胺基)丙醯胺,鏡像異構物1。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC-3;管柱:YMC Amylose SA 10µ,250×50;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:甲醇;等度:50% A+50% B;流速:100 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 1.28 min 儀器:Thermo Fisher UltiMate 3000;管柱:YMC Amylose SA 3µ,100×4.6;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:50% A+50% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 174.2 | 2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-甲氧基-苯胺基)丙醯胺(鏡像異構物2) | 實例174 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.15 (d,J =7.35 Hz, 3 H), 3.73 (s, 3H), 5.06 (q,J =7.35 Hz, 1 H), 7.01 (d,J =9.13 Hz, 2 H), 7.16 (m, 2 H), 7.21 (s, 1 H), 7.27 (t,J =72 Hz, 1 H), 7.46 (m, 2 H), 7.54 (m, 3 H), 8.15 (m, 2 H) LC-MS (方法2)Rt = 1.08 min MS (ESIpos): m/z = 463.2 [M+H]+ 31%產率 |
| 對掌性HPLC實例174.2 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-甲氧基-苯胺基)丙醯胺(316 mg,0.66 mmol,實例174),得到121 mg (31%產率) 2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-甲氧基-苯胺基)丙醯胺,鏡像異構物2。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC-3;管柱:YMC Amylose SA 10µ,250×50;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:甲醇;等度:50% A+50% B;流速:100 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 1.62 min 儀器:Thermo Fisher UltiMate 3000;管柱:YMC Amylose SA 3µ,100×4.6;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:50% A+50% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 175 | 外消旋-2-(N-[4-胺基-5-(4-硝基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物116,外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.16 (d, J=7.35 Hz, 3 H), 5.07 (q, J=7.35 Hz, 1 H), 7.26 (br s, 1 H), 7.33 (m, 3 H), 7.59 (br s, 1 H), 7.63 (m, 3 H), 7.71 (m, 2 H), 8.23 (m, 3 H), 8.38 (m, 1 H) Biotage (方法X) LC-MS (方法2)Rt = 1.05 min MS (ESIpos): m/z = 430.1 [M+H]+ 66%產率 |
| 176 | 外消旋-2-(4-氟-N-[5-(4-甲氧基苯甲醯基)-4-甲基-噻唑-2-基]苯胺基)丙醯胺 | 中間物117,外消旋-2-溴丙醯胺 | 1 H NMR (500 MHz, DMSO-d 6 ) δ ppm = 1.16 (d,J =7.57 Hz, 3 H), 2.29 (s, 3 H), 3.80 (s, 3 H), 5.11 (q,J =7.35 Hz, 1 H), 6.99 (d,J =8.83 Hz, 2 H), 7.20 (s, 1 H), 7.36 (dd,J =8.83 Hz, 2 H), 7.58 (m, 2 H), 7.61 (s, 1 H), 7.68 (m, 2 H) LC-MS (方法2)Rt = 1.16 min MS (ESIpos): m/z = 414.5 [M+H]+ 79%產率 |
| 176.1 及176.2 | (R)-2-(4-氟-N-[5-(4-甲氧基苯甲醯基)-4-甲基-噻唑-2-基]苯胺基)丙醯胺及(S)-2-(4-氟-N-[5-(4-甲氧基苯甲醯基)-4-甲基-噻唑-2-基]苯胺基)丙醯胺 | ||
| 176.1 | 2-(4-氟-N-[5-(4-甲氧基苯甲醯基)-4-甲基-噻唑-2-基]苯胺基)丙醯胺(鏡像異構物1) | 實例176 | 1 H NMR (500 MHz, DMSO-d 6 ) δ ppm = 1.16 (d,J =7.57 Hz, 3 H), 2.29 (s, 3 H), 3.80 (s, 3 H), 5.11 (q,J =7.35 Hz, 1 H), 6.99 (d,J =8.83 Hz, 2 H), 7.20 (s, 1 H), 7.36 (dd,J =8.83 Hz, 2 H), 7.58 (m, 2 H), 7.61 (s, 1 H), 7.68 (m, 2 H) LC-MS (方法2)Rt = 1.16 min MS (ESIpos): m/z = 414.5 [M+H]+ 49%產率 |
| 對掌性HPLC實例176.1 在對掌性管柱上HPLC分離外消旋-2-(4-氟-N-[5-(4-甲氧基苯甲醯基)-4-甲基-噻唑-2-基]苯胺基)丙醯胺(80 mg,0.19 mmol,實例176),得到39 mg (49%產率) 2-(4-氟-N-[5-(4-甲氧基苯甲醯基)-4-甲基-噻唑-2-基]苯胺基)丙醯胺,鏡像異構物1。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC-4;管柱:YMC Cellulose SC 10µ,250×50;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:乙醇;等度:80% A+20% B;流速:100 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 4.20 min 儀器:Thermo Fisher UltiMate 3000;管柱:YMC Cellulose SC 3µ,100×4.6;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:乙醇;等度:80% A+20% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 176.2 | 2-(4-氟-N-[5-(4-甲氧基苯甲醯基)-4-甲基-噻唑-2-基]苯胺基)丙醯胺(鏡像異構物2) | 實例176 | 1 H NMR (500 MHz, DMSO-d 6 ) δ ppm = 1.16 (d,J =7.57 Hz, 3 H), 2.29 (s, 3 H), 3.80 (s, 3 H), 5.11 (q,J =7.35 Hz, 1 H), 6.99 (d,J =8.83 Hz, 2 H), 7.20 (s, 1 H), 7.36 (dd,J =8.83 Hz, 2 H), 7.58 (m, 2 H), 7.61 (s, 1 H), 7.68 (m, 2 H) LC-MS (方法2)Rt = 1.16 min MS (ESIpos): m/z = 414.5 [M+H]+ 49%產率 |
| 對掌性HPLC實例176.2 在對掌性管柱上HPLC分離外消旋-2-(4-氟-N-[5-(4-甲氧基苯甲醯基)-4-甲基-噻唑-2-基]苯胺基)丙醯胺(80 mg,0.19 mmol,實例176),得到31 mg (39%產率) 2-(4-氟-N-[5-(4-甲氧基苯甲醯基)-4-甲基-噻唑-2-基]苯胺基)丙醯胺,鏡像異構物2。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC-4;管柱:YMC Cellulose SC 10µ,250×50;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:乙醇;等度:80% A+20% B;流速:100 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 4.84 min 儀器:Thermo Fisher UltiMate 3000;管柱:YMC Cellulose SC 3µ,100×4.6;溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:乙醇;等度:80% A+20% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 177 | 外消旋-4-[4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氟-苯胺基)噻唑-5-羰基]苯基]環丙烷甲醯胺 | 中間物118,外消旋-2-溴丙醯胺 | 1 H NMR (500 MHz, DMSO-d 6 ) δ ppm = 0.75 - 0.80 (m, 4 H), 1.16 (d,J =7.31 Hz, 3 H), 1.77 (m, 1 H), 5.05 (m, 1 H), 7.24 (br s, 1 H), 7.32 (dd,J =8.74 Hz, 2 H), 7.45 (d,J =8.58 Hz, 2 H), 7.57 (m, 3 H), 7.64 (dd,J =8.74, 4.93 Hz, 2 H), 8.11 (m, 2 H), 10.34 (s, 1 H) RP-HPLC (方法C鹼性) LC-MS (方法1)Rt = 0.99 min MS (ESIpos): m/z = 468.5 [M+H]+ 57%產率 |
| 178 | 外消旋-2-(N-[4-胺基-5-(4-(N-𠰌啉基)苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物119,外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 3.16 (m, 4 H), 3.70 (m, 4 H), 5.06 (q,J =7.35 Hz, 1 H), 6.90 (d,J =8.87 Hz, 2 H), 7.24 (br s, 1 H), 7.34 (dd,J =8.74 Hz, 2 H), 7.43 (m,J =8.87 Hz, 2 H), 7.57 (br s, 1 H), 7.65 (m, 2 H), 7.97 (m, 2 H) LC-MS (方法2)Rt = 1.01 min MS (ESIpos): m/z = 470.3 [M+H]+ 48%產率 |
| 179 | 外消旋-2-(N-[4-胺基-5-[4-(吡唑-1-基甲基)苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物120,外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.14 (d,J =7.35 Hz, 3 H), 5.04 (q,J =7.35 Hz, 1 H), 5.32 (m, 2 H), 6.27 (dd,J =2.03 Hz, 1 H), 7.15 (d,J =8.36 Hz, 2 H), 7.23 (s, 1 H), 7.31 (m, 2 H), 7.43 (m, 2 H), 7.45 (m, 1 H), 7.60 (m, 3 H), 7.82 (dd,J =2.28, 0.76 Hz, 1 H), 8.18 (m, 2 H) RP-HPLC (方法C鹼性) LC-MS (方法1)Rt = 1.0 min MS (ESIpos): m/z = 465.6 [M+H]+ 66%產率 |
| 180 | 外消旋-2-(N-[4-胺基-5-[4-(二甲基胺基)苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物121,外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 2.92 (s, 6 H), 5.05 (q,J =7.35 Hz, 1 H), 6.65 (m, 2 H), 7.23 (s, 1 H), 7.34 (dd,J =8.87 Hz, 2 H), 7.43 (m, 2 H), 7.57 (br d,J =0.76 Hz, 1 H), 7.65 (m, 2 H), 7.96 (m, 2 H) RP-HPLC (方法D鹼性) LC-MS (方法2)Rt = 1.13 min MS (ESIpos): m/z = 428.5 [M+H]+ 63%產率 |
| 181 | 外消旋-2-(N-[4-胺基-5-(4-吡咯啶-1-基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物122,外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.16 (br d,J =7.35 Hz, 3 H), 1.93 (m, 4 H), 3.23 (m, 4 H), 5.06 (m, 1 H), 6.47 (br d,J =8.62 Hz, 2 H), 7.24 (m, 1 H), 7.34 (s, 2 H), 7.42 (br d,J =8.36 Hz, 2 H), 7.57 (br s, 1 H), 7.65 (m, 2 H), 7.97 (m, 2 H) LC-MS (方法2)Rt = 1.21 min MS (ESIpos): m/z = 454.3 [M+H]+ 82%產率 |
| 182 | 外消旋-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-苯甲氧基-苯胺基)丙醯胺 | 中間物123,外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.15 (d,J =7.35 Hz, 3 H), 5.03 - 5.06 (m, 1 H), 5.08 - 5.12 (m, 2 H), 7.09 - 7.14 (m, 4 H), 7.22 (s, 1 H), 7.28 (s, 1 H), 7.35 - 7.45 - 7.62 (m, 10 H), 8.10 - 8.15 (m, 2 H) Biotage (方法X) LC-MS (方法2)Rt = 1.29 min MS (ESIpos): m/z = 539.4 [M+H]+ 73%產率 |
| 182.1 及182.2 | (R)-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-苯甲氧基-苯胺基)丙醯胺及(S)-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-苯甲氧基-苯胺基)丙醯胺 | ||
| 182.1 | 2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-苯甲氧基-苯胺基)丙醯胺(鏡像異構物1) | 實例182 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.15 (d,J =7.35 Hz, 3 H), 5.05 (m, 1 H), 5.11 (m, 2 H), 7.13 (m, 4 H), 7.22 (s, 1 H), 7.28 (s, 1 H), 7.35 - 7.55 (m, 10 H), 8.13 (m, 2 H) LC-MS (方法2)Rt = 1.29 min MS (ESIpos): m/z = 539.4 [M+H]+ 44%產率 |
| 對掌性HPLC實例182.1 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-苯甲氧基-苯胺基)丙醯胺(813 mg,1.51 mmol,實例182),得到360 mg (44%產率) 2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-苯甲氧基-苯胺基)丙醯胺,鏡像異構物1。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC-3;管柱:YMC Cellulose SB 10µ,250×50; 溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:乙醇+ 0.1 vol%二乙胺;等度:60% A+40% B;流速:100 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 2.76 min 儀器:Waters Alliance 2695;管柱:YMC Cellulose SB 3µ,100×4.6; 溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:乙醇;等度:60% A+40% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 182.2 | 2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-苯甲氧基-苯胺基)丙醯胺(鏡像異構物2) | 實例182 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.15 (d,J =7.35 Hz, 3 H), 5.03 - 5.06 (m, 1 H), 5.09 - 5.12 (m, 2 H), 7.09 - 7.14 (m, 4 H), 7.22 (s, 1 H), 7.28 (s, 1 H), 7.35 - 7.55 (m, 10 H), 8.10 - 8.15 (m, 2 H) LC-MS (方法2)Rt = 1.29 min MS (ESIpos): m/z = 539.4 [M+H]+ 45%產率 |
| 對掌性HPLC實例182.2 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-苯甲氧基-苯胺基)丙醯胺(813 mg,1.51 mmol,實例182),得到365 mg (45%產率) 2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-苯甲氧基-苯胺基)丙醯胺,鏡像異構物2。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC-3;管柱:YMC Cellulose SB 10µ,250×50; 溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:乙醇+ 0.1 vol%二乙胺;等度:60% A+40% B;流速:100 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 3.49 min 儀器:Waters Alliance 2695;管柱:YMC Cellulose SB 3µ,100×4.6; 溶離劑A:己烷+ 0.1 vol%二乙胺;溶離劑B:乙醇;等度:60% A+40% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 183 | 外消旋-2-(N-[4-胺基-5-[3-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物124,外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.15 (d,J =7.35 Hz, 3 H), 5.03 - 5.06 (m, 1 H), 7.20 - 7.28 (m, 4 H), 7.33 (d,J =8.87 Hz, 3 H), 7.42 (d,J =8.11 Hz, 1 H), 7.59 - 7.63 (m, 3 H), 8.17 - 8.21 (m, 2 H) RP-HPLC (方法D鹼性) LC-MS (方法2)Rt = 1.13 min MS (ESIpos): m/z = 451.5 [M+H]+ 41%產率 |
| 184 | 外消旋-2-(N-[4-胺基-5-(吡啶-3-羰基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺 | 中間物125,外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.19 (d,J =7.35 Hz, 3 H), 4.97 - 5.09 (m, 1 H), 7.30 (s, 1 H), 7.40 - 7.48 (m, 1 H), 7.48 - 7.53 (m, 1 H), 7.55 - 7.61 (m, 1 H), 7.63 (s, 1 H), 7.74 - 7.81 (m, 1 H), 7.85 - 7.90 (m, 1 H), 8.07 - 8.41 (m, 2 H), 8.61 (dd,J =4.82, 1.52 Hz, 1 H), 8.69 (dd,J =2.28, 0.76 Hz, 1 H) RP-HPLC (方法D鹼性) LC-MS (方法2)Rt = 0.92 min MS (ESIpos): m/z = 404.3 [M+H]+ 54%產率 |
| 184.1 及184.2 | (R)-2-(N-[4-胺基-5-(吡啶-3-羰基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺及(S)-2-(N-[4-胺基-5-(吡啶-3-羰基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺 | ||
| 184.1 | 2-(N-[4-胺基-5-(吡啶-3-羰基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺(鏡像異構物1) | 實例184 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.19 (d,J =7.35 Hz, 3 H), 4.97 - 5.09 (m, 1 H), 7.30 (s, 1 H), 7.40 - 7.48 (m, 1 H), 7.48 - 7.53 (m, 1 H), 7.55 - 7.61 (m, 1 H), 7.63 (s, 1 H), 7.74 - 7.81 (m, 1 H), 7.85 - 7.90 (m, 1 H), 8.07 - 8.41 (m, 2 H), 8.61 (dd,J =4.82, 1.52 Hz, 1 H), 8.69 (dd,J =2.28, 0.76 Hz, 1 H) LC-MS (方法2)Rt = 0.92 min MS (ESIpos): m/z = 404.3 [M+H]+ 39%產率 |
| 對掌性HPLC實例184.1 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-(吡啶-3-羰基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺(115 mg,0.29 mmol,實例184),得到45 mg (39%產率) 2-(N-[4-胺基-5-(吡啶-3-羰基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺,鏡像異構物1。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC-4;管柱:YMC Cellulose SC 10µ,250×50;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:50% A+50% B;流速:100 mL/min;溫度:25℃;UV:280 nm 分析型對掌性 HPLC : Rt = 2.11 min 儀器:Thermo Fisher UltiMate 3000;管柱:YMC Cellulose SC 3µ,100×4.6;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:50% A+50% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 184.2 | 2-(N-[4-胺基-5-(吡啶-3-羰基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺(鏡像異構物2) | 實例184 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.19 (d,J =7.35 Hz, 3 H), 4.97 - 5.09 (m, 1 H), 7.30 (s, 1 H), 7.40 - 7.48 (m, 1 H), 7.48 - 7.53 (m, 1 H), 7.55 - 7.61 (m, 1 H), 7.63 (s, 1 H), 7.74 - 7.81 (m, 1 H), 7.85 - 7.90 (m, 1 H), 8.07 - 8.41 (m, 2 H), 8.61 (dd,J =4.82, 1.52 Hz, 1 H), 8.69 (dd,J =2.28, 0.76 Hz, 1 H) LC-MS (方法2)Rt = 0.92 min MS (ESIpos): m/z = 404.3 [M+H]+ 43%產率 |
| 對掌性HPLC實例184.2 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-(吡啶-3-羰基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺(115 mg,0.29 mmol,實例184),得到50 mg (43%產率) 2-(N-[4-胺基-5-(吡啶-3-羰基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺,鏡像異構物2。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC-4;管柱:YMC Cellulose SC 10µ,250×50;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:50% A+50% B;流速:100 mL/min;溫度:25℃;UV:280 nm 分析型對掌性 HPLC : Rt = 2.83 min 儀器:Thermo Fisher UltiMate 3000;管柱:YMC Cellulose SC 3µ,100×4.6;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:50% A+50% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | |||
| 185 | 外消旋-2-(N-[5-(4-乙醯胺基苯甲醯基)-4-胺基-噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物126,外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.15 (d,J =7.35 Hz, 3 H), 2.03 (s, 3 H), 5.05 (q,J =7.35 Hz, 1 H), 7.24 (s, 1 H), 7.32 (dd,J =8.87 Hz, 2 H), 7.44 (d,J =8.87 Hz, 2 H), 7.55 (d,J =8.62 Hz, 2 H), 7.58 (br s, 1 H), 7.61 - 7.66 (m, 2 H), 7.81 - 8.39 (m, 2 H), 10.11 (br s, 1 H) RP-HPLC (方法C鹼性) LC-MS (方法1)Rt = 0.87 min MS (ESIpos): m/z = 442.4 [M+H]+ 54%產率 |
| 186 | 外消旋-2-(N-[4-胺基-5-(2-氯吡啶-4-羰基)噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物127,外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.16 (d,J =7.60 Hz, 3 H), 5.00 - 5.13 (m, 1 H), 7.27 (s, 1 H), 7.34 (dd,J =8.87 Hz, 2 H), 7.41 (dd,J =5.07, 1.27 Hz, 1 H), 7.49 (s, 1 H), 7.59 (s, 1 H), 7.64 (dd,J =8.87, 5.07 Hz, 2 H), 8.20 - 8.42 (m, 2 H), 8.45 (d,J =5.07 Hz, 1 H) RP-HPLC (方法C鹼性) LC-MS (方法2)Rt = 1.03 min MS (ESIpos): m/z = 420.3 [M+H]+ 25%產率 |
| 187 | 外消旋-2-(N-[4-胺基-5-(2-甲基吡啶-4-羰基)噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物128,外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.15 (d,J =7.60 Hz, 3 H), 2.45 (s, 3 H), 5.06 (br s, 1 H), 7.10 - 7.23 (m, 1 H), 7.23 - 7.28 (m, 2 H), 7.33 (dd,J =8.74 Hz, 2 H), 7.59 (br s, 1 H), 7.63 (dd,J =8.87, 5.07 Hz, 2 H), 8.05 - 8.42 (m, 2 H), 8.46 (d,J =5.07 Hz, 1 H) RP-HPLC (方法C鹼性) LC-MS (方法2)Rt = 0.90 min MS (ESIpos): m/z = 400.5 [M+H]+ 66%產率 |
| 187.1 及187.2 | (R)-2-(N-[4-胺基-5-(2-甲基吡啶-4-羰基)噻唑-2-基]-4-氟-苯胺基)丙醯胺及(S)-2-(N-[4-胺基-5-(2-甲基吡啶-4-羰基)噻唑-2-基]-4-氟-苯胺基)丙醯胺 | ||
| 187.1 | 2-(N-[4-胺基-5-(2-甲基吡啶-4-羰基)噻唑-2-基]-4-氟-苯胺基)丙醯胺(鏡像異構物1) | 實例187 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.15 (d,J =7.60 Hz, 3 H), 2.45 (s, 3 H), 5.06 (br s, 1 H), 7.10 - 7.23 (m, 1 H), 7.23 - 7.28 (m, 2 H), 7.33 (dd,J =8.74 Hz, 2 H), 7.59 (br s, 1 H), 7.63 (dd,J =8.87, 5.07 Hz, 2 H), 8.05 - 8.42 (m, 2 H), 8.46 (d,J =5.07 Hz, 1 H) 32%產率 |
| 對掌性HPLC實例187.1 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-(2-甲基吡啶-4-羰基)噻唑-2-基]-4-氟-苯胺基)丙醯胺(333 mg,0.83 mmol,實例187),得到105 mg (32%產率) 2-(N-[4-胺基-5-(2-甲基吡啶-4-羰基)噻唑-2-基]-4-氟-苯胺基)丙醯胺,鏡像異構物1。 製備型對掌性 HPLC 儀器:Sepiatec:Prep SFC100;管柱:Chiralpak IG 5µ 250×30mm;溶離劑A:CO2 ;溶離劑B:乙醇+ 0.2 vol%氨水(32%);等度:15% B;流速:100 mL/min;溫度:40℃;BPR:150巴;UV:254 nm 分析型對掌性 HPLC : Rt = 2.81 min 儀器:Agilent:1260,Aurora SFC-模組;管柱:Chiralpak IG 5µ 100×4.6mm;溶離劑A:CO2 ;溶離劑B:乙醇+ 0.2 vol%氨水(32%);等度:25% B;流速:4 mL/min;溫度:37.5℃;BPR:100巴;UV:254 nm | |||
| 187.2 | 2-(N-[4-胺基-5-(2-甲基吡啶-4-羰基)噻唑-2-基]-4-氟-苯胺基)丙醯胺(鏡像異構物2) | 實例187 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.15 (d,J =7.60 Hz, 3 H), 2.45 (s, 3 H), 5.06 (br s, 1 H), 7.10 - 7.23 (m, 1 H), 7.23 - 7.28 (m, 2 H), 7.33 (dd,J =8.74 Hz, 2 H), 7.59 (br s, 1 H), 7.63 (dd,J =8.87, 5.07 Hz, 2 H), 8.05 - 8.42 (m, 2 H), 8.46 (d,J =5.07 Hz, 1 H) 23%產率 |
| 對掌性HPLC實例187.2 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-(2-甲基吡啶-4-羰基)噻唑-2-基]-4-氟-苯胺基)丙醯胺(333 mg,0.83 mmol,實例187),得到78 mg (23%產率) 2-(N-[4-胺基-5-(2-甲基吡啶-4-羰基)噻唑-2-基]-4-氟-苯胺基)丙醯胺,鏡像異構物2。 製備型對掌性 HPLC 儀器:Sepiatec:Prep SFC100;管柱:Chiralpak IG 5µ 250×30mm;溶離劑A:CO2 ;溶離劑B:乙醇+ 0.2 vol%氨水(32%);等度:15% B;流速:100 mL/min;溫度:40℃;BPR:150巴;UV:254 nm 分析型對掌性 HPLC : Rt = 3.56 min 儀器:Agilent:1260,Aurora SFC-模組;管柱:Chiralpak IG 5µ 100×4.6mm;溶離劑A:CO2 ;溶離劑B:乙醇+ 0.2 vol%氨水(32%);等度:25% B;流速:4 mL/min;溫度:37.5℃;BPR:100巴;UV:254 nm | |||
| 188 | 外消旋-2-(N-[4-胺基-5-[2-(二氟甲基)吡啶-4-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物129,外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 4.99 - 5.13 (m, 1 H), 6.97 (t,J =52 Hz, 1 H), 7.27 (s, 1 H), 7.33 (t,J =8.87 Hz, 2 H), 7.56 - 7.61 (m, 2 H), 7.64 (dd,J =8.87, 5.07 Hz, 2 H), 7.67 (s, 1 H), 8.20 - 8.57 (m, 2 H), 8.73 (d,J =4.56 Hz, 1 H) RP-HPLC (方法C鹼性) LC-MS (方法2)Rt = 1.00 min MS (ESIpos): m/z = 436.3 [M+H]+ 13%產率 |
| 189 | 外消旋-2-[(4-胺基-5-苯甲醯基-噻唑-2-基)-(4-吡啶基)胺基]丙醯胺 | 中間物130,外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.22 (d,J =7.35 Hz, 3 H), 5.05 (q,J =7.35 Hz, 1 H), 5.74 (s, 1 H), 7.32 (s, 1 H), 7.37 - 7.44 (m, 2 H), 7.48 - 7.55 (m, 2 H), 7.56 - 7.65 (m, 3 H), 8.06 - 8.42 (m, 2 H), 8.68 - 8.73 (m, 2 H) RP-HPLC (方法C鹼性) LC-MS (方法2)Rt = 0.80 min MS (ESIpos): m/z = 368.2 [M+H]+ 17%產率 |
| 190 | 外消旋-2-(N-[4-胺基-5-(2-甲氧基吡啶-4-羰基)噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 中間物131,外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.15 (d,J =7.35 Hz, 3 H), 3.83 (s, 3H), 5.00 - 5.11 (m, 1 H), 6.76 (s, 1 H), 6.99 (dd,J =5.20, 1.39 Hz, 1 H), 7.26 (s, 1 H), 7.30 - 7.37 (m, 2 H), 7.59 (s, 1 H), 7.63 (dd,J =8.87, 5.07 Hz, 2 H), 8.17 - 8.20 (m, 1 H), 8.21 - 8.48 (m, 2 H) RP-HPLC (方法C鹼性) LC-MS (方法2)Rt = 0.98 min MS (ESIpos): m/z = 416.2 [M+H]+ 29%產率 |
| 191 | 外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-3-氟-4-甲氧基-苯胺基)丙醯胺 | 中間物133;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 8.12 (br s, 2H), 7.57 (s, 1H), 7.46-7.53 (m, 3H), 7.34-7.44 (m, 4H), 7.21-7.28 (m, 2H), 4.98-5.10 (m, 1H), 3.87 (s, 3H), 1.16 (d, J = 7.4 Hz, 3H)。 LC-MS (方法2)Rt = 1.06 min MS (ESIpos): m/z = 415.3 [M+H]+ 78%產率 |
| 192 | 外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-氰基-3-氟-苯胺基)丙醯胺 | 中間物134;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1H NMR (400 MHz, DMSO-d6, 22ºC): Shift = 7.95-8.40 (m, 3H), 7.86 (dd, J = 10.4, 1.8 Hz, 1H), 7.64-7.72 (m, 2H), 7.50-7.55 (m, 2H), 7.38-7.48 (m, 3H), 7.36 (s, 1H), 5.01 (q, J = 7.4 Hz, 1H), 1.22 (d, J = 7.4 Hz, 3H) LC-MS (方法2)Rt = 1.04 min MS (ESIpos): m/z = 410.3 [M+H]+ 18%產率 |
| 193 | 外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-溴-苯胺基)丙醯胺 | 中間物135;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 8.17 (br s, 2H), 7.66-7.72 (m, 2H), 7.59 (s, 1H), 7.51-7.57 (m, 2H), 7.46-7.51 (m, 2H), 7.36-7.44 (m, 3H), 7.26 (s, 1H), 5.05 (q, J = 7.3 Hz, 1H), 1.16 (d, J = 7.6 Hz, 3H)。 LC-MS (方法2)Rt = 1.19 min MS (ESIpos): m/z = 445.3 [M+H]+ 47%產率 |
| 194 | 外消旋-2-[N-(4-胺基-5-苯甲醯基-噻唑-2-基)-3-氯-4-(二氟甲氧基)苯胺基]丙醯胺 | 中間物136;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 8.13 (br s, 2H), 7.90 (d, J = 2.5 Hz, 1H), 7.60-7.68 (m, 2H), 7.45-7.52 (m, 3H), 7.39-7.44 (m, 3H), 7.39 (t, J = 73.0 Hz, 1H), 7.29 (s, 1H), 5.02 (q, J = 7.1 Hz, 1H), 1.18 (d, J = 7.4 Hz, 3H)。 LC-MS (方法2)Rt = 1.18 min MS (ESIpos): m/z = 467.4 [M+H]+ 68%產率 |
| 195 | 外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-乙氧基-苯胺基)丙醯胺 | 中間物137;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 8.11 (br s, 2H), 7.52 (s, 1H), 7.41-7.49 (m, 4H), 7.34-7.41 (m, 3H), 7.20 (s, 1H), 6.98 (d, J = 9.1 Hz, 2H), 5.00-5.12 (m, 1H), 4.03 (q, J = 6.8 Hz, 2H), 1.32 (t, J = 7.0 Hz, 3H), 1.14 (d, J = 7.4 Hz, 3H)。 LC-MS (方法2)Rt = 1.15 min MS (ESIpos): m/z = 411.5 [M+H]+ 61%產率 |
| 196 | 外消旋-2-[(4-胺基-5-苯甲醯基-噻唑-2-基)-(1,3-苯并間二氧雜環戊烯-5-基)胺基]丙醯胺 | 中間物138;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 8.08 (br s, 2H), 7.54 (s, 1H), 7.46-7.51 (m, 2H), 7.36-7.44 (m, 3H), 7.22 (s, 1H), 7.14 (d, J = 1.8 Hz, 1H), 7.01-7.07 (m, 1H), 6.96-7.00 (m, 1H), 6.10 (s, 2H), 4.97-5.09 (m, 1H), 1.18 (d, J = 7.4 Hz, 3H)。 LC-MS (方法2)Rt = 1.03 min MS (ESIpos): m/z = 411.4 [M+H]+ 67%產率 |
| 197 | 外消旋-2-[(4-胺基-5-苯甲醯基-噻唑-2-基)-(2,2-二氟-1,3-苯并間二氧雜環戊烯-5-基)胺基]丙醯胺 | 中間物139;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 8.13 (br s, 2H), 7.71 (d, J = 2.0 Hz, 1H), 7.61 (s, 1H), 7.45-7.56 (m, 4H), 7.35-7.44 (m, 3H), 7.28 (s, 1H), 5.03 (br d, J = 6.8 Hz, 1H), 1.18 (d, J = 7.4 Hz, 3H)。 LC-MS (方法2)Rt = 1.2 min MS (ESIpos): m/z = 447.3 [M+H]+ 51%產率 |
| 198 | 外消旋-2-[N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-(二氟甲氧基)-3-氟-苯胺基]丙醯胺 | 中間物140;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 8.14 (br s, 2H), 7.69-7.76 (m, 1H), 7.62 (s, 1H), 7.46-7.52 (m, 4H), 7.36-7.46 (m, 3H), 7.34 (t, J = 73.0 Hz, 1H), 7.29 (s, 1H), 5.03 (q, J = 7.1 Hz, 1H), 1.18 (d, J = 7.4 Hz, 3H)。 LC-MS (方法2)Rt = 1.12 min MS (ESIpos): m/z = 451.3 [M+H]+ 49%產率 |
| 199 | 外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-苯甲氧基-苯胺基)丙醯胺 | 中間物141;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 8.12 (br s, 2H), 7.53 (s, 1H), 7.44-7.51 (m, 6H), 7.32-7.43 (m, 6H), 7.21 (s, 1H), 7.09 (d, J = 9.1 Hz, 2H), 4.99-5.15 (m, 3H), 1.15 (d, J = 7.4 Hz, 3H)。 LC-MS (方法2)Rt = 1.28 min MS (ESIpos): m/z = 473.4 [M+H]+ 57%產率 |
| 200 | 外消旋-2-[N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-3-氯-4-(二氟甲氧基)苯胺基]丙醯胺 | 中間物142;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 7.93-8.45 (m, 2H), 7.91 (d, J = 2.3 Hz, 1H), 7.63-7.67 (m, 1H), 7.62 (s, 1H), 7.47-7.53 (m, 3H), 7.40 (t, J = 73.0 Hz, 1H), 7.29 (s, 1H), 6.92-6.96 (m, 2H), 4.98-5.07 (m, 1H), 3.76 (s, 3H), 1.18 (d, J = 7.4 Hz, 3H)。 LC-MS (方法2)Rt = 1.17 min MS (ESIpos): m/z = 497.3 [M+H]+ 63%產率 |
| 201 | 外消旋-2-[N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-3-氯-4-(二氟甲氧基)苯胺基]丙醯胺 | 中間物143;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 7.93-8.54 (m, 2H), 7.91 (d, J = 2.5 Hz, 1H), 7.61-7.68 (m, 2H), 7.55-7.61 (m, 2H), 7.08-7.53 (m, 6H), 4.98-5.08 (m, 1H), 1.18 (d, J = 7.4 Hz, 3H)。 LC-MS (方法2)Rt = 1.21 min MS (ESIpos): m/z = 533.3 [M+H]+ 58%產率 |
| 202 | 外消旋-2-[N-[4-胺基-5-(4-氯苯甲醯基)噻唑-2-基]-3-氯-4-(二氟甲氧基)苯胺基]丙醯胺 | 中間物144;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 7.92-8.51 (m, 2H), 7.90 (d, J = 2.5 Hz, 1H), 7.60-7.68 (m, 2H), 7.50-7.55 (m, 2H), 7.45-7.50 (m, 3H), 7.39 (t, J = 73.0 Hz, 1H), 7.30 (s, 1H), 4.98-5.08 (m, 1H), 1.18 (d, J = 7.4 Hz, 3H)。 LC-MS (方法2)Rt = 1.28 min MS (ESIpos): m/z = 501.3 [M+H]+ 56%產率 |
| 203 | 外消旋-2-[N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-3-氯-4-(二氟甲氧基)苯胺基]丙醯胺 | 中間物145;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 8.61-8.66 (m, 2H), 8.06-8.54 (m, 2H), 7.90 (d, J = 2.5 Hz, 1H), 7.61-7.67 (m, 2H), 7.48 (d, J = 8.6 Hz, 1H), 7.40-7.45 (m, 2H), 7.39 (t, J = 72.7 Hz, 1H), 7.31 (s, 1H), 4.98-5.07 (m, 1H), 1.18 (d, J = 7.4 Hz, 3H)。 LC-MS (方法2)Rt = 0.98 min MS (ESIpos): m/z = 468.3 [M+H]+ 47%產率 |
| 204 | 外消旋-2-[N-[4-胺基-5-[6-(二氟甲氧基)吡啶-3-羰基]噻唑-2-基]-3-氯-4-(二氟甲氧基)苯胺基]丙醯胺 | 中間物146;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 8.41 (d, J = 1.8 Hz, 1H), 8.05-8.38 (m, 2H), 8.02 (dd, J = 8.6, 2.5 Hz, 1H), 7.91 (d, J = 2.5 Hz, 1H), 7.72 (t, J = 72.5 Hz, 1H), 7.61-7.68 (m, 2H), 7.47-7.52 (m, 1H), 7.40 (t, J = 72.8 Hz, 1H), 7.31 (s, 1H), 7.10-7.15 (m, 1H), 4.98-5.08 (m, 1H), 1.19 (d, J = 7.4 Hz, 3H)。 LC-MS (方法2)Rt = 1.21 min MS (ESIpos): m/z = 534.3 [M+H]+ 42%產率 |
| 205 | 外消旋-2-[N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-4-(二氟甲氧基)-3-氟-苯胺基]丙醯胺 | 中間物147;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 7.77-8.42 (m, 2H), 7.74 (dd, J = 11.4, 1.3 Hz, 1H), 7.62 (s, 1H), 7.47-7.53 (m, 4H), 7.35 (t, J = 73.0 Hz, 1H), 6.91-6.97 (m, 2H), 4.99-5.08 (m, 1H), 3.76 (s, 3H), 1.19 (d, J = 7.4 Hz, 3H)。 LC-MS (方法2)Rt = 1.13 min MS (ESIpos): m/z = 481.3 [M+H]+ 57%產率 |
| 206 | 外消旋-2-[N-[4-胺基-5-(4-氯苯甲醯基)噻唑-2-基]-4-(二氟甲氧基)-3-氟-苯胺基]丙醯胺 | 中間物148;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 7.80-8.55 (m, 2H), 7.73 (dd, J = 11.3, 1.4 Hz, 1H), 7.62 (s, 1H), 7.46-7.55 (m, 6H), 7.35 (t, J = 72.8 Hz, 1H), 7.30 (s, 1H), 4.99-5.08 (m, 1H), 1.19 (d, J = 7.4 Hz, 3H)。 LC-MS (方法2)Rt = 1.24 min MS (ESIpos): m/z = 485.3 [M+H]+ 53%產率 |
| 207 | 外消旋-2-[N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-(二氟甲氧基)-3-氟-苯胺基]丙醯胺 | 中間物149;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 7.78-8.47 (m, 2H), 7.73 (dd, J = 11.2, 1.3 Hz, 1H), 7.62 (s, 1H), 7.55-7.60 (m, 2H), 7.34-7.54 (m, 3H), 7.09-7.32 (m, 4H), 4.98-5.08 (m, 1H), 1.19 (d, J = 7.4 Hz, 3H)。 LC-MS (方法2)Rt = 1.18 min MS (ESIpos): m/z = 517.3 [M+H]+ 50%產率 |
| 208 | 外消旋-2-[N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-4-(二氟甲氧基)-3-氟-苯胺基]丙醯胺 | 中間物150;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 8.61-8.65 (m, 2H), 8.30 (br s, 2H), 7.73 (dd, J = 11.0, 1.4 Hz, 1H), 7.63 (s, 1H), 7.48-7.52 (m, 2H), 7.39-7.45 (m, 2H), 7.35 (t, J = 73.0 Hz, 1H), 7.31 (s, 1H), 4.98-5.08 (m, 1H), 1.19 (d, J = 7.4 Hz, 3H)。 LC-MS (方法2)Rt = 0.94 min MS (ESIpos): m/z = 452.3 [M+H]+ 48%產率 |
| 209 | 外消旋-2-[N-[4-胺基-5-[6-(二氟甲氧基)吡啶-3-羰基]噻唑-2-基]-4-(二氟甲氧基)-3-氟-苯胺基]丙醯胺 | 中間物151;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 8.41 (d, J = 2.0 Hz, 1H), 8.02 (dd, J = 8.5, 2.4 Hz, 3H), 7.74 (dd, J = 11.4, 1.3 Hz, 1H), 7.72 (t, J = 72.5 Hz, 1H), 7.63 (s, 1H), 7.49-7.53 (m, 2H), 7.36 (t, J = 73.0 Hz, 1H), 7.31 (s, 1H), 7.10-7.15 (m, 1H), 4.99-5.09 (m, 1H), 1.19 (d, J = 7.4 Hz, 3H)。 LC-MS (方法2)Rt = 1.18 min MS (ESIpos): m/z = 518.3 [M+H]+ 51%產率 |
| 210 | 外消旋-2-[N-[4-胺基-5-[6-(二氟甲氧基)吡啶-3-羰基]噻唑-2-基]-4-(二氟甲氧基)-3-氟-苯胺基]丙醯胺 | 中間物152;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 8.41 (d, J = 2.0 Hz, 1H), 8.02 (dd, J = 8.5, 2.4 Hz, 3H), 7.74 (dd, J = 11.4, 1.3 Hz, 1H), 7.72 (t, J = 72.5 Hz, 1H), 7.63 (s, 1H), 7.49-7.53 (m, 2H), 7.36 (t, J = 73.0 Hz, 1H), 7.31 (s, 1H), 7.10-7.15 (m, 1H), 4.99-5.09 (m, 1H), 1.19 (d, J = 7.4 Hz, 3H)。 LC-MS (方法2)Rt = 1.18 min MS (ESIpos): m/z = 518.3 [M+H]+ 51%產率 |
| 211 | 外消旋-2-[N-(4-胺基-5-苯甲醯基-噻唑-2-基)-3-氯-4-(三氟甲氧基)苯胺基]丙醯胺 | 中間物153;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 8.01 (dd, J = 1.9, 0.9 Hz, 3H), 7.74 (d, J = 1.8 Hz, 2H), 7.66 (s, 1H), 7.49-7.55 (m, 2H), 7.37-7.47 (m, 3H), 7.32 (s, 1H), 4.95-5.05 (m, 1H), 1.19 (d, J = 7.4 Hz, 3H)。 LC-MS (方法2)Rt = 1.29 min MS (ESIpos): m/z = 485.3 [M+H]+ 48%產率 |
| 212 | 外消旋-2-[[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-(2,2-二氟-1,3-苯并間二氧雜環戊烯-5-基)胺基]丙醯胺 | 中間物154;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 7.80-8.36 (m, 2H), 7.72 (d, J = 1.8 Hz, 1H), 7.61 (s, 1H), 7.46-7.57 (m, 4H), 7.28 (s, 1H), 6.90-6.97 (m, 2H), 5.03 (br d, J = 7.6 Hz, 1H), 3.76 (s, 3H), 1.18 (d, J = 7.4 Hz, 3H)。 LC-MS (方法2)Rt = 1.19 min MS (ESIpos): m/z = 476.3 [M+H]+ 67%產率 |
| 213 | 外消旋-2-[[4-胺基-5-(4-氯苯甲醯基)噻唑-2-基]-(2,2-二氟-1,3-苯并間二氧雜環戊烯-5-基)胺基]丙醯胺 | 中間物155;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 8.19 (br s, 2H), 7.71 (d, J = 2.0 Hz, 1H), 7.61 (s, 1H), 7.44-7.56 (m, 6H), 7.29 (s, 1H), 4.98-5.09 (m, 1H), 1.18 (d, J = 7.4 Hz, 3H)。 LC-MS (方法2)Rt = 1.31 min MS (ESIpos): m/z = 481.2 [M+H]+ 59%產率 |
| 214 | 外消旋-2-[[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-(2,2-二氟-1,3-苯并間二氧雜環戊烯-5-基)胺基]丙醯胺 | 中間物156;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 7.80-8.54 (m, 2H), 7.72 (d, J = 1.8 Hz, 1H), 7.61 (s, 1H), 7.53-7.60 (m, 3H), 7.47-7.52 (m, 1H), 7.30 (br s, 1H), 7.28 (t, J = 73.8 Hz, 1H), 7.18 (d, J = 8.6 Hz, 2H), 5.04 (br d, J = 6.3 Hz, 1H), 1.18 (d, J = 7.4 Hz, 3H)。 LC-MS (方法2)Rt = 1.23 min MS (ESIpos): m/z = 513.3 [M+H]+ 37%產率 |
| 215 | 外消旋-2-[[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-(2,2-二氟-1,3-苯并間二氧雜環戊烯-5-基)胺基]丙醯胺 | 中間物157;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 8.60-8.65 (m, 2H), 8.07-8.53 (m, 2H), 7.71 (d, J = 2.0 Hz, 1H), 7.63 (s, 1H), 7.52-7.58 (m, 1H), 7.46-7.51 (m, 1H), 7.39-7.45 (m, 2H), 7.30 (s, 1H), 4.95-5.13 (m, 1H), 1.18 (d, J = 7.4 Hz, 3H)。 LC-MS (方法2)Rt = 0.99 min MS (ESIpos): m/z = 448.3 [M+H]+ 64%產率 |
| 216 | 外消旋-2-[[4-胺基-5-[6-(二氟甲氧基)吡啶-3-羰基]噻唑-2-基]-(2,2-二氟-1,3-苯并間二氧雜環戊烯-5-基)胺基]丙醯胺 | 中間物158;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 8.41 (d, J = 2.3 Hz, 3H), 8.02 (dd, J = 8.5, 2.4 Hz, 1H), 7.72 (d, J = 2.0 Hz, 1H), 7.71 (t, J = 72.5 Hz, 1H), 7.62 (s, 1H), 7.54-7.58 (m, 1H), 7.51 (d, J = 1.8 Hz, 1H), 7.30 (s, 1H), 7.11 (d, J = 8.4 Hz, 1H), 4.96-5.12 (m, 1H), 1.19 (d, J = 7.4 Hz, 3H)。 LC-MS (方法2)Rt = 1.23 min MS (ESIpos): m/z = 514.3 [M+H]+ 59%產率 |
| 217 | 外消旋-2-[N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-3-氟-4-(三氟甲氧基)苯胺基]丙醯胺 | 中間物159;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 7.88-8.42 (m, 2H), 7.85 (dd, J = 11.2, 2.5 Hz, 1H), 7.75 (td, J = 8.7, 1.0 Hz, 1H), 7.64 (s, 1H), 7.58-7.63 (m, 1H), 7.48-7.55 (m, 2H), 7.32 (s, 1H), 6.91-6.97 (m, 2H), 5.01 (q, J = 7.4 Hz, 1H), 3.77 (s, 3H), 1.20 (d, J = 7.4 Hz, 3H)。 LC-MS (方法2)Rt = 1.23 min MS (ESIpos): m/z = 499.3 [M+H]+ 55%產率 |
| 218 | 外消旋-2-[N-[4-胺基-5-(4-氯苯甲醯基)噻唑-2-基]-3-氟-4-(三氟甲氧基)苯胺基]丙醯胺 | 中間物160;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 7.90-8.49 (m, 2H), 7.85 (dd, J = 11.2, 2.3 Hz, 1H), 7.75 (td, J = 8.7, 1.0 Hz, 1H), 7.65 (s, 1H), 7.58-7.62 (m, 1H), 7.51-7.56 (m, 2H), 7.45-7.50 (m, 2H), 7.32 (s, 1H), 4.97-5.06 (m, 1H), 1.20 (d, J = 7.4 Hz, 3H)。 LC-MS (方法2)Rt = 1.34 min MS (ESIpos): m/z = 503.3 [M+H]+ 46%產率 |
| 219 | 外消旋-2-[N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-3-氟-4-(三氟甲氧基)苯胺基]丙醯胺 | 中間物161;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 7.89-8.50 (m, 2H), 7.85 (dd, J = 11.2, 2.3 Hz, 1H), 7.70-7.80 (m, 1H), 7.65 (s, 1H), 7.57-7.63 (m, 3H), 7.32 (s, 1H), 7.29 (t, J = 73.8 Hz, 1H), 7.19 (d, J = 8.6 Hz, 2H), 5.02 (q, J = 7.4 Hz, 1H), 1.20 (d, J = 7.4 Hz, 3H)。 LC-MS (方法2)Rt = 1.26 min MS (ESIpos): m/z = 525.3 [M+H]+ 40%產率 |
| 220 | 外消旋-2-[N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-3-氟-4-(三氟甲氧基)苯胺基]丙醯胺 | 中間物162;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 8.61-8.66 (m, 2H), 8.05-8.54 (m, 2H), 7.85 (dd, J = 11.2, 2.3 Hz, 1H), 7.71-7.78 (m, 1H), 7.66 (s, 1H), 7.60 (dd, J = 8.7, 1.4 Hz, 1H), 7.41-7.46 (m, 2H), 7.33 (s, 1H), 4.97-5.06 (m, 1H), 1.20 (d, J = 7.4 Hz, 3H)。 LC-MS (方法2)Rt = 1.04 min MS (ESIpos): m/z = 470.3 [M+H]+ 40%產率 |
| 221 | 外消旋-2-[N-[4-胺基-5-[6-(二氟甲氧基)吡啶-3-羰基]噻唑-2-基]-3-氟-4-(三氟甲氧基)苯胺基]丙醯胺 | 中間物163;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 8.42 (d, J = 2.0 Hz, 1H), 8.23 (br s, 2H), 8.03 (dd, J = 8.5, 2.4 Hz, 1H), 7.86 (dd, J = 11.2, 2.3 Hz, 1H), 7.73-7.79 (m, 1H), 7.72 (t, J = 72.5 Hz, 1H), 7.66 (s, 1H), 7.58-7.64 (m, 1H), 7.34 (s, 1H), 7.13 (dd, J = 8.6, 0.8 Hz, 1H), 4.97-5.06 (m, 1H), 1.20 (d, J = 7.4 Hz, 3H)。 LC-MS (方法2)Rt = 1.29 min MS (ESIpos): m/z = 536.3 [M+H]+ 51%產率 |
| 222 | 外消旋-2-[N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-3-氯-4-(三氟甲氧基)苯胺基]丙醯胺 | 中間物164;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 7.78-8.36 (m, 2H), 7.74 (s, 2H), 7.66 (s, 1H), 7.49-7.55 (m, 2H), 7.32 (s, 1H), 6.91-6.98 (m, 2H), 5.00 (q, J = 7.0 Hz, 1H), 3.77 (s, 3H), 1.19 (d, J = 7.4 Hz, 3H)。 LC-MS (方法2)Rt = 1.29 min MS (ESIpos): m/z = 515.3 [M+H]+ 46%產率 |
| 223 | 外消旋-2-[N-[4-胺基-5-(4-氯苯甲醯基)噻唑-2-基]-3-氯-4-(三氟甲氧基)苯胺基]丙醯胺 | 中間物165;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 8.03-8.45 (m, 2H), 8.01 (t, J = 1.4 Hz, 1H), 7.74 (s, 2H), 7.66 (s, 1H), 7.51-7.57 (m, 2H), 7.45-7.50 (m, 2H), 7.33 (s, 1H), 4.96-5.05 (m, 1H), 1.19 (d, J = 7.4 Hz, 3H)。 LC-MS (方法2)Rt = 1.4 min MS (ESIpos): m/z = 519.2 [M+H]+ 40%產率 |
| 224 | 外消旋-2-[N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-3-氯-4-(三氟甲氧基)苯胺基]丙醯胺 | 中間物166;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 8.04-8.37 (m, 2H), 8.01 (t, J = 1.3 Hz, 1H), 7.74 (s, 2H), 7.66 (s, 1H), 7.57-7.62 (m, 2H), 7.33 (s, 1H), 7.29 (t, J = 73.8 Hz, 1H), 7.19 (d, J = 8.6 Hz, 2H), 5.00 (q, J = 7.0 Hz, 1H), 1.19 (d, J = 7.6 Hz, 3H)。 LC-MS (方法2)Rt = 1.32 min MS (ESIpos): m/z = 551,3 [M+H]+ 42%產率 |
| 225 | 外消旋-2-[N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-3-氯-4-(三氟甲氧基)苯胺基]丙醯胺 | 中間物167;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 8.62-8.66 (m, 2H), 8.03-8.60 (m, 2H), 8.01 (t, J = 1.4 Hz, 1H), 7.74 (s, 2H), 7.67 (s, 1H), 7.41-7.46 (m, 2H), 7.34 (s, 1H), 4.95-5.04 (m, 1H), 1.19 (d, J = 7.4 Hz, 3H)。 LC-MS (方法2)Rt = 1.09 min MS (ESIpos): m/z = 486.2 [M+H]+ 42%產率 |
| 226 | 外消旋-2-[N-[4-胺基-5-[6-(二氟甲氧基)吡啶-3-羰基]噻唑-2-基]-3-氯-4-(三氟甲氧基)苯胺基]丙醯胺 | 中間物168;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 8.42 (d, J = 1.8 Hz, 1H), 8.07-8.40 (m, 2H), 8.01-8.06 (m, 2H), 7.75 (s, 2H), 7.72 (t, J = 72.2 Hz, 1H), 7.67 (s, 1H), 7.34 (s, 1H), 7.13 (d, J = 9.1 Hz, 1H), 4.96-5.05 (m, 1H), 1.20 (d, J = 7.6 Hz, 3H)。 LC-MS (方法2)Rt = 1.33 min MS (ESIpos): m/z = 552.2 [M+H]+ 34%產率 |
| 227 | 外消旋-2-[(4-胺基-5-苯甲醯基-噻唑-2-基)-(6-甲氧基-3-吡啶基)胺基]丙醯胺 | 中間物169;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 8.32 (d, J = 2.5 Hz, 1H), 7.93 (dd, J = 8.9, 2.8 Hz, 3H), 7.61 (s, 1H), 7.47-7.52 (m, 2H), 7.35-7.44 (m, 3H), 7.26 (s, 1H), 6.93 (d, J = 8.9 Hz, 1H), 4.98-5.16 (m, 1H), 3.87 (s, 3H), 1.17 (d, J = 7.4 Hz, 3H)。 LC-MS (方法2)Rt = 1.01 min MS (ESIpos): m/z = 398.3 [M+H]+ 75%產率 |
| 228 | 外消旋-2-[(4-胺基-5-苯甲醯基-噻唑-2-基)-[6-(三氟甲氧基)-3-吡啶基]胺基]丙醯胺 | 中間物170;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 8.56 (d, J = 2.5 Hz, 1H), 8.30 (dd, J = 8.7, 2.7 Hz, 1H), 8.15 (br s, 2H), 7.68 (s, 1H), 7.52 (dd, J = 7.6, 1.5 Hz, 2H), 7.37-7.48 (m, 4H), 7.33 (s, 1H), 4.97-5.07 (m, 1H), 1.19 (d, J = 7.4 Hz, 3H)。 LC-MS (方法2)Rt = 1.16 min MS (ESIpos): m/z = 452.3 [M+H]+ 50%產率 |
| 229 | 外消旋-2-[(4-胺基-5-苯甲醯基-噻唑-2-基)-[6-(二氟甲氧基)-3-吡啶基]胺基]丙醯胺 | 中間物171;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 8.46 (d, J = 2.3 Hz, 1H), 8.18 (dd, J = 8.7, 2.7 Hz, 3H), 7.74 (t, J = 72.2 Hz, 1H), 7.66 (s, 1H), 7.47-7.53 (m, 2H), 7.36-7.46 (m, 3H), 7.31 (s, 1H), 7.23 (d, J = 8.6 Hz, 1H), 5.04 (br d, J = 5.6 Hz, 1H), 1.18 (d, J = 7.4 Hz, 3H)。 LC-MS (方法2)Rt = 1.1 min MS (ESIpos): m/z = 434.3 [M+H]+ 68%產率 |
| 230 | 外消旋-2-[(4-胺基-5-苯甲醯基-噻唑-2-基)-[6-(三氟甲基)-3-吡啶基]胺基]丙醯胺 | 中間物172;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 8.95 (s, 1H), 8.35-8.40 (m, 1H), 8.09 (br d, J = 8.4 Hz, 3H), 7.72 (s, 1H), 7.50-7.56 (m, 2H), 7.34-7.47 (m, 4H), 4.97-5.04 (m, 1H), 1.21 (br d, J = 7.1 Hz, 3H)。 LC-MS (方法2)Rt = 1.1 min MS (ESIpos): m/z = 436.3 [M+H]+ 20%產率 |
| 231 | 外消旋-2-[(4-胺基-5-苯甲醯基-噻唑-2-基)-[6-(二氟甲基)-3-吡啶基]胺基]丙醯胺 | 中間物173;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 8.86 (d, J = 2.3 Hz, 1H), 7.89-8.50 (m, 3H), 7.86 (d, J = 8.4 Hz, 1H), 7.70 (s, 1H), 7.49-7.54 (m, 2H), 7.37-7.46 (m, 3H), 7.34 (s, 1H), 7.03 (t, J = 54.7 Hz, 1H), 5.03 (q, J = 7.4 Hz, 1H), 1.19 (d, J = 7.4 Hz, 3H)。 LC-MS (方法2)Rt = 1.0 min MS (ESIpos): m/z = 418.3 [M+H]+ 39%產率 |
| 232 | 外消旋-2-[(4-胺基-5-苯甲醯基-噻唑-2-基)-(6-氯-3-吡啶基)胺基]丙醯胺 | 中間物174;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 8.61 (d, J = 2.8 Hz, 1H), 8.14 (dd, J = 8.4, 2.8 Hz, 3H), 7.69 (d, J = 8.6 Hz, 2H), 7.48-7.55 (m, 2H), 7.37-7.46 (m, 3H), 7.33 (br s, 1H), 4.96-5.07 (m, 1H), 1.19 (d, J = 7.4 Hz, 3H)。 LC-MS (方法2)Rt = 1.03 min MS (ESIpos): m/z = 402.2 [M+H]+ 49%產率 |
| 233 | 外消旋-2-[(4-胺基-5-苯甲醯基-噻唑-2-基)-(6-氟-3-吡啶基)胺基]丙醯胺 | 中間物175;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 8.46 (d, J = 2.3 Hz, 1H), 7.72-8.42 (m, 3H), 7.67 (s, 1H), 7.48-7.54 (m, 2H), 7.33-7.47 (m, 4H), 7.32 (s, 1H), 4.97-5.10 (m, 1H), 1.19 (d, J = 7.6 Hz, 3H)。 LC-MS (方法2)Rt = 0.97 min MS (ESIpos): m/z = 386.3 [M+H]+ 65%產率 |
| 234 | 外消旋-2-[(4-胺基-5-苯甲醯基-噻唑-2-基)-(6-甲基-3-吡啶基)胺基]丙醯胺 | 中間物176;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 8.58 (d, J = 2.3 Hz, 1H), 7.90 (dd, J = 8.1, 2.5 Hz, 3H), 7.62 (s, 1H), 7.46-7.52 (m, 2H), 7.35-7.44 (m, 4H), 7.27 (s, 1H), 5.01-5.12 (m, 1H), 1.16 (d, J = 7.6 Hz, 3H)。 LC-MS (方法2)Rt = 0.91 min MS (ESIpos): m/z = 382.3 [M+H]+ 69%產率 |
| 235 | 外消旋-2-[N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-氟-3-(三氟甲氧基)苯胺基]丙醯胺 | 中間物177;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 7.78-8.47 (m, 3H), 7.73 (td, J = 4.3, 2.5 Hz, 1H), 7.62-7.70 (m, 2H), 7.47-7.54 (m, 2H), 7.35-7.46 (m, 3H), 7.30 (s, 1H), 5.02 (br d, J = 6.8 Hz, 1H), 1.17 (d, J = 7.4 Hz, 3H)。 LC-MS (方法2)Rt = 1.26 min MS (ESIpos): m/z = 469.3 [M+H]+ 52%產率 |
| 236 | 外消旋-2-[N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-氯-3-(三氟甲氧基)苯胺基]丙醯胺 | 中間物178;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 7.97 (dd, J = 2.0, 1.3 Hz, 3H), 7.85 (d, J = 8.6 Hz, 1H), 7.65-7.73 (m, 2H), 7.48-7.55 (m, 2H), 7.36-7.47 (m, 3H), 7.32 (s, 1H), 5.03 (q, J = 7.4 Hz, 1H), 1.18 (d, J = 7.6 Hz, 3H)。 LC-MS (方法2)Rt = 1.33 min MS (ESIpos): m/z = 485.2 [M+H]+ 44%產率 |
| 237 | 外消旋-2-[N-(4-胺基-5-苯甲醯基-噻唑-2-基)-3-(二氟甲氧基)-4-氟-苯胺基]丙醯胺 | 中間物179;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 7.77-8.54 (m, 2H), 7.72 (d, J = 7.6 Hz, 1H), 7.62 (s, 1H), 7.48-7.58 (m, 4H), 7.36-7.44 (m, 3H), 7.27 (s, 1H), 7.26 (t, J = 72.8 Hz, 1H), 4.97-5.08 (m, 1H), 1.18 (d, J = 7.4 Hz, 3H)。 LC-MS (方法2)Rt = 1.15 min MS (ESIpos): m/z = 451.3 [M+H]+ 66%產率 |
| 238 | 外消旋-2-[N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-氯-3-(二氟甲氧基)苯胺基]丙醯胺 | 中間物180;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 7.78-8.54 (m, 2H), 7.69-7.77 (m, 2H), 7.63 (s, 1H), 7.48-7.55 (m, 3H), 7.36-7.45 (m, 3H), 7.09-7.33 (m, 2H), 5.02 (q, J = 7.4 Hz, 1H), 1.19 (d, J = 7.6 Hz, 3H)。 LC-MS (方法2)Rt = 1.22 min MS (ESIpos): m/z = 467.3 [M+H]+ 51%產率 |
| 239 | 外消旋-2-[N-(4-胺基-5-苯甲醯基-噻唑-2-基)-2-氟-4-(三氟甲氧基)苯胺基]丙醯胺 | 中間物181;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 8.03-8.39 (m, 2H), 7.93-8.03 (m, 1H), 7.61-7.72 (m, 2H), 7.52 (br d, J = 4.3 Hz, 2H), 7.42 (br d, J = 7.1 Hz, 4H), 7.34 (br s, 1H), 4.65-5.38 (m, 1H), 1.09-1.27 (m, 3H)。 LC-MS (方法2)Rt = 1.19 min MS (ESIpos): m/z = 469.2 [M+H]+ 50%產率 |
| 240 | 外消旋-2-[N-(4-胺基-5-苯甲醯基-噻唑-2-基)-2-氯-4-(三氟甲氧基)苯胺基]丙醯胺 | 中間物182;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 7.88-8.43 (m, 3H), 7.64-7.87 (m, 2H), 7.60 (br d, J = 8.4 Hz, 1H), 7.27-7.56 (m, 6H), 4.93-5.30 (m, 1H), 1.09 (d, J = 7.4 Hz, 3H)。 LC-MS (方法2)Rt = 1.24 min MS (ESIpos): m/z = 485.1 [M+H]+ 41%產率 |
| 241 | 外消旋-2-[N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-(二氟甲氧基)-2-氟-苯胺基]丙醯胺 | 中間物183;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 7.94-8.49 (m, 2H), 7.88 (br s, 1H), 7.63 (br s, 1H), 7.50 (br s, 2H), 7.39-7.45 (m, 3H), 7.38 (t, J = 73.3 Hz, 1H), 7.35 (br d, J = 2.0 Hz, 1H), 7.31 (br s, 1H), 7.18 (br d, J = 8.9 Hz, 1H), 4.82-5.40 (m, 1H), 1.15 (br d, J = 1.3 Hz, 3H)。 LC-MS (方法2)Rt = 1.09 min MS (ESIpos): m/z = 451.2 [M+H]+ 38%產率 |
| 242 | 外消旋-2-[N-(4-胺基-5-苯甲醯基-噻唑-2-基)-2-氯-4-(二氟甲氧基)苯胺基]丙醯胺 | 中間物184;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 8.01 (d, J = 8.9 Hz, 3H), 7.60-7.72 (m, 1H), 7.20-7.59 (m, 9H), 4.97-5.21 (m, 1H), 1.09 (d, J = 7.4 Hz, 3H)。 LC-MS (方法2)Rt = 1.13 min MS (ESIpos): m/z = 467.1 [M+H]+ 44%產率 |
| 243 | 外消旋-2-[N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-4-(二氟甲基)苯胺基]丙醯胺 | 中間物185;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 7.77-8.41 (m, 2H), 7.67-7.76 (m, 4H), 7.60 (s, 1H), 7.45-7.52 (m, 2H), 7.27 (s, 1H), 7.10 (t, J = 55.8 Hz, 1H), 6.90-6.95 (m, 2H), 5.08 (q, J = 7.3 Hz, 1H), 3.75 (s, 3H), 1.17 (d, J = 7.4 Hz, 3H)。 LC-MS (方法2)Rt = 1.05 min MS (ESIpos): m/z = 447.2 [M+H]+ 54%產率 |
| 244 | 外消旋-2-[N-[4-胺基-5-(4-氯苯甲醯基)噻唑-2-基]-4-(二氟甲基)苯胺基]丙醯胺 | 中間物186;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 7.81-8.54 (m, 2H), 7.67-7.75 (m, 4H), 7.60 (s, 1H), 7.48-7.53 (m, 2H), 7.43-7.48 (m, 2H), 7.28 (s, 1H), 7.09 (t, J = 55.5 Hz, 1H), 5.08 (q, J = 7.3 Hz, 1H), 1.17 (d, J = 7.4 Hz, 3H)。 LC-MS (方法2)Rt = 1.15 min MS (ESIpos): m/z = 451.1 [M+H]+ 48%產率 |
| 245 | 外消旋-2-[N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-(二氟甲基)苯胺基]丙醯胺 | 中間物187;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 7.76-8.57 (m, 2H), 7.67-7.76 (m, 4H), 7.61 (s, 1H), 7.52-7.59 (m, 2H), 7.14-7.20 (m, 2H), 6.93-7.48 (m, 3H), 5.08 (q, J = 7.5 Hz, 1H), 1.17 (d, J = 7.4 Hz, 3H)。 LC-MS (方法2)Rt = 1,09 min MS (ESIpos): m/z = 483.2 [M+H]+ 45%產率 |
| 246 | 外消旋-2-[N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-4-(二氟甲基)苯胺基]丙醯胺 | 中間物188;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 8.59-8.64 (m, 2H), 8.06-8.55 (m, 2H), 7.67-7.76 (m, 4H), 7.62 (s, 1H), 7.37-7.43 (m, 2H), 7.29 (s, 1H), 7.09 (t, J = 55.8 Hz, 1H), 5.02-5.13 (m, 1H), 1.17 (d, J = 7.4 Hz, 3H)。 LC-MS (方法2)Rt = 0.85 min MS (ESIpos): m/z = 418.2 [M+H]+ 49%產率 |
| 247 | 外消旋-2-[N-[4-胺基-5-[6-(二氟甲氧基)吡啶-3-羰基]噻唑-2-基]-4-(二氟甲基)苯胺基]丙醯胺 | 中間物189;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 8.03-8.53 (m, 3H), 8.00 (dd, J = 8.5, 2.4 Hz, 1H), 7.50-7.91 (m, 6H), 7.29 (s, 1H), 6.94-7.26 (m, 2H), 5.08 (q, J = 7.1 Hz, 1H), 1.18 (d, J = 7.6 Hz, 3H)。 LC-MS (方法2)Rt = 1.13 min MS (ESIpos): m/z = 484.5 [M+H]+ 53%產率 |
| 248 | 外消旋-2-[[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-[6-(三氟甲氧基)-3-吡啶基]胺基]丙醯胺 | 中間物190;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 8.57 (d, J = 2.5 Hz, 1H), 8.31 (dd, J = 8.6, 2.5 Hz, 1H), 7.90-8.28 (m, 2H), 7.65-7.71 (m, 1H), 7.50-7.55 (m, 2H), 7.46 (d, J = 8.6 Hz, 1H), 7.33 (s, 1H), 6.92-6.97 (m, 2H), 5.03 (q, J = 6.8 Hz, 1H), 3.77 (s, 3H), 1.20 (d, J = 7.4 Hz, 3H)。 LC-MS (方法2)Rt = 1.14 min MS (ESIpos): m/z = 482.4 [M+H]+ 47%產率 |
| 249 | 外消旋-2-[[4-胺基-5-(4-氯苯甲醯基)噻唑-2-基]-[6-(三氟甲氧基)-3-吡啶基]胺基]丙醯胺 | 中間物191;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 8.56 (d, J = 2.5 Hz, 1H), 8.30 (dd, J = 8.7, 2.7 Hz, 3H), 7.69 (s, 1H), 7.51-7.57 (m, 2H), 7.43-7.50 (m, 3H), 7.34 (s, 1H), 5.03 (br d, J = 7.1 Hz, 1H), 1.19 (d, J = 7.4 Hz, 3H)。 LC-MS (方法2)Rt = 1.24 min MS (ESIpos): m/z = 486.3 [M+H]+ 23%產率 |
| 250 | 外消旋-2-[[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-[6-(三氟甲氧基)-3-吡啶基]胺基]丙醯胺 | 中間物192;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 8.57 (d, J = 2.5 Hz, 1H), 8.30 (dd, J = 8.7, 2.7 Hz, 1H), 8.11 (br s, 2H), 7.68 (s, 1H), 7.57-7.62 (m, 2H), 7.45 (d, J = 9.1 Hz, 1H), 7.34 (s, 1H), 7.29 (t, J = 73.8 Hz, 1H), 7.19 (d, J = 8.6 Hz, 2H), 5.03 (br d, J = 6.6 Hz, 1H), 1.20 (d, J = 7.4 Hz, 3H)。 LC-MS (方法2)Rt = 1.19 min MS (ESIpos): m/z = 518.3 [M+H]+ 31%產率 |
| 251 | 外消旋-2-[[4-胺基-5-[6-(二氟甲氧基)吡啶-3-羰基]噻唑-2-基]-[6-(三氟甲氧基)-3-吡啶基]胺基]丙醯胺 | 中間物293;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 8.57 (d, J = 2.5 Hz, 1H), 8.43 (d, J = 2.3 Hz, 1H), 8.31 (dd, J = 8.7, 2.7 Hz, 3H), 8.04 (dd, J = 8.5, 2.4 Hz, 1H), 7.72 (t, J = 72.5 Hz, 1H), 7.70 (s, 1H), 7.46 (d, J = 9.1 Hz, 1H), 7.35 (s, 1H), 7.13 (d, J = 9.1 Hz, 1H), 5.03 (br d, J = 6.8 Hz, 1H), 1.20 (d, J = 7.4 Hz, 3H)。 LC-MS (方法2)Rt = 1.21 min MS (ESIpos): m/z = 519.4 [M+H]+ 26%產率 |
| 252 | 外消旋-2-[[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-[6-(二氟甲氧基)-3-吡啶基]胺基]丙醯胺 | 中間物194;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 8.47 (d, J = 2.5 Hz, 1H), 8.19 (dd, J = 8.6, 2.8 Hz, 3H), 7.75 (t, J = 72.2 Hz, 1H), 7.65 (s, 1H), 7.48-7.53 (m, 2H), 7.30 (s, 1H), 7.25 (d, J = 8.1 Hz, 1H), 6.92-6.96 (m, 2H), 5.05 (br d, J = 5.8 Hz, 1H), 3.76 (s, 3H), 1.19 (d, J = 7.4 Hz, 3H)。 LC-MS (方法2)Rt = 1.09 min MS (ESIpos): m/z = 464.3 [M+H]+ 65%產率 |
| 253 | 外消旋-2-[[4-胺基-5-(4-氯苯甲醯基)噻唑-2-基]-[6-(二氟甲氧基)-3-吡啶基]胺基]丙醯胺 | 中間物195;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 8.46 (d, J = 2.3 Hz, 1H), 8.18 (dd, J = 8.7, 2.7 Hz, 3H), 7.74 (t, J = 72.5 Hz, 1H), 7.66 (s, 1H), 7.50-7.55 (m, 2H), 7.44-7.49 (m, 2H), 7.31 (s, 1H), 7.22-7.27 (m, 1H), 5.05 (br s, 1H), 1.18 (d, J = 7.4 Hz, 3H)。 LC-MS (方法2)Rt = 1.19 min MS (ESIpos): m/z = 468.3 [M+H]+ 51%產率 |
| 254 | 外消旋-2-[[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-[6-(二氟甲氧基)-3-吡啶基]胺基]丙醯胺 | 中間物196;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 8.47 (d, J = 2.5 Hz, 1H), 8.19 (dd, J = 8.7, 2.7 Hz, 3H), 7.75 (t, J = 72.5 Hz, 1H), 7.66 (s, 1H), 7.56-7.61 (m, 2H), 7.31 (s, 1H), 7.29 (t, J = 73.8 Hz, 1H), 7.25 (d, J = 8.6 Hz, 1H), 7.18 (d, J = 8.6 Hz, 2H), 5.05 (br s, 1H), 1.19 (d, J = 7.4 Hz, 3H)。 LC-MS (方法2)Rt = 1.14 min MS (ESIpos): m/z = 500.4 [M+H]+ 44%產率 |
| 255 | 外消旋-2-[[4-胺基-5-[6-(二氟甲氧基)吡啶-3-羰基]噻唑-2-基]-[6-(二氟甲氧基)-3-吡啶基]胺基]丙醯胺 | 中間物197;外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 8.47 (d, J = 2.5 Hz, 1H), 8.41 (d, J = 2.0 Hz, 1H), 8.19 (dd, J = 8.6, 2.5 Hz, 3H), 8.03 (dd, J = 8.6, 2.5 Hz, 1H), 7.75 (t, J = 72.5 Hz, 1H), 7.72 (t, J = 72.3 Hz, 1H), 7.67 (s, 1H), 7.32 (s, 1H), 7.25 (d, J = 9.1 Hz, 1H), 7.12 (d, J = 8.6 Hz, 1H), 5.06 (br s, 1H), 1.19 (d, J = 7.4 Hz, 3H)。 LC-MS (方法2)Rt = 1.13 min MS (ESIpos): m/z = 501.5 [M+H]+ 56%產率 |
| 256 | 外消旋-N-[5-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氟-苯胺基)噻唑-5-羰基]-2-吡啶基]胺基甲酸苯甲酯 | 中間物217,外消旋-2-溴丙醯胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.17 (d,J =7.35 Hz, 3 H), 5.05 (m,J =6.34 Hz, 1 H), 5.18 (s, 2 H), 7.26 (s, 1 H), 7.29 - 7.44 (m, 7 H), 7.59 (s, 1 H), 7.64 (dd,J =8.87, 5.07 Hz, 2 H), 7.80 - 7.85 (m, 1 H), 7.85 - 7.91 (m, 1 H), 7.94 - 8.36 (m, 2 H), 8.40 (d,J =1.77 Hz, 1 H), 10.49 (s, 1 H) RP-HPLC (方法C) LC-MS (方法2)Rt = 1.16 min MS (ESIpos): m/z = 535.4 [M+H]+ 7%產率 |
將4-[4-胺基-2-(4-氟苯胺基)噻唑-5-羰基]苯甲酸乙酯(14.2 g,36.9 mmol,中間物210)懸浮於DMF (300 mL)中,且用外消旋-2-溴丙醯胺(7.9 g,52 mmol)及碳酸鉀(9 g,65 mmol)處理。在室溫攪拌反應混合物隔夜且接著用水處理。在30 min之後,用乙酸乙酯萃取反應混合物三次。經合併之有機相用鹽水洗滌,經由拒水過濾圈(MN 617 WA)過濾且蒸發至乾燥,得到15.47 g (33 mmol,89%產率)標題化合物。
LC-MS (方法2):Rt = 1.17 min; MS(ESIpos) m/z = 457.3 [M+H]+
將4-[4-胺基-2-(4-氯-3-氟-苯胺基)噻唑-5-羰基]苯甲酸乙酯(1.24 g,2.52 mmol,中間物212)懸浮於DMF (18 mL)中,且用外消旋-2-溴丙醯胺(765.5 mg,5.04 mmol)及碳酸鉀(522 mg,3.78 mmol)處理。攪拌反應混合物3 h且接著用水處理。在30 min之後,用乙酸乙酯萃取反應混合物三次。經合併之有機相用鹽水洗滌,經由拒水過濾圈(MN 617 WA)過濾且蒸發至乾燥。藉由Biotage (方法X)純化粗產物,得到1.02 g (82%產率)標題化合物。
1
H NMR (400 MHz, DMSO-d 6
) δ ppm = 1.19 (m,J
=8.0 Hz, 3 H), 1.31 (t,J
=7.1 Hz, 3 H), 4.30 (q,J
=7.10 Hz, 2 H), 5.02 (m, 1 H), 7.31 (s, 1 H), 7.51 (dt,J
=8.49, 1.20 Hz, 1 H), 7.62 (m, 3 H), 7.74 (m, 2 H), 7.97 (m, 2 H), 8.28 (m, 2 H)。
LC-MS (方法2):Rt = 1.20 min; MS(ESIpos) m/z = 491.2 [M+H]+
將外消旋-2-[4-[4-胺基-2-(4-氟苯胺基)噻唑-5-羰基]苯氧基]-2-甲基-丙酸乙酯(1.01 g,2.28 mmol,中間物214)懸浮於DMF (20 mL)中,且用外消旋-2-溴丙醯胺(519 mg,3.4 mmol)及碳酸鉀(1.57 g,11.4 mmol)處理。在室溫攪拌反應混合物隔夜且接著用水處理。在30 min之後,用乙酸乙酯萃取反應混合物三次。經合併之有機相用鹽水洗滌,經由拒水過濾圈(MN 617 WA)過濾且蒸發至乾燥。藉由Biotage (方法X)純化粗產物,得到926 mg (1.79 mmol,78%產率)標題化合物。
1
H NMR (400 MHz, DMSO-d 6
) δ ppm = 1.07 (t,J
=7.1 Hz, 3 H), 1.16 (d,J
=7.35 Hz, 3 H), 1.53 (s, 6 H), 4.13 (q,J
=7.1 Hz, 2 H), 5.06 (m, 1 H), 6.74 (m, 2 H), 7.24 (s, 1 H), 7.33 (t,J
=8.74 Hz, 2 H), 7.44 (m, 2 H), 7.57 (s, 1 H), 7.63 (m, 2 H), 8.13 (m, 2 H)。
LC-MS (方法2):Rt = 1.22 min; MS(ESIpos) m/z = 515.5 [M+H]+
將4-[(4-胺基-2-{[(2RS)-1-胺基-1-側氧基丙-2-基](4-氟苯基)胺基}-1,3-噻唑-5-基)羰基]苯甲酸(中間物211,75 mg,0.175 mmol)及環己烷胺(35 mg,0.35 mmol)溶解於1 mL DMF中,且用HATU (133 mg,0.35 mmol)、N,N-二異丙基乙基胺(68 mg,0.53 mmol)及DMAP (1 mg,9 µM)處理。在室溫攪拌反應混合物隔夜,過濾且藉由RP-HPLC (方法D)純化,得到48 mg (0.09 mmol,53%)標題化合物。
1
H NMR (400 MHz, DMSO-d 6
) δ ppm = 1.06 - 1.14 (m, 1 H), 1.16 (d,J
=7.35 Hz, 3 H), 1.20 - 1.36 (m, 4 H), 1.55 - 1.64 (m, 1 H), 1.68 - 1.76 (m, 2 H), 1.76 - 1.83 (m, 2 H), 3.66 - 3.79 (m, 1 H), 5.01 - 5.12 (m, 1 H), 7.25 (s, 1 H), 7.32 (t,J
=8.74 Hz, 2 H), 7.52 (d,J
=8.36 Hz, 2 H), 7.58 (s, 1 H), 7.64 (dd,J
=8.87, 5.07 Hz, 2 H), 7.78 (d,J
=8.36 Hz, 2 H), 7.98 - 8.12 (br s, 1H), 8.23 (d,J
=7.86 Hz, 1 H), 8.20 - 8.50 (br s, 1H)。
LC-MS (方法2):Rt = 1.15 min; MS(ESIpos) m/z = 510.4 [M+H]+
以下實例由下表10中陳述之起始材料,使用關於實例260之程序製備。
必要時,在沈澱、萃取或過濾反應混合物之後,藉由RP-HPLC (方法A至D,視極性而定)或藉由製備型急驟層析(方法X、Y或Z,視極性而定)純化粗產物。
使用所陳述管柱及溶劑條件藉由對掌性HPLC將鏡像異構物與其外消旋體分離。
表10:實例261至273
| 實例編號 | 化學結構 化學名稱 | 起始材料 | 分析/純化/產率 |
| 261 | 外消旋-4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氟-苯胺基)噻唑-5-羰基]-N-異丙基-苯甲醯胺 | 中間物211,丙-2-胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.11 - 1.19 (m, 9 H), 3.99 - 4.11 (m, 1 H), 5.00 - 5.13 (m, 1 H), 7.25 (s, 1 H), 7.32 (t,J =8.87 Hz, 2 H), 7.53 (d,J =8.62 Hz, 2 H), 7.58 (s, 1 H), 7.60 - 7.67 (m, 2 H), 7.79 (d,J =8.36 Hz, 2 H), 7.94 - 8.22 (m, 1 H), 8.24 (d,J =7.86 Hz, 1 H), 8.27 - 8.48 (m, 1 H) RP-HPLC (方法C鹼性) LC-MS (方法2)Rt = 1.00 min MS (ESIpos): m/z = 470.7 [M+H]+ 73%產率 |
| 262 | 外消旋-4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氟-苯胺基)噻唑-5-羰基]-N-苯甲基-苯甲醯胺 | 中間物211,1-苯基甲胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 4.46 (d,J =6.08 Hz, 2 H), 5.01 - 5.11 (m, 1 H), 7.21 - 7.28 (m, 2 H), 7.28 - 7.35 (m, 6 H), 7.53 - 7.57 (m, 2 H), 7.58 (s, 1 H), 7.60 - 7.66 (m, 2 H), 7.83 - 7.87 (m, 2 H), 8.09 (br s, 1 H), 8.38 (br s, 1 H), 9.07 (t,J =5.96 Hz, 1 H) RP-HPLC (方法C鹼性) LC-MS (方法2)Rt = 1.10 min MS (ESIpos): m/z = 518.4 [M+H]+ 59%產率 |
| 263 | 4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氟-苯胺基)噻唑-5-羰基]-N-[(2S)-2-羥基丙基]苯甲醯胺(立體異構物之混合物) | 中間物211, S-1-胺基丙-2-醇 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.04 (d,J =6.34 Hz, 3 H), 1.13 - 1.19 (m, 3 H), 3.17 (td,J =5.96, 1.52 Hz, 2 H), 3.70 - 3.81 (m, 1 H), 4.73 (d,J =4.82 Hz, 1 H), 5.01 - 5.13 (m, 1 H), 7.26 (s, 1 H), 7.32 (t,J =8.74 Hz, 2 H), 7.53 (d,J =8.36 Hz, 2 H), 7.58 (s, 1 H), 7.61 - 7.66 (m, 2 H), 7.81 (d,J =8.62 Hz, 2 H), 7.91 - 8.14 (m, 1 H), 8.17 - 8.38 (m, 1 H), 8.43 (t,J =5.83 Hz, 1 H) RP-HPLC (方法C鹼性) LC-MS (方法2)Rt = 0.83 min MS (ESIpos): m/z = 486.6 [M+H]+ 73%產率 |
| 264 | 外消旋-4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氟-苯胺基)噻唑-5-羰基]-N-(2-甲氧基乙基)苯甲醯胺 | 中間物211, 2-甲氧基乙胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 3.25 (s, 3 H), 3.36 - 3.46 (m, 4 H), 5.00 - 5.12 (m, 1 H), 7.26 (s, 1 H), 7.29 - 7.36 (m, 2 H), 7.54 (d,J =8.36 Hz, 2 H), 7.58 (s, 1 H), 7.63 (dd,J =8.87, 5.07 Hz, 2 H), 7.80 (d,J =8.36 Hz, 2 H), 7.90 - 8.16 (m, 1 H), 8.17 - 8.47 (m, 1 H), 8.55 (t,J =5.20 Hz, 1 H) RP-HPLC (方法C鹼性) LC-MS (方法2)Rt = 0.90 min MS (ESIpos): m/z = 486.6 [M+H]+ 68%產率 |
| 265 | 4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氟-苯胺基)噻唑-5-羰基]-N-[(2R)-2-羥基丙基]苯甲醯胺(立體異構物之混合物) | 中間物211, R-1-胺基丙-2-醇 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.04 (d,J =6.08 Hz, 3 H), 1.16 (d,J =7.60 Hz, 3 H), 3.17 (td,J =6.02, 1.65 Hz, 2 H), 3.70 - 3.80 (m, 1 H), 4.73 (d,J =4.82 Hz, 1 H), 5.01 - 5.12 (m, 1 H), 7.25 (s, 1 H), 7.32 (t,J =8.74 Hz, 2 H), 7.51 - 7.57 (m, 2 H), 7.58 (s, 1 H), 7.60 - 7.67 (m, 2 H), 7.81 (d,J =8.36 Hz, 2 H), 7.92 - 8.17 (m, 1 H), 8.18 - 8.38 (m, 1 H), 8.43 (t,J =5.70 Hz, 1 H) RP-HPLC (方法C鹼性) LC-MS (方法2)Rt = 0.83 min MS (ESIpos): m/z = 486.6 [M+H]+ 64%產率 |
| 266 | 外消旋-4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氟-苯胺基)噻唑-5-羰基]-N-環丙基-苯甲醯胺 | 中間物211, 環丙胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 0.51 - 0.58 (m, 2 H), 0.64 - 0.71 (m, 2 H), 1.16 (d,J =7.35 Hz, 3 H), 2.82 (m,J =4.06 Hz, 1 H), 5.06 (m,J =7.10 Hz, 1 H), 7.25 (s, 1 H), 7.32 (t,J =8.87 Hz, 2 H), 7.52 (d,J =8.36 Hz, 2 H), 7.58 (s, 1 H), 7.61 - 7.67 (m, 2 H), 7.73 - 7.81 (m, 2 H), 7.92 - 8.17 (m, 1 H), 8.18 - 8.40 (m, 1 H), 8.44 (d,J =4.31 Hz, 1 H) RP-HPLC (方法C鹼性) LC-MS (方法2)Rt = 0.93 min MS (ESIpos): m/z = 468.5 [M+H]+ 68%產率 |
| 267 | 外消旋-4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氟-苯胺基)噻唑-5-羰基]-N-環戊基-苯甲醯胺 | 中間物211, 環戊胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 1.47 - 1.58 (m, 4 H), 1.63 - 1.73 (m, 2 H), 1.81 - 1.93 (m, 2 H), 4.14 - 4.26 (m, 1 H), 5.01 - 5.13 (m, 1 H), 7.25 (s, 1 H), 7.32 (t,J =8.87 Hz, 2 H), 7.50 - 7.55 (m, 2 H), 7.58 (s, 1 H), 7.61 - 7.66 (m, 2 H), 7.75 - 7.82 (m, 2 H), 7.94 - 8.11 (m, 1 H), 8.12 - 8.27 (m, 1 H), 8.31 (d,J =7.35 Hz, 1 H) RP-HPLC (方法C鹼性) LC-MS (方法2)Rt = 1.08 min MS (ESIpos): m/z = 496.4 [M+H]+ 47%產率 |
| 268 | 外消旋-4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氯-3-氟-苯胺基)噻唑-5-羰基]-N-(2-苯氧基乙基)苯甲醯胺 | 中間物213, 2-苯氧基乙胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.19 (d,J =7.35 Hz, 3 H), 3.58 - 3.65 (m, 2 H), 4.09 (t,J =5.83 Hz, 2 H), 4.98 - 5.08 (m, 1 H), 6.90 - 6.97 (m, 3 H), 7.23 - 7.34 (m, 3 H), 7.48 - 7.53 (m, 1 H), 7.55 - 7.59 (m, 2 H), 7.61 - 7.66 (m, 1 H), 7.71 - 7.78 (m, 2 H), 7.81 - 7.87 (m, 2 H), 7.96 - 8.57 (m, 2 H), 8.71 - 8.77 (m, 1 H) RP-HPLC (方法D鹼性) LC-MS (方法2)Rt = 1.15 min MS (ESIpos): m/z = 582.2 [M+H]+ 16%產率 |
| 269 | 外消旋-4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氯-3-氟-苯胺基)噻唑-5-羰基]-N-[2-(三氟甲氧基)乙基]苯甲醯胺 | 中間物213, 2-(三氟甲氧基)乙胺鹽酸鹽(1:1) | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.20 (d,J =7.35 Hz, 3 H), 3.55 (q,J =5.35 Hz, 2 H), 4.18 (dd,J =5.35 Hz, 2 H), 4.99 - 5.07 (m, 1 H), 7.30 (s, 1 H), 7.51 (dt,J =8.62, 1.14 Hz, 1 H), 7.56 - 7.61 (m, 2 H), 7.63 (s, 1 H), 7.72 - 7.78 (m, 2 H), 7.79 - 7.88 (m, 2 H), 8.02 - 8.47 (m, 2 H), 8.78 (t,J =5.58 Hz, 1 H) RP-HPLC (方法D鹼性) LC-MS (方法2)Rt = 1.11 min MS (ESIpos): m/z = 574.1 [M+H]+ 32%產率 |
| 270 | 外消旋-4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氯-3-氟-苯胺基)噻唑-5-羰基]-N-[2-(二氟甲氧基)乙基]苯甲醯胺 | 中間物213, 2-(二氟甲氧基)乙胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.20 (d,J =7.35 Hz, 3 H), 3.48 (q,J =5.58 Hz, 2 H), 3.91 - 3.96 (m, 2 H), 4.98 - 5.09 (m, 1 H), 6.68 (t, J=76 Hz, 1 H), 7.30 (s, 1 H), 7.48 - 7.53 (m, 1 H), 7.56 - 7.60 (m, 2 H), 7.63 (s, 1 H), 7.70 - 7.79 (m, 2 H), 7.79 - 7.86 (m, 2 H), 7.95 - 8.51 (m, 2 H), 8.66 - 8.71 (m, 1 H) RP-HPLC (方法D鹼性) LC-MS (方法2)Rt = 1.02 min MS (ESIpos): m/z = 556.1 [M+H]+ 18%產率 |
| 271 | 外消旋-4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氯-3-氟-苯胺基)噻唑-5-羰基]-N-(2-三級丁氧基乙基)苯甲醯胺 | 中間物213, 2-三級丁氧基乙胺鹽酸鹽(1:1) | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.12 (s, 9 H), 1.20 (d,J =7.35 Hz, 3 H), 3.27 - 3.33 (m, 2 H), 3.37 - 3.43 (m, 2 H), 4.98 - 5.07 (m, 1 H), 7.30 (s, 1 H), 7.47 - 7.54 (m, 1 H), 7.54 - 7.59 (m, 2 H), 7.63 (s, 1 H), 7.71 - 7.78 (m, 2 H), 7.79 - 7.84 (m, 2 H), 7.97 - 8.45 (m, 2 H), 8.52 (t,J =5.58 Hz, 1 H) RP-HPLC (方法D鹼性) LC-MS (方法2)Rt = 1.02 min MS (ESIpos): m/z = 562.2 [M+H]+ 33%產率 |
| 272 | 外消旋-4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氯-3-氟-苯胺基)噻唑-5-羰基]-N-(2-甲氧基乙基)苯甲醯胺 | 中間物213, 2-甲氧基乙胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.20 (d,J =7.35 Hz, 3 H), 3.25 (s, 3 H), 3.37 - 3.47 (m, 4 H), 4.98 - 5.08 (m, 1 H), 7.31 (s, 1 H), 7.49 - 7.54 (m, 1 H), 7.54 - 7.59 (m, 2 H), 7.63 (s, 1 H), 7.71 - 7.78 (m, 2 H), 7.80 - 7.85 (m, 2 H), 7.97 - 8.46 (m, 2 H), 8.53 - 8.59 (m, 1 H) RP-HPLC (方法C鹼性) LC-MS (方法2)Rt = 0.95 min MS (ESIpos): m/z = 520.2 [M+H]+ 17%產率 |
| 273 | 外消旋-2-[4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氟-苯胺基)噻唑-5-羰基]苯氧基]-N-[(4-氯苯基)甲基]-2-甲基-丙醯胺 | 中間物215, 1-(4-氯苯基)甲胺 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 1.45 (s, 6 H), 4.23 (d,J =6.08 Hz, 2 H), 5.00 - 5.13 (m, 1 H), 6.77 - 6.82 (m, 2 H), 7.13 - 7.19 (m, 2 H), 7.24 (s, 1 H), 7.27 - 7.36 (m, 4 H), 7.38 - 7.45 (m, 2 H), 7.57 (s, 1 H), 7.64 (dd,J =8.87, 5.07 Hz, 2 H), 7.80 - 8.57 (m, 2 H), 8.68 (t,J =6.08 Hz, 1 H) RP-HPLC (方法C鹼性) LC-MS (方法2)Rt = 1.23 min MS (ESIpos): m/z = 610.4 [M+H]+ 77%產率 |
將[4-胺基-2-(4-氟苯胺基)-1,3-噻唑-5-基](6-溴吡啶-3-基)甲酮(2.52 g,6.4 mmol,中間物218)懸浮於DMF (100 mL)中,且用外消旋-2-溴丙醯胺(1.46 g,9.6 mmol)及碳酸鉀(4.43 g,32 mmol)處理。在室溫攪拌反應混合物隔夜且接著用水處理。在30 min之後,過濾出沈澱,用水洗滌且真空乾燥,得到2.2 g (4.4 mmol,69%產率)標題化合物。
1
H NMR (400 MHz, DMSO-d 6
) δ ppm = 1.16 (d,J
=7.35 Hz, 3 H), 5.05 (m, 1 H), 7.27 (m, 1 H), 7.34 (t,J
=8.87 Hz, 2 H), 7.65 (m, 4 H), 7.80 (dd,J
=8.24, 2.41 Hz, 1 H), 8.25 (m, 2 H), 8.48 (d,J
=2.03 Hz, 1 H)。
LC-MS (方法2):Rt = 1.08 min; MS(ESIpos) m/z = 466.1 [M+H]+
將2-(N-[4-胺基-5-(6-溴吡啶-3-羰基)噻唑-2-基]-4-氟-苯胺基)丙醯胺(50 mg,0.11 mmol,實例274)、4-(三氟甲基)哌啶(25 mg,0.16 mmol)、碘化四丁銨(4 mg,0.01 mmol)及碳酸鉀(18 mg,0.13 mmol)懸浮於DMSO中,且在50℃攪拌隔夜。過濾反應混合物且藉由RP-HPLC (方法D)純化,得到24 mg (0.04 mmol,41%)標題化合物。
1
H NMR (400 MHz, DMSO-d 6
) δ ppm = 1.17 (d,J
=7.35 Hz, 3 H), 1.30 - 1.43 (m, 2 H), 1.84 (br d,J
=11.15 Hz, 2 H), 2.56 - 2.65 (m, 1 H), 2.87 (td,J
=12.86, 2.15 Hz, 2 H), 4.42 - 4.51 (m, 2 H), 5.00 - 5.11 (m, 1 H), 6.84 (d,J
=8.87 Hz, 1 H), 7.25 (s, 1 H), 7.35 (t,J
=8.87 Hz, 2 H), 7.58 (s, 1 H), 7.61 - 7.72 (m, 3 H), 7.80 - 8.26 (m, 2 H), 8.31 (d,J
=2.28 Hz, 1 H)。
LC-MS (方法2):Rt = 1.25 min; MS(ESIpos) m/z = 537.5 [M+H]+
以下實例由下表11中陳述之起始材料,使用關於實例275之程序製備。
必要時,在沈澱、萃取或過濾反應混合物之後,藉由RP-HPLC (方法A至D,視極性而定)或藉由製備型急驟層析(方法X、Y或Z,視極性而定)純化粗產物。
使用所陳述管柱及溶劑條件藉由對掌性HPLC將鏡像異構物與其外消旋體分離。
表11:實例276至285.2
| 實例編號 | 化學結構 化學名稱 | 起始材料 | 分析/純化/產率 | |
| 276 | 外消旋-2-(N-[4-胺基-5-[6-(4-甲基-1-哌啶基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 實例274, 4-甲基哌啶 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 0.89 (d,J =6.08 Hz, 3 H), 0.97 - 1.09 (m, 2 H), 1.17 (d,J =7.35 Hz, 3 H), 1.57 - 1.68 (m, 3 H), 2.76 - 2.87 (m, 2 H), 4.32 (br d,J =13.18 Hz, 2 H), 5.01 - 5.10 (m, 1 H), 6.78 (d,J =8.87 Hz, 1 H), 7.25 (s, 1 H), 7.35 (t,J =8.87 Hz, 2 H), 7.58 (br s, 1 H), 7.62 - 7.69 (m, 3 H), 7.86 - 8.24 (m, 2 H), 8.29 (d,J =2.28 Hz, 1 H) RP-HPLC (方法D鹼性) LC-MS (方法2)Rt = 1.28 min MS (ESIpos): m/z = 438.3 [M+H]+ 56%產率 | |
| 277 | 外消旋-2-(N-[4-胺基-5-[6-[4-(氧環丁-3-基)-1-哌啶基]吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 實例274, 4-(氧環丁-3-基)哌啶 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 0.94 (br dd,J =12.29, 3.42 Hz, 2 H), 1.16 (d,J =7.35 Hz, 3 H), 1.61 (br d,J =11.15 Hz, 2 H), 1.81 - 1.94 (m, 1 H), 2.63 - 2.73 (m, 1 H), 2.79 - 2.89 (m, 2 H), 4.30 - 4.40 (m, 4 H), 4.59 (dd,J =7.86, 6.08 Hz, 2 H), 5.05 (q,J =7.10 Hz, 1 H), 6.79 (d,J =8.87 Hz, 1 H), 7.25 (s, 1 H), 7.34 (t,J =8.87 Hz, 2 H), 7.58 (s, 1 H), 7.60 - 7.70 (m, 3 H), 7.80 - 8.23 (m, 2 H), 8.29 (d,J =2.53 Hz, 1 H) RP-HPLC (方法D鹼性) LC-MS (方法2)Rt = 1.06 min MS (ESIpos): m/z = 525.5 [M+H]+ 60%產率 | |
| 278 | 外消旋-2-(N-[4-胺基-5-[6-(二甲基胺基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 實例274, N-甲基甲胺 | 1 H NMR (500 MHz, DMSO-d 6 ) δ ppm = 1.17 (d,J =7.25 Hz, 3 H), 3.03 (s, 6 H), 5.01 - 5.09 (m, 1 H), 6.61 (d,J =8.83 Hz, 1 H), 7.25 (s, 1 H), 7.35 (t,J =8.83 Hz, 2 H), 7.58 (s, 1 H), 7.63 - 7.70 (m, 3 H), 7.82 - 8.26 (m, 2 H), 8.30 (d,J =2.21 Hz, 1 H) RP-HPLC (方法D鹼性) LC-MS (方法2)Rt = 1.04 min MS (ESIpos): m/z = 429.5 [M+H]+ 51%產率 | |
| 279 | 外消旋-2-(N-[4-胺基-5-[6-(4,4-二甲基-1-哌啶基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 實例274, 4,4-二甲基哌啶鹽酸鹽(1:1) | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 0.95 (s, 6 H), 1.17 (d,J =7.35 Hz, 3 H), 1.28 - 1.34 (m, 4 H), 3.52 - 3.60 (m, 4 H), 5.00 - 5.12 (m, 1 H), 6.78 (d,J =9.13 Hz, 1 H), 7.25 (s, 1 H), 7.35 (t,J =8.87 Hz, 2 H), 7.55 - 7.61 (m, 1 H), 7.62 - 7.69 (m, 3 H), 7.80 - 8.24 (m, 2 H), 8.29 (d,J =2.53 Hz, 1 H) RP-HPLC (方法D鹼性) LC-MS (方法2)Rt = 1.37 min MS (ESIpos): m/z = 497.5 [M+H]+ 59%產率 | |
| 280 | 外消旋-2-(N-[4-胺基-5-[6-(3-氮雜雙環[3.2.1]辛-3-基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 實例274, 3-氮雜雙環[3.2.1]辛烷鹽酸鹽(1:1) | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.16 (d,J =7.35 Hz, 3 H), 1.37 - 1.46 (m, 2 H), 1.50 - 1.56 (m, 2 H), 1.56 - 1.67 (m, 2 H), 2.26 - 2.32 (m, 2 H), 2.85 (d,J =10.39 Hz, 2 H), 3.93 (br d,J =10.65 Hz, 2 H), 4.99 - 5.10 (m, 1 H), 6.67 (d,J =8.87 Hz, 1 H), 7.25 (s, 1 H), 7.34 (t,J =8.87 Hz, 2 H), 7.58 (s, 1 H), 7.61 - 7.69 (m, 3 H), 7.75 - 8.25 (m, 2 H), 8.29 (d,J =2.53 Hz, 1 H) RP-HPLC (方法D鹼性) LC-MS (方法2)Rt = 1.29 min MS (ESIpos): m/z = 495.3 [M+H]+ 60%產率 | |
| 281 | 外消旋-2-(N-[4-胺基-5-[6-(3,5-二甲基-1-哌啶基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 實例274, 3,5-二甲基哌啶 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 0.87 (d,J =6.59 Hz, 6 H), 1.17 (d,J =7.60 Hz, 3 H), 1.44 - 1.57 (m, 2 H), 1.75 (br d,J =12.42 Hz, 1 H), 2.25 - 2.34 (m, 2 H), 4.34 (br d,J =9.89 Hz, 2 H), 5.01 - 5.12 (m, 1 H), 6.80 (d,J =8.87 Hz, 1 H), 7.25 (s, 1 H), 7.35 (t,J =8.74 Hz, 2 H), 7.58 (s, 1 H), 7.62 - 7.70 (m, 3 H), 7.81 - 8.26 (m, 2 H), 8.29 (d,J =2.53 Hz, 1 H), 0.78 (q, J=12 Hz, 1 H) RP-HPLC (方法D鹼性) LC-MS (方法2)Rt = 1.37 min MS (ESIpos): m/z = 497.3 [M+H]+ 59%產率 | |
| 282 | 外消旋-2-(N-[4-胺基-5-[6-(3-氮雜雙環[3.1.0]己-3-基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 實例274, 3-氮雜雙環[3.1.0]己烷鹽酸鹽(1:1) | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 0.13 (d,J =4.31 Hz, 1 H), 0.72 (td,J =7.67, 4.69 Hz, 1 H), 1.16 (d,J =7.35 Hz, 3 H), 1.63 - 1.69 (m, 2 H), 3.34 - 3.41 (m, 2 H), 3.63 (br d,J =10.39 Hz, 2 H), 5.05 (br d,J =7.35 Hz, 1 H), 6.42 (d,J =8.62 Hz, 1 H), 7.25 (s, 1 H), 7.34 (t,J =8.74 Hz, 2 H), 7.58 (s, 1 H), 7.60 - 7.70 (m, 3 H), 7.83 - 8.22 (m, 2 H), 8.27 (d,J =2.28 Hz, 1 H) RP-HPLC (方法D鹼性) LC-MS (方法2)Rt = 1.12 min MS (ESIpos): m/z = 467.3 [M+H]+ 72%產率 | |
| 283 | 外消旋-2-(N-[4-胺基-5-[6-(1-哌啶基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 實例274,哌啶 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.17 (d,J =7.35 Hz, 3 H), 1.45 - 1.55 (m, 4 H), 1.56 - 1.64 (m, 2 H), 3.53 - 3.59 (m, 4 H), 5.00 - 5.10 (m, 1 H), 6.78 (d,J =9.12 Hz, 1 H), 7.25 (s, 1 H), 7.35 (t,J =8.74 Hz, 2 H), 7.58 (s, 1 H), 7.62 - 7.70 (m, 3 H), 7.80 - 8.23 (m, 2 H), 8.29 (d,J =2.28 Hz, 1 H) RP-HPLC (方法D鹼性) LC-MS (方法2)Rt = 1.22 min MS (ESIpos): m/z = 469.5 [M+H]+ 100%產率 | |
| 284 | 外消旋-2-(N-[4-胺基-5-[6-(4,4-二氟-1-哌啶基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 實例274,4,4-二氟哌啶鹽酸鹽(1:1) | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.17 (d,J =7.60 Hz, 3 H), 1.90 - 2.03 (m, 4 H), 3.69 - 3.76 (m, 4 H), 5.00 - 5.11 (m, 1 H), 6.93 (d,J =9.13 Hz, 1 H), 7.25 (s, 1 H), 7.35 (t,J =8.74 Hz, 2 H), 7.58 (s, 1 H), 7.62 - 7.72 (m, 3 H), 7.80 - 8.26 (m, 2 H), 8.31 - 8.34 (m, 1 H) RP-HPLC (方法D鹼性) LC-MS (方法2)Rt = 1.09 min MS (ESIpos): m/z = 466.2 [M+H]+ 26%產率 | |
| 285 | 外消旋-2-(N-[4-胺基-5-[6-(4-氰基-4-甲基-1-哌啶基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | 實例274,4-甲基哌啶-4-甲腈鹽酸鹽(1:1) | 1 H NMR (500 MHz, DMSO-d 6 ) δ ppm = 1.17 (d,J =7.25 Hz, 3 H), 1.35 (s, 3 H), 1.49 (td,J =12.77, 4.10 Hz, 2 H), 1.90 (br d,J =13.87 Hz, 2 H), 2.97 - 3.05 (m, 2 H), 4.36 (br d,J =13.87 Hz, 2 H), 5.01 - 5.10 (m, 1 H), 6.86 (d,J =8.83 Hz, 1 H), 7.25 (s, 1 H), 7.35 (t,J =8.83 Hz, 2 H), 7.58 (s, 1 H), 7.63 - 7.70 (m, 3 H), 7.78 - 8.29 (m, 2 H), 8.31 (d,J =2.21 Hz, 1 H) RP-HPLC (方法D鹼性) LC-MS (方法2)Rt = 1.04 min MS (ESIpos): m/z = 508.8 [M+H]+ 64%產率 | |
| 285.1 及285.2 | (R)-2-(N-[4-胺基-5-[6-(4-氰基-4-甲基-1-哌啶基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺及(S)-2-(N-[4-胺基-5-[6-(4-氰基-4-甲基-1-哌啶基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺 | |||
| 285.1 | 2-(N-[4-胺基-5-[6-(4-氰基-4-甲基-1-哌啶基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺(鏡像異構物1) | 實例285 | 1 H NMR (500 MHz, DMSO-d 6 ) δ ppm = 1.17 (d,J =7.25 Hz, 3 H), 1.35 (s, 3 H), 1.49 (td,J =12.77, 4.10 Hz, 2 H), 1.90 (br d,J =13.87 Hz, 2 H), 2.97 - 3.05 (m, 2 H), 4.36 (br d,J =13.87 Hz, 2 H), 5.01 - 5.10 (m, 1 H), 6.86 (d,J =8.83 Hz, 1 H), 7.25 (s, 1 H), 7.35 (t,J =8.83 Hz, 2 H), 7.58 (s, 1 H), 7.63 - 7.70 (m, 3 H), 7.78 - 8.29 (m, 2 H), 8.31 (d,J =2.21 Hz, 1 H) LC-MS (方法2)Rt = 1.04 min MS (ESIpos): m/z = 508.8 [M+H]+ 39%產率 | |
| 對掌性HPLC實例285.1 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-[6-(4-氰基-4-甲基-1-哌啶基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺(98 mg,0.19 mmol,實例285),得到38 mg (39%產率) 2-(N-[4-胺基-5-[6-(4-氰基-4-甲基-1-哌啶基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺,鏡像異構物1。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC-4;管柱:YMC Cellulose SC 10µ,250×50;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:50% A+50% B;流速:100 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 2.37 min 儀器:Thermo Fisher UltiMate 3000;管柱:YMC Cellulose SC 3µ,100×4.6;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:50% A+50% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm | ||||
| 285.2 | 2-(N-[4-胺基-5-[6-(4-氰基-4-甲基-1-哌啶基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺(鏡像異構物2) | 實例285 | 1 H NMR (500 MHz, DMSO-d 6 ) δ ppm = 1.17 (d,J =7.25 Hz, 3 H), 1.35 (s, 3 H), 1.49 (td,J =12.77, 4.10 Hz, 2 H), 1.90 (br d,J =13.87 Hz, 2 H), 2.97 - 3.05 (m, 2 H), 4.36 (br d,J =13.87 Hz, 2 H), 5.01 - 5.10 (m, 1 H), 6.86 (d,J =8.83 Hz, 1 H), 7.25 (s, 1 H), 7.35 (t,J =8.83 Hz, 2 H), 7.58 (s, 1 H), 7.63 - 7.70 (m, 3 H), 7.78 - 8.29 (m, 2 H), 8.31 (d,J =2.21 Hz, 1 H) LC-MS (方法2)Rt = 1.04 min MS (ESIpos): m/z = 508.8 [M+H]+ 42%產率 | |
| 對掌性HPLC實例285.2 在對掌性管柱上HPLC分離外消旋-2-(N-[4-胺基-5-[6-(4-氰基-4-甲基-1-哌啶基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺(98 mg,0.19 mmol,實例285),得到41 mg (42%產率) 2-(N-[4-胺基-5-[6-(4-氰基-4-甲基-1-哌啶基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺,鏡像異構物2。 製備型對掌性 HPLC 儀器:PrepCon Labomatic HPLC-4;管柱:YMC Cellulose SC 10µ,250×50;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:50% A+50% B;流速:100 mL/min;溫度:25℃;UV:254 nm 分析型對掌性 HPLC : Rt = 3.22 min 儀器:Thermo Fisher UltiMate 3000;管柱:YMC Cellulose SC 3µ,100×4.6;溶離劑A:甲基三級丁基醚+ 0.1 vol%二乙胺;溶離劑B:乙腈;等度:50% A+50% B;流速:1.4 mL/min;溫度:25℃;UV:254 nm |
將2-(N-[4-胺基-5-(4-苯甲氧基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺(鏡像異構物2,實例170.2,41 mg,0.084 mmol)溶解於乙醇(1 mL)中。在氮氣下,添加Pd/C (133 mg),且反應混合物用H2
吹掃且在常壓H2
下在室溫攪拌5 h。經由矽藻土過濾混合物,且減壓蒸發溶劑。藉由RP-HPLC (方法B)純化殘餘物,得到22 mg (0.05 mmol,61%)標題化合物。
1
H NMR (400 MHz, DMSO-d 6
) δ ppm = 1.16 (d,J
=7.35 Hz, 3 H), 4.99 - 5.10 (m, 1 H), 6.70 - 6.75 (m, 2 H), 7.24 (s, 1 H), 7.30 - 7.40 (m, 4 H), 7.57 (s, 1 H), 7.61 - 7.66 (m, 2 H), 7.84 - 8.32 (m, 2 H), 9.90 (br s, 1 H)。
LC-MS (方法2):Rt = 0.68 min; MS(ESIpos) m/z = 401.3 [M+H]+
以下實例由下表12中陳述之起始材料,使用關於實例286之程序製備。
必要時,在沈澱、萃取或過濾反應混合物之後,藉由RP-HPLC (方法A至D,視極性而定)或藉由製備型急驟層析(方法X、Y或Z,視極性而定)純化粗產物。
使用所陳述管柱及溶劑條件藉由對掌性HPLC將鏡像異構物與其外消旋體分離。
表12:實例287至291
| 實例編號 | 化學結構 化學名稱 | 起始材料 | 分析/純化/產率 |
| 287 | 2-(N-[4-胺基-5-(4-羥基苯甲醯基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺(鏡像異構物1) | 實例165.1 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.18 (d,J =7.35 Hz, 3 H), 4.96 - 5.06 (m, 1 H), 6.72 (d,J =8.62 Hz, 2 H), 7.28 (s, 1 H), 7.37 - 7.43 (m, 2 H), 7.48 - 7.54 (m, 1 H), 7.55 - 7.64 (m, 2 H), 7.72 - 7.83 (m, 1 H), 7.83 - 8.25 (m, 2 H) RP-HPLC (方法B鹼性) LC-MS (方法2)Rt = 0.68 min MS (ESIpos): m/z = 419.3 [M+H]+ 49%產率 |
| 288 | 2-(N-[4-胺基-5-(4-羥基苯甲醯基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺(鏡像異構物2) | 實例165.2 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.18 (d,J =7.35 Hz, 3 H), 4.96 - 5.06 (m, 1 H), 6.72 (d,J =8.62 Hz, 2 H), 7.28 (s, 1 H), 7.37 - 7.43 (m, 2 H), 7.48 - 7.54 (m, 1 H), 7.55 - 7.64 (m, 2 H), 7.72 - 7.83 (m, 1 H), 7.83 - 8.25 (m, 2 H) RP-HPLC (方法B鹼性) LC-MS (方法2)Rt = 0.68 min MS (ESIpos): m/z = 419.3 [M+H]+ 43%產率 |
| 289 | 2-(N-[4-胺基-5-(4-羥基苯甲醯基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺(鏡像異構物1) | 實例166.1 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.19 (d,J =7.35 Hz, 3 H), 4.97 - 5.06 (m, 1 H), 6.72 - 6.78 (m, 2 H), 7.29 (s, 1 H), 7.38 - 7.46 (m, 2 H), 7.51 (dt,J =8.49, 1.20 Hz, 1 H), 7.62 (s, 1 H), 7.71 - 7.79 (m, 2 H), 7.83 - 8.26 (m, 2 H), 9.93 (s, 1 H) Biotage (方法X) LC-MS (方法2)Rt = 0.76 min MS (ESIpos): m/z = 435.2 [M+H]+ 21%產率 |
| 290 | 2-(N-[4-胺基-5-(4-羥基苯甲醯基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺(鏡像異構物2) | 實例166.2 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.19 (d,J =7.35 Hz, 3 H), 4.97 - 5.06 (m, 1 H), 6.72 - 6.78 (m, 2 H), 7.29 (s, 1 H), 7.38 - 7.46 (m, 2 H), 7.51 (dt,J =8.49, 1.20 Hz, 1 H), 7.62 (s, 1 H), 7.71 - 7.79 (m, 2 H), 7.83 - 8.26 (m, 2 H), 9.93 (s, 1 H) Biotage (方法X) LC-MS (方法2)Rt = 0.76 min MS (ESIpos): m/z = 435.2 [M+H]+ 27%產率 |
| 291 | 2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-羥基-苯胺基)丙醯胺(單一鏡像異構物) | 實例182.2 | 1 H NMR (400 MHz, DMSO-d 6 ) δ ppm = 1.14 (d,J =7.35 Hz, 3 H), 4.96 - 5.13 (m, 1 H), 6.80 (d,J =8.87 Hz, 2 H), 7.14 - 7.21 (m, 3 H), 7.27 (t, J=72 Hz, 1H), 7.32 (d,J =8.62 Hz, 2 H), 7.49 (s, 1 H), 7.52 - 7.58 (m, 2 H), 7.78 - 8.55 (m, 2 H), 9.85 (s, 1 H) RP-HPLC (方法B鹼性) LC-MS (方法2)Rt = 0.68 min MS (ESIpos): m/z = 449.3 [M+H]+ 47%產率 |
將[4-胺基-2-(4-氟苯胺基)噻唑-5-基]-[4-(2-羥基乙氧基)苯基]甲酮(中間物209,74 mg,0.2 mmol)懸浮於DMF (4 mL)中,且用外消旋-2-溴丙醯胺(30 mg,0.2 mmol)及碳酸鉀(137 mg,0.2 mmol)處理。在室溫攪拌反應混合物4天。藉由RP-HPLC (方法C,鹼性)純化濾液,得到47 mg (53%產率)標題化合物。
1
H NMR (400 MHz, DMSO-d 6
) δ ppm = 1.15 (d,J
=7.35 Hz, 3 H) 3.64 - 3.71 (m, 2 H) 3.98 (t,J
=4.94 Hz, 2 H) 4.87 - 4.93 (m, 1 H) 5.00 - 5.11 (m, 1 H) 6.88 - 6.95 (m, 2 H) 7.23 (s, 1 H) 7.30 - 7.36 (m, 2 H) 7.44 - 7.49 (m, 2 H) 7.56 - 7.60 (m, 1 H) 7.61 - 7.66 (m, 2 H) 7.74 - 8.34 (m, 2 H) 9.02 - 9.07 (m, 1 H)。
LC-MS (方法1):Rt = 0.84 min; MS(ESIpos) m/z = 445.6 [M+H]+
。
實驗章節——藉助於X射線分析判定絕對立體化學
實例49.2之絕對組態之判定 (R)-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺
實例49.2之晶體學資料以及描繪熱橢球及對結構編號之圖顯示於表13及圖6中。藉由緩慢蒸發乙醇溶液獲得實例49.2之無色晶體。使用保護性油將單晶體固定於冷凍環上。在使用Cu X射線輻射(CuKα, = 1.54178 Å)之具有κ測角計及HyPix-6000HE雜交光子偵測器之Rigaku XtaLAB Synergy S系統上,在100 K收集單晶X射線繞射資料。使用CrysAlisPRO程式整合資料。SHELXM用於結構溶液,且SHELXL用於基於F2之全矩陣最小平方細分。在不對稱單元中,存在兩個實例49.2分子及兩個水分子。經由環系統之180°旋轉,兩個分子中之二-氟化苯基環變為無序的。替代位置之佔有率分別細分為0.25/0.75 (分子A中)及0.35/0.65 (分子B)。異向性地細分所有非氫原子。在所計算位置中添加所有氫原子,且細分其駐留原子上之騎乘(riding)。49.2中與氮原子連接以及在水分子處之氫位於差異性傅里葉圖譜(Fourier map)中且手動地置放。氫原子之等向性溫度因子分別細分為對應重原子之溫度因子之大小的1.2及1.5倍。絕對立體化學(R-組態)可用0.008(7)之Flack參數明確地指定。針對分子表示,使用XP程式。
表13:實例49.2之晶體資料及結構細分 識別碼 實例49.2
經驗式 C40 H36 F8 N8 O8 S2
式量 972.89
溫度 100(2) K
波長 1.54184 Å
晶體系統 三斜晶系
空間群 P1
單位晶胞尺寸 a = 7.59740(10) Å a= 78.1410(10)°。
b = 9.28630(10) Å b= 89.0340(10)°。
c = 15.1835(2) Å g = 83.8330(10)°。
體積 1042.28(2) Å3
Z 1
密度(計算值) 1.550 Mg/m3
吸光係數 2.049 mm-1
F(000) 500
晶體大小 0.050 × 0.040 × 0.160 mm3
資料收集之θ範圍 2.974至68.246°。
指標(Index)範圍 -9<=h<=9,-11<=k<=11,-18<=l<=18
反射收集 74868
獨立反射 7441 [R(int) = 0.0428]
對於θ = 67.684°之完整性 99.9%
細分方法 基於F2
之全矩陣最小平方
資料/限制/參數 7441 / 153 / 651
基於F2
之適合度 1.044
最終R指標[I>2sigma(I)] R1 = 0.0425,wR2 = 0.1062
R指標(所有資料) R1 = 0.0437,wR2 = 0.1072
絕對結構參數 0.008(7)
消光係數 n/a
最大差異峰及谷 0.879及-0.502 e.Å-3
實例59.1之絕對組態之判定 (R)-2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺
實例59.1之晶體學資料以及描繪熱橢球及對結構編號之圖顯示於表14及圖7中。藉由自甲苯溶液中緩慢蒸發獲得實例59.1之無色晶體。使用保護性油將單晶體固定於冷凍環上。在使用Cu X射線輻射(CuKα, = 1.54178 Å)之具有κ測角計及HyPix-6000HE雜交光子偵測器之Rigaku XtaLAB Synergy S系統上,在100 K收集單晶X射線繞射資料。使用CrysAlisPRO程式整合資料。SHELXM用於結構溶液,且SHELXL用於基於F2之全矩陣最小平方細分。在不對稱單元中,存在四個實例59.1分子及一個無序甲苯分子。經由環系統之180°旋轉,四個分子中之三者中之氟化苯基環系統變為無序的。替代位置之佔有率分別細分為0.30/0.70 (分子B中)、0.20/0.80 (分子C中)及0.15/0.85 (分子D中)。甲苯溶劑分子在假2倍軸上為無序的,且兩個替代位置之佔有率用0.45/0.55之比率細分。異向性地細分所有非氫原子。在所計算位置中添加氫原子,且細分其駐留原子上之騎乘。與胺及醯胺氮原子連接之氫位於差異性傅里葉圖譜中且手動地置放或使用騎乘模型細分。氫原子之等向性溫度因子分別細分為對應重原子之溫度因子之大小的1.2及1.5倍。絕對立體化學(R-組態)可用0.015(11)之Flack參數明確地指定。針對分子表示,使用XP程式。
表14:實例59.1之晶體資料及結構細分 識別碼 59.1
經驗式 C20 H18 N4 O3 F Cl S + 0.25 (C7 H8)
式量 448.9 + 23.0
溫度 100(2) K
波長 1.54178 Å
晶體系統 三斜晶系
空間群 P1
單位晶胞尺寸 a = 8.9781(2) Å a= 103.099(2)°。
b = 13.3867(3) Å b= 92.827(2)°。
c = 18.9350(3) Å g = 101.417(2)°。
體積 2162.07(8) Å3
Z 4
密度(計算值) 1.450 Mg/m3
吸光係數 2.827 mm-1
F(000) 978
晶體大小 0.070 × 0.060 × 0.005 mm3
資料收集之θ範圍 2.407至68.401°。
指標範圍 -10<=h<=10,-16<=k<=16,-22<=l<=22
反射收集 76934
獨立反射 15381 [R(int) = 0.0650]
對於θ = 67.679°之完整性 100.0%
細分方法 基於F2
之全矩陣最小平方
資料/限制/參數 15381 / 1400 / 1272
基於F2
之適合度 1.003
最終R指標[I>2sigma(I)] R1 = 0.0496,wR2 = 0.1120
R指標(所有資料) R1 = 0.0605,wR2 = 0.1185
絕對結構參數 0.015(11)
消光係數 n/a
最大差異峰及谷 0.462及-0.430 e.Å-3
實例61.2之絕對組態之判定 (R)-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-氟-苯胺基)丙醯胺
實例61.2之晶體學資料以及描繪熱橢球及對結構編號之圖顯示於表15及圖8中。藉由自乙腈溶液緩慢蒸發獲得實例61.2之無色晶體。使用保護性油將單晶體固定於冷凍環上。在使用Cu X射線輻射(CuKα, = 1.54178 Å)之具有κ測角計及HyPix-6000HE雜交光子偵測器之Rigaku XtaLAB Synergy S系統上,在100 K收集單晶X射線繞射資料。使用CrysAlisPRO程式整合資料。SHELXM用於結構溶液,且SHELXL用於基於F2之全矩陣最小平方細分。在不對稱單元中,存在八個實例61.2分子及兩個水分子。異向性地細分所有非氫原子。在所計算位置中添加所有氫原子,且細分其駐留原子上之騎乘。與胺及醯胺氮原子連接之氫位於差異性傅里葉圖譜中且手動地置放或使用騎乘模型細分。氫原子之等向性溫度因子分別細分為對應重原子之溫度因子之大小的1.2及1.5倍。絕對立體化學(R-組態)可用0.027(11)之Flack參數明確地指定。針對分子表示,使用XP程式。
表15:實例61.2之晶體資料及結構細分 識別碼 實例61.2
經驗式 C19 H20 F N4 O2 S + 0.1875 H2 O
式量 390.45
溫度 100(2) K
波長 1.54178 Å
晶體系統 四方晶系
空間群 P4(1)
單位晶胞尺寸 a = 17.135 Å a= 90°。
b = 17.135 Å b= 90°。
c = 49.3911(2) Å g = 90°。
體積 14502.48(6) Å3
Z 32
密度(計算值) 1.431 Mg/m3
吸光係數 1.886 mm-1
F(000) 6544
晶體大小 0.3 × 0.2 × 0.1 mm3
資料收集之θ範圍 2.58至77.25°。
指標範圍 -14<=h<=15,0<=k<=21,-59<=l<=61
反射收集 178451
獨立反射 26790 [R(int) = 0.0513]
對於θ= 77.25°之完整性 91.2%
細分方法 基於F2
之全矩陣最小平方
資料/限制/參數 26790 / 1889 / 2043
基於F2
之適合度 1.315
最終R指標[I>2sigma(I)] R1 = 0.0508,wR2 = 0.1276
R指標(所有資料) R1 = 0.0538,wR2 = 0.1292
絕對結構參數 0.027(11)
最大差異峰及谷 0.475及-0.425 e.Å-3
實例62.2之絕對組態之判定 (R)-2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺
實例62.2之晶體學資料以及描繪熱橢球及對結構編號之圖顯示於表16及圖9中。純化樣品中已經存在實例62.2之無色晶體。使用保護性油將單晶體固定於冷凍環上。在使用Cu X射線輻射(CuKα, = 1.54178 Å)之具有κ測角計及HyPix-6000HE雜交光子偵測器之Rigaku XtaLAB Synergy S系統上,在100 K收集單晶X射線繞射資料。使用CrysAlisPRO程式整合資料。SHELXM用於結構溶液,且SHELXL用於基於F2之全矩陣最小平方細分。在不對稱單元中,存在兩個實例62.2分子。異向性地細分所有非氫原子。在所計算位置中添加所有氫原子,且細分其駐留原子上之騎乘。與氮原子連接之氫位於差異性傅里葉圖譜中且手動地置放。氫原子之等向性溫度因子分別細分為對應重原子之溫度因子之大小的1.2及1.5倍。絕對立體化學(R-組態)可用0.004(3)之Flack參數明確地指定。針對分子表示,使用XP程式。
表16:實例62.2之晶體資料及結構細分 識別碼 實例62.2
經驗式 C40 H38 F2 N8 O6 S2
式量 828.90
溫度 100(2) K
波長 1.54184 Å
晶體系統 單斜晶系
空間群 I2
單位晶胞尺寸 a = 14.128 Å a= 90°。
b = 13.01730(10) Å b= 92.60°。
c = 21.74910(10) Å g = 90°。
體積 3995.63(4) Å3
Z 4
密度(計算值) 1.378 Mg/m3
吸光係數 1.778 mm-1
F(000) 1728
晶體大小 0.100 × 0.070 × 0.020 mm3
資料收集之θ範圍 3.656至77.353°。
指標範圍 -17<=h<=17,-16<=k<=15,-27<=l<=27
反射收集 75900
獨立反射 8071 [R(int) = 0.0302]
對於θ = 67.684°之完整性 100.0%
細分方法 基於F2
之全矩陣最小平方
資料/限制/參數 8071 / 1 / 551
基於F2
之適合度 1.065
最終R指標[I>2sigma(I)] R1 = 0.0226,wR2 = 0.0591
R指標(所有資料) R1 = 0.0227,wR2 = 0.0592
絕對結構參數 -0.004(3)
消光係數 n/a
最大差異峰及谷 0.151及-0.239 e.Å-3
實驗章節——生物測定及生物學資料 下表17列出本段及分析章節中所用之縮寫,只要其在本文正文內未加解釋。其他縮寫具有熟習此項技術者本身慣用之含義。
表17:縮寫 nL 奈升
µL 微升
mL 毫升
nM 奈莫耳
µM 微莫耳
mM 毫莫耳
min 分鐘
s 秒
kDa 千道爾頓
MW 分子量
cAMP 環單磷酸腺苷
ADP 二磷酸腺苷
ATP 三磷酸腺苷
FCS 胎牛血清(fetal calf serum)
FBS 胎牛血清(fetal bovine serum)
PBS 磷酸鹽緩衝鹽水
RPMI 洛斯維·帕克紀念研究所(Roswell Park Memorial Institute)
ACK溶解緩衝液 銨-氯-鉀溶解緩衝液
DMEM 杜爾貝科氏改良伊格爾氏培養基(Dulbecco's Modified Eagle's Medium)
HEPES 2-[4-(2-羥基乙基)哌𠯤-1-基]乙磺酸
MOPS 3-(N-(N-𠰌啉基))丙磺酸
Pen/Strep 青黴素及鏈黴素
HBS-P+ 含有0.1 M HEPES、1.5 M NaCl及0.5% v/v界面活性劑P20之緩衝液
DTT DL-二硫蘇糖醇
BGG 牛γ球蛋白
PBMC 周邊血液單核細胞
APC 抗原呈遞細胞
CD 分化簇
IgG 免疫球蛋白G
OKT3 CD3單株抗體
FLAG-Tag 胺基酸序列DYKDDDDK
DNA 去氧核糖核酸
CFSE 羧基螢光素丁二醯亞胺基酯
OVA 卵白蛋白抗原
FACS 螢光活化細胞分選
s.c. 皮下
i.v. 靜脈內
i.p. 腹膜內
n.d. 未測定
實例在所選生物學測定中測試一或多次。當測試超過一次時,資料係以平均值形式或以中位值形式報導,其中
● 平均值(亦稱為算術平均值)表示所得值之總和除以所測試次數,且
● 中位值表示該組值當以升序或降序排列時之中間數。若資料集中之值個數為奇數,則中位值為中間值。若資料集中之值數目為偶數,則中位值為兩個中間值之算術平均值。
合成實例一或多次。當合成超過一次時,來自生物測定之資料表示利用獲自一或多個合成批次之測試的資料集計算之平均值或中位值。
本發明化合物之活體外活性可在以下分析中證明:
人類DGKζ激酶活性抑制分析. 本發明化合物之人類二醯基甘油激酶澤塔(DGKζ)抑制活性採用如以下段落中所描述之人類DGKζ激酶活性分析來定量。本質上,酶活性藉由經由來自公司Promega之「ADP-Glo™激酶分析」套組定量產生為酶反應之副產物的二磷酸腺苷(adenosine-di-phosphate;ADP)來量測。此偵測系統如下工作:在第一步驟中,在激酶反應中未消耗之三磷酸腺苷(ATP)係使用腺苷酸環化酶(「ADP-Glo-試劑」)定量轉化為環單磷酸腺苷(cAMP),接著終止腺苷酸環化酶且使激酶反應中產生之ADP轉化為ATP,其隨後在基於螢光素酶之反應中產生輝光發光信號(「激酶偵測試劑」)。
C端Flag標記之重組全長人類DGKζ (在經桿狀病毒感染之昆蟲細胞中內部表現,使用抗Flag下拉及尺寸排阻層析純化)用作酶。作為替代方案,可使用Carnabio之市售酶。作為激酶之受質,使用在辛基-β-D-葡萄哌喃糖苷微胞中復原之1,2-二油醯基-sn-甘油。為了製備微胞,使用氮氣流使1體積之16.1 mM 1,2-二油醯基-sn-甘油(Avanti,目錄號O8001-25G)於氯仿中之溶液緩慢蒸發。隨後,添加22.55體積之510 mM辛基-β-D-葡萄哌喃糖苷(Sigma-Aldrich,目錄號O8001-10G)於50 mM MOPS緩衝液(pH 7.4)中之溶液,且將混合物在超音波浴中音波處理20 s。接著,添加35體積之50 mM MOPS緩衝液(pH 7.4),得到0.28 mM 1,2 二油醯基-sn-甘油及200 mM辛基-β-D-葡萄哌喃糖苷之溶液,使其等分且在液氮中急驟冷凍,且儲存在-20℃直至使用。對於各實驗,使新鮮等分試樣快速解凍且用含有95.7 µM三磷酸腺苷(Promega)之水性分析緩衝液(下文所描述)稀釋24倍,得到1.67倍濃縮受質溶液。
為了分析,將50 nl測試化合物於二甲基亞碸(DMSO,sigma)中之100倍濃縮溶液移液至白色1536孔或白色低體積384孔微量滴定盤中(均為Greiner Bio-One, Frickenhausen, Germany)。隨後,將2 µl人類DGKζ於水性分析緩衝液[50 mM (3-(N-(N-𠰌啉基))丙磺酸(MOPS,pH 7.4,Sigma-Aldrich)、1 mM二硫蘇糖醇(DTT,Sigma-Aldrich)、100 mM NaCl (Sigma-Aldrich)、10 mM MgCl2
(Sigma-Aldrich)、0.1% (w/v)牛γ球蛋白(BGG,Sigma-Aldrich)、1 µM CaCl2
(Sigma-Aldrich)]之溶液添加至孔中,且將混合物在22℃培育15 min以使測試化合物與酶預結合。藉由添加3 µl受質溶液[如上文所描述製備;於分析緩衝液中之11.7 µM 1,2-二油醯基-sn-甘油(=>5 µl分析體積中之最終濃度為7 µM),8.33 mM辛基-β-D-葡萄哌喃糖苷(=>5 µl分析體積中之最終濃度為5 mM)及91.67 µM三磷酸腺苷(=>5 µl分析體積中之最終濃度為55 µM)]起始反應且將所得混合物在22℃培育20 min之反應時間。視酶批次活性而定調整DGKζ之濃度且經選擇適合於使分析在線性範圍中,通常濃度為約0.1 nM。藉由添加2.5 µl「ADP-Glo-試劑」(1:1.5,用水稀釋)來終止反應且將所得混合物在22℃培育1 h以將激酶反應中未消耗之ATP完全轉化為cAMP。隨後添加2.5 µl「激酶偵測試劑」(比生產商建議的濃度高1.2倍),將所得混合物在22℃培育1 h,且接著用適合的量測儀器(例如Viewlux™,來自Perkin-Elmer)量測發光。將發射光之量視為所產生之ADP之量的量度,且由此視為DGKζ之活性的量度。
將資料標準化(無抑制劑之酶反應= 0%抑制,不包括酶的所有其他分析組分= 100%抑制)。通常,在相同微量滴定盤上以20 µM至0.07 nM範圍內之11個不同濃度(20 µM、5.7 µM、1.6 µM、0.47 µM、0.13 µM、38 nM、11 nM、3.1 nM、0.9 nM、0.25 nM及0.07 nM,在分析前藉由連續稀釋以於DMSO中之100倍濃溶液的水準單獨地製備之稀釋系列,確切濃度可視所使用移液器而變化),對各濃度以一式兩份值對測試化合物進行測試,且使用Genedata Screener™軟體計算IC50
值。
表18:活體外人類DGKζ激酶活性抑制分析中實例之IC50
值.
表19:活體外人類DGKζ激酶活性抑制分析中中間物之IC50
值。
| 實例編號 | IC50 [nM] |
| 1 | 946 |
| 2 | 935 |
| 3 | 927 |
| 4 | 833 |
| 5 | 757 |
| 6 | 740 |
| 7 | 705 |
| 8 | 618 |
| 9 | 536 |
| 10 | 425 |
| 11 | 406 |
| 12 | 364 |
| 13 | 357 |
| 14 | 334 |
| 15 | 266 |
| 16 | 283 |
| 17 | 261 |
| 18 | 207 |
| 19 | 200 |
| 20 | 161 |
| 21 | 142 |
| 21.1 | 5510 |
| 21.2 | 51 |
| 22 | 130 |
| 23 | 130 |
| 24 | 115 |
| 25 | 101 |
| 26 | 74.8 |
| 27 | 69.6 |
| 27.1 | 8650 |
| 27.2 | 43.6 |
| 28 | 61 |
| 29 | 58.4 |
| 29.1 | 12500 |
| 29.2 | 46.2 |
| 30 | 57.5 |
| 31 | 43.5 |
| 32 | 38.7 |
| 33 | 42.8 |
| 33.1 | 8610 |
| 33.2 | 22.8 |
| 34 | 34.4 |
| 35 | 25.3 |
| 36 | 22.2 |
| 37 | 19.8 |
| 37.1 | 2000 |
| 37.2 | 9.46 |
| 38 | 19.3 |
| 38.1 | 2000 |
| 38.2 | 7.37 |
| 39 | 19 |
| 40 | 15.4 |
| 40.1 | 792 |
| 40.2 | 7.08 |
| 41 | 13.5 |
| 41.1 | 2930 |
| 41.2 | 7.73 |
| 42 | 11.3 |
| 43 | 11.1 |
| 43.1 | 2730 |
| 43.2 | 5.93 |
| 44 | 8.83 |
| 44.1 | 1390 |
| 44.2 | 6.72 |
| 45 | 338 |
| 45.1 | 201 |
| 45.2 | 8910 |
| 45.3 | 1050 |
| 45.4 | > 20000 |
| 46 | 7.07 |
| 46.1 | 1470 |
| 46.2 | 5.69 |
| 47 | 3.77 |
| 47.1 | 1020 |
| 47.2 | 1.96 |
| 48 | 3.72 |
| 48.1 | 1.76 |
| 48.2 | 120 |
| 49 | 2.76 |
| 49.1 | 1030 |
| 49.2 | 2.1 |
| 50 | 378 |
| 50.1 | 127 |
| 50.2 | 14300 |
| 51 | 16.6 |
| 51.1 | 8.85 |
| 51.2 | 872 |
| 52 | 99.2 |
| 52.1 | 72.7 |
| 52.2 | 11400 |
| 53 | 30.8 |
| 53.1 | 20.3 |
| 53.2 | 1780 |
| 54 | 20.7 |
| 55 | 9.74 |
| 55.1 | 6 |
| 55.2 | 835 |
| 56 | 120 |
| 56.1 | 50.5 |
| 56.2 | 7640 |
| 57 | 155 |
| 57.1 | 137 |
| 57.2 | 14638 |
| 58 | 16.7 |
| 58.1 | 8 |
| 58.2 | 1047 |
| 59 | 10.3 |
| 59.1 | 4 |
| 59.2 | 424 |
| 60 | 403 |
| 61 | 93.2 |
| 61.1 | 5180 |
| 61.2 | 108 |
| 62 | 32.2 |
| 62.1 | 4620 |
| 62.2 | 23.2 |
| 63 | 33.9 |
| 63.1 | 5170 |
| 63.2 | 18.5 |
| 64 | 55.8 |
| 65 | 101 |
| 66 | 363 |
| 67 | 2270 |
| 68 | 457 |
| 69 | 64.1 |
| 70 | 196 |
| 71 | 2310 |
| 72 | 985 |
| 73 | 148 |
| 73.1 | 3720 |
| 73.2 | 82.1 |
| 74 | 190 |
| 74.1 | 17100 |
| 74.2 | 81.4 |
| 75 | 419 |
| 75.1 | > 20000 |
| 75.2 | 214 |
| 76 | 252 |
| 76.1 | 114 |
| 76.2 | 11000 |
| 77 | 533 |
| 77.1 | 234 |
| 77.2 | 10200 |
| 78 | 7220 |
| 78.1 | > 20000 |
| 78.2 | 7550 |
| 79 | 6790 |
| 79.1 | 1660 |
| 79.2 | 2390 |
| 80 | 10.8 |
| 81 | 8.71 |
| 81.1 | 1020 |
| 81.2 | 10.1 |
| 82 | 89.6 |
| 83 | 24.3 |
| 84 | 24.6 |
| 85 | 20.3 |
| 86 | 759 |
| 87 | 8.53 |
| 88 | 667 |
| 89 | 131 |
| 90 | 63.3 |
| 91 | 701 |
| 92 | 16.7 |
| 93 | 187 |
| 94 | 25.7 |
| 95 | 39 |
| 96 | 31.4 |
| 97 | 24.7 |
| 98 | 73.5 |
| 99 | 75.8 |
| 100 | 176 |
| 101 | 329 |
| 102 | 506 |
| 103 | 41.9 |
| 104 | 234 |
| 105 | 6.45 |
| 106 | 33.3 |
| 107 | 77.3 |
| 108 | 19.4 |
| 109 | 51.7 |
| 110 | 366 |
| 111 | 334 |
| 112 | 300 |
| 113 | 703 |
| 114 | 658 |
| 115 | 272 |
| 116 | 581 |
| 117 | 14.9 |
| 118 | 22.4 |
| 119 | 4.54 |
| 120 | 16.7 |
| 121 | 19.9 |
| 122 | 9.07 |
| 123 | 100 |
| 124 | 48.3 |
| 125 | 44 |
| 126 | 28.8 |
| 127 | 73.1 |
| 128 | 72.2 |
| 129 | 97.1 |
| 130 | 46.5 |
| 131 | 180 |
| 132 | 93.3 |
| 133 | 42.5 |
| 134 | 76.8 |
| 135 | 49.5 |
| 136 | 740 |
| 137 | 238 |
| 138 | 61.6 |
| 139 | 56.9 |
| 140 | 37.5 |
| 141 | 389 |
| 142 | 14.5 |
| 143 | 12.7 |
| 144 | 8.79 |
| 145 | 2.66 |
| 146 | 21.6 |
| 147 | 291 |
| 148 | 76.4 |
| 149 | 405 |
| 150 | 372 |
| 151 | 387 |
| 152 | 111 |
| 153 | 107 |
| 154 | 55.6 |
| 155 | 200 |
| 156 | 231 |
| 157 | 190 |
| 158 | 6.71 |
| 159 | 214 |
| 160 | 187 |
| 160.1 | 115 |
| 160.2 | 8448 |
| 161 | 15 |
| 161.1 | 9 |
| 161.2 | 2573 |
| 162 | 22 |
| 162.1 | 12 |
| 162.2 | 6574 |
| 163 | 9 |
| 163.1 | 5 |
| 163.2 | 1091 |
| 164 | 7 |
| 164.1 | 5 |
| 164.2 | 944 |
| 165 | 3 |
| 165.1 | 2 |
| 165.2 | 331 |
| 166 | 3 |
| 166.1 | 2 |
| 166.2 | 129 |
| 167 | 2 |
| 167.1 | 3 |
| 167.2 | 303 |
| 168 | 19 |
| 169 | 3 |
| 169.1 | 3 |
| 169.2 | 859 |
| 170 | 7 |
| 170.1 | 5 |
| 170.2 | 1000 |
| 171 | 11 |
| 172 | 46 |
| 172.1 | 24 |
| 172.2 | 4892 |
| 173 | 25 |
| 174 | 51 |
| 174.1 | 26 |
| 174.2 | 3793 |
| 175 | 20 |
| 176 | 91 |
| 176.1 | 34 |
| 176.2 | 672 |
| 177 | 40 |
| 178 | 48 |
| 179 | 57 |
| 180 | 62 |
| 181 | 65 |
| 182 | 91 |
| 182.1 | 84 |
| 182.2 | 10527 |
| 183 | 222 |
| 184 | 428 |
| 184.1 | 297 |
| 184.2 | > 20000 |
| 185 | 301 |
| 186 | 392 |
| 187 | 1400 |
| 187.1 | 553 |
| 187.2 | > 20000 |
| 188 | 1240 |
| 189 | 6352 |
| 190 | 553 |
| 191 | 356 |
| 192 | 224 |
| 193 | 35 |
| 194 | 66 |
| 195 | 1000 |
| 196 | 128 |
| 197 | 90 |
| 198 | 88 |
| 199 | 396 |
| 200 | 70 |
| 201 | 25 |
| 202 | 69 |
| 203 | 381 |
| 204 | 73 |
| 205 | 54 |
| 206 | 48 |
| 207 | 22 |
| 208 | 672 |
| 209 | 45 |
| 210 | 69 |
| 211 | 183 |
| 212 | 41 |
| 213 | 42 |
| 214 | 16 |
| 215 | 279 |
| 216 | 32 |
| 217 | 41 |
| 218 | 64 |
| 219 | 13 |
| 220 | 219 |
| 221 | 31 |
| 222 | 108 |
| 223 | 235 |
| 224 | 45 |
| 225 | 252 |
| 226 | 87 |
| 227 | 393 |
| 228 | 218 |
| 229 | 193 |
| 230 | 199 |
| 231 | 662 |
| 232 | 112 |
| 233 | 267 |
| 234 | 1640 |
| 235 | 542 |
| 236 | 730 |
| 237 | 749 |
| 238 | 667 |
| 239 | 236 |
| 240 | 1328 |
| 241 | 382 |
| 242 | 2031 |
| 243 | 51 |
| 244 | 30 |
| 245 | 22 |
| 246 | 662 |
| 247 | 40 |
| 248 | 136 |
| 249 | 120 |
| 250 | 36 |
| 251 | 87 |
| 252 | 106 |
| 253 | 59 |
| 254 | 32 |
| 255 | 76 |
| 256 | 9 |
| 257 | n.d. |
| 258 | 19 |
| 259 | 19 |
| 260 | 29 |
| 261 | 90 |
| 262 | 6 |
| 263 | 539 |
| 264 | 376 |
| 265 | 459 |
| 266 | 287 |
| 267 | 63 |
| 268 | 3 |
| 269 | 12 |
| 270 | 13 |
| 271 | 18 |
| 272 | 39 |
| 273 | 20 |
| 274 | 107 |
| 275 | 29 |
| 276 | 29 |
| 277 | 494 |
| 278 | 230 |
| 279 | 48 |
| 280 | 43 |
| 281 | 98 |
| 282 | 53 |
| 283 | 36 |
| 284 | 33 |
| 285 | 68 |
| 285.1 | 34 |
| 285.2 | 432 |
| 286 | 31 |
| 287 | 18 |
| 288 | 3442 |
| 289 | 10 |
| 290 | 936 |
| 291 | 178 |
| 292 | 282 |
| 中間物編號 | IC50 [nM] |
| 41 | > 20000 |
| 43 | > 20000 |
| 62 | > 20000 |
| 63 | > 20000 |
| 64 | > 20000 |
| 65 | > 20000 |
| 66 | > 20000 |
| 67 | > 20000 |
Jurkat IL2- 報導細胞株中之反式活化分析
在IL2啟動子控制下經螢火蟲螢光素酶報導基因構築體穩定轉染之購自Promega之Jurkat細胞(Promega,#CS187001)中進行反式活化分析。如製造商所規定培養細胞。在大致1E+06個細胞/毫升之培養密度時收穫散裝細胞,將其懸浮於冷凍儲存介質(70%RPMI/20% FCS/10% DMSO)中,以-1°/min之受控速率冷凍於1.8 mL冷凍小瓶中,其中細胞密度為每瓶1E+07至1E+08個細胞,且儲存在-150℃或更低,直至進一步使用。解凍冷凍細胞且在培養基中以3.5E+05個細胞/毫升之起始密度培養6天。在第6天,使細胞在300×g下離心5 min,傾析培養基且用新鮮分析培養基(500 mLRPMI (Gibco,# 22400) + 5 mL L-麩醯胺酸(Sigma,#G7513) + 5 mL青黴素/鏈黴素(Sigma #P0781) + 5 mL非必需胺基酸(Invitrogen,#11140) + 5 mL丙酮酸鈉(Gibco #1136088)、5 mL FBS (Biochrom,#S0615))將細胞濃度調整至5.0E+06個細胞/毫升。將細胞工作儲備液分成兩份:使用EC30刺激之中性對照及化合物,使用EC100刺激之較高對照。
藉由以1/1/4比率在分析培養基中以2倍最終濃度(最終濃度視細胞批次而定,通常對於中性對照0.055/0.055/0.22 µg/mL,對於較高對照0.5/0.5/2 mg/mL)稀釋抗CD3 (BD Pharmingen,#555329)、抗CD28 (BD Pharmingen,#555725)及山羊抗小鼠抗IgG (ThermoFisher,#31160)抗體來製備抗體預混物。在使用之前將預混物溶液以1+1體積添加至細胞中。
將五十奈升測試化合物於DMSO中之100倍濃縮溶液轉移至白色微量滴定測試盤(384,Greiner Bio-One,Germany)中。對此使用Hummingbird液體處置器(Digilab, USA)或Echo聲學系統(Labcyte, USA)。將五微升新製備的細胞懸浮液添加至測試盤之孔中,且將其在37℃在5% CO2
氛圍中培育。在完成4小時培育後,將3 µl Bio-Glo螢光素酶分析試劑(Promega,#G7941,如由供應商推薦製備)添加至所有孔中。將測試盤在20℃培育10 min,之後在微量盤讀取器(通常BMG, Germany之Pherastar或Perkin-Elmer, USA之ViewLux)中量測發光。使資料標準化(中性對照=0%效果,較高對照=100%效果)。在高達11個濃度(通常20 µM、5.7 µM、1.6 µM、0.47 µM、0.13 µM、38 nM、11 nM、3.1 nM、0.89 nM、0.25 nM及0.073 nM)下測試化合物,重複兩次。製備稀釋系列,隨後藉由連續稀釋以100倍濃縮形式進行分析。藉由4參數擬合使用商業套裝軟體(Genedata Analyzer, Switzerland)計算EC50
值。
人類PBMC之多純系活化 為了測試本發明DGKζ抑制劑對於人類周邊血液單核細胞(PBMC)之IL-2及IFN-γ分泌之效果,作為篩選分析進行24 h人類PBMC分析。為此,將96孔平底盤在4℃以50 µL PBS/孔用次最佳刺激條件(EC 10-30)之人類aCD3 (Invitrogen,純系OKT3)抗體塗覆隔夜。將在液體N2
下自白血球樣品分離及冷凍之PBMC解凍且再懸浮於培養基(X-Vivo-20)中。塗鋪4 × 105
個細胞/孔。以各別濃度(自10 µM至3 nM之5倍稀釋步驟)用本發明DGKζ抑制劑處理孔,且最終每孔DMSO濃度為0.1%。使用培養基+DMSO (0.1%)作為基線值。使用1000 ng/mL aCD3 + aCD28 (1 µg/mL)及DGKζ參考抑制劑作為陽性對照。在24 h之後,收集培養基且進行hIL-2或hIFN-γ ELISA。計算以下參數:EC50
值,在50%增加時之濃度;最大增加%及各別濃度以及標準化為所選擇DGKζ參考抑制劑之最大濃度(10 µM)的最大效果。
小鼠 OT-I 抗原特異性 T 細胞 之活體外活化
為了測試本發明DGKζ抑制劑在鼠類抗原特異性T細胞中之效果,收集OT-I小鼠之脾及淋巴結且經由40 µm細胞過濾器搗碎且在1 mL ACK溶解緩衝液(Gibco)/脾臟中培育1 min。在50 mL falcon管中之含有0.05 ng/mL SIINFEKL(圖2)之培養基中,在37℃培育4×106
個細胞/毫升30 min。之後,使細胞離心且使4×106
個細胞/毫升再懸浮於新鮮培養基中(DMEM;10% FCS,1% Pen/Strep,0.1% β-巰基乙醇,1% HEPES)。在96孔圓底盤中每孔塗鋪4×105
個細胞。以於最終濃度為0.1%之DMSO中之各別濃度(自10 µM至3 nM之5倍稀釋步驟),用本發明DGKζ抑制劑處理孔。使用培養基+ DMSO (0.1%)作為基線值。使用與4× SIINFEKL濃度(0.2 ng/ml)及DGKζ參考抑制劑一起培育之細胞作為陽性對照。將盤離心以在培育之前減少T細胞與APC之間的距離。在24 h之後,收集培養基,且進行mIL-2或mIFN-γ ELISA。計算以下參數:EC50
值,在50%增加時之濃度;最大增加%及各別濃度以及標準化為所選擇DGKζ參考抑制劑之最大濃度(10 µM)的最大效果。
DGKζ表面電漿子共振相互作用分析 使用表面電漿子共振(surface plasmonResonance;SPR)測定本發明中所描述之化合物與DGKζ結合之能力。此允許依據平衡解離常數(KD
[M])以及結合及解離速率常數(分別為kon
[1/Ms]及koff
[1/s])來定量結合。使用Biacore® T200、Biacore® S200或Biacore® 8K (GE Healthcare)進行量測。
此章節中所描述之所有緩衝液均用補充有如下文所指示之額外緩衝組分:二硫蘇糖醇(DTT來自Sigma,#D0632-25G)、腺苷5′-三磷酸(ATP來自Sigma,#A26209-10G)、MgCl2
(Sigma,#M1028-100ML)、二甲基亞碸(DMSO來自Biomol,#54686.500)的10×HBS-P+緩衝液(GE Healthcare,#BR100671)製備。
對於SPR量測而言,經由卵白素-生物素相互作用將重組及生物素化人類DGKζ (獲自Carna Biosciences,產品編號:12-410-20N)固定至一系列S感測器晶片Sa (GE Healthcare,#BR-1005-31)上。簡言之,將DGKζ在固定緩衝液(10 mM HEPES,150 mM NaCl,0.05% v/v界面活性劑P20,2 mM MgCl2
,1 mM DTT,pH 7.4)中稀釋至10 µg/mL之濃度且在10℃之溫度使用10 µL/min之流速在SA晶片表面上捕捉500秒。通常達成大致6000RU之固定量。參考表面由不含經固定蛋白質之卵白素表面組成。將化合物自10 mM DMSO儲備溶液稀釋至操作緩衝液(10 mM HEPES,150 mM NaCl,0.05% v/v界面活性劑P20,2 mM MgCl2
,1 mM DTT,0.2 mM ATP及1% v/v DMSO,pH 7.4)中。對於SPR結合量測而言,將連續稀釋液(通常1:3稀釋,得到8個濃度,直至2 µM或20 µM)注射於經固定蛋白質上。在18℃及在100 µL/min之流速下量測結合親和力及動力學。
藉由以30 µL/min之流速注射不含ATP之再生緩衝器(10 mM HEPES,150 mM NaCl,0.05% v/v界面活性劑P20,1 mM DTT及1% v/v DMSO,pH 7.4)200 s進行具有額外再生步驟之分析的變化形式。
使雙參考感測器圖譜擬合至如Biacore® T200、S200及8K評價軟體(Biacore T200評價軟體版本2.0,Biacore S200評價軟體版本1.0,Biacore 8K評價軟體,GE Healthcare)中實施的單個可逆朗格繆爾(Langmuir) 1:1反應機制。
使用桿狀病毒系統之昆蟲細胞中DGKζ之表現 表現構築體:
編碼人類DGKζ (UniprotQ13574-2
)之全長序列的cDNA針對真核細胞中之表現加以最佳化且藉由Life Technologies的GeneArt Technology合成。
DNA序列編碼以下序列:
構築體DGKζ_hu 胺基酸M1至V928
另外,表現構築體編碼:用於轉譯起始之Kozak DNA序列(GCCACC)、甲硫胺酸隨後胺基酸甘胺酸之轉譯起始密碼子、在DGKζ N端及在DGKζ之C端之Flag (DYKDDDDK)序列、兩個終止密碼子及此外用於閘道選殖之5'及3' att-DNA序列。
使用閘道技術將DGKζ構築體次選殖至目的載體pD-INS中。載體pD-INS為能夠表現Flag-DGKζ蛋白質之桿狀病毒轉移載體(基於載體pVL1393,Pharmingen)。各別蛋白質命名為DGKz_hu_1。
重組桿狀病毒之產生
使用Fugene HD (Roche),將DGKζ轉移載體與桿狀病毒DNA (Flashbac Gold DNA, Oxford Expression Technologies)一起共轉染於Sf9細胞中。在5天之後,將含有編碼各種DGK蛋白質之重組桿狀病毒的經轉染細胞之上清液用於進一步感染Sf9細胞以便病毒擴增,從而使用qPCR監測病毒效價。
使用生物反應器之Sf9細胞中之DGKζ表現
將具有拋棄式培養袋之Wave生物反應器中培養的Sf9細胞(Insect-xpress medium,Lonza,27℃)以106
個細胞/毫升之細胞密度與重組桿狀病毒儲備液中之一者一起以感染倍率1感染,且培育72 h。隨後,藉由離心(800 xg)收穫細胞,且將細胞集結粒(cell pellet)冷凍在-80℃。
DGKz_hu_1蛋白之純化:
藉由如下之兩步層析程序來達成DGKz_hu_1蛋白之純化。
將集結細胞(來自8 L細胞培養物)再懸浮於溶解緩衝液(25 mM Tris HCl 8.0;500 mM NaCl;250 mM蔗糖,1 mM DTT;0.1% Triton X-100;完全蛋白酶抑制劑混合物-(Roche))中且藉由凍融循環溶解,隨後在冰上在核酸酶(25 U/mL)存在下培育60 min。使溶解物在63.000 xg下在4℃離心30 min。接著,將可溶性上清液與40 mL抗Flag M2瓊脂糖(Sigma)一起在塑膠燒瓶中在4℃在旋轉情況下培育16 h以為了使結合加標籤之DGKζ蛋白,隨後用5 × 50 mL洗滌緩衝液(25 mM Tris HCl 8.0;500 mM NaCl;250 mM蔗糖;1 mM DTT)沖洗,及最後使用溶離緩衝液(具有250 μg/mL FLAG-肽之洗滌緩衝液在4℃以3 × 25 mL培育30 min)溶離經結合蛋白質。
將來自親和層析之溶離級分濃縮(使用Amicon Ultra 15,離心過濾器,30 kDa MW截止;Millipore #UFC903024)至25 mL且應用於尺寸排阻層析管柱(S200製備級26/60,GE Healthcare),且收集所得單體峰級分,合併且再次濃縮。針對尺寸排阻層析及最終濃縮樣品,使用具有300 mM NaCl之洗滌緩衝液。最終蛋白質樣品濃度為5至10 mg/mL,且產量為每公升細胞培養物5 mg最終蛋白質。
本發明化合物之活體內活性可在以下分析中證明:
鼠類抗原特異性OT-I T細胞之活體內活化 經口投與化合物增強活體內抗原特異性T細胞活化。
活體內直接偵測抗原特異性T細胞增殖在技術上具有挑戰性,因為其需要存在對同源抗原具有特異性之T細胞以及對細胞增殖具有特異性的量測程序。此等要求皆滿足於OT-I轉移模型中,其利用直接轉移CD8 T細胞轉殖基因用於識別卵白蛋白衍生肽作為抗原之T細胞受體。
在轉移之前,用螢光染料CFSE標記OT-I T細胞,該螢光染料CFSE藉由每一次細胞分裂稀釋且因此允許偵測細胞增殖。在轉移經CFSE標記之T細胞之後,用卵白蛋白抗原OVA-30 (圖3)對小鼠進行疫苗接種。僅轉移的OT-I細胞能夠識別APC所呈遞之OVA-抗原且接著僅此等轉移的T細胞得以活化。OT-I細胞中之CFSE量之流動式細胞量測分析可與多種活化標記(如CD69、CD25及PD1)之量測組合。
特定言之,野生型C57Bl6小鼠接受2×106
個經CFSE標記之OT-I T細胞,且在一天後藉由靜脈內施加2.5 µg OVA-30進行疫苗接種。接著,將小鼠分為接受單獨媒劑、單獨本發明DGKζ抑制劑或本發明DGKζ抑制劑與其他免疫調節劑組合之群組。處理小鼠2至20天,且藉由FACS分析脾、血液及淋巴結之T細胞組成(包括轉移OT-1細胞)。
活體內同基因型腫瘤模型 將小鼠歸屬於在6-8週年齡之研究。畜牧業、飼養及健康狀況均根據動物福祉指南。同基因型腫瘤細胞株用適當培養基培養且在接種之前拆分至少3次。視模型而定,對雌性小鼠s.c、i.v.或i.p接種適當量之含腫瘤細胞之培養基或培養基/基質膠混合物。在4至10天之後,將小鼠隨機分組且當腫瘤達到大致40至70mm2
之大小時開始治療性治療。
使用測徑規測定長度(a)及寬度(b)來量測腫瘤大小。根據以下計算腫瘤體積:
v=(a x b^2)/2
計算單一療法及組合治療相對於對照組之顯著性,如藉由二因子變異數分析測定。
圖1:編碼人類DGKζ M1至V928加N端Flag標籤之DGKz_hu_1,如在SEQ ID No. 1下所描述。
圖2:SIINFEKL胺基酸序列,如在SEQ ID No. 2下所描述。
圖3:OVA-30肽序列,如在SEQ ID No. 3下所描述。
圖4:FLAG-標籤,如在SEQ ID No. 4下所描述。
圖5:用於轉譯起始之Kozak序列,如在SEQ ID No. 5下所描述。
圖6:實例49.2之50%熱橢球,分子1.F171及F151表示在C13-C16軸上180°病症之兩個細分位置。
圖7:實例59.1分子1之50%熱橢球
圖8:實例61.2分子1之50%熱橢球
圖9:實例62.2分子1之50%熱橢球
Claims (16)
- 一種通式(I)化合物: 其中: R1 表示視情況經取代一次、兩次或三次之苯基或6員雜芳基,各取代基獨立地選自鹵素原子或選自以下之基團:羥基、氰基、硝基、C1 -C6 -烷基、(苯基)-(C1 -C3 -烷基)-、C1 -C6 -鹵烷基、C1 -C6 -烷氧基、(苯基)-(C1 -C3 -烷氧基)-、C1 -C6 -鹵烷氧基、-N(R5 )(R6 ), 其中該(苯基)-(C1 -C3 -烷基)-基團及該(苯基)-(C1 -C3 -烷氧基)-基團中之苯基視情況經取代一次或兩次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、甲基、乙基、三氟甲基、甲氧基、乙氧基、二甲胺基及三氟甲氧基, 或與該苯基或6員雜芳基之相鄰碳原子連接之兩個取代基一起形成選自以下之二價基團:-(CH2 )3 -、-(CH2 )4 -、-(CH2 )2 -O-、-(CH2 )3 -O-、-CH2 -O-CH2 -、-(CH2 )2 -O-CH2 -、-O-CH2 -O-、-O-CH2 -CH2 -O-、-O-CF2 -O-、-O-CH2 -CF2 -O-及-O-CF2 -CF2 -O-, 或 R1 表示視情況經取代一次或兩次之5員雜芳基,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、C1 -C3 -烷基及C1 -C3 -烷氧基; R2 表示基團, 其中「*」指示與連接R2 之氮原子連接之點; R3 表示選自甲基及-NH2 之基團; R4 表示視情況經取代一次、兩次或三次之苯基或6員雜芳基,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、硝基、C1 -C6 -烷基、(苯基)-(C1 -C3 -烷基)-、(5或6員雜芳基)-(C1 -C3 -烷基)-、(C3 -C7 -環烷基)-(C1 -C3 -烷基)-、((R9 )O)-(C1 -C6 -烷基)-、C1 -C6 -鹵烷基、C3 -C7 -環烷基、-OR9 、-N(R10 )(R11 )、((R10 )(R11 )N)-(C1 -C3 -烷基alkyl)-、-C(=O)-N(R12 )(R13 )、-S(=O)n -R14 、-C(=O)R14 、-C(=O)-OR17 ,及自身視情況經一或兩個選自鹵素原子及甲基之取代基取代的5或6員雜芳基, 或與該苯基或6員雜芳基之相鄰碳原子連接之兩個取代基一起形成選自以下之二價基團:-(CH2 )3 -、-(CH2 )4 -、-(CH2 )2 -O-、-(CH2 )3 -O-、-CH2 -O-CH2 -、-(CH2 )2 -O-CH2 -、-O-CH2 -O-、-O-CH2 -CH2 -O-、-O-CF2 -O-、-O-CH2 -CF2 -O-及-O-CF2 -CF2 -O-; R5 及R6 在每次出現時獨立地表示氫原子或選自以下之基團:C1 -C4 -烷基、(C1 -C4 -烷基)-C(=O)-、C3 -C4 -環烷基及(苯基)-(C1 -C3 -烷基)-, 或 R5 及R6 連同其所連接之氮原子一起表示視情況經取代一次、兩次或三次之單環含氮4至7員雜環烷基,各取代基獨立地選自鹵素原子或選自以下之基團:側氧基、羥基、C1 -C4 -烷基、(C1 -C4 -烷基)-C(=O)-、C3 -C4 -環烷基及C1 -C4 -烷氧基; R7 表示氫原子或C1 -C2 -烷基; R8 表示選自-C(=O)-NH2 及-S(=O)2 -NH2 之基團; R9 表示氫原子或選自以下之基團:C1 -C6 -烷基、(5或6員雜芳基)-(C1 -C3 -烷基)-、(苯基)-(C1 -C3 -烷基)-、C1 -C6 -鹵烷基、C2 -C4 -羥烷基、(C1 -C3 -烷氧基)-C2 -C3 -烷基-、((C1 -C3 -烷基)-C(=O)-O)-C2 -C3 -烷基-、-C(R18 )(R19 )-C(=O)-OR17 、-C(R18 )(R19 )-C(=O)-N(R20 )(R21 )、-C(=O)-N(R20 )(R21 )、苯基及5或6員雜芳基, 其中該(苯基)-(C1 -C3 -烷基)-基團內之苯基及該苯基自身以及該(5或6員雜芳基)-(C1 -C3 -烷基)-基團內之5或6員雜芳基及該5或6員雜芳基自身視情況經取代一次或兩次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、甲基、乙基、三氟甲基、甲氧基、乙氧基、二甲胺基及三氟甲氧基; R10 及R11 在每次出現時獨立地表示氫原子或選自以下之基團:C1 -C4 -烷基、C1 -C4 -鹵烷基、C2 -C4 -羥烷基、(C1 -C3 -烷氧基)-C2 -C3 -烷基-、((R22 )(R23 )N)-C2 -C3 -烷基、(C3 -C7 -環烷基)-(C1 -C3 -烷基)-、(C1 -C4 -烷基)-C(=O)-、C3 -C7 -環烷基、(C3 -C7 -環烷基)-C(=O)-、(苯基)-(C1 -C3 -烷基)-、(苯基)-(C1 -C3 -烷基)-C(=O)-、(苯基)-(C1 -C3 -烷基)-O-C(=O)-、苯基及5或6員雜芳基, 其中C3 -C7 -環烷基以及該(C3 -C7 -環烷基)-(C1 -C3 -烷基)-基團及(C3 -C7 -環烷基)-C(=O)-基團內之C3 -C7 -環烷基視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自氰基、C1 -C2 -烷基及C1 -C2 -鹵烷基之基團, 且其中該苯基及該5或6員雜芳基、以及該(苯基)-(C1 -C3 -烷基)-基團、(苯基)-(C1 -C3 -烷基)-C(=O)-基團及(苯基)-(C1 -C3 -烷基)-O-C(=O)-基團內之苯基視情況經取代一次或兩次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、甲基、乙基、三氟甲基、甲氧基、乙氧基、二甲胺基及三氟甲氧基, 或 R10 及R11 連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基或雙環含氮5至11員雜環烷基,其視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、側氧基、羥基、C1 -C4 -烷基、C1 -C4 -鹵烷基、(C1 -C4 -烷基)-C(=O)-、C3 -C7 -環烷基、C1 -C4 -烷氧基、-N(R22 )(R23 )及單環4至7員雜環烷基; R12 及R13 在每次出現時獨立地表示氫原子或選自以下之基團:C1 -C4 -烷基、C1 -C4 -鹵烷基、C1 -C4 -羥烷基、(C1 -C4 -烷氧基)-C2 -C3 -烷基-、(C1 -C4 -鹵烷氧基)-C2 -C3 -烷基-、(苯氧基)-C2 -C3 -烷基-、C3 -C7 -環烷基、單環4至7員雜環烷基及(苯基)-(C1 -C3 -烷基)-, 其中C3 -C7 -環烷基及單環4至7員雜環烷基視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、側氧基、羥基、C1 -C4 -烷基、(C1 -C4 -烷基)-C(=O)-、C3 -C4 -環烷基及C1 -C4 -烷氧基, 且其中該(苯氧基)-C2 -C3 -烷基-基團及該(苯基)-(C1 -C3 -烷基)-基團內之苯基視情況經取代一次或兩次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、甲基、乙基、三氟甲基、甲氧基、乙氧基、二甲胺基及三氟甲氧基, 或 R12 及R13 連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、側氧基、羥基、C1 -C4 -烷基、(C1 -C4 -烷基)-C(=O)-、C3 -C4 -環烷基及C1 -C4 -烷氧基; R14 表示選自C1 -C4 -烷基、C1 -C4 -鹵烷基及苯基之基團, 其中苯基視情況經取代一次或兩次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、甲基、乙基、三氟甲基、甲氧基、乙氧基、二甲胺基及三氟甲氧基; R17 表示C1 -C4 -烷基; R18 及R19 在每次出現時獨立地表示氫原子或C1 -C4 -烷基; R20 表示氫原子或選自以下之基團:C1 -C6 -烷基、C3 -C4 -烯基、C3 -C4 -炔基、C1 -C3 -烷氧基、C3 -C7 -環烷基、雙環C5 -C11 -環烷基、金剛烷基、單環4至7員雜環烷基、雙環5至11員雜環烷基、苯基、萘基及5至10員雜芳基, 其中該C1 -C6 -烷基視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:羥基、氰基、C1 -C3 -烷氧基、-N(R22 )(R23 )、C3 -C7 -環烷基、雙環C5 -C11 -環烷基、金剛烷基、單環4至7員雜環烷基、雙環5至11員雜環烷基、苯基及5至10員雜芳基,該苯基取代基及該5至10員雜芳基取代基自身視情況經取代一次或兩次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、甲基、乙基、三氟甲基、甲氧基、乙氧基、二甲胺基及三氟甲氧基, 且其中C3 -C7 -環烷基、雙環C5 -C11 -環烷基、金剛烷基、單環4至7員雜環烷基及雙環5至11員雜環烷基視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、側氧基、羥基、C1 -C4 -烷基、(C1 -C4 -烷基)-C(=O)-、C3 -C4 -環烷基及C1 -C4 -烷氧基, 且其中該苯基、該萘基及該5至10員雜芳基視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、C1 -C4 -烷基、C1 -C4 -鹵烷基、C1 -C4 -烷氧基、C1 -C4 -鹵烷氧基、-N(R22 )(R23 )及-C(=O)-N(R24 )(R25 ), R21 表示氫原子或C1 -C4 -烷基, 或 R20 及R21 連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況為苯并縮合的且其視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、側氧基、羥基、C1 -C4 -烷基、C1 -C4 -鹵烷基、(苯基)-(C1 -C3 -烷基)-、(C1 -C4 -烷基)-C(=O)-、C3 -C4 -環烷基、C1 -C4 -烷氧基、C1 -C3 -鹵烷氧基、-N(R22 )(R23 )及-C(=O)-N(R24 )(R25 ); R22 及R23 在每次出現時獨立地表示氫原子或選自C1 -C2 -烷基及(C1 -C2 -烷基)-C(=O)-之基團; R24 及R25 在每次出現時獨立地表示氫原子或C1 -C4 -烷基,及 n 表示整數0、1或2, 或其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物或鹽,或其混合物。
- 如請求項1之化合物,其中: R1 表示視情況經取代一次、兩次或三次之苯基或吡啶基,各取代基獨立地選自鹵素原子或選自以下之基團:羥基、氰基、硝基、C1 -C4 -烷基、(苯基)-(C1 -C2 -烷基)-、C1 -C4 -鹵烷基、C1 -C4 -烷氧基、(苯基)-(C1 -C2 -烷氧基)-、C1 -C4 -鹵烷氧基、-N(R5 )(R6 ), 其中該(苯基)-(C1 -C2 -烷基)-基團及該(苯基)-(C1 -C2 -烷氧基)-基團中之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及溴原子或選自甲基、三氟甲基及甲氧基之基團, 或與該苯基或吡啶基之相鄰碳原子連接之兩個取代基一起形成選自以下之二價基團:-(CH2 )3 -、-(CH2 )4 -、-(CH2 )2 -O-、-(CH2 )3 -O-、-CH2 -O-CH2 -、-O-CH2 -O-、-O-CH2 -CH2 -O-及-O-CF2 -O-, 或 R1 表示視情況經取代一次或兩次之吡唑基,各取代基獨立地選自鹵素原子或選自氰基、C1 -C2 -烷基及C1 -C2 -烷氧基之基團; R2 表示基團, 其中「*」指示與連接R2 之氮原子連接之點; R3 表示選自甲基及-NH2 之基團; R4 表示視情況經取代一次、兩次或三次之苯基或吡啶基,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、硝基、C1 -C4 -烷基、(苯基)-(C1 -C2 -烷基)-、(5員雜芳基)-(C1 -C2 -烷基)-、(C3 -C7 -環烷基)-(C1 -C2 -烷基)-、((R9 )O)-(C1 -C4 -烷基)-、C1 -C4 -鹵烷基、C3 -C7 -環烷基、-OR9 、-N(R10 )(R11 )、((R10 )(R11 )N)-(C1 -C3 -烷基)-、-C(=O)-N(R12 )(R13 )、S(=O)n -R14 、-C(=O)R14 、-C(=O)-OR17 及自身視情況經一或兩個甲基取代5員雜芳基, 或與該苯基或吡啶基之相鄰碳原子連接之兩個取代基一起形成選自以下之二價基團:-(CH2 )3 -、-(CH2 )4 -、-(CH2 )2 -O-、-(CH2 )3 -O-、-CH2 -O-CH2 -、-O-CH2 -O-、-O-CH2 -CH2 -O-及-O-CF2 -O-; R5 及R6 在每次出現時獨立地表示氫原子或選自C1 -C2 -烷基及(C1 -C2 -烷基)-C(=O)-之基團, 或 R5 及R6 連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:側氧基、羥基、C1 -C2 -烷基及(C1 -C2 -烷基)-C(=O)-; R7 表示氫原子或C1 -C2 -烷基; R8 表示-C(=O)-NH2 基團; R9 表示氫原子或選自以下之基團:C1 -C4 -烷基、(苯基)-(C1 -C2 -烷基)-、C1 -C4 -鹵烷基、C2 -C3 -羥烷基、(C1 -C2 -烷氧基)-C2 -烷基-、((C1 -C2 -烷基)-C(=O)-O)-C2 -烷基-、-C(R18 )(R19 )-C(=O)-OR17 、-C(R18 )(R19 )-C(=O)-N(R20 )(R21 )、-C(=O)-N(R20 )(R21 )及苯基, 其中該(苯基)-(C1 -C2 -烷基)-基團內之苯基及該苯基自身視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:氰基、甲基、三氟甲基及甲氧基; R10 及R11 在每次出現時獨立地表示氫原子或選自以下之基團:C1 -C2 -烷基、C1 -C2 -鹵烷基、C2 -C3 -羥烷基、(C1 -C2 -烷氧基)-C2 -烷基-、((R22 )(R23 )N)-C2 -烷基、(C3 -C7 -環烷基)-(C1 -C2 -烷基)-、(C1 -C2 -烷基)-C(=O)-、C3 -C7 -環烷基、(C3 -C7 -環烷基)-C(=O)-、(苯基)-(C1 -C2 -烷基)-、(苯基)-(C1 -C2 -烷基)-C(=O)-及(苯基)-(C1 -C2 -烷基)-O-C(=O)-, 其中C3 -C7 -環烷基以及該(C3 -C7 -環烷基)-(C1 -C2 -烷基)-基團及該(C3 -C7 -環烷基)-C(=O)-基團內之C3 -C7 -環烷基視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自以下之基團:氰基、C1 -C2 -烷基及C1 -C2 -鹵烷基, 且其中該(苯基)-(C1 -C2 -烷基)-基團、該(苯基)-(C1 -C2 -烷基)-C(=O)-基團及該(苯基)-(C1 -C2 -烷基)-C(=O)-基團內之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:甲基、三氟甲基及甲氧基, 或 R10 及R11 連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基或雙環含氮5至10員雜環烷基,其視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、側氧基、羥基、C1 -C2 -烷基、C1 -C2 -鹵烷基、(C1 -C2 -烷基)-C(=O)-、C1 -C2 -烷氧基、-N(R22 )(R23 )及單環4至7員雜環烷基; R12 及R13 在每次出現時獨立地表示氫原子或選自以下之基團:C1 -C4 -烷基、C1 -C4 -鹵烷基、C1 -C4 -羥烷基、(C1 -C4 -烷氧基)-C2 -C3 -烷基-、(C1 -C4 -鹵烷氧基)-C2 -C3 -烷基-、(苯氧基)-C2 -C3 -烷基-、C3 -C7 -環烷基、單環4至7員雜環烷基及(苯基)-(C1 -C3 -烷基)-, 其中C3 -C7 -環烷基及單環4至7員雜環烷基視情況經取代一次或兩次,各取代基獨立地選自鹵素原子或選自以下之基團:側氧基、C1 -C2 -烷基及(C1 -C2 -烷基)-C(=O)-, 且其中該(苯氧基)-C2 -C3 -烷基-基團及該(苯基)-(C1 -C3 -烷基)-基團內之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:氰基、甲基、三氟甲基及甲氧基, 或 R12 及R13 連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況經取代一次或兩次,各取代基獨立地選自鹵素原子或選自以下之基團:側氧基、C1 -C2 -烷基及(C1 -C2 -烷基)-C(=O)-; R14 表示選自以下之基團:C1 -C2 -烷基、C1 -C2 -鹵烷基及苯基, 其中苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:甲基、三氟甲基及甲氧基; R17 表示C1 -C4 -烷基; R18 及R19 在每次出現時獨立地表示氫原子或C1 -C2 -烷基; R20 表示氫原子或選自以下之基團:C1 -C6 -烷基、C3 -C4 -烯基、C3 -C4 -炔基、C1 -C3 -烷氧基、C3 -C7 -環烷基、雙環C5 -C11 -環烷基、金剛烷基、單環4至7員雜環烷基、雙環5至10員雜環烷基、苯基、萘基及5至10員雜芳基, 其中該C1 -C6 -烷基視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:羥基、氰基、C1 -C3 -烷氧基、-N(R22 )(R23 )、C3 -C7 -環烷基、雙環C5 -C11 -環烷基、金剛烷基、單環4至7員雜環烷基、雙環5至10員雜環烷基、苯基及5至10員雜芳基,該苯基取代基及該5至10員雜芳基取代基自身視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:甲基、三氟甲基及甲氧基, 且其中C3 -C7 -環烷基、雙環C5 -C11 -環烷基、金剛烷基、單環4至7員雜環烷基、雙環5至10員雜環烷基視情況經取代一次或兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、側氧基、羥基、C1 -C2 -烷基及(C1 -C2 -烷基)-C(=O)-, 且其中該苯基、該萘基及該5至10員雜芳基視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、C1 -C2 -烷基、C1 -C2 -鹵烷基、C1 -C2 -烷氧基、C1 -C2 -鹵烷氧基、-N(R22 )(R23 )及-C(=O)-N(R24 )(R25 ), R21 表示氫原子或C1 -C2 -烷基, 或 R20 及R21 連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況為苯并縮合的且其視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、側氧基、羥基、C1 -C2 -烷基、C1 -C2 -鹵烷基、(苯基)-(C1 -C2 -烷基)-、(C1 -C2 -烷基)-C(=O)-、C3 -C4 -環烷基、C1 -C2 -烷氧基、C1 -C2 -鹵烷氧基、-N(R22 )(R23 )及-C(=O)-N(R24 )(R25 ); R22 及R23 在每次出現時獨立地表示氫原子或選自C1 -C2 -烷基及(C1 -C2 -烷基)-C(=O)-之基團; R24 及R25 在每次出現時獨立地表示氫原子或C1 -C2 -烷基,及 n 表示整數0、1或2, 或其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物或鹽,或其混合物。
- 如請求項1或2之化合物,其中: R1 表示視情況經取代一次、兩次或三次之苯基或吡啶基,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:羥基、氰基、C1 -C4 -烷基、C1 -C2 -氟烷基、C1 -C2 -烷氧基、(苯基)-(C1 -C2 -烷氧基)-、C1 -C2 -氟烷氧基及-N(R5 )(R6 ), 或與該苯基或吡啶基之相鄰碳原子連接之兩個取代基一起形成選自以下之二價基團:-(CH2 )3 -、-O-CH2 -O-及-O-CF2 -O-, 或 R1 表示視情況經一個甲基取代之吡唑基; R2 表示基團, 其中「*」指示與連接R2 之氮原子連接之點; R3 表示選自甲基及-NH2 之基團; R4 表示視情況經取代一次、兩次或三次之苯基或吡啶基,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、C1 -C3 -烷基、((R9 )O)-(C1 -C3 -烷基)-、C1 -C3 -氟烷基、-OR9 、-N(R10 )(R11 )、-C(=O)-N(R12 )(R13 )、S(=O)n -R14 及-C(=O)-OR17 , 或與該苯基或吡啶基之相鄰碳原子連接之兩個取代基一起形成選自以下之二價基團:-(CH2 )3 -、-O-CH2 -O-及-O-CF2 -O-; R5 及R6 在每次出現時獨立地表示氫原子或C1 -C2 -烷基, 或 R5 及R6 連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自以下之基團:羥基及C1 -C2 -烷基; R7 表示氫原子或C1 -C2 -烷基; R8 表示-C(=O)-NH2 基團; R9 表示氫原子或選自以下之基團:C1 -C2 -烷基、苯甲基、C1 -C2 -氟烷基、C2 -羥烷基、(C1 -C2 -烷氧基)-C2 -烷基-、((C1 -C2 -烷基)-C(=O)-O)-C2 -烷基-、-C(R18 )(R19 )-C(=O)-OR17 、-C(R18 )(R19 )-C(=O)-N(R20 )(R21 )、-C(=O)-N(R20 )(R21 )及苯基, 其中該苯甲基內之苯基及該苯基自身視情況經取代一次或兩次,各取代基獨立地選自氟原子及氯原子或選自以下之基團:氰基及甲基; R10 及R11 在每次出現時獨立地表示氫原子或選自以下之基團:C1 -C2 -烷基、C1 -C2 -氟烷基、(C3 -C5 -環烷基)-(C1 -C2 -烷基)- (C1 -C2 -烷基)-C(=O)-、C3 -C7 -環烷基、C3 -C7 -環烷基-(C=O)-、(苯基)-(C1 -C2 -烷基)-、(苯基)-(C1 -C2 -烷基)-C(=O)-及(苯基)-(C1 -C2 -烷基)-O-C(=O)-, 其中C3 -C7 -環烷基、及該(C3 -C5 -環烷基)-(C1 -C2 -烷基)-內之C3 -C5 -環烷基以及C3 -C7 -環烷基-(C=O)-基團內之C3 -C7 -環烷基視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自以下之基團:氰基、C1 -C2 -烷基及C1 -C2 -氟烷基, 且其中該(苯基)-(C1 -C2 -烷基)-基團、該(苯基)-(C1 -C2 -烷基)-C(=O)-基團及該(苯基)-(C1 -C2 -烷基)-O-C(=O)-基團內之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及甲基, 或 R10 及R11 連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自以下之基團:氰基、側氧基、C1 -C2 -烷基、C1 -C2 -氟烷基及(C1 -C2 -烷基)-C(=O)-; R12 及R13 在每次出現時獨立地表示氫原子或選自以下之基團:C1 -C4 -烷基、C1 -C4 -氟烷基、C1 -C4 -羥烷基、(C1 -C4 -烷氧基)-C2 -C3 -烷基-、(C1 -C2 -氟烷氧基)-C2 -C3 -烷基-、(苯氧基)-C2 -C3 -烷基-、C3 -C7 -環烷基、單環4至7員雜環烷基及(苯基)-(C1 -C2 -烷基)-, 其中C3 -C7 -環烷基及單環4至7員雜環烷基視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自以下之基團:側氧基、C1 -C2 -烷基及(C1 -C2 -烷基)-C(=O)-, 且其中該(苯氧基)-C2 -C3 -烷基-基團及該(苯基)-(C1 -C2 -烷基)-基團內之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子及氯原子或選自以下之基團:甲基、三氟甲基及甲氧基, 或 R12 及R13 連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況經取代一次或兩次,各取代基獨立地選自鹵素原子或選自以下之基團:側氧基、C1 -C2 -烷基及(C1 -C2 -烷基)-C(=O)-; R14 表示選自甲基及三氟甲基之基團; R17 表示C1 -C2 -烷基; R18 及R19 在每次出現時獨立地表示氫原子或甲基; R20 表示氫原子或選自以下之基團:視情況經取代C1 -C3 -烷基、未經取代C4 -C6 -烷基、丙-2-炔基、甲氧基、C3 -C6 -環烷基、金剛烷基、單環4至7員雜環烷基、苯基及5至10員雜芳基, 其中該C1 -C3 -烷基視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:羥基、氰基、C1 -C3 -烷氧基、-N(R22 )(R23 )、C3 -C6 -環烷基、金剛烷基、單環4至7員雜環烷基、苯基及5至10員雜芳基,該苯基取代基及該5至10員雜芳基取代基自身視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及甲基, 且其中該C3 -C6 -環烷基、該金剛烷基及該單環4至7員雜環烷基視情況經取代一次或兩次或三次,各取代基獨立地選自氟原子或選自以下之基團:側氧基、C1 -C2 -烷基及(C1 -C2 -烷基)-C(=O)-, 且其中該苯基及該5至10員雜芳基視情況經取代一次、兩次或三次,各取代基獨立地選自氟原子及氯原子或選自以下之基團:氰基、C1 -C2 -烷基、C1 -C2 -氟烷基、C1 -C2 -烷氧基、C1 -C2 -氟烷氧基、-N(R22 )(R23 )及-C(=O)-N(R24 )(R25 ), R21 表示氫原子或C1 -C2 -烷基, 或 R20 及R21 連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況為苯并縮合的且其視情況經取代一次、兩次或三次,各取代基獨立地選自鹵素原子或選自以下之基團:氰基、側氧基、羥基、C1 -C2 -烷基、C1 -C2 -氟烷基、苯甲基、(C1 -C2 -烷基)-C(=O)-、C3 -C4 -環烷基、C1 -C2 -烷氧基、C1 -C2 -氟烷氧基、-N(R22 )(R23 )及-C(=O)-N(R24 )(R25 ); R22 及R23 在每次出現時獨立地表示氫原子或選自C1 -C2 -烷基及(C1 -C2 -烷基)-C(=O)-之基團; R24 及R25 在每次出現時獨立地表示氫原子或C1 -C2 -烷基,及 n 表示整數2, 或其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物或鹽,或其混合物。
- 2或3之化合物,其中: R1 表示視情況經取代一次或兩次之苯基或吡啶基,各取代基獨立地選自氟原子及氯原子或選自以下之基團:氰基、C1 -C2 -烷基、C1 -C2 -氟烷基、C1 -C2 -烷氧基、C1 -C2 -氟烷氧基; R2 表示基團, 其中「*」指示與連接R2 之氮原子連接之點; R3 表示選自甲基及-NH2 之基團; R4 表示視情況經取代一次或兩次之苯基或吡啶基,各取代基獨立地選自氟原子及氯原子或選自以下之基團:C1 -C2 -烷基、C1 -C2 -氟烷基、-OR9 ; R7 表示氫原子或C1 -C2 -烷基; R8 表示-C(=O)-NH2 基團,及 R9 表示選自以下之基團:C1 -C2 -烷基、苯甲基、C1 -C2 -氟烷基、(C1 -C2 -烷氧基)-C2 -烷基-及苯基, 其中該苯甲基內之苯基及該苯基自身視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及甲基; 或其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物或鹽,或其混合物。
- 2或3之化合物,其中: R1 表示視情況經取代一次或兩次苯基或吡啶基,各取代基獨立地選自氟原子、氯原子及溴原子或選自以下之基團:氰基、二氟甲基、三氟甲基、甲氧基、苯甲氧基、二氟甲氧基及三氟甲氧基, 或與該苯基或吡啶基之相鄰碳原子連接之兩個取代基一起形成二價基團-O-CF2 -O-; R2 表示基團, 其中「*」指示與連接R2 之氮原子連接之點; R3 表示選自甲基及-NH2 之基團; R4 表示視情況經取代一次或兩次之苯基或吡啶基,各取代基獨立地選自鹵素原子或選自以下之基團:C1 -C2 -烷基、C1 -C2 -氟烷基、-OR9 , -N(R10 )(R11 )、-C(=O)-N(R12 )(R13 )及-C(=O)-OR17 ; R7 表示氫原子或C1 -C2 -烷基; R8 表示-C(=O)-NH2 基團; R9 表示氫原子或選自以下之基團:C1 -C2 -烷基、苯甲基、C1 -C2 -氟烷基、(C1 -C2 -烷氧基)-C2 -烷基-、((C1 -C2 -烷基)-C(=O)-O)-C2 -烷基-、-C(R18 )(R19 )-C(=O)-N(R20 )(R21 )、-C(=O)-N(R20 )(R21 )及苯基, 其中該苯甲基內之苯基及該苯基自身視情況經取代一次或兩次,各取代基獨立地選自氟原子及氯原子或選自以下之基團:氰基及甲基; R10 及R11 在每次出現時獨立地表示氫原子或選自以下之基團:C1 -C2 -烷基、(C3 -C5 -環烷基)-(C1 -C2 -烷基)-、C3 -C7 -環烷基及(苯基)-(C1 -C2 -烷基)-O-C(=O)-, 其中C3 -C7 -環烷基及該(C3 -C5 -環烷基)-(C1 -C2 -烷基)-基團內之C3 -C5 -環烷基視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自以下之基團:氰基、甲基及C1 -氟烷基, 且其中該(苯基)-(C1 -C2 -烷基)-O-C(=O)-基團內之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及甲基, 或 R10 及R11 連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自以下之基團:氰基、甲基及C1 -氟烷基; R12 及R13 在每次出現時獨立地表示氫原子或選自以下之基團:C1 -C4 -烷基、C1 -C2 -氟烷基、C1 -C2 -羥烷基、(C1 -C4 -烷氧基)-C2 -C3 -烷基-、(C1 -C2 -氟烷氧基)-C2 -C3 -烷基-、(苯氧基)-C2 -C3 -烷基-、C3 -C7 -環烷基及(苯基)-(C1 -C2 -烷基)-, 其中C3 -C7 -環烷基視情況經取代一次或兩次,各取代基獨立地選自氟原子或甲基, 且其中該(苯氧基)-C2 -C3 -烷基-基團及該(苯基)-(C1 -C2 -烷基)-基團內之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子及氯原子或選自以下之基團:甲基、三氟甲基及甲氧基; R17 表示C1 -C2 -烷基; R18 及R19 在每次出現時獨立地表示氫原子或甲基; R20 表示氫原子或選自以下之基團:C1 -C3 -烷基及苯基, 其中該C1 -C3 -烷基視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自羥基、C1 -C3 -烷氧基及苯基之基團,該苯基自身視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及甲基, 且其中該苯基視情況經取代一次、兩次或三次,各取代基獨立地選自氟原子及氯原子或選自以下之基團:甲基、三氟甲基、甲氧基及三氟甲氧基,及 R21 表示氫原子或C1 -C2 -烷基, 或其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物或鹽,或其混合物。
- 2或3之化合物,其中: R1 表示基團, 其中「**」指示與連接R1 之氮原子連接之點; R2 表示基團, 其中「*」指示與連接R2 之氮原子連接之點; R3 表示選自甲基及-NH2 之基團; R4 表示基團 其中「#」指示與連接R4 之羰基連接之點; R7 表示氫原子或C1 -C2 -烷基; R8 表示-C(=O)-NH2 基團; R9 表示氫原子或選自以下之基團:C1 -C2 -烷基、苯甲基、C1 -C2 -氟烷基、(C1 -C2 -烷氧基)-C2 -烷基-、((C1 -C2 -烷基)-C(=O)-O)-C2 -烷基-、-C(R18 )(R19 )-C(=O)-N(R20 )(R21 )、-C(=O)-N(R20 )(R21 )及苯基, 其中該苯甲基內之苯基及該苯基自身視情況經取代一次或兩次,各取代基獨立地選自氟原子及氯原子或選自以下之基團:氰基及甲基; R10 及R11 在每次出現時獨立地表示氫原子或選自以下之基團:C1 -C2 -烷基、C3 -C7 -環烷基及(苯甲基)-O-C(=O)-, 其中C3 -C7 -環烷基視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自以下之基團:甲基及三氟甲基, 且其中該(苯甲基)-O-C(=O)-基團內之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及甲基, 或 R10 及R11 連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自以下之基團:氰基、甲基及三氟甲基; R12 及R13 在每次出現時獨立地表示氫原子或選自以下之基團:C1 -C4 -烷基、C1 -C2 -氟烷基、C1 -C2 -羥烷基、(C1 -C4 -烷氧基)-C2 -烷基-、(C1 -C2 -氟烷氧基)-C2 -烷基-、(苯氧基)-C2 -烷基-、C3 -C7 -環烷基及(苯基)-(C1 -C2 -烷基)-, 其中該(苯氧基)-C2 -烷基-基團及該(苯基)-(C1 -C2 -烷基)-基團內之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子及氯原子或選自以下之基團:甲基、三氟甲基及甲氧基, R17 表示C1 -C2 -烷基; R18 及R19 在每次出現時獨立地表示氫原子或甲基; R20 表示選自苯甲基及苯基之基團, 其中該苯基及該苯甲基內之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及甲基, R21 表示氫原子或甲基, Y1 表示-C(H)=、-C(F)=、-C(Cl)=、-C(CN)=或-N=; Y2 表示-C(H)=或-N=; Y3 表示-C(R27 )=或-N=, 其限制條件為,若Y2 表示-N=,則Y3 表示-C(R27 )=;且若Y3 表示-N=,則Y2 表示-C(H)=; R26 表示氟原子、氯原子或溴原子或選自以下之基團:甲基、二氟甲基、三氟甲基、甲氧基、苯甲氧基、二氟甲氧基及三氟甲氧基,及 R27 表示鹵素原子或選自以下之基團:C1 -C2 -烷基、C1 -C2 -氟烷基、-OR9 、-N(R10 )(R11 )、-C(=O)-N(R12 )(R13 )及-C(=O)-OR17 , 或其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物或鹽,或其混合物。
- 2、3、5或6之化合物,其中: R1 表示基團, 其中「**」指示與連接R1 之氮原子連接之點; R2 表示基團, 其中「*」指示與連接R2 之氮原子連接之點; R3 表示選自甲基及-NH2 之基團; R4 表示基團 其中「#」指示與連接R4 之羰基連接之點; R7 表示氫原子或C1 -C2 -烷基; R8 表示-C(=O)-NH2 基團; R9 表示氫原子或選自以下之基團:C1 -C2 -烷基、苯甲基、C1 -C2 -氟烷基及苯基, 其中該苯甲基內之苯基及該苯基自身視情況經取代一次或兩次,各取代基獨立地選自氟原子及氯原子或選自以下之基團:氰基及甲基; R10 及R11 在每次出現時獨立地表示氫原子或選自以下之基團:C1 -C2 -烷基及(苯甲基)-O-C(=O)-, 且其中該(苯甲基)-O-C(=O)-基團內之苯基視情況經取代一次或兩次,各取代基獨立地選自氟原子、氯原子及甲基, 或 R10 及R11 連同其所連接之氮原子一起表示單環含氮4至7員雜環烷基,其視情況經取代一次或兩次,各取代基獨立地選自氟原子或選自以下之基團:氰基、甲基及三氟甲基; R12 及R13 在每次出現時獨立地表示氫原子或選自以下之基團:C1 -C2 -烷基、(C1 -C4 -烷氧基)-C2 -烷基-、(C1 -C2 -氟烷氧基)-C2 -烷基-、(苯氧基)-C2 -烷基-、C3 -C7 -環烷基及(苯基)-(C1 -C2 -烷基)-; Y1 表示-C(H)=、-C(F)=、-C(Cl)=或-N=; Y2 表示-C(H)=或-N=; Y3 表示-C(R27 )=或-N=, 其限制條件為,若Y2 表示-N=,則Y3 表示-C(R27 )=;且若Y3 表示-N=,則Y2 表示-C(H)=; R26 表示氟原子、氯原子或溴原子或選自以下之基團:二氟甲基、甲氧基、苯甲氧基、二氟甲氧基及三氟甲氧基,及 R27 表示鹵素原子或選自以下之基團:-OR9 、-N(R10 )(R11 )及-C(=O)-N(R12 )(R13 ), 或其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物或鹽,或其混合物。
- 如請求項1之化合物,其選自由以下組成之群: 外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-甲氧基-2-甲基-苯胺基)丙醯胺, 外消旋-2-[N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-(二甲基胺基)苯胺基]丙醯胺, 外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-異丙氧基-苯胺基)丙醯胺, 外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-2,4,6-三氟-苯胺基)丙醯胺, 外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-2-溴-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-(6-甲基吡啶-3-羰基)噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-(2-氟苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-氰基-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-氯-3-(三氟甲基)苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-2-氯-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-(3-氰基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-[N-(4-胺基-5-苯甲醯基-噻唑-2-基)-3-氯-4-(二甲基胺基)苯胺基]丙醯胺, 外消旋-2-(N-[4-胺基-5-(6-甲氧基吡啶-3-羰基)噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-4-[4-胺基-2-(N-[2-胺基-1-甲基-2-側氧基-乙基]-4-氟-苯胺基)噻唑-5-羰基]-N-甲基-苯甲醯胺, 外消旋-2-(N-[4-胺基-5-(3-氟苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-3-氯-4-甲氧基-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-(4-氟苯甲醯基)噻唑-2-基]-4-甲氧基-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-(4-甲磺醯基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-(4-咪唑-1-基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-(4-氰基-3-氟-苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺, (R)-2-(N-[4-胺基-5-(4-氰基-3-氟-苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺, (S)-2-(N-[4-胺基-5-(4-氰基-3-氟-苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-(4-氰基-2-氟-苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-(2-氟-4-甲氧基-苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-[N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-(三氟甲氧基)苯胺基]丙醯胺, 外消旋-2-(N-[4-胺基-5-(3,4-二氟苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-(3,4-二氯苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-[N-[4-胺基-5-(4-氟苯甲醯基)噻唑-2-基]-4-(三氟甲氧基)苯胺基]丙醯胺, (R)-2-[N-[4-胺基-5-(4-氟苯甲醯基)噻唑-2-基]-4-(三氟甲氧基)苯胺基]丙醯胺, (S)-2-[N-[4-胺基-5-(4-氟苯甲醯基)噻唑-2-基]-4-(三氟甲氧基)苯胺基]丙醯胺, 外消旋-2-[N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-(三氟甲基)苯胺基]丙醯胺, 外消旋-2-(N-[4-胺基-5-[6-(三氟甲基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, (R)-2-(N-[4-胺基-5-[6-(三氟甲基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, (S)-2-(N-[4-胺基-5-[6-(三氟甲基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-氯-2-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-(茚烷-5-羰基)噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-3,4-二氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-(4-氰基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺, (R)-2-(N-[4-胺基-5-(4-氰基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺, (S)-2-(N-[4-胺基-5-(4-氰基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-氯-苯胺基)丙醯胺, 外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-3,4-二氯-苯胺基)丙醯胺, 外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-氯-3-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-(4-氟苯甲醯基)噻唑-2-基]-4-氯-苯胺基)丙醯胺, (R)-2-(N-[4-胺基-5-(4-氟苯甲醯基)噻唑-2-基]-4-氯-苯胺基)丙醯胺, (S)-2-(N-[4-胺基-5-(4-氟苯甲醯基)噻唑-2-基]-4-氯-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-(4-氯苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺, (R)-2-(N-[4-胺基-5-(4-氯苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺, (S)-2-(N-[4-胺基-5-(4-氯苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-[4-[4-胺基-2-(N-[2-胺基-1-甲基-2-側氧基-乙基]-4-氟-苯胺基)噻唑-5-羰基]苯氧基]-2-甲基-丙酸乙酯, 外消旋-2-(N-[4-胺基-5-[4-(三氟甲氧基)苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, (R)-2-(N-[4-胺基-5-[4-(三氟甲氧基)苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, (S)-2-(N-[4-胺基-5-[4-(三氟甲氧基)苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-(4-氯苯甲醯基)噻唑-2-基]-4-氯-苯胺基)丙醯胺, (R)-2-(N-[4-胺基-5-(4-氯苯甲醯基)噻唑-2-基]-4-氯-苯胺基)丙醯胺, (S)-2-(N-[4-胺基-5-(4-氯苯甲醯基)噻唑-2-基]-4-氯-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-(三氟甲基)苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-[N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-(三氟甲基)苯胺基]丙醯胺, (R)-2-[N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-(三氟甲基)苯胺基]丙醯胺, (S)-2-[N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-(三氟甲基)苯胺基]丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, (R)-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, (S)-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 2-(N-[4-胺基-5-[4-[2-胺基-1-甲基-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]苯胺基)丙醯胺(立體異構物之混合物), (2R)-(N-[4-胺基-5-[4-[2-胺基-(1R)-甲基-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]苯胺基)丙醯胺, (2R)-(N-[4-胺基-5-[4-[2-胺基-(1S)-甲基-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]苯胺基)丙醯胺, (2S)-(N-[4-胺基-5-[4-[2-胺基-(1R)-甲基-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]苯胺基)丙醯胺, (2S)-(N-[4-胺基-5-[4-[2-胺基-(1S)-甲基-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-氯-2-氟-苯胺基)丙醯胺, (R)-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-氯-2-氟-苯胺基)丙醯胺, (S)-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-氯-2-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-氯-苯胺基)丙醯胺, (R)-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-氯-苯胺基)丙醯胺, (S)-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-氯-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺, (R)-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺, (S)-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺, (R)-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺, (S)-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺, (R)-2-(N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺, (S)-2-(N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺, (R)-2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺, (S)-2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-(6-甲氧基吡啶-3-羰基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺, (R)-2-(N-[4-胺基-5-(6-甲氧基吡啶-3-羰基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺, (S)-2-(N-[4-胺基-5-(6-甲氧基吡啶-3-羰基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[6-(三氟甲基)吡啶-3-羰基]噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺, (R)-2-(N-[4-胺基-5-[6-(三氟甲基)吡啶-3-羰基]噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺, (S)-2-(N-[4-胺基-5-[6-(三氟甲基)吡啶-3-羰基]噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺, 外消旋-2-(N-[5-[4-(二氟甲氧基)苯甲醯基]-4-甲基-噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[5-[4-(二氟甲氧基)苯甲醯基]-4-甲基-噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺, (R)-2-(N-[5-[4-(二氟甲氧基)苯甲醯基]-4-甲基-噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺, (S)-2-(N-[5-[4-(二氟甲氧基)苯甲醯基]-4-甲基-噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺, (R)-2-(N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺, (S)-2-(N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-4-氯-苯胺基)丙醯胺, (R)-2-(N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-4-氯-苯胺基)丙醯胺, (S)-2-(N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-4-氯-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-4-氯-苯胺基)丙醯胺, (R)-2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-4-氯-苯胺基)丙醯胺, (S)-2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-4-氯-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺, (R)-2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺, (S)-2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺 外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)苯胺基)丙醯胺, 外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-氟-苯胺基)丙醯胺, (R)-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-氟-苯胺基)丙醯胺, (S)-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺, (R)-2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺, (S)-2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-(4-甲基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺, (R)-2-(N-[4-胺基-5-(4-甲基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺, (S)-2-(N-[4-胺基-5-(4-甲基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-(4-氟苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-2,4-二氟-苯胺基)丙醯胺, 外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-甲氧基-苯胺基)丙醯胺, 外消旋-2-[(4-胺基-5-苯甲醯基-1,3-噻唑-2-基)(苯基)胺基]丁醯胺, 外消旋-2-[(4-胺基-5-苯甲醯基-1,3-噻唑-2-基)(4-氟苯基)胺基]丁醯胺, 2-(N-[4-胺基-5-[4-(2-胺基-1-甲基-2-側氧基-乙氧基)苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺(立體異構物之混合物), 外消旋-2-{[4-胺基-5-(4-甲氧基苯甲醯基)-1,3-噻唑-2-基](4-氟苯基)胺基}丁醯胺, 2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-氟-苯胺基)乙醯胺, 2-(N-[4-胺基-5-(4-甲基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)乙醯胺, 外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-甲基-苯胺基)丙醯胺, (R)-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-甲基-苯胺基)丙醯胺, (S)-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-甲基-苯胺基)丙醯胺, 外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-3-氟-苯胺基)丙醯胺, (R)-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-3-氟-苯胺基)丙醯胺, (S)-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-3-氟-苯胺基)丙醯胺, 外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-2-氟-苯胺基)丙醯胺, (R)-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-2-氟-苯胺基)丙醯胺, (S)-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-2-氟-苯胺基)丙醯胺, 外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-3-甲基-苯胺基)丙醯胺, (R)-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-3-甲基-苯胺基)丙醯胺, (S)-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-3-甲基-苯胺基)丙醯胺, 外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-2-甲基-苯胺基)丙醯胺, (R)-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-2-甲基-苯胺基)丙醯胺, (S)-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-2-甲基-苯胺基)丙醯胺, 外消旋-2-[(4-胺基-5-苯甲醯基-噻唑-2-基)-(1-甲基吡唑-4-基)胺基]丙醯胺, (R)-2-[(4-胺基-5-苯甲醯基-噻唑-2-基)-(1-甲基吡唑-4-基)胺基]丙醯胺, (S)-2-[(4-胺基-5-苯甲醯基-噻唑-2-基)-(1-甲基吡唑-4-基)胺基]丙醯胺, 外消旋-2-[(4-胺基-5-苯甲醯基-噻唑-2-基)-(3-吡啶基)胺基]丙醯胺, (R)-2-[(4-胺基-5-苯甲醯基-噻唑-2-基)-(3-吡啶基)胺基]丙醯胺, (S)-2-[(4-胺基-5-苯甲醯基-噻唑-2-基)-(3-吡啶基)胺基]丙醯胺, 外消旋-2-(N-[4-胺基-5-(4-溴苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-[4-[4-胺基-2-(4-氟-N-[2-胺基-1-甲基-2-側氧基-乙基]苯胺基)噻唑-5-羰基]苯氧基]乙酸乙酯, (R)-2-[4-[4-胺基-2-(4-氟-N-[2-胺基-1-甲基-2-側氧基-乙基]苯胺基)噻唑-5-羰基]苯氧基]乙酸乙酯, (S)-2-[4-[4-胺基-2-(4-氟-N-[2-胺基-1-甲基-2-側氧基-乙基]苯胺基)噻唑-5-羰基]苯氧基]乙酸乙酯, 外消旋-2-(N-[4-胺基-5-[4-[2-(異丙基胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-[2-(間甲苯基甲基胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-[2-(鄰甲苯基甲基胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-[2-[(3-氯苯基)甲基胺基]-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-[2-(4-甲基哌𠯤-1-基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-[2-(3-甲基苯胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-(2-(N-𠰌啉基)-2-側氧基-乙氧基)苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-[2-側氧基-2-[2-(1-哌啶基)乙基胺基]乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-[2-(4-苯甲基-1-哌啶基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-[2-(2-甲氧基乙基胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-[2-(4-氰基苯胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-[2-[甲基(丙-2-炔基)胺基]-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-[2-[(2-甲氧基苯基)甲基胺基]-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-[2-[(3-甲氧基苯基)甲基胺基]-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-[2-[(2-氟苯基)甲基胺基]-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-[2-[(4-氟苯基)甲基胺基]-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-[2-(1H-苯并咪唑-2-基甲基胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-[2-側氧基-2-(2,2,2-三氟乙基胺基)乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-[2-[甲基(2-吡啶基)胺基]-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-[2-[甲基-(1-甲基-4-哌啶基)胺基]-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-[2-(甲氧基胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-[2-[(5-甲基異㗁唑-3-基)胺基]-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-[2-(乙基胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-[2-(4-甲基苯胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-[2-(環己基胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-3-[[2-[4-[4-胺基-2-(N-[2-胺基-1-甲基-2-側氧基-乙基]-4-氟-苯胺基)噻唑-5-羰基]苯氧基]乙醯基]胺基]苯甲醯胺, 外消旋-2-(N-[4-胺基-5-[4-[2-側氧基-2-(6-喹啉基胺基)乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-4-[[2-[4-[4-胺基-2-(N-[2-胺基-1-甲基-2-側氧基-乙基]-4-氟-苯胺基)噻唑-5-羰基]苯氧基]乙醯基]胺基]苯甲醯胺, (2S)-1-[2-[4-[4-胺基-2-(N-[2-胺基-(1RS)-甲基-2-側氧基-乙基]-4-氟-苯胺基)噻唑-5-羰基]苯氧基]乙醯基]吡咯啶-2-甲醯胺(兩種非鏡像異構物之混合物), 外消旋-2-(N-[4-胺基-5-[4-[2-[乙基(甲基)胺基]-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-[2-[(3-甲基異㗁唑-5-基)胺基]-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-[2-[3-(二甲基胺基)丙基-甲基-胺基]-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[5-[4-[2-(4-乙醯基哌𠯤-1-基)-2-側氧基-乙氧基]苯甲醯基]-4-胺基-噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-[2-側氧基-2-(3-吡啶基甲基胺基)乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 2-(N-[4-胺基-5-[4-[2-(2,3-二羥基丙基胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺(立體異構物之混合物), 外消旋-2-(N-[4-胺基-5-[4-[2-(4-甲氧基苯胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-[2-[苯甲基(甲基)胺基]-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-[2-(4-氯苯胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-[2-[(2-氯苯基)甲基胺基]-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-[2-[(4-氯苯基)甲基胺基]-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-[2-(4-氟苯胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-[2-(氮𠰢-1-基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-[2-[(4-甲氧基苯基)甲基胺基]-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 2-(N-[4-胺基-5-[4-[2-側氧基-2-(1-苯基乙基胺基)乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺(立體異構物之混合物), 外消旋-2-(N-[4-胺基-5-[4-[2-側氧基-2-(對甲苯基甲基胺基)乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-[2-[甲基(2-苯基乙基)胺基]-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 2-(N-[4-胺基-5-[4-[2-(3-甲基-1-哌啶基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺(立體異構物之混合物), 外消旋-2-(N-[4-胺基-5-[4-[2-(4-甲基-1-哌啶基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[5-[4-[2-(4-乙醯胺基苯胺基)-2-側氧基-乙氧基]苯甲醯基]-4-胺基-噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-[2-側氧基-2-(1H-吡唑并[3,4-d]嘧啶-4-基胺基)乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-[2-(環戊基胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-[2-(3,4-二氫-1H-異喹啉-2-基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-(2-異吲哚啉-2-基-2-側氧基-乙氧基)苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-[2-[2-呋喃基甲基(甲基)胺基]-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-[2-[4-(二甲基胺基)-1-哌啶基]-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-[2-[甲基(3-吡啶基甲基)胺基]-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-[2-(N,2-二甲基苯胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-[2-(N,4-二甲基苯胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-[2-(N,3-二甲基苯胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-[2-(2,2-二甲基丙基胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 2-(N-[5-[4-[2-(1-金剛烷基胺基)-2-側氧基-乙氧基]苯甲醯基]-4-胺基-噻唑-2-基]-4-氟-苯胺基)丙醯胺(單一立體異構物), 2-(N-[5-[4-[2-(1-金剛烷基甲基胺基)-2-側氧基-乙氧基]苯甲醯基]-4-胺基-噻唑-2-基]-4-氟-苯胺基)丙醯胺(單一立體異構物), 2-(N-[5-[4-[2-[2-(1-金剛烷基)乙基胺基]-2-側氧基-乙氧基]苯甲醯基]-4-胺基-噻唑-2-基]-4-氟-苯胺基)丙醯胺(單一立體異構物), 2-(N-[4-胺基-5-[4-[2-(4-氯苯胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺(單一立體異構物), 4-[[2-[4-[4-胺基-2-(4-氟-N-[2-胺基-1-甲基-2-側氧基-乙基]苯胺基)噻唑-5-羰基]苯氧基]乙醯基]胺基]苯甲醯胺(單一立體異構物), 2-(N-[4-胺基-5-[4-[2-((2RS),3-二羥基丙基胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺(兩種非鏡像異構物之混合物), 2-(N-[4-胺基-5-[4-[2-側氧基-2-[2-(1-哌啶基)乙基胺基]乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺(單一立體異構物), 2-(N-[4-胺基-5-[4-(2-胺基-2-側氧基-乙氧基)苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺(單一立體異構物), (R)-2-(N-[4-胺基-5-[4-[2-(甲基胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, (S)-2-(N-[4-胺基-5-[4-[2-(甲基胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, (R)-2-(N-[4-胺基-5-[4-[2-(異丙基胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, (S)-2-(N-[4-胺基-5-[4-[2-(異丙基胺基)-2-側氧基-乙氧基]苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-[4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氟-苯胺基)噻唑-5-羰基]苯氧基]-N-異丙基-2-甲基-丙醯胺, 外消旋-2-[4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氟-苯胺基)噻唑-5-羰基]苯氧基]-2-甲基-丙醯胺, 外消旋-2-(N-(5-苯甲醯基-4-甲基-噻唑-2-基)-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-(4-羥基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-(4-苯甲氧基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[6-(二氟甲基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-3-氯-4-氟-苯胺基)丙醯胺, (R)- 2-(N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-3-氯-4-氟-苯胺基)丙醯胺, (S)- 2-(N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-3-氯-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-3-氯-4-氟-苯胺基)丙醯胺, (R)- 2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-3-氯-4-氟-苯胺基)丙醯胺, (S)- 2-(N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-3-氯-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[6-(二氟甲氧基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, (R)-2-(N-[4-胺基-5-[6-(二氟甲氧基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, (S)-2-(N-[4-胺基-5-[6-(二氟甲氧基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[6-(二氟甲氧基)吡啶-3-羰基]噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺, (R)-(N-[4-胺基-5-[6-(二氟甲氧基)吡啶-3-羰基]噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺, (S)-(N-[4-胺基-5-[6-(二氟甲氧基)吡啶-3-羰基]噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[6-(二氟甲氧基)吡啶-3-羰基]噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺, (R)-2-(N-[4-胺基-5-[6-(二氟甲氧基)吡啶-3-羰基]噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺, (S)-2-(N-[4-胺基-5-[6-(二氟甲氧基)吡啶-3-羰基]噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-(4-苯甲氧基苯甲醯基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺, (R)-2-(N-[4-胺基-5-(4-苯甲氧基苯甲醯基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺, (S)-2-(N-[4-胺基-5-(4-苯甲氧基苯甲醯基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-(4-苯甲氧基苯甲醯基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺, (R)-2-(N-[4-胺基-5-(4-苯甲氧基苯甲醯基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺, (S)-2-(N-[4-胺基-5-(4-苯甲氧基苯甲醯基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺, 外消旋- N-[4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-3,4-二氟-苯胺基)噻唑-5-羰基]苯基]胺基甲酸苯甲酯, (R)-N-[4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-3,4-二氟-苯胺基)噻唑-5-羰基]苯基]胺基甲酸苯甲酯, (S)-N-[4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-3,4-二氟-苯胺基)噻唑-5-羰基]苯基]胺基甲酸苯甲酯, 外消旋-2-[4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氟-苯胺基)噻唑-5-羰基]苯氧基]乙酸乙酯, 外消旋-N-[4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氟-苯胺基)噻唑-5-羰基]苯基]胺基甲酸苯甲酯, (R)-N-[4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氟-苯胺基)噻唑-5-羰基]苯基]胺基甲酸苯甲酯, (S)-N-[4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氟-苯胺基)噻唑-5-羰基]苯基]胺基甲酸苯甲酯, 外消旋-2-(N-[4-胺基-5-(4-苯甲氧基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺, (R)-2-(N-[4-胺基-5-(4-苯甲氧基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺, (S)-2-(N-[4-胺基-5-(4-苯甲氧基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-(4-碘苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-(6-甲氧基吡啶-3-羰基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺, (R)-2-(N-[4-胺基-5-(6-甲氧基吡啶-3-羰基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺, (S)-2-(N-[4-胺基-5-(6-甲氧基吡啶-3-羰基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-(4-苯氧基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-甲氧基-苯胺基)丙醯胺, (R)-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-甲氧基-苯胺基)丙醯胺, (S)-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-甲氧基-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-(4-硝基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(4-氟-N-[5-(4-甲氧基苯甲醯基)-4-甲基-噻唑-2-基]苯胺基)丙醯胺, (R)-2-(4-氟-N-[5-(4-甲氧基苯甲醯基)-4-甲基-噻唑-2-基]苯胺基)丙醯胺, (S)-2-(4-氟-N-[5-(4-甲氧基苯甲醯基)-4-甲基-噻唑-2-基]苯胺基)丙醯胺, 外消旋-4-[4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氟-苯胺基)噻唑-5-羰基]苯基]環丙烷甲醯胺, 外消旋-2-(N-[4-胺基-5-(4-(N-𠰌啉基)苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-(吡唑-1-基甲基)苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-(二甲基胺基)苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-(4-吡咯啶-1-基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-苯甲氧基-苯胺基)丙醯胺, (R)-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-苯甲氧基-苯胺基)丙醯胺, (S)-2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-苯甲氧基-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[3-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-(吡啶-3-羰基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺, (R)-2-(N-[4-胺基-5-(吡啶-3-羰基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺, (S)-2-(N-[4-胺基-5-(吡啶-3-羰基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺, 外消旋-2-(N-[5-(4-乙醯胺基苯甲醯基)-4-胺基-噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-(2-氯吡啶-4-羰基)噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-(2-甲基吡啶-4-羰基)噻唑-2-基]-4-氟-苯胺基)丙醯胺, (R)-2-(N-[4-胺基-5-(2-甲基吡啶-4-羰基)噻唑-2-基]-4-氟-苯胺基)丙醯胺, (S)-2-(N-[4-胺基-5-(2-甲基吡啶-4-羰基)噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[2-(二氟甲基)吡啶-4-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-[(4-胺基-5-苯甲醯基-噻唑-2-基)-(4-吡啶基)胺基]丙醯胺, 外消旋-2-(N-[4-胺基-5-(2-甲氧基吡啶-4-羰基)噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-3-氟-4-甲氧基-苯胺基)丙醯胺, 外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-氰基-3-氟-苯胺基)丙醯胺, 外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-溴-苯胺基)丙醯胺, 外消旋-2-[N-(4-胺基-5-苯甲醯基-噻唑-2-基)-3-氯-4-(二氟甲氧基)苯胺基]丙醯胺, 外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-乙氧基-苯胺基)丙醯胺, 外消旋-2-[(4-胺基-5-苯甲醯基-噻唑-2-基)-(1,3-苯并間二氧雜環戊烯-5-基)胺基]丙醯胺, 外消旋-2-[(4-胺基-5-苯甲醯基-噻唑-2-基)-(2,2-二氟-1,3-苯并間二氧雜環戊烯-5-基)胺基]丙醯胺, 外消旋-2-[N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-(二氟甲氧基)-3-氟-苯胺基]丙醯胺, 外消旋-2-(N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-苯甲氧基-苯胺基)丙醯胺, 外消旋-2-[N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-3-氯-4-(二氟甲氧基)苯胺基]丙醯胺, 外消旋-2-[N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-3-氯-4-(二氟甲氧基)苯胺基]丙醯胺, 外消旋-2-[N-[4-胺基-5-(4-氯苯甲醯基)噻唑-2-基]-3-氯-4-(二氟甲氧基)苯胺基]丙醯胺, 外消旋-2-[N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-3-氯-4-(二氟甲氧基)苯胺基]丙醯胺, 外消旋-2-[N-[4-胺基-5-[6-(二氟甲氧基)吡啶-3-羰基]噻唑-2-基]-3-氯-4-(二氟甲氧基)苯胺基]丙醯胺, 外消旋-2-[N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-4-(二氟甲氧基)-3-氟-苯胺基]丙醯胺, 外消旋-2-[N-[4-胺基-5-(4-氯苯甲醯基)噻唑-2-基]-4-(二氟甲氧基)-3-氟-苯胺基]丙醯胺, 外消旋-2-[N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-(二氟甲氧基)-3-氟-苯胺基]丙醯胺, 外消旋-2-[N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-4-(二氟甲氧基)-3-氟-苯胺基]丙醯胺, 外消旋-2-[N-[4-胺基-5-[6-(二氟甲氧基)吡啶-3-羰基]噻唑-2-基]-4-(二氟甲氧基)-3-氟-苯胺基]丙醯胺, 外消旋-2-[N-(4-胺基-5-苯甲醯基-噻唑-2-基)-3-氯-4-(三氟甲氧基)苯胺基]丙醯胺, 外消旋-2-[[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-(2,2-二氟-1,3-苯并間二氧雜環戊烯-5-基)胺基]丙醯胺, 外消旋-2-[[4-胺基-5-(4-氯苯甲醯基)噻唑-2-基]-(2,2-二氟-1,3-苯并間二氧雜環戊烯-5-基)胺基]丙醯胺, 外消旋-2-[[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-(2,2-二氟-1,3-苯并間二氧雜環戊烯-5-基)胺基]丙醯胺, 外消旋-2-[[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-(2,2-二氟-1,3-苯并間二氧雜環戊烯-5-基)胺基]丙醯胺, 外消旋-2-[[4-胺基-5-[6-(二氟甲氧基)吡啶-3-羰基]噻唑-2-基]-(2,2-二氟-1,3-苯并間二氧雜環戊烯-5-基)胺基]丙醯胺, 外消旋-2-[N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-3-氟-4-(三氟甲氧基)苯胺基]丙醯胺, 外消旋-2-[N-[4-胺基-5-(4-氯苯甲醯基)噻唑-2-基]-3-氟-4-(三氟甲氧基)苯胺基]丙醯胺, 外消旋-2-[N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-3-氟-4-(三氟甲氧基)苯胺基]丙醯胺, 外消旋-2-[N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-3-氟-4-(三氟甲氧基)苯胺基]丙醯胺, 外消旋-2-[N-[4-胺基-5-[6-(二氟甲氧基)吡啶-3-羰基]噻唑-2-基]-3-氟-4-(三氟甲氧基)苯胺基]丙醯胺, 外消旋-2-[N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-3-氯-4-(三氟甲氧基)苯胺基]丙醯胺, 外消旋-2-[N-[4-胺基-5-(4-氯苯甲醯基)噻唑-2-基]-3-氯-4-(三氟甲氧基)苯胺基]丙醯胺, 外消旋-2-[N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-3-氯-4-(三氟甲氧基)苯胺基]丙醯胺, 外消旋-2-[N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-3-氯-4-(三氟甲氧基)苯胺基]丙醯胺, 外消旋-2-[N-[4-胺基-5-[6-(二氟甲氧基)吡啶-3-羰基]噻唑-2-基]-3-氯-4-(三氟甲氧基)苯胺基]丙醯胺, 外消旋-2-[(4-胺基-5-苯甲醯基-噻唑-2-基)-(6-甲氧基-3-吡啶基)胺基]丙醯胺, 外消旋-2-[(4-胺基-5-苯甲醯基-噻唑-2-基)-[6-(三氟甲氧基)-3-吡啶基]胺基]丙醯胺, 外消旋-2-[(4-胺基-5-苯甲醯基-噻唑-2-基)-[6-(二氟甲氧基)-3-吡啶基]胺基]丙醯胺, 外消旋-2-[(4-胺基-5-苯甲醯基-噻唑-2-基)-[6-(三氟甲基)-3-吡啶基]胺基]丙醯胺, 外消旋-2-[(4-胺基-5-苯甲醯基-噻唑-2-基)-[6-(二氟甲基)-3-吡啶基]胺基]丙醯胺, 外消旋-2-[(4-胺基-5-苯甲醯基-噻唑-2-基)-(6-氯-3-吡啶基)胺基]丙醯胺, 外消旋-2-[(4-胺基-5-苯甲醯基-噻唑-2-基)-(6-氟-3-吡啶基)胺基]丙醯胺, 外消旋-2-[(4-胺基-5-苯甲醯基-噻唑-2-基)-(6-甲基-3-吡啶基)胺基]丙醯胺, 外消旋-2-[N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-氟-3-(三氟甲氧基)苯胺基]丙醯胺, 外消旋-2-[N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-氯-3-(三氟甲氧基)苯胺基]丙醯胺, 外消旋-2-[N-(4-胺基-5-苯甲醯基-噻唑-2-基)-3-(二氟甲氧基)-4-氟-苯胺基]丙醯胺, 外消旋-2-[N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-氯-3-(二氟甲氧基)苯胺基]丙醯胺, 外消旋-2-[N-(4-胺基-5-苯甲醯基-噻唑-2-基)-2-氟-4-(三氟甲氧基)苯胺基]丙醯胺, 外消旋-2-[N-(4-胺基-5-苯甲醯基-噻唑-2-基)-2-氯-4-(三氟甲氧基)苯胺基]丙醯胺, 外消旋-2-[N-(4-胺基-5-苯甲醯基-噻唑-2-基)-4-(二氟甲氧基)-2-氟-苯胺基]丙醯胺, 外消旋-2-[N-(4-胺基-5-苯甲醯基-噻唑-2-基)-2-氯-4-(二氟甲氧基)苯胺基]丙醯胺, 外消旋-2-[N-[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-4-(二氟甲基)苯胺基]丙醯胺, 外消旋-2-[N-[4-胺基-5-(4-氯苯甲醯基)噻唑-2-基]-4-(二氟甲基)苯胺基]丙醯胺, 外消旋-2-[N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-(二氟甲基)苯胺基]丙醯胺, 外消旋-2-[N-[4-胺基-5-(吡啶-4-羰基)噻唑-2-基]-4-(二氟甲基)苯胺基]丙醯胺, 外消旋-2-[N-[4-胺基-5-[6-(二氟甲氧基)吡啶-3-羰基]噻唑-2-基]-4-(二氟甲基)苯胺基]丙醯胺, 外消旋-2-[[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-[6-(三氟甲氧基)-3-吡啶基]胺基]丙醯胺, 外消旋-2-[[4-胺基-5-(4-氯苯甲醯基)噻唑-2-基]-[6-(三氟甲氧基)-3-吡啶基]胺基]丙醯胺, 外消旋-2-[[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-[6-(三氟甲氧基)-3-吡啶基]胺基]丙醯胺, 外消旋-2-[[4-胺基-5-[6-(二氟甲氧基)吡啶-3-羰基]噻唑-2-基]-[6-(三氟甲氧基)-3-吡啶基]胺基]丙醯胺, 外消旋-2-[[4-胺基-5-(4-甲氧基苯甲醯基)噻唑-2-基]-[6-(二氟甲氧基)-3-吡啶基]胺基]丙醯胺, 外消旋-2-[[4-胺基-5-(4-氯苯甲醯基)噻唑-2-基]-[6-(二氟甲氧基)-3-吡啶基]胺基]丙醯胺, 外消旋-2-[[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-[6-(二氟甲氧基)-3-吡啶基]胺基]丙醯胺, 外消旋-2-[[4-胺基-5-[6-(二氟甲氧基)吡啶-3-羰基]噻唑-2-基]-[6-(二氟甲氧基)-3-吡啶基]胺基]丙醯胺, 外消旋-N-[5-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氟-苯胺基)噻唑-5-羰基]-2-吡啶基]胺基甲酸苯甲酯, 外消旋-4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氟-苯胺基)噻唑-5-羰基]苯甲酸乙酯, 外消旋-4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氯-3-氟-苯胺基)噻唑-5-羰基]苯甲酸乙酯, 外消旋-2-[4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氟-苯胺基)噻唑-5-羰基]苯氧基]-2-甲基-丙酸乙酯, 外消旋-4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氟-苯胺基)噻唑-5-羰基]-N-環己基-苯甲醯胺, 外消旋-4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氟-苯胺基)噻唑-5-羰基]-N-異丙基-苯甲醯胺, 外消旋-4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氟-苯胺基)噻唑-5-羰基]-N-苯甲基-苯甲醯胺, 4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氟-苯胺基)噻唑-5-羰基]-N-[(2S)-2-羥基丙基]苯甲醯胺(立體異構物之混合物), 外消旋-4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氟-苯胺基)噻唑-5-羰基]-N-(2-甲氧基乙基)苯甲醯胺, 4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氟-苯胺基)噻唑-5-羰基]-N-[(2R)-2-羥基丙基]苯甲醯胺(立體異構物之混合物), 外消旋-4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氟-苯胺基)噻唑-5-羰基]-N-環丙基-苯甲醯胺, 外消旋-4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氟-苯胺基)噻唑-5-羰基]-N-環戊基-苯甲醯胺, 外消旋-4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氯-3-氟-苯胺基)噻唑-5-羰基]-N-(2-苯氧基乙基)苯甲醯胺, 外消旋-4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氯-3-氟-苯胺基)噻唑-5-羰基]-N-[2-(三氟甲氧基)乙基]苯甲醯胺, 外消旋-4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氯-3-氟-苯胺基)噻唑-5-羰基]-N-[2-(二氟甲氧基)乙基]苯甲醯胺, 外消旋-4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氯-3-氟-苯胺基)噻唑-5-羰基]-N-(2-三級丁氧基乙基)苯甲醯胺, 外消旋-4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氯-3-氟-苯胺基)噻唑-5-羰基]-N-(2-甲氧基乙基)苯甲醯胺, 外消旋-2-[4-[4-胺基-2-(N-(2-胺基-1-甲基-2-側氧基-乙基)-4-氟-苯胺基)噻唑-5-羰基]苯氧基]-N-[(4-氯苯基)甲基]-2-甲基-丙醯胺, 外消旋-2-(N-[4-胺基-5-(6-溴吡啶-3-羰基)噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[6-[4-(三氟甲基)-1-哌啶基]吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[6-(4-甲基-1-哌啶基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[6-[4-(氧環丁-3-基)-1-哌啶基]吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[6-(二甲基胺基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[6-(4,4-二甲基-1-哌啶基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[6-(3-氮雜雙環[3.2.1]辛-3-基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[6-(3,5-二甲基-1-哌啶基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[6-(3-氮雜雙環[3.1.0]己-3-基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[6-(1-哌啶基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[6-(4,4-二氟-1-哌啶基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 外消旋-2-(N-[4-胺基-5-[6-(4-氰基-4-甲基-1-哌啶基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, (R)-2-(N-[4-胺基-5-[6-(4-氰基-4-甲基-1-哌啶基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, (S)-2-(N-[4-胺基-5-[6-(4-氰基-4-甲基-1-哌啶基)吡啶-3-羰基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 2-(N-[4-胺基-5-(4-羥基苯甲醯基)噻唑-2-基]-4-氟-苯胺基)丙醯胺(單一鏡像異構物), (R)-2-(N-[4-胺基-5-(4-羥基苯甲醯基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺, (S)-2-(N-[4-胺基-5-(4-羥基苯甲醯基)噻唑-2-基]-3,4-二氟-苯胺基)丙醯胺, 2-(N-[4-胺基-5-(4-羥基苯甲醯基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺(鏡像異構物1), 2-(N-[4-胺基-5-(4-羥基苯甲醯基)噻唑-2-基]-4-氯-3-氟-苯胺基)丙醯胺(鏡像異構物2), 2-(N-[4-胺基-5-[4-(二氟甲氧基)苯甲醯基]噻唑-2-基]-4-羥基-苯胺基)丙醯胺(單一鏡像異構物),及 外消旋-2-(N-[4-胺基-5-[4-(2-羥基乙氧基)苯甲醯基]噻唑-2-基]-4-氟-苯胺基)丙醯胺, 或其立體異構物、互變異構物、N-氧化物、水合物、溶劑合物或鹽,或其混合物。
- 如請求項1至8中任一項之通式(I)化合物,其用於治療或預防疾病。
- 一種醫藥組合物,其包含如請求項1至8中任一項之通式(I)化合物及一或多種醫藥學上可接受之賦形劑。
- 一種醫藥組合,其包含: 一或多種第一活性成分,特定言之,如請求項1至8中任一項之通式(I)化合物,及 一或多種其他活性成分,特定言之,免疫檢查點抑制劑。
- 如請求項11之醫藥組合,其中該免疫檢查點抑制劑為aPD-1/-L1軸拮抗劑。
- 如請求項11之醫藥組合,其中該免疫檢查點抑制劑為DGKα之抑制劑。
- 一種如請求項1至8中任一項之通式(I)化合物之用途,其用於治療或預防疾病。
- 一種如請求項1至8中任一項之通式(I)化合物之用途,其用於製備用於治療或預防疾病之藥物。
- 如請求項14或15之用途,其中該疾病為癌症或具有失調免疫反應之病狀或與異常DGKζ信號傳導相關之病症,舉例而言,諸如液體及實體腫瘤。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP20171280 | 2020-04-24 | ||
| EP20171280.9 | 2020-04-24 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| TW202200552A true TW202200552A (zh) | 2022-01-01 |
Family
ID=70464845
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| TW110114675A TW202200552A (zh) | 2020-04-24 | 2021-04-23 | 作為用於免疫活化之DGKζ抑制劑之經取代胺基噻唑 |
Country Status (19)
| Country | Link |
|---|---|
| US (3) | US20230167078A1 (zh) |
| EP (2) | EP4139287A1 (zh) |
| JP (2) | JP2023522251A (zh) |
| KR (1) | KR20230005247A (zh) |
| CN (2) | CN115697979A (zh) |
| AR (1) | AR121929A1 (zh) |
| AU (1) | AU2021261524A1 (zh) |
| BR (1) | BR112022019057A2 (zh) |
| CA (2) | CA3180670A1 (zh) |
| CL (1) | CL2022002919A1 (zh) |
| CO (1) | CO2022014876A2 (zh) |
| CR (1) | CR20220536A (zh) |
| DO (1) | DOP2022000223A (zh) |
| EC (1) | ECSP22080829A (zh) |
| IL (1) | IL297499A (zh) |
| MX (1) | MX2022013388A (zh) |
| PE (1) | PE20230322A1 (zh) |
| TW (1) | TW202200552A (zh) |
| WO (2) | WO2021214019A1 (zh) |
Families Citing this family (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN117736207A (zh) | 2019-12-24 | 2024-03-22 | 卡尔那生物科学株式会社 | 二酰基甘油激酶调节化合物 |
| EP4139287A1 (en) | 2020-04-24 | 2023-03-01 | Bayer Aktiengesellschaft | Substituted aminothiazoles as dgkzeta inhibitors for immune activation |
| KR20230116838A (ko) | 2020-11-30 | 2023-08-04 | 아스테라스 세이야쿠 가부시키가이샤 | 헤테로아릴카르복시아미드 화합물 |
| CN117396478A (zh) | 2021-06-23 | 2024-01-12 | 吉利德科学公司 | 二酰基甘油激酶调节化合物 |
| EP4359411A1 (en) | 2021-06-23 | 2024-05-01 | Gilead Sciences, Inc. | Diacylglyercol kinase modulating compounds |
| US11932634B2 (en) | 2021-06-23 | 2024-03-19 | Gilead Sciences, Inc. | Diacylglycerol kinase modulating compounds |
| EP4359415A1 (en) | 2021-06-23 | 2024-05-01 | Gilead Sciences, Inc. | Diacylglyercol kinase modulating compounds |
| WO2024036100A1 (en) * | 2022-08-08 | 2024-02-15 | Bristol-Myers Squibb Company | Substituted tetrazolyl compounds useful as t cell activators |
| WO2024165469A1 (en) | 2023-02-06 | 2024-08-15 | Bayer Aktiengesellschaft | Combinations of dgk (diacylglycerol kinase) inhibitors and immune checkpoint inhibitors and modulators |
| WO2024200410A1 (en) | 2023-03-31 | 2024-10-03 | Bayer Aktiengesellschaft | Microcrystalline forms of (r)-2-(n-[4-amino-5-(4-methoxybenzoyl)thiazol-2-yl]-4-fluoroanilino)propanamide and processes for their preparation |
| WO2024208198A1 (zh) * | 2023-04-06 | 2024-10-10 | 微境生物医药科技(上海)有限公司 | 作为DGKζ抑制剂的噻唑类化合物 |
Family Cites Families (40)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP1539722A1 (en) | 2002-08-07 | 2005-06-15 | F. Hoffmann-La Roche Ag | Thiazole derivatives |
| US20050137239A1 (en) | 2003-12-17 | 2005-06-23 | Hines Michelle D. | Thiazole derivatives |
| WO2005102325A1 (en) | 2004-04-20 | 2005-11-03 | Ab Science | Use of c-kit inhibitors for treating inflammatory muscle disorders including myositis and muscular dystrophy |
| WO2005102318A1 (en) | 2004-04-20 | 2005-11-03 | Ab Science | Use of c-kit inhibitors for treating hiv related diseases |
| CN1946703A (zh) | 2004-04-20 | 2007-04-11 | 特兰斯泰克制药公司 | 取代的噻唑和嘧啶衍生物作为黑素细胞皮质激素受体调节剂 |
| JP2007533732A (ja) | 2004-04-23 | 2007-11-22 | アブ サイエンス | 線維症を処置するためのc−kit阻害剤の使用法 |
| WO2005102326A2 (en) | 2004-04-23 | 2005-11-03 | Ab Science | Use of c-kit inhibitors for treating renal diseases |
| US20080004279A1 (en) | 2004-04-23 | 2008-01-03 | Alain Moussy | Use of C-Kit Inhibitors for Treating Plasmodium Related Diseases |
| WO2006078287A2 (en) | 2004-05-06 | 2006-07-27 | Plexxikon, Inc. | Pde4b inhibitors and uses therefor |
| CA2566104A1 (en) | 2004-05-18 | 2005-12-01 | Ab Science | Use of mast cells inhibitors for treating patients exposed to chemical or biological weapons |
| WO2005115304A2 (en) | 2004-05-24 | 2005-12-08 | Ab Science | Use of c-kit inhibitors for treating fibrodysplasia |
| WO2005115385A1 (en) | 2004-05-24 | 2005-12-08 | Ab Science | Use of c-kit inhibitors for treating acne |
| KR20080019213A (ko) | 2005-05-09 | 2008-03-03 | 아칠리온 파르마세우티칼스 인코포레이티드 | 티아졸 화합물 및 그 사용방법 |
| BRPI0611187A2 (pt) | 2005-06-03 | 2010-08-24 | Xenon Pharmaceuticals Inc | derivados aminotiazàis como inibidores da estearoil-coa desaturase humana |
| WO2007022415A2 (en) | 2005-08-18 | 2007-02-22 | Pharmacopeia, Inc. | Substituted 2-aminothiazoles for treating neurodegenerative diseases |
| GB0701426D0 (en) | 2007-01-25 | 2007-03-07 | Univ Sheffield | Compounds and their use |
| KR100903974B1 (ko) | 2007-09-27 | 2009-06-25 | 한국화학연구원 | 2,4,5-삼중치환-1,3-티아졸 유도체 및 약제학적으로 허용가능한 그의 염, 그의 제조방법 및 그를 유효성분으로함유하는 spc 수용체 활성으로 유발되는 염증관련 질환치료제 |
| US9315449B2 (en) | 2008-05-15 | 2016-04-19 | Duke University | Substituted pyrazoles as heat shock transcription factor activators |
| MX338530B (es) | 2008-06-03 | 2016-04-21 | Siga Technologies Inc | Inhibidores de molecula pequeña para el tratamiento o prevencion de infeccion de virus del dengue. |
| JP5322296B2 (ja) | 2008-08-20 | 2013-10-23 | 日本曹達株式会社 | テトラゾイルオキシム誘導体を含む植物病害防除剤の使用方法 |
| WO2012075393A2 (en) | 2010-12-02 | 2012-06-07 | President And Fellows Of Harvard College | Activators of proteasomal degradation and uses thereof |
| EP2675440B1 (en) | 2011-02-14 | 2020-03-25 | Merck Sharp & Dohme Corp. | Cathepsin cysteine protease inhibitors |
| WO2013033037A2 (en) | 2011-08-26 | 2013-03-07 | The Regents Of The University Of California | Novel antiprion compounds |
| CN103058949A (zh) | 2011-10-18 | 2013-04-24 | 华东理工大学 | 做为dhodh抑制剂的噻唑衍生物及其应用 |
| CN103159695B (zh) | 2011-12-08 | 2015-08-12 | 首都师范大学 | 可抑制hiv复制并对耐药hiv病毒株有效的噻唑类化合物及其制备方法和用途 |
| GB201307233D0 (en) | 2013-04-22 | 2013-05-29 | Vib Vzw | Compounds and uses thereof |
| WO2014181287A1 (en) | 2013-05-09 | 2014-11-13 | Piramal Enterprises Limited | Heterocyclyl compounds and uses thereof |
| WO2015046193A1 (ja) | 2013-09-25 | 2015-04-02 | 塩野義製薬株式会社 | Trpv4阻害活性を有する芳香族複素環式アミン誘導体 |
| WO2015199206A1 (ja) | 2014-06-27 | 2015-12-30 | 塩野義製薬株式会社 | Trpv4阻害活性を有する6員環誘導体 |
| CN106109467B (zh) | 2016-06-20 | 2020-04-17 | 中国药科大学 | 三类羧基取代芳香化合物在耐吡嗪酰胺结核病及结核病治疗中的医药用途 |
| WO2019133445A1 (en) | 2017-12-28 | 2019-07-04 | Inception Ibd, Inc. | Aminothiazoles as inhibitors of vanin-1 |
| PT3814347T (pt) * | 2018-06-27 | 2023-07-18 | Bristol Myers Squibb Co | Compostos de naftiridinona úteis como ativadores de células t |
| HUE064531T2 (hu) * | 2018-06-27 | 2024-04-28 | Bristol Myers Squibb Co | Szubsztituált naftiridinon vegyületek mint T-sejt aktivátorok |
| EP4013508A1 (en) | 2019-08-12 | 2022-06-22 | Bayer Aktiengesellschaft | [1,2,4]triazolo[1,5-c]quinazolin-5-amines |
| AR119821A1 (es) | 2019-08-28 | 2022-01-12 | Bristol Myers Squibb Co | Compuestos de piridopirimidinonilo sustituidos útiles como activadores de células t |
| WO2021043966A1 (en) | 2019-09-06 | 2021-03-11 | Inflazome Limited | Nlrp3 inhibitors |
| KR20220092918A (ko) | 2019-11-04 | 2022-07-04 | 알렉터 엘엘씨 | Siglec-9 ecd 융합 분자 및 이의 사용 방법 |
| AR120896A1 (es) | 2019-12-25 | 2022-03-30 | Astellas Pharma Inc | COMPUESTO DE PIRIDAZINIL-TIAZOLCARBOXAMIDA COMO INHIBIDORES DE DGKz |
| MX2022013230A (es) | 2020-04-24 | 2022-11-14 | Boehringer Ingelheim Int | Analogos de glucagon como agonistas de accion prolongada del receptor de glp-1/glucagon para usarse en el tratamiento de enfermedad del higado graso y esteatohepatitis. |
| EP4139287A1 (en) | 2020-04-24 | 2023-03-01 | Bayer Aktiengesellschaft | Substituted aminothiazoles as dgkzeta inhibitors for immune activation |
-
2021
- 2021-04-20 EP EP21720251.4A patent/EP4139287A1/en active Pending
- 2021-04-20 CA CA3180670A patent/CA3180670A1/en active Pending
- 2021-04-20 AU AU2021261524A patent/AU2021261524A1/en active Pending
- 2021-04-20 KR KR1020227040664A patent/KR20230005247A/ko active Search and Examination
- 2021-04-20 JP JP2022564009A patent/JP2023522251A/ja active Pending
- 2021-04-20 CA CA3180819A patent/CA3180819A1/en active Pending
- 2021-04-20 WO PCT/EP2021/060167 patent/WO2021214019A1/en active Application Filing
- 2021-04-20 PE PE2022002433A patent/PE20230322A1/es unknown
- 2021-04-20 EP EP21720249.8A patent/EP4139286A1/en active Pending
- 2021-04-20 JP JP2022564007A patent/JP2023522250A/ja active Pending
- 2021-04-20 WO PCT/EP2021/060170 patent/WO2021214020A1/en unknown
- 2021-04-20 CN CN202180037365.XA patent/CN115697979A/zh active Pending
- 2021-04-20 CR CR20220536A patent/CR20220536A/es unknown
- 2021-04-20 MX MX2022013388A patent/MX2022013388A/es unknown
- 2021-04-20 IL IL297499A patent/IL297499A/en unknown
- 2021-04-20 CN CN202180043311.4A patent/CN115697980A/zh active Pending
- 2021-04-20 US US17/920,679 patent/US20230167078A1/en active Pending
- 2021-04-20 BR BR112022019057A patent/BR112022019057A2/pt active Search and Examination
- 2021-04-20 US US17/921,043 patent/US20230167103A1/en active Pending
- 2021-04-23 TW TW110114675A patent/TW202200552A/zh unknown
- 2021-04-23 AR ARP210101100A patent/AR121929A1/es unknown
-
2022
- 2022-09-14 US US17/944,922 patent/US11964953B2/en active Active
- 2022-10-17 EC ECSENADI202280829A patent/ECSP22080829A/es unknown
- 2022-10-17 DO DO2022000223A patent/DOP2022000223A/es unknown
- 2022-10-19 CO CONC2022/0014876A patent/CO2022014876A2/es unknown
- 2022-10-21 CL CL2022002919A patent/CL2022002919A1/es unknown
Also Published As
| Publication number | Publication date |
|---|---|
| US20230139936A1 (en) | 2023-05-04 |
| CN115697980A (zh) | 2023-02-03 |
| US11964953B2 (en) | 2024-04-23 |
| CR20220536A (es) | 2023-01-17 |
| CN115697979A (zh) | 2023-02-03 |
| AR121929A1 (es) | 2022-07-27 |
| CL2022002919A1 (es) | 2023-03-31 |
| WO2021214020A1 (en) | 2021-10-28 |
| KR20230005247A (ko) | 2023-01-09 |
| JP2023522250A (ja) | 2023-05-29 |
| EP4139286A1 (en) | 2023-03-01 |
| JP2023522251A (ja) | 2023-05-29 |
| WO2021214019A1 (en) | 2021-10-28 |
| CO2022014876A2 (es) | 2023-03-17 |
| CA3180819A1 (en) | 2021-10-28 |
| CA3180670A1 (en) | 2021-10-28 |
| BR112022019057A2 (pt) | 2022-11-08 |
| MX2022013388A (es) | 2022-11-30 |
| EP4139287A1 (en) | 2023-03-01 |
| DOP2022000223A (es) | 2022-11-15 |
| IL297499A (en) | 2022-12-01 |
| ECSP22080829A (es) | 2022-11-30 |
| US20230167103A1 (en) | 2023-06-01 |
| PE20230322A1 (es) | 2023-02-22 |
| AU2021261524A1 (en) | 2022-11-24 |
| US20230167078A1 (en) | 2023-06-01 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| TW202200552A (zh) | 作為用於免疫活化之DGKζ抑制劑之經取代胺基噻唑 | |
| CA2996318C (en) | Heteroaryl compounds as irak inhibitors and uses thereof | |
| CN112204009B (zh) | 整合应激通路的调节剂 | |
| US20230062100A1 (en) | Substituted aminoquinolones as dgkalpha inhibitors for immune activation | |
| US20230064809A1 (en) | Substituted aminoquinolones as dgkalpha inhibitors for immune activation | |
| JP2021502356A (ja) | Hpk1阻害剤として有用なイソフラノン化合物 | |
| JP2022533023A (ja) | 統合的ストレス経路の調節剤としての置換シクロアルキル | |
| UA123785C2 (uk) | Сполуки піролотриазину як інгібітори tam | |
| TW201827430A (zh) | 4,5-環化1,2,4-三唑酮 | |
| TW201840549A (zh) | 2-雜芳基-3-氧代-2,3-二氫噠嗪-4-甲醯胺 | |
| JP2017536369A (ja) | Irakインヒビターとしてのヘテロアリール化合物及びその使用 | |
| BR112016013632B1 (pt) | Carboxamidas, seus usos, seus intermediários e seu processo de preparação, e medicamento | |
| EP3390387B1 (en) | Heteroarylbenzimidazole compounds | |
| KR20230035311A (ko) | Nek7 키나제의 억제제 | |
| US11267824B2 (en) | Inhibitors of indoleamine 2,3-dioxygenase and/or tryptophan 2,3-dioxygenase | |
| CN112566697B (zh) | 作为IRAK4抑制剂的吡咯并[1,2-b]哒嗪衍生物 | |
| TW202023551A (zh) | 作為布魯頓氏酪胺酸激酶(btk)之可逆抑制劑的稠合咪唑并吡啶 | |
| TW201726657A (zh) | 雜芳基苯并咪唑化合物 |