RU2463304C1 - Трисдикетонатные комплексы лантанидов с лигандами пиридинового ряда в качестве люминофоров и способ их получения - Google Patents
Трисдикетонатные комплексы лантанидов с лигандами пиридинового ряда в качестве люминофоров и способ их получения Download PDFInfo
- Publication number
- RU2463304C1 RU2463304C1 RU2011114874/05A RU2011114874A RU2463304C1 RU 2463304 C1 RU2463304 C1 RU 2463304C1 RU 2011114874/05 A RU2011114874/05 A RU 2011114874/05A RU 2011114874 A RU2011114874 A RU 2011114874A RU 2463304 C1 RU2463304 C1 RU 2463304C1
- Authority
- RU
- Russia
- Prior art keywords
- formula
- complexes
- iii
- pyridine
- lanthanides
- Prior art date
Links
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 title claims abstract description 28
- 229910052747 lanthanoid Inorganic materials 0.000 title claims abstract description 22
- 239000003446 ligand Substances 0.000 title claims abstract description 21
- 150000002602 lanthanoids Chemical class 0.000 title claims abstract description 20
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 title claims abstract description 15
- 238000000034 method Methods 0.000 title claims abstract description 6
- 229910052693 Europium Inorganic materials 0.000 claims abstract description 12
- OGPBJKLSAFTDLK-UHFFFAOYSA-N europium atom Chemical compound [Eu] OGPBJKLSAFTDLK-UHFFFAOYSA-N 0.000 claims abstract description 11
- 125000000217 alkyl group Chemical group 0.000 claims abstract description 9
- 125000000175 2-thienyl group Chemical group S1C([*])=C([H])C([H])=C1[H] 0.000 claims abstract description 7
- 229910052771 Terbium Inorganic materials 0.000 claims abstract description 7
- 125000001624 naphthyl group Chemical group 0.000 claims abstract description 4
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims abstract description 3
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 claims abstract 2
- GZCRRIHWUXGPOV-UHFFFAOYSA-N terbium atom Chemical compound [Tb] GZCRRIHWUXGPOV-UHFFFAOYSA-N 0.000 claims description 5
- 230000003993 interaction Effects 0.000 claims description 2
- 150000001768 cations Chemical class 0.000 claims 2
- 238000005401 electroluminescence Methods 0.000 abstract description 11
- 239000000463 material Substances 0.000 abstract description 6
- 238000005424 photoluminescence Methods 0.000 abstract description 5
- -1 terbium cation Chemical class 0.000 abstract description 5
- 239000013110 organic ligand Substances 0.000 abstract description 4
- 239000010409 thin film Substances 0.000 abstract description 4
- 239000000126 substance Substances 0.000 abstract description 3
- 150000001875 compounds Chemical class 0.000 description 22
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 18
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 17
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 12
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 12
- 239000010410 layer Substances 0.000 description 12
- 239000000243 solution Substances 0.000 description 12
- 239000000203 mixture Substances 0.000 description 10
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 9
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 9
- 239000007983 Tris buffer Substances 0.000 description 8
- 238000010521 absorption reaction Methods 0.000 description 7
- 238000000354 decomposition reaction Methods 0.000 description 7
- 235000019441 ethanol Nutrition 0.000 description 7
- 239000000843 powder Substances 0.000 description 7
- 239000011541 reaction mixture Substances 0.000 description 7
- SLUNEGLMXGHOLY-UHFFFAOYSA-N benzene;hexane Chemical compound CCCCCC.C1=CC=CC=C1 SLUNEGLMXGHOLY-UHFFFAOYSA-N 0.000 description 6
- 230000015572 biosynthetic process Effects 0.000 description 6
- NBPGPQJFYXNFKN-UHFFFAOYSA-N 4-methyl-2-(4-methylpyridin-2-yl)pyridine Chemical group CC1=CC=NC(C=2N=CC=C(C)C=2)=C1 NBPGPQJFYXNFKN-UHFFFAOYSA-N 0.000 description 5
- NNMXSTWQJRPBJZ-UHFFFAOYSA-K europium(iii) chloride Chemical compound Cl[Eu](Cl)Cl NNMXSTWQJRPBJZ-UHFFFAOYSA-K 0.000 description 5
- 229920000767 polyaniline Polymers 0.000 description 5
- 239000002244 precipitate Substances 0.000 description 5
- XKRFYHLGVUSROY-UHFFFAOYSA-N Argon Chemical compound [Ar] XKRFYHLGVUSROY-UHFFFAOYSA-N 0.000 description 4
- UXVMQQNJUSDDNG-UHFFFAOYSA-L Calcium chloride Chemical compound [Cl-].[Cl-].[Ca+2] UXVMQQNJUSDDNG-UHFFFAOYSA-L 0.000 description 4
- 239000001110 calcium chloride Substances 0.000 description 4
- 229910001628 calcium chloride Inorganic materials 0.000 description 4
- 150000003222 pyridines Chemical class 0.000 description 4
- 238000010992 reflux Methods 0.000 description 4
- 238000003786 synthesis reaction Methods 0.000 description 4
- 150000000918 Europium Chemical class 0.000 description 3
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 3
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 3
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 3
- 239000011159 matrix material Substances 0.000 description 3
- 229920003227 poly(N-vinyl carbazole) Polymers 0.000 description 3
- 238000006862 quantum yield reaction Methods 0.000 description 3
- 230000005855 radiation Effects 0.000 description 3
- 238000003756 stirring Methods 0.000 description 3
- 239000000758 substrate Substances 0.000 description 3
- XNYBCXGYJYRPQV-UHFFFAOYSA-N 4-naphthalen-2-ylpyridine Chemical compound C1=CC2=CC=CC=C2C=C1C1=CC=NC=C1 XNYBCXGYJYRPQV-UHFFFAOYSA-N 0.000 description 2
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 2
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 2
- 239000004793 Polystyrene Substances 0.000 description 2
- 229910006404 SnO 2 Inorganic materials 0.000 description 2
- 238000000862 absorption spectrum Methods 0.000 description 2
- 229910052786 argon Inorganic materials 0.000 description 2
- 239000012298 atmosphere Substances 0.000 description 2
- 239000011575 calcium Substances 0.000 description 2
- NZZIMKJIVMHWJC-UHFFFAOYSA-N dibenzoylmethane Chemical compound C=1C=CC=CC=1C(=O)CC(=O)C1=CC=CC=C1 NZZIMKJIVMHWJC-UHFFFAOYSA-N 0.000 description 2
- 238000002347 injection Methods 0.000 description 2
- 239000007924 injection Substances 0.000 description 2
- 230000002262 irrigation Effects 0.000 description 2
- 238000003973 irrigation Methods 0.000 description 2
- AWJUIBRHMBBTKR-UHFFFAOYSA-N isoquinoline Chemical compound C1=NC=CC2=CC=CC=C21 AWJUIBRHMBBTKR-UHFFFAOYSA-N 0.000 description 2
- 238000001748 luminescence spectrum Methods 0.000 description 2
- 238000004020 luminiscence type Methods 0.000 description 2
- 238000002360 preparation method Methods 0.000 description 2
- 229910052761 rare earth metal Inorganic materials 0.000 description 2
- 239000000523 sample Substances 0.000 description 2
- 230000003595 spectral effect Effects 0.000 description 2
- TXBBUSUXYMIVOS-UHFFFAOYSA-N thenoyltrifluoroacetone Chemical compound FC(F)(F)C(=O)CC(=O)C1=CC=CS1 TXBBUSUXYMIVOS-UHFFFAOYSA-N 0.000 description 2
- 238000012546 transfer Methods 0.000 description 2
- SHXHPUAKLCCLDV-UHFFFAOYSA-N 1,1,1-trifluoropentane-2,4-dione Chemical compound CC(=O)CC(=O)C(F)(F)F SHXHPUAKLCCLDV-UHFFFAOYSA-N 0.000 description 1
- BSXCLFYNJYBVPM-UHFFFAOYSA-N 1-thiophen-2-ylbutane-1,3-dione Chemical compound CC(=O)CC(=O)C1=CC=CS1 BSXCLFYNJYBVPM-UHFFFAOYSA-N 0.000 description 1
- ROFVEXUMMXZLPA-UHFFFAOYSA-N Bipyridyl Chemical class N1=CC=CC=C1C1=CC=CC=N1 ROFVEXUMMXZLPA-UHFFFAOYSA-N 0.000 description 1
- 229920001609 Poly(3,4-ethylenedioxythiophene) Polymers 0.000 description 1
- DGEZNRSVGBDHLK-UHFFFAOYSA-N [1,10]phenanthroline Chemical compound C1=CN=C2C3=NC=CC=C3C=CC2=C1 DGEZNRSVGBDHLK-UHFFFAOYSA-N 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 229910052782 aluminium Inorganic materials 0.000 description 1
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 239000012300 argon atmosphere Substances 0.000 description 1
- 150000004982 aromatic amines Chemical class 0.000 description 1
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 1
- KGYGBOORGRYDGQ-UHFFFAOYSA-N benzene;methanol Chemical compound OC.C1=CC=CC=C1 KGYGBOORGRYDGQ-UHFFFAOYSA-N 0.000 description 1
- 230000008033 biological extinction Effects 0.000 description 1
- 239000004305 biphenyl Substances 0.000 description 1
- 238000007664 blowing Methods 0.000 description 1
- 238000005119 centrifugation Methods 0.000 description 1
- 238000006243 chemical reaction Methods 0.000 description 1
- 239000008367 deionised water Substances 0.000 description 1
- 229910021641 deionized water Inorganic materials 0.000 description 1
- 239000003599 detergent Substances 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- SWXVUIWOUIDPGS-UHFFFAOYSA-N diacetone alcohol Natural products CC(=O)CC(C)(C)O SWXVUIWOUIDPGS-UHFFFAOYSA-N 0.000 description 1
- 238000004090 dissolution Methods 0.000 description 1
- 239000002019 doping agent Substances 0.000 description 1
- 238000001194 electroluminescence spectrum Methods 0.000 description 1
- 238000000921 elemental analysis Methods 0.000 description 1
- 239000010408 film Substances 0.000 description 1
- 239000012634 fragment Substances 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 238000010438 heat treatment Methods 0.000 description 1
- 150000002466 imines Chemical class 0.000 description 1
- 150000002500 ions Chemical class 0.000 description 1
- 229910021644 lanthanide ion Inorganic materials 0.000 description 1
- 150000002601 lanthanoid compounds Chemical class 0.000 description 1
- 239000002346 layers by function Substances 0.000 description 1
- 238000004519 manufacturing process Methods 0.000 description 1
- 239000008204 material by function Substances 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- QSHDDOUJBYECFT-UHFFFAOYSA-N mercury Chemical compound [Hg] QSHDDOUJBYECFT-UHFFFAOYSA-N 0.000 description 1
- 229910052753 mercury Inorganic materials 0.000 description 1
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 1
- 230000007935 neutral effect Effects 0.000 description 1
- 125000004433 nitrogen atom Chemical group N* 0.000 description 1
- 239000012454 non-polar solvent Substances 0.000 description 1
- 230000003287 optical effect Effects 0.000 description 1
- 125000002524 organometallic group Chemical group 0.000 description 1
- 230000003647 oxidation Effects 0.000 description 1
- 238000007254 oxidation reaction Methods 0.000 description 1
- MPQXHAGKBWFSNV-UHFFFAOYSA-N oxidophosphanium Chemical class [PH3]=O MPQXHAGKBWFSNV-UHFFFAOYSA-N 0.000 description 1
- 239000001301 oxygen Substances 0.000 description 1
- 229910052760 oxygen Inorganic materials 0.000 description 1
- 125000004430 oxygen atom Chemical group O* 0.000 description 1
- 238000000103 photoluminescence spectrum Methods 0.000 description 1
- 239000002798 polar solvent Substances 0.000 description 1
- 229920000642 polymer Polymers 0.000 description 1
- 229920002223 polystyrene Polymers 0.000 description 1
- 239000011241 protective layer Substances 0.000 description 1
- 150000002910 rare earth metals Chemical class 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- PYWVYCXTNDRMGF-UHFFFAOYSA-N rhodamine B Chemical compound [Cl-].C=12C=CC(=[N+](CC)CC)C=C2OC2=CC(N(CC)CC)=CC=C2C=1C1=CC=CC=C1C(O)=O PYWVYCXTNDRMGF-UHFFFAOYSA-N 0.000 description 1
- 229940043267 rhodamine b Drugs 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 239000002904 solvent Substances 0.000 description 1
- 238000001228 spectrum Methods 0.000 description 1
- 125000001424 substituent group Chemical group 0.000 description 1
- 150000003462 sulfoxides Chemical class 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- GFISHBQNVWAVFU-UHFFFAOYSA-K terbium(iii) chloride Chemical compound Cl[Tb](Cl)Cl GFISHBQNVWAVFU-UHFFFAOYSA-K 0.000 description 1
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 230000007704 transition Effects 0.000 description 1
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 1
- 238000007738 vacuum evaporation Methods 0.000 description 1
Images
Abstract
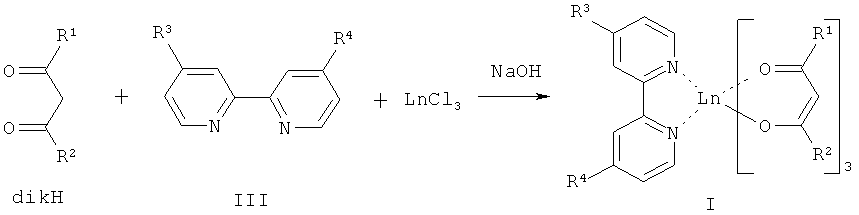
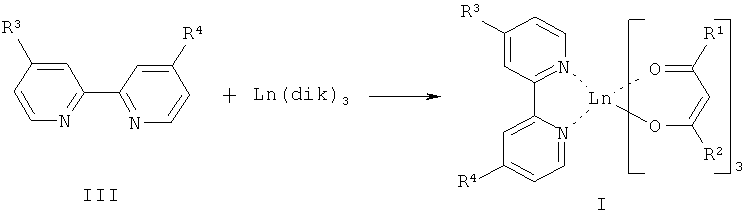
Изобретение относится к новым люминесцентным комплексам лантанидов, которые могут быть использованы в качестве люминофоров, активных компонентов или в составе функциональных материалов в светоизлучающих устройствах. Описываются комплексы лантанидов с органическими лигандами формулы (I):
где Ln - трехзарядный катион европия или тербия; dik - β-дикетонат формулы (II): где - R1, R2 - низший алкил, фторированный алкил, фенил, 2-тиенил; Q - пиридинсодержащий лиганд формулы (III) или (IV), где R3, R4 - низший алкил, нафтил; n=1 или 2. Описывается также способ получения комплексов лантанидов формулы (I) взаимодействием β-дикетона (dikH) и пиридинсодержащего лиганда Q формулы (III) или (IV) с хлоридом лантанида (III) (LnCl3), или реакцией пиридинсодержащего лиганда Q формулы (III) с комплексом Ln(dik)3. Предложенные люминесцентные комплексы лантанидов обладают интенсивной фото- и электролюминесценцией и способны образовывать тонкие пленки, что позволяет использовать их не только как фотолюминофоры, но и в электролюминесцентных устройствах в качестве активного слоя или в составе функционального материала. 2 н.п. ф-лы, 1 ил., 1 табл., 6 пр.
Description
Изобретение относится к области координационной химии и химии материалов, а именно - к новым люминесцентным комплексам лантанидов. Описываются комплексы редкоземельных металлов с органическими лигандами общей формулы (I):
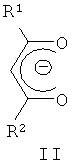
в которой Ln - трехвалентный катион редкоземельного металла; dik - β-дикетонат формулы (II):
где - R1, R2 - низший алкил, фторированный алкил, фенил, 2-тиенил;
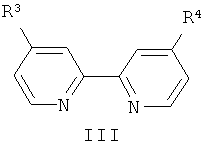
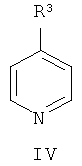
Q - пиридинсодержащий лиганд формулы (III) или (IV):
где R3, R4 - низший алкил, нафтил;
n=1 или 2.
Предлагаемые соединения и материалы на их основе могут быть использованы в качестве люминофоров, активного слоя в светоизлучающих диодах, люминесцентных сенсорах. Изобретение также относится к способу получения таких соединений.
Указанный тип соединений, их свойства и способ получения в литературе не описаны. Заявляемый тип соединений имеет структуру, относящуюся к комплексам β-дикетонатов лантанидов с нейтральными пиридинсодержащими лигандами. В описываемых комплексах ион лантанида (преимущественно Eu и Tb) находится в степени окисления +3, с координационным числом, равным 8. Центральный ион Ln3+ координирует шесть атомов кислорода трех хелатных β-дикетонатных лиганда и два атома азота одного или двух замещенных пиридинсодержащих лиганда. Заявляемый тип соединений содержит неизвестное ранее сочетание замещенных лигандов, совокупность которых позволяет их отнести к новым люминесцентным комплексам лантанидов.
Комплексы лантанидов с ароматическими азотсодержащими соединениями иного строения используются в качестве люминесцентных зондов и сенсоров в биомедицинских исследованиях [например, Bünzli G.J.-C., Piguet С., Chem. Rev. 2002, 102, 1897; Tsukube H., Shinoda S., Chem. Rev. 2002, 102, 2389; Yang H., Cairns N., Патент US 5,858,676, 1999; Murray G.M., Заявка на патент US 20030003587 A1, 2003].
Известны β-дикетонатные комплексы лантанидов с ароматическими карбоновыми кислотами, ароматическими аминами, фенантролином, фосфиноксидами, сульфоксидами, которые используются в качестве светоизлучающих слоев в электролюминесцентных устройствах
Показано, что эти соединения обладают интенсивной фото- и электролюминесценцией, которая проявляется в виде узких характеристических полос, получаемый цвет излучения близок к монохроматическому.
Наиболее близкими по составу к заявляемым люминофорам являются трисдикетонатные комплексы лантанидов с иминиевыми лигандами [Radu N.S., Lecloux D.D., Herron N., Clarkson L.M., Патент US 7,575,816 B2, 2009]. В патенте описываются комплексы лантанидов, содержащие в качестве лигандов еноляты β-дикетонов. В качестве иминиевых лигандов используются изохинолин, замещенные пиридин и 2,2'-дипиридил. Особенностью строения описываемых соединений является наличие заместителей в пиридинсодержащих лигандах, в качестве которых используются t-Bu-, F3C-, CN-, Me2N-, Ph, 4-FC6H4, 2-FC6H4, 2-F3CC6H4, 3-F3CC6H4, 2-тиенил. Описываемые соединения обладают интенсивной фото- и электролюминесценцией. Однако существует необходимость улучшения люминесцентных свойств соединений лантанидов в комбинации с такими характеристиками, как способность к электролюминесценции и способность образовывать тонкие пленки. Кроме того, синтез и люминесцентные свойства β-дикетонатов лантанидов с пиридинсодержащими лигандами в основном остаются неизученными несмотря на многообещающий потенциал таких соединений [Moleski R., Stathatos Е., Bekiari V., Lianos P., Thin Solid Films, 2002, 416, 279; Biju S., Ambili Raj D.B., Reddy M.L.P., Kariuki B.M., Inorg. Chem., 2006, 45, 10651; Li X.-L., Dai F.-R., Zhang L.-Y., Zhu Y.-M., Peng Q., Chen Z.-N., Organometallics, 2007, 26, 4483]. В этом отношении перспективными лигандами являются производные пиридина, содержащие метильный и в качестве эффективного флуоресцентного фрагмента нафтильный остаток.
Задачей настоящего изобретения является создание новых люминесцентных комплексов лантанидов, обладающих интенсивной фото- и электролюминесценцией, способных образовывать тонкие пленки. Это позволит использовать их не только как фотолюминофоры, но и в электролюминесцентных устройствах в качестве активного слоя или в составе функционального материала. Задачей изобретения является также разработка методов синтеза целевых соединений.
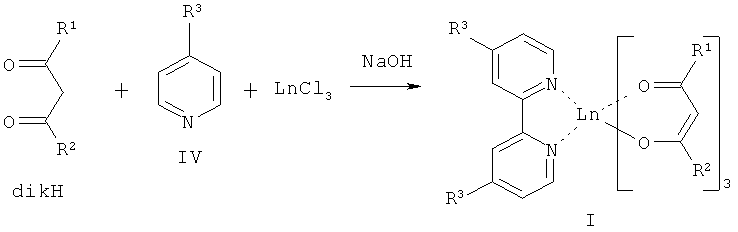
Решение поставленной задачи достигается структурой заявляемых новых люминесцентных комплексов лантанидов общей формулы (I) и способом их получения, заключающимся в том, что взаимодействие β-дикетона (dikH) и пиридинсодержащего лиганда формулы (III) или (IV) с хлоридом лантанида (III) (LnCl3) в присутствии гидроксида натрия приводит к образованию целевого соединения общей формулы (I), или пиридинсодержащий лиганд формулы (III) подвергают взаимодействию с комплексом Ln(dik)3. В первом случае реакция, по-видимому, протекает в две стадии. В начале образуется трисдикетонатный комплекс Ln(dik)3, который затем присоединяет в качестве дополнительного лиганда производное пиридина Q, в результате чего координационное число Ln (III) возрастает до 8. Все комплексы были синтезированы с хорошими выходами (40-88%).
Строение полученных соединений (I) (примеры 1-6) подтверждено данными элементного анализа.
Пример 1. (4,4'-Диметил-2,2'-дипиридил)трис[1-(2-тиенил)-3,3,3-трифтор-1,3-бутандионато]европия (III)
В колбе емкостью 20 мл, снабженной обратным холодильником и хлоркальциевой трубкой, смешивают 18 мг (0.1 ммоля) 4,4'-диметил-2,2'-дипиридила и 67 мг (0.3 ммоля) 4,4,4-трифтор-1-(2-тиенил)-1,3-бутандиона, 12 мг (0.3 ммоля) NaOH и 2 мл этилового спирта. Реакционную смесь перемешивают 10 мин при 60°С, затем при перемешивании по каплям добавляют раствор 37 мг (0.1 ммоля) хлорида европия (III) (EuCl3·6H2O) в 0.5 мл воды. Реакционную смесь нагревают 1.5 ч при 60°С, затем охлаждают, разбавляют водой, выпавший осадок отфильтровывают, перекристаллизовывают из бензола. Получают 72 мг (72%) комплекса в виде бело-розового порошка, т.пл. 219-225°С (с разложением; из бензола).
Найдено, %: С 43.36; Н 2.21; N 2.65.
C36H24EuF9N2O6S3.
Вычислено, %: С 43.25; Н 2.42; N 2.80.
Пример 2. (4-Метил-4'-нафтил-2,2'-дипиридил)трис[1-(2-тиенил)-3,3,3-трифтор-1,3-бутандионато]европия (III)
Получен аналогично примеру 1 из 4-метил-4'-нафтил-2,2'-дипиридила, 4,4,4-трифтор-1-(2-тиенил)-1,3-бутандиона и хлорида европия (III) (EuCl3·6Н2О) с выходом 76% в виде бело-розового порошка, т.пл. 138-145°С (с разложением; из смеси бензол - метиловый спирт в соотношении 1:1).
Найдено, %: С 48.78; Н 2.64; N 2.58.
C45H28EuF9N2O6S3.
Вычислено, %: С 48.61; Н 2.54; N 2.52.
Пример 3. (4-Метил-4'-нафтил-2,2'-дипиридил)трис[1,3-дифенил-1,3-пропандионато]европия (III)
В колбе емкостью 20 мл, снабженной обратным холодильником и хлоркальциевой трубкой, смешивают 89 мг (0.3 ммоля) 4-метил-4'-нафтил-2,2'-дипиридила, 202 мг (0.9 ммоля) дибензоилметана, 36 мг (0.9 ммоля) NaOH и 15 мл этилового спирта. Реакционную смесь перемешивают 10 мин при 60°С, затем при перемешивании по каплям добавляют раствор 101 мг (0.3 ммоля) хлорида европия (III) (EuCl3·6Н2О) в 0.5 мл воды. Реакционную смесь нагревают 1.5 ч при 60°С, затем раствор упаривают в вакууме до выпадения осадка, выпавший осадок отфильтровывают, перекристаллизовывают из смеси бензол - гексан. Получают 297 мг (88%) комплекса в виде бело-розового порошка, т.пл. 112-124°С (с разложением; из смеси бензол - гексан).
Найдено, %: С 70.96; Н 4.33; N 2.51.
C66H48EuN2O6.
Вычислено, %: С 70.84; Н 4.39; N 2.61.
Пример 4. (4,4'-Диметил-2,2'-дипиридил)трис[1,1,1-трифтор-2,4-пентандионато]тербия (III)
Получен аналогично примеру 3 из 4,4'-диметил-2,2'-дипиридила, 1,1,1-трифтор-2,4-пентандиона и хлорида тербия (III) (TbCl3·6Н2О) с выходом 64% в виде белого порошка, т.пл. 282-286°С (с разложением; из смеси бензол - гексан).
Найдено, %: С 41.42; Н 2.86; N 3.24.
C27H24F9N2O6Tb.
Вычислено, %: С 41.65; Н 3.13; N 3.41.
Пример 5. (4,4'-Диметил-2,2'-дипиридил)трис[1,3-дифенил-1,3-пропандионато]европия (III)
А. Синтез трис[1,3-дифенил-1,3-пропандионато]европия (III). В колбе емкостью 20 мл, снабженной обратным холодильником и хлоркальциевой трубкой, смешивают 202 мг (0.9 ммоля) дибензоилметана и 5 мл метилового спирта, затем при нагревании и перемешивании добавляют раствор 36 мг (0.9 ммоля) NaOH в 0.5 мл воды, реакционную смесь перемешивают 15 мин при 60°С, затем по каплям добавляют раствор 110 мг (0.3 ммоля) хлорида европия (III) (EuCl3·6H2O) в 0.5 мл воды. Реакционную смесь нагревают 2 ч при 60°С, затем охлаждают, выпавший осадок отфильтровывают, промывают бензолом. Получают 38 мг (44%) комплекса в виде светло-розового порошка, т.пл. 178-191°С (с разложением).
В. В колбе емкостью 20 мл, снабженной обратным холодильником и хлоркальциевой трубкой, смешивают 824 мг (0.1 ммоля) трис[1,3-дифенил-1,3-пропандионато]европия (III), 184 мг (0.1 ммоля) 4,4'-диметил-2,2'-дипиридила и 2 мл этилового спирта. Реакционную смесь нагревают 2 ч при 60°С, затем охлаждают, разбавляют водой, выпавший осадок отфильтровывают, перекристаллизовывают из смеси бензол - гексан. Получают 40 мг (40%) комплекса в виде светло-розового порошка, т.пл. 178-191°С (с разложением; из смеси бензол - гексан).
Найдено, %: С 68.12; Н 4.25; N 2.53.
C57H45EuN2O6.
Вычислено, %: С 68.06; Н 4.51; N 2.79.
Пример 6. Бис(4-(2-Нафтил)пиридин)трис[1-(2-тиенил)-3,3,3-трифтор-1,3-бутандионато]европия (III)
Получен аналогично примеру 1 из 4-(2-нафтил)пиридина, 4,4,4-трифтор-1-(2-тиенил)-1,3-бутандиона и хлорида европия (III) (EuCl3·6Н2О) с выходом 48% в виде бело-розового порошка, т.пл. 77-92°С (с разложением; из смеси бензол - гексан).
Найдено, %: С 54.44; Н 2.78; N 2.44.
C54H34EuF9N2O6S3·0.5С6Н6.
Вычислено, %: С 54.11; Н 2.79; N 2.28.
Были исследованы физико-химические и люминесцентные свойства полученных соединений формулы (I).
Было найдено, что заявляемые соединения хорошо растворимы как в полярных растворителях, таких как этиловый спирт, ацетонитрил, так и в неполярных растворителях, таких как гексан и бензол. Установлено, что лучше всего комплексы растворяются в ацетонитриле; без остатка растворяются в этаноле; в гексане - при концентрациях порядка 2 - 7×10-4 моль·л-1 остается заметное количество нерастворенного вещества, при этом с течением времени наблюдается дополнительное растворение. В воде при концентрациях 3 - 6×10-5 моль·л-1 остается небольшое количество взвеси, но с течением времени наблюдается медленный переход вещества в растворенное состояние.
Была изучена устойчивость комплексов европия к действию света: растворы в воде, этаноле и гексане облучали ртутной лампой светом с длиной волны 313 и 365 нм. При этом изменений в спектрах поглощения в процессе облучения в течение 4 ч не наблюдалось.
Были исследованы спектрально-абсорбционные и спектрально-люминесцентные свойства полученных комплексов в растворах ацетонитрила при 296 К. Максимумы длинноволновых полос поглощения находятся в области 330-350 нм для комплексов европия и в области 280-290 нм для комплекса тербия. Комплексы имеют высокую поглощательную способность: молярные коэффициенты экстинкции в максимумах полос поглощения составляют 50000-70000 л·моль-1·см-1. В спектре люминесценции у каждого комплекса имеется несколько узких пиков. У комплексов европия они расположены в желто-красной области, у тербия - в зелено-голубой области. Длины волн основных максимумов представлены в таблице 1. Величины квантовых выходов достигают десятков %, что указывает на эффективную передачу энергии от органических лигандов на катион лантанида, например, соединения из примеров 1, 2 и 6.
В таблице 1 представлены данные, полученные для ацетонитрильных растворов комплексов общей формулы (I).
| Таблица 1 | ||||
| Абсорбционные и люминесцентные характеристики комплексов лантанидов с органическими лигандами | ||||
| Соединение | Поглощение а) | Люминесценция а) | ||
| λmax, нм | εmax×10-4, л·моль-1·см-1 б) | λmax; нмв) | Квантовый выход, %г) | |
| Пример 1 | 339 | 6.6 | 613 | 30 |
| Пример 2 | 339 | 6.5 | 613 | 30 |
| Пример 3 | 349 | 6.4 | 613 | 1 |
| Пример 4 | 285 | 5.4 | 546 | 1 |
| Пример 5А | 349 | 5.3 | 613 | 1 |
| Пример 5В | 349 | 6.1 | 613 | 1 |
| Пример 6 | 339 | 6.1 | 613 | 22 |
| а) В ацетонитриле в присутствии кислорода воздуха при 23°С. | ||||
| б) Молярный коэффициент поглощения при λmax длинноволновой полосы. | ||||
| в) Основной максимум в исправленном спектре люминесценции. | ||||
| г) Измерен относительно Родамина Б в этаноле (квантовый выход 50%) с поправкой на разное время жизни люминесценции соединения сравнения и комплексов и разную рефракцию растворителей. | ||||
Полученные соединения были исследованы в составе электролюминесцентных материалов. Для этого было изготовлено электролюминесцентное устройство.
Работа проводилась в условиях чистой атмосферы класса 1000. Стеклянные подложки размером 2×2 см с нанесенным прозрачным токопроводящим слоем In2O3/SnO2 с поверхностным сопротивлением 14 Ом/квадрат последовательно обрабатывались в ультразвуковой ванне в течение 15 мин в растворе детергента, деионизированной воде, ацетоне и изопропиловом спирте. Подложки сушились путем обдува струей чистого аргона. На очищенную таким образом поверхность методом центрифугирования наносили дырочный инжектирующий слой из водного раствора полианилина (ПАНИ), полученного методом матричного синтеза. Использованный ПАНИ обладает повышенной способностью к инжекции дырок по сравнению со смесью полиэтилендиокситиофена с полисульфоновой кислотой. Слой сушился в две стадии: при 110°С в течение 1 мин в атмосфере сухого аргона и в вакууме при 60°С в течение 8 ч.
В качестве светоизлучающего слоя использовался поливинилкарбазол (ПВК), допированный комплексом из примера 1 (2% по массе), который формировали методом полива из раствора хлороформа на заранее нанесенный инжектирующий слой ПАНИ. Далее наносили электронный транспортный слой также путем полива на центрифуге раствора толуола, содержащего смесь полистирола (ПС) с (3-(4-дифенил)-4-фенил-5-(4-трет-бутилфенил)-1,2,4-триазолом (ТАЗ) (30 мольных %). Таким образом, в процессе формирования соответствующих функциональных слоев были исключены две энергозатратные стадии термического вакуумного испарения (ТВИ). На конечной стадии наносили катодный слой (Са) методом ТВИ и защитный слой алюминия. Оптимальные толщины слоев составляли: 50 нм ПАНИ, 60 нм (ПВК/комплекс), 25 нм (ТАЗ+ПС), 10 нм (Са) и 150 (AL). Электрические и оптические измерения проводили в атмосфере аргона. Излучение регистрировали через прозрачную подложку. Генерацию ЭЛ в светоизлучающем слое осуществляли путем приложения к образцу (In2O3/SnO2 - анод) положительного смещения от 0 до 30 В.
Для примера (фиг.1) представлен спектр электролюминесценции (ЭЛ) светодиодной структуры, содержащей комплекс 1 (пример 1), а также приведены спектры поглощения и фотолюминесценции для этого соединения в ацетонитриле. Излучение ЭЛ имеет красный цвет с максимальной величиной яркости 50 кд/м2 при плотности тока 20 мА/см2 и напряжении 15 В, что сравнимо с известными характеристиками светодиодных структур на основе других комплексов лантанидов. Спектр ЭЛ практически совпадает с полосой ФЛ. Отсюда следует, что излучение принадлежит комплексу европия. ЭЛ полимерной матрицы отсутствовала, что указывает на полный перенос энергии с матрицы на допант.
Предварительные исследования физико-химических свойств полученных соединений общей формулы (I) показали, что заявляемые соединения способны к образованию тонких пленок, обладают интенсивной фото- и электролюминесценцией. Заявляемые соединения формулы (I) и материалы на их основе могут быть использованы в качестве люминофоров, активных компонентов, в составе функциональных материалов в светоизлучающих диодах, люминесцентных сенсорах и других светоизлучающих устройствах.
Claims (2)
1. Люминесцентные комплексы лантанидов общей формулы (I)
в которой Ln - трехзарядный катион европия или тербия; dik - β-дикетонат формулы (II)
где R1, R2 - низший алкил, фторированный алкил, фенил, 2-тиенил;
Q - пиридинсодержащий лиганд формулы (III) или (IV)
где R3, R4 - низший алкил, нафтил; n=1 или 2.
в которой Ln - трехзарядный катион европия или тербия; dik - β-дикетонат формулы (II)
где R1, R2 - низший алкил, фторированный алкил, фенил, 2-тиенил;
Q - пиридинсодержащий лиганд формулы (III) или (IV)
где R3, R4 - низший алкил, нафтил; n=1 или 2.
2. Способ получения люминесцентных комплексов лантанидов общей формулы (I) по п.1, характеризующийся тем, что он включает взаимодействие β-дикетона (dikH) и пиридинсодержащего лиганда Q формулы (III) или (IV)
где R3, R4 и n имеют указанные по п.1 значения, с хлоридом лантанида (III) (LnCl3), или пиридинсодержащий лиганд Q формулы (III) подвергают взаимодействию с комплексом
Ln(dik)3,
где Ln - трехзарядный катион европия или тербия; dik - β-дикетонат формулы (II)
где R1, R2 имеют указанные по п.1 значения.
где R3, R4 и n имеют указанные по п.1 значения, с хлоридом лантанида (III) (LnCl3), или пиридинсодержащий лиганд Q формулы (III) подвергают взаимодействию с комплексом
Ln(dik)3,
где Ln - трехзарядный катион европия или тербия; dik - β-дикетонат формулы (II)
где R1, R2 имеют указанные по п.1 значения.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2011114874/05A RU2463304C1 (ru) | 2011-04-18 | 2011-04-18 | Трисдикетонатные комплексы лантанидов с лигандами пиридинового ряда в качестве люминофоров и способ их получения |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2011114874/05A RU2463304C1 (ru) | 2011-04-18 | 2011-04-18 | Трисдикетонатные комплексы лантанидов с лигандами пиридинового ряда в качестве люминофоров и способ их получения |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| RU2463304C1 true RU2463304C1 (ru) | 2012-10-10 |
Family
ID=47079512
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2011114874/05A RU2463304C1 (ru) | 2011-04-18 | 2011-04-18 | Трисдикетонатные комплексы лантанидов с лигандами пиридинового ряда в качестве люминофоров и способ их получения |
Country Status (1)
| Country | Link |
|---|---|
| RU (1) | RU2463304C1 (ru) |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE102014108142A1 (de) | 2014-03-27 | 2015-10-01 | Fraunhofer-Gesellschaft zur Förderung der angewandten Forschung e.V. | Mit einer oder mehreren Koordinationsverbindungen der Seltenen Erden belegter Nanodiamant und dessen Verwendung als lumineszierendes Material in Schichten und Formkörpern |
| RU2584208C1 (ru) * | 2014-11-17 | 2016-05-20 | Открытое акционерное общество "Центральный научно-исследовательский институт "ЦИКЛОН" | Способ получения электролюминесцентного материала 1,10-фенантролин-три-(теноилтрифторацетоната) европия (iii) для использования в производстве органических светоизлучающих диодов (осид) и структур на их основе |
| RU2620117C2 (ru) * | 2014-07-23 | 2017-05-23 | Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования "Московский государственный университет имени М.В. Ломоносова" (МГУ) | Разнолигандные комплексные соединения тербия с фенантролином, интенсивность люминесценции которых зависит от температуры |
| RU2703227C1 (ru) * | 2018-07-04 | 2019-10-15 | Федеральное государственное бюджетное учреждение науки Физический институт им. П.Н. Лебедева Российской академии наук (ФГБУН ФИАН) | Сенсорный люминесцирующий материал, способ его получения и способ определения содержания воды в исследуемой жидкости |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| SU555103A1 (ru) * | 1975-12-22 | 1977-04-25 | Институт Физической Химии Им.Л.В.Писаржевского Ан Украинской Сср | Координационные соединени лантанидов с фторированным -дикетоном в качестве лантанидного сдвигающего реагента дл мр спектроскопии |
| US20050147843A1 (en) * | 2002-03-26 | 2005-07-07 | Sumitomo Chemical Company, Limited | Metal complex and organic letroluminescent devices |
| WO2006043110A1 (en) * | 2004-10-22 | 2006-04-27 | The Queen's University Of Belfast | Light emitting complex salts |
| US7087323B2 (en) * | 2001-07-05 | 2006-08-08 | E. I. Du Pont De Nemours And Company | Photoactive lanthanide complexes with phosphine oxides, phosphine oxide-sulfides, pyridine N-oxides, and phosphine oxide-pyridine N-oxides, and devices made with such complexes |
| RU2412435C1 (ru) * | 2009-08-05 | 2011-02-20 | Государственное образовательное учреждение высшего профессионального образования Кабардино-Балкарский государственный университет им. Х.М. Бербекова | Люминесцентный способ определения тербия |
-
2011
- 2011-04-18 RU RU2011114874/05A patent/RU2463304C1/ru not_active IP Right Cessation
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| SU555103A1 (ru) * | 1975-12-22 | 1977-04-25 | Институт Физической Химии Им.Л.В.Писаржевского Ан Украинской Сср | Координационные соединени лантанидов с фторированным -дикетоном в качестве лантанидного сдвигающего реагента дл мр спектроскопии |
| US7087323B2 (en) * | 2001-07-05 | 2006-08-08 | E. I. Du Pont De Nemours And Company | Photoactive lanthanide complexes with phosphine oxides, phosphine oxide-sulfides, pyridine N-oxides, and phosphine oxide-pyridine N-oxides, and devices made with such complexes |
| US20050147843A1 (en) * | 2002-03-26 | 2005-07-07 | Sumitomo Chemical Company, Limited | Metal complex and organic letroluminescent devices |
| WO2006043110A1 (en) * | 2004-10-22 | 2006-04-27 | The Queen's University Of Belfast | Light emitting complex salts |
| RU2412435C1 (ru) * | 2009-08-05 | 2011-02-20 | Государственное образовательное учреждение высшего профессионального образования Кабардино-Балкарский государственный университет им. Х.М. Бербекова | Люминесцентный способ определения тербия |
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE102014108142A1 (de) | 2014-03-27 | 2015-10-01 | Fraunhofer-Gesellschaft zur Förderung der angewandten Forschung e.V. | Mit einer oder mehreren Koordinationsverbindungen der Seltenen Erden belegter Nanodiamant und dessen Verwendung als lumineszierendes Material in Schichten und Formkörpern |
| DE102014108142B4 (de) | 2014-03-27 | 2022-07-07 | Fraunhofer-Gesellschaft zur Förderung der angewandten Forschung e.V. | Mit einer oder mehreren Koordinationsverbindungen der Seltenen Erden belegter Nanodiamant und dessen Verwendung als lumineszierendes Material in Schichten und Formkörpern sowie Verfahren zu dessen Herstellung |
| RU2620117C2 (ru) * | 2014-07-23 | 2017-05-23 | Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования "Московский государственный университет имени М.В. Ломоносова" (МГУ) | Разнолигандные комплексные соединения тербия с фенантролином, интенсивность люминесценции которых зависит от температуры |
| RU2584208C1 (ru) * | 2014-11-17 | 2016-05-20 | Открытое акционерное общество "Центральный научно-исследовательский институт "ЦИКЛОН" | Способ получения электролюминесцентного материала 1,10-фенантролин-три-(теноилтрифторацетоната) европия (iii) для использования в производстве органических светоизлучающих диодов (осид) и структур на их основе |
| RU2703227C1 (ru) * | 2018-07-04 | 2019-10-15 | Федеральное государственное бюджетное учреждение науки Физический институт им. П.Н. Лебедева Российской академии наук (ФГБУН ФИАН) | Сенсорный люминесцирующий материал, способ его получения и способ определения содержания воды в исследуемой жидкости |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN104804045B (zh) | 近红外发光材料及有机电致发光器件 | |
| Taydakov et al. | Effective electroluminescent materials for OLED applications based on lanthanide 1.3-diketonates bearing pyrazole moiety | |
| Pertegás et al. | Host–guest blue light-emitting electrochemical cells | |
| US7862908B2 (en) | Conjugated compounds containing hydroindoloacridine structural elements, and their use | |
| JP3302945B2 (ja) | 新規な有機金属発光物質およびそれを含む有機電気発光素子 | |
| JP5924266B2 (ja) | 希土類金属錯体 | |
| KR101591484B1 (ko) | 희토 유로퓸 착물 및 발광 재료로서의 응용 | |
| WO2019153980A1 (zh) | 一种喹啉三唑类稀土配合物及其制备方法和应用 | |
| JP2020509996A (ja) | イリジウム金属配位化合物、その応用及び有機エレクトロルミネッセンス素子 | |
| Dai et al. | Iridium (iii) complexes with enhanced film amorphism as guests for efficient orange solution-processed single-layer PhOLEDs with low efficiency roll-off | |
| Huo et al. | Comparative studies on OLED performances of chloro and fluoro substituted Zn (II) 8-hydroxyquinolinates | |
| RU2463304C1 (ru) | Трисдикетонатные комплексы лантанидов с лигандами пиридинового ряда в качестве люминофоров и способ их получения | |
| TW201641509A (zh) | 雜配銥錯合物、與使用該化合物之發光材料及有機發光元件 | |
| Maheshwaran et al. | High performance solution-processed green phosphorescent organic light-emitting diodes with high current efficiency and long-term stability | |
| JP2006160724A (ja) | 金属錯体化合物及びそれを用いた有機エレクトロルミネッセンス素子 | |
| Pu et al. | Solution processable phosphorescent rhenium (I) dendrimers | |
| Rozhkov et al. | Copper (i) ionic complexes based on imidazo [4, 5-f][1, 10] phenanthrolin diimine chelating ligands: crystal structures, and photo-and electroluminescence properties | |
| KR20140117432A (ko) | 이종 리간드 금속 착물의 제조 | |
| TWI397516B (zh) | 含聯三伸苯基之芳香族化合物及有機發光二極體 | |
| WO2011125627A1 (ja) | 希土類金属錯体 | |
| WO2006080515A1 (ja) | 置換エチニル金-含窒素へテロ環カルベン錯体及びそれを用いた有機エレクトロルミネッセンス素子 | |
| CN102414178A (zh) | 具有含氮原子的芳香环配位体的金属络合物 | |
| Yu et al. | Synthesis, characterization, and photo-and electro-luminescence of new Ir (III) complexes with carrier transporting group-functionalized dibenzoylmethane ligand for green phosphorescent OLEDs | |
| RU2657496C1 (ru) | Разнолигандные фторзамещенные ароматические карбоксилаты лантанидов, проявляющие люминесцентные свойства, и органические светодиоды на их основе | |
| US20090131670A1 (en) | Bis-triphenylsilyl compounds and their application on organic electronic device |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20160419 |