RU2381103C2 - Контейнер для жидких фармацевтических композиций с высокими влагозащитными свойствами - Google Patents
Контейнер для жидких фармацевтических композиций с высокими влагозащитными свойствами Download PDFInfo
- Publication number
- RU2381103C2 RU2381103C2 RU2005139050/04A RU2005139050A RU2381103C2 RU 2381103 C2 RU2381103 C2 RU 2381103C2 RU 2005139050/04 A RU2005139050/04 A RU 2005139050/04A RU 2005139050 A RU2005139050 A RU 2005139050A RU 2381103 C2 RU2381103 C2 RU 2381103C2
- Authority
- RU
- Russia
- Prior art keywords
- container according
- liquid
- container
- polymer film
- test
- Prior art date
Links
Images
Classifications
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B32—LAYERED PRODUCTS
- B32B—LAYERED PRODUCTS, i.e. PRODUCTS BUILT-UP OF STRATA OF FLAT OR NON-FLAT, e.g. CELLULAR OR HONEYCOMB, FORM
- B32B27/00—Layered products comprising a layer of synthetic resin
- B32B27/06—Layered products comprising a layer of synthetic resin as the main or only constituent of a layer, which is next to another layer of the same or of a different material
- B32B27/08—Layered products comprising a layer of synthetic resin as the main or only constituent of a layer, which is next to another layer of the same or of a different material of synthetic resin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61J—CONTAINERS SPECIALLY ADAPTED FOR MEDICAL OR PHARMACEUTICAL PURPOSES; DEVICES OR METHODS SPECIALLY ADAPTED FOR BRINGING PHARMACEUTICAL PRODUCTS INTO PARTICULAR PHYSICAL OR ADMINISTERING FORMS; DEVICES FOR ADMINISTERING FOOD OR MEDICINES ORALLY; BABY COMFORTERS; DEVICES FOR RECEIVING SPITTLE
- A61J1/00—Containers specially adapted for medical or pharmaceutical purposes
- A61J1/05—Containers specially adapted for medical or pharmaceutical purposes for collecting, storing or administering blood, plasma or medical fluids ; Infusion or perfusion containers
- A61J1/10—Bag-type containers
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B32—LAYERED PRODUCTS
- B32B—LAYERED PRODUCTS, i.e. PRODUCTS BUILT-UP OF STRATA OF FLAT OR NON-FLAT, e.g. CELLULAR OR HONEYCOMB, FORM
- B32B1/00—Layered products having a non-planar shape
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B32—LAYERED PRODUCTS
- B32B—LAYERED PRODUCTS, i.e. PRODUCTS BUILT-UP OF STRATA OF FLAT OR NON-FLAT, e.g. CELLULAR OR HONEYCOMB, FORM
- B32B1/00—Layered products having a non-planar shape
- B32B1/08—Tubular products
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B32—LAYERED PRODUCTS
- B32B—LAYERED PRODUCTS, i.e. PRODUCTS BUILT-UP OF STRATA OF FLAT OR NON-FLAT, e.g. CELLULAR OR HONEYCOMB, FORM
- B32B27/00—Layered products comprising a layer of synthetic resin
- B32B27/28—Layered products comprising a layer of synthetic resin comprising synthetic resins not wholly covered by any one of the sub-groups B32B27/30 - B32B27/42
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B32—LAYERED PRODUCTS
- B32B—LAYERED PRODUCTS, i.e. PRODUCTS BUILT-UP OF STRATA OF FLAT OR NON-FLAT, e.g. CELLULAR OR HONEYCOMB, FORM
- B32B27/00—Layered products comprising a layer of synthetic resin
- B32B27/30—Layered products comprising a layer of synthetic resin comprising vinyl (co)polymers; comprising acrylic (co)polymers
- B32B27/304—Layered products comprising a layer of synthetic resin comprising vinyl (co)polymers; comprising acrylic (co)polymers comprising vinyl halide (co)polymers, e.g. PVC, PVDC, PVF, PVDF
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B32—LAYERED PRODUCTS
- B32B—LAYERED PRODUCTS, i.e. PRODUCTS BUILT-UP OF STRATA OF FLAT OR NON-FLAT, e.g. CELLULAR OR HONEYCOMB, FORM
- B32B27/00—Layered products comprising a layer of synthetic resin
- B32B27/32—Layered products comprising a layer of synthetic resin comprising polyolefins
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61J—CONTAINERS SPECIALLY ADAPTED FOR MEDICAL OR PHARMACEUTICAL PURPOSES; DEVICES OR METHODS SPECIALLY ADAPTED FOR BRINGING PHARMACEUTICAL PRODUCTS INTO PARTICULAR PHYSICAL OR ADMINISTERING FORMS; DEVICES FOR ADMINISTERING FOOD OR MEDICINES ORALLY; BABY COMFORTERS; DEVICES FOR RECEIVING SPITTLE
- A61J1/00—Containers specially adapted for medical or pharmaceutical purposes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M2207/00—Methods of manufacture, assembly or production
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B32—LAYERED PRODUCTS
- B32B—LAYERED PRODUCTS, i.e. PRODUCTS BUILT-UP OF STRATA OF FLAT OR NON-FLAT, e.g. CELLULAR OR HONEYCOMB, FORM
- B32B2307/00—Properties of the layers or laminate
- B32B2307/40—Properties of the layers or laminate having particular optical properties
- B32B2307/412—Transparent
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B32—LAYERED PRODUCTS
- B32B—LAYERED PRODUCTS, i.e. PRODUCTS BUILT-UP OF STRATA OF FLAT OR NON-FLAT, e.g. CELLULAR OR HONEYCOMB, FORM
- B32B2307/00—Properties of the layers or laminate
- B32B2307/70—Other properties
- B32B2307/724—Permeability to gases, adsorption
- B32B2307/7242—Non-permeable
- B32B2307/7246—Water vapor barrier
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B32—LAYERED PRODUCTS
- B32B—LAYERED PRODUCTS, i.e. PRODUCTS BUILT-UP OF STRATA OF FLAT OR NON-FLAT, e.g. CELLULAR OR HONEYCOMB, FORM
- B32B2323/00—Polyalkenes
- B32B2323/04—Polyethylene
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B32—LAYERED PRODUCTS
- B32B—LAYERED PRODUCTS, i.e. PRODUCTS BUILT-UP OF STRATA OF FLAT OR NON-FLAT, e.g. CELLULAR OR HONEYCOMB, FORM
- B32B2323/00—Polyalkenes
- B32B2323/10—Polypropylene
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B32—LAYERED PRODUCTS
- B32B—LAYERED PRODUCTS, i.e. PRODUCTS BUILT-UP OF STRATA OF FLAT OR NON-FLAT, e.g. CELLULAR OR HONEYCOMB, FORM
- B32B2327/00—Polyvinylhalogenides
- B32B2327/12—Polyvinylhalogenides containing fluorine
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B32—LAYERED PRODUCTS
- B32B—LAYERED PRODUCTS, i.e. PRODUCTS BUILT-UP OF STRATA OF FLAT OR NON-FLAT, e.g. CELLULAR OR HONEYCOMB, FORM
- B32B2439/00—Containers; Receptacles
- B32B2439/80—Medical packaging
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10T—TECHNICAL SUBJECTS COVERED BY FORMER US CLASSIFICATION
- Y10T428/00—Stock material or miscellaneous articles
- Y10T428/13—Hollow or container type article [e.g., tube, vase, etc.]
- Y10T428/1334—Nonself-supporting tubular film or bag [e.g., pouch, envelope, packet, etc.]
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10T—TECHNICAL SUBJECTS COVERED BY FORMER US CLASSIFICATION
- Y10T428/00—Stock material or miscellaneous articles
- Y10T428/13—Hollow or container type article [e.g., tube, vase, etc.]
- Y10T428/1352—Polymer or resin containing [i.e., natural or synthetic]
Landscapes
- Health & Medical Sciences (AREA)
- Mechanical Engineering (AREA)
- Engineering & Computer Science (AREA)
- Animal Behavior & Ethology (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Hematology (AREA)
- Medical Preparation Storing Or Oral Administration Devices (AREA)
- Bag Frames (AREA)
- Laminated Bodies (AREA)
- Packages (AREA)
- Wrappers (AREA)
- Compositions Of Macromolecular Compounds (AREA)
Abstract
Изобретение относится к контейнеру для хранения фармацевтического раствора, содержащего консервант в водонепроницаемой камере. Материал стенок камеры содержит два слоя. Внутренний слой выполнен из полиэтиленовой или полипропиленовой пленки. Внешний слой выполнен из полихлортрифторэтиленовой пленки. Слои неразрывно соединены между собой. Контейнер является прозрачным и оснащен устройством, через которое жидкость может выходить из него, когда это желательно. Полученный контейнер можно безопасно использовать для хранения растворов без снижения содержания в них консервантов, таких как фенол, мета-крезол и бензиловый спирт. 4 н. и 58 з.п. ф-лы, 5 ил.
Description
Область техники
Настоящее изобретение относится к прозрачному пластиковому контейнеру, который можно использовать для хранения жидких растворов или суспензий, например лекарств, которые могут содержать консерванты.
Предшествующий уровень техники
Некоторые лекарства доставляют пациентам в твердой форме, другие в жидкой форме. Часто жидкие лекарства поставляют в контейнере. Некоторые контейнеры состоят полностью или главным образом из стекла, другие контейнеры состоят полностью или главным образом из других материалов, таких как пластик. Лекарства в твердой форме часто продают в стеклянном контейнере или в пластиковом контейнере. Примером пластикового контейнера является блистерная упаковка.
В фармацевтической композиции в жидкой форме активный ингредиент находится в растворенной или суспендированной форме. В дополнение к активному ингредиенту фармацевтическая композиция может содержать фармацевтически активный носитель, разрыхлитель, стабилизатор или буферное вещество.
Для введения различных лекарств применяют разные пути введения. Некоторые лекарства вводят пероральным путем, другие вводят путем инъекции, например, внутривенной или подкожной. Многие лекарства, представляющие собой пептиды, например инсулин, вводят путем инъекций. Ранее для инъекций использовали шприцы. Теперь становится все более распространенным для введения инсулина использовать так называемые системы для инъекций карандашного типа. Кроме того, применение помп для инъекций может стать популярным путем введения лекарств посредством инъекций. В некоторых помпах водная композиция будет представлена в стеклянном резервуаре или в другом твердом резервуаре, в других помпах водная композиция будет представлена в гибком резервуаре, например в резервуаре, который полностью или главным образом выполнен из материала, иного, чем стекло, например из пластика.
Для многих водных композиций крайне затруднительно найти не стеклянный материал, который можно безопасно использовать для хранения указанной водной композиции до ее применения пациентом. Одно из множества затруднений состоит в высокой подвижности консервантов в сварном слое из полимеров, подобных полиэтилену (здесь обозначен ПЭ), полипропилену (здесь обозначен ПП), полиэтилентерефталату (здесь обозначен ПЭТ) или аналогичных, в сочетании с высоким сродством консервантов к широко применяемым клеям на полиуретановой основе, используемым для приклеивания сварного слоя к влагонепроницаемому материалу, подобному полихлортрифторэтилену (здесь обозначен ПХТФЭ). Результаты тестов известных из уровня техники пластиковых изделий, содержащих раствор лекарства с консервантами, свидетельствуют о том, что имеет место быстрое и нежелательное снижение содержания консерванта в растворе лекарства. Главной задачей авторов данного изобретения был поиск материала или комбинации материалов, которые можно использовать для изготовления прозрачного гибкого контейнера, удовлетворяющего требованиям безопасности для хранения фармацевтических растворов, содержащих консервант, такой как фенол, мета-крезол и бензиловый спирт. Было крайне сложно найти материал, удовлетворяющий этим требованиям.
Кратко, задачей данного изобретения является преодоление или уменьшение, по меньшей мере, некоторых недостатков предшествующего уровня техники.
Более конкретной задачей изобретения является создание контейнера или резервуара.
Другой задачей изобретения является создание гибкого контейнера.
Другой задачей изобретения является создание прозрачного контейнера.
Другой задачей изобретения является создание контейнера, позволяющего осуществлять стерилизацию.
Другой задачей изобретения является создание материалов, которые можно сваривать с образованием вышеупомянутого резервуара.
Другой задачей данного изобретения является создание контейнера, который можно использовать для хранения жидких растворов или суспензий лекарств, которые могут содержать консерванты.
Другой задачей изобретения является создание контейнера, который обладает достаточной прозрачностью, чтобы обеспечить контроль содержимого контейнера.
Другой задачей изобретения является создание контейнера, который можно использовать для хранения жидких растворов или суспензий лекарств, возможно, содержащих консерванты, и который не состоит или только в минимальной степени состоит из стекла.
Другой задачей изобретения является создание контейнера, обладающего барьерными свойствами, гарантирующими, что концентрация активного ингредиента в водной композиции по существу не меняется во время хранения в течение достаточного периода времени.
Другой задачей изобретения является создание контейнера, обладающего барьерными свойствами, гарантирующими, что концентрация любого консерванта, присутствующего в водной композиции, по существу не меняется во время хранения в течение достаточного периода времени.
Другой задачей изобретения является создание контейнера, который можно плотно сваривать с подходящим материалом перегородки.
Другой задачей изобретения является создание контейнера, который можно плотно склеивать с подходящим материалом перегородки иными способами, чем сварка.
Следующей задачей изобретения является создание пленки для пакета, который можно использовать для хранения лекарственного препарата на основе стерильной воды.
Следующей задачей изобретения является создание пакета, который можно использовать в качестве резервуара для помпы, и предпочтительно указанный резервуар содержит лекарственный препарат на водной основе.
Следующей задачей изобретения является создание пленочного материала для указанного пакета, удовлетворяющего некоторым функциональным требованиям, таким как физические свойства материала после стерилизации, химические требования к материалу после стерилизации и чистота.
Таким образом, одной задачей изобретения является создание пленочного материала для указанного пакета, который можно стерилизовать, например, используя гамма-излучение, электронный пучок, пар или этиленоксид.
Следующей задачей изобретения является создание пленочного материала для указанного пакета, который после стерилизации удовлетворяет большинству или всем из приведенных ниже физических требований: 1) материал должен быть прозрачным; 2) материал должен обеспечивать хороший барьер против воды; 3) материал должен обеспечивать хороший барьер против газов (например, кислорода и двуокиси углерода); 4) материал должен обеспечивать хороший барьер против консервантов (например, фенола и мета-крезола); 5) материал должен обеспечивать хороший барьер против запахов (например, консервантов); 6) материал должен быть устойчивым к разрушению стрессовыми нагрузками окружающей среды (например, масла, парфюмерия); 7) материал должен быть устойчивым к образованию трещин при изгибе; 8) материал должен обладать хорошими свойствами герметизации (например, с помощью сварки); 9) материал не должен расслаиваться после стерилизации, во время обработки или хранения и 10) материал не должен претерпевать значительную релаксацию во время хранения и использования.
Следующей задачей изобретения является создание пленочного материала для указанного пакета, который после стерилизации удовлетворяет большинству или всем из приведенных ниже химических требований: 1) материал не должен высвобождать в лекарство вещества, которые могут влиять на здоровье и безопасность пациента (выщелачиваемые вещества); 2) материал должен иметь очень низкий уровень экстрагируемых веществ и 3) материал должен быть совместимым с лекарственным препаратом.
Следующей задачей изобретения является создание пленочного материала для указанного пакета, который после стерилизации удовлетворяет приведенным ниже требованиям к чистоте: 1) должно быть возможно изготовление материала в гигиеничных условиях и 2) конечный продукт должен быть свободен от пыли и частиц.
Следующей задачей данного изобретения является создание пленочного материала для указанного пакета, который удовлетворяет некоторым требованиям здоровья и безопасности, предпочтительно большинству требований, упомянутых в 1) Европейской Фармакопее (Ph. Eur.) 2002, 4 издание; 2) Фармакопее США (USP) 25; 3) Японской Фармакопее (JP) XIV; 4) Директиве ЕЭС 90/128 + поправки (EEC Directive 90/128 + amendments) "Relating to plastics materials and articles intended to come into contact with foodstuffs"; 5) Кодексе федеральных инструкций США (CFR), Глава 21, Продукты и лекарства, часть 170-190; 6) III/9090/90 EN. Plastic Primary Packaging Materials. Note for Guidance и 7) Guidance for Industry. Container Closure Systems for Packaging Human Drugs and Biologies, Chemistry, Manufacturing, and Controls Documentation. FDA, May 1999.
Определения
Соэкструзия представляет собой процесс, при котором два или более чем два полимерных материала плавят в двух или более чем двух экструдерах и экструдируют вместе через плоскую щель или систему плоских щелей и охлаждают с получением соэкструдированной полимерной пленки.
Экструзия-ламинирование (также обозначенная как соэкструзия-ламинирование) представляет собой процесс, при котором сырье в форме полимерной пленки одного материала покрывают через плоскую щель или систему плоских щелей из одного или более чем одного экструдера одним слоем или более чем одним слоем расплавленного материала или материалов, а затем охлаждают с образованием экструзионно-ламинированной полимерной пленки.
Ламинирование представляет собой процесс, при котором два исходных материала полимерной пленки соединяют вместе путем добавления соответствующего клея к одной полимерной пленке с последующим наложением второй полимерной пленки с образованием ламинированной полимерной пленки.
Соединительный слой представляет собой слой, который помещают между двумя полимерными слоями с целью обеспечения соединения этих двух слоев вместе.
Термин “контейнер”, который здесь также обозначает пакет или резервуар, представляет собой изделие, которое может содержать жидкость. Этот контейнер выполнен из пленочного или листового материала.
Внутренний слой камеры указанного контейнера находится в непосредственном контакте с жидкостью, которая подлежит хранению в указанном контейнере.
“Наружный слой камеры контейнера” представляет собой слой, который не находится в непосредственном контакте с жидкостью, которая подлежит хранению в указанном контейнере. Иными словами, внутренний слой расположен между наружным слоем и указанной жидкостью. В отношении слоев термины “внутренний” и “наружный” относятся к положению двух слоев по отношению друг к другу, причем положение жидкости определяет направление от внутреннего к наружному. Например, данная терминология не противоречит тому, что следующий слой может быть приклеен к наружному слою с его наружной стороны, в результате чего в действительности так называемый наружный слой помещен между, с одной стороны, так называемым внутренним слоем и, с другой стороны, дополнительным слоем, приклеенным к так называемому наружному слою с его внешней стороны.
Гибкий предмет представляет собой предмет, который можно сгибать или можно легко сгибать и который не ломается (пока его не сгибают слишком сильно). Стекло не является гибким. Здесь термин “гибкий” в связи с контейнерами указывает на то, что, если контейнер подвергают воздействию силы, например, посредством наполнения его жидкостью, он будет менять свою форму не ломаясь.
Здесь термин “инсулин” относится к инсулину любого вида, такому как свиной инсулин, бычий инсулин и человеческий инсулин, и к его солям, таким как цинковые соли и протаминовые соли, а также к активным производным инсулина и аналогам инсулина. Термин “активные производные инсулина” означает то, что специалисты в данной области техники обычно рассматривают как производные, см. ряд общих учебников, например, инсулин, имеющий заместитель, не присутствующий в исходной молекуле инсулина. Термин “аналоги инсулина” относится к инсулину, где один или более чем один из аминокислотных остатков заменен другим аминокислотным остатком, и/или из которого один или более чем один из аминокислотных остатков удален, и/или в котором один или более чем один из аминокислотных остатков добавлен, при условии, что указанный аналог инсулина обладает достаточной активностью инсулина. Используя результаты так называемого анализа свободных жировых клеток, любой специалист в данной области техники, например врач, знает, когда и в каких дозировках вводить аналог инсулина. Примеры аналогов инсулина описаны в приведенных ниже патентах и их эквивалентах: US 5618913, ЕР 254516, ЕР 280534, US 5750497 и US 6011007. Примерами конкретных аналогов инсулина являются инсулин аспарт (человеческий инсулин, в котором аминокислота пролин в положении В28 замещена на аспарагиновую кислоту AspB28), инсулин лизпро (человеческий инсулин, где заместителями являются LysB28, ProB29) и инсулин гларгин (человеческий инсулин, где заместителями являются GlyA21, ArgB31, ArgB32). Здесь термин “инсулин” также охватывает соединения, которые можно считать как производными инсулина, так и аналогами инсулина. Примеры таких соединений описаны в патентах US 5750497 и US 6011007 и их эквивалентах. Примером особого аналога и производного инсулина является инсулин детемир (то есть дез-ThrB30 человеческий инсулин γ LysB29 тетрадеканоил).
Термин "U", когда его используют здесь, относится к единицам инсулина. Большинство применяемых в настоящее время (имеющихся в продаже) инсулинов (бычий, свиной, человеческий, лизпро, аспарт и гларгин) обладает эффективностью в одну единицу, которая эквивалентна 6 нмоль. Длительно действующие инсулины обладают сниженной эффективностью по сравнению с человеческим инсулином. Таким образом, для инсулина детемир одна единица соответствует 24 нмоль. Для других инсулинов отношение между U и нмоль можно определить, если оно еще не известно, например, путем определения количества, дающего фармакологический эффект (снижение глюкозы в крови), подобный эффекту человеческого инсулина.
Сущность изобретения
Кратко, данное изобретение относится к гибкому прозрачному водонепроницаемому контейнеру, состоящему из пленки, содержащей два слоя, внутренний слой и наружный слой, которые соединены вместе с образованием пленки, причем этой пленке придана форма прозрачного пакета, который обладает достаточной влагостойкостью, устойчивостью к фенолу и мета-крезолу, что дает возможность длительного хранения раствора или суспензии лекарства, содержащих воду, фенол и/или мета-крезол, без значительных изменений концентрации воды, фенола и мета-крезола в течение длительного периода времени, и который можно стерилизовать облучением.
В другом аспекте данное изобретение относится к способу хранения жидкого раствора и/или суспензии инсулина в течение значительного периода времени для применения в устройстве для доставки, включающему стадии образования пакета из прозрачной полимерной пленки, которая является достаточно водонепроницаемой, устойчивой к фенолу и мета-крезолу, что дает возможность хранения инсулина в течение двух лет без ухудшения его фармацевтических свойств; стерилизации этого пакета и помещения инсулинового соединения внутрь этого пакета для хранения в течение значительного периода времени.
Краткое описание графических материалов
Фиг.1 и 2 представляют примеры воплощений данного изобретения.
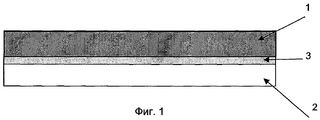
На фиг.1 показан поперечный разрез через стенку камеры в контейнере по данному изобретению. Внутренний слой 2 находится в непосредственном контакте с жидкостью, которую хранят в указанном контейнере. Обычно наружный слой 1 (который может представлять собой слой ПХТФЭ) не находится в контакте с жидкостью в контейнере. В данном воплощении изобретения, показанном на фиг.1, внутренний и наружный слои соединены вместе с использованием связующего слоя 3.
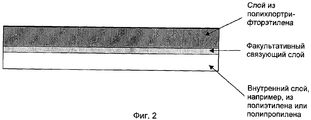
Фиг.2 идентична фиг.1, но на фиг.2 цифры из фиг.1 заменены соответствующим пояснительным текстом.
На фиг.3 изображена одна сторона гибкого контейнера. Сварная зона 4, показанная на этой фигуре, обеспечивает герметичность контейнера. Внутренняя часть 5 контейнера может быть заполнена жидкостью.
На фиг.4 изображен разрез по линии 1-1 на фиг.3, выполненный перпендикулярно поверхности, показанной на фиг.3. Стенка 6 контейнера состоит из наружного слоя 1, внутреннего слоя 2 и связующего слоя 3.
На фиг.5 показан поперечный разрез через стенку контейнера в конкретном воплощении данного изобретения и часть помещенной в контейнер жидкости.
Раскрытие предпочтительных вариантов изобретения
Было неожиданно обнаружено, что контейнер, описанный в приведенной ниже формуле изобретения, соответствует требованиям, предъявляемым к контейнеру, который следует применять для хранения водного раствора, в частности раствора лекарства, содержащего консерванты, такие как фенол или мета-крезол.
В одном аспекте данное изобретение относится к гибкому, по меньшей мере частично прозрачному контейнеру для хранения жидкости в водонепроницаемой камере, материал стенок которой содержит по меньшей мере два слоя, внутренний слой которой находится в непосредственном контакте с указанной жидкостью, когда указанная камера содержит жидкость, а наружный слой которой не находится в контакте или находится только в минимальной или в самой низкой степени в контакте с указанной жидкостью, когда указанная камера содержит жидкость, где указанные внутренний и наружный слои неразрывно соединены вместе, характеризующемуся тем, что при заполнении камеры водой и ее хранении при температуре примерно 5°С в течение 24 месяцев менее 10 мас.% воды диффундирует из контейнера и при заполнении камеры водой, содержащей примерно 1,8 мг/мл (19 мМ) фенола, и ее хранении при температуре примерно 5°С в течение 24 месяцев изменение концентрации фенола в жидкости составляет менее примерно 10 мас.%.
В другом аспекте данное изобретение относится к гибкому, по меньшей мере частично прозрачному контейнеру для хранения жидкости в водонепроницаемой камере, материал стенок которой содержит по меньшей мере два слоя, внутренний слой которой находится в непосредственном контакте с указанной жидкостью, когда камера содержит жидкость, и наружный слой которой не находится в контакте или находится только в минимальной или в самой низкой степени в контакте с указанной жидкостью, когда камера содержит жидкость, где указанные внутренний и наружный слои неразрывно соединены вместе, характеризующемуся тем, что при заполнении камеры водой и ее хранении при температуре примерно 5°С в течение 24 месяцев менее чем 10 мас.% воды диффундирует из контейнера и при заполнении камеры водой, содержащей примерно 1,8 мг/мл (19 мМ) фенола, и ее хранении при температуре примерно 37°С в течение 12 недель изменение концентрации фенола в жидкости составляет менее примерно 10 мас.%.
В предпочтительном воплощении изобретения наружный слой камеры контейнера выполнен таким образом, что он обеспечивает соблюдение требования, когда при заполнении камеры водой и ее хранении при температуре примерно 5°С в течение 24 месяцев менее чем 10 мас.%, предпочтительно менее чем 5 мас.%, более предпочтительно менее чем 3 мас.% воды диффундирует из контейнера.
В другом предпочтительном воплощении изобретения внутренний слой камеры контейнера выполнен таким образом, что он обеспечивает соблюдение требования, когда при заполнении камеры водой, содержащей примерно 1,8 мг/мл (19 мМ) фенола, и ее хранении при температуре примерно 5°С в течение 24 месяцев изменение концентрации фенола в жидкости составляет менее чем примерно 10 мас.% или когда при заполнении камеры водой, содержащей примерно 1,8 мг/мл (19 мМ) фенола, и ее хранении при температуре примерно 37°С в течение 12 недель изменение концентрации фенола в жидкости составляет менее чем примерно 10 мас.%.
Согласно другому предпочтительному воплощению изобретения внутренний слой камеры контейнера, описанного выше, является свариваемым.
Согласно другому предпочтительному воплощению изобретения внутренний слой камеры контейнера, описанного выше, имеет толщину более примерно 10 мкм, предпочтительно более примерно 20 мкм, и менее примерно 60 мкм, предпочтительно менее примерно 50 мкм, более предпочтительно менее примерно 40 мкм.
Согласно другому предпочтительному воплощению изобретения оно относится к контейнеру, описанному выше, из которого при заполнении водой и при хранении при температуре примерно 5°С в течение 24 месяцев диффундирует менее 10 мас.%, предпочтительно менее 5 мас.%, более предпочтительно менее 2 мас.% воды.
Согласно другому предпочтительному воплощению изобретения оно относится к контейнеру, описанному выше, в котором при заполнении водой, содержащей примерно 1,8 мг/мл (19 мМ) фенола, и его хранении при температуре примерно 5°С в течение 24 месяцев изменение концентрации фенола составляет менее примерно 10 мас.%, предпочтительно менее примерно 5 мас.%, более предпочтительно менее примерно 2 мас.%.
Согласно другому предпочтительному воплощению изобретения оно относится к контейнеру, описанному выше, в котором при заполнении водой, содержащей примерно 1,8 мг/мл (19 мМ) фенола, и его хранении при температуре примерно 37°С в течение 12 недель изменение концентрации фенола составляет менее примерно 10 мас.%, предпочтительно менее примерно 5 мас.%, более предпочтительно менее примерно 2 мас.%.
Согласно другому предпочтительному воплощению изобретения оно относится к контейнеру, описанному выше, в котором при заполнении водой, содержащей примерно 2,06 мг/мл (19 мМ) мета-крезола, и его хранении при температуре примерно 5°С в течение 24 месяцев изменение концентрации мета-крезола составляет менее примерно 10 мас.%, предпочтительно менее примерно 5 мас.%, более предпочтительно менее примерно 2 мас.%.
Согласно другому предпочтительному воплощению изобретения оно относится к контейнеру, описанному выше, в котором при заполнении водой, содержащей примерно 2,06 мг/мл (19 мМ) мета-крезола, и его хранении при температуре примерно 37°С в течение 12 недель изменение концентрации мета-крезола составляет менее примерно 10 мас.%, предпочтительно менее примерно 5 мас.%, более предпочтительно менее примерно 2 мас.%.
Согласно другому предпочтительному воплощению данного изобретения оно относится к контейнеру, описанному выше, который изготовлен из пакетной полимерной пленки, которая при тестировании, как описано в тесте А ниже, дает максимальную потерю мета-крезола примерно 10%, предпочтительно не более чем примерно 5%.
Согласно другому предпочтительному воплощению данного изобретения оно относится к контейнеру, описанному выше, который изготовлен из пакетной полимерной пленки, которая при тестировании, как описано в тесте А ниже, дает изменение в значении рН, которое составляет примерно +/- 0,2.
Согласно другому предпочтительному воплощению данного изобретения оно относится к контейнеру, описанному выше, который изготовлен из пакетной полимерной пленки, которая при тестировании, как описано в тесте В ниже, дает максимальную потерю массы примерно 2,5%, предпочтительно не более чем примерно 1%.
Согласно другому предпочтительному воплощению данного изобретения оно относится к контейнеру, описанному выше, который изготовлен из пакетной полимерной пленки, которая при тестировании, как описано в тесте В ниже, дает максимальную потерю мета-крезола примерно 10%, предпочтительно не более чем примерно 5%.
Согласно другому предпочтительному воплощению данного изобретения оно относится к контейнеру, описанному выше, который изготовлен из пакетной полимерной пленки, которая при тестировании, как описано в тесте В ниже, дает изменение в значении рН, которое составляет примерно +/- 0,2.
Согласно другому предпочтительному воплощению данного изобретения оно относится к контейнеру, описанному выше, который изготовлен из пакетной полимерной пленки, которая при тестировании, как описано в тесте С ниже, дает максимальную потерю массы примерно 2,5%, предпочтительно не более чем примерно 2%.
Согласно другому предпочтительному воплощению данного изобретения оно относится к контейнеру, описанному выше, который изготовлен из пакетной полимерной пленки, которая при тестировании, как описано в тесте С ниже, дает максимальную потерю мета-крезола примерно 10%, предпочтительно не более чем примерно 5%.
Согласно другому предпочтительному воплощению данного изобретения оно относится к контейнеру, описанному выше, который изготовлен из пакетной полимерной пленки, которая при тестировании, как описано в тесте С ниже, дает максимальную потерю фенола примерно 10%, предпочтительно не более чем примерно 5%.
Согласно другому предпочтительному воплощению данного изобретения оно относится к контейнеру, описанному выше, который изготовлен из пакетной полимерной пленки, которая при тестировании, как описано в тесте С ниже, дает изменение в значении рН, которое составляет примерно +/- 0,2.
Согласно другому предпочтительному воплощению данного изобретения оно относится к контейнеру, описанному выше, который изготовлен из пакетной полимерной пленки, которая удовлетворяет тесту D, описанному ниже, для разведения 1:50, предпочтительно для разведения 1:100, более предпочтительно для разведения 1:200, даже более предпочтительно для разведения 1:400.
Согласно другому предпочтительному воплощению данного изобретения оно относится к контейнеру, описанному выше, который является гибким.
Согласно другому предпочтительному воплощению данного изобретения оно относится к контейнеру, описанному выше, который оснащен устройством, посредством которого указанную жидкость можно выталкивать из указанного контейнера.
Согласно другому предпочтительному воплощению данного изобретения оно относится к контейнеру, описанному выше, который содержит дополнительный третий полимерный слой с внешней стороны слоя из ПХТФЭ.
Согласно другому предпочтительному воплощению данного изобретения оно относится к контейнеру, описанному выше, который, когда он полностью заполнен жидкостью, может содержать количество жидкости, которое составляет по меньшей мере примерно 0,5 мл, предпочтительно по меньшей мере примерно 1 мл, и не более чем примерно 10 мл, предпочтительно не более чем примерно 5 мл, более предпочтительно не более чем примерно 2 мл, и наиболее предпочтительно объем составляет примерно 1,5 мл. Согласно конкретному предпочтительному воплощению данного изобретения оно относится к контейнеру, содержащему от примерно 2 мл до примерно 4 мл, предпочтительно примерно 3 мл.
Согласно другому предпочтительному воплощению данного изобретения оно относится к контейнеру, описанному выше, который частично или полностью наполняют жидкой фармацевтической композицией.
Согласно другому предпочтительному воплощению данного изобретения оно относится к контейнеру, описанному выше, где по меньшей мере 95 объемных %, предпочтительно по меньшей мере 98 объемных %, более предпочтительно по меньшей мере 99 объемных % и даже более предпочтительно по меньшей мере 99,9 объемных % внутренней части контейнера содержит жидкую фармацевтическую композицию.
Согласно другому предпочтительному воплощению данного изобретения оно относится к контейнеру, описанному выше, который частично или полностью наполняют жидкой фармацевтической композицией, где активный ингредиент представляет собой пептид.
Согласно другому предпочтительному воплощению данного изобретения оно относится к контейнеру, описанному выше, который частично или полностью наполняют жидкой фармацевтической композицией, где активный ингредиент представляет собой инсулин.
Согласно другому предпочтительному воплощению данного изобретения оно относится к контейнеру, описанному выше, где содержание инсулина в указанном контейнере находится в интервале от примерно 10 U/мл до примерно 1500 U/мл.
Согласно другому предпочтительному воплощению данного изобретения оно относится к контейнеру, описанному выше, содержащему раствор или суспензию, которые содержат консервант.
Согласно другому предпочтительному воплощению данного изобретения оно относится к контейнеру, описанному выше, который частично или полностью наполняют жидкой фармацевтической композицией, содержащей фенол.
Согласно другому предпочтительному воплощению данного изобретения оно относится к контейнеру, описанному выше, который частично или полностью наполняют жидкой фармацевтической композицией, содержащей мета-крезол.
Согласно другому предпочтительному воплощению данного изобретения оно относится к контейнеру, описанному выше, который частично или полностью наполняют жидкой фармацевтической композицией, содержащей бензиловый спирт.
В другом аспекте данное изобретение относится к применению контейнера, описанному выше, для хранения жидкой фармацевтической композиции, как упомянуто выше.
Еще в одном аспекте данное изобретение относится к контейнеру для хранения жидкости в водонепроницаемой камере, где материал стенок этой камеры содержит по меньшей мере два слоя, где внутренний слой находится в непосредственном контакте с указанной жидкостью, когда указанная камера содержит жидкость, а другой слой, состоящий из ПХТФЭ пленки, не находится или находится только в минимальной или в самой низкой степени в контакте с указанной жидкостью, когда указанная камера содержит жидкость, где указанный внутренний слой состоит из ПЭ или ПП пленки, и либо указанный внутренний слой и указанный ПХТФЭ слой представляют собой соэкструдат или экструдат-ламинат, либо указанный внутренний слой и указанный ПХТФЭ слой соединены вместе, и толщина указанного слоя ПХТФЭ составляет более чем примерно 40 мкм и менее чем примерно 100 мкм, предпочтительно менее чем примерно 75 мкм.
Согласно предпочтительному воплощению данного изобретения оно относится к контейнеру, описанному выше, который является по меньшей мере частично прозрачным.
Согласно предпочтительному воплощению данного изобретения оно относится к контейнеру, описанному выше, который является полностью прозрачным.
Внутренний слой контейнера по данному изобретению может состоять из полиэтилена (здесь обозначен ПЭ) или полипропилена (здесь обозначен ПП) либо из смесей ПЭ и ПП. ПЭ состоит по меньшей мере из 75 мас.%, предпочтительно по меньшей мере из 90 мас.%, более предпочтительно по меньшей мере из 95 мас.% полиэтилена. ПП состоит по меньшей мере из 75 мас.%, предпочтительно по меньшей мере из 90 мас.%, более предпочтительно по меньшей мере из 95 мас.% полипропилена.
В предпочтительном воплощении данного изобретения ПЭ является таким, как определено в Европейской Фармакопее 2001, 4 издание, пункт 3.1.5, содержание которой включено здесь путем ссылки. Примеры компонентов, присутствующих в ПЭ, представляют собой гомологи высших алкенов (С3-С10) и других добавок, упомянутых там.
В предпочтительном воплощении данного изобретения ПП является таким, как определено в Европейской Фармакопее 2001, 4 издание, пункт 3.1.6, содержание которого включено здесь путем ссылки. Кратко, ПП состоит из гомополимера пропилена или из сополимера пропилена не более чем с 25% этилена или смеси (сплава) полипропилена не более чем с 25% полиэтилена. Он может содержать добавки, см. пункт 3.1.6 выше.
В предпочтительном воплощении данного изобретения внутренний слой представляет собой слой ПХТФЭ, состоящий по меньшей мере из 75%, предпочтительно по меньшей мере из 90%, более предпочтительно по меньшей мере из 95 мас.% полихлортрифторэтиленовой пленки, например, Aclar® от Honeywell, Morris Town, New Jersey, USA.
В другом предпочтительном воплощении данного изобретения наружный слой представляет собой слой ПХТФЭ, состоящий по меньшей мере из 75 мас.%, предпочтительно по меньшей мере из 90 мас.%, более предпочтительно по меньшей мере из 95 мас.% полихлортрифторэтиленовой пленки, например, Aclar® от Honeywell, Morris Town, New Jersey, USA.
Связующий слой, который можно использовать для того, чтобы внутренний и наружный слои, например ПХТФЭ слой, были соединены вместе, может состоять из клея, например полиэтиленимина (здесь обозначен ПЭИ), или любого другого подходящего связующего слоя. Альтернативно связующий слой может представлять собой полиолефин, имеющий по меньшей мере одну функциональную группу ненасыщенной карбоновой кислоты или ее ангидрида. Альтернативно связующий слой может представлять собой полиолефин, имеющий по меньшей мере одну функциональную группу ненасыщенной карбоновой кислоты или ее ангидрида. Примерами являются: Lotader, Lotryl, Evatane и Orevac, например, ATOFINA, Lavamelt, например, BAYER, PROVISTA и EASTAR, например, EASTMAN, Bynel, например, DuPont, AMPLIFY и INTEGRAL, например, Dow.
Дополнительные примеры связующих слоев упомянуты в WO 98/25762, содержание которой включено здесь путем ссылки. В качестве примера конкретного связующего слоя можно также сделать ссылку на используемый в Aclar® Сх 130 от Honeywell.
Важно выбрать связующий слой, который не влияет каким-либо нежелательным образом на готовый материал. В предпочтительном воплощении данного изобретения связующий слой является таким, что только самое низкое количество фенола, мета-крезола или бензилового спирта исчезает за период 24 месяца при температуре 5°С или за период 12 недель при температуре 27°С, когда водный раствор, содержащий примерно 1,8 мг/мл фенола помещают в контейнер согласно данному изобретению, см. тесты, описанные ниже.
Известные связующие слои имеют толщину, например, 2 или 8 мкм. Согласно предпочтительному воплощению данного изобретения оно относится к контейнеру, описанному выше, где связующий слой или связующие слои в полимерной пленке имеют толщину в интервале от примерно 1 мкм до примерно 10 мкм, предпочтительно менее чем примерно 8 мкм, более предпочтительно менее чем примерно 6 мкм.
Для изготовления контейнеров согласно данному изобретению использование соэкструдированных-ламинированных продуктов не ограничено некоторыми из конкретных полимерных слоев, упомянутых выше, таких как ПП или ПЭ и ПХТФЭ.
Примером соэкструдированного-ламинированного продукта, не изготовленного из ПП или ПЭ и ПХТФЭ, является соэкструдированная полимерная пленка ПЭ-ПЭТ, ламинированная с ПХТФЭ, которую можно изготовить путем использования стандартных методик ламинирования, известных в данной области техники. Эта структура обладает значительным барьером против подвижных молекул, подобных мета-крезолу.
Третий полимерный слой может быть нанесен на внешнюю сторону наружного слоя, например на внешнюю сторону слоя ПХТФЭ. Примерами такого третьего слоя являются ПП, ПЭ, ПЭТ-G (модифицированный полиэтилентерептатглицерин) и ТПЭ (термопластический эластомер), дающие возможность сварки с наружной стороны резервуара. На фиг.5 показан пример, где используют такой третий полимерный слой. В данном примере дополнительный слой может быть таким же или иным, чем внутренний слой. В предпочтительном воплощении данного изобретения дополнительный слой и внутренний слой идентичны или почти идентичны.
В предпочтительном воплощении данного изобретения толщина внутреннего слоя составляет по меньшей мере примерно 20 мкм, предпочтительно по меньшей мере примерно 30 мкм, и не более чем примерно 100 мкм, предпочтительно не более чем примерно 75 мкм.
Полимерная пленка для изготовления контейнера по данному изобретению, состоящая из соэкструдата, может быть изготовлена, как описано ниже.
Сырье ПХТФЭ (гранулы или порошок), сырье связующего слоя и сырье ПЭ плавят в трех отдельных экструдерах и соэкструзируют в расплавленном состоянии через плоские щели предпочтительной толщины и охлаждают, а затем формуют полимерную пленку.
Полимерная пленка для изготовления контейнера по данному изобретению, состоящая из экструдата-ламината, может быть изготовлена, как описано ниже.
Сырье полимерной пленки ПХТФЭ предпочтительной толщины обрабатывают с помощью процесса экструзии-ламинирования, где расплавленный связующий слой, который действует как уплотнитель, добавляют к полимерной пленке ПХТФЭ с последующим добавлением расплавленного сваривающего слоя, например, из ПЭ, ПП или любого другого полимера. Экструдат-ламинат охлаждают на охлаждающем барабане или подобном устройстве и вентилируют. Химическая природа связующего слоя такова, что он обладает низким сродством к ароматическим консервантам, подобным мета-крезолу и фенолу.
Полимерная пленка, полезная для производства контейнера по данному изобретению, состоящая из ламината, может быть изготовлена, как описано ниже.
Другим полезным способом изготовления ламината является использование сырья полимерной пленки ПХТФЭ предпочтительной толщины в сочетании со связующим с последующим ламинированием с полимерной пленкой предпочтительного сваривающего слоя, например, соэкструдированного ПЭТ-ПЭ предпочтительной толщины. Основой связующего, как правило, является полиуретан, обладающий низким сродством к ароматическим консервантам, подобным мета-крезолу и фенолу.
Контейнер по данному изобретению, где два слоя соединены вместе посредством сваривания, может быть изготовлен, как описано ниже.
Свариваемые слои накладывают друг на друга и сваривают вместе путем использования любой соответствующей методики сварки, известной в данной области техники, например с помощью нагревания, ультразвука, лазера или тому подобного. Наружную и внутреннюю периферию сварной зоны определяют, учитывая размер и форму резервуара.
Контейнер по данному изобретению должен обладать гибкостью, которая позволяет наполнить контейнер, так что его можно использовать в качестве пакета.
Если водная композиция содержит консервант, важно, чтобы его концентрация была достаточной для поддержания противомикробной эффективности.
В предпочтительном воплощении контейнер по данному изобретению состоит из материала, который дает возможность стерилизовать контейнер удобным способом, например β- или γ-облучением или нагреванием.
В предпочтительном воплощении контейнер по данному изобретению состоит из материала, который удовлетворят приведенному ниже тесту на гибкость.
Два прямоугольных куска тестируемого материала, оба имеющие размер 60 мм × 20 мм, сваривают вместе с 3 мм сварной зоной, образуя сваренный тестируемый пакет, а затем этот пакет наполняют 1,5 мл воды. Если избыточное давление находится ниже 100 мбар, материал обладает достаточной гибкостью.
В предпочтительном воплощении данного изобретения контейнер по данному изобретению следует использовать для хранения водной фармацевтической композиции, например раствора или суспензии фармацевтически активного соединения.
В предпочтительном воплощении данного изобретения активный ингредиент в указанной фармацевтической композиции представляет собой белок. В следующем предпочтительном воплощении данного изобретения активный ингредиент представляет собой инсулин, гормон роста или фактор VII или их аналоги. В предпочтительном воплощении данного изобретения количество инсулина в водном растворе или суспензии находится в интервале с нижним пределом примерно 10 U/мл, предпочтительно примерно 40 U/мл, более предпочтительно примерно 100 U/мл и даже более предпочтительно примерно 150 U/мл, и с верхним пределом примерно 1500 U/мл, предпочтительно примерно 1000 U/мл, более предпочтительно примерно 500 U/мл, наиболее предпочтительно примерно 300 U/мл.
В предпочтительном воплощении данного изобретения водный препарат содержит стабилизатор. В более предпочтительном воплощении данного изобретения водный препарат содержит фенол. В другом предпочтительном воплощении данного изобретения водный препарат содержит мета-крезол. В другом предпочтительном воплощении данного изобретения водный препарат содержит бензиловый спирт. В следующем предпочтительном воплощении данного изобретения суммарная концентрация фенола и/или мета-крезола в водном препарате находится в интервале от примерно 20 мМ до примерно 50 мМ, предпочтительно в интервале от примерно 30 мМ до примерно 45 мМ. Концентрация фенола и/или мета-крезола среди прочего зависит от концентрации инсулина в водном препарате. В предпочтительном воплощении данного изобретения количество фенола в водном растворе находится в интервале от примерно 15 до примерно 25 мМ. В другом предпочтительном воплощении данного изобретения количество мета-крезола в водном растворе находится в интервале от примерно 15 до примерно 25 мМ. В другом предпочтительном воплощении данного изобретения количество бензилового спирта в водном препарате находится в интервале от примерно 15 до примерно 25 мМ. В другом предпочтительном воплощении данного изобретения бензиловый спирт в водном препарате отсутствует.
При выборе материалов, которые следует использовать для изготовления контейнера по данному изобретению, важно выбрать материалы, которые не абсорбируют слишком много активного ингредиента и других ингредиентов, присутствующих в водной фармацевтической композиции.
Как указано в приведенной ниже формуле изобретения, контейнер по данному изобретению может быть оснащен устройством, посредством которого указанную жидкость можно выталкивать из указанного контейнера (когда это желательно). Примером такого устройства может быть перегородка для проникновения иглы, изготовленная из резинового материала, приклеенного к внутренней или внешней стороне полимерной пленки контейнера или в зоне сварки между двумя полимерными пленками. Другим примером может быть активный или пассивный запирающий клапан, приклеенный к контейнеру. Контейнер по данному изобретению можно опустошить путем приложения внешнего давления к резервуару или путем всасывания из помпового устройства.
Контейнер по данному изобретению можно использовать во многих устройствах, например помпе, шприце или шприце карандашного типа. Удобно, чтобы контейнер по данному изобретению был одноразовым.
Данное изобретение также относится к материалу пленки, содержащей по меньшей мере два слоя, где указанные слои неразрывно соединены вместе, который можно использовать для изготовления прозрачного контейнера согласно данному изобретению. В предпочтительном воплощении данного изобретения материал пленки можно использовать непосредственно для изготовления контейнеров, заявленных здесь. Например, материал пленки по изобретению не нужно обрабатывать, чтобы полностью прикрепить дополнительную пленку к одной из двух поверхностей.
Упоминание здесь ссылок не допускает, чтобы они составляли предшествующий уровень техники.
Слово "содержать" должно интерпретироваться в широком смысле и означает "включать", "содержать" или "состоять из" (см. Guidelines for Examination in the European Patent Office 2000, part C, chapter III, 4.13).
Методы тестирования
В предпочтительном воплощении контейнер по данному изобретению изготовлен из пакетных полимерных пленок, удовлетворяющих всем или некоторым из приведенных ниже тестов.
Тест А
Тест на потерю мета-крезола и изменение рН
Сначала стопку плоских листов А4 полимерной пленки суммарной толщиной менее 1 см подвергают облучению электронным пучком 2×25 кГц.
Затем 10 см2 (2×5 см2) полимерной пленки режут на 15 частей меньшего размера (0,7×1 см2) и погружают в 1,5 мл раствора, содержащего примерно 1,80 мг/мл (19 мМ) фенола, 2,06 мг/мл (19 мМ) мета-крезола, 16,0 мг/мл (174 мМ) глицерина, 1,25 мг/мл (7 мМ) двузамещенного гидрофосфата натрия, 0,58 мг/мл (10 мМ) хлорида натрия и рН 7,40. Погруженный образец и образец сравнения помещают в инкубатор при 37°С на 1 неделю.
Содержание мета-крезола в растворе анализируют с использованием хроматографического метода.
Этот тест должен показать суммарную миграцию мета-крезола, включая абсорбцию непосредственно в связующий слой по краю. При хранении при вышеупомянутых условиях должно выполняться следующее требование: максимальная потеря мета-крезола должна составлять 10%, а предпочтительная потеря менее чем 5%. Значение рН раствора не должно измениться более чем на +/- 0,2.
Тест В
Тест на проницаемость, потерю мета-крезола и рН
Модифицированный Тест “Чашка Паддингтона” (DS/EN 13726-2 с изменениями).
Тестируемую полимерную пленку помещают между двумя фланцами так, что 10 см2 внутренней полимерной пленки (ПЭ, ПП или любого другого сварного слоя) находятся в контакте с 5 мл раствора с рН 7,40, содержащего примерно 1,80 мг/мл (19 мМ) фенола, 2,06 мг/мл (19 мМ) мета-крезола, 16,0 мг/мл (174 мМ) глицерина, 1,25 мг/мл (7 мМ) двузамещенного гидрофосфата натрия, 0,58 мг/мл (10 мМ) хлорида натрия. Чашку Паддингтона помещают вверх дном, давая возможность прямого контакта между раствором и полимерной пленкой, в инкубаторе при 37°С и относительной влажности максимум 15% на 1 неделю параллельно со образцом сравнения, где используют чашку Паддингтона с инертной алюминиевой фольгой. Чашки Паддингтона взвешивают до и после инкубации. Содержание мета-крезола анализируют с использованием хроматографического метода. Этот тест полезен для тестирования суммарного испарения и должен показать барьерные свойства против консервантов, подобных мета-крезолу и фенолу. При хранении при вышеупомянутых условиях должно выполняться следующее требование: максимальная потеря массы должна составлять 2,5%, предпочтительно менее чем 1%, максимальная потеря мета-крезола должна составлять 10% и предпочтительно менее чем 5%, а значение рН должно измениться не более чем на +/- 0,2.
Тест С
Тестирование пакетов с носителем
В данном тесте пакеты изготавливают путем сваривания полимерной пленки и наполняют их носителем. Несколько пакетов взвешивают перед хранением при 37°С и относительной влажности 15%, а затем взвешивают в течение 12 недель. Несколько пакетов хранят при 37°С и тестируют на содержание мета-крезола и фенола через регулярные промежутки в течение 12 недель. Стеклянные флаконы используют в качестве сравнительных образцов. При хранении при вышеупомянутых условиях в течение 12 недель должно выполняться следующее требование: максимальная потеря массы должна составлять 2,5%, предпочтительно менее чем 1%, максимальная потеря мета-крезола должна составлять 10% и предпочтительно менее чем 5%, максимальная потеря фенола должна составлять 10% и предпочтительно менее чем 5%, а значение рН должно измениться не более чем на +/- 0,2.
Тест D
Прозрачность наполненного пакета
Наполненный пакет должен удовлетворять требованию к прозрачности Европейской Фармакопеи 2001, 4 издание, часть 3.2.2.1, касающемуся пластиковых контейнеров для водных растворов для парентеральной инфузии. Для данного метода раствор S разводят 1:200 (для ПЭ или ПП) или 1:400 для других контейнеров. Этот тест можно модифицировать тестированием раствора S, разведенного 1:50 или 1:100.
Приведенные ниже примеры предложены для иллюстрации, но они не ограничивают рамок изобретения.
Осуществление изобретения
Пример 1
Полихлортрифторэтилен (50 микрон) соэкструдируют с полиэтиленимином, модифицированным эпокси (связующий слой) и полиэтиленом (50 микрон). Эту соэкструдированную полимерную пленку используют для изготовления контейнера с объемом примерно 1,5 мл путем сварки нагреванием.
Пример 2
Соэкструдат ПЭ-ПЭТ ламинируют, используя клей на основе полиуретана для ламинирования Aclar® UltrR×2000 и ПЭТ, с получением структуры, подобной ПЭ-ПЭТ/Aclar® UltrR×2000/ПЭТ, где "/" показывает использование клея. Эту соэкструдированную полимерную пленку используют для изготовления контейнера с объемом примерно 1,5 мл путем сварки нагреванием.
Пример 3
Полипропилен (50 микрон) ламинируют на слой ПХТФЭ полимерной пленки, изготовленной в примере 1. Полимерная пленка, состоящая из 3 полимеров, будет полезна для изготовления пакетов с использованием сваривающего ПЭ слоя, который даст возможность приклеивания элемента, состоящего из вещества, позволяющего осуществить сварку с ПП слоем, с внешней стороны пакета.
Пример 4
Многослойную экспериментальную пленку, состоящую из ПЭ (25 мкм) и ПХТФЭ (50 мкм) со связующим слоем, полученную согласно заявке РСТ/ВЕ 03/000226 заявителя Tekni-Plex Europe N.V., с которым было заключено соглашение о конфиденциальности, тестировали с помощью упомянутых выше тестов А, В и С. Результаты этих тестов были следующими:
Тест А: Потеря мета-крезола составляла 1%. Значение рН изменилось с 7,43 до 7,35.
Тест В: Потеря мета-крезола составляла 1%. Потеря массы составляла 0,1%.
Тест С: Потеря массы составляла 1,3%. Потеря мета-крезола составляла 8,7%. Потеря фенола составляла 2,1%. Значение рН изменилось с 7,35 до 7,20 для лекарственного продукта.
Claims (62)
1. Гибкий, по меньшей мере частично прозрачный контейнер для хранения фармацевтического раствора, содержащего консервант, в водонепроницаемой камере, материал стенок которой содержит по меньшей мере два слоя, внутренний слой которой находится в непосредственном контакте с указанной жидкостью, когда камера содержит жидкость, и наружный слой которой не находится в контакте с указанной жидкостью, когда камера содержит жидкость, где указанные внутренний и наружный слои неразрывно соединены вместе, характеризующийся тем, что при заполнении камеры водой и ее хранении при температуре примерно 5°С в течение 24 месяцев, менее 10 мас.%, предпочтительно менее 5 мас.%, более предпочтительно менее 3 мас.% воды диффундирует из контейнера; и при заполнении камеры водой, содержащей примерно 1,8 мг/мл фенола и ее хранении при температуре примерно 5°С в течение 24 месяцев или ее хранении при температуре примерно 37°С в течение 12 недель, изменение концентрации фенола в жидкости составляет менее примерно 10 мас.%, предпочтительно менее 5 мас.%, более предпочтительно менее 3 мас.%, и при заполнении камеры водой, содержащей примерно 2,06 мг/мл метакрезола, и хранении при температуре примерно 5°С в течение 24 месяцев или хранении при температуре примерно 37°С в течение 12 недель, изменение концентрации метакрезола составляет менее примерно 10 мас.%, предпочтительно менее примерно 5 мас.%, более предпочтительно менее примерно 2 мас.%.
2. Контейнер по п.1, в котором толщина внутреннего слоя составляет более примерно 10 мкм, предпочтительно более примерно 20 мкм, и менее примерно 60 мкм, предпочтительно менее примерно 50 мкм, более предпочтительно менее примерно 40 мкм.
3. Контейнер по п.1, из которого при наполнении водой и при хранении при температуре примерно 5°С в течение 24 месяцев диффундирует менее 10 мас.%, предпочтительно менее 5 мас.%, более предпочтительно менее 2 мас.% воды.
4. Контейнер по п.1, где наружный слой камеры контейнера выполнен таким образом, что он обеспечивает соблюдение требования, когда при заполнении камеры водой и ее хранении при температуре примерно 5°С в течение 24 месяцев, менее 10 мас.%, предпочтительно менее 5 мас.%, более предпочтительно менее 3 мас.% воды диффундирует из контейнера.
5. Контейнер по п.1, где внутренний слой камеры контейнера выполнен таким образом, что он обеспечивает соблюдение требования, когда при заполнении камеры водой, содержащей примерно 1,8 мг/мл фенола, и ее хранении при температуре примерно 5°С в течение 24 месяцев, изменение концентрации фенола в жидкости составляет менее примерно 10 мас.%, предпочтительно менее 5 мас.%, более предпочтительно менее 3 мас.%; или когда при заполнении камеры водой, содержащей примерно 1,8 мг/мл фенола, и ее хранении при температуре примерно 37°С в течение 12 недель, изменение концентрации фенола в жидкости составляет менее примерно 10 мас.%, предпочтительно менее 5 мас.%, более предпочтительно менее 3 мас.%.
6. Контейнер по п.1, где внутренний слой является свариваемым.
7. Контейнер по п.1, отличающийся тем, что изготовлен из пакетной полимерной пленки, которая при тестировании тестом А, описанным выше, дает максимальную потерю метакрезола примерно 10 мас.%, предпочтительно не более примерно 5 мас.%.
8. Контейнер п.1, который изготовлен из пакетной полимерной пленки, которая при тестировании тестом А, описанным выше, дает изменение значения рН не более примерно +/- 0,2.
9. Контейнер по п.1, который изготовлен из пакетной полимерной пленки, которая при тестировании тестом В, описанным выше, дает максимальную потерю массы примерно 2,5 мас.%, предпочтительно не более примерно 1 мас.%.
10. Контейнер по п.1, который изготовлен из пакетной полимерной пленки, которая при тестировании тестом В, описанным выше, дает максимальную потерю метакрезола примерно 10 мас.%, предпочтительно не более примерно 5 мас.%.
11. Контейнер по п.1, который изготовлен из пакетной полимерной пленки, которая при тестировании тестом В, описанным выше, дает изменение значения рН не более примерно +/- 0,2.
12. Контейнер по п.1, который изготовлен из пакетной полимерной пленки, которая при тестировании тестом С, описанным выше, дает максимальную потерю массы примерно 2,5 мас.%, предпочтительно не более примерно 1 мас.%.
13. Контейнер по п.1, который изготовлен из пакетной полимерной пленки, которая при тестировании тестом С, описанным выше, дает максимальную потерю метакрезола примерно 10 мас.%, предпочтительно не более примерно 5 мас.%.
14. Контейнер по п.1, который изготовлен из пакетной полимерной пленки, которая при тестировании тестом С, описанным выше, дает максимальную потерю фенола примерно 10 мас.%, предпочтительно не более чем примерно 5 мас.%.
15. Контейнер по п.1, который изготовлен из пакетной полимерной пленки, которая при тестировании тестом С, описанным выше, дает изменение значения рН не более чем примерно +/- 0,2.
16. Контейнер по п.1, который изготовлен из пакетной полимерной пленки, которая удовлетворяет тесту D, описанному выше, для разведения 1:50, предпочтительно для разведения 1:100, более предпочтительно для разведения 1:200, наиболее предпочтительно для разведения 1:400.
17. Контейнер по п.1, в котором толщина связующего слоя или связующих слоев в полимерной пленке находится в интервале от примерно 1 мкм до примерно 10 мкм, предпочтительно менее примерно 8 мкм, более предпочтительно менее примерно 6 мкм.
18. Контейнер по п.1, отличающийся тем, что оснащен устройством, посредством которого из него можно выталкивать жидкость.
19. Контейнер по п.1, отличающийся тем, что содержит дополнительный третий полимерный слой с внешней стороны полихлортрифторэтиленового слоя.
20. Контейнер по п.1, отличающийся тем, что когда он полностью заполнен жидкостью, может содержать по меньшей мере примерно 0,5 мл жидкости, предпочтительно по меньшей мере примерно 1 мл жидкости, и не более примерно 10 мл жидкости, предпочтительно не более примерно 5 мл жидкости, более предпочтительно не более примерно 2 мл жидкости, и предпочтительно объем жидкости составляет примерно 1,5 мл.
21. Контейнер по п.1, отличающийся тем, что когда он полностью заполнен жидкостью, может содержать от примерно 2 мл до примерно 4 мл жидкости, предпочтительно примерно 3 мл жидкости.
22. Контейнер по п.1, частично или полностью наполненный жидкой фармацевтической композицией.
23. Контейнер по п.22, в котором содержащаяся жидкая фармацевтическая композиция занимает по меньшей мере 95 об.%, предпочтительно по меньшей мере 98 об.%, более предпочтительно по меньшей мере 99 об.% и наиболее предпочтительно по меньшей мере 99,9 об.% внутренней части контейнера.
24. Контейнер по п.1, частично или полностью наполненный жидкой фармацевтической композицией, где активный ингредиент представляет собой пептид.
25. Контейнер по п.24, где пептид представляет собой инсулин.
26. Контейнер по п.25, где содержание инсулина находится в интервале от примерно 10 U/мл до примерно 1500 U/мл.
27. Контейнер по п.1, содержащий консервант.
28. Контейнер по п.1, частично или полностью наполненный жидкой фармацевтической композицией, содержащей фенол.
29. Контейнер по п.1, частично или полностью наполненный жидкой фармацевтической композицией, содержащей метакрезол.
30. Контейнер по п.1, частично или полностью наполненный жидкой фармацевтической композицией, содержащей бензиловый спирт.
31. Контейнер для хранения фармацевтического раствора, содержащего консервант, в водонепроницаемой камере, материал стенок которой содержит по меньшей мере два слоя, внутренний слой которой находится в непосредственном контакте с указанной жидкостью, когда камера содержит жидкость, а другой слой, состоящий из полихлортрифторэтиленовой пленки, которая не находится в контакте с указанной жидкостью, когда камера содержит жидкость, где указанный внутренний слой состоит из полиэтиленовой или полипропиленовой пленки, и либо указанный внутренний слой и указанный полихлортрифторэтиленовый слой представляют собой соэкструдат или экструдат-ламинат, либо указанный внутренний слой и указанный полихлотрифторэтиленовый слой соединены вместе, и толщина полихлортрифторэтиленового слоя составляет более примерно 40 мкм и менее примерно 100 мкм, предпочтительно менее примерно 75 мкм.
32. Контейнер по п.31, отличающийся тем, что является по меньшей мере частично прозрачный.
33. Контейнер по п.31, отличающийся тем, что является полностью прозрачным.
34. Контейнер по п.1, отличающийся тем, что изготовлен из пакетной полимерной пленки, которая при тестировании тестом А, описанным выше, дает максимальную потерю метакрезола примерно 10 мас.%, предпочтительно не более примерно 5 мас.%.
35. Контейнер п.31, который изготовлен из пакетной полимерной пленки, которая при тестировании тестом А, описанным выше, дает изменение значения рН не более примерно +/- 0,2.
36. Контейнер по п.31, который изготовлен из пакетной полимерной пленки, которая при тестировании тестом В, описанным выше, дает максимальную потерю массы примерно 2,5 мас.%, предпочтительно не более примерно 1 мас.%.
37. Контейнер по п.31, который изготовлен из пакетной полимерной пленки, которая при тестировании тестом В, описанным выше, дает максимальную потерю метакрезола примерно 10 мас.%, предпочтительно не более примерно 5 мас.%.
38. Контейнер по п.31, который изготовлен из пакетной полимерной пленки, которая при тестировании тестом В, описанным выше, дает изменение значения рН не более примерно +/- 0,2.
39. Контейнер по п.31, который изготовлен из пакетной полимерной пленки, которая при тестировании тестом С, описанным выше, дает максимальную потерю массы примерно 2,5 мас.%, предпочтительно не более примерно 1 мас.%.
40. Контейнер по п.31, который изготовлен из пакетной полимерной пленки, которая при тестировании тестом С, описанным выше, дает максимальную потерю метакрезола примерно 10 мас.%, предпочтительно не более примерно 5 мас.%.
41. Контейнер по п.31, который изготовлен из пакетной полимерной пленки, которая при тестировании тестом С, описанным выше, дает максимальную потерю фенола примерно 10 мас.%, предпочтительно не более чем примерно 5 мас.%.
42. Контейнер по п.31, который изготовлен из пакетной полимерной пленки, которая при тестировании тестом С, описанным выше, дает изменение значения рН не более чем примерно +/- 0,2.
43. Контейнер по п.31, который изготовлен из пакетной полимерной пленки, которая удовлетворяет тесту D, описанному выше, для разведения 1:50, предпочтительно для разведения 1:100, более предпочтительно для разведения 1:200, наиболее предпочтительно для разведения 1:400.
44. Контейнер по п.31, в котором толщина связующего слоя или связующих слоев в полимерной пленке находится в интервале от примерно 1 мкм до примерно 10 мкм, предпочтительно менее примерно 8 мкм, более предпочтительно менее примерно 6 мкм.
45. Контейнер по п.31, отличающийся тем, что он является гибким.
46. Контейнер по п.31, отличающийся тем, что оснащен устройством, посредством которого из него можно выталкивать жидкость.
47. Контейнер по п.31, отличающийся тем, что содержит дополнительный третий полимерный слой с внешней стороны полихлортрифторэтиленового слоя.
48. Контейнер по п.31, отличающийся тем, что когда он полностью заполнен жидкостью, может содержать по меньшей мере примерно 0,5 мл жидкости, предпочтительно по меньшей мере примерно 1 мл жидкости, и не более примерно 10 мл жидкости, предпочтительно не более примерно 5 мл жидкости, более предпочтительно не более примерно 2 мл жидкости, и предпочтительно объем жидкости составляет примерно 1,5 мл.
49. Контейнер по п.31, отличающийся тем, что когда он полностью заполнен жидкостью, может содержать от примерно 2 мл до примерно 4 мл жидкости, предпочтительно примерно 3 мл жидкости.
50. Контейнер по п.31, частично или полностью наполненный жидкой фармацевтической композицией.
51. Контейнер по п.31, в котором содержащаяся жидкая фармацевтическая композиция занимает по меньшей мере 95 об.%, предпочтительно по меньшей мере 98 об.%, более предпочтительно по меньшей мере 99 об.% и наиболее предпочтительно по меньшей мере 99,9 об.% внутренней части контейнера.
52. Контейнер по п.31, частично или полностью наполненный жидкой фармацевтической композицией, где активный ингредиент представляет собой пептид.
53. Контейнер по п.52, где пептид представляет собой инсулин.
54. Контейнер по п.53, где содержание инсулина находится в интервале от примерно 10 U/мл до примерно 1500 U/мл.
55. Контейнер по п.31, содержащий консервант.
56. Контейнер по п.31, частично или полностью наполненный жидкой фармацевтической композицией, содержащей фенол.
57. Контейнер по п.31, частично или полностью наполненный жидкой фармацевтической композицией, содержащей метакрезол.
58. Контейнер по п.31, частично или полностью наполненный жидкой фармацевтической композицией, содержащей бензиловый спирт.
59. Контейнер по п.31, в котором при заполнении его водой, содержащей примерно 2,06 мг/мл метакрезола, и хранении при температуре примерно 5°С в течение 24 месяцев, изменение концентрации метакрезола составляет менее примерно 10 мас.%, предпочтительно менее примерно 5 мас.%, более предпочтительно менее примерно 2 мас.%.
60. Контейнер по п.31, в котором при заполнении его водой, содержащей примерно 2,06 мг/мл метакрезола, и хранении при температуре примерно 37°С в течение 12 недель, изменение концентрации метакрезола составляет менее примерно 10 мас.%, предпочтительно менее примерно 5 мас.%, более предпочтительно менее примерно 2 мас.%.
61. Применение контейнера по любому из пп.1-60 для хранения жидкой фармацевтической композиции, упомянутой в любом из предшествующих пунктов.
62. Материал пленки, содержащей по меньшей мере два слоя, где указанные слои неразрывно соединены вместе, который можно использовать для изготовления прозрачного контейнера по любому из пп.1-60.
Applications Claiming Priority (17)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DKPA200300971 | 2003-06-27 | ||
| DKPA200300971 | 2003-06-27 | ||
| US50471503P | 2003-09-22 | 2003-09-22 | |
| US60/504,715 | 2003-09-22 | ||
| US52334903P | 2003-11-19 | 2003-11-19 | |
| DKPA200301717 | 2003-11-19 | ||
| US60/523,349 | 2003-11-19 | ||
| DKPA200301717 | 2003-11-19 | ||
| US52479303P | 2003-11-25 | 2003-11-25 | |
| DKPA200301741 | 2003-11-25 | ||
| US60/524,793 | 2003-11-25 | ||
| DKPA200301741 | 2003-11-25 | ||
| US52546903P | 2003-11-26 | 2003-11-26 | |
| DKPA200301746 | 2003-11-26 | ||
| US60/525,469 | 2003-11-26 | ||
| DKPA200301746 | 2003-11-26 | ||
| PCT/DK2004/000440 WO2005000580A1 (en) | 2003-06-27 | 2004-06-23 | High moisture barrier container for medical liquid compositions |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU2005139050A RU2005139050A (ru) | 2006-06-27 |
| RU2381103C2 true RU2381103C2 (ru) | 2010-02-10 |
Family
ID=36596200
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2005139050/04A RU2381103C2 (ru) | 2003-06-27 | 2004-06-23 | Контейнер для жидких фармацевтических композиций с высокими влагозащитными свойствами |
Country Status (12)
| Country | Link |
|---|---|
| US (1) | US8399078B2 (ru) |
| EP (2) | EP1641616B1 (ru) |
| JP (1) | JP4781264B2 (ru) |
| KR (1) | KR20060029154A (ru) |
| CN (1) | CN1791511A (ru) |
| AT (1) | ATE505323T1 (ru) |
| AU (1) | AU2004251810B2 (ru) |
| CA (1) | CA2529023A1 (ru) |
| DE (1) | DE602004032237D1 (ru) |
| PL (1) | PL1641616T3 (ru) |
| RU (1) | RU2381103C2 (ru) |
| WO (1) | WO2005000580A1 (ru) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2545451C2 (ru) * | 2010-11-15 | 2015-03-27 | Ф. Хоффманн-Ля Рош Аг | Контейнер для хранения медицинских или фармацевтических жидкостей |
| RU2813063C2 (ru) * | 2019-06-26 | 2024-02-06 | Сева Санте Анималь | Полимерная упаковка, ее применение для хранения стерильной фармацевтической композиции и способ хранения стерильной фармацевтической композиции |
Families Citing this family (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE602004032237D1 (de) | 2003-06-27 | 2011-05-26 | Novo Nordisk As | Behälter für medizinische flüssigkeiten mit hoher wasserdampfsperre |
| DE602004029496D1 (de) * | 2003-12-22 | 2010-11-18 | Novo Nordisk As | Offbehälter zur lagerung von pharmazeutischen flüssigkeiten |
| EP1738896A1 (en) * | 2005-06-28 | 2007-01-03 | Novo Nordisk A/S | Multilayer film with septum layer |
| CN101365505A (zh) * | 2006-01-06 | 2009-02-11 | 诺沃-诺迪斯克有限公司 | 使用收缩式储存器的药物输送设备 |
| ATE506080T1 (de) | 2006-02-28 | 2011-05-15 | Novo Nordisk As | Verfahren zur strahlungs-sterilisation von kunststoff-verpackungsmaterial für insulin |
| WO2008058997A2 (en) * | 2006-11-14 | 2008-05-22 | Novo Nordisk A/S | Adaptive hypoglycaemia alert system and method |
| WO2008148176A1 (en) * | 2007-06-08 | 2008-12-11 | Tekni-Plex Europe, Naamloze Vennootschap | Multi-layer high moisture barrier film for use in the production of pharmaceutical or medical thermoformed blister packs and a method for manufacturing such a film |
| WO2011083055A1 (en) | 2010-01-05 | 2011-07-14 | Novo Nordisk A/S | Method for forming collapsible reservoir |
| EP2556815A1 (en) * | 2011-08-10 | 2013-02-13 | Debiotech S.A. | Container for storing a drug such as insulin |
| JP5849001B2 (ja) * | 2012-03-23 | 2016-01-27 | 第一三共株式会社 | Ptp又はブリスターパック用積層体、及びこれを用いて成形されたptp又はブリスターパック |
| US9068565B2 (en) * | 2012-05-03 | 2015-06-30 | Becton, Dickinson And Company | Container and method for storing a pharmaceutical agent |
| CN102794961B (zh) * | 2012-08-28 | 2015-05-13 | 常州大学 | 一种三层共挤输液用膜及其制备方法 |
| JP7071063B2 (ja) | 2017-05-01 | 2022-05-18 | 藤森工業株式会社 | 包装袋 |
| US20200346445A1 (en) * | 2019-05-02 | 2020-11-05 | Honeywell International Inc. | Multi-layer article for storing a product |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3403064A (en) * | 1963-09-12 | 1968-09-24 | Baxter Laboratories Inc | Method of forming a composite plastic container with an inner and outer seal |
| RU2208517C2 (ru) * | 1997-02-24 | 2003-07-20 | Бакстер Биотек Текнолоджи С.А.Р.Л. | Совместно экструдированные многослойные пленки для стерилизуемых емкостей для жидкости |
| RU2291681C2 (ru) * | 1996-05-13 | 2007-01-20 | Б. Браун Медикал, Инк. | Гибкая имеющая множество отделений емкость многоцелевого назначения |
| RU2300365C2 (ru) * | 2005-03-02 | 2007-06-10 | Михаил Юрьевич Попов | Контейнер для крови и/или компонентов крови |
Family Cites Families (72)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3087491A (en) * | 1958-03-14 | 1963-04-30 | Baxter Laboratories Inc | Parenteral solution equipment and method of making |
| CA1079231A (en) | 1976-12-16 | 1980-06-10 | Baxter Travenol Laboratories | Flexible collapsible container defining relatively rigid shoulder and base at opposite end |
| US4212299A (en) * | 1977-06-07 | 1980-07-15 | Toppan Printing Co., Ltd. | Container bag |
| JPS5950342B2 (ja) | 1978-01-27 | 1984-12-07 | 凸版印刷株式会社 | 冷凍保存用袋 |
| JPS6051438B2 (ja) * | 1979-12-21 | 1985-11-13 | 三井化学株式会社 | ラミネ−ト物の製造方法及びそれに用いる押出用ダイ |
| US4435135A (en) | 1981-04-03 | 1984-03-06 | Seaquist Valve Company | Pump assembly with improved seal |
| DE3275711D1 (en) | 1982-12-24 | 1987-04-23 | Toppan Printing Co Ltd | Multi-layered hollow container |
| EP0132583B1 (en) | 1983-08-01 | 1988-09-14 | Ausimont, U.S.A., Inc. | Coextrusion of thermoplastic fluoropolymers with thermoplastic polymers |
| DK347086D0 (da) | 1986-07-21 | 1986-07-21 | Novo Industri As | Novel peptides |
| PH25772A (en) | 1985-08-30 | 1991-10-18 | Novo Industri As | Insulin analogues, process for their preparation |
| US4874386A (en) * | 1986-12-05 | 1989-10-17 | Sta-Set Corporation | Fluid dispensing device |
| FI884914A7 (fi) | 1987-02-25 | 1988-10-24 | Novo Nordisk As | Uusia insuliinijohdannaisia |
| JPS63224944A (ja) | 1987-03-16 | 1988-09-20 | 住友ベークライト株式会社 | 多層フイルムの製造方法 |
| US5000739A (en) * | 1988-07-12 | 1991-03-19 | Pinewood Medical, Inc. | Programmable infusion pump |
| US4857053A (en) | 1988-08-29 | 1989-08-15 | Dalton Michael J | Matrix septum |
| US5205820A (en) * | 1989-06-16 | 1993-04-27 | Science, Incorporated | Fluid delivery apparatus |
| US5176634A (en) * | 1990-08-02 | 1993-01-05 | Mcgaw, Inc. | Flexible multiple compartment drug container |
| US5366839A (en) * | 1990-08-03 | 1994-11-22 | Tomoegawa Paper Co., Ltd. | Toner for electrostatic charge image |
| JPH06511271A (ja) | 1991-09-27 | 1994-12-15 | アライド−シグナル・インコーポレーテッド | 高バリヤー性pctfeフィルム |
| EP0605558A1 (en) | 1991-09-27 | 1994-07-13 | AlliedSignal Inc. | Barrier film |
| US6011007A (en) | 1993-09-17 | 2000-01-04 | Novo Nordisk A/S | Acylated insulin |
| DK0792290T3 (da) | 1993-09-17 | 2001-10-01 | Novo Nordisk As | Acyleret insulin |
| CH686881A5 (it) | 1993-12-17 | 1996-07-31 | Bieffe Medital Sa | Film a strati coestrusi per contenitori di soluzioni parenterali. |
| JP3672617B2 (ja) * | 1994-05-25 | 2005-07-20 | 呉羽化学工業株式会社 | ポリクロロトリフルオロエチレン延伸フィルム、その製造方法および該フィルムを用いる包装体 |
| JP3125636B2 (ja) * | 1994-08-10 | 2001-01-22 | 住友化学工業株式会社 | 包装袋又は包装容器 |
| DE19509632C1 (de) | 1995-03-17 | 1996-03-28 | Fresenius Ag | Implantierbare Infusionspumpe |
| US5928213A (en) * | 1996-05-13 | 1999-07-27 | B. Braun Medical, Inc. | Flexible multiple compartment medical container with preferentially rupturable seals |
| US5944709A (en) * | 1996-05-13 | 1999-08-31 | B. Braun Medical, Inc. | Flexible, multiple-compartment drug container and method of making and using same |
| US5910138A (en) * | 1996-05-13 | 1999-06-08 | B. Braun Medical, Inc. | Flexible medical container with selectively enlargeable compartments and method for making same |
| US5945221A (en) | 1996-06-20 | 1999-08-31 | Alliedsignal Inc. | Biaxial orientation of fluoropolymer films |
| US5874035A (en) * | 1996-06-20 | 1999-02-23 | Alliedsignal Inc. | Highly oriented fluoropolymer films |
| JP2001501504A (ja) * | 1996-09-20 | 2001-02-06 | ノボ ノルディスク アクティーゼルスカブ | 作動シリンダ |
| PL334252A1 (en) * | 1996-12-23 | 2000-02-14 | Novo Nordisk As | Cyclic hydrocarbon polymer therapeutic agent holding container for storing a liquid therapeutic agent |
| US6530900B1 (en) | 1997-05-06 | 2003-03-11 | Elan Pharma International Limited | Drug delivery device |
| US6306503B1 (en) * | 1997-06-11 | 2001-10-23 | Alliedsignal Inc. | Multilayer fluoropolymer films with improved adhesion |
| US6139931A (en) * | 1997-07-10 | 2000-10-31 | Tri-Seal Holdings, Inc. | High barrier closure liner for carbonated beverage containers and the like |
| EP1445910A3 (de) * | 1997-10-15 | 2005-03-02 | Nokia Corporation | Verfahren zum Bereitstellen von Information in einem Kommunikationssystem mittels eines mobilen Telefons |
| US6432542B1 (en) * | 1997-11-06 | 2002-08-13 | Alliedsignal Inc. | Multicomponent structures having improved adhesion |
| DE19753266B4 (de) | 1997-12-01 | 2010-10-07 | H.B. Fuller Licensing & Financing, Inc., St. Paul | Verfahren zum Verbinden luftundurchlässiger Materialien |
| US6183460B1 (en) | 1998-01-22 | 2001-02-06 | Baxter International Inc. | Multi-use solution container having flaps |
| DE19850607A1 (de) | 1998-11-03 | 2000-05-04 | Rolf Siegel | Behältnis für in flüssiger Phase vorliegende biologisch aktive Substanzen, Zellen oder Zellorganellen, sowie diesbezügliches Herstellungsverfahren |
| US6287652B2 (en) | 1998-12-09 | 2001-09-11 | Color Prelude, Inc. | Fluid product sampler package with clear moisture vapor barrier film |
| AR024246A1 (es) | 1999-03-01 | 2002-09-25 | Johnson & Johnson Vision Care | Contenedor para dispositivo medico. |
| BE1012589A3 (fr) | 1999-04-08 | 2000-12-05 | Solvay | Structure thermoplastique multicouche. |
| AU3403201A (en) * | 2000-02-10 | 2001-08-20 | Power Paper Ltd. | Drug delivery device and method |
| JP4492985B2 (ja) | 2000-02-24 | 2010-06-30 | 三菱商事プラスチック株式会社 | 液体医薬品用プラスチック容器及び液体医薬品の保存回収方法 |
| US6572542B1 (en) * | 2000-03-03 | 2003-06-03 | Medtronic, Inc. | System and method for monitoring and controlling the glycemic state of a patient |
| US6692472B2 (en) * | 2000-05-04 | 2004-02-17 | Novo Nordisk A/S | Injection device, a preassembled dose setting and injection mechanism for an injection device, and a method of assembling an injection device |
| JP2002028999A (ja) * | 2000-05-11 | 2002-01-29 | Mitsui Chemicals Inc | ガスバリアフィルム積層体 |
| EP2363061A1 (en) * | 2000-06-16 | 2011-09-07 | BodyMedia, Inc. | System for monitoring and managing body weight and other physiological conditions including iterative and personalized planning, intervention and reporting capability |
| ES2267784T3 (es) | 2000-06-23 | 2007-03-16 | Honeywell International Inc. | Peliculas de alta proteccion contra la humedad. |
| ATE386560T1 (de) * | 2000-11-03 | 2008-03-15 | Allergan Medical S A | Implantierbare medizinische vorrichtung zum abgeben einer flüssigkeit |
| US6699218B2 (en) | 2000-11-09 | 2004-03-02 | Insulet Corporation | Transcutaneous delivery means |
| AU2002222820A1 (en) | 2001-11-23 | 2003-06-10 | Medit As | A cluster system for remote monitoring and diagnostic support |
| US6592978B1 (en) * | 2002-02-01 | 2003-07-15 | Kloeckner Pentaplast Of America, Inc. | Three part high moisture barrier for packages |
| US20030203141A1 (en) | 2002-04-25 | 2003-10-30 | Blum John B. | Blister package |
| US6979316B1 (en) | 2002-05-23 | 2005-12-27 | Seedlings Life Science Ventures Llc | Apparatus and method for rapid auto-injection of medication |
| US7025754B2 (en) * | 2002-07-01 | 2006-04-11 | Ventaira Pharmaceuticals, Inc. | Drug containment system |
| FR2850027B1 (fr) | 2003-01-21 | 2005-09-16 | Medex Sa | Dispositif d'injection de liquide medical |
| DE20306931U1 (de) | 2003-05-06 | 2003-07-10 | Kka Kleinewefers Anlagen Gmbh | Vorrichtung zur Beschichtung einer Warenbahn |
| AU2003902187A0 (en) | 2003-05-08 | 2003-05-22 | Aimedics Pty Ltd | Patient monitor |
| DE602004032237D1 (de) | 2003-06-27 | 2011-05-26 | Novo Nordisk As | Behälter für medizinische flüssigkeiten mit hoher wasserdampfsperre |
| PL1677668T3 (pl) | 2003-10-13 | 2010-12-31 | Novo Nordisk As | Sposób i urządzenie do określania stanu fizjologicznego |
| EP1525873A1 (en) | 2003-10-23 | 2005-04-27 | Novo Nordisk A/S | Container with septum member |
| ES2354814T3 (es) * | 2003-12-18 | 2011-03-18 | Tekni-Plex Europe Nv | Película para envasar líquidos o similares y método para fabricar tal película. |
| DE602004029496D1 (de) * | 2003-12-22 | 2010-11-18 | Novo Nordisk As | Offbehälter zur lagerung von pharmazeutischen flüssigkeiten |
| GB0405798D0 (en) | 2004-03-15 | 2004-04-21 | E San Ltd | Medical data display |
| US8554480B2 (en) * | 2004-03-25 | 2013-10-08 | Siemens Medical Solutions Usa, Inc. | Treatment data processing and planning system |
| US8313308B2 (en) * | 2004-03-26 | 2012-11-20 | Hospira, Inc. | Medical infusion pump with closed loop stroke feedback system and method |
| JP2008510476A (ja) * | 2004-08-27 | 2008-04-10 | ノボ ノルディスク ヘルス ケア アクチェンゲゼルシャフト | 生物学的材料からのxiii因子ポリペプチドの精製 |
| CN101365505A (zh) | 2006-01-06 | 2009-02-11 | 诺沃-诺迪斯克有限公司 | 使用收缩式储存器的药物输送设备 |
| WO2008058997A2 (en) | 2006-11-14 | 2008-05-22 | Novo Nordisk A/S | Adaptive hypoglycaemia alert system and method |
-
2004
- 2004-06-23 DE DE602004032237T patent/DE602004032237D1/de not_active Expired - Lifetime
- 2004-06-23 PL PL04738937T patent/PL1641616T3/pl unknown
- 2004-06-23 CN CNA2004800132575A patent/CN1791511A/zh active Pending
- 2004-06-23 RU RU2005139050/04A patent/RU2381103C2/ru not_active IP Right Cessation
- 2004-06-23 AU AU2004251810A patent/AU2004251810B2/en not_active Ceased
- 2004-06-23 EP EP04738937A patent/EP1641616B1/en not_active Expired - Lifetime
- 2004-06-23 WO PCT/DK2004/000440 patent/WO2005000580A1/en not_active Ceased
- 2004-06-23 CA CA002529023A patent/CA2529023A1/en not_active Abandoned
- 2004-06-23 KR KR1020057025112A patent/KR20060029154A/ko not_active Withdrawn
- 2004-06-23 AT AT04738937T patent/ATE505323T1/de not_active IP Right Cessation
- 2004-06-23 JP JP2006515727A patent/JP4781264B2/ja not_active Expired - Fee Related
- 2004-06-23 EP EP10178128A patent/EP2301749A1/en not_active Withdrawn
-
2005
- 2005-11-21 US US11/283,653 patent/US8399078B2/en active Active
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3403064A (en) * | 1963-09-12 | 1968-09-24 | Baxter Laboratories Inc | Method of forming a composite plastic container with an inner and outer seal |
| RU2291681C2 (ru) * | 1996-05-13 | 2007-01-20 | Б. Браун Медикал, Инк. | Гибкая имеющая множество отделений емкость многоцелевого назначения |
| RU2208517C2 (ru) * | 1997-02-24 | 2003-07-20 | Бакстер Биотек Текнолоджи С.А.Р.Л. | Совместно экструдированные многослойные пленки для стерилизуемых емкостей для жидкости |
| RU2300365C2 (ru) * | 2005-03-02 | 2007-06-10 | Михаил Юрьевич Попов | Контейнер для крови и/или компонентов крови |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2545451C2 (ru) * | 2010-11-15 | 2015-03-27 | Ф. Хоффманн-Ля Рош Аг | Контейнер для хранения медицинских или фармацевтических жидкостей |
| RU2813063C2 (ru) * | 2019-06-26 | 2024-02-06 | Сева Санте Анималь | Полимерная упаковка, ее применение для хранения стерильной фармацевтической композиции и способ хранения стерильной фармацевтической композиции |
Also Published As
| Publication number | Publication date |
|---|---|
| ATE505323T1 (de) | 2011-04-15 |
| JP2007506464A (ja) | 2007-03-22 |
| PL1641616T3 (pl) | 2011-09-30 |
| EP1641616A1 (en) | 2006-04-05 |
| RU2005139050A (ru) | 2006-06-27 |
| AU2004251810B2 (en) | 2010-03-04 |
| CN1791511A (zh) | 2006-06-21 |
| KR20060029154A (ko) | 2006-04-04 |
| US8399078B2 (en) | 2013-03-19 |
| AU2004251810A1 (en) | 2005-01-06 |
| EP1641616B1 (en) | 2011-04-13 |
| US20060134358A1 (en) | 2006-06-22 |
| JP4781264B2 (ja) | 2011-09-28 |
| DE602004032237D1 (de) | 2011-05-26 |
| EP2301749A1 (en) | 2011-03-30 |
| CA2529023A1 (en) | 2005-01-06 |
| WO2005000580A1 (en) | 2005-01-06 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US7807242B2 (en) | Transparent, flexible, impermeable plastic container for storage of pharmaceutical liquids | |
| RU2381103C2 (ru) | Контейнер для жидких фармацевтических композиций с высокими влагозащитными свойствами | |
| US11452811B2 (en) | Application arrangement with a medicinal substance fluid | |
| RU2215656C2 (ru) | Материал для упаковки содержащего никотин продукта | |
| EP2033615B1 (en) | Liquid container | |
| JP5012585B2 (ja) | アルブミン収容プラスチック容器 | |
| US20020132359A1 (en) | Dispensing unit for oxygen-sensitive drugs | |
| JP2003205972A (ja) | 非経口流体用改良型容器 | |
| CN107049929B (zh) | 甲状腺激素t3和/或t4的单次剂量药物制剂 | |
| JP4607609B2 (ja) | 薬液バッグ、薬液バッグ収容体および薬液バッグ収容体の製造方法 | |
| JP4254117B2 (ja) | アルブミン溶液収容プラスチック容器 | |
| US20080311321A1 (en) | Multilayer Film With Septum Layer | |
| JP4225416B2 (ja) | タンパク質製剤の安定性を改善する方法 | |
| JPH07100185A (ja) | 医薬液入り容器 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20120624 |