RU2018114512A - Способ получения соединений индолина и новая соль индолина - Google Patents
Способ получения соединений индолина и новая соль индолина Download PDFInfo
- Publication number
- RU2018114512A RU2018114512A RU2018114512A RU2018114512A RU2018114512A RU 2018114512 A RU2018114512 A RU 2018114512A RU 2018114512 A RU2018114512 A RU 2018114512A RU 2018114512 A RU2018114512 A RU 2018114512A RU 2018114512 A RU2018114512 A RU 2018114512A
- Authority
- RU
- Russia
- Prior art keywords
- silodosin
- indole
- phenoxy
- dihydro
- hydroxypropyl
- Prior art date
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D209/00—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D209/02—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom condensed with one carbocyclic ring
- C07D209/04—Indoles; Hydrogenated indoles
- C07D209/10—Indoles; Hydrogenated indoles with substituted hydrocarbon radicals attached to carbon atoms of the hetero ring
- C07D209/14—Radicals substituted by nitrogen atoms, not forming part of a nitro radical
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D209/00—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D209/02—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom condensed with one carbocyclic ring
- C07D209/04—Indoles; Hydrogenated indoles
- C07D209/08—Indoles; Hydrogenated indoles with only hydrogen atoms or radicals containing only hydrogen and carbon atoms, directly attached to carbon atoms of the hetero ring
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/40—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil
- A61K31/403—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil condensed with carbocyclic rings, e.g. carbazole
- A61K31/404—Indoles, e.g. pindolol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/40—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil
- A61K31/403—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil condensed with carbocyclic rings, e.g. carbazole
- A61K31/404—Indoles, e.g. pindolol
- A61K31/405—Indole-alkanecarboxylic acids; Derivatives thereof, e.g. tryptophan, indomethacin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/08—Drugs for disorders of the urinary system of the prostate
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07B—GENERAL METHODS OF ORGANIC CHEMISTRY; APPARATUS THEREFOR
- C07B2200/00—Indexing scheme relating to specific properties of organic compounds
- C07B2200/13—Crystalline forms, e.g. polymorphs
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Animal Behavior & Ethology (AREA)
- Life Sciences & Earth Sciences (AREA)
- Epidemiology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Engineering & Computer Science (AREA)
- Urology & Nephrology (AREA)
- Indole Compounds (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Claims (82)
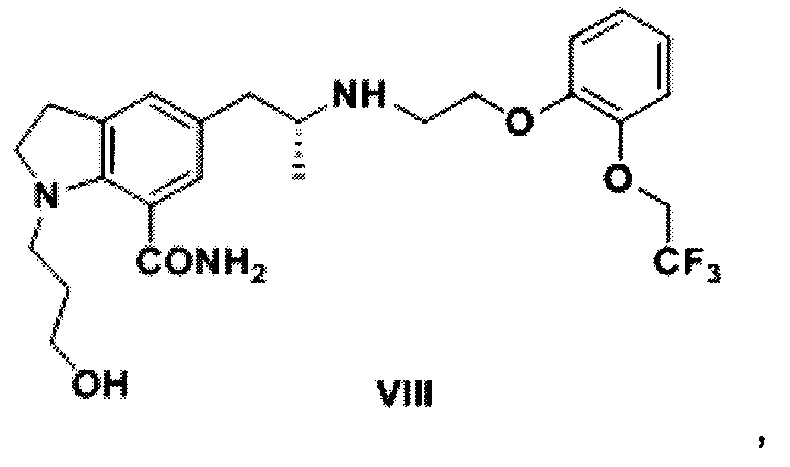
1. Способ получения 1-(3-гидроксипропил)-5-[(2R)-2-({2-[2-(2,2,2-трифтор-этокси)фенокси]этил}амино)пропил]-2,3-дигидро-1Н-индол-7-карбоксамида структурной формулы (VIII):
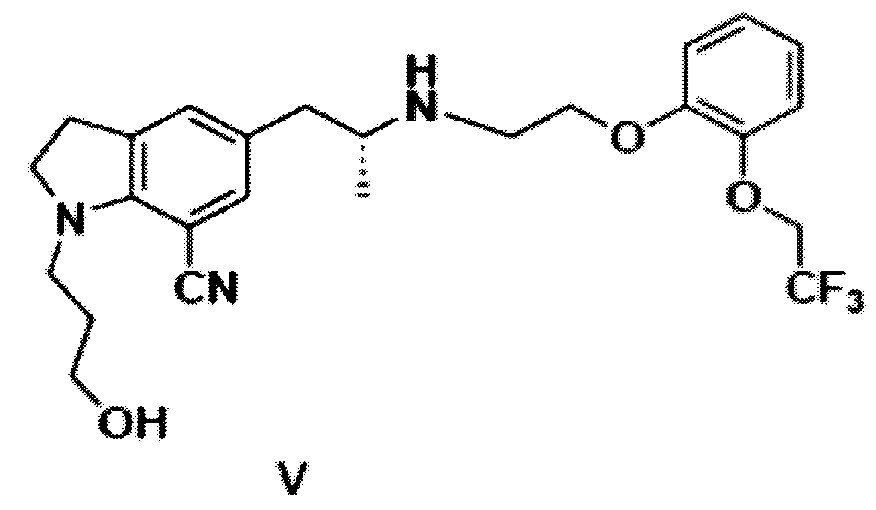
включающий переведение 1-(3-гидроксипропил)-5-[(2R)-2-({2-[2-(2,2,2-трифтор-этокси)фенокси]этил}амино)пропил]-2,3-дигидро-1Н-индол-7-карбонитрила структурной формулы (V)
в карбоксилатную соль, последующую нейтрализацию и гидролиз с получением 1-(3-гидроксипропил)-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)-пропил]-2,3-дигидро-1Н-индол-7-карбоксамида структурной формулы (VIII).
2. Способ получения по п. 1, касающийся получения 1-(3-гидроксипропил)-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)-пропил]-2,3-дигидро-1Н-индол-7-карбоксамида структурной формулы (VIII),:
где 1-(3-гидроксипропил)-5-[(2R)-2-{{2-[2-(2,2,2-трифторэтокси)фенокси]этил}-амино)пропил]-2,3-дигидро-1Н-индол-7-карбонитрил структурной формулы (V):
смешивают с N-ацетилглутаминовой кислотой с получением 1-(3-гидроксипропил)-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1Н-индол-7-карбонитрила N-ацетилмоноглутамата структурной формулы (VI):
с последующей нейтрализацией глутамата и гидролизом с получением 1-(3-гидроксипропил)-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)-пропил]-2,3-дигидро-1Н-индол-7-карбоксамида структурной формулы (VIII).
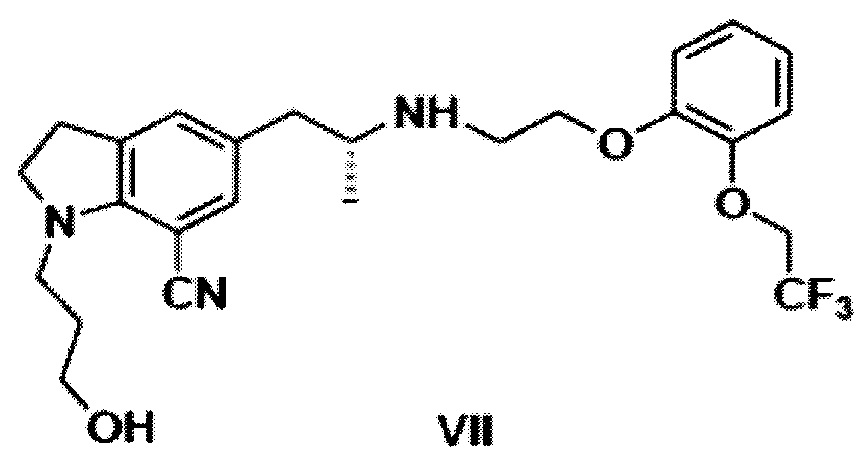
3. Способ получения по п. 1, включающий нейтрализацию 1-(3-гидроксипропил)-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)-пропил]-2,3-дигидро-1Н-индол-7-карбонитрила N-ацетилмоноглутамата до 1-(3-гидроксипропил)-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)-пропил]-2,3-дигидро-1Н-индол-7-карбонитрила структурной формулы (VII)
4. Однореакторный способ получения 1-(3-гидроксипропил)-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1Н-индол-7-карбоксамида структурной формулы (VIII) в виде кристаллической гамма-формы, включающий:
a) введение в реакцию 1-(3-гидроксипропил)-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1Н-индол-7-карбонитрила (VII) с щелочным раствором
в присутствии окислителя при более низкой температуре;
b) гашение реакционной массы стадии а) раствором сульфита натрия;
c) разбавление реакционной массы стадии b) галогенированным алифатическим углеводородным растворителем и удаление водного слоя;
d) разбавление органического слоя стадии с) ароматическим углеводородным растворителем и удаление галогенированного алифатического углеводорода;
e) охлаждение раствора стадии d) до комнатной температуры;
f) добавление С1-С6-алифатического простого эфира к раствору ароматического углеводорода стадии е);
g) фильтрацию силодозина в виде кристаллической гамма-формы.
5. Однореакторный способ получения 1-(3-гидроксипропил)-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1Н-индол-7-карбоксамида структурной формулы (VIII) в виде кристаллической гамма-формы по п. 4, включающий:
a) введение в реакцию 1-(3-гидроксипропил)-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1Н-индол-7-карбонитрила (VII) с водным раствором гидроксида натрия
в присутствии перекиси водорода при 5-10°С;
b) гашение реакционной массы стадии а) раствором сульфита натрия;
c) разбавление реакционной массы стадии b) дихлорметаном и удаление водного слоя;
d) разбавление органического слоя стадии с) толуолом и удаление дихлорметана;
e) охлаждение раствора стадии d) до комнатной температуры;
f) добавление метил-трет-бутилового эфира к раствору стадии е);
е) фильтрацию силодозина в виде кристаллической гамма-формы.
6. Способ получения кристаллической гамма-формы силодозина, включающий растворение силодозина в смеси С1-С6-спирта и ароматического углеводорода, возможно при повышенной температуре, с последующим добавлением анти-растворителя, предпочтительно простого эфира, при более низкой температуре, с последующим перемешиванием и фильтрацией.
7. Способ получения по п. 6, где С1-С6-спирт представляет собой изопропиловый спирт, метанол, этанол и пропанол.
8. Способ получения по п. 7, где С1-С6-спирт представляет собой изопропиловый спирт.
9. Способ получения по п. 6, где ароматический углеводородный растворитель представляет собой толуол, бензол, этилбензол и ксилол.
10. Способ получения по п. 9, где углеводородный растворитель представляет собой толуол.
11. Способ получения по п. 6, где простой эфир представляет собой метил-трет-бутиловый эфир, диэтиловый эфир, метилэтиловый эфир и метилфениловый эфир.
12. Способ получения по п. 11, где простой эфир представляет собой метил-трет-бутиловый эфир.
13. Способ получения кристаллической гамма-формы силодозина по п. 6, где остаточное содержание толуола составляет менее чем 890 м.д., полученной способом, включающим следующие стадии:
a) суспендирование кристаллической гамма-формы силодозина в простом эфире, предпочтительно в метил-трет-бутиловом эфире, при комнатной температуре или при более низкой температуре, с последующим перемешиванием и фильтрацией;
b) высушивание полученного соединения;
c) выделение полиморфной гамма-формы силодозина с содержанием толуола менее чем 890 м.д.
14. Кристаллическая форма 1-(3-Гидроксипропил)-5-[(2R)-2-({2-(2,2,2-трифторэтокси)фенокси]этил)-амино)пропил]2,3-дигидро-1Н-индол-7-карбонитрил N-ацетилмоноглутамат.
15. Кристаллическая форма 1-(3-гидроксипропил)-5-[(2R)-2-({2-(2,2,2-трифторэтокси)фенокси]этил}амино)-пропил]2,3-дигидро-1Н-индол-7-карбонитрила N-ацетилмоноглутамата, характеризующаяся рентгеновской дифрактограммой, имеющей выраженные пики при значениях 5,38; 6,69; 8,55; 12,0; 15,08; 16,38; 17,35; 18,80; 19,42; 20,12; 21,17; 21,87; 22,18; 23,7; 24,87; 25,26; 26,19; 26,98; 27,51; 29,10±0,2 градусов 2θ.
16. Кристаллическая форма 1-(3-гидроксипропил)-5-[(2R)-2-({2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]2,3-дигидро-1Н-индол-7-карбонитрила N-ацетилмоноглутамата по п. 15, характеризующаяся рентгеновской дифрактограммой, представленной на Фиг. 1.
17. Однореакторный способ получения 1-(3-гидроксипропил)-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1Н-индол-7-карбоксамида структурной формулы (VIII) в виде кристаллической бета-формы, включающий:
a) введение в реакцию 1-(3-гидроксипропил)-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1Н-индол-7-карбонитрила (VII) с водным щелочным раствором
в присутствии окислителя при более низкой температуре;
b) гашение реакционной массы раствором сульфита натрия;
c) разбавление реакционной массы галогенированным алифатическим углеводородным растворителем и удаление водного слоя;
d) разбавление органического слоя ароматическим углеводородным растворителем и удаление галогенированного алифатического углеводорода;
e) добавление С1-С6-алифатического простого эфира к раствору ароматического углеводорода при повышенной температуре;
f) частичное охлаждение раствора стадии е), внесение затравки кристаллического бета-силодозина;
g) медленное охлаждение до комнатной температуры и фильтрацию силодозина в виде кристаллической бета-формы.
18. Однореакторный способ получения 1-(3-гидроксипропил)-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1Н-индол-7-карбоксамида структурной формулы (VIII) в виде кристаллической бета-формы по п. 17, включающий:
a) введение в реакцию 1-(3-гидроксипропил)-5-[(2R)-2-({2-[2-(2,2,2-трифторэтокси)фенокси]этил}амино)пропил]-2,3-дигидро-1Н-индол-7-карбонитрила (VII) с водным раствором гидроксида натрия
в присутствии перекиси водорода при 5-10°С;
b) гашение реакционной массы раствором сульфита натрия;
c) разбавление реакционной массы дихлорметаном и удаление водного слоя;
d) разбавление органического слоя толуолом и удаление дихлорметана;
e) добавление метил-трет-бутилового эфира к органическому слою стадии d) при 75-80°С;
f) частичное охлаждение раствора стадии е) до 65-70°С, внесение затравки кристаллического бета-силодозина;
g) медленное охлаждение до комнатной температуры и фильтрацию силодозина в виде кристаллической бета-формы.
19. Способ получения кристаллической бета-формы силодозина из кристаллической гамма-формы силодозина, включающий следующие стадии:
a) растворение кристаллической гамма-формы силодозина в ароматическом углеводородном растворителе при повышенной температуре;
b) добавление растворителя - С1-С6-алифатического простого эфира к раствору ароматического углеводорода стадии а) при повышенной температуре;
c) частичное охлаждение раствора стадии b), внесение затравки кристаллического бета-силодозина;
d) медленное охлаждение до комнатной температуры и фильтрацию силодозина в виде кристаллической бета-формы.
20. Способ получения кристаллической бета-формы силодозина из кристаллической гамма-формы силодозина по п. 19, включающий следующие стадии:
a) растворение кристаллической гамма-формы силодозина в толуоле при 75°С;
b) добавление метил-трет-бутилового эфира к раствору стадии а) при 75°С;
c) частичное охлаждение раствора стадии b) до 60°С, внесение затравки кристаллического бета-силодозина;
d) медленное охлаждение до комнатной температуры и фильтрацию силодозина в виде кристаллической бета-формы.
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| IN5079CH2015 | 2015-09-23 | ||
| IN5079/CHE/2015 | 2015-09-23 | ||
| IN201641017352 | 2016-05-19 | ||
| IN201641017352 | 2016-05-19 | ||
| PCT/IB2016/055625 WO2017051324A1 (en) | 2015-09-23 | 2016-09-21 | The process of preparing indoline compounds and a novel indoline salt |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| RU2018114512A true RU2018114512A (ru) | 2019-10-23 |
Family
ID=58386325
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2018114512A RU2018114512A (ru) | 2015-09-23 | 2016-09-21 | Способ получения соединений индолина и новая соль индолина |
Country Status (9)
| Country | Link |
|---|---|
| US (1) | US20180339964A1 (ru) |
| EP (1) | EP3353149A4 (ru) |
| JP (1) | JP2018528233A (ru) |
| KR (1) | KR20180052728A (ru) |
| AU (1) | AU2016327159A1 (ru) |
| BR (1) | BR112018005930A2 (ru) |
| CA (1) | CA2999417A1 (ru) |
| RU (1) | RU2018114512A (ru) |
| WO (1) | WO2017051324A1 (ru) |
Families Citing this family (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| ES2607639B1 (es) | 2015-09-30 | 2018-02-28 | Urquima, S.A | Sal de ácido maleico de un intermedio de silodosina |
| CN107056675B (zh) * | 2017-05-10 | 2019-09-03 | 浙江天宇药业股份有限公司 | 一种西洛多辛及其中间体的合成方法 |
| CN111410626B (zh) * | 2019-01-04 | 2022-11-04 | 上海汇伦医药股份有限公司 | 赛洛多辛α-晶型的制备方法 |
Family Cites Families (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| ATE508113T1 (de) * | 2004-10-27 | 2011-05-15 | Kissei Pharmaceutical | Indolinverbindung und verfahren zu deren herstellung |
| CN101993407B (zh) * | 2009-08-27 | 2014-01-29 | 浙江华海药业股份有限公司 | 用于制备西洛多辛的吲哚啉化合物及其制备方法 |
| CN103159664B (zh) * | 2013-03-29 | 2016-03-23 | 深圳市海滨制药有限公司 | 一种赛洛多辛原料药及其制备方法、药物组合物 |
| CN104140389A (zh) * | 2013-05-06 | 2014-11-12 | 昆明积大制药股份有限公司 | 一种赛洛多辛及其中间体的制备方法 |
| WO2015015512A2 (en) * | 2013-07-29 | 2015-02-05 | Ind-Swift Laboratories Limited | Process for the preparation of silodosin and its gamma form |
| IN2014MU00483A (ru) * | 2014-02-11 | 2015-11-13 |
-
2016
- 2016-09-21 WO PCT/IB2016/055625 patent/WO2017051324A1/en active Application Filing
- 2016-09-21 JP JP2018515460A patent/JP2018528233A/ja active Pending
- 2016-09-21 KR KR1020187010382A patent/KR20180052728A/ko unknown
- 2016-09-21 CA CA2999417A patent/CA2999417A1/en not_active Abandoned
- 2016-09-21 AU AU2016327159A patent/AU2016327159A1/en not_active Abandoned
- 2016-09-21 EP EP16848238.8A patent/EP3353149A4/en not_active Withdrawn
- 2016-09-21 BR BR112018005930A patent/BR112018005930A2/pt not_active Application Discontinuation
- 2016-09-21 US US15/763,030 patent/US20180339964A1/en not_active Abandoned
- 2016-09-21 RU RU2018114512A patent/RU2018114512A/ru not_active Application Discontinuation
Also Published As
| Publication number | Publication date |
|---|---|
| EP3353149A1 (en) | 2018-08-01 |
| AU2016327159A1 (en) | 2018-04-26 |
| EP3353149A4 (en) | 2019-09-11 |
| WO2017051324A1 (en) | 2017-03-30 |
| US20180339964A1 (en) | 2018-11-29 |
| KR20180052728A (ko) | 2018-05-18 |
| JP2018528233A (ja) | 2018-09-27 |
| BR112018005930A2 (pt) | 2018-10-09 |
| CA2999417A1 (en) | 2017-03-30 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2018114512A (ru) | Способ получения соединений индолина и новая соль индолина | |
| CN101993405B (zh) | 吲哚啉衍生物、及其制备方法和用途 | |
| AU2011281421A1 (en) | Process for preparing aminobenzoylbenzofuran derivatives | |
| BRPI0807197A2 (pt) | Processo para a preparação de um derivado de benzimidazol | |
| RU2018106948A (ru) | Способ получения замещенных производных 3-(2-анилино-1-циклогексил -1н-бензимидазол-5-ил)пропановой кислоты | |
| RU2016135762A (ru) | Способ получения (r)-1,1,3-триметил-4-аминоиндана | |
| TW201408634A (zh) | 新穎製法 | |
| RU2011139325A (ru) | Аморфная соль макроциклического ингибитора hcv | |
| PT2042497E (pt) | Processo de síntese industrial do ranelato de estrôncio e dos seus hidratos | |
| ES2927193T3 (es) | Proceso para la preparación de 2-(5-metoxiisocroman-1-il)-4,5-dihidro-1H-imidazol y su sal hidrogenosulfato | |
| JP2012251113A5 (ru) | ||
| RU2016134404A (ru) | КРИСТАЛЛИЧЕСКАЯ ФОРМА α МОНОБЕНЗОАТА СОЕДИНЕНИЯ А, СПОСОБ ЕЕ ПОЛУЧЕНИЯ И СОДЕРЖАЩАЯ ЕЕ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | |
| RU2009115852A (ru) | Способ получения абакавира | |
| CN107935866B (zh) | 盐酸达泊西汀杂质的制备方法 | |
| JP5305593B2 (ja) | 高化学的r−5−(2−(2−エトキシフェノキシエチルアミノ)プロピル)−2−メトキシベンゼンスルホンアミド塩酸塩の調製 | |
| CN103508898B (zh) | 一种新的枸橼酸阿尔维林的制备方法 | |
| RU2019106531A (ru) | Кристалл соли производного хиназолина | |
| KR20160027536A (ko) | 실로도신 합성에 유용한 중간체의 제조방법 | |
| TW200948352A (en) | Methods of preparing substituted heterocycles-149 | |
| CN105439977A (zh) | 一种阿考替胺及其盐酸盐的制备方法 | |
| EA017767B1 (ru) | Способ получения золмитриптана | |
| CN110452149B (zh) | 二氢吲哚化合物的制备方法、二氢吲哚化合物及用途 | |
| CN105523939B (zh) | 一种来那度胺中间体的制备方法 | |
| RU2558145C1 (ru) | Способ промышленного получения азотзамещенного амино-5,6,7,8-тетрагидронафтола | |
| JP2016064988A (ja) | 1‐(3‐ベンゾイルオキシプロピル)‐7‐シアノ‐5‐[(2r)‐2‐({2‐[2‐(2,2,2‐トリフルオロエトキシ)フェノキシ]エチル}アミノ)プロピル]インドリンの酒石酸塩を製造する方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| FA93 | Acknowledgement of application withdrawn (no request for examination) |
Effective date: 20190923 |