JP7697371B2 - 組換えc反応性タンパク質 - Google Patents
組換えc反応性タンパク質 Download PDFInfo
- Publication number
- JP7697371B2 JP7697371B2 JP2021561228A JP2021561228A JP7697371B2 JP 7697371 B2 JP7697371 B2 JP 7697371B2 JP 2021561228 A JP2021561228 A JP 2021561228A JP 2021561228 A JP2021561228 A JP 2021561228A JP 7697371 B2 JP7697371 B2 JP 7697371B2
- Authority
- JP
- Japan
- Prior art keywords
- reactive protein
- crp
- seq
- recombinant
- amino acid
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/46—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates
- C07K14/47—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates from mammals
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/536—Immunoassay; Biospecific binding assay; Materials therefor with immune complex formed in liquid phase
- G01N33/537—Immunoassay; Biospecific binding assay; Materials therefor with immune complex formed in liquid phase with separation of immune complex from unbound antigen or antibody
- G01N33/539—Immunoassay; Biospecific binding assay; Materials therefor with immune complex formed in liquid phase with separation of immune complex from unbound antigen or antibody involving precipitating reagent, e.g. ammonium sulfate
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/46—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates
- C07K14/47—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates from mammals
- C07K14/4701—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates from mammals not used
- C07K14/4737—C-reactive protein
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/96—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving blood or serum control standard
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/01—Fusion polypeptide containing a localisation/targetting motif
- C07K2319/02—Fusion polypeptide containing a localisation/targetting motif containing a signal sequence
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12R—INDEXING SCHEME ASSOCIATED WITH SUBCLASSES C12C - C12Q, RELATING TO MICROORGANISMS
- C12R2001/00—Microorganisms ; Processes using microorganisms
- C12R2001/01—Bacteria or Actinomycetales ; using bacteria or Actinomycetales
- C12R2001/185—Escherichia
- C12R2001/19—Escherichia coli
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2333/00—Assays involving biological materials from specific organisms or of a specific nature
- G01N2333/435—Assays involving biological materials from specific organisms or of a specific nature from animals; from humans
- G01N2333/46—Assays involving biological materials from specific organisms or of a specific nature from animals; from humans from vertebrates
- G01N2333/47—Assays involving proteins of known structure or function as defined in the subgroups
- G01N2333/4701—Details
- G01N2333/4737—C-reactive protein
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Immunology (AREA)
- Molecular Biology (AREA)
- Engineering & Computer Science (AREA)
- Hematology (AREA)
- Urology & Nephrology (AREA)
- Organic Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Biomedical Technology (AREA)
- Biochemistry (AREA)
- Cell Biology (AREA)
- Microbiology (AREA)
- Gastroenterology & Hepatology (AREA)
- Biophysics (AREA)
- Biotechnology (AREA)
- Genetics & Genomics (AREA)
- Zoology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Toxicology (AREA)
- Food Science & Technology (AREA)
- Physics & Mathematics (AREA)
- Analytical Chemistry (AREA)
- General Physics & Mathematics (AREA)
- Pathology (AREA)
- Peptides Or Proteins (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
Description
非特許文献2:臨床検査,Vol.46,No.9,p973-981(2002年9月)
項1.遺伝子組換えにより生産されたC反応性タンパク質であって、該C反応性タンパク質の55%以上のN末端がピログルタミル化されている組換えC反応性タンパク質。
項2.該C反応性タンパク質の65%以上のN末端がピログルタミル化されている、項1に記載の組換えC反応性タンパク質。
項3.該C反応性タンパク質の75%以上のN末端がピログルタミル化されている、項1に記載の組換えC反応性タンパク質。
項4.該C反応性タンパク質の85%以上のN末端がピログルタミル化されている、項1に記載の組換えC反応性タンパク質。
項5.組換えC反応性タンパク質が、細菌による組換えタンパク質である、項1から4のいずれかに記載の組換えC反応性タンパク質。
項6.細菌が大腸菌である項5に記載の組換えC反応性タンパク質。
項7.C反応性タンパク質がヒト由来である、項1から6のいずれかに記載の組換えC反応性タンパク質。
項8.C反応性タンパク質が、下記の(a)から(c)のいずれかのポリペプチドからなる、項1から7のいずれかに記載の組換えC反応性タンパク質。
(a)配列番号1または配列番号2に記載されたポリペプチド
(b)配列番号1または配列番号2に示されるアミノ酸配列において、1若しくは数個のアミノ酸残基が置換、欠失、挿入および/または付加したアミノ酸配列からなり、かつ、抗C反応性タンパク質抗体に対する抗原性を有するポリペプチド
(c)配列番号1または配列番号2に示されるアミノ酸配列との同一性が90%以上であるアミノ酸配列からなり、かつ、抗C反応性タンパク質抗体に対する抗原性を有するポリペプチド
項9.項1から8のいずれかに記載のC反応性タンパク質を含むキャリブレーター。
項10.項1から8のいずれかに記載のC反応性タンパク質を含む管理血清項11.項9に記載のC反応性タンパク質を含むキャリブレーターを用いて検体中のC反応性タンパク質を定量する方法。
項12.項10に記載のC反応性タンパク質を含む管理血清を用いて検体中のC反応性タンパク質を定量する方法。
項13.抗C反応性タンパク質抗体が固定化されたラテックス粒子を用いた、ラテックス免疫比濁法により、項11または12に記載の検体中のC反応性タンパク質を定量する方法。
本発明の組換えCRPは、例えばヒト、イヌ、ネコ、マウス、ラット、ウサギ、ヤギなどに哺乳類に由来するCRPが挙げられる。その中でも、ヒト、イヌ又はネコ由来のCRPがより好ましく、さらにはヒト由来のCRPが特に好ましい。
(a)配列番号1または配列番号2に記載されたポリペプチド。
(b)配列番号1または配列番号2に示されるアミノ酸配列において、1若しくは数個のアミノ酸残基が置換、欠失、挿入および/または付加したアミノ酸配列からなり、かつ、抗C反応性タンパク質抗体に対する抗原性を有するポリペプチド。
(c)配列番号1または配列番号2に示されるアミノ酸配列との同一性が90%以上であるアミノ酸配列からなり、かつ、抗C反応性タンパク質抗体に対する抗原性を有するポリペプチド。
(b)配列番号1または配列番号2に示されるアミノ酸配列において、1若しくは数個のアミノ酸残基が置換、欠失、挿入および/または付加したアミノ酸配列からなり、かつ、抗C反応性タンパク質抗体に対する抗原性を有するポリペプチド、または、
(c)配列番号1または配列番号2に示されるアミノ酸配列との同一性が90%以上であるアミノ酸配列からなり、かつ、抗C反応性タンパク質抗体に対する抗原性を有するポリペプチド、
であってもよい。
本発明の組換えCRPをコードするDNAは、例えばヒト、イヌ、ネコ、マウス、ラット、ウサギ、ヤギなどに哺乳類に由来するCRPをコードするDNAが挙げられる。その中でも、ヒト、イヌ又はネコ由来のCRPをコードするDNAがより好ましく、さらにはヒト由来のCRPをコードするDNAが好ましい。
(d)上記(a)から(c)のいずれかのCRPのアミノ酸配列をコードするDNA
(e)配列番号5または配列番号6に示される塩基配列からなるDNA
(f)配列番号5または配列番号6に示される塩基配列において、1若しくは数個の塩基が置換、欠失、挿入および/または付加した塩基配列からなり、かつ、抗C反応性タンパク質抗体に対する抗原性を有するポリペプチドをコードするDNA
(g)配列番号5または配列番号6に示される塩基配列との同一性が80%以上である塩基配列からなり、かつ、抗C反応性タンパク質抗体に対する抗原性を有するポリペプチドをコードするDNA。
(f)配列番号5または配列番号6に示される塩基配列において、1若しくは数個の塩基が置換、欠失、挿入および/または付加した塩基配列からなり、かつ、抗C反応性タンパク質抗体に対する抗原性を有するポリペプチドをコードするDNA、または、
(g)配列番号5または配列番号6に示される塩基配列との同一性が80%以上である塩基配列からなり、かつ、抗C反応性タンパク質抗体に対する抗原性を有するポリペプチドをコードするDNA、
であってもよい。
本発明の別の実施形態は、上記のDNAを組み込んだベクター、該ベクターを含む形質転換体、または、該形質転換体を培養することを含む組換えCRPを製造する方法である。本発明の組換えCRPは、その遺伝子を適当なベクターに挿入して組換えベクターを調製し、この組換えベクターで適当な宿主細胞を形質転換して形質転換体を調製し、この形質転換体を培養することによって容易に行うことができる。
本発明の組換えCRPは、全体の55%以上のN末端がピログルタミル化されている組換えCRPであり、具体的には、N末端環化率が55%以上と算出された組換えCRPである。
本発明において、CRP濃度測定は以下の条件で行う。該CRP濃度測定方法は、抗C反応性タンパク質抗体が固定化されたラテックス粒子と被検試料中のCRP(被検物質)が抗原抗体反応を起こし、当該ラテックス粒子の凝集反応の程度からCRP濃度を測定する方法である。なお、本発明で「CRP濃度」という場合は、具体的には、特に記載のない限り、以下の方法で測定した値を意味する。
・デンカ生研社製CRPラテックスX2「生研」R1試薬(緩衝液)
・デンカ生研社製CRPラテックスX2「生研」R2試薬(ラテックス(抗ヒトCRPポリクローナル抗体(ウサギ)結合ラテックス)浮遊液)
・デンカ生研社製CRPX2標準液H
<測定試料>
測定試料は、CRP溶液であり、必要に応じて20mM Tris-HCl緩衝溶液(0.14M 塩化ナトリウム、2mM 塩化カルシウム;pH7.5)で希釈された後、使用する。また特定のCRP濃度に調製する場合は、ブラッドフォードプロテインアッセイにおいて値付けされたタンパク質濃度を基準として、希釈倍率を決定する。
<測定方法>
上記の測定試料、上記のR1試薬及び上記R2試薬を下記条件で日立7180形自動分析装置を用いて、試料中のCRP濃度(mg/dL)を測定する。CRP濃度は、式(I)により算出される。
試料: 2.2μL
R1試薬: 120μL
R2試薬: 120μL
測定方法: 2ポイントエンド法(18-34)
主波長: 546nm
副波長: 800nm
本発明において、組換えCRPのN末端環化率測定は、以下の条件で行う。本測定方法は、質量分析により未環化型CRPのスペクトルと環化型CRPのスペクトルの10価の各イオン強度を測定し、各イオン強度から未環化型CRPと環化型CRPの比率を算出する方法である。本発明で「未環化型CRPのスペクトル」とは、分子量23045に該当するスペクトルのことをいい、また「環化型CRPのスペクトル」とは、分子量23027に該当するスペクトルのことをいう。なお、本発明で「CRPのN末端環化率」という場合は、具体的には、特に記載がない限り、以下の方法で測定した値を意味する。
測定試料は、CRP溶液であり、必要に応じて超純水で希釈された後に使用する。
<測定方法>
上記の測定試料を、下記条件でLC/MS装置を用いて、試料中の未環化型CRPのスペクトルと環化型CRPのスペクトルを測定する。
LC条件
装置:Waters製 ACQUITY UPLC
カラム:Waters製 Mass PREP Micro Desalting Column 20μm,2.1×5mm
移動相:A 水/ギ酸混液(1000:1),B IPA/ACN/メタノール/ギ酸混液(500:300:200:1)
カラム温度:50℃
注入量:5μL
MS条件
装置:BRUKERDALTONICS製 microOTOF
イオン化法:ESIポジティブ
上記測定方法で得られた各CRPスペクトルの溶出時間1.7~2.0分の平均スペクトルの10価の各イオン強度(intensity)を用いて、未環化型CRPと環化型CRPの比率を算出する方法による。本発明の「比率」とは、未環化型CRPと環化型CRPの2つのイオン強度の合計を100とした場合の、環化型CRPのイオン強度の比率をいい、下記の式(II)により算出される。
(1)変異の導入
大腸菌由来アルカリホスファターゼ分泌シグナル配列(ATGAAACAAAGCACTATTGCACTGGCACTCTTACCGTTACTGTTTACCCCTGTGACAAAAGCC)と配列番号5または配列番号6のヒト由来成熟型CRP配列を連結させた配列番号7または配列番号8の人工合成遺伝子を鋳型とし、配列番号9,10のプライマーを用いて、CRP遺伝子を増幅した。配列番号9はフォワードプライマー、配列番号10はリバースプライマーである。本プライマーには制限酵素サイトNdeI、または制限酵素サイトBamHIがそれぞれ付加されている。増幅した遺伝子断片と、制限酵素NdeIとBamHIで切断されたベクタープラスミドpBluescript KSN(+)、In-Fusion Reaction Mix(タカラバイオ製)を加えてインキュベーションすることにより、プラスミドを構築した。このようにして、CRP遺伝子を大量に発現できるように設計された、配列番号7を含む組換えプラスミドpBKSN_CRP1と、配列番号8を含む組換えプラスミドpBKSN_CRP2を取得した。
(1)で構築したプラスミドを用いて、エシェリヒア・コリー(Escherichia coli)JM109株コンピテントセル(東洋紡製)を形質転換し、SOC培地中で1hr、37℃で培養後、LB寒天培地(グルコース1.0%、アンピシリン50μg/mLを含む)に展開し、コロニーである該形質転換体を取得した。pBKSN_CRP1の導入で得られた形質転換体をエシェリヒア・コリーJM109(pBKSN_CRP1)と命名した。また上記と同様の方法でpBKSN_CRP2の導入で得られた形質転換体をエシェリヒア・コリーJM109(pBKSN_CRP2)と命名した。
実施例1にて取得した形質転換体エシェリヒア・コリーJM109(pBKSN_CRP1)のコロニーを、試験管内にて滅菌した5mLのLB液体培地(グルコース1.0%、アンピシリン100μg/mLを含む)へ植菌し、37℃で16時間培養した。得られた培養液を種培養液とし、10本の2L容の坂口フラスコに入った500mLのLB液体培地(グリセロール0.5%、塩化カルシウム0.05%、IPTG 1mM、アンピシリン50μg/mLを含む)に植菌し、振とう数180rpmで30℃、24時間培養した。培養終了より菌体を遠心分離により集菌し、20mM Tris-HCl緩衝液(0.14M 塩化ナトリウム、2mM 塩化カルシウム、pH7.5)に懸濁した後、フレンチプレス(Niro Soavi製)にて破砕し、更に遠心分離を行い、上清液を粗精製液1として得た。また上記と同様の方法でエシェリヒア・コリーJM109(pBKSN_CRP2)から粗精製液2も取得した。
実施例2にて取得した粗精製液1に対し、PierceTM p-Aminophenyl Phosphoryl Choline Agarose(Thermo SCIENTIFIC製)を用いたアフィニティー精製を行った。実施例2で使用した緩衝液20mM Tris-HCl緩衝液(0.14M 塩化ナトリウム、2mM 塩化カルシウム、pH7.5)で平衡化した前記樹脂を、粗精製液と混合して吸着させた樹脂を、前記緩衝液で洗浄し、20mM Tris-HCl緩衝液(0.14M 塩化ナトリウム、2mM EDTA2mM、pH7.5)で溶出させた、組換えCRP溶液1を取得した。この溶液はさらに、中空糸膜を用いた加水濃縮によりEDTAを除きつつ、実施例2で使用した緩衝液20mM Tris-HCl緩衝液(0.14M 塩化ナトリウム、2mM 塩化カルシウム、pH7.5)へ置換され、さらに遠心式限外ろ過フィルター(メルク製)で適当な濃度まで濃縮して、純度の高い組換えCRP1を得た。取得した組換えCRP1を用いてSDS-PAGEを行った結果を図1に示す。その結果、不純タンパク質がSDS-PAGEでは検出できないレベルにまで、純度を向上させることに成功した。また上記と同様の方法で粗精製液2から純度の高い組換えCRP2も得た。得られたCRP2について、SDS-PAGEを行った結果を図2に示す。CRP1と同様に、不純タンパク質がSDS-PAGEでは検出できないレベルにまで、純度を向上させることに成功した。
実施例3にて取得した組換えCRP1を、37℃で8日間加温し、組換えCRPのN末端がピログルタミル化により環化された、環化型組換えCRP1を取得した。環化処理では実施例2で使用した緩衝液20mM Tris-HCl緩衝液(0.14M 塩化ナトリウム、2mM 塩化カルシウム、pH7.5)を使用し、CRP濃度は300mg/dLで実施した。また上記と同様の方法で組換えCRP2から環化型組換えCRP2を取得した。
実施例3にて取得した組換えCRP1と組換えCRP2、実施例4にて取得した環化型組換えCRP1と環化型組換えCRP2、及びポジティブコントロールとして天然型ヒトCRP(Yashraj製)を、超純水にてCRP濃度150mg/dLに調製したCRP溶液を上述した通りのLC/MS条件で測定した(表1参照)。組換えCRP1の各サンプルの質量スペクトルにおいて、溶出時間1.7~2.0分の平均の10価のイオンを拡大したものを図3に示す。
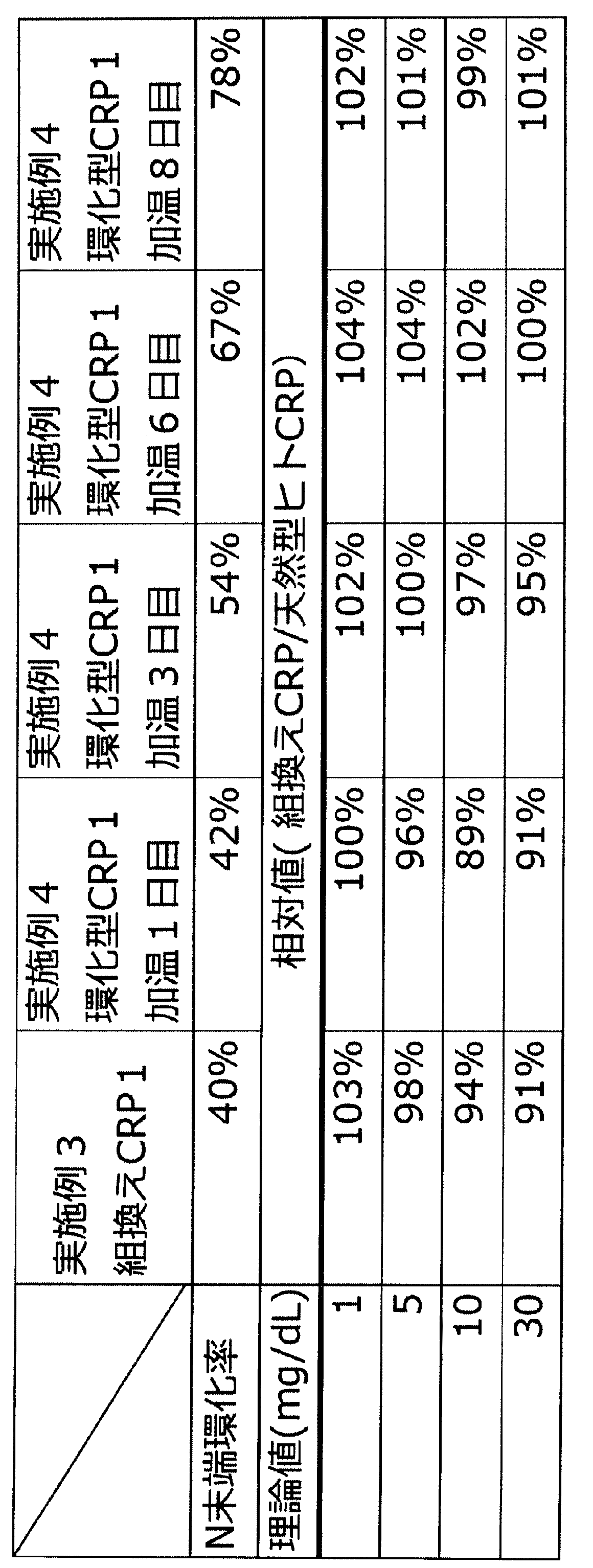
ウシ血清アルブミン(シグマ製)を超純水にて、0.1、0.2、0.4、及び0.75mg/mLに希釈して標準液を調製した。各標準液60μLにプロテインアッセイ濃縮色素試薬(BioRad製)600μLと超純水2.4mLを添加し、室温にて5分間静置後に595nmの吸光度を測定した。上述の595nmの吸光度の測定値とウシ血清アルブミン濃度から検量線を作成した。実施例3にて取得した組換えCRP1と組換えCRP2、実施例4取得した環化型組換えCRP1と環化型組換えCRP2、及び天然型ヒトCRPを超純水にておいて、適当な濃度になるよう希釈し、標準液と同様な試薬、条件で調製し、595nmの吸光度を測定した。各種CRPの測定値から、上述の検量線よりタンパク質濃度を算出した。上述のタンパク質濃度をもとに、タンパク質濃度1mg/dL、5mg/dL、10mg/dL、30mg/dLになるように20mM Tris-HCl緩衝溶液(0.14M 塩化ナトリウム、2mM 塩化カルシウム、pH7.5)で希釈してCRP溶液を調製した。
Claims (7)
- 下記の(a)から(c)のいずれかのポリペプチドからなる、ヒト由来のC反応性タンパク質を大腸菌で遺伝子組換えにより発現させ、取得したC反応性タンパク質の環化処理を行うことにより、該C反応性タンパク質の65%以上のN末端がピログルタミル化されている、組換えC反応性タンパク質の製造方法。
(a)配列番号1または配列番号2に記載されたポリペプチド
(b)配列番号1または配列番号2に示されるアミノ酸配列において、1若しくは数個の アミノ酸残基が置換、欠失、挿入および/または付加したアミノ酸配列からなり、かつ、 抗C反応性タンパク質抗体に対する抗原性を有するポリペプチド
(c)配列番号1または配列番号2に示されるアミノ酸配列との同一性が90%以上であ るアミノ酸配列からなり、かつ、抗C反応性タンパク質抗体に対する抗原性を有するポリペプチド - C反応性タンパク質の環化処理を、pH7から10の緩衝液中で、37℃から50℃の温度で6日以上行う、請求項1に記載の組換えC反応性タンパク質の製造方法。
- 該C反応性タンパク質の75%以上のN末端がピログルタミル化されている、請求項1または2に記載の組換えC反応性タンパク質の製造方法。
- 該C反応性タンパク質の85%以上のN末端がピログルタミル化されている、請求項1または2に記載の組換えC反応性タンパク質の製造方法。
- 下記の(a)から(c)のいずれかのポリペプチドからなる、65%以上のN末端がピログルタミル化されている組換えC反応性タンパク質の、抗C反応性タンパク質抗体が固定化されたラテックス粒子を用いた、ラテックス免疫比濁法により、検体中のC反応性タンパク質の定量における使用。
(a)配列番号1または配列番号2に記載されたポリペプチド
(b)配列番号1または配列番号2に示されるアミノ酸配列において、1若しくは数個の アミノ酸残基が置換、欠失、挿入および/または付加したアミノ酸配列からなり、かつ、 抗C反応性タンパク質抗体に対する抗原性を有するポリペプチド
(c)配列番号1または配列番号2に示されるアミノ酸配列との同一性が90%以上であ るアミノ酸配列からなり、かつ、抗C反応性タンパク質抗体に対する抗原性を有するポリペプチド - 該C反応性タンパク質の75%以上のN末端がピログルタミル化されている、請求項5に記載の検体中のC反応性タンパク質の定量における使用。
- 該C反応性タンパク質の85%以上のN末端がピログルタミル化されている、請求項5に記載の検体中のC反応性タンパク質の定量における使用。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2025012968A JP2025066156A (ja) | 2019-11-29 | 2025-01-29 | 組換えc反応性タンパク質 |
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2019216784 | 2019-11-29 | ||
| JP2019216784 | 2019-11-29 | ||
| JP2020140434 | 2020-08-21 | ||
| JP2020140434 | 2020-08-21 | ||
| PCT/JP2020/039893 WO2021106453A1 (ja) | 2019-11-29 | 2020-10-23 | 組換えc反応性タンパク質 |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2025012968A Division JP2025066156A (ja) | 2019-11-29 | 2025-01-29 | 組換えc反応性タンパク質 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JPWO2021106453A1 JPWO2021106453A1 (ja) | 2021-06-03 |
| JP7697371B2 true JP7697371B2 (ja) | 2025-06-24 |
Family
ID=76129330
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2021561228A Active JP7697371B2 (ja) | 2019-11-29 | 2020-10-23 | 組換えc反応性タンパク質 |
| JP2025012968A Pending JP2025066156A (ja) | 2019-11-29 | 2025-01-29 | 組換えc反応性タンパク質 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2025012968A Pending JP2025066156A (ja) | 2019-11-29 | 2025-01-29 | 組換えc反応性タンパク質 |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US20230039528A1 (ja) |
| EP (1) | EP4067372A4 (ja) |
| JP (2) | JP7697371B2 (ja) |
| CN (1) | CN114761561B (ja) |
| WO (1) | WO2021106453A1 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2025066156A (ja) * | 2019-11-29 | 2025-04-22 | 東洋紡株式会社 | 組換えc反応性タンパク質 |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2000014388A (ja) | 1998-07-03 | 2000-01-18 | Oriental Yeast Co Ltd | 組換えcrpおよびその製造方法 |
| JP2006300758A (ja) | 2005-04-21 | 2006-11-02 | Apro Life Science Institute Inc | 内部標準ペプチドを用いて生体由来試料に含まれる標的タンパク質を定量する方法 |
| WO2011155358A1 (ja) | 2010-06-11 | 2011-12-15 | 日東紡績株式会社 | 5量体crpの製造方法、5量体crpを製造する遺伝子組換えカイコとその製造方法、単量体イヌcrpをコードするdna及びそのdnaを含む発現ベクター |
| JP2011257243A (ja) | 2010-06-08 | 2011-12-22 | Shino-Test Corp | 試料中のc反応性蛋白質の測定試薬、測定方法及び測定範囲の拡大方法 |
| JP2018535394A (ja) | 2015-09-17 | 2018-11-29 | アムジェン インコーポレイテッド | Il23経路バイオマーカーを使用するil23アンタゴニストに対する臨床応答の予測 |
Family Cites Families (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2971290B2 (ja) * | 1993-04-27 | 1999-11-02 | オリエンタル酵母工業株式会社 | プラスミド及びそれで形質転換されたエシェリチア・コリ |
| JPH08233816A (ja) * | 1995-02-27 | 1996-09-13 | Wako Pure Chem Ind Ltd | 免疫学的測定法 |
| JPWO2009107170A1 (ja) * | 2008-02-29 | 2011-06-30 | 学校法人日本大学 | 抗crp抗体及びその利用 |
| JP5798720B2 (ja) * | 2010-03-30 | 2015-10-21 | 積水メディカル株式会社 | ヒトc反応性タンパク質(crp)測定用イムノクロマト試薬 |
| CN101974556B (zh) * | 2010-11-11 | 2015-02-11 | 中国计量科学研究院 | 一种同位素标记的重组c反应蛋白的制备方法 |
| CN103185798A (zh) * | 2011-12-27 | 2013-07-03 | 苏州德沃生物技术有限公司 | 一种心肌梗塞纳米免疫增强比浊快速检测试剂盒及使用方法 |
| CN106153933B (zh) * | 2015-03-26 | 2018-09-04 | 广州瑞博奥生物科技有限公司 | 一种高效定量检测c反应蛋白的免疫学试剂盒 |
| CN105158476A (zh) * | 2015-06-03 | 2015-12-16 | 南京闻智生物科技有限公司 | 一种全量程c反应蛋白胶乳增强免疫比浊检测试剂盒 |
| CN106699884B (zh) * | 2017-01-19 | 2020-04-17 | 江苏众红生物工程创药研究院有限公司 | 抗人c-反应蛋白抗体及其应用 |
| CN107022527B (zh) * | 2017-03-24 | 2019-12-27 | 菲鹏生物股份有限公司 | 可分泌抗c反应蛋白单克隆抗体的杂交瘤细胞、c反应蛋白检测试剂及其制备方法和应用 |
| JP7697371B2 (ja) * | 2019-11-29 | 2025-06-24 | 東洋紡株式会社 | 組換えc反応性タンパク質 |
-
2020
- 2020-10-23 JP JP2021561228A patent/JP7697371B2/ja active Active
- 2020-10-23 EP EP20893352.3A patent/EP4067372A4/en active Pending
- 2020-10-23 US US17/780,893 patent/US20230039528A1/en active Pending
- 2020-10-23 WO PCT/JP2020/039893 patent/WO2021106453A1/ja not_active Ceased
- 2020-10-23 CN CN202080082456.0A patent/CN114761561B/zh active Active
-
2025
- 2025-01-29 JP JP2025012968A patent/JP2025066156A/ja active Pending
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2000014388A (ja) | 1998-07-03 | 2000-01-18 | Oriental Yeast Co Ltd | 組換えcrpおよびその製造方法 |
| JP2006300758A (ja) | 2005-04-21 | 2006-11-02 | Apro Life Science Institute Inc | 内部標準ペプチドを用いて生体由来試料に含まれる標的タンパク質を定量する方法 |
| JP2011257243A (ja) | 2010-06-08 | 2011-12-22 | Shino-Test Corp | 試料中のc反応性蛋白質の測定試薬、測定方法及び測定範囲の拡大方法 |
| WO2011155358A1 (ja) | 2010-06-11 | 2011-12-15 | 日東紡績株式会社 | 5量体crpの製造方法、5量体crpを製造する遺伝子組換えカイコとその製造方法、単量体イヌcrpをコードするdna及びそのdnaを含む発現ベクター |
| JP2018535394A (ja) | 2015-09-17 | 2018-11-29 | アムジェン インコーポレイテッド | Il23経路バイオマーカーを使用するil23アンタゴニストに対する臨床応答の予測 |
Non-Patent Citations (2)
| Title |
|---|
| OLIVEIRA, E. B. et al.,Primary structure of human C-reactive protein,Proc. Natl. Acad. Sci. USA,1977年,Vol.74, No.8,pp.3148-3151 |
| XIA, D. Y. et al.,Primary Structure of Anodonta C-reactive Protein,Chin. J. Biochem. Mol. Biol.,2000年,Vol.16, No.2,pp.215-223 |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2025066156A (ja) * | 2019-11-29 | 2025-04-22 | 東洋紡株式会社 | 組換えc反応性タンパク質 |
Also Published As
| Publication number | Publication date |
|---|---|
| JPWO2021106453A1 (ja) | 2021-06-03 |
| CN114761561B (zh) | 2024-04-30 |
| EP4067372A1 (en) | 2022-10-05 |
| JP2025066156A (ja) | 2025-04-22 |
| CN114761561A (zh) | 2022-07-15 |
| WO2021106453A1 (ja) | 2021-06-03 |
| US20230039528A1 (en) | 2023-02-09 |
| EP4067372A4 (en) | 2023-11-08 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN101042403A (zh) | 一种检测耐除草剂大豆中epsps基因的酶联免疫试剂盒及其使用方法 | |
| CN109975536A (zh) | 抗缪勒激素胶乳增强比浊法检测试剂盒及其制备使用方法 | |
| JP2025066156A (ja) | 組換えc反応性タンパク質 | |
| KR20220144822A (ko) | 재조합 칼프로텍틴 | |
| CN114276445A (zh) | 轮状病毒重组蛋白特异性抗体、质粒载体及方法 | |
| CN110763839A (zh) | 一种timp-i胶乳增强比浊法检测试剂盒及其制备使用方法 | |
| CN112852840A (zh) | 一种牛纽布病毒重组vp1基因、重组蛋白及其应用 | |
| WO2017204325A1 (ja) | 改変型ストレプトリジンo | |
| CN102221616B (zh) | 一种鸡毒支原体间接elisa诊断试剂盒 | |
| CN117700539A (zh) | 抗犬瘟热病毒单克隆抗体、质粒载体及制备方法 | |
| CN106554411B (zh) | 可用作标准物质的胱抑素c产品、其制备方法及其用途 | |
| CN114908113B (zh) | 人白细胞介素-5重组蛋白的制备方法 | |
| CN109721651B (zh) | 一种视黄醇结合蛋白检测试剂盒及其临床应用 | |
| CN114277021B (zh) | 胱硫醚-β-裂解酶及其制备方法和应用 | |
| CN103304645A (zh) | 重组链球菌溶血素o蛋白、核苷酸序列、制备方法及应用 | |
| JP6174778B1 (ja) | 肝型脂肪酸結合蛋白質標品、該標品を評価する方法、該標品を用いる測定における肝型脂肪酸結合蛋白質に起因する測定値の変動幅を抑制する方法、肝型脂肪酸結合蛋白質の検量線を作成する方法、及び該蛋白質を定量する方法 | |
| CN108956988B (zh) | 一种羊口疮病毒抗体间接elisa检测试剂盒、检测方法及应用 | |
| CN103387971B (zh) | 一种重组人胃蛋白酶原ii同工酶嵌合蛋白、制备方法及其应用 | |
| JP6218983B1 (ja) | 肝型脂肪酸結合蛋白質標品、該標品を評価する方法、該標品を用いる測定における肝型脂肪酸結合蛋白質に起因する測定値の変動幅を抑制する方法、肝型脂肪酸結合蛋白質の検量線を作成する方法、及び該蛋白質を定量する方法 | |
| CN103834667A (zh) | 化学合成的肺炎链球菌PspA蛋白胞外区基因片段及其表达、应用 | |
| CN102718871A (zh) | 结核分枝杆菌特异性标志物Rv1284的重组蛋白、其制备方法及用途 | |
| CN112979767B (zh) | 检测牛支原体抗体的抗原组合物、试剂盒及其应用 | |
| CN118580319B (zh) | 一种检测非洲猪瘟病毒p30抗体的试剂盒及其应用 | |
| CN101906420B (zh) | 人聚角微丝蛋白基因原核表达系统及其表达蛋白的应用 | |
| CN115947803B (zh) | 一种用于定量检测鼠疫耶尔森菌抗体的诊断抗原 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20230818 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20240709 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20240826 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20241119 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20250129 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20250513 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20250526 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7697371 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |