JP7637166B2 - 凝固第ix因子および凝固第x因子に結合する二重特異性抗体 - Google Patents
凝固第ix因子および凝固第x因子に結合する二重特異性抗体 Download PDFInfo
- Publication number
- JP7637166B2 JP7637166B2 JP2023017261A JP2023017261A JP7637166B2 JP 7637166 B2 JP7637166 B2 JP 7637166B2 JP 2023017261 A JP2023017261 A JP 2023017261A JP 2023017261 A JP2023017261 A JP 2023017261A JP 7637166 B2 JP7637166 B2 JP 7637166B2
- Authority
- JP
- Japan
- Prior art keywords
- amino acid
- acid sequence
- seq
- nos
- antibody
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/46—Hybrid immunoglobulins
- C07K16/468—Immunoglobulins having two or more different antigen binding sites, e.g. multifunctional antibodies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
- A61P7/04—Antihaemorrhagics; Procoagulants; Haemostatic agents; Antifibrinolytic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/36—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against blood coagulation factors
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/31—Immunoglobulins specific features characterized by aspects of specificity or valency multispecific
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/34—Identification of a linear epitope shorter than 20 amino acid residues or of a conformational epitope defined by amino acid residues
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/55—Fab or Fab'
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
- C07K2317/565—Complementarity determining region [CDR]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/75—Agonist effect on antigen
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/92—Affinity (KD), association rate (Ka), dissociation rate (Kd) or EC50 value
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Immunology (AREA)
- Hematology (AREA)
- Biochemistry (AREA)
- Biophysics (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Molecular Biology (AREA)
- Genetics & Genomics (AREA)
- Animal Behavior & Ethology (AREA)
- Diabetes (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Pharmacology & Pharmacy (AREA)
- General Chemical & Material Sciences (AREA)
- Peptides Or Proteins (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Description
本出願は、2016年11月23日に出願の米国仮特許出願第62/425,921号、2017年1月31日に出願の米国仮特許出願第62/452,809号、2017年7月7日に出願の米国仮特許出願第62/529,805号、および2017年11月16日に出願の米国仮特許出願第62/587,284号への利益を主張するものであり、これらは、その全体が参照により本明細書に組み入れられる。
本出願と共に出願された電子提出済み配列表の内容(名称:4159.485PC04_Sequence_listing_ST25.txt;サイズ:1,053,370バイト;および作成日は2017年11月21日)は、その全体が参照により本明細書に組み入れられる。
はFIXzと比べて、遊離FIXaに優先的に結合するか、および/またはFIXa-SMもしくはFIXzに対する抗FIXa抗体またはその抗原結合部分の結合親和性よりも高い結合親和性で、遊離FIXaに結合する。一部の態様では、抗FIXa抗体またはその抗原結合部分は、図3B中の抗体からなる群から選択される参照抗体と交差競合する。一部の態様では、抗FIXa抗体またはその抗原結合部分は、図3B中の抗体からなる群から選択される参照抗体と同じエピトープに結合する。一部の態様では、抗FIXa抗体またはその抗原結合部分は、FXzと比べて遊離FIXaもしくはFIXa-SMに優先的に結合するか、および/または抗FIXa抗体またはその抗原結合部分のFIXzに対する結合親和性よりも高い結合親和性で、遊離FIXaまたはFIXa-SMに結合する。一部の態様では、抗FIXa抗体またはその抗原結合部分は、図3C中の抗体からなる群から選択される参照抗体と交差競合する。一部の態様では、抗FIXa抗体またはその抗原結合部分は、図3C中の抗体からなる群から選択される参照抗体と同じエピトープに結合する。一部の態様では、このような参照抗体は、BIIB-9-882、BIIB-9-433およびそれらの組合せから選択される。一部の態様では、抗FIXa抗体またはその抗原結合部分は、CDR1、CDR2およびCDR3を含み、CDR3は、図3A、図3Bおよび図3C中のVH CDR3または1つもしくは2つの変異を有するVH CDR3からなる群から選択されるVH CDR3を含む。一部の態様では、抗FIXa抗体またはその抗原結合部分は、CDR1、CDR2およびCDR3を含み、CDR3は、ARDX1X2X3X4X5X6YYX7MDV(配列番号753)を含み、X1はVまたはGであり、X2は、GまたはVであり、X3は、GまたはRであり、X4は、YまたはVであり、X5は、AまたはSであり、X6は、GまたはDであり、X7は、Gであるか、または存在しない。一部の態様では、CDR3は、ARDVGGYAGYYGMDV(配列番号905、BIIB-9-484、1335、1336)、ARDISTDGESSLYYYMDV(配列番号901、BIIB-9-460)、ARGPTDSSGYLDMDV(配列番号1186、BIIB-9-882)またはARDGPRVSDYY MDV(配列番号912、BIIB-9-619)を含む。一部の態様では、抗FIXa抗体またはその抗原結合部分は、CDR1、CDR2およびCDR3を含み、CDR1は、図3A、図3Bおよび図3C中のVH CDR1または1つもしくは2つの変異を有するVH CDR1からなる群から選択されるVH CDR1を含む。一部の態様では、抗FIXa抗体またはその抗原結合部分は、VH CDR1、CDR2およびCDR3を含み、CDR2は、図3A、図3Bおよび図3C中のVH CDR2または1つもしくは2つの変異を有するVH CDR2からなる群から選択されるVH CDR2を含む。一部の態様では、抗FIXa抗体またはその抗原結合部分は、VL CDR1、CDR2およびCDR3を含み、CDR1は、図3A、図3Bおよび図3C中のVL CDR1または1つもしくは2つの変異を有するVL CDR1からなる群から選択されるVL CDR1を含む。一部の態様では、抗FIXa抗体またはその抗原結合部分は、VL CDR1、CDR2およびCDR3を含み、CDR2は、図3A、図3Bおよび図3C中のVL CDR2または1つもしくは2つの変異を有するVL CDR2からなる群から選択されるVL CDR2を含む。一部の態様では、抗FIXa抗体またはその抗原結合部分は、VL CDR1、CDR2およびCDR3を含み、CDR3は、図3A、図3Bおよび図3C中のVL CDR3または1つもしくは2つの変異を有するVL CDR3からなる群から選択されるVL CDR3を含む。
およびCDR3配列、ならびに/またはそれぞれ、配列番号950、995および1040を含むVL CDR1、CDR2およびCDR3配列(BIIB-9-484)を含む。一部の態様では、抗FIXa抗体またはその抗原結合部分は、それぞれ、配列番号809、配列番号854および配列番号899を含む、VH CDR1、CDR2およびCDR3配列、ならびに/またはそれぞれ、配列番号944、配列番号989および配列番号1034を含むVL CDR1、VL CDR2およびVL CDR3配列(BIIB-9-440)を含む。一部の態様では、抗FIXa抗体またはその抗原結合部分は、それぞれ、配列番号1102、配列番号1144および配列番号1186を含む、VH CDR1、CDR2およびCDR3配列、ならびに/またはそれぞれ、配列番号1228、配列番号1270および配列番号1312を含むVL CDR1、VL CDR2およびVL CDR3配列(BIIB-9-882)を含む。一部の態様では、抗FIXa抗体またはその抗原結合部分は、それぞれ、配列番号811、配列番号856および配列番号901を含む、VH CDR1、CDR2およびCDR3配列、ならびに/またはそれぞれ、配列番号946、配列番号991および配列番号1036を含むVL CDR1、VL
CDR2およびVL CDR3配列(BIIB-9-460)を含む。一部の態様では、抗FIXa抗体またはその抗原結合部分は、それぞれ、配列番号1108、配列番号1150および配列番号1192を含む、VH CDR1、CDR2およびCDR3配列、ならびに/またはそれぞれ、配列番号1234、配列番号1276および配列番号1318を含むVL CDR1、VL CDR2およびVL CDR3配列(BIIB-9-433)を含む。一部の態様では、抗FIXa抗体またはその抗原結合部分は、それぞれ、配列番号822、配列番号867および配列番号912を含む、VH CDR1、CDR2およびCDR3配列、ならびに/またはそれぞれ、配列番号957、配列番号1002および配列番号1047を含むVL CDR1、VL CDR2およびVL CDR3配列(BIIB-9-619)を含む。一部の態様では、抗FIXa抗体またはその抗原結合部分は、それぞれ、配列番号843、配列番号888および配列番号933を含むVH
CDR1、CDR2およびCDR3配列、ならびに/またはそれぞれ、配列番号950、配列番号995および配列番号1040を含むVL CDR1、VL CDR2およびVL CDR3配列を含むか、または(ii)抗FIXa抗体またはその抗原結合部分は、それぞれ、配列番号844、配列番号889および配列番号934を含むVH CDR1、CDR2およびCDR3配列、ならびに/またはそれぞれ、配列番号950、配列番号995および配列番号1040を含むVL CDR1、VL CDR2およびVL CDR3配列(BIIB-9-1335およびBIIB-9-1336)を含む。抗FIXa抗体またはその抗原結合部分は、VHおよびVLを含み、VHは、配列番号1、3、5、7、9、11、13、15、17、19、21、23、25、27、29、31、33、35、37、39、41、43、45、47、49、51、53、55、57、59、61、63、65、67、69、71、73、75、77、79、81、83、85、87、89、91、93、95、97、99、101、103、105、107、109、111、113、115、117、119、121、123、125、127、129、131、133、135、137、139、141、143、145、147、149、151、153、155、157、159、161、163、165、167、169、171、173、175、177、179、および181からなる群から選択されるアミノ酸配列と、少なくとも約80%、少なくとも約85%、少なくとも約90%、少なくとも約95%、少なくとも約96%、少なくとも約97%、少なくとも約98%、少なくとも約99%または約100%同一のアミノ酸配列を含む。一部の態様では、抗FIXa抗体またはその抗原結合部分は、VHおよびVLを含み、VLは、配列番号191、193、195、197、199、201、203、205、207、209、211、213、215、217、219、221、223、225、227、229、231、233、235、237、239、241、243、245、247、249、251、253、255、257、259、261、263、265、267、269、271、273、275、277、279、281、283、285、287、289、291、293
、295、297、299、301、303、305、307、309、311、313、315、317、319、321、323、325、327、329、331、333、335、337、339、341、343、345、347、349、351、353、355、357、359、361、363、365、および367からなる群から選択されるアミノ酸配列と、少なくとも約80%、少なくとも約85%、少なくとも約90%、少なくとも約95%、少なくとも約96%、少なくとも約97%、少なくとも約98%、少なくとも約99%または約100%同一のアミノ酸配列を含む。一部の態様では、抗FIXa抗体またはその抗原結合部分は、VHおよびVLを含み、VHは、VH1-46.0、VH1-46.4、VH1-46.5、VH1-46.7、VH1-46.9、VH1-69.9、VH3-07.0、VH3-21.0、VH3-21.2、VH3-23.0、VH3-23.1、VH4-31.0、VH4-34.0、VH4-39.0、VH4-39.2、VH4-39.3、VH4-39.5、VH4-39.6、VH4-39.8、VH4-59.6、VH4-0B.4、またはVH4-0B.6の生殖系配列から誘導される。一部の態様では、抗FIXa抗体またはその抗原結合部分は、VHおよびVLを含み、VLは、VK1-05.0、VK1-05.6、VK1-05.9、VK1-05.21、VK1-12.0、VK1-12.3、VK1-33.0、VK1-33.1、VK1-33.2、VK1-33.8、VK1-33.10、VK1-39.0、VK1-39.6、VK2-28.0、VK2-28.1、VK3-11.0、VK3-11.2、VK3-11.6、VK3-11.10、VK3-11.14、VK3-15.0、VK3-15.6、VK3-15.8、VK3-15.11、VK3-15.20、VK3-15.26、VK3-20.0、VK3-20.4、VK3-20.5、VK3-20.8、またはVK4-01.0の生殖系配列から誘導される。一部の態様では、抗FIXa抗体またはその抗原結合部分は、VHおよびVLを含み、(a1)VHおよびVLは、それぞれ、配列番号31および221(BIIB-9-484)を含み;(a2)VHおよびVLは、それぞれ、配列番号19および209(BIIB-9-440)を含み;(a3)VHおよびVLは、それぞれ、配列番号115および301(BIIB-9-882)を含み;(a4)VHおよびVLは、それぞれ、配列番号23および213(BIIB-9-460)を含み;(a5)VHおよびVLは、それぞれ、配列番号127および313(BIIB-9-433)を含み;(a6)VHおよびVLは、それぞれ、配列番号45および235(BIIB-9-619)を含み;(a7)VHおよびVLは、それぞれ、配列番号185および371(BIIB-9-578)を含み;(a8)VHおよびVLは、それぞれ、配列番号87および221(BIIB-9-1335)を含み;または(a9)VHおよびVLは、それぞれ、配列番号89および221(BIIB-9-1336)を含む。
R3を含み、CDR1は、図3D中のVH CDR1または1つもしくは2つの変異を有するVH CDR1からなる群から選択されるVH CDR1を含む。一部の態様では、抗FIXz抗体またはその抗原結合部分は、VH CDR1、CDR2およびCDR3を含み、CDR2は、図3D中のVH CDR2または1つもしくは2つの変異を有するVH CDR2からなる群から選択されるVH CDR2を含む。一部の態様では、抗FIXz抗体またはその抗原結合部分は、VL CDR1、CDR2およびCDR3を含み、CDR1は、図3D中のVL CDR1または1つもしくは2つの変異を有するVL CDR1からなる群から選択されるVL CDR1を含む。一部の態様では、抗FIXz抗体またはその抗原結合部分は、VL CDR1、CDR2およびCDR3を含み、CDR2は、図3D中のVL CDR2または1つもしくは2つの変異を有するVL CDR2からなる群から選択されるVL CDR2を含む。一部の態様では、抗FIXz抗体またはその抗原結合部分は、VL CDR1、CDR2およびCDR3を含み、CDR3は、図3D中のVL CDR3または1つもしくは2つの変異を有するVL CDR3からなる群から選択されるVL CDR3を含む。一部の態様では、抗FIX抗体は、IgG1、IgG2、IgG3、IgG4またはそれらのバリアントからなる群から選択される。一部の態様では、抗FIX抗体はIgG4抗体である。一部の態様では、抗FIX抗体は、エフェクターのない(effectorless)IgG4 Fcを含む。一部の態様では、抗FIX抗体またはその抗原結合部分は、重鎖定常領域を含む。一部の態様では、抗FIX抗体は、ヒト抗体、操作された抗体またはヒト化抗体である。一部の態様では、抗FIX抗原結合部分は、Fab、Fab’、F(ab’)2、Fvまたは一本鎖Fv(scFv)を含む。
抗FXz抗体またはその抗原結合部分は、抗体またはその抗原結合部分のFXaへの結合親和性よりも高い結合親和性でFXzに結合する。同様に、抗体またはその抗原結合部分のFXaへの結合親和性よりも高い結合親和性でFXzに結合する、単離された抗FXz抗体またはその抗原結合部分が提供される。一部の態様では、抗FXz抗体またはその抗原結合部分は、BLIによって測定すると、約100nM以下、約90nM以下、約80nM以下、約70nM以下、約60nM以下、約50nM以下、約40nM以下、約30nM以下、約20nM以下、約10nM以下、約9nM以下、約8nM以下、約7nM以下、約6nM以下、約5nM以下、約4nM以下、約3nM以下、約2nM以下、約1nM以下のKDで、FXzに結合する。一部の態様では、FXaは、遊離FXa、またはEGR-CMKに共有結合により連結されているFXa(FIXa-SM)である。一部の態様では、FXzは、活性化不能型第X因子(FXn)を含む。一部の態様では、抗FXz抗体またはその抗原結合部分は、図12Aおよび図12B中の抗体からなる群から選択される参照抗体と交差競合する。一部の態様では、抗FXz抗体またはその抗原結合部分は、図12Aおよび図12B中の抗体からなる群から選択される参照抗体と同じエピトープに結合する。一部の態様では、抗FXz抗体またはその抗原結合部分は、BIIB-12-915、BIIB-12-917、BIIB-12-932、およびそれらの任意の組合せからなる群から選択される参照抗体と同じエピトープに結合する。一部の態様では、抗FXz抗体またはその抗原結合部分は、CDR1、CDR2およびCDR3を含み、CDR3は、図12Aおよび図12中のVH CDR3または1つもしくは2つの変異を有するVH CDR3からなる群から選択されるVH CDR3を含む。一部の態様では、抗FXz抗体またはその抗原結合部分は、CDR1、CDR2およびCDR3を含み、CDR3は、ARX1X2X3RX4X5X6X7FDX8(配列番号766)を含み、X1は、GまたはLであり、X2は、RまたはGであり、X3は、FまたはYであり、X4は、PまたはGであり、X5は、RまたはAであり、X6は、GまたはSであり、X7は、RまたはAであり、X8は、YまたはIである。一部の態様では、抗FXz抗体またはその抗原結合部分は、CDR1、CDR2およびCDR3を含み、CDR3は、ARGRFRPRGRFDY(配列番号1575、BIIB-12-917)、ARLGYRGASAFDI(配列番号1589、BIIB-12-932)またはARVGGGYANP(配列番号1573、BIIB-12-915)を含む。一部の態様では、抗FXz抗体またはその抗原結合部分は、VH CDR1、CDR2およびCDR3を含み、CDR1は、図12Aおよび図12B中のVH CDR1または1つもしくは2つの変異を有するVH CDR1からなる群から選択されるVH CDR1を含む。一部の態様では、抗FXz抗体またはその抗原結合部分は、VH CDR1、CDR2およびCDR3を含み、CDR2は、図12Aおよび図12B中のVH CDR2または1つもしくは2つの変異を有するVH CDR2からなる群から選択されるVH CDR2を含む。一部の態様では、抗FXz抗体またはその抗原結合部分は、VL CDR1、CDR2およびCDR3を含み、CDR1は、図12Aおよび図12B中のVL CDR1または1つもしくは2つの変異を有するVL CDR1からなる群から選択されるVL CDR1を含む。一部の態様では、抗FXz抗体またはその抗原結合部分は、VL CDR1、CDR2およびCDR3を含み、CDR2は、図12Aおよび図12B中のVL CDR2または1つもしくは2つの変異を有するVL CDR2からなる群から選択されるVL CDR2を含む。一部の態様では、抗FXz抗体またはその抗原結合部分は、VL CDR1、CDR2およびCDR3を含み、CDR3は、図12Aおよび図12B中のVL CDR3または1つもしくは2つの変異を有するVL CDR3からなる群から選択されるVL CDR3を含む。
、CDR2およびCDR3、ならびにVL CDR1、CDR2およびCDR3を含む。一部の態様では、抗FXz抗体またはその抗原結合部分は、それぞれ、配列番号1393、1483または1573を含む、VH CDR1、CDR2およびCDR3配列、ならびに/またはそれぞれ、配列番号1663、1753および1843を含むVL CDR1、VL CDR2およびVL CDR3配列(BIIB-12-915)を含む。一部の態様では、抗FXz抗体またはその抗原結合部分は、それぞれ、配列番号1395、1485または1575を含む、VH CDR1、CDR2およびCDR3配列、ならびに/またはそれぞれ、配列番号1665、1755および1845を含むVL CDR1、VL CDR2およびVL CDR3配列(BIIB-12-917)を含む。一部の態様では、抗FXz抗体またはその抗原結合部分は、それぞれ、配列番号1409、1499または1589を含む、VH CDR1、CDR2およびCDR3配列、ならびに/またはそれぞれ、配列番号1679、1769および1859を含むVL CDR1、VL
CDR2およびVL CDR3配列(BIIB-12-932)を含む。一部の態様では、抗FXz抗体またはその抗原結合部分は、VHおよびVLを含み、VHは、配列番号377、379、381、383、385、387、389、391、393、395、397、399、401、403、405、407、409、411、413、415、417、419、421、423、425、427、429、431、433、435、437、439、441、443、445、447、449、451、453、455、457、459、461、463、465、467、469、471、473、475、477、479、481、483、485、487、489、491、493、495、497、499、501、503、505、507、509、511、513、515、517、519、521、523、525、527、529、531、533、535、537、539、541、543、545、547、549、551、553、および555からなる群から選択されるアミノ酸配列と、少なくとも約80%、少なくとも約85%、少なくとも約90%、少なくとも約95%、少なくとも約96%、少なくとも約97%、少なくとも約98%、少なくとも約99%または約100%同一のアミノ酸配列を含む。一部の態様では、抗FXz抗体またはその抗原結合部分は、VHおよびVLを含み、VLは、配列番号565、567、569、571、573、575、579、581、583、585、587、589、591、593、595、597、599、601、603、605、607、609、611、613、615、617、619、621、623、625、627、629、631、633、635、637、639、641、643、645、647、649、651、653、655、657、659、661、663、665、667、669、671、673、675、677、679、681、683、685、687、689、691、693、695、697、699、701、703、705、707、709、711、713、715、717、719、721、723、725、727、729、731、733、735、737、739、741、および743からなる群から選択されるアミノ酸配列と、少なくとも約80%、少なくとも約85%、少なくとも約90%、少なくとも約95%、少なくとも約96%、少なくとも約97%、少なくとも約98%、少なくとも約99%または約100%同一のアミノ酸配列を含む。一部の態様では、抗FXz抗体またはその抗原結合部分は、VHおよびVLを含み、VHは、VH1-18.0、VH1-18.1、VH1-18.8、VH1-46.0、VH1-46.4、VH1-46.5、VH1-46.6、VH1-46.7、VH1-46.8、VH1-46.9、VH3-21.0、VH3-23.0、VH3-23.2、VH3-23.6、VH3-30.0、VH4-31.5、VH4-39.0、VH4-39.5、VH4-0B.4、またはVH5-51.1の生殖系配列から誘導される。一部の態様では、抗FXz抗体またはその抗原結合部分は、VHおよびVLを含み、VLは、VK1-05.6、VK1-05.12、VK1-12.0、VK1-12.4、VK1-12.7、VK1-12.10、VK1-12.15、VK1-39.0、VK1-39.3、VK1-39.15、VK2-28.0、VK2-28.1、VK2-28.5、VK3-11.0、VK3-11.2、VK3-11.6、VK3-11
.14、VK3-15.0、VK3-15.8、VK3-15.10、VK3-20.0、VK3-20.1、VK3-20.4、VK3-20.5、VK4-01.0、VK4-01.4、VK4-01.20の生殖系配列から誘導される。一部の態様では、抗FX抗体またはその抗原結合部分は、VHおよびVLを含み、(b1)VHおよびVLは、それぞれ、配列番号423および611(BIIB-12-915)を含み;(b2)VHおよびVLは、それぞれ、配列番号427および615(BIIB-12-917)を含み;または(b3)VHおよびVLは、それぞれ、配列番号455および643(BIIB-12-932)を含む。
それぞれ、配列番号559および747(BIIB-12-925)を含む。一部の態様では、抗FX抗体またはその抗原結合部分は、IgG1、IgG2、IgG3、IgG4またはそれらのバリアントからなる群から選択される。一部の態様では、抗FX抗体またはその抗原結合部分はIgG4抗体である。一部の態様では、抗FX抗体またはその抗原結合部分は、エフェクターのないIgG4 Fcを含む。一部の態様では、抗FX抗体またはその抗原結合部分は、重鎖定常領域を含む。一部の態様では、抗FX抗体は、ヒト抗体、操作された抗体またはヒト化抗体である。一部の態様では、その抗原結合部分は、Fab、Fab’、F(ab’)2、Fvまたは一本鎖Fv(scFv)を含む。本開示はまた、第2の結合特異性を有する分子に連結している、本明細書に開示される抗FX抗体を含む二重特異性分子を提供する。同様に、本明細書に開示される抗FX抗体もしくはその抗原結合部分の重鎖および/もしくは軽鎖可変領域、または本明細書に開示される抗FX抗体もしくはその抗原結合部分を含む二重特異性分子をコードする核酸が提供される。同様に、核酸分子を含む発現ベクターが提供される。同様に、発現ベクターにより形質転換された細胞が提供される。同様に、抗体もしくはその抗原結合部分、または二重特異性分子を含むイムノコンジュゲートであって、薬剤に連結されているイムノコンジュゲートが提供される。同様に、(i)抗体もしくはその抗原結合部分、または二重特異性分子、またはイムノコンジュゲート、および(ii)担体を含む組成物が提供される。同様に、(i)抗体もしくはその抗原結合部分、または二重特異性分子、またはイムノコンジュゲート、および(ii)使用のための指示書を含むキットが提供される。同様に、抗FX抗体またはその抗原結合部分を製造する方法であって、細胞中で抗体またはその抗原結合部分を発現させる工程、およびこの細胞からこの抗体またはその抗原結合部分を単離する工程を含む、方法が提供される。
、(a)抗FIX抗体またはその抗原結合部分は、(a1)それぞれ、配列番号815、860または905を含む、VH CDR1、CDR2およびCDR3配列、ならびに/またはそれぞれ、配列番号950、995または1040を含むVL CDR1、VL CDR2およびVL CDR3配列(BIIB-9-484);(a2)それぞれ、配列番号822、867および912を含む、VH CDR1、CDR2およびCDR3配列、ならびに/またはそれぞれ、配列番号957、1002および1047を含むVL CDR1、CDR2およびCDR3配列(BIIB-9-619);(a3)それぞれ、配列番号1347、1351および1355を含む、VH CDR1、CDR2およびCDR3配列、ならびに/またはそれぞれ、配列番号1359、1363および1367を含むVL CDR1、CDR2およびCDR3配列(BIIB-9-578);(a4)それぞれ、配列番号843、888および933を含む、VH CDR1、CDR2およびCDR3配列、ならびに/またはそれぞれ、配列番号978、1023および1068を含むVL CDR1、CDR2およびCDR3配列(BIIB-9-1335)を含み;または(a5)それぞれ、配列番号844、889および934を含む、VH CDR1、CDR2およびCDR3配列、ならびに/またはそれぞれ、配列番号979、1024および1069を含むVL CDR1、CDR2およびCDR3配列(BIIB-9-1336)を含み;(b)抗FX抗体またはその抗原結合部分は、(b1)それぞれ、配列番号1393、1483および1573を含む、VH CDR1、CDR2およびCDR3配列、ならびに/またはそれぞれ、配列番号1663、1753および1843を含むVL CDR1、CDR2およびCDR3配列(BIIB-12-915);(b2)それぞれ、配列番号1395、1485および1575を含む、VH CDR1、CDR2およびCDR3配列、ならびに/またはそれぞれ、配列番号1665、1755および1845を含むVL CDR1、CDR2およびCDR3配列(BIIB-12-917);(b3)それぞれ、配列番号1911、1915および1919を含む、VH CDR1、CDR2およびCDR3配列、ならびに/またはそれぞれ、配列番号1923、1927および1931を含むVL CDR1、CDR2およびCDR3配列(BIIB-12-925);(b4)それぞれ、配列番号1409、1499および1589を含む、VH CDR1、CDR2およびCDR3配列、ならびに/またはそれぞれ、配列番号1679、1769および1859を含むVL CDR1、CDR2およびCDR3配列(BIIB-12-932);または(b5)それぞれ、配列番号1433、1523および1613を含む、VH CDR1、CDR2およびCDR3配列、ならびに/またはそれぞれ、配列番号1703、1793および1883を含むVL CDR1、CDR2およびCDR3配列(BIIB-12-1306)を含む。本明細書に開示される二重特異性分子の一部の態様では、(a)抗FIX抗体またはその抗原結合部分は、(a1)それぞれ、配列番号31および221を含むVHおよびLV(BIIB-9-484);(a2)それぞれ、配列番号45および235を含むVHおよびVL(BIIB-9-619);(a3)それぞれ、配列番号185および371を含むVHおよびVL(BIIB-9-578);(a4)それぞれ、配列番号87および221を含むVHおよびVL(BIIB-9-1335);または(a5)それぞれ、配列番号89および221を含むVHおよびVL(BIIB-9-1336)を含み;(b)抗FX抗体またはその抗原結合部分は、(b1)それぞれ、配列番号423および611を含むVHおよびLV(BIIB-12-915);(b2)それぞれ、配列番号427および615を含むVHおよびVL(BIIB-12-917);(b3)それぞれ、配列番号559および747を含むVHおよびVL(BIIB-12-925);(b4)それぞれ、配列番号455および643を含むVHおよびVL(BIIB-12-932);または(b5)それぞれ、配列番号503および691を含むVHおよびVL(BIIB-12-1306)を含む。本明細書に開示される二重特異性分子の一部の態様では、(i)抗FIX抗体またはその抗原結合部分は、それぞれ、配列番号31および221を含むVHおよびLV(BIIB-9-484)を含み;および抗FX抗体またはその抗原結合部分は、それぞれ、配列番号423および611を含むVHおよびVL(BIIB-12-915)を含み;また
は(ii)抗FIX抗体またはその抗原結合部分は、それぞれ、配列番号31および221を含むVHおよびVL(BIIB-9-484)を含み;抗FX抗体またはその抗原結合部分は、それぞれ、配列番号427および615を含むVHおよびVL(BIIB-12-917)を含み;または(iii)抗FIX抗体またはその抗原結合部分は、それぞれ、配列番号31および221を含むVHおよびVL(BIIB-9-484)を含み;抗FX抗体またはその抗原結合部分は、それぞれ、配列番号559および747を含むVHおよびVL(BIIB-12-925)を含み;または(iv)抗FIX抗体またはその抗原結合部分は、それぞれ、配列番号31および221を含むVHおよびVL(BIIB-9-484)を含み;抗FX抗体またはその抗原結合部分は、それぞれ、配列番号455および643を含むVHおよびVL(BIIB-12-932)を含み;または(v)抗FIX抗体またはその抗原結合部分は、それぞれ、配列番号185および371を含むVHおよびVL(BIIB-9-578)を含み;抗FX抗体またはその抗原結合部分は、それぞれ、配列番号423および611を含むVHおよびVL(BIIB-12-915)を含み;または(vi)抗FIX抗体またはその抗原結合部分は、それぞれ、配列番号185および371を含むVHおよびVL(BIIB-9-578)を含み;抗FX抗体またはその抗原結合部分は、それぞれ、配列番号427および615を含むVHおよびVL(BIIB-12-917)を含み;または(vii)抗FIX抗体またはその抗原結合部分は、それぞれ、配列番号45および235を含むVHおよびVL(BIIB-9-619)を含み;抗FX抗体またはその抗原結合部分は、それぞれ、配列番号427および615を含むVHおよびVL(BIIB-12-917)を含み;または(viii)抗FIX抗体またはその抗原結合部分は、それぞれ、配列番号45および235を含むVHおよびVL(BIIB-9-619)を含み;および抗FX抗体またはその抗原結合部分は、それぞれ、配列番号559および747を含むVHおよびVL(BIIB-12-925)を含む。一部の態様では、二重特異性分子は、少なくとも1つのFVIIIa活性アッセイにおいて、活性化第VIII因子(FVIIIa)補因子を機能的に擬似する。一部の態様では、FVIIIa活性アッセイは、発色FXa生成アッセイ、一段階凝固アッセイまたはそれらの組合せから選択される。一部の態様では、FVIIIa活性は、同一のアッセイにおいて、普通なら、FVIIIにより実現される活性の、少なくとも10%、20%、30%、35%、40%、45%、50%、60%、70%、80%、90%、100%、110%、120%、130%、140%、150%、160%、170%、180%、190%または200%を実現する。一部の態様では、二重特異性分子は、インビトロまたはインビボで、プロトロンビンからトロンビンを、フィブリノゲンからフィブリンを、および/またはフィブリン凝塊を生成することができる。一部の態様では、二重特異性分子は、BLIによって決定すると、FIXaとFXの両方に同時に結合する。一部の態様では、二重特異性分子は、IgGアイソタイプのものである。一部の態様では、IgGアイソタイプは、IgG1部分クラスのものである。一部の態様では、IgGアイソタイプは、IgG4部分クラスのものである。一部の態様では、二重特異性分子は、二重特異性IgGフォーマットのものであり、表2中の抗体からなる群から選択される。一部の態様では、二重特異性分子は、二重特異性ヘテロ二量体フォーマットのものである。一部の態様では、二重特異性分子は、2つの異なる重鎖および2つの異なる軽鎖を含む。一部の態様では、二重特異性分子は、2つの同一の軽鎖および2つの異なる重鎖を含む。一部の態様では、二重特異性分子は、血友病を有する対象における、出血エピソードの出現率を制御または低減することが可能である。一部の態様では、二重特異性分子は、血友病を有する対象における、ホメオスタシスを維持することができる。一部の態様では、二重特異性分子は、血友病を有する対象における、決まった手順の予防を実現することができる。一部の態様では、対象は、第VIII因子に対して中和抗体を発達させる、または発達させることが予想される。
重特異性分子または二重特異性分子を含むイムノコンジュゲート、および(ii)担体を含む組成物が提供される。同様に、(i)本明細書に開示される二重特異性分子または二重特異性分子を含むイムノコンジュゲート、および(ii)使用のための指示書を含むキットが提供される。同様に、本明細書に開示される二重特異性分子をコードする核酸配列が提供される。同様に、核酸を含むベクター、およびベクターを含む宿主細胞が提供される。一部の態様では、宿主細胞は、原核細胞、真核細胞、原生生物細胞、動物細胞、植物細胞、真菌細胞、酵母細胞、Sf9細胞、哺乳動物細胞、鳥類細胞、昆虫細胞、CHO細胞、HEK細胞またはCOS細胞である。同様に、本明細書に開示される二重特異性分子を生成する方法であって、二重特異性分子の発現を可能にする条件下で、本明細書に開示される宿主細胞を培養する工程を含む方法が提供される。一部の態様では、本明細書に開示される二重特異性分子を生成する方法は、ヘテロ二量化を増強する条件を使用することをさらに含む。
番号2194)を含み、X1は、S、GまたはEであり、X2は、YまたはFであり、X3は、S、E、GまたはDであり、X4は、N、V、AまたはTである;および/または(ii)VH CDR2は、アミノ酸配列X5ISX6X7X8X9X10IYYADSVKG(配列番号2195)を含み、X5は、S、A、YまたはGであり、X6は、SまたはAであり、X7は、S、AまたはGであり、X8は、S、GまたはDであり、X9は、S、TまたはGであり、X10は、YまたはTである。
VH CDR1は、配列番号2048~2052から選択され、VH CDR2は、配列番号2074~2078から選択され、VH CDR3は、配列番号2100~2104から選択されるVH CDR1、CDR2およびCDR3、ならびに/または(ii)VL CDR1、CDR2およびCDR3であって、VL CDR1は、配列番号2126~2130から選択され、VL CDR2は、配列番号2152~2156から選択され、VL CDR3は、配列番号2178~2182から選択される、VL CDR1、CDR2およびCDR3を含む。
S(配列番号2206)を含み、X6は、SまたはYであり、X7は、S、Y、R、TまたはQであり、X8は、Y、G、PまたはAであり、X9は、SまたはQであり、X10は、Sまたはであり、X11は、YまたはQである。
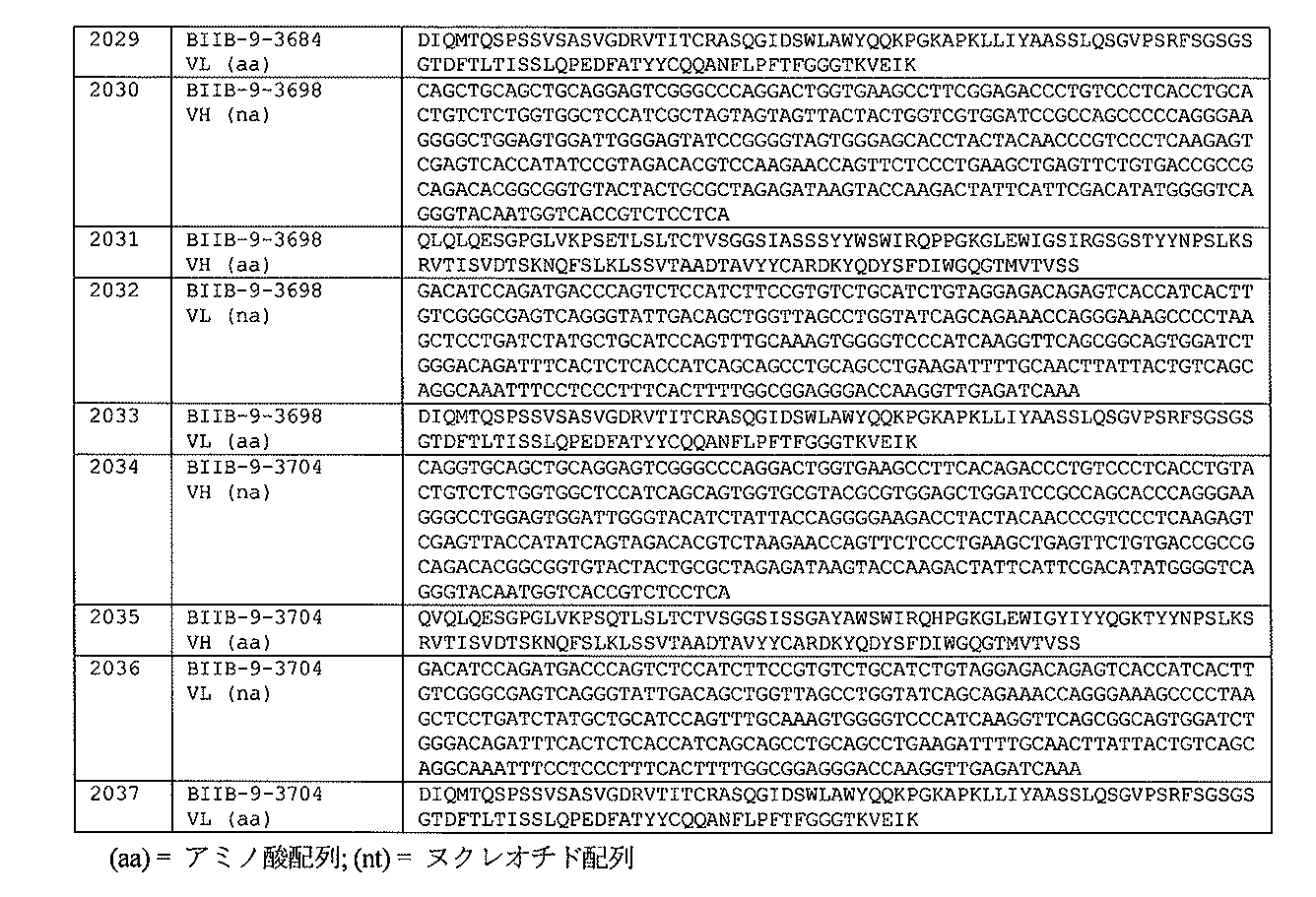
れ、配列番号1967および1969(BIIB-9-3650)を含み;(a10)VHおよびVLは、それぞれ、配列番号1971および1973(BIIB-9-3654)を含み;(a11)VHおよびVLは、それぞれ、配列番号1975および1977(BIIB-9-3753)を含み;(a12)VHおよびVLは、それぞれ、配列番号1979および1981(BIIB-9-3754)を含み;(a13)VHおよびVLは、それぞれ、配列番号1983および1985(BIIB-9-3756)を含み;(a14)VHおよびVLは、それぞれ、配列番号1987および1989(BIIB-9-3764)を含み;(a15)VHおよびVLは、それぞれ、配列番号1991および1993(BIIB-9-3766)を含み;(a16)VHおよびVLは、それぞれ、配列番号1995および1997(BIIB-9-3707)を含み;(a17)VHおよびVLは、それぞれ、配列番号1999および2001(BIIB-9-3709)を含み;(a18)VHおよびVLは、それぞれ、配列番号2003および2005(BIIB-9-3720)を含み;(a19)VHおよびVLは、それぞれ、配列番号2007および2009(BIIB-9-3727)を含み;(a20)VHおよびVLは、それぞれ、配列番号2011および2013(BIIB-9-3745)を含み;(a21)VHおよびVLは、それぞれ、配列番号2015および2017(BIIB-9-3780)を含み;(a22)VHおよびVLは、それぞれ、配列番号2019および2021(BIIB-9-3675)を含み;(a23)VHおよびVLは、それぞれ、配列番号2023および2025(BIIB-9-3681)を含み;(a24)VHおよびVLは、それぞれ、配列番号2027および2029(BIIB-9-3684)を含み;(a25)VHおよびVLは、それぞれ、配列番号2031および2033(BIIB-9-3698)を含み;または(a26)VHおよびVLは、それぞれ、配列番号2035および2037(BIIB-9-3704)を含む。
実施形態1. 活性化第IX因子(FIXa)に特異的に結合する、単離された抗体またはその抗原結合部分(「抗FIXa抗体またはその抗原結合部分」)であって、抗FIXa抗体またはその抗原結合部分が、FIXaおよび第IX因子チモーゲン(FIXz)の存在下でFIXaに優先的に結合する、抗FIXa抗体またはその抗原結合部分。
れらの任意の組合せから選択される、実施形態18または19の抗FIXa抗体またはその抗原結合部分。
CDR2からなる群から選択されるVH CDR2を含む、前記実施形態のいずれかの抗FIXa抗体またはその抗原結合部分。
CDR1からなる群から選択されるVL CDR1を含む、前記実施形態のいずれかの抗FIXa抗体またはその抗原結合部分。
CDR2からなる群から選択されるVL CDR2を含む、前記実施形態のいずれかの抗FIXa抗体またはその抗原結合部分。
CDR3からなる群から選択されるVL CDR3を含む、前記実施形態のいずれかの抗FIXa抗体またはその抗原結合部分。
にVL CDR1、CDR2およびCDR3が、それぞれ、図3A、図3Bおよび図3Cの、VH CDR1、VH CDR2およびVH CDR3、ならびにVL CDR1、CDR2およびCDR3を含む、抗FIXa抗体またはその抗原結合部分。
(a2)抗体が、それぞれ、配列番号1102、配列番号1144および配列番号1186を含む、VH CDR1、CDR2およびCDR3配列、ならびに/またはそれぞれ、配列番号1228、配列番号1270および配列番号1312を含むVL CDR1、VL CDR2およびVL CDR3配列(BIIB-9-882)を含み;
(a3)抗体が、それぞれ、配列番号811、配列番号856および配列番号901を含む、VH CDR1、CDR2およびCDR3配列、ならびに/またはそれぞれ、配列番号946、配列番号991および配列番号1036を含むVL CDR1、VL CDR2およびVL CDR3配列(BIIB-9-460)を含み;または
(a4)抗体が、それぞれ、配列番号1108、配列番号1150および配列番号1192を含む、VH CDR1、CDR2およびCDR3配列、ならびに/またはそれぞれ、配列番号1234、配列番号1276および配列番号1318を含むVL CDR1、VL CDR2およびVL CDR3配列(BIIB-9-433)を含む、実施形態29の抗FIXa抗体またはその抗原結合部分。
、155、157、159、161、163、165、167、169、171、173、175、177、179、および181からなる群から選択されるアミノ酸配列と、少なくとも約80%、少なくとも約85%、少なくとも約90%、少なくとも約95%、少なくとも約96%、少なくとも約97%、少なくとも約98%、少なくとも約99%または約100%同一のアミノ酸配列を含む、前記実施形態のいずれかの抗FIXa抗体またはその抗原結合部分。
(a1)VHおよびVLは、それぞれ、配列番号31および221(BIIB-9-484)を含み;
(a2)VHおよびVLは、それぞれ、配列番号19および209(BIIB-9-440)を含み;
(a3)VHおよびVLは、それぞれ、配列番号115および301(BIIB-9-882)を含み;
(a4)VHおよびVLは、それぞれ、配列番号23および213(BIIB-9-460)を含み;
(a5)VHおよびVLは、それぞれ、配列番号127および313(BIIB-9-4
33)を含み;
(a6)VHおよびVLは、それぞれ、配列番号45および235(BIIB-9-619)を含み;
(a7)VHおよびVLは、それぞれ、配列番号185および371(BIIB-9-578)を含み;
(a8)VHおよびVLは、それぞれ、配列番号87および221(BIIB-9-1335)を含み;または
(a9)VHおよびVLは、それぞれ、配列番号89および221(BIIB-9-1336)を含む
前記実施形態のいずれかの抗FIXa抗体またはその抗原結合部分。
1、VH1-18.8、VH1-46.0、VH1-46.4、VH1-46.5、VH1-46.6、VH1-46.7、VH1-46.8、VH1-46.9、VH3-21.0、VH3-23.0、VH3-23.2、VH3-23.6、VH3-30.0、VH4-31.5、VH4-39.0、VH4-39.5、VH4-0B.4またはVH5-51.1のうちの生殖系配列から誘導される、実施形態66から88のいずれか1つの抗FXz抗体またはその抗原結合部分。
(b1)VHおよびVLが、それぞれ、配列番号423および611(BIIB-12-915)を含み;
(b2)VHおよびVLが、それぞれ、配列番号427および615(BIIB-12-917)を含み;または
(b3)VHおよびVLが、それぞれ、配列番号455および643(BIIB-12-932)を含む、実施形態66から90のいずれか1つの抗FXz抗体またはその抗原結合部分。
CDR3配列(BIIB-12-925)を含む、実施形態103の抗FXaまたはその抗原結合部分。
6の抗FX抗体またはその抗原結合部分。
いずれか1つの抗FX抗体またはその抗原結合部分を含む、二重特異性分子。
(ii)抗FX抗体またはその抗原結合部分が、VH CDR1、CDR2およびCDR3、ならびにVL CDR1、CDR2およびCDR3を含み、VH CDR1、CDR2およびCDR3、ならびにVL CDR1、CDR2およびCDR3が、図16A、図16B、図16Cおよび図16D中の抗FX(BIIB-12)抗体の、VH CDR1、VH CDR2およびVH CDR3ならびにVL CDR1、VL CDR2およびVL CDR3からなる群から選択される、実施形態122から124のいずれか1つの二重特異性分子。
(a1)それぞれ、配列番号815、860または905を含む、VH CDR1、CDR2およびCDR3配列、ならびに/またはそれぞれ、配列番号950、995または1040を含むVL CDR1、VL CDR2およびVL CDR3配列(BIIB-9-484);
(a2)それぞれ、配列番号822、867および912を含む、VH CDR1、CDR2およびCDR3配列、ならびに/またはそれぞれ、配列番号957、1002および1047を含むVL CDR1、CDR2およびCDR3配列(BIIB-9-619);
(a3)それぞれ、配列番号1347、1351および1355を含む、VH CDR1、CDR2およびCDR3配列、ならびに/またはそれぞれ、配列番号1359、1363および1367を含むVL CDR1、CDR2およびCDR3配列(BIIB-9-578);
(a4)それぞれ、配列番号843、888および933を含む、VH CDR1、CDR2およびCDR3配列、ならびに/またはそれぞれ、配列番号978、1023および1068を含むVL CDR1、CDR2およびCDR3配列(BIIB-9-1335);または
(a5)それぞれ、配列番号844、889および934を含む、VH CDR1、CDR2およびCDR3配列、ならびに/またはそれぞれ、配列番号979、1024および1069を含むVL CDR1、CDR2およびCDR3配列(BIIB-9-1336)を含み;
(b)抗FX抗体またはその抗原結合部分が、
(b1)それぞれ、配列番号1393、1483および1573を含む、VH CDR1、CDR2およびCDR3配列、ならびに/またはそれぞれ、配列番号1663、1753および1843を含むVL CDR1、CDR2およびCDR3配列(BIIB-12-915);
(b2)それぞれ、配列番号1395、1485および1575を含む、VH CDR1、CDR2およびCDR3配列、ならびに/またはそれぞれ、配列番号1665、1755および1845を含むVL CDR1、CDR2およびCDR3配列(BIIB-12-917);
(b3)それぞれ、配列番号1911、1915および1919を含む、VH CDR1、CDR2およびCDR3配列、ならびに/またはそれぞれ、配列番号1923、1927および1931を含むVL CDR1、CDR2およびCDR3配列(BIIB-12-925);
(b4)それぞれ、配列番号1409、1499および1589を含む、VH CDR1、CDR2およびCDR3配列、ならびに/またはそれぞれ、配列番号1679、1769および1859を含むVL CDR1、CDR2およびCDR3配列(BIIB-12-932);または
(b5)それぞれ、配列番号1433、1523および1613を含む、VH CDR1、CDR2およびCDR3配列、ならびに/またはそれぞれ、配列番号1703、1793および1883を含むVL CDR1、CDR2およびCDR3配列(BIIB-12-1306)を含む、実施形態122から124のいずれか1つの二重特異性分子。
(a1)それぞれ、配列番号31および221を含むVHおよびVL(BIIB-9-484);
(a2)それぞれ、配列番号45および235を含むVHおよびVL(BIIB-9-619);
(a3)それぞれ、配列番号185および371を含むVHおよびVL(BIIB-9-578);
(a4)それぞれ、配列番号87および221を含むVHおよびVL(BIIB-9-1335);または
(a5)それぞれ、配列番号89および221を含むVHおよびVL(BIIB-9-1336)を含み;
(b)抗FX抗体またはその抗原結合部分が、
(b1)それぞれ、配列番号423および611を含むVHおよびVL(BIIB-12-915);
(b2)それぞれ、配列番号427および615を含むVHおよびVL(BIIB-12-917);
(b3)それぞれ、配列番号559および747を含むVHおよびVL(BIIB-12-925);
(b4)それぞれ、配列番号455および643を含むVHおよびVL(BIIB-12-932);または
(b5)それぞれ、配列番号503および691を含むVHおよびVL(BIIB-12-1306)を含む、実施形態122から124のいずれか1つの二重特異性分子。
(ii)抗FIX抗体またはその抗原結合部分が、それぞれ、配列番号31および221を含むVHおよびVL(BIIB-9-484)を含み、抗FX抗体またはその抗原結合
部分が、それぞれ、配列番号427および615を含むVHおよびVL(BIIB-12-917)を含み;
(iii)抗FIX抗体またはその抗原結合部分が、それぞれ、配列番号31および221を含むVHおよびVL(BIIB-9-484)を含み、抗FX抗体またはその抗原結合部分が、それぞれ、配列番号559および747を含むVHおよびVL(BIIB-12-925)を含み;
(iv)抗FIX抗体またはその抗原結合部分が、それぞれ、配列番号31および221を含むVHおよびVL(BIIB-9-484)を含み、抗FX抗体またはその抗原結合部分が、それぞれ、配列番号455および643を含むVHおよびVL(BIIB-12-932)を含み;
(v)抗FIX抗体またはその抗原結合部分が、それぞれ、配列番号185および371を含むVHおよびVL(BIIB-9-578)を含み、抗FX抗体またはその抗原結合部分が、それぞれ、配列番号423および611を含むVHおよびVL(BIIB-12-915)を含み;
(vi)抗FIX抗体またはその抗原結合部分が、それぞれ、配列番号185および371を含むVHおよびVL(BIIB-9-578)を含み、抗FX抗体またはその抗原結合部分が、それぞれ、配列番号427および615を含むVHおよびVL(BIIB-12-917)を含み;
(vii)抗FIX抗体またはその抗原結合部分が、それぞれ、配列番号45および235を含むVHおよびVL(BIIB-9-619)を含み、抗FX抗体またはその抗原結合部分が、それぞれ、配列番号427および615を含むVHおよびVL(BIIB-12-917)を含み;または
(viii)抗FIX抗体またはその抗原結合部分が、それぞれ、配列番号45および235を含むVHおよびVL(BIIB-9-619)を含み、抗FX抗体またはその抗原結合部分が、それぞれ、配列番号559および747を含むVHおよびVL(BIIB-12-925)を含む、実施形態122から127のいずれか1つの二重特異性分子。
。
5の抗FIXa抗体またはその抗原結合部分。
(i)VH CDR1は、表7中のVH CDR1または1つもしくは2つの変異を有するVH CDR1からなる群から選択されるVH CDR1を含み;および/または
(ii)VH CDR2は、表7中のVH CDR2または1つもしくは2つの変異を有するVH CDR2からなる群から選択されるVH CDR2を含み;および/または
(iii)VH CDR3は、表7中のVH CDR3または1つもしくは2つの変異を有するVH CDR3からなる群から選択されるVH CDR3を含み;および/または(iv)VL CDR1は、表7中のVL CDR1または1つもしくは2つの変異を有するVL CDR1からなる群から選択されるVL CDR1を含み;および/または
(v)VL CDR2は、表7中のVL CDR2または1つもしくは2つの変異を有するVL CDR2からなる群から選択されるVL CDR2を含み;および/または
(vi)VL CDR3は、表7中のVL CDR3または1つもしくは2つの変異を有するVL CDR3からなる群から選択されるVL CDR3を含む。
実施形態1から12のいずれか1つの抗FIXa抗体またはその抗原結合部分。
(ii)VH CDR2が、アミノ酸配列X5ISX6X7X8X9X10IYYADSVKG(配列番号2195)を含み、X5が、S、A、YまたはGであり、X6が、SまたはAであり、X7が、S、AまたはGであり、X8が、S、GまたはDであり、X9が、S、TまたはGであり、X10が、YまたはTである、実施形態183の単離された抗FIXa抗体またはその抗原結合部分。
184のいずれか1つの単離された抗FIXa抗体またはその抗原結合部分。
(i)VL CDR1が、アミノ酸配列QASQDIANYLN(配列番号2116)を含み;および/または
(ii)VL CDR2が、アミノ酸配列DASNLET(配列番号2142)を含む、実施形態185の単離された単離された抗FIXa抗体またはその抗原結合部分。
(ii)VH CDR2が、アミノ酸配列SISX1X2X3SYIX4YAX5SVKG(配列番号2197)を含み、X1が、SまたはDであり、X2が、GまたはSであり、X3が、EまたはAであり、X4が、YまたはAであり、X5が、EまたはDである、実施形態188の単離された抗FIXa抗体またはその抗原結合部分。
(i)VL CDR1が、アミノ酸配列X1AX2X3X4IX5X6YLN(配列番号2199)を含み、X1が、Q、GまたはEであり、X2が、SまたはNであり、X3が、QまたはEであり、X4が、DまたはYであり、X5が、AまたはSであり、X6が、NまたはDである;および/または
(ii)VL CDR2が、アミノ酸配列DAX7NLX8X9(配列番号2200)であり、X7が、SまたはAであり、X8が、E、HまたはQであり、X9が、TまたはYである、実施形態190の単離された単離された抗FIXa抗体またはその抗原結合部分。
選択されるVL CDR3を含むVL CDR1、CDR2およびCDR3を含む、実施形態182の抗FIXa抗体またはその抗原結合部分。
(i)VH CDR1が、アミノ酸配列YTFX1X2YX3MH(配列番号2202)を含み、X1が、TまたはHであり、X2が、S、GまたはHであり、X3が、YまたはPである;および/または
(ii)VH CDR2が、アミノ酸配列X4INPSX5GX6TX7YAQKFQG(配列番号2203)を含み、X4が、IまたはSであり、X5が、GまたはRであり、X6が、SまたはRであり、X7が、SまたはEである、実施形態193の単離された抗FIXa抗体またはその抗原結合部分。
(i)VL CDR1が、アミノ酸配列RASQSVSSYLA(配列番号2116)を含み;および/または
(ii)VL CDR2が、アミノ酸配列DASNRAT(配列番号2116)を含む、実施形態195の単離された単離された抗FIXa抗体またはその抗原結合部分。
(i)VH CDR1が、アミノ酸配列GSIX1SX2X3YX4WX5(配列番号2205)を含み、X1が、SまたはAであり、X2が、S、T、GまたはVであり、X3が、SまたはAであり、X4が、YまたはAであり、X5が、G、V、NまたはSである;および/または
(ii)VH CDR2が、アミノ酸配列X6IX7X8X9GX10TX11YNPSLKS(配列番号2206)を含み、X6が、SまたはYであり、X7が、S、Y、R、TまたはQであり、X8が、Y、G、PまたはAであり、X9が、SまたはQであり、X
10が、SまたはKであり、X11が、YまたはQである、実施形態198の単離された単離された抗FIXa抗体またはその抗原結合部分。
(i)VL CDR1が、アミノ酸配列RASQGIDSWLA(配列番号2136)を含み;および/または
(ii)VL CDR2が、アミノ酸配列AASSLQS(配列番号2162)を含む、実施形態200の単離された抗FIXa抗体またはその抗原結合部分。
(i)VHが、配列番号1935、1939、1943、1947、1951、1955、1959、1963、1967、1971、1975、1979、1983、1987、1991、1995、1999、2003、2007、2011、2015、2019、2023、2027、2031および2035からなる群から選択されるアミノ酸配列と少なくとも約80%、少なくとも約85%、少なくとも約90%、少なくとも約95%、少なくとも約96%、少なくとも約97%、少なくとも約98%、少なくとも約99%または約100%同一のアミノ酸配列を含み;および/または
(ii)VLが、配列番号1937、1941、1945、1949、1953、1957、1961、1965、1969、1973、1977、1981、1985、1989、1993、1997、2001、2005、2009、2013、2017、2021、2025、2029、2033および2037からなる群から選択されるアミノ酸配列と少なくとも約80%、少なくとも約85%、少なくとも約90%、少なくとも約95%、少なくとも約96%、少なくとも約97%、少なくとも約98%、少なくとも約99%または約100%同一のアミノ酸配列を含む、実施形態182から202のいずれか1つの抗FIXa抗体またはその抗原結合部分。
(a1)VHおよびVLは、それぞれ、配列番号1935および1937(BIIB-9-3595)を含み;
(a2)VHおよびVLは、それぞれ、配列番号1939および1941(BIIB-9-3601)を含み;
(a3)VHおよびVLは、それぞれ、配列番号1943および1945(BIIB-9-3604)を含み;
(a4)VHおよびVLは、それぞれ、配列番号1947および1949(BIIB-9-3617)を含み;
(a5)VHおよびVLは、それぞれ、配列番号1951および1953(BIIB-9-3618)を含み;
(a6)VHおよびVLは、それぞれ、配列番号1955および1957(BIIB-9
-3621)を含み;
(a7)VHおよびVLは、それぞれ、配列番号1959および1961(BIIB-9-3647)を含み;
(a8)VHおよびVLは、それぞれ、配列番号1963および1965(BIIB-9-3649)を含み;
(a9)VHおよびVLは、それぞれ、配列番号1967および1969(BIIB-9-3650)を含み;
(a10)VHおよびVLは、それぞれ、配列番号1971および1973(BIIB-9-3654)を含み;
(a11)VHおよびVLは、それぞれ、配列番号1975および1977(BIIB-9-3753)を含み;
(a12)VHおよびVLは、それぞれ、配列番号1979および1981(BIIB-9-3754)を含み;
(a13)VHおよびVLは、それぞれ、配列番号1983および1985(BIIB-9-3756)を含み;
(a14)VHおよびVLは、それぞれ、配列番号1987および1989(BIIB-9-3764)を含み;
(a15)VHおよびVLは、それぞれ、配列番号1991および1993(BIIB-9-3766)を含み;
(a16)VHおよびVLは、それぞれ、配列番号1995および1997(BIIB-9-3707)を含み;
(a17)VHおよびVLは、それぞれ、配列番号1999および2001(BIIB-9-3709)を含み;
(a18)VHおよびVLは、それぞれ、配列番号2003および2005(BIIB-9-3720)を含み;
(a19)VHおよびVLは、それぞれ、配列番号2007および2009(BIIB-9-3727)を含み;
(a20)VHおよびVLは、それぞれ、配列番号2011および2013(BIIB-9-3745)を含み;
(a21)VHおよびVLは、それぞれ、配列番号2015および2017(BIIB-9-3780)を含み;
(a22)VHおよびVLは、それぞれ、配列番号2019および2021(BIIB-9-3675)を含み;
(a23)VHおよびVLは、それぞれ、配列番号2023および2025(BIIB-9-3681)を含み;
(a24)VHおよびVLは、それぞれ、配列番号2027および2029(BIIB-9-3684)を含み;
(a25)VHおよびVLは、それぞれ、配列番号2031および2033(BIIB-9-3698)を含み;または
(a26)VHおよびVLは、それぞれ、配列番号2035および2037(BIIB-9-3704)を含む、実施形態182から203のいずれか1つの抗FIXa抗体またはその抗原結合部分。
本開示を一層容易に理解することができるために、ある用語を最初に定義する。本出願において使用される通り、本明細書において特に明示的に提示している場合を除き、以下の用語の各々は、以下に説明されている意味を有するものとする。さらなる定義は、本出願全体にわたり説明されている。
「A」(単独)および「B」(単独)を含むことが意図されている。同様に、「A、Bおよび/またはC」などの言い回しで使用される用語「および/または」は、以下の態様:A、BおよびC;A、BまたはC;AまたはC;AまたはB;BまたはC;AおよびC;AおよびB;BおよびC;A(単独);B(単独);およびC(単独)の各々を包含することが意図されている。
間隔は±10%である。
York、N.Y.(1992年);および本明細書に記載される方法を参照されたい)。
ー、およびスキャッチャード解析が挙げられる。KDが使用される場合、抗体に対する「高い親和性」という用語は、約1×10-7M未満、または約1×10-8M未満、または約1×10-9M未満、または約1×10-10M未満、または約1×10-11M未満、または約1×10-12M未満、または約1×1013M未満、または約1×10-14M未満、またはそれ未満の平衡解離定数(KD)を指す。
cksonら(1995年)J.Immunol.154巻(7号):3310~9頁;およびHawkinsら(1992年)J.Mol.Biol.226巻:889~896頁により記載されている。活性を増強するアミノ酸残基による選択的変異誘発位置、接触または超変異位置における変異は、米国特許第6,914,128号に記載される。
合せを含み、この場合、例えば、scFvは、典型的な抗体の重鎖および/または軽鎖のどちらか一方のN末端に共有結合により連結(例えば、ペプチド結合により、または化学リンカーによる)されているか、または典型的な抗体の重鎖および/または軽鎖にインターカレートされている。
Immunological Interest(第5版、1991年、米国国立衛生研究所、Bethesda Md.)、および(2)抗原-抗体複合体の結晶学的検討に基づく手法(Al-lazikaniら(1997年)J.Molec.Biol.273巻:927~948年))。さらに、これらの2つの手法の組合せが時として、当分野において使用されて、CDRを決定する。Kabatの番号付けシステムは、可変ドメインにおける残基を参照する際に、一般に使用される(およそ、軽鎖の残基1~107、および重鎖の残基1~113)(例えば、Kabatら、Sequences of Immunological Interest.第5版、Public Health Service、米国国立衛生研究所、Bethesda、Md.(1991年))。
Proteins of Immunological Interest、第5版、米国国立衛生研究所(United States Public Health Service, National Institutes of Health)、Bethesdaにも説明されている。したがって、言い回し「Kabatに
説明されているEU指標」または「KabatのEU指標」および「Kabatに説明されているEU指標による位置」およびその文法上の変化形は、Kabat 1991年に説明されているEdelmanらのヒトIgG1 EU抗体に基づく残基の番号付けシステムを指す。
」と互換的に使用することができ、無傷抗体と同じエピトープへの特異的結合が可能な無傷抗体の部分を指す。特に、抗原結合部分は、無傷抗体の1つまたはそれ以上のCDRを含む無傷抗体の一部分または部分を指す。抗体の抗原結合機能は、完全長抗体の断片により行われることは当分野で公知である。抗体断片の例には、以下に限定されないが、Fab、Fab’、F(ab’)2およびFv断片、線状抗体、一本鎖抗体、および抗体断片から形成された多重特異性抗体が含まれる。
体のことである。一部の実施形態では、参照抗体は、同一特異性を有する別の抗体(例えば、本明細書に開示される抗FIXaの場合、参照抗体は、当分野で公知の別の抗FIXまたは抗FIXa抗体とすることができる)である。一部の実施形態では、結合親和性の増大は、同じ凝固因子(例えば、FIXまたはFX)、因子の形態(例えば、FIXaまたはFXz)または抗原結合部位(例えば、エピトープ)に対する参照抗体の結合親和性よりも、例えば、少なくとも約10%、少なくとも約20%、少なくとも約30%、少なくとも約40%、少なくとも約50%、少なくとも約60%、少なくとも約70%、少なくとも約80%、少なくとも約90%または少なくとも約100%高いとすることができる。一部の実施形態では、結合親和性の増大は、同じ凝固因子(例えば、FIXまたはFX)、因子の形態(例えば、FIXaまたはFXz)または抗原結合部位(例えば、エピトープ)に対する参照抗体の結合親和性よりも、例えば、少なくとも約2倍、少なくとも約3倍、少なくとも約4倍、少なくとも約5倍、少なくとも約6倍、少なくとも約7倍、少なくとも約8倍、少なくとも約9倍または少なくとも約10倍高いとすることができる。
(i)結合特異性:用語「特異性」とは、結合性分子、例えば抗体が、様々な抗原性部位に対して、1つの抗原性部位(例えば、エピトープ)に優先的に結合する能力を指し、高い親和性を必ずしも暗示するものではない。用語「結合特異性」および「特異性」は、互換的に使用され、(i)結合性分子の特定の部分、と(ii)特定のエピトープに特異的に結合する(以下の「特異的結合」の定義を参照されたい)結合性分子の能力の両方を指すことができる。例えば、一部の実施形態では、本明細書に開示される二重特異性抗体は、2つの結合特異性、すなわち、例えばFIXaへの第1の結合特異性、および例えばFXzへの第2の結合特異性を含む(この文脈では、特定の抗原決定基への二重特異性抗体の結合の特異的領域などの「結合特異性」は、「結合ドメイン」と等価である)。
(ii)特異的結合:結合性分子、例えば、抗体は、抗原と結合性分子との間の特異的相互作用の免疫学的反応が存在する場合、「特異的に結合する」。用語「特異的に結合する」は、抗体が生成して、その可変領域を介して、抗原に結合することを意味する。用語「非特異的な結合」は、抗体が抗原に特異的に結合するよう生成しないが、非特異的な手段を介して、抗原にいくらか結合することを意味する。一例として、抗体は、抗体分子のFc部分を介して、Fc受容体に非特異的に結合すると予想される。別の例として、ある種の抗体は、それらが生成しない抗原と誤って交差反応することがある。
(iii)優先的な結合:結合性分子、例えば、抗体は、これが他の物質に結合するよりも、より大きな親和性、アビディティーで、一層容易に、および/またはより長い期間で結合する場合、抗原に「優先的に結合する」。例えば、FIXaエピトープに優先的に結合する抗体は、それらが、他のFIXaエピトープまたは非FIXaエピトープに結合するよりも、より大きな親和性、アビディティー、一層容易に、および/またはより長い期間でこのエピトープに結合する抗体である。例えば、抗FIX抗体の50%、60%、70%、80%、90%または95%超が、FIXaとFIXzの両方の存在下で、FIXaに結合する場合、抗FIX抗体は、FIXチモーゲンよりも活性化FIXに優先的に結合する。例えば、第1の標的に優先的に結合する抗体(または部分もしくはエピトープ)は、第2の標的に優先的に結合することがあり、または優先的に結合しないことがあることが、この定義を一読することによりやはり理解される。したがって、「優先的な結合」は、排他的な結合を必ずしも必要としない(排他的な結合を含むことができる)。したがって、一部の態様では、「優先的な結合」は、「排他的な結合」とすることができる。これらの概念を例示するため、抗FIXの50%が、FIXチモーゲンに特異的に結合し、FIXaに50%特異的に結合する場合、このような結合は、「非選択的」または「非優先的」となる。抗FIXの50%未満しか、FIXチモーゲンに結合せず、50%を超えてFXaに結合する場合、抗FIXは、FIXaに「優先的に結合する」。抗FIXが、
FIXチモーゲンに結合せず、FIXaにしか結合しない場合、抗FIXは、FIXaに「排他的に結合する」。
法は、例えば、EP1870459A1、Xie,Z.ら、J Immunol Methods 286巻(2005年)95~101頁に記載されており、FC部分に関してノブイントゥーホール技術と組み合わせてscFvを使用する二重特異性抗体のフォーマットを指す。
(i)鎖Aは、T336W変異を含み、鎖Bは、T366W、L368AおよびY407V変異を含む(ノブインホールフォーマット);
(ii)鎖Aは、F405L変異を含み、鎖Bは、K409R変異を含む(デュオボディフォーマット);
(iii)鎖Aは、T350V、L351Y、F405AおよびY407V変異を含み、鎖Bは、T350V、T366L、K392LおよびT394W変異を含む(azymetricフォーマット);
(iv)鎖Aは、K409DおよびK392D変異を含み、鎖Bは、D399KおよびE356K変異を含む(電荷対フォーマット);
(v)鎖Aは、D221E、P228EおよびL368E変異を含み、鎖Bは、D221R、P228RおよびK409R変異を含む(電荷対フォーマット);
(vi)鎖Aは、S364HおよびF405A変異を含み、鎖Bは、Y349TおよびT394F変異を含む(HA-TFフォーマット);または
(vii)鎖Aは、IgG/Aキメラを含み、鎖Bもまた、IgG/Aキメラ(SEEDボディフォーマット)を含む。
またはscFv)または操作されたタンパク質足場を含む。一部の態様では、本発明の二重特異性分子は、二重特異性抗体断片を含む。二重特異性抗体定常ドメインのいくつかまたはすべてを欠く、多数の二重特異性断片形態が、当分野において公知である。一部の態様では、本発明の二重特異性分子は、二重特異性融合タンパク質、例えば、ImmTAC(親和性の成熟した受容体に連結したscFv)である。他の態様では、二重特異性分子は、二重特異性抗体コンジュゲートである。
たはD-オルニチンのいずれか1つとすることができる。一般に、単離されたポリペプチドの特性の変化を誘発することが予想される機能的に重要な領域における置換は、(i)極性残基、例えば、セリンまたはトレオニンは、疎水性残基、例えば、ロイシン、イソロイシン、フェニルアラニンまたはアラニンに(またはこれにより)置き換えられている;(ii)システイン残基は、他の任意の残基に(またはこれにより)置き換えられている;(iii)電気陽性側鎖を有する残基、例えば、リシン、アルギニンまたはヒスチジンは、電気陰性側鎖を有する残基、例えば、グルタミン酸またはアスパラギン酸に(またはこれにより)置き換えられている;または(iv)かさ高い側鎖を有する残基、例えば、フェニルアラニンは、このような側鎖を有さないもの、例えばグリシンに(またはこれにより)置き換えられている。上述の非保存的置換の1つが、タンパク質の機能的な特性を改変することができる可能性は、タンパク質の機能的に重要な領域に関して、置換位置にもやはり関連する:したがって、一部の非保存的置換は、生物学的特性にほとんどまたは全く影響を及ぼし得ない。
知の技法(例えば、培養細胞での組換え発現、またはトランスジェニック動物での発現)のいずれかを使用して作製された、ヒトにより産生される抗体に相当するアミノ酸配列を有する抗体を意味する。したがって、用語ヒト抗体はまた、ヒトによって元々産生されたが、非ヒト系(例えば、化学合成により生成した;細菌、哺乳動物または昆虫細胞で組換え発現した;または動物対象において発現した)で発現される、抗体に対応するアミノ酸配列を有する抗体(または操作されたバリアントまたはその誘導体)を包含する。したがって、ヒト対象から、またはヒト細胞(例えば、ハイブリドーマ、または組換え抗体もしくはその断片を発現する細胞株)から得られ、続いて動物、例えばマウスにおいて発現した抗体は、ヒト抗体と見なされる。ヒト抗体のこの定義には、無傷または完全長抗体、その断片、ならびに/または例えばマウス軽鎖およびヒト重鎖ペプチドを含む抗体などの、少なくとも1つのヒトの重鎖および/または軽鎖ポリペプチドを含む抗体が含まれる。
と同じヌクレオチドによって占有されている場合、この分子は、その位置で同一である。2つの配列の間の同一性のパーセントは、配列が共有する同一の位置の数と相関し、2つの配列の最適アライメントに対して導入する必要があるギャップの数および各ギャップの長さが考慮される。配列の比較、および2つの配列の間の同一性率の決定は、算術アルゴリズムを使用して行うことができる。DNAおよびRNAを比較する場合、チミン(T)およびウラシル(U)は、等価と見なすことができる。
結合性分子(例えば、抗FIXa、抗FXzまたは生体特異的抗FIXa/抗FXz)、および1つまたはそれ以上の部分、例えば、結合性分子に化学的にコンジュゲートされている治療部分または診断部分を含む化合物を指す。一般に、イムノコンジュゲートは、一般式:A-(L-M)nによって定義され、式中、Aは、結合性分子(例えば、抗体)であり、Lは、任意選択のリンカーであり、Mは、例えば、治療剤、検出可能な標識などとすることができる非相同性部分であり、nは整数である。イムノコンジュゲートはまた、反対の順序で一般式によって定義することもできる。一部の態様では、イムノコンジュゲートは、「抗体-薬物コンジュゲート」(「ADC」)である。本開示の文脈では、用語「イムノコンジュゲート」は、化学的にまたは酵素によるコンジュゲート分子に限定されない。本開示に使用される用語「イムノコンジュゲート」はまた、遺伝的融合を含む。
明細書の実施例の項目に記載される発色アッセイである。一態様では、本明細書に開示される結合性分子(例えば、二重特異性抗体)は、観察されるFXa基質切断の速度が、加える結合性分子(例えば、二重特異性抗体)の非存在下で、平均基本速度より少なくとも3標準偏差高いと、「FVIIIa活性を擬似する」と言われる。別の例示的な方法は、活性化部分トロンボプラスチン時間(aPTT)アッセイである。用語「活性化部分トロンボプラスチン時間(APTT)」は、試験のリン脂質濃度のみが制御(リン脂質および表面アクチベータ濃度とは反対に)され、名称「部分トロンボプラスチン」が、凝固を加速するが、血友病性血漿の凝固時間の延長を補正しないリン脂質調製までの時間に適用される試験(1953年に考案された)の元々の形態から導かれる。実質的に、この用語「部分的な」は、リン脂質が存在するが組織因子は存在しないことを意味する。aPTTはまた、カオリンセファリン凝固時間(KCCT)またはカオリン加部分トロンボプラスチン時間(PTTK)としても知られている。他の有用な方法は、上記の従来的なaPTTアッセイから修正された一段階(OS)凝固アッセイを含む。一段階凝固アッセイは、FVIII欠乏血漿および希釈試験サンプルを使用し、FVIII活性に対して定量的とすることができる。実施例4を参照されたい。対照的に、aPTTアッセイは、aPTT試薬およびカルシウムを含むサンプル血漿を使用し、凝固時間を報告するものである。
を指す。このような組成物は滅菌されている。
酸塩、マレイン酸塩、マロン酸塩、メタンスルホン酸塩、2-ナフタレンスルホン酸塩、ニコチン酸塩、硝酸塩、オレイン酸塩、シュウ酸塩、パルミチン酸塩、パモ酸塩、ペクチン酸塩、過硫酸塩、3-フェニルプロピオン酸塩、リン酸塩、ピクリン酸塩、ピバル酸塩、プロピオン酸塩、ステアリン酸塩、コハク酸塩、硫酸塩、酒石酸塩、チオシアン酸塩、トルエンスルホン酸塩、ウンデカン酸塩、吉草酸塩などが含まれる。代表的なアルカリまたはアルカリ土類金属塩には、ナトリウム、リチウム、カリウム、カルシウム、マグネシウムなど、および以下に限定されないが、アンモニウム、テトラメチルアンモニウム、テトラエチルアンモニウム、メチルアミン、ジメチルアミン、トリメチルアミン、トリエチルアミン、エチルアミンを含めた非毒性アンモニウム、第四級アンモニウムおよびアミン陽イオンなどが含まれる。本開示の薬学的に許容される塩は、例えば、非毒性の無機酸または有機酸から形成される、親化合物の慣用的な非毒性塩を含む。本開示の薬学的に許容される塩は、従来の化学的方法によって、塩基性または酸性の部分を含んでいる親化合物から合成することができる。一般に、このような塩は、水中、もしくは有機溶媒中、または上記2つの混合物中、遊離酸または遊離塩基の形態のこれらの化合物を、化学量論量の適切な塩基または酸と反応させることにより製造することができる;一般に、エーテル、酢酸エチル、エタノール、イソプロパノールまたはアセトニトリルのような非水性媒体が使用される。好適な塩の一覧は、Remington’s Pharmaceutical Sciences、第17版、Mack Publishing Company、Easton、Pa.、1985年、1418頁、Pharmaceutical Salts:Properties,Selection,and Use、P.H.StahlおよびC.G.Wermuth(編)、Wiley-VCH、2008年およびBergeら、Journal of Pharmaceutical Science、66巻、1~19頁(1977年)に見出され、それらのそれぞれの全体が参照により本明細書に組み入れられる。
がって、この用語は、三本鎖、二本鎖および一本鎖のデオキシリボ核酸(「DNA」)、ならびに三本鎖、二本鎖および一本鎖のリボ核酸(「RNA」)を含む。それはまた、例えば、アルキル化によりおよび/またはキャッピングによる、ポリヌクレオチドの修飾形態、ならびにその非修飾形態を含む。より詳細には、用語「ポリヌクレオチド」には、ポリデオキシリボヌクレオチド(2-デオキシ-D-リボースを含む)、スプライシングされているかスプライシングされていないに関わらず、tRNA、rRNA、hRNA、siRNAおよびmRNAを含めたポリリボヌクレオチド(D-リボースを含む)、プリン塩基もしくはピリミジン塩基のNグリコシドまたはCグリコシドであるポリヌクレオチドの任意の他のタイプ、および非ヌクレオチド主鎖を含有する他のポリマー、例えばポリアミド(例えば、ペプチド核酸「PNA」)、およびポリモルホリノポリマー、および他の合成による配列特異的核酸ポリマーが含まれるが、但し、これらのポリマーは、DNAおよびRNAに見出されるような塩基対および塩基スタッキングを可能にする立体配置の核酸塩基を含有することを条件とする。特定の態様では、ポリヌクレオチドは、mRNAを含む。他の態様では、mRNAは、合成mRNAである。一部の態様では、合成mRNAは、少なくとも1つの非天然核酸塩基を含む。一部の態様では、ある種のクラスの核酸塩基はすべて、非天然の核酸塩基(例えば、本明細書に開示されるポリヌクレオチド中のウリジンがすべて、非天然核酸塩基、例えば5-メトキシウリジンにより置き換えられている)で置き換えられている。一部の態様では、ポリヌクレオチド(例えば、合成RNAまたは合成DNA)は、天然核酸塩基しか、すなわち合成DNAの場合、A,C、TおよびUしか、または合成RNAの場合、A、C、TおよびUしか含まない。
467頁およびそこに引用されている参照文献の方法により製造される;およびイソグアニンヌクレオチドは、上記のSwitzerら、1993年、およびMantschら(1993年)Biochem.14巻:5593~5601頁によって記載されている方法を使用して、またはCollinsらへの米国特許第5,780,610号に記載される方法によって製造することができる。他の非天然塩基対は、2,6-ジアミノピリミジンおよびその補体(1-メチルピラゾロ-[4,3]ピリミジン-5,7-(4H,6H)-ジオンの合成に関する、Piccirilliら(1990年)Nature 343巻:33~37頁に記載される方法により合成することができる。上記のLeachら(1992年)J.Am.Chem.Soc.114巻:3675~3683頁およびSwitzerらに記載されるものなどの固有の塩基対を形成する他のこのような修飾ヌクレオチド単位が公知である。
障害および/または状態(例えば、がん)に罹患し易い個体は、以下:(1)疾患、障害および/または状態の発症に関連する遺伝子変異;(2)疾患、障害および/または状態の発症に関連する遺伝的多形;(3)疾患、障害および/もしくは状態に関連するタンパク質ならびに/もしくは核酸の発現量ならびに/もしくは活性の向上および/または低下;(4)疾患、障害および/または状態の発症に関連する習慣および/または生活スタイル;(5)疾患、障害および/または状態の家族歴;(6)疾患、障害および/または状態の発症に関連する微生物への曝露および/またはこの微生物による感染症のうちの1つまたはそれ以上を特徴とすることができる。一部の実施形態では、疾患、障害および/または状態に罹患し易い個体は、疾患、障害および/または状態を発症すると予想される。一部の実施形態では、疾患、障害および/または状態に罹患し易い個体は、疾患、障害および/または状態を発症しないであろう。
、他の場合では、インビボ(例えば、対象へのmRNAの投与)、またはエクスビボ(例えば、それを必要とする対象への投与のための自家移植または非相同性細胞に導入されるDNAまたはRNA)で行うことができる。同様に、記載している通りの機能の1つ超をもたらすベクターが含まれる。
本開示は、第IX因子および第X因子、ならびにそれらの抗原結合部分に結合する抗体を提供する。これらの抗体は、これらの凝固因子の特定の機能的形態への優先的な結合が可能である。例えば、一部の実施形態では、FIXに対する開示されている抗体は、活性部位において、擬似基質に共有結合により連結されている、活性化FIX(FIXa)、例えば遊離FIXaまたはFIXaに優先的に結合する(FXa+EGR-CMK)。他の実施形態では、開示される抗体は、遊離FIXaまたはFIXチモーゲンよりも、FIXa-SMに優先的に結合する。さらに他の実施形態では、開示される抗体は、FIXa-SMまたはFIXチモーゲンよりも、遊離FIXaに優先的に結合する。対照的に、一部の実施形態では、FXに対する開示される抗体は、活性化FX(FXa)よりもFXチモーゲン(FXz)に優先的に結合する。この優先的な結合は、FIXaおよびFXzに特異的かつ同時に結合することができる、抗FIXa部分および抗FXz部分を含む二重特異性分子を生成するのに重要である。第VIII因子は、Ca2+およびリン脂質の存在下で、FXを活性化FXaに変換するFXとの複合体を形成するFIXaに対する補因子である。したがって、FIXaとFXzとの間の抗体を媒介とする複合体の形成は、FVIIIaの作用を擬似する。
本開示は、抗FIX結合性分子、例えば、FIXチモーゲンよりも活性化FIX(FIXa)に優先的に結合する抗FIX抗体、またはその抗原結合部分を含む分子を提供する
。
nら、J Biol Chem.1981年4月10日;256巻(7号):3433~42頁)。この巨大分子の活性化は、Ca2+を含めた、低分子量アゴニストによって支援される(Mathurら、Biol.Chem.、272巻(1997年)、23418~23426頁)。いくつかの一連の証拠により、Ca2+結合は、立体構造の再配列を伴うことが示されている(Bajajら、Proc.Natl.Acad.Sci.USA、89巻(1992年)、152~156頁、EnfieldおよびThompson、Blood、64巻(1984年)、821~831頁)。テナーゼ複合体におけるこの非常に活性なFIXaは、擬似基質(例えば、Glu-Gly-Arg-クロロメチルケトン(EGR-CMK))をFIXaの活性部位への共有結合によって擬似される(FXa+EGR-CMK、FIXa-SMとも呼ばれる)。したがって、FIXa-SMは、遊離FIXaと比べて、非常に活性なFIXa(テナーゼ複合体中)に優先的に結合する、抗体またはその抗体結合部分を区別するための重要な手段として使用することができる。
、Nature 299巻:178~180頁(1982年);Fairら、Blood64巻:194~204頁(1984年);およびKurachiら.、Proc.Natl.Acad.Sci.、U.S.A.79巻:6461~6464頁(1982年)を参照されたい)。Simioniらによって2009年に特徴付けられたR338L FIX(Padua)バリアントである、FIXの1つの具体的なバリアントは、機能獲得型変異を含んでおり、これは、天然FIXと比べて、Paduaバリアントの活性がほぼ8倍、向上していることに相関している。FIXバリアントはまた、FIXポリペプチドのFIX活性に影響を及ぼさない、1つまたはそれ以上の保存的アミノ酸置換を有する、いかなるFIXポリペプチドを含むことができる。
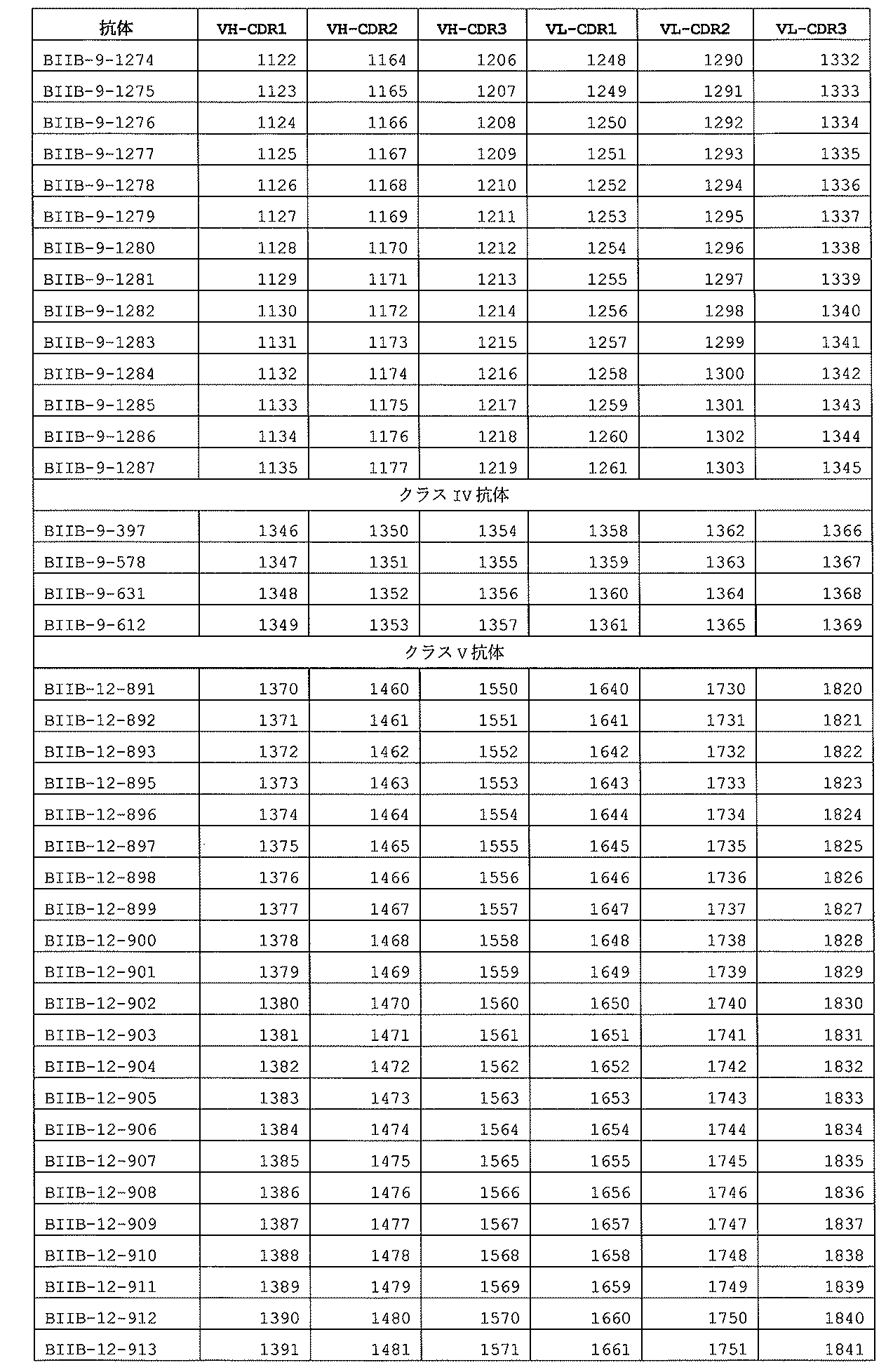
クラスI:遊離FIXaまたはFIXzよりもFIXa-SMに優先的に結合する、抗FIXa抗体またはその抗原結合部分(図3Aの抗体);
クラスII:FIXa-SMまたはFIXzよりも遊離FIXaに優先的に結合する、抗FIXa抗体またはその抗原結合部分(図3Bの抗体);および
クラスIII:ほぼ等価に遊離FIXaおよびFIXa-SMに結合するが、FIXzに顕著なほどに結合しない、抗FIXa抗体またはその抗原結合部分(図3Cの抗体)。
(i)図3A中のVH CDR3配列からなる群から選択されるVH CDR3配列と同一のVH CDR3配列、または
(ii)1つ、2つまたは3つのアミノ酸置換を除く、図3A中のVH CDR3配列からなる群から選択されるVH CDR3配列と同一のVH CDR3配列
を含む。
(i)図3B中のVH CDR3配列からなる群から選択されるVH CDR3配列と同一のVH CDR3配列、または
(ii)1つ、2つまたは3つのアミノ酸置換を除く、図3B中のVH CDR3配列からなる群から選択されるVH CDR3配列と同一のVH CDR3配列
を含む。
(i)図3C中のVH CDR3配列からなる群から選択されるVH CDR3配列と同一のVH CDR3配列、または
(ii)1つ、2つまたは3つのアミノ酸置換を除く、図3C中のVH CDR3配列からなる群から選択されるVH CDR3配列と同一のVH CDR3配列
を含む。
(i)図3A中で開示されているVH CDR1配列からなる群から選択される配列と同一のVH CDR1配列、または
(ii)1つ、2つまたは3つのアミノ酸置換を除く、図3A中で開示されているVH
CDR1配列からなる群から選択される配列と同一のVH CDR1配列
を含む。
(i)図3B中で開示されているVH CDR1配列からなる群から選択される配列と同一のVH CDR1配列、または
(ii)1つ、2つまたは3つのアミノ酸置換を除く、図3B中で開示されているVH
CDR1配列からなる群から選択される配列と同一のVH CDR1配列
を含む。
(i)図3C中で開示されているVH CDR1配列からなる群から選択される配列と同一のVH CDR1配列、または
(ii)1つ、2つまたは3つのアミノ酸置換を除く、図3C中で開示されているVH
CDR1配列からなる群から選択される配列と同一のVH CDR1配列
を含む。
(i)図3A中で開示されているVH CDR2配列からなる群から選択される配列と同一のVH CDR2配列、または
(ii)1つ、2つまたは3つのアミノ酸置換を除く、図3A中で開示されているVH
CDR2配列からなる群から選択される配列と同一のVH CDR2配列
を含む。
(i)図3B中で開示されているVH CDR2配列からなる群から選択される配列と同一のVH CDR2配列、または
(ii)1つ、2つまたは3つのアミノ酸置換を除く、図3B中で開示されているVH
CDR2配列からなる群から選択される配列と同一のVH CDR2配列
を含む。
(i)図3C中で開示されているVH CDR2配列からなる群から選択される配列と同一のVH CDR2配列、または
(ii)1つ、2つまたは3つのアミノ酸置換を除く、図3C中で開示されているVH
CDR2配列からなる群から選択される配列と同一のVH CDR2配列
を含む。
(i)図3A中で開示されているVL CDR1配列からなる群から選択される配列と同一のVL CDR1配列、または
(ii)1つ、2つまたは3つのアミノ酸置換を除く、図3A中で開示されているVL
CDR1配列からなる群から選択される配列と同一のVL CDR1配列
を含む。
(i)図3B中で開示されているVL CDR1配列からなる群から選択される配列と同一のVL CDR1配列、または
(ii)1つ、2つまたは3つのアミノ酸置換を除く、図3B中で開示されているVL
CDR1配列からなる群から選択される配列と同一のVL CDR1配列
を含む。
(i)図3C中で開示されているVL CDR1配列からなる群から選択される配列と同一のVL CDR1配列、または
(ii)1つ、2つまたは3つのアミノ酸置換を除く、図3C中で開示されているVL
CDR1配列からなる群から選択される配列と同一のVL CDR1配列
を含む。
(i)図3A中のVL CDR2配列からなる群から選択される配列と同一のVL CDR2配列、または
(ii)1つ、2つまたは3つのアミノ酸置換を除く、図3A中のVL CDR2配列からなる群から選択される配列と同一のVL CDR2配列
を含む。
(i)図3B中のVL CDR2配列からなる群から選択される配列と同一のVL CDR2配列、または
(ii)1つ、2つまたは3つのアミノ酸置換を除く、図3B中のVL CDR2配列からなる群から選択される配列と同一のVL CDR2配列
を含む。
(i)図3C中のVL CDR2配列からなる群から選択される配列と同一のVL CDR2配列、または
(ii)1つ、2つまたは3つのアミノ酸置換を除く、図3C中のVL CDR2配列からなる群から選択される配列と同一のVL CDR2配列
を含む。
(i)図3A中で開示されているVL CDR3配列からなる群から選択される配列と同一のVL CDR3配列、または
(ii)1つ、2つまたは3つのアミノ酸置換を除く、図3A中で開示されているVL
CDR3配列からなる群から選択される配列と同一のVL CDR3配列
を含む。
(i)図3B中で開示されているVL CDR3配列からなる群から選択される配列と同一のVL CDR3配列、または
(ii)1つ、2つまたは3つのアミノ酸置換を除く、図3B中で開示されているVL
CDR3配列からなる群から選択される配列と同一のVL CDR3配列
を含む。
(i)図3C中で開示されているVL CDR3配列からなる群から選択される配列と同一のVL CDR3配列、または
(ii)1つ、2つまたは3つのアミノ酸置換を除く、図3C中で開示されているVL
CDR3配列からなる群から選択される配列と同一のVL CDR3配列
を含む。
B-9-611、BIIB-9-619、BIIB-9-626、BIIB-9-883、BIIB-9-419、BIIB-9-451、BIIB-9-473、BIIB-9-565、BIIB-9-573、BIIB-9-579、BIIB-9-581、BIIB-9-582、BIIB-9-585、BIIB-9-587、BIIB-9-590、BIIB-9-592、BIIB-9-606、BIIB-9-608 BIIB-9-616、BIIB-9-621、BIIB-9-622、BIIB-9-627、BIIB-9-1335、およびBIIB-9-1336からなる群から選択される抗FIXa抗体のVH CDR1、VH CDR2およびVH CDR3ならびにVL CDR1、VL CDR2およびVL CDR3を含む。
CDR1、VH CDR2およびVH CDR3ならびにVL CDR1、VL CDR2およびVL CDR3を含む。
CDR2およびVL CDR3を含む。
~1089および配列番号1090~1093を含むVL CDR1、VL CDR2およびVL CDR3配列を含む(クラスII抗体のVL CDR)。
CDR)、ならびに/またはそれぞれ、配列番号1220~1261、配列番号1262~1303および配列番号1304~1345を含むVL CDR1、VL CDR2およびVL CDR3配列を含む(クラスIII抗体のVL CDR)。
(a1)それぞれ、配列番号809、配列番号854および配列番号899を含む、VH CDR1、VH CDR2およびVH CDR3配列(BIIB-9-440抗体の
VH CDR)、ならびに/またはそれぞれ、配列番号944、配列番号989および配列番号1034を含むVL CDR1、VL CDR2およびVL CDR3配列(BIIB-9-440抗体のVL CDR);
(a2)それぞれ、配列番号1102、配列番号1144および配列番号1186を含む、VH CDR1、VH CDR2およびVH CDR3配列(BIIB-9-882抗体のVH CDR)、ならびに/またはそれぞれ、配列番号1228、配列番号1270および配列番号1312を含むVL CDR1、VL CDR2およびVL CDR3配列(BIIB-9-882抗体のVL CDR);
(a3)それぞれ、配列番号811、配列番号856および配列番号901を含む、VH CDR1、VH CDR2およびVH CDR3配列(BIIB-9-460抗体のVH CDR)、ならびに/またはそれぞれ、配列番号946、配列番号991および配列番号1036を含むVL CDR1、VL CDR2およびVL CDR3配列(BIIB-9-460抗体のVL CDR);または
(a4)それぞれ、配列番号1108、配列番号1150および配列番号1192を含む、VH CDR1、VH CDR2およびVH CDR3配列(BIIB-9-433抗体のVH CDR)、ならびに/またはそれぞれ、配列番号1234、配列番号1276および配列番号1318を含むVL CDR1、VL CDR2およびVL CDR3配列(BIIB-9-433抗体のVL CDR);
を含む。
(i)それぞれ、配列番号843、配列番号888および配列番号933を含む、VH CDR1、VH CDR2およびVH CDR3配列(BIIB-9-1335抗体のVH CDR)、ならびに/またはそれぞれ、配列番号950、配列番号995および配列番号1040を含むVL CDR1、VL CDR2およびVL CDR3配列(BIIB-9-1335抗体のVL CDR);または
(ii)それぞれ、配列番号844、配列番号889および配列番号934を含む、VH
CDR1、VH CDR2およびVH CDR3配列(BIIB-9-1336抗体のVH CDR)、ならびに/またはそれぞれ、配列番号950、配列番号995および配列番号1040を含むVL CDR1、VL CDR2およびVL CDR3配列(BIIB-9-1336抗体のVL CDR)
を含む。
5、27、29、31、33、35、37、39、41、43、45、47、49、51、53、55、57、59、61、63、65、67、69、71、73、75、77、79、81、83、85、87、および89;クラスII抗体の場合、配列番号91、93、95および97;ならびにクラスIII抗体の場合、配列番号99、101、103、105、107、109、111、113、115、117、119、121、123、125、127、129、131、133、135、137、139、141、143、145、147、149、151、153、155、157、159、161、163、165、167、169、171、173、175、177、179、および181)からなる群から選択されるアミノ酸配列と、少なくとも約70%、少なくとも約75%、少なくとも約80%、少なくとも約85%、少なくとも約90%、少なくとも約95%、少なくとも約96%、少なくとも約97%、少なくとも約98%、少なくとも約99%または約100%同一のアミノ酸配列を含む。
73、75、77、79、81、83、85、87、および89;クラスII抗体の場合、配列番号91、93、95および97;ならびにクラスIII抗体の場合、配列番号99、101、103、105、107、109、111、113、115、117、119、121、123、125、127、129、131、133、135、137、139、141、143、145、147、149、151、153、155、157、159、161、163、165、167、169、171、173、175、177、179、および181)からなる群から選択されるアミノ酸配列と、少なくとも約70%、少なくとも約75%、少なくとも約80%、少なくとも約85%、少なくとも約90%、少なくとも約95%、少なくとも約96%、少なくとも約97%、少なくとも約98%、少なくとも約99%または約100%同一のアミノ酸配列を含み;
(ii)VLは、配列番号191、193、195、197、199、201、203、205、207、209、211、213、215、217、219、221、223、225、227、229、231、233、235、237、239、241、243、245、247、249、251、253、255、257、259、261、263、265、267、269、271、273、275、277、279、281、283、285、287、289、291、293、295、297、299、301、303、305、307、309、311、313、315、317、319、321、323、325、327、329、331、333、335、337、339、341、343、345、347、349、351、353、355、357、359、361、363、365、および367(クラスI抗体の場合、配列番号191、193、195、197、199、201、203、205、207、209、211、213、215、217、219、221、223、225、227、229、231、233、235、237、239、241、243、245、247、249、251、253、255、257、259、261、263、265、267、269、271、273、および275;クラスII抗体の場合、配列番号277、279、281および283;クラスIII抗体の場合、配列番号285、287、289、291、293、295、297、299、301、303、305、307、309、311、313、315、317、319、321、323、325、327、329、331、333、335、337、339、341、343、345、347、349、351、353、355、357、359、361、363、365、および367)からなる群から選択されるアミノ酸配列と、少なくとも約70%、少なくとも約75%、少なくとも約80%、少なくとも約85%、少なくとも約90%、少なくとも約95%、少なくとも約96%、少なくとも約97%、少なくとも約98%、少なくとも約99%または約100%同一のアミノ酸配列を含む。
5、VH4-39.0、VH4-39.5、VH4-0B.4、VH5-51.1、およびそれらの任意の組合せからなる群から選択される。
96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含む(それぞれ、BIIB-9-484のVHおよびVL);
(a2)VHは、配列番号19と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み、VLは、配列番号209と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含む(それぞれ、BIIB-9-440のVHおよびVL);
(a3)VHは、配列番号115と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み、VLは、配列番号301と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含む(それぞれ、BIIB-9-882のVHおよびVL);
(a4)VHは、配列番号23と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み、VLは、配列番号213と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含む(それぞれ、BIIB-9-460のVHおよびVL);
(a5)VHは、配列番号127と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み、VLは、配列番号313と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含む(それぞれ、BIIB-9-433のVHおよびVL);
(a6)VHは、配列番号45と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み、VLは、配列番号235と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含む(それぞれ、BIIB-9-619のVHおよびVL);
(a7)VHは、配列番号87と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み、VLは、配列番号221と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含む(それぞれ、BIIB-9-1335のVHおよびVL);または(a8)VHは、配列番号89と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み、VLは、配列番号221と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含む(それぞれ、BIIB-9-1336のVHおよびVL)。
よび179、または232および241(配列番号758では、それぞれ、位置76~88、112~115、153~167および222~231に対応する)の間に位置する、少なくとも1つのアミノ酸を含む、エピトープ領域に結合する。
179、S232、R233、Y234、V235、N236、W237、E240およびK241(配列番号758において、それぞれ、位置H76、H77、N78、H88、D112、K113、E114、Y115、R153、Y165、N166、N167、S222、R223、Y224、V225、N226、W227、E230およびK231に対応する)のうちの少なくとも1つを含むエピトープに結合する。一部の態様では、抗FIXa抗体またはその抗原結合部分は、FIXaの重鎖の配列における、キモトリプシノーゲン番号付けによるアミノ酸残基H91、H92、N93、H101、D125、K126、E127、Y128、R165、Y177、N178、N179、S232、R233、Y234、V235、N236、W237、E240およびK241(配列番号758において、それぞれ、位置H76、H77、N78、H88、D112、K113、E114、Y115、R153、Y165、N166、N167、S222、R223、Y224、V225、N226、W227、E230およびK231に対応する)からなる群から選択される、少なくとも2、3、4、5、6、7、8、9、10、11,12、13、14、15、16、17、18または19のアミノ酸残基を含むエピトープに結合する。
開示されているVL CDR1配列からなる群から選択されるVL CDR1配列を含む。
(i)VH CDR1は、アミノ酸配列FTFX1SX2X3MX4(配列番号2194)を含み、X1は、S、GまたはEであり、X2は、YまたはFであり、X3は、S、E、GまたはDであり、X4は、N、V、AまたはTである;および/または
(ii)VH CDR2は、アミノ酸配列X5ISX6X7X8X9X10IYYADSVKG(配列番号2195)を含み、X5は、S、A、YまたはGであり、X6は、SまたはAであり、X7は、S、AまたはGであり、X8は、S、GまたはDであり、X9は、S、TまたはGであり、X10は、YまたはTである;および/または
(iii)VH CDR3は、アミノ酸配列ARDX11GGYAGYYGMDV(配列番号2196)を含み、X11は、LまたはVである。
(i)VL CDR1は、アミノ酸配列QASQDIANYLN(配列番号2116)を含み;および/または
(ii)VL CDR2は、アミノ酸配列DASNLET(配列番号2142)を含み;および/または
(iii)VL CDR3は、アミノ酸配列QQYANFPYT(配列番号2168)を含む。
(i)VH CDR1は、アミノ酸配列FTFX1SX2X3MX4(配列番号2194)を含み、X1は、S、GまたはEであり、X2は、YまたはFであり、X3は、S、E、GまたはDであり、X4は、N、V、AまたはTである;および/または
(ii)VH CDR2は、アミノ酸配列X5ISX6X7X8X9X10IYYADSVKG(配列番号2195)を含み、X5は、S、A、YまたはGであり、X6は、SまたはAであり、X7は、S、AまたはGであり、X8は、S、GまたはDであり、X9
は、S、TまたはGであり、X10は、YまたはTである;および/または
(iii)VH CDR3は、アミノ酸配列ARDX11GGYAGYYGMDV(配列番号2196)を含み、X11は、LまたはVである;および
単離された抗FIXa抗体またはその抗原結合部分は、VL CDR1、CDR2およびCDR3をさらに含み、VL CDR1は、アミノ酸配列QASQDIANYLN(配列番号2116)を含み;および/またはVL CDR2は、アミノ酸配列DASNLET(配列番号2142)を含み;および/またはVL CDR3は、アミノ酸配列QQYANFPYT(配列番号2168)を含む。
(i)VH CDR1は、アミノ酸配列FTFGSYDMN(配列番号2048)を含み;および/または
(ii)VH CDR2は、アミノ酸配列SISX1X2X3SYIX4YAX5SVKG(配列番号2197)を含み、X1は、SまたはDであり、X2は、GまたはSであり、X3は、EまたはAであり、X4は、YまたはAであり、X5は、EまたはDである;および/または
(iii)VH CDR3は、アミノ酸配列X6RDVX7GYAGX8YGMDV(配列番号2198)を含み、X6は、AまたはVであり、X7は、GまたはSであり、X8は、YまたはFである。
(i)VL CDR1は、アミノ酸配列X1AX2X3X4IX5X6YLN(配列番号2199)を含み、X1は、Q、GまたはEであり、X2は、SまたはNであり、X3は、QまたはEであり、X4は、DまたはYであり、X5は、AまたはSであり、X6は、NまたはDである;および/または
(ii)VL CDR2は、アミノ酸配列DAX7NLX8X9(配列番号2200)であり、X7は、SまたはAであり、X8は、E、HまたはQであり、X9は、TまたはYである;および/または
(iii)VL CDR3は、アミノ酸配列X10QYAX11FPYT(配列番号2201)を含み、X10は、QまたはSであり、X11は、NまたはRである。
(i)VH CDR1は、アミノ酸配列FTFGSYDMN(配列番号2048)を含み;および/または
(ii)VH CDR2は、アミノ酸配列SISX1X2X3SYIX4YAX5SVKG(配列番号2197)を含み、X1は、SまたはDであり、X2は、GまたはSであり、X3は、EまたはAであり、X4は、YまたはAであり、X5は、EまたはDである;および/または
(iii)VH CDR3は、アミノ酸配列X6RDVX7GYAGX8YGMDV(
配列番号2198)を含み、X6は、AまたはVであり、X7は、GまたはSであり、X8は、YまたはFである;および、
単離された抗FIXa抗体またはその抗原結合部分は、VL CDR1、CDR2およびCDR3をさらに含み、
(iv)VL CDR1は、アミノ酸配列X1AX2X3X4IX5X6YLN(配列番号2199)を含み、X1は、Q、GまたはEであり、X2は、SまたはNであり、X3は、QまたはEであり、X4は、DまたはYであり、X5は、AまたはSであり、X6は、NまたはDである;および/または
(v)VL CDR2が、アミノ酸配列DAX7NLX8X9(配列番号2200)であり、X7は、SまたはAであり、X8は、E、HまたはQであり、X9は、TまたはYである;および/または
(vi)VL CDR3は、アミノ酸配列X10QYAX11FPYT(配列番号2201)を含み、X10は、QまたはSであり、X11は、NまたはRである。
(i)VH CDR1は、アミノ酸配列YTFX1X2YX3MH(配列番号2202)を含み、X1は、TまたはHであり、X2は、S、GまたはHであり、X3は、YまたはPである;および/または
(ii)VH CDR2は、アミノ酸配列X4INPSX5GX6TX7YAQKFQG(配列番号2203)を含み、X4は、IまたはSであり、X5は、GまたはRであり、X6は、SまたはRであり、X7は、SまたはEである;および/または
(iii)VH CDR3は、アミノ酸配列ARDGPX8X9X10DYYMDV(配列番号2204)を含み、X8は、RまたはQであり、X9は、V、D、LまたはEであり、X10は、SまたはVである。
(i)VH CDR1は、アミノ酸配列YTFX1X2YX3MH(配列番号2202)を含み、X1は、TまたはHであり、X2は、S、GまたはHであり、X3は、YまたはPである;および/または
(ii)VH CDR2は、アミノ酸配列X4INPSX5GX6TX7YAQKFQG(配列番号2203)を含み、X4は、IまたはSであり、X5は、GまたはRであり、X6は、SまたはRであり、X7は、SまたはEである;および/または
(iii)VH CDR3は、アミノ酸配列ARDGPX8X9X10DYYMDV(配列番号2204)を含み、X8は、RまたはQであり、X9は、V、D、LまたはEで
あり、X10は、SまたはVである;および、
単離された抗FIXa抗体またはその抗原結合部分は、VL CDR1、CDR2およびCDR3をさらに含み、VL CDR1は、アミノ酸配列RASQSVSSYLA(配列番号2116)を含み;および/またはVL CDR2は、アミノ酸配列DASNRAT(配列番号2116)を含み;および/または(iii)VL CDR3は、アミノ酸配列QQRDNWPFT(配列番号2116)を含む。
(i)VH CDR1は、アミノ酸配列GSIX1SX2X3YX4WX5(配列番号2205)を含み、X1は、SまたはAであり、X2は、S、T、GまたはVであり、X3は、SまたはAであり、X4は、YまたはAであり、X5は、G、V、NまたはSである;および/または
(ii)VH CDR2は、アミノ酸配列X6IX7X8X9GX10TX11YNPSLKS(配列番号2206)を含み、X6は、SまたはYであり、X7は、S、Y、R、TまたはQであり、X8は、Y、G、PまたはAであり、X9は、SまたはQであり、X10は、SまたはKであり、X11は、YまたはQである;および/または
(iii)VH CDR3は、アミノ酸配列ARDKYQDYSX12DI(配列番号2207)を含み、X12は、FまたはVである。
(i)VH CDR1は、アミノ酸配列GSIX1SX2X3YX4WX5(配列番号2205)を含み、X1は、SまたはAであり、X2は、S、T、GまたはVであり、X3は、SまたはAであり、X4は、YまたはAであり、X5は、G、V、NまたはSである;および/または
(ii)VH CDR2は、アミノ酸配列X6IX7X8X9GX10TX11YNPSLKS(配列番号2206)を含み、X6は、SまたはYであり、X7は、S、Y、R、TまたはQであり、X8は、Y、G、PまたはAであり、X9は、SまたはQであり、X10は、SまたはKであり、X11は、YまたはQである、および/または
(iii)VH CDR3は、アミノ酸配列ARDKYQDYSX12DI(配列番号2207)を含み、X12は、FまたはVである;および
単離された抗FIXa抗体またはその抗原結合部分は、VL CDR1、CDR2およびCDR3をさらに含み、VL CDR1は、アミノ酸配列RASQGIDSWLA(配列番号2136)を含み;および/またはVL CDR2は、アミノ酸配列AASSLQS(配列番号2162)を含み;および/またはVL CDR3は、アミノ酸配列QQAN
FLPFT(配列番号2188)を含む。
(ii)VLは、配列番号1937、1941、1945、1949、1953、1957、1961、1965、1969、1973、1977、1981、1985、1989、1993、1997、2001、2005、2009、2013、2017、2021、2025、2029、2033および2037からなる群から選択されるアミノ酸配列と少なくとも約80%、少なくとも約85%、少なくとも約90%、少なくとも約95%、少なくとも約96%、少なくとも約97%、少なくとも約98%、少なくとも約99%または約100%同一のアミノ酸配列を含む、
酸配列を含む(それぞれ、BIIB-9-1336のVHおよびVL)。
(a1)VHは、配列番号1935と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み、VLは、配列番号1937と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み;
(a2)VHは、配列番号1939と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み、VLは、配列番号1941と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み;
(a3)VHは、配列番号1943と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み、VLは、配列番号1945と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み;
(a4)VHは、配列番号1947と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み、VLは、配列番号1949と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み;
(a5)VHは、配列番号1951と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み、VLは、配列番号1953と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み;
(a6)VHは、配列番号1955と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み、VLは、配列番号1957と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み;
(a7)VHは、配列番号1959と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み、VLは、配列番号1961と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み;
(a8)VHは、配列番号1963と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み、VLは、配列番号1965と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100
%が同一のアミノ酸配列を含み;
(a9)VHは、配列番号1967と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み、VLは、配列番号1969と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み;
(a10)VHは、配列番号1971と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み、VLは、配列番号1973と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み;
(a11)VHは、配列番号1975と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み、VLは、配列番号1977と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み;
(a12)VHは、配列番号1979と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み、VLは、配列番号1981と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み;
(a13)VHは、配列番号1983と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み、VLは、配列番号1985と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み;
(a14)VHは、配列番号1987と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み、VLは、配列番号1989と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み;
(a15)VHは、配列番号1991と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み、VLは、配列番号1993と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み;
(a16)VHは、配列番号1995と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み、VLは、配列番号1997と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み;
(a17)VHは、配列番号1999と少なくとも70%、少なくとも80%、少なく
とも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み、VLは、配列番号2001と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み;
(a18)VHは、配列番号2003と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み、VLは、配列番号2005と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み;
(a19)VHは、配列番号2007と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み、VLは、配列番号2009と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み;
(a20)VHは、配列番号2011と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み、VLは、配列番号2013と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み;
(a21)VHは、配列番号2015と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み、VLは、配列番号2017と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み;
(a22)VHは、配列番号2019と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み、VLは、配列番号2021と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み;
(a23)VHは、配列番号2023と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み、VLは、配列番号2025と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み;
(a24)VHは、配列番号2027と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み、VLは、配列番号2029と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み;
(a25)VHは、配列番号2031と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み、VLは、配列番号2
033と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み;または
(a26)VHは、配列番号2035と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含み、VLは、配列番号2037と少なくとも70%、少なくとも80%、少なくとも90%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%または100%が同一のアミノ酸配列を含む。
(a2)VHおよびVLは、それぞれ、配列番号1939および1941(BIIB-9-3601)を含み;
(a3)VHおよびVLは、それぞれ、配列番号1943および1945(BIIB-9-3604)を含み;
(a4)VHおよびVLは、それぞれ、配列番号1947および1949(BIIB-9-3617)を含み;
(a5)VHおよびVLは、それぞれ、配列番号1951および1953(BIIB-9-3618)を含み;
(a6)VHおよびVLは、それぞれ、配列番号1955および1957(BIIB-9-3621)を含み;
(a7)VHおよびVLは、それぞれ、配列番号1959および1961(BIIB-9-3647)を含み;
(a8)VHおよびVLは、それぞれ、配列番号1963および1965(BIIB-9-3649)を含み;
(a9)VHおよびVLは、それぞれ、配列番号1967および1969(BIIB-9-3650)を含み;
(a10)VHおよびVLは、それぞれ、配列番号1971および1973(BIIB-9-3654)を含み;
(a11)VHおよびVLは、それぞれ、配列番号1975および1977(BIIB-9-3753)を含み;
(a12)VHおよびVLは、それぞれ、配列番号1979および1981(BIIB-9-3754)を含み;
(a13)VHおよびVLは、それぞれ、配列番号1983および1985(BIIB-9-3756)を含み;
(a14)VHおよびVLは、それぞれ、配列番号1987および1989(BIIB-9-3764)を含み;
(a15)VHおよびVLは、それぞれ、配列番号1991および1993(BIIB-9-3766)を含み;
(a16)VHおよびVLは、それぞれ、配列番号1995および1997(BIIB-9-3707)を含み;
(a17)VHおよびVLは、それぞれ、配列番号1999および2001(BIIB-9-3709)を含み;
(a18)VHおよびVLは、それぞれ、配列番号2003および2005(BIIB-9-3720)を含み;
(a19)VHおよびVLは、それぞれ、配列番号2007および2009(BIIB-9-3727)を含み;
(a20)VHおよびVLは、それぞれ、配列番号2011および2013(BIIB-
9-3745)を含み;
(a21)VHおよびVLは、それぞれ、配列番号2015および2017(BIIB-9-3780)を含み;
(a22)VHおよびVLは、それぞれ、配列番号2019および2021(BIIB-9-3675)を含み;
(a23)VHおよびVLは、それぞれ、配列番号2023および2025(BIIB-9-3681)を含み;
(a24)VHおよびVLは、それぞれ、配列番号2027および2029(BIIB-9-3684)を含み;
(a25)VHおよびVLは、それぞれ、配列番号2031および2033(BIIB-9-3698)を含み;または
(a26)VHおよびVLは、それぞれ、配列番号2035および2037(BIIB-9-3704)を含む。
50%、少なくとも60%、少なくとも70%、少なくとも80%、少なくとも90%、少なくとも100%、少なくとも120%、少なくとも140%、少なくとも160%、少なくとも180%、少なくとも200%、少なくとも220%、少なくとも240%、少なくとも260%、少なくとも280%、少なくとも300%、少なくとも320%、少なくとも340%、少なくとも360%、少なくとも380%、または少なくとも400%、ATIIIによるFIXa阻害の速度を向上することができる。
したがって、本開示は、FIXチモーゲン(FIXz)に特異的に結合する抗体(例えば、単離された抗体)またはその抗原結合部分であって、FIXaおよびFIXzの存在下でFIXzに優先的に結合する、抗体またはその抗原結合部分(「抗FIXz抗体またはその抗原結合部分」)を提供する。
(i)図3D中のVH CDR3配列からなる群から選択されるVH CDR3配列と同一のVH CDR3配列、または
(ii)1つ、2つまたは3つのアミノ酸置換を除く、図3D中のVH CDR3配列
からなる群から選択されるVH CDR3配列と同一のVH CDR3配列
を含む。
(i)図3D中で開示されているVH CDR1配列からなる群から選択される配列と同一のVH CDR1配列、または
(ii)1つ、2つまたは3つのアミノ酸置換を除く、図3D中で開示されているVH
CDR1配列からなる群から選択される配列と同一のVH CDR1配列
を含む。
(i)図3D中で開示されているVH CDR2配列からなる群から選択される配列と同一のVH CDR2配列、または
(ii)1つ、2つまたは3つのアミノ酸置換を除く、図3D中で開示されているVH
CDR2配列からなる群から選択される配列と同一のVH CDR2配列
を含む。
(i)図3D中で開示されているVL CDR1配列からなる群から選択される配列と同一のVL CDR1配列、または
(ii)1つ、2つまたは3つのアミノ酸置換を除く、図3D中で開示されているVL
CDR1配列からなる群から選択される配列と同一のVL CDR1配列
を含む。
(i)図3D中のVL CDR2配列からなる群から選択される配列と同一のVL CDR2配列、または
(ii)1つ、2つまたは3つのアミノ酸置換を除く、図3D中のVL CDR2配列からなる群から選択される配列と同一のVL CDR2配列
を含む。
(i)図3D中で開示されているVL CDR3配列からなる群から選択される配列と同一のVL CDR3配列、または
(ii)1つ、2つまたは3つのアミノ酸置換を除く、図3D中で開示されているVL
CDR3配列からなる群から選択される配列と同一のVL CDR3配列
を含む。
CDR2およびVH CDR3ならびにVL CDR1、VL CDR2およびVL CDR3を含む。
(i)VHは、配列番号183、185、187および189からなる群から選択されるアミノ酸配列と、少なくとも約70%、少なくとも約75%、少なくとも約80%、少なくとも約85%、少なくとも約90%、少なくとも約95%、少なくとも約96%、少なくとも約97%、少なくとも約98%、少なくとも約99%または約100%同一のアミノ酸配列を含み;
(ii)VLは、配列番号369、371、373および375からなる群から選択されるアミノ酸配列と、少なくとも約70%、少なくとも約75%、少なくとも約80%、少なくとも約85%、少なくとも約90%、少なくとも約95%、少なくとも約96%、少なくとも約97%、少なくとも約98%、少なくとも約99%または約100%同一のアミノ酸配列を含む。
本開示はまた、FXに特異的に結合する、抗FX結合性分子、例えば、抗FX抗体、またはそのFX結合性断片を含む分子を提供する。本開示の一部の態様では、開示されている抗FX結合性分子、例えば、抗FX抗体、またはそのFX結合性断片を含む分子は、FXチモーゲン(FXz)(本開示全体を通して、「抗FXz抗体」と称される)に優先的に結合する。
8のアミノ酸にあるシグナルペプチドを含むプレプロペプチドとして製造される。FXチモーゲン(FXz)のアミノ酸配列は、以下に提示されている(シグナル配列(1~23)は、下線が引かれており、プロペプチド(24~40)は、太字で記載されている):
る。
(i)図12Aまたは図12B中のVH CDR3配列からなる群から選択されるVH
CDR3配列と同一のVH CDR3配列、または
(ii)1つ、2つまたは3つのアミノ酸置換を除く、図12Aまたは図12B中のVH CDR3配列からなる群から選択されるVH CDR3配列と同一のVH CDR3配列
を含む。
(i)図12Aまたは図12B中で開示されているVH CDR1配列からなる群から選択される配列と同一のVH CDR1配列、または
(ii)1つ、2つまたは3つのアミノ酸置換を除く、図12Aまたは図12B中で開示されているVH CDR1配列からなる群から選択される配列と同一のVH CDR1配列
を含む。
(i)図12Aまたは図12B中で開示されているVH CDR2配列からなる群から選択される配列と同一のVH CDR2配列、または
(ii)1つ、2つまたは3つのアミノ酸置換を除く、図12Aまたは図12B中で開示されているVH CDR2配列からなる群から選択される配列と同一のVH CDR2配列
を含む。
(i)図12Aまたは図12B中で開示されているVL CDR1配列からなる群から選択される配列と同一のVL CDR1配列、または
(ii)1つ、2つまたは3つのアミノ酸置換を除く、図12Aまたは図12B中で開
示されているVL CDR1配列からなる群から選択される配列と同一のVL CDR1配列
を含む。
(i)図12Aまたは図12B中のVL CDR2配列からなる群から選択される配列と同一のVL CDR2配列、または
(ii)1つ、2つまたは3つのアミノ酸置換を除く、図12Aまたは図12B中のVL CDR2配列からなる群から選択される配列と同一のVL CDR2配列
を含む。
(i)図12Aまたは図12B中で開示されているVL CDR3配列からなる群から選択される配列と同一のVL CDR3配列、または
(ii)1つ、2つまたは3つのアミノ酸置換を除く、図12Aまたは図12B中で開示されているVL CDR3配列からなる群から選択される配列と同一のVL CDR3配列
を含む。
(i)図12Aまたは図12B中で開示されているVL CDR3配列からなる群から選択される配列と同一のVL CDR3配列、または
(ii)1つ、2つまたは3つのアミノ酸置換を除く、図12Aまたは図12B中で開示されているVL CDR3配列からなる群から選択される配列と同一のVL CDR3配列
からなるか、または実質的になる。
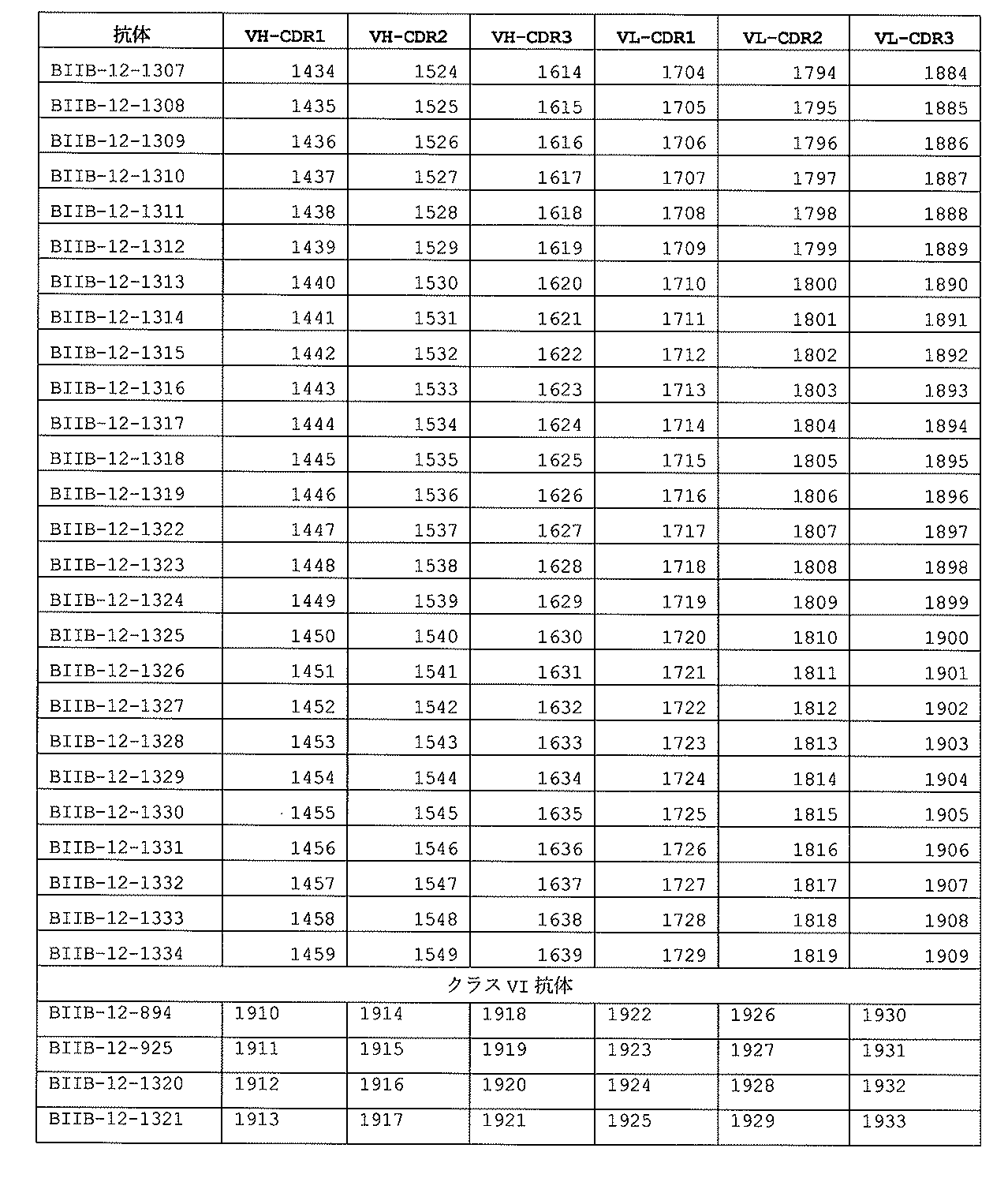
、BIIB-12-1296、BIIB-12-1297、BIIB-12-1298、BIIB-12-1299、BIIB-12-1300、BIIB-12-1301、BIIB-12-1302、BIIB-12-1303、BIIB-12-1304、BIIB-12-1305、BIIB-12-1306、BIIB-12-1307、BIIB-12-1308、BIIB-12-1309、BIIB-12-1310、BIIB-12-1311、BIIB-12-1312、BIIB-12-1313、BIIB-12-1314、BIIB-12-1315、BIIB-12-1316、BIIB-12-1317、BIIB-12-1318、BIIB-12-1319、BIIB-12-1322、BIIB-12-1323、BIIB-12-1324、BIIB-12-1325、BIIB-12-1326、BIIB-12-1327、BIIB-12-1328、BIIB-12-1329、BIIB-12-1330、BIIB-12-1331、BIIB-12-1332、BIIB-12-1333、またはBIIB-12-1334からなる群から選択される抗FXz抗体のVH CDR1、VH CDR2およびVH CDR3ならびにVL CDR1、VL CDR2およびVL CDR3を含む。
なくとも約99%または約100%同一のアミノ酸配列を含む。
(i)VHは、配列番号377、379、381、383、385、387、389、391、393、395、397、399、401、403、405、407、409、411、413、415、417、419、421、423、425、427、429、431、433、435、437、439、441、443、445、447、449、451、453、455、457、459、461、463、465、467、469、471、473、475、477、479、481、483、485、487、489、491、493、495、497、499、501、503、505、507、509、511、513、515、517、519、521、523、525、527、529、531、533、535、537、539、541、543、545、547、549、551、553、および555からなる群から選択されるアミノ酸配列と、少なくとも約70%、少なくとも約75%、少なくとも約80%、少なくとも約85%、少なくとも約90%、少なくとも約95%、少なくとも約96%、少なくとも約97%、少なくとも約98%、少なくとも約99%または約100%同一のアミノ酸配列を含み;
(ii)VLは、565、567、569、571、573、575、579、581、583、585、587、589、591、593、595、597、599、601、603、605、607、609、611、613、615、617、619、621、623、625、627、629、631、633、635、637、639、641、643、645、647、649、651、653、655、657、659、661、663、665、667、669、671、673、675、677、679、681、683、685、687、689、691、693、695、697、699、701、703、705、707、709、711、713、715、717、719、721、723、725、727、729、731、733、735、737、739、741、および743からなる群から選択されるアミノ酸配列と、少なくとも約70%、少なくとも約75%、少なくとも約80%、少なくとも約85%、少なくとも約90%、少なくとも約95%、少なくとも約96%、少なくとも約97%、少なくとも約98%、少なくとも約99%または約100%同一のアミノ酸配列を含む。
ことができず、または4、3、2もしくは1以下のアミノ酸しか差異を示さないことさえあり得る。
(i)少なくとも1つのVHは、配列番号423、427または455から選択される配列からなるか、またはこれらから実質的になる;および、
(ii)少なくとも1つのVLは、配列番号611、615または643から選択される配列からなるか、またはこれらから実質的になる。
(b1)VHおよびVLは、それぞれ、配列番号423および611を含む、これらからなる、またはこれらから実質的になる;
(b2)VHおよびVLは、それぞれ、配列番号427および615を含む、これらからなる、またはこれらから実質的になる;または
(b3)VHおよびVLは、それぞれ、配列番号455および643を含む、これらからなる、またはこれらから実質的になる。
本開示は、活性化第X因子(FXa)に特異的に結合する抗体(例えば、単離された抗体)またはその抗原結合部分であって、抗FX抗体またはその抗原結合部分が、FXzおよびFXaの存在下で、FXaに優先的に結合する、抗体またはその抗原結合部分を提供する。一実施形態では、FXaは、擬似基質(すなわち、EGR-CMK)に共有結合しているFXaである。
(i)図12C中のVH CDR3配列からなる群から選択されるVH CDR3配列と同一のVH CDR3配列;または
(ii)1つ、2つまたは3つのアミノ酸置換を除く、図12C中のVH CDR3配列からなる群から選択されるVH CDR3配列と同一のVH CDR3配列
を含む。
(i)図12C中で開示されているVH CDR1配列からなる群から選択される配列と同一のVH CDR1配列、または
(ii)1つ、2つまたは3つのアミノ酸置換を除く、図12C中で開示されているVH
CDR1配列からなる群から選択される配列と同一のVH CDR1配列
を含む。
(i)図12C中で開示されているVH CDR2配列からなる群から選択される配列と同一のVH CDR2配列、または
(ii)1つ、2つまたは3つのアミノ酸置換を除く、図12C中で開示されているVH
CDR2配列からなる群から選択される配列と同一のVH CDR2配列
を含む。
(i)図12C中で開示されているVL CDR1配列からなる群から選択される配列と同一のVL CDR1配列、または
(ii)1つ、2つまたは3つのアミノ酸置換を除く、図12C中で開示されているVL CDR1配列からなる群から選択される配列と同一のVL CDR1配列
を含む。
(i)図12C中のVL CDR2配列からなる群から選択される配列と同一のVL CDR2配列、または
(ii)1つ、2つまたは3つのアミノ酸置換を除く、図12C中のVL CDR2配列からなる群から選択される配列と同一のVL CDR2配列
を含む。
(i)図12C中で開示されているVL CDR3配列からなる群から選択される配列と同一のVL CDR3配列、または
(ii)1つ、2つまたは3つのアミノ酸置換を除く、図12C中で開示されているVL CDR3配列からなる群から選択される配列と同一のVL CDR3配列
を含む。
(i)図12C中で開示されているVL CDR3配列からなる群から選択される配列と同一のVL CDR3配列、または
(ii)1つ、2つまたは3つのアミノ酸置換を除く、図12C中で開示されているVL CDR3配列からなる群から選択される配列と同一のVL CDR3配列
からなるか、またはこれらから実質的になる。
(i)VHは、配列番号557、559、561および563からなる群から選択されるアミノ酸配列と、少なくとも約70%、少なくとも約75%、少なくとも約80%、少なくとも約85%、少なくとも約90%、少なくとも約95%、少なくとも約96%、少なくとも約97%、少なくとも約98%、少なくとも約99%または約100%同一のアミノ酸配列を含み;
(ii)VLは、配列番号745、747、749および751からなる群から選択されるアミノ酸配列と、少なくとも約70%、少なくとも約75%、少なくとも約80%、少なくとも約85%、少なくとも約90%、少なくとも約95%、少なくとも約96%、少なくとも約97%、少なくとも約98%、少なくとも約99%または約100%同一のアミノ酸配列を含む。
本開示のある種の態様は、本明細書に開示されるVHおよびVL CDR配列を含み、さらに本明細書に開示される抗体とは異なるフレームワーク配列を含有する、本明細書に開示される抗FIX抗体(例えば、抗FIXa抗体または抗FIXz抗体)および抗FX抗体(例えば、抗FXa抗体または抗FXz抗体)に関する。このようなフレームワーク配列は、公のDNAデータベース、または生殖系抗体遺伝子配列を含む公表されている参考文献から得ることができる。例えば、ヒト重鎖および軽鎖可変領域遺伝子の生殖系DNA配列は、「VBase」ヒト生殖系配列データベース(www.mrc-cpe.cam.ac.uk/vbaseにてインターネットで入手可能である)、およびKabat,E.A.ら(1991年)Sequences of Proteins of Immunological Interest、第5版、U.S.Department of Health and Human Services、NIH Publica
tion 91~3242頁;Tomlinson,I.M.ら(1992年)「The
Repertoire of Human Germline VH Sequences Reveals about Fifty Groups of VH Segments with Different Hypervariable Loops」、Mol.Biol.227巻:776~798頁;およびCox,J.P.L.ら(1994年)、「A Directory of Human Germ-line VH
Segments Reveals a Strong Bias in their
Usage」、Eur.J.Immunol.24巻:827~836頁において見出すことができる;これらの各々の内容は、参照により本明細書に明示的に組み入れられる。
分解、およびその後の効能の低下をもたらすことができる。したがって、同様に、酸化的分解を受けないアミノ酸残基により置き換えられた重鎖および/または軽鎖CDR中の1つまたはそれ以上のメチオニン残基を有する抗FIX/FX抗体も提供される。一実施形態では、本明細書に開示される抗体のCDRにおけるメチオニン残基は、酸化的分解を受けないアミノ酸残基により置き換えられる。同様に、脱アミド部位は、抗体のいずれかから、特にCRDにおいて除去することができる。
FXz抗体)は、多価である。特定の態様では、抗FIX抗体(例えば、抗FIXa抗体または抗FIXz抗体)または抗FX抗体(例えば、抗FXa抗体または抗FXz抗体)は、二価の、例えば、いくつかの特異的抗原結合部位を含む抗体である。特定の態様では、抗FIX抗体(例えば、抗FIXa抗体または抗FIXz抗体)または抗FX抗体(例えば、抗FXa抗体または抗FXz抗体)は、二重特異性である、すなわち、この分子は、2つの異なる抗原(例えば、同一または異なる分子の2つの異なるエピトープ)に特異的に結合することができる。いくつかの特定の態様では、抗FIX抗体(例えば、抗FIXa抗体または抗FIXz抗体)または抗FX抗体(例えば、抗FXa抗体または抗FXz抗体)は、二価および二重特異性である、例えば、2つの異なる抗原(例えば、同一または異なる分子の2つの異なるエピトープ)に結合することができる4つの二結合部位を含む抗体である。
本開示はまた、第2の結合特異性を有する分子に連結されている、抗FIX特異性(例えば、本明細書に開示される抗FIXa抗体もしくは抗原結合部分、または本明細書に開示される抗FIXz抗体もしくはその抗原結合部分)を含む二重特異性分子を提供する。同様に、第2の結合特異性を有する分子に連結されている、抗FX特異性(例えば、本明細書に開示される抗FXz抗体もしくはその抗原結合部分、または本明細書に開示される抗FXa抗体もしくはその抗原結合部分)を含む二重特異性分子を提供する。同様に、(ii)抗FXz特異性(例えば、本明細書に開示される抗FXz抗体もしくはその抗原結合部分または本明細書に開示される抗FXa抗体もしくはその抗原結合部分)に連結している、(i)抗FIX特異性(例えば、本明細書に開示される抗FIXa抗体もしくは抗原結合部分または抗FIXz抗体もしくはその抗原結合部分)を含む二重特異性分子が提供される。本明細書に開示される二重特異性分子は、免疫グロブリン構造、または例えば、ドメインを再配列することにより抗体から誘導される構造を有する二重特異性分子に限定されない。本明細書に開示される二重特異性分子は、本明細書に開示されるCDRまたはその組合せが、グラフトされている分子足場(例えば、フィブロネクチンIIIまたはテネシイン-C足場)も含む。
およびVL、ならびに図12Aおよび図12B中の抗FXz抗体からなる群から選択される抗FXz抗体のVHおよびVLを含む。
(i)VH CDR1、VH CDR2およびVH CDR3ならびにVL CDR1、VL CDR2およびVL CDR3を含む抗FIXa抗体またはその抗原結合部分であって、VH CDR1、VH CDR2およびVH CDR3ならびにVL CDR1、VL CDR2およびVL CDR3が、図3A、3B、3Cおよび3D中の抗FIXa(BIIB-9)抗体の、VH CDR1、VH CDR2およびVH CDR3ならびにVL CDR1、VL CDR2およびVL CDR3(例えば、図15A、15B、15Cおよび15DのCDR)からなる群から選択される、抗FIXa抗体またはその抗原結合部分;および
(ii)VH CDR1、VH CDR2およびVH CDR3ならびにVL CDR1、VL CDR2およびVL CDR3を含む抗FX抗体またはその抗原結合部分であって、VH CDR1、VH CDR2およびVH CDR3ならびにVL CDR1、VL CDR2およびVL CDR3が、図12Aおよび12B中の抗FX(BIIB-12)抗体の、VH CDR1、VH CDR2およびVH CDR3ならびにVL CDR1、VL CDR2およびVL CDR3(例えば、図15A、15B、15Cおよび15DのCDR)からなる群から選択される、抗FX抗体またはその抗原結合部分
を含む。
(a)抗FIX抗体またはその抗原結合部分であって:
(a1)それぞれ、配列番号815、860または905を含む、VH CDR1、VH CDR2およびVH CDR3配列、および/またはそれぞれ、配列番号950、995または1040を含むVL CDR1、VL CDR2およびVL CDR3配列(BIIB-9-484)
(a2)それぞれ、配列番号822、867または912を含む、VH CDR1、VL CDR2およびVL CDR3配列、および/またはそれぞれ、配列番号957、1002または1047を含むVL CDR1、VL CDR2およびVL CDR3配列(BIIB-9-619)
(a3)それぞれ、配列番号1347、1351または1355を含む、VH CDR1、VH CDR2およびVH CDR3配列、および/またはそれぞれ、配列番号1359、1363または1367を含むVL CDR1、VL CDR2およびVL CDR3配列(BIIB-9-578)
(a4)それぞれ、配列番号843、888または933を含む、VH CDR1、VH CDR2およびVH CDR3配列、および/またはそれぞれ、配列番号978、1023または1068を含むVL CDR1、VL CDR2およびVL CDR3配列(BIIB-9-1335)、または
(a5)それぞれ、配列番号844、889または934を含む、VH CDR1、VH CDR2およびVH CDR3配列、および/またはそれぞれ、配列番号979、1024または1069を含むVL CDR1、VL CDR2およびVL CDR3配列(BIIB-9-1336)
を含む、抗FIX抗体またはその抗原結合部分ならびに
(b)抗FX抗体またはその抗原結合部分であって:
(b1)それぞれ、配列番号1393、1483または1573を含む、VH CDR1、VH CDR2およびVH CDR3配列、および/またはそれぞれ、配列番号1663、1753または1843を含むVL CDR1、VL CDR2およびVL CDR3配列(BIIB-12-915)
(b2)それぞれ、配列番号1395、1485または1575を含む、VH CDR1、VH CDR2およびVH CDR3配列、および/またはそれぞれ、配列番号1665、1755または1845を含むVL CDR1、VL CDR2およびVL CD
R3配列(BIIB-12-917)
(b3)それぞれ、配列番号1911、1915または1919を含む、VH CDR1、VH CDR2およびVH CDR3配列、および/またはそれぞれ、配列番号1923、1927または1931を含むVL CDR1、VL CDR2およびVL CDR3配列(BIIB-12-925)
(b4)それぞれ、配列番号1409、1499または1589を含む、VH CDR1、VH CDR2およびVH CDR3配列、および/またはそれぞれ、配列番号1679、1769または1859を含むVL CDR1、VL CDR2およびVL CDR3配列(BIIB-12-932)
(b5)それぞれ、配列番号1433、1523または1613を含む、VH CDR1、VH CDR2およびVH CDR3配列、および/またはそれぞれ、配列番号1703、1793または1883を含むVL CDR1、VL CDR2およびVL CDR3配列(BIIB-12-1306)
を含む、抗FX抗体またはその抗原結合部分を含む。
(a)抗FIX抗体またはその抗原結合部分であって:
(a1)それぞれ、配列番号31および221を含むVHおよびVL;(BIIB-9-484)
(a2)それぞれ、配列番号45および235を含むVHおよびVL;(BIIB-9-619)
(a3)それぞれ、配列番号185および371を含むVHおよびVL;(BIIB-9-578)
(a4)それぞれ、配列番号87および221を含むVHおよびVL;(BIIB-9-1335)
(a5)それぞれ、配列番号89および221を含むVHおよびVL(BIIB-9-1336)
を含む、抗FIX抗体またはその抗原結合部分、
(b)抗FX抗体またはその抗原結合部分であって:
(b1)それぞれ、配列番号423および611を含むVHおよびVL;(BIIB-12-915)
(b2)それぞれ、配列番号427および615を含むVHおよびVL;(BIIB-12-917)
(b3)それぞれ、配列番号559および747を含むVHおよびVL;(BIIB-12-925)
(b4)それぞれ、配列番号455および643を含むVHおよびVL;(BIIB-12-932)または
(b5)それぞれ、配列番号503および691を含むVHおよびVL(BIIB-12-1306)
を含む、抗FX抗体またはその抗原結合部分
を含む。
(i)抗FIXa抗体またはその抗原結合部分は、それぞれ、配列番号31および221を含むVHおよびVL;(BIIB-9-484)を含み、抗FXz抗体またはその抗原結合部分は、それぞれ、配列番号423および611を含むVHおよびVL;(BIIB-12-915)を含み;
(ii)抗FIXa抗体またはその抗原結合部分は、それぞれ、配列番号31および221を含むVHおよびVL;(BIIB-9-484)を含み、抗FXz抗体またはその抗原結合部分は、それぞれ、配列番号427および615を含むVHおよびVL;(BIIB-12-917)を含み;
(iii)抗FIXa抗体またはその抗原結合部分は、それぞれ、配列番号31および221を含むVHおよびVL;(BIIB-9-484)を含み、抗FXa抗体またはその抗原結合部分は、それぞれ、配列番号559および747を含むVHおよびVL;(BIIB-12-925)を含み;
(iv)抗FIXa抗体またはその抗原結合部分は、それぞれ、配列番号31および221を含むVHおよびVL;(BIIB-9-484)を含み、抗FXz抗体またはその抗原結合部分は、それぞれ、配列番号455および643を含むVHおよびVL;(BIIB-12-932)を含み;
(v)抗FIXz抗体またはその抗原結合部分は、それぞれ、配列番号185および371を含むVHおよびVL;(BIIB-9-578)を含み、抗FXz抗体またはその抗原結合部分は、それぞれ、配列番号423および611を含むVHおよびVL;(BIIB-12-915)を含み;
(vi)抗FIXz抗体またはその抗原結合部分は、それぞれ、配列番号185および371を含むVHおよびVL;(BIIB-9-578)を含み、抗FXz抗体またはその抗原結合部分は、それぞれ、配列番号427および615を含むVHおよびVL;(BIIB-12-917)を含み;
(vii)抗FIXa抗体またはその抗原結合部分は、それぞれ、配列番号45および235を含むVHおよびVL;(BIIB-9-619)を含み、抗FXz抗体またはその抗原結合部分は、それぞれ、配列番号427および615を含むVHおよびVL;(BIIB-12-917)を含み;または
(viii)抗FIXa抗体またはその抗原結合部分は、それぞれ、配列番号45および235を含むVHおよびVL(BIIB-9-619)を含み;抗FXa抗体またはその抗原結合部分は、それぞれ、配列番号559および747を含むVHおよびVL(BIIB-12-925)を含む。
(iii)表7中に開示されているVH CDR1配列からなる群から選択される配列と同一のVH CDR1配列、または
(iv)1つ、2つまたは3つのアミノ酸置換を除く、表7中に開示されているVH CDR1配列からなる群から選択される配列と同一のVH CDR1配列
を含む。
(iii)表7中のVH CDR2配列からなる群から選択される配列と同一のVH CDR2配列、または
(iv)1つ、2つまたは3つのアミノ酸置換を除く、表7中のVH CDR2配列か
らなる群から選択される配列と同一のVH CDR2配列
を含む。
(iii)表7中に開示されているVH CDR3配列からなる群から選択される配列と同一のVH CDR3配列、または
(iv)1つ、2つまたは3つのアミノ酸置換を除く、表7中に開示されているVH CDR3配列からなる群から選択される配列と同一のVH CDR3配列
を含む。
(v)表7中に開示されているVL CDR1配列からなる群から選択される配列と同一のVL CDR1配列、または
(vi)1つ、2つまたは3つのアミノ酸置換を除く、表7中に開示されているVL CDR1配列からなる群から選択される配列と同一のVL CDR1配列
を含む。
(v)表7中のVL CDR2配列からなる群から選択される配列と同一のVL CDR2配列、または
(vi)1つ、2つまたは3つのアミノ酸置換を除く、表7中のVL CDR2配列からなる群から選択される配列と同一のVL CDR2配列
を含む。
(v)表7中に開示されているVL CDR3配列からなる群から選択される配列と同一のVL CDR3配列、または
(vi)1つ、2つまたは3つのアミノ酸置換を除く、表7中に開示されているVL CDR3配列からなる群から選択される配列と同一のVL CDR3配列
を含む。
CDR2およびVL CDR3配列から選択される、VH CDR1、VH CDR2およびVH CDR3ならびにVL CDR1、VL CDR2およびVL CDR3を含む。
20%/80%)の存在下での同一実験条件下で観察される活性よりも、少なくとも約
50%、少なくとも約60%、少なくとも約70%、少なくとも約80%、少なくとも約90%、少なくとも約100%、少なくとも約110%、少なくとも約120%、少なくとも約130%、少なくとも約140%、少なくとも約150%、少なくとも約160%、少なくとも約170%、少なくとも約180%、少なくとも約190%、少なくとも約200%、少なくとも約210%、少なくとも約220%、少なくとも約230%、少なくとも約240%、少なくとも約250%、少なくとも約260%、少なくとも約270%、少なくとも約280%、少なくとも約290%または少なくとも約300%高い。
性抗体を含み、それらはすべて、その全体が参照によって本明細書に組み入れられる。
ドメインの1つは、第1の標的分子(例えば、FIXa)に特異的に結合する/これと相互作用することが可能な抗体の可変領域(またはその部分)、その抗体断片または誘導体からなる。第2の結合ドメインは、第2の標的分子(例えば、FXz)に特異的に結合する/これと相互作用することが可能な抗体の可変領域(またはその部分)、その抗体断片または誘導体からなる。
Laboratory Manual:Cold Spring Harbor La
boratory Press、第2版(1989年)および第3版(2001年);Gerhardtら、Methods for General and Molecular Bacteriology ASM Press(1994年);Lefkovits、Immunology Methods Manual:The Comprehensive Sourcebook of Techniques;Academic
Press(1997年);Golemis、Protein-Protein Interactions:A Molecular Cloning Manual Cold Spring Harbor Laboratory Press(2002年)を参照されたい)。
(i)「一本鎖Fv」または「scFv」:抗体のVHおよびVLドメインを有する抗体断片であり、これらのドメインは、一本鎖ポリペプチド中に存在する。一般に、scFvポリペプチドは、scFvが抗原結合にとって所望の構造の形成を可能にする、VHとVLドメインとの間のポリペプチドリンカーをさらに含む。一本鎖抗体の生成に関して記載されている技法は、例えば、Pluckhun in The Pharmacology of Monoclonal Antibodies、Rosenburg and
Moore(編).Springer-Verlag、N.Y.113巻(1994年)、269~315頁に記載される。
(ii)「Fab断片」:1つの軽鎖、ならびに1つの重鎖のCH1および可変領域からなる。Fab分子の重鎖は、別の重鎖分子とジスルフィド結合を形成することができない。
(iii)「Fab断片」:1つの軽鎖、およびVHドメインおよびCH1ドメインを含有する1つの重鎖の部分、およびやはりまたCH1とCH2ドメインとの間の領域を含み、こうして、鎖間ジスルフィド結合が、2つのFab’断片の2つの重鎖の間に形成されて、F(ab’)2分子を形成することができる。
(iv)「F(ab’)2断片」:CH1ドメインとCH2ドメインとの間の定常領域の一部を含有する2つの軽鎖および2つの重鎖を含み、こうして鎖間ジスルフィド結合は、2つの重鎖の間に形成される。したがって、F(ab’)2断片は、2つの重鎖間のジスルフィド結合により一緒に保持される2つのFab’断片からなる。「Fv領域」は、重鎖および軽鎖の両方からの可変領域を含むが、定常領域を欠いている。
一重特異性、二重特異性または多重特異性分子として、本明細書に記載される抗FIX可変領域(例えば、抗FIXa可変領域または抗FIXz可変領域)および/または抗FX可変領域(例えば、抗FXa可変領域または抗FXz可変領域)は、Fc、例えば、IgG1、IgG2、IgG3またはIgG4 Fcに連結されており(例えば、共有結合により連結されているかまたは融合されている)、これらは、任意のアロタイプまたはイソアロタイプ、例えば、IgG1の場合:Glm、Glm1(a)、Glm2(x)、Glm3(f)、Glml7(z);IgG2の場合:G2m、G2m23(n);IgG3の場合:G3m、G3m21(g1)、G3m28(g5)、G3m11(b0)、G3m5(b1)、G3ml3(b3)、G3ml4(b4)、G3m10(b5)、G3m15(s)、G3m16(t)、G3m6(c3)、G3m24(c5)、G3m26(u)、G3m27(v);およびKの場合:Km、Km1、Km2、Km3(例えば、
Jefferiesら(2009年)mAbs 1:1を参照されたい)のいずれかとすることができる。
び/または(d)親Fcに比べてFc受容体に対する親和性が増大している、または低下している、Fcバリアントを生成するため、Fc領域に修飾を行うことができる。このようなFc領域バリアントは、一般に、Fc領域中に少なくとも1つのアミノ酸修飾を含むであろう。アミノ酸修飾を組み合わせることは、特に望ましいことと考えられる。例えば、バリアントFc領域は、その中に、例えば、本明細書において特定されている指定Fc領域の位置の、2つ、3つ、4つ、5つなどの置換を含むことができる。
用を低下させるための他の修飾には、置換297A、234A、235A、237A、318A、228P、236E、268Q、309L、330S、331S、220S、226S、229S、238S、233Pおよび234V、ならびに変異手段もしくは酵素手段による、またはタンパク質をグリコシル化しない細菌などの生物中での産生による、位置297におけるグリコシル化の除去が含まれる。これら修飾および他の修飾は、Strohl、2009年、Current Opinion in Biotechnology 20巻:685~691頁に概説されている。
ることにより行うことができる。例えば、米国特許第6,277,375号に記載される通り、以下の残基:252、254、256、433、435、436のうちの多くの1つまたはそれ以上を変異させることができる。特定の例示的な置換は、以下:T252L、T254Sおよび/またはT256Fのうちの1つまたはそれ以上を含む。代替的に、生物学的半減期を増加させるため、抗体は、Prestaらによる米国特許第5,869,046号および同第6,121,022号に記載される通り、CHIまたはCL領域内で改変されて、IgGのFc領域のCH2ドメインの2つのループから採取されるサルベージ受容体結合エピトープを含有することができる。FcRnへの結合を高める、および/または薬物動態特性を改善する他の例示的なバリアントには、例えば、2591、308F、428L、428M、434S、434l l、434F、434Yおよび434Xlを含めた、位置259、308、428および434における置換を含む。FcRnへのFc結合を増大する他のバリアントには、250E、250Q、428L、428F、250Q/428L(Hintonら、2004年、J.Biol.Chem.279巻(8号):6213~6216頁、Hintonら、2006年、Journal of Immunology 176巻:346~356頁)、256A、272A、286A、305A、307A、307Q、311A、312A、376A、378Q、380A、382A、434A(Shieldsら、Journal of Biological Chemistry、2001年、276巻(9号):6591~6604頁)、252F、252T、252Y、252W、254T、256S、256R、256Q、256E、256D、256T、309P、311S、433R、433S、433l、433P、433Q、434H、434F、434Y、252Y/254T/256E、433K/434F/436H、308T/309P/311S(Dall’Acquaら Journal of Immunology、2002年、169巻:5171~5180頁、Dall’Acquaら、2006年、Journal of Biological Chemistry 281巻:23514~23524頁)が含まれる。FcRn結合をモジュレートするための他の修飾は、Yeungら、2010年、J Immunol、182巻:7663~7671頁に記載される。ある種の実施形態では、特定の生物学的特徴を有するハイブリッド型IgGアイソタイプを使用することができる。例えば、IgG1/IgG3ハイブリッド型バリアントは、CH2および/またはCH3領域におけるIgG1の位置を2つのアイソタイプが異なる位置のIgG3からのアミノ酸と置き換えることにより構築することができる。したがって、1つまたはそれ以上の置換、例えば、274Q、276K、300F、339T、356E、358M、384S、392N、397M、422l、435Rおよび436Fを含むハイブリッド型バリアントIgG抗体を構築することができる。本明細書に記載される他の実施形態では、IgG1/IgG2ハイブリッド型バリアントは、CH2および/またはCH3領域におけるIgG2の位置を2つのアイソタイプが異なる位置のIgG1からのアミノ酸と置き換えることにより構築することができる。したがって、1つまたはそれ以上の置換、例えば、以下のアミノ酸置換:233E、234L、235L、-236G(位置236におけるグリシンの挿入を指す)および321hのうちの1つまたはそれ以上を含むハイブリッド型バリアントIgG抗体を構築することができる。
FcγRIIIaに対する親和性の最も大きな増大、FcγRIIb結合の低下および強力な毒性活性を示した、S239D/I332EおよびS239D/I332E/A330L変異を有するバリアントを含めた、FcγRIIIaへの結合を強力に増強させた他のIgG1バリアントが特定されている(Lazarら、2006年)。ADCC活性がインビトロでかなり増大するよう翻訳された、アレムツズマブ(CD52特異的、トラスツズマブ(HER2/neu特異的)、リツキシマブ(CD20特異的)およびセツキシマブ(EGFR特異的)などの抗体への三重変異の導入、およびS239D/I332Eバリアントが、サルにおいてB細胞を枯渇させる能力の増大を示した(Lazarら、2006年)。さらに、B細胞悪性腫瘍および乳がんのモデルにおいて、FcγRIIIaへの結合の増大、およびヒトFcγRIIIaを発現するトランスジェニックマウスにおけるADCC活性の同時増大を示した、L235V、F243L、R292P、Y300LおよびP396L変異を含有するIgG1変異体が特定されている(Stavenhagenら、2007年;Nordstromら、2011年)。使用することができる他のFc変異体は以下:S298A/E333A/L334A、S239D/I332E、S239D/I332E/A330L、L235V/F243L/R292P/Y300L/P396LおよびM428L/N434Sを含む。
上で言及したように、開示されている結合性分子の定常領域は、生じた構築物のプロファイルを増強する1つまたはそれ以上のアミノ酸の変異または置換によって修飾することができる。この点で、修飾された抗体またはその抗原結合断片の構造および免疫原性プロファイルを実質的に維持しながら、保存された結合部位(例えば、Fc結合)によってもたらされる活性を混乱させることが可能である。ある種の態様は、定常領域への1つまたはそれ以上のアミノ酸の付加を含んで、エフェクター機能の低下などの所望の特徴を向上させる、またはより多くの治療剤または診断剤の結合を実現することができる。このような態様では、選択された定常領域ドメインに由来する特定の配列が挿入または複製される。
化するため、抗体またはその断片を、通常、1つまたはそれ以上のPEG基を抗体または抗体断片に結合する条件下で、PEGの反応性エステル誘導体またはアルデヒド誘導体などのポリエチレングリコール(PEG)と反応させる。好ましくは、PEG化は、反応性PEG分子(または反応性水溶性ポリマーの類似体)とのアシル化反応またはアルキル化反応により行われる。本明細書で使用する場合、用語「ポリエチレングリコール」は、モノ(C1-C10)アルコキシ-またはアリールオキシ-ポリエチレングリコールまたはポリエチレングリコール-マレイミドなどの、他のタンパク質を誘導するために使用されるPEGの任意の形態を包含することが意図されている。ある種の実施形態では、PEG化されている抗体は、非グリコシル化抗体である。タンパク質をPEG化する方法は、当分野で公知であり、本明細書に記載される抗体に適用することができる。例えば、NishimuraらによるEP0154316、およびIshikawaらによるEP0401384を参照されたい。
本開示はまた、本明細書に開示される結合性分子(例えば、抗体)のいずれかを含むイムノコンジュゲートを提供する(例えば、本明細書に開示される抗FIX、抗FXまたは二重特異性抗FIX/抗FX抗体)。一態様では、イムノコンジュゲートは、薬剤に連結されている、本明細書に開示される抗体または抗原結合部分を含む。特定の一態様では、イムノコンジュゲートは、薬剤(例えば、治療剤として、または診断剤として)に連結している本明細書に開示される二重特異性分子を含む。
いる。
本開示はまた、本明細書に開示される結合性分子、例えば、本明細書に開示される抗体または結合性分子のいずれかをコードする核酸を提供する。一部の態様では、核酸は、本明細書に開示される抗体またはその抗原結合部分の重鎖および/または軽鎖可変領域、または本明細書に開示される二重特異性分子もしくは多重特異性分子(例えば、抗体)をコードする。本開示のポリヌクレオチドは、RNAの形態、またはDNAの形態をとることができる。DNAには、cDNA、ゲノムDNAおよび合成DNAが含まれる;および一本鎖がコード鎖または非コード(アンチセンス)鎖とすることができる場合、二本鎖または一本鎖とすることができる。ある種の態様では、DNAは、非天然組換え抗体を生成するために使用されるcDNAである。一部の態様では、RNAは、それを必要とする対象に投与した後、ここで開示されている結合性分子を発現することができるmRNAである。一部の態様では、mRNAの発現は、インビボとすることができる。mRNA発現はまた、インビトロまたはエクスビボとすることができる。一部の態様では、本明細書に開示
される結合性分子(例えば、抗FIX抗体、抗FX抗体または二重特異性抗FIX/抗FX抗体)をコードするmRNAは、化学的に修飾されて、例えば、修飾ヌクレオシド間連結基(例えば、ホスホロチオエート)、または修飾塩基(例えば、シュードウリジン、チオウリジンなど)を含むことができる。
ゴヌクレオチドは、一般的に、相補的集合体(complementary assembly)のための5’または3’突出部を含む。
、本明細書に開示される発現ベクター(単数または複数)で形質転換される。一部の態様では、細胞は、組換え発現のための宿主細胞である。例えば、一部の態様では、宿主細胞は、原核細胞、真核細胞、原生生物細胞、動物細胞、植物細胞、真菌細胞、酵母細胞、Sf9細胞、哺乳動物細胞、鳥類細胞、昆虫細胞、CHO細胞、HEK細胞またはCOS細胞である。原核生物には、グラム陰性またはグラム陽性生物、例えば、大腸菌または桿菌が含まれる。高等真核細胞には、哺乳動物起源の確立された細胞株が含まれる。細胞不含の翻訳系も使用することができる。細菌、真菌、酵母および哺乳動物細胞の宿主と使用するのに好適なクローニングおよび発現ベクターは、Pouwelsら(Cloning Vectors:A Laboratory Manual、Elsevier、N.Y.、1985年)により記載されており、この関連開示は、参照により本明細書に組み入れられる。抗体生成を含むタンパク質生成の方法に関する追加情報は、例えば、米国特許出願第2008/0187954号、米国特許第6,413,746号および同第6,660,501号、および国際特許出願WO04009823に見出すことができ、その各々の全体が参照により明細書に組み入れられる。
ルまたは他の脂肪族基を有するシリカゲルを使用する、1つまたはそれ以上の逆相高速液体クロマトグラフィー(RP-HPLC)工程を使用して、本明細書に開示される結合性分子またはその抗原結合部分をさらに精製することができる。上述の精製工程の一部またはすべてが、様々に組み合わされてさらに使用され、均一な組換えタンパク質を得ることができる。
本開示はまた、本明細書に開示される結合性分子、例えば抗体を製造する方法を提供する。一部の態様では、(i)抗FIX抗体またはその抗原結合部分、(ii)抗FX抗体またはその抗原結合部分、または(iii)本明細書に開示される二重特異性分子を生成する方法は、細胞において(例えば、宿主細胞において)、その抗体、その抗原結合部分または二重特異性分子を発現させる工程、および細胞からの抗体、その抗体結合部分または二重特異性分子を単離する工程を含む。
腫瘍としてインビボでのどちらかで増殖させることができる。次に、モノクローナル抗体は、上記のポリクローナル抗体に関して記載されている培養培地または腹水から精製することができる。
boomおよびWinter、J.Mol.Biol.227巻:381号(1991年)およびMarksら、J.Mol.Biol.222巻:581頁(1991年)に記載される、非相同性ファージタンパク質との融合タンパク質として、ヒト抗体またはその断片を発現する。抗体ファージライブラリーの生成および使用に関する技法はまた、そのそれぞれの全体が参照により組み入れられる、米国特許第5,969,108号、同第6,172,197、同第5,885,793号、同第6,521,404号;同第6,544,731号;同第6,555,313号;同第6,582,915号;同第6,593,081号;同第6,300,064号;同第6,653,068号;同第6,706,484号;および同第7,264,963号に記載される。
セイ)、「サンドイッチ」免疫アッセイ、免疫沈降アッセイ、沈降素反応、ゲル拡散沈降素反応、イムノ拡散アッセイ、凝集アッセイ、補体結合アッセイ、免疫放射定量アッセイ、蛍光免疫アッセイ、プロテインA免疫アッセイを含む。このようなアッセイは、決まった手順であり、当分野で周知である(例えば、その全体が参照により本明細書に組み入れられる、Ausubelら(編)、(1994年)Current Protocols
in Molecular Biology(John Wiley&Sons、Inc.、NY)、第1巻を参照されたい)。
Laboratory Press);Sambrookら、(編)(1992年)Molecular Cloning:A Laboratory Manual、(Cold Springs Harbor Laboratory、NY);D.N.Glover(編)(1985年)DNA Cloning、I巻およびII巻;Gait(編)(1984年)Oligonucleotide Synthesis;Mullisら、米国特許第4,683,195号;HamesおよびHiggins(編)(1984年)Nucleic Acid Hybridization;HamesおよびHiggins(編)(1984)Transcription And Translation;Freshney(1987年)Culture Of Animal Cells(Alan R.Liss,Inc.);Immobilized Cells And Enzymes(IRL Press)(1986年);Perbal(1984年)A Practical Guide To Molecular Cloning;the treatise、Methods In Enzymology(Academic Press,Inc.、N.Y.);MillerおよびCalos(編)(1987)Gene Transfer Vectors For Mammalian
Cells(Cold Spring Harbor Laboratory);Wuら(編)、Methods In Enzymology、154巻および155巻;MayerおよびWalker(編)(1987年)Immunochemical Methods In Cell And Molecular Biology(Academic Press、London);WeirおよびBlackwell(編)(1986年)Handbook Of Experimental Immunology、I~IV巻;Manipulating the Mouse Embryo、Cold Spring Harbor Laboratory Press、Cold Spring Harbor、N.Y.、(1986年);およびAusubelら(1989年)Current Protocols in Molecular Biolog
y(John Wiley and Sons、Baltimore、Md.)を参照されたい。
Engineering(第2版;Oxford Univ.Press)に説明されている。タンパク質操作の一般原理は、Rickwoodら(編)(1995年)Protein Engineering,A Practical Approach(IRL Press at Oxford Univ.Press、Oxford、Eng.)に説明されている。抗体および抗体-ハプテン結合の一般原理は、Nisonoff(1984年)Molecular Immunology(第2版;Sinauer Associates、Sunderland、Mass.);およびSteward(1984年)Antibodies,Their Structure and Function(Chapman and Hall、New York、N.Y.)に説明されている。さらに、当分野で公知であり、具体的に記載されていない免疫学における標準法は、一般に、Current Protocols in Immunology、John Wiley&Sons、New York;Stitesら(編)(1994年)Basic and Clinical Immunology(第8版;Appleton&Lange、Norwalk、Conn.)およびMishellおよびShiigi(編)(1980年)Selected Methods in Cellular Immunology(W.H.Freeman and Co.、NY)に従う。
Manual(Cold Spring Harbor Press);Lewin(2003年)Genes VIII(Prentice Hall 2003年);HarlowおよびLane(1988年)Antibodies:A Laboratory Manual(Cold Spring Harbor Press);DieffenbachおよびDveksler(2003年)PCR Primer(Cold Spring Harbor Press)が含まれる。
本開示はまた、例えば、(i)本明細書において開示されている抗体もしくはその抗原結合部分、本明細書において開示されている二重特異性分子(例えば、二重特異性抗体)、または本明細書において開示されているイムノコンジュゲート、および(ii)担体を
含む医薬組成物を提供する。
(1)以下からなる群から選択される、少なくとも1つの治療活性構成成分または診断活性構成成分、
(i)本明細書において開示されている結合性分子、例えば抗FIX抗体またはその抗原結合部分、抗FX抗体またはその抗原結合部分、抗FIX特異性および/または抗FX特異性を含む二重特異性分子;
(ii)それらの誘導体、例えば本明細書において開示されている結合性分子に所望の特性(例えば、血漿中半減期の延長)をもたらす、非相同性部分を有するイムノコンジュゲート、融合タンパク質または誘導体;
(iii)(i)の結合性分子をコードするポリヌクレオチドおよび/または(ii)の誘導体;
(iv)(iii)のポリヌクレオチドを含むベクター;
(v)(iii)のポリヌクレオチドまたは(iv)のベクターを含む細胞;または
(vi)それらの組合せ、および
(2)1つまたはそれ以上の担体、添加剤および/または賦形剤
を含む、医薬組成物(例えば、治療用または診断用組成物)を提供する。
どの多価糖アルコール、例えば三価またはそれより多価の糖アルコールを含む。
本開示はまた、本明細書において開示されている結合性分子(例えば、抗FIX抗体、抗FX抗体または二重特異性抗FIX/抗FX抗体)または本開示の他の組成物(例えば、核酸、ベクター、細胞)の使用を含む処置方法および診断方法を提供する。
一態様では、本明細書において開示されている結合性分子(例えば、抗FIX抗体、抗
FX抗体または二重特異性抗FIX/抗FX抗体)または本開示の他の組成物(例えば、核酸、ベクター、細胞)を使用して、凝固障害または出血性障害を予防、処置または反転させることができる。別の態様では、本方法は、それを必要とする対象に、本明細書において開示されている結合性分子(例えば、抗FIX抗体、抗FX抗体または二重特異性抗FIX/抗FX抗体)または本開示の他の組成物(例えば、核酸、ベクター、細胞)を投与する工程を含む。対象は、以下に限定されないが、ヒト、マウス、ラット、モルモット、以下に限定されないが、ウシ、ウマ、ヒツジ、ブタ、ヤギ、ネコ、イヌ、ハムスター、ロバなどの飼育動物などの哺乳動物とすることができる。一態様では、対象はヒトである。
FIX/抗FX抗体)または本開示の他の組成物(例えば、核酸、ベクター、細胞)は、血友病Aを有する、または血友病Aを有することが疑われ、1週間に1回、2回またはそれ超で、出血を経験した対象に投与することができる。
、生じる傾向を有する、および生じるリスクにある。一部の態様では、FVIIIに対する阻害剤は、FVIIIに対する中和抗体である。一部の態様では、対象は、FVIIIによる処置を受けているか、またはFVIII、例えばFVIII補充療法による処置の候補である。
本開示は、FIXおよびFXなどの、凝固因子の発現異常または欠陥を特徴とする疾患の診断に有用な診断的方法をさらに提供する。一部の態様では、診断は、個体からの組織
または体液中の、FIX(例えば、FIXa)および/またはFX(例えば、FXz)の発現レベルの測定、および測定された発現レベルと、正常組織または体液中のFIX(例えば、FIXa)および/またはFX(例えば、FXz)の標準発現レベルとを比較することを含み、それにより、標準品と比較した発現レベルの向上または低下が、障害の指標となる。
あって、クラスVにおける、抗FXz抗体またはその抗原結合部分を、好適な条件下、対象から得たサンプルに接触させる工程、およびこのサンプル中の抗FX抗体またはその抗原結合部分のFXzへの結合を測定する工程を含む、方法が提供される。他の実施形態では、クラスVIにおける抗FXa抗体またはその抗原結合部分を使用して、FIXチモーゲンと比較した、活性化FXのレベルを測定することができる。一部の態様では、サンプルは、血液または血清である。
本明細書において開示されている結合性分子(例えば、抗FIX抗体、抗FX抗体または二重特異性抗FIX/抗FX抗体)は、単独の活性剤として投与することができるか、または例えば、併用療法として様々な疾患の処置において有用な1つもしくはそれ以上の追加医薬または治療剤と組み合わせて投与することもできる。例えば、追加剤は、本明細書において提供される二重特異性抗体によって処置される、疾患または状態を処置するのに有用なものとして、当分野で認識されている治療剤とすることができる。この組合せ物はまた、1種超の追加剤、例えば、2種または3種の追加剤を含むことができる。
本開示はまた、本明細書に記載されている方法を行うために使用することができる、本明細書において開示されている結合性分子またはその抗原結合部分を含むキットを提供する。ある種の態様では、キットは、(i)本明細書において開示されている抗体、二重特異性分子、イムノコンジュゲート、医薬組成物、核酸(例えば、DNAまたはmRNA)、ベクターまたは細胞(例えば、宿主細胞)またはそれらの組合せ、および(ii)使用
のための指示書を含む。一部の態様では、キットは、1つまたはそれ以上の容器中に、本明細書において開示されている抗体、二重特異性分子、イムノコンジュゲート、医薬組成物、核酸(例えば、DNAまたはmRNA)、ベクターまたは細胞(例えば、宿主細胞)またはそれらの組合せを含む。
抗体選択および抗体生成の設計:ヒト活性化FIXに対する一連のヒト抗体は、ヒト抗体Adimab酵母ライブラリー(ADIMAB、7Lucent Drive、Lebanon、NH03766)から選択した。抗体選択は、3種の異なる第IX因子バリアントを使用して行った:
(i)その活性化を阻止し、チモーゲン形態(FIXz)中の第IX因子を維持する180位(成熟番号付け)において、アルギニンにアラニン変異もたらす第IX因子である、「活性化不能型FIX」(FIXnとしても略される);
(ii)活性化FIXの形態にあり、テナーゼ複合体中でFVIIIaに結合されていない場合、活性化FIXの立体構造にあると考えられる「遊離FIXa」;および
(iii)活性化FIXの最も活性な立体構造に擬似するよう意図されている、活性部位に共有結合している擬似基質(例えば、L-Glu-Gly-Argクロロメチルケトン、すなわち、EGR-CMK)との活性化FIXの形態にある「FIXa-SM」。
生成するため、カルシウムおよび30%エチレングリコールの存在下で、6時間、5倍モル濃度過剰のペプチドと共に遊離FIXaをインキュベートした。過剰ペプチドをサイズ排除クロマトグラフィーまたは透析のどちらか一方によって除去し、質量分析法により活性部位の飽和を確認した。
21巻(2号):163~170頁;BoderおよびWittrup(1997年)Nature Biotechnology 15巻(6号):553~557頁を参照されたい。
M CaCl2を含むまたは含まない緩衝液を用いて行った。特定の実験に関するさらなる詳細は、以下の実施例に示されている。特定の抗原に対する様々な抗体の相対的結合は、「応答」、または開始から結合期の終わりまでのナノメートルのシフト変化として一般に報告される。抗原結合応答は、ロード期の間にプローブにロードされた抗体の量に依存する。したがって、プローブにロードされた抗体の量が同じである場合、ならびに抗原の濃度および結合期の長さが同じである場合、これらの応答が比較可能となる。他の例では、ForteBioデータ解析ソフトウェアを使用して、KDを算出することができる。すべての場合において、抗ヒトIgG AHQプローブへの抗原の非特異的な結合の欠如が確認された。
クラスI:抗体は、遊離FIXaまたは活性化不能型FIXのどちらかと比べて、FIXa-SMに優先的に結合する。図9Aに示される通り、BIIB-9-460およびBIIB-9-484が、このクラスの例となる;
クラスII:抗体は、BIIB-9-885およびBIIB-9-416によって示される通り、FIXa-SMまたは活性化不能型FIXに対するよりも遊離FIXaに優先的に結合する(図9B);
クラスIII:抗体は、ほぼ等しくFIXa-SMまたは遊離FIXaのどちらかと結合
するが、活性化不能型FIXとほとんど結合しない。BIIB-9-1287は、このクラスの例として働く(図9C);および、
クラスIV:抗体は、遊離FIXaまたはFIXa-SMに比べて、活性化不能型FIXに優先的に結合する(図9D)。BIIB-9-397は、このクラスの例として働く。
抗体選別および抗体生成の設計:活性化第X因子(FXa)よりもFXチモーゲン(例えば、活性化不能型第X因子(FX))に選択的に結合する抗体を得る目的で、酵母Adimabヒト抗体ライブラリーからの抗体選別は、3つの異なる第X因子バリアントを使用して行った:
(i)その活性化を阻止し、チモーゲン形態にあるFXを維持する194位(成熟番号付け)において、アルギニンからアラニンへの変異を有するFXである、「活性化不能型第X因子」(「FXn」)。これは、BLI実験に使用したFXz(チモーゲンFX)であった。FXnを生成し、以下に記載されている通り、自家でビオチン化した。
(ii)いかなる擬似基質も含まない活性化FXの形態にあり、野生型の活性化FX立体構造(HTI、カタログ番号HCXA-0060)にあると考えられている「遊離FX」(「FXa」);
(iii)活性部位に共有結合した擬似基質(例えば、EGR-CMK)を有する活性化第X因子の形態にある「FXa-SM」(HTI、カタログHCXA-EGR)。一部の場合、擬似基質をビオチン化(BEGR-CMK)し、活性部位に共有結合させた(HTI、カタログ番号HCXA-BEGR)。
秒間、バイオセンサーをインキュベートした。次に、このバイオセンサーを、180秒間、代表的なIgG(TBSFCa中の200nM)を含有するウェルに移した。この後、バイオセンサーは、TBSFCa中で60秒間、インキュベートし、ベースラインを確立した。次に、このバイオセンサーを所望の抗原(TBSFCa中の200nM)を含有するウェルに移して、90秒間、結合を行った。最後に、90秒間のインキュベートを行うため、このセンサーをTBSFCa単独に移した。200nMのFXnまたはFXa-SMのどちらかに対する、結合期後の極大応答値(nm)を、選別で特定した94種の抗体の各々に関してプロットした。FXn特異性を指向する選別において特定された抗体はほとんどすべて、共有結合により修飾されたFXaに対してよりも、FXへの結合親和性が大きくなることを実証した(図13)。
2つの異なるFabのアームからなる二重特異性抗体であって、そのアームの1つが、FIXチモーゲンよりも活性化FIX(「FXa」)に優先的に結合し(クラスI、IIおよびIII抗体)、第2のアームは、FXa(クラスV抗体)よりもFXチモーゲンに優先的に結合している、上記の二重特異性抗体を実施例1および2に記載されている個々の抗体から生成した。FIXaよりもFIXチモーゲンに優先的に結合する第1のFabアーム(クラスIVの抗体)およびFXaよりもFXzに優先的に結合する(クラスVの抗体)、またはFXzよりもFXaに優先的に結合する(クラスVIの抗体)第2のFabからなる、さらなる二重特異性抗体を生成した。FIXzよりもFIXaに優先的に結合する(クラスI、IIおよびIIIの抗体)第1のFabアームおよびFXzよりもFXaに優先的に結合する(クラスVIの抗体)第2のFabアームからなる他の二重特異性抗体も生成した。
Immunology 67巻:95~106頁およびその中に引用されている参照文献;Byrneら(2013年)Trends in Biotechnology 31巻:621~632頁およびその中に引用されている参照文献;Stropら(2012年)J.Mol.Biol.420巻:204~219頁およびその中に引用されている参照文献を参照されたい;それらはすべて、その全体が参照によって本明細書に組み入れられる。同様に、上記は、その全体が参照によって本明細書に組み入れられることをやはり参照されたい。
発色アッセイにおける、FVIIIa活性を置き換えるおよび/または擬似することが可能な二重特異性抗体を、血漿中の一段階凝固アッセイにおけるFVIIIa様活性を置き換えるその能力についてさらに試験した。上に記載されている発色アッセイにおける最高の活性を示す二重特異性抗体のみをこの検討に選択した。
二重特異性活性が、抗体:抗原相互作用の操作により改善されるかどうかを決定するた
め、BIIB-9-484VHのCDR1およびCDR2領域を修飾して、生殖系配列にアミノ酸の多様性を導入した。次に、BIIB-9-484の106の配列誘導体のライブラリーを、Adimabプラットフォームに導入した。
アーム、または抗FIXaのアーム(BIIB-9-1335およびBIIB-9-1336)の親和成熟娘のどちらかと対を形成した、1つのこのような実施例を図23に示す(図23)。親抗FIXaのアームと比べて、親和性成熟抗FIXaのアームを含有する二重特異性抗体の凝固時間のさらなる低下は、抗FIXaのアームの親和性増大により、生じる二重特異性抗体の活性の増大がもたらされることを示す。
いくつかの活性アッセイを使用して、参照二重特異性抗体(bsAb)および本開示であるBS-027125の二重特異性抗体を組換えFVIII(rFVIII)と比較した。bsAb BS-027125はBIIB-9-1336およびBIIB-12-917を含む。参照二重特異性抗体は、ACE910/エミシズマブ(「エミシズマブバイオシミラー」)と同一の配列を有する;ACE910は、活性化第IX因子および第X因子に結合して、第VIII因子(FVIII)の補因子機能を擬似する組換えヒト化二重特異性抗体である。ACE910は、参照により本明細書に組み入れられる、米国特許第8,062,635号に開示されている。エミシズマブバイオシミラーおよびBS-027125は、図24Aおよび図24Bにそれぞれ図示されている。エミシズマブバイオシミラーは、第IX因子チモーゲン、第IXa因子、第X因子チモーゲンおよび第Xa因子の各々に、約1μMとなるKdで結合する(図24A)。BS-027125はまた、第IX因子チモーゲン(KD=8nM)、第IXa因子(KD=2nM)および第X因子チモーゲン(KD=20nM)に結合するが、第Xa因子には結合しない(図24B)。したがって、BS-027125は、エミシズマブバイオシミラーよりも、活性化第IX因子および/または第X因子チモーゲンに対して高い親和性および高い特異性を有する。
テナーゼ複合体の一部として、活性化第VIII因子(FVIIIa)は、細胞膜上の露出しているホスファチジルセリン(PS)に結合して、活性化第IXa因子および第X因子と集合する。FVIIIaは、PS(ホスファチジルセリン)およびホスファチジルエタノールアミン(PE)の両方を含有するリン脂質に優先的に結合することが示されている。ホスファチジルコリン(PC)リン脂質ベシクル中にホスファチジルエタノールアミン(PE)が存在すると、最適凝固因子活性に必要なPSの量が低下することを示す一方、PSおよびPCのみで構成されているベシクルは、最適活性化に一層高いレベルのPSを必要とする。最近、FVIIIaの擬似二重特異性抗体(エミシズマブ)は、阻害剤を有するおよびこれを有さない血友病A患者に対する潜在的処置として開発されたものである。FVIII擬似二重特異性抗体BS-027125は、エミシズマブよりも標的特
異性が改善している。リン脂質の組成がテンナーゼ活性に影響を及ぼすこと、および抗体が、リン脂質に直接、結合しないことを考慮すると、FVIIIa擬似抗体は、類似したリン脂質優先性を示すかどうか明確ではない。
Enzymol、2003年に記載されている通り、単層リン脂質ベシクルを押し出しにより製造した。試験した合成リン脂質のベシクルは、PS(ホスファチジルセリン)/PE(ホスファチジルエタノールアミン)/PC(ホスファチジルコリン)(20%/40%/40%)またはPS/PC(20%/80%)のいずれかからなった。
様々な対の抗FIXa抗体が固有の部位に結合しているかどうかを決定するため、本発明者らは、製造業者の指示書に従い、Octet HTX系におけるバイオレイヤー干渉法を使用して、ビニング実験を行った。手短に言えば、抗ヒトIgG定量(AHQ)ディップアンドリードバイオセンサー(Pall Fortebio:カタログ番号18-5005)をTBSFCa中で60秒間、平衡にした。続いて、第1の抗体(TBSFCa中で200nM)を180秒にわたり、バイオセンサーの先端にロードし、次いで、緩衝液単独中で60秒間、ベースライン工程を行った。
ること、およびそれらの抗体は、非競合的であることを示しており、これらの抗体は、同じビンに収まらなかったことを意味する(図31A)。しかし、シグナルのさらなる向上が観察されなかった場合、このことは、抗体1および抗体2が、同時に抗原に結合することができないことを示しており、したがってそれらの抗体は、競合的であると言われ、これらの抗体は、同じビンに収まったことを意味する(図31B)。
BIIB-9-484の固有のビニングプロファイルのために、本発明者らは、この抗体および親和性の成熟した娘BIIB-9-1336のさらなる特性を検討した。FIXaの場合を含む、多数の凝固因子の活性および結合特性が、カルシウム依存性であるので、本発明者らは、バイオレイヤー干渉法(BLI)を使用して、これらの2つの抗体が、カルシウムの存在または非存在によって影響を受けるかどうかを最初に試験した。
BIIB-9-1336が、FIXaの酵素機能に及ぼす効果を有するかどうか決定するため、本発明者らは、TBSCa中で5分間、250nMのFIXaと共に、様々な量の抗体をインキュベートした。続いて、ペプチド基質であるADG299を加えて、最終濃度を0.8mMにし、FIXaによる基質切断の速度を経時的なODの変化により測定した(図33A)。
よびネガティブ対照として抗FX抗体であるBIIB-12-917のアミド分解活性に影響を及ぼす能力があるかを試験した。BIIB-9-1336は、FIXaによる基質切断の速度を3倍、向上させることができた一方、BIIB-9-579およびBIIB-12-917は、影響を及ぼさなかった。
抗トロンビンIIIは、セリンプロテアーゼ阻害剤であり、ATIIIとFIXaの活性部位のセリンとの間の非可逆的結合の形成をもたらす。したがって、阻害の機構は、FIXa活性部位の反応性に依存する。BIIB-9-1336は、FIXaのアミド分解活性を増大することができるので、BIIB-9-1336はまた、ATIIIによってFIXa阻害の速度を向上させるはずであることは理にかなっている。これを試験するため、本発明者らは、1500nMのBIIB-9-1336、もしくはBIIB-9-484の親和性成熟の間に特定された別の抗FIXa抗体であるBIIB-9-1335の存在下または非存在下で、TBSCa中、5000nMのATIIIと共に500nMのFIXaをインキュベートした。サンプルは、1、30、60および120分間時に抜き取り、非還元性SDSローディング用緩衝液と混合し、4~20%のBioRadstain-freeゲル上で泳動させた(図34A)。
BIIB-9-484およびBIIB-9-1336とFIXaとの相互作用のさらなる本発明者らの理解のために、本発明者らは、これらの抗体の正確なエピトープを決定しようとした。これを行うため、本発明者らは、標準法を使用して、これらの抗体の各々のFab部分のみを最初に、クローニングして発現させて、精製した。続いて、本発明者らは、緩衝液を含有するカルシウム中で、各FabをFIXaと1.5:1のモル比で混合し、サイズ排除クロマトグラフィーを使用して、過剰のFabから得られた複合体を精製した。
本発明者らは、FX上のBIIB-12-917のエピトープは、BIIB-9-484またはBIIB-9-1336と対を形成すると、高いFVIIIa様活性で、生産性のある二重特異性抗体を形成するので、上記のBIIB-12-917のエピトープを特徴付けようとした。BLIを使用して、本発明者らは、野生型チモーゲンFX(FXz)、野生型活性化FX(FXa)、活性化ペプチドを維持する活性化FX(FXa+AP)、活性化ペプチドを欠如するチモーゲンFX(FX-AP)、およびFXに由来する活性化ペプチドを含むチモーゲンFIX(FIX+FX AP)を含めた、異なる組換えFXバリアントのパネルへのBIIB-12-917の結合を試験した。バリアントの概略図は、図38B中に示されている。
BIIB-9-484、BIIB-9-1336、BIIB-9-578またはBIIB-9-619から誘導される一連の抗体は、CDR H1およびCDR H2;またはCDR H3;またはCDR L1、CDR L2およびCDR L3;またはこれらの組合せにアミノ酸多様性を導入することにより生成した。FIXa特異性および/または親和性の向上した抗体は、実施例1および5に記載されている方法を使用して、これらの
ライブラリーから特定した。これらの抗体のVHおよびVLドメインの配列およびそれらのCDRの配列は、以下の表6および7に提示されている。
二重特異性抗体の前臨床薬物動態評価を、血友病Aのヒト化マウスモデルで行う。ヒトFIXおよびヒトFX遺伝子を、胚性幹細胞遺伝子標的を使用して、非相同性再結合により、個々のマウス遺伝子座位の各々に、個別にノックインする。続いて、ヒトFIXのノックインマウスのFVIII遺伝子を、CRISPR/Cas9技術により編集して、FVIII遺伝子ノックアウトを生成した。ヒトFIXノックインとヒトFXノックインとの間の品種交雑により、ヒトFIXとヒトFXの両方に対する同型接合マウス(FIX-X-KI)となるであろう。このマウスモデルは、下大静脈閉塞モデルまたは頸動脈塩化第二鉄損傷モデルなどの、血栓モデルを行うのに有用である。マウスFVIII遺伝子を欠如するヒトFIXノックインとヒトFXノックインとの間の品種交雑により、ヒトFIX、ヒトFXおよびFVIII欠乏の同型接合マウス(FIX-X-KI/FVIII-def)となるであろう。このマウスモデルは、尾部クリップモデルおよび尾静脈切断モデルなどの止血モデルを行うのに有用である。
二重特異性抗体の急性効能は、尾部クリップ出血モデルを用いて決定し、ここでは、尾部先端を切断し、ある範囲の量の二重特異性抗体、対照抗体、rFVIII、および/またはrFVIIaもしくはaPCCなどのバイパス治療を投与したFIX-X-KI/FVIII-defマウスからの全血液損失分を、既に記載されている通り測定する(Dumontら、2012年、Blood、119巻(13号):3024~3030頁)。二重特異性抗体の延長された効能は、既に記載した尾静脈切断モデルを用いて決定する(Panら、2009年、Blood、114巻(13号):2802~2811頁)で決定する。手短に言えば、FIX-FX-KI/FVIII-defマウスに、ある範囲の量の二重特異性抗体、対照抗体、rFVIII、および/またはrFVIIaまたはaPCCなどのバイパス治療を投与し、投与の24時間後に安楽死させて、尾部静脈の切開を施す。出血時間を記録し、マウスを最大24時間、ケージに戻し、この時点で、これらのマウスの再出血、総合的な応答、活性および生存率を評価する。
血栓症モデルを使用して、潜在的な血栓形成促進特性について二重特異性抗体を評価する。下大静脈閉塞モデル(Alemanら、2014年、J Clin Invest、124巻(8号):3590~3600頁)または頸動脈塩化第二鉄損傷モデル(Machlusら、2011年、Blood、117巻(18号):4953~4963頁)を行う。手短に言えば、下大静脈モデルの場合、FIX-FX-KIマウスを安楽死させ、これにrFVIIaまたはaPCCなどのある範囲の量の二重特異性抗体、対照抗体、rFVIIIおよび/またはバイパス治療を投与し、無菌開腹術を施し、下大静脈を完全に
ライゲーションする。24時間後、マウスを安楽死させて、血栓重量を測定する。頸動脈塩化第二鉄損傷モデルの場合、FIX-FX-KIマウスを安楽死させ、これにある範囲の量の二重特異性抗体、対照抗体、rFVIII、および/またはrFVIIaまたはaPCCなどのバイパス治療を投与する。頸動脈を10%の塩化第二鉄溶液で損傷させる。血流の変化をドップラー超音波法によりモニタリングし、頸動脈の閉塞時間を記録する。
カニクイザルにおける二重特異性抗体の薬物動態および薬力学評価も、記載されている通り行う(Dumontら、2015年、Thromb Res、136巻(6号):1266~1272頁)。手短に言えば、Mutoら、2014年、Blood、124巻(20号):3165~3171頁に記載されているように、後天性血友病Aモデルを開発する。血友病のサルに、ある範囲の量の二重特異性抗体、対照抗体、rFVIII、および/またはrFVIIaもしくはaPCCなどのバイパス治療を投与する。投与後のある範囲の時間点に、血液サンプルを採集する。ROTEM解析に血液の一部を使用するか、または他の活性をベースとするアッセイおよび残留血液を血漿に処理して、ELISAにより二重特異性抗体の循環レベルを決定する。
Claims (8)
- 活性化第IX因子(FIXa)に結合する単離された抗体またはその抗原結合部分であって、該抗FIXa抗体またはその抗原結合部分が、該抗FIXa抗体またはその抗原結合部分のFIXチモーゲン(FIXz)に対する結合親和性よりも高い結合親和性でFIXaに結合し、該抗FIXa抗体またはその抗原結合部分が重鎖可変領域(VH)および軽鎖可変領域(VL)を含み、該VHがVH CDR1、VH CDR2、およびVH CDR3を含み、該VLがVL CDR1、VL CDR2、およびVL CDR3を含み、該VH CDR1、VH CDR2、VH CDR3、VL CDR1、VL CDR2、およびVL CDR3がそれぞれ、(a1)配列番号800、845、890、935、980、および1025;(b1)配列番号801、846、891、936、981、および1026;(c1)配列番号802、847、892、937、982、および1027;(d1)配列番号803、848、893、938、983、および1028;(e1)配列番号804、849、894、939、984、および1029;(f1)配列番号805、850、895、940、985、および1030;(g1)配列番号806、851、896、941、986、および1031;(h1)配列番号807、852、897、942、987、および1032;(i1)配列番号808、853、898、943、988、および1033;(j1)配列番号810、855、900、945、990、および1035;(k1)配列番号812、857、902、947、992、および1037;(l1)配列番号813、858、903、948、993、および1038;(m1)配列番号814、859、904、949、994、および1039;(n1)配列番号816、861、906、951、996、および1041;(o1)配列番号817、862、907、952、997、および1042;(p1)配列番号818、863、908、953、998、および1043;(q1)配列番号819、864、909、954、999、および1044;(r1)配列番号820、865、910、955、1000、および1045;(s1)配列番号821、866、911、956、1001、および1046;(t1)配列番号823、868、913、958、1003、および1048;(u1)配列番号824、869、914、959、1004、および1049;(v1)配列番号825、870、915、960、1005、および1050;(w1)配列番号826、871、916、961、1006、および1051;(x1)配列番号827、872、917、962、100
7、および1052;(y1)配列番号828、873、918、963、1008、および1053;(z1)配列番号829、874、919、964、1009、および1054;(a2)配列番号830、875、920、965、1010、および1055;(b2)配列番号831、876、921、966、1011、および1056;(c2)配列番号832、877、922、967、1012、および1057;(d2)配列番号833、878、923、968、1013、および1058;(e2)配列番号834、879、924、969、1014、および1059;(f2)配列番号835、880、925、970、1015、および1060;(g2)配列番号836、881、926、971、1016、および1061;(h2)配列番号837、882、927、972、1017、および1062;(i2)配列番号838、883、928、973、1018、および1063;(j2)配列番号839、884、929、974、1019、および1064;(k2)配列番号840、885、930、975、1020、および1065;(l2)配列番号841、886、931、976、1021、および1066;(m2)配列番号842、887、932、977、1022、および1067;(n2)配列番号844、889、934、979、1024、および1069;(o2)配列番号1070、1074、1078、1082、1086、および1090;(p2)配列番号1071、1075、1079、1083、1087、および1091;(q2)配列番号1072、1076、1080、1084、1088、および1092;(r2)配列番号1073、1077、1081、1085、1089、および1093;(s2)配列番号1094、1136、1178、1220、1262、および1304;(t2)配列番号1095、1137、1179、1221、1263、および1305;(u2)配列番号1096、1138、1180、1222、1264、および1306;(v2)配列番号1097、1139、1181、1223、1265、および1307;(w2)配列番号1098、1140、1182、1224、1266、および1308;(x2)配列番号1099、1141、1183、1225、1267、および1309;(y2)配列番号1100、1142、1184、1226、1268、および1310;(z3)配列番号1101、1143、1185、1227、1269、および1311;(a3)配列番号1103、1145、1187、1229、1271、および1313;(b3)配列番号1104、1146、1188、1230、1272、および1314;(c3)配列番号1105、1147、1189、1231、1273、および1315;(d3)配列番号1106、1148、1190、1232、1274、および1316;(e3)配列番号1107、1149、1191、1233、1275、および1317;(f3)配列番号1109、1151、1193、1235、1277、および1319;(g3)配列番号1110、1152、1194、1236、1278、および1320;(h3)配列番号1111、1153、1195、1237、1279、および1321;(i3)配列番号1112、1154、1196、1238、1280、および1322;(j3)配列番号1113、1155、1197、1239、1281、および1323;(k3)配列番号1114、1156、1198、1240、1282、および1324;(l3)配列番号1115、1157、1199、1241、1283、および1325;(m3)配列番号1116、1158、1200、1242、1284、および1326;(n3)配列番号1117、1159、1201、1243、1285、および1327;(o3)配列番号1118、1160、1202、1244、1286、および1328;(p3)配列番号1119、1161、1203、1245、1287、および1329;(q3)配列番号1120、1162、1204、1246、1288、および1330;(r3)配列番号1121、1163、1205、1247、1289、および1331;(s3)配列番号1122、1164、1206、1248、1290、および1332;(t3)配列番号1123、1165、1207、1249、1291、および1333;(u3)配列番号1124、1166、1208、1250、1292、および1334;(v3)配列番号1125、1167、1209、1251、1293、および1335;(w3)
配列番号1126、1168、1210、1252、1294、および1336;(x3)配列番号1127、1169、1211、1253、1295、および1337;(y3)配列番号1128、1170、1212、1254、1296、および1338;(z3)配列番号1129、1171、1213、1255、1297、および1339;(a4)配列番号1130、1172、1214、1256、1298、および1340;(b4)配列番号1131、1173、1215、1257、1299、および1341;(c4)配列番号1132、1174、1216、1258、1300、および1342;(d4)配列番号1133、1175、1217、1259、1301、および1343;(e4)配列番号1134、1176、1218、1260、1302、および1344;または(f4)配列番号1135、1177、1219、1261、1303、および1345に示されるアミノ酸配列を含み、
(a1)のVHが配列番号1のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(b1)のVHが配列番号3のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(c1)のVHが配列番号5のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(d1)のVHが配列番号7のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(e1)のVHが配列番号9のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(f1)のVHが配列番号11のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(g1)のVHが配列番号13のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(h1)のVHが配列番号15のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(i1)のVHが配列番号17のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(j1)のVHが配列番号21のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(k1)のVHが配列番号25のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(l1)のVHが配列番号27のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(m1)のVHが配列番号29のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(n1)のVHが配列番号33のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(o1)のVHが配列番号35のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(p1)のVHが配列番号37のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(q1)のVHが配列番号39のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(r1)のVHが配列番号41のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(s1)のVHが配列番号43のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(t1)のVHが配列番号47のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(u1)のVHが配列番号49のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(v1)のVHが配列番号51のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(w1)のVHが配列番号53のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(x1)のVHが配列番号55のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(y1)のVHが配列番号57のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(z1)のVHが配列番号59のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(a2)のVHが配列番号61のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(b2)のVHが配列番号63のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(c2)のVHが配列番号65のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(d2)のVHが配列番号67のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(e2)のVHが配列番号69のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(f2)のVHが配列番号71のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(g2)のVHが配列番号73のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(h2)のVHが配列番号75のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(i2)のVHが配列番号77のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(j2)のVHが配列番号79のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(k2)のVHが配列番号81のア
ミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(l2)のVHが配列番号83のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(m2)のVHが配列番号85のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(n2)のVHが配列番号89のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(o2)のVHが配列番号91のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(p2)のVHが配列番号93のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(q2)のVHが配列番号95のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(r2)のVHが配列番号97のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(s2)のVHが配列番号99のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(t2)のVHが配列番号101のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(u2)のVHが配列番号103のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(v2)のVHが配列番号105のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(w2)のVHが配列番号107のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(x2)のVHが配列番号109のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(y2)のVHが配列番号111のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(z2)のVHが配列番号113のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(a3)のVHが配列番号117のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(b3)のVHが配列番号119のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(c3)のVHが配列番号121のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(d3)のVHが配列番号123のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(e3)のVHが配列番号125のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(f3)のVHが配列番号129のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(g3)のVHが配列番号131のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(h3)のVHが配列番号133のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(i3)のVHが配列番号135のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(j3)のVHが配列番号137のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(k3)のVHが配列番号139のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(l3)のVHが配列番号141のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(m3)のVHが配列番号143のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(n3)のVHが配列番号145のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(o3)のVHが配列番号147のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(p3)のVHが配列番号149のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(q3)のVHが配列番号151のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(r3)のVHが配列番号153のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(s3)のVHが配列番号155のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(t3)のVHが配列番号157のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(u3)のVHが配列番号159のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(v3)のVHが配列番号161のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(w3)のVHが配列番号163のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(x3)のVHが配列番号165のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(y3)のVHが配列番号167のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(z3)のVHが配列番号169のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(a4)のVHが配列番号171のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(b4)のVHが配列番号173のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(c4)のVHが配列番号175のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(d4)のVHが配列番号177のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(
e4)のVHが配列番号179のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、または(f4)のVHが配列番号181のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、前記抗体またはその抗原結合部分。 - 活性化第IX因子(FIXa)に結合する単離された抗体またはその抗原結合部分であって、該抗FIXa抗体またはその抗原結合部分が、該抗FIXa抗体またはその抗原結合部分のFIXチモーゲン(FIXz)に対する結合親和性よりも高い結合親和性でFIXaに結合し、該抗FIXa抗体またはその抗原結合部分が重鎖可変領域(VH)および軽鎖可変領域(VL)を含み、該VHがVH CDR1、VH CDR2、およびVH CDR3を含み、該VLがVL CDR1、VL CDR2、およびVL CDR3を含み、該VH CDR1、VH CDR2、VH CDR3、VL CDR1、VL CDR2、およびVL CDR3がそれぞれ、(a1)配列番号800、845、890、935、980、および1025;(b1)配列番号801、846、891、936、981、および1026;(c1)配列番号802、847、892、937、982、および1027;(d1)配列番号803、848、893、938、983、および1028;(e1)配列番号804、849、894、939、984、および1029;(f1)配列番号805、850、895、940、985、および1030;(g1)配列番号806、851、896、941、986、および1031;(h1)配列番号807、852、897、942、987、および1032;(i1)配列番号808、853、898、943、988、および1033;(j1)配列番号810、855、900、945、990、および1035;(k1)配列番号812、857、902、947、992、および1037;(l1)配列番号813、858、903、948、993、および1038;(m1)配列番号814、859、904、949、994、および1039;(n1)配列番号816、861、906、951、996、および1041;(o1)配列番号817、862、907、952、997、および1042;(p1)配列番号818、863、908、953、998、および1043;(q1)配列番号819、864、909、954、999、および1044;(r1)配列番号820、865、910、955、1000、および1045;(s1)配列番号821、866、911、956、1001、および1046;(t1)配列番号823、868、913、958、1003、および1048;(u1)配列番号824、869、914、959、1004、および1049;(v1)配列番号825、870、915、960、1005、および1050;(w1)配列番号826、871、916、961、1006、および1051;(x1)配列番号827、872、917、962、1007、および1052;(y1)配列番号828、873、918、963、1008、および1053;(z1)配列番号829、874、919、964、1009、および1054;(a2)配列番号830、875、920、965、1010、および1055;(b2)配列番号831、876、921、966、1011、および1056;(c2)配列番号832、877、922、967、1012、および1057;(d2)配列番号833、878、923、968、1013、および1058;(e2)配列番号834、879、924、969、1014、および1059;(f2)配列番号835、880、925、970、1015、および1060;(g2)配列番号836、881、926、971、1016、および1061;(h2)配列番号837、882、927、972、1017、および1062;(i2)配列番号838、883、928、973、1018、および1063;(j2)配列番号839、884、929、974、1019、および1064;(k2)配列番号840、885、930、975、1020、および1065;(l2)配列番号841、886、931、976、1021、および1066;(m2)配列番号842、887、932、977、1022、および1067;(n2)配列番号1070、1074、1078、1082、1086、および1090;(o2)配列番号1071、1075、1079、1083、1087、および1091;(p2)配列番号1072、1076、1080、1084、1088、
および1092;(q2)配列番号1073、1077、1081、1085、1089、および1093;(r2)配列番号1094、1136、1178、1220、1262、および1304;(s2)配列番号1095、1137、1179、1221、1263、および1305;(t2)配列番号1096、1138、1180、1222、1264、および1306;(u2)配列番号1097、1139、1181、1223、1265、および1307;(v2)配列番号1098、1140、1182、1224、1266、および1308;(w2)配列番号1099、1141、1183、1225、1267、および1309;(x2)配列番号1100、1142、1184、1226、1268、および1310;(y2)配列番号1101、1143、1185、1227、1269、および1311;(z2)配列番号1103、1145、1187、1229、1271、および1313;(a3)配列番号1104、1146、1188、1230、1272、および1314;(b3)配列番号1105、1147、1189、1231、1273、および1315;(c3)配列番号1106、1148、1190、1232、1274、および1316;(d3)配列番号1107、1149、1191、1233、1275、および1317;(e3)配列番号1109、1151、1193、1235、1277、および1319;(f3)配列番号1110、1152、1194、1236、1278、および1320;(g3)配列番号1111、1153、1195、1237、1279、および1321;(h3)配列番号1112、1154、1196、1238、1280、および1322;(i3)配列番号1113、1155、1197、1239、1281、および1323;(j3)配列番号1114、1156、1198、1240、1282、および1324;(k3)配列番号1115、1157、1199、1241、1283、および1325;(l3)配列番号1116、1158、1200、1242、1284、および1326;(m3)配列番号1117、1159、1201、1243、1285、および1327;(n3)配列番号1118、1160、1202、1244、1286、および1328;(o3)配列番号1119、1161、1203、1245、1287、および1329;(p3)配列番号1120、1162、1204、1246、1288、および1330;(q3)配列番号1121、1163、1205、1247、1289、および1331;(r3)配列番号1122、1164、1206、1248、1290、および1332;(s3)配列番号1123、1165、1207、1249、1291、および1333;(t3)配列番号1124、1166、1208、1250、1292、および1334;(u3)配列番号1125、1167、1209、1251、1293、および1335;(v3)配列番号1126、1168、1210、1252、1294、および1336;(w3)配列番号1127、1169、1211、1253、1295、および1337;(x3)配列番号1128、1170、1212、1254、1296、および1338;(y3)配列番号1129、1171、1213、1255、1297、および1339;(z3)配列番号1130、1172、1214、1256、1298、および1340;(a4)配列番号1131、1173、1215、1257、1299、および1341;(b4)配列番号1132、1174、1216、1258、1300、および1342;(c4)配列番号1133、1175、1217、1259、1301、および1343;(d4)配列番号1134、1176、1218、1260、1302、および1344;または(e4)配列番号1135、1177、1219、1261、1303、および1345
に示されるアミノ酸配列を含み、
(a1)のVLが配列番号191のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(b1)のVLが配列番号193のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(c1)のVLが配列番号195のアミノ酸配列と少なくとも
80%同一のアミノ酸配列を含む、(d1)のVLが配列番号197のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(e1)のVLが配列番号199のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(f1)のVLが配列番号201の
アミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(g1)のVLが配列番号203のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(h1)のVLが配列番号205のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(i1)のVLが配列番号207のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(j1)のVLが配列番号211のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(k1)のVLが配列番号215のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(l1)のVLが配列番号217のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(m1)のVLが配列番号219のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(n1)のVLが配列番号223のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(o1)のVLが配列番号225のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(p1)のVLが配列番号227のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(q1)のVLが配列番号229のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(r1)のVLが配列番号231のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(s1)のVLが配列番号233のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(t1)のVLが配列番号237のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(u1)のVLが配列番号239のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(v1)のVLが配列番号241のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(w1)のVLが配列番号243のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(x1)のVLが配列番号245のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(y1)のVLが配列番号247のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(z1)のVLが配列番号249のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(a2)のVLが配列番号251のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(b2)のVLが配列番号253のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(c2)のVLが配列番号255のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(d2)のVLが配列番号257のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(e2)のVLが配列番号259のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(f2)のVLが配列番号261のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(g2)のVLが配列番号263のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(h2)のVLが配列番号265のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(i2)のVLが配列番号267のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(j2)のVLが配列番号269のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(k2)のVLが配列番号271のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(l2)のVLが配列番号273のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(m2)のVLが配列番号275のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(n2)のVLが配列番号277のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(o2)のVLが配列番号279のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(p2)のVLが配列番号281のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(q2)のVLが配列番号283のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(r2)のVLが配列番号285のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(s2)のVLが配列番号287のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(t2)のVLが配列番号289のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(u2)のVLが配列番号291のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(v2)のVLが配列番号293のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(w2)のVLが配列番号295のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(x2)のVLが配列番号297のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(y2)のVLが配列番号299のアミノ酸配列と少なくとも80%同一のアミ
ノ酸配列を含む、(z2)のVLが配列番号303のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(a3)のVLが配列番号305のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(b3)のVLが配列番号307のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(c3)のVLが配列番号309のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(d3)のVLが配列番号311のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(e3)のVLが配列番号315のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(f3)のVLが配列番号317のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(g3)のVLが配列番号319のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(h3)のVLが配列番号321のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(i3)のVLが配列番号323のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(j3)のVLが配列番号325のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(k3)のVLが配列番号327のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(l3)のVLが配列番号329のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(m3)のVLが配列番号331のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(n3)のVLが配列番号333のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(o3)のVLが配列番号335のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(p3)のVLが配列番号337のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(q3)のVLが配列番号339のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(r3)のVLが配列番号341のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(s3)のVLが配列番号343のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(t3)のVLが配列番号345のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(u3)のVLが配列番号347のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(v3)のVLが配列番号349のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(w3)のVLが配列番号351のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(x3)のVLが配列番号353のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(y3)のVLが配列番号355のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(z3)のVLが配列番号357のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(a4)のVLが配列番号359のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(b4)のVLが配列番号361のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(c4)のVLが配列番号363のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(d4)のVLが配列番号365のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、または(e4)のVLが配列番号367のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、前記抗体またはその抗原結合部分。 - 請求項1または2に記載の抗体またはその抗原結合部分および第X因子チモーゲン(FXz)に結合する抗体またはその抗原結合部分(「抗FXz抗体またはその抗原結合部分」)を含む二重特異性分子であって、該抗FXz抗体またはその抗原結合部分がVHおよびVLを含み、該VHがVH CDR1、VH CDR2、およびVH CDR3を含み、該VLがVL CDR1、VL CDR2、およびVL CDR3を含み、該抗FXz抗体またはその抗原結合部分が、
(a)それぞれ、配列番号1370、1460、1550、1640、1730、および1820;
(b)それぞれ、配列番号1371、1461、1551、1641、1731、および1821;
(c)それぞれ、配列番号1372、1462、1552、1642、1732、および1822;
(d)それぞれ、配列番号1373、1463、1553、1643、1733、および
1823;
(e)それぞれ、配列番号1374、1464、1554、1644、1734、および1824;
(f)それぞれ、配列番号1375、1465、1555、1645、1735、および1825;
(g)それぞれ、配列番号1376、1466、1556、1646、1736、および1826;
(h)それぞれ、配列番号1377、1467、1557、1647、1737、および1827;
(i)それぞれ、配列番号1378、1468、1558、1648、1738、および1828;
(j)それぞれ、配列番号1379、1469、1559、1649、1739、および1829;
(k)それぞれ、配列番号1380、1470、1560、1650、1740、および1830;
(l)それぞれ、配列番号1381、1471、1561、1651、1741、および1831;
(m)それぞれ、配列番号1382、1472、1562、1652、1742、および1832;
(n)それぞれ、配列番号1383、1473、1563、1653、1743、および1833;
(o)それぞれ、配列番号1384、1474、1564、1654、1744、および1834;
(p)それぞれ、配列番号1385、1475、1565、1655、1745、および1835;
(q)それぞれ、配列番号1386、1476、1566、1656、1746、および1836;
(r)それぞれ、配列番号1387、1477、1567、1657、1747、および1837;
(s)それぞれ、配列番号1388、1478、1568、1658、1748、および1838;
(t)それぞれ、配列番号1389、1479、1569、1659、1749、および1839;
(u)それぞれ、配列番号1390、1480、1570、1660、1750、および1840;
(v)それぞれ、配列番号1391、1481、1571、1661、1751、および1841;
(w)それぞれ、配列番号1392、1482、1572、1662、1752、および1842;
(x)それぞれ、配列番号1393、1483、1573、1663、1753、および1843;
(y)それぞれ、配列番号1394、1484、1574、1664、1754、および1844;
(z)それぞれ、配列番号1395、1485、1575、1665、1755、および1845;
(aa)それぞれ、配列番号1396、1486、1576、1666、1756、および1846;
(bb)それぞれ、配列番号1397、1487、1577、1667、1757、および1847;
(cc)それぞれ、配列番号1398、1488、1578、1668、1758、およ
び1848;
(dd)それぞれ、配列番号1399、1489、1579、1669、1759、および1849;
(ee)それぞれ、配列番号1400、1490、1580、1670、1760、および1850;
(ff)それぞれ、配列番号1401、1491、1581、1671、1761、および1851;
(gg)それぞれ、配列番号1402、1492、1582、1672、1762、および1852;
(hh)それぞれ、配列番号1403、1493、1583、1673、1763、および1853;
(ii)それぞれ、配列番号1404、1494、1584、1674、1764、および1854;
(jj)それぞれ、配列番号1405、1495、1585、1675、1765、および1855;
(kk)それぞれ、配列番号1406、1496、1586、1676、1766、および1856;
(ll)それぞれ、配列番号1407、1497、1587、1677、1767、および1857;
(mm)それぞれ、配列番号1408、1498、1588、1678、1768、および1858;
(nn)それぞれ、配列番号1409、1499、1589、1679、1769、および1859;
(oo)それぞれ、配列番号1410、1500、1590、1680、1770、および1860;
(pp)それぞれ、配列番号1411、1501、1591、1681、1771、および1861;
(qq)それぞれ、配列番号1412、1502、1592、1682、1772、および1862;
(rr)それぞれ、配列番号1413、1503、1593、1683、1773、および1863;
(ss)それぞれ、配列番号1414、1504、1594、1684、1774、および1864;
(tt)それぞれ、配列番号1415、1505、1595、1685、1775、および1865;
(uu)それぞれ、配列番号1416、1506、1596、1686、1776、および1866;
(vv)それぞれ、配列番号1417、1507、1597、1687、1777、および1867;
(ww)それぞれ、配列番号1418、1508、1598、1688、1778、および1868;
(xx)それぞれ、配列番号1419、1509、1599、1689、1779、および1869;
(yy)それぞれ、配列番号1420、1510、1600、1690、1780、および1870;
(zz)それぞれ、配列番号1421、1511、1601、1691、1781、および1871;
(aaa)それぞれ、配列番号1422、1512、1602、1692、1782、および1872;
(bbb)それぞれ、配列番号1423、1513、1603、1693、1783、お
よび1873;
(ccc)それぞれ、配列番号1424、1514、1604、1694、1784、および1874;
(ddd)それぞれ、配列番号1425、1515、1605、1695、1785、および1875;
(eee)それぞれ、配列番号1426、1516、1606、1696、1786、および1876;
(fff)それぞれ、配列番号1427、1517、1607、1697、1787、および1877;
(ggg)それぞれ、配列番号1428、1518、1608、1698、1788、および1878;
(hhh)それぞれ、配列番号1429、1519、1609、1699、1789、および1879;
(iii)それぞれ、配列番号1430、1520、1610、1700、1790、および1880;
(jjj)それぞれ、配列番号1431、1521、1611、1701、1791、および1881;
(kkk)それぞれ、配列番号1432、1522、1612、1702、1792、および1882;
(lll)それぞれ、配列番号1433、1523、1613、1703、1793、および1883;
(mmm)それぞれ、配列番号1434、1524、1614、1704、1794、および1884;
(nnn)それぞれ、配列番号1435、1525、1615、1705、1795、および1885;
(ooo)それぞれ、配列番号1436、1526、1616、1706、1796、および1886;
(ppp)それぞれ、配列番号1437、1527、1617、1707、1797、および1887;
(qqq)それぞれ、配列番号1438、1528、1618、1708、1798、および1888;
(rrr)それぞれ、配列番号1439、1529、1619、1709、1799、および1889;
(sss)それぞれ、配列番号1440、1530、1620、1710、1800、および1890;
(ttt)それぞれ、配列番号1441、1531、1621、1711、1801、および1891;
(uuu)それぞれ、配列番号1442、1532、1622、1712、1802、および1892;
(vvv)それぞれ、配列番号1443、1533、1623、1713、1803、および1893;
(www)それぞれ、配列番号1444、1534、1624、1714、1804、および1894;
(xxx)それぞれ、配列番号1445、1535、1625、1715、1805、および1895;
(yyy)それぞれ、配列番号1446、1536、1626、1716、1806、および1896;
(zzz)それぞれ、配列番号1447、1537、1627、1717、1807、および1897;
(aaaa)それぞれ、配列番号1448、1538、1628、1718、1808、
および1898;
(bbbb)それぞれ、配列番号1449、1539、1629、1719、1809、および1899;
(cccc)それぞれ、配列番号1450、1540、1630、1720、1810、および1900;
(dddd)それぞれ、配列番号1451、1541、1631、1721、1811、および1901;
(eeee)それぞれ、配列番号1452、1542、1632、1722、1812、および1902;
(ffff)それぞれ、配列番号1453、1543、1633、1723、1813、および1903;
(gggg)それぞれ、配列番号1454、1544、1634、1724、1814、および1904;
(hhhh)それぞれ、配列番号1455、1545、1635、1725、1815、および1905;
(iiii)それぞれ、配列番号1456、1546、1636、1726、1816、および1906;
(jjjj)それぞれ、配列番号1457、1547、1637、1727、1817、および1907;
(kkkk)それぞれ、配列番号1458、1548、1638、1728、1818、および1908;または
(llll)それぞれ、配列番号1459、1549、1639、1729、1819、および1909
を含むVH CDR1、VH CDR2、VH CDR3、VL CDR1、VL CDR2、およびVL CDR3を含み、
(a)のVHが配列番号377のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(b)のVHが配列番号379のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(c)のVHが配列番号381のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(d)のVHが配列番号383のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(e)のVHが配列番号385のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(f)のVHが配列番号387のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(g)のVHが配列番号389のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(h)のVHが配列番号391のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(i)のVHが配列番号393のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(j)のVHが配列番号395のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(k)のVHが配列番号397のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(l)のVHが配列番号399のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(m)のVHが配列番号401のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(n)のVHが配列番号403のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(o)のVHが配列番号405のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(p)のVHが配列番号407のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(q)のVHが配列番号409のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(r)のVHが配列番号411のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(s)のVHが配列番号413のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(t)のVHが配列番号415のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(u)のVHが配列番号417のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(v)のVHが配列番号419のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(w)のVHが配列番号421のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(x)のVHが配列番
号423のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(y)のVHが配列番号425のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(z)のVHが配列番号427のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(aa)のVHが配列番号429のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(bb)のVHが配列番号431のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(cc)のVHが配列番号433のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(dd)のVHが配列番号435のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(ee)のVHが配列番号437のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(ff)のVHが配列番号439のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(gg)のVHが配列番号441のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(hh)のVHが配列番号443のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(ii)のVHが配列番号445のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(jj)のVHが配列番号447のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(kk)のVHが配列番号449のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(ll)のVHが配列番号451のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(mm)のVHが配列番号453のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(nn)のVHが配列番号455のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(oo)のVHが配列番号457のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(pp)のVHが配列番号459のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(qq)のVHが配列番号461のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(rr)のVHが配列番号463のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(ss)のVHが配列番号465のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(tt)のVHが配列番号467のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(uu)のVHが配列番号469のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(vv)のVHが配列番号471のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(ww)のVHが配列番号473のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(xx)のVHが配列番号475のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(yy)のVHが配列番号477のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(zz)のVHが配列番号479のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(aaa)のVHが配列番号481のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(bbb)のVHが配列番号483のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(ccc)のVHが配列番号485のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(ddd)のVHが配列番号487のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(eee)のVHが配列番号489のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(fff)のVHが配列番号491のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(ggg)のVHが配列番号493のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(hhh)のVHが配列番号495のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(iii)のVHが配列番号497のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(jjj)のVHが配列番号499のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(kkk)のVHが配列番号501のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(lll)のVHが配列番号503のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(mmm)のVHが配列番号505のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(nnn)のVHが配列番号507のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(ooo)のVHが配列番号509のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(ppp)のVHが配列番号511のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(qqq)のVHが配列番号513の
アミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(rrr)のVHが配列番号5115のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(sss)のVHが配列番号517のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(ttt)のVHが配列番号519のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(uuu)のVHが配列番号521のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(vvv)のVHが配列番号523のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(www)のVHが配列番号525のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(xxx)のVHが配列番号527のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(yyy)のVHが配列番号529のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(zzz)のVHが配列番号531のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(aaaa)のVHが配列番号533のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(bbbb)のVHが配列番号535のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(cccc)のVHが配列番号537のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(dddd)のVHが配列番号539のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(eeee)のVHが配列番号541のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(ffff)のVHが配列番号543のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(gggg)のVHが配列番号545のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(hhhh)のVHが配列番号547のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(iiii)のVHが配列番号549のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(jjjj)のVHが配列番号551のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(kkkk)のVHが配列番号553のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、または(llll)のVHが配列番号555のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、前記二重特異性分子。 - (a)のVLが配列番号565のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(b)のVLが配列番号567のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(c)のVLが配列番号569のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(d)のVLが配列番号571のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(e)のVLが配列番号573のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(f)のVLが配列番号575のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(g)のVLが配列番号577のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(h)のVLが配列番号579のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(i)のVLが配列番号581のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(j)のVLが配列番号583のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(k)のVLが配列番号585のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(l)のVLが配列番号587のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(m)のVLが配列番号589のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(n)のVLが配列番号591のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(o)のVLが配列番号593のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(p)のVLが配列番号595のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(q)のVLが配列番号597のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(r)のVLが配列番号599のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(s)のVLが配列番号601のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(t)のVLが配列番号603のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(u)のVLが配列番号605のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(v)のVLが配列番号607のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(w)のVLが配列番号60
9のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(x)のVLが配列番号611のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(y)のVLが配列番号613のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(z)のVLが配列番号615のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(aa)のVLが配列番号617のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(bb)のVLが配列番号619のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(cc)のVLが配列番号621のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(dd)のVLが配列番号623のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(ee)のVLが配列番号625のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(ff)のVLが配列番号627のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(gg)のVLが配列番号629のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(hh)のVLが配列番号631のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(ii)のVLが配列番号633のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(jj)のVLが配列番号635のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(kk)のVLが配列番号637のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(ll)のVLが配列番号639のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(mm)のVLが配列番号641のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(nn)のVLが配列番号643のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(oo)のVLが配列番号645のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(pp)のVLが配列番号647のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(qq)のVLが配列番号649のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(rr)のVLが配列番号651のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(ss)のVLが配列番号653のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(tt)のVLが配列番号655のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(uu)のVLが配列番号657のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(vv)のVLが配列番号659のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(ww)のVLが配列番号661のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(xx)のVLが配列番号663のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(yy)のVLが配列番号665のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(zz)のVLが配列番号667のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(aaa)のVLが配列番号669のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(bbb)のVLが配列番号671のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(ccc)のVLが配列番号673のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(ddd)のVLが配列番号675のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(eee)のVLが配列番号677のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(fff)のVLが配列番号679のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(ggg)のVLが配列番号681のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(hhh)のVLが配列番号683のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(iii)のVLが配列番号685のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(jjj)のVLが配列番号687のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(kkk)のVLが配列番号689のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(lll)のVLが配列番号691のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(mmm)のVLが配列番号693のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(nnn)のVLが配列番号695のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(ooo)のVLが配列番号697のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(ppp)のVLが配列番号699のアミノ酸配
列と少なくとも80%同一のアミノ酸配列を含む、(qqq)のVLが配列番号701のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(rrr)のVLが配列番号703のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(sss)のVLが配列番号705のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(ttt)のVLが配列番号707のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(uuu)のVLが配列番号709のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(vvv)のVLが配列番号711のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(www)のVLが配列番号713のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(xxx)のVLが配列番号715のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(yyy)のVLが配列番号717のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(zzz)のVLが配列番号719のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(aaaa)のVLが配列番号721のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(bbbb)のVLが配列番号723のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(cccc)のVLが配列番号725のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(dddd)のVLが配列番号727のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(eeee)のVLが配列番号729のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(ffff)のVLが配列番号731のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(gggg)のVLが配列番号733のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(hhhh)のVLが配列番号735のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(iiii)のVLが配列番号737のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(jjjj)のVLが配列番号739のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、(kkkk)のVLが配列番号741のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、または(llll)のVLが配列番号743のアミノ酸配列と少なくとも80%同一のアミノ酸配列を含む、請求項3に記載の二重特異性分子。 - 請求項1もしくは2に記載の抗体もしくはその抗原結合部分または請求項3もしくは4に記載の二重特異性分子をコードする、核酸。
- 請求項1もしくは2に記載の抗体もしくはその抗原結合部分または請求項3もしくは4に記載の二重特異性分子、および薬学的に許容される担体を含む、医薬組成物。
- 治療において使用するための、請求項1もしくは2に記載の抗体もしくはその抗原結合部分、請求項3もしくは4に記載の二重特異性分子、または請求項6に記載の医薬組成物。
- 血友病A患者を処置するのに使用するための、請求項3もしくは4に記載の二重特異性分子、または請求項6に記載の医薬組成物。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2025022258A JP2025081447A (ja) | 2016-11-23 | 2025-02-14 | 凝固第ix因子および凝固第x因子に結合する二重特異性抗体 |
Applications Claiming Priority (10)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201662425921P | 2016-11-23 | 2016-11-23 | |
| US62/425,921 | 2016-11-23 | ||
| US201762452809P | 2017-01-31 | 2017-01-31 | |
| US62/452,809 | 2017-01-31 | ||
| US201762529805P | 2017-07-07 | 2017-07-07 | |
| US62/529,805 | 2017-07-07 | ||
| US201762587284P | 2017-11-16 | 2017-11-16 | |
| US62/587,284 | 2017-11-16 | ||
| PCT/US2017/063135 WO2018098363A2 (en) | 2016-11-23 | 2017-11-22 | Bispecific antibodies binding to coagulation factor ix and coagulation factor x |
| JP2019547608A JP7227146B2 (ja) | 2016-11-23 | 2017-11-22 | 凝固第ix因子および凝固第x因子に結合する二重特異性抗体 |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2019547608A Division JP7227146B2 (ja) | 2016-11-23 | 2017-11-22 | 凝固第ix因子および凝固第x因子に結合する二重特異性抗体 |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2025022258A Division JP2025081447A (ja) | 2016-11-23 | 2025-02-14 | 凝固第ix因子および凝固第x因子に結合する二重特異性抗体 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2023058589A JP2023058589A (ja) | 2023-04-25 |
| JP7637166B2 true JP7637166B2 (ja) | 2025-02-27 |
Family
ID=60766147
Family Applications (3)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2019547608A Active JP7227146B2 (ja) | 2016-11-23 | 2017-11-22 | 凝固第ix因子および凝固第x因子に結合する二重特異性抗体 |
| JP2023017261A Active JP7637166B2 (ja) | 2016-11-23 | 2023-02-08 | 凝固第ix因子および凝固第x因子に結合する二重特異性抗体 |
| JP2025022258A Ceased JP2025081447A (ja) | 2016-11-23 | 2025-02-14 | 凝固第ix因子および凝固第x因子に結合する二重特異性抗体 |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2019547608A Active JP7227146B2 (ja) | 2016-11-23 | 2017-11-22 | 凝固第ix因子および凝固第x因子に結合する二重特異性抗体 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2025022258A Ceased JP2025081447A (ja) | 2016-11-23 | 2025-02-14 | 凝固第ix因子および凝固第x因子に結合する二重特異性抗体 |
Country Status (21)
| Country | Link |
|---|---|
| US (1) | US20230192896A1 (ja) |
| EP (1) | EP3545002A2 (ja) |
| JP (3) | JP7227146B2 (ja) |
| KR (1) | KR20190080949A (ja) |
| CN (1) | CN110662770A (ja) |
| AU (1) | AU2017363309A1 (ja) |
| BR (1) | BR112019010349A2 (ja) |
| CA (1) | CA3044574A1 (ja) |
| CL (1) | CL2019001372A1 (ja) |
| CO (1) | CO2019006500A2 (ja) |
| CR (1) | CR20190297A (ja) |
| DO (1) | DOP2019000127A (ja) |
| EC (1) | ECSP19044484A (ja) |
| IL (1) | IL266749A (ja) |
| MA (1) | MA46893A (ja) |
| MX (1) | MX2019005772A (ja) |
| PE (1) | PE20200012A1 (ja) |
| PH (1) | PH12019501126A1 (ja) |
| TN (1) | TN2019000164A1 (ja) |
| TW (1) | TW201819417A (ja) |
| WO (1) | WO2018098363A2 (ja) |
Families Citing this family (43)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| MA40835A (fr) | 2014-10-23 | 2017-08-29 | Biogen Ma Inc | Anticorps anti-gpiib/iiia et leurs utilisations |
| MA40861A (fr) * | 2014-10-31 | 2017-09-05 | Biogen Ma Inc | Anticorps anti-glycoprotéines iib/iiia |
| FR3038517B1 (fr) | 2015-07-06 | 2020-02-28 | Laboratoire Francais Du Fractionnement Et Des Biotechnologies | Utilisation de fragments fc modifies en immunotherapie |
| EP3577140A1 (en) | 2017-02-01 | 2019-12-11 | Novo Nordisk A/S | Procoagulant antibodies |
| GB201709970D0 (en) | 2017-06-22 | 2017-08-09 | Kymab Ltd | Bispecific antigen-binding molecules |
| EP3672990A1 (en) | 2017-08-25 | 2020-07-01 | Five Prime Therapeutics, Inc. | B7-h4 antibodies and methods of use thereof |
| AR113142A1 (es) * | 2017-09-29 | 2020-01-29 | Chugai Pharmaceutical Co Ltd | Moléculas de unión al antígeno multiespecíficas que tienen actividad de sustitución de la función de cofactor del factor viii de coagulación de sangre (fviii), y formulaciones farmacéuticas que contienen dicha molécula como ingrediente activo |
| US11787874B2 (en) | 2017-11-15 | 2023-10-17 | Novo Nordisk A/S | Factor X binders enhancing FX activation |
| JP2021514379A (ja) | 2018-02-21 | 2021-06-10 | ファイブ プライム セラピューティクス, インコーポレイテッド | B7−h4抗体製剤 |
| MA52416A (fr) | 2018-03-02 | 2021-04-21 | Five Prime Therapeutics Inc | Anticorps b7-h4 et leurs procédés d'utilisation |
| FR3082427B1 (fr) * | 2018-06-14 | 2020-09-25 | Lab Francais Du Fractionnement | Combinaison de facteur vii et d'un anticorps bispecifique anti-facteurs ix et x |
| JP2021530223A (ja) * | 2018-07-09 | 2021-11-11 | スロゼン, インコーポレイテッド | 組織特異性Wntシグナル増強分子及びその使用 |
| JP6761142B1 (ja) * | 2018-08-01 | 2020-09-23 | ノヴォ ノルディスク アー/エス | 改良された血液凝固促進抗体 |
| US11220554B2 (en) | 2018-09-07 | 2022-01-11 | Novo Nordisk A/S | Procoagulant antibodies |
| US12331110B2 (en) | 2018-09-05 | 2025-06-17 | The Board Of Regents Of The University Of Texas System | Monoclonal antibodies against endotrophin and the use thereof |
| WO2020115283A1 (en) * | 2018-12-07 | 2020-06-11 | Baxalta GmbH | Bispecific antibodies binding factor ixa and factor x |
| WO2020114614A1 (en) * | 2018-12-07 | 2020-06-11 | Baxalta GmbH | Proteinaceous molecules binding factor ixa and factor x |
| WO2020115281A1 (en) * | 2018-12-07 | 2020-06-11 | Baxalta GmbH | Proteinaceous molecules binding factor ixa and factor x |
| WO2020114615A1 (en) * | 2018-12-07 | 2020-06-11 | Baxalta GmbH | Bispecific antibodies binding factor ixa and factor x |
| BR112021011393A2 (pt) * | 2018-12-13 | 2021-08-31 | Surface Oncology, Inc. | Anticorpos anti-il-27 e usos dos mesmos |
| PL3723858T3 (pl) | 2018-12-21 | 2022-03-07 | Kymab Limited | Przeciwciało dwuswoiste fixaxfx o wspólnym łańcuchu lekkim |
| AU2020232691B2 (en) | 2019-03-05 | 2023-06-29 | Nkarta, Inc. | CD19-directed chimeric antigen receptors and uses thereof in immunotherapy |
| CN115052898B (zh) * | 2020-01-30 | 2025-09-16 | 诺和诺德股份有限公司 | 双特异性因子viii模拟抗体 |
| US11365239B2 (en) * | 2020-03-20 | 2022-06-21 | Tsb Therapeutics (Beijing) Co., Ltd. | Anti-SARS-COV-2 antibodies and uses thereof |
| JP2023106635A (ja) | 2020-04-17 | 2023-08-02 | 中外製薬株式会社 | 二重特異性抗原結合分子ならびに、それに関連する組成物、組成物の製造のための使用、キット、および方法 |
| WO2021231237A2 (en) * | 2020-05-11 | 2021-11-18 | Augmenta Bioworks, Inc. | Antibodies for sars-cov-2 and uses thereof |
| WO2021252804A1 (en) * | 2020-06-12 | 2021-12-16 | Nkarta, Inc. | Genetically modified natural killer cells for cd70-directed cancer immunotherapy |
| TW202233656A (zh) | 2020-11-16 | 2022-09-01 | 美商蘇羅森營運公司 | 肝特異性wnt訊號增強分子及其用途 |
| CA3214653A1 (en) * | 2021-04-09 | 2022-10-13 | Heyue Zhou | Antigen binding proteins that bind ror1 |
| WO2023111018A1 (en) * | 2021-12-17 | 2023-06-22 | F. Hoffmann-La Roche Ag | Antibodies against coagulation factor x and uses thereof |
| WO2023147574A2 (en) * | 2022-01-31 | 2023-08-03 | The Children's Hospital Of Philadelphia | Compositions and methods for treating factor ix deficiency |
| EP4522659A1 (en) * | 2022-05-12 | 2025-03-19 | Merck Sharp & Dohme LLC | Anti-integrin antibodies and uses thereof |
| AR129879A1 (es) | 2022-07-08 | 2024-10-09 | Novo Nordisk As | Compuestos de isvd altamente potentes capaces de sustituir al fviii(a) |
| CA3266237A1 (en) * | 2022-08-29 | 2024-03-07 | Invivyd, Inc. | Anti-SARS-CoV-2 antibodies and their uses |
| TW202432584A (zh) * | 2022-11-15 | 2024-08-16 | 美商嘉來克生命科學有限責任公司 | 抗papp-a抗體及其使用方法 |
| WO2024108158A1 (en) * | 2022-11-18 | 2024-05-23 | Byomass Inc. | Anti-activin a/b antibodies and uses thereof |
| CN116589588B (zh) * | 2023-04-14 | 2023-12-22 | 北京基科晟斯医药科技有限公司 | 结合凝血因子x的抗体 |
| WO2024216106A1 (en) * | 2023-04-14 | 2024-10-17 | Triveni Bio, Inc. | Dual inhibitor trypsin antibodies and uses thereof |
| WO2024233955A1 (en) * | 2023-05-11 | 2024-11-14 | Avantgen, Inc. | Agents that bind to cd16a and uses thereof |
| AU2024272787A1 (en) * | 2023-05-17 | 2025-11-20 | Adimab, Llc | Anti-cd28 antibodies and methods related thereto |
| WO2025076507A1 (en) * | 2023-10-06 | 2025-04-10 | The Children's Hospital Of Philadelphia | Engineered proteins and methods of use thereof |
| GB202316779D0 (en) * | 2023-11-01 | 2023-12-13 | Ucl Business Ltd | Antigen binding protein |
| CN121299112B (zh) * | 2024-09-12 | 2026-04-17 | 中国食品药品检定研究院 | 一种检测九型hpv疫苗或抗原原液体外相对效力的方法 |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2011137000A (ja) | 2003-10-10 | 2011-07-14 | Chugai Pharmaceut Co Ltd | 機能蛋白質を代替する二種特異性抗体 |
Family Cites Families (102)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4816567A (en) | 1983-04-08 | 1989-03-28 | Genentech, Inc. | Recombinant immunoglobin preparations |
| EP0154316B1 (en) | 1984-03-06 | 1989-09-13 | Takeda Chemical Industries, Ltd. | Chemically modified lymphokine and production thereof |
| US4683195A (en) | 1986-01-30 | 1987-07-28 | Cetus Corporation | Process for amplifying, detecting, and/or-cloning nucleic acid sequences |
| US6492107B1 (en) | 1986-11-20 | 2002-12-10 | Stuart Kauffman | Process for obtaining DNA, RNA, peptides, polypeptides, or protein, by recombinant DNA technique |
| GB2183661B (en) | 1985-03-30 | 1989-06-28 | Marc Ballivet | Method for obtaining dna, rna, peptides, polypeptides or proteins by means of a dna recombinant technique |
| ATE74164T1 (de) | 1985-04-22 | 1992-04-15 | Genetics Inst | Herstellung mit hoher leistung des aktivfaktors ix. |
| US4676980A (en) | 1985-09-23 | 1987-06-30 | The United States Of America As Represented By The Secretary Of The Department Of Health And Human Services | Target specific cross-linked heteroantibodies |
| US5618920A (en) | 1985-11-01 | 1997-04-08 | Xoma Corporation | Modular assembly of antibody genes, antibodies prepared thereby and use |
| DE3600905A1 (de) | 1986-01-15 | 1987-07-16 | Ant Nachrichtentech | Verfahren zum dekodieren von binaersignalen sowie viterbi-dekoder und anwendungen |
| US5681718A (en) | 1986-03-14 | 1997-10-28 | Celltech Limited | Methods for enhanced production of tissue plasminogen activator in cell culture using alkanoic acids or salts thereof |
| US5225539A (en) | 1986-03-27 | 1993-07-06 | Medical Research Council | Recombinant altered antibodies and methods of making altered antibodies |
| WO1988007089A1 (en) | 1987-03-18 | 1988-09-22 | Medical Research Council | Altered antibodies |
| US5677425A (en) | 1987-09-04 | 1997-10-14 | Celltech Therapeutics Limited | Recombinant antibody |
| EP0401384B1 (en) | 1988-12-22 | 1996-03-13 | Kirin-Amgen, Inc. | Chemically modified granulocyte colony stimulating factor |
| US5530101A (en) | 1988-12-28 | 1996-06-25 | Protein Design Labs, Inc. | Humanized immunoglobulins |
| CA2016842A1 (en) | 1989-05-16 | 1990-11-16 | Richard A. Lerner | Method for tapping the immunological repertoire |
| WO1990014443A1 (en) | 1989-05-16 | 1990-11-29 | Huse William D | Co-expression of heteromeric receptors |
| CA2016841C (en) | 1989-05-16 | 1999-09-21 | William D. Huse | A method for producing polymers having a preselected activity |
| GB9015198D0 (en) | 1990-07-10 | 1990-08-29 | Brien Caroline J O | Binding substance |
| US6172197B1 (en) | 1991-07-10 | 2001-01-09 | Medical Research Council | Methods for producing members of specific binding pairs |
| CA2405246A1 (en) | 1990-12-03 | 1992-06-11 | Genentech, Inc. | Enrichment method for variant proteins with alterred binding properties |
| WO1993008829A1 (en) | 1991-11-04 | 1993-05-13 | The Regents Of The University Of California | Compositions that mediate killing of hiv-infected cells |
| ES2341666T3 (es) | 1991-12-02 | 2010-06-24 | Medimmune Limited | Produccion de autoanticuerpos de repertorios de segmentos de anticue rpos expresados en la superficie de fagos. |
| EP1291360A1 (en) | 1991-12-13 | 2003-03-12 | Xoma Corporation | Methods and materials for preparation of modified antibody variable domains and therapeutic uses thereof |
| US5714350A (en) | 1992-03-09 | 1998-02-03 | Protein Design Labs, Inc. | Increasing antibody affinity by altering glycosylation in the immunoglobulin variable region |
| WO1993022332A2 (en) | 1992-04-24 | 1993-11-11 | Board Of Regents, The University Of Texas System | Recombinant production of immunoglobulin-like domains in prokaryotic cells |
| US5639641A (en) | 1992-09-09 | 1997-06-17 | Immunogen Inc. | Resurfacing of rodent antibodies |
| AU691811B2 (en) | 1993-06-16 | 1998-05-28 | Celltech Therapeutics Limited | Antibodies |
| US5681702A (en) | 1994-08-30 | 1997-10-28 | Chiron Corporation | Reduction of nonspecific hybridization by using novel base-pairing schemes |
| US5731168A (en) | 1995-03-01 | 1998-03-24 | Genentech, Inc. | Method for making heteromultimeric polypeptides |
| US5641870A (en) | 1995-04-20 | 1997-06-24 | Genentech, Inc. | Low pH hydrophobic interaction chromatography for antibody purification |
| US5869046A (en) | 1995-04-14 | 1999-02-09 | Genentech, Inc. | Altered polypeptides with increased half-life |
| US6121022A (en) | 1995-04-14 | 2000-09-19 | Genentech, Inc. | Altered polypeptides with increased half-life |
| US6096871A (en) | 1995-04-14 | 2000-08-01 | Genentech, Inc. | Polypeptides altered to contain an epitope from the Fc region of an IgG molecule for increased half-life |
| AU725609C (en) | 1995-08-18 | 2002-01-03 | Morphosys Ag | Protein/(poly)peptide libraries |
| US6696248B1 (en) | 1995-08-18 | 2004-02-24 | Morphosys Ag | Protein/(poly)peptide libraries |
| MA24512A1 (fr) * | 1996-01-17 | 1998-12-31 | Univ Vermont And State Agrienl | Procede pour la preparation d'agents anticoagulants utiles dans le traitement de la thrombose |
| JP4046354B2 (ja) | 1996-03-18 | 2008-02-13 | ボード オブ リージェンツ,ザ ユニバーシティ オブ テキサス システム | 増大した半減期を有する免疫グロブリン様ドメイン |
| US5714352A (en) | 1996-03-20 | 1998-02-03 | Xenotech Incorporated | Directed switch-mediated DNA recombination |
| US6277375B1 (en) | 1997-03-03 | 2001-08-21 | Board Of Regents, The University Of Texas System | Immunoglobulin-like domains with increased half-lives |
| WO1998052976A1 (en) | 1997-05-21 | 1998-11-26 | Biovation Limited | Method for the production of non-immunogenic proteins |
| US6194551B1 (en) | 1998-04-02 | 2001-02-27 | Genentech, Inc. | Polypeptide variants |
| ES2434961T5 (es) | 1998-04-20 | 2018-01-18 | Roche Glycart Ag | Ingeniería de glicosilación de anticuerpos para mejorar la citotoxicidad celular dependiente del anticuerpo |
| HU230769B1 (hu) | 1999-01-15 | 2018-03-28 | Genentech Inc. | Módosított effektor-funkciójú polipeptid-változatok |
| US6737056B1 (en) | 1999-01-15 | 2004-05-18 | Genentech, Inc. | Polypeptide variants with altered effector function |
| US6914128B1 (en) | 1999-03-25 | 2005-07-05 | Abbott Gmbh & Co. Kg | Human antibodies that bind human IL-12 and methods for producing |
| EP1176195B1 (en) | 1999-04-09 | 2013-05-22 | Kyowa Hakko Kirin Co., Ltd. | Method for controlling the activity of immunologically functional molecule |
| ATE482275T1 (de) | 1999-07-02 | 2010-10-15 | Morphosys Ag | Erzeugung spezifischer bindungspartner die an von genomischen dns-fragmenten oder ests kodierten (poly)peptiden binden |
| AT411997B (de) * | 1999-09-14 | 2004-08-26 | Baxter Ag | Faktor ix/faktor ixa aktivierende antikörper und antikörper-derivate |
| HUP0204475A2 (en) | 2000-02-11 | 2003-04-28 | Merck Patent Gmbh | Enhancing the circulating half-life of antibody-based fusion proteins |
| CN101289511A (zh) | 2000-04-11 | 2008-10-22 | 杰南技术公司 | 多价抗体及其应用 |
| US6725230B2 (en) | 2000-07-18 | 2004-04-20 | Aegis Analytical Corporation | System, method and computer program for assembling process data of multi-database origins using a hierarchical display |
| US7117096B2 (en) | 2001-04-17 | 2006-10-03 | Abmaxis, Inc. | Structure-based selection and affinity maturation of antibody library |
| HUP0600342A3 (en) | 2001-10-25 | 2011-03-28 | Genentech Inc | Glycoprotein compositions |
| US20040002587A1 (en) | 2002-02-20 | 2004-01-01 | Watkins Jeffry D. | Fc region variants |
| US20040132101A1 (en) | 2002-09-27 | 2004-07-08 | Xencor | Optimized Fc variants and methods for their generation |
| AU2003217912A1 (en) | 2002-03-01 | 2003-09-16 | Xencor | Antibody optimization |
| US7317091B2 (en) | 2002-03-01 | 2008-01-08 | Xencor, Inc. | Optimized Fc variants |
| SI1916001T1 (sl) * | 2002-03-04 | 2011-10-28 | Imclone Llc | Äśloveĺ ka protitelesa specifiäśna za kdr in njihova uporaba |
| US7538195B2 (en) | 2002-06-14 | 2009-05-26 | Immunogen Inc. | Anti-IGF-I receptor antibody |
| GB0216648D0 (en) | 2002-07-18 | 2002-08-28 | Lonza Biologics Plc | Method of expressing recombinant protein in CHO cells |
| EP1534335B9 (en) | 2002-08-14 | 2016-01-13 | Macrogenics, Inc. | Fcgammariib-specific antibodies and methods of use thereof |
| WO2004029207A2 (en) | 2002-09-27 | 2004-04-08 | Xencor Inc. | Optimized fc variants and methods for their generation |
| DE60334141D1 (de) | 2002-10-15 | 2010-10-21 | Facet Biotech Corp | VERÄNDERUNG VON FcRn-BINDUNGSAFFINITÄTEN ODER VON SERUMHALBWERTSZEITEN VON ANTIKÖRPERN MITTELS MUTAGENESE |
| BR0316101A (pt) | 2002-11-07 | 2005-09-27 | Immunogen Inc | Anticorpos anticd33 e processo para tratamento de leucemia melóide aguda usando os mesmos |
| JP2006524039A (ja) | 2003-01-09 | 2006-10-26 | マクロジェニクス,インコーポレーテッド | 変異型Fc領域を含む抗体の同定および作製ならびにその利用法 |
| US7297336B2 (en) * | 2003-09-12 | 2007-11-20 | Baxter International Inc. | Factor IXa specific antibodies displaying factor VIIIa like activity |
| US8101720B2 (en) | 2004-10-21 | 2012-01-24 | Xencor, Inc. | Immunoglobulin insertions, deletions and substitutions |
| AU2003271174A1 (en) * | 2003-10-10 | 2005-04-27 | Chugai Seiyaku Kabushiki Kaisha | Double specific antibodies substituting for functional protein |
| GB0324368D0 (en) | 2003-10-17 | 2003-11-19 | Univ Cambridge Tech | Polypeptides including modified constant regions |
| CA2552788C (en) | 2004-01-12 | 2013-09-24 | Applied Molecular Evolution, Inc. | Fc region variants |
| WO2005075514A2 (en) | 2004-03-10 | 2005-08-18 | Lonza Ltd. | Method for producing antibodies |
| EP1737890A2 (en) | 2004-03-24 | 2007-01-03 | Xencor, Inc. | Immunoglobulin variants outside the fc region |
| PL1776384T3 (pl) | 2004-08-04 | 2013-10-31 | Mentrik Biotech Llc | WARIANTY REGIONÓW Fc |
| US20080312425A1 (en) | 2004-08-30 | 2008-12-18 | Lonza Biologics Plc. | Ion Exchange Chromatography and Purification of Antibodies |
| EP3050963B1 (en) | 2005-03-31 | 2019-09-18 | Chugai Seiyaku Kabushiki Kaisha | Process for production of polypeptide by regulation of assembly |
| WO2007147901A1 (en) | 2006-06-22 | 2007-12-27 | Novo Nordisk A/S | Production of bispecific antibodies |
| US8236932B2 (en) * | 2007-01-03 | 2012-08-07 | Morphotek, Inc. | High affinity antibodies that neutralize Staphylococcus enterotoxin B |
| US7691980B2 (en) | 2007-01-09 | 2010-04-06 | Bio-Rad Laboratories, Inc. | Enhanced capacity and purification of antibodies by mixed mode chromatography in the presence of aqueous-soluble nonionic organic polymers |
| US7700734B2 (en) | 2007-01-09 | 2010-04-20 | Shu-Wha Lin | Recombinant human factor IX and use thereof |
| US8877688B2 (en) | 2007-09-14 | 2014-11-04 | Adimab, Llc | Rationally designed, synthetic antibody libraries and uses therefor |
| US8691730B2 (en) | 2007-09-14 | 2014-04-08 | Adimab, Llc | Rationally designed, synthetic antibody libraries and uses therefor |
| US9266967B2 (en) | 2007-12-21 | 2016-02-23 | Hoffmann-La Roche, Inc. | Bivalent, bispecific antibodies |
| US20090162359A1 (en) | 2007-12-21 | 2009-06-25 | Christian Klein | Bivalent, bispecific antibodies |
| US8227577B2 (en) | 2007-12-21 | 2012-07-24 | Hoffman-La Roche Inc. | Bivalent, bispecific antibodies |
| US8242247B2 (en) | 2007-12-21 | 2012-08-14 | Hoffmann-La Roche Inc. | Bivalent, bispecific antibodies |
| ES2563027T3 (es) | 2008-01-07 | 2016-03-10 | Amgen Inc. | Método para fabricación de moléculas heterodímeras Fc de anticuerpos utilizando efectos de conducción electrostática |
| EP2275431A3 (en) | 2008-01-18 | 2011-05-25 | Bio-Rad Laboratories, Inc. | Enhanced fractionation of phosphorylated and nonphosphorylated biomolecules by apatite chromotography |
| PE20120591A1 (es) | 2009-04-02 | 2012-05-23 | Roche Glycart Ag | Anticuerpos multiespecificos que comprenden anticuerpos de longitud completa y fragmentos fab de cadena sencilla |
| JP5616428B2 (ja) | 2009-04-07 | 2014-10-29 | ロシュ グリクアート アクチェンゲゼルシャフト | 三価の二重特異性抗体 |
| JP2012525149A (ja) | 2009-04-27 | 2012-10-22 | オンコメッド ファーマシューティカルズ インコーポレイテッド | ヘテロ多量体分子を作製するための方法 |
| TW201100543A (en) | 2009-05-27 | 2011-01-01 | Hoffmann La Roche | Tri-or tetraspecific antibodies |
| US9676845B2 (en) | 2009-06-16 | 2017-06-13 | Hoffmann-La Roche, Inc. | Bispecific antigen binding proteins |
| US8703132B2 (en) | 2009-06-18 | 2014-04-22 | Hoffmann-La Roche, Inc. | Bispecific, tetravalent antigen binding proteins |
| KR20120108967A (ko) | 2009-09-16 | 2012-10-05 | 제넨테크, 인크. | 코일드 코일 및/또는 테더 함유 단백질 복합체 및 그의 용도 |
| TW201138821A (en) | 2010-03-26 | 2011-11-16 | Roche Glycart Ag | Bispecific antibodies |
| CN102946906B (zh) | 2010-04-23 | 2015-07-15 | 弗·哈夫曼-拉罗切有限公司 | 生产异源多聚体蛋白质 |
| DK2593594T3 (en) | 2010-07-16 | 2017-12-11 | Adimab Llc | ANTIBODY LIBRARIES |
| PH12016502073B1 (en) * | 2010-11-17 | 2024-04-05 | Chugai Pharmaceutical Co Ltd | Multi-specific antigen-binding molecule having alternative function to function of blood coagulation factor viii |
| CN107266577B (zh) | 2011-10-11 | 2022-09-13 | 弗·哈夫曼-拉罗切有限公司 | 双特异性抗体的改进的组装 |
| WO2013119966A2 (en) | 2012-02-10 | 2013-08-15 | Genentech, Inc. | Single-chain antibodies and other heteromultimers |
| CA2978038A1 (en) * | 2015-04-17 | 2016-10-20 | F. Hoffmann-La Roche Ag | Combination therapy with coagulation factors and multispecific antibodies |
-
2017
- 2017-11-22 US US16/462,878 patent/US20230192896A1/en not_active Abandoned
- 2017-11-22 KR KR1020197017712A patent/KR20190080949A/ko not_active Withdrawn
- 2017-11-22 CA CA3044574A patent/CA3044574A1/en not_active Abandoned
- 2017-11-22 PE PE2019001058A patent/PE20200012A1/es unknown
- 2017-11-22 WO PCT/US2017/063135 patent/WO2018098363A2/en not_active Ceased
- 2017-11-22 AU AU2017363309A patent/AU2017363309A1/en not_active Abandoned
- 2017-11-22 MA MA046893A patent/MA46893A/fr unknown
- 2017-11-22 JP JP2019547608A patent/JP7227146B2/ja active Active
- 2017-11-22 EP EP17817962.8A patent/EP3545002A2/en active Pending
- 2017-11-22 BR BR112019010349A patent/BR112019010349A2/pt not_active Application Discontinuation
- 2017-11-22 CR CR20190297A patent/CR20190297A/es unknown
- 2017-11-22 CN CN201780084392.6A patent/CN110662770A/zh active Pending
- 2017-11-22 MX MX2019005772A patent/MX2019005772A/es unknown
- 2017-11-22 TN TNP/2019/000164A patent/TN2019000164A1/en unknown
- 2017-11-23 TW TW106140758A patent/TW201819417A/zh unknown
-
2019
- 2019-05-20 CL CL2019001372A patent/CL2019001372A1/es unknown
- 2019-05-20 IL IL266749A patent/IL266749A/en unknown
- 2019-05-21 DO DO2019000127A patent/DOP2019000127A/es unknown
- 2019-05-21 PH PH12019501126A patent/PH12019501126A1/en unknown
- 2019-06-20 CO CONC2019/0006500A patent/CO2019006500A2/es unknown
- 2019-06-21 EC ECSENADI201944484A patent/ECSP19044484A/es unknown
-
2023
- 2023-02-08 JP JP2023017261A patent/JP7637166B2/ja active Active
-
2025
- 2025-02-14 JP JP2025022258A patent/JP2025081447A/ja not_active Ceased
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2011137000A (ja) | 2003-10-10 | 2011-07-14 | Chugai Pharmaceut Co Ltd | 機能蛋白質を代替する二種特異性抗体 |
Non-Patent Citations (1)
| Title |
|---|
| NATURE MEDICINE, 2012, Vol.18, No.10, p.1570-1574 |
Also Published As
| Publication number | Publication date |
|---|---|
| JP2019535325A (ja) | 2019-12-12 |
| ECSP19044484A (es) | 2019-08-30 |
| DOP2019000127A (es) | 2019-10-15 |
| MA46893A (fr) | 2019-10-02 |
| PH12019501126A1 (en) | 2019-08-19 |
| EP3545002A2 (en) | 2019-10-02 |
| US20230192896A1 (en) | 2023-06-22 |
| JP7227146B2 (ja) | 2023-02-21 |
| PE20200012A1 (es) | 2020-01-06 |
| JP2025081447A (ja) | 2025-05-27 |
| MX2019005772A (es) | 2019-10-02 |
| KR20190080949A (ko) | 2019-07-08 |
| CL2019001372A1 (es) | 2019-11-04 |
| CR20190297A (es) | 2019-11-01 |
| CA3044574A1 (en) | 2018-05-31 |
| CO2019006500A2 (es) | 2019-06-28 |
| TW201819417A (zh) | 2018-06-01 |
| WO2018098363A3 (en) | 2018-09-20 |
| BR112019010349A2 (pt) | 2019-10-08 |
| AU2017363309A1 (en) | 2019-07-11 |
| JP2023058589A (ja) | 2023-04-25 |
| CN110662770A (zh) | 2020-01-07 |
| TN2019000164A1 (en) | 2020-10-05 |
| IL266749A (en) | 2019-07-31 |
| WO2018098363A2 (en) | 2018-05-31 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7637166B2 (ja) | 凝固第ix因子および凝固第x因子に結合する二重特異性抗体 | |
| JP7807367B2 (ja) | 抗klk7抗体、抗klk5抗体、多重特異性抗klk5/klk7抗体および使用方法 | |
| ES2778498T3 (es) | Anticuerpos anti-tau(pS422) humanizados y procedimientos de uso | |
| US20230383008A1 (en) | ANTI-HtrA1 ANTIBODIES AND METHODS OF USE THEREOF | |
| TW201835107A (zh) | 促凝血抗體 | |
| JP2022529036A (ja) | 二重特異性抗体 | |
| JP7829547B2 (ja) | 抗Notch2抗体及び使用方法 | |
| JP2024512377A (ja) | 抗klk7抗体、抗klk5抗体、多重特異性抗klk5/klk7抗体、及び使用方法 | |
| JP2016537965A (ja) | Nsp4阻害剤及び使用方法 | |
| KR20260028190A (ko) | 칼리크레인 항체 및 이의 용도 | |
| TW202517673A (zh) | 與C3bBb結合之抗體 | |
| IL323628A (en) | Anti-alpha v beta 8 integrin antibodies and methods of use | |
| CN121175339A (zh) | 抗fxi抗体及其用途 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20230309 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20230309 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20240123 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20240423 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20240508 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20240730 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20241023 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20241217 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20250114 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20250214 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7637166 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |