JP7601758B2 - Mta依存的に抗原に対する結合活性が変化する抗原結合ドメインを含む抗原結合分子及び当該抗原結合ドメイン取得用ライブラリ - Google Patents
Mta依存的に抗原に対する結合活性が変化する抗原結合ドメインを含む抗原結合分子及び当該抗原結合ドメイン取得用ライブラリ Download PDFInfo
- Publication number
- JP7601758B2 JP7601758B2 JP2021507411A JP2021507411A JP7601758B2 JP 7601758 B2 JP7601758 B2 JP 7601758B2 JP 2021507411 A JP2021507411 A JP 2021507411A JP 2021507411 A JP2021507411 A JP 2021507411A JP 7601758 B2 JP7601758 B2 JP 7601758B2
- Authority
- JP
- Japan
- Prior art keywords
- antigen
- binding
- mta
- antibody
- binding domain
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/10—Processes for the isolation, preparation or purification of DNA or RNA
- C12N15/1034—Isolating an individual clone by screening libraries
- C12N15/1037—Screening libraries presented on the surface of microorganisms, e.g. phage display, E. coli display
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/005—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies constructed by phage libraries
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/24—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against cytokines, lymphokines or interferons
- C07K16/244—Interleukins [IL]
- C07K16/248—IL-6
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2803—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily
- C07K16/2818—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily against CD28 or CD152
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2866—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against receptors for cytokines, lymphokines, interferons
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/42—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against immunoglobulins
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/44—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material not provided for elsewhere, e.g. haptens, metals, DNA, RNA, amino acids
-
- C—CHEMISTRY; METALLURGY
- C40—COMBINATORIAL TECHNOLOGY
- C40B—COMBINATORIAL CHEMISTRY; LIBRARIES, e.g. CHEMICAL LIBRARIES
- C40B40/00—Libraries per se, e.g. arrays, mixtures
- C40B40/04—Libraries containing only organic compounds
- C40B40/06—Libraries containing nucleotides or polynucleotides, or derivatives thereof
- C40B40/08—Libraries containing RNA or DNA which encodes proteins, e.g. gene libraries
-
- C—CHEMISTRY; METALLURGY
- C40—COMBINATORIAL TECHNOLOGY
- C40B—COMBINATORIAL CHEMISTRY; LIBRARIES, e.g. CHEMICAL LIBRARIES
- C40B40/00—Libraries per se, e.g. arrays, mixtures
- C40B40/04—Libraries containing only organic compounds
- C40B40/10—Libraries containing peptides or polypeptides, or derivatives thereof
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/68—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids
- G01N33/6803—General methods of protein analysis not limited to specific proteins or families of proteins
- G01N33/6845—Methods of identifying protein-protein interactions in protein mixtures
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/68—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids
- G01N33/6854—Immunoglobulins
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/21—Immunoglobulins specific features characterized by taxonomic origin from primates, e.g. man
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/24—Immunoglobulins specific features characterized by taxonomic origin containing regions, domains or residues from different species, e.g. chimeric, humanized or veneered
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/31—Immunoglobulins specific features characterized by aspects of specificity or valency multispecific
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/55—Fab or Fab'
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/92—Affinity (KD), association rate (Ka), dissociation rate (Kd) or EC50 value
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2500/00—Screening for compounds of potential therapeutic value
- G01N2500/02—Screening involving studying the effect of compounds C on the interaction between interacting molecules A and B (e.g. A = enzyme and B = substrate for A, or A = receptor and B = ligand for the receptor)
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Organic Chemistry (AREA)
- Immunology (AREA)
- Molecular Biology (AREA)
- Biochemistry (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Genetics & Genomics (AREA)
- Engineering & Computer Science (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Biophysics (AREA)
- Biomedical Technology (AREA)
- Urology & Nephrology (AREA)
- Hematology (AREA)
- Physics & Mathematics (AREA)
- Biotechnology (AREA)
- General Chemical & Material Sciences (AREA)
- Microbiology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Pathology (AREA)
- General Physics & Mathematics (AREA)
- Analytical Chemistry (AREA)
- Food Science & Technology (AREA)
- Cell Biology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Virology (AREA)
- Wood Science & Technology (AREA)
- Zoology (AREA)
- General Engineering & Computer Science (AREA)
- Pharmacology & Pharmacy (AREA)
- Bioinformatics & Computational Biology (AREA)
- Plant Pathology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Crystallography & Structural Chemistry (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Peptides Or Proteins (AREA)
Description
さらに、本発明者らは、MTA自体に対して特異的に結合する抗原結合分子の取得にも成功した。
[A1] 5’-Methylthioadenosine(MTA)依存的に抗原に対する結合活性が 変化する抗原結合ドメインを含む抗原結合分子。
[A2] 前記抗原結合ドメインのMTA存在下における前記抗原に対する結合活性がMTA非存在下における前記抗原に対する結合活性と異なる、抗原結合分子。
[A3] [A1]または[A2]に記載の抗原結合分子であって、当該抗原結合分子に含まれる抗原結合ドメインの前記抗原に対する結合活性はアデノシンに実質的に影響されない、抗原結合分子。
[A4] [A1]から[A3]に記載の抗原結合分子であって、当該抗原結合分子に含まれる抗原結合ドメインの前記抗原に対する結合活性はS-(5'-Adenosyl)-L-homocysteine (SAH)に実質的に影響されない、抗原結合分子。
[A5] [A1]から[A4]に記載の抗原結合分子であって、当該抗原結合分子に含まれる抗原結合ドメインの前記抗原に対する結合活性はAMP、ADPまたはATPに実質的に影響されない、抗原結合分子。
[A6] [A1]または[A2]に記載の抗原結合分子であって、当該抗原結合分子に含まれる抗原結合ドメインの前記抗原に対する結合活性はアデノシンに対しても依存的に変化する、抗原結合分子。
[A7] [A1]、[A2]または[A6]に記載の抗原結合分子であって、当該抗原結合分子に含まれる抗原結合ドメインの前記抗原に対する結合活性はS-(5'-Adenosyl)-L-homocysteine (SAH)に対しても依存的に変化する、抗原結合分子。
[A8] [A1]、[A2]、[A6]または[A7]に記載の抗原結合分子であって、当該抗原結合分子に含まれる抗原結合ドメインの前記抗原に対する結合活性はAMP、ADPおよび/または ATPに対しても依存的に変化する、抗原結合分子。
[A9] 前記抗原結合ドメインは抗体可変領域または/及び単ドメイン抗体を含む、[A1]から[A8]のいずれか一つに記載の抗原結合分子。
[A10] 前記抗原結合分子が抗体である、[A1]から[A9]のいずれか一つに記載の抗原結合分子。
[A11] 抗体Fc領域を含む[A1]から[A10]のいずれか一つに記載の抗原結合分子。
[A12] 前記抗体Fc領域が天然型Fc領域または改変Fc領域である、[A11]に記載の抗原結合分子。
[A13] 前記抗原結合ドメインのMTA存在下における抗原に対する結合活性が、前記抗原結合ドメインのMTA非存在下における抗原に対する結合活性より強い、[A1]から[A12]のいずれか一つに記載の抗原結合分子。
[A14] 前記抗原結合ドメインのMTA存在下における抗原に対する結合活性が、前記抗原結合ドメインのMTA非存在下における抗原に対する結合活性より弱い、[A1]から[A12]のいずれか一つに記載の抗原結合分子。
[A15] 前記抗原結合ドメインはMTAと相互作用するアミノ酸残基を有する、[A1]から[A14]いずれか一つに記載の抗原結合分子。
[A16] 前記MTAと相互作用するアミノ酸残基は、前記抗原結合ドメインの抗原と結合している状態においてMTAと相互作用する、[A15]に記載の抗原結合分子。
[A17] 前記抗原結合ドメインは抗体可変領域または単ドメイン抗体を含んでおり、前記MTAと相互作用するアミノ酸残基は前記抗体可変領域または前記単ドメイン抗体のCDR中に位置する、[A15]または[A16]に記載の抗原結合分子。
[A18] 前記抗原結合ドメインは抗体可変領域であり、前記MTAと相互作用するアミノ酸残基は、前記抗体可変領域のアミノ酸配列の内、Kabatナンバリングで特定される重鎖34位、35a位、47位、52位、52e位、101位、軽鎖32位、34位、36位、46位、49位、50位、89位、90位、91位及び96位のアミノ酸部位の群から選択される少なくとも一つ以上のアミノ酸部位に位置するアミノ酸残基である、[A15]から[A17]のいずれか一つに記載の抗原結合分子。
[A19] 前記抗原結合ドメインは抗体可変領域であり、当該抗体可変領域は重鎖W34、C35a、W47、F52、Y52e、E101、軽鎖R32、S34、Y36、L46、Y49、S50、A89、G90、L91、及びP96(Kabatナンバリング)から選択される少なくとも一つ以上のアミノ酸を含む [A15]から[A18]のいずれか一つに記載の抗原結合分子。
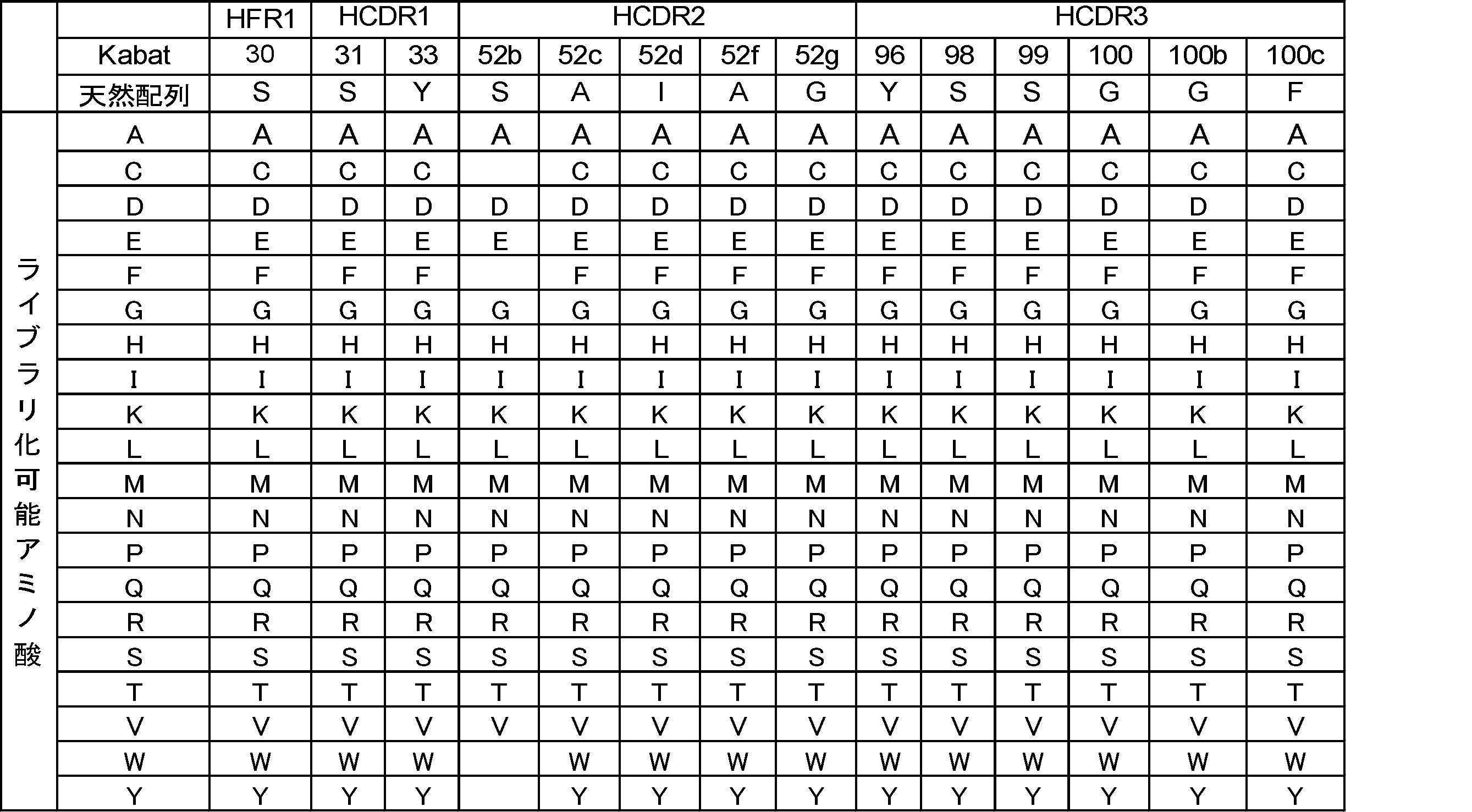
[A20] 前記抗原結合ドメインは抗体可変領域であり、当該抗体可変領域は下記アミノ酸の群から選択される少なくとも一つ以上のアミノ酸を含む、[A1]から[A19]のいずれか一つに記載の抗原結合分子(Kabatナンバリング):
重鎖30位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖31位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖32位に位置するA;
重鎖33位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖34位に位置するW;
重鎖35位に位置するM;
重鎖35a位に位置するC;
重鎖50位に位置するC;
重鎖51位に位置するI;
重鎖52位に位置するF;
重鎖52a位に位置するA;
重鎖52b位に位置するA、D、E、G、H、I、K、L、M、N、P、Q、R、S、TまたはVのいずれか;
重鎖52c位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖52d位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖52e位に位置するY;
重鎖52f位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖52g位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖53位に位置するS;
重鎖54位に位置するG;
重鎖55位に位置するG;
重鎖56位に位置するS;
重鎖57位に位置するT;
重鎖58位に位置するY;
重鎖59位に位置するY;
重鎖60位に位置するA;
重鎖61位に位置するS;
重鎖62位に位置するW;
重鎖63位に位置するA;
重鎖64位に位置するK;
重鎖65位に位置するG;
重鎖95位に位置するG;
重鎖96位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖97位に位置するG;
重鎖98位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖99位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖100位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖100a位に位置するG;
重鎖100b位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖100c位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖101位に位置するE;
重鎖102位に位置するL;
軽鎖24位に位置するQ;
軽鎖25位に位置するS;
軽鎖26位に位置するS;
軽鎖27位に位置するE;
軽鎖27a位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖28位に位置するV;
軽鎖29位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖30位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖31位に位置するA、D、E、G、H、I、K、L、M、N、P、Q、R、S、TまたはVのいずれか;
軽鎖32位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖33位に位置するL;
軽鎖34位に位置するS;
軽鎖49位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖50位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖51位に位置するA;
軽鎖52位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖53位に位置するT;
軽鎖54位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖55位に位置するP;
軽鎖56位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖89位に位置するA;
軽鎖90位に位置するG;
軽鎖91位に位置するL;
軽鎖92位に位置するY;
軽鎖93位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖94位に位置するG;
軽鎖95位に位置するN;
軽鎖95a位に位置するI;
軽鎖96位に位置するP;
軽鎖97位に位置するA。
[A21] 前記抗原結合ドメインは抗体可変領域であり、前記MTAと相互作用するアミノ酸残基は、前記抗体可変領域のアミノ酸配列の内、Kabatナンバリングで特定される重鎖34位、47位、50位、58位、95位、98位、99位、100a位、軽鎖28位、91位、95b位、95c位及び96位のアミノ酸部位の群から選択される少なくとも一つ以上のアミノ酸部位に位置するアミノ酸残基である、[A15]から[A17]のいずれか一つに記載の抗原結合分子。
[A22] 前記抗原結合ドメインは抗体可変領域であり、当該抗体可変領域は重鎖W34、W47、C50、Y58、E95、F98、G99、G100a、軽鎖Y28、T91、F95b、Y95c、及びF96(Kabatナンバリング)から選択される少なくとも一つ以上のアミノ酸を含む、[A15]から[A17]、および[A21]のいずれか一つに記載の抗原結合分子。
[A23] 前記抗原結合ドメインは抗体可変領域であり、当該抗体可変領域は下記アミノ酸の群から選択される少なくとも一つ以上のアミノ酸を含む、[A1]から[A17]のいずれかまたは[A21]から[A22]のいずれか一つに記載の抗原結合分子(Kabatナンバリング):
重鎖31位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖32位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖33位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖34位に位置するW;
重鎖35位に位置するM;
重鎖35a位に位置するC;
重鎖50位に位置するC;
重鎖51位に位置するI;
重鎖52位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖52a位に位置するS;
重鎖53位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖54位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖55位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖56位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖57位に位置するT;
重鎖58位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖59位に位置するY;
重鎖60位に位置するA;
重鎖61位に位置するS;
重鎖62位に位置するW;
重鎖63位に位置するV;
重鎖64位に位置するN;
重鎖65位に位置するG;
重鎖95位に位置するE;
重鎖96位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖97位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖98位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖99位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖100位に位置するS;
重鎖100a位に位置するG;
重鎖100b位に位置するA;
重鎖100c位に位置するL;
重鎖101位に位置するN;
重鎖102位に位置するL;
軽鎖24位に位置するH;
軽鎖25位に位置するS;
軽鎖26位に位置するS;
軽鎖27位に位置するK;
軽鎖27a位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖27b位に位置するV;
軽鎖28位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖29位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖30位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖31位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖32位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖33位に位置するL;
軽鎖34位に位置するA;
軽鎖49位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖50位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖51位に位置するA;
軽鎖52位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖53位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖54位に位置するL;
軽鎖55位に位置するA;
軽鎖56位に位置するS;
軽鎖89位に位置するQ;
軽鎖90位に位置するG;
軽鎖91位に位置するT;
軽鎖92位に位置するY;
軽鎖93位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖94位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖95位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖95a位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖95b位に位置するF;
軽鎖95c位に位置するY;
軽鎖96位に位置するF;
軽鎖97位に位置するA。
[A24] 前記抗原結合ドメインは抗体可変領域であり、前記MTAと相互作用するアミノ酸残基は、前記抗体可変領域のアミノ酸配列の内、Kabatナンバリングで特定される重鎖33位、50位、52位、54位、56位、57位、58位、99位、100位、100a位、軽鎖91位、95c位、及び96位のアミノ酸部位の群から選択される少なくとも一つ以上のアミノ酸部位に位置するアミノ酸残基である、[A15]から[A17]のいずれか一つに記載の抗原結合分子。
[A25] 前記抗原結合ドメインは抗体可変領域であり、当該抗体可変領域は重鎖A33、I50、G52、D54、S56、T57、W58、G99、Y100、T100a、軽鎖S91、Y95c、及びN96(Kabatナンバリング)から選択される少なくとも一つ以上のアミノ酸を含む、 [A15]から[A17]、および[A24]のいずれか一つに記載の抗原結合分子。
[A26] 前記抗原結合ドメインは抗体可変領域であり、当該抗体可変領域は下記アミノ酸の群から選択される少なくとも一つ以上のアミノ酸を含む、[A1]から[A17]のいずれかまたは[A24]から[A25]のいずれか一つに記載の抗原結合分子(Kabatナンバリング):
重鎖26位に位置するA、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖28位に位置するA、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖29位に位置するAまたはLのいずれか;
重鎖30位に位置するA、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖31位に位置するA、D、E、F、G、H、I、K、L、N、Q、R、S、T、V、WまたはYのいずれか;
重鎖32位に位置するD、E、F、H、N、P、RまたはYのいずれか;
重鎖33位に位置するA、I、P、TまたはVのいずれか;
重鎖34位に位置するA、E、F、H、I、K、L、M、N、Q、S、T、V、WまたはYのいずれか;
重鎖35位に位置するG;
重鎖50位に位置するD、IまたはVのいずれか;
重鎖51位に位置するI;
重鎖52位に位置するG;
重鎖53位に位置するA、D、E、G,I、K、QまたはRのいずれか;
重鎖54位に位置するD、E、F、G、H、I、K、L、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖55位に位置するA、D、E、F、GまたはHのいずれか;
重鎖56位に位置するA、D、E、F、G、H、I、K、L、N、Q、R、S、T、V、WまたはYのいずれか;
重鎖57位に位置するA、D、E、G、H、I、K、L、N、P、Q、R、S、TまたはVのいずれか;
重鎖58位に位置するW;
重鎖59位に位置するA、D、E、F、G、H、I、K、L、Q、R、S、T、V、WまたはYのいずれか;
重鎖60位に位置するP;
重鎖61位に位置するA、F、Q、R、S、T、V、WまたはYのいずれか;
重鎖62位に位置するW;
重鎖63位に位置するV;
重鎖64位に位置するK;
重鎖65位に位置するA、FまたはG;
重鎖95位に位置するG;
重鎖96位に位置するA、E、F、G、H、K、L、Q、R、S、T、WまたはYのいずれか;
重鎖97位に位置するA、F、H、K、N、WまたはYのいずれか;
重鎖98位に位置するA、D、E、F、G、H、I、K、L、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖99位に位置するA、D、E、G、H、QまたはSのいずれか;
重鎖100位に位置するFまたはY;
重鎖100a位に位置するN、TまたはV
重鎖100b位に位置するN;
重鎖100c位に位置するA;
重鎖100d位に位置するFまたはW;
重鎖101位に位置するD;
重鎖102位に位置するP;
軽鎖24位に位置するQ;
軽鎖25位に位置するS;
軽鎖26位に位置するS;
軽鎖27位に位置するQ;
軽鎖27e位に位置するS;
軽鎖27f位に位置するV;
軽鎖28位に位置するA、E、F、H、I、K、L、N、R、S、T、V、WまたはYのいずれか;
軽鎖29位に位置するA、D、E、F、G、H、I、K、L、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖30位に位置するN;
軽鎖31位に位置するN ;
軽鎖32位に位置するA、E、F、G、H、SまたはYのいずれか;
軽鎖33位に位置するL;
軽鎖34位に位置するS;
軽鎖50位に位置するD ;
軽鎖51位に位置するA;
軽鎖52位に位置するS ;
軽鎖53位に位置するT ;
軽鎖54位に位置するL;
軽鎖55位に位置するA;
軽鎖56位に位置するS;
軽鎖89位に位置するH;
軽鎖90位に位置するG;
軽鎖91位に位置するA、SまたはTのいずれか;
軽鎖92位に位置するA、D、E、F、G、H、I、K、L、M、N、Q、R、S、T、V、WまたはYのいずれか;
軽鎖93位に位置するA、D、E、F、G、H、L、N、Q、R、S、T、VまたはYのいずれか;
軽鎖94位に位置するA、E、F、G、H、I、K、L、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖95位に位置するA、D、E、F、G、H、I、K、L、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖95a位に位置するA、D、E、F、G、H、I、K、L、N、P、Q、R、V、WまたはYのいずれか;
軽鎖95b位に位置するA、D、E、F、G、H、I、K、L、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖95c位に位置するA、F、H、I、K、L、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖96d位に位置するD;
軽鎖96位に位置するN;
軽鎖97位に位置するAまたはG;
軽鎖98位に位置するA、F、I、LまたはV。
[A27] 前記抗原はMTA以外の分子である、またはMTA以外の分子でありヒトの生体内で免疫原性を有する分子である[A1]から[A26]のいずれか一つに記載の抗原結合分子。
[A28] 前記抗原はペプチド、ポリペプチド、タンパク質のいずれかである、[A1]から[A27]のいずれか一つに記載の抗原結合分子。
[A29] 前記抗原結合分子は更に第2の抗原結合ドメインを有し、前記第2の抗原結合ドメインは前記抗原結合ドメインが結合する抗原と異なる第2の抗原に対して結合活性を有する、[A1]から[A28]のいずれか一つに記載の抗原結合分子。
[A30] 前記第2の抗原結合ドメインの前記第2の抗原に対する結合活性はMTAに実質的に影響されない、[A29]に記載の抗原結合分子。
[A31] 前記第2の抗原結合ドメインの前記第2の抗原に対する結合活性はMTA依存的に変化する、[A29]に記載の抗原結合分子。
[A32] 前記第2の抗原結合ドメインのMTA存在下における前記第2の抗原に対する結合活性が、前記第2の抗原結合ドメインのMTA非存在下における前記第2の抗原に対する結合活性と異なる、[A31]に記載の抗原結合分子。
[A33] 前記抗原が膜型分子または可溶型分子である、[A1]から[A32]のいずれか一つに記載の抗原結合分子。
[A34] 前記抗原が膜型分子であり、且つ疾患組織で発現している抗原である[A33]に記載の抗原結合分子。
[A35] 前記抗原が可溶型分子であり、且つがん組織で発現している抗原である[A33]に記載の抗原結合分子。
[A36] 前記がん組織で発現している抗原ががん細胞に発現している抗原、もしくはがん組織中のがん間質細胞や免疫組織で発現している抗原である[A35]に記載の抗原結合分子。
[A37] 前記がん組織はMTAが蓄積しているがん組織である、[A35]または[A36]に記載の抗原結合分子。
[A38] 前記がん組織は、MTA phospholylase (MTAP)をコードしている遺伝子が欠損もしくは発現低下している、または酵素活性を低下させる変異もしくはスプライシングバリアントを有しているがん組織である[A35]から[A37]のいずれか一つに記載の抗原結合分子。
[A39] 前記がん組織は、MTAPの活性が欠損または低下しているがん組織である[A35]から[A37]のいずれか一つに記載の抗原結合分子。
[A40] [A1]から[A39]のいずれか一つに記載の抗原結合分子であって、前記抗原が膜型分子であり、前記抗原結合分子は前記抗原を発現する細胞に対して細胞傷害活性を示す、抗原結合分子。
[A41] ADCC活性、ADCP活性またはCDC活性の中から選択される少なくとも1つ以上の細胞傷害活性を示す[A40]に記載の抗原結合分子。
[A42] 前記抗原対してアゴニスト活性を有する[A1]から[A39]に記載の抗原結合分子。
[A43] 前記抗原と前記第2の抗原の一方は標的細胞において発現している抗原であり、他方はエフェクター細胞において発現している抗原である[A29]から[A32]のいずれか一つに記載の抗原結合分子。
[A44] 前記標的細胞はがん細胞である、[A43]に記載の抗原結合分子。
[A45] 前記がん細胞はMTAPをコードしている遺伝子が欠損もしくは発現低下している、または酵素活性を低下させる変異もしくはスプライシングバリアントを有しているがん細胞、または前記MTAPをコードしている遺伝子が欠損もしくは発現低下している、または酵素活性を低下させる変異もしくはスプライシングバリアントを有しているがん細胞の周囲に存在するがん細胞である[A44]に記載の抗原結合分子。
[A46] 前記標的細胞はMTAPをコードしている遺伝子が欠損もしくは発現低下している、または酵素活性を低下させる変異もしくはスプライシングバリアントを有しているがん細胞の周囲に存在するがん細胞以外の細胞である[A43]に記載の抗原結合分子。
[A47] 前記がん細胞の周囲に存在するがん細胞以外の細胞はcancer - associated fibroblasts (CAF) またはtumor associated macrophages (TAM)である[A43]に記載の抗原結合分子。
[A48] 前記エフェクター細胞がT細胞である、[A43]から[47]のいずれか一つに記載の抗原結合分子。
[A49] 前記エフェクター細胞において発現している抗原がT細胞レセプター(TCR)複合体である、[A48]に記載の抗原結合分子。
[A50] 前記エフェクター細胞において発現している抗原がCD3である、[A48]または[A49]のいずれか記載の抗原結合分子。
[A51] エフェクター細胞を活性化することで、標的細胞に対して細胞傷害活性を惹起する[A48]から[A50]のいずれか一つに記載の抗原結合分子。
[A52] TDCC活性を有する、[A48]から[A51]のいずれか一つに記載の抗原結合分子。
[A53] [A1]から[A39]のいずれか一つに記載の抗原結合分子であって、前記抗原が可溶型分子であり、前記抗原結合分子は前記抗原に対して中和活性を示す、抗原結合分子。
[A54] 前記抗原結合ドメインのMTA非存在下における前記抗原に対するKD値と前記抗原結合ドメインのMTA存在下における前記抗原に対するKD値が異なる[A1]から[A53]のいずれか一つに記載の抗原結合分子。
[A55] [A1]から[A54]のいずれか一つに記載の抗原結合分子を含む医薬組成物。
[A56] [A1]から[A55]のいずれか一つに記載の抗原結合分子を有効成分として含むがんの治療用医薬組成物。
[A57] 前記がんが、MTAが組織中に蓄積しているがんである[A56]に記載の医薬組成物。
[A58] 前記がんが、MTAPをコードしている遺伝子が欠損もしくは発現低下している、または酵素活性を低下させる変異もしくはスプライシングバリアントを有しているがんである、[A56]から[A57]のいずれか一つに記載の医薬組成物。
[A59] 前記がんが、MTAPの活性が欠損または低下しているであるがんある、[A56]から[A58]のいずれか一つに記載の医薬組成物。
[A60] [A1]から[A54]のいずれか一つに記載の抗原結合分子を製造する方法。
[A61] [A1]から[A52]のいずれか一つに記載の抗原結合分子コードするポリヌクレオチド。
[A62] [A61]に記載のポリヌクレオチドを含むベクター
[A63] [A62]に記載のベクターを保持する細胞。
[A64] [A63]に記載の細胞を培養し、培養上清から回収される抗原結合分子。
[G1] MTAの濃度依存的に結合しない対照の抗原結合分子と比較して、高い血漿中滞留性を有する、および/または低い血漿中抗原蓄積能を有する、[A1]から[A54]のいずれか一つに記載の抗原結合分子。
[G2] [G1]に記載の抗原結合分子および薬学的に許容される担体を含む、薬学的製剤。
[G3] 対照の抗原結合分子と比較して、高い血漿中滞留性を有する、および/または低い血漿中抗原蓄積能を有する抗原結合分子を製造する方法であって、(a) MTAの濃度が高まるにつれて抗原結合活性が増大する抗原結合分子を製造する工程、および(b) (a)で製造された抗原結合分子の血漿中滞留性、および/または血漿中抗原蓄積能を測定する工程を含む、方法。
[B1] お互いに配列の異なる複数の抗原結合ドメインを含む抗原結合分子、または/および互いに配列の異なる複数の抗原結合ドメインを含む抗原結合分子をコードする核酸からなるライブラリであって、MTAと相互作用するアミノ酸残基を有する抗原結合ドメインを含む抗原結合分子、または/および前記抗原結合分子をコードする核酸から主としてなるライブラリ。
[B2] 前記抗原結合ドメインが抗体可変領域である、[B1]に記載のライブラリ。
[B3] MTAに対する結合活性を有する抗体可変領域未改変体中の1つまたは複数のアミノ酸部位に位置するアミノ酸と異なるアミノ酸を有し、互いに配列が異なる複数の抗体可変領域改変体、または/およびMTAに対する結合活性を有する抗体可変領域未改変体中の1つまたは複数のアミノ酸部位に位置するアミノ酸と異なるアミノ酸を有し、互いに配列が異なる複数の抗体可変領域改変体をそれぞれコードする核酸を含む[B2]に記載のライブラリ。
[B4] 前記抗体可変領域改変体中の、前記抗体可変領域未改変体と異なるアミノ酸を有するアミノ酸部位は、下記のアミノ酸部位の群から選ばれる一つまたは複数のアミノ酸部位である、[B3]に記載のライブラリ:
1) 前記抗体可変領域未改変体中のMTAとの結合に関与しないアミノ酸部位に対応するアミノ酸部位、
2) 前記抗体可変領域改変体と比較して、前記抗体可変領域改変体のMTAとの結合を著しく減弱させないアミノ酸部位、及び
3) 前記抗体可変領域改変体の抗原に対するMTA依存的結合に寄与しやすいアミノ酸部位。
[B5] 前記抗体可変領域改変体中の、前記抗体可変領域未改変体と異なるアミノ酸を有するアミノ酸部位は、下記のアミノ酸部位の群から選ばれる一つまたは複数のアミノ酸部位である、[B3]に記載のライブラリ:
1) 前記抗体可変領域未改変体中のMTAとの結合に関与しないアミノ酸部位に対応するアミノ酸部位、
2) 前記抗体可変領域改変体と比較して、前記抗体可変領域改変体のMTAとの結合を著しく減弱させないアミノ酸部位、
3) 前記抗体可変領域未改変体の表面に露出するアミノ酸部位に対応するアミノ酸部位、及び
4) 前記抗体可変領域未改変体においてMTA結合/非結合時に構造変化率が大きい領域に位置するアミノ酸部位に対応するアミノ酸部位。
[B6] 前記抗体可変領域の未改変体はアデノシンまたは/及びS-(5'-Adenosyl)-L-homocysteine (SAH)に実質的に結合しない、[B3]から[B5]のいずれかに記載のライブラリ。
[B7] 前記抗体可変領域の未改変体は下記いずれかである、[B3]から[B6]のいずれか一つに記載のライブラリ:
a) 配列番号:46で示す重鎖可変領域と配列番号:47で示す軽鎖可変領域を含む抗体可変領域;
b) 配列番号:50で示す重鎖可変領域と配列番号:51で示す軽鎖可変領域を含む抗体可変領域;
c) 配列番号:48で示す重鎖可変領域と配列番号:49で示す軽鎖可変領域を含む抗体可変領域;
d) 配列番号:52で示す重鎖可変領域と配列番号:53で示す軽鎖可変領域を含む抗体可変領域。
[B8] 前記複数の抗体可変領域は、下記:
XAXWMC(配列番号:65)を含むH-CDR1;
CIFAXXXYXXSGGSTYYASWAKG(配列番号:66)を含むH-CDR2;
GXGXXXGXXDEL(配列番号:67)を含むH-CDR3;
QSSEXVXXXXLS(配列番号:68)を含むL-CDR1;
XAXTXPX(配列番号:69)を含むL-CDR2;及び
AGLYXGNIPA(配列番号:70)を含むL-CDR3;
を含む抗体可変領域であり、Xは任意のアミノ酸を指し、異なる位置に存在するXは同種のアミノ酸でなくて良い、[B2]に記載のライブラリ。
[B9] 前記複数の抗体可変領域は、下記:
XAXWMC(配列番号:65)を含むH-CDR1;
CIFAX1XXYXXSGGSTYYASWAKG(配列番号:71)を含むH-CDR2;
GXGXXXGXXDEL(配列番号:67)を含むH-CDR3;
QSSEXVXXX1XLS(配列番号:72)を含むL-CDR1;
XAXTXPX(配列番号:69)を含むL-CDR2;及び
AGLYXGNIPA(配列番号:70)を含むL-CDR3;
を含む抗体可変領域であり、
Xは任意のアミノ酸、
X1はA、D、E、G、H、I、K、L、M、N、P、Q、R、S、TおよびVから選ばれるアミノ酸であり、異なる位置に存在するXもしくはX1は同種のアミノ酸でなくて良い、[B2]に記載のライブラリ。
[B10] 前記複数の抗体可変領域は、下記:
XXAXWMC(配列番号:73)を含むH-CDR1;
CIFAX1XXYXXSGGSTYYASWAKG(配列番号:71)を含むH-CDR2;
GXGXXXGXXDEL(配列番号:67)を含むH-CDR3;
QSSEXVXXX1XLS(配列番号:72)を含むL-CDR1;
XAXTXPX(配列番号:69)を含むL-CDR2;及び
AGLYXGNIPA(配列番号:70)を含むL-CDR3;
を含む抗体可変領域であり、
Xは任意のアミノ酸、
X1はA、D、E、G、H、I、K、L、M、N、P、Q、R、S、TおよびVから選ばれるアミノ酸であり、異なる位置に存在するXもしくはX1は同種のアミノ酸でなくて良い、[B2]に記載のライブラリ。
[B11] 前記複数の抗体可変領域は、下記:
XXXWMC(配列番号:74)を含むH-CDR1;
CIXSXXXXTXYASWVNG(配列番号:75)を含むH-CDR2;
EXXXXSGALNL(配列番号:76)を含むH-CDR3;
HSSKXVXXXXXLA(配列番号:77)を含むL-CDR1;
XAXXLAS(配列番号:78)を含むL-CDR2;及び
QGTYXXXXFYFA(配列番号:79)を含むL-CDR3;
を含む抗体可変領域であり、Xは任意のアミノ酸を指し、異なる位置に存在するXは同種のアミノ酸でなくて良い、[B2]に記載のライブラリ。
[B12] 前記抗体可変領域の未改変体はアデノシンに対しても結合活性を有する、[B3]から[B5]のいずれか一つに記載のライブラリ。
[B13] 前記抗体可変領域の未改変体は(5'-Adenosyl)-L-homocysteine (SAH)、AMP,ADPまたは/及びATPに対しても結合活性を有する[B12]に記載のライブラリ。
[B14] 前記抗体可変領域の未改変体は、配列番号:31で示す重鎖可変領域と配列番号:32で示す軽鎖可変領域を有する抗体可変領域である、[B3]から[B5]、[B12]のいずれか一つに記載のライブラリ。
[B15] 前記複数の抗体可変領域は、下記:
X2X3X4X5G(配列番号:80)を含むH-CDR1;
X6IGX7X8X9X10X11WX12PX13WVKX14(配列番号:81)を含むH-CDR2;
GX15X16X17X18X19X20NAX21DP(配列番号:82)を含むH-CDR3;
QSSQSVX22X23NNX24LS(配列番号:83)を含むL-CDR1;
DASTLAS(配列番号:84)を含むL-CDR2;及び
HGX25X26X27X28X29X30X31X32DNX33(配列番号:85)を含むL-CDR3;
を含む抗体可変領域であり、
X2はA、D、E、F、G、H、I、K、L、N、Q、R、S、T、V、WおよびYから選ばれるアミノ酸、
X3はD、E、F、H、K、N、P、RおよびYから選ばれるアミノ酸、
X4はA、I、P、TおよびVから選ばれるアミノ酸、
X5はA、E、F、H、I、K、L、M、N、Q、S、T、V、WおよびYから選ばれるアミノ酸、
X6はD、IおよびVから選ばれるアミノ酸、
X7はA、D、E、G、I、K、QおよびRから選ばれるアミノ酸、
X8はD、E、F、G、H、I、K、L、P、Q、R、S、T、V、WおよびYから選ばれるアミノ酸、
X9はA、D、E、F、G、HおよびSから選ばれるアミノ酸、
X10はA、D、E、F、G、H、I、K、L、N、Q、R、S、T、V、WおよびYから選ばれるアミノ酸、
X11はA、D、E、G、H、I、K、L、N、P、Q、R、S、TおよびVから選ばれるアミノ酸、
X12はA、D、E、F、G、H、I、K、L、Q、R、S、T、V、WおよびYから選ばれるアミノ酸、
X13はA、F、Q、R、S、T、V、WおよびYから選ばれるアミノ酸、
X14はA、FおよびGから選ばれるアミノ酸、
X15はA、E、F、G、H、K、L、Q、R、S、T、WおよびYから選ばれるアミノ酸、
X16はF、H、K、N、WおよびYから選ばれるアミノ酸、
X17はA、D、E、F、G、H、I、K、L、N、P、Q、R、S、T、V、WおよびYから選ばれるアミノ酸、
X18はA、D、E、G、H、QおよびSから選ばれるアミノ酸、
X19はFおよびYから選ばれるアミノ酸、
X20はN、TおよびVから選ばれるアミノ酸、
X21はFおよびWから選ばれるアミノ酸、
X22はA、E、F、H、I、K、L、N、R、S、T、V、WおよびYから選ばれるアミノ酸、
X23はA、D、E、F、G、H、I、K、L、N、P、Q、R、S、T、V、WおよびYから選ばれるアミノ酸、
X24はA、E、F、G、H、SおよびYから選ばれるアミノ酸、
X25はA、SおよびTから選ばれるアミノ酸、
X26はA、D、E、F、G、H、I、K、L、M、N、Q、R、S、T、V、WおよびYから選ばれるアミノ酸、
X27はA、D、E、F、G、H、L、N、Q、R、S、T、VおよびYから選ばれるアミノ酸、
X28はA、E、F、G、H、I、K、L、N、P、Q、R、S、T、V、WおよびYから選ばれるアミノ酸、
X29はA、D、E、F、G、H、I、K、L、N、P、Q、R、S、T、V、W、Yから選ばれるアミノ酸、
X30はA、D、E、F、G、H、I、K、L、N、P、Q、R、V、WおよびYから選ばれるアミノ酸、
X31はA、D、E、F、G、H、I、K、L、N、P、Q、R、S、T、V、WおよびYから選ばれるアミノ酸、
X32はA、F、H、I、K、L、N、P、Q、R、S、T、V、WおよびYから選ばれるアミノ酸、
X33はAおよびGから選ばれるアミノ酸である、[B2]に記載のライブラリ。
[B16] [B15]に記載のライブラリから、MTAに結合する抗原結合ドメインを含む抗原結合分子をコードする核酸が濃縮されたライブラリ。
[B17] 前記抗原結合ドメインのMTAに対する結合は、抗原の非存在下におけるMTAに対する結合である、[B16]に記載のライブラリ。
[B18] 前記濃縮は、以下(1)~(2)の工程:
(1) [B15]に記載のライブラリからディスプレイされた抗原結合ドメインをMTAと接触させる工程、及び
(2) 前記工程(1)でMTAに結合した抗原結合ドメインを選択する工程、
を含む、[B16]または[B17]に記載のライブラリ。
[B19] [B15]に記載のライブラリから、アデノシンに結合する抗原結合ドメインをコードする核酸が濃縮されたライブラリ。
[B20] 前記抗原結合ドメインのアデノシンに対する結合は、抗原の非存在下におけるアデノシンに対する結合である、[B19]に記載のライブラリ。
[B21] 前記濃縮は、以下(1)~(2)の工程:
(1) [B15]に記載のライブラリからディスプレイされた抗原結合ドメインをアデノシンと接触させる工程、及び
(2) 前記工程(1)でアデノシンに結合した抗原結合ドメインを選択する工程、
を含む、[B19]または[B20]に記載のライブラリ。
[C1] 以下(a)および(b)の工程:
(a) MTAに対する結合活性を有する抗原結合ドメインにおいて、以下(i)乃至(vi)の少なくとも一つ以上を満たすアミノ酸部位を特定する工程:
(i) 前記抗原結合ドメインの表面に露出するアミノ酸部位;
(ii) 前記抗原結合ドメインがMTAに結合したときの構造とMTAに結合していない時の構造を比較するときに構造変化率が大きい領域に位置するアミノ酸部位;
(iii) MTAとの結合に関与しないアミノ酸部位;
(iv) MTAとの結合を著しく減弱させないアミノ酸部位;
(v) 前記抗原結合ドメインが属する動物種において、アミノ酸出現頻度の多様性のあるアミノ酸部位;または
(vi) Canonical structureの形成に重要でないアミノ酸部位;
(b) 前記抗原結合ドメインにおいて、未改変体をコードする核酸及び工程(a)で特定された1または複数のアミノ酸部位にアミノ酸改変を有する、互いに配列が異なる、前記抗原結合ドメインの複数の改変体をそれぞれコードする核酸を含むライブラリを設計する工程、
を含むライブラリの製造方法。
[C2] 前記工程(b)のアミノ酸改変は、以下(1)乃至(3)の少なくとも一つ以上を満たす:
(1) 当該アミノ酸改変を有する抗原結合ドメイン改変体がMTAに結合したときの構造とMTAに結合していないときの構造を比較する場合、当該改変後アミノ酸が位置するアミノ酸部位の構造変化率が大きい;
(2) 当該アミノ酸改変を有する抗原結合ドメイン改変体がMTAに結合したときの構造とMTAに結合していないときの構造を比較する場合、当該改変後アミノ酸が存在することにより前記抗原結合ドメイン改変体の構造変化が阻害されない;
(3) 当該アミノ酸改変を有する抗原結合ドメイン改変体が、前記抗原結合ドメイン未改変体と比べて、MTAに対する結合活性が著しく減弱されていない;
[C1]に記載の製造方法。
[C3] 前記MTAに対する結合活性を有する抗原結合ドメインは、アデノシンに実質的に結合しない、[C1]から[C2]のいずれか一つに記載の製造方法。
[C4] 前記MTAに対する結合活性を有する抗原結合ドメインは、(5'-Adenosyl)-L-homocysteine (SAH)、AMP,ADPまたは/及びATPに対して結合しない[C3]に記載の製造方法。
[C5] [C1]から[C4]のいずれか一つに記載の製造方法により製造されたライブラリ。
[C6] 以下(a)および(b)の工程:
(a) 低分子化合物に対する結合活性を有する抗原結合ドメインにおいて、以下(i)乃至(ii)の少なくとも一つを満たすアミノ酸部位を特定する工程:
(i) 前記抗原結合ドメインの表面に露出するアミノ酸部位;
(ii) 前記抗原結合ドメインが前記低分子化合物に結合したときの構造と前記低分子化合物に結合していない時の構造を比較するときに構造変化率が大きい領域に位置するアミノ酸部位;
(b) 前記抗原結合ドメインにおいて、未改変体をコードする核酸及び工程(a)で特定された1または複数のアミノ酸部位にアミノ酸改変を有する、互いに配列が異なる、前記抗原結合ドメインの複数の改変体をそれぞれコードする核酸を含むライブラリを設計する工程、
を含むライブラリの製造方法。
[C7] 前記工程(b)のアミノ酸改変は、以下(1)乃至(3)の少なくとも一つ以上を満たす:
(1) 当該アミノ酸改変を有する抗原結合ドメイン改変体が前記低分子化合物に結合したときの構造と前記低分子化合物に結合していないときの構造を比較する場合、当該改変後アミノ酸が位置するアミノ酸部位の構造変化率が大きい;
(2) 当該アミノ酸改変を有する抗原結合ドメイン改変体が前記低分子化合物に結合したときの構造と前記低分子化合物に結合していないときの構造を比較する場合、当該改変後アミノ酸が存在することにより前記抗原結合ドメイン改変体の構造変化が阻害されない;
(3) 当該アミノ酸改変を有する抗原結合ドメイン改変体が、前記抗原結合ドメイン未改変体と比べて、前記低分子化合物に対する結合活性が著しく減弱されていない;
[C5]に記載の製造方法。
[C8] 以下(a)および(b)の工程:
(a) 低分子化合物に対して相互作用する抗原結合ドメインにおいて、以下(i)乃至(iv)の少なくとも一つを満たすアミノ酸部位を特定する工程:
(i) 前記抗原結合ドメインの表面に露出するアミノ酸部位;
(ii) 前記抗原結合ドメインが前記低分子化合物に結合したときの構造と前記低分子化合物に結合していない時の構造を比較するときに構造変化率が大きい領域に位置するアミノ酸部位;
(iii) 前記低分子化合物との結合に関与しないアミノ酸部位;
(iv) 前記低分子化合物との結合を著しく減弱させないアミノ酸部位;
(v) 前記抗原結合ドメインが属する動物種において、アミノ酸出現頻度の多様性のあるアミノ酸部位;または
(vi) Canonical structureの形成に重要でないアミノ酸部位;
(b) 前記抗原結合ドメインにおいて、未改変体をコードする核酸及び工程(a)で特定された1または複数のアミノ酸部位に以下の(1)乃至(2)の少なくとも一つを満たすアミノ酸改変を有する、互いに配列が異なる、前記抗原結合ドメインの複数の改変体をそれぞれコードする核酸を含むライブラリを設計する工程:
(1) 当該アミノ酸改変を有する抗原結合ドメイン改変体が前記低分子化合物に結合したときの構造と前記低分子化合物に結合していないときの構造を比較する場合、当該改変後アミノ酸が位置するアミノ酸部位の構造変化率が大きい;
(2) 当該アミノ酸改変を有する抗原結合ドメイン改変体が前記低分子化合物に結合したときの構造と前記低分子化合物に結合していないときの構造を比較する場合、当該改変後アミノ酸が存在することにより前記抗原結合ドメイン改変体の構造変化が阻害されない;
を含むライブラリの製造方法。
[C9] 前記低分子化合物はアデノシン、アデノシン3リン酸、アデノシン2リン酸、アデノシン1リン酸、S-(5'-Adenosyl)-L-homocysteine (SAH)から選択される少なくとも一つから選ばれる、[C6]から[C8]のいずれか一つに記載の製造方法。
[C10] [C6]から[C8]のいずれか一つに記載の製造方法により製造されたライブラリ。
[D1] MTA依存的に抗原に対する結合活性が変化する抗原結合ドメインを含む抗原結合分子をスクリーニングする方法。
[D2] 抗原結合ドメインの第1濃度のMTA存在下における抗原に対する結合活性と第1濃度と異なる濃度(第2濃度)のMTA存在下における抗原に対する結合活性を比較することを含む、[D1]に記載の方法。
[D3] 第1濃度のMTA存在下における抗原に対する結合活性と第2濃度のMTA存在下における抗原に対する結合活性が異なる抗原結合ドメインを含む抗原結合分子を選択する工程含む、[D1]または[D2]に記載の方法。
[D4] 前記第1濃度のMTA存在下における抗原に対する結合活性が前記第2濃度のMTA存在下における抗原に対する結合活性より高い抗原結合ドメインを含む抗原結合分子を選択する工程含む、[D2]から[D3]のいずれか一つに記載の方法。
[D5] 前記第1濃度のMTA存在下における抗原に対する結合活性が前記第2濃度のMTA存在下における抗原に対する結合活性より低い抗原結合ドメインを含む抗原結合分子を選択する工程含む、[D2]から[D3]のいずれか一つに記載の方法。
[D6] 以下(a)~(c)の工程:
(a) 抗原結合ドメインを含む抗原結合分子を第1濃度のMTA存在下で抗原と接触させる工程、
(b) 前記工程(a)で結合した抗原結合ドメインを含む抗原結合分子を第2濃度のMTA存在下に置く工程、及び
(c) 前記工程(b)で解離した抗原結合ドメインを含む抗原結合分子を単離する工程、
を含む、[D1]に記載の方法。
[D7] 以下の(a)~(d)の工程;
(a) 抗原結合ドメインを含む抗原結合分子を第1濃度のMTA存在下で抗原と接触させる工程、
(b) 前記工程(a)で前記抗原結合ドメインを含む抗原結合分子が抗原に結合したことを確認する工程、
(c) 前記抗原に結合した前記抗原結合ドメインを含む抗原結合分子を第2濃度のMTA存在下に置く工程、及び
(d) 前記工程(c)で抗原結合活性が、前記工程(b)で抗原に結合したことを確認した基準より弱い抗原結合ドメインを含む抗原結合分子を単離する工程、
を含む、[D1]に記載の方法。
[D8] 前記(a)工程を行う前に、抗原結合ドメインがMTAに結合可能であることを確認する、[D6]または[D7]に記載の方法。
[D9] 以下(a)~(d)の工程:
(a) 第1濃度のMTA存在下で抗原結合ドメインを含む抗原結合分子を抗原に接触させる工程、
(b) 前記工程(a)で前記抗原結合ドメインを含む抗原結合分子が抗原に結合しないことを確認する工程、
(c) 前記抗原に結合しない抗原結合ドメインを含む抗原結合分子を第2濃度のMTA存在下で抗原に結合させる工程、及び
(d) 前記工程(c)で抗原に結合した抗原結合ドメインを含む抗原結合分子を単離する工程、
を含む、[D1]に記載の方法。
[D10] 以下(a)~(c)の工程:
(a) 抗原結合ドメインを含む抗原結合分子がディスプレイされたライブラリを第1濃度のMTA存在下で抗原と接触させる工程、
(b) 前記工程(a)で結合した抗原結合ドメインを含む抗原結合分子を第2濃度のMTA存在下に置く工程、及び
(c) 前記工程(b)で解離した抗原結合ドメインを含む抗原結合分子を単離する工程、
を含む、[D1]に記載の方法。
[D11] 以下の(a)~(d)の工程;
(a) 抗原結合ドメインを含む抗原結合分子がディスプレイされたライブラリを第1濃度のMTA存在下で抗原と接触させる工程、
(b) 前記工程(a)で抗原に結合した抗原結合ドメインを含む抗原結合分子を選択する工程、
(c) 前記工程(b)で選択した抗原結合ドメインを含む抗原結合分子を第2濃度のMTA存在下に置く工程、及び
(d) 前記工程(c)で抗原結合活性が、前記工程(b)で選択した基準より弱い抗原結合ドメインを含む抗原結合分子を単離する工程、
を含む、[D1]に記載の方法。
[D12] 前記(a)工程の前に、以下(1)から(2)の工程:
(1) 抗原結合ドメインを含む抗原結合分子がディスプレイされたライブラリをMTAと接触させる工程、及び
(2) 前記工程(1)でMTAに結合した抗原結合ドメインを含む抗原結合分子を選択する工程、
を含み、前記工程(a)で第1濃度のMTA存在下で抗原と接触させるライブラリは、前記工程(1)及び(2)で選択された抗原結合ドメインを含む抗原結合分子がディスプレイされたライブラリである、[D10]または[D11]に記載の方法。
[D13] 以下(a)~(d)の工程:
(a) 第1濃度のMTA存在下で抗原結合ドメインを含む抗原結合分子がディスプレイされたライブラリを抗原に接触させる工程、
(b) 前記工程(a)で抗原に結合しない抗原結合ドメインを含む抗原結合分子を選択する工程、
(c) 前記工程(b)で選択された抗原結合ドメインを含む抗原結合分子を第2濃度のMTA存在下で抗原に結合させる工程、及び
(d) 前記工程(c)で抗原に結合した抗原結合ドメインを含む抗原結合分子を単離する工程、
を含む、[D1]に記載の方法。
[D14] 前記第1濃度は前記第2濃度より高い濃度である、[D2]から[D8]のいずれか一つに記載の方法。
[D15] 抗原結合ドメインのMTA存在下における抗原に対する結合活性とMTA非存在における抗原に対する結合活性を比較することを含む、[D1]に記載の方法。
[D16] MTA存在下における抗原に対する結合活性とMTA非存在下における抗原に対する結合活性が異なる抗原結合ドメインを選択する工程含む、[D1]または[D15]に記載の方法。
[D17] MTA存在下における抗原に対する結合活性がMTA非存在下における抗原に対する結合活性より高い抗原結合ドメインを選択する工程含む、[D1]または[D15]に記載の方法。
[D18] 以下(a)~(c)の工程:
(a) 抗原結合ドメインを含む抗原結合分子をMTAの存在下で抗原と接触させる工程、
(b) 前記工程(a)で結合した抗原結合ドメインを含む抗原結合分子をMTAの非存在下に置く工程、及び
(c) 前記工程(b)で解離した抗原結合ドメインを含む抗原結合分子を単離する工程、
を含む、[D1]に記載の方法。
[D19] 以下の(a)~(d)の工程;
(a) 抗原結合ドメインを含む抗原結合分子をMTAの存在下で抗原と接触させる工程、
(b) 前記工程(a)で前記抗原結合ドメインを含む抗原結合分子が抗原に結合したことを確認する工程、
(c) 前記抗原に結合した前記抗原結合ドメインを含む抗原結合分子をMTAの非存在下に置く工程、及び
(d) 前記工程(c)で抗原結合活性が、前記工程(b)で抗原に結合したことを確認した基準より弱い抗原結合ドメインを含む抗原結合分子を単離する工程、
を含む、[D1]に記載の方法。
[D20] 前記(a)工程を行う前に、抗原結合ドメインを含む抗原結合分子がMTAに結合可能であることを確認する、[D18]または[D19]に記載の方法。
[D21] 以下(a)~(d)の工程:
(a) MTAの存在下で抗原結合ドメインを含む抗原結合分子を抗原に接触させる工程、
(b) 前記工程(a)で前記抗原結合ドメインを含む抗原結合分子が抗原に結合しないことを確認する工程、
(c) 前記抗原に結合しない抗原結合ドメインを含む抗原結合分子をMTAの非存在下で抗原に結合させる工程、及び
(d) 前記工程(c)で抗原に結合した抗原結合ドメインを含む抗原結合分子を単離する工程、
を含む、[D1]に記載の方法。
[D22] 以下(a)~(c)の工程:
(a) 抗原結合ドメインを含む抗原結合分子がディスプレイされたライブラリを MTAの存在下で抗原と接触させる工程、
(b) 前記工程(a)で結合した抗原結合ドメインを含む抗原結合分子をMTAの非存在下に置く工程、及び
(c) 前記工程(b)で解離した抗原結合ドメインを含む抗原結合分子を単離する工程、
を含む、[D1]に記載の方法。
[D23] 以下の(a)~(d)の工程;
(a) 抗原結合ドメインを含む抗原結合分子がディスプレイされたライブラリをMTAの存在下で抗原と接触させる工程、
(b) 前記工程(a)で抗原に結合した抗原結合ドメインを含む抗原結合分子を選択する工程、
(c) 前記工程(b)で選択した抗原結合ドメインを含む抗原結合分子をMTAの非存在下に置く工程、及び
(d) 前記工程(c)で抗原結合活性が、前記工程(b)で選択した基準より弱い抗原結合ドメインを含む抗原結合分子を単離する工程、
を含む、[D1]に記載の方法。
[D24] 前記(a)工程の前に、以下(1)から(2)の工程:
(1) 抗原結合ドメインを含む抗原結合分子がディスプレイされたライブラリをMTAと接触させる工程、及び
(2) 前記工程(1)でMTAに結合した抗原結合ドメインを含む抗原結合分子を選択する工程、
を含み、前記工程(a)でMTAの存在下で抗原と接触させるライブラリは、前記工程(1)及び(2)で選択された抗原結合ドメインを含む抗原結合分子がディスプレイされたライブラリである、[D22]または[D23]に記載の方法。
[D25] 以下(a)~(d)の工程:
(a) MTAの存在下で抗原結合ドメインを含む抗原結合分子がディスプレイされたライブラリを抗原に接触させる工程、
(b) 前記工程(a)で抗原に結合しない抗原結合ドメインを含む抗原結合分子を選択する工程、
(c) 前記工程(b)で選択された抗原結合ドメインを含む抗原結合分子をMTAの非存在下で抗原に結合させる工程、及び
(d) 前記工程(c)で抗原に結合した抗原結合ドメインを含む抗原結合分子を単離する工程、
を含む、[D1]に記載の方法。
[D26] 前記抗原結合ドメインを含む抗原結合分子がディスプレイされたライブラリは、またはナイーブヒト抗体ディスプレイライブラリ、または合成ヒト抗体ディスプレイライブラリ、または[B1]から[B14]のいずれか一つに記載のライブラリ、または[C5]に記載のライブラリである、[D10]から[D14]または[D22]から[D25]のいずれか一つに記載の方法。
[D27] 前記抗原結合ドメインが抗体可変領域もしくは単ドメイン抗体である、[D1]から[D26]のいずれか一つに記載の方法。
[F1] MTA依存的に抗原に対する結合活性が変化する抗原結合ドメインを含む抗原結合分子を製造する方法。
[F2] 抗原結合ドメインの第1濃度のMTA存在下における抗原に対する結合活性と第1濃度とは異なる濃度(第2濃度)のMTA存在下における抗原に対する結合活性を比較することを含む、[F1]に記載の方法。
[F3] 第1濃度のMTA存在下における抗原に対する結合活性と第2濃度のMTA存在下における抗原に対する結合活性が異なる抗原結合ドメインを選択する工程含む、[F1]または[F2]に記載の方法。
[F4] 前記第1濃度のMTA存在下における抗原に対する結合活性が前記第2濃度のMTA存在下における抗原に対する結合活性より高い抗原結合ドメインを選択する工程含む、[F2]から[F3]のいずれか一つに記載の方法。
[F5] 前記第1濃度のMTA存在下における抗原に対する結合活性が前記第2濃度のMTA存在下における抗原に対する結合活性より低い抗原結合ドメインを選択する工程含む、[F2]から[F3]のいずれか一つに記載の方法。
[F6] 前記選択された抗原結合ドメインを含む抗原結合分子をコードするポリヌクレオチドが作動可能に連結されたベクターが導入された細胞を培養し、細胞の培養液から抗原結合ドメインを含む抗原結合分子を回収する工程を更に含む、[F3]から[F5]のいずれか一つに記載の方法。
[F7] 以下(a)~(d)の工程:
(a) 抗原結合ドメインを第1濃度のMTA存在下で抗原と接触させる工程、
(b) 前記工程(a)で結合した抗原結合ドメインを第2濃度のMTA存在下に置く工程、
(c) 前記工程(b)で解離した抗原結合ドメインを単離する工程、及び
(d) 前記工程(c)で単離された抗原結合ドメインを含む抗原結合分子をコードするポリヌクレオチドが作動可能に連結されたベクターが導入された細胞を培養し、細胞の培養液から抗原結合ドメインを含む抗原結合分子を回収する工程、
を含む、[F1]に記載の方法。
[F8] 以下の(a)~(e)の工程;
(a) 抗原結合ドメインを第1濃度のMTA存在下で抗原と接触させる工程、
(b) 前記工程(a)で前記抗原結合ドメインが抗原に結合したことを確認する工程、
(c) 前記抗原に結合した前記抗原結合ドメインを第2濃度のMTA存在下に置く工程、
(d) 前記工程(c)で抗原結合活性が、前記工程(b)で抗原に結合したことを確認した基準より弱い抗原結合ドメインを単離する工程、及び
(e) 前記工程(d)で単離された抗原結合ドメインを含む抗原結合分子をコードするポリヌクレオチドが作動可能に連結されたベクターが導入された細胞を培養し、細胞の培養液から抗原結合ドメインを含む抗原結合分子を回収する工程、
を含む、[F1]に記載の方法。
[F9] 前記(a)工程を行う前に、抗原結合ドメインがMTAに結合可能であることを確認する、[F7]または[F8]に記載の方法。
[F10] 以下(a)~(e)の工程:
(a) 第1濃度のMTA存在下で抗原結合ドメインを抗原に接触させる工程、
(b) 前記工程(a)で前記抗原結合ドメインが抗原に結合しないことを確認する工程、
(c) 前記抗原に結合しない抗原結合ドメインを第2濃度のMTA存在下で抗原に結合させる工程、
(d) 前記工程(c)で抗原に結合した抗原結合ドメインを単離する工程、及び
(e) 前記工程(d)で単離された抗原結合ドメインを含む抗原結合分子をコードするポリヌクレオチドが作動可能に連結されたベクターが導入された細胞を培養し、細胞の培養液から抗原結合ドメインを含む抗原結合分子を回収する工程、
を含む、[F1]に記載の方法。
[F11] 以下(a)~(d)の工程:
(a) 抗原結合ドメインがディスプレイされたライブラリを第1濃度のMTA存在下で抗原と接触させる工程、
(b) 前記工程(a)で結合した抗原結合ドメインを第2濃度のMTA存在下に置く工程、
(c) 前記工程(b)で解離した抗原結合ドメインを単離する工程、及び
(d) 前記工程(c)で単離された抗原結合ドメインを含む抗原結合分子をコードするポリヌクレオチドが作動可能に連結されたベクターが導入された細胞を培養し、細胞の培養液から抗原結合ドメインを含む抗原結合分子を回収する工程、
を含む、[F1]に記載の方法。
[F12] 以下の(a)~(e)の工程;
(a) 抗原結合ドメインがディスプレイされたライブラリを第1濃度のMTA存在下で抗原と接触させる工程、
(b) 前記工程(a)で抗原に結合した抗原結合ドメインを選択する工程、
(c) 前記工程(b)で選択した抗原結合ドメインを第2濃度のMTA存在下に置く工程、
(d) 前記工程(c)で抗原結合活性が、前記工程(b)で選択した基準より弱い抗原結合ドメインを単離する工程、及び
(e) 前記工程(d)で単離された抗原結合ドメインを含む抗原結合分子をコードするポリヌクレオチドが作動可能に連結されたベクターが導入された細胞を培養し、細胞の培養液から抗原結合ドメインを含む抗原結合分子を回収する工程、
を含む、[F1]に記載の方法。
[F13] 前記(a)工程の前に、以下(1)から(2)の工程:
(1) 抗原結合ドメインがディスプレイされたライブラリをMTAと接触させる工程、及び
(2) 前記工程(1)でMTAに結合した抗原結合ドメインを選択する工程、
を含み、前記工程(a)で第1濃度のMTA存在下で抗原と接触させるライブラリは、前記工程(1)及び(2)で選択された抗原結合ドメインがディスプレイされたライブラリである、[F11]または[F12]に記載の方法。
[F14] 以下(a)~(e)の工程:
(a) 第1濃度のMTA存在下で抗原結合ドメインがディスプレイされたライブラリを抗原に接触させる工程、
(b) 前記工程(a)で抗原に結合しない抗原結合ドメインを選択する工程、
(c) 前記工程(b)で選択された抗原結合ドメインを第2濃度のMTA存在下で抗原に結合させる工程、
(d) 前記工程(c)で抗原に結合した抗原結合ドメインを単離する工程、及び
(e) 前記工程(d)で単離された抗原結合ドメインを含む抗原結合分子をコードするポリヌクレオチドが作動可能に連結されたベクターが導入された細胞を培養し、細胞の培養液から抗原結合ドメインを含む抗原結合分子を回収する工程、
を含む、[F1]に記載の方法。
[F15] 前記第1濃度は前記第2濃度より高い濃度である、[F2]から[F14]のいずれか一つに記載の方法。
[F16] 抗原結合ドメインのMTA存在下における抗原に対する結合活性とMTA非存在における抗原に対する結合活性を比較することを含む、[F1]に記載の方法。
[F17] MTA存在下における抗原に対する結合活性とMTA非存在下における抗原に対する結合活性が異なる抗原結合ドメインを選択する工程含む、[F1]または[F16]に記載の方法。
[F18] MTA存在下における抗原に対する結合活性がMTA非存在下における抗原に対する結合活性が高い抗原結合ドメインを選択する工程含む、[F1]または[F16]に記載の方法。
[F19] 前記選択された抗原結合ドメインを含む抗原結合分子をコードするポリヌクレオチドが作動可能に連結されたベクターが導入された細胞を培養し、細胞の培養液から抗原結合ドメインを含む抗原結合分子を回収する工程を更に含む、[F16]から[F18]のいずれか一つに記載の方法。
[F20] 以下(a)~(d)の工程:
(a) 抗原結合ドメインをMTAの存在下で抗原と接触させる工程、
(b) 前記工程(a)で結合した抗原結合ドメインをMTAの非存在下に置く工程、
(c) 前記工程(b)で解離した抗原結合ドメインを単離する工程、及び
(d) 前記工程(c)で単離された抗原結合ドメインを含む抗原結合分子をコードするポリヌクレオチドが作動可能に連結されたベクターが導入された細胞を培養し、細胞の培養液から抗原結合ドメインを含む抗原結合分子を回収する工程、
を含む、[F1]に記載の方法。
[F21] 以下の(a)~(e)の工程;
(a) 抗原結合ドメインをMTAの存在下で抗原と接触させる工程、
(b) 前記工程(a)で前記抗原結合ドメインが抗原に結合したことを確認する工程、
(c) 前記抗原に結合した前記抗原結合ドメインをMTAの非存在下に置く工程、
(d) 前記工程(c)で抗原結合活性が、前記工程(b)で抗原に結合したことを確認した基準より弱い抗原結合ドメインを単離する工程、及び
(e) 前記工程(d)で単離された抗原結合ドメインを含む抗原結合分子をコードするポリヌクレオチドが作動可能に連結されたベクターが導入された細胞を培養し、細胞の培養液から抗原結合ドメインを含む抗原結合分子を回収する工程、
を含む、[F1]に記載の方法。
[F22] 前記(a)工程を行う前に、抗原結合ドメインがMTAに結合可能であることを確認する、[F20]または[F21]に記載の方法。
[F23] 以下(a)~(e)の工程:
(a) MTAの存在下で抗原結合ドメインを抗原に接触させる工程、
(b) 前記工程(a)で前記抗原結合ドメインが抗原に結合しないことを確認する工程、
(c) 前記抗原に結合しない抗原結合ドメインをMTAの非存在下で抗原に結合させる工程、
(d) 前記工程(c)で抗原に結合した抗原結合ドメインを単離する工程、及び
(e) 前記工程(d)で単離された抗原結合ドメインを含む抗原結合分子をコードするポリヌクレオチドが作動可能に連結されたベクターが導入された細胞を培養し、細胞の培養液から抗原結合ドメインを含む抗原結合分子を回収する工程、
を含む、[F1]に記載の方法。
[F24] 以下(a)~(d)の工程:
(a) 抗原結合ドメインがディスプレイされたライブラリを MTAの存在下で抗原と接触させる工程、
(b) 前記工程(a)で結合した抗原結合ドメインをMTAの非存在下に置く工程、
(c) 前記工程(b)で解離した抗原結合ドメインを単離する工程、及び
(d) 前記工程(c)で単離された抗原結合ドメインを含む抗原結合分子をコードするポリヌクレオチドが作動可能に連結されたベクターが導入された細胞を培養し、細胞の培養液から抗原結合ドメインを含む抗原結合分子を回収する工程、
を含む、[F1]に記載の方法。
[F25] 以下の(a)~(e)の工程;
(a) 抗原結合ドメインがディスプレイされたライブラリをMTAの存在下で抗原と接触させる工程、
(b) 前記工程(a)で抗原に結合した抗原結合ドメインを選択する工程、
(c) 前記工程(b)で選択した抗原結合ドメインをMTAの非存在下に置く工程、
(d) 前記工程(c)で抗原結合活性が、前記工程(b)で選択した基準より弱い抗原結合ドメインを単離する工程、及び
(e) 前記工程(d)で単離された抗原結合ドメインを含む抗原結合分子をコードするポリヌクレオチドが作動可能に連結されたベクターが導入された細胞を培養し、細胞の培養液から抗原結合ドメインを含む抗原結合分子を回収する工程、
を含む、[F1]に記載の方法。
[F26] 前記(a)工程の前に、以下(1)から(2)の工程:
(1) 抗原結合ドメインがディスプレイされたライブラリをMTAと接触させる工程、及び
(2) 前記工程(1)でMTAに結合した抗原結合ドメインを選択する工程、
を含み、前記工程(a)でMTAの存在下で抗原と接触させるライブラリは、前記工程(1)及び(2)で選択された抗原結合ドメインがディスプレイされたライブラリである、[F24]または[F25]に記載の方法。
[F27] 以下(a)~(e)の工程:
(a) MTAの存在下で抗原結合ドメインがディスプレイされたライブラリを抗原に接触させる工程、
(b) 前記工程(a)で抗原に結合しない抗原結合ドメインを選択する工程、
(c) 前記工程(b)で選択された抗原結合ドメインをMTAの非存在下で抗原に結合させる工程、
(d) 前記工程(c)で抗原に結合した抗原結合ドメインを単離する工程、及び
(e) 前記工程(d)で単離された抗原結合ドメインを含む抗原結合分子をコードするポリヌクレオチドが作動可能に連結されたベクターが導入された細胞を培養し、細胞の培養液から抗原結合ドメインを含む抗原結合分子を回収する工程、
を含む、[F1]に記載の方法。
[F28] 前記抗原結合ドメインがディスプレイされたライブラリは、またはナイーブヒト抗体ディスプレイライブラリ、または合成ヒト抗体ディスプレイライブラリ、または[B1]から[B14]のいずれか一つに記載のライブラリ、または[C5]に記載のライブラリである、[F11]から[F15]または[F24]から[F27]のいずれか一つに記載の方法。
[F29] 前記抗原結合ドメインが抗体可変領域もしくは単ドメイン抗体である、[F1]から[F28]のいずれか一つに記載の方法。
[E1] MTAに特異的に結合する抗原結合分子。
[E2] MTAに結合する抗原結合分子であって、当該抗原結合分子はアデノシンに実質的に結合しない[E1]に記載の抗原結合分子。
[E3] MTAに結合する抗原結合分子であって、当該抗原結合分子は(5'-Adenosyl)-L-homocysteine (SAH)、AMP,ADPまたは/及びATPに実質的に結合しない[E1]または[E2]に記載の抗原結合分子。
[E4] [E1]から[E3]のいずれか一つに記載の抗原結合分子を用いる、MTA濃度測定方法。
[E5] 前記MTA濃度は、組織中のMTA濃度である、[E4]に記載の測定方法。
[E6] 抗原抗体反応を利用してMTA濃度を測定する[E4]または[E5]のいずれか一つに記載の測定方法。
[E7] 免疫組織染色法を用いる、[E4]から[E5]のいずれか一つに記載の測定方法。
[E8] imaging法を用いる、[E4]から[E5]のいずれか一つに記載の測定方法。
[E9] in vivo imaging法を用いる、[E4]から[E5]のいずれか一つに記載の測定方法。
[E10] [E1]から[E3]のいずれか一つに記載の抗原結合分子を用いる、疾患の診断方法。
[E11] 前記診断は、疾患の罹患有無を判断する、または疾患に対する治療効果を予測する、[E10]に記載の方法。
[E12] 前記疾患はがんである、[E10]から[E11]のいずれか一つに記載の方法。
[E13] 前記がんは、がん組織中にMTAが蓄積されているがんである、[E12]に記載の方法。
[E14] 前記がんは、MTAPをコードしている遺伝子が欠損もしくは発現低下している、または酵素活性を低下させる変異もしくはスプライシングバリアントを有しているがん組織である[E12]または[E13]のいずれかに一つに記載の方法。
[E15] [E1]から[E3]のいずれか一つに記載の抗原結合分子を含む、疾患の診断キット。
[E16] 前記診断は、疾患の罹患有無を判断する、または疾患に対する治療効果を予測する、[E15]に記載のキット。
[E17] 前記疾患はがんである、[E15]から[E16]のいずれか一つに記載のキット。
[E18] 前記がんは、がん組織中にMTAが蓄積されているがんである、[E17]に記載のキット。
さらに、本開示の、互いに配列の異なる複数の、MTA依存的に抗原に対する結合活性が変化する抗原結合ドメインを含む抗原結合分子を含むライブラリを用いれば、上述したとおりの、がん組織特異的な疾患の治療に有用なMTA依存的に抗原に対する結合活性が変化する様々な抗原結合分子を、短時間で効率良く取得することが可能である。
アミノ酸
本明細書において、たとえば、Ala/A、Leu/L、Arg/R、Lys/K、Asn/N、Met/M、Asp/D、Phe/F、Cys/C、Pro/P、Gln/Q、Ser/S、Glu/E、Thr/T、Gly/G、Trp/W、His/H、Tyr/Y、Ile/I、Val/Vと表されるように、アミノ酸は1文字コードまたは3文字コード、またはその両方で表記されている。
抗原結合分子のアミノ酸配列中のアミノ酸の改変のためには、部位特異的変異誘発法(Kunkelら(Proc. Natl. Acad. Sci. USA (1985) 82, 488-492))やOverlap extension PCR等の公知の方法が適宜採用され得る。また、天然のアミノ酸以外のアミノ酸に置換するアミノ酸の改変方法として、複数の公知の方法もまた採用され得る(Annu. Rev. Biophys. Biomol. Struct. (2006) 35, 225-249、Proc. Natl. Acad. Sci. U.S.A. (2003) 100 (11), 6353-6357)。例えば、終止コドンの1つであるUAGコドン(アンバーコドン)の相補的アンバーサプレッサーtRNAに非天然アミノ酸が結合されたtRNAが含まれる無細胞翻訳系システム(Clover Direct(Protein Express))等も好適に用いられる。
(a) 33位、(b)55位、(c)96位、(d)33位および55位、(e)33位および96位、(f)55位および96位、(g)33位および55位および96位。
本明細書において「抗原」は抗原結合ドメインが結合するエピトープを含む限りその構造は特定の構造に限定されない。ある態様において、抗原は4アミノ酸以上のペプチド、またはポリペプチド、またはタンパク質である。抗原としては下記のような分子;17-IA、4-1BB、4Dc、6-ケト-PGF1a、8-イソ-PGF2a、8-オキソ-dG、A1 アデノシン受容体、A33、ACE、ACE-2、アクチビン、アクチビンA、アクチビンAB、アクチビンB、アクチビンC、アクチビンRIA、アクチビンRIA ALK-2、アクチビンRIB ALK-4、アクチビンRIIA、アクチビンRIIB、ADAM、ADAM10、ADAM12、ADAM15、ADAM17/TACE、ADAM8、ADAM9、ADAMTS、ADAMTS4、ADAMTS5、アドレシン、aFGF、ALCAM、ALK、ALK-1、ALK-7、アルファ-1-アンチトリプシン、アルファ-V/ベータ-1アンタゴニスト、ANG、Ang、APAF-1、APE、APJ、APP、APRIL、AR、ARC、ART、アルテミン、抗Id、ASPARTIC、心房性ナトリウム利尿因子、av/b3インテグリン、Axl、b2M、B7-1、B7-2、B7-H、B-リンパ球刺激因子(BlyS)、BACE、BACE-1、Bad、BAFF、BAFF-R、Bag-1、BAK、Bax、BCA-1、BCAM、Bcl、BCMA、BDNF、b-ECGF、bFGF、BID、Bik、BIM、BLC、BL-CAM、BLK、BMP、BMP-2 BMP-2a、BMP-3 オステオゲニン(Osteogenin)、BMP-4 BMP-2b、BMP-5、BMP-6 Vgr-1、BMP-7(OP-1)、BMP-8(BMP-8a、OP-2)、BMPR、BMPR-IA(ALK-3)、BMPR-IB(ALK-6)、BRK-2、RPK-1、BMPR-II(BRK-3)、BMP、b-NGF、BOK、ボンベシン、骨由来神経栄養因子、BPDE、BPDE-DNA、BTC、補体因子3(C3)、C3a、C4、C5、C5a、C10、CA125、CAD-8、カルシトニン、cAMP、癌胎児性抗原(CEA)、癌関連抗原、カテプシンA、カテプシンB、カテプシンC/DPPI、カテプシンD、カテプシンE、カテプシンH、カテプシンL、カテプシンO、カテプシンS、カテプシンV、カテプシンX/Z/P、CBL、CCI、CCK2、CCL、CCL1、CCL11、CCL12、CCL13、CCL14、CCL15、CCL16、CCL17、CCL18、CCL19、CCL2、CCL20、CCL21、CCL22、CCL23、CCL24、CCL25、CCL26、CCL27、CCL28、CCL3、CCL4、CCL5、CCL6、CCL7、CCL8、CCL9/10、CCR、CCR1、CCR10、CCR10、CCR2、CCR3、CCR4、CCR5、CCR6、CCR7、CCR8、CCR9、CD1、CD2、CD3、CD3E、CD4、CD5、CD6、CD7、CD8、CD10、CD11a、CD11b、CD11c、CD13、CD14、CD15、CD16、CD18、CD19、CD20、CD21、CD22、CD23、CD25、CD27L、CD28、CD29、CD30、CD30L、CD32、CD33(p67タンパク質)、CD34、CD38、CD40、CD40L、CD44、CD45、CD46、CD49a、CD52、CD54、CD55、CD56、CD61、CD64、CD66e、CD74、CD80(B7-1)、CD89、CD95、CD123、CD137、CD138、CD140a、CD146、CD147、CD148、CD152、CD164、CEACAM5、CFTR、cGMP、CINC、ボツリヌス菌毒素、ウェルシュ菌毒素、CKb8-1、CLC、CMV、CMV UL、CNTF、CNTN-1、COX、C-Ret、CRG-2、CT-1、CTACK、CTGF、CTLA-4、PD1、PDL1、LAG3、TIM3、galectin-9、CX3CL1、CX3CR1、CXCL、CXCL1、CXCL2、CXCL3、CXCL4、CXCL5、CXCL6、CXCL7、CXCL8、CXCL9、CXCL10、CXCL11、CXCL12、CXCL13、CXCL14、CXCL15、CXCL16、CXCR、CXCR1、CXCR2、CXCR3、CXCR4、CXCR5、CXCR6、サイトケラチン腫瘍関連抗原、DAN、DCC、DcR3、DC-SIGN、補体制御因子(Decay accelerating factor)、des(1-3)-IGF-I(脳IGF-1)、Dhh、ジゴキシン、DNAM-1、Dnase、Dpp、DPPIV/CD26、Dtk、ECAD、EDA、EDA-A1、EDA-A2、EDAR、EGF、EGFR(ErbB-1)、EMA、EMMPRIN、ENA、エンドセリン受容体、エンケファリナーゼ、eNOS、Eot、エオタキシン1、エフリンB2/EphB4、EPO、ERCC、E-セレクチン、ET-1、ファクターIIa、ファクターVII、ファクターVIIIc、ファクターIX、線維芽細胞活性化タンパク質(FAP)、Fas、FcR1、FEN-1、フェリチン、FGF、FGF-19、FGF-2、FGF3、FGF-8、FGFR、FGFR-3、フィブリン、FL、FLIP、Flt-3、Flt-4、卵胞刺激ホルモン、フラクタルカイン、FZD1、FZD2、FZD3、FZD4、FZD5、FZD6、FZD7、FZD8、FZD9、FZD10、G250、Gas6、GCP-2、GCSF、GD2、GD3、GDF、GDF-1、GDF-3(Vgr-2)、GDF-5(BMP-14、CDMP-1)、GDF-6(BMP-13、CDMP-2)、GDF-7(BMP-12、CDMP-3)、GDF-8(ミオスタチン)、GDF-9、GDF-15(MIC-1)、GDNF、GDNF、GFAP、GFRa-1、GFR-アルファ1、GFR-アルファ2、GFR-アルファ3、GITR、グルカゴン、Glut4、糖タンパク質IIb/IIIa(GPIIb/IIIa)、GM-CSF、gp130、gp72、GRO、成長ホルモン放出因子、ハプテン(NP-capまたはNIP-cap)、HB-EGF、HCC、HCMV gBエンベロープ糖タンパク質、HCMV gHエンベロープ糖タンパク質、HCMV UL、造血成長因子(HGF)、Hep B gp120、ヘパラナーゼ、Her2、Her2/neu(ErbB-2)、Her3(ErbB-3)、Her4(ErbB-4)、単純ヘルペスウイルス(HSV) gB糖タンパク質、HSV gD糖タンパク質、HGFA、高分子量黒色腫関連抗原(HMW-MAA)、HIV gp120、HIV IIIB gp 120 V3ループ、HLA、HLA-DR、HM1.24、HMFG PEM、HRG、Hrk、ヒト心臓ミオシン、ヒトサイトメガロウイルス(HCMV)、ヒト成長ホルモン(HGH)、HVEM、I-309、IAP、ICAM、ICAM-1、ICAM-3、ICE、ICOS、IFNg、Ig、IgA受容体、IgE、IGF、IGF結合タンパク質、IGF-1R、IGFBP、IGF-I、IGF-II、IL、IL-1、IL-1R、IL-2、IL-2R、IL-4、IL-4R、IL-5、IL-5R、IL-6、IL-6R、IL-8、IL-9、IL-10、IL-12、IL-13、IL-15、IL-18、IL-18R、IL-21、IL-23、IL-27、インターフェロン(INF)-アルファ、INF-ベータ、INF-ガンマ、インヒビン、iNOS、インスリンA鎖、インスリンB鎖、インスリン様増殖因子1、インテグリンアルファ2、インテグリンアルファ3、インテグリンアルファ4、インテグリンアルファ4/ベータ1、インテグリンアルファ4/ベータ7、インテグリンアルファ5(アルファV)、インテグリンアルファ5/ベータ1、インテグリンアルファ5/ベータ3、インテグリンアルファ6、インテグリンベータ1、インテグリンベータ2、インターフェロンガンマ、IP-10、I-TAC、JE、カリクレイン2、カリクレイン5、カリクレイン6、カリクレイン11、カリクレイン12、カリクレイン14、カリクレイン15、カリクレインL1、カリクレインL2、カリクレインL3、カリクレインL4、KC、KDR、ケラチノサイト増殖因子(KGF)、ラミニン5、LAMP、LAP、LAP(TGF-1)、潜在的TGF-1、潜在的TGF-1 bp1、LBP、LDGF、LECT2、レフティ、ルイス-Y抗原、ルイス-Y関連抗原、LFA-1、LFA-3、Lfo、LIF、LIGHT、リポタンパク質、LIX、LKN、Lptn、L-セレクチン、LT-a、LT-b、LTB4、LTBP-1、肺表面、黄体形成ホルモン、リンホトキシンベータ受容体、Mac-1、MAdCAM、MAG、MAP2、MARC、MCAM、MCAM、MCK-2、MCP、M-CSF、MDC、Mer、METALLOPROTEASES、MGDF受容体、MGMT、MHC(HLA-DR)、MIF、MIG、MIP、MIP-1-アルファ、MK、MMAC1、MMP、MMP-1、MMP-10、MMP-11、MMP-12、MMP-13、MMP-14、MMP-15、MMP-2、MMP-24、MMP-3、MMP-7、MMP-8、MMP-9、MPIF、Mpo、MSK、MSP、ムチン(Muc1)、MUC18、ミュラー管抑制物質、Mug、MuSK、NAIP、NAP、NCAD、N-Cアドヘリン、NCA 90、NCAM、NCAM、ネプリライシン、ニューロトロフィン-3、-4、または-6、ニュールツリン、神経成長因子(NGF)、NGFR、NGF-ベータ、nNOS、NO、NOS、Npn、NRG-3、NT、NTN、OB、OGG1、OPG、OPN、OSM、OX40L、OX40R、p150、p95、PADPr、副甲状腺ホルモン、PARC、PARP、PBR、PBSF、PCAD、P-カドヘリン、PCNA、PDGF、PDGF、PDK-1、PECAM、PEM、PF4、PGE、PGF、PGI2、PGJ2、PIN、PLA2、胎盤性アルカリホスファターゼ(PLAP)、PlGF、PLP、PP14、プロインスリン、プロレラキシン、プロテインC、PS、PSA、PSCA、前立腺特異的膜抗原(PSMA)、PTEN、PTHrp、Ptk、PTN、R51、RANK、RANKL、RANTES、RANTES、レラキシンA鎖、レラキシンB鎖、レニン、呼吸器多核体ウイルス(RSV)F、RSV Fgp、Ret、リウマイド因子、RLIP76、RPA2、RSK、S100、SCF/KL、SDF-1、SERINE、血清アルブミン、sFRP-3、Shh、SIGIRR、SK-1、SLAM、SLPI、SMAC、SMDF、SMOH、SOD、SPARC、Stat、STEAP、STEAP-II、TACE、TACI、TAG-72(腫瘍関連糖タンパク質-72)、TARC、TCA-3、T細胞受容体(例えば、T細胞受容体アルファ/ベータ)、TdT、TECK、TEM1、TEM5、TEM7、TEM8、TERT、睾丸PLAP様アルカリホスファターゼ、TfR、TGF、TGF-アルファ、TGF-ベータ、TGF-ベータ Pan Specific、TGF-ベータRI(ALK-5)、TGF-ベータRII、TGF-ベータRIIb、TGF-ベータRIII、TGF-ベータ1、TGF-ベータ2、TGF-ベータ3、TGF-ベータ4、TGF-ベータ5、トロンビン、胸腺Ck-1、甲状腺刺激ホルモン、Tie、TIMP、TIQ、組織因子、TMEFF2、Tmpo、TMPRSS2、TNF、TNF-アルファ、TNF-アルファベータ、TNF-ベータ2、TNFc、TNF-RI、TNF-RII、TNFRSF10A(TRAIL R1 Apo-2、DR4)、TNFRSF10B(TRAIL R2 DR5、KILLER、TRICK-2A、TRICK-B)、TNFRSF10C(TRAIL R3 DcR1、LIT、TRID)、TNFRSF10D(TRAIL R4 DcR2、TRUNDD)、TNFRSF11A(RANK ODF R、TRANCE R)、TNFRSF11B(OPG OCIF、TR1)、TNFRSF12(TWEAK R FN14)、TNFRSF13B(TACI)、TNFRSF13C(BAFF R)、TNFRSF14(HVEM ATAR、HveA、LIGHT R、TR2)、TNFRSF16(NGFR p75NTR)、TNFRSF17(BCMA)、TNFRSF18(GITR AITR)、TNFRSF19(TROY TAJ、TRADE)、TNFRSF19L(RELT)、TNFRSF1A(TNF RI CD120a、p55-60)、TNFRSF1B(TNF RII CD120b、p75-80)、TNFRSF26(TNFRH3)、TNFRSF3(LTbR TNF RIII、TNFC R)、TNFRSF4(OX40 ACT35、TXGP1 R)、TNFRSF5(CD40 p50)、TNFRSF6(Fas Apo-1、APT1、CD95)、TNFRSF6B(DcR3 M68、TR6)、TNFRSF7(CD27)、TNFRSF8(CD30)、TNFRSF9(4-1BB CD137、ILA)、TNFRSF21(DR6)、TNFRSF22(DcTRAIL R2 TNFRH2)、TNFRST23(DcTRAIL R1 TNFRH1)、TNFRSF25(DR3 Apo-3、LARD、TR-3、TRAMP、WSL-1)、TNFSF10(TRAIL Apo-2リガンド、TL2)、TNFSF11(TRANCE/RANKリガンド ODF、OPGリガンド)、TNFSF12(TWEAK Apo-3リガンド、DR3リガンド)、TNFSF13(APRIL TALL2)、TNFSF13B(BAFF BLYS、TALL1、THANK、TNFSF20)、TNFSF14(LIGHT HVEMリガンド、LTg)、TNFSF15(TL1A/VEGI)、TNFSF18(GITRリガンド AITRリガンド、TL6)、TNFSF1A(TNF-a コネクチン(Conectin)、DIF、TNFSF2)、TNFSF1B(TNF-b LTa、TNFSF1)、TNFSF3(LTb TNFC、p33)、TNFSF4(OX40リガンド gp34、TXGP1)、TNFSF5(CD40リガンド CD154、gp39、HIGM1、IMD3、TRAP)、TNFSF6(Fasリガンド Apo-1リガンド、APT1リガンド)、TNFSF7(CD27リガンド CD70)、TNFSF8(CD30リガンド CD153)、TNFSF9(4-1BBリガンド CD137リガンド)、TP-1、t-PA、Tpo、TRAIL、TRAIL R、TRAIL-R1、TRAIL-R2、TRANCE、トランスフェリン受容体、TRF、Trk、TROP-2、TLR(Toll-like receptor)1、TLR2、TLR3、TLR4、TLR5、TLR6、TLR7、TLR8、TLR9、TLR10、TSG、TSLP、腫瘍関連抗原CA125、腫瘍関連抗原発現ルイスY関連炭水化物、TWEAK、TXB2、Ung、uPAR、uPAR-1、ウロキナーゼ、VCAM、VCAM-1、VECAD、VE-Cadherin、VE-cadherin-2、VEFGR-1(flt-1)、VEGF、VEGFR、VEGFR-3(flt-4)、VEGI、VIM、ウイルス抗原、VLA、VLA-1、VLA-4、VNRインテグリン、フォン・ヴィレブランド因子、WIF-1、WNT1、WNT2、WNT2B/13、WNT3、WNT3A、WNT4、WNT5A、WNT5B、WNT6、WNT7A、WNT7B、WNT8A、WNT8B、WNT9A、WNT9A、WNT9B、WNT10A、WNT10B、WNT11、WNT16、XCL1、XCL2、XCR1、XCR1、XEDAR、XIAP、XPD、HMGB1、IgA、Aβ、CD81、CD97、CD98、DDR1、DKK1、EREG、Hsp90、IL-17/IL-17R、IL-20/IL-20R、酸化LDL、PCSK9、prekallikrein 、RON、TMEM16F、SOD1、Chromogranin A、Chromogranin B、tau、VAP1、高分子キニノーゲン、IL-31、IL-31R、Nav1.1、Nav1.2、Nav1.3、Nav1.4、Nav1.5、Nav1.6、Nav1.7、Nav1.8、Nav1.9、EPCR、C1、C1q、C1r、C1s、C2、C2a、C2b、C3、C3a、C3b、C4、C4a、C4b、C5、C5a、C5b、C6、C7、C8、C9、factor B、factor D、factor H、properdin、sclerostin、fibrinogen、fibrin、prothrombin、thrombin、組織因子、factor V、factor Va、factor VII、factor VIIa、factor VIII、factor VIIIa、factor IX、factor IXa、factor X、factor Xa、factor XI、factor XIa、factor XII、factor XIIa、factor XIII、factor XIIIa、TFPI、antithrombin III、EPCR、トロンボモデュリン、TAPI、tPA、plasminogen、plasmin、PAI-1、PAI-2、GPC3、Syndecan-1、Syndecan-2、Syndecan-3、Syndecan-4、LPA、S1Pならびにホルモンおよび成長因子のための受容体が例示され得る。抗原としてはがん組織におけるがん細胞・免疫細胞・ストローマ細胞等に発現する抗原
が好ましい。
本明細書において、「抗原結合ドメイン」は目的とする抗原に結合するかぎりどのような構造のドメインも使用され得る。そのようなドメインの例として、例えば、抗体の重鎖および軽鎖の可変領域、生体内に存在する細胞膜タンパクであるAvimerに含まれる35アミノ酸程度のAドメインと呼ばれるモジュール(国際公開WO2004/044011、WO2005/040229)、細胞膜に発現する糖たんぱく質であるfibronectin中のタンパク質に結合するドメインである10Fn3ドメインを含むAdnectin(国際公開WO2002/032925)、ProteinAの58アミノ酸からなる3つのヘリックスの束(bundle)を構成するIgG結合ドメインをscaffoldとするAffibody(国際公開WO1995/001937)、33アミノ酸残基を含むターンと2つの逆並行ヘリックスおよびループのサブユニットが繰り返し積み重なった構造を有するアンキリン反復(ankyrin repeat:AR)の分子表面に露出する領域であるDARPins(Designed Ankyrin Repeat proteins)(国際公開WO2002/020565)、好中球ゲラチナーゼ結合リポカリン(neutrophil gelatinase-associated lipocalin(NGAL))等のリポカリン分子において高度に保存された8つの逆並行ストランドが中央方向にねじれたバレル構造の片側を支える4つのループ領域であるAnticalin等(国際公開WO2003/029462)、ヤツメウナギ、ヌタウナギなど無顎類の獲得免疫システムとしてイムノグロブリンの構造を有さない可変性リンパ球受容体(variable lymphocyte receptor(VLR))のロイシン残基に富んだリピート(leucine-rich-repeat(LRR))モジュールが繰り返し積み重なった馬てい形の構造の内部の並行型シート構造のくぼんだ領域(国際公開WO2008/016854)が好適に挙げられる。
本開示の抗原結合ドメインの好適な例として、抗体の重鎖および軽鎖の可変領域を含む抗原結合ドメインが挙げられる。こうした抗原結合ドメインの例としては、「scFv(single chain Fv)」、「単鎖抗体(single chain antibody)」、「Fv」、「scFv2(single chain Fv 2)」、「Fab」または「F(ab')2」等が好適に挙げられる。
本開示において、抗原結合ドメインを含む抗原結合分子は最も広義な意味として使用されており、具体的には、それらが抗原結合ドメインを含む限り、様々な分子型が含まれる。抗原結合分子は、抗原結合ドメインのみからなる分子であっても良く、抗原結合ドメイン及び他のドメインを含む分子であっても良い。例えば、抗原結合分子が抗原結合ドメインとFc領域が結合した分子で有る場合、例として、完全抗体や抗体断片が挙げられる。抗体には、単一のモノクローナル抗体(アゴニストおよびアンタゴニスト抗体を含む)、ヒト抗体、ヒト化抗体、キメラ抗体等が含まれ得る。既存の安定なα/βバレルタンパク質構造等の立体構造が scaffold(土台)として用いられ、その一部分の構造のみが抗原結合ドメインの構築のためにライブラリ化されたスキャフォールド分子も、本開示の抗原結合分子に含まれ得る 。
本明細書において、抗体とは、天然のものであるかまたは部分的もしくは完全合成により製造された免疫グロブリンをいう。抗体はそれが天然に存在する血漿や血清等の天然資源や抗体を産生するハイブリドーマ細胞の培養上清から単離され得るし、または遺伝子組換え等の手法を用いることによって部分的にもしくは完全に合成され得る。抗体の例としては免疫グロブリンのアイソタイプおよびそれらのアイソタイプのサブクラスが好適に挙げられる。ヒトの免疫グロブリンとして、IgG1、IgG2、IgG3、IgG4、IgA1、IgA2、IgD、IgE、IgMの9種類のクラス(アイソタイプ)が知られている。本開示の抗体には、これらのアイソタイプのうちIgG1、IgG2、IgG3、IgG4が含まれ得る。ヒトIgG1、ヒトIgG2、ヒトIgG3、ヒトIgG4定常領域としては、遺伝子多型による複数のアロタイプ配列がSequences of proteins of immunological interest, NIH Publication No.91-3242 に記載されているが、本開示においてはそのいずれであっても良い。特にヒトIgG1の配列としては、EUナンバリングで表される356-358位のアミノ酸配列がDELであってもEEMであってもよい。また、ヒトIgκ(Kappa)定常領域とヒトIgλ (Lambda)定常領域としては、遺伝子多型による複数のアロタイプ配列がSequences of proteins of immunological interest, NIH Publication No.91-3242に記載されているが、本開示においてはそのいずれであっても良い。
本開示で使用されている方法によると、抗体のCDRとFRに割り当てられるアミノ酸位置はKabatにしたがって規定される(Sequences of Proteins of Immunological Interest(National Institute of Health, Bethesda, Md., 1987年および1991年)。本明細書において、抗原結合分子が抗体または抗原結合断片である場合、可変領域のアミノ酸はKabatナンバリングにしたがい、定常領域のアミノ酸はKabatのアミノ酸位置に準じたEUナンバリングにしたがって表される。
用語「可変領域」または「可変ドメイン」は、抗体を抗原へと結合させることに関与する、抗体の重鎖または軽鎖のドメインのことをいう。天然型抗体の重鎖および軽鎖の可変ドメイン(それぞれVHおよびVL)は、通常、各ドメインが4つの保存されたフレームワーク領域 (FR) および3つの超可変領域 (HVR) を含む、類似の構造を有する。(例えば、Kindt et al. Kuby Immunology, 6th ed., W.H. Freeman and Co., page 91 (2007) 参照。)1つのVHまたはVLドメインで、抗原結合特異性を与えるに充分であろう。さらに、ある特定の抗原に結合する抗体は、当該抗原に結合する抗体からのVHまたはVLドメインを使ってそれぞれVLまたはVHドメインの相補的ライブラリをスクリーニングして、単離されてもよい。例えばPortolano et al., J. Immunol. 150:880-887 (1993); Clarkson et al., Nature 352:624-628 (1991) 参照。
本明細書で用いられる用語「超可変領域」または「HVR」は、配列において超可変であり(「相補性決定領域」または「CDR」(complementarity determining region))、および/または構造的に定まったループ(「超可変ループ」)を形成し、および/または抗原接触残基(「抗原接触」)を含む、抗体の可変ドメインの各領域のことをいう。通常、抗体は6つのHVRを含む:VHに3つ(H1、H2、H3)、およびVLに3つ(L1、L2、L3)である。本明細書での例示的なHVRは、以下のものを含む:
(a) アミノ酸残基26-32 (L1)、50-52 (L2)、91-96 (L3)、26-32 (H1)、53-55 (H2)、および96-101 (H3)のところで生じる超可変ループ (Chothia and Lesk, J. Mol. Biol. 196:901-917 (1987));
(b) アミノ酸残基24-34 (L1)、50-56 (L2)、89-97 (L3)、31-35b (H1)、50-65 (H2)、 および95-102 (H3)のところで生じるCDR (Kabat et al., Sequences of Proteins of Immunological Interest, 5th Ed. Public Health Service, National Institutes of Health, Bethesda, MD (1991));
(c) アミノ酸残基27c-36 (L1)、46-55 (L2)、89-96 (L3)、30-35b (H1)、47-58 (H2)、および93-101 (H3) のところで生じる抗原接触 (MacCallum et al. J. Mol. Biol. 262: 732-745 (1996));ならびに、
(d) HVRアミノ酸残基46-56 (L2)、47-56 (L2)、48-56 (L2)、49-56 (L2)、26-35 (H1)、26-35b (H1)、49-65 (H2)、93-102 (H3)、および94-102 (H3)を含む、(a)、(b)、および/または(c)の組合せ。
別段示さない限り、HVR残基および可変ドメイン中の他の残基(例えば、FR残基)は、本明細書では上記のKabatらにしたがって番号付けされる。
「フレームワーク」または「FR」は、超可変領域 (HVR) 残基以外の、可変ドメイン残基のことをいう。可変ドメインのFRは、通常4つのFRドメイン:FR1、FR2、FR3、およびFR4からなる。それに応じて、HVRおよびFRの配列は、通常次の順序でVH(またはVL)に現れる:FR1-H1(L1)-FR2-H2(L2)-FR3-H3(L3)-FR4。
Fc領域は、抗体重鎖の定常領域に由来するアミノ酸配列を含む。Fc領域は、EUナンバリングで表されるおよそ216位のアミノ酸における、パパイン切断部位のヒンジ領域のN末端から、当該ヒンジ、CH2およびCH3ドメインを含める抗体の重鎖定常領域の部分である。Fc領域は、ヒトIgG1から取得され得るが、IgGの特定のサブクラスに限定されるものでもない。当該Fc領域の好適な例として、後述されるようにpH酸性域におけるFcRnに対する結合活性を有するFc領域が挙げられる。また当該Fc領域の好適な例として、後述されるようにFcγレセプターに対する結合活性を有するFc領域が挙げられる。そのようなFc領域の非限定な一態様として、ヒトIgG1(配列番号:5)、IgG2(配列番号:6)、IgG3(配列番号:7)、またはIgG4(配列番号:8)で表されるFc領域が例示される。
本開示で使用される抗体は、抗体の全長分子に限られず、低分子化抗体またはその修飾物であってもよい。低分子化抗体は、全長抗体(例えば、whole IgG等のwhole antibody)の一部分が欠損している抗体断片を含み、抗原に対する結合活性を有していれば特に限定されない。本開示の低分子化抗体は、全長抗体の一部分であれば特に限定されないが、重鎖可変領域(VH)又は/及び軽鎖可変領域(VL)を含んでいることが好ましい。VHまたはVLのアミノ酸配列は、置換、欠失、付加及び/又は挿入がされていてもよい。さらに抗原に対する結合活性を有する限り、VH又は/及びVLの一部を欠損させてもよい。又、可変領域はキメラ化やヒト化されていてもよい。抗体断片の具体例としては、例えば、Fab、Fab'、F(ab')2、Fvなどを挙げることができる。また、低分子化抗体の具体例としては、例えば、Fab、Fab'、F(ab')2、Fv、scFv(single chain Fv)、Diabody、sc(Fv)2(single chain (Fv)2)などを挙げることができる。これら抗体の多量体(例えば、ダイマー、トリマー、テトラマー、ポリマー)も、本開示の低分子化抗体に含まれる。
-[VL]リンカー[VH]リンカー[VH]リンカー[VL]
-[VH]リンカー[VL]リンカー[VL]リンカー[VH]
-[VH]リンカー[VH]リンカー[VL]リンカー[VL]
-[VL]リンカー[VL]リンカー[VH]リンカー[VH]
-[VL]リンカー[VH]リンカー[VL]リンカー[VH]
-[VH]ペプチドリンカー(15アミノ酸)[VL]ペプチドリンカー(15アミノ酸)[VH]ペプチドリンカー(15アミノ酸)[VL]
4つの抗体可変領域を結合する場合には、通常、3つのリンカーが必要となるが、全て同じリンカーを用いてもよいし、異なるリンカーを用いてもよい。
本発明の抗原結合ドメインの好適な例の一つとして、単ドメイン抗体(sdAb)が挙げられる。
MTAを含む低分子化合物に依存的でなく、低分子化合物と異なる分子である抗原に対して所望の結合活性を有する抗体を作製する方法は当業者において公知である。以下に、IL-6Rに結合する抗体(抗IL-6R抗体)を作製する方法が例示される。IL-6R以外の抗原に結合する抗体も下記の例示に準じて適宜作製され得る。
-IL-6Rのような膜蛋白質の構造を維持して免疫刺激が与えられ得る。
-免疫抗原を精製する必要が無い。
-グアニジン超遠心法(Biochemistry (1979) 18 (24), 5294-5299)
-AGPC法(Anal. Biochem. (1987) 162 (1), 156-159)
(1)ハイブリドーマから得られたcDNAによってコードされるV領域を含む抗体をIL-6R発現細胞に接触させる工程、
(2)IL-6R発現細胞と抗体との結合を検出する工程、および
(3)IL-6R発現細胞に結合する抗体を選択する工程。
(1)哺乳類細胞、:CHO(Chinese hamster ovary cell line)、COS(Monkey kidney cell line)、ミエローマ(Sp2/0、NS0等)、BHK (baby hamster kidney cell line)、Hela、Vero、HEK293(human embryonic kidney cell line with sheared adenovirus (Ad)5 DNA)、PER.C6 cell (human embryonic retinal cell line transformed with the Adenovirus Type 5 (Ad5) E1A and E1B genes)など(Current Protocols in Protein Science (May, 2001, Unit 5.9, Table 5.9.1))
(2)両生類細胞:アフリカツメガエル卵母細胞など
(3)昆虫細胞:sf9、sf21、Tn5など
-酵母:サッカロミセス・セレビシエ(Saccharomyces serevisiae)などのサッカロミセス(Saccharomyces )属、メタノール資化酵母(Pichia pastoris)などのPichia属。
-糸状菌:アスペスギルス・ニガー(Aspergillus niger)などのアスペルギルス(Aspergillus )属。
また、低分子化合物に連結させる抗原はKLHに限定されるものではなく、例えばビオチンなどと連結したものを感作抗原として使用してもよく、さらにKLH、ビオチン以外にも低分子化合物に連結可能であれば使用可能され得る。
本開示はまた、以下に例示的に記載する態様を包含するものである。
[1] ビオチン化MTA。
[2] Biotin-2’-MTA。
[3] 6’-MTA-biotin。
[4]MTAに結合する抗原結合分子をスクリーニングするための[1]から[3]に記載のビオチン化MTAの使用。
[5] MTAに結合する抗原結合分子を取得するための免疫原としての[1]から[3]に記載のビオチン化MTAの使用。
[6] [1]から[3]に記載のビオチン化MTAを用いて、MTAに結合する抗原結合分子をスクリーニングする方法。
その少なくとも一つの抗原結合ドメインが抗原分子中の第一のエピトープに結合し、その少なくとも一つの別の抗原結合ドメインが抗原分子中の第二のエピトープに結合する特徴を有する、少なくとも二つの抗原結合ドメインを含む抗原結合分子は、その反応の特異性という観点から多重特異性抗原結合分子と呼ばれる。一分子の抗原結合分子に含まれる二種類の抗原結合ドメインによって当該抗原結合分子が、二つの異なるエピトープに結合する場合、当該抗原結合分子は二重特異性抗原結合分子と呼ばれる。また、一分子の抗原結合分子に含まれる三種類の抗原結合ドメインによって当該抗原結合分子が、三つの異なるエピトープに結合する場合、当該抗原結合分子は三重特異性抗原結合分子と呼ばれる。
一つまたは複数の抗原結合ドメインを含む多価の多重特異性または多重パラトピック抗原結合分子とその調製方法は、Conrathら(J.Biol.Chem. (2001) 276 (10) 7346-7350)、Muyldermans(Rev. Mol. Biotech. (2001) 74, 277-302)およびKontermann R.E. (2011) Bispecific Antibodies(Springer-Verlag)等の非特許文献、ならびに国際公開WO1996/034103またはWO1999/023221等の特許文献等にも記載されている。これらに記載された多重特異性または多重パラトピック抗原結合分子とその調製方法を用いることによって、本開示の抗原結合分子を作製することが可能である
本明細書において、「がん」という用語は、一般に、悪性新生物を表すために用いられ、それは、転移性または非転移性であってよい。例えば、消化管や皮膚等の上皮組織から発生した癌腫の非限定な例として、脳腫瘍、皮膚癌、頸頭部癌、食道癌、肺癌、胃癌、十二指腸癌、乳癌、前立腺癌、子宮頸癌、子宮体癌、膵臓癌、肝臓癌、大腸癌、結腸癌、膀胱癌、および卵巣癌等が例示される。また、筋肉等の非上皮性組織(間質)から発生した肉腫の非限定な例として、骨肉腫、軟骨肉腫、横紋筋肉腫、平滑筋肉腫、脂肪肉腫、および血管肉腫等が例示される。さらに、造血器由来の血液がんの非限定な例として、ホジキンリンパ腫(Hodgkin's lymphoma)および非ホジキンリンパ腫(non Hodgkin's lymphoma)を含む悪性リンパ腫、急性(acute myelocytic leukemia)または慢性骨髄性白血病(chronic myelocytic leukemia)、および急性(acute lymphatic leukemia)または慢性リンパ性白血病(chronic lymphatic leukemia)を含む白血病、ならびに多発性骨髄腫(multiple myeloma)が例示される。本明細書で広く用いられる「新生物」という用語は、新たに生じたいかなる病的組織腫瘍をも意味する。本開示においては、新生物は腫瘍の形成を生じ、それは部分的に血管形成を特徴とする。新生物は、例えば、血管腫、神経膠腫、奇形腫等の良性、あるいは、例えば、癌腫、肉腫、膠細胞腫、星状膠細胞腫、神経芽細胞腫、網膜芽腫等の悪性でありうる。
また、MTAを代謝するメチルチオアデノシンホスフォリラーゼ(MTAP:methylthioadenosine phosphorylase)が欠損したがん組織やMTAPの機能が低下しているがん組織もMTAが蓄積しているがん組織の一態様である。具体的には、MTAPをコードしている遺伝子が欠損もしくは発現低下しているがん組織、MTAPの活性を低下させる変異もしくはスプライシングバリアントを発現しているがん組織、またはMTAPの酵素活性が低下しているがん組織が、MTAが蓄積しているがん組織の一態様である。MTAPの発現または機能の低下は、正常組織と比較することで決定することができ、比較対象となる正常組織の非限定な一例としては、がん組織の隣接正常組織や健常人の組織が例示され得る。
本開示において「Cancer-associated fibroblast (CAF)」とは、がん組織周辺部に存在す内皮細胞等,多様な起源を持つheterogeneous な集団である。非限定なCAFの特徴としては、がん細胞の増殖促進,血管新生の促進,がん細胞の脈管浸潤促進,免疫応答の制御等を通じてがんの進展に有利な微小環境を構築する等がある。さらに、非限定なCAFの一態様として、α-smooth muscle actin (α-SMA)、fibroblast activation protein (FAP)、tenascin-C (TN-C)、periostin (POSTN)、NG2 chondroitin sulfate proteoglycan (NG2)、platelet derived growth factor receptor (PDGFR)、vimentin、desmin、fibroblast specific protein-1 (FSP1)、fibronectinから選ばれるマーカーが発現している細胞が例示される。
本開示において「Tumor-associated macrophage(TAM)」とは、がん組織およびその周辺部に存在するマクロファージをいう。例えば、線維芽細胞や血管内皮細胞などとともに、がんの微小環境を形成するマクロファージ集団が例示される。非限定なTAMの特徴として、抗炎症性因子の産生や制御性T細胞の浸潤を促すことで抗腫瘍免疫を抑制するなど、種々の血管新生因子の産生によって新生血管を誘導することが例示される。さらに、非限定なTAMの一態様として、CD163、CD204、IL-10、TGF-β、Prastaglandin E2から選ばれるマーカーが発現している細胞が例示される。
本開示において、「エフェクター細胞」とは、T細胞(CD4+(ヘルパーリンパ球)T細胞および/またはCD8+(細胞傷害性)T細胞)、多核白血球(好中球、好酸球、好塩基球、肥満細胞)、単球、マクロファージ、組織球またはナチュラルキラー細胞(NK細胞)、NK様T細胞、クッパー細胞、ランゲルハンス細胞、またはリンフォカイン活性化キラー細胞(LAK細胞)等の白血球、Bリンパ球、もしくは樹状細胞またはマクロファージ等の抗原提示細胞を含む最も広義な意味で使用され得るが、好適なエフェクター細胞の例としては、CD8+(細胞傷害性)T細胞、NK細胞、またはマクロファージが挙げられる。エフェクター細胞の細胞膜に発現する膜型分子であれば、本開示の抗原結合分子に含まれる少なくとも1つの抗原結合ドメインが結合する抗原として使用され得るが、好適な膜型分子としては、TCRを構成するポリペプチド、CD3、CD2、CD28、CD44、CD16、CD32、CD64、またはNKG2DもしくはNK細胞活性化リガンドが非限定な例として例示され得る。
本明細書中で用いられる用語「MTA」は、メチルチオアデノシン(Methylthioadenosine)を指しており、具体的には、下記化学式で示される化合物を指す。
本明細書中で用いられる用語「MTA類縁体」は、MTAと一部共通の構造を有するMTA以外の低分子化合物を指す。MTA類縁体として、分子中にアデノシンを共通骨格として有する低分子化合物が例示されうるし、またアデノシン中の5位の炭素に硫黄原子や酸素原子を含む側鎖を有する低分子化合物が例示される。さらにMTA類縁体として、これらに限定されるものではないが、例えば、S-アデノシルメチオニン(SAM:S-adenoshylmethionine)、S-アデノシルホモシステイン(SAH:S-adenosylhomocystein、S-(5'-Adenosyl)-L-homocysteine)等のポリアミン生合成経路の代謝物(Stevensら(J Chromatogr A. 2010 May 7;1217(19):3282-8))が好適に挙げられる。
また、MTA類縁体の非限定的な一態様として、アデノシン、アデノシン3リン酸(ATP)、アデノシン2リン酸(ADP)、アデノシン1リン酸(AMP)が挙げられる。
本開示中で用いられる用語「低分子化合物」は、生体に存在する「生体高分子」以外の天然由来の化学物質又は非天然由来の化学物質をいう。低分子化合物として、これらに限定されるものではないが、例えば、天然に存在する、もしくは人工的に合成される分子量が10000以下の化合物、好ましくは分子量が1000以下の化合物が列挙される。低分子化合物の非限定的な態様として、例えば、がん組織特異的化合物、炎症組織特異的化合物、非天然化合物が例示される。
本明細書中で用いられる、用語「がん組織特異的な化合物(がん組織特異的化合物)」とは、非がん組織と比較してがん組織中に差示的に存在する化合物をいう。
用語「代謝」は、生物の組織内で生ずる化学変化のことをいい、「同化」および「異化」が含まれる。同化とは、分子の生合成または蓄積のことをいい、異化は分子の分解のことをいう。「代謝産物」は、物質代謝に起因する中間体または生成物である。「一次代謝産物」とは、細胞または生物の成長もしくは繁殖の過程に直接関わる代謝産物を指し、「二次代謝産物」とはそれらの成長もしくは繁殖の過程には直接関わらず、細胞または生物に共通の生命現象に直接関与しない物質を生合成する代謝の結果生じる抗生物質や色素等の生産物をいう。代謝産物は、「生体高分子」の代謝産物でもあり得るし、「低分子」の代謝産物でもあり得る。「生体高分子」は、一種類以上の反復単位からなる高分子である。生体高分子は、一般に生物系で見出され、生物を組織する細胞およびそれに付着する細胞間マトリックス、組織間マトリックス等の構造物を形成する分子量がおよそ5000以上の分子、特に多糖類(炭水化物等)およびペプチド(この用語はポリペプチドおよびタンパク質を含むようにして用いられる)およびポリヌクレオチド、同様にそれらの類似体、例えばアミノ酸類似体もしくは非アミノ酸基から構成もしくは含むそれらの化合物が挙げられる。
本明細書中で用いられる、用語「炎症組織特異的な化合物(炎症組織特異的化合物)」とは、非炎症組織と比較して炎症組織中に差示的に存在する化合物をいう。本明細書において、「炎症組織」とは、例えば、以下が例示的に挙げられる。
・関節リウマチや変形性関節症における関節
・気管支喘息やCOPDにおける肺(肺胞)
・炎症性腸疾患やクローン病や潰瘍性大腸炎における消化器官
・肝臓、腎臓、肺における線維化症における線維化組織
・臓器移植における拒絶反応が起こっている組織
・動脈硬化や心不全における血管、心臓(心筋)
・メタボリック症候群における内臓脂肪
・アトピー性皮膚炎その他皮膚炎における皮膚組織
・椎間板ヘルニアや慢性腰痛における脊髄神経
炎症組織特異的代謝産物とは、炎症性組織に浸潤にしている免疫細胞が高く産生する代謝産物、および、炎症組織において傷害を受けている正常細胞特異的が高く産生する代謝産物である。浸潤する免疫細胞としては、エフェクターT細胞、成熟樹状細胞、好中球、顆粒細胞(肥満細胞)、好塩基球等が例示される。また、本発明における代謝産物には、炎症組織に存在する細胞(免疫細胞、正常細胞)が、アポトーシスやネクローシス等によって細胞死した際に、細胞内から細胞外に放出される化合物も含まれる。
本発明で使用される低分子化合物、またはがん組織特異的化合物、とくにがん細胞特異的代謝産物の非限定な一態様として、乳酸、コハク酸、クエン酸等の周囲に存在する非がん部組織よりもがん組織において高濃度に存在するグルコース代謝の結果生成される一次代謝産物が好適に挙げられる。ピルビン酸キナーゼ、ヘキソキナーゼ、および乳酸脱水素酵素(LDH)等の解糖系(Embden-Myerhof経路)酵素の上方調節(アップレギュレーション)として特徴付けられる解糖系表現型は、Warburg効果として固形腫瘍の特徴であることが従来から知られている。
上述されたグルコース代謝以外にも、嫌気条件下における生体高分子の生合成に必要な必須アミノ酸および非必須アミノ酸の連続供給が必要な腫瘍細胞ではアミノ酸代謝も変化していることが知られている。グルタミンはその側鎖に二つの窒素を含む窒素運搬体として作用する、生体においてもっとも広範に分布するアミノ酸である。グルタミンの細胞内への取込み速度が上昇している腫瘍細胞はグルタミントラップ(glutamine trap)として機能しているといわれている。こうしたグルタミンの取込みとグルタミン酸および乳酸へ変換される活性の上昇は「グルタミン分解(glutaminolysis)」と呼ばれ、形質転換された(腫瘍)細胞の特徴であると思われている(MazurekおよびEigenbrodt(Anticancer Res. (2003) 23, 1149-1154、ならびにMazurekら(J. Cell. Physiol. (1999) 181, 136-146))。その結果、がん患者は血漿中のグルタミンのレベルの減少の一方でグルタミン酸濃度の増大を示す(Drogeら(Immunobiology (1987) 174, 473-479)。そして、肺癌組織の13C放射標識されたグルコースの代謝研究によって13C標識コハク酸、 13C 標識アラニン、13C 標識グルタミン酸、および13C 標識クエン酸の濃度間で相関が観察された。本発明で使用される低分子化合物、がん組織特異的化合物の非限定な一態様として、こうしたグルタミン分解等によってがん組織において高濃度に蓄積する、アラニン、グルタミン酸、アスパラギン酸等が好適に挙げられる。
インドールアミン2, 3-ジオキシゲナーゼ(IDO)はメラノーマ、結腸癌、および腎臓癌等の多くのがんで高発現しているトリプトファン代謝酵素であり(Uyttenhoveら(Nat. Med. (2003) 9, 1269-127)、二つのアイソフォームが存在することが知られている(Lobら(CancerImmunol. Immunother. (2009) 58, 153-157))。IDOはトリプトファンのキヌレニン(下記式で表される)への変換を触媒しニコチンアミドヌクレオチド(NAD)の新生経路の最初の酵素である。また、IDOを発現しないグリオーマでは肝臓のトリプトファン2, 3-ジオキシゲナーゼ(TDO)によって、トリプトファンからキヌレニンが生成する(Opitzら(Nature (2011) 478, 7368, 197-203))。またIDOはがん組織に浸潤している樹状細胞にも発現しており、樹状細胞もキヌレニンを産生する(J. Immunol. (2008) 181, 5396-5404)。またIDOはがん組織の 骨髄系由来抑制細胞(MDSC)にも発現しており、MDSCもキヌレニンを産生する(Yuら(J. Immunol. (2013) 190, 3783-3797))。
プロスタグランジンE2(PGE2)(下記式で表される)は、シクロオキシゲナーゼ(COX)-1/2によって合成されるプロスタグランジンおよびトロンボキサンを含むプラストノイドと呼ばれるアラキドン酸の代謝物である(WarnerおよびMitchell(FASEB J. (2004) 18, 790-804))。PGE2結腸癌細胞の増殖を促進し、そのアポトーシスを抑制する(Shengら(Cancer Res. (1998) 58, 362-366))。 多くのがん細胞ではシクロオキシゲナーゼの発現が変化していることが知られている。すなわち、COX-1はほぼすべての組織において構成的に発現しているのに対して、COX-2は腫瘍においてある種の炎症性サイトカインおよびがん遺伝子によって誘導されることが主に見出されている(WarnerおよびMitchell(前掲))。COX-2の過剰発現は乳癌の予後の悪さ(Denkertら(Clin. Breast Cancer (2004) 4, 428-433)、および卵巣癌の急速な疾患の進行(Denkerら(Mod. Pathol. (2006) 19, 1261-1269)と関連性があることも報告されている。またがん組織に浸潤している抑制性T細胞もプロスタグランジンE2を産生している(Curr. Med. Chem. (2011) 18, 5217-5223)。アラキドン酸の代謝物のプロスタグランジン、ロイコトリエン等の低分子化合物ががんのオートクライン、および/またはパラクラインな増殖を制御する刺激因子として作用していることが知られている(Nat. Rev. Cancer (2012) 12 (11) 782-792)。本発明で使用される低分子化合物、がん組織特異的化合物、とくにがん細胞特異的代謝産物やがん組織に浸潤している免疫細胞特異的代謝物の非限定な一態様として、こうしたプロスタグランジンE2等のアラキドン酸の代謝産物が好適に挙げられる。プロスタグランジンE2以外にも、トロンボキサンA2 (TXA2)が大腸癌等のがん組織で産生が亢進しており(J. Lab. Clin. Med. (1993) 122, 518-523)、本発明のアラキドン酸の代謝産物の非限定な一態様として好適に挙げられる。
がん細胞が細胞死すると細胞内の大量のATPが細胞外に漏出することが知られている。そのため、がん組織におけるATP濃度は正常組織と比較して著しく高い(PLoS One. (2008) 3, e2599)。複数の型の細胞がATP、ADPおよびAMPの型のアデニンヌクレオチドを遊離する。細胞外-5'-ヌクレオチダーゼ(eco-5'-nucleotidase)(CD73)のような細胞表面の細胞外酵素によって代謝される(RestaおよびThompson(Immunol. Rev. (1998) 161, 95-109)ならびにSadejら(Melanoma Res. (2006) 16, 213-222)。アデノシンは低濃度で細胞外環境に構成的に存在するプリンヌクレオシドであるが、固形癌で見出される低酸素組織では細胞外アデノシン濃度の顕著な増加が報告されている(BlayおよびHoskin(Cancer Res. (1997) 57, 2602-2605)。CD73は腫瘍および免疫細胞の表面に発現しており(Kobieら(J. Immunol. (2006) 177, 6780-6786)、乳癌(Canbolatら(Breast Cancer Res. Treat. (1996) 37, 189-193)、胃癌(Durakら(Cancer Lett. (1994) 84, 199-202)、膵臓癌(FlockeおよびMannherz(Biochim. Biophys. Acta (1991) 1076, 273-281)およびグリオブラストーマ(Bardotら(Br. J. Cancer (1994) 70, 212-218))において活性の上昇が見出されている。がん組織におけるアデノシンの蓄積は、細胞質の5'-ヌクレオチダーゼによるAMPの脱リン酸によって細胞内アデノシン生成が増加することに起因している可能性が提唱されている(HeadrickおよびWillis(Biochem. J. (1989) 261, 541-550)。さらにがん組織に浸潤している抑制性T細胞等もATP分解酵素を発現しており、アデノシンを産生している(Proc. Natl. Acad. Sci. (2006) 103 (35), 13132-13137、Curr. Med. Chem. (2011) 18, 5217-5223)。産生されたアデノシンは、A2Aレセプター等のアデノシンレセプターを介してがん組織を免疫抑制的な環境にしていると考えられている(Curr. Med. Chem. (2011),18,5217-23)。本発明で使用される低分子化合物、がん組織特異的化合物の非限定な一態様として、こうしたATP等のプリンヌクレオチドの代謝によってがん組織において高濃度に蓄積する、ATP、ADP、AMP、またはアデノシン等が好適に挙げられる。さらにアデノシンは、adenosine deaminaseによってイノシンに分解されるため、イノシンが高濃度に蓄積する。
尿酸は生体内におけるプリンヌクレオシドの代謝経路の産物であり、血液または間質腔等の細胞外に遊離される。また、近年では、がん組織等の病変部位に存在する死細胞から遊離されることが明らかとなっている(Nat. Med. (2007) 13, 851-856)。本発明で使用される低分子化合物、がん組織特異的化合物の非限定な一態様として、こうしたATP等のプリンヌクレオチドの代謝によってがん組織において高濃度に蓄積する尿酸も好適に挙げられる。
複数のヒトがん組織において酵素ニコチンアミドN-メチルトランスフェラーゼが高発現していることが知られている。本酵素がニコチンアミドから安定的な代謝物である1-メチルニコチンアミドを産生する際、メチル供与体となるS-アデノシルメチオニン(SAM)のメチル基を消費するために、がん細胞におけるSAM濃度の減少に伴ったDNAのメチル化能を損ねる機構を通じて、ニコチンアミドN-メチルトランスフェラーゼの高発現が腫瘍化(tumorigenesis)に寄与していることが提唱されている(Ulanovskayaら(Nat. Chem. Biol. (2013) 9 (5) 300-306))。本酵素の安定的な代謝産物である1-メチルニコチンアミドは、がん細胞の細胞外に分泌することが知られており(Yamadaら(J. Nutr. Sci. Vitaminol. (2010) 56, 83-86))、本発明で使用される低分子化合物、がん組織特異的化合物の非限定な一態様として、こうしたニコチンアミドの代謝によってがん組織において高濃度に蓄積する1-メチルニコチンアミド等も好適に挙げられる。
本開示における低分子化合物は抗原結合分子と相互作用し得る。低分子化合物と相互作用し得る抗原結合分子中のアミノ酸残基は、抗原結合分子中の抗原結合ドメインに存在しても良いし、抗原結合ドメイン以外の部位に存在しても良い。抗原結合分子中の低分子化合物と相互作用する部位として、抗原結合ドメインが例示されるがこれに限定されるものではない。
本明細書において、「抗原に特異的に結合する抗原結合ドメイン」は、抗原結合ドメインが、ある抗原中に含まれる複数のエピトープのうち特定のエピトープに対して特異的である場合に用いられる。また、抗原結合ドメインが結合するエピトープが複数の異なる抗原に含まれる場合には、当該抗原結合ドメインを有する抗原結合分子は当該エピトープを含む様々な抗原と結合することができる。ここで、実質的に結合しないとは上記結合活性の項で記載される方法に準じて決定され、前記相手方以外の分子に対する特異的結合分子の結合活性が、前記相手方の分子に対するの結合活性の80%以下、通常50%以下、好ましくは30%以下、特に好ましくは15%以下の結合活性を示すことをいう。抗原結合ドメインがMTAまたはMTA以外の低分子化合物依存的に抗原に対する結合活性が変化する抗原結合ドメインの場合、抗原に対する当該抗原結合ドメインの結合は、当該抗原結合ドメインの抗原に対する結合活性が高い条件(例えば、MTAの特定濃度下またはMTA非存在下、MTA以外の低分子化合物の特定濃度下またはMTA以外の低分子化合物非存在下)にて測定される。
用語「結合活性(binding activity)」は、分子(例えば、抗体)の1個またはそれ以上の結合部位と、分子の結合パートナー(例えば、抗原)との間の、非共有結合的な相互作用の合計の強度のことをいう。ここで、「結合活性(binding activity)」は、ある結合対のメンバー(例えば、抗体と抗原)の間の1:1相互作用に厳密に限定されない。例えば、結合対のメンバーが1価での1:1相互作用を反映する場合、結合活性は固有の結合アフィニティ(「アフィニティ」)のことをいう。結合対のメンバーが、1価での結合および多価での結合の両方が可能である場合、結合活性は、これらの結合力の総和となる。分子XのそのパートナーYに対する結合活性は、一般的に、解離定数 (KD) または「単位リガンド量当たりのアナライト結合量」により表すことができる。結合活性は、本明細書に記載のものを含む、当該技術分野において知られた通常の方法によって測定され得る。標的組織特異的な化合物の濃度以外の条件については当業者が適宜決定することが可能である。
結合活性を測定するための具体的な実例となるおよび例示的な態様については、下で述べる。
特定の態様において、本明細書で提供される抗原結合分子は抗体であり、抗体の結合活性(binding activity)は、≦1μM、≦100nM、≦10nM、≦1nM、≦0.1nM、≦0.01nMまたは≦0.001nM(例えば、10-8M以下、例えば10-8M~10-13M、例えば10-9M~10-13M)の解離定数 (KD) である。
特定の低分子化合物が非存在の条件において抗原結合活性を示さない抗原結合分子が、当該低分子化合物存在下において当該抗原に対する結合活性を示す場合は、当該低分子化合物存在下において結合活性を評価することができる。同様に、特定の低分子化合物存在下において抗原に対する結合活性を示さず、当該低分子化合物の非存在下で当該抗原に対する結合活性を示す場合は、当該低分子化合物の非存在下において結合活性を評価することができる。特定の低分子化合物が低濃度で存在する条件における抗原結合活性が当該低分子化合物が高濃度で存在する条件における抗原結合活性より高い場合、当該低分子化合物が高濃度で存在する条件において結合活性を評価することができる。同様に、特定の低分子化合物が高濃度で存在する条件における抗原結合活性が当該低分子化合物が低濃度で存在する条件における抗原結合活性より低い場合、当該低分子化合物が低濃度で存在する条件において結合活性を評価することができる。抗原と抗原結合分子の結合活性に影響を与えうる条件は、低分子化合物の存在下/非存在下やその低分子化合物の濃度に限定されず、イオン濃度、イオン組成または温度などが例示されるがこれらに限定されるものではない。さらに前記の異なる複数の因子が組み合わされた条件下で結合活性を評価することも当然あり得る。
抗原中に存在する抗原決定基を意味するエピトープは、本明細書において開示される抗原結合分子中の抗原結合ドメインが結合する抗原上の部位を意味する。本開示における抗原結合分子が結合する抗原上の部位は、当該抗原結合分子の結合の有無を評価することによって定義されうる。
FACSCantoTM II
FACSAriaTM
FACSArrayTM
FACSVantageTM SE
FACSCaliburTM (いずれもBD Biosciences社の商品名)
EPICS ALTRA HyPerSort
Cytomics FC 500
EPICS XL-MCL ADC EPICS XL ADC
Cell Lab Quanta / Cell Lab Quanta SC(いずれもBeckman Coulter社の商品名)
IL-6Rに対する抗原結合ドメインを含む被験抗原結合分子が、ある抗原結合分子とエピトープを共有することは、両者の同じエピトープに対する競合によって確認され得る。抗原結合分子間の競合は、交叉ブロッキングアッセイなどによって検出される。例えば競合ELISAアッセイは、好ましい交叉ブロッキングアッセイである。
ΔGeo-Mean=Geo-Mean(ポリペプチド会合体存在下)/Geo-Mean(ポリペプチド会合体非存在下)
本明細書において、「低分子化合物依存的に抗原に対する結合活性が変化する抗原結合ドメイン」とは、異なる低分子化合物濃度存在下において、前記低分子化合物とは異なる分子である抗原に対する結合活性が変化する抗原結合ドメインを意味する。
本開示におけるMTA依存的に抗原に対する結合活性が変化する抗原結合ドメインは、MTA濃度の異なる条件下において、MTAとは異なる分子である抗原に対する結合活性が異なる抗原結合ドメインである。これらの抗原結合ドメインが結合する抗原は、膜型分子であっても良く、可溶型分子であっても良い。また、これらの抗原結合ドメインが結合する抗原は、疾患組織で発現している抗原、より好ましくはがん組織で発現している抗原、更に好ましくはMTAが蓄積しているがん組織で発現する抗原である。がん組織で発現する抗原は、がん細胞に発現している抗原でもよく、がん組織中のがん間質細胞や免疫組織で発現している抗原でもよい。
MTA存在下における抗原に対する結合活性が、MTA非存在下における抗原に対する結合活性より強い抗原結合ドメインは、MTA非存在下において抗原に実質的に結合しない抗原結合ドメインを含む。
MTA存在下における抗原に対する結合活性が、前記抗原結合ドメインのMTA非存在下における抗原に対する結合活性より弱い抗原結合ドメインの場合、MTA存在下において抗原に実質的に結合しない抗原結合ドメインを含む。
高濃度のMTA存在下における抗原結合活性低濃度のMTA存在下における抗原結合活性より強い抗原結合ドメインは、低濃度のMTA存在下において抗原に実質的に結合しない抗原結合ドメインを含む。
高濃度のMTA存在下における抗原結合活性低濃度のMTA存在下における抗原結合活性より弱い抗原結合ドメインは、高濃度のMTA存在下において抗原に実質的に結合しない抗原結合ドメインを含む。
本明細書において、「抗原に対する結合活性が低分子化合物に実質的に影響されない」は、当該低分子化合物存在下における抗原結合ドメインの抗原結合活性と当該低分子化合物非存在下における抗原結合ドメインの抗原結合活性が、お互いの少なくとも0.5倍~2倍であることをいう。
別の非限定的な一態様において、本開示のMTA依存的に抗原に対する結合活性の変化する抗原結合ドメインの抗原結合活性は、S-(5'-Adenosyl)-L-homocysteine (SAH)に実質的に影響されない。
別の非限定的な一態様において、本開示のMTA依存的に抗原に対する結合活性の変化する抗原結合ドメインの抗原結合活性は、SAMに実質的に影響されない。
別の非限定的な一態様において、本開示のMTA依存的に抗原に対する結合活性の変化する抗原結合ドメインの抗原結合活性は、アデノシン、AMP、ADP、ATPのいずれにも実質的に影響されない。
別の非限定的な一態様において、本開示のMTA依存的に抗原に対する結合活性の変化する抗原結合ドメインの抗原結合活性は、アデノシン、S-(5'-Adenosyl)-L-homocysteine (SAH)のいずれにも実質的に影響されない。
別の非限定的な一態様において、本開示のMTA依存的に抗原に対する結合活性の変化する抗原結合ドメインの抗原結合活性は、アデノシン、S-(5'-Adenosyl)-L-homocysteine (SAH)、SAMのいずれにも実質的に影響されない。
別の非限定的な一態様において、本開示のMTA依存的に抗原に対する結合活性の変化する抗原結合ドメインの抗原結合活性は、アデノシン、S-(5'-Adenosyl)-L-homocysteine (SAH)、SAM、AMP、ADP、ATPのいずれにも実質的に影響されない。
非限定的な一態様において、本開示のMTA依存的に抗原に対する結合活性の変化する抗原結合ドメインの抗原結合活性は、アデノシン依存的にも変化する。MTAとアデノシンの両方の分子に依存的に結合活性が変化する抗原結合ドメインは、特定の理論に拘束されるものではないが、MTAとアデノシンの両方の分子において共通の構造と相互作用することにより抗原に対する結合活性が変化すると理解することができる。その場合、結合活性を評価する溶媒中において仮にMTAの濃度が減少したとしても、アデノシンの濃度がMTAの濃度の減少による結合活性の低下の程度を上回る濃度で存在する場合は、結合活性が維持される、もしくは強く検出されることはあり得る。また、結合活性を評価する溶媒中において仮にMTAの濃度が増加したとしても、MTAの濃度の増加による結合活性の増加の程度を越えてアデノシンの濃度が低下する場合は、結合活性が維持される、もしくは低く検出されることはあり得る。
別の非限定的な一態様において、本開示のMTA依存的に抗原に対する結合活性の変化する抗原結合ドメインの抗原結合活性は、S-(5'-Adenosyl)-L-homocysteine (SAH)依存的にも変化する。
別の非限定的な一態様において、本開示のMTA依存的に抗原に対する結合活性の変化する抗原結合ドメインの抗原結合活性は、SAM依存的にも変化する。
別の非限定的な一態様において、本開示のMTA依存的に抗原に対する結合活性の変化する抗原結合ドメインの抗原結合活性は、アデノシン、AMP、ADP、ATPのいずれにも依存的にも変化する。
別の非限定的な一態様において、本開示のMTA依存的に抗原に対する結合活性の変化する抗原結合ドメインの抗原結合活性は、アデノシン、S-(5'-Adenosyl)-L-homocysteine (SAH)のいずれにも依存的にも変化する。
別の非限定的な一態様において、本開示のMTA依存的に抗原に対する結合活性の変化する抗原結合ドメインの抗原結合活性は、アデノシン、S-(5'-Adenosyl)-L-homocysteine (SAH)、SAMのいずれにも依存的にも変化する。
別の非限定的な一態様において、本開示のMTA依存的に抗原に対する結合活性の変化する抗原結合ドメインの抗原結合活性は、アデノシン、S-(5'-Adenosyl)-L-homocysteine (SAH)、SAM、AMP、ADP、ATPのいずれにも依存的にも変化する。
重鎖30位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖31位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖32位に位置するA;
重鎖33位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖34位に位置するW;
重鎖35位に位置するM;
重鎖35a位に位置するC;
重鎖50位に位置するC;
重鎖51位に位置するI;
重鎖52位に位置するF;
重鎖52a位に位置するA;
重鎖52b位に位置するA、D、E、G、H、I、K、L、M、N、P、Q、R、S、TまたはVのいずれか;
重鎖52c位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖52d位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖52e位に位置するY;
重鎖52f位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖52g位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖53位に位置するS;
重鎖54位に位置するG;
重鎖55位に位置するG;
重鎖56位に位置するS;
重鎖57位に位置するT;
重鎖58位に位置するY;
重鎖59位に位置するY;
重鎖60位に位置するA;
重鎖61位に位置するS;
重鎖62位に位置するW;
重鎖63位に位置するA;
重鎖64位に位置するK;
重鎖65位に位置するG;
重鎖95位に位置するG;
重鎖96位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖97位に位置するG;
重鎖98位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖99位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖100位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖100a位に位置するG;
重鎖100b位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖100c位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖101位に位置するE;
重鎖102位に位置するL;
軽鎖24位に位置するQ;
軽鎖25位に位置するS;
軽鎖26位に位置するS;
軽鎖27位に位置するE;
軽鎖27a位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖28位に位置するV;
軽鎖29位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖30位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖31位に位置するA、D、E、G、H、I、K、L、M、N、P、Q、R、S、TまたはVのいずれか;
軽鎖32位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖33位に位置するL;
軽鎖34位に位置するS;
軽鎖49位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖50位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖51位に位置するA;
軽鎖52位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖53位に位置するT;
軽鎖54位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖55位に位置するP;
軽鎖56位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖89位に位置するA;
軽鎖90位に位置するG;
軽鎖91位に位置するL;
軽鎖92位に位置するY;
軽鎖93位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖94位に位置するG;
軽鎖95位に位置するN;
軽鎖95a位に位置するI;
軽鎖96位に位置するP;
軽鎖97位に位置するA。
重鎖31位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖32位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖33位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖34位に位置するW;
重鎖35位に位置するM;
重鎖35a位に位置するC;
重鎖50位に位置するC;
重鎖51位に位置するI;
重鎖52位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖52a位に位置するS;
重鎖53位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖54位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖55位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖56位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖57位に位置するT;
重鎖58位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖59位に位置するY;
重鎖60位に位置するA;
重鎖61位に位置するS;
重鎖62位に位置するW;
重鎖63位に位置するV;
重鎖64位に位置するN;
重鎖65位に位置するG;
重鎖95位に位置するE;
重鎖96位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖97位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖98位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖99位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖100位に位置するS;
重鎖100a位に位置するG;
重鎖100b位に位置するA;
重鎖100c位に位置するL;
重鎖101位に位置するN;
重鎖102位に位置するL;
軽鎖24位に位置するH;
軽鎖25位に位置するS;
軽鎖26位に位置するS;
軽鎖27位に位置するK;
軽鎖27a位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖27b位に位置するV;
軽鎖28位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖29位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖30位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖31位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖32位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖33位に位置するL;
軽鎖34位に位置するA;
軽鎖49位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖50位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖51位に位置するA;
軽鎖52位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖53位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖54位に位置するL;
軽鎖55位に位置するA;
軽鎖56位に位置するS;
軽鎖89位に位置するQ;
軽鎖90位に位置するG;
軽鎖91位に位置するT;
軽鎖92位に位置するY;
軽鎖93位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖94位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖95位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖95a位に位置するA、C、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖95b位に位置するF;
軽鎖95c位に位置するY;
軽鎖96位に位置するF;
軽鎖97位に位置するA。
重鎖26位に位置するA、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖28位に位置するA、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖29位に位置するAまたはLのいずれか;
重鎖30位に位置するA、D、E、F、G、H、I、K、L、M、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖31位に位置するA、D、E、F、G、H、I、K、L、N、Q、R、S、T、V、WまたはYのいずれか;
重鎖32位に位置するD、E、F、H、N、P、RまたはYのいずれか;
重鎖33位に位置するA、I、P、TまたはVのいずれか;
重鎖34位に位置するA、E、F、H、I、K、L、M、N、Q、S、T、V、WまたはYのいずれか;
重鎖35位に位置するG;
重鎖50位に位置するD、IまたはVのいずれか;
重鎖51位に位置するI;
重鎖52位に位置するG;
重鎖53位に位置するA、D、E、G,I、K、QまたはRのいずれか;
重鎖54位に位置するD、E、F、G、H、I、K、L、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖55位に位置するA、D、E、F、GまたはHのいずれか;
重鎖56位に位置するA、D、E、F、G、H、I、K、L、N、Q、R、S、T、V、WまたはYのいずれか;
重鎖57位に位置するA、D、E、G、H、I、K、L、N、P、Q、R、S、TまたはVのいずれか;
重鎖58位に位置するW;
重鎖59位に位置するA、D、E、F、G、H、I、K、L、Q、R、S、T、V、WまたはYのいずれか;
重鎖60位に位置するP;
重鎖61位に位置するA、F、Q、R、S、T、V、WまたはYのいずれか;
重鎖62位に位置するW;
重鎖63位に位置するV;
重鎖64位に位置するK;
重鎖65位に位置するA、FまたはG;
重鎖95位に位置するG;
重鎖96位に位置するA、E、F、G、H、K、L、Q、R、S、T、WまたはYのいずれか;
重鎖97位に位置するA、F、H、K、N、WまたはYのいずれか;
重鎖98位に位置するA、D、E、F、G、H、I、K、L、N、P、Q、R、S、T、V、WまたはYのいずれか;
重鎖99位に位置するA、D、E、G、H、QまたはSのいずれか;
重鎖100位に位置するFまたはY;
重鎖100a位に位置するN、TまたはV
重鎖100b位に位置するN;
重鎖100c位に位置するA;
重鎖100d位に位置するFまたはW;
重鎖101位に位置するD;
重鎖102位に位置するP;
軽鎖24位に位置するQ;
軽鎖25位に位置するS;
軽鎖26位に位置するS;
軽鎖27位に位置するQ;
軽鎖27e位に位置するS;
軽鎖27f位に位置するV;
軽鎖28位に位置するA、E、F、H、I、K、L、N、R、S、T、V、WまたはYのいずれか;
軽鎖29位に位置するA、D、E、F、G、H、I、K、L、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖30位に位置するN;
軽鎖31位に位置するN ;
軽鎖32位に位置するA、E、F、G、H、SまたはYのいずれか;
軽鎖33位に位置するL;
軽鎖34位に位置するS;
軽鎖50位に位置するD ;
軽鎖51位に位置するA;
軽鎖52位に位置するS ;
軽鎖53位に位置するT ;
軽鎖54位に位置するL;
軽鎖55位に位置するA;
軽鎖56位に位置するS;
軽鎖89位に位置するH;
軽鎖90位に位置するG;
軽鎖91位に位置するA、SまたはTのいずれか;
軽鎖92位に位置するA、D、E、F、G、H、I、K、L、M、N、Q、R、S、T、V、WまたはYのいずれか;
軽鎖93位に位置するA、D、E、F、G、H、L、N、Q、R、S、T、VまたはYのいずれか;
軽鎖94位に位置するA、E、F、G、H、I、K、L、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖95位に位置するA、D、E、F、G、H、I、K、L、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖95a位に位置するA、D、E、F、G、H、I、K、L、N、P、Q、R、V、WまたはYのいずれか;
軽鎖95b位に位置するA、D、E、F、G、H、I、K、L、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖95c位に位置するA、F、H、I、K、L、N、P、Q、R、S、T、V、WまたはYのいずれか;
軽鎖96d位に位置するD;
軽鎖96位に位置するN;
軽鎖97位に位置するAまたはG;
軽鎖98位に位置するA、F、I、LまたはV。
本明細書における「分子間相互作用を形成している状態」については,例えばMTAと抗原結合分子二者の複合体の結晶構造解析から、抗原結合分子を形成するアミノ酸の側鎖又は主鎖を構成する非水素原子とMTAを構成する非水素原子との原子間距離をもとに判定できる。たとえば,上記原子間距離は3.0Å、3.2Å、3.4Å、3.6Å、3.8Å、4.0Å、4.2Å、4.4Å、4.6Å、4.8Å又は5.0Å以内が好ましいがこれに限定されることはない。更に好ましい上記原子間距離は3.6Å、3.8Å、4.0Å又は4.2Å以内である。
より詳しくは、立体構造上での原子間距離と形成される分子間相互作用の種類ならびに原子の種類の情報をもとに直接的に相互作用している可能性が判定できる。さらに正確にはAlaやGlyへの改変といったアミノ酸残基の変異導入が低分子化合物の活性に与える影響から判断することができるが、これに限定されるわけではない。
本明細書における「間接的に影響している状態」についても,例えば、MTAと抗原結合分子二者の複合体の立体構造から各アミノ酸残基のコンフォメーションや周囲の残基との分子間相互作用の状況を詳細に解析することで、MTAの結合に間接的に影響しているかどうかを推定できるが、より正確にはAlaやGlyへの改変といったアミノ酸残基の変異導入がMTAの活性に与える影響から判断することができる。
本明細書における「分子間相互作用を形成している状態」については,例えばMTA、抗原、抗原結合分子三者の複合体の結晶構造解析から、抗原存在下で抗原結合分子を形成するアミノ酸の側鎖又は主鎖を構成する非水素原子とMTAを構成する非水素原子との原子間距離をもとに判定できる。たとえば,上記原子間距離は3.0Å、3.2Å、3.4Å、3.6Å、3.8Å、4.0Å、4.2Å、4.4Å、4.6Å、4.8Å又は5.0Å以内が好ましいがこれに限定されることはない。更に好ましい上記原子間距離は3.6Å、3.8Å、4.0Å又は4.2Å以内である。
より詳しくは、立体構造上での原子間距離と形成される分子間相互作用の種類ならびに原子の種類の情報をもとに直接的に相互作用している可能性が判定できる。さらに正確にはAlaやGlyへの改変といったアミノ酸残基の変異導入が低分子化合物の活性に与える影響から判断することができるが、これに限定されるわけではない。
本明細書における「間接的に影響している状態」についても,例えば、MTA、抗原、抗原結合分子三者の複合体の立体構造から各アミノ酸残基のコンフォメーションや周囲の残基との分子間相互作用の状況を詳細に解析することで、抗原存在下でのMTAの結合に間接的に影響しているかどうかを推定できるが、より正確にはAlaやGlyへの改変といったアミノ酸残基の変異導入がMTAの活性に与える影響から判断することができる。
非限定な一態様として、前記抗原結合ドメインは抗体可変領域であり、当該抗体可変領域は重鎖W34、C35a、W47、F52、Y52e、E101、軽鎖R32、S34、Y36、L46、Y49、S50、A89、G90、L91、及びP96(Kabatナンバリング)から選択される少なくとも一つ以上のアミノ酸を含む抗原結合ドメインが例示される。
非限定な一態様として、前記抗原結合ドメインは抗体可変領域であり、当該抗体可変領域は重鎖W34、W47、C50、Y58、E95、F98、G99、G100a、軽鎖Y28、T91、F95b、Y95c、及びF96(Kabatナンバリング)から選択される少なくとも一つ以上のアミノ酸を含む抗原結合ドメインが例示される。
また、前記抗原結合ドメインは抗体可変領域であり、当該抗体可変領域は重鎖A33、I50、G52、D54、S56、T57、W58、G99、Y100、T100a、軽鎖S91、Y95c、及びN96(Kabatナンバリング)から選択される少なくとも一つ以上のアミノ酸を含む抗原結合ドメインが例示されうる。
非限定な一態様においては、本開示にMTA依存的に抗原に対する結合活性の変化する抗原結合ドメインを含む抗原結合分子は抗体Fc領域を含む分子である。本開示の抗原結合分子に含まれる抗体Fc領域は、天然型Fc領域であっても改変Fc領域であっても良い。天然型Fc領域として、ヒトIgG1(配列番号:5)、IgG2(配列番号:6)、IgG3(配列番号:7)、またはIgG4(配列番号:8)で表されるFc領域が例示される。
Ser
Gly・Ser
Gly・Gly・Ser
Ser・Gly・Gly
Gly・Gly・Gly・Ser(配列番号:19)
Ser・Gly・Gly・Gly(配列番号:20)
Gly・Gly・Gly・Gly・Ser(配列番号:21)
Ser・Gly・Gly・Gly・Gly(配列番号:22)
Gly・Gly・Gly・Gly・Gly・Ser(配列番号:23)
Ser・Gly・Gly・Gly・Gly・Gly(配列番号:24)
Gly・Gly・Gly・Gly・Gly・Gly・Ser(配列番号:25)
Ser・Gly・Gly・Gly・Gly・Gly・Gly(配列番号:26)
(Gly・Gly・Gly・Gly・Ser(配列番号:21))n
(Ser・Gly・Gly・Gly・Gly(配列番号22))n
[nは1以上の整数である]等が好適に挙げられる。但し、ペプチドリンカーの長さや配列は目的に応じて当業者が適宜選択することができる。
本発明における抗原結合分子が高い血漿中滞留性を有しているかどうかの判断は、対照となる抗原結合分子との相対的な比較によって行うことができる。いくつかの態様において、MTAの濃度が高まるにつれて抗原結合活性が増大する抗原結合分子は、対照となる抗原結合分子と比べて、高い血漿中滞留性を有する。一態様において、対照となる抗原結合分子は、MTAの濃度に依存した抗原結合活性を有していない抗原結合分子である。特定の態様において、化合物の濃度に依存した抗原結合活性を有していない抗原結合分子とは、MTAの存在下と非存在下における抗原結合活性の差が、例えば2倍より小さい、1.8倍より小さい、1.5倍より小さい、1.3倍より小さい、1.2倍より小さい、または1.1倍より小さい抗原結合分子を意味する。比較の観点からすると、本開示の抗原結合分子と、対照となる抗原結合分子とでは、十分量のMTAの存在下における抗原結合活性が互いに実質的に等しいことが望ましい。
もよい。
Fcγレセプター(FcγRとも記載される)とは、IgG1、IgG2、IgG3、IgG4モノクローナル抗体のFc領域に結合し得るレセプターをいい、実質的にFcγレセプター遺伝子にコードされるタンパク質のファミリーのいかなるメンバーをも意味する。ヒトでは、このファミリーには、アイソフォームFcγRIa、FcγRIbおよびFcγRIcを含むFcγRI(CD64);アイソフォームFcγRIIa(アロタイプH131およびR131を含む。即ち、FcγRIIa (H)およびFcγRIIa (R))、FcγRIIb(FcγRIIb-1およびFcγRIIb-2を含む)およびFcγRIIcを含むFcγRII(CD32);およびアイソフォームFcγRIIIa(アロタイプV158およびF158を含む。即ち、FcγRIIIa (V)およびFcγRIIIa (F))およびFcγRIIIb(アロタイプFcγRIIIb-NA1およびFcγRIIIb-NA2を含む)を含むFcγRIII(CD16)、並びにいかなる未発見のヒトFcγR類またはFcγRアイソフォームまたはアロタイプも含まれるが、これらに限定されるものではない。FcγRは、ヒト、マウス、ラット、ウサギおよびサルを含むが、これらに限定されるものではない、いかなる生物由来でもよい。マウスFcγR類には、FcγRI(CD64)、FcγRII(CD32)、FcγRIII(CD16)およびFcγRIII-2(FcγRIV、CD16-2)、並びにいかなる未発見のマウスFcγR類またはFcγRアイソフォームまたはアロタイプも含まれるが、これらに限定されない。こうしたFcγレセプターの好適な例としてはヒトFcγRI(CD64)、FcγRIIa(CD32)、FcγRIIb(CD32)、FcγRIIIa(CD16)及び/又はFcγRIIIb(CD16)が挙げられる。ヒトFcγRIのポリヌクレオチド配列及びアミノ酸配列はそれぞれ配列番号:9(NM_000566.3)及び10(NP_000557.1)に、ヒトFcγRIIa(アロタイプH131)のポリヌクレオチド配列及びアミノ酸配列はそれぞれ配列番号:11(BC020823.1)及び12(AAH20823.1)に(アロタイプR131は配列番号:12の166番目のアミノ酸がArgに置換されている配列である)、FcγRIIbのポリヌクレオチド配列及びアミノ酸配列はそれぞれ配列番号:13(BC146678.1)及び14(AAI46679.1)に、FcγRIIIaのポリヌクレオチド配列及びアミノ酸配列はそれぞれ配列番号:15(BC033678.1)及び16(AAH33678.1)に、及びFcγRIIIbのポリヌクレオチド配列及びアミノ酸配列は、それぞれ配列番号:17(BC128562.1)及び18(AAI28563.1)に記載されている(カッコ内はRefSeq等のデータベース登録番号を示す)。Fcγレセプターが、IgG1、IgG2、IgG3、IgG4モノクローナル抗体のFc領域に結合活性を有するか否かは、上記に記載されるFACSやELISAフォーマットのほか、ALPHAスクリーン(Amplified Luminescent Proximity Homogeneous Assay)や表面プラズモン共鳴(SPR)現象を利用したBIACORE法等によって確認され得る(Proc. Natl. Acad. Sci. U.S.A. (2006) 103 (11), 4005-4010)。
前述されるように、本開示の抗原結合分子に含まれるFc領域として、Fcγレセプターに対する結合活性を有するFc領域が挙げられる。そのようなFc領域の非限定な一態様として、ヒトIgG1(配列番号:5)、IgG2(配列番号:6)、IgG3(配列番号:7)、またはIgG4(配列番号:8)で表されるFc領域が例示される。Fcγレセプターが、IgG1、IgG2、IgG3、IgG4モノクローナル抗体のFc領域に結合活性を有するか否かは、上記に記載されるFACSやELISAフォーマットのほか、ALPHAスクリーン(Amplified Luminescent Proximity Homogeneous Assay)や表面プラズモン共鳴(SPR)現象を利用したBIACORE法等によって確認され得る(Proc. Natl. Acad. Sci. U.S.A. (2006) 103 (11), 4005-4010)。
本開示が含むFc領域として、ヒトIgG1(配列番号:5)、IgG2(配列番号:6)、IgG3(配列番号:7)、またはIgG4(配列番号:8)で表されるFc領域のほかに、天然型ヒトIgGのFc領域のFcγレセプターに対する結合活性よりもFcγレセプターに対する結合活性が高いFcγR結合改変Fc領域も適宜使用され得る。本明細書において、「天然型ヒトIgGのFc領域」とは、配列番号:5、6、7または8で例示されるヒトIgG1、IgG2、IgG3またはIgG4のFc領域のEUナンバリング297位に結合した糖鎖がフコース含有糖鎖であるFc領域を意味する。そのようなFcγR結合改変Fc領域は、天然型ヒトIgGのFc領域のアミノ酸を改変することによって作製され得る。FcγR結合改変Fc領域のFcγRに対する結合活性が、天然型ヒトIgGのFc領域のFcγRに対する結合活性より高いか否かは、前記の結合活性の項で記載された方法を用いて適宜実施され得る。
また、本開示において好適に用いられる、Fcγレセプター結合ドメインの例として、特定のFcγレセプターに対する結合活性がそのほかのFcγレセプターに対する結合活性よりも高い性質を有するFcγレセプター結合ドメイン(選択的なFcγレセプターに対する結合活性を有するFcγレセプター結合ドメイン)もまた好適に挙げられる。抗原結合分子として抗体が(Fcγレセプター結合ドメインとしてFc領域が)用いられる場合には、一分子の抗体は一分子のFcγレセプターとしか結合できないため、一分子の抗原結合分子は抑制型Fcγレセプターに結合した状態で他の活性型FcγRに結合することはできないし、活性型Fcγレセプターに結合した状態で他の活性型Fcγレセプターや抑制型Fcγレセプターに結合することはできない。
前記したように、活性型Fcγレセプターとしては、FcγRIa、FcγRIbおよびFcγRIcを含むFcγRI(CD64)、FcγRIIaならびにFcγRIIIa(アロタイプV158およびF158を含む)およびFcγRIIIb(アロタイプFcγRIIIb-NA1およびFcγRIIIb-NA2を含む)を含むFcγRIII(CD16)が好適に挙げられる。また、FcγRIIb(FcγRIIb-1およびFcγRIIb-2を含む)が抑制型Fcγレセプターの好適な例として挙げられる。
本明細書において、特定のFcγレセプターに対する結合活性がそれ以外のFcγレセプターに対する結合活性よりも高い例として、例えば、抑制型Fcγレセプターに対する結合活性が活性型Fcγレセプターに対する結合活性よりも高い場合が挙げられる。この場合、Fc領域のFcγRIIbに対する結合活性が、FcγRIa、FcγRIIa、FcγRIIIa及び/又はFcγRIIIbのいずれかのヒトFcγレセプターに対する結合活性よりも高いことをいう。例えば、上記の解析方法にもとづいて、Fc領域を含む抗原結合分子のFcγRIIbに対する結合活性が、FcγRIa、FcγRIIa、FcγRIIIa及び/又はFcγRIIIbのいずれかのヒトFcγレセプターに対する結合活性の、105%以上、好ましくは110%以上、120%以上、130%以上、140%以上、特に好ましくは150%以上、160%以上、170%以上、180%以上、190%以上、200%%以上、250%以上、300%以上、350%以上、400%以上、450%以上、500%以上、750%以上、10倍以上、20倍以上、30倍以上、40倍以上、50倍、60倍、70倍、80倍、90倍、100倍以上の結合活性を示すことをいう。抑制型Fcγレセプターに対する結合活性が活性型Fcγレセプターに対する結合活性よりも高いFc領域は、抗原結合ドメインが可溶型分子に結合する本開示の抗原結合分子に好適に含まれ得る。
本開示が提供する抗原結合分子に含まれるFc領域として、Fc領域に結合した糖鎖の組成がフコース欠損糖鎖を結合したFc領域の割合が高くなるように、またはバイセクティングN-アセチルグルコサミンが付加したFc領域の割合が高くなるように修飾されたFc領域も含まれ得る。抗体Fc領域に結合するN -グリコシド結合複合型糖鎖還元末端のN -アセチルグルコサミンからフコース残基を除去すると、FcγRIIIaに対する親和性が増強されることが知られている(非特許文献6)。こうしたFc領域を含むIgG1抗体は、後述するADCC活性が増強されていることが知られていることから、当該Fc領域を含む抗原結合分子は、本開示の医薬組成物に含まれる抗原結合分子としても有用である。抗体Fc領域に結合するN -グリコシド結合複合型糖鎖還元末端のN -アセチルグルコサミンからフコース残基が除去された抗体としては、例えば、次のような抗体;
グリコシル化が修飾された抗体(国際公開WO1999/054342等)、
糖鎖に付加するフコースが欠損した抗体(国際公開WO2000/061739、WO2002/031140、WO2006/067913等)、
FcRnとIgG抗体との結晶学的研究によって、FcRn-IgG複合体は、二分子のFcRnに対して一分子のIgGから構成され、IgGのFc領域の両側に位置するCH2およびCH3ドメインの接触面付近において、二分子の結合が起こると考えられている(Burmeisterら(Nature (1994) 372, 336-343)。一方、PCT/JP2012/058603の実施例3において確認されたように、抗体のFc領域が二分子のFcRnおよび一分子の活性型Fcγレセプターの四者を含む複合体を形成できることが明らかとなった(PCT/JP2012/058603)。このヘテロ複合体の形成は、pH中性域の条件下でFcRnに対する結合活性を有するFc領域を含む抗原結合分子の性質について解析を進めた結果明らかとなった現象である。
(様態1) pH中性域の条件下でのFcRnに対する結合活性を有し、活性型FcγRに対する結合活性が天然型Fc領域の活性型FcγRに対する結合活性より低いFc領域を含む抗原結合分子
234位のアミノ酸をAla、Arg、Asn、Asp、Gln、Glu、Gly、His、Lys、Met、Phe、Pro、Ser、ThrまたはTrpのいずれか、
235位のアミノ酸をAla、Asn、Asp、Gln、Glu、Gly、His、Ile、Lys、Met、Pro、Ser、Thr、ValまたはArgのいずれか、
236位のアミノ酸をArg、Asn、Gln、His、Leu、Lys、Met、Phe、ProまたはTyrのいずれか、
237位のアミノ酸をAla、Asn、Asp、Gln、Glu、His、Ile、Leu、Lys、Met、Pro、Ser、Thr、Val、TyrまたはArgのいずれか、
238位のアミノ酸をAla、Asn、Gln、Glu、Gly、His、Ile、Lys、Thr、TrpまたはArgのいずれか、
239位のアミノ酸をGln、His、Lys、Phe、Pro、Trp、TyrまたはArgのいずれか、
265位のアミノ酸をAla、Arg、Asn、Gln、Gly、His、Ile、Leu、Lys、Met、Phe、Ser、Thr、Trp、TyrまたはValのいずれか、
266位のアミノ酸をAla、Arg、Asn、Asp、Gln、Glu、Gly、His、Lys、Phe、Pro、Ser、Thr、TrpまたはTyrのいずれか、
267位のアミノ酸をArg、His、Lys、Phe、Pro、TrpまたはTyrのいずれか、
269位のアミノ酸をAla、Arg、Asn、Gln、Gly、His、Ile、Leu、Lys、Met、Phe、Pro、Ser、Thr、Trp、TyrまたはValのいずれか、
270位のアミノ酸をAla、Arg、Asn、Gln、Gly、His、Ile、Leu、Lys、Met、Phe、Pro、Ser、Thr、Trp、TyrまたはValのいずれか、
271位のアミノ酸をArg、His、Phe、Ser、Thr、TrpまたはTyrのいずれか、
295位のアミノ酸をArg、Asn、Asp、Gly、His、Phe、Ser、TrpまたはTyrのいずれか、
296位のアミノ酸をArg、Gly、LysまたはProのいずれか、
297位のアミノ酸をAla、
298位のアミノ酸をArg、Gly、Lys、Pro、TrpまたはTyrのいずれか、
300位のアミノ酸をArg、LysまたはProのいずれか、
324位のアミノ酸をLysまたはProのいずれか、
325位のアミノ酸をAla、Arg、Gly、His、Ile、Lys、Phe、Pro、Thr、TrpTyr、もしくはValのいずれか、
327位のアミノ酸をArg、Gln、His、Ile、Leu、Lys、Met、Phe、Pro、Ser、Thr、Trp、TyrまたはValのいずれか、
328位のアミノ酸をArg、Asn、Gly、His、LysまたはProのいずれか、
329位のアミノ酸をAsn、Asp、Gln、Glu、Gly、His、Ile、Leu、Lys、Met、Phe、Ser、Thr、Trp、Tyr、ValまたはArgのいずれか、
330位のアミノ酸をProまたはSerのいずれか、
331位のアミノ酸をArg、GlyまたはLysのいずれか、もしくは
332位のアミノ酸をArg、LysまたはProのいずれか、
のいずれか一つ以上に改変されているFc領域が好適に挙げられる。
免疫グロブリンスーパーファミリーに属するFcγレセプターと異なり、ヒトFcRnは構造的には主要組織不適合性複合体(MHC)クラスIのポリペプチドに構造的に類似しクラスIのMHC分子と22から29%の配列同一性を有する(Ghetieら,Immunol. Today (1997) 18 (12), 592-598)。FcRnは、可溶性βまたは軽鎖(β2マイクログロブリン)と複合体化された膜貫通αまたは重鎖よりなるヘテロダイマーとして発現される。MHCのように、FcRnのα鎖は3つの細胞外ドメイン(α1、α2、α3)よりなり、短い細胞質ドメインはタンパク質を細胞表面に繋留する。α1およびα2ドメインが抗体のFc領域中のFcRn結合ドメインと相互作用する(Raghavanら(Immunity (1994) 1, 303-315)。
MTAと相互作用するアミノ酸残基が位置する部位として、抗原結合分子の抗原結合ドメインとは異なる部分が例示される。抗原結合分子の抗原結合ドメインとは異なる部分のアミノ酸残基がMTAと相互作用することにより抗原結合ドメインの構造が変化し、間接的にMTA依存的に抗原結合活性が変化し得る。
非限定的な一態様として、本開示の抗原結合分子は更に第2の抗原結合ドメインを有し、前記第2の抗原結合ドメインは前記抗原結合ドメインが結合する抗原と異なる第2の抗原に対して結合活性を有する。
抗原結合分子が異なる複数の抗原結合ドメインを有する場合、その内の少なくとも一つの抗原結合ドメインがMTAまたはMTA以外の低分子化合物依存的に抗原に対する結合活性が変化する抗原結合ドメインを有しても良いし、抗原結合分子が含む全ての抗原結合ドメインがMTAまたはMTA以外の低分子化合物依存的に抗原に対する結合活性が変化する抗原結合ドメインであっても良い。また複数の抗原結合ドメインがそれぞれ異なる低分子化合物依存的に抗原に対する結合活性が変化する抗原ドメインであっても良いし、一つの抗原結合分子の中に低分子化合物依存的に抗原に対する結合活性が変化する抗原結合ドメインと低分子化合物の濃度に抗原に対する結合活性が影響されない抗原結合ドメインが同時に存在しても良い。
更なる一態様において、前記第2の抗原結合ドメインの前記第2の抗原に対する結合活性はMTAに実質的に影響されない。
更なる一態様において、前記第2の抗原結合ドメインの前記第2の抗原に対する結合活性はMTA依存的に変化する。より詳細な一態様において、前記第2の抗原結合ドメインのMTA存在下における前記第2の抗原に対する結合活性が、前記第2の抗原結合ドメインのMTA非存在下における前記第2の抗原に対する結合活性と異なる。
2つ以上の複数の抗原結合ドメインを有し、さらに複数の異なる抗原に対して同時に結合し得る抗原結合分子の非限定な例示として、二重特異性抗体が例示され得るが、これに限定されるものではない。
エフェクター細胞の細胞膜に結合する膜型分子として、これらに限るものではないが、TCR複合体、CD3、CD3eが例示される。
一方のパラトープががん細胞やがん組織に浸潤している細胞等(標的細胞とも呼ぶ)の細胞膜に結合する膜型分子に存在するエピトープに結合し、もう一方のパラトープがエフェクター細胞の細胞膜に発現する膜型分子中に存在するエピトープに結合する二重パラトピック抗原結合分子の一態様いおいては、当該二重パラトピック抗原結合分子が標的細胞とエフェクター細胞の両方に結合することで、エフェクター細胞を活性化され、標的細胞に対して細胞傷害活性を惹起することが出来る。エフェクター細胞がT細胞である場合、惹起される細胞傷害活性はT細胞による細胞傷害(T-cell-dependent cytotoxicity: TDCC)活性である。
本開示の抗原結合分子ががん細胞に結合し、細胞傷害活性を発揮するために、抗原結合分子に細胞傷害性物質が結合されていてもよい。細胞傷害性物質としては、以下に例示される化学療法剤であってもよく、またCurr Opin Chem Biol (2010) 14, 529-37や国際公開2009/140242に開示されている化合物であってもよく、これらの化合物が適切なリンカー等で抗原結合分子に結合される。本開示の抗原結合分子が医薬組成物として使用される場合、対象(被験者、患者、等)に当該抗原結合分子を投与する前にこれらの細胞傷害性物質を結合させることも可能であるし、投与の前後または同時に投与することも可能である。
ジフテリアトキシンA鎖(Diphtheria toxin A Chain)(Langoneら(Methods in Enzymology (1983) 93, 307-308));
シュードモナスエンドトキシン(Pseudomonas Exotoxin)(Nature Medicine (1996) 2, 350-353);
リシン鎖(Ricin A Chain)(Fultonら(J. Biol. Chem. (1986) 261, 5314-5319)、Sivamら(Cancer Res. (1987) 47, 3169-3173)、Cumberら、(J. Immunol. Methods (1990) 135,15-24、Wawrzynczakら(Cancer Res. (1990) 50, 7519-7562)、およびGheeite ら(J. Immunol.Methods (1991) 142,223-230));
無糖鎖リシンA鎖(Deglicosylated Ricin A Chain)(Thorpeら(Cancer Res. (1987) 47, 5924-5931));
アブリンA鎖(Abrin A Chain)(Wawrzynczakら(Br. J. Cancer (1992) 66, 361-366)、Wawrzynczakら(Cancer Res. (1990) 50, 7519-7562)、Sivamら(Cancer Res. (1987) 47, 3169-3173)、およびThorpeら(Cancer Res. (1987) 47, 5924-5931));
ゲロニン(Gelonin)(Sivamら(Cancer Res. (1987) 47, 3169-3173)、Cumberら(J. Immunol. Methods (1990) 135, 15-24)、Wawrzynczakら(Cancer Res., (1990) 50, 7519-7562)、およびBolognesiら(Clin. exp. Immunol. (1992) 89, 341-346));
ポークウイード抗ウィルス蛋白(PAP-s; Pokeweed anti-viral protein fromseeds)(Bolognesiら(Clin. exp. Immunol. (1992) 89, 341-346));
ブリオジン(Briodin)(Bolognesiら(Clin. exp. Immunol. (1992) 89, 341-346));
サポリン(Saporin)(Bolognesiら(Clin. exp. Immunol. (1992) 89, 341-346));
モモルジン(Momordin)(Cumberら(J. Immunol. Methods (1990) 135, 15-24);Wawrzynczakら(Cancer Res. (1990) 50, 7519-7562)、およびBolognesiら(Clin. exp. Immunol. (1992) 89, 341-346));
モモルコキン(Momorcochin)(Bolognesiら(Clin. exp. Immunol. (1992) 89, 341-346));
ジアンシン32(Dianthin 32)(Bolognesiら(Clin. exp. Immunol. (1992) 89, 341-346));
ジアンシン30(Dianthin 30)(Stirpe F., Barbieri L.(FEBS letter (1986) 195, 1-8));
モデッシン(Modeccin)(Stirpe F., Barbieri L.(FEBS letter (1986) 195, 1-8));
ビスカミン(Viscumin)(Stirpe F., Barbieri L.(FEBS letter (1986) 195, 1-8));
ボルケシン(Volkesin)(Stirpe F., Barbieri L.(FEBS letter (1986) 195, 1-8));
ドデカンドリン(Dodecandrin)(Stirpe F., Barbieri L.(FEBS letter (1986) 195, 1-8));
トリチン(Tritin)(Stirpe F., Barbieri L.(FEBS letter (1986) 195, 1-8));
ルフィン(Luffin)(Stirpe F., Barbieri L.(FEBS letter (1986) 195, 1-8));および
トリコキリン(Trichokirin)(Casellasら(Eur. J. Biochem. (1988) 176, 581-588)、およびBolognesiら(Clin. exp. Immunol., (1992) 89, 341-346))。
本開示の非限定な一態様では、MTA依存的に抗原に対する結合活性が変化する抗原結合ドメインを含み、膜型分子をその細胞膜に発現する細胞に対する細胞傷害活性を有する抗原結合分子、および当該抗原結合分子を有効成分として含む医薬組成物が提供される。本開示において細胞傷害活性とは、例えば抗体依存性細胞介在性細胞傷害(antibody-dependent cell-mediated cytotoxicity:ADCC)活性、補体依存性細胞傷害(complement-dependent cytotoxicity:CDC)活性、T細胞による細胞傷害(T-cell-dependent cytotoxicity: TDCC)活性および抗体依存性細胞貪食(Antibody-Dependent Cellular Phagocytosis:ADCP)活性等が挙げられる。本開示において、CDC活性とは補体系による細胞傷害活性を意味する。またADCC活性とは、標的細胞の細胞膜に発現された膜型分子に結合する抗原結合ドメインを含む抗原結合分子のFc領域に、免疫細胞等が当該免疫細胞に発現したFcγレセプターを介して結合し、当該免疫細胞が標的細胞に傷害を与える活性を意味する。またTDCC活性とは、標的細胞の細胞膜に発現された膜型分子に結合する抗原結合ドメイン、およびT細胞上のT細胞レセプター(TCR)複合体の構成サブユニットのいずれかに対する抗原結合ドメイン、特にCD3 epsilon鎖に結合する抗原結合ドメインを含むbi-specific抗体を用いることで標的細胞とT細胞を接近させることにより、T細胞が標的細胞に障害を与える活性を意味する。目的の抗原結合分子がADCC活性、CDC活性、TDCC活性またはADCP活性を有するか否かは公知の方法により測定され得る。
(1)エフェクター細胞の調製
CBA/Nマウスなどから摘出された脾臓から、RPMI1640培地(Invitrogen)中で脾臓細胞が分離される。10%ウシ胎児血清(FBS、HyClone)を含む同培地で洗浄された当該脾臓細胞の濃度を5×106/mLに調製することによって、エフェクター細胞が調製され得る。
(2)補体溶液の調製
10% FBS含有培地(Invitrogen)によってBaby Rabbit Complement(CEDARLANE)を10倍に希釈することによって、補体溶液が調製され得る。
(3)標的細胞の調製
(1)ヒトPBMC溶液の調製
5000単位/5mlのヘパリン溶液が予め500μl注入された注射器を用い、健常人より末梢血50 mlを採取する。PBSを用いて2倍に希釈された当該末梢血を4等分し、15 mlのFicoll-Paque PLUSが予め注入されて遠心操作が行なわれたLeucosepリンパ球分離管(GE Healthcare)に加える。当該末梢血が分注された分離管に1000 gの速度によって10分間室温にて遠心分離の操作をした後、単核球画分層を分取する。10%FBSを含むRPMI-1640(10%FBS/RPMI-1640)によって1回当該各分層に含まれる細胞を洗浄した後、当該細胞を各標的細胞の培養液中にその細胞密度が2 x 106 細胞/ mlとなるように懸濁する。当該細胞懸濁液をエフェクター細胞として以後の実験に供する。
TDCC活性はLDHリリース法(LDH Cytotoxicity Detection Kit: TAKARA)にて評価され得る。まず、各標的細胞の培養液で終濃度の4倍に希釈した各濃度(0.000004、0.00004、0.0004、0.004、0.04、0.4、4、40μg/ml)の抗体溶液を96ウェルU底プレートの各ウェル中に50μlずつ添加する。次に、各標的細胞の培養液で2 x 105細胞/mlに調製した標的細胞を50μlずつ播種し(1 x 104細胞/ウェル)室温にて15分間静置する。各ウェル中に(1)で調製した各標的細胞の培養液中で調製したヒトPBMC溶液各100μl(2 x 105細胞/ウェル)を加えた当該プレートを、5%炭酸ガスインキュベータ中において37℃で約24時間静置した後に、遠心操作する。当該プレートの各ウェル中の100μlの培養上清を96ウェル平底プレートに移す。前記LDH Cytotoxicity Detection Kit のcatalyst溶液を1 mlのH2Oに溶解し、dye溶液と1:45で混合する。catalyst溶液およびdye溶液の混合溶液を100μl/ウェルで培養上清を移した96ウェル平底プレートに分注し、15-30分、室温で静置した。490-492nmの吸光度をプレートリーダーで測定する。対照波長は600-620nmとして、490-492nmの吸光度から引いた。培養液のみのウェル(ブランク)の平均値を引いた値を以下の式に当てはめる。
下式:
Cytotoxicty (TDCC) (%) = ((A-B)-C))×100 / (D-C)
に基づいて細胞傷害活性を求めることができる。 ここでAは標的細胞、エフェクター細胞、抗体の混合の吸光度、Bはエフェクター細胞の吸光度、Cは標的細胞の吸光度、Dは標的細胞にTriton X-100を添加した吸光度とする。
本開示の非限定な一態様では、MTA依存的に抗原に対する結合活性が変化する抗原結合ドメインを含み、T細胞上のT細胞レセプター(TCR)複合体の構成サブユニットのいずれかに結合することでT細胞の活性化能を有する抗原結合分子、および当該抗原結合分子を有効成分として含む医薬組成物が提供される。標的細胞の細胞膜に発現された膜型分子に結合する抗原結合ドメイン、およびT細胞上のT細胞レセプター(TCR)複合体の構成サブユニットのいずれかに対する抗原結合ドメイン、特にCD3 epsilon鎖に結合する抗原結合ドメインを含むbi-specific抗体を用いることで標的細胞とT細胞を接近させることにより、T細胞の活性化を誘導することができる。T細胞の活性化能の測定は、例えばGloResponse NFAT-RE-Luc2 Jurkat細胞(Promega)を用いて測定することができる。前記細胞にはNuclear factor of activated T cells(NFAT)応答配列であるNFAT response element(NFAT-RE)により発現が誘導されるルシフェラーゼレポーターが組み込まれており、Jurkatの細胞膜に発現しているTCR複合体の活性化を、レポータータンパク質の発現を測定することにより検出することが可能である。当該細胞を用いることでTCR複合体を活性化可能なTCRリガンドや抗TCR抗体、抗CD3抗体によるT細胞活性化能を測定することが可能である。T細胞の活性化能の測定は、前記細胞を用いた方法に限定されず同様のNFAT response element(NFAT-RE)およびレポータータンパク質を導入したT細胞系の細胞を構築して用いて測定することも可能である。また、T細胞の活性化能の測定は前記手法に限定されず、例えばCD69やCD25等のT細胞活性化マーカーの発現確認をフローサイトメトリー法や遺伝子発現解析法により行っても良いし、TNF-α、IFN-γ、IL-6 及びIL-2等の活性化したT細胞が分泌するサイトカインを測定することで行っても良いが、これらの手法に限定されずT細胞の活性化を測定できる方法であれば使用する細胞株や測定方法によらず使用することができる。
本開示の非限定な一態様では、MTA依存的に抗原に対する結合活性が変化する抗原結合ドメインを含み、当該膜型分子に対する中和活性を有する抗原結合分子を有効成分として含む医薬組成物が提供される。本開示の非限定な別の一態様では、低分子化合物依存的に抗原に対する結合活性が変化する抗原結合ドメインを含み、膜型分子をその細胞膜に発現する細胞に対する細胞傷害活性に加えて、当該膜型分子に対する中和活性を有する抗原結合分子を有効成分として含む医薬組成物が提供される。一般的に、中和活性とは、ウイルスや毒素など、細胞に対して生物学的活性を有するリガンドの当該生物学的活性を阻害する活性をいう。即ち、中和活性を有する物質とは、当該リガンド又は当該リガンドが結合するレセプターに結合し、当該リガンドとレセプターの結合を阻害する物質をさす。中和活性によりリガンドとの結合を阻止されたレセプターは、当該レセプターを通じた生物学的活性を発揮することができなくなる。抗原結合分子が抗体である場合、このような中和活性を有する抗体は一般に中和抗体と呼ばれる。ある被検物質の中和活性は、リガンドの存在下における生物学的活性をその被検物質の存在又は非存在下の条件の間で比較することにより測定され得る。
本明細書において記載される抗原結合分子がヒトに投与される場合、当該抗原結合分子における抗原結合ドメインとして、ヒトに対する異種抗原性を低下させること等を目的として人為的に改変した遺伝子組換え型抗体由来の抗原結合ドメインが適宜採用され得る。遺伝子組換え型抗体には、例えば、ヒト化(Humanized)抗体等が含まれる。これらの改変抗体は、公知の方法を用いて適宜製造される。
本開示によって、副作用を回避しつつ薬効を発揮するために、正常組織や血液中において全身的に作用せず、がんにおいて作用する抗原結合分子を含む医薬組成物が提供される。本開示の医薬組成物に含まれる抗原結合分子は、MTA依存的に標的抗原への結合が制御されることから、例えば、該抗原結合分子が、がん組織における抗原を標的とする場合、がん組織におけるがん細胞・免疫細胞・ストローマ細胞等に発現する抗原、あるいはがん組織に分泌されている抗原に結合することが出来ないため、正常組織に対する細胞傷害作用や中和作用等による副作用を回避しつつ、がんに対する強力な細胞傷害作用や増殖抑制作用、免疫亢進作用等を発揮する。例えば、MTA依存的にT細胞に発現するCD3に対する結合活性が変化する抗原結合ドメインと、がん細胞に発現するEGFRに結合する抗原結合ドメインを含む二重特異性抗原結合分子または二重パラトピックな抗原結合分子は、正常組織に発現するEGFRに結合せず、がん細胞に発現しているEGFRに結合するため、副作用を回避しつつ強力な抗腫瘍効果を発揮する。すなわち、がん細胞近傍にいるT細胞に発現しているCD3にはMTAに依存的に結合するが、がん細胞近傍以外にいるT細胞に発現しているCD3に結合しないため、がん細胞近傍にいるT細胞を活性化し副作用を回避しつつ強力な抗腫瘍効果を発揮する。
本開示におけるMTA依存的に結合する抗原結合分子は、様々な既存の医薬用途の技術と組み合わることが可能である。そのような技術の組み合わせの非限定な一態様として、MTA依存的に結合する抗原結合分子を利用したキメラ抗原受容体 T細胞(CAR-T細胞)の作成が例示される。CAR-Tの非限定な作成手法の一つとしては、TCRの細胞外ドメインに腫瘍関連抗原に特異的に結合する抗原結合分子を連結し、またT細胞の活性化を増強する目的でCD28等の共刺激分子のシグナルドメインを細胞内に連結したキメラ受容体を遺伝子改変技術によりT細胞を主とするエフェクター細胞に導入する手法が挙げられる。前記腫瘍関連抗原に特異的に結合する抗原結合分子として、本開示におけるMTA依存的に結合する抗原結合分子を使用することで、MTAが蓄積した腫瘍組織特異的にCAR-T細胞が抗原に結合することが可能となる。
また、本開示のMTA依存的に結合する抗原結合分子と組み合わせ可能な技術の非限定な例として、ウィルスベクター等を用いてMTA依存的に結合する抗原結合分子をコードする核酸を生体内に組み込み、当該抗原結合分子を直接発現させる方法が挙げられる。ウィルスベクターとして、アデノウィルスが例示されるがこれに限定されるものではない。またウィルスベクターを用いることなくエレクトロポレーション法や核酸を直接投与する手法等によりMTA依存的に結合する抗原結合分子をコードする核酸を直接生体内に組み込むことも可能であるし、当該抗原結合分子を分泌発現させるように遺伝子改変した細胞を生体に投与することで、当該抗原結合分子を継続的に生体内で分泌させることも可能である。
本明細書で用いられる「オリゴヌクレオチド」は、通常約200ヌクレオチド長未満であるがそうである必要はない、通常一本鎖である合成ポリヌクレオチドのことをいう。用語「オリゴヌクレオチド」および「ポリヌクレオチド」は、相互に排他的ではない。ポリヌクレオチドに関する上記の説明は、オリゴヌクレオチドに等しくかつ完全に適用可能である。本明細書において、「オリゴヌクレオチド」及び「核酸」は互換的に使用される。
本明細書で用いられる用語「ベクター」は、それが連結されたもう1つの核酸を増やすことができる、核酸分子のことをいう。この用語は、自己複製核酸構造としてのベクター、および、それが導入された宿主細胞のゲノム中に組み入れられるベクターを含む。あるベクターは、自身が動作的に連結された核酸の、発現をもたらすことができる。そのようなベクターは、本明細書では「発現ベクター」とも称される。発現ベクターはウィルスを用いる方法やエレクトロポレーション法などにより宿主細胞に導入することができるが、発現ベクターの導入は生体外での導入に限られるものではなく、ベクターを直接生体に導入することも可能である。
用語「宿主細胞」、「宿主細胞株」、および「宿主細胞培養物」は、相互に交換可能に用いられ、外来核酸を導入された細胞(そのような細胞の子孫を含む)のことをいう。宿主細胞は「形質転換体」および「形質転換細胞」を含み、これには初代の形質転換細胞および継代数によらずその細胞に由来する子孫を含む。子孫は、親細胞と核酸の内容において完全に同一でなくてもよく、変異を含んでいてもよい。オリジナルの形質転換細胞がスクリーニングされたまたは選択された際に用いられたものと同じ機能または生物学的活性を有する変異体子孫も、本明細書では含まれる。
例えば、米国特許第4,816,567号に記載されるとおり、抗原結合分子は組み換えの方法や構成を用いて製造することができる。一態様において、本明細書に記載のMTA依存的に抗原に対する結合活性が変化する抗原結合ドメインを含む抗原結合分子をコードする、単離された核酸が提供される。MTA依存的に抗原に対する結合活性が変化する抗原結合ドメインが抗体可変領域を含む態様において、そのような核酸は、抗体のVLを含むアミノ酸配列および/またはVHを含むアミノ酸配列(例えば、抗体の軽鎖および/または重鎖)をコードしてもよい。さらなる態様において、このような核酸を含む1つまたは複数のベクター(例えば、発現ベクター)が提供される。さらなる態様において、このような核酸を含む宿主細胞が提供される。このような態様の1つでは、宿主細胞は、(1)抗原結合分子のVLを含むアミノ酸配列および抗原結合分子のVHを含むアミノ酸配列をコードする核酸を含むベクター、または、(2)抗原結合分子のVLを含むアミノ酸配列をコードする核酸を含む第一のベクターと抗原結合分子のVHを含むアミノ酸配列をコードする核酸を含む第二のベクターを含む(例えば、形質転換されている)。一態様において、宿主細胞は、真核性である(例えば、チャイニーズハムスター卵巣 (CHO) 細胞)またはリンパ系の細胞(例えば、Y0、NS0、Sp2/0細胞))。一態様において、MTA依存的に抗原に対する結合活性が変化する抗原結合ドメインを含む抗原結合分子の発現に好適な条件下で、上述のとおり当該抗原結合分子をコードする核酸を含む宿主細胞を培養すること、および任意で、当該抗体を宿主細胞(または宿主細胞培養培地)から回収することを含む、MTA依存的に抗原に対する結合活性が変化する抗原結合ドメインを含む抗原結合分子を作製する方法が提供される。
本開示は、MTA依存的に抗原に対する結合活性が変化する抗原結合ドメインを含む抗原結合分子をスクリーニングする方法を提供する。 本開示の記載事項に従いMTA依存的に抗原に対する結合活性が変化する抗原結合ドメイン(または当該ドメインを含む抗原結合分子)が取得され得る。取得する方法の非限定な一態様として、以下にその具体例がいくつか例示される。
例えば、第1濃度のMTAの存在下における抗原に対する抗原結合ドメイン(または当該ドメインを含む抗原結合分子)の結合活性と第2濃度のMTAの存在下における抗原に対する抗原結合ドメイン(または当該ドメインを含む抗原結合分子)の結合活性の方が異なることを確認するためには、第1濃度のMTA存在下および第2濃度のMTA存在下における抗原に対する抗原結合ドメイン(または当該ドメインを含む抗原結合分子)の結合活性が比較される。MTA依存的に抗原に対する結合活性がの変化する抗原結合ドメインを選択するには、第1濃度のMTA存在下および第2濃度のMTA存在下における抗原に対する抗原結合ドメイン(または当該ドメインを含む抗原結合分子)の結合活性が異なる抗原結合ドメインが選択される。第1濃度と第2濃度は異なる濃度であり、これらの濃度のどちらか一方を0(即ち、MTAが非存在する)とすることが出来る。
MTAの高濃度存在下における抗原結合活性がMTAの低濃度存在下における抗原結合活性より高い抗原結合ドメイン(または当該ドメインを含む抗原結合分子)を取得するには、第1濃度における抗原結合活性が第2濃度における抗原結合活性が高い抗原結合ドメイン(または当該ドメインを含む抗原結合分子)が選択される。
(a) 抗原結合ドメインを含む抗原結合分子を第1濃度のMTA存在下で抗原と接触させる工程、
(b) 前記工程(a)で結合した抗原結合ドメインを含む抗原結合分子を第2濃度のMTA存在下に置く工程、及び
(c) 前記工程(b)で解離した抗原結合ドメインを含む抗原結合分子を単離する工程、
を含む抗原結合分子のスクリーニング方法を提供する。
(a) 抗原結合ドメインを含む抗原結合分子を第1濃度のMTA存在下で抗原と接触させる工程、
(b) 前記工程(a)で前記抗原結合ドメインを含む抗原結合分子が抗原に結合したことを確認する工程、
(c) 前記抗原に結合した前記抗原結合ドメインを含む抗原結合分子を第2濃度のMTA存在下に置く工程、及び
(d) 前記工程(c)で抗原結合活性が、前記工程(b)で抗原に結合したことを確認した基準より弱い抗原結合ドメインを含む抗原結合分子を単離する工程、
を含む、抗原結合分子のスクリーニング方法を提供する。
(a) MTAに結合可能な抗原結合ドメインを含む抗原結合分子を第1濃度のMTA存在下で抗原と接触させる工程、
(b) 前記工程(a)で結合した抗原結合ドメインを含む抗原結合分子を第2濃度のMTA存在下に置く工程、及び
(c) 前記工程(b)で解離した抗原結合ドメインを含む抗原結合分子を単離する工程、
を含む抗原結合分子のスクリーニング方法を提供する。
(a) MTAに結合可能な抗原結合ドメインを含む抗原結合分子を第1濃度のMTA存在下で抗原と接触させる工程、
(b) 前記工程(a)で前記抗原結合ドメインを含む抗原結合分子が抗原に結合したことを確認する工程、
(c) 前記抗原に結合した前記抗原結合ドメインを含む抗原結合分子を第2濃度のMTA存在下に置く工程、及び
(d) 前記工程(c)で抗原結合活性が、前記工程(b)で抗原に結合したことを確認した基準より弱い抗原結合ドメインを含む抗原結合分子を単離する工程、
を含む、抗原結合分子のスクリーニング方法を提供する。
(a) 第1濃度のMTA存在下で抗原結合ドメインを含む抗原結合分子を抗原に接触させる工程、
(b) 前記工程(a)で前記抗原結合ドメインを含む抗原結合分子が抗原に結合しないことを確認する工程、
(c) 前記抗原に結合しない抗原結合ドメインを含む抗原結合分子を第2濃度のMTA存在下で抗原に結合させる工程、及び
(d) 前記工程(c)で抗原に結合した抗原結合ドメインを含む抗原結合分子を単離する工程、
を含む抗原結合分子のスクリーニング方法を提供する。
(a) 抗原結合ドメインを含む抗原結合分子がディスプレイされたライブラリを第1濃度のMTA存在下で抗原と接触させる工程、
(b) 前記工程(a)で結合した抗原結合ドメインを含む抗原結合分子を第2濃度のMTA存在下に置く工程、及び
(c) 前記工程(b)で解離した抗原結合ドメインを含む抗原結合分子を単離する工程、
を含む抗原結合分子のスクリーニング方法を提供する。
(a) 抗原結合ドメインを含む抗原結合分子がディスプレイされたライブラリを第1濃度のMTA存在下で抗原と接触させる工程、
(b) 前記工程(a)で抗原に結合した抗原結合ドメインを含む抗原結合分子を選択する工程、
(c) 前記工程(b)で選択した抗原結合ドメインを含む抗原結合分子を第2濃度のMTA存在下に置く工程、及び
(d) 前記工程(c)で抗原結合活性が、前記工程(b)で選択した基準より弱い抗原結合ドメインを含む抗原結合分子を単離する工程、
を含む抗原結合分子のスクリーニング方法を提供する。
(1) 抗原結合ドメインを含む抗原結合分子がディスプレイされたライブラリをMTAと接触させる工程、及び
(2) 前記工程(1)でMTAに結合した抗原結合ドメインを含む抗原結合分子を選択する工程、
(a) 前記工程(1)及び(2)で選択された抗原結合ドメインを含む抗原結合分子がディスプレイされたライブラリを第1濃度のMTA存在下で抗原と接触させる工程、
(b) 前記工程(a)で結合した抗原結合ドメインを含む抗原結合分子を第2濃度のMTA存在下に置く工程、及び
(c) 前記工程(b)で解離した抗原結合ドメインを含む抗原結合分子を単離する工程、
を含む抗原結合分子のスクリーニング方法を提供する。
(1) 抗原結合ドメインを含む抗原結合分子がディスプレイされたライブラリをMTAと接触させる工程、及び
(2) 前記工程(1)でMTAに結合した抗原結合ドメインを含む抗原結合分子を選択する工程、
(a) 前記工程(1)及び(2)で選択された抗原結合ドメインを含む抗原結合分子がディスプレイされたライブラリを第1濃度のMTA存在下で抗原と接触させる工程、
(b) 前記工程(a)で抗原に結合した抗原結合ドメインを含む抗原結合分子を選択する工程、
(c) 前記工程(b)で選択した抗原結合ドメインを含む抗原結合分子を第2濃度のMTA存在下に置く工程、及び
(d) 前記工程(c)で抗原結合活性が、前記工程(b)で選択した基準より弱い抗原結合ドメインを含む抗原結合分子を単離する工程、
を含む抗原結合分子のスクリーニング方法を提供する。
(a) 第1濃度のMTA存在下で抗原結合ドメインを含む抗原結合分子がディスプレイされたライブラリを抗原に接触させる工程、
(b) 前記工程(a)で抗原に結合しない抗原結合ドメインを含む抗原結合分子を選択する工程、
(c) 前記工程(b)で選択された抗原結合ドメインを含む抗原結合分子を第2濃度のMTA存在下で抗原に結合させる工程、及び
(d) 前記工程(c)で抗原に結合した抗原結合ドメインを含む抗原結合分子を単離する工程、
を含む抗原結合分子のスクリーニング方法を提供する。
(a) 抗原結合ドメインを含む抗原結合分子をMTAの存在下で抗原と接触させる工程、
(b) 前記工程(a)で結合した抗原結合ドメインを含む抗原結合分子をMTAの非存在下に置く工程、及び
(c) 前記工程(b)で解離した抗原結合ドメインを含む抗原結合分子を単離する工程、
を含む、抗原結合分子のスクリーニング方法を提供する。
(a) 抗原結合ドメインを含む抗原結合分子をMTAの存在下で抗原と接触させる工程、
(b) 前記工程(a)で前記抗原結合ドメインを含む抗原結合分子が抗原に結合したことを確認する工程、
(c) 前記抗原に結合した前記抗原結合ドメインを含む抗原結合分子をMTAの非存在下に置く工程、及び
(d) 前記工程(c)で抗原結合活性が、前記工程(b)で抗原に結合したことを確認した基準より弱い抗原結合ドメインを含む抗原結合分子を単離する工程、を含む抗原結合分子のスクリーニング方法を提供する。
(a) MTAに結合可能な抗原結合ドメインを含む抗原結合分子をMTAの存在下で抗原と接触させる工程、
(b) 前記工程(a)で結合した抗原結合ドメインを含む抗原結合分子をMTAの非存在下に置く工程、及び
(c) 前記工程(b)で解離した抗原結合ドメインを含む抗原結合分子を単離する工程、
を含む、抗原結合分子のスクリーニング方法を提供する。
(a) MTAに結合可能な抗原結合ドメインを含む抗原結合分子をMTAの存在下で抗原と接触させる工程、
(b) 前記工程(a)で前記抗原結合ドメインを含む抗原結合分子が抗原に結合したことを確認する工程、
(c) 前記抗原に結合した前記抗原結合ドメインを含む抗原結合分子をMTAの非存在下に置く工程、及び
(d) 前記工程(c)で抗原結合活性が、前記工程(b)で抗原に結合したことを確認した基準より弱い抗原結合ドメインを含む抗原結合分子を単離する工程、を含む抗原結合分子のスクリーニング方法を提供する。
(a) MTAの存在下で抗原結合ドメインを含む抗原結合分子を抗原に接触させる工程、
(b) 前記工程(a)で前記抗原結合ドメインを含む抗原結合分子が抗原に結合しないことを確認する工程、
(c) 前記抗原に結合しない抗原結合ドメインを含む抗原結合分子をMTAの非存在下で抗原に結合させる工程、及び
(d) 前記工程(c)で抗原に結合した抗原結合ドメインを含む抗原結合分子を単離する工程、
を含む抗原結合分子のスクリーニング方法を提供する。
(a) 抗原結合ドメインを含む抗原結合分子がディスプレイされたライブラリを MTAの存在下で抗原と接触させる工程、
(b) 前記工程(a)で結合した抗原結合ドメインを含む抗原結合分子をMTAの非存在下に置く工程、及び
(c) 前記工程(b)で解離した抗原結合ドメインを含む抗原結合分子を単離する工程、
を含む抗原結合分子のスクリーニング方法を提供する。
(a) 抗原結合ドメインを含む抗原結合分子がディスプレイされたライブラリをMTAの存在下で抗原と接触させる工程、
(b) 前記工程(a)で抗原に結合した抗原結合ドメインを含む抗原結合分子を選択する工程、
(c) 前記工程(b)で選択した抗原結合ドメインを含む抗原結合分子をMTAの非存在下に置く工程、及び
(d) 前記工程(c)で抗原結合活性が、前記工程(b)で選択した基準より弱い抗原結合ドメインを含む抗原結合分子を単離する工程、
を含む抗原結合分子のスクリーニング方法を提供する。
(1) 抗原結合ドメインを含む抗原結合分子がディスプレイされたライブラリをMTAと接触させる工程、及び
(2) 前記工程(1)でMTAに結合した抗原結合ドメインを含む抗原結合分子を選択する工程、
(a) 前記工程(1)及び(2)で選択された抗原結合ドメインを含む抗原結合分子がディスプレイされたライブラリをMTAの存在下で抗原と接触させる工程、
(b) 前記工程(a)で結合した抗原結合ドメインを含む抗原結合分子をMTAの非存在下に置く工程、及び
(c) 前記工程(b)で解離した抗原結合ドメインを含む抗原結合分子を単離する工程、
を含む抗原結合分子のスクリーニング方法を提供する。
(1) 抗原結合ドメインを含む抗原結合分子がディスプレイされたライブラリをMTAと接触させる工程、及び
(2) 前記工程(1)でMTAに結合した抗原結合ドメインを含む抗原結合分子を選択する工程、
(a) 前記工程(1)及び(2)で選択された抗原結合ドメインを含む抗原結合分子がディスプレイされたライブラリをMTAの存在下で抗原と接触させる工程、
(b) 前記工程(a)で抗原に結合した抗原結合ドメインを含む抗原結合分子を選択する工程、
(c) 前記工程(b)で選択した抗原結合ドメインを含む抗原結合分子をMTAの非存在下に置く工程、及び
(d) 前記工程(c)で抗原結合活性が、前記工程(b)で選択した基準より弱い抗原結合ドメインを含む抗原結合分子を単離する工程、
を含む抗原結合分子のスクリーニング方法を提供する。
(a) MTAの存在下で抗原結合ドメインを含む抗原結合分子がディスプレイされたライブラリを抗原に接触させる工程、
(b) 前記工程(a)で抗原に結合しない抗原結合ドメインを含む抗原結合分子を選択する工程、
(c) 前記工程(b)で選択された抗原結合ドメインを含む抗原結合分子をMTAの非存在下で抗原に結合させる工程、及び
(d) 前記工程(c)で抗原に結合した抗原結合ドメインを含む抗原結合分子を単離する工程、
を含む抗原結合分子のスクリーニング方法を提供する。
本開示の一側面はMTA依存的に抗原に対する結合活性が変化する抗原結合ドメインを含む抗原結合分子の製造方法を提供する。
本開示の記載事項に従いMTA依存的に抗原に対する結合活性が変化する抗原結合ドメイン(または当該ドメインを含む抗原結合分子)が取得され得る。取得する方法の非限定な一態様として、以下にその具体例がいくつか例示される。
例えば、第1濃度のMTAの存在下における抗原に対する抗原結合ドメイン(または当該ドメインを含む抗原結合分子)の結合活性と第2濃度のMTAの存在下における抗原に対する抗原結合ドメイン(または当該ドメインを含む抗原結合分子)の結合活性の方が異なることを確認するためには、第1濃度のMTA存在下および第2濃度のMTA存在下における抗原に対する抗原結合ドメイン(または当該ドメインを含む抗原結合分子)の結合活性が比較される。MTA依存的に抗原に対する結合活性がの変化する抗原結合ドメインを選択するには、第1濃度のMTA存在下および第2濃度のMTA存在下における抗原に対する抗原結合ドメイン(または当該ドメインを含む抗原結合分子)の結合活性が異なる抗原結合ドメインが選択される。第1濃度と第2濃度は異なる濃度であり、これらの濃度のどちらか一方を0(即ち、MTAが非存在する)とすることが出来る。
MTAの高濃度存在下における抗原結合活性がMTAの低濃度存在下における抗原結合活性より高い抗原結合ドメイン(または当該ドメインを含む抗原結合分子)を取得するには、第1濃度における抗原結合活性が第2濃度における抗原結合活性が高い抗原結合ドメイン(または当該ドメインを含む抗原結合分子)が選択される。
MTA存在下における抗原結合活性がMTA非存在下における抗原結合活性より高い抗原結合ドメイン(または当該ドメインを含む抗原結合分子)を取得するには、第2濃度を0と設定した上、第1濃度における抗原結合活性が第2濃度における抗原結合活性が高い抗原結合ドメイン(または当該ドメインを含む抗原結合分子)が選択される。
(a) 抗原結合ドメインを第1濃度のMTA存在下で抗原と接触させる工程、
(b) 前記工程(a)で結合した抗原結合ドメインを第2濃度のMTA存在下に置く工程、
(c) 前記工程(b)で解離した抗原結合ドメインを単離する工程、及び
(d) 前記工程(c)で単離された抗原結合ドメインを含む抗原結合分子をコードするポリヌクレオチドが作動可能に連結されたベクターが導入された細胞を培養し、細胞の培養液から抗原結合ドメインを含む抗原結合分子を回収する工程、
を含む抗原結合分子の製造方法を提供する。
(a) 抗原結合ドメインを第1濃度のMTA存在下で抗原と接触させる工程、
(b) 前記工程(a)で前記抗原結合ドメインが抗原に結合したことを確認する工程、
(c) 前記抗原に結合した前記抗原結合ドメインを第2濃度のMTA存在下に置く工程、
(d) 前記工程(c)で抗原結合活性が、前記工程(b)で抗原に結合したことを確認した基準より弱い抗原結合ドメインを単離する工程、及び
(e) 前記工程(d)で単離された抗原結合ドメインを含む抗原結合分子をコードするポリヌクレオチドが作動可能に連結されたベクターが導入された細胞を培養し、細胞の培養液から抗原結合ドメインを含む抗原結合分子を回収する工程、
を含む抗原結合分子の製造方法を提供する。
(a) MTAに結合可能な抗原結合ドメインを第1濃度のMTA存在下で抗原と接触させる工程、
(b) 前記工程(a)で結合した抗原結合ドメインを第2濃度のMTA存在下に置く工程、
(c) 前記工程(b)で解離した抗原結合ドメインを単離する工程、及び
(d) 前記工程(c)で単離された抗原結合ドメインを含む抗原結合分子をコードするポリヌクレオチドが作動可能に連結されたベクターが導入された細胞を培養し、細胞の培養液から抗原結合ドメインを含む抗原結合分子を回収する工程、
を含む抗原結合分子の製造方法を提供する。
(a) MTAに結合可能な抗原結合ドメインを第1濃度のMTA存在下で抗原と接触させる工程、
(b) 前記工程(a)で前記抗原結合ドメインが抗原に結合したことを確認する工程、
(c) 前記抗原に結合した前記抗原結合ドメインを第2濃度のMTA存在下に置く工程、
(d) 前記工程(c)で抗原結合活性が、前記工程(b)で抗原に結合したことを確認した基準より弱い抗原結合ドメインを単離する工程、及び
(e) 前記工程(d)で単離された抗原結合ドメインを含む抗原結合分子をコードするポリヌクレオチドが作動可能に連結されたベクターが導入された細胞を培養し、細胞の培養液から抗原結合ドメインを含む抗原結合分子を回収する工程、
を含む抗原結合分子の製造方法を提供する。
(a) 第1濃度のMTA存在下で抗原結合ドメインを抗原に接触させる工程、
(b) 前記工程(a)で前記抗原結合ドメインが抗原に結合しないことを確認する工程、
(c) 前記抗原に結合しない抗原結合ドメインを第2濃度のMTA存在下で抗原に結合させる工程、
(d) 前記工程(c)で抗原に結合した抗原結合ドメインを単離する工程、及び
(e) 前記工程(d)で単離された抗原結合ドメインを含む抗原結合分子をコードするポリヌクレオチドが作動可能に連結されたベクターが導入された細胞を培養し、細胞の培養液から抗原結合ドメインを含む抗原結合分子を回収する工程、
を含む抗原結合分子の製造方法を提供する。
(a) 抗原結合ドメインがディスプレイされたライブラリを第1濃度のMTA存在下で抗原と接触させる工程、
(b) 前記工程(a)で結合した抗原結合ドメインを第2濃度のMTA存在下に置く工程、
(c) 前記工程(b)で解離した抗原結合ドメインを単離する工程、及び
(d) 前記工程(c)で単離された抗原結合ドメインを含む抗原結合分子をコードするポリヌクレオチドが作動可能に連結されたベクターが導入された細胞を培養し、細胞の培養液から抗原結合ドメインを含む抗原結合分子を回収する工程、
を含む抗原結合分子の製造方法を提供する。
(a) 抗原結合ドメインがディスプレイされたライブラリを第1濃度のMTA存在下で抗原と接触させる工程、
(b) 前記工程(a)で抗原に結合した抗原結合ドメインを選択する工程、
(c) 前記工程(b)で選択した抗原結合ドメインを第2濃度のMTA存在下に置く工程、
(d) 前記工程(c)で抗原結合活性が、前記工程(b)で選択した基準より弱い抗原結合ドメインを単離する工程、及び
(e) 前記工程(d)で単離された抗原結合ドメインを含む抗原結合分子をコードするポリヌクレオチドが作動可能に連結されたベクターが導入された細胞を培養し、細胞の培養液から抗原結合ドメインを含む抗原結合分子を回収する工程、
を含む抗原結合分子の製造方法を提供する。
(1) 抗原結合ドメインがディスプレイされたライブラリをMTAと接触させる工程、及び
(2) 前記工程(1)でMTAに結合した抗原結合ドメインを選択する工程、
(a) 前記工程(1)及び(2)で選択された抗原結合ドメインがディスプレイされたライブラリを第1濃度のMTA存在下で抗原と接触させる工程、
(b) 前記工程(a)で結合した抗原結合ドメインを第2濃度のMTA存在下に置く工程、
(c) 前記工程(b)で解離した抗原結合ドメインを単離する工程、及び
(d) 前記工程(c)で単離された抗原結合ドメインを含む抗原結合分子をコードするポリヌクレオチドが作動可能に連結されたベクターが導入された細胞を培養し、細胞の培養液から抗原結合ドメインを含む抗原結合分子を回収する工程、
を含む抗原結合分子の製造方法を提供する。
(1) 抗原結合ドメインがディスプレイされたライブラリをMTAと接触させる工程、及び
(2) 前記工程(1)でMTAに結合した抗原結合ドメインを選択する工程、
(a) 前記工程(1)及び(2)で選択された抗原結合ドメインがディスプレイされたライブラリを第1濃度のMTA存在下で抗原と接触させる工程、
(b) 前記工程(a)で抗原に結合した抗原結合ドメインを選択する工程、
(c) 前記工程(b)で選択した抗原結合ドメインを第2濃度のMTA存在下に置く工程、
(d) 前記工程(c)で抗原結合活性が、前記工程(b)で選択した基準より弱い抗原結合ドメインを単離する工程、及び
(e) 前記工程(d)で単離された抗原結合ドメインを含む抗原結合分子をコードするポリヌクレオチドが作動可能に連結されたベクターが導入された細胞を培養し、細胞の培養液から抗原結合ドメインを含む抗原結合分子を回収する工程、
を含む抗原結合分子の製造方法を提供する。
(a) 第1濃度のMTA存在下で抗原結合ドメインがディスプレイされたライブラリを抗原に接触させる工程、
(b) 前記工程(a)で抗原に結合しない抗原結合ドメインを選択する工程、
(c) 前記工程(b)で選択された抗原結合ドメインを第2濃度のMTA存在下で抗原に結合させる工程、
(d) 前記工程(c)で抗原に結合した抗原結合ドメインを単離する工程、及び
(e) 前記工程(d)で単離された抗原結合ドメインを含む抗原結合分子をコードするポリヌクレオチドが作動可能に連結されたベクターが導入された細胞を培養し、細胞の培養液から抗原結合ドメインを含む抗原結合分子を回収する工程、
を含む抗原結合分子の製造方法を提供する。
(a) 抗原結合ドメインをMTAの存在下で抗原と接触させる工程、
(b) 前記工程(a)で結合した抗原結合ドメインをMTAの非存在下に置く工程、
(c) 前記工程(b)で解離した抗原結合ドメインを単離する工程、及び
(d) 前記工程(c)で単離された抗原結合ドメインを含む抗原結合分子をコードするポリヌクレオチドが作動可能に連結されたベクターが導入された細胞を培養し、細胞の培養液から抗原結合ドメインを含む抗原結合分子を回収する工程、
を含む抗原結合分子の製造方法を提供する。
(a) 抗原結合ドメインをMTAの存在下で抗原と接触させる工程、
(b) 前記工程(a)で前記抗原結合ドメインが抗原に結合したことを確認する工程、
(c) 前記抗原に結合した前記抗原結合ドメインをMTAの非存在下に置く工程、
(d) 前記工程(c)で抗原結合活性が、前記工程(b)で抗原に結合したことを確認した基準より弱い抗原結合ドメインを単離する工程、及び
(e) 前記工程(d)で単離された抗原結合ドメインを含む抗原結合分子をコードするポリヌクレオチドが作動可能に連結されたベクターが導入された細胞を培養し、細胞の培養液から抗原結合ドメインを含む抗原結合分子を回収する工程、
を含む抗原結合分子の製造方法を提供する。
(a) MTAに結合可能な抗原結合ドメインをMTAの存在下で抗原と接触させる工程、
(b) 前記工程(a)で結合した抗原結合ドメインをMTAの非存在下に置く工程、
(c) 前記工程(b)で解離した抗原結合ドメインを単離する工程、及び
(d) 前記工程(c)で単離された抗原結合ドメインを含む抗原結合分子をコードするポリヌクレオチドが作動可能に連結されたベクターが導入された細胞を培養し、細胞の培養液から抗原結合ドメインを含む抗原結合分子を回収する工程、
を含む抗原結合分子の製造方法を提供する。
(a) MTAに結合可能な抗原結合ドメインをMTAの存在下で抗原と接触させる工程、
(b) 前記工程(a)で前記抗原結合ドメインが抗原に結合したことを確認する工程、
(c) 前記抗原に結合した前記抗原結合ドメインをMTAの非存在下に置く工程、
(d) 前記工程(c)で抗原結合活性が、前記工程(b)で抗原に結合したことを確認した基準より弱い抗原結合ドメインを単離する工程、及び
(e) 前記工程(d)で単離された抗原結合ドメインを含む抗原結合分子をコードするポリヌクレオチドが作動可能に連結されたベクターが導入された細胞を培養し、細胞の培養液から抗原結合ドメインを含む抗原結合分子を回収する工程、
を含む抗原結合分子の製造方法を提供する。
(a) MTAの存在下で抗原結合ドメインを抗原に接触させる工程、
(b) 前記工程(a)で前記抗原結合ドメインが抗原に結合しないことを確認する工程、
(c) 前記抗原に結合しない抗原結合ドメインをMTAの非存在下で抗原に結合させる工程、
(d) 前記工程(c)で抗原に結合した抗原結合ドメインを単離する工程、及び
(e) 前記工程(d)で単離された抗原結合ドメインを含む抗原結合分子をコードするポリヌクレオチドが作動可能に連結されたベクターが導入された細胞を培養し、細胞の培養液から抗原結合ドメインを含む抗原結合分子を回収する工程、
を含む抗原結合分子の製造方法を提供する。
(a) 抗原結合ドメインがディスプレイされたライブラリを MTAの存在下で抗原と接触させる工程、
(b) 前記工程(a)で結合した抗原結合ドメインをMTAの非存在下に置く工程、
(c) 前記工程(b)で解離した抗原結合ドメインを単離する工程、及び
(d) 前記工程(c)で単離された抗原結合ドメインを含む抗原結合分子をコードするポリヌクレオチドが作動可能に連結されたベクターが導入された細胞を培養し、細胞の培養液から抗原結合ドメインを含む抗原結合分子を回収する工程、
を含む抗原結合分子の製造方法を提供する。
(a) 抗原結合ドメインがディスプレイされたライブラリをMTAの存在下で抗原と接触させる工程、
(b) 前記工程(a)で抗原に結合した抗原結合ドメインを選択する工程、
(c) 前記工程(b)で選択した抗原結合ドメインをMTAの非存在下に置く工程、
(d) 前記工程(c)で抗原結合活性が、前記工程(b)で選択した基準より弱い抗原結合ドメインを単離する工程、及び
(e) 前記工程(d)で単離された抗原結合ドメインを含む抗原結合分子をコードするポリヌクレオチドが作動可能に連結されたベクターが導入された細胞を培養し、細胞の培養液から抗原結合ドメインを含む抗原結合分子を回収する工程、
を含む抗原結合分子の製造方法を提供する。
(1) 抗原結合ドメインがディスプレイされたライブラリをMTAと接触させる工程、及び
(2) 前記工程(1)でMTAに結合した抗原結合ドメインを選択する工程、
(a) 前記工程(1)及び(2)で選択された抗原結合ドメインがディスプレイされたライブラリをMTAの存在下で抗原と接触させる工程、
(b) 前記工程(a)で結合した抗原結合ドメインをMTAの非存在下に置く工程、
(c) 前記工程(b)で解離した抗原結合ドメインを単離する工程、及び
(d) 前記工程(c)で単離された抗原結合ドメインを含む抗原結合分子をコードするポリヌクレオチドが作動可能に連結されたベクターが導入された細胞を培養し、細胞の培養液から抗原結合ドメインを含む抗原結合分子を回収する工程、
を含む抗原結合分子の製造方法を提供する。
(1) 抗原結合ドメインがディスプレイされたライブラリをMTAと接触させる工程、及び
(2) 前記工程(1)でMTAに結合した抗原結合ドメインを選択する工程、
(a) 前記工程(1)及び(2)で選択された抗原結合ドメインがディスプレイされたライブラリをMTAの存在下で抗原と接触させる工程、
(b) 前記工程(a)で抗原に結合した抗原結合ドメインを選択する工程、
(c) 前記工程(b)で選択した抗原結合ドメインをMTAの非存在下に置く工程、
(d) 前記工程(c)で抗原結合活性が、前記工程(b)で選択した基準より弱い抗原結合ドメインを単離する工程、及び
(e) 前記工程(d)で単離された抗原結合ドメインを含む抗原結合分子をコードするポリヌクレオチドが作動可能に連結されたベクターが導入された細胞を培養し、細胞の培養液から抗原結合ドメインを含む抗原結合分子を回収する工程、
を含む抗原結合分子の製造方法を提供する。
(a) MTAの存在下で抗原結合ドメインがディスプレイされたライブラリを抗原に接触させる工程、
(b) 前記工程(a)で抗原に結合しない抗原結合ドメインを選択する工程、
(c) 前記工程(b)で選択された抗原結合ドメインをMTAの非存在下で抗原に結合させる工程、
(d) 前記工程(c)で抗原に結合した抗原結合ドメインを単離する工程、及び
(e) 前記工程(d)で単離された抗原結合ドメインを含む抗原結合分子をコードするポリヌクレオチドが作動可能に連結されたベクターが導入された細胞を培養し、細胞の培養液から抗原結合ドメインを含む抗原結合分子を回収する工程、
を含む抗原結合分子の製造方法を提供する。
本明細書において「ライブラリ」とは互いに配列の異なる複数の抗原結合ドメインを含む抗原結合分子、または/および互いに配列の異なる複数の抗原結合ドメインを含む抗原結合分子をコードする核酸若しくはポリヌクレオチドをいう。ライブラリ中に含まれる抗原結合ドメインを含む抗原結合分子、または/および抗原結合ドメインを含む抗原結合分子をコードする核酸の配列は単一の配列ではなく、互いに配列の異なる複数の抗原結合分子または/および互いに配列の異なる複数の抗原結合分子をコードする核酸である。
XAXWMC(配列番号:65)を含むH-CDR1;
CIFAXXXYXXSGGSTYYASWAKG(配列番号:66)を含むH-CDR2;
GXGXXXGXXDEL(配列番号:67)を含むH-CDR3;
QSSEXVXXXXLS(配列番号:68)を含むL-CDR1;
XAXTXPX(配列番号:69)を含むL-CDR2;及び
AGLYXGNIPA(配列番号:70)を含むL-CDR3;
を含む抗体可変領域である。ここで、Xは任意のアミノ酸を指し、異なる位置に存在するXは同種のアミノ酸であっても良く、同種のアミノ酸でなくても良い。
XAXWMC(配列番号:65)を含むH-CDR1;
CIFAX1XXYXXSGGSTYYASWAKG(配列番号:71)を含むH-CDR2;
GXGXXXGXXDEL(配列番号:67)を含むH-CDR3;
QSSEXVXXX1XLS(配列番号:72)を含むL-CDR1;
XAXTXPX(配列番号:69)を含むL-CDR2;及び
AGLYXGNIPA(配列番号:70)を含むL-CDR3;
を含む抗体可変領域である。ここで、Xは任意のアミノ酸、X1はA、D、E、G、H、I、K、L、M、N、P、Q、R、S、TおよびVから選ばれるアミノ酸である。更に、異なる位置に存在するXもしくはX1は同種のアミノ酸であっても良く、同種のアミノ酸でなくても良い。
XXAXWMC(配列番号:73)を含むH-CDR1;
CIFAX1XXYXXSGGSTYYASWAKG(配列番号:71)を含むH-CDR2;
GXGXXXGXXDEL(配列番号:67)を含むH-CDR3;
QSSEXVXXX1XLS(配列番号:72)を含むL-CDR1;
XAXTXPX(配列番号:69)を含むL-CDR2;及び
AGLYXGNIPA(配列番号:70)を含むL-CDR3;
を含む抗体可変領域である。ここで、Xは任意のアミノ酸、X1はA、D、E、G、H、I、K、L、M、N、P、Q、R、S、TおよびVから選ばれるアミノ酸であ。更に、異なる位置に存在するXもしくはX1は同種のアミノ酸であっても良く、同種のアミノ酸でなくても良い。
XXXWMC(配列番号:74)を含むH-CDR1;
CIXSXXXXTXYASWVNG(配列番号:75)を含むH-CDR2;
EXXXXSGALNL(配列番号:76)を含むH-CDR3;
HSSKXVXXXXXLA(配列番号:77)を含むL-CDR1;
XAXXLAS(配列番号:78)を含むL-CDR2;及び
QGTYXXXXFYFA(配列番号:79)を含むL-CDR3;
を含む抗体可変領域である。ここで、Xは任意のアミノ酸を指し、異なる位置に存在するXは同種のアミノ酸であっても良く、同種のアミノ酸でなくても良い。
X2X3X4X5G(配列番号:80)を含むH-CDR1;
X6IGX7X8X9X10X11WX12PX13WVKX14(配列番号:81)を含むH-CDR2;
GX15X16X17X18X19X20NAX21DP(配列番号:82)を含むH-CDR3;
QSSQSVX22X23NNX24LS(配列番号:83)を含むL-CDR1;
DASTLAS(配列番号:84)を含むL-CDR2;及び
HGX25X26X27X28X29X30X31X32DNX33(配列番号:85)を含むL-CDR3;
を含む抗体可変領域であり、
X2はA、D、E、F、G、H、I、K、L、N、Q、R、S、T、V、WおよびYから選ばれるアミノ酸、
X3はD、E、F、H、K、N、P、RおよびYから選ばれるアミノ酸、
X4はA、I、P、TおよびVから選ばれるアミノ酸、
X5はA、E、F、H、I、K、L、M、N、Q、S、T、V、WおよびYから選ばれるアミノ酸、
X6はD、IおよびVから選ばれるアミノ酸、
X7はA、D、E、G、I、K、QおよびRから選ばれるアミノ酸、
X8はD、E、F、G、H、I、K、L、P、Q、R、S、T、V、WおよびYから選ばれるアミノ酸、
X9はA、D、E、F、G、HおよびSから選ばれるアミノ酸、
X10はA、D、E、F、G、H、I、K、L、N、Q、R、S、T、V、WおよびYから選ばれるアミノ酸、
X11はA、D、E、G、H、I、K、L、N、P、Q、R、S、TおよびVから選ばれるアミノ酸、
X12はA、D、E、F、G、H、I、K、L、Q、R、S、T、V、WおよびYから選ばれるアミノ酸、
X13はA、F、Q、R、S、T、V、WおよびYから選ばれるアミノ酸、
X14はA、FおよびGから選ばれるアミノ酸、
X15はA、E、F、G、H、K、L、Q、R、S、T、WおよびYから選ばれるアミノ酸、
X16はF、H、K、N、WおよびYから選ばれるアミノ酸、
X17はA、D、E、F、G、H、I、K、L、N、P、Q、R、S、T、V、WおよびYから選ばれるアミノ酸、
X18はA、D、E、G、H、QおよびSから選ばれるアミノ酸、
X19はFおよびYから選ばれるアミノ酸、
X20はN、TおよびVから選ばれるアミノ酸、
X21はFおよびWから選ばれるアミノ酸、
X22はA、E、F、H、I、K、L、N、R、S、T、V、WおよびYから選ばれるアミノ酸、
X23はA、D、E、F、G、H、I、K、L、N、P、Q、R、S、T、V、WおよびYから選ばれるアミノ酸、
X24はA、E、F、G、H、SおよびYから選ばれるアミノ酸、
X25はA、SおよびTから選ばれるアミノ酸、
X26はA、D、E、F、G、H、I、K、L、M、N、Q、R、S、T、V、WおよびYから選ばれるアミノ酸、
X27はA、D、E、F、G、H、L、N、Q、R、S、T、VおよびYから選ばれるアミノ酸、
X28はA、E、F、G、H、I、K、L、N、P、Q、R、S、T、V、WおよびYから選ばれるアミノ酸、
X29はA、D、E、F、G、H、I、K、L、N、P、Q、R、S、T、V、W、Yから選ばれるアミノ酸、
X30はA、D、E、F、G、H、I、K、L、N、P、Q、R、V、WおよびYから選ばれるアミノ酸、
X31はA、D、E、F、G、H、I、K、L、N、P、Q、R、S、T、V、WおよびYから選ばれるアミノ酸、
X32はA、F、H、I、K、L、N、P、Q、R、S、T、V、WおよびYから選ばれるアミノ酸、
X33はAおよびGから選ばれるアミノ酸である。
本開示の一態様において、MTA依存的に抗原に対する結合活性を変化させるアミノ酸残基を有する抗原結合ドメインを含む抗原結合分子ライブラリ中の抗原結合ドメインは抗体可変領域であり、当該ライブラリに含まれるもしくは当該ライブラリに含まれる核酸にコードされる「複数の抗原結合分子」に含まれる抗原結合ドメインは、MTAに対する結合活性を有する抗体可変領域未改変体中の1つまたは複数のアミノ酸部位に位置するアミノ酸と異なるアミノ酸を有し、互いに配列が異なる複数の抗体可変領域改変体を含む。
MTA依存的に抗原に対する結合活性を変化させるアミノ酸残基を有する抗原結合ドメインを含む抗原結合分子ライブラリをデザインするときに出発分子として使用することが出来るため、本明細書で「鋳型」または「テンプレート」と称する場合もある。
a) 配列番号:46で示す重鎖可変領域と配列番号:47で示す軽鎖可変領域を含む抗体可変領域;
b) 配列番号:50で示す重鎖可変領域と配列番号:51で示す軽鎖可変領域を含む抗体可変領域;
c) 配列番号:48で示す重鎖可変領域と配列番号:49で示す軽鎖可変領域を含む抗体可変領域;
d) 配列番号:52で示す重鎖可変領域と配列番号:53で示す軽鎖可変領域を含む抗体可変領域;
e) 配列番号:31で示す重鎖可変領域と配列番号:32で示す軽鎖可変領域を有する抗体可変領域。
また、前記のスクリーニング方法によって取得される本開示の抗原結合ドメイン又は抗原結合分子の調製法の非限定の一態様として、あらかじめ存在している低分子化合物に結合活性を有する抗原結合ドメインを用いることが可能である。例えば、これに限定されるわけではないが、MTAを例にした場合、MTAに結合活性を有する抗原結合ドメイン、MTA依存的に抗原に対する結合活性が変化する抗原結合ドメイン、MTAと相互作用するアミノ酸残基を有する抗原結合ドメインを用いることが可能である。
本開示における「改変体」とは、親配列の未改変体に対して、少なくとも1又はそれ以上のアミノ酸が置換されている親配列の各々異なる改変体をいう。
一態様において本開示の抗体可変領域改変体を作製するため、前記の抗体可変領域未改変体の重鎖可変領域または軽鎖可変領域の配列、もしくはCDR配列またはフレームワーク配列に含まれる抗原結合分子を作製するために部位特異的変異誘発法(Kunkelら(Proc. Natl. Acad. Sci. U.S.A. (1985) 82, 488-492))やOverlap extension PCR等の公知の方法が適宜採用され得る。
非限定的な一態様において、前記抗原結合ドメイン改変体が抗原結合ドメイン未改変体と異なるアミノ酸を有するアミノ酸部位は、下記のアミノ酸部位の群から選ばれる一つまたは複数のアミノ酸部位である:
1) 前記抗原結合ドメイン未改変体中のMTAとの結合に関与しないアミノ酸部位に対応するアミノ酸部位、
2) 前記抗原結合ドメイン改変体と比較して、前記抗原結合ドメイン改変体のMTAとの結合を著しく減弱させないアミノ酸部位、及び
3) 前記抗原結合ドメイン改変体の抗原に対するMTA依存的結合に寄与しやすいアミノ酸部位。
1) 前記抗原結合ドメイン未改変体中のMTAとの結合に関与しないアミノ酸部位に対応するアミノ酸部位、
2) 前記抗原結合ドメイン改変体と比較して、前記抗原結合ドメイン改変体のMTAとの結合を著しく減弱させないアミノ酸部位、
3) 前記抗原結合ドメイン未改変体の表面に露出するアミノ酸部位に対応するアミノ酸部位、及び
4) 前記抗原結合ドメイン未改変体においてMTA結合/非結合時に構造変化率が大きい領域に位置するアミノ酸部位に対応するアミノ酸部位。
前記抗原結合ドメイン未改変体の配列が抗原結合ドメイン改変体の配列と異なるアミノ酸を有するアミノ酸部位は、ライブラリを設計するときに、多様なアミノ酸が含まれるように設計することが可能な部位とし、本開示において、「多様化可能なアミノ酸部位」とも呼ばれる。多様化可能なアミノ酸部位は、以下を含むことが出来る:
(i) 抗原結合ドメインの表面に露出するアミノ酸部位;
(ii) 抗原結合ドメインがMTAに結合したときの構造とMTAに結合していない時の構造を比較するときに構造変化率が大きい領域に位置するアミノ酸部位;
(iii) MTAとの結合に関与しないアミノ酸部位;
(iv) MTAとの結合を著しく減弱させないアミノ酸部位;
(v) 抗原結合ドメインが属する動物種において、アミノ酸出現頻度の多様性のあるアミノ酸部位;
(vi) Canonical structureの形成に重要でないアミノ酸部位;
(vii) 抗原結合ドメイン改変体の抗原に対するMTA依存的結合に寄与しやすいアミノ酸部位。
本開示における「MTAとの結合に関与しないアミノ酸部位」は、MTAと抗原結合分子の複合体の結晶構造解析、NMRを用いた立体構造解析、又はアミノ酸の変異導入等の手法によって同定することができる。本開示の非限定の一態様として、MTAと抗原結合分子の複合体の結晶構造解析から、MTAとの結合に関与していない抗原結合分子のアミノ酸残基、特にMTAとの結合に関与していない抗原結合ドメインのアミノ酸残基を同定することができる。ここで、「MTAとの結合に関与」とは、抗原結合ドメインが抗体可変領域である場合、抗体可変領域のH鎖又はL鎖を形成するアミノ酸における側鎖又は主鎖の原子とMTAの原子が、結合活性に効果を及ぼしうる距離で分子間相互作用を形成している状態、又は、あるアミノ酸残基がCDRループ等の立体構造をMTAが結合する際のコンフォメーションに安定化させる等の間接的な影響を含む、MTAの結合に寄与している状態、ならびにその双方を満たす状態のことをいう。
別の一態様では、MTAに対する結合に関与しないアミノ酸部位の判定は、MTAとの結合に関与しているアミノ酸部位のうちから選択される、いずれか一つ以上のアミノ酸部位以外のアミノ酸部位であるとも考えることができる。
本明細書における「分子間相互作用を形成している状態」については、抗原結合ドメインが抗体可変領域である場合、例えばMTAと抗原結合分子の複合体の結晶構造解析から、抗体可変領域のH鎖又はL鎖を形成するアミノ酸の側鎖又は主鎖を構成する非水素原子とMTAを構成する非水素原子との原子間距離をもとに判定できる。たとえば,上記原子間距離は3.0Å、3.2Å、3.4Å、3.6Å、3.8Å、4.0Å、4.2Å、4.4Å、4.6Å、4.8Å又は5.0Å以内が好ましいがこれに限定されることはない。更に好ましい上記原子間距離は3.6Å、3.8Å、4.0Å又は4.2Å以内である。
より詳しくは、立体構造上での原子間距離と形成される分子間相互作用の種類ならびに原子の種類の情報をもとに直接的に相互作用している可能性が判定できる。さらに正確にはAlaやGlyへの改変といったアミノ酸残基の変異導入がMTAの活性に与える影響から判断することができるが、これに限定されるわけではない。
本明細書における「間接的に影響している状態」についても,例えば、MTAと抗原結合分子の複合体の立体構造から各アミノ酸残基のコンフォメーションや周囲の残基との分子間相互作用の状況を詳細に解析することで、MTAの結合に間接的に影響しているかどうかを推定できるが、より正確にはAlaやGlyへの改変といったアミノ酸残基の変異導入がMTAの活性に与える影響から判断することができる。
本開示における非限定の一態様として、「MTAとの結合を著しく減弱させないアミノ酸部位」は、アミノ酸の変異導入の方法によって同定することができる。例えば、可変領域のアミノ酸を網羅的に改変して、個々の改変体のMTAへの結合が、Biacore等を用いた公知の方法で測定され、個々の改変体のMTAに対する結合活性(アフィニティ)がKD値として算出される。当該KD値が親配列である未改変体のKD値と比較され、一定の基準を上回る結合を示す改変箇所が、「MTAとの結合を著しく減弱させないアミノ酸部位」と判定される。例えば、Biacore等の公知の方法を用いた測定の結果、個々の改変体のMTAに対する結合活性(アフィニティ)がKD値として算出され、重鎖の部位としては改変によってMTA結合能が未改変体の1/100、1/50、1/10、1/9、1/8、1/7、1/6、1/5、1/4、1/3又は1/2の結合能を下回らないもの、および軽鎖の部位としては改変によってMTA結合能が未改変体の1/100、1/50、1/10、1/9、1/8、1/7、1/6、1/5、1/4、1/3又は1/2の結合能を下回らないものがMTAとの結合を著しく減弱させないアミノ酸部位と判定されるが、上記基準に限定されるものではない。あるいは、親配列である未改変体のKD値との比較ではなく、個々の改変体のMTAに対する結合活性(アフィニティ)がKD値として算出され、重鎖の部位としては10mM、1mM、100uM、10uM、1uM、100nM、10nM、1nM、100pM、10pM、又は1pMの結合能を下回らないもの、および軽鎖の部位としては10mM、1mM、100uM、10uM、1uM、100nM、10nM、1nM、100pM、10pM、又は1pMの結合能を下回らないものがMTAとの結合を著しく減弱させないアミノ酸部位と判定されるが、上記基準に限定されるものではない。未改変及び改変体のMTAに対する結合活性の測定は、当業者公知の方法(Biacore、ELISA、ECL等)から適宜選択して実施することができる。
別の一態様では、MTAとの結合を著しく減弱させないアミノ酸部位の判定は、MTAとの結合に関与しているアミノ酸部位のうちから選択される、いずれか一つ以上のアミノ酸部位以外のアミノ酸部位であるとも考えることができる。
本開示における「MTA依存的結合に寄与しやすいアミノ酸部位」は、MTAと抗原結合分子の複合体の結晶構造解析、NMRを用いた立体構造解析、又はアミノ酸の変異導入等の手法によって同定または推定することができる。「MTA依存的結合に寄与しやすいアミノ酸部位」を推定する非限定な手法として、抗原結合分子蛋白の表面に露出しているアミノ酸残基が位置するアミノ酸部位、もしくはMTAが結合したときに非結合時と比較して構造変化する領域に位置するアミノ酸部位を同定する手法が例示される。
本開示における「抗原結合ドメインの表面に露出するアミノ酸部位」は、タンパク質の立体構造上の表面に位置するアミノ酸部位をいう。抗原結合ドメインを含む抗原結合分子単体、またはMTAと抗原結合分子の複合体に対して、結晶構造解析やNMRを用いた立体構造解析等の手法によって、抗原結合ドメインのタンパク質表面に位置するアミノ酸残基およびアミノ酸部位を同定することができる。抗原結合ドメインの表面に露出するアミノ酸部位を同定する非限定な一手法として、溶媒露出表面積(Accessible surface area)を算出することで、表面に露出するアミノ酸部位を同定する手法が挙げられる。
本開示における「抗原結合ドメインのMTA結合/非結合時に構造変化率が大きい領域」は、結晶構造解析やNMRを用いた立体構造解析等の手法を用いて、抗原結合ドメインを含む抗原結合分子単体、及びMTAと抗原結合分子の複合体の構造を比較することにより、構造変化する領域を同定することにより同定することが出来る。
また、「抗原結合ドメインのMTA結合/非結合時に構造変化率が大きい領域に位置するアミノ酸部位」は、抗原結合ドメインを含む抗原結合分子単体、及びMTAと抗原結合分子の複合体の構造を比較することにより直接同定することもできる。抗原結合ドメインが抗体可変領域の場合、MTAに結合した時の抗体H鎖およびL鎖の構造と、MTAに結合していない時の抗体H鎖、L鎖構造を重ね合わせたときに計算される、MTA結合時/非結合時の各アミノ酸残基のCα原子間の距離をもとに、当該アミノ酸残基が位置するアミノ酸部位が「抗原結合ドメインのMTA結合/非結合時に構造変化率が大きい領域に位置するアミノ酸部位」であるか否かを判定できる。例えば、 MTA結合時/非結合時のCα原子間の距離が可変領域全アミノ酸残基のMTA結合時/非結合時のCα原子間距離の平均値以上であるアミノ酸残基が位置するアミノ酸部位を「抗原結合ドメインのMTA結合/非結合時に構造変化率が大きい領域に位置するアミノ酸部位」と判定することが出来るが、これに限定されることはない。
このような、抗原結合ドメインのMTA結合/非結合時に構造変化率が大きい領域に位置するアミノ酸部位のアミノ酸を多様なアミノ酸に置換することにより、MTA依存的な抗原結合活性をもたらすことが期待される。これにより、このようなアミノ酸部位において多様なアミノ酸が出現するライブラリを設計することができる。この場合において、抗原結合ドメインのMTA結合/非結合時に構造変化率が大きい領域に位置するアミノ酸部位に異なるアミノ酸を有する抗原結合分子の集合となるように、複数の抗原結合分子から主としてなるライブラリを設計することが可能である。
本開示における「アミノ酸出現頻度の多様性のあるアミノ酸部位」とは、親配列が属する動物種の抗体のレパートリーとして、1%以上の出現頻度で存在が認められるアミノ酸の種類として2種以上が認められるアミノ酸部位のことをいう。
本開示における「Canonical structureの形成に重要でないアミノ酸部位」において、抗体のcanonical structureとは、抗体重鎖及び軽鎖の主にCDR1、2の立体構造のクラスタリングを示しており、構造は抗体のサブグループや、CDRの長さや配列によって分類されることができる。各canonical structureにおいて、構造の維持に重要な残基は既に公知であり、Chothiaら(J. Mol. Biol. (1992) 227, 799-817)、Al-Lazikaniら(J. Mol. Biol. (1997) 273, 927-948)、Tomlinsonら(J. Mol. Biol.(1992) 227, 776-798)等の報告を参照することにより、該当する親抗原結合分子が分類されるcanonical structure、及びその構造に重要な残基を特定することが可能である。
また、抗体以外の抗原結合ドメインにおいても、構造の維持に重要な残基が存在していることは公知であり、これに限定されるわけではないが、作製した変異体の構造解析等により、個々の抗原結合ドメインにおいてcanonical structureの形成に重要でないアミノ酸部位を同定することが可能である。
本開示の一態様として、以下(a)および(b)の工程:
(a) MTAに対する結合活性を有する抗原結合ドメインにおいて、以下(i)乃至(vi)の少なくとも一つ以上を満たすアミノ酸部位を特定する工程:
(i) 前記抗原結合ドメインの表面に露出するアミノ酸部位;
(ii) 前記抗原結合ドメインがMTAに結合したときの構造とMTAに結合していない時の構造を比較するときに構造変化率が大きい領域に位置するアミノ酸部位;
(iii) MTAとの結合に関与しないアミノ酸部位;
(iv) MTAとの結合を著しく減弱させないアミノ酸部位;
(v) 前記抗原結合ドメインが属する動物種において、アミノ酸出現頻度の多様性のあるアミノ酸部位;または
(vi) Canonical structureの形成に重要でないアミノ酸部位;
(b) 前記抗原結合ドメインにおいて、未改変体をコードする核酸及び工程(a)で特定された1または複数のアミノ酸部位にアミノ酸改変を有する、互いに配列が異なる、前記抗原結合ドメインの複数の改変体をそれぞれコードする核酸を含むライブラリを設計する工程、
を含む方法によって製造されるライブラリが提供される。
(a) MTAに対する結合活性を有する抗原結合ドメインにおいて、以下(i)乃至(vi)の少なくとも一つ以上を満たすアミノ酸部位を特定する工程:
(i) 前記抗原結合ドメインの表面に露出するアミノ酸部位;
(ii) 前記抗原結合ドメインがMTAに結合したときの構造とMTAに結合していない時の構造を比較するときに構造変化率が大きい領域に位置するアミノ酸部位;
(iii) MTAとの結合に関与しないアミノ酸部位;
(iv) MTAとの結合を著しく減弱させないアミノ酸部位;
(v) 前記抗原結合ドメインが属する動物種において、アミノ酸出現頻度の多様性のあるアミノ酸部位;または
(vi) Canonical structureの形成に重要でないアミノ酸部位;
(b) 前記抗原結合ドメインにおいて、未改変体をコードする核酸及び工程(a)で特定された1または複数のアミノ酸部位にアミノ酸改変を有する、互いに配列が異なる、前記抗原結合ドメインの複数の改変体をそれぞれコードする核酸を含むライブラリを設計する工程、
を含む方法により製造されたライブラリであって、
工程(b)のアミノ酸改変は、以下(1)乃至(3)の少なくとも一つ以上を満たす:
(1) 当該アミノ酸改変を有する抗原結合ドメイン改変体がMTAに結合したときの構造とMTAに結合していないときの構造を比較する場合、当該改変後アミノ酸が位置するアミノ酸部位の構造変化率が大きい;
(2) 当該アミノ酸改変を有する抗原結合ドメイン改変体がMTAに結合したときの構造とMTAに結合していないときの構造を比較する場合、当該改変後アミノ酸が存在することにより前記抗原結合ドメイン改変体の構造変化が阻害されない;
(3) 当該アミノ酸改変を有する抗原結合ドメイン改変体が、前記抗原結合ドメイン未改変体と比べて、MTAに対する結合活性が著しく減弱されていない。
非限定的な一態様において、本開示のライブラリはMTAに結合する抗原結合ドメインを含む抗原結合分子をコードする核酸が濃縮されたライブラリが提供される。
本開示における「濃縮する」とは、濃縮作業実施前のライブラリとの比較において、目的の活性を有する改変体をコードする核酸の存在比率を上昇させることを言う。目的の活性を有する改変体をコードする核酸の存在比率が上昇した状態を、「濃縮された」と言う。
一例として、これに限定されるわけではないが、MTAに結合する抗原結合分子をコードする核酸を濃縮するとは、パンニングによりMTAに対して結合活性を有する抗原結合分子をコードする核酸の存在比率を上昇させることによって達成可能である。より具体的には、一例として、複数の抗原結合分子を含むライブラリがファージディスプレイ法により表面に提示されたファージをMTAと接触させ、洗浄作業により結合活性を有していない分子を提示しているファージ及び分子を提示していないファージを除去したのち、結合を維持している抗原結合分子を提示しているファージのみを回収することによって、パンニングによりMTAに対して結合活性を有する抗原結合分子をコードする核酸の存在比率を上昇させることが可能であるが、これに限定されることはない。このような方法は、即ち、以下(1)~(2)の工程:
(1) ライブラリからディスプレイされた抗原結合ドメインをMTAと接触させる工程、及び
(2) 前記工程(1)でMTAに結合した抗原結合ドメインを選択する工程、を含む方法である。
目的の活性を有する抗原結合分子コードする核酸の存在比率が、濃縮作業実施前のライブラリとの比較において、1.1倍以上上昇することが好ましい。より好ましくは、目的の活性を有する抗原結合分子をコードする核酸の存在比率を、1.2倍以上、1.5倍以上、2倍以上、4倍以上、10倍以上、25倍以上、100倍以上上昇させることにより、本開示に記載のライブラリを製造することが可能である。非限定的な一態様において、このような方法で濃縮されたライブラリ中の抗原結合分子がMTAに対する結合活性は、MTAとは異なる種類の分子である抗原の非存在下でも示される。
濃縮対象となるライブラリは、MTA依存的に抗原に対する結合活性が変化する抗原結合ドメインを含んでいる限りその種類は限定されない。より具体的に、これらに限定されないが、ナイーブヒト抗体ディスプレイライブラリ、合成ヒト抗体ディスプレイライブラリ、後述する本明細書の方法に沿って設計されるライブラリ、本明細書実施例に記載のライブラリが挙げられる。
(1) ライブラリからディスプレイされた抗原結合ドメインをアデノシンと接触させる工程、及び
(2) 前記工程(1)でアデノシンに結合した抗原結合ドメインを選択する工程、を含む方法である。
目的の活性を有する抗原結合分子コードする核酸の存在比率が、濃縮作業実施前のライブラリとの比較において、1.1倍以上上昇することが好ましい。より好ましくは、目的の活性を有する抗原結合分子をコードする核酸の存在比率を、1.2倍以上、1.5倍以上、2倍以上、4倍以上、10倍以上、25倍以上、100倍以上上昇させることにより、本開示に記載のライブラリを製造することが可能である。非限定的な一態様において、このような方法で濃縮されたライブラリ中の抗原結合分子がアデノシンに対する結合活性は、アデノシンとは異なる種類の分子である抗原の非存在下でも示される。
濃縮対象となるライブラリは、アデノシン依存的に抗原に対する結合活性が変化する抗原結合ドメインを含んでいる限りその種類は限定されない。より具体的に、これらに限定されないが、ナイーブヒト抗体ディスプレイライブラリ、合成ヒト抗体ディスプレイライブラリ、本明細書のライブラリ製造方法に沿って製造されるライブラリ、本明細書に記載のライブラリが挙げられる。
本開示はまた、上記に説明した本開示に包含される様々な態様の「ライブラリ」を製造する方法に関する。
本開示に係る「ライブラリの製造方法」は、以下に例示するようないずれかの特定の方法に限定されるものではなく、上述した本開示の「ライブラリ」を製造し得る方法であればいずれの方法も包含される。
本開示に係る「ライブラリの製造方法」としては、例えば、以下に例示するような方法を挙げることができる。
なお、以下に例示する「ライブラリの製造方法」における各特定事項は、上記で本開示の「ライブラリ」から「濃縮された」について詳述したとおりの技術的意義を有する。
(a) MTAに対する結合活性を有する抗原結合ドメインにおいて、以下(i)乃至(vi)の少なくとも一つ以上を満たすアミノ酸部位を特定する工程:
(i) 前記抗原結合ドメインの表面に露出するアミノ酸部位;
(ii) 前記抗原結合ドメインがMTAに結合したときの構造とMTAに結合していない時の構造を比較するときに構造変化率が大きい領域に位置するアミノ酸部位;
(iii) MTAとの結合に関与しないアミノ酸部位;
(iv) MTAとの結合を著しく減弱させないアミノ酸部位;
(v) 前記抗原結合ドメインが属する動物種において、アミノ酸出現頻度の多様性のあるアミノ酸部位;または
(vi) Canonical structureの形成に重要でないアミノ酸部位;
(b) 前記抗原結合ドメインにおいて、未改変体をコードする核酸及び工程(a)で特定された1または複数のアミノ酸部位にアミノ酸改変を有する、互いに配列が異なる、前記抗原結合ドメインの複数の改変体をそれぞれコードする核酸を含むライブラリを設計する工程、
を含むライブラリの製造方法が提供される。
(a) MTAに対する結合活性を有する抗原結合ドメインにおいて、以下(i)乃至(vi)の少なくとも一つ以上を満たすアミノ酸部位を特定する工程:
(i) 前記抗原結合ドメインの表面に露出するアミノ酸部位;
(ii) 前記抗原結合ドメインがMTAに結合したときの構造とMTAに結合していない時の構造を比較するときに構造変化率が大きい領域に位置するアミノ酸部位;
(iii) MTAとの結合に関与しないアミノ酸部位;
(iv) MTAとの結合を著しく減弱させないアミノ酸部位;
(v) 前記抗原結合ドメインが属する動物種において、アミノ酸出現頻度の多様性のあるアミノ酸部位;または
(vi) Canonical structureの形成に重要でないアミノ酸部位;
(b) 前記抗原結合ドメインにおいて、未改変体をコードする核酸及び工程(a)で特定された1または複数のアミノ酸部位にアミノ酸改変を有する、互いに配列が異なる、前記抗原結合ドメインの複数の改変体をそれぞれコードする核酸を含むライブラリを設計する工程、
工程(b)のアミノ酸改変は、以下(1)乃至(3)の少なくとも一つ以上を満たす:
(1) 当該アミノ酸改変を有する抗原結合ドメイン改変体がMTAに結合したときの構造とMTAに結合していないときの構造を比較する場合、当該改変後アミノ酸が位置するアミノ酸部位の構造変化率が大きい;
(2) 当該アミノ酸改変を有する抗原結合ドメイン改変体がMTAに結合したときの構造とMTAに結合していないときの構造を比較する場合、当該改変後アミノ酸が存在することにより前記抗原結合ドメイン改変体の構造変化が阻害されない;
(3) 当該アミノ酸改変を有する抗原結合ドメイン改変体が、前記抗原結合ドメイン未改変体と比べて、MTAに対する結合活性が著しく減弱されていない;
を含むライブラリの製造方法が提供される。
以下に例示するライブラリの製造方法における各特定事項は、上記で詳述したMライブラリの製造方法と同様な技術的意義を有し、当業者は、「MTA」を「低分子化合物」と読み替えることにより様々な特定事項の意味を理解できる。
(a) 低分子化合物に対する結合活性を有する抗原結合ドメインにおいて、以下(i)乃至(ii)の少なくとも一つを満たすアミノ酸部位を特定する工程:
(i) 前記抗原結合ドメインの表面に露出するアミノ酸部位;
(ii) 前記抗原結合ドメインが前記低分子化合物に結合したときの構造と前記低分子化合物に結合していない時の構造を比較するときに構造変化率が大きい領域に位置するアミノ酸部位;
(b) 前記抗原結合ドメインにおいて、未改変体をコードする核酸及び工程(a)で特定された1または複数のアミノ酸部位にアミノ酸改変を有する、互いに配列が異なる、前記抗原結合ドメインの複数の改変体をそれぞれコードする核酸を含むライブラリを設計する工程、
を含むライブラリの製造方法が提供される。
(a) 低分子化合物に対する結合活性を有する抗原結合ドメインにおいて、以下(i)乃至(ii)の少なくとも一つを満たすアミノ酸部位を特定する工程:
(i) 前記抗原結合ドメインの表面に露出するアミノ酸部位;
(ii) 前記抗原結合ドメインが前記低分子化合物に結合したときの構造と前記低分子化合物に結合していない時の構造を比較するときに構造変化率が大きい領域に位置するアミノ酸部位;
(b) 前記抗原結合ドメインにおいて、未改変体をコードする核酸及び工程(a)で特定された1または複数のアミノ酸部位にアミノ酸改変を有する、互いに配列が異なる、前記抗原結合ドメインの複数の改変体をそれぞれコードする核酸を含むライブラリを設計する工程、
工程(b)のアミノ酸改変は、以下(1)乃至(3)の少なくとも一つ以上を満たす:
(1) 当該アミノ酸改変を有する抗原結合ドメイン改変体が前記低分子化合物に結合したときの構造と前記低分子化合物に結合していないときの構造を比較する場合、当該改変後アミノ酸が位置するアミノ酸部位の構造変化率が大きい;
(2) 当該アミノ酸改変を有する抗原結合ドメイン改変体が前記低分子化合物に結合したときの構造と前記低分子化合物に結合していないときの構造を比較する場合、当該改変後アミノ酸が存在することにより前記抗原結合ドメイン改変体の構造変化が阻害されない;
(3) 当該アミノ酸改変を有する抗原結合ドメイン改変体が、前記抗原結合ドメイン未改変体と比べて、前記低分子化合物に対する結合活性が著しく減弱されていない;
を含むライブラリの製造方法が提供される。
(a) 低分子化合物に対して相互作用する抗原結合ドメインにおいて、以下(i)乃至(iv)の少なくとも一つを満たすアミノ酸部位を特定する工程:
(i) 前記抗原結合ドメインの表面に露出するアミノ酸部位;
(ii) 前記抗原結合ドメインが前記低分子化合物に結合したときの構造と前記低分子化合物に結合していない時の構造を比較するときに構造変化率が大きい領域に位置するアミノ酸部位;
(iii) 前記低分子化合物との結合に関与しないアミノ酸部位;
(iv) 前記低分子化合物との結合を著しく減弱させないアミノ酸部位;
(v) 前記抗原結合ドメインが属する動物種において、アミノ酸出現頻度の多様性のあるアミノ酸部位;または
(vi) Canonical structureの形成に重要でないアミノ酸部位;
(b) 前記抗原結合ドメインにおいて、未改変体をコードする核酸及び工程(a)で特定された1または複数のアミノ酸部位に以下の(1)乃至(2)の少なくとも一つを満たすアミノ酸改変を有する、互いに配列が異なる、前記抗原結合ドメインの複数の改変体をそれぞれコードする核酸を含むライブラリを設計する工程:
(1) 当該アミノ酸改変を有する抗原結合ドメイン改変体が前記低分子化合物に結合したときの構造と前記低分子化合物に結合していないときの構造を比較する場合、当該改変後アミノ酸が位置するアミノ酸部位の構造変化率が大きい;
(2) 当該アミノ酸改変を有する抗原結合ドメイン改変体が前記低分子化合物に結合したときの構造と前記低分子化合物に結合していないときの構造を比較する場合、当該改変後アミノ酸が存在することにより前記抗原結合ドメイン改変体の構造変化が阻害されない;
を含むライブラリの製造方法が提供される。
本開示はまた、MTAに特異的に結合する抗原結合分子に関する。MTAに特異的に結合する抗原結合分子の非限定な一例として、S-(5'-Adenosyl)-L-homocysteine (SAH)、SAM、AMP、ADP、ATPから選ばれる一つまたは複数の低分子化合物に実質的に結合しない抗原結合分子が例示される。
ここで、実質的に結合しないとは本明細書結合活性の項で記載される方法に準じて決定され、前記MTA以外の低分子化合物に対し、前記MTAに対する結合活性の85%以下、通常50%以下、好ましくは30%以下、特に好ましくは20%以下の結合活性を示すことをいう。
別の非限定的な一態様において、本開示のMTAに特異的に結合する抗原結合分子は、S-(5'-Adenosyl)-L-homocysteine (SAH)に実質的に結合しない。
別の非限定的な一態様において、本開示のMTAに特異的に結合する抗原結合分子は、SAMに実質的に結合しない。
別の非限定的な一態様において、本開示のMTAに特異的に結合する抗原結合分子は、アデノシン、AMP、ADP、ATPのいずれにも実質的に結合しない。
別の非限定的な一態様において、本開示のMTAに特異的に結合する抗原結合分子は、アデノシン、S-(5'-Adenosyl)-L-homocysteine (SAH)のいずれにも実質的に結合しない。
別の非限定的な一態様において、本開示のMTAに特異的に結合する抗原結合分子は、アデノシン、S-(5'-Adenosyl)-L-homocysteine (SAH)、SAMのいずれにも実質的に結合しない。
別の非限定的な一態様において、本開示のMTAに特異的に結合する抗原結合分子は、アデノシン、S-(5'-Adenosyl)-L-homocysteine (SAH)、SAM、AMP、ADP、ATPのいずれにも実質的に結合しない。
a) 配列番号:46で示す重鎖可変領域と配列番号:47で示す軽鎖可変領域を含む抗体可変領域;
b) 配列番号:50で示す重鎖可変領域と配列番号:51で示す軽鎖可変領域を含む抗体可変領域;
c) 配列番号:48で示す重鎖可変領域と配列番号:49で示す軽鎖可変領域を含む抗体可変領域;
d) 配列番号:52で示す重鎖可変領域と配列番号:53で示す軽鎖可変領域を含む抗体可変領域をのいずれか一つ含む抗原結合分子が挙げられる。
特定の態様において、本明細書で提供されるMTAに特異的に結合する抗原結合分子のいずれも、生物学的サンプルにおけるMTAの存在を検出するのに有用である。本明細書で用いられる用語「検出」は、定量的または定性的な検出を包含する。特定の態様において、生物学的サンプルは、細胞または組織、例えば、がん組織を含む。
被験体を選択するための使用の非限定な一態様として、MTAが蓄積しているがんであるか否かの判断が例示される。本開示において、MTAががん組織にて蓄積されていることが検証されたことにより、組織中または/および末梢中のMTAを検出することによりそれらのがんに罹患しているかどうかの診断が可能である。
また治療効果を予測するための使用の非限定な一態様として、組織中または/および抹消中のMTAを検出することにより、がん組織の縮小や増悪を間接的に診断し得る。
実験に使用する細胞株として、ATCCからHCC827, HPAC, HT-1376, NCI-H2228, SK-LU-1, SK-MES-1, U-87 MGを、DainipponからMia-PaCa2を、NCIからKM12を、JCRBからKM12-Lucを、RIKENからPK-1を入手した。KM12-Luc以外の細胞株について、Barretina JらNature. (2012)483:603-7.が公開した細胞株のSNPsアレイデータセットを参照して、MTAP欠損状態を判定した。KM12-Lucはこのデータセットに含まれていないが、KM12の派生株であることから、MTAP欠損状態はKM12と同じであるとみなした。
MTAP欠損細胞のMia-PaCa2, NCI-H2228, SK-LU-1, U-87 MG、およびMTAP非欠損細胞のHCC827, HPAC, KM12-Lucを75cm2 bottleに106個撒き、48時間培養した。細胞をTrypsinで剥がして回収し、回収された細胞にH2Oを加え、Sonicationによる細胞破砕を実施して細胞破砕液を得た。細胞破砕液に、細胞破砕液の3倍量のMeOHを加えてVortexし、更に遠心でDebrisを除去し、遠心後上清中のMTA濃度をLC-MS(TSQ vantage, ThermoFisher)を用いて測定した。Reinoso RF et al., Drug Metab Dispos. 2001 Apr;29(4 Pt 1):453-9.の論文報告を参照し、細胞体積を106細胞あたり4.0uLと仮定し、遠心後上清中のMTA濃度から細胞内MTA濃度を算出した。図1で示すように、MTAP非欠損細胞に比べ、MTAP欠損細胞のいずれも高い細胞内MTA濃度を有することが分かった。
MTAP欠損細胞のMia-PaCa2, NCI-H2228, SK-LU-1, U-87 MGおよびMTAP非欠損細胞のHCC827, KM12-Lucを75cm2 bottleに106個撒き、培地を14mL加え培養した。24, 48時間の各タイムポイントで培養液を回収し、回収された培養液に3倍量のMeOHを加え、遠心してDebrisを除去したのちに上清を取得し、取得された培養液上清中のMTA濃度をLC-MS(LTQ VelosおよびTSQ vantage, ThermoFisher)で測定した。その結果、MTAP欠損細胞の培養液中ではMTA濃度の経時的上昇(MTAの蓄積)が観察された。一方、MTAP非欠損細胞のHCC827の培養液中では、いずれのタイムポイントにおいてもMTAは検出限界の5nMを下回り、MTAP非欠損細胞のKM12-Lucの培養液中のMTA濃度も、5nMをやや上回る程度であった(図2)。
MTAP欠損細胞の培養液中のMTA濃度が経時的に増加することから、細胞内から細胞外へのMTA移行経路があることが推測される。しかし、MTAP非欠損細胞では、細胞内に~1uMのMTAがあると予想される(図1)にも関わらず、培養液中のMTA濃度が非常に低かった(図2)。MTAP非欠損細胞培養液中のMTA蓄積が見られない理由に関する手がかりを得るため、MTAP非欠損細胞のHT-1376、SK-MES-1を6-wells plateに3 x 105個撒き、培地を3mL加え、24hrインキュベーションして細胞を接着させた。その後、MTA濃度が100nMになるようにMTA溶液を培養液に加え、所定の時間培養した(MTA: Sigma, Catalog No. D5011-100MG)。0, 4, 24, 48, 72時間の各タイムポイントで培養液を回収し、回収した培養液中のMTA濃度をLC-MSで測定したところ、培養開始後に培養液中のMTA濃度が経時的に減少することが観察された(図3)。細胞がMTAPを使ってMTAを代謝できる場合、細胞外のMTAが細胞に吸収され、速やかに消失することが示唆された。
MTA添加培地でMTAP非欠損細胞を培養するとき、培養液中MTAが速やかに消失したことを受け、正常組織でもMTAが細胞に吸収され速やかに消失するかを検討した。
マウスから新鮮血液を採取した。予め37℃で加温しておいたマウス血液に終濃度5 ng/mLになるようにMTAの安定同位体(SIL-MTA)を添加し、5秒後に等量のアセトニトリルを添加した。アセトニトリルで除タンパクした血液試料にメタノールならびに内標準物質を添加し、遠心濾過後の濾液をLC-MS/MSで分析し、SIL-MTA添加5秒後のマウス血液中SIL-MTA濃度を測定した。マウス血液とアセトニトリルを等量混合した溶液に終濃度5 ng/mLとなるようにSIL-MTAを添加したサンプルを用いて測定したSIL-MTA濃度をSIL-MTA濃度の初期値とした。SIL-MTA濃度の初期値とSIL-MTA添加5秒後のマウス血液中SIL-MTA濃度から、血液からのSIL-MTA消失速度定数を算出し、消失速度定数にマウス単位体重当たりの血液量(85 mL/kg)を乗じて算出した全血液クリアランスは46685 mL/h/kgと推定された。この結果から、マウス血液中に添加されたMTAは、血液から速やかに消失することが分かった。
実施例(1-4)の検討から、in vitroではMTA血液クリアランスが大きいことが示唆されたため、実際にin vivoでもMTAのクリアランスが大きいかを検討するためにMTAの薬物動態試験を実施した。内因性MTAと区別するために被験物質にSIL-MTAを用いた。NOD-scidマウスにSIL-MTAを0.1~100 μg/min/kg、25 mL/kg(n=3)で定速静脈内投与して、投与開始後2, 5, 10, 30分に血液を採取した。血液採取後、12000rpm、5分間、4℃で遠心して細胞を除去し、血漿を得た。血漿中SIL-MTA濃度はLC-MS/MSで測定した。投与開始後30分の血漿中SIL-MTA濃度とSIL-MTAの投与速度から算出されたSIL-MTA全身クリアランスは38961 mL/h/kg以上であり、in vivoにおいてもMTAは速やかに血漿から消失することが明らかとなった。
MTAP欠損細胞のMia-PaCa2とMTAP非欠損細胞のPK-1をNOD SCIDマウスの皮下に移植して担癌マウスを作製し、腫瘍体積が188~347mm3の時点で腫瘍を採取した(n=3)。腫瘍重量の3倍量のメタノールを添加してステンレスビーズを用いてホモジェナイズし、12000rpm、10分間遠心分離して上清を得た。得られた上清を75%メタノールで10倍希釈し、内標準物質を含む水溶液を添加して10000rpm、10分間遠心分離した。上清をフィルターで濾過し、濾液をLC-MS/MS分析してMTA濃度を測定し、濾液中のMTA量と腫瘍重量から腫瘍中のMTA濃度(pmol/g tissue)を計算した。その結果、MTAP欠損細胞のMia-PaCa2を移植したNOD SCIDマウスにおいて高い腫瘍中MTA濃度が検出された(図4)。
Asterand社およびILS社から購入した膀胱がん8例と、食道がん10例のFresh frozen臨床サンプルにおいてMTAP 欠損に伴うMTA蓄積が見られるかを調べた。
臨床サンプルからQIAamp Fast DNA Tissue Kit [QIAGEN, cat.no. 51404] を用いてDNAを抽出した。抽出されたDNAを鋳型にして、RealTime-PCR法でMTAPの遺伝子領域の増幅を行って、MTAP遺伝子のCt値を求めた。Ct値は増幅DNA量が閾値に達するまでのPCRサイクル数であり、初期DNA量が少ないと大きい値となる。実験間の増幅効率の差を補正するため、M’soka TJら(Leukemia (2000) 14, 935-940)に倣い、別染色体上にあるMTAP偽遺伝子のΨX4のCt値も求めた。各サンプルについて、MTAP遺伝子のCt値からΨX4遺伝子のCt値を引いてΔCtを求めた。
臨床サンプル重量の3倍量のメタノールを添加してステンレスビーズを用いてホモジェナイズし、12000rpm、10分間遠心分離して上清を得た。得られた上清を75%メタノールで10倍希釈し、内標準物質を含む水溶液を添加して10000rpm、10分間遠心分離した。上清をフィルターで濾過し、濾液をLC-MS/MS分析してMTA濃度を測定し、濾液中のMTA量と臨床サンプル重量から各サンプルの組織中MTA濃度(pmol/g tissue)を計算した。検出限界(30 pmol/g tissue)を下回ったサンプルに関しては、検出下限の値を測定値とした。
ΔCt値を横軸に、組織中のMTA量を縦軸に作図し、MTAP DNA量とMTA濃度の相関性を分析した(図5)。膀胱がん臨床サンプルと食道がん臨床サンプルのいずれにおいても、ΔCtが大きくなる、すなわち組織中MTAP DNA量が少なくなるにつれ、MTA濃度が大きくなることが観察された。
MTAP欠損細胞のMia-PaCa2とMTAP非欠損細胞のKM12をBALB/c nu/nuマウスの皮下に移植し、担癌マウス(以下、Mia-PaCa2モデル、KM12モデル)を作成した。移植した腫瘍体積が200mm3以上になった時点でイソフルラン麻酔下、マイクロダイアリスプローブを腫瘍および肝臓(対照としての正常組織)に挿入し、組織間質液を採取した。プローブ挿入後90-120分に採取された組織間質液中のMTA濃度をLC-MS/MS法で定量した。BSA溶液(0, 1, 10,100mg/mL)にMTAを既知濃度添加した標準溶液を作製し、マイクロダイリシスのプローブから回収されたMTA濃度と標準溶液のMTA濃度の比から、MTA回収率を算出した。採取された組織間質液中MTA濃度に対して、MTA回収率(16.3%)で補正し、組織中の細胞外MTA濃度が算出された。
腫瘍中細胞外MTA濃度については、Mia-PaCa2モデルの方がKM12モデルより高く、MTAP欠損細胞からMTAが間質液に排出されていることが示唆された(図6)。一方、肝臓中細胞外MTA濃度については、両担癌マウスモデル間では差が見られなかった。以上結果から、MTAP欠損細胞からMTAが排出されているが、MTAP欠損細胞由来のMTAは速やかに体内から消失するため正常組織中の細胞外MTA濃度は低く保たれていると推察された。
ナイーブライブラリもしくは合成ライブラリからのMTA依存的に抗原に結合する抗体の取得
(2-1)MTA依存的に抗原に結合する抗体を取得するためのパニング
ヒトのナイーブ抗体レパートリーを模したライブラリから、MTA存在下でヒトIL-6レセプター(hIL-6R)に対して結合活性を示す抗体がスクリーニングされた。
ヒトPBMCから調製したポリA RNAや、市販されているヒトポリA RNAなどを鋳型として、当業者に公知な方法に従い、互いに異なるヒト抗体配列のFabドメインを提示する複数のファージからなるナイーブヒト抗体ファージディスプレイライブラリ(ナイーブライブラリと呼称する)が構築された。
またヒトのナイーブ抗体レパートリーを参考に人為的に設計したデザインをもとに、当業者に公知な方法に従い、互いに異なるヒト抗体配列のFabドメインを提示する複数のファージからなる合成ヒト抗体ファージディスプレイライブラリ(合成ライブラリと呼称する)が構築された。
具体的には、構築されたファージミドベクターを保持する大腸菌に対して、M13KO7TC(WO2015046554A1)もしくはM13KO7ΔpIII(ハイパーファージと呼称される)(PROGEN Biotechnik)を感染させ、30℃で一晩培養した上清からファージが回収された。ファージ産生が行われた大腸菌の培養液に2.5M NaCl/10%PEGを添加することによって沈殿させたファージの集団を、TBSにて希釈することによって抗体提示ファージライブラリ液が調製された。
パニングで得られた大腸菌のシングルコロニーらから、それぞれ常法(Methods mol. Biol. (2002) 178, 133-145)に倣い、ファージ含有培養上清が回収された。ヘルパーファージとしてハイパーファージを用い、抗体多価提示ファージが回収された。NucleoFast96(MACHERY-NAGEL)を用いて、回収されたファージ培養上清が限外濾過された。
TBSまたは終濃度100 μMのMTAを含むTBSに希釈されたファージが以下の手順でELISAに供された。384 Well Microplates Streptavidin-coated(greiner)に、ビオチン標識hIL-6Rを含むTBSが10 μl添加され1時間以上静置された。当該プレートの各ウェルをTBSTで洗浄した後、各ウェルは80uLの0.2%スキムミルク-TBSで1時間以上ブロッキングされた。各ウェルをTBSTで洗浄した後、当該ウェルに調製されたファージが加えられ一時間静置することで、ファージに提示する抗体をMTA非存在下もしくは存在下においてビオチン標識hIL-6Rに結合させた。当該ウェルをTBSTもしくは終濃度100 μMのMTAを含むTBSTで洗浄した後、当該ウェルにTBSまたは終濃度100 μMのMTAを含むTBSで希釈されたHRP結合抗M13抗体(GE Healthcare)が加えられ一時間静置された。当該ウェルをTBSTもしくは終濃度100 μMのMTAを含むTBSTで洗浄した後、TMB single溶液(ZYMED)が加えられ、一定時間後溶液の発色反応が硫酸の添加により停止された後、450nm波長の吸光度が測定された。解析の結果、評価した384クローン中、100μMのMTA存在下とMTAの非存在下でhIL-6Rに対する結合活性が変化する抗体を提示するファージが4クローン確認された。
実施例(2-2)において確認された、100μMのMTA存在下とMTAの非存在下でhIL-6Rに対する結合活性が変化する抗体の重鎖および軽鎖の可変領域配列は、重鎖抗体定常領域配列(配列番号:56)もしくは軽鎖kappa定常領域配列(配列番号:39)を有する動物発現用プラスミドへとそれぞれ挿入された。プライマー(配列番号:44および45)を用いて増幅された抗体遺伝子の塩基配列を解析したところ、一種類の抗体可変領域配列(重鎖可変領域:配列番号:54、軽鎖可変領域:配列番号:55)が同定された。参考実施例1の方法を用いて抗体(C03H- BH076N17/C03L-KT0)が発現された。
Biacore T200(GE Healthcare)を用いて、C03H- BH076N17/C03L-KT0とhIL-6Rとの抗原抗体反応におけるMTAとアデノシンの影響が評価された。ランニングバッファーとして、TBS、0.02%(w/v)Tween20、pH7.4が用いられた。センサーチップCM5(GE Healthcare)上にアミンカップリングによりProA/G(Pierce)を固定化し、その上に抗体を固相化した後、各種抗原をアナライトとして相互作用させることで、抗原抗体間の結合量の変化が観察された。抗原の希釈には、ランニングバッファーおよびランニングバッファーにMTA、またはアデノシンのいずれかがそれぞれ添加されたバッファーが使用され、数段階の濃度系列で調製された。パラメーターの算出にはBiacore T200 Evaluation Software(GE Healthcare)が用いられた。
MTAもしくはアデノシンの異なる濃度下での、C03H- BH076N17/C03L-KT0のhIL-6Rに対する結合量を図7に示した。C03H- BH076N17/C03L-KT0はMTA濃度が高いほどhIL-6Rに対して強い結合活性を示すことが確認された。またアデノシン存在下ではいかなる濃度においてもhIL-6Rへの結合は観察されなかった。したがってC03H- BH076N17/C03L-KT0はMTA特異的に依存的にhIL-6Rに結合する抗体であることが示された。
MTA依存的に抗原に結合する抗体を取得するための、ヒト化SMB0002を鋳型としたライブラリのデザイン
(3-1)ヒト化SMB0002のMTA結合性評価
MTAとアデノシンの構造の類似性から、アデノシンに結合する抗体は、MTAに交差反応する可能性があり、MTAに交差反応するアデノシン抗体は、MTA依存的に抗原に結合する抗体を取得するためのライブラリをデザインするときの鋳型抗体として使用できる可能性がある。アデノシンに結合すると報告されたヒト化SMB0002(重鎖可変領域:配列番号:31;軽鎖可変領域:配列番号:32)が、MTA依存的に抗原に結合する抗体を取得するためのライブラリをデザインするときの鋳型抗体として利用できるか検証するため、Biacore T200 (GE Healthcare)を用いて、ヒト化SMB0002のMTAに対する結合性が解析された。
測定で得られたセンサーグラムから算出されたカイネティクスパラメーターである結合速度定数 ka(1/Ms)、および解離速度定数 kd(1/s)をもとに、解離定数KD(M)が算出された。あるいは、衡状態解析法 (Steady state analysis) を用いて、解離定数KD(M)が算出された。各パラメーターの算出には Biacore T200 Evaluation Software(GE Healthcare)が用いられた。
この測定によって、ヒト化SMB0002のMTAおよびアデノシンに対する結合活性が表1のように決定され、ヒト化SMB0002はアデノシンだけでなくMTAに対しても結合活性を有すると確認された。
ヒト化SMB0002のFab断片(SMB0002hFab)単独、およびSMB0002hFabとアデノシンの複合体の結晶構造が解析された。
結晶化用ヒト化SMB0002全長抗体の調製及び精製は当業者公知の方法により行われた。
SMB0002hFabは、ヒト化SMB0002全長抗体をEndoproteinase Lys-C(Roche、カタログ番号11047825001)による制限消化し、続いて、Fc断片を除去するためのプロテインAカラム(MabSlect SuRe、GE Healthcare)、カチオン交換カラム(HiTrap SP HP、GE Healthcare)、およびゲル濾過カラム(Superdex200 16/60、GE Healthcare)へのローディングを用いるという、従来の方法により調製された。Fab断片を含む画分はプールされ、-80℃で保存された。
結晶化は、当業者公知の方法で精製され、約13mg/mLまで濃縮されたSMB0002hFabを用いて、シッティングドロップ蒸気拡散法により5℃で行われた。リザーバー溶液は、0.1 M リン酸水素二ナトリウム・クエン酸 pH 4.2、40 %w/v ポリエチレングリコール200から成るものであった。
得られた結晶は、液体窒素で凍結され、高エネルギー加速器研究機構の放射光施設フォトンファクトリーのBL-17AでX線回折データが測定された。測定中、結晶は常に-178℃の窒素流下に置おくことで凍結状態が維持された。X線回折画像は、ビームラインに接続されたPilatus 6M検出器(DECTRIS)を用いて、結晶を1回に0.25°回転させながら、合計720枚が収集された。得られた回折画像は、Xia2 (J. Appl. Cryst. (2010). 43, 186-190)を用いて処理され、分解能2.24 Åまでの回折強度データが取得された。結晶学的統計値が表2に示される。
得られたX線回折強度データを用いて、既知のFabの結晶構造をサーチモデルとして、Phaser(J. Appl. Cryst. (2007) 40, 658-674)を用いた分子置換法を実施し、初期構造が決定された。その後、Coot(Acta Cryst. D66: 486-501 (2010))とRefmac5(Acta Cryst. D67: 355-467 (2011))によるモデル構築と精密化が繰り返され、最終的な精密化座標が得られた。結晶学的統計値は、表2に示される。
当業者公知の方法で精製されたSMB0002hFabは、尿素により変性された後、透析法によってリフォールディングされ、続いて、ゲル濾過クロマトグラフィー(Superdex200 10/300 increase、GE Healthcare)により精製された。結晶化は、約13mg/mLまで濃縮されたSMB0002hFabを用いて、シッティングドロップ蒸気拡散法により20℃で行われた。リザーバー溶液は、0.1 M Morpheus buffer 2 pH 7.5、37.5% w/v M1K3350、0.1M Morpheus Carboxylic acids(Morpheus、Molecular Dimensions)から成るものであった。
得られた結晶は、液体窒素で凍結され、高エネルギー加速器研究機構の放射光施設フォトンファクトリーのBL-17AでX線回折データが測定された。測定中、結晶は常に-178℃の窒素流下に置おくことで凍結状態が維持された。X線回折画像は、ビームラインに接続されたPilatus 6M検出器(DECTRIS)を用いて、結晶を1回に0.25°回転させながら、合計4320枚が収集された。得られた回折画像は、autoPROC(Acta Cryst. D67: 293-302 (2011))を用いて処理され、分解能1.83 Åまでの回折強度データが取得された。結晶学的統計値が表2に示される。
得られたX線回折強度データを用いて、既知のFabの結晶構造をサーチモデルとして、Phaser(J. Appl. Cryst. (2007) 40, 658-674)を用いた分子置換法により初期構造が決定された。その後、Coot(Acta Cryst. D66: 486-501 (2010))とRefmac5(Acta Cryst. D67: 355-467 (2011))によるモデル構築と精密化が繰り返され、最終的な精密化座標が得られた。結晶学的統計値は、表2に示される。
SMB0002hFabとアデノシンの複合体(SMB0002hFab-アデノシン複合体)の結晶構造の非対称単位は、2つのSMB0002hFabとアデノシンの複合体を含んでいた。両者の構造は良好に重ね合わせることができる。以下で説明する図8は、一方の分子のみを用いて作成された。
SMB0002hFab-アデノシン複合体の結晶構造より、アデノシンは、主に当該抗体Fab断片の重鎖と軽鎖の間に形成されるポケットに、アデニン環部分がポケットの奥に向かう形で結合することが明らかになった。
図8に示すように、アデノシンのアデニン環部分は、ヒト化SMB0002の軽鎖S91、N96及び重鎖A33、I50、Y100の各側鎖ならびに、重鎖T100a、G99の各主鎖により認識される。特に、アデニン環の1位Nと抗体軽鎖N96の側鎖の間および、アデニン環の6位のNH2と抗体軽鎖N96およびS91の側鎖、抗体重鎖T100aの主鎖のカルボニル酸素の間、並びにアデニン環の7位Nと抗体重鎖T100aの主鎖のアミドNHの間には水素結合が形成されている。また、アデニン環の8位CHと抗体重鎖G99の主鎖のカルボニル酸素の間には、弱い水素結合が形成されている。さらに、アデニン環と抗体重鎖A33、I50、Y100の各側鎖の間には、CH-πまたはπ-πなどといったアデニン環部分のパイ電子を利用した相互作用が形成されている。また、リボース部分の3’位のOは、抗体重鎖D54、S56の各側鎖と水素結合を形成している。さらにこれらの相互作用に加えて、アデノシンは、抗体重鎖T57、G52、W58、N100b、F100d、抗体軽鎖Y95cにより取り囲まれており、ファンデルワールス相互作用が形成されている。これらの相互作用によって、アデノシンはヒト化SMB0002に認識されていることが推察される。なお、Fabのアミノ酸の残基番号付けは、Kabat番号付けスキームに基づく。
SMB0002hFabの結晶構造の非対称単位は、2つのSMB0002hFab分子(分子1、分子2)を含んでいた。図9は、分子1(SMB0002hFab_1)と分子2(SMB0002hFab_2)から可変領域を抽出した重ね合わせを示す図9で示されるように、両者の構造は、重鎖CDR1の構造と重鎖と軽鎖の間のねじれ角が異なっていることが示された。
SMB0002hFab-アデノシン複合体の結晶構造と、SMB0002hFab_1の重ね合わせを示す図10から、両者の構造は良好に重ね合わせることができることが明らかになり、SMB0002hFab_1は、アデノシン結合時と同様な構造を取っているのではないかと推察される。一方で、SMB0002hFab_2の構造は、アデノシンが結合した複合体の構造とは異なっており、アデノシンが結合していない時の構造であることが推察される。
図11は、SMB0002hFab-アデノシン複合体の結晶構造とSMB0002hFab_2の結晶構造の重ね合わせを示す図である。ヒト化SMB0002の構造は、アデノシンの結合によって、SMB0002hFab-アデノシン複合体のような1つの構造に固定される可能性が示唆される。具体的には重鎖CDR1の構造及び、重鎖と軽鎖の間のねじれ角がアデノシンの結合により変化する。
つまり、アデノシン依存的に抗原に結合する抗体中では、抗原は、アデノシンにより固定化された構造を取っている抗体に結合することができる一方で、アデノシン非存在下では、抗原は抗体に結合しにくいということが想定される。従って、アデノシンの結合に伴い構造変化が生じる領域の利用はアデノシン依存的な抗原結合能の発揮に有効であると期待される。アデノシンの結合により固定される抗体の抗原結合界面を利用することが、アデノシン依存的な抗原結合能の発揮に重要であると考えられる。
以上のヒト化SMB0002の結晶構造解析の結果より、アデノシンの結合に大きく関与していないアミノ酸部位、もしくは抗原とのアデノシン依存的な結合に関与しやすいと想定されるアミノ酸部位(抗体蛋白の表面に露出しているアミノ酸残基が位置するアミノ酸部位、もしくはアデノシンが結合したときに構造変化する抗体領域に位置するアミノ酸部位)が選抜された。
結晶構造解析の結果から、ヒト化SMB0002中の、ヒト化SMB0002のアデノシンもしくはMTAへの結合に大きく関与していないアミノ酸部位、もしくは抗原とのアデノシン依存的結合もしくは抗原とのMTA依存的結合に関与しやすいと想定されるアミノ部位が推定された。これらの部位のアミノ酸をヒト化SMB0002と異なるアミノ酸に改変しても、MTAもしくはアデノシンとの相互作用を保持する可能性が高いと考えられるため、ライブラリ設計のための多様化可能なアミノ酸部位となると考えられた。多様化可能なアミノ酸部位において、配置しても抗体とアデノシンもしくはMTAと相互作用に影響しないアミノ酸の種類を同定するため、ヒト化SMB0002のこれらの多様化可能なアミノ酸部位のアミノ酸を一つ改変した、ヒト化SMB0002一置換改変体が網羅的に作製された。
重鎖のうちアデノシンとの相互作用に関する考察に基づいた多様化可能なアミノ酸部位(表中、「Kabat」と記載されるKabatナンバリングで表される部位)ならびに当該部位における改変前のアミノ酸(表中、「天然配列」と記載される、ヒト化SMB0002の当該部位に出現するアミノ酸)および改変後のアミノ酸(表中、「改変アミノ酸」と記載されるアミノ酸)は表3に示した。
センサーチップ上にキャプチャーされた抗体に対して、アデノシン希釈液/MTA希釈液とブランクであるランニングバッファーが添加され、アデノシン/MTAと抗体の結合が観察された。その後ランニングバッファーが流され、アデノシン/MTAの抗体からの解離が観察された。各パラメーターの算出にはBiacore T200 Evaluation Software(GE Healthcare)が用いられた。
ライブラリの設計にあたり、一置換改変体の網羅的評価で得られた情報をもとに、以下の条件のうち少なくとも一つを満たすアミノ酸が多様化に使用可能なアミノ酸として選定された。
条件1)MTAあるいはアデノシンに対する結合に大きく関与しないアミノ酸;
条件2)アデノシン結合時と非結合時でヒト化SMB0002の構造変化率が大きいと予想されるアミノ酸。
選定された多様化可能なアミノ酸のうち、少なくともいずれか一つ以上のアミノ酸が出現するライブラリを設計することによって、MTAもしくはアデノシン依存的に抗原に結合する抗体を取得するためのライブラリ(以下、S02ライブラリ)が構築された。S02ライブラリの重鎖におけるアミノ酸多様化されたアミノ酸部位、ならびに当該部位におけるアミノ酸レパートリーは表11に示した。S02ライブラリの軽鎖におけるアミノ酸多様化されたアミノ酸部位、ならびに当該部位におけるアミノ酸レパートリーは表12に示した。表中、「Kabat」と記載されるKabatナンバリングで表される部位はアミノ酸多様化されたアミノ酸部位を、「天然配列」と記載されるアミノ酸は当該部位における未改変体ヒト化SMB0002のアミノ酸を、「ライブラリ化可能アミノ酸」と記載されるアミノ酸は当該部位におけるアミノ酸レパートリーを、それぞれ示す。重鎖に含まれる各多様化可能なアミノ酸部位において、選出されたアミノ酸レパートリーに含まれるアミノ酸のうち、少なくともいずれか一つが出現するライブラリが設計された。また、軽鎖に含まれる各多様化可能なアミノ酸部位において、選出されたアミノ酸レパートリーに含まれるアミノ酸のうち、少なくともいずれか一つが出現するライブラリが設計された。
MTA依存的に抗原に結合する抗体を取得するためのライブラリの構築及び当該ライブラリMTA依存的に抗原に結合する抗体の取得
(4-1-1)重鎖もしくは軽鎖可変領域ファージディスプレイライブラリの構築
設計されたS02ライブラリ中の重鎖可変領域部分はTRIM技術(Tiller T et al. MAbs 2013)を利用して遺伝子合成され、ヒト化SMB0002の軽鎖可変領域配列(配列番号:32)と組み合わせヒトIgG由来CH1配列およびヒトIgG由来軽鎖定常領域配列を有する適切なファージミドベクターに導入された。このファージミドベクターをエレクトロポレーションにより大腸菌へと導入することで、MTAもしくはアデノシン依存的に抗原に結合する抗体を取得するための重鎖可変領域ファージディスプレイライブラリが構築された。
設計されたS02ライブラリ中の軽鎖可変領域部分はTRIM技術(Tiller T et al. MAbs 2013)を利用して遺伝子合成され、ヒト化SMB0002の重鎖可変領域配列(配列番号:64)と組み合わせヒトIgG由来CH1配列およびヒトIgG由来軽鎖定常領域配列を有する適切なファージミドベクターに導入された。このファージミドベクターをエレクトロポレーションにより大腸菌へと導入することで、MTAもしくはアデノシン依存的に抗原に結合する抗体を取得するための軽鎖可変領域ファージディスプレイライブラリが構築された。
実施例(4-1-1)で構築された重鎖可変領域ファージディスプレイライブラリ、軽鎖可変領域ファージディスプレイライブラリのそれぞれから、MTAに結合する抗体群を濃縮するために、ビオチン化標識MTA(Biotin-2’-MTA)を用いたパニングが実施された。
具体的には、構築された重鎖可変領域ファージディスプレイライブラリまたは軽鎖可変領域ファージディスプレイライブラリのファージミドベクターを保持する大腸菌に対して、M13KO7ΔpIII(ハイパーファージと呼称される)(PROGEN Biotechnik)を感染させ、25℃で一晩培養した上清からファージが回収された。ファージ産生が行われた大腸菌の培養液に2.5M NaCl/10%PEGを添加することによって沈殿させたファージの集団をTBSにて希釈することによって抗体多価提示ファージライブラリ液が調製された。
実施例(4-1-2)で濃縮されたMTAに結合する抗体群中の抗体を提示するファージを感染させた大腸菌のシングルコロニーから、常法(Methods mol. Biol. (2002) 178, 133-145)に倣い、ファージ含有培養上清が回収された。ヘルパーファージとしてハイパーファージを用い、抗体多価提示ファージが回収され、ELISAに供された。384 Well Microplates Streptavidin-coated(greiner)に、Biotin-2’-MTAを含むTBSが10 μL添加され、1時間以上静置された。当該プレートの各ウェルをTBSTで洗浄した後、各ウェルは80μLの0.2%スキムミルク-TBSで1時間以上ブロッキングされた。各ウェルをTBSTで洗浄した後、各ウェルに調製されたファージが加えられ一時間静置することで、ファージに提示される抗体をBiotin-2’-MTAに結合させた。各ウェルをTBSTで洗浄した後、各ウェルにTBSで希釈されたHRP結合抗M13抗体(GE Healthcare)が加えられ一時間静置された。各ウェルをTBSTで洗浄した後、TMB single溶液(ZYMED)が加えられ、一定時間後溶液の発色反応が硫酸の添加により停止された後、450nm波長の吸光度が測定された。解析の結果、Biotin-2’-MTAに結合する抗体を提示するファージが複数確認された。ファージELISAの結果を図12(重鎖可変領域ファージディスプレイライブラリから濃縮された抗体群)、図13(軽鎖可変領域ファージディスプレイライブラリから濃縮された抗体群)、表13に示した。ELISAの結果から、実施例(4-1-2)のパニングにより濃縮された抗体群中にMTA結合抗体が多数含まれていることが示された。
ファージELISAで評価されたクローンについて、プライマー(配列番号:33および34)を用いて増幅された抗体遺伝子の塩基配列が解析された。解析の結果、ファージELISAで評価された192クローンの中での抗体配列重複サンプル2クローン以下であり、実施例(4-1-2)の濃縮を経てもライブラリが高い配列多様性を保持していることが示された。
実施例(4-1-2)で濃縮されたMTA結合抗体群について、当該抗体群に含まれる改変重鎖と改変軽鎖を組み合わせることにより作製されるFab提示ファージライブラリもMTAに対する結合を維持する抗体が多数含まれることが予想され、MTA依存的に抗原に結合する抗体を取得するためのライブラリが構築できると考えられた。
実施例(4-1-2)で濃縮されたMTA結合抗体群を提示するファージが感染した大腸菌から、当業者公知の方法で抗体遺伝子が抽出された。重鎖可変領域ファージライブラリから濃縮された抗体群に対して、重鎖可変領域を増幅できるプライマー(配列番号:34, 35)を用いて重鎖可変領域遺伝子が増幅された。軽鎖可変領域ファージライブラリから濃縮された抗体群に対して、ヒト化SMB0002の重鎖可変領域配列を制限酵素処理により除去し、軽鎖可変領域ライブラリ遺伝子とヒトIgG由来軽鎖定常領域配列とヒトIgG由来CH1配列を含むファージミド断片が調製された。前記ファージミドベクター断片に重鎖可変領域ライブラリから増幅された重鎖可変領域遺伝子を挿入することで、重鎖/軽鎖可変領域ライブラリ遺伝子が導入されたファージミドベクターが構築された。このベクターをエレクトロポレーションにより大腸菌へと導入することで、ヒト抗体可変領域と定常領域からなるFabドメインを提示し、MTA依存的に抗原に結合する抗体を取得するためのライブラリ(以下、MTA濃縮S02ライブラリ)が構築された。
実施例(4-1-5)で構築されたMTA濃縮S02ライブラリから、MTA存在下でヒトIL-6レセプター(hIL-6R)、ヒトIL-6(hIL-6)、ヒトIgA(hIgA)のそれぞれに対して結合活性を示す抗体がスクリーニングされた。
具体的には、構築されたMTA濃縮S02ライブラリのファージミドベクターを保持する大腸菌に対して、M13KO7ΔpIII(ハイパーファージと呼称される)(PROGEN Biotechnik)を感染させ、25℃で一晩培養した上清からファージが回収された。ファージ産生が行われた大腸菌の培養液に2.5M NaCl/10%PEGを添加することによって沈殿させたファージの集団をTBSにて希釈することによって抗体多価提示ファージライブラリ液が調製された。
実施例(4-2)のパニングで得られた大腸菌のシングルコロニーから、常法(Methods mol. Biol. (2002) 178, 133-145)に倣い、ファージ含有培養上清が回収された。ヘルパーファージとしてハイパーファージを用い、抗体多価提示ファージが回収された。NucleoFast96(MACHERY-NAGEL)を用いて、回収されたファージ培養上清が限外濾過された。具体的には培養上清各0.2 mLがNucleoFast96の各ウェルに添加され、6000 g、40分間遠心分離を行いフロースルーが除去された。その後H2O 0.2 mLが各ウェルに添加され、6000 g、20分間遠心分離を行いフロースルーが除去された。その後TBS 0.2 mLが各ウェルに添加され、室温で5分間静置された後、抗体多価提示ファージ溶液が回収された。
ファージELISAで評価された抗体群のいくつかについて、プライマー(配列番号:33および34)を用いて増幅された抗体遺伝子の塩基配列が解析された。
抗体の重鎖可変領域と軽鎖可変領域配列はそれぞれ、重鎖抗体定常領域配列(配列番号:38)もしくは軽鎖kappa定常領域配列(配列番号:39)を有する動物発現用プラスミドへとそれぞれ挿入された。表15で示す抗体を参考実施例1の方法を用いて発現させ、精製した。
Biacore T200(GE Healthcare)を用いて、実施例(4-5)で精製製された抗体と標的抗原との抗原抗体反応におけるMTAとアデノシンの影響が評価された。ランニングバッファーとして、20 mM ACES、150 mM NaCl、0.05%(w/v)Tween20、pH7.4が用いられ、25℃で測定された。センサーチップCM4上にアミンカップリングによりProA/Gを固定化し、その上に抗体を固相化した後、各種抗原をアナライトとして相互作用させることで、抗原抗体間の結合量の変化が観察された。抗原の希釈には、ランニングバッファーおよびランニングバッファーにMTAまたはアデノシンのいずれかがそれぞれ終濃度100 μMの濃度で添加されたバッファーが使用された。また抗原は数段階の濃度系列で調製され、各抗原濃度に対するセンサーグラムからシングルサイクルカイネティクス解析により各クローンの解離定数KDが算出された。パラメーターの算出にはBiacore T200 Evaluation Software(GE Healthcare)が用いられた。100 μM MTA存在下での各クローンの解離定数KDを表16に示した。また100 μMアデノシン存在下では抗原への結合は観察されなかった。
MTA依存的に結合する抗体がMTA依存的に機能することを確認するために、MTA依存的に結合する抗体を用いてMTAの存在下および非存在下におけるT細胞の活性化能を評価した。評価には、実施例(4-5)でクローニングされたMTA依存性抗hIL-6R抗体(6RS2T007H-F760mnN17/6RS2T007L-KT0)、および抗CD3抗体(重鎖可変領域:配列番号:40、重鎖定常領域:配列番号:42、軽鎖可変領域:配列番号:41、軽鎖定常領域:配列番号:39)からなる抗hIL-6R/hCD3二重特異性抗体を用いた。
上記MTA依存性抗hIL-6R抗体および抗CD3抗体はそれぞれ参考実施例1の方法に従い調製した。取得されたMTA依存性抗IL-6R抗体および抗CD3抗体を混合し25 mM 2-MEA(2-メルカプトエチルアミン)存在下で37℃、90分間反応させることで、両抗体の重鎖および軽鎖を有し、MTA依存的にhIL-6Rに結合する抗原結合ドメインとCD3に結合する抗原結合ドメインを有する二重特異性抗体を作製した。作製した二重特異性抗体は透析によりPBSへ溶媒置換した後、分光光度計を用いて280nmでの吸光度を測定した。得られた吸光度の測定値から参考実施例1に記載のPACE法により算出された吸光係数を用いて精製抗体の濃度が算出された。抗体は10% FBSを含むRPMI1640培地(アッセイバッファー)またはMTAもしくはアデノシンを含むアッセイバッファーで希釈してT細胞活性化能の評価に用いた。
実施例(4-5)でクローニングされたMTA依存的に結合する抗hIL-6R抗体(6RS2T007H-F760mnN17/6RS2T007L-KT0)について、MTA濃度依存的な抗原結合量の変化をBiacore T200(GE Healthcare)を用いて検証した。測定はランニングバッファーとして、MTAが終濃度0.1、 1、 10、 100 μMの濃度で添加された20 mM ACES、150 mM NaCl、0.05%(w/v)Tween20、pH7.4を用いて、25℃で測定した。センサーチップとしてSeries S Sensor Chip CM4を使用し、アミンカップリングによりProA/Gを固定化し、その上に抗体を固相化した後、hIL-6Rをアナライトとして相互作用させることで、抗原抗体間の結合量の変化を測定した。抗原の希釈には、ランニングバッファーを用いた。各MTA濃度における抗体の抗原結合量変化を図29に示した。この結果からMTA依存的に結合する抗体がMTA濃度に応じて抗原への結合量が段階的に変化することが確認され、MTAの濃度依存的に結合していることが確認された。
(5-1)ウサギB細胞クローニングによる抗MTA抗体の取得
(5-1-1)抗MTA抗体取得用の免疫原のデザイン
ウサギに免疫する免疫原として6’-MTA- Keyhole Limpet Hemocyanin(6’-MTA-KLH)が用いられた。Mariculture Keyhole Limpet Hemocyanin(KLH)は、ヘルパーT細胞上に発現するT細胞受容体が認識できる抗原性の高い蛋白質であり、抗体産生を活性化することが知られているため、MTAと連結させることでMTAに対する抗体の産生を亢進させることが期待される。
また、KLHの代わりにビオチンをMTAに連結させた6’-MTA-biotinが作製された。
(2R,3R,4S,5S)-2-(6-アミノ-9H-プリン-9-イル)-5-(クロロメチル)オキソラン-3,4-ジオール
1H-NMR(400MHz,DMSO-d6,ppm) δ 8.35(s,1H),8.17(s,1H),7.30(s,2H),5.94(d,J=5.6Hz,1H),5.60 (d,J=6.0Hz,1H),5.46(d,J=5.2Hz,1H),4.76(q,J =5.6Hz,1H),4.23(q,J=4.8Hz,1H),4.14-4.06(m, 1H),3.96(dd,J=11.6,5.1Hz,1H),3.85(dd,J=11.6, 6.4Hz,1H).
LC-MS(ES,m/z):298[M+H]+
1H-NMR(400MHz,DMSO-d6,ppm) δ 8.36(s,1H),8.16(s,1H),7.28(s,2H),5.90(d,J=5.7Hz,1H),5.52 (d,J=5.7Hz,1H),5.37-5.31(m,1H),4.76(q,J=5.0 Hz,1H),4.16(q,J=3.6Hz,1H),4.04(td,J=6.3,3.6 Hz,1H),2.94-2.71(m,2H),2.06(s,3H).
LC-MS(ES,m/z):338[M+H]+
1H-NMR(300MHz,Chloroform-d,ppm) δ 8.32(s, 1H),7.91(s,1H),6.06(d,J=2.2Hz,1H),5.89(s,2H),5.49(dd,J=6.4,2.2Hz,1H),5.04(dd,J=6.4,3.2 Hz,1H),4.45-4.33(m,1H),2.75(qt,J=18.4,9.8 Hz,2H),2.08(s,3H),1.59(s,3H),1.38(s,3H).
LC-MS(ES,m/z):480[M+H]+
LC-MS(ES,m/z):412[M+H]+
1H-NMR(400MHz,DMSO-d6,ppm) δ 11.81(s,1H),8.35(s,1H),8.22(s,1H),7.82(s,1H),5.90(d,J=5.7 Hz,1H),5.49(s,1H),5.31(s,1H),4.75(t,J=5.3Hz,1H),4.16(t,J=4.3Hz,1H),4.04(ddd,J=6.9,5.8, 3.7Hz,1H),3.47(s,2H),2.94-2.74(m,2H),2.20(t, J=7.3Hz,2H),2.07(s,3H),1.56(dp,J=25.6,7.4Hz,4H),1.33(qd,J=8.4,6.0Hz,2H).
LC-MS(ES,m/z):893[M+H]+
1H-NMR(400MHz,DMSO-d6,ppm) δ 8.35(s,1H), 8.25(dd,J=13.4,7.7Hz,2H),7.89-7.78(m,3H),6.41(s,1H),6.35(s,1H),5.90(d,J=5.7Hz, 1H),5.48(d,J=6.0Hz,1H),5.31(d,J=5.0Hz, 1H),4.75(q,J=5.6Hz,1H),4.49(t,J=5.3Hz, 2H),4.29(dd,J=14.3,6.7Hz,3H),4.20-4.08(m, 2H),4.04(td,J=6.3,3.7Hz,1H),3.80(t,J=5.3Hz,2H),3.55-3.27(m,14H),3.23-3.04(m,3H), 2.94-2.74(m,3H),2.58(d,J=12.4Hz,1H),2.14-2.02(m,7H),1.53(ddtd,J=35.3,28.2,13.8,7.6Hz,8H),1.38-1.22(m,4H)
6-([9-[(2R,3R,4S,5S)-3,4-ジヒドロキシ-5-[(メチルスルファニル)メチル]オキソラン-2-イル]-9H-プリン-6-イル]アミノ)ヘキサン酸(4.94mg,0.012mmol,1等量))のDMSO (200μl)溶液に1-エチル-3-(3-ジメチルアミノプロピル)カルボジイミド塩酸塩(2.30mg,0.012mmol, 1.0等量),ヒドロキシ-2,5-ジオキソピロリジン-3-スルホン酸 ナトリウム塩(2.61mg,0.012mmol,1.0等量)を加え20℃にて2時間撹拌した。この溶液を50μl取り、KLH(10mg,ThermoFisher Scientific社,77600)のリン酸バッファー溶液(pH8.4,0.95μL)を4℃にて加え緩やかに撹拌し4℃にて24時間静置した。得られたコンジュゲートを含む溶液を、そのまま動物免疫に用いた。
実施例(5-1-2)で合成された6’-MTA-KLHを用いて、ウサギが当業者公知の方法で免疫された。免疫されたウサギの血液または脾臓から採取された細胞懸濁液から、autoMACS Pro SeparatorとFACSAria(BD)を用いた未標識アデノシン共存下でもMTA結合活性を有する細胞の候補が選抜された。次に選抜された細胞の培養上清中に分泌された抗体を用いて細胞がスクリーニングされた。具体的には、ELISA法により、6’-MTA-biotinに対する結合活性の有無、及び未標識MTA共存下における6’-MTA-biotinへの結合活性の有無が評価された。6’-MTA-biotinに結合し、未標識MTA共存下においてアデノシンの共存有無にかかわらず6’-MTA-biotinへの結合が抑制される抗体を分泌することを指標に選抜された細胞からPCR法を用いて重鎖可変領域遺伝子および軽鎖可変領域遺伝子が取得された。取得された可変領域遺伝子から、ヒトIgG1重鎖定常領域、およびヒト軽鎖定常領域と組み合わせて抗体を発現させた。
実施例(5-1-3)で取得された抗体について、プライマー(配列番号:44および45)を用いて増幅された抗体遺伝子の塩基配列が解析された。配列を以下の表17に示す。
ウサギB細胞クローニングから得られたクローンがMTA特異的に結合するか否かを検証するため、Biacore T200 (GE Healthcare)を用いて、MTAおよびその類縁体に対する結合性が解析された。
Protein Aがあらかじめ固定化されたSensor chip Protein A (GE healthcare)、またはストレプトアビジンがあらかじめ固定化されたSensor chip SA(GE Healthcare)にビオチン化された抗ヒトIgG CH1分子であるCaptureSelect Biotin Anti-IgG-Fc (Hu) (Thermo fisher scientific) を結合させた固定化表面に対し、目的の抗体をキャプチャーさせ、MTA (sigma-aldrich)またはMTA類縁体を相互作用させた。MTA類縁体として、MTAとの構造類似性及びMTAP欠損細胞株の担癌マウスの腫瘍組織内濃度から、アデノシン (Wako)(腫瘍組織内測定濃度:182 nM)およびS-(5'-Adenosyl)-L-homocysteine, (SAH) (sigma-aldrich)(腫瘍組織内測定濃度:30 nM)が選抜された。ランニングバッファーには20mM ACES-NaOH, 150mM NaCl, 0.05% Tween20, 0.05%DMSOが用いられた。MTAまたはアデノシンまたはSAHは流速30μL/minで、120秒間相互作用させ、その後ランニングバッファーにて解離させた。相互作用は25℃で測定され、MTAおよびその類縁体の希釈にはランニングバッファーと同じバッファーが使用された。
測定で得られたセンサーグラムから算出されたカイネティクスパラメーターである結合速度定数 ka(1/Ms)、および解離速度定数 kd(1/s)をもとに、解離定数KD(M)が算出された。あるいは、衡状態解析法 (Steady state analysis) を用いて、解離定数KD(M)が算出された。各パラメーターの算出には Biacore T200 Evaluation Software(GE Healthcare)が用いられた。
この測定によって、各抗体のMTAおよびその類縁体に対する結合活性が表18のように決定され、選択された抗体のいずれもMTAに対して高い選択性を有することが確認された。
MTA0303の Fab断片(MTA0303Fab)とメチルチオアデノシン(MTA)の複合体(MTA0303Fab-MTA)の結晶構造が解析された。
結晶化用MTA0303全長抗体の調製及び精製は当業者公知の方法により行われた。
MTA0303Fabは、MTA0303全長抗体をEndoproteinase Lys-C(Roche、カタログ番号11047825001)により制限消化し、続いて、Fc断片を除去するためのプロテインAカラム(MabSlect SuRe、GE Healthcare)、カチオン交換カラム(HiTrap SP HP、GE Healthcare)、およびゲル濾過カラム(Superdex75 16/60、GE Healthcare)へのローディングを用いるという、従来の方法により調製された。Fab断片を含む画分はプールされ、-80℃で保存された。
結晶化は、当業者公知の方法で精製され、約16 mg/mLまで濃縮されたMAT0303Fabに終濃度2mMになるようにMTAを混合した溶液を用いて、シーディング法と、株式会社 創晶において行われたフェムト秒レーザーの照射(J. Appl. Phys. 42: L798-L800 (2003)) を組み合わせたシッティングドロップ蒸気拡散法により5℃で行われた。リザーバー溶液は、0.1 M HEPES pH 7.5、70 % v/v (+/-)-2-Methyl-2,4-pentanediolから成るものであった。
得られた結晶は、液体窒素で凍結され、ポール・シェラー研究所の放射光施設Swiss Light Source X10SAにてX線回折データが測定された。測定中、結晶は常に-178℃の窒素流下に置おくことで凍結状態が維持された。X線回折画像は、ビームラインに接続されたPilatus 6M検出器(DECTRIS)を用いて、結晶を1回に0.25°回転させながら、合計720枚が収集された。得られた回折画像は、autoPROC(Acta Cryst. D67: 293-302 (2011))を用いて処理され、分解能1.95Åまでの回折強度データが取得された。結晶学的統計値が表19に示される。
得られたX線回折強度データを用いて、既知のFabの結晶構造をサーチモデルとして、Phaser(J. Appl. Cryst. (2007) 40, 658-674)を用いた分子置換法を実施し、初期構造が決定された。その後、Coot(Acta Cryst. D66: 486-501 (2010))とRefmac5(Acta Cryst. D67: 355-467 (2011))によるモデル構築と精密化が繰り返され、最終的な精密化座標が得られた。結晶学的統計値は、表19に示される。
図20に示すMTA0303Fab-MTA複合体の結晶構造より、MTAは、MTA0303Fabの重鎖と軽鎖の間に形成されるポケットにチオメチル基部分がポケットの奥に向かう形で結合することが明らかになった。また、図15に示されるように、MTAは、重鎖CDR2に覆いかぶさられるように、奥深くに埋もれるように結合していた。
MTA非存在下における当該抗体の構造と、MTA存在下における当該抗体の構造が異なることは、MTA依存的な抗原への結合に重要であると考えられる。つまり、蛋白質抗原は、MTAの結合に伴い構造が変化した抗体のみに結合することができる一方で、MTA非存在下では、当該抗体の構造は、MTA存在下における構造とは異なるため、MTAが存在しない状態では、蛋白質抗原は抗体に結合することができないということが想定される。従って、MTAの結合に伴い構造変化を生じる領域の利用はMTA依存的な抗原結合能の発揮に有効であると期待される。当該抗体においては、MTAの結合に伴う重鎖CDR2の構造変化が考えられるため、重鎖CDR2の利用によるMTA依存的に抗原に結合する抗体の取得が期待される。なお、Fabのアミノ酸の残基番号付けは、Kabat番号付けスキームに基づく。
MTA0330のFab断片(MTA0330Fab)とMTAの複合体(MTA0330Fab-MTA)の結晶構造が解析された。
結晶化用MTA0330全長抗体の調製及び精製は当業者公知の方法により行われた。
MTA0330Fabは、MTA0330全長抗体をEndoproteinase Lys-C(Roche、カタログ番号11047825001)により制限消化し、続いて、Fc断片を除去するためのプロテインAカラム(MabSlect SuRe、GE Healthcare)、カチオン交換カラム(HiTrap SP HP、GE Healthcare)、およびゲル濾過カラム(Superdex75 16/60、GE Healthcare)へのローディングを用いるという、従来の方法により調製された。Fab断片を含む画分はプールされ、-80℃で保存された。
結晶化は、当業者公知の方法で精製され、約13.3 mg/mLまで濃縮されたMAT0330 Fabに終濃度2mMになるようにMTAを混合した溶液を用いて、シッティングドロップ蒸気拡散法により20℃で行われた。リザーバー溶液は、30.0 %w/v P550MME_P20K、 0.1 M Morpheus buffer 1 pH 6.5、60 mM Morpheus Divalents (Morpheus、Molecular Dimensions)から成るものであった。
得られた結晶は、液体窒素で凍結され、ポール・シェラー研究所の放射光施設Swiss Light Source X10SAにてX線回折データが測定された。測定中、結晶は常に-178℃の窒素流下に置おくことで凍結状態が維持された。X線回折画像は、ビームラインに接続されたPilatus 6M検出器(DECTRIS)を用いて、結晶を1回に0.25°回転させながら、合計1440枚が収集された。得られた回折画像は、autoPROC(Acta Cryst. D67: 293-302 (2011))を用いて処理され、分解能1.46Åまでの回折強度データが取得された。結晶学的統計値が表19に示される。
得られたX線回折強度データを用いて、既知のFabの結晶構造をサーチモデルとして、Phaser(J. Appl. Cryst. (2007) 40, 658-674)を用いた分子置換法により初期構造が決定された。その後、Coot(Acta Cryst. D66: 486-501 (2010))とRefmac5(Acta Cryst. D67: 355-467 (2011))によるモデル構築と精密化が繰り返され、最終的な精密化座標が得られた。結晶学的統計値は、表19に示される。
図21に示すMTA0330Fab-MTA複合体の結晶構造より、MTAは、MTA0330Fabの重鎖と軽鎖の間に形成されるポケットにチオメチル基部分がポケットの奥に向かう形で、また、図18に示すようにMTAのアデニン環部分は当該抗体の表面から露出するように結合することが明らかになった。
図19に示すように、MTAのアデニン環部分は、当該抗体の軽鎖F95bおよび、重鎖F98の各側鎖の間で、π-π相互作用が形成されることで認識される。また、リボース部分は、2’位のOおよび3’位のOと重鎖E95の側鎖と水素結合を形成することで認識される。チオメチル基部分は、軽鎖F96の側鎖との間でCH-π相互作用が形成されている。さらにこれらの相互作用に加えて、MTAは、重鎖W34、W47、C50、Y58、G99、G100aおよび、軽鎖Y28、T91、Y95cにより取り囲まれており、ファンデルワールス相互作用が形成されている。これらの相互作用によって、MTAは当該抗体により強く認識されていることが推察される。なお、Fabのアミノ酸の残基番号付けは、Kabat番号付けスキームに基づく。
(5-5-1)NMR用MTA0303およびMTA0330全長抗体の調製
NMR用MTA0303およびMTA0330全長抗体の調製及び精製は当業者公知の方法により行われた。但し、アミノ酸の安定同位体標識を実施するため、培地中に200mg/L [d-13CH3, 15N, 2H]Isoleucine, 300mg/L [d2-13CH3, 2H, 15N]Leucine, 190mg/L [g1-13CH3, 2H, 15N]Valine, 360mg/L [b-13CH3, 2H, 15N]Alanine, 60mg/L β-chloro-L-Alanineを添加した。
MTA0303のFab断片(MTA0303Fab)およびMTA0330のFab断片(MTA0330Fab)を、Lys-C(Roche、カタログ番号11 047 825 001)による制限消化、続いて、Fc断片を除去するためのプロテインAカラム(MabSlect SuRe、GE Healthcare)を用いるという、従来の方法により調製された。Fab断片を含む画分はプールされ、5mM d-citrate, pH6.5, 20mM NaCl, 5% D2Oに置換し、0.15mM~0.3mMとなるまで濃縮した。
実施例(5-5-2)で調製した試料を用いて、AvanceIII 600 (Bruker社)でNMRスペクトルを測定した。測定温度を305Kとした。1H-15N TROSYスペクトルおよび1H-13C SOFAST-HMQCスペクトルを取得するため、それぞれtrosyetf3gpiasi、sfhmqcf2gpphパルスプログラム(Bruker社標準パルスプログラム)を用いた。スペクトルのフーリエ変換には、TopSpin (Bruker社)を使用した。
実施例(5-5-2)で調製した資料に、終濃度が0.4 mMになるようにMTAを添加し、Avance III 600でNMRスペクトルを測定した。測定温度を305Kとした。1H-15N TROSYスペクトルおよび1H-13C SOFAST-HMQCスペクトルを取得するため、それぞれtrosyetf3gpiasi、sfhmqcf2gpphパルスプログラム(Bruker社標準パルスプログラム)を用いた。スペクトルのフーリエ変換には、TopSpin (Bruker社)を使用した。
NMRスペクトル表示ソフトウエアであるSparky(UCSF)を用いて、MTA0303FabのNMRスペクトルとMTA0303Fab―MTA複合体のNMRスペクトルを重ね合わせた後、スペクトルの比較を行った。結果を図22に示す。MTA結合状態と非結合状態で化学シフトがピーク1個分以上、変化しているシグナルは17個あった。
NMRスペクトル表示ソフトウエアであるSparky(UCSF)を用いて、MTA0303FabのNMRスペクトルとMTA0303Fab-MTA複合体のNMRスペクトルを重ね合わせた後、スペクトルの比較を行った。結果を図23に示す。MTA結合状態と非結合状態で化学シフトがピーク1個分以上、変化しているシグナルは20個あった。
NMRスペクトル表示ソフトウエアであるSparky(UCSF)を用いて、MTA0330FabのNMRスペクトルとMTA0330Fab―MTA複合体のNMRスペクトルを重ね合わせた後、スペクトルの比較を行った。結果を図24に示す。MTA結合状態と非結合状態で化学シフトがピーク1個分以上、変化しているシグナルは7個あった。
NMRスペクトル表示ソフトウエアであるSparky(UCSF)を用いて、MTA0330FabのNMRスペクトルとMTA0330Fab―MTA複合体のNMRスペクトルを重ね合わせた後、スペクトルの比較を行った。結果を図25に示す。MTA結合状態と非結合状態で化学シフトがピーク1個分以上、変化しているシグナルは7個あった。
実施例5で取得した抗MTA抗体のMTA0303、MTA0330を鋳型として、MTA依存的に抗原に結合する抗体を取得するためのライブラリをデザインした。
MTA0303とMTA0330のヒト化が当業者公知の方法で実施された(欧州特許公開EP239400、国際公開WO1996/00257、WO1993/012227、WO1992/003918、WO1994/002602、WO1994/025585、WO1996/034096、WO1996/033735、WO1992/001047、WO1992/020791、WO1993/006213、WO1993/011236、WO1993/019172、WO1995/001438、WO1995/015388、Cancer Res.,(1993)53, 851-856, BBRC.,(2013)436(3):543-50等)。ヒト化抗体の配列を以下の表20に示す。
ヒト化MTA0303、ヒト化MTA0330がMTAに特異的に結合するか否かを検証するため、Biacore T200 (GE Healthcare)を用いて、MTAおよびMTA類縁体(アデノシン、SAH)に対する結合性が解析された。
Protein Aがあらかじめ固定化されたSensor chip Protein A (GE healthcare)、またはストレプトアビジンがあらかじめ固定化されたSensor chip SA(GE Healthcare)にビオチン化された抗ヒトIgG CH1分子であるCaptureSelect Biotin Anti-IgG-Fc (Hu) (Thermo fisher scientific) を結合させた固定化表面に対し、目的の抗体をキャプチャーさせ、MTA (sigma-aldrich)、またはアデノシン (Wako)、またはS-(5'-Adenosyl)-L-homocysteine (SAH) (sigma-aldrich) を相互作用させた。ランニングバッファーには20mM ACES-NaOH, 150mM NaCl, 0.05% Tween20, 0.05%DMSOが用いられた。MTAまたはアデノシンまたはSAHは流速30μL/minで、120秒間相互作用させ、その後ランニングバッファーにて解離させた。相互作用は25℃で測定され、MTAまたはアデノシンまたはSAHの希釈にはランニングバッファーと同じバッファーが使用された。
測定で得られたセンサーグラムから算出されたカイネティクスパラメーターである結合速度定数 ka(1/Ms)、および解離速度定数 kd(1/s)をもとに、解離定数KD(M)が算出された。あるいは、衡状態解析法 (Steady state analysis) を用いて、解離定数KD(M)が算出された。各パラメーターの算出には Biacore T200 Evaluation Software(GE Healthcare)が用いられた。
この測定によって、各抗体のMTAおよびMTA類縁体に対する結合活性が表21のように決定され、ヒト化抗体のいずれもMTAに対して高い選択性を有することが確認された。
実施例(5-3)のMTA0303結晶構造解析の結果から、ヒト化MTA0303中のMTAへの結合に大きく関与していないアミノ酸部位、もしくは抗原とのMTA依存的な結合に関与しやすいと想定される抗体可変領域のアミノ酸部位が推定された。これらの部位は多様化してもMTAに対する結合性を保持する可能性が高いと考えられるため、ライブラリのための多様化部位の候補となると考えられた。推定した部位の中で実際にMTAへの結合に大きく関与しない部位を同定するため、各部位のアミノ酸に対するAla/Val置換改変体が作製された。
各MTA0303重鎖改変体の、改変された部位(表中、「Kabat」と記載されるKabatナンバリングで表される部位)および当該部位における改変前のアミノ酸(表中、「天然配列」と記載されるアミノ酸)および改変後のアミノ酸(表中、「改変アミノ酸」と記載されるアミノ酸)は表22に示した。
ライブラリの設計にあたり、得られた情報をもとに、結合評価した改変体の中で、以下の条件を満たす部位を多様化可能なアミノ酸部位として選定された:
改変体の網羅的評価の結果から、MTAに対する結合に大きく関与しないアミノ酸部位。
判定された多様化可能なアミノ酸部位に、少なくともいずれか一つ以上のライブラリ化可能なアミノ酸が出現するライブラリを設計することによって、MTA依存的に抗原に結合する抗体取得用のライブラリが構築された。ライブラリ化可能なアミノ酸として全種類のアミノ酸を採用し、X線結晶構造解析の結果から、重鎖S52b、軽鎖N31についてのみ、MTAが結合した際の抗体の構造変化を抑制すると予想されるアミノ酸を除いた。
ヒト化MTA0303の重鎖における多様化可能なアミノ酸部位、ならびに当該部位におけるアミノ酸レパートリーは表24に示した。ヒト化MTA0303の軽鎖における多様化可能なアミノ酸位、ならびに当該部位におけるアミノ酸レパートリーは表25に示した。表中、「Kabat」と記載されるKabatナンバリングで表される部位は多様化可能なアミノ酸部位を、「天然配列」と記載されるアミノ酸は当該部位におけるヒト化MTA0303のアミノ酸を、「ライブラリ化可能アミノ酸」と記載されるアミノ酸)は当該部位における多様化可可能アミノ酸を、それぞれ示す。重鎖の各多様化可能アミノ酸部位において、表中のアミノ酸レパートリーに含まれるアミノ酸のうち、少なくともいずれか一つが出現するライブラリが設計された。軽鎖の各多様化可能アミノ酸部位において、表中のアミノ酸レパートリーに含まれるアミノ酸のうち、少なくともいずれか一つが出現するライブラリが構築された。
実施例(5-4)のMTA0330の結晶構造解析の結果から、ヒト化MTA0330中のMTAへの結合に大きく関与していないアミノ酸部位、もしくは抗原とのMTA依存的な結合に関与しやすいと想定される抗体可変領域のアミノ酸部位が推定された。これらの部位は多様化してもMTAに対する結合性を保持する可能性が高いと考えられるため、ライブラリのための多様化部位の候補となると考えられた。推定した部位の中で実際にMTAへの結合に大きく関与しない部位を同定するため、各部位のアミノ酸に対するAla置換改変体が作製された。
各MTA0330重鎖改変体の、改変された部位(表中、「Kabat」と記載されるKabatナンバリングで表される部位)および当該部位における改変前のアミノ酸(表中、「天然配列」と記載されるアミノ酸)および改変後のアミノ酸(表中、「改変アミノ酸」と記載されるアミノ酸)は表26に示した。
ライブラリの設計にあたり、得られた情報をもとに、結合評価した改変体の中で、以下の条件を満たす部位を多様化可能なアミノ酸部位として選定された:
改変体の網羅的評価の結果から、MTAに対する結合に大きく関与しないアミノ酸部位。
ヒト化MTA0330の重鎖における多様化可能なアミノ酸部位、ならびに当該部位におけるアミノ酸レパートリーは表28に示した。ヒト化MTA0330の軽鎖における多様化可能なアミノ酸位、ならびに当該部位におけるアミノ酸レパートリーは表29に示した。表中、「Kabat」と記載されるKabatナンバリングで表される部位は多様化可能なアミノ酸部位を、「天然配列」と記載されるアミノ酸は当該部位におけるヒト化MTA0330のアミノ酸を、「ライブラリ化可能アミノ酸」と記載されるアミノ酸)は当該部位における多様化可可能アミノ酸を、それぞれ示す。重鎖の各多様化可能アミノ酸部位において、表中のアミノ酸レパートリーに含まれるアミノ酸のうち、少なくともいずれか一つが出現するライブラリが設計された。軽鎖の各多様化可能アミノ酸部位において、表中のアミノ酸レパートリーに含まれるアミノ酸のうち、少なくともいずれか一つが出現するライブラリが構築された。
(6-7-1)ヒト化MTA0330重鎖もしくは軽鎖可変領域ファージディスプレイライブラリの構築
実施例(6-6)で構築したヒト化MTA0330を鋳型として設計した重鎖可変領域ライブラリを遺伝子合成し、合成したヒト化MTA0330の重鎖可変領域をヒト化MTA0330の軽鎖可変領域、およびヒトIgG由来重鎖CH1配列およびヒトIgG由来軽鎖定常領域配列含むファージミドベクターに導入した。同様の手法を用いてヒト化MTA0330を鋳型として設計された軽鎖可変領域ライブラリを遺伝子合成し、合成したヒト化MTA0330の軽鎖可変領域をヒト化MTA0330の重鎖可変領域、およびヒトIgG由来重鎖CH1配列およびヒトIgG由来軽鎖定常領域配列を含むファージミドベクターに導入した。作成した上記ファージミドベクターをエレクトロポレーションにより大腸菌へと導入することで、MTA依存的に抗原に結合できる重鎖・軽鎖可変領域を取得可能なファージディスプレイライブラリが構築された。
実施例(6-7-1)において構築された重鎖可変領域、軽鎖可変領域のそれぞれのファージディスプレイライブラリから、MTAに結合する抗体可変領域を有するファージの集団を取得するために、ビオチン化標識MTAを用いたパニングを実施した。具体的には、構築されたファージミドベクターを保持する大腸菌に対して、M13KO7ΔpIII(ハイパーファージと呼称される)(PROGEN Biotechnik)を感染させ、25℃で一晩培養した上清からファージが回収された。ファージ産生が行われた大腸菌の培養液をTBSに溶媒置換し抗体多価提示ファージライブラリ液が調製された。
重鎖、軽鎖可変領域ファージディスプレイライブラリそれぞれから取得されたMTAに対して結合する重鎖および軽鎖の集団について、その集団の中の重鎖と軽鎖を組み合わせることにより作製されるFab提示ファージライブラリもMTAに対する結合を維持するクローンが多数含まれることが予想され、より効率よくMTA依存性抗体を取得できるライブラリが構築できると考えられた。
MTAに対するパニングで取得された重鎖、軽鎖それぞれのファージライブラリが感染した大腸菌から当業者公知の方法で遺伝子が抽出された。パンニング後重鎖可変領域ファージライブラリにおいては、重鎖可変領域遺伝子が重鎖可変領域を増幅できるプライマー(配列番号:88、89)を用いて増幅された。
構築されたMTA依存性抗体取得用ファージディスプレイライブラリ(M30ライブラリと呼称する)から、MTA存在下でヒトIL-6レセプター(hIL-6R)、ヒトIL-6(hIL-6)、ヒトIgA(hIgA)のそれぞれに対して結合活性を示す抗体がスクリーニングされた。
具体的には、構築されたファージミドベクターを保持する大腸菌に対して、M13KO7ΔpIII(ハイパーファージと呼称される)(PROGEN Biotechnik)を感染させ、25℃で一晩培養した上清からファージが回収された。ファージ産生が行われた大腸菌の培養液をTBSに溶媒置換し抗体多価提示ファージライブラリ液が調製された。
パンニングで得られた重鎖および軽鎖の可変領域配列は、重鎖抗体定常領域配列(配列番号:86)もしくは軽鎖kappa定常領域配列(配列番号:87)を有する動物発現用プラスミドへと挿入された。播種されたExpi293株(Thermo Fisher Scientific)に、調製されたプラスミドがリポフェクション法により導入された。CO2インキュベーター(37 ℃、8% CO2、1000 rpm)で4日間培養された培養上清を回収した。
培養上清は以下の手順でフローサイトメトリーを利用した抗原結合評価に供された。384ウェルマイクロプレート(greiner)に各ビオチン標識抗原を固相した磁気ビーズ、培養上清、0.1% BSA/5mM Mg2CL2/PBSもしくは終濃度100 μMのMTAを含む0.1% BSA/5mM Mg2CL2/PBSが添加され30分間以上静置された。当該プレートのビーズを0.1% BSA/5mM Mg2CL2/PBSまたは100 μMのMTAを含む0.1% BSA/5mM Mg2CL2/PBSで洗浄した後、当該ウェルにPBSもしくは終濃度100 μMのMTAを含む0.1% BSA/5mM Mg2CL2/PBSで希釈されたDyLight488標識抗ヒトFc抗体(invitrogen)が加えられ30分間以上静置された。当該ウェルを0.1% BSA/5mM Mg2CL2/PBSもしくは終濃度100 μMのMTAを含む0.1% BSA/5mM Mg2CL2/PBSで洗浄した後、iQue screener(Intellicyt)でサンプルの蛍光強度を測定した。解析の結果、ビオチン標識hIL-6R、hIL-6、hIgAのそれぞれを用いてパンニングされた各条件について、MTA依存的に抗原に結合する抗体が複数確認された。結果を表31に示した。
(7-1)重鎖および軽鎖可変領域ファージディスプレイライブラリを用いたアデノシンに結合する抗体群の濃縮
実施例(4-1-1)で構築された重鎖可変領域ファージディスプレイライブラリ、軽鎖可変領域ファージディスプレイライブラリのそれぞれから、アデノシンに結合する抗体群を濃縮するために、Biotin-2’-アデノシンとBiotin-5’-アデノシンの混合物(Biotin-アデノシン混合物)を用いたパニングが実施された。
具体的には、構築された重鎖可変領域ファージディスプレイライブラリまたは軽鎖可変領域ファージディスプレイライブラリのファージミドベクターを保持する大腸菌に対して、M13KO7ΔpIII(ハイパーファージと呼称される)(PROGEN Biotechnik)を感染させ、25℃で一晩培養した上清からファージが回収された。ファージ産生が行われた大腸菌の培養液に2.5M NaCl/10%PEGを添加することによって沈殿させたファージの集団をTBSにて希釈することによって抗体多価提示ファージライブラリ液が調製された。
実施例(7-1)で濃縮されたアデノシンに結合する抗体群中の抗体を提示するファージを感染させた大腸菌のシングルコロニーから、常法(Methods mol. Biol. (2002) 178, 133-145)に倣い、ファージ含有培養上清が回収された。ヘルパーファージとしてハイパーファージを用い、抗体多価提示ファージが回収され、ELISAに供された。384 Well Microplates Streptavidin-coated(greiner)に、Biotin-アデノシン混合物を含むTBSが10 μL添加され、1時間以上静置された。当該プレートの各ウェルをTBSTで洗浄した後、各ウェルは80uLの0.2%スキムミルク-TBSで1時間以上ブロッキングされた。各ウェルをTBSTで洗浄した後、各ウェルに調製されたファージが加えられ一時間静置することで、ファージに提示される抗体をBiotin-アデノシン混合物に結合させた。各ウェルをTBSTで洗浄した後、各ウェルにTBSで希釈されたHRP結合抗M13抗体(GE Healthcare)が加えられ一時間静置された。各ウェルをTBSTで洗浄した後、TMB single溶液(ZYMED)が加えられ、一定時間後溶液の発色反応が硫酸の添加により停止された後、450nm波長の吸光度が測定された。解析の結果、Biotin-2’-アデノシンに結合する抗体を提示するファージが複数確認された。ファージELISAの結果を表30に示した。ELISAの結果から、実施例(7-1)のパニングにより濃縮された抗体群中にアデノシン結合抗体が多数含まれていることが示された。
実施例(7-2)で濃縮されたアデノシン結合抗体群について、当該抗体群に含まれる改変重鎖と改変軽鎖を組み合わせることにより作製されるFab提示ファージライブラリもアデノシンに対する結合を維持する抗体が多数含まれることが予想され、アデノシン依存的に抗原に結合する抗体を取得するためのライブラリが構築できると考えられた。
実施例(7-2)で濃縮されたアデノシン結合抗体群を提示するファージが感染した大腸菌から、当業者公知の方法で抗体遺伝子が抽出された。重鎖可変領域ファージライブラリから濃縮された抗体群に対して、重鎖可変領域を増幅できるプライマー(配列番号:34、35)を用いて重鎖可変領域遺伝子が増幅された。軽鎖可変領域ファージライブラリおよびそのライブラリから濃縮された抗体群に対して、ヒト化SMB0002の重鎖可変領域配列を制限酵素処理により除去し、軽鎖可変領域ライブラリ遺伝子とヒトIgG由来軽鎖定常領域配列とヒトIgG由来CH1配列を含むファージミド断片が調製された。前記ファージミドベクター断片に重鎖可変領域ライブラリから増幅された重鎖可変領域遺伝子を挿入することで、重鎖/軽鎖可変領域ライブラリ遺伝子が導入されたファージミドベクターが構築された。このベクターをエレクトロポレーションにより大腸菌へと導入することで、ヒト抗体可変領域と定常領域からなるFabドメインを提示し、アデノシン依存的に抗原に結合する抗体を取得するためのライブラリ(アデノシン濃縮S02ライブラリ)が構築された。
以下の方法を用いて抗体蛋白が発現された。播種されたヒト胎児腎細胞由来FreeStyle293株またはExpi293株(Thermo Fisher Scientific)に、調製されたプラスミドがリポフェクション法により導入された。CO2インキュベーター(37 ℃、8% CO2、1000 rpm)で4日間培養された培養上清から、rProtein A Sepharose Fast Flow(Amersham Biosciences)またはMonoSpin ProA(ジーエルサイエンス)を用いて当業者公知の方法で抗体が精製された。分光光度計を用いて、精製された抗体溶液の280nmでの吸光度が測定された。得られた測定値からPACE法により算出された吸光係数を用いて精製抗体の濃度が算出された(Protein Science(1995) 4、2411-2423)。
さらに、本開示の、互いに配列の異なる複数の、MTA依存的に抗原に対する結合活性が変化する抗原結合ドメインまたは抗原結合ドメインを含む抗原結合分子を含むライブラリを用いれば、MTA依存的に抗原に対する結合活性が変化する抗原結合ドメイン及び当該抗原結合ドメインを含む抗原結合分子を、短時間で効率良く取得することが可能である。
Claims (7)
- i)5’-Methylthioadenosine(MTA)の濃度に応じて抗原に対する結合活性が変化し、および
ii)MTAの非存在下、且つ100μMのアデノシンの存在下において前記抗原に対する結合活性を有しない、
抗原結合ドメインを含む抗原結合分子であり、
前記抗原結合ドメインは、抗体重鎖可変領域(VH)および抗体軽鎖可変領域(VL)を含み、
前記抗原は、MTA以外の分子である、
抗原結合分子。 - 前記抗原結合分子が、抗体である、請求項1記載の抗原結合分子。
- 前記抗原結合分子が、二重特異性抗体である、請求項1または2記載の抗原結合分子。
- 前記抗原が、膜型分子であり、且つがん組織で発現している抗原である、請求項1乃至3のいずれか一項記載の抗原結合分子。
- 前記二重特異性抗体が、CD3に結合する抗原結合ドメインおよびがん細胞に発現する抗原に結合する抗原結合ドメインを含む、請求項3記載の抗原結合分子。
- 請求項1乃至5のいずれか一項記載の抗原結合分子を含む医薬組成物。
- 請求項1乃至5のいずれか一項記載の抗原結合分子の製造方法であって、
請求項1乃至5のいずれか一項記載の抗原結合分子をコードするポリヌクレオチドが作動可能に連結されたベクターを提供する工程、
前記ベクターが導入された細胞を提供する工程、
前記細胞を培養する工程、および
前記細胞の培養液から前記抗原結合分子を回収する工程、
を含む、方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2024211901A JP2025038000A (ja) | 2019-03-19 | 2024-12-05 | Mta依存的に抗原に対する結合活性が変化する抗原結合ドメインを含む抗原結合分子及び当該抗原結合ドメイン取得用ライブラリ |
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2019051965 | 2019-03-19 | ||
| JP2019051965 | 2019-03-19 | ||
| PCT/JP2020/012189 WO2020189748A1 (ja) | 2019-03-19 | 2020-03-19 | Mta依存的に抗原に対する結合活性が変化する抗原結合ドメインを含む抗原結合分子及び当該抗原結合ドメイン取得用ライブラリ |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2024211901A Division JP2025038000A (ja) | 2019-03-19 | 2024-12-05 | Mta依存的に抗原に対する結合活性が変化する抗原結合ドメインを含む抗原結合分子及び当該抗原結合ドメイン取得用ライブラリ |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JPWO2020189748A1 JPWO2020189748A1 (ja) | 2020-09-24 |
| JP7601758B2 true JP7601758B2 (ja) | 2024-12-17 |
Family
ID=72520304
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2021507411A Active JP7601758B2 (ja) | 2019-03-19 | 2020-03-19 | Mta依存的に抗原に対する結合活性が変化する抗原結合ドメインを含む抗原結合分子及び当該抗原結合ドメイン取得用ライブラリ |
| JP2024211901A Pending JP2025038000A (ja) | 2019-03-19 | 2024-12-05 | Mta依存的に抗原に対する結合活性が変化する抗原結合ドメインを含む抗原結合分子及び当該抗原結合ドメイン取得用ライブラリ |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2024211901A Pending JP2025038000A (ja) | 2019-03-19 | 2024-12-05 | Mta依存的に抗原に対する結合活性が変化する抗原結合ドメインを含む抗原結合分子及び当該抗原結合ドメイン取得用ライブラリ |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US20220153875A1 (ja) |
| EP (1) | EP3943108A4 (ja) |
| JP (2) | JP7601758B2 (ja) |
| CN (2) | CN113613676A (ja) |
| WO (1) | WO2020189748A1 (ja) |
Families Citing this family (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| SG10202006507XA (en) | 2012-05-30 | 2020-08-28 | Chugai Pharmaceutical Co Ltd | Target-tissue-specific antigen-binding molecule |
| KR102454360B1 (ko) | 2013-12-04 | 2022-10-12 | 추가이 세이야쿠 가부시키가이샤 | 화합물의 농도에 따라 항원 결합능이 변화되는 항원 결합 분자 및 그의 라이브러리 |
| CN117130035A (zh) * | 2017-08-18 | 2023-11-28 | 南京中硼联康医疗科技有限公司 | 生物剂量计及具有其的中子捕获治疗系统 |
| KR102697702B1 (ko) | 2018-08-10 | 2024-08-22 | 추가이 세이야쿠 가부시키가이샤 | 항cd137 항원 결합 분자 및 그의 사용 |
| JP2023529853A (ja) * | 2020-06-17 | 2023-07-12 | ティジアーナ ライフ サイエンシズ パブリック リミティド カンパニー | キメラ抗原受容体(car)t細胞療法を増強するための組成物および方法 |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2007531724A (ja) | 2004-04-05 | 2007-11-08 | クアーク・ファーマスーティカルス、インコーポレイテッド | 5’−デオキシ−5’−メチルチオアデノシンに対する抗体及びその使用 |
| WO2013180200A1 (ja) | 2012-05-30 | 2013-12-05 | 中外製薬株式会社 | 標的組織特異的抗原結合分子 |
| WO2015083764A1 (ja) | 2013-12-04 | 2015-06-11 | 中外製薬株式会社 | 化合物の濃度に応じて抗原結合能の変化する抗原結合分子及びそのライブラリ |
| JP2018537473A (ja) | 2015-12-03 | 2018-12-20 | アジオス ファーマシューティカルズ, インコーポレイテッド | Mtapヌル癌を処置するためのmat2a阻害剤 |
Family Cites Families (80)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4816567A (en) | 1983-04-08 | 1989-03-28 | Genentech, Inc. | Recombinant immunoglobin preparations |
| US4737456A (en) | 1985-05-09 | 1988-04-12 | Syntex (U.S.A.) Inc. | Reducing interference in ligand-receptor binding assays |
| GB8607679D0 (en) | 1986-03-27 | 1986-04-30 | Winter G P | Recombinant dna product |
| FI903489A0 (fi) | 1988-11-11 | 1990-07-10 | Medical Res Council | Ligander med en enda sektion, receptorer innehaollande naemnda ligander, foerfaranden foer deras framstaellning samt anvaendning av liganderna och receptorerna. |
| DE3920358A1 (de) | 1989-06-22 | 1991-01-17 | Behringwerke Ag | Bispezifische und oligospezifische, mono- und oligovalente antikoerperkonstrukte, ihre herstellung und verwendung |
| US5959177A (en) | 1989-10-27 | 1999-09-28 | The Scripps Research Institute | Transgenic plants expressing assembled secretory antibodies |
| JPH06508511A (ja) | 1990-07-10 | 1994-09-29 | ケンブリッジ アンティボディー テクノロジー リミティド | 特異的な結合ペアーの構成員の製造方法 |
| GB9015198D0 (en) | 1990-07-10 | 1990-08-29 | Brien Caroline J O | Binding substance |
| ES2108048T3 (es) | 1990-08-29 | 1997-12-16 | Genpharm Int | Produccion y utilizacion de animales inferiores transgenicos capaces de producir anticuerpos heterologos. |
| EP0604580A1 (en) | 1991-09-19 | 1994-07-06 | Genentech, Inc. | EXPRESSION IN E. COLI OF ANTIBODY FRAGMENTS HAVING AT LEAST A CYSTEINE PRESENT AS A FREE THIOL, USE FOR THE PRODUCTION OF BIFUNCTIONAL F(ab') 2? ANTIBODIES |
| ATE181571T1 (de) | 1991-09-23 | 1999-07-15 | Medical Res Council | Methoden zur herstellung humanisierter antikörper |
| JPH07501451A (ja) | 1991-11-25 | 1995-02-16 | エンゾン・インコーポレイテッド | 多価抗原結合タンパク質 |
| ATE463573T1 (de) | 1991-12-02 | 2010-04-15 | Medimmune Ltd | Herstellung von autoantikörpern auf phagenoberflächen ausgehend von antikörpersegmentbibliotheken |
| EP0746609A4 (en) | 1991-12-17 | 1997-12-17 | Genpharm Int | NON-HUMAN TRANSGENIC ANIMALS CAPABLE OF PRODUCING HETEROLOGOUS ANTIBODIES |
| EP0656941B1 (en) | 1992-03-24 | 2005-06-01 | Cambridge Antibody Technology Limited | Methods for producing members of specific binding pairs |
| JPH07509137A (ja) | 1992-07-24 | 1995-10-12 | セル ジェネシス,インク. | 異種抗体の生産 |
| US5648267A (en) | 1992-11-13 | 1997-07-15 | Idec Pharmaceuticals Corporation | Impaired dominant selectable marker sequence and intronic insertion strategies for enhancement of expression of gene product and expression vector systems comprising same |
| JPH08509612A (ja) | 1993-04-26 | 1996-10-15 | ジェンファーム インターナショナル インコーポレイテッド | 異種抗体を産生することができるトランスジェニック非ヒト動物 |
| GB9313509D0 (en) | 1993-06-30 | 1993-08-11 | Medical Res Council | Chemisynthetic libraries |
| FR2707189B1 (fr) | 1993-07-09 | 1995-10-13 | Gradient Ass | Procédé de traitement de résidus de combustion et installation de mise en Óoeuvre dudit procédé. |
| EP0731842A1 (en) | 1993-12-03 | 1996-09-18 | Medical Research Council | Recombinant binding proteins and peptides |
| ATE172218T1 (de) | 1994-06-24 | 1998-10-15 | Ici Plc | Geschäumte formteile aus styrol - und acryl - polymer - zusammensetzung |
| KR100261941B1 (ko) | 1994-07-13 | 2000-07-15 | 나가야마 오사무 | 사람의 인터루킨-8에 대한 재구성 사람항체 |
| US5789199A (en) | 1994-11-03 | 1998-08-04 | Genentech, Inc. | Process for bacterial production of polypeptides |
| US5731168A (en) | 1995-03-01 | 1998-03-24 | Genentech, Inc. | Method for making heteromultimeric polypeptides |
| US5840523A (en) | 1995-03-01 | 1998-11-24 | Genetech, Inc. | Methods and compositions for secretion of heterologous polypeptides |
| EP0739981A1 (en) | 1995-04-25 | 1996-10-30 | Vrije Universiteit Brussel | Variable fragments of immunoglobulins - use for therapeutic or veterinary purposes |
| EP0822830B1 (en) | 1995-04-27 | 2008-04-02 | Amgen Fremont Inc. | Human anti-IL-8 antibodies, derived from immunized xenomice |
| CA2219486A1 (en) | 1995-04-28 | 1996-10-31 | Abgenix, Inc. | Human antibodies derived from immunized xenomice |
| US6040498A (en) | 1998-08-11 | 2000-03-21 | North Caroline State University | Genetically engineered duckweed |
| EP1027439B1 (en) | 1997-10-27 | 2010-03-17 | Bac Ip B.V. | Multivalent antigen-binding proteins |
| ES2434961T5 (es) | 1998-04-20 | 2018-01-18 | Roche Glycart Ag | Ingeniería de glicosilación de anticuerpos para mejorar la citotoxicidad celular dependiente del anticuerpo |
| KR101077001B1 (ko) | 1999-01-15 | 2011-10-26 | 제넨테크, 인크. | 효과기 기능이 변화된 폴리펩티드 변이체 |
| EP1176195B1 (en) | 1999-04-09 | 2013-05-22 | Kyowa Hakko Kirin Co., Ltd. | Method for controlling the activity of immunologically functional molecule |
| US7125978B1 (en) | 1999-10-04 | 2006-10-24 | Medicago Inc. | Promoter for regulating expression of foreign genes |
| DE60022369T2 (de) | 1999-10-04 | 2006-05-18 | Medicago Inc., Sainte Foy | Verfahren zur regulation der transkription von fremden genen in gegenwart von stickstoff |
| CA2421447C (en) | 2000-09-08 | 2012-05-08 | Universitat Zurich | Collections of repeat proteins comprising repeat modules |
| CN102311986B (zh) | 2000-10-06 | 2015-08-19 | 协和发酵麒麟株式会社 | 产生抗体组合物的细胞 |
| JP2004526419A (ja) | 2000-10-16 | 2004-09-02 | フィロス インク. | 抗体模倣物および他の結合タンパク質のためのタンパク質骨格 |
| PT1355919E (pt) | 2000-12-12 | 2011-03-02 | Medimmune Llc | Moléculas com semivida longa, composições que as contêm e suas utilizações |
| JP2005500018A (ja) | 2001-04-02 | 2005-01-06 | アイデック ファーマスーティカルズ コーポレイション | GnTIIIと同時発現する組換え抗体 |
| US20030157561A1 (en) | 2001-11-19 | 2003-08-21 | Kolkman Joost A. | Combinatorial libraries of monomer domains |
| ES2312586T3 (es) | 2001-06-22 | 2009-03-01 | Chugai Seiyaku Kabushiki Kaisha | Inhibidor del crecimiento celular que contenga un anticuerpo anti-clipicano 3. |
| WO2003029462A1 (en) | 2001-09-27 | 2003-04-10 | Pieris Proteolab Ag | Muteins of human neutrophil gelatinase-associated lipocalin and related proteins |
| US20040132101A1 (en) | 2002-09-27 | 2004-07-08 | Xencor | Optimized Fc variants and methods for their generation |
| WO2003104453A1 (ja) | 2002-06-05 | 2003-12-18 | 中外製薬株式会社 | 抗体作製方法 |
| WO2004022595A1 (ja) | 2002-09-04 | 2004-03-18 | Chugai Seiyaku Kabushiki Kaisha | MRL/lprマウスを用いた抗体の作製 |
| WO2004029207A2 (en) | 2002-09-27 | 2004-04-08 | Xencor Inc. | Optimized fc variants and methods for their generation |
| DK1562972T3 (da) | 2002-10-15 | 2010-12-06 | Facet Biotech Corp | Modifikation af FcRn-bindingsaffiniteter eller serumhalveringstider for antistoffer ved mutagenese |
| PL222222B1 (pl) | 2003-01-22 | 2016-07-29 | Glycart Biotechnology Ag | Sposób wytwarzania polipeptydu |
| WO2005040229A2 (en) | 2003-10-24 | 2005-05-06 | Avidia, Inc. | Ldl receptor class a and egf domain monomers and multimers |
| EP1706424B1 (en) | 2004-01-12 | 2009-07-22 | Applied Molecular Evolution, Inc. | Fc region variants |
| PL1674111T3 (pl) | 2004-07-09 | 2011-04-29 | Chugai Pharmaceutical Co Ltd | Przeciwciała anty-glipikan 3 |
| ES2426817T3 (es) | 2004-08-04 | 2013-10-25 | Mentrik Biotech, Llc | Regiones Fc variantes |
| WO2006023420A2 (en) | 2004-08-16 | 2006-03-02 | Medimmune, Inc. | Integrin antagonists with enhanced antibody dependent cell-mediated cytotoxicity activity |
| US20060067930A1 (en) | 2004-08-19 | 2006-03-30 | Genentech, Inc. | Polypeptide variants with altered effector function |
| US7632497B2 (en) | 2004-11-10 | 2009-12-15 | Macrogenics, Inc. | Engineering Fc Antibody regions to confer effector function |
| EP2208783A1 (en) | 2004-12-22 | 2010-07-21 | Chugai Seiyaku Kabushiki Kaisha | Method of producing an antibody using a cell in which the function of fucose transporter is inhibited |
| EP1871808A2 (en) | 2005-03-31 | 2008-01-02 | Xencor, Inc. | Fc VARIANTS WITH OPTIMIZED PROPERTIES |
| TWI671403B (zh) | 2005-03-31 | 2019-09-11 | 中外製藥股份有限公司 | 控制組裝之多肽的製造方法 |
| WO2006116260A2 (en) | 2005-04-26 | 2006-11-02 | Medimmune, Inc. | Modulation of antibody effector function by hinge domain engineering |
| CA2618681C (en) | 2005-08-10 | 2015-10-27 | Macrogenics, Inc. | Identification and engineering of antibodies with variant fc regions and methods of using same |
| AU2006299429B2 (en) | 2005-10-03 | 2012-02-23 | Xencor, Inc. | Fc variants with optimized Fc receptor binding properties |
| WO2007104529A2 (en) * | 2006-03-13 | 2007-09-20 | Ablynx N.V. | Amino acid sequences directed against il-6 and polypeptides comprising the same for the treatment of diseases and disorders associated with il-6-mediated signalling |
| AU2007281284A1 (en) | 2006-08-02 | 2008-02-07 | The Uab Research Foundation | Methods and compositions related to soluble monoclonal variable lymphocyte receptors of defined antigen specificity |
| WO2008092117A2 (en) | 2007-01-25 | 2008-07-31 | Xencor, Inc. | Immunoglobulins with modifications in the fcr binding region |
| DK2176298T3 (en) | 2007-05-30 | 2018-02-12 | Xencor Inc | Methods and compositions for inhibiting CD32B-expressing cells |
| PL2808343T3 (pl) | 2007-12-26 | 2019-11-29 | Xencor Inc | Warianty Fc ze zmienionym wiązaniem do FcRn |
| TWI700293B (zh) | 2008-04-11 | 2020-08-01 | 日商中外製藥股份有限公司 | 重複結合複數個抗原的抗體 |
| WO2009140242A1 (en) | 2008-05-13 | 2009-11-19 | Genentech, Inc. | Analysis of antibody drug conjugates by bead-based affinity capture and mass spectrometry |
| EP2669298A3 (en) | 2008-05-23 | 2014-02-26 | Ablexis, LLC | Single variable immunoglobulin domain comprising VL-DH-JL |
| TWI667257B (zh) | 2010-03-30 | 2019-08-01 | 中外製藥股份有限公司 | 促進抗原消失之具有經修飾的FcRn親和力之抗體 |
| KR102568454B1 (ko) | 2010-11-30 | 2023-08-18 | 추가이 세이야쿠 가부시키가이샤 | 복수 분자의 항원에 반복해서 결합하는 항원 결합 분자 |
| EP3604330A1 (en) | 2011-02-25 | 2020-02-05 | Chugai Seiyaku Kabushiki Kaisha | Fcgammariib-specific fc antibody |
| EP2698431B1 (en) | 2011-03-30 | 2020-09-09 | Chugai Seiyaku Kabushiki Kaisha | Retention of antigen-binding molecules in blood plasma and method for modifying immunogenicity |
| US9890218B2 (en) | 2011-06-30 | 2018-02-13 | Chugai Seiyaku Kabushiki Kaisha | Heterodimerized polypeptide |
| TW201817745A (zh) | 2011-09-30 | 2018-05-16 | 日商中外製藥股份有限公司 | 具有促進抗原清除之FcRn結合域的治療性抗原結合分子 |
| TW202500756A (zh) | 2012-02-24 | 2025-01-01 | 日商中外製藥股份有限公司 | 經FcγRIIB促進抗原消失之抗原結合分子 |
| KR102282691B1 (ko) | 2013-09-30 | 2021-07-27 | 추가이 세이야쿠 가부시키가이샤 | 개변된 헬퍼 파지를 사용하여 항원 결합 분자를 제작하는 방법 |
| SG10201808225TA (en) | 2014-03-21 | 2018-10-30 | Regeneron Pharma | Non-human animals that make single domain binding proteins |
-
2020
- 2020-03-19 WO PCT/JP2020/012189 patent/WO2020189748A1/ja not_active Ceased
- 2020-03-19 US US17/438,993 patent/US20220153875A1/en active Pending
- 2020-03-19 EP EP20773939.2A patent/EP3943108A4/en active Pending
- 2020-03-19 CN CN202080021856.0A patent/CN113613676A/zh active Pending
- 2020-03-19 CN CN202511354577.7A patent/CN121159688A/zh active Pending
- 2020-03-19 JP JP2021507411A patent/JP7601758B2/ja active Active
-
2024
- 2024-12-05 JP JP2024211901A patent/JP2025038000A/ja active Pending
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2007531724A (ja) | 2004-04-05 | 2007-11-08 | クアーク・ファーマスーティカルス、インコーポレイテッド | 5’−デオキシ−5’−メチルチオアデノシンに対する抗体及びその使用 |
| WO2013180200A1 (ja) | 2012-05-30 | 2013-12-05 | 中外製薬株式会社 | 標的組織特異的抗原結合分子 |
| WO2015083764A1 (ja) | 2013-12-04 | 2015-06-11 | 中外製薬株式会社 | 化合物の濃度に応じて抗原結合能の変化する抗原結合分子及びそのライブラリ |
| JP2018537473A (ja) | 2015-12-03 | 2018-12-20 | アジオス ファーマシューティカルズ, インコーポレイテッド | Mtapヌル癌を処置するためのmat2a阻害剤 |
Non-Patent Citations (2)
| Title |
|---|
| European Journal of Cancer,2014年,Vol.50, pp.2714-2724 |
| Journal of Chromatography B,2008年,Vol.876, pp.123-128 |
Also Published As
| Publication number | Publication date |
|---|---|
| CN121159688A (zh) | 2025-12-19 |
| CN113613676A (zh) | 2021-11-05 |
| EP3943108A4 (en) | 2023-01-04 |
| US20220153875A1 (en) | 2022-05-19 |
| JP2025038000A (ja) | 2025-03-18 |
| WO2020189748A1 (ja) | 2020-09-24 |
| EP3943108A1 (en) | 2022-01-26 |
| JPWO2020189748A1 (ja) | 2020-09-24 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7765428B2 (ja) | 標的組織特異的抗原結合分子 | |
| JP7488843B2 (ja) | 化合物の濃度に応じて抗原結合能の変化する抗原結合分子及びそのライブラリ | |
| JP7601758B2 (ja) | Mta依存的に抗原に対する結合活性が変化する抗原結合ドメインを含む抗原結合分子及び当該抗原結合ドメイン取得用ライブラリ |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20230317 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20240304 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20240419 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20240422 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20240628 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20241001 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20241030 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20241108 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20241205 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7601758 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |