以下、本発明の実施形態について詳細に説明する。しかし、本発明は、以下の実施形態に何ら限定されない。本発明は、本発明の目的の範囲内で、適宜変更を加えて実施できる。なお、説明が重複する箇所については、適宜説明を省略する場合があるが、発明の要旨は限定されない。
以下、化合物名の後に「系」を付けて、化合物及びその誘導体を包括的に総称する場合がある。また、化合物名の後に「系」を付けて重合体名を表す場合には、重合体の繰返し単位が化合物又はその誘導体に由来することを意味する。更に、反応式(R−1)〜(R−19)で表される反応を各々、反応(R−1)〜(R−19)と記載することがある。一般式(1)〜(7)、(6−1)、(6−2)及び(6−3)で表される化合物を各々、化合物(1)〜(7)、(6−1)、(6−2)及び(6−3)と記載することがある。化学式(2a)、(3a)、(4a)、(5a)、(6a)〜(6c)、(7a)、(8)、(10a)、(10b)、(11a)、(12a)、(12b)、(13a)〜(13e)及び(14a)〜(14e)で表される化合物を各々、化合物(2a)、(3a)、(4a)、(5a)、(6a)〜(6c)、(7a)、(8)、(10a)、(10b)、(11a)、(12a)、(12b)、(13a)〜(13e)及び(14a)〜(14e)と記載することがある。
以下、ハロゲン原子、炭素原子数1以上6以下のアルキル基、炭素原子数1以上6以下のアルコキシ基、炭素原子数6以上14以下のアリール基は、何ら規定していなければ、各々次の意味である。
ハロゲン原子は、例えば、フッ素(フルオロ基)、塩素(クロロ基)又は臭素(ブロモ基)である。
炭素原子数1以上6以下のアルキル基は、直鎖状又は分枝鎖状で非置換の炭素原子数1以上6以下のアルキル基である。炭素原子数1以上6以下のアルキル基の例としては、メチル基、エチル基、プロピル基、イソプロピル基、n−ブチル基、s−ブチル基、t−ブチル基、ペンチル基、イソペンチル基、ネオペンチル基又はヘキシル基が挙げられる。
炭素原子数1以上6以下のアルコキシ基は、直鎖状又は分枝鎖状で非置換の炭素原子数1以上6以下のアルコキシ基である。炭素原子数1以上6以下のアルコキシ基の例としては、メトキシ基、エトキシ基、n−プロポキシ基、イソプロポキシ基、n−ブトキシ基、s−ブトキシ基、t−ブトキシ基、ペンチルオキシ基、イソペンチルオキシ基、ネオペンチルオキシ基又はヘキシルオキシ基が挙げられる。
炭素原子数6以上14以下のアリール基は、例えば、炭素原子数6以上14以下の非置換の芳香族単環炭化水素基、炭素原子数6以上14以下の非置換の芳香族縮合二環炭化水素基又は素原子数6以上14以下の非置換の芳香族縮合三環炭化水素基である。炭素原子数6以上14以下のアリール基の例としては、フェニル基、ナフチル基、アントリル基又はフェナントリル基が挙げられる。
<第一実施形態:化合物(1)>
本発明の第一実施形態は、化合物(1)である。化合物(1)は、トリアリールアミンヒドラゾン化合物、すなわちトリアリールアミン構造を含むヒドラゾン化合物である。化合物(1)は、下記一般式(1)で表される。
一般式(1)中、R1、R2、R3、R4、R5及びR6は、各々独立して、ハロゲン原子、置換基を有してもよい炭素原子数1以上6以下のアルキル基、置換基を有してもよい炭素原子数1以上6以下のアルコキシ基又は置換基を有してもよい炭素原子数6以上14以下のアリール基を表す。aは、1以上3以下の整数を表す。b及びcは、各々独立して、0又は1を表す。d、e、f、g、h及びiは、各々独立して、0以上5以下の整数を表す。dが2以上5以下の整数を表すとき複数のR1は同一でも異なっていてもよい。eが2以上5以下の整数を表すとき複数のR2は同一でも異なっていてもよい。fが2以上5以下の整数を表すとき複数のR3は同一でも異なっていてもよい。gが2以上5以下の整数を表すとき複数のR4は同一でも異なっていてもよい。hが2以上5以下の整数を表すとき複数のR5は同一でも異なっていてもよい。iが2以上5以下の整数を表すとき複数のR6は同一でも異なっていてもよい。
化合物(1)は、電子写真感光体(以下、感光体と記載することがある)の電気特性を向上させることができる。その理由は以下のように推測される。
第一に、化合物(1)は、2個のトリフェニルアミン部位を有する。2個のトリフェニルアミン部位の間には、1個以上3個以下(一般式(1)中のaに相当)の共役結合が存在する。そのため、化合物(1)の分子構造が適度に大きくなる。これにより、感光層中に存在する一の化合物(1)のπ電子雲と他の化合物(1)のπ電子雲との距離(ホッピング距離)が小さくなる傾向がある。その結果、化合物(1)の間での正孔の移動性が向上し、感光体の電気特性が向上すると考えられる。
第二に、化合物(1)は、化学式「−CH=N−N=」で表される基を2個有する。化学式「−CH=N−N=」で表される基は極性基である。そのため、化合物(1)は感光層を形成するための溶剤に溶解し易い。また、バインダー樹脂が極性基(例えばカルボニル基)を有する場合に、極性基を有する化合物(1)とバインダー樹脂との相溶性が向上すると考えられる。これにより、化合物(1)が均一に分散した感光層が得られ易くなる。その結果、感光体の電気特性が向上すると考えられる。
第三に、化合物(1)は、平面構造を有する電荷発生剤と重なり易い構造を有している。化合物(1)と電荷発生剤との重なる面積が広くなると、電荷発生剤から化合物(1)へ正孔が効率良く受け渡される傾向がある。その結果、感光体の電気特性が向上すると考えられる。
一般式(1)のR1〜R6で表される炭素原子数1以上6以下のアルキル基としては、炭素原子数1以上3以下のアルキル基が好ましく、メチル基がより好ましい。R1〜R6で表される炭素原子数1以上6以下のアルキル基は、置換基を有してもよい。炭素原子数1以上6以下のアルキル基が有する置換基としては、ハロゲン原子、炭素原子数1以上6以下のアルコキシ基又は炭素原子数6以上14以下のアリール基が挙げられる。置換基の数は特に限定されないが、3個以下であることが好ましい。
一般式(1)のR1〜R6で表される炭素原子数1以上6以下のアルコキシ基としては、炭素原子数1以上3以下のアルコキシ基が好ましく、メトキシ基又はエトキシ基がより好ましい。R1〜R6で表される炭素原子数1以上6以下のアルコキシ基は、置換基を有してもよい。炭素原子数1以上6以下のアルコキシ基が有する置換基としては、ハロゲン原子、炭素原子数1以上6以下のアルコキシ基又は炭素原子数6以上14以下のアリール基が挙げられる。置換基の数は特に限定されないが、3個以下であることが好ましい。
一般式(1)のR1〜R6で表される炭素原子数6以上14以下のアリール基としては、炭素原子数6以上14以下の芳香族単環炭化水素基又は炭素原子数6以上14以下の芳香族縮合二環炭化水素基が好ましく、フェニル基がより好ましい。R1〜R6で表される炭素原子数6以上14以下のアリール基は、置換基を有してもよい。炭素原子数6以上14以下のアリール基が有する置換基としては、ハロゲン原子、炭素原子数1以上6以下のアルキル基、炭素原子数1以上6以下のアルコキシ基又は炭素原子数6以上14以下のアリール基が挙げられる。置換基の数は特に限定されないが、3個以下であることが好ましい。
感光体の電気特性を向上させるためには、R1〜R6は、各々独立して、炭素原子数1以上6以下のアルキル基、炭素原子数1以上6以下のアルコキシ基又は炭素原子数6以上14以下のアリール基を表すことが好ましい。
一般式(1)中、aは2又は3を表すことが好ましい。aが2又は3であると、化合物(1)の分子構造が適度に大きくなり、感光層中に存在する一の化合物(1)のπ電子雲と他の化合物(1)のπ電子雲との距離(ホッピング距離)が小さくなる傾向がある。その結果、化合物(1)の間での正孔の移動性が向上し、感光体の電気特性が向上すると考えられる。
感光体の電気特性を向上させるためには、一般式(1)中、d、e、f、g、h及びiは、各々独立して、0以上2以下の整数を表すことが好ましい。同様の理由から、d及びgは、各々独立して1又は2を表すことがより好ましい。同様の理由から、e、f、h及びiは、各々、0を表すことがより好ましい。
d、e、f、g、h又はiが2以上5以下の整数を表すとき、対応する複数のR1、R2、R3、R4、R5及びR6は同一でも異なっていてもよい。例えば、dが2を表すとき、2個のR1は互いに同一であっても異なっていてもよい。例えば、dが2を表すとき、2個のR1は各々メチル基であってもよいし、2個のR1の一方がメチル基であり他方がメトキシ基であってもよい。
d、e、f、g、h又はiが1以上5以下の整数を表すとき、対応するR1、R2、R3、R4、R5及びR6の置換位置は特に限定されない。R1、R2、R3、R4、R5又はR6は、R1、R2、R3、R4、R5又はR6が結合するフェニル基のパラ位、メタ位又はオルト位の何れに結合してもよい。R1、R2、R3、R4、R5又はR6は、フェニル基のオルト位及び/又はパラ位に結合することが好ましい。
一般式(1)中、下記一般式(1−1)で表される基は、下記一般式(1−2)で表される基と同一であることが好ましい。感光体の電気特性を維持しつつ、反応工程を減らして効率的に化合物(1)を製造できるためである。
一般式(1−1)中、R1、R2、R3、b、d、e及びfは、一般式(1)中のR1、R2、R3、b、d、e及びfと同義である。一般式(1−1)中のR1、R2、R3、b、d、e及びfの好適な例は、一般式(1)中のR1、R2、R3、b、d、e及びfの好適な例と同じである。Y1は、結合部位を表す。
一般式(1−2)中、R4、R5、R6、c、g、h及びiは、一般式(1)中のR4、R5、R6、c、g、h及びiと同義である。一般式(1−2)中のR4、R5、R6、c、g、h及びiの好適な例は、一般式(1)中のR4、R5、R6、c、g、h及びiの好適な例と同じである。Y2は、結合部位を表す。
一般式(1−1)で表される基のY1は、下記一般式(1−3)で表される基のY1と結合する。そして、一般式(1−1)中のY1が結合する窒素原子と、一般式(1−3)中のY1が結合する炭素原子との間に、単結合が形成される。一般式(1−2)で表される基のY2は、一般式(1−3)で表される基のY2と結合する。そして、一般式(1−2)中のY2が結合する窒素原子と、一般式(1−3)中のY2が結合する炭素原子との間に、単結合が形成される。
一般式(1−3)中、aは、一般式(1)中のaと同義である。一般式(1−3)中のaの好適な例は、一般式(1)中のaの好適な例と同じである。Y1及びY2は各々、結合部位を表す。
一般式(1−1)で表される基が一般式(1−2)で表される基と同一である場合、一般式(1)中のR1〜R6及びb〜iは次の関係を有する。一般式(1)中、R1及びR4は、互いに同じ基を表す。R2及びR5は、互いに同じ基を表す。R3及びR6は、互いに同じ基を表す。b及びcは、互いに同じ整数を表す。d及びgは、互いに同じ整数を表す。e及びhは、互いに同じ整数を表す。f及びiは、互いに同じ整数を表す。d及びgが互いに2以上5以下の同じ整数を表すとき、複数のR1は同一でも異なってもよく、複数のR4は同一でも異なってもよい。この場合、一のフェニル基の一の結合位置に結合するR1と、別のフェニル基のこのR1に対応する置換位置に結合するR4とは、同一である。理解を容易にするために一例を挙げて説明する。例えば、一のフェニル基のパラ位に結合するR1と、オルト位に結合するR1とは同一でも異なっていてもよい。この場合、別のフェニル基のパラ位に結合するR4と、オルト位に結合するR4とは同一でも異なっていてもよい。この場合、一のフェニル基のパラ位に結合するR1と、別のフェニル基のパラ位に結合するR4とは同一である。一のフェニル基のオルト位に結合するR1と、別のフェニル基のオルト位に結合するR4とは同一である。e及びhが互いに2以上5以下の同じ整数を表すときも、複数のR2及び複数のR5は同様の関係を有する。f及びiが互いに2以上5以下の同じ整数を表すときも、複数のR3及び複数のR6は同様の関係を有する。
一般式(1−1)で表される基が一般式(1−2)で表される基と同一である場合、一般式(1)中のR2、R3、R5及びR6は互いに同じ基を表し、e、f、h及びiは互いに同じ整数を表すことが好ましい。
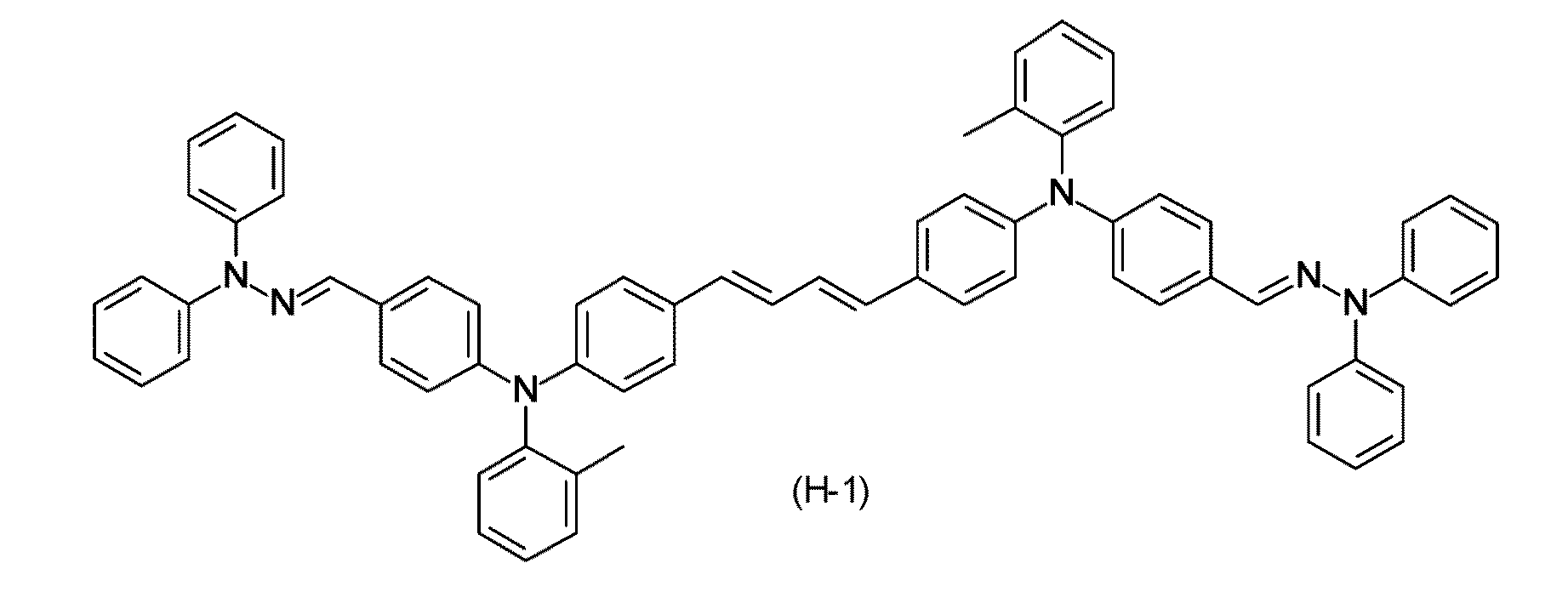
化合物(1)の具体例としては、下記化学式(H−1)、(H−2)、(H−3)、(H−4)又は(H−5)で表される化合物(以下、化合物(H−1)、(H−2)、(H−3)、(H−4)又は(H−5)と記載することがある)が挙げられる。代表例として化合物(H−2)及び(H−4)の1H−NMRスペクトルを、図1及び図2に示す。
[化合物(1)の製造方法]
化合物(1)は、例えば、下記の反応(R−1)〜(R−10)に従って又はこれに準ずる方法によって製造される。これらの反応以外に、必要に応じて適宜な工程が含まれてもよい。反応(R−1)〜(R−10)で示す反応式において、R1〜R6及びa〜iは、一般式(1)中のR1〜R6及びa〜iと同義である。Xは、ハロゲン原子を表す。
[化合物(6)の製造]
まず、化合物(6)を製造する。化合物(6)は、下記一般式(6)で表される。化合物(6)は、化合物(1)を製造するための原料である。化合物(6)の製造方法として、化合物(6−1)、(6−2)及び(6−3)の製造方法を例に挙げて説明する。化合物(6−1)、(6−2)及び(6−3)は各々、一般式(6)中のaが1、2及び3である化合物である。
化合物(6−1)は、下記反応(R−1)及び(R−2)に従って製造される。化合物(6−2)は、下記反応(R−1)及び(R−3)に従って製造される。
反応(R−1)では、1モル当量の化合物(2)と1モル当量の亜リン酸トリエチルとを反応させて、1モル当量の化合物(3)を得る。反応(R−1)では、1モルの化合物(2)に対して、1モル以上2.5モル以下の亜リン酸トリエチルを添加することが好ましい。反応(R−1)の反応温度は160℃以上200℃以下であることが好ましい。反応(R−1)の反応時間は2時間以上10時間以下であることが好ましい。
反応(R−2)では、1モル当量の化合物(3)と1モル当量の化合物(4)とを反応させて、1モル当量の化合物(6−1)を得る。反応(R−2)は、ウィッティヒ(Wittig)反応である。反応(R−2)では、1モルの化合物(3)に対して、1モル以上5モル以下の化合物(4)を添加することが好ましい。反応(R−2)の反応温度は0℃以上50℃以下であることが好ましい。反応(R−2)の反応時間は2時間以上24時間以下であることが好ましい。
反応(R−2)は、塩基の存在下で行われてもよい。塩基としては、例えば、ナトリウムアルコキシド(具体的には、ナトリウムメトキシド又はナトリウムエトキシド)、金属水素化物(具体的には、水素化ナトリウム又は水素化カリウム)又は金属塩(具体的には、n−ブチルリチウム)が挙げられる。これらの塩基は1種を単独で用いてもよく、2種以上を組み合わせて用いてもよい。塩基の添加量は、1モルの化合物(3)に対して、1モル以上2モル以下であることが好ましい。
反応(R−2)は、溶媒中で行われてもよい。溶媒としては、例えば、エーテル類(具体的には、テトラヒドロフラン、ジエチルエーテル又はジオキサン)、ハロゲン化炭化水素(具体的には、塩化メチレン、クロロホルム又はジクロロエタン)又は芳香族炭化水素(具体的には、ベンゼン又はトルエン)が挙げられる。
反応(R−3)では、1モル当量の化合物(3)と1モル当量の化合物(5)とを反応させて、1モル当量の化合物(6−2)を得る。反応(R−3)は、ウィッティヒ(Wittig)反応である。反応(R−3)は、化合物(4)の代わりに化合物(5)を使用する以外は、反応(R−2)と同様の方法で行うことができる。
化合物(6−3)は、下記反応(R−4)及び(R−5)に従って製造される。
反応(R−4)では、1モル当量の化合物(7)と2モル当量の亜リン酸トリエチルとを反応させて、1モル当量の化合物(8)を得る。反応(R−4)では、1モルの化合物(7)に対して、2モル以上5モル以下の亜リン酸トリエチルを添加することが好ましい。反応(R−4)の反応温度は160℃以上200℃以下であることが好ましい。反応(R−4)の反応時間は2時間以上10時間以下であることが好ましい。
反応(R−5)では、1モル当量の化合物(8)と2モル当量の化合物(4)とを反応させて、1モル当量の化合物(6−3)を得る。反応(R−5)は、ウィッティヒ(Wittig)反応である。反応(R−5)では、1モルの化合物(8)に対して、2モル以上10モル以下の化合物(4)を添加することが好ましい。反応(R−5)は、塩基の存在下で行われてもよい。反応(R−5)は、溶媒中で行われてもよい。反応(R−5)で使用される塩基及び溶媒の例は、反応(R−2)で使用される塩基及び溶媒の例と同様である。反応(R−5)の反応温度は0℃以上50℃以下であることが好ましい。反応(R−5)の反応時間は2時間以上24時間以下であることが好ましい。
[化合物(12)の製造]
次に、下記反応(R−6)に従って、化合物(12)を製造する。化合物(12)は、化合物(14)を製造するための原料である。
反応(R−6)では、1モル当量の化合物(10)と1モル当量の化合物(11、ジフェニルヒドラジン誘導体の塩酸塩)とを反応させて、1モル当量の化合物(12)を得る。反応(R−6)では、1モルの化合物(10)に対して、1モル以上2.5モル以下の化合物(11)を添加することが好ましい。反応(R−6)の反応温度は80℃以上150℃以下であることが好ましい。反応(R−6)の反応時間は2時間以上10時間以下であることが好ましい。
反応(R−6)は、触媒の存在下で行われてもよい。触媒としては、例えば、酸触媒が挙げられ、より具体的には、p−トルエンスルホン酸、カンファースルホン酸又はピリジニウム−p−トルエンスルホン酸が挙げられる。これらの触媒は1種を単独で用いてもよく、2種以上を組み合わせて用いてもよい。触媒の添加量は、1モルの化合物(10)に対して、少量であり、具体的には0.01モル以上0.5モル以下であることが好ましい。
反応(R−6)は、溶媒中で行われてもよい。反応(R−6)で使用される溶媒の例は、反応(R−2)で使用される溶媒の例と同様である。
[化合物(14)の製造]
次に、下記反応(R−7)に従って、化合物(14)を製造する。化合物(14)は、化合物(1)を製造するための原料である。
反応(R−7)では、1モル当量の化合物(12)と1モル当量の化合物(13)とを反応させて、1モル当量の化合物(14)を得る。反応(R−7)は、カップリング反応である。反応(R−7)では、1モルの化合物(12)に対して、1モル以上2.5モル以下の化合物(13)を添加することが好ましい。反応(R−7)の反応温度は80℃以上140℃以下であることが好ましい。反応(R−7)の反応時間は2時間以上10時間以下であることが好ましい。
反応(R−7)では、触媒としてパラジウム化合物を用いてもよい。パラジウム化合物としては、例えば、四価パラジウム化合物、二価パラジウム化合物又はその他のパラジウム化合物が挙げられる。四価パラジウム化合物としては、例えば、ヘキサクロルパラジウム(IV)酸ナトリウム四水和物又はヘキサクロルパラジウム(IV)酸カリウム四水和物が挙げられる。二価パラジウム化合物としては、例えば、塩化パラジウム(II)、臭化パラジウム(II)、酢酸パラジウム(II)、パラジウムアセチルアセテート(II)、ジクロロビス(ベンゾニトリル)パラジウム(II)、ジクロルビス(トリフェニルホスフィン)パラジウム(II)、ジクロロテトラミンパラジウム(II)又はジクロロ(シクロオクタ−1,5−ジエン)パラジウム(II)が挙げられる。その他のパラジウム化合物としては、例えば、トリス(ジベンジリデンアセトン)ジパラジウム(0)、トリス(ジベンジリデンアセトン)ジパラジウムクロロホルム錯体(0)又はテトラキス(トリフェニルホスフィン)パラジウム(0)が挙げられる。パラジウム化合物は1種を単独で用いてもよく、2種以上を組み合わせて用いてもよい。パラジウム化合物の添加量は、1モルの化合物(12)に対して、0.0005モル以上20モル以下であることが好ましく、0.001モル以上1モル以下であることがより好ましい。
パラジウム化合物は、配位子を含む構造であってもよい。これにより、反応(R−7)の反応性を向上させ易くなる。配位子としては、例えば、トリシクロヘキシルホスフィン、トリフェニルホスフィン、メチルジフェニルホスフィン、トリフリルホスフィン、トリ(o−トリル)ホスフィン、ジシクロヘキシルフェニルホスフィン、トリ(t−ブチル)ホスフィン、2,2’−ビス(ジフェニルホスフィノ)−1,1’−ビナフチル又は2,2’−ビス[(ジフェニルホスフィノ)ジフェニル]エーテルが挙げられる。配位子は1種を単独で用いてもよく、2種以上を組み合わせて用いてもよい。配位子の添加量は、1モルの化合物(12)に対して、0.0005モル以上20モル以下であることが好ましく、0.001モル以上1モル以下であることがより好ましい。
反応(R−7)は、塩基の存在下で行われてもよい。これにより、触媒活性を向上できると考えられる。塩基は、無機塩基であってもよいし、有機塩基であってもよい。有機塩基としては、例えば、アルカリ金属アルコシドが挙げられ、具体的には、ナトリウムメトキシド、ナトリウムエトキシド、カリウムメトキシド、カリウムエトキシド、リチウムtert−ブトキシド、ナトリウムtert−ブトキシド又はカリウムtert−ブトキシドが挙げられる。無機塩基としては、例えば、リン酸三カリウム又はフッ化セシウムが挙げられる。1モルの化合物(12)に対して、パラジウム化合物を0.0005モル以上20モル以下添加する場合、塩基の添加量は、1モル以上50モル以下であることが好ましく、1モル以上30モル以下であることがより好ましい。
反応(R−7)は、溶媒中で行われてもよい。溶媒としては、例えば、キシレン(具体的には、o−キシレン)、トルエン、テトラヒドロフラン又はジメチルホルムアミドが挙げられる。
[化合物(17)の製造]
次に、下記反応(R−8)に従って、化合物(17)を製造する。化合物(17)は、化合物(19)を製造するための原料である。
反応(R−8)では、1モル当量の化合物(15)と1モル当量の化合物(16、ジフェニルヒドラジン誘導体の塩酸塩)とを反応させて、1モル当量の化合物(17)を得る。反応(R−8)は、化合物(10)の代わりに化合物(15)を使用すること、及び化合物(11)の代わりに化合物(16)を使用すること以外は、反応(R−6)と同様の方法で行うことができる。
[化合物(19)の製造]
次に、下記反応(R−9)に従って、化合物(19)を製造する。化合物(19)は、化合物(1)を製造するための原料である。
反応(R−9)では、1モル当量の化合物(17)と1モル当量の化合物(18)とを反応させて、1モル当量の化合物(19)を得る。反応(R−9)は、カップリング反応である。反応(R−9)は、化合物(12)の代わりに化合物(17)を使用すること、及び化合物(13)の代わりに化合物(18)を使用すること以外は、反応(R−7)と同様の方法で行うことができる。
[化合物(1)の製造]
次に、下記反応(R−10)に従って、目的化合物である化合物(1)を製造する。
反応(R−10)では、1モル当量の化合物(6)と1モル当量の化合物(14)と1モル当量の化合物(19)とを反応させて、1モル当量の化合物(1)を得る。反応(R−10)は、カップリング反応である。反応(R−10)では、1モルの化合物(6)に対して、1モル以上2.5モル以下の化合物(14)及び1モル以上2.5モル以下の化合物(19)を添加することが好ましい。反応(R−10)の反応温度は80℃以上140℃以下であることが好ましい。反応(R−10)の反応時間は2時間以上10時間以下であることが好ましい。
反応(R−10)では、触媒としてパラジウム化合物を用いてもよい。パラジウム化合物は、配位子を含む構造であってもよい。反応(R−10)は、塩基の存在下で行われてもよい。反応(R−10)は、溶媒中で行われてもよい。反応(R−10)で使用される触媒、配位子、塩基及び溶媒の例は、反応(R−7)で使用される触媒、配位子、塩基及び溶媒の例と同様である。
なお、一般式(1−1)で表される基が一般式(1−2)で表される基と同一である化合物(1)を製造する場合、化合物(14)と化合物(19)とは同じ化合物になる。この場合、反応(R−10)では、1モル当量の化合物(6)と、2モル当量の化合物(14)又は化合物(19)とを反応させて、1モル当量の化合物(1)を得ればよい。化合物(14)を製造する工程及び化合物(19)を製造する工程の何れかを割愛することができる。
反応(R−10)で得られた反応生成物を、必要に応じて精製することにより、目的化合物である化合物(1)を単離することができる。精製方法としては、公知の方法が適宜採用される。精製は、例えば晶析又はシリカゲルクロマトグラフィーにより行われてもよい。精製に使用する溶媒として、例えば、クロロホルム及びヘキサンの混合溶媒を使用してもよい。
<第二実施形態:感光体>
第二実施形態は、感光体に関する。感光体は、積層型感光体であってもよく、単層型感光体であってもよい。感光体は、第一実施形態で述べた化合物(1)を含有する感光層を備える。
<1.積層型感光体>
以下、図3を参照して、感光体1が積層型感光体である場合の感光体1の構造について説明する。図3は、本実施形態に係る感光体1の一例である積層型感光体を示す概略断面図である。
図3(a)に示すように、感光体1としての積層型感光体は、例えば、導電性基体2と感光層3とを備える。積層型感光体には、感光層3として、電荷発生層3aと電荷輸送層3bとが備えられる。
図3(b)に示すように、感光体1としての積層型感光体では、導電性基体2上に電荷輸送層3bが設けられ、電荷輸送層3b上に電荷発生層3aが設けられてもよい。ただし、一般に電荷輸送層3bの膜厚は、電荷発生層3aの膜厚に比べ厚いため、電荷輸送層3bは、電荷発生層3aに比べ破損し難い。このため、積層型感光体の耐摩耗性を向上させるためには、図3(a)に示すように、導電性基体2上に電荷発生層3aが設けられ、電荷発生層3a上に電荷輸送層3bが設けられることが好ましい。
図3(c)に示すように、感光体1としての積層型感光体は、導電性基体2と感光層3と中間層(下引き層)4とを備えていてもよい。中間層4は、導電性基体2と感光層3との間に備えられる。また、感光層3上には、保護層5(図4参照)が設けられていてもよい。
電荷発生層3a及び電荷輸送層3bの厚さは、それぞれの層としての機能を十分に発現できる限り、特に限定されない。電荷発生層3aの厚さは、0.01μm以上5μm以下であることが好ましく、0.1μm以上3μm以下であることがより好ましい。電荷輸送層3bの厚さは、2μm以上100μm以下であることが好ましく、5μm以上50μm以下であることがより好ましい。
感光層3のうちの電荷発生層3aは、電荷発生剤を含有する。電荷発生層3aは、電荷発生層用バインダー樹脂(以下、ベース樹脂と記載することがある)を含有してもよい。電荷発生層3aは、必要に応じて、各種添加剤を含有してもよい。
感光層3のうちの電荷輸送層3bは、正孔輸送剤を含有する。電荷輸送層3bは、バインダー樹脂を含有してもよい。電荷輸送層3bは、必要に応じて、電子アクセプター化合物及び各種添加剤を含有してもよい。以上、図3を参照して、感光体1が積層型感光体である場合の感光体1の構造について説明した。
<2.単層型感光体>
以下、図4を参照して、感光体1が単層型感光体である場合の感光体1の構造について説明する。図4は、本実施形態に係る感光体1の別の例である単層型感光体を示す概略断面図である。
図4(a)に示すように、感光体1としての単層型感光体は、例えば、導電性基体2と感光層3とを備える。感光体1としての単層型感光体には、感光層3として、単層型感光層3cが備えられる。単層型感光層3cは、一層の感光層3である。
図4(b)に示すように、感光体1としての単層型感光体は、導電性基体2と、単層型感光層3cと、中間層(下引き層)4とを備えてもよい。中間層4は、導電性基体2と単層型感光層3cとの間に設けられる。また、図4(c)に示すように、単層型感光層3c上に保護層5が設けられてもよい。
単層型感光層3cの厚さは、単層型感光層としての機能を十分に発現できる限り、特に限定されない。単層型感光層3cの厚さは、5μm以上100μm以下であることが好ましく、10μm以上50μm以下であることがより好ましい。
感光層3としての単層型感光層3cは、電荷発生剤と正孔輸送剤とを一層に含有する。単層型感光層3cは、電子輸送剤及びバインダー樹脂のうちの一以上を更に含有してもよい。単層型感光層3cは、必要に応じて、各種添加剤を含有してもよい。感光体1が単層型感光体である場合、電荷発生剤と、正孔輸送剤と、必要に応じて添加される成分(例えば、電子輸送剤、バインダー樹脂又は添加剤)とは、一層の感光層3(単層型感光層3c)に含有される。以上、図4を参照して、感光体1が単層型感光体である場合の感光体1の構造について説明した。
次に、感光体である積層型感光体及び単層型感光体の要素について説明する。
<3.導電性基体>
導電性基体は、感光体の導電性基体として用いることができる限り、特に限定されない。導電性基体は、少なくとも表面部が導電性を有する材料で形成されていればよい。導電性基体の一例としては、導電性を有する材料で形成される導電性基体が挙げられる。導電性基体の別の例としては、導電性を有する材料で被覆される導電性基体が挙げられる。導電性を有する材料としては、例えば、アルミニウム、鉄、銅、錫、白金、銀、バナジウム、モリブデン、クロム、カドミウム、チタン、ニッケル、パラジウム、インジウム、ステンレス鋼又は真鍮が挙げられる。これらの導電性を有する材料を単独で用いてもよいし、2種以上を組み合わせて(例えば、合金として)用いてもよい。これらの導電性を有する材料のなかでも、感光層から導電性基体への電荷の移動が良好であることから、アルミニウム又はアルミニウム合金が好ましい。
導電性基体の形状は、画像形成装置の構造に合わせて適宜選択される。導電性基体の形状としては、例えば、シート状又はドラム状が挙げられる。また、導電性基体の厚さは、導電性基体の形状に応じて適宜選択される。
<4.正孔輸送剤>
感光層は、正孔輸送剤として、第一実施形態に係る化合物(1)を含有する。感光体が積層型感光体である場合、電荷輸送層は、正孔輸送剤として化合物(1)を含有する。感光体が単層型感光体である場合、単層型感光層は、正孔輸送剤として化合物(1)を含有する。感光層に化合物(1)が含有されることにより、第一実施形態で述べたように、感光体の電気特性を向上させることができる。
感光体が積層型感光体である場合、正孔輸送剤としての化合物(1)の含有量は、電荷輸送層に含有されるバインダー樹脂100質量部に対して、10質量部以上200質量部以下であることが好ましく、20質量部以上100質量部以下であることがより好ましい。
感光体が単層型感光体である場合、正孔輸送剤としての化合物(1)の含有量は、単層型感光層に含有されるバインダー樹脂100質量部に対して、10質量部以上200質量部以下であることが好ましく、10質量部以上100質量部以下であることがより好ましく、10質量部以上75質量部以下であることが特に好ましい。
電荷輸送層は、化合物(1)に加えて、更に別の正孔輸送剤を含有してもよい。別の正孔輸送剤としては、例えば、化合物(1)以外の含窒素環式化合物又は縮合多環式化合物を使用することができる。含窒素環式化合物及び縮合多環式化合物としては、例えば、のジアミン化合物(例えば、N,N,N’,N’−テトラフェニルフェニレンジアミン誘導体、N,N,N’,N’−テトラフェニルナフチレンジアミン誘導体又はN,N,N’,N’−テトラフェニルフェナントリレンジアミン誘導体)、オキサジアゾール系化合物(例えば、2,5−ジ(4−メチルアミノフェニル)−1,3,4−オキサジアゾール)、スチリル化合物(例えば、9−(4−ジエチルアミノスチリル)アントラセン)、カルバゾール化合物(例えば、ポリビニルカルバゾール)、有機ポリシラン化合物、ピラゾリン系化合物(例えば、1−フェニル−3−(p−ジメチルアミノフェニル)ピラゾリン)、ヒドラゾン系化合物、インドール系化合物、オキサゾール系化合物、イソオキサゾール系化合物、チアゾール系化合物、チアジアゾール系化合物、イミダゾール系化合物、ピラゾール系化合物又はトリアゾール系化合物が挙げられる。正孔輸送剤の合計質量に対する化合物(1)の含有量は、80質量%以上であることが好ましく、90質量%以上であることが好ましく、100質量%であることが特に好ましい。
<5.電荷発生剤>
感光体が積層型感光体である場合、電荷発生層は、電荷発生剤を含有する。感光体が単層型感光体である場合、単層型感光層は、電荷発生剤を含有する。
電荷発生剤は、感光体用の電荷発生剤である限り、特に限定されない。電荷発生剤としては、例えば、フタロシアニン系顔料、ペリレン系顔料、ビスアゾ顔料、トリスアゾ顔料、ジチオケトピロロピロール顔料、無金属ナフタロシアニン顔料、金属ナフタロシアニン顔料、スクアライン顔料、インジゴ顔料、アズレニウム顔料、シアニン顔料、無機光導電材料(例えば、セレン、セレン−テルル、セレン−ヒ素、硫化カドミウム又はアモルファスシリコン)の粉末、ピリリウム顔料、アンサンスロン系顔料、トリフェニルメタン系顔料、スレン系顔料、トルイジン系顔料、ピラゾリン系顔料又はキナクリドン系顔料が挙げられる。電荷発生剤は、1種を単独で用いてもよいし、2種以上を組み合わせて用いてもよい。
フタロシアニン系顔料としては、例えば、化学式(C−1)で表される無金属フタロシアニン又は金属フタロシアニンが挙げられる。金属フタロシアニンとしては、例えば、化学式(C−2)で表されるチタニルフタロシアニン、ヒドロキシガリウムフタロシアニン又はクロロガリウムフタロシアニンが挙げられる。フタロシアニン系顔料は、結晶であってもよく、非結晶であってもよい。フタロシアニン系顔料の結晶形状(例えば、α型、β型、Y型、V型又はII型)については特に限定されず、種々の結晶形状を有するフタロシアニン系顔料が使用される。
無金属フタロシアニンの結晶としては、例えば、無金属フタロシアニンのX型結晶(以下、X型無金属フタロシアニンと記載することがある)が挙げられる。チタニルフタロシアニンの結晶としては、例えば、チタニルフタロシアニンのα型、β型又はY型結晶(以下、α型、β型又はY型チタニルフタロシアニンと記載することがある)が挙げられる。ヒドロキシガリウムフタロシアニンの結晶としては、ヒドロキシガリウムフタロシアニンのV型結晶が挙げられる。クロロガリウムフタロシアニンの結晶としては、クロロガリウムフタロシアニンのII型結晶が挙げられる。
例えば、デジタル光学式の画像形成装置(例えば、半導体レーザーのような光源を使用した、レーザービームプリンター又はファクシミリ)には、700nm以上の波長領域に感度を有する感光体を用いることが好ましい。700nm以上の波長領域で高い量子収率を有することから、電荷発生剤としては、フタロシアニン系顔料が好ましく、無金属フタロシアニン又はチタニルフタロシアニンがより好ましく、X型無金属フタロシアニン又はY型チタニルフタロシアニンが更に好ましい。感光層に正孔輸送剤として化合物(1)が含有される場合に電気特性を特に向上させるためには、電荷発生剤としてはY型チタニルフタロシアニンがより好ましい。
Y型チタニルフタロシアニンは、CuKα特性X線回折スペクトルにおいて、例えば、ブラッグ角(2θ±0.2°)の27.2°に主ピークを有する。CuKα特性X線回折スペクトルにおける主ピークとは、ブラッグ角(2θ±0.2°)が3°以上40°以下である範囲において、1番目又は2番目に大きな強度を有するピークである。
CuKα特性X線回折スペクトルの測定方法の一例について説明する。試料(チタニルフタロシアニン)をX線回折装置(例えば、株式会社リガク製「RINT(登録商標)1100」)のサンプルホルダーに充填して、X線管球Cu、管電圧40kV、管電流30mA、かつCuKα特性X線の波長1.542Åの条件で、X線回折スペクトルを測定する。測定範囲(2θ)は、例えば3°以上40°以下(スタート角3°、ストップ角40°)であり、走査速度は、例えば10°/分である。
短波長レーザー光源(例えば、350nm以上550nm以下の波長を有するレーザー光源)を用いた画像形成装置に適用される感光体には、電荷発生剤として、アンサンスロン系顔料が好適に用いられる。
感光体が積層型感光体である場合、電荷発生剤の含有量は、電荷発生層に含有されるベース樹脂100質量部に対して、5質量部以上1000質量部以下であることが好ましく、30質量部以上500質量部以下であることがより好ましい。
感光体が単層型感光体である場合、電荷発生剤の含有量は、単層型感光層に含有されるバインダー樹脂100質量部に対して、0.1質量部以上50質量部以下であることが好ましく、0.5質量部以上30質量部以下であることがより好ましく、0.5質量部以上4.5質量部以下であることが特に好ましい。
<6.電子輸送剤及び電子アクセプター化合物>
感光体が積層型感光体である場合、電荷輸送層は、必要に応じて、電子アクセプター化合物を含有してもよい。これにより、正孔輸送剤の正孔輸送能が向上する傾向がある。一方、感光体が単層型感光体である場合、単層型感光層は、必要に応じて、電子輸送剤を含有してもよい。これにより、単層型感光層は電子を輸送することができ、単層型感光層にバイポーラー(両極性)の特性を付与し易くなる。
電子輸送剤又は電子アクセプター化合物の例としては、キノン系化合物、ジイミド系化合物、ヒドラゾン系化合物、マロノニトリル系化合物、チオピラン系化合物、トリニトロチオキサントン系化合物、3,4,5,7−テトラニトロ−9−フルオレノン系化合物、ジニトロアントラセン系化合物、ジニトロアクリジン系化合物、テトラシアノエチレン、2,4,8−トリニトロチオキサントン、ジニトロベンゼン、ジニトロアクリジン、無水コハク酸、無水マレイン酸又はジブロモ無水マレイン酸が挙げられる。キノン系化合物としては、例えば、ジフェノキノン系化合物、アゾキノン系化合物、アントラキノン系化合物、ナフトキノン系化合物、ニトロアントラキノン系化合物又はジニトロアントラキノン系化合物が挙げられる。電子輸送剤は、1種単独で用いてもよいし、2種以上を組み合わせて用いてもよい。電子アクセプター化合物も、1種単独で用いてもよいし、2種以上を組み合わせて用いてもよい。
電子輸送剤又は電子アクセプターとしては、例えば、一般式(20)又は(21)で表される化合物が挙げられる。
一般式(20)及び(21)中、R20〜R25は、各々独立して、水素原子、シアノ基、置換基を有してもよいアルキル基、置換基を有してもよいアルケニル基、置換基を有してもよいアルコキシ基、置換基を有してもよいアルコキシカルボニル基、置換基を有してもよいアリール基又は置換基を有してもよい複素環基を表す。
一般式(20)及び(21)中のR20〜R25で表されるアルキル基は、例えば、炭素原子数1以上6以下のアルキル基である。炭素原子数1以上6以下のアルキル基としては、炭素原子数1以上5以下のアルキル基が好ましく、メチル基、tert−ブチル基又は1,1−ジメチルプロピル基がより好ましい。アルキル基は置換基を有してもよい。置換基としては、例えば、ハロゲン原子、ヒドロキシル基、炭素原子数1以上6以下のアルコキシ基、置換基を更に有してもよい炭素原子数6以上14以下のアリール基又はシアノ基が挙げられる。置換基の数は、特に限定されないが、3個以下であることが好ましい。置換基としての炭素原子数6以上14以下のアリール基が更に有する置換基としては、例えば、ハロゲン原子、ヒドロキシル基、炭素原子数1以上6以下のアルキル基、炭素原子数1以上6以下のアルコキシ基、ニトロ基、シアノ基、炭素原子数2以上7以下のアルカノイル基(カルボニル基に炭素原子数1以上6以下のアルキル基が結合した基)、ベンゾイル基、フェノキシ基、炭素原子数2以上7以下のアルコキシカルボニル基(カルボニル基に炭素原子数1以上6以下のアルコキシ基が結合した基)又はフェノキシカルボニル基が挙げられる。
一般式(20)及び(21)中のR20〜R25で表されるアルケニル基は、例えば、直鎖状又は分枝鎖状で非置換の炭素原子数2以上6以下のアルケニル基である。炭素原子数2以上6以下のアルケニル基は、例えば、1個以上3個以下の二重結合を有する。炭素原子数2以上6以下のアルケニル基の例としては、ビニル基、プロペニル基、ブテニル基、ペンテニル基、ペンタジエニル基、ヘキセニル基又はヘキサジエニル基が挙げられる。アルケニル基は置換基を有してもよい。置換基としては、例えば、ハロゲン原子、ヒドロキシル基、炭素原子数1以上6以下のアルコキシ基、炭素原子数6以上14以下のアリール基又はシアノ基が挙げられる。置換基の数は、特に限定されないが、3個以下であることが好ましい。
一般式(20)及び(21)中のR20〜R25で表されるアルコキシ基は、例えば、炭素原子数1以上6以下のアルコキシ基である。炭素原子数1以上6以下のアルコキシ基としては、炭素原子数1以上3以下のアルコキシ基が好ましく、メトキシ基がより好ましい。アルコキシ基は置換基を有してもよい。置換基としては、例えば、ハロゲン原子、ヒドロキシル基、炭素原子数1以上6以下のアルコキシ基、炭素原子数6以上14以下のアリール基又はシアノ基が挙げられる。置換基として好ましくは、フェニル基である。置換基の数は、特に限定されないが、3個以下であることが好ましく、1個であることがより好ましい。
一般式(20)及び(21)中のR20〜R25で表されるアルコキシカルボニル基は、例えば、炭素原子数2以上7以下のアルコキシカルボニル基である。炭素原子数2以上7以下のアルコキシカルボニル基は、カルボニル基に直鎖状又は分枝鎖状で非置換の炭素原子数1以上6以下のアルコキシ基が結合した基である。アルコキシカルボニル基は置換基を有してもよい。置換基としては、例えば、ハロゲン原子、ヒドロキシル基、炭素原子数1以上6以下のアルコキシ基、炭素原子数6以上14以下のアリール基又はシアノ基が挙げられる。置換基の数は、特に限定されないが、3個以下であることが好ましい。
一般式(20)及び(21)中のR20〜R25で表されるアリール基は、例えば、炭素原子数6以上14以下のアリール基である。炭素原子数6以上14以下のアリール基としては、フェニル基が好ましい。アリール基は置換基を有してもよい。置換基としては、例えば、ハロゲン原子、ヒドロキシル基、炭素原子数1以上6以下のアルキル基、炭素原子数1以上6以下のアルコキシ基、ニトロ基、シアノ基、炭素原子数2以上7以下のアルカノイル基(カルボニル基に炭素原子数1以上6以下のアルキル基が結合した基)、ベンゾイル基、フェノキシ基、炭素原子数2以上7以下のアルコキシカルボニル基(カルボニル基に炭素原子数1以上6以下のアルコキシ基が結合した基)、フェノキシカルボニル基、炭素原子数6以上14以下のアリール基又はビフェニル基が挙げられる。置換基の数は、特に限定されないが、3個以下であることが好ましい。
一般式(20)及び(21)中のR20〜R25で表される複素環基は、例えば、N、S及びOからなる群より選択される1以上のヘテロ原子を含む5員又は6員の単環の複素環基;このような単環同士が縮合した複素環基;又は、このような単環と、5員又は6員の炭化水素環とが縮合した複素環基である。複素環基が縮合環である場合、縮合環に含まれる環の数は2個又は3個であることが好ましい。複素環基が有してもよい置換基としては、例えば、ハロゲン原子、ヒドロキシル基、炭素原子数1以上6以下のアルキル基、炭素原子数1以上6以下のアルコキシ基、ニトロ基、シアノ基、炭素原子数2以上7以下のアルカノイル基(カルボニル基に炭素原子数1以上6以下のアルキル基が結合した基)、ベンゾイル基、フェノキシ基、炭素原子数2以上7以下のアルコキシカルボニル基(カルボニル基に炭素原子数1以上6以下のアルコキシ基が結合した基)又はフェノキシカルボニル基が挙げられる。置換基の数は、特に限定されないが、3個以下であることが好ましい。
一般式(20)で表される化合物の具体例としては、化学式(E−1)で表される化合物が挙げられる。一般式(21)で表される化合物の具体例としては、化学式(E−2)で表される化合物が挙げられる。以下、化学式(E−1)及び(E−2)で表される化合物を各々、化合物(E−1)及び(E−2)と記載することがある。
感光体が積層型感光体である場合、電子アクセプター化合物の含有量は、電荷輸送層に含有されるバインダー樹脂100質量部に対して、0.1質量部以上20質量部以下であることが好ましく、0.5質量部以上10質量部以下であることがより好ましい。
感光体が単層型感光体である場合、電子輸送剤の含有量は、単層型感光層に含有されるバインダー樹脂100質量部に対して、5質量部以上100質量部以下であることが好ましく、10質量部以上80質量部以下であることがより好ましく、30質量部以上50質量部以下であることが特に好ましい。
<7.バインダー樹脂>
感光体が積層型感光体である場合、電荷輸送層は、バインダー樹脂を含有する。感光体が単層型感光体である場合、単層型感光層は、バインダー樹脂を含有する。
バインダー樹脂としては、例えば、熱可塑性樹脂、熱硬化性樹脂又は光硬化性樹脂が挙げられる。熱可塑性樹脂としては、例えば、ポリカーボネート樹脂、ポリアリレート樹脂、スチレン−ブタジエン共重合体、スチレン−アクリロニトリル共重合体、スチレン−マレイン酸共重合体、アクリル酸重合体、スチレン−アクリル酸共重合体、ポリエチレン樹脂、エチレン−酢酸ビニル共重合体、塩素化ポリエチレン樹脂、ポリ塩化ビニル樹脂、ポリプロピレン樹脂、アイオノマー樹脂、塩化ビニル−酢酸ビニル共重合体、アルキド樹脂、ポリアミド樹脂、ウレタン樹脂、ポリスルホン樹脂、ジアリルフタレート樹脂、ケトン樹脂、ポリビニルブチラール樹脂、ポリエステル樹脂又はポリエーテル樹脂が挙げられる。熱硬化性樹脂としては、例えば、シリコーン樹脂、エポキシ樹脂、フェノール樹脂、尿素樹脂又はメラミン樹脂が挙げられる。光硬化性樹脂としては、例えば、エポキシアクリレート(エポキシ化合物のアクリル酸付加物)又はウレタン−アクリレート(ウレタン化合物のアクリル酸付加物)が挙げられる。これらのバインダー樹脂は、1種を単独で使用してもよく、2種以上を組み合わせて使用してもよい。
これらの樹脂の中では、加工性、機械的特性、光学的特性及び耐摩耗性のバランスに優れた単層型感光層及び電荷輸送層が得られることから、ポリカーボネート樹脂が好ましい。ポリカーボネート樹脂の例としては、下記化学式で表されるビスフェノールZ型ポリカーボネート樹脂、ビスフェノールZC型ポリカーボネート樹脂、ビスフェノールC型ポリカーボネート樹脂又はビスフェノールA型ポリカーボネート樹脂が挙げられる。
バインダー樹脂の粘度平均分子量は、40,000以上であることが好ましく、40,000以上52,500以下であることがより好ましい。バインダー樹脂の粘度平均分子量が40,000以上であると、感光体の耐摩耗性を向上させ易い。バインダー樹脂の粘度平均分子量が52,500以下であると、感光層の形成時にバインダー樹脂が溶剤に溶解し易くなり、電荷輸送層用塗布液又は単層型感光層用塗布液の粘度が高くなり過ぎない。その結果、電荷輸送層又は単層型感光層を形成し易くなる。
<8.ベース樹脂>
感光体が積層型感光体である場合、電荷発生層は、ベース樹脂を含有する。ベース樹脂は、感光体に適用できるベース樹脂である限り、特に制限されない。ベース樹脂としては、熱可塑性樹脂、熱硬化性樹脂又は光硬化性樹脂が挙げられる。熱可塑性樹脂としては、例えば、スチレン−ブタジエン共重合体、スチレン−アクリロニトリル共重合体、スチレン−マレイン酸共重合体、スチレン−アクリル酸共重合体、アクリル酸重合体、ポリエチレン樹脂、エチレン−酢酸ビニル共重合体、塩素化ポリエチレン樹脂、ポリ塩化ビニル樹脂、ポリプロピレン樹脂、アイオノマー、塩化ビニル−酢酸ビニル共重合体、アルキド樹脂、ポリアミド樹脂、ウレタン樹脂、ポリカーボネート樹脂、ポリアリレート樹脂、ポリスルホン樹脂、ジアリルフタレート樹脂、ケトン樹脂、ポリビニルブチラール樹脂、ポリエーテル樹脂又はポリエステル樹脂が挙げられる。熱硬化性樹脂としては、例えば、シリコーン樹脂、エポキシ樹脂、フェノール樹脂、尿素樹脂、メラミン樹脂又はその他架橋性の熱硬化性樹脂が挙げられる。光硬化性樹脂としては、例えば、エポキシアクリレート(エポキシ化合物のアクリル酸付加物)又はウレタン−アクリレート(ウレタン化合物のアクリル酸付加物)が挙げられる。ベース樹脂は1種を単独で使用してもよいし、2種以上を組み合わせて使用してもよい。
電荷発生層に含有されるベース樹脂は、電荷輸送層に含有されるバインダー樹脂とは異なることが好ましい。積層型感光体の製造では、例えば、導電性基体上に電荷発生層が形成され、電荷発生層上に電荷輸送層が形成される。その際に、電荷発生層上に、電荷輸送層用塗布液が塗布される。そのため、電荷発生層は、電荷輸送層用塗布液の溶剤に溶解しないことが好ましいからである。
<9.添加剤>
感光体の感光層(電荷発生層、電荷輸送層又は単層型感光層)は、必要に応じて、各種の添加剤を含有してもよい。添加剤としては、例えば、劣化防止剤(例えば、酸化防止剤、ラジカル捕捉剤、1重項消光剤又は紫外線吸収剤)、軟化剤、表面改質剤、増量剤、増粘剤、分散安定剤、ワックス、アクセプター、ドナー、界面活性剤、可塑剤、増感剤又はレベリング剤が挙げられる。酸化防止剤としては、例えば、ヒンダードフェノール(例えば、ジ(tert−ブチル)p−クレゾール)、ヒンダードアミン、パラフェニレンジアミン、アリールアルカン、ハイドロキノン、スピロクロマン、スピロインダノン若しくはこれらの誘導体、有機硫黄化合物又は有機燐化合物が挙げられる。
<10.中間層>
中間層(下引き層)は、例えば、無機粒子及び中間層に用いられる樹脂(中間層用樹脂)を含有する。中間層が存在することにより、リーク発生を抑制し得る程度の絶縁状態を維持しつつ、感光体を露光した時に発生する電流の流れを円滑にして、抵抗の上昇が抑えられると考えられる。
無機粒子としては、例えば、金属(例えば、アルミニウム、鉄又は銅)、金属酸化物(例えば、酸化チタン、アルミナ、酸化ジルコニウム、酸化スズ又は酸化亜鉛)の粒子又は非金属酸化物(例えば、シリカ)の粒子が挙げられる。これらの無機粒子は、1種を単独で用いてもよいし、2種以上を併用してもよい。
中間層用樹脂としては、中間層を形成する樹脂として用いることができる限り、特に限定されない。中間層は、各種の添加剤を含有してもよい。添加剤は、感光層の添加剤と同様である。
<11.感光体の製造方法>
感光体が積層型感光体である場合、積層型感光体は、例えば、以下のように製造される。まず、電荷発生層用塗布液及び電荷輸送層用塗布液を調製する。電荷発生層用塗布液を導電性基体上に塗布し、乾燥することによって、電荷発生層を形成する。続いて、電荷輸送層用塗布液を電荷発生層上に塗布し、乾燥することによって、電荷輸送層を形成する。これにより、積層型感光体が製造される。
電荷発生層用塗布液は、電荷発生剤及び必要に応じて添加される成分(例えば、ベース樹脂及び各種の添加剤)を、溶剤に溶解又は分散させることにより調製される。電荷輸送層用塗布液は、正孔輸送剤及び必要に応じて添加される成分(例えば、バインダー樹脂、電子アクセプター化合物及び各種添加剤)を、溶剤に溶解又は分散させることにより調製される。
次に、感光体が単層型感光体である場合、単層型感光体は、例えば、以下のように製造される。単層型感光体は、単層型感光層用塗布液を導電性基体上に塗布し、乾燥することによって製造される。単層型感光層用塗布液は、電荷発生剤、正孔輸送剤及び必要に応じて添加される成分(例えば、電子輸送剤、バインダー樹脂及び各種添加剤)を、溶剤に溶解又は分散させることにより製造される。
塗布液(電荷発生層用塗布液、電荷輸送層用塗布液又は単層型感光層用塗布液)に含有される溶剤は、塗布液に含まれる各成分を溶解又は分散できる限り、特に限定されない。溶剤の例としては、アルコール類(例えば、メタノール、エタノール、イソプロパノール又はブタノール)、脂肪族炭化水素(例えば、n−ヘキサン、オクタン又はシクロヘキサン)、芳香族炭化水素(例えば、ベンゼン、トルエン又はキシレン)、ハロゲン化炭化水素(例えば、ジクロロメタン、ジクロロエタン、四塩化炭素又はクロロベンゼン)、エーテル類(例えば、ジメチルエーテル、ジエチルエーテル、テトラヒドロフラン、エチレングリコールジメチルエーテル、ジエチレングリコールジメチルエーテル又はプロピレングリコールモノメチルエーテル)、ケトン類(例えば、アセトン、メチルエチルケトン又はシクロヘキサノン)、エステル類(例えば、酢酸エチル又は酢酸メチル)、ジメチルホルムアルデヒド、ジメチルホルムアミド又はジメチルスルホキシドが挙げられる。これらの溶剤は、1種単独で又は2種以上を組み合わせて用いられる。感光体の製造時の作業性を向上させるためには、溶剤として非ハロゲン溶剤(ハロゲン化炭化水素以外の溶剤)を用いることが好ましい。
塗布液は、各成分を混合し、溶剤に分散することにより調製される。混合又は分散には、例えば、ビーズミル、ロールミル、ボールミル、アトライター、ペイントシェーカー又は超音波分散機を用いることができる。
塗布液(電荷発生層用塗布液、電荷輸送層用塗布液又は単層型感光層用塗布液)は、各成分の分散性を向上させるために、例えば、界面活性剤を含有してもよい。
塗布液(電荷発生層用塗布液、電荷輸送層用塗布液又は単層型感光層用塗布液)を塗布する方法としては、塗布液を導電性基体上に均一に塗布できる方法である限り、特に限定されない。塗布方法としては、例えば、ディップコート法、スプレーコート法、スピンコート法又はバーコート法が挙げられる。
塗布液(電荷発生層用塗布液、電荷輸送層用塗布液又は単層型感光層用塗布液)を乾燥する方法としては、塗布液中の溶剤を蒸発させ得る限り、特に限定されない。例えば、高温乾燥機又は減圧乾燥機を用いて、熱処理(熱風乾燥)する方法が挙げられる。熱処理条件は、例えば、40℃以上150℃以下の温度、かつ3分間以上120分間以下の時間である。
なお、感光体の製造方法は、必要に応じて、中間層を形成する工程及び保護層を形成する工程の一方又は両方を更に含んでもよい。中間層を形成する工程及び保護層を形成する工程では、公知の方法が適宜選択される。
以下、実施例を用いて本発明を更に具体的に説明する。しかし、本発明は実施例の範囲に何ら限定されない。
<1.感光体の材料>
積層型感光体の電荷発生層及び電荷輸送層を形成するための材料として、以下の正孔輸送剤及び電荷発生剤を準備した。単層型感光体の単層型感光層を形成するための材料として、以下の正孔輸送剤、電荷発生剤及び電子輸送剤を準備した。
<1−1.正孔輸送剤>
正孔輸送剤として、第一実施形態で述べた化合物(H−1)〜(H−5)を準備した。化合物(H−1)〜(H−5)は、各々以下の方法で製造した。
<1−1−1.化合物(6a)〜(6c)の製造>
まず、化合物(H−1)〜(H−5)を製造するための原料として、化合物(6a)〜(6c)を製造した。下記反応(R−11)及び(R−12)に従って、化合物(6c)を製造した。下記反応(R−11)及び(R−13)に従って、化合物(6a)を製造した。下記反応(R−14)及び(R−15)に従って、化合物(6b)を製造した。
反応(R−11)では、化合物(2a)と亜リン酸トリエチルとを反応させて、化合物(3a)を得た。詳しくは、容量200mLのフラスコに、化合物(2a)16.1g(0.10モル)と、亜リン酸トリエチル25.0g(0.15モル)とを投入した。フラスコ内容物を、180℃で8時間攪拌した後、室温まで冷却した。続いて、フラスコ内容物に含まれる未反応の亜リン酸トリエチルを減圧留去した。これにより、白色液体である化合物(3a)を得た。化合物(3a)の収量は24.1gであり、化合物(2a)からの化合物(3a)の収率は92mol%であった。
反応(R−12)では、化合物(3a)と化合物(4a)とを反応させて化合物(6c)を得た。反応(R−12)は、ウィッティヒ(Wittig)反応である。詳しくは、反応(R−11)で得られた化合物(3a)13.1g(0.05モル)を、容量500mLの二口フラスコに0℃で加えた。フラスコ内の空気を、アルゴンガスで置換した。続いて、フラスコ内に、乾燥テトラヒドロフラン(100mL)及び28%ナトリウムメトキシド9.3g(0.05モル)を添加した。フラスコ内容物を30分間攪拌した。続いて、フラスコ内に、化合物(4a)7.0g(0.05モル)の乾燥テトラヒドロフラン(300mL)溶液を添加した。フラスコ内容物を、室温で12時間攪拌した。フラスコ内容物を、イオン交換水に注ぎ、トルエンで抽出した。得られた有機層を、イオン交換水で5回洗浄し、無水硫酸ナトリウムを用いて乾燥させた。続いて、有機層に含有される溶媒を留去し、残渣を得た。得られた残渣を、トルエン/メタノール(20mL/100mL)を用いて晶析した。これにより、化合物(6c)を得た。化合物(6c)の収量は9.4gであり、化合物(3a)からの化合物(6c)の収率は75mol%であった。
反応(R−13)では、化合物(3a)と化合物(5a)とを反応させて化合物(6a)を得た。反応(R−13)は、ウィッティヒ(Wittig)反応である。詳しくは、反応(R−11)で得られた化合物(3a)13.1g(0.05モル)を、容量500mLの二口フラスコに0℃で加えた。フラスコ内の空気を、アルゴンガスで置換した。続いて、フラスコ内に、乾燥テトラヒドロフラン(100mL)及び28%ナトリウムメトキシド9.3g(0.05モル)を添加した。フラスコ内容物を30分間攪拌した。続いて、フラスコ内に、化合物(5a)8.4g(0.05モル)の乾燥テトラヒドロフラン(300mL)溶液を添加した。フラスコ内容物を、室温で12時間攪拌した。フラスコ内容物を、イオン交換水に注ぎ、トルエンで抽出した。得られた有機層を、イオン交換水で5回洗浄し、無水硫酸ナトリウムを用いて乾燥させた。続いて、有機層に含有される溶媒を留去し、残渣を得た。得られた残渣を、トルエン/メタノール(20mL/100mL)を用いて晶析した。これにより、白色結晶である化合物(6a)を得た。化合物(6a)の収量は9.6gであり、化合物(3a)からの化合物(6a)の収率は69mol%であった。
反応(R−14)では、化合物(7a)と亜リン酸トリエチルとを反応させて、化合物(8)を得た。詳しくは、容量200mLのフラスコに、化合物(7a)15.2g(0.05モル)と、亜リン酸トリエチル25.0g(0.15モル)とを投入した。フラスコ内容物を、180℃で8時間攪拌した後、室温まで冷却した。続いて、フラスコ内容物に含まれる未反応の亜リン酸トリエチルを減圧留去した。これにより、化合物(8)を得た。化合物(8)の収量は14.5gであり、化合物(7a)からの化合物(8)の収率は88mol%であった。
反応(R−15)では、化合物(8)と化合物(4a)とを反応させて化合物(6b)を得た。反応(R−15)は、ウィッティヒ(Wittig)反応である。詳しくは、反応(R−14)で得られた化合物(8)16.4g(0.05モル)を、容量500mLの二口フラスコに0℃で加えた。フラスコ内の空気を、アルゴンガスで置換した。続いて、フラスコ内に、乾燥テトラヒドロフラン(100mL)及び28%ナトリウムメトキシド9.3g(0.05モル)を添加した。フラスコ内容物を30分間攪拌した。続いて、フラスコ内に、化合物(4a)14.1g(0.10モル)の乾燥テトラヒドロフラン(300mL)溶液を添加した。フラスコ内容物を、室温で12時間攪拌した。フラスコ内容物を、イオン交換水に注ぎ、トルエンで抽出した。得られた有機層を、イオン交換水で5回洗浄し、無水硫酸ナトリウムを用いて乾燥させた。続いて、有機層に含有される溶媒を留去し、残渣を得た。得られた残渣を、トルエン/メタノール(20mL/100mL)を用いて晶析した。これにより、化合物(6b)を得た。化合物(6b)の収量は3.8gであり、化合物(8)からの化合物(6b)の収率は25mol%であった。
<1−1−2.化合物(12a)及び(12b)の製造>
次に、化合物(14a)〜(14e)を製造するための原料として、化合物(12a)及び(12b)を製造した。下記反応(R−16)に従って、化合物(12a)を製造した。下記反応(R−17)に従って、化合物(12b)を製造した。
反応(R−16)では、化合物(10a)と化合物(11a)とを反応させて化合物(12a)を得た。詳しくは、ディーン・スターク管に、化合物(10a)6.3g(0.0450モル)、化合物(11a、ジフェニルヒドラジン塩酸塩)10.0g(0.0450モル)、トルエン(100mL)及びp−トルエンスルホン酸(0.0045モル)を加えた。混合物を、100℃で4時間還流しながら攪拌した。得られた混合物を、イオン交換水に注ぎ、トルエンで抽出した。得られた有機層を、イオン交換水で5回洗浄し、無水硫酸ナトリウムで乾燥した後、溶媒を留去した。得られた残渣を、トルエン/メタノール(体積比1:1)で晶析し、白色結晶である化合物(12a)を得た。化合物(12a)の収量は12.1gであり、化合物(10a)からの化合物(12a)の収率は88mol%であった。
反応(R−17)では、化合物(10b)と化合物(11a)とを反応させて化合物(12b)を得た。反応(R−17)は、化合物(10a)6.3g(0.0450モル)の代わりに化合物(10b)7.5g(0.0450モル)を使用した以外は、反応(R−16)と同様の方法で行った。その結果、化合物(12b)が得られた。化合物(12b)の収量は11.8gであり、化合物(10b)からの化合物(12b)の収率は79mol%であった。
<1−1−3.化合物(14a)〜(14e)の製造>
次に、下記反応(R−18)に従って、化合物(14a)を製造した。
反応(R−18)では、化合物(12a)と化合物(13a)とを反応させて化合物(14a)を得た。以下、化合物(12a)を反応(R−18)の第一原料と、化合物(13a)を反応(R−18)の第二原料と記載することがある。反応(R−18)は、カップリング反応である。詳しくは、三口フラスコに、化合物(12a)6.1g(0.020モル)、トリシクロヘキシルホスフィン0.0662g(1.89×10-4モル)、トリス(ジベンジリデンアセトン)ジパラジウム(0)0.0864g(9.44×10-5モル)、ナトリウムtert−ブトキシド4.0g(0.042モル)、化合物(13a)2.1g(0.020モル)及び蒸留したо−キシレン(500mL)を投入した。フラスコ内の空気をアルゴンガスで置換した。続いて、フラスコ内容物を120℃で5時間攪拌した後、室温まで冷却した。フラスコ内容物をイオン交換水で3回洗浄し、有機層を得た。有機層に無水硫酸ナトリウムと活性白土とを加え、乾燥処理及び吸着処理を行った。乾燥処理及び吸着処理後の有機層を減圧留去し、о−キシレンを除去した。これにより、残渣を得た。得られた残渣を、クロロホルム/ヘキサン(体積比1:1)を用いて晶析した。これにより、反応(R−18)の反応生成物として化合物(14a)が得られた。化合物(14a)の収量は5.1gであり、化合物(12a)からの化合物(14a)の収率は69mol%であった。
以下の点を変更した以外は、化合物(14a)の製造と同様の方法で、化合物(14b)〜(14e)を各々製造した。なお、化合物(14b)〜(14e)の製造において使用される各原料は、化合物(14a)の製造において使用される対応する原料のモル数と同じモル数で添加した。
反応(R−18)の第一原料を、化合物(H−1)の製造における化合物(12a)から、表1に示す第一原料(化合物(12a)又は(12b))に変更した。反応(R−18)の第二原料を、化合物(H−1)の製造における化合物(13a)から、表1に示す第二原料(化合物(13b)、(13c)、(13d)又は(13e))に変更した。その結果、反応(R−18)の反応生成物として、化合物(14a)の代わりに、化合物(14b)、(14c)、(14d)及び(14e)の何れかが得られた。反応(R−18)で得られた化合物(14b)、(14c)、(14d)及び(14e)の収量を表1に示す。また、第一原料(化合物(12a)又は(12b))からの化合物(14b)、(14c)、(14d)及び(14e)の収率を表1に示す。
表1中、化合物(12a)及び(12b)、(13a)〜(13e)、並びに(14a)〜(14e)は、各々、下記化学式(12a)及び(12b)、(13a)〜(13e)、並びに(14a)〜(14e)で表される。
<1−1−4.化合物(H−1)〜(H−5)の製造>
次に、下記反応(R−19)に従って、化合物(H−1)を製造した。
反応(R−19)では、化合物(6a)と化合物(14a)とを反応させて化合物(H−1)を得た。以下、化合物(6a)を反応(R−19)の第一原料と、化合物(14a)を反応(R−19)の第二原料と記載することがある。反応(R−19)は、カップリング反応である。詳しくは、三口フラスコに、反応(R−13)で得られた化合物(6a)1.40g(0.005モル)、トリシクロヘキシルホスフィン0.0356g(1.02×10-4モル)、トリス(ジベンジリデンアセトン)ジパラジウム(0)0.0465g(5.09×10-5モル)、ナトリウムtert−ブトキシド1.00g(0.010モル)、反応(R−18)で得られた化合物(14a)3.60g(0.010モル)及び蒸留したо−キシレン(200mL)を投入した。フラスコ内の空気をアルゴンガスで置換した。続いて、フラスコ内容物を120℃で5時間攪拌した後、室温まで冷却した。フラスコ内容物をイオン交換水で3回洗浄し、有機層を得た。有機層に無水硫酸ナトリウムと活性白土とを加え、乾燥処理及び吸着処理を行った。乾燥処理及び吸着処理後の有機層を減圧留去し、о−キシレンを除去した。これにより、残渣を得た。得られた残渣を、クロロホルム/ヘキサン(体積比1:1)を用いて晶析した。その結果、化合物(H−1)が得られた。化合物(H−1)の収量は3.2gであり、化合物(6a)からの化合物(H−1)の収率は66mol%であった。
以下の点を変更した以外は、化合物(H−1)の製造と同様の方法で、化合物(H−2)〜(H−5)を各々製造した。なお、化合物(H−2)〜(H−5)の製造において使用される各原料は、化合物(H−1)の製造において使用される対応する原料のモル数と同じモル数で添加した。
反応(R−19)の第一原料を、化合物(H−1)の製造における化合物(6a)から、表2に示す第一原料(化合物(6a)、(6b)又は(6c))に変更した。反応(R−19)の第二原料を、化合物(H−1)の製造における化合物(14a)から、表1に示す第二原料(化合物(14b)、(14c)、(14d)又は(14e))に変更した。その結果、反応(R−19)の反応生成物として、化合物(H−1)の代わりに、化合物(H−2)、(H−3)、(H−4)及び(H−5)の何れかが得られた。反応(R−19)で得られた化合物(H−2)、(H−3)、(H−4)及び(H−5)の収量を表2に示す。また、第一原料(化合物(6a)、(6b)又は(6c))からの化合物(H−2)、(H−3)、(H−4)及び(H−5)の収率を表2に示す。
次に、1H−NMR(プロトン核磁気共鳴分光計)を用いて、製造した化合物(H−1)〜(H−5)の1H−NMRスペクトルを測定した。磁場強度は300MHzに設定した。溶媒として、重水素化クロロホルム(CDCl3)を使用した。内部標準物質としてテトラメチルシラン(TMS)を使用した。
化合物(H−1)〜(H−5)のうちの代表例として、化合物(H−2)及び(H−4)の1H−NMRスペクトルを、図1及び図2に示す。化合物(H−2)及び(H−4)の1H−NMRスペクトルの化学シフト値を以下に示す。なお、図1及び図2中の1.50ppm付近のピークは、化合物(H−2)及び(H−4)に残る水に由来するピークである。
化合物(H−2):1H−NMR(300MHz,CDCl3)δ=7.35−7.42(m,8H),7.11−7.25(m,22H),6.83−7.06(m,16H),6.72−6.80(m,4H),6.41(d,2H),3.80(s,6H),2.01(s,6H).
化合物(H−4):1H−NMR(300MHz,CDCl3)δ=7.35−7.42(m,8H),7.11−7.24(m,20H),6.82−7.06(m,20H),6.41(d,2H),2.33(s,6H),1.99(s,6H).
1H−NMRスペクトル及び化学シフト値により、化合物(H−2)及び(H−4)が各々得られていることを確認した。他の化合物(H−1)、(H−3)及び(H−5)も同様にして、1H−NMRスペクトル及び化学シフト値により、それぞれ化合物(H−1)、(H−3)及び(H−5)が得られていることを確認した。
<1−1−5.化合物(H−A)及び(H−B)の準備>
正孔輸送剤として、下記化学式(H−A)及び(H−B)で表される化合物も準備した。以下、化学式(H−A)及び(H−B)で表される化合物を各々、化合物(H−A)及び(H−B)と記載することがある。
<1−2.電荷発生剤>
電荷発生剤として、化合物(C−1X)及び(C−2Y)を準備した。化合物(C−1X)は、第二実施形態で述べた化学式(C−1)で表される無金属フタロシアニンであった。また、化合物(C−1X)の結晶構造はX型であった。
化合物(C−2Y)は、第二実施形態で述べた化学式(C−2)で表されるチタニルフタロシアニンであった。また、化合物(C−2Y)の結晶構造はY型であった。
<1−3.電子輸送剤>
単層型感光体の単層型感光層に含有させる電子輸送剤として、第二実施形態で述べた化合物(E−1)及び(E−2)を準備した。
<2.積層型感光体の製造>
上述した感光層を形成するための材料を用いて、積層型感光体(P−1)〜(P−7)を製造した。
<2−1.積層型感光体(P−1)の製造>
表面処理された酸化チタン(テイカ株式会社製「試作品SMT−02」、数平均一次粒子径10nm)を準備した。詳しくは、アルミナとシリカとを用いて酸化チタンを表面処理し、表面処理された酸化チタンを湿式分散しながらメチルハイドロジェンポリシロキサンを用いて更に表面処理したものを準備した。
次に、下引き層用塗布液を調製した。具体的には、容器内に、表面処理された酸化チタン2.8質量部、共重合ポリアミド樹脂(ダイセル・エボニック株式会社製「ダイアミドX4685」)1質量部、溶剤としてのエタノール10質量部及び溶剤としてのブタノール2質量部を投入した。容器の内容物を、ビーズミルを用いて5時間混合し、溶剤中に材料を分散させた。これにより、下引き層用塗布液を得た。
次に、下引き層を形成した。具体的には、得られた下引き層用塗布液を5μmのフィルターを用いてろ過した。その後、下引き層用塗布液を、導電性基体としてのアルミニウム製のドラム状支持体(直径30mm、全長238.5mm)の表面に、ディップコート法を用いて塗布した。続いて、塗布した下引き層用塗布液を、130℃で30分間加熱した。これにより、導電性基体上に下引き層(膜厚1.5μm)を形成した。
次に、電荷発生層用塗布液を調製した。具体的には、容器内に、電荷発生剤としての化合物(C−2Y)1質量部、ベース樹脂としてのポリビニルブチラール樹脂(電気化学工業株式会社製「デンカブチラール ♯6000EP」)1質量部、分散媒としてのプロピレングリコールモノメチルエーテル40質量部及び分散媒としてのテトラヒドロフラン40質量部を投入した。容器の内容物を、ビーズミルを用いて2時間混合し、分散媒に材料を分散させた。これにより、電荷発生層用塗布液を得た。次に、得られた電荷発生層用塗布液を3μmのフィルターを用いてろ過した。その後、電荷発生層用塗布液を、形成された下引き層上に、ディップコート法を用いて塗布した。続いて、塗布した電荷発生層用塗布液を、50℃で5分間乾燥させた。これにより、下引き層上に、電荷発生層(膜厚0.3μm)が形成された。
次に、電荷輸送層用塗布液を調製した。具体的には、正孔輸送剤としての化合物(H−1)70質量部、バインダー樹脂としてのビスフェノールZ型ポリカーボネート樹脂(帝人株式会社製「パンライト(登録商標)TS−2050」、粘度平均分子量50,000)100質量部、添加剤としてのジ(tert−ブチル)p−クレゾール(BHT)5質量部、溶剤としてのテトラヒドロフラン430質量部及び溶剤としてのトルエン430質量部を、容器内に投入した。容器の内容物を混合し、溶剤に材料を溶解させた。これにより、電荷輸送層用塗布液を得た。次に、得られた電荷輸送層用塗布液を、電荷発生層用塗布液と同様の方法で、形成された電荷発生層上に塗布した。続いて、塗布した電荷輸送層用塗布液を、130℃で30分間乾燥させた。これにより、電荷発生層上に、電荷輸送層(膜厚20μm)が形成された。その結果、積層型感光体(P−1)が得られた。
<2−2.積層型感光体(P−2)〜(P−7)の製造>
以下の点を変更した以外は、積層型感光体(P−1)の製造と同様の方法で、積層型感光体(P−2)〜(P−7)を各々製造した。積層型感光体(P−1)の製造に用いた正孔輸送剤としての化合物(H−1)を、表3に示す種類の正孔輸送剤に変更した。
<3.単層型感光体の製造>
感光層を形成するための材料を用いて、単層型感光体(P−8)〜(P−28)を製造した。
<3−1.単層型感光体(P−8)の製造>
容器内に、電荷発生剤としての化合物(C−1X)5質量部、正孔輸送剤としての化合物(H−1)80質量部、電子輸送剤としての化合物(E−1)50質量部、バインダー樹脂としてのビスフェノールZ型ポリカーボネート樹脂(帝人株式会社製「パンライト(登録商標)TS−2050」、粘度平均分子量50,000)100質量部及び溶剤としてのテトラヒドロフラン800質量部を投入した。容器の内容物を、ボールミルを用いて50時間混合して、溶剤に材料を分散させた。これにより、単層型感光層用塗布液を得た。単層型感光層用塗布液を、導電性基体としてのアルミニウム製のドラム状支持体(直径30mm、全長238.5mm)上に、ディップコート法を用いて塗布した。塗布した単層型感光層用塗布液を、100℃で30分間熱風乾燥させた。これにより、導電性基体上に、単層型感光層(膜厚25μm)を形成した。その結果、単層型感光体(P−8)が得られた。
<3−2.単層型感光体(P−9)〜(P−28)の製造>
以下の点を変更した以外は、単層型感光体(P−8)の製造と同様の方法で、単層型感光体(P−9)〜(P−28)を各々製造した。単層型感光体(P−8)の製造に用いた電荷発生剤としての化合物(C−1X)を、表4に示す種類の電荷発生剤に変更した。単層型感光体(P−8)の製造に用いた正孔輸送剤としての化合物(H−1)を、表4に示す種類の正孔輸送剤に変更した。単層型感光体(P−8)の製造に用いた電子輸送剤としての化合物(E−1)を、表4に示す種類の電子輸送剤に変更した。
<4.積層型感光体の電気特性の評価>
製造した積層型感光体(P−1)〜(P−7)の各々に対して、電気特性を評価した。電気特性の評価は、温度23℃及び相対湿度60%RHの環境下で行った。まず、ドラム感度試験機(ジェンテック株式会社製)を用いて、積層型感光体の表面を−700Vに帯電させた。次いで、バンドパスフィルターを用いて、ハロゲンランプの白色光から単色光(波長780nm、半値幅20nm、光エネルギー0.4μJ/cm2)を取り出した。取り出された単色光を、積層型感光体の表面に照射した。照射が終了してから0.5秒経過した時の積層型感光体の表面電位を測定した。測定された表面電位を、感度電位(VL、単位V)とした。測定された積層型感光体の感度電位(VL)を、表3に示す。なお、感度電位(VL)の絶対値が小さいほど、積層型感光体の電気特性が優れていることを示す。
<5.単層型感光体の電気特性の評価>
製造した単層型感光体(P−8)〜(P−28)の各々に対して、電気特性を評価した。電気特性の評価は、温度23℃及び湿度60%RHの環境下で行った。まず、ドラム感度試験機(ジェンテック株式会社製)を用いて、単層型感光体の表面を+700Vに帯電させた。次いで、バンドパスフィルターを用いて、ハロゲンランプの白色光から単色光(波長780nm、半値幅20nm、光エネルギー1.5μJ/cm2)を取り出した。取り出された単色光を、単層型感光体の表面に照射した。照射が終了してから0.5秒経過した時の単層型感光体の表面電位を測定した。測定された表面電位を、感度電位(VL、単位V)とした。測定された単層型感光体の感度電位(VL)を、表4に示す。なお、感度電位(VL)の絶対値が小さいほど、単層型感光体の電気特性が優れていることを示す。
<6.感光体の結晶化の評価>
積層型感光体(P−1)〜(P−5)の各々に対して、積層型感光体の表面を目視にて観察し、結晶化の有無を評価した。単層型感光体(P−8)〜(P−22)の各々に対して、単層型感光体の表面を目視にて観察し、結晶化の有無を評価した。その結果、積層型感光体(P−1)〜(P−5)及び単層型感光体(P−8)〜(P−22)の何れも結晶化は確認されなかった。
表3及び表4中、CGM、HTM、ETM及びVLは、各々、電荷発生剤、正孔輸送剤、電子輸送剤及び感度電位を示す。
積層型感光体(P−1)〜(P−5)及び単層型感光体(P−8)〜(P−22)の感光層は、正孔輸送剤として化合物(1)を、具体的には化合物(H−1)〜(H−5)の何れかを含有していた。そのため、表3及び表4から明らかなように、これらの感光体では、感度電位(VL)の絶対値が小さく、電気特性が優れていた。
一方、積層型感光体(P−6)〜(P−7)及び単層型感光体(P−23)〜(P−28)の感光層は、正孔輸送剤として、化合物(1)を含有していなかった。そのため、表3及び表4から明らかなように、これらの感光体では、感度電位(VL)の絶対値が大きく、電気特性が劣っていた。
以上のことから、化合物(1)は、感光層に含有された場合に、感光体の電気特性を向上させることが示された。また、化合物(1)を含有する感光層を備える感光体は、電気特性に優れることが示された。