JP6445429B2 - 少なくとも2つの異なる標的化実体を含むテーラーメイドで選択的かつ多重特異性治療用分子を選択および作製するための方法およびその使用 - Google Patents
少なくとも2つの異なる標的化実体を含むテーラーメイドで選択的かつ多重特異性治療用分子を選択および作製するための方法およびその使用 Download PDFInfo
- Publication number
- JP6445429B2 JP6445429B2 JP2015519058A JP2015519058A JP6445429B2 JP 6445429 B2 JP6445429 B2 JP 6445429B2 JP 2015519058 A JP2015519058 A JP 2015519058A JP 2015519058 A JP2015519058 A JP 2015519058A JP 6445429 B2 JP6445429 B2 JP 6445429B2
- Authority
- JP
- Japan
- Prior art keywords
- binding
- antibody
- dna
- linker
- binding pair
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2863—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against receptors for growth factors, growth regulators
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/32—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against translation products of oncogenes
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/46—Hybrid immunoglobulins
- C07K16/468—Immunoglobulins having two or more different antigen binding sites, e.g. multifunctional antibodies
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/26—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving oxidoreductase
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/58—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving urea or urease
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/66—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving luciferase
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/563—Immunoassay; Biospecific binding assay; Materials therefor involving antibody fragments
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/575—Immunoassay; Biospecific binding assay; Materials therefor for cancer
- G01N33/5758—Immunoassay; Biospecific binding assay; Materials therefor for cancer involving compounds serving as markers for tumours, cancers or neoplasias, e.g. cellular determinants, receptors, heat shock/stress proteins, A-protein, oligosaccharides or metabolites
- G01N33/5759—Immunoassay; Biospecific binding assay; Materials therefor for cancer involving compounds serving as markers for tumours, cancers or neoplasias, e.g. cellular determinants, receptors, heat shock/stress proteins, A-protein, oligosaccharides or metabolites involving compounds localised on the membrane of tumour or cancer cells
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/68—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids
- G01N33/6854—Immunoglobulins
- G01N33/6857—Antibody fragments
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/31—Immunoglobulins specific features characterized by aspects of specificity or valency multispecific
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/55—Fab or Fab'
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/60—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments
- C07K2317/62—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments comprising only variable region components
- C07K2317/622—Single chain antibody (scFv)
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/94—Stability, e.g. half-life, pH, temperature or enzyme-resistance
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2333/00—Assays involving biological materials from specific organisms or of a specific nature
- G01N2333/435—Assays involving biological materials from specific organisms or of a specific nature from animals; from humans
- G01N2333/705—Assays involving receptors, cell surface antigens or cell surface determinants
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2333/00—Assays involving biological materials from specific organisms or of a specific nature
- G01N2333/435—Assays involving biological materials from specific organisms or of a specific nature from animals; from humans
- G01N2333/705—Assays involving receptors, cell surface antigens or cell surface determinants
- G01N2333/71—Assays involving receptors, cell surface antigens or cell surface determinants for growth factors; for growth regulators
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2333/00—Assays involving biological materials from specific organisms or of a specific nature
- G01N2333/90—Enzymes; Proenzymes
- G01N2333/91—Transferases (2.)
- G01N2333/912—Transferases (2.) transferring phosphorus containing groups, e.g. kinases (2.7)
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Immunology (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Molecular Biology (AREA)
- General Health & Medical Sciences (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Biochemistry (AREA)
- Medicinal Chemistry (AREA)
- Biophysics (AREA)
- Genetics & Genomics (AREA)
- Urology & Nephrology (AREA)
- Hematology (AREA)
- Biomedical Technology (AREA)
- Biotechnology (AREA)
- Analytical Chemistry (AREA)
- Physics & Mathematics (AREA)
- Microbiology (AREA)
- Wood Science & Technology (AREA)
- Zoology (AREA)
- Cell Biology (AREA)
- General Physics & Mathematics (AREA)
- Pathology (AREA)
- Food Science & Technology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- General Engineering & Computer Science (AREA)
- Oncology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Peptides Or Proteins (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
Description
過去数年の間に、細胞表面受容体に対する抗体、抗体断片、およびリガンドを含む多種多様な腫瘍特異的治療用タンパク質が開発されており、臨床試験されている。これらの治療用タンパク質は、数種類の治療用毒素、例えば、低分子薬物、酵素、放射性同位体、タンパク質毒素、および患者に特異的に送達するための他の毒素に結合体化されている。
(i)細胞を含有する試料に存在する細胞表面マーカーを決定する工程およびi)少なくとも第1の細胞表面マーカー、任意で第2の細胞表面マーカーを選択する工程、またはii)多重特異性結合分子の結合特異性の数に対応する多数の細胞表面マーカーを選択する工程、
(ii)(a)多数の結合実体であって、それぞれが結合ペアの第1のパートナーまたはメンバーを含み、それによって、結合実体のそれぞれが異なる細胞表面マーカーもしくはそのリガンドまたは同じ細胞表面マーカーのエピトープに特異的に結合し、それによって、結合ペアのそれぞれの第1のパートナーまたはメンバーがその対応する第2のパートナーまたはメンバーにしか結合せず、結合ペアの他の第2のパートナーまたはメンバーのいずれにも結合しない多数の結合実体、および(b)結合ペアの対応する第2のメンバーを含むリンカーをインキュベートし、かつそれによって多重特異性結合分子を生成する工程。
(i)試料中の細胞の表面に存在する細胞表面マーカーを決定し、第1の表面マーカーおよび第2の表面マーカーを選択する工程、
(ii)(a)第1の結合ペアの第1のパートナーもしくはメンバーを含む、または第1の結合ペアの第1のパートナーもしくはメンバーと結合体化された抗体Fab断片またはscFv抗体断片であって、それによって第1の細胞表面マーカーに特異的に結合する、抗体Fab断片またはscFv抗体断片、(b)第2の結合ペアの第1のパートナーもしくはメンバーを含む、または第2の結合ペアの第1のパートナーもしくはメンバーと結合体化された抗体Fab断片またはscFv抗体断片であって、それによって第2の細胞表面マーカーに特異的に結合する、抗体Fab断片またはscFv抗体断片、および(c)末端の一方において第1の結合ペアの第2のメンバーを含み、それぞれの他方の末端において第2の結合ペアの第2のメンバーを含むリンカー
をインキュベートし、かつそれによって二重特異性抗体を生成する工程。
(i)多数の多重特異性結合分子の結合特異性および/または選択性および/または親和性および/またはエフェクター機能および/またはインビボ半減期を決定し、それによって、結合実体のそれぞれの(可能性のある)組み合わせが多数の多重特異性結合分子の中に含まれる工程、
(ii)適切な結合特異性および/または選択性および/または親和性および/またはエフェクター機能および/またはインビボ半減期を有する多重特異性結合分子を選択し、それによって、抗原結合実体の組み合わせを決定する工程。
(i)第1の結合ペアの第1のメンバーを含む、または第1の結合ペアの第1のメンバーと結合体化された第1の多数群の抗体Fab断片またはscFv抗体断片の各メンバーを、第2の結合ペアの第1のメンバーを含む、または第2の結合ペアの第1のメンバーと結合体化された第2の多数群の抗体Fab断片またはscFv抗体断片の各メンバーと、および末端の一方において第1の結合ペアの第2のメンバーを含み、かつそれぞれの他方の末端において第2の結合ペアの第2のメンバーを含むリンカーと組み合わせることによって調製された多数の二重特異性抗体の結合特異性および/または選択性および/または親和性および/またはエフェクター機能および/またはインビボ半減期を決定する工程であって、第1の多数群が第1の細胞表面マーカーに特異的に結合し、第2の多数群が第2の細胞表面マーカーに特異的に結合する工程、ならびに
(ii)適切な結合特異性および/または選択性および/または親和性および/またはエフェクター機能および/またはインビボ半減期を有する二重特異性抗体を選択し、それによって、抗原結合部位の組み合わせを決定する工程。
(a)(i)第1の表面マーカーに特異的に結合し、
(ii)第1の結合ペアの第1のメンバーと結合体化された、
第1のFab断片またはscFv抗体断片、
(b)(i)第2の表面マーカーに特異的に結合し、かつ
(ii)第2の結合ペアの第1のメンバーと結合体化された、
第2のFab断片またはscFv抗体断片、および
(c)(i)第1の結合ペアの第2のメンバーと結合体化され、かつ
(ii)第2の結合ペアの第2のメンバーと結合体化された
エナンチオマーDNAポリヌクレオチドリンカー
を含む二重特異性抗体であって、第1および第2のFab断片またはscFv抗体断片が非共有結合複合体を形成する、二重特異性抗体である。
(a)(i)第1の細胞表面マーカーまたはそのリガンドに特異的に結合し、かつ
(ii)第1の結合ペアの第1のメンバーと結合体化された、
第1の結合実体、
(b)(i)第2の細胞表面マーカーまたはそのリガンドに特異的に結合し、かつ
(ii)第2の結合ペアの第1のメンバーと結合体化された、
第2の結合実体、および
(c)(i)第1の結合ペアの第2のメンバーと結合体化され、かつ
(ii)第2の結合ペアの第2のメンバーと結合体化された、
ポリヌクレオチドリンカー
を含む複合体である。
(a)(i)第1の細胞表面マーカーに特異的に結合し、かつ
(ii)第1の結合ペアの第1のメンバー結合体化された、
第1のFab断片またはscFv抗体断片、
(b)(i)第2の細胞表面マーカーに特異的に結合し、かつ
(ii)第2の結合ペアの第1のメンバー結合体化された、
第2のFab断片またはscFv抗体断片、および
(c)(i)第1の結合ペアの第2のメンバーと結合体化され、かつ
(ii)第2の結合ペアの第2のメンバー結合体化された、
ポリヌクレオチドリンカー
を含む複合体である。
(a)第1の細胞表面マーカーまたはそのリガンドに特異的に結合し、かつ第1の結合ペアの第1のメンバーと結合体化された第1の結合実体、またはFab断片、またはscFv抗体断片を合成する工程、
(b)第2の細胞表面マーカーまたはそのリガンドに特異的に結合し、かつ第2の結合ペアの第1のメンバーと結合体化された第2の結合実体、またはFab断片、またはscFv抗体断片を合成する工程、
(c)第1の結合ペアの第2のメンバーと結合体化され、かつ第2の結合ペアの第2のメンバーと結合体化されたポリヌクレオチドリンカーを合成する工程、および
(d)合成された成分を組み合わせることによって複合体を形成する工程。
[本発明1001]
(i)試料中の細胞の表面に存在する表面マーカーを決定し、かつ第1の表面マーカーおよび第2の表面マーカーを選択する工程、
(ii)(a)第1の結合ペアの第1のメンバーと結合体化された抗体Fab断片またはscFv抗体断片であって、それによって第1の表面マーカーに特異的に結合する、抗体Fab断片またはscFv抗体断片、(b)第2の結合ペアの第1のメンバーと結合体化された抗体Fab断片またはscFv抗体断片であって、それによって第2の表面マーカーに特異的に結合する、抗体Fab断片またはscFv抗体断片、および(c)末端の一方において第1の結合ペアの第2のメンバーを含み、それぞれの他方の末端において第2の結合ペアの第2のメンバーを含むエナンチオマーDNAポリヌクレオチドリンカー
をインキュベートし、かつそれによって二重特異性抗体を生成する工程
を含む、二重特異性抗体を生成するための方法。
[本発明1002]
(i)それぞれが第1の結合ペアの同じ第1のメンバーに連結された第1の多数群の抗体Fab断片またはscFv抗体断片の各メンバーを、それぞれが第2の結合ペアの同じ第1のメンバーに連結された第2の多数群の抗体Fab断片またはscFv抗体断片の各メンバーと、および末端の一方において第1の結合ペアの第2のメンバーを含み、かつそれぞれの他方の末端において第2の結合ペアの第2のメンバーを含むエナンチオマーDNAポリヌクレオチドリンカーと、組み合わせることによって調製された多数の二重特異性抗体の結合特異性および/または親和性および/またはエフェクター機能および/またはインビボ半減期を決定する工程であって、それによって第1の多数群が第1の細胞表面マーカーに特異的に結合し、第2の多数群が第2の細胞表面マーカーに特異的に結合する、工程、ならびに
(ii)適切な結合特異性および/または親和性および/またはエフェクター機能および/またはインビボ半減期を有する二重特異性抗体を選択し、かつそれによって抗原結合部位の組み合わせを決定する工程
を含む、抗原結合部位の組み合わせを決定するための方法。
[本発明1003]
二重特異性抗体が、
(a)(i)第1の表面マーカーに特異的に結合し、かつ
(ii)第1の結合ペアの第1のメンバーと結合体化された
第1のFab断片またはscFv抗体断片、
(b)(i)第2の表面マーカーに特異的に結合し、かつ
(ii)第2の結合ペアの第1のメンバーと結合体化された
第2のFab断片またはscFv抗体断片、および
(c)(i)第1の結合ペアの第2のメンバーと結合体化され、かつ
(ii)第2の結合ペアの第2のメンバーと結合体化された
エナンチオマーDNAポリヌクレオチドリンカー
を含む複合体であることを特徴とする、前記本発明のいずれかの方法。
[本発明1004]
複合体が非共有結合複合体であることを特徴とする、前記本発明のいずれかの方法。
[本発明1005]
結合ペアがポリヌクレオチドの相補的ペアであることを特徴とする、前記本発明のいずれかの方法。
[本発明1006]
複合体が、リンカーの少なくとも一部に相補的なポリヌクレオチドと結合体化されたエフェクター部分をさらに含む、前記本発明のいずれかの方法。
[本発明1007]
第1のエフェクター部分と結合体化されたポリヌクレオチドの少なくとも一部に相補的であり、かつ(ii)ポリヌクレオチドリンカーに相補的でない、ポリヌクレオチド
と結合体化された第2のエフェクター部分を、複合体が含むことを特徴とする、本発明1006の方法。
[本発明1008]
第1および第2のFab断片またはscFv抗体断片が、同じ標的およびその上にある非重複エピトープに結合することを特徴とする、前記本発明のいずれかの方法。
[本発明1009]
ポリヌクレオチドリンカーが8〜1000個のヌクレオチドを含むことを特徴とする、前記本発明のいずれかの方法。一つの態様において、ポリヌクレオチドリンカーは10〜500個のヌクレオチドを含む。
[本発明1010]
エナンチオマーDNAがL-DNAであることを特徴とする、前記本発明のいずれかの方法。
[本発明1011]
L-DNAが一本鎖L-DNA(ss-L-DNA)であることを特徴とする、本発明1010の方法。
[本発明1012]
本発明1001〜1011のいずれかの方法によって得られた二重特異性抗体と、任意で薬学的に許容される担体とを含む、薬学的製剤。
[本発明1013]
医薬として使用するための、本発明1001〜1011のいずれかの方法によって得られた二重特異性抗体。
[本発明1014]
医薬の製造における、本発明1001〜1011のいずれかの方法によって得られた二重特異性抗体の使用。
[本発明1015]
癌を有する個体を治療する方法であって、本発明1001〜1011のいずれかの方法によって得られた二重特異性抗体の有効量を該個体に投与する工程を含む、方法。
[本発明1016]
(a)(i)第1の表面マーカーに特異的に結合し、かつ
(ii)第1の結合ペアの第1のメンバーと結合体化された
第1のFab断片またはscFv抗体断片、
(b)(i)第2の表面マーカーに特異的に結合し、かつ
(ii)第2の結合ペアの第1のメンバーと結合体化された
第2のFab断片またはscFv抗体断片、および
(c)(i)第1の結合ペアの第2のメンバーと結合体化され、かつ
(ii)第2の結合ペアの第2のメンバーと結合体化された
エナンチオマーDNAポリヌクレオチドリンカー
を含む二重特異性抗体であって、それによって第1および第2のFab断片またはscFv抗体断片ならびにエナンチオマーDNAポリヌクレオチドリンカーが非共有結合複合体を形成する、二重特異性抗体。
I.定義
冠詞「1つの(a)」および「1つの(an)」は、冠詞の1つまたは複数(すなわち、少なくとも1つ)の文法上の目的語を指すために本明細書において用いられる。一例として、「1つの(an)抗体」は1つの抗体または複数の抗体を意味する。
ほとんどの細胞に基づく疾患では、抗体に基づく受容体分子の結合を介した疾患関連細胞の標的化は有望なアプローチの1つである。しかしながら、臨床的に関連する表面受容体(=標的)の発現レベルは患者ごとに異なり、従って、標準化された抗体に基づく薬物の効力はかなり異なる。このことは、2つの異なるエピトープ/受容体を同時に標的化するという作用様式をもつ二重特異性抗体および多重特異性結合分子に特に当てはまる。
- ホスホチロシンキナーゼのリン酸化状況の確認
- JNK阻害の確認
- 分子によって誘導されたアポトーシスの確認
- 単一特異性結合分子対多重特異性結合分子を用いた結合アッセイの実施
- 増殖阻害の確認
について様々な細胞インビトロアッセイ/細胞試料において試験することができる。
第1の結合実体、例えば、抗体Fab断片を別の特異的結合実体、例えば、第2の抗体Fab断片と組み合わせることが望ましい。さらに、第1の結合実体を多くの異なる他の結合実体に連結した時に第1の結合実体がさらに優れた特性を示すかどうかスクリーニングすることが可能である。いわゆるコンビマトリックスアプローチを用いると、簡単な手法で結合実体の多数の組み合わせを扱うことができる。第2の結合実体は異なる標的/エピトープ/抗原に結合してもよく、同じ抗原であるが異なるエピトープに結合してもよく、同じエピトープに結合するが単一の結合実体の異なる変種(例えば、ヒト化候補)でもよいことを指摘しなければならない。
本明細書において報告される一局面は、二重特異性抗体を生成するための方法であって、以下の工程を含む方法である:
(i)試料中の細胞の表面に存在する表面マーカーを決定し、第1の表面マーカーおよび第2の表面マーカーを選択する工程、
(ii)(a)第1の結合ペアの第1のパートナーまたはメンバーと結合体化された抗体Fab断片またはscFv抗体断片であって、それによって第1の表面マーカーに特異的に結合する、抗体Fab断片またはscFv抗体断片、(b)第2の結合ペアの第1のメンバーと結合体化された抗体Fab断片またはscFv抗体断片であって、それによって第2の表面マーカーに特異的に結合する、抗体Fab断片またはscFv抗体断片、および(c)末端の一方において第1の結合ペアの第2のメンバーを含み、それぞれの他方の末端において第2の結合ペアの第2のメンバーを含むリンカー
をインキュベートし、かつそれによって二重特異性抗体を生成する工程。
(i)第1の多数群の抗体Fab断片またはscFv抗体断片の各メンバーを、第2の多数群の抗体Fab断片またはscFv抗体断片の各メンバーと、および末端の一方において第1の結合ペアの第2のメンバーを含み、かつそれぞれの他方の末端において第2の結合ペアの第2のメンバーを含むリンカーと組み合わせることによって調製された多数の二重特異性抗体の結合特異性および/または親和性および/またはエフェクター機能および/またはインビボ半減期を決定する工程であって、第1の多数群が第1の細胞表面分子に特異的に結合し、第2の多数群が第2の細胞表面分子に特異的に結合する工程、ならびに
(ii)適切な結合特異性および/または親和性および/またはエフェクター機能および/またはインビボ半減期を有する二重特異性抗体を選択し、それによって、抗原結合部位の組み合わせを決定する工程。
(a)(i)第1の表面マーカーに特異的に結合し、かつ
(ii)第1の結合ペアの第1のメンバーと結合体化された
第1のFab断片またはscFv抗体断片、
(b)(i)第2の表面マーカーに特異的に結合し、かつ
(ii)第2の結合ペアの第1のメンバーと結合体化された、
第2のFab断片またはscFv抗体断片、および
(c)(i)第1の結合ペアの第2のメンバーと結合体化され、かつ
(ii)第2の結合ペアの第2のメンバーと結合体化された
ポリヌクレオチドリンカー
を含む複合体である。
(a)第1の細胞表面マーカーに特異的に結合し、かつ第1の結合ペアの第1のメンバーと結合体化された第1のFab断片またはscFv抗体断片を合成する工程、
(b)第2の細胞表面マーカーに特異的に結合し、かつ第2の結合ペアの第1のメンバーと結合体化された第2のFab断片またはscFv抗体断片を合成する工程、
(c)第1の結合ペアの第2のメンバーと結合体化され、かつ第2の結合ペアの第2のメンバーと結合体化されたポリヌクレオチドリンカーを合成する工程、および
(d)合成された成分を組み合わせることによって複合体を形成する工程
を含む。
多重特異性結合分子、例えば、二重特異性抗体、すなわち、非共有結合相互作用によってつながれ、それによって、単離されたRNAまたはDNA、特に、D-DNAよりインビボでのタンパク質分解および酵素分解に対する耐性が高くなった少なくとも2つの成分を含む複合体が本明細書において報告される。この複合体は、結合アビディティを利用して、その標的に対して高親和性を有し、優れた溶解度を有する。この複合体は、1つまたは複数のエフェクター部分を標的に送達するのに使用することができる。
(A-a':a-S-b:b'-B)-X(n)または(A-a':a-S-b:b'-B):X(n)
のポリペプチド-ポリヌクレオチド-複合体であり、
式中、
AならびにBは、標的に特異的に結合する結合実体であり、
a':aならびにb:b'は結合ペアであり、a'およびaはbとb'の結合を妨げず、逆もまた同じであり、
Sはリンカーポリヌクレオチドであり、
(:X)は、共有結合的に、または結合ペアを介して、a'、a、b、b'、またはSの少なくとも1つに結合されたエフェクター部分を意味し、
(n)は整数であり、
-は共有結合を表し、
:は非共有結合を表す。
(A-a':a-S-b:b'-B)-X(n)または(A-a':a-S-b:b'-B):X(n)
のポリペプチド-ポリヌクレオチド-複合体を生成するための方法も本明細書において報告され、本方法は、
(a)A-a'およびb'-Bをそれぞれ合成する工程、
(b)リンカーa-S-bを合成する工程、および
(c)前記式の複合体を形成する工程
を含み、エフェクター部分Xは工程(a)、(b)、または(c)においてa'、a、b、b'またはSの少なくとも1つに結合される。
(a)標的に特異的に結合し、かつ結合ペアの第1のメンバーと結合体化された結合実体、例えば、ポリペプチド、
(b)その第1の末端において結合ペアの第2のメンバーと結合体化されたポリヌクレオチドリンカー、および
(c)ポリヌクレオチドリンカーの少なくとも一部に相補的なポリヌクレオチドと結合体化されたエフェクター部分
を含む結合実体-ポリヌクレオチド-複合体を生成する方法であって、
(a)(i)標的に特異的に結合し、かつ結合ペアの第1のメンバーと結合体化された結合実体、および(ii)ポリヌクレオチドリンカーの少なくとも一部に相補的なポリヌクレオチドと結合体化されたエフェクター部分をそれぞれ合成する工程、
(b)その第1の末端において結合ペアの第2のメンバーと結合体化されたポリヌクレオチドリンカーを合成する工程、ならびに
(c)合成された成分をハイブリダイズすることによって結合実体-ポリヌクレオチド-複合体を形成する工程
を含む方法である。
(a)第1の標的に特異的に結合し、第1の結合ペアの第1のメンバーと結合体化された第1の結合実体、例えば、ポリペプチド、
(b)第2の標的に特異的に結合し、第2の結合ペアの第1のメンバーと結合体化された第2の結合実体、例えば、ポリペプチド、および
(c)その第1の末端において第1の結合ペアの第2のメンバーと結合体化され、かつその第2の末端において第2の結合ペアの第2のメンバーと結合体化されたポリヌクレオチドリンカー
を含む結合実体-ポリヌクレオチド-複合体を生成する方法であって、
(a)第1の標的に特異的に結合し、第1の結合ペアの第1のメンバーと結合体化された第1の結合実体、第2の標的に特異的に結合し、第2の結合ペアの第1のメンバーと結合体化された第2の結合実体をそれぞれ合成する工程、および
(b)その第1の末端において第1の結合ペアの第2のメンバーと結合体化され、かつその第2の末端において第2の結合ペアの第2のメンバーに結合体化されたポリヌクレオチドリンカーを合成する工程、ならびに
(c)合成された成分をハイブリダイズすることによって結合実体-ポリヌクレオチド-複合体を形成する工程
を含む方法である。
(a)第1の標的に特異的に結合し、かつ第1の一本鎖L-DNA部分と結合体化された結合実体(例えば、ポリペプチド)、
(b)第2の標的に特異的に結合し、かつ第2の一本鎖L-DNA部分と結合体化された第2の結合実体(例えば、ポリペプチド)、および
(c)その第1の(または3')末端において、第1の一本鎖L-DNA部分に相補的な第1の一本鎖L-DNAリンカー部分を含み、その第2の(または5')末端において、第2の一本鎖L-DNA部分に相補的な第2の一本鎖L-DNAリンカー部分を含むリンカー
を含む複合体である。
(a)第1の標的に特異的に結合し、第1の一本鎖L-DNA部分と結合体化された抗体FAB断片またはscFv、
(b)第2の標的に特異的に結合し、第2の一本鎖L-DNA部分と結合体化された抗体FAB断片またはscFv、および
(c)その第1の(または3')末端に、第1の一本鎖L-DNA部分に相補的な第1の一本鎖L-DNAリンカー部分を含み、その第2の(または5')末端に、第2の一本鎖L-DNA部分に相補的な第2の一本鎖L-DNAリンカー部分を含むリンカー
を含む複合体である。
(a)第1の標的に特異的に結合し、かつ第1の一本鎖L-DNA部分と結合体化されたポリペプチド、
(b)第2の標的に特異的に結合し、かつ第2の一本鎖L-DNA部分と結合体化されたポリペプチド、および
(c)その第1の(または3')末端に、第1の一本鎖L-DNA部分に相補的な第1の一本鎖L-DNAリンカー部分を含み、その第2の(または5')末端に、第2の一本鎖L-DNA部分に相補的な第2の一本鎖L-DNAリンカー部分を含み、第1の一本鎖L-DNA部分と第2の一本鎖L-DNA部分との間に第3の一本鎖L-DNAリンカー部分を含むリンカー
を含む。
- 第1の一本鎖L-DNA部分に相補的な第1の一本鎖L-DNAリンカー部分、
- ドッキング一本鎖L-DNA部分、および
- 第2の一本鎖L-DNA部分に相補的な第2の一本鎖L-DNAリンカー部分
を含む。
- 第1の一本鎖L-DNA部分に相補的な第1の一本鎖L-DNAリンカー部分、
- 直鎖非ヌクレオチド部分、
- ドッキング一本鎖L-DNA部分、および
- 第2の一本鎖L-DNA部分に相補的な第2の一本鎖L-DNAリンカー部分
を含む。
- 第1の一本鎖L-DNA部分に相補的な第1の一本鎖L-DNAリンカー部分、
- ドッキング一本鎖L-DNA部分、
- 非ヌクレオチド部分、および
- 第2の一本鎖L-DNA部分に相補的な第2の一本鎖L-DNAリンカー部分
を含む。
- 第1の一本鎖L-DNA部分に相補的な第1の一本鎖L-DNAリンカー部分、
- 非ヌクレオチド部分、
- ドッキング一本鎖L-DNA部分、および
- 第2の一本鎖L-DNA部分に相補的な第2の一本鎖L-DNAリンカー部分
を含む。
- 第1の一本鎖L-DNA部分に相補的な第1の一本鎖L-DNAリンカー部分、
- 第1の非ヌクレオチド部分、
- ドッキング一本鎖L-DNA部分、
- 第2の非ヌクレオチド部分、
- 第2の一本鎖L-DNA部分に相補的な第2の一本鎖L-DNAリンカー部分
を含む。
モノクローナル抗体法は、特異的に結合するモノクローナル抗体またはその断片の形で特異的に結合する薬剤の生成を可能にする。モノクローナル抗体またはその断片を作り出すために、マウス、ウサギ、ハムスター、または他の任意の哺乳動物をポリペプチドすなわち抗体の標的または/およびポリペプチドをコードする核酸で免疫するなどの技法を使用することができる。代替として、モノクローナル抗体またはその断片は、scFv(単鎖可変領域)、具体的にはヒトscFvのファージライブラリーを使用することによって得ることができる(例えば、US5,885,793、WO92/01047、WO99/06587を参照されたい)。
本明細書において報告される複合体は(ポリヌクレオチド)リンカーを含む。リンカーはポリペプチドに共有結合されてもよく、(ポリヌクレオチド)リンカーおよびポリペプチドは特異的結合ペアによって互いに結合されてもよい。
式II:
式中、PGは、酸不安定保護基、特に、モノメトキシトリチル、ジメトキシトリチル、ピキシル、キサンチル、特に、ジメトキシトリチルであり、Yは、C2-C18アルキル、アルケニルアルキニルであり、アルキル、アルケニル、アルキニルはエチレンオキシ部分および/またはアミド部分を含んでもよく、Yは、好ましくは、C4-C18アルキル、アルケニル、またはアルキニルであり、1つのアミド部分を含有し、Xは機能的部分である。
1つの態様において、結合ペアの各メンバーは10kDa以下の分子量のものである/10kDa以下の分子量を有する。1つの態様において、結合ペアの各メンバーの分子量は、8kDa、または7kDa、または6kDa、または5kDa、または4kDa、またはそれより小さい。
エフェクター部分は、結合部分、標識部分、生物学的に活性な部分、および反応性部分からなる群より選択することができる。複数のエフェクター部分が複合体に存在するのであれば、それぞれのこのようなエフェクター部分は、それぞれの場合において、独立して、結合部分、標識部分、生物学的に活性な部分、および反応性部分でもよい。結合部分は、結合ペアのそれぞれと干渉しないように選択される。
[M(L1L2L3)]n-Y-XmA (i)
の構造を有する。式中、Mは希土類イオンまたは遷移金属イオンより選択される二価または三価の金属カチオンであり、L1、L2、およびL3は同じあるか、または異なり、少なくとも2つの窒素含有複素環を有する配位子を示し、L1、L2、およびL3は窒素原子を介して金属カチオンに結合し、Xは、リンカーYを介して配位子L1、L2、およびL3の少なくとも1つに共有結合された反応性官能基であり、nは、1〜10、特に、1〜4の整数であり、mは1または2であるか、または特に1であり、Aは電荷を等しくするために必要とされ得る対イオンを示す。
一般的に、抗体断片または結合ペアのメンバーなどの結合実体は、例えば、US4,816,567に記載のように組換え方法および組成物を用いて産生され得る。
標的またはリンカーに特異的に結合する結合実体の少なくとも1つが、1つまたは複数のエフェクター部分、例えば、細胞傷害剤、例えば、化学療法剤または化学療法薬物、増殖阻害剤、毒素(例えば、タンパク質毒素、細菌、真菌、植物、もしくは動物に由来する酵素活性のある毒素、またはその断片)、あるいは放射性同位体とさらに結合体化された複合体も本明細書において提供される。
本明細書において報告される多重特異性結合分子(例えば、二重特異性抗体)の薬学的製剤は、望ましい程度の純度を有する、このような多重特異性結合分子を凍結乾燥製剤または水溶液の形で1種類または複数種の最適な薬学的に許容される担体(Osol, A. (ed.), Remington's Pharmaceutical Sciences, 16th edition, Mack Publishing Company (1980))と混合することによって調製される。薬学的に許容される担体は、一般的に、使用される投与量および濃度でレシピエントに無毒であり、緩衝液、例えば、リン酸、クエン酸、および他の有機酸;アスコルビン酸およびメチオニンを含む抗酸化物質;防腐剤(例えば、オクタデシルジメチルベンジル塩化アンモニウム、塩化ヘキサメトニウム、塩化ベンザルコニウム、塩化ベンゼトニウム、フェノール、ブチルアルコールもしくはベンジルアルコール、アルキルパラベン、例えば、メチルパラベンもしくはプロピルパラベン、カテコール、レゾルシノール、シクロヘキサノール、3-ペンタノール、およびm-クレゾール)、低分子量(約10残基未満)ポリペプチド、タンパク質、例えば、血清アルブミン、ゼラチン、もしくは免疫グロブリン、親水性ポリマー、例えば、ポリビニルピロリドン、アミノ酸、例えば、グリシン、グルタミン、アスパラギン、ヒスチジン、アルギニン、もしくはリジン、グルコース、マンノース、もしくはデキストリンを含む単糖、二糖、および他の炭水化物、キレート剤、例えば、EDTA、糖、例えば、スクロース、マンニトール、トレハロース、もしくはソルビトール、塩形成対イオン、例えば、ナトリウム、金属複合体(例えば、Zn-タンパク質複合体)、ならびに/または非イオン界面活性剤、例えば、ポリエチレングリコール(PEG)を含むが、これに限定されない。本明細書において例示的な薬学的に許容される担体は、間質性薬物分散剤、例えば、可溶性中性活性ヒアルロニダーゼ糖タンパク質(sHASEGP)、例えば、ヒト可溶性PH-20ヒアルロニダーゼ糖タンパク質、例えば、rHuPH20(HYLENEX(登録商標), Baxter International, Inc.)をさらに含む。rHuPH20を含む、ある特定の例示的なsHASEGPおよび使用方法はUS2005/0260186およびUS2006/0104968に記載されている。一局面において、sHASEGPは1つまたは複数のさらなるグリコサミノグリカナーゼ(glycosaminoglycanase)、例えば、コンドロイチナーゼと組み合わされる。
本明細書において報告される任意の多重特異性結合分子(例えば、二重特異性抗体)を治療方法において使用することができる。
本明細書において報告される一局面において、前記の障害の治療、予防、および/または診断に有用な材料を含有する製造物品が提供される。製造物品は、容器および容器に貼られている、または容器に関連するラベルまたは添付文書を備える。適切な容器には、例えば、瓶、バイアル、注射器、IV溶液バック(IV solution bag)などが含まれる。容器はガラスまたはプラスチックなどの様々な材料から形成されてもよい。容器は、単独の組成物、または状態の治療、予防、および/もしくは診断に有効な別の組成物と組み合わされる組成物を保持し、滅菌アクセスポートを有してもよい(例えば、容器は、静脈内溶液バックまたは皮下注射針で穴を開けることができるストッパーを有するバイアルでもよい)。組成物中の少なくとも1種類の活性薬剤は、本明細書において報告される複合体である。ラベルまたは添付文書は、組成物が、えり抜きの状態を治療するのに用いられることを示す。さらに、製造物品は、(a)本明細書において報告される複合体を含む組成物が中に入れられている第1の容器;および(b)さらなる細胞傷害剤または他の治療剤を含む組成物が中に入れられている第2の容器を備えてもよい。本発明のこの態様における製造物品は、ある特定の状態を治療するために組成物を使用できることを示す添付文書をさらに備えてもよい。代替としてまたはさらに、製造物品は、薬学的に許容される緩衝液、例えば、無菌注射用水(BWFI)、リン酸緩衝食塩水、リンガー液、およびデキストロース液を含む第2の(または第3の)容器をさらに備えてもよい。これは、他の緩衝液、希釈剤、フィルター、針、および注射器を含む商業的観点および使用者の観点から望ましい他の材料をさらに備えてもよい。
SEQ ID NO:01 VH(mAb 1.4.168)
SEQ ID NO:02 VL(mAb 1.4.168)
SEQ ID NO:03 VH(mAb 8.1.2)
SEQ ID NO:04 VL(mAb 8.1.2)
SEQ ID NO:05 17merのss-DNA(5'末端が抗トロポニンT MAB aのFAB'およびIGF-1Rに対するFAB'1.4.168にそれぞれ共有結合している)
SEQ ID NO:06 19merのss-DNA(3'末端が抗トロポニンT MAB bのFAB'およびリン酸化IGF-1Rに対すFAB'8.1.2にそれぞれ共有結合している)
SEQ ID NO:07 相補的19merのss-DNA(リンカーの一部として使用した)
SEQ ID NO:08 相補的17merのss-DNA(リンカーの一部として使用した)
SEQ ID NO:09 抗トロポニン抗体aに対するエピトープ「A」
SEQ ID NO:10 抗トロポニン抗体bに対するエピトープ「B」
SEQ ID NO:11 IGF-1R(1340-1366)
SEQ ID NO:12 hInsR(1355-1382)
SEQ ID NO:13 35merのL-DNAポリヌクレオチドリンカー
SEQ ID NO:14 75merのL-DNAポリヌクレオチドリンカー
SEQ ID NO:15 95merのL-DNAポリヌクレオチドリンカー
SEQ ID NO:16 4D5 FAB'重鎖アミノ酸配列
SEQ ID NO:17 4D5 FAB'軽鎖アミノ酸配列
SEQ ID NO:18 2C4 FAB'重鎖アミノ酸配列
SEQ ID NO:19 2C4 FAB'軽鎖アミノ酸配列
SEQ ID NO:20 ErbB2の細胞外ドメイン(ECD)内の残基22-645
SEQ ID NO:21
式中、X=ホスホルアミダイトC3(3-(4,4'-ジメトキシトリチルオキシ)プロピル-1-[(2-シアノエチル)-(N,N-ジイソプロピル)]-ホスホルアミダイト(Glen Research)を介して導入されたプロピレン-ホスフェート、Y=(6-(4-モノメトキシトリチルアミノ)ヘキシル-(2-シアノエチル)-(N,N-ジイソプロピル)-ホスホルアミダイト(Glen Research)を介して導入された5'-アミノ-修飾因子C6、およびZ=スルホスクシンイミジル4-[N-マレイミドメチル]シクロヘキサン-1-カルボキシレート(Thermo Fischer)を介して導入された4[N-マレイニミドメチル]シクロヘキサン-1-カルボキシ
SEQ ID NO:22
式中、X=ホスホルアミダイトC3(3-(4,4'-ジメトキシトリチルオキシ)プロピル-1-[(2-シアノエチル)-(N,N-ジイソプロピル)]-ホスホルアミダイト(Glen Research)を介して導入されたプロピレン-ホスフェート、Y=(6-(4-モノメトキシトリチルアミノ)ヘキシル-(2-シアノエチル)-(N,N-ジイソプロピル)-ホスホルアミダイト(Glen Research)を介して導入された5'-アミノ-修飾因子C6、およびZ=スルホスクシンイミジル4-[N-マレイミドメチル]シクロヘキサン-1-カルボキシレート(Thermo Fischer)を介して導入された4[N-マレイニミドメチル]シクロヘキサン-1-カルボキシ
SEQ ID NO:23
SEQ ID NO:24
SEQ ID NO:25
SEQ ID NO:26 抗HER2抗体4D5重鎖可変ドメイン
SEQ ID NO:27 VH CDR1
SEQ ID NO:28 VH CDR2
SEQ ID NO:29 VH CDR3
SEQ ID NO:30 抗HER2抗体4D5重鎖軽鎖可変ドメイン
SEQ ID NO:31 VL CDR1
SEQ ID NO:32 VL CDR2
SEQ ID NO:33 VL CDR3
SEQ ID NO:34 抗HER2抗体2C4重鎖可変ドメイン
SEQ ID NO:35 VH CDR1
SEQ ID NO:36 VH CDR2
SEQ ID NO:37 VH CDR3
SEQ ID NO:38 抗HER2抗体2C4軽鎖可変ドメイン
SEQ ID NO:39 VL CDR1
SEQ ID NO:40 VL CDR2
SEQ ID NO:41 VL CDR3
SEQ ID NO:42
; X=フルオレセイン Y=C7アミノリンカー Z=C3スペーサー
SEQ ID NO:43
;X=Cy5 Y=C7アミノリンカー Z=C3スペーサー
SEQ ID NO:44
;X=アミノリンカー Y=フルオレセイン Z=C3スペーサー
SEQ ID NO:45
;X=フルオレセイン Y=C7アミノリンカー Z=C3スペーサー
SEQ ID NO:46
;X=アミノリンカー Y=フルオレセイン Z=C3スペーサー
SEQ ID NO:47
SEQ ID NO:48
SEQ ID NO:49
SEQ ID NO:69 IgG1定常ドメイン
SEQ ID NO:70 IgG2定常ドメイン
SEQ ID NO:71 IgG4定常ドメイン
SEQ ID NO:72
SEQ ID NO:73
SEQ ID NO:74 ソルターゼタグ
SEQ ID NO:75 結合ペアメンバーオリゴヌクレオチド
SEQ ID NO:76 L-DNAリンカー
FAB-ss-DNA-結合体の形成
ヒト心臓トロポニンTの異なる非重複エピトープであるエピトープaおよびエピトープbにそれぞれ結合する2種類のモノクローナル抗体を使用した。これらの抗体は両方とも、トロポニンTがサンドイッチイムノアッセイ形式で検出される最新のRoche Elecsys(商標)Troponin Tアッセイにおいて用いられる。
抗トロポニンT<エピトープa>抗体FAB-ss-DNAa-結合体Aを調製するために、SEQ ID NO:05の誘導体、すなわち、
を使用する。式中、X=ホスホルアミダイトC3(3-(4,4'-ジメトキシトリチルオキシ)プロピル-1-[(2-シアノエチル)-(N,N-ジイソプロピル)]-ホスホルアミダイト(Glen Research)を介して導入されたプロピレン-ホスフェート、Y=3'-アミノ修飾因子TFAアミノC-6 lcaa CPG(ChemGenes)を介して導入された3''-アミノ-修飾因子C6、Z=スルホスクシンイミジル4-[N-マレイミドメチル]シクロヘキサン-1-カルボキシレート(ThermoFischer)を介して導入された4[N-マレイニミドメチル]シクロヘキサン-1-カルボキシ。
抗トロポニンT<エピトープb>抗体FAB-ss-DNAb-結合体Bを調製するために、SEQ ID NO:06の誘導体、すなわち、
を使用する。式中、X=ホスホルアミダイトC3(3-(4,4'-ジメトキシトリチルオキシ)プロピル-1-[(2-シアノエチル)-(N,N-ジイソプロピル)]-ホスホルアミダイト(Glen Research)を介して導入されたプロピレン-ホスフェート、Y=(6-(4-モノメトキシトリチルアミノ)ヘキシル-(2-シアノエチル)-(N,N-ジイソプロピル)-ホスホルアミダイト(Glen Research)を介して導入された5'-アミノ-修飾因子C6、Z=スルホスクシンイミジル4-[N-マレイミドメチル]シクロヘキサン-1-カルボキシレート(ThermoFischer)を介して導入された4[N-マレイニミドメチル]シクロヘキサン-1-カルボキシ。
ビオチン化リンカー分子の形成
ss-DNAリンカーL1、L2、およびL3において用いられるオリゴヌクレオチドはそれぞれ、最新式のオリゴヌクレオチド合成法によって、およびビオチン化のためにビオチン化ホスホルアミダイト試薬を用いて合成された。
を有する。これは、それぞれ、SEQ ID NO:7およびSEQ ID NO:8のss-DNAオリゴヌクレオチドを含み、ビオチン-dT(5'-ジメトキシトリチルオキシ-5-[N-((4-t-ブチルベンゾイル)-ビオチニル)-アミノヘキシル)-3-アクリルイミド]-2'-デオキシウリジン-3'-[(2-シアノエチル)-(N,N-ジイソプロピル)]-ホスホルアミダイト(Glen Research)を使用することによってビオチン化された。
を有する。これは、それぞれ、SEQ ID NO:7およびSEQ ID NO:8のss-DNAオリゴヌクレオチドを含み、それぞれ5個のチミジンからなるオリゴヌクレオチド領域が2回現れ、ビオチン-dT(5'-ジメトキシトリチルオキシ-5-[N-((4-t-ブチルベンゾイル)-ビオチニル)-アミノヘキシル)-3-アクリルイミド]-2'-デオキシウリジン-3'-[(2-シアノエチル)-(N,N-ジイソプロピル)]-ホスホルアミダイト(Glen Research)を使用することによってビオチン化された。
を有する。これは、それぞれ、SEQ ID NO:7 および SEQ ID NO:8のss-DNAオリゴヌクレオチドを含み、それぞれ15個のチミジンからなるオリゴヌクレオチド領域が2回現れ、ビオチン-dT(5'-ジメトキシトリチルオキシ-5-[N-((4-t-ブチルベンゾイル)-ビオチニル)-アミノヘキシル)-3-アクリルイミド]-2'-デオキシウリジン-3'-[(2-シアノエチル)-(N,N-ジイソプロピル)]-ホスホルアミダイト(Glen Research)を使用することによってビオチン化された。
一価トロポニンT結合剤aおよびbそれぞれに対するエピトープ
それぞれ、抗トロポニンT抗体aおよびbに由来する対応するFAB'断片に対して個々に中等度の親和性しか有さない合成ペプチドが構築されてきた。
a)抗体aに対するエピトープ「A」は、
に含まれる。式中、Uはβ-アラニンを表す。
b)抗体bに対するエピトープ「B」は、
に含まれる。式中、Oはアミノ-トリオキサ-オクタン酸を表す。
生体分子相互作用分析
この実験のために、BIAcore 3000機器(GE Healthcare)を、このシステムに取り付けたBIAcore SAセンサーと一緒にT=25℃で使用した。プレコンディショニング(preconditioning)は、100μl/minで、50mM NaOHに溶解した1M NaClの3x1分間の注入および1分間の10mM HClを用いて行った。
表5および表6に示した実験データはそれぞれ、一価dsDNA FAB AまたはB結合体それぞれと比較した時の分析物(TnT1またはTnT2)それぞれと様々なヘテロ二価FAB-FAB結合体A-Bとの間の複合体安定性の増加を示す。この効果を、それぞれの表において列2および3と比較して列1に示した。
FAB'-ss-DNA-結合体の形成
ヒトHER2(ErbB2またはp185neu)の異なる非重複エピトープAおよびBに結合する2種類のモノクローナル抗体を使用した。第1の抗体は、抗HER2抗体4D5(huMAb4D5-8、rhuMab HER2、トラスツズマブ、またはハーセプチン(登録商標);その全体が参照により本明細書に組み入れられるUS5,821,337を参照されたい)である。第2の抗体は抗HER2抗体2C4(ペルツズマブ)である。
抗HER2抗体4D5 FAB'-ss-DNA-結合体を調製するために、
SED ID NO:05の誘導体、すなわち、
を使用する。式中、X=ホスホルアミダイトC3(3-(4,4'-ジメトキシトリチルオキシ)プロピル-1-[(2-シアノエチル)-(N,N-ジイソプロピル)]-ホスホルアミダイト(Glen Research)を介して導入されたプロピレン-ホスフェート、Y=(6-(4-モノメトキシトリチルアミノ)ヘキシル-(2-シアノエチル)-(N,N-ジイソプロピル)-ホスホルアミダイト(Glen Research)を介して導入された5'-アミノ-修飾因子C6、Z=スルホスクシンイミジル4-[N-マレイミドメチル]シクロヘキサン-1-カルボキシレート(ThermoFischer)を介して導入された4[N-マレイニミドメチル]シクロヘキサン-1-カルボキシ。
抗HER2抗体2C4 FAB'-ss-DNA-結合体Bを調製するために、SEQ ID NO:06の誘導体、すなわち、
を使用する。式中、X=ホスホルアミダイトC3(3-(4,4'-ジメトキシトリチルオキシ)プロピル-1-[(2-シアノエチル)-(N,N-ジイソプロピル)]-ホスホルアミダイト(GlenResearch)を介して導入されたプロピレン-ホスフェート、Y=(6-(4-モノメトキシトリチルアミノ)ヘキシル-(2-シアノエチル)-(N,N-ジイソプロピル)-ホスホルアミダイト(Glen Research)を介して導入された5'-アミノ-修飾因子C6、Z=スルホスクシンイミジル4-[N-マレイミドメチル]シクロヘキサン-1-カルボキシレート(ThermoFischer)を介して導入された4[N-マレイニミドメチル]シクロヘキサン-1-カルボキシ。
生体分子相互作用分析
この実験のために、BIAcore T100機器(GE Healthcare)を、このシステムに取り付けたBIAcore SAセンサーと一緒にT=25℃で使用した。プレコンディショニングは、100μl/minで、50mM NaOH、pH8.0に溶解した1M NaClの3x1分間の注入、その後に10mM HClの1分間の注入を用いて行われた。システムバッファーはHBS-EP(10mM HEPES pH7.4、150mM NaCl、1mM EDTA、0.05%P20)であった。サンプルバッファーは、1mg/ml CMD(カルボキシメチルデキストラン)を補充したシステムバッファーであった。
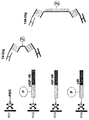
ss-D-DNA標識FAB断片をシステムに注入した時に、HER2-ECD相互作用を観察することができなかった。なぜなら、ss-D-DNA標識FAB断片は、センサー表面に提示されたスピゲルマーss-L-DNAリンカーとハイブリダイズしなかったからである(図2)。
リンカー:表面に提示されたビオチン化ss-L-DNAポリヌクレオチドリンカー、リンカー長が異なるオリゴ_35mer-Bi、オリゴ_75mer-Bi、およびオリゴ_95mer-Bi。ss-L-DNA-FAB:2C4-ss-L-DNA:19mer-フルオレセインで標識された抗HER2抗体2C4-FAB'-ss-L-DNA。4D5-ss-L-DNA:17mer-フルオレセインで標識された抗HER2抗体4D5-FAB'-ss-L-DNA。4D5-+2C4-ss-L-DNA:表面に提示された両断片の組み合わせ。LRU:センサー表面にハイブリダイズされた応答単位での質量(mass)。抗原:87kDa HER2-ECDを分析物として溶解状態で使用した。ka:(1/Ms)での会合速度。kd:(1/s)での解離速度。t1/2 diss:一次反応速度式の解ln(2)/kD*3600に従って時間単位で計算された抗原複合体半減時間。kD:モル濃度での親和性。kD:ピコモル濃度で計算された親和性。Rmax:応答単位(RU)での飽和状態での最大分析物反応シグナル。MR:モル比。相互作用の化学量論を示す。Chi2、U値:測定の質の指標。
さらなる生体分子相互作用分析
BIAcore 3000機器をCM-5センサーチップと一緒に取り付けた。製造業者(GE healthcare, Uppsala, Sweden)により推奨されるようにセンサーをプレコンディショニングした。システムバッファーは、(10mM HEPES pH7.4、150mM NaCl、1mM EDTA、0.05%Tween(登録商標)20)であった。システムバッファーをサンプルバッファーとしても使用した。システムを制御ソフトウェア4.1の下で25℃で操作した。
さらなる複合体-合成および特徴付け
ハイブリダイズ可能なオリゴヌクレオチドの合成
SEQ ID NO:05およびSEQ ID NO:06それぞれに示した配列を含む以下のアミノ改変前駆体を標準的な方法に従って合成した。以下に示したオリゴヌクレオチドはいわゆるアミノリンカーだけでなく蛍光色素も含む。当業者が容易に認めるように、オリゴヌクレオチドそのもの、ならびにオリゴヌクレオチドを含む成分の精製を容易にするために、この蛍光色素は非常に便利である。
- スペーサーホスホルアミダイトC3(3-(4,4'-ジメトキシトリチルオキシ)プロピル-1-[(2-シアノエチル)-(N,N-ジイソプロピル)]-ホスホルアミダイト(Glen Research);
- 5'-アミノ-修飾因子C6(6-(4-モノメトキシトリチルアミノ)ヘキシル-(2-シアノエチル)-(N,N-ジイソプロピル)-ホスホルアミダイト(Glen Research)を使用することによって5'アミノ修飾因子を導入する;
- 5'-フルオレセインホスホルアミダイト6-(3',6'-ジピバロイルフルオレセイニル-6-カルボキサミド)-ヘキシル-1-O-(2-シアノエチル)-(N,N-ジイソプロピル)-ホスホルアミダイト(GlenResearch);
- Cy5(商標)ホスホルアミダイト1-[3-(4-モノメトキシトリチルオキシ)プロピル]-1'-[3-[(2-シアノエチル)-(N,N-ジイソプロピルホスホルアミジチル]プロピル]-3,3,3',3'-テトラメチルインドジカルボシアニンクロリド(Glen Research);
- LightCyclerフルオレセインCPG 500A(Roche Applied Science);および
- 3'-アミノ修飾因子TFAアミノC-6 lcaa CPG 500A(ChemGenes)
実施例2からのアミノ改変オリゴヌクレオチドを0.1Mホウ酸ナトリウム緩衝液pH8.5緩衝液(c=600μmol)に溶解し、Thermo ScientificからのDMF(c=3mg/100μl)に溶解した18倍モル過剰のSulfo SMCC(スルホスクシンイミジル4-[N-マレイミドメチル]シクロヘキサン-1-カルボキシレートと反応させた。スルホ-SMCC 4-[N-マレイミドメチル]シクロヘキサン-1-カルボキシレートの加水分解産物を除去するために反応産物を水に対して徹底的に透析した。
オリゴヌクレオチドを、標準的な方法によってABI394合成機において固体支持体として市販のdT-CPGならびに標準的なdA(bz)、dT、dG(iBu)、およびdC(Bz)ホスホルアミダイト(Sigma Aldrich)を用いて10μmolスケールでトリチルオン形式で合成した。
- スペーサーホスホルアミダイト18(18-O-ジメトキシトリチルヘキサエチレングリコール,1-[(2-シアノエチル)-(N,N-ジイソプロピル)]-ホスホルアミダイト(Glen Research);
- ビオチン-dT(5'-ジメトキシトリチルオキシ-5-[N-((4-t-ブチルベンゾイル)-ビオチニル)-アミノヘキシル)-3-アクリルイミド]-2'-デオキシウリジン-3'-[(2-シアノエチル)-(N,N-ジイソプロピル)]-ホスホルアミダイト(Glen Research);
- ビオチンホスホルアミダイト1-ジメトキシトリチルオキシ-2-(N-ビオチニル-4-アミノブチル)-プロピル-3-O-(2-シアノエチル)-(N,N-ジイソプロピル)-ホスホルアミダイト、ならびに
- アミノ改変の場合は、5'-ジメトキシトリチル-5-[N-(トリフルオロアセチルアミノヘキシル)-3-アクリルイミド]-2'-デオキシウリジン、3'-[(2-シアノエチル)-(N,N-ジイソプロピル)]-ホスホルアミダイト、およびジゴキシゲニン-N-ヒドロキシル-スクシンイミジルエステルによる後標識。
A)IgGの切断およびss-DNAによるFAB'断片の標識
精製モノクローナル抗体をペプシンプロテアーゼの助けを借りて切断して、F(ab')2断片を得る。その後、低濃度のシステアミンを用いて37℃で処理することによってF(ab')2断片をFAB'断片に還元する。PD10カラムによってシステアミンを分離することによって反応を止める。実施例3に従って生成されたように、FAB'断片を活性化オリゴヌクレオチドで標識する。この一本鎖DNA(=ss-DNA)は、FAB'ヒンジ領域のシステインと反応するチオール反応性マレイミド基を有する。高いパーセントの単一標識FAB'断片を得るために、ss-DNAとFAB'断片との相対モル比を低く保つ。単一標識FAB'断片(ss-DNA:FAB'=1:1)の精製はイオン交換クロマトグラフィー(カラム: Source 15 Q PE 4.6/100, Pharmacia/GE)を介して行われる。効率的な精製の検証は分析用ゲル濾過およびSDS-PAGEによって達成される。
抗pIGF-1R複合体は、IGF-1Rの細胞内ドメインの異なるエピトープを標的とする2つのFAB'断片に基づいている。すなわち、FAB'8.1.2は標的タンパク質のリン酸化部位(pTyr1346)を検出し、FAB'1.4.168は標的タンパク質の非リン酸化部位を検出する。FAB'断片は一本鎖DNA(ss-DNA)と共有結合的に連結されている。すなわち、FAB'1.4.168は、SEQ ID NO:05を含み、蛍光マーカーとしてフルオレセインを含有する17merのss-DNAに共有結合的に連結され、FAB'8.1.2は、SEQ ID NO:06を含み、蛍光マーカーとしてCy5を含有する19merのss-DNAに共有結合的に連結されている。以下では、共有結合的に結合された17merまたは19merのss-DNAを有する、これらのFABをそれぞれss-FAB'1.4.168およびss-FAB'8.1.2と名付けた。複合体の組み立ては、ss-FAB'断片の対応するss-DNAにハイブリダイズするリンカー(すなわち、2つの相補的ss-DNAオリゴヌクレオチド(それぞれ、SEQ ID NO:7およびSEQ ID NO:8)を含む架橋構築物によって媒介される。複合体の2つのss-FAB'断片間の距離は、それぞれ、スペーサー、例えば、C18スペーサー、または長さの異なるDNAを使用することによって改変することができる。
および(2)(=実施例2.4のリンカー10)
を等モル量で室温で混合した。1分間のインキュベーション工程後、反応ミックスを分析用ゲル濾過カラム(Superdex(商標)200, 10/300 GL, GE Healthcare)によって分析した。単一複合体成分の溶出量(VE)を反応ミックスのVEと比較することによって、複合体は首尾よく形成されたことが証明される(図10)。
この実験のために、BIAcore 2000機器(GE Healthcare)を、このシステムに組み込んだBIAcore SAセンサーと一緒にT=25℃で使用した。プレコンディショニングは、100μl/minで、50mM NaOHに溶解した1M NaClの3x1分間の注入および10mM HClの1分間の注入を用いて行われた。
上にハイブリダイズしたss-FAB'8.1.2およびss-FAB'1.4.168からなる100nM二価結合剤、ならびにリンカー(1)
上にハイブリダイズしたss-FAB'8.1.2およびss-FAB'1.4.168からなる100nM二価結合剤の1つをそれぞれ4つ全てのフローセルに注入した。
BIAcore T100機器(GE Healthcare)を、このシステムに取り付けたBIAcore CM5センサーと一緒に使用した。0.1%SDS、50mM NaOH、10mM HCl、および100mM H3PO4を100μl/minで1分間注入することによってセンサーをプレコンディショニングした。
BIAcore 3000機器(GE Healthcare)を、このシステムに組み込んだBIAcore SAセンサーと一緒にT=25℃で使用した。50mM NaOHに溶解した1M NaClを3x1分間および10mM HClを1分間、注入することによって100μl/minでセンサーをプレコンディショニングした。
および1042RUビオチン化23.7kDa T40-Bi 77 merのss-DNA-リンカー(2)
を捕獲した。
結合アッセイ-インビトロおよびエクスビボ
検出オリゴヌクレオチドプローブ-Cy5
ss-L-DNA検出オリゴヌクレオチドプローブ-Cy5
は最新式のオリゴヌクレオチド合成法によって合成された。Cy5色素の導入はアミノ基とCy5単一反応性(monoreactive)NHSエステル(GE Healthcare Lifescience, STADT, LAND)との反応を介して行われた。ヌクレオチドの場合、L-DNAアミダイト(ChemGenes, STADT, LAND)を使用した。固相オリゴヌクレオチド合成プロセスの間に5'アミノ基および3'アミノ基を導入した。式中、Y=(6-(4-モノメトキシトリチルアミノ)ヘキシル-(2-シアノエチル)-(N,N-ジイソプロピル)-ホスホルアミダイト(Glen Research)を介して導入された5'-アミノ-修飾因子C6、およびZ=3'アミノ修飾因子(Aminomodifier)TFAアミノC6長鎖アミノアルキル多孔性ガラス1000A(ChemGenes)を介して導入された3'-アミノ修飾因子C6。
等モル化学量論のFITC標識抗HER2抗体2C4-FAB'-ss-L-DNAおよびFITC標識抗HER2抗体4D5-FAB'-ss-L-DNAをSEQ ID NO:73のss-L-DNAリンカーとハイブリダイズすることによって複合体を組み立てた。複合体の正しい組み立てを検証するために、複合体をSECクロマトグラフィー工程に供し、滅菌フィルターで濾過した。
2x106細胞/mlの濃度のヒト乳癌KPL-4細胞を30μlの体積でμ-slides VI(ibidi, Germany)に播種した。3時間後、細胞が付着するように70μlの培地(RPMI1640、2mM L-グルタミン、10%FCS)を添加した。
(同所に移植した)確立したKPL-4腫瘍を有する免疫不全SCIDベージュマウスに、100μlのPBSに溶解した50μgの複合体をi.v.注射し、18時間後に等モル濃度(2.63μg/マウス)のCy5標識DNAプローブを注射した。48時間後に腫瘍を外植し、MAESTROシステム(CRi, Cambridge, USA)を用いてマルチスペクトル蛍光分析によって調べた。
インビトロ結合アッセイ
複合体を、そのFAB'-ss-L-DNA成分のそれぞれを介してFITCで二重標識する。検出プローブは二重Cy5標識ss-L-DNA 20merオリゴヌクレオチドプローブであり、複合体の95 merのss-L-DNAリンカーにハイブリダイズすることができる。
図24(左画像)に図示したように、試料を最初に複合体とインキュベートし、その後にCy5標識検出プローブとインキュベートした実験の場では強い蛍光シグナルを検出することができる。対照的に(右画像)、KPL-4異種移植片にCy5標識検出プローブのみを予め注射した腫瘍では蛍光シグナルを検出することはできなかった。
MDA-MB-175乳癌細胞株における細胞増殖の阻害
10%胎仔ウシ血清、2mMグルタミン、およびペニシリン/ストレプトマイシンを補充したDMEM/F12培地中で培養した2x104個のMDA-MB-175乳癌細胞を96ウェルプレートに播種した。翌日、示された濃度(40〜0.0063μg/ml)の抗体および複合体をそれぞれ添加した。6日間のインキュベーション後に、Alamar Blueを添加し、プレートを組織培養インキュベーターに入れて3〜4時間インキュベートした。蛍光を測定した(励起530nm/発光590)。パーセント阻害を参照として未処理細胞を用いて計算した。
抗HER2抗体2C4(ペルツズマブ)は44%の最大阻害を示した。抗HER2抗体ハーセプチンは9%の最大阻害を示した。ペルツズマブおよびハーセプチン(登録商標)のFAB断片を含む、本明細書において報告される複合体は46%の最大阻害を示す。
複合体の凍結融解-安定性
等モル化学量論のFITC標識抗HER2抗体2C4-FAB'-ss-L-DNAおよびFITC標識抗HER2抗体4D5-FAB'-ss-L-DNAをSEQ ID NO:73のss-L-DNAリンカーとハイブリダイズすることによって複合体を組み立てた。複合体の正しい組み立てを検証するために、複合体をSECクロマトグラフィー工程に供し、滅菌フィルターで濾過した。
結合実体のクローニングおよび発現
基本的/標準的な哺乳動物発現プラスミドの説明
望ましいタンパク質をヒト胎児由来腎臓細胞(HEK293)の一過的トランスフェクションによって発現させた。望ましい遺伝子/タンパク質を発現させるために、以下の機能エレメント:
- イントロンAを含むヒトサイトメガロウイルス(P-CMV)に由来する最初期エンハンサーおよびプロモーター、
- ヒト重鎖免疫グロブリン5'-非翻訳領域(5'UTR)、
- マウス免疫グロブリン重鎖シグナル配列(SS)、
- 発現させようとする遺伝子/タンパク質(例えば、完全長抗体重鎖)、および
- ウシ成長ホルモンポリアデニル化配列(BGHpA)
を含む転写単位を使用した。
- 大腸菌において、このプラスミドの複製を可能にする、ベクターpUC18に由来する複製起点、および
- 大腸菌においてアンピシリン耐性を付与するβラクタマーゼ遺伝子
を含有する。
最初に、結合実体(例えば、抗体Fab断片)をコードする構築物のクローニングを行った。結合実体をコードする核酸を有するプラスミドは、通常、遺伝子合成によって得られ、それによって、コードされる結合実体のC末端領域はソルターゼ-モチーフおよびHis-タグを含有する。プラスミドを個々にマルチウェルプレートの別々のウェルに移す(プレート全体に添加することができる)。その後、プラスミドを、結合実体コード領域を切断する制限酵素ミックスで消化する。全てのプラスミドに1つだけの制限酵素ミックスが必要とされるやり方で全ての遺伝子合成を設計することが望ましい。その後、最適な洗浄工程によって、精製されたDNA断片が得られる。これらの断片を、前述されたものと同じ制限ミックスを用いてアクセプターベクターから切断されたプラスミドバックボーンに連結する。代替として、SLICを介したクローニング工程によってクローニング手順を実施することができる。連結後、自動プラットフォームによって、全ての連結ミックスが、コンピテントな大腸菌細胞(例えば、Top 10 Multi Shot, Invitrogen)が入っているさらなるマルチウェルプレートに移され、形質転換反応が行われる。細胞を望ましい密度まで培養する。培養混合物のアリコートからグリセロールストックを入手することができる。(例えば、プラスミド単離ミニキット(例えば、NucleoSpin 96 Plasmid, Macherey& Nagel)を用いて)培養物からプラスミドを単離する。アリコートを適切な制限ミックスによる消化およびSDS-ゲル電気泳動(例えば、E-Gel 48, Invitrogen)によってプラスミド同一性をチェックする。その後、対照配列決定反応を行うために新たなプレートにプラスミドアリコートを添加することができる。
F17 Medium(Invitrogen Corp.)中で培養したHEK293細胞(ヒト胎児由来腎臓細胞株293由来)の一過的トランスフェクションによって抗体Fab断片を作製した。トランスフェクションのために、「293-Fectin」Transfection Reagent (Invitrogen)を使用した。抗体Fab断片を、完全長軽鎖およびC末端LPXTG配列(SEQ ID NO:74)を含有する対応する切断型重鎖をコードする2つの異なるプラスミドから発現させた。トランスフェクションの際に2つのプラスミドを等モルプラスミド比で使用した。製造業者の説明書に明記されたようにトランスフェクションを行った。トランスフェクションの7日後に、抗体Fab断片を含有する細胞培養上清を収集した。精製するまで上清を凍結温度で保管した。
抗体Fab断片-オリゴヌクレオチド結合体の連結を解した二重特異性結合分子の作製
抗体Fab断片とオリゴヌクレオチドとのカップリングを酵素ソルターゼAを用いて行った。これによって、LPXTGペプチド(SEQ ID NO:74)を含有する部分を有する分子を、GG部分を有する別の分子に共有結合的に取り付けた。従って、オリゴヌクレオチドには部分の一方があったが、抗体Fab断片にはそれぞれの他方の部分があった。酵素反応はターンオーバーが多く、特異性が高く、副産物が少なく、有害な廃棄物が少ないので化学反応より有利な場合がある。
インキュベーションは37℃で4〜16時間であった。
を含めて一緒にピペットで取る。リンカーDNAはその5'末端が第1の抗体Fab断片-オリゴヌクレオチド結合体とハイブリダイズするのに対して、その3'末端は第2の抗体Fab断片-オリゴヌクレオチド結合体に相補的であり、それによって、2つの異なる抗体Fab断片-オリゴヌクレオチド結合体の間に物理的な接続が確立される。適切なハイブリダイゼーションのために、溶液を60℃に加熱し、次いで、ゆっくりと室温まで冷却し、その後に保管のために4℃まで冷却する。短期間のプロトコールの場合、室温で数分間でも十分である。
多量の二重特異性結合分子が必要とされる場合、または他の制約がある場合、いわゆる調製アプローチを適用することができる。これによって、ソルターゼ反応混合物をランニングバッファーとして1xPBSを用いてSuperdex200カラムにアプライする。画分を0.4ml体積で収集する。その後、抗体Fab断片-オリゴヌクレオチド結合体を含有する画分を確かめるために全ての関連画分のアリコートをLabChipシステム(Perkin Elmer)を介して分析する。さらに、全ての関連画分のアリコートをアガロース-ゲルに添加し、それによって、いわゆるキャッチャー(catcher)オリゴヌクレオチドを試料に添加した後に、ゲルにアプライする。このキャッチャーオリゴヌクレオチドは抗体Fab断片-オリゴヌクレオチド結合体のオリゴヌクレオチドに相補的であり、その結果としてdsDNA部分となり、抗体Fab断片-オリゴヌクレオチド結合体のssDNA単独より容易にアガロースゲル上で容易に視覚化することができる。(LabChipシステム上で分かるように)抗体Fab断片-オリゴヌクレオチド結合体を含有し、かつ(アガロースゲル上で分かるように)遊離オリゴヌクレオチドを含有しない画分をプールし、必要に応じて、限外濾過、例えば、Amicon Ultra 0.5ML,10K(Millipore)を用いた限外濾過によって濃縮する。連結反応のために、2つの抗体Fab断片-オリゴヌクレオチド結合体分子を等モル比でリンカーL-DNAを含めて一緒にピペットで取り、前のセクションにおいて概説したように処理する。
Claims (18)
- (i)試料中の細胞の表面に存在する表面マーカーを決定し、かつ第1の表面マーカーおよび第2の表面マーカーを選択する工程、
(ii)(a)第1の結合ペアの第1のメンバーと結合体化された抗体Fab断片またはscFv抗体断片であって、それによって第1の表面マーカーに特異的に結合する、抗体Fab断片またはscFv抗体断片、(b)第2の結合ペアの第1のメンバーと結合体化された抗体Fab断片またはscFv抗体断片であって、それによって第2の表面マーカーに特異的に結合する、抗体Fab断片またはscFv抗体断片、および(c)末端の一方において第1の結合ペアの第2のメンバーを含み、それぞれの他方の末端において第2の結合ペアの第2のメンバーを含むエナンチオマーDNAポリヌクレオチドリンカー
をインキュベートし、かつそれによって二重特異性抗体を生成する工程
を含む、二重特異性抗体を生成するための方法。 - (i)それぞれが第1の結合ペアの同じ第1のメンバーに連結された第1の多数群の抗体Fab断片またはscFv抗体断片の各メンバーを、それぞれが第2の結合ペアの同じ第1のメンバーに連結された第2の多数群の抗体Fab断片またはscFv抗体断片の各メンバーと、および末端の一方において第1の結合ペアの第2のメンバーを含み、かつそれぞれの他方の末端において第2の結合ペアの第2のメンバーを含むエナンチオマーDNAポリヌクレオチドリンカーと、組み合わせることによって調製された多数の二重特異性抗体の結合特異性および/または親和性および/またはエフェクター機能および/またはインビボ半減期を、インビトロで、エクスビボで、および/または非ヒト動物においてインビボで決定する工程であって、それによって第1の多数群が第1の細胞表面マーカーに特異的に結合し、第2の多数群が第2の細胞表面マーカーに特異的に結合する、工程、ならびに
(ii)適切な結合特異性および/または親和性および/またはエフェクター機能および/またはインビボ半減期を有する二重特異性抗体を選択し、かつそれによって抗原結合部位の組み合わせを決定する工程
を含む、抗原結合部位の組み合わせを決定するための方法。 - 二重特異性抗体が、
(a)(i)第1の表面マーカーに特異的に結合し、かつ
(ii)第1の結合ペアの第1のメンバーと結合体化された
第1のFab断片またはscFv抗体断片、
(b)(i)第2の表面マーカーに特異的に結合し、かつ
(ii)第2の結合ペアの第1のメンバーと結合体化された
第2のFab断片またはscFv抗体断片、および
(c)(i)第1の結合ペアの第2のメンバーと結合体化され、かつ
(ii)第2の結合ペアの第2のメンバーと結合体化された
エナンチオマーDNAポリヌクレオチドリンカー
を含む複合体であることを特徴とする、請求項1または2記載の方法。 - 複合体が非共有結合複合体であることを特徴とする、請求項3記載の方法。
- 結合ペアがポリヌクレオチドの相補的ペアであることを特徴とする、請求項1〜4のいずれか一項記載の方法。
- 複合体が、リンカーの少なくとも一部に相補的なポリヌクレオチドと結合体化されたエフェクター部分をさらに含む、請求項3または4記載の方法。
- 第1のエフェクター部分と結合体化されたポリヌクレオチドの少なくとも一部に相補的であり、かつ(ii)ポリヌクレオチドリンカーに相補的でない、ポリヌクレオチド
と結合体化された第2のエフェクター部分を、複合体が含むことを特徴とする、請求項6記載の方法。 - 第1および第2のFab断片またはscFv抗体断片が、同じ標的およびその上にある非重複エピトープに結合することを特徴とする、請求項1〜7のいずれか一項記載の方法。
- ポリヌクレオチドリンカーが8〜1000個のヌクレオチドを含むことを特徴とする、請求項1〜8のいずれか一項記載の方法。
- ポリヌクレオチドリンカーが10〜500個のヌクレオチドを含むことを特徴とする、請求項1〜9のいずれか一項記載の方法。
- エナンチオマーDNAがL-DNAであることを特徴とする、請求項1〜10のいずれか一項記載の方法。
- L-DNAが一本鎖L-DNA(ss-L-DNA)であることを特徴とする、請求項11記載の方法。
- 請求項1〜12のいずれか一項記載の方法によって得られた二重特異性抗体と、任意で薬学的に許容される担体とを含む、癌を治療するための薬学的製剤。
- 請求項1〜12のいずれか一項記載の方法によって得られた二重特異性抗体を含む、癌を治療するための医薬。
- 癌を治療するための医薬の製造における、請求項1〜12のいずれか一項記載の方法によって得られた二重特異性抗体の使用。
- 二重特異性抗体と、任意で薬学的に許容される担体とを含む、癌を治療するための薬学的製剤であって、該二重特異性抗体が
(a)(i)第1の表面マーカーに特異的に結合し、かつ
(ii)第1の結合ペアの第1のメンバーと結合体化された
第1のFab断片またはscFv抗体断片、
(b)(i)第2の表面マーカーに特異的に結合し、かつ
(ii)第2の結合ペアの第1のメンバーと結合体化された
第2のFab断片またはscFv抗体断片、および
(c)(i)第1の結合ペアの第2のメンバーと結合体化され、かつ
(ii)第2の結合ペアの第2のメンバーと結合体化された
エナンチオマーDNAポリヌクレオチドリンカー
を含む二重特異性抗体であって、それによって第1および第2のFab断片またはscFv抗体断片ならびにエナンチオマーDNAポリヌクレオチドリンカーが非共有結合複合体を形成する二重特異性抗体であることを特徴とする、薬学的製剤。 - 二重特異性抗体を含む、癌を治療するための医薬であって、該二重特異性抗体が
(a)(i)第1の表面マーカーに特異的に結合し、かつ
(ii)第1の結合ペアの第1のメンバーと結合体化された
第1のFab断片またはscFv抗体断片、
(b)(i)第2の表面マーカーに特異的に結合し、かつ
(ii)第2の結合ペアの第1のメンバーと結合体化された
第2のFab断片またはscFv抗体断片、および
(c)(i)第1の結合ペアの第2のメンバーと結合体化され、かつ
(ii)第2の結合ペアの第2のメンバーと結合体化された
エナンチオマーDNAポリヌクレオチドリンカー
を含む二重特異性抗体であって、それによって第1および第2のFab断片またはscFv抗体断片ならびにエナンチオマーDNAポリヌクレオチドリンカーが非共有結合複合体を形成する二重特異性抗体であることを特徴とする、医薬。 - 癌を治療するための医薬の製造における、二重特異性抗体の使用であって、該二重特異性抗体が
(a)(i)第1の表面マーカーに特異的に結合し、かつ
(ii)第1の結合ペアの第1のメンバーと結合体化された
第1のFab断片またはscFv抗体断片、
(b)(i)第2の表面マーカーに特異的に結合し、かつ
(ii)第2の結合ペアの第1のメンバーと結合体化された
第2のFab断片またはscFv抗体断片、および
(c)(i)第1の結合ペアの第2のメンバーと結合体化され、かつ
(ii)第2の結合ペアの第2のメンバーと結合体化された
エナンチオマーDNAポリヌクレオチドリンカー
を含む二重特異性抗体であって、それによって第1および第2のFab断片またはscFv抗体断片ならびにエナンチオマーDNAポリヌクレオチドリンカーが非共有結合複合体を形成する二重特異性抗体であることを特徴とする、使用。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP12173878 | 2012-06-27 | ||
| EP12173878.5 | 2012-06-27 | ||
| PCT/EP2013/063260 WO2014001326A1 (en) | 2012-06-27 | 2013-06-25 | Method for the selection and production of tailor-made, selective and multi-specific therapeutic molecules comprising at least two different targeting entities and uses thereof |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2015522265A JP2015522265A (ja) | 2015-08-06 |
| JP6445429B2 true JP6445429B2 (ja) | 2018-12-26 |
Family
ID=48748178
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2015519058A Expired - Fee Related JP6445429B2 (ja) | 2012-06-27 | 2013-06-25 | 少なくとも2つの異なる標的化実体を含むテーラーメイドで選択的かつ多重特異性治療用分子を選択および作製するための方法およびその使用 |
Country Status (10)
| Country | Link |
|---|---|
| US (1) | US20150232560A1 (ja) |
| EP (1) | EP2867255B1 (ja) |
| JP (1) | JP6445429B2 (ja) |
| KR (1) | KR20150023906A (ja) |
| CN (1) | CN104395340B9 (ja) |
| BR (1) | BR112014029888A2 (ja) |
| CA (1) | CA2871386A1 (ja) |
| MX (1) | MX2014014065A (ja) |
| RU (1) | RU2644263C2 (ja) |
| WO (1) | WO2014001326A1 (ja) |
Families Citing this family (67)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN102369214B (zh) | 2009-04-07 | 2019-04-12 | 罗氏格黎卡特股份公司 | 三价、双特异性抗体 |
| US9676845B2 (en) | 2009-06-16 | 2017-06-13 | Hoffmann-La Roche, Inc. | Bispecific antigen binding proteins |
| WO2011034605A2 (en) | 2009-09-16 | 2011-03-24 | Genentech, Inc. | Coiled coil and/or tether containing protein complexes and uses thereof |
| AR080793A1 (es) | 2010-03-26 | 2012-05-09 | Roche Glycart Ag | Anticuerpos biespecificos |
| RU2013110875A (ru) | 2010-08-24 | 2014-09-27 | Ф.Хоффманн-Ля Рош Аг | БИСПЕЦИФИЧЕСКИЕ АНТИТЕЛА, СОДЕРЖАЩИЕ СТАБИЛИЗИРОВАННЫЙ ДИСУЛЬФИДОМ ФРАГМЕНТ Fv |
| JP5766296B2 (ja) | 2010-12-23 | 2015-08-19 | エフ.ホフマン−ラ ロシュ アーゲーF. Hoffmann−La Roche Aktiengesellschaft | ポリペプチド−ポリヌクレオチド複合体、およびエフェクター成分の標的化された送達におけるその使用 |
| JP5764677B2 (ja) | 2011-02-28 | 2015-08-19 | エフ・ホフマン−ラ・ロシュ・アクチェンゲゼルシャフト | 抗原結合タンパク質 |
| MX2014009565A (es) | 2012-02-10 | 2014-11-10 | Genentech Inc | Anticuerpos monocatenarios y otros heteromultimeros. |
| RU2015100656A (ru) | 2012-06-27 | 2016-08-20 | Ф. Хоффманн-Ля Рош Аг | Способ получения конъюгатов fc-фрагмента антитела, включающих по меньшей мере одну связывающую группировку, которая специфически связывается с мишенью, и их применения |
| JP6203838B2 (ja) | 2012-06-27 | 2017-09-27 | エフ.ホフマン−ラ ロシュ アーゲーF. Hoffmann−La Roche Aktiengesellschaft | 少なくとも2つの異なる結合実体を含む、テーラーメイドの高度に選択的かつ多重特異的なターゲティング実体を選択および作製するための方法、ならびにその使用 |
| WO2014041072A1 (en) | 2012-09-14 | 2014-03-20 | F. Hoffmann-La Roche Ag | Method for the production and selection of molecules comprising at least two different entities and uses thereof |
| JP6346265B2 (ja) | 2013-03-21 | 2018-06-20 | ジェニスフィア・エルエルシー | Dnaインターカレーティング剤の細胞送達 |
| BR112016006929A2 (pt) | 2013-10-11 | 2017-09-19 | Hoffmann La Roche | Anticorpo, ácido nucleico, vetor de expressão, célula hospedeira, métodos de preparação de anticorpo, de tratamento de pacientes e de geração de um anticorpo, composição farmacêutica e uso do anticorpo |
| WO2015148126A1 (en) * | 2014-03-12 | 2015-10-01 | Invictus Oncology Pvt. Ltd. | Targeted drug delivery through affinity based linkers |
| GB2587768B (en) * | 2014-04-03 | 2021-08-18 | T Gjerde Douglas | Devices and methods for purification, detection and use of biological cells |
| GB201409558D0 (en) * | 2014-05-29 | 2014-07-16 | Ucb Biopharma Sprl | Method |
| GB201412659D0 (en) | 2014-07-16 | 2014-08-27 | Ucb Biopharma Sprl | Molecules |
| GB201412658D0 (en) | 2014-07-16 | 2014-08-27 | Ucb Biopharma Sprl | Molecules |
| WO2016087416A1 (en) | 2014-12-03 | 2016-06-09 | F. Hoffmann-La Roche Ag | Multispecific antibodies |
| WO2016145416A2 (en) * | 2015-03-11 | 2016-09-15 | The Broad Institute, Inc. | Proteomic analysis with nucleic acid identifiers |
| AR104368A1 (es) * | 2015-04-03 | 2017-07-19 | Lilly Co Eli | Anticuerpos biespecíficos anti-cd20- / anti-baff |
| GB201601077D0 (en) | 2016-01-20 | 2016-03-02 | Ucb Biopharma Sprl | Antibody molecule |
| GB201601075D0 (en) | 2016-01-20 | 2016-03-02 | Ucb Biopharma Sprl | Antibodies molecules |
| GB201601073D0 (en) | 2016-01-20 | 2016-03-02 | Ucb Biopharma Sprl | Antibodies |
| GB201521389D0 (en) | 2015-12-03 | 2016-01-20 | Ucb Biopharma Sprl | Method |
| GB201521382D0 (en) | 2015-12-03 | 2016-01-20 | Ucb Biopharma Sprl | Antibodies |
| GB201521383D0 (en) * | 2015-12-03 | 2016-01-20 | Ucb Biopharma Sprl And Ucb Celltech | Method |
| GB201521391D0 (en) * | 2015-12-03 | 2016-01-20 | Ucb Biopharma Sprl | Antibodies |
| GB201521393D0 (en) * | 2015-12-03 | 2016-01-20 | Ucb Biopharma Sprl | Antibodies |
| IL260983B (en) | 2016-02-19 | 2022-07-01 | Genisphere Llc | Nucleic acid carriers and methods of medical use |
| EP3416691A4 (en) | 2016-02-19 | 2020-02-26 | Genisphere, LLC | SUPPORTS OF NUCLEIC ACIDS AND THEIR THERAPEUTIC METHODS OF USE |
| WO2017153336A1 (en) | 2016-03-07 | 2017-09-14 | F. Hoffmann-La Roche Ag | Detection of anti-p53 antibodies |
| CA3016563A1 (en) | 2016-03-21 | 2017-09-28 | Elstar Therapeutics, Inc. | Multispecific and multifunctional molecules and uses thereof |
| US10738338B2 (en) | 2016-10-18 | 2020-08-11 | The Research Foundation for the State University | Method and composition for biocatalytic protein-oligonucleotide conjugation and protein-oligonucleotide conjugate |
| CN108264561B (zh) * | 2016-12-30 | 2021-09-10 | 惠和生物技术(上海)有限公司 | 一种结合cd19、cd3和t细胞负共刺激分子的三功能分子及其应用 |
| US20200291089A1 (en) | 2017-02-16 | 2020-09-17 | Elstar Therapeutics, Inc. | Multifunctional molecules comprising a trimeric ligand and uses thereof |
| JP7373998B2 (ja) | 2017-05-02 | 2023-11-06 | コーネル・ユニバーシティー | 有効性がより大きくかつ毒性がより少ない腫瘍標的指向方法及び試薬 |
| CN108866635B (zh) * | 2017-05-09 | 2021-11-26 | 安升(上海)医药科技有限公司 | 多特异性蛋白药物及其文库、以及制备方法和应用 |
| WO2018222901A1 (en) | 2017-05-31 | 2018-12-06 | Elstar Therapeutics, Inc. | Multispecific molecules that bind to myeloproliferative leukemia (mpl) protein and uses thereof |
| WO2019035938A1 (en) | 2017-08-16 | 2019-02-21 | Elstar Therapeutics, Inc. | MULTISPECIFIC MOLECULES BINDING TO BCMA AND USES THEREOF |
| CN108179134B (zh) * | 2017-12-27 | 2020-11-24 | 武汉大学 | 基于EpCAM/PSMA双抗体功能化微流控芯片及其制备方法和应用 |
| US12247060B2 (en) | 2018-01-09 | 2025-03-11 | Marengo Therapeutics, Inc. | Calreticulin binding constructs and engineered T cells for the treatment of diseases |
| WO2019178362A1 (en) | 2018-03-14 | 2019-09-19 | Elstar Therapeutics, Inc. | Multifunctional molecules that bind to calreticulin and uses thereof |
| WO2019178364A2 (en) | 2018-03-14 | 2019-09-19 | Elstar Therapeutics, Inc. | Multifunctional molecules and uses thereof |
| GB201810327D0 (en) * | 2018-06-22 | 2018-08-08 | Bicycletx Ltd | Peptide ligands for binding to IL-17 |
| CA3105448A1 (en) | 2018-07-03 | 2020-01-09 | Elstar Therapeutics, Inc. | Anti-tcr antibody molecules and uses thereof |
| EP3670666A1 (en) * | 2018-12-20 | 2020-06-24 | Freie Universität Berlin | Method for optical imaging a target molecule in a sample, a protein-oligonuleotide conjugate for use in the method and a kit for carrying out the method |
| WO2020167447A2 (en) | 2019-02-15 | 2020-08-20 | Illumina, Inc. | Sensing systems |
| CN114127112A (zh) | 2019-02-21 | 2022-03-01 | 马伦戈治疗公司 | 与t细胞结合的多功能分子及其治疗自身免疫性病症的用途 |
| EP3927744A1 (en) | 2019-02-21 | 2021-12-29 | Marengo Therapeutics, Inc. | Multifunctional molecules that bind to t cell related cancer cells and uses thereof |
| EP3927431A1 (en) | 2019-02-21 | 2021-12-29 | Marengo Therapeutics, Inc. | Anti-tcr antibody molecules and uses thereof |
| EP3927746A1 (en) | 2019-02-21 | 2021-12-29 | Marengo Therapeutics, Inc. | Multifunctional molecules that bind to calreticulin and uses thereof |
| GB2597851B (en) | 2019-02-21 | 2024-05-29 | Marengo Therapeutics Inc | Antibody molecules that bind to NKP30 and uses thereof |
| FR3099066B1 (fr) | 2019-07-26 | 2021-08-13 | Novasep Process | Procédé de purification d’une substance cible avec inactivation virale |
| WO2021071876A1 (en) * | 2019-10-10 | 2021-04-15 | University Of Massachusetts | Photolytic compounds and triplet-triplet annihilation mediated photolysis |
| CN112746331A (zh) * | 2019-10-29 | 2021-05-04 | 安升(上海)医药科技有限公司 | 半衰期延长的药物及其文库、以及制备方法和应用 |
| WO2021138407A2 (en) | 2020-01-03 | 2021-07-08 | Marengo Therapeutics, Inc. | Multifunctional molecules that bind to cd33 and uses thereof |
| EP4084823A4 (en) | 2020-01-03 | 2024-05-15 | Marengo Therapeutics, Inc. | ANTI-TCR ANTIBODY MOLECULES AND THEIR USES |
| CA3180321A1 (en) | 2020-04-24 | 2021-10-28 | Marengo Therapeutics, Inc. | Multifunctional molecules that bind to t cell related cancer cells and uses thereof |
| WO2022046920A2 (en) | 2020-08-26 | 2022-03-03 | Marengo Therapeutics, Inc. | Multifunctional molecules that bind to calreticulin and uses thereof |
| JP2023540248A (ja) | 2020-08-26 | 2023-09-22 | マレンゴ・セラピューティクス,インコーポレーテッド | Trbc1またはtrbc2を検出する方法 |
| GB2616128A (en) | 2020-08-26 | 2023-08-30 | Marengo Therapeutics Inc | Antibody molecules that bind to NKp30 and uses thereof |
| KR20240004462A (ko) | 2021-04-08 | 2024-01-11 | 마렝고 테라퓨틱스, 인크. | Tcr에 결합하는 다기능성 분자 및 이의 용도 |
| US12060148B2 (en) | 2022-08-16 | 2024-08-13 | Honeywell International Inc. | Ground resonance detection and warning system and method |
| WO2026011013A1 (en) | 2024-07-02 | 2026-01-08 | Epibiologics, Inc. | Binding agents and uses thereof |
| WO2026037839A2 (en) | 2024-08-12 | 2026-02-19 | ONA Therapeutics S.L. | Anti-fgfr4 molecules and uses thereof |
| WO2026050572A2 (en) | 2024-08-29 | 2026-03-05 | Marengo Therapeutics, Inc. | Multifunctional molecules binding to tcr and uses thereof |
Family Cites Families (81)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4150149A (en) | 1976-11-29 | 1979-04-17 | Professional Staff Association Of The Los Angeles County Harbor General Hospital | Method and means for the early detection and diagnosis of certain types of cancers |
| USRE30985E (en) | 1978-01-01 | 1982-06-29 | Serum-free cell culture media | |
| US4444744A (en) | 1980-03-03 | 1984-04-24 | Goldenberg Milton David | Tumor localization and therapy with labeled antibodies to cell surface antigens |
| US4361544A (en) | 1980-03-03 | 1982-11-30 | Goldenberg Milton David | Tumor localization and therapy with labeled antibodies specific to intracellular tumor-associated markers |
| GB2095818B (en) | 1981-03-27 | 1985-10-02 | Exxon Research Engineering Co | Staged adsorption/resorption heat pump |
| US4560655A (en) | 1982-12-16 | 1985-12-24 | Immunex Corporation | Serum-free cell culture medium and process for making same |
| US4657866A (en) | 1982-12-21 | 1987-04-14 | Sudhir Kumar | Serum-free, synthetic, completely chemically defined tissue culture media |
| US4816567A (en) | 1983-04-08 | 1989-03-28 | Genentech, Inc. | Recombinant immunoglobin preparations |
| US4767704A (en) | 1983-10-07 | 1988-08-30 | Columbia University In The City Of New York | Protein-free culture medium |
| GB8516415D0 (en) | 1985-06-28 | 1985-07-31 | Celltech Ltd | Culture of animal cells |
| US4927762A (en) | 1986-04-01 | 1990-05-22 | Cell Enterprises, Inc. | Cell culture medium with antioxidant |
| US5606040A (en) | 1987-10-30 | 1997-02-25 | American Cyanamid Company | Antitumor and antibacterial substituted disulfide derivatives prepared from compounds possessing a methyl-trithio group |
| US5770701A (en) | 1987-10-30 | 1998-06-23 | American Cyanamid Company | Process for preparing targeted forms of methyltrithio antitumor agents |
| DE68925971T2 (de) | 1988-09-23 | 1996-09-05 | Cetus Oncology Corp | Zellenzuchtmedium für erhöhtes zellenwachstum, zur erhöhung der langlebigkeit und expression der produkte |
| FI903489A0 (fi) | 1988-11-11 | 1990-07-10 | Medical Res Council | Ligander med en enda sektion, receptorer innehaollande naemnda ligander, foerfaranden foer deras framstaellning samt anvaendning av liganderna och receptorerna. |
| DE3920358A1 (de) | 1989-06-22 | 1991-01-17 | Behringwerke Ag | Bispezifische und oligospezifische, mono- und oligovalente antikoerperkonstrukte, ihre herstellung und verwendung |
| CA2026147C (en) | 1989-10-25 | 2006-02-07 | Ravi J. Chari | Cytotoxic agents comprising maytansinoids and their therapeutic use |
| US5208020A (en) | 1989-10-25 | 1993-05-04 | Immunogen Inc. | Cytotoxic agents comprising maytansinoids and their therapeutic use |
| US5959177A (en) | 1989-10-27 | 1999-09-28 | The Scripps Research Institute | Transgenic plants expressing assembled secretory antibodies |
| GB9015198D0 (en) | 1990-07-10 | 1990-08-29 | Brien Caroline J O | Binding substance |
| US5122469A (en) | 1990-10-03 | 1992-06-16 | Genentech, Inc. | Method for culturing Chinese hamster ovary cells to improve production of recombinant proteins |
| US5571894A (en) | 1991-02-05 | 1996-11-05 | Ciba-Geigy Corporation | Recombinant antibodies specific for a growth factor receptor |
| EP0940468A1 (en) | 1991-06-14 | 1999-09-08 | Genentech, Inc. | Humanized antibody variable domain |
| GB9114948D0 (en) | 1991-07-11 | 1991-08-28 | Pfizer Ltd | Process for preparing sertraline intermediates |
| EP0604580A1 (en) | 1991-09-19 | 1994-07-06 | Genentech, Inc. | EXPRESSION IN E. COLI OF ANTIBODY FRAGMENTS HAVING AT LEAST A CYSTEINE PRESENT AS A FREE THIOL, USE FOR THE PRODUCTION OF BIFUNCTIONAL F(ab') 2? ANTIBODIES |
| FI941572L (fi) | 1991-10-07 | 1994-05-27 | Oncologix Inc | Anti-erbB-2-monoklonaalisten vasta-aineiden yhdistelmä ja käyttömenetelmä |
| ATE463573T1 (de) | 1991-12-02 | 2010-04-15 | Medimmune Ltd | Herstellung von autoantikörpern auf phagenoberflächen ausgehend von antikörpersegmentbibliotheken |
| DE69333807T2 (de) | 1992-02-06 | 2006-02-02 | Chiron Corp., Emeryville | Marker für krebs und biosynthetisches bindeprotein dafür |
| WO1994010308A1 (en) | 1992-10-23 | 1994-05-11 | Immunex Corporation | Methods of preparing soluble, oligomeric proteins |
| EP1005870B1 (en) | 1992-11-13 | 2009-01-21 | Biogen Idec Inc. | Therapeutic application of chimeric antibodies to human B lymphocyte restricted differentiation antigen for treatment of B cell lymphoma |
| US5635483A (en) | 1992-12-03 | 1997-06-03 | Arizona Board Of Regents Acting On Behalf Of Arizona State University | Tumor inhibiting tetrapeptide bearing modified phenethyl amides |
| US5780588A (en) | 1993-01-26 | 1998-07-14 | Arizona Board Of Regents | Elucidation and synthesis of selected pentapeptides |
| DE4310141A1 (de) | 1993-03-29 | 1994-10-06 | Boehringer Mannheim Gmbh | Homobidentale trifunktionelle Linker |
| US5635602A (en) | 1993-08-13 | 1997-06-03 | The Regents Of The University Of California | Design and synthesis of bispecific DNA-antibody conjugates |
| CA2156924A1 (en) | 1993-12-27 | 1995-07-06 | Ton That Hai | Water soluble non-immunogenic polyamide cross-linking agents |
| US5773001A (en) | 1994-06-03 | 1998-06-30 | American Cyanamid Company | Conjugates of methyltrithio antitumor agents and intermediates for their synthesis |
| US5789199A (en) | 1994-11-03 | 1998-08-04 | Genentech, Inc. | Process for bacterial production of polypeptides |
| US5840523A (en) | 1995-03-01 | 1998-11-24 | Genetech, Inc. | Methods and compositions for secretion of heterologous polypeptides |
| US5869046A (en) | 1995-04-14 | 1999-02-09 | Genentech, Inc. | Altered polypeptides with increased half-life |
| US5714586A (en) | 1995-06-07 | 1998-02-03 | American Cyanamid Company | Methods for the preparation of monomeric calicheamicin derivative/carrier conjugates |
| AU6163196A (en) * | 1995-06-07 | 1996-12-30 | Smithkline Beecham Corporation | Method for obtaining receptor agonist antibodies |
| US5712374A (en) | 1995-06-07 | 1998-01-27 | American Cyanamid Company | Method for the preparation of substantiallly monomeric calicheamicin derivative/carrier conjugates |
| SE504798C2 (sv) * | 1995-06-16 | 1997-04-28 | Ulf Landegren | Immunanalys och testkit med två reagens som kan tvärbindas om de adsorberats till analyten |
| US6267958B1 (en) | 1995-07-27 | 2001-07-31 | Genentech, Inc. | Protein formulation |
| US6171586B1 (en) | 1997-06-13 | 2001-01-09 | Genentech, Inc. | Antibody formulation |
| JP2002501721A (ja) | 1997-08-01 | 2002-01-22 | モルフォシス・アクチェンゲゼルシャフト | 多量体(ポリ)ペプチドコンプレックスのメンバーをコードする核酸配列を同定するための新規方法およびファージ |
| US6040498A (en) | 1998-08-11 | 2000-03-21 | North Caroline State University | Genetically engineered duckweed |
| US6573043B1 (en) | 1998-10-07 | 2003-06-03 | Genentech, Inc. | Tissue analysis and kits therefor |
| EP1074563A1 (en) | 1999-08-02 | 2001-02-07 | F. Hoffmann-La Roche Ag | Chimeric polypeptides enhancing dimer formation through electrostatic interactions and disulfide bond, method for production and uses thereof |
| US7125978B1 (en) | 1999-10-04 | 2006-10-24 | Medicago Inc. | Promoter for regulating expression of foreign genes |
| DE60022369T2 (de) | 1999-10-04 | 2006-05-18 | Medicago Inc., Sainte Foy | Verfahren zur regulation der transkription von fremden genen in gegenwart von stickstoff |
| EP1242438B1 (en) | 1999-12-29 | 2006-11-08 | Immunogen, Inc. | Cytotoxic agents comprising modified doxorubicins and daunorubicins and their therapeutic use |
| US6511809B2 (en) * | 2000-06-13 | 2003-01-28 | E. I. Du Pont De Nemours And Company | Method for the detection of an analyte by means of a nucleic acid reporter |
| WO2002072141A2 (en) | 2001-03-09 | 2002-09-19 | William Herman | Targeted ligands |
| AU2004204763A1 (en) | 2003-01-09 | 2004-07-29 | Arizeke Pharmaceuticals Inc. | Compositions and methods for targeted biological delivery of molecular carriers |
| US20060104968A1 (en) | 2003-03-05 | 2006-05-18 | Halozyme, Inc. | Soluble glycosaminoglycanases and methods of preparing and using soluble glycosaminogly ycanases |
| US7871607B2 (en) | 2003-03-05 | 2011-01-18 | Halozyme, Inc. | Soluble glycosaminoglycanases and methods of preparing and using soluble glycosaminoglycanases |
| GB0305702D0 (en) | 2003-03-12 | 2003-04-16 | Univ Birmingham | Bispecific antibodies |
| US20050163782A1 (en) | 2003-06-27 | 2005-07-28 | Biogen Idec Ma Inc. | Modified binding molecules comprising connecting peptides |
| US20050095627A1 (en) * | 2003-09-03 | 2005-05-05 | The Salk Institute For Biological Studies | Multiple antigen detection assays and reagents |
| CN107213469A (zh) | 2003-11-06 | 2017-09-29 | 西雅图基因公司 | 能够与配体偶联的单甲基缬氨酸化合物 |
| JP2007536254A (ja) * | 2004-05-05 | 2007-12-13 | メリマック ファーマシューティカルズ インコーポレーティッド | 生物活性を調節するための二重特異性結合剤 |
| JO3000B1 (ar) | 2004-10-20 | 2016-09-05 | Genentech Inc | مركبات أجسام مضادة . |
| AU2005333156B2 (en) | 2004-11-03 | 2011-05-26 | Iris Molecular Diagnostics, Inc. | Homogeneous analyte detection |
| US7795009B2 (en) | 2005-06-15 | 2010-09-14 | Saint Louis University | Three-component biosensors for detecting macromolecules and other analytes |
| EP1940470B1 (en) | 2005-09-26 | 2013-04-17 | Medarex, Inc. | Antibody-drug conjugates and their use |
| DE502005008153D1 (de) | 2005-11-23 | 2009-10-29 | Roche Diagnostics Gmbh | Polynukleotid mit Phosphatmimetikum |
| US20100266620A1 (en) | 2006-01-20 | 2010-10-21 | Le Sun | Immunoconjugates for treatment of infectious diseases |
| US8008026B2 (en) * | 2006-04-21 | 2011-08-30 | Peoplebio, Inc. | Methods for differentially detecting a multimeric form from a monomeric form of a multimer-forming polypeptide through three-dimensional interactions |
| WO2008052774A2 (en) * | 2006-10-31 | 2008-05-08 | Noxxon Pharma Ag | Methods for detection of a single- or double-stranded nucleic acid molecule |
| WO2008137120A1 (en) * | 2007-05-03 | 2008-11-13 | Tethys Bioscience, Inc. | Binding reagents that contain small epitope binding molecules |
| JP5191537B2 (ja) * | 2007-06-18 | 2013-05-08 | エム・エス・ディー・オス・ベー・フェー | ヒトのプログラムされたデスレセプターpd−1に対する抗体 |
| EP2195461B1 (en) * | 2007-09-17 | 2015-05-27 | Mattias Strömberg | Magnetic detection of small entities |
| CN101918027A (zh) | 2007-11-02 | 2010-12-15 | 森托科尔奥索生物科技公司 | 半合成GLP-1肽-Fc融合构造、方法及其用途 |
| US11260133B2 (en) | 2008-02-21 | 2022-03-01 | Sanford-Burnham Medical Research Institute | Methods and compositions related to peptides and proteins with C-terminal elements |
| CN102458442B (zh) | 2009-04-08 | 2016-06-29 | 加利福尼亚大学董事会 | 具有受控血清药代动力学的人蛋白支架 |
| CN103384825B (zh) * | 2010-12-23 | 2017-05-24 | 霍夫曼-拉罗奇有限公司 | 通过二价结合剂检测经翻译后修饰的多肽 |
| JP5766296B2 (ja) * | 2010-12-23 | 2015-08-19 | エフ.ホフマン−ラ ロシュ アーゲーF. Hoffmann−La Roche Aktiengesellschaft | ポリペプチド−ポリヌクレオチド複合体、およびエフェクター成分の標的化された送達におけるその使用 |
| EP2655414B1 (en) * | 2010-12-23 | 2018-08-29 | Roche Diagniostics GmbH | Bispecific binding agent |
| EP2659275B1 (en) * | 2010-12-23 | 2017-11-22 | Roche Diagnostics GmbH | Detection of a polypeptide dimer by a bivalent binding agent |
| GB201409558D0 (en) * | 2014-05-29 | 2014-07-16 | Ucb Biopharma Sprl | Method |
-
2013
- 2013-06-25 CA CA2871386A patent/CA2871386A1/en not_active Abandoned
- 2013-06-25 JP JP2015519058A patent/JP6445429B2/ja not_active Expired - Fee Related
- 2013-06-25 MX MX2014014065A patent/MX2014014065A/es unknown
- 2013-06-25 KR KR20157002302A patent/KR20150023906A/ko not_active Withdrawn
- 2013-06-25 WO PCT/EP2013/063260 patent/WO2014001326A1/en not_active Ceased
- 2013-06-25 RU RU2015100231A patent/RU2644263C2/ru not_active IP Right Cessation
- 2013-06-25 BR BR112014029888-2A patent/BR112014029888A2/pt not_active IP Right Cessation
- 2013-06-25 EP EP13734693.8A patent/EP2867255B1/en active Active
- 2013-06-25 CN CN201380033855.8A patent/CN104395340B9/zh not_active Expired - Fee Related
-
2014
- 2014-12-22 US US14/579,165 patent/US20150232560A1/en not_active Abandoned
Also Published As
| Publication number | Publication date |
|---|---|
| CN104395340A (zh) | 2015-03-04 |
| BR112014029888A2 (pt) | 2020-05-12 |
| RU2015100231A (ru) | 2016-08-20 |
| EP2867255A1 (en) | 2015-05-06 |
| MX2014014065A (es) | 2015-02-04 |
| WO2014001326A1 (en) | 2014-01-03 |
| KR20150023906A (ko) | 2015-03-05 |
| JP2015522265A (ja) | 2015-08-06 |
| CN104395340B (zh) | 2018-10-02 |
| EP2867255B1 (en) | 2017-07-19 |
| RU2644263C2 (ru) | 2018-02-08 |
| CA2871386A1 (en) | 2014-01-03 |
| HK1207865A1 (en) | 2016-02-12 |
| CN104395340B9 (zh) | 2018-11-30 |
| US20150232560A1 (en) | 2015-08-20 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6445429B2 (ja) | 少なくとも2つの異なる標的化実体を含むテーラーメイドで選択的かつ多重特異性治療用分子を選択および作製するための方法およびその使用 | |
| JP5766296B2 (ja) | ポリペプチド−ポリヌクレオチド複合体、およびエフェクター成分の標的化された送達におけるその使用 | |
| JP6148729B2 (ja) | 共有結合している抗原−抗体結合体 | |
| JP6476194B2 (ja) | 二重特異性抗ハプテン/抗血液脳関門受容体抗体、それらの複合体、及び血液脳関門シャトルとしてのそれらの使用 | |
| CN107531788B (zh) | 对her2和血脑屏障受体特异性的三特异性抗体及使用方法 | |
| Yamada | Therapeutic monoclonal antibodies | |
| JP2023156299A (ja) | FcRH5に対するヒト化親和性成熟抗体及び使用方法 | |
| CN107001475B (zh) | 抗tim3抗体及使用方法 | |
| RU2617970C2 (ru) | Антитела, не содержащие fc-фрагмента, включающие два fab-фрагмента, и способы их применения | |
| JP2021048860A (ja) | 抗her2抗体及び使用方法 | |
| JP6602304B2 (ja) | 共有結合で連結されたヘリカー−抗ヘリカー抗体コンジュゲートおよびその用途 | |
| JP7373588B2 (ja) | 抗ctla-4抗体およびその使用 | |
| JP2018520642A (ja) | マスク抗cd3抗体及びその使用方法 | |
| RU2705299C2 (ru) | Антитела против 5-бром-2'-дезоксиуридина и способы применения | |
| KR20200118065A (ko) | 이중특이적 항원-결합 분자 및 이의 사용 방법 | |
| HK1207865B (zh) | 包含至少两个不同靶向实体的定制选择性和多特异性治疗分子的方法及其用途 | |
| CN117794953A (zh) | 双特异性抗体及使用方法 | |
| HK40108333A (zh) | 双特异性抗体及使用方法 | |
| HK1223954B (zh) | 双特异性抗-半抗原/抗-血脑屏障受体的抗体、其复合物及它们作为血脑屏障穿梭物的应用 | |
| HK1248719B (en) | Trispecific antibodies specific for her2 and a blood brain barrier receptor and methods of use |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20150513 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20160426 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20170201 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20170425 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20170511 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20170823 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20171121 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20180402 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20180627 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20180823 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20181121 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20181129 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6445429 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |