JP4439079B2 - プラバスタチンの製造方法 - Google Patents
プラバスタチンの製造方法 Download PDFInfo
- Publication number
- JP4439079B2 JP4439079B2 JP2000104278A JP2000104278A JP4439079B2 JP 4439079 B2 JP4439079 B2 JP 4439079B2 JP 2000104278 A JP2000104278 A JP 2000104278A JP 2000104278 A JP2000104278 A JP 2000104278A JP 4439079 B2 JP4439079 B2 JP 4439079B2
- Authority
- JP
- Japan
- Prior art keywords
- pravastatin
- mevastatin
- culture
- formula
- salt
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Landscapes
- Preparation Of Compounds By Using Micro-Organisms (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
Description
【発明の属する技術分野】
本発明は、抗高脂血症剤として有用なプラバスタチン、その塩またはそのラクトン閉環体の生物学的変換による製造方法に関する。
【0002】
【従来の技術】
プラバスタチンの製造方法、特に生物学的変換方法によるものとしては、イヌおよびウサギ肝臓ホモジネートを用いて、メバスタチンから変換する方法が、特開昭57−2240号に開示されている。微生物を用いてメバスタチンから変換する方法として、アブシディア(Absidia)属、カニンガメラ(cunninghamella)属、シンセファロスポラム(Syncephalosporum)属およびストレプトマイセス(Streptomyces)属を用いる製法が、特開昭57−50894号および特開昭57−67575号に開示されている。また、特開昭57−155995号および特開昭58−10572号には、ムコール(Mucor)、リゾープス(Rhisopus)、チゴリンクス(Zygorynchus)、シルシネラ(Cireinella)、アクチノムコール(Actinomucor)、ゴングロネラ(Gongronella)、フィコマイセス(Phycomyces)、モルチエレラ(Mortierella)、ピタノポラス(Pythanoporus)およびリゾクトニア(Rhizoctonia)の各属に属する微生物を用いる方法が開示されている。
【0003】
【発明が解決しようとする課題】
本発明は、メバスタチンを出発原料とした、生物学的変換方法によるプラバスタチンの新規な製造方法を提供するものである。
【0004】
【課題を解決するための手段】
本発明者は、上記目的を達成するために広範な微生物群からメバスタチンの6β位水素原子を水酸基に変換しうる微生物のスクリーニングを試みたところ、希少放線菌に分類されるミクロテトラスポーラ(Microtetraspora)属に属する菌株が前記変換能を有することを見出した。
【0005】
従って、本発明は、 式(I)、
【化3】
で示されるメバスタチン、そのラクトン開環体またはその塩(以下、これらを総称してメバスタチン類ということがある)の、
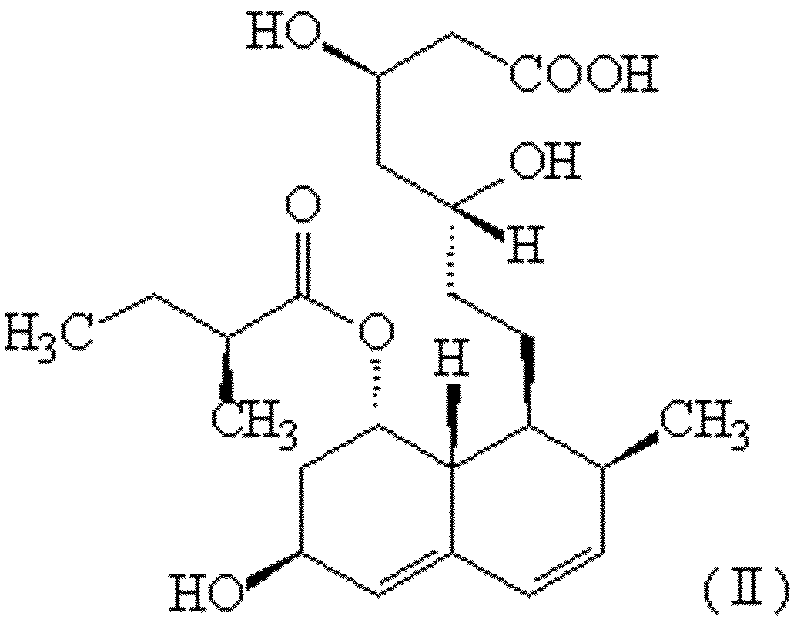
式(II)、
【化4】
で示されるプラバスタチン、その塩またはそのラクトン閉環体(以下、これらを総称してプラバスタチン類ということがある)への生物学的変換方法による、式(II)で示されるプラバスタチン、その塩またはそのラクトン閉環体の製造方法であって、
(A)前記生物学的変換方法を行いうるものであって、かつ、ミクロテトラスポーラ(Microtetraspora)属に属する菌株またはその培養菌体の調製物の存在下で、式(I)で示されるメバスタチン、そのラクトン開環体またはその塩をインキュベーション処理する工程、
(B)インキュベーション処理液から式(II)で示されるプラバスタチン、その塩またはそのラクトン閉環体の少なくとも1種を採取する工程、
を含んでなる方法を、提供することにより達成できる。
【0006】
本発明の生物学的変換方法では、ミクロテトラスポーラ(Microtetraspora)属に属する微生物であって、前記式(I)で示されるメバスタチン類から前記式(II)で示されるプラバスタチン類へ変換する能力を有する微生物、並びにそれらの培養菌体調製物であれば、種および株の種類を問うことなく使用できる。好ましい微生物として、ミクロテトラスポーラ・レクチカテナ(Microtetraspora recticatena)IFO14525株を挙げることができる。本菌株は、IFO((財)発酵研究所;INSTITUTE FOR FERMENTATION,OSAKA)から容易に入手できる。
【0007】
なお、本菌株の菌学的性状は次のとおりである。
1.形態
基生菌糸より直鎖状(Rectiflexibiles)の気中菌糸を伸長する。成熟した気中菌糸の先に4個の円筒形の胞子からなる胞子鎖を形成する。胞子のうは認められない。胞子の大きさは1.0×2.0μmくらいで、胞子の表面は瘤状(knobby)又は粗面状(rugose)を示し、鞭毛は認められない。
【0008】
2.各種培地における生育状態
培養は全て28℃で行い、各種培地での生育結果を以下に示す。
(1)イースト・麦芽寒天培地
生育は良好で、その表面に気中菌糸を着生し、白色の胞子が見られる。培養裏面は薄い茶色である。溶解性色素は産生しない。
(2)オートミール寒天培地
生育は中程度で、その表面に気中菌糸を僅かに着生し、白色の胞子が見られる。培養裏面は薄い茶色である。茶色の溶解性色素を僅かに産生する。
(3)スターチ・無機塩寒天培地
生育は中程度で表面に気中菌糸を着生しない。培養裏面は無色である。溶解性色素は産生しない。
(4)グリセリン・アスパラギン寒天培地
生育は中程度で、その表面に気中菌糸を僅かに着生し、白色の胞子が見られる。培養裏面は無色である。溶解性色素は産生しない。
(5)チロシン寒天培地
生育は中程度で、その表面に気中菌糸を僅かに着生し、白色の胞子が見られる。培養裏面は無色である。培地中にメラニン色素を産生しない。
【0009】
3.各種炭素源の同化性
プリードハム・ゴトリーブ寒天培地に各種の炭素源を加え生育を見た。
(1)L−アラビノース +
(2)D−キシロース +
(3)D−グルコース +
(4)D−フルクトース −
(5)シュークロース ±
(6)イノシトール ±
(7)L−ラムノース +
(8)D−マンニトール −
(9)D−ラフィノース −
+は同化する、±は多少同化する、−は殆ど同化しない。
【0010】
4.化学分類学的性質
本菌の細胞壁成分であるジアミノピメリン酸(diamino pimericacid)の異性体型はmeso型であった。全菌体の糖組成としてガラクトース、グルコース、マンノース、リボース、及びマジュロースらしき糖が検出された。
【0011】
本発明によれば、これらの菌株またはその培養菌体調製物、さらに酸素の存在下で、出発原料(基質)であるメバスタチン類がインキュベーション処理される。この処理は前記菌株を好気的条件下で培養する際に、その培養液中に基質を添加して行うか、あるいは場合により前記菌株の培養菌体を、例えばそのまま、もしくはホモジナイズした調製物の懸濁液中に基質を添加し、酸素を含む気体、例えば空気を通気しながらインキュベーションして行うこともできる。
【0012】
培養液への基質の添加は、培養前または培養開始後一定期間経過したときのいずれの時期に行ってもよい。上記菌体は上記いずれかの菌株を栄養源含有培地に接種し、好気的に培養することにより製造できる。かかる培養菌体の調製物を用意するための菌株の培養または基質が添加された状態で行われる菌株の培養は、原則的には一般微生物の培養方法に準じて行うことができるが、通常は液体培養による振とう培養、通気攪拌培養などの好気的条件下で実施するのが好ましい。
【0013】
培養に用いられる培地としては、ミクロテトラスポーラ(Microtetraspora)属に属する微生物が利用できる栄養源を含有する培地であればよく、各種の合成培地、半合成培地、天然培地などいずれも利用可能である。培地組成としては炭素源としてのグルコース、マルトース、キシロース、フルクトース、シュークロース等を単独または組合せて用いることができる。これらの炭素源は、培養途中で随時添加してもよく、例えばグルコースを3〜7g/lの濃度範囲となるようにフィードするとメバスタチン類からプラバスタチン類への変換速度を相対的に増大させることができる。
【0014】
窒素源としては、ペプトン、肉エキス、大豆粉、カゼイン、アミノ酸、麦芽エキス、酵母エキス、尿素等の有機窒素源、硝酸ナトリウム、硫酸アンモニウム等の無機窒素源を、単独または組合せて用いることができる。その他、例えば塩化ナトリウム、塩化カリウム、炭酸カルシウム、硫酸マグネシウム、リン酸ナトリウム、リン酸カリウム、塩化コバルト等の塩類、重金属類塩、ビタミン類も必要に応じ添加使用することができる。なお、培養中発泡が著しい場合には、公知の各種消泡剤を適宜培地中に添加することもできる。
【0015】
培養条件は、該菌株が良好に生育し得る範囲内で適宜選択することができる。通常、pH6〜9.5、28〜30℃で2〜8日程度培養する。上述した各種の培養条件は、使用微生物の種類や特性、外部条件等に応じて適宜変更でき、最適条件を選択できる。
【0016】
また、培養菌体調製物は、培養終了後、遠心分離または濾過により分離した菌体またはホモジナイズした菌体を適当な溶液に懸濁して調製する。菌体の懸濁に使用できる溶液は、前記した培地であるか、あるいはトリス−酢酸、トリス−塩酸、コハク酸ナトリウム、クエン酸ナトリウム、リン酸ナトリウム、リン酸カリウムなどの緩衝液を単独または混合したものである。緩衝液のpHは、好ましくは6.0〜9.0、さらに好ましくは7.0〜8.5である。
【0017】
基質となるメバスタチン類は、粉末のままか、あるいは水溶性有機溶媒、例えばエタノールなどに溶解して培養液または菌体の懸濁液に添加することができ、その添加量は、例えば、培養液の場合、培養液1l当り200〜800mgが好ましい。添加量を1000mg/lより多くすると、変換速度が著しく遅くなり好ましくない。基質添加後は、27〜31℃で3〜10日間、好ましくは約6〜8日間、振とうあるいは通気攪拌などの操作を行い、好気的条件下で反応を進行させることにより基質であるメバスタチン類を目的のプラバスタチン類に変換することができる。
【0018】
こうして生成した目的のプラバスタチン類を反応混合から単離するには、種々の既知精製手段を選択、組合せて行うことができる。例えば、疎水性吸着樹脂への吸着・溶出、酢酸エチル、n−ブタノール等を用いた溶媒抽出、シリカゲル等によるカラム法あるいは薄層クロマトグラフィー、逆相カラムを用いた分取用高速液体クロマトグラフィー等を、単独あるいは適宜組合せ、場合により反復使用することにより、分離精製することができる。
【0019】
【実施例】
以下、本発明について具体例を挙げてより詳細に説明するが、本発明をこれらの例に限定することを意図するものではない。なお、下記の例中のパーセント(%)は、特に断りのない限り、容量パーセントを示す。
【0020】
例1〜6
表1に示した各種成分を含む各培地5mlを試験管に入れ、121℃、20分間加熱滅菌した。これにミクロテトラスポーラ・レクチカテナ(Microtetraspora recticatena)IFO14525株を接種し、表1に示した時期にメバスタチンを最終濃度で500mg/lとなるように添加し、28℃にて10日間培養した。
【0021】
このようにして得られた培養液を2ml分取し、同量のメタノールを加えて振とうし、3000rpmにて10分間遠心分離した。この上清をさらに12000rpmにて10分間遠心し、得られた上清を下記の条件にて高速液体クロマトグラフィー(HPLC)分析し、プラバスタチン濃度を測定した。なお、この条件では、プラバスタチンの保持時間は17.6分である。結果を表1にまとめて示す。
【0022】
【表1】
【0023】
(HPLC分析条件)
カラム:STR ODS−II(4.6φ×150mm)
移動相:メタノール/水/酢酸/トリエチルアミン(500:500:1:1)混液
流速:1.0ml/分
検出:238nm
【0024】
例7
グルコース1.0%、マルトエキス0.2%、酵母エキス0.5%を含む培地50mlを500ml容三角フラスコに入れ、121℃、20分間加熱滅菌した。これにミクロテトラスポーラ・レクチカテナ(Microtetrasporarecticatena)IFO14525株を接種し、28℃で4日間、ロータリーシェーカー(220rpm)上で培養した。これにメバスタチンを最終濃度で500mg/lとなるように添加し、さらに8日間、同条件で培養した。得られた培養液を前述の条件でHPLC分析したところ、プラバスタチンの濃度は91.0mg/lであり、メバスタチンからプラバスタチンへの変換率は、15.6%であった。
【0025】
例8〜16
表2に示した濃度のグルコースを含み、さらにマルトエキス0.2%、酵母エキス0.5%、炭酸カルシウム0.2%を含む各種培地50mlを500ml容三角フラスコに入れ、121℃、20分間加熱滅菌した。これにミクロテトラスポーラ・レクチカテナ(Microtetraspora recticatena)IFO14525株を接種し、28℃で4日間、ロータリーシェーカー(220rpm)上で培養した。これにメバスタチンを表2に示す濃度となるように添加し、さらに6日間、同条件で培養した。得られた培養液を前述の条件でHPLC分析した結果を表2に示す。プラバスタチン生産量は、メバスタチン添加量500mg/lまでは増加したが、1000mg/lでは逆に減少した。
【0026】
【表2】
【0027】
例17
グルコース0.5%、マルトエキス0.2%、酵母エキス0.5%、炭酸カルシウム0.2%からなる前培養用培地50mlを500ml容三角フラスコに入れ、121℃、20分間加熱滅菌した。これにミクロテトラスポーラ・レクチカテナ(Microtetraspora recticatena)IFO14525株を接種し、28℃で2日間、ロータリーシェーカー(220rpm)上で培養し、前培養液を調製した。次に3l容のジャーファーメンテーター(MDL300:丸菱株式会社製)に前培養用培地と同組成の変換培養用培地1.5lを準備し、121℃、20分間加熱滅菌した。これに前培養液150mlを接種し、温度28℃、攪拌数300rpm、通気量1.0vvmの条件で培養した。1日後、菌体が十分に増殖したことを確認してメバスタチンを濃度500mg/lとなるように添加し、培養を継続した。メバスタチンを添加して1日後、40mg/lのプラバスタチンが生産され、6日後には、100mg/lに達した。この時の変換率は20%であった。
【0028】
例18
例17と同様に前培養液を調製し、3l容ジャーファーメンターでの変換培養を行った。ただし、変換培養の培地は、次の組成を有する。溶性でんぷん6.0%、大豆粉2.0%、KR−酵母0.3%、ファーマメディア0.7%、酵母エキス0.1%、硫酸マグネシウム・7水和物0.05%、リン酸一カリウム0.05%、プルロニック(旭電化社製)0.05%。培養方法は、基本的に例17と同様であるが、培養開始後、3日目にメバスタチンを濃度500mg/lとなるように添加した。メバスタチンを添加して5日後、190mg/lのプラバスタチンが生産され、この時の変換率は38%であった。
【0029】
例19
例17と同様に前培養液を調製し、例18で用いた変換培地を用いて、3l容ジャーファーメンターでのpH制御による変換培養を行った。ただし、pHの制御は2M水酸化ナトリウムを用い、pH8.0に維持した。培養開始後、4日目にメバスタチンを濃度500mg/lとなるように添加した。メバスタチンを添加して6日後、プラバスタチンの濃度は285mg/lに達し、この時の変換率は57%であった。
Claims (4)
- 式(I)、
式(II)、
(A)前記生物学的変換方法を行いうるものであって、かつ、ミクロテトラスポーラ(Microtetraspora)属に属する菌株またはその培養菌体の調製物の存在下で、式(I)で示されるメバスタチン、そのラクトン開環体またはその塩をインキュベーション処理する工程、
(B)インキュベーション処理液から式(II)で示されるプラバスタチン、その塩またはそのラクトン閉環体の少なくとも1種を採取する工程、
を含んでなる方法。 - インキュベーション処理される物質が、メバスタチンである請求項1記載の方法。
- インキュベーション処理液から採取される物質がプラバスタチンまたはその塩である請求項1または2記載の方法。
- ミクロテトラスポーラ(Microtetraspora)属に属する菌株が、ミクロテトラスポーラ・レクチカテナ(Microtetraspora recticatena)IFO14525株である請求項1〜3のいずれかに記載の方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2000104278A JP4439079B2 (ja) | 2000-04-06 | 2000-04-06 | プラバスタチンの製造方法 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2000104278A JP4439079B2 (ja) | 2000-04-06 | 2000-04-06 | プラバスタチンの製造方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2001286293A JP2001286293A (ja) | 2001-10-16 |
| JP4439079B2 true JP4439079B2 (ja) | 2010-03-24 |
Family
ID=18617853
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2000104278A Expired - Fee Related JP4439079B2 (ja) | 2000-04-06 | 2000-04-06 | プラバスタチンの製造方法 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP4439079B2 (ja) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP4485081B2 (ja) * | 2001-02-23 | 2010-06-16 | メルシャン株式会社 | プラバスタチンの生産に関与するdnaおよびその使用 |
| CN112553262B (zh) * | 2020-12-31 | 2023-04-07 | 广东蓝宝制药有限公司 | 一种普伐他汀的发酵工艺 |
-
2000
- 2000-04-06 JP JP2000104278A patent/JP4439079B2/ja not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| JP2001286293A (ja) | 2001-10-16 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR880002483B1 (ko) | 3-히드록시-ml-236b 유도체의 제조방법 | |
| JP4439401B2 (ja) | マクロライド系化合物の製造方法 | |
| WO2005054491A1 (ja) | 光学活性テトラヒドロチオフェン誘導体の製造方法、および、光学活性テトラヒドロチオフェン-3-オールの晶析方法 | |
| US5407826A (en) | Isolated cultures of microorganisms of Clonostachys Cylindrospora, Gliocladium and Nectria Gliocladioides | |
| JP4439079B2 (ja) | プラバスタチンの製造方法 | |
| JP3957053B2 (ja) | 新規な微生物及びプラバスタチンの製造方法 | |
| JPS637757B2 (ja) | ||
| AU620595B2 (en) | Process for the preparation of macrolide compounds | |
| JP4399234B2 (ja) | 有用変換微生物 | |
| JPH0639480B2 (ja) | 新規マクロライド系抗生物質m119 | |
| JP4449015B2 (ja) | シクロスポリン誘導体の製造方法 | |
| JPWO1997008336A1 (ja) | 生物学的変換によるヒドロキシル化コレステロールの製造方法およびジヒドロキシコレステロール | |
| JP4179760B2 (ja) | 不飽和脂肪酸又はその誘導体の製造法 | |
| JPH0378107B2 (ja) | ||
| JPH0378106B2 (ja) | ||
| WO1997008336A1 (fr) | Procede de production de cholesterols hydroxyles par conversion biologique et dihydroxycholesterols obtenus selon ce procede | |
| JPH0738792B2 (ja) | プロトカテキュ酸の製造方法 | |
| JP2004115380A (ja) | 新規メバスタチン誘導体及びその製造方法 | |
| JPH0434555B2 (ja) | ||
| JPH0378108B2 (ja) | ||
| JPH05331181A (ja) | ファルネシルトランスフェラーゼ阻害物質oh−4652物質およびその製造法 | |
| JPS5820596B2 (ja) | コプロボルフイリン 3 ノ セイホウ | |
| JPS6037991A (ja) | 抗生物質ss8228c及びその製造法 | |
| JPH0378104B2 (ja) | ||
| JPS6225356B2 (ja) |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20070116 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20091125 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20091125 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20091125 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20100104 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20100105 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20130115 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| LAPS | Cancellation because of no payment of annual fees |