JP4040736B2 - 耐熱性フルクトシルアミノ酸オキシダーゼ - Google Patents
耐熱性フルクトシルアミノ酸オキシダーゼ Download PDFInfo
- Publication number
- JP4040736B2 JP4040736B2 JP02816998A JP2816998A JP4040736B2 JP 4040736 B2 JP4040736 B2 JP 4040736B2 JP 02816998 A JP02816998 A JP 02816998A JP 2816998 A JP2816998 A JP 2816998A JP 4040736 B2 JP4040736 B2 JP 4040736B2
- Authority
- JP
- Japan
- Prior art keywords
- faod
- amino acid
- fusion protein
- gst
- acid oxidase
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Lifetime
Links
Images
Landscapes
- Enzymes And Modification Thereof (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Peptides Or Proteins (AREA)
Description
【発明の属する技術分野】
本発明は、熱安定性の優れたフルクトシルアミノ酸オキシダーゼ活性を有する組換えタンパク質に関する。
【0002】
【従来の技術】
フルクトシルアミノ酸オキシダーゼ(以下、FAODと略称する)は酸化還元酵素の1つであって、例えば、臨床及び食品の分野でアマドリ化合物の分析に有用であることが知られている。アマドリ化合物とは、タンパク質等のアミノ基を有する物質のアミノ基と、アルドース等の還元性の糖のアルデヒド基とが非酵素的かつ非可逆的に結合し、アマドリ転移して生成する糖化タンパクである。生体内では、グルコースとアミノ酸が結合してフルクトシルアミン誘導体が生成し、血液中のヘモグロビンが糖化されたフルクトシルアミン誘導体はグリコヘモグロビン、アルブミンが糖化された誘導体はグリコアルブミン、血液中のタンパクが糖化された誘導体はフルクトサミンと呼ばれる。これらの血中濃度は、過去の一定期間の平均血糖値を反映していることから、その測定値は、糖尿病の症状の重要な指標となり得るために、測定手段の確立は臨床上、極めて有用である。また、食品中のアマドリ化合物を定量することにより、その食品の製造後の保存状況や期間を知ることができ、品質管理に役立つと考えられる。
【0003】
アマドリ化合物の定量は、以下の反応式で表されるように、酸化還元酵素の作用によって生成する過酸化水素の量、又は消費される酸素の量に基づいて行われる。
R1−CO−CH2−NH−R2 + O2 + H2O→
R1−CO−CHO + R2−NH2 + H2O2
(式中、R1はアルドース残基、R2はアミノ酸、タンパク質又はペプチド残基を表す)
上記反応に用いうる酵素として、本出願人は、アスペルギルス属(A spergillus)由来の菌が産生するフルクトシルアミノ酸オキシダーゼ(以下、FAOD−Lという)を見出し、そのDNA組換え技術による製造に成功した(特願平8−193344)。
【0004】
【発明が解決すべき課題】
しかしながら、これら天然又は組換え技術で得られた酵素は、40℃付近で不安定になる傾向があるために、保管、輸送に際して失活する恐れがあり、取り扱いが困難であった。また、通常、測定に先立って被検試料をプロテアーゼ処理するが、プロテアーゼを不活化するためにインヒビターを用いている。そのために、操作手順が繁雑になり、自動分析装置や測定者に過大な負担がかかるという問題点があった。また、従来法によれば、硫安沈殿、ゲルろ過及びイオン交換樹脂等のカラム精製及び透析等の様々な工程を経て酵素を精製する必要があり、時間及び手間がかかる上、十分な収率をあげることができなかった。
【0005】
【課題を解決するための手段】
本発明は、従来のFAOD−Lに比較して熱安定性に優れた酵素であって、配列表の配列番号1に記載のアミノ酸配列、該配列において1若しくは数個のアミノ酸が欠失、置換若しくは付加されたアミノ酸配列を有するポリペプチドと、グルタチオン S−トランスフェラーゼ(以下、GSTと略す)との融合タンパク質であって、FAOD活性を有する組換えタンパク質を提供するものである。
【0006】
本発明の組換えタンパク質は、アスペルギルス・テレウスGP1(A spergillus terreus GP1;FERM BP-5684)が産生するFAOD−Lと、GSTとの融合タンパクであり、後述するように、FAOD−Lの酵素活性は維持したまま、極めて優れた熱安定性を示すことから、上記の従来技術における課題を解決し、例えば、プロテアーゼインヒビターを使用せず、加熱処理により、プロテアーゼを不活化することができ、実用性に優れた、有用な酵素である。しかも、精製工程が極めて簡単であり、収率が低下する恐れも少ないという利点がある。
GST(EC2.5.1.18)は様々な生物に見出され、立体構造研究が最も進んでいる薬物代謝酵素である(ファルマシア、360-364頁、Vol.33, No.4,1997)。本発明に用いたGSTは、Schistosoma japonicumより見出されたものであって、分子量は約26,000である。
本発明の組換えタンパク質は、FAODが使用される様々な分野で、それら酵素と同様に用いることができ、特に、上記のアマドリ化合物の分析に有用である。
【0007】
【発明の実施の形態】
FAOD−LをコードするDNAは、一般に入手可能なE.coli SOLR/pFAL2 FERM BP-5981から常法に従って単離することができる。そのようにして得られるFAOD−LをコードするDNAの塩基配列と推定のアミノ酸配列を配列番号1に示す。本発明の目的には、配列番号1に示した全アミノ酸配列を有するFAOD−Lのみならず、所望の酵素活性を有するそのアミノ酸配列における変異体も同様に有用である。そのような変異体は、当業者既知の方法で、アミノ酸の欠失、置換及び/又は挿入により誘導することができる。
【0008】
本発明の融合タンパク質の製造に際しては、まず、E.coli SOLR/pFAL2 FERM BP-5981からFAOD−LのcDNAを抽出する。次いで、このcDNAとGSTをコードするDNAとを適当な発現ベクター内で連結して融合タンパク質の発現ベクターを構築する。そのような発現ベクターは、予め、FAOD−LのcDNAとGST DNAとを連結した後、適当な発現ベクターに挿入するか、あるいは、後述の実施例に記載のごとく、融合タンパク質としてGST及びFAOD−LをコードするDNAが発現されるように、適当なGSTの発現ベクター(例、pGEX)にFAOD−LのcDNAを挿入することにより、構築することができる。このようにして得られた発現ベクターで宿主細胞を形質転換し、適当な培地で培養すると、目的の融合タンパク質が生産される。得られた融合タンパク質の精製については、無細胞抽出液をGlutathion Sepharose 4B カラム(ファルマシア製)に吸着させ、トリス−塩酸緩衝液で洗浄した後、グルタチオンを含む同緩衝液で溶出する。なお、一連の操作は、当該技術分野で入手可能な制限酵素、宿主細胞、発現ベクターを用い、当業者既知の方法で行うことができる。
【0009】
以下に実施例を挙げて本発明を詳しく説明するが、これらは本発明を制限するものではない。以下の実施例で用いたプラスミド類、様々な制限酵素やT4DNAリガーゼ、その他の酵素類は、市販品から入手し、供給者の指示に従って使用した。また、DNAのクローニング、各プラスミドの構築、宿主の形質転換、形質転換体の培養及び培養物からの酵素の回収は、当業者既知の方法、あるいは文献記載の方法に準じて行なった。また、酵素活性は以下の力価の測定法に従って測定した。
【0010】
力価測定法
生成する過酸化水素を比色法により測定する方法(速度法)
100mM FZL(Nα−Z−リジン)溶液はあらかじめ得られたFZLを蒸留水で溶解することによって調製する。45mM 4−アミノアンチピリン、60ユニット/mlパーオキシダーゼ溶液、及び60mM フェノール溶液それぞれ100μlと、0.1M トリス−塩酸緩衝液(pH8.0)1ml、及び酵素溶液50μlを混合し、全量を蒸留水で3.0mlとする。30℃で平衡化した後、100mM FZL溶液50μlを添加し、505nmにおける吸光度を経時的に測定する。生成するキノン色素の分子吸光係数(5.16×103M-1cm-1)から、1分間に生成する過酸化水素のマイクロモルを算出し、この数字を酵素活性単位とする。
【0011】
実施例1 融合タンパク質の製造
1.FAOD−LのcDNAの抽出
E.coli SOLR/pFAL2 (FERM BP-5981)は、アスペルギルス・テレウスGP1(Aspergillus terreus GP1;FERM BP-5684)からクローニングされたFAOD−LのcDNAを有する形質転換体である。このE.coli SOLR/pFAL2(FERM BP-5981)を50μl/mlのアンピシリンを含む2×YT培地5mlで、37℃、10時間培養し、次いで、菌体を集菌し、以下の方法に従ってプラスミドの抽出を行った。
培養液3mlから得た菌体をTE緩衝液で洗浄する。次に、Solution I(50mMグルコース、25mMトリス−塩酸(pH8.0)、10mM EDTA)50μlに菌体を懸濁したのち、10mg/mlのリゾチーム50μlを加え、軽くボルテックスし、室温で5分間放置する。次に、Solution II(0.2N水酸化ナトリウム、1%SDS)を加えて穏やかに撹拌し、5分間氷冷する。次に、5Mの酢酸カリウムを150μl加えて撹拌後、5分間氷冷する。氷冷終了後、4℃、12,000rpm、5分間の遠心を行い、上清を別のマイクロチューブに移す。これを2度、フェノール/クロロホルムで抽出して精製し、2倍量のエタノールを加えてエタノール沈殿させる。これを70%エタノールで洗浄した後、減圧して乾燥させる。
【0012】
次いで、これを50μlのTE緩衝液に溶解し、RNaseを1μl加えて37℃で30分間反応させる。反応終了後、20%PEG/2.5N塩化ナトリウムを30μl加え、穏やかにボルテックスした後、1時間氷冷する。その後、4℃、14,000rpm、20分間遠心し、プラスミドを沈殿させる。そして、70%エタノールで洗浄後、減圧乾燥し、20μlのTE緩衝液に溶解する。
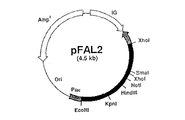
上の操作で得たプラスミドpFAL2の制限地図を図1に示す。pFAL2は約4.5kbのプラスミドで、lacプロモーターの下流にFAOD−LのcDNAがEcoRI〜XhoIで挿入されている。
【0013】
2.FAOD−LのcDNAの増幅
配列番号1に記載のFAOD−Lの塩基配列のN−末端およびC−末端からPCR用のプライマーを設計した。プライマーには、プラスミドへの接続のための制限酵素部位(EcoRI)を接続した。2つのプライマー(pFAL5(配列番号2)及びpFAL3(配列番号3))を合成した。上記(1)で得たプラスミドpFAL2とこれら2つのプライマー、及びTaqポリメラーゼ(TaKaRa Ex Taq;宝酒造社製)を用い、供給者の指示に従って、以下の手順でPCRを行った。すなわち、(94℃,1分;60℃,1分;72℃,2分)からなる一連の処理を30サイクル行った後、72℃で2分処理してPCRを行った。
この操作により、約1.5kbのFAOD−LのcDNAが増幅された。そして、このPCR産物をアガロースゲル電気泳動にかけ、Sephaglas Band Prep Kit (ファルマシア社製)を用いて切り出した。
【0014】
3.FAOD−LのcDNAの、GST発現ベクターへのライゲーション
上の操作で得たFAOD−LのcDNAをGST発現ベクターであるpGEX−4T−1(ファルマシア社製、以下、pGEXベクターという)に接続した。このpGEXベクターのマルチクローニングサイト(MCS)の上流には、GSTをコードするDNAが挿入されている。
まず、pGEXベクターを制限酵素EcoRIで処理し、得られた制限酵素処理物をアルカリホスファターゼ(Calfintestine;宝酒造社製)で、供給者の指示に従って処理した。次に、PCRで得たFAOD−LのcDNAを制限酵素EcoRIで処理した。
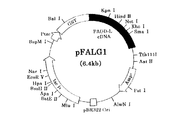
次いで、pGEXの制限酵素処理物とFAOD−LのcDNAの制限酵素処理物とを、T4DNA Ligase(宝酒造社製)を用い、供給者の指示に従ってライゲーションした。この操作により、FAOD−LのcDNAがpGEXベクターのEcoRI部位に挿入され、GST DNAとFAOD−L DNAとが、5’側から直列に並んで挿入されているプラスミドpFALG1を得た。このプラスミドpFALG1の制限地図を図2に示す。
【0015】
4.大腸菌の形質転換
上記の操作で得たプラスミドpFALG1を用いて大腸菌JM109株を形質転換した。大腸菌のコンピテントセルの調製は常法に従って行った。大腸菌形質転換株をアンピシリン、IPTGを含む2×TYプレートで培養し、形質転換株のみを常法通り選別した。
【0016】
5.FAOD−LのcDNA挿入株の選別
上で得た大腸菌を培養したプレートをろ紙に転写し、1%のリゾチーム溶液で30℃、30分間処理して溶菌した。次に、これを室温下で風乾し、下記のFAOD発色液に浸漬させ、上記のFAOD酵素活性測定法(速度法)と同様、FAOD−Lを発現させている株を発色に基づいて特定し、それに対応する株をプレーから選別した。
【0017】
6.大腸菌組組換え株でのFAOD−L−GST融合タンパク質の発現
上の操作で選別した大腸菌形質転換株E.coli JM109/pFALG1をジャーファーメンターで、28℃にて培養した。培地として50μl/mlのアンピシリンを含むLB培地(1L)を用い、100mM IPTG溶液を培養開始2時間後に培地の1/1000容量加えて発現を誘導した。培養中、2時間毎に菌体を1部集菌し、増殖(Growth;OD606)と比活性(U/mg)を調べたところ、IPTG添加後8時間でFAOD生産が最大となった(図3参照)。図3中、上側の曲線(白丸)は、菌体の増殖、下側の曲線(黒丸)はFAODの発現量(比活性)を表している。
【0018】
7.FAOD−L−GST融合タンパク質の精製
融合タンパク質の精製については、無細胞抽出液をGlutathion Sepharose 4B カラム(ファルマシア製)に吸着させ、供給者の指示に従って、トリス−塩酸緩衝液で洗浄した後、グルタチオンを含む同緩衝液で溶出してアフィニティー精製し、12.2U/mgの精製酵素を得た。この精製酵素をそのまま、以下の実験に用いた。なお、一連の操作は、当該技術分野で入手可能な制限酵素、宿主細胞、発現ベクターを用い、当業者既知の方法で行うことができる。
【0019】
8.FAOD−L−GST融合タンパク質の性質
1)分子量
FAOD−L−GST融合タンパク質の分子量は、SDS−PAGEで確認した結果、74kDaであった。これは、FAOD−L(分子量51kDa)とGST(分子量26kDa)との融合タンパク質であることを示している。
2)基質特異性
融合タンパク質の基質特異性は、速度法で求めた場合、FZLに対して、12.2U/mg、FV(フルクトシルバリン)に対して4.36U/mgであり、FZL/FVは約3であった。これは、A.テレウスGP1から精製したFAOD−LのFZL/FVが約3であることと一致しており、非融合型のFAOD−Lとの基質特異性における同一性が確認された。
【0020】
3)熱安定性
熱安定性は、対象となる温度で、上記7で精製した酵素を10分間インキュベートした後、以下の組成の反応液で、30℃、30分間反応させ、505nmにおけるキノン色素の分子吸光係数(5.16×103M-1cm-1)から、1分間に生成する過酸化水素のマイクロモルを算出し、この数字を酵素活性単位とした。
そして、20℃処理で得た数値を100とし、20〜60℃における処理で得た数値を図4に表した。図4から明らかなように、FAOD−Lの場合には、50℃、10分間のインキュベーションでほぼ完全に失活するのに対し、本発明のFAOD−L−GST融合タンパク質の場合には、ほぼ100%の活性が維持されていた。40℃においても、活性の相違が認められた。
【0021】
【配列表】
【0022】
【0023】
【0024】
【図面の簡単な説明】
【図1】 FAOD−LをコードするDNAを含むプラスミドpFAL2の制限地図。
【図2】 FAOD−L−GSTをコードするDNAを含むプラスミドpFALG1の制限地図。
【図3】 大腸菌形質転換株E.coli JM109/pFALG1の増殖(OD606)と比活性(U/mg)との関係を示すグラフ。図中、白丸は、菌体の増殖(OD606)、黒丸はFAODの発現量(U/mg)を表している。
【図4】 FAOD−L−GST融合タンパク質とFAOD−Lの熱安定性を示すグラフ。
Claims (4)
- 配列表の配列番号1に記載のアミノ酸配列、該配列において1若しくは数個のアミノ酸が欠失、置換若しくは付加されたアミノ酸配列を有するポリペプチドと、グルタチオンS−トランスフェラーゼとの融合タンパク質であって、フルクトシルアミノ酸オキシダーゼ活性を有する組換えタンパク質。
- 請求項1記載のタンパク質をコードするDNA。
- 請求項2記載のDNAを導入された形質転換体。
- 請求項3記載の形質転換体を培養し、その培養物からフルクトシルアミノ酸オキシダーゼ活性を有する生成物を回収することからなる、グルタチオンS−トランスフェラーゼとフルクトシルアミノ酸オキシダーゼ活性を有するポリペプチドとの融合タンパク質の製造方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP02816998A JP4040736B2 (ja) | 1998-02-10 | 1998-02-10 | 耐熱性フルクトシルアミノ酸オキシダーゼ |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP02816998A JP4040736B2 (ja) | 1998-02-10 | 1998-02-10 | 耐熱性フルクトシルアミノ酸オキシダーゼ |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JPH11221081A JPH11221081A (ja) | 1999-08-17 |
| JP4040736B2 true JP4040736B2 (ja) | 2008-01-30 |
Family
ID=12241250
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP02816998A Expired - Lifetime JP4040736B2 (ja) | 1998-02-10 | 1998-02-10 | 耐熱性フルクトシルアミノ酸オキシダーゼ |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP4040736B2 (ja) |
Families Citing this family (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP5074386B2 (ja) * | 2006-04-25 | 2012-11-14 | キッコーマン株式会社 | 熱安定性に優れた真核型アマドリアーゼ、その遺伝子及び組換え体dna、並びに熱安定性に優れた真核型アマドリアーゼの製造法 |
| JP5476021B2 (ja) * | 2008-10-17 | 2014-04-23 | 東洋紡株式会社 | フルクトシルアミノ酸オキシダーゼ改変体およびその利用 |
| CN103122338B (zh) * | 2012-12-29 | 2014-05-07 | 宁波美康生物科技股份有限公司 | 热稳定性高的果糖赖氨酸氧化酶及其制备方法 |
| CN103695380B (zh) * | 2013-12-27 | 2016-05-25 | 宁波美康生物科技股份有限公司 | 果糖氨基酸氧化酶、制备方法及含该酶的糖化白蛋白检测试剂盒 |
-
1998
- 1998-02-10 JP JP02816998A patent/JP4040736B2/ja not_active Expired - Lifetime
Also Published As
| Publication number | Publication date |
|---|---|
| JPH11221081A (ja) | 1999-08-17 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP2508600B1 (en) | Mutant enzyme and application thereof | |
| CN102292439A (zh) | 黄素结合型葡萄糖脱氢酶 | |
| JPWO2010053161A1 (ja) | 改変型フラビンアデニンジヌクレオチド依存性グルコースデヒドロゲナーゼ | |
| WO2021149675A1 (ja) | 3-ヒドロキシ酪酸脱水素酵素及びその製造方法 | |
| JP6455430B2 (ja) | キサンチンオキシダーゼ遺伝子とそれをコードするアミノ酸配列 | |
| JP4040736B2 (ja) | 耐熱性フルクトシルアミノ酸オキシダーゼ | |
| JP2546554B2 (ja) | Dna、細胞、n−メチルヒダントイナーゼ活性を有する蛋白質の取得法 | |
| WO2002072839A1 (en) | Glucose dehydrogenase | |
| JP4133326B2 (ja) | 新規なフルクトシルアミノ酸オキシダーゼ | |
| JP5289801B2 (ja) | ウリカーゼ活性を有する蛋白質 | |
| Bakke et al. | Thermostabilization of porcine kidney d‐amino acid oxidase by a single amino acid substitution | |
| JPH10248574A (ja) | 新規な乳酸酸化酵素 | |
| JP2011217731A (ja) | 改変型フラビンアデニンジヌクレオチド依存性グルコースデヒドロゲナーゼ | |
| Ferri et al. | Cloning and Expression of Fructosyl-amine Oxidase from Marine Yeast Pichia Species N1-1: Stefano Ferri et al. | |
| JP4890133B2 (ja) | 安定な尿酸測定試薬 | |
| JP3904098B2 (ja) | 改変ザルコシンオキシダーゼおよびその用途 | |
| JP2003079386A (ja) | 新規なフルクトシルアミノ酸オキシダーゼ | |
| EP2695939A1 (en) | Modified glucose dehydrogenase | |
| JP2003339385A (ja) | 新規3−ヒドロキシ酪酸脱水素酵素遺伝子、新規3−ヒドロキシ酪酸脱水素酵素の製造法、ならびに、新規3−ヒドロキシ酪酸脱水素酵素を用いたケトン体の測定方法および測定用組成物 | |
| JP6476542B2 (ja) | 変異型グルコース−6−リン酸脱水素酵素 | |
| JP2012019756A (ja) | フラビンアデニンジヌクレオチド依存性グルコースデヒドロゲナーゼを用いるグルコース測定方法 | |
| JP4963888B2 (ja) | 安定なウリカーゼ製剤 | |
| JP3112146B2 (ja) | 耐熱性マレートデヒドロゲナーゼ活性を有する蛋白質 | |
| JP2008022766A (ja) | ウリカーゼの比活性を向上させる方法、および比活性の向上した改変型ウリカーゼ | |
| JP4591074B2 (ja) | 加熱処理を施した脱水素酵素 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20050202 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20071009 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20071108 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20101116 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20111116 Year of fee payment: 4 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20121116 Year of fee payment: 5 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20131116 Year of fee payment: 6 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| EXPY | Cancellation because of completion of term |