JP2015060799A - リチウムイオン電池用電極材料とその製造方法及びリチウムイオン電池用電極並びにリチウムイオン電池 - Google Patents
リチウムイオン電池用電極材料とその製造方法及びリチウムイオン電池用電極並びにリチウムイオン電池 Download PDFInfo
- Publication number
- JP2015060799A JP2015060799A JP2013195495A JP2013195495A JP2015060799A JP 2015060799 A JP2015060799 A JP 2015060799A JP 2013195495 A JP2013195495 A JP 2013195495A JP 2013195495 A JP2013195495 A JP 2013195495A JP 2015060799 A JP2015060799 A JP 2015060799A
- Authority
- JP
- Japan
- Prior art keywords
- particles
- lithium ion
- ion battery
- electrode
- less
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/10—Energy storage using batteries
Landscapes
- Battery Electrode And Active Subsutance (AREA)
Abstract
【課題】高い放電容量、高い出力特性を実現するリチウムイオン電池用電極材料とその製造方法及びリチウムイオン電池用電極並びにリチウムイオン電池を提供する。【解決手段】本発明のリチウムイオン電池用電極材料は、LiFePO4粒子またはLiFexM1−xPO4(但し、MはCo、Mn及びNiの群から選択された1種または2種以上、0<x<1)粒子の表面が炭素質被膜により被覆されてなる一次粒子が複数個凝集した凝集粒子からなり、一次粒子の平均一次粒子径は10nm以上かつ1000nm以下であり、凝集粒子は、累積粒度分布における累積百分率30%の粒子径(D30)の累積百分率70%の粒子径(D70)に対する比(D30/D70)が0.20以上かつ0.48以下、タップ密度が1.0g/cm3以上かつ1.7g/cm3以下、圧粉体密度が電極活物質粒子の真密度の50%以上かつ75%以下である。【選択図】なし
Description
本発明は、リチウムイオン電池用電極材料とその製造方法及びリチウムイオン電池用電極並びにリチウムイオン電池に関し、特に詳しくは、高い放電容量、高い出力特性を実現可能なリチウムイオン電池用電極材料と、このリチウムイオン電池用電極材料の製造方法、及びリチウムイオン電池用電極並びにリチウムイオン電池に関するものである。
近年、小型、軽量、高容量の電池として、リチウムイオン電池等の非水電解液系の二次電池が提案され、実用に供されている。
このリチウムイオン電池は、リチウムイオンを可逆的に脱挿入可能な性質を有する正極及び負極と非水系の電解液とにより構成されている。
このリチウムイオン電池の負極材料としては、一般的に、負極活物質である炭素系材料またはチタン酸リチウム(Li4Ti5O12)等のリチウムイオンを可逆的に脱挿入可能な性質を有するLi含有金属酸化物が用いられる。
このリチウムイオン電池は、リチウムイオンを可逆的に脱挿入可能な性質を有する正極及び負極と非水系の電解液とにより構成されている。
このリチウムイオン電池の負極材料としては、一般的に、負極活物質である炭素系材料またはチタン酸リチウム(Li4Ti5O12)等のリチウムイオンを可逆的に脱挿入可能な性質を有するLi含有金属酸化物が用いられる。
一方、リチウムイオン電池の正極活物質としては、マンガン酸リチウム(LiMn2O4)、コバルト酸リチウム(LiCoO2)等のリチウムイオンを可逆的に脱挿入可能な性質を有するLi含有金属酸化物が用いられる。このLi含有金属酸化物は、バインダー等の有機化合物により電極材料合剤を構成しており、この電極材料合剤を集電体と称される金属箔の表面に塗布し固化することにより、リチウムイオン電池の正極が形成される。
このようなリチウムイオン電池は、従来の鉛蓄電池、ニッケルカドミウム電池、ニッケル水素電池と比べて、軽量かつ小型であるとともに、高エネルギーを有していることから、携帯用電話機、多機能型携帯用電話機、携帯用情報端末、ノート型パーソナルコンピューター等の各種携帯用機器に用いられる小型電源のみならず、定置式の非常用大型電池用途として注目されている。
このようなリチウムイオン電池は、従来の鉛蓄電池、ニッケルカドミウム電池、ニッケル水素電池と比べて、軽量かつ小型であるとともに、高エネルギーを有していることから、携帯用電話機、多機能型携帯用電話機、携帯用情報端末、ノート型パーソナルコンピューター等の各種携帯用機器に用いられる小型電源のみならず、定置式の非常用大型電池用途として注目されている。
また、近年では、リチウムイオン電池は、プラグインハイブリッド自動車、ハイブリッド自動車、電動工具等の高出力電源として検討されており、これらの高出力電源として用いられる電池には高速の充放電特性が求められている。
このような大型用途向け電池、さらには電池の高機能化、高容量化、低コスト化等の観点から、レアメタルフリーの正極活物質として種々の材料が検討されている。
これらのなかでも、LiFePO4に代表されるオリビン系リン酸塩系電極活物質は、安全性、高資源量及び低コストである電極活物質として注目されている。
このような大型用途向け電池、さらには電池の高機能化、高容量化、低コスト化等の観点から、レアメタルフリーの正極活物質として種々の材料が検討されている。
これらのなかでも、LiFePO4に代表されるオリビン系リン酸塩系電極活物質は、安全性、高資源量及び低コストである電極活物質として注目されている。
しかしながら、これらオリビン系リン酸塩系電極活物質には、電子伝導性が低いという問題点があり、したがって、コバルト酸リチウム(LiCoO2)のような電子伝導性が高いリチウム含有金属酸化物と比べると、電池特性が劣っている。そこで、このオリビン系リン酸塩系電極活物質の電子伝導性を高めるために、この電極活物質の粒子表面を有機化合物にて覆い、その後、この有機化合物を炭化することにより、電極活物質粒子の表面に炭素質被膜を形成し、この炭素質被膜の炭素を電子伝導性物質とした電極材料が提案されている(特許文献1)。
この電極材料では、電極活物質粒子を球状の粒子とするとともに、この球状の粒子の累積粒度分布における累積百分率30%の粒子径(D30)の累積百分率70%の粒子径(D70)に対する比(D30/D70)を0.5以上とすることにより、電極作製時に導電助材を使用せず、しかも最低限の量の粘着材にて電極を作製することができ、この電極中の電極活物質の密度を高くすることができるとされている。
この電極材料では、電極活物質粒子を球状の粒子とするとともに、この球状の粒子の累積粒度分布における累積百分率30%の粒子径(D30)の累積百分率70%の粒子径(D70)に対する比(D30/D70)を0.5以上とすることにより、電極作製時に導電助材を使用せず、しかも最低限の量の粘着材にて電極を作製することができ、この電極中の電極活物質の密度を高くすることができるとされている。
ところで、従来の表面に炭素質被膜が形成された電極材料においては、電極活物質の粒子表面に有機化合物を炭化してなる炭素質被膜を形成していることから、確かに電極活物質の電子伝導性は高まるものの、この電極活物質の電極における充填率が低い場合には、電極活物質間の接触点が減少し、その結果、電極材料としての導電性が低下することとなり、よって、この電極活物質を用いてリチウムイオン電池の正電極を作製した際に、0.1C以下の低レートから3C以上の高レートまで安定した高容量かつ高出力のリチウムイオン電池を得ることができないという問題点があった。
特に、特許文献1に記載された電極材料では、シャープ性が高いために単位体積に占める電極活物質粒子の割合が低くなる傾向にある。単一粒子径に近い真球状粒子では、約半分は空間が占めるので、プレスで正極層の密度を上げるためには大きな電極活物質粒子の体積変動を伴うこことなり、集電体自体へダメージを与え、密着不良が起こり易くなるという問題点があった。
本発明は、上記の課題を解決するためになされたものであって、0.1C以下の低レートから3C以上の高レートまで安定した高い放電容量、高い出力特性を実現することが可能なリチウムイオン電池用電極材料とその製造方法及びリチウムイオン電池用電極並びにリチウムイオン電池を提供することを目的とする。
本発明者等は、上記課題を解決するために鋭意検討を行った結果、LiFePO4またはLiFexM1−xPO4(但し、MはCo、Mn及びNiの群から選択された1種または2種以上、0<x<1)からなる電極活物質粒子の表面が炭素質被膜により被覆されてなる一次粒子が複数個凝集した凝集粒子からなるリチウムイオン電池用電極材料について、一次粒子の平均一次粒子径を10nm以上かつ1000nm以下、凝集粒子については、その累積粒度分布における累積百分率30%の粒子径(D30)の累積百分率70%の粒子径(D70)に対する比(D30/D70)を0.20以上かつ0.48以下、タップ密度を1.0g/cm3以上かつ1.7g/cm3以下、圧粉体密度を電極活物質粒子の真密度の50%以上かつ75%以下とすれば、導電性が低下することなく、高い放電容量及び高い出力特性を実現することができることを見出し、本発明を完成するに至った。
すなわち、本発明のリチウムイオン電池用電極材料は、LiFePO4またはLiFexM1−xPO4(但し、MはCo、Mn及びNiの群から選択された1種または2種以上、0<x<1)からなる電極活物質粒子の表面が炭素質被膜により被覆されてなる一次粒子が複数個凝集した凝集粒子からなるリチウムイオン電池用電極材料であって、前記一次粒子の平均一次粒子径は10nm以上かつ1000nm以下であり、前記凝集粒子は、累積粒度分布における累積百分率30%の粒子径(D30)の累積百分率70%の粒子径(D70)に対する比(D30/D70)が0.20以上かつ0.48以下、タップ密度が1.0g/cm3以上かつ1.7g/cm3以下、圧粉体密度が前記電極活物質粒子の真密度の50%以上かつ75%以下であることを特徴とする。
本発明のリチウムイオン電池用電極材料では、前記一次粒子の表面の炭素質被膜による被覆率が80%以上であり、前記凝集粒子は、その平均粒子径が0.5μm以上かつ100μm以下、体積密度が該凝集粒子を中実とした場合の体積密度の50体積%以上かつ80体積%以下であり、かつ前記一次粒子により包囲された空孔が多数存在する多孔質体であることが好ましい。
前記炭素質被膜の含有率は、前記一次粒子の全質量に対して0.5質量%以上かつ5.0質量%以下であることが好ましい。
前記炭素質被膜の含有率は、前記一次粒子の全質量に対して0.5質量%以上かつ5.0質量%以下であることが好ましい。
本発明のリチウムイオン電池用電極材料の製造方法は、上記のリチウムイオン電池用電極材料を製造する方法であって、
水熱合成法により、LiFePO4またはLiFexM1−xPO4(但し、MはCo、Mn及びNiの群から選択された1種または2種以上、0<x<1)からなる粒子またはその前駆体を作製し、
次いで、前記粒子またはその前駆体に炭素源を添加して焼成することにより、生成する粒子の表面を炭素質被膜にて覆う一次粒子とするとともに該一次粒子を複数個凝集する凝集粒子を生成することを特徴とする。
水熱合成法により、LiFePO4またはLiFexM1−xPO4(但し、MはCo、Mn及びNiの群から選択された1種または2種以上、0<x<1)からなる粒子またはその前駆体を作製し、
次いで、前記粒子またはその前駆体に炭素源を添加して焼成することにより、生成する粒子の表面を炭素質被膜にて覆う一次粒子とするとともに該一次粒子を複数個凝集する凝集粒子を生成することを特徴とする。
本発明のリチウムイオン電池用電極は、本発明のリチウムイオン電池用電極材料を含有してなることを特徴とする。
本発明のリチウムイオン電池は、本発明のリチウムイオン電池用電極を正極として備えてなることを特徴とする。
本発明のリチウムイオン電池用電極材料によれば、LiFePO4またはLiFexM1−xPO4(但し、MはCo、Mn及びNiの群から選択された1種または2種以上、0<x<1)からなる電極活物質粒子の表面が炭素質被膜により被覆されてなる一次粒子の平均一次粒子径を10nm以上かつ1000nm以下、この一次粒子を複数個凝集した凝集粒子の累積粒度分布における累積百分率30%の粒子径(D30)の累積百分率70%の粒子径(D70)に対する比(D30/D70)を0.20以上かつ0.48以下、タップ密度を1.0g/cm3以上かつ1.7g/cm3以下、圧粉体密度を電極活物質粒子の真密度の50%以上かつ75%以下としたので、導電性が低下することなく、放電容量を大幅に向上させることができ、出力特性も大幅に向上させることができる。
したがって、0.1C以下の低レートから3C以上の高レートまで安定した高い放電容量及び高い出力特性を有するリチウムイオン電池用電極材料を提供することができる。
したがって、0.1C以下の低レートから3C以上の高レートまで安定した高い放電容量及び高い出力特性を有するリチウムイオン電池用電極材料を提供することができる。
本発明のリチウムイオン電池用電極材料の製造方法によれば、水熱合成法により、LiFePO4またはLiFexM1−xPO4(但し、MはCo、Mn及びNiの群から選択された1種または2種以上、0<x<1)からなる粒子またはその前駆体を作製し、次いで、この粒子またはその前駆体に炭素源を添加して焼成することにより、生成する粒子の表面を炭素質被膜にて覆う一次粒子とするとともに該一次粒子を複数個凝集する凝集粒子を生成するので、導電性が低下することなく、0.1C以下の低レートから3C以上の高レートまで安定した高い放電容量及び高い出力特性を有するリチウムイオン電池用電極材料を、効率よく、安定して製造することができる。
本発明のリチウムイオン電池用電極によれば、本発明のリチウムイオン電池用電極材料を含有したので、このリチウムイオン電池用電極をリチウムイオン電池に適用した場合に、導電性が低下することなく、放電容量を大幅に向上させることができ、出力特性も大幅に向上させることができる。
本発明のリチウムイオン電池によれば、本発明のリチウムイオン電池用電極を正極として備えたので、導電性が低下することなく、放電容量を大幅に向上させることができ、出力特性も大幅に向上させることができる。
本発明のリチウムイオン電池用電極材料とその製造方法及びリチウムイオン電池用電極並びにリチウムイオン電池を実施するための形態について説明する。
なお、この形態は、発明の趣旨をより良く理解させるために具体的に説明するものであり、特に指定のない限り、本発明を限定するものではない。
なお、この形態は、発明の趣旨をより良く理解させるために具体的に説明するものであり、特に指定のない限り、本発明を限定するものではない。
[リチウムイオン電池用電極材料]
本発明の一実施形態のリチウムイオン電池用電極材料は、LiFePO4、または該LiFePO4のFeの一部を異種元素であるCo、Mn及びNiの群から選択された1種または2種以上により置換したLiFexM1−xPO4(但し、MはCo、Mn及びNiの群から選択された1種または2種以上、0<x<1)からなる電極活物質粒子の表面が炭素質被膜により被覆されてなる一次粒子が複数個凝集した凝集粒子からなるリチウムイオン電池用電極材料であって、この一次粒子の平均一次粒子径は10nm以上かつ1000nm以下であり、上記の凝集粒子は、累積粒度分布における累積百分率30%の粒子径(D30)の累積百分率70%の粒子径(D70)に対する比(D30/D70)が0.20以上かつ0.48以下、タップ密度が1.0g/cm3以上かつ1.7g/cm3以下、圧粉体密度が電極活物質粒子の真密度の50%以上かつ75%以下の電極材料である。
本発明の一実施形態のリチウムイオン電池用電極材料は、LiFePO4、または該LiFePO4のFeの一部を異種元素であるCo、Mn及びNiの群から選択された1種または2種以上により置換したLiFexM1−xPO4(但し、MはCo、Mn及びNiの群から選択された1種または2種以上、0<x<1)からなる電極活物質粒子の表面が炭素質被膜により被覆されてなる一次粒子が複数個凝集した凝集粒子からなるリチウムイオン電池用電極材料であって、この一次粒子の平均一次粒子径は10nm以上かつ1000nm以下であり、上記の凝集粒子は、累積粒度分布における累積百分率30%の粒子径(D30)の累積百分率70%の粒子径(D70)に対する比(D30/D70)が0.20以上かつ0.48以下、タップ密度が1.0g/cm3以上かつ1.7g/cm3以下、圧粉体密度が電極活物質粒子の真密度の50%以上かつ75%以下の電極材料である。
「一次粒子」
この一次粒子は、LiFePO4またはLiFexM1−xPO4(但し、MはCo、Mn及びNiの群から選択された1種または2種以上、0<x<1)からなる粒子の表面が炭素質被膜により被覆されてなる粒子である。
この一次粒子は、LiFePO4またはLiFexM1−xPO4(但し、MはCo、Mn及びNiの群から選択された1種または2種以上、0<x<1)からなる粒子の表面が炭素質被膜により被覆されてなる粒子である。
この一次粒子の平均一次粒子径は10nm以上かつ1000nm以下が好ましく、より好ましくは20nm以上かつ800nm以下、さらに好ましくは25nm以上かつ500nm以下である。
ここで、この一次粒子の平均一次粒子径を上記の範囲に限定した理由は、この一次粒子の平均一次粒子径が10nm未満では、この一次粒子の表面を薄膜状の炭素にて十分に被覆することが困難であり、高速充放電レートにおける放電容量が低くなり、充分な充放電レート性能を実現することが困難となるので好ましくなく、一方、この一次粒子の平均一次粒子径が1000nmを超えると、この一次粒子の内部抵抗が大きくなり、その結果、高速充放電レートにおける放電容量が不十分になるので好ましくない。
ここで、この一次粒子の平均一次粒子径を上記の範囲に限定した理由は、この一次粒子の平均一次粒子径が10nm未満では、この一次粒子の表面を薄膜状の炭素にて十分に被覆することが困難であり、高速充放電レートにおける放電容量が低くなり、充分な充放電レート性能を実現することが困難となるので好ましくなく、一方、この一次粒子の平均一次粒子径が1000nmを超えると、この一次粒子の内部抵抗が大きくなり、その結果、高速充放電レートにおける放電容量が不十分になるので好ましくない。
炭素質被膜は、一次粒子に所望の電子伝導性を付与するためのもので、この一次粒子の表面の炭素質被膜による被覆率は、80%以上が好ましく、より好ましくは90%以上、さらに好ましくは95%以上である。
ここで、炭素質被膜による被覆率が80%未満では、一次粒子の表面における炭素質被膜の被覆が不十分なものとなり、よって、一次粒子の電子導電性が大きく低下することにより粒子自体の抵抗が高くなり、その結果、高速充放電レートにおける放電容量が低くなり、充分な充放電レート性能を実現することが困難となるので好ましくない。
ここで、炭素質被膜による被覆率が80%未満では、一次粒子の表面における炭素質被膜の被覆が不十分なものとなり、よって、一次粒子の電子導電性が大きく低下することにより粒子自体の抵抗が高くなり、その結果、高速充放電レートにおける放電容量が低くなり、充分な充放電レート性能を実現することが困難となるので好ましくない。
この炭素質被膜の含有率は、一次粒子の全質量に対して0.5質量%以上かつ5.0質量%以下であることが好ましく、より好ましくは0.7質量%以上かつ4.5質量%以下、さらに好ましくは0.8質量%以上かつ4.0質量%以下である。
ここで、この炭素質被膜の含有率が0.5質量%未満では、炭素量が一次粒子の全質量に対して少なすぎてしまい、よって、一次粒子自体の電子導電性が低下することとなり、その結果、高速充放電レートにおける放電容量が低くなり、充分な充放電レート性能を実現することが困難となるので好ましくない。
一方、この炭素質被膜の含有率が5.0質量%を超えると、炭素量が一次粒子の全質量に対して多すぎてしまい、よって、この炭素質被膜に対する一次粒子自体の割合が減少し、活物質としての特性を有効に利用され難くなるので好ましくない。
ここで、この炭素質被膜の含有率が0.5質量%未満では、炭素量が一次粒子の全質量に対して少なすぎてしまい、よって、一次粒子自体の電子導電性が低下することとなり、その結果、高速充放電レートにおける放電容量が低くなり、充分な充放電レート性能を実現することが困難となるので好ましくない。
一方、この炭素質被膜の含有率が5.0質量%を超えると、炭素量が一次粒子の全質量に対して多すぎてしまい、よって、この炭素質被膜に対する一次粒子自体の割合が減少し、活物質としての特性を有効に利用され難くなるので好ましくない。
「凝集粒子」
上記の一次粒子が複数個凝集した凝集粒子である。
この凝集粒子の平均粒子径(平均二次粒子径)は0.5μm以上かつ100.0μm以下が好ましく、より好ましくは1.0μm以上かつ50.0μm以下である。
ここで、この凝集粒子の平均粒子径が0.5μm未満では、凝集粒子が小さくなりすぎてしまい、その結果、高速充放電レートにおける放電容量が低くなり、充分な充放電レート性能を実現することが困難となるので好ましくなく、一方、この凝集粒子の平均粒子径が100μmを超えると、この凝集粒子が大きすぎるために、この凝集粒子を用いて電極形成用塗料またはペーストを作製し、この電極形成用塗料またはペーストを用いて金属箔の表面に正極層を形成してリチウムイオン電池用正極とした場合に、この正極層の表面に凝集粒子に起因する凹凸が生じ、その結果、高速充放電の際に局所的に充放電ルートが生じ、放電容量が低下する要因になるので好ましくない。
上記の一次粒子が複数個凝集した凝集粒子である。
この凝集粒子の平均粒子径(平均二次粒子径)は0.5μm以上かつ100.0μm以下が好ましく、より好ましくは1.0μm以上かつ50.0μm以下である。
ここで、この凝集粒子の平均粒子径が0.5μm未満では、凝集粒子が小さくなりすぎてしまい、その結果、高速充放電レートにおける放電容量が低くなり、充分な充放電レート性能を実現することが困難となるので好ましくなく、一方、この凝集粒子の平均粒子径が100μmを超えると、この凝集粒子が大きすぎるために、この凝集粒子を用いて電極形成用塗料またはペーストを作製し、この電極形成用塗料またはペーストを用いて金属箔の表面に正極層を形成してリチウムイオン電池用正極とした場合に、この正極層の表面に凝集粒子に起因する凹凸が生じ、その結果、高速充放電の際に局所的に充放電ルートが生じ、放電容量が低下する要因になるので好ましくない。
この凝集粒子は、累積粒度分布における累積百分率30%の粒子径(D30)の累積百分率70%の粒子径(D70)に対する比(D30/D70)が0.20以上かつ0.48以下であることが好ましく、より好ましくは0.25以上かつ0.45以下である。
ここで、比(D30/D70)が0.20未満では、累積百分率30%の粒子径(D30)の粒子が少なすぎてしまい、その結果、ペーストの粘度が高く、溶剤が多く必要となるので好ましくなく、一方、比(D30/D70)が0.48を超えると、粒度分布がシャープとなり、後述するタップ密度及び圧粉体密度が低下し、この凝集粒子を用いて電極を作製した際に、この凝集粒子内に存在する空孔が埋まり難くなるので好ましくない。
ここで、比(D30/D70)が0.20未満では、累積百分率30%の粒子径(D30)の粒子が少なすぎてしまい、その結果、ペーストの粘度が高く、溶剤が多く必要となるので好ましくなく、一方、比(D30/D70)が0.48を超えると、粒度分布がシャープとなり、後述するタップ密度及び圧粉体密度が低下し、この凝集粒子を用いて電極を作製した際に、この凝集粒子内に存在する空孔が埋まり難くなるので好ましくない。
この凝集粒子は、タップ密度が1.0g/cm3以上かつ1.7g/cm3以下であることが好ましく、より好ましくは1.2g/cm3以上かつ1.6g/cm3以下である。
ここで、タップ密度が1.0g/cm3未満では、プレス時に凝集粒子の体積変動に伴う集電体との密着が不良となるので好ましくなく、一方、タップ密度が1.7g/cm3を超えると、細孔の形成が不足し、電解質の拡散抵抗が大きくなるので好ましくない。
ここで、タップ密度が1.0g/cm3未満では、プレス時に凝集粒子の体積変動に伴う集電体との密着が不良となるので好ましくなく、一方、タップ密度が1.7g/cm3を超えると、細孔の形成が不足し、電解質の拡散抵抗が大きくなるので好ましくない。
圧粉体密度は、所定量の凝集粒子を所定の圧力、例えば0.38t/cm2の圧力にて成形し、得られた成形体の質量と容積から圧粉体密度を算出することができる。
この圧粉体密度は、電極活物質粒子の真密度の50%以上かつ75%以下であることが好ましく、より好ましくは真密度の55%以上かつ70%以下である。
ここで、圧粉体密度が電極活物質粒子の真密度の50%未満では、単位体積の電極活物質占有率が低くなり、電気容量を高くできなくなるので好ましくなく、一方、圧粉体密度が電極活物質粒子の真密度の75%を超えると、圧粉体中の細孔容量が不足し、電解質の拡散抵抗が大きくなるので好ましくない。
この圧粉体密度は、電極活物質粒子の真密度の50%以上かつ75%以下であることが好ましく、より好ましくは真密度の55%以上かつ70%以下である。
ここで、圧粉体密度が電極活物質粒子の真密度の50%未満では、単位体積の電極活物質占有率が低くなり、電気容量を高くできなくなるので好ましくなく、一方、圧粉体密度が電極活物質粒子の真密度の75%を超えると、圧粉体中の細孔容量が不足し、電解質の拡散抵抗が大きくなるので好ましくない。
なお、低い圧力で大きな圧粉体密度が得られる凝集粒子は、高電気容量の正極層が形成され易いばかりか、集電体への影響も最小限にできるので好ましい。
さらに、凝集粒子の崩れ易さを考慮すると、圧粉体密度/タップ密度比が1.6以上の凝集粒子は、崩れ易く、低い圧力で大きな圧粉体密度が得られ、高電気容量の正極層が形成され易いばかりか、集電体への影響も最小限にできるので好ましい。
さらに、凝集粒子の崩れ易さを考慮すると、圧粉体密度/タップ密度比が1.6以上の凝集粒子は、崩れ易く、低い圧力で大きな圧粉体密度が得られ、高電気容量の正極層が形成され易いばかりか、集電体への影響も最小限にできるので好ましい。
この凝集粒子の体積密度は、水銀ポロシメーターを用いて測定することができる。ここでいう体積密度とは、上記の測定によって得られるそれぞれの凝集粒子の間隙の体積と、それぞれの凝集粒子の全質量に基づき算出される。
この凝集粒子は、体積密度が該凝集粒子を中実とした場合の体積密度の50体積%以上かつ80体積%以下であることが好ましく、より好ましくは60体積%以上かつ75体積%以下である。
この凝集粒子は、体積密度が該凝集粒子を中実とした場合の体積密度の50体積%以上かつ80体積%以下であることが好ましく、より好ましくは60体積%以上かつ75体積%以下である。
ここで、体積密度が中実とした場合の体積密度の50体積%未満では、凝集体強度が低くなり易く、ペースト時に凝集が崩壊し粘度調整が困難となるので好ましくなく、一方、体積密度が中実とした場合の体積密度の80%を超えると、凝集体の内部の密度が高くなりすぎて、この凝集体の外殻内部のチャネル状(網目状)の細孔が小さくなってしまい、その結果、凝集体の内部に有機化合物の炭化の際に生成するタール状物質が閉じ込められてしまうので好ましくない。
このように、この凝集粒子の体積密度を上記の範囲とすることで、凝集粒子が緻密化することにより凝集粒子の強度が増加し、この凝集粒子を、例えば、バインダー、導電助剤、溶媒と混合して電極スラリーを調製する際に凝集粒子が崩れ難くなり、その結果、電極スラリーの粘度の上昇が抑制され、かつ流動性が保たれることにより、塗工性が改善され、電極スラリーの塗膜における凝集粒子の充填性の向上をも図ることができる。
この凝集粒子は、上述した一次粒子(表面被膜LiFePO4粒子または表面被膜LiFexM1−xPO4粒子)により包囲された空孔が多数存在する多孔質体である。
ここで、「一次粒子により包囲された空孔が多数存在する」とは、一次粒子が3個以上会合することで形成される空隙を意味する。
この凝集粒子では、空孔が多数存在することにより、凝集状態が緩やかとなり、崩れやすくなる。そこで、この凝集粒子を用いてリチウムイオン電池用電極を作製した際には、空孔が潰れることにより凝集粒子の充填密度が上昇し、得られた電極の密度が増大することとなる。
ここで、「一次粒子により包囲された空孔が多数存在する」とは、一次粒子が3個以上会合することで形成される空隙を意味する。
この凝集粒子では、空孔が多数存在することにより、凝集状態が緩やかとなり、崩れやすくなる。そこで、この凝集粒子を用いてリチウムイオン電池用電極を作製した際には、空孔が潰れることにより凝集粒子の充填密度が上昇し、得られた電極の密度が増大することとなる。
この凝集粒子の炭素含有率は、この凝集粒子の全質量に対して0.5質量%以上かつ5.0質量%以下であることが好ましく、より好ましくは0.7質量%以上かつ4.5質量%以下である。
ここで、この凝集粒子の炭素含有率が0.5質量%より低い場合、炭素質被膜の被覆率が80%を下回ることとなり、この凝集粒子を用いてリチウムイオン電池の電極を形成した場合に高速充放電レートにおける放電容量が低くなり、充分な充放電レート性能を実現することが困難となるので好ましくない。一方、この凝集粒子の炭素含有率が5.0質量%を超えると、相対的に電極活物質(LiFePO4またはLiFexM1−xPO4)の含有率が低くなり、この凝集粒子を用いてリチウムイオン電池の電極を形成した場合に電池の容量が低くなるとともに、炭素質被膜の過剰な担持により電極活物質が嵩高くなり、したがって、電極密度が低くなり、単位体積あたりのリチウムイオン電池の電池容量の低下が無視できなくなるので好ましくない。
ここで、この凝集粒子の炭素含有率が0.5質量%より低い場合、炭素質被膜の被覆率が80%を下回ることとなり、この凝集粒子を用いてリチウムイオン電池の電極を形成した場合に高速充放電レートにおける放電容量が低くなり、充分な充放電レート性能を実現することが困難となるので好ましくない。一方、この凝集粒子の炭素含有率が5.0質量%を超えると、相対的に電極活物質(LiFePO4またはLiFexM1−xPO4)の含有率が低くなり、この凝集粒子を用いてリチウムイオン電池の電極を形成した場合に電池の容量が低くなるとともに、炭素質被膜の過剰な担持により電極活物質が嵩高くなり、したがって、電極密度が低くなり、単位体積あたりのリチウムイオン電池の電池容量の低下が無視できなくなるので好ましくない。
このように、凝集粒子の平均粒子径(平均二次粒子径)、比(D30/D70)、タップ密度、圧粉体密度、体積密度及び炭素含有率を上記の範囲に限定したことにより、凝集粒子が高密度となるように分布することとなり、その結果、導電性が低下することなく、放電容量を大幅に向上させることができ、出力特性も大幅に向上させることができる。
[リチウムイオン電池用電極材料の製造方法]
本実施形態のリチウムイオン電池用電極材料の製造方法は、
(1)粒子またはその前駆体の作製工程
水熱合成法により、LiFePO4またはLiFexM1−xPO4(但し、MはCo、Mn及びNiの群から選択された1種または2種以上、0<x<1)からなる粒子またはその前駆体を作製する工程。
(2)凝集粒子生成工程
前記粒子またはその前駆体に炭素源を添加して焼成することにより、生成する粒子の表面を炭素質被膜にて覆う一次粒子とするとともに該一次粒子を複数個凝集する凝集粒子を生成する工程。
を有する。
次に、これらの工程を詳細に説明する。
本実施形態のリチウムイオン電池用電極材料の製造方法は、
(1)粒子またはその前駆体の作製工程
水熱合成法により、LiFePO4またはLiFexM1−xPO4(但し、MはCo、Mn及びNiの群から選択された1種または2種以上、0<x<1)からなる粒子またはその前駆体を作製する工程。
(2)凝集粒子生成工程
前記粒子またはその前駆体に炭素源を添加して焼成することにより、生成する粒子の表面を炭素質被膜にて覆う一次粒子とするとともに該一次粒子を複数個凝集する凝集粒子を生成する工程。
を有する。
次に、これらの工程を詳細に説明する。
(1)粒子またはその前駆体の作製工程
水熱合成法により、LiFePO4またはLiFexM1−xPO4(但し、MはCo、Mn及びNiの群から選択された1種または2種以上、0<x<1)からなる粒子またはその前駆体を作製する。
水熱合成法により、LiFePO4またはLiFexM1−xPO4(但し、MはCo、Mn及びNiの群から選択された1種または2種以上、0<x<1)からなる粒子またはその前駆体を作製する。
LiFePO4粒子は、Li源、Fe源及びP源を、これらのモル比(Li源:Fe源:P源)が1:1:1となるように水を主成分とする溶媒に投入し、撹拌してLiFePO4の前駆体溶液とし、この前駆体溶液を耐圧容器に入れ、高温、高圧下、例えば、120℃以上かつ250℃以下、0.2MPa以上にて、1時間以上かつ24時間以下、水熱処理を行うことにより得ることができる。
Li源としては、例えば、水酸化リチウム(LiOH)、炭酸リチウム(Li2CO3)、塩化リチウム(LiCl)、リン酸リチウム(Li3PO4)等のリチウム無機酸塩、酢酸リチウム(LiCH3COO)、蓚酸リチウム((COOLi)2)等のリチウム有機酸塩、及びこれらの水和物の群から選択された1種または2種以上が好適に用いられる。特に、塩化リチウム、酢酸リチウム等のようなFe源及びP源と均一な溶液相を形成する原料が好ましい。
Fe源としては、例えば、塩化鉄(II)(FeCl2)、硫酸鉄(II)(FeSO4)、酢酸鉄(II)(Fe(CH3COO)2)等の鉄化合物またはその水和物が好適に用いられる。
P源としては、オルトリン酸(H3PO4)、メタリン酸(HPO3)等のリン酸、リン酸二水素アンモニウム(NH4H2PO4)、リン酸水素二アンモニウム((NH4)2HPO4)、リン酸アンモニウム((NH4)3PO4)、及びこれらの水和物等の群から選択された1種または2種以上が好適に用いられる。
特に、オルトリン酸は、Li源及びP源と均一な溶液相を形成するので好ましい。
特に、オルトリン酸は、Li源及びP源と均一な溶液相を形成するので好ましい。
LiFexM1−xPO4粒子もLiFePO4粒子と同様、Li源、Fe源、M源及びP源を、これらのモル比(Li源:Fe源:M源:P源)が1:x:1−x:1となるように水を主成分とする溶媒に投入し、撹拌してLiFexM1−xPO4の前駆体溶液とし、この前駆体溶液を耐圧容器に入れ、高温、高圧下、例えば、120℃以上かつ250℃以下、0.2MPa以上にて、1時間以上かつ24時間以下、水熱処理を行うことにより得ることができる。
M源としては、例えば、塩化コバルト(II)(CoCl2)、炭酸コバルト(II)(CoCO3)、硫酸コバルト(II)(CoSO4)、酢酸コバルト(II)(Co(CH3COO)2)、蓚酸コバルト(II)(Co(COO)2)等のコバルト化合物またはその水和物、または、塩化マンガン(II)(MnCl2)、炭酸マンガン(II)(MnCO3)、硫酸マンガン(II)(MnSO4)、酢酸マンガン(II)(Mn(CH3COO)2)等のマンガン化合物またはその水和物、あるいは、塩化ニッケル(II)(NiCl2)、炭酸ニッケル(II)(NiCO3)、硫酸ニッケル(II)(NiSO4)、酢酸ニッケル(II)(Ni(CH3COO)2)等のニッケル化合物またはその水和物、が好適に用いられる。
(2)凝集粒子生成工程
上記の水熱合成法により得られたLiFePO4またはLiFexM1−xPO4(但し、MはCo、Mn及びNiの群から選択された1種または2種以上、0<x<1)からなる粒子またはその前駆体に、炭素源を添加して焼成する。
上記の水熱合成法により得られたLiFePO4またはLiFexM1−xPO4(但し、MはCo、Mn及びNiの群から選択された1種または2種以上、0<x<1)からなる粒子またはその前駆体に、炭素源を添加して焼成する。
上記の炭素源としては、非酸化性雰囲気下にて熱処理することにより炭素を生成する有機化合物であればよく、特に制限はされないが、例えば、ポリビニルアルコール(PVA)、ポリビニルピロリドン、メチルセルロースあるいはエチルセルロース等のセルロース、デンプン、ゼラチン、ヒアルロン酸、ブドウ糖(D−グルコース)、果糖(D−フルクトース)、ショ糖、乳糖等の糖類、ヘキサノール、オクタノール等の高級一価アルコール、アリルアルコール、プロピノール(プロパルギルアルコール)、テルピネオール等の不飽和一価アルコール、ポリ酢酸ビニル、ポリエーテル等が挙げられる。特に、ブドウ糖(D−グルコース)、果糖(D−フルクトース)、ポリビニルアルコール(PVA)等は、スラリーを作製する際に均一な溶液相を形成するので好ましい。
この有機化合物の濃度は、特に限定されるものではないが、LiFePO4粒子(またはLiFexM1−xPO4粒子)の表面に、所定の厚みの炭素質被膜を均一に形成するためには、1質量%以上かつ25質量%以下が好ましい。
ここでは、LiFePO4(またはLiFexM1−xPO4)からなる粒子またはその前駆体と、炭素源とを所定量、水中に分散させてスラリーを作製する。分散させる装置としては、遊星ミル、振動ミル、ボールミル等が好適に用いられる。
分散粒子の凝集状態をコントロールするには、凝集剤を使用したり、等電点を利用することで行う。
凝集剤には無機系と有機系があり、無機系凝集剤としては、Al、Fe、Ca、Mg等の多価金属の水酸化物または塩を、有機系凝集剤としては、アルギン酸ナトリウム、アクリル酸ナトリウム、マレイン酸共重合物塩、ポリアクリルアミド部分加水分解物塩等のアニオン性、デンプン、水溶性尿素樹脂、ポリアクリルアミド、ポリオキシエチレン等のノニオン性、水溶性アニリン樹脂塩酸塩、ポリチオ尿酸酢酸塩、クロライド、ポリエチレンイミン、ビニルピリジン共重合物塩等のカチオン性、ゼラチン等の両性凝集剤を、適宜使用することができる。
分散粒子の凝集状態をコントロールするには、凝集剤を使用したり、等電点を利用することで行う。
凝集剤には無機系と有機系があり、無機系凝集剤としては、Al、Fe、Ca、Mg等の多価金属の水酸化物または塩を、有機系凝集剤としては、アルギン酸ナトリウム、アクリル酸ナトリウム、マレイン酸共重合物塩、ポリアクリルアミド部分加水分解物塩等のアニオン性、デンプン、水溶性尿素樹脂、ポリアクリルアミド、ポリオキシエチレン等のノニオン性、水溶性アニリン樹脂塩酸塩、ポリチオ尿酸酢酸塩、クロライド、ポリエチレンイミン、ビニルピリジン共重合物塩等のカチオン性、ゼラチン等の両性凝集剤を、適宜使用することができる。
また、分散粒子の等電点を調整することで粒子間の反発をコントロールすることにより、凝集状態をコントロールしてもよい。
次いで、このスラリーを噴霧乾燥法を用いて乾燥造粒し、造粒物を得る。噴霧乾燥法が適用される装置としては、略球形の造粒体が得られることからスプレイドライヤーが好適である。
次いで、このスラリーを噴霧乾燥法を用いて乾燥造粒し、造粒物を得る。噴霧乾燥法が適用される装置としては、略球形の造粒体が得られることからスプレイドライヤーが好適である。
この工程では、LiFePO4(またはLiFexM1−xPO4)粒子またはその前駆体と、炭素源とを所定量、水中に分散させたスラリーを、例えば、70℃以上かつ250℃以下の大気中に噴霧し乾燥造粒することにより、このLiFePO4(またはLiFexM1−xPO4)粒子またはその前駆体の表面を炭素源(有機化合物)にて覆った一次粒子またはその前駆体を集合した略球状の造粒物が得られる。
次いで、得られた造粒物を、非酸化性雰囲気中、例えば、窒素ガス等の不活性ガス雰囲気中、あるいは、酸化を防止したい場合には窒素ガスに数体積%程度の水素ガスを混入させた還元性ガス雰囲気中、600℃以上かつ1000℃以下の温度にて、0.1時間以上かつ40時間以下、焼成する。なお、焼成時に非酸化性雰囲気中に蒸発した炭素源(有機化合物)を除去する目的で、酸素等の支燃性または可燃性ガスを不活性雰囲気中に導入することとしてもよい。
これにより、LiFePO4(またはLiFexM1−xPO4)粒子が生成するとともに、LiFePO4(またはLiFexM1−xPO4)粒子は、表面を被覆する炭素源が炭化して、LiFePO4(またはLiFexM1−xPO4)粒子の表面を有機化合物由来の炭素質被膜にて覆う一次粒子(表面被膜LiFePO4粒子または表面被膜LiFexM1−xPO4粒子)になるとともに、この一次粒子(表面被膜LiFePO4粒子または表面被膜LiFexM1−xPO4粒子)は複数個凝集して凝集粒子となる。
この凝集粒子の形状は、特に限定されないが、球状、特に真球状の二次粒子からなる電極材料が生成しやすいことから、球状、特に真球状のものが好ましい。
以上により、LiFePO4粒子またはLiFexM1−xPO4粒子の表面が炭素質被膜により被覆されてなる一次粒子が複数個凝集した凝集粒子からなるリチウムイオン電池用電極材料を作製することができる。
以上により、LiFePO4粒子またはLiFexM1−xPO4粒子の表面が炭素質被膜により被覆されてなる一次粒子が複数個凝集した凝集粒子からなるリチウムイオン電池用電極材料を作製することができる。
[リチウムイオン電池]
本実施形態のリチウムイオン電池は、本実施形態のリチウムイオン電池用電極材料を含有してなるリチウムイオン電池用電極を、正極として備えている。
本実施形態の正極を作製するには、上記のリチウムイオン電池用電極材料と、バインダー樹脂からなる結着剤と、溶媒とを混合して、電極形成用塗料または電極形成用ペーストを調整する。この際、必要に応じてカーボンブラック等の導電助剤を添加してもよい。
本実施形態のリチウムイオン電池は、本実施形態のリチウムイオン電池用電極材料を含有してなるリチウムイオン電池用電極を、正極として備えている。
本実施形態の正極を作製するには、上記のリチウムイオン電池用電極材料と、バインダー樹脂からなる結着剤と、溶媒とを混合して、電極形成用塗料または電極形成用ペーストを調整する。この際、必要に応じてカーボンブラック等の導電助剤を添加してもよい。
上記の結着剤、すなわちバインダー樹脂としては、例えば、ポリテトラフルオロエチレン(PTFE)樹脂、ポリフッ化ビニリデン(PVdF)樹脂、フッ素ゴム等が好適に用いられる。
上記のリチウムイオン電池用電極材料とバインダー樹脂との配合比は、特に限定されないが、例えば、リチウムイオン電池用電極材料100質量部に対してバインダー樹脂を1質量部以上かつ30質量部以下、好ましくは3質量部以上かつ20質量部以下とする。
上記のリチウムイオン電池用電極材料とバインダー樹脂との配合比は、特に限定されないが、例えば、リチウムイオン電池用電極材料100質量部に対してバインダー樹脂を1質量部以上かつ30質量部以下、好ましくは3質量部以上かつ20質量部以下とする。
この電極形成用塗料または電極形成用ペーストに用いる溶媒としては、例えば、水、メタノール、エタノール、1−プロパノール、2−プロパノール(イソプロピルアルコール:IPA)、ブタノール、ペンタノール、ヘキサノール、オクタノール、ジアセトンアルコール等のアルコール類、酢酸エチル、酢酸ブチル、乳酸エチル、プロピレングリコールモノメチルエーテルアセテート、プロピレングリコールモノエチルエーテルアセテート、γ−ブチロラクトン等のエステル類、ジエチルエーテル、エチレングルコールモノメチルエーテル(メチルセロソルブ)、エチレングルコールモノエチルエーテル(エチルセロソルブ)、エチレングルコールモノブチルエーテル(ブチルセロソルブ)、ジエチレングリコールモノメチルエーテル、ジエチレングリコールモノエチルエーテル等のエーテル類が挙げられる。
また、アセトン、メチルエチルケトン(MEK)、メチルイソブチルケトン(MIBK)、アセチルアセトン、シクロヘキサノン等のケトン類、ジメチルホルムアミド、N,N−ジメチルアセトアセトアミド、N−メチルピロリドン等のアミド類、エチレングリコール、ジエチレングリコール、プロピレングリコール等のグリコール類等も挙げることができる。これらは、1種のみを単独で用いてもよく、2種以上を混合して用いてもよい。
次いで、この電極形成用塗料または電極形成用ペーストを、金属箔の一方の面に塗布し、その後、乾燥し、上記のリチウムイオン電池用電極材料とバインダー樹脂との混合物からなる塗膜が一方の面に形成された金属箔を得る。
次いで、この塗膜を加圧圧着し、乾燥して、金属箔の一方の面に正極層を有する集電体(電極)を作製する。
この集電体(電極)を正極とすることで、リチウムイオン電池を得ることができる。
次いで、この塗膜を加圧圧着し、乾燥して、金属箔の一方の面に正極層を有する集電体(電極)を作製する。
この集電体(電極)を正極とすることで、リチウムイオン電池を得ることができる。
以上説明したように、本実施形態のリチウムイオン電池用電極材料によれば、LiFePO4またはLiFexM1−xPO4(但し、MはCo、Mn及びNiの群から選択された1種または2種以上、0<x<1)からなる電極活物質粒子の表面が炭素質被膜により被覆されてなる一次粒子の平均一次粒子径を10nm以上かつ1000nm以下、この一次粒子を複数個凝集した凝集粒子の累積粒度分布における累積百分率30%の粒子径(D30)の累積百分率70%の粒子径(D70)に対する比(D30/D70)を0.20以上かつ0.48以下、タップ密度を1.0g/cm3以上かつ1.7g/cm3以下、圧粉体密度を電極活物質粒子の真密度の50%以上かつ75%以下としたので、導電性が低下することなく、放電容量を大幅に向上させることができ、出力特性も大幅に向上させることができる。
本実施形態のリチウムイオン電池用電極材料の製造方法によれば、水熱合成法により、LiFePO4またはLiFexM1−xPO4(但し、MはCo、Mn及びNiの群から選択された1種または2種以上、0<x<1)からなる粒子またはその前駆体を作製し、次いで、この粒子またはその前駆体に炭素源を添加して焼成することにより、生成する粒子の表面を炭素質被膜にて覆う一次粒子とするとともに該一次粒子を複数個凝集する凝集粒子を生成するので、導電性が低下することなく、高い放電容量及び高い出力特性を有するリチウムイオン電池用電極材料を、効率よく、安定して製造することができる。
本実施形態のリチウムイオン電池によれば、本実施形態のリチウムイオン電池用電極材料を含有してなるリチウムイオン電池用電極を、正極として備えたので、導電性が低下することなく、放電容量を大幅に向上させることができ、出力特性も大幅に向上させることができる。
以下、実施例1〜8及び比較例1〜4により本発明を具体的に説明するが、本発明はこれらの実施例によって限定されるものではない。
(実施例1)
凝集粒子の合成を行った。
ここでは、まず、Li源として酢酸リチウム(LiCH3COO)を、Fe源として硫酸鉄(II)(FeSO4)を、P源としてオルトリン酸(H3PO4)を、それぞれ用い、これらをモル比でLi:Fe:P=1:1:1となるように、純水に溶解して、0.1モル/kgの原料スラリーを作製して耐圧容器に収納し、170℃にて1時間、水熱合成を行った。
凝集粒子の合成を行った。
ここでは、まず、Li源として酢酸リチウム(LiCH3COO)を、Fe源として硫酸鉄(II)(FeSO4)を、P源としてオルトリン酸(H3PO4)を、それぞれ用い、これらをモル比でLi:Fe:P=1:1:1となるように、純水に溶解して、0.1モル/kgの原料スラリーを作製して耐圧容器に収納し、170℃にて1時間、水熱合成を行った。
この反応後に室温になるまで冷却し、沈殿しているケーキ状の反応生成物を得た。
このケーキ状物質を70℃にて2時間真空乾燥させ、乾燥粉体を得た。
この乾燥粉体から若干量の試料を採取し、この試料をX線回折法にて同定したところ、単相のLiFePO4が生成していることが確認された。
この乾燥粉体を走査型電子顕微鏡にて観察し、無作為に500個の粒子を選び出して、各々の一次粒子径を測定し、平均一次粒子径を算出した。その結果、平均一次粒子径は15nmであった。
このケーキ状物質を70℃にて2時間真空乾燥させ、乾燥粉体を得た。
この乾燥粉体から若干量の試料を採取し、この試料をX線回折法にて同定したところ、単相のLiFePO4が生成していることが確認された。
この乾燥粉体を走査型電子顕微鏡にて観察し、無作為に500個の粒子を選び出して、各々の一次粒子径を測定し、平均一次粒子径を算出した。その結果、平均一次粒子径は15nmであった。
次いで、この反応生成物93質量部と、有機化合物として固形分換算で5質量部となるように調製したポリビニルアルコール10%水溶液と、凝集剤としてゼラチン2質量部を、純水中に投入し、撹拌することにより、懸濁したスラリーを得た。
次いで、このスラリーを、スプレードライヤーを用いて、100℃の大気雰囲気下にて、凝集粒子径が3μm程度になるようにスラリー濃度および送液速度を調整し、乾燥造粒した。乾燥造粒後の粉体は球形であった。
次いで、このスラリーを、スプレードライヤーを用いて、100℃の大気雰囲気下にて、凝集粒子径が3μm程度になるようにスラリー濃度および送液速度を調整し、乾燥造粒した。乾燥造粒後の粉体は球形であった。
次いで、この粉体を、窒素ガス雰囲気中、600℃にて1時間、焼成を行うことにより、粒子表面に炭素質被膜を形成するとともに、これらの粒子を凝集してなる凝集粒子を得た。
このようにして得られた凝集粒子の平均粒子径(平均二次粒子径)、比(D30/D70)、体積密度、比表面積、タップ密度、圧粉体密度、炭素量、炭素質被膜の被覆率、凝集粒子の崩れ易さ、をそれぞれ評価した。
評価方法は、次のとおりである。
このようにして得られた凝集粒子の平均粒子径(平均二次粒子径)、比(D30/D70)、体積密度、比表面積、タップ密度、圧粉体密度、炭素量、炭素質被膜の被覆率、凝集粒子の崩れ易さ、をそれぞれ評価した。
評価方法は、次のとおりである。
(1)平均粒子径及び比(D30/D70)
レーザー式回折粒度分布測定装置 SALD−1000(島津製作所(株)社製)を用いて測定した。
(2)体積密度
水銀ポロシメーターを用いて、凝集粒子全体の質量と、凝集粒子の粒子間隙の体積とを測定し、これらの質量及び体積を基に凝集粒子の体積密度(%)を算出した。
(3)比表面積
比表面積計 BELSORP−mini(日本ベル社製)を用いて、凝集粒子の比表面積を、窒素(N2)吸着によるBET法により測定した。
レーザー式回折粒度分布測定装置 SALD−1000(島津製作所(株)社製)を用いて測定した。
(2)体積密度
水銀ポロシメーターを用いて、凝集粒子全体の質量と、凝集粒子の粒子間隙の体積とを測定し、これらの質量及び体積を基に凝集粒子の体積密度(%)を算出した。
(3)比表面積
比表面積計 BELSORP−mini(日本ベル社製)を用いて、凝集粒子の比表面積を、窒素(N2)吸着によるBET法により測定した。
(4)タップ密度
凝集粒子から所定の質量の試料を採取し、この試料を容積10mLのガラス製のメスシリンダーに投入し、この試料をメスシリンダーとともに振動させ、この試料の容積が変化しなくなった時点で試料の容積を測定し、この試料の質量を容積で除した値をタップ密度とした。
(5)圧粉体密度
所定量の凝集粒子を0.38t/cm2の圧力にて成形し、得られた成形体の質量と容積から圧粉体密度を算出した。
(6)炭素量
凝集粒子の炭素量を、炭素分析計を用いて測定した。
凝集粒子から所定の質量の試料を採取し、この試料を容積10mLのガラス製のメスシリンダーに投入し、この試料をメスシリンダーとともに振動させ、この試料の容積が変化しなくなった時点で試料の容積を測定し、この試料の質量を容積で除した値をタップ密度とした。
(5)圧粉体密度
所定量の凝集粒子を0.38t/cm2の圧力にて成形し、得られた成形体の質量と容積から圧粉体密度を算出した。
(6)炭素量
凝集粒子の炭素量を、炭素分析計を用いて測定した。
(7)炭素質被膜の被覆率
凝集粒子の炭素質被膜を、透過型電子顕微鏡(TEM)及びエネルギー分散型X線分光器(EDX)を用いて観察し、凝集粒子の表面のうち炭素質被膜が覆っている部分の割合を算出し、被覆率とした。
(8)凝集粒子の崩れ易さ
凝集粒子の崩れ易さを、圧粉体密度/タップ密度比により評価した。
ここでは、圧粉体密度/タップ密度比が1.6以上となったものを崩れ易い(○)とし、圧粉体密度/タップ密度比が1.6未満となったものを崩れ難い(×)とした。
凝集粒子の炭素質被膜を、透過型電子顕微鏡(TEM)及びエネルギー分散型X線分光器(EDX)を用いて観察し、凝集粒子の表面のうち炭素質被膜が覆っている部分の割合を算出し、被覆率とした。
(8)凝集粒子の崩れ易さ
凝集粒子の崩れ易さを、圧粉体密度/タップ密度比により評価した。
ここでは、圧粉体密度/タップ密度比が1.6以上となったものを崩れ易い(○)とし、圧粉体密度/タップ密度比が1.6未満となったものを崩れ難い(×)とした。
このようにして得られた凝集粒子の平均粒子径は1.20μm、比(D30/D70)は0.23、体積密度は71.6%、比表面積は14.87m2/g、タップ密度は1.62g/cm3、圧粉体密度は2.6g/cm3、炭素量は4.87%、凝集粒子の崩れ易さは「○」であった。
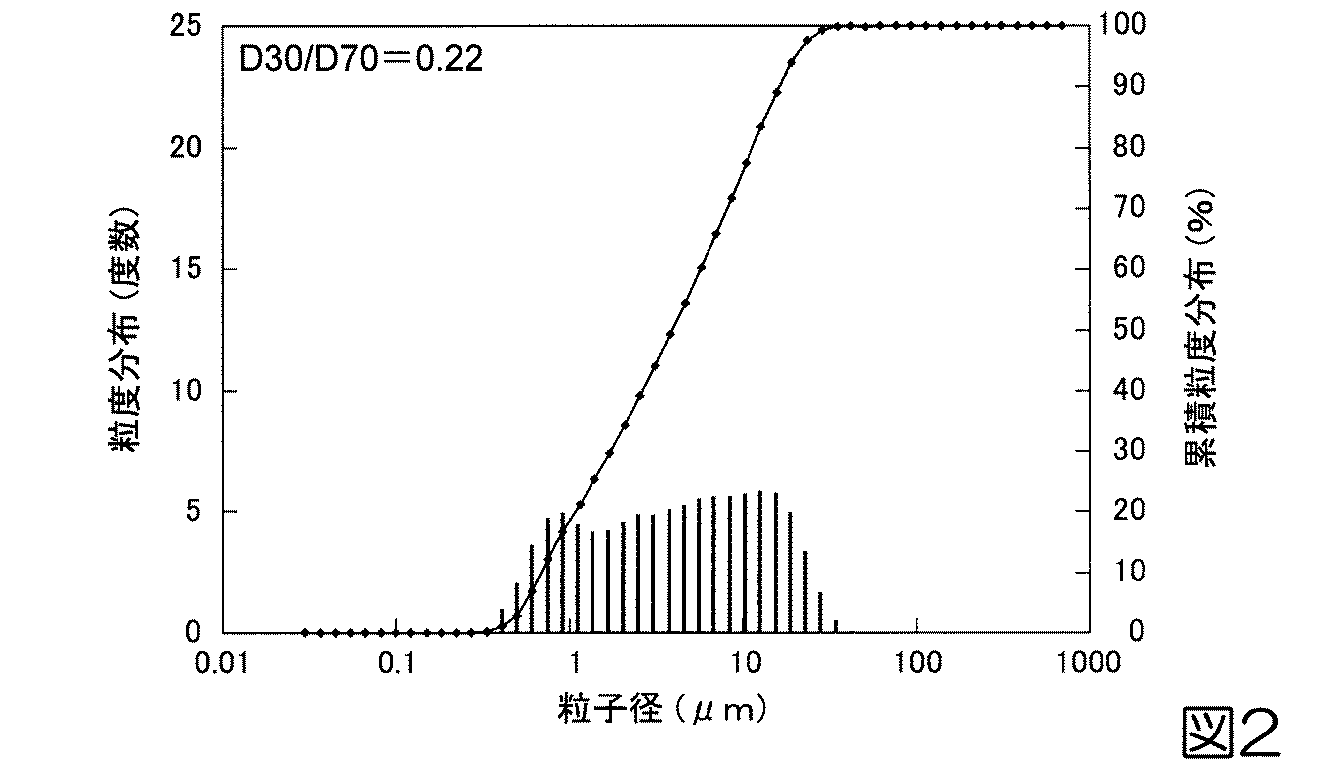
これらの評価結果を表1に示す。また、凝集粒子の粒度分布及び累積粒度分布を図1に示す。
これらの評価結果を表1に示す。また、凝集粒子の粒度分布及び累積粒度分布を図1に示す。
(実施例2)
Li源として酢酸リチウム(LiCH3COO)を、Fe源として硫酸鉄(II)(FeSO4)を、P源としてオルトリン酸(H3PO4)を、それぞれ用い、これらをモル比でLi:Fe:P=1:1:1となるように、純水に溶解して、0.1モル/kgの原料スラリーを作製して耐圧容器に収納し、170℃にて5時間、水熱合成を行った。得られたケーキ状の反応生成物の平均一次粒子径は98nmであった。
Li源として酢酸リチウム(LiCH3COO)を、Fe源として硫酸鉄(II)(FeSO4)を、P源としてオルトリン酸(H3PO4)を、それぞれ用い、これらをモル比でLi:Fe:P=1:1:1となるように、純水に溶解して、0.1モル/kgの原料スラリーを作製して耐圧容器に収納し、170℃にて5時間、水熱合成を行った。得られたケーキ状の反応生成物の平均一次粒子径は98nmであった。
次いで、この反応生成物93質量部と、有機化合物として固形分換算で5質量部となるように調製したポリビニルアルコール10%水溶液と、凝集剤としてゼラチン2質量部を、純水中に投入し、撹拌することにより、懸濁したスラリーを得た。
次いで、このスラリーを、スプレードライヤーを用いて、100℃の大気雰囲気下にて、凝集粒子径が5μm程度になるようにスラリー濃度および送液速度を調整し、乾燥造粒した。乾燥造粒後の粉体は球形であった。
次いで、この粉体を、窒素ガス雰囲気中、600℃にて1時間、焼成を行い、実施例2の凝集粒子を得た。
次いで、このスラリーを、スプレードライヤーを用いて、100℃の大気雰囲気下にて、凝集粒子径が5μm程度になるようにスラリー濃度および送液速度を調整し、乾燥造粒した。乾燥造粒後の粉体は球形であった。
次いで、この粉体を、窒素ガス雰囲気中、600℃にて1時間、焼成を行い、実施例2の凝集粒子を得た。
このようにして得られた凝集粒子の平均粒子径は7.50μm、比(D30/D70)は0.32、体積密度は70.3%、比表面積は8.99m2/g、タップ密度は1.23g/cm3、圧粉体密度は2.2g/cm3、炭素量は1.04%、凝集粒子の崩れ易さは「○」であった。
これらの評価結果を表1に示す。
これらの評価結果を表1に示す。
(実施例3)
Li源として酢酸リチウム(LiCH3COO)を、Fe源として硫酸鉄(II)(FeSO4)を、P源としてオルトリン酸(H3PO4)を、それぞれ用い、これらをモル比でLi:Fe:P=1:1:1となるように、純水に溶解して、0.1モル/kgの原料スラリーを作製して耐圧容器に収納し、170℃にて10時間、水熱合成を行った。得られたケーキ状の反応生成物の平均一次粒子径は130nmであった。
Li源として酢酸リチウム(LiCH3COO)を、Fe源として硫酸鉄(II)(FeSO4)を、P源としてオルトリン酸(H3PO4)を、それぞれ用い、これらをモル比でLi:Fe:P=1:1:1となるように、純水に溶解して、0.1モル/kgの原料スラリーを作製して耐圧容器に収納し、170℃にて10時間、水熱合成を行った。得られたケーキ状の反応生成物の平均一次粒子径は130nmであった。
次いで、この反応生成物93質量部と、有機化合物として固形分換算で5質量部となるように調製したポリビニルアルコール10%水溶液と、凝集剤としてゼラチン2質量部を、純水中に投入し、撹拌することにより、懸濁したスラリーを得た。
次いで、このスラリーを、スプレードライヤーを用いて、100℃の大気雰囲気下にて、凝集粒子径が10μm程度になるようにスラリー濃度および送液速度を調整し、乾燥造粒した。乾燥造粒後の粉体は球形であった。
次いで、この粉体を、窒素ガス雰囲気中、600℃にて1時間、焼成を行い、実施例3の凝集粒子を得た。
次いで、このスラリーを、スプレードライヤーを用いて、100℃の大気雰囲気下にて、凝集粒子径が10μm程度になるようにスラリー濃度および送液速度を調整し、乾燥造粒した。乾燥造粒後の粉体は球形であった。
次いで、この粉体を、窒素ガス雰囲気中、600℃にて1時間、焼成を行い、実施例3の凝集粒子を得た。
このようにして得られた凝集粒子の平均粒子径は10.50μm、比(D30/D70)は0.40、体積密度は72.0%、比表面積は7.29m2/g、タップ密度は1.34g/cm3、圧粉体密度は2.2g/cm3、炭素量は2.68%、凝集粒子の崩れ易さは「○」であった。
これらの評価結果を表1に示す。
これらの評価結果を表1に示す。
(実施例4)
Li源として酢酸リチウム(LiCH3COO)を、Fe源として硫酸鉄(II)(FeSO4)を、P源としてオルトリン酸(H3PO4)を、それぞれ用い、これらをモル比でLi:Fe:P=1:1:1となるように、純水に溶解して、0.1モル/kgの原料スラリーを作製して耐圧容器に収納し、200℃にて1時間、水熱合成を行った。得られたケーキ状の反応生成物の平均一次粒子径は560nmであった。
Li源として酢酸リチウム(LiCH3COO)を、Fe源として硫酸鉄(II)(FeSO4)を、P源としてオルトリン酸(H3PO4)を、それぞれ用い、これらをモル比でLi:Fe:P=1:1:1となるように、純水に溶解して、0.1モル/kgの原料スラリーを作製して耐圧容器に収納し、200℃にて1時間、水熱合成を行った。得られたケーキ状の反応生成物の平均一次粒子径は560nmであった。
次いで、この反応生成物93質量部と、有機化合物として固形分換算で5質量部となるように調製したポリビニルアルコール10%水溶液と、凝集剤としてゼラチン2質量部を、純水中に投入し、撹拌することにより、懸濁したスラリーを得た。
次いで、このスラリーを、スプレードライヤーを用いて、100℃の大気雰囲気下にて、凝集粒子径が50μm程度になるようにスラリー濃度および送液速度を調整し、乾燥造粒した。乾燥造粒後の粉体は球形であった。
次いで、この粉体を、窒素ガス雰囲気中、600℃にて1時間、焼成を行い、実施例4の凝集粒子を得た。
次いで、このスラリーを、スプレードライヤーを用いて、100℃の大気雰囲気下にて、凝集粒子径が50μm程度になるようにスラリー濃度および送液速度を調整し、乾燥造粒した。乾燥造粒後の粉体は球形であった。
次いで、この粉体を、窒素ガス雰囲気中、600℃にて1時間、焼成を行い、実施例4の凝集粒子を得た。
このようにして得られた凝集粒子の平均粒子径は52.30μm、比(D30/D70)は0.37、体積密度は58.5%、比表面積は7.65m2/g、タップ密度は1.32g/cm3、圧粉体密度は2.4g/cm3、炭素量は1.94%、凝集粒子の崩れ易さは「○」であった。
これらの評価結果を表1に示す。
これらの評価結果を表1に示す。
(実施例5)
Li源として酢酸リチウム(LiCH3COO)を、Fe源として硫酸鉄(II)(FeSO4)を、P源としてオルトリン酸(H3PO4)を、それぞれ用い、これらをモル比でLi:Fe:P=1:1:1となるように、純水に溶解して、0.1モル/kgの原料スラリーを作製して耐圧容器に収納し、200℃にて5時間、水熱合成を行った。得られたケーキ状の反応生成物の平均一次粒子径は920nmであった。
Li源として酢酸リチウム(LiCH3COO)を、Fe源として硫酸鉄(II)(FeSO4)を、P源としてオルトリン酸(H3PO4)を、それぞれ用い、これらをモル比でLi:Fe:P=1:1:1となるように、純水に溶解して、0.1モル/kgの原料スラリーを作製して耐圧容器に収納し、200℃にて5時間、水熱合成を行った。得られたケーキ状の反応生成物の平均一次粒子径は920nmであった。
次いで、この反応生成物93質量部と、有機化合物として固形分換算で5質量部となるように調製したポリビニルアルコール10%水溶液と、凝集剤としてゼラチン2質量部を、純水中に投入し、撹拌することにより、懸濁したスラリーを得た。
次いで、このスラリーを、スプレードライヤーを用いて、100℃の大気雰囲気下にて、凝集粒子径が100μm程度になるようにスラリー濃度および送液速度を調整し、乾燥造粒した。乾燥造粒後の粉体は球形であった。
次いで、この粉体を、窒素ガス雰囲気中、600℃にて1時間、焼成を行い、実施例5の凝集粒子を得た。
次いで、このスラリーを、スプレードライヤーを用いて、100℃の大気雰囲気下にて、凝集粒子径が100μm程度になるようにスラリー濃度および送液速度を調整し、乾燥造粒した。乾燥造粒後の粉体は球形であった。
次いで、この粉体を、窒素ガス雰囲気中、600℃にて1時間、焼成を行い、実施例5の凝集粒子を得た。
このようにして得られた凝集粒子の平均粒子径は81.60μm、比(D30/D70)は0.41、体積密度は64.5%、比表面積は4.58m2/g、タップ密度は1.02g/cm3、圧粉体密度は1.7g/cm3、炭素量は0.98%、凝集粒子の崩れ易さは「○」であった。
これらの評価結果を表1に示す。
これらの評価結果を表1に示す。
(実施例6)
Li源として酢酸リチウム(LiCH3COO)を、Mn源として硫酸マンガン(II)(MnSO4)を、P源としてオルトリン酸(H3PO4)を、それぞれ用い、これらをモル比でLi:Mn:P=1:1:1となるように、純水に溶解して、0.1モル/kgの原料スラリーを作製して耐圧容器に収納し、170℃にて1時間、水熱合成を行った。得られたケーキ状の反応生成物の平均一次粒子径は21nmであった。
Li源として酢酸リチウム(LiCH3COO)を、Mn源として硫酸マンガン(II)(MnSO4)を、P源としてオルトリン酸(H3PO4)を、それぞれ用い、これらをモル比でLi:Mn:P=1:1:1となるように、純水に溶解して、0.1モル/kgの原料スラリーを作製して耐圧容器に収納し、170℃にて1時間、水熱合成を行った。得られたケーキ状の反応生成物の平均一次粒子径は21nmであった。
次いで、この反応生成物93質量部と、有機化合物として固形分換算で5質量部となるように調製したポリビニルアルコール10%水溶液と、凝集剤としてゼラチン2質量部を、純水中に投入し、撹拌することにより、懸濁したスラリーを得た。
次いで、このスラリーを、スプレードライヤーを用いて、100℃の大気雰囲気下にて、凝集粒子径が5μm程度になるようにスラリー濃度および送液速度を調整し、乾燥造粒した。乾燥造粒後の粉体は球形であった。
次いで、この粉体を、窒素ガス雰囲気中、600℃にて1時間、焼成を行い、実施例6の凝集粒子を得た。
次いで、このスラリーを、スプレードライヤーを用いて、100℃の大気雰囲気下にて、凝集粒子径が5μm程度になるようにスラリー濃度および送液速度を調整し、乾燥造粒した。乾燥造粒後の粉体は球形であった。
次いで、この粉体を、窒素ガス雰囲気中、600℃にて1時間、焼成を行い、実施例6の凝集粒子を得た。
このようにして得られた凝集粒子の平均粒子径は3.55μm、比(D30/D70)は0.22、体積密度は72.2%、比表面積は30.12m2/g、タップ密度は1.44g/cm3、圧粉体密度は2.5g/cm3、炭素量は1.96%、凝集粒子の崩れ易さは「○」であった。
これらの評価結果を表1に示す。
これらの評価結果を表1に示す。
(実施例7)
Li源として酢酸リチウム(LiCH3COO)を、Mn源として硫酸マンガン(II)(MnSO4)を、P源としてオルトリン酸(H3PO4)を、それぞれ用い、これらをモル比でLi:Mn:P=1:1:1となるように、純水に溶解して、0.1モル/kgの原料スラリーを作製して耐圧容器に収納し、170℃にて5時間、水熱合成を行った。得られたケーキ状の反応生成物の平均一次粒子径は120nmであった。
Li源として酢酸リチウム(LiCH3COO)を、Mn源として硫酸マンガン(II)(MnSO4)を、P源としてオルトリン酸(H3PO4)を、それぞれ用い、これらをモル比でLi:Mn:P=1:1:1となるように、純水に溶解して、0.1モル/kgの原料スラリーを作製して耐圧容器に収納し、170℃にて5時間、水熱合成を行った。得られたケーキ状の反応生成物の平均一次粒子径は120nmであった。
次いで、この反応生成物93質量部と、有機化合物として固形分換算で5質量部となるように調製したポリビニルアルコール10%水溶液と、凝集剤としてゼラチン2質量部を、純水中に投入し、撹拌することにより、懸濁したスラリーを得た。
次いで、このスラリーを、スプレードライヤーを用いて、100℃の大気雰囲気下にて、凝集粒子径が20μm程度になるようにスラリー濃度および送液速度を調整し、乾燥造粒した。乾燥造粒後の粉体は球形であった。
次いで、この粉体を、窒素ガス雰囲気中、600℃にて1時間、焼成を行い、実施例7の凝集粒子を得た。
次いで、このスラリーを、スプレードライヤーを用いて、100℃の大気雰囲気下にて、凝集粒子径が20μm程度になるようにスラリー濃度および送液速度を調整し、乾燥造粒した。乾燥造粒後の粉体は球形であった。
次いで、この粉体を、窒素ガス雰囲気中、600℃にて1時間、焼成を行い、実施例7の凝集粒子を得た。
このようにして得られた凝集粒子の平均粒子径は20.80μm、比(D30/D70)は0.27、体積密度は73.1%、比表面積は52.30m2/g、タップ密度は1.65g/cm3、圧粉体密度は2.7g/cm3、炭素量は2.73%、凝集粒子の崩れ易さは「○」であった。
これらの評価結果を表1に示す。
これらの評価結果を表1に示す。
(実施例8)
Li源として酢酸リチウム(LiCH3COO)を、Mn源として硫酸マンガン(II)(MnSO4)を、P源としてオルトリン酸(H3PO4)を、それぞれ用い、これらをモル比でLi:Mn:P=1:1:1となるように、純水に溶解して、0.1モル/kgの原料スラリーを作製して耐圧容器に収納し、200℃にて1時間、水熱合成を行った。得られたケーキ状の反応生成物の平均一次粒子径は720nmであった。
Li源として酢酸リチウム(LiCH3COO)を、Mn源として硫酸マンガン(II)(MnSO4)を、P源としてオルトリン酸(H3PO4)を、それぞれ用い、これらをモル比でLi:Mn:P=1:1:1となるように、純水に溶解して、0.1モル/kgの原料スラリーを作製して耐圧容器に収納し、200℃にて1時間、水熱合成を行った。得られたケーキ状の反応生成物の平均一次粒子径は720nmであった。
次いで、この反応生成物93質量部と、有機化合物として固形分換算で5質量部となるように調製したポリビニルアルコール10%水溶液と、凝集剤としてゼラチン2質量部を、純水中に投入し、撹拌することにより、懸濁したスラリーを得た。
次いで、このスラリーを、スプレードライヤーを用いて、100℃の大気雰囲気下にて、凝集粒子径が100μm程度になるようにスラリー濃度および送液速度を調整し、乾燥造粒した。乾燥造粒後の粉体は球形であった。
次いで、この粉体を、窒素ガス雰囲気中、600℃にて1時間、焼成を行い、実施例8の凝集粒子を得た。
次いで、このスラリーを、スプレードライヤーを用いて、100℃の大気雰囲気下にて、凝集粒子径が100μm程度になるようにスラリー濃度および送液速度を調整し、乾燥造粒した。乾燥造粒後の粉体は球形であった。
次いで、この粉体を、窒素ガス雰囲気中、600℃にて1時間、焼成を行い、実施例8の凝集粒子を得た。
このようにして得られた凝集粒子の平均粒子径は92.10μm、比(D30/D70)は0.36、体積密度は62.0%、比表面積は20.12m2/g、タップ密度は1.10g/cm3、圧粉体密度は2.0g/cm3、炭素量は1.20%、凝集粒子の崩れ易さは「○」であった。
これらの評価結果を表1に示す。
これらの評価結果を表1に示す。
(比較例1)
Li源として酢酸リチウム(LiCH3COO)を、Fe源として硫酸鉄(II)(FeSO4)を、P源としてオルトリン酸(H3PO4)を、それぞれ用い、これらをモル比でLi:Fe:P=1:1:1となるように、純水に溶解して、0.1モル/kgの原料スラリーを作製して耐圧容器に収納し、170℃にて0.5時間、水熱合成を行った。得られたケーキ状の反応生成物の平均一次粒子径は7nmであった。
Li源として酢酸リチウム(LiCH3COO)を、Fe源として硫酸鉄(II)(FeSO4)を、P源としてオルトリン酸(H3PO4)を、それぞれ用い、これらをモル比でLi:Fe:P=1:1:1となるように、純水に溶解して、0.1モル/kgの原料スラリーを作製して耐圧容器に収納し、170℃にて0.5時間、水熱合成を行った。得られたケーキ状の反応生成物の平均一次粒子径は7nmであった。
次いで、この反応生成物93質量部と、有機化合物として固形分換算で5質量部となるように調製したポリビニルアルコール10%水溶液とを、純水中に投入し撹拌することにより、懸濁したスラリーを得た。この懸濁したスラリーには凝集剤を添加しなかった。
次いで、このスラリーを、スプレードライヤーを用いて、100℃の大気雰囲気下にて、凝集粒子径が1μm程度になるようにスラリー濃度および送液速度を調整し、乾燥造粒した。乾燥造粒後の粉体は球形であった。
次いで、この粉体を、窒素ガス雰囲気中、600℃にて1時間、焼成を行い、比較例1の凝集粒子を得た。
次いで、このスラリーを、スプレードライヤーを用いて、100℃の大気雰囲気下にて、凝集粒子径が1μm程度になるようにスラリー濃度および送液速度を調整し、乾燥造粒した。乾燥造粒後の粉体は球形であった。
次いで、この粉体を、窒素ガス雰囲気中、600℃にて1時間、焼成を行い、比較例1の凝集粒子を得た。
このようにして得られた凝集粒子の平均粒子径は0.32μm、比(D30/D70)は0.63、体積密度は48.3%、比表面積は18.90m2/g、タップ密度は1.76g/cm3、圧粉体密度は2.6g/cm3、炭素量は6.26%、凝集粒子の崩れ易さは「×」であった。
これらの評価結果を表1に示す。
これらの評価結果を表1に示す。
(比較例2)
Li源として酢酸リチウム(LiCH3COO)を、Fe源として硫酸鉄(II)(FeSO4)を、P源としてオルトリン酸(H3PO4)を、それぞれ用い、これらをモル比でLi:Fe:P=1:1:1となるように、純水に溶解して、0.1モル/kgの原料スラリーを作製して耐圧容器に収納し、200℃にて10時間、水熱合成を行った。得られたケーキ状の反応生成物の平均一次粒子径は1180nmであった。
Li源として酢酸リチウム(LiCH3COO)を、Fe源として硫酸鉄(II)(FeSO4)を、P源としてオルトリン酸(H3PO4)を、それぞれ用い、これらをモル比でLi:Fe:P=1:1:1となるように、純水に溶解して、0.1モル/kgの原料スラリーを作製して耐圧容器に収納し、200℃にて10時間、水熱合成を行った。得られたケーキ状の反応生成物の平均一次粒子径は1180nmであった。
次いで、この反応生成物93質量部と、有機化合物として固形分換算で5質量部となるように調製したポリビニルアルコール10%水溶液とを、純水中に投入し撹拌することにより、懸濁したスラリーを得た。この懸濁したスラリーには凝集剤を添加しなかった。
次いで、このスラリーを、スプレードライヤーを用いて、100℃の大気雰囲気下にて、凝集粒子径が100μm程度になるようにスラリー濃度および送液速度を調整し、乾燥造粒した。乾燥造粒後の粉体は球形であった。
次いで、この粉体を、窒素ガス雰囲気中、600℃にて1時間、焼成を行い、比較例2の凝集粒子を得た。
次いで、このスラリーを、スプレードライヤーを用いて、100℃の大気雰囲気下にて、凝集粒子径が100μm程度になるようにスラリー濃度および送液速度を調整し、乾燥造粒した。乾燥造粒後の粉体は球形であった。
次いで、この粉体を、窒素ガス雰囲気中、600℃にて1時間、焼成を行い、比較例2の凝集粒子を得た。
このようにして得られた凝集粒子の平均粒子径は121.80μm、比(D30/D70)は0.19、体積密度は71.1%、比表面積は3.79m2/g、タップ密度は0.98g/cm3、圧粉体密度は1.3g/cm3、炭素量は0.31%、凝集粒子の崩れ易さは「×」であった。
これらの評価結果を表1に示す。
これらの評価結果を表1に示す。
(比較例3)
Li源として酢酸リチウム(LiCH3COO)を、Mn源として硫酸マンガン(II)(MnSO4)を、P源としてオルトリン酸(H3PO4)を、それぞれ用い、これらをモル比でLi:Mn:P=1:1:1となるように、純水に溶解して、0.1モル/kgの原料スラリーを作製して耐圧容器に収納し、170℃にて0.5時間、水熱合成を行った。得られたケーキ状の反応生成物の平均一次粒子径は8nmであった。
Li源として酢酸リチウム(LiCH3COO)を、Mn源として硫酸マンガン(II)(MnSO4)を、P源としてオルトリン酸(H3PO4)を、それぞれ用い、これらをモル比でLi:Mn:P=1:1:1となるように、純水に溶解して、0.1モル/kgの原料スラリーを作製して耐圧容器に収納し、170℃にて0.5時間、水熱合成を行った。得られたケーキ状の反応生成物の平均一次粒子径は8nmであった。
次いで、この反応生成物93質量部と、有機化合物として固形分換算で5質量部となるように調製したポリビニルアルコール10%水溶液を、純水中に投入し撹拌することにより、懸濁したスラリーを得た。この懸濁したスラリーには凝集剤を添加しなかった。
次いで、このスラリーを、スプレードライヤーを用いて、100℃の大気雰囲気下にて、凝集粒子径が1μm程度になるようにスラリー濃度および送液速度を調整し、乾燥造粒した。乾燥造粒後の粉体は球形であった。
次いで、この粉体を、窒素ガス雰囲気中、600℃にて1時間、焼成を行い、比較例3の凝集粒子を得た。
次いで、このスラリーを、スプレードライヤーを用いて、100℃の大気雰囲気下にて、凝集粒子径が1μm程度になるようにスラリー濃度および送液速度を調整し、乾燥造粒した。乾燥造粒後の粉体は球形であった。
次いで、この粉体を、窒素ガス雰囲気中、600℃にて1時間、焼成を行い、比較例3の凝集粒子を得た。
このようにして得られた凝集粒子の平均粒子径は0.88μm、比(D30/D70)は0.79、体積密度は42.6%、比表面積は20.90m2/g、タップ密度は1.79g/cm3、圧粉体密度は2.7g/cm3、炭素量は5.91%、凝集粒子の崩れ易さは「×」であった。
これらの評価結果を表1に示す。
これらの評価結果を表1に示す。
(比較例4)
Li源として酢酸リチウム(LiCH3COO)を、Mn源として硫酸マンガン(II)(MnSO4)を、P源としてオルトリン酸(H3PO4)を、それぞれ用い、これらをモル比でLi:Mn:P=1:1:1となるように、純水に溶解して、0.1モル/kgの原料スラリーを作製して耐圧容器に収納し、200℃にて10時間、水熱合成を行った。得られたケーキ状の反応生成物の平均一次粒子径は1240nmであった。
Li源として酢酸リチウム(LiCH3COO)を、Mn源として硫酸マンガン(II)(MnSO4)を、P源としてオルトリン酸(H3PO4)を、それぞれ用い、これらをモル比でLi:Mn:P=1:1:1となるように、純水に溶解して、0.1モル/kgの原料スラリーを作製して耐圧容器に収納し、200℃にて10時間、水熱合成を行った。得られたケーキ状の反応生成物の平均一次粒子径は1240nmであった。
次いで、この反応生成物93質量部と、有機化合物として固形分換算で5質量部となるように調製したポリビニルアルコール10%水溶液を、純水中に投入し撹拌することにより、懸濁したスラリーを得た。この懸濁したスラリーには凝集剤を添加しなかった。
次いで、このスラリーを、スプレードライヤーを用いて、100℃の大気雰囲気下にて、凝集粒子径が100μm程度になるようにスラリー濃度および送液速度を調整し、乾燥造粒した。乾燥造粒後の粉体は球形であった。
次いで、この粉体を、窒素ガス雰囲気中、600℃にて1時間、焼成を行い、比較例4の凝集粒子を得た。
次いで、このスラリーを、スプレードライヤーを用いて、100℃の大気雰囲気下にて、凝集粒子径が100μm程度になるようにスラリー濃度および送液速度を調整し、乾燥造粒した。乾燥造粒後の粉体は球形であった。
次いで、この粉体を、窒素ガス雰囲気中、600℃にて1時間、焼成を行い、比較例4の凝集粒子を得た。
このようにして得られた凝集粒子の平均粒子径は132.50μm、比(D30/D70)は0.15、体積密度は41.2%、比表面積は3.24m2/g、タップ密度は0.88g/cm3、圧粉体密度は1.3g/cm3、炭素量は0.38%、凝集粒子の崩れ易さは「×」であった。
これらの評価結果を表1に示す。
これらの評価結果を表1に示す。
(リチウムイオン電池の作製)
実施例1〜8及び比較例1〜4各々の正極を作製した。
ここでは、実施例1〜8及び比較例1〜4各々にて得られた凝集粒子をリチウムイオン電池用電極材料とし、導電助剤としてアセチレンブラック(AB)、バインダーとしてポリフッ化ビニリデン(PVdF)、溶媒としてN−メチル−2−ピロリジノン(NMP)を用い、これらを混合し、実施例1〜8及び比較例1〜4各々のペーストを作製した。なお、ペースト中の質量比、リチウムイオン電池用電極材料:AB:PVdFは85:10:5であった。
次いで、これらのペーストを厚み30μmのアルミニウム(Al)箔上に、300μm程度の厚みで塗布し、乾燥した。その後、40MPaの圧力にて圧密し、100μm程度の厚みの正極とした。
実施例1〜8及び比較例1〜4各々の正極を作製した。
ここでは、実施例1〜8及び比較例1〜4各々にて得られた凝集粒子をリチウムイオン電池用電極材料とし、導電助剤としてアセチレンブラック(AB)、バインダーとしてポリフッ化ビニリデン(PVdF)、溶媒としてN−メチル−2−ピロリジノン(NMP)を用い、これらを混合し、実施例1〜8及び比較例1〜4各々のペーストを作製した。なお、ペースト中の質量比、リチウムイオン電池用電極材料:AB:PVdFは85:10:5であった。
次いで、これらのペーストを厚み30μmのアルミニウム(Al)箔上に、300μm程度の厚みで塗布し、乾燥した。その後、40MPaの圧力にて圧密し、100μm程度の厚みの正極とした。
次いで、この正極を成形機を用いて面積が2cm2の円板状に打ち抜き、真空乾燥後、乾燥Ar雰囲気下にてステンレススチール(SUS)製の2032コイン型セルを用いて、実施例1〜8及び比較例1〜4各々のリチウムイオン電池を作製した。なお、負極には金属Liを、セパレーターには多孔質ボリプロピレン膜を、電解質溶液には1MのLiPF6溶液を、それぞれ用いた。このLiPF6溶液の溶媒としては、炭酸エチレンと炭酸ジエチルとの比が1:1のものを用いた。
「電池特性試験」
実施例1〜8及び比較例1〜4各々のリチウムイオン電池の電池特性試験を、環境温度25℃、充電電流1Cで10秒間充電し、その後10分間休止し、次いで、0.1C放電を行ったときの放電容量(0.1C放電容量)を測定し、さらに、第2サイクルとして、3C充電を10秒間行った後、10分休止し、次いで、3C放電を行ったときの放電容量(3C放電容量)を測定した。
ここでは、3C放電容量の0.1C放電容量に対する比(3C放電容量/0.1C放電容量)が83%以上を「良品」とし、83%未満を「不良品」とした。
実施例1〜8及び比較例1〜4各々のリチウムイオン電池の放電容量を表2に示す。
実施例1〜8及び比較例1〜4各々のリチウムイオン電池の電池特性試験を、環境温度25℃、充電電流1Cで10秒間充電し、その後10分間休止し、次いで、0.1C放電を行ったときの放電容量(0.1C放電容量)を測定し、さらに、第2サイクルとして、3C充電を10秒間行った後、10分休止し、次いで、3C放電を行ったときの放電容量(3C放電容量)を測定した。
ここでは、3C放電容量の0.1C放電容量に対する比(3C放電容量/0.1C放電容量)が83%以上を「良品」とし、83%未満を「不良品」とした。
実施例1〜8及び比較例1〜4各々のリチウムイオン電池の放電容量を表2に示す。
これらの評価結果によれば、実施例1〜8では、比(D30/D70)が0.2以上かつ0.48以下、タップ密度が1.0g/cm3以上かつ1.7g/cm3以下、圧粉体密度が真密度の50%以上かつ80%以下であることから、0.1C放電容量及び3C放電容量共に優れていることが分かった。
一方、比較例1〜4では、比(D30/D70)が0.20以上かつ0.48以下、タップ密度が1.0g/cm3以上かつ1.7g/cm3以下、圧粉体密度が真密度の50%以上かつ75%以下のいずれも満足していないことから、0.1C放電容量及び3C放電容量共に、実施例1〜8と比べて劣っていることが分かった。
一方、比較例1〜4では、比(D30/D70)が0.20以上かつ0.48以下、タップ密度が1.0g/cm3以上かつ1.7g/cm3以下、圧粉体密度が真密度の50%以上かつ75%以下のいずれも満足していないことから、0.1C放電容量及び3C放電容量共に、実施例1〜8と比べて劣っていることが分かった。
Claims (6)
- LiFePO4またはLiFexM1−xPO4(但し、MはCo、Mn及びNiの群から選択された1種または2種以上、0<x<1)からなる電極活物質粒子の表面が炭素質被膜により被覆されてなる一次粒子が複数個凝集した凝集粒子からなるリチウムイオン電池用電極材料であって、
前記一次粒子の平均一次粒子径は10nm以上かつ1000nm以下であり、
前記凝集粒子は、累積粒度分布における累積百分率30%の粒子径(D30)の累積百分率70%の粒子径(D70)に対する比(D30/D70)が0.20以上かつ0.48以下、タップ密度が1.0g/cm3以上かつ1.7g/cm3以下、圧粉体密度が前記電極活物質粒子の真密度の50%以上かつ75%以下であることを特徴とするリチウムイオン電池用電極材料。 - 前記一次粒子の表面の炭素質被膜による被覆率が80%以上であり、
前記凝集粒子は、その平均粒子径が0.5μm以上かつ100μm以下、体積密度が該凝集粒子を中実とした場合の体積密度の50体積%以上かつ80体積%以下であり、かつ前記一次粒子により包囲された空孔が多数存在する多孔質体であることを特徴とする請求項1記載のリチウムイオン電池用電極材料。 - 前記炭素質被膜の含有率は、前記一次粒子の全質量に対して0.5質量%以上かつ5.0質量%以下であることを特徴とする請求項1または2記載のリチウムイオン電池用電極材料。
- 請求項1ないし3のいずれか1項記載のリチウムイオン電池用電極材料の製造方法であって、
水熱合成法により、LiFePO4またはLiFexM1−xPO4(但し、MはCo、Mn及びNiの群から選択された1種または2種以上、0<x<1)からなる粒子またはその前駆体を作製し、
次いで、前記粒子またはその前駆体に炭素源を添加して焼成することにより、生成する粒子の表面を炭素質被膜にて覆う一次粒子とするとともに該一次粒子を複数個凝集する凝集粒子を生成することを特徴とするリチウムイオン電池用電極材料の製造方法。 - 請求項1ないし3のいずれか1項記載のリチウムイオン電池用電極材料を含有してなることを特徴とするリチウムイオン電池用電極。
- 請求項5記載のリチウムイオン電池用電極を正極として備えてなることを特徴とするリチウムイオン電池。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2013195495A JP2015060799A (ja) | 2013-09-20 | 2013-09-20 | リチウムイオン電池用電極材料とその製造方法及びリチウムイオン電池用電極並びにリチウムイオン電池 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2013195495A JP2015060799A (ja) | 2013-09-20 | 2013-09-20 | リチウムイオン電池用電極材料とその製造方法及びリチウムイオン電池用電極並びにリチウムイオン電池 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2015060799A true JP2015060799A (ja) | 2015-03-30 |
Family
ID=52818145
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2013195495A Pending JP2015060799A (ja) | 2013-09-20 | 2013-09-20 | リチウムイオン電池用電極材料とその製造方法及びリチウムイオン電池用電極並びにリチウムイオン電池 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2015060799A (ja) |
Cited By (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP5880757B1 (ja) * | 2015-03-31 | 2016-03-09 | 住友大阪セメント株式会社 | リチウムイオン二次電池用正極材料、リチウムイオン二次電池用正極、リチウムイオン二次電池、リチウムイオン二次電池用正極材料の製造方法 |
| JP6288338B1 (ja) * | 2017-03-24 | 2018-03-07 | 住友大阪セメント株式会社 | リチウムイオン二次電池用正極材料、リチウムイオン二次電池用正極、リチウムイオン二次電池 |
| JP6288340B1 (ja) * | 2017-03-24 | 2018-03-07 | 住友大阪セメント株式会社 | リチウムイオン二次電池用電極材料、及びリチウムイオン二次電池 |
| JP2018055868A (ja) * | 2016-09-27 | 2018-04-05 | 太平洋セメント株式会社 | ポリアニオン系正極活物質及びその製造方法 |
| JP2018163742A (ja) * | 2017-03-24 | 2018-10-18 | 住友大阪セメント株式会社 | リチウムイオン二次電池用正極材料、リチウムイオン二次電池用正極、リチウムイオン二次電池、リチウムイオン二次電池用正極材料の評価方法 |
| JP6471821B1 (ja) * | 2018-02-28 | 2019-02-20 | 住友大阪セメント株式会社 | リチウムイオン二次電池用電極材料、リチウムイオン二次電池用電極、及びリチウムイオン二次電池 |
| EP3462523A1 (en) | 2017-09-29 | 2019-04-03 | Sumitomo Osaka Cement Co., Ltd. | Electrode material for lithium ion battery and lithium ion battery |
| CN113451548A (zh) * | 2020-03-25 | 2021-09-28 | 比亚迪股份有限公司 | 磷酸铁锂正极片及制备方法、磷酸铁锂锂离子电池 |
| JP7010402B1 (ja) * | 2021-03-31 | 2022-01-26 | 住友大阪セメント株式会社 | リチウムイオン二次電池用正極材料、リチウムイオン二次電池用正極、リチウムイオン二次電池 |
| CN115295797A (zh) * | 2022-07-13 | 2022-11-04 | 深圳市德方创域新能源科技有限公司 | 铁系正极补锂材料及其制备方法与应用 |
-
2013
- 2013-09-20 JP JP2013195495A patent/JP2015060799A/ja active Pending
Cited By (22)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2016195003A (ja) * | 2015-03-31 | 2016-11-17 | 住友大阪セメント株式会社 | リチウムイオン二次電池用正極材料、リチウムイオン二次電池用正極、リチウムイオン二次電池、リチウムイオン二次電池用正極材料の製造方法 |
| US9508989B2 (en) | 2015-03-31 | 2016-11-29 | Sumitomo Osaka Cement Co., Ltd. | Positive electrode material for lithium ion secondary batteries, positive electrode for lithium ion secondary batteries, lithium ion secondary battery, and method of producing positive electrode material for lithium ion secondary batteries |
| JP5880757B1 (ja) * | 2015-03-31 | 2016-03-09 | 住友大阪セメント株式会社 | リチウムイオン二次電池用正極材料、リチウムイオン二次電池用正極、リチウムイオン二次電池、リチウムイオン二次電池用正極材料の製造方法 |
| JP2018055868A (ja) * | 2016-09-27 | 2018-04-05 | 太平洋セメント株式会社 | ポリアニオン系正極活物質及びその製造方法 |
| US10897044B2 (en) | 2017-03-24 | 2021-01-19 | Sumitomo Osaka Cement Co., Ltd. | Cathode material for lithium-ion secondary battery, cathode for lithium-ion secondary battery, and lithium-ion secondary battery |
| JP6288340B1 (ja) * | 2017-03-24 | 2018-03-07 | 住友大阪セメント株式会社 | リチウムイオン二次電池用電極材料、及びリチウムイオン二次電池 |
| JP2018163763A (ja) * | 2017-03-24 | 2018-10-18 | 住友大阪セメント株式会社 | リチウムイオン二次電池用電極材料、及びリチウムイオン二次電池 |
| JP2018163742A (ja) * | 2017-03-24 | 2018-10-18 | 住友大阪セメント株式会社 | リチウムイオン二次電池用正極材料、リチウムイオン二次電池用正極、リチウムイオン二次電池、リチウムイオン二次電池用正極材料の評価方法 |
| JP2018163746A (ja) * | 2017-03-24 | 2018-10-18 | 住友大阪セメント株式会社 | リチウムイオン二次電池用正極材料、リチウムイオン二次電池用正極、リチウムイオン二次電池 |
| JP6288338B1 (ja) * | 2017-03-24 | 2018-03-07 | 住友大阪セメント株式会社 | リチウムイオン二次電池用正極材料、リチウムイオン二次電池用正極、リチウムイオン二次電池 |
| EP3462523A1 (en) | 2017-09-29 | 2019-04-03 | Sumitomo Osaka Cement Co., Ltd. | Electrode material for lithium ion battery and lithium ion battery |
| KR20190038250A (ko) | 2017-09-29 | 2019-04-08 | 스미토모 오사카 세멘토 가부시키가이샤 | 리튬 이온 전지용 전극 재료 및 리튬 이온 전지 |
| US10547048B2 (en) | 2017-09-29 | 2020-01-28 | Sumitomo Osaka Clement Co., Ltd. | Electrode material for lithium ion battery and lithium ion battery |
| JP2019149355A (ja) * | 2018-02-28 | 2019-09-05 | 住友大阪セメント株式会社 | リチウムイオン二次電池用電極材料、リチウムイオン二次電池用電極、及びリチウムイオン二次電池 |
| CN109768228A (zh) * | 2018-02-28 | 2019-05-17 | 住友大阪水泥股份有限公司 | 锂离子二次电池用电极材料、锂离子二次电池用电极及锂离子二次电池 |
| JP6471821B1 (ja) * | 2018-02-28 | 2019-02-20 | 住友大阪セメント株式会社 | リチウムイオン二次電池用電極材料、リチウムイオン二次電池用電極、及びリチウムイオン二次電池 |
| CN113451548A (zh) * | 2020-03-25 | 2021-09-28 | 比亚迪股份有限公司 | 磷酸铁锂正极片及制备方法、磷酸铁锂锂离子电池 |
| CN113451548B (zh) * | 2020-03-25 | 2022-09-09 | 比亚迪股份有限公司 | 磷酸铁锂正极片及制备方法、磷酸铁锂锂离子电池 |
| JP7010402B1 (ja) * | 2021-03-31 | 2022-01-26 | 住友大阪セメント株式会社 | リチウムイオン二次電池用正極材料、リチウムイオン二次電池用正極、リチウムイオン二次電池 |
| EP4068423A1 (en) * | 2021-03-31 | 2022-10-05 | Sumitomo Metal Mining Co., Ltd. | Positive electrode material for lithium ion secondary battery, positive electrode for lithium ion secondary battery, and lithium ion secondary battery |
| CN115295797A (zh) * | 2022-07-13 | 2022-11-04 | 深圳市德方创域新能源科技有限公司 | 铁系正极补锂材料及其制备方法与应用 |
| CN115295797B (zh) * | 2022-07-13 | 2023-07-04 | 深圳市德方创域新能源科技有限公司 | 铁系正极补锂材料及其制备方法与应用 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6216965B2 (ja) | 電極材料と電極板及びリチウムイオン電池並びに電極材料の製造方法、電極板の製造方法 | |
| JP2015060799A (ja) | リチウムイオン電池用電極材料とその製造方法及びリチウムイオン電池用電極並びにリチウムイオン電池 | |
| JP6288340B1 (ja) | リチウムイオン二次電池用電極材料、及びリチウムイオン二次電池 | |
| JP5621740B2 (ja) | 電極材料及び電極並びに電極材料の製造方法 | |
| JP6288339B1 (ja) | リチウムイオン二次電池用電極材料、その製造方法、リチウムイオン二次電池用電極およびリチウムイオン二次電池 | |
| JP6156537B1 (ja) | リチウムイオン二次電池用電極材料、リチウムイオン二次電池用電極およびリチウムイオン二次電池 | |
| JP2014216240A (ja) | 電極活物質と電極材料及び電極、リチウムイオン電池並びに電極材料の製造方法 | |
| JP2018056051A (ja) | リチウムイオン二次電池、及びリチウムイオン二次電池用正極材料 | |
| JPWO2013146168A1 (ja) | 電極材料 | |
| JP2013182689A (ja) | 電極活物質の製造方法及び電極活物質 | |
| JP6077205B2 (ja) | 電極材料及びその製造方法 | |
| JP6841362B1 (ja) | リチウムイオン二次電池用正極材料、リチウムイオン二次電池用正極及びリチウムイオン二次電池 | |
| JP5821722B2 (ja) | リチウムイオン電池用正極材料及びリチウムイオン電池用正極並びにリチウムイオン電池 | |
| WO2014030691A1 (ja) | 電極材料、リチウムイオン電池用電極ペースト、リチウムイオン電池用電極、およびリチウムイオン電池 | |
| JP2016072135A (ja) | 電極材料及びその製造方法、電極、並びにリチウムイオン電池 | |
| JP6501014B1 (ja) | リチウムイオン二次電池用正極材料、その製造方法、リチウムイオン二次電池用電極、及びリチウムイオン二次電池 | |
| JP2018142420A (ja) | リチウムイオン二次電池用電極、リチウムイオン二次電池 | |
| JP2018056054A (ja) | リチウムイオン二次電池用電極材料、及びリチウムイオン二次電池 | |
| JP2015088317A (ja) | 電極材料及び電極並びにリチウムイオン電池 | |
| JP5838994B2 (ja) | 電極材料と電極形成用ペースト、電極板及びリチウムイオン電池並びに電極材料の製造方法 | |
| JP2018170186A (ja) | リチウムイオン二次電池用正極材料、及びリチウムイオン二次電池 | |
| JP5783295B2 (ja) | 電極材料、ペースト、電極板及びリチウムイオン電池 | |
| KR102643519B1 (ko) | 리튬 이온 전지용 전극 재료 및 리튬 이온 전지 | |
| JP2017069177A (ja) | リチウムイオン二次電池用電極材料、リチウムイオン二次電池用電極およびリチウムイオン二次電池 | |
| JP6132062B1 (ja) | リチウムイオン二次電池用正極材料、その製造方法、リチウムイオン二次電池用電極、及びリチウムイオン二次電池 |