JP2010070455A - ジスチリルベンゼン化合物混合物 - Google Patents
ジスチリルベンゼン化合物混合物 Download PDFInfo
- Publication number
- JP2010070455A JP2010070455A JP2008236008A JP2008236008A JP2010070455A JP 2010070455 A JP2010070455 A JP 2010070455A JP 2008236008 A JP2008236008 A JP 2008236008A JP 2008236008 A JP2008236008 A JP 2008236008A JP 2010070455 A JP2010070455 A JP 2010070455A
- Authority
- JP
- Japan
- Prior art keywords
- general formula
- distyrylbenzene
- group
- compound
- substituent
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
- 0 CC=C(N(C1=CCCCC1)C(CC1)=CC=C1C=O)I=I(*)I Chemical compound CC=C(N(C1=CCCCC1)C(CC1)=CC=C1C=O)I=I(*)I 0.000 description 3
Images
Landscapes
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Photoreceptors In Electrophotography (AREA)
Abstract
Description
以下、電子写真感光体を例に挙げ、従来の電荷輸送剤について述べる。電子写真感光体は可視光から赤外光まで各種露光光源に対応した材料が開発しやすいこと、環境汚染の影響が少ない材料を選択できること、製造コストが安いことなどの理由により、無機感光体に対して有利な点が多い。電子写真感光体の電荷輸送剤としては、例えばオキサジアゾール化合物(例えば、特許文献1参照)、オキサゾール化合物(例えば、特許文献2参照)、ピラゾリン化合物(例えば、特許文献3参照)、ヒドラゾン化合物(例えば、特許文献4〜7参照)、ジアミン化合物(例えば、特許文献8参照)、スチルベン化合物(例えば、特許文献9〜11参照)、ブタジエン化合物(例えば、特許文献12参照)等がある。これらの電荷輸送剤は優れた特性を有し、実用化されているものがあるが、近年、画像形成装置の高速化並びに小型化が急速に進行するに伴って、電荷輸送機能の更なる向上が必要不可欠となっており、特に高移動度を有する電荷輸送剤の開発が強く求められている。
高移動度を有する電荷輸送剤は、π共役が発達した分子構造が有利であるが、その場合に分子サイズが大きくなり、溶解性が低下したり、結晶化しやすくなるなどの不具合が生じる。感光体の電荷輸送層に用いる場合は、電荷輸送剤をバインダー樹脂とともに溶剤に溶解させ膜を形成する必要がある。例え、移動度に優れる電荷輸送剤があったとしても、溶剤に溶解できなければ実用性はないことになる。
バインダー樹脂への相溶性を改善したジスチリルベンゼン化合物を得る手法もあるが(特許文献14参照)、ジスチリルベンゼン化合物の対称性を考慮したものではなく、また製造工程が長く、安価に製造することが困難であり、実用レベルにあるとは言い難い。また、一段階の反応で得た複数のスチリル基を有する化合物混合物を電子写真感光体の材料として使用しているものがある(特許文献15参照)。この方法で得られる混合物はオリゴマーであり、不純物を多く含んでいる。そのため、電荷輸送剤としての機能が高くはない。また、一段階の反応でp−ターフェニル化合物混合物を合成しているものがある(特許文献16参照)。この方法で得られる混合物は有機溶剤に対する溶解性が高く、純度も高い。しかしながら、電荷輸送剤の移動度は今後の電子写真感光体のさらなる特性向上には十分ではない。このように高いドリフト移動度を有し、低コストで製造可能であり、有機溶剤に対する優れた溶解性を有する電荷輸送剤は見出されていない。
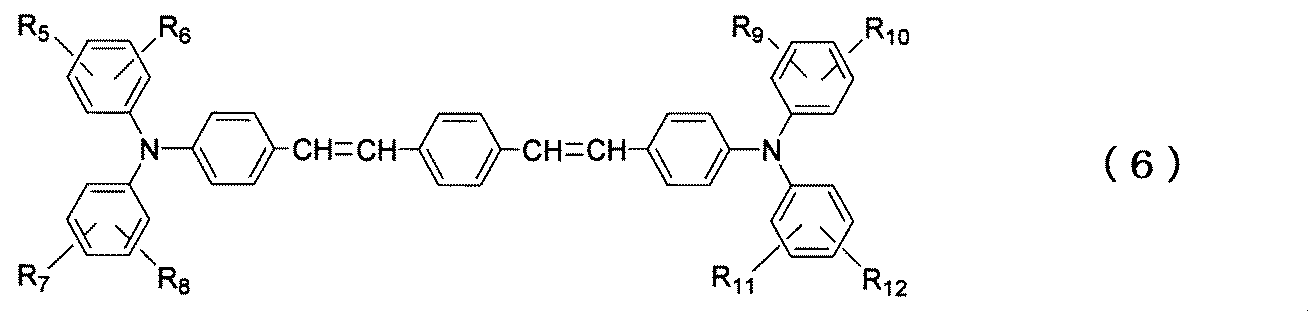
(1)「下記一般式(1)、一般式(2)および一般式(3)で表わされる3種類の対称型ジスチリルベンゼン化合物から選択される2種類または3種類と、下記一般式(4)、一般式(5)および一般式(6)で表わされる非対称型ジスチリルベンゼン化合物から選択される1〜3種類とを含むことを特徴とするジスチリルベンゼン化合物混合物;
(2)「前記一般式(4)〜(6)で表わされる非対称型ジスチリルベンゼン化合物のうち、最大含有率を示す化合物の含有率が1〜50質量%であることを特徴とする前記第(1)項に記載のジスチリルベンゼン化合物混合物」、
(3)「下記一般式(7)、一般式(8)で表わされる2種類のジフェニルアミノベンズアルデヒド化合物とp−キシレン−α,α'−ジイルジホスホン酸テトラエチルとの一段階の反応によって合成されることを特徴とするジスチリルベンゼン化合物混合物;
(4)「下記一般式(7)、一般式(8)で表わされる2種類のジフェニルアミノベンズアルデヒド化合物とp−キシレン−α,α'−ジイルジホスホン酸テトラエチルとの一段階の反応によって合成される下記一般式(1)、一般式(2)で表わされる2種類の対称型ジスチリルベンゼン化合物と、下記一般式(4)で表わされる1種類の非対称型ジスチリルベンゼン化合物からなることを特徴とするジスチリルベンゼン化合物混合物;
(5)「下記一般式(7)、一般式(8)および一般式(9)で表わされる3種類のジフェニルアミノベンズアルデヒド化合物とp−キシレン−α,α'−ジイルジホスホン酸テトラエチルとの一段階の反応によって合成されることを特徴とするジスチリルベンゼン化合物混合物。
(6)「下記一般式(7)、一般式(8)および一般式(9)で表わされる3種類のジフェニルアミノベンズアルデヒド化合物とp−キシレン−α,α'−ジイルジホスホン酸テトラエチルとの一段階の反応によって合成される下記一般式(1)、一般式(2)および一般式(3)で表わされる3種類の対称型ジスチリルベンゼン化合物と、下記一般式(4)、一般式(5)および一般式(6)で表わされる3種類の非対称型ジスチリルベンゼン化合物とからなることを特徴とするジスチリルベンゼン化合物混合物;
(7)「下記一般式(7)、一般式(8)および一般式(9)で表わされる3種類のジフェニルアミノベンズアルデヒド化合物から選択される2種類または3種類とp−キシレン−α,α'−ジイルジホスホン酸テトラエチルとの一段階の反応によって、3〜6種類のジスチリルベンゼン化合物混合物を得ることを特徴とするジスチリルベンゼン化合物混合物の製造方法;
本発明のジスチリルベンゼン化合物混合物の有機溶剤に対する溶解性が向上した理由として、混合物が類似構造の化合物の混合物であることが挙げられる。また、この混合物は、嵩高いフェニルアミノ基の構造が異なり立体障害を有するため、分散性に優れ、良好な電荷輸送能をも発現する。
ジスチリルベンゼン化合物混合物を一段階の反応で合成すると、類似構造の化合物の混合物を晶析で得られる。この混晶は、フェニルアミノ基の構造が異なるジスチリルベンゼン化合物がランダムに存在するため、立体障害により、分子レベルでの隙間が多くなるため、さらに溶解性が向上すると考えられる。
また、本発明の前記一般式(1)、一般式(2)および一般式(3)で表わされる3種類の対称型ジスチリルベンゼン化合物の内、2〜3種類と、該化合物のそれぞれの置換基群を併せ持つ一般式(4)、一般式(5)および一般式(6)で表わされる非対称型ジスチリルベンゼン化合物の内、1〜3種類からなるジスチリルベンゼン化合物混合物は、下記一般式(7)、一般式(8)および一般式(9)で表わされる3種類のジフェニルアミノベンズアルデヒド化合物から選択される2種類または3種類とp−キシレン−α,α’−ジイルジホスホン酸テトラエチルとの一段階の反応によっても、3〜6種類のジスチリルベンゼン化合物混合物を合成することができる。一段階の反応でジスチリルベンゼン化合物混合物を合成する方法は、嵩高いフェニルアミノ基の構造が異なる対称型ジスチリルベンゼンと非対称型ジスチリルベンゼンとが同時に合成されるため、分子同士が整列し難く、前記混合物の混晶は、分子レベルで隙間が多く存在し、各々の化合物を別々に合成して混合したものに比べ、より溶解性が向上する。
一段階ではなく、個々の化合物を混合してジスチリルベンゼン化合物混合物を作製することも可能であり、その際一般式(4)〜(6)で表わされる非対称型ジスチリルベンゼン化合物のうち、最大含有率を示す化合物の含有率は50質量%を超えることができる。
しかしながら、非対称型ジスチリルベンゼン化合物と対称型ジスチリルベンゼン化合物とが高度に分散し、溶解性に優れる点、及び、コスト面から、有利である。
化合物の同定は、対称型ジスチリルベンゼン化合物については、個々の化合物についての単一合成を実施し、元素分析によってその構造を確認した後、高速液体クロマトグラフィーによるリテンションタイムの比較によって行なった。また、非対称型ジスチリルベンゼン化合物については、ジスチリルベンゼン化合物混合物からの分取高速液体クロマトグラフィーを用いた単離を実施し、元素分析によってその構造を確認した後、高速液体クロマトグラフィーによるリテンションタイムの比較によって行なった。化合物の同定および混合比を測定するための高速液体クロマトグラフィーの側定条件は以下の通りである。
カラム:ODS系カラム、
溶離液:テトラヒドロフラン/メタノール=1/10(v/v)、
測定波長:254nm。
p−キシレン−α,α’−ジイルジホスホン酸テトラエチル11.35g(30.0mmol)と4−ジフェニルアミノベンズアルデヒド8.61g(31.5mmol)、4−(ジ−p−トリルアミノ)−ベンズアルデヒド9.49g(31.5mmol)にテトラヒドロフラン34mlを加え、これにカリウム−t−ブトキシド8.06g(72mmol)を30〜45℃に加温しながら加えた。さらに、45〜50℃で1時間撹拌した後、メタノール100mlを加え、析出した結晶をろ過した。結晶をメタノールで洗浄した後、乾燥し、粗晶18.80g(収率;97.2%)を得た。さらに、粗晶15.00gにトルエン300mlを加え、50℃に加温して溶解した後、活性白土強(日本活性白土株式会社製)7.50gを加え、45〜50℃で1時間撹拌した。さらに活性白土強7.50gを加え、45〜50℃で1時間撹拌した後、ろ過し、トルエンを留去した。テトラヒドロフラン/メタノールの混合溶媒で晶析を行ない、化合物No.1、No.11およびNo.13からなるジスチリルベンゼン化合物混合物を、化合物No.1:化合物No.11:化合物No.13=48.5:25.4:25.9(高速液体クロマトグラフィーによるピーク面積比)の混合比で14.59g(精製収率;97.3%)得た。
化合物No.1;炭素:89.42%(89.40%)、水素:6.24%(6.25%)、窒素:4.34%(4.35%)、化合物No.11;炭素:89.55%(89.58%)、水素:5.90%(5.88%)、窒素:4.55%(4.54%)、化合物No.13;炭素:89.24%(89.25%)、水素:6.60%(6.59%)、窒素:4.15%(4.16%)(計算値をかっこ内に示す。)。
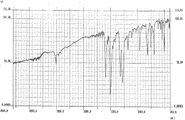
図1に合成実施例1で作製した化合物No.1、No.11およびNo.13からなるジスチリルベンゼン化合物混合物のIRスペクトルを示す。
ジフェニルアミノベンズアルデヒド化合物として4−(N−フェニル−N−p−トリルアミノ)−ベンズアルデヒド7.24g(25.2mmol)、4−(ジ−p−トリルアミノ)−ベンズアルデヒド11.39g(37.8mmol)を使用した他は、合成実施例1と同様にして反応、後処理を行ない、粗晶18.86g(収率;95.0%)得た。粗晶15.00gを合成実施例1と同様にして活性白土による吸着精製、晶析を行ない、化合物No.2、No.12およびNo.13からなるジスチリルベンゼン化合物混合物を、化合物No.2:化合物No.12:化合物No.13=45.7:12.6:40.9(高速液体クロマトグラフィーによるピーク面積比)の混合比で14.43g(収率;96.2%)得た。
化合物No.2;炭素:89.34%(89.32%)、水素:6.42%(6.43%)、窒素:4.23%(4.25%)、化合物No.12;炭素:89.38%(89.40%)、水素:6.26%(6.25%)、窒素:4.35%(4.35%)、化合物No.13;炭素:89.24%(89.25%)、水素:6.60%(6.59%)、窒素:4.15%(4.16%)(計算値をかっこ内に示す。)。
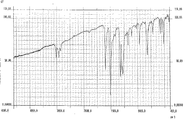
図2に合成実施例2で作製した化合物No.2、No.12およびNo.13からなるジスチリルベンゼン化合物混合物のIRスペクトルを示す。
ジフェニルアミノベンズアルデヒド化合物として4−(N−フェニル−N−p−トリルアミノ)−ベンズアルデヒド1.81g(6.3mmol)、4−(ジ−p−トリルアミノ)−ベンズアルデヒド17.09g(56.7mmol)を使用した他は、合成実施例1と同様にして反応、後処理を行ない、粗晶19.01g(収率;94.6%)得た。粗晶15.00gを合成実施例1と同様にして活性白土による吸着精製、晶析を行ない、化合物No.2、No.12およびNo.13からなるジスチリルベンゼン化合物混合物を、化合物No.2:化合物No.12:化合物No.13=16.8:0.9:80.6(高速液体クロマトグラフィーによるピーク面積比)の混合比で14.36g(収率;95.7%)得た。
化合物No.2;炭素:89.34%(89.32%)、水素:6.42%(6.43%)、窒素:4.23%(4.25%)、化合物No.12;炭素:89.38%(89.40%)、水素:6.26%(6.25%)、窒素:4.35%(4.35%)、化合物No.13;炭素:89.24%(89.25%)、水素:6.60%(6.59%)、窒素:4.15%(4.16%)。(計算値をかっこ内に示す。)。
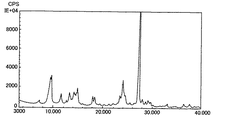
図3に合成実施例3で作製した化合物No.2、No.12およびNo.13からなるジスチリルベンゼン化合物混合物のIRスペクトルを示す。
ジフェニルアミノベンズアルデヒド化合物として4−(ジ−p−トリルアミノ)−ベンズアルデヒド15.19g(50.4mmol)、4−〔N−フェニル−N−(5,6,7,8−テトラヒドロナフタレン−1−イル)−アミノ〕−ベンズアルデヒド1.38g(4.2mmol)、4−〔N−フェニル−N−(5,6,7,8−テトラヒドロナフタレン−2−イル)−アミノ〕−ベンズアルデヒド2.75g(8.4mmol)を使用した他は、合成実施例1と同様にして反応、後処理を行ない、粗晶18.94g(収率;92.4%)得た。粗晶15.00gを合成実施例1と同様にして活性白土による吸着精製、晶析を行ない、化合物No.3、No.4、No.5、No.13、No.18およびNo.19からなるジスチリルベンゼン化合物混合物を、化合物No.3:化合物No.4:化合物No.5:化合物No.13:化合物No.18:化合物No.19=6.2:19.1:0.3:73.0:0.1:0.9(高速液体クロマトグラフィーによるピーク面積比)の混合比で13.23g(収率;88.2%)得た。
化合物No.3;炭素:89.39%(89.36%)、水素:6.61%(6.63%)、窒素:4.00%(4.01%)、化合物No.4;炭素:89.36%(89.36%)、水素:6.62%(6.63%)、窒素:4.02%(4.01%)、化合物No.5;炭素:89.49%(89.46%)、水素:6.67%(6.68%)、窒素:3.84%(3.86%)、化合物No.13;炭素:89.24%(89.25%)、水素:6.60%(6.59%)、窒素:4.15%(4.16%)、化合物No.18;炭素:89.50%(89.46%)、水素:6.66%(6.68%)、窒素:3.84%(3.86%)、化合物No.19;炭素:89.43%(89.46%)、水素:6.71%(6.68%)、窒素:3.86%(3.86%)(計算値をかっこ内に示す。)。
図4に合成実施例4で作製した化合物No.3、No.4、No.5およびNo.13、No.18、No.19からなるジスチリルベンゼン化合物混合物のIRスペクトルを示す。
合成実施例1〜4のジスチリルベンゼン化合物混合物および単一合成したジスチリルベンゼン化合物(化合物No.11、No.12およびNo.13)の25℃におけるトルエンまたはテトラヒドロフランに対する溶解度を測定した。結果を表1に示した。溶解度の単位は%(重量/重量)で表わした。
本発明のジスチリルベンゼン化合物混合物を用いた応用例として、電子写真感光体の作製例を示す。
<電子写真感光体1>
導電性支持体としての直径30mmのアルミニウムシリンダーに、下記組成の下引き層塗工液、電荷発生層塗工液、電荷輸送層塗工液を、順次塗布・乾燥し、約3.5μmの下引き層、約0.2μmの電荷発生層、約23μmの電荷輸送層を形成し、積層感光体を作製した。なお、各層の塗工後に指触乾燥を行なった後、下引き層は130℃、電荷発生層は95℃、電荷輸送層は120℃で各々20分乾燥を行なうことにより、導電性支持体/下引き層/電荷発生層/電荷輸送層からなる電子写真感光体を得た。
(下引き層用塗工液)
酸化チタン 50部
(CR−EL、平均一次粒径:約0.25μm、石原産業(株)製)
アルキッド樹脂 14部
(ベッコライトM6401−50、固形分:50%、
大日本インキ化学工業(株)製)
メラミン樹脂 8部
(L−145−60、固形分:60%、大日本インキ化学工業(株)製)
2−ブタノン 70部
はじめに、電荷発生剤に用いたチタニルフタロシアニン結晶の合成方法について述べる。合成は、特開2004−83859号公報に準じた。
即ち、1,3−ジイミノイソインドリン292部とスルホラン1800部を混合し、窒素気流下でチタニウムテトラブトキシド204部を滴下する。滴下終了後、徐々に180℃まで昇温し、反応温度を170℃〜180℃の間に保ちながら5時間撹拌して反応を行なった。反応終了後、放冷した後、析出物を濾過し、クロロホルムで粉体が青色になるまで洗浄し、次にメタノールで数回洗浄し、更に80℃の熱水で数回洗浄した後乾燥し、粗チタニルフタロシアニンを得た。粗チタニルフタロシアニンを20倍量の濃硫酸に溶解し、100倍量の氷水に撹拌しながら滴下し、析出した結晶を濾過し、次いで、洗浄液が中性になるまでイオン交換水(pH:7.0、比伝導度:1.0μS/cm)により水洗いを繰り返し(洗浄後のイオン交換水のpH値は6.8、比伝導度は2.6μS/cmであった)、チタニルフタロシアニン顔料のウェットケーキ(水ペースト)を得た。
(X線回折スペクトル測定条件)
X線管球:Cu
電圧:50kV
電流:30mA
走査速度:2°/分
走査範囲:3°〜40°
時定数:2秒
作製したチタニルフタロシアニン結晶を下記組成の処方にて、下記に示す条件にて分散を行ない、電荷発生層用塗工液を作製した。
チタニルフタロシアニン結晶 15部
ポリビニルブチラール(積水化学製:BX−1) 10部
2−ブタノン 280部
市販のビーズミル分散機に直径0.5mmのPSZボールを用い、ポリビニルブチラールを溶解した2−ブタノン溶液及び上記顔料を投入し、ローター回転数1200r.p.m.にて30分間分散を行ない、電荷発生層用塗工液を作製した。
なお、電荷発生層の膜厚は、780nmにおける電荷発生層の透過率が25%になるように調整した。電荷発生層の透過率は、下記組成の電荷発生層塗工液を、ポリエチレンテレフタレートフィルムを巻き付けたアルミシリンダーに感光体作製と同じ条件で塗工を行ない、電荷発生層を塗工していないポリエチレンテレフタレートフィルムを比較対照とし、市販の分光光度計(島津:UV−3100)にて、780nmの透過率を評価した。
合成実施例1のジスチリルベンゼン化合物混合物 7部
ビスフェノールZポリカーボネート 10部
(パンライトTS−2050、帝人化成製)
テトラヒドロフラン/トルエン(8/2)混合溶媒 80部
1%シリコーンオイル 溶媒:テトラヒドロフラン/トルエン(8/2)混合溶液
0.2部
(KF50−1CS、信越化学工業製)
電荷輸送層の電荷輸送剤を合成実施例2のジスチリルベンゼン化合物混合物に換えた以外は応用例1と同様に電子写真感光体を作製した。
電荷輸送層の電荷輸送剤を合成実施例3のジスチリルベンゼン化合物混合物に換えた以外は応用例1と同様に電子写真感光体を作製した。
電荷輸送層の電荷輸送剤を合成実施例4のジスチリルベンゼン化合物混合物に換えた以外は応用例1と同様に電子写真感光体を作製した。
電荷輸送層の電荷輸送剤をジスチリルベンゼン化合物No.11に換えた以外は応用例1と同様に電子写真感光体を作製した。
電荷輸送層の電荷輸送剤をジスチリルベンゼン化合物No.12に換えた以外は応用例1と同様に電子写真感光体を作製した。
電荷輸送層の電荷輸送剤をジスチリルベンゼン化合物No.13に換えた以外は応用例1と同様に電子写真感光体を作製した。
明部電位測定にはリコー製imagio Neo270を用いた。
imagio Neo270の現像ユニットを分解し、表面電位計に接続された電位計プローブを現像ユニットに取り付け、それに感光体をセットして、暗部電位が−800(V)になるように印加電位を調節した後、黒ベタ画像を出力することによって、明部電位を測定した。表面電位計はTREK MODEL344を用いた。
下記組成の溶液に電荷輸送剤を7部添加し、25℃で攪拌した。電荷輸送剤が溶解するまでに要した時間で溶解性を評価した。
ビスフェノールZポリカーボネート 10部
(パンライトTS−2050、帝人化成製)
テトラヒドロフラン/トルエン(8/2)混合溶媒 68部
1%シリコーンオイル 溶媒:テトラヒドロフラン/トルエン(8/2)混合溶液
0.2部
(KF50−1CS、信越化学工業製)
電荷輸送剤の溶解性は以下の基準で判定した。
5:5分以内に溶解
4:10分以内に溶解
3:20分以内に溶解
2:30分以内に溶解
1:25℃では溶解せず
測定結果を以下の表に示す。
Claims (7)
- 下記一般式(1)、一般式(2)および一般式(3)で表わされる3種類の対称型ジスチリルベンゼン化合物から選択される2種類または3種類と、下記一般式(4)、一般式(5)および一般式(6)で表わされる非対称型ジスチリルベンゼン化合物から選択される1〜3種類とを含むことを特徴とするジスチリルベンゼン化合物混合物。
- 前記一般式(4)〜(6)で表わされる非対称型ジスチリルベンゼン化合物のうち、最大含有率を示す化合物の含有率が1〜50質量%であることを特徴とする請求項1に記載のジスチリルベンゼン化合物混合物。
- 下記一般式(7)、一般式(8)で表わされる2種類のジフェニルアミノベンズアルデヒド化合物とp−キシレン−α,α'−ジイルジホスホン酸テトラエチルとの一段階の反応によって合成されることを特徴とするジスチリルベンゼン化合物混合物。
- 下記一般式(7)、一般式(8)で表わされる2種類のジフェニルアミノベンズアルデヒド化合物とp−キシレン−α,α'−ジイルジホスホン酸テトラエチルとの一段階の反応によって合成される下記一般式(1)、一般式(2)で表わされる2種類の対称型ジスチリルベンゼン化合物と、下記一般式(4)で表わされる1種類の非対称型ジスチリルベンゼン化合物からなることを特徴とするジスチリルベンゼン化合物混合物。
- 下記一般式(7)、一般式(8)および一般式(9)で表わされる3種類のジフェニルアミノベンズアルデヒド化合物とp−キシレン−α,α'−ジイルジホスホン酸テトラエチルとの一段階の反応によって合成されることを特徴とするジスチリルベンゼン化合物混合物。
- 下記一般式(7)、一般式(8)および一般式(9)で表わされる3種類のジフェニルアミノベンズアルデヒド化合物とp−キシレン−α,α'−ジイルジホスホン酸テトラエチルとの一段階の反応によって合成される下記一般式(1)、一般式(2)および一般式(3)で表わされる3種類の対称型ジスチリルベンゼン化合物と、下記一般式(4)、一般式(5)および一般式(6)で表わされる3種類の非対称型ジスチリルベンゼン化合物とからなることを特徴とするジスチリルベンゼン化合物混合物。
- 下記一般式(7)、一般式(8)および一般式(9)で表わされる3種類のジフェニルアミノベンズアルデヒド化合物から選択される2種類または3種類とp−キシレン−α,α'−ジイルジホスホン酸テトラエチルとの一段階の反応によって、3〜6種類のジスチリルベンゼン化合物混合物を得ることを特徴とするジスチリルベンゼン化合物混合物の製造方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008236008A JP5412074B2 (ja) | 2008-09-16 | 2008-09-16 | ジスチリルベンゼン化合物混合物 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008236008A JP5412074B2 (ja) | 2008-09-16 | 2008-09-16 | ジスチリルベンゼン化合物混合物 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2010070455A true JP2010070455A (ja) | 2010-04-02 |
| JP5412074B2 JP5412074B2 (ja) | 2014-02-12 |
Family
ID=42202594
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2008236008A Active JP5412074B2 (ja) | 2008-09-16 | 2008-09-16 | ジスチリルベンゼン化合物混合物 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP5412074B2 (ja) |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2001098176A (ja) * | 1999-09-29 | 2001-04-10 | Kyocera Mita Corp | スチルベン誘導体、その製造方法およびそれを用いた電子写真感光体 |
| JP2003286234A (ja) * | 2002-03-27 | 2003-10-10 | Kyocera Mita Corp | 電子写真感光体および画像形成装置 |
| JP2005107500A (ja) * | 2003-09-11 | 2005-04-21 | Kyocera Mita Corp | 画像形成装置 |
| JP2010072023A (ja) * | 2008-09-16 | 2010-04-02 | Ricoh Co Ltd | ジスチリルベンゼン化合物混合物及び該化合物混合物を用いた電子写真感光体 |
-
2008
- 2008-09-16 JP JP2008236008A patent/JP5412074B2/ja active Active
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2001098176A (ja) * | 1999-09-29 | 2001-04-10 | Kyocera Mita Corp | スチルベン誘導体、その製造方法およびそれを用いた電子写真感光体 |
| JP2003286234A (ja) * | 2002-03-27 | 2003-10-10 | Kyocera Mita Corp | 電子写真感光体および画像形成装置 |
| JP2005107500A (ja) * | 2003-09-11 | 2005-04-21 | Kyocera Mita Corp | 画像形成装置 |
| JP2010072023A (ja) * | 2008-09-16 | 2010-04-02 | Ricoh Co Ltd | ジスチリルベンゼン化合物混合物及び該化合物混合物を用いた電子写真感光体 |
Also Published As
| Publication number | Publication date |
|---|---|
| JP5412074B2 (ja) | 2014-02-12 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR101196635B1 (ko) | p?터페닐 화합물 및 이 화합물을 이용한 전자 사진용 감광체 | |
| JP2010235909A (ja) | 複合アゾ顔料の製造方法およびそれにより得られた複合アゾ顔料 | |
| JP2000112157A (ja) | 電子写真感光体 | |
| JPH11228851A (ja) | ジスチリル化合物及びそれを用いた電子写真感光体 | |
| JP5412074B2 (ja) | ジスチリルベンゼン化合物混合物 | |
| JPH0311466B2 (ja) | ||
| JPH10312072A (ja) | 電子写真感光体 | |
| JP3780544B2 (ja) | 新規フタロシアニン化合物及びそれを用いた電子写真感光体 | |
| JP2748497B2 (ja) | オキシチタニウムフタロシアニン結晶の製造法 | |
| JP5733685B2 (ja) | ビスジアザペンタジエン誘導体およびそれらの製造方法 | |
| JP2000098640A (ja) | 電子写真感光体 | |
| JP3765324B2 (ja) | 電子写真感光体 | |
| JP4460224B2 (ja) | 新規なイミド化合物、および該化合物を用いた電子写真感光体、電子写真装置 | |
| JP4233388B2 (ja) | 新規なキノン化合物、および該化合物を用いた電子写真感光体、電子写真装置 | |
| JPS60111248A (ja) | 感光体 | |
| JP3845080B2 (ja) | 非対称トリスアゾ顔料 | |
| JP2000219689A (ja) | ジニトロアントリンイミン誘導体とそれを用いた電子写真感光体 | |
| JPH0428302B2 (ja) | ||
| JP3855032B2 (ja) | 電子写真感光体 | |
| JPH11143098A (ja) | 電子写真感光体 | |
| JPH1039529A (ja) | 電子写真感光体 | |
| JPS60196772A (ja) | 感光体 | |
| JPH0117571B2 (ja) | ||
| JPH02165156A (ja) | 電子写真感光体 | |
| JPWO2018163597A1 (ja) | 電子写真感光体 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20110902 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20130621 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20130815 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20131018 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20131111 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5412074 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| S531 | Written request for registration of change of domicile |
Free format text: JAPANESE INTERMEDIATE CODE: R313531 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |