JP2008520739A - 長鎖多価不飽和脂肪酸由来のオキシリピンならびにその作製および使用方法 - Google Patents
長鎖多価不飽和脂肪酸由来のオキシリピンならびにその作製および使用方法 Download PDFInfo
- Publication number
- JP2008520739A JP2008520739A JP2007543444A JP2007543444A JP2008520739A JP 2008520739 A JP2008520739 A JP 2008520739A JP 2007543444 A JP2007543444 A JP 2007543444A JP 2007543444 A JP2007543444 A JP 2007543444A JP 2008520739 A JP2008520739 A JP 2008520739A
- Authority
- JP
- Japan
- Prior art keywords
- dpan
- dihydroxy
- oil
- lcpufa
- hydroxy
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P7/00—Preparation of oxygen-containing organic compounds
- C12P7/64—Fats; Fatty oils; Ester-type waxes; Higher fatty acids, i.e. having at least seven carbon atoms in an unbroken chain bound to a carboxyl group; Oxidised oils or fats
- C12P7/6436—Fatty acid esters
- C12P7/6445—Glycerides
- C12P7/6472—Glycerides containing polyunsaturated fatty acid [PUFA] residues, i.e. having two or more double bonds in their backbone
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/185—Acids; Anhydrides, halides or salts thereof, e.g. sulfur acids, imidic, hydrazonic or hydroximic acids
- A61K31/19—Carboxylic acids, e.g. valproic acid
- A61K31/20—Carboxylic acids, e.g. valproic acid having a carboxyl group bound to a chain of seven or more carbon atoms, e.g. stearic, palmitic, arachidic acids
- A61K31/202—Carboxylic acids, e.g. valproic acid having a carboxyl group bound to a chain of seven or more carbon atoms, e.g. stearic, palmitic, arachidic acids having three or more double bonds, e.g. linolenic
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
- A61P7/10—Antioedematous agents; Diuretics
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C59/00—Compounds having carboxyl groups bound to acyclic carbon atoms and containing any of the groups OH, O—metal, —CHO, keto, ether, groups, groups, or groups
- C07C59/40—Unsaturated compounds
- C07C59/42—Unsaturated compounds containing hydroxy or O-metal groups
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D303/00—Compounds containing three-membered rings having one oxygen atom as the only ring hetero atom
- C07D303/02—Compounds containing oxirane rings
- C07D303/38—Compounds containing oxirane rings with hydrocarbon radicals, substituted by carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P7/00—Preparation of oxygen-containing organic compounds
- C12P7/64—Fats; Fatty oils; Ester-type waxes; Higher fatty acids, i.e. having at least seven carbon atoms in an unbroken chain bound to a carboxyl group; Oxidised oils or fats
- C12P7/6409—Fatty acids
- C12P7/6427—Polyunsaturated fatty acids [PUFA], i.e. having two or more double bonds in their backbone
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P7/00—Preparation of oxygen-containing organic compounds
- C12P7/64—Fats; Fatty oils; Ester-type waxes; Higher fatty acids, i.e. having at least seven carbon atoms in an unbroken chain bound to a carboxyl group; Oxidised oils or fats
- C12P7/6409—Fatty acids
- C12P7/6427—Polyunsaturated fatty acids [PUFA], i.e. having two or more double bonds in their backbone
- C12P7/6432—Eicosapentaenoic acids [EPA]
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P7/00—Preparation of oxygen-containing organic compounds
- C12P7/64—Fats; Fatty oils; Ester-type waxes; Higher fatty acids, i.e. having at least seven carbon atoms in an unbroken chain bound to a carboxyl group; Oxidised oils or fats
- C12P7/6409—Fatty acids
- C12P7/6427—Polyunsaturated fatty acids [PUFA], i.e. having two or more double bonds in their backbone
- C12P7/6434—Docosahexenoic acids [DHA]
Abstract
Description
本発明は一般に、新規オキシピリンの産生用基質としてのドコサペンタエン酸(C22:5n-6)(DPAn-6)、ドコサペンタエン酸(C22:5n-3)(DPAn-3)、およびドコサテトラエン酸(DTAn-6:C22:4n-6)の使用、ならびにそれらによって産生されるオキシリピンに関する。本発明はさらに、特に抗炎症化合物としてのDPAn-6、DPAn-3、DTAn-6、および/またはそれら由来のオキシリピンの使用に関する。本発明はまた、強化量かつ有効量の長鎖多価不飽和酸(LCPUFA)由来オキシリピン、特にドコサノイドを含有する、LCPUFAに富んだ油および組成物を生成する新規な方法に関する。
1990年代の研究者らは、大型藻類(海草)中にいくつかの脂肪酸のヒドロキシ誘導体を同定し、生物体での創傷治癒および細胞シグナル伝達におけるこれら化合物の果たし得る役割について記載した(Gerwick & Bernart 1993;Gerwick et al 1993;Gerwick 1994)。彼らは、これらの化合物が、リポキシゲナーゼ経路を介して人体で産生されるものと類似していることを認めた。彼らはまた、紅藻、褐藻、および緑藻類においてC18脂肪酸(リノール酸、リノレン酸)およびアラキドン酸(C20:4n-6)(ARA)からエイコサノイドおよび関連オキシリピンを産生させるために、これら海草の細胞懸濁培養液を開発することを試みた。しかしながら、これらの培養系における海草バイオマスの産生は非常に乏しいことが判明し(例えば、15日後に約0.6〜1.0 g/L海草バイオマス(Rorrer et al. 1996))、重要な脂肪酸を培養液に直接添加しても、オキシリピンの産生は対照よりも最小限に増加するにすぎなかった(Rorrer et al. 1997)。さらに、場合によっては、添加した遊離脂肪酸が培養物に対して毒性があることが判明した(Rorrer et al. 1997)。そのため、これらの系はこれらの脂肪酸の酸化型の産生に関する学術的興味として留まるのみであり、研究はこれら海草中のC18およびC20オキシリピンに対して継続されている(例えば、Bouarab et al. 2004)。
本発明の1つの態様は一般に、ドコサペンタエン酸(DPAn-6)の単離されたドコサノイドに関する。そのようなドコサノイドには、これらに限定されないが、DPAn-6のモノヒドロキシ誘導体、DPAn-6のジヒドロキシ誘導体、およびDPAn-6のトリヒドロキシ誘導体から選択されるドコサノイドのRまたはSエピマーが含まれ得る。そのようなドコサノイドには、より詳細には、これらに限定されないが、7-ヒドロキシDPAn-6;8-ヒドロキシDPAn-6;10-ヒドロキシDPAn-6;11-ヒドロキシDPAn-6;13-ヒドロキシDPAn-6;14-ヒドロキシDPAn-6;17-ヒドロキシDPAn-6;7,17-ジヒドロキシDPAn-6;10,17-ジヒドロキシDPAn-6;13,17-ジヒドロキシDPAn-6;7,14-ジヒドロキシDPAn-6;8,14-ジヒドロキシDPAn-6;16,17-ジヒドロキシDPAn-6;4,5-ジヒドロキシDPAn-6;7,16,17-トリヒドロキシDPAn-6;および4,5,17-トリヒドロキシDPAn-6から選択されるドコサノイドのRもしくはSエピマー;またはその類似体、誘導体、もしくは塩が含まれ得る。
新規な抗炎症化合物に関する、ならびに上記のリポキシン、レゾルビン、およびドコサトリエンなどの公知の抗炎症化合物を提供する別の方法に関する当技術分野における必要性を認識して、本発明者らは、抗炎症用途において使用するための新規な抗炎症試薬および改良組成物の提供をもたらす、いくつかの相互に関係のある発見をした。
本出願の目的のため、長鎖多価不飽和脂肪酸(LCPUFA)を、3つまたはそれ以上の二重結合を含む、18またはそれ以上の炭素鎖長の脂肪酸、好ましくは20またはそれ以上の炭素鎖長の脂肪酸と定義する。ω-6系のLCPUFAには、ジ-ホモ-ガンマリノール酸(C20:3n-6)、アラキドン酸(C20:4n-6)、ドコサテトラエン酸またはアドレン酸(C22:4n-6)、およびドコサペンタエン酸(C22:5n-6)が含まれる。ω-3系のLCPUFAには、エイコサトリエン酸(C20:3n-3)、エイコサテトラエン酸(C20:4n-3)、エイコサペンタエン酸(C20:5n-3)、ドコサペンタエン酸(C22:5n-3)、およびドコサヘキサエン酸(C22:6n-3)酸が含まれる。LCPUFAには、これらに限定されないがC24:6(n-3)およびC28:8(n-3)をはじめとする、22個を超える炭素および4つまたはそれ以上の二重結合を有する脂肪酸もまた含まれる。
本発明の1つの態様は、DPAn-6、DPAn-3、もしくはDTAn-6由来の新規オキシリピン、およびそのようなオキシリピンの任意の類似体または誘導体、加えてそのようなオキシリピンまたはその類似体もしくは誘導体を含有する任意の組成物または製剤または生成物、ならびに任意のLCPUFAオキシリピンまたはその類似体もしくは誘導体、詳細にはDHA、EPA、DPAn-6、DPAn-3、またはDTAn-6由来の任意のオキシリピン、より詳細には任意のドコサノイド、さらにより詳細にはDPAn-6、DPAn-3、またはDTAn-6由来の任意のオキシリピンが任意の方法により強化された油またはその他の組成物もしくは製剤もしくは生成物に関する。本発明はまた、油もしくは組成物中のオキシリピンの質、量、もしくは安定性を改善するため、ならびに/または油もしくは組成物中に含まれるオキシリピンの吸収、生物学的利用能、および/もしくは有効性を改善するために、そのようなオキシリピン(DHA、EPA、DPAn-6、DPAn-3、またはDTAn-6由来の任意のオキシリピン、より詳細には任意のドコサノイド)が油または組成物中で安定化または維持された任意の油またはその他の組成物もしくは製剤もしくは生成物に関する。
本発明において有用なEPA由来のオキシリピンには、これらに限定されないが、15-エピ-リポキシンA4(5S,6R,15R-トリヒドロキシエイコサテトラエン酸)およびその中間体15R-ヒドロキシエイコサペンタエン酸(15R-HEPE);レゾルビンE1(5,12,18-トリヒドロキシEPA)、ならびにその中間体5,6-エポキシ,18R-ヒドロキシ-EPE、および5S-ヒドロ(ペルオキシ),18R-ヒドロキシ-EPE、および18R-ヒドロキシ-EPE(18R-HEPE);ならびにレゾルビンE2(5S,18R-ジヒドロキシ-EPEまたは5S,18R-ジHEPE)およびその中間体が含まれる。これらのEPA誘導体の構造については、図13を参照されたい。EPA由来オキシリピンはSerhan (2005)に詳述されており、これはその全体が参照により本明細書に組み入れられる。
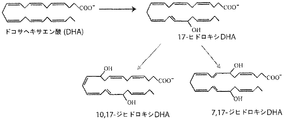
本発明において有用なDHA由来のオキシリピンには、これらに限定されないが、レゾルビンD1(7,8,17R-トリヒドロキシDHA)およびレゾルビンD2(7,16,17R-トリヒドロキシDHA)、加えてそれらのSエピマー、ならびに17S/R-ヒドロペルオキシDHA、および7S-ヒドロペルオキシ,17S/R-OH-DHA、および7(8)-エポキシ-17S/R-OH-DHAを含むそれらの中間体;レゾルビンD4(4,5,17R-トリヒドロキシDHA)およびレゾルビンD3(4,11,17RトリヒドロキシDHA)、加えてそれらのSエピマー、ならびに17S/R-ヒドロペルオキシDHA、および4S-ヒドロペルオキシ,17S/R-OH DHA、および4(5)-エポキシ-17S/R-OH DHAを含むそれらの中間体;ならびにニューロプロテクチンD1(10,17S-ドコサトリエン、プロテクチンD1)、加えてそのRエピマー、ならびにジヒドロキシ生成物16,17-エポキシ-ドコサトリエン(16,17-エポキシ-DT)およびヒドロペルオキシ生成物17S-ヒドロペルオキシDHAを含むそれらの中間体;レゾルビンD5(7S,17S-ジヒドロキシDHA)およびレゾルビンD6ならびにそれらのヒドロキシル含有中間体;ならびにエポキシド誘導体7,8エポキシDPA、10,11-エポキシDPA、13,14-エポキシDPA、および19,20-エポキシDPA、ならびにジヒドロキシ誘導体13,14-ジヒドロキシドコサペンタエン酸;7-ヒドロキシDHA、10-ヒドロキシDHA、11-ヒドロキシDHA、13-ヒドロキシDHA、14-ヒドロキシDHA、16-ヒドロキシDHA、および17-ヒドロキシDHAのRおよびSエピマーを含むその他のモノヒドロキシDHA誘導体;ならびに10,20-ジヒドロキシDHA、7,14-ジヒドロキシDHA、および8,14-ジヒドロキシDHAのRおよびSエピマーを含むその他のジヒドロキシDHA誘導体が含まれる。これらのDHA誘導体の説明および構造については、以下の実施例2、7、および10、ならびに図2A〜2D、図7、図10、および図14AおよびBを参照されたい。DHA由来オキシリピンはSerhan (2005)およびYe et al (2002)に詳述されており、これらはその全体が参照により本明細書に組み入れられる。
本発明の1つの態様は、DPAn-6、DTAn-6、またはDPA-n-3に由来する新規オキシリピンに関する。本発明の別の態様は、C22 PUFAに由来し得る新規ドコサノイドに関する。具体的には、本発明者らは本明細書において、その構造がC22脂肪酸構造から新たに設計された新規ドコサノイドについて記載する。本発明により包含されるオキシリピンには、DPAn-6、DTAn-6、もしくはDPAn-3に由来するか、または一般にC22脂肪酸に由来し、より詳細には本明細書においてドコサノイドと称される任意のオキシリピンが含まれる。新規ドコサノイドには、DPAn-6、DTAn-6、DPAn-3の任意の酸化誘導体、またはC22脂肪酸のその他の新規酸化誘導体(例えば、図23を参照されたい)、加えてそれらの任意の誘導体もしくは類似体が含まれる。詳細には、本発明のドコサノイドには、これらに限定されないが、DPAn-6、DTAn-6、もしくはDPAn-3、またはC22脂肪酸のいずれかの任意のモノヒドロキシ、ジヒドロキシ、またはトリヒドロキシ誘導体の任意のRまたはSエピマーが含まれ、このドコサノイドは、参照LCPUFA中の炭素-炭素二重結合を形成する任意の炭素において誘導体化を含み得る。本発明のドコサノイドには、DPAn-6、DTAn-6、またはDPAn-3を基質として使用し、かつこれらに限定されないが、表1に記載するような(以下を参照されたい)リポキシゲナーゼ、シクロオキシゲナーゼ、シトクロムP450酵素、およびその他のヘム含有酵素を含むオキシリピン生成酵素によって触媒される酵素反応の任意の生成物もまた含まれる。表1に、酵素の正式名称、正式記号、別名、生物、および/または配列データベースアクセッション番号を含め、列挙した公知の酵素を同定するのに十分な情報を提供する。
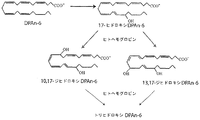
DPAn-6由来オキシリピン(DPAn-6由来のオキシリピン、またはより詳細にはDPAn-6由来のドコサノイドとも称する)には、これらに限定されないが、DPAn-6の任意のモノヒドロキシ、ジヒドロキシ、トリヒドロキシ、または多ヒドロキシ誘導体の任意のRまたはSエピマーが含まれ、このオキシリピンは、DPAn-6中の炭素-炭素二重結合を形成する任意の炭素においてヒドロキシ誘導体化を含み得る。本発明のいくつかの例示的な新規DPAn-6由来オキシリピンには、これらに限定されないが、7-ヒドロキシDPAn-6、8-ヒドロキシDPAn-6、10-ヒドロキシDPAn-6、11-ヒドロキシDPAn-6、13-ヒドロキシDPAn-6、14-ヒドロキシDPAn-6、および17-ヒドロキシDPAn-6(特に17-ヒドロキシDPAn-6)を含む、DPAn-6のモノヒドロキシ生成物のRおよびSエピマー;7,17-ジヒドロキシDPAn-6、10,17-ジヒドロキシDPAn-6、13,17-ジヒドロキシDPAn-6、7,14-ジヒドロキシDPAn-6、8,14-ジヒドロキシDPAn-6、16,17-ジヒドロキシDPAn-6、および4,5-ジヒドロキシDPAn-6(特に10,17-ヒドロキシDPAn-6)を含む、DPAn-6のジヒドロキシ誘導体のRおよびSエピマー;ならびに7,16,17-トリヒドロキシDPAn-6および4,5,17-トリヒドロキシDPAn-6のRおよびSエピマーを含む、DPAn-6のトリヒドロキシ誘導体が含まれる。DPAn-6オキシリピンの構造を、実施例3、6、8、および11、ならびに図3A〜3D、図6、図8、図11、および図15に記載および/または表示する。
DPAn-3由来オキシリピン(DPAn-3由来のオキシリピン、またはより詳細にはDPAn-3由来のドコサノイドとも称する)には、これらに限定されないが、DPAn-3の任意のモノヒドロキシ、ジヒドロキシ、トリヒドロキシ、または多ヒドロキシ誘導体の任意のRまたはSエピマーが含まれ、このオキシリピンは、DPAn-3中の炭素-炭素二重結合を形成する任意の炭素においてヒドロキシ誘導体化を含み得る。本発明のいくつかの例示的な新規DPAn-3由来オキシリピンには、これらに限定されないが、7-ヒドロキシDPAn-3、10-ヒドロキシDPAn-3、11-ヒドロキシDPAn-3、13-ヒドロキシDPAn-3、14-ヒドロキシDPAn-3、16-ヒドロキシDPAn-3、および17-ヒドロキシDPAn-3を含む、DPAn-3のモノヒドロキシ生成物のRおよびSエピマー;7,17-ジヒドロキシDPAn-3、10,17-ジヒドロキシDPAn-3、8,14-ジヒドロキシDPAn-3、16,17-ジヒドロキシDPAn-3、13,20-ジヒドロキシDPAn-3、および10,20-ジヒドロキシDPAn-3を含む、DPAn-3のジヒドロキシ誘導体のRおよびSエピマー;ならびに7,16,17-トリヒドロキシDPAn-3のRおよびSエピマーを含む、DPAn-3のトリヒドロキシ誘導体が含まれる。DPAn-3オキシリピンの構造を、実施例4、9、および12、ならびに図4A〜4D、図9、図12、および図16に記載および/または表示する。
DTAn-6由来オキシリピン(DTAn-6由来のオキシリピン、またはより詳細にはDTAn-6由来のドコサノイドとも称する)には、これらに限定されないが、DTAn-6の任意のモノヒドロキシ、ジヒドロキシ、トリヒドロキシ、または多ヒドロキシ誘導体の任意のRまたはSエピマーが含まれ、このオキシリピンは、DTAn-6中の炭素-炭素二重結合を形成する任意の炭素においてヒドロキシ誘導体化を含み得る。本発明のいくつかの例示的な新規DTAn-6由来オキシリピンには、これらに限定されないが、7-ヒドロキシDTAn-6、10-ヒドロキシDTAn-6、13-ヒドロキシDTAn-6、および17-ヒドロキシDTAn-6を含む、DTAn-6のモノヒドロキシ生成物のRおよびSエピマー;7,17-ジヒドロキシDTAn-6、10,17-ジヒドロキシDTAn-6、および16,17-ジヒドロキシDTAn-6を含む、DTAn-6のジヒドロキシ誘導体のRおよびSエピマー;ならびに7,16,17-トリヒドロキシDTAn-6のRおよびSエピマーを含む、DTAn-6のトリヒドロキシ誘導体が含まれる。DTAn-6オキシリピンの構造を、実施例5、ならびに図5A〜5Cおよび図17に記載および/または表示する。
その他の新規C22-PUFA由来オキシリピン(C22-PUFA由来のオキシリピン、またはより詳細にはC22-PUFA由来由来のドコサノイドとも称する)には、これらに限定されないが、C22-PUFAの任意のモノヒドロキシ、ジヒドロキシ、トリヒドロキシ、または多ヒドロキシ誘導体の任意のRまたはSエピマーが含まれ、このオキシリピンは、C22-PUFA中の炭素-炭素二重結合を形成する任意の炭素においてヒドロキシ誘導体化を含み得る。本発明により包含されるいくつかの例示的な新規ドコサノイドには、これらに限定されないが、4,5-エポキシ-17-ヒドロキシDPA、7,8-エポキシDHA、10,11-エポキシDHA、13,14-エポキシDHA、19,20-エポキシDHA、13,14-ジヒドロキシDHA、16,17-ジヒドロキシDTAn-6、7,16,17-トリヒドロキシDTAn-6、4,5,17-トリヒドロキシDTAn-6、7,16,17-トリヒドロキシDTAn-3、16,17-ジヒドロキシDTAn-3、16,17-ジヒドロキシDTRAn-6、7,16,17-トリヒドロキシDTRAn-6、4,5-ジヒドロキシDTAn-6、および10,16,17-トリヒドロキシDTRAn-6が含まれる。これらのC22-PUFA由来ドコサノイドの構造を図23に示す。
本発明は、本明細書に記載のLCPUFAおよび/またはLCPUFAオキシリピンを含む油、組成物、製剤、および生成物を含む。本発明によれば、「生成物」という用語は、本発明の任意の油、組成物、または製剤を一般的にまたは総称して説明するために用い得るが、生成物の使用の状況に応じて1つの用語は別の用語よりも好ましいと考えられる。本発明の1つの態様において、油、組成物、および製剤は、少なくともDPAn-6、DTAn-6、もしくはDPAn-3、またはそれら由来のオキシリピン、またはそれらの組み合わせを含み、任意の他のLCPUFAおよび/またはそれ由来の任意のオキシリピンをさらに含んでもよい。そのようなオキシリピンは、新規合成、任意の供給源からの酵素変換(例えば、リポキシゲナーゼ、シクロオキシゲナーゼ、シトクロムP450酵素、および他のヘム含有酵素を含む酵素による)、任意の供給源からの精製、および任意の生物学的供給源(例えば、細菌、植物、動物源)からの産生を含む、任意の化学的または生物学的(生体)方法により産生され得る。
例えば、動物(無脊椎動物および脊椎動物)、植物、および細菌源を含むLCPUFAの任意の供給源を用いて、本発明のLCPUFA、オキシリピン、油、組成物、または製剤を生成することができる。
本明細書に記載のLCPUFAのオキシリピンを含有する油は、本発明以前に記載されているような化学合成されたまたはインビトロでの酵素変換により産生されたオキシリピンと比較して、独特の特徴を有する。LCPUFAオキシリピン、特にドコサノイドは、遊離型および/またはエステル型として油中に存在する。エステル型としては、LCPUFAオキシリピン、特にドコサノイドは、トリグリセリド、ジグリセリド、モノグリセリド、リン脂質、ステロールエステル、および/またはろうエステル型として存在し得る。オキシリピンはこれまでは遊離脂肪酸型としてしか記載されていなかったため、エステル型はオキシリピンの新規な形態であり、その存在は本発明の油または組成物中で強化、安定化、または保持され得る。理論に縛られることはないが、本発明者らは、いったんLCPUFAオキシリピン、特にドコサノイドが遊離脂肪酸型として形成されると、これがエステル型の1つに再エステル化され得ると考えている。または、脂肪酸分子は、エステル型であるままオキシリピンに変換され得る。
本発明の1つの態様は、抗炎症薬または神経保護薬としてのLCPUFA自体、特にDPAn-6および/またはDPAn-3の使用を含む(すなわち、LCPUFAは、単独でまたはそのオキシリピン代謝産物と組み合わせて提供される)。DPAn-6および/またはDPAn-3は、単独でまたは他のLCPUFA、好ましくはDHAおよび/またはEPAと組み合わせて提供され得る。抗炎症特性または神経保護特性を有するDTAn-6もまた、本発明により包含される。好ましくは、本発明において用いられるDPAn-6、DPAn-3、またはDTAn-6は、以下の形態の1つとして提供される:DPAn-6、DTAn-6、および/またはDPAn-3を含有するトリグリセリドとして、DPAn-6、DTAn-6、および/またはDPAn-3を含有するリン脂質として、遊離脂肪酸として、DPAn-6、DTAn-6、および/またはDPAn-3のエチルまたはメチルエステルとして。
本発明に従って、油、補助剤、化粧用、治療組成物、および本明細書に記載のその他の製剤または生成物中で用いられるLCPUFAおよび/またはそのオキシリピン誘導体は、種々の形態で提供される。例えば、そのような形態には、これらに限定されないが以下のものが含まれる:好ましくは本明細書に記載するように産生された、LCPUFAおよび/またはそのオキシリピン誘導体を含む藻類油;好ましくは本明細書に記載するように産生された、PUFAおよび/またはそのオキシリピン誘導体を含む植物油;PUFAを含むトリグリセリド油;PUFAを含むリン脂質;PUFAを含むタンパク質、トリグリセリド、および/またはリン脂質の組み合わせ;PUFAを含む乾燥海洋微細藻類;PUFAを含むスフィンゴ脂質;PUFAのエステル;遊離脂肪酸;PUFAと別の生理活性分子との複合体;およびこれらの組み合わせ。長鎖脂肪酸は、供給源の混合、精製、強化(例えば、培養および/または処理技法を介して)、および遺伝子操作によるなどして、脂肪酸の天然源中で生じる量または比率と異なる量および/または比率で提供され得る。生理活性分子には、これらに限定されないが、タンパク質、アミノ酸(例えば、DHA-グリシン、DHA-リジン、またはアミノ酸類似体などの天然アミノ酸)、薬物、および炭水化物を含む任意の適切な分子が含まれ得る。本明細書に概説する形態によって、高い官能的品質を有する食品、食事または栄養補助剤、および薬学的物質の製剤化における柔軟性が可能になる。
本発明の1つの態様においては、LCPUFAおよび/またはそのオキシリピン誘導体の供給源のいずれもが、そのようなLCPUFAまたはそのオキシリピン誘導体を含有するいずれの油または組成物または製剤も含めて、本発明の方法において有用であり得る1つまたは複数の追加成分と共に提供され得る。このような追加成分には、任意のさらなる抗炎症薬、栄養補助剤(例えば、ビタミン、ミネラル、および栄養補給剤を含むその他の栄養剤)、治療薬、または薬学的もしくは栄養的担体(例えば、薬学的(治療を含む)組成物または栄養組成物と併用され得る任意の賦形剤、希釈剤、送達媒体、または担体化合物および製剤)が含まれるが、これらに限定されない。
細菌技術を用いてLCPUFA含有油(DHAおよびDPAn-6を含む)を産生する方法は、当技術分野において教示されている。米国特許第5,130,242号および米国特許第5,340,594号は、シゾキトリウム種およびヤブレツボカビ種を用いた発酵により、DHAおよびDPAに富んだ脂質を産生する方法を教示している。米国特許出願公開第2003/0161866号は、推定的ウルケニア属に属する微生物を培養することにより、DHAおよびDPAn-6を含有する油を調製する工程について記載している。
産生または発酵条件を最適化して、LCPUFAオキシリピン(特に、ドコサノイド)の産生を増強すること、および/または産生された時点でそれらを安定化することができる。これらの方法は、これらの化合物を産生する酵素の活性および/または発現を増強する培養条件を選択する段階を含む。例えば、細胞濃度および/または培養物の特定の増殖速度を変更する任意の培養条件は、潜在的に細胞組成を変更し得る。微生物における代謝産物または二次代謝産物の産生を改変することが知られている培養条件には、これらに限定されないが以下のものが含まれる:低浸透圧性または高浸透圧性塩分ストレス、栄養制限ストレス(窒素、リン、炭素、および/または微量金属)、温度ストレス(慣例より高いまたは低い)、酸素および/または二酸化炭素レベルの増強もしくは減少、ならびに剪断などの物理的ストレス。さらに、細胞中の代謝産物または二次代謝産物のレベルは、増殖相(対数期 対 定常期)により、および微生物による生物変換のための種々の前駆体分子を提供することにより、変動し得る。
酵素はLCPUFAのヒドロキシ誘導体の形成において重要な役割を果たすため、これら酵素とLCPUFAとの接触を増強して、ヒドロキシ誘導体の形成を増強する好ましい方法が存在する。1つの好ましい工程においては、細菌細胞または油糧種子を破裂させ(例えば、細菌細胞をホモジナイズすることによる、または油糧種子を粉砕することによる)、得られた油およびバイオマス混合物を最適な条件下(例えば、温度、pH、残留水分活性、イオン濃度、および任意の必須補因子の存在)で一定時間インキュベートして、バイオマス中に遊離された酵素をLCPUFAと直接反応させる。同様に、自動酸化工程もこの様式で促進され得る。
好ましい油処理法には、油を最小限に処理することに焦点をおいた方法が含まれる。慣用的な油糧種子処理において用いられる工程は、遊離脂肪酸または遊離脂肪酸様化合物を除去し、それによって脂肪酸様のLCPUFAのヒドロキシ誘導体を除去してしまう傾向がある。特に、遊離脂肪酸の除去に焦点をおいた油の苛性処置(一般に油の純化と称される)は、回避すべきである。好ましくは、油はアルコール(例えば、イソプロピルアルコール)もしくはその他の有機溶媒(例えば、ヘキサン)、またはその混合物、または超臨界流体(例えば、二酸化炭素)を用いて抽出し、得られた油を冷却濾過し、漂白し、再度冷却濾過し、次いで脱臭する。より好ましい方法においては、冷却濾過段階を除いて、抽出後に油を単に漂白および脱臭する。さらにより好ましい方法においては、油の抽出後の唯一の処理段階は、油の脱臭に限定される。上記の抽出では、油の抽出における使用には、ヘキサンなどの有機溶媒を使用するよりもアルコールまたはアルコール水混合液が好ましい。化学的抽出の別法として、圧搾により、または第一級アルコールもしくはキャリアーオイルなどの分離処理助剤を用いた、破壊およびその後の遠心分離により、油をバイオマスから分離することができる。これらの粗製油は、上記の方法の1つまたは複数により精製および安定化され得る。
1つの好ましい方法では、上記の方法により、または任意の他の適切な方法により油が抽出および処理された時点で、油中のLCPUFAオキシリピン(特に、ドコサノイド)の安定化を支援するために、抗酸化剤を油に添加する。別の好ましい方法では、オキシリピンおよび/またはLCPUFAの酸化的分解の可能性を最小限に抑えるために、抗酸化剤を抽出および精製工程の一つまたは複数の時点で添加し得る。さらに、オキシリピンは、より多くのヒドロキシ基が取り込まれるほどより極性の高い分子となり、極性型および極性の低い形態のLCPUFAオキシリピン(特に、ドコサノイド)両方の含量/溶解性/安定性を増強するために、ならびに例えば油成分形態のみの使用に利用できる食物および薬学的用途よりも幅広い種類のそれらにおける使用を容易にするために、油は乳濁液形態で調製することができる。
本発明は、ヒトおよびその他の動物において抗炎症、抗増殖、神経保護、および/または血管調節効果を提供するための、DPAn-6、DTAn-6、および/もしくはDPAn-3を含むLCPUFA、ならびに/またはそのオキシリピン誘導体、ならびに/またはC20およびそれ以上のPUFAのオキシリピン誘導体、特にドコサノイドが強化された種々の油の使用に基づく。このような効果は、個体の全般的健康を増強するのに、ならびに個体における種々の疾患および状態を治療または予防する上で有用である。例えば、本発明は、代謝不均衡、ならびにLCPUFAおよびオキシリピン、特にドコサノイド、加えて本明細書に記載の組成物および油によって提供される炎症の調節から恩恵を受け得る疾患状態を治療する方法を含む。
実施例1
以下の実施例は、DPAn-6が15-リポキシゲナーゼによってモノヒドロキシジエン誘導体に完全に変換され得、DPAn-3またはDHAよりも効率的に変換されることを実証する。
以下の実施例は、DHAの主要な15-リポキシゲナーゼ生成物について記載する。
以下の実施例は、DPAn-6の主要な15-リポキシゲナーゼ生成物を示し、DHAから産生されるモノヒドロキシおよびジヒドロキシ誘導体(実施例2を参照されたい)と類似しているそのような誘導体の産生を実証する。
以下の実施例は、DPAn-3の主要な15-リポキシゲナーゼ生成物を示し、DHA(実施例2)およびDPAn-6(実施例3)から産生されるモノヒドロキシおよびジヒドロキシ誘導体と類似しているそのような誘導体の産生を実証する。
以下の実施例は、DTAn-6の主要な15-リポキシゲナーゼ生成物を示し、DHA(実施例2)、DPAn-6(実施例3)、およびDPAn-3(実施例4)から形成されるモノヒドロキシおよびジヒドロキシ誘導体と類似しているそのような誘導体の産生を実証する。
以下の実施例は、15-リポキシゲナーゼおよびその後のヘモグロビンによる順次的処置後にDPAn-6から産生された酵素オキシリピン生成物の構造を示す。
以下の実施例は、DHAの主要な5-リポキシゲナーゼ生成物を示す。
以下の実施例は、DPAn-6の主要な5-リポキシゲナーゼ生成物を示し、DHAの5-LOX生成物(実施例7)と類似しているモノヒドロキシ誘導体の産生を示す。
以下の実施例は、DPAn-3の主要な5-リポキシゲナーゼ生成物を示し、DHAの5-LOX生成物(実施例7)と類似しているモノヒドロキシおよびジヒドロキシ誘導体の産生を示す。
以下の実施例は、DHAの主要な12-リポキシゲナーゼ生成物を示す。
以下の実施例は、DPAn-6の主要な12-リポキシゲナーゼ生成物を示し、DHA/12-LOX反応によるモノヒドロキシおよびジヒドロキシ誘導体(実施例10)と類似しているそのような誘導体の産生を示す。
以下の実施例は、DPAn-3の主要な12-リポキシゲナーゼ生成物を示し、DHA/12-LOX反応(実施例10)およびDPAn-6/12-LOX反応(実施例11)から産生されるモノヒドロキシおよびジヒドロキシ誘導体と類似しているそのような誘導体の産生を示す。
以下の実施例は、藻類DHA/DPAn-6 LCPUFA油中のオキシリピンの質量スペクトル解析について記載する。
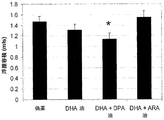
以下の実施例は、LCPUFAの種々の組み合わせを動物に与えたラット肢浮腫実験の結果を示す。
以下の実施例では、マウス背部空気嚢モデルにおいて、DPAn-6由来オキシリピン、17-ヒドロキシDPAn-6および10,17-ジヒドロキシ-DPAn-6の強力な抗炎症効果を実証する。
以下の実施例は、細胞培養物におけるDHAおよびDPAn-6由来ドコサノイドの抗炎症効果を示す。
以下の実施例は、培養でのヒトリンパ球に及ぼす10,17-ジヒドロキシDPAn-6の抗炎症効果をさらに例証し、抗CD3/抗CD28抗体で刺激したTリンパ球によるTNFα分泌の減少において、ジヒドロキシDPAn-6化合物がDHA類似体(10,17,ジヒドロキシDHA)よりも強力であることを実証する。
Claims (112)
- ドコサペンタエン酸(DPAn-6)の単離されたドコサノイド。
- DPAn-6のモノヒドロキシ誘導体、DPAn-6のジヒドロキシ誘導体、およびDPAn-6のトリヒドロキシ誘導体からなる群より選択されるドコサノイドのRまたはSエピマーである、請求項1記載の単離されたドコサノイド。
- 7-ヒドロキシDPAn-6;8-ヒドロキシDPAn-6;10-ヒドロキシDPAn-6;11-ヒドロキシDPAn-6;13-ヒドロキシDPAn-6;14-ヒドロキシDPAn-6;17-ヒドロキシDPAn-6;7,17-ジヒドロキシDPAn-6;10,17-ジヒドロキシDPAn-6;13,17-ジヒドロキシDPAn-6;7,14-ジヒドロキシDPAn-6;8,14-ジヒドロキシDPAn-6;16,17-ジヒドロキシDPAn-6;4,5-ジヒドロキシDPAn-6;7,16,17-トリヒドロキシDPAn-6;および4,5,17-トリヒドロキシDPAn-6からなる群より選択されるドコサノイドのRもしくはSエピマー;またはその類似体、誘導体、もしくは塩である、請求項1記載の単離されたドコサノイド。
- ドコサペンタエン酸(DPAn-3)の単離されたドコサノイド。
- DPAn-3のモノヒドロキシ誘導体、DPAn-3のジヒドロキシ誘導体、およびDPAn-3のトリヒドロキシ誘導体からなる群より選択されるドコサノイドのRまたはSエピマーである、請求項4記載の単離されたドコサノイド。
- 7-ヒドロキシDPAn-3;10-ヒドロキシDPAn-3;11-ヒドロキシDPAn-3;13-ヒドロキシDPAn-3;14-ヒドロキシDPAn-3;16-ヒドロキシDPAn-3;17-ヒドロキシDPAn-3;7,17-ジヒドロキシDPAn-3;10,17-ジヒドロキシDPAn-3;8,14-ジヒドロキシDPAn-3;16,17-ジヒドロキシDPAn-3;13,20-ジヒドロキシDPAn-3;10,20-ジヒドロキシDPAn-3;および7,16,17-トリヒドロキシDPAn-3からなる群より選択されるドコサノイドのRもしくはSエピマー;またはその類似体、誘導体、もしくは塩である、請求項5記載の単離されたドコサノイド。
- ドコサテトラエン酸(DTAn-6)の単離されたドコサノイド。
- DTAn-6のモノヒドロキシ誘導体、DTAn-6のジヒドロキシ誘導体、およびDTAn-6のトリヒドロキシ誘導体からなる群より選択されるドコサノイドのRまたはSエピマーである、請求項7記載の単離されたドコサノイド。
- 7-ヒドロキシDTAn-6;10-ヒドロキシDTAn-6;13-ヒドロキシDTAn-6;17-ヒドロキシDTAn-6;7,17-ジヒドロキシDTAn-6;10,17-ジヒドロキシDTAn-6;16,17-ジヒドロキシDTAn-6;および7,16,17-トリヒドロキシDTAn-6からなる群より選択されるドコサノイドのRもしくはSエピマー;またはその類似体、誘導体、もしくは塩である、請求項8記載の単離されたドコサノイド。
- 4,5-エポキシ-17-ヒドロキシDPA;7,8-エポキシDHA;10,11-エポキシDHA;13,14-エポキシDHA;19,20-エポキシDHA;13,14-ジヒドロキシDHA;16,17-ジヒドロキシDTAn-6;7,16,17-トリヒドロキシDTAn-6;4,5,17-トリヒドロキシDTAn-6;7,16,17-トリヒドロキシDTAn-3;16,17-ジヒドロキシDTAn-3;16,17-ジヒドロキシDTRAn-6;7,16,17-トリヒドロキシDTRAn-6;4,5-ジヒドロキシDTAn-6;および10,16,17-トリヒドロキシDTRAn-6からなる群より選択されるドコサノイドのRもしくはSエピマー;またはその類似体、誘導体、もしくは塩である、C22多価不飽和脂肪酸の単離されたドコサノイド。
- 請求項1〜10のいずれか一項記載の少なくとも1つのドコサノイドを含む組成物。
- 治療組成物である、請求項11記載の組成物。
- 栄養組成物である、請求項11記載の組成物。
- 化粧用組成物である、請求項11記載の組成物。
- アスピリンをさらに含む、請求項11記載の組成物。
- DPAn-6、DPAn-3、DTAn-6、DHA、EPA、DHAのオキシリピン誘導体、およびEPAのオキシリピン誘導体からなる群より選択される化合物をさらに含む、請求項11記載の組成物。
- スタチン、非ステロイド性抗炎症薬、抗酸化剤、および神経保護薬からなる群より選択される少なくとも1つの薬剤をさらに含む、請求項11記載の組成物。
- 薬学的に許容される担体をさらに含む、請求項11記載の組成物。
- 微生物油、植物種子油、および水生動物油からかなる群より選択される油を含む、請求項11記載の組成物。
- 油1グラム当たり少なくとも約10μgのドコサノイドを含む油。
- 油1グラム当たり少なくとも約20μgのドコサノイドを含む、請求項20記載の油。
- 油1グラム当たり少なくとも約50μgのドコサノイドを含む、請求項20記載の油。
- 油1グラム当たり少なくとも約100μgのドコサノイドを含む、請求項20記載の油。
- ドコサノイドが、ドコサテトラエン酸(DTAn-6)、ドコサペンタエン酸(DPAn-6)、ドコサペンタエン酸(DPAn-3)、ドコサヘキサエン酸(DHA)、およびエイコサペンタエン酸(EPA)からなる群より選択される多価不飽和脂肪酸に由来する、請求項20〜23のいずれか一項記載の油。
- ドコサノイドが、ドコサテトラエン酸(DTAn-6)、ドコサペンタエン酸(DPAn-6)、およびドコサペンタエン酸(DPAn-3)からなる群より選択される多価不飽和脂肪酸に由来する、請求項20〜23のいずれか一項記載の油。
- ドコサノイドがドコサペンタエン酸(DPAn-6)に由来する、請求項20〜23のいずれか一項記載の油。
- ドコサノイドが、DPAn-6のモノヒドロキシ誘導体、DPAn-6のジヒドロキシ誘導体、およびDPAn-6のトリヒドロキシ誘導体からなる群より選択されるドコサノイドのRまたはSエピマーである、請求項26記載の油。
- ドコサノイドが、7-ヒドロキシDPAn-6;8-ヒドロキシDPAn-6;10-ヒドロキシDPAn-6;11-ヒドロキシDPAn-6;13-ヒドロキシDPAn-6;14-ヒドロキシDPAn-6;17-ヒドロキシDPAn-6;7,17-ジヒドロキシDPAn-6;10,17-ジヒドロキシDPAn-6;13,17-ジヒドロキシDPAn-6;7,14-ジヒドロキシDPAn-6;8,14-ジヒドロキシDPAn-6;16,17-ジヒドロキシDPAn-6;4,5-ジヒドロキシDPAn-6;7,16,17-トリヒドロキシDPAn-6;および4,5,17-トリヒドロキシDPAn-6からなる群より選択されるドコサノイドのRもしくはSエピマー;またはその類似体、誘導体、もしくは塩である、請求項26記載の油。
- ドコサノイドがドコサペンタエン酸(DPAn-3)に由来する、請求項20〜23のいずれか一項記載の油。
- ドコサノイドが、DPAn-3のモノヒドロキシ誘導体、DPAn-3のジヒドロキシ誘導体、およびDPAn-3のトリヒドロキシ誘導体からなる群より選択されるドコサノイドのRまたはSエピマーである、請求項29記載の油。
- ドコサノイドが、7-ヒドロキシDPAn-3;10-ヒドロキシDPAn-3;11-ヒドロキシDPAn-3;13-ヒドロキシDPAn-3;14-ヒドロキシDPAn-3;16-ヒドロキシDPAn-3;17-ヒドロキシDPAn-3;7,17-ジヒドロキシDPAn-3;10,17-ジヒドロキシDPAn-3;8,14-ジヒドロキシDPAn-3;16,17-ジヒドロキシDPAn-3;13,20-ジヒドロキシDPAn-3;10,20-ジヒドロキシDPAn-3;および7,16,17-トリヒドロキシDPAn-3からなる群より選択されるドコサノイドのRもしくはSエピマー;またはその類似体、誘導体、もしくは塩である、請求項29記載の油。
- ドコサノイドがドコサテトラエン酸(DTAn-6)に由来する、請求項20〜23のいずれか一項記載の油。
- ドコサノイドが、DTAn-6のモノヒドロキシ誘導体、DTAn-6のジヒドロキシ誘導体、およびDTAn-6のトリヒドロキシ誘導体からなる群より選択されるドコサノイドのRまたはSエピマーである、請求項32記載の油。
- ドコサノイドが、7-ヒドロキシDTAn-6;10-ヒドロキシDTAn-6;13-ヒドロキシDTAn-6;17-ヒドロキシDTAn-6;7,17-ジヒドロキシDTAn-6;10,17-ジヒドロキシDTAn-6;16,17-ジヒドロキシDTAn-6;および7,16,17-トリヒドロキシDTAn-6からなる群より選択されるドコサノイドのRもしくはSエピマー;またはその類似体、誘導体、もしくは塩である、請求項32記載の油。
- 微生物油、植物種子油、および水生動物油からかなる群より選択される、請求項20〜34のいずれか一項記載の油。
- 請求項20〜35のいずれか一項記載の油を含む組成物。
- 治療組成物である、請求項36記載の組成物。
- 栄養組成物である、請求項36記載の組成物。
- 化粧用組成物である、請求項36記載の組成物。
- DPAn-6、DPAn-3、およびDTAn-6からなる群より選択される長鎖多価不飽和脂肪酸、ならびに薬学的または栄養学的に許容される担体を含む組成物。
- アスピリンをさらに含む、請求項40記載の組成物。
- DPAn-6、DTAn-6、またはDPAn-3からのドコサノイドの産生を触媒する酵素をさらに含む、請求項40記載の組成物。
- 個体における炎症または神経変性の少なくとも1つの症状を予防または軽減する方法であって、個体における炎症または神経変性の少なくとも1つの症状を軽減するために、炎症もしくは神経変性またはそれらに関連する状態もしくは疾患を有するリスクがある、それらを有すると診断された、またはそれらを有すると疑われる個体に、DPAn-6、DPAn-3、DPAn-6のオキシリピン誘導体、およびDPAn-3のオキシリピン誘導体からなる群より選択される薬剤を投与する段階を含む、方法。
- 薬剤が、Tリンパ球による腫瘍壊死因子-α(TNF-α)の産生を減少させるのに有効である、請求項43記載の方法。
- 薬剤が、炎症部位への好中球およびマクロファージの遊走を減少させるのに有効である、請求項43記載の方法。
- 薬剤が、個体におけるインターロイキン-1β(IL-1β)産生を減少させるのに有効である、請求項43記載の方法。
- 薬剤が、個体におけるマクロファージ走化性タンパク質-1(MCP-1)を減少させるのに有効である、請求項43記載の方法。
- 少なくとも1つの長鎖ω-3脂肪酸および/またはそのオキシリピン誘導体を個体に投与する段階をさらに含む、請求項43記載の方法。
- ω-3脂肪酸が、DHAおよびEPAからなる群より選択される、請求項48記載の方法。
- DPAn-6またはDPAn-3が、以下の形態:DPAn-6またはDPAn-3を含有するトリグリセリド、DPAn-6またはDPAn-3を含有するリン脂質、遊離脂肪酸、DPAn-6またはDPAn-3のエチルまたはメチルエステルの、1つとして提供される、請求項43記載の方法。
- DPAn-6もしくはDPAn-3またはそれらのオキシリピン誘導体が、微生物油、動物油、または長鎖多価不飽和脂肪酸を産生するように遺伝子改変された油糧種子植物に由来する植物油の形態で提供される、請求項43記載の方法。
- オキシリピン誘導体が、DPAn-6またはDPAn-3からそのオキシリピン誘導体への酵素変換により産生される、請求項43記載の方法。
- オキシリピン誘導体が新規に化学合成される、請求項43記載の方法。
- オキシリピン誘導体が、DPAn-6のモノヒドロキシ生成物のRエピマー、DPAn-6のモノヒドロキシ生成物のSエピマー、DPAn-3のモノヒドロキシ生成物のRエピマー、DPAn-3のモノヒドロキシ生成物のSエピマー、DPAn-6のジヒドロキシ生成物のRエピマー、DPAn-6のジヒドロキシ生成物のSエピマー、DPAn-3のジヒドロキシ生成物のRエピマー、DPAn-3のジヒドロキシ生成物のSエピマー、DPAn-6のトリヒドロキシ生成物のRエピマー、DPAn-6のトリヒドロキシ生成物のSエピマー、DPAn-3のトリヒドロキシ生成物のRエピマー、およびDPAn-3のトリヒドロキシ生成物のSエピマーからなる群より選択される、請求項43記載の方法。
- オキシリピン誘導体が、7-ヒドロキシDPAn-6;8-ヒドロキシDPAn-6;10-ヒドロキシDPAn-6;11-ヒドロキシDPAn-6;13-ヒドロキシDPAn-6;14-ヒドロキシDPAn-6;17-ヒドロキシDPAn-6;7,17-ジヒドロキシDPAn-6;10,17-ジヒドロキシDPAn-6;13,17-ジヒドロキシDPAn-6;7,14-ジヒドロキシDPAn-6;8,14-ジヒドロキシDPAn-6;16,17-ジヒドロキシDPAn-6;4,5-ジヒドロキシDPAn-6;7,16,17-トリヒドロキシDPAn-6;および4,5,17-トリヒドロキシDPAn-6からなる群より選択されるドコサノイドのRもしくはSエピマー;またはその類似体、誘導体、もしくは塩である、請求項43記載の方法。
- オキシリピン誘導体が、7-ヒドロキシDPAn-3;10-ヒドロキシDPAn-3;11-ヒドロキシDPAn-3;13-ヒドロキシDPAn-3;14-ヒドロキシDPAn-3;16-ヒドロキシDPAn-3;17-ヒドロキシDPAn-3;7,17-ジヒドロキシDPAn-3;10,17-ジヒドロキシDPAn-3;8,14-ジヒドロキシDPAn-3;16,17-ジヒドロキシDPAn-3;13,20-ジヒドロキシDPAn-3;10,20-ジヒドロキシDPAn-3;および7,16,17-トリヒドロキシDPAn-3からなる群より選択されるドコサノイドのRもしくはSエピマー;またはその類似体、誘導体、もしくは塩である、請求項43記載の方法。
- 薬剤が、17-ヒドロキシDPAn-6および10,17-ジヒドロキシDPAn-6、またはそれらの誘導体もしくは類似体からなる群より選択される、請求項43記載の方法。
- 薬剤が、17-ヒドロキシDPAn-6、またはその誘導体もしくは類似体である、請求項43記載の方法。
- 薬剤が、10,17-ジヒドロキシDPAn-6、またはその誘導体もしくは類似体である、請求項43記載の方法。
- 薬剤がDPAn-6である、請求項43記載の方法。
- 薬剤がDPAn-3である、請求項43記載の方法。
- 個体にアスピリンを投与する段階をさらに含む、請求項43〜61のいずれか一項記載の方法。
- スタチン、非ステロイド性抗炎症薬、抗酸化剤、および神経保護薬からなる群より選択される少なくとも1つの薬剤を投与する段階をさらに含む、請求項43〜61のいずれか一項記載の方法。
- 請求項1〜10のいずれか一項記載のドコサノイドを化学合成する段階を含む、ドコサノイドを産生する方法。
- DPAn-6基質、DTAn-6基質、またはDPAn-3基質を該DPAn-6基質、該DTAn-6基質、または該DPAn-3基質からのドコサノイドの産生を触媒する酵素と接触させることにより、ドコサノイドを触媒的に産生する段階を含む、ドコサノイドを産生する方法。
- ドコサノイドを産生させるために、22炭素長鎖多価不飽和脂肪酸(LCPUFA)からのドコサノイドの産生を触媒する酵素を過剰発現するように遺伝子改変された長鎖多価不飽和脂肪酸(LCPUFA)産生微生物を培養するか、またはそのように遺伝子改変されたLCPUFA産生植物を栽培する段階を含む、ドコサノイドを産生する方法。
- 長鎖多価不飽和脂肪酸(LCPUFA)産生微生物、LCPUFA産生植物、またはLCPUFA産生動物によって産生される長鎖多価不飽和脂肪酸(LCPUFA)を、該LCPUFAのドコサノイドへの変換を触媒する酵素と接触させる段階を含む、ドコサノイドを産生する方法。
- 酵素が、リポキシゲナーゼ、シクロオキシゲナーゼ、およびシトクロムP450酵素からなる群より選択される、請求項65〜67のいずれか一項記載の方法。
- 酵素が、12-リポキシゲナーゼ、5-リポキシゲナーゼ、15-リポキシゲナーゼ、シクロオキシゲナーゼ-2、ヘモグロビンα1、ヘモグロビンβ、ヘモグロビンγA、CYP4A11、CYP4B1、CYP4F11、CYP4F12、CYP4F2、CYP4F3、CYP4F8、CYP4V2、CYP4X1、CYP41、CYP2J2、CYP2C8、トロンボキサンA合成酵素1、プロスタグランジンI2合成酵素、およびプロスタサイクリン合成酵素からなる群より選択される、請求項65〜67のいずれか一項記載の方法。
- LCPUFAがDPAn-6、DTAn-6、およびDPAn-3からなる群より選択される、請求項66または67記載の方法。
- LCPUFA産生微生物またはLCPUFA産生植物が、LCPUFAを産生するように遺伝子改変されている、請求項66または67記載の方法。
- LCPUFA産生微生物がLCPUFAを内因的に産生する、請求項66または67記載の方法。
- LCPUFA産生微生物がトラウスキトリド(Thraustochytrid)である、請求項72記載の方法。
- LCPUFA由来の少なくとも1つのオキシリピンの存在に関して油を強化するか、または油中の該オキシリピンを安定化する方法であって、LCPUFA産生微生物を、LCPUFAのオキシリピンへの変換を触媒する酵素の酵素活性を増強する化合物と共に培養する段階を含む方法。
- 化合物が酵素の発現を促進する、請求項74記載の方法。
- 化合物がLCPUFAの自動酸化を増強または惹起する、請求項74記載の方法。
- 化合物がアセトサリチル酸(acetosalicylic acid)である、請求項74記載の方法。
- LCPUFAのオキシリピンへの変換を触媒する酵素の存在下で、細菌または植物油糧種子を破裂させる段階であって、細菌および植物油糧種子は少なくとも1つのLCPUFAを産生する段階を含む、LCPUFA由来の少なくとも1つのオキシリピンの存在に関して油を強化するか、または油中の該オキシリピンを安定化する方法。
- 酵素が、リポキシゲナーゼ、シクロオキシゲナーゼ、およびシトクロムP450酵素からなる群より選択される、請求項78記載の方法。
- オキシリピンを回収および精製する段階をさらに含む、請求項74〜79のいずれか一項記載の方法。
- オキシリピンがさらに処理され、オキシリピンの誘導体またはその塩として回収される、請求項80記載の方法。
- 以下の段階を含む、LCPUFAのオキシリピン誘導体を含有する油を処理する方法:
a) 細菌、植物、または動物源によって産生されたLCPUFAのオキシリピン誘導体を含有する油を回収する段階;および
b) LCPUFAのオキシリピン誘導体を保持する油を産生するために、油からの遊離脂肪酸の除去を最小限に抑える工程を用いて油を純化する段階。 - 動物が水生動物である、請求項82記載の方法。
- 動物が魚である、請求項82記載の方法。
- 植物が油糧種子植物である、請求項82記載の方法。
- 細菌源がトラウスキトリドである、請求項82記載の方法。
- 純化段階がアルコール、アルコール:水混合液、または有機溶媒による油の抽出を含む、請求項82〜86のいずれか一項記載の方法。
- 純化段階が非極性有機溶媒による油の抽出を含む、請求項82〜86のいずれか一項記載の方法。
- 純化段階がアルコールまたはアルコール:水混合液による油の抽出を含む、請求項82〜86のいずれか一項記載の方法。
- 純化段階が、油を冷却濾過する段階、漂白する段階、さらに冷却濾過する段階、および脱臭する段階をさらに含む、請求項82〜89のいずれか一項記載の方法。
- 純化段階が、冷却濾過段階なしで、油を漂白する段階および脱臭する段階をさらに含む、請求項82〜89のいずれか一項記載の方法。
- 純化段階が、冷却濾過段階も漂白段階もなしで、油を脱臭する段階をさらに含む、請求項82〜89のいずれか一項記載の方法。
- 抗酸化剤を油に添加する段階をさらに含む、請求項82〜86のいずれか一項記載の方法。
- 純化段階が油を乳濁液として調製する段階を含む、請求項82〜86のいずれか一項記載の方法。
- 油が、LCPUFAのオキシリピンへの変換を触媒する酵素と接触させることによりさらに処理される、請求項82〜89のいずれか一項記載の方法。
- 酵素が、リポキシゲナーゼ、シクロオキシゲナーゼ、およびシトクロムP450酵素からなる群より選択される、請求項95記載の方法。
- 酵素が基体上に固定化されている、請求項95記載の方法。
- 油中のLCPUFAからLCPUFAオキシリピン誘導体を分離する段階をさらに含む、請求項82〜97のいずれか一項記載の方法。
- 分離段階がクロマトグラフィーによる、請求項98記載の方法。
- 分離されたLCPUFAオキシリピンを油または組成物に添加する段階をさらに含む、請求項98記載の方法。
- 以下の段階を含む、LCPUFAのオキシリピン誘導体を含有する油を処理する方法:
a) 細菌、植物、または動物源によって産生されたLCPUFAのオキシリピン誘導体を含有する油を回収する段階;
b) 油を純化する段階;および
c) 油中のLCPUFAからLCPUFAオキシリピンを分離する段階。 - 段階(c)の前に、化学的または生物学的工程により油中のLCPUFAをLCPUFAオキシリピンに変換する段階をさらに含む、請求項101記載の方法。
- 分離されたLCPUFAオキシリピンを生成物に添加する段階をさらに含む、請求項101または102記載の方法。
- 個体における炎症または神経変性の少なくとも1つの症状を予防または軽減する方法であって、個体における炎症または神経変性の少なくとも1つの症状を軽減するために、炎症もしくは神経変性またはそれらに関連する状態もしくは疾患を有するリスクがある、それらを有すると診断された、またはそれらを有すると疑われる患者に、DTAn-6およびDTAn-6のオキシリピン誘導体からなる群より選択される薬剤を投与する段階を含む、方法。
- 薬剤が、DTAn-6のモノヒドロキシ誘導体、DTAn-6のジヒドロキシ誘導体、およびDTAn-6のトリヒドロキシ誘導体からなる群より選択されるドコサノイドのRまたはSエピマーである、請求項104記載の方法。
- 薬剤が、7-ヒドロキシDTAn-6;10-ヒドロキシDTAn-6;13-ヒドロキシDTAn-6;17-ヒドロキシDTAn-6;7,17-ジヒドロキシDTAn-6;10,17-ジヒドロキシDTAn-6;16,17-ジヒドロキシDTAn-6;および7,16,17-トリヒドロキシDTAn-6からなる群より選択されるドコサノイドのRもしくはSエピマー;またはその類似体、誘導体、もしくは塩である、請求項104記載の方法。
- LCPUFAをオキシリピンに変換する酵素を発現するように遺伝的に形質転換された、PUFA PKS経路を含む生物。
- 植物および微生物からなる群より選択される、請求項107記載の生物。
- PUFA PKS経路を発現して長鎖多価不飽和脂肪酸を産生するように遺伝子改変された油糧種子植物である、請求項107記載の生物。
- 微生物である、請求項107記載の生物。
- 微生物が内因性PUFA PKS経路を含む、請求項110記載の生物。
- 酵素が、リポキシゲナーゼ、シクロオキシゲナーゼ、およびシトクロムP450酵素からなる群より選択される、請求項107記載の生物。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US62984204P | 2004-11-19 | 2004-11-19 | |
| US72903805P | 2005-10-21 | 2005-10-21 | |
| PCT/US2005/042462 WO2006055965A2 (en) | 2004-11-19 | 2005-11-21 | Oxylipins from long chain polyunsaturated fatty acids and methods of making and using the same |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2008520739A true JP2008520739A (ja) | 2008-06-19 |
| JP2008520739A5 JP2008520739A5 (ja) | 2009-01-15 |
Family
ID=36407879
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2007543444A Pending JP2008520739A (ja) | 2004-11-19 | 2005-11-21 | 長鎖多価不飽和脂肪酸由来のオキシリピンならびにその作製および使用方法 |
Country Status (13)
| Country | Link |
|---|---|
| US (2) | US7884131B2 (ja) |
| EP (1) | EP1824809A4 (ja) |
| JP (1) | JP2008520739A (ja) |
| KR (1) | KR20070090928A (ja) |
| CN (1) | CN101102988B (ja) |
| AU (1) | AU2005306320B2 (ja) |
| BR (1) | BRPI0516803A (ja) |
| CA (1) | CA2588166A1 (ja) |
| EA (1) | EA010802B1 (ja) |
| IL (1) | IL183246A0 (ja) |
| MX (1) | MX2007006049A (ja) |
| NZ (1) | NZ555394A (ja) |
| WO (1) | WO2006055965A2 (ja) |
Cited By (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2012026106A1 (ja) * | 2010-08-25 | 2012-03-01 | 国立大学法人 東京大学 | 光学活性な新規抗炎症性化合物及びその製造方法 |
| JP2013500966A (ja) * | 2009-07-31 | 2013-01-10 | ユニバーシティー オブ ピッツバーグ − オブ ザ コモンウェルス システム オブ ハイヤー エデュケーション | 抗炎症剤としての脂肪酸 |
| JP2015522535A (ja) * | 2012-05-10 | 2015-08-06 | ソルテックス エヌエー エルエルシー | 天然の特異的炎症収束性メディエータおよびその前駆物質を含有する、抗炎症活性を有する油 |
| JP2016505016A (ja) * | 2013-01-11 | 2016-02-18 | マサチューセッツ アイ アンド イヤー インファーマリー | 炎症及び血管形成を減少させるcyp450脂質メタボライト |
| JP2016520612A (ja) * | 2013-05-30 | 2016-07-14 | ザ ブリガム アンド ウィメンズ ホスピタル インコーポレイテッドThe Brigham and Women’s Hospital, Inc. | 新規n−3イムノリソルベント:構造及び作用 |
| JP2018506584A (ja) * | 2015-02-09 | 2018-03-08 | ボード オブ スーパーバイザーズ オブ ルイジアナ ステート ユニバーシティ アンド アグリカルチュアル アンド メカニカル カレッジ | 炎症性、変性及び神経変性疾患の治療のための化合物、組成物及び方法 |
| US10537541B2 (en) | 2015-10-02 | 2020-01-21 | Complexa Inc. | Treatment of focal segmental glomerular sclerosis (FSGS) using therapeutically effective oral doses of 10-nitro-9(E)-octadec-9-enoic acid |
| US11608342B2 (en) | 2015-07-07 | 2023-03-21 | H. Lundbeck A/S | PDE9 inhibitors with imidazo triazinone backbone and imidazo pyrazinone backbone for treatment of peripheral diseases |
Families Citing this family (53)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20090318394A1 (en) * | 2004-11-19 | 2009-12-24 | Julie Nauroth | Long Chain Polyunsaturated Fatty Acids and Methods of Making and Using the Same |
| US7893106B2 (en) * | 2004-11-19 | 2011-02-22 | Martek Biosciences, Corporation | Oxylipins from stearidonic acid and γ-linolenic acid and methods of making and using the same |
| KR20130101596A (ko) * | 2005-07-08 | 2013-09-13 | 마텍 바이오싸이언스스 코포레이션 | 치매 및 치매-전단계와 관련된 용태의 치료를 위한 다중불포화 지방산 |
| WO2007041440A2 (en) * | 2005-10-03 | 2007-04-12 | The Brigham And Women's Hospital, Inc. | Anti-inflammatory actions of neuroprotectin d1/protectin d1 and its natural stereoisomers |
| EP1983977A4 (en) * | 2006-01-31 | 2011-11-30 | Martek Biosciences Corp | OXYLIPINES FROM STEARIDONIC ACID AND GAMMA-LINOLIC ACID AND METHOD FOR THE PRODUCTION AND USE THEREOF |
| GB0604647D0 (en) | 2006-03-08 | 2006-04-19 | Shchepinov Mikhail | Stabilized food supplements and their derivatives |
| WO2007127377A2 (en) * | 2006-04-28 | 2007-11-08 | Resolvyx Pharmaceuticals, Inc. | Combinations comprising omega-3 fatty acid compounds for the treatment of cardiovascular disease |
| US20100035989A1 (en) * | 2006-07-19 | 2010-02-11 | Resolvyx Pharmaceuticals, Inc. | Compositions and methods for the treatment of mucositis |
| EP2131833A2 (en) * | 2006-10-26 | 2009-12-16 | Resolvyx Pharmaceuticals, Inc. | Use of resolvins for inhibition of bone loss |
| US20080161275A1 (en) * | 2006-12-05 | 2008-07-03 | Resolvyx Pharmaceuticals, Inc. | Compositions and methods for the treatment of inflammatory disease |
| WO2008103753A2 (en) * | 2007-02-20 | 2008-08-28 | Martek Biosciences Corporation | Oxylipins from long chain polyunsaturated fatty acids and methods of making and using the same |
| NZ579852A (en) * | 2007-03-23 | 2012-03-30 | Novartis Ag | Use of a masked or coated copper salt for the treatment of macular degeneration |
| US20100159540A1 (en) * | 2007-03-26 | 2010-06-24 | Ana Rodriguez | Synthesis of resolvins and intermediates, compounds prepared thereby, and uses thereof |
| DK2180787T3 (da) | 2007-08-01 | 2014-02-03 | Univ Pittsburgh | Nitrooliesyremodulering af type ii-diabetes |
| AU2008301895A1 (en) * | 2007-09-14 | 2009-03-26 | Resolvyx Pharmaceuticals, Inc. | Oxylipin compounds for treating autoimmune diseases |
| CA2702475A1 (en) * | 2007-10-12 | 2009-04-23 | Resolvyx Pharmaceuticals, Inc. | Compositions and methods for the treatment of ophthalmic conditions |
| WO2009086281A1 (en) * | 2007-12-21 | 2009-07-09 | Martek Biosciences Corporation | Method for preparation of oxylipins |
| CN102083787A (zh) | 2008-05-01 | 2011-06-01 | 康普雷克萨公司 | 乙烯基取代的脂肪酸 |
| US20140024713A1 (en) | 2008-06-19 | 2014-01-23 | University Of Utah Research Foundation | Use of nitrated lipids for treatment of side effects of toxic medical therapies |
| EP2299997A4 (en) | 2008-06-19 | 2012-01-11 | Univ Utah Res Found | USE OF NITRATED LIPIDS FOR THE TREATMENT OF SIDE EFFECTS OF TOXIC MEDICAL THERAPIES |
| ES2792676T3 (es) * | 2008-09-16 | 2020-11-11 | Brigham & Womens Hospital Inc | Compuestos del ácido 14-hidroxi-docosahexaenoico |
| PT2349250T (pt) * | 2008-10-31 | 2017-07-25 | Lipid Pharmaceuticals Ehf | Ácidos gordos para uso como um medicamento |
| US8853437B2 (en) | 2009-02-20 | 2014-10-07 | The University Of Tokyo | Anti-inflammatory compounds |
| ES2345241B1 (es) | 2009-03-16 | 2011-09-08 | Lipopharma Therapeutics | Uso de 2-hidroxiderivados de acidos grasos poliinsaturados como medicamentos. |
| KR101759353B1 (ko) * | 2009-04-17 | 2017-07-18 | 나타크 파마 에스.엘 | 오메가-3 지방산이 풍부하고 피탄산 함량이 적은 조성물 |
| USRE46608E1 (en) | 2009-09-01 | 2017-11-14 | Catabasis Pharmaceuticals, Inc. | Fatty acid niacin conjugates and their uses |
| DK2473045T3 (en) | 2009-09-01 | 2016-12-12 | Catabasis Pharmaceuticals Inc | Niacin-FATTY ACID CONJUGATES AND THEIR USES |
| CA2781276A1 (en) | 2009-10-02 | 2011-04-07 | Complexa, Inc. | Heteroatom containing substituted fatty acids |
| WO2011053870A1 (en) | 2009-10-30 | 2011-05-05 | Retrotope, Inc. | Alleviating oxidative stress disorders with pufa derivatives |
| JP5909183B2 (ja) * | 2010-08-19 | 2016-04-26 | 国立大学法人 東京大学 | オメガ3系脂肪酸由来の新規抗炎症性代謝物 |
| US11712429B2 (en) | 2010-11-29 | 2023-08-01 | Amarin Pharmaceuticals Ireland Limited | Low eructation composition and methods for treating and/or preventing cardiovascular disease in a subject with fish allergy/hypersensitivity |
| NZ611606A (en) | 2010-11-29 | 2015-10-30 | Amarin Pharmaceuticals Ie Ltd | Low eructation composition and methods for treating and/or preventing cardiovascular disease in a subject with fish allergy/hypersensitivity |
| AU2012249920B2 (en) | 2011-04-26 | 2017-06-15 | Biojiva Llc | Disorders implicating PUFA oxidation |
| KR102014524B1 (ko) | 2011-04-26 | 2019-08-26 | 레트로토프 인코포레이티드 | 산화성 망막 질환 |
| JP6093756B2 (ja) | 2011-04-26 | 2017-03-08 | レトロトップ、 インコーポレイテッドRetrotope, Inc. | 損なわれたエネルギー処理障害およびミトコンドリア欠損症 |
| EP2701695B1 (en) | 2011-04-26 | 2019-04-03 | Retrotope, Inc. | Neurodegenerative disorders and muscle diseases implicating pufas |
| US9416118B2 (en) | 2011-06-10 | 2016-08-16 | The Brigham And Women's Hospital, Inc. | Docosahexaenoyl ethanolamides |
| EP2744491B1 (en) | 2011-08-19 | 2020-07-29 | The University of Utah Research Foundation | Combination therapy with nitrated lipids and inhibitors of the renin-angiotensin-aldosterone system |
| US10322118B2 (en) * | 2012-04-10 | 2019-06-18 | Trustees Of Dartmouth College | Compounds and methods for inhibiting Cif virulence factor |
| EP2861227A4 (en) | 2012-06-17 | 2016-01-27 | Matinas Biopharma Inc | OMEGA-3 PENTAIC ACID COMPOSITIONS AND METHODS OF USE |
| DK2887923T3 (da) | 2012-08-24 | 2023-07-03 | Sun Pharmaceutical Ind Ltd | Oftalmisk opløsning af polyoxyllipid eller polyoxylfedtsyre og behandling af øjentilstande |
| WO2014130894A1 (en) * | 2013-02-21 | 2014-08-28 | University Of Southern California | Compositions for the treatment of inflammatory diseases |
| EP2968246A4 (en) * | 2013-03-13 | 2016-08-03 | Matinas Biopharma Inc | OMEGA 3 PENTANOIC ACID COMPOSITIONS AND METHODS OF USE |
| WO2017015271A1 (en) | 2015-07-20 | 2017-01-26 | The Brigham And Women's Hospital, Inc. | Elucidation of novel 13-series resolvins that increase with atorvastatin and clear infections |
| WO2017041094A1 (en) | 2015-09-03 | 2017-03-09 | Solutex Na Llc | Compositions comprising omega-3 fatty acids, 17-hdha and 18- hepe and methods of using same |
| EP3373976B1 (en) | 2015-11-10 | 2024-01-03 | Sun Pharmaceutical Industries Limited | Topical formulations and uses thereof |
| ES2871130T3 (es) | 2015-11-23 | 2021-10-28 | Retrotope Inc | Marcado isotópico específico del sitio de sistemas de 1, 4-dieno |
| WO2019104311A1 (en) * | 2017-11-27 | 2019-05-31 | Brown University | Compositions and methods for suppressing neurological disease |
| WO2019104315A1 (en) * | 2017-11-27 | 2019-05-31 | Brown University | Compositions and methods using lipids for treating neurological disease |
| CN111989399A (zh) * | 2018-04-16 | 2020-11-24 | 韩国生命工学研究院 | 多不饱和脂肪酸的多羟基衍生物的制备方法 |
| JP7020756B2 (ja) | 2018-09-24 | 2022-02-16 | アマリン ファーマシューティカルズ アイルランド リミテッド | 対象の心血管イベントのリスクを低減する方法 |
| KR20200042285A (ko) * | 2018-10-15 | 2020-04-23 | (주)아모레퍼시픽 | 피부장벽 강화용 조성물 |
| US11779910B2 (en) | 2020-02-21 | 2023-10-10 | Biojiva Llc | Processes for isotopic modification of polyunsaturated fatty acids and derivatives thereof |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS63238075A (ja) * | 1987-03-24 | 1988-10-04 | Mitsumaru Kagaku Kk | 高度不飽和脂肪酸からのラクトン類の製造法 |
| JPH05286956A (ja) * | 1992-04-06 | 1993-11-02 | Nippon Suisan Kaisha Ltd | ドコサペンタエン酸モノエポキシ体、及びその製造法 |
| JPH11209259A (ja) * | 1998-01-20 | 1999-08-03 | Noevir Co Ltd | 皮膚化粧料 |
| WO2002092540A1 (en) * | 2001-05-14 | 2002-11-21 | Martek Biosciences Corporation | Production and use of a polar lipid-rich fraction containing omega-3 and/or omega-6 highly unsatruated fatty acids from microbes, genetically modified plant seeds and marine organisms |
| JP2003525880A (ja) * | 2000-02-16 | 2003-09-02 | ザ・ブリガーム・アンド・ウーメンズ・ホスピタル・インコーポレーテッド | アスピリン誘発脂質メディエータ |
Family Cites Families (22)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4866046A (en) * | 1988-05-31 | 1989-09-12 | Top Laboratories, Inc. | Low-dosage sublingual aspirin |
| US5102670A (en) * | 1990-09-14 | 1992-04-07 | Abraham Nader G | Method for treating eye disorders by reducing 12(r)-hydroxyeicosatetraenoic acid and 12(r)-dihydroxyeicosatrienoic acid levels |
| US6887901B1 (en) * | 1993-06-15 | 2005-05-03 | Brigham & Women's Hospital, Inc. | Lipoxin compounds and their use in treating cell proliferative disorders |
| GB9403857D0 (en) * | 1994-03-01 | 1994-04-20 | Scotia Holdings Plc | Fatty acid derivatives |
| CZ281096B6 (cs) * | 1994-06-30 | 1996-06-12 | Jindřich Mudr. Drsc. Mourek | Tuková složka mléčné výživy a dětská výživa |
| US5955496A (en) * | 1996-08-13 | 1999-09-21 | The Regents Of The University Of California | Dihydroxy-oxy-eicosadienoates |
| CN1109543C (zh) * | 1996-10-11 | 2003-05-28 | 斯卡里斯塔有限公司 | 包括二十碳五烯酸和/或十八碳四烯酸的药物制剂 |
| US6174695B1 (en) * | 1997-08-12 | 2001-01-16 | The Regents Of The University Of California | Epoxide hydrolase inhibitor methods |
| DE19757414A1 (de) * | 1997-12-23 | 1999-07-01 | Nutricia Nv | Fettmischung |
| WO2000051444A1 (fr) * | 1999-03-04 | 2000-09-08 | Suntory Limited | Utilisation d'une matiere contenant de l'acide docosapentaenoique |
| AU5850000A (en) * | 1999-07-07 | 2001-01-30 | Kyowa Hakko Kogyo Co. Ltd. | Process for producing hydroxylated fatty acid and delta-lactone |
| CA2386636A1 (en) | 1999-11-09 | 2001-05-17 | Alcon, Inc. | 15-hydroxyeicosatetraenoic acid-related compounds and methods of use |
| DE10046541A1 (de) * | 2000-09-19 | 2002-03-28 | Knoll Ag | Mechanisch stabile darreichungsformen, enthaltend Ubichinone |
| WO2002029018A2 (en) * | 2000-10-06 | 2002-04-11 | Michigan State University | Divinyl ether synthase gene and protein, and uses thereof |
| US7030159B2 (en) * | 2001-12-18 | 2006-04-18 | The Brigham And Women's Hospital, Inc. | Approach to anti-microbial host defense with molecular shields with EPA and DHA analogs |
| US7527935B2 (en) * | 2002-03-19 | 2009-05-05 | Mitsubishi Tanabe Pharma Corporation | G-protein coupled receptor having eicosanoid as ligand and gene thereof |
| US7582785B2 (en) * | 2002-04-01 | 2009-09-01 | University Of Southern California | Trihydroxy polyunsaturated eicosanoid derivatives |
| AU2003260687A1 (en) * | 2002-04-01 | 2003-10-20 | University Of Southern California | Trihydroxy polyunsaturated eicosanoids |
| FR2843124B1 (fr) * | 2002-08-02 | 2004-10-15 | Goemar Lab Sa | Procede de preparation d'acides gras polyinsatures libres et de leurs metabolites d'oxydation |
| EP3584235A3 (en) * | 2002-08-12 | 2020-04-22 | Brigham and Women's Hospital | Resolvins: biotemplates for novel therapeutic interventions |
| US20040166130A1 (en) * | 2002-12-23 | 2004-08-26 | L'oreal | Lanolin-free cosmetic composition comprising a hydroxylated fatty acid aromatic ester |
| US7893106B2 (en) * | 2004-11-19 | 2011-02-22 | Martek Biosciences, Corporation | Oxylipins from stearidonic acid and γ-linolenic acid and methods of making and using the same |
-
2005
- 2005-11-21 BR BRPI0516803-1A patent/BRPI0516803A/pt not_active IP Right Cessation
- 2005-11-21 EP EP05846821A patent/EP1824809A4/en not_active Withdrawn
- 2005-11-21 CA CA002588166A patent/CA2588166A1/en not_active Abandoned
- 2005-11-21 NZ NZ555394A patent/NZ555394A/en not_active IP Right Cessation
- 2005-11-21 EA EA200701100A patent/EA010802B1/ru not_active IP Right Cessation
- 2005-11-21 JP JP2007543444A patent/JP2008520739A/ja active Pending
- 2005-11-21 MX MX2007006049A patent/MX2007006049A/es active IP Right Grant
- 2005-11-21 AU AU2005306320A patent/AU2005306320B2/en not_active Ceased
- 2005-11-21 WO PCT/US2005/042462 patent/WO2006055965A2/en active Application Filing
- 2005-11-21 KR KR1020077013738A patent/KR20070090928A/ko not_active Application Discontinuation
- 2005-11-21 US US11/284,790 patent/US7884131B2/en not_active Expired - Fee Related
- 2005-11-21 CN CN2005800468877A patent/CN101102988B/zh not_active Expired - Fee Related
-
2007
- 2007-05-15 IL IL183246A patent/IL183246A0/en unknown
-
2010
- 2010-12-29 US US12/981,261 patent/US20110178047A1/en not_active Abandoned
Patent Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS63238075A (ja) * | 1987-03-24 | 1988-10-04 | Mitsumaru Kagaku Kk | 高度不飽和脂肪酸からのラクトン類の製造法 |
| JPH05286956A (ja) * | 1992-04-06 | 1993-11-02 | Nippon Suisan Kaisha Ltd | ドコサペンタエン酸モノエポキシ体、及びその製造法 |
| JPH11209259A (ja) * | 1998-01-20 | 1999-08-03 | Noevir Co Ltd | 皮膚化粧料 |
| JP2003525880A (ja) * | 2000-02-16 | 2003-09-02 | ザ・ブリガーム・アンド・ウーメンズ・ホスピタル・インコーポレーテッド | アスピリン誘発脂質メディエータ |
| WO2002092540A1 (en) * | 2001-05-14 | 2002-11-21 | Martek Biosciences Corporation | Production and use of a polar lipid-rich fraction containing omega-3 and/or omega-6 highly unsatruated fatty acids from microbes, genetically modified plant seeds and marine organisms |
| JP2004536059A (ja) * | 2001-05-14 | 2004-12-02 | マーテック バイオサイエンシズ ボールダー コーポレーション | 微生物、遺伝的に改変された植物種子および海洋生物由来のω−3および/またはω−6高度不飽和脂肪酸を含有する極性脂質の豊富な画分の生成および使用 |
Non-Patent Citations (7)
| Title |
|---|
| JPN6011060206; MILKS,M.M. and SPRECHER,H.: 'Metabolism of 4,7,10,13,16-docosapentaenoic acid by human platelet cyclooxygenase and lipoxygenase' Biochimica et Biophysica Acta, Lipids and Lipid Metabolism Vol.835, No.1, 1985, p.29-35 * |
| JPN6011060209; SPRECHER,H. and CAREAGA,M.M.: 'Metabolism of (n-6) and (n-3) polyunsaturated fatty acids by human platelets' Prostaglandins, Leukotrienes and Medicine Vol.23, No.2-3, 1986, p.129-134 * |
| JPN6011060211; OLIW,E.H. and SPRECHER,H.: 'Metabolism of polyunsaturated fatty acids by an (n-6)-lipoxygenase associated with human ejaculates' Biochimica et Biophysica Acta, Lipids and Lipid Metabolism Vol.1002, No.3, 1989, p.283-291 * |
| JPN6011060212; GUERRIERO,A. et al.: 'Hydroxyeicosatetraenoic, hydroxyeicosapentaenoic, hydroxydocosapentaenoic, and hydroxydocosahexaenoi' Journal of Natural Products Vol.53, No.1, 1990, p.57-61 * |
| JPN6011060213; KARANIAN,J.W. et al.: 'Inhibitory effects of n-6 and n-3 hydroxy fatty acids on thromboxane (U46619)-induced smooth muscle' Journal of Pharmacology and Experimental Therapeutics Vol.270, No.3, 1994, p.1105-1109 * |
| JPN6011060215; HAVIV,F. et al.: 'Structural requirements for the inhibition of 5-lipoxygenase by 15-hydroxyeicosa-5,8,11,13-tetraenoi' Journal of Medicinal Chemistry Vol.30, No.2, 1987, p.254-263 * |
| JPN6011060216; MANCINI,I. et al.: 'Novel 10-hydroxydocosapolyenoic acids from deep-water scleractinian corals' Helvetica Chimica Acta Vol.82, No.5, 1999, p.677-684 * |
Cited By (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2017114897A (ja) * | 2009-07-31 | 2017-06-29 | ユニバーシティー オブ ピッツバーグ − オブ ザ コモンウェルス システム オブ ハイヤー エデュケーション | 抗炎症剤としての脂肪酸 |
| JP2013500966A (ja) * | 2009-07-31 | 2013-01-10 | ユニバーシティー オブ ピッツバーグ − オブ ザ コモンウェルス システム オブ ハイヤー エデュケーション | 抗炎症剤としての脂肪酸 |
| JPWO2012026106A1 (ja) * | 2010-08-25 | 2013-10-28 | 国立大学法人 東京大学 | 光学活性な新規抗炎症性化合物及びその製造方法 |
| WO2012026106A1 (ja) * | 2010-08-25 | 2012-03-01 | 国立大学法人 東京大学 | 光学活性な新規抗炎症性化合物及びその製造方法 |
| JP2015522535A (ja) * | 2012-05-10 | 2015-08-06 | ソルテックス エヌエー エルエルシー | 天然の特異的炎症収束性メディエータおよびその前駆物質を含有する、抗炎症活性を有する油 |
| JP2018193378A (ja) * | 2012-05-10 | 2018-12-06 | ソルテックス エヌエー エルエルシー | 天然の特異的炎症収束性メディエータおよびその前駆物質を含有する、抗炎症活性を有する油 |
| JP2016505016A (ja) * | 2013-01-11 | 2016-02-18 | マサチューセッツ アイ アンド イヤー インファーマリー | 炎症及び血管形成を減少させるcyp450脂質メタボライト |
| JP2016520612A (ja) * | 2013-05-30 | 2016-07-14 | ザ ブリガム アンド ウィメンズ ホスピタル インコーポレイテッドThe Brigham and Women’s Hospital, Inc. | 新規n−3イムノリソルベント:構造及び作用 |
| JP2019163265A (ja) * | 2013-05-30 | 2019-09-26 | ザ ブリガム アンド ウィメンズ ホスピタル インコーポレイテッドThe Brigham and Women’s Hospital, Inc. | 新規n−3イムノリソルベント:構造及び作用 |
| US11667598B2 (en) | 2013-05-30 | 2023-06-06 | The Brigham & Women's Hospital Inc. | N-3 immunoresolvents: structures and actions |
| JP2018506584A (ja) * | 2015-02-09 | 2018-03-08 | ボード オブ スーパーバイザーズ オブ ルイジアナ ステート ユニバーシティ アンド アグリカルチュアル アンド メカニカル カレッジ | 炎症性、変性及び神経変性疾患の治療のための化合物、組成物及び方法 |
| JP7025212B2 (ja) | 2015-02-09 | 2022-02-24 | ボード オブ スーパーバイザーズ オブ ルイジアナ ステート ユニバーシティ アンド アグリカルチュアル アンド メカニカル カレッジ | 炎症性、変性及び神経変性疾患の治療のための化合物、組成物及び方法 |
| US11608342B2 (en) | 2015-07-07 | 2023-03-21 | H. Lundbeck A/S | PDE9 inhibitors with imidazo triazinone backbone and imidazo pyrazinone backbone for treatment of peripheral diseases |
| US10537541B2 (en) | 2015-10-02 | 2020-01-21 | Complexa Inc. | Treatment of focal segmental glomerular sclerosis (FSGS) using therapeutically effective oral doses of 10-nitro-9(E)-octadec-9-enoic acid |
Also Published As
| Publication number | Publication date |
|---|---|
| CN101102988B (zh) | 2011-12-14 |
| EP1824809A2 (en) | 2007-08-29 |
| AU2005306320B2 (en) | 2011-09-08 |
| EP1824809A4 (en) | 2010-03-03 |
| CN101102988A (zh) | 2008-01-09 |
| US7884131B2 (en) | 2011-02-08 |
| WO2006055965A3 (en) | 2006-11-30 |
| KR20070090928A (ko) | 2007-09-06 |
| IL183246A0 (en) | 2007-08-19 |
| CA2588166A1 (en) | 2006-05-26 |
| EA010802B1 (ru) | 2008-12-30 |
| BRPI0516803A (pt) | 2008-09-23 |
| AU2005306320A1 (en) | 2006-05-26 |
| US20060241088A1 (en) | 2006-10-26 |
| MX2007006049A (es) | 2007-07-24 |
| NZ555394A (en) | 2010-07-30 |
| WO2006055965A2 (en) | 2006-05-26 |
| US20110178047A1 (en) | 2011-07-21 |
| EA200701100A1 (ru) | 2007-10-26 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2008520739A (ja) | 長鎖多価不飽和脂肪酸由来のオキシリピンならびにその作製および使用方法 | |
| JP2010519311A (ja) | 長鎖多価不飽和脂肪酸由来のオキシリピンならびにその作製およびその使用方法 | |
| US7893106B2 (en) | Oxylipins from stearidonic acid and γ-linolenic acid and methods of making and using the same | |
| US20090318394A1 (en) | Long Chain Polyunsaturated Fatty Acids and Methods of Making and Using the Same | |
| JP5973503B2 (ja) | アスピリン誘発脂質メディエータ | |
| JP2010519311A5 (ja) | ||
| AU2014358123B2 (en) | Dihomo-gamma-linolenic acid-containing microbial oil and dihomo-gamma-linolenic acid-containing microbial biomass | |
| BRPI0311916B1 (pt) | processo para a produção de um óleo microbiano compreendendo ácido araquidônico | |
| JP7242769B2 (ja) | 遊離多価不飽和脂肪酸含有組成物及びその製造方法 | |
| US20090320148A1 (en) | Oxylipins from stearidonic acid and gamma-linolenic acid and methods of making and using the same | |
| AU2011253846A1 (en) | Oxylipins from long chain polyunsaturated fatty acids and methods of making and using the same | |
| US20110027841A1 (en) | Method for preparation of oxylipins |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20081120 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20081120 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20111109 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20111116 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20120214 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20120221 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20121017 |