JP2008519070A - プロトンポンプ阻害剤用の新規な改変された放出の錠剤製剤 - Google Patents
プロトンポンプ阻害剤用の新規な改変された放出の錠剤製剤 Download PDFInfo
- Publication number
- JP2008519070A JP2008519070A JP2007540284A JP2007540284A JP2008519070A JP 2008519070 A JP2008519070 A JP 2008519070A JP 2007540284 A JP2007540284 A JP 2007540284A JP 2007540284 A JP2007540284 A JP 2007540284A JP 2008519070 A JP2008519070 A JP 2008519070A
- Authority
- JP
- Japan
- Prior art keywords
- layer
- tablet
- dosage form
- coating
- ppi
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 0 Cc1nc2c(C)c(*)c(*)c(*)c2[n]1 Chemical compound Cc1nc2c(C)c(*)c(*)c(*)c2[n]1 0.000 description 1
- JWWJICXMFDZFBP-UHFFFAOYSA-N Cc1nc2c[s]cc2[nH]1 Chemical compound Cc1nc2c[s]cc2[nH]1 JWWJICXMFDZFBP-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/28—Dragees; Coated pills or tablets, e.g. with film or compression coating
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/4427—Non condensed pyridines; Hydrogenated derivatives thereof containing further heterocyclic ring systems
- A61K31/4439—Non condensed pyridines; Hydrogenated derivatives thereof containing further heterocyclic ring systems containing a five-membered ring with nitrogen as a ring hetero atom, e.g. omeprazole
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/16—Agglomerates; Granulates; Microbeadlets ; Microspheres; Pellets; Solid products obtained by spray drying, spray freeze drying, spray congealing,(multiple) emulsion solvent evaporation or extraction
- A61K9/1605—Excipients; Inactive ingredients
- A61K9/1617—Organic compounds, e.g. phospholipids, fats
- A61K9/1623—Sugars or sugar alcohols, e.g. lactose; Derivatives thereof; Homeopathic globules
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/16—Agglomerates; Granulates; Microbeadlets ; Microspheres; Pellets; Solid products obtained by spray drying, spray freeze drying, spray congealing,(multiple) emulsion solvent evaporation or extraction
- A61K9/1605—Excipients; Inactive ingredients
- A61K9/1629—Organic macromolecular compounds
- A61K9/1652—Polysaccharides, e.g. alginate, cellulose derivatives; Cyclodextrin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/16—Agglomerates; Granulates; Microbeadlets ; Microspheres; Pellets; Solid products obtained by spray drying, spray freeze drying, spray congealing,(multiple) emulsion solvent evaporation or extraction
- A61K9/1682—Processes
- A61K9/1694—Processes resulting in granules or microspheres of the matrix type containing more than 5% of excipient
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2072—Pills, tablets, discs, rods characterised by shape, structure or size; Tablets with holes, special break lines or identification marks; Partially coated tablets; Disintegrating flat shaped forms
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2072—Pills, tablets, discs, rods characterised by shape, structure or size; Tablets with holes, special break lines or identification marks; Partially coated tablets; Disintegrating flat shaped forms
- A61K9/2086—Layered tablets, e.g. bilayer tablets; Tablets of the type inert core-active coat
- A61K9/209—Layered tablets, e.g. bilayer tablets; Tablets of the type inert core-active coat containing drug in at least two layers or in the core and in at least one outer layer
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/28—Dragees; Coated pills or tablets, e.g. with film or compression coating
- A61K9/2806—Coating materials
- A61K9/2813—Inorganic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/28—Dragees; Coated pills or tablets, e.g. with film or compression coating
- A61K9/2806—Coating materials
- A61K9/2833—Organic macromolecular compounds
- A61K9/284—Organic macromolecular compounds obtained by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyvinyl pyrrolidone
- A61K9/2846—Poly(meth)acrylates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/28—Dragees; Coated pills or tablets, e.g. with film or compression coating
- A61K9/2806—Coating materials
- A61K9/2833—Organic macromolecular compounds
- A61K9/286—Polysaccharides, e.g. gums; Cyclodextrin
- A61K9/2866—Cellulose; Cellulose derivatives, e.g. hydroxypropyl methylcellulose
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/4808—Preparations in capsules, e.g. of gelatin, of chocolate characterised by the form of the capsule or the structure of the filling; Capsules containing small tablets; Capsules with outer layer for immediate drug release
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/04—Drugs for disorders of the alimentary tract or the digestive system for ulcers, gastritis or reflux esophagitis, e.g. antacids, inhibitors of acid secretion, mucosal protectants
Abstract
【選択図】 図3
Description
Het1は
ベンゾイミダゾール部分におけるNは、R6〜R9で置換された環炭素原子のうちの1つが、置換基を有さない窒素原子と場合により交換されてもよいことを意味し;
R1、R2及びR3は、同じであるかまたは異なり、そして水素、アルキル、場合によりフッ素で置換されるアルコキシ、アルキルチオ、アルコキシアルコキシ、ジアルキルアミノ、ピペリジノ、モルホリノ、ハロゲン、フェニル及びフェニルアルコキシより選択され;
R4及びR5は、同じか又は異なり、そして水素、アルキル及びアリールアルキルより選択され;
R6’は、水素、ハロゲン、トリフルオロメチル、アルキル又はアルコキシであり;
R6〜R9は、同じか若しくは異なり、そして水素、アルキル、アルコキシ、ハロゲン、ハロ−アルコキシ、アルキルカルボニル、アルコキシカルボニル、オキサゾリニル、及びトリフルオロアルキルより選択されるか、又は隣接する基R6〜R9が、さらに置換され得る環構造を形成し;
R10は、水素であるか又はR3と共にアルキレン鎖を形成し、そして
R11及びR12は、同じか又は異なり、そして水素、ハロゲン又はアルキルより選択される]
の化合物、そのアルカリ性塩、その単一の鏡像異性体のうちの1つ又は鏡像異性体のうちの1つのアルカリ性塩である。
本発明の使用される二重パルス実施態様において使用されると予測される用量は、等用量(例えば60mg+60mg)で適切に組み合わされた、酸感受性PPIの1つの即時放出部分と1つの遅延放出部分に分割された2〜500mgの範囲である。
酸感受性プロトンポンプ阻害剤含有コアは、場合により薬学的に許容しうる賦形剤と共に従来の方法による直径が5mmより小さいか又は5mmに等しい小錠剤の形態のコア材料中に活性薬物を入れて製剤化されている。小錠剤が非対称である場合、それらの最長軸は5mmより小さいか又は5mmに等しい。
本発明による酸性化合物は、10%w/wの濃度で(室温すなわち約20℃にて)精製水に溶解または懸濁され、そしてガラス電極またはISFET電極を備えたpHメーターで測定した場合に5またはそれ以下のpHを示す化合物である。
当該分野で公知のあらゆる適切な造粒手順、例えば湿式造粒、乾式造粒又は溶融造粒を利用し得る。
コア材料上に塗布され、そして遅滞時間制御層をPPI含有コアと分離している遅延放出改変層は、水溶性ポリマーベースの層に疎水性化剤及びタルクを組み込むことにより疎水性にされる。
遅滞時間制御層は、例えばヒドロキシプロピルメチルセルロース 4000のような高粘性水溶性ポリマーを必須成分として含む。用語「水溶性ポリマー」は、本明細書で使用される場合、水溶性ポリマー、水溶性コポリマー、又はこのようなポリマーの混合物を意味する。本発明における「高粘性」は、1つ目の選択肢として欧州薬局方及び2つ目の選択肢として米国薬局方に従って試験されて100mPas(cps)から15000mPas(cps)までのみかけ粘度とみなされる。試験が両方の薬局方に記載される場合、欧州薬局方における方法が普及している。
最も好ましい高粘性水溶性ポリマーは、HPMC若しくはHEC又はそれらの混合物である。
以前に記載した遅滞時間制御層を有する錠剤は、本発明の1つの代替の実施態様として、水溶性結合剤、崩壊剤及び場合により界面活性剤とともに、活性物質の第2の部分/用量を含む分散液/溶液/懸濁液で、例えばスプレーされてコーティングを施される。このコーティングは、適切なコーティング装置で行われて、遅滞時間制御層の上面上に堆積されたPPIの第2の部分を含む層を有するコアを得、これが最終製剤を投与した場合に即時放出パルスを生じる。
PPIの第2の部分を含むこの層は、活性成分に加えて、結合剤並びに場合により崩壊剤及びアルカリ性pH調節化合物のような他の賦形剤を含む。
層を形成された錠剤上に腸溶性コーティング層を塗布する前に、それらを、例えばpH−緩衝化化合物のようなアルカリ性化合物を場合により含む医薬賦形剤を含む1つまたはそれ以上の水溶性かまたは水中で急速に崩壊するサブコーティング層で場合により被覆し得る。このサブコーティング層は、層を形成された錠剤の組成物を外部腸溶性コーティング層と分離する。
本発明の最終製剤は、第1の代替の実施態様についての以下の原則的な方法に従って製造される;
I) 唯一の活性薬物として酸感受性プロトンポンプ阻害剤を含む小錠剤の形態のコア材料を調製する工程;
II) 工程I)で得られた錠剤コアを、遅延放出改変層でコーティングする工程;
III) 工程II)から得られた遅延放出改変層を形成された錠剤コアを、必須成分として高粘性水溶性ポリマーを含む遅滞時間制御層でコーティングする工程;
IV) 工程III)から得られた遅滞時間制御層を形成された錠剤を、外部腸溶性コーティングでコーティングする工程であって、任意のサブコーティング層が、腸溶性コーティング層が塗布される前に塗布される、工程;
V) 工程IV)で得られた錠剤生成物を、外部腸溶性コーティング及び任意のサブコーティング層を有しPPIの即時放出を生じるペレットと共に、カプセル剤、サシェ剤又は複数単位ペレット系錠剤に組み込む工程。
I) 唯一の活性薬物として酸感受性プロトンポンプ阻害剤を含む小錠剤の形態のコア材料を調製する工程;
II) 工程I)から得られた錠剤コアを、遅延放出改変層でコーティングする工程;
III) 工程II)から得られた遅延放出改変層を形成された錠剤コアを、必須成分として高粘性水溶性ポリマーを含む遅滞時間制御層でコーティングする工程;
IV) 工程III)から得られた遅滞時間制御層を形成された錠剤を、第2のPPI部分を含む層でコーティングする工程;
V) 工程IV)から得られた錠剤を、任意のサブコーティング層で場合によりコーティングする工程;並びに
VI) 工程V)から得られた錠剤生成物を、外部腸溶性コーティングでコーティングする工程;
VII) 場合により、工程VI)から得られた腸溶性コーティングを施された錠剤を、カプセル剤、サシェ剤、又は複数単位ペレット系錠剤に製剤化する工程。
a)高粘性水溶性ポリマーを非溶媒中に分散すること;及び
b)水性液体又は水を加えて分散したポリマー粒子の水和形態を形成すること;
により製造された高粘性水溶性ポリマーの分散液を利用することが特に有益である。
このような分散系が、最初にポリマーを含水液体に溶解し、次いでその系を沈降させることでは得ることができないことは理解されるべきである。
実施態様は、1〜10時間の範囲、好ましくは1〜8時間の範囲、そして最も好ましくは1〜6時間の範囲の遅滞時間を有するように設計される。
代替として、実施態様は、2〜10時間の範囲、好ましくは2〜8時間の範囲、そして最も好ましくは2〜6時間の範囲の遅滞時間を有するように設計される。
さらなる代替として、実施態様は、4〜10時間の範囲、好ましくは4〜8時間の範囲、そして最も好ましくは4〜6時間の範囲の遅滞時間を有するように設計される。
患者への提示前の本発明の剤形を、カプセル剤、サシェ剤、複数単位ペレット系錠剤、又は即時パルス及び遅延パルスの両方を含む錠剤の形態になるように仕上げることが企図されている。完成した剤形は、それぞれ遅延放出パルス、即時放出パルスを生じる、錠剤、他の種類の錠剤及びペレットの選択的組み合わせを含み得る。遅延放出パルスは、本発明によれば錠剤を起源とする。
錠剤コア中の1つのPPI部分及びコーティング層に含まれる第2のPPI部分、そして外部層として腸溶性コーティングを有すると短く記載された本発明の「他の代替の実施態様」についての方法の説明に従って製造された錠剤もまた、それ自体完成剤形であることが企図されている。
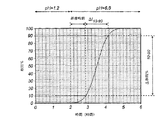
遅滞時間/遅延時間:ペレット/錠剤の形態の腸溶性コーティングを施されたコアが露出された後でさえも、pH1.2を有する第1の溶出媒体については2時間、次いでpH6.8を有する第2の溶解媒体中で、インビトロでの薬物の溶出が遅延されることを本発明については意味する。
遅滞時間は、(第2の)溶出媒体中において、(遅延パルスにおける用量の)薬物の10%が放出されるまでに要する時間として定義される。例証のため、図1を参照のこと。
勾配は、溶出した量(80%)を(遅延用量の)10−90%の間の溶出に必要な時間(分)で割ったものとして定義される。これは、1分あたりの%(10-90)で表わされるので、この期間の平均速度としての勾配を与える。例証のために、図1を参照のこと。
11mgのエソメプラゾールMg三水和物を含む遅延放出錠剤
遅延放出錠剤の製造のための原則的な方式は、活性成分(PPI)を含む錠剤コアを作製し、そして以下の順序でそれらに層をコーティングすることによる;遅延放出改変層→遅滞時間制御層→腸溶性コーティング層。
錠剤コアを概略的に、活性物質を賦形剤と共に造粒し、乾燥し、そして得られた顆粒を粉砕し、顆粒をさらなる添加剤と混合し、そしてその混合物を圧縮することにより製造した。
賦形剤 量(g)
エソメプラゾール−Mg三水和物 450
マンニトール 349
微結晶セルロース 188
グリコールデンプンナトリウム 60
ヒドロキシプロピルメチルセルロース(HPMC)6cps 60
水 350
得られた湿った塊をトレイ上に置き、そして50℃で乾燥オーブン中で終夜乾燥させた。
得られた顆粒を粉砕して、1.0mmの開口を有する篩に通した。
成分 量(g)
エソメプラゾール顆粒 900
タルク 41.5
微結晶セルロース 51.5
ステアリルフマル酸ナトリウム 20.8
混合物を、円形で直径4mmの寸法の平均重量31mgを有する錠剤を生じるパンチを備えた回転式プレスKorsch 106で圧縮した。
成分 量(g)
コア材料
エソメプラゾール錠剤 150
コーティング懸濁液
タルク 33.8
ヒドロキシプロピルセルロース(75−150cps) 9.0
Mgステアレート 2.3
水 315
直径0.8mmの開口を有する液体ノズルを備えたWurster方式に従って作動する流動床装置でコーティングを行った。入口空気温度は75℃であり、流動空気流量は40Nm3/時、噴霧装置空気圧は2.0bar、噴霧装置空気流量は2.2Nm3/時、スプレー速度は8−11g/分であり、結果として約45℃の出口空気温度となった。
成分 量(g)
コア材料
遅延放出改変層でコーティングされた錠剤 150
コーティング懸濁液
ヒドロキシプロピルメチルセルロース4000cps* 66.7
ヒドロキシプロピルメチルセルロース6cps 9.2
エタノール99.5% 1125
水 143.3
* 欧州薬局方に従って試験したpHは7.5であった。
成分 量(g)
コア材料
遅滞時間層コーティングを施された錠剤 150
コーティング懸濁液
メタクリル酸コポリマー、C型30%分散液 75
タルク 4
クエン酸トリエチル 2.3
水 94.5
前の工程と同じコーティング装置でコーティングを行った。
入口空気温度は65℃であり、流動空気流量は約40m3/時、噴霧装置空気圧は2.5bar、噴霧装置空気流量は2.6Nm3/時、スプレー速度は6−7g/分であり、結果として約38℃の出口空気温度となった。
得られた生成物のサンプルをインビトロ溶出について試験した。得られた溶出プロフィールを図2に示す。
放出されたエソメプラゾールマグネシウムの量を、UV−分光計で302nmにて測定した。
放出曲線(吸収値曲線)の一部の下降している最終段階は、溶解媒体中での一部の分解の結果であると考えられ得る。
評価された遅滞時間は約5時間である。
エソメプラゾールマグネシウム(40mg+11mg)の即時放出パルス及び遅延放出パルスを示すカプセル
二相性パルス放出カプセル剤の製造のための概要の方式は、即時放出のペレット及び遅延放出の錠剤の両方(すなわち、本発明によるサブコーティングおよび遅滞時間制御層の組み合わせを有する錠剤)を、硬ゼラチンカプセルに充てんすることによる。
すなわち以下の順序に従った;
遅延放出錠剤(本発明による遅滞時間ペレット)を実施例1に記載されるように調製する→錠剤をカプセルに充てんする→得られた錠剤含有カプセルに即時放出ペレットを充てんする。
エソメプラゾールマグネシウム(10mg+11mg)の即時放出パルス及び遅延放出パルスを示す腸溶性コーティングを施された錠剤。
遅延及び即時放出錠剤の製造のための概要の方式は、実施例1に従って製造されたPPIを含むコア、遅延放出改変層及び遅滞時間制御層を有する錠剤で開始して、そしてそれらを以下の順序で層でコーティングする;第2PPI部分を含む層(即時放出を生じる)→サブコーティング層→腸溶性コーティング層。
錠剤を、実施例1において記載されるものと同じ、直径0.8mmの開口を有する液体ノズルを備えたWurster方式に従って作動する流動床装置でコーティングした。入口空気温度を80℃に設定し、流動空気流量を約45Nm3/時、噴霧装置空気圧を2.8bar、噴霧装置空気流量を2.8Nm3/時、スプレー速度を6−11g/分に設定した。
成分 量(g)
コア材料
実施例1からの遅滞時間層をコーティングされた錠剤
(それぞれ約54mg) 216
コーティング懸濁液
エソメプラゾール−Mg三水和物 61.1
ポリソルベート80 1.2
ヒドロキシプロピルメチルセルロース6cps 9.1
クロスカルメロースナトリウム 4
水 373
懸濁液重量: 448.4
平均錠剤重量が13mg増加するまでコーティングを続けた。
成分 量(g)
コア材料
上記からの錠剤 268
コーティング懸濁液
タルク粉末 49.2
ヒドロキシプロピルセルロース(75−150cps) 13.6
Mg−ステアレート 3.2
水 480
懸濁液重量: 546
平均錠剤重量が12−14mg増加するまでコーティングを続けた。
成分 量(g)
コア材料
上記からのサブコーティングを施された錠剤 240
コーティング懸濁液
メタクリル酸コポリマー、C型 30%分散液 156
タルク 8.3
クエン酸トリエチル 4.8
水 196
前の工程と同じコーティング装置でコーティングを行った。
入口空気温度は65℃であり、流動空気流量は約40m3/時、噴霧装置空気圧は2.5bar、噴霧装置空気流量は2.6Nm3/時、スプレー速度は6−7g/分であった。
平均錠剤重量が約16mg増加するまでコーティングを続けた。
ランソプラゾール(10mg)の即時放出パルス及びエソメプラゾールマグネシウム(10mg)の遅延放出パルスを示す遅延放出錠剤(後の腸溶性コーティング用)
遅延放出錠剤の製造のための原則的な方式は、実施例1に従うコアを有する錠剤で開始し、そしてそれらに以下の順序で層をコーティングする;→遅延放出改変層→遅滞時間制御層→第2PPI部分を含む層(即時放出を生じる)。
本実施例に従う錠剤が腸溶性コーティングを施されていないことに留意するべきである。実施例1のような前の実施例に従ってこれらに後で腸溶性コーティングを施して、特許請求された本発明の実施態様を得てもよい。
成分 量(g)
コア材料
エソメプラゾール錠剤コア(実施例1に従う) 150
コーティング懸濁液
タルク 33.8
ヒドロキシプロピルセルロース(75−150cps) 9.0
ステアリルフマル酸ナトリウム 2.3
水 315
直径0.8mmの開口を有する液体ノズルを備えたWurster方式に従って作動する流動床装置でコーティングを行った。入口空気温度は65℃であり、流動空気流量は60Nm3/時、噴霧装置空気圧は1.5bar、噴霧装置空気流量は1.6Nm3/時、スプレー速度は8−11g/分であり、結果として約50℃の出口空気温度となった。
成分 量(g)
コア材料
(上記からの)遅延放出改変層でコーティングされた錠剤 150
コーティング懸濁液
ヒドロキシエチルセルロース250HHX 70
ヒドロキシエチルセルロースPLUS330CS 7.5
エタノール99.5% 751
水 183
直径0.8mmの開口を有する液体ノズルを備えたWurster方式に従って作動する流動床装置でコーティングを行った。入口空気温度は42℃であり、流動空気流量は60Nm3/時、噴霧装置空気圧は1.5bar、噴霧装置空気流量は1.6Nm3/時、スプレー速度は11−14g/分であり、結果として約32℃の出口空気温度となった。
成分 量(g)
コア材料
(上記からの)遅滞時間層をコーティングした錠剤 150
コーティング懸濁液
ランソプラゾール 29.4
ポリソルベート80 0.6
ヒドロキシプロピルメチルセルロース6cps 4.4
クロスカルメロースナトリウム 5.1
水 498
溶出試験を、パドル及び固定バスケットを備えたUSP溶出装置No.2で行った。パドルを75rpmで作動させた。溶出媒体は1000mlのリン酸緩衝液pH6.8(37℃)であった。これらのサンプルについてはHClへの予備暴露は行わなかった。
放出されたランソプラゾール量を、UV−分光計で285nm(時間段階0−360分)にて測定した。放出されたエソメプラゾールマグネシウム量を、UV−分光計で302nm(時間段階420−1020分)にて測定した。
評価された遅滞時間は約10時間である。
Claims (23)
- 活性薬物として酸感受性プロトンポンプ阻害剤(PPI)を含む経口用固形医薬剤形であって、該剤形は、2つのPPI放出部分、遅延放出パルスでPPIを放出する錠剤、及び即時放出パルスでPPIを放出するペレットを含み、PPIは、小錠剤の形態のコア材料中に配合されており、そして遅延放出パルスを生じる錠剤が、所定の順序でコア材料上に以下の層;
−遅延放出改変層;
−必須成分として高粘性水溶性ポリマーを含む遅滞時間制御層;
−任意のサブコーティング層;及び
−外部腸溶性コーティング層;
を有し、
そして即時放出パルスを生じるペレットが、ペレットの形態のコア材料上に以下の層;
−任意のサブコーティング層;及び
−外部腸溶性コーティング層
を有することを特徴とする、上記剤形。 - 活性薬物として酸感受性プロトンポンプ阻害剤(PPI)を含む経口用固形医薬剤形であって、該剤形は2つのPPI放出部分を有する錠剤であり、各錠剤は、遅延放出パルス及び即時放出パルスを生じ、PPIが小錠剤の形態のコア材料中に配合されており、そして錠剤が所定の順序でコア材料上に以下の層;
−遅延放出改変層;
−必須成分として高粘性水溶性ポリマーを含む遅滞時間制御層;
−PPIの第2の部分を含む層;
−任意のサブコーティング層;及び
−外部腸溶性コーティング層
を有することを特徴とする、上記剤形。 - 最終剤形がカプセル剤である、請求項1又は2に記載の経口用医薬剤形。
- 最終剤形がサシェ剤である、請求項1又は2に記載の経口用医薬剤形。
- 即時放出パルスを生じるペレットが1つ又はそれ以上の錠剤の形態であり、そして最終剤形が遅延放出パルスの錠剤及び即時放出パルスの錠剤を含む、請求項1、3又は4のいずれか1項に記載の経口用医薬剤形。
- 酸感受性プロトンポンプ阻害剤が、エソメプラゾールのアルカリ性塩である、請求項1〜5のいずれか1項に記載の経口用医薬剤形。
- 酸感受性プロトンポンプ阻害剤が、エソメプラゾールマグネシウムである、請求項1〜5のいずれか1項に記載の経口用医薬剤形。
- 酸感受性プロトンポンプ阻害剤が、オメプラゾールマグネシウムである、請求項1〜5のいずれか1項に記載の経口用医薬剤形。
- 1〜10時間の範囲の、遅延(第2)パルスについての遅滞時間を有する、請求項1〜8のいずれか1項に記載の経口用医薬剤形。
- 2〜8時間の範囲の遅滞時間を有する、請求項9に記載の経口用医薬剤形。
- 遅滞時間制御層が、コーティング過程からのあらゆる残留物以外の唯一の成分として高粘性水溶性ポリマーを含む、請求項1〜10のいずれか1項に記載の経口用医薬剤形。
- 遅滞時間制御層における必須成分が、高粘性ヒドロキシプロピルメチルセルロース又は高粘性ヒドロキシエチルセルロースである、請求項1〜11のいずれか1項に記載の経口用医薬剤形。
- 高粘性ヒドロキシプロピルメチルセルロース又はヒドロキシエチルセルロースが、欧州薬局方に従って測定した場合に7.0〜9.0の間のpHを示す、請求項12に記載の経口用医薬剤形。
- 遅延放出改変層が、水溶性ポリマー、タルク並びにMg−ステアレート、ベヘン酸グリセリル及びステリルフマル酸ナトリウムからなる群より選択される疎水性化剤を含む、請求項1〜13のいずれか1項に記載の経口用医薬剤形。
- 遅延放出改変層が、溶媒/水の微量痕跡を無視すれば、ヒドロキシプロピルセルロース、タルク、並びにMg−ステアレートのみから構成される、請求項1〜14のいずれか1項に記載の経口用医薬剤形。
- 請求項1に記載の経口用医薬剤形を製造するための方法であって、以下の工程;
I) 活性薬物として酸感受性プロトンポンプ阻害剤を含む小錠剤の形態のコア材料を調製する工程;
II) 工程I)からの錠剤コアを、遅延放出改変層でコーティングする工程;
III) 工程II)からの遅延放出改変層を形成された錠剤コアを、必須成分として高粘性水溶性ポリマーを含む遅滞時間制御層でコーティングする工程;
IV) 工程III)からの遅滞時間制御層を形成された錠剤を、外部腸溶性コーティングでコーティングする工程であって、任意のサブコーティング層が、腸溶性コーティング層の前に塗布される工程;並びに
V) 工程IV)で得られた錠剤生成物を、外部腸溶性コーティング及び任意のサブコーティング層を有しPPIの即時放出を生じるペレットと共に、カプセル剤、サシェ剤又は複数単位ペレット系錠剤に組み込む工程、
を含む、上記方法。 - 請求項2に記載の経口用医薬剤形を製造するための方法であって、以下の工程;
I) 活性薬物として酸感受性プロトンポンプ阻害剤を含む小錠剤の形態のコア材料を調製する工程;
II) 工程I)からの錠剤コアを、遅延放出改変層でコーティングする工程;
III) 工程II)からの遅延放出改変層を形成された錠剤コアを、必須成分として高粘性水溶性ポリマーを含む遅滞時間制御層でコーティングする工程;
IV) 工程III)からの遅滞時間制御層を形成された錠剤を、第2のPPI部分を含む層でコーティングする工程;
V) 工程IV)から得られた錠剤を、任意のサブコーティング層で場合によりコーティングする工程;並びに
VI) 工程V)から得られた錠剤生成物を、外部腸溶性コーティングでコーティングする工程;
VII) 場合により、工程VI)から得られた腸溶性コーティングを施された錠剤を、カプセル剤、サシェ剤、又は複数単位ペレット系錠剤に製剤化する工程、
を含む、上記方法。 - 工程V)における即時放出パルスを生じるペレットが、1つ又はそれ以上の錠剤の形態であり、そして剤形が遅延放出パルスの錠剤及び即時放出パルスの錠剤を含む、請求項16に記載の方法。
- 工程II)からの遅延放出改変層を形成された錠剤コアを遅滞時間制御層でコーティングする工程III)が、
a) 高粘性水溶性ポリマーを非溶媒中に分散させること;及び
b) 水性液体又は水を加えて分散したポリマー粒子の水和形態を形成すること、
により製造される高粘性水溶性ポリマーの分散液を利用することにより行われる、請求項16又は17に記載の方法。 - 工程IIにより得られる遅延放出改変層が、コーティング過程からの溶媒/分散媒体/懸濁媒体のあらゆる残留物以外はヒドロキシプロピルセルロース、タルク及びMg−ステアレートの成分のみから構成される、請求項16〜19のいずれか1項に記載の方法。
- 得られた生成物が、1〜10時間の範囲の遅滞時間を有する、請求項16〜20のいずれか1項に記載の方法。
- 胃酸分泌の抑制を改善することを必要とする患者に、請求項1〜15のいずれか1項に規定される経口用医薬剤形を投与することからなる胃酸分泌の抑制を改善するための方法。
- 胃腸疾患の処置における、請求項1〜15のいずれか1項に記載の医薬剤形の使用。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US62564904P | 2004-11-04 | 2004-11-04 | |
| PCT/SE2005/001643 WO2006049565A1 (en) | 2004-11-04 | 2005-11-02 | New modified release tablet formulations for proton pump inhibitors |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2008519070A true JP2008519070A (ja) | 2008-06-05 |
| JP2008519070A5 JP2008519070A5 (ja) | 2008-12-11 |
Family
ID=36319458
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2007540284A Pending JP2008519070A (ja) | 2004-11-04 | 2005-11-02 | プロトンポンプ阻害剤用の新規な改変された放出の錠剤製剤 |
Country Status (17)
| Country | Link |
|---|---|
| US (1) | US20080003281A1 (ja) |
| EP (1) | EP1809262A4 (ja) |
| JP (1) | JP2008519070A (ja) |
| KR (1) | KR20070083956A (ja) |
| CN (1) | CN101094661A (ja) |
| AR (1) | AR052225A1 (ja) |
| AU (1) | AU2005301369A1 (ja) |
| BR (1) | BRPI0517954A (ja) |
| CA (1) | CA2584419A1 (ja) |
| IL (1) | IL182686A0 (ja) |
| MX (1) | MX2007004987A (ja) |
| NO (1) | NO20072257L (ja) |
| RU (1) | RU2007115544A (ja) |
| TW (1) | TW200624126A (ja) |
| UY (1) | UY29193A1 (ja) |
| WO (1) | WO2006049565A1 (ja) |
| ZA (1) | ZA200703111B (ja) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2014504633A (ja) * | 2011-02-03 | 2014-02-24 | ルピン・リミテッド | 経口投与用放出制御医薬組成物 |
| WO2018110683A1 (ja) * | 2016-12-15 | 2018-06-21 | 大原薬品工業株式会社 | 化学的安定性が改善されたエソメプラゾール塩を含有する錠剤 |
Families Citing this family (20)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| AR051654A1 (es) * | 2004-11-04 | 2007-01-31 | Astrazeneca Ab | Nuevas formulaciones de pellets de liberacion modificada para inhibidores de la bomba de protones |
| EP1970056A1 (en) * | 2007-03-15 | 2008-09-17 | Polichem S.A. | Time-specific delayed/pulsatile release dosage forms |
| CA2694602A1 (en) * | 2007-07-27 | 2009-02-05 | Depomed, Inc. | Pulsatile gastric retentive dosage forms |
| ITFI20070253A1 (it) * | 2007-11-09 | 2009-05-10 | Valpharma Internat S P A | Formulazioni farmaceutiche per la somministrazione di ipp. |
| US20090280173A1 (en) * | 2008-05-09 | 2009-11-12 | Ishwar Chauhan | Multilayer Omeprazole Tablets |
| US20090280175A1 (en) * | 2008-05-09 | 2009-11-12 | Ishwar Chauhan | Multilayer Proton Pump Inhibitor Tablets |
| US10485770B2 (en) * | 2009-12-21 | 2019-11-26 | Aptapharma, Inc. | Functionally-coated multilayer tablets |
| EP2384746A3 (en) * | 2010-05-05 | 2012-03-07 | Sanovel Ilac Sanayi ve Ticaret A.S. | Dual release oral tablet compositions of dexlansoprazole |
| EP2384745A3 (en) | 2010-05-05 | 2012-01-18 | Sanovel Ilac Sanayi ve Ticaret A.S. | Modified release pharmaceutical compositions of dexlansoprazole |
| EP2384747A3 (en) * | 2010-05-05 | 2012-01-18 | Sanovel Ilac Sanayi ve Ticaret A.S. | Oral Tablet Compositions Of Dexlansoprazole |
| US8563035B2 (en) | 2010-05-05 | 2013-10-22 | Sanovel Ilac Sanayi Ve Ticaret Anomin Sirketi | Oral tablet compositions of dexlansoprazole |
| WO2012111024A1 (en) * | 2011-02-18 | 2012-08-23 | Suven Nishtaa Pharma Pvt Ltd | Pharmaceutical compositions of dexlansoprazole |
| EP3288556A4 (en) | 2015-04-29 | 2018-09-19 | Dexcel Pharma Technologies Ltd. | Orally disintegrating compositions |
| CN104856971B (zh) * | 2015-05-15 | 2019-05-14 | 暨南大学 | 一种脉冲双释放制剂及其制备方法与应用 |
| CN105012274A (zh) * | 2015-06-27 | 2015-11-04 | 上海信谊万象药业股份有限公司 | 一种奥美拉唑微片胶囊制剂及其制备方法 |
| CN104940170A (zh) * | 2015-07-23 | 2015-09-30 | 浙江亚太药业股份有限公司 | 一种埃索美拉唑镁肠溶胶囊及其制备方法 |
| CA3009332A1 (en) * | 2015-12-22 | 2017-06-29 | Imprimis Pharmaceuticals, Inc. | Pharmaceutical formulations for treating kidney stones and methods for fabricating and using thereof |
| US10076494B2 (en) | 2016-06-16 | 2018-09-18 | Dexcel Pharma Technologies Ltd. | Stable orally disintegrating pharmaceutical compositions |
| KR101877350B1 (ko) | 2016-10-28 | 2018-08-09 | 한미약품 주식회사 | 에스오메프라졸 함유 복합 캡슐제 및 그 제조방법 |
| WO2019030610A1 (en) * | 2017-08-11 | 2019-02-14 | Solutions In Innovative Research Pvt. Ltd. | PHARMACEUTICAL COMPOSITIONS WITH DUAL DIRECTLY COMPRESSIBLE MEDICAMENT RELEASE |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2001526213A (ja) * | 1997-12-22 | 2001-12-18 | アストラゼネカ・アクチエボラーグ | 経口医薬パルス放出剤形 |
| JP2003171277A (ja) * | 2001-12-07 | 2003-06-17 | Wyeth Lederle Japan Ltd | 薬物放出時間制御型固形製剤 |
Family Cites Families (24)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| IL75400A (en) * | 1984-06-16 | 1988-10-31 | Byk Gulden Lomberg Chem Fab | Dialkoxypyridine methyl(sulfinyl or sulfonyl)benzimidazoles,processes for the preparation thereof and pharmaceutical compositions containing the same |
| US4704285A (en) * | 1985-11-18 | 1987-11-03 | The Dow Chemical Company | Sustained release compositions comprising hydroxypropyl cellulose ethers |
| IT1230576B (it) * | 1988-10-20 | 1991-10-28 | Angeli Inst Spa | Formulazioni farmaceutiche per via orale a liberazione selettiva nel colon |
| JPH07223970A (ja) * | 1994-02-10 | 1995-08-22 | Tanabe Seiyaku Co Ltd | 消化管内適所放出製剤 |
| US5945124A (en) * | 1995-07-05 | 1999-08-31 | Byk Gulden Chemische Fabrik Gmbh | Oral pharmaceutical composition with delayed release of active ingredient for pantoprazole |
| US20050054682A1 (en) * | 1996-01-04 | 2005-03-10 | Phillips Jeffrey O. | Pharmaceutical compositions comprising substituted benzimidazoles and methods of using same |
| SE9600072D0 (sv) * | 1996-01-08 | 1996-01-08 | Astra Ab | New oral formulation of two active ingredients II |
| AU5179898A (en) * | 1996-11-06 | 1998-05-29 | Sharmatek, Inc. | Delayed delivery system for acid-sensitive drugs |
| US5885616A (en) * | 1997-08-18 | 1999-03-23 | Impax Pharmaceuticals, Inc. | Sustained release drug delivery system suitable for oral administration |
| PT1126826E (pt) * | 1998-11-02 | 2008-11-25 | Elan Pharma Int Ltd | Composição de metilfenidato de libertação modificada multiparticulada |
| US6632451B2 (en) * | 1999-06-04 | 2003-10-14 | Dexcel Pharma Technologies Ltd. | Delayed total release two pulse gastrointestinal drug delivery system |
| EP1064938A1 (en) * | 1999-06-28 | 2001-01-03 | Sanofi-Synthelabo | Pharmaceutical dosage forms for controlled release producing at least a timed pulse |
| EP1074249A1 (en) * | 1999-07-27 | 2001-02-07 | Jagotec Ag | A pharmaceutical tablet system for releasing at least one active substance during a release period subsequent to a no-release period |
| ES2168043B1 (es) * | 1999-09-13 | 2003-04-01 | Esteve Labor Dr | Forma farmaceutica solida oral de liberacion modificada que contiene un compuesto de bencimidazol labil en medio acido. |
| GB9923436D0 (en) * | 1999-10-04 | 1999-12-08 | American Home Prod | Pharmaceutical compositions |
| US20030180352A1 (en) * | 1999-11-23 | 2003-09-25 | Patel Mahesh V. | Solid carriers for improved delivery of active ingredients in pharmaceutical compositions |
| US6627223B2 (en) * | 2000-02-11 | 2003-09-30 | Eurand Pharmaceuticals Ltd. | Timed pulsatile drug delivery systems |
| US6749867B2 (en) * | 2000-11-29 | 2004-06-15 | Joseph R. Robinson | Delivery system for omeprazole and its salts |
| CN100408029C (zh) * | 2001-09-28 | 2008-08-06 | 麦克内尔-Ppc股份有限公司 | 有镶嵌部分的组合剂型 |
| CA2496044A1 (en) * | 2002-08-16 | 2004-02-26 | Themis Laboratories Private Limited | A process for manufacture of stable oral multiple units pharamceutical composition containing benzimidazoles |
| US8487002B2 (en) * | 2002-10-25 | 2013-07-16 | Paladin Labs Inc. | Controlled-release compositions |
| WO2004071374A2 (en) * | 2003-02-11 | 2004-08-26 | Torrent Pharmaceuticals Limited | Once a day orally administered pharmaceutical compositions |
| US7670624B2 (en) * | 2004-01-29 | 2010-03-02 | Astella Pharma Inc. | Gastrointestinal-specific multiple drug release system |
| US20050239845A1 (en) * | 2004-04-16 | 2005-10-27 | Santarus, Inc. | Combination of proton pump inhibitor, buffering agent, and prokinetic agent |
-
2005
- 2005-10-31 AR ARP050104549A patent/AR052225A1/es not_active Application Discontinuation
- 2005-11-02 AU AU2005301369A patent/AU2005301369A1/en not_active Abandoned
- 2005-11-02 MX MX2007004987A patent/MX2007004987A/es not_active Application Discontinuation
- 2005-11-02 US US11/718,571 patent/US20080003281A1/en not_active Abandoned
- 2005-11-02 EP EP05801796A patent/EP1809262A4/en not_active Withdrawn
- 2005-11-02 KR KR1020077010117A patent/KR20070083956A/ko not_active Application Discontinuation
- 2005-11-02 WO PCT/SE2005/001643 patent/WO2006049565A1/en active Application Filing
- 2005-11-02 JP JP2007540284A patent/JP2008519070A/ja active Pending
- 2005-11-02 RU RU2007115544/15A patent/RU2007115544A/ru unknown
- 2005-11-02 CN CNA2005800458269A patent/CN101094661A/zh active Pending
- 2005-11-02 BR BRPI0517954-8A patent/BRPI0517954A/pt not_active Application Discontinuation
- 2005-11-02 CA CA002584419A patent/CA2584419A1/en not_active Abandoned
- 2005-11-04 TW TW094138678A patent/TW200624126A/zh unknown
- 2005-11-04 UY UY29193A patent/UY29193A1/es not_active Application Discontinuation
-
2007
- 2007-04-16 ZA ZA200703111A patent/ZA200703111B/xx unknown
- 2007-04-19 IL IL182686A patent/IL182686A0/en unknown
- 2007-05-02 NO NO20072257A patent/NO20072257L/no not_active Application Discontinuation
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2001526213A (ja) * | 1997-12-22 | 2001-12-18 | アストラゼネカ・アクチエボラーグ | 経口医薬パルス放出剤形 |
| JP2003171277A (ja) * | 2001-12-07 | 2003-06-17 | Wyeth Lederle Japan Ltd | 薬物放出時間制御型固形製剤 |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2014504633A (ja) * | 2011-02-03 | 2014-02-24 | ルピン・リミテッド | 経口投与用放出制御医薬組成物 |
| WO2018110683A1 (ja) * | 2016-12-15 | 2018-06-21 | 大原薬品工業株式会社 | 化学的安定性が改善されたエソメプラゾール塩を含有する錠剤 |
| JP2018095632A (ja) * | 2016-12-15 | 2018-06-21 | 大原薬品工業株式会社 | 化学的安定性が改善されたエソメプラゾール塩を含有する錠剤 |
Also Published As
| Publication number | Publication date |
|---|---|
| IL182686A0 (en) | 2007-09-20 |
| AU2005301369A1 (en) | 2006-05-11 |
| KR20070083956A (ko) | 2007-08-24 |
| AR052225A1 (es) | 2007-03-07 |
| BRPI0517954A (pt) | 2008-10-21 |
| EP1809262A1 (en) | 2007-07-25 |
| TW200624126A (en) | 2006-07-16 |
| US20080003281A1 (en) | 2008-01-03 |
| RU2007115544A (ru) | 2008-12-10 |
| ZA200703111B (en) | 2009-09-30 |
| NO20072257L (no) | 2007-08-03 |
| UY29193A1 (es) | 2006-06-30 |
| CN101094661A (zh) | 2007-12-26 |
| EP1809262A4 (en) | 2012-09-05 |
| CA2584419A1 (en) | 2006-05-11 |
| WO2006049565A1 (en) | 2006-05-11 |
| MX2007004987A (es) | 2007-06-14 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2008519070A (ja) | プロトンポンプ阻害剤用の新規な改変された放出の錠剤製剤 | |
| KR101752014B1 (ko) | 고용량 및 저용량 약물들의 조합을 포함하는 구강붕해정 조성물 | |
| JP4907765B2 (ja) | 経口医薬パルス放出剤形 | |
| JP2008519069A (ja) | プロトンポンプ阻害剤用の新規な改変された放出のペレット製剤 | |
| JP4885347B2 (ja) | 酸に不安定ベンズイミダゾールを含有する修飾された放出特性の経口用固形製剤 | |
| JP2002532425A (ja) | 新規な医薬製剤 | |
| JP5925318B2 (ja) | 有核錠 | |
| AU2009224254A2 (en) | Orally-disintegrating solid preparation | |
| KR20080104132A (ko) | 약 염기성 약물과 유기산을 포함하는 약물 전달 시스템 | |
| SG190905A1 (en) | Orally disintegrating tablet | |
| KR20080098627A (ko) | 약 염기성 선택성 세로토닌 5-ht3 차단제와 유기산을 포함하는 약물 전달 시스템 | |
| JP6364406B2 (ja) | 口腔内崩壊錠 | |
| MX2013006247A (es) | Tableta oralmente desintegradora. | |
| JP2014533656A5 (ja) | ||
| WO2021018414A1 (en) | Pharmaceutical composition comprising dabigatran etexilate | |
| WO2005034924A1 (en) | Enteric coated pellets comprising esomeprazole, hard gelatin capsule containing them, and method of preparation | |
| JP2019099567A (ja) | 多層構造を有する粒子状医薬組成物 | |
| JP2009542669A (ja) | ピペリジノアルカノールと充血除去剤の組み合わせを含んで成る医薬組成物 | |
| EP2535045A1 (en) | Pharmaceutical composition of lansoprazole | |
| JP5919173B2 (ja) | 徐放性塩酸アンブロキソール口腔内崩壊錠 | |
| WO2010018593A2 (en) | Gastric acid resistant benzimidazole multiple unit tablet composition | |
| EP3380084B1 (en) | Omeprazole formulations | |
| CA3160869A1 (en) | Dosage form for use in treating or preventing of a disease |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20081022 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20081022 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20111121 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20111129 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20120515 |