JP2008511649A - 最適化液相酸化 - Google Patents
最適化液相酸化 Download PDFInfo
- Publication number
- JP2008511649A JP2008511649A JP2007530229A JP2007530229A JP2008511649A JP 2008511649 A JP2008511649 A JP 2008511649A JP 2007530229 A JP2007530229 A JP 2007530229A JP 2007530229 A JP2007530229 A JP 2007530229A JP 2008511649 A JP2008511649 A JP 2008511649A
- Authority
- JP
- Japan
- Prior art keywords
- reaction medium
- reactor
- reaction zone
- oxidation
- reaction
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 239000007791 liquid phase Substances 0.000 title claims abstract description 250
- 238000007254 oxidation reaction Methods 0.000 title claims abstract description 211
- 230000003647 oxidation Effects 0.000 title claims abstract description 191
- URLKBWYHVLBVBO-UHFFFAOYSA-N Para-Xylene Chemical group CC1=CC=C(C)C=C1 URLKBWYHVLBVBO-UHFFFAOYSA-N 0.000 claims abstract description 451
- 238000006243 chemical reaction Methods 0.000 claims abstract description 300
- KKEYFWRCBNTPAC-UHFFFAOYSA-N Terephthalic acid Chemical compound OC(=O)C1=CC=C(C(O)=O)C=C1 KKEYFWRCBNTPAC-UHFFFAOYSA-N 0.000 claims abstract description 246
- 238000000034 method Methods 0.000 claims abstract description 98
- 239000012429 reaction media Substances 0.000 claims description 558
- 230000001590 oxidative effect Effects 0.000 claims description 308
- 239000007800 oxidant agent Substances 0.000 claims description 307
- 239000007789 gas Substances 0.000 claims description 167
- 239000007788 liquid Substances 0.000 claims description 129
- 239000002245 particle Substances 0.000 claims description 101
- 239000007787 solid Substances 0.000 claims description 99
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 claims description 70
- QQVIHTHCMHWDBS-UHFFFAOYSA-N isophthalic acid Chemical compound OC(=O)C1=CC=CC(C(O)=O)=C1 QQVIHTHCMHWDBS-UHFFFAOYSA-N 0.000 claims description 70
- 239000001301 oxygen Substances 0.000 claims description 70
- 229910052760 oxygen Inorganic materials 0.000 claims description 70
- 239000012071 phase Substances 0.000 claims description 70
- MYMOFIZGZYHOMD-UHFFFAOYSA-N Dioxygen Chemical compound O=O MYMOFIZGZYHOMD-UHFFFAOYSA-N 0.000 claims description 58
- 229910001882 dioxygen Inorganic materials 0.000 claims description 57
- 230000008569 process Effects 0.000 claims description 33
- 239000003054 catalyst Substances 0.000 claims description 29
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 claims description 19
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 claims description 19
- 229910052794 bromium Inorganic materials 0.000 claims description 19
- 239000011148 porous material Substances 0.000 claims description 19
- 239000010941 cobalt Substances 0.000 claims description 18
- 229910017052 cobalt Inorganic materials 0.000 claims description 18
- GUTLYIVDDKVIGB-UHFFFAOYSA-N cobalt atom Chemical compound [Co] GUTLYIVDDKVIGB-UHFFFAOYSA-N 0.000 claims description 18
- 239000011572 manganese Substances 0.000 claims description 15
- PWHULOQIROXLJO-UHFFFAOYSA-N Manganese Chemical compound [Mn] PWHULOQIROXLJO-UHFFFAOYSA-N 0.000 claims description 14
- 229910052748 manganese Inorganic materials 0.000 claims description 14
- 230000001186 cumulative effect Effects 0.000 claims description 11
- 238000007599 discharging Methods 0.000 claims description 9
- PNVDDTCIZTWBNJ-UHFFFAOYSA-N 1-oxofluorene-2,6-dicarboxylic acid Chemical compound C1=C(C(O)=O)C=C2C3=CC=C(C(=O)O)C(=O)C3=CC2=C1 PNVDDTCIZTWBNJ-UHFFFAOYSA-N 0.000 claims description 6
- 230000005540 biological transmission Effects 0.000 claims description 6
- DZFAKQZRZPHYLG-UHFFFAOYSA-N 4-(2-phenylethenyl)cyclohexa-2,4-diene-1,1-dicarboxylic acid Chemical compound C1=CC(C(=O)O)(C(O)=O)CC=C1C=CC1=CC=CC=C1 DZFAKQZRZPHYLG-UHFFFAOYSA-N 0.000 claims 1
- 150000001875 compounds Chemical class 0.000 abstract description 214
- 238000005457 optimization Methods 0.000 abstract 1
- 239000002904 solvent Substances 0.000 description 223
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 173
- 239000002002 slurry Substances 0.000 description 113
- 239000012535 impurity Substances 0.000 description 109
- 239000005711 Benzoic acid Substances 0.000 description 85
- 235000010233 benzoic acid Nutrition 0.000 description 85
- 238000007872 degassing Methods 0.000 description 79
- 125000003118 aryl group Chemical group 0.000 description 74
- GOUHYARYYWKXHS-UHFFFAOYSA-N 4-formylbenzoic acid Chemical compound OC(=O)C1=CC=C(C=O)C=C1 GOUHYARYYWKXHS-UHFFFAOYSA-N 0.000 description 72
- 238000004519 manufacturing process Methods 0.000 description 71
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 64
- 238000009826 distribution Methods 0.000 description 60
- 230000036961 partial effect Effects 0.000 description 55
- 239000000203 mixture Substances 0.000 description 50
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 49
- 229910001868 water Inorganic materials 0.000 description 47
- 150000001491 aromatic compounds Chemical class 0.000 description 46
- 239000007790 solid phase Substances 0.000 description 44
- 230000015572 biosynthetic process Effects 0.000 description 43
- 239000000047 product Substances 0.000 description 42
- 238000010992 reflux Methods 0.000 description 41
- 239000000706 filtrate Substances 0.000 description 38
- CTQNGGLPUBDAKN-UHFFFAOYSA-N O-Xylene Chemical group CC1=CC=CC=C1C CTQNGGLPUBDAKN-UHFFFAOYSA-N 0.000 description 37
- LPNBBFKOUUSUDB-UHFFFAOYSA-N p-toluic acid Chemical compound CC1=CC=C(C(O)=O)C=C1 LPNBBFKOUUSUDB-UHFFFAOYSA-N 0.000 description 35
- XNGIFLGASWRNHJ-UHFFFAOYSA-N phthalic acid Chemical class OC(=O)C1=CC=CC=C1C(O)=O XNGIFLGASWRNHJ-UHFFFAOYSA-N 0.000 description 35
- 229910002090 carbon oxide Inorganic materials 0.000 description 34
- 125000001183 hydrocarbyl group Chemical group 0.000 description 33
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 description 31
- UGFAIRIUMAVXCW-UHFFFAOYSA-N Carbon monoxide Chemical compound [O+]#[C-] UGFAIRIUMAVXCW-UHFFFAOYSA-N 0.000 description 30
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 30
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 30
- 239000012530 fluid Substances 0.000 description 30
- ARCGXLSVLAOJQL-UHFFFAOYSA-N trimellitic acid Chemical compound OC(=O)C1=CC=C(C(O)=O)C(C(O)=O)=C1 ARCGXLSVLAOJQL-UHFFFAOYSA-N 0.000 description 28
- 238000013019 agitation Methods 0.000 description 26
- 239000008096 xylene Substances 0.000 description 26
- -1 aromatic dicarboxylic acids Chemical class 0.000 description 25
- 238000000746 purification Methods 0.000 description 25
- 238000004090 dissolution Methods 0.000 description 24
- 238000000926 separation method Methods 0.000 description 24
- IVSZLXZYQVIEFR-UHFFFAOYSA-N m-xylene Chemical group CC1=CC=CC(C)=C1 IVSZLXZYQVIEFR-UHFFFAOYSA-N 0.000 description 22
- 239000006185 dispersion Substances 0.000 description 19
- 230000000694 effects Effects 0.000 description 19
- 239000000463 material Substances 0.000 description 19
- 238000002156 mixing Methods 0.000 description 19
- YNQLUTRBYVCPMQ-UHFFFAOYSA-N Ethylbenzene Chemical compound CCC1=CC=CC=C1 YNQLUTRBYVCPMQ-UHFFFAOYSA-N 0.000 description 18
- 239000000126 substance Substances 0.000 description 17
- 230000008901 benefit Effects 0.000 description 16
- 239000005020 polyethylene terephthalate Substances 0.000 description 16
- 229920000139 polyethylene terephthalate Polymers 0.000 description 16
- 238000001556 precipitation Methods 0.000 description 16
- 238000004364 calculation method Methods 0.000 description 15
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 14
- 239000002253 acid Substances 0.000 description 14
- 239000002609 medium Substances 0.000 description 14
- 238000005984 hydrogenation reaction Methods 0.000 description 13
- 230000007246 mechanism Effects 0.000 description 13
- 230000002829 reductive effect Effects 0.000 description 13
- 230000001276 controlling effect Effects 0.000 description 12
- 238000002425 crystallisation Methods 0.000 description 12
- 229910052751 metal Inorganic materials 0.000 description 12
- 239000002184 metal Substances 0.000 description 12
- FXLOVSHXALFLKQ-UHFFFAOYSA-N p-tolualdehyde Chemical compound CC1=CC=C(C=O)C=C1 FXLOVSHXALFLKQ-UHFFFAOYSA-N 0.000 description 12
- 229910002091 carbon monoxide Inorganic materials 0.000 description 11
- 230000008025 crystallization Effects 0.000 description 11
- 238000012546 transfer Methods 0.000 description 11
- KNSIQMPBRNAYMV-UHFFFAOYSA-N 2-(4-carboxyphenyl)terephthalic acid Chemical group C1=CC(C(=O)O)=CC=C1C1=CC(C(O)=O)=CC=C1C(O)=O KNSIQMPBRNAYMV-UHFFFAOYSA-N 0.000 description 10
- XBDQKXXYIPTUBI-UHFFFAOYSA-M Propionate Chemical compound CCC([O-])=O XBDQKXXYIPTUBI-UHFFFAOYSA-M 0.000 description 10
- KXKVLQRXCPHEJC-UHFFFAOYSA-N acetic acid trimethyl ester Natural products COC(C)=O KXKVLQRXCPHEJC-UHFFFAOYSA-N 0.000 description 10
- 238000013461 design Methods 0.000 description 10
- 238000010790 dilution Methods 0.000 description 10
- 239000012895 dilution Substances 0.000 description 10
- 230000007704 transition Effects 0.000 description 10
- SBBQDUFLZGOASY-OWOJBTEDSA-N 4-[(e)-2-(4-carboxyphenyl)ethenyl]benzoic acid Chemical compound C1=CC(C(=O)O)=CC=C1\C=C\C1=CC=C(C(O)=O)C=C1 SBBQDUFLZGOASY-OWOJBTEDSA-N 0.000 description 9
- FJKROLUGYXJWQN-UHFFFAOYSA-N 4-hydroxybenzoic acid Chemical class OC(=O)C1=CC=C(O)C=C1 FJKROLUGYXJWQN-UHFFFAOYSA-N 0.000 description 9
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 9
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 9
- 238000005273 aeration Methods 0.000 description 9
- 229910052799 carbon Inorganic materials 0.000 description 9
- 229910002092 carbon dioxide Inorganic materials 0.000 description 9
- 239000001569 carbon dioxide Substances 0.000 description 9
- 238000007796 conventional method Methods 0.000 description 9
- 230000007423 decrease Effects 0.000 description 9
- 229940058172 ethylbenzene Drugs 0.000 description 9
- 238000010586 diagram Methods 0.000 description 8
- 238000005259 measurement Methods 0.000 description 8
- 238000011084 recovery Methods 0.000 description 8
- 125000004432 carbon atom Chemical group C* 0.000 description 7
- 125000005842 heteroatom Chemical group 0.000 description 7
- 229910052757 nitrogen Inorganic materials 0.000 description 7
- 239000000700 radioactive tracer Substances 0.000 description 7
- 238000006722 reduction reaction Methods 0.000 description 7
- 239000007921 spray Substances 0.000 description 7
- 238000003756 stirring Methods 0.000 description 7
- CQQSQBRPAJSTFB-UHFFFAOYSA-N 4-(bromomethyl)benzoic acid Chemical compound OC(=O)C1=CC=C(CBr)C=C1 CQQSQBRPAJSTFB-UHFFFAOYSA-N 0.000 description 6
- BJCTXUUKONLPPK-UHFFFAOYSA-N 9-oxofluorene-2-carboxylic acid Chemical compound C1=CC=C2C(=O)C3=CC(C(=O)O)=CC=C3C2=C1 BJCTXUUKONLPPK-UHFFFAOYSA-N 0.000 description 6
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 6
- 238000004458 analytical method Methods 0.000 description 6
- 125000002843 carboxylic acid group Chemical group 0.000 description 6
- 238000001816 cooling Methods 0.000 description 6
- 230000029087 digestion Effects 0.000 description 6
- 238000007922 dissolution test Methods 0.000 description 6
- 238000011143 downstream manufacturing Methods 0.000 description 6
- 238000004817 gas chromatography Methods 0.000 description 6
- 238000010438 heat treatment Methods 0.000 description 6
- 230000006872 improvement Effects 0.000 description 6
- 239000012452 mother liquor Substances 0.000 description 6
- 229940078552 o-xylene Drugs 0.000 description 6
- 230000036284 oxygen consumption Effects 0.000 description 6
- 239000000376 reactant Substances 0.000 description 6
- 238000004064 recycling Methods 0.000 description 6
- 230000009467 reduction Effects 0.000 description 6
- 238000007086 side reaction Methods 0.000 description 6
- 239000000243 solution Substances 0.000 description 6
- 238000012360 testing method Methods 0.000 description 6
- LFEWXDOYPCWFHR-UHFFFAOYSA-N 4-(4-carboxybenzoyl)benzoic acid Chemical compound C1=CC(C(=O)O)=CC=C1C(=O)C1=CC=C(C(O)=O)C=C1 LFEWXDOYPCWFHR-UHFFFAOYSA-N 0.000 description 5
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 5
- 150000004056 anthraquinones Chemical class 0.000 description 5
- 235000010290 biphenyl Nutrition 0.000 description 5
- 150000001732 carboxylic acid derivatives Chemical class 0.000 description 5
- 238000011109 contamination Methods 0.000 description 5
- 230000002349 favourable effect Effects 0.000 description 5
- 150000008376 fluorenones Chemical class 0.000 description 5
- 239000011521 glass Substances 0.000 description 5
- 238000004128 high performance liquid chromatography Methods 0.000 description 5
- 238000000589 high-performance liquid chromatography-mass spectrometry Methods 0.000 description 5
- 239000000543 intermediate Substances 0.000 description 5
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 5
- 238000011002 quantification Methods 0.000 description 5
- AFQYQSWTVCNJQT-UHFFFAOYSA-N 9-oxofluorene-4-carboxylic acid Chemical compound O=C1C2=CC=CC=C2C2=C1C=CC=C2C(=O)O AFQYQSWTVCNJQT-UHFFFAOYSA-N 0.000 description 4
- IKHGUXGNUITLKF-UHFFFAOYSA-N Acetaldehyde Chemical compound CC=O IKHGUXGNUITLKF-UHFFFAOYSA-N 0.000 description 4
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 4
- UFWIBTONFRDIAS-UHFFFAOYSA-N Naphthalene Chemical compound C1=CC=CC2=CC=CC=C21 UFWIBTONFRDIAS-UHFFFAOYSA-N 0.000 description 4
- NBBJYMSMWIIQGU-UHFFFAOYSA-N Propionic aldehyde Chemical compound CCC=O NBBJYMSMWIIQGU-UHFFFAOYSA-N 0.000 description 4
- MWPLVEDNUUSJAV-UHFFFAOYSA-N anthracene Chemical compound C1=CC=CC2=CC3=CC=CC=C3C=C21 MWPLVEDNUUSJAV-UHFFFAOYSA-N 0.000 description 4
- 239000012965 benzophenone Substances 0.000 description 4
- ZTQSAGDEMFDKMZ-UHFFFAOYSA-N butyric aldehyde Natural products CCCC=O ZTQSAGDEMFDKMZ-UHFFFAOYSA-N 0.000 description 4
- 150000001721 carbon Chemical group 0.000 description 4
- 230000003197 catalytic effect Effects 0.000 description 4
- 238000006555 catalytic reaction Methods 0.000 description 4
- 239000007806 chemical reaction intermediate Substances 0.000 description 4
- 238000002591 computed tomography Methods 0.000 description 4
- 238000012937 correction Methods 0.000 description 4
- WOZVHXUHUFLZGK-UHFFFAOYSA-N dimethyl terephthalate Chemical class COC(=O)C1=CC=C(C(=O)OC)C=C1 WOZVHXUHUFLZGK-UHFFFAOYSA-N 0.000 description 4
- ZUOUZKKEUPVFJK-UHFFFAOYSA-N diphenyl Chemical compound C1=CC=CC=C1C1=CC=CC=C1 ZUOUZKKEUPVFJK-UHFFFAOYSA-N 0.000 description 4
- 150000002148 esters Chemical class 0.000 description 4
- 238000001704 evaporation Methods 0.000 description 4
- 230000008020 evaporation Effects 0.000 description 4
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 4
- GPSDUZXPYCFOSQ-UHFFFAOYSA-N m-toluic acid Chemical compound CC1=CC=CC(C(O)=O)=C1 GPSDUZXPYCFOSQ-UHFFFAOYSA-N 0.000 description 4
- 238000012423 maintenance Methods 0.000 description 4
- 125000001624 naphthyl group Chemical group 0.000 description 4
- 230000035515 penetration Effects 0.000 description 4
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 4
- 229920000642 polymer Polymers 0.000 description 4
- 238000012545 processing Methods 0.000 description 4
- 238000005070 sampling Methods 0.000 description 4
- 230000001629 suppression Effects 0.000 description 4
- KUCOHFSKRZZVRO-UHFFFAOYSA-N terephthalaldehyde Chemical compound O=CC1=CC=C(C=O)C=C1 KUCOHFSKRZZVRO-UHFFFAOYSA-N 0.000 description 4
- ZRPXGXYVWGQWRD-UHFFFAOYSA-N 1-oxofluorene-2,7-dicarboxylic acid Chemical compound OC(=O)C1=CC=C2C3=CC=C(C(=O)O)C(=O)C3=CC2=C1 ZRPXGXYVWGQWRD-UHFFFAOYSA-N 0.000 description 3
- BSZXAFXFTLXUFV-UHFFFAOYSA-N 1-phenylethylbenzene Chemical compound C=1C=CC=CC=1C(C)C1=CC=CC=C1 BSZXAFXFTLXUFV-UHFFFAOYSA-N 0.000 description 3
- SGKSQSJLZBTPEL-UHFFFAOYSA-N 2-(4-carboxybenzoyl)terephthalic acid Chemical compound C1=CC(C(=O)O)=CC=C1C(=O)C1=CC(C(O)=O)=CC=C1C(O)=O SGKSQSJLZBTPEL-UHFFFAOYSA-N 0.000 description 3
- NEQFBGHQPUXOFH-UHFFFAOYSA-N 4-(4-carboxyphenyl)benzoic acid Chemical group C1=CC(C(=O)O)=CC=C1C1=CC=C(C(O)=O)C=C1 NEQFBGHQPUXOFH-UHFFFAOYSA-N 0.000 description 3
- ZUTFCPOKQHJATC-UHFFFAOYSA-N 9,10-dioxoanthracene-2,6-dicarboxylic acid Chemical compound OC(=O)C1=CC=C2C(=O)C3=CC(C(=O)O)=CC=C3C(=O)C2=C1 ZUTFCPOKQHJATC-UHFFFAOYSA-N 0.000 description 3
- RWQUWTMOHXGTNN-UHFFFAOYSA-N 9-n,10-n-bis(4-butylphenyl)-9-n,10-n-bis(4-methylphenyl)phenanthrene-9,10-diamine Chemical compound C1=CC(CCCC)=CC=C1N(C=1C2=CC=CC=C2C2=CC=CC=C2C=1N(C=1C=CC(C)=CC=1)C=1C=CC(CCCC)=CC=1)C1=CC=C(C)C=C1 RWQUWTMOHXGTNN-UHFFFAOYSA-N 0.000 description 3
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 3
- PJANXHGTPQOBST-VAWYXSNFSA-N Stilbene Chemical class C=1C=CC=CC=1/C=C/C1=CC=CC=C1 PJANXHGTPQOBST-VAWYXSNFSA-N 0.000 description 3
- 150000001299 aldehydes Chemical class 0.000 description 3
- 125000004429 atom Chemical group 0.000 description 3
- 150000004074 biphenyls Chemical group 0.000 description 3
- 239000003795 chemical substances by application Substances 0.000 description 3
- 238000005859 coupling reaction Methods 0.000 description 3
- 230000006324 decarbonylation Effects 0.000 description 3
- 238000006606 decarbonylation reaction Methods 0.000 description 3
- 238000006114 decarboxylation reaction Methods 0.000 description 3
- 238000000151 deposition Methods 0.000 description 3
- 238000003795 desorption Methods 0.000 description 3
- 238000004821 distillation Methods 0.000 description 3
- 238000005516 engineering process Methods 0.000 description 3
- 238000001914 filtration Methods 0.000 description 3
- 230000006870 function Effects 0.000 description 3
- 229910052739 hydrogen Inorganic materials 0.000 description 3
- 238000010191 image analysis Methods 0.000 description 3
- 125000005647 linker group Chemical group 0.000 description 3
- 238000000691 measurement method Methods 0.000 description 3
- 150000002739 metals Chemical class 0.000 description 3
- ZWLPBLYKEWSWPD-UHFFFAOYSA-N o-toluic acid Chemical compound CC1=CC=CC=C1C(O)=O ZWLPBLYKEWSWPD-UHFFFAOYSA-N 0.000 description 3
- 150000002894 organic compounds Chemical class 0.000 description 3
- 150000004965 peroxy acids Chemical class 0.000 description 3
- 239000002244 precipitate Substances 0.000 description 3
- ODLMAHJVESYWTB-UHFFFAOYSA-N propylbenzene Chemical compound CCCC1=CC=CC=C1 ODLMAHJVESYWTB-UHFFFAOYSA-N 0.000 description 3
- 238000010926 purge Methods 0.000 description 3
- 238000000935 solvent evaporation Methods 0.000 description 3
- 230000003068 static effect Effects 0.000 description 3
- PJANXHGTPQOBST-UHFFFAOYSA-N stilbene Chemical class C=1C=CC=CC=1C=CC1=CC=CC=C1 PJANXHGTPQOBST-UHFFFAOYSA-N 0.000 description 3
- 235000021286 stilbenes Nutrition 0.000 description 3
- 150000001911 terphenyls Chemical group 0.000 description 3
- 238000010977 unit operation Methods 0.000 description 3
- 238000009423 ventilation Methods 0.000 description 3
- FYGHSUNMUKGBRK-UHFFFAOYSA-N 1,2,3-trimethylbenzene Chemical class CC1=CC=CC(C)=C1C FYGHSUNMUKGBRK-UHFFFAOYSA-N 0.000 description 2
- QNLZIZAQLLYXTC-UHFFFAOYSA-N 1,2-dimethylnaphthalene Chemical class C1=CC=CC2=C(C)C(C)=CC=C21 QNLZIZAQLLYXTC-UHFFFAOYSA-N 0.000 description 2
- YJTKZCDBKVTVBY-UHFFFAOYSA-N 1,3-Diphenylbenzene Chemical group C1=CC=CC=C1C1=CC=CC(C=2C=CC=CC=2)=C1 YJTKZCDBKVTVBY-UHFFFAOYSA-N 0.000 description 2
- QUBBAXISAHIDNM-UHFFFAOYSA-N 1-ethyl-2,3-dimethylbenzene Chemical class CCC1=CC=CC(C)=C1C QUBBAXISAHIDNM-UHFFFAOYSA-N 0.000 description 2
- PGXYDLMTTDWCIZ-UHFFFAOYSA-N 1-oxofluorene-3,5-dicarboxylic acid Chemical compound C1=CC(C(O)=O)=C2C3=CC(C(=O)O)=CC(=O)C3=CC2=C1 PGXYDLMTTDWCIZ-UHFFFAOYSA-N 0.000 description 2
- ZWEHNKRNPOVVGH-UHFFFAOYSA-N 2-Butanone Chemical compound CCC(C)=O ZWEHNKRNPOVVGH-UHFFFAOYSA-N 0.000 description 2
- SYBYTAAJFKOIEJ-UHFFFAOYSA-N 3-Methylbutan-2-one Chemical compound CC(C)C(C)=O SYBYTAAJFKOIEJ-UHFFFAOYSA-N 0.000 description 2
- 229940090248 4-hydroxybenzoic acid Drugs 0.000 description 2
- JKOCGAMDKVAHCI-UHFFFAOYSA-N 6,7-Benzocoumarin Chemical compound C1=CC=C2C=C(OC(=O)C=C3)C3=CC2=C1 JKOCGAMDKVAHCI-UHFFFAOYSA-N 0.000 description 2
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 2
- WVDDGKGOMKODPV-UHFFFAOYSA-N Benzyl alcohol Chemical class OCC1=CC=CC=C1 WVDDGKGOMKODPV-UHFFFAOYSA-N 0.000 description 2
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 2
- CPELXLSAUQHCOX-UHFFFAOYSA-N Hydrogen bromide Chemical compound Br CPELXLSAUQHCOX-UHFFFAOYSA-N 0.000 description 2
- XEEYBQQBJWHFJM-UHFFFAOYSA-N Iron Chemical compound [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 description 2
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 2
- AMIMRNSIRUDHCM-UHFFFAOYSA-N Isopropylaldehyde Chemical compound CC(C)C=O AMIMRNSIRUDHCM-UHFFFAOYSA-N 0.000 description 2
- ZOKXTWBITQBERF-UHFFFAOYSA-N Molybdenum Chemical compound [Mo] ZOKXTWBITQBERF-UHFFFAOYSA-N 0.000 description 2
- LRHPLDYGYMQRHN-UHFFFAOYSA-N N-Butanol Chemical compound CCCCO LRHPLDYGYMQRHN-UHFFFAOYSA-N 0.000 description 2
- SECXISVLQFMRJM-UHFFFAOYSA-N N-Methylpyrrolidone Chemical compound CN1CCCC1=O SECXISVLQFMRJM-UHFFFAOYSA-N 0.000 description 2
- PXHVJJICTQNCMI-UHFFFAOYSA-N Nickel Chemical compound [Ni] PXHVJJICTQNCMI-UHFFFAOYSA-N 0.000 description 2
- KFSLWBXXFJQRDL-UHFFFAOYSA-N Peracetic acid Chemical compound CC(=O)OO KFSLWBXXFJQRDL-UHFFFAOYSA-N 0.000 description 2
- ISWSIDIOOBJBQZ-UHFFFAOYSA-N Phenol Chemical compound OC1=CC=CC=C1 ISWSIDIOOBJBQZ-UHFFFAOYSA-N 0.000 description 2
- RTAQQCXQSZGOHL-UHFFFAOYSA-N Titanium Chemical compound [Ti] RTAQQCXQSZGOHL-UHFFFAOYSA-N 0.000 description 2
- 238000002835 absorbance Methods 0.000 description 2
- 238000009825 accumulation Methods 0.000 description 2
- 125000000218 acetic acid group Chemical group C(C)(=O)* 0.000 description 2
- 150000007513 acids Chemical class 0.000 description 2
- WNLRTRBMVRJNCN-UHFFFAOYSA-N adipic acid Chemical compound OC(=O)CCCCC(O)=O WNLRTRBMVRJNCN-UHFFFAOYSA-N 0.000 description 2
- 150000001298 alcohols Chemical class 0.000 description 2
- 150000001335 aliphatic alkanes Chemical class 0.000 description 2
- 125000001931 aliphatic group Chemical group 0.000 description 2
- PYKYMHQGRFAEBM-UHFFFAOYSA-N anthraquinone Natural products CCC(=O)c1c(O)c2C(=O)C3C(C=CC=C3O)C(=O)c2cc1CC(=O)OC PYKYMHQGRFAEBM-UHFFFAOYSA-N 0.000 description 2
- 230000009286 beneficial effect Effects 0.000 description 2
- UJMDYLWCYJJYMO-UHFFFAOYSA-N benzene-1,2,3-tricarboxylic acid Chemical class OC(=O)C1=CC=CC(C(O)=O)=C1C(O)=O UJMDYLWCYJJYMO-UHFFFAOYSA-N 0.000 description 2
- QMKYBPDZANOJGF-UHFFFAOYSA-N benzene-1,3,5-tricarboxylic acid Chemical compound OC(=O)C1=CC(C(O)=O)=CC(C(O)=O)=C1 QMKYBPDZANOJGF-UHFFFAOYSA-N 0.000 description 2
- RWCCWEUUXYIKHB-UHFFFAOYSA-N benzophenone Chemical compound C=1C=CC=CC=1C(=O)C1=CC=CC=C1 RWCCWEUUXYIKHB-UHFFFAOYSA-N 0.000 description 2
- 150000008366 benzophenones Chemical class 0.000 description 2
- 230000033228 biological regulation Effects 0.000 description 2
- 239000004305 biphenyl Substances 0.000 description 2
- 238000009835 boiling Methods 0.000 description 2
- QARVLSVVCXYDNA-UHFFFAOYSA-N bromobenzene Chemical class BrC1=CC=CC=C1 QARVLSVVCXYDNA-UHFFFAOYSA-N 0.000 description 2
- 125000002915 carbonyl group Chemical group [*:2]C([*:1])=O 0.000 description 2
- 150000001735 carboxylic acids Chemical class 0.000 description 2
- 230000006835 compression Effects 0.000 description 2
- 238000007906 compression Methods 0.000 description 2
- 238000005094 computer simulation Methods 0.000 description 2
- 229910052802 copper Inorganic materials 0.000 description 2
- 239000010949 copper Substances 0.000 description 2
- 230000008878 coupling Effects 0.000 description 2
- 238000010168 coupling process Methods 0.000 description 2
- 239000012043 crude product Substances 0.000 description 2
- RWGFKTVRMDUZSP-UHFFFAOYSA-N cumene Chemical compound CC(C)C1=CC=CC=C1 RWGFKTVRMDUZSP-UHFFFAOYSA-N 0.000 description 2
- 230000003247 decreasing effect Effects 0.000 description 2
- 230000002950 deficient Effects 0.000 description 2
- 230000001934 delay Effects 0.000 description 2
- 230000008021 deposition Effects 0.000 description 2
- 238000001514 detection method Methods 0.000 description 2
- XBDQKXXYIPTUBI-UHFFFAOYSA-N dimethylselenoniopropionate Natural products CCC(O)=O XBDQKXXYIPTUBI-UHFFFAOYSA-N 0.000 description 2
- 238000001035 drying Methods 0.000 description 2
- 238000010828 elution Methods 0.000 description 2
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 2
- 239000000835 fiber Substances 0.000 description 2
- 238000011049 filling Methods 0.000 description 2
- YLQWCDOCJODRMT-UHFFFAOYSA-N fluoren-9-one Chemical class C1=CC=C2C(=O)C3=CC=CC=C3C2=C1 YLQWCDOCJODRMT-UHFFFAOYSA-N 0.000 description 2
- RMBPEFMHABBEKP-UHFFFAOYSA-N fluorene Chemical compound C1=CC=C2C3=C[CH]C=CC3=CC2=C1 RMBPEFMHABBEKP-UHFFFAOYSA-N 0.000 description 2
- 230000005251 gamma ray Effects 0.000 description 2
- 230000005484 gravity Effects 0.000 description 2
- 150000002432 hydroperoxides Chemical class 0.000 description 2
- ZXEKIIBDNHEJCQ-UHFFFAOYSA-N isobutanol Chemical compound CC(C)CO ZXEKIIBDNHEJCQ-UHFFFAOYSA-N 0.000 description 2
- 239000005351 kimble Substances 0.000 description 2
- OVWYEQOVUDKZNU-UHFFFAOYSA-N m-tolualdehyde Chemical compound CC1=CC=CC(C=O)=C1 OVWYEQOVUDKZNU-UHFFFAOYSA-N 0.000 description 2
- 238000010907 mechanical stirring Methods 0.000 description 2
- TZIHFWKZFHZASV-UHFFFAOYSA-N methyl formate Chemical compound COC=O TZIHFWKZFHZASV-UHFFFAOYSA-N 0.000 description 2
- 229910052750 molybdenum Inorganic materials 0.000 description 2
- 239000011733 molybdenum Substances 0.000 description 2
- 238000012544 monitoring process Methods 0.000 description 2
- 150000002762 monocarboxylic acid derivatives Chemical class 0.000 description 2
- NIHNNTQXNPWCJQ-UHFFFAOYSA-N o-biphenylenemethane Natural products C1=CC=C2CC3=CC=CC=C3C2=C1 NIHNNTQXNPWCJQ-UHFFFAOYSA-N 0.000 description 2
- 230000003287 optical effect Effects 0.000 description 2
- 238000003921 particle size analysis Methods 0.000 description 2
- 239000013618 particulate matter Substances 0.000 description 2
- 230000037361 pathway Effects 0.000 description 2
- FDPIMTJIUBPUKL-UHFFFAOYSA-N pentan-3-one Chemical compound CCC(=O)CC FDPIMTJIUBPUKL-UHFFFAOYSA-N 0.000 description 2
- 238000011020 pilot scale process Methods 0.000 description 2
- 238000009428 plumbing Methods 0.000 description 2
- 125000005575 polycyclic aromatic hydrocarbon group Chemical group 0.000 description 2
- 239000002243 precursor Substances 0.000 description 2
- UOHMMEJUHBCKEE-UHFFFAOYSA-N prehnitene Chemical class CC1=CC=C(C)C(C)=C1C UOHMMEJUHBCKEE-UHFFFAOYSA-N 0.000 description 2
- BDERNNFJNOPAEC-UHFFFAOYSA-N propan-1-ol Chemical compound CCCO BDERNNFJNOPAEC-UHFFFAOYSA-N 0.000 description 2
- 230000010349 pulsation Effects 0.000 description 2
- 230000002285 radioactive effect Effects 0.000 description 2
- 230000009257 reactivity Effects 0.000 description 2
- 230000001105 regulatory effect Effects 0.000 description 2
- 238000001226 reprecipitation Methods 0.000 description 2
- 230000004043 responsiveness Effects 0.000 description 2
- 238000001179 sorption measurement Methods 0.000 description 2
- 229910001220 stainless steel Inorganic materials 0.000 description 2
- 239000010935 stainless steel Substances 0.000 description 2
- 239000010936 titanium Substances 0.000 description 2
- 229910052719 titanium Inorganic materials 0.000 description 2
- 229910052723 transition metal Inorganic materials 0.000 description 2
- 150000003624 transition metals Chemical class 0.000 description 2
- 238000002834 transmittance Methods 0.000 description 2
- 150000003628 tricarboxylic acids Chemical class 0.000 description 2
- 230000005514 two-phase flow Effects 0.000 description 2
- 239000012808 vapor phase Substances 0.000 description 2
- 239000002918 waste heat Substances 0.000 description 2
- WQONPSCCEXUXTQ-UHFFFAOYSA-N 1,2-dibromobenzene Chemical class BrC1=CC=CC=C1Br WQONPSCCEXUXTQ-UHFFFAOYSA-N 0.000 description 1
- UUCHLIAGHZJJER-UHFFFAOYSA-N 1,2-diethylnaphthalene Chemical class C1=CC=CC2=C(CC)C(CC)=CC=C21 UUCHLIAGHZJJER-UHFFFAOYSA-N 0.000 description 1
- MARCAKLHFUYDJE-UHFFFAOYSA-N 1,2-xylene;hydrate Chemical compound O.CC1=CC=CC=C1C MARCAKLHFUYDJE-UHFFFAOYSA-N 0.000 description 1
- QSSXJPIWXQTSIX-UHFFFAOYSA-N 1-bromo-2-methylbenzene Chemical class CC1=CC=CC=C1Br QSSXJPIWXQTSIX-UHFFFAOYSA-N 0.000 description 1
- KTADSLDAUJLZGL-UHFFFAOYSA-N 1-bromo-2-phenylbenzene Chemical class BrC1=CC=CC=C1C1=CC=CC=C1 KTADSLDAUJLZGL-UHFFFAOYSA-N 0.000 description 1
- OBWNDFMWFPAURN-UHFFFAOYSA-N 1-ethyl-2-methyl-3-phenylbenzene Chemical class CCC1=CC=CC(C=2C=CC=CC=2)=C1C OBWNDFMWFPAURN-UHFFFAOYSA-N 0.000 description 1
- HYFLWBNQFMXCPA-UHFFFAOYSA-N 1-ethyl-2-methylbenzene Chemical class CCC1=CC=CC=C1C HYFLWBNQFMXCPA-UHFFFAOYSA-N 0.000 description 1
- RZTDESRVPFKCBH-UHFFFAOYSA-N 1-methyl-4-(4-methylphenyl)benzene Chemical class C1=CC(C)=CC=C1C1=CC=C(C)C=C1 RZTDESRVPFKCBH-UHFFFAOYSA-N 0.000 description 1
- KJCVRFUGPWSIIH-UHFFFAOYSA-N 1-naphthol Chemical class C1=CC=C2C(O)=CC=CC2=C1 KJCVRFUGPWSIIH-UHFFFAOYSA-N 0.000 description 1
- LJRFPYMJMQVHQU-UHFFFAOYSA-N 1-oxofluorene-2-carboxylic acid Chemical class C1=CC=C2C3=CC=C(C(=O)O)C(=O)C3=CC2=C1 LJRFPYMJMQVHQU-UHFFFAOYSA-N 0.000 description 1
- MNLKGWIYXCKWBU-UHFFFAOYSA-N 2,3,4,5,6-pentamethylbenzoic acid Chemical class CC1=C(C)C(C)=C(C(O)=O)C(C)=C1C MNLKGWIYXCKWBU-UHFFFAOYSA-N 0.000 description 1
- JEBOPSGVIIUIQD-UHFFFAOYSA-N 2,3,4,5-tetramethylbenzoic acid Chemical class CC1=CC(C(O)=O)=C(C)C(C)=C1C JEBOPSGVIIUIQD-UHFFFAOYSA-N 0.000 description 1
- HDIJZFORGDBEKL-UHFFFAOYSA-N 2,3,4-trimethylbenzoic acid Chemical class CC1=CC=C(C(O)=O)C(C)=C1C HDIJZFORGDBEKL-UHFFFAOYSA-N 0.000 description 1
- YNVNFMCYBIBHLH-UHFFFAOYSA-N 2,3-dibromobenzoic acid Chemical class OC(=O)C1=CC=CC(Br)=C1Br YNVNFMCYBIBHLH-UHFFFAOYSA-N 0.000 description 1
- RXKWXQVRFBMHCY-UHFFFAOYSA-N 2,3-diethylbenzoic acid Chemical class CCC1=CC=CC(C(O)=O)=C1CC RXKWXQVRFBMHCY-UHFFFAOYSA-N 0.000 description 1
- OYBOMOHJZRNFPM-UHFFFAOYSA-N 2,3-dimethyl-6-phenylbenzoic acid Chemical class OC(=O)C1=C(C)C(C)=CC=C1C1=CC=CC=C1 OYBOMOHJZRNFPM-UHFFFAOYSA-N 0.000 description 1
- RIZUCYSQUWMQLX-UHFFFAOYSA-N 2,3-dimethylbenzoic acid Chemical class CC1=CC=CC(C(O)=O)=C1C RIZUCYSQUWMQLX-UHFFFAOYSA-N 0.000 description 1
- QWBBPBRQALCEIZ-UHFFFAOYSA-N 2,3-dimethylphenol Chemical class CC1=CC=CC(O)=C1C QWBBPBRQALCEIZ-UHFFFAOYSA-N 0.000 description 1
- PVIVWSKQVHYIEI-UHFFFAOYSA-N 2-(bromomethyl)benzaldehyde Chemical class BrCC1=CC=CC=C1C=O PVIVWSKQVHYIEI-UHFFFAOYSA-N 0.000 description 1
- QSLMPDKYTNEMFQ-UHFFFAOYSA-N 2-(bromomethyl)benzoic acid Chemical class OC(=O)C1=CC=CC=C1CBr QSLMPDKYTNEMFQ-UHFFFAOYSA-N 0.000 description 1
- MKWTUDDFTJUKNR-UHFFFAOYSA-N 2-(hydroperoxymethyl)benzoic acid Chemical class OOCC1=CC=CC=C1C(O)=O MKWTUDDFTJUKNR-UHFFFAOYSA-N 0.000 description 1
- UXFFHMWQBGYRBN-UHFFFAOYSA-N 2-(hydroxymethyl)-6-methylbenzaldehyde Chemical class CC1=CC=CC(CO)=C1C=O UXFFHMWQBGYRBN-UHFFFAOYSA-N 0.000 description 1
- SKUCUVAJYLXPGU-UHFFFAOYSA-N 2-(hydroxymethyl)-6-methylbenzoic acid Chemical class CC1=CC=CC(CO)=C1C(O)=O SKUCUVAJYLXPGU-UHFFFAOYSA-N 0.000 description 1
- MGMNPSAERQZUIM-UHFFFAOYSA-N 2-(hydroxymethyl)benzoic acid Chemical class OCC1=CC=CC=C1C(O)=O MGMNPSAERQZUIM-UHFFFAOYSA-N 0.000 description 1
- PGTSKBVCLZBQFK-UHFFFAOYSA-N 2-Phenylmalonaldehyde Chemical class O=CC(C=O)C1=CC=CC=C1 PGTSKBVCLZBQFK-UHFFFAOYSA-N 0.000 description 1
- QXOPAHUDEPTDQJ-UHFFFAOYSA-N 2-bromo-2-phenylethanol Chemical compound OCC(Br)C1=CC=CC=C1 QXOPAHUDEPTDQJ-UHFFFAOYSA-N 0.000 description 1
- JVLVVWMRMZYJLU-UHFFFAOYSA-N 2-bromo-3-(hydroxymethyl)-6-methylbenzaldehyde Chemical class CC1=CC=C(CO)C(Br)=C1C=O JVLVVWMRMZYJLU-UHFFFAOYSA-N 0.000 description 1
- CQNHMBLWYPOGGW-UHFFFAOYSA-N 2-bromo-3-(hydroxymethyl)benzoic acid Chemical class OCC1=CC=CC(C(O)=O)=C1Br CQNHMBLWYPOGGW-UHFFFAOYSA-N 0.000 description 1
- JQJPYFDYIPZQLU-UHFFFAOYSA-N 2-bromo-3-hydroxy-6-methylbenzoic acid Chemical class CC1=CC=C(O)C(Br)=C1C(O)=O JQJPYFDYIPZQLU-UHFFFAOYSA-N 0.000 description 1
- GBPZLKQDSNPABG-UHFFFAOYSA-N 2-bromo-3-hydroxybenzoic acid Chemical class OC(=O)C1=CC=CC(O)=C1Br GBPZLKQDSNPABG-UHFFFAOYSA-N 0.000 description 1
- ICXBPDJQFPIBSS-UHFFFAOYSA-N 2-bromo-6-methylbenzoic acid Chemical class CC1=CC=CC(Br)=C1C(O)=O ICXBPDJQFPIBSS-UHFFFAOYSA-N 0.000 description 1
- NDOPHXWIAZIXPR-UHFFFAOYSA-N 2-bromobenzaldehyde Chemical class BrC1=CC=CC=C1C=O NDOPHXWIAZIXPR-UHFFFAOYSA-N 0.000 description 1
- XRXMNWGCKISMOH-UHFFFAOYSA-N 2-bromobenzoic acid Chemical class OC(=O)C1=CC=CC=C1Br XRXMNWGCKISMOH-UHFFFAOYSA-N 0.000 description 1
- VADKRMSMGWJZCF-UHFFFAOYSA-N 2-bromophenol Chemical class OC1=CC=CC=C1Br VADKRMSMGWJZCF-UHFFFAOYSA-N 0.000 description 1
- SMNNDVUKAKPGDD-UHFFFAOYSA-N 2-butylbenzoic acid Chemical class CCCCC1=CC=CC=C1C(O)=O SMNNDVUKAKPGDD-UHFFFAOYSA-N 0.000 description 1
- GLVYLTSKTCWWJR-UHFFFAOYSA-N 2-carbonoperoxoylbenzoic acid Chemical class OOC(=O)C1=CC=CC=C1C(O)=O GLVYLTSKTCWWJR-UHFFFAOYSA-N 0.000 description 1
- UJCIERMQHAXPRF-UHFFFAOYSA-N 2-ethyl-1-methylnaphthalene Chemical class C1=CC=CC2=C(C)C(CC)=CC=C21 UJCIERMQHAXPRF-UHFFFAOYSA-N 0.000 description 1
- CGMMPMYKMDITEA-UHFFFAOYSA-N 2-ethylbenzoic acid Chemical class CCC1=CC=CC=C1C(O)=O CGMMPMYKMDITEA-UHFFFAOYSA-N 0.000 description 1
- DYNFCHNNOHNJFG-UHFFFAOYSA-N 2-formylbenzoic acid Chemical compound OC(=O)C1=CC=CC=C1C=O DYNFCHNNOHNJFG-UHFFFAOYSA-N 0.000 description 1
- ZORGKHKVEAHWEJ-UHFFFAOYSA-N 2-methyl-6-phenylbenzoic acid Chemical class CC1=CC=CC(C=2C=CC=CC=2)=C1C(O)=O ZORGKHKVEAHWEJ-UHFFFAOYSA-N 0.000 description 1
- QTWJRLJHJPIABL-UHFFFAOYSA-N 2-methylphenol;3-methylphenol;4-methylphenol Chemical class CC1=CC=C(O)C=C1.CC1=CC=CC(O)=C1.CC1=CC=CC=C1O QTWJRLJHJPIABL-UHFFFAOYSA-N 0.000 description 1
- JCYPDKSGYHGCCY-UHFFFAOYSA-N 2-pentylbenzoic acid Chemical class CCCCCC1=CC=CC=C1C(O)=O JCYPDKSGYHGCCY-UHFFFAOYSA-N 0.000 description 1
- BXGXGTXWGGOFSP-UHFFFAOYSA-N 2-phenylethaneperoxoic acid Chemical class OOC(=O)CC1=CC=CC=C1 BXGXGTXWGGOFSP-UHFFFAOYSA-N 0.000 description 1
- GADSJKKDLMALGL-UHFFFAOYSA-N 2-propylbenzoic acid Chemical class CCCC1=CC=CC=C1C(O)=O GADSJKKDLMALGL-UHFFFAOYSA-N 0.000 description 1
- RFTPZYBPPSJAGJ-UHFFFAOYSA-N 3,4,5,6-tetramethylphthalaldehyde Chemical class CC1=C(C)C(C)=C(C=O)C(C=O)=C1C RFTPZYBPPSJAGJ-UHFFFAOYSA-N 0.000 description 1
- KKESUPMSPXDMHO-UHFFFAOYSA-N 3,4,5-trimethylphthalaldehyde Chemical class CC1=CC(C=O)=C(C=O)C(C)=C1C KKESUPMSPXDMHO-UHFFFAOYSA-N 0.000 description 1
- RLPJNKOWKHELHS-UHFFFAOYSA-N 3,4-dimethylphthalaldehyde Chemical class CC1=CC=C(C=O)C(C=O)=C1C RLPJNKOWKHELHS-UHFFFAOYSA-N 0.000 description 1
- SDAMTPCXBPNEQC-UHFFFAOYSA-N 3,4-dimethylphthalic acid Chemical class CC1=CC=C(C(O)=O)C(C(O)=O)=C1C SDAMTPCXBPNEQC-UHFFFAOYSA-N 0.000 description 1
- YNJSNEKCXVFDKW-UHFFFAOYSA-N 3-(5-amino-1h-indol-3-yl)-2-azaniumylpropanoate Chemical compound C1=C(N)C=C2C(CC(N)C(O)=O)=CNC2=C1 YNJSNEKCXVFDKW-UHFFFAOYSA-N 0.000 description 1
- LNTOZTQSWAIFMD-UHFFFAOYSA-N 3-(hydroperoxymethyl)-2-hydroxybenzoic acid Chemical class OOCC1=CC=CC(C(O)=O)=C1O LNTOZTQSWAIFMD-UHFFFAOYSA-N 0.000 description 1
- HZRKCDROLLYLRQ-UHFFFAOYSA-N 3-(hydroxymethyl)phthalic acid Chemical class OCC1=CC=CC(C(O)=O)=C1C(O)=O HZRKCDROLLYLRQ-UHFFFAOYSA-N 0.000 description 1
- ZZGXRPGQPAPARK-UWVGGRQHSA-N 3-[(5r,6r)-1-azabicyclo[3.2.1]octan-6-yl]-4-propylsulfanyl-1,2,5-thiadiazole Chemical compound C1([C@H]2CN3C[C@@]2(CCC3)[H])=NSN=C1SCCC ZZGXRPGQPAPARK-UWVGGRQHSA-N 0.000 description 1
- STBGLXMINLWCNL-UHFFFAOYSA-N 3-bromo-2-hydroxybenzaldehyde Chemical class OC1=C(Br)C=CC=C1C=O STBGLXMINLWCNL-UHFFFAOYSA-N 0.000 description 1
- SRZMKSSXAIRFNR-UHFFFAOYSA-N 3-ethyl-2-methylbenzoic acid Chemical class CCC1=CC=CC(C(O)=O)=C1C SRZMKSSXAIRFNR-UHFFFAOYSA-N 0.000 description 1
- NCZBKZVYANUNBE-UHFFFAOYSA-N 3-formylphthalic acid Chemical class OC(=O)C1=CC=CC(C=O)=C1C(O)=O NCZBKZVYANUNBE-UHFFFAOYSA-N 0.000 description 1
- WLUMYMROFLMGPY-UHFFFAOYSA-N 3-methyl-6-phenylphthalic acid Chemical class OC(=O)C1=C(C(O)=O)C(C)=CC=C1C1=CC=CC=C1 WLUMYMROFLMGPY-UHFFFAOYSA-N 0.000 description 1
- WHSXTWFYRGOBGO-UHFFFAOYSA-N 3-methylsalicylic acid Chemical class CC1=CC=CC(C(O)=O)=C1O WHSXTWFYRGOBGO-UHFFFAOYSA-N 0.000 description 1
- MQLISDXRPCTWDV-UHFFFAOYSA-N 4,5,6-trimethylbenzene-1,2,3-tricarbaldehyde Chemical class CC1=C(C)C(C=O)=C(C=O)C(C=O)=C1C MQLISDXRPCTWDV-UHFFFAOYSA-N 0.000 description 1
- RGHHSNMVTDWUBI-UHFFFAOYSA-N 4-hydroxybenzaldehyde Chemical class OC1=CC=C(C=O)C=C1 RGHHSNMVTDWUBI-UHFFFAOYSA-N 0.000 description 1
- MMFMTASDTOCTLC-UHFFFAOYSA-N 4-methylbenzene-1,2,3-tricarboxylic acid Chemical class CC1=CC=C(C(O)=O)C(C(O)=O)=C1C(O)=O MMFMTASDTOCTLC-UHFFFAOYSA-N 0.000 description 1
- JSBBGWWJLQNXNQ-UHFFFAOYSA-N 4-phenylbenzene-1,2,3-tricarboxylic acid Chemical class OC(=O)C1=C(C(O)=O)C(C(=O)O)=CC=C1C1=CC=CC=C1 JSBBGWWJLQNXNQ-UHFFFAOYSA-N 0.000 description 1
- DUQVVZHRGRVMPF-UHFFFAOYSA-N 5,6-dimethylbenzene-1,2,3,4-tetracarbaldehyde Chemical compound CC1=C(C)C(C=O)=C(C=O)C(C=O)=C1C=O DUQVVZHRGRVMPF-UHFFFAOYSA-N 0.000 description 1
- MTIJWROEGVTEIJ-UHFFFAOYSA-N CC1=CC(=C(C(=C1C=O)C=O)C=O)C Chemical class CC1=CC(=C(C(=C1C=O)C=O)C=O)C MTIJWROEGVTEIJ-UHFFFAOYSA-N 0.000 description 1
- VYZAMTAEIAYCRO-UHFFFAOYSA-N Chromium Chemical compound [Cr] VYZAMTAEIAYCRO-UHFFFAOYSA-N 0.000 description 1
- XDTMQSROBMDMFD-UHFFFAOYSA-N Cyclohexane Chemical compound C1CCCCC1 XDTMQSROBMDMFD-UHFFFAOYSA-N 0.000 description 1
- VGGSQFUCUMXWEO-UHFFFAOYSA-N Ethene Chemical compound C=C VGGSQFUCUMXWEO-UHFFFAOYSA-N 0.000 description 1
- 239000005977 Ethylene Substances 0.000 description 1
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- 206010024769 Local reaction Diseases 0.000 description 1
- 101710092224 Phosphate propanoyltransferase Proteins 0.000 description 1
- QCWXUUIWCKQGHC-UHFFFAOYSA-N Zirconium Chemical compound [Zr] QCWXUUIWCKQGHC-UHFFFAOYSA-N 0.000 description 1
- 230000002159 abnormal effect Effects 0.000 description 1
- IKHGUXGNUITLKF-XPULMUKRSA-N acetaldehyde Chemical compound [14CH]([14CH3])=O IKHGUXGNUITLKF-XPULMUKRSA-N 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 239000001361 adipic acid Substances 0.000 description 1
- 235000011037 adipic acid Nutrition 0.000 description 1
- 230000002411 adverse Effects 0.000 description 1
- 125000004067 aliphatic alkene group Chemical group 0.000 description 1
- 150000001338 aliphatic hydrocarbons Chemical class 0.000 description 1
- 150000001336 alkenes Chemical class 0.000 description 1
- 239000012491 analyte Substances 0.000 description 1
- 238000013459 approach Methods 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 150000003934 aromatic aldehydes Chemical class 0.000 description 1
- 230000000712 assembly Effects 0.000 description 1
- 238000000429 assembly Methods 0.000 description 1
- HULHOBUIBFPLGZ-UHFFFAOYSA-N benzene-1,2,3-tricarbaldehyde Chemical class O=CC1=CC=CC(C=O)=C1C=O HULHOBUIBFPLGZ-UHFFFAOYSA-N 0.000 description 1
- IZALUMVGBVKPJD-UHFFFAOYSA-N benzene-1,3-dicarbaldehyde Chemical class O=CC1=CC=CC(C=O)=C1 IZALUMVGBVKPJD-UHFFFAOYSA-N 0.000 description 1
- AGEZXYOZHKGVCM-UHFFFAOYSA-N benzyl bromide Chemical compound BrCC1=CC=CC=C1 AGEZXYOZHKGVCM-UHFFFAOYSA-N 0.000 description 1
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 1
- 125000001246 bromo group Chemical class Br* 0.000 description 1
- 230000005587 bubbling Effects 0.000 description 1
- 239000006227 byproduct Substances 0.000 description 1
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 1
- 239000003060 catalysis inhibitor Substances 0.000 description 1
- 238000009903 catalytic hydrogenation reaction Methods 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 230000000739 chaotic effect Effects 0.000 description 1
- 238000012512 characterization method Methods 0.000 description 1
- 238000012824 chemical production Methods 0.000 description 1
- 239000007795 chemical reaction product Substances 0.000 description 1
- 239000007805 chemical reaction reactant Substances 0.000 description 1
- 239000003638 chemical reducing agent Substances 0.000 description 1
- 239000013626 chemical specie Substances 0.000 description 1
- 229910052804 chromium Inorganic materials 0.000 description 1
- 239000011651 chromium Substances 0.000 description 1
- 238000000975 co-precipitation Methods 0.000 description 1
- JQGDUUUFOWPCQL-UHFFFAOYSA-N cobalt;naphthalene Chemical class [Co].C1=CC=CC2=CC=CC=C21 JQGDUUUFOWPCQL-UHFFFAOYSA-N 0.000 description 1
- 230000002301 combined effect Effects 0.000 description 1
- 238000010960 commercial process Methods 0.000 description 1
- 238000004891 communication Methods 0.000 description 1
- 230000000052 comparative effect Effects 0.000 description 1
- 239000002131 composite material Substances 0.000 description 1
- 238000010276 construction Methods 0.000 description 1
- 239000004035 construction material Substances 0.000 description 1
- 239000000356 contaminant Substances 0.000 description 1
- 238000010411 cooking Methods 0.000 description 1
- 238000005260 corrosion Methods 0.000 description 1
- 230000007797 corrosion Effects 0.000 description 1
- 239000013078 crystal Substances 0.000 description 1
- 150000001924 cycloalkanes Chemical class 0.000 description 1
- 238000000354 decomposition reaction Methods 0.000 description 1
- 239000008367 deionised water Substances 0.000 description 1
- 229910021641 deionized water Inorganic materials 0.000 description 1
- 230000001627 detrimental effect Effects 0.000 description 1
- 125000004177 diethyl group Chemical class [H]C([H])([H])C([H])([H])* 0.000 description 1
- 238000007865 diluting Methods 0.000 description 1
- 229910001873 dinitrogen Inorganic materials 0.000 description 1
- 150000002009 diols Chemical class 0.000 description 1
- 238000006073 displacement reaction Methods 0.000 description 1
- 239000012153 distilled water Substances 0.000 description 1
- 229910001039 duplex stainless steel Inorganic materials 0.000 description 1
- 230000032050 esterification Effects 0.000 description 1
- 238000005886 esterification reaction Methods 0.000 description 1
- WBJINCZRORDGAQ-UHFFFAOYSA-N ethyl formate Chemical compound CCOC=O WBJINCZRORDGAQ-UHFFFAOYSA-N 0.000 description 1
- 238000002474 experimental method Methods 0.000 description 1
- 238000000605 extraction Methods 0.000 description 1
- 239000004744 fabric Substances 0.000 description 1
- 239000012526 feed medium Substances 0.000 description 1
- 229930003944 flavone Natural products 0.000 description 1
- 150000002213 flavones Chemical class 0.000 description 1
- 235000011949 flavones Nutrition 0.000 description 1
- 238000011010 flushing procedure Methods 0.000 description 1
- 230000004907 flux Effects 0.000 description 1
- 239000006260 foam Substances 0.000 description 1
- 238000005187 foaming Methods 0.000 description 1
- 230000004927 fusion Effects 0.000 description 1
- 238000000227 grinding Methods 0.000 description 1
- 229910052736 halogen Inorganic materials 0.000 description 1
- 150000002367 halogens Chemical class 0.000 description 1
- YUWFEBAXEOLKSG-UHFFFAOYSA-N hexamethylbenzene Chemical class CC1=C(C)C(C)=C(C)C(C)=C1C YUWFEBAXEOLKSG-UHFFFAOYSA-N 0.000 description 1
- 229930195733 hydrocarbon Natural products 0.000 description 1
- 150000002430 hydrocarbons Chemical class 0.000 description 1
- 239000001257 hydrogen Substances 0.000 description 1
- 229910000042 hydrogen bromide Inorganic materials 0.000 description 1
- MEUKEBNAABNAEX-UHFFFAOYSA-N hydroperoxymethane Chemical compound COO MEUKEBNAABNAEX-UHFFFAOYSA-N 0.000 description 1
- YVJRCWCFDJYONJ-UHFFFAOYSA-N hydroperoxymethylbenzene Chemical class OOCC1=CC=CC=C1 YVJRCWCFDJYONJ-UHFFFAOYSA-N 0.000 description 1
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 1
- 125000004029 hydroxymethyl group Chemical group [H]OC([H])([H])* 0.000 description 1
- 229950006430 hydroxytoluic acid Drugs 0.000 description 1
- ZQLCWPXBHUALQC-UHFFFAOYSA-N hydroxytoluic acid Natural products CC1=CC=C(C(O)=O)C=C1O ZQLCWPXBHUALQC-UHFFFAOYSA-N 0.000 description 1
- 239000004615 ingredient Substances 0.000 description 1
- 230000003993 interaction Effects 0.000 description 1
- 229910052742 iron Inorganic materials 0.000 description 1
- 150000002576 ketones Chemical class 0.000 description 1
- 239000005367 kimax Substances 0.000 description 1
- 230000002045 lasting effect Effects 0.000 description 1
- 238000004811 liquid chromatography Methods 0.000 description 1
- 238000011068 loading method Methods 0.000 description 1
- 230000007774 longterm Effects 0.000 description 1
- 238000013178 mathematical model Methods 0.000 description 1
- GQKZBCPTCWJTAS-UHFFFAOYSA-N methoxymethylbenzene Chemical compound COCC1=CC=CC=C1 GQKZBCPTCWJTAS-UHFFFAOYSA-N 0.000 description 1
- 150000004702 methyl esters Chemical class 0.000 description 1
- 230000005012 migration Effects 0.000 description 1
- 238000013508 migration Methods 0.000 description 1
- 239000002480 mineral oil Substances 0.000 description 1
- 235000010446 mineral oil Nutrition 0.000 description 1
- 238000012821 model calculation Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 239000002808 molecular sieve Substances 0.000 description 1
- 239000000178 monomer Substances 0.000 description 1
- 125000001971 neopentyl group Chemical group [H]C([*])([H])C(C([H])([H])[H])(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 229910052759 nickel Inorganic materials 0.000 description 1
- QJGQUHMNIGDVPM-UHFFFAOYSA-N nitrogen(.) Chemical compound [N] QJGQUHMNIGDVPM-UHFFFAOYSA-N 0.000 description 1
- 230000006911 nucleation Effects 0.000 description 1
- 238000010899 nucleation Methods 0.000 description 1
- BTFQKIATRPGRBS-UHFFFAOYSA-N o-tolualdehyde Chemical class CC1=CC=CC=C1C=O BTFQKIATRPGRBS-UHFFFAOYSA-N 0.000 description 1
- 238000004806 packaging method and process Methods 0.000 description 1
- 239000011236 particulate material Substances 0.000 description 1
- BEZDDPMMPIDMGJ-UHFFFAOYSA-N pentamethylbenzene Chemical class CC1=CC(C)=C(C)C(C)=C1C BEZDDPMMPIDMGJ-UHFFFAOYSA-N 0.000 description 1
- 230000008447 perception Effects 0.000 description 1
- 150000002978 peroxides Chemical class 0.000 description 1
- XCRBXWCUXJNEFX-UHFFFAOYSA-N peroxybenzoic acid Chemical class OOC(=O)C1=CC=CC=C1 XCRBXWCUXJNEFX-UHFFFAOYSA-N 0.000 description 1
- 150000002989 phenols Chemical class 0.000 description 1
- 229910052698 phosphorus Inorganic materials 0.000 description 1
- 230000000704 physical effect Effects 0.000 description 1
- 239000004033 plastic Substances 0.000 description 1
- 229920003023 plastic Polymers 0.000 description 1
- 230000010287 polarization Effects 0.000 description 1
- 238000006068 polycondensation reaction Methods 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 238000011175 product filtration Methods 0.000 description 1
- 235000019260 propionic acid Nutrition 0.000 description 1
- 239000012264 purified product Substances 0.000 description 1
- CYIDZMCFTVVTJO-UHFFFAOYSA-N pyromellitic acid Chemical compound OC(=O)C1=CC(C(O)=O)=C(C(O)=O)C=C1C(O)=O CYIDZMCFTVVTJO-UHFFFAOYSA-N 0.000 description 1
- 239000010453 quartz Substances 0.000 description 1
- IUVKMZGDUIUOCP-BTNSXGMBSA-N quinbolone Chemical compound O([C@H]1CC[C@H]2[C@H]3[C@@H]([C@]4(C=CC(=O)C=C4CC3)C)CC[C@@]21C)C1=CCCC1 IUVKMZGDUIUOCP-BTNSXGMBSA-N 0.000 description 1
- 230000005855 radiation Effects 0.000 description 1
- 239000012066 reaction slurry Substances 0.000 description 1
- 230000008707 rearrangement Effects 0.000 description 1
- 238000007670 refining Methods 0.000 description 1
- 230000008521 reorganization Effects 0.000 description 1
- 230000004044 response Effects 0.000 description 1
- 238000006798 ring closing metathesis reaction Methods 0.000 description 1
- 230000000630 rising effect Effects 0.000 description 1
- 150000003839 salts Chemical class 0.000 description 1
- 238000004062 sedimentation Methods 0.000 description 1
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N silicon dioxide Inorganic materials O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 1
- 239000002356 single layer Substances 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- URGAHOPLAPQHLN-UHFFFAOYSA-N sodium aluminosilicate Chemical compound [Na+].[Al+3].[O-][Si]([O-])=O.[O-][Si]([O-])=O URGAHOPLAPQHLN-UHFFFAOYSA-N 0.000 description 1
- 239000012265 solid product Substances 0.000 description 1
- 230000007480 spreading Effects 0.000 description 1
- 238000003892 spreading Methods 0.000 description 1
- 239000012258 stirred mixture Substances 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
- 238000000859 sublimation Methods 0.000 description 1
- 230000008022 sublimation Effects 0.000 description 1
- 238000006467 substitution reaction Methods 0.000 description 1
- 239000008399 tap water Substances 0.000 description 1
- 235000020679 tap water Nutrition 0.000 description 1
- CIHOLLKRGTVIJN-UHFFFAOYSA-N tert‐butyl hydroperoxide Chemical compound CC(C)(C)OO CIHOLLKRGTVIJN-UHFFFAOYSA-N 0.000 description 1
- 238000010998 test method Methods 0.000 description 1
- 150000000000 tetracarboxylic acids Chemical class 0.000 description 1
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 1
- QENJZWZWAWWESF-UHFFFAOYSA-N tri-methylbenzoic acid Natural products CC1=CC(C)=C(C(O)=O)C=C1C QENJZWZWAWWESF-UHFFFAOYSA-N 0.000 description 1
- 229910052721 tungsten Inorganic materials 0.000 description 1
- 238000009827 uniform distribution Methods 0.000 description 1
- 238000011144 upstream manufacturing Methods 0.000 description 1
- 238000003828 vacuum filtration Methods 0.000 description 1
- 229910052720 vanadium Inorganic materials 0.000 description 1
- 238000011179 visual inspection Methods 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
- 239000003643 water by type Substances 0.000 description 1
- 238000005303 weighing Methods 0.000 description 1
- 238000010626 work up procedure Methods 0.000 description 1
- 229910052726 zirconium Inorganic materials 0.000 description 1
Images
Classifications
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J8/00—Chemical or physical processes in general, conducted in the presence of fluids and solid particles; Apparatus for such processes
- B01J8/0015—Feeding of the particles in the reactor; Evacuation of the particles out of the reactor
- B01J8/003—Feeding of the particles in the reactor; Evacuation of the particles out of the reactor in a downward flow
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J10/00—Chemical processes in general for reacting liquid with gaseous media other than in the presence of solid particles, or apparatus specially adapted therefor
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J8/00—Chemical or physical processes in general, conducted in the presence of fluids and solid particles; Apparatus for such processes
- B01J8/18—Chemical or physical processes in general, conducted in the presence of fluids and solid particles; Apparatus for such processes with fluidised particles
- B01J8/1818—Feeding of the fluidising gas
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J8/00—Chemical or physical processes in general, conducted in the presence of fluids and solid particles; Apparatus for such processes
- B01J8/18—Chemical or physical processes in general, conducted in the presence of fluids and solid particles; Apparatus for such processes with fluidised particles
- B01J8/1872—Details of the fluidised bed reactor
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J8/00—Chemical or physical processes in general, conducted in the presence of fluids and solid particles; Apparatus for such processes
- B01J8/18—Chemical or physical processes in general, conducted in the presence of fluids and solid particles; Apparatus for such processes with fluidised particles
- B01J8/20—Chemical or physical processes in general, conducted in the presence of fluids and solid particles; Apparatus for such processes with fluidised particles with liquid as a fluidising medium
- B01J8/22—Chemical or physical processes in general, conducted in the presence of fluids and solid particles; Apparatus for such processes with fluidised particles with liquid as a fluidising medium gas being introduced into the liquid
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J8/00—Chemical or physical processes in general, conducted in the presence of fluids and solid particles; Apparatus for such processes
- B01J8/18—Chemical or physical processes in general, conducted in the presence of fluids and solid particles; Apparatus for such processes with fluidised particles
- B01J8/20—Chemical or physical processes in general, conducted in the presence of fluids and solid particles; Apparatus for such processes with fluidised particles with liquid as a fluidising medium
- B01J8/22—Chemical or physical processes in general, conducted in the presence of fluids and solid particles; Apparatus for such processes with fluidised particles with liquid as a fluidising medium gas being introduced into the liquid
- B01J8/222—Chemical or physical processes in general, conducted in the presence of fluids and solid particles; Apparatus for such processes with fluidised particles with liquid as a fluidising medium gas being introduced into the liquid in the presence of a rotating device only
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C51/00—Preparation of carboxylic acids or their salts, halides or anhydrides
- C07C51/16—Preparation of carboxylic acids or their salts, halides or anhydrides by oxidation
- C07C51/21—Preparation of carboxylic acids or their salts, halides or anhydrides by oxidation with molecular oxygen
- C07C51/255—Preparation of carboxylic acids or their salts, halides or anhydrides by oxidation with molecular oxygen of compounds containing six-membered aromatic rings without ring-splitting
- C07C51/265—Preparation of carboxylic acids or their salts, halides or anhydrides by oxidation with molecular oxygen of compounds containing six-membered aromatic rings without ring-splitting having alkyl side chains which are oxidised to carboxyl groups
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C51/00—Preparation of carboxylic acids or their salts, halides or anhydrides
- C07C51/42—Separation; Purification; Stabilisation; Use of additives
- C07C51/487—Separation; Purification; Stabilisation; Use of additives by treatment giving rise to chemical modification
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C63/00—Compounds having carboxyl groups bound to a carbon atoms of six-membered aromatic rings
- C07C63/14—Monocyclic dicarboxylic acids
- C07C63/15—Monocyclic dicarboxylic acids all carboxyl groups bound to carbon atoms of the six-membered aromatic ring
- C07C63/26—1,4 - Benzenedicarboxylic acid
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2208/00—Processes carried out in the presence of solid particles; Reactors therefor
- B01J2208/00008—Controlling the process
- B01J2208/00017—Controlling the temperature
- B01J2208/00106—Controlling the temperature by indirect heat exchange
- B01J2208/00265—Part of all of the reactants being heated or cooled outside the reactor while recycling
- B01J2208/00292—Part of all of the reactants being heated or cooled outside the reactor while recycling involving reactant solids
- B01J2208/003—Part of all of the reactants being heated or cooled outside the reactor while recycling involving reactant solids involving reactant slurries
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2208/00—Processes carried out in the presence of solid particles; Reactors therefor
- B01J2208/00743—Feeding or discharging of solids
- B01J2208/00761—Discharging
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2208/00—Processes carried out in the presence of solid particles; Reactors therefor
- B01J2208/00796—Details of the reactor or of the particulate material
- B01J2208/00823—Mixing elements
- B01J2208/00831—Stationary elements
- B01J2208/0084—Stationary elements inside the bed, e.g. baffles
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2208/00—Processes carried out in the presence of solid particles; Reactors therefor
- B01J2208/00796—Details of the reactor or of the particulate material
- B01J2208/00823—Mixing elements
- B01J2208/00858—Moving elements
- B01J2208/00867—Moving elements inside the bed, e.g. rotary mixer
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2219/00—Chemical, physical or physico-chemical processes in general; Their relevant apparatus
- B01J2219/00002—Chemical plants
- B01J2219/00004—Scale aspects
- B01J2219/00006—Large-scale industrial plants
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2219/00—Chemical, physical or physico-chemical processes in general; Their relevant apparatus
- B01J2219/00002—Chemical plants
- B01J2219/00027—Process aspects
- B01J2219/0004—Processes in series
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Engineering & Computer Science (AREA)
- Combustion & Propulsion (AREA)
- Oil, Petroleum & Natural Gas (AREA)
- General Chemical & Material Sciences (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Physical Or Chemical Processes And Apparatus (AREA)
- Low-Molecular Organic Synthesis Reactions Using Catalysts (AREA)
Abstract
Description
図1は、本発明の一実施態様に従って構築された酸化反応器の側面図であり、反応器中への供給流、酸化剤流及び還流の導入、反応器中における多相反応媒体の存在並びに反応器の頂部(top)及び底部(bottom)のそれぞれからの気体及びスラリーの回収を特に示し;
図2は、図3のライン2−2に沿った気泡塔型反応器の底部の拡大側断面図であり、反応器への酸化剤流の導入に使用される酸化剤スパージャーの位置及び構造を特に示し;
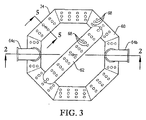
図3は、図2の酸化剤スパージャーの上面図であり、酸化剤スパージャー頂部の酸化剤用開口部を特に示し;
図4は、図2の酸化剤スパージャーの底面図であり、酸化剤スパージャーの底部の開口部を特に示し;
図5は、図3のライン5−5に沿った酸化剤スパージャーの側断面図であり、酸化剤スパージャーの頂部及び底部の酸化剤用開口部の幾何学的配置を特に示し;
図6は、気泡塔型反応器の底部の拡大側面図であり、垂直方向に間隔をあけられた複数の位置において反応器中へ供給流を導入するためのシステムを特に示し;
図7は、図6のライン7−7に沿った上断面図であり、図6に示される供給材料導入システムが好ましい半径方向供給ゾーン(FZ)及び方位角の1つより多いクアドラント(Q1、Q2、Q3、Q4)に供給流を分配する様子を特に示し;
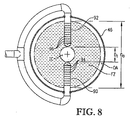
図8は、図7と同様な上断面図であるが、多数の小さい供給開口部をそれぞれ有するバヨネットチューブを用いて反応器中に供給流を排出するための代替手段を示し;
図9は、多数の容器貫通を必要とせずに垂直方向に間隔をあけられた複数の位置において反応ゾーン中に供給流を導入するための代替システムの等角図であり、供給材料分配システムが酸化剤スパージャー上で少なくとも部分的に支持され得ることを示し;
図10は、図9に示された貫通が1つの供給材料分配システム及び酸化剤スパージャーの側面図であり;
図11は、酸化剤スパージャー上において支持された貫通が1つの供給材料分配系を更に示す、図10のライン11−11に沿った上断面図であり;
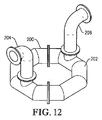
図12は、酸化剤用開口部の全てがリング部材の底部に配置された代替酸化剤スパージャーの等角図であり;
図13は、図12の代替酸化剤スパージャーの上面図であり;
図14は、図12の代替酸化剤スパージャーの底面図であり、反応ゾーン中に酸化剤流を導入するための底部開口部の位置を特に示し;
図15は、図13のライン15−15に沿った酸化剤スパージャーの側断面図であり、下方の酸化剤用開口部の幾何学的配置を特に示し;
図16は、反応器の底部出口近くに内部脱気容器を装着した気泡塔型反応器の側面図であり;
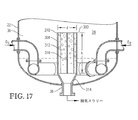
図17は、図18のライン17−17に沿った図16の気泡塔型反応器の下部(lower portion)の拡大側断面図であり、気泡塔型反応器の底部出口に配置された内部脱気容器の形状を特に示し;
図18は、図16のライン18−18に沿った上断面図であり、脱気容器中に配設されたボルテックスブレーカーを特に示し;
図19は、外部脱気容器を装着した気泡塔型反応器の側面図であり、脱気容器の底部から出る脱気されたスラリーの一部が、反応器の底部に連結されたデ−インベントリー・ライン(de-inventorying line)を流し出すのに用いられる様子を示し;
図20は、反応器の側部の高い位置から回収される反応媒体の気相を離脱させるための内部/外部複合型脱気容器を装着した気泡塔型反応器の側面図であり;
図21は、反応器の底部近くに代替複合型脱気容器を装着した気泡塔型反応器の側面図であり;
図22は、図21の気泡塔型反応器の下部の拡大側断面図であり、反応器の底部ヘッドを通して酸化剤流を受ける入口導管を用いる代替酸化剤スパージャーの使用を特に示し;
図23は、図22と同様な拡大側断面図であり、反応器中において酸化剤流をより均一に分配するための衝突板を場合によっては用いて、反応器の下部ヘッド中の多数の開口部を経て反応器中に酸化剤流を導入するための代替手段を特に示し;
図24は、反応器の上部(upper portion)から反応器の下部に反応媒体の一部を循環させることによって被酸化性化合物の分散の改善に役立つ内部流通導管を用いる気泡塔型反応器の側面図であり;
図25は、反応器の上部から反応器の下部に反応媒体の一部を循環させることによって被酸化性化合物の分散の改善に役立つ外部流通導管を用いる気泡塔型反応器の側面図であり;
図26は、酸化反応器内における被酸化性化合物の分散を改良するために使用できる横型エダクターの側断面図であり、反応媒体をエダクター中に引き込むために流入液体供給材料を用い且つ供給材料と反応媒体との混合物を高速で反応ゾーン中に排出するエダクターを特に示し;
図27は、酸化反応器中における被酸化性化合物の分散を改良するために使用できる縦型エダクターの側断面図であり、液体供給材料と流入ガスを合し、そして合した二相流体を用いて、反応媒体をエダクター中に引き込み且つ液体供給材料、流入気体及び反応媒体の混合物を高速で反応ゾーン中に排出するエダクターを特に示し;
図28は、多相反応媒体を含む気泡塔型反応器の側面図であり、反応媒体中のいくつかの勾配を定量化するために等容積の30個の水平スライスに理論的に分割されている反応媒体を特に示し;
図29は、多相反応媒体を含む気泡塔型反応器の側面図であり、かなり異なる酸素濃度及び/又は酸素消費速度を有する、第1及び第2の独立した20%連続容量の反応媒体を特に示し;
図30は、任意の機械的撹拌を用いる又は用いない、多相反応媒体を含む2つの積み重ね反応器の側面図であり、反応器が、かなり異なる酸素濃度及び/又は酸素消費速度を有する、独立した20%連続容量の反応媒体を含むことを特に示し;
図31は、任意の機械的撹拌を用いる又は用いない、多相反応媒体を含む3つの並列反応器の側面図であり、反応器が、かなり異なる酸素濃度及び/又は酸素消費速度を有する、独立した20%連続容量の反応媒体を含むことを特に示し;
図32A及び32Bは、本発明の一実施態様に従って製造された粗製テレフタル酸(CTA)粒子の拡大図であり、各CTA粒子が、多数の緩く結合したCTA子粒子から成る低密度高表面積の粒子であることを特に示し;
図33A及び33Bは、常法に従って製造されたCTAの拡大図であり、従来のCTA粒子は、図32A及び32Bの本発明のCTA粒子よりも粒度が大きく、密度が低く且つ表面積が小さいことを特に示し;
図34は、先行技術の精製テレフタル酸(PTA)の製造方法の簡略化した工程系統図であり;そして
図35は、本発明の一実施態様に係るPTA製造方法の簡略化した工程系統図である。
このプロットから、Vm及びCを求めた。次に、77°Kにおける窒素の断面積を用いて下記式によってVmを表面積に変換した:
S=A+B*(1−exp(−C*t))
[式中、t=時間(単位:分);
S=時間tにおける溶解度(単位:THF中ppm);
exp=2の自然対数の底における指数関数;
A,B=回帰定数(regressed constant)(単位:THF中のppm)(Aは、非常に短い時間における比較的小さい粒子の急速な溶解に主に関連し;A+Bの和は、指定された試験期間の終わり近くにおける全溶解量に主に関連する);
C=回帰時定数(regressed time constant)(単位:レシプロカル分)]。
USA,80 Skyline Drive,Plainview,NY 11803)。中に入れる。Agilent 8453 Diode Array Spectrophtometerを用いて、この充填フローセルを通して種々の波長の光の透過率を測定する(Agilent Technologies,395 Page Mill Raod,Palo Alto,CA 94303)。セル及び使用溶媒を含む(これらに限定するものではない)バックグラウンドから吸光度を補正後、溶液を透過する入射光線の割合を表すパーセント透過率の結果を、機械によって直接的に記録する。波長340nm及び400nmにおけるパーセント透過率値は、純粋なTPAを、その中に典型的によく見られる多くの不純物と識別するのに特に有用である。
(生成される一酸化炭素のモル数)対(供給される被酸化性芳香族化合物のモル数)の比は、好ましくは約0.005:1超、より好ましくは約0.010:1超、更に好ましくは約0.015:1超、最も好ましくは0.020:1超である。同時に、(生成される一酸化炭素のモル数)対(供給される被酸化性芳香族化合物のモル数)の比は好ましくは約0.09:1未満、より好ましくは約0.07:1未満、更に好ましくは約0.05:1未満、最も好ましくは0.04:1未満である。
これは、気泡塔型反応器中におけるp−キシレンの商業的酸化からの操作例である。この例は、例えば本発明の態様に従って適当な幾何学的条件及びプロセス条件を用いる場合にはp−キシレンの濃度に関して大きな垂直方向勾配(vertical gradients)が存在することを示す。
例2〜5は、例1の反応器と全く同一の又は特定の改良を加えられたが例1とほぼ同様な気泡塔型反応器の計算モデルである。例2〜5を生成するために行った計算上の流体動態(CFD)モデリングは、係属中の米国特許出願第60/594,774号(タイトル:Modeling of Liquid−Phase Oxidation)に開示されたモデルリング方法に従って実施した。この特許出願を引用することによってここに組み入れる。
この例は、例1の機械的構造に関する計算を発展させ、例3及び4に対する比較基準を設定する。この例において、気泡塔型反応器の機械的構造は例1と同一であり、p−キシレン及び濾液溶媒を含む供給流のための、反応器壁を貫通する直径0.076mの円形入口孔を有する。p−キシレンの供給速度は約1.84kg/秒であり、例1よりも速い。p−キシレンと充分に混合すて供給する濾液溶媒の供給速度は約18.4gk/秒である。従って、壁孔を通って入ってくるp−キシレン+濾液溶媒の合わさった流れの空塔速度は約4m/秒である。気体離脱ヘッドスペース中における還流溶媒の供給速度は12.8kg/秒である。酸化剤スパージャーを通る圧縮空気の供給速度は約9kg/秒である。反応スラリーの固形分は約31重量%である。生成物スラリーは、反応器下部ヘッドの中央から、反応媒体の約25mの概ね定常の液面を保持する効果的な定常速度を用いて回収する。反応媒体の中央高さの平均ガス・ホールドアップは面積平均、時間平均基準で約55%であり、時間平均の長さは少なくとも約100秒のCFDモデル時間である。反応媒体の上方のヘッドスペース中の圧力は約0.50メガパスカル(ゲージ)である。反応媒体の中央高さ近くで測定された温度は約160℃である。反応媒体の液体部分内の水、コバルト、臭素及びマンガンの含量は例1と本質的に同じである。
この例は、本発明の一態様に従って、反応媒体に入る点における、p−キシレンを含む液相供給材料の空塔速度を増加させることによるp−キシレン供給材料の分散の改善に関して計算を発展させる。この例において、気泡塔型反応器の機械的構造は、p−キシレンを含む液体供給材料が入る壁孔の円直径を0.025mまで減少させる以外は例2と同一である。p−キシレン供給速度及び他のプロセス条件は、壁孔を通って入るp−キシレン+濾液溶媒の合わさった液相供給流の空塔速度がここでは約36m/秒である以外は、例2の場合と同一である。
この例は、酸化剤及びp−キシレンを気泡塔型反応器中に導入するための改良された機械的手段に関して計算を発展させる。この例は、例1〜3において使用するのと同じ気泡塔型反応器内で行う。しかし、反応器は、反応媒体中への酸化剤及びp−キシレンの入れ方に関して修正した。例4の説明においては、第一に、p−キシレンを反応媒体に入れるための修正装置、従ってp−キシレン濃度の高いゾーンの減少に注意を向ける。第二に、酸化剤を反応体に入れるための修正装置、従って通気の不良なゾーンの減少に注意を向ける。これは、2つの修正が結果の点で完全に独立していることを前提とするものではなく、単に段階的な提示である。
例5及び6は、商業用気泡塔型反応器において、本発明の開示に従って、通気の不良な領域を最小化すること、垂直方向、方位角及び半径方向により分散されるように商用純度p−キシレンの導入方法を改良すること、並びに分子状酸素の利用可能性が最高の点により近くなるように商用純度p−キシレンの入口を下げることの重要性を示す操作例である。更にこれらの例は高位置スラリー出口による収率のメリットを示す。
この例において使用される気泡塔型反応器は、例1及び2の反応器と実質的に同じ機械的構造を有する。この反応器は、例6に匹敵するプロセス条件で運転し、比較基準を提供する。運転液面は反応媒体の約25mの高さであった。商用純度のp−キシレンの供給が約81kg/分の速度で効果的に定常であった。濾液溶媒は約793kg/分の効果的な定常速度で供給した。この濾液溶媒の未計量の部分は導管サイズ及び圧力低下から約20kg/分であると推定して、液体フラッシとして酸化剤スパージャーに供給した。濾液の残り約773kg/分は商用純度のp−キシレンとよく混合して供給した。濾液溶媒及び商用純度のp−キシレンの合わさった液相供給流は約854kg/分となった。この濾液溶媒はプラント再循還システムに由来し、酢酸及び水約97%超を含んでいた。濾液溶媒中の触媒成分の濃度は、反応媒体の液相内の組成がコバルト約2,158ppmw、臭素約1,911ppmw及びマンガン約118ppmwとなるようなものであった。還流溶媒の別の流れを、反応媒体の運転液面の上方の気体離脱ゾーン中に液滴として約546kg/分の効果的な定常速度で供給した。この還流溶媒は酢酸及び水約99重量%超からなり;還流溶媒は、触媒成分レベルをほとんど含まない別のプラント再循還システムに由来する。濾液供給材料及び還流溶媒供給材料の合わさった含水量は、反応媒体の液相内の水の濃度が約5.8重量%となるようなものであった。酸化剤は、約352kg/分の効果的な定常速度で圧縮空気供給した。反応器ヘッド気体中の運転圧は定常的に約0.42メパスカル(ゲージ)であった。この反応器は、反応熱が入ってくる供給材料の温度を上昇させ且つ入ってくる溶媒の多くを蒸発させるように、実質的に断熱的に運転した。反応媒体の中央高さ近くで測定した運転温度は約154.6℃であった。粗製テレフタル酸(CTA)を含む、出て行くスラリーは、反応器の下部楕円形ヘッドの底部近くか約428kg/分の効果的な定常速度で除去した。
この例の気泡塔型反応器は、計算例である例4において発展させた機械的構造に相当する。この例の反応器は、p−キシレン供給材料の入口の高さ、速度、数及び間隔の改善を含み、従って、p−キシレン供給材料の分配を改善し且つ分子状酸素に対する改良された段階付け(staging)をもたらす。この例の反応器は、改善された酸化剤スパージャーを用いることによる、反応媒体を出ていくスラリーを除去及び脱気するための高さ及び方法における、反応媒体内の通気の質の改善を更に含む。例5に比較して、p−キシレンの収率に関して重要な改善が見られ、不純物の生成に関して重要な減少が見られる。
例7〜10は、特に反応媒体へのp−キシレンの初期分散に関連する計算例であるが、本発明の他の態様も示す。
この例は、蒸発したp−キシレンの供給に関する。この計算例において、p−キシレン供給材料は、反応媒体に入る前に加熱及び蒸発させる。これはp−キシレンの初期分散を助ける。これは、入ってくる容量を増大させ、速度の増加を容易にする。更に、これは、入ってくるp−キシレンのバルク液相への移動を遅らせ、p−キシレン供給材料を、分子状酸素の気体供給とよりよく調和させて反応性液相に向けて移動させる。
この例は部分蒸発されたp−キシレンの供給に関する。この計算例において、p−キシレン供給材料は、反応媒体に入る前に酸化剤供給材料と混合することによって部分蒸発させる。これは、p−キシレンの初期分散を助ける。これは、入ってくる容量を増大させ、速度の増加を容易にし、p−キシレンの濃度を稀釈する。更に、これは、入ってくるp−キシレンのバルク液相への移動を遅らせ、p−キシレン供給材料を、分子状酸素の気体供給とよりよく調和させて、反応性液相に向けて移動させる。
この例は、液体エダクターを用いた、反応器壁から離れた位置からのp−キシレンの供給に関する。この計算例においては、p−キシレン液体供給材料の初期分散を、推進力として液体流を使用するエダクターを用いることによって改善する。この例の反応器は、以下の点を除いて例4と同じ機械的構造及びプロセス境界条件を有する。p−キシレン+濾液溶媒の混合液相流は、同一の公称3インチの流通導管を通って同一高さで反応器壁に流れ込む。しかし、例4の内部液相供給分配システムではなく、図26の図に示されるような、当業界で知られたフローエダクター中の駆動流体として、混合液相流を反応媒体中に放出する。エダクターは、駆動流体に0.1メガパスカルの圧力差を生じるように設計する。エダクターは、フロープルームが下部TLの上方約4.5mの高さで反応器の軸中心線に沿って垂直方向上向きに出ていくように位置及び向きを設定する。排出され且つ駆動液体と混合される反応媒体の容積は、排出口における気泡塔中の気泡群の確率現象に応じて経時的に変動する。しかし、時間平均排出流は、駆動流体流よりも大きく、従って、入ってくるp−キシレンがより急速に稀釈される。その後の混合及び化学反応は気泡塔における通常の確率現象に従って起こる。
この例は、気液エダクターを用いて反応器壁から離れた位置にp−キシレンを供給することに関する。この計算例においては、推進力として気体流を使用するエダクターを用いることによってp−キシレンの初期稀釈を改善する。この例の反応器は、以下の点を除いて例4と同じ機械的構造及びプロセス境界条件を有する。八角形の酸化剤スパージャー及び液相供給分配システムを共に取り除く。代わりに、入ってくる酸化剤流とp−キシレン+濾液溶媒の混合液相流とを別々の導管を通して反応器内部に運搬する。両流れは図27のダイアグラムに示されるような、当業界において知られるフローエダクターの入口において駆動流体として一緒になる。このエダクターは反応器の軸中心線に沿って垂直にまっすぐ配置する。このエダクターは、出口が下向きであって且つ反応器の下部接線の下方0.2mに位置するように配置する。このエダクターは、駆動流体に0.1メガパスカルの圧力差を生じるように設計する。2つの温度センサーを、圧縮空気供給材料とp−キシレン供給材料とが最初に一緒になる位置の近くに配置する。これらの温度センサーは、高温が検知されたら酸化剤及びp−キシレンの供給を止めるように、アラーム及びインターロックに接続する。
例11〜13は、導管中において反応媒体からの液体の流れを用いてp−キシレンの反応媒体中への初期分散を助けることに特に関する計算例であるが、本発明の他の態様も示す。
この例は、液体の運搬に反応器内の流通導管を用いて、入ってくるp−キシレンの初期分散を助けることに関する。この例の反応器は、以下の点を除いて例4と同じ機械的構造及びプロセス境界条件を有する。図24のダイアグラムを参照する。p−キシレン+濾液溶媒の混合液相流は例4と同様な公称3インチの流通導管を通って反応器に入る。しかし、例4の内部液相供給分配系は取り除き、代わりに混合液体流を流通導管中に放出する。流通導管は、反応器の下部TLの上方1mにあるその下端を含むその全長のほとんどが約0.15mの円内径を有する。流通導管は反応器の下部TLから上方に21mの全高まで垂直に伸びる。反応器の下部TLの上方20mの高さにおいて、流通導管はm高さが更に1m上昇する間に、流通導管は内部断面積が0.5m2となるように拡大する。前記流通導管のこのより直径の大きい上部セクションを内部脱気容器と考えることができ、それが実際には一部分は反応器壁を用いて形成される。この流通導管全体を反応器の内側に配置する。流通導管への頂部入口において、反応媒体はp−キシレン及びp−トルアルデヒドが非常に欠乏しているが、p−トルイル酸及び4−カルボキシベンズアルデヒドの重要な濃度が存在する。前記流通導管の頂部に入る反応媒体は実質的に脱気され、反応器の他の部分よりもこの流通導管の内側に密度の高い媒体を生じる。流通導管内のスラリーは約150kg/秒と推定される速度で下向きに移動し、その時点で、流通導管の全長にわたって積算された流動圧降下が、この流通導管の全長にわたって積算された内側と外側の密度差とバランスのとれた状態になる。スラリーのこの下向きの流れのうち約104kg/秒が液体であり、約69重量%に相当する。合計約20.2kg/秒の、充分に混合されたp−キシレンと濾液溶媒の供給流は、下部TLの上方約5mの高さで前記流通導管に入る。この混合物は次に、1秒未満で流通導管の下方へ更に4m(約27導管直径)進み、感知できる程度まで混合される。このようにして、p−キシレンの濃度は、気泡塔内の反応媒体本体中に放出される前に、約15,000ppmwまで有効に低下される。その後の混合及び化学反応は気泡塔における通常の確率現象に従って起こる。
この例は、液体の運搬に反応器の外側の流通導管を用いて、入ってくるp−キシレンの初期分散を助けることに関する。この例の反応器は、以下の点を除いて例11と同じ機械的構造及びプロセス境界条件を有し、図25のダイアグラムに関連する。内部流通導管は取り除き、代わりに外部流通導管が用いる。反応器を外部脱気セクションに接続する導管の部分は0.30mの内側円直径を有し、下部TLの上方20mに位置する。外部脱気セクションの内側円直径は1mであり、その高さは2mである。脱気セクションの下方の流通導管の内側円直径は0.20mであり、ほぼ同じの利用可能な高さのヘッドを用いてより大きな流速を可能にする。流速を所望の範囲に調節するために、流量センサー及び流量調節弁を流通導管に装着する。例えば、流量調節は、例11の内部流通導管を経て行われると推定されるのと同じ150kg/秒のスラリー運搬を実現するように設定する。p−キシレン及び濾液溶媒の混合液相流は反応器の下部TLから上方約5mで外部流通導管に入る。外部流通導管の出口は反応器の下部ヘッドに接続する。従って、p−キシレン濃度は再び気泡塔内の反応媒体本体中に放出する前に約15,000ppmwまで有効に低下させる。その後の混合及び化学反応は、気泡塔における通常の確率現象に従って起こる。後処理のための生成物スラリーの回収は、脱気セクションの下方で、p−キシレン及び濾液溶媒の液相流の添加の前にこの流通導管の枝管を経て行い、その結果、スラリーの除去脱気のための別のシステムが必要ない。
この例は、液体の運搬に反応器外部及び内部の両方のセクションからなる流通導管を用いて、入っていくp−キシレンの初期分散を助けることに関する。この計算例は、外部流通導管中の第2の枝管が反応器の下部TLから上方約3mに位置し且つそれがp−キシレン及び濾液溶媒の混合液相流の添加点より下方であることを除いて、例12と同じである。第2の分岐流通導管も0.20mの内側円直径を有する。別の流量調節弁を、再び流量を調節するために、第2の分岐流通導管中に配置する。この分岐流通導管は下部TLから上方3mにおいて反応器側壁を貫通し、分岐流通導管は反応器壁内側に0.4m伸びる。従って、分岐導管は反応器の外部及び内部の両方のセクションを含む。流れは、底部ヘッドの導管出口又は側壁内部の導管出口の一方を通って又は任意の比率で両方を通って反応器に入ることができる。
Claims (27)
- (a)分子状酸素を含む酸化剤流を気泡塔型反応器の反応ゾーン中に導入し;
(b)p−キシレンを含む供給流を、最大直径(D)を有する、前記反応ゾーン中に導入し(但し、p−キシレンの少なくとも30重量%は、前記分子状酸素が前記反応ゾーンに入る最低位置の約1.5D以内において前記反応ゾーンに入る);そして
(c)前記反応ゾーンに含まれる多相反応媒体の液相中において前記p−キシレンを酸化させる
ことを含んでなる方法。 - 前記p−キシレンの少なくとも約50重量%を、前記分子状酸素が前記反応ゾーンに入る最低位置の約2.5D以内において、前記反応ゾーン中に導入する請求項1に記載の方法。
- 前記p−キシレンの少なくとも約75重量%を、前記分子状酸素が前記反応ゾーンに入る最低位置の約5D以内において、前記反応ゾーン中に導入する請求項1に記載の方法。
- 前記供給流を、複数の供給開口部を経て、前記反応ゾーン中に導入し、前記供給開口部の少なくとも2つを、互いに垂直方向に少なくとも約0.5Dの間隔をあけて配置する請求項1に記載の方法。
- 前記供給開口部の少なくとも2つを、互いに垂直方向に少なくとも約1.5Dの間隔をあけて配置する請求項4に記載の方法。
- 前記供給流を、前記反応ゾーンを1対の交差垂直面によって等容積の4つの垂直クアドラント(quadrant)に理論的に分割する場合に、前記p−キシレンの約80重量%以下が前記垂直クアドラントの単一のクアドラント中において前記反応ゾーンに入るように、前記反応ゾーン中に導入する請求項1に記載の方法。
- 前記反応ゾーンの少なくとも一部分を、前記反応器の1つ又はそれ以上の直立側壁によって規定し、前記p−キシレンの少なくとも約25重量%が、前記直立側壁から内側に少なくとも0.05Dの間隔をあけて配置された1つ又はそれ以上の位置において、前記反応ゾーンに入る請求項1に記載の方法。
- 前記反応媒体が最大高さ(H)、最大幅(W)及び少なくとも約3:1のH:W比を有する請求項1に記載の方法。
- 前記H:W比が約8:1〜約20:1の範囲である請求項8に記載の方法。
- 前記分子状酸素の大部分が、前記反応ゾーンの底部の約0.25W以内において、前記反応ゾーンに入る請求項8に記載の方法。
- 前記酸化が、前記反応媒体中で前記p−キシレンの少なくとも約10重量%に、固体を形成させる請求項1に記載の方法。
- 前記酸化を、コバルト、臭素及びマンガンを含む触媒系の存在下で、実施する請求項1に記載の方法。
- 前記酸化を、前記反応ゾーンを等容積の30個の水平スライスに理論的に分割した場合に、pX−max水平スライスが前記の30個の水平スライスの全ての最大p−キシレン濃度を有し且つpX−minが前記pX−max水平スライスの上方に位置するすべての水平スライスの最小p−キシレン濃度を有するように、実施し、前記p−キシレン濃度を前記反応媒体の液相中で時間平均及び容積平均重量基準で測定し、そして(前記pX−max水平スライスのp−キシレン濃度)対(前記pX−min水平スライスのp−キシレン濃度)の比が少なくとも約5:1である請求項1に記載の方法。
- 前記酸化を、前記反応ゾーンを、等容積の30個の水平スライスに理論的に分割した場合に、O2−max水平スライスが前記の30個の水平スライスの全ての最大酸素濃度を有し且つO2−min水平スライスが前記O2−max水平スライスの上方に位置するすべての水平スライスの最小酸素濃度を有するように、実施し、前記酸素濃度を前記反応媒体の気相中で時間平均及び容積平均モル湿潤基準で測定し、そして(前記O2−max水平スライスの酸素濃度)対(前記O2−min水平スライスの酸素濃度)の比が少なくとも約2:1である請求項1に記載の方法。
- 前記方法が、前記粗製テレフタル酸の少なくとも一部を二次酸化反応器における酸化に供することを含む請求項1に記載の方法。
- 前記二次酸化反応器中における前記酸化を、前記気泡塔型反応器中における前記酸化よりも少なくとも約10℃高い平均温度において、実施する請求項15に記載の方法。
- 前記二次酸化反応器中における前記酸化を、前記気泡塔型の平均温度よりも約20〜約80℃高い範囲の平均温度において実施し、前記気泡塔型反応器中における前記酸化を約140〜約180℃の範囲の平均温度において実施し、前記二次酸化反応器中における前記酸化を約180〜約220℃の範囲の平均温度において実施する請求項15に記載の方法。
- 前記酸化が前記反応媒体中において前記粗製テレフタル酸の固体粒子を形成させ、前記粗製テレフタル酸粒子の代表サンプルが以下の特性:
(i)約12ppmw未満の4,4−ジカルボキシスチルベン(4,4−DCS)を含み、
(ii)約800ppmw未満のイソフタル酸(IPA)を含み、
(iii)約100ppmw未満の2,6−ジカルボキシフルオレノン(2,6−DCF)を含み、
(iv)340nmにおけるパーセント透過率(%T340)が約25より高い
の1つ又はそれ以上を有する請求項1に記載の方法。 - 主に液相の流れと主に気相の流れとを反応させるための気泡塔型反応器であって、
常態での直立中心シェル軸に沿って伸びる細長い反応ゾーンを規定する容器シェル(前記反応ゾーンは、互いに最大距離(L)をあけて配置された常態での(垂直)下端及び常態での(垂直)上端を有し、前記反応ゾーンは最大直径(D)を有し、前記反応ゾーンは少なくとも約3:1のL:D比を有する);
前記気相流を前記反応ゾーン中に排出するための1つ又はそれ以上の気体用開口部(前記気体用開口部の少なくとも1つは、前記の常態での下端の約0.25D以内に配置する);及び
前記液相流を前記反応ゾーン中に導入するための1つ又はそれ以上の液体用開口部(前記液体用開口部の全てによって規定される累積孔面積の少なくとも約30%が、前記の常態での下端の最も近くに位置する気体用開口部から約1.5Dの軸距離を開けて配置された液体用開口部による)
を含んでなる気泡塔型反応器。 - 前記液体用開口部の全てによって規定される累積孔面積の少なくとも約50%が、前記の常態での下端の最も近くに位置する気体用開口部から約2.5D未満の軸距離をあけて配置された液体用開口部によるものである請求項19に記載の気泡塔型反応器。
- 前記液体用開口部の全てによって規定される累積孔面積の少なくとも約75%が、前記の常態での下端の最も近くに位置する気体用開口部から約5D未満の軸距離をあけて配置された液体用開口部によるものである請求項19に記載の気泡塔型反応器。
- 前記反応器が、互いに少なくとも約0.5Dの間隔をあけて配置された少なくとも2つの液体用開口部を含む請求項19に記載の気泡塔型反応器。
- 前記反応器が、互いに少なくとも約1.5Dの間隔をあけて配置された少なくとも2つの液体用開口部を含む請求項19に記載の気泡塔型反応器。
- 前記反応ゾーンを1対の交差垂直面によって等容積の4つの垂直クアドラントに理論的に分割する場合に、前記液体用開口部の全てによって規定される累積孔面積の約80%以下を前記垂直クアドラントの共通の1つに配置した請求項19に記載の気泡塔型反応器。
- 前記反応ゾーンの少なくとも一部を、前記反応器の1つ又はそれ以上の直立側壁によって規定し、前記液体用開口部の全てによって規定される累積孔面積の少なくとも約25%が、前記直立側壁から内側に少なくとも0.05Dの間隔をあけて配置された液体用開口部によるものである請求項19に記載の気泡塔型反応器。
- 前記気体用開口部の全てによって規定される累積孔面積の大部分を、前記反応ゾーンの前記の常態での下端の約0.022L以内に配置した請求項19に記載の気泡塔型反応器。
- Lが約20〜約75mの範囲であり、Dが約2〜約10の範囲であり、前記L:D比が約8:1〜約20:1の範囲である請求項19に記載の気泡塔型反応器。
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US60665304P | 2004-09-02 | 2004-09-02 | |
| US63155904P | 2004-11-29 | 2004-11-29 | |
| US11/153,994 US7910769B2 (en) | 2004-09-02 | 2005-06-16 | Optimized liquid-phase oxidation |
| PCT/US2005/030659 WO2006028771A2 (en) | 2004-09-02 | 2005-08-29 | Optimized liquid-phase oxidation |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2008511649A true JP2008511649A (ja) | 2008-04-17 |
| JP2008511649A5 JP2008511649A5 (ja) | 2008-10-16 |
Family
ID=35781255
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2007530229A Pending JP2008511649A (ja) | 2004-09-02 | 2005-08-29 | 最適化液相酸化 |
Country Status (13)
| Country | Link |
|---|---|
| US (2) | US7910769B2 (ja) |
| EP (1) | EP1786556B1 (ja) |
| JP (1) | JP2008511649A (ja) |
| KR (2) | KR101281442B1 (ja) |
| CN (1) | CN101010134B (ja) |
| BR (2) | BR122015022124B8 (ja) |
| CA (1) | CA2576795A1 (ja) |
| ES (1) | ES2617727T3 (ja) |
| LT (1) | LT1786556T (ja) |
| MX (1) | MX2007002515A (ja) |
| PL (1) | PL1786556T3 (ja) |
| PT (1) | PT1786556T (ja) |
| WO (1) | WO2006028771A2 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2016040312A (ja) * | 2010-01-29 | 2016-03-24 | グルーポ ペトロテメックス,ソシエダ アノニマ デ カピタル バリアブレ | 側方取り出し式の第2の反応器を備える酸化システム |
Families Citing this family (21)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2006031422A2 (en) * | 2004-09-02 | 2006-03-23 | Eastman Chemical Company | Optimized liquid-phase oxidation |
| US7692036B2 (en) | 2004-11-29 | 2010-04-06 | Eastman Chemical Company | Optimized liquid-phase oxidation |
| US7910769B2 (en) | 2004-09-02 | 2011-03-22 | Eastman Chemical Company | Optimized liquid-phase oxidation |
| US7987613B2 (en) * | 2004-10-12 | 2011-08-02 | Great River Energy | Control system for particulate material drying apparatus and process |
| US20070155987A1 (en) * | 2006-01-04 | 2007-07-05 | O'meadhra Ruairi S | Oxidative digestion with optimized agitation |
| US20070208194A1 (en) | 2006-03-01 | 2007-09-06 | Woodruff Thomas E | Oxidation system with sidedraw secondary reactor |
| US7393973B2 (en) * | 2006-03-01 | 2008-07-01 | Eastman Chemical Company | Polycarboxylic acid production system with enhanced residence time distribution for oxidative digestion |
| US7501537B2 (en) * | 2006-03-01 | 2009-03-10 | Eastman Chemical Company | Polycarboxylic acid production system employing oxidative digestion with reduced or eliminated upstream liquor exchange |
| US7326807B2 (en) * | 2006-03-01 | 2008-02-05 | Eastman Chemical Company | Polycarboxylic acid production system with enhanced heating for oxidative digestion |
| US7816556B2 (en) * | 2006-03-01 | 2010-10-19 | Eastman Chemical Company | Polycarboxylic acid production system employing enhanced multistage oxidative digestion |
| US7772424B2 (en) * | 2006-03-01 | 2010-08-10 | Eastman Chemical Company | Polycarboxylic acid production system employing enhanced evaporative concentration downstream of oxidative digestion |
| US7420082B2 (en) * | 2006-03-01 | 2008-09-02 | Eastman Chemical Company | Polycarboxylic acid production system employing hot liquor removal downstream of oxidative digestion |
| US7326808B2 (en) * | 2006-03-01 | 2008-02-05 | Eastman Chemical Company | Polycarboxylic acid production system employing cooled mother liquor from oxidative digestion as feed to impurity purge system |
| CN101143811B (zh) * | 2007-09-29 | 2010-06-23 | 中国石化仪征化纤股份有限公司 | 利用鼓泡塔氧化反应器生产芳香酸的方法 |
| FR2953596B1 (fr) * | 2009-12-09 | 2013-12-20 | Rhodia Operations | Procede et installation de determination, d'au moins un parametre d'une transformation faisant intervenir un transfert entre un gaz et un liquide |
| US8790601B2 (en) * | 2010-01-29 | 2014-07-29 | Grupo Petrotemex, S.A. De C.V. | Oxidation system with sidedraw secondary reactor |
| US8936767B2 (en) * | 2010-01-29 | 2015-01-20 | Grupo Petrotemex. S.A. de C.V. | Oxidation system with sidedraw secondary reactor |
| CN102826522A (zh) * | 2012-08-28 | 2012-12-19 | 滨海雅克化工有限公司 | 一种用氧气氧化法生产三氯氧磷的环流反应装置 |
| EP2837424A1 (de) * | 2013-08-13 | 2015-02-18 | TARTECH eco industries AG | Schlackenbrecher |
| US10000435B1 (en) | 2017-02-28 | 2018-06-19 | Grupo Petrotemex, S.A. De C.V. | Energy and environmentally integrated method for production of aromatic dicarboxylic acids by oxidation |
| CN114950284B (zh) * | 2022-05-19 | 2023-01-10 | 台州学院 | 一种气液鼓泡流化床的气体射流优选方法 |
Citations (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS5257134A (en) * | 1975-10-31 | 1977-05-11 | Mitsubishi Chem Ind Ltd | Process for preparation of aromatic polycarboxylic acids |
| JPS62192490A (ja) * | 1986-02-19 | 1987-08-24 | Nippon Steel Corp | 酸化処理用気泡塔 |
| JPH01160476A (ja) * | 1987-12-16 | 1989-06-23 | Nippon Sharyo Seizo Kaisha Ltd | 気泡塔型反応装置 |
| JPH09278709A (ja) * | 1996-02-13 | 1997-10-28 | Mitsubishi Chem Corp | 芳香族カルボン酸の製造方法 |
| JPH10330292A (ja) * | 1996-12-12 | 1998-12-15 | Praxair Technol Inc | 気泡塔反応器への直接的酸素注入法 |
| JP2001247511A (ja) * | 2000-03-07 | 2001-09-11 | Mitsubishi Chemicals Corp | 芳香族カルボン酸の製造方法 |
| US6504051B1 (en) * | 2001-06-04 | 2003-01-07 | Eastman Chemical Company | Process for production of aromatic carboxylic acids with improved water removal technique |
| JP2006509044A (ja) * | 2002-12-09 | 2006-03-16 | イーストマン ケミカル カンパニー | 粗製カルボン酸スラリーの精製方法 |
| JP2008511645A (ja) * | 2004-09-02 | 2008-04-17 | イーストマン ケミカル カンパニー | 最適化液相酸化 |
| JP2008511648A (ja) * | 2004-09-02 | 2008-04-17 | イーストマン ケミカル カンパニー | 最適化液相酸化 |
Family Cites Families (253)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US1902550A (en) | 1930-01-31 | 1933-03-21 | Nat Synthetic Corp | Process of oxidizing cyclic organic compounds |
| US1936427A (en) | 1930-01-31 | 1933-11-21 | Nat Synthetic Corp | Process of oxidizing naphthalene and related condensed aromatic ring compounds |
| US2572575A (en) | 1949-09-23 | 1951-10-23 | Monsanto Chemicals | Preparation of terephthalic acid |
| US2572710A (en) | 1949-09-23 | 1951-10-23 | Monsanto Chemicals | Preparation of terephthalic acid |
| US3064044A (en) * | 1957-08-15 | 1962-11-13 | Standard Oil Co | Multistage oxidation system for preparing dicarboxylic acid |
| US3082250A (en) | 1958-05-05 | 1963-03-19 | Standard Oil Co | Recovery of phthalic acid products |
| US3071447A (en) | 1958-09-09 | 1963-01-01 | Whiting Corp | Hydraulic classifier |
| US3029278A (en) | 1958-12-11 | 1962-04-10 | Standard Oil Co | Process for separation of phthalic acids |
| US3257363A (en) | 1961-05-22 | 1966-06-21 | Phillips Petroleum Co | Control of the composition of a reaction mixture |
| GB1007570A (en) | 1961-07-24 | 1965-10-13 | Socaty | Process for the catalytic oxidation of xylenes or industrial mixtures of xylenes |
| BE621323A (ja) | 1961-08-14 | |||
| US3216481A (en) | 1962-04-17 | 1965-11-09 | Badger Co | Recovery of phthalic and maleic acid from solutions |
| NL294776A (ja) * | 1962-10-06 | |||
| US3244744A (en) | 1963-02-27 | 1966-04-05 | Standard Oil Co | Separation process for isophthalic acid and terephthalic acid |
| FR1394471A (fr) | 1963-04-30 | 1965-04-02 | Standard Oil Co | Perfectionnements aux procédés pour la préparation d'acides benzène-polycarboxyliques de haute pureté |
| DE1493192A1 (de) | 1963-04-30 | 1969-02-20 | Standard Oil Co | Verfahren zur Herstellung von aromatischen Saeuren |
| DE1276628C2 (de) | 1963-05-20 | 1975-01-16 | Rudzki, Henryk Stanislaw, Dr., Los Angeles, Calif. (V.St.A.) | Verfahren zur herstellung von isophtalsaeure und/oder terephthalsaeure |
| US3410897A (en) | 1963-10-10 | 1968-11-12 | Maruzen Oil Company Ltd | Purification of terephthalic acid |
| US3388157A (en) | 1965-02-10 | 1968-06-11 | Ethyl Corp | Process for the production of dicarboxylic acids |
| NL6606774A (ja) | 1965-05-17 | 1966-11-18 | ||
| GB1142864A (en) | 1965-11-15 | 1969-02-12 | Ici Ltd | Crystallisation process |
| US3497552A (en) | 1966-07-18 | 1970-02-24 | Standard Oil Co | Continuous crystallization in a plurality of cooling stages using dilutions by cooled solvent of feed to each stage |
| US3549695A (en) | 1966-09-01 | 1970-12-22 | Mobil Oil Corp | Method for downflow leaching |
| US3534090A (en) | 1966-11-04 | 1970-10-13 | Mobil Oil Corp | Hydrocarbon oxidation |
| US3584039A (en) | 1967-08-30 | 1971-06-08 | Standard Oil Co | Fiber-grade terephthalic acid by catalytic hydrogen treatment of dissolved impure terephthalic acid |
| US3556733A (en) | 1968-04-05 | 1971-01-19 | Struthers Scientific Int Corp | Fines dissolver for crystallizers |
| FR2006269A1 (ja) | 1968-04-16 | 1969-12-26 | Celanese Corp | |
| US3850981A (en) | 1968-04-16 | 1974-11-26 | Celanese Corp | Liquid phase oxidation of p-xylene to terephthalic acid |
| US3626001A (en) | 1968-05-09 | 1971-12-07 | Atlantic Richfield Co | Method for the production of high-purity isophthalic or terephthalic acid |
| AT282466B (de) | 1968-07-25 | 1970-06-25 | Oemv Ag | Bitumenblasverfahren und Einrichtung zur Durchführung desselben |
| DE1792402A1 (de) | 1968-08-29 | 1971-11-11 | Dynamit Nobel Ag | Verfahren zur Durchfuehrung exothermer chemischer Reaktionen in heterogenen Gas-Fluessigkeits-Gemischen |
| GB1250222A (ja) | 1968-10-25 | 1971-10-20 | ||
| CA849014A (en) | 1968-10-25 | 1970-08-11 | Ichikawa Yataro | Apparatus for continuous gas-liquid contact and process for refining crude terephthalic acid |
| US3660476A (en) | 1968-10-30 | 1972-05-02 | Teijin Ltd | Method for the preparation of terephthalic acid |
| US3708532A (en) | 1968-11-04 | 1973-01-02 | Teijin Ltd | Process for the continuous purification of crude terephthalic acid |
| BE724040A (ja) | 1968-11-18 | 1969-05-02 | ||
| US3700731A (en) | 1969-02-28 | 1972-10-24 | Du Pont | Process for oxidizing xylenes to phthalic acids |
| US3629321A (en) | 1969-05-26 | 1971-12-21 | Standard Oil Co | Integration of para-xylene oxidation to terephthalic acid and its esterification to dimethyl terephthalate |
| US3683018A (en) | 1969-05-26 | 1972-08-08 | Standard Oil Co | Integrated oxidation of isomeric xylene mixture to isomeric phthalic acid mixture and separation of mixture of isomeric phthalic acids into individual isomer products |
| US3839436A (en) | 1969-05-26 | 1974-10-01 | Standard Oil Co | Integration of para-or meta-xylene oxidation to terephthalic acid or isophthalic acid and its purification by hydrogen treatment of aqueous solution |
| DE1927937A1 (de) | 1969-05-31 | 1970-12-17 | Dynamit Nobel Ag | Verfahren zur Herstellung von Benzoldicarbonsaeuren bzw. Benzoldicarbonsaeureestern |
| US3873275A (en) | 1969-09-29 | 1975-03-25 | Whiting Corp | Crystallization apparatus and method |
| BE759284A (fr) | 1969-11-24 | 1971-05-24 | Shell Int Research | Procede et appareil pour la mise en contact d'un liquide avec des particules solides |
| GB1301291A (ja) | 1969-12-01 | 1972-12-29 | ||
| US3686293A (en) | 1970-07-13 | 1972-08-22 | Giorgio Gualdi | Process for the preparation of aromatic carboxylic acids |
| JPS5328419B1 (ja) | 1971-04-26 | 1978-08-15 | ||
| US3785779A (en) | 1971-08-02 | 1974-01-15 | Exxon Research Engineering Co | Gas liquid inlet distributor |
| JPS5544644B2 (ja) | 1971-09-23 | 1980-11-13 | ||
| GB1373230A (en) | 1971-12-23 | 1974-11-06 | Mitsui Petrochemical Ind | Process for producing terephthalic acid |
| JPS5234590B2 (ja) | 1971-12-28 | 1977-09-03 | ||
| NL169993C (nl) * | 1972-01-13 | 1982-09-16 | Maruzen Oil Co Ltd | Werkwijze ter bereiding van tereftaalzuur. |
| DE2217003C2 (de) * | 1972-04-08 | 1983-12-15 | Chemische Werke Hüls AG, 4370 Marl | Verfahren und Vorrichtung zur kontinuierlichen Herstellung von gesättigten aliphatischen Dicarbonsäuren |
| GB1428831A (en) | 1972-05-20 | 1976-03-17 | Teijin Ltd | Separation of aromatic carboxylic acids |
| US3845117A (en) | 1972-12-14 | 1974-10-29 | Halcon International Inc | Process for preparation of phthalic acids |
| JPS5328421B2 (ja) | 1973-05-15 | 1978-08-15 | ||
| US3931305A (en) | 1973-08-20 | 1976-01-06 | Standard Oil Company | Terephthalic acid recovery by continuous flash crystallization |
| JPS5328902B2 (ja) | 1973-09-14 | 1978-08-17 | ||
| US4053506A (en) | 1975-05-02 | 1977-10-11 | Standard Oil Company (Indiana) | Production of fiber-grade terephthalic acid |
| US3997620A (en) | 1975-10-28 | 1976-12-14 | Uop Inc. | Process for separating para-xylene |
| JPS5278846A (en) | 1975-12-25 | 1977-07-02 | Matsuyama Sekyu Kagaku Kk | Continuous production of high purity telephthalic acid |
| NL170133C (nl) | 1976-02-24 | 1982-10-01 | Matsuyama Petrochemicals Inc | Werkwijze voor de bereiding van een aromatisch dicarbonzuur. |
| SU1126202A3 (ru) | 1976-05-28 | 1984-11-23 | Институт Фор Атомэнерги (Фирма) | Способ непрерывной многостадийной кристаллизации из раствора |
| DE2623977C3 (de) | 1976-05-28 | 1979-04-12 | Nukem Gmbh, 6450 Hanau | Verfahren und Vorrichtung zur Herstellung von rieselfähigem, direkt verpressbarem Urandioxid-Pulver |
| US4081464A (en) | 1976-07-26 | 1978-03-28 | Standard Oil Company | Iso- or terephthalic acid production in and recovery from benzoic acid-water solvent system |
| US4185073A (en) | 1976-07-26 | 1980-01-22 | Standard Oil Company (Indiana) | Apparatus for iso- or terephthalic acid production in and recovery from benzoic acid-water solvent system |
| GB1542320A (en) | 1976-10-26 | 1979-03-14 | Labofina Sa | Process for the preparation of aromatic dicarboxylic acids |
| NL188282C (nl) | 1977-04-04 | 1992-05-18 | Montedison Spa | Werkwijze voor de synthese van tereftaalzuur door oxyderen van p-xyleen in azijnzuuroplossing. |
| US4158738A (en) | 1977-05-26 | 1979-06-19 | E. I. Du Pont De Nemours And Company | Process for the production of fiber-grade terephthalic acid |
| US4482524A (en) | 1978-01-31 | 1984-11-13 | Ari Technologies, Inc. | Autocirculation apparatus |
| DE2805915C3 (de) | 1978-02-13 | 1981-11-05 | Dynamit Nobel Ag, 5210 Troisdorf | Reaktor zur Oxidation von Gemischen aus p-Xylol und p-Toluylsäuremethylester mit sauerstoffhaltigen Gasen in flüssiger Phase |
| US4233269A (en) | 1978-11-09 | 1980-11-11 | Exxon Research & Engineering Co. | Gas liquid distributor |
| US4263448A (en) | 1979-03-30 | 1981-04-21 | Halcon Research And Development Corp. | Process for oxidation of hydrocarbons |
| US4255590A (en) | 1979-11-08 | 1981-03-10 | Standard Oil Company (Indiana) | Combination of pyrolysis and incineration of solid mixture of oxygen-containing aromatic compounds obtained as residue of manufacture of benzene di- and tricarboxylic acids |
| IT1129759B (it) | 1980-01-23 | 1986-06-11 | Montedison Spa | Metodo per ricuperare in forma attiva i componenti del sistema catalitico della sintesi dell'acido tereftalico |
| GB2072162B (en) | 1980-03-21 | 1984-03-21 | Labofina Sa | Process for the production and the recovery of terephthalic acid |
| DE3047101A1 (de) | 1980-12-13 | 1982-07-22 | Hoechst Ag, 6000 Frankfurt | Verfahren zum verbessern der gasverteilung in mammut-schlaufenreaktoren |
| US4342876A (en) | 1980-12-22 | 1982-08-03 | Bechtel International Corporation | Method for oxidation of p-xylene and method for preparing dimethylterephthalate |
| US4334086A (en) | 1981-03-16 | 1982-06-08 | Labofina S.A. | Production of terephthalic acid |
| US4459365A (en) * | 1981-05-29 | 1984-07-10 | Mitsubishi Gas Chemical Company, Inc. | Method of recovering a catalytic metal |
| US4456767A (en) * | 1981-07-27 | 1984-06-26 | Rhone-Poulenc, Inc. | Solvent and catalyst recovery and recycle in the manufacture of phenoxybenzoic acid |
| US4391985A (en) | 1981-11-16 | 1983-07-05 | Eastman Kodak Company | Process for the separation of isophthalic acid from terephthalic acid |
| DE3363127D1 (en) | 1982-02-09 | 1986-05-28 | Bbc Brown Boveri & Cie | Method and apparatus for treating a liquid with a gas |
| JPS59104345A (ja) | 1982-12-03 | 1984-06-16 | Kuraray Yuka Kk | 直接重合用に適したテレフタル酸の製造方法 |
| JPS59106435A (ja) | 1982-12-10 | 1984-06-20 | Mitsubishi Chem Ind Ltd | 高純度テレフタル酸の製法 |
| JPS6036439A (ja) | 1983-08-09 | 1985-02-25 | Mitsubishi Chem Ind Ltd | テレフタル酸の製法 |
| US4500732A (en) | 1983-09-15 | 1985-02-19 | Standard Oil Company (Indiana) | Process for removal and recycle of p-toluic acid from terephthalic acid crystallizer solvent |
| US4769487A (en) | 1984-08-20 | 1988-09-06 | Amoco Corporation | Multistage oxidation in a single reactor |
| US4605763A (en) | 1984-08-31 | 1986-08-12 | Eastman Kodak Company | Process for the purification of terephthalic acid |
| US4777287A (en) | 1984-10-29 | 1988-10-11 | Amoco Corporation | Recycle of vaporized solvent in liquid phase oxidation of an alkyl aromatic |
| US4835307A (en) | 1984-12-13 | 1989-05-30 | Amoco Corporation | Method and apparatus for controlling the manufacture of terephthalic acid to control the level and variability of the contaminant content and the optical density |
| US4648999A (en) | 1985-07-22 | 1987-03-10 | M. W. Kellogg Company | Apparatus for contacting fluid with solid |
| GB8527335D0 (en) | 1985-11-06 | 1985-12-11 | Ici Plc | Fermentation process |
| US4892970A (en) | 1985-12-30 | 1990-01-09 | Amoco Corporation | Staged aromatics oxidation in aqueous systems |
| US5099064A (en) | 1985-12-30 | 1992-03-24 | Amoco Corporation | Method for increasing conversion efficiency for oxidation of an alkyl aromatic compound to an aromatic carboxylic acid |
| DE3625261A1 (de) | 1986-07-25 | 1988-02-04 | Basf Ag | Verfahren zur kontinuierlichen hydroformylierung olefinisch ungesaettigter verbindungen |
| US4769489A (en) | 1986-07-28 | 1988-09-06 | Amoco Corporation | Catalyst recovery method |
| US4914230A (en) | 1986-07-28 | 1990-04-03 | Amoco Corporation | Catalyst recovery method |
| JPH078821B2 (ja) | 1986-09-26 | 1995-02-01 | 三井石油化学工業株式会社 | 芳香族カルボン酸の製造方法 |
| JPH078823B2 (ja) | 1986-10-20 | 1995-02-01 | 三井石油化学工業株式会社 | 高純度テレフタル酸の製造方法 |
| US5166420A (en) | 1986-10-20 | 1992-11-24 | Mitsui Petrochemical Industries, Ltd. | Process for the production of high purity terephthalic acid |
| US4900480A (en) | 1986-10-21 | 1990-02-13 | Union Carbide Corporation | Gas-liquid mixing |
| DE3641305C1 (de) | 1986-12-03 | 1988-03-24 | Kalk Chemische Fabrik Gmbh | Verfahren und Vorrichtung zur Herstellung einer suspendiertes Calciumcarbonat enthaltenden Ammoniumnitratloesung |
| DE3704720A1 (de) | 1987-02-14 | 1988-08-25 | Huels Troisdorf | Verfahren und vorrichtung zur herstellung von benzolcarbonsaeuren bzw. benzoldicarbonsaeureestern |
| JP2504461B2 (ja) | 1987-04-24 | 1996-06-05 | 三菱化学株式会社 | 高品質テレフタル酸の製法 |
| DE3839229A1 (de) | 1988-11-19 | 1990-05-23 | Krupp Koppers Gmbh | Verfahren zur gewinnung von p-xylol mit einer reinheit von mehr als 99,8 gew.-% |
| US5211924A (en) | 1988-02-29 | 1993-05-18 | Amoco Corporation | Method and apparatus for increasing conversion efficiency and reducing power costs for oxidation of an aromatic alkyl to an aromatic carboxylic acid |
| US4855491A (en) | 1988-04-25 | 1989-08-08 | Amoco Corporation | Method for selectively removing process stream impurities utilizing reverse osmosis |
| US4863888A (en) | 1988-04-29 | 1989-09-05 | Amoco Corporation | Catalyst containing cobalt boron and oxygen and optionally aluminum of preparation and process |
| GB8811114D0 (en) | 1988-05-11 | 1988-06-15 | Ici Plc | Fermentation process & apparatus |
| US4855492A (en) | 1988-05-27 | 1989-08-08 | Amoco Corporation | Process for production of aromatic polycarboxylic acids |
| US4833269A (en) | 1988-08-05 | 1989-05-23 | Amoco Corporation | Method for purifying terephthalic acid recycle streams |
| US4939297A (en) * | 1989-06-05 | 1990-07-03 | Eastman Kodak Company | Extraction process for removal of impurities from terephthalic acid filtrate |
| US5068406A (en) | 1989-09-06 | 1991-11-26 | Amoco Corporation | Compartmented oxidation method |
| US5004830A (en) * | 1989-11-29 | 1991-04-02 | Amoco Corporation | Process for oxidation of alkyl aromatic compounds |
| US5126037A (en) | 1990-05-04 | 1992-06-30 | Union Oil Company Of California | Geopreater heating method and apparatus |
| DE4016063A1 (de) | 1990-05-18 | 1991-11-21 | Hoechst Ag | Verfahren zur teilweisen elektrolytischen enthalogenierung von di- und trichloressigsaeure sowie elektrolyseloesung |
| KR920004602B1 (ko) | 1990-06-07 | 1992-06-11 | 재단법인 한국화학연구소 | 1-옥소-1, 2, 3, 4-테트라하이드로나프탈렌의 제조방법 |
| DE69104280T2 (de) | 1990-06-25 | 1995-02-16 | Mitsubishi Gas Chemical Co | Verfahren zur Herstellung von hochreiner Isophthalsäure. |
| US5356600A (en) | 1990-09-24 | 1994-10-18 | Praxair Technology, Inc. | Oxygen enrichment method and system |
| US5095145A (en) | 1990-11-05 | 1992-03-10 | Amoco Corporation | Preparation of purified terephthalic acid from waste polyethylene terephthalate |
| US5095142A (en) | 1990-11-29 | 1992-03-10 | Amoco Corporation | Solvent recovery during production of aromatic polycarboxylic acids |
| GB9102393D0 (en) | 1991-02-05 | 1991-03-20 | Ici Plc | Production of terephthalic acid |
| GB9104776D0 (en) | 1991-03-07 | 1991-04-17 | Ici Plc | Process for the production of terephthalic acid |
| US5175355A (en) | 1991-04-12 | 1992-12-29 | Amoco Corporation | Improved process for recovery of purified terephthalic acid |
| US5227570A (en) | 1991-12-02 | 1993-07-13 | Taiwan Styrene Monomer Corporation | Process for separation of ethylbenzene or ethylbenzene/p-xylene from a xylene isomers mixture |
| US6489527B1 (en) | 1992-05-26 | 2002-12-03 | John Di-Yi Ou | Process for improving purity of para-xylene product |
| GB9310070D0 (en) | 1992-05-29 | 1993-06-30 | Ici Plc | Process for the production of purified terephthalic acid |
| US5292934A (en) | 1992-06-18 | 1994-03-08 | Amoco Corporation | Method for preparing aromatic carboxylic acids |
| KR970000136B1 (ko) | 1993-09-28 | 1997-01-04 | 브이.피. 유리예프 | 고순도 벤젠디카르복실산 이성질체의 제조방법 |
| FR2715395B1 (fr) | 1994-01-26 | 1997-02-07 | Anjou Rech | Unite de traitement d'eau par ozonation, et installation de production d'eau ozonee correspondante |
| US5523474A (en) | 1994-05-11 | 1996-06-04 | Praxair Technology, Inc. | Terephthalic acid production using evaporative cooling |
| US5518700A (en) | 1994-06-25 | 1996-05-21 | Shell Oil Company | Cyclonic reactor |
| DE69422623T2 (de) | 1994-09-27 | 2000-06-29 | Chevron Chem Co | Herstellung von reinem Benzol und Paraxylenen durch Kombinieren einer Aromatisierung und einer Disproportionierung von unreinem Toluol |
| US5567842A (en) | 1994-11-16 | 1996-10-22 | Mitsubishi Chemical Corporation | Process for producing terephthalic acid |
| US5712412A (en) | 1994-12-26 | 1998-01-27 | Mitsubishi Gas Chemical Co., Inc. | Process for producing highly pure terephthalic acid |
| FR2728894A1 (fr) | 1994-12-29 | 1996-07-05 | Inst Francais Du Petrole | Procede de separation de paraxylene comportant au moins deux etages de cristallisation a haute temperature |
| SI9500109A (en) | 1995-04-05 | 1996-10-31 | Levec Janez Dipl Ing Prof Dr | Apparatus and Process for Thermal Oxidative Treatment of Waste Waters |
| GB2299767B (en) | 1995-04-07 | 1998-05-13 | Norske Stats Oljeselskap | Regneration of fischer-tropsch catalysts |
| JP3979505B2 (ja) | 1995-05-17 | 2007-09-19 | 三菱瓦斯化学株式会社 | 高純度テレフタル酸の製造方法 |
| JPH08325197A (ja) | 1995-05-30 | 1996-12-10 | Mitsubishi Gas Chem Co Inc | テレフタル酸の製造方法 |
| US5767311A (en) | 1995-06-07 | 1998-06-16 | Glitsch International, Inc. | Method and apparatus for preparing purified terephtalic acid |
| US5580531A (en) | 1995-06-07 | 1996-12-03 | Twenty-First Century Research Corporation | Devices for making reaction products by controlling transient conversion in an atomized liquid |
| US5801282A (en) | 1995-06-07 | 1998-09-01 | Twenty-First Century Research Corporation | Methods of making intermediate oxidation products by controlling pre-coalescing temperature and transient temperature difference in an atomized liquid |
| US5929274A (en) | 1995-06-07 | 1999-07-27 | Hfm International, Inc. | Method to reduce carboxybenzaldehyde isomers in terephthalic acid or isophthalic acid |
| US5883292A (en) | 1996-01-17 | 1999-03-16 | Twenty-First Century Research Corporation | Reaction control by regulating internal condensation inside a reactor |
| US6013835A (en) | 1995-06-07 | 2000-01-11 | Hfm International, Inc. | Method and apparatus for preparing purified terephthalic acid |
| US5840968A (en) | 1995-06-07 | 1998-11-24 | Hfm International, Inc. | Method and apparatus for preparing purified terephthalic acid |
| ES2104512B1 (es) | 1995-09-21 | 1998-07-01 | Interquisa | Procedimiento industrial para la fabricacion de acidos carboxilicos aromaticos. |
| FR2739375B1 (fr) | 1995-09-29 | 1997-12-05 | Inst Francais Du Petrole | Production de paraxylene a partir d'un effluent de dismutation paraselective du toluene par un procede de cristallisation associe a une adsorption en lit mobile simule |
| US5696285A (en) | 1995-12-29 | 1997-12-09 | Praxair Technology, Inc. | Production of terephthalic acid with excellent optical properties through the use of pure or nearly pure oxygen as the oxidant in p-xylene oxidation |
| US5693856A (en) * | 1996-01-16 | 1997-12-02 | The Boc Group, Inc. | Production of terephthalic acid |
| US6376733B1 (en) | 1996-01-25 | 2002-04-23 | Exxonmobil Chemical Patents Inc. | Process for production of paraxylene |
| US5756833A (en) | 1996-02-01 | 1998-05-26 | Amoco Corporation | Catalytic purification and recovery of dicarboxylic aromatic acids |
| ID15851A (id) | 1996-02-13 | 1997-08-14 | Mitsubishi Chem Corp | Proses untuk menghasilkan suatu asam aromatik karboksilik |
| US6084125A (en) | 1996-02-27 | 2000-07-04 | Praxair Technology, Inc. | Process for producing aliphatic acids using a reactor system having a shell and a tube reactor configuration to force circulation of reaction liquid |
| US5824207A (en) | 1996-04-30 | 1998-10-20 | Novetek Octane Enhancement, Ltd. | Method and apparatus for oxidizing an organic liquid |
| US6242643B1 (en) | 1996-05-17 | 2001-06-05 | Toray Industries, Inc. | Method for preparing aromatic carboxylic acids, aromatic aldehydes, and aromatic alcohols |
| US6288270B1 (en) | 1996-06-24 | 2001-09-11 | Rpc Inc. | Methods for controlling the reaction rate of a hydrocarbon to an acid by making phase-related adjustments |
| JP3757995B2 (ja) | 1996-07-12 | 2006-03-22 | 三菱瓦斯化学株式会社 | 高純度イソフタル酸の製造方法 |
| US5928615A (en) | 1996-07-12 | 1999-07-27 | Mcdermott Technology, Inc. | Wet scrubber oxidation air sparger arrangement |
| JPH1045667A (ja) | 1996-07-29 | 1998-02-17 | Mitsubishi Gas Chem Co Inc | 分散媒置換装置を用いた高純度テレフタル酸の製造方法 |
| EP0923524A1 (en) | 1996-08-21 | 1999-06-23 | Twenty-First Century Research Corporation | Methods and devices for controlling the reaction by adjusting the oxidant consumption rate |
| US6133476A (en) | 1996-09-17 | 2000-10-17 | Lin; Tsong-Dar Vincent | Process for purification of aromatic polycarboxylic acids |
| ATE343400T1 (de) * | 1996-09-24 | 2006-11-15 | Merck & Co Inc | Verbindungen zur hemmung der angiogenese durch gentherapie |
| IT1288760B1 (it) | 1996-10-17 | 1998-09-24 | Fiat Ricerche | Motore elettrostatico lineare |
| US5817868A (en) | 1996-11-12 | 1998-10-06 | Twenty-First Century Research Corporation | Method and devices for controlling the oxidation of a hydrocarbon to an acid by regulating temperature/conversion relationship in multi-stage arrangements |
| US5824819A (en) | 1996-12-18 | 1998-10-20 | Twenty-First Century Research Corporation | Methods of preparing an intermediate oxidation product from a hydrocarbon by utilizing an activated initiator |
| GB9701251D0 (en) | 1997-01-22 | 1997-03-12 | Bp Chem Int Ltd | Process |
| KR100264749B1 (ko) | 1997-02-17 | 2000-09-01 | 나까니시 히로유끼 | 고순도 테레프탈산의 제조 방법 |
| CN1095822C (zh) | 1997-02-27 | 2002-12-11 | 纳幕尔杜邦公司 | 对苯二酸的生产 |
| US6288273B1 (en) | 1997-02-27 | 2001-09-11 | Basf Aktiengesellschaft | Method for producing shell catalysts for catalytic gas-phase oxidation of aromatic hydrocarbons |
| US5811363A (en) | 1997-05-02 | 1998-09-22 | Exxon Research And Engineering Company | Catalyst rejuvenation in hydrocarbon synthesis slurry with reduced slurry recontamination |
| US5817702A (en) | 1997-05-02 | 1998-10-06 | Exxon Research And Engineering Company | Hydrocarbon synthesis catalyst slurry rejuvenation with gas disengagement |
| US5811468A (en) | 1997-05-06 | 1998-09-22 | Exxon Research And Engineering Company | Combination gas disengaging downcomer-rejuvenation tube for in-situ slurry catalyst rejuvenation (LAW541) |
| US5770629A (en) | 1997-05-16 | 1998-06-23 | Exxon Research & Engineering Company | Slurry hydrocarbon synthesis with external product filtration |
| US6037491A (en) | 1997-07-25 | 2000-03-14 | Rpc Inc. | Methods and devices for controlling hydrocarbon oxidations to respective acids by adjusting the solvent to hydrocarbon ratio |
| US5939313A (en) | 1997-09-12 | 1999-08-17 | Praxair Technology, Inc. | Stationary vortex system for direct injection of supplemental reactor oxygen |
| FR2768724B1 (fr) | 1997-09-23 | 1999-12-03 | Inst Francais Du Petrole | Procede de production de paraxylene comprenant une etape d'adsorption et une etape d'isomerisation en phase liquide |
| US6004452A (en) | 1997-11-14 | 1999-12-21 | Chevron Chemical Company Llc | Process for converting hydrocarbon feed to high purity benzene and high purity paraxylene |
| KR20010040818A (ko) | 1998-02-09 | 2001-05-15 | 알피시 인코포레이티드 | 탄화수소의 이염기산 산화반응 혼합물내 코발트 촉매 처리방법 |
| JP3664867B2 (ja) | 1998-03-13 | 2005-06-29 | 三菱重工業株式会社 | Pcb分解反応容器 |
| ES2273468T3 (es) | 1998-04-20 | 2007-05-01 | Givaudan Sa | Compuestos con grupos hidroxilo protegidos. |
| US6133470A (en) | 1998-07-28 | 2000-10-17 | Mobil Oil Corporation | Integration of p-xylene production and subsequent conversion process |
| DE19837723A1 (de) | 1998-08-20 | 2000-02-24 | Phenolchemie Gmbh & Co Kg | Verfahren zur Reinigung von Abwässern aus dem Hock-Verfahren |
| US6080372A (en) | 1998-09-11 | 2000-06-27 | Air Products And Chemicals, Inc. | Two stage reactor for continuous three phase slurry hydrogenation and method of operation |
| DE19843573A1 (de) | 1998-09-23 | 2000-03-30 | Degussa | Blasensäule und deren Verwendung |
| JP2000128824A (ja) * | 1998-10-27 | 2000-05-09 | Mitsui Chemicals Inc | 芳香族カルボン酸の製造方法 |
| US6392091B2 (en) | 1998-11-24 | 2002-05-21 | Tsong-Dar Vincent Lin | Process of purifying and producing high purity aromatic polycarboxylic acids |
| US6291707B1 (en) | 1999-03-12 | 2001-09-18 | Tsong-Dar Vincent Lin | Process of purifying and producing high purity aromatic polycarboxylic acids and derivatives thereof |
| US6153790A (en) | 1998-12-01 | 2000-11-28 | Shell Oil Company | Method to produce aromatic dicarboxylic acids using cobalt and zirconium catalysts |
| JP2000191583A (ja) | 1998-12-25 | 2000-07-11 | Mitsui Chemicals Inc | 芳香族カルボン酸の製造方法 |
| IT1311976B1 (it) | 1999-03-25 | 2002-03-22 | Franco Codignola | Procedimento per la produzione di acidi aromatici. |
| US6143926A (en) | 1999-09-21 | 2000-11-07 | E. I. Du Pont De Nemours And Company | Process for producing pure terephthalic acid with improved recovery of precursors, solvent and methyl acetate |
| US6639104B2 (en) | 1999-12-10 | 2003-10-28 | Inca International S.P.A. | Process for the recovery of purified terephthalic acid (PTA) |
| US20010007910A1 (en) | 2000-01-12 | 2001-07-12 | Housley Samuel D. | Process for producing carboxylic acids |
| US20020091285A1 (en) | 2001-01-10 | 2002-07-11 | Housley Samuel Duncan | Method for increasing oxidation reactor production capacity |
| US7060853B2 (en) | 2000-01-12 | 2006-06-13 | Invista North America S.A R.L. | Method for increasing oxidation reactor production capacity |
| US6949673B2 (en) * | 2000-01-12 | 2005-09-27 | E.I. Du Pont De Nemours And Company | Process for producing carboxylic acids |
| CN1227208C (zh) | 2000-01-21 | 2005-11-16 | Bp北美公司 | 在苯甲酸和水溶剂中氧化生产高纯芳香羧酸的方法 |
| JP2001226315A (ja) | 2000-02-10 | 2001-08-21 | Mitsubishi Chemicals Corp | テレフタル酸の製造方法 |
| KR100374785B1 (ko) | 2000-06-29 | 2003-03-04 | 학교법인 포항공과대학교 | 액상 산화 반응기 |
| JP4243912B2 (ja) | 2000-07-05 | 2009-03-25 | 三菱瓦斯化学株式会社 | スラリーからの結晶回収方法 |
| US6765113B2 (en) | 2000-07-19 | 2004-07-20 | E.I. Du Pont De Nemours And Company | Production of aromatic carboxylic acids |
| PT1453883E (pt) | 2000-12-07 | 2013-03-04 | Grupo Petrotemex Sa De Cv | Processo de preparação de poliéster de baixo custo utilizando um reactor tubular |
| JP4809534B2 (ja) | 2001-01-22 | 2011-11-09 | 三菱瓦斯化学株式会社 | 芳香族カルボン酸の製造法 |
| US20020137805A1 (en) * | 2001-01-26 | 2002-09-26 | Huang Jui-Hsin Ray | Process for operating a fischer-tropsch reactor |
| US6743400B2 (en) | 2001-03-21 | 2004-06-01 | The Boc Group, Inc. | Sparger configuration for fluidized bed hydrocarbon partial oxidation reactors |
| US6541525B2 (en) | 2001-03-27 | 2003-04-01 | Exxonmobil Research And Engineering Company | Slurry catalyst rejuvenation in-situ in slurry reactor |
| WO2002092549A1 (en) | 2001-05-15 | 2002-11-21 | Inca International S.P.A. | Agitation system for alkylbenzene oxidation reactors |
| US7485747B2 (en) | 2001-06-04 | 2009-02-03 | Eastman Chemical Company | Two stage oxidation process for the production of aromatic dicarboxylic acids |
| US7196215B2 (en) | 2001-06-04 | 2007-03-27 | Eastman Chemical Company | Process for the production of purified terephthalic acid |
| US6689903B2 (en) | 2001-06-04 | 2004-02-10 | Eastman Chemical Company | Crystallization method for production of purified aromatic dicarboxylic acids |
| EP1422214A4 (en) | 2001-08-29 | 2007-07-11 | Mitsubishi Chem Corp | PROCESS FOR PREPARING AROMATIC DICARBOXYLIC ACID |
| WO2005068407A1 (en) | 2004-01-07 | 2005-07-28 | Conocophillips Company | Systems and methods for catalyst/hydrocarbon product separation |
| CN2562866Y (zh) | 2002-02-01 | 2003-07-30 | 中国石油天然气股份有限公司 | 多级环流反应器 |
| US6908601B2 (en) | 2002-02-08 | 2005-06-21 | The Boc Group, Inc. | Method for the production of nitrogen trifluoride |
| DE10211907A1 (de) | 2002-03-18 | 2003-10-02 | Basf Ag | Oxidation von o-Xylol zu o-Tolylsäure und anderen Oxidationsprodukten durch gestaffelte Zufuhr eines sauerstoffhaltigen Gases |
| US7135596B2 (en) | 2002-04-23 | 2006-11-14 | Bp Corporation North America Inc. | Method of removing iron contaminants from liquid streams during the manufacture and/or purification of aromatic acids |
| JP2004168716A (ja) | 2002-11-20 | 2004-06-17 | Mitsubishi Chemicals Corp | テレフタル酸の製造方法 |
| US7132566B2 (en) | 2003-09-22 | 2006-11-07 | Eastman Chemical Company | Process for the purification of a crude carboxylic acid slurry |
| US7161027B2 (en) | 2002-12-09 | 2007-01-09 | Eastman Chemical Company | Process for the oxidative purification of terephthalic acid |
| US7074954B2 (en) | 2002-12-09 | 2006-07-11 | Eastman Chemical Company | Process for the oxidative purification of terephthalic acid |
| US20040133057A1 (en) | 2003-01-02 | 2004-07-08 | Conocophillips Company | Gaseous hydrocarbon-oxygen bubble tank mixer |
| US6825278B2 (en) | 2003-01-16 | 2004-11-30 | Resolution Specialty Materials Llc | Modified pressure sensitive adhesive |
| US6804609B1 (en) | 2003-04-14 | 2004-10-12 | Conocophillips Company | Property prediction using residual stepwise regression |
| RU2268086C2 (ru) | 2003-04-17 | 2006-01-20 | Общество с ограниченной ответственностью "Научно-исследовательский и производственный центр "ВНИПИМ-ТОС" (ООО "НИиПЦ" ВНИПИМ-ТОС") | Противоточный секционированный газлифтный реактор для газожидкостных процессов |
| US20040215036A1 (en) | 2003-04-25 | 2004-10-28 | Robert Lin | Method for heating a crude carboxylic acid slurry in a post oxidation zone by the addition of steam |
| US7153480B2 (en) | 2003-05-22 | 2006-12-26 | David Robert Bickham | Apparatus for and method of producing aromatic carboxylic acids |
| US7381386B2 (en) | 2003-06-05 | 2008-06-03 | Eastman Chemical Company | Extraction process for removal of impurities from mother liquor in the synthesis of carboxylic acid |
| US7494641B2 (en) | 2003-06-05 | 2009-02-24 | Eastman Chemical Company | Extraction process for removal of impurities from an oxidizer purge stream in the synthesis of carboxylic acid |
| US7273950B2 (en) * | 2003-06-13 | 2007-09-25 | Tereftalatos Mexicanos, S.A. De C.V. | Process and apparatus for the efficient oxidation of alkyl aromatic compounds |
| CN1208301C (zh) | 2003-08-08 | 2005-06-29 | 中国纺织工业设计院 | 一种生产对苯二甲酸用的气升式外循环鼓泡塔氧化装置 |
| CN1228302C (zh) | 2003-10-12 | 2005-11-23 | 浙江大学 | 一种生产对苯二甲酸用的鼓泡塔氧化反应装置 |
| US7485746B2 (en) | 2003-11-14 | 2009-02-03 | Bp Corporation North America Inc. | Staged countercurrent oxidation |
| US6838487B1 (en) | 2003-12-04 | 2005-01-04 | Rentech, Inc. | Method and apparatus for regenerating an iron-based Fischer-Tropsch catalyst |
| US7615663B2 (en) | 2004-09-02 | 2009-11-10 | Eastman Chemical Company | Optimized production of aromatic dicarboxylic acids |
| US7381836B2 (en) * | 2004-09-02 | 2008-06-03 | Eastman Chemical Company | Optimized liquid-phase oxidation |
| US7683210B2 (en) | 2004-09-02 | 2010-03-23 | Eastman Chemical Company | Optimized liquid-phase oxidation |
| US7608733B2 (en) | 2004-09-02 | 2009-10-27 | Eastman Chemical Company | Optimized liquid-phase oxidation |
| US7692036B2 (en) | 2004-11-29 | 2010-04-06 | Eastman Chemical Company | Optimized liquid-phase oxidation |
| US7572932B2 (en) | 2004-09-02 | 2009-08-11 | Eastman Chemical Company | Optimized liquid-phase oxidation |
| US7692037B2 (en) | 2004-09-02 | 2010-04-06 | Eastman Chemical Company | Optimized liquid-phase oxidation |
| US7910769B2 (en) | 2004-09-02 | 2011-03-22 | Eastman Chemical Company | Optimized liquid-phase oxidation |
| US7589231B2 (en) | 2004-09-02 | 2009-09-15 | Eastman Chemical Company | Optimized liquid-phase oxidation |
| US7399882B2 (en) | 2004-09-02 | 2008-07-15 | Eastman Chemical Company | Optimized liquid-phase oxidation |
| US7504535B2 (en) | 2004-09-02 | 2009-03-17 | Eastman Chemical Company | Optimized liquid-phase oxidation |
| US7586000B2 (en) | 2004-09-02 | 2009-09-08 | Eastman Chemical Company | Optimized liquid-phase oxidation |
| US7568361B2 (en) * | 2004-09-02 | 2009-08-04 | Eastman Chemical Company | Optimized liquid-phase oxidation |
| US7582793B2 (en) | 2004-09-02 | 2009-09-01 | Eastman Chemical Company | Optimized liquid-phase oxidation |
| US7884232B2 (en) | 2005-06-16 | 2011-02-08 | Eastman Chemical Company | Optimized liquid-phase oxidation |
| CN100417437C (zh) | 2005-11-18 | 2008-09-10 | 浙江大学 | 带有阻尼内构件的鼓泡塔反应器 |
| US7358389B2 (en) | 2006-01-04 | 2008-04-15 | Eastman Chemical Company | Oxidation system employing internal structure for enhanced hydrodynamics |
| US7501537B2 (en) | 2006-03-01 | 2009-03-10 | Eastman Chemical Company | Polycarboxylic acid production system employing oxidative digestion with reduced or eliminated upstream liquor exchange |
-
2005
- 2005-06-16 US US11/153,994 patent/US7910769B2/en active Active
- 2005-08-29 EP EP05804200.3A patent/EP1786556B1/en active Active
- 2005-08-29 BR BR122015022124A patent/BR122015022124B8/pt active IP Right Grant
- 2005-08-29 PT PT58042003T patent/PT1786556T/pt unknown
- 2005-08-29 WO PCT/US2005/030659 patent/WO2006028771A2/en active Application Filing
- 2005-08-29 MX MX2007002515A patent/MX2007002515A/es active IP Right Grant
- 2005-08-29 CN CN2005800295030A patent/CN101010134B/zh active Active
- 2005-08-29 PL PL05804200T patent/PL1786556T3/pl unknown
- 2005-08-29 CA CA002576795A patent/CA2576795A1/en not_active Abandoned
- 2005-08-29 ES ES05804200.3T patent/ES2617727T3/es active Active
- 2005-08-29 LT LTEP05804200.3T patent/LT1786556T/lt unknown
- 2005-08-29 JP JP2007530229A patent/JP2008511649A/ja active Pending
- 2005-08-29 KR KR1020077006864A patent/KR101281442B1/ko active IP Right Grant
- 2005-08-29 KR KR1020127031375A patent/KR101363742B1/ko active IP Right Grant
- 2005-08-29 BR BRPI0514779-4A patent/BRPI0514779B1/pt active IP Right Grant
-
2011
- 2011-02-11 US US13/025,682 patent/US8685334B2/en active Active
Patent Citations (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS5257134A (en) * | 1975-10-31 | 1977-05-11 | Mitsubishi Chem Ind Ltd | Process for preparation of aromatic polycarboxylic acids |
| JPS62192490A (ja) * | 1986-02-19 | 1987-08-24 | Nippon Steel Corp | 酸化処理用気泡塔 |
| JPH01160476A (ja) * | 1987-12-16 | 1989-06-23 | Nippon Sharyo Seizo Kaisha Ltd | 気泡塔型反応装置 |
| JPH09278709A (ja) * | 1996-02-13 | 1997-10-28 | Mitsubishi Chem Corp | 芳香族カルボン酸の製造方法 |
| JPH10330292A (ja) * | 1996-12-12 | 1998-12-15 | Praxair Technol Inc | 気泡塔反応器への直接的酸素注入法 |
| JP2001247511A (ja) * | 2000-03-07 | 2001-09-11 | Mitsubishi Chemicals Corp | 芳香族カルボン酸の製造方法 |
| US6504051B1 (en) * | 2001-06-04 | 2003-01-07 | Eastman Chemical Company | Process for production of aromatic carboxylic acids with improved water removal technique |
| JP2006509044A (ja) * | 2002-12-09 | 2006-03-16 | イーストマン ケミカル カンパニー | 粗製カルボン酸スラリーの精製方法 |
| JP2008511645A (ja) * | 2004-09-02 | 2008-04-17 | イーストマン ケミカル カンパニー | 最適化液相酸化 |
| JP2008511648A (ja) * | 2004-09-02 | 2008-04-17 | イーストマン ケミカル カンパニー | 最適化液相酸化 |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2016040312A (ja) * | 2010-01-29 | 2016-03-24 | グルーポ ペトロテメックス,ソシエダ アノニマ デ カピタル バリアブレ | 側方取り出し式の第2の反応器を備える酸化システム |
Also Published As
| Publication number | Publication date |
|---|---|
| BRPI0514779B1 (pt) | 2020-12-08 |
| BR122015022124B8 (pt) | 2021-10-05 |
| KR20130028750A (ko) | 2013-03-19 |
| EP1786556A2 (en) | 2007-05-23 |
| US20060047143A1 (en) | 2006-03-02 |
| US7910769B2 (en) | 2011-03-22 |
| CN101010134A (zh) | 2007-08-01 |
| PT1786556T (pt) | 2017-03-14 |
| WO2006028771A2 (en) | 2006-03-16 |
| KR101281442B1 (ko) | 2013-07-02 |
| BRPI0514779A (pt) | 2008-06-24 |
| BR122015022124B1 (pt) | 2021-05-04 |
| US20110256037A1 (en) | 2011-10-20 |
| KR20070054699A (ko) | 2007-05-29 |
| CN101010134B (zh) | 2012-03-07 |
| WO2006028771A3 (en) | 2006-08-10 |
| CA2576795A1 (en) | 2006-03-16 |
| MX2007002515A (es) | 2007-05-04 |
| US8685334B2 (en) | 2014-04-01 |
| PL1786556T3 (pl) | 2017-08-31 |
| KR101363742B1 (ko) | 2014-02-14 |
| EP1786556B1 (en) | 2016-11-30 |
| LT1786556T (lt) | 2017-02-27 |
| ES2617727T3 (es) | 2017-06-19 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2008511649A (ja) | 最適化液相酸化 | |
| JP2008511650A (ja) | 最適化液相酸化 | |
| JP2008511639A (ja) | 最適化液相酸化 | |
| KR101363707B1 (ko) | 최적화된 액상 산화를 위한 기포탑 반응기 | |
| JP2008511640A (ja) | 最適化液相酸化 | |
| JP2008511664A (ja) | 最適化液相酸化 | |
| JP2008511656A (ja) | 粗製テレフタル酸組成物及びその製造方法 | |
| JP2008511646A (ja) | 気泡塔型反応器中における最適化液相酸化 | |
| KR101364801B1 (ko) | 최적화된 액상 산화 | |
| JP2008511638A (ja) | 最適化液相酸化 | |
| US7582793B2 (en) | Optimized liquid-phase oxidation | |
| JP2008511645A (ja) | 最適化液相酸化 | |
| US7608733B2 (en) | Optimized liquid-phase oxidation | |
| JP2008511648A (ja) | 最適化液相酸化 | |
| JP2008511647A (ja) | 最適化液相酸化 | |
| JP2008511655A (ja) | 最適化液相酸化 | |
| JP2008511665A (ja) | 最適化液相酸化 | |
| JP2008511641A (ja) | 最適化液相酸化 | |
| WO2006028817A2 (en) | Optimized liquid-phase oxidation | |
| WO2006028768A2 (en) | Optimized liquid-phase oxidation of paraxylene |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20080828 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20080828 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20110627 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20110712 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20130205 |