-
Die
vorliegende Erfindung betrifft neue Verbindungen, Verfahren zu ihrer
Herstellung, pharmazeutische Zusammensetzungen, die diese Verbindungen
enthalten, und ihre Verwendung bei der Therapie.
-
Chemokine
spielen eine wichtige Rolle bei der Immun- und Entzündungsantwort bei verschiedenen Krankheiten
und Störungen,
einschließlich
Asthma und allergischen Krankheiten sowie Autoimmunpathologien,
wie rheumatoider Arthritis und Atherosklerose. Bei diesen kleinen
sezernierten Molekülen
handelt es sich um eine wachsende Superfamilie von Proteinen mit
einem Molekulargewicht von 8–14
kDa, die durch ein Strukturmotiv mit vier konservierten Cysteinen
gekennzeichnet ist. Die Chemokin-Superfamilie kann in zwei Hauptgruppen
mit charakteristischen Strukturmotiven unterteilt werden, die Cys-X-Cys-(C-X-C-)
und die Cys-Cys-(C-C-)Familie.
Diese unterscheiden sich voneinander durch Einschub einer einzigen
Aminosäure zwischen
den beiden NH-proximalen Cysteinresten und Sequenzähnlichkeit.
-
Zu
den C-X-C-Chemokinen gehören
mehrere hochwirksame Chemoattraktantien und Aktivatoren von Neutrophilen,
wie Interleukin-8 (IL-8) und Neutrophile aktivierendes Peptid 2
(NAP-2).
-
Zu
den C-C-Chemokinen gehören
hochwirksame Chemoattraktantien für Monozyten und Lymphozyten,
aber nicht für
Neutrophile, wie beispielsweise humanes MCP-1, MCP-2 und MCP-3 (MCP = Monocyte Chemotactic
Protein), RANTES (Regulated an Activation, Normal T Expressed and
Secreted), Eotaxin sowie MIP-1α und
MIP-1β (MIP = Macrophage
Inflammatory Protein).
-
Untersuchungen
haben gezeigt, daß die
Wirkungen der Chemokine durch Unterfamilien von G-Protein-gekoppelten
Rezeptoren vermittelt werden, zu denen unter anderem die Rezeptoren
mit der Bezeichnung CCR1, CCR2, CCR2A, CCR2B, CCR3, CCR4, CCR5,
CCR6, CCR7, CCR8, CCR9, CCR10, CXCR1, CXCR2, CXCR3 und CXCR4 gehören. Diese
Rezeptoren stellen gute Ziele für
die Arzneistoffentwicklung dar, da Mittel, die diese Rezeptoren
modulieren, zur Verwendung bei der Behandlung von Störungen und
Krankheiten wie den oben beschriebenen geeignet wären.
-
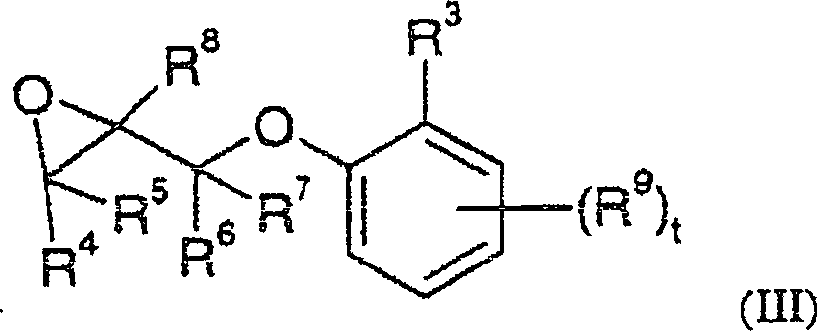
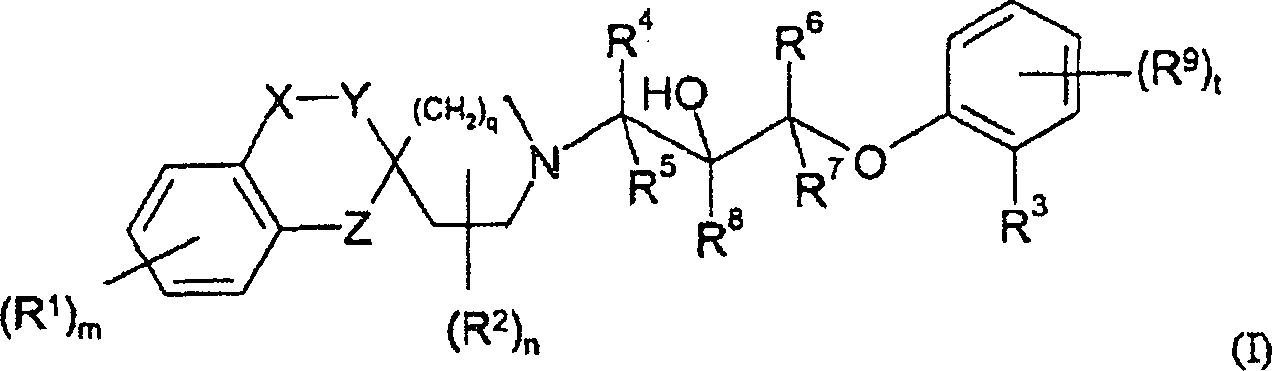
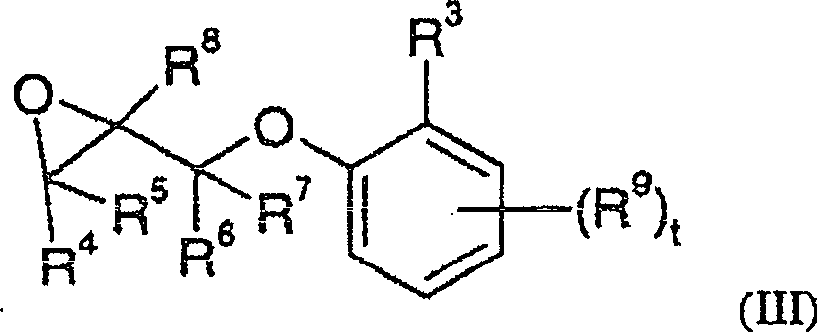
Gegenstand
der vorliegenden Erfindung sind daher Verbindungen der allgemeinen
Formel
wobei
m
für 0,
1, 2, 3 oder 4 steht;
R
1 jeweils unabhängig für Halogen,
Cyano, Hydroxy, C
1-C
6-Alkyl,
C
1-C
6-Halogenalkyl,
C
1-C
6-Alkoxy oder
Sulfonamido (-SO
2NH
2)
steht;
X entweder für
eine Bindung, -CH
2-, -O- steht und Y für eine Bindung,
-CH
2-, -O- steht oder X und Y zusammen für eine Gruppe
-CH-C(CH
3)- oder -C(CH
3)=CH- stehen und Z für eine Bindung,
-O-, -NH- oder -CH
2- steht, mit der Maßgabe, daß nur einer der Reste X, Y
und Z jeweils für
eine Bindung stehen kann, und mit der Maßgabe, daß X und Y nicht beide gleichzeitig
für -O-
stehen;
n für
0, 1 oder 2 steht;
R
2 jeweils unabhängig für Halogen
oder C
1-C
6-Alkyl
steht;
q für
0 oder 1 steht;
R
3 für -NHC(O)R
10, -C(O)NR
11R
12 oder -COOR
12a steht;
R
4, R
5, R
6,
R
7 und R
8 jeweils
unabhängig
voneinander für
ein Wasserstoffatom oder eine C
1-C
6-Alkylgruppe stehen;
t für 0, 1 oder
2 steht;
R
9 jeweils unabhängig für Halogen,
Cyano, Hydroxy, Carboxyl, C
1-C
6-Alkoxy,
C
1-C
6-Alkoxycarbonyl,
C
1-C
6-Halogenalkyl oder
gegebenenfalls durch wenigstens einen Substituenten ausgewählt aus
Carboxyl und C
1-C
6-Alkoxycarbonyl
substituiertes C
1-C
6-Alkyl
steht;
R
10 für eine Gruppe C
1-C
6-Alkyl, C
2-C
6-Alkenyl, C
3-C
6-Cycloalkyl,
Adamantyl, C
5-C
6-Cycloalkenyl,
Phenyl oder ein gesättigtes
oder ungesättigtes
5- bis 10-gliedriges
heterocyclisches
R
10 für eine Gruppe
C
1-C
6-Alkyl, C
2-C
6-Alkenyl, C
3-C
6-Cycloalkyl, Adamantyl, C
5-C
6-Cycloalkenyl, Phenyl oder ein gesättigtes
oder ungesättigtes
5- bis 10-gliedriges
heterocyclisches Ringsystem mit wenigstens einem Ringheteroatom
ausgewählt
aus Stickstoff, Sauerstoff und Schwefel, die jeweils gegebenenfalls
durch einen oder mehrere Substituenten unabhängig voneinander ausgewählt aus
Nitro, Hydroxy, Oxo, Halogen, Carboxyl, C
1-C
6-Alkyl,
C
1-C
6-Alkoxy, C
1-C
6-Alkylthio, C
1-C
6-Alkylcarbonyl, C
1-C
6-Alkoxycarbonyl,
Phenyl und -NHC(O)-R
13 substituiert sein
können,
steht, oder R
10 für eine Gruppe -NR
14R
15 oder -O-R
16 steht;
R
11 und R
12 jeweils
unabhängig
voneinander für
(i) ein Wasserstoffatom, (ii) einen 3- bis 6-gliedrigen gesättigten oder ungesättigten
Ring, der gegebenenfalls wenigstens ein Ringheteroatom ausgewählt aus
Stickstoff, Sauerstoff und Schwefel enthält und gegebenenfalls weiterhin
eine verbrückende
Gruppe enthält,
wobei der Ring gegebenenfalls durch wenigstens einen Substituenten
ausgewählt
aus Halogen, Hydroxy, C
1-C
6-Alkyl, C
1-C
6-Hydroxyalkyl
und C
1-C
6-Halogenalkyl
substituiert ist,
(iii) eine C
1-C
6-Alkylgruppe, gegebenenfalls substituiert
durch wenigstens einen Substituenten ausgewählt aus Halogen, Amino (-NH
2), Hydroxy, C
1-C
6-Halogenalkyl,
Carboxyl, C
1-C
6-Alkoxy,
C
1-C
6-Alkoxycarbonyl, C
1-C
6-Alkylcarbonylamino
und einem 3- bis 6-gliedrigen gesättigten oder ungesättigten
Ring, der gegebenenfalls wenigstens ein Ringheteroatom ausgewählt aus
Stickstoff, Sauerstoff und Schwefel enthält und gegebenenfalls weiterhin
eine verbrückende
Gruppe enthält,
wobei der Ring gegebenenfalls durch wenigstens einen Substituenten
ausgewählt
aus Halogen, Hydroxy, Oxo (=O), C
1-C
6-Alkyl, C
1-C
6-Hydroxyalkyl und C
1-C
6-Halogenalkyl substituiert
ist, oder (iv) C
1-C
6-Alkylsulfonyl stehen,
oder
R
11 und R
12 zusammen
mit dem Stickstoffatom, an das sie gebunden sind, einen 4- bis 7-gliedrigen
gesättigten heterocyclischen
Ring bilden, der gegebenenfalls weiterhin ein Ringstickstoff-, -sauerstoff-
oder -schwefelatom enthält
und der gegebenenfalls unter Bildung eines 8- bis 11-gliedrigen Ringsystems
an einen Benzolring kondensiert ist, wobei der heterocyclische Ring
bzw. das Ringsystem gegebenenfalls durch wenigstens einen Substituenten
ausgewählt
aus Halogen, Hydroxy, Amino (-CONH
2), C
1-C
6-Alkyl, C
1-C
6-Hydroxyalkyl, C
1-C
6-Alkoxy, C
1-C
6-Alkoxycarbonyl, C
1-C
6-Halogenalkyl, C
1-C
6-Alkylamino, Di-C
1-C
6-alkylamino,
C
1-C
6-Alkylcarbonyl,
C
1-C
6-Alkylcarbonylamino,
C
1-C
6-Alkylaminocarbonyl,
Di-C
1-C
6-alkylaminocarbonyl, Phenyl, Halogenphenyl,
Phenylcarbonyl, Phenylcarbonyloxy und Hydroxydiphenylmethyl substituiert
ist;
R
12a für ein Wasserstoffatom oder
eine C
1-C
6-Alkylgruppe steht;
R
13 für
eine C
1-C
6-Alkyl-,
Amino- (-NH
2) oder Phenylgruppe steht;
R
14 und R
15 jeweils
unabhängig
voneinander für
ein Wasserstoffatom oder eine Gruppe C
1-C
6-Alkyl, C
1-C
6-Alkylsulfonyl,
Phenyl oder ein gesättigtes
oder ungesättigtes
5- bis 10-gliedriges heterocyclisches Ringsystem mit wenigstens
einem Ringheteroatom ausgewählt
aus Stickstoff, Sauerstoff und Schwefel stehen, wobei die Gruppen
jeweils gegebenenfalls wie oben für R
10 definiert
substituiert sind, oder
R
14 und R
15 zusammen mit dem Stickstoffatom, an das
sie gebunden sind, einen 4- bis 7-gliedrigen gesättigten heterocyclischen Ring
bilden, der gegebenenfalls weiterhin ein Ringstickstoff-, -sauerstoff-
oder -schwefelatom enthält,
wobei der heterocyclische Ring gegebenenfalls durch wenigstens ein
Hydroxy substituiert ist; und
R
16 für ein Wasserstoffatom
oder eine Gruppe C
1-C
6-Alkyl, Phenyl oder
ein gesättigtes
oder ungesättigtes
5- bis 10-gliedriges heterocyclisches Ringsystem mit wenigstens
einem Ringheteroatom ausgewählt
aus Stickstoff, Sauerstoff und Schwefel steht, wobei die Gruppen
jeweils gegebenenfalls wie oben für R
10 definiert
substituiert sind;
und deren pharmazeutisch annehmbare Salze
und Solvate.
-
Im
Rahmen der vorliegenden Beschreibung kann, soweit nichts anderes
angegeben ist, eine Alkyl- oder Alkenylsubstituentengruppe oder
eine Alkyleinheit in einer Substituentengruppe geradkettig oder
verzweigt sein. Die Alkyleinheiten in einer Dialkylamino- oder Dialkylaminocarbonylsubstituentengruppe
können gleich
oder verschieden sein. Eine Halogenalkyl- oder Halogenphenylsubstituentengruppe
enthält
wenigstens ein Halogenatom, beispielsweise ein, zwei, drei oder
vier Halogenatome. Ein Hydroxyalkylsubstituent kann eine oder mehrere
Hydroxylgruppen enthalten, enthält
jedoch vorzugsweise eine oder zwei Hydroxylgruppen. In dem durch
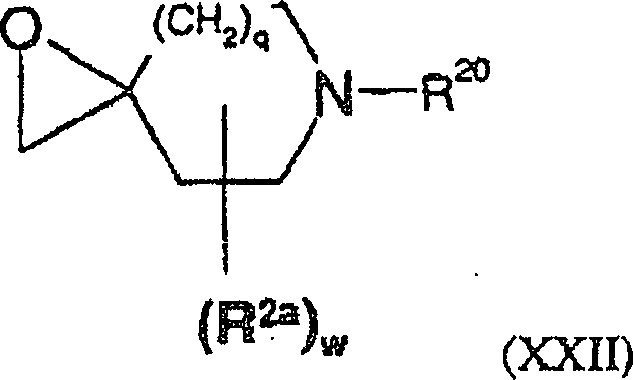
R2 substituierten Ring kann R2 an
ein beliebiges geeignetes Ringatom einschließlich des Kohlenstoffatoms
von (CH2)q gebunden
sein. Stehen R11 und R12 oder
R14 und R15 für einen
4- bis 7-gliedrigen gesättigten Heterocyclus,
so versteht sich, daß der
Heterocyclus nicht mehr als zwei Ringheteroatome enthält: das
Stickstoff-Ringatom, an das R11 und R12 bzw. R14 und R15 gebunden sind, und gegebenenfalls ein
Stickstoff-, Sauerstoff- oder Schwefel-Ringatom. Zur Definition
von R10 (oder R14,
R15 oder R16) sollte
angemerkt werden, daß das
gesättigte
oder ungesättigte
5- bis 10-gliedrige heterocyclische Ringsystem alicyclische oder aromatische
Eigenschaften aufweisen kann. In ähnlicher Weise kann in der
Definition von R11 bzw. R12 ein
3- bis 6-gliedriger
gesättigter
oder ungesättigter
Ring, der gegebenenfalls wenigstens ein Ringheteroatom enthält, alicyclische
oder aromatische Eigenschaften aufweisen. Ein ungesättigtes
Ringsystem ist teilweise oder vollständig ungesättigt.
-
Bei
einer Ausführungsform
der Erfindung steht m für
0 oder 1.
-
R1 steht jeweils unabhängig für Halogen (zum Beispiel Chlor,
Fluor, Brom oder Iod), Cyano, Hydroxy, C1-C6-Alkyl,
vorzugsweise C1-C4-Alkyl,
(zum Beispiel Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, Isobutyl, tert.-Butyl, n-Pentyl oder
n-Hexyl), C1-C6-Halogenalkyl,
vorzugsweise C1-C4-Halogenalkyl,
(zum Beispiel Trifluormethyl), C1-C6-Alkoxy, vorzugsweise C1-C4-Alkoxy, (zum Beispiel Methoxy, Ethoxy,
n-Propoxy oder n-Butoxy) oder Sulfonamido.
-
Bei
einer Ausführungsform
der Erfindung steht R1 jeweils unabhängig für Halogen,
C1-C6-Alkyl, vorzugsweise
C1-C4-Alkyl, oder C1-C6-Halogenalkyl,
vorzugsweise C1-C4-Halogenalkyl.
-
Bei
einer anderen Ausführungsform
steht R1 jeweils unabhängig für Fluor, Chlor, Methyl oder
Trifluormethyl.
-
Kombinationen
von X und Y von besonderem Interesse schließen eine oder mehrere der folgenden ein:
| X | Y |
| Bindung | O |
| O | Bindung |
| CH2 | Bindung |
| Bindung | CH2 |
| CH2 | O |
| O | CH2 |
| CH2 | CH2 |
| -CH=C(CH3)- |
-
Bei
einer Ausführungsform
der Erfindung haben X und Y die unten gezeigten Bedeutungen:
| X | Y |
| Bindung | O |
| O | Bindung |
| CH2 | O |
| O | CH2 |
| CH2 | CH2 |
| -CH=C(CH3)- |
-
Bei
einer Ausführungsform
der Erfindung steht Z für
eine Bindung, -O- oder -CH2-.
-
Kombinationen
von X, Y und Z von besonderem Interesse schließen eine oder mehrere der folgenden ein:
| X | Y | Z |
| Bindung | O | CH2 |
| O | Bindung | CH2 |
| CH2 | Bindung | O |
| Bindung | CH2 | O |
| CH2 | O | Bindung |
| CH2 | CH2 | Bindung |
| O | Bindung | O |
| Bindung | O | O |
| CH2 | CH2 | O |
| O | CH2 | CH2 |
| -CH=C(CH3)- | Bindung |
-
Bei
einer Ausführungsform
der Erfindung haben X, Y und Z die unten gezeigten Bedeutungen:
| X | Y | Z |
| Bindung | O | CH2 |
| O | Bindung | CH2 |
| CH2 | O | Bindung |
| O | CH2 | Bindung |
| CH2 | CH2 | Bindung |
| Bindung | O | O |
| O | Bindung | O |
| -CH=C(CH3)- | Bindung |
-
Bei
einer anderen Ausführungsform
der Erfindung haben X, Y und Z die unten gezeigten Bedeutungen:
| X | Y | Z |
| Bindung | O | CH2 |
| O | Bindung | CH2 |
| CH2 | Bindung | O |
| Bindung | CH2 | O |
| CH2 | O | Bindung |
-
Bei
noch einer anderen Ausführungsform
der Erfindung haben X, Y und Z die unten gezeigten Bedeutungen:
| X | Y | Z |
| Bindung | O | CH2 |
| O | Bindung | CH2 |
| CH2 | O | Bindung |
-
R2 steht jeweils unabhängig für Halogen (zum Beispiel Chlor,
Fluor, Brom oder Iod) oder C1-C6-Alkyl, vorzugsweise
C1-C4-Alkyl, (zum
Beispiel Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, Isobutyl,
tert.-Butyl, n-Pentyl
oder n-Hexyl).
-
Bei
einer Ausführungsform
der Erfindung steht n für
1 und R2 für Halogen, insbesondere Fluor.
-
Bei
einer Ausführungsform
der Erfindung steht R3 für -NHC(O)R10.
-
Bei
einer anderen Ausführungsform
der Erfindung steht R3 für -C(O)NR11R12.
-
R4, R5, R6,
R7 und R8 stehen
jeweils unabhängig
voneinander für
ein Wasserstoffatom oder eine C1-C6-Alkylgruppe,
vorzugsweise eine C1-C4-Alkylgruppe,
(zum Beispiel Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, Isobutyl,
tert.-Butyl, n-Pentyl oder n-Hexyl).
-
Bei
einer Ausführungsform
der Erfindung stehen R4, R5,
R6, R7 und R8 jeweils unabhängig voneinander für ein Wasserstoffatom
oder eine Methylgruppe.
-
Bei
einer anderen Ausführungsform
der Erfindung stehen R4, R5,
R6 und R7 jeweils
für ein
Wasserstoffatom und R8 steht für eine Methylgruppe.
-
Bei
einer Ausführungsform
der Erfindung stehen R4, R5,
R6, R7 und R8 jeweils für ein Wasserstoffatom.
-
Bei
einer Ausführungsform
der Erfindung steht t für
0, 1 oder 2.
-
R9 steht jeweils unabhängig für Halogen (zum Beispiel Chlor,
Fluor, Brom oder Iod), Cyano, Hydroxy, Carboxyl, C1-C6-Alkoxy, vorzugsweise C1-C4-Alkoxy, (zum Beispiel Methoxy, Ethoxy,
n-Propoxy oder n-Butoxy), C1-C6-Alkoxycarbonyl, vorzugsweise
C1-C4-Alkoxycarbonyl,
(zum Beispiel Methoxycarbonyl, Ethoxycarbonyl, n-Propoxycarbonyl oder n-Butoxycarbonyl),
C1-C6-Halogen alkyl,
vorzugsweise C1-C4-Halogenalkyl,
(zum Beispiel Trifluormethyl), oder C1-C6-Alkyl, vorzugsweise C1-C4-Alkyl,
(zum Beispiel Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, Isobutyl,
tert.-Butyl, n-Pentyl oder n-Hexyl), gegebenenfalls substituiert
durch wenigstens einen Substituenten (zum Beispiel einen, zwei oder
drei Substituenten) unabhängig
voneinander ausgewählt
aus Carboxyl und C1-C6-Alkoxycarbonyl,
vorzugsweise C1-C4-Alkoxycarbonyl,
(zum Beispiel Methoxycarbonyl, Ethoxycarbonyl, n-Propoxycarbonyl
oder n-Butoxycarbonyl).
-
Bei
einer Ausführungsform
der Erfindung steht R9 jeweils unabhängig für Halogen,
Cyano, Hydroxy, Carboxyl, C1-C6-Alkoxy, vorzugsweise
C1-C4-Alkoxy, C1-C6-Alkoxycarbonyl,
vorzugsweise C1-C4-Alkoxycarbonyl,
C1-C6-Halogenalkyl,
vorzugsweise C1-C4-Halogenalkyl,
oder C1-C6-Alkyl,
vorzugsweise C1-C4-Alkyl.
-
Bei
einer anderen Ausführungsform
der Erfindung steht R9 jeweils unabhängig für Halogen,
Hydroxy, Carboxyl, Methyl, Methoxy, Methoxycarbonyl oder Trifluormethyl.
-
R
9 ist vorzugsweise an ein Kohlenstoffatom
gebunden, das sich in der para-Stellung zum Kohlenstoffatom befindet,
an das entweder das Sauerstoffatom oder die Gruppe R
3 gebunden
ist, wie durch die Sternchen in der unten gezeigten Teilstruktur
angegeben:
R
10 kann
für eine
C
1-C
6-Alkylgruppe,
vorzugsweise eine C
1-C
4-Alkylgruppe
(zum Beispiel Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, Isobutyl,
tert.-Butyl, n-Pentyl oder n-Hexyl), C
2-C
6-Alkenyl, vorzugsweise C
2-C
4-Alkenyl, C
3-C
6-Cycloalkyl (Cyclopropyl, Cyclobutyl, Cyclopentyl oder
Cyclohexyl), Adamantyl, C
5-C
6-Cycloalkenyl,
Phenyl oder ein gesättigtes
oder ungesättigtes
5- bis 10-gliedriges
heterocyclisches Ringsystem, das wenigstens ein Ringheteroatom (zum
Beispiel ein, zwei, drei oder vier Ringheteroatome unabhängig voneinander)
ausgewählt
aus Stickstoff, Sauerstoff und Schwefel enthält, die jeweils (d. h. jede
der angeführten
Gruppen und das Ringsystem) gegebenenfalls durch einen oder mehrere
(zum Beispiel einen, zwei, drei oder vier) Substituenten unabhängig voneinander
ausgewählt
aus Nitro, Hydroxy, Oxo, Halogen (zum Beispiel Fluor, Chlor, Brom
oder Iod), Carboxyl, C
1-C
6-Alkyl,
vorzugsweise C
1-C
4-Alkyl,
(zum Beispiel Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, Isobutyl,
tert.-Butyl, n-Pentyl
oder n-Hexyl), C
1-C
6-Alkoxy,
vorzugsweise C
1-C
4-Alkoxy, (zum Beispiel
Methoxy, Ethoxy, n-Propoxy oder n-Butoxy), C
1-C
6-Alkylthio, vorzugsweise C
1-C
4-Alkylthio, (zum Beispiel Methylthio oder
Ethylthio), C
1-C
6-Alkylcarbonyl, vorzugsweise
C
1-C
4-Alkylcarbonyl,
(zum Beispiel Methylcarbonyl, Ethylcarbonyl, n-Propylcarbonyl, Isopropylcarbonyl, n-Butylcarbonyl,
n-Pentylcarbonyl
oder n-Hexylcarbonyl), C
1-C
6-Alkoxycarbonyl, vorzugsweise
C
1-C
4-Alkoxycarbonyl,
(zum Beispiel Methoxycarbonyl oder Ethoxycarbonyl), Phenyl und -NHC(O)-R
13 substituiert sein können, stehen.
-
Das
gesättigte
oder ungesättigte
5- bis 10-gliedrige heterocyclische Ringsystem in R10 kann
monocyclisch oder polycyclisch (zum Beispiel bicyclisch) sein; Beispiele
hierfür
schließen
Pyrrolidinyl, Piperidinyl, Pyrazolyl, Thiazolidinyl, Thienyl, Isoxazolyl,
Thiadiazolyl, Pyrrolyl, Furanyl, Thiazolyl, Indolyl, Chinolinyl,
Benzimidazolyl, Triazolyl, Tetrazolyl, Pyridinyl und Kombinationen
von zwei oder mehr davon ein.
-
Bei
einer Ausführungsform
der Erfindung steht R10 für eine Gruppe
C1-C6-Alkyl, C3-C6-Cycloalkyl,
Phenyl oder ein gesättigtes
oder ungesättigtes
5- bis 6-gliedriges heterocyclisches Ringsystem mit wenigstens einem Ringheteroatom
(zum Beispiel einem oder zwei Ringheteroatomen unabhängig voneinander)
ausgewählt aus
Stickstoff, Sauerstoff und Schwefel, die jeweils (d. h. jede der
angeführten
Gruppen und das Ringsystem) gegebenenfalls durch einen, zwei, drei
oder vier Substituenten unabhängig
voneinander ausgewählt
aus Nitro, Hydroxy, Oxo, Halogen, Carboxyl, C1-C6-Alkyl, vorzugsweise C1-C4-Alkyl, C1-C6-Alkoxy, vorzugsweise C1-C4-Alkoxy,
C1-C6-Alkylthio,
vorzugsweise C1-C4-Alkylthio,
C1-C6-Alkylcarbonyl,
vorzugsweise C1-C4-Alkylcarbonyl,
C1-C6-Alkoxycarbonyl,
vorzugsweise C1-C4-Alkoxycarbonyl,
Phenyl und -NHC(O)-R13 substituiert sein
können.
-
Bei
einer anderen Ausführungsform
der Erfindung steht R10 für eine Gruppe
C1-C6-Alkyl, C3-C6-Cycloalkyl oder
Phenyl, die jeweils gegebenenfalls durch einen oder zwei Substituenten
unabhängig
voneinander ausgewählt
aus Halogen, C1-C6-Alkyl,
vorzugsweise C1-C4-Alkyl,
und C1-C6-Alkoxy,
vorzugsweise C1-C4-Alkoxy,
substituiert sein können.
-
Bei
noch einer anderen Ausführungsform
der Erfindung steht R10 für C1-C6-Alkyl, Cyclopentyl
oder Phenyl.
-
Alternativ
dazu kann R10 für eine Gruppe -NR14R15 oder -O-R16 stehen.
-
R14 und R15 stehen
jeweils unabhängig
voneinander für
ein Wasserstoffatom, oder eine Gruppe C1-C6-Alkyl, vorzugsweise C1-C4-Alkyl, (zum Beispiel Methyl, Ethyl, n-Propyl, Isopropyl,
n-Butyl, Isobutyl, tert.-Butyl, n-Pentyl oder n-Hexyl), C1-C6-Alkylsulfonyl, vorzugsweise C1-C4-Alkylsulfonyl, (zum Beispiel Methylsulfonyl,
Ethylsulfonyl, n-Propylsulfonyl, Isopropylsulfonyl, n-Butylsulfonyl, Isobutylsulfonyl,
tert.-Butylsulfonyl, n-Pentylsulfonyl oder n-Hexylsulfonyl), Phenyl
oder ein gesättigtes
oder ungesättigtes
5- bis 10-gliedriges heterocyclisches Ringsystem, das wenigstens
ein Ringheteroatom (zum Beispiel ein, zwei, drei oder vier Ringheteroatome
unabhängig
voneinander) ausgewählt
aus Stickstoff, Sauerstoff und Schwefel enthält, wobei jede Gruppe (d. h.
jede der angeführten
Gruppen einschließlich
des Ringsystems) gegebenenfalls wie oben für R10 definiert
substituiert ist (d. h. gegebenenfalls durch einen oder mehrere
(zum Beispiel einen, zwei, drei oder vier) Substituenten unabhängig voneinander
ausgewählt
aus Nitro, Hydroxy, Oxo, Halogen (zum Beispiel Fluor, Chlor, Brom
oder Iod), Carboxyl, C1-C6-Alkyl, vorzugsweise
C1-C4-Alkyl, (zum
Beispiel Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, Isobutyl,
tert.-Butyl, n-Pentyl
oder n-Hexyl), C1-C6-Alkoxy,
vorzugsweise C1-C4-Alkoxy,
(zum Beispiel Methoxy, Ethoxy, n-Propoxy oder n-Butoxy), C1-C6-Alkylthio, vorzugsweise C1-C4-Alkylthio, (zum
Beispiel Methylthio oder Ethylthio), C1-C6-Alkylcarbonyl, vorzugsweise C1-C4-Alkylcarbonyl,
(zum Beispiel Methylcarbonyl, Ethylcarbonyl, n-Propylcarbonyl, Isopropylcarbonyl,
n-Butylcarbonyl, n-Pentylcarbonyl
oder n-Hexylcarbonyl), C1-C6-Alkoxycarbonyl,
vorzugsweise C1-C4-Alkoxycarbonyl,
(zum Beispiel Methoxycarbonyl oder Ethoxycarbonyl), Phenyl und -NHC(O)-R13 substituiert ist), oder R14 und
R15 zusammen mit dem Stickstoffatom, an
das sie gebunden sind, bilden einen 4- bis 7-gliedrigen gesättigten
heterocyclischen Ring, der gegebenenfalls weiterhin ein Ringstickstoff-,
Ringsauerstoff- oder Ringschwefelatom enthält (zum Beispiel Pyrrolidinyl,
Piperidinyl, Morpholino, Piperadinyl oder Thiomorpholinyl), wobei
der heterocyclische Ring gegebenenfalls durch wenigstens eine Hydroxylgruppe
(zum Beispiel eine oder zwei Hydroxylgruppen) substituiert ist.
-
Bei
R14 bzw. R15 kann
das gesättigte
oder ungesättigte
5- bis 10-gliedrige
heterocyclische Ringsystem monocyclisch oder polycyclisch (zum Beispiel
bicyclisch) sein; Beispiele hierfür schließen Pyrrolidinyl, Piperidinyl,
Pyrazolyl, Thiazolidinyl, Thienyl, Isoxazolyl, Thiadiazolyl, Pyrrolyl,
Furanyl, Thiazolyl, Indolyl, Chinolinyl, Benzimidazolyl, Triazolyl,
Tetrazolyl, Pyridinyl und Kombinationen von zwei oder mehr davon
ein.
-
Bei
einer Ausführungsform
der Erfindung stehen R14 und R15 jeweils
unabhängig
voneinander für
ein Wasserstoffatom oder eine C1-C6-Alkyl- oder C1-C6-Alkylsulfonylgruppe, wobei jede Gruppe
gegebenenfalls wie oben für
R10 definiert substituiert ist, oder R14 und R15 bilden
zusammen mit dem Stickstoffatom, an das sie gebunden sind, einen
5- oder 6-gliedrigen gesättigten
heterocyclischen Ring, der gegebenenfalls weiterhin ein Ringstickstoff-,
Ringsauerstoff- oder Ringschwefelatom enthält, wobei der heterocyclische
Ring gegebenenfalls durch wenigstens eine Hydroxylgruppe substituiert
ist.
-
Bei
einer anderen Ausführungsform
stehen R14 und R15 jeweils
unabhängig
voneinander für
ein Wasserstoffatom oder eine C1-C6-Alkylsulfonylgruppe, oder R14 und
R15 bilden zusammen mit dem Stickstoffatom, an
das sie gebunden sind, einen 5- oder 6-gliedrigen gesättigten
heterocyclischen Ring, der gegebenenfalls durch wenigstens eine
Hydroxylgruppe substituiert ist.
-
Bei
noch einer anderen Ausführungsform
stehen R14 und R15 jeweils
unabhängig
voneinander für
ein Wasserstoffatom oder eine Methylsulfonylgruppe, oder R14 und R15 bilden
zusammen mit dem Stickstoffatom, an das sie gebunden sind, einen
Pyrrolidinyl- oder Piperidinylring, der gegebenenfalls durch eine
Hydroxylgruppe substituiert ist.
-
R16 steht für ein Wasserstoffatom, oder
eine Gruppe C1-C6-Alkyl, vorzugsweise
C1-C4-Alkyl, (zum
Beispiel Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, Isobutyl,
tert.-Butyl, n-Pentyl oder n-Hexyl), Phenyl oder ein gesättigtes
oder ungesättigtes
5- bis 10-gliedriges heterocyclisches Ringsystem, das wenigstens
ein Ringheteroatom (zum Beispiel ein, zwei, drei oder vier Ringheteroatome
unabhängig
voneinander) ausgewählt
aus Stickstoff, Sauerstoff und Schwefel enthält, wobei jede Gruppe (d. h.
jede der angeführten
Gruppen einschließlich
des Ringsystems) gegebenenfalls wie oben für R10 definiert
substituiert ist (d. h. gegebenenfalls durch einen oder mehrere
(zum Beispiel einen, zwei, drei oder vier) Substituenten unabhängig voneinander
ausgewählt
aus Nitro, Hydroxy, Oxo, Halogen (zum Beispiel Fluor, Chlor, Brom
oder Iod), Carboxyl, C1-C6-Alkyl, vorzugsweise
C1-C4-Alkyl, (zum
Beispiel Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, Isobutyl,
tert.-Butyl, n-Pentyl oder
n-Hexyl), C1-C6-Alkoxy,
vorzugsweise C1-C4-Alkoxy,
(zum Beispiel Methoxy, Ethoxy, n-Propoxy oder n-Butoxy), C1-C6-Alkylthio, vorzugsweise
C1-C4-Alkylthio,
(zum Beispiel Methylthio oder Ethylthio), C1-C6-Alkylcarbonyl, vorzugsweise C1-C4-Alkylcarbonyl,
(zum Beispiel Methylcarbonyl, Ethylcarbonyl, n-Propylcarbonyl, Isopropylcarbonyl,
n-Butylcarbonyl,
n-Pentylcarbonyl oder n-Hexylcarbonyl), C1-C6-Alkoxycarbonyl, vorzugsweise C1-C4-Alkoxycarbonyl, (zum Beispiel Methoxycarbonyl
oder Ethoxycarbonyl), Phenyl und -NHC(O)-R13 substituiert
ist).
-
Bei
R16 kann das gesättigte oder ungesättigte 5-
bis 10-gliedrige
heterocyclische Ringsystem monocyclisch oder polycyclisch (zum Beispiel
bicyclisch) sein; Beispiele heirfür schließen Pyrrolidinyl, Piperidinyl,
Pyrazolyl, Thiazolidinyl, Thienyl, Isoxazolyl, Thiadiazolyl, Pyrrolyl,
Furanyl, Thiazolyl, Indolyl, Chinolinyl, Benzimidazolyl, Triazolyl,
Tetrazolyl, Pyridinyl und Kombinationen von zwei oder mehr davon
ein.
-
R11 und R12 stehen
jeweils unabhängig
voneinander für
- (i) ein Wasserstoffatom,
- (ii) einen 3- bis 6-gliedrigen gesättigten oder ungesättigten
Ring, der gegebenenfalls wenigstens ein Ringheteroatom (zum Beispiel
ein, zwei, drei oder vier Ringheteroatome unabhängig voneinander) ausgewählt aus
Stickstoff, Sauerstoff und Schwefel enthält und gegebenenfalls weiterhin
eine verbrückende
Gruppe enthält
(wobei Beispiele hierfür
Cyclopropyl, Cyclobutyl, Cyclopentyl, Cyclohexyl, Bicyclo[2.2.1]heptyl,
Phenyl, Pyrolyl, Imidazolyl, Pyridinyl, Pyrazinyl, Pyridazinyl,
Tetrazolyl, Pyrimidinyl, Thienyl, Furanyl, Tetrahydrofuranyl und
Kombinationen von zwei oder mehr davon einschließen), wobei der Ring gegebenenfalls durch
wenigstens einen Substituenten (zum Beispiel einen, zwei oder drei
Substituenten unabhängig
voneinander) ausgewählt
aus Halogen (zum Beispiel Fluor, Chlor, Brom oder Iod), Hydroxy,
C1-C6-Alkyl, vorzugsweise
C1-C5-Alkyl, (zum
Beispiel Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, Isobutyl,
tert.-Butyl, n-Pentyl, 1,1-Dimethylpropyl oder n-Hexyl), C1-C6-Hydroxyalkyl, vorzugsweise C1-C4-Hydroxyalkyl,
(zum Beispiel -CH2OH, -CH2CH2OH, -CH2CH2CH2OH oder -CH(OH)CH3) und C1-C6-Halogenalkyl, vorzugsweise C1-C4-Halogenalkyl, (zum Beispiel Trifluormethyl)
substituiert ist,
- (iii) eine C1-C6-Alkylgruppe,
gegebenenfalls substituiert durch wenigstens einen Substituenten
(zum Beispiel einen, zwei, drei oder vier Substituenten unabhängig voneinander)
ausgewählt
aus Halogen (zum Beispiel Fluor, Chlor, Brom oder Iod), Amino(-NH2), Hydroxy, C1-C6-Halogenalkyl, vorzugsweise C1-C4-Halogenalkyl, (zum Beispiel Trifluormethyl),
Carboxyl, C1-C6-Alkoxy,
vorzugsweise C1-C4-Alkoxy,
(zum Beispiel Methoxy, Ethoxy, n-Propoxy oder n-Butoxy), C1-C6-Alkoxycarbonyl,
vorzugsweise C1-C4-Alkoxycarbonyl (zum
Beispiel Methoxycarbonyl oder Ethoxycarbonyl), C1-C6-Alkylcarbonylamino, vorzugsweise C1-C4-Alkylcarbonylamino,
(zum Beispiel Methylcarbonylamino oder Ethylcarbonylamino) und einem
3- bis 6-gliedrigen gesättigten
oder ungesättigten
Ring, der gegebenenfalls wenigstens ein Ringheteroatom (zum Beispiel
ein, zwei, drei oder vier Ringheteroatome unabhängig voneinander) ausgewählt aus
Stickstoff, Sauerstoff und Schwefel enthält und gegebenenfalls weiterhin
eine verbrückende
Gruppe enthält
(wobei Beispiele hierfür
Cyclopropyl, Cyclobutyl, Cyclopentyl, Cyclohexyl, Bicyclo[2.2.1]heptyl,
Phenyl, Pyrolyl, Imidazolyl, Pyridinyl, Pyrazinyl, Pyridazinyl,
Tetrazolyl, Pyrimidinyl, Thienyl, Furanyl, Tetrahydrofuranyl und
Kombinationen von zwei oder mehr davon einschließen), wobei der Ring gegebenenfalls
durch wenigstens einen Substituenten (zum Beispiel einen, zwei oder
drei Substituenten unabhängig
voneinander) ausgewählt aus
Halogen (zum Beispiel Fluor, Chlor, Brom oder Iod), Hydroxy, Oxo(=O),
C1-C6-Alkyl, vorzugsweise C1-C4-Alkyl, (zum
Beispiel Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, Isobutyl,
tert.-Butyl, n-Pentyl,
oder n-Hexyl), C1-C6-Hydroxyalkyl,
vorzugsweise C1-C4-Hydroxyalkyl,
(zum Beispiel -CH2OH, -CH2CH2OH, -CH2CH2CH2OH oder -CH(OH)CH3) und C1-C6-Halogenalkyl, vorzugsweise C1-C4-Halogenalkyl, (zum Beispiel Trifluormethyl)
substituiert ist, oder
- (iv) C1-C6-Alkylsulfonyl,
vorzugsweise C1-C4-Alkylsulfonyl, (zum
Beispiel Methylsulfonyl oder Ethylsulfonyl), oder R11 und
R12 bilden zusammen mit dem Stickstoffatom,
an das sie gebunden sind, einen 4- bis 7-gliedrigen gesättigten
heterocyclischen Ring, der gegebenenfalls weiterhin ein Ringstickstoff-,
-sauerstoff- oder -schwefelatom enthält (zum Beispiel Pyrrolidinyl,
Piperidinyl, Piperazinyl, Morpholinyl oder Thiomorpholinyl) und
der gegebenenfalls unter Bildung eines 8- bis 11-gliedrigen Ringsystems an einen Benzolring
kondensiert ist (zum Beispiel Dihydroisochinolinyl oder Dihydroisoindolyl),
wobei der heterocyclische Ring bzw. das Ringsystem gegebenenfalls
durch wenigstens einen Substituenten (zum Beispiel einen, zwei,
drei oder vier Substituenten unabhängig voneinander) ausgewählt aus
Halogen (zum Beispiel Fluor, Chlor, Brom oder Iod), Hydroxy, Amido (-CONH2), C1-C6-Alkyl,
vorzugsweise C1-C4-Alkyl,
(zum Beispiel Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, Isobutyl,
tert.-Butyl, n-Pentyl oder n-Hexyl),
C1-C6-Hydroxyalkyl,
vorzugsweise C1-C4-Hydroxyalkyl, (zum
Beispiel -CH2OH, -CH2CH2OH, -CH2CH2CH2OH oder -CH(OH)CH3), C1-C6-Alkoxy,
vorzugsweise C1-C4-Alkoxy,
(zum Beispiel Methoxy, Ethoxy, n-Propoxy oder n-Butoxy), C1-C6-Alkoxycarbonyl,
vorzugsweise C1-C4-Alkoxycarbonyl,
(zum Beispiel Methoxycarbonyl oder Ethoxycarbonyl), C1-C6-Halogenalkyl,
vorzugsweise C1-C4-Halogenalkyl,
(zum Beispiel Trifluormethyl), C1-C6-Alkylamino, vorzugsweise C1-C4-Alkylamino, (zum Beispiel Methylamino oder
Ethylamino), Di-C1-C6-alkylamino,
vorzugsweise Di-C1-C4-alkylamino,
(zum Beispiel Dimethylamino), C1-C6-Alkylcarbonyl, vorzugsweise C1-C4-Alkylcarbonyl, (zum Beispiel Methylcarbonyl
oder Ethylcarbonyl), C1-C6-Alkylcarbonylamino,
vorzugsweise C1-C4-Alkylcarbonylamino,
(zum Beispiel Methylcarbonylamino oder Ethylcarbonylamino), C1-C6-Alkylaminocarbonyl, vorzugsweise C1-C4-Alkylaminocarbonyl,
(zum Beispiel Methylaminocarbonyl oder Ethylaminocarbonyl), Di-C1-C6-alkylaminocarbonyl,
vorzugsweise Di-C1-C4-alkylaminocarbonyl,
(zum Beispiel Dimethylaminocarbonyl), Phenyl, Halogenphenyl (zum
Beispiel Fluorphenyl oder Chlorphenyl), Phenylcarbonyl, Phenylcarbonyloxy
und Hydroxydiphenylmethyl substituiert ist.
-
Bei
einer Ausführungsform
der Erfindung stehen R11 und/oder R12 für
einen 3- bis 6-gliedrigen gesättigten
oder ungesättigten
Ring, der gegebenenfalls wenigstens ein Ringheteroatom (zum Beispiel
ein, zwei, drei oder vier Ringheteroatome unabhängig voneinander) ausgewählt aus
Stickstoff, Sauerstoff und Schwefel enthält und gegebenenfalls weiterhin
eine verbrückende
Gruppe enthält,
wobei der Ring gegebenenfalls durch wenigstens einen Substituenten
(zum Beispiel einen, zwei oder drei Substituenten unabhängig voneinander) ausgewählt aus Hydroxy,
C1-C6-Alkyl, vorzugsweise
C1-C5-Alkyl, (zum
Beispiel Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, Isobutyl,
tert.-Butyl, n-Pentyl, 1,1-Dimethylpropyl oder n-Hexyl), C1-C6-Hydroxyalkyl,
vorzugsweise C1-C4-Hydroxyalkyl, (zum
Beispiel -CH2OH, -CH2CH2OH, -CH2CH2CH2OH oder -CH(OH)CH3) substituiert ist.
-
Bei
einer anderen Ausführungsform
der Erfindung stehen R11 und/oder R12 für
einen 3- bis 6-gliedrigen gesättigten
oder ungesättigten
Ring, der gegebenenfalls wenigstens ein Ringstickstoffatom und gegebenenfalls
weiterhin eine verbrückende
Gruppe (insbesondere, Cyclopropyl, Cyclopentyl, Cyclohexyl, Bicyclo[2.2.1]heptyl,
Phenyl, Pyrrolidinyl und Tetrazolyl) enthält, wobei der Ring gegebenenfalls
durch wenigstens einen Substituenten (zum Beispiel einen, zwei oder
drei Substituenten unabhängig
voneinander) ausgewählt aus
Hydroxy, C1-C5-Alkyl
und C1-C2-Hydroxyalkyl substituiert ist.
-
Bei
einer Ausführungsform
der Erfindung stehen R11 und/oder R12 für
eine C1-C6-Alkylgruppe,
die gegebenenfalls substituiert ist durch wenigstens einen Substituenten
(zum Beispiel einen, zwei, drei oder vier Substituenten unabhängig voneinander)
ausgewählt
aus Amino, Hydroxy, C1-C6-Alkoxy,
vorzugsweise C1-C4-Alkoxy,
(zum Beispiel Methoxy, Ethoxy, n-Propoxy oder n-Butoxy), C1-C6-Alkoxycarbonyl, vorzugsweise C1-C4-Alkoxycarbonyl, (zum Beispiel Methoxycarbonyl
oder Ethoxycarbonyl), C1-C6-Alkylcarbonylamino,
vorzugsweise C1-C4-Alkylcarbonylamino,
(zum Beispiel Methylcarbonylamino oder Ethylcarbonylamino) und einem
3- bis 6-gliedrigen gesättigten
oder ungesättigten
Ring, der gegebenenfalls wenigstens ein Ringheteroatom (zum Beispiel
ein, zwei, drei oder vier Ringheteroatome unabhängig voneinander) ausgewählt aus
Stickstoff und Sauerstoff enthält
und gegebenenfalls weiterhin eine verbrückende Gruppe enthält, wobei
der Ring gegebenenfalls durch wenigstens einen Substituenten (zum
Beispiel einen, zwei oder drei Substituenten unabhängig voneinander)
ausgewählt
aus Halogen (zum Beispiel Fluor, Chlor, Brom oder Iod), Hydroxy,
Oxo, C1-C6-Alkyl,
vorzugsweise C1-C4-Alkyl,
(zum Beispiel Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, Isobutyl, tert.-Butyl,
n-Pentyl oder n-Hexyl), C1-C6-Hydroxyalkyl, vorzugsweise
C1-C4-Hydroxyalkyl,
(zum Beispiel -CH2OH, -CH2CH2OH, -CH2CH2CH2OH oder -CH(OH)CH3) und C1-C6-Halogenalkyl, vorzugsweise C1-C4-Halogenalkyl, (zum Beispiel Trifluormethyl)
substituiert ist.
-
Bei
einer anderen Ausführungsform
der Erfindung stehen R11 und/oder R12 für
eine C1-C6-Alkylgruppe, die
gegebenenfalls substituiert ist durch wenigstens einen Substituenten
(zum Beispiel einen, zwei, drei oder vier Substituenten unabhängig voneinander)
ausgewählt
aus Amino, Hydroxy, C1-C4-Alkoxy,
C1-C2-Alkoxycarbonyl,
C1-C2-Alkylcarbonylamino und einem 3- bis 6-gliedrigen
gesättigten
oder ungesättigten
Ring, der gegebenenfalls ein oder zwei Ringheteroatom ausgewählt aus
Stickstoff und Sauerstoff enthält
und gegebenenfalls weiterhin eine verbrückende Gruppe (insbesondere
Cyclopropyl, Bicyclo[2,2,1]heptyl, Phenyl oder Tetrahydrofuranyl,
enthält,
wobei der Ring gegebenenfalls durch wenigstens einen Substituenten
(zum Beispiel einen, zwei oder drei Substituenten unabhängig voneinander)
ausgewählt
aus Oxo (zum Beispiel unter Bildung eines 2,5-Dioxoimidazolidinylrings) und C1-C2-Alkyl substituiert
ist.
-
Bei
einer Ausführungsform
der Erfindung bilden R11 und R12 zusammen
mit dem Stickstoffatom, an das sie gebunden sind, einen 4- bis 7-gliedrigen
gesättigten
heterocyclischen Ring, der gegebenenfalls weiterhin ein Ringstickstoff-,
-sauerstoff- oder -schwefelatom enthält (zum Beispiel Pyrrolidinyl,
Piperidinyl, Piperazinyl, Morpholinyl oder Thiomorpholinyl) und
der gegebenenfalls mit einem Benzolring kondensiert ist und ein
8- bis 11-gliedriges
Ringsystem (zum Beispiel Dihydroisochinolinyl oder Dihydroisoindolyl)
bildet, wobei der heterocylische Ring bzw. das heterocyclische Ringsystem
gegebenenfalls substituiert ist durch wenigstens einen Substituenten
(zum Beispiel einen, zwei, drei oder vier Substituenten unabhängig voneinander)
ausgewählt aus
Halogen (zum Beispiel Fluor, Chlor, Brom oder Iod), Hydroxy, Amido,
C1-C6-Alkyl, vorzugsweise
C1-C4-Alkyl, (zum
Beispiel Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, Isobutyl, tert.-Butyl, n-Pentyl
oder n-Hexyl), C1-C6-Hydroxyalkyl,
vorzugsweise C1-C4-Hydroxyalkyl,
(zum Beispiel -CH2OH, -CH2CH2OH, -CH2CH2CH2OH oder -CH(OH)CH3), C1-C6-Alkoxy,
vorzugsweise C1-C4-Alkoxy,
(zum Beispiel Methoxy, Ethoxy, n-Propoxy oder n-Butoxy), C1-C6-Alkoxycarbonyl, vorzugsweise
C1-C4-Alkoxycarbonyl,
(zum Beispiel Methoxycarbonyl oder Ethoxycarbonyl), C1-C6-Halogenalkyl,
vorzugsweise C1-C4-Halogenalkyl,
(zum Beispiel Trifluormethyl), Di-C1-C6-alkylamino, vorzugsweise Di-C1-C4-alkylamino, (zum Beispiel Dimethylamino),
C1-C6-Alkylcarbonylamino,
vorzugsweise C1-C4-Alkylcarbonylamino,
(zum Beispiel Methylcarbonylamino oder Ethylcarbonylamino), Di-C1-C6-alkylaminocarbonyl,
vorzugsweise Di-C1-C4-alkylaminocarbonyl,
(zum Beispiel Dimethylaminocarbonyl), Phenyl, Halogenphenyl (zum
Beispiel Fluorphenyl oder Chlorphenyl), Phenylcarbonyloxy und Hydroxydiphenylmethyl.
-
Bei
einer Ausführungsform
der Erfindung bilden R11 und R12 zusammen
mit dem Stickstoffatom, an das sie gebunden sind, einen 5- bis 6-gliedrigen
gesättigten
heterocyclischen Ring, der gegebenenfalls weiterhin ein Ringstickstoff-,
-sauerstoff- oder -schwefelatom enthält und der gegebenenfalls mit
einem Benzolring kondensiert ist und ein 9- bis 10-gliedriges Ringsystem
bildet, wobei der heterocylische Ring bzw. das heterocyclische Ringsystem
gegebenenfalls substituiert ist durch einen oder zwei Substituenten
unabhängig
voneinander ausgewählt
aus Fluor, Hydroxy, Amido, C1-C2-Alkyl, C1-C2-Hydroxyalkyl, C1-C2-Alkoxy, C1-C2-Alkoxycarbonyl,
C1-C2Halogenalkyl,
Di-C1-C2-alkylamino,
C1-C2-Alkylcarbonylamino,
Di-C1-C2-alkylaminocarbonyl, Phenyl, Chlorphenyl,
Phenylcarbonyloxy und Hydroxydiphenylmethyl.
-
Bei
einer anderen Ausführungsform
der Erfindung bilden R11 und R12 zusammen
mit dem Stickstoffatom, an das sie gebunden sind, einen heterocyclischen
Ring oder ein heterocyclisches Ringsystem ausgewählt aus Pyrrolidinyl, Piperidinyl,
Piperazinyl, Morpholinyl, Thiomorpholinyl, Dihydroisochinolinyl
und Dihydroisoindolyl, wobei der heterocyclische Ring bzw. das heterocyclische
Ringsystem gegebenenfalls substituiert ist durch einen oder zwei
Substituenten unabhängig
voneinander ausgewählt
aus Fluor, Hydroxy, Amido, Methyl, Hydroxymethyl, 2-Hydroxyethyl,
Methoxy, Methoxycarbonyl, Trifluormethyl, Dimethylamino, Methylcarbonylamino,
Dimethylaminocarbonyl, Phenyl, Chlorphenyl, Phenylcarbonyloxy und
Hydroxydiphenylmethyl.
-
R12a steht für ein Wasserstoffatom oder
eine C1-C6-Alkylgruppe, vorzugsweise
eine C1-C4-Alkylgruppe, (zum
Beispiel Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, Isobutyl,
tert.-Butyl, n-Pentyl oder n-Hexyl).
-
Bei
einer Ausführungsform
der Erfindung steht R12a für ein Wasserstoffatom
oder eine Methylgruppe.
-
R13 steht für eine C1-C6-Alkylgruppe, vorzugsweise eine C1-C4-Alkylgruppe,
(zum Beispiel Methyl, Ethyl, n-Propyl,
Isopropyl, n-Butyl, Isobutyl, tert.-Butyl, n-Pentyl oder n-Hexyl), Amino- oder Phenylgruppe.
-
Bei
einer Ausführungsform
der Erfindung:
steht R1 jeweils unabhängig für Halogen
oder C1-C6-Alkyl;
steht
einer der Reste X und Y für
eine Bindung und der andere der Reste X und Y steht für ein Sauerstoffatom und
Z steht für
-CH2-, oder X steht für -CH2-,
Y steht für
ein Sauerstoffatom und Z steht für
eine Bindung;
stehen R4, R5,
R6 und R7 jeweils
für ein
Wasserstoffatom und R8 steht für ein Wasserstoffatom
oder eine C1-C5-Alkylgruppe;
steht
t für 1
oder 2; und
steht R9 jeweils unabhängig für Hydroxy
(zum Beispiel in der para-Position zu R3)
oder Halogen (zum Beispiel entweder in der para-Position zu R3 oder in der para-Position zu -O-).
-
Bei
einer Ausführungsform
der Erfindung:
steht m für
0 oder 1;
steht R1 jeweils unabhängig für Fluor,
Chlor, Methyl oder Trifluormethyl;
steht entweder X für eine Bindung,
-CH2- oder -O- und Y steht für eine Bindung, -CH2- oder -O-, oder X und Y zusammen stehen
für eine
Gruppe -CH=C(CH3), und Z steht für eine Bindung,
-O- oder -CH2-, mit der Maßgabe, daß jeweils
nur einer der Reste X, Y und Z für
eine Bindung stehen kann und mit der Maßgabe, daß X und Y nicht beide gleichzeitig
für -O-
stehen;
steht n für
0 oder 1;
steht R2 für Fluor;
steht
q für 0
oder 1;
steht R3 für -NHC(O)R10,
-C(O)NR11R12 oder
-COOR12a;
stehen R4,
R5, R6, R7 und R8 jeweils
unabhängig
voneinander für
ein Wasserstoffatom oder eine Methylgruppe;
steht t für 0, 1 oder
2;
steht R9 jeweils unabhängig für Halogen,
Hydroxy, Carboxyl, Methyl, Methoxy, Methoxycarbonyl oder Trifluormethyl;
steht
R10 für
Methyl, Cyclopentyl, Phenyl oder eine Gruppe -NR14R15;
stehen R11 und
R12 jeweils unabhängig voneinander für
- (i) ein Wasserstoffatom,
- (ii) einen 3- bis 6-gliedrigen gesättigten oder ungesättigten
Ring, der gegebenenfalls wenigstens ein Ringstickstoffatom enthält und gegebenenfalls
weiterhin eine verbrückende
Gruppe enthält,
wobei der Ring gegebenenfalls substituiert ist durch wenigstens
einen Substituenten ausgewählt
aus Hydroxy, C1-C5-Alkyl und C1-C2-Hydroxyalkyl,
- (iii) eine C1-C6-Alkylgruppe,
gegebenenfalls substituiert durch wenigstens einen Substituenten
ausgewählt aus
Amino, Hydroxy, C1-C4-Alkoxy, C1-C2-Alkoxycarbonyl,
C1-C2-Alkylcarbonylamino
und einem 3- bis 6-gliedrigen gesättigten oder ungesättigten
Ring, der gegebenenfalls ein oder zwei Ringheteroatome ausgewählt aus
Stickstoff und Sauerstoff enthält
und gegebenenfalls weiterhin eine verbrückende Gruppe enthält, wobei
der Ring gegebenenfalls durch wenigstens einen Substituenten ausgewählt aus
Oxo und C1-C2-Alkyl substituiert
ist, oder
- (iv) Methylsulfonyl, oder
R11 und
R12 bilden zusammen mit dem Stickstoffatom,
an das sie gebunden sind, einen 5- bis 6-gliedrigen gesättigten heterocyclischen Ring,
der gegebenenfalls weiterhin ein Ringstickstoff-, sauerstoff- oder
-schwefelatom enthält
und gegebenenfalls an einen Bezolring kondensiert ist und ein 9-
bis 10-gliedriges Ringsystem bildet, wobei der heterocyclische Ring
bzw. das heterocyclische Ringsystem gegebenenfalls substituiert
ist durch einen oder zwei Substituenten unabhängig voneinander ausgewählt aus
Fluor, Hydroxy, Amido, C1-C2-Alkyl, C1-C2-Hydroxyalkyl, C1-C2-Alkoxy, C1-C2-Alkoxycarbonyl,
C1-C2-Halogenalkyl,
Di-C1-C2-alkylamino,
C1-C2- Alkylcarbonylamino,
Di-C1-C2-alkylaminocarbonyl,
Phenyl, Chlorphenyl, Phenylcarbonyloxy und Hydroxydiphenylmethyl;
steht
R12a für
ein Wasserstoffatom oder eine Methylgruppe; und
stehen R14 und R15 jeweils
unabhängig
voneinander für
ein Wasserstoffatom oder eine C1-C6-Alkylsulfonylgruppe, oder R14 und
R15 bilden zusammen mit dem Stickstoffatom,
an das sie gebunden sind, einen 5- bis 6-gliedrigen gesättigten
heterocyclischen Ring, der gegebenenfalls durch wenigstens ein Hydroxy
substituiert ist.
-
Bei
einer Ausführungsform
der Erfindung:
steht m für
0 oder 1;
steht R1 für Halogen;
steht
entweder X für
eine Bindung, -CH2- oder -O- und Y steht für eine Bindung,
-CH2- oder -O-, oder X und Y zusammen stehen
für eine
Gruppe -CH=C(CH3), und Z steht für eine Bindung,
-O- oder -CH2-, mit der Maßgabe, daß jeweils
nur einer der Reste X, Y und Z für
eine Bindung stehen kann und mit der Maßgabe, daß X und Y nicht beide gleichzeitig
für -O-
stehen;
steht n für
0;
steht q für
0 oder 1;
steht R3 für -NHC(O)R10, C(O)NR11R12 oder -COOR12a;
stehen R4, R5, R6, R7 und R8 jeweils unabhängig voneinander für ein Wasserstoffatom
oder eine Methylgruppe;
steht t für 0 oder 1;
steht R9 für
Halogen, Hydroxy, Methoxy oder Trifluormethyl;
steht R10 für
Methyl;
stehen R11 und R12 jeweils
unabhängig
voneinander für
Wasserstoff, Methyl, Cyclopropyl, Hydroxyethyl oder Aminoethyl,
oder R11 und R12 bilden
zusammen mit dem Stickstoffatom, an das sie gebunden sind, eine
Morpholinylgruppe oder bilden eine durch Hydroxy substituierte Piperidinylgruppe;
und
steht R12a für ein Wasserstoffatom.
-
Beispiele
für erfindungsgemäße Verbindungen
schließen
die folgenden ein:
N-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}phenyl)acetamid,
N-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-fluorphenyl)acetamid,
N-(2-{E(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-methoxyphenyl)acetamid,
N-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxyphenyl)acetamid,
N-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-5-(trifluormethyl)phenyl]acetamid,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-N-cyclopropylbenzamid,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-N-cyclopropyl-4-fluorbenzamid,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-N-cyclopropyl-4-methoxybenzamid,
N-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxy-2-methylpropyl]oxy}-4-hydroxyphenyl}acetamidtrifluoracetat,
N-(5-Chlor-2-{[(2S)-3-(6-chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}phenyl)acetamid,
N-(2-{[(2S)-3-(6-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-fluorphenyl)acetamid,
N-(2-{(2S)-3-(6-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}phenyl)acetamid,
N-(2-{[(2S)-3-(6-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-methoxyphenyl)acetamid,
2-{[(2S)-3-(6-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-N-cyclopropyl-4-fluorbenzamid,
N-(2-{[(2S)-3-(5-Fluor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl}phenyl)acetamid,
N-Cyclopropyl-2-{[(2S)-2-hydroxy-3-(1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)propyl]oxy}benzamid,
N-(4-Chlor-2-{[(2S)-2-hydroxy-3-(1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)propyl]oxy}phenyl)acetamid,
N-(5-Chlor-2-{[(2S)-2-hydroxy-3-(1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)propyl]oxy}phenyl)acetamid,
N-[2-{[(2S)-2-Hydroxy-2-methyl-3-(1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)propyl]oxy}-4-methoxyphenyl)acetamid,
N-(2-{[(2S)-2-Hydroxy-3-(1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)propyl]oxy}-5-(trifluormethyl)phenyl]acetamid,
N-(2-{[(2S)-2-Hydroxy-3-(2-methyl-1'H-spiro[inden-1,4'-piperidin]-1'-yl)propyl]oxy}phenyl)acetamid,
N-(2-{[(2S)-3-(2,3-Dihydro-1'H-spiro[inden-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}phenyl)acetamid,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-N-cyclopropyl-4-hydroxybenzamid,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran- 2,4'-piperidin]-1'-yl)-2-hydroxy-2-methylpropyl]oxy}-N-cyclopropyl-4-hydroxybenzamid,
N-(4-Hydroxy-2-{[(2S)-2-hydroxy-3-(1'H,4H-spiro[chromen-3,4'-piperidin]-1'-yl)propyl]oxy}phenyl)acetamid,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxy-2-methylpropyl]oxy}-4-hydroxy-N-methylbenzamid(trifluoracetat),
2-{[(2S)-3-(S-Chlor-1'H,3H-spiro(1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxy]oxy}-4-hydroxy-N-methylbenzamid,
N-(2-{[(2S)-3-(5-Chlor-1'H-spiro[1,3-benzodioxol-2,4'-piperidin]-1-yl)-2-hydroxypropyl]oxy}-4-hydroxyphenyl)acetamidtrifluoracetat,
N-(2-{[(2S)-3-(5-Chlor-1'H-spiro[1,3-benzodioxol-2,4'-piperidin]-1'-yl)-2-hydroxy-2-methylpropyl]oxy}-4-hydroxyphenyl)acetamidtrifluoracetat,
N-(4-Hydroxy-2-{[(2S)-2-hydroxy-3-(1'H-spiro[1,3-benzodioxol-2,4'-piperidin]-1'-yl)propyl]oxy}phenyl)acetamidtrifluoracetat,
N-(4-Hydroxy-2-{[(2S)-2-hydroxy-2-methyl-3-(1'H-spiro[1,3-benzodioxol-2,4'-piperidin]-1'-yl)propyl]oxy}phenyl)acetamidtrifluoracetat,
N-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxyphenyl)acetamid,
N-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}phenyl)acetamid,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-methylbenzamid,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxy-2-methoxypropyl]oxy}-N-cyclopropyl-4-hydroxybenzamid,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran- 2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-(2-hydroxyethyl)benzamid,
N-(2-Aminoethyl)-2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzamid,
2-{[(2S)-3-(5-Fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-methylbenzamid,
N-(2-{[(2S)-3-(5-Fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxyphenyl)acetamid,
N-(2-{[(2S)-3-(5-Fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}phenyl)acetamid,
N-[2-({(2S)-3[(2S)-5-Chlor-1'H,3H-spiro[1-benzofuran-2,3'-pyrrolidin]-1'-yl]-2-hydroxypropyl}oxy)phenyl]acetamid,
N-[2-({(2S)-3[(2R)-5-Chlor-1'H,3H-spiro[1-benzofuran-2,3'-pyrrolidin]-1'-yl]-2-hydroxypropyl}oxy)phenyl]acetamid,
N-[2-({(2S)-3[(2S)-5-Chlor-1'H,3H-spiro[1-benzofuran-2,3'-pyrrolidin]-1'-yl]-2-hydroxypropyl}oxy)-4-methoxyphenyl]acetamid,
N-[2-({(2S)-3[(2R)-5-Chlor-1'H,3H-spiro[1-benzofuran-2,3'-pyrrolidin]-1'-yl]-2-hydroxypropyl}oxy)-4-methoxyphenyl]acetamid,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,3'-pyrrolidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-methylbenzamid,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoesäure(trifluoracetat),
3(S)-1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)pyrrolidin-3-ol,
3(R)-1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)pyrrolidin-3-ol,
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran- 2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-(morpholin-4-ylcarbonyl)phenol,
2-{[(2S)-3-(5-Chlor-1'H-spiro[1,3-benzodioxol-2,4'-piperidin]-1-yl)-2-hydroxypropyl]oxy}-N-methylbenzamidtrifluoracetat,
N-(2-{[(2S)-3-(6-Chlor-3,4-dihydro-1'H-spiro[chromen-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}phenyl)acetamidtrifluoracetat,
N-(2-{[(2S)-3-(6-Chlor-3,4-dihydro-1'H-spiro[chromen-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-fluorphenyl)acetamidtrifluoracetat,
2-{[(2S)-3-(6-Chlor-3,4-dihydro-1'H-spiro[chromen-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-N-methylbenzamidtrifluoracetat,
N-(2-{[(2S)-3-(6-Chlor-3,4-dihydro-1'H-spiro[chromen-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxyphenyl)acetamidtrifluoracetat,
N-(2-{[(2S)-3-(6-Chlor-3,4-dihydro-1'H-spiro[chromen-2,4'-piperidin]-1'-yl)-2-hydroxy-2-methylpropyl]oxy}-4-hydroxyphenyl)acetamidtrifluoracetat,
N-[2-({(2S)-3-[(2R)-5-Chlor-1'H,3H-spiro[1-benzofuran-2,3'-pyrrolidin]-1'-yl]-2-hydroxypropyl}oxy)-4-hydroxyphenyl]acetamid,
N-[2-({(2S)-3-[(2S)-5-Chlor-1'H,3H-spiro[1-benzofuran-2,3'-pyrrolidin]-1'-yl)-2-hydroxypropyl}oxy)-4-hydroxyphenyl]acetamid,
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-(pyrrolidin-1-ylcarbonyl)phenol,
1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)piperidin-4-ol,
(3S)-1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}benzoyl)pyrrolidin-3-ol,
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4- (piperidin-1-ylcarbonyl)phenol,
(3S)-1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)pyrrolidin-3-ol,
1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)piperidin-4-ol,
N-[4-Hydroxy-2-({(2S)-2-hydroxy-3-[5-(trifluormethyl)-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)propyl}oxy)phenyl]acetamid,
(3S)-1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)pyrrolidin-3-ylbenzoesäure,
(3S)-1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-fluorbenzoyl)pyrrolidin-3-ol,
(3S)-1-[4-Hydroxy-2-({(2S)-2-hydroxy-3-[5-(trifluormethyl)-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-i'-yl]propyl}oxy)benzoyl]pyrrolidin-3-ol,
(3S)-1-[4-Fluor-2-{[(2S)-2-hydroxy-3-(1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)propyl]oxy}benzoyl)pyrrolidin-3-ol,
4-Fluor-2-{[(2S)-3-(5-fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}benzoesäure(hydrochlorid),
(3S)-1-[4-Fluor-2-{[(2S)-3-(5-fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyi]oxy}benzoyl)pyrrolidin-3-ol,
N-[(3S)-1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)pyrrolidin-3-yl]acetamid,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-methyl-benzoesäurehydrochlorid,
(3S)-1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzo furan-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-methylbenzoyl)pyrrolidin-3-ol,
2-{[(2S)-3-(5-Fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-methylbenzoesäurehydrochlorid,
(2S)-1-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-3-(2-{[2-(hydroxymethyl)morpholin-4-yl]carbonyl}-5-methylphenoxy)propan-2-ol,
(3S)-1-(2-{[(2S)-3-(5-Fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-methylbenzoyl)pyrrolidin-3-ol,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-N-{[(4R)-2,5-dioxoimidazolidin-4-yl]methyl}-4-hydroxybenzamid,
1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)-3-(trifluormethyl)pyrrolidin-3-ol,
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-{[3-(trifluormethyl)pyrrolidin-1-yl]carbonyl}phenol,
N-[2-(Acetylamino)ethyl]-2-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzamid,
N-(5-Chlor-2-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-methoxyphenyl)acetamid,
(3S)-N-(5-Chlor-2-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}phenyl)-3-hydroxypyrrolidin-1-carbonsäureamid,
(3S)-N-(2-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}phenyl)-3-hydroxypyrrolidin-1-carbonsäureamid,
N-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-phenyl)-4-hydroxypiperidin-1-carbonsäureamid,
N-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran- 2,4-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-phenyl)harnstofftrifluoracetat,
N-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxyphenyl)harnstofftrifluoracetat,
N-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-fluorphenyl)harnstofftrifluoracetat,
N-{[(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxyphenyl)amino]carbonyl}methansulfonamidtrifluoracetat,
(4S)-2-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)isoxazolidin-4-oltrifluoracetat,
(4R)-2-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)isoxazolidin-4-oltrifluoracetat,
(4S)-2-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)-4-methylisoxazolidin-4-oltrifluoracetat,
(4R)-2-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)-4-methylisoxazolidin-4-oltrifluoracetat,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-N-(methylsulfonyl)benzamidtrifluoracetat,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-N-1H-tetrazol-5-ylbenzamidbis(trifluoracetat),
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-{[(3R)-3-(dimethylamino)pyrrolidin-1-yl]carbonyl}phenol-bis(trifluoracetat),
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-{[(3S)-3-(dimethylamino)pyrrolidin-1-yl]carbonyl}phenol bis(trifluoracetat),
(3S)-1-(5-Chlor-2-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)pyrrolidin-3-oltrifluoracetat,
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-{[(3S)-3-methoxypyrrolidin-1-yl]carbonyl}phenoltrifluoracetat,
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-{[(2R)-2-(hydroxymethyl)pyrrolidin-1-yl]carbonyl}phenoltrifluoracetat,
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-{[(2S)-2-(hydroxymethyl)pyrrolidin-1-yl]carbonyl}phenoltrifluoracetat,
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-{[3-(hydroxymethyl)pyrrolidin-1-yl]carbonyl}phenoltrifluoracetat,
1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)-D-prolinamidtrifluoracetat,
N-(4-Hydroxy-2-{[(2S)-2-hydroxy-3-(1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)propyl]oxy}-phenyl)acetamidtrifluoracetat,
N-(4-Hydroxy-2-{[(2S)-2-hydroxy-3-(5-methyl-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)propyl]oxy}phenyl)acetamidtrifluoracetat,
N-(5-Chlor-2-{[(2S)-2-hydroxy-3-(1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)propyl]oxy}-4-methoxyphenyl)acetamidtrifluoracetat,
N-(5-Chlor-4-hydroxy-2-{[(2S)-2-hydroxy-3-(1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)propyl]oxy}phenyl)acetamidtrifluoracetat,
(3S)-N-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-methoxyphenyl)-3-hydroxypyrrolidin-1-carbon säureamidtrifluoracetat,
(3S)-N-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxyphenyl)-3-hydroxypyrrolidin-1-carbonsäureamidtrifluoracetat,
(3S)-1-(4-Hydroxy-2-{[(2S)-2-hydroxy-3-(1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)propyl]-oxy}benzoyl)pyrrolidin-3-oltrifluoracetat,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-5-methylbenzoesäurehydrochlorid,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-methoxybenzoesäurehydrochlorid,
(3S)-1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-5-methylbenzoyl)pyrrolidin-3-oltrifluoracetat,
(3S)-1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-methoxybenzoyl)pyrrolidin-3-oltrifluoracetat,
5-Chlor-2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}benzoesäurehydrochlorid,
(3S)-1-(5-Chlor-2-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}benzoyl)pyrrolidin-3-oltrifluoracetat,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofurau-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-5-fluorbenzoesäurehydrochlorid,
(3S)-1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-5-fluorbenzoyl)pyrrolidin-3-oltrifluoracetat,
N-(2-{[(2S)-3-(5-Chlor-1H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-phenyl)pyrrolidin-1-carbonsäureamidtrifluoracetat,
4-(Acetylamino)-3-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}benzoesäuremethylestertrifluoracetat,
4-(Acetylamino)-3-{[(2S)-3-(5-chlor-1'H,3H-spiro[1- benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}benzoesäuretrifluoracetat,
N-(2-{[(2S)-3-(5-Chlor-3'-fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxyphenyl)acetamid,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-(2-hydroxypropyl)benzamid,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-(2-hydroxy-1,1-dimethylethyl)benzamid,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-N-cyclopentyl-4-hydroxybenzamid,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-(2-methoxyethyl)benzamid,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-(2-hydroxyphenyl)benzamid,
N-(tert-Butyl)-2-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzamid,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-(2-hydroxy-1-methylethyl)benzamid,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-isobutylbenzamid,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-(4-hydroxycyclohexyl)benzamid,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-N-(2,3-dihydroxypropyl)-4-hydroxybenzamid,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-(2-hydroxyethyl)-N-methylbenzamid,
N-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran- 2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)serinmethylester,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-N-(1-ethylpropyl)-4-hydroxybenzamid,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-(tetrahydrofuran-2-ylmethyl)benzamid,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-[1-(hydroxymethyl)-2,2-dimethylpropyl]benzamid,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-N-{[(1S,2R,5S)-6,6-dimethylbicyclo[3.1.1]hept-2-yl]-methyl}-4-hydroxybenzamid,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy]-4-hydroxy-N-[1-(hydroxymethyl)-2-methylpropyl]benzamid,
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-{[4-(2-hydroxyethyl)piperazin-1-yl]carbonyl}phenol,
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-{[3-(hydroxymethyl)piperidin-1-yl]carbonyl}phenol,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-N-[5-(1,1-dimethylpropyl)-2-hydroxyphenyl]-4-hydroxybenzamid,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-[3-(1-hydroxyethyl)phenyl]benzamid,
2-{[(2S)-3-(5-Chlor-1H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-N-(cyclopropylmethyl)-4-hydroxybenzamid,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-pyrrolidin-1-ylbenzamid,
N-[(1R,4S)-Bicyclo[2.2.1]hept-2-yl]-2-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'- yl)-2-hydroxypropyl]oxy}-4-hydroxybenzamid,
4-(4-Chlorphenyl)-1-(2-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)piperidin-4-ol,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-(2-hydroxy-1-phenylethyl)benzamid,
1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)-4-phenylpiperidin-4-ol,
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-(3,4-dihydroisochinolin-2-(1H)-ylcarbonyl)phenol,
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-{[2-(hydroxymethyl)piperidin-1-yl]carbonyl}phenol,
1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)-N,N-dimethylprolinamid,
(4R)-1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)-4-hydroxyprolinmethylester,
(3R)-1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)piperidin-3-ol,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-(2-hydroxycyclohexyl)benzamid,
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-phenylpiperidin-1-yl)carbonyl]phenol,
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-(thiomorpholin-4-ylcarbonyl)phenol,
1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)piperidin-3-ol,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-N-(cyclo propylmethyl)-4-hydroxy-N-propylbenzamid,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N,N-diisobutylbenzamid,
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro(1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-(1,3-dihydro-2H-isoindol-2-ylcarbonyl)phenol,
N-(2-tert-Butoxyethyl)-2-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-isobutylbenzamid,
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-fluorpiperidin-1-yl)carbonyl]phenol,
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4,4-difluorpiperidin-1-yl)carbonyl]phenol,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-N-phenylbenzamid,
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-({(2R)-2-[hydroxy(diphenyl)methyl]pyrrolidin-1-yl}carbonyl]phenol,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-(2-hydroxyethyl)-N-methylbenzamid,
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-(pyrrolidin-1-ylcarbonyl)phenol,
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-{[4-(2-hydroxyethyl)piperazin-1-yl]carbonyl}phenol,
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-{[3-(hydroxymethyl)piperidin-1-yl]carbonyl}phenol,
4-(4-Chlorphenyl)-1-(2-{[(2S)-3-(5-chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)piperidin-4-ol,
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'- piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-{[4-(hydroxymethyl)piperidin-1-yl]carbonyl}phenol,
1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)-4-phenylpiperidin-4-ol,
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-{3,4-dihydroisochinolin-2(1H)-ylcarbonyl)phenol,
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-{[2-(hydroxymethyl)piperidin-1-yl]carbonyl}phenol,
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-{[3-(dimethylamino)pyrrolidin-1-yl]carbonyl}phenol,
1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)-N,N-dimethylprolinamid,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-N-cyclohexyl-4-hydroxy-N-(2-hydroxyethyl)benzamid,
(4R)-1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)-4-hydroxyprolinmethylester,
(3R)-1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)piperidin-3-ol,
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-phenylpiperidin-1-yl)carbonyl]phenol,
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-(thiomorpholin-4-ylcarbonyl)phenol,
1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)piperidin-3-ol,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-N-(cyclopropylmethyl)-4-hydroxy-N-propylbenzamid,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'- piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N,N-diisobutylbenzamid,
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-(1,3-dihydro-2H-isoindol-2-ylcarbonyl)phenol,
N-(2-tert-Butoxyethyl)-2-{[(2S)-3-(5-chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-isobutylbenzamid,
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-fluorpiperidin-1-yl)carbonyl]phenol,
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4,4-difluorpiperidin-1-yl)carbonyl]phenol,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-(2-hydroxypropyl)benzamid,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-(2-hydroxy-1,1-dimethylethyl)benzamid,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-N-cyclopentyl-4-hydroxybenzamid,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-(2-methoxyethyl)benzamid,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-(2-hydroxyphenyl)benzamid,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-(2-hydroxy-1-methylethyl)benzamid,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-isobutylbenzamid,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-(2-hydroxyethyl)benzamid,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'- piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-(4-hydroxycyclohexyl)benzamid,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-N-(2,3-dihydroxypropyl)-4-hydroxybenzamid,
N-2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)serinmethylester,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-N-(1-ethylpropyl)-4-hydroxybenzamid,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-(tetrahydrofuran-2-ylmethyl)benzamid,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-[1-(hydroxymethyl)-2,2-dimethylpropyl]benzamid,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-[1-(hydroxymethyl)-2-methylpropyl]benzamid,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-[3-(1-(hydroxyethyl)phenyl]benzamid,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-N-(cyclopropylmethyl)-4-hydroxybenzamid,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-pyrrolidin-1-ylbenzamid,
N-[(1R,4S)-Bicyclo[2.2.1]hept-2-yl]-2-{[(2S)-3-(5-chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzamid,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-(2-hydroxy-1-phenylethyl)benzamid,
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-(2-hydroxycyclohexyl)benzamid,
1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran- 2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)pyrrolidin-3-carbonsäureamidtrifluoracetat,
1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)-L-prolinamidtrifluoracetat,
2-Chlor-5-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-{[(3R)-3-(dimethylamino)pyrrolidin-1-yl]carbonyl}phenolbis(trifluoracetat),
2-Chlor-5-{((2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-{[(3R)-3-(hydroxymethyl)pyrrolidin-1-yl]carbonyl}phenoltrifluoracetat,
2-Chlor-5-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-{[(3S)-3-(hydroxymethyl)pyrrolidin-1-yl]carbonyl}phenoltrifluoracetat,
2-Chlor-5-{[(2S)-3-(5-fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-(pyrrolidin-1-ylcarbonyl}phenoltrifluoracetat,
N-(2-{[(2R)-3-(5-Fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-methoxyphenyl)acetamid,
2-{[(2S)-3-(5-Fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]-oxy}benzoesäuremethylester,
2-{[(2S)-3-(5-Fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}benzoesäure-(hydrochlorid),
(3S)-1-(2-{[(2S)-3-(5-Fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-benzoyl)pyrrolidin-3-ol,
3-{[(2S)-3-(5-Fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-(pyrrolidin-1-ylcarbonyl)phenol,
N-(4-Fluor-2-{[(2S)-3-(5-Fluor-1'H,3H-spiro[1-benzofuran-2,4-piperidin]-1-yl)-2-hydroxypropyl]-oxy}phenyl)acetamid,
N-(5-Chlor-2-[3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropoxy]-4-hydroxyphenyl}cyclopentancarbonsäureamid,
N-{5-Chlor-2-[3-(5-fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropoxy]-4-hydroxyphenyl}cyclopentancarbonsäureamid,
N-(5-Chlor-4-hydroxy-2-[2-hydroxy-3-(1'H,3H-spiro-[1-benzofuran-2,4'-piperidin]-1'-yl)propoxy]-phenyl}cyclopentancarbonsäureamid,
N-(5-Chlor-2-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]-oxy}-4-hydroxyphenyl)benzamidtrifluoracetat,
N-(5-Chlor-2-{[(2S)-3-(5-fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]-oxy}-4-hydroxyphenyl)benzamidtrifluoracetat,
N-(5-Chlor-2-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]-oxy}-4-hydroxyphenyl)harnstofftrifluoracetat,
N-(5-Chlor-2-{[(2S)-3-(5-fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]-oxy}-4-hydroxyphenyl)harnstofftrifluoracetat,
N-(5-Chlor-2-{[(2S)-3-(5-fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]-oxy}phenyl)harnstoff,
N-(5-Chlor-2-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]-oxy}phenyl)harnstoff,
N-(2-{[(2S)-3-(5-Fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]-oxy}phenyl)harnstoff,
N-(2-{[(2S)-2-Hydroxy-3-(1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)propyl]oxy}phenyl)harnstoff,
N-(4-Fluor-2-{[(2S)-3-(5-fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]-oxy}phenyl)harnstoff,
N-(4-Fluor-2-{[(2S)-2-hydroxy-3-(1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)propyl]oxy}-phenyl)harnstoff,
und
deren pharmazeutisch annehmbaren Salze und Solvate.
-
Die
vorliegende Erfindung stellt weiterhin ein Verfahren zur Herstellung
von Verbindungen der Formel (I) und deren pharmazeutisch annehmbaren
Salzen oder Solvaten wie oben definiert bereit, bei dem man
- (a) eine Verbindung der Formel in welcher m, R1,
n, R2, q, X, Y und Z wie in Formel (I) definiert
sind, mit einer Verbindung der Formel in welcher R3,
R4, R5, R6, R7, R8,
t und R9 wie in Formel (I) definiert sind,
umsetzt; oder
- (b) eine Verbindung der Formel in welcher m, R1,
n, R2, q, X, Y, Z, R4,
R5, R6, R7 und R8 wie in Formel
(I) definiert sind, mit einer Verbindung der Formel in welcher R3,
t und R9 wie in Formel (I) definiert sind,
in Gegenwart einer geeigneten Base umsetzt; oder
- (c) wenn R3 für -NHC(O)R10 steht,
eine Verbindung der Formel in welcher
m, R1, n, R2, q,
X, Y, Z, R4, R5,
R6, R7, R8, t und R9 wie in
Formel (I) definiert sind, mit einer Verbindung der Formel in welcher L1 für eine Abgangsgruppe
(z. B. eine Hydroxylgruppe oder ein Halogenatom wie Chlor) steht und
R10 wie in Formel (I) definiert ist, umsetzt;
oder
- (d) wenn R3 für -C(O)NR11R12 steht, eine Verbindung der Formel in welcher
L2 für
eine Abgangsgruppe (z. B. eine Hydroxylgruppe oder ein Halogenatom
wie Chlor) steht und m, R1, n, R2, q, X, Y, Z, R4,
R5, R6, R7, R8, t und R9 wie in Formel (I) definiert sind, mit einer
Verbindung der Formel (IX), NHR11R12, in welcher R11 und
R12 wie in Formel (I) definiert sind, umsetzt;
oder
- (e) wenn R9 für -NHC(O)R10 steht,
R10 für
-NR14R15 steht und
R14 und R15 beide
für Wasserstoff
stehen, eine wie oben in (c) definierte Verbindung der Formel (VI)
mit Kaliumcyanat umsetzt;
-
und
gegebenenfalls im Anschluß an
(a), (b), (c), (d) und (e) ein pharmazeutisch annehmbares Salz oder
Solvat bildet.
-
Die
erfindungsgemäßen Verfahren
können
zweckmäßigerweise
in Gegenwart eines Lösungsmittels, zum
Beispiel eines organischen Lösungsmittels
wie eines Alkohols (zum Beispiel Methanol oder Ethanol), eines Kohlenwasserstoffs
(zum Beispiel Toluol) oder Tetrahydrofuran, Dimethylformamid, N-Methylpyrrolidinon oder
Acetonitril bei einer Temperatur von zum Beispiel 0°C oder darüber, wie
bei einer Temperatur im Bereich von 0, 5, 10, 15 oder 20°C bis 100,
110 oder 120°C
durchgeführt
werden.
-
Bestimmte
Verbindungen der Formel (II) sind neu. So stellt die vorliegende
Erfindung weiterhin Zwischenprodukte der Formel
bereit, wobei R
1a ausgewählt ist
aus Fluor, Chlor, Methyl und Trifluormethyl; s für 1 oder 2 steht; q für 0 oder
1 steht; w für
0 oder 1 steht; und R
2a für Fluor
steht.
-
Spezifische
Beispiele für
Verbindungen der Formel (IIR) schließen die folgenden ein: 5-Fluor-3H-spiro[1-benzofuran-2,4'-piperidin]
5-Methyl-3H-spiro[1-benzofuran-2,4'-piperidin]
5-
(Trifluormethyl)-3H-spiro[1-benzofuran-2,4'-piperidin]
5-Chlor-3'-fluor-3H-spiro[1-benzofuran-2,4'-piperidin]
5-Chlor-3H-spiro[1-benzofuran-2,3'-pyrrolidin]
und 6-Chlor-3,4-dihydrospiro[chromen-2,4'-piperidin]
-
Andere
Verbindungen der Formel (II) und Verbindungen der Formeln (III),
(IV), (V), (VI), (VII), (VIII) und (IX) sind entweder im Handel
erhältlich,
aus der Literatur bekannt oder lassen sich nach bekannten Verfahren darstellen.
-
Verbindungen
der Formel (II), in denen m für
1 steht, R
1 für Chlor oder Fluor steht, n
für 0 steht,
q für 1
steht, einer der Reste X und Y für
eine Bindung steht und der andere der Reste X und Y für ein Sauerstoffatom
steht und Z für
CH
2 steht, lassen sich gemäß den folgenden
Reaktionsschemata darstellen, in denen DMF für Dimethylformamid steht, EtOH
für Ethanol
steht, DME für
1,2-Dimethoxyethan steht, i-Pr für
Isopropyl steht, THF für
Tetrahydrofuran steht, KOtBu für
Kalium-tert.-butanolat
steht und HOAc für
Essigsäure
steht:
-
Die
Verbindungen der Formel (II), in denen m für 1 steht, R
1 für Chlor
steht, n für
0 steht, q für
1 steht, X für
CH
2 steht, Y für ein Sauerstoffatom steht
und Z für
eine Bindung steht, lassen sich gemäß. dem folgenden Reaktionsschema
darstellen, in welchem THF für
Tetrahydrofuran steht:
-
Verbindungen
der Formel (II), in denen m für
1 steht, R
1 für Chlor steht, n für 0 steht,
q für 0
steht, einer der Reste X und Y für
eine Bindung steht und der andere der Reste X und Y für ein Sauerstoffatom
steht und Z für
CH
2 steht, lassen sich gemäß dem folgenden Reaktionsschema
darstellen, in welchem DMF für
Dimethylformamid steht und EtOH für Ethanol steht:
-
Die
Verbindungen der Formel (II), in denen m für 1 steht, R
1 für Methyl
steht, n für
0 steht, q für
1 steht, der eine der Reste X und Y für eine Bindung steht und der
andere der Reste X und Y für
ein Sauerstoffatom steht und Z für
CH
2 steht, lassen sich gemäß dem folgenden
Reaktionsschema darstellen, in welchem DMSO für Dimethylsulfoxid steht:
-
Die
Verfahrensrouten (C), (D) und (H) oben sind neu.
-
Die
vorliegende Erfindung stellt somit weiterhin ein Verfahren zur Herstellung
von wie oben definierten Verbindungen der Formel (IIA), in denen
s für 1
steht, bereit, bei dem man eine Verbindung der Formel
in welcher L
1 für eine geeignete
Abgangsgruppe (z. B. eine Elektronenabzugsgruppe wie ein Halogenatom) oder
eine Alkoxygruppe, insbesondere eine Methoxygruppe, steht, L
2 für
eine geeignete Abgangsgruppe wie ein Halogenatom steht und R
1a wie in Formel (IIA) definiert ist, mit
einer Verbindung der Formel
in welcher R
20 für eine Schutzgruppe
wie eine Benzylgruppe oder eine Gruppe -C(O)-O-R
21,
in welcher R
21 für eine Alkylgruppe (z. B. C
1-C
6-Alkyl, insbesondere
tert.-Butyl) oder eine Arylgruppe (z. B. Phenyl) steht und q, w
und R
2a wie in Formel (IIA) definiert sind,
unter Bildung einer Verbindung der Formel
umsetzt und anschließend cyclisiert
und dann die Schutzgruppe R
20 entfernt.
-
Wie
für den
Fachmann leicht ersichtlich ist, müssen bei den erfindungsgemäßen Verfahren
bestimmte funktionelle Gruppen, wie Hydroxyl- oder Aminogruppen,
in den Reagentien möglicherweise
durch Schutzgruppen geschützt werden.
Somit kann die Herstellung der Verbindungen der Formel (I) die Abspaltung
einer oder mehrerer Schutzgruppen in einer geeigneten Stufe umfassen.
-
Die
Schätzung
und Entschützung
funktioneller Gruppen wird in „Protective
Groups in Organic Chemistry",
Herausgeber J. W. F. McOmie, Plenum Press (1973), und „Protective
Groups in Organic Synthesis", 3.
Auflage, T. W. Greene & P.
G. M. Wuts, Wiley-Interscience (1999), beschrieben.
-
Die
Verbindungen der obigen Formel (I) können in ein pharmazeutisch
annehmbares Salz oder Solvat davon, vorzugsweise ein Säureadditionssalz,
wie z. B. ein Hydrochlorid, Hydrobromid, Phosphat, Acetat, Fumarat,
Maleat, Tartrat, Citrat, Oxalat, Methansulfonat oder p-Toluolsulfonat, umgewandelt
werden.
-
Verbindungen
der Formel (I) können
in stereoisomeren Formen vorliegen. Es versteht sich, daß die Erfindung
die Verwendung aller geometrischen und optischen Isomere (einschließlich von
Atropisomeren) der Verbindungen der Formel (I) und Gemische davon
einschließlich
von Racematen einschließt.
Die Verwendung von Tautomeren und Gemischen davon bildet ebenfalls
eine Ausgestaltung der vorliegenden Erfindung. Enantiomerenreine
Formen sind besonders erwünscht.
-
Die
Verbindungen der Formel (I) haben Wirkung als Pharmazeutika, insbesondere
als Modulatoren der Aktivität
von Chemokinrezeptoren (insbesondere des MIP-1α-Chemokinrezeptors),
und können
zur Behandlung von Autoimmunerkrankungen, entzündlichen Erkrankungen, proliferativen
und hyperproliferativen Erkrankungen und durch das Immunsystem vermittelten
Krankheiten einschließlich
der Abstoßung
transplantierter Organe oder Gewebe und AIDS (Acquired Immunodeficiency
Syndrome) verwendet werden.
-
Beispiele
für diese
Beschwerden sind:
- (1) (Atemwege) Atemwegserkrankungen
einschließlich
von chronischer obstruktiver Lungenerkrankung (COPD) wie irreversibler
COPD; Asthma, wie z. B. Bronchialasthma, allergisches Asthma, Intrinsic-Asthma, Extrinsic-Asthma
und stauballergisches Asthma, insbesondere chronisches oder inveteriertes
Asthma (z. B. Spätasthma
und Überreaktion
der Atemwege); Bronchitis; akute, allergische, atrophische Rhinitis
und chronische Rhinitis einschließlich Rhinitis caseosa, hypertrophischer
Rhinitis, Rhinitis purulenta, Rhinitis sicca und Rhinitis medicamentosa;
membranöse
Rhinitis einschließlich
kruppöser,
fibrinöser
und pseudomembranöser
Rhinitis und skrofulöser
Rhinitis; saisonale Rhinitis einschließlich Rhinitis nervosa (Heuschnupfen)
und vasomotorischer Rhinitis; Sarkoidose, Drescherkrankheit und
verwandte Krankheiten, Lungenfibrose und idiopathische interstitielle
Pneumonie;
- (2) (Knochen und Gelenke) rheumatoide Arthritis, seronegative
Spondyloarthropathien (einschließlich Spondylitis ankylosans,
Arthritis psoriatica und Reiter-Krankheit), Behcet-Krankheit, Sjögren-Syndrom und systemische
Sklerose;
- (3) (Haut) Psoriasis, atopische Dermatitis, Kontaktdermatitis
und andere Arten von Ekzemen, seborrhoische Dermatitis, Lichen planus,
Pemphigus, bullöser
Pemphigus, Epidermolysis bullosa, Urticaria, angioneurotische Ödeme, Gefäßentzündungen,
Erytheme, kutane Eosinophilien, Uveitis, Alopecia areata und Frühjahrskonjunktivitis;
- (4) (Magen-Darm-Trakt) Zöliakie,
Proctitis, eosinophile Gastroenteritis, Mastozytose, Morbus Crohn,
Colitis ulcerosa, nahrungsbedingte Allergien mit Wirkung auf darmferne
Stellen, z. B. Migräne,
Rhinitis und Ekzem;
- (5) (andere Gewebe und systemische Krankheiten) multiple Sklerose,
Atherosklerose, AIDS (Acquired Immunodeficiency Syndrome), Lupus
erythematodes, systemischer Lupus erythematodes, Hashimoto-Thyroiditis, Myasthenia
gravis, Typ-I-Diabetes, nephrotisches Syndrom, Eosinophilia fascitis,
Hyper-IgE-Syndrom, lepromatöse
Lepra, Sézary-Syndrom und idiopathische
thrombozytopenische Purpura;
- (6) (Allograft-Abstoßung)
akut und chronisch, beispielsweise nach Transplantation von Niere,
Herz, Leber, Lunge, Knochenmark, Haut und Hornhaut; und chronische
Graft-Versus-Host-Reaktion;
- (7) Krebs, insbesondere nicht-kleinzelliges Bronchialkarzinom
(NSCLC) und Plattenepithelsarkom;
- (8) Krankheiten, bei denen die Angiogenese mit erhöhten Chemokinspiegeln
assoziiert ist; und
- (9) zystische Fibrose, Schlaganfall, Reperfusionsverletzungen
in Herz, Gehirn und peripheren Gliedmaßen und Sepsis.
-
Gegenstand
der vorliegenden Erfindung ist demgemäß eine Verbindung der Formel
(I) oder ein pharmazeutisch annehmbares Salz oder Solvat davon gemäß obiger
Definition zur Verwendung bei der Therapie.
-
Einen
weiteren Gegenstand der vorliegenden Erfindung bildet die Verwendung
einer Verbindung der Formel (I) oder eines pharmazeutisch annehmbaren
Salzes oder Solvats davon gemäß obiger
Definition bei der Herstellung eines Arzneimittels zur Verwendung
bei der Therapie.
-
Im
Rahmen der vorliegenden Beschreibung schließt der Begriff „Therapie" auch „Prophylaxe" ein, sofern nicht
ausdrücklich
anders vermerkt. Der Begriff „therapeutisch" ist entsprechend
aufzufassen.
-
Einen
weiteren Gegenstand der vorliegenden Erfindung bildet die Verwendung
einer Verbindung der Formel (I) oder eines pharmazeutisch annehmbaren
Salzes oder Solvats davon gemäß obiger
Definition bei der Herstellung eines Arzneimittels zur Verwendung
bei der Behandlung einer entzündlichen
Erkrankung.
-
Einen
weiteren Gegenstand der vorliegenden Erfindung bildet die Verwendung
einer Verbindung der Formel (I) oder eines pharmazeutisch annehmbaren
Salzes oder Solvats davon gemäß obiger
Definition bei der Herstellung eines Arzneimittels zur Verwendung
bei der Behandlung einer Atemwegserkrankung.
-
Für die obigen
therapeutischen Anwendungen variiert die verabreichte Dosierung
natürlich
mit der eingesetzten Verbindung, der Verabreichungsart, der gewünschten
Behandlung und der indizierten Störung. Die Tagesdosis der Verbindung
der Formel (I) kann im Bereich von 0,001 mg/kg bis 30 mg/kg liegen.
-
Die
Verbindungen der Formel (I) und pharmazeutisch annehmbare Salze
und Solvate davon können für sich allein
verwendet werden, werden aber im allgemeinen in Form einer pharmazeutischen
Zusammensetzung verabreicht, in der die Verbindung der Formel (I)
bzw. das Salz bzw. das Solvat (Wirkstoff) zusammen mit einem pharmazeutisch
annehmbaren Hilfsstoff, Verdünnungsmittel
oder Träger
vorliegt. Je nach der Verabreichungsart enthält die pharmazeutische Zusammensetzung
vorzugsweise 0,05 bis 99 Gew.-% (Gewichtsprozent), besonders bevorzugt
0,05 bis 80 Gew.-%, noch weiter bevorzugt 0,10 bis 70 Gew.-% und
noch weiter bevorzugt 0,10 bis 50 Gew.-% Wirkstoff, wobei sich alle
Gewichtsprozentangaben auf die gesamte Zusammensetzung beziehen.
-
Gegenstand
der vorliegenden Erfindung ist auch eine pharmazeutische Zusammensetzung,
enthaltend eine Verbindung der Formel (I) oder ein pharmazeutisch
annehmbares Salz oder Solvat davon gemäß obiger Definition zusammen
mit einem pharmazeutisch annehmbaren Hilfsstoff, Verdünnungsmittel
oder Träger.
-
Gegenstand
der Erfindung ist ferner ein Verfahren zur Herstellung einer erfindungsgemäßen pharmazeutischen
Zusammensetzung, bei dem man eine Verbindung der Formel (I) oder
ein pharmazeutisch annehmbares Salz oder Solvat davon gemäß obiger
Definition mit einem pharmazeutisch annehmbaren Hilfsstoff, Verdünnungsmittel
oder Träger
vermischt.
-
Die
pharmazeutischen Zusammensetzungen können topisch (z. B. in die
Lunge und/oder die Atemwege oder auf die Haut) in Form von Cremes,
Lösungen,
Suspensionen, Heptafluoralkan-Aerosolen und Trockenpulverformulierungen,
oder systemisch, z. B. durch orale Verabreichung in Form von Tabletten,
Kapseln, Sirupen, Pulvern oder Granulaten, oder durch parenterale
Verabreichung in Form von Lösungen
oder Suspensionen oder durch subkutane Verabreichung oder durch
rektale Verabreichung in Form von Suppositorien oder transdermal
verabreicht werden.
-
Die
Erfindung wird nun anhand der folgenden Ausführungsbeispiele näher erläutert, in
welchen 1H-NMR-Spektren auf einem Spektrometer der
Bauart Unity Inova 400 von Varian aufgenommen wurden. Dabei wurde
der zentrale Lösungsmittelpeak
von Chloroform-d (δH 7,27 ppm), Aceton-d6 (δH 2,05
ppm), DMSO-d6 (δH 2,50
ppm), oder Methanol-d4 (δH 4,87
ppm) als interner Standard verwendet. Niedrigaufgelöste Massenspektren
und genaue Massenbestimmungen wurden auf einem LC-MS-System 1100
von Hewlett-Packard mit APCI/ESI-Ionisationskammern aufgenommen.
Alle Lösungsmittel
und im Handel erhältlichen
Reagentien waren von Laborqualität
und wurden in Lieferform verwendet. Die für die Verbindungen verwendete
Nomenklatur wurde mit ACD/IUPAC Name Pro generiert. Die in den Beispielen
verwendeten Abkürzungen
bzw. Ausdrücke haben
die folgenden Bedeutungen:
- BuLi:
- Butyllithium
- DCM:
- Dichlormethan
- DEAD:
- Azodicarbonsäurediethylester
- DMAP:
- 4-Dimethylaminopyridin
- DME:
- 1,2-Dimethoxyethan
- DMF:
- N,N-Dimethylformamid
- DMSO:
- Dimethylsulfoxid
- Et2O:
- Diethylether
- EtOAc:
- Essigsäureethylester
- EtOH:
- Ethanol
- HOAc:
- Essigsäure
- KotBu:
- Kalium-tert.-butanolat
- MeCN:
- Acetonitril
- MeOH:
- Methanol
- NMP:
- 1-Methyl-2-pyrrolidinon
- TEA:
- Triethylamin
- TFA:
- Trifluoressigsäure
- THF:
- Tetrahydrofuran
- TMSCI:
- Chlortrimethylsilan
- SELECTFLUORTM
- Fluorierungsreagens(Aldrich)
-
Chemische
Bezeichnung: 1-(Chlormethyl)-4-fluor-1,4-diazoniabicyclo[2.2.2]octan[bis(tetrafluorborat)]
PS-Carbodiimid:
ein harzgebundenes Kupplungsmittel Chemische Bezeichnung: N-Cyclohexylcarbodiimid-N'-propyloxymethylpolystyrol
-
Beispiele
-
Zwischenprodukt: 5-Chlor-3H-spiro[1-benzofuran-2,4'-piperidin]
-
Methode A:
-
Diese
Verbindung wurde wie von Effland, R. C.; Gardner, B. A.; Strupczewski,
J., J. Heterocyclic Chem., 1981, 18, 811-814 beschrieben dargestellt. Methode
B:
-
i) 1-Oxa-6-azaspiro[2,5]octan-6-carbonsäure-1,1-dimethylethylester
-
Kalium-t-butanolat
(31 g) wurde bei 20°C
zu einer gerührten
Suspension von Trimethylsulfoxoniumiodid (60,8 g) in 1,2-Dimethoxyethan
(250 ml) gegeben. Nach 1 Stunde wurde die Mischung im Verlauf von
30 Minuten bei 0°C
portionsweise zu einer gerührten
Lösung
von 4-Oxo-1-piperidincarbonsäure-1,1-dimethylethylester
(50 g) in 1,2-Dimethoxyethan (50 ml) gegeben. Nach weiteren 2 Stunden
wurde mit Wasser (500 ml) versetzt, und die Mischung wurde mit tert.-Butylmethylether
(2 × 500
ml) extrahiert. Die organischen Extrakte wurden getrennt mit einer
gesättigten
Natriumhydrogencarbonatlösung
(250 ml) gewaschen, vereinigt, über wasserfreiem
Magnesiumsulfat getrocknet, filtriert und im Vakuum eingedampft.
Das verbliebene Öl
wurde zusammen mit Toluol (100 ml) eingedampft, wodurch man die
im Untertitel genannte Verbindung (43,25 g, 81%) in Form eines Feststoffs
erhielt.
1H-NMR (400 MHz, CDCl3): δ 1,46
(9H, s), 1,43-1,48 (2H, m), 1,75-1,84 (2H, m), 2,69 (2H, s), 3,38-3,47
(2H, m), 3,70-3,75 (2H, m).
-
(ii) 5-Chlorspiro[1-benzofuran-2,4'-piperidin]-1'-carbonsäure-1,1-dimethylester
-
Eine
Lösung
von Isopropylmagnesiumchlorid in Tetrahydrofuran (2 M, 106,6 ml)
wurde bei 0°C
unter Stickstoff im Verlauf von 15 Minuten tropfenweise zu einer
gerührten
Lösung
von 2-Brom-4-chlor-1-fluorbenzol (42,5 g) in wasserfreiem Tetrahydrofuran
(250 ml) gegeben. Nach weiteren 15 Minuten wurde eine Lösung von 1-Oxa-6-azaspiro[2,5]octan-6-carbonsäure-1,1-dimethylethylester
(43,2 g) in wasserfreiem Tetrahydrofuran (50 ml) zugesetzt, gefolgt
von einem Kupfer(I)-bromid Dimethylsulfid-Komplex (0,4 g). Die Mischung
wurde 18 Stunden lang bei 40°C
gerührt,
auf 20°C
abgekühlt,
mit Wasser verdünnt
(300 ml) und mit tert.-Butylmethylether
(2 × 300
ml) extrahiert. Die organischen Extrakte wurden über wasserfreiem Magnesiumsulfat
getrocknet, filtriert und im Vakuum eingedampft. Das verbliebene Öl wurde
in 1,2-Dimethoxypropan (200 ml) gelöst. Kalium-tert.-butanolat
(22,8 g) wurde zugegeben, und die Mischung wurde 16 Stunden lang
bei 40°C
und dann 24 Stunden lang bei 50°C
gerührt.
Weiteres Kalium-tert.-butanolat (5,7 g) wurde zugesetzt, und es
wurde weitere 2 Stunden lang bei 50°C und dann 4 Stunden lang bei
55°C gerührt. Wasser
(500 ml) wurde zugegeben, und die Mischung wurde mit tert.-Butylmethylether
(2 × 300
ml) extrahiert. Die organischen Extrakte wurden über wasserfreiem Magnesiumsulfat
getrocknet, filtriert und im Vakuum eingedampft, wodurch man die
im Untertitel genannte Verbindung (47,45 g, 67%) in Form eines Öls erhielt.
1H-NMR (400 MHz, CDCl3): δ 1,47 (9H,
s), 1,67 (2H, td), 1,85-1,93 (2H, m), 2,94 (2H, s), 3,39 (2H, td), 3,65-3,80 (2H, m), 6,67
(1H, d), 7,06 (1H, d), 7,10 (1H, s).
-
iii) 5-Chlorspiro[1-benzofuran-2,4'-piperidin]
-
Konzentrierte
Salzsäure
(23 ml) wurde zu einer Lösung
von 5-Chlorspiro[1-benzofuran-2,4'-piperidin]-1'-carbonsäure-1,1-dimethylester (46,43
g) in Tetrahydrofuran (230 ml) gegeben. Die Mischung wurde 6 Stunden
lang bei 50°C
gerührt,
auf 20°C
abgekühlt,
mit Wasser (230 ml) verdünnt
und mit tert.-Butylmethylether (2 × 230 ml) extrahiert. Die wäßrige Phase
wurde durch Zugabe einer 50 Gew.-% Natriumhydroxidlösung auf
einen pH-Wert von > 10
eingestellt und mit tert.-Butylmethylether (3 × 300 ml) extrahiert. Die organischen Extrakte
wurden über
wasserfreiem Magnesiumsulfat getrocknet, filtriert und im Vakuum
eingedampft. Das verbliebene Öl
wurde in Tetrahydrofuran (240 ml) gelöst und mit konzentrierter Salzsäure (12
ml) versetzt, und die Mischung wurde 16 Stunden lang bei 20°C gerührt. Der
ausgefallene Feststoff wurde abfiltriert und in Wasser (100 ml)
gelöst.
Die Lösung
wurde durch Zugabe einer 50 Gew.-% Natriumhydroxidlösung auf
einen pH-Wert von > 10
eingestellt und mit tert.-Butylmethylether (3 × 100 ml) extrahiert, wodurch
man die Titelverbindung (13,3 g, 45%) in Form eines Feststoffs erhielt.
1H-NMR (400 MHz, CDCl3): δ 1,69-1,76
(2H, m), 1,83-1,87 (2H, m), 2,78-2,84 (2H, m), 2,98-3,03 (4H, m),
6,65 (1H, d), 7,04 (1H, d), 7,13 (1H, s).
APCI-MS: m/z 224/6
[M+H]+
-
Zwischenprodukt: 5-Fluor-3H-spiro[1-benzofuran-2,4'-piperidin]
-
Methode A:
-
i) 1'-Benzyl-5-fluor-3H-spiro[1-benzofuran-2,4'-piperidin]
-
In
eine gerührte
Suspension von Magnesiumband (763 mg) in Diethylether (7 ml) wurde
ein Iodkristall gegeben, gefolgt von 0,4 ml 2-(Brommethyl)-1,4-difluorbenzol
unter Stickstoff. Die Reaktionsmischung wurde mit einer Heißluftpistole
gestartet, und 2-(Brommethyl)-1,4-difluorbenzol (5,0 g, 24,25 mmol)
in Diethylether (7 ml) wurde so zugesetzt, daß die Mischung unter leichtem
Rückfluß blieb.
Nach dem Ende der Zugabe wurde die Reaktionsmischung 100 Minuten
unter Rückfluß gerührt und
auf Raumtemperatur abgekühlt.
Diese Reaktionsmischung wurde unter kräftigem Rühren tropfenweise mit einer
Lösung
von 1-Benzylpiperidin-4-on (4,57 g, 24,25 mmol) in Diethylether
(12 ml) versetzt. Nach dem Ende der Zugabe wurde die Reaktionsmischung über Nacht
bei Raumtemperatur gelassen. Eine wäßrige Lösung von NH4Cl
wurde zugesetzt, und die Mischung wurde bis zum Ende der Hydrolyse
bei Raumtemperatur gerührt
und dann mit Diethylether extrahiert. Die organische Phase wurde
mit H2O gewaschen, über Na2SO4 getrocknet, filtriert und im Vakuum eingeengt. Der
Rückstand
wurde durch Flash-Chromatographie
an Kieselgel (0–1%
Methanol in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man das Zwischenprodukt 1-Benzyl-4-(2,5-difluorbenzyl)piperidin-4-ol
(2,74 g) erhielt, das große
Mengen an unbekannten Verunreinigungen enthielt. Eine Suspension
von NaH (55%, 1,12 g, 26,0 mmol) in Toluol (10 ml) wurde langsam
mit einer Lösung
von 1-Benzyl-4-(2,5-difluorbenzyl)piperidin-4-ol in Toluol (15 ml)
versetzt. Nach dem Ende der Zugabe wurde die Reaktionsmischung bei
110°C gerührt (in
einem vorgeheizten Ölbad),
nach 5 Minuten wurde mit DMF (9 ml) versetzt, und es wurde weitere
2 Stunden lang bei Rückflußtemperatur
gerührt.
Die Reaktionsmischung wurde auf Raumtemperatur abgekühlt, mit
H2O (20 ml) versetzt und mit Essigsäureethylester
extrahiert. Die organische Phase wurde über Na2SO4 getrocknet, filtriert und eingeengt. Der
Rückstand
wurde durch Flash-Chromatographie an Kieselgel (0–1,5% Methanol
in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die im Untertitel genannte Verbindung (190 mg) erhielt.
1H-NMR (CDCl3, 400
MHz): δ 7,39-7,26
(m, 5H); 6,88-6,76 (m, 2H); 6,67 (dd, J = 4,2, 8,7 Hz, 1H); 3,59
(s, 2H); 2,99 (s, 2H); 2,68-2,47 (m, 4H); 2,03-1,94 (m, 2H); 1,86-1,76
(m, 2H).
APCI-MS : m/z 298 (MH+).
-
(ii) 5-Fluor-3H-spiro[1-benzofuran-2,4'-piperidin]
-
Chlorameisensäureethylester
(65,6 mg, 0,604 mmol) wurde zu einer Lösung von 1'-Benzyl-5-fluor-3H-spiro[1-benzofuran-2,4'-piperidin] (150
mg, 0,504 mmol) in Toluol (2 ml) gegeben, und die Reaktionsmischung
wurde über
Nacht unter Rückfluß erhitzt.
Die Reaktionsmischung wurde auf Raumtemperatur abgekühlt, durch
Zugabe von Toluol verdünnt
und nacheinander mit wäßriger NaHCO3 und H2O gewaschen.
Die organische Phase wurde über
Na2SO4 getrocknet,
filtriert und im Vakuum eingeengt. Der Rückstand wurde in Ethanol (3,5
ml) gelöst,
wäßrige KOH
(800 mg KOH in 0,8 ml H2O) wurde zugesetzt,
die Reaktionsmischung wurde über
Nacht bei Rückflußtemperatur
gerührt,
auf Raumtemperatur abgekühlt
und das Ethanol wurde im Vakuum entfernt. Die wäßrige Phase wurde mit Et2O extrahiert, und die vereinigten Etherphasen
wurden mit 3 N wäßriger HCl
gewaschen. Die vereinigten wäßrigen Phasen
wurden durch Zugabe von wäßriger NaOH
auf einen pH-Wert von 10 eingestellt. Die basische Lösung wurde
mit Essigsäureethylester
extrahiert. Die vereinigten organischen Phasen wurden mit H2O gewaschen, über Na2SO4 getrocknet, filtriert und eingeengt. Der Rückstand
wurde durch HPLC (10–55%
CH3CN in H2O, 0,1%
NH4OH) aufgereinigt, wodurch man die Titelverbindung
(49 mg) erhielt.
1H-NMR (CD3OD, 400 MHz): δ 6,92-6,87 (m, 1H); 6,81-6,75
(m, 1H); 6,64 (dd, J = 4,2, 8,7 Hz, 1H); 3,08-2,98 (m, 4H); 2,89-2,81
(m, 2H); 1,91-1,83 (m, 2H); 1,78-1,71 (m, 2H).
APCI-MS: m/z
208 (MH+).
-
-
(i) 4-[(5-Fluor-2-methoxyphenyl)methyl]-4-hydroxy-1-piperidincarbonsäure-1,1-dimethylethylester
-
Eine
Lösung
von Isopropylmagnesiumchlorid in Tetrahydrofuran (2 M, 130 ml) wurde
bei 30°C
unter Stickstoff im Verlauf von 30 Minuten tropfenweise zu einer
gerührten
Lösung
von 2-Brom-4-fluoranisol (34,2 ml) in wasserfreiem Tetrahydrofuran
(400 ml) gegeben. Nach weiteren 16 Studen bei 30°C wurde mit Kupfer(I)-bromid-Dimethylsulfid-Komplex
(0,4 g) versetzt, gefolgt von einer Lösung von 1-Oxa-6-azaspiro[2.5]octan-6-carbonsäure-1,1-dimethylethylester
(56,2 g) in wasserfreiem Tetrahydrofuran (110 ml). Nach weiteren
3 Stunden bei 30°C
wurde die Lösung
auf 20°C
abgekühlt,
mit Wasser (600 ml) verdünnt
und mit tert.-Butylmethylether (600 ml) und dann mit Essigsäureethylester
(600 ml) extrahiert. Die vereinigten organischen Extrakte wurden über wasserfreiem
Magnesiumsulfat getrocknet, filtriert und im Vakuum eingedampft,
wodurch man das im Untertitel genannte Rohprodukt (86 g) in Form
eines Feststoffs erhielt.
APCI-MS : m/z 240 [M+H-(CH3)2CCH2-CO2]+
-
(ii) 5-Fluorspiro[1-benzofuran-2,4'-piperidin]hydrochlorid
-
Bromwasserstoffsäure (48%,
60 ml) wurde zu einer Lösung
von rohem 4-[(5-Fluor-2-methoxyphenyl)methyl]-4-hydroxy-1-piperidincarbonsäure-1,1-dimethylethylester
in Essigsäure
(300 ml) gegeben. Die Mischung wurde 5 Stunden lang unter Rückfluß erhitzt.
Weitere Bromwasserstoffsäure
(48%, 60 ml) wurde zugegeben, und es wurde weitere 24 Stunden lang
unter Rückfluß erhitzt.
Die Mischung wurde auf Raumtemperatur abgekühlt, in Wasser gegossen (2
l) und mit tert.-Butylmethylether
(2 × 500
ml) extrahiert. Die wäßrige Phase
wurde durch Zugabe einer 50 Gew.-%igen Natriumhydroxidlösung auf
einen pH-Wert von > 10
eingestellt und mit tert.-Butylmethylether (2 l + 1 l) extrahiert.
Die organischen Extrakte wurden über
wasserfreiem Magnesiumsulfat getrocknet, filtriert und im Vakuum
eingedampft. Das verbliebene Öl
wurde in Tetrahydrofuran (200 ml) gelöst und mit konzentrierter Salzsäure (13
ml) versetzt, und die Lösung
wurde im Vakuum eingedampft. Der verbliebene Feststoff wurde aus
Tetrahydrofuran/tert.-Butylmethylether (4:1, 500 ml) aus kristallisiert,
wodurch man die Titelverbindung (20,0 g, Gesamtausbeute 31%) erhielt.
1H-NMR (CD3OD, 400
MHz): δ 1,86-1,98
(2H, m), 2,03-2,07 (2H, m), 3,05 (2H, s), 3,16-3,27 (4H, m), 6,61
(1H, dd), 6,74 (1H, dt), 6,81 (1H, dd).
APCI-MS: m/z 208 [M+H]+
-
Zwischenprodukt: 3H-Spiro[1-benzofuran-2,4'-piperidin]
-
Diese
Verbindung wurde wie von Effland, R. C; Gardner, B. A; Strupczewski,
J., J. Heterocyclic Chem., 1981, 18, 811-814 beschrieben dargestellt.
-
Zwischenprodukt:
5-Methyl-3H-spiro[1-benzofuran-2,4'-piperidin]
-
(i) 6-Benzyl-1-oxa-6-azaspiro[2.5]octan
-
Natriumhydrid
(55%ige Suspension in Mineralöl,
1,57 g, 35 mmol) wurde mit Heptan gewaschen, unter einem Stickstoffstrom
getrocknet und in trockenem DMSO (10 ml) suspendiert. Unter Stickstoff
wurde tropfenweise mit einer Lösung
von Trimethylsulfoxoniumiodid (4,8 g, 22 mmol) in DMSO (45 ml) versetzt.
Nach 20 Minuten Rühren
wurde tropfenweise mit einer Lösung
von 1-Benzylpiperidin-4-on
(3,78 g, 20 mmol) versetzt. Die Mischung wurde über Nacht bei Raumtemperatur
gerührt
und dann auf Eis (200 g) gegeben und mit Dichlormethan (2 × 200 ml)
extrahiert. Die vereinigten Extrakte wurden mit Wasser (3 × 100 ml)
gewaschen und über
Na2SO4 getrocknet.
Das Lösungsmittel
wurde im Vakuum entfernt. Der Rückstand
wurde in Diethylether gelöst,
und das unlösliche
Material wurde abfiltriert. Durch Abdampfen des Lösungsmittels
erhielt man ein hellgelbes Öl
(2,95 g, 73%).
1H-NMR (CDCl3, 400 MHz): δ 7,2-7,4 (m, 5H); 3,57 (s, 2H);
2,5-2,7 (m, 4H); 1,85 (m, 2H); 1,55 (m, 2H).
-
(ii) 1-Benzyl-4-(2-fluor-5-methylbenzyl)piperidin-4-ol
-
Eine
Lösung
von 2-Brom-1-fluor-4-methylbenzol (0,76 g, 4 mmol) in THF (15 ml)
wurde bei –70°C unter Ar
tropfenweise mit einer Lösung
von n-BuLi (1,6 M in Hexan, 2,5 ml, 4 mmol) versetzt. Die Reaktionsmischung
wurde 1 Stunde lang bei –70°C gerührt und
dann mit BF3·Et2O
(0,5 ml, 4 mmol) versetzt. Nach 20 Minuten Rühren bei –70°C wurde tropfenweise mit einer
Lösung
von 6-Benzyl-1-oxa-6-azaspiro[2.5]octan (0,41 g, 2 mmol) in trockenem
THF (5 ml) versetzt. Es wurde weitere 2 Stunden lang bei –70°C gerührt, und
dann wurde die Reaktionsmischung mit wäßriger gesättigter NH4Cl
(20 ml) gequencht. Die Phasen wurden getrennt, und die wäßrige Phase
wurde mit THF extrahiert. Die vereinigten organischen Phasen wurden über Na2SO getrocknet. Das Lösungsmittel wurde im Vakuum
entfernt. Der Rückstand
wurde mit Diethylether (50 ml) versetzt, gefolgt von 2 M HCl in
Et2O (5 ml). Der Niederschlag wurde gesammelt,
mit Et2O gewaschen und in der kleinstmöglichen
Menge an Methanol (etwa 5 ml) gelöst. Wasser (50 ml) wurde zugesetzt,
und der pH-Wert wurde durch Zugabe von 2 M wäßriger NaOH auf 10 eingestellt.
Die Mischung wurde mit Essigsäureethylester (2 × 25 ml)
extrahiert, und die vereinigten organischen Extrakte wurden über Na2SO4 getrocknet.
Durch Abdampfen des Lösungsmittels
erhielt man ein bräunliches Öl.
APCI-MS:
m/z 314 [M+H]+
-
(iii) 1'-Benzyl-5-methyl-3H-spiro[1-benzofuran-2,4'-piperidin]
-
Eine
Suspension von NaH (55% in Mineralöl, 200 mg, 5 mmol) in Toluol
(10 ml) wurde langsam mit einer Lösung von rohem 1-Benzyl-4-(2-fluor-5-methylbenzyl)piperidin-4-ol
in Toluol (15 ml) versetzt. Nach dem Ende der Zugabe wurde die Reaktionsmischung
auf 110°C
erhitzt und 5 Minuten lang gerührt.
DMF (9 ml) wurde zugegeben, und es wurde weitere 10 Stunden lang
bei Rückflußtemperatur
gerührt.
Die Reaktionsmischung wurde auf Raumtemperatur abgekühlt, in
Wasser (50 ml) gegossen und mit Essigsäureethylester (2 × 25 ml)
extrahiert. Die organische Phase wurde über Na2SO4 getrocknet, filtriert und eingeengt. Der
Rückstand wurde
durch Flash-Chromatographie an Kieselgel (Essigsäureethylester/n-Heptan) aufgereinigt,
wodurch man die im Untertitel genannte Verbindung (240 mg, 41%)
erhielt.
1H-NMR (CDCl3,
400 MHz): δ 7,2-7,4
(m, 5H); 6,8-6,9 (m, 2H); 6,64 (d, J = 10,8 Hz, 1H), 3,54 (s, 2H);
2,91 (s, 2H); 2,4-2,7 (m, 4H); 2,24 (s, 3H); 1,92 (m, 2H); 1,78
(m, 2H)
APCI-MS: m/z 294 [M+H]+
-
(iv) 5-Methyl-3H-spiro[1-benzofuran-2,4'-piperidin]
-
Eine
Lösung
von 1'-Benzyl-5-methyl-3H-spiro[1-benzofuran-2,4'-piperidin] (0,12
g, 0,41 mol) in Dichlormethan (3 ml) wurde mit Chlorameisensäure-1-chlorethylester (87
mg, 0,61 mmol) versetzt. Die Lösung wurde über Nacht
bei Raumtemperatur gerührt.
Das Lösungsmittel
wurde im Vakuum entfernt. Der Rückstand wurde
in Methanol (3 ml) gelöst,
und die Lösung
wurde 2 Stunden lang auf 70°C
erhitzt. Das Lösungsmittel wurde
abgedampft, und der Rückstand
wurde mit Diethylether versetzt. Der gebildete Niederschlag wurde
abfiltriert, mit Diethylether gewaschen und in Methanol (1 ml) gelöst. Wasser
(25 ml) wurde zugesetzt, und der pH-Wert wurde durch Zugabe von
2 M wäßriger NaOH
auf 10 eingestellt. Die Mischung wurde mit Dichlormethan (2 × 25 ml)
extrahiert, und die vereinigten organischen Extrakte wurden über Na2SO4 getrocknet.
Durch Abdampfen des Lösungsmittels
erhielt man ein bräunliches Öl (64 mg,
77%).
1H-NMR (CDCl3,
400 MHz): δ 6,95
(s, 1H); 6,90 (d, J = 8 Hz, 1H); 6,64 (d, J = 8 Hz, 1H); 3,11 (m,
2H); 2,95 (s, 2H); 2,85 (m, 2H); 2,26 (s, 3H); 1,88 (m, 2H); 1,72
(m, 2H).
APCI-MS: m/z 204 [M+H]+
-
Zwischenprodukt: 5-(Trifluormethyl)-3H-spiro[1-benzofuran-2,4'-piperidin]
-
(i) 1-Benzyl-4-[2-fluor-5-(trifluormethyl)benzyl]-piperidin-4-ol
-
Eine
gerührte
Suspension von Mg-Band (308 mg) in Et2O (5
ml) wurde unter Argon mit einem Iodkristall gefolgt von 0,3 ml 2-(Brommethyl)-1-fluor-4-(trifluormethyl)-benzol versetzt.
Die Reaktion wurde mit einer Heißluftpistole gestartet, und
dann wurde langsam mit 2-(Brommethyl)-1-fluor-4-(trifluormethyl)benzol
(2,5 g, 9,73 mmol) in Et2O (5 ml) versetzt
(wobei der Rückfluß aufrechterhalten
wurde). Nach dem Ende der Zugabe wurde die Reaktionsmischung 50
Minuten lang unter Rückfluß erhitzt
und auf Raumtemperatur abgekühlt.
Eine Lösung
von 1-Benzylpiperidin-4-on (1,84 g, 9,73 mmol) in Et2O
(10 ml) wurde langsam unter kräftigem
Rühren zugesetzt.
Nach dem Ende der Zugabe wurde die Reaktionsmischung 50 Minuten
lang bei Raumtemperatur belassen, eine gesättigte wäßrige Lösung von NH4Cl
wurde zugesetzt und die Mischung wurde bis zum Ende der Hydrolyse
bei Raumtemperatur gerührt
und dann mit Essigsäureethylester
extrahiert. Die vereinigten organischen Phasen wurden mit Wasser
gewaschen, über
Na2SO4 getrocknet,
filtriert und eingeengt. Der Rückstand
wurde durch Flash-Chromatographie an Kieselgel (0–1% Methanol
in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die im Untertitel genannte Verbindung (720 mg) erhielt.
APCI-MS:
m/z 368 (MH+).
-
(ii) 1'-Benzyl-5-(trifluormethyl)-3H-spiro[1-benzofuran-2,4'-piperidin]
-
Eine
Suspension von NaH (55%) (127 mg, 2,91 mmol) in Toluol (4 ml) wurde
bei Raumtemperatur langsam zu einer Lösung von 1-Benzyl-4-[2-fluor-5-(trifluormethyl)benzyl]piperidin-4
(715 mg, 1,94 mmol) in Toluol (5 ml) gegeben. Nach dem Ende der
Zugabe wurde die Reaktionsmischung 5 Minuten lang bei 110°C gerührt und
dann mit DMF (3 ml) versetzt, und die Reaktionsmischung wurde 40
Minuten lang bei Rückflußtemperatur
gerührt,
auf Raumtemperatur abgekühlt,
mit H2O (3 ml) versetzt und mit Essigsäureethylester
extrahiert. Die organische Phase wurde über Na2SO4 getrocknet, filtriert und eingeengt. Der
Rückstand
wurde durch Flash-Chromato graphie an Kieselgel (0–1% Methanol
in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die im Untertitel genannte Verbindung (380 mg) erhielt.
1H-NMR (CDCl3, 400
MHz): δ 7,45-7,23
(m, 6H); 6,82 (d, J = 9,0 Hz, 1H); 3,60 (s, 2H); 3,02 (s, 2H); 2,70-2,45 (m,
4H); 2,00 (m, 2H); 1,85 (m, 2H).
APCI-MS: m/z 348 (MH+).
-
(iii) 5-(Trifluormethyl)-3H-spiro[1-benzofuran-2,4'-piperidin]
-
Eine
Lösung
von 1'-Benzyl-5-(trifluormethyl)-3H-spiro[1-benzofuran-2,4'-piperidin) (280
mg, 0,806 mmol) in Toluol (3 ml) wurde mit Chlorameisensäureethylester
(0,093 ml, 0,967 mmol) versetzt, und die Reaktionsmischung wurde über Nacht
bei Rückflußtemperatur
gerührt,
auf Raumtemperatur abgekühlt,
durch Zugabe von Toluol verdünnt
und nacheinander mit wäßriger NaHCO3 und Wasser gewaschen. Die organische Phase
wurde über
Na2SO4 getrocknet,
filtriert und eingeengt. Der Rückstand
wurde in Ethanol (4 ml) gelöst und
mit wäßriger KOH
(1,14 g KOH in 1,2 ml H2O) versetzt, die
Reaktionsmischung wurde über
Nacht unter Rückfluß erhitzt
und auf Raumtemperatur abgekühlt
und das Ethanol wurde im Vakuum entfernt. Die wäßrige Phase wurde mit Et2O extrahiert, und die vereinigten Etherphasen
wurden mit 3 N wäßriger HCl
gewaschen. Die vereingten sauren Phasen wurden durch Zugabe von
wäßriger NaOH
auf einen pH-Wert von 10 eingestellt. Die basische Lösung wurde
mit Essigsäureethylester
extrahiert. Die vereinigten organischen Phasen wurden mit Wasser
gewaschen, über
Na2SO4 getrocknet,
filtriert und eingeengt. Der Rückstand
wurde durch Flash-Chromatographie an Kieselgel (0–2% Methanol
in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die im Untertitel genannte Verbindung (156 mg) erhielt.
1H-NMR (CD3OD, 400
MHz): δ 7,29
(s, 1H); 7,39 (d, J = 8,4 Hz, 1H); 6,82 (d, J = 8,4 Hz, 1H); 3,10-3,00
(m, 4H); 2,89-2,81 (m, 2H); 1,94-1,86 (m, 2H); 1,82-1,74 (m, 2H).
APCI-MS:
m/z 258 (MH+).
-
Zwischenprodukt:
5-Chlor-3'-fluor-3H-spiro[1-benzofuran-2,4,-piperidin]
-
(i) 4-[(Trimethylsilyl)oxy]-3,6-dihydropyridin-1(2H)-carbonsäure-tert.-butylester
-
Eine
Lösung
von 4-Oxopiperidin-1-carbonsäure-tert.-butylester (10,13
g, 50,84 mmol) in DMF wurde unter Argon mit TMSCl (7,74 ml, 61,27
mmol) versetzt, gefolgt von Et3N (17 ml).
Die Mischung wurde über Nacht
bei 80°C
gerührt.
Die Lösung
wurde auf Raumtemperatur abgekühlt
und dann mit Heptan verdünnt
und mit konzentrierter wäßriger NaHCO3 und Wasser gewaschen. Die organische Phase
wurde anschließend über Natriumsulfat
getrocknet, filtriert und eingeengt. Die chromatographische Aufreinigung
an Kieselgel (EtOAc:Petrolether 40-60 1:9) lieferte 9,6 g (69%)
eines Öls,
das beim Stehenlassen fest wurde.
1H-NMR
(CDCl3, 300 MHz): δ 4,79 (m, 1H); 3,87 (m, 2H);
3,52 (t, J = 5,8 Hz, 2H); 2,11 (m, 2H); 1,47 (s, 9H); 0,19 (s, 9H)
APCI-MS:
m/z 272 (M+H)+.
-
(ii) 3-Fluor-4-oxopiperidin-1-carbonsäure-tert.-butylester
-
Eine
Lösung
von 4-[(Trimethylsilyl)oxy]-3,6-dihydropyridin-1(2H)-carbonsäure-tert.-butylester
(9,52 g, 35,07 mmol) in CH3CN wurde unter
Argon mit Selectfluor-Reagens
(13,7 g, 38,6 mmol) versetzt, und die Mischung wurde 2 Stunden lang
bei Raumtemperatur gerührt.
Die Reaktionsmischung wurde mit EtOAc (1000 ml verdünnt), mit
verdünnter
Kochsalzlösung
und Wasser gewaschen, über
Natriumsulfat getrocknet, filtriert und im Vakuum eingeengt. Die
chromatographische Aufreinigung an Kieselgel (MeOH:EtOAc, 0:1 bis
2:98) lieferte 5,35 g (70%) eines Öls, das beim Stehenlassen fest
wurde.
1H-NMR (CDCl3,
300 MHz): δ 4,73-4,94
(m, 1H), 4,14-4,23 (m, 2H), 3,30-3,20 (m, 2H) 2,49-2,66 (m, 2H),
1,50 (s, 9H).
APCI-MS: m/z 218 (M+H)+
-
(iii) 4-(5-Chlor-2-fluorbenzyl)-3-fluor-4-hydroxypiperidin-1-carbonsäure-tert.-butylester
-
Mit
Ether bedeckte Magnesiumspäne
wurden mit einer kleinen Menge einer Lösung von 2-(Brommethyl)-4-chlor-1-fluorbenzol in
Diethylether versetzt, und die Reaktion wurde mit Hilfe einer Heizpistole
gestartet. Die Mischung wurde unter Rückfluß tropfenweise mit der restlichen
Lösung
(150 ml) versetzt, wobei der Rückfluß beibehalten
wurde. Nachdem die gesamte Lösung
zugesetzt worden war, wurde die Mischung gerührt, bis der Rückfluß stoppte.
Eine Lösung
von 3-Fluor-4-oxopiperidin-1-carbonsäure-tert.-butylester in Diethylether (50
ml) wurde langsam zugegeben. Die auf diese Weise erhaltene Mischung
wurde weitere 4 s bei Raumtemperatur gerührt und dann durch die langsame
Zugabe von gesättigter
wäßriger Ammoniumchloridlösung (125 m)
gequencht. Es wurde mit EtOAc (2 × 150 mml) extrahiert, mit
Kochsalzlösung
und Wasser gewaschen, über Natriumsulfat
getrocknet, filtriert und eingeengt. Der auf diese Weise erhaltene
Rückstand
wurde an Kieselgel (Heptan-Et2O 4:1-2:1)
aufgereinigt, wodurch man 1,61 g (18%) der im Untertitel genannten
Verbindung erhielt.
1H-NMR (CDCl3 300 MHz): δ 6,74 (s, 1H), 7,15 (s, 1H),
7,10-7,14 (m, 1H), 4,85-5,02 (m, 1H), 3,78-3,88 (m, 2H), 3,50 (m,
2H) 2,74 (s, 2H), 1,63-1,67 (m, 2H), 1,44 (s, 9H)
APCI-MS:
m/z 362 (M+H)+
-
(iv) 5-Chlor-3'-fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-carbonsäure-tert.-butylester
-
Eine
Suspension von NaH (60% in Mineralöl, 1,38 g, 4,35 mmol) in Benzol
(30 ml) wurde mit einer Lösung
von 4-(5-Chlor-2-fluorbenzyl)-3-fluor-4-hydroxypiperidin-1-carbonsäure-tert.-butylester
in Benzol (50 mml) versetzt, und die Mischung wurde auf Rückfluß erhitzt.
DMF (20 mml) wurde zugesetzt und es wurde 6 Stunden lang bei Rückfluß gehalten.
Die Mischung wurde auf Raumtemperatur abgekühlt, in Wasser gegossen und
mit EtOAc extrahiert. Die organische Phase wurde über Natriumsulfat
getrocknet, filtriert und eingeengt. Der Rückstand wurde durch Chromatographie
an SiO2 (Essigsäureethylester:n-Heptan) aufgereinigt,
wodurch man das Produkt (10 mg, 26%) erhielt.
APCI-MS m/z 342
[M+H]+
-
(v) 5-Chlor-3'-fluor-3H-spiro[1-benzofuran-2,4'-piperidin]
-
Eine
Lösung
von 5-Chlor-3'-fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-carbonsäure-tert.-butylester
in DCM/TFA (20 ml, 5:2) wurde 2 Stunden lang bei Raumtemperatur
gerührt.
Das Lösungsmittel
wurde im Vakuum entfernt, und der Rückstand wurde mit EtOAc verdünnt und
mit gesättigter
wäßriger NaHCO
3-Lösung
und Wasser gewaschen. Die organische Phase wurde über Na
2SO
4 getrocknet,
filtriert und eingeengt, wodurch man die Titelverbindung (60 mg)
erhielt.
APCI-MS m/z 242 [M+H]
+ Zwischenprodukt:
4H-Spiro[chromen-3,4'-piperidin]
-
(i) 1-Benzyl-4-(2-fluorbenzyl)piperidin-4-carbonsäure-ethylester
-
1-Benzylpiperidin-4-carbonsäureethylester
(2,47 g, 10 mmol) wurde in Tetrahydrofuran (20 ml) gelöst und auf –78°C abgekühlt. Lithiumbis(trimethylsilyl)amid
(11 ml, 1,0 M in Tetrahydrofuran) wurde langsam zugesetzt, und es
wurde 30 Minuten lang gerührt.
2-Fluorbenzylbromid (1,34 ml, 11 mmol) in 5 ml Tetrahydrofuran wurde
langsam zugefügt.
Die auf diese Weise erhaltene Lösung
wurde auf Raumtemperatur kommen gelassen und über Nacht gerührt. Der
Ansatz wurde mit Ammoniumchlorid (wäßrig, gesättigt) gequencht und zwischen
Wasser und Essigsäureethylester
verteilt. Die organische Phase wurde mit Kochsalzlösung gewaschen und über Magnesiumsulfat
getrocknet, filtriert und eingeengt. Das Rohprodukt wurde an Kieselgel
(Heptan/Essigsäureethylester)
aufgereinigt, wodurch man 2,7 g (77%) der im Untertitel genannten
Verbindung in Form eines farblosen Öls erhielt.
APCI-MS: m/z
356 [MH+]
-
(ii) [1-Benzyl-4-(2-fluorbenzyl)piperidin-4-yl]methanol
-
Eine
gerührte
Lösung
von 1-Benzyl-4-(2-fluorbenzyl)-piperidin-4-carbonsäureethylester
(1,85 g, 5,2 mmol) in Diethylether wurde auf Eis/Natriumchlorid
abgekühlt.
Es wurde tropfenweise mit Lithiumaluminiumhydrid (5,8 ml, 1,0 M
in Diethylether) versetzt. Nach 2 Stunden Rühren bei Raumtemperatur wurde
die Mischung wieder auf Eis abgekühlt und mit Wasser/Natriumhydroxid
(10%) gequencht, und die Mischung wurde 1 Stunde lang bei Raumtemperatur
gerührt.
Die festen Bestandteile wurden abfiltriert, und die organische Phase
wurde über
Dinatriumsulfat getrocknet, filtriert und eingeengt. Das Rohprodukt
wurde an Kieselgel (Dichlormethan/Ethanol) aufgereinigt, wodurch
man 1,0 g (61%) der im Untertitel genannten Verbindung erhielt.
APCI-MS:
m/z 314 [MH+]
-
(iii) 1'-Benzyl-4H-spiro[chromen-3,4'-piperidin]
-
Natriumhydrid
(350 mg, 7,0 mmol, 50%ige Dispersion in 61) wurde unter einer Stickstoffatmosphäre dreimal
mit Heptan gewaschen und dann in Tetrahydrofuran (50 ml) gelöst. Eine
Lösung
von [1-Benzyl-4-(2-fluorbenzyl)-piperidin-4-yl)methanol
(1 g, 3,2 mmol) in Tetrahydrofuran (30 ml) wurde zugesetzt, und
die auf diese Weise erhaltene Mischung wurde 3 Stunden lang unter
Rückfluß erhitzt.
Die abgekühlte
Lösung
wurde zwischen Wasser und Essigsäureethylester
verteilt, und die organische Phase wurde über Magnesiumsulfat getrocknet
und eingeengt. Das Rohprodukt wurde an Kieselgel (Dichlormethan/Methanol)
aufgereinigt, wodurch man 0,83 g (89%) der im Untertitel genannten
Verbindung erhielt.
APCI-MS: m/z 294 [MH+]
-
(iv) 4H-Spiro[chromen-3,4'-piperidin]
-
1'-Benzyl-4H-spiro[chromen-3,4'-piperidin] (800
mg, 2,7 mmol) wurde in Methanol (100 ml) gelöst. Essigsäure (5 ml) und Palladium auf
Aktivkohle (kat. Menge, 10%) wurden zugesetzt. Durch eine 18stündige Umsetzung
in einem Parr-Apparat bei 35 psi und anschließendes Filtrieren, Eindampfen
und Aufreinigen durch HPLC an C18 (Acetonitril/Wasser) erhielt man
500 mg (92%) der Titelverbindung.
1H-NMR
(400 MHz, DMSO-d6) δ: 8,86 (1H, bs); 7,10-7,05 (2H,
m); 6,85 (1H, dt); 6,76 (1H, d); 3,93 (2H, s); 3,15-3,01 (4H, m);
2,71 (2H, s); 1,66-1,51 (4H, m).
APCI-MS: m/z 204 [MH+]
-
Zwischenprodukt:
6-Chlor-3,4-dihydrospiro[chromen-2,4'-piperidin]
-
(i) 1'-Benzyl-6-chlorspiro[chromen-2,4'-piperidin]-4(3H)-on
-
Eine
Lösung
von 1-(5-Chlor-2-hydroxyphenyl)ethanon (1,7 g, 10 mmol), 1-Benzylpiperidin-4-on
(2,08 g, 11 mmol) und Pyrrolidin (1,07 g, 15 mmol) in Methanol (2
ml) wurde 3 Stunden lang auf 70°C
erhitzt. Nach dem Abkühlen
auf Raumtemperatur wurde die Reaktionsmischung in Wasser gegossen
(20 ml) und mit Essigsäureethylester
(50 ml) extrahiert. Die organische Phase wurde mit 1 N wäßriger HCl
(2 × 50
ml), 2 N wäßriger NaOH
(50 ml) und Wasser gewaschen. Trocknen über Na2SO4 gefolgt vom Abdampfen des Lösungsmittels lieferte
die im Untertitel genannte Verbindung in Form eines orangefarbenen Öls (2,61
g, 77%).
APCI-MS: m/z 342 [M+H]+
-
(ii) 1'-Benzyl-6-chlor-3,4-dihydrospiro[chromen-2,4'-piperidin]
-
Eine
gerührte
Suspension von AlCl3 (3,04 g, 22,8 mmol)
in Dichlormethan (75 ml) wurde bei 0°C mit tert.-Butylamin-Boran (1:1) (3,98 g, 45,8
mmol) versetzt, und es wurde weitere 15 Minuten lang bei dieser
Temperatur gerührt,
wodurch man eine klare Lösung
erhielt. Eine Lösung
von 1'-Benzyl-6-chlorspiro[chromen-2,4'-piperidin]-4(3H)-on
(2,61 g, 7,6 mmol) in Dichlormethan (15 ml) wurde tropfenweise zugesetzt.
Es wurde weitere 2 Stunden lang bei 0°C und 3 Stunden lang bei Raumtemperatur
gerührt.
Die Reaktionsmischung wurde durch tropfenweise Zugabe von 0,1 N
wäßriger HCl
gequencht. Nach dem Ende der Gasentwicklung wurden die Phasen getrennt.
Die organische Phase wurde mit 0,1 N HCl (2 × 50 ml) und mit Kochsalzlösung (50
ml) gewaschen und über
Na2SO4 getrocknet.
Das Lösungsmittel
wurde im Vakuum entfernt, wodurch man die im Untertitel genannte
Verbindung in Form eines farblosen Feststoffs (1,63 g, 65%) erhielt.
APCI-MS:
m/z 328 [M+H]+
-
(iii) 6-Chlor-3,4-dihydrospiro[chromen-2,4'-piperidin]-hydrochlorid
-
Eine
Lösung
von 1'-Benzyl-6-chlor-3,4-dihydrospiro[chromen-2,4'-piperidin] (1,63
g, 5,0 mmol) und Chlorameisensäure-1-chlorethylester
(1,07 g, 7,5 mmol) in Toluol (5 ml) wurde über Nacht unter Rückfluß erhitzt.
Das Lösungsmittel
wurde im Vakuum entfernt, und der ölige Rückstand wurde in Methanol (10
ml) gelöst und über Nacht
unter Rückfluß erhitzt.
Das Lösungsmittel
wurde im Vakuum entfernt, und der Rückstand wurde mit Diethylether
(50 ml) behandelt. Der weiße
Niederschlag wurde abfiltriert, mit Diethylether gewaschen und getrocknet,
wodurch man die im Untertitel genannte Verbindung in Form eines
weißen
Pulvers (0,58 g, 49%) erhielt.
1H-NMR
(CDCl3, 400 MHz): δ 7,07 (d, J = 10,0 Hz, 2H);
7,63 (d, J = 8,4 Hz, 1H); 3,2-3,5 (m, 4H); 2,77 (t, J = 6,6 Hz,
2H); 1,9-2,2 (m, 4H); 1,88 (t, J = 6,6 Hz, 2H).
APCI-MS: m/z
238 [M+H]+
-
Zwischenprodukt: 6-Chlor-3H-spiro[2-benzofuran-1,4'-piperidin]
-
(i) 1'-Benzyl-6-chlor-3H-spiro(2-benzofuran-1,4'-piperidin]-3-on
-
Eine
Lösung
von 2-Brom-4-chlorbenzoesäure
(2,35 g, 10,0 mmol) in Tetrahydrofuran (THF) (15 ml) wurde bei –78°C unter Stickstoff
langsam mit einer 1,6 M Lösung
von n-Butyllithium in Hexan (Parham, W. E.; Egberg, D. C.; Sayed,
Y. A.; Thraikill, R. W.; Keyser, G. E.; William, M. N.; Montgomery,
M. C.; Jones, L. D., J. Org. Chem., 1976, 41, 2628-2633) (20 ml,
32,0 mmol) versetzt. Nach dem Ende der Zugabe wurde die Reaktionsmischung
3 Stunden (h) lang bei –78°C gerührt. Anschließend wurde
eine Lösung
von 1-Benzylpiperidin-4-on
(3,78 g, 20,0 mmol) in THF (10 ml) bei –78°C langsam zur Reaktionsmischung
gegeben. Nach dem Ende der Zugabe wurde die Reaktionstemperatur
auf Raumtemperatur erhöhrt,
und die Reaktionsmischung wurde über
Nacht bei Raumtemperatur gerührt.
Die Reaktionsmischung wurde in eine Mischung aus Wasser (H2O) (60 ml) und Diethylether (60 ml) gegossen,
und die Phasen wurden getrennt. Anschließend wurde die wäßrige Phase
mit Diethylether (2 × 20
ml) extrahiert. Die wäßrige Phase
wurde mit 6 M wäßriger HCl
auf einen pH-Wert von 2 angesäuert,
1 Stunde lang gekocht und auf 0°C
abgekühlt,
der pH-Wert wurde
durch Zugabe von wäßrigem Natriumhydroxid
(NaOH) (6 M) auf 10 eingestellt und die Mischung wurde schnell mit
Trichlormethan (CHCl3) extrahiert. Die organische
Phase wurde mit H2O gewaschen, über Natriumsulfat
(Na2SO4) getrocknet,
filtriert und im Vakuum eingeengt, wodurch man die im Untertitel
genannte Verbindung (1,22 g) erhielt, die rein genug für den nächsten Schritt
war.
1H-NMR (CDCl3,
400 MHz): δ 7,84
(d, J = 8,2 Hz, 1H); 7,51 (dd, J = 1,7, 8,2 Hz, 1H); 7,45-7,25 (m,
6H); 3,67 (s, 2H); 3,00 (bd; J = 9,4 Hz, 2H); 2,61 (bt, J = 11,2
Hz, 2H); 2,32 (breit, s, 2H); 1,74 (d, J = 12,2 Hz, 2H).
APCI-MS:
m/z 328 (MH+).
-
(ii) 1'-Benzyl-6-chlor-3H-spiro[2-benzofuran-1,4'-piperidin]
-
Eine
Lösung
von 1'-Benzyl-6-chlor-3H-spiro[2-benzofuran-1,4'-piperidin]-3-on
(1,1 g, 3,35 mmol) in THF (15 ml) wurde bei 0°C langsam mit einer 1 M-Lösung von
Boran (Marxer, A.; Rodriguez, H. R.; McKenna, J. M.; Tsai, H. M.,
J. Org. Chem., 1975, 40, 1427-1430) in THF (7 ml, 7,0 mmol) versetzt.
Nach dem Ende der Zugabe wurde die Reaktionsmischung 30 Minuten
(min) lang auf Raumtemperatur gehalten und dann über Nacht unter Rückfluß gehalten,
auf 0°C
abgekühlt
und langsam mit wäßriger 6
M Salzsäure
(HCl) (3,5 ml) versetzt. Die Reaktionsmischung wurde 5 Stunden lang
unter Rückfluß gehalten,
auf 0°C
abgekühlt,
der pH-Wert wurde durch Zugaben von 6 M wäßriger NaOH auf 10 eingestellt
und das Ganze wurde mit Essigsäureethylester
extrahiert. Die organische Phase wurde mit H2O
gewaschen, über
Na2SO4 getrocknet,
filtriert und im Vakuum eingeengt. Der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (0–30%
Essigsäureethylester
in Petrolether) aufgereinigt, wodurch man die im Untertitel genannte
Verbindung (900 mg) erhielt.
1H-NMR
(CDCl3, 400 MHz): δ 7,44-7,22 (m, 6H); 7,18 (m,
2H); 5,03 (s, 2H); 3,60 (s, 2H) 2,87 (bd, J = 10,5 Hz, 2H); 2,45
(bt, J = 11,2 Hz, 2H); 2,00 (bs, 2H); 1,79 (d, J = 11,2 Hz, 2H).
APCI-MS:
m/z 314 (MH+).
-
(iii) 6-Chlor-3H-spiro[2-benzofuran-1,4'-piperidin]
-
Eine
Lösung
von 1'-Benzyl-6-chlor-3H-spiro[2-benzofuran-1,4'-piperidin] (850
mg, 2,7 mmol) in Dichlormethan (CH2Cl2) (8 ml) wurde bei 0°C langsam mit Chlorameisensäurechlorethylester
(Yang, B. V.; O'Rourke,
D.; Li, J., Synlett, 1993, 195-196) (772 mg, 5,4 mmol) versetzt.
Nach dem Ende der Zugabe wurde die Reaktionsmischung 30 Minuten
lang bei 0°C
gerührt.
Die flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde in Methanol (10
ml) gelöst
und 40 Minuten lang unter Rückfluß gehalten.
Die flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie an
Kieselgel (0–6%
Methanol in Dichlormethan, 0,2% Ammoniumhydroxid (NH4OH))
aufgereinigt, wodurch man die Titelverbindung (170 mg) erhielt und
1'-Benzyl-6-chlor-3H-spiro[2-benzofuran-1,4'-piperidin] (200
mg) zurückgewann.
1H-NMR (CD3OD, 400
MHz): δ 7,29-7,21
(m, 3H); 5,00 (s, 2H); 2,99 (m, 4H); 1,90-181 (m, 2H); 1,70 (m,
2H).
APCI-MS: m/z 224 (MH+).
-
Zwischenprodukt: 5-Fluor-3H-spiro[2-benzofuran-1,4'-piperidin]
-
(iv) 1'-Benzyl-5-fluor-3H-spiro[2-benzofuran-1,4'-piperidin]-3-on
-
Diese
Umsetzung wurde wie für
(i) oben beschrieben unter Verwendung von 2-Brom-5-fluorbenzoesäure (2,19
g, 10,0 mmol), 1-Benzylpiperidin-4-on (3,78 g, 20,0 mmol), n-Butyllithium
(n-BuLi) (20 ml) und THF (20 ml) durchgeführt, wodurch man die im Untertitel
genannte Verbindung erhielt.
1H-NMR
(CDCl3, 400 MHz): δ 7,58-7,23 (m, 8H); 3,68 (S,
2H); 2,98 (m, 2H); 2,59 (m, 2H); 2,28 (m, 2H); 1,74 (m, 2H).
APCI-MS:
m/z 312 (MH+).
-
(v) 1'-Benzyl-5-fluor-3H-spiro[2-benzofuran-1,4'-piperidin]
-
Diese
Umsetzung wurde wie für
(ii) oben beschrieben unter Verwendung von 1'-Benzyl-5-fluor-3H-spiro[2-benzofuran-1,4'-piperidin]-3-on
(200 mg, 0,642 mmol), einer 1 M Lösung von Boran-THF-Komplex
(1,34 ml, 1,34 mmol) und THF (3 ml) durchgeführt, wodurch man die im Untertitel
genannte Verbindung (148 mg) erhielt.
1H-NMR
(CDCl3, 400 MHz): δ 7,41-7,27 (m, 5H); 7,08 (dd,
J = 4,8, 8,3 Hz, 1H); 6,97 (m, 1H); 6,89 (m, 1H); 5,08 (s, 2H);
3,60 (s, 2H); 2,87 (m, 2H); 2,46 (m, 2H); 1,97 (m, 2H); 1,88 (m,
2H).
APCI-MS: m/z 298 (MH+).
-
(vi) 5-Fluor-3H-spiro[2-benzofuran-1,4'-piperidin]
-
Diese
Umsetzung wurde wie für
(iii) oben beschrieben unter Verwendung von 1'-Benzyl-5-fluor-3H-spiro[2-benzofuran-1,4'-piperidin] (145
mg, 0,487 mmol) und Chlorameisensäurechlorethylester (0,07 ml)
durchgeführt,
wodurch man die Titelverbindung erhielt.
1H-NMR
(CD3OD, 400 MHz): δ 7,18 (dd, J = 4,9, 8,1 Hz,
1H); 7,03-6,96 (m, 2H); 5,01 (s, 2H); 3,09-2,93 (m, 4H); 1,91-1,81
(m, 2H); 1,73-1,66 (m 2H).
APCI-MS: m/z 208 (MH+).
-
Zwischenprodukt: 3-Nitrobenzolsulfonsäure-[(2S)-2-methyloxiran-2-yl]methylester
-
Dargestellt
wie von Eriksson, T.; Klingstedt, T.; Mussie, T., offengelegte internationale
Patentanmeldung Nr.
WO 01/98273 ,
beschrieben.
-
Beispiel 1
-
N-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}phenyl)acetamid
-
Schritt I:
-
N-{2-[(2S)-Oxiran-2-ylmethoxy]phenyl}acetamid
-
Eine
Mischung von N-(2-Hydroxyphenyl)acetamid (1,51 g, 10 mmol), (2S)-Oxiran-2-ylmethyl-3-nitrobenzolsulfonat
(2,59 g, 10 mmol) und Caesiumcarbonat (CS2CO3) (3,9 g, 12 mmol) in Dimethylformamid (DMF) (30
ml) wurde über Nacht
bei Raumtemperatur gerührt.
Die Reaktionsmischung wurde zwischen Essigsäureethylester und H2O verteilt. Die organische Phase wurde über Na2SO4 getrocknet,
filtriert und eingeengt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel aufgereinigt, wodurch man die im Untertitel genannte
Verbindung (1,34 g) erhielt.
1H-NMR
(CDCl3, 400 MHz): δ 8,40 (m, 1H); 7,90 (bs, 1H);
7,05 (m, 2H); 6,92 (m, 1H); 4,37 (dd, J = 2,5, 11,3 Hz, 1H); 3,98
(dd, J = 5,9, 11,3 Hz, 1H); 3,40 (m, 1H); 2,97 (t, J = 4,8 Hz, 1H);
2,81 (dd, J = 2,7, 4,8 Hz, 1H); 2,20 (s, 3H).
-
Schritt II:
-
N-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}phenyl)acetamid
-
Eine
Mischung von 5-Chlor-3H-spiro[1-benzofuran-2,4'-piperidin]
(36 mg, 0,16 mmol) und N-{2-[(2S)-Oxiran-2-ylmethoxy]phenyl}acetamid (33 mg, 0,16
mmol) in Ethanol (3 ml) wurde über
Nacht bei 80°C
gerührt.
Die flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (0–3%
Methanol in Dichlormethan mit 0,2% Ammoniumhydroxid) aufgereinigt,
wodurch man die Titelverbindung (25 mg) erhielt.
1H-NMR
(CDCl3, 400 MHz): δ 7,82 (d, J = 4,8 Hz, 1H); 7,22
(m, 1H); 7,13 (m, 2H); 7,05 (d, J = 7,5 Hz, 1H); 6,98 (m, 1H); 6,74
(d, J = 8,6 Hz, 1H); 4,49 (m, 1H); 4,08 (d, J = 4,8 Hz, 2H); 3,70
(m, 2H); 3,43 (m, 4H); 3,12 (s, 2H); 2,20 (m, 7H).
APCI-MS:
m/z 433 (MH+).
-
Beispiel 2
-
N-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-fluorphenyl)acetamid
-
Schritt I:
-
N-(4-Fluor-2-hydroxyphenyl)acetamid
-
Eine
Mischung von 5-Fluor-2-nitrophenol (5 g, 31,8 mmol), Essigsäureanhydrid
(4,86 g, 47,7 mmol) und Platin auf Aktivkohle (5%, 200 mg) in Methanol
wurde 3 Stunden lang unter 35 psi hydriert. Der Katalysator wurde
abfiltriert und der Rückstand
wurde durch Flash-Chromatographie
an Kieselgel aufgereinigt, wodurch man die im Untertitel genannte
Verbindung (4,7 g) erhielt.
1H-NMR
(CD3OD, 300 MHz): δ 7,56-7,51 (m, 1H); 6,61-6,50
(m, 2H); 2,15 (s, 3H).
APCI-MS: m/z 170 (MH+).
-
Schritt II:
-
N-{4-Fluor-2-[(2S)-oxiran-2-ylmethoxy]phenyl}acetamid
-
Eine
Mischung von N-(4-Fluor-2-hydroxyphenyl)acetamid (1,69 g, 10,0 mmol),
(2S)-Oxiran-2-ylmethyl-3-nitrobenzolsulfonat
(2,59 g, 10,0 mmol) und Cs2CO3 (4,87
g, 15,0 mmol) in DMF (15 ml) wurde 2 Stunden lang bei Raumtemperatur
gerührt.
Die Reaktionsmischung wurde zwischen Essigsäureethylester und H2O verteilt. Die organische Phase wurde über Na2SO4 getrocknet,
filtriert und eingeengt. Der Rückstand
wurde durch Flash-Chromatographie
an Kieselgel aufgereinigt, wodurch man die im Untertitel genannte
Verbindung (1,35 g) erhielt.
1H-NMR
(CDCl3, 400 MHz): δ 8,33-8,29 (m, 1H); 7,71 (bs,
1H), 6,74-6,66 (m, 2H); 4,39-4,36 (m, 1H); 3,95-3,90 (m, 1H); 3,41-3,39
(m, 1H); 2,99-2,97 (m, 1H); 2,80-2,79
(m, 1H).
APCI-MS: m/z 226 (MH+).
-
Schritt III:
-
N-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-fluorphenyl)-acetamid
-
Eine
Mischung von 5-Chlor-3H-spiro[1-benzofuran-2,4'-piperidin]
(45 mg, 0,201 mmol) und N-{4-Fluor-2-[(2S)-oxiran-2-ylmethoxy]phenyl}acetamid (45,3
mg, 0,201 mmol) in Ethanol (3 ml) wurde über Nacht bei 80°C gerührt. Die
flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie an
Kieselgel (0–3%
Methanol in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die Titelverbindung (33 mg) erhielt.
1H-NMR
(CDCl3, 400 MHz): δ 8,52 (s, 1H); 8,20 (dd, J =
6,4, 8,9 Hz, 1H); 7,18 (s, 1H); 7,13 (dd, J = 2,0, 8,5 Hz, 1H);
6,74 (dd, J = 2,6, 8,6 Hz, 1H); 6,69 (d, J = 8,6 Hz, 1H); 6,59 (dd,
J = 2,6, 9,8 Hz, 1H); 4,48 (m, 1H); 4,17 (dd, J = 3,7, 9,8 Hz, 1H);
4,00 (dd, J = 2,2, 9,8 Hz, 1H); 3,79 (m, 2H); 3,59 (bd, J = 11,7
Hz, 1H); 3,38 (m, 1H); 3,27 (m, 1H); 3,12 (s, 2H); 3,05 (m, 1H);
2,48 (m, 1H); 2,37 (m, 1H); 2,24 (s, 3H); 2,17 (m, 2H).
APCI-MS:
m/z 451 (MH+).
-
Beispiel 3
-
N-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-methoxyphenyl)acetamid
-
Schritt I:
-
N-(2-Hydroxy-4-methoxyphenyl)acetamid
-
2-Nitro-5-methoxyphenol
(dargestellt ausgehend von 3-Methoxyphenol,
R. J. Maleski, Synthetic Communications, 1993, 23, 343-348) (48,5
g, 0,287 mol) gelöst
in THF (1,5 l) wurde bei Raumtemperatur über Nacht über 10% Palladium auf Aktivkohle
(10 g) bis zur Aufnahme von 20,3 l Wasserstoff hydriert. Nach dem Filtrieren
und Eindampfen wurde der Rückstand
in entgastem Wasser (1,7 l) suspendiert und unter Rühren mit Essigsäureanhydrid
(42,5 ml) versetzt. Die Mischung wurde 1 Stunde lang auf 60°C erhitzt
und dann auf Raumtemperatur abgekühlt. Die flüchtigen Bestandteile wurden
im Vakuum entfernt und der Feststoff wurde gründlich mit Wasser gewaschen
und im Vakuum getrocknet, wodurch man ziegelsteinrote Kristalle
(41,7 g, 80%) erhielt.
1H-NMR (400
MHz, CDCl3): δ 8,98 (s, 1H); 7,34 (bs, 1H);
6,81 (d, 1H); 6,58 (d, 1H); 6,44 (dd, 1H); 3,78 (s, 3H); 2,26 (s,
3H)
-
Schritt II:
-
N-{4-Methoxy-2[(2S)-oxiran-2-ylmethoxy]phenyl}acetamid
-
N-(2-Hydroxy-4-methoxyphenyl)acetamid
(18,12 g, 0,1 mol) und (2S)-Oxiran-2-ylmethyl-3-nitrobenzolsulfonat
(25,92 g, 0,1 mol) wurden in trockenem DMF (75 ml) gelöst und unter
Stickstoff (N2) auf einem Eisbad gerührt. Caesiumcarbonat
(35,8 g, 0,11 mol) wurde zugesetzt, und es wurde über Nacht
bei Raumtemperatur unter N2 weitergerührt. Die
Mischung wurde in Essigsäureethylester
(1 l) und Wasser (250 ml) gegossen. Die organische Phase wurde mit
Wasser (3 × 250
ml) gewaschen, über
Na2SO4 getrocknet,
filtriert und im Vakuum eingeengt, wodurch man ein orangefarbenes
festes Rohprodukt (29 g) erhielt, das aus Ethanol (100 ml) umkristallisiert
und mit Ether gewaschen wurde, wodurch man weiße Kristalle erhielt. Weitere
weiße
Kristalle wurden nach Eindampfen und Umkristallisieren aus 2-Propanol
aus den Mutterlaugen erhalten. Gesamtausbeute 15 g (63%).
1H-NMR (CDCl3): δ 8,22 (d,
1H); 7,64 (bs, 1H); 6,53 (dd, 1H); 6,50 (d, 1H); 4,34 (dd, 1H);
3,92 (dd, 1H); 3,79 (s, 3H); 3,38 (m, 1H); 2,96 (t, 1H); 2,78 (dd,
1H); 2,20 (s, 3H)
-
Schritt III:
-
N-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-methoxy-phenyl)acetamid
-
Eine
Mischung von 5-Chlor-3H-spiro[1-benzofuran-2,4'-piperidin]
(200 mg, 0,894 mmol) und N-{4-Methoxy-2[(2S)-oxiran-2-ylmethoxy]phenyl}acetamid
(212 mg, 0,894 mmol) in Ethanol (5 ml) wurde über Nacht bei 80°C gerührt. Die
flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie an
Kieselgel (0–2%
Methanol in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die Titelverbindung (400 mg) erhielt.
1H-NMR
(CD3OD, 400 MHz): δ 7,74 (d, J = 8,9 Hz, 1H); 7,13
(m, 1H); 7,04 (dd, J = 2,3, 8,5 Hz, 1H); 6,65 (d, J = 8,5 Hz, 1H);
6,61 (d, J = 2,7 Hz, 1H); 6,51 (dd, J = 2,7, 8,8 Hz, 1H); 4,17 (m,
1H); 4,08 (dd, J = 3,4, 10,0 Hz, 1H); 3,98 (dd, J = 6,3, 9,9 Hz,
1H); 3,79 (s, 3H); 3,03 (s, 2H); 2,72 (m, 4H); 2,62 (m, 2H); 2,15
(s, 3H); 1,95 (m, 2H); 1,84 (m, 2H).
APCI-MS: m/z 461 (MH+).
-
Beispiel 4
-
N-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxyphenyl)acetamid
-
Eine
kalte Lösung
(0°C) von
N-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-methoxyphenyl)acetamid
(380 mg, 0,82 mmol) in Dichlormethan (8 ml) wurde langsam mit einer
1 M-Lösung
von Bortribromid (BBr3) in Dichlormethan
(2,47 ml, 2,47 mmol) versetzt. Nach dem Ende der Zugabe wurde das
Eisbad entfernt, und die Reaktionsmischung wurde 2 h 30 min bei
Raumtemperatur gerührt.
Die Reaktionsmischung wurde auf 0°C
abgekühlt
und im Verlauf von 10 Minuten unter Rühren langsam mit Methanol (2
ml) versetzt. Die flüchtigen
Bestandteile wurden im Vakuum entfernt. Der Rückstand wurde in einem großen Volumen
Essigsäureethylester
gelöst
und nacheinander mit einer wäßrigen Lösung von
Natriumhydrogencarbonat (NaHCO3) und mit
Wasser gewaschen. Die organische Phase wurde über Na2SO4 getrocknet, filtriert und eingeengt und
der Rückstand
wurde durch Flash-Chromatographie an Kieselgel (0–3% Methanol
in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die Titelverbindung (155 mg) erhielt.
1H-NMR
(CD3OD, 400 MHz): δ 7,57 (d, J = 8,7 Hz, 1H); 7,14
(m, 1H); 7,04 (dd, J = 2,3, 8,5 Hz, 1H); 6,66 (d, J = 8,5 Hz, 1H);
6,48 (d, J = 2,5 Hz, 1H); 6,32 (dd, J = 2,5, 8,6 Hz, 1H); 4,17 (m,
1H); 4,06 (dd, J = 3,4, 9,8 Hz, 1H); 3,93 (dd, J = 6,2, 9,8 Hz,
1H); 3,03 (s, 2H); 2,70 (m, 4H); 2,59 (m, 2H); 2,13 (s, 3H); 1,95
(m, 2H); 1,84 (m, 2H).
APCI-MS: m/z 447 (MH+).
-
Beispiel 5
-
N- [2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-5-(trifluormethyl)phenyl]acetamid
-
Schritt I:
-
N-[2-{[(2S)-2-Methyloxiran-2-yl]methoxy}-5-(trifluormethyl)phenyl]acetamid
-
Eine
Mischung von 2-Nitro-4-(trifluormethyl)phenol (310 mg, 1,5 mmol),
Palladium auf Aktivkohle (10%, 125 mg) und Essigsäureanhydrid
(306,3 mg, 3,0 mmol) in Methanol wurde 2 Stunden lang bei Normaldruck
hydriert. Der Katalysator wurde abfiltriert und das Filtrat wurde
im Vakuum eingeengt, wodurch man rohes N-[2-Hydroxy-5-(trifluormethyl)phenyl]acetamid
(331 mg) erhielt. Ein Teil (219,16 mg, 1,0 mmol) des N-[2-Hydroxy-5-(trifluormethyl)phenyl]acetamids
wurde in Gegenwart von Cs2CO3 (406,25
mg, 1,25 mmol) in DMF (5 ml) bei Raumtemperatur 5 Stunden lang mit
[(2S)-2-Methyloxiran-2-yl]- methyl-3-nitrobenzolsulfonat (273,27
mg, 1,0 mmol) behandelt. Die Reaktionsmischung wurde zwischen Essigsäureethylester
und Wasser verteilt. Die organische Phase wurde über Na2SO4 getrocknet, filtriert und eingeengt. Der
Rückstand
wurde durch Flash-Chromatographie an Kieselgel (0–40% Essigsäureethylester
in Petrolether) aufgereinigt, wodurch man die im Untertitel genannte
Verbindung (230 mg) erhielt.
1H-NMR
(CDCl3, 400 MHz): δ 8,86 (s, 1H); 8,00 (bs, 1H);
7,29 (m, 1H); 6,97 (d, J = 8,5 Hz, 1H); 4,23 (d, J = 11,0 Hz, 1H);
4,04 (d, J = 11,03 Hz, 1H) 2,93 (m, 1H); 2,81 (d, J = 4,6 Hz, 1H);
2,22 (s, 31H); 1,42 (s, 3H).
-
Schritt II:
-
N-[2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-5-(trifluormethyl)phenyl]acetamid
-
Eine
Mischung von 5-Chlor-3H-spiro[1-benzofuran-2,4'-piperidin]
(35 mg, 0,155 mmol) und N-[2-{[(2S)-2-Methyloxiran-2-yl]methoxy}-5-(trifluormethyl)-phenyl]acetamid (45
mg, 0,155 mmol) in Ethanol (2 ml) wurde über Nacht bei 80°C gerührt. Die
flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (0–1,5%
Methanol in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die Titelverbindung (28 mg) erhielt.
1H-NMR
(CD3OD, 400 MHz): δ 8,40 (d, J = 1,8 Hz, 1H); 7,40
(dd, J = 1,4, 8,7 Hz, 1H); 7,18 (d, J = 8,6 Hz, 1H); 7,13 (m, 1H);
7,03 (dd, J = 2,2, 8,5 Hz, 1H); 6,63 (d, J = 8,5 Hz, 1H); 4,13 (d,
J = 9,3 Hz, 1H); 3,98 (d, J = 9,3 Hz, 1H); 2,99 (s, 2H); 2,78 (m,
1H); 2,68 (m, 3H); 2,58 (m, 1H); 2,22 (s, 3H); 1,88 (m, 2H); 1,78
(m, 2H); 1,32 (s, 3H).
APCI-MS: m/z 513 (MH+).
-
Beispiel 6
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-N-cyclopropyl-benzamid
-
Schritt I:
-
N-Cyclopropyl-2-hydroxybenzamid
-
Eine
Mischung von Salicylsäuremethylester
(4,36 g, 28,69 mmol) und Cyclopropylamin (1,64 g) wurde in einem
verschlossenen Röhrchen
3 Stunden lang auf 80–100°C erhitzt.
Weitere 0,5 g Cyclopropylamin wurden zugesetzt, und es wurde über Nacht
auf 70°C
erhitzt. Die flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel aufgereinigt, wodurch man die im Untertitel genannte
Verbindung (2,71 g) erhielt.
1H-NMR
(CDCl3, 400 MHz): δ 12,40 (s, 1H); 7,40 (m, 1H);
7,38 (m, 1H); 7,01 (m, 1H); 6,81 (m, 1H); 6,48 (bs, 1H); 2,85 (m,
1H); 0,98 (m, 2H); 0,82 (m, 2H).
-
Schritt II:
-
N-Cyclopropyl-2-[(2S)-oxiran-2-ylmethoxy]benzamid
-
Eine
Mischung von N-Cyclopropyl-2-hydroxybenzamid (270 mg, 1,52 mmol),
(2S)-Oxiran-2-ylmethyl-3-nitrobenzolsulfonat (378 mg, 1,68 mmol)
und Caesiumcarbonat (645 mg, 1,98 mmol) in DMF (4 ml) wurde über Nacht
bei Raumtemperatur gerührt.
Die Reaktionsmischung wurde zwischen Essigsäureethylester und Wasser verteilt.
Die organische Phase wurde über
Na2SO4 getrocknet,
filtriert und eingeengt. Der Rückstand
wurde durch Flash-Chromatographie
an Kieselgel (40% Heptan in Essigsäureethylester) aufgereinigt, wodurch
man die im Untertitel genannte Verbindung (354 mg) erhielt.
1H-NMR (CDCl3, 400
MHz): δ 8,22
(dd, J = 1,8, 7,8 Hz, 1H); 7,95 (bs, 1H); 7,42 (m, 1H); 7,10 (m,
1H); 6,93 (d, J = 8,3 Hz, 1H); 4,44 (dd, J = 2,5, 10,7 Hz, 1H);
4,08 (dd, J = 5,1, 10,8 Hz, 1H); 3,40 (m, 1H); 3,04-2,95 (m, 2H);
2,83 (dd, J = 2,7, 4,5 Hz, 1H); 0,86 (m, 2H); 0,65 (m, 2H).
-
Schritt III:
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-N-cyclopropyl-benzamid
-
Eine
Mischung von 5-Chlor-3H-spiro[1-benzofuran-2,4'-piperidin]
(9 mg, 0,04 mmol) und N-Cyclopropyl-2-[(2S)-oxiran-2-ylmethoxy]benzamid (9,4 mg,
0,4 mmol) in Ethanol (1,5 ml) wurde über Nacht bei 80°C gerührt. Die
flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (0–1,5%
Methanol in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die Titelverbindung (7 mg) erhielt.
1H-NMR
(CD3OD, 400 MHz): δ 7,92 (m, 1H); 7,47 (m, 1H);
7,13 (m, 2H); 7,05 (m, 2H); 6,65 (d, J = 8,5 Hz, 1H); 4,23 (dd,
J = 3,0, 9,4 Hz, 1H); 4,16 (m, 1H); 4,09 (dd, J = 5,5, 9,4 Hz, 1H);
3,03 (s, 2H); 2,93 (m, 1H); 2,70 (bs, 4H); 2,60 (d, J = 6,3 Hz,
1H); 1,96 (m, 2H); 1,85 (m, 2H); 0,81 (m, 2H); 0,69 (m, 2H).
APCI-MS:
m/z 457 (MH+).
-
Beispiel 7
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-N-cyclopropyl-4-fluorbenzamid
-
Schritt I:
-
N-Cyclopropyl-4-fluor-2-hydroxybenzamid
-
Eine
Suspension von 4-Fluor-2-hydroxybenzoesäuremethyl-ester (510 mg, 3,0 mmol) in Cyclopropylamin
(5 ml) wurde über
Nacht bei Raumtemperatur gerührt,
wodurch man eine klare Lösung
erhielt. Die flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (0–30%
Essigsäureethylester
in Petrolether) aufgereinigt, wodurch man die im Untertitel genannte
Verbindung (493 mg) erhielt.
1H-NMR
(CD3OD, 400 MHz): δ 12,65 (s, 1H); 7,28 (m, 1H);
6,69 (dd, J = 2,6, 10,4 Hz, 1H); 6,56 (ddd, J = 2,6, 8,0, 10,4 Hz,
1H); 6,30 (bs, 1H); 2,88 (m, 1H); 0,98 (m, 2H); 0,66 (m, 2H).
APCI-MS:
m/z 196 (MH+).
-
Schritt II:
-
N-Cyclopropyl-4-fluor-2-(oxiran-2-ylmethoxy)benzamid
-
Eine
Mischung von N-Cyclopropyl-4-fluor-2-hydroxybenzamid (195 mg, 1,0
mmol), (2S)-Oxiran-2-ylmethyl-3-nitrobenzolsulfonat
(259 mg, 1,0 mmol) und Cs2CO3 (390
mg, 1,2 mmol) in DMF (5 ml) wurde über Nacht bei Raumtemperatur
gerührt.
Die Reaktionsmischung wurde zwischen Essigsäureethylester und Wasser verteilt.
Die organische Phase wurde über
Na2SO4 getrocknet,
filtriert. und eingeengt. Der Rückstand
wurde durch Flash-Chromatographie
an Kieselgel (0–30%
Essigsäureethylester
in Petrolether) aufgereinigt, wodurch man die im Untertitel genannte
Verbindung (150 mg) erhielt.
1H-NMR
(CDCl3, 400 MHz): δ 8,24 (dd, J = 7,0, 8,8 Hz,
1H); 7,80 (bs, 1H); 6,82 (ddd, J = 2,3, 7,6, 10,2 Hz, 1H); 6,66
(dd, J = 2,3, 10,2 Hz, 1H); 4,45 (dd, J = 2,4, 10,7 Hz, 1H); 4,05
(dd, J = 5,1, 10,7 Hz, 1H); 3,40 (m, 1H); 3,00 (m, 2H); 2,84 (dd,
J = 2,6, 4,8 Hz, 1H); 0,86 (m, 2H); 0,65 (m, 2H).
APCI-MS:
m/z 252 (MH+).
-
Schritt III:
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-N-cyclopropyl-4-fluorbenzamid
-
Eine
Mischung von 5-Chlor-3H-spiro[1-benzofuran-2,4'-piperidin]
(30 mg, 0,134 mmol) und N-Cyclopropyl-4-fluor-2-(oxiran-2-ylmethoxy)benzamid
(33,6 mg, 0,134 mmol) in Ethanol (2 ml) wurde über Nacht bei 80°C gerührt. Die
flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie an
Kieselgel (0–2%
Methanol in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die Titelverbindung (36 mg) erhielt.
1H-NMR
(CD3OD, 400 MHz): δ 7,97 (dd, J = 6,9, 8,7 Hz,
1H); 7,14 (m, 1H); 7,05 (dd, J = 2,3, 8,5 Hz, 1H); 6,96 (dd, J =
2,4, 10,4 Hz, 1H); 6,82 (ddd, J = 2,4, 8,0, 10,4 Hz, 1H); 6,66 (d,
J = 8,5 Hz, 1H); 4,24 (dd, J = 3,0, 9,4 Hz, 1H); 4,17 (m, 1H); 4,10
(dd, J = 5,5, 9,4 Hz, 1H); 3,05 (s, 2H); 2,82 (m, 1H); 2,71 (bs,
4H); 2,60 (d, J = 6,3 Hz, 2H); 1,99 (m, 2H); 1,88 (m, 2H); 0,83
(m, 2H); 0,58 (m, 2H).
APCI-MS: m/z 252 (MH+).
-
Beispiel 8
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-N-cyclopropyl-4-methoxybenzamid
-
Schritt I:
-
N-Cyclopropyl-2-hydroxy-4-methoxybenzamid
-
Eine
Suspension von 2-Hydroxy-4-methoxybenzoesäuremethylester (5,1 g, 28,0
mmol) in Cyclopropylamin (24 ml) wurde 5 Tage lang bei Raumtemperatur
gerührt.
Die flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (0–60%
Essigsäureethylester
in Petrolether) aufgereinigt, wodurch man die im Untertitel genannte
Verbindung (1,8 g) erhielt.
1H-NMR
(CD3OD, 400 MHz): δ 7,61 (d, J = 8,8 Hz, 1H); 6,42
(m, 2H); 3,80 (s, 3H); 2,80 (m, 1H); 0,80 (m, 2H); 0,62 (m, 2H).
APCI-MS:
m/z 208 (MH+)
-
Schritt II:
-
N-Cyclopropyl-4-methoxy-2-[(2S)-oxiran-2-ylmethoxy]-benzamid
-
Eine
Mischung von N-Cyclopropyl-2-hydroxy-4-methoxybenzamid (700 mg,
3,38 mmol), (2S)-Oxiran-2-ylmethyl-3-nitrobenzolsulfonat (876 mg, 3,38 mmol)
und Cs2CO3 (1,31
g, 4,05 mmol) in DMF (12 ml) wurde über Nacht bei Raumtemperatur
gerührt.
Die Reaktionsmischung wurde zwischen Essigsäureethylester und Wasser verteilt.
Die organische Phase wurde über
Na2SO4 getrocknet,
filtriert und eingeengt. Der Rückstand
wurde durch Flash-Chromatographie an Kieselgel (0–80% Essigsäureethylester
in Petrolether) aufgereinigt, wodurch man die im Untertitel genannte
Verbindung (1,0 g) erhielt.
1H-NMR
(CDCl3, 400 MHz): δ 8,20 (d, J = 8,8 Hz, 1H); 7,85
(bs, 1H); 6,63 (dd, J = 2,3, 8,8 Hz, 1H); 6,45 (d, J = 2,3 Hz, 1H);
4,42 (dd, J = 2,5, 10,8 Hz, 1H); 4,05 (dd, J = 5,2, 10,8 Hz, 1H);
3,82 (s, 3H); 3,40 (m, 1H); 3,00 (m, 2H); 2,83 (dd, J = 2,6, 4,8
Hz, 1H); 0,88 (m, 2H); 0,68 (m, 2H).
APCI-MS: m/z 264 (MH+).
-
Schritt III:
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-N-cyclopropyl-4-methoxybenzamid
-
Eine
Mischung von 5-Chlor-3H-spiro[1-benzofuran-2,4'-piperidin]
(100 mg, 0,447 mmol) und N-Cyclopropyl-4-methoxy-2-[(2S)-oxiran-2-ylmethoxy]benzamid
(117,7 mg, 0,447 mmol) in Ethanol (3 ml) wurde über Nacht bei 80°C gerührt. Die
flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie an
Kieselgel (0–1,5%
Methanol in Dichlormethan, 0,2% NH4OH) aufgereinigt, wodurch
man die Titelverbindung (145 mg) erhielt.
1H-NMR
(CDCl3, 400 MHz): δ 8,18 (m, 2H); 7,12 (m, 1H);
7,09 (dd, J = 2,3, 8,5 Hz, 1H); 6,70 (d, J = 8,5 Hz, 1H); 6,63 (dd,
J = 2,3, 8,8 Hz, 1H); 6,44 (d, J = 2,3 Hz, 1H); 4,19 (dd, J = 3,3,
9,4 Hz, 1H); 4,13 (m, 1H); 3,97 (dd, J = 5,0, 9,4 Hz, 1H); 3,88
(s, 3H); 3,02 (m, 3H); 2,92 (m, 1H); 2,81 (m, 1H); 2,63 (m, 3H);
2,53 (dd, J = 3,6, 12,4 Hz, 1H); 2,04 (m, 2H); 1,88 (m, 2H); 0,85
(m, 2H); 0,06 (m, 2H).
APCI-MS: m/z 487 (MH+).
-
Beispiel 9
-
N-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxy-2-methylpropyl]oxy}-4-hydroxyphenyl)acetamidtrifluoracetat
-
Schritt I:
-
2-Methyl-1,3-benzoxazol-6-ol
-
Eine
gerührte
Lösung
von 1-(2,4-Dihydroxyphenyl)ethanon (20 g, 131 mmol) in Pyridin (80
ml) wurde bei Raumtemperatur im Verlauf von 15 Minuten in kleinen
Portionen mit Hydroxylaminhydrochlorid (9,1 g, 131 mmol) versetzt.
Die Reaktionsmischung wurde 20 Stunden lang gerührt und dann mit Wasser (600
ml) verdünnt
und mit Essigsäureethylester
(2 × 250
ml) extrahiert. Die vereinigten organischen Extrakte wurden mit Wasser
(2 × 250
ml) und wäßriger 5%iger
HCl (250 ml) gewaschen. Das Lösungsmittel
wurde im Vakuum entfernt. Der Rückstand
wurde mit Wasser (200 ml) versetzt und dann im Vakuum eingeengt,
dann wurde mit Toluol versetzt (200 ml) und im Vakuum eingeengt.
Der Rückstand
wurde in einer Mischung aus Acetonitril (150 ml) und Dimethylacetamid
(25 ml) gelöst.
Die Lösung
wurde auf 5°C
abgekühlt
und tropfenweise mit Phosphoroxychlorid (20,4 g, 12,2 ml, 133 mmol)
versetzt, wobei die Temperatur auf über 10°C ansteigen gelassen wurde.
Nach dem Ende der Zugabe wurde die Reaktionsmischung 1 Stunde lang
bei Raumtemperatur gerührt und
dann langsam auf eine Mischung aus Natriumcarbonat (55 g) und Eis
(etwa 800 g) gegossen. Nachdem das Eis geschmolzen war, wurde die
auf diese Weise erhaltene Suspension filtriert und der gesammelte
Feststoff wurde mit Wasser (2 × 150
ml) gewaschen. Das Produtk wurde im Vakuum getrocknet, wodurch man
ein gelbes Pulver (14,4 g, 97 mmol, 76%) erhielt.
1H-NMR
(400 MHz, DMSO-d6): δ 9,68 (bs, 1H), 7,38 (d, J =
8,5 Hz, 1H), 6,94 (d, J = 2,2 Hz, 1H), 6,74 (dd, J = 8,5, 2,2 Hz,
1H), 2,50 (s, 3H).
-
Schritt II:
-
Benzoesäure-2-methyl-1,3-benzoxazol-6-ylester
-
Eine
gerührte
Suspension von 2-Methyl-1,3-benzoxazol-6-ol (2,99 g, 20 mmol) in Dichlormethan
(50 ml) wurde mit Triethylamin (4,05 g, 5,58 ml, 40 mmol) versetzt.
Eine Lösung
von Benzoylchlorid (3,09 g, 2,56 ml, 22 mmol) in Dichlormethan (20
ml) wurde im Verlauf von 10 Minuten tropfenweise zugesetzt. Die
Reaktionsmischung wurde 2,5 Stunden lang bei Raumtemperatur gerührt, dann
mit Wasser (2 × 50
ml) gewaschen und über
Na2SO4 getrocknet,
filtriert und im Vakuum eingeengt, wodurch man die im Untertitel
genannte Verbindung in Form eines farblosen Feststoffs (5,05 g,
20 mmol) erhielt.
1H-NMR (400 MHz,
CDCl3): δ 8,22
(m, 2H), 7,66 (m, 2H), 7,53 (m, 2H), 7,40 (d, 1H), 7,16 (dd, 1H),
2,65 (s, 3H).
APCI-MS: m/z 254 [MH+].
-
Schritt III:
-
Benzoesäure-4-(acetylamino)-3-hydroxyphenylester
-
Eine
Lösung
von Benzoesäure-2-methyl-1,3-benzoxazol-6-ylester (5,05 g,
20 mmol) in THF (100 ml) wurde mit einer Mischung aus Trifluoressigsäure und
Wasser (4 ml/10 ml) versetzt. Die Reaktionsmischung wurde 16 Stunden
lang bei Raumtemperatur gerührt
und dann mit gesättigter
wäßriger NaHCO3-Lösung
(150 ml) versetzt. Die Mischung wurde mit Essigsäureethylester (150 ml) extrahiert, über Na2SO4 getrocknet,
filtriert und im Vakuum eingeengt, wodurch man die im Untertitel
genannte Verbindung erhielt.
1H-NMR
(400 MHz, Aceton-d6): δ 9,76 (bs, 1H), 9,32 (bs, 1H),
8,15 (m, 2H), 7,71 (m, 1H), 7,60 (m, 2H), 7,47 (d, 1H), 6,85 (m,
1H), 6,75 (m, 1H), 2,20 (s, 3H).
APCI-MS: m/z 272 [MH+]
-
Schritt IV:
-
Benzoesäure-4-(acetylamino)-3-{[(2S)-2-methyloxiran-2-yl]methoxy}phenylester
-
Diese
Verbindung wurde ausgehend von Benzoesäure-4-(acetylamino)-3-hydroxyphenylester (2,71
g, 10 mmol) und 3-Nitrobenzolsulfonsäure-[(2S)-2-methyloxiran-2-yl]methylester unter
Anwendung der Standardvorschrift und unter Verwendung von 1-Methylpyrrolidin-2-on
als Lösungsmittel
dargestellt. Durch Flash-Chromatographie an Kieselgel (Essigsäureethylester/n-Heptan)
erhielt man die im Untertitel genannte Verbindung in Form eines
farblosen Feststoffs (1,31 g, 3,9 mmol, 39%).
1H-NMR
(400 MHz, CDCl3): δ 8,4 (d, 1H), 8,18 (m, 2H),
7,91 (bs, 1H), 7,63 (m, 1H), 7,50 (m, 2H), 6,83 (m, 1H), 4,15 (d,
J = 10,8 Hz, 1H), 4,03 (d, J = 10,8 Hz, 1H), 3,99 (d, J = 10,8 Hz,
1H), 2,92 (d, J = 4,6 Hz, 1H), 2,78 (d, J = 4,6 Hz, 1H), 2,22 (s,
3H), 1,48 (s, 3H).
APCI-MS: m/z 342 [MH+].
-
Schritt V:
-
N-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxy-2-methylpropyl]oxy}-4-hydroxyphenyl)acetamidtrifluoracetat
-
Eine
Lösung
von 5-Chlor-3H-spiro[1-benzofuran-2,4'-piperidin]
(20,0 mg, 0,09 mmol) und Benzoesäure-4-(acetylamino)-3-{[(2S)-2-methyloxiran-2-yl]methoxy}-phenylester (30,5
mg, 0,09 mmol) in Methanol (2 ml) wurde 3 Stunden lang auf Rückfluß erhitzt.
Die Reaktionsmischung wurde auf Raumtemperatur abgekühlt und mit
1 Tropfen von 20% NaOH in Ethanol versetzt. Die Mischung wurde 3
Stunden lang bei Raumtemperatur gerührt. Das Lösungsmittel wurde im Vakuum
abdestilliert. Der Rückstand
wurde durch HPLC ("Kromasil"-Säule; Laufmittel:
[Acetonitril + 0,1% Trifluoressigsäure (TFA)/Wasser + 0,1% TFA])
aufgereinigt, wodurch man einen farblosen Feststoff (41 mg, 0,07
mmol, 79%) erhielt.
1H-NMR (400 MHz,
Aceton-d6): δ 8,67 (bs, 1H), 7,71 (d, J =
7,0 Hz, 1H), 7,22 (s, 1H), 7,12 (dd, J = 2,3, 8,5 Hz, 1H), 6,75
(d, J = 8,5 Hz, 1H), 6,59 (d, J = 2,6 Hz, 1H), 6,42 (dd, J = 2,6,
8,6 Hz, 1H), 4,03 (d, 1H), 3,97 (d, J = 9,7 Hz, 1H), 3,92 (bs, 1H),
3,82 (bs, 1H), 3,70 (d, J = 13,6 Hz, 1H), 3,52 (m, 3H), 2,1-2,5
(m, 4H), 2,10 (s, 3H), 1,51 (s, 3H).
APCI-MS: m/z 461 [MH+].
-
Beispiel 10
-
N-(5-Chlor-2-{[(2S)-3-(6-chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-phenyl)acetamid
-
Schritt I:
-
N-(5-Chlor-2-hydroxyphenyl)acetamid
-
Eine
Suspension von 2-Amino-4-chlorphenol (1,43 g, 10,0 mmol) in Methanol
wurde mit Essigsäureanhydrid
(0,945 ml, 10,0 mmol) versetzt, und die Reaktionsmischung wurde
2 Stunden lang bei Raumtemperatur gerührt. Die flüchtigen Bestandteile wurden
im Vakuum entfernt, wodurch man die im Untertitel genannte Verbindung
(1,5 g) erhielt.
1H-NMR (DMSO-d6, 400 MHz): δ 10,20 (bs, 1H); 9,21 (s, 1H);
8,00 (d, J = 2,6 Hz, 1H); 6,94 (dd, J = 2,6, 8,7 Hz, 1H); 6,84 (d,
J = 8,7 Hz, 1H); 2,02 (s, 3H).
-
Schritt II:
-
N-{5-Chlor-2-[(2S)-oxiran-2-ylmethoxy]phenyl}acetamid
-
Eine
Mischung von N-(5-Chlor-2-hydroxyphenyl)acetamid (500 mg, 2,69 mmol),
(2S)-Oxiran-2-ylmethyl-3-nitrobenzolsulfonat (697 mg, 2,69 mmol)
und Cs2CO3 (1,04
g, 3,22 mmol) in DMF (10 ml) wurde über Nacht bei Raumtemperatur
gerührt.
Die Reaktionsmischung wurde zwischen Essigsäureethylester und Wasser verteilt.
Die organische Phase wurde über
Na2SO4 getrocknet,
filtriert und eingeengt. Der Rückstand
wurde durch Flash-Chromatographie an Kieselgel (Essigsäureethylester
0–50%
in Petrolether) aufgereinigt, wodurch man die im Untertitel genannte
Verbindung (600 mg) erhielt.
1H-NMR
(CDCl3, 400 MHz): δ 8,47 (d, J = 2,3 Hz, 1H); 7,93
(bs, 1H); 6,98 (dd, J = 2,3, 8,7 Hz, 1H); 6,83 (d, J = 8,7 Hz, 1H);
4,36 (dd, J = 2,4, 11,3 Hz, 1H); 3,94 (dd, J = 6,1, 11,3 Hz, 1H);
3,39 (m, 1H); 2,98 (m, 1H); 2,81 (dd, J = 2,7, 4,8 Hz, 1H); 2,22
(s, 3H).
APCI-MS: m/z 242 (MH+)
-
Schritt III:
-
N-(5-Chlor-2-{[(2S)-3-(6-chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-phenyl)acetamid
-
Eine
Mischung von 6-Chlor-3H-spiro[2-benzofuran-1,4'-piperidin]
(26 mg, 0,116 mmol) und N-{5-Chlor-2-[(2S)-oxiran-2-ylmethoxy]phenyl}acetamid (28
mg, 0,116 mmol) in Ethanol (3 ml) wurde über Nacht bei 80°C gerührt. Die
flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (0–2%
Methanol in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die Titelverbindung (28 mg) erhielt.
1H-NMR
(CD3OD, 400 MHz): δ 8,18 (d, J = 2,4 Hz, 1H); 7,30-7,20 (m, 3H); 7,10-7,00
(m, 2H); 5,02 (s, 2H); 4,23 (m, 1H); 4,14 (dd, J = 3,1, 9,9 Hz,
1H); 3,99 (dd, J = 6,5, 9,9 Hz, 1H); 2,93 (m, 2H); 2,63 (d, J =
6,3 Hz, 2H); 2,55 (m, 2H); 2,21 (s, 3H); 2,00 (m, 2H); 1,73 (m,
2H).
APCI-MS: m/z 467 (MH+).
-
Beispiel 11
-
N-(2-{[(2S)-3-(6-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-fluorphenyl)-acetamid
-
Eine
Mischung von 6-Chlor-3H-spiro[2-benzofuran-1,4'-piperidin]
(30 mg, 0,134 mmol) und N-{4-Fluor-2-[(2S)-oxiran-2-ylmethoxy]phenyl}acetamid (30
mg, 0,134 mmol) in Ethanol (3 ml) wurde über Nacht bei 80°C gerührt. Die
flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (Methanol 0–1%
in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die Titelverbindung (40 mg) erhielt.
1H-NMR
(CD3OD, 400 MHz): δ 7,90 (dd, J = 6,2, 8,9 Hz,
1H); 7,29-7,20 (m, 3H); 6,89 (dd, J = 2,7, 10,5 Hz, 1H); 6,67 (m,
1H); 5,02 (s, 2H); 4,23 (m, 1H); 4,13 (dd, J = 3,1, 9,9 Hz, 1H);
4,01 (dd, J = 6,3, 9,9 Hz, 1H); 2,93 (m, 2H); 2,69-2,50 (m, 4H);
2,20 (s, 3H); 2,00 (m, 2H); 1,73 (bd, J = 13,5 Hz, 2H).
APCI-MS:
m/z 451 (MH+).
-
Beispiel 12
-
N-(2-{[(2S)-3-(6-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}phenyl)acetamid
-
Eine
Mischung von 6-Chlor-3H-spiro[2-benzofuran-1,4'-piperidin]
(25 mg, 0,111 mmol) und N-{2-[(2S)-Oxiran-2-ylmethoxy]phenyl}acetamid (23 mg, 0,111
mmol) in Ethanol (2 ml) wurde über
Nacht bei 80°C
gerührt.
Die flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (0–1%
Methanol in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die Titelverbindung (20 mg) erhielt.
1H-NMR
(CD3OD, 400 MHz): δ 8,00 (dd, J = 1,3, 8,0 Hz,
1H; 7,30-7,20 (m, 3H); 7,12-7,05 (m, 2H); 6,93 (m, 1H); 5,01 (s,
2H); 4,22 (m, 1H); 4,14 (dd, J = 3,3, 9,9 Hz, 1H); 4,00 (dd, J =
6,4, 9,9 Hz, 1H); 2,94 (m, 2H); 2,69-2,52 (m, 4H); 2,20 (s, 3H); 2,01 (m,
2H); 1,74 (bd, J = 13,5 Hz, 2H).
APCI-MS: m/z 433 (MH+).
-
Beispiel 13
-
N-(2-{[(2S)-3-(6-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-methoxyphenyl)acetamid
-
Eine
Mischung von 6-Chlor-3H-spiro[2-benzofuran-1,4'-piperidin]
(46 mg, 0,205 mmol) und N-{4-Methoxy-2[(2S)-oxiran-2-ylmethoxy]phenyl}acetamid (48,6
mg, 0,205 mmol) in Ethanol (2 ml) wurde über Nacht bei 80°C gerührt. Die
flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie an
Kieselgel (0–1,5%
Methanol in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die Titelverbindung (80 mg) erhielt.
1H-NMR
(CD3OD, 400 MHz): δ 7,75 (d, J = 8,9 Hz, 1H); 7,29-7,20 (m, 3H); 6,64
(d, J = 2,7 Hz, 1H); 6,51 (dd, J = 2,7, 8,9 Hz, 1H); 5,02 (s, 2H);
4,44 (m, 1H); 4,12 (dd, J = 3,3, 10,0 Hz, 1H); 3,98 (dd, J = 6,2,
10,0 Hz, 1H); 3,80 (s, 3H); 2,96 (m, 2H); 2,68-2,50 (m, 4H); 2,18
(s, 3H); 2,00 (m, 2H); 1,74 (bd, J = 13,2 Hz, 2H).
APCI-MS:
m/z 461 (MH+).
-
Beispiel 14
-
2-{[(2S)-3-(6-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-N-cyclopropyl-4-fluorbenzamid
-
Eine
Mischung von 6-Chlor-3H-spiro[2-benzofuran-1,4'-piperidin]
(25 mg, 0,111 mmol) und N-Cyclopropyl-4-fluor-2-(oxiran-2-ylmethoxy)benzamid
(28 mg, 0,111 mmol) in Ethanol wurde über Nacht bei 80°C gerührt. Die
flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie an
Kieselgel (0–1%
Methanol in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die Titelverbindung (32 mg) erhielt.
1H-NMR
(CD3OD, 400 MHz): δ 7,98 (dd, J = 6,9, 8, Hz, 1H);
7,29-7,20 (m, 3H); 6,98 (dd, J = 2,4, 10,8 Hz, 1H); 6,82 (ddd, J
= 2,4, 8,0, 8,8 Hz, 1H); 5,01 (s, 2H); 4,25 (dd, J = 3,1, 9,4 Hz,
1H); 4,19 (m, 1H); 4,11 (dd, J = 5,5, 9,4 Hz, 1H); 2,92 (m, 3H);
2,59 (m, 4H); 2,01 (m, 2H); 1,73 (m, 2H); 0,80 (m, 2H); 0,69 (m,
2H).
APCI-MS: m/z 477 (MH+).
-
Beispiel 15
-
N-(2-{[(2S)-3-(5-Fluor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]phenyl)acetamid
-
Eine
Mischung von 5-Fluor-3H-spiro[2-benzofuran-1,4'-piperidin]
(15 mg, 0,072 mmol) und N-{2-[(2S)-Oxiran-2- ylmethoxy]phenyl}acetamid (15 mg, 0,072
mmol) in Ethanol (1,5 ml) wurde über
Nacht bei 80°C
gerührt.
Die flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (0–2%
Methanol in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die Titelverbindung (9 mg) erhielt.
1H-NMR
(CD3OD, 400 MHz): δ 7,99 (dd, J = 1,2, 8,0 Hz,
1H); 7,18 (dd, J = 4,9, 8,0 Hz, 1H); 7,11-6,90 (m, 5H); 5,00 (s,
2H); 4,27 (m, 1H); 4,13 (dd, J = 3,2, 9,9 Hz, 1H); 3,99 (dd, J =
6,4, 9,9 Hz, 1H); 2,99 (m, 2H); 2,72-2,52 (m, 4H); 2,20 (s, 3H);
2,02 (m, 2H); 1,73 (bd, J = 13,6 Hz, 2H).
APCI-MS: m/z 415
(MH+).
-
Eine
Suspension von 2-Amino-5-chlorphenol (1,01 g, 7,0 mmol) in Methanol
(10 ml) wurde mit Essigsäureanhydrid
(1,08 g, 10,55 mmol) versetzt, und die Reaktionsmischung wurde 30
Minuten lang bei Raumtemperatur gerührt. Die flüchtigen Bestandteile wurden
im Vakuum entfernt und der Rückstand
wurde durch Flash-Chromatographie an Kieselgel (Hexan:Essigsäureethylester
5:2) aufgereinigt, wodurch man die im Untertitel genannte Verbindung
(1,19 g) erhielt.
1H-NMR (DMSO-d6, 400 MHz): δ 10,29 (bs, 1H); 9,26 (bs, 1H);
7,77 (d, J = 8,6 Hz, 1H); 6,86 (d, J = 2,4 Hz, 1H); 6,80 (dd, J
= 2,4, 8,6 Hz, 1H); 2,12 (s, 3H).
APCI-MS: m/z 186 (MH+).
-
Schritt II:
-
N-{4-Chlor-2-[(2S)-oxiran-2-ylmethoxy]phenyl}acetamid
-
Eine
Mischung von 3-Nitrobenzolsulfonsäure-(28)-oxiran-2-ylmethylester (3,37
g, 13,25 mmol), N-(4-Chlor-2-hydroxyphenyl)acetamid
(2,46 g, 17,23 mmol) und Cs2CO3 (6,48
g, 19,88 mmol) wurde bei 0°C mit
DMF (20 ml) versetzt, und die Reaktionsmischung wurde 3 Stunden
lang bei 0°C
gerührt.
Die Reaktionsmischung wurde zwischen Essigsäureethylester und Wasser verteilt.
Die organische Phase wurde über Na2SO4 getrocknet,
filtriert und eingeengt. Der Rückstand
wurde durch Flash-Chromatographie an Kieselgel (Hexan:Essigsäureethylester
3:2) aufgereinigt, wodurch man die im Untertitel genannte Verbindung
(2,36 g) erhielt.
1H-NMR (CD3COCD3, 400 MHz): δ 8,67 (bs,
1H); 8,30 (d, J = 8,7 Hz, 1H); 7,07 (d, J = 2,3 Hz, 1H); 6,95 (dd,
J = 2,2, 8,7 Hz, 1H); 4,46 (dd, J = 2,3, 11,5 Hz, 1H); 3,94 (dd,
J = 6,6, 11,5 Hz, 1H); 3,34 (m, 1H); 2,87 (dd, J = 4,3, 5,0 Hz,
1H); 2,73 (dd, J = 2,7, 5,0 Hz, 1H); 2,18 (s, 3H).
-
Schritt III
-
N-(4-Chlor-2-{[(2S)-2-hydroxy-3-(3-oxo-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)propyl]oxy}phenyl)-acetamid
-
Eine
Mischung von 3H-Spiro[2-benzofuran-1,4'-piperidin]-3-on (Marxer, A.; Rodriguez,
H. R.; McKenna, J. M.; Tsai, H. M., J. Org. Chem., 1975, 40, 1427-1433)
(61 mg, 0,3 mmol) und N-(4-Chlor-2-[(29)-oxiran-2-ylmethoxy]phenyl)acetamid
(72,5 mg, 0,3 mmol) in Ethanol (3 ml) wurde über Nacht bei 80°C gerührt. Die
flüchtigen
Bestandteile wurden im Vakuum entfernt und der
-
Beispiel 17
-
N-Cyclopropyl-2-{[(2S)-2-hydroxy-3-(1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)propyl]oxy}benzamid
-
Eine
Mischung von 3H-Spiro[2-benzofuran-1,4'-piperidin] (Marxer, A.; Rodriguez,
H. R.; McKenna, J. M.; Tsai, H. M., J. Org. Chem., 1975, 40, 1427-1433)
(46,5 mg, 0,246 mmol) und N-Cyclopropyl-2-[(2S)-oxiran-2-ylmethoxy]benzamid
(57,4 mg, 0,246 mmol) in Ethanol (3 ml) wurde über Nacht bei 80°C gerührt. Die flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie an
Kieselgel (0–2%
Methanol in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die Titelverbindung (55 mg) erhielt.
1H-NMR
(CDCl3, 400 MHz): δ 8,43 (d, J = 1,8 Hz, 1H); 8,20
(dd, J = 1,8, 7,8 Hz, 1H); 7,40 (m, 1H); 7,30 (m, 2H); 7,23 (m,
1H); 7,18 (m, 1H); 7,08 (t, J = 7,5 Hz, 1H); 6,93 (d, J = 8,2 Hz,
1H); 5,10 (s, 2H); 4,20 (m, 2H); 4,00 (dd, J = 5,0, 9,3 Hz, 1H);
3,02 (m, 2H); 2,85 (m, 2H); 2,69 (m, 1H); 2,58 (m, 2H); 2,02 (m,
2H); 1,82 (d, 2H); 0,85 (m, 2H); 0,63 (m, 2H).
APCI-MS: m/z
423 (MH+).
bei 80°C über Nacht. Die flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie an
Kieselgel (0–1,5%
Methanol in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die Titelverbindung (35 mg) erhielt.
1H-NMR
(CDCl3, 400 MHz): δ 8,05 (d, J = 8,7 Hz, 1H); 7,29-7,18 (m, 4H); 7,10
(d, J = 2,2 Hz, 1H); 6,94 (dd, J = 2,2, 8,7 Hz, 1H); 5,08 (s, 2H);
4,26 (m, 1H); 4,16 (dd, J = 3,0, 10,0 Hz, 1H); 4,01 (dd, J = 6,4,
9,9 Hz, 1H); 2,97 (m, 2H); 2,69-2,52 (m, 4H); 2,19 (s, 3H); 2,07
(m, 2H); 1,73 (m, 2H).
APCI-MS: m/z 433 (MH+).
-
Beispiel 19
-
N-(5-Chlor-2-{[(2S)-2-hydroxy-3-(1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)propyl]oxy}phenyl)-acetamid
-
Eine
Mischung von 3H-Spiro[2-benzofuran-1,4'-piperidin] (63 mg, 0,33 mmol) und N-{5-Chlor-2-[(2S)-oxiran-2-ylmethoxy]phenyl}acetamid
(80 mg, 0,33 mmol) in Ethanol (5 ml) wurde 4 Stunden lang bei 77°C gerührt. Die
flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (0–3%
Methanol in Chloroform) aufgereinigt, wodurch man die Titelverbindung
(77 mg) erhielt.
1H-NMR (CDCl3, 400 MHz): δ 8,50 (m, 1H); 7,31 (m, 3H);
7,18 (m, 1H); 6,98 (m, 1H); 6,83 (m, 1H); 5,10 (s, 2H); 4,10 (m,
1H); 4,03 (dd, 1H); 3,91 (dd, 1H); 2,97 (m, 1H); 2,76 (m, 2H); 2,60-2,43
(m, 3H); 2,20 (s, 3H); 2,05-1,89 (m, 2H); 1,60 (m, 2H).
APCI-MS:
m/z 431 (MH+).
-
Beispiel 20
-
N-(2-{[(2S)-2-Hydroxy-2-methyl-3-(1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)propyl]oxy}-4-methoxyphenyl)acetamid
-
Schritt I:
-
3-Nitrobenzolsulfonsäure-[(2S)-2-methyloxiranyl]-methylester
-
In
einen ofengetrockneten 1000-ml-Dreihalskolben wurden gepulverte,
aktivierte Molekularsiebe (8,0 g, 4 Å) und CH2Cl2 (440 ml) gegeben, es wurde mit D-(–)-Weinsäurediisopropylester
(4 ml, 14,2 mmol) und 2-Methyl-2-propen-1-ol
(20 ml, 240 mmol) versetzt und die Mischung wurde auf –20°C abgekühlt. Titantetraisopropanolat
(3,5 ml, 11,9 mmol) mit einigen ml CH2Cl2 wurden zugesetzt, und die Mischung wurde
30 Minuten bei –20°C gerührt. Es
wurde über
1,5 Stunden tropfenweise mit Cumenhydroperoxid (75 ml, 430 mmol)
versetzt, wobei die Temperatur auf –20°C gehalten wurde. Die Mischung
wurde über
Nacht bei dieser Temperatur gerührt.
Es wurde über
5 Stunden tropfenweise mit Trimethylphosphit (40 ml, 340 mmol) versetzt,
wobei die Temperatur auf –20°C gehalten
wurde. Triethylamin (50 ml, 360 mmol) und 4-Dimethylaminopyridin (DMAP) (3,48 g,
28,5 mmol) wurden zugegeben, gefolgt von einer Lösung von 3-Nitrobenzolsulfonylchlorid
(47 g, 212 mmol) in CH2Cl2 (400
ml). Die Temperatur wurde auf –10°C erhöht, und
die Mischung wurde über
Nacht bei dieser Temperatur gerührt.
Nach dem Entfernen des Kühlbads
wurde die Reaktionsmischung über
Celite filtriert. Die organische Phase wurde mit 10%iger Weinsäure (500
ml), gesättigter
NaHCO3 (300 ml) und Kochsalzlösung (300
ml) gewaschen. Die organische Phase wurde über wasserfreiem Magnesiumsulfat
(MgSO4) getrocknet und im Vakuum eingeengt,
wodurch man 150 g eines gelben Öls
erhielt. Das Rohprodukt wurde durch Flash-Chromatographie an Kieselgel
(0–50%
Essigsäureethylester
in Heptan) aufgereinigt, wodurch man die im Untertitel genannte
Verbindung (48,8 g) erhielt.
1H-NMR
(CDCl3, 400 MHz): δ 8,79-8,75 (m, 1H); 8,52 (ddd,
J = 1,1, 2,3, 8,3 Hz, 1H); 8,25 (ddd, J = 1,1, 1,8, 7,8 Hz, 1H);
7,81 (t, J = 8,5 Hz, 1H); 4,28 (d, J = 11,3 Hz, 1H); 4,05 (d, J
= 11,3 Hz, 1H); 2,73 (d, J = 4,4 Hz, 1H); 2,67 (d, J = 4,4 Hz, 1H);
1,56 (s, 3H).
-
Schritt II:
-
N-(4-Methoxy-2-{[(2S)-2-methyloxiran-2-yl]methoxy}-phenyl)acetamid
-
Eine
Mischung von 3-Nitrobenzolsulfonsäure-[(2S)-2-methyloxiran-2-yl]methylester (2,04
g, 7,46 mmol), N-(2-Hydroxy-4-methoxyphenyl)acetamid
((1,04 g, 5,74 mmol) und Cs2CO3 (2,80
g, 8,61 mmol) in DMF (12 ml) wurde über Nacht bei Raumtemperatur
gerührt.
Die Reaktionsmischung wurde zwischen Essigsäureethylester und Wasser verteilt.
Die organische Phase wurde über
Na2SO4 getrocknet,
filtriert und eingeengt. Der Rückstand
wurde durch Flash-Chromatographie an Kieselgel (Essigsäureethylester:Hexan
1:1) aufgereinigt, wodurch man die im Untertitel genannte Verbindung
(1,19 g) erhielt.
1H-NMR (CDCl3, 400 MHz): δ 8,20 (d, J = 8,8 Hz, 1H); 7,72
(bs, 1H); 6,52 (m, 2H); 4,12 (d, J = 11,0 Hz, 1H); 3,98 (d, J =
11,0 Hz, 1H); 3,77 (s, 3H); 2,91 (d, J = 4,7 Hz, 1H); 2,77 (d, J
= 4,7 Hz, 1H); 2,20 (s, 3H); 1,48 (s, 3H).
-
Schritt III:
-
N-(2-{[(2S)-2-Hydroxy-2-methyl-3-(1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)propyl]oxy}-4-methoxyphenyl)acetamid
-
Eine
Mischung von 3H-Spiro[2-benzofuran-1,4'-piperidin] (57 mg, 0,3 mmol) und N-(4-Methoxy-2-{[(2S)-2-methyloxiran-2-yl]methoxy}phenyl)acetamid
(75,4 mg, 0,3 mmol) in Ethanol (3 ml) wurde über Nacht bei 80°C gerührt. Die
flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie an
Kieselgel (0–1,5%
Methanol in Dichlormethan, 0,2% NH4OH) aufgereinigt, wodurch
man die Titelverbindung (70 mg) erhielt.
1H-NMR
(CD3OD, 400 MHz): δ 7,65 (d, J = 8,8 Hz, 1H); 7,28-7,15 (m, 4H); 6,61
(d, J = 2,7 Hz, 1H); 6,50 (dd, J = 2,7, 8,8 Hz, 1H); 5,10 (s, 2H);
3,99 (d, J = 9,2 Hz, 1H); 3,90 (d, J = 9,2 Hz; 1H); 3,79 (s, 3H);
2,88 (m, 2H); 2,73-2,53
(m, 4H); 2,16 (s, 3H); 2,00 (m, 2H); 1,63 (m, 2H); 1,31 (s, 3H).
APCI-MS:
m/z 441 (MH+).
-
Beispiel 21
-
N-[2-{[(2S)-2-Hydroxy-3-(1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)propyl]oxy)-5-(trifluormethyl)-phenyl]acetamid
-
Schritt I:
-
N-[2-[(2S)-Oxiran-2-ylmethoxy]-5-(trifluormethyl)-phenyl]acetamid
-
Eine
Mischung von N-[2-Hydroxy-5-(trifluormethyl)phenyl]acetamid (282
mg, 1,28 mmol), (2S)-Oxiran-2-ylmethyl-3-nitrobenzolsulfonat
(331,5 mg, 1,28 mmol) und Cs2CO3 (487,5
mg, 1,28 mmol) in DMF (5 ml) wurde über Nacht bei Raumtemperatur
gerührt.
Die Reaktionsmischung wurde zwischen Essigsäureethylester und Wasser verteilt.
Die organische Phase wurde über
Na2SO4 getrocknet,
filtriert und eingeengt. Der Rückstand
wurde durch Flash-Chromatographie an Kieselgel (0–40% Essigsäureethylester
in Petrolether) aufgereinigt, wodurch man die im Untertitel genannte
Verbindung (150 mg) erhielt.
1H-NMR
(CDCl3, 400 MHz): δ 8,72 (bs, 1H); 7,90 (bs, 1H);
7,31 (m, 1H); 6,97 (d, 1H); 4,46 (dd, J = 2,4, 11,3 Hz, 1H); 4,00
(dd, J = 6,3, 11,3 Hz, 1H); 3,44 (m, 1H); 3,00 (d, J = 4,5 Hz, 1H);
2,80 (dd, J = 2,7, 4,8 Hz, 1H); 2,25 (s, 3H).
-
Schritt II:
-
N-[2-{E(2S)-2-Hydroxy-3-(1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)propyl]oxy}-5-(trifluormethyl)-phenyl]acetamid
-
Eine
Mischung von 3H-Spiro[2-benzofuran-1,4'-piperidin] (47,3 mg, 0,25 mmol) und
N-[2-[(2S)-Oxiran-2-yl-methoxy]-5-(trifluormethyl)phenyl]acetamid
(69 mg, 0,25 mmol) in Ethanol (3 ml) wurde über Nacht bei 80°C gerührt. Die
flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (0–1,5%
Methanol in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die Titelverbindung (38 mg) erhielt.
1H-NMR
(CD3OD, 400 MHz): δ 8,49 (d, 1H); 7,39 (dd, 1H);
7,30-7,17 (m, 5H); 5,08 (s, 2H); 4,28 (m, 2H); 4,10 (dd, J = 6,5,
9,8 Hz, 1H); 2,98 (m, 2H); 2,68-2,53 (m, 4H); 2,22 (s, 3H); 2,02
(m, 2H); 1,73 (m, 2H)
APCI-MS: m/z 465 (MH+).
-
Beispiel 22
-
N-(2-{[(2S)-2-Hydroxy-3-(2-methyl-1'H-spiro[inden-1,4'-piperidin]-1'-yl)propyl]oxy}phenyl)acetamid
-
Eine
Mischung von 2-Methylspiro[inden-1,4'-piperidin] (Efange, S. M. N.; Khare,
A. B.; Foulon, C.; Akella, S. K.; Parsons, S. M., J. Med. Chem.,
1994, 37, 2574-2582) (82,5 mg, 0,35 mmol) und N-{2-[(2S)-Oxiran-2-ylmethoxy]phenyl}acetamid
(72,5 mg, 0,35 mmol) in Ethanol (3 ml) wurde über Nacht bei 80°C gerührt. Die
flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (0–2%
Methanol in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die Titelverbindung (80 mg) erhielt.
-
Der
Rückstand
wurde durch Flash-Chromatographie an Kieselgel (0–2% Methanol
in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die Titelverbindung (80 mg) erhielt.
1H-NMR
(CD3OD, 400 MHz): δ 7,84 (m, 2H); 7,28 (m, 2H);
7,16 (m, 2H); 7,07 (m, 1H); 6,98 (m, 1H); 6,53 (bs, 1H); 4,58 (m,
1H); 4,14 (m, 2H); 3,90-3,49 (m, 6H); 2,45 (m, 2H); 2,19 (s, 3H);
1,99 (s, 3H); 1,40 (bt, J = 14,0 Hz, 2H).
APCI-MS: m/z 407
(MH+).
-
Beispiel 23
-
N-(2-{[(2S)-3-(2,3-Dihydro-1'H-spiro[inden-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}phenyl)acetamid
-
Eine
Mischung von 2,3-Dihydrospiro[inden-1,4'-piperidin] (Efange, S. M. N.; Khare,
A. B.; Foulon, C.; Akella, S. K.; Parsons, S. M., J. Med. Chem.,
1994, 37, 2574-2582;
Chambers, M. S.; Baker, R.; Billington, D. C.; Knight, A. K.; Middlemiss,
D. N.; Wong, E. H. F., J. Med. Chem., 1992, 35, 2033-2039) (78,3
mg, 0,35 mmol) und N-{2-[(2S)-Oxiran-2-ylmethoxy]phenyl}acetamid
(72,5 mg, 0,35 mmol) in Ethanol (3 ml) wurde über Nacht bei 80°C gerührt. Die
flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromato graphie
an Kieselgel (0–2%
Methanol in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die Titelverbindung (65 mg) erhielt.
1H-NMR
(CD3OD, 400 MHz): δ 7,82 (m, 1H); 7,26-7,12 (m,
5H); 7,06 (m, 1H); 6,98 (m, 1H); 4,50 (m, 1H); 4,10 (d, 2H); 3,72
(m, 2H); 3,45-3,22 (m, 5H); 2,99 (t, J = 7,3 Hz, 2H); 2,33-2,13
(m, 6H); 1,82 (m, 2H).
APCI-MS: m/z 395 (MH+).
-
Beispiel 25
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-N-cyclopropyl-4-hydroxybenzamid
-
Schritt I:
-
2-Hydroxy-4-(trityloxy)benzoesäuremethylester
Eine Lösung
von 2,4-Dihydroxybenzoesäuremethylester
(388 mg, 2,0 mmol) in Dimethylformamid (5 ml) wurde mit Triethylamin,
Et3N, (0,556 ml, 4,0 mmol) versetzt, gefolgt
von Tritylchlorid (557,5 mg, 2,0 mmol) und 4-Dimethylaminopyridin (DMAP) (20 mg).
Die Reaktionsmischung wurde über
Nacht bei Raumtemperatur gerührt
und dann in eine Eis-Wasser-Mischung gegossen, und der weiße Niederschlag
wurde abfiltriert. Dieser Niederschlag wurde einer Flash-Chromatographie an
Kieselgel (Essigsäureethylester
0–5% in
Petrolether) unterzogen, wodurch man die im Untertitel genannte Verbindung
(350 mg) erhielt.
1H-NMR (CDCl3, 400 MHz): δ 10,65 (s, 1H); 7,58-7,22 (m,
16H); 6,38 (m, 2H); 3,89 (s, 3H).
-
Schritt II:
-
N-Cyclopropyl-2-hydroxy-4-(trityloxy)benzamid
-
2-Hydroxy-4-(trityloxy)benzoesäuremethylester
(340 mg, 0,83 mmol) wurde in Cyclopropylamin (3 ml) gelöst und eine
Woche lang bei Raumtemperatur belassen. Die flüchtigen Bestandteile wurden
im Vakuum entfernt und der Rückstand
wurde durch Flash-Chromatographie an Kieselgel (Essigsäureethylester
0–20%
in Petrolether) aufgereinigt, wodurch man die im Untertitel genannte
Verbindung (210 mg) erhielt.
1H-NMR
(CDCl3, 400 MHz): δ 12,30 (s, 1H); 7,48 (m, 6H);
7,35-7,22 (m, 9H); 6,92 (d, J = 9,0 Hz, 1H); 6,31 (d, J = 2,4 Hz,
1H); 6,24 (dd, J = 2,4, 8,8 Hz, 1H); 6,08 (bs, 1H); 2,80 (m, 1H);
0,85 (m, 2H); 0,60 (m, 2H).
-
Schritt III:
-
N-Cyclopropyl-2-[(2S)-oxiran-2-ylmethoxy]-4-(trityloxy)benzamid
-
Eine
Mischung von (2S)-Oxiran-2-ylmethyl-3-nitrobenzolsulfonat (119 mg,
0,459 mmol), N-Cyclopropyl-2-hydroxy-4-(trityloxy)benzamid (200 mg, 0,459
mmol) und Caesiumcarbonat, Cs2CO3, (186,2 mg, 0,573 mmol) in Dimethylformamid
(3 ml) wurde über
Nacht bei Raumtemperatur gerührt.
Die Reaktionsmischung wurde zwischen Essigsäureethylester und Wasser verteilt.
Die organische Phase wurde über
Natriumsulfat, Na2SO4,
getrocknet, filtriert und eingeengt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (0–40%
Essigsäureethylester
in Petrolether) aufgereinigt, wodurch man die im Untertitel genannte
Verbindung (160 mg) erhielt.
1H-NMR
(CDCl3, 400 MHz): δ 8,04 (s, 1H); 7,86 (d, J =
8,8 Hz, 1H); 7,73 (bd, J = 3,0 Hz, 1H); 7,46-7,39 (m, 5H); 7,34-7,23
(m, 9H); 6,44 (dd, J = 2,2, 8,8 Hz, 1H); 6,23 (d, J = 2,2 Hz, 1H);
4,03 (dd, J = 2,7, 10,8 Hz, 1H); 3,68 (dd, J = 5,0, 10,8 Hz, 1H);
3,23 (m, 1H); 2,88 (m, 2H); 2,70 (dd, J = 2,7, 4,9 Hz, 1H); 0,80
(m, 2H); 0,58 (m, 2H).
-
Schritt IV:
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy)-N-cyclopropyl-4-hydroxybenzamid
-
Eine
Mischung von N-Cyclopropyl-2-[(2S)-oxiran-2-yl-methoxy]-4-(trityloxy)benzamid (152
mg, 0,307 mmol) und 5-Chlor-3H-spiro[1-benzofuran-2,4'-piperidin] (69 mg,
0,307 mmol) in Ethanol (3 ml) wurde über Nacht bei 80°C gerührt. Die
flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde unter Rückfluß 90 Minuten
lang mit 80%iger wäßriger Essigsäure (10
ml) behandelt. Die flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (0–3%
Methanol in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die Titelverbindung (75 mg) erhielt.
1H-NMR
(CD3OD, 400 MHz): δ 7,83 (d, J = 8,4 Hz, 1H); 7,13
(m, 1H); 6,94 (dd, J = 2,3, 8,4 Hz, 1H); 6,65 (d, J = 8,4 Hz, 1H);
6,51-6,45 (m, 2H); 4,21-4,13 (m, 2H); 4,08-4,02 (m, 1H); 3,01 (s,
2H); 2,90 (m, 1H); 2,75 (bs, 4H); 2,58 (d, J = 6,2 Hz, 2H); 1,98
(m, 2H); 1,88 (m, 2H); 0,80 (m, 2H); 0,65 (m, 2H).
APCI-MS:
m/z 473 (MH+)
-
Beispiel 26
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxy-2-methylpropyl]oxy)-N-cyclopropyl-4-hydroxybenzamid
-
Schritt I:
-
N-Cyclopropyl-2-hydroxy-4-[(4-methoxybenzyl)oxy]-benzamid
-
2-Hydroxy-4-[(4-methoxybenzyl)oxy]benzoesäuremethylester
(Percec, V.; Tomazos, D. J. Mater. Chem. 1993, 3, 643-650) (530
mg, 1,83 mmol) wurde in Cyclopropylamin (3 ml) gelöst und eine
Woche lang bei Raumtemperatur belassen. Die flüchtigen Bestandteile wurden
im Vakuum entfernt und der Rückstand
wurde durch Flash-Chromatographie an Kieselgel (Essigsäureethylester
0–40%
in Petrolether) aufgereinigt, wodurch man die im Untertitel genannte
Verbindung (407 mg) erhielt.
1H-NMR
(DMSO-d6, 400 MHz): δ 13,20 (bs, 1H); 8,56 (d, J
= 2,7 Hz, 1H); 7,72 (d, J = 8,7 Hz, 1H); 7,38-7,33 (m, 2H); 6,96-6,92
(m, 2H); 6,49-6,45 (m, 2H); 5,00 (s, 2H); 3,79 (s, 3H); 2,80 (m,
1H); 0,78 (m, 2H); 0,58 (m, 2H).
-
Schritt II:
-
[(2S)-2-Methyloxiranyl]methyl-3-nitrobenzolsulfonat
-
In
einen ofengetrockneten 1000-ml-Dreihalskolben wurden gepulverte,
aktivierte Molekularsiebe (8,0 g, 4 Å) und Dichlormethan, CH2Cl2, (440 ml) gegeben,
es wurde mit D-(–)-Weinsäurediisopropylester
(4 ml, 14,2 mmol) und 2-Methyl-2-propen-1-ol
(20 ml, 240 mmol) versetzt und die Mischung wurde auf –20°C abgekühlt. Titantetraisopropanolat
(3,5 ml, 11,9 mmol) mit einigen ml Dichlormethan wurden zugesetzt,
und die Mischung wurde 30 Minuten bei –20°C gerührt. Es wurde über 1,5
Stunden tropfenweise mit Cumenhydroperoxid (75 ml, 430 mmol) versetzt,
wobei die Temperatur auf –20°C gehalten
wurde. Die Mischung wurde über
Nacht bei dieser Temperatur gerührt.
Es wurde über
5 Stunden tropfenweise mit Trimethylphosphit (40 ml, 340 mmol) versetzt,
wobei die Temperatur auf –20°C gehalten
wurde. Triethylamin (50 ml, 360 mmol) und 4-Dimethylaminopyridin
(DMAP) (3,48 g, 28,5 mmol) wurden zugegeben, gefolgt von einer Lösung von
3-Nitrobenzolsulfonylchlorid (47 g, 212 mmol) in Dichlormethan (400
ml). Die Temperatur wurde auf –10°C erhöht, und
die Mischung wurde über
Nacht bei dieser Temperatur gerührt.
Nach dem Entfernen des Kühlbads
wurde die Reaktionsmischung über
Celite filtriert. Die organische Phase wurde mit 10%iger Weinsäure (500
ml), gesättigtem Natriumhydrogencarbonat,
NaHCO3 (300 ml) und Kochsalzlösung (300
ml) gewaschen. Die organische Phase wurde über wasserfreiem Magnesiumsulfat
(MgSO4) getrocknet und im Vakuum eingeengt,
wodurch man 150 g eines gelben Öls
erhielt. Das Rohprodukt wurde durch Flash-Chromatographie an Kieselgel
(0–50%
Essigsäureethylester
in Heptan) aufgereinigt, wodurch man die im Untertitel genannte
Verbindung (48,8 g) erhielt.
1H-NMR
(CDCl3, 400 MHz): δ 8,79-8,75 (m, 1H); 8,52 (ddd,
J = 1,1, 2,3, 8,3 Hz, 1H); 8,25 (ddd, J = 1,1, 1,8, 7,8 Hz, 1H);
7,81 (t, J = 8,5 Hz, 1H); 4,28 (d, J = 11,3 Hz, 1H); 4,05 (d, J
= 11,3 Hz, 1H); 2,73 (d, J = 4,4 Hz, 1H); 2,67 (d, J = 4,4 Hz, 1H);
1,56 (s, 3H).
-
Schritt III:
-
N-Cyclopropyl-4-[(4-methoxybenzyl)oxy]-2-{[(2S)-2-methyloxiran-2-yl]methoxy}benzamid
-
Eine
Mischung von [(2S)-2-Methyloxiran-2-yl]methyl-3-nitrobenzolsulfonat (218 mg, 0,797 mmol), N-Cyclopropyl-2-hydroxy-4-[(4-methoxybenzyl)oxy]benzamid
(250 mg, 0,797 mmol) und Caesiumcarbonat, Cs2CO3, (311 mg, 0,956 mmol) in Dimethylformamid
(5 ml) wurde über
Nacht bei Raumtemperatur gerührt.
Die Reaktionsmischung wurde zwischen Essigsäureethylester und Wasser verteilt.
Die organische Phase wurde über
Natriumsulfat, Na2SO4,
getrocknet, filtriert und eingeengt und der Rückstand wurde durch Flash-Chromatographie an
Kieselgel (0–40%
Essigsäureethylester
in Petrolether) aufgereinigt, wodurch man die im Untertitel genannte
Verbindung (260 mg) erhielt.
1H-NMR
(CDCl3, 400 MHz): δ 8,19 (d, J = 8,8 Hz, 1H); 7,90
(d, J = 3,0 Hz, 1H); 7,38-7,33 (m, 2H); 6,96-6,92 (m, 2H); 6,70
(dd, J = 2,3, 8,8 Hz, 1H); 6,48 (d, J = 2,3 Hz, 1H); 5,02 (s, 2H);
4,14 (d, J = 10,3 Hz, 1H); 4,06 (d, J = 10,3 Hz, 1H); 3,80 (s, 3H);
3,04-2,98 (m, 1H); 2,94 (d, J = 4,7 Hz, 1H); 2,87 (d, J = 4,7 Hz,
1H); 1,50 (s, 3H); 0,86 (m, 2H); 0,65 (m, 2H).
APCI-MS: m/z
384 (MH+).
-
Schritt IV:
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxy-2-methylpropyl]oxy}-N-cyclopropyl-4-[(4-methoxybenzyl)oxy]benzamid
-
Eine
Mischung von 5-Chlor-3H-spiro(1-benzofuran-2,4'-piperidin]
(70 mg, 0,313 mmol) und N-Cyclopropyl-4-[(4-methoxybenzyl)oxy]-2-{[(2S)-2-methyloxiran-2-yl]-methoxy}benzamid
(120 mg, 0,313 mmol) in Ethanol (3 ml) wurde 6 Stunden lang bei
80°C gerührt. Die
flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (0–1%
Methanol in Dichlormethan, 0,2% Ammoniumhydroxid, NH4OH)
aufgereinigt, wodurch man die im Untertitel genannte Verbindung
(100 mg) erhielt.
1H-NMR (CDCl3, 400 MHz): δ 8,22–8,15 (m, 2H); 7,39–7,34 (m,
2H); 7,13-7,06 (m, 2H); 6,97-6,92 (m, 2H); 6,72-6,66 (m, 2H); 6,50 (d, J = 2,3 Hz, 1H);
5,08 (s, 2H); 3,88 (s, 3H); 3,05 (m, 1H); 2,99 (s, 2H); 2,90 (m,
2H); 2,75 (m, 1H); 2,66 (d, J = 13,8 Hz, 1H); 2,64 (m, 1H); 2,49
(d, J = 13,8 Hz, 1H); 1,99 (m, 2H); 1,82 (m, 2H); 1,60 (bs, 2H);
1,33 (s, 3H); 0,86 (m, 2H); 0,65 (m, 2H).
APCI-MS: m/z 607
(MH+).
-
Schritt V:
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxy-2-methylpropyl]oxy}-N-cyclopropyl-4-hydroxybenzamid
-
2-[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxy-2-methylpropyl]oxy}-N-cyclopropyl-4-[(4-methoxybenzyl)oxy]benzamid
(80 mg, 0,131 mmol) wurde bei Raumtemperatur 15 Minuten lang mit Trifluoressigsäure 10%
in Dichlormethan (10 ml) behandelt. Die flüchtigen Bestandteile wurden
im Vakuum entfernt und der Rückstand
wurde durch Flash-Chromatographie
an Kieselgel (0–2%
Methanol in Dichlormethan, 0,2% Ammoniumhydroxid, NH4OH)
aufgereinigt, wodurch man die Titelverbindung (40 mg) erhielt.
1H-NMR (CD3OD, 400
MHz): δ 7,83
(m, 1H); 7,12 (m, 1H); 7,03 (dd, J = 2,3, 8,5 Hz, 1H); 6,64 (d,
J = 8,5 Hz, 1H); 6,49-6,45 (m, 2H); 4,09 (d, J = 9,2 Hz, 1H); 3,90
(d, J = 9,2 Hz, 1H); 2,99 (s, 2H); 2,92 (m, 1H); 2,79 (m, 2H); 2,66
(m, 2H); 2,58 (d, J = 13,9 Hz, 1H); 2,50 (d, J = 13,9 Hz, 1H); 1,93-1,75
(m, 4H); 1,31 (s, 3H); 0,80 (m, 2H); 0,68 (m, 2H).
APCI-MS:
m/z 487 (MH+).
-
Beispiel 27
-
N-(4-Hydroxy-2-{[(2S)-2-hydroxy-3-(1'H,4H-spiro-[chromen-3,4'-piperidin]-1'-yl)propyl]oxy}phenyl)-acetamid
-
Schritt I:
-
(1Z)-1-(2,4-Dihydroxyphenyl)ethanonoxim
-
1-(2,4-Dihydroxyphenyl)ethanon
(4,5 g, 29,6 mmol) wurde in Pyridin (17 ml) gelöst. Hydroxylaminhydrochlorid
(2,1 g, 29,6 mmol) wurde im Verlauf von 10 Minuten in kleinen Portionen
zugesetzt. Nach Rühren bei
Raumtemperatur über
Nacht wurde die grün-gelbliche
Lösung
zwischen Wasser und Essigsäureethylester verteilt.
Die organische Phase wurde zweimal mit Wasser und einmal mit 0,2
M Salzsäure
gewaschen und anschließend
eingeengt. Der ölige
Rückstand
wurde mit Wasser versetzt und eingedampft, wodurch man einen weißen, halbfesten
Rückstand
erhielt, der mit Toluol versetzt und eingedampft wurde, wodurch
man die Titelverbindung (4,8 g, 98%) in Form eines weißen Feststoffs
erhielt.
-
Schritt II:
-
2-Methyl-1,3-benzoxazol-6-ol
-
Eine
gekühlte
(5°C) Lösung von
(1Z)-1-(2,4-Dihydroxyphenyl)ethanonoxim (9,7 g, 57,7 mmol) in Acetonitril
(65 ml) und Dimethylacetamid (11 ml) wurde tropfenweise mit Phosphoroxychlorid
(5,6 ml, 60,3 mmol) versetzt. Während
der Zugabe wurde die Temperatur unter 10°C gehalten. Nach 1 Stunde Rühren bei
Raumtemperatur wurde die gelbe Suspension auf eine Mischung aus
Natriumhydrogencarbonat und Eis gegossen. Der auf diese Weise erhaltene
Niederschlag wurde filtriert und getrocknet, wodurch man 6,3 g (73%)
der Titelverbindung erhielt.
-
Schritt III:
-
Essigsäure-2-methyl-1,3-benzoxazol-6-ylester
-
Eine
Suspension von 2-Methyl-1,3-benzoxazol-6-ol (7,1 g, 47,8 mmol) in
Tetrahydrofuran wurde auf 10°C
abgekühlt
und in einer Portion mit Triethylamin (5,8 ml, 81,3 mmol) versetzt,
gefolgt von der Zugabe von Acetylchlorid (11,3 ml, 81,6 mmol) in
kleinen Portionen. Nach Rühren
bei Raumtemperatur über
Nacht wurde die Reaktionsmischung zwischen Wasser und Essigsäureethylester
verteilt. Die organische Phase wurde zweimal mit Wasser gewaschen
und eingeengte, wodurch man die Titelverbindung (8,2 g, 90%) in
Form eines beigefarbenen Feststoffs erhielt.
-
Schritt IV:
-
Essigsäure-4-(acetylamino)-3-hydroxyphenylester
-
Essigsäure-2-methyl-1,3-benzoxazol-6-ylester
(8,1 g, 42,3 mmol) wurde in Tetrahydrofuran (60 ml) gelöst und mit
Trifluoressigsäure
(4 ml, 53,2 mmol) versetzt. Die hellbraune Lösung wurde über Nacht bei Raumtemperatur
gerührt.
Natriumhydrogenocarbonat (wäßrig, gesättigt) wurde
zugesetzt, und die Lösung
wurde zweimal mit Essigsäureethylester
extrahiert. Die vereinigten organischen Phasen wurden eingeengt,
wodurch man die Titelverbindung (8,0 g, 91%) in Form eines beigefarbenen
Feststoffs erhielt.
-
Schritt V:
-
Essigsäure-4-(acetylamino)-3-[(2S)-oxiran-2-ylmethoxy]-phenylester
-
Eine
Lösung
von Essigsäure-4-(acetylamino)-3-hydroxyphenylester
(669 mg, 3,2 mmol), 3-Nitrobenzolsulfonsäure-(2S)-oxiran-2-ylmethylester
(748 mg, 2,9 mol) und Caesiumcarbonat (1,05 g, 3,2 mmol) in 1-Methylpyrrolidinon
(10 ml) wurde über
Nacht bei Raumtemperatur gerührt
und dann zwischen Wasser und Essigsäureethylester verteilt. Die
organische Phase wurde zweimal mit Wasser gewaschen und zu einem
gelben Öl
eingeengt, das in Methanol/Diethylether 1/2 suspendiert wurde. Der
feste beigefarbene Niederschlag wurde abfiltriert und getrocknet,
wodurch man die Titelverbindung (296 mg, 38%) erhielt.
-
Schritt VI:
-
N-(4-Hydroxy-2-{[(2S)-2-hydroxy-3-(1'H,4H-spiro-[chromen-3,4'-piperidin]-1'-yl)propyl]oxy}phenyl)-acetamid
-
Eine
Lösung
von Essigsäure-4-(acetylamino)-3-[(2S)-oxiran-2-ylmethoxy]phenylester
(56 mg, 0,21 mmol) und 4H-Spiro[chromen-3,4'-piperidin] (43 mg, 0,21 mmol) in Methanol
(1 ml) wurde über
Nacht bei 60°C gerührt und
dann eingeengt. Der dunkelgraue Rückstand wurde durch HPLC an
C18 ("Kromasil"-Säule, 5 μm, Acetonitril/Wasser 10/90
bis 60/40 über
20 Minuten mit 0,1% Trifluoressigsäure) aufgereinigt, wodurch
man die Titelverbindung (39 mg, 33%), Trifluoracetatsalz, erhielt.
1H-NMR (Aceton-d6,
400 MHz,) δ:
11,27 (1H, bs); 8,52 (1H, bs); 7,95 (1H, d); 7,10 (2H, t); 6,86
(1H, t); 6,78 (1H, d); 6,53 (1H, d); 6,40 (1H, dd); 4,55-4,48 (1H,
m); 4,21 (1H, s); 4,09-4,01 (2H, m); 3,91 (1H, s); 3,83-3,65 (2H,
m); 3,65-3,49 (2H, m); 3,49-3,35 (2H, m); 3,00 (1H, s); 2,70 (1H,
s); 2,08 (3H, s); 2,02-1,74 (4H, m).
APCI-MS: m/z 427 [MH+]
-
Beispiel 28
-
2-([(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxy-2-methylpropyl]oxy}-4-hydroxy-N-methylbenzamid
(Trifluoracetat)
-
Schritt I:
-
2-Hydroxy-4-[(4-methoxybenzyl)oxy]-N-methylbenzamid
Eine Suspension von 2-Hydroxy-4-[(4-methoxybenzyl)oxy]benzoesäuremethylester
(500 mg, 1,73 mmol) in Methanol (15 ml) wurde bei 0°C langsam
mit 40%igem wäßrigem Methylamin
(3 ml) versetzt. Nach dem Ende der Zugabe wurde die Reaktionsmischung
2 Tage lang bei Raumtemperatur gerührt. Die flüchtigen Bestandteile wurden
im Vakuum entfernt, wodurch man die im Untertitel genannte Verbindung
(500 mg) erhielt.
1H-NMR (DMSO-d6, 400 MHz): δ 13,20 (bs, 1H); 8,60 (m, 1H);
7,70 (d, J = 8,8 Hz, 1H); 7,35 (m, 2H); 6,96-6,92 (m, 2H); 6,50
(dd, J = 2,6, 8,8 Hz, 1H); 6,42 (d, J = 2,6 Hz, 1H); 5,04 (s, 2H);
3,76 (s, 3H); 2,79 (d, J = 4,6 Hz, 3H).
APCI-MS: m/z 288 (MH+).
-
Schritt II:
-
4-[(4-Methoxybenzyl)oxy]-N-methyl-2-{[(2S)-2-methyloxiran-2-yl]methoxy]benzamid
-
Eine
Mischung von 3-Nitrobenzolsulfonsäure-[(2S)-2-methyloxiran-2-yl]methylester (133 mg,
0,487 mmol), 2-Hydroxy-4-[(4-methoxybenzyl)oxy]-N-methylbenzamid
(140 mg, 0,487 mmol) und Caesiumcarbonat, Cs2CO3, (198 mg, 0,608 mmol) in Dimethylformamid
(5 ml) wurde über
Nacht bei Raumtemperatur gerührt.
Die Reaktionsmischung wurde zwischen Essigsäureethylester und Wasser verteilt.
Die organische Phase wurde über
Natriumsulfat, Na2SO4,
getrocknet, filtriert und eingeengt. Der Rückstand wurde durch Flash-Chromatographie an
Kieselgel (0–60%
Essigsäureethylester
in Petrolether) aufgereinigt, wodurch man die im Untertitel genannte
Verbindung (130 mg) erhielt.
1H-NMR
(CDCl3, 400 MHz): δ 8,18 (d, J = 8,8 Hz, 1H); 7,82
(m, 1H); 7,37 (m, 2H); 6,97-6,92 (m, 2H); 6,71 (dd, J = 2,3, 8,8
Hz, 1H); 6,53 (d, J = 2,3 Hz, 1H); 5,01 (s, 2H); 4,18 (d, J = 10,5
Hz, 1H); 4,10 (d, J = 10,5 Hz, 1H); 3,85 (s, 3H); 3,02 (d, J = 4,9
Hz, 3H); 2,97 (d, J = 4,6 Hz, 1H); 2,80 (d, J = 4,6 Hz, 1H); 1,50
(s, 3H).
APCI-MS: m/z 358 (MH+).
-
Schritt III:
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxy-2-methylpropyl]oxy}-4-[(4-methoxybenzyl)oxy]-N-methylbenzamid
-
Eine
Mischung von 5-Chlor-3H-spiro[1-benzofuran-2,4'-piperidin]
(70 mg, 0,313 mmol) und Methoxybenzyl)oxy]-N-methyl-2-{[(2S)-2-methyloxiran-2-yl]methoxy}benzamid
(112 mg, 0,313 mmol) in Ethanol (2 ml) wurde 4,5 Stunden lang bei
80°C gerührt. Die
flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (0–1,5%
Methanol in Dichlormethan, 0,2% Ammoniumhydroxid, NH4OH)
aufgereinigt, wodurch man die im Untertitel genannte Verbindung
(135 mg) erhielt.
1H-NMR (CDCl3, 400 MHz): δ 8,18 (d, J = 8,7 Hz, 1H); 8,12
(m, 1H); 7,39-7,35 (m, 2H); 7,12 (m, 2H); 7,08 (dd, J = 2,3, 8,5
Hz, 1H); 6,97-6,92 (m, 2H); 6,72-6,66 (m, 2H); 6,52 (d, J = 2,3
Hz, 1H); 5,05 (s, 2H); 3,90 (m, 2H); 3,82 (s, 3H); 3,0 (d, J = 4,9
Hz, 3H); 2,98 (s, 2H); 2,94-2,84 (m, 2H); 2,73 (m, 1H); 2,69 (d,
J = 13,9 Hz, 1H); 2,63 (m, 1H); 2,49 (d, J = 13,9 Hz, 1H); 1,99
(m, 2H); 1,82 (m, 2H).
APCI-MS: m/z 581 (MH+)
-
Schritt IV:
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxy-2-methylpropyl]oxy}-4-hydroxy-N-methylbenzamid
(Trifluoracetat)
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxy-2-methylpropyl]oxy}-4-[(4-methoxybenzyl)oxy]-N-methylbenzamid
(125 mg, 0,215 mmol) wurde bei Raumtemperatur 20 Minuten lang mit
10% Trifluoressigsäure
in Dichlormethan (10 ml) behandelt. Die flüchtigen Bestandteile wurden
im Vakuum entfernt und der Rückstand
wurde durch HPLC (Acetonitril/Wasser (CH3CN/H2O), 0,1% Trifluoressigsäure) aufgereinigt, wodurch
man die Titelverbindung (50 mg) erhielt.
1H-NMR
(CD3OD, 400 MHz): δ 7,52-7,47 (m, 1H); 7,20 (bs,
1H); 7,10 (dd, J = 2,3, 8,5 Hz, 1H); 6,75 (d, J = 8,5 Hz, 1H); 6,52
(bs, 1H); 6,49 (dd, J = 2,1, 8,5 Hz, 1H); 4,20 (m, 2H); 4,00 (m,
1H); 3,62-3,35 (m, 4H); 3,18 (2xs, 2H); 3,90 (2xs, 3H); 2,60 (m,
2H); 2,32-2,05 (m, 3H); 1,39 (s, 3H).
APCI-MS: m/z 461 (MH+).
-
Beispiel 29
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxy]oxy}-4-hydroxy-N-methylbenzamid
-
Schritt I:
-
4-[4-Methoxybenzyl)oxy]-N-methyl-2-[(2S)-oxiran-2-yl-methoxy]benzamid
-
Eine
Mischung von 3-Nitrobenzolsulfonsäure-(2S)-oxiran-2-ylmethylester (151
mg, 0,584 mmol), 2-Hydroxy-4-[(4-methoxybenzyl)oxy]benzoesäuremethylester
(168 mg, 0,584 mmol) und Caesiumcarbonat, Cs2CO3, (228 mg, 0,70 mmol) in Dimethylformamid
(4 ml) wurde über
Nacht bei Raumtemperatur gerührt.
Die Reaktionsmischung wurde zwischen Essigsäureethylester und Wasser verteilt.
Die organische Phase wurde über
Natriumsulfat getrocknet, Na2SO4,
filtriert und eingeengt. Der Rückstand
wurde durch Flash-Chromatographie an Kieselgel (Essigsäureethylester
0–90%
in Petrolether) aufgereinigt, wodurch man die im Untertitel genannte
Verbindung (150 mg) erhielt.
1H-NMR
(DMSO-d6, 400 MHz): δ 7,90 (m, 1H); 7,75 (d, J =
8,7 Hz, 1H); 7,37 (d, J = 8,6 Hz, 2H); 6,96-6,91 (m, 2H); 6,74 (d,
J = 2,3 Hz, 1H); 6,68 (dd, J = 2,3, 8,7 Hz, 1H); 5,08 (s, 2H); 4,48
(dd, J = 2,5, 11,5 Hz, 1H); 4,04 (dd, J = 6,0, 11,5 Hz, 1H); 3,78
(s, 3H); 3,45 (m, 1H); 2,86 (t, J = 4,9 Hz, 1H); 2,79 (d, J = 4,7
Hz, 3H); 2,73 (dd, J = 2,7, 5,0 Hz, 1H).
APCI-MS: m/z 344 (MH+).
-
Schritt II:
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]-N-methylbenzamid
-
Eine
Mischung von 5-Chlor-3H-spiro[1-benzofuran-2,4'-piperidin]
(70 mg, 0,313 mmol) und 4-[4-Methoxybenzyl)-oxy]-N-methyl-2-[(2S)-oxiran-2-ylmethoxy]benzamid (107,5
mg, 0,313 mmol) in Ethanol (3 ml) wurde 6 Stunden lang bei 80°C gerührt. Die
flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (0–1%
Methanol in Dichlormethan, 0,2% Ammoniumhydroxid, NH4OH)
aufgereinigt, wodurch man die im Untertitel genannte Verbindung
(122 mg) erhielt.
1H-NMR (CDCl3, 400 MHz): δ 8,18 (d, J = 8, 8 Hz, 1H);
8,10 (m, 1H); 7,34 (d, J = 8,7 Hz, 2H); 7,14 (bs, 1H); 7,08 (m,
1H); 6,95 (d, J = 8,7 Hz, 2H); 6,70 (m, 2H); 6,5 (d, J = 2,1 Hz,
1H); 5,08 (s, 2H); 4,22-4,12 (m, 2H); 3,98 (dd, J = 5,3, 9,3 Hz,
1H); 3,85 (s, 3H); 3,01 (s, 2H); 3,00 (d, J = 4,8 Hz, 3H); 2,95-2,87
(m, 1H); 2,80 (m, 1H); 2,65-2,50 (m, 4H); 2,01 (m, 2H); 1,82 (m,
2H).
APCI-MS: m/z 567 (MH+).
-
Schritt III:
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxy]oxy}-4-hydroxy-N-methylbenzamid
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]-N-methylbenzamid
(110 mg, 0,194 mmol) wurde bei Raumtemperatur 20 Minuten lang mit
10% Trifluoressigsäure
in Dichlormethan (10 ml) behandelt. Die flüchtigen Bestandteile wurden
im Vakuum entfernt und der Rückstand
wurde durch Flash-Chromatographie an Kieselgel (0–3% Methanol
in Dichlormethan, 0,2% Ammoniumhydroxid, NH4OH)
aufgereinigt, wodurch man die Titelverbindung (45 mg) erhielt.
1H-NMR (CD3OD, 400
MHz): δ 7,81
(d, J = 8,7 Hz, 1H); 7,13 (m, 1H); 7,04 (dd, J = 2,3, 8,5 Hz, 1H);
6,66 (d, J = 8,5 Hz, 1H); 6,52 (d, J = 2,2 Hz, 1H); 6,48 (dd, J
= 2,2, 8,6 Hz, 1H); 4,25-4,17 (m, 2H); 4,05 (m, 1H); 3,02 (s, 2H);
2,92 (s, 3H); 2,70 (bs, 4H); 2,60 (d, J = 6,2 Hz, 2H); 1,94 (m,
2H); 1,84 (m, 2H).
APCI-MS: m/z 447 (MH+).
-
Beispiel 30
-
N-(2-{[(2S)-3-(5-Chlor-1'H-spiro[1,3-benzodioxol-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy)-4-hydroxyphenyl)acetamidtrifluoracetat
-
Schritt I:
-
5-Chlor-1'H-spiro[1,3-benzodioxol-2,4'-piperidin]-1'-carbonsäureethylester
-
Eine
Mischung von 4-Oxopiperidin-1-carbonsäureethylester (1,71 g, 10 mmol),
4-Chlorbenzol-1,2-diol (1,73 g, 12 mmol) und einer katalytischen
Menge an 4-Methylbenzolsulfonsäure-hydrat
in trockenem Toluol (30 ml) wurde 7 Stunden lang an einem Wasserabscheider
erhitzt. Nach dem Abkühlen
wurde die Reaktionsmischung mit 2 N Natriumhydroxid (2 × 25 ml)
gewaschen, und das Lösungsmittel
wurde im Vakuum entfernt. Flash-Chromatographie
an Kieselgel (Heptan/Essigsäureethylester,
2:1) des verbliebenen halbfesten Produkts lieferte 5-Chlor-1'H-spiro[1,3-benzodioxol-2,4'-piperidin]-1'-carbonsäureethylester
in Form farbloser Kristalle (0,43 g, 15%).
APCI-MS: m/z 298
[MH+].
1H-NMR
(400 MHz, CDCl3): δ 6,77 (m, 2H), 6,67 (m, 1H),
4,16 (q, 2H, J = 7,1 Hz), 3,67 (t, 4H, J = 5,7 Hz), 1,98 (t, 4H,
J = 5,7 Hz), 1,28 (t, 3H, J = 7,1 Hz).
-
Schritt II:
-
5-Chlorspiro[1,3-benzodioxol-2,4'-piperidin]
-
5-Chlor-1'H-spiro[1,3-benzodioxol-2,4'-piperidin]-1'-carbonsäureethylester (0,43 g, 1,45
mmol) wurde in Ethanol (5 ml) und Wasser (0,4 ml) gelöst. Es wurde
mit Natriumhydroxid (0,2 g) versetzt und anschließend 2 Tage
lang unter Rückfluß erhitzt.
Nach dem Abkühlen wurde
die Lösung
im Vakuum eingeengt und mit 10%iger HCl auf einen pH-Wert von < 1 angesäuert. Nach
Ende der Gasentwicklung wurde die Lösung durch die Zugabe von gesättigtem
wäßrigem Natriumhydrogencarbonat,
NaHCO3, alkalisch gestellt und mit Dichlormethan
extrahiert. Trocknen über
Natriumsulfat, Na2SO4,
und anschließendes
Abdampfen des Lösungsmittels lieferte
einen farblosen Feststoff (0,28 g, 1,2 mol, 86%).
APCI-MS:
m/z 226 [MH+].
1H-NMR
(400 MHz, CDCl3): δ 6,6-6,9 (m, 3H), 3,06 (t, 4H,
J = 5,0 Hz), 1,99 (t, 4H, J = 5,2 Hz).
-
Schritt III:
-
N-2-{[(2S)-3-(5-Chlor-1'H-spiro[1,3-benzodioxol-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxyphenyl)acetamidtrifluoracetat
-
Eine
Lösung
von 5-Chlorspiro[1,3-benzodioxol-2,4'-piperidin]
(45 mg, 0,2 mmol) und Essigsäure-4-(acetylamino)-3-[(2S)-oxiran-2-ylmethoxy]phenylester
(53 mg, 0,2 mmol) in Methanol (5 ml) wurde 15 Stunden lang unter
Rückfluß erhitzt.
Das Lösungsmittel
wurde im Vakuum abdestilliert. Der Rückstand wurde durch präparative
HPLC ("Kromasil"-Säule; Laufmittel:
[Acetonitril + 0,1% Trifluoressigsäure (TFA)/Wasser + 0,1% TFA])
aufgereinigt, wodurch man die Titelverbindung in Form eines farblosen
Feststoffs (37 mg, 0,07 mmol, 33%) erhielt.
APCI-MS: m/z 449
[MH+].
1H-NMR
(400 MHz, Aceton-d6): δ 8,47 (bs, 1H), 7,93 (d, 1H,
J = 8,7 Hz), 6,8-7,0 (m, 3H), 6,53 (d, 1H, J = 2,6 Hz), 6,41 (dd,
1H, J = 2,6 Hz, J = 8,7 Hz), 4,54 (m, 1H), 4,08 (m, 2H), 3,66 (m,
2H), 2,51 (m, 4H), 2,08 (s, 3H), 2,06 (m, 4H).
-
Beispiel 31
-
N-(2-{[(2S)-3-(5-Chlor-1'H-spiro[1,3-benzodioxol-2,4'-piperidin]-1'-yl)-2-hydroxy-2-methylpropyl]oxy}-4-hydroxyphenyl)acetamidtrifluoracetat
-
Die
Titelverbindung wurde wie in Beispiel 9 beschrieben ausgehend von
5-Chlorspiro[1,3-benzodioxol-2,4'-piperidin]
(45 mg, 0,2 mmol) und Benzoesäure-4-(acetylamino)-3-{[(2S)-2-methyloxiran-2-yl]methoxy}phenylester
(68 mg, 0,2 mmol) in Form eines farblosen Feststoffs (30 mg, 0,05
mmol, 26%) dargestellt.
APCI-MS: m/z 463 [MH+].
1H-NMR (400 MHz, Aceton-d6): δ 8,59 (bs,
1H), 7,73 (d, 1H, J = 8,7 Hz), 6,8-7,0 (m, 3H), 6,58 (d, 1H, J =
2,6 Hz), 6,42 (dd, 1H, J = 2,6 Hz, J = 8,7 Hz), 4,42 (d, 1H, J =
9,7 Hz), 3,97 (d, 1H, J = 9,7 Hz), 3,71 (d, 1H, J = 14 Hz), 3,54
(d, 1H, J = 14 Hz), 2,52 (m, 4H), 2,09 (s, 3H), 2,06 (m, 4H), 1,51
(s, 3H).
-
Beispiel 32
-
N-4-(Hydroxy-2-{[(2S)-2-hydroxy-3-(1'H-spiro[1,3-benzodioxol-2,4'-piperidin]-1'-yl)propyl]oxy}-phenyl)acetamidtrifluoracetat
-
Die
Titelverbindung wurde ausgehend von Spiro[1,3-benzodioxol-2,4'-piperidin] (E. K. Moltzen, J. Perrengaard,
E. Meier, J. Med. Chem. 1995, 38 (11), 2009-2007) (38 mg, 0,2 mmol)
wie in Beispiel 30 beschrieben dargestellt. Ausbeute 78 mg, 0,15
mmol, 74%.
APCI-MS: m/z 415 [MH+].
1H-NMR (400 MHz, Aceton-d6): δ 7,90 (d,
1H, J = 8,7 Hz), 6,87 (s, 4H), 6,53 (d, 1H, J = 2,6 Hz), 6,75 (dd,
1H, J = 2,6 Hz, J = 8,7 Hz), 4,56 (m, 1H,), 4,08 (m, 2H), 3,69 (m,
2H), 2,46 (m, 4H), 2,09 (s, 3H), 2,07 (m, 4H).
-
Beispiel 33
-
N-(4-Hydroxy-2-{[(2S)-2-hydroxy-2-methyl-3-(1'H-spiro(1,3-benzodioxol-2,4'-piperidin)-1'-yl)-propyl]oxy)phenyl)acetamidtrifluoracetat
-
Die
Titelverbindung wurde ausgehend von Spiro[1,3-benzodioxol-2,4'-piperidin] (38 mg, 0,2 mmol) wie in
Beispiel 9 beschrieben dargestellt. Ausbeute 88 mg, 0,16 mmol, 81%.
APCI-MS:
m/z 429 [MH+].
1H-NMR
(400 MHz, Aceton-d6): δ 7,68 (d, 1H, J = 8,7 Hz), 6,86
(s, 4H), 6,60 (d, 1H, J = 2,5 Hz), 6,43 (dd, 1H, J = 2,6 Hz, J =
8,7 Hz), 4,06 (d, 1H, J = 9,7 Hz), 3,98 (d, 1H, J = 9,7 Hz), 4,03
(d, 1H, J = 9,7 Hz), 3,77 (d, 1H, J = 13,6 Hz), 3,60 (d, 1H, J =
13,6 Hz), 2,51 (m, 4H), 2,10 (s, 3H), 2,08 (m, 4H), 1,52 (s, 3H).
-
Zwischenprodukt: 5-Chlor-3H-spiro[2-benzofuran-1,4'-piperidin]
-
Schritt I:
-
1'-Benzyl-5-chlor-3H-spiro(2-benzofuran-1,4'-piperidin]-3-on
-
Eine
Lösung
von 2-Brom-5-chlorbenzoesäure
(2,35 g, 10,0 mmol) in Tetrahydrofuran (THF) (15 ml) wurde bei –78°C unter Stickstoff
langsam mit einer 1,6 M Lösung
von n-Butyllithium in Hexan (20 ml, 32,0 mmol) versetzt. Nach dem
Ende der Zugabe wurde die Reaktionsmischung noch weitere 3 Stunden
lang bei –78°C gerührt. Dann
wurde die Reaktionsmischung bei –78°C langsam mit einer Lösung von
1-Benzylpiperidin-4-on (3,78 g, 20,0 mmol) in THF (10 ml) versetzt.
Nach dem Ende der Zugabe wurde die Reaktionstemperatur auf Raumtemperatur
erhöht,
und die Reaktionsmischung wurde über
Nacht bei Raumtemperatur gerührt. Die
Reaktionsmischung wurde in eine Mischung von Wasser (60 ml) und
Diethylether (60 ml) gegossen, und die Phasen wurden getrennt. Anschließend wurde
die wäßrige Phase
mit Diethylether (2 × 20
ml) extrahiert. Die wäßrige Phase
wurde mit 6 M wäßriger Salzsäure (HCl)
auf einen pH-Wert von 2 angesäuert
und 1 Stunde lang gekocht, auf 0°C
abgekühlt,
durch Zugabe von wäßrigem (6
M) Natriumhydroxid (NaOH) auf einen pH-Wert von 10,0 eingestellt
und schnell mit Trichlormethan (CHCl3) extrahiert.
Die organische Phase wurde mit Wasser gewaschen, über Natriumsulfat
(Na2SO4) getrocknet,
filtriert und im Vakuum eingeengt, wodurch man die im Untertitel
genannte Verbindung (1,22 g) erhielt, die ausreichend rein für den nächsten Schritt
war.
1H-NMR (CDCl3,
400 MHz): δ 7,85
(m, 1H); 7,65 (dd, J = 1,9, 8,2 Hz, 1H); 7,41-7, 26-1,69 (m, 2H).
APCI-MS:
m/z 328 (MH+).
-
Schritt II:
-
1'-Benzyl-5-chlor-3H-spiro[2-benzofuran-1,4'-piperidin]
-
Eine
Lösung
von 1'-Benzyl-5-chlor-3H-spiro[2-benzofuran-1,4'-piperidin]-3-on
(1,1 g, 3,35 mmol) in THF (12 ml) wurde bei 0°C langsam mit einer 1 M Lösung von
Boran-Komplex in THF (7 ml, 7,0 mmol) versetzt. Nach dem Ende der
Zugabe wurde die Reaktionsmischung 30 Minuten lang bei Raumtemperatur
und dann über
Nacht unter Rückfluß gehalten,
auf 0°C
abgekühlt
und langsam mit wäßriger 6
M HCl (3,5 ml) versetzt. Die Reaktionsmischung wurde 5 Stunden lang
unter Rückfluß gehalten,
auf 0°C
abgekühlt
und durch Zugabe von wäßriger NaOH
(6 M) auf einen pH-Wert von 10 eingestellt, und das Ganze wurde
mit Essigsäureethylester
extrahiert. Die organische Phase wurde mit Wasser gewaschen, über Natriumsulfat
getrocknet (Na2SO4), filtriert
und im Vakuum eingeengt. Der Rückstand
wurde durch Flash-Chromatographie
an Kieselgel (0–30% Essigsäureethylester
in Petrolether) aufgereinigt, wodurch man die im Untertitel genannte
Verbindung (1,0 g) erhielt.
1H-NMR
(CDCl3, 400 MHz): δ 7,40-7,06 (m, 8H); 5,03 (s,
2H); 3,60 (s, 2H), 2,87 (m, 2H); 2,45 (m, 2H); 1,95 (m, 2H); 1,80
(m, 2H).
APCI-MS: m/z 314 (MH+).
-
Schritt III:
-
5-Chlor-3H-spiro[2-benzofuran-1,4'-piperidin]
-
Eine
Lösung
von 1'-Benzyl-5-chlor-3H-spiro[2-benzofuran-1,4'-piperidin] (950
mg, 3,02 mmol) in Dichlormethan (CH2Cl2) (6 ml) wurde bei 0°C langsam mit Chlorameisensäurechlorethylester
(560,6 mg, 3,92 mmol) versetzt. Nach dem Ende der Zugabe wurde die
Reaktionsmischung 25 Minuten lang bei 0°C gerührt. Die flüchtigen Bestandteile wurden
im Vakuum entfernt, und der Rückstand
wurde in Methanol (6 ml) gelöst und
40 Minuten lang unter Rückfluß gehalten.
Die flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (0–5%
Methanol in Dichlormethan, 0,2% Ammoniumhydroxid, NH4OH)
aufgereinigt, wodurch man die Titelverbindung (300 mg) erhielt und
1'-Benzyl-5-chlor-3H-spiro[2-benzofuran-1,4'-piperidin] (320
mg) zurückgewann.
1H-NMR (CD3OD, 400
MHz): δ 7,28-7,24
(m, 2H); 7,18-7,13 (m, 1H); 5,00 (s, 2H); 2,95 (m, 4H); 1,90-1,77
(m, 2H); 1,72-1,63 (m, 2H).
APCI-MS: m/z 224 (MH+).
-
Zwischenprodukt: 5-Fluor-3H-spiro[1-benzofuran-2,4'-piperidin]
-
Schritt I:
-
1'-Benzyl-5-fluor-3H-spiro[1-benzofuran-2,4'-piperidin]
-
In
eine gerührte
Suspension von Magnesiumband (763 mg) in Diethylether (7 ml) wurde
ein Iodkristall gegeben, gefolgt von 0,4 ml 2-(Brommethyl)-1,4-difluorbenzol
unter Stickstoff. Die Reaktionsmischung wurde mit einer Heißluftpistole
gestartet, und 2-(Brommethyl)-1,4-difluorbenzol (5,0 g, 24,25 mmol)
in Diethylether (7 ml) wurde so zugesetzt, daß die Mischung unter leichtem
Rückfluß bleib.
Nach dem Ende der Zugabe wurde die Reaktionsmischung 100 Minuten
unter Rückfluß gerührt und
auf Raumtemperatur abgekühlt.
Diese Reaktionsmischung wurde unter kräftigem Rühren tropfenweise mit einer
Lösung
von 1-Benzylpiperidin-4-on (4,57 g, 24,25 mmol) in Diethylether
(12 ml) versetzt. Nach dem Ende der Zugabe bildete sich ein weißer Kuchen, der über Nacht
bei Raumtemperatur belassen wurde. Der Kuchen wurde durch Behandeln
mit einer wäßrigen Lösung von
Ammoniumchlorid (NH4Cl) hydrolysiert und
dann mit Diethylether extrahiert. Die organische Phase wurde mit
Wasser gewaschen, über
Natriumsulfat getrocknet (Na2SO4),
filtriert und eingeengt, und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (0–1%
Methanol in Dichlormethan, 0,1% Ammoniumhydroxid, NH4OH)
aufgereinigt, wodurch man das Zwischenprodukt 1-Benzyl-4-(2,5-difluorbenzyl)piperidin-4-ol
(2,74 g) erhielt, das eine große
Menge an Verunreinigungen erhielt. Eine Suspension von Natriumhydrid
(NaH) (55%, 1,12 g, 26,0 mmol) in Toluol (10 ml) wurde langsam mit
einer Lösung
von 1-Benzyl-4-(2,5-difluorbenzyl)piperidin-4-ol in Toluol (15 ml)
versetzt. Nach dem Ende der Zugabe wurde die Reaktionsmischung bei
110°C (in
einem vorgeheizten Ölbad)
gerührt,
nach 5 Minuten wurde mit Dimethylformamid (9 ml) versetzt und es
wurde weitere 2 Stunden lang unter Rückfluß gerührt. Die Reaktionsmischung
wurde auf Raumtemperatur abgekühlt,
mit Wasser (20 ml) versetzt und mit Essigsäureethylester extrahiert. Die
organische Phase wurde über
Natriumsulfat (Na2SO4)
getrocknet, filtriert und eingeengt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (0–1,5%
Methanol in Dichlormethan, 0,1% Ammoniumhydroxid, NH4OH)
aufgereinigt, wodurch man die im Untertitel genannte Verbindung
(190 mg) erhielt.
1H-NMR (CDCl3, 400 MHz): δ 7,39-7,26 (m, 5H); 6,88-6,76
(m, 2H); 6,67 (dd, J = 4,2, 8,7 Hz, 1H); 3,59 (s, 2H); 2,99 (s,
2H); 2,68-2,47 (m, 4H); 2,03-1,94 8 M, 2H); 1,86-1,76 (m, 2H).
APCI-MS:
m/z 298 (MH+)
-
Schritt II:
-
5-Fluor-3H-spiro[1-benzofuran-2,4'-piperidin]
-
Chlorameisensäureethylester
(65,6 mg, 0,604 mmol) wurde zu einer Lösung von 1'-Benzyl-5-fluor-3H-spiro[1-benzofuran-2,4'-piperidin] (150
mg, 0,504 mmol) in Toluol (2 ml) gegeben, und die Reaktionsmischung
wurde über
Nacht unter Rückfluß erhitzt.
Die Reaktionsmischung wurde auf Raumtemperatur abgekühlt, durch
Zugabe von Toluol verdünnt
und nacheinander mit wäßrigem Natriumhydrogencarbonat
(NaHCO3) und Wasser gewaschen. Die organische
Phase wurde über
Natriumsulfat (Na2SO4)
getrocknet, filtriert und im Vakuum eingeengt. Der Rückstand
wurde in Ethanol (3,5 ml) gelöst,
wäßriges Kaliumhydroxid
(KOH) (800 mg KOH in 0,8 ml Wasser) wurde zugesetzt, die Reaktionsmischung
wurde über
Nacht bei Rückflußtemperatur gerührt, auf
Raumtemperatur abgekühlt
und mit Essigsäureethylester
extrahiert. Die organische Phase wurde gut mit Wasser gewaschen, über Natriumsulfat
(Na2SO4) getrocknet,
filtriert und eingeengt. Der Rückstand wurde
durch HPLC (10% Acetonitril (CH3CN) –55% CH3CN in Wasser mit 0,1% Ammoniumhydroxid (NH4OH)) aufgereinigt, wodurch man die Titelverbindung
(49 mg) erhielt.
1H-NMR (CD3OD, 400 MHz): δ 6,92-6,87 (m, 1H); 6,81-6,75
(m, 1H); 6,64 (dd, J = 4,2, 8,7 Hz, 1H); 3,08-2,98 (m, 4H); 2,89-2,81
(m, 2H); 1,92-1,83 (m, 2H); 1,78-1,71 (m, 2H).
APCI-MS: m/z
208 (MH+).
-
Zwischenprodukt: 5-Chlor-3H-spiro[1-benzofuran-2,3'-pyrrolidin]
-
Schritt I:
-
1-Benzyl-3-(5-chlor-2-fluorbenzyl)pyrrolidin-3-ol
-
Eine
gerührte
Suspension von Magnesiumband (1,39 g, 57,06 mmol) in Diethylether
(10 ml) wurde unter Stickstoff mit einem Iodkristall versetzt, gefolgt
von 0,5 ml 2-(Brommethyl)-4-chlor-1-fluorbenzol. Die Reaktion wurde
mit einer Heizluftpistole gestartet, und dann wurde so mit einer
Lösung
von 2-(Brommethyl)-4-chlor-1-fluorbenzol
(12,75 g, 57,06 mmol) in Diethylether versetzt, daß ein leichter
Rückfluß aufrechterhalten
wurde. Nach dem Ende der Zugabe wurde die Reaktionsmischung 3,5
Stunden lang unter Rückfluß gerührt, auf
Raumtemperatur abgekühlt
und unter kräftigem
Rühren
tropfenweise mit einer Lösung
von 1-Benzylpyrrolidin-3-on
(10,0 g, 57,06 mmol) in Diethylether (20 ml) versetzt. Nach dem
Ende der Zugabe wurde die Reaktionsmischung über Nacht bei Raumtemperatur
belassen. Die Reaktionsmischung wurde mit einer wäßrigen Lösung von
Ammoniumchlorid (NH4Cl) behandelt und mit
Essigsäureethylester
extrahiert. Die organische Phase wurde mit Wasser gewaschen, über Natriumsulfat
(Na2SO4) getrocknet,
filtriert und eingeengt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (0–2%
Methanol in Dichlormethan, 0,2% Ammoniumhydroxid, NH4OH)
aufgereinigt, wodurch man die im Untertitel genannte Verbindung
(650 mg) erhielt.
1H-NMR (CDCl3, 400 MHz): δ 7,39-7,23 (m, 6H); 7,21-7,15
(m, 1H); 6,98 (t, J = 9,0 Hz, 1H); 3,68 (d, J = 13,0 Hz, 1H); 3,63
(d, J = 13,0 Hz, 1H); 3,01-2,89 (m, 3H); 2,65 (d, J = 9,5 Hz, 1H);
2,42-2,34 (m, 2H); 2,07-1,98 (m, 1H); 1,88-1,75 (m, 1H); 1,64 (bs,
1H).
APCI-MS: m/z 320 (MH+).
-
Schritt II:
-
1'-Benzyl-5-chlor-3H-spiro[1-benzofuran-2‚3'-pyrrolidin]
-
Eine
Suspension von Natriumhydrid (NaH) (55%, 612 mg, 14,0 mmol) in Toluol
(10 ml) wurde mit einer Lösung
von 1-Benzyl-3-(5-chlor-2-fluorbenzyl)pyrrolidin-3-ol (1,3 g, 4,06
mmol) in Toluol (20 ml) versetzt, und die Reaktionsmischung wurde
unter Rückfluß gerührt und
nach 5 Minuten wurde mit Dimethylformamid (10 ml) versetzt, und
die Reaktionsmischung wurde 90 Minuten lang unter Rückfluß erhitzt,
auf Raumtemperatur abgekühlt,
mit Wasser (20 ml) versetzt und mit Essigsäureethylester extrahiert. Die
organische Phase wurde über Natriumsulfat
getrocknet (Na2SO4),
filtriert und eingeengt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (0–1,5%
Methanol in Dichlormethan, 0,2% Ammoniumhydroxid, NH4OH)
aufgereinigt, wodurch man die im Untertitel genannte Verbindung
(560 mg) erhielt.
1H-NMR (CD3OD, 400 MHz): δ 7,39-7,24 (m, 5H); 7,10 (s,
1H); 7,06 (dd, J = 2,3, 8,5 Hz, 1H); 6,68 (d, J = 8,4 Hz, 1H); 3,73
(d, J = 13,0 Hz, 1H); 3,70 (d, J = 13,0 Hz, 1H); 3,24 (d, J = 16,0
Hz, 1H); 3,20 (d, J = 16,0 Hz, 1H); 2,99 (d, J = 10,4 Hz, 1H); 2,95-2,88
(m, 1H); 2,74-2,64 (m, 2H); 2,43-2,34 (m, 1H); 2,11-2,02 (m, 1H).
APCI-MS:
m/z 300 (MH+).
-
Schritt III:
-
5-Chlor-3H-spiro[1-benzofuran-2,3'-pyrrolidin]
-
Die
experimentelle Vorschrift ist die gleiche wie oben für das entsprechende
Piperidinderivat beschrieben, wobei 1'-Benzyl-5-chlor-3H-spiro[1-benzofuran-2,3'-pyrrolidin] (555 mg, 1,85 mmol), Chlorameisensäureethylester
(261 mg, 2,4 mmol), Toluol (5 ml), Kaliumhydroxid (KOH) (3,0 g),
Wasser (3 ml) und Ethanol (6 ml) verwendet wurden und man die Titelverbindung
(240 mg) nach Flash-Chromatographie an Kieselgel (0–2% Methanol
in Dichlormethan, 0,2% Ammoniumhydroxid, NH4OH)
erhielt.
1H-NMR (CDCl3,
400 MHz): δ 7,13
(s, 1H); 7,08 (dd, J = 2,3, 8,5 Hz, 1H); 6,65 (d, J = 8,5 Hz, 1H);
3,32-3,16 (m, 4H); 3,07 (ddd, J = 4,8, 9,1, 11,2 Hz, 1H); 2,80 (d,
J = 12,3 Hz, 1H); 2,33-2,24 (m, 1H); 1,93 (ddd, J = 7,3, 9,1, 13,7
Hz, 1H).
APCI-MS: m/z 210 (MH+).
-
Beispiel 34
-
N-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxyphenyl)acetamid
-
Eine
Mischung von 5-Chlor-3H-spiro[2-benzofuran-1,4'-piperidin]
(29,3 mg, 0,131 mmol) und Essigsäure-4-(acetylamino)-3-[(2S)-oxiran-2-ylmethoxy]phenylester
(35 mg, 0,131 mmol) in Ethanol (1,5 ml) wurde über Nacht bei 80°C gerührt. Die
flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch HPLC (10–55% Acetonitril
(CH3CN) in Wasser, 0,1% Trifluoressigsäure, CF3COOH) aufgereinigt, wodurch man die Titelverbindung
(35 mg) erhielt.
1H-NMR (CD3OD, 400 MHz): δ 7,36 (m, 3H); 7,21 (d, J =
8,7 Hz, 1H); 6,50 (d, J = 2,4 Hz, 1H); 6,40 (dd, J = 2,4, 8,7 Hz,
1H); 5,10 (s, 2H); 4,48 (m, 1H); 4,05 (d, J = 4,6 Hz, 2H); 3,78-3,63
(m, 2H); 3,56-3,35 (m, 4H); 2,40-2,21 (m, 2H); 2,13 (s, 3H); 2,08-1,95
(m, 2H).
APCI-MS: m/z 447 (MH+).
-
Beispiel 35
-
N-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}phenyl)acetamid
-
Eine
Mischung von 5-Chlor-3H-spiro[2-benzofuran-1,4'-piperidin]
(35 mg, 0,156 mmol) und N-{2-[(2S)-Oxiran-2-ylmethoxy]phenyl}acetamid (32,3 mg,
0,156 mmol) in Ethanol (1,5 ml) wurde über Nacht bei 80°C gerührt. Die
flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (0–1%
Methanol in Dichlormethan, 0,1% Ammoniumhydroxid, NH4OH) aufgereinigt,
wodurch man die Titelverbindung (45 mg) erhielt.
1H-NMR
(CD3OD, 400 MHz): δ 7,99 (dd, J = 1,3, 7,9 Hz,
1H); 7,29-7,25 (m, 2H); 7,18 (d, J = 7,8 Hz, 1H); 7,12-7,01 (m,
2H); 6,96-6,91 (m, 1H); 5,00 (s, 2H); 4,25 (m, 1H); 4,13 (dd, J
= 3,2, 9,9 Hz, 1H); 3,99 (dd, J = 6,4, 9,9 Hz, 1H); 3,00-2,89 (m,
2H); 2,67-2,50 (m, 4H); 2,20 (s, 3H); 2,08-1,96 (m, 2H); 1,73 (m,
2H).
APCI-MS: m/z 431 (MH+).
-
Beispiel 36
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-methylbenzamid
-
Schritt I:
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]-N-methylbenzamid
-
Eine
Mischung von 5-Chlor-3H-spiro[2-benzofuran-1,4'-piperidin]
(26 mg, 0,116 mmol) und 4-[(4-Methoxybenzyl)oxy]-N-methyl-2-[(2S)-oxiran-2-ylmethoxy]-benzamid (40 mg,
0,116 mmol) in Ethanol (2 ml) wurde über Nacht bei 80°C gerührt. Die
flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (0–1%
Methanol in Dichlormethan, 0,1% Ammoniumhydroxid, NH4OH)
aufgereinigt, wodurch man die im Untertitel genannte Verbindung
(50 mg) erhielt.
1H-NMR (CDCl3, 400 MHz): δ 78,18 (d, J = 8,8 Hz, 1H);
8,14 (m, 1H); 7,37 (d, J = 8,7 Hz, 2H); 7,28 (m, 2H); 7,22 (s, 1H);
7,09 (d, J = 8,0 Hz, 1H); 6,97-6,92 (m, 2H); 6,71 (dd, J = 2,3,
8,8 Hz, 1H); 6,52 (d, J = 2,3 Hz, 1H); 5,08 (s, 2H); 5,05 (s, 2H);
4,25-4,15 (m, 2H); 3,85 (s, 3H); 3,00 (m, 4H); 2,88-2,75 (m, 2H);
2,66-2,46 (m, 3H); 2,06-1,90 (m, 2H); 1,82 (d, J = 12,9 Hz, 2H).
APCI-MS:
m/z 567 (MH+).
-
Schritt II:
-
2-{((2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-methylbenzamid
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]-N-methylbenzamid
(45 mg, 0,079 mmol) wurde bei Raumtemperatur 25 Minuten lang mit
10% Trifluoressigsäure
(CF3COOH) in Dichlormethan (CH2Cl2) (3 ml) behandelt. Die flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch HPLC (10–45% Acetonitril
(CH3CN) in Wasser, 0,1% Ammoniumhydroxid,
NH4OH) aufgereinigt, wodurch man die Titelverbindung
(17 mg) erhielt.
1H-NMR (CD3OD, 400 MHz): δ 7,82 (d, J = 8,7 Hz, 1H); 7,30-7,25 (m, 2H); 7,18
(d, J = 7,9 Hz, 1H); 6,55 (d, J = 2,2 Hz, 1H); 6,48 (dd, J = 2,2,
8,7 Hz, 1H); 5,05 (s, 2H); 4,26-4,19 (m, 2H); 4,09-4,04 (m, 1H);
2,98-2,87 (m, 5H); 2,64-2,50 (m, 4H); 2,09-1,97 (m, 2H); 1,73 (d,
J = 13,2 Hz, 2H).
APCI-MS: m/z 447 (MH+).
-
Beispiel 37
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxy-2-methoxypropyl]oxy)-N-cyclopropyl-4-hydroxybenzamid
-
Schritt I:
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxy-2-methylpropyl]oxy}-N-cyclopropyl-4[(4-methoxybenzyl)oxy]benzamid
-
Eine
Mischung von 5-Chlor-3H-spiro[2-benzofuran-1,4'-piperidin]
(40 mg, 0,178 mmol) und N-Cyclopropyl-4-[(4-methoxybenzyl)oxy]-2-{[(2S)-2-methyloxiran-2-yl]- methoxy}benzamid
(68 mg, 0,178 mmol) in Ethanol (2 ml) wurde 6 Stunden lang bei 80°C gerührt. Die
flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (0–0,9%
Methanol in Dichlormethan, 0,1% Ammoniumhydroxid, NH4OH)
aufgereinigt, wodurch man die im Untertitel genannte Verbindung
(45 mg) erhielt.
1H-NMR (CDCl3, 400 MHz): δ 8,21 (bs, 1H); 7,99 (d, J =
8,7 Hz, 1H); 7,36 (d, J = 8,7 Hz, 2H) 7,27 (m, 1H); 7,20 (s, 1H);
7,03 (d, J = 8,0 Hz, 1H); 6,92 (m, 2H); 6,70 (dd, J = 2,3, 8,8 Hz,
1H); 6,50 (d, J = 2,3 Hz, 1H); 5,03 (s, 2H); 5,01 (s, 2H); 3,86
(s, 2H); 2,85 (s, 3H); 3,05 (m, 1H); 2,91-2,80 (m, 3H); 2,75 (m,
1H); 2,67 (d, J = 13,9 Hz, 1H); 2,50 (d, J = 13,9 Hz, 1H); 1,95
(m, 2H); 1,75 (m, 2H); 1,30 (s, 3H); 0,83 (m, 2H); 0,62 (m, 2H).
APCI-MS:
m/z 607 (MH+).
-
Schritt II:
-
2-([(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxy-2-methoxypropyl]oxy}-N-cyclopropyl-4-hydroxybenzamid
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxy-2-methylpropyl]oxy}-N-cyclopropyl-4-[(4-methoxybenzyl)oxy]benzamid
(40 mg, 0,065 mmol) wurde bei Raumtemperatur 25 Minuten lang mit 10%iger
Trifluoressigsäure
(CF3COOH) (3 ml) behandelt. Die flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch HPLC (10–55% Acetonitril
(CH3CN) in Wasser, 0,1% Ammoniumhydroxid,
NH4OH) aufgereinigt, wodurch man die Titelverbindung
(30 mg) erhielt.
1H-NMR (CD3OD, 400 MHz): δ 7,84 (d, J = 8,4 Hz, 1H); 7,25
(m, 2H); 7,16 (d, J = 7,6 Hz, 1H); 6,45 (m, 2H); 5,00 (s, 2H); 4,11
(d, J = 9,0 Hz, 1H); 3,93 (d, J = 9,0 Hz, 1H); 2,93 (m, 1H); 2,88
(m, 2H); 2,74-2,49 (m, 4H); 1,99 (m, 2H); 1,62 (m, 2H); 1,31 (s,
3H); 0,79 (m, 2H); 0,65 (m, 2H).
APCI-MS: m/z 487 (MH+).
-
Beispiel 38
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-(2-hydroxyethyl)benzamid
-
Schritt I:
-
4-[(4-Methoxybenzyl)oxy]-2-[(2S)-oxiran-2-ylmethoxy]benzoesäuremethylester
-
Eine
Mischung von 3-Nitrobenzolsulfonsäure-2(S)-oxiran-2-ylmethylester (518
mg, 2,0 mmol), 2-Hydroxy-4-[(4-methoxybenzyl)oxy]benzoesäuremethylester
(576,6 mg, 2,0 mmol) und Caesiumcarbonat (Cs2CO3) (812,5 mg, 2,5 mmol) in Dimethylformamid
(10 ml) wurde bei Raumtemperatur über Nacht gerührt. Die
Reaktionsmischung wurde zwischen Essigsäureethylester und Wasser verteilt.
Die organische Phase wurde über
Natriumsulfat, Na2SO4,
getrocknet, filtriert und im Vakuum eingeengt, und der Rückstand
wurde durch Flash-Chromatographie
an Kieselgel (Essigsäureethylester
0–30%
in Petrolether) aufgereinigt, wodurch man die im Untertitel genannte
Verbindung (600 mg) erhielt.
1H-NMR
(CDCl3, 400 MHz): δ 7,87 (d, J = 8,7 Hz, 1H); 7,39-7,34 (m, 2H); 6,97-6,92
(m, 2H); 6,61 (dd, J = 2,4, 8,7 Hz, 1H); 6,59 (d, J = 2,2 Hz, 1H);
5,04 (s, 2H); 4,31 (dd, J = 2,9, 11,1 Hz, 1H); 4,07 (dd, J = 4,8,
11,1 Hz, 1H); 3,88 (s, 3H); 3,85 (s, 3H); 3,40 (m, 1H); 2,92 (m,
2H).
APCI-MS: m/z 345 (MH+).
-
Schritt II:
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoesäuremethylester
-
Eine
Mischung von 5-Chlor-3H-spiro[1-benzofuran-2,4'-piperidin]
(150 mg, 0,67 mmol) und 4-[(4-Methoxybenzyl)oxy]-2-[(2S)-oxiran-2-ylmethoxy]benzoesäuremethylester
(230,5 mg, 0,67 mmol) in Ethanol (3 ml) wurde über Nacht bei 80°C gerührt. Die
flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (0–3%
Methanol in Dichlormethan) aufgereinigt, wodurch man die im Untertitel
genannte Verbindung (370 mg) erhielt.
1H-NMR
(CDCl3, 400 MHz): δ 7,87 (d, J = 8,8 Hz, 1H); 7,40-7,35 (m, 2H); 7,12
(m, 1H); 7,07 (dd, J = 2,2, 8,4 Hz, 1H); 6,98-6,93 (m, 2H); 6,69
(d, J = 8,4 Hz, 1H); 6,63 (d, J = 2,2 Hz, 1H); 6,60 (s, 1H); 5,06
(s, 2H); 4,19 (m, 2H); 4,03 (m, 1H); 3,89 (s, 3H); 3,85 (s, 3H);
3,00 (s, 2H); 2,80 (m, 1H); 2,73-2,58 (m, 5H); 2,00 (m, 2H); 1,82
(m, 2H).
APCI-MS: m/z 568 (MH+).
-
Schritt III:
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-N-(2-hydroxyethyl)-4-[(4-methoxybenzyl)oxy]benzamid
-
Eine
Mischung von 2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoesäuremethylester
(60 mg, 0,105 mmol) und 2-Aminoethanol (0,256 ml, 4,2 mmol) in Methanol
(2 ml) wurde 72 Stunden lang unter Rückfluß erhitzt. Die flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie an
Kieselgel (0–3%
Methanol in Dichlormethan, 0,2% Ammoniumhydroxid, NH4OH)
aufgereinigt, wodurch man die im Untertitel genannte Verbindung
(30 mg) erhielt.
1H-NMR (CDCl3, 400 MHz): δ 8,49 (t, J = 5,4 Hz, 1H); 8,17
(d, J = 8,8 Hz, 1H); 7,40-7,35 (m, 2H); 7,12 (s, 1H); 7,09 (dd,
J = 2,2, 8,4 Hz, 1H); 6,98-6,93 (m, 2H); 6,72 (dd, J = 2,2, 8,8
Hz, 1H); 6,69 (d, J = 8,5 Hz, 1H); 6,55 (d, J = 2,2 Hz, 1H); 5,06
(s, 2H); 4,21 (m, 2H); 3,94 (dd, J = 7,2, 10,1 Hz, 1H); 3,85 (s,
3H); 3,83 (d, J = 4,8 Hz, 2H); 3,70 (m, 1H); 3,60 (m, 1H); 3,00
(s, 2H); 2,91-2,76 (m, 2H); 2,68-2,53 (m, 4H); 2,00 (m, 2H); 1,80
(m, 2H).
APCI-MS: m/z 597 (MH+).
-
Schritt IV:
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-(2-hydroxyethyl)benzamid
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-N-(2-hydroxyethyl)-4-[(4-methoxybenzyl)oxy]benzamid
(27 mg, 0,045 mmol) wurde bei Raumtemperatur 30 Minuten lang mit
10% Trifluoressigsäure
(CF3COOH) in Dichlormethan (CH2Cl2) (3 ml) behandelt. Die flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (0–4%
Methanol in Dichlormethan, Ammoniumhydroxid, 0,2% NH4OH)
aufgereinigt, wodurch man die Titelverbindung (16 mg) erhielt.
1H-NMR (CD3OD, 400
MHz): δ 7,85
(d, J = 8,6 Hz, 1H); 7,13 (m, 1H); 7,19 (dd, J = 2,4, 8,5 Hz, 1H);
6,65 (d, J = 8,5 Hz, 1H); 6,52 (d, J = 2,2 Hz, 1H); 6,49 (dd, J
= 2,2, 8,6 Hz, 1H); 4,27-4,17 (m, 2H); 4,06 (dd, J = 5,9, 9,4 Hz,
1H); 3,73 (t, J = 5,6 Hz, 2H); 3,53 (m, 2H); 3,00 (s, 2H); 2,70
(m, 4H); 2,62 (d, J = 6,4 Hz, 2H); 1,95 (m, 2H); 1,84 (m, 2H).
APCI-MS:
m/z 477 (MH+).
-
Beispiel 39
-
N-(2-Aminoethyl)-2-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzamid
-
Schritt I:
-
N-(2-Aminoethyl)-2-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzamid
-
Eine
Mischung von 2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoesäure (50
mg, 0,084 mmol) und N,N-Carbonyldiimidazol
(14 mg, 0,084 mmol) in Dimethylformamid (3 ml) wurde 1 Stunde lang
bei Raumtemperatur gerührt.
Anschließend
wurde mit Ethylendiamin (11 mg, 0,168 mmol) versetzt, und die Reaktionsmischung
wurde über
Nacht bei Raumtemperatur gerührt.
Die Reaktionsmischung wurde zwischen Essigsäureethylester und Wasser verteilt,
die organische Phase wurde über
Natriumsulfat, Na2SO4,
getrocknet, filtriert und im Vakuum eingeengt und der Rückstand
wurde durch Flash-Chromatographie an Kieselgel (0–3% Methanol
in Dichlormethan, Ammoniumhydroxid, 0,2% NH4OH)
aufgereinigt, wodurch man die im Untertitel genannte Verbindung
(22 mg) erhielt.
1H-NMR (CD3OD, 400 MHz): δ 7,93 (d, J = 8,9 Hz, 1H); 7,45
(m, 2H); 7,12 (s, 1H); 7,04 (dd, J = 2,3, 8,6 Hz, 1H); 6,95-6,90
(m, 2H); 6,73 (s, 1H); 6,70 (d, J = 2,2 Hz, 1H); 6,64 (d, J = 8,5
Hz, 1H); 5,08 (s, 2H); 4,27 (dd, J = 2,7, 9,7 Hz, 1H); 4,23-4,15
(m, 1H); 4,05 (dd, J = 6,6, 9,8 Hz, 1H); 3,80 (s, 3H); 3,48 (t,
J = 5,9 Hz, 2H); 2,96 (s, 2H); 2,86 (t, J = 6,1 Hz, 2H); 2,68 (m,
4H); 2,56 (d, J = 6,4 Hz, 2H); 1,90 (m, 2H); 1,80 (m, 2H)
APCI-MS:
m/z 596 (MH+).
-
Schritt II:
-
N-(2-Aminoethyl)-2-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzamid
-
N-(2-Aminoethyl)-2-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzamid
((22 mg, 0,037 mmol) wurde bei Raumtemperatur 20 Minuten lang mit
10% Trifluoressigsäure
(CF3COOH) in Dichlormethan (2 ml) behandelt.
Die flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch HPLC (10–60% Acetonitril
(CH3CN) in Wasser, 0,1% Ammoniumhydroxid,
NH4OH) aufgereinigt, wodurch man die Titelverbindung
(8 mg) erhielt.
1H-NMR (CD3OD,
400 MHz): δ 7,83
(d, J = 8,6 Hz, 1H); 7,14 (m, 1H); 7,04 (dd, J = 2,2, 8,4 Hz, 1H);
6,65 (d, J = 8,4 Hz, 1H); 6,50 (d, J = 2,1 Hz, 1H); 6,47 (dd, J
= 2,2, 8,6 Hz, 1H); 4,27-4,19 (m, 2H); 4,04 (m, 1H); 3,50 (t, J
= 6,0 Hz, 2H); 3,02 (s, 2H); 2,90 (t, J = 6,0 Hz, 2H); 2,69 (m,
4H); 2,60 (d, J = 6,2 Hz, 2H); 1,94 (m, 2H); 1,84 (m, 2H).
APCI-MS:
m/z 476 (MH+).
-
Beispiel 40
-
2-{[(2S)-3-(5-Fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-methylbenzamid
-
Schritt I:
-
2-{[(2S)-3-(5-Fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]-N-methylbenzamid
-
Eine
Mischung von 5-Fluor-3H-spiro[1-benzofuran-2,4'-piperidin]
(20 mg, 0,096 mmol) und 4-[(4-Methoxybenzyl)oxy]-N-methyl-2-[(2S)-oxiran-2-ylmethoxy]-benzamid (34,3 mg,
0,099 mmol) in Ethanol (2 ml) wurde über Nacht bei 80°C gerührt. Die
flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (0–0,8%
Methanol in Dichlormethan, 0,1% Ammoniumhydroxid, NH4OH)
aufgereinigt, wodurch man die im Untertitel genannte Verbindung
(36 mg) erhielt.
1H-NMR (CDCl3, 400 MHz): δ 8,16 (d, J = 8,7 Hz, 1H); 8,10
(m, 1H); 7,36 (m, 2H); 6,96-6,91 (m, 2H); 6,89-6,77 (m, 2H); 7,72-6,64
(m, 2H); 6,54 (d, J = 2,3 Hz, 1H); 5,00 (s, 2H); 4,20-4,10 (m, 2H);
3,96 (dd, J = 5,4, 9,4 Hz, 1H); 3,83 (s, 3H); 3,01 (s, 3H); 3,00
(s, 2H); 2,90 (m, 1H); 2,80 (m, 1H); 2,64-2,50 (m, 4H); 2,00 (m,
2H); 1,83 (m, 2H).
APCI-MS: m/z 551 (MH+).
-
Schritt II:
-
2-{[(2S)-3-(5-Fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-methylbenzamid
-
2-{[(2S)-3-(5-Fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]-N-methylbenzamid
(32 mg, 0,058 mmol) wurde bei Raumtemperatur 20 Minuten lang mit
10% Trifluoressigsäure
(CF3COOH) in Dichlormethan (2,5 ml) behandelt.
Die flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch HPLC (10–50% Acetonitril
(CH3CN) in Wasser, 0,1% Ammoniumhydroxid,
NH4OH) aufgereinigt, wodurch man die Titelverbindung
(11 mg) erhielt.
1H-NMR (CDCl3, 400 MHz): δ 7,82 (d, J = 8,6 Hz, 1H); 6,50
(dd, J = 2,7, 8,1 Hz, 1H); 6,81-6,74 (m, 1H); 6,62 (dd, J = 4,2,
8,7 Hz, 1H); 6,52 (d, J = 2,2 Hz, 1H); 6,48 (dd, J = 2,2, 8,6 Hz,
1H); 4,24-4,17 (m, 2H); 4,08-4,02 (m, 1H); 3,01 (s, 2H); 2,92 (s,
3H); 2,77-2,63 (m, 4H); 2,60 (d, J = 6,2 Hz, 2H); 1,94 (m, 2H);
1,84 (m, 2H).
APCI-MS: m/z 431 (MH+).
-
Beispiel 41
-
N-(2-{[(2S)-3-(5-Fluor-1'H,3H-spiro[-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxyphenyl)acetamid
-
Eine
Mischung von 5-Fluor-3H-spiro[1-benzofuran-2,4'-piperidin]
(20 mg, 0,096 mmol) und Essigsäure-4-(acetylamino)-3-[(2S)-oxiran-2-ylmethoxy]phenylester
(25,5 mg, 0,096 mmol) in Ethanol (2 ml) wurde über das Wochenende bei 80°C gerührt. Die
flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch HPLC (10–35% Acetonitril
(CH3CN) in Wasser, 0,1% Ammoniumhydroxid,
NH4OH) aufgereinigt, wodurch man die Titelverbindung
(14 mg) erhielt.
1H-NMR (CD3OD, 400 MHz): δ 7,57 (d, J = 8,7 Hz, 1H); 6,90
(m, 1H); 6,81-6,74 (m, 1H); 6,63 (dd, J = 4,2, 8,7 Hz, 1H); 6,48
(d, J = 2,5 Hz, 1H); 6,36 (dd, J = 2,6, 8,7 Hz, 1H); 4,18 (m, 1H);
4,05 (dd, J = 3,4, 9,8 Hz, 1H); 3,93 (dd, J = 6,2, 9,8 Hz, 1H);
3,01 (s, 2H); 2,70 (m, 4H); 2,61 (t, J = 7,0 Hz, 2H); 2,14 (s, 3H);
1,96 (m, 2H); 1,85 (m, 2H).
APCI-MS: m/z 431 (MH+).
-
Beispiel 42
-
N-(2-{[(2S)-3-(5-Fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}phenyl)acetamid
-
Eine
Mischung von 5-Fluor-3H-spiro[1-benzofuran-2,4'-piperidin]
(8 mg, 0,038 mmol) und N-{2-[(2S)-Oxiran-2-ylmethoxy]phenyl}acetamid (8 mg, 0,038
mmol) in Ethanol (1,5 ml) wurde über
Nacht bei 80°C
gerührt.
Die flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch HPLC (10–70% Acetonitril
(CH3CN) in Wasser, 0,1% Ammoniumhydroxid,
NH4OH) aufgereinigt, wodurch man die Titelverbindung
(11 mg) erhielt.
1H-NMR (CD3OD, 400 MHz): δ 7,99 (dd, J = 1,5, 8,1 Hz,
1H); 7,08 (m, 1H); 7,03 (m, 1H); 6,94 (m, 1H); 6,90 (m, 1H); 6,77
(m, 1H); 6,63 (dd, J = 4,2, 8,8 Hz, 1H); 4,19 (m, 1H); 4,12 (dd,
J = 3,2, 9,9 Hz, 1H); 3,98 (dd, J = 6,4, 9,9 Hz, 1H); 3,05 (s, 2H);
2,70 (m, 4H); 2,62 (m, 2H); 2,19 (s, 3H); 1,94 (m, 2H); 1,85 (m,
2H).
APCI-MS: m/z 415 (MH+)
-
Beispiel 43
-
N-(2-({(2S)-3[(2S)-5-Chlor-1'H,3H-spiro[1-benzofuran-2,3'-pyrrolidin]-1'-yl]-2-hydroxypropyl}oxy)phenyl]-acetamid
-
Eine
Mischung von 5-Chlor-3H-spiro[1-benzofuran-2,3'-pyrrolidin]
(34,5 mg, 0,167 mmol) und N-{2-[(2S)-Oxiran-2-ylmethoxy]phenyl}acetamid (35
mg, 0,167 mmol) in Ethanol (1,5 ml) wurde über Nacht bei 80°C gerührt. Die
flüchtigen
Bestandteile wurden im Vakuum entfernt, und der Rückstand
wurde durch Flash-Chromatographie an Kieselgel (0–1% Methanol
(CH3OH) in Dichlormethan (CH2Cl2), 0,2% Ammoniumhydroxid, NH4OH)
aufgereinigt, wodurch man eine Mischung von zwei Isomeren (55 mg)
erhielt. Diese Mischung wurde einer chiralen HPLC unterzogen, wodurch
man die Titelverbindung (17 mg) und das andere Isomer (14 mg) erhielt.
1H-NMR (CD3OD, 400
MHz): δ 7,99
(dd, J = 1,4, 8,0 Hz, 1H); 7,15 (m, 1H); 7,11-7,01 (m, 3H); 6,93
(m, 1H); 6,66 (d, J = 8,5 Hz, 1H); 4,18-4,11 (m, 2H); 3,99 (dd,
J = 7,0, 10,6 Hz, 1H); 3,25 (m, 2H); 3,11 (d, J = 10,8 Hz, 1H);
3,00 (m, 1H); 2,86-2,69 (m, 4H); 2,33-2,25 (m, 1H); 2,18 (s, 3H);
2,13-2,05 (m, 1H).
APCI-MS: m/z 417 (MH+).
-
Beispiel 44
-
N-[2-({(2S)-3[(2R)-5-Chlor-1'H,3H-spiro[1-benzofuran-2,3'-pyrrolidin]-1'-yl]-2-hydroxypropyl}oxy)phenyl]-acetamid
-
- 1H-NMR (CD3OD,
400 MHz): δ 7,99
(dd, J = 1,4, 8,0 Hz, 1H); 7,15 (m, 1H); 7,11-7,01 (m, 3H); 6,93
(m, 1H); 6,66 (d, J = 8,5 Hz, 1H); 4,18-4,11 (m, 2H); 3,99 (dd,
J = 7,0, 10,6 Hz, 1H); 3,25 (m, 2H); 3,11 (d, J = 10,8 Hz, 1H); 3,00
(m, 1H); 2,86-2,69 (m, 4H); 2,33-2,25 (m, 1H); 2,18 (s, 3H); 2,13-2,05
(m, 1H).
- APCI-MS: m/z 417 (MH+).
-
Beispiel 45
-
N-[2-({(2S)-3-[(2S)-5-Chlor-1'H,3H-spiro[1-benzofuran-2,3'-pyrrolidin]-1'-yl]-2-hydroxypropyl}oxy)-4-methoxyphenyl]acetamid
-
Eine
Mischung von 5-Chlor-3H-spiro[1-benzofuran-2,3'-pyrrolidin]
(60 mg, 0,286 mmol) und N-{4-Methoxy-2-[(2S)-oxiran-2-ylmethoxy]phenyl}acetamid
(68 mg, 0,286 mmol) in Ethanol (2 ml) wurde über Nacht bei 80°C gerührt. Die
flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie an
Kieselgel (0–1%
Methanol (CH3OH) in Dichlormethan (CH2Cl2), 0,2% Ammoniumhydroxid,
NH4OH) aufgereinigt, wodurch man eine Mischung
von zwei Isomeren erhielt, die einer chiralen HPLC unterzogen wurde,
wodurch man die Titelverbindung (35 mg) und das andere Isomer (35
mg) erhielt.
1H-NMR (CD3OD,
400 MHz): δ 7,73
(d, J = 8,8 Hz, 1H); 7,14 (m, 1H); 7,04 (dd, J = 2,2, 8,4 Hz, 1H);
6,65 (d, J = 8,5 Hz, 1H); 6,60 (d, J = 2,5 Hz, 1H); 6,49 (dd, J
= 2,6, 8,8 Hz, 1H); 4,15-4,06 (m, 2H); 3,96 (dd, J = 6,2, 9,8 Hz,
1H); 3,79 (s, 3H); 3,25 (m, 2H); 3,11 (dd, J = 10,7, 15,9 Hz, 1H);
2,99 (m, 1H); 2,85-2,64 (m, 4H); 2,25 (m, 1H); 2,13 (s, 3H); 2,08
(m, 1H).
APCI-MS: m/z 447 (MH+).
-
Beispiel 46
-
N-[2-({(2S)-3-[(2R)-5-Chlor-1'H,3H-spiro[1-benzofuran-2,3'-pyrrolidin]-1'-yl]-2-hydroxypropyl}oxy)-4-methoxyphenyl]acetamid
-
- 1H-NMR (CD3OD,
400 MHz): δ 7,73
(d, J = 8,8 Hz, 1H); 7,14 (m, 1H); 7,04 (dd, J = 2,2, 8,4 Hz, 1H);
6,65 (d, J = 8,5 Hz, 1H); 6,60 (d, J = 2,5 Hz, 1H); 6,49 (dd, J
= 2,6, 8,8 Hz, 1H); 4,15-4,06 (m, 2H); 3,96 (dd, J = 6,2, 9,8 Hz,
1H); 3,79 (s, 3H); 3,25 (m, 2H); 3,11 (dd, J = 10,7, 15,9 Hz, 1H);
2,99 (m, 1H); 2,85-2,64 (m, 4H); 2,25 (m, 1H); 2,13 (s, 3H); 2,08
(m, 1H).
- APCI-MS: m/z 447 (MH+).
-
Beispiel 47
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,3'-pyrrolidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-methylbenzamid
-
Schritt I:
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,3'-pyrrolidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]-N-methylbenzamid
-
Eine
Mischung von 5-Chlor-3H-spiro[1-benzofuran-2,3'-pyrrolidin]
(80 mg, 0,381 mmol) und 4-[(4-Methoxybenzyl)oxy]-N-methyl-2-[(2S)-oxiran-2-ylmethoxy]-benzamid (130,8 mg,
0,381 mmol) in Ethanol (3 ml) wurde über Nacht bei 80°C gerührt. Die
flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (0–1%
Methanol in Dichlormethan, 0,2% Ammoniumhydroxid, NH4OH)
aufgereinigt, wodurch man die im Untertitel genannte Verbindung
(165 mg) erhielt.
1H-NMR (CDCl3, 400 MHz): δ 8,15 (d, J = 8,8 Hz, 1H); 8,04
(m, 1H); 7,36 (m, 2H); 7,13 (breit, s, 1H); 7,09 (m, 1H); 6,93 (m,
2H); 6,72-6,66 (m, 2H); 6,54 (d, J = 2,2 Hz, 1H); 5,05 (s, 2H);
4,17 (dd, J = 3,2, 9,5 Hz, 1H); 4,09 (m, 1H); 3,98 (dd, J = 5,7,
9,5 Hz, 1H); 3,83 (s, 3H); 3,30-2,83 (m, 9H); 2,72 (m, 1H); 2,60
(dd, J = 3,4, 12,1 Hz, 1H); 2,34 (m, 2H); 2,08 (m, 2H).
APCI-MS:
m/z 553 (MH+).
-
Schritt II:
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,3'-pyrrolidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-methylbenzamid
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,3'-pyrrolidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]-N-methylbenzamid
(160 mg, 0,289 mmol) wurde bei Raumtemperatur 25 Minuten lang mit
10% Trifluoressigsäure
(CF3COOH) in Dichlormethan (CH2Cl2) behandelt. Die flüchtigen Bestandteile wurden
im Vakuum entfernt und der Rückstand
wurde durch Flash-Chromatographie
an Kieselgel (0–3%
Methanol (CH3OH) in Dichlormethan (CH2Cl2), 0,2% Ammoniumhydroxid,
NH4OH) aufgereinigt, wodurch man die Titelverbindung
(80 mg) erhielt.
APCI-MS: m/z 433 (MH+).
-
Beispiel 48
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoesäure(trifluoracetat)
-
Schritt I:
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl]benzoesäure
-
Eine
Lösung
von 2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoesäuremethylester
(150 mg, 0,264 mmol) in Ethanol (2 ml) wurde mit einer wäßrigen Lösung von Kaliumhydroxid
(KOH) (770 mg, KOH in 0,77 ml Wasser) versetzt, und die Reaktionsmischung
wurde über Nacht
unter Rückfluß gerührt, auf
0°C abgekühlt und
durch die Zugabe von wäßriger Salzsäure (HCl)
auf einen pH-Wert von 2,0 eingestellt. Das Ganze wurde mit Essigsäureethylester
extrahiert. Die organische Phase wurde über Natriumsulfat, Na2SO4, getrocknet,
filtriert und eingeengt, wodurch man die im Untertitel genannte
Verbindung (145 mg) erhielt.
1H-NMR
(CD3OD, 400 MHz): δ 7,78 (d, J = 8,4 Hz, 1H); 7,35
(m, 2H); 7,19 (m, 1H); 7,09 (dd, J = 2,2, 8,4 Hz, 1H); 6,93 (m,
2H); 6,75-6,65 (m, 3H); 5,09 (s, 2H); 4,40 (m, 1H); 4,24 (dd, J
= 4,0, 9,3 Hz, 1H); 4,06 (dd, J = 5,5, 9,3 Hz, 1H); 3,80 (s, 3H);
3,70-3,53 (m, 2H); 3,51-3,35 (m, 4H); 3,14 (s, 2H); 2,33 (m, 2H);
2,12 (d, J = 14,8 Hz, 2H).
APCI-MS: m/z 554 (MH+)
-
Schritt II:
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoesäure(trifluoracetat)
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl]benzoesäure (31
mg, 0,052 mmol) wurde bei Raumtemperatur 20 Minuten lang mit 10%
Trifluoressigsäure
(CF3COOH) in Dichlormethan (CH2Cl2) (2 ml) behandelt. Die flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch HPLC (10–55% Acetonitril
(CH3CN) in Wasser, 0,1% Trifluoressigsäure (CF3COOH)) aufgereinigt, wodurch man die Titelverbindung
(15 mg) erhielt.
APCI-MS: m/z 434 (MH+).
-
Beispiel 49
-
3(S)-1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)pyrrolidin-3-ol
-
Schritt I:
-
(3S)-1-{2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoyl}pyrrolidin-3-ol
-
Eine
Mischung von 2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoesäure (100
mg, 0,169 mmol) und N,N-Carbonyldiimidazol
(30 mg, 0,186 mmol) in Dimethylformamid (3 ml) wurde 1 Stunde lang
bei Raumtemperatur gerührt.
Anschließend
wurde mit (3S)-Pyrrolidin-3-ol (76,3 mg, 0,845 mmol) versetzt, und
die Reaktionsmischung wurde über
Nacht bei Raumtemperatur gerührt.
Die Reaktionsmischung wurde zwischen Essigsäureethylester und Wasser verteilt,
die organische Phase wurde über
Natriumsulfat, Na2SO4,
getrocknet, filtriert und im Vakuum eingeengt und der Rückstand wurde
durch Flash-Chromatographie an Kieselgel (0–2,5% Methanol in Dichlormethan,
0,2% Ammoniumhydroxid, NH4OH) aufgereinigt,
wodurch man die im Untertitel genannte Verbindung (55 mg) erhielt.
APCI-MS:
m/z 623 (MH+).
-
Schritt II:
-
3(S)-1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)pyrrolidin-3-ol
-
(3S)-1-{2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoyl}pyrrolidin-3-ol
(50 mg, 0,08 mmol) wurde bei Raumtemperatur 20 Minuten lang mit
10% Trifluoressigsäure
(CF3COOH) in Dichlormethan (CH2Cl2) (3 ml) behandelt. Die flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (0–4,5%
Methanol (CH3OH) in Dichlormethan (CH2Cl2), 0,2% Ammoniumhydroxid,
NH4OH) aufgereinigt, wodurch man die Titelverbindung
(25 mg) erhielt.
1H-NMR (CD3OD, 400 MHz): δ 7,13 (m, 1H); 7,08 (dd, J =
2,5, 8,2 Hz, 1H); 7,03 (dd, J = 2,3, 8,5 Hz, 1H); 6,65 (d, J = 8,4
Hz, 1H); 6,49 (m, 1H); 6,44 (m, 1H); 4,48 (m, 0, 5H); 4,35 (m, 0,5H);
4,10 (m, 1H); 4,03 (m, 1H); 3,96 (dd, J = 5,6, 9,7 Hz, 1H); 3,67
(m, 1H); 3,62-3,50 (m, 2H); 3,30 (m, 1H); 3,00 (s, 2H); 2,78-2,52
(m, 6H); 2,12-1,77 (m, 6H).
APCI-MS: m/z 503 (MH+).
-
Beispiel 50
-
3(R)-1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy)-4-hydroxybenzoyl)pyrrolidin-3-ol
-
Schritt I:
-
(3R)-1-{2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoyl}pyrrolidin-3-ol
-
Eine
Mischung von 2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoesäure (60
mg, 0,101 mmol) und N,N-Carbonyldiimidazol
(17,5 mg, 0,108 mmol) in Dimethylformamid (3 ml) wurde 1 Stunde
lang bei Raumtemperatur gerührt.
Anschließend
wurde mit (3R)-Pyrrolidin-3-ol
(47 mg, 0,540 mmol) versetzt, und die Reaktionsmischung wurde über Nacht
bei Raumtemperatur gerührt.
Die Reaktionsmischung wurde zwischen Essigsäureethylester und Wasser verteilt,
die organische Phase wurde über
Natriumsulfat getrocknet, Na2SO4,
filtriert und im Vakuum eingeengt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (0–3%
Methanol in Dichlormethan, 0,2% Ammoniumhydroxid, NH4OH)
aufgereinigt, wodurch man die im Untertitel genannte Verbindung
(64 mg) erhielt.
APCI-MS: m/z 623 (MH+).
-
Schritt II:
-
3(R)-1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)pyrrolidin-3-ol
-
(3R)-1-{2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoyl}pyrrolidin-3-ol
(60 mg, 0,096 mmol) wurde bei Raumtemperatur 20 Minuten lang mit
10% Trifluoressigsäure
(CF3COOH) in Dichlormethan (CH2Cl2) (3 ml) behandelt. Die flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (0–5%
Methanol (CH3OH) in Dichlormethan (CH2Cl2), 0,2% Ammoniumhydroxid,
NH4OH) aufgereinigt, wodurch man die Titelverbindung
(8 mg) erhielt.
1H-NMR (CD3OD,
400 MHz): δ 7,13
(m, 1H); 7,08 (dd, J = 2,5, 8,2 Hz, 1H); 7,03 (dd, J = 2,3, 8,5
Hz, 1H); 6,65 (d, J = 8,4 Hz, 1H); 6,49 (m, 1H); 6,44 (m, 1H); 4,48
(m, 0, 5H); 4,35 (m, 0, 5H); 4,10 (m, 1H); 4,03 (m, 1H); 3,96 (dd,
J = 5,6, 9,7 Hz, 1H); 3,67 (m, 1H); 3,62-3,50 (m, 2H); 3,30 (m,
1H); 3,00 (s, 2H); 2,78-2,52 (m, 6H); 2,12-1,77 (m, 6H).
APCI-MS:
m/z 503 (MH+).
-
Beispiel 51
-
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-(morpholin-4-ylcarbonyl)phenol
-
Schritt I:
-
(2S)-1-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-3-[5-[(4-methoxybenzyl)oxy]-2-(morpholin-4-ylcarbonyl)phenoxy]propan-2-ol
-
Eine
Mischung von 2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1- benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoesäure (100
mg, 0,169 mmol) und N,N-Carbonyldiimidazol
(35 mg, 0,215 mmol) in Dimethylformamid (3 ml) wurde 1 Stunde lang
bei Raumtemperatur gerührt.
Anschließend
wurde mit Morpholin (250 mg, 2,86 mmol) versetzt, und die Reaktionsmischung
wurde über
Nacht bei Raumtemperatur gerührt.
Die Reaktionsmischung wurde zwischen Essigsäureethylester und Wasser verteilt,
die organische Phase wurde über
Natriumsulfat, Na2SO4,
getrocknet, filtriert und im Vakuum eingeengt und der Rückstand
wurde durch Flash-Chromatographie an Kieselgel (0–1,5% Methanol
in Dichlormethan, 0,2% Ammoniumhydroxid, NH4OH) aufgereinigt,
wodurch man die im Untertitel genannte Verbindung (58 mg) erhielt.
APCI-MS:
m/z 623 (MH+).
-
Schritt II:
-
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-(morpholin-4-ylcarbonyl)phenol
-
(2S)-1-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-3-[5-[(4-methoxybenzyl)oxy]-2-(morpholin-4-ylcarbonyl)phenoxy]propan-2-ol
(55 mg, 0,088 mmol) wurde bei Raumtemperatur 25 Minuten lang mit
10% Trifluoressigsäure
(CF3COOH) in Dichlormethan (CH2Cl2) (3 ml) behandelt. Die flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (0–3%
Methanol (CH3OH) in Dichlormethan (CH2Cl2), 0,2% Ammoniumhydroxid,
NH4OH) aufgereinigt, wodurch man die Titelverbindung
(24 mg) erhielt.
1H-NMR (CD3OD, 400 MHz): δ 7,13 (m, 1H); 7,07-7,01 (m,
2H); 6,65 (d, J = 8,5 Hz, 1H); 6,50 (d, J = 2,1 Hz, 1H); 6,45 (dd,
J = 2,1, 8,2 Hz, 1H); 4,15-3,92 (m, 3H); 3,87-3,37 (m, 8H); 3,00 (s, 2H); 2,78-2,49
(m, 6H); 1,94 (m, 2H); 1,83 (m, 2H).
APCI-MS: m/z 503 (MH+).
-
Beispiel 52
-
2-([(2S)-3-(5-Chlor-1'H-spiro[1,3-benzodioxol-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-N-methylbenzamidtrifluoracetat
(Salz)
-
Schritt I:
-
2-Hydroxy-N-methylbenzamid
-
Eine
Lösung
von Salicylsäuremethylester
(5,16 ml, 40 mmol) in Methanol (10 ml) wurde bei 0°C tropfenweise
mit wäßrigem 40%igem
Methylamin (18,1 ml, 210 mmol) versetzt. Nach dem Ende der Zugabe
wurde die Reaktionsmischung über
Nacht bei Raumtemperatur gerührt.
Die flüchtigen
Bestandteile wurden im Vakuum entfernt, wodurch man die im Untertitel
genannte Verbindung (5,48 g) erhielt.
1H-NMR
(CD3OD, 400 MHz): δ 7,70 (dd, J = 1,5, 7,9 Hz,
1H); 7,38-7,32 (2H); 6,90-6,83 (m, 2H); 2,85 (s, 3H).
-
Schritt II:
-
N-Methyl-2-[(2S)-oxiran-2-ylmethoxy]benzamid
-
Eine
Mischung von (2S)-Oxiran-2-ylmethyl-3-nitrobenzol-sulfonat (388,5 mg,
1,50 mmol), 2-Hydroxy-N-methylbenzamid (226,5 mg, 1,50 mmol) und
Caesiumcarbonat (586 mg, 1,80 mmol) in Dimethylformamid (6 ml) wurde über Nacht
bei Raumtemperatur gerührt.
Die Reaktionsmischung wurde zwischen Essigsäureethylester und Wasser verteilt.
Die organische Phase wurde über
Natriumsulfat, Na2SO4,
getrocknet, filtriert und eingeengt. Der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (0–50%
Essigsäureethylester
in Petrolether) aufgereinigt, wodurch man die im Untertitel genannte
Verbindung (284 mg) erhielt.
1H-NMR
(CDCl3, 400 MHz): δ 8,39 (m, 1H); 7,90 (bs, 1H);
7,06-6,98 (m, 2H); 6,95-6,89 (m, 1H); 4,38 (dd, J = 2,5, 11,4 Hz,
1H); 3,98 (dd, J = 6,0, 11,4 Hz, 1H); 3,40 (m, 1H); 2,97 (t, J =
5,0 Hz, 1H); 2,81 (dd, J = 2,7, 4,8 Hz, 1H); 2,21 (s, 3H).
APCI-MS:
m/z 208 (MH+).
-
Schritt III:
-
2-{[(2S)-3-(5-Chlor-1'H-spiro[1,3-benzodioxol-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-N-methylbenzamidtrifluoracetat
(Salz)
-
Eine
Mischung von 5-Chlorspiro[1,3-benzodioxol-2,4'-piperidin]
(22,5 mg, 0,1 mmol) und N-Methyl-2-[(2S)-oxiran-2-ylmethoxy]benzamid (20,7 mg,
0,1 mmol) in Ethanol (2 ml) wurde über Nacht bei 80°C gerührt. Die
flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch präparative HPLC
(Laufmittel: [Acetonitril/Wasser + 0,1% TFA]) aufgereinigt, wodurch
man die Titelverbindung in Form eines farblosen Feststoffs (28 mg,
51%) erhielt.
1H-NMR (Aceton-d6, 400 MHz): δ 7,94 (dd, J = 7,7, 1,7 Hz,
1H), 7,46 (td, J = 7,8, 1,8 Hz, 1H), 7,15 (d, J = 8,3 Hz, 1H), 7,07
(t, J = 7,5 Hz, 1H), 6,93-6,86 (m, 3H), 4,73 (m, 1H), 4,27 (m, 2H),
3,71 (dd, J = 13,4, 2,9 Hz, 2H), 3,58 (dd, J = 13,4, 9,5 Hz, 2H),
2,92 (s, 3H), 2,55 (bs, 4H), 2,08 (m, 2H, vom Signal des Lösungsmittels überdeckt).
APCI-MS:
m/z 433 (MH+).
-
Beispiel 53
-
N-(2-{[(2S)-3-(6-Chlor-3,4-dihydro-1'H-spiro[chromen-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-phenyl)acetamidtrifluoracetat
(Salz)
-
Eine
Mischung von 6-Chlor-3,4-dihydrospiro[chromen-2,4'-piperidin]
(23,8 mg, 0,1 mmol) und N-(2-[(2S)- Oxiran-2-ylmethoxy]phenyl}acetamid (20,7
mg, 0,1 mmol) in Ethanol (3 ml) wurde über Nacht bei 80°C gerührt. Die
flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch präparative
HPLC (Laufmittel: [Acetonitril/Wasser + 0,1% TFA]) aufgereinigt,
wodurch man die Titelverbindung in Form eines farblosen Feststoffs
(40 mg, 71%) erhielt.
1H-NMR (Aceton-d6, 400 MHz): δ 8,74 (bs, 1H), 8,29 (d, J =
7,5 Hz, 1H), 7,15 (s, 1H), 7,11 (d, J = 8,8 Hz, 1H), 6,99 (d, J
= 3,8 Hz, 2H), 6,97-6,85 (m, 2H), 4,54 (m, 1H), 4,11 (m, 2H), 3,81-3,43
(m, 6H), 2,88 (t, J = 6,8 Hz, 2H), 2,24-2,09 (m, 2H), 2,13 (s, 3H),
2,08 (m, 2H, vom Signal des Lösungsmittels überdeckt),
1,95 (t, J = 6,8 Hz, 2H).
APCI-MS: m/z 445 (MH+).
-
Beispiel 54
-
N-(2-{[(2S)-3-(6-Chlor-3,4-dihydro-1'H-spiro[chromen-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-fluorphenyl)acetamidtrifluoracetat
(Salz)
-
Dargestellt
wie in Beispiel 53 beschrieben unter Verwendung von N-{4-Fluor-2-[(2S)-oxiran-2-ylmethoxy]phenyl}acetamid.
1H-NMR (Aceton-d6,
400 MHz): δ 8,69
(bs, 1H), 8,24 (m, 1H), 7,15 (s, 1H), 7,11 (dd, J = 8,7, 2,6 Hz,
1H), 6,85 (m, 2H), 6,69 (td, J = 8,7, 2,8 Hz, 1H), 4,55 (m, 1H),
4,13 (m, 2H), 3,80-3,44 (m, 6H), 2,88 (t, J = 6,8 Hz, 2H), 2,29-2,05
(m, 4H, vom Signal des Lösungsmittels überdeckt),
2,12 (s, 3H), 1,95 (t, J = 6,6 Hz, 2H).
APCI-MS: m/z 463 (MH+).
-
Beispiel 55
-
2-{[(2S)-3-(6-Chlor-3,4-dihydro-1'H-spiro[chromen-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-N-methylbenzamidtrifluoracetat
(Salz)
-
Dargestellt
wie in Beispiel 53 beschrieben unter Verwendung von N-Methyl-2-[(2S)-oxiran-2-ylmethoxy]benzamid.
1H-NMR (Aceton-d6,
400 MHz): δ 8,08
(bs, 1H), 7,96 (dd, J = 7,7, 1,5 Hz, 1H), 7,44 (ddd, J = 8,3, 7,3,
1,8 Hz, 1H), 7,15-7,05 (m, 4H), 6,86 (d, J = 8,7 Hz, 1H), 4,70 (m,
1H), 4,24 (m, 2H), 3,77 (m, 2H), 3,60-3,45 (m, 4H), 2,91 (d, J =
4,4 Hz, 3H), 2,87 (t, J = 6,9 Hz, 2H), 2,24 (td, J = 14,5, 4,3 Hz,
2H), 2,11-2,05 (m, 2H, vom Signal des Lösungsmittels überdeckt),
1,92 (m, 2H).
APCI-MS: m/z 445 (MH+).
-
Beispiel 56
-
N-(2-{[(2S)-3-(6-Chlor-3,4-dihydro-1'H-spiro[chromen-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxyphenyl)acetamidtrifluoracetat
(Salz)
-
Dargestellt
ausgehend von 6-Chlor-3,4-dihydrospiro[chromen-2,4'-piperidin] wie in
Beispiel 27 beschrieben.
1H-NMR (Aceton-d6, 400 MHz): δ 7,92 (d, J = 8,7 Hz, 1H), 7,14
(s, 1H), 7,11 (dd, J = 8,7, 2,5 Hz, 1H), 6,86 (d, J = 8,6 Hz, 1H),
6,52 (d, J = 2,4 Hz, 1H), 6,40 (dd, J = 8,7, 2,5 Hz, 1H), 4,52 (m,
1H), 4,06 (m, 2H), 3,83-3,41 (m, 6H), 2,87 (t, J = 6,8 Hz, 2H),
2,27-2,08 (m, 4H, vom Signal des Lösungsmittels überdeckt),
2,08 (s, 3H), 1,93 (t, J = 6,7 Hz, 2H).
APCI-MS: m/z 461 (MH+).
-
Beispiel 57
-
N-(2-{[(2S)-3-(6-Chlor-3,4-dihydro-1'H-spiro[chromen-2,4'-piperidin]-1'-yl)-2-hydroxy-2-methylpropyl]oxy}-4-hydroxyphenyl)acetamidtrifluoracetat
-
Dargestellt
ausgehend von 6-Chlor-3,4-dihydrospiro[chromen-2,4'-piperidin] wie in
Beispiel 9 beschrieben.
1H-NMR (Aceton-d6, 400 MHz): δ 7,72 (d, J = 7,3 Hz, 1H), 7,11
(m, 2H), 6,86 (d, J = 8,5 Hz, 2H), 6,58 (s, 1H), 6,42 (d, J = 8,7
Hz, 1H), 3,99 (dd, J = 22,2, 9,3 Hz, 2H), 3,91-3,46 (m, 6H), 2,85
(t, J = 6,7 Hz, 2H), 2,29 (t, J = 12,6 Hz, 2H), 2,08 (s, 3H, vom
Signal des Lösungsmittels überdeckt),
2,07 (m, 2H, vom Signal des Lösungsmittels überdeckt),
1,90 (s, 28H), 1,50 (s, 3H).
APCI-MS: m/z 475 (MH+).
-
Beispiel 58
-
N-[2-({(2S)-3-[(2R)-5-Chlor-1'H,3H-spiro[1-benzofuran-2,3'-pyrrolidin]-1'-yl-2-hydroxypropyl}oxy)-4-hydroxyphenyl]acetamid
-
Eine
kalte Lösung
(Eisbad) von N-[2-({(2S)-3-[(2R)-5-Chlor-1'H,3H-spiro[1-benzofuran-2,3'-pyrrolidin]-1'-yl]-2-hydroxypropyl}oxy)-4-methoxyphenyl]acetamid
(30 mg, 0,067 mmol) in CH2Cl2 (1,5
ml) wurde langsam mit einer 1 M Lösung von BBr3 in
CH2Cl2 (0,2 ml)
versetzt. Nach dem Ende der Zugabe wurde die Reaktionsmischung 3
Stunden lang bei 0°C
gerührt.
Nach Zugabe von Methanol (0,2 ml) wurde weitere 10 Minuten lang
gerührt.
Die flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde in Essigsäureethylester
gelöst
und nacheinander mit einer wäßrigen Lösung von
NaHCO3 und H2O gewaschen.
Die organische Phase wurde über
Na2SO4 getrocknet,
filtriert und im Vakuum eingeengt. Der Rückstand wurde durch HPLC (10–60% CH3CN in H2O in Gegenwart
von 0,1% NH4OH) aufgereinigt, wodurch man
die Titelverbindung (14 mg) erhielt.
1H-NMR
(CD3OD, 400 MHz): δ 7,57 (d, J = 8,7 Hz, 1H); 7,15
(bs, 1H); 7,05 (dd, J = 2,3, 8,6 Hz, 1H); 6,66 (d, J = 8,5 Hz, 1H);
6,47 (d, J = 2,5 Hz, 1H); 6,36 (dd, J = 2,5, 8,7 Hz, 1H); 4,14-4,08
(m, 1H); 4,05 (dd, J = 3,5, 9,7 Hz, 1H); 3,92 (dd, J = 6,2, 9,7
Hz, 1H); 3,25 (m, 2H); 3,09 (d, J = 10,6 Hz, 1H); 3,02 (2,92 (m,
1H); 2,86-2,75 (m,
3H); 2,69 (dd, J = 7,3, 12,2 Hz, 1H); 2,32-2,24 (m, 1H); 2,13-2,05
(m, 4H).
APCI-MS: m/z 433 (MH).
-
Beispiel 59
-
N-[2-({(2S)-3-[(2S)-5-Chlor-1'H,3H-spiro[1-benzofuran-2,3'-pyrrolidin]-1'-yl]-2-hydroxypropyl}oxy)-4-hydroxyphenyl]acetamid
-
Eine
kalte Lösung
(Eisbad) von N-[2-({(2S)-3-[(2S)-5-Chlor-1''H,3H-spiro[1-benzofuran-2,3'-pyrrolidin]-1'-yl]-2-hydroxypropyl}oxy)-4-methoxyphenyl]acetamid
(30 mg, 0,067 mmol) in CH2Cl2 (1,5
ml) wurde langsam mit einer 1 M Lösung von BBr3 in
CH2Cl2 (0,2 ml)
versetzt. Nach dem Ende der Zugabe wurde die Reaktionsmischung 3
Stunden lang bei 0°C
gerührt.
Nach der Zugabe von Methanol (0,2 ml) wurde noch weitere 10 Minuten
lang gerührt.
Die flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde in Essigsäureethylester
gelöst
und nacheinander mit einer wäßrigen Lösung von
NaHCO3 und H2O gewaschen.
Die organische Phase wurde über
Na2SO4 getrocknet,
filtriert und im Vakuum eingeengt. Der Rückstand wurde durch HPLC (CH3CN 10–60%
in H2O in Gegenwart von 0,1% NH4OH)
aufgereinigt, wodurch man die Titelverbindung (15 mg) erhielt.
1H-NMR (CD3OD, 400
MHz): δ 7,57
(d, J = 8,7 Hz, 1H); 7,15 (m, 1H); 7,05 (dd, J = 2,3, 8,5 Hz, 1H);
6,65 (d, J = 8,5 Hz, 1H); 6,47 (d, J = 2,5 Hz, 1H); 6,36 (dd, J
= 2,5, 8,5 Hz, 1H); 4,14-4,07 (m, 1H); 4,04 (dd, J = 3,7, 9,9 Hz,
1H); 3,93 (dd, J = 6,1, 9,9 Hz, 1H); 3,25 (m, 2H); 3,13 (d, J =
10,7 Hz, 1H); 3,03-2,96 (m, 1H); 2,82-2,73 (m, 3H); 3,93 (dd, J = 6,1, 9,9
Hz, 1H); 2,32-2,24 (m, 1H); 2,14-2,05 (m, 4H).
APCI-MS: m/z
433 (MH+).
-
Beispiel 60
-
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-(pyrrolidin-1-ylcarbonyl)phenol
-
Schritt I:
-
(2S)-1-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-3-[5-[(4-methoxybenzyl)oxy]-2-(pyrrolidin-1-ylcarbonyl)phenoxy]propan-2-ol
-
Eine
Mischung von 2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl]benzoesäure (Hydrochlorid)
(100 mg, 0,169 mmol) und N,N-Carbonyldiimidazol (27,5 mg, 0,169
mmol) in DMF (3 ml) wurde 1 Stunde lang bei Raumtemperatur gerührt. Anschließend wurde mit
Pyrrolidin (120 mg, 1,69 mmol) in DMF (1 ml) versetzt, und die Reaktionsmischung
wurde über
Nacht bei Raumtemperatur gerührt.
Die Reaktionsmischung wurde zwischen Essigsäureethylester und Wasser verteilt. Die
organische Phase wurde über
Na2SO4 getrocknet,
filtriert und eingeengt. Der Rückstand
wurde durch Flash-Chromatographie an Kieselgel (0–1% Methanol
in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die im Untertitel genannte Verbindung (38 mg) erhielt.
1H-NMR (CDCl3, 400
MHz): δ 7,39-7,34
(m, 2H); 7,27-7,20 (m, 1H); 7,13 (m, 1H); 7,05 (dd, J = 2,3, 8,5
Hz, 1H); 6,95 (m, 1H); 6,69 (d, J = 8,4 Hz, 1H); 6,64-6,59 (m, 2H);
4,13-3,98 (m, 3H); 3,87 (s, 3H); 3,64 (t, J = 6,9 Hz, 2H); 3,38
(m, 2H); 3,00 (s, 2H); 2,80 (m, 1H); 2,73-2,49 (m, 5H); 2,03-1,76
(m, 8H).
APCI-MS: m/z 607 (MH+).
-
Schritt II:
-
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-(pyrrolidin-1-ylcarbonyl)phenol
-
(25)-1-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-3-[5-[(4-methoxybenzyl)oxy]-2-(pyrrolidin-1-ylcarbonyl)phenoxy]propan-2-ol
(35 mg, 0,057 mmol) wurde bei Raumtemperatur 25 Minuten lang mit
10% CF3CO2H in CH2Cl2 (3 ml) behandelt.
Die flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (0–3%
Methanol in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die Titelverbindung (20 mg) erhielt.
1H-NMR
(CD3OD, 400 MHz): δ 7,09 (m, 1H); 7,04-6,97 (m,
2H); 6,61 (d, J = 8,5 Hz, 1H); 6,45 (d, J = 2,2 Hz, 1H); 6,39 (dd,
J = 2,0, 8,3 Hz, 1H); 4,09-4,02 (m, 1H); 3,97 (dd, J = 4,3, 9,7
Hz, 1H); 3,91 (dd, J = 5,7, 9,7 Hz, 1H); 3,51 (t, J = 6,8 Hz, 2H);
3,30 (m, 2H); 2,99 (s, 2H); 2,74-2,46 (m, 6H); 1,98-1,74 (m, 8H).
APCI-MS:
m/z 487 (MH+).
-
Beispiel 61
-
1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)piperidin-4-ol
-
Schritt I:
-
1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoyl}piperidin-4-ol
-
Eine
Mischung von 2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)benzoesäure (Hydrochlorid)
(100 mg, 0,169 mmol) und N,N-Carbonyldiimidazol (27,5 mg, 0,169
mmol) in DMF (3 ml) wurde 1 Stunde lang bei Raumtemperatur gerührt. Anschließend wurde mit
Piperidin-4-ol (20,5 mg, 0,202 mmol) in DMF versetzt, und die Reaktionsmischung
wurde über
Nacht bei Raumtemperatur gerührt.
Die Reaktionsmischung wurde zwischen Essigsäureethylester und Wasser verteilt. Die
organische Phase wurde über
Na2SO4 getrocknet,
filtriert und eingeengt. Der Rückstand
wurde durch Flash-Chromatographie
an Kieselgel (0–2%
Methanol in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die im Untertitel genannte Verbindung (50 mg) erhielt.
APCI-MS:
m/z 637 (MH+).
-
Schritt II:
-
1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro(1-benzofuran-2,4'-piperidin-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)piperidin-4-ol
-
1-{2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoyl}piperidin-4-ol
(45 mg, 0,07 mmol) wurde bei Raumtemperatur 25 Minuten mit 10% CF3CO2H in CH2Cl2 (3 ml) behandelt.
Die flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (0–4,5%
Methanol in Dichlormethan, 0,2% NH4OH) aufgereinigt, wodurch
man die Titelverbindung (20 mg) erhielt.
1H-NMR
(CD3OD, 400 MHz): δ 7,09 (m, 1H); 7,02-6,92 (m,
2H); 6,60 (d, J = 8,5 Hz, 1H); 6,47-6,37 (m, 2H); 4,21-3,78 (m, 4H); 3,58-3,03
(m, 4H); 3,00 (s, 2H); 2,76-2,44
(m, 6H); 1,96-1,22 (m, 8H).
APCI-MS: m/z 637 (MH+).
-
Beispiel 62
-
(3S)-1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}benzoyl)-pyrrolidin-3-ol
-
Eine
Mischung von 2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl]benzoesäure (Hydrochlorid)
(60 mg, 0,132 mmol) und N,N-Carbonyldiimidazol (30 mg, 0,184 mmol)
in DMF (1,5 ml) wurde 1 Stunde lang bei Raumtemperatur gerührt. Anschließend wurde mit
3(S)-Pyrrolidin-3-ol
(57,5 mg, 0,66 mmol) in DMF (1 ml) versetzt, und die Reaktionsmischung
wurde über Nacht bei
Raumtemperatur gerührt.
Die Reaktionsmischung wurde zwischen Essigsäureethylester und Wasser verteilt.
Die organische Phase wurde über
Na2SO4 getrocknet,
filtriert und eingeengt. Der Rückstand
wurde durch Flash-Chromatographie
an Kieselgel (0–2,5%
Methanol in Dichlormethan, 0,2% NH4OH) aufgereinigt, wodurch
man die Titelverbindung (13 mg) erhielt.
1H-NMR
(CD3OD, 400 MHz): δ 7,45-7,39 (m, 1H); 7,26 (bd,
J = 7,2 Hz, 1H); 7,15-7,09 (m, 2H); 7,08-7,01 (m, 2H); 6,65 (d,
J = 8,5 Hz, 1H); 4,50 (m, 0,5H); 4,38 (m, 0,5H); 4,17-3,98 (m, 3H);
3,77-3,42 (m, 3H); 3,25 (m, 1H); 3,02 (s, 2H); 2,77-2,52 (m, 6H);
2,14-1,77 (m, 6H).
APCI-MS: m/z 487 (MH+).
-
Beispiel 63
-
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-(piperidin-1-ylcarbonyl)phenol
-
Schritt I:
-
(2S)-1-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4,-piperidin]-1'-yl)-3-[5-[(4-methoxybenzyl)oxy]-2-(piperidin-1-ylcarbonyl)phenoxy]propan-2-ol
-
Eine
Mischung von 2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl]benzoesäure (Hydrochlorid)
(100 mg, 0,169 mmol) und N,N-Carbonyldiimidazol (41 mg, 0,253 mmol)
in DMF (1,5 ml) wurde 1 Stunde lang bei Raumtemperatur gerührt. Anschließend wurde mit
Piperidin (144 mg, 1,79 mmol) in DMF versetzt, und die Reaktionsmischung
wurde über
Nacht bei Raumtemperatur gerührt.
Die Reaktionsmischung wurde zwischen Essigsäureethylester und Wasser verteilt.
Die organische Phase wurde über
Na2SO4 getrocknet,
filtriert und eingeengt. Der Rückstand
wurde durch Flash-Chromatographie an Kieselgel (0–1% Methanol
in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die im Untertitel genannte Verbindung (24 mg) erhielt.
APCI-MS:
m/z 621 (MH+).
-
Schritt II:
-
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-(piperidin-1-ylcarbonyl)phenol
-
(2S)-1-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-3-[5-[(4-methoxybenzyl)oxy]-2-(piperidin-1-ylcarbonyl)phenoxy]propan-2-ol
(23 mg, 0,037 mmol) wurde bei Raumtemperatur 30 Minuten lang mit
10% CF3CO2H in CH2Cl2 (3 ml) behandelt.
Die flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (0–2,5%
Methanol in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die Titelverbindung (10 mg) erhielt.
1H-NMR
(CD3OD, 400 MHz): δ 7,13 (m, 1H); 7,03 (dd, J =
2,2, 8,5 Hz, 1H); 7,00 (d, J = 8,2 Hz, 1H); 6,65 (d, J = 8,5 Hz,
1H); 6,50 (d, J = 2,1 Hz, 1H); 6,44 (dd, J = 2,1, 8,2 Hz, 1H); 4,10
(m, 1H); 4,07-3,93 (m, 2H); 3,80 (m, 1H); 3,58 (m, 1H); 3,30 (m,
2H, innerhalb des Methanol-Peaks);
3,00 (s, 2H); 2,78-2,51 (m, 6H); 1,98-1,80 (m, 4H); 1,75-1,40 (m,
6H).
APCI-MS: m/z 503 (MH+).
-
Beispiel 64
-
(3S)-1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)pyrrolidin-3-ol
-
Schritt I:
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoesäuremethylester
-
Eine
Mischung von 5-Chlor-3H-spiro[2-benzofuran-1,4'-piperidin]
(195 mg, 0,87 mmol) und 4-[(4-Methoxybenzyl)oxy]-2-[(2S)-oxiran-2-ylmethoxy]benzoesäuremethylester
(300 mg, 0,87 mmol) in Ethanol (4 ml) wurde über Nacht bei 80°C gerührt. Die
flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (0–2%
Methanol in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die im Untertitel genannte Verbindung (450 mg) erhielt.
1H-NMR (CDCl3, 400
MHz): δ 7,89-7,85
M, 1H); 7,39-7,35 (m, 2H); 7,26 (dd, J = 1,8, 8,1 Hz, 1H); 7,20
(breit, s, 1H); 7,08 (d, J = 8,0 Hz, 1H); 6,97-6,93 (m, 2H); 6,64-6,59 (m, 2H); 5,08
(s, 4H); 4,24-4,15 (m, 2H); 4,03 (dd, J = 5,8, 9,0 Hz, 1H); 3,88
(s, 3H); 3,84 (s, 3H); 2,98-2,85 (m, 2H); 2,75-2,46 (m, 4H); 2,03-1,90
(m, 2H); 1,77 (breit, d, J = 13,5 Hz, 2H).
APCI-MS: m/z 570
(MH+).
-
Schritt II:
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoesäure (Hydrochlorid)
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoesäuremethylester
(450 mg, 0,792 mmol) wurde in Ethanol (6 ml) aufgenommen. Wäßriges KOH (2,31
g KOH in 2,3 ml H2O) wurde zugesetzt, und
die Reaktionsmischung wurde über
Nacht unter Rückfluß erhitzt,
auf 0°C
abgekühlt
und durch die Zugabe von wäßriger HCl
auf einen pH-Wert von 2,0 eingestellt, und mit Essigsäureethylester
extrahiert. Die organische Phase wurde mit H2O
gewaschen, über
Na2SO4 getrocknet,
filtriert und eingeengt, wodurch man die im Untertitel genannte
Verbindung (370 mg) erhielt.
1H-NMR
(CD3OD, 400 MHz): δ 7,97-7,93 (m, 1H); 7,39-7,32
(m, 5H); 6,96-6,91 (m, 2H); 6,75-6,70 (m, 2H); 5,10 (s, 4H); 4,48-4,42
(m, 1H); 4,30 (dd, J = 4,0, 9,5 Hz, 1H); 4,11 (dd, J = 5,3, 9,5
Hz, 1H); 3,81 (s, 3H); 3,80-3,42 (m, 6H); 2,55-2,41 (m, 2H); 1,98-1,88
(m, 2H).
APCI-MS: m/z 554 (MH+).
-
Schritt III:
-
(3S)-1-{2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoyl)pyrrolidin-3-ol
-
Eine
Mischung von 2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoesäure (Hydrochlorid)
(150 mg, 0,254 mmol) und N,N-Carbonyldiimidazol (54 mg, 0,33 mmol)
in DMF (4 ml) wurde 1 Stunde lang bei Raumtemperatur gerührt und
mit 3(S)-Pyrrolidin-3-ol (111 mg, 1,27 mmol) in DMF (1,5 ml) versetzt,
und die Reaktionsmischung wurde über
Nacht bei Raumtemperatur gerührt
und zwischen Essigsäureethylester
und Wasser verteilt. Die organische Phase wurde über Na2SO4 getrocknet, filtriert und eingeengt. Der
Rückstand
wurde durch Flash-Chromatographie an Kieselgel (0–2% Methanol
in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die im Untertitel genannte Verbindung (100 mg) erhielt.
APCI-MS:
m/z 623 (MH+).
-
Schritt IV:
-
(3S)-1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)pyrrolidin-3-ol
-
(3S)-1-{2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoyl}pyrrolidin-3-ol
(95 mg, 0,152 mmol) wurde bei Raumtemperatur 25 Minuten lang mit
10% CF3CO2H in CH2Cl2 (4 ml) behandelt.
Die flüchti gen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (Methanol 0–5%
in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die Titelverbindung (34 mg) erhielt.
1H-NMR
(CD3OD, 400 MHz): δ 7,31-7,27 (m, 2H); 7,20 (d,
J = 8,3 Hz, 1H); 7,10 (d, J = 8,3 Hz, 1H); 6,52 (t, J = 2,5 Hz,
1H); 6,46 (dt, J = 2,0 Hz, 1H); 5,02 (s, 2H); 4,49 (m, 0, 5H); 4,38
(m, 0,5H); 4,20 (m, 1H); 4,08-3,98 (m, 2H); 3,73-3,49 (m, 3H); 3,30
(m, 1H); 3,12 (bs, 2H); 2,95-2,70 (m, 4H); 2,18-1,75 (m, 6H).
APCI-MS:
m/z 503 (MH+).
-
Beispiel 65
-
1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)piperidin-4-ol
-
Schritt I:
-
1-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoyl}piperidin-4-ol
-
Eine
Mischung von 2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoesäure (Hydrochlorid)
(150 mg, 0,254 mmol) und N,N-Carbonyldiimidazol (54 mg, 0,33 mmol)
in DMF (4 ml) wurde 1 Stunde lang bei Raumtemperatur gerührt und
mit Piperidin-4-ol (77 mg, 0,762 mmol) versetzt, und die Reaktionsmischung
wurde über
Nacht bei Raumtemperatur gerührt
und zwischen Essigsäureethylester
und Wasser verteilt. Die organische Phase wurde über Na2SO4 getrocknet, filtriert und eingeengt. Der
Rückstand
wurde durch Flash-Chromatographie an Kieselgel (0–2,5% Methanol
in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die im Untertitel genannte Verbindung (70 mg) erhielt.
APCI-MS:
m/z 637 (MH+).
-
Schritt II:
-
1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)piperidin-4-ol
-
1-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoyl}piperidin-4-ol
(65 mg, 0,102 mmol) wurde bei Raumtemperatur 25 Minuten lang mit
10% CF3CO2H in Dichlormethan
(3 ml) behandelt. Die flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (0–5%
Methanol in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die Titelverbindung (26 mg) erhielt.
1H-NMR
(CD3OD, 400 MHz): δ 7,30-7,25 (m, 2H); 7,19 (d,
J = 8,1 Hz, 1H); 7,07-6,98 (m, 1H); 6,53 (bs, 1H); 6,45 (d, J =
8,2 Hz, 1H); 5,01 (s, 2H); 4,30-3,70 (m, 5H); 3,62-3,10 (m, 3H);
3,00 (bs, 2H); 2,73-2,50 (m, 4H); 2,10-1,32 (m, 8H).
APCI-MS:
m/z 517 (MH+).
-
Beispiel 66
-
N-[4-Hydroxy-2-({(2S)-2-hydroxy-3-[5-(trifluormethyl)-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl]-propyl}oxy)phenyl]acetamid
-
Eine
Mischung von Essigsäure-4-(acetylamino)-3-[(2S)-oxiran-2-ylmethoxy]phenylester
(41 mg, 0,155 mmol) und 5-(Trifluormethyl)-3H-spiro[1-benzofuran-2,4'-piperidin] (40 mg,
0,155 mmol) in Ethanol (2 ml) wurde über Nacht bei 80°C gerührt. Die
flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (0–2,5%
Methanol in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die Titelverbindung (54 mg) erhielt.
1H-NMR
(CD3OD, 400 MHz): δ 7,57 (d, J = 8,7 Hz, 1H); 7,45
(s, 1H); 7,39 (d, J = 8,5 Hz, 1H); 6,82 (d, J = 8,4 Hz, 1H); 6,48
(d, J = 2,5 Hz, 1H); 6,46 (dd, J = 2,6, 8,7 Hz, 1H); 4,20-4,14 (m,
1H); 4,05 (dd, J = 3,5, 9,9 Hz, 1H); 3,93 (dd, J = 6,2, 9,9 Hz,
1H); 3,08 (s, 2H); 2,80-2,55 (m, 6H); 2,13 (s, 3H); 2,02-1,83 (m,
4H).
APCI-MS: m/z 481 (MH+).
-
Beispiel 67
-
(3S)-1-{[2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)pyrrolidin-3-ylbenzoat
-
Schritt I:
-
(3S)-3-(Benzoyloxy)pyrrolidin-1-carbonsäure-tert.-butylester
-
Eine
Lösung
von (3S)-Pyrrolidin-3-ol (0,87 g, 10,0 mmol) in THF (20 ml) wurde
bei Raumtemperatur langsam mit einer Lösung von Dikohlensäure-di-tert.-butylester (2,18
g, 10,0 mmol) in THF (10 ml) versetzt. Nach dem Ende der Zugabe
wurde die Reaktionsmischung über
Nacht bei Raumtemperatur gerührt.
Die flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (0–2,5%
Methanol in Dichlormethan) aufgereinigt, wodurch man das (3S)-3-Hydroxypyrrolidin-1-carbonsäure-tert.-butylester-Zwischenprodukt
erhielt. Eine Lösung
von (3S)-3-Hydroxypyrrolidin-1-carbonsäuretert.-butylester (900 mg,
4,8 mmol) in CH2Cl2 (6
ml) wurde bei 0°C
mit Et3N (699 mg, 6,91 mmol) versetzt, gefolgt
von Benzoylchlorid (809 mg, 5,76 mmol). Nach dem Ende der Zugabe
die Reaktionsmischung wurde über Nacht
bei Raumtemperatur gerührt.
Die Reaktionsmischung wurde zwischen CH2Cl2 und H2O verteilt.
Die organische Phase wurde nacheinander mit wäßriger NaHCO3 und
Wasser gewaschen, über
Na2SO4 getrocknet, filtriert
und eingeengt. Der Rückstand
wurde durch Flash-Chromatographie an Kieselgel (0–1% Methanol
in Dichlormethan) aufgereinigt, wodurch man die im Untertitel genannte
Verbindung (642 mg) erhielt.
1H-NMR
(CDCl3, 400 MHz): δ 8,03 (d, J = 7,3 Hz, 2H); 7,59
(t, J = 7,3 Hz, 1H); 7,46 (t, J = 7,7 Hz, 2H); 5,58 (m, 1H); 3,75-3,45
(m, 4H); 2,20 (s, 2H); 1,50 (s, 9H).
APCI-MS: m/z 192 (MH+-Boc).
-
Schritt II:
-
(3S)-Pyrrolidin-3-yl-benzoat (Trifluoracetat)
-
(3S)-3-(Benzoyloxy)pyrrolidin-1-carbonsäure-tert.-butylester (635 mg,
2,18 mmol) wurde bei Raumtemperatur über Nacht mit 20% CF3CO2H in CH2Cl2 (20 ml) behandelt.
Die flüchtigen
Bestandteile wurden im Vakuum entfernt, wodurch man die im Untertitel
genannte Verbindung erhielt (800 mg).
1H-NMR
(CDCl3, 400 MHz): δ 9,29 (bd, 2H); 8,06 (m, 2H);
7,64-7,59 (m, 1H); 7,47 (t, J = 7,9 Hz, 2H); 5,70 (m, 1H); 3,72-3,50
(m, 4H); 2,40 (m, 2H).
APCI-MS: m/z 192 (MH+).
-
Schritt III:
-
(3S)-1-{2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoyl}pyrrolidin-3-yl-benzoat
-
Eine
Mischung von 2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl]benzoesäure (Hydrochlorid)
(218 mg, 0,369 mmol) und N,N-Carbonyldiimidazol (77,5 mg, 0,478
mmol) in DMF (3 ml) wurde 50 Minuten lang bei Raumtemperatur gerührt. Anschließend wurde mit
(3S)-Pyrrolidin-3-yl-benzoat
(Trifluoracetat) (225 mg, 0,738 mmol) in DMF (1 ml) gefolgt von
Et3N (0,102 ml, 0,738 mmol) versetzt, und
die Reaktionsmischung wurde über
Nacht bei Raumtemperatur gerührt.
Die Reaktionsmischung wurde zwischen Essigsäureethylester und Wasser verteilt.
Die organische Phase wurde über Na2SO4 getrocknet,
filtriert und eingeengt. Der Rückstand
wurde durch Flash-Chromatographie an Kieselgel (0–2,5% Methanol
in Dichlormethan) aufgereinigt, wodurch man die im Untertitel genannte
Verbindung (140 mg) erhielt.
APCI-MS: m/z 727 (MH+).
-
Schritt IV:
-
(3S)-1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)pyrrolidin-3-ylbenzoat
-
(3S)-1-{2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoyl}pyrrolidin-3-yl-benzoat
(135 mg, 0,185 mmol) wurde bei Raumtemperatur 35 Minuten lang mit
10% CF3CO2H in CH2Cl2 (3 ml) behandelt.
Die flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie an
Kieselgel (0–3,5%
Methanol in Dichlormethan) aufgereinigt, wodurch man die Titelverbindung
(73 mg) erhielt.
1H-NMR (CDCl3, 400 MHz): δ 8,06 (d, J = 7,4 Hz, 1H); 8,00
(d, J = 7,4 Hz, 1H); 7,61-7,56 (m, 1H); 7,52-7,43 (m, 2H); 7,17-7,04
(m, 3H); 6,71 (dd, J = 2,4, 8,5 Hz, 1H); 6,56-6,45 (m, 2H); 5,16
(m, 0,5H); 5,50 (m, 0,5H); 4,45 (m, 1H); 4,05-3,48 (m, 7H); 3,33-2,92
(m, 8H); 2,40-1,95
(m, 5H).
APCI-MS: m/z 607 (MH+).
-
Beispiel 68
-
(3S)-1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-fluorbenzoyl)pyrrolidin-3-ol
-
Schritt I:
-
4-Fluor-2-[(2S)-oxiran-2-ylmethoxy]benzoesäuremethylester
-
Eine
Mischung von 4-Fluor-2-hydroxybenzoesäuremethylester (456,3 mg, 1,76
mmol), 3-Nitrobenzolsulfonsäure-(2S)-oxiran-2-ylmethylester
(300 mg, 1,76 mmol) und Cs2CO3 (687,4
mg, 2,11 mmol) in DMF (4,5 ml) wurde über Nacht bei Raumtemperatur
gerührt.
Die Reaktionsmischung wurde zwischen Essigsäureethylester und H2O verteilt, und die organische Phase wurde über Na2SO4 getrocknet,
filtriert und im Vakuum eingeengt. Der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (0–30%
Essigsäureethylester
in Petrolether) aufgereinigt, wodurch man die im Untertitel genannte
Verbindung (385 mg) erhielt.
1H-NMR
(CDCl3, 400 MHz): δ 7,93-7,85 (m, 1H); 6,77-6,69
(m, 2H); 4,36 (dd, J = 2,6, 11,2 Hz, 1H); 4,08 (dd, J = 4,9, 11,2
Hz, 1H); 3,90 (s, 3H); 3,44 (m, 1H); 2,95 (m, 2H).
APCI-MS:
m/z 227 (MH+).
-
Schritt II:
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-fluorbenzoesäuremethylester
-
Eine
Mischung von 5-Chlor-3H-spiro[1-benzofuran-2,4'-piperidin]
(224 mg, 1,0 mmol) und 4-Fluor-2-[(2S)-oxiran-2-ylmethoxy]benzoesäuremethylester
(226 mg, 1,0 mmol) in Ethanol (2 ml) wurde über Nacht bei 80°C gerührt. Die
flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie an
Kieselgel (0–2,5%
Methanol in Dichlormethan) aufgereinigt, wodurch man die im Untertitel
genannte Verbindung (290 mg) erhielt.
1H-NMR
(CDCl3, 400 MHz): δ 7,90 (m, 1H); 7,12 (s, 1H);
7,07 (dd, J = 2,2, 8,4 Hz, 1H); 6,77-6,67 (m, 3H); 4,25-4,14 (m, 2H); 4,06
(dd, J = 5,6, 9,0 Hz, 1H); 3,90 (s, 3H); 3,00 (s, 2H); 2,90-2,60
(m, 6H); 2,00 (m, 2H); 1,86 (m, 2H).
APCI-MS: m/z 452 (MH+).
-
Schritt III:
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-fluorbenzoesäure (Hydrochlorid)
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-fluorbenzoesäuremethylester
(286 mg, 0,635 mmol) in THF (3 ml) wurde bei Raumtemperatur 7 Stunden
lang mit wäßriger KOH
(106 mg KOH in 1 ml H2O) behandelt. Die
Reaktionsmischung wurde auf 0°C
abgekühlt
und durch Zugabe von wäßriger HCl
auf einen pH-Wert von 2 eingestellt, und dann mit Essigsäureethylester
extrahiert. Die organische Phase wurde mit H2O
gewaschen, über
Na2SO4 getrocknet,
filtriert und eingeengt, wodurch man die im Untertitel genannte
Verbindung (250 mg) erhielt.
1H-NMR
(CD3OD, 400 MHz): δ 7,98 (dd, J = 6,9, 8,8 Hz,
1H); 7,20 (s, 1H); 7,11 (dd, J = 2,0, 8,6 Hz, 1H); 6,97 (dd, J =
2,3, 10,9 Hz, 1H); 6,86-6,79 (m, 1H); 6,74 (d, J = 8,5 Hz, 1H);
4,50-4,43 (m, 1H); 4,27 (dd, J = 4,0, 9,6 Hz, 1H); 4,13 (dd, J =
5,3, 9,6 Hz, 1H); 3,80-3,43 (m, 6H); 3,15 (s, 2H); 2,10 (m, 2H);
2,18 (m, 2H).
APCI-MS: m/z 436 (MH+).
-
Schritt IV:
-
(3S)-1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-fluorbenzoyl)pyrrolidin-3-ol
-
Eine
Mischung von 2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1- benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-fluorbenzoesäure (Hydrochlorid)
(200 mg, 0,423 mmol) und N,N-Carbonyldiimidazol (89,2 mg, 0,55 mmol)
in DMF (3 ml) wurde 50 Minuten lang bei Raumtemperatur gerührt. Anschließend wurde
mit (3S)-Pyrrolidin-3-ol (184 mg, 2,11 mmol) in DMF (1 ml) versetzt,
und die Reaktionsmischung wurde über
Nacht bei Raumtemperatur gerührt
und zwischen Essigsäureethylester
und H2O verteilt. Die organische Phase wurde über Na2SO4 getrocknet,
filtriert und eingeengt. Der Rückstand
wurde durch Flash-Chromatographie an Kieselgel (0–2,5% Methanol
in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die Titelverbindung (60 mg) erhielt.
1H-NMR
(CD3OD, 400 MHz): δ 7,28 (m, 1H); 7,13 (s, 1H);
7,07-7,02 (m, 1H); 6,97-6,91 (m, 1H); 6,81-6,75 (m, 1H); 6,65 (d,
J = 8,5 Hz, 1H); 4,49 (m, 0,5H); 4,38 (m, 0,5H); 4,16-3,99 (m, 3H);
3,70 (dd, J = 5,2, 9,3 Hz, 1H); 3,64-3,46 (m, 2H); 3,37-3,19 (m,
1H); 3,00 (s, 2H); 2,75-2,52 (m, 6H); 2,14-1,78 (m, 6H).
APCI-MS:
m/z 506 (MH+).
-
Beispiel 69
-
(3S)-1-[4-Hydroxy-2-({(2S)-2-hydroxy-3-(5-(trifluormethyl)-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl]propyl}oxy)benzoyl]pyrrolidin-3-ol
-
Schritt I:
-
2-({(2S)-2-Hydroxy-3-[5-(trifluormethyl)-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl]propyl}oxy)-4-[(4-methoxybenzyl)oxy]benzoesäuremethylester
-
Eine
Mischung von 5-(Trifluormethyl)-3H-spiro[1-benzofuran-2,4'-piperidin] (107 mg, 0,416 mmol) und 4-[(4-Methoxybenzyl)oxy]-2-[(2S)-oxiran-2-ylmethoxy]-benzoesäuremethylester
(143,25 mg, 0,416 mmol) in Ethanol (2 ml) wurde über das Wochenende bei 75°C gerührt. Die
flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie an
Kieselgel (0–2,5%
Methanol in Dichlormethan) aufgereinigt, wodurch man die im Untertitel
genannte Verbindung (200 mg) erhielt.
APCI-MS: m/z 602 (MH+).
-
Schritt II:
-
2-({(2S)-2-Hydroxy-3-[5-(trifluormethyl)-1'H,3H-spiro-1-benzofuran-2,4'-piperidin]-1'-yl]propyl}oxy)-4-[(4-methoxybenzyl)oxy]benzoesäure (Hydrochlorid)
-
2-({(2S)-2-Hydroxy-3-[5-(trifluormethyl)-1'H,3H-spiro-q [1-benzofuran-2,4'-piperidin]-1'-yl]propyl}oxy)-4-[(4-methoxybenzyl)oxy]benzoesäuremethylester
(190 mg, 0,315 mmol) wurde in Ethanol (4 ml) aufgenommen und mit
wäßriger KOH
(918 mg KOH in 1 ml H2O) versetzt, und die
Reaktionsmischung wurde über Nacht
bei Rückflußtemperatur
gerührt,
auf 0°C
abgekühlt
und durch die Zugabe von wäßriger HCl
auf einen pH-Wert von 2 eingestellt und dann mit Essigsäureethylester
extrahiert. Die organische Phase wurde mit H2O gewaschen, über Na2SO4 getrocknet,
filtriert und eingeengt, wodurch man die im Untertitel genannte
Verbindung (170 mg) erhielt.
1H-NMR
(CD3OD, 400 MHz): δ 7,93 (d, J = 9,0 Hz, 1H); 7,52
(s, 1H); 7,45 (d, J = 8,6 Hz, 1H); 7,36 (d, J = 8,6 Hz, 2H); 6,96-6,88
(m, 3H); 6,75-6,69 (m, 2H); 5,10 (S, 2H); 4,44 (m, 1H); 4,28 (dd,
J = 4,0, 9,5 Hz, 1H); 4,11 (dd, J = 5,3, 9,5 Hz, 1H); 3,80 (s, 3H);
3,77-3,43 (m, 6H); 3,22 (s, 2H); 2,38 (m, 2H); 2,20 (m, 2H)
APCI-MS:
m/z 588 (MH+).
-
Schritt III:
-
(3S)-1-{2-({(2S)-2-Hydroxy-3-[5-(trifluormethyl)-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl]-propyl}oxy)-4-[(4-methoxybenzyl)oxy]benzoyl}pyrrolidin-3-ol
-
Eine
Mischung von 2-({(2S)-2-Hydroxy-3-[5-(trifluormethyl)-1'H,3H-spiro-(1-benzofuran-2,4'-piperidin]-1'-yl]propyl}oxy)-4-[(4-methoxybenzyl)oxy]benzoesäure (Hydrochlorid)
(150 mg, 0,24 mmol) und N,N-Carbonyldiimidazol
(47 mg, 0,288 mmol) in DMF (3 ml) wurde 50 Minuten lang bei Raumtemperatur
gerührt.
Anschließend
wurde mit (3S)-Pyrrolidin-3-ol (104,5 mg, 1,2 mmol) in DMF (1 ml)
versetzt, und die Reaktionsmischung wurde über Nacht bei Raumtemperatur
gerührt.
Die Reaktionsmischung wurde zwischen Essigsäureethylester und H2O verteilt. Die organische Phase wurde über Na2SO4 getrocknet,
filtriert und eingeengt. Der Rückstand
wurde durch Flash-Chromatographie an Kieselgel (0–2,5% Methanol
in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die im Untertitel genannte Verbindung (80 mg) erhielt.
APCI-MS:
m/z 657 (MH+).
-
Schritt IV:
-
(3S)-1-(4-Hydroxy-2-({(2S)-2-hydroxy-3-(5-(trifluormethyl)-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl]propyl}oxy)benzoyl]pyrrolidin-3-ol
-
(3S)-1-{2-({(2S)-2-Hydroxy-3-[5-(trifluormethyl)-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl]propyl}oxy)-4-[(4-methoxybenzyl)oxy]benzoyl}pyrrolidin-3-ol (75 mg, 0,114
mmol) wurde bei Raumtemperatur 20 Minuten lang mit 10% CF3CO2H in CH2Cl2 (3 ml) behandelt.
Die flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (0–3%
Methanol in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die Titelverbindung (26 mg) erhielt.
1H-NMR
(CD3OD, 400 MHz): δ 7,45 (s, 1H); 7,39 (d, J =
8,5 Hz, 1H); 7,09 (dd, J = 2,4, 8,2 Hz, 1H); 6,82 (d, J = 8,4 Hz,
1H); 6,50 (m, 1H); 6,45 (m, 1H); 4,48 (m, 0,5H); 4,36 (m, 0,5H);
4,15-4,01 (m, 2H); 3,97 (dd, J = 5,6, 9,7 Hz, 1H); 3,72-3,50 (m,
3H); 3,38-3,23 (m, 1H); 3,06 (s, 2H); 2,79-2,52 (m, 6H); 2,12-1,80
(m, 6H).
APCI-MS: m/z 537 (MH+).
-
Beispiel 70
-
(3S)-1-(4-Fluor-2-{[(2S)-2-hydroxy-3-(1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)propyl]oxy}benzoyl)-pyrrolidin-3-ol
-
Schritt I:
-
4-Fluor-2-{[(2S)-2-hydroxy-3-(1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)propyl]oxy}benzoesäuremethylester
-
Eine
Mischung von 3H-Spiro[1-benzofuran-2,4'-piperidin) (55 mg, 0,29 mmol) und 4-Fluor-2[(2S)-oxiran-2-yl-methoxy]benzoesäuremethylester
(66 mg, 0,29 mmol) in Ethanol (1,5 ml) wurde über Nacht bei 78°C gerührt. Die
flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (0–1%
Methanol in Dichlormethan) aufgereinigt, wodurch man die im Untertitel
genannte Verbindung (50 mg) erhielt.
APCI-MS: m/z 416 (MH+).
-
Schritt II:
-
4-Fluor-2-{[(2S)-2-hydroxy-3-(1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)propyl]oxy}benzoesäure (Hydrochlorid)
-
4-Fluor-2-{[(2S)-2-hydroxy-3-(1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)propyl]oxy}benzoesäuremethylester
(50 mg, 0,12 mmol) wurde in THF (1,5 ml) gelöst. Wäßrige KOH (20 mg KOH in 0,5
ml H2O) wurde zugesetzt, und die Reaktionsmischung
wurde 24 Stunden lang bei Raumtemperatur gerührt, auf 0°C abgekühlt und durch Zugabe von wäßriger HCl
auf einen pH-Wert von 2 eingestellt und dann mit Essigsäureethylester extrahiert.
Die organische Phase wurde mit H2O gewaschen, über Na2SO4 getrocknet,
filtriert und eingeengt, wodurch man die im Untertitel genannte
Verbindung (37 mg) erhielt.
1H-NMR
(CD3OD, 400 MHz): δ 7,96 (dd, J = 6,9, 8,8 Hz,
1H); 7,20 (d, J = 7,2 Hz, 1H); 7,12 (t, J = 7,5 Hz, 1H); 6,97 (dd,
J = 2,4, 11,0 Hz, 1H); 6,88-6,78 (m, 2H); 6,76 (d, J = 8,0 Hz, 1H);
4,43 (m, 1H); 4,27 (dd, J = 4,1, 9,5 Hz, 1H); 4,13 (dd, J = 5,3,
9,5 Hz, 1H); 3,79-3,42 (m, 6H); 3,14 (s, 2H); 2,30 (m, 2H); 2,16
(m, 2H).
APCI-MS: m/z 402 (MH+).
-
Schritt III:
-
(3S)-1-(4-Fluor-2-{[(2S)-2-hydroxy-3-(1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)propyl]oxy}benzoyl)-pyrrolidin-3-ol
-
Eine
Mischung von 4-Fluor-2-{[(2S)-2-hydroxy-3-(1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)propyl]oxy}-benzoesäure (Hydrochlorid)
(35 mg, 0,079 mmol) und N,N-Carbonyldiimidazol
(15,4 mg, 0,095 mmol) in DMF (1,5 ml) wurde 45 Minuten lang bei
Raumtemperatur gerührt
und mit (3S)-Pyrrolidin-3-ol (34,4 mg, 0,395 mmol) in DMF (0,5 ml)
versetzt, und die Reaktionsmischung wurde über Nacht bei Raumtemperatur
gerührt.
Die Reaktionsmischung wurde zwischen Essigsäureethylester und H2O verteilt. Die organische Phase wurde über Na2SO4 getrocknet,
filtriert und eingeengt. Der Rückstand
wurde durch Flash-Chromatographie an Kieselgel (0–2,5% Methanol
in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die Titelverbindung (15 mg) erhielt.
1H-NMR
(CD3OD, 400 MHz): δ 7,32-7,26 (m, 1H); 7,13 (d,
J = 7,3 Hz, 1H); 7,05 (t, J = 7,6 Hz, 1H); 6,94 (dt, J = 2,2 Hz,
1H); 6,82-6,75 (m, 2H); 6,67 (d, J = 7,9 Hz, 1H); 4,48 (m, 0,5H);
4,38 (m, 0,5H); 4,18-3,98 (m, 3H); 3,70 (dd, J = 5,3, 9,3 Hz, 1H);
3,66-3,46 (m, 2H); 3,37-3,18
(m, 1H); 3,00 (s, 2H); 2,78-2,51 (m, 6H); 2,15-1,78 (m, 6H).
APCI-MS: m/z 471
(MH+).
-
Beispiel 71
-
4-Fluor-2-{[(2S)-3-(5-fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy)benzoesäure (Hydrochlorid)
-
Schritt I:
-
4-Fluor-2-{[(2S)-3-(5-fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}benzoesäure-methylester
-
Eine
Mischung von 5-Fluor-3H-spiro[1-benzofuran-2,4'-piperidin]
(50 mg, 0,241 mmol) und 4-Fluor-2-[(2S)-oxiran-2-ylmethoxy]benzoesäuremethylester
(54,5 mg, 0,241 mmol) in Ethanol (1,5 ml) wurde über Nacht bei 77°C gerührt. Die
flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie an
Kieselgel (0–2,5%
Methanol in Dichlormethan) aufgereinigt, wodurch man die im Untertitel
genannte Verbindung (80 mg) erhielt.
APCI-MS: m/z 434 (MH+).
-
Schritt II:
-
4-Fluor-2-{[(2S)-3-(5-fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}benzoesäure (Hydrochlorid)
-
Eine
Lösung
von 4-Fluor-2-{[(2S)-3-(5-fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}benzoesäuremethylester
(80 mg, 0,184 mmol) in THF (1,5 ml) wurde mit einer wäßrigen Lösung von
KOH (31 mg KOH in 0,5 ml H2O) versetzt,
und die Reaktionsmischung wurde 24 Stunden lang bei Raumtemperatur
gerührt,
auf 0°C
abgekühlt
und durch Zugabe von wäßriger HCl
auf einen pH-Wert von 2 eingestellt und dann mit Essigsäureethylester
extrahiert. Die organische Phase wurde mit H2O
gewaschen, über
Na2SO4 getrocknet,
filtriert und eingeengt, wodurch man die Titelverbindung (60 mg)
erhielt.
1H-NMR (CD3OD,
400 MHz): δ 7,97
(dd, J = 6,9, 8,7 Hz, 1H); 6,97 (m, 2H); 6,88-6,79 (m, 2H); 6,72
(dd, J = 4,2, 8,8 Hz, 1H); 4,45 (m, 1H); 4,27 (dd, J = 4,1, 9,6
Hz, 1H); 4,13 (dd, J = 5,3, 9,6 Hz, 1H); 3,78-3,42 (m, 6H); 3,14
(s, 2H); 2,30 (m, 2H); 2,16 (m, 2H).
APCI-MS: m/z 420 (MH+).
-
Beispiel 72
-
(3S)-1-(4-Fluor-2-{[(2S)-3-(5-fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}benzoyl)pyrrolidin-3-ol
-
Eine
Mischung von 4-Fluor-2-{[(2S)-3-(5-fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}benzoesäure (Hydrochlorid)
(50 mg, 0,109 mmol) und N,N-Carbonyldiimidazol (21,2 mg, 0,131 mmol)
in DMF (1,5 ml) wurde 1 Stunde lang bei Raumtemperatur gerührt und
mit (3S)-Pyrrolidin-3-ol (47,5 mg, 0,545 mmol) in DMF (0,5 ml) versetzt,
und die Reaktionsmischung wurde über
Nacht bei Raumtemperatur gerührt.
Die Reaktionsmischung wurde zwischen Essigsäureethylester und H2O verteilt. Die organische Phase wurde über Na2SO4 getrocknet,
filtriert und eingeengt. Der Rückstand
wurde durch Flash-Chromatographie an Kieselgel (0–2,5% Methanol
in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die Titelverbindung (21 mg) erhielt.
1H-NMR
(CD3OD, 400 MHz): δ 7,29 (m, 1H); 6,97-6,87 (m,
2H); 6,82-6,74 (m, 2H); 6,93 (dd, J = 4,1, 8,7 Hz, 1H); 4,48 (m,
0,5H); 4,37 (m, 0,5H); 4,16-3,98 (m, 3H); 3,70 (dd, J = 5,3, 9,4
Hz, 1H); 3,67-3,47 (m, 2H); 3,36-3,18 (m, 1H); 3,05 (s, 2H); 2,78-2,52
(m, 6H); 2,16-1,78 (m, 6H).
APCI-MS: m/z 489 (MH+).
-
Beispiel 73
-
N-[(3S)-1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)pyrrolidin-3-yl]acetamid
-
Schritt I:
-
N-((3S)-1-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoyl}pyrrolidin-3-yl)acetamid
-
Eine
Mischung von 2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl]benzoesäure (Hydrochlorid)
(150 mg, 0,254 mmol) und N,N-Carbonyldiimidazol (50 mg, 0,308 mmol)
in DMF (2 ml) wurde 50 Minuten lang bei Raumtemperatur gerührt. Anschließend wurde mit
N-[(3S)-pyrrolidin-3-yl]acetamid
(110 mg, 1,26 mmol) in DMF (0,5 ml) versetzt, und die Reaktionsmischung wurde über Nacht
bei Raumtemperatur gerührt.
Die Reaktionsmischung wurde zwischen Essigsäureethylester und Wasser verteilt.
Die organische Phase wurde über
Na2SO4 getrocknet,
filtriert und eingeengt. Der Rückstand
wurde durch Flash-Chromatographie an Kieselgel (0–2% Methanol
in Dichlormethan) aufgereinigt, wodurch man die im Untertitel genannte
Verbindung (100 mg) erhielt.
APCI-MS: m/z 664 (MH+).
-
Schritt II:
-
N-[(3S)-1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)pyrrolidin-3-yl]acetamid
-
N-((3S)-1-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoyl}pyrrolidin-3-yl)acetamid
(100 mg, 0,15 mmol) wurde bei Raumtemperatur 25 Minuten lang mit
10% CF3CO2H in CH2Cl2 (3 ml) behandelt.
Die flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (0–4%
Methanol in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die Titelverbindung (22 mg) erhielt.
1H-NMR
(CD3OD, 400 MHz): δ 7,13 (m, 1H); 7,09 (dd, J =
3,7, 8,2 Hz, 1H); 7,04 (dd, J = 1,7, 8,5 Hz, 1H); 6,65 (d, J = 8,5
Hz, 1H); 6,50 (t, J = 2,0 Hz, 1H); 6,45 (dt, J = 2,2 Hz, 1H); 4,44
(m, 0,5H); 4,26 (m, 0,5H); 4,16-3,77 (m,
3H); 3,74-3,58 (m, 2H); 3,52-3,14 (m, 2H); 3,00 (s, 2H); 2,77-2,52
(m, 6H); 2,28-2,10 (m, 1H); 1,98-1,78 (m, 8H).
APCI-MS: m/z
545 (MH+).
-
Beispiel 74
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-methylbenzoesäure (Hydrochlorid)
-
Schritt I:
-
4-Methyl-2-[(2S)-oxiran-2-ylmethoxy]benzoesäuremethylester
-
Eine
Mischung von 3-Nitrobenzolsulfonsäure-(2S)-oxiran-2-ylmethylester (777,7
mg, 3,0 mmol), 2-Hydroxy-4-methylbenzoesäuremethylester
(498,5 mg, 3,0 mmol) und Cs2CO3 (1,17
g, 3,6 mmol) in DMF (10 ml) wurde über Nacht bei Raumtemperatur
gerührt.
Die Reaktionsmischung wurde zwischen Essigsäureethylester und H2O verteilt. Die organische Phase wurde über Na2SO4 getrocknet,
filtriert und eingeengt. Der Rückstand wurde
durch Flash-Chromatographie an Kieselgel (0–20% Essigsäureethylester in Petrolether)
aufgereinigt, wodurch man die im Untertitel genannte Verbindung
(500 mg) erhielt.
1H-NMR (CDCl3, 400 MHz): δ 7,75 (d, J = 7,9 Hz, 1H); 6,84
(d, J = 7,9 Hz, 1H); 6,81 (s, 1H); 4,33 (dd, J = 3,0, 11,2 Hz, 1H);
4,12 (dd, J = 4,8, 11,2 Hz, 1H); 3,89 (s, 3H); 3,42 (m, 1H); 2,94
(m, 2H); 2,38 (s, 3H).
APCI-MS: m/z 223 (MH+).
-
Schritt II:
-
2-{((2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-methylbenzoesäuremethylester
-
Eine
Mischung von 5-Chlor-3H-spiro[1-benzofuran-2,4'-piperidin]
(223,7 mg, 1,0 mmol) und 4-Methyl-2-[(2S)-oxiran-2-ylmethoxy]benzoesäuremethylester
(222,24 mg, 1,0 mmol) in Ethanol (2 ml) wurde 5 Stunden lang bei
80°C gerührt. Die
flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie an
Kieselgel (0–2%
Methanol in Dichlormethan) aufgereinigt, wodurch man die im Untertitel
genannte Verbindung (410 mg) erhielt.
1H-NMR
(CDCl3, 400 MHz): δ 7,76 (d, J = 8,4 Hz, 1H); 7,13
(s, 1H); 7,08 (dd, J = 2,2, 8,5 Hz, 1H); 6,85 (m, 2H); 6,68 (d,
J = 8,4 Hz, 1H); 4,24 (m, 1H); 4,19 (dd, J = 4,3, 9,2 Hz, 1H); 4,08
(dd, J = 6,0, 9,1 Hz, 1H); 3,90 (s, 3H); 3,02 (s, 2H); 2,94-2,67
(m, 6H); 2,40 (s, 3H); 2,06-1,86 (m, 4H).
APCI-MS: m/z 448
(MH+).
-
Schritt III:
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'yl)-2-hydroxypropyl]oxy}-4-methylbenzoesäure (Hydrochlorid)
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'- piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-methylbenzoesäuremethylester
(400 mg, 0,89 mmol) wurde in Ethanol aufgenommen und mit einer wäßrigen Lösung von KOH
(2,6 g KOH 2,6 ml H2O) versetzt, und die
Reaktionsmischung wurde 5 Stunden lang bei Rückflußtemperatur gerührt, auf
0°C abgekühlt und
durch Zugabe von wäßriger HCl
auf einen pH-Wert von 2 eingestellt und dann mit Essigsäureethylester
extrahiert. Die organische Phase wurde mit H2O
gewaschen, über
Na2SO4 getrocknet,
filtriert und eingeengt, wodurch man die Titelverbindung (330 mg)
erhielt.
1H-NMR (CD3OD,
400 MHz): δ 7,82
(d, J = 7,9 Hz, 1H); 7,20 (s, 1H); 7,10 (dd, J = 2,2, 8,5 Hz, 1H);
6,98 (s, 1H); 6,90 (d, J = 8,1 Hz, 1H), 6,74 (d, J = 8,5 Hz, 1H);
4,44 (m, 1H); 4,29 (dd, J = 4,0, 9,5 Hz, 1H); 4,12 (dd, J = 5,4,
9,6 Hz, 1H); 3,78-3,42 (m, 6H); 3,14 (s, 2H); 2,40 (s, 3H); 2,30
(m, 2H); 2,16 (m, 2H).
APCI-MS: m/z 432 (MH+).
-
Beispiel 75
-
(3S)-1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy])4-methylbenzoyl)pyrrolidin-3-ol
-
Eine
Mischung von 2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'yl)-2-hydroxypropyl]oxy}-4-methylbenzoesäure (Hydrochlorid)
(150 mg, 0,32 mmol) und N,N-Carbonyldiimidazol (65 mg, 0,4 mmol)
in DMF (2,5 ml) wurde 45 Minuten lang bei Raumtemperatur gerührt. Anschließend wurde
mit (3S)-Pyrrolidin-3-ol (139,4 mg, 1,6 mmol in DMF (0,5 ml) versetzt,
und die Reaktionsmischung wurde über
Nacht bei Raumtemperatur gerührt.
Die Reaktionsmischung wurde zwischen Essigsäureethylester und H2O verteilt. Die organische Phase wurde über Na2SO4 getrocknet,
filtriert und eingeengt. Der Rückstand
wurde durch Flash-Chromatographie an Kieselgel (0–2,5% Methanol
in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die Titelverbindung (90 mg) erhielt.
1H-NMR
(CD3OD, 400 MHz): δ 7,13 (m, 2H); 7,04 (dd, J =
2,1, 8,5 Hz, 1H); 6,92 (s, 1H); 6,85 (d, J = 7,6 Hz, 1H); 6,60 (d,
J = 8,5 Hz, 1H); 4,47 (m, 0,5H); 4,35 (m, 0,5H); 4,17-3,96 (m, 3H);
3,74-3,44 (m, 3H); 3,37-3,18 (m, 1H); 3,00 (s, 2H); 2,77-2,50 (m,
6H); 2,36 (s, 3H); 2,14-1,78 (m, 6H).
APCI-MS: m/z 501 (MH+).
-
Beispiel 76
-
2-{[(2S)-3-(5-Fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-methylbenzoesäure (Hydrochlorid)
-
Schritt I:
-
2-{[(2S)-3-(5-Fluor-1'H,3H-spiro-[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-methylbenzoesäuremethylester
-
Eine
Mischung von 5-Fluor-3H-spiro[1-benzofuran-2,4'-piperidin]
(85 mg, 0,41 mmol) und 4-Methyl-2-[(2S)-oxiran-2-ylmethoxy]benzoesäuremethylester
(91 mg, 0,41 mmol) in Ethanol (2 ml) wurde 4,5 Stunden lang bei
85°C gerührt. Die
flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie an
Kieselgel (0–2,5%
Methanol in Dichlormethan) aufgereinigt, wodurch man die im Untertitel
genannte Verbindung (136 mg) erhielt.
APCI-MS: m/z 430 (MH+).
-
Schritt II:
-
2-{[(2S)-3-(5-Fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-methylbenzoesäure (Hydrochlorid)
-
2-{[(2S)-3-(5-Fluor-1'H,3H-spiro[1-benzofuran-2,4'- piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-methylbenzoesäuremethylester
(133 mg, 0,309 mmol) wurde in Ethanol (2,5 ml) aufgenommen und mit
wäßriger KOH (902
mg KOH in 1 ml H2O) versetzt. Die Reaktionsmischung
wurde 5 Stunden lang bei Rückflußtemperatur gerührt, auf
0°C abgekühlt und
durch Zugabe von wäßriger HCl
auf einen pH-Wert von 2 eingestellt und dann mit Essigsäureethylester
extrahiert. Die organische Phase wurde mit H2O
gewaschen, über
Na2SO4 getrocknet,
filtriert und eingeengt, wodurch man die Titelverbindung (50 mg)
erhielt.
1H-NMR (CD3OD,
400 MHz): δ 7,74
(d, J = 7,9 Hz, 1H); 6,96 (m, 2H); 6,89 (d, J = 8,0 Hz, 1H); 6,84
(m, 1H); 6,71 (dd, J = 4,1, 8,7 Hz, 1H); 4,43 (m, 1H); 4,28 (dd,
J = 4,0, 9,4 Hz, 1H); 4,11 (dd, J = 5,6, 9,5 Hz, 1H); 3,75-3,40
(m, 6H); 3,14 (s, 2H); 2,39 (s, 3H); 2,32 (m, 2H); 2,14 (m, 2H).
APCI-MS:
m/z 416 (MH+).
-
Beispiel 77
-
(2S)-1-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-3-(2-{[2-(hydroxymethyl)morpholin-4-yl]carbonyl)-5-methylphenoxy)propan-2-ol
-
Schritt I:
-
2,4-Morpholindicarbonsäure-4-(tert.-butyl)ester-2-methylester
-
Methyliodid
(9,38 ml, 150 mmol) wurde zu einer Suspension von 4-(tert.-Butoxycarbonyl)-2-morpholincarbonsäure (14,5
g, 62,6 mmol) und trockenem K2CO3 (17,3 g, 125 mmol) in trockenem DMF (360
ml) gegeben. Die Mischung wurde über
Nacht bei Raumtemperatur gerührt, über Celite
filtriert und eingeengt. Der Rückstand
wurde zwischen CH2Cl2 und
H2O verteilt. Die organische Phase wurde über Na2SO4 getrocknet,
filtriert und eingeengt, wodurch man die im Untertitel genannte Verbindung
(22 g) erhielt.
1H-NMR (CDCl3, 400 MHz): δ 4,07 (dd, 2H); 3,99 (m, 1H);
3,77 (s, 3H); 3,73 (m, 1H); 3,55 (m, 1H); 3,07 (m, 2H); 1,45 (s,
9H).
-
Schritt II:
-
2-(Hydroxymethyl)-4-morpholincarbonsäure-tert.-butylester
-
2,4-Morpholindicarbonsäure-4-(tert.-butyl)ester-2-methylester (62,6
mmol) wurde in trockenem THF (100 ml) gelöst und bei 0°C tropfenweise
mit einer Suspension von Lithiumborhydid (2,5 g, 115 mmol) in trockenem
THF (100 ml) versetzt. Nach dem Ende der Zugabe wurde die Reaktionsmischung über Nacht
bei Raumtemperatur gerührt.
Wasser (10 ml) wurde zugesetzt, und die Mischung wurde 1 Stunde
lang bei Raumtemperatur gerührt.
Die flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde zwischen Essigsäureethylester
und H2O verteilt. Die organische Phase wurde
nacheinander mit 0,5 M wäßriger HCl,
gesättigter
wäßriger NaHCO3-Lösung und
H2O gewaschen. Die organische Phase wurde über Na2SO4 getrocknet,
filtriert und eingeengt, wodurch man die im Untertitel genannte
Verbindung (13,3 g) erhielt.
1H-NMR
(CDCl3, 400 MHz): δ 3,88 (m, 3H); 3,46-3,42 (m,
4H); 2,93 (m, 1H); 2,75 (m, 1H); 2,09 (m, 1H); 1,46 (s, 9H).
-
Schritt III:
-
Trifluoressigsäuremorpholin-2-ylmethylester
(Trifluoressigsäuresalz)
-
2-(Hydroxymethyl)-4-morpholincarbonsäure-tert.-butylester
(5,13 g, 23,61 mmol) wurde bei Raumtemperatur 3 Stunden lang mit
CF3CO2H (20 ml)
in CH2Cl2 (50 ml)
behandelt. Die flüchtigen
Bestandteile wurden im Vakuum entfernt, wodurch man die im Untertitel
genannte Verbindung erhielt (7,6 g).
1H-NMR
(DMSO-d6, 400 MHz): δ 9,25 (bs, 2H); 3,86 (dd, J
= 3,3, 12,6 Hz, 1H); 3,62 (m, 2H); 3,39 (m, 2H); 3,19 (m, 2H); 2,96
(t, J = 11,2 Hz, 1H); 2,76 (t, J = 11,2 Hz, 1H).
-
Schritt IV:
-
(2S)-1-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-3-(2-{[2-(hydroxymethyl)morpholin-4-yl]carbonyl)-5-methylphenoxy)propan-2-ol
-
Eine
Mischung von 2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'yl)-2-hydroxypropyl]oxy}-4-methylbenzoesäure (Hydrochlorid)
(100 mg, 0,213 mmol) und N,N-Carbonyldiimidazol (41,5 mg, 0,255
mmol) in DMF (2,5 ml) wurde 50 Minuten lang bei Raumtemperatur gerührt und
dann mit Trifluoressigsäuremorpholin-2-ylmethylester (Trifluoressigsäuresalz)
(347 mg, 1,06 mmol) in DMF (1 ml) gefolgt von Et3N (0,3
ml) versetzt, und die Reaktionsmischung wurde 5 Stunden lang bei
Raumtemperatur gerührt.
Die Reaktionsmischung wurde zwischen Essigsäureethylester und H2O verteilt. Die organische Phase wurde über Na2SO4 getrocknet,
filtriert und eingeengt. Der Rückstand
wurde durch Flash-Chromatographie an Kieselgel aufgereinigt (0–2,5% Methanol
in Dichlormethan, 0,2% NH4OH), wodurch man
die Titelverbindung (58 mg) erhielt.
APCI-MS: m/z 531 (MH+).
-
Beispiel 78
-
(3S)-1-(2-{[(2S)-3-(5-Fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-methylbenzoyl)pyrrolidin-3-ol
-
Eine
Mischung von 2-{[(2S)-3-(5-Fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}- 4-methylbenzoesäure (Hydrochlorid)
(45 mg, 0,099 mmol) und N,N-Carbonyldiimidazol (20 mg, 0,123 mmol)
in DMF (2 ml) wurde 50 Minuten lang bei Raumtemperatur gerührt und
mit (3S)-Pyrrolidin-3-ol (43 mg, 0,495 mmol) in DMF (1 ml) versetzt,
und die Reaktionsmischung wurde über
Nacht bei Raumtemperatur gerührt.
Die Reaktionsmischung wurde zwischen Essigsäureethylester und H2O verteilt. Die organische Phase wurde über Na2SO4 getrocknet,
filtriert und eingeengt. Der Rückstand
wurde durch Flash-Chromatographie an Kieselgel (0–2,5% Methanol
in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die Titelverbindung (35 mg) erhielt.
1H-NMR
(CD3OD, 400 MHz): δ 7,14 (dd, J = 1,0, 7,6 Hz,
1H); 6,94-6,84 (m, 3H); 6,77 (m, 1H); 6,62 (dd, J = 4,2, 8,8 Hz,
1H); 4,48 (m, 0,5H); 4,35 (m, 0,5H); 4,16-3,96 (m, 3H); 3,73-3,43
(m, 3H); 3,38-3,18 (m, 1H); 3,00 (s, 2H); 2,76-2,52 (m, 6H); 2,35
(s, 3H); 2,12-1,77 (m, 6H).
APCI-MS: m/z 485 (MH+).
-
Beispiel 79
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-N-{[(4R)-2,5-dioxoimidazolidin-4-yl]methyl)-4-hydroxybenzamid
-
Schritt I:
-
2-{((2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2‚4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-N-{[(4R)-2,5-dioxoimidazolidin-4-yl]methyl}-4-[(4-methoxybenzyl)-oxy]benzamid
-
Eine
Mischung von 2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy)-4-[(4-methoxybenzyl]benzoesäure (Hydrochlorid)
(125 mg, 0,211 mmol) und N,N-Carbonyldiimidazol (43 mg, 0,264 mmol)
in DMF (3 ml) wurde 40 Minuten lang bei Raumtemperatur gerührt. Anschließend wurde mit
(5R)-5- (Aminomethyl)imidazolidin-2,4-dion
(Hydrochlorid) (150 mg, 0,906 mmol) gefolgt von Et3N
(0,54 ml (3,62 mmol) versetzt, und die Reaktionsmischung wurde über Nacht
bei Raumtemperatur gerührt.
Die Reaktionsmischung wurde zwischen Essigsäureethylester und Wasser verteilt.
Die organische Phase wurde über Na2SO4 getrocknet,
filtriert und eingeengt. Der Rückstand
wurde durch Flash-Chromatographie an Kieselgel (0–2,5% Methanol
in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die im Untertitel genannte Verbindung (30 mg) erhielt.
APCI-MS:
m/z 665 (MH+).
-
Schritt II:
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-N-{[(4R)-2,5-dioxoimidazolidin-4-yl]methyl}-4-hydroxybenzamid
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-N-{[(4R)-2,5-dioxoimidazolidin-4-yl]methyl}-4-[(4-methoxybenzyl]-oxy]benzamid (28
mg, 0,042 mmol) wurde bei Raumtemperatur 25 Minuten lang mit 10%
CF3CO2H in CH2Cl2 (3 ml) behandelt.
Die flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie an
Kieselgel (0–5%
Methanol in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die Titelverbindung (9 mg) erhielt.
1H-NMR
(CD3OD, 400 MHz): δ 7,83 (d, J = 8,6 Hz, 1H); 7,14
(s, 1H); 7,04 (dd, J = 1,9, 8,3 Hz, 1H); 6,65 (d, J = 8,5 Hz, 1H);
6,53 (s, 1H); 6,48 (m, 1H); 4,37-4,17 (m, 3H); 4,07 (m, 1H); 3,90-3,64
(m, 2H); 3,03 (s, 2H); 2,85-2,59 (m, 6H); 2,02-1,82 (m, 4H).
APCI-MS:
m/z 545 (MH+).
-
Beispiel 80
-
1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)-3-(trifluormethyl)pyrrolidin-3-ol
-
Schritt I:
-
3-Hydroxy-3-(trifluormethyl)pyrrolidin-1-carbonsäure-tert.-butylester
-
3-Oxopyrrolidin-1-carbonsäure-tert.-butylester
(926 mg, 5,0 mmol) wurde in THF (10 ml) gelöst, und die Lösung wurde
auf 0°C
abgekühlt
und mit Trimethyl(trifluormethyl)silan (0,872 ml) und Tetrabutylammoniumfluorid
(TBAF) (176 mg, 0,557 mmol) versetzt. Das Eisbad wurde entfernt
und die Reaktionsmischung wurde über
Nacht bei Raumtemperatur gerührt.
Eine gesättigte
wäßrige Lösung von
NH4Cl (8 ml) wurde zugegeben, und es wurde
weitergerührt.
Nach 15 Minuten wurde mit TBAF (2,36 g TBAF in 7,5 ml THF) versetzt,
und die Reaktionsmischung wurde 1 Stunde lang bei Raumtemperatur
gerührt.
Die Reaktionsmischung wurde mit Essigsäureethylester extrahiert, mit
H2O gewaschen, über Na2SO4 getrocknet, filtriert und eingeengt. Der Rückstand
wurde durch Flash-Chromatographie an Kieselgel (0–40% Essigsäureethylester
in Petrolether) aufgereinigt, wodurch man die im Untertitel genannte
Verbindung (800 mg) erhielt.
1H-NMR
(CDCl3, 400 MHz): δ 3,78-3,38 (m, 4H); 2,25 (m,
1H); 2,00 (m, 1H); 1,40 (s, 9H)
-
Schritt II:
-
3-(Trifluormethyl)pyrrolidin-3-ol (Trifluoracetat)
-
3-Hydroxy-3-(trifluormethyl)pyrrolidin-1-carbonsäuretert.-butylester
(310 mg, 1,21 mmol) wurde bei Raumtemperatur 4 Stunden lang mit
20% CF3CO2H in CH2Cl2 behandelt. Die
flüchtigen
Bestandteile wurden im Vakuum entfernt, wodurch man die im Untertitel
genannte Verbindung (330 mg) erhielt.
1H-NMR
(CD3OD, 400 MHz): δ 3,72-3,59 (m, 4H); 2,38 (m,
1H); 2,22 (m, 1H).
APCI-MS: m/z 156 (MH+).
-
Schritt III:
-
1-{2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoyl}-3-(trifluormethyl)pyrrolidin-3-ol
-
Eine
Mischung von 2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl]benzoesäure (Hydrochlorid)
(150 mg, 0,254 mmol) und N,N-Carbonyldiimidazol (51,5 mg, 0,317
mmol) in DMF (3 ml) wurde 40 Minuten lang bei Raumtemperatur gerührt. Anschließend wurde mit
(3-(Trifluormethyl)pyrrolidin-3-ol
(Trifluoracetat) (326 mg, 1,21 mmol) gefolgt von Et3N
(0,337 ml 2,42 mmol) versetzt, und die Reaktionsmischung wurde 20
Stunden lang bei Raumtemperatur gerührt. Die Reaktionsmischung
wurde zwischen Essigsäureethylester
und Wasser verteilt. Die organische Phase wurde über Na2SO4 getrocknet, filtriert und eingeengt. Der
Rückstand
wurde durch Flash-Chromatographie an Kieselgel (0–2,0% Methanol
in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die im Untertitel genannte Verbindung (83 mg) erhielt.
APCI-MS:
m/z 691 (MH+).
-
Schritt IV:
-
1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)-3-(trifluormethyl)pyrrolidin-3-ol
-
1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoyl}-3-(trifluormethyl)pyrrolidin-3-ol
(83 mg, 0,12 mmol) wurde bei Raumtemperatur 25 Minuten lang mit
10% CF3CO2H in CH2Cl2 (3 ml) behandelt.
Die flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (0–3%
Methanol in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die Titelverbindung (15 mg) erhielt.
1H-NMR
(CD3OD, 400 MHz): δ 7,16-7,09 (m, 2H); 7,05 (m,
1H); 6,66 (d, J = 8,5 Hz, 1H); 6,50 (s, 1H); 6,46 (d, J = 8,3 Hz,
1H); 4,12 (m, 1H); 4,00 (m, 2H); 3,89-3,40 (m, 4H); 3,02 (s, 2H);
2,87-2,60 (m, 6H); 2,35-1,80 (m, 6H).
APCI-MS: m/z 571 (MH+).
-
Beispiel 81
-
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-{[3-(trifluormethyl)pyrrolidin-1-yl]carbonyl}phenol
-
Schritt I:
-
3-(Trifluormethyl)pyrrolidin-1-carbonsäure-tert.-butylester
-
Eine
Lösung
von 3-Hydroxy-3-(trifluormethyl)pyrrolidin-1-carbonsäure-tert.-butylester (468 mg,
1,83 mmol) in Pyridin (10 ml) wurde mit SOCl2 (1,71
ml) versetzt, und die Reaktionsmischung wurde unter Stickstoff 25
Minuten lang bei Rückflußtemperatur
gerührt,
auf Raumtemperatur abgekühlt,
mit H2O (20 ml) versetzt und mit Essigsäureethylester
extrahiert. Die vereinigten organischen Phasen wurden nacheinander
mit verdünnter wäßriger HCl,
gesättigter
wäßriger NaHCO3-Lösung
und H2O gewaschen. Die organische Phase
wurde über Na2SO4 getrocknet,
filtriert und eingeengt. Der Rückstand
wurde in Ethanol (10 ml) gelöst
und mit Pd/C (10%) (300 mg) versetzt, und die Mischung wurde über das
Wochenende bei Raumtemperatur hydriert. Der Katalysator wurde abfiltriert.
Das Filtrat wurde im Vakuum eingeengt, wodurch man die im Untertitel
genannte Verbindung (100 mg) erhielt.
APCI-MS: m/z 140 (MH+-Boc).
-
Schritt II:
-
3-(Trifluormethyl)pyrrolidin (Trifluoracetat)
-
3-(Trifluormethyl)pyrrolidin-1-carbonsäure-tert.-butylester
(100 mg, 0,42 mmol) wurde bei Raumtemperatur über Nacht mit 20% CF3CO2H in CH2Cl2 behandelt. Die
flüchtigen
Bestandteile wurden im Vakuum entfernt, wodurch man die im Untertitel
genannte Verbindung (106 mg) erhielt.
APCI-MS: m/z 140 (MH+).
-
Schritt III:
-
(2S)-1-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-3-(5-[(4-methoxybenzyl)oxy]-2-{[3-(trifluormethyl)pyrrolidin-1-yl]carbonyl}phenoxy)-propan-2-ol
-
Eine
Mischung von 2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl]benzoesäure (Hydrochlorid)
(177 mg, 0,3 mmol) und N,N-Carbonyldiimidazol (61 mg, 0,375 mmol)
in DMF (3 ml) wurde 45 Minuten lang bei Raumtemperatur gerührt und
mit 3-(Trifluormethyl)pyrrolidin (Trifluoracetat) (106 mg, 0,42
mmol) in DMF (1 ml) gefolgt von Et3N (0,17
ml, 1,2 mmol) versetzt, und die Reaktionsmischung wurde über Nacht
bei Raumtemperatur gerührt.
Die Reaktionsmischung wurde zwischen Essigsäureethylester und H2O verteilt. Die organische Phase wurde über Na2SO4 getrocknet,
filtriert und eingeengt. Der Rückstand
wurde durch Flash-Chromatographie
an Kieselgel (0–1%
Methanol in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die im Untertitel genannte Verbindung (89 mg) erhielt.
APCI-MS:
m/z 675 (MH+).
-
Schritt IV:
-
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-{[3-(trifluormethyl)pyrrolidin-1-yl]carbonyl)phenol
-
(2S)-1-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-3-(5-[(4-methoxybenzyl)oxy]-2-{[3-(trifluormethyl)pyrrolidin-1-yl]carbonyl}phenoxy)propan-2-ol (88 mg, 0,13 mmol)
wurde bei Raumtemperatur 25 Minuten lang mit 10% CF3CO2H in CH2Cl2 (3 ml) behandelt. Die flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (0–3%
Methanol in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die Titelverbindung (22 mg) erhielt.
1H-NMR
(CD3OD, 400 MHz): δ 7,14 (s, 1H); 7,08 (dd, J =
4,3, 8,3 Hz, 1H); 7,05 (m, 1H); 6,66 (d, J = 8,5 Hz, 1H); 6,51 (m,
1H); 6,46 (m, 1H); 4,15-3,42 (m, 7H); 3,18 (m, 1H); 3,02 (s, 2H);
2,78-2,52 (m, 6H); 2,34-1,80
(m, 6H).
APCI-MS: m/z 555 (MH+).
-
Beispiel 82
-
N-[2-(Acetylamino)ethyl]-2-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzamid
-
Schritt I:
-
N-[2-(Acetylamino)ethyl]-2-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzamid
-
Eine
Mischung von 2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl]benzoesäure (Hydrochlorid)
(100 mg, 0,169 mmol) und N,N-Carbonyldiimidazol (834 mg, 0,211 mmol)
in DMF (3 ml) wurde 45 Minuten lang bei Raumtemperatur gerührt und
mit N-(2-Aminoethyl)acetamid (86 mg, 0,845 mmol) versetzt, und die
Reaktionsmischung wurde über
Nacht bei Raumtemperatur gerührt.
Die Reaktionsmischung wurde zwischen Essigsäureethylester und H2O verteilt. Die organische Phase wurde über Na2SO4 getrocknet,
filtriert und eingeengt. Der Rückstand
wurde durch Flash-Chromatographie an Kieselgel (0–2% Methanol
in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die im Untertitel genannte Verbindung (77 mg) erhielt.
1H-NMR (CDCl3, 400
MHz): δ 8,38
(t, J = 5,6 Hz, 1H); 8,10 (d, J = 8,8 Hz, 1H); 7,36 (d, J = 8,6
Hz, 2H); 7,13 (m, 2H); 7,07 (dd, J = 2,1, 8,4 Hz, 1H); 6,94 (d,
J = 8,6 Hz, 2H); 6,73-6,65 (m, 3H); 6,57 (d, J = 2,2 Hz, 1H); 5,02
(s, 2H); 4,34 (m, 1H); 4,22 (dd, J = 3,0, 9,7 Hz, 1H); 4,00 (dd,
J = 6,3, 9,7 Hz, 1H); 3,83 (s, 3H); 3,65 (m, 2H); 3,48 (m, 2H);
3,06-2,67 (m, 8H); 2,08 (m, 4H); 1,97 (s, 3H).
APCI-MS: m/z
638 (MH+).
-
Schritt II:
-
N-(2-(Acetylamino)ethyl]-2-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy)-4-hydroxybenzamid
-
N-[2-(Acetylamino) ethyl]-2-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzamid
(72 mg, 0,112 mmol) wurde bei Raumtemperatur 25 Minuten lang mit
10% CF3CO2H in CH2Cl2 (3 ml) behandelt.
Die flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (0–3,5%
Methanol in Dichlormethan, 0,2% NH4OH) aufgereinigt, wodurch
man die Titelverbindung (32 mg) erhielt.
1H-NMR
(CD3OD, 400 MHz): δ 7,82 (d, J = 8,7 Hz, 1H); 7,14 (s,
1H); 7,04 (dd, J = 2,2, 8,5 Hz, 1H); 6,66 (d, J = 8,5 Hz, 1H); 6,53
(d, J = 2,1 Hz, 1H); 6,49 (dd, J = 2,1, 8,7 Hz, 1H); 4,23 (m, 2H);
4,07 (dd, J = 7,0, 10,7 Hz, 1H); 3,51 (t, J = 6,1 Hz, 2H); 3,39
(t, J = 6,1 Hz, 2H); 3,02 (s, 2H); 2,74 (bs, 4H); 2,64 (d, J = 6,0
Hz, 2H); 1,99-1,82 (m, 7H)
APCI-MS: m/z 518 (MH+).
-
Beispiel 83
-
N-(5-Chlor-2-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-methoxyphenyl)acetamid
-
Schritt I:
-
N-(5-Chlor-2-hydroxy-4-methoxyphenyl)acetamid
-
Diese
Verbindung wurde wie von Kun Hoe Chung; Kyong Mahn Kim; Jae Nyoung
Kim und Eung Kul Ryu, Synth. Comm., 1991, 21 (18&19), 1917-1922, beschrieben unter
Verwendung von N-(2-Hydroxy-4-methoxyphenyl)acetamid als Ausgangsmaterial
dargestellt.
APCI-MS: m/z 216 [MH+]
-
Schritt II:
-
N-{5-Chlor-4-methoxy-2-[(2S)-oxiran-2-ylmethoxy]-phenyl}acetamid
-
Eine
Suspension von N-(5-Chlor-2-hydroxy-4-methoxyphenyl)acetamid (227
mg, 1,05 mmol) und Caesiumcarbonat (376 mg, 1,25 mmol) in 1-Methyl-2-pyrrolidinon
(2 ml), wurde tropfenweise mit 3-Nitrobenzolsulfonsäure-(2S)-oxiran-2-ylmethylester
(301 mg, 1,16 mmol) gelöst
in 2-Methyl-2-pyrrolidin
(2 ml) versetzt. Die auf diese Weise erhaltene braune Suspension
wurde über
Nacht bei Raumtemperatur gerührt.
Die Mischung wurde zwischen Wasser und Essigsäureethylester verteilt. Die
organi sche Phase wurde über
wasserfreiem Magnesiumsulfat getrocknet, filtriert und eingeengt,
wodurch man als Rohausbeute 280 mg (98%) der Titelverbindung erhielt.
APCI-MS:
m/z 272 [MH+]
-
Schritt III:
-
N-(5-Chlor-2-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-methoxyphenyl)acetamid
-
Eine
Lösung
von N-(5-Chlor-4-methoxy-2-[(2S)-oxiran-2-ylmethoxy]phenyl}acetamid (101 mg, 0,37 mmol)
und 5-Chlor-3H-spiro[1-benzofuran-2,4'-piperidin] (83,5
mg, 0,37 mmol) in Ethanol (10 ml) wurde über Nacht unter Rückfluß erhitzt
und dann eingeengt. Das Rohprodukt wurde an C18 ("Kromasil"-Säule, 10 μm, Acetonitril/Wasser
25/75 bis 50/50 im Verlauf von 30 Minuten mit 0,1% Trifluoressigsäure) aufgereinigt.
Die reinen Fraktionen wurden gesammelt und lyophilisiert, wodurch
man 116 mg (51%) der Titelverbindung in Form des Trifluoracetatsalzes
erhielt.
1H-NMR (400 MHz, (CD3)2CO) δ: 8,36 (1H,
s); 7,24 (1H, bs); 7,14 (1H, dd); 6,87 (1H, s); 6,76 (1H, d); 4,59-4,52 (1H, m); 4,25-4,15
(2H, m); 3,89-3,40 (6H, m); 3,88 (3H, s); 3,20 (2H, bs); 2,45-2,19
(4H, m); 2,12 (3H, s).
APCI-MS: m/z 495 [MH+]
-
Beispiel 84
-
(3S)-N-(5-Chlor-2-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-phenyl)-3-hydroxypyrrolidin-1-carbonsäureamid
-
Schritt I:
-
(3S)-N-(5-Chlor-2-hydroxyphenyl)-3-hydroxypyrrolidin-1-carbonsäureamid
-
Eine
Mischung von 5-Chlor-1,3-benzoxazol-2(3H)-on (577 mg, 0,34 mmol)
und (3S)-Pyrrolidin-3-ol (0,6 ml, 0,74 mmol) wurde 2 Stunden lang
auf 90°C
erhitzt. Das auf diese Weise erhaltene verfestigte Öl wurde an
Kieselgel (Dichlormethan/Methanol) aufgereinigt, wodurch man die
Titelverbindung (768 mg, 88%) erhielt.
APCI-MS: m/z 257 [MH+]
-
Schritt II:
-
(3S)-N-(5-Chlor-2-[(2S)-oxiran-2-ylmethoxy]phenyl)-3-hydroxypyrrolidin-1-carbonsäureamid
-
Eine
Lösung
von (3S)-N-(5-Chlor-2-hydroxyphenyl)-3-hydroxypyrrolidin-1-carbonsäureamid
(232 mg, 0,90 mmol), 3-Nitrobenzolsulfonsäure-(2S)-oxiran-2-ylmethylester (234
mg, 0,90 mmol) und Caesiumcarbonat (369 mg, 1,13 mmol) in Dimethylformamid
(9 ml) wurde über
Nacht bei Raumtemperatur gerührt.
Die Mischung wurde zwischen Wasser und Essigsäureethylester verteilt, und
die organische Phase wurde zweimal mit Wasser und einmal mit Kochsalzlösung gewaschen
und anschließend
eingeengt. Das Rohprodukt wurde durch HPLC an C18 ("Kromasil"-Säule, 10 μm, Acetonitril/Wasser
35/65 a 85/15 sur 30 Minuten) aufgereinigt, wodurch man die Titelverbindung
(82 mg, 29%) erhielt.
APCI-MS: m/z 313 [MH+]
-
(3S)-N-(5-Chlor-2-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4-piperidin]-1'-yl)-2-hydroxypropyl]oxy)-phenyl)-3-hydroxypyrrolidin-1-carbonsäureamid
-
Eine
Lösung
von (3S)-N-{5-Chlor-2-[(2S)-oxiran-2-yl-methoxy]phenyl}-3-hydroxypyrrolidin-1-carbonsäureamid
(63,2 mg, 0,20 mmol) und 5-Chlor-3H-spiro[1-benzofuran-2,4'-piperidin] (45,4
mg, 0,20 mmol) in Isopropanol (8 ml) wurde über Nacht bei 80°C gerührt. Das
eingeengte Rohprodukt wurde durch HPLC an C18 ("Kromasil"- Säule, 10 μm, Acetonitril/Wasser
50/50 bis 85/15 im Verlauf von 45 Minuten, mit 0,1% Trifluoressigsäure) aufgereinigt.
Die reinen Fraktionen wurden gesammelt und lyophilisiert, wodurch
man die Titelverbindung (83 mg, 65%) in Form des Trifluoracetatsalzes
erhielt.
1H-NMR (400 MHz, DMSO-d6) δ:
9,69 (1H, bs); 9,60 (1H, bs); 8,00 (1H, d); 7,39 (1H, bs); 7,29
(1H, bs); 7,16 (1H, d); 7,06 (1H, d); 7,00 (1H, dd); 6,78 (1H, d);
4,41-4,34 (1H, m); 4,32 (1H, bs); 4,09-3,97 (2H, m); 3,62-3,40 (7H,
m); 3,36-3,16 (4H, m); 3,10 (2H, s); 2,22-2,03 (3H, m); 2,03-1,90
(1H, m); 1,88-1,79 (1H, m).
APCI-MS: m/z 536 [MH+]
-
Beispiel 85
-
(3S)-N-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}phenyl)-3-hydroxypyrrolidin-1-carbonsäureamid
-
Die
Titelverbindung wurde unter Verwendung von 1,3-Benzoxazol-2(3H)-on nach Verfahren analog den
in Beispiel 84 beschriebenen Verfahren dargestellt.
1H-NMR (400 MHz, DMSO-d6) δ: 9,70 (1H,
bs); 9,62 (1H, bs); 7,82 (1H, d); 7,36 (1H, s); 7,29 (1H, bs); 7,00 (2H,
dt); 6,91 (1H, t); 6,80 (1H, d); 4,41-4,34 (1H, m); 4,32 (1H, bs);
4,09-3,97 (2H, m); 3,62-3,41 (7H, m); 3,35-3,15 (4H, m); 3,10 (2H,
s); 2,22-2,03 (3H, m); 2,03-1,90 (1H, m); 1,88-1,79 (1H, m).
APCI-MS:
m/z 502 [MH+]
-
Beispiel 86
-
N-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin)-1'-yl)-2-hydroxypropyl]oxy]phenyl)-4-hydroxypiperidin-1-carbonsäureamid
-
Die
Titelverbindung wurde unter Verwendung von 1,3-Benzoxazol-2(3H)-on und 4-Hydroxypiperidin nach Verfahren
analog den in Beispiel 84 beschriebenen Verfahren dargestellt.
1H-NMR (400 MHz, DMSO-d6) δ: 9,67 (1H,
bs); 9,60 (1H, bs); 7,81 (1H, s); 7,63 (1H, d); 7,30 (1H, d); 7,15
(1H, d); 7,06-6,98 (2H, m); 6,91 (1H, dt); 6,80 (1H, d); 4,41-4,28
(2H, m); 4,08-3,95 (2H, m); 3,84-3,75 (2H, m); 3,69 (1H, sept);
3,63-3,41 (3H, m); 3,32-3,04 (4H, m); 3,10 (2H, s); 2,22-1,98 (4H,
m); 1,80-1,71 (2H, m); 1,41-1,29 (2H, m).
APCI-MS: m/z 516
[MH+]
-
Beispiel 87
-
N-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy)phenyl)harnstofftrifluoracetat
(Salz)
-
Schritt I:
-
(2S)-3-(2-Aminophenoxy)-1-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)propan-2-olbis(hydrochlorid)
(Salz)
-
N-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}phenyl)acetamid
(117 mg, 0,27 mmol) wurde bei 100°C
2 Stunden lang in 1 M Salzsäure
(2 ml) gerührt.
Die Lösung wurde
mit Wasser verdünnt
und lyophilisiert, wodurch man die im Untertitel genannte Verbindung
in Form eines weißen
amorphen Feststoffs (112 mg) erhielt.
1H-NMR
(MeOH-d4, 400 MHz): δ 7,49-7,44 (m, 1H); 7,40 (d,
J = 8,0 Hz, 1H); 7,25 (d, J = 8,4 Hz, 1H); 7,21 (bs, 1H); 7,15-7,09
(m, 2H); 6,75 (d, J = 8,4 Hz, 1H); 4,64-4,52 (m, 1H); 4,21 (d, J
= 4,8 Hz, 2H); 3,84-3,65 (m, 2H); 3,49 (dd, J = 10,3, 13,1 Hz, 2H);
3,62-3,38 (m, 2H); 3,16 (bs, 2H); 2,33-2,15 (m, 4H).
APCI-MS:
m/z 389 (MH+)
-
Schritt II:
-
N-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy)phenyl)harnstofftrifluoracetat
(Salz)
-
(2S)-3-(2-Aminophenoxy)-1-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)propan-2-olbis(hydrochlorid)
(46,2 mg, 0,1 mmol) gelöst
in Essigsäure/Wasser
(1/1 ml) wurde mit du Kaliumcyanat (16,2 mg, 0,2 mmol) gelöst in Wasser
(0,5 ml) versetzt. Die Mischung wurde über Nacht bei Raumtemperatur
gerührt.
Nach Aufreinigung durch präparative
HPLC unter Verwendung von Acetonitril/Wasser mit 0,1% TFA als Laufmittel und
anschließendem
Lyophilisieren erhielt man die Titelverbindung in Form eines weißen amorphen
Feststoffs (43 mg, 78%).
1H-NMR (400
MHz, Aceton-d6): δ 8,38-8,34 (m, 1H); 7,83 (bs,
1H); 7,25 & 7,21
(s, 1H); 7,14 (d, J = 8,4 Hz, 1H); 6,93-6,81 (m, 3H); 6,77 (d, J
= 8,4 Hz, 1H); 5,95 (bs, 2H); 4,60-4,52 (m, 1H); 4,18 (d, J = 9,6
Hz, 1H); 4,07-4,00 (m,
1H); 3,92-3,71 (m, 3H); 3,70-3,40 (m, 3H); 3,30 & 3,22 (s, 2H); 2,44-2,19 (m, 4H).
APCI-MS:
m/z 432 (MH+)
-
Beispiel 88
-
N-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxyphenyl)harnstofftrifluoracetat
(Salz)
-
Schritt I:
-
4-Amino-3-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy)phenolbis(trifluoracetat)
(Salz)
-
Die
Verbindung wurde analog der Verbindung Beispiel 87 Schritt I ausgehend
von N-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypro pyl]oxy}-4-hydroxyphenyl)acetamid
(135 mg, 0,3 mmol) und 1 M Salzsäure
(3 ml) dargestellt. Nach Aufreinigung durch präparative HPLC unter Verwendung
von Acetonitril/Wasser mit 0,1% TFA als Laufmittel und anschließendem Lyophilisieren
erhielt man die im Untertitel genannte Verbindung in Form eines
weißen
amorphen Feststoffs (150 mg).
1H-NMR
(MeOH-d4, 400 MHz): δ 7,21 (bs, 1H); 7,18 (d, J =
8,8 Hz, 1H); 7,11 (dd, J = 2,0, 8,4 Hz, 1H); 6,74 (d, J = 8,4 Hz,
1H); 6,62 (d, J = 2,4 Hz, 1H); 6,49 (dd, J = 2,4, 8,8 Hz, 1H); 4,58-4,49
(m, 1H); 4,13 (d, J = 4,8 Hz, 2H); 3,8-3,6 (m, 2H); 3,6-3,4 (m,
2H); 3,48 (d, J = 13,2 Hz, 1H); 3,45 (d, J = 13,2 Hz, 1H); 3,16
(s, 2H); 2,31-2,17 (m, 4H).
APCI-MS: m/z 405 (MH+)
-
Schritt II:
-
N-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxyphenyl)harnstofftrifluoracetat
(Salz)
-
Die
Verbindung wurde analog der Verbindung Beispiel 87 Schritt II ausgehend
von 4-Amino-3-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}phenolbis(hydrochlorid)
(63,3 mg, 0,1 mmol) und Kaliumcyanat (16,2 mg, 0,2 mmol) dargestellt.
Nach Aufreinigung und anschließendem
Lyophilisieren erhielt man die Titelverbindung in Form eines weißen amorphen
Feststoffs (51 mg, 90%).
1H-NMR (400
MHz, Aceton-d6): δ 8,01 (d, J = 8,8 Hz, 1H); 7,60
(s, 1H); 7,25 & 7,21
(s, 1H); 7,14 (dd, J = 2,2, 8,4 Hz, 1H); 6,77 (d, J = 8,4 Hz, 1H);
6,45 (d, J = 2,5 Hz, 1H); 6,37 (dd, J = 2,5, 8,8 Hz, 1H); 4,57-4,49
(m, 1H); 4,12 (dd, J = 9,7, 2,6 Hz, 1H); 4,01 (dd, J = 9,7, 5,1
Hz, 1H); 3,95-3,65 (m, 3H); 3,62-3,40 (m, 3H); 3,33 & 3,21 (s, 3H);
2,44-2,20 (m, 4H).
APCI-MS: m/z 448 (MH+)
-
Beispiel 89
-
N-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,
4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-fluorphenyl)harnstofftrifluoracetat
(Salz)
-
Schritt I:
-
(2S)-1-(2-Amino-5-fluorphenoxy)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)propan-2-ol-bis (hydrochlorid)
(Salz)
-
Die
im Untertitel genannte Verbindung wurde analog der Verbindung Beispiel
87 Schritt I ausgehend von N-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-fluorphenyl)-acetamid (150 mg,
0,27 mmol) und 1 M Salzsäure
(2 ml) dargestellt.
APCI-MS: m/z 407 (MH+)
-
Schritt II:
-
N-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2‚4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-fluorphenyl)-harnstofftrifluoracetat
(Salz)
-
Die
in Schritt 1 erhaltene Reaktionslösung wurde mit Ammoniumacetat
(200 mg) gelöst
in Essigsäure (1
ml) gepuffert. Kaliumcyanat (44 mg, 0,54 mmol) gelöst in Wasser
(0,5 ml) wurde zugesetzt, und die Mischung wurde über Nacht
bei Raumtemperatur gerührt.
Nach Aufreinigung der Reaktionsmischung durch präparative HPLC unter Verwendung
von Acetonitril/Wasser mit 0,1% TFA als Laufmittel und anschließendem Lyophilisieren
erhielt man die Titelverbindung in Form eines weißen amorphen
Feststoffs (105 mg).
1H-NMR (MeOH-d4, 300 MHz): δ 7,70 (dd, J = 8,7, 6,3 Hz,
1H); 7,22-7,19 (m, 1H); 7,11 (dd, J = 8,4, 2,4 Hz, 1H); 6,86 (dd,
J = 10,2, 2,7 Hz, 1H); 6,74 (d, J = 8,4 Hz, 1H); 6,69 (ddd, J =
8,4, 8,4, 2,7 Hz, 1H); 4,53-4,43 (m, 1H); 4,09 (d, J = 5,1 Hz, 2H);
3,76-3,62 (m, 2H); 3,56-3,34 (m, 4H); 3,21 & 3,14 (S, 2H); 2,30-2,05 (m, 4H).
APCI-MS:
m/z 450 (MH+)
-
Beispiel 90
-
N-{[(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxyphenyl)amino]carbonyl}methanesulfonamidtrifluoracetat
(Salz)
-
Eine
Lösung
von Chlorameisensäure-4-nitrophenylester
(50 mg, 0,25 mmol) in DCM (3 ml) wurde mit DMAP (30 mg, 0,25 mmol)
versetzt. Die Mischung wurde 5 Minuten lang gerührt und dann mit Methansulfonamid
(24 mg, 0,25 mmol) und TEA (25 μl,
0,25 mmol) versetzt, und es wurde 1 weitere Stunde lang gerührt. 4-Amino-3-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}phenol (78 mg,
0,12 mmol) gelöst
in DCM (2 ml) und TEA (75 μl,
0,75 mmol) wurden zugegeben, und es wurde weiter bei Raumtemperatur
gerührt.
Nach LCMS-Kontrolle war die Umsetzung nach 2 Stunden beendet. Nach
dem Abdampfen des Lösungsmittels
wurde das Rohprodukt durch präparative
HPLC unter Verwendung von Acetonitril/Wasser mit 0,1% TFA als Laufmittel
aufgereinigt. Die Titelverbindung wurde nach dem Lyophilisieren
in Form eines weißen
amorphen Feststoffs (7 mg) erhalten.
1H-NMR
(Aceton-d6, 300 MHz): δ 8,32 (bs, 1H); 7,91 (d, J =
8,7 Hz, 1H); 7,24 (bs, 1H); 7,14 (dd, J = 8,4, 2,2 Hz, 1H); 6,78
(d, J = 8,6 Hz, 1H); 6,51 (d, J = 2,4 Hz, 1H); 6,43 (dd, J = 8,6,
2,6 Hz, 1H); 4,61-4,52 (m, 1H); 4,11 (dd, J = 9,5, 3,8 Hz, 1H);
3,98 (dd, J = 9,5, 6,4 Hz, 1H); 4,01-3,78 (m, 2H); 3,65 (d, J =
9,4 Hz, 1H); 3,74-3,42 (m, 4H); 3,27 (s, 3H); 3,30-3,15 (m, 2H);
2,43-2,20 (m, 4H).
APCI-MS: m/z 526 (MH+)
-
Beispiel 91
-
(4S)-2-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)isoxazolidin-4-oltrifluoracetat
(Salz)
-
Schritt I:
-
(S)-2-[4-Hydroxyisoxazolidin-2-yl]carbonylbenzoesäuremethylester
-
Triethylamin
(0,28 ml) wurde unter Stickstoff zu einer Lösung von N-Hydroxyphtalimid
(5,00 g, 30 mmol) und (R)-(–)-Epichlorhydrin
(2,40 ml, 30,6 mmol) in wasserfreiem Dioxan (10 ml) gegeben. Die
Mischung wurde 48 Stunden lang bei 50°C gerührt, weiteres (2R)-2-(Chlormethyl)oxiran
(0,24 ml) und Triethylamin (0,28 ml) wurden zugegeben, und es wurde
weitere 24 Stunden lang bei 50°C
gerührt.
Methanol (10 ml) und weiteres Triethylamin (4,27 ml) wurden zugesetzt,
und es wurde weitere 2 Stunden lang bei 50°C gerührt. Die Mischung wurde im
Vakuum eingedampft, und der Rückstand
wurde in einer gesättigten
wäßrigen Lösung von
Natriumhydrogencarbonat (100 ml) gelöst und mit Essigsäureethylester
(6 × 100
ml) extrahiert. Die vereinigten organischen Extrakte wurden über wasserfreiem
Magnesiumsulfat getrocknet, filtriert und im Vakuum eingedampft. Der
Rückstand
wurde aus Essigsäureethylester
umkristallisiert, wodurch man die im Untertitel genannte Verbindung
(3,4 g) erhielt.
1H-NMR (CDCl3; 400 MHz): δ 3,66 (1H, d, breit), 3,79 (1H,
d, breit), 3,89-3,99 (1H, m), 3,99-4,10 (1H, m), 4,74-4,81 (1H,
m), 7,46 (1H, d), 7,49 (1H, t), 7,62 (1H, t), 7,99 (1H, d).
SM
(ESI): m/z 252 [M+H]+
-
Schritt II:
-
(S)-4-Isoxazolidinolhydrochlorid
-
Salzsäure (4 M,
15 ml) wurde zu (S)-2-[4-Hydroxyisoxazolidin-2-yl]carbonylbenzoesäuremethylester (1,87
g, 7,4 mmol) gegeben, und die Lösung
wurde 3 Stunden lang auf Rückfluß erhitzt.
Die Mischung wurde auf Raumtemperatur abgekühlt, filtriert und im Vakuum
eingedampft. Der Rückstand
wurde aus Propan-2-ol umkristallisiert, wodurch man die im Untertitel
genannte Verbindung in Form weißer
Nadeln (0,78 g) erhielt.
1H-NMR (DMSO-d6; 400 MHz): δ 3,35 (1H, d), 3,47 (1H, dd),
4,03 (1H, dd), 4,07 (1H, d), 4,78-4,81 (1H, m).
-
Schritt III:
-
(4S)-2-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoyl}isoxazolidin-4-ol
-
Nachdem
PS-Carbodiimid (1,28 mmol/g) (312 mg, 0,4 mmol) 15 Minuten lang
in DCM (5 ml) gerührt worden
war, wurde mit 2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoesäure (118
mg, 0,2 mmol) gelöst
in DCM (2 ml) versetzt, und es wurde weitere 30 Minuten lang gerührt. Eine
Lösung
von (S)-4-Isoxazolidinolhydrochlorid (25 mg, 0,2 mmol) und TEA (70 μl, 0,5 mmol)
in DCM (1 ml) wurde zugesetzt, und es wurde weiter über Nacht
bei Raumtemperatur gerührt.
Gemäß LCMS-Kontrolle
was die Umsetzung beendet. Alle Feststoffe wurden abfiltriert, und
das Filtrat wurde im Vakuum eingedampft. Der Rückstand wurde zwischen Essigsäureethylester
und Wasser verteilt, und die organische Phase wurde mit Wasser gewaschen,
getrocknet und im Vakuum eingedampft, wodurch man ein Öl (93 mg)
erhielt.
APCI-MS: m/z 625 (MH+)
-
Schritt IV:
-
(4S)-2-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)isoxazolidin-4-oltrifluoracetat
(Salz)
-
(4S)-2-{2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoyl}isoxazolidin-4-ol
(93 mg, 0,15 mmol) wurde in einer TFA/DCM-Mischung 1/9 (10 ml) gelöst, und
die Lösung
wurde 30 Minuten lang bei Raumtemperatur gerührt. Nach Abdampfen des Lösungsmittels
im Vakuum wurde der Rückstand
durch präparative
HPLC unter Verwendung von Acetonitril/Wasser mit 0,1% TFA als Laufmittel
aufgereinigt. Die Titelverbindung wurde nach dem Lyophilisieren
in Form eines weißen amorphen
Feststoffs (18 mg) erhalten.
1H-NMR
(Aceton-d6, 300 MHz): δ 7,23 (bs, 1H); 7,22 (d, J =
8,2 Hz, 1H); 7,14 (dd, J = 8,5, 2,4 Hz, 1H); 6,78 (d, J = 8,5 Hz,
1H); 6,61 (d, J = 2,0 Hz, 1H); 6,50 (dd, J = 8,3, 2,0 Hz, 1H); 4,88-4,81
(m, 1H); 4,60-4,48 (m, 1H); 4,15 (dd, J = 9,5, 4,5 Hz, 1H); 4,02
(dd, J 9,5, 6,3 Hz, 1H); 3,97 (dd, J = 11,7, 5,9 Hz, 1H); 3,94-3,87
(m, 2H); 3,86-3,72
(bs, 2H); 3,70 (d, J = 11,7 Hz, 2H); 3,56-3,40 (bs, 2H); 3,41 (dd,
J = 13,5, 9,2 Hz, 1H); 3,17 (bs, 2H); 2,48-2,14 (m, 4H).
APCI-MS:
m/z 505 (MH+)
-
Beispiel 92
-
(4R)-2-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)isoxazolidin-4-oltrifluoracetat
(Salz)
-
Schritt I:
-
(R)-2-[4-Hydroxyisoxazolidin-2-yl]carbonylbenzoesäuremethylester
-
Dargestellt
ausgehend von (2S)-2-(Chlormethyl)oxiran nach dem in Beispiel 91
Schritt I beschriebenen Verfahren.
1H-NMR
(CDCl3; 400 MHz): δ 3,66 (1H, d, breit), 3,79 (1H,
d, breit), 3,89-3,99 (1H, m), 3,99-4,10 (1H, m), 4,74-4,81 (1H,
m), 7,46 (1H, d), 7,49 (1H, t), 7,62 (1H, t), 7,99 (1H, d).
SM
(ESI): m/z 252 [M+H]+.
-
Schritt II:
-
(R)-4-Isoxazolidinolhydrochlorid
-
Dargestellt
ausgehend von (R)-2-[4-Hydroxyisoxazolidin-2-yl]carbonylbenzoesäuremethylester nach der Vorschrift
von Beispiel 91 Schritt II.
1H-NMR
(CDCl3; 400 MHz): δ 3,3 (1H, d), 3,47 (1H, dd),
4,03 (1H, dd), 4,07 (1H, d), 4,78-4,81 (1H, m).
-
Schritt III:
-
(4R)-2-{2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoyl}isoxazolidin-4-ol
-
Die
im Untertitel genannte Verbindung wurde analog der Verbindung Beispiel
91 Schritt III ausgehend von 2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoesäure (118
mg, 0,2 mmol) und (R)-4-Isoxazolidinolhydrochlorid (25 mg, 0,2 mmol)
dargestellt.
APCI-MS: m/z 625 (MH+)
-
Schritt IV:
-
(4R)-2-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)isoxazolidin-4-oltrifluoracetat
(Salz)
-
Die
Titelverbindung wurde analog der Verbindung Beispiel 91 Schritt
IV ausgehend von (4R)-2-{2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoyl}isoxazolidin-4-ol
und TFA/DCM 1/9 dargestellt. Nach Aufreinigung und anschließendem Lyophilisieren
erhielt man die Titelverbindung in Form eines weißen amorphen
Feststoffs (26 mg).
1H-NMR (Aceton-d6, 300 MHz): δ 7,23 (bs, 1H); 7,22 (d, J =
8,2 Hz, 1H); 7,14 (dd, J = 8,5, 2,4 Hz, 1H); 6,78 (d, J = 8,5 Hz,
1H); 6,61 (d, J = 2,0 Hz, 1H); 6,50 (dd, J = 8,3, 2,0 Hz, 1H); 4,88-4,81
(m, 1H); 4,60-4,48 (m, 1H); 4,15 (dd, J = 9,5, 4,5 Hz, 1H); 4,02
(dd, J = 9,5, 6,3 Hz, 1H) 3,97 (dd, J = 11,7, 5,9 Hz, 1H); 3,94-3,87
(m, 2H); 3,86-3,72
(bs, 2H); 3,70 (d, J = 11,7 Hz, 2H); 3,56-3,40 (bs, 2H); 3,41 (dd,
J = 13,5, 9,2 Hz, 1H); 3,17 (bs, 2H); 2,48-2,14 (m, 4H).
APCI-MS:
m/z 505 (MH+)
-
Beispiel 93
-
(4S)-2-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)-4-methylisoxazolidin-4-oltrifluoracetat
(Salz)
-
Schritt I:
-
2-{[(2S)-2-Methyloxiranyl]methoxy]-1H-isoindol-1,3(2H)-dion
-
Eine
Mischung von N-Hydroxyphtalimid (5,3 g, 32,5 mmol), 3-Nitrobenzolsulfonsäure-[(2S)-2-methyloxiran-2-yl]methylester
(5,9 g, 21,6 mmol) und Triethylamin (10,6 ml) in Dichlormethan (15
ml) wurde unter Stickstoff 24 Stunden lang bei Raumtemperatur gerührt. Die
Reaktionsmischung wurde auf eine Kieselgelsäule aufgetragen und mit Dichlormethan
eluiert, wodurch man die im Untertitel genannte Verbindung in Form
eines farblosen Feststoffs (3,1 g) erhielt.
1H-NMR
(CDCl3; 400 MHz): δ 1,63 (3H, s), 2,69 (1H, d),
2,76 (1H, d), 4,17 (1H, d), 4,21 (1H, d), 7,73-7,78 (2H, m), 7,82-7,87
(2H, m)
MS (APCI) 234 [M+H]+
-
Schritt II:
-
2-[[(2R)-3-Chlor-2-hydroxy-2-methylpropyl]oxy]-1H-isoindol-1,3(2H)-dion
-
2-[[(2S)-2-Methyloxiranyl]methoxy]-1H-isoindol-1,3(2H)-dion (3,0 g, 12,9
mmol) wurde mit konzentrierter Salzsäure (12 ml) versetzt, und die
Mischung wurde 2 Stunden lang bei Raumtemperatur gerührt. Die
Mischung wurde zwischen Wasser und Dichlormethan verteilt, und die
organische Phase wurde getrocknet und durch Chromatographie (EtOAc)
aufgereinigt, wodurch man die im Untertitel genannte Verbindung
in Form eines farblosen Feststoffs (3,3 g) erhielt.
1H-NMR (CDCl3; 400
MHz): δ 1,29
(3H, S), 3,67 (1H, d), 3,76 (1H, d), 4,09 (1H, d), 4,15 (1H, d),
7,86 (4H, s), 5,24 (1H, s)
-
Schritt III:
-
2-[[(4S)-4-Hydroxy-4-methyl-2-isoxazolidinyl]carbonyl]-benzoesäuremethylester
-
Eine
Lösung
von 2-[[(2R)-3-Chlor-2-hydroxy-2-methylpropyl]oxy]-1H-isoindol-1,3(2H)-dion
(3,3 g, 12,2 mmol) in Methanol (25 ml) wurde mit Triethylamin (3,4
ml) versetzt und unter Stickstoff 1 Stunde lang auf Rückfluß erhitzt.
Die Mischung wurde zur Trockne eingeengt und durch Chromatographie
unter Anwendung eines Laufmittelgradienten aus Dichlormethan bis
5% Methanol in Dichlormethan aufgereinigt. Die chirale Reinheit des
Produkts wurde durch zweimaliges Umkristallisieren aus Acetonitrol
verbessert, wodurch man die im Untertitel genannte Verbindung in
Form eines farblosen Feststoffs (1,92 g) erhielt.
1H-NMR
(CDCl3; 400 MHz): δ 1,52 (3H, s), 3,59 (1H, d),
3,81 (1H, d), 3,88 (1H, d), 4,04 (1H, s), 4,34 (1H, d), 3,92 (3H,
s), 7,45 (1H, d), 7,49 (1H, t), 7,62 (1H, t), 8,00 (1H, d). HPLC:
(9010THIP.M) 50-mm-Chiracel AD-, ee > 99%
-
Schritt IV:
-
(4S)-4-Methyl-4-isoxazolidinolhydrochlorid
-
Eine
Lösung
von 2-[[(4S)-4-Hydroxy-4-methyl-2-isoxazolidinyl]carbonyl]benzoesäuremethylester
(4,9 g, 19,5 mmol) in 2 N Salzsäure
(30 ml) wurde unter Stickstoff 4 Stunden lang auf Rückfluß erhitzt.
Nach dem Abkühlen
wurde der Niederschlag abfiltriert und die Mutterlaugen wurden im
Vakuum zur Trockne eingeengt. Der Rückstand wurde mit Acetonitril
verrieben, wodurch man die im Untertitel genannte Verbindung in
Form eines weißen
Feststoffs (1,79 g) erhielt.
1H-NMR
(CDCl3; 400 MHz): δ 1,42 (3H, s), 3,29 (1H, d),
3,41 (1H, dd), 3,87 (1H, d), 4,05 (1H, dd)
-
Schritt V:
-
(4S)-2-{2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoyl}-4-methylisoxazolidin-4-ol
-
Die
im Untertitel genannte Verbindung wurde analog der Verbindung Beispiel
91 Schritt III ausgehend von 2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoesäure (118
mg, 0,2 mmol) und (4S)-4-Methyl-4-isoxazolidinolhydrochlorid
(28 mg, 0,2 mmol) dargestellt.
APCI-MS: m/z 639 (MH+)
-
Schritt VI:
-
(4S)-2-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)-4-methylisoxazolidin-4-oltrifluoracetat
(Salz)
-
Die
Titelverbindung wurde analog der Verbindung Beispiel 91 Schritt
IV ausgehend von (4S)-2-{2-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]-benzoyl}4-methylisoxazolidin-4-ol
(Rohprodukt erhalten aus (4S)-2-{2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoyl)}4-methylisoxazolidin-4-ol)
und TFA/DCM 1/9 dargestellt. Nach Aufreinigung und anschließendem Lyophilisieren
wurde die Titelverbindung in Form eines amorphen weißen Feststoffs
(33 mg) erhalten.
1H-NMR (Aceton-d6, 300 MHz): δ 7,23 (bs, 1H); 7,22 (d, J =
8,2 Hz, 1H); 7,14 (dd, J = 8,5, 2,4 Hz, 1H); 6,78 (d, J = 8,5 Hz,
1H); 6,61 (d, J = 2,0 Hz, 1H); 6,50 (dd, J = 8,3, 2,0 Hz, 1H); 4,59-4,47
(m, 1H); 4,15 (dd, J = 9,8, 5,1 Hz, 1H); 4,06 (dd, J = 9,8, 5,6
Hz, 1H); 3,92 (d, J = 8,3 Hz, 1H); 3,86-3,74 (bs, 2H); 3,85 (d,
J = 11,2 Hz, 1H); 3,77 (d, J = 8,3 Hz, 1H); 3,66 (d, J = 11,2 Hz,
1H); 3,65-3,56 (m, 2H); 3,50 (d, J = 9,0 Hz, 1H); 3,55-3,40 (m,
2H); 3,46 (d, J = 9,0 Hz, 1H); 3,16 (bs, 2H); 2,48-2,14 (m, 4H); 1,48
(s, 3H).
APCI-MS: m/z 519 (MH+)
-
Beispiel 94
-
(4R)-2-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)-4-methylisoxazolidin-4-oltrifluoracetat
(Salz)
-
Schritt I:
-
2-[[(2R)-2-Methyloxiranyl]methoxy]-1H-isoindol-1,3(2H)-dion
-
Dargestellt
aus N-Hydroxyphthalimid und 3-Nitrobenzolsulfonsäure-[(2R)-2-methyloxiran-2-yl]methylester
(Chen, J.; Shum, W., Tetrahedron Letters, 1993, 34(48), 7663-6)
nach der Methode von Beispiel 93, Schritt I.
1H-NMR
(CDCl3; 400 MHz): δ 1,63 (3H, s), 2,69 (1H, d),
2,76 (1H, d), 4,17 (1H, d), 4,21 (1H, d), 7,73-7,78 (2H, m), 7,82-7,87
(2H, m).
MS (APCI) 234 [M+H]+
-
Schritt II:
-
2-[((2R)-3-Chlor-2-hydroxy-2-methylpropyl]oxy]-1H-isoindol-1‚3(2H)-dion
-
Dargestellt
aus 2-[[(2R)-2-Methyloxiranyl]methoxy]-1H-isoindol-1,3(2H)-dion nach der Methode
von Beispiel 93, Schritt II.
1H-NMR
(CDCl3; 400 MHz): δ 1,29 (3H, S), 3,67 (1H, d),
3,76 (1H, d), 4,09 (1H, d), 4,15 (1H, d), 7,86 (4H, s), 5,24 (1H,
s)
-
Schritt III:
-
2-[[(4R)-4-Hydroxy-4-methyl-2-isoxazolidinyl]carbonyl]benzoesäuremethylester
-
Dargestellt
aus 2-[[(2R)-3-Chlor-2-hydroxy-2-methylpropyl]oxy]-1H-isoindol-1,3(2H)-dion
nach der Methode von Beispiel 93, Schritt III.
1H-NMR
(CDCl3; 400 MHz): δ 1,52 (3H, s), 3,59 (1H, d),
3,81 (1H, d), 3,88 (1H, d), 4,04 (1H, s), 4,34 (1H, d), 3,92 (3H,
s), 7,45 (1H, d), 7,49 (1H, t), 7,62 (1H, t), 8,00 (1H, d)
-
Schritt IV:
-
(4R)-4-Methyl-4-isoxazolidinolhydrochlorid
-
Dargestellt
aus 2-[[(4R)-4-hydroxy-4-methyl-2-isoxazolidinyl]oarbonyl]benzoesäuremethylester
nach der Methode von Beispiel 93, Schritt IV.
1H-NMR
(CDCl3; 400 MHz): δ 1,42 (3H, s), 3,29 (1H, d),
3,41 (1H, dd), 3,87 (1H, d), 4,05 (1H, dd)
-
Schritt V:
-
(4R)-2-{2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoyl}-4-methylisoxazolidin-4-ol
-
Die
im Untertitel genannte Verbindung wurde analog der Verbindung Beispiel
91 Schritt III ausgehend von 2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoesäure (118
mg, 0,2 mmol) und (4R)-4-Methyl-4-isoxazolidinolhydrochlorid
(28 mg, 0,2 mmol) dargestellt.
APCI-MS: m/z 639 (MH+)
-
Schritt VI:
-
(4R)-2-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)-4-methylisoxazolidin-4-oltrifluoracetat
(Salz)
-
Die
Titelverbindung wurde analog der Verbindung Beispiel 91 Schritt
IV ausgehend von (4R)-2-{2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]-benzoyl}-4-methylisoxazolidin-4-ol
und TFA/DCM 1/9 dargestellt. Nach der Aufreinigung und anschließendem Lyophilisieren
wurde die Titelverbindung in Form eines weißen amorphen Feststoffs (30
mg) erhalten.
1H-NMR (Aceton-d6, 300 MHz): δ 7,23 (bs, 1H); 7,22 (d, J =
8,2 Hz, 1H); 7,14 (dd, J = 8,5, 2,4 Hz, 1H); 6,78 (d, J = 8,5 Hz,
1H); 6,61 (d, J = 2,0 Hz, 1H); 6,50 (dd, J = 8,3, 2,0 Hz, 1H); 4,60-4,48
(m, 1H); 4,15 (dd, J = 9,5, 4,5 Hz, 1H); 4,03 (dd, J = 9,5, 6,3
Hz, 1H); 3,92 (d, J = 8,4 Hz, 1H); 3,87-3,72 (bs, 2H); 3,82 (d,
J = 10,9 Hz, 1H); 3,75 (d, J = 8,4 Hz, 1H); 3,69 (d, J = 10,9 Hz,
1H); 3,66 (bs, 1H); 3,56-3,38 (m, 2H); 3,42 (dd, J = 8,8, 13,5 Hz,
1H); 3,17 (bs, 2H); 2,48-2,14 (m, 4H); 1,48 (s, 3H)
APCI-MS:
m/z 519 (MH+)
-
Beispiel 95
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy)-N-(methylsulfonyl)benzamidtrifluoracetat
-
Schritt I:
-
2-[(2S)-Oxiran-2-ylmethoxy]benzoesäure-tert.-butylester
-
Eine
Mischung von Salicylsäure-tert.-butylester
(2,01 g, 10,3 mmol), 3-Nitrobenzolsulfonsäure-(2S)-oxiran-2-ylmethylester (2,69 g, 10,4
mmol) und Caesiumcarbonat (4,05 g, 12,4 mmol) in Dimethylformamid
(20 ml) wurde über
Nacht bei Raumtemperatur gerührt.
Die Reaktionsmischung wurde zwischen Essigsäureethylester und Wasser verteilt.
Die organische Phase wurde über
Natriumsulfat, Na2SO4,
getrocknet, filtriert und im Vakuum eingeengt. Der Rückstand
wurde durch Flash-Chromatographie
an Kieselgel (40% Essigsäureethylester,
60% Heptan) aufgereinigt, wodurch man die im Untertitel genannte
Verbindung (2,3 g, 89%) erhielt.
1H-NMR
(CDCl3, 400 MHz): δ 7,71 (dd, J = 1,8, 7,7 Hz,
1H); 7,41 (dd, J = 1,8, 7,8 Hz, 1H); (dd, J = 0,8, 7,5 Hz, 1H);
6,98 (d, J = 8,4 Hz, 1H); 4,29 (dd, J = 3,2, 11,0 Hz, 1H); 4,06
(dd, J = 5,2, 11,0 Hz, 1H); 3,42-3,37 (m, 1H); 2,93-2,89 (m, 1H); 2,86-2,83
(m, 1H).
APCI-MS: m/z 25 (MH+)
-
Schritt II:
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy)benzoesäure-tert.-butylester
-
Eine
Mischung von 5-Chlor-3H-spiro[1-benzofuran-2,4'-piperidin]
(390 mg, 1,6 mmol) und 2-[(2S)-Oxiran-2-ylmethoxy]benzoesäure-tert.-butylester (350 mg,
1,6 mmol) in Ethanol wurde über
Nacht unter Rückfluß erhitzt.
Die flüchtigen
Bestandteile wurden im Vakuum entfernt, und der Rückstand
wurde ohne weitere Aufreinigung verwendet.
APCI-MS: m/z 474
(MH+)
-
Schritt III:
-
2-({(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-[(4-methoxybenzyl)oxy]propyl)-oxy)benzoesäure
-
Eine
Suspension von Natriumhydrid (170 mg, 4,2 mmol) in THF (10 ml) wurde
unter Argon bei 0°C
mit 2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}benzoesäure-tert.-butylester
(750 mg, 1,6 mmol) in THF (10 ml) und 1-(Chlormethyl)-4-methoxybenzol (250
mg, 1,6 mmol) in THF (10 ml) versetzt. Die Mischung wurde über Nacht
bei Raumtemperatur gerührt,
auf Eis gegossen und mit HCl (aq.) auf einen pH-Wert von 1 eingestellt.
Anschließend
wurde mit Essigsäureethylester
extrahiert, die organische Phase wurde über Natriumsulfat getrocknet
(Na2SO4) und die
flüchtigen
Bestandteile wurden im Vakuum entfernt. Der Rückstand wurde durch HPLC (Acetonitril/Wasser,
0,025% Ammoniumhydroxid) aufgereinigt, wodurch man die im Untertitel
genannte Verbindung (91 mg) erhielt.
APCI-MS: m/z 538 (MH+)
-
Schritt IV:
-
2-({(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-[(4-methoxybenzyl)oxy]propyl}oxy)-N-(methylsulfonyl)benzamid
-
Eine
Mischung von 2-({(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-[(4-methoxybenzyl)oxy]propyl}oxy)benzoesäure (90
mg, 0,17 mmol), N,N-Dimethylpyridin-4-amin
(22 mg, 0,18 mmol), Methansulfonamid (18 mg, 0,19 mmol) und N-[3-(Dimethylamino)propyl]-N'-ethylcarbodiimidhydrochlorid
(35 mg, 0,18 mmol) in Dichlormethan (5 ml) wurde unter Argon über Nacht
bei Raumtemperatur gerührt.
Die Mischung wurde in 1 M HCl (aq) gegossen, die beiden Phasen wurden
getrennt und die wäßrige Phase
wurde mit Dichlormethan extrahiert. Die vereinigten organischen
Phasen wurden über
Natriumsulfat getrocknet, die flüchtigen
Bestandteile wurden im Vakuum entfernt, und der Rückstand
(117 mg) wurde ohne weitere Aufreinigung verwendet.
APCI-MS:
m/z 615 (MH+)
-
Schritt V:
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy)-N-(methylsulfonyl)benzamid
-
2-({(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-[(4-methoxybenzyl)oxy]propyl}oxy)-N-(methylsulfonyl)benzamid
(104 mg, 0,17 mmol) wurde bei Raumtemperatur 1 Stunde lang in einer
Mischung aus Trifluoressigsäure
(500 μl)
und Dichlormethan (3 ml) gerührt.
Die flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch HPLC (Acetonitril/Wasser,
0,025% Ammoniumhydroxid) aufgereinigt, wodurch man die im Untertitel
genannte Verbindung (31 mg, Gesamtausbeute über die Stufen II-V 3,9%) erhielt.
1H-NMR (Aceton-d6,
400 MHz): δ 7,92
(dd, J = 1,8, 7,8 Hz, 1H); 7,62 (dd, J = 1,8, 8,3 Hz, 1H); 7,28-7,22
(m, 2H); 7,19-7,11 (m, 2H); 6,77 (d, J = 8,5 Hz, 1H); 4,76-4,69
(m, 1H); 4,42-4,32 (m, 2H); 3,98-3,44 (m, 6H); 3,42 (s, 3H); 3,19
(bs, 2H); 2,41-2,19 (m, 4H).
APCI-MS: m/z 495 (MH+)
-
Schritt VI:
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-N-(methylsulfonyl)benzamidtrifluoracetat
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-N-(methylsulfonyl)benzamid
(31 mg, 0,06 mmol) wurde in Dichlormethan gelöst und mit Trifluoressigsäure (100 μl) versetzt. Die
flüchtigen
Bestandteile wurden im Vakuum entfernt, wodurch man die im Untertitel
genannte Verbindung (35 mg) erhielt.
APCI-MS: m/z 495 (MH+)
-
Beispiel 96
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-N-1H-tetrazol-5-ylbenzamidbis(trifluoracetat)
-
Schritt I:
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}benzoesäurehydrochlorid
-
Eine
Mischung von 2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-benzoesäure-tert.-butylester
(200 mg, 0,42 mmol) und wäßriger konz.
HCl (3 ml) in Dichlormethan (25 ml) wurde 48 Stunden lang bei Raumtemperatur
gerührt.
Die flüchtigen
Bestandteile wurden im Vakuum entfernt, und der braune Rückstand
wurde ohne weitere Aufreinigung verwendet.
APCI-MS: m/z 418
(MH+)
-
Schritt II:
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-N-1H-tetrazol-5-ylbenzamidbis(Trifluoracetat)
-
Eine
Mischung von 2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy)-benzoesäurehydropchlorid
(110 mg, 0,24 mmol), 1H-Tetrazol-5-amin (27 mg, 0,26 mmol) und PS-Carbodiimid
(850 mg, 1 mmol) wurde bei Raumtemperatur über Nacht in Dichlormethan
(10 ml) gerührt.
Die flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch HPLC (Acetonitril/Wasser, 0,1%
Trifluoressigsäure)
aufgereinigt, wodurch man die im Untertitel genannte Verbindung
(23 mg, Gesamtausbeute über
die Stufen I-II 11%) erhielt.
1H-NMR
(Aceton-d6, 400 MHz): δ 11,43 (bs, 1H); 8,03 (dd, J
= 1,7, 7,8 Hz, 1H); 7,65 (dd, J = 1,9, 7,1 Hz, 1H); 7,32 (d, J =
8,3 Hz, 1H); 7,25-7,17 (m, 2H); 7,14 (dd, J = 2,4, 8,5 Hz, 1H);
6,79 (d, J = 8,5 Hz, 1H); 4,85-4,78 (m, 1H); 4,52-4,39 (m, 2H);
3,98-3,76 (m, 2H); 3,75-3,67 (m, 2H); 3,66-3,50 (m, 2H); 3,22 (bs,
2H); 2,47-2,32 (m, 2H); 2,31-2,20 (m, 2H).
APCI-MS: m/z 485
(MH+)
-
Beispiel 97
-
3-{{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4{[(3R)-3-(dimethylamino)pyrrolidin-1-yl]carbonyl}phenolbis-(trifluoracetat)
(Salz)
-
Schritt I:
-
(2S)-1-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-3-{2-{[(3R)-3-(dimethylamino)-pyrrolidin-1-yl]carbonyl)-5-[(4-methoxybenzyl)oxy]-phenoxy}propan-2-ol
-
Eine
Mischung von PS-Carbodiimid (530 mg, 0,68 mmol) und Dichlormethan
(6 ml) wurde 15 Minuten lang bei Raumtemperatur gerührt und
mit einer Lösung
von 2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoesäurehydrochlorid
(200 mg, 0,32 mmol) in NMP (1 ml) und Dichlormethan (2 ml) versetzt,
und die Mischung wurde 30 Minuten lang gerührt und mit einer Lösung von
(3R)-N,N-Dimethylpyrrolidin-3-amin (48 mg, 0,42 mmol) in Dichlormethan
(2 ml) versetzt. Die Mischung wurde über Nacht bei Raumtemperatur
gerührt und
dann filtriert, und das Filtrat wurde mit Kochsalzlösung gewaschen
und über
Natriumsulfat getrocknet. Die flüchtigen
Bestandteile wurden im Vakuum entfernt, und der Rückstand
wurde ohne weitere Aufreinigung verwendet.
APCI-MS: m/z 650
(MH+)
-
Schritt II:
-
3-{{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-{[(3R)-3-isopropylpyrrolidin-1-yl]carbonyl}phenolbis(trifluoracetat)
-
Eine
Lösung
von (2S)-1-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1-yl)-3-{2-{[(3R)-3-isopropylpyrrolidin-1-yl]carbonyl)-5-[(4-methoxybenzyl)oxy]-phenoxy}propan-2-ol
(das aus dem vorherigen Schritt erhaltene Rohprodukt) und Dichlormethan
(3 ml) wurde mit Trifluoressigsäure
(600 μl)
versetzt. Die Mischung wurde 1 Stunde lang bei Raumtemperatur gerührt, die
flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch HPLC (Acetonitril/Wasser,
0,1% Trifluoressigsäure)
aufgereinigt, wodurch man die im Untertitel genannte Verbindung
(60 mg, Gesamtausbeute über
die Stufen I-II 25%) erhielt.
1H-NMR
(Aceton-d6, 400 MHz): δ 7,22 (s, 1H); 7,15-7,11 (m,
2H); 6,77 (d, J = 8,5 Hz, 1H); 6,64-6,60 (m, 1H); 6,53-6,49 (m,
1H); 4,63-4,49 (m, 2H); 4,17-3,96 (m, 4H); 3,96-3,72 (m, 4H); 3,71-3,38
(m, 6H); 3,17 (bs, 2H); 3,00 (bs, 3H); 2,94 (bs, 3H); 2,60-2,18
(m, 6H).
APCI-MS: m/z 530 (MH+)
-
Beispiel 98
-
3-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-([(3S)-3-(dimethylamino)pyrrolidin-1-yl]carbonyl}phenolbis(trifluoracetat)
-
Die
Titelverbindung wurde unter Verwendung von (3S)-N,N-Dimethylpyrrolidin-3-amin wie in
Beispiel 97 beschrieben dargestellt.
1H-NMR
(Aceton-d6, 300 MHz): δ 7,25-7,20 (m, 1H); 7,16-7,11 (m, 2H); 6,77
(d, J = 8,5 Hz, 1H); 6,63-6,58 (m, 1H); 6,54-6,48 (m, 1H); 4,70-4,52
(m, 1H); 4,20-3,98 (m, 3H); 3,96-3,72 (m, 4H); 3,70-3,36 (m, 6H);
3,17 (bs, 2H); 3,00 (s, 3H); 2,95 (s, 3H); 2,62-2,16 (m, 6H).
APCI-MS:
m/z 530 (MH+)
-
Beispiel 99
-
(3S')-1-(5-Chlor-2-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)pyrrolidin-3-oltrifluoracetat
-
Schritt I:
-
5-Chlor-2,4-dihydroxybenzoesäuremethylester
-
Dargestellt
ausgehend von 2,4-Dihydroxybenzoesäure methylester unter Anwendung
der in Anderson, W. K., et al., J. Med. Chem. 1996, 39, 46-55 beschriebenen
Vorschrift.
1H-NMR (CDCl3,
400 MHz): δ 10,85
(s, 1H), 7,84 (s, 1H), 6,63 (s, 1H), 5,99 (s, 1H), 3,95 (s, 3H)
-
Schritt II:
-
5-Chlor-2-hydroxy-4-[(4-methoxybenzyl)oxy]benzoesäuremethylester
-
Eine
Lösung
von 5-Chlor-2,4-dihydroxybenzoesäuremethylester
(0,41 g, 2 mmol) in Aceton wurde mit 1-(Chlormethyl)-4-methoxybenzol
(0,32 g, 2 mmol) und K2CO3 (0,28
g, 2 mmol) versetzt. Die Reaktionsmischung wurde 3 Tage lang unter
Rückfluß erhitzt
und dann auf Raumtemperatur abgekühlt. Das anorganische Material
wurde abfiltriert. Das Lösungsmittel
wurde im Vakuum abdestilliert, und der Rückstand wurde aus Methanol
umkristallisiert, wodurch man einen weißen Feststoff (0,37 g, 60%)
erhielt.
1H-NMR (CDCl3,
400 MHz): δ 10,89
(s, 1H), 7,82 (s, 1H), 7,37 (d, J = 8,7 Hz, 2H), 6,92 (d, J = 8,7
Hz, 2H), 6,56 (s, 1H), 5,09 (s, 2H), 3,92 (s, 3H), 3,82 (s, 3H)
-
Schritt III:
-
5-Chlor-4-[(4-methoxybenzyl)oxy]-2-[(2S)-oxiran-2-yl-methoxy]benzoesäuremethylester
-
Eine
Lösung
von 5-Chlor-2-hydroxy-4-[(4-methoxybenzyl)-oxy]benzoesäuremethylester (0,37 g, 1,16 mmol),
3-Nitrobenzolsulfonsäure-(2S)-oxiran-2-ylmethylester
(0,30 g, 1,16 mmol) und Caesiumcarbonat (0,45 g, 1,4 mmol) in Dimethylformamid
(15 ml) wurde über
Nacht bei Raumtemperatur gerührt.
Die Mischung wurde zwischen Wasser und Essigsäureethylester verteilt, und
die organische Phase wurde zweimal mit Wasser und einmal mit Kochsalzlösung gewaschen
und anschließend
eingeengt. Das Rohprodukt wurde durch Flash-Chromatographie an Kieselgel
(Laufmittel: Essigsäureethylester/n-Heptan) aufgereinigt,
wodurch man die Titelverbindung (0,33, 74%) erhielt.
1H-NMR (CDCl3, 400
MHz): δ 7,91
(s, 1H), 7,37 (d, J = 8,7 Hz, 2H), 6,92 (dd, J = 6,7, 2,0 Hz, 2H),
6,66 (s, 1H), 5,14 (m, 2H), 4,33 (dd, J = 11,4, 2,6 Hz, 1H), 3,98
(dd, J = 11,5, 5,1 Hz, 1H), 3,86 (s, 3H), 3,82 (s, 3H), 3,36 (m,
1H), 2,93-2,87 (m, 2H).
APCI-MS: m/z 379 (MH+)
-
Schritt IV:
-
5-Chlor-2-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoesäuremethylestertrifluoracetat
(Salz)
-
Eine
Lösung
von 5-Chlor-3H-spiro[1-benzofuran-2,4'-piperidin)
(100 mg, 0,45 mmol) und 5-Chlor-4-[(4-methoxybenzyl)oxy]-2-[(2S)-oxiran-2-ylmethoxy]-benzoesäuremethylester
(170 mg, 0,45 mmol) in Ethanol (5 ml) wurde 6 Stunden lang unter
Rückfluß erhitzt.
Das Lösungsmittel
wurde im Vakuum abdestilliert. Der Rückstand wurde durch HPLC (Laufmittel:
[Acetonitril/Wasser + 0,1% TFA]) aufgereinigt, wodurch man einen
farblosen Feststoff (218 mg, 67%) erhielt.
APCI-MS: m/z 602
(MH+)
-
Schritt V:
-
5-Chlor-2-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoesäurehydrochlorid
-
Eine
Mischung von 5-Chlor-2-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoesäuremethyl estertrifluoracetat
(220 mg, 0,3 mmol) in Ethanol (10 ml) wurde mit einer Lösung von
Kaliumhydroxid (4 g) und Wasser (4 ml) versetzt. Die Mischung wurde
3 Stunden lang bei Raumtemperatur gerührt, mit wäßriger HCl (37%) auf einen
pH-Wert von 1 eingestellt, mit Essigsäureethylester extrahiert und über Natriumsulfat
getrocknet. Die flüchtigen
Bestandteile wurden im Vakuum entfernt, die im Untertitel genannte
Verbindung (180 mg) erforderte keine weitere Aufreinigung.
APCI-MS:
m/z 588 (MH+)
-
Schritt VI:
-
(3S)-1-{5-Chlor-2-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoyl}pyrrolidin-3-oltrifluoracetat
-
Eine
Mischung von PS-Carbodiimid (250 mg, 0,32 mmol) und Dichlormethan
(3 ml) wurde 15 Minuten lang bei Raumtemperatur gerührt und
mit einer Lösung
von 5-Chlor-2-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoesäurehydrochlorid
(100 mg, 0,16 mmol) in NMP (0,5 ml) und Dichlormethan (1 ml) versetzt, und
die Mischung wurde 30 Minuten lang gerührt und wurde mit einer Lösung von
(3S)-Pyrrolidin-3-ol
(18 mg, 0,21 mmol) in Dichlormethan (1 ml) versetzt. Die Mischung
wurde über
Nacht bei Raumtemperatur gerührt
und dann filtriert, und das Filtrat wurde mit Kochsalzlösung gewaschen
und über
Natriumsulfat getrocknet. Die flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch HPLC (Acetonitril/Wasser, 0,1%
Trifluoressigsäure)
aufgereinigt, wodurch man die im Untertitel genannte Verbindung.
(45 mg) erhielt.
APCI-MS: m/z 657 (MH+)
-
Schritt VII:
-
(3S)-1-(5-Chlor-2-{[(2S)-3-(5-chlor-1'H,3H-spiro-[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)pyrrolidin-3-oltrifluoracetat
-
Eine
Lösung
von (3S)-1-{5-Chlor-2-{[(2S)-3-(5-chlor-1'H,3H-spiro-[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoyl}-pyrrolidin-3-oltrifluoracetat
(45 mg, 0,05 mmol) in Dichlormethan (3 ml) wurde mit Trifluoressigsäure (0,3
ml) versetzt. Die Mischung wurde 20 Minuten lang bei Raumtemperatur
gerührt,
und die flüchtigen
Bestandteile wurden im Vakuum entfernt. Der Rückstand wurde durch HPLC (Acetonitril/Wasser, 0,1%
Trifluoressigsäure)
aufgereinigt, wodurch man die im Untertitel genannte Verbindung
(22 mg, Gesamtausbeute über
die Stufen V-VII 11%) erhielt.
1H-NMR
(Aceton-d6, 400 MHz): δ 7,24-7,22 (m, 2H); 7,13 (d,
J = 8,4 Hz, 1H); 6,87 (d, J = 13,7 Hz, 1H); 6,77 (d, J = 8,5 Hz,
1H); 4,56-4,46 (m, 2H); 4,44-4,39 (m, 1H); 4,17-4,02 (m, 2H); 3,87-3,72
(m, 2H); 3,70-3,60 (m, 2H); 3,60-3,26 (m, 7H); 3,16 (bs, 2H); 2,45-2,16
(m, 4H); 2,03-1,80 (m, 2H).
APCI-MS: m/z 537 (MH+)
-
Beispiel 100
-
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-([(3S)-3-methoxypyrrolidin-1-yl]carbonyl)phenoltrifluoracetat
-
Schritt I:
-
(2S)-1-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-3-(5-[(4-methoxybenzyl)oxy]-2-{[(3S)-3-methoxypyrrolidin-1-yl]carbonyl)phenoxy)propan-2-ol
-
Eine
Mischung von PS-Carbodiimid (277 mg, 0,35 mmol) und Dichlormethan
(3 ml) wurde 15 Minuten lang bei Raumtemperatur gerührt und
mit einer Lösung
von 2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoesäurehydrochlorid
(100 mg, 0,16 mmol) in NMP (0,5 ml) und Dichlormethan (1 ml) versetzt,
und die Mischung wurde 30 Minuten lang gerührt und mit einer Lösung von
(3S)-3-Methoxypyrrolidin (27 mg, 0,27 mmol) in Dichlormethan (1
ml) versetzt. Die Mischung wurde über Nacht bei Raumtemperatur
gerührt
und dann filtriert, und das Filtrat wurde mit Kochsalzlösung gewaschen
und über
Natriumsulfat getrocknet. Die flüchtigen Bestandteile
wurden im Vakuum entfernt und der Rückstand wurde durch HPLC (Acetonitril/Wasser,
0,025% Ammoniumhydroxid) aufgereinigt, wodurch man (35 mg) der im
Untertitel genannten Verbindung erhielt.
APCI-MS: m/z 637 (MH+)
-
Schritt II:
-
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-([(3S)-3-methoxypyrrolidin-1-yl]carbonyl}phenoltrifluoracetat
-
Eine
Lösung
von (2S)-1-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-3-(5-[(4-methoxybenzyl)-oxy]-2-{[(3S)-3-methoxypyrrolidin-1-yl]carbonyl}-phenoxy)propan-2-ol
(35 mg, 0,05 mmol) in Dichlormethan (3 ml) wurde mit Trifluoressigsäure (0,3
ml) versetzt. Die Mischung wurde 2 Stunden lang bei Raumtemperatur
gerührt,
die flüchtigen Bestandteile
wurden entfernt und der Rückstand
wurde durch HPLC (Acetonitril/Wasser, 0,1% Trifluoressigsäure) aufgereinigt,
wodurch man 25 mg (Gesamtausbeute über die Stufen I-II 25%) der
Titelverbindung erhielt.
1H-NMR (Aceton-d6, 400 MHz): δ 7,23 (s, 1H); 7,16-7,10 (m,
2H); 6,77 (d, J = 8,7 Hz, 1H); 6,64-6,61 (m, 1H); 6,52 (dd, J =
2,1, 8,2 Hz, 1H); 4,54-4,45 (m, 1H); 4,17-3,95 (m, 3H); 3,88-3,70 (m, 2H); 3,69-3,60
(m, 2H); 3,60-3,42 (m, 4H); 3,40-3,31 (m, 3H); 3,26 (s, 2H); 3,17 (bs,
2H); 2,46-2,17 (m, 4H); 2,10-1,92 (m, 2H).
APCI-MS: m/z 517
(MH+)
-
Beispiel 101
-
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-{[(2R)-2-(hydroxymethyl)pyrrolidin-1-yl]carbonyl)phenoltrifluoracetat
-
Schritt I:
-
(2S)-1-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-3-{2-{([(2R)-2-(hydroxymethyl)-pyrrolidin-1-yl]carbonyl}-5-[(4-methoxybenzyl)oxy]-phenoxy}propan-2-ol
-
Eine
Mischung von PS-Carbodiimid (280 mg, 0,36 mmol) und Dichlormethan
(2,5 ml) wurde 15 Minuten lang bei Raumtemperatur gerührt und
mit einer Lösung
von 2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoesäurehydrochlorid
(100 mg, 0,16 mmol) in NMP (0,6 ml) und Dichlormethan (1 ml) versetzt,
und die Mischung wurde 30 Minuten lang gerührt und mit einer Lösung von
(2R)-Pyrrolidin-2-ylmethanol (30 mg, 0,30 mmol) in Dichlormethan
(1 ml) versetzt. Die Mischung wurde über Nacht bei Raumtemperatur
gerührt
und filtriert. Die flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch HPLC (Acetonitril/Wasser,
0,025% Ammoniumhydroxid) aufgereinigt, wodurch man die im Untertitel
genannte Verbindung (51 mg) erhielt.
APCI-MS: m/z 637 (MH+)
-
Schritt II:
-
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-([(2R)-2-(hydroxymethyl)pyrrolidin-1-yl]carbonyl}phenoltrifluoracetat
-
Eine
Lösung
von (2S)-1-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-3-{2-{[(2R)-2-(hydroxymethyl)pyrrolidin-1-yl]carbonyl}-5-[(4-methoxybenzyl)oxy]phenoxy}propan-2-ol
(51 mg, 0,08 mmol) in Dichlormethan (3 ml) wurde mit Trifluoressigsäure (0,3
ml) versetzt. Die Mischung wurde 30 Minuten lang bei Raumtemperatur
gerührt,
die flüchtigen
Bestandteile wurden entfernt und der Rückstand wurde durch HPLC (Acetonitril/Wasser,
0,1% Trifluoressigsäure)
aufgereinigt, wodurch man 20 mg (Gesamtausbeute über die Stufen I-II 20%) der
Titelverbindung erhielt.
1H-NMR (Aceton-d6, 400 MHz): δ 7,23 (s, 1H); 7,15-7,10 (m,
2H); 6,77 (d, J = 8,6 Hz, 1H); 6,60-6,57 (m, 1H); 6,50 (dd, J =
2,1, 8,2 Hz, 1H); 4,58-4,48 (m, 1H), 4,32-4,24 (m, 1H); 4,14-4,06 (m, 2H); 3,90-3,60
(m, 4H); 3,60-3,40 (m, 4H); 3,32-3,20 (m, 2H); 3,16 (bs, 2H); 2,46-2,16
(m, 4H); 1,95-1,66 (m, 2H); 1,35-1,29 (m, 2H).
APCI-MS: m/z
517 (MH+)
-
Beispiel 102
-
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-{[(2S)-2-(hydroxymethyl)pyrrolidin-1-yl]carbonyl}phenoltrifluoracetat
-
Die
Titelverbindung wurde wie in Beispiel 101 beschrieben unter Verwendung
von (2R)-Pyrrolidin-2-ylmethanol dargestellt.
1H-NMR
(Aceton-d6, 400 MHz): δ 7,23 (s, 1H); 7,16-7,05 (m,
2H); 6,77 (d, J = 8,5 Hz, 1H); 6,64-6,57 (m, 1H); 6,50 (dd, J =
2,2, 8,4 Hz, 1H); 4,60-4,51 (m, 1H), 4,30-4,22 (m, 1H); 4,14-4,10 (m, 2H); 3,90-3,72
(m, 2H); 3,70-3,24 (m, 8H); 3,17 (bs, 2H); 2,44-2,14 (m, 4H); 1,92-1,68
(m, 4H).
APCI-MS: m/z 517 (MH+)
-
Beispiel 103
-
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-{[3-(hydroxymethyl)pyrrolidin-1-yl]carbonyl}phenoltrifluoracetat
-
Die
Titelverbindung wurde wie in Beispiel 101 beschrieben unter Verwendung
von Pyrrolidin-3-ylmethanolhydrochlorid dargestellt.
1H-NMR (Aceton-d6,
400 MHz): δ 7,23
(s, 1H); 7,16-7,08 (m, 2H); 6,80-6,75 (m, 1H); 6,67-6,62 (m, 1H); 6,53-6,48 (m, 1H); 4,52-4,44
(m, 1H), 4,17-4,02 (m, 2H); 3,90-3,10 (m, 15H); 2,50-2,16 (m, 4H);
2,02-1,68 (m, 2H).
APCI-MS: m/z 517 (MH+)
-
Beispiel 104
-
1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)-D-prolinamidtrifluoracetat
-
Schritt I:
-
1-{2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoyl}-D-prolinamid
-
Eine
Mischung von PS-Carbodiimid (280 mg, 0,36 mmol) und Dichlormethan
(2,5 ml) wurde 15 Minuten lang bei Raumtemperatur gerührt und
mit einer Lösung
von 2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoesäurehydrochlorid
(100 mg, 0,16 mmol) in NMP (0,6 ml) und Dichlormethan (1 ml) versetzt,
und die Mischung wurde 30 Minuten lang gerührt und mit einer Lösung von
D-Prolinamid (29 mg, 0,25 mmol) in Dichlormethan (1 ml) versetzt.
Die Mischung wurde bei Raumtemperatur über Nacht gerührt und
filtriert. Die flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch HPLC (Acetonitril/Wasser, 0,025%
Ammoniumhydroxid) aufgereinigt, wodurch man (68 mg) die im Untertitel
genannte Verbindung erhielt.
APCI-MS: m/z 650 (MH+)
-
Schritt II:
-
1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)-D-prolinamidtrifluoracetat
-
Eine
Lösung
von 1-{2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoyl}-D-prolinamid
(68 mg, 0,10 mmol) in Dichlormethan wurde mit Trifluoressigsäure (0,3
ml) versetzt. Die Mischung wurde 30 Minuten lang bei Raumtemperatur
gerührt,
die flüchtigen
Bestandteile wurden entfernt und der Rückstand wurde durch HPLC (Acetonitril/Wasser,
0,1% Trifluoressigsäure)
aufgereinigt, wodurch man 28 mg (Gesamtausbeute über die Stufen I-II 27%) der
Titelverbindung erhielt.
1H-NMR (Aceton-d6, 400 MHz, 2 Rotamere): δ 7,23 (s, 1H); 7,22-7,16 und
6,64-6,54 (m, 3H); 7,15-7,10 und 7,06-7,02 (m, 2H); 6,77 (d, J = 8,4 Hz, 1H);
6,53-6,48 und 6,46-6,41 (m, 1H); 4,62-4,47 (m, 2H); 4,16-4,02 (m, 2H);
3,92-3,42 (m, 8H); 3,34-3,22 (m, 2H); 3,16 (bs, 2H); 2,46-2,14 (m,
4H); 2,12-1,76 (m, 2H).
APCI-MS: m/z 530 (MH+)
-
Beispiel 105
-
N-(4-Hydroxy-2-{[(2S)-2-hydroxy-3-(1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)propyl]oxy)phenyl)-acetamidtrifluoracetat
(Salz)
-
Die
Titelverbindung wurde ausgehend von 3H-Spiro[1- benzofuran-2,4'-piperidin] wie in Beispiel 27 beschrieben
dargestellt.
1H-NMR (Aceton-d6, 400 MHz): δ 8,52 (s, 1H), 7,93 (d, J =
8,7 Hz, 1H), 7,21 (d, J = 7,2 Hz, 1H), 7,12 (t, J = 7,7 Hz, 1H),
6,86 (t, J = 7,3 Hz, 1H), 6,75 (d, J = 7,9 Hz, 1H), 6,53 (d, J =
2,4 Hz, 1H), 6,40 (dd, J = 8,8, 2,4 Hz, 1H), 4,53 (m, 1H), 4,08
(m, 2H), 3,94-3,39 (m, 6H), 3,15 (s, 2H), 2,45-2,15 (m, 4H), 2,09
(s, 3H).
APCI-MS: m/z 413 (MH+).
-
Beispiel 106
-
N-(4-Hydroxy-2-{[(2S)-2-hydroxy-3-(5-methyl-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)propyl]oxy}-phenyl)acetamidtrifluoracetat
(Salz)
-
Die
Titelverbindung wurde ausgehend von 5-Methyl-3H-spiro[1-benzofuran-2,4'-piperidin] wie in
Beispiel 27 beschrieben dargestellt.
1H-NMR
(Aceton-d6, 400 MHz): δ 8,56 (s, 1H), 7,90 (d, J =
8,7 Hz, 1H), 7,01 (s, 1H), 6,92 (d, J = 8,1 Hz, 1H), 6,63 (d, J
= 8,1 Hz, 1H), 6,53 (d, J = 2,4 Hz, 1H), 6,41 (dd, J = 8,7, 2,4
Hz, 1H), 4,52 (s, 1H), 4,07 (d, J = 3,8 Hz, 2H), 3,92-3,38 (m, 6H),
3,09 (s, 2H), 2,42-2,13
(m, 4H), 2,24 (s, 3H), 2,10 (s, 3H).
APCI-MS: m/z 427 (MH+).
-
Beispiel 107
-
N-(5-Chlor-2-{[(2S)-2-hydroxy-3-(1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)propyl]oxy}-4-methoxyphenyl)acetamidtrifluoracetat
(Salz)
-
Die
Titelverbindung wurde ausgehend von 3H-Spiro[1-benzofuran-2,4'-piperidin] wie in Beispiel 83 beschrieben
dargestellt.
1H-NMR (DMSO-d6, 400 MHz): δ 9,61 (bs, 1H), 9,02 (m, 1H),
7,91 (s, 1H), 7,21 (d, J = 7,3 Hz, 1H), 7,11 (m, 1H), 6,85 (m, 2H),
6,77 (d, J = 7,9 Hz, 1H), 4,38 (m, 1H), 4,06 (m, 2H), 3,85 (s, 3H),
3,66-3,12 (m, 6H), 3,08 (s, 2H), 2,23-1,94 (m, 7H).
APCI-MS:
m/z 461 (MH+).
-
Beispiel 108
-
N-(5-Chlor-4-hydroxy-2-{[(2S)-2-hydroxy-3-(1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)propyl]oxy}-phenyl)acetamidtrifluoracetat
(Salz)
-
Eine
gerührte
Lösung
von N-(5-Chlor-2-{[(2S)-2-hydroxy-3-(1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-propyl]oxy}-4-methoxyphenyl)acetamidtrifluoracetat
(116 mg, 0,2 mmol) in Dichlormethan (50 ml) wurde bei 0°C unter Argon
mit einer Lösung
von BBr3 (1 M in Dichlormethan, 2 ml, 2
mmol) versetzt. Es wurde weitere 6 Stunden lang bei 0°C gerührt, und
dann wurde die Reaktionsmischung mit Methanol gequencht. Das Lösungsmittel
wurde im Vakuum entfernt und der Rückstand wurde durch HPLC (Laufmittel:
[Acetonitril/Wasser + 0,1% TFA]) aufgereinigt, wodurch man einen
farblosen Feststoff (12 mg, 10%) erhielt.
1H-NMR
(Aceton-d6, 400 MHz): δ 8,62 (s, 1H), 8,26 (s 1H),
7,21 (d, J = 7,3 Hz, 1H), 7,12 (t, J = 7,7 Hz, 1H), 6,86 (t, J =
7,4 Hz, 1H), 6,75 (m, 2H), 4,55 (m, 1H), 4,10 (m, 2H), 3,93-3,19
(m, 8H), 3,16 (s, 2H), 2,43-2,15 (m,
4H), 2,11 (s, 3H).
APCI-MS: m/z 447 (MH+).
-
Beispiel 109
-
(3S)-N-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-methoxyphenyl)-3-hydroxypyrrolidin-1-carbonsäureamidtrifluoracetat
(Salz)
-
Die
Titelverbindung wurde unter Verwendung von 6-Methoxy-1,3-benzoxazol-2(3H)on wie in
Beispiel 84 beschrieben dargestellt.
1H-NMR
(Aceton-d6, 400 MHz): δ 7,74 (m, 1H), 7,23 (s, 1H),
7,13 (dd, J = 8,5, 2,2 Hz, 1H), 7,03 (s, 1H), 6,77 (d, J = 8,5 Hz,
1H), 6,61 (d, J = 2,7 Hz, 1H), 6,49 (dd, J = 8,8, 2,7 Hz, 1H), 4,59
(m, 1H), 4,47 (m, 1H), 4,14 (m, 2H), 3,80 (m, 2H), 3,75 (s, 3H),
3,64-3,40 (m, 8H), 3,16 (s, 2H), 2,44-2,16 (m, 4H), 2,09-1,89 (m,
2H).
APCI-MS: m/z 532 (MH+).
-
Beispiel 110
-
(3S)-N-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxyphenyl)-3-hydroxypyrrolidin-1-carbonsäureamidtrifluoracetat
(Salz)
-
Eine
gerührte
Lösung
von (3S)-N-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-methoxyphenyl)-3-hydroxypyrrolidin-1-carbonsäureamidtrifluoracetat
(59 mg, 0,09 mmol) in Dichlormethan (50 ml) wurde unter Argon bei
0°C mit
einer Lösung
von BBr3 (1 M in Dichlormethan, 1,8 ml,
1,8 mmol) versetzt. Es wurde weitere 4 Stunden lang bei 0°C gerührt, und
die Reaktionsmischung wurde dann mit Methanol gequencht. Das Lösungsmittel
wurde im Vakuum entfernt und der Rückstand wurde durch HPLC (Laufmittel:
[Acetonitril/Wasser + 0,1% TFA]) aufgereinigt, wodurch man einen
farblosen Feststoff (30 mg, 53%) erhielt.
1H-NMR
(Aceton-d6, 400 MHz): δ 7,52 (m, 1H), 7,23 (s, 1H),
7,13 (dd, J = 8,5, 2,3 Hz, 1H), 6,99 (s, 1H), 6,77 (d, J = 8,5 Hz,
1H), 6,57 (d, J = 2,5 Hz, 1H), 6,39 (dd, J = 8,6, 2,6 Hz, 1H), 4,56
(m, 1H), 4,46 (m, 1H), 4,07 (m, 2H), 3,90-3,21 (m, 10H), 3,16 (s,
2H), 2,42-2,16 (m, 4H), 2,09-1,90 (m, 2H).
APCI-MS: m/z 518
(MH+).
-
Beispiel 111
-
(3S)-1-(4-Hydroxy-2-{[(2S)-2-hydroxy-3-(1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)propyl]oxy)benzoyl)-pyrrolidin-3-oltrifluoracetat
(Salz)
-
Schritt I:
-
2-{[(2S)-2-Hydroxy-3-(1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)propyl]oxy}-4-[(4-methoxybenzyl)oxy]-benzoesäuremethylestertrifluoracetat
(Salz)
-
Eine
Lösung
von 3H-Spiro[1-benzofuran-2,4'-piperidin]
(50 mg, 0,26 mmol) und 4-[(4-Methoxybenzyl)oxy]-2-[(2S)-oxiran-2-ylmethoxy]benzoesäuremethylester
(91 mg, 0,26 mmol) in Ethanol (3 ml) wurde 6 Stunden lang unter
Rückfluß erhitzt.
Das Lösungsmittel
wurde im Vakuum abdestilliert. Der Rückstand wurde durch HPLC (Laufmittel:
[Acetonitril/Wasser + 0,1% TFA]) aufgereinigt, wodurch man einen
farblosen Feststoff (103 mg, 61%) erhielt.
APCI-MS: m/z 534
(MH+)
-
Schritt II:
-
2-{[(2S)-2-Hydroxy-3-(1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)propyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoesäurehydrochlorid
-
Eine
Mischung von 2-{[(2S)-2-Hydroxy-3-(1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)propyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoesäuremethylestertrifluoracetat
(103 mg, 0,16 mmol) in Ethanol (5 ml) wurde mit einer 10 N wäßrigen Lösung von
NaOH (1 ml) und Wasser (1 ml) versetzt. Die Mischung wurde über Nacht
bei Raumtemperatur gerührt,
mit wäßriger HCl
(2 M) auf einen pH-Wert
von 1 eingestellt, mit Essigsäureethylester
extrahiert und über Natriumsulfat
getrocknet. Die flüchtigen
Bestandteile wurden im Vakuum entfernt, wodurch man die im Untertitel
genannte Verbindung erhielt, die ohne weitere Aufreinigung verwendet
wurde.
APCI-MS: m/z 520 (MH+)
-
Schritt III:
-
(3S)-1-(4-Hydroxy-2-{[(2S)-2-hydroxy-3-(1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-propyl]oxy)benzoyl)pyrrolidin-3-oltrifluoracetat
(Salz)
-
Eine
Mischung von PS-Carbodiimid (250 mg, 0,32 mmol) und Dichlormethan
(5 ml) wurde 15 Minuten lang bei Raumtemperatur gerührt und
dann mit 2-{[(2S)-2-Hydroxy-3-(1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-propyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoesäurehydrochlorid
(89 mg, 0,16 mmol) versetzt, und die Mischung wurde 30 Minuten lang
gerührt.
Eine Lösung
von (3S)-Pyrrolidin-3-ol
(14 mg, 0,16 mmol) in Dichlormethan (1 ml) wurde zugesetzt. Die
Mischung wurde 24 Stunden lang bei Raumtemperatur gerührt und
dann filtriert. Trifluoressigsäure
(10% in Dichlormethan, 5 ml) wurde zugefügt, und es wurde 1 weitere
Stunde lang bei Raumtemperatur gerührt. Die flüchtigen Bestandteile wurden
im Vakuum entfernt und der Rückstand
wurde durch HPLC (Acetonitril/Wasser, 0,1% Trifluoressigsäure) aufgereinigt,
wodurch man die Titelverbindung (14 mg, Gesamtausbeute über die
Stufen II-III 15%) erhielt.
1H-NMR
(Aceton-d6, 400 MHz): δ 7,20 (d, J = 7,2 Hz, 1H), 7,12
(m, 2H), 6,85 (t, J = 7,4 Hz, 1H), 6,76 (d, J = 7,9 Hz, 1H), 6,60
(dd, J = 7,4, 2,0 Hz, 1H), 6,51 (dt, J = 8,2, 2,4 Hz, 1H), 4,49
(s, 2H), 4,40 (m, 1H), 4,17-4,00 (m,
3H), 3,87-3,25 (m, 8H), 3,12 (s, 2H), 2,45-2,12 (m, 4H), 2,10-1,85 (m, 2H).
APCI-MS:
m/z 469 (MH+).
-
Beispiel 112
-
2-([(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy)-5-methylbenzoesäurehydrochlorid
-
Schritt I:
-
5-Methyl-2-[(2S)-oxiran-2-ylmethoxy]benzoesäuremethylester
-
Eine
Lösung
von 2-Hydroxy-5-methylbenzoesäuremethylester
(0,166 g, 1 mmol), 3-Nitrobenzolsulfonsäure-(2S)-oxiran-2-ylmethylester (0,26 g, 1 mmol)
und Caesiumcarbonat (0,39 g, 1,2 mmol) in Dimethylformamid (5 ml)
wurde über
Nacht bei Raumtemperatur gerührt.
Die Mischung wurde zwischen Wasser und Essigsäureethylester verteilt, und
die organische Phase wurde zweimal mit Wasser und einmal mit Kochsalzlösung gewaschen,
und anschließend
eingeengt. Das Rohprodukt wurde durch Flash-Chromatographie an Kieselgel (Laufmittel:
Essigsäureethylester/n-Heptan)
aufgereinigt, wodurch man die Titelverbindung (0,16 g, 72%) in Form
eines farblosen Öls
erhielt.
1H-NMR (CDCl3,
400 MHz): δ 7,61
(d, J = 2,0 Hz, 1H), 7,25 (d, J = 9,9 Hz, 1H), 6,89 (d, J = 8,4
Hz, 1H), 4,28 (dd, J = 11,2, 3,0 Hz, 1H), 4,07 (dd, J = 11,2, 4,9
Hz, 1H), 3,89 (s, 3H), 3,38 (m, 1H), 2,89 (m, 2H), 2,30 (s, 3H)
-
Schritt II:
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy)-5-methylbenzoesäuremethylestertrifluoracetat
(Salz)
-
Eine
Lösung
von 5-Chlor-3H-spiro[1-benzofuran-2,4'-piperidin]
(112 mg, 0,5 mmol) und 5-Methyl-2-[(2S)-oxiran-2-ylmethoxy]benzoesäuremethylester
(111 mg, 0,5 mmol) in Ethanol (5 ml) wurde 6 Stunden lang unter
Rückfluß erhitzt.
Das Lösungsmittel
wurde im Vakuum abdestilliert. Der Rückstand wurde durch HPLC (Laufmittel:
[Acetonitril/Wasser + 0,1% TFA]) aufgereinigt, wodurch man einen
farblosen Feststoff (153 mg, 54%) erhielt.
APCI-MS: m/z 446
(MH+)
-
Schritt III:
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy)-5-methylbenzoesäurehydrochlorid
-
Eine
Mischung von 2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-5-methylbenzoesäuremethylestertrifluoracetat
(153 mg, 0,27 mmol) in Ethanol (5 ml) wurde mit einer 10 N wäßrigen Lösung von NaOH
(1 ml) und Wasser (1 ml) versetzt. Die Mischung wurde 3 Stunden
lang bei Raumtemperatur gerührt, mit
wäßriger HCl
(2 M) auf einen pH-Wert von 1 eingestellt, mit Essigsäureethylester
extrahiert und über
Natriumsulfat getrocknet. Die flüchtigen
Bestandteile wurden im Vakuum entfernt, wodurch man die im Untertitel genannte
Verbindung (123 mg, 96%) erhielt.
1H-NMR
(Aceton-d6, 400 MHz): δ 7,68 (d, J = 2,1 Hz, 1H), 7,36
(dd, J = 8,6, 2,1 Hz, 1H), 7,22 (s, 1H), 7,11 (m, 2H), 6,76 (d,
J = 8,5 Hz, 1H), 4,68 (m, 1H), 4,27 (m, 1H), 4,17 (m, 1H), 3,72
(bs, 2H), 3,67 (d, J = 13,7 Hz, 1H), 3,51 (bs, 2H), 3,43 (dd, J
= 13,5, 8,8 Hz, 1H), 3,19 (s, 2H), 2,47 (bs, 2H), 2,30 (s, 3H),
2,22 (bs, 2H).
APCI-MS: m/z 423 (MH+)
-
Beispiel 113
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-methoxybenzoesäurehydrochlorid
-
Die
Titelverbindung wurde unter Verwendung von 2-Hydroxy-4-methoxybenzoesäuremethylester
wie in Beispiel 112 beschrieben dargestellt.
1H-NMR
(Aceton-d6, 400 MHz): δ 7,89 (d, J = 8,8 Hz, 1H), 7,23
(m, 1H), 7,12 (dd, J = 8,5, 2,3 Hz, 1H), 6,76 (d, J = 8,6 Hz, 2H),
6,74 (d, J = 2,3 Hz, 2H), 6,65 (dd, J = 8,8, 2,3 Hz, 1H), 4,70 (m,
1H), 4,31 (m, 1H), 4,22 (m, 1H), 3,89 (s, 3H), 3,73 (bs, 2H), 3,67
(dd, J = 13,4, 1,9 Hz, 1H), 3,58-3,45 (m, 2H), 3,41 (dd, J = 13,5,
8,7 Hz, 1H), 3,19 (s, 2H), 2,49 (m, 2H), 2,24 (dl, J = 14,0 Hz,
2H)
APCI-MS: m/z 448 (MH+)
-
Beispiel 114
-
(3S)-1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy)-5-methylbenzoyl)pyrrolidin-3-oltrifluoracetat
(Salz)
-
Eine
Mischung von PS-Carbodiimid (78 mg, 0,1 mmol) und Dichlormethan
(5 ml) wurde 15 Minuten lang bei Raumtemperatur gerührt und
dann mit 2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-5-methylbenzoesäurehydrochlorid
(23 mg, 0,05 mmol) versetzt, und die Mischung wurde 30 Minuten lang
gerührt.
Eine Lösung
von (3S)-Pyrrolidin-3-ol (5 mg, 0,05 mmol) in Dichlormethan (1 ml)
wurde zugesetzt. Die Mischung wurde 24 Stunden lang bei Raumtemperatur
gerührt
und filtriert. Die flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch HPLC (Acetonitril/Wasser,
0,1% Trifluoressigsäure)
aufgereinigt, wodurch man (6 mg, 21%) die Titelverbindung erhielt.
1H-NMR (Aceton-d6,
400 MHz): δ 7,17
(s, 2H), 7,08 (d, J = 8,5 Hz, 2H), 7,04 (d, J = 1,6 Hz, 2H), 6,99
(dd, J = 8,3, 5,3 Hz, 2H), 6,70 (d, J = 8,4 Hz, 1H), 4,49 (m, 1H),
4,39 (m, 1H), 4,15 (m, 2H), 3,98 (m, 3H), 3,63 (dd, J = 9,1, 5,4
Hz, 2H), 3,59-3,40 (m, 3H), 3,28 (m, 2H), 3,04 (s, 3H), 2,75-2,49
(m, 4H), 2,27 (d, J = 2,2 Hz, 4H).
APCI-MS: m/z 501 (MH+)
-
Beispiel 115
-
(3S)-1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-methoxybenzoyl)pyrrolidin-3-oltrifluoracetat
(Salz)
-
Die
Titelverbindung wurde ausgehend 2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-methoxybenzoesäurehydrochlorid
wie in Beispiel 114 beschrieben dargestellt.
1H-NMR
(Aceton-d6, 400 MHz): δ 7,23 (s, 1H), 7,19 (dd, J =
8,4, 3,1 Hz, 1H), 7,13 (d, J = 8,6 Hz, 1H), 6,77 (d, J = 8,5 Hz,
1H), 6,67 (t, J = 2,4 Hz, 1H), 6,60 (dt, J = 8,4, 2,2 Hz, 1H), 4,51
(m, 2H), 4,39 (m, 1H), 4,22-4,12 (m, 2H), 4,08 (m, 1H), 3,83 (s,
3H), 3,85-3,25 (m, 8H), 3,16 (s, 2H), 2,35 (bs, 2H), 2,21 (bs, 2H).
APCI-MS:
m/z 517 (MH+)
-
Beispiel 116
-
5-Chlor-2-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy)benzoesäurehydrochlorid
-
Die
Titelverbindung wurde unter Verwendung von 5-Chlor-2-hydroxybenzoesäuremethylester
wie in Beispiel 112 beschrieben dargestellt. 1H-NMR
(Aceton-d6, 400 MHz): δ 7,81 (d, J = 2,8 Hz, 1H), 7,57
(dd, J = 9,0, 2,8 Hz, 1H), 7,26 (d, J = 9,0 Hz, 1H), 7,23 (s, 1H),
7,13 (dd, J = 8,5, 2,2 Hz, 1H), 6,77 (d, J = 8,5 Hz, 1H), 4,66 (m,
2H), 4,32 (m, 1H), 4,19 (m, 1H), 3,73 (bs, 2H), 3,69 (d, J = 13,3
Hz, 1H), 3,54 (bs, 2H), 3,45 (dd, J = 13,5, 8,9 Hz, 1H), 3,20 (s,
2H), 2,46 (bs, 2H), 2,24 (dl, J = 12,3 Hz, 2H).
APCI-MS: m/z
452 (MH+)
-
Beispiel 117
-
(3S)-1-(5-Chlor-2-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}benzoyl)pyrrolidin-3-oltrifluoracetat
(Salz)
-
Die
Titelverbindung wurde ausgehend von 5-Chlor-2-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-pipe ridin]-1'-yl)-2-hydroxypropyl]oxy}benzoesäurehydrochlorid
wie in Beispiel 114 beschrieben dargestellt.
1H-NMR
(Aceton-d6, 400 MHz): δ 7,39 (dt, J = 8,8, 2,4 Hz,
1H), 7,25 (dd, J = 4,1, 2,8 Hz, 1H), 7,23 (s, 1H), 7,15 (d, J =
8,7 Hz, 1H), 7,12 (s, 1H), 6,77 (d, J = 8,5 Hz, 1H), 4,53 (m, 2H),
4,42 (m, 1H), 4,23-4,06 (m, 3H), 3,76-3,14 (m, 12H), 2,33 (bs, 2H),
2,23 (bs, 2H).
APCI-MS: m/z 521 (MH+)
-
Beispiel 118
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy)-5-fluorbenzoesäurehydrochlorid
-
Die
Titelverbindung wurde unter Verwendung von 5-Fluor-2-hydroxybenzoesäuremethylester
wie in Beispiel 112 beschrieben dargestellt.
1H-NMR
(Aceton-d6, 400 MHz): δ 7,56 (dd, J = 8,9, 3,2 Hz,
1H), 7,35 (m, 1H), 7,27 (dd, J = 9,2, 4,4 Hz, 1H), 7,13 (dd, J =
8,4, 2,1 Hz, 1H), 6,76 (d, J = 8,5 Hz, 1H), 4,68 (m, 1H), 4,29 (m,
1H), 4,18 (m, 1H), 3,72 (bs, 2H), 3,68 (dl, J = 13,1 Hz, 3H), 3,51
(bs, 1H), 3,41 (dd, J = 13,4, 9,0 Hz, 3H), 3,19 (s, 2H), 2,53 (bs,
2H), 2,22 (bs, 2H).
APCI-MS: m/z 436 (MH+)
-
Beispiel 119
-
(3S)-1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy)-5-fluorbenzoyl)pyrrolidin-3-oltrifluoracetat
(Salz)
-
Die
Titelverbindung wurde ausgehend von 5-Fluor-2-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}benzoesäurehydrochlorid
wie in Beispiel 114 beschrieben dargestellt.
1H-NMR
(Aceton-d6, 400 MHz): δ 7,23 (s, 1H), 7,16 (m, 2H),
7,12 (s, 1H), 7,04 (m, 1H), 6,77 (d, J = 8,5 Hz, 1H), 4,51 (m, 2H),
4,41 (m, 1H), 4,19-4,04 (m, 3H), 3,70-3,13 (m, 12H), 2,32 (bs, 2H),
2,23 (bs, 2H).
APCI-MS: m/z 505 (MH+)
-
Beispiel 120
-
N-(2-{((2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy)phenyl)pyrrolidin-1-carbonsäureamidtrifluoracetat
(Salz)
-
Die
Titelverbindung wurde unter Verwendung von 1,3-Benzoxazol-2(3H)-on und Pyrrolidin wie
in Beispiel 84 beschrieben dargestellt.
1H-NMR
(Aceton-d6, 400 MHz): δ 8,14 (m, 1H), 7,23 (s, 2H),
7,13 (dd, J = 8,5, 2,2 Hz, 1H), 6,99 (m, 1H), 6,90 (m, 2H), 6,76
(d, J = 8,6 Hz, 1H), 4,64 (m, 1H), 4,13 (m, 1H), 3,82 (bs, 2H),
3,61 (dl, J = 13,1 Hz, 2H), 3,55-3,42 (m, 8H), 3,18 (s, 2H), 2,35
(bs, 2H), 2,25 (bs, 2H), 1,93 (m, 4H).
APCI-MS: m/z 486 (MH+).
-
Beispiel 121
-
4-(Acetylamino)-3-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy)-benzoesäuremethylestertrifluoracetat
(Salz)
-
Schritt I:
-
4-(Acetylamino)-3-hydroxybenzoesäuremethylester
-
Eine
Lösung
von 3-Hydroxy-4-nitrobenzoesäuremethylester
(0,78 g, 3,96 mmol) in THF (40 ml) mit Pd auf Aktivkohle (10%, 0,15
g) wurde über
Nacht bei Normaldruck unter einer Wasserstoffatmosphäre gerührt. Die
Mischung wurde über
Celite filtriert. Das Lösungsmittel
wurde im Vakuum entfernt. Der Rückstand
wurde in Wasser (20 ml) aufgenommen und mit Essigsäureanhydrid
(0,5 ml, 5,29 mmol) versetzt. Die Mischung wurde 30 Minuten lang
kräftig
bei 65°C
gerührt.
Nach dem Abkühlen
auf Raumtemperatur wurde der Niederschlag abfiltriert, mit Wasser
gewaschen und getrocknet. Weißes
Pulver (0,64 g, 77%).
-
Schritt II:
-
4-(Acetylamino)-3-[(2S)-oxiran-2-ylmethoxy]benzoesäuremethylester
-
Eine
Lösung
von 4-(Acetylamino)-3-hydroxybenzoesäuremethylester (0,209 g, 1
mmol), 3-Nitrobenzolsulfonsäure-(2S)-oxiran-2-ylmethylester
(0,26 g, 1 mmol) und Caesiumcarbonat (0,39 g, 1,2 mmol) in Dimethylformamid
(5 ml) wurde bei Raumtemperatur über
Nacht gerührt.
Die Mischung wurde zwischen Wasser und Essigsäureethylester verteilt, und
die organische Phase wurde zweimal mit Wasser und einmal mit Kochsalzlösung gewaschen
und anschließend
eingeengt. Das Rohprodukt wurde durch Flash-Chromatographie an Kieselgel
(Laufmittel: Essigsäureethylester/n-Heptan)
aufgereinigt, wodurch man die im Untertitel genannte Verbindung
(96 mg, 36%) in Form eines farblosen Öls erhielt.
1H-NMR
(CDCl3, 400 MHz): δ 8,45 (d, J = 8,5 Hz, 1H), 8,12
(s, 1H), 7,69 (dd, J = 8,5, 1,6 Hz, 1H), 7,54 (d, J = 1,7 Hz, 1H),
4,43 (dd, J = 11,3, 2,3 Hz, 1H), 3,96 (dd, J = 11,3, 6,3 Hz, 1H),
3,89 (s, 3H), 3,41 (m, 1H), 2,96 (t, J = 4,5 Hz, 1H), 2,79 (dd,
J = 4,7, 2,6 Hz, 1H), 2,24 (s, 3H).
APCI-MS: m/z 266 (MH+).
-
Schritt III:
-
4-(Acetylamino)-3-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-benzoesäuremethylestertrifluoracetat
(Salz)
-
Eine
Lösung
von 5-Chlor-3H-spiro[1-benzofuran-2,4'-piperidin]
(81 mg, 0,36 mmol) und 4-(Acetylamino)-3- [(2S)-oxiran-2-ylmethoxy]benzoesäuremethylester
(96 mg, 0,36 mmol) in Ethanol (5 ml) wurde 5 Stunden lang auf Rückfluß erhitzt.
Das Lösungsmittel
wurde im Vakuum abdestilliert. Der Rückstand wurde durch HPLC (Laufmittel:
[Acetonitril/Wasser + 0,1% TFA]) aufgereinigt, wodurch man einen
farblosen Feststoff (177 mg, 82%) erhielt.
1H-NMR
(Aceton-d6, 400 MHz): δ 8,97 (s, 1H), 8,49 (d, J =
8,5 Hz, 1H), 7,64 (dd, J = 8,6, 1,7 Hz, 1H), 7,57 (d, J = 1,4 Hz,
1H), 7,24 (s, 1H), 7,13 (dd, J = 8,5, 2,0 Hz, 1H), 6,76 (d, J =
8,5 Hz, 1H), 4,60 (m, 1H), 4,22 (m, 2H), 3,93-3,69 (m, 6H), 3,85
(s, 3H), 3,21 (s, 2H), 2,44-2,22 (m, 4H), 2,20 (s, 3H).
APCI-MS:
m/z 489 (MH+).
-
Beispiel 122
-
4-(Acetylamino)-3-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1-yl)-2-hydroxypropyl]oxy)benzoesäuretrifluoracetat
(Salz)
-
Eine
gerührte
Lösung
von 4-(Acetylamino)-3-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}benzoesäuremethylestertrifluoracetatsalz
(175 mg, 0,29 mmol) in Ethanol (4 ml) wurde mit 2 M wäßriger NaOH
(4 ml) versetzt. Die Reaktionsmischung wurde über Nacht bei Raumtemperatur
gerührt.
Der pH-Wert wurde dann zurch Zugabe von TFA auf 5 eingestellt.
-
Die
Mischung wurde im Vakuum eingeengt und durch HPLC (Laufmittel: [Acetonitril/Wasser
+ 0,1% TFA]) aufgereinigt, wodurch man einen farblosen Feststoff
(114 mg, 67%) erhielt.
1H-NMR (Aceton-d6, 400 MHz): δ 8,96 (s, 1H), 8,48 (d, J =
8,4 Hz, 1H), 7,67 (dd, J = 8,5, 1,6 Hz, 1H), 7,58 (d, J = 1,1 Hz,
1H), 7,24 (s, 1H), 7,13 (dd, J = 8,5, 2,1 Hz, 1H), 6,76 (d, J =
8,5 Hz, 1H), 4,61 (m, 1H), 4,23 (m, 2H), 3,96-3,42 (m, 6H), 3,21
(s, 2H), 2,48-2,21 (m, 4H), 2,20 (s, 3H).
APCI-MS: m/z 475
(MH+).
-
Beispiel 123
-
N-(2-{[(2S)-3-(5-Chlor-3'-fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxyphenyl)acetamid
-
Die
Titelverbindung wurde wie in Beispiel 27 beschrieben ausgehend von
5-Chlor-3'-fluor-3H-spiro(1-benzofuran-2,4'-piperidin) (57,3
mg, 0,212 mmol) und 4-{(Acetylamino)-3-(2S)-oxiran-2-ylmethoxy]phenylester
(51,2 mg, 0,216 mmol) dargestellt, wodurch man 18 mg (18%) der Titelverbindung
erhielt.
APCI-MS: m/z 465 (M+H)+
-
Beispiel 124
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-(2-hydroxypropyl)benzamid
-
Harzgebundenes
Carbodiimid (60 mg, 0,08 mmol) wurde 30 Minuten in Dichlormethan
(0,5 ml) aufquellen gelassen. 2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoesäure (24,7
mg, 0,045 mmol, 0,3 M in 1-Methyl-2-pyrrolidinon) wurde zugegeben,
und nach weiteren 30 Minuten wurde mit 1-Aminopropan-2-ol (0,21
ml, 0,3 M in 1-Methyl-2-pyrrolidinon) versetzt. Es wurde über Nacht
bei Raumtemperatur reagieren gelassen, worauf das Harz abfiltiert
und mit mehreren Portionen Dichlormethan gewaschen wurde. Die organischen
Phasen wurden gesammelt und eingedampft. Das Rohprodukt 2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-N-(2-hydroxypropyl)-4-[(4-methoxybenzyl)oxy)benzamid
wurde in Trifluoressigsäure/Dichlormethan
(1,2 ml 70/30) gelöst
und über Nacht
bei Raumtemperatur gerührt.
Die Lösungsmittel
wurden abgedampft und das auf diese Weise erhaltene Rohprodukt wurde
mit Acetonitril/Wasser + 0,1% Trifluoressigsäure als Laufmittel an C18 aufgereinigt.
Die reinen Fraktionen wurden gesammelt, vereinigt und eingedampft,
wodurch man die Titelverbindung in Form des Trifluoracetats erhielt.
APCI-MS
m/z: 490 [MH+]
-
Die
folgenden Verbindungen in den Beispielen 125 bis 166 wurden nach
Verfahren analog dem in Beispiel 124 beschriebenen Verfahren dargestellt.
-
Beispiel 125
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-(2-hydroxy-1,1-dimethylethyl)benzamid
-
-
Beispiel 126
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-N-cyclopentyl-4-hydroxybenzamid
-
-
Beispiel 127
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-(2-methoxyethyl)benzamid
-
-
Beispiel 128
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro(1-benzofuran-2‚4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N{2-hydroxyphenyl)benzamid
-
-
Beispiel 129
-
N-(tert.-Butyl)-2-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzamid
-
-
Beispiel 130
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-(2-hydroxy-1-methylethyl)benzamid
-
-
Beispiel 131
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-isobutylbenzamid
-
-
Beispiel 132
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-(4-hydroxycyclohexyl)benzamid
-
-
Beispiel 133
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-N-(2,3-dihydroxypropyl)-4-hydroxybenzamid
-
-
Beispiel 134
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}hydroxy-N-(2-hydroxyethyl)-N-methylbenzamid
-
-
Beispiel 135
-
N-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)serinmethylester
-
-
Beispiel 136
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy)-N-(1-ethylpropyl)-4-hydroxybenzamid
-
-
Beispiel 137
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-(tetrahydrofuran-2-ylmethyl)benzamid
-
-
Beispiel 138
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-[1-(hydroxymethyl)-2,2-dimethylpropyl]benzamid
-
-
Beispiel 139
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy)-N-{[(1S,2R,5S)-6,6-dimethylbicyclo[3.1.1]hept-2-yl]methyl}4-hydroxybenzamid
-
-
Beispiel 140
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-[1-(hydroxymethyl)-2-methylpropyl]benzamid
-
-
Beispiel 141
-
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-{[4-(2-hydroxyethyl)piperazin-1-yl]carbonyl}phenol
-
-
Beispiel 142
-
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-{[3-(hydroxymethyl)piperidin-1-yl]carbonyl)phenol
-
-
Beispiel 143
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-N-[5-(1,1-dimethylpropyl)-2-hydroxyphenyl]4-hydroxybenzamid
-
-
Beispiel 144
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-[3-(1-hydroxyethyl)phenyl]benzamid
-
-
Beispiel 145
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy)-N-(cyclopropylmethyl)-4-hydroxybenzamid
-
-
Beispiel 146
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-pyrrolidin-1-ylbenzamid
-
-
Beispiel 147
-
N-[(1R,4S)-Bicyclo[2.2.1]hept-2-yl]-2-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzamid
-
-
Beispiel 148
-
4-(4-Chlorphenyl)-1-(2-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy)-4-hydroxybenzoyl)piperidin-4-ol
-
-
Beispiel 149
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-(2-hydroxy-1-phenylethyl)benzamid
-
-
Beispiel 150
-
1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)-4-phenylpiperidin-4-ol
-
-
Beispiel 151
-
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-(3,4-dihydroisochinolin-2(1H)-ylcarbonyl)phenol
-
-
Beispiel 152
-
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin-1'-yl)-2-hydroxypropyl]oxy}-4-{[2-(hydroxymethyl)piperidin-1-yl]carbonyl)phenol
-
-
Beispiel 153
-
1-(2-{((2S)-3-(5-Chlor-1'H,3H-spiro[I-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)-N,N-dimethylprolinamid
-
-
Beispiel 154
-
(4R)-1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)-4-hydroxyprolinmethylester
-
-
Beispiel 155
-
(3R)-1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1-yl)-2-hydroxypropyl]oxy)-4-hydroxybenzoyl)piperidin-3-ol
-
-
Beispiel 156
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-(2-hydroxycyclohexyl)benzamid
-
-
Beispiel 157
-
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-phenylpiperidin-1-yl)carbonyl]phenol
-
-
Beispiel 158
-
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-(thiomorpholin-4-ylcarbonyl)phenol
-
-
Beispiel 159
-
1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy)}hydroxybenzoyl)-piperidin-3-ol
-
-
Beispiel 160
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-N-(cyclopropylmethyl)-4-hydroxy-N-propylbenzamid
-
-
Beispiel 161
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N,N-diisobutylbenzamid
-
-
Beispiel 162
-
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy)-4-(1,3-dihydro-2H-isoindol-2-ylcarbonyl)phenol
-
-
Beispiel 163
-
N-(2-tert.-Butoxyethyl)-2-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-isobutylbenzamid
-
-
Beispiel 164
-
3-([(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-fluorpiperidin-1-yl)carbonyl]phenol
-
-
Beispiel 165
-
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy)-4-[(4,4-difluorpiperidin-1-yl)carbonyl]phenol
-
-
Beispiel 166
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy)-N-phenylbenzamid
-
-
Die
folgenden Verbindungen in den Beispielen 167 bis 211 wurden wie
in Beispiel 124 unter Verwendung von 6-Chlor-3H-spiro[2-benzofuran-1,4'-piperidin] als Ausgangsmaterial
dargestellt.
-
Beispiel 167
-
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-({(2R)-2-[hydroxy(diphenyl)methyl]pyrrolidin-1-yl}carbonyl)-phenol
-
-
Beispiel 168
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-(2-hydroxyethyl)-N-methylbenzamid
-
-
Beispiel 169
-
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-(pyrrolidin-1-ylcarbonyl)phenol
-
-
Beispiel 170
-
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro(2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-{[4-(2-hydroxyethyl)piperazin-1-yl]carbonyl}phenol
-
-
Beispiel 171
-
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-{[3-(hydroxymethyl)piperidin-1-yl]carbonyl)phenol
-
-
Beispiel 172
-
4-(4-Chlorphenyl)-1-(2-{[(2S)-3-(5-chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)piperidin-4-ol
-
-
Beispiel 173
-
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-{[4-(hydroxymethyl)piperidin-1-yl]carbonyl)phenol
-
-
Beispiel 174
-
1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy)-4-hydroxybenzoyl)-4-phenylpiperidin-4-ol
-
-
Beispiel 175
-
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-(3,4-dihydroisochinolin-2(1H)-ylcarbonyl)phenol
-
-
Beispiel 176
-
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-{[2-(hydroxymethyl)piperidin-1-yl]carbonyl}phenol
-
-
Beispiel 177
-
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-{[3-(dimethylamino)pyrrolidin-1-yl]carbonyl}phenol
-
-
Beispiel 178
-
1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)-N,N-dimethylprolinamid
-
-
Beispiel 179
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-N-cyclohexyl-4-hydroxy-N-(2-hydroxyethyl)benzamid
-
-
Beispiel 180
-
(4R)-1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl}-4-hydroxyprolinmethylester
-
-
Beispiel 181
-
(3R)-1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)piperidin-3-ol
-
-
Beispiel 182
-
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy)-4-[(4-phenylpiperidin-1-yl)carbonyl]phenol
-
-
Beispiel 183
-
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-(thiomorpholin-4-ylcarbonyl)phenol
-
-
Beispiel 184
-
1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)piperidin-3-ol
-
-
Beispiel 185
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-N-(cyclopropylmethyl)-4-hydroxy-N-propylbenzamid
-
-
Beispiel 186
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N,N-diisobutylbenzamid
-
-
Beispiel 187
-
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro(2-benzofuran-1,4'-piperidin)-1'-yl)-2-hydroxypropyl]oxy}-4-(1,3-dihydro-2H-isoindol-2-ylcarbonyl)phenol
-
-
Beispiel 188
-
N-(2-tert.-Butoxyethyl)-2-{[(2S)-3-(5-chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-isobutylbenzamid
-
-
Beispiel 189
-
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-fluorpiperidin-1-yl)carbonyl]phenol
-
-
Beispiel 190
-
3-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4,4-difluorpiperidin-1-yl)carbonyl]phenol
-
-
Beispiel 191
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-(2-hydroxypropyl)benzamid
-
-
Beispiel 192
-
2-1{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1‚4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy)-4-hydroxy-N-(2-hydroxy-1,1-dimethylethyl)benzamid
-
-
Beispiel 193
-
2-{[1(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-N-cyclopentyl-4-hydroxybenzamid
-
-
Beispiel 194
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-(2-methoxyethyl)benzamid
-
-
Beispiel 195
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-(2-hydroxyphenyl)benzamid
-
-
Beispiel 196
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-(2-hydroxy-1-methylethyl)benzamid
-
-
Beispiel 197
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-isobutylbenzamid
-
-
Beispiel 198
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-(2-hydroxyethyl)benzamid
-
-
Beispiel 199
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-(4-hydroxycyclohexyl)benzamid
-
-
Beispiel 200
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy)-N-(2,3-dihydroxypropyl)-4-hydroxybenzamid
-
-
Beispiel 201
-
N-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)serinmethylester
-
-
Beispiel 202
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy)-N-(1-ethylpropyl)-4-hydroxybenzamid
-
-
Beispiel 203
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-(tetrahydrofuran-2-ylmethyl)benzamid
-
-
Beispiel 204
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-[1-(hydroxymethyl)-2,2-dimethylpropyl]benzamid
-
-
Beispiel 205
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-[1-(hydroxymethyl)-2-methylpropyl]benzamid
-
-
Beispiel 206
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-[3-(1-hydroxyethyl)phenyl]benzamid
-
-
Beispiel 207
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy)-N-(cyclopropylmethyl)-4-hydroxybenzamid
-
-
Beispiel 208
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-pyrrolidin-1-ylbenzamid
-
-
Beispiel 209
-
N-[(1R,4S)-Bicyclo[2.2.1]-hept-2-yl]-2-{[(2S)-3-(5-chlor-1'H,3H-spiro[2-benzofuran-1‚4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzamid
-
-
Beispiel 210
-
2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxy-N-(2-hydroxy-1-phenylethyl)benzamid
-
-
Beispiel 211
-
2-([(2S)-3-(5-Chlor-1'H,3H-spiro[2-benzofuran-1,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}hydroxy-N-(2-hydroxycyclohexyl)benzamid
-
-
Beispiel 212
-
1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)pyrrolidin-3-carbonsäureamidtrifluoracetat
-
Schritt I:
-
1-{2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoyl}pyrrolidin-3-carbonsäureamid
-
Eine
Mischung von PS-Carbodiimid (425 mg, 0,54 mmol) und Dichlormethan
(5 ml) wurde 15 Minuten lang bei Raumtemperatur gerührt und
mit einer Lösung
von 2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoesäurehydrochlorid
(160 mg, 0,27 mmol) in NMP (2,5 ml) und Dichlormethan (2,5 ml) versetzt.
Die Mischung wurde 30 Minuten lang gerührt und mit einer Mischung
von Pyrrolidin-3-carbonsäureamid
(73 mg, 0,48 mmol) und Triethylamin (73 μl, 52 mmol) in Dichlormethan
(2,5 ml) versetzt. Die Mischung wurde über Nacht bei Raumtemperatur
gerührt
und dann filtriert. Die flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch HPLC (Acetonitril/Wasser,
0,025% Ammoniumhydroxid) aufgereinigt, wodurch man die im Untertitel
genannte Verbindung (55 mg, Ausbeute 31%) erhielt.
APCI-MS:
m/z 650 (MH+)
-
Schritt II:
-
1-{2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)pyrrolidin-3-carbonsäureamidtrifluoracetat
-
Eine
Lösung
von 1-{2-{[(2S)-3-(5-Chlor-1'H,3H-spiro(1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoyl}pyrrolidin-3-carbonsäureamid
(55 mg, 0,084 mmol) in Dichlormethan (3 ml) wurde mit Trifluoressigsäure (0,3
ml) versetzt. Die Mischung wurde 1 Stunde lang bei Raumtemperatur
gerührt,
die flüchtigen Bestandteile
wurden entfernt und der Rückstand
wurde durch HPLC (Acetonitril/Wasser, 0,1% Trifluoressigsäure) aufgereinigt,
wodurch man 23 mg (42%) der Titelverbindung erhielt.
1H-NMR (Aceton-d6,
400 MHz): δ 7,28-7,22
(m, 1H); 7,18-7,07
(m, 2H); 6,83-6,75 (m, 1H); 6,67-6,57 (m, 1H); 6,56-6,48 (m, 1H);
4,62-4,46 (m, 1H); 4,21-3,92 (m, 2H); 3,91-3,44 (m, 8H); 3,44-3,26
(m, 2H); 3,26-3,06 (m, 3H); 2,50-2,01 (m, 6H).
APCI-MS: m/z
530 (MH+)
-
Beispiel 213
-
1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxybenzoyl)-L-prolinamidtrifluoracetat
-
Schritt I:
-
1-{2-{((2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoyl}-L-prolinamid
-
Eine
Mischung von PS-Carbodiimid (425 mg, 0,54 mmol) und Dichlormethan
(3 ml) wurde 15 Minuten lang bei Raumtemperatur gerührt, und
wurde mit einer Lösung
von 2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'- piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoesäurehydrochlorid
(160 mg, 0,27 mmol) in NMP (1,5 ml) und Dichlormethan (2 ml) versetzt.
Die Mischung wurde 30 Minuten lang gerührt und mit einer Mischung
von L-Prolinamid (46 mg, 0,40 mmol) in Dichlormethan (2 ml) versetzt.
Die Mischung wurde über
Nacht bei Raumtemperatur gerührt
und filtriert. Die flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch HPLC (Acetonitril/Wasser, 0,025%
Ammoniumhydroxid) aufgereinigt, wodurch man 85 mg (48%) der im Untertitel
genannten Verbindung erhielt.
APCI-MS: m/z 650 (MH+)
-
Schritt II:
-
1-(2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin-1'-yl)-2-hydroxypropyl]oxy)}hydroxybenzoyl)-L-prolinamidtrifluoracetat
-
Eine
Lösung
von 1-{2-{[(2S)-3-(5-Chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoyl}-L-prolinamid
(85 mg, 0,13 mmol) in Dichlormethan (3 ml) wurde mit Trifluoressigsäure (0,3
ml) versetzt. Die Mischung wurde 1 Stunde lang bei Raumtemperatur
gerührt,
die flüchtigen
Bestandteile wurden entfernt und der Rückstand wurde durch HPLC (Acetonitril/Wasser,
0,1% Trifluoressigsäure)
aufgereinigt, wodurch man 37 mg (44%) der Titelverbindung erhielt.
1H-NMR (Aceton-d6,
400 MHz): δ 7,23
(s, 1H); 7,19-7,10, 7,06-7,03 und 6,61-6,54 (m, 5H); 6,77 (d, J
= 8,3 Hz, [H); 6,53-6,48 und 6,46-6,42 (m, 1H); 4,61-4,55 (m, 1H);
4,55-4,47 (m, 1H); 4,17-4,08 (m, 1H); 4,05-3,94 (m, 1H); 3,88-3,70
(m, 2H); 3,70-3,28 (m, 6H); a 3,16 (bs, 2H); 2,47-2,14 (m, 4H);
2,10-1,77 (m, 4H). Die Verbindung liegt in Lösung als eine Mischung von
zwei Rotameren vor.
APCI-MS: m/z 530 (MH+)
-
Beispiel 214
-
2-Chlor-5-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-{[(3R)-3-(dimethylamino)pyrrolidin-1-yl]carbonyl}phenolbis(trifluoracetat)
-
Schritt I:
-
5-Chlor-2-hydroxy-4-[(4-methoxybenzyl)oxy]benzoesäuremethylester
-
Eine
Mischung von 1-(Chlormethyl)-4-methoxybenzol (1,53 g, 9,8 mmol),
5-Chlor-2,4-dihydroxybenzoesäuremethylester
(1,98 g, 9,8 mmol) und Kaliumcarbonat (1,3 g, 9,8 mmol) in Aceton
(15 ml) wurde über Nacht
unter Rückfluß gerührt. Die
Mischung wurde filtriert, das Lösungsmittel
wurde im Vakuum entfernt und der Rückstand wurde in Essigsäureethylester
gelöst
und zweimal mit Kochsalzlösung
gewaschen. Die organische Phase wurde über Natriumsulfat getrocknet,
das Lösungsmittel
wurde im Vakuum entfernt und der Rückstand wurde durch Umkristallisieren
aus Methanol aufgereinigt. Man erhielt 1,46 g (46%) der Titelverbindung.
1H-NMR (CDCl3, 400
MHz): δ 10,90
(s, 1H); 7,84 (s, 1H); 7,39 (d, J = 8,5 Hz, 2H); 6,94 (d, J = 8,7
Hz, 2H); 6,57 (s, 1H); 5,10 (s, 2H); 3,93 (s, 3H); 3,83 (s, 3H).
-
Schritt II:
-
5-Chlor-4-[(4-methoxybenzyl)oxy]-2-[(2S)-oxiran-2-yl-methoxy]benzoesäuremethylester
-
Eine
Mischung von 5-Chlor-2-hydroxy-4-[(4-methoxybenzyl)oxy]benzoesäuremethylester
(1,78 g, 5,5 mmol), 3-Nitrobenzolsulfonsäure-(2S)-oxiran-2-ylmethylester
(1,43 g, 5,5 mmol) und Caesiumcarbonat (2,15 g, 6,6 mmol) in NMP
(15 ml) wurde über
Nacht bei Raumtemperatur gerührt.
Die Mischung wurde mit Wasser versetzt und anschließend dreimal
mit Essigsäureethylester
extrahiert. Die vereinigten organischen Phasen wurden mit Wasser
gewaschen und über
Natriumsulfat getrocknet, und das Lösungsmittel wurde im Vakuum entfernt.
Der Rückstand
wurde durch Flash-Chromatographie an Kieselgel (10–30% Essigsäureethylester/Heptan)
aufgereinigt, wodurch man 1,66 g (79%) der Titelverbindung erhielt.
1H-NMR (CDCl3, 300
MHz): δ 7,92
(s, 1H); 7,39 (d, J = 8,8 Hz, 2H); 6,93 (d, J = 8,7 Hz, 2H); 6,67
(s, 1H); 5,15 (s, 2H); 4,35 (dd, J = 2,5, 11,5 Hz, 1H); 4,02-3,96
(m, 1H); 3,87 (s, 1H); 3,83 (s, 3H); 3,41-3,35 (m, 1H); 2,95-2,88
(m, 2H).
APCI-MS: m/z 379 (MH+)
-
Schritt III:
-
5-Chlor-2-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoesäuremethylester
-
Eine
Mischung von 5-Chlor-3H-spiro[1-benzofuran-2,4'-piperidin]
(420 mg, 1,9 mmol) und 5-Chlor-4-[(4-methoxybenzyl)oxy]-2-[(2S)-oxiran-2-ylmethoxy]benzoesäuremethylester
(710 mg, 1,9 mmol) in Ethanol (15 ml) wurde unter Rühren über Nacht
auf Rückfluß erhitzt.
Das Lösungsmittel
wurde im Vakuum entfernt, der Rückstand
erforderte keine weitere Aufreinigung. Man erhielt 1,13 g (100%)
der Titelverbindung.
APCI-MS: m/z 602 (MH+)
-
Schritt IV:
-
5-Chlor-2-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoesäurehydrochlorid
-
Eine
Mischung von 5-Chlor-2-{[(2S)-3-(5-chlor-1'H,3H- spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoesäuremethylester
(1,13 g, 1,9 mmol), Kaliumhydroxid (15 g), Wasser (15 ml) und Ethanol (50
ml) wurde zwei Stunden lang bei Raumtemperatur gerührt. Das
Ethanol wurde im Vakuum entfernt, es wurde mit wäßriger Salzsäure (37%)
bis zu einem pH-Wert von 1 versetzt, und die Mischung wurde mit
Essigsäureethylester
extrahiert, mit Kochsalzlösung
gewaschen und über
Natriumsulfat getrocknet. Das Lösungsmittel wurde
im Vakuum entfernt, eine weitere Aufreinigung war nicht erforderlich,
man erhielt 1,05 g (89%) der Titelverbindung.
APCI-MS: m/z
588 (MH+)
-
Schritt V:
-
(2S)-1-{4-Chlor-2-{[(3R)-3-(dimethylamino)pyrrolidin-1-yl]carbonyl}-5-[(4-methoxybenzyl)oxy]phenoxy)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-propan-2-ol
-
Eine
Mischung von PS-Carbodiimid (380 mg, 0,49 mmol) und Dichlormethan
(3 ml) wurde 15 Minuten lang bei Raumtemperatur gerührt und
mit einer Lösung
von 5-Chlor-2-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoesäurehydrochlorid
(150 mg, 0,24 mmol) in NMP (0,5 ml) und Dichlormethan (2,5 ml) versetzt.
Die Mischung wurde 30 Minuten lang gerührt, und mit einer Mischung
von (3R)-N,N-Dimethylpyrrolidin-3-amin
(56 mg, 0,49 mmol) in Dichlormethan (2,5 ml) versetzt. Die Mischung
wurde über
Nacht bei Raumtemperatur gerührt
und dann filtriert. Die flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch HPLC (Acetonitril/Wasser,
0,025% Ammoniumhydroxid) aufgereinigt, wodurch man 110 mg, (67%)
der im Untertitel genannten Verbindung erhielt.
APCI-MS: m/z
684 (MH+)
-
Schritt VI:
-
2-Chlor-5-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-{[(3R)-3-(dimethylamino)pyrrolidin-1-yl]carbonyl}phenolbis(trifluoracetat)
-
Eine
Lösung
von (2S)-1-{4-Chlor-2-{[(3R)-3-(dimethylamino)pyrrolidin-1-yl]carbonyl}-5-[(4-methoxybenzyl)-oxy]phenoxy)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)propan-2-ol (10 mg, 0,16 mmol) in
Dichlormethan (3 ml) wurde mit Trifluoressigsäure (0,3 ml) versetzt. Die
Mischung wurde 1 Stunde lang bei Raumtemperatur gerührt, die
flüchtigen
Bestandteile wurden entfernt und der Rückstand wurde durch HPLC (Acetonitril/Wasser,
0,1% Trifluoressigsäure)
aufgereinigt, wodurch man 45 mg (35%) der Titelverbindung erhielt.
1H-NMR (Aceton-d6,
400 MHz,): δ 7,24-7,21
(m, 2H); 7,13 (d, J = 8,9 Hz, 1H); 7,07 und 6,98 (m, 1H); 6,77 (d, J
= 8,5 Hz, 1H); 4,66-4,50 (m, 1H); 4,20-3,96 (m, 2H); 3,94-3,70 (m,
2H); 3,68-3,46 (m, 4H); 3,44-3,35 (m, 1H); 3,19 (bs, 2H); 2,97 (s,
3H); 2,93 (s, 3H); 2,58-2,19
(m, 6H). Die Verbindung liegt in Lösung als eine Mischung von
zwei Rotameren vor.
APCI-MS: m/z 564 (MH+)
-
Beispiel 215
-
2-Chlor-5-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-{[(3R)-3-(hydroxymethyl)pyrrolidin-1-yl]carbonyl}phenoltrifluoracetat
-
Schritt I:
-
(2S)-1-(4-Chlor-2-([(3R)-3-(hydroxymethyl)pyrrolidin-1-yl]carbonyl)-5-[(4-methoxybenzyl)oxy]phenoxy)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)propan-2-ol
-
Eine
Mischung von PS-Carbodiimid (380 mg, 0,49 mmol) und Dichlormethan
(3 ml) wurde 15 Minuten lang bei Raumtemperatur gerührt und
wurde mit einer Lösung
von 5-Chlor-2-{[(2S)-3-(5-chlor-1'H,3H-spiro(1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoesäurehydrochlorid
(150 mg, 0,24 mmol) in NMP (1 ml) und Dichlormethan (2,5 ml) versetzt. Die
Mischung wurde 30 Minuten lang gerührt und mit einer Mischung
von (3R)-Pyrrolidin-3-ylmethanol (82 mg, 0,59 mmol) und Triethylamin
(85 μl,
61 mmol) in Dichlormethan (2,5 ml) versetzt. Die Mischung wurde
48 h bei Raumtemperatur gerührt
und dann filtriert. Die flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch HPLC (Acetonitril/Wasser,
Ammoniumhydroxid, 0,025%) aufgereinigt, wodurch man 87 mg (54%)
der im Untertitel genannten Verbindung erhielt.
APCI-MS: m/z
671 (MH+)
-
Schritt II:
-
2-Chlor-5-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-{[(3R)-3-(hydroxymethyl)pyrrolidin-1-yl]carbonyl}phenoltrifluoracetat
-
Eine
Lösung
von (2S)-1-{4-Chlor-2-{[(3R)-3-(hydroxymethyl)pyrrolidin-1-yl]carbonyl}-5-[(4-methoxybenzyl)-oxy]phenoxy}-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)propan-2-ol (87 mg, 0,13 mmol) in
Dichlormethan (3 ml) wurde mit Trifluoressigsäure (0,3 ml) versetzt. Die
Mischung wurde 1 Stunde lang bei Raumtemperatur gerührt, die
flüchtigen
Bestandteile wurden entfernt und der Rückstand wurde durch HPLC (Acetonitril/Wasser,
0,1% Trifluoressigsäure)
aufgereinigt, wodurch man 23 mg (26%) der Titelverbindung erhielt.
1H-NMR (Aceton-d6,
300 MHz): δ 7,24-7,21
(m, 2H); 7,13 (dd, J = 2,4, 8,6 Hz, 1H); 6,97-6,92 (m, 1H); 6,77
(dd, J = 1,2, 8,6 Hz, 1H); 4,57-4,46 (m, 1H); 4,18-4,04 (m, 2H);
3,92-3,70 (m, 2H); 3,70-3,30 (m, 10H); 3,29-3,12 (m, 3H); 2,52-2,16
(m, 4H); 2,10-1,68 (m, 2H).
APCI-MS: m/z 551 (MH+)
-
Beispiel 216
-
2-Chlor-5-{(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-{[(3S)-3-(hydroxymethyl)pyrrolidin-1-yl]carbonyl}-phenoltrifluoracetat
-
Die
Titelverbindung wurde unter Verwendung von (3S)-Pyrrolidin-3-ylmethanol wie in Beispiel
215 beschrieben dargestellt.
1H-NMR
(Aceton-d6, 300 MHz): δ 7,26-7,21 (m, 2H); 7,13 (dd,
J = 2,3, 8,5 Hz, 1H); 6,97-6,90 (m, 1H); 6,77 (dd, J = 1,2, 8,4
Hz, 1H); 4,56-4,46 (m, 1H); 4,17-4,03 (m, 2H); 3,92-3,70 (m, 2H);
3,70-3,33 (m, 10H); 3,30-3,22 (m, 1H); 3,17 (bs, 2H); 2,52-2,16
(m, 4H); 2,10-1,68 (m, 2H).
APCI-MS: m/z 551 (MH+)
-
Beispiel 217
-
2-Chlor-5-{[(2S)-3-(5-fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl}2-hydroxypropyl]oxy}-4-(pyrrolidin-1-ylcarbonyl)phenoltrifluoracetat
-
Schritt I:
-
5-Chlor-2-{[(2S)-3-(5-fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoesäuremethylester
-
Eine
Mischung von 5-Fluor-3H-spiro[1-benzofuran-2,4'-piperidin]
(390 mg, 1,9 mmol) und 5-Chlor-4-[(4- methoxybenzyl)oxy]-2-[(2S)-oxiran-2-ylmethoxy]benzoesäuremethylester
(710 mg, 1,9 mmol) in Ethanol (15 ml) wurde unter Rühren über Nacht
auf Rückfluß erhitzt.
Das Lösungsmittel
wurde im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (Dichlormethan/Methanol 0–3%) aufgereinigt, wodurch
man die im Untertitel genannte Verbindung erhielt.
APCI-MS:
m/z 586 (MH+)
-
Schritt II:
-
5-Chlor-2-{[(2S)-3-(5-fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoesäurehydrochlorid
-
Eine
Mischung von 5-Chlor-2-{[(2S)-3-(5-fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoesäuremethylester
(910 mg, 1,5 mmol), Kaliumhydroxid (15 g), Wasser (1 ml) und Ethanol (50
ml) wurde drei Stunden lang bei Raumtemperatur gerührt. Das
Ethanol wurde im Vakuum entfernt, es wurde mit wäßriger Salzsäure (37%)
bis zu einem pH-Wert von 1 versetzt, und die Mischung wurde mit
Essigsäureethylester
extrahiert, mit Kochsalzlösung
gewaschen und über
Natriumsulfat getrocknet. Das Lösungsmittel wurde
im Vakuum entfernt, eine weitere Aufreinigung war nicht erforderlich.
Man erhielt 0,91 g (80% Gesamtausbeute über die Stufen I-II) der Titelverbindung.
APCI-MS:
m/z 572 (MH+)
-
Schritt III:
-
(2S)-1-[4-Chlor-5-[(4-methoxybenzyl)oxy]-2-(pyrrolidin-1-ylcarbonyl)phenoxy]-3-(5-fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)propan-2-ol
-
Eine
Mischung von PS-Carbodiimid (380 mg, 0,49 mmol) und Dichlormethan
(3 ml) wurde 15 Minuten lang bei Raumtemperatur gerührt und
mit einer Lösung
von 5-Chlor-2-{[(2S)-3-(5-fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoesäurehydrochlorid
(150 mg, 0,25 mmol) in NMP (0,5 ml) und Dichlormethan (2,5 ml) versetzt.
Die Mischung wurde 30 Minuten lang gerührt und mit einer Mischung
von Pyrrolidin (56 mg, 0,49 mmol) in Dichlormethan (2,5 ml) versetzt.
Die Mischung wurde 48 Stunden lang bei Raumtemperatur gerührt und dann
filtriert. Die flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch HPLC (Acetonitril/Wasser,
0,025% Ammoniumhydroxid) aufgereinigt, wodurch man die im Untertitel
genannte Verbindung (45 mg, Ausbeute 29%) erhielt.
APCI-MS:
m/z 625 (MH+)
-
Schritt IV:
-
2-Chlor-5-{[(2S)-3-(5-fluor-1'H,3H-spiro(1-benzofuran-2,4'-piperidin-1'-yl)-2-hydroxypropyl]oxy}-4-(pyrrolidin-1-ylcarbonyl)phenoltrifluoracetat
-
Eine
Lösung
von (2S)-1-[4-Chlor-5-[(4-methoxybenzyl)-oxy]-2-(pyrrolidin-1-ylcarbonyl)phenoxy]-3-(5-fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)propan-2-ol (45 mg, 0,07
mmol) in Dichlormethan (3 ml) wurde mit Trifluoressigsäure (0,3
ml) versetzt. Die Mischung wurde 1 Stunde lang bei Raumtemperatur
gerührt,
die flüchtigen
Bestandteile wurden entfernt und der Rückstand wurde durch HPLC (Acetonitril/Wasser,
0,1% Trifluoressigsäure)
aufgereinigt, wodurch man 38 mg (87%) der Titelverbindung erhielt.
1H-NMR (Aceton-d6,
300 MHz): δ 7,24
(s, 1H); 7,04-6,98 (m, 1H); 6,97-6,94 (m, 1H); 6,94-6,84 (m, 1H); 6,77-6,72 (m, 1H); 4,56-4,45
(m, 1H); 4,17-4,06 (m, 2H); 3,90-3,69 (m, 2H); 3,60-3,44 (m, 4H);
3,44-3,28 (m, 4H); 3,16 (bs, 2H); 2,46-2,14 (m, 4H); 2,00-1,82 (m,
4H).
APCI-MS: m/z 505 (MH+)
-
Beispiel 218
-
N-(2-{[(2R)-3-(5-Fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-methoxyphenyl)acetamid
-
Schritt I:
-
(2R)-2-[(5-Methoxy-2-nitrophenoxy)methyl]oxiran
-
Eine
Mischung von (2S)-Oxiran-2-ylmethanol (296,3 mg, 4,0 mmol), 5-Methoxy-2-nitrophenol
(676,6 mg, 4,0 mmol) und Triphenylphosphin (1,05 g, 4,0 mmol) in
THF (10 ml) wurde bei Raumtemperatur tropfenweise mit Diethylazodicarboxylat
(DEAD, 704,6 mg, 4,0 mmol) in THF (5 ml) versetzt. Nach dem Ende
der Zugabe wurde die Reaktionsmischung über Nacht bei Raumtemperatur
gerührt.
Die flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (0-40% Essigsäureethylester
in Petrolether) aufgereinigt, wodurch man die im Untertitel genannte
Verbindung (650 mg) erhielt.
1H-NMR
(CDCl3, 400 MHz): δ 8,00 (d, J = 9,0 Hz, 1H), 6,60
(d, J = 2,5 Hz, 1H); 6,55 (dd, J = 2,5, 9,2 Hz, 1H); 4,41 (dd, J
= 2,7, 11,3 Hz, 1H); 4,12 (dd, J = 5,0, 11,3 Hz, 1H); 3,90 (s, 3H);
3,41 (m, 1H); 2,93 (m, 2H).
-
Schritt II:
-
N-(4-Methoxy-2-[(2R)-oxiran-2-ylmethoxy]phenyl)acetamid
-
Eine
Mischung von (2R)-2-[(5-Methoxy-2-nitrophenoxy)-methyl]oxiran (620 mg, 2,75 mmol), Pd
auf Aktivkohle (10%) (250 mg), N-Ethyldiisopropylamin (0,941 ml)
und Essigsäureanhydrid
(0,52 ml, 5,5 mmol) in Essigsäureethylester
(25 ml) wurde 40 Minuten lang unter Normaldruck hydriert. Der Katalysator
wurde filtriert und das Filtrat wurde eingeengt. Der Rückstand
wurde durch Flash-Chromatographie an Kieselgel (0–60% Essigsäureethylester
in Petrolether) aufgereinigt, wodurch man die im Untertitel genannte
Verbindung (155 mg) erhielt.
1H-NMR
(CDCl3, 400 MHz): δ 8,21 (d, J = 8,7 Hz, 1H); 6,52
(m, 2H); 4,35 (dd, J = 2,5, 11,4 Hz, 1H); 3,93 (dd, J = 6,0, 11,4
Hz, 1H); 3,80 (s, 3H); 3,40 (m, 1H); 2,96 (t, J = 4,6 Hz, 1H); 2,78
(dd, J = 2,7, 4,8 Hz, 1H).
APCI-MS: m/z 238 (MH+).
-
Schritt III:
-
N-(2-{[(2R)-3-(5-Fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-methoxyphenyl)acetamid
-
Eine
Mischung von 5-Fluor-3H-spiro[1-benzofuran-2,4'-piperidin]hydrochlorid
(154 mg, 0,632 mmol), N-{4-Methoxy-2-[(2R)-oxiran-2-ylmethoxy]phenyl}acetamid
(150 mg, 0,632 mmol) und K2CO3 (87
mg, 0,632 mmol) in Ethanol (3 ml) wurde 3 Stunden lang bei 80°C gerührt. Die
Reaktionsmischung wurde zwischen Essigsäureethylester und H2O verteilt. Die organische Phase wurde über Na2SO4 getrocknet,
filtriert und im Vakuum eingeengt. Der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (0–1,5%
Methanol in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die Titelverbindung (100 mg) erhielt.
1H-NMR
(CDCl3, 400 MHz): δ 8,18 (d, J = 8,6 Hz, 1H); 8,02
(bs, 1H); 6,87 (m, 1H); 6,80 (m, 1H); 6,66 (dd, J = 4,2, 8,7 Hz,
1H); 6,56-6,51 (m, 2H); 4,18 (m, 1H); 4,04 (dd, J = 3,3, 10,1 Hz,
1H); 3,96 (dd, J = 5,7, 10,1 Hz, 1H); 3,79 (s, 3H); 3,01 (s, 2H);
2,91 (m, 2H); 2,78-2,57 (m, 4H); 2,20 (s, 3H); 2,07-1,84 (m, 4H).
APCI-MS:
m/z 445 (MH+).
-
Beispiel 219
-
2-([(2S)-3-(5-Fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}benzoesäure methylester
-
Eine
Mischung von 5-Fluor-3H-spiro[1-benzofuran-2,4'-piperidin]
(155,4 mg, 0,75 mmol) und 2-[(2S)-Oxiran-2-ylmethoxy]benzoesäuremethylester (157 mg, 0,75
mmol) in Methanol (4 ml) wurde über Nacht
bei 80°C
gerührt.
Die flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (0–1%
Methanol in Dichlormethan, 0,1% NH4OH) aufgereinigt,
wodurch man die Titelverbindung (250 mg) erhielt.
1H-NMR
(CDCl3, 400 MHz): δ 7,83 (dd, J = 1,9, 4,1 Hz,
1H); 7,48 (m, 1H); 7,02 (m, 2H); 6,86 (m, 1H); 6,79 (m, 1H); 6,66
(dd, J = 4,2, 8,7 Hz, 1H); 4,26-4,16 (m, 2H); 4,09 (dd, J = 5,7,
9,2 Hz, 1H); 3,90 (s, 3H); 3,00 (s, 2H); 2,90-2,68 (m, 6H); 2,00
(m, 2H); 1,90 (m, 2H)
APCI-MS: m/z 416 (MH+).
-
Beispiel 220
-
2-{[(2S)-3-(5-Fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}benzoesäure (Hydrochlorid)
-
2-{[(2S)-3-(5-Fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}benzoesäuremethylester
(240 mg, 0,58 mmol) wurde in THF (4 ml) gelöst und mit wäßriger KOH
(67 mg KOH in 1 ml H2O) versetzt, und die
Reaktionsmischung wurde über
Nacht bei Raumtemperatur gerührt.
Die aus diese Weise erhaltene Mischung wurde auf einen pH-Wert von
2,0 durch Zugabe von wäßriger HCl
eingestellt und mit Essigsäureethylester
extrahiert. Die organische Phase wurde mit H2O
gewaschen, über
Na2SO4 getrocknet,
filtriert und eingeengt, wodurch man die Titelverbindung (210 mg)
erhielt.
1H-NMR (CD3OD,
400 MHz): δ7,93
(dd, J = 1,8, 7,8 Hz, 1H); 7,57 (m, 1H); 7,18 (d, J = 8,4 Hz, 1H);
7,10 (t, J = 7,6 Hz, 1H); 6,97 (dd, J = 2,6, 8,1 Hz, 1H); 6,85 (m, 1H);
6,73 (dd, J = 4,2, 8,8 Hz, 1H); 4,46 (m, 1H); 4,31 (dd, J = 4,0,
9,5 Hz, 1H); 4,15 (dd, J = 5,4, 9,5 Hz, 1H); 3,76-3,40 (m, 6H);
3,16 (s, 2H); 2,30 (m, 2H); 2,19 (m, 2H).
APCI-MS: m/z 403
(MH+).
-
Beispiel 221
-
(3S)-1-(2-{[(2S)-3-(5-Fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin)-1'-yl)-2-hydroxypropyl]oxy}benzoyl)-pyrrolidin-3-ol
-
Eine
Mischung von 2-{[(2S)-3-(5-Fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-benzoesäure (Hydrochlorid)
(200 mg, 0,456 mmol) und N,N-Carbonyldiimidazol (89 mg, 0,548 mmol) in
DMF (3 ml) wurde 40 Minuten lang bei Raumtemperatur gerührt und
mit einer Lösung
von 3(S)-Pyrrolidin-3-ol (199 mg, 2,28 mmol) in DMF (1 ml) versetzt,
und die Reaktionsmischung wurde über
Nacht bei Raumtemperatur gerührt.
Die Mischung wurde zwischen Essigsäureethylester und H2O verteilt, und die organische Phase wurde über Na2SO4 getrocknet,
filtriert und eingeengt. Der Rückstand
wurde durch Flash-Chromatographie an Kieselgel (0–2% Methanol
in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die Titelverbindung (96 mg) erhielt.
1H-NMR
(CD3OD, 400 MHz): δ 7,42 (m, 1H); 7,27 (d, J =
7,4 Hz, 1H); 7,11 (dd, J = 2,8, 8,4 Hz, 1H); 7,04 (t, J = 7,4 Hz,
1H); 6,90 (dd, J = 2,5, 8,0 Hz, 1H); 6,78 (m, 1H); 6,63 (dd, J =
4,2, 8,7 Hz, 1H); 4,50 (m, 0,5H); 4,38 (m, 0,5H); 4,17-4,00 (m,
3H); 3,72 (m 1H); 3,63 (m, 1H); 3,50 (m, 1H); 3,373,18 (m, 1H, sous
le pic du Methanol); 3,02 (s, 2H); 2,77-2,54 (m, 6H); 2,18-1,78
(m, 6H)
APCI-MS: m/z 471 (MH+).
-
Beispiel 222
-
3-{[(2S)-3-(5-Fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-(pyrrolidin-1-ylcarbonyl)phenol
-
Schritt I:
-
2-{((2S)-3-(5-Fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy)-4-[(4-methoxybenzyl)oxy]benzoesäuremethylester
-
Eine
Mischung von 5-Fluor-3H-spiro[1-benzofuran-2,4'-piperidin]
(119 mg, 0,577 mmol) und 4-[(4-Methoxybenzyl)oxy]-2-[(2S)-oxiran-2-ylmethoxy]benzoesäuremethylester
(199 mg, 0,577 mmol) in Methanol (3 ml) wurde über Nacht bei 80°C gerührt. Die
flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (0–1,5%
Methanol in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die im Untertitel genannte Verbindung (228 mg) erhielt.
1H-NMR (CDCl3, 400
MHz): δ 7,85
(d, J = 8,6 Hz, 1H); 7,36 (d, J = 8,6 Hz, 1H); 6,94 (m, 2H); 6,89-6,77
(m, 2H); 6,66 (dd, J = 4,1, 8,7 Hz, 1H); 6,62-6,57 (m, 2H); 4,28
(m, 1H); 4,12 (dd, J = 4,7, 9,3 Hz, 1H); 4,06 (dd, J = 5,9, 9,3
Hz, 1H); 3,88 (s, 3H); 3,85 (s, 3H); 3,00 (s, 2H); 2,98-2,74 (m,
6H); 2,00 (breit, s, 4H).
APCI-MS: m/z 552 (MH+).
-
Schritt II:
-
2-{((2S)-3-(5-Fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoesäure (Hydrochlorid)
-
2-{[(2S)-3-(5-Fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoesäuremethylester
(220 mg, 0,398 mmol) wurde in Ethanol (3 ml) und mit wäßriger KOH
(224 mg KOH in 1 ml H2O) versetzt, und die
Mischung wurde über
Nacht bei Rückflußtemperatur
gerührt
und auf 0°C abgekühlt, bis
zu dem Erreichen eines pH-Wertes von 2,0 mit wäßriger HCl versetzt, mit Essigsäureethylester extrahiert,
mit H2O gewaschen, über Na2SO4 getrocknet, filtriert und eingeengt, wodurch
man die im Untertitel genannte Verbindung (180 mg) erhielt.
1H-NMR (CD3OD, 400
MHz): δ 7,90
(d, J = 9,1 Hz, 1H); 7,36 (d, J = 8,7 Hz, 2H); 6,98-6,91 (m, 3H);
6,83 (m, 1H); 6,74-6,68 (m, 3H); 5,10 (s, 2H); 4,44 (m, 1H); 4,27
(dd, J = 4,0, 9,4 Hz, 1H); 4,10 (dd, J = 5,4, 9,4 Hz, 1H); 3,80
(s, 3H); 3,77-3,40 (m, 6H); 3,12 (s, 2H); 2,30 (m, 2H); 2,15 (m,
2H).
APCI-MS: m/z 538 (MH+)
-
Schritt III:
-
(2S)-1-(5-Fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'yl)-3-(5-[(4-methoxybenzyl)oxy]-2-(pyrrolidin-1-ylcarbonyl)phenoxy]propan-2-ol
-
2-{[(2S)-3-(5-Fluor-1'H,3H-spiro[1-benzofuran-2,4'piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoesäure (Hydrochlorid)
(136 mg, 0,237 mmol) und N,N-Carbonyldiimidazol (46 mg, 0,284 mmol)
wurden in DMF (3 ml) aufgenommen, die Mischung wurde 55 Minuten
lang bei Raumtemperatur gerührt und
mit Pyrrolidin (168,5 mg, 2,37 mmol) versetzt und die Mischung wurde über Nacht
bei Raumtemperatur gerührt.
Die Reaktionsmischung wurde zwischen Essigsäureethylester und H2O verteilt. Die organische Phase wurde über Na2SO4 getrocknet,
filtriert und eingeengt. Der Rückstand
wurde durch Flash-Chromatographie
an Kieselgel (Methanol 0–1,5%
in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die im Untertitel genannte Verbindung (70 mg) erhielt.
APCI-MS:
m/z 552 (MH+).
-
Schritt IV:
-
3-{[(2S)-3-(5-Fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4(pyrrolidin-1-yl-carbonyl)phenol
-
(2S)-1-(5-Fluor-1'H,3H-Spiro[1-benzofuran-2,4'-piperidin]-1'yl)-3-[5-[(4-methoxybenzyl)oxy]-2-(pyrrolidin-1-ylcarbonyl)phenoxy]propan-2-ol
(65 mg, 0,11 mmol) wurde bei Raumtemperatur 25 Minuten lang mit
10% CF3CO2H in CH2Cl2 (3 ml) behandelt.
Die flüchtigen
Bestandteile wurden im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel (0–2,5%
Methanol in Dichlormethan, 0,2% NH4OH) aufgereinigt,
wodurch man die Titelverbindung (28 mg) erhielt.
1H-NMR
(CD3OD, 400 MHz): δ 7,07 (d, J = 8,2 Hz, 1H); 6,90
(dd, J = 2,6, 8,2 Hz, 1H); 6,77 (m, 1H); 6,63 (dd, J = 4,2, 8,7
Hz, 1H); 6,50 (d, J = 2,1 Hz, 1H); 6,44 (dd, J = 2,1, 8,3 Hz, 1H);
4,10 (m, 1H); 4,03 (dd, J = 4,3, 9,7 Hz, 1H); 3,96 (dd, J = 5,6,
9,7 Hz, 1H); 3,56 (t, J = 7,0 Hz, 2H); 3,34 (m, 2H, innerhalb des
Methanol-Peaks); 3,01 (s, 2H); 2,70 (bs, 4H); 2,56 (m, 2H); 2,01-1,78
(m, 8H).
APCI-MS: m/z 471 (MH+).
-
Beispiel 223
-
N-(4-Fluor-2-{[(2S)-3-(5-fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy)-phenyl)acetamid
-
Die
Titelverbindung wurde unter Verwendung von 5-Fluor-3H-spiro[1-benzofuran-2,4'-piperidin] wie in Beispiel
2 beschrieben dargestellt.
1H-NMR (Aceton-d6, 300 MHz): δ 8,63 (bs, 1H); 8,26-8,17 (m,
1H); 6,99-6,88 (m, 2H); 6,87-6,76 (m, 1H); 6,74-6,62 (m, 2H); 4,25-4,19 (m, 1H); 4,19-4,09
(m, 1H); 4,07-3,99 (m, 1H); 3,03 (s, 2H); 2,85 (bs, 1H); 2,78-2,60 (m, 4H); 2,60-2,54
(m, 2H); 2,10 (s, 3H); 1,97-1,76
(m, 4H).
APCI-MS: m/z 433 (MH+)
-
Beispiel 224
-
N-(5-Chlor-2-[3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropoxy]-4-hydroxyphenyl]cyclopentancarbonsäureamid
-
Schritt I:
-
5-Chlor-6-[(triisopropylsilyl)oxy]-1,3-benzoxazol-2(3H)-on
-
5-Chlor-6-hydroxy-1,3-benzoxazol-2(3H)-on
(0,93 g, 5 mmol) und Imidazol (1,00 g, 15 mmol) wurden unter Rühren in
einer inerten Atmosphäre
in Dimethylformamid (10 ml) gelöst.
Triisopropylsilylchlorid (1,15 g, 6 mmol) wurde zugegeben, und die
auf diese Weise erhaltene Lösung
wurde 3 Tage lang gerührt.
Die Reaktionsmischung wurde zwischen Wasser und Heptan verteilt.
Die organische Phase wurde mit Wasser gewaschen und über wasserfreiem
Magnesiumsulfat getrocknet, filtriert und eingeengt, wodurch man
1,45 g (85%) der im Untertitel genannten Verbindung in Form eines
grauen Feststoffs erhielt.
APCI-MS: m/z 342 [MH+]
-
Schritt II:
-
N-{5-Chlor-2-hydroxy-4-[(triisopropylsilyl)oxy]phenyl)-cyclopentancarbonsäureamid
-
Brom(cyclopentyl)magnesium
(0,58 ml, 1,16 mmol, 2 M in Diethylether) wurde unter einer inerten
Atmosphäre
zu einer Lösung
von 5-Chlor-6-[(triisopropylsilyl)oxy]-1,3-benzoxazol-2(3H)-on (66 mg, 0,19
mmol) in Tetrahydrofuran (3 ml) gegeben. Nach Rühren über Nacht bei 70°C wurde die
Lösung
eingedampft und in Essigsäureethylester
gelöst.
Die organische Phase wurde mit Wasser und 1 M Salzsäure gewaschen,
getrocknet und anschließend
eingeengt, wodurch man 68 mg (89%) der im Untertitel genannten Verbindung
in Form eines braunen Feststoffs erhielt.
APCI-MS: m/z 412
[MH+]
-
Schritt III:
-
N-{5-Chlor-2-(oxiran-2-ylmethoxy)-4-[(triisopropylsilyl)oxy]phenyl}cyclopentancarbonsäureamid
-
N-{5-Chlor-2-hydroxy-4-[(triisopropylsilyl)oxy]phenyl}-cyclopentancarbonsäureamid
(140 mg, 0,3 mmol) wurde in 1,4-Dioxan (20 ml) gelöst. Caesiumcarbonat
(170 mg, 0,5 mmol) wurde zugesetzt, gefolgt von 3-Nitrobenzolsulfonsäure-(2S)-oxiran-2-ylmethylester
(90 mg, 0,3 mmol). Nach Rühren über Nacht
bei Raumtemperatur wurde die Mischung zwischen Essigsäureethylester
und Wasser verteilt. Die organische Phase wurde mit Wasser gewaschen
und eingeengt. Die Aufreinigung durch HPLC an C18 (Xterra, 5 μm, 19 × 50 mm;
Acetonitril/Wasser 60/40 bis 100/0 im Verlauf von 15 Minuten) lieferte
25 mg (17%) des im Titel genannten Zwischenprodukts.
1H-NMR (300 MHz, (CDCl3) δ: 8,45 (1H,
s); 7,70 (1H, bs); 6,51 (1H, s); 4,27 (1H, dd); 3,88 (1H, dd); 3,39-3,34 (1H,
m); 2,98-2,95 (1H, m); 2,80 (1H, dd); 2,79-2,67 (1H, m); 2,02-1,61
(8H, m); 1,36-1,22 (3H, m); 1,17-1,05 (18H,
m).
APCI-MS: m/z 468 [MH+]
-
Schritt IV:
-
N-{5-Chlor-2-[3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropoxy]-4-hydroxyphenyl)cyclopentancarbonsäureamid
-
Eine
Lösung
von 5-Chlor-3H-spiro[1-benzofuran-2,4'-piperidin]
(11 mg, 0,05 mmol) und N-{5-Chlor-2-(oxiran-2-ylmethoxy)-4-[(triisopropylsilyl)oxy]phenyl}cyclopentancarbonsäureamid
(25 mg, 0,05 mmol) in Isopropanol (15 ml) wurde über Nacht bei 65°C gerührt und
dann eingeengt, wodurch man 34 mg (98%) N-{5-Chlor-2-[3-(5- chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropoxy]-4-[(triisopropylsilyl)oxy]phenyl}-cyclopentancarbonsäureamid
in Form eines hellbraunen Feststoffs erhielt, welcher in Dimethylformamid
(15 ml) und Wasser (1,5 ml) gelöst
wurde. Caesium carbonat (32 mg, 0,10 mmol) wurde zugesetzt. Die
Lösung
wurde über
Nacht bei Raumtemperatur gerührt
und dann zwischen Wasser und Essigsäureethylester verteilt. Die
organische Phase wurde mehrmals mit Wasser gewaschen, getrocknet
und eingeengt. Der Rückstand
wurde durch HPLC an C18 (Kromasil, 5 μm, Acetonitril/Wasser 10/90
bis 60/40 über
20 Minuten) aufgereinigt, wodurch man die Titelverbindung erhielt.
APCI-MS:
m/z 535 [MH+]
-
Beispiel 225
-
N-{5-Chlor-2-(3-(5-fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropoxy]-4-hydroxyphenyl}cyclopentancarbonsäureamid
-
Die
Titelverbindung wurde wie in Beispiel 224 beschrieben unter Verwendung
von 5-Fluor-3H-spiro[1-benzofuran-2,4'-piperidin] dargestellt.
APCI-MS:
m/z 519 [MH+]
-
Beispiel 226
-
N-{5-Chlor-4-hydroxy-2-12-hydroxy-3-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)propoxy]phenyl}cyclopentancarbonsäureamid
-
Die
Titelverbindung wurde wie in Beispiel 224 beschrieben unter Verwendung
von 3H-spiro[1-benzofuran-2,4'-piperidin] dargestellt.
APCI-MS:
m/z 501 [MH+]
-
Beispiel 227
-
N-(5-Chlor-2-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxyphenyl)benzamidtrifluoracetat
(Salz)
-
Schritt I:
-
N-(5-Chlor-2,4-dimethoxyphenyl)benzamid
Eine gerührte
Lösung
von (5-Chlor-2,4-dimethoxyphenyl)-amin (1,88 g, 10 mmol) und Triethylamin
(2,1 ml, 15 mmol) in DCM (50 ml) wurde unter Kühlen tropfenweise mit Benzoylchlorid
(1,3 ml, 11 mmol) versetzt. Die Umsetzung war nach 5 abgeschlossen.
Die Lösung wurde
nacheinander mit einer 1 M Lösung
von Natriumhydrogencarbonat (10 ml) und Wasser (3 × 10 ml)
gewaschen, getrocknet und im Vakuum eingeengt, wodurch man einen
Feststoff erhielt, welcher aus Essigsäureethylester (25 ml) umkristallisiert
wurde, wodurch man einen hellgrauen Feststoff (1,975 g, 67%) erhielt.
APCI-MS:
m/z 292 (MH+)
-
Schritt II:
-
N-(5-Chlor-2,4-dihydroxyphenyl)benzamid
-
Eine
gerührte
Lösung
von N-(5-Chlor-2,4-dimethoxyphenyl)benzamid (292 mg, 1 mmol) in
DCM (10 ml) wurde bei Raumtemperatur tropfenweise mit Bortribromid
in DCM (3 ml, 3 mmol) versetzt. Nach 30 Minuten bildete sich ein
Niederschlag. Es wurde über
Nacht weitergerührt.
Die Mischung wurde mit Methanol (5 ml) gequencht und im Vakuum eingeengt,
wodurch man ein Öl
erhielt, das ohne weitere Aufreinigung verwendet wurde.
APCI-MS:
m/z 264 (MH+)
-
Schritt III:
-
Benzoesäure-4-(benzoylamino)-2-chlor-5-hydroxyphenyl
ester
-
Rohes
N-(5-Chlor-2,4-dihydroxyphenyl)benzamid (1 mmol) in Aceton (10 ml)
wurde mit Kaliumcarbonat (280 mg, 2 mmol) und Benzoylchlorid (140
mg, 1 mmol) versetzt. Die Mischung wurde über Nacht bei Raumtemperatur
gerührt.
Das Lösungsmittel
wurde im Vakuum entfernt und der Rückstand wurde durch Flash-Chromatographie
an Kieselgel unter Verwendung eines Gradienten aus DCM und Methanol
aufgereinigt. Man erhielt die reine Verbindung in Form eines weißen Feststoffs
(153 mg, 42%).
1H-NMR (Aceton-d6, 400 MHz): δ 9,81 (bs, 1H); 9,39 (bs, 1H);
8,21 (d, J = 7,3 Hz, 2H); 8,16 (s, 1H); 8,06 (d, J = 7,3 Hz, 2H);
7,77 (t, J = 7,6 Hz, 1H); 7,68-7,55 (m, 5H); 7,07 (s, 1H).
APCI-MS:
m/z 368 (MH+)
-
Schritt IV:
-
Benzoesäure-4-(benzoylamino)-2-chlor-5-[(2S)-oxiran-2-ylmethoxy]phenylester
-
Eine
gerührte
Lösung
von Benzoesäure-4-(benzoylamino)-2-chlor-5-hydroxyphenylester
(103 mg, 0,28 mmol) und 3-Nitrobenzolsulfonsäure-[(2S)-2-methyloxiran-2-yl]-methylester (73 mg,
0,28 mmol) in DMF (3 ml) wurde mit Caesiumcarbonat (98 mg, 0,3 mmol)
versetzt. Es wurde über
Nacht weiter bei Raumtemperatur gerührt. Die Mischung wurde in
Wasser gegossen und zwischen Wasser und Essigsäureethylester verteilt. Die
organische Phase wurde mit Wasser gewaschen, getrocknet und im Vakuum
eingeengt, wodurch man einen weißen Feststoff (117 mg, 98%)
erhielt. Der Feststoff wurde ohne weitere Aufreinigung verwendet.
1H-NMR (Aceton-d6,
400 MHz): δ 9,06
(bs, 1H); 8,66 (s, 1H); 8,22 (d, J = 7,5 Hz, 2H); 8,02 (d, J = 7,5
Hz, 2H); 7,77 (t, J = 7,7 Hz, 1H); 7,64 (t, J = 7,7 Hz, 2H); 7,57
(t, J = 7,7 Hz, 2H); 7,30 (s, 1H); 4,57 (dd, J = 2,4, 11,5 Hz, 1H);
4,11 (dd, J = 6,2, 11,5 Hz, 1H); 3,49-3,43 (m, 1H); 2,90-2,87 (m,
1H); 2,81-2,78 (m, 2H).
APCI-MS: m/z 424 (MH+)
-
Schritt V:
-
N-(5-Chlor-2-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy)-4-hydroxyphenyl)benzamidtrifluoracetat
(Salz)
-
Eine
Lösung
von 5-Chlor-3H-spiro[1-benzofuran-2,4'-piperidin
(29 mg, 0,13 mmol) und Benzoesäure-4-(benzoylamino)-2-chlor-5-[(2S)-oxiran-2-ylmethoxy]-phenylester (55 mg,
0,13 mmol) in Ethanol (3 ml) wurde 2 Stunden lang bei 80°C gerührt. 1 M
NaOH (0,15 ml, 0,15 mmol) wurde zugesetzt, und es wurde 1 Stunde
lang bei 80°C
weitergerührt.
Das Lösungsmittel
wurde im Vakuum abgedampft und das Rohprodukt durch Flash-Chromatographie (Kieselgel,
Gradient von DCM und Methanol) aufgereinigt, wodurch man ein Öl (32 mg)
erhielt, das in Essigsäure
gelöst
und mit TFA angesäuert
wurde. Nach dem Lyophilisieren erhielt man die Titelverbindung in
Form eines weißen
amorphen Feststoffs (36 mg, 42%).
1H-NMR
(Aceton-d6, 400 MHz): δ 9,01 (s, 1H); 8,95 (bs, 1H);
8,24 (s, 1H); 8,23 (s, 1H); 8,03-7,98 (m, 2H); 7,59-7,49 (m, 3H);
7,24-7,22 (m, 1H); 7,14 (dd, J = 8,5, 2,3 Hz, 1H); 6,92 (s, 1H);
6,76 (d, J = 8,5 Hz, 1H); 4,66-4,58 (m, 1H); 4,21-4,12 (m, 2H);
3,80-3,53 (m, 3H); 3,53-3,36 (m, 3H); 3,17 (s, 2H); 2,38-2,16 (m,
4H).
APCI-MS: m/z 543 (MH+)
-
Beispiel 228
-
N-(5-Chlor-2-{[(2S)-3-(5-fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxyphenyl)benzamidtrifluoracetat
(Salz)
-
Die
Verbindung wurde unter Verwendung von 5-Fluor-3H- spiro[1-benzofuran-2,4'-piperidin] wie in
Beispiel 227 beschrieben dargestellt.
1H-NMR
(Aceton-d6, 400 MHz): δ 9,02 (bs, 2H); 8,23 (s, 1H);
8,22 (s, 1H); 8,01 (d, J = 7,3 Hz, 2H); 7,59-7,49 (m, 3H); 7,01
(d, J = 8,3 Hz, 1H); 6,94 (s, 1H); 6,88 (ddd, J = 9,0, 2,3 Hz, 1H);
6,73 (dd, J = 8,7, 4,2 Hz, 1H); 4,69-4,59 (m, 1H); 4,21-4,12 (m,
2H); 3,86-3,57 (m, 3H); 3,57-3,36 (m, 3H); 3,17 (s, 2H); 2,40-2,14
(m, 4H).
APCI-MS: m/z 527 (MH+)
-
Beispiel 229
-
N-(5-Chlor-2-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin)-1'-yl)-2-hydroxypropyl]oxy)-4-hydroxyphenyl)harnstofftrifluoracetat
(Salz)
-
Schritt I:
-
5-Chlor-2-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoylazid
-
Eine
gerührte
Suspension von 5-Chlor-2-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy)benzoesäurehydrochlorid
(235 mg, 0,4 mmol) in DCM (10 ml) wurde mit Triethylamin (60 μl, 0,4 ml)
versetzt, wodurch man eine Lösung
erhielt. Die Lösung
wurde mit Diphenylphosphorylazid (90 μl, 0,4 mmol) und Triethylamin
(60 μl,
0,4 mmol) versetzt. Die Mischung wurde über Nacht bei Raumtemperatur
gerührt.
Das Lösungsmittel
wurde im Vakuum abgedampft und der Rückstand wurde durch Flash-Chromatographie
(Kieselgel, DCM) aufgereinigt, worauf die im Untertitel genannte
Verbindung in Form eines unreinen farblosen Öls (235 mg) zurückblieb,
das ohne weitere Aufreinigung in dem nächsten Schritt eingesetzt wurde.
APCI-MS:
m/z 585 (MH+, Isocyanat)
-
Schritt II:
-
N-(5-Chlor-2-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxyphenyl)harnstofftrifluoracetat
(Salz)
-
Rohes 5-Chlor-2-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoylazid
(235 mg, < 0,4
mmol) wurde in Toluol (3 ml) gelöst
und unter Rühren
3 Stunden lang erhitzt. Die gelbe Lösung wurde auf Raumtemperatur
abgekühlt
und mit 0,5 M Ammoniak in Dioxan (1,6 ml, 0,8 mmol) versetzt, und
die Mischung wurde über
Nacht stehengelassen. Das Lösungsmittel
wurde im Vakuum abgedampft und der Rückstand wurde in 10% TFA in
DCM (5 ml) gelöst
und 1 Stunde lang stehengelassen. Das Lösungsmittel wurde im Vakuum
abgedampft, und der dunkle Rückstand
wurde durch präparative
HPLC unter Verwendung von Acetonitril/Wasser mit 0,1% TFA als Laufmittel
aufgereinigt. Die Titelverbindung wurde nach dem Lyophilisieren
in Form eines weißen
amorphen Feststoffs (6 mg, 2,5%) erhalten.
1H-NMR
(Aceton-d6, 400 MHz): δ 8,35 (s, 1H), 7,70 (bs, 1H),
7,25 (s, 1H), 7,14 (dd, J = 8,5, 2,0 Hz, 1H), 6,77 (d, J = 8,5 Hz,
1H), 6,65 (s, 1H), 5,92 (bs, 2H), 4,54 (m, 1H), 4,14 (d, J = 9,7
Hz, 1H), 4,02 (dd, J = 9,4, 5,1 Hz, 1H), 3,95-3,65 (m, 2H), 3,60-3,39
(m, 4H), 3,21 (s, 2H), 2,43-2,18 (m, 4H).
APCI-MS: m/z 482
(MH+)
-
Beispiel 230
-
N-(5-Chlor-2-{[(2S)-3-(5-fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-4-hydroxyphenyl)harnstofftrifluoracetat
(Salz)
-
Die
Verbindung wurde ausgehend von 5-Chlor-2-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'- yl)-2-hydroxypropyl]oxy}-4-[(4-methoxybenzyl)oxy]benzoesäure wie
in Beispiel 229 beschrieben dargestellt.
APCI-MS: m/z 466 (MH+)
-
Beispiel 231
-
N-(5-Chlor-2-{[(2S)-3-(5-fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy)-phenyl)harnstoff
-
Schritt I:
-
N-(5-Chlor-2-hydroxyphenyl)harnstoff
-
2-Amino-4-chlorphenol
(1,3 g, 8,9 mmol) wurde in 1 M HCl (10 ml) gelöst. Zum Einstellen des pH-Wertes
auf 5 wurde Ammoniumacetat zur Lösung
gegeben. Die gerührte
Mischung wurde mit einer Suspension von Kaliumcyanat (0,80 mg, 9,8
mmol) in Wasser versetzt und dann über Nacht bei Raumtemperatur
belassen. Das Wasser wurde abgedampft und der Rückstand wurde aus Wasser umkristallisiert,
wodurch man einen rosafarbenen Niederschlag (0,9 g, 55%) erhielt.
APCI-MS:
m/z 187 [MH+]
-
Schritt II:
-
N-{5-Chlor-2-[(2S)-oxiran-2-ylmethoxy]phenyl}harnstoff
-
Eine
Lösung
von N-(5-Chlor-2-hydroxyphenyl)harnstoff (0,9 g, 4,9 mmol) und 3-Nitrobenzolsulfonsäure-(2S)-oxiran-2-ylmethylester
(1,0 g, 3,8 mmol) in Dimethylformamid wurde unter Stickstoff gerührt. Die
Mischung wurde mit Caesiumcarbonat (1,9 g, 5,7 mmol) versetzt, und
der Ansatz wurde über
Nacht bei Raumtemperatur unter Stickstoff gerührt. Die Mischung wurde zwischen
Wasser und Dichlormethan verteilt, und die organische Phase wurde
mit Wasser gewaschen. Nach Trocknen, Filtrieren und Abdampfen des
Lösungsmittels
erhielt man 0,48 g (52%) der im Untertitel genannten Verbindung.
APCI-MS:
m/z 243 [MH+].
-
Schritt III:
-
N-(5-Chlor-2-{[(2S)-3-(5-fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-phenyl)harnstoff
-
N-{5-Chlor-2-[(2S)-oxiran-2-ylmethoxy]phenyl}harnstoff
(0,48 g, 2,0 mmol) und 5-Fluor-3H-spiro[1-benzofuran-2,4'-piperidin] (0,49
g, 2,0 mmol) wurden in 3 ml Ethanol gelöst. Die Reaktionsmischung wurde über Nacht
bei 80°C
gerührt.
Das Ethanol wurde abgedampft und die Mischung wurde durch Säulenchromatographie
(Dichlormethan/Methanol) und HPLC an C18 (Xterra) aufgereinigt,
wodurch man 35 mg (39%) der Titelverbindung erhielt.
1H-NMR (DMSO-d6,
400 MHz): δ 8,18
(d, J = 2,6 Hz, 1H); 7,92 (s, 1H); 7,07-6,97 (m, 2H); 6,91-6,84
(m, 2H); 6,73-6,68 (m, 1H); 6,33 (s, 2H); 4,88 (bs, 1H); 4,15-3,98 (m, 2H); 3,97-3,85
(m, 1H); 3,00 (s, 2H); 2,76-2,30
(m breit, 6H, teilweise vom Signal des Lösungsmittels überdeckt);
1,94-1,65 (m breit, 4H).
APCI-MS: m/z 450 [MH+]
-
Beispiel 232
-
N-(5-Chlor-2-{[(2S)-3-(5-chlor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}-phenyl)harnstoff
-
Die
Titelverbindung wurde unter Verwendung von 5-Chlor-3H-spiro[1-benzofuran-2,4'-piperidin] wie in Beispiel
231 beschrieben dargestellt.
APCI-MS: m/z 466 [MH+]
-
Beispiel 233
-
N-(2-{[(2S)-3-(5-Fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)-2-hydroxypropyl]oxy}phenyl)harnstoff
-
Die
Titelverbindung wurde ausgehend von 2-Aminophenol nach der in Beispiel
231 beschriebenen Vorschrift dargestellt.
1H-NMR
(DMSO-d6, 400 MHz): δ 8,08-8,01 (m, 1H); 7,77 (s,
1H); 7,08-7,03 (m, 1H); 7,00-6,95 (m, 1H); 6,92-6,80 (m, 3H); 6,75-6,69
(m, 1H); 6,16 (s, 2H); 4,90 (bs, 1H); 4,20-4,00 (m breit, 2H); 3,97-3,86
(m, 1H); 3,02 (s, 2H); 2,86-2,35 (m breit, 6H, teilweise vom Signal
des Lösungsmittels überdeckt);
2,02-1,67 (m breit, 4H).
APCI-MS: m/z 416,2 [MH+]
-
Beispiel 234
-
N-(2-{[(2S)-2-Hydroxy-3-(1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)propyl]oxy}phenyl)harnstoff
-
Die
Titelverbindung wurde ausgehend von 2-Aminophenol und 3H-Spiro[1-benzofuran-2,4'-piperidin] nach
der in Beispiel 231 beschriebenen Vorschrift dargestellt.
1H-NMR (Aceton-d6,
400 MHz): δ 8,25-8,21
(m, 1H); 7,81 (bs, 1H); 7,17-7,13 (m, 1H); 7,10-7,04 (m, 1H); 7,02-6,96 (m, 1H); 6,92-6,84
(m, 2H); 6,81-6,75 (m, 1H); 6,69 (d, J = 7,6 Hz, 1H); 5,60 (bs,
2H); 4,18-4,09 (m, 2H); 4,02-3,94 (m, 1H); 3,01 (s, 2H); 2,82-2,53
(m, 6H, teilweise vom Signal des Lösungsmittels überdeckt); 1,95-1,77
(m, 4H).
APCI-MS: m/z 398 [MH+]
-
Beispiel 235
-
N-(4-Fluor-2-{[(2S)-3-(5-fluor-1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl}-2-hydroxypropyl]oxy)-phenyl)harnstoff
-
Die
Titelverbindung wurde ausgehend von 2-Amino-5-fluorphenol und 5-Fluor-3H-spiro[1-benzofuran-2,4'- piperidin] nach der in Beispiel 231
beschriebenen Vorschrift dargestellt.
1H-NMR
(Aceton-d6, 400 MHz): δ 8,17 (dd, J = 9,0, 6,4 Hz,
1H); 7,75 (bs, 1H); 6,97-6,92 (m, 1H); 6,87-6,79 (m, 2H); 6,69-6,60
(m, 2H); 5,68 (bs, 2H); 4,21-4,12 (m, 2H); 4,06-3,97 (m, 1H); 3,04
(s, 2H); 2,81-2,55 (m, 6H, teilweise vom Signal des Lösungsmittels überdeckt);
1,97-1,79 (m, 4H).
APCI-MS: m/z 434,2 [MH+]
-
Beispiel 236
-
N-(4-Fluor-2-{[(2S)-2-hydroxy-3-(1'H,3H-spiro[1-benzofuran-2,4'-piperidin]-1'-yl)propyl]oxy}phenyl)-harnstoff
-
Die
Titelverbindung wurde ausgehend von 2-Amino-5-fluorphenol und 3H-Spiro[1-benzofuran-2,4'-piperidin] nach
der in Beispiel 231 beschriebenen Vorschrift dargestellt.
1H-NMR (Aceton-d6,
400 MHz): δ 8,21-8,15
(m, 1H); 7,71 (bs, 1H); 7,15 (d, J = 7,3 Hz, 1H); 7,07 (t, J = 7,7
Hz, 1H); 6,88-6,82 (m, 1H); 6,79 (t, J = 7,4 Hz, 1H); 6,69 (d, J
= 7,9 Hz, 1H); 6,67-6,60 (m, 1H); 5,64 (bs, 2H); 4,22-4,11 (m, 3H);
4,05-4,00 (m, 1H); 3,02 (s, 2H); 2,90-2,57 (m, 6H, teilweise vom
Signal des Lösungsmittels überdeckt);
1,97-1,79 (m, 4H).
APCI-MS: m/z 416,2 [MH+]
-
THP-1-Chemotaxis-Assay
-
Einführung
-
Mit
dem Assay mißt
man die durch MIP-1α-Chemokin
in der humanen monozytischen Zellinie THP-1 hervorgerufenen chemotaktischen
Reaktionen. Die Verbindungen der Beispiele wurden anhand ihrer Fähigkeit,
die chemotaktische Reaktion auf eine Standardkonzentration. von
MIP-1α-Chemokin
zu unterdrücken, beurteilt.
-
Methoden
-
Kultivierung von THP-1-Zellen
-
Die
Zellen wurden aus gefrorenen Aliquots bei 37°C schnell aufgetaut und in einem
25-cm-Kolben mit 5 ml RPMI-1640-Medium mit Glutamax und 10% hitzeinaktiviertem
fetalem Kälberserum
ohne Antibiotika (RPMI + 10%HIFCS) resuspendiert. An Tag 3 wird
das Medium verworfen und durch frisches Medium ersetzt.
-
THP-1-Zellen
werden routinemäßig in RPMI-1640-Medium
mit 10% hitzeinaktiviertem fetalem Kälberserum und Glutamax, aber
ohne Antibiotika kultiviert. Für
ein optimales Wachstum der Zellen ist es erforderlich, daß sie alle
3 Tage passagiert werden und die minimale Dichte der Subkultur 4 × 105 Zellen/ml beträgt.
-
Chemotaxis-Assay
-
Zellen
wurden aus dem Kolben entnommen und durch Zentrifugieren in RPMI
+ 10%HIFCS + Glutamax gewaschen. Die Zellen wurden dann zu 2 × 107 Zellen/ml in frischem Medium (RPMI + 10%HIFCS
+ Glutamax), dem Calcein-AM (5 μl
einer Stammlösung
auf 1 ml für
eine Endkonzentration von 5 × 10–6 M)
zugesetzt worden war, resuspendiert. Nach vorsichtigem Mischen wurden
die Zellen in einem CO2-Inkubator 30 Minuten bei
37°C inkubiert.
Die Zellen wurden dann mit Medium auf 50 ml verdünnt und zweimal durch Zentrifugieren bei
400 × g
gewaschen. Die markierten Zellen wurden dann bei einer Zellkonzentration
von 1 × 107 Zellen/ml resuspendiert und bei 37°C in einem
CO2-Feuchtinkubator 30 Minuten mit dem gleichen
Volumen an MIP-1α-Antagonist
(Endkonzentration 10–10 M bis 10–6 M)
inkubiert.
-
Der
Chemotaxis-Assay wurde mit Neuroprobe-Chemotaxisplatten mit 96 Vertiefungen
unter Verwendung von 8-μm- Filtern (Kat.-Nr.
101-8) durchgeführt.
In dreifacher Ausführung
wurden zu den unteren Vertiefungen der Platte 30 Mikroliter Chemoattraktans,
ergänzt
mit verschiedenen Konzentrationen von Antagonisten oder Vehikel,
gegeben. Dann wurde das Filter vorsichtig darauf angeordnet, wonach
25 μl der
mit der entsprechenden Konzentration von Antagonist oder Vehikel
vorinkubierten Zellen auf die Oberfläche des Filters gegeben wurden.
Die Platte wurde dann bei 37°C
in einem CO2-Feuchtinkubator 2 Stunden inkubiert.
Die auf der Oberfläche
verbliebenen Zellen wurden dann durch Adsorption entfernt, wonach
die gesamte Platte 10 Minuten bei 2000 U/min zentrifugiert wurde.
Nach Entfernung des Filters wurden die Zellen, die in die unteren Vertiefungen
gewandert waren, durch die Fluoreszenz von zellassoziiertem Calcein-AM
quantitativ bestimmt. Die Zellmigration wurde dann nach Subtraktion
des Reagens-Blindwerts in Fluoreszenzeinheiten ausgedrückt, und
die Werte wurden durch Vergleich der Fluoreszenzwerte mit dem Wert
einer bekannten Zahl markierter Zellen auf Migration standardisiert.
Durch Vergleich der Zahl der gewanderten Zellen mit Vehikel wurde
die Wirkung von Antagonisten als % Inhibierung berechnet.